-
Gebiet der Erfindung
-
Diese
Erfindung betrifft im allgemeinen getragene Katalysatoren auf der
Basis von anderen Übergangsmetallen
als Platin und deren Verwendung in Brennstoffzellen, die für eine Vielzahl
von Verwendungen als Anoden und Kathoden in Brennstoffzellen, Reformerkatalysatoren,
Oxidationskatalysatoren, Wassergas-Verschiebungskatalysatoren, Metall-Luftbatterien,
Sauerstoffsensoren und Sauerstoffrekombinationskatalysatoren geeignet
sind. Insbesondere betrifft diese Erfindung Katalysatoren, die spezifisch
für die
Anwendung als Alkohol-Toleranzkathodenmaterialien für die katalytische
Sauerstoffreduktion oder Anodenmaterialien für die katalytische Oxidation
von Brennstoffmolekülen
bestimmt sind.
-
Stand der Technik
-
Brennstoffzellen
sind elektrochemische Vorrichtungen, die chemische Energie einer
Reaktion direkt in elektrische Leistung umwandeln. In solchen Zellen
werden ein Brennstoff (allgemein Wasserstoff, Alkohole oder gesättigte Kohlenwasserstoffe)
und ein Oxidationsmittel (allgemein Sauerstoff von Luft) kontinuierlich
zu den Elektroden geführt.
Theoretisch kann eine Brennstoffzelle elektrische Energie erzeugen,
so lange der Brennstoff und das Oxidationsmittel zu den Elektroden
geführt
werden. In der Realität
beschränkt
der Abbau oder die schlechte Funktion der Komponenten die praktische
Arbeitsdauer der Brennstoffzellen.
-
Eine
Vielzahl von Brennstoffzellen befindet sich in unterschiedlichen
Entwicklungsstufen; insbesondere unter der Berücksichtigung, dass Brennstoffzellen,
bei denen Elektrokatalysatoren des in dieser Erfindung beschriebenen
und beanspruchten Typs verwendet werden können, können folgende Beispiele erwähnt werden:
polymere Elektrolyt-Brennstoffzellen (PEFC), angetrieben mit H2, direkte Oxidations-Brennstoffzellen (DOFC),
angetrieben mit Alkoholen (direkte Alkohol-Brennstoffzelle, DAFC)
oder mit irgendwelchen anderen wasserstoffhaltigen flüssigen oder
gasförmigen
Brennstoffen (Alkohole, Glycole, Aldehyde, gesättigte Kohlenwasserstoffe,
Carbonsäuren
etc.), Phosphorsäure-Brennstoffzellen
(PAFC) und geschmolzene Carbonat-Brennstoffzellen (MCFC).
-
Essentielle
Komponenten von jeder Brennstoffzelle der erwähnten Arten sind die Elektroden,
die im allgemeinen Metalle oder Metallteilchen enthalten, die auf
porösen
Kohlenstoffmaterialien getragen werden, die an einen geeigneten
Leiter gebunden sind. Üblicherweise
für die
Reduktion von Sauerstoff verwendete Katalysatoren umfassen Übergangsmetalle
wie Platin, Nickel, Kobalt, Silber, um einige zu erwähnen. Üblicherweise
für die
Oxidation des Brennstoffes verwendete Katalysatoren (beispielsweise
H2 bei PEFC und Methanol bei den direkten
Methanol-Brennstoffzellen (DMFC)) sind Platin, Platin-Ruthen, Platin-Ruthen-Molybdän und Platin-Zinn-Mischungen.
Alle Brennstoffzellen, die ein akzeptables Zellpotential (> 0,5 V) erzeugen, enthalten Platin
alleine oder zusammen mit anderen Metallen, bevorzugt Ruthen an
der Anode, während
die Kathode im allgemeinen durch Platin gebildet wird, wobei andere
Metalle gleichermaßen
verwendet werden können.
Das bevorzugte Vorhandensein von Platin, allgemein in hohen Beladungen,
bedeutet eine hauptsächliche ökonomische
Beschränkung
bezüglich
der Massenproduktion von Brennstoffzellen für den Transport, Funktelephone
und elektrische Vorrichtungen im allgemeinen. Tatsächlich tragen
die hohen Kosten von Platin (gegenwärtig etwa 25-30 USD/g) dazu
bei, dass die Kosten der Energie, erzeugt durch eine Brennstoffzelle,
viel höher
sind als die Kosten von anderen Energieerzeugungsalternativen. Darüber hinaus
sind Kathoden auf Platinbasis in DMFC bezüglich Methanol empfindlich.
Angesichts der höheren
Effizienz von Brennstoffzellen im Vergleich zu traditionellen Energieerzeugungsmethoden
ebenso wie deren umweltschädliche
Natur ist es sehr gewünscht, Brennstoffzellen
zu entwickeln, die kein Platin erfordern.
-
Nach
Kenntnis des Anmelders ist Platin eine essentielle Komponente in
den Anoden für
DOFCS oder PEFC, die gegenwärtig
erhältlich
sind.
-
US-A-4,828,941
beschreibt Methanol/Luft-Brennstoffzellen, bei denen die Kathode
als katalytische Komponente eine Co(Salen)Verbindung oder ein Polymer
mit dieser Verbindung enthält.
Es ist nicht möglich, auf
Platin als Katalysator für
die Oxidation von Methanol in der beanspruchten elektrochemischen
Zelle zu verzichten.
-
in
US-A-6,245,707 wird die Synthese von methanoltoleranten Kathoden
für die
Sauerstoffreduktion erläutert,
erhalten durch Vermischen und Wärmebehandeln
von zumindest zwei unterschiedlichen Übergangsmetall-haltigen Stickstoffchelaten.
Die Stickstoffchelate umfassen Metallporphyrine und bevorzugte Übergangsmetalle
sind Eisen, Kobalt, Nickel, Kupfer, Mangan, Ruthen, Vanadium und
Zink.
-
Katalysierte
Kathoden für
Brennstoffzellen, umfassend eine Mischung von Kobaltacetat und Polyacrylnitril
sind in US-A-5,358,803 beschrieben.
-
US-A-5,240,893
beschreibt ein Verfahren zur Herstellung von Elektroden, insbesondere
Kathoden, gebildet mit einem pyrolisierten Metall-Heterokohlenstoff-Stickstoffmaterial,
bei dem das Metall Kobalt, Nickel, Eisen, Kupfer, Vanadium, Chrom
und Mangan und Mischungen davon ist. Ein Polymer wird erhalten durch
Reaktion einer Aminverbindung mit Formaldehyd oder polymerisiertem
Formaldehyd in der Gegenwart eines Alkalikatalysators. Das isolierte
oder in situ gebildete Polymer wird mit Kohlenstoffteilchen und
einem Metallsalz reagiert, unter Erhalt eines polymerisierten Produkts
in Form eines Gels, das für
1 h bei 800°C
gebacken wird. Das resultierende Pulver wird mit einem Bindemittel
gemischt und verwendet, um Elektroden zu erzeugen. Unabhängig vom
Metalldotiermittel besteht die spezifische Energie, die durch diese
Kathoden erhalten wird, aus einigen zehn mW/cm2 bei
einer niedrigen Stromdichte.
-
DE-A-25
49 083 berichtet von der Herstellung von platinfreien Kathoden für Brennstoffzellen
auf der Basis von Eisenphthalocyaninen.
-
WO-A-0196264
beschreibt Fischer-Tropsch-Katalysatoren, die durch eine Matrix
mit einem Polymer, im allgemeinen Polyacrylat oder Polymethacrylat,
und zumindest zwei Metallen aufgebaut ist, von denen eines Eisen,
Kobalt, Nickel und Chrom ist und das andere Metall Eisen, Silber,
Zinn, Platin, Zirkonium oder Mischungen davon.
-
Beschreibung der Zeichnungen
-
1 bedeutet
eine schematische Querschnittsansicht einer vereinfachten Brennstoffzelle,
die mit dem Katalysator dieser Erfindung arbeitet.
-
2 zeigt
anodische Polarisationskurven für
unterschiedliche Materialien in 2N H2SO4-1N CH3OH Lösung, die
mit Luft gesättigt
ist.
-
3 zeigt
die kathodischen Polarisationskurven für unterschiedliche Materialien
in 2N H2SO4-1N CH3OH Lösung,
die mit Luft gesättigt
ist.
-
4 zeigt
anodische Polarisationskurven für
unterschiedliche Materialien in 1N KOH-1N CH3OH
Lösung,
die mit Luft gesättigt
ist.
-
5 zeigt
die kathodischen Polarisationskurven für unterschiedliche Materialien
in 1N KOH-1N CH3OH Lösung, die mit Luft gesättigt ist.
-
6 zeigt
die Änderung
der Leistung eines DMFC unter Verwendung der Elektroden, die mit
Katalysatoren dieser Erfindung erzeugt sind, im Verlaufe der Zeit.
-
7 zeigt
in einem Fließdiagramm
die verschiedenen Arbeitsschritte von den Ausgangsreagenzien zur
Herstellung des Polymers bis zu den metall dotierten katalytischen
Materialien, die zur Erzeugung der Elektroden verwendet werden.
-
Detaillierte
Beschreibung der Erfindung
-
Der
Anmelder hat nun festgestellt, dass neue bestimmte Polymere gebildet
durch Kondensation von 4-{1-[(2,4-Di(substituiertem)-phenyl)-hydrazono]-alkyl}-benzol-1,3-diol
mit einem 3,5-disubstituierten Phenol und Formaldehyd oder Paraformaldehyd,
Koordinaten-Übergangsmetallsalze
nach Behandlung mit angemessenen Reduktionsmitteln und Immobilisierung
auf Trägermaterialien
(porösen
Kohlenstoffen, Graphit, metallischen Pulvern etc.), die sehr effiziente
Katalysatoren für
elektrochemische Zellen sind, die beispielsweise Energien bei Umgebungstemperatur
und einem Druck von 160 mW/cm2 ergeben können, wenn
die Verbrennung direkt mit Methanol erfolgt, und 300 mW/cm2 ergeben können, wenn mit H2 angetrieben
wird, erhalten werden.
-
Gemäß einem
ersten Ausführungsbeispiel
betrifft dieser Erfindung daher Stickstoff-Sauerstoff-Kohlenstoff-Polymere
(nachfolgend mit P bezeichnet), die für die Koordination von anderen
Metallsalzen als Platinsalzen geeignet sind.
-
Gemäß dieser
Erfindung sind mit Stickstoff-Sauerstoff-Kohlenstoff-Polymeren Polymere
gemeint, erhalten durch Kondensation eines 4-{1-[(2,4-Di(substituierten)-phenyl)-hydrazono]-alkyl}-benzol-1,3-diols
mit einem 3,5-disubstituierten Phenol und Formaldehyd oder Paraformaldehyd
in der Gegenwart eines basischen (z.B. NaOH) oder sauren (z.B. HCl)
Katalysators in Wasser/Alkohol-Mischungen als Lösungsmittel und bei einer Temperatur,
die zur Bildung einer Methylol-Zwischenverbindung (entsprechend
Schema I) ausreichend ist.
-
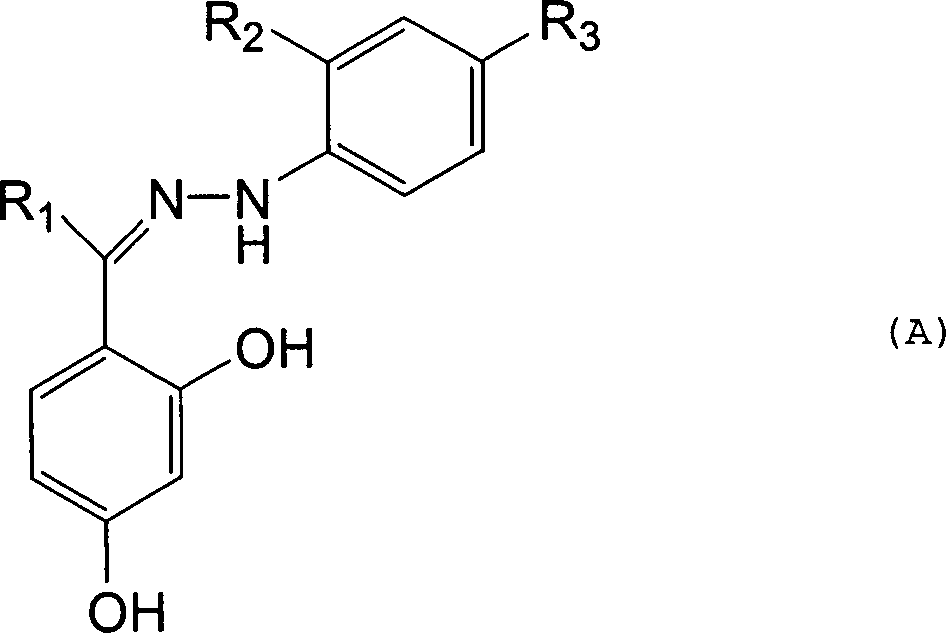
Als
4-{1-[(2,4-Di(substituiertes)-phenyl)-hydrazono]-alkyl}-benzol-1,3-diol gemäß dieser
Erfindung ist eine Verbindung mit der Formel (A) gemein
worin R
1 aus
der Gruppe ausgewählt
ist, bestehend aus: Wasserstoff und einem Kohlenwasserstoffradikal,
bevorzugt aliphatisch, mit 1 bis 10 Kohlenstoffatomen, gegebenenfalls
halogeniert, mehr bevorzugt Methyl oder Ethyl.
-
R2 und R3 sind jeweils
unabhängig
bevorzugt eine Elektronen ziehende Gruppe, ausgewählt aus
der Gruppe bestehend aus Wasserstoff, Halogen, Acyl, Ester, Carbonsäure, Formyl,
Nitril, Sulfonsäure,
linearen oder verzweigten Alkyl- oder Arylgruppen mit 1 bis 15 Kohlenstoffatomen,
wahlweise funktionalisiert mit Halogenen oder aneinander gebunden,
zur Bildung von einem oder mehreren kondensierten Ringen mit dem
Phenylring, und Nitrogruppen.
-
Als
3,5-disubstituiertes Phenol gemäß dieser
Erfindung ist eine Verbindung der Formel (B) gemeint:
worin R
4 und
R
5 jeweils unabhängig eine Elektronen gebende
Gruppe sind, ausgewählt
aus der Gruppe bestehend aus Wasserstoff, Hydroxyl, Ether, Aminen,
Aryl- und linearen und verzweigten Alkylgruppen mit 1 bis 15 Kohlenstoffatomen.
-
Gemäß dieser
Erfindung bedeutet Acyl eine COR'-Gruppe,
worin R' bevorzugt
C1-10-Alkyl oder Aryl ist, Ester eine Gruppe
COOR' ist, worin
R' wie oben definiert
ist, Ether eine Gruppe OR' ist,
worin R' wie oben
definiert ist, Amine eine Gruppe NR''R''' sind,
worin R'' und R''' gleich
oder verschieden voneinander sind und H, C1-6-Alkyl,
Aryl bedeuten, wobei in den oben angegebenen Definitionen Aryl bevorzugt
Phenyl, Naphthyl und höhere
Homologe bedeutet.
-
Unter
Formaldehyd und Paraformaldehyd ist das zweitgenannte bevorzugt.
-
Die
Stickstoff-Sauerstoff-Kohlenstoff-Polymere P werden wie nachfolgend
gezeigt als ziegelrote Feststoffe erhalten, die im allgemeinen in
polaren organischen Lösungsmitteln
wie Dimethylsulfoxid, Dimethylformamid, 1,4-Dioxan, Aceton, Tetrahydrofuran
löslich
sind.
-
Die
wahrscheinlichste Struktur von P ist ähnlich zu der eines phenolischen
Harzes (Bakelit) mit Phenoleinheiten, die durch 4-{1-[(2,4-Di(substituierte)-phenyl)-hydrazono]-alkyl}-benzol-1,3-diol-Einheiten
ersetzt sind, die zum Modulieren der chemisch-physikalischen Eigenschaften
des Polymers selbst beitragen. Weil die beiden Phenolderivate (A)
und (B) jeweils mit Formaldehyd reagieren können, unter Erzeugung eines
makromolekularen Struk tur, kann eine weitere Modulierung von P durch
Variieren des anfänglichen
molaren Verhältnisses
(A/B) erzielt werden; bevorzugt ist erfindungsgemäß ein solches
anfängliches
molares Verhältnis
a/b zwischen 0,5 und 2, und mehr bevorzugt 0,7.
-
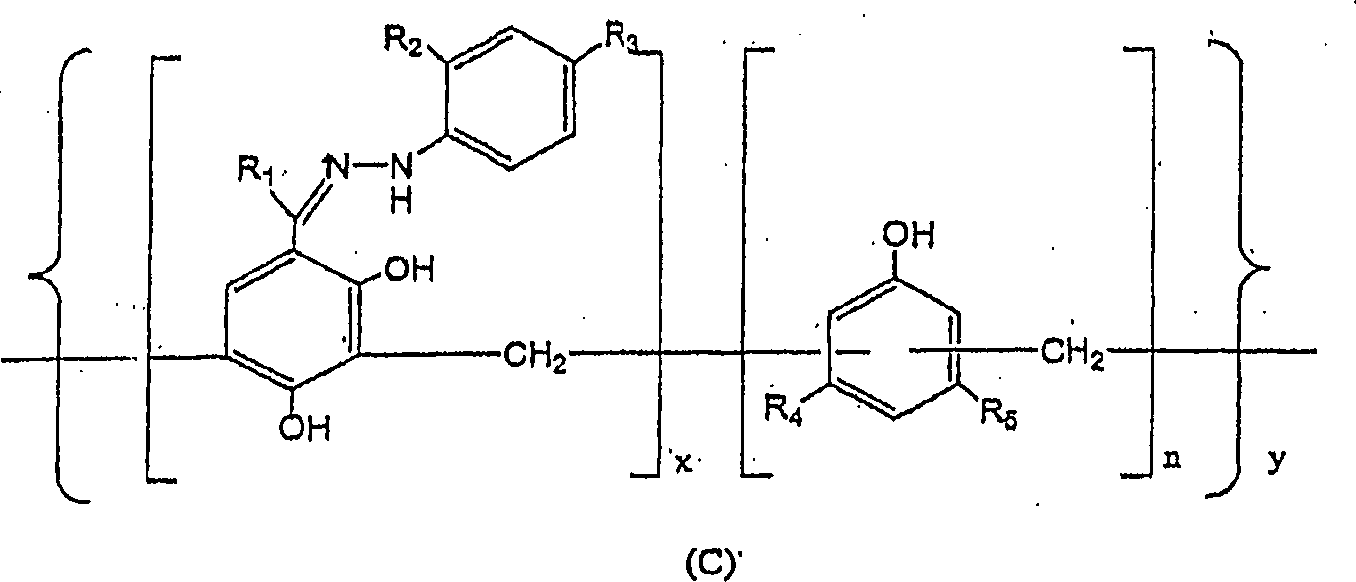
Das
Polymer dieser Erfindung kann ebenfalls durch die folgende Formel
(C) dargestellt werden:
worin
y von 2 bis 120 variieren kann, x zwischen 1 und 2 variieren kann,
n zwischen 1 und 3 variieren kann und R
1,
R
2, R
3, R
4 und R
5 wie oben
definiert sind.
-
Wie
ein Fachmann realisieren kann, der die obige Formel betrachtet,
hat das Polymer P gemäß dieser Erfindung
verfügbare
Stickstoff- und Sauerstoffatome zum Binden von Metallzentren, bevorzugt
auf Chelatisierungsart. IR- und NMR-Spektren von P zeigen eindeutig
das Vorhandensein von NH- und OH-Gruppen. Die P-Materialien können bei
150°C für einige
Stunden an Luft ohne Zersetzung getrocknet werden. Die Molekulargewichte
im Zahlenmittel können
in einem breiten Bereich moduliert werden, und zwar zwischen etwa
1.000 bis etwa 50.000, indem angemessen die experimentellen Bedingungen
variiert werden.
-
Gemäß einem
bevorzugten Verfahren zur Herstellung werden die Polymere P dieser
Erfindung durch Kondensation eines 4-{1-[(2,4-Di(substituierten)-phenyl)-hydrazono]-alkyl}-benzol-1,3-diols
mit einem 3,5-disubstituierten Phenol und Formaldehyd oder Paraformaldehyd
in Gegenwart eines basischen (z.B. NaOH) oder sauren (z.B. HCl)
Katalysators in Wasser/Alkohol-Mischungen als Lösungsmittel bei einer Temperatur
erhalten, die zur Bildung einer Methylol-Zwischenproduktverbindung
ausreichend ist (entsprechend dem folgenden Schema I):
Schema
I worin R
1, R
2,
R
3, R
4 und R
5 wie oben definiert sind.
-
Die
4-{1-[(2,4-Di(substituierten)-phenyl)-hydrazono]-alkyl}-benzol-1,3-diol-Reagenzien
werden über Kondensation
von angemessenen 4-Acyl/Formyl-benzol-1,3-diolen mit 2,4-disubstituierten
Phenylhydrazinen synthetisiert.
-
Die
Polymere P werden ebenfalls in einem Ein-Topf- oder Kaskadenvorgang
unter Verwendung von 4-Acyl/Formyl-benzol-1,3-diol, 2,4-disubstituiertem
Phenylhydrazin, 3,5-disubstituierten Phenolen und Formaldehyd oder
Paraformaldehyd mit den oben erwähnten
Substituenten als getrennte Komponenten erhalten.
-
Bevorzugt
ist die Reaktionstemperatur zwischen etwa 20 bis etwa 150°C und der
pH-Wert liegt im Bereich von etwa 1 bis etwa 14.
-
Gemäß einem
zweiten Ausführungsbeispiel
betrifft diese Erfindung einen Komplex, bestehend aus einem Polymer
wie oben beschrieben und einem Metallsalz.
-
Tatsächlich ermöglichen
die ausgezeichneten Bindeeigenschaften von P die stabile Komplexierung
einer großen
Vielzahl von Metallsalzen, bevorzugt Übergangsmetallsalzen und mehr
bevorzugt Eisen-, Kobalt- und Nickelcarboxylaten, -halogeniden,
-alcoholaten, -acetylacetonaten, -formiaten, -oxalaten, -malonaten
und analogen organischen Salzen und Mischungen davon.
-
Anorganische
Salze wie Carbonate, Oxide und Bicarbonate etc. und Mischungen davon
sind ebenfalls geeignet für
den Zweck, vorausgesetzt, dass sie gemäß der Kenntnis der anorganischen
Chemie in der Lage sind, mit dem Polymer P in der Reaktionsumgebung
zur Bildung eines Koordinationskomplexes zu interagieren.
-
Fe-,
Co- und Ni-Acetate (und Mischungen davon) sind besonders bevorzugt.
-
Die
Komplexe dieser Erfindung können
durch Rühren
einer Suspension von P mit einem Metallsalz oder einer Mischung
von Metallsalzen, mehr bevorzugt Nickel(II)-, Eisen(II)- und Kobalt(II)-Salzen,
aufgelöst bevorzugt
in Wasser oder Wasser/Alkohol, erhalten werden. Die Reaktion erzeugt
ein Material, bei dem die Metallsalze stark an P gebunden sind und
den Oxidationszustand der molekularen Vorläufer aufrechterhalten. Die
erhaltenen metalldotierten Materialien, nachfolgend als P-M angegeben
(M = Hauptgruppe oder Übergangsmetall)
sind sehr stabil; sie können
mehrere Male mit siedendem Wasser ohne Verlust der verankerten Metallsalze
gewaschen werden.
-
Nach
dem oben beschriebenen bevorzugten Vorgang kann die gesamte Metallkonzentration
in den metalldotierten Materialien P-M angemessen in dem Bereich
von 0,5 bis 10 Gew.% variiert werden.
-
Die
Reaktion von P mit zwei Metallsalzen in einem gewünschten
Verhältnis
oder die Reaktion von P mit n-Metallsalzen in den gewünschten
Verhältnissen
ergibt P-M-Materialien, bei denen das ursprüngliche Verhältnis der
zugegebenen Metalle vollständig
aufrechterhalten wird. Daher ergibt die Reaktion von P mit beispielsweise
Fe(OAc)2, Ni(OAc)2 und
Co(OAc)2 (OAc = Acetat) in einem stöchiometrischen
1:1:1 Verhältnis
ein P-M-Material, umfassend Eisen(II)-, Nickel(II)- und Kobalt(II)-Ionen
in einem molaren 1:1:1 Verhältnis.
-
Gemäß einem
weiteren Ausführungsbeispiel
betrifft diese Erfindung Katalysatoren, erhalten aus den beschriebenen
P-M-Materialien, und Elektroden für Brennstoffzellen, umfassend
solche Katalysatoren zusammen mit einem geeigneten leitenden Träger. Darüber hinaus
betrifft diese Erfindung auch Brennstoffzellen, umfassend die Elektroden
gemäß dieser
Erfindung.
-
Die
Katalysatoren dieser Erfindung umfassen andere Metalle als Platin,
mehr bevorzugt Nickel, Kobalt, Eisen und Mischungen davon, und sind
unerwartet in der Lage, die Reduktion von Sauerstoff ebenso wie die
Oxidation von verschiedenen gasförmigen
und flüssigen
Substraten (H2, Methancl, Ethylenglycol
und höhere
Glycole, Benzin, Formaldehyd, Hydrazin, um einige zu nennen) zu
katalysieren. Der Anmelder hat auch festgestellt, dass diese Katalysatoren
effiziente Elektroden für
unterschiedliche Arten von Brennstoffzellen bilden. Insbesondere
hat der Anmelder überraschenderweise
festgestellt, dass die Anode das Vorhandensein von Nickel alleine
oder in binären
und ternären
Kombinationen mit Kobalt und Eisen erfordert, während gemäß einem bevorzugten Verfahren
die Kathode Nickel oder Kobalt alleine enthält. Darüber hinaus sind die Kathoden
dieser Erfindung vollständig
tolerant gegenüber
vorhandenen Alkoholen, was die Verwendung von höheren Alkoholkonzentrationen
(bis zu 50 Vol.%) als bei DAFC auf Platinbasis ermöglicht.
-
Zur
Erzeugung der Katalysatoren dieser Erfindung werden die P-M-Materialien
mit Reduktionsmitteln entweder im festen Zustand mit H2 oder
in Fluidlösungssystemen
behandelt. Daher wird eine feste Probe des P-M-Materials in einem Lösungsmittel dispergiert, bevorzugt
Wasser/Alkohol-Mischungen,
und wird dann mit einer Lösung
eines Reduktionsmittels, bevorzugt einer wässrigen Hydrazinlösung, mehr
bevorzugt einer Lösung
aus einem Tetrahydroboratsalz [Y]BH4 bei
einer Temperatur zwischen –10
und 30°C
behandelt, worin Y ein Alkalimetallkation wie Li+,
Na+, K+ oder ein
organisches Kation wie Tetraalkylammonium (NR4)+ und Bis(triphenylphosphoranyliden)ammonium
(PPM+), um nur einige zu nennen, ist.
-
Gemäß einem
anderen Verfahren zur Erzeugung der erfindungsgemäßen Katalysatoren
wird eine feste Probe des P-M-Materials bei einer angemessenen Temperatur
zwischen 50 und 1.000°C,
bevorzugt 800°C, unter
Inertgasschutz (z.B. N2, Ar) für etwa 2
Stunden gebacken.
-
In
einem bevorzugten Verfahren zur Erzeugung der erfindungsgemäßen Katalysatoren,
insbesondere zur Bildung von Anoden für Brennstoffzellen, wie schematisch
in 1 veranschaulicht, werden die P-M-Materialien
zuvor entweder auf einem porösen
Kohlenstoffträgermaterial
(Vulkan XC-72, Aktivkohle RBDA, Standard R-5000, NSM-III, Ketjen-Ruß und Raven-1020,
Graphit etc.) oder anderen leitenden Trägermaterialien wie feingepulvertem
Silber, Nickel und anderen vor der Behandlung mit Reduktionsmitteln
entweder im festen Zustand oder in Fluidlösungssystemen getragen. Die
Reduktion der Metallzentren tritt mit der Bildung von Heterokohlenstoff-getragenen
Metallteilchen (HC-P-M) auf, worin M durch ein Einzelmetall oder
eine Mischung von anderen Metallen als Platin gebildet ist.
-
Gemäß einem
anderen bevorzugten Verfahren zur Erzeugung von Anoden für Brennstoffzellen
werden feste P-M-Materialien mit einem H2-Fluß bei etwa
350 bis 400°C
für etwa
1 bis 2 Stunden behandelt.
-
Aufgrund
der ausgezeichneten Affinität
von P für
Metallsalze kann der Heterokohlenstoff-getragene Katalysator HC-P-M
ebenfalls in einem Ein-Topf- oder
Kaskadenvorgang durch Mischen von P, einem Metallsalz oder mehr
als einem Salz von unterschiedlichen Metallen und dem Kohlenstoffträger in einem
angemessenen Lösungsmittel
hergestellt werden, und die resultierende Mischung wird mit einem
Reduktionsmittel wie Hydrazin oder Tetrahydroboratsalz, um einige
zu nennen, behandelt. Gemäß einem
bevorzugten Verfahren zur Erzeugung der erfindungsgemäßen Katalysatoren
HC-P-M, insbesondere zur Bil dung von Kathoden für Brennstoffzellen, werden
die P-M-Materialien vorher auf einem porösen Kohlenstoffträgermaterial
(Vulkan XC-72, Aktivkohle RBDA, Standard R-5000, NSM-III, Ketjen-Ruß und Raven-1020,
Graphit etc.) oder anderen leitenden Trägermaterialien wie feingepulvertem
Silber, Nickel und anderen vor der Wärmebehandlung bei einer angemessenen
Temperatur zwischen 500 und 1.000°C,
bevorzugt 800°C,
unter Inertgasschutz (beispielsweise N2,
Ar) für
etwa 2 Stunden getragen.
-
Ein
allgemeiner Vorgang zur Herstellung der Anoden und Kathoden aus
den erfindungsgemäßen Katalysatoren
ist der folgende:
Ein Anteil von HC-P-M wird in einer 1:1 Mischung
aus Wasser/Alkohol unter heftigem Rühren bei Raumtemperatur suspendiert.
Zu dieser Suspension wird unter Rühren ein Nichtbenetzungsmittel
wie Polytetrafluorethylen (PTFE) (60 Gew.%ige Dispersion in Wasser,
Aldrich) (ca. 20 Gew.% im Hinblick auf HC-P-M) gegeben. Das heftige
Rühren
wird für
circa 10 min fortgesetzt, unter Erhalt eines Flokkulationsmaterials.
Der Reaktionsbehälter
wird mit Ultraschall behandelt, bis ein gummiartiges Material gebildet
wird, das durch Dekantieren getrennt wird. Dieses Material wird
auf Kohlenstoffpapier, gesinterten Graphit oder Metallnetze (Stahl,
Nickel etc.) aufgerollt und bei etwa 100 kg/cm2 gepreßt. Die
so gebildete Elektrode wird bei 350 bis 400°C unter Inertgasatmosphäre (N2, Ar) gebacken.
-
Diese
Erfindung wird weiter unter Bezugnahme auf die folgenden Beispiele
erläutert,
die jedoch nur zur Erläuterung
dienen und nicht den Gesamtumfang der Erfindung selbst einschränken.
-
Drei
bevorzugte Vorgänge
zur Erzeugung des Polymers P werden in den Beispielen 1, 2 und 3
beschrieben.
-
Beispiel 1
-
Zu
einer Suspension aus 32 g fein zerteiltem 4-{1-[(2,4-Dinitro-phenyl)-hydrazono]-ethyl}-benzol-1,3-diol
in 200 ml Wasser werden 10 g Phenol und 10 ml wässriges Formaldehyd (40 Gew.%)
bei Raumtemperatur gegeben. Zu dieser Mischung wird festes NaOH
(0,5 g) unter Rühren
gegeben. Die resultierende dunkelbraune Suspension wird 8 Stunden
bei 100°C
unter Rückfluß gehalten,
unter Erhalt eines dunkelbraunen Feststoffes. Der Feststoff wird
filtriert, mehrere Male mit kaltem Wasser gewaschen und dann zu
500 ml destilliertem Wasser gegeben. Die resultierende Suspension
wird sanft mit konzentrierter HCl (37 %) auf pH 7 neutralisiert.
Das Polymer P trennt sich als dunkelroter Feststoff, der gesammelt
und mehrere Male mit kalten Wasser/Aceton-Mischungen (1:1, V:V)
gewaschen wird zur Entfernung von nicht reagierten Monomeren und niedermolekularen
Fraktionen. Nach der Reinigung wird P bei 60°C 3-4 Stunden getrocknet. Ausbeute
38 g.
-
Beispiel 2
-
Zu
einer Suspension aus 32 g fein zerteiltem 4-{1-[(2,4-Dinitrophenyl)-hydrazono]-ethyl}-benzol-1,3-diol
in 200 ml Wasser werden 10 g Phenol und 10 ml wässriges Formaldehyd (40 Gew.%)
bei Raumtemperatur gegeben. Zu dieser Mischung wird konzentriertes
(37 %) HCl (10 ml) unter Rühren
gegeben. Die resultierende dunkelbraune Suspension wird 8 Stunden
bei 110°C
unter Rückfluß gehalten,
unter Erhalt eines dunkelbraunen Feststoffes. Der Feststoff wird
filtriert, mehrere Male mit kaltem Wasser gewaschen und dann zu
500 ml destilliertem Wasser gegeben. Die resultierende Suspension
wird sanft mit einer wässrigen
Lösung aus
1N NaOH auf pH 7 neutralisiert. Das Polymer P trennt sich als dunkelroter
Feststoff, der gesammelt und mehrere Male mit kalten Wasser/Aceton-Mischungen
(1:1, V:V) gewaschen wird zur Entfernung von nicht reagierten Monomeren
und niedermolekularen Fraktionen. Nach der Reinigung wird P bei
60°C 3-4
Stunden getrocknet. Ausbeute 36 g.
-
Beispiel 3
-
Zu
einer Lösung
aus 5,0 g (2,4-Dichlorphenyl)hydrazin in 1.000 ml Methanol werden
langsam 10 ml konzentrierte Schwefelsäure gegeben. Nach der Auflösung wird
eine moläquivalente
Menge von (2,4-Dihydroxy)benzophenon bei Raumtemperatur zugegeben.
Nach 5 Minuten wird die Lösung
orange und ein dunkelbrauner Feststoff beginnt sich auszufällen. Der
Feststoff wird filtriert, mehrere Male mit kaltem Wasser gewaschen
und dann in Wasser suspendiert. Die Suspension wird auf pH 7 mit
konzentriertem NaOH neutralisiert. Der gesammelte dunkelbraune Feststoff
wird mehrere Male mit kaltem Wasser gewaschen und dann zu 500 ml
destilliertem Wasser gegeben. Eine äquivalente Menge 3,5-Dimethylphenol
wird zugegeben und die Lösung
mit 10 ml HCl (37 %) angesäuert.
Nach vollständiger
Auflösung
wird eine moläquivalente
Menge Formaldehyd (40 Gew.%ige Lösung)
langsam unter Rühren
hinzugegeben. Die resultierende Lösung wird bei 100°C unter Rühren unter
Rückfluß gehalten.
Nach etwa 8 Stunden trennt sich P als dunkelroter Feststoff, der
gesammelt und mehrere Male mit kalten Wasser/Aceton-Mischungen (1:1,
V:V) gewaschen wird, zur Entfernung von nicht reagierten Monomeren
und niedermolekularen Fraktionen. Nach der Reinigung wird P bei
60°C 3-4 Stunden
getrocknet. Ausbeute 3,9 g.
-
Charakterisierung
einer typischen Probe des Polymers P, erhalten von 4-{1-[(2,4-Dinitrophenyl)-hydrazono]-ethyl}-benzol-1,3-diol,
Phenol und Paraformaldehyd, unter Verwendung der Elementaranalyse,
Fourier-Transform-Infrarotspektroskopie
(FT-IR), W-sichtbare Spektroskopie (W-Vis) und 1H
und 13C{1H}-NMR-Spektroskopie.
Elementaranalyse:
C 58,60 %, H 4,24 %, N 12,15 %. (Diese Analyse paßt gut zu
einem Polymer mit der Formel C, worin x = 1 und n = 1; berechnet:
C 58,67 %, H 4,00 %, N 12,44 %).
FT-IR: 3600-3200 (vO-H), 3290
(vN-H), 3100 (v aromatisch C-H), 1620 (v C=N), 1615 (v aromatisch
C=C), 1590 (δ N-H),
1530 (vs·NO2),
1514 (vas·NO2)
1330 (δ O-H),
830 (v aromatisch C-NO2), 710 (δ aromatisch
C-H) cm-1.
UV-Vis: λmax = 390 nm; Schulter bei 420 nm.
1H-NMR (400,13 MHz, 298 K): (CD3COCD3): δ =
2,4-2,6 (N=C-CH3), 3,7-4,1 (Ar-CH2-Ar), 6,4-6,3 (C-H, aromatisch), 7,0-6,8
(C-H, Phenolring), 7,6-7,4 (C-H, aromatisch), 8,5-8,3 (H, Phenolring),
9,0-8,9 (H, aromatisch, 9,1-9,0 (Ar-NH-N), 11,4-11,2 (Ar-OH), 12,0-11,8
(Ar-OH).
13C NMR: (CD3COCD3): δ =
40 (Ar-CH2-Ar), 102-130 (aromatisch), 137
(O2N-C aromatisch), 143 (HN-C aromatisch),
159 (Ar-C=N-), 160-161 (HO-C aromatisch) ppm.
-
Das
Polymer P zersetzt sich vor dem Schmelzen bei Temperaturen von mehr
als 300°C.
-
Die
beiden bevorzugten Vorgänge
für die
Erzeugung der Katalysatoren dieser Erfindung werden in den Beispielen
4 und 5 beschrieben.
-
Beispiel 4
-
In
100 ml Aceton werden 0,50 g P und 0,30 g Nickel(II)-Acetattetrahydrat
(Aldrich) bei Raumtemperatur aufgelöst. Die Lösung wird bei Raumtemperatur
gerührt,
bis das gesamte Aceton verdampft ist, wodurch ein rötlicher
Rest zurückbleibt.
Dieser Feststoff, das P-M, wird in einen Quarzreaktor, der auf 800°C erwärmt ist,
unter einem Schutzfluß aus
Stickstoff 2 Stunden eingegeben. 0,30 g eines schwarzen gepulverten
Materials werden erhalten, umfassend Nickel mit 7,1 Gew.% (ICP-AES-Analyse).
-
Beispiel 5
-
In
100 ml Aceton werden 0,5 g P, 0,13 g Nickel(II)-Acetattetrahydrat
(Aldrich), 0,08 g Eisen(II)-Acetattetrahydrat (Aldrich) und 0,08
g Kobalt(II)-Acetattetrahydrat (Aldrich) bei Raumtemperatur gegeben.
Die resultierende Lösung
wird bei Raumtemperatur gerührt,
bis das gesamte Aceton verdampft ist, wodurch ein violetter Rest
zurückbleibt.
Dieses rohe Produkt, das P-M, wird in einen Quarzreaktor gegeben,
der dann auf 360°C unter
einem H2-Fluß 2 Stunden erwärmt wird.
0,6 g eines schwarzen pulverförmigen
Materials wird erhalten, umfassend Eisen, Kobalt und Nickel in einem
ca. 1:1:1 Verhältnis
für einen
Gesamtmetall-Prozentsatz im Produkt von 9,2 Gew.% (ICP-AES-Analyse).
-
Ein
bevorzugter Vorgang zur Erzeugung einer Kathode aus einem HC-P-M-Material dieser Erfindung ist
in Beispiel 6 beschrieben.
-
Beispiel 6
-
In
100 ml Aceton werden 0,50 g P und 0,30 g Nickel(II)-Acetattetrahydrat
(Aldrich) bei Raumtemperatur aufgelöst. Zu dieser Mischung, die
das P-M enthält,
werden 5,0 g Vulkan XC-72R (zuvor aktiviert durch Erwärmen auf
800°C unter
N2 für
2 Stunden, mit anschließendem
Rückfluß in wässrigem
HNO2 (50 %) aktiviert) gegeben. Die resultierende
Mischung wird bei Raumtemperatur gerührt, bis das ganze Aceton verdampft
ist, unter Erhalt eines schwarzen Restes. Das gesamte Aceton wird
bei vermindertem Druck entfernt. Der feste Rest wird in einen Quarzreaktor,
der auf 800°C
erwärmt
wird, in einem Fluß aus
Stickstoff für
2 Stunden eingeführt.
-
Das
feste Produkt wird in einer 1:1 (VV) Mischung aus Wasser/Ethanol
unter Rühren
dispergiert. Zur resultierenden Suspension werden 2,5 g PTFE (60
Gew.%ige Dispersion in Wasser, Aldrich) gegeben. Das heftige Rühren wird
für etwa
10 min aufrechterhalten, unter Erhalt eines Flokkulatmaterials.
Der Reaktionsbehälter
wird mit Ultraschall bearbeitet, bis ein gummiartiges Material gebildet
wird, das durch Dekantieren getrennt wird. Dieses Material wird
auf eine mit Teflon® behandeltes Kohlenstoffpapier
(Toray) aufgerollt und bei 100 kg/cm2 gepreßt. Die
so gebildete Elektrode wird bei 350°C unter einer Stickstoffatmosphäre gebacken.
-
Die
zwei bevorzugten Vorgänge
zur Erzeugung einer Anode dieser Erfindung sind in den Beispielen
7 und 8 beschrieben.
-
Beispiel 7
-
In
100 ml Aceton werden 0,5 g P, 0,10 g Nickel(II)-Acetattetrahydrat
(Aldrich), 0,065 g Eisen(II)-Acetattetrahydrat (Aldrich) und 0,065
g Kobalt(II)-Acetattetrahydrat (Aldrich) bei Raumtemperatur aufgelöst. Zu dieser
Mischung, die das P-M enthält,
werden 5 g Vulkan XC-72R (zuvor durch Erwärmen auf 800°C unter N2 für
2 Stunden aktiviert, mit anschließendem Rückfluß in wässrigem HNO3 (50
%)) gegeben. Aceton wird bei vermindertem Druck entfernt. Der feste
Rest wird in einen Quarzreaktor gegeben, der dann auf 360°C 2 Stunden
unter einem H2-Fluß erwärmt wird. Das feste Produkt
wird in einer 1:1 Mischung (W) auf Wasser/Ethanol unter Rühren dispergiert.
Zur resultierenden Suspension werden 2,5 g PTFE (60 Gew.%ige Dispersion
in Wasser, Aldrich) gegeben. Das heftige Rühren wird für etwa 10 min aufrechterhalten,
unter Erhalt eines Flokkulatmaterials. Der Reaktions behälter wird
mit Ultraschall behandelt, bis ein gummiartiges Aufschlämmungsmaterial
gebildet wird, das durch Dekantieren getrennt wird. Dieses Material
wird bei 400 kg/cm2 auf ein kreisförmiges Stahldrahtnetz
mit einer Drahtdicke von 0,2 mm, einer Meshgröße von 0,2 mm und einem Radius
von 1,75 cm gepreßt.
-
Beispiel 8
-
In
100 ml Aceton werden 0,5 g P, 0,10 g Nickel(II)-Acetattetrahydrat
(Aldrich), 0,065 g Eisen(II)-Acetattetrahydrat (Aldrich) und 0,065
g Kobalt(II)-Acetattetrahydrat (Aldrich) bei Raumtemperatur aufgelöst. Zu dieser
Mischung, die das P-M enthält,
werden 5,0 g Vulkan XC-72R (zuvor aktiviert durch Erwärmen auf
800°C unter
N2 für
2 Stunden mit anschließendem
Rückfluß in wässrigem
HNO3 (50 %)) gegeben. Nach 10-minütigem Rühren bei
0°C werden
10 ml einer wässrigen
Lösung
aus NaBH4 (10 Gew.%) tropfenweise zugegeben
(Vorsicht: das evolvierte H2-Gas kann mit
dem festen Katalysator, der sich an den Reaktorwänden niedergeschlagen hat,
reagieren). Das Rühren
wird 30 min bei Raumtemperatur fortgesetzt. Das feste Produkt wird
durch Filtration getrennt und mehrere Male mit Wasser/Ethanol (1:1,
VV) gewaschen. Dann wird das feste Produkt zu einer 1:1 (VV) Mischung
aus Wasser/Ethanol unter Rühren
gegeben. Zu der resultierenden Suspension werden 2,5 g PTFE (60
Gew.%ige Dispersion in Wasser, Aldrich) gegeben. Das heftige Rühren wird
für ca.
10 min aufrechterhalten, unter Erhalt eines Flokkulatmaterials.
Der Reaktionsbehälter
wird mit Ultraschall behandelt, bis ein gummiartiges Material gebildet
wird, das durch Dekantieren getrennt wird. Dieses Material wird
bei 400 kg/cm2 auf ein kreisförmiges Stahldrahtnetz
mit einer Drahtdicke von 0,2 mm, einer Meshgröße von 0,2 mm und einem Radius
von 1,75 cm gepreßt.
-
Elektrochemische
Messungen
-
Proben
der Elektroden gemäß dieser
Erfindung wurden als quadratische planare Plättchen mit einer Größe von 0,5
cm2 hergestellt. Die zyklische Voltametrie
wurde verwendet, um die Anoden gegenüber der Ferrocen(FcH)oxidation
zu testen, während
die Kathoden gegenüber
der Tetracyanoethylen(TCNE)reduktion untersucht wurden. In beiden
Fällen
wurden CH2Cl2-Lösungen mit [NBu4][PF6] (0,2 M) als tragenden Elektrolyt verwendet.
-
Tabelle
1 faßt
die erhaltenen elektrochemischen Ergebnisse mit der erfindungsgemäßen Anode,
umfassend Fe-Co-Ni in einem 1:1:1 molaren Verhältnis, und einer Kathode dieser
Erfindung, umfassend Ni, zusammen und berichtet ebenfalls von den
Vergleichen mit bekannten Elektrodenmaterialien zur allgemeinen Verwendung
bei Brennstoffzellen. Die elektrochemischen Daten werden nur zur
Erläuterung
angegeben und beschränken
die elektrochemische Leistung der Katalysatoren dieser Erfindung
nicht. Tabelle
1 Formale
Elektrodenpotentiale (V vs. SCE) und Peak-to-Peak-Trennung (mv)
für die
Einelektronenoxidation von FcH und die Einelektronenreduktion von
TCNE bei unterschiedlichen Elektrodenmaterialien (CH2CL2-Lösung; [NBu
4][PF
6] (0,2 M))
- a gemessen bei
0,05 nVs-1
- b + c von der
Brennstoffzell-Wissenschaft
-
Angesichts
der Tatsache, dass die elektrochemische Reversibilität von Einelektrodenverfahren
durch eine Peak-zu-Peak-Trennung von 59 mV bei Umgebungstemperatur
gezeigt wird, ist ersichtlich, dass die erfindungsgemäßen Elektroden
sich als effektive Elektronenaustauscher verhalten und in diesem
Sinn besser sind als die kommerziellen untersuchten Elektroden auf
Pt-Basis.
-
Die
Elektroden dieser Erfindung wurden unter typischen Brennstoffzell-Arbeitsbedingungen
untersucht, beispielsweise 2N H2SO4 und 1N KOH bei 25°C, 1 M CH3OH
und Sättigung
mit Luft. Wie in den 1 bis 4 gezeigt
ist, zeigen in sauren oder basischen Lösungen die Elektrodenmaterialien
dieser Erfindung hohe Stromdichten, die vergleichbar oder sogar
besser sind als solche von kommerziell erhältlichen Materialien, die untersucht
wurden.
-
Die 2 und 3 zeigen
die anodischen und kathodischen Polarisationskurven, aufgezeichnet durch
Einzelablenkungsvoltametrie für
unterschiedliche Anoden- und Kathodenmaterialien in 2N H2SO4-Lösung.
-
Die
Vergleiche werden mit dem entsprechenden Verhalten unter entlüfteten wässrigen
Bedingungen erhalten. Die Zeichen für den Strom entsprechen der
IUPAC-Konvention. Die 3 und 4 zeigen
die pertinenten Polarisierungskurven, aufgezeichnet in KOH-Lösung.
-
Die
mit den erfindungsgemäßen Katalysatoren
erzeugten Elektroden, bevorzugt Anoden, gebildet mit ternären oder
binären
Kombinationen von Fe, Co und Ni auf einem leitenden Trägermaterial,
und Kathoden, umfassend Ni oder Co alleine auf einem leitenden Trägermaterial
enthalten, können
in einzelnen, selbstlüftenden
direkten Oxidationsbrennstoffzellen (DOFC), bevorzugten direkten
Alkohol-Brennstoffzellen (DAFC) und mehr bevorzugt direkten Methanol-Brennstoffzellen
(DMFC) oder in polymeren Elektrolyt-Brennstoffzellen (PEFC), die im Stand
der Technik bekannt sind, verwendet werden, wobei offene Kreislaufspannungen
(OCV) von 1,18 V bei Umgebungstemperatur (angetrieben von H2) gezeigt werden. Angemessene Kombinationen
der Metalle im Katalysator dieser Erfindung können eine spezifische Leistung
von 300 mW/cm2 bei Umgebungstemperatur und
-druck ergeben. Die erfindungsgemäßen Kathoden sind gegenüber Alkoholen
vollständig
tolerant, wodurch Alkohole in DAFC verbunden werden. Kommerziell
erhältliche
kationische und anionische Membranen können gleichermaßen verwendet
werden.
-
Als
Beispiel zeigt 6 die Leistung von DMFC, gebildet
mit Elektroden dieser Erfindung (Kathode auf Ni-Basis, Anode auf
Fe-Co-Ni-Basis).