-
Gebiet der Erfindung
-
Diese Erfindung bezieht sich auf
neue Liganden für
Dopaminrezeptoren. Insbesondere bezieht sich die vorliegende Erfindung
auf wahlweise substituierte 1,2,3,11b-Tetrahydrochromeno[4,3,2-de] isochinolinverbindungen
und deren Verwendung in pharmazeutischen Formulierungen zur Behandlung
von Dopamin-bezogenen Dysfunktionen des zentralen und peripheren
Nervensystems.
-
Hintergrund
und Zusammenfassung der Erfindung
-
Dopamin, ein Neurotransmitter in
dem zentralen Nervensystem, wurde in eine Vielzahl von neurologischen
Störungen
verwickelt. Beispielsweise wurde es hypothetischerweise angenommen,
dass eine überschüssige Stimulation
von Subtypen von Dopaminrezeptoren mit Schizophrenie verknüpft ist.
Des Weiteren wird es im Allgemeinen anerkannt, dass entweder eine überschüssige oder
nicht ausreichende funktionelle dopaminerge Aktivität in dem
zentralen und/oder peripheren Nervensystem Bluthochdruck, Narkolepsie
und andere verhaltensmäßige, neurologische,
physiologische und die Bewegung betreffende Störungen einschließlich Parkinson'sche
Krankheit, eine chronische, fortschreitende Krankheit, die durch
ein Unvermögen
der Kontrolle des spontanen motorischen Systems charakterisiert
ist, bewirken kann.
-
Dopaminrezeptoren wurden traditionell
in zwei Familien (die D1- und D2-Dopaminrezeptorfamilien)
basierend auf pharmakologischen und funktionellen Befunden klassifiziert.
D1-Rezeptoren erkennen vorzugsweise das
Phenyltetrahydrobenzazepin und führen
im Allgemeinen zu einer Stimulation des Enzyms Adenylatcyclase,
wobei D2-Rezeptoren die Butyrophenone und
Benzamide erkennen und oftmals mit Adenylatcyclase negativ gekoppelt
(oder überhaupt
nicht gekoppelt) sind. Es ist nunmehr bekannt, dass wenigstens 5
Gene existieren, die für
Subtypen von Dopaminrezeptoren kodieren: die D1,
D2, D3, D9 und D5-Rezeptorsubtypen.
Die traditionelle Klassifikation bleibt jedoch bei der Dl-artigen Klasse nützlich, die die D1 (D1A) und die D5 (D1B) Rezeptorsubtypen aufweisen, wobei die
D2-artige Klasse aus den D2, D3 und D9 Rezeptorsubtypen besteht. Eine Variation
kann auch durch Spleiß-Varianten
(z. B. die D2L und D2S Spleiß-Varianten)
sowie auch durch unterschiedliche Allele (z. B. multiple Wiederholungen
des D4-Gens) auftreten.
-
Arzneimittel des zentralen Nervensystems,
die eine Affinität
für die
Dopaminrezeptoren zeigen, werden im Allgemeinen nicht nur durch
deren Rezeptorselektivität
klassifiziert, sondern des Weiteren durch die Aktivität ihres
Agonisten (rezeptoraktivierend) oder Antagonisten (rezeptorblockierend).
Während
die mit der Wechselwirkung von Dopamin mit den verschiedenen Rezeptorsubtypen
verbundenen physiologischen Aktivitäten nicht voll-ständig verstanden
sind, ist es bekannt, dass Liganden, die eine Selektivität für einen
besonderen Rezeptorsubtyp zeigen, mehr oder weniger vorhersagbare
neuropharmakologische Ergebnisse produzieren werden. Die Verfügbarkeit
von Antagonist- und Agonistverbindungen selektiver Dopaminrezeptoren
gestattet die Gestaltung von Experimenten, um das Verständnis der
vielen funktionellen Rollen von D1-Rezeptoren
zu steigern und kann zu neuen Behandlungen für verschiedene Störungen des
zentralen und peripheren Nervensystems führen. Des Weiteren, wenn Agonisten mit
hoher Affinität
für sowohl
D1- und D2-Rezeptoren erhältlich sind,
können
diese Agonisten unter Umständen
verwendet werden, in denen eine Bindung zu sowohl D1-
und D2-Rezeptoren nützlich
ist.
-
Der frühe Blickpunkt der Studien von
Dopaminrezeptoren lag auf der D
2-Familie,
aber eine kritische Rolle von den Dopamin D
1-Rezeptoren in der
Funktion des Nervensystems ist kürzlich
sichtbar geworden. Diese frühe
Arbeit an selektiven D
1-Rezeptorliganden fokussierte sich primär auf Moleküle aus einer
einzelnen chemischen Klasse, den Phenyltetrahydrobenzazepinen, wie
beispielsweise dem Antagonisten SCH23390 (1):
Es wurde gefunden, dass
verschiedene der Phenyltetrahydrobenzazepine Agoniste von D
1-Rezeptoren sind; die aus dieser Klasse
erhaltenen Agoniste [einschließlich
beispielsweise SKF38393 (+)-2] wären
jedoch im Allgemeinen teilweise Agoniste. Selbst bei SKF82958, welches
ein vollständiger
Agonist sein sollte, wurde es kürzlich
gezeigt, dass dieses nicht die volle intrinsische Wirksamkeit in
Präparationen
mit verminderter Rezeptorreserve hat. Die Differenzierung zwischen
D
1-Agonisten mit voller und teilweiser Wirksamkeit
ist für
die Gemeinschaft der medizinischen Forschung von Bedeutung, da dieses
die Wirkungen von diesen Verbindungen auf komplexe, durch das zentrale
Nervensystem vermittelte Ereignisse haben kann. Beispielsweise haben zwei
Vollagoniste (Dihydrexidin und A-77636) außergewöhnliche Wirksamkeiten gegen
Parkinson sche Krankheit in dem MPTP behandelten Affenmodell, wobei
teilweise Agoniste ohne signifikante Aktivität sind. Erst kürzlich erhaltene
Daten legen nahe, dass volle und teilweise Agoniste sich ebenfalls
in deren Effekten auf andere komplexe neurale Funktionen unterscheiden.
Des Weiteren bestehen Rezeptor-vermittelte Ereignisse (beispielsweise
Rekrutierung von G-Proteinen und assoziierten Rezeptorkinasen),
die sich auf die Agonistaktivität auswirken
können:
Diese letzteren biochemischen Ereignisse können unabhängig von den Veränderungen
in den Niveaus von sekundären
Messengern (beispielsweise cAMP), die durch ein Arzneimittel vermittelt
sind, auftreten.
-
Demgemäss haben Forscher ihre Anstrengungen
darauf gerichtet, Liganden zu gestalten, die volle Agonisten für die D
1-Rezeptoren
sind (d.h. die volle intrinsische Wirksamkeit haben). Eine derartige
Verbindung ist Dihydrexidin (3), ein Hexahydrobenzo[a]phenanthridin
der Formel:
Die Struktur von Dihydrexidin
(3) ist einzigartig von anderen D
1-Agonisten,
da das zusätzliche
Ringsystem angebunden ist, wodurch das Molekül vergleichsweise starr gemacht
wird. Studien zur Molekülmodellierung
von Dihydrexidin (3) haben gezeigt, dass die Verbindung eine begrenzte
Anzahl von Konformationen niedriger Energie hat und dass die aromatischen
Ringe in einer vergleichsweise coplanaren Anordnung in allen von
diesen Konformationen gehalten sind. Die kürzlich erfolgte Aufklärung der Konfiguration
des aktiven Enantiomers von Dihydrexidin (3) war mit den Vorhersagen
aus diesem Modell konsistent.
-
Im Gegensatz zu anderen D1-Agonisten mit hoher Affinität und hoher
intrinsischer Aktivität
wie 3-substituierte Aminomethylisochromane stellt Dihydrexidin (3)
ein halbstarres Templat zur Entwicklung eines Modells eines Dopaminliganden
bereit. Die essenziellen Merkmale dieses Modells umfassen die Anwesenheit
einer transoiden β-Phenyldopamineinheit,
ein äquatorial
orientiertes einsames Elektronenpaar an dem basischen Stickstoffatom
und nahezu eine Coplanarität
des anhängenden
Phenylringes mit dem Catecholring. Das auf Dihydrexidin basierende
Modell hat eine transoide β-Phenyldopamineinheit,
wohingegen das dopaminerge Phenyltetrahydrobenzazepin eine cisoide β-Phenyldopaminkonfor-mation
hat. Das auf Dihydrexidin basierende Modell hatte als Basis für die Gestaltung
von zusätzlichen
D1-Rezeptoragonisten
gedient. Die Gestaltung und Synthese der D1-Rezeptoragonisten,
die eine hohe intrinsische Aktivität haben, ist für die forschende
medizinische Gemeinschaft aufgrund der potenziellen Verwendung von
Vollagonisten zur Behandlung komplexer, durch das zentrale Nervensystem
vermittelter Ereignisse von Bedeutung, und ebenso Bedingungen, in
welchen periphere Dopaminrezeptoren involviert sind. Beispielsweise
haben die Zusammensetzungen nach der vorliegenden Erfindung eine
potenzielle Verwendung als Mittel zur Blutdrucksenkung und zur Beeinflussung der
Lungen- und Nierenfunktion.
-
Ein Ausführungsbeispiel der vorliegenden
Erfindung ist eine neue Klasse von Dopaminrezeptoragonisten der
allgemeinen Formel:
und pharmazeutisch akzeptable
Salze von dieser und pharmazeutische Formulierungen von solchen
Verbindungen. Die vorliegenden Verbindungen sind zur Behandlung
von Patienten nützlich,
die eine Dopamin-bezogene Funktionsstörung des zentralen Nervensystems
haben (wie durch eine offensichtliche neurologische, psychologische,
physiologische oder verhaltensmäßige Störung bewiesen
wird), sowie auch Bedingungen, in welchen periphere Dopaminrezeptoren
involviert sind (einschließlich
Zielgewebe wie beispielsweise der Niere, der Lunge, endokrine Gewebe
und Gewebe des cardiovascularen Systems).
-
Kurzbeschreibung
der Zeichnungen
-
1 ist
eine graphische Darstellung der Affinität von Dinoxylin (Kreise), Dinapsolin
(Diamanten) und (+)-SCH23390 (Dreiecke) für striatale D1-Rezeptoren.
Striatale D1-Rezeptoren von Ratten sind
mit [3H]SCH23390(1) gekennzeichnet
und ungekennzeichnetes Dinoxylin, Dinapsolin oder (+)-SCH23390 wurde zugefügt, um die
spezifische Bindung von jeder Verbindung zu dem D1-Rezeptor
zu bestimmen.
-
2 ist
eine graphische Darstellung der Affinität von Dinoxylin (Kreisen),
Dinapsolin (Diamanten) und (+)-SCH23390 (Dreiecke) für D1-Rezeptoren von Primaten, die in C-6 Zellen
expremiert sind. D1-Rezeptoren wurden mit
[3H]SCH23390(1) gekennzeichnet,
und ungekennzeichnetes Dinoxylin, Dinapsolin oder (+)-SCH23390 wurden
zugefügt,
um die spezifische Bindung von jeder der Verbindungen zu dem D1-Rezeptor zu bestimmen.
-
3 ist
eine graphische Darstellung der Affinität von Dinoxylin (Kreise), Dinapsolin
(Diamanten) und Chlorpromazin (Dreiecke) für striatale D2-Rezeptoren,
die mit [3H]Spiperon gekennzeichnet sind.
Ungekennzeichnetes Dinoxylin, Dinapsolin oder Chlorpromazin wurde
zugefügt,
um die spezifische Bindung von jeder der Verbindungen zu dem D2-Rezeptor zu bestimmen.
-
4 ist
eine graphische Darstellung der Anzahl von kontralateralen Rotationen über die
Zeit (Stunden) von Ratten, die in dem unilateralen 6-OHDA-Läsionsmodell
mit Dinoxylin (Quadrate) oder Dihydrexidin (Kreise) behandelt wurden.
-
Detaillierte
Beschreibung der Erfindung
-
Es wird in Übereinstimmung mit der vorliegenden
Erfindung eine Verbindung der allgemeinen Formel:
und pharmazeutisch akzeptable
Salze derselben bereitgestellt, wobei R
1-R
3 Wasserstoff sind, C
1-C
4 Alkyl oder C
2-C
4 Alkenyl; R
8 ist
Wasserstoff, C
1-C
4 Alkyl
oder eine Phenoxyschutzgruppe; X
9 ist Wasserstoff,
Halogen einschließlich
Chlor, Fluor und Brom oder eine Gruppe der Formel -oR, wobei R Wasserstoff,
C
1-C
4 AL-kyl oder eine Phenoxyschutzgruppe
ist, und R
4, R
5 und
R
6 sind unabhängig voneinander ausgewählt aus
der Gruppe bestehend aus Wasserstoff, C
1-C
4 Alkyl, Phenyl, Halogen oder eine Gruppe
-OR, wobei R wie oben definiert ist, und wenn X
9 eine
Gruppe der Formel -OR ist, können
die Gruppen R
8 und R zusammengefasst werden, um
eine Gruppe der Formel -CH
2- zu bilden.
-
Der Begriff „C2-C4 Alkenyl" bezieht sich auf Allyl, 2-Butenyl,
3-Butenyl und Vinyl.
-
Der Begriff „C1-C4 Alkyl" wie er hier benutzt wird, bezieht
sich auf verzweigte oder gradkettige Alkylgruppen, die ein bis vier
Kohlenstoffatome umfassen, einschließlich, aber nicht beschränkt auf,
Methyl, Ethyl, Propyl, Isopropyl, n-Butyl, t- Butyl und Cyclopropylmethyl.
-
In einem Ausführungsbeispiel ist wenigstens
ein Rest von R4, R5 oder
R6 Wasserstoff. In einem anderen Ausführungsbeispiel
sind wenigstens zwei Reste von R4, R5 oder R6 Wasserstoff.
-
Der Begriff „pharmazeutisch akzeptable
Salze" bezieht sich auf solche Salze, die unter Verwendung von organischen
oder anorganischen Säuren
gebildet werden, deren Salze zur Verwendung in Menschen und niederen
Tieren ohne unerwünschte
Toxizität,
Irritation, allergische Antwort und dergleichen geeignet sind. Geeignete
Säuren
zur Bildung von pharmazeutisch akzeptablen Salzen von biologisch
aktiven Verbindungen, die eine Aminfunktionalität haben, sind auf diesem Fachgebiet
gut bekannt. Die Salze können
gemäß herkömmlichen
Verfahren in situ während
der endgültigen
Isolation und Reinigung der vorliegenden Erfindungen hergestellt
werden, oder separat, durch Reaktion der isolierten Verbindungen
in der Form freier Basen mit einer geeigneten salzbildenden Säure.
-
Der Begriff „Phenoxyschutzgruppe", wie
er hier verwendet wird, bezieht sich auf Substituenten des phenolischen
Sauerstoffs, welche unerwünschte
Reaktionen und Abbau während
der Synthesen verhindern und welche später ohne Wirkung auf andere
funktionelle Gruppen des Moleküls
entfernt werden können.
Derartige Schutzgruppen und Verfahren zu deren Anwendung und Entfernung
sind auf dem Fachgebiet gut bekannt. Sie schließen ein Ether, wie beispielsweise
Cyclopropylmethyl-, Cyclohexyl-, Allylether und dergleichen; Alkoxyalkylether
wie beispielsweise Methoxymethyl- oder Methoxyethoxymethylether
und dergleichen; Alkylthioalkylether wie beispielsweise Methylthiomethylether;
Tetrahydropyranylether; Arylalkylether wie beispielsweise Benzyl-,
o-Nitrobenzyl-, p-Methoxybenzyl-, 9-Anthrylmethyl-, 4-Picolylether und
dergleichen; Trialkylsilylether wie beispielsweise Trimethylsilyl-,
Triethylsilyl-, t-Butyldimethylsilyl-, t-Butyldiphenylsilylether
und dergleichen; Alkyl- und Arylester wie beispielsweise Acetate,
Propionate, Butyrate, Isobutyrate, Trimethylacetate, Benzoate und
dergleichen; Karbonate wie beispielsweise Methyl-, Ethyl-, 2,2,2-Trichloroethyl-,
2-Trimethylsilylethyl-,
Benzyl- und dergleichen; und Carbamate wie beispielsweise Methyl,
Isobutyl, Phenyl, Benzyl, Dimethyl und dergleichen.
-
Der Begriff „C1-C4 Alkoxy", wie er hier verwendet wird, bezieht
sich auf verzweigte oder geradkettige Alkylgruppen mit ein bis vier
Kohlenstoffatomen, welche durch ein Sauerstoffatom gebunden sind,
einschließlich
aber nicht beschränkt
auf Methoxy, Ethoxy, Propoxy und t-Butoxy.
-
Des Weiteren können die vorliegenden Verbindungen
in Übereinstimmung
mit anderen Ausführungsbeispielen
dieser Erfindung in herkömmlichen
Formen der Arzneimitteldosierung zur Verwendung in Verfahren zur
Behandlung eines Patienten, der an einer Dopamin-bezogenen Fehlfunktion
des zentralen oder peripheren Nervensystems leidet,. formuliert
werden. Wirksame Dosen der vorliegenden Verbindungen hängen von
vielen Faktoren ab, einschließlich
der zu behandelnden Indikation, dem Weg der Verabreichung und dem
allgemeinen Zustand des Patienten. Für eine orale Verabreichung
wird es beispielsweise angenommen, dass wirksame Dosen der vorliegenden
Verbindungen in dem Bereich von ungefähr 0,1 bis ungefähr 50 mg/kg,
typischerweise von ungefähr
0,5 bis ungefähr
25 mg/kg betragen. Wirksame parenterale Dosen können in dem Bereich von ungefähr 0,01
bis ungefähr
5 mg/kg des Körpergewichtes
liegen. Im Allgemeinen weisen Behandlungsschema unter Verwendung
von Verbindungen in Übereinstimmung
mit der vorliegenden Erfindung eine Verabreichung von ungefähr 1 mg
bis ungefähr
500 mg der Verbindungen nach dieser Erfindung je Tag in mehrfachen
Dosierungen oder in einer einzigen Dosierung auf .
-
Flüssige Dosierungsformen für eine orale
Verabreichung können
pharmazeutisch akzeptable Emulsionen, Mikroemulsionen, Lösun gen,
Suspensionen und Sirups einschließen, die inerte Verdünnungsmittel
enthalten, die üblicherweise
auf dem Fachgebiet verwendet werden, wie beispielsweise Wasser.
Derartige Zusammensetzungen können
auch zusätzliche
Hilfsmittel wie Benetzungsmittel, Emulgierungs- und Suspendierungsmittel,
Süßmittel
und Geschmacksmittel enthalten. Injizierbare Zubereitungen der Verbindungen
nach der vorliegenden Erfindung können unter Verwendung von auf
dem Fachgebiet bekannter Produkte durch Dispergierung oder Lösung einer
wirksamen Dosis der Verbindung in einem parenteral akzeptablen Verdünnungsmittel
wie beispielsweise Wasser, oder mehr bevorzugt isotonischer Natriumchloridlösung, formuliert
werden. Die parenteralen Formulierungen können unter Verwendung von auf
dem Fachgebiet bekannter Mikrofiltrationstechniken sterilisiert
werden.
-
Die Verbindungen dieser Erfindung
können
auch als Dosierungen in fester Form für eine orale Verabreichung
wie beispielsweise als Kapseln, Tabletten, Pulver, Pillen und dergleichen
formuliert werden. Typischerweise ist die aktive Verbindung mit
einem inerten Verdünnungsmittel
oder Träger
wie beispielsweise Zucker oder Stärke und anderen für die Dosierungsform
geeigneten Excipienten vermischt. Daher werden Tablettenformulierungen
akzeptable Gleitmittel, Bindemittel und/oder Zerfallmittel umfassen.
Wahlweise können pulverförmige Zusammensetzungen,
die eine aktive Verbindung gemäß dieser
Erfindung und beispielsweise einen Stärke- oder Zuckerträger aufweisen,
in Gelatinekapseln zur oralen Verabreichung gefüllt werden. Andere Dosierungsformen
der Verbindungen nach der vorliegenden Erfindung können unter
Benutzung auf dem Fachgebiet bekannter Techniken in Formen formuliert
werden, die für
die spezifische Verabreichungsweise angepasst sind.
-
Eine Verbindung, die in Übereinstimmung
mit der vorliegenden Verbindung bereitgestellt wird, ist (±)-8,9-Dihydroxy-1,2,3,11b-tetrahydrochromeno[4,3,2-de]isochinolin-Hydrobromid,
welches nachfolgend hierzu als „Dinoxylin" bezeichnet wird.
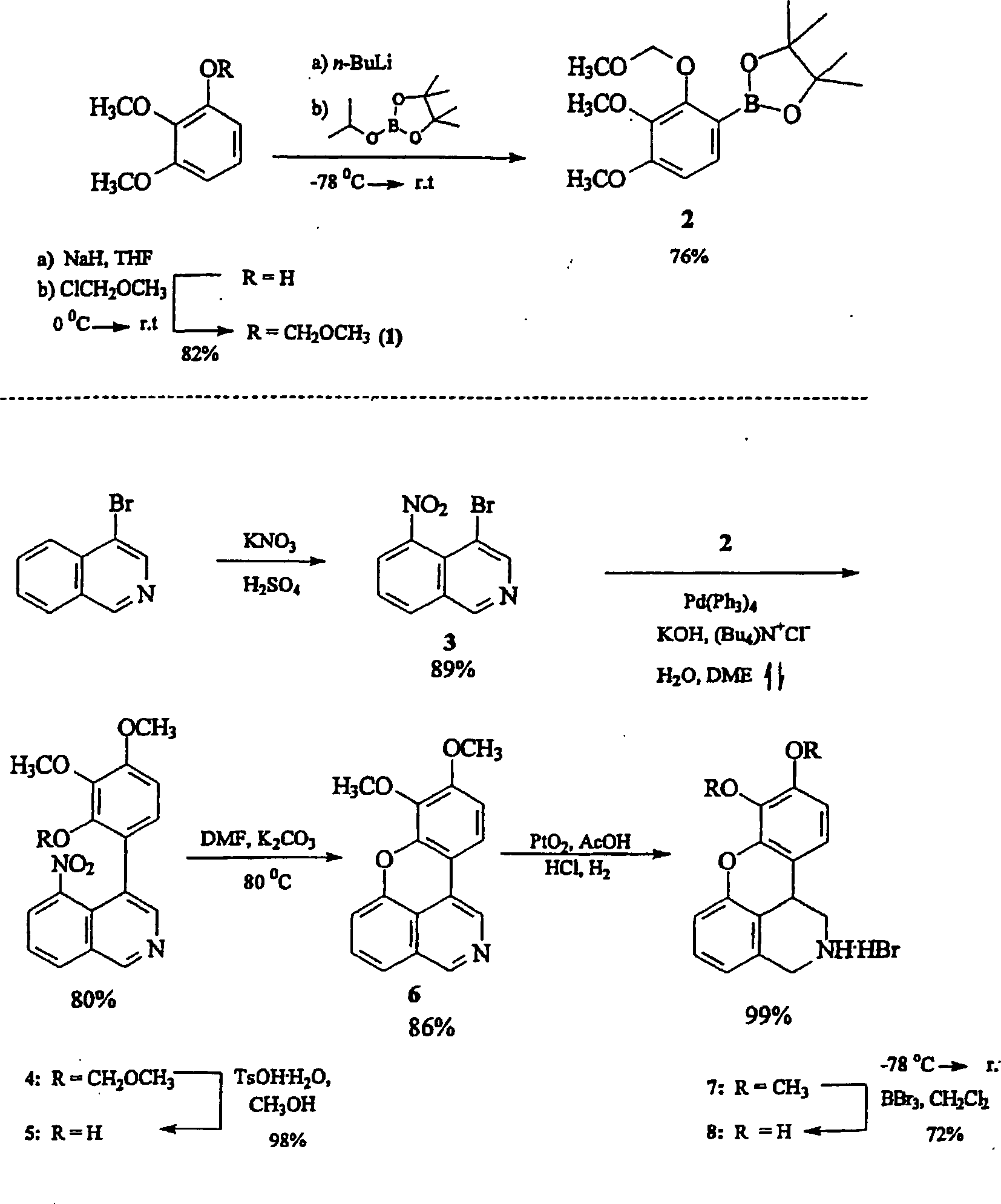
Di noxylin wird aus 2,3-Dimethoxyphenol synthetisiert, wie in Schema
1 dargestellt ist. Die Phenolgruppe wird als Methoxymethyl („MOM")-Derivat
geschützt,
gefolgt durch eine Behandlung mit Butyllithium, anschließend mit
dem veranschaulichten substituierten Borolan, um das Borolan-Derivat 2 zu
ergeben.
-
Wie in Schema 1 gezeigt ist, wird
dieses Borolan-Derivat anschließend
in einer Pd-katalysierten Überkreuz-Kopplungsreaktion
des Suzuki-Typs mit 5-Nitro-4-bromoisochinolin eingesetzt. Das resultierende
Kopplungsprodukt 4 wird anschließend mit Toluolsulfonsäure in Methanol
behandelt, um die MOM-Schutzgruppe des
Phenols zu entfernen. Eine einfache Behandlung dieses Nitrophenols 5 mit
Kaliumkarbonat in DMF bei 80°C
führt zu
einem Ringschluss mit einem Verlust der Nitro-Gruppe, was zu dem
grundlegenden tetrazyklischen Chromenoisochinolinkern 6 führt. Eine
einfache katalytische Hydrogenierung bewirkt eine Reduktion des
Stickstoff enthaltenden Ringes, um die Verbindung 7 zu
ergeben. Die Verwendung von Bortribromid zur Spaltung der Methylether-Verknüpfungen
ergibt die vorläufige
Verbindung 8.
-
Es ist offensichtlich, dass durch
geeignete Substitution des Isochinolinringes eine breite Vielfalt
von substituierten Verbindungen erhalten werden kann. Eine Substitution
an dem Stickstoffatom in entweder der Verbindung 6 oder 7,
gefolgt von einer Reduktion wird schnell eine Serie von Verbindungen
ergeben, die mit niedrigen Alkylgruppen an dem Stickstoffatom substituiert
ist. Gleichermaßen
würde die
Verwendung von Alkylsubstituenten an den 1,3,6,7 oder 8-Positionen
des Nitroisochinolins 3 zu einer Vielzahl von Ring-substituierten
Verbindungen führen.
Zusätzlich
kann die 3-Position der Verbindung 6 auch direkt mit einer
Vielfalt von Alkylgruppen substituiert werden. Auf ähnliche
Weise führt
eine Ersetzung der 4-Methoxygruppe der Verbindung 2 in
dem Schema 1 mit Fluoro-, Chloro- oder Al-kylgruppen zu den jeweiligen Verbindungen
mit Variationen an X9. Wenn Gruppen an dem
Kern anwesend sind, die gegenüber
den katalytischen Hydrogenierungsbedingungen nicht stabil sind,
die zur Überführung von 6 in 7 verwendet
werden, haben wir gefunden, dass die Reduktion durch Verwendung
von Natriumcyanoborhydrid bei geringfügig saurem pH-Wert durchgeführt werden
kann. Des Weiteren ergibt die Bildung von quarternären N-Alkylsalzen der Derivate
der Verbindung 6 Verbindungen, die ebenfalls leicht mit
Natriumborhydrid reduziert werden, um zu Derivaten der Verbindung
7 zu führen.
-
Raumfüllende Repräsentationen der Konformationen
mit niedriger Energie für
(+)-trans-10,11, Dihydroxy-5,6,6a,7,8,12bhexahydrobenzo[a]phenanthridin[(+)-dihydrexidin]
und des 11bR-Enantiomers
von Dinoxylin, welches an dessen 12bS chiralen Zentrum homochiral
mit (+)-Dihydrexidin ist, wurden verglichen. Zwei hauptsächliche
strukturelle Eigenschaften sind schnell ersichtlich. Als erstes
ist die sterisch massige Form, die durch die C(7) –C(8) Ethanbrücke in Dihydrexidin
(3) bereitgestellt wurde, entfernt worden. Zum zweiten
ist der Winkel des anhängenden
Phenylrings mit Hinsicht auf die Ebene des Catecholrings geringfügig verändert worden.
Dies ist aus Draufsicht-Ansichten am meisten ersichtlich, wobei
das aromatische Wasserstoffatom H(1) in Dihydrexidin (3) über den
Catecholring vorsteht. In Dinoxylin wird jedoch diese Position verwendet,
um den anhängigen
Phenylring durch ein Sauerstoffatom an den Catecholring anzubinden;
dies wirkt auf den anhängenden
Phenylring, um diesen in eine Richtung im Uhrzeigersinn relativ
zu Dihydrexidin (3), bei einer Ansicht von oben, zu vertwisten.
Die Aminogruppen sind in ähnlichen
Positionen, was den Grad an konformatorischer Flexibilität der heterozyklischen
Ringe ergibt. Des Weiteren können
beide Moleküle
einen N-H-Vektor in einer äquatorialen
Orientierung aufweisen, ein Merkmal des Pharmacophors, von welchem
angenommen wird, dass dieses für
D1-Rezeptoragonisten von Bedeutung ist.
In Übereinstimmung
mit jenen Beobachtungen sind die pharmakologischen Eigenschaften
dieser beiden Moleküle ähnlich.
-
-
Schema 1. Schema für die Synthese
von 8,9-Dihydroxy-1,2,3,11btetrahydrochromeno[4,3,2-de]Isochinolinhydrobromid Experimente
wurden durchgeführt,
um die Bindung von Dinoxylin an D1-Rezeptoren
zu bestimmen. Es wurde gefunden, dass Dinoxylin eine ähnliche
Affinität
(K0,5 < 5nM)
wie Dinapsolin bezüglich striatalen
D1-Rezeptoren von Ratten hat. Des Weiteren
demonstrieren kompetitive Experimente unter Verwendung von unmarkiertem
SCH23390 (1) als einen Kompetitor, dass Dinoxylin mit hoher
Affinität
konkurriert und eine flache Konkurrenzkurve (nH =
ca. 0,7) hat, die mit den Agonisteigenschaften (siehe 1 und 2) konsistent ist. Die Agonisteigenschaften
von Dinoxylin bei D1-Rezeptoren wurden in
vitro durch Messung des Vermögens
von Dinoxylin zur Erhöhung
der cAMP-Produktion in dem Striatum von Ratten und C-6-mD1-Zellen bestätigt. In sowohl dem Striatum
von Ratten als auch den C-6-mD1-Zellen hat
Dinoxylin eine volle Agonistaktivität mit einem EC50 von
weniger als 30 nM bei der Stimulierung der Synthese von CAMP über die
D1-Rezeptoren.
-
Die pharmakologischen Daten bestätigen daher,
dass Dinoxylin eine hohe Affinität
für Dopamin
D1-Rezeptoren hat, die mit [3H]SCH23390
markiert sind, die geringfügig
größer als
die von (+)-trans-10,11-Dihydroxy-5,6,6a,7,8,12b-hexahydrobenzo[a]
phenantridin (Dihydrexidin 3) ist. Des Weiteren war Dinoxylin
sowohl in striatalen Membranen von Ratten als auch in kloniert exprimierten
D1A-Rezeptoren von Primaten ein voller Agonist
relativ zu Dopamin, ähnlich
zu Dihydrexidin (3) aber im Unterschied zu dem teilweisen
Agonist (+)-SKF 38393 (siehe 2 und 3: (+)-SKF 38393 = (+)-2;
(±)-trans-10,11-Dihydroxy-5,6,6a,7,8,12b-hexahydrobenzo[a]phenanthridin
= (±)-3,
und (±)-8,9-Dihydroxy-2,3,7,11b-tetrahydro-lH-naphto[1,2,3-de]isochinolin = 4;
Dinapsolin).
-
Basierend auf dem zugrundeliegenden
Modell des D1-Pharmacophors ist es zu erwarten,
dass sowohl die Affinität
und die intrinsische Aktivität
von racemischem Dinoxylin (und substituierten Analoga von diesem) in
nur einem von dessen Enantiomeren vorliegen – dem Enantiomer mit der absoluten
Konfiguration 11bR (und dessen homochiralen Analoga). Es wird erwartet,
dass die Auflösung
des Racemats unter Verwendung von auf dem Fachgebiet bekannter Trennungstechniken
ein Dinoxylinisomer ergibt, welches ungefähr die zweifache D1-Affinität zeigt,
wie das Racemat.
-
Es wurde bestimmt, dass Dihydrexidin
ungefähr
zehnfach D1 : D2 selektiv
ist. Darüber
hinaus hat Dihydrexidin, während
es die erwartete Dopaminagonistenaktivität hat, des Weiteren eine ungewöhnliche
Eigenschaft, die hier als „funktionelle
Selektivität"
bezeichnet wird. Insbesondere wirkt Dihydrexidin (in vivo oder in vitro)
in Ratten als ein Agonist bei D2-artigen
Rezeptoren, die hinter den Synapsen angeordnet sind, aber als ein
Antagonist bei D2-artigen Rezeptoren, die
vorsynaptisch angeordnet sind. Es wird angenommen, dass dies aufgrund
der Unterschiede in dem Komplex Ligand-Rezeptor-G Protein gegeben.
ist, der postsynaptisch bzw. vorsynaptisch angeordnet ist, wie durch
die spezifischen G-Proteine bestimmt wird, die in dem gegebenen
zellulären
Milieu vorliegen. Wie in 1 gezeigt
ist, hat Dinoxylin eine größere Affinität für D2-artige Rezeptoren, als dies Dihydrexidin
hat, was den ersten vollen Agonisten bereitstellt, der eine sehr
hohe Affinität
für sowohl D1
als auch D2-Rezeptoren in dem Gehirn von Säugetieren
hat. Des Weiteren unterscheidet sich Dinoxylin von Dihydrexidin
in dessen Eigenschaften der „funktionellen
Selektivität".
-
Es wurde gezeigt, dass diese D2-Eigenschaften von Dihydrexidin in demselben
Enantiomer (d. h. 6aR, 12bS) vorliegen, welches der volle Agonist
mit hoher Affinität
an dem D1-Rezeptor ist. Auf dieser Basis
wird es angenommen, dass sowohl die D1 und
D2-Eigenschaften
von Dinoxylin ebenfalls in dem homochiralen Enantiomer liegen. Das
optische Isomer von Dinoxylin und geeigneter Analoga konstituieren
signifikante Werkzeuge, um das Phänomen der „funktionellen Selektivität" zu studieren.
-
Die antiparkinsonschen Wirkungen
von Dihydrexidin in dem MPTP Modell der Parkinson'schen Krankheit
wurden früher
berichtet und es ist erwartet, dass Dinoxylin ähnliche Wirkungen zeigen wird.
Wie in 4 gezeigt ist,
ist Dinoxylin in dem unilateralen Ratten-6-OHDA-Läsionsmodell
getestet worden, einem Paradigma, das eine Dopaminagonistaktivität in vivo
zeigt, und es wurde durch einige Personen vorgeschlagen, die Antiparkinson-Wirksamkeit der Arzneimittel
vorherzusagen. Wie gesehen werden kann, bewirkt Dinoxylin eine signifikante
Rotation, die für
ungefähr.5
Stunden nach einer einzelnen subkutanen Dosis bestehen bleibt. Es ist
mehr als das zweifache der Dauer der Wirkung einer ähnlichen
Dosis von Dihydrexidin, die über
den gleichen Weg verabreicht wird. In Übereinstimmung mit diesen Daten
wurden vorläufige
Studien mit Krallenaffen (marmosets) durchgeführt, die eine mittelschwere
MPTP-induzierte Dopamindenervierung haben. Es wurde gefunden, dass
Dinoxylin signifikante antiparkinson'sche Wirkungen hat, die eine
Erhöhung
in der Fortbewegung und Erregung und eine Verringerung der Parkinson-Anzeichen
bewirken. Dementsprechend haben Dinoxylin und dessen Derivate eine
potentielle klinische Verwendbarkeit bei Parkinson'scher Krankheit
und bei anderen Bedingungen, in welchen eine Störung von Dopaminrezeptoren
therapeutisch sein kann. Darüber
hinaus ist es berichtet worden, dass eine geeignete Modifikation
von Dihydrexidin Analoga erzeugen wird, welche auf spezifische Subpopulationen
der Dopamin-Rezeptorfamilie abzielen. Wohingegen ähnliche
Strategien mit Dinoxylin in Verbindungen mit einer neuen Rezeptorsubtypselektivität und/oder
funktionellen Profilen resultieren sollten, ist der Effekt von diesen
Substitutionen nicht der gleiche wie mit dem Dihydrexidin-Rückgrat.
-
Dopamin selber wird selten als ein
Arzneimittel verwendet, da, obwohl es alle Dopamin-Rezeptoren aktiviert,
es intravenös
verabreicht werden muss, es eine sehr kurze pharmacokinetische Halbwertszeit
hat und es auch andere Monoaminrezeptoren aktivieren kann. Diese
Serien unterscheiden sich von früheren
starren Dopaminanaloga in mehreren wichtigen Weisen. Als erstes
ist dies die erste Serie von Voll-D1-Agonisten mit
hoher Affinität, die
auch eine wenigstens gleich hohe Affinität für D2-Rezeptoren haben.
Daher hat, wobei Dihydrexidin zehnfach D1 D2 selektiv und Dinapsolin fünffach D1 : D2 selektiv ist,
Dinoxylin tatsächlich
eine gleich hohe Affinität
für beide
Rezeptoren. In den zwei früheren
Serien war es möglich,
die D2-Affinität zu erhöhen, aber
nur auf Kosten der D1-Affinität. Diese
Serie stellt das Vermögen
bereit, Arzneimittel mit hoher Affinität für beide Populationen von Rezeptoren
zu haben. Arzneimittel mit hoher Affinität gleichzeitig für sowohl D1 als auch D2 bieten
spezifische klinische Vorteile gegenüber Mitteln mit hoher Affinität für nur eine
der Hauptfamilien an. Die Neuheit dieser Serien wird klarer, wenn
die Wechselwirkung mit den spezifischen Dopaminrezeptorisoformen
untersucht wird. Ein wichtiger Unterschied zwischen diesen Serien
und früheren
Arzneimitteln wie beispielsweise Dihydrexidin und Dinapsolin ist
die, dass diese Mittel im Wesentlichen keine Affinität für die D4-Rezeptorisoform aufweisen. Umgekehrt hat
Dinoxylin einen K0,5-Wert von weniger als
45 nM an dem klonierten menschlichen D4-Rezeptor,
verglichen mit > 1.000
für entweder
Dinapsolin oder Dihydrexidin oder deren Derivate. Obwohl es gezeigt
wurde, dass D4-Antagonisten eine Wirksamkeit
bei der Behandlung von Schizophrenie fehlt, besteht ein großes Potenzial
für die
Verwendung von D4-Agonisten mit hoher Wirksamkeit
für ausgewählte psychiatrische
und neurologische Krankheiten.
-
Ein weiterer Hauptunterschied zu
diesen Serien ist der Effekt von Substituenten auf die Rezeptoraktivität. Basierend
auf den verfügbaren
Daten mit Dihydrexidin würde
es vorhergesagt worden sein, dass Zufügungen von N-Propyl oder N-Allyl
die D2-Affinität der vorliegenden
Liganden merklich erhöht
hätten.
Tatsächlich
verringerten diese N-Substituenten die D2-Affinität der vorliegenden
Verbindung signifikant. Dieser dramatische Unterschied legt nahe,
dass Dinoxylin an den D2-Rezeptor in einer
unvorhergesehenen Art und Weise bindet und auch eine einzigartige
therapeutische Verwendung haben sollte.
-
Mit Bezugnahme auf die nachfolgend
beschriebenen experimentellen Prozeduren, wurden Schmelzpunkte mit
einem Thomas-Hoover-Schmelzpunktapparat
bestimmt und wurden nicht korrigiert. 1H
NMR Spektren wurden mit einem Varian VXR 500S (500 MHZ) NMR Instrument
aufgenommen und die chemischen Verschiebungen wurden in Werten (ppm)
relativ zu TMS berichtet. Die IR Spektren wurden als KBr Tabletten
oder als flüssiger
Film mit einem FTIR Spektrometer der Serie Perkin Elmer 1600 aufgenommen.
Chemische Ionisationsmassenspektren (CIMS) wurden auf einem Finnigan
4000 Quadrupolmassenspektrometer aufgenommen. Hochauflösende CI
Spektren wurden unter Verwendung eines Kratos MS50 Spektrometers
aufgenommen. Daten von Elementaranalysen wurden von dem mikroanalytischen
Labor der Purdue University, West Lafayette, IN erhalten.
-
THF wurde von Benzophenon-Natrium
unter Stickstoff unmittelbar vor der Verwendung abdestilliert; 1,2-Dichlorethan
wurde von Phosphorpentoxid vor der Verwendung abdestilliert.
-
Beispiel 1A
-
Synthese von 8,9-Dihydroxy-1,2,3,11b-tetrahydrochromeno[4,3,2-de]isochinolinhydrobromid
(Dinoxylin)
-
1,2-Dimethoxy-3-methoxymethoxybenzol
(1)
-
Eine Aufschlämmung von Natriumhydrid wurde
durch Zugabe von 1000 ml von trockenem THF zu 7,06 g (0,18 mol)
von Natriumhydrid (60.%ige Dispersion in Mineralöl) unter einer Argonatmosphäre bei 0°C hergestellt.
Zu der Aufschlämmung
wurde 2,3-Dimethoxyphenol
(23,64 g; 0,153 mol) über
eine Spritze zugefügt.
Der resultierenden Lösung
wurde gestattet, sich auf Raumtemperatur zu erwärmen, und wurde für zwei Stunden
gerührt.
Die schwarze Lösung
wurde auf 0°C
abgekühlt
und 13,2 ml von Chlormethylmethylether (14 g; 0,173 mol) wurden
langsam über
eine Spritze zugefügt.
Der Lösung
wurde gestattet, Raumtemperatur zu erreichen und wurde für weitere
acht Stunden gerührt.
Die gelbe Mischung wurde zu einem Öl konzentriert, welches in
1000 ml Diethylether gelöst
wurde. Die resultierende Lösung
wurde mit Wasser (500 ml) und 2N NaOH (3 × 400 ml) gewaschen, getrocknet
(MgSO4), filtriert und konzentriert. Nach
einer Destillation im Kugelrohr (90–100°C, 0,3 atm) wurden 24,6 g eines
klaren Öles
(84%) erhalten: 1H NMR: (300 MHz, CDCl3): 6,97 (t, 1H, J = 8,7 Hz); 6,79 (dd, 1H,
J = 7,2, 1,8 Hz); 6,62 (dd, 1H, J = 6,9, 1,2 Hz); 5,21 (s, 2H);
3,87 (s, 3H); 3,85 (s, 3H); 3,51 (s, 3H) . CIMS m/z: 199 (M + H+, 50%); 167 (M + H+-CH3OH, 100%). Berechnete Analyse für C10H14O4:
C 60,59; H 7,12. Gefunden: C 60,93; H 7, 16.
-
2-(3,4-Dimethoxy-2-methoxymethoxyphenyl)-4,4,5,5-tetramethyl[1,3,2]dioxaborolan
(2).
-
Das MOM-geschützte Phenol 1 (10 g; 0,0505
mol) wurde in 1000 ml trockenem Diethylether gelöst und auf –78°C abgekühlt. Eine Lösung von n-Butyllithium (22,2
ml von 2,5 M) wurde anschließend über eine Spritze
zugefügt.
Das Kühlbad
wurde entfernt und der Lösung
wurde gestattet, sich auf Raumtemperatur zu erwärmen. Nach Rühren der
Lösung
bei Raumtemperatur für
zwei Stunden wurde ein gelber Niederschlag beobachtet. Die Mischung
wurde auf – 78°C abgekühlt und
15 ml von 2-Isopropoxy-4,4,5,5-tetramethyl-1,3,2-dioxyborolan (0,080 mol) wurden über eine
Spritze zugefügt.
Das Kühlbad
wurde nach zwei Stunden entfernt. Das Rühren wurde für vier Stunden
bei Raumtemperatur fortgesetzt. Die Mischung wurde anschließend in
300 ml Wasser geleert und mehrere Male mit Diethylether extrahiert
(3 x 300 ml), getrocknet (Na2SO4)
und auf ein gelbes Öl
(12,37 g, 76%) konzentriert, welches ohne weitere Reinigung verwendet
wurde: 1H NMR: (300 MHz, CDCl3)
: 7,46 (d, 1H, J = 8,4 Hz); 6,69 (d, 1H, J = 8,4 Hz); 5,15 (s, 2H);
3,87 (s, 3H); 3,83 (s, 3H); 1,327 (s, 12H).
-
4-Bromo-5-nitroisochinolin
(3)
-
Kaliumnitrat (5,34 g; 0,052 mol)
wurde zu 20 ml von konzentrierter Schwefelsäure zugefügt und langsam durch sorgfältiges Erwärmen gelöst. Die
resultierende Lösung
wurde tropfenweise zu einer Lösung
von 4-Bromoisochinolin (10 g; 0,048 mol), welches in 40 ml der gleichen
Säure bei
0°C gelöst wurde,
zugefügt. Nach
Entfernung des Kühlbades
wurde die Lösung
für eine
Stunde bei Raumtemperatur gerührt.
Die Reaktionsmischung wurde anschließend auf gestoßenes Eis
(400 g) geleert und mit Ammoniumhydroxid basisch gemacht. Der resultierende
gelbe Niederschlag wurde durch Filtration gesammelt und das Filtrat
wurde mit Diethylether (3 x 500 ml) extrahiert, getrocknet (Na2SO4) und konzentriert,
um einen gelben Feststoff zu ergeben, welcher mit dem ursprünglichen
Niederschlag kombiniert wurde. Eine Rekristallisation aus Methanol
ergab 12,1 g (89%) von leicht gelben Kristallen: Smp 172–174°C; 1H NMR: (300 MHz, CDCl3):
9,27 (s, 1H); 8,87 (s, 1H); 8,21 (dd, 1H, J = 6,6, 1,2 Hz); 7,96
(dd, 1H, J = 6,6, 1,2 Hz); 7,73 (t, 1H, J = 7,5 Hz). CIMS m/z: 253
(M + H+, 100%); 255 (M + H+ +
2, 100%). Berechnete Analyse für
C9H5BrN2O2: C 42,72; H 1,99; N 11,07. Gefunden: C
42,59; H 1,76; N 10,87.
-
4-(3,4-Dimethoxy-2rmethoaymethoxyphenyl)-5-nitroisochinolin
(4)
-
Isochinolin 3 (3,36 g; 0,0143 mol)
Pinacolboronatester 2 (5,562 g; 0,0172 mol) und 1,0 g (6 mol%) von Tetrakis
(triphenylphosphin)palladium(0) wurden in 100 ml von Dimethoxyethan
(DME) suspendiert. Kaliumhydroxid (3,6 g; 0,064 mol) und 0,46 g
(10 mol%) von Tetrabutylammoniumbromid wurden in 14,5 ml von Wasser gelöst und zu
der DME-Mischung zugefügt.
Die resultierende Suspension wurde für 30 min mit Argon entgast und
anschließend
unter Rückfluss
für vier
Stunden erwärmt.
Der resultierenden schwarzen Lösung
wurde gestattet, auf Raumtemperatur abzukühlen, in 500 ml Wasser geleert,
mit Diethylether (3 x 500 ml) extrahiert, getrocknet (Na2SO4) und konzentriert.
Das Produkt wurde anschließend
durch Säulenchromatographie
(Silicagel, 50% Ethylacetat : Hexan) gereinigt, was 5,29 g an gelben
Kristallen ergab (80,10: Smp 138–140°C; 1H NMR:
(300 MHz, CDCl3): 9,33 (s, 1H); 8,61 (s,
1H); 8,24 (dd, 1H, J = 7,2, 0,9 Hz); 8,0 (dd, 1H, J = 6,3 1,2 Hz); 7,67
(t, 1H, J = 7,8 Hz); 7,03 (d, 1H, J = 9,6 Hz); 6,81 (d, 1H, J =
8,1 Hz); 4,86 (d, 1H, J = 6 Hz); 4,70 (d, 1H, J = 5,4 Hz); 3,92
(s, 3H); 3,89 (s, 3H); 2,613 (s, 3H). CIMS m/z: 371 (M + H+, 100%). Berechnete Analyse für C19H18N2O6: C 61,62; H 4, 90; N 7, 56. Gefunden: C
61, 66; H 4,90; N 7,56.
-
2,3-Dimethoxy-6-(5-nitroisochinolin-4-yl)phenol
(5).
-
Nach Lösen von Isochinolin 4 (5,285
g, 0,014 mol) in 200 ml von Methanol durch gelindes Erwärmen wurde
p-Toluolsulfonsäuremonohydrat
(8,15 g; 0,043 mol) in verschiedenen Portionen zugefügt. Das
Rühren wurde
für vier
Stunden bei Raumtemperatur fortgesetzt. Nach Vervollständigung
der Reaktion wurde die Lösung
durch Zugabe von gesättigtem
Natriumhydrogencarbonat basisch gemacht. Das Produkt wurde anschließend mit
Dichlormethan (3 x 250 ml) extrahiert, getrocknet (Na2SO4) und konzentriert. Der resultierende gelbe Feststoff
(4,65 g; 98%) wurde direkt in der nächsten Reaktion verwendet.
Eine analytische Probe wurde aus Methanol umkristallisiert: Smp
170–174°C; 1H NMR: (300 MHz, CDCl3)
: 9,33 (s, 1H); 8,62 (s, 1H); 8,24 (dd, 1H, J = 7,2, 0,9 Hz); 7,99
(dd, 1H, J = 6,3, 1,2 Hz); 7,67 (t, 1H, J = 7,8 Hz); 6,96 (d, 1H,
J = 8,7 Hz); 6,59 (d, 1H, J = 8,7 Hz); 5,88 (bs, 1H); 3,94 (s, 3H);
3,92 (s, 3H) . CIMS m/z: 327 (M + H+, 100%).
Berechnete Analyse für
C17H19N2O5: C 62, 57; H 4,32; N 8,58; Gefunden: C
62,18; H 4,38; N 8,35.
-
8,9-Diaaethoxychromeno[4,3,2-de]isochinolin
(6).
-
Phenol 5 (4,65 g, 0,014 mol) wurde
in 100 ml von trockenem N,N-Dimethylformamid
gelöst.
Die Lösung
wurde mit Argon für
30 Minuten entgast. Kaliumcarbonat (5,80 g, 0,042 mol) wurde zu
der gelben Lösung in
einer Portion zugefügt.
Nach Erwärmen
bei 80°C
für eine
Stunde wurde die Mischung braun und kein Ausgangsmaterial verblieb
mehr. Nachdem die Lösung
auf Raumtemperatur abgekühlt
wurde, wurden 200 ml von Wasser zugefügt. Die wässrige Schicht wurde mit Dichlormethan
(3 × 500
ml) extrahiert, dieses organische Extrakt wurde mit Wasser gewaschen
(3 x 500 ml), getrocknet (Na2SO4)
und konzentriert. Ein weißes
Pulver (3,65 g 92%) wurde erhalten, welches in der nächsten Reaktion
ohne weitere Reinigung verwendet wurde. Eine analytische Probe wurde
aus Ethylacetat : Hexan umkristallisiert: Smp 195–196°C; 1H NMR: (300 MHz, CDCl3):
9,02 (s, 1H); 8,82 (s, 1H); 7,87 (d, 1H, J = 8,7 Hz); 7,62 (m, 3H);
7,32 (dd, 1H, J = 6,0, 1,5 Hz); 6,95 (d, J = 9,6 Hz); 3,88 (s, 3H);
3,82 (s, 3H). CIMS m/z: 280 (M + H+, 100%).
-
8,9-Dimethoxy-1,2,3,11b-tetrahydrochromaeno[4,3,2-ds]isochinolin
(7)
-
Platin (IV)oxid (200 mg) wurde zu
einer Lösung
enthaltend 50 ml Essigsäure
und Isochinolin 6 (1 g; 3,5 mmol) zugefügt. Nach Zugabe von 2,8 ml
von konzentrierter HCl wurde die Mischung auf einem Parr Hydrogenator
bei 60 psi für
24 Stunden geschüttelt.
Die grüne
Lösung
wurde durch Celite filtriert, um den Katalysator zu entfernen und
der Hauptanteil der Essigsäure
wurde durch Verflüchtigung
an einem Rotationsverdampfer entfernt. Die verbleibende Säure wurde
unter Verwendung von einer gesättigten
Lösung
von Natriumhydrogencarbonat neutralisiert, mit Diethylether extrahiert
(3 x 250 ml), getrocknet (Na2SO4)
und konzentriert. Das resultierende Öl (0,997 g; 99%) wurde ohne
weitere Reinigung verwendet: 1H NMR: (300
MHz, CDCl3): 7,10 (t, 1H, J = 7,5 Hz); 7,
00 (d, 1H, J = 8, 4 Hz); 6, 78 (m, 2H); 6, 60 (d, 1H, J = 9 Hz)
; 4, 10 (s, 2H); 3, 84 (m, 8H); 2, 93 (t, 1H, J = 12, 9 Hz) .
-
8,9-Dihydroxy-1,2,3,11b-tetrahydrochroeno[4,3,2-de]isochinolin
hydrobromid (8)
-
Das rohe Produkt 7 (0,834 g; 3,0
mmol) wurde in 50 ml wasserfreiem Dichlormethan gelöst. Die
Lösung
wurde auf –78°C abgekühlt und
15,0 ml einer Bortribromid-Lösung
(1,0 M in Di chlormethan) wurden langsam zugefügt. Die Lösung wurde über Nacht gerührt, während die
Reaktion langsam auf Raumtemperatur erwärmt wurde. Die Lösung wurde
wieder auf –78°C abgekühlt, 50
ml von Methanol wurden langsam zugegeben, um die Reaktion zu quenchen.
Die Lösung
wurde anschließend
bis zur Trockne konzentriert. Methanol wurde zugefügt und die
Lösung
wurde konzentriert. Dieser Prozess wurde drei Mal wiederholt. Der
resultierende braune Feststoff wurde mit aktivierter Holzkohle behandelt
und aus Ethanol umkristallisiert: Smp 298–302°C dec; 1H
NMR: (300 MHz, D2O): 7,32 (t, 1H, J = 6,6
Hz); 7,13 (d, 1H, J = 8,4 Hz); 7,04 (d, 1H, J = 8,4 Hz); 4,37 (m,
2H); 4,20 (t, 3H, J = 10 Hz) . Berechnete Analyse für C15H14BrNO3H2O: C 50,87; H
4,55; N 3,82. Gefunden: C 51,18; H 4,31; N 3,95.
-
N-Allyl-8,9-dimethoxy-1,2,3,11b-tetrahydroehromeno[4,3,2-de]isochinolin (10)
.
-
Tetrahydroisochinolin 7 (1,273 g;
4,5 mmol) wurde in 150 ml Aceton gelöst. Kaliumcarbonat (0,613 g; 4,5
mmol) und 0,4 ml (4,6 mmol) von Allylbromid wurden zugefügt. Die
Reaktion wurde anschließend
bei Raumtemperatur für
vier Stunden gerührt.
Der Feststoff wurde anschließend
durch Filtration entfernt und auf dem Filter mehrere Male mit Ether
gewaschen. Das Filtrat wurde konzentriert und durch Flashchromatographie gereinigt
(Silicagel, 50% Ethylacetat : Hexan), um 1,033 g (71%) eines gelben Öls zu ergeben,
welches ohne weitere Reinigung verwendet wurde: 1H
NMR (300 MHz, CDCl3): 7,15 (t, 1H, J = 9
Hz); 7,04 (d, 1H, J = 9 Hz); 6,83 (m, 2H); 6,65 (d, 1H, J = 6 Hz);
5,98 (m, 1H); 5,27 (m, 2H); 4,10 (m, 3H); 3,95 (s, 3H); 3,86 (s,
3H); 3,46 (d, 1H, J = 15 Hz); 3,30 (d, 2H, J = 6 Hz); 2,56 (t, 1H,
J = 12 Hz).
-
N-Allyl-8,9-Dihydroxy-1,2,3,11b-tetrahydrochromeno[4,3,2-de]isochinolin (11).
-
N-Allylamin 10 (0,625 g; 1,93 mmol)
wurde in 50 ml Dichlor methan gelöst.
Die Lösung
wurde auf –78°C gekühlt und
10,0 ml von BBr3-Lösung (1,0 M in Dichlormethan)
wurden langsam zugefügt.
Die Lösung
wurde über
Nacht gerührt,
während
die Reaktion sich langsam auf Raumtemperatur erwärmte. Nach Rückkühlung der
Lösung
auf –78°C wurden
50 ml von Methanol langsam zugefügt,
um die Reaktion zu quenchen. Die Reaktionsmischung wurde anschließend bis
zur Trockne konzentriert. Methanol wurde zugefügt und die Lösung wurde
konzentriert. Dieser Prozess wurde drei Mal wiederholt. Eine Rekristallisation
des braunen Feststoffes aus Ethanol ergab 0,68 g (61%) eines weißen Feststoffes:
Smp 251-253°C dec; 1H NMR: (300 MHz, D2O): 10,55
(s, 1H); 10,16 (s, 1H); 8,61 (t, 1H, J = 9 Hz); 8,42 (d, 1H, J =
9 Hz); 8,31 (d, 1H, J = 9 Hz); 7,87 (d, 1H, J = 9 Hz), 7,82 (d,
1H, J = 9 Hz); 7,36 (q, 1H, J = 9 Hz), 6,89 (m, 2H); 6,85 (d, 1H,
J = 15 Hz); 5,58 (m, 3H); 5,28 (m, 2H); 3,76 (d, 1H, J = 3 Hz).
HRCIMS m/z: Berechnet: 295,1208; Gefunden: 295,1214.
-
N-Propyl-8,9-dimethoxy-1,2,3,11b-tetrahydrochromeno-(4,3,2-de)isochinolin
(12)
-
N-Allylamin 10 (1,033 g;
3,2 mmol) wurde in 50 ml Ethanol gelöst. Palladium auf Kohle (10%
trocken; 0,103 g) wurden anschließend zugefügt. Die Mischung wurde auf
einem Parr-Hydrogenator
unter 60 psi H2 für drei Stunden geschüttelt. Nachdem
TLC nicht mehr ein Ausgangsmaterial zeigte, wurde die Mischung durch Celite
filtriert und konzentriert, um 0,95 g (91%) eines Öls zu ergeben,
welches ohne weitere Reinigung verwendet wurde: 1H
NMR: (300 MHz, CDCl3): 7,15 (t, 1H, J =
7,2 Hz); 7,04 (d, 1H, J = 8,1 Hz); 6,84 (t, 2H, J = 7,5 Hz); 6,65
(d, 1H, J = 8,4 Hz); 4,07 (m, 2H); 3,95 (s, 3H); 3,86 (s, 3H); 3,71
(q, 1H, J = 5,1 Hz); 3,42 (d, 2H, J = 15,6 Hz); 2,62 (m, 2H); 2,471
(t, J = 10,5 Hz); 1,69 (h, 2H, J = 7,2 Hz); 0,98 (t, 3H, J = 7,5
Hz) . CIMS m/z: 326 (M + H+, 100%) .
-
N-propyl-8,9-dihydroxy-1,2,3,11b-tetrahydrochromeno[4,3,2-de]isochinolin (13).
-
Das N-Propylamin 12 (0,90
g; 2,8 mmol) wurde in 200 ml Dichlormethan gelöst und auf –78°C abgekühlt. In einem separaten 250
ml Rundbodenkolben wurden 125 ml von trockenem Dichlormethan auf –78°C gekühlt und
1,4 ml (14,8 mmol) von BBr3 wurden über eine
Spritze zugefügt.
Die BBr3-Lösung wurde unter Verwendung
einer Kanüle
in den Kolben, welcher das Ausgangsmaterial enthielt, überführt. Die
Lösung
wurde über
Nacht gerührt,
während
die Reaktionsmischung sich langsam auf Raumtemperatur erwärmte. Nach
Kühlung
der Lösung
auf –78°C wurden
50 ml von Methanol langsam zugefügt,
um die Reaktion zu quenchen. Die Reaktionsmischung wurde anschließend zur
Trockne konzentriert. Methanol wurde zugefügt und die Lösung wurde
konzentriert. Dieser Prozess wurde drei Mal wiederholt. Der resultierende
braune Feststoff wurde in heißem
Isopropylalkohol suspendiert. Langsame Abkühlung auf Raumtemperatur resultierte
in einem feinen gelben Niederschlag. Der Feststoff wurde durch Filtration
gesammelt (0, 660 g; 63): Smp 259–264°C dec; 1H NMR:
(300 MHz, CDCl3) 7,16 (t, 1H, J = 9 Hz);
6,97 (d, 1H, J = 12 Hz); 6,83 (d, 1H, J = 9 Hz); 6,55 (d, 1H, J
= 9 Hz); 6,46 (d, 1H, J = 9 Hz); 4,45 (d, 1H, J = 15 Hz); 4,10 (m,
3H); 3,17 (q, 2H, J = 6 Hz); 3,04 (t, 1H, J = 9 Hz); 1,73 (q, 2H,
J = 9 Hz); 0,90 (t, 3H, J = 6 Hz) . Berechnete Analyse für C18H20BrNO3: C 57, 16; H 5, 33; N 3,70. Gefunden: C
56,78; H 5,26; N 3,65.
-
Pharmakologie von Dinoxylin
-
Verfahren: Radiorezeptorstudien
in Hirngewebe
-
Gefrorenes Striatum von Ratten wurde
durch sieben manuelle Schläge
in einem Wheaton Teflon-Glas Homogenisator in 8 ml eisgekühltem 50
mM HEPES Puffer mit 4,0 mM MgCl2 (pH-Wert
7,4) homogenisiert. Das Gewebe wurde bei 27.000 × g für 10 min zentrifugiert, der Überstand
wurde verworfen und das Pellet wurde ho mogenisiert (5 Schläge) und
in einem eisgekühlten
Puffer resuspendiert und wiederum zentrifugiert. Das endgültige Pellet
wurde bei einer Konzentration von ungefähr 2,0 mg Nassgewicht/ml suspendiert.
Die Menge von Gewebe, welches zu jedem Probenröhrchen zugefügt wurde,
betrug 1,0 mg in einem endgültigen
Probenvolumen von 1,0 ml. D1-Rezeptoren
wurden mit [3H] SCH23390 (0,30 nM) markiert.
D2-Rezeptoren wurden mit [3H]Spiperon
(0,07 nM) markiert; unmarkiertes Ketanserin (50 nM) wurde zugefügt, um eine
Bindung an die 5HT2-Stellen zu maskieren.
Die gesamte Bindung wurde als Radioligand definiert, der in der
Abwesenheit von jeglichen konkurrierenden Arzneimitteln band. Eine
unspezifische Bindung wurde durch Zugabe von unmarkiertem SCH23390
(1μM) oder
unmarkiertem Chlorpromazin (1 M) für jeweils D1-
und D2-Rezeptorbindungsassays abgeschätzt. Dreifache
Bestimmungen wurden für
jede Arzneimittelkonzentration in jedem Assay durchgeführt. Die
Probenröhrchen
wurden bei 37°C
für 15
min inkubiert. Die Bindung wurde durch Filtrierung mit eisgekühltem Puffer
auf einem Skatron 12 Well Zellernter (Skatron Inc., Sterling, VA)
unter Verwendung von Glasfasermatten (Skatron Nr. 7034) filtriert.
Den Filtern wurde gestattet, zu trocknen und 2,0 ml von Optiphase
HI-SAF II Szintillationsflüssigkeit
wurde zugefügt.
Nach 30-minütigem
Schütteln
wurde die Radioaktivität
auf einem LKB Wallac 1219 RackBeta Flüssigszintillationszähler (Wallac,
Gaithersburg, MD) bestimmt. Gewebeproteinniveaus wurden unter Verwendung
des BCA Proteinassayreagenzes abgeschätzt.
-
Funktionelle
Studien in Hirngewebe
-
Gefrorenes striatales Gewebe (ca.
40 mg) wurde in 4 ml eines Puffers (5 mM Hepes, 2 mM EGTA, pH-Wert
7,5) unter Verwendung von 10 Schlägen in einem Wheaton Teflon-Glas
Homogenisator homogenisiert. 4 ml von 50 mM Hepes mit 2 mM EGTA
Puffer (pH-Wert 7,5) wurden zugefügt und das Gewebe wurde durch
weitere drei Schläge
homogenisiert. Ein Aliquot von 20 μ1 von diesem homogenisierten
Gewebe wurde zu einer vorbereiteten Reaktionsmischung zugefügt. Die
Reaktionsmischung bestand aus 100 mM Hepes (pH-Wert 7,4), 100 mM NaCl, 4 mM MgCl2, 2 mM EDTA, 500 μM Isobutylmethylxanthin (IBMX),
0,01% Ascorbinsäure,
10 μM Pargylin,
2 mM ATP, 5 μM
GTP, 20 mM Phosphocreatin, 5 Einheiten von Ceratinphosphokinase
(CPK) und ausgewählte
Konzentrationen von DA. Das endgültige
Reaktionsvolumen betrug 100 μ1.
Die basale cAMP-Aktivität wurde
durch Inkubation von Gewebe in die Reaktionsmischung ohne zugefügtem Arzneimittel
bestimmt. Röhrchen
wurden im Doppel untersucht. Nach einer 15minütigen Inkubation bei 30°C wurde die
Reaktion durch die Zugabe von 500 μ1 von 0,1 N HCl gestoppt. Die
Röhrchen
wurden kurz in einem Vortex behandelt und anschließend in
einer BHG Hermle Z 230 M Mikrozentrifuge für 5 min bei 15.000 × g gedreht,
um große
Teilchen zu beseitigen.
-
Die Konzentration von cAMP in jeder
Probe wurde mit einem RIA von acetyliertem cAMP bestimmt, welcher
gegenüber
dem zuvor beschriebenen (Harper und Brooker, 1975) modifiziert wurde.
Eine Iodierung von cAMP wurde unter Verwendung eines zuvor beschriebenen
Verfahrens (Patel und Linden, 1988) durchgeführt. Als Puffer des Assays
wurde 50 mM Natriumacetatpuffer mit 0,1 Natriumazid (pH-Wert 4,75)
verwendet. Standardkurven von CAMP wurden in einem Puffer bei Konzentrationen
von 2 bis 500 fmol/Probenröhrchen erstellt.
Um die Sensitivität
des Assays zu erhöhen,
wurden sämtliche
Proben und Standards mit 10 μ1
einer 2 : 1 Lösung
von Triethylamin : Essigsäureanhydrid
acetyliert. Proben wurden im Doppel untersucht. Jedes Röhrchen des
Assays enthielt 100 μ1
an verdünnter
Probe, 100 μ1
von primären
Antikörpern
(Schaf, Anti-cAMP, 1 : 100.000 Verdünnung mit 1% BSA in einem Puffer)
und 100 μ1
von [125I]-cAMP (50.000 dpm/100 μ1 des Puffer);
das gesamte Volumen des Assays betrug 300 μ1. Die Röhrchen wurden in einem Vortex
behandelt und bei 4°C über Nacht
(ungefähr
18 Stunden) gelagert. Die Antikörper-gebundene
Radioaktivität
wurde anschließend
durch Zugabe von 25 μL
von BioMag von Kaninchen, Anti-Ziege IgG (Advanced Magnetics, Cambridge
MA) gefolgt durch eine Behandlung im Vortex und weitere Inkubation
bei 4°C
für eine
Stunde separiert. Zu diesen Proben wurde 1 ml von 12% Polyethylenglycol/50mM
Natriumacetatpuffer (pH-Wert 6,75) zugefügt und alle Röhrchen wurden
bei 1.700 × g
für 10
Minuten zentrifugiert. Die Überstände wurden
aspiriert und die Radioaktivität
in dem resultierenden Pellet wurde unter Verwendung eines LKB Wallac
Gammazählers (Gaithersburg,
MD) bestimmt.
-
Radiorezeptorstudien
mit exprimierten Rezeptoren
-
Radiorezeptor- und Funktionsstudien
wurden ebenfalls für
klonierte menschliche Rezeptoren oder Rezeptoren von Affen durchgeführt, die
in eine von mehreren Zelllinien [z. B. C-6 Gliomazellen oder chinesische Ovarienzellen
von Hamstern (CHO)] transfektiert waren. Die Zellen wurden in einem
geeigneten Medium wachsen gelassen und bei Konfluenz zur Membranherstellung
geerntet. Kolben der Zellen in dem gleichen Durchgang wurden unter
Verwendung eines Gummiwischers (policeman) ausgekratzt und in 50
ml Zentrifugenröhrchen
gesammelt. Diese wurden für
10 Minuten bei 1.200 × g
gedreht, um die gesamten Zellen zu pelletieren. Der Überstand
wurde verworfen und anschließend
wurden 5 ml von PBS (mit Phosphat gepufferte Salzlösung)/Kolben
zu den Zentrifugenröhrchen
zugefügt,
um die Zellen wieder zu suspendieren. Die Röhrchen wurden dann anschließend erneut
für 20
Minuten bei 28.500 × g
zentrifugiert. Das PBS wurde entfernt und das Pellet wurde in einer
Lösung
von 10% DMSO in PBS suspendiert. Die Zellen wurden mit einem Polytron
für 10
Sekunden auf Stufe 5 homogenisiert. 1 ml der Aliquote wurde bei –80°C gelagert,
bis diese in den Studien zur Rezeptorbindung verwendet wurden. Die
Aliquote enthielten ungefähr
1 mg/ml an Protein, wie unter Verwendung des BCA Proteinassayreagenzes
(Pierce, Rockford, IL) gemessen wurde.
-
Für
D1-artige Rezeptoren wurde ein Membranprotein
(50–75
g) mit jeder Testverbindung und [3H] SCH23390
(0,3 nM) in 50 mM Tris-HCl
(pH-Wert 7,4) zusammen mit 120 mM NaCl, 5 mM KCl, 2 mM CaCl2 und 1 mM MgCl2 inkubiert.
SCH23390 (5 μM)
wurde verwendet, um die nicht spezifische Bindung zu definieren.
Die Röhrchen
wurden in drei Exemplaren in einem endgültigen Volumen von 500 μ1 durchgetestet.
Nach einer Inkubation für
30 Minuten bei 37°C
wurden die Röhrchen
schnell durch Skatron Glasfaserfiltermatten (11734) filtriert und
mit 5 ml von eisgekühltem
Waschpuffer (50 mM Tris, pH-Wert 7,4) unter Verwendung eines Skatron
Mikrozellernters (Skatron Instruments Inc., Sterling, VA) gespült. Den
Filtern wurde ermöglicht,
zu trocknen und diese wurden anschließend in Szintillationsgefäße (Skatron
Instruments Inc., Sterling, VA) überführt. Ein
OptiPhase „HiSafe"
II Szintillationscocktail (1 ml) wurde zu jedem Gefäß zugefügt. Nach
Schütteln für 30 min
wurde die Radioaktivität
in jeder Probe auf einem LKB Wallac 1219 Rackbeta Flüssigkeitsszintillationszähler (Wallac
Inc., Gaithersburg, MD) bestimmt. Ein ähnliches Protokoll wurde für D2-artige Rezeptoren verwendet, mit der Ausnahme,
dass [3H] Spiperon (0,07 nM) als Radioligand
verwendet wurde.
-
Funktionelle
Studien mit exprimierten Rezeptoren
-
Die intrinsische Agonistaktivität wurde
durch das Vermögen
von ausgewählten
Verbindungen eingeschätzt,
Adenylatcyclase zu stimulieren, wie durch die cAMP-Bildung in ganzen
Zellen gemessen wurde. In C-6 Zellen wurde beispielsweise die Dosis-Antwortkurve für jedes
Arzneimittel unter Verwendung einer sigmoiden Funktion angepasst,
um die maximal wirksame Konzentration (oberes Plateau der Kurve)
sowie auch ECSO-Werte zu bestimmen. Sämtliche Arzneimittel wurden
in dem gleichen Assay überprüft, um die
Variabilität über die
Zelldurchläufe
zu verringern. Konfluente Platten von Zellen wurden mit Arzneimitteln
inkubiert, die in DMEM-H klaren Medien gelöst waren, denen 20 mM Hepes,
0,01% Ascorbinsäure
und 500 μM
iso-Butylmethylxanthin (IBMX; pH-Wert 7,2; Medium A) zugefügt worden
waren. Das endgültige
Volumen für
jede Vertiefung betrug 500 μ1.
Zusätzlich
zu den Dosis-Antwortkurven, die für jedes Arzneimittel laufen gelassen
wurden, wurden für
jede Platte Basisniveaus von cAMP und Isoproterenol-stimulierte
(durch endogene β2-Rezeptoren, positive Kontrolle) CAMP-Niveaus
evaluiert. Jede Bedingung wurde zweifach in den Vertiefungen durchlaufen. Nachfolgend
zu einer 10minütigen
Inkubation bei 37°C
wurden die Zellen kurz mit den Medien gespült und die Reaktion wurde durch
die Zugabe von 500 μ1
0,1 N HCl abgebrochen. Den Zellen wurde anschließend gestattet, für 5–10 min
bei 4°C
abzukühlen,
die Vertiefungen wurden ausgekratzt und das Volumen wurde in 1,7
ml Zentrifugenröhrchen überführt. Eine
zusätzlich
Menge von 1 ml von 0,1 N HCl wurde zu jedem Röhrchen zugefügt, um ein
endgültiges
Volumen von 1,5 ml/Röhrchen
zu ergeben. Die Röhrchen
wurden kurz in einem Vortex behandelt und anschließend in
einer BHG Hermle Z 230 M Mikrozentrifuge für 5 min bei 15.000 × g gedreht, um
große
zelluläre
Teilchen zu beseitigen. Die Niveaus von zyklischem AMP wurden für jede Probe
wie oben beschrieben bestimmt.
-
Die Daten wurden für jede Probe
berechnet und ursprünglich
als pmol/mg/min CAMP ausgedrückt.
Die Basislinienwerte von CAMP wurden von der Gesamtmenge von CAMP,
welches für
jede Arzneimittelbedingung erzeugt wurde, subtrahiert. Um die Variation
zwischen Assays zu minimieren, wurde eine Referenzverbindung (DA;
100 μM)
in jedem Assay eingefügt,
um als ein interner Standard zu dienen, der eine Normalisation der
Daten ermöglichte.
Die Daten für
jedes Arzneimittel wurden relativ zu der Prozentzahl der durch 100 M
DA erzeugten Stimulation ausgedrückt.
Normalisierte Dosis-Antwortkurven wurden durch nichtlineare Regression
unter Verwendung eines Algorithmus für sigmoide Kurven in dem Kurvenanpassungsprogramm
InPlot (Graphpad, Inc.; San Francisco, CA) analysiert. Für jede Kurve
stellte das Programm abgeschätzte
Punkte für
sowohl die EC50-Werte und die maximal erzeugte
Stimulation (d.h. oberes Plateau der sigmoiden Kurven) bereit.
-
Zusätzliche
beanspruchte Variationen der erfindungsgemäßen Verbindungen
-
Unter Verwendung der gleichen allgemeinen
Prozeduren, wie sie in Beispiel 1 oben beschrieben wurden, wurden
die Verbindungen in den Beispielen 1 bis 56, wie sie in der Tabelle
II unten weiter ausgeführt
sind, unter Verwendung der Ausgangsverbindungen, die mit den in
dem Schema 1 veranschaulichten Verbindungen korrespondieren, synthetisiert,
aber mit funktionellen Gruppen substituiert, die geeignet sind,
die Substitutionsmuster bereitzustellen, die auf dem für jedes
Beispiel gezeigten zusammenfassten Chromenoisochinolinprodukt dargestellt
sind. Daher stellen beispielsweise 6, 7 und/oder 8-substituierte
Analoga der Verbindung 3 (Schema 1) jeweils die korrespondierenden
Substituenten R6, R5 und R4 der
Formel I dar. Die Verwendung von anderen 1 und 3 substituierten
Isochinolinen (Analoga der Verbindung 3 in Schema 1) stellen
die korrespondierenden Substitutionsmuster an C3 und
Cl in Formel I dar.
-
-
-
Die oben angegebenen Beispiele stellen
die Erfindung illustrierend dar und sind nicht beabsichtigt, um die
Erfindung auf die offenbarten Beispiele zu beschränken. Es
ist beabsichtigt, dass Variationen und Modifikationen der beispielhaft
veranschaulichten Verbindungen, die dem Fachmann auf diesem Fachgebiet
offensichtlich sind, innerhalb des Schutzumfangs und der Natur der
Erfindung liegen, wie sie in den nachfolgenden Ansprüchen spezifiziert
ist.