WO2019131579A1 - たばこ抽出物、たばこ抽出物の製造方法、およびたばこ抽出物を用いた非燃焼型香味吸引器 - Google Patents
たばこ抽出物、たばこ抽出物の製造方法、およびたばこ抽出物を用いた非燃焼型香味吸引器 Download PDFInfo
- Publication number
- WO2019131579A1 WO2019131579A1 PCT/JP2018/047439 JP2018047439W WO2019131579A1 WO 2019131579 A1 WO2019131579 A1 WO 2019131579A1 JP 2018047439 W JP2018047439 W JP 2018047439W WO 2019131579 A1 WO2019131579 A1 WO 2019131579A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- tobacco extract
- tobacco
- fraction
- extract according
- organic solvent
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A24—TOBACCO; CIGARS; CIGARETTES; SIMULATED SMOKING DEVICES; SMOKERS' REQUISITES
- A24B—MANUFACTURE OR PREPARATION OF TOBACCO FOR SMOKING OR CHEWING; TOBACCO; SNUFF
- A24B15/00—Chemical features or treatment of tobacco; Tobacco substitutes, e.g. in liquid form
- A24B15/10—Chemical features of tobacco products or tobacco substitutes
- A24B15/12—Chemical features of tobacco products or tobacco substitutes of reconstituted tobacco
-
- A—HUMAN NECESSITIES
- A24—TOBACCO; CIGARS; CIGARETTES; SIMULATED SMOKING DEVICES; SMOKERS' REQUISITES
- A24B—MANUFACTURE OR PREPARATION OF TOBACCO FOR SMOKING OR CHEWING; TOBACCO; SNUFF
- A24B15/00—Chemical features or treatment of tobacco; Tobacco substitutes, e.g. in liquid form
- A24B15/18—Treatment of tobacco products or tobacco substitutes
- A24B15/24—Treatment of tobacco products or tobacco substitutes by extraction; Tobacco extracts
- A24B15/241—Extraction of specific substances
- A24B15/243—Nicotine
-
- A—HUMAN NECESSITIES
- A24—TOBACCO; CIGARS; CIGARETTES; SIMULATED SMOKING DEVICES; SMOKERS' REQUISITES
- A24B—MANUFACTURE OR PREPARATION OF TOBACCO FOR SMOKING OR CHEWING; TOBACCO; SNUFF
- A24B15/00—Chemical features or treatment of tobacco; Tobacco substitutes, e.g. in liquid form
- A24B15/10—Chemical features of tobacco products or tobacco substitutes
- A24B15/16—Chemical features of tobacco products or tobacco substitutes of tobacco substitutes
-
- A—HUMAN NECESSITIES
- A24—TOBACCO; CIGARS; CIGARETTES; SIMULATED SMOKING DEVICES; SMOKERS' REQUISITES
- A24B—MANUFACTURE OR PREPARATION OF TOBACCO FOR SMOKING OR CHEWING; TOBACCO; SNUFF
- A24B15/00—Chemical features or treatment of tobacco; Tobacco substitutes, e.g. in liquid form
- A24B15/10—Chemical features of tobacco products or tobacco substitutes
- A24B15/16—Chemical features of tobacco products or tobacco substitutes of tobacco substitutes
- A24B15/167—Chemical features of tobacco products or tobacco substitutes of tobacco substitutes in liquid or vaporisable form, e.g. liquid compositions for electronic cigarettes
-
- A—HUMAN NECESSITIES
- A24—TOBACCO; CIGARS; CIGARETTES; SIMULATED SMOKING DEVICES; SMOKERS' REQUISITES
- A24B—MANUFACTURE OR PREPARATION OF TOBACCO FOR SMOKING OR CHEWING; TOBACCO; SNUFF
- A24B15/00—Chemical features or treatment of tobacco; Tobacco substitutes, e.g. in liquid form
- A24B15/18—Treatment of tobacco products or tobacco substitutes
- A24B15/24—Treatment of tobacco products or tobacco substitutes by extraction; Tobacco extracts
- A24B15/241—Extraction of specific substances
-
- A—HUMAN NECESSITIES
- A24—TOBACCO; CIGARS; CIGARETTES; SIMULATED SMOKING DEVICES; SMOKERS' REQUISITES
- A24B—MANUFACTURE OR PREPARATION OF TOBACCO FOR SMOKING OR CHEWING; TOBACCO; SNUFF
- A24B15/00—Chemical features or treatment of tobacco; Tobacco substitutes, e.g. in liquid form
- A24B15/18—Treatment of tobacco products or tobacco substitutes
- A24B15/24—Treatment of tobacco products or tobacco substitutes by extraction; Tobacco extracts
- A24B15/26—Use of organic solvents for extraction
Definitions
- the present invention relates to a tobacco extract, a method for producing the tobacco extract, and a non-burning type flavor aspirator using the tobacco extract.
- the tobacco extract or its extraction method is used for the purpose of improving the flavor of the tobacco material and for the purpose of reducing the content of components in the tobacco material.
- the residue obtained by extracting leaf tobacco material with a low polarity solvent is further extracted with a high polarity solvent, and the extract extracted with the low polarity solvent is returned to the residue to obtain a tobacco raw material with good flavor ( Patent document 1)
- a tobacco material is extracted with a solvent to give an extract and a residue
- the extract is treated with a phenol oxidizing enzyme to reduce the amount of a phenol compound, and then it is combined with a tobacco residue to obtain a phenol compound.
- Patent Document 2 Methods for preparing reduced amounts of tobacco products (Patent Document 2), methods in which a fraction obtained by steam-distilling leaf tobacco is mixed with other materials as essential oils (Patent Document 3), etc. have been reported. Moreover, the method (patent document 4) of distilling a tobacco raw material (vacuum distillation etc.), and preparing a distillate is reported.
- the extraction means is solvent extraction and a volatile organic solvent or a halogen-based organic solvent is used as the extraction solvent, some glycosides and higher fatty acids, a ring structure and a substituent Contains a large number of hydrophobic components consisting of different high molecular weight compounds.
- a tobacco extract obtained by water extraction when it is applied to a non-burning type flavor suction device using propylene glycol, glycerin or the like as a solvent, insoluble particles are generated. This is because the water extract contains components insoluble in propylene glycol and glycerin, such as proteins and inorganic salts.
- the obtained water-insoluble fraction contains a large amount of hydrophobic components such as essential oils. These hydrophobic components are considered to be the main cause of the generation of insoluble particles when propylene glycol, glycerin or a mixture thereof is applied as a solvent.
- the mixed solution is heated by the heat source unit, and the boiling point of polyols (propylene glycol, glycerin etc.) which is a solvent of the mixed solution, or
- the non-volatile components which are vaporized at a temperature close to the boiling point of the mixture but which are not vaporized at this temperature remain in the heat source and burnt to cause a change in flavor.
- the problem to be solved by the present invention is that, when applied to a non-combustion type flavor suction device, insoluble particles are not generated in the mixed liquid etc., and burning of the heat source portion can be suppressed to suppress flavor change. It is providing a tobacco extract.
- the inventors of the present invention conducted intensive studies to solve such problems, and solvent-extraction of a fraction obtained by steam-distilling all or part of a tobacco plant with a suitable organic solvent removes the organic solvent.
- the tobacco extract produced has a low content of hydrophobic components and non-volatile components, so that when it is applied to a non-combustion type flavor suction device, insoluble particles are not generated in the mixed liquid etc., and in particular the non-combustion type flavor
- the present inventors have found that when used in a mixed liquid used in a heating type flavor aspirator, which is one form of aspirator, it is possible to suppress the burning of the heat source portion and to suppress the change of the flavor, thereby completing the present invention.
- the present invention includes, but not limited to, the following aspects.
- [1] Sum of peak areas of component groups having a retention index (RI) of less than 2100 when analyzed by gas chromatography (hydrogen flame ionization detector) using a column in which the stationary phase is 100% dimethylpolysiloxane Tobacco extract, which is at least 78% of the total of the total peak area.
- [2] The tobacco extract according to [1], wherein the total of the peak areas of the component groups having a retention index (RI) of less than 2100 is 81% or more of the total of the total peak areas.
- [3] The tobacco extract according to [1] or [2], wherein the content of linolenic acid is 0.02% by weight or less of the total tobacco extract.
- the tobacco extract according to [7] or [8] further comprising the step of adjusting the pH of the fraction to 6.0 or less before the step of extracting the fraction with an organic solvent.
- the tobacco extract according to [9] wherein the pH of the fraction is 4.0 or less.
- the non-combustion type flavor suction device does not cause problems such as precipitation due to insoluble components in the solvent, and prevents non-burning of the heat source and suppresses flavor change. It becomes possible to provide a combustion type flavor suction device.
- by maintaining the acidity of the fraction obtained by steam distillation in the extraction step it is possible to further reduce the alkaloid content or provide a tobacco extract from which the alkaloid has been removed by liquid-liquid transfer with a solvent. .
- the fraction obtained by steam-distilling tobacco leaves is subjected to liquid-liquid transfer using ethyl acetate, and the upper ethyl acetate layer is separated and extracted, and then ethyl acetate is removed under reduced pressure.
- the vertical line in the chromatogram indicates the retention time at which the retention index (RI) is 2100.
- the peak of linolenic acid is indicated by an arrow.
- the fraction obtained by steam-distilling tobacco leaves is subjected to liquid-liquid transfer using diethyl ether, and the upper diethyl ether layer is separated and extracted, and then diethyl ether is removed under reduced pressure.
- the vertical line in the chromatogram indicates the retention time at which RI is 2100.
- the peak of linolenic acid is indicated by an arrow.
- the fraction obtained by steam distillation of tobacco leaves is subjected to liquid-liquid transfer using chloroform, and the lower chloroform layer is separated and extracted, and then chloroform is removed under reduced pressure.
- FIG. 5 is a chromatogram by GC / FID of a tobacco extract obtained by solvent immersion extraction of tobacco leaves with ethyl acetate. The vertical line in the chromatogram indicates the retention time at which RI is 2100.
- FIG. 6 is a chromatogram by GC / FID of a tobacco extract obtained by solvent immersion extraction of tobacco leaves with diethyl ether. The vertical line in the chromatogram indicates the retention time at which RI is 2100.
- FIG. 7 is a chromatogram by GC / FID of a tobacco extract obtained by solvent immersion extraction of tobacco leaves with chloroform.
- FIG. 8 is a chromatogram by GC / FID of a tobacco extract obtained by solvent immersion extraction of tobacco leaves with n-hexane. The vertical line in the chromatogram indicates the retention time at which RI is 2100.
- FIG. 9 is a chromatogram by GC / FID of a tobacco extract obtained by solvent immersion extraction of tobacco leaves with acetone. The vertical line in the chromatogram indicates the retention time at which RI is 2100.
- FIG. 10 is a chromatogram by GC / FID of a tobacco extract obtained by solvent immersion extraction of tobacco leaves with ethanol. The vertical line in the chromatogram indicates the retention time at which RI is 2100.
- FIG. 8 is a chromatogram by GC / FID of a tobacco extract obtained by solvent immersion extraction of tobacco leaves with n-hexane. The vertical line in the chromatogram indicates the retention time at which RI is 2100.
- FIG. 9 is a chromatogram by GC / FID of a tobacco extract obtained by
- FIG. 11 is a chromatogram by GC / FID of a tobacco extract obtained by solvent immersion extraction of tobacco leaves with methanol. The vertical line in the chromatogram indicates the retention time at which RI is 2100.
- FIG. 12 is a chromatogram by GC / FID of a tobacco extract obtained by solvent extraction with ethyl acetate of a hot water extract obtained by hot water extraction of tobacco leaves. The vertical line in the chromatogram indicates the retention time at which RI is 2100.
- FIG. 13 is a chromatogram by GC / FID of a tobacco extract obtained by solvent extraction with diethyl ether of a hot water extract obtained by hot water extraction of tobacco leaves. The vertical line in the chromatogram indicates the retention time at which RI is 2100.
- FIG. 12 is a chromatogram by GC / FID of a tobacco extract obtained by solvent extraction with ethyl acetate of a hot water extract obtained by hot water extraction of tobacco leaves. The vertical line in the chromatogram indicates
- FIG. 14 is a chromatogram by GC / FID of a tobacco extract obtained by solvent extraction with chloroform of a hot water extract obtained by hot water extraction of tobacco leaves.
- the vertical line in the chromatogram indicates the retention time at which RI is 2100.
- FIG. 15 is a chromatogram by GC / FID of a tobacco extract obtained by solvent extraction of a hot water extract obtained by extracting hot water of tobacco leaves with n-hexane.
- the vertical line in the chromatogram indicates the retention time at which RI is 2100.
- the present invention provides the sum of peak areas of components having a retention index (RI) of less than 2100 when analyzed by gas chromatography using a column in which the stationary phase is 100% dimethylpolysiloxane.
- RI retention index
- the analysis is performed by gas chromatography (hydrogen flame ionization detector).
- the tobacco extract of the present invention is produced using all or part of a tobacco plant as a raw material.
- the "part of tobacco plant body” is a part of a tobacco plant body, for example, leaves (including upper leaves, true leaves, combined leaves, middle leaves, and lower leaves), core parts, sprouts, stems, stems, flowers , Roots and species, or mixtures thereof, preferably leaves, sprouts and stems.
- the whole or a part of the tobacco plant body may be used as it is, or may be cut, crushed or ground to be in the form of flakes, slurry or fine powder.
- the whole or part of the tobacco plant may be harvested from a field or the like as it is, or may be left indoors or outdoors for a predetermined period to dissipate some of the water, or it may be dried (freezer (freeze) It is also possible to use one that almost dissipates water, such as a drier.
- retention index (RI) refers to the carbon number of linear hydrocarbon (n-alkane) in analysis by gas chromatography, and the retention ratio of n-alkane and the compound to be analyzed is relative It refers to the indicator expressed in When a column having a predetermined stationary phase is used, the retention index (RI) becomes theoretically the same value if the same compound is used even if the column length, the carrier gas flow rate, and the like change. Specifically, the retention index (RI) is calculated by the following equation.
- the retention index (RI) is calculated using an n-alkane mixture in the range of n-hexane (C 6 , RI: 600) to n-pentatricontane (C 35 , RI: 3500) Although values are used, the n-alkane mixture used in calculating the retention index (RI) is not limited thereto.
- the column used in gas chromatography has, for example, a nonpolar or low polar stationary phase, preferably a nonpolar stationary phase.
- a column having a nonpolar stationary phase for example, a column having a stationary phase of 100% dimethylpolysiloxane can be used.
- DB-1 manufactured by Agilent Technologies
- Agilent Technologies can be used, but it is not limited thereto.
- a column having a low polarity stationary phase for example, a column having a stationary phase of 95% dimethylpolysiloxane / 5% diphenylsiloxane can be used.
- DB-5 manufactured by Agilent Technologies
- DB-5 can be used as a column having a stationary phase of 95% dimethylpolysiloxane / 5% diphenylsiloxane, but is not limited thereto.
- the “refractory component” or the “refractory compound” is dissolved in the solvent polyol and is azeotroped with a substance having a boiling point higher than the temperature at which the solvent vaporizes, or the solvent
- the compound itself refers to a tobacco component or compound having the property of not vaporizing.
- the less volatile component or compound include glycosides, proteins, polymer compounds having different ring structures and substituents, long chain fatty acids, long chain hydrocarbons and the like.
- non-volatile components or compounds are typically used after the retention time of n-henicosane (C 21 , retention index (RI): 2100) It has a retention time, ie it exhibits a retention index (RI) of 2100 or more.
- component group having a retention index (RI) of less than 2100 is a component group having a retention time earlier than the retention time of n-henicosane (C 21 , RI: 2100) It means a group of components that vaporize at a low boiling point of 200 ° C. to 240 ° C. or less.
- the total of the peak areas of the "components less than 2100 for the retention index (RI)" is, for example, 78% or more of the total of the total peak areas. Preferably it is 80% or more, more preferably 81% or more.
- Peak area is the point at which the tangent of the inflection point on either side with the baseline of the waveform of the separated tobacco component or compound peak meets the baseline on the chromatogram obtained by gas chromatography analysis It refers to the area of the part enclosed by the line segment which connected.
- the present invention provides the aforementioned tobacco extract, wherein the content of linolenic acid is 0.02% by weight or less of the total tobacco extract.
- Linolenic acid is a linear unsaturated fatty acid having three double bonds and the molecular formula is represented by C 18 H 30 O 2 and is a highly hydrophobic and hardly volatile component, and is for non-combustible flavor suction devices It is insoluble in a relatively polar organic solvent such as propylene glycol used as a solvent for the mixture.
- the content of linolenic acid is, for example, 0.02% by weight or less, preferably 0.01% by weight or less, and more preferably 0.006% by weight or less of the whole tobacco extract.
- the present invention provides the peak area of one or more alkaloids selected from the group consisting of nicotine, nornicotine, myosmin, nicotilin, nicotine-N-oxide, anabacin, anatabin, and cotinine as a total peak area
- the tobacco extract is provided, which has been reduced to 5% or less of the total area.
- the total peak area of the alkaloid is, for example, 5% or less, preferably 3.5% or less, more preferably 2.5% or less of the total peak area, and most preferably the alkaloid No peaks are detected.
- the present invention provides the above-mentioned tobacco extract for use in a non-burning type flavor inhaler.
- non-combustion type flavor suction device generates aerosol by means such as heating with a heat source without burning the aerosol generating article held in the aerosol generating article holding unit, or by atomizing with ultrasonic waves, etc.
- aerosol-generating articles include, but are not limited to, liquid or solid aerosol sources containing flavor components contained in tobacco raw materials, and tobacco materials such as compressed tobacco pellets and tobacco powder.
- the non-combustion flavor suction device may be any tobacco product that produces an aerosol (which may be a flavored aerosol) which the user inhales, for example, a heating flavor suction of a type using an aerosol source in liquid form Containers, a heating type flavor suction unit of a type using an aerosol generated by heating a cigarette as an aerosol source, a non-heating type flavor suction unit suctioning the flavor without heating the cigarette, and the like.
- a heating flavor suction of a type using an aerosol source in liquid form Containers for example, a heating flavor suction of a type using an aerosol source in liquid form Containers, a heating type flavor suction unit of a type using an aerosol generated by heating a cigarette as an aerosol source, a non-heating type flavor suction unit suctioning the flavor without heating the cigarette, and the like.
- the non-combustible flavor aspirator product is not particularly limited, but a heated flavor aspirator of a type preferably using a liquid aerosol source can be used.
- liquid aerosol source used for a non-burning type flavor suction device for example, a mixed liquid for non-burning type flavor suction device containing flavor components contained in a tobacco raw material in a polyol such as glycerin or propylene glycol can be mentioned.
- the mixed solution for non-combustion type flavor suction device can also contain the above-mentioned tobacco extract of the present invention as one for providing the flavor component contained in the tobacco raw material.
- the present invention comprises 1) steam distillation of all or part of tobacco plants to obtain a fraction, 2) extracting the obtained fraction with an organic solvent, 3) extraction
- a method for producing the tobacco extract comprising a method comprising the step of removing an organic solvent from the obtained organic phase.
- the variety of tobacco (plant of Nicotiana genus) plant used for steam distillation is not particularly limited.
- yellow species, burley species, orient species etc. can be used.
- the tobacco plant used for steam distillation can be used in its entirety without selecting the site, or only a desired site can be selected and used in part.
- all or part of the tobacco plant used for steam distillation may be subjected to steam distillation without cutting, or appropriately cut into a desired size, for example, cut into about 2 cm square and subjected to steam distillation It is also good.
- the whole or a part of the tobacco plant which has been pulverized or ground in a usual manner and which has been cut into pieces, slurry or powder may be subjected to steam distillation.
- All or part of the tobacco plants used for steam distillation may be those harvested from the field or the like as they are, or they may be left indoors or outdoors for a predetermined period to dissipate some of the water, or It is also possible to use one which almost dissipates water with a dryer (including a lyophilizer).
- Steam distillation is a method of distilling a high boiling point compound having a low vapor pressure at a temperature equal to or lower than the boiling point.
- the heating vessel is continuously filled with the heating steam by continuously introducing the heating steam into the distillation vessel containing the target sample containing the target compound, and the target compound is distilled together with the steam.
- liquid-liquid transfer or “liquid-liquid extraction” refers to organic solvent extraction of a target compound from a liquid-phase sample. Specifically, it is a method of extracting a compound using an organic solvent as a solvent. An organic solvent is added to a sample of a liquid phase containing a target compound to form two separated phases, and the target compound is extracted into the added organic solvent by utilizing the difference in distribution to the two phases by shaking. Do.
- solvent immersion extraction refers to organic solvent extraction of a target compound from a solid phase sample.
- the target compound is extracted into the organic solvent by immersing the solid phase sample containing the target compound in the organic solvent.
- the organic solvent used in the step of extraction with an organic solvent may be any solvent immiscible with water, for example, ethyl acetate, diethyl ether, propyl acetate, isopropyl acetate etc., preferably ethyl acetate or diethyl ether.
- ethyl acetate diethyl ether
- propyl acetate isopropyl acetate etc.
- isopropyl acetate preferably ethyl acetate or diethyl ether.
- the method used in the step of removing the organic solvent from the organic phase obtained by the extraction is not particularly limited.
- a method such as removal of a reduced pressure solvent by an evaporator or the like, removal of a heated solvent by a heater, removal of a solvent by spraying a purge gas, or the like can be used.
- the present invention provides a method for producing the above tobacco extract, which further comprises the step of adjusting the pH of the steam distillation fraction to 3.0 to 6.0.
- the alkaloid content is adjusted by shifting the equilibrium between the molecular form and the ionic form of the alkaloid to the ionic form by adjusting the pH of the steam distillation fraction to the above pH, and inhibiting the extraction into the organic solvent.
- a reduced or alkaloid removed tobacco extract can be produced.
- the pH of the steam distillation fraction is adjusted to, for example, 6.0 or less, preferably 5.0 or less, more preferably 4.0 or less.
- the pH of the steam distillation fraction is adjusted to, for example, 1.0 or more, preferably 2.0 or more, more preferably 3.0 or more.
- warm water extraction refers to solvent extraction using heated water as a solvent.
- hot water extraction for example, water is heated to 50 to 60 ° C., and when the raw material is immersed, the condition is about 40 ° C. to 45 ° C.
- the present invention provides the above-mentioned tobacco extract produced by the above production method.
- the tobacco extract is produced by using the whole or a part of the tobacco plant as a raw material, and depending on the species of the tobacco plant used as the raw material, the part to be used, and the components contained originally depending on the growth environment. Although the amount may vary greatly, and it may be conceivable that the specification of the tobacco extract of the present invention based on the content of the component in the extract is not practical, the use of the above-mentioned production method results in poor volatility. It is expected that a tobacco extract of the present invention having a certain level of quality with reduced components and / or reduced alkaloid content or removal of alkaloid can be obtained, which exhibits the effects of the present invention. is there.
- Example 1 Preparation of Tobacco Extract by Steam Distillation and Organic Solvent Extraction A tobacco extract of the U.S. yellow species was manufactured according to the following procedure.
- the organic phase was transferred to a 300 mL Erlenmeyer flask, 20 g of anhydrous sodium sulfate was added, and after gentle penetration, it was dehydrated by leaving it to stand at room temperature for 30 minutes.
- the chromatograms obtained by GC / FID analysis of the tobacco extract when solvent-extracted with ethyl acetate, diethyl ether, chloroform and n-hexane are shown in FIGS. 1 to 4, respectively.
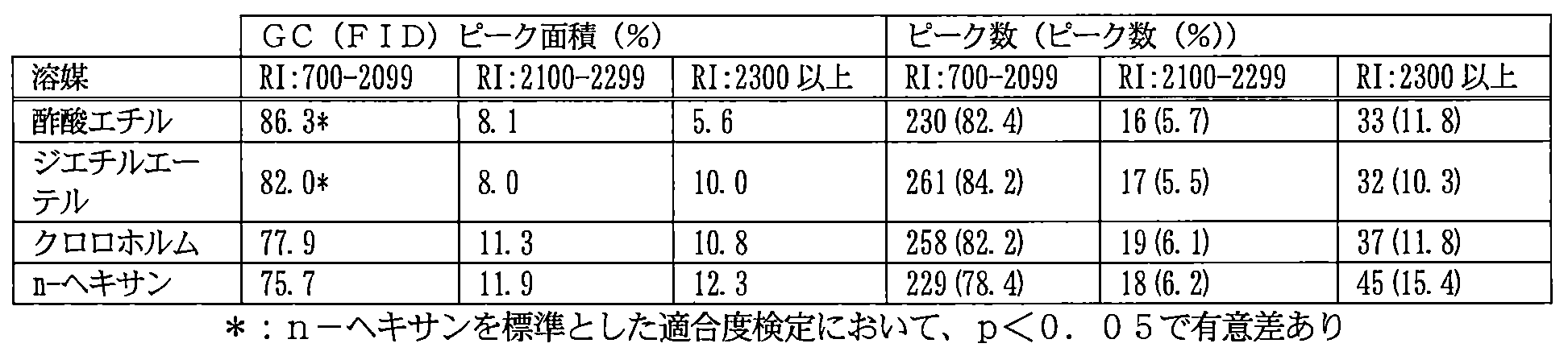
- the peaks on the chromatogram are classified into retention index (RI) 700 to 2099, 2100 to 2299, and 2300 or more numerical values, the sum of the peak areas of the component groups in each range is the area of the entire peak.
- the ratio (%) to the total, and the ratio (%) to the total of the peak number of the component groups in each range and the total peak number are shown in Table 1 below.
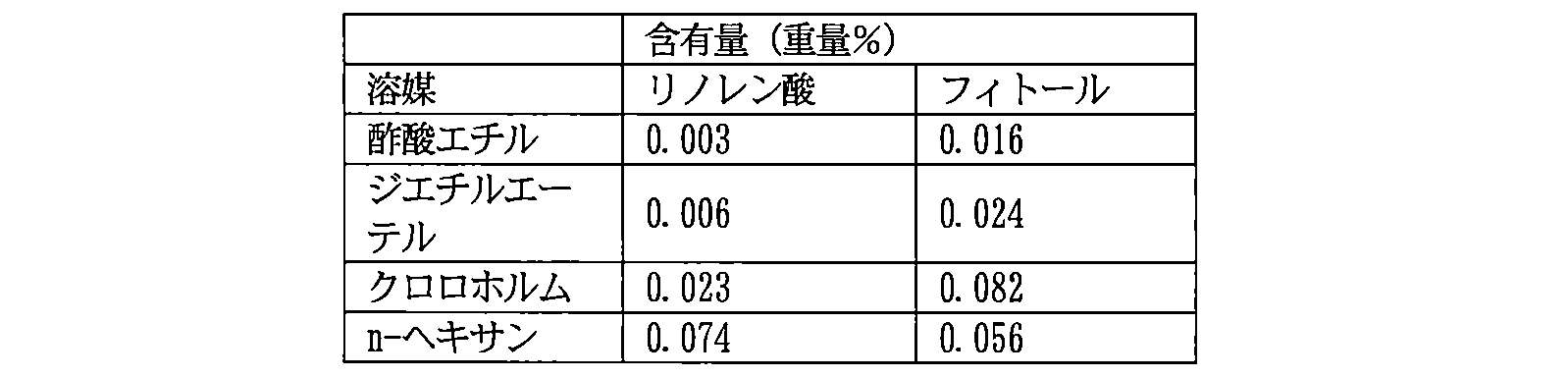
- the content (% by weight) of linolenic acid and phytol, which are highly hydrophobic and hardly volatile compounds, in the entire tobacco extract is shown in Table 2 below.
- the retention index (RI) is obtained when the fraction after steam distillation is subjected to solvent extraction with either ethyl acetate, diethyl ether, chloroform or n-hexane.
- the peak of the component group having a relatively high boiling point of 2100 or more and low volatility is small, and the peak of linolenic acid, which is an index of the hydrophobic compound having high hydrophobicity, is also small.
- the peak of the component group having RI of 2100 or more is smaller and the peak of linolenic acid is even compared to the case of solvent extraction with chloroform or n-hexane. It was small.
- the ratio of the peak area of the component group having a relatively low boiling point of RI less than 2100 and being volatile tends to exceed 78%.
- the content of linolenic acid is about 0.1% by weight or less even when solvent extraction is carried out with any of ethyl acetate, diethyl ether, chloroform or n-hexane. I found that. In particular, the content of linolenic acid was about 0.02% by weight or less when solvent extraction was performed with ethyl acetate or diethyl ether, and was extremely low as compared with the solvent extraction with chloroform or n-hexane. Therefore, it was shown that solvent extraction of the fraction after steam distillation with ethyl acetate or diethyl ether can provide a tobacco extract with significantly reduced non-volatile components.
- Example 2 Solubility Test of Tobacco Extract in Propylene Glycol
- the tobacco extract obtained as a dry solid in Example 1 is converted to propylene glycol, which is also used as a solvent for a mixed liquid for a heating type flavor suction device. It was tested for solubility. Specifically, after adding a predetermined amount of propylene glycol, heating to 42 ° C. and returning to room temperature, 150 ⁇ m (primary particles), 1500 ⁇ m (aggregation using a particle size distribution measuring device (LV-950A manufactured by Horiba, Ltd.) The particle size distribution of the substance was measured to confirm the presence or absence of insoluble particles.
- LV-950A particle size distribution measuring device
- the tobacco extract produced by liquid-liquid extraction of the fraction after steam distillation with ethyl acetate or diethyl ether is dissolved by adding propylene glycol having a weight of 4 times the weight of the extract, and is not less than 0.45 ⁇ m No insoluble particles were identified.
- the tobacco extract produced by solvent extraction of the fraction after steam distillation with chloroform or n-hexane has a diameter of 0.45 ⁇ m when propylene glycol having a weight of 4 times the weight of the extract is added.
- the above insoluble particles were confirmed and were not completely dissolved.
- propylene glycol was added stepwise, the tobacco extract produced by solvent extraction of the steam-distilled fraction with chloroform, even when propylene glycol of 20 times the weight of the extract was added, was used.
- a tobacco extract produced by solvent extraction of the fraction after steam distillation with n-hexane is 0.45 ⁇ m or more even when propylene glycol having a weight of 50 times the weight of the extract is added.
- Insoluble particles were confirmed. Such insoluble particles are considered to be generated due to extraction of hydrophobic components in tobacco leaves.
- Comparative Example 1 Production of tobacco extract by organic solvent extraction and solubility test in propylene glycol (1) Production of tobacco extract by organic solvent extraction Ethyl acetate, diethyl ether, chloroform, n-hexane, acetone as an organic solvent , Ethanol and methanol were used. Into a 500 mL conical beaker, tobacco leaf (10 g) of the same U.S. yellow species same as Example 1 cut into about 2 cm square was placed, and 100 mL of an organic solvent was added and immersed. Shake extraction at room temperature for 1 hour (solvent immersion extraction), filter the organic solvent after extraction through a filter paper (Advantec Toyo No.
- the chromatograms obtained by analysis by GC / FID are shown in FIGS. 5 to 11, respectively.
- the peaks on the chromatogram are classified into retention index (RI) 700 to 2099, 2100 to 2299, and 2300 or more numerical values, the sum of the peak areas of the component groups in each range is the area of the entire peak.
- the ratio (%) to the total, and the ratio (%) to the total of the peak number of the component group of each range and the total peak number are shown in Table 3 below.
- Hot Water Extraction Distilled water is heated to prepare 500 mL of hot water at about 60 ° C., and tobacco leaf of US yellow variety cut into about 2 cm square (50 g) was added, kept at 40-45 ° C., and extracted for 10 minutes while stirring with a stirrer.
- the extracted warm water was cooled to room temperature in a 6 ° C. refrigerator, and filtered through filter paper (ADVANTEC, No. 5A) to remove solids, to obtain 470 mL of a warm water extract.
- Example 2 150 mm loaded with a small amount of anhydrous sodium sulfate and rotary evaporated in a water bath at 40 ° C. until evaporation to dryness. The solvent was removed under reduced pressure to obtain 8.2 to 12.5 mg of a tobacco extract as a dry matter. 1 mL of the organic solvent used for extraction was added to the extract to make a sample for analysis, and analysis by GC / FID was performed under the same conditions as in Example 1 (4).
- the chromatograms obtained by analysis by GC / FID are shown in FIGS. 12 to 15, respectively.
- the peaks on the chromatogram are classified into retention index (RI) 700 to 2099, 2100 to 2299, and 2300 or more numerical values, the sum of the peak areas of the component groups in each range is the area of the entire peak.
- the ratio (%) to the total, and the ratio (%) to the total of the peak number of the component group of each range and the total peak number are shown in Table 4 below.
- Example 3 Production of tobacco extract with reduced alkaloid content or removal of alkaloid Using tobacco leaves of US yellow species, a tobacco extract with reduced alkaloid content or removal of alkaloid was manufactured according to the following procedure . That is, by adjusting the pH of the steam distillation fraction obtained in the same manner as in Example 1, the equilibrium between the molecular form and the ionic form of the alkaloid is shifted to the ionic form and the extraction to the organic solvent is inhibited. By reducing the alkaloid content or removing the alkaloid.
- Example 4 Preparation of Yellow Seed Tobacco Extract by Steam Distillation and Organic Solvent Extraction and Solubility Test in Propylene Glycol A tobacco extract was produced according to the following procedure using French yellow seed tobacco.
- Example 2 The obtained fraction is divided into 500 mL portions and extracted with various organic solvents (ethyl acetate, diethyl ether, chloroform and n-hexane) in the same procedure as in Example 1 (2) and (3), The solvent was removed to give 187-280 mg of tobacco extract as a dry product.
- organic solvents ethyl acetate, diethyl ether, chloroform and n-hexane
- the above tobacco extract was tested for solubility in propylene glycol. Specifically, a predetermined amount of propylene glycol was added, and the presence or absence of insoluble particles was visually confirmed. Further, the particle size distribution was measured with a wet particle size measuring device (LA-960 manufactured by Horiba, Ltd.), and the presence or absence of insoluble particles having a particle diameter of 0.45 ⁇ m or more was confirmed. The results are shown in Tables 6 and 7 below.
- the yellow seed tobacco extract produced by solvent extraction of the fraction after steam distillation with ethyl acetate or diethyl ether is 20 times and 50 times the weight of the extract weight
- the solution was dissolved by adding propylene glycol.
- the yellow seed tobacco extract produced by solvent extraction of the fraction after steam distillation with chloroform is not dissolved when propylene glycol having a weight of 20 times the weight of the extract is added, and the particle size is not However, insoluble particles having a size of not less than 0.45 ⁇ m were confirmed, and were finally dissolved by adding 50 times the weight of propylene glycol.
- the yellow seed tobacco extract produced by solvent extraction of the fraction after steam distillation with n-hexane does not dissolve even when propylene glycol having a weight of 50 times the weight of the extract is added, Insoluble particles having a particle diameter of 0.45 ⁇ m or more were confirmed.
- a tobacco extract having a significantly reduced amount of non-volatile components in tobacco leaves a method for producing the tobacco extract, a non-combustion flavor aspirator containing the tobacco extract, and the tobacco extract
- the heating type flavor suction device which is one form of a non-burning type flavor suction device can be provided. Furthermore, a tobacco extract from which alkaloid content has been reduced or from which the alkaloid has been removed, a method for producing the tobacco extract, a non-combustion type flavor suction device containing the tobacco extract, and a non-combustion type flavor suction containing the tobacco extract It is possible to provide a heating type flavor aspirator which is one form of the vessel.
Landscapes
- Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Manufacture Of Tobacco Products (AREA)
Abstract
非燃焼型香味吸引器に供した場合に、混合液などで不溶粒子を発生せず、熱源部の焦げ付きを抑えて喫味の変容も抑えることができるたばこ抽出物を提供する。 たばこ植物体の全部またはその一部を水蒸気蒸留した留分を適当な有機溶媒で溶媒抽出し、有機溶媒を除去して製造したたばこ抽出物を提供する。
Description
本発明は、たばこ抽出物、該たばこ抽出物の製造方法、および該たばこ抽出物を用いた非燃焼型香味吸引器に関する。
たばこ抽出物またはその抽出法は、たばこ原料の香味を改善する目的やたばこ原料中の成分の含有量を低下させる目的で用いられている。例えば、葉たばこ材料を低極性溶媒で抽出した後の残渣をさらに高極性溶媒で抽出し、その残渣へ低極性溶媒で抽出した抽出物をかけ戻すことにより、香味が良好なたばこ原料を得る方法(特許文献1)、たばこ材料を溶媒で抽出してエキスと残渣とを供し、そのエキスをフェノール酸化酵素で処理してフェノール系化合物の量を低下させ、たばこ残渣と組合せることでフェノール系化合物の量の低下したたばこ製品を調製する方法(特許文献2)、葉たばこを水蒸気蒸留した留分を精油としてその他材料と混合する方法(特許文献3)などが報告されている。
また、たばこ原料を蒸留(減圧蒸留など)して留出液を調製する方法(特許文献4)が報告されている。
また、たばこ原料を蒸留(減圧蒸留など)して留出液を調製する方法(特許文献4)が報告されている。
たばこ抽出物を非燃焼型香味吸引器に供する場合、抽出する手段として一般的なたばこ抽出法である有機溶媒や水等からなる溶媒による抽出、高圧炭酸ガス抽出、水蒸気蒸留などの方法がある。しかし、それらの方法で得たたばこ抽出物をプロピレングリコールやグリセリンなどを溶媒として非燃焼型香味吸引器に適用すると、例えばプロピレングリコールやグリセリンに対する不溶性分が存在する場合、不溶粒子が発生し、沈殿などの品質異常が問題となる。この不溶粒子は、抽出手段が溶媒抽出であり、かつ抽出溶媒として揮発性有機溶媒やハロゲン系有機溶媒を用いた場合には、一部の配糖体類や高級脂肪酸類、環構造や置換基の異なる高分子化合物からなる疎水性成分を多く含む。また、水抽出で得られるたばこ抽出物についても、プロピレングリコールやグリセリンなどを溶媒として非燃焼型香味吸引器に適用した際には、不溶粒子が発生する。これは、水抽出物中にタンパク質、無機塩類などのプロピレングリコールやグリセリンに不溶な成分が含まれているためである。また、抽出手段が水蒸気蒸留の場合は、得られた水に不溶な画分には精油などの疎水性成分が多く含まれる。これらの疎水性成分が、プロピレングリコール、グリセリン、あるいはそれらの混合物などを溶媒として適用した際に不溶粒子が発生する主な原因と考えられる。
また、非燃焼型香味吸引器の一形態である加熱型香味吸引器では、混合液を熱源部で加熱し、混合液の溶媒であるポリオール類、(プロピレングリコール、グリセリンなど)の沸点、または、それらの混合物の沸点に近接した温度で蒸気化しているが、この温度で気化されない難揮発性成分は熱源部に留まり焦げて香味の変容の原因となる。
したがって、本発明が解決しようとする課題は、非燃焼型香味吸引器に供した場合に、混合液などで不溶粒子を発生せず、熱源部の焦げ付きを抑えて香味の変容も抑えることができるたばこ抽出物を提供することである。
本発明者らは、かかる課題を解決するために鋭意研究を進めたところ、たばこ植物体の全部またはその一部を水蒸気蒸留した留分を適当な有機溶媒で溶媒抽出し、有機溶媒を除去して製造したたばこ抽出物は疎水性成分および難揮発性成分の含有量が低く、非燃焼型香味吸引器に供した場合に、混合液などで不溶粒子が発生しないこと、また特に非燃焼型香味吸引器の一形態である加熱型香味吸引器に使用する混合液に供した場合に熱源部の焦げ付きを抑えて香味の変容も抑えることができることを見出し、本発明を完成させた。
すなわち、本発明は非限定的に以下の態様を含む。
[1]固定相が100%ジメチルポリシロキサンであるカラムを用いてガスクロマトグラフィー(水素炎イオン化検出器)で分析をした場合に、保持指標(RI)が2100未満の成分群のピーク面積の合計が全体のピーク面積の合計の78%以上である、たばこ抽出物。
[2]保持指標(RI)が2100未満の成分群のピーク面積の合計が全体のピーク面積の合計の81%以上である、[1]に記載のたばこ抽出物。
[3]リノレン酸の含有量がたばこ抽出物全体の0.02重量%以下である、[1]または[2]に記載のたばこ抽出物。
[4]リノレン酸のピーク面積が全体のピーク面積の合計の0.01重量%以下である、[1]~[3]のいずれかに記載のたばこ抽出物。
[5]ニコチン、ノルニコチン、ミオスミン、ニコチリン、ニコチン-N-オキシド、アナバシン、アナタビン、およびコチニンから選択される1種以上のアルカロイドのピーク面積の合計が全体のピーク面積の合計の5%以下まで減少している、[1]~[4]のいずれかに記載のたばこ抽出物。
[6]固定相が100%ジメチルポリシロキサンであるカラムを用いてガスクロマトグラフィー(水素炎イオン化検出器)で分析をした場合に、ニコチン、ノルニコチン、ミオスミン、ニコチリン、ニコチン-N-オキシド、アナバシン、アナタビン、およびコチニンからなる群から選択される1種以上のアルカロイドのピークが検出されない、[1]~[5]のいずれかに記載のたばこ抽出物。
[7]1)たばこ植物体の全部またはその一部を水蒸気蒸留して留分を得る工程、
2)得られた留分を有機溶媒で抽出する工程、
3)抽出により得られた有機相から有機溶媒を除去する工程
を含む方法によって製造される、[1]~[6]のいずれかに記載のたばこ抽出物。
[8]有機溶媒が、酢酸エチルまたはジエチルエーテルである、[7]に記載のたばこ抽出物。
[9]留分を有機溶媒で抽出する工程の前に、留分のpHを6.0以下に調製する工程をさらに含む、[7]または[8]に記載のたばこ抽出物。
[10]留分のpHが4.0以下である、[9]に記載のたばこ抽出物。
[11]非燃焼型香味吸引器に用いるための、[1]~[10]のいずれかに記載のたばこ抽出物。
[12]加熱型香味吸引器に用いるための、[1]~[11]のいずれかに記載のたばこ抽出物。
[13][1]~[11]のいずれかに記載のたばこ抽出物を含む、非燃焼型香味吸引器。
[14][1]~[12]のいずれかに記載のたばこ抽出物を含む、加熱型香味吸引器。
[15][1]~[12]のいずれかに記載のたばこ抽出物を含む、加熱型香味吸引器用混合液。
[16][15]に記載の加熱型香味吸引器用混合液を含む、加熱型香味吸引器。
[17]1)たばこ植物体の全部またはその一部を水蒸気蒸留して留分を得る工程、
2)得られた留分を有機溶媒で抽出する工程、
3)抽出により得られた有機相から有機溶媒を除去する工程
を含む、[1]~[12]に記載のたばこ抽出物の製造方法。
[18]有機溶媒が、酢酸エチルまたはジエチルエーテルである、[17]に記載のたばこ抽出物の製造方法。
[19]留分を有機溶媒で抽出する工程の前に、留分のpHを6.0以下に調製する工程をさらに含む、[17]または[18]に記載のたばこ抽出物の製造方法。
[20]留分のpHが4.0以下である、[19]に記載のたばこ抽出物の製造方法。
[21][1]~[11]のいずれかに記載のたばこ抽出物の、非燃焼型香味吸引器への使用。
[22][1]~[12]のいずれかに記載のたばこ抽出物の、加熱型香味吸引器への使用。
[1]固定相が100%ジメチルポリシロキサンであるカラムを用いてガスクロマトグラフィー(水素炎イオン化検出器)で分析をした場合に、保持指標(RI)が2100未満の成分群のピーク面積の合計が全体のピーク面積の合計の78%以上である、たばこ抽出物。
[2]保持指標(RI)が2100未満の成分群のピーク面積の合計が全体のピーク面積の合計の81%以上である、[1]に記載のたばこ抽出物。
[3]リノレン酸の含有量がたばこ抽出物全体の0.02重量%以下である、[1]または[2]に記載のたばこ抽出物。
[4]リノレン酸のピーク面積が全体のピーク面積の合計の0.01重量%以下である、[1]~[3]のいずれかに記載のたばこ抽出物。
[5]ニコチン、ノルニコチン、ミオスミン、ニコチリン、ニコチン-N-オキシド、アナバシン、アナタビン、およびコチニンから選択される1種以上のアルカロイドのピーク面積の合計が全体のピーク面積の合計の5%以下まで減少している、[1]~[4]のいずれかに記載のたばこ抽出物。
[6]固定相が100%ジメチルポリシロキサンであるカラムを用いてガスクロマトグラフィー(水素炎イオン化検出器)で分析をした場合に、ニコチン、ノルニコチン、ミオスミン、ニコチリン、ニコチン-N-オキシド、アナバシン、アナタビン、およびコチニンからなる群から選択される1種以上のアルカロイドのピークが検出されない、[1]~[5]のいずれかに記載のたばこ抽出物。
[7]1)たばこ植物体の全部またはその一部を水蒸気蒸留して留分を得る工程、
2)得られた留分を有機溶媒で抽出する工程、
3)抽出により得られた有機相から有機溶媒を除去する工程
を含む方法によって製造される、[1]~[6]のいずれかに記載のたばこ抽出物。
[8]有機溶媒が、酢酸エチルまたはジエチルエーテルである、[7]に記載のたばこ抽出物。
[9]留分を有機溶媒で抽出する工程の前に、留分のpHを6.0以下に調製する工程をさらに含む、[7]または[8]に記載のたばこ抽出物。
[10]留分のpHが4.0以下である、[9]に記載のたばこ抽出物。
[11]非燃焼型香味吸引器に用いるための、[1]~[10]のいずれかに記載のたばこ抽出物。
[12]加熱型香味吸引器に用いるための、[1]~[11]のいずれかに記載のたばこ抽出物。
[13][1]~[11]のいずれかに記載のたばこ抽出物を含む、非燃焼型香味吸引器。
[14][1]~[12]のいずれかに記載のたばこ抽出物を含む、加熱型香味吸引器。
[15][1]~[12]のいずれかに記載のたばこ抽出物を含む、加熱型香味吸引器用混合液。
[16][15]に記載の加熱型香味吸引器用混合液を含む、加熱型香味吸引器。
[17]1)たばこ植物体の全部またはその一部を水蒸気蒸留して留分を得る工程、
2)得られた留分を有機溶媒で抽出する工程、
3)抽出により得られた有機相から有機溶媒を除去する工程
を含む、[1]~[12]に記載のたばこ抽出物の製造方法。
[18]有機溶媒が、酢酸エチルまたはジエチルエーテルである、[17]に記載のたばこ抽出物の製造方法。
[19]留分を有機溶媒で抽出する工程の前に、留分のpHを6.0以下に調製する工程をさらに含む、[17]または[18]に記載のたばこ抽出物の製造方法。
[20]留分のpHが4.0以下である、[19]に記載のたばこ抽出物の製造方法。
[21][1]~[11]のいずれかに記載のたばこ抽出物の、非燃焼型香味吸引器への使用。
[22][1]~[12]のいずれかに記載のたばこ抽出物の、加熱型香味吸引器への使用。
本発明のたばこ抽出物によれば、非燃焼型香味吸引器に供する際に溶媒への不溶性成分による沈殿などの問題を起こすことなく、かつ熱源部の焦げ付きを抑えて香味の変容も抑えた非燃焼型香味吸引器を提供することが可能となる。また、抽出工程において水蒸気蒸留で得られた留分を酸性に保ちながら溶媒による液液転溶することで、さらにアルカロイド含有量を低減またはアルカロイドを除去したたばこ抽出物を提供することが可能となる。
以下に本発明の態様を具体的に説明するが、本発明はこれらに限定されるものではない。
本明細書で特段に定義されない限り、本発明に関連して用いられる化学用語および技術用語は、当業者によって一般に理解される意味を有するものとする。
1つの態様として、本発明は、固定相が100%ジメチルポリシロキサンであるカラムを用いてガスクロマトグラフィーで分析をした場合に、保持指標(RI)が2100未満の成分群のピーク面積の合計が、全体のピーク面積の合計の78%以上である、たばこ抽出物を提供する。好ましい態様として、分析はガスクロマトグラフィー(水素炎イオン化検出器)で行う。
本発明のたばこ抽出物は、たばこ植物体の全部またはその一部を原材料として製造される。「たばこ植物体の一部」とは、たばこ植物体の部分であり、例えば葉(上葉、本葉、合葉、中葉、および下葉を含む)、摘芯部、腋芽、茎、幹、花、根、および種、またはそれらの混合物を含み、好ましくは葉、腋芽、および幹である。
たばこ植物体の全部またはその一部は、そのまま用いても、あるいは裁断、粉砕または磨砕して細片状、スラリー状、または微粉状としたものを用いてもよい。たばこ植物体の全部またはその一部は、畑地などから収穫したものをそのまま用いても、所定期間屋内または屋外に放置して水分を一部放散させたものを用いても、あるいは乾燥器(凍結乾燥器も含む)などで水分をほとんど放散させたものを用いてもよい。
本明細書で「保持指標(RI)」とは、ガスクロマトグラフィーによる分析において、直鎖炭化水素(n-アルカン)の炭素数を基準とし、n-アルカンと分析対象の化合物の保持比を相対的に表した指標を指す。保持指標(RI)は、所定の固定相を有するカラムを用いた場合、カラムの長さ、キャリアガス流量などが変化しても同一の化合物であれば理論上同じ値となる。保持指標(RI)は、具体的には以下の式で算出される。
本明細書において、保持指標(RI)は、n-ヘキサン(C6、RI:600)からn-ペンタトリコンタン(C35、RI:3500)の範囲のn-アルカン混合物を用いて算出された値を用いるが、保持指標(RI)を算出する際に用いられるn-アルカン混合物はこれに限定されない。
本明細書において、ガスクロマトグラフィーで用いるカラムは、例えば無極性または低極性の固定相、好ましくは無極性の固定相を有する。
無極性の固定相を有するカラムとしては、例えば100%ジメチルポリシロキサンの固定相を有するカラムを用いることができる。
100%ジメチルポリシロキサンの固定相を有するカラムとしては、例えばDB-1(アジレント・テクノロジー製)を用いることができるが、これに限定されない。
低極性の固定相を有するカラムとしては、例えば95%ジメチルポリシロキサン/5%ジフェニルシロキサンの固定相を有するカラムを用いることができる。
95%ジメチルポリシロキサン/5%ジフェニルシロキサンの固定相を有するカラムとしては、例えばDB-5(アジレント・テクノロジー製)を用いることができるが、これに限定されない。
本明細書において、「難揮発性成分」または「難揮発性化合物」とは、溶媒となるポリオール類に溶解し、かつ溶媒が気化する温度よりも高い沸点を有する物質、または溶媒と共沸せずその化合物自体は気化しない特性を有するたばこ成分または化合物を指す。難揮発性成分または化合物としては、配糖体類、タンパク質、環構造や置換基の異なる高分子化合物、長鎖脂肪酸類、長鎖炭化水素類などがある。
上記難揮発性成分または化合物は、無極性または低極性のカラムを用いたガスクロマトグラフィーによる分析において、典型的にはn-ヘンイコサン(C21、保持指標(RI):2100)の保持時間以後の保持時間を有し、すなわち2100以上の保持指標(RI)を示す。
したがって、本発明において、「保持指標(RI)2100未満の成分群」とは、n-ヘンイコサン(C21、RI:2100)の保持時間よりも前の保持時間を有する成分群であり、比較的沸点が低く200℃~240℃以下で気化する成分群を意味する。
本発明において、「保持指標(RI)2100未満の成分群」のピーク面積の合計は、全体のピーク面積の合計の例えば78%以上である。好ましくは80%以上、より好ましくは81%以上である。
「ピーク面積」とは、ガスクロマトグラフィーによる分析で得られたクロマトグラム上における、分離されたたばこ成分または化合物のピークの波形の頂点に対して左右の変曲点の接線とベースラインが交わる地点を結んだ線分で囲まれた部分の面積を指す。
別の態様として、本発明は、リノレン酸の含有量がたばこ抽出物全体の0.02重量%以下である、前記たばこ抽出物を提供する。
リノレン酸は二重結合を3つ有する、分子式がC18H30O2で表される直鎖の不飽和脂肪酸であり、疎水性が高い難揮発性の成分であり、非燃焼型香味吸引器用混合液の溶媒として用いられるプロピレングリコールなどの比較的極性の高い有機溶媒に不溶である。
本発明において、リノレン酸の含有量は、たばこ抽出物全体の例えば0.02重量%以下、好ましくは0.01重量%以下、より好ましくは0.006重量%以下である。
別の態様として、本発明は、ニコチン、ノルニコチン、ミオスミン、ニコチリン、ニコチン-N-オキシド、アナバシン、アナタビン、およびコチニンからなる群から選択される1種以上のアルカロイドのピーク面積の合計が全体のピーク面積の合計の5%以下まで減少している、前記たばこ抽出物を提供する。
本発明において、上記アルカロイドのピーク面積の合計は、全体のピーク面積の合計の例えば5%以下、好ましくは3.5%以下、より好ましくは2.5%以下であり、最も好ましくは上記アルカロイドのピークは検出されない。
別の態様として、本発明は、非燃焼型香味吸引器に用いるための、前記たばこ抽出物を提供する。
「非燃焼型香味吸引器」とは、エアロゾル発生物品保持部に保持されたエアロゾル発生物品を燃焼させずに熱源で加熱する、または超音波で霧化する等の手段でエアロゾルを発生させ、吸口部材を通じて口中にデリバリーするたばこ製品を指す。例えば、エアロゾル発生物品は、たばこ原料に含まれる香味成分を含有する液体状または固体状のエアロゾル源、圧縮たばこペレットやたばこ粉末等のたばこ材料などがあるがこれに限定されない。
非燃焼型香味吸引器は、ユーザーが吸引するエアロゾル(香味が付与されたエアロゾルであってもよい)を生成するたばこ製品であればよく、例えば液体状のエアロゾル源を用いるタイプの加熱型香味吸引器、たばこを加熱し発生するエアロゾルをエアロゾル源として用いるタイプの加熱型香味吸引器、たばこを加熱せずにその香味を吸引する非加熱型香味吸引器などが挙げられる。
本発明においては、非燃焼型香味吸引器製品は特に限定されないが、好ましくは液体状のエアロゾル源を用いるタイプの加熱型香味吸引器を用いることができる。
非燃焼型香味吸引器に用いる液体状のエアロゾル源としては、例えばたばこ原料に含まれる香味成分をグリセリンまたはプロピレングリコールなどのポリオールに含有する、非燃焼型香味吸引器用混合液が挙げられる。
本明細書において、非燃焼型香味吸引器用混合液は、たばこ原料に含まれる香味成分を提供するものとして、本発明の前記たばこ抽出物を含むこともできる。
別の態様として、本発明は、1)たばこ植物体の全部またはその一部を水蒸気蒸留して留分を得る工程、2)得られた留分を有機溶媒で抽出する工程、3)抽出により得られた有機相から有機溶媒を除去する工程を含む方法を含む、前記たばこ抽出物の製造方法を提供する。
本発明において、水蒸気蒸留に用いるたばこ(Nicotiana属の植物)植物体の品種は特に限定されない。例えば黄色種、バーレー種、オリエント種などを用いることができる。
本発明において、水蒸気蒸留に用いるたばこ植物体は部位を選別せずに全部を用いることもできるし、所望の部位のみを選別して一部を用いることもできる。また、水蒸気蒸留に用いるたばこ植物体の全部またはその一部は、裁断せずに水蒸気蒸留に供してもよいし、適宜所望のサイズに裁断、例えば2cm角程度に裁断して水蒸気蒸留に供してもよい。定法により粉砕または磨砕して細片状、スラリー状、または微粉状としたたばこ植物体の全部またはその一部を水蒸気蒸留に供してもよい。水蒸気蒸留に用いるたばこ植物体の全部またはその一部は、畑地などから収穫したものをそのまま用いても、所定期間屋内または屋外に放置して水分を一部放散させたものを用いても、あるいは乾燥機(凍結乾燥機も含む)などで水分をほとんど放散させたものを用いてもよい。
「水蒸気蒸留」とは、蒸気圧の低い高沸点の化合物を沸点以下の温度で蒸留する方法である。目的化合物を含む対象試料を入れた蒸留容器に連続的に加熱水蒸気を導入することで、蒸留容器を加熱水蒸気で満たされた加熱状態にし、水蒸気とともに目的化合物を留出させる。
本明細書において、「液液転溶」または「液液抽出」とは、液相の試料からの目的化合物の有機溶媒抽出を指す。具体的には、有機溶媒を溶媒とした化合物の抽出方法である。目的化合物を含む液相の試料に対して有機溶媒を加えて分離した二相を形成し、振とうすることにより、二相に対する分配の差を利用して加えた有機溶媒中に目的化合物を抽出する。
本明細書において、「溶媒浸漬抽出」とは、固相の試料からの目的化合物の有機溶媒抽出を指す。目的化合物を含む固相の試料を有機溶媒中に浸漬することにより、有機溶媒中に目的化合物を抽出する。
本発明において、有機溶媒で抽出する工程で用いる有機溶媒は、水と混和しない溶媒であればよく、例えば酢酸エチル、ジエチルエーテル、酢酸プロピル、酢酸イソプロピルなど、好ましくは酢酸エチルまたはジエチルエーテルを用いることができる。
本発明において、抽出により得られた有機相から有機溶媒を除去する工程で用いる方法は、特に限定されない。エバポレーターなどによる減圧溶媒除去、ヒーターによる加熱溶媒除去、パージガスの吹き付けによる溶媒除去などの方法を用いることができる。
別の態様として、本発明は、水蒸気蒸留の留分のpHを3.0~6.0に調製する工程をさらに含む、前記たばこ抽出物の製造方法を提供する。水蒸気蒸留の留分のpHを上記pHに調整することでアルカロイドの分子形とイオン形の間の平衡をイオン形の方へシフトさせ、有機溶媒への抽出を阻害することで、アルカロイド含有量を低減またはアルカロイドを除去したたばこ抽出物を製造することができる。
本発明においては、水蒸気蒸留の留分のpHを、例えば6.0以下、好ましくは5.0以下、より好ましくは4.0以下に調整する。
また、本発明においては、水蒸気蒸留の留分のpHを、例えば1.0以上、好ましくは2.0以上、より好ましくは3.0以上に調整する。
本明細書において、「温水抽出」とは、加熱した水を溶媒として用いた溶媒抽出を指す。
温水抽出においては、例えば50~60℃に水を加熱して、原材料を浸漬したときに約40℃~45℃になる条件とする。
別の態様として、本発明は、上記製造方法で製造される、前記たばこ抽出物を提供する。
前記たばこ抽出物は、たばこ植物体の全部またはその一部を原材料として製造されるものであり、原材料として用いるたばこ植物体の種、用いる部分や生育環境によっては、元々含有される各成分の含有量が大きく変動する場合もあり、抽出物中の成分の含有量を指標とした本発明のたばこ抽出物の特定が実際的でない場合も考えられうるが、上記製造方法を用いれば、難揮発性成分が減少し、および/またはアルカロイド含有量が低減もしくはアルカロイドが除去された、ある程度一定の品質を有する本発明のたばこ抽出物が得られることが期待され、これは本発明の効果を奏するものである。
以下に本発明の実施例を説明する。本発明の技術的範囲は、これらの実施例によって限定されない。
実施例1:水蒸気蒸留および有機溶媒抽出によるたばこ抽出物の製造
米国産黄色種のたばこ葉を用いて、下記の手順でたばこ抽出物を製造した。
実施例1:水蒸気蒸留および有機溶媒抽出によるたばこ抽出物の製造
米国産黄色種のたばこ葉を用いて、下記の手順でたばこ抽出物を製造した。
(1)水蒸気蒸留
水を入れて1時間程度内部をクリーニングした水蒸気蒸留装置(東京製作所製ハーブオイルメーカー(ラージタイプ))に2Lの水を入れてヒーターで加熱(250℃)した。沸騰後、米国産黄色種のたばこ葉(500g)を入れて蒸留を開始した。その後蒸留を続け、2時間の蒸留で、1000mLの留分を採取した。得られた留分は、ビーカーに移してラップをし、5℃の冷蔵庫で一晩保存した。
水を入れて1時間程度内部をクリーニングした水蒸気蒸留装置(東京製作所製ハーブオイルメーカー(ラージタイプ))に2Lの水を入れてヒーターで加熱(250℃)した。沸騰後、米国産黄色種のたばこ葉(500g)を入れて蒸留を開始した。その後蒸留を続け、2時間の蒸留で、1000mLの留分を採取した。得られた留分は、ビーカーに移してラップをし、5℃の冷蔵庫で一晩保存した。
(2)留分の有機溶媒抽出
有機溶媒として、酢酸エチル、ジエチルエーテル、クロロホルム、およびn-ヘキサンを用いた。
1L容の分液ロートに留分500mL(留分に浮いていたオイルも含む)を入れ、有機溶媒200mLおよび塩化ナトリウム30gを添加して振とうした。水相を除去した後、有機相に残りの留分500mLおよび塩化ナトリウム30gを添加して振とうした(計1000mLの留分を抽出)。水相を除去した後、有機相を300mL用の三角フラスコに移し、無水硫酸ナトリウム20gを添加し、緩やかに浸透した後、室温で30分放置することにより脱水した。
有機溶媒として、酢酸エチル、ジエチルエーテル、クロロホルム、およびn-ヘキサンを用いた。
1L容の分液ロートに留分500mL(留分に浮いていたオイルも含む)を入れ、有機溶媒200mLおよび塩化ナトリウム30gを添加して振とうした。水相を除去した後、有機相に残りの留分500mLおよび塩化ナトリウム30gを添加して振とうした(計1000mLの留分を抽出)。水相を除去した後、有機相を300mL用の三角フラスコに移し、無水硫酸ナトリウム20gを添加し、緩やかに浸透した後、室温で30分放置することにより脱水した。
(3)有機相からの有機溶媒の除去
脱水後の有機相を、少量の無水硫酸ナトリウムを載せたろ紙(アドバンテック東洋製,No.2,150mm)でろ過し、ロータリーエバポレーターにより、蒸発乾固するまで40℃の湯浴中で減圧溶媒除去した。5mLの純度99%エタノール(和光特級)をさらに添加し、ロータリーエバポレーターにより、減圧条件下にて残留する有機溶媒を完全に除去し、乾固物として17mgのたばこ抽出物を得た。該抽出物の重量に対して100倍の重量の有機溶媒(抽出に用いたものと同じ)を添加して溶解した。溶解物を0.45μmの孔径のフィルター(PTFE)でろ過し、たばこ抽出液とした。
脱水後の有機相を、少量の無水硫酸ナトリウムを載せたろ紙(アドバンテック東洋製,No.2,150mm)でろ過し、ロータリーエバポレーターにより、蒸発乾固するまで40℃の湯浴中で減圧溶媒除去した。5mLの純度99%エタノール(和光特級)をさらに添加し、ロータリーエバポレーターにより、減圧条件下にて残留する有機溶媒を完全に除去し、乾固物として17mgのたばこ抽出物を得た。該抽出物の重量に対して100倍の重量の有機溶媒(抽出に用いたものと同じ)を添加して溶解した。溶解物を0.45μmの孔径のフィルター(PTFE)でろ過し、たばこ抽出液とした。
(4)たばこ抽出液のガスクロマトグラフィー(GC/FID)による分析
(3)で得たたばこ抽出液について、以下の条件で分析を行った。
ガスクロマトグラフィー(GC/FID)
装置:アジレント・テクノロジー製7890A GC
カラム:DB-1(アジレント・テクノロジー製),内径0.25mm×長さ30m,膜厚0.25μm
注入量:1μL
注入モード:スプリット(10:1)
注入口温度:290℃
セプタムパージ流量:5mL/分
キャリアガス:ヘリウム(He)
カラム流量:1mL/分
オーブン:40℃(3分)-4℃/分-290℃(10分)(計75.5分)
検出器:水素炎イオン化検出器(FID)
検出器温度:300℃
水素(H2)流量:40mL/分
空気(Air)流量:450mL/分
メークアップガス(He)流量:1mL/分
(3)で得たたばこ抽出液について、以下の条件で分析を行った。
ガスクロマトグラフィー(GC/FID)
装置:アジレント・テクノロジー製7890A GC
カラム:DB-1(アジレント・テクノロジー製),内径0.25mm×長さ30m,膜厚0.25μm
注入量:1μL
注入モード:スプリット(10:1)
注入口温度:290℃
セプタムパージ流量:5mL/分
キャリアガス:ヘリウム(He)
カラム流量:1mL/分
オーブン:40℃(3分)-4℃/分-290℃(10分)(計75.5分)
検出器:水素炎イオン化検出器(FID)
検出器温度:300℃
水素(H2)流量:40mL/分
空気(Air)流量:450mL/分
メークアップガス(He)流量:1mL/分
酢酸エチル、ジエチルエーテル、クロロホルム、およびn-ヘキサンで溶媒抽出した場合のたばこ抽出液のGC/FIDによる分析で得られたクロマトグラムを、図1~4にそれぞれ示す。また、クロマトグラム上のピークを、保持指標(RI)700~2099、2100~2299、および2300以上の数値範囲で分類した場合の各範囲の成分群のピーク面積の合計が全体のピークの面積の合計に占める割合(%)、ならびに各範囲の成分群のピーク数および全体のピーク数の合計に占める割合(%)を以下の表1に示す。さらに、疎水性が高い難揮発性化合物であるリノレン酸およびフィトールの、たばこ抽出物全体における含有量(重量%)を以下の表2に示す。
図1~4のクロマトグラムから明らかであるように、水蒸気蒸留後の留分を酢酸エチル、ジエチルエーテル、クロロホルム、またはn-ヘキサンのいずれで溶媒抽出した場合であっても、保持指標(RI)が2100以上の比較的沸点が高く揮発しにくい成分群のピークが小さく、疎水性が高い難揮発性化合物の指標であるリノレン酸のピークも小さいことが分かった。特に、酢酸エチルまたはジエチルエーテルのそれぞれで溶媒抽出した場合には、クロロホルムまたはn-ヘキサンで溶媒抽出した場合と比較しても、RIが2100以上の成分群のピークが小さく、リノレン酸のピークが小さかった。そして、表1から明らかであるように、酢酸エチルまたはジエチルエーテルで溶媒抽出した場合には、RIが2100未満の比較的沸点が低く揮発しやすい成分群のピーク面積の割合が78%を超えていることが分かった。また、表2から明らかであるように、酢酸エチル、ジエチルエーテル、クロロホルム、またはn-ヘキサンのいずれで溶媒抽出した場合であっても、リノレン酸の含有量が0.1重量%程度以下であることが分かった。特に、酢酸エチルまたはジエチルエーテルで溶媒抽出した場合にはリノレン酸の含有量が0.02重量%程度以下であり、クロロホルムまたはn-ヘキサンで溶媒抽出した場合と比較しても極めて低かった。したがって、水蒸気蒸留後の留分を酢酸エチルまたはジエチルエーテルで溶媒抽出することで、難揮発性成分を大幅に減少したたばこ抽出物が得られることが示された。
実施例2:たばこ抽出物のプロピレングリコールへの溶解性試験
実施例1で乾固物として得られたたばこ抽出物について、加熱型香味吸引器用混合液の溶媒としても用いられているプロピレングリコールへの溶解性について試験した。具体的には、所定量のプロピレングリコールを添加して42℃に加温し、室温に戻した後に粒子径分布測定装置(堀場製作所製LV-950A)で150μm(1次粒子)、1500μm(凝集物)の粒度分布を測定し、不溶粒子の有無を確認した。
実施例1で乾固物として得られたたばこ抽出物について、加熱型香味吸引器用混合液の溶媒としても用いられているプロピレングリコールへの溶解性について試験した。具体的には、所定量のプロピレングリコールを添加して42℃に加温し、室温に戻した後に粒子径分布測定装置(堀場製作所製LV-950A)で150μm(1次粒子)、1500μm(凝集物)の粒度分布を測定し、不溶粒子の有無を確認した。
水蒸気蒸留後の留分を酢酸エチルまたはジエチルエーテルにより液液抽出することにより製造したたばこ抽出物は、該抽出物重量の4倍の重量のプロピレングリコールを添加することで溶解し、0.45μm以上の不溶粒子は確認されなかった。
一方、水蒸気蒸留後の留分をクロロホルムまたはn-ヘキサンにより溶媒抽出することにより製造したたばこ抽出物は、該抽出物の重量の4倍の重量のプロピレングリコールを添加した場合に、直径0.45μm以上の不溶粒子が確認され、完全に溶解していなかった。プロピレングリコールを段階的に追加したところ、水蒸気蒸留後の留分をクロロホルムにより溶媒抽出することにより製造したたばこ抽出物は、該抽出物の重量の20倍の重量のプロピレングリコールを添加した場合においても、そして水蒸気蒸留後の留分をn-ヘキサンにより溶媒抽出することにより製造したたばこ抽出物は、該抽出物の重量の50倍の重量のプロピレングリコールを添加した場合においても、0.45μm以上の不溶粒子が確認された。このような不溶粒子は、たばこ葉中の疎水性成分が抽出されたことにより発生したものと考えられる。
したがって、水蒸気蒸留後の留分を酢酸エチルまたはジエチルエーテルにより溶媒抽出することにより、たばこ葉中の疎水性成分を大幅に減少し、プロピレングリコールに容易に溶解するたばこ抽出物が得られることが示された。
比較例1:有機溶媒抽出によるたばこ抽出物の製造およびプロピレングリコールへの溶解性試験
(1)有機溶媒抽出によるたばこ抽出物の製造
有機溶媒として、酢酸エチル、ジエチルエーテル、クロロホルム、n-ヘキサン、アセトン、エタノール、およびメタノールを用いた。
500mL容のコニカルビーカーに、2cm角程度に裁断した実施例1と同じ米国産黄色種のたばこ葉(10g)を入れ、有機溶媒100mLを添加して浸漬させた。室温で1時間振とう抽出を行い(溶媒浸漬抽出)、抽出後の有機溶媒を少量の無水硫酸ナトリウムを載せたろ紙(アドバンテック東洋製,No.2,150mm)でろ過し、ロータリーエバポレーターにより、蒸発乾固するまで40℃の湯浴中で減圧溶媒除去し、乾固物として9.3mg~16.0mgのたばこ抽出物を得た。該抽出物の抽出に用いた有機溶媒1mLを添加して分析用試料とし、実施例1(4)と同様の条件で、GC/FIDによる分析を行った。ただし、注入モードはスプリット(50:1)とした。
(1)有機溶媒抽出によるたばこ抽出物の製造
有機溶媒として、酢酸エチル、ジエチルエーテル、クロロホルム、n-ヘキサン、アセトン、エタノール、およびメタノールを用いた。
500mL容のコニカルビーカーに、2cm角程度に裁断した実施例1と同じ米国産黄色種のたばこ葉(10g)を入れ、有機溶媒100mLを添加して浸漬させた。室温で1時間振とう抽出を行い(溶媒浸漬抽出)、抽出後の有機溶媒を少量の無水硫酸ナトリウムを載せたろ紙(アドバンテック東洋製,No.2,150mm)でろ過し、ロータリーエバポレーターにより、蒸発乾固するまで40℃の湯浴中で減圧溶媒除去し、乾固物として9.3mg~16.0mgのたばこ抽出物を得た。該抽出物の抽出に用いた有機溶媒1mLを添加して分析用試料とし、実施例1(4)と同様の条件で、GC/FIDによる分析を行った。ただし、注入モードはスプリット(50:1)とした。
GC/FIDによる分析で得られたクロマトグラムを、図5~11にそれぞれ示す。また、クロマトグラム上のピークを、保持指標(RI)700~2099、2100~2299、および2300以上の数値範囲で分類した場合の各範囲の成分群のピーク面積の合計が全体のピークの面積の合計に占める割合(%)、ならびに各範囲の成分群のピーク数および全体のピーク数の合計に占める割合(%)を以下の表3に示す。
図5~11のクロマトグラムから明らかであるように、全ての有機溶媒において、RIが2100以上の比較的沸点が高く揮発しにくい成分群のピークが、RIが2100未満の比較的沸点が低く揮発しやすい成分群のピークと比較して、実施例1の結果(図1~4)よりも大きいことが分かった。そして、表3から明らかであるように、全ての有機溶媒において、RIが2100未満の比較的沸点が低く揮発しやすい成分群のピーク面積の割合が高くても70%強(メタノールの場合)と、実施例1の結果(表1)と比較して低く、ピーク数も少ないことが分かった。一方、RIが2100以上の比較的沸点が高く揮発しにくい成分群のピーク面積の割合が、実施例1の結果(表1)と比較して高く、ピーク数も多い傾向があることも分かった。したがって、有機溶媒抽出のみでは、難揮発性成分を効果的に減少したたばこ抽出物は得られないことが示された。
(2)たばこ抽出物のプロピレングリコールへの溶解性試験
実施例2と同様の試験を、有機溶媒抽出のみにより製造したたばこ抽出物に対して行ったところ、いずれのたばこ抽出物とも、該抽出物の重量の50倍の重量のプロピレングリコールを添加した場合においても、0.45μm以上の不溶粒子が確認された。したがって、有機溶媒抽出のみでは、たばこ葉中の疎水性成分を大幅に減少し、プロピレングリコールに容易に溶解するたばこ抽出物は得られないことが示された。
実施例2と同様の試験を、有機溶媒抽出のみにより製造したたばこ抽出物に対して行ったところ、いずれのたばこ抽出物とも、該抽出物の重量の50倍の重量のプロピレングリコールを添加した場合においても、0.45μm以上の不溶粒子が確認された。したがって、有機溶媒抽出のみでは、たばこ葉中の疎水性成分を大幅に減少し、プロピレングリコールに容易に溶解するたばこ抽出物は得られないことが示された。
比較例2:温水抽出および有機溶媒抽出によるたばこ抽出物の製造
(1)温水抽出
蒸留水を加熱して約60℃の温水500mLを用意し、2cm角程度に裁断した米国産黄色種のたばこ葉(50g)を入れて40~45℃になるように保温し、スターラーで撹拌しながら10分間抽出した。抽出後の温水を6℃の冷蔵庫内で室温まで冷まし、ろ紙(ADVANTEC,No.5A)でろ過して固体を除去し、470mLの温水抽出液を得た。
(1)温水抽出
蒸留水を加熱して約60℃の温水500mLを用意し、2cm角程度に裁断した米国産黄色種のたばこ葉(50g)を入れて40~45℃になるように保温し、スターラーで撹拌しながら10分間抽出した。抽出後の温水を6℃の冷蔵庫内で室温まで冷まし、ろ紙(ADVANTEC,No.5A)でろ過して固体を除去し、470mLの温水抽出液を得た。
(2)温水抽出液からの有機溶媒抽出
有機溶媒として、酢酸エチル、ジエチルエーテル、クロロホルム、およびn-ヘキサンを用いた。
500mL容の分液ロートに温水抽出液100mLを入れ、有機溶媒50mLおよび塩化ナトリウム20gを添加し、5分間振とうした。振とう後6℃の冷蔵庫で3時間静置し、有機相と水相が良好に分離していることを確認し、水相を除去した。水相を除去した後、有機相を少量の無水硫酸ナトリウムを載せたろ紙(アドバンテック東洋製,No.2,150mm)でろ過し、ロータリーエバポレーターにより、蒸発乾固するまで40℃の湯浴中で減圧溶媒除去し、乾固物として8.2~12.5mgのたばこ抽出物を得た。該抽出物に抽出に用いた有機溶媒1mLを添加して分析用試料とし、実施例1(4)と同様の条件で、GC/FIDによる分析を行った。
有機溶媒として、酢酸エチル、ジエチルエーテル、クロロホルム、およびn-ヘキサンを用いた。
500mL容の分液ロートに温水抽出液100mLを入れ、有機溶媒50mLおよび塩化ナトリウム20gを添加し、5分間振とうした。振とう後6℃の冷蔵庫で3時間静置し、有機相と水相が良好に分離していることを確認し、水相を除去した。水相を除去した後、有機相を少量の無水硫酸ナトリウムを載せたろ紙(アドバンテック東洋製,No.2,150mm)でろ過し、ロータリーエバポレーターにより、蒸発乾固するまで40℃の湯浴中で減圧溶媒除去し、乾固物として8.2~12.5mgのたばこ抽出物を得た。該抽出物に抽出に用いた有機溶媒1mLを添加して分析用試料とし、実施例1(4)と同様の条件で、GC/FIDによる分析を行った。
GC/FIDによる分析で得られたクロマトグラムを、図12~15にそれぞれ示す。また、クロマトグラム上のピークを、保持指標(RI)700~2099、2100~2299、および2300以上の数値範囲で分類した場合の各範囲の成分群のピーク面積の合計が全体のピークの面積の合計に占める割合(%)、ならびに各範囲の成分群のピーク数および全体のピーク数の合計に占める割合(%)を以下の表4に示す。
図12~15のクロマトグラムから明らかであるように、温水抽出液を有機溶媒抽出した場合には、全ての有機溶媒において、検出されたすべての成分群のピークが、実施例1の結果(図1~4)よりも小さいことが分かった。また、RIが2100以上の比較的沸点が高く揮発しにくい成分群のピークが、RIが2100未満の比較的沸点が低く揮発しやすい成分群のピークと比較して、実施例1の結果(図1~4)よりも大きいことが分かった。そして、表4から明らかであるように、全ての有機溶媒において、RIが2100未満の比較的沸点が低く揮発しやすい成分群のピーク面積の割合が高くても55%弱(酢酸エチルの場合)であり、実施例1の結果(表1)と比較して低く、ピーク数も少ないことが分かった。一方、RIが2100以上の比較的沸点が高く揮発しにくい成分群のピーク面積の割合が、実施例1の結果(表1)と比較して高いことも分かった。したがって、温水抽出および有機溶媒抽出では、難揮発性成分を効果的に減少したたばこ抽出物は得られない上、抽出の過程での成分のロスも大きいことが示された。
実施例3:アルカロイド含有量を低減またはアルカロイドを除去したたばこ抽出物の製造
米国産黄色種のたばこ葉を用いて、下記の手順でアルカロイド含有量を低減またはアルカロイドを除去したたばこ抽出物を製造した。すなわち、実施例1と同様に得た水蒸気蒸留の留分のpHを調整することでアルカロイドの分子形とイオン形の間の平衡をイオン形の方へシフトさせ、有機溶媒への抽出を阻害することで、アルカロイド含有量を低減またはアルカロイドを除去した。
米国産黄色種のたばこ葉を用いて、下記の手順でアルカロイド含有量を低減またはアルカロイドを除去したたばこ抽出物を製造した。すなわち、実施例1と同様に得た水蒸気蒸留の留分のpHを調整することでアルカロイドの分子形とイオン形の間の平衡をイオン形の方へシフトさせ、有機溶媒への抽出を阻害することで、アルカロイド含有量を低減またはアルカロイドを除去した。
(1)水蒸気蒸留
実施例1(1)と同様に、黄色種のたばこ葉の水蒸気蒸留を行い、留分1000mLを得た。
実施例1(1)と同様に、黄色種のたばこ葉の水蒸気蒸留を行い、留分1000mLを得た。
(2)留分の有機溶媒抽出
有機溶媒としてジエチルエーテルを用いた。
(1)で得た留分に1.5M硫酸を撹拌しながら徐々に添加し、pH6.0、5.0、4.0、または3.0に調整した。実施例1(2)と同様の手順でpHを調整した留分のジエチルエーテルによる溶媒抽出を行い、ジエチルエーテル相を脱水した。
有機溶媒としてジエチルエーテルを用いた。
(1)で得た留分に1.5M硫酸を撹拌しながら徐々に添加し、pH6.0、5.0、4.0、または3.0に調整した。実施例1(2)と同様の手順でpHを調整した留分のジエチルエーテルによる溶媒抽出を行い、ジエチルエーテル相を脱水した。
(3)有機相からの有機溶媒の除去
脱水後のジエチルエーテル相から、実施例1(3)と同様の手順でジエチルエーテルを除去し、乾固物として18mgのたばこ抽出物を得た。該抽出物の重量に対して100倍の重量のジエチルエーテルを添加して溶解した。溶解物を0.45μmの孔径のフィルター(PTFE)でろ過し、たばこ抽出液とした。
脱水後のジエチルエーテル相から、実施例1(3)と同様の手順でジエチルエーテルを除去し、乾固物として18mgのたばこ抽出物を得た。該抽出物の重量に対して100倍の重量のジエチルエーテルを添加して溶解した。溶解物を0.45μmの孔径のフィルター(PTFE)でろ過し、たばこ抽出液とした。
(4)たばこ抽出液のガスクロマトグラフィー(GC/FID)による分析
(3)で得たたばこ抽出液について、実施例1(4)と同様の条件で、GC/FIDによる分析を行った。
留分をpH6.0、5.0、4.0、または3.0でジエチルエーテルにより溶媒抽出した場合のたばこ抽出液のGC/FIDによる分析で得られたクロマトグラム上のニコチン、ノルニコチン、ミオスミン、ニコチリン、ニコチン-N-オキシド、アナバシン、アナタビン、およびコチニンの各アルカロイドのピーク面積が、全体のピークの面積の合計に占める割合(%)を以下の表5に示す。
(3)で得たたばこ抽出液について、実施例1(4)と同様の条件で、GC/FIDによる分析を行った。
留分をpH6.0、5.0、4.0、または3.0でジエチルエーテルにより溶媒抽出した場合のたばこ抽出液のGC/FIDによる分析で得られたクロマトグラム上のニコチン、ノルニコチン、ミオスミン、ニコチリン、ニコチン-N-オキシド、アナバシン、アナタビン、およびコチニンの各アルカロイドのピーク面積が、全体のピークの面積の合計に占める割合(%)を以下の表5に示す。
表5から明らかであるように、pH6.0、5.0でジエチルエーテルにより溶媒抽出した場合には検出されていたニコチン(RI:1348)が、pH4.0、3.0では検出されないことが分かった。そして、pH6.0で溶媒抽出した場合には各アルカロイドのピーク面積の割合の合計が3.1%であり、pH5.0で溶媒抽出した場合には2.0%であり、pH4.0または3.0で溶媒抽出した場合には上記のアルカロイドのピークは検出されなかった。したがって、pH6.0、5.0ではアルカロイド含有量が低減されており、pH4.0、3.0ではアルカロイドが除去されていることが示された。
実施例4:水蒸気蒸留および有機溶媒抽出による黄色種たばこ抽出物の製造およびプロピレングリコールへの溶解性試験
フランス産黄色種たばこを用いて、下記の手順でたばこ抽出物を製造した。
フランス産黄色種たばこを用いて、下記の手順でたばこ抽出物を製造した。
(1)フランス産黄色種たばこ(958.5g)について、水蒸気蒸留装置(東京製作所製ハーブオイルメーカー(3kg用))を、3Lの水とともにヒーターで加熱(設定:280℃、実温度:126~128℃)して水蒸気蒸留を行い、2.3Lの留分を得た。留分の滴下速度は9.5~10ml/分であった。
(2)得られた留分を500mLずつに分け、実施例1(2)および(3)と同様の手順で各種有機溶媒(酢酸エチル、ジエチルエーテル、クロロホルム、およびn-ヘキサン)で抽出し、溶媒を除去して、乾固物として187~280mgのたばこ抽出物を得た。
上記のたばこ抽出物について、プロピレングリコールへの溶解性について試験した。具体的には、所定量のプロピレングリコールを添加して、目視で不溶粒子の有無を確認した。また、湿式粒子測定器(堀場製作所製LA-960)で粒度分布を測定し、粒子径が0.45μm以上の不溶粒子の有無を確認した。結果を以下の表6および7に示す。
表6および7から明らかであるように、水蒸気蒸留後の留分を酢酸エチルまたはジエチルエーテルにより溶媒抽出することにより製造した黄色種たばこ抽出物は、該抽出物重量の20倍および50倍の重量のプロピレングリコールを添加することで溶解した。
一方、水蒸気蒸留後の留分をクロロホルムにより溶媒抽出することにより製造した黄色種たばこ抽出物は、該抽出物の重量の20倍の重量のプロピレングリコールを添加した場合には溶解せず、粒子径が0.45μm以上の不溶粒子が確認され、50倍の重量のプロピレングリコールを添加することでようやく溶解した。また、水蒸気蒸留後の留分をn-ヘキサンにより溶媒抽出することにより製造した黄色種たばこ抽出物は、該抽出物の重量の50倍の重量のプロピレングリコールを添加した場合においても溶解せず、粒子径が0.45μm以上の不溶粒子が確認された。
したがって、水蒸気蒸留後の留分を酢酸エチルまたはジエチルエーテルにより溶媒抽出することにより、フランス産黄色種においても、たばこ葉中の疎水性成分を大幅に減少し、プロピレングリコールに容易に溶解するたばこ抽出物が得られることが示された。
本発明により、たばこ葉中の難揮発性成分量を大幅に減少したたばこ抽出物、該たばこ抽出物の製造方法、該たばこ抽出物を含む非燃焼型香味吸引器、さらに該たばこ抽出物を含む非燃焼型香味吸引器の一形態である加熱型香味吸引器を提供することができる。また、さらにアルカロイド含有量を低減またはアルカロイドを除去したたばこ抽出物、該たばこ抽出物の製造方法、該たばこ抽出物を含む非燃焼型香味吸引器、さらに該たばこ抽出物を含む非燃焼型香味吸引器の一形態である加熱型香味吸引器を提供することができる。
Claims (22)
- 固定相が100%ジメチルポリシロキサンであるカラムを用いてガスクロマトグラフィー(水素炎イオン化検出器)で分析をした場合に、保持指標(RI)が2100未満の成分群のピーク面積の合計が全体のピーク面積の合計の78%以上である、たばこ抽出物。
- 保持指標(RI)が2100未満の成分群のピーク面積の合計が全体のピーク面積の合計の81%以上である、請求項1に記載のたばこ抽出物。
- リノレン酸の含有量がたばこ抽出物全体の0.02重量%以下である、請求項1または2に記載のたばこ抽出物。
- リノレン酸のピーク面積が全体のピーク面積の合計の0.01重量%以下である、請求項1~3のいずれか一項に記載のたばこ抽出物。
- 固定相が100%ジメチルポリシロキサンであるカラムを用いてガスクロマトグラフィー(水素炎イオン化検出器)で分析をした場合に、ニコチン、ノルニコチン、ミオスミン、ニコチリン、ニコチン-N-オキシド、アナバシン、アナタビン、およびコチニンから選択される1種以上のアルカロイドのピーク面積の合計が全体のピーク面積の合計の5%以下まで減少している、請求項1~4のいずれか一項に記載のたばこ抽出物。
- ニコチン、ノルニコチン、ミオスミン、ニコチリン、ニコチン-N-オキシド、アナバシン、アナタビン、およびコチニンからなる群から選択される1種以上のアルカロイドのピークが検出されない、請求項1~5のいずれか一項に記載のたばこ抽出物。
- 1)たばこ植物体の全部またはその一部を水蒸気蒸留して留分を得る工程、
2)得られた留分を有機溶媒で抽出する工程、
3)抽出により得られた有機相から有機溶媒を除去する工程
を含む方法によって製造される、請求項1~6のいずれか一項に記載のたばこ抽出物。 - 有機溶媒が、酢酸エチルまたはジエチルエーテルである、請求項7に記載のたばこ抽出物。
- 留分を有機溶媒で抽出する工程の前に、留分のpHを6.0以下に調製する工程をさらに含む、請求項7または8に記載のたばこ抽出物。
- 留分のpHが4.0以下である、請求項9に記載のたばこ抽出物。
- 非燃焼型香味吸引器に用いるための、請求項1~10のいずれか一項に記載のたばこ抽出物。
- 加熱型香味吸引器に用いるための、請求項1~11のいずれか一項に記載のたばこ抽出物。
- 請求項1~11のいずれか一項に記載のたばこ抽出物を含む、非燃焼型香味吸引器。
- 請求項1~12のいずれか一項に記載のたばこ抽出物を含む、加熱型香味吸引器。
- 請求項1~12のいずれか一項に記載のたばこ抽出物を含む、加熱型香味吸引器用混合液。
- 請求項15に記載の加熱型香味吸引器用混合液を含む、加熱型香味吸引器。
- 1)たばこ植物体の全部またはその一部を水蒸気蒸留して留分を得る工程、
2)得られた留分を有機溶媒で抽出する工程、
3)抽出により得られた有機相から有機溶媒を除去する工程
を含む、請求項1~12に記載のたばこ抽出物の製造方法。 - 有機溶媒が、酢酸エチルまたはジエチルエーテルである、請求項17に記載のたばこ抽出物の製造方法。
- 留分を有機溶媒で抽出する工程の前に、留分のpHを6.0以下に調製する工程をさらに含む、請求項17または18に記載のたばこ抽出物の製造方法。
- 留分のpHが4.0以下である、請求項19に記載のたばこ抽出物の製造方法。
- 請求項1~11のいずれか一項に記載のたばこ抽出物の、非燃焼型香味吸引器への使用。
- 請求項1~12のいずれか一項に記載のたばこ抽出物の、加熱型香味吸引器への使用。
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201880083925.3A CN111511224B (zh) | 2017-12-27 | 2018-12-25 | 烟草提取物、烟草提取物的制造方法、以及使用了烟草提取物的非燃烧型香味抽吸器 |
| JP2019561686A JP7054708B2 (ja) | 2017-12-27 | 2018-12-25 | たばこ抽出物、たばこ抽出物の製造方法、およびたばこ抽出物を用いた非燃焼型香味吸引器 |
| EP18894936.6A EP3732998A4 (en) | 2017-12-27 | 2018-12-25 | TOBACCO EXTRACT, PROCESS FOR THE PRODUCTION OF TOBACCO EXTRACT AND NON-BURNING AROMA INHALER WITH TOBACCO EXTRACT |
| US16/913,934 US20200359672A1 (en) | 2017-12-27 | 2020-06-26 | Tobacco extract, method for producing tobacco extract, and non-combustion flavor inhaler including tobacco extract |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2017-250959 | 2017-12-27 | ||
| JP2017250959 | 2017-12-27 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| US16/913,934 Continuation US20200359672A1 (en) | 2017-12-27 | 2020-06-26 | Tobacco extract, method for producing tobacco extract, and non-combustion flavor inhaler including tobacco extract |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2019131579A1 true WO2019131579A1 (ja) | 2019-07-04 |
Family
ID=67067327
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2018/047439 WO2019131579A1 (ja) | 2017-12-27 | 2018-12-25 | たばこ抽出物、たばこ抽出物の製造方法、およびたばこ抽出物を用いた非燃焼型香味吸引器 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US20200359672A1 (ja) |
| EP (1) | EP3732998A4 (ja) |
| JP (1) | JP7054708B2 (ja) |
| CN (1) | CN111511224B (ja) |
| TW (1) | TWI735834B (ja) |
| WO (1) | WO2019131579A1 (ja) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN112924597A (zh) * | 2021-01-27 | 2021-06-08 | 上海烟草集团有限责任公司 | 一种烟支内部梗丝分布均匀性的测定方法 |
| CN113933432A (zh) * | 2021-10-22 | 2022-01-14 | 中国烟草总公司郑州烟草研究院 | 一种适用于烟叶中生物碱检测的高灵敏和高精密度的分析方法 |
| WO2024142149A1 (ja) * | 2022-12-26 | 2024-07-04 | 日本たばこ産業株式会社 | 風味原料付香構成部材及び喫煙物品 |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN115381132A (zh) * | 2021-05-20 | 2022-11-25 | 湖南中烟工业有限责任公司 | 一种利用烟草制备的烟用香料及其制备方法和应用 |
| CN113303493A (zh) * | 2021-05-21 | 2021-08-27 | 林建辉 | 一种用于电子雾化棒的植物源抑菌精油及其制备方法 |
| CN113917045B (zh) * | 2021-11-17 | 2023-06-30 | 云南省烟草农业科学研究院 | 气相色谱-氢焰检测器定量分析烟叶11种酰胺生物碱方法 |
| CN114504118B (zh) * | 2022-02-15 | 2023-01-13 | 河北中烟工业有限责任公司 | 加热卷烟的加料液及其制备方法和加热卷烟 |
| CN114711455B (zh) * | 2022-03-10 | 2022-12-23 | 浙江中烟工业有限责任公司 | 加拿大烟叶烟气特征碱性香味成分的制备方法及其应用 |
| CN114788576B (zh) * | 2022-04-07 | 2023-05-16 | 河南中烟工业有限责任公司 | 一种烤甜香突出的豫烟浸膏美拉德反应香料及其制备方法和应用 |
| CN114894936A (zh) * | 2022-05-27 | 2022-08-12 | 云南中烟工业有限责任公司 | 烟草及烟草制品中六种生物碱的液相色谱检测方法 |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS6045909A (ja) | 1984-07-25 | 1985-03-12 | Hitachi Ltd | 磁気ヘツド |
| JPH1137986A (ja) * | 1997-05-19 | 1999-02-12 | Nkk Corp | クロロベンゼン類の自動分析装置および自動分析方法 |
| JP2002520005A (ja) | 1998-07-08 | 2002-07-09 | ノボザイムス アクティーゼルスカブ | タバコの処理におけるフェノール酸化酵素の利用 |
| WO2015029977A1 (ja) | 2013-08-27 | 2015-03-05 | 日本たばこ産業株式会社 | たばこ原料及びその製造方法並びにたばこ製品 |
| CN104757703A (zh) | 2014-12-31 | 2015-07-08 | 贵州中烟工业有限责任公司 | 一种烟草馏出液及其制备和应用 |
| CN106324130A (zh) * | 2016-08-15 | 2017-01-11 | 国家烟草质量监督检验中心 | 一种卷烟烟丝中烟碱的手性分析方法 |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS6045909B2 (ja) * | 1983-04-04 | 1985-10-12 | 日本たばこ産業株式会社 | たばこ香喫味の改善方法 |
| US6298859B1 (en) * | 1998-07-08 | 2001-10-09 | Novozymes A/S | Use of a phenol oxidizing enzyme in the treatment of tobacco |
| CN103278592A (zh) * | 2013-05-17 | 2013-09-04 | 云南省烟草农业科学研究院 | 一种气相色谱保留指数的高效获取方法及其系统 |
| CN104585865B (zh) * | 2015-01-20 | 2016-02-03 | 川渝中烟工业有限责任公司 | 一种含烟草提取物的电子烟烟液及其制备方法 |
| CN104939305B (zh) * | 2015-05-20 | 2016-04-20 | 湖南中烟工业有限责任公司 | 一种烟草提取物及电子烟液 |
| CN105954402B (zh) * | 2016-04-27 | 2018-07-06 | 中国烟草总公司郑州烟草研究院 | 一种卷烟主流烟气中生物碱的气相色谱-火焰离子化/串联质谱检测方法 |
| CN106617265B (zh) * | 2016-11-22 | 2018-05-08 | 中国烟草总公司郑州烟草研究院 | 一种电子烟烟液及其制备方法 |
| GB201706778D0 (en) * | 2017-04-28 | 2017-06-14 | British American Tobacco Investments Ltd | Method |
-
2018
- 2018-12-25 TW TW107146967A patent/TWI735834B/zh active
- 2018-12-25 CN CN201880083925.3A patent/CN111511224B/zh active Active
- 2018-12-25 EP EP18894936.6A patent/EP3732998A4/en active Pending
- 2018-12-25 WO PCT/JP2018/047439 patent/WO2019131579A1/ja unknown
- 2018-12-25 JP JP2019561686A patent/JP7054708B2/ja active Active
-
2020
- 2020-06-26 US US16/913,934 patent/US20200359672A1/en active Pending
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS6045909A (ja) | 1984-07-25 | 1985-03-12 | Hitachi Ltd | 磁気ヘツド |
| JPH1137986A (ja) * | 1997-05-19 | 1999-02-12 | Nkk Corp | クロロベンゼン類の自動分析装置および自動分析方法 |
| JP2002520005A (ja) | 1998-07-08 | 2002-07-09 | ノボザイムス アクティーゼルスカブ | タバコの処理におけるフェノール酸化酵素の利用 |
| WO2015029977A1 (ja) | 2013-08-27 | 2015-03-05 | 日本たばこ産業株式会社 | たばこ原料及びその製造方法並びにたばこ製品 |
| CN104757703A (zh) | 2014-12-31 | 2015-07-08 | 贵州中烟工业有限责任公司 | 一种烟草馏出液及其制备和应用 |
| CN106324130A (zh) * | 2016-08-15 | 2017-01-11 | 国家烟草质量监督检验中心 | 一种卷烟烟丝中烟碱的手性分析方法 |
Non-Patent Citations (1)
| Title |
|---|
| See also references of EP3732998A4 |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN112924597A (zh) * | 2021-01-27 | 2021-06-08 | 上海烟草集团有限责任公司 | 一种烟支内部梗丝分布均匀性的测定方法 |
| CN113933432A (zh) * | 2021-10-22 | 2022-01-14 | 中国烟草总公司郑州烟草研究院 | 一种适用于烟叶中生物碱检测的高灵敏和高精密度的分析方法 |
| CN113933432B (zh) * | 2021-10-22 | 2023-08-25 | 中国烟草总公司郑州烟草研究院 | 一种适用于烟叶中生物碱检测的高灵敏和高精密度的分析方法 |
| WO2024142149A1 (ja) * | 2022-12-26 | 2024-07-04 | 日本たばこ産業株式会社 | 風味原料付香構成部材及び喫煙物品 |
Also Published As
| Publication number | Publication date |
|---|---|
| CN111511224A (zh) | 2020-08-07 |
| JP7054708B2 (ja) | 2022-04-14 |
| US20200359672A1 (en) | 2020-11-19 |
| CN111511224B (zh) | 2022-04-19 |
| JPWO2019131579A1 (ja) | 2020-12-17 |
| TW201929695A (zh) | 2019-08-01 |
| TWI735834B (zh) | 2021-08-11 |
| EP3732998A1 (en) | 2020-11-04 |
| EP3732998A4 (en) | 2021-11-17 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| WO2019131579A1 (ja) | たばこ抽出物、たばこ抽出物の製造方法、およびたばこ抽出物を用いた非燃焼型香味吸引器 | |
| JP5856572B2 (ja) | セルロース系材料から構成物質を抽出、単離する方法 | |
| KR100362918B1 (ko) | 용매추출방법 | |
| US20170231267A1 (en) | Tobacco flavor extract with reduced tsnas | |
| BR102017017521B1 (pt) | Método de extração, extrato de tabaco e uso do mesmo, produto de tabaco e método de preparação do mesmo | |
| KR102269022B1 (ko) | 담배 향을 모방하는데 유용한 조성물 | |
| US20230337717A1 (en) | Ground tobacco composition | |
| KR20220016455A (ko) | 액체 담배 추출물을 제조하는 개선 방법 | |
| KR20220016818A (ko) | 둘 이상의 담배로부터 배합된 액체 담배 추출물을 생산하는 방법 | |
| KR20230118622A (ko) | 액체 담배 추출물을 제조하는 개선 방법 | |
| CN110373273B (zh) | 一种植物蜡质的脱除添加剂及脱除方法 | |
| RU2818243C2 (ru) | Способ получения смешанного жидкого табачного экстракта из двух или более видов табака | |
| CN109793261A (zh) | 一种烟用黄葵提取物的制备方法及其应用 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 18894936 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2019561686 Country of ref document: JP Kind code of ref document: A |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| ENP | Entry into the national phase |
Ref document number: 2018894936 Country of ref document: EP Effective date: 20200727 |