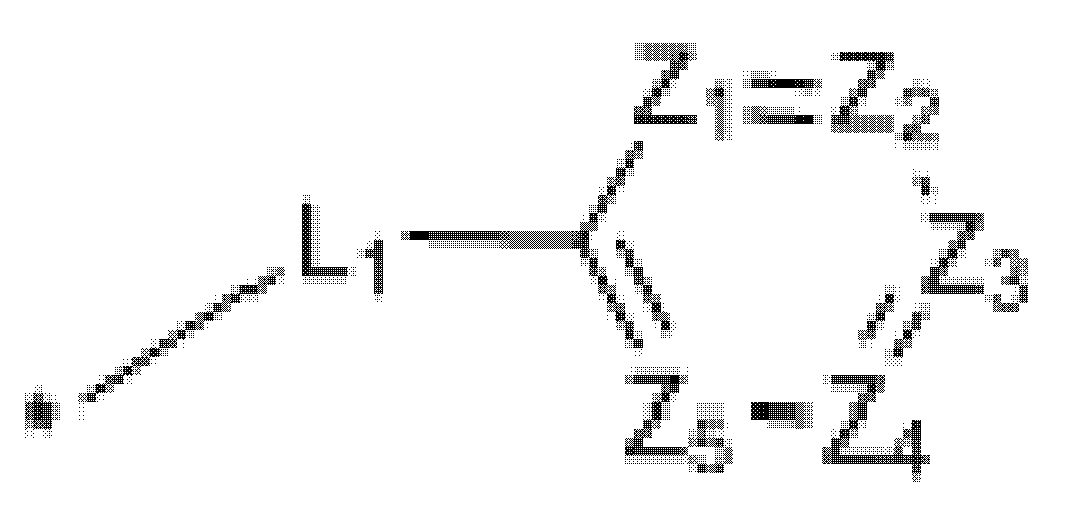WO2016105165A2 - 유기 발광 화합물 및 이를 이용한 유기 전계 발광 소자 - Google Patents
유기 발광 화합물 및 이를 이용한 유기 전계 발광 소자 Download PDFInfo
- Publication number
- WO2016105165A2 WO2016105165A2 PCT/KR2015/014271 KR2015014271W WO2016105165A2 WO 2016105165 A2 WO2016105165 A2 WO 2016105165A2 KR 2015014271 W KR2015014271 W KR 2015014271W WO 2016105165 A2 WO2016105165 A2 WO 2016105165A2
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- group
- aryl
- alkyl
- formula
- boron
- Prior art date
Links
- 150000001875 compounds Chemical class 0.000 title claims abstract description 148
- 238000002347 injection Methods 0.000 claims abstract description 29
- 239000007924 injection Substances 0.000 claims abstract description 29
- 230000005525 hole transport Effects 0.000 claims abstract description 13
- 125000003118 aryl group Chemical group 0.000 claims description 220
- 125000000217 alkyl group Chemical group 0.000 claims description 166
- ZOXJGFHDIHLPTG-UHFFFAOYSA-N Boron Chemical group [B] ZOXJGFHDIHLPTG-UHFFFAOYSA-N 0.000 claims description 126
- 125000001072 heteroaryl group Chemical group 0.000 claims description 104
- 125000000753 cycloalkyl group Chemical group 0.000 claims description 84
- 125000000592 heterocycloalkyl group Chemical group 0.000 claims description 84
- XYFCBTPGUUZFHI-UHFFFAOYSA-N phosphine group Chemical group P XYFCBTPGUUZFHI-UHFFFAOYSA-N 0.000 claims description 84
- 125000003545 alkoxy group Chemical group 0.000 claims description 83
- 125000005103 alkyl silyl group Chemical group 0.000 claims description 83
- 125000005104 aryl silyl group Chemical group 0.000 claims description 82
- 125000004104 aryloxy group Chemical group 0.000 claims description 79
- 238000000034 method Methods 0.000 claims description 76
- 125000005264 aryl amine group Chemical group 0.000 claims description 71
- 125000003342 alkenyl group Chemical group 0.000 claims description 69
- 125000000304 alkynyl group Chemical group 0.000 claims description 69
- -1 diaryl phosphine Chemical compound 0.000 claims description 59
- 125000004429 atom Chemical group 0.000 claims description 56
- 239000000126 substance Substances 0.000 claims description 53
- 125000001424 substituent group Chemical group 0.000 claims description 46
- YZCKVEUIGOORGS-OUBTZVSYSA-N Deuterium Chemical compound [2H] YZCKVEUIGOORGS-OUBTZVSYSA-N 0.000 claims description 37
- 125000004093 cyano group Chemical group *C#N 0.000 claims description 37
- 229910052805 deuterium Inorganic materials 0.000 claims description 37
- 229910052736 halogen Inorganic materials 0.000 claims description 37
- 150000002367 halogens Chemical class 0.000 claims description 37
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 claims description 34
- 239000008280 blood Substances 0.000 claims description 33
- 210000004369 blood Anatomy 0.000 claims description 33
- 229910000073 phosphorus hydride Inorganic materials 0.000 claims description 33
- 150000004982 aromatic amines Chemical class 0.000 claims description 27
- 239000011368 organic material Substances 0.000 claims description 27
- 229910052757 nitrogen Inorganic materials 0.000 claims description 25
- 229910052739 hydrogen Inorganic materials 0.000 claims description 22
- 239000001257 hydrogen Substances 0.000 claims description 22
- YCWSUKQGVSGXJO-NTUHNPAUSA-N nifuroxazide Chemical group C1=CC(O)=CC=C1C(=O)N\N=C\C1=CC=C([N+]([O-])=O)O1 YCWSUKQGVSGXJO-NTUHNPAUSA-N 0.000 claims description 21
- 229910052799 carbon Inorganic materials 0.000 claims description 19
- 238000009833 condensation Methods 0.000 claims description 19
- 230000005494 condensation Effects 0.000 claims description 19
- 150000002431 hydrogen Chemical class 0.000 claims description 19
- 125000005328 phosphinyl group Chemical group [PH2](=O)* 0.000 claims description 16
- 229910052760 oxygen Inorganic materials 0.000 claims description 14
- 229910052717 sulfur Inorganic materials 0.000 claims description 14
- 125000004432 carbon atom Chemical group C* 0.000 claims description 12
- 229910052796 boron Inorganic materials 0.000 claims description 7
- 125000000609 carbazolyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3NC12)* 0.000 claims description 7
- 125000002529 biphenylenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3C12)* 0.000 claims description 6
- 125000005549 heteroarylene group Chemical group 0.000 claims description 6
- 125000000843 phenylene group Chemical group C1(=C(C=CC=C1)*)* 0.000 claims description 6
- 125000006751 (C6-C60) aryloxy group Chemical group 0.000 claims description 5
- 125000000732 arylene group Chemical group 0.000 claims description 5
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 5
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 3
- 125000006749 (C6-C60) aryl group Chemical group 0.000 claims 1
- 125000003277 amino group Chemical group 0.000 claims 1
- 125000001820 oxy group Chemical group [*:1]O[*:2] 0.000 claims 1
- 238000006467 substitution reaction Methods 0.000 claims 1
- 239000012044 organic layer Substances 0.000 abstract description 5
- 230000015572 biosynthetic process Effects 0.000 description 205
- 238000003786 synthesis reaction Methods 0.000 description 205
- 239000010410 layer Substances 0.000 description 117
- 239000000463 material Substances 0.000 description 55
- 238000002360 preparation method Methods 0.000 description 41
- 238000005160 1H NMR spectroscopy Methods 0.000 description 21
- UJOBWOGCFQCDNV-UHFFFAOYSA-N 9H-carbazole Chemical compound C1=CC=C2C3=CC=CC=C3NC2=C1 UJOBWOGCFQCDNV-UHFFFAOYSA-N 0.000 description 14
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 12
- 0 Cc1c2C(C(*)=C)=C(C(*)=C(*)C=*)C(*(*)/C=C(\*)/CC(*)C3*)=C3N(*)c2c(*)c(I)c1*C(*)=C(*)I*=** Chemical compound Cc1c2C(C(*)=C)=C(C(*)=C(*)C=*)C(*(*)/C=C(\*)/CC(*)C3*)=C3N(*)c2c(*)c(I)c1*C(*)=C(*)I*=** 0.000 description 10
- 239000002019 doping agent Substances 0.000 description 10
- 230000006872 improvement Effects 0.000 description 10
- PAYRUJLWNCNPSJ-UHFFFAOYSA-N Aniline Chemical compound NC1=CC=CC=C1 PAYRUJLWNCNPSJ-UHFFFAOYSA-N 0.000 description 8
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 8
- HKSMIGRZEXQMDZ-UHFFFAOYSA-N [N+](=O)([O-])C1=C(C=CC=C1)C1=CC2=C(N(C3=C(C4=C2C=CC=C4)C=CC=C3)C2=CC=CC=C2)C=C1 Chemical compound [N+](=O)([O-])C1=C(C=CC=C1)C1=CC2=C(N(C3=C(C4=C2C=CC=C4)C=CC=C3)C2=CC=CC=C2)C=C1 HKSMIGRZEXQMDZ-UHFFFAOYSA-N 0.000 description 7
- RFFLAFLAYFXFSW-UHFFFAOYSA-N 1,2-dichlorobenzene Chemical compound ClC1=CC=CC=C1Cl RFFLAFLAYFXFSW-UHFFFAOYSA-N 0.000 description 6
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 6
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 6
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 6
- FWESVNIHRVSDDV-UHFFFAOYSA-N 2-(4-bromophenyl)triphenylene Chemical group C1=CC(Br)=CC=C1C1=CC=C(C=2C(=CC=CC=2)C=2C3=CC=CC=2)C3=C1 FWESVNIHRVSDDV-UHFFFAOYSA-N 0.000 description 5
- XLOMVQKBTHCTTD-UHFFFAOYSA-N Zinc monoxide Chemical compound [Zn]=O XLOMVQKBTHCTTD-UHFFFAOYSA-N 0.000 description 4
- 150000004945 aromatic hydrocarbons Chemical class 0.000 description 4
- 238000006243 chemical reaction Methods 0.000 description 4
- 229910052751 metal Inorganic materials 0.000 description 4
- 239000002184 metal Substances 0.000 description 4
- 150000002894 organic compounds Chemical class 0.000 description 4
- 239000000758 substrate Substances 0.000 description 4
- RRCMGJCFMJBHQC-UHFFFAOYSA-N (2-chlorophenyl)boronic acid Chemical compound OB(O)C1=CC=CC=C1Cl RRCMGJCFMJBHQC-UHFFFAOYSA-N 0.000 description 3
- UIHRXFQYSLTTIP-UHFFFAOYSA-N 10-azatetracyclo[8.6.1.05,17.011,16]heptadeca-1,3,5(17),6,8,11,13,15-octaene Chemical compound C1=CC=CN2C3=CC=CC=C3C3=CC=CC1=C32 UIHRXFQYSLTTIP-UHFFFAOYSA-N 0.000 description 3
- OBHJJRTXDMGYAE-UHFFFAOYSA-N 2,3-dibromodibenzo-p-dioxin Chemical compound O1C2=CC=CC=C2OC2=C1C=C(Br)C(Br)=C2 OBHJJRTXDMGYAE-UHFFFAOYSA-N 0.000 description 3
- VQGHOUODWALEFC-UHFFFAOYSA-N 2-phenylpyridine Chemical compound C1=CC=CC=C1C1=CC=CC=N1 VQGHOUODWALEFC-UHFFFAOYSA-N 0.000 description 3
- VPHUKLCBQWLRBX-UHFFFAOYSA-N 3-bromo-2-(2-chlorophenyl)-9-phenylcarbazole Chemical compound BrC=1C(=CC=2N(C3=CC=CC=C3C=2C=1)C1=CC=CC=C1)C1=C(C=CC=C1)Cl VPHUKLCBQWLRBX-UHFFFAOYSA-N 0.000 description 3
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 3
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- XYOVOXDWRFGKEX-UHFFFAOYSA-N azepine Chemical compound N1C=CC=CC=C1 XYOVOXDWRFGKEX-UHFFFAOYSA-N 0.000 description 3
- 230000000052 comparative effect Effects 0.000 description 3
- 230000009477 glass transition Effects 0.000 description 3
- 238000004519 manufacturing process Methods 0.000 description 3
- ONYWFLRJXLAVPG-UHFFFAOYSA-N 2-[2-(2-chlorophenyl)-9-phenylcarbazol-3-yl]aniline Chemical compound ClC1=C(C=CC=C1)C1=CC=2N(C3=CC=CC=C3C=2C=C1C1=C(N)C=CC=C1)C1=CC=CC=C1 ONYWFLRJXLAVPG-UHFFFAOYSA-N 0.000 description 2
- NIWMTLKBRAGRBS-UHFFFAOYSA-N 2-[3-(2-chlorophenyl)dibenzo-p-dioxin-2-yl]aniline Chemical compound ClC1=C(C=CC=C1)C=1C(=CC2=C(OC3=C(O2)C=CC=C3)C=1)C1=C(N)C=CC=C1 NIWMTLKBRAGRBS-UHFFFAOYSA-N 0.000 description 2
- OCDRZNMKIPLRKX-UHFFFAOYSA-N 2-bromo-3-(2-chlorophenyl)dibenzo-p-dioxin Chemical compound BrC1=CC2=C(OC3=C(O2)C=CC=C3)C=C1C1=C(C=CC=C1)Cl OCDRZNMKIPLRKX-UHFFFAOYSA-N 0.000 description 2
- QENGPZGAWFQWCZ-UHFFFAOYSA-N 3-Methylthiophene Chemical compound CC=1C=CSC=1 QENGPZGAWFQWCZ-UHFFFAOYSA-N 0.000 description 2
- AWXGSYPUMWKTBR-UHFFFAOYSA-N 4-carbazol-9-yl-n,n-bis(4-carbazol-9-ylphenyl)aniline Chemical compound C12=CC=CC=C2C2=CC=CC=C2N1C1=CC=C(N(C=2C=CC(=CC=2)N2C3=CC=CC=C3C3=CC=CC=C32)C=2C=CC(=CC=2)N2C3=CC=CC=C3C3=CC=CC=C32)C=C1 AWXGSYPUMWKTBR-UHFFFAOYSA-N 0.000 description 2
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 2
- 101000837344 Homo sapiens T-cell leukemia translocation-altered gene protein Proteins 0.000 description 2
- YNAVUWVOSKDBBP-UHFFFAOYSA-N Morpholine Chemical compound C1COCCN1 YNAVUWVOSKDBBP-UHFFFAOYSA-N 0.000 description 2
- GLUUGHFHXGJENI-UHFFFAOYSA-N Piperazine Chemical compound C1CNCCN1 GLUUGHFHXGJENI-UHFFFAOYSA-N 0.000 description 2
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical group C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 2
- 102100028692 T-cell leukemia translocation-altered gene protein Human genes 0.000 description 2
- YTPLMLYBLZKORZ-UHFFFAOYSA-N Thiophene Chemical compound C=1C=CSC=1 YTPLMLYBLZKORZ-UHFFFAOYSA-N 0.000 description 2
- 229910045601 alloy Inorganic materials 0.000 description 2
- 239000000956 alloy Substances 0.000 description 2
- MWPLVEDNUUSJAV-UHFFFAOYSA-N anthracene Chemical compound C1=CC=CC2=CC3=CC=CC=C3C=C21 MWPLVEDNUUSJAV-UHFFFAOYSA-N 0.000 description 2
- IOJUPLGTWVMSFF-UHFFFAOYSA-N benzothiazole Chemical group C1=CC=C2SC=NC2=C1 IOJUPLGTWVMSFF-UHFFFAOYSA-N 0.000 description 2
- 239000011203 carbon fibre reinforced carbon Substances 0.000 description 2
- 238000000576 coating method Methods 0.000 description 2
- 239000003086 colorant Substances 0.000 description 2
- 238000004440 column chromatography Methods 0.000 description 2
- 239000012153 distilled water Substances 0.000 description 2
- 239000011521 glass Substances 0.000 description 2
- 125000005842 heteroatom Chemical group 0.000 description 2
- AMGQUBHHOARCQH-UHFFFAOYSA-N indium;oxotin Chemical compound [In].[Sn]=O AMGQUBHHOARCQH-UHFFFAOYSA-N 0.000 description 2
- 125000001041 indolyl group Chemical group 0.000 description 2
- 238000004020 luminiscence type Methods 0.000 description 2
- 150000002739 metals Chemical class 0.000 description 2
- 125000002950 monocyclic group Chemical group 0.000 description 2
- 125000001181 organosilyl group Chemical group [SiH3]* 0.000 description 2
- 239000002985 plastic film Substances 0.000 description 2
- 125000003367 polycyclic group Chemical group 0.000 description 2
- 125000002098 pyridazinyl group Chemical group 0.000 description 2
- 125000000714 pyrimidinyl group Chemical group 0.000 description 2
- 238000001953 recrystallisation Methods 0.000 description 2
- 150000003839 salts Chemical class 0.000 description 2
- 229910052710 silicon Inorganic materials 0.000 description 2
- 239000007787 solid Substances 0.000 description 2
- 239000000243 solution Substances 0.000 description 2
- 239000002904 solvent Substances 0.000 description 2
- RIOQSEWOXXDEQQ-UHFFFAOYSA-N triphenylphosphine Chemical compound C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 RIOQSEWOXXDEQQ-UHFFFAOYSA-N 0.000 description 2
- 229930195735 unsaturated hydrocarbon Natural products 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Chemical compound O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 2
- 239000011787 zinc oxide Substances 0.000 description 2
- SFUIGUOONHIVLG-UHFFFAOYSA-N (2-nitrophenyl)boronic acid Chemical compound OB(O)C1=CC=CC=C1[N+]([O-])=O SFUIGUOONHIVLG-UHFFFAOYSA-N 0.000 description 1
- HKKGIHCPNBYMFD-UHFFFAOYSA-N 1$l^{3}-iodacyclohexa-1,3,5-triene Chemical compound C1=CC=IC=C1 HKKGIHCPNBYMFD-UHFFFAOYSA-N 0.000 description 1
- JYEUMXHLPRZUAT-UHFFFAOYSA-N 1,2,3-triazine Chemical group C1=CN=NN=C1 JYEUMXHLPRZUAT-UHFFFAOYSA-N 0.000 description 1
- YJTKZCDBKVTVBY-UHFFFAOYSA-N 1,3-Diphenylbenzene Chemical group C1=CC=CC=C1C1=CC=CC(C=2C=CC=CC=2)=C1 YJTKZCDBKVTVBY-UHFFFAOYSA-N 0.000 description 1
- KVGZZAHHUNAVKZ-UHFFFAOYSA-N 1,4-Dioxin Chemical compound O1C=COC=C1 KVGZZAHHUNAVKZ-UHFFFAOYSA-N 0.000 description 1
- KRVWTVYQGIOXQE-UHFFFAOYSA-N 1-(2,6-diphenoxyphenoxy)naphthalene Chemical group C=1C=CC(OC=2C=CC=CC=2)=C(OC=2C3=CC=CC=C3C=CC=2)C=1OC1=CC=CC=C1 KRVWTVYQGIOXQE-UHFFFAOYSA-N 0.000 description 1
- GJDSGEWWFYYOFU-UHFFFAOYSA-N 1-[1-(9h-carbazol-1-yl)-4-phenylcyclohexa-2,4-dien-1-yl]-9h-carbazole Chemical group C1=CC(C=2C3=C(C4=CC=CC=C4N3)C=CC=2)(C=2C3=C(C4=CC=CC=C4N3)C=CC=2)CC=C1C1=CC=CC=C1 GJDSGEWWFYYOFU-UHFFFAOYSA-N 0.000 description 1
- HNZUKQQNZRMNGS-UHFFFAOYSA-N 2-(3-bromophenyl)-4,6-diphenyl-1,3,5-triazine Chemical compound BrC1=CC=CC(C=2N=C(N=C(N=2)C=2C=CC=CC=2)C=2C=CC=CC=2)=C1 HNZUKQQNZRMNGS-UHFFFAOYSA-N 0.000 description 1
- 125000004974 2-butenyl group Chemical group C(C=CC)* 0.000 description 1
- DDGPPAMADXTGTN-UHFFFAOYSA-N 2-chloro-4,6-diphenyl-1,3,5-triazine Chemical compound N=1C(Cl)=NC(C=2C=CC=CC=2)=NC=1C1=CC=CC=C1 DDGPPAMADXTGTN-UHFFFAOYSA-N 0.000 description 1
- YTTFZSLFNVFHAQ-UHFFFAOYSA-N 2-chloro-4-(4-naphthalen-1-ylphenyl)quinazoline Chemical compound C1=CC=CC2=NC(Cl)=NC(C=3C=CC(=CC=3)C=3C4=CC=CC=C4C=CC=3)=C21 YTTFZSLFNVFHAQ-UHFFFAOYSA-N 0.000 description 1
- 125000002941 2-furyl group Chemical group O1C([*])=C([H])C([H])=C1[H] 0.000 description 1
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 description 1
- 125000001494 2-propynyl group Chemical group [H]C#CC([H])([H])* 0.000 description 1
- DIVZFUBWFAOMCW-UHFFFAOYSA-N 4-n-(3-methylphenyl)-1-n,1-n-bis[4-(n-(3-methylphenyl)anilino)phenyl]-4-n-phenylbenzene-1,4-diamine Chemical compound CC1=CC=CC(N(C=2C=CC=CC=2)C=2C=CC(=CC=2)N(C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C=C(C)C=CC=2)C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C=C(C)C=CC=2)=C1 DIVZFUBWFAOMCW-UHFFFAOYSA-N 0.000 description 1
- VFUDMQLBKNMONU-UHFFFAOYSA-N 9-[4-(4-carbazol-9-ylphenyl)phenyl]carbazole Chemical compound C12=CC=CC=C2C2=CC=CC=C2N1C1=CC=C(C=2C=CC(=CC=2)N2C3=CC=CC=C3C3=CC=CC=C32)C=C1 VFUDMQLBKNMONU-UHFFFAOYSA-N 0.000 description 1
- NGIGFZSCOGZEPN-UHFFFAOYSA-N C1=CC=C2C(=C1)C3=CC=CC=C3N4C5=C(C=CC=C25)C6=C4C(=CC=C6)C7=CC=CC=C7[N+](=O)[O-] Chemical compound C1=CC=C2C(=C1)C3=CC=CC=C3N4C5=C(C=CC=C25)C6=C4C(=CC=C6)C7=CC=CC=C7[N+](=O)[O-] NGIGFZSCOGZEPN-UHFFFAOYSA-N 0.000 description 1
- WVNAFJAWGUFQMJ-UHFFFAOYSA-N C1=CC=C2C(=C1)C3=CC=CC=C3N4C5=CC=CC(=C5C6=C4C2=CC=C6)C7=CC=CC=C7[N+](=O)[O-] Chemical compound C1=CC=C2C(=C1)C3=CC=CC=C3N4C5=CC=CC(=C5C6=C4C2=CC=C6)C7=CC=CC=C7[N+](=O)[O-] WVNAFJAWGUFQMJ-UHFFFAOYSA-N 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- VYZAMTAEIAYCRO-UHFFFAOYSA-N Chromium Chemical compound [Cr] VYZAMTAEIAYCRO-UHFFFAOYSA-N 0.000 description 1
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- 229910052688 Gadolinium Inorganic materials 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- AFCARXCZXQIEQB-UHFFFAOYSA-N N-[3-oxo-3-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)propyl]-2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidine-5-carboxamide Chemical compound O=C(CCNC(=O)C=1C=NC(=NC=1)NCC1=CC(=CC=C1)OC(F)(F)F)N1CC2=C(CC1)NN=N2 AFCARXCZXQIEQB-UHFFFAOYSA-N 0.000 description 1
- CBENFWSGALASAD-UHFFFAOYSA-N Ozone Chemical compound [O-][O+]=O CBENFWSGALASAD-UHFFFAOYSA-N 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 1
- BQCADISMDOOEFD-UHFFFAOYSA-N Silver Chemical compound [Ag] BQCADISMDOOEFD-UHFFFAOYSA-N 0.000 description 1
- 229910006404 SnO 2 Inorganic materials 0.000 description 1
- ATJFFYVFTNAWJD-UHFFFAOYSA-N Tin Chemical compound [Sn] ATJFFYVFTNAWJD-UHFFFAOYSA-N 0.000 description 1
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical compound [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 description 1
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- CUJRVFIICFDLGR-UHFFFAOYSA-N acetylacetonate Chemical compound CC(=O)[CH-]C(C)=O CUJRVFIICFDLGR-UHFFFAOYSA-N 0.000 description 1
- ORILYTVJVMAKLC-UHFFFAOYSA-N adamantane Chemical compound C1C(C2)CC3CC1CC2C3 ORILYTVJVMAKLC-UHFFFAOYSA-N 0.000 description 1
- 229910001573 adamantine Inorganic materials 0.000 description 1
- 239000012790 adhesive layer Substances 0.000 description 1
- 125000001931 aliphatic group Chemical group 0.000 description 1
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 150000001412 amines Chemical group 0.000 description 1
- 239000010405 anode material Substances 0.000 description 1
- 150000001454 anthracenes Chemical class 0.000 description 1
- 125000005428 anthryl group Chemical group [H]C1=C([H])C([H])=C2C([H])=C3C(*)=C([H])C([H])=C([H])C3=C([H])C2=C1[H] 0.000 description 1
- 230000004888 barrier function Effects 0.000 description 1
- 230000000903 blocking effect Effects 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 239000006229 carbon black Substances 0.000 description 1
- 229910052804 chromium Inorganic materials 0.000 description 1
- 239000011651 chromium Substances 0.000 description 1
- 229920001940 conductive polymer Polymers 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 239000010949 copper Substances 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 230000008025 crystallization Effects 0.000 description 1
- 125000004122 cyclic group Chemical group 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 1
- 238000009792 diffusion process Methods 0.000 description 1
- 238000003618 dip coating Methods 0.000 description 1
- 238000005401 electroluminescence Methods 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 230000005281 excited state Effects 0.000 description 1
- UIWYJDYFSGRHKR-UHFFFAOYSA-N gadolinium atom Chemical compound [Gd] UIWYJDYFSGRHKR-UHFFFAOYSA-N 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 229910052737 gold Inorganic materials 0.000 description 1
- 239000010931 gold Substances 0.000 description 1
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 238000004770 highest occupied molecular orbital Methods 0.000 description 1
- 125000002962 imidazol-1-yl group Chemical group [*]N1C([H])=NC([H])=C1[H] 0.000 description 1
- 229910052738 indium Inorganic materials 0.000 description 1
- APFVFJFRJDLVQX-UHFFFAOYSA-N indium atom Chemical compound [In] APFVFJFRJDLVQX-UHFFFAOYSA-N 0.000 description 1
- 229910003437 indium oxide Inorganic materials 0.000 description 1
- PJXISJQVUVHSOJ-UHFFFAOYSA-N indium(iii) oxide Chemical compound [O-2].[O-2].[O-2].[In+3].[In+3] PJXISJQVUVHSOJ-UHFFFAOYSA-N 0.000 description 1
- 150000002475 indoles Chemical class 0.000 description 1
- 238000007641 inkjet printing Methods 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- 239000011630 iodine Substances 0.000 description 1
- 229910052741 iridium Inorganic materials 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000001972 isopentyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000000555 isopropenyl group Chemical group [H]\C([H])=C(\*)C([H])([H])[H] 0.000 description 1
- 238000010030 laminating Methods 0.000 description 1
- 239000002346 layers by function Substances 0.000 description 1
- 229910052744 lithium Inorganic materials 0.000 description 1
- 238000004768 lowest unoccupied molecular orbital Methods 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- 229910044991 metal oxide Inorganic materials 0.000 description 1
- 150000004706 metal oxides Chemical class 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 125000001624 naphthyl group Chemical group 0.000 description 1
- 239000007773 negative electrode material Substances 0.000 description 1
- 125000002868 norbornyl group Chemical group C12(CCC(CC1)C2)* 0.000 description 1
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 1
- 125000005561 phenanthryl group Chemical group 0.000 description 1
- 229920006255 plastic film Polymers 0.000 description 1
- 229910052697 platinum Inorganic materials 0.000 description 1
- 229920000767 polyaniline Polymers 0.000 description 1
- 229920000128 polypyrrole Polymers 0.000 description 1
- 229920000123 polythiophene Polymers 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 125000000561 purinyl group Chemical group N1=C(N=C2N=CNC2=C1)* 0.000 description 1
- 125000003373 pyrazinyl group Chemical group 0.000 description 1
- 125000004076 pyridyl group Chemical group 0.000 description 1
- 125000000246 pyrimidin-2-yl group Chemical group [H]C1=NC(*)=NC([H])=C1[H] 0.000 description 1
- 239000010453 quartz Substances 0.000 description 1
- 125000005493 quinolyl group Chemical group 0.000 description 1
- 229930195734 saturated hydrocarbon Natural products 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 229910052711 selenium Inorganic materials 0.000 description 1
- 239000010703 silicon Substances 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N silicon dioxide Inorganic materials O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- 229910052709 silver Inorganic materials 0.000 description 1
- 239000004332 silver Substances 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 238000004528 spin coating Methods 0.000 description 1
- 238000000859 sublimation Methods 0.000 description 1
- 230000008022 sublimation Effects 0.000 description 1
- 238000010189 synthetic method Methods 0.000 description 1
- 238000010345 tape casting Methods 0.000 description 1
- 239000010409 thin film Substances 0.000 description 1
- 229930192474 thiophene Natural products 0.000 description 1
- 229910052718 tin Inorganic materials 0.000 description 1
- 229910052719 titanium Inorganic materials 0.000 description 1
- 239000010936 titanium Substances 0.000 description 1
- 125000004306 triazinyl group Chemical group 0.000 description 1
- 125000005580 triphenylene group Chemical group 0.000 description 1
- 238000004506 ultrasonic cleaning Methods 0.000 description 1
- 238000001771 vacuum deposition Methods 0.000 description 1
- 229910052720 vanadium Inorganic materials 0.000 description 1
- GPPXJZIENCGNKB-UHFFFAOYSA-N vanadium Chemical compound [V]#[V] GPPXJZIENCGNKB-UHFFFAOYSA-N 0.000 description 1
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 1
- 229920002554 vinyl polymer Polymers 0.000 description 1
- 235000012431 wafers Nutrition 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- 229910052727 yttrium Inorganic materials 0.000 description 1
- VWQVUPCCIRVNHF-UHFFFAOYSA-N yttrium atom Chemical compound [Y] VWQVUPCCIRVNHF-UHFFFAOYSA-N 0.000 description 1
- 229910052725 zinc Inorganic materials 0.000 description 1
- 239000011701 zinc Substances 0.000 description 1
- YVTHLONGBIQYBO-UHFFFAOYSA-N zinc indium(3+) oxygen(2-) Chemical compound [O--].[Zn++].[In+3] YVTHLONGBIQYBO-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D223/00—Heterocyclic compounds containing seven-membered rings having one nitrogen atom as the only ring hetero atom
- C07D223/14—Heterocyclic compounds containing seven-membered rings having one nitrogen atom as the only ring hetero atom condensed with carbocyclic rings or ring systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/06—Luminescent, e.g. electroluminescent, chemiluminescent materials containing organic luminescent materials
Abstract
본 발명은 정공 주입 및 수송능과 발광능 등이 우수한 신규 유기 화합물과 이를 하나 이상의 유기물층에 포함함으로써 낮은 구동 전압과, 높은 발광 효율 및 향상된 수명 특성을 갖는 유기 전계 발광 소자에 관한 것이다.
Description
본 발명은 신규한 유기 발광 화합물 및 이를 이용한 유기 전계 발광 소자에 관한 것으로, 보다 상세하게는 정공 주입 및 수송능과 발광능 등이 우수한 신규한 아제핀계 화합물 및 이를 하나 이상의 유기물층에 포함함으로써 낮은 구동 전압과, 높은 발광 효율 및 향상된 수명 특성을 갖는 유기 전계 발광 소자에 관한 것이다.
1950년대 베르나소스(Bernanose)의 유기 박막 발광 관측을 시점으로 1965년 안트라센 단결정을 이용한 청색 전기발광으로 이어진 유기 전계 발광 (electroluminescent, EL) 소자(이하, 간단히 '유기 EL 소자'로 칭함)에 대한 연구는 1987년 탕(Tang)에 의하여 정공층과 발광층의 기능층으로 나눈 적층구조의 유기 EL 소자가 제시되었다. 이후 고효율, 고수명의 유기 EL 소자를 만들기 위하여, 소자 내 각각의 특징적인 유기물 층을 도입하는 형태로 발전하여 왔으며, 이에 사용되는 특화된 물질의 개발로 이어졌다.
유기 EL 소자는 두 전극 사이에 전압을 걸어 주면 양극에서는 정공이 주입되고, 음극에서는 전자가 유기물층으로 주입된다. 주입된 정공과 전자가 만났을 때 엑시톤(exciton)이 형성되며, 이 엑시톤이 바닥상태로 떨어질 때 빛이 나게 된다. 이때 유기물층으로 사용되는 물질은 그 기능에 따라, 발광 물질, 정공 주입 물질, 정공 수송 물질, 전자 수송 물질, 전자 주입 물질 등으로 분류될 수 있다.
유기 EL 소자의 발광층 형성재료는 발광색에 따라 청색, 녹색, 적색 발광 재료로 구분될 수 있다. 그 밖에, 보다 나은 천연색을 구현하기 위한 발광재료로 노란색 및 주황색 발광재료도 사용된다. 또한, 색순도의 증가와 에너지 전이를 통한 발광 효율을 증가시키기 위하여, 발광 재료로서 호스트/도펀트 계를 사용할 수 있다. 도펀트 물질은 유기 물질을 사용하는 형광 도펀트와 Ir, Pt 등의 중원자(heavy atoms)가 포함된 금속 착체 화합물을 사용하는 인광 도펀트로 나눌 수 있다. 이러한 인광 재료의 개발은 이론적으로 형광에 비해 4배까지의 발광 효율을 향상시킬 수 있어 인광 도펀트 뿐만 아니라 인광 호스트 재료들에 대해 관심이 집중되고 있다.
현재까지 정공 주입층, 정공 수송층, 정공 차단층, 전자 수송층으로는, 하기 화학식으로 표현된 NPB, BCP, Alq3 등이 널리 알려져 있고, 발광 재료는 안트라센 유도체들이 형광 도펀트/호스트 재료로서 보고되고 있다. 특히 발광재료 중 효율 향상 측면에서 큰 장점을 가지고 있는 인광 재료로서는 Firpic, Ir(ppy)3, (acac)Ir(btp)2 등과 같은 Ir을 포함하는 금속 착체 화합물이 청색, 녹색, 적색 도판트 재료로 사용되고 있다. 현재까지는 4,4-디카바졸릴비페닐(4,4-dicarbazolybiphenyl, CBP)가 인광 호스트 재료로 우수한 특성을 나타내고 있다.
그러나 기존의 재료들은 발광 특성 측면에서는 유리한 면이 있으나, 유리전이온도가 낮고 열적 안정성이 매우 좋지 않아 유기 EL 소자에서의 수명 측면에서 만족할만한 수준이 되지 못하고 있다. 따라서, 보다 성능이 뛰어난 재료의 개발이 요구되고 있다.
본 발명은 유기 전계 발광 소자에 적용할 수 있으며, 정공 주입 및 수송능과 발광능 등이 모두 우수한 신규 유기 화합물을 제공하는 것을 목적으로 한다.
또한, 본 발명은 상기 신규 유기 화합물을 포함하여 낮은 구동 전압과 높은 발광 효율을 나타내며 수명 특성이 향상된 유기 전계 발광 소자를 제공하는 것을 또 다른 목적으로 한다.
상기 목적을 달성하기 위하여, 본 발명은 하기 화학식 1로 표시되는 화합물을 제공한다:
[화학식 1]
상기 화학식 1에서,
R1과 R2, R2과 R3, R3과 R4, R5와 R6, R6과 R7, R7과 R8, R9과 R10, R10과 R11 및 R11과 R12 중 적어도 하나는 하기 화학식 2로 표시되는 고리와 축합되어 축합 고리를 형성하고;
하기 화학식 2로 표시되는 고리와 축합을 형성하지 않는 R1 내지 R12은 각각 독립적으로 수소, 중수소, 할로겐, 시아노기, 니트로기, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되거나, 인접하는 기와 결합하여 축합 고리를 형성할 수 있으며;
Ar1은 C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되며;
상기 R1 내지 R12 및 Ar1의 알킬기, 시클로알킬기, 헤테로시클로알킬기, 아릴기, 헤테로아릴기, 알킬옥시기, 아릴옥시기, 알킬실릴기, 아릴실릴기, 알킬보론기, 아릴보론기, 아릴포스핀기, 모노 또는 디아릴포스피닐기 및 아릴아민기는 각각 독립적으로, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택된 1종 이상으로 치환되거나 비치환되고, 복수 개의 치환기로 치환되는 경우 이들은 서로 동일하거나 상이할 수 있으며;
[화학식 2]
상기 화학식 2에서,
점선은 상기 화학식 1과 축합이 이루어지는 부분이고;
X1 및 X2는 각각 독립적으로 단일결합, O, S, N(Ar2), C(Ar3)(Ar4) 및 Si(Ar5)(Ar6)으로 구성된 군으로부터 선택되나, X1 및 X2가 모두 단일결합은 아니며, 바람직하게는 X1 및 X2 중 적어도 하나는 N(Ar2)이고;
Y1 내지 Y4은 각각 독립적으로 N 또는 C(R13)이고, 바람직하게는 Y1 내지 Y4 모두가 C(R13)이거나, 상기 Y1 내지 Y4 중 적어도 한 개가 N이며;
R13이 복수 개인 경우 이들은 서로 동일하거나 상이하며, 상기 R13은 수소, 중수소, 할로겐, 시아노기, 니트로기, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되거나, 인접하는 기와 결합하여 축합 고리를 형성할 수 있으며;
Ar2 내지 Ar6는 각각 독립적으로 C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되며;
상기 R13 및 Ar2 내지 Ar6의 알킬기, 시클로알킬기, 헤테로시클로알킬기, 아릴기, 헤테로아릴기, 알킬옥시기, 아릴옥시기, 알킬실릴기, 아릴실릴기, 알킬보론기, 아릴보론기, 아릴포스핀기, 모노 또는 디아릴포스피닐기 및 아릴아민기는 각각 독립적으로, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택된 1종 이상으로 치환되거나 비치환되고, 복수 개의 치환기로 치환되는 경우 이들은 서로 동일하거나 상이할 수 있다.
본 발명의 바람직한 한 구현 예에 따르면, 상기 화학식 1로 표시되는 화합물은 하기 화학식 3 내지 화학식 7 중 어느 하나로 표시되는 화합물인 것을 특징으로 한다:
[화학식 3]
[화학식 4]
[화학식 5]
[화학식 6]
[화학식 7]
상기 화학식 3 내지 화학식 7에 있어서,
X1, X2, Ar1, Y1 내지 Y4 및 R1 내지 R12 각각은 상기 화학식 1 및 화학식 2 에서 정의된 바와 같다.
본 발명의 바람직한 한 구현 예에 따르면, 상기 화학식 1로 표시되는 화합물은 하기 화학식 8 내지 화학식 10 중 어느 하나로 표시되는 화합물인 것을 특징으로 한다:
[화학식 8]
[화학식 9]
[화학식 10]
상기 화학식 8 내지 화학식 10에 있어서,
R2와 R3, R3과 R4, R5와 R6, R6과 R7, R7과 R8, R9과 R10, R10과 R11, R11과 R12 및 R15와 R16 중 적어도 하나는 하기 화학식 2로 표시되는 고리와 축합되어 축합 고리를 형성하고;
하기 화학식 2로 표시되는 고리와 축합을 형성하지 않는 R2 내지 R12 및 R15 내지 R16는 각각 독립적으로 수소, 중수소, 할로겐, 시아노기, 니트로기, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되거나, 인접하는 기와 결합하여 축합 고리를 형성할 수 있으며;
X3은 O, S, N(Ar7), C(Ar8)(Ar9) 및 Si(Ar10)(Ar11)으로 구성된 군으로부터 선택되고, 바람직하게는 N(Ar7)이며;
Ar7 내지 Ar11은 각각 독립적으로 C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~6C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되며;
n은 0 내지 4의 정수이며;
R14는 중수소, 할로겐, 시아노기, 니트로기, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되거나, 인접하는 기와 결합하여 축합 고리를 형성할 수 있으며, 상기 R14가 복수 개인 경우 이들은 서로 동일하거나 상이하며;
상기 Ar7 내지 Ar11, R2 내지 R12 및 R14 내지 R16의 알킬기, 시클로알킬기, 헤테로시클로알킬기, 아릴기, 헤테로아릴기, 알킬옥시기, 아릴옥시기, 알킬실릴기, 아릴실릴기, 알킬보론기, 아릴보론기, 아릴포스핀기, 모노 또는 디아릴포스피닐기 및 아릴아민기는 각각 독립적으로, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택된 1종 이상으로 치환되거나 비치환되고, 복수 개의 치환기로 치환되는 경우 이들은 서로 동일하거나 상이할 수 있으며;
[화학식 2]
상기 화학식 2에서,
점선은 상기 화학식 8 내지 10 중 어느 하나와 축합이 이루어지는 부분이고;
X1 및 X2는 각각 독립적으로 단일결합, O, S, N(Ar2), C(Ar3)(Ar4) 및 Si(Ar5)(Ar6)으로 구성된 군으로부터 선택되나, X1 및 X2가 모두 단일결합은 아니며;
Y1 내지 Y4은 각각 독립적으로 N 또는 C(R13)이며;
R13이 복수 개인 경우 이들은 서로 동일하거나 상이하며, 상기 R13은 수소, 중수소, 할로겐, 시아노기, 니트로기, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되거나, 인접하는 기와 결합하여 축합 고리를 형성할 수 있으며;
Ar2 내지 Ar6는 각각 독립적으로 C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되며;
상기 R13 및 Ar2 내지 Ar6의 알킬기, 시클로알킬기, 헤테로시클로알킬기, 아릴기, 헤테로아릴기, 알킬옥시기, 아릴옥시기, 알킬실릴기, 아릴실릴기, 알킬보론기, 아릴보론기, 아릴포스핀기, 모노 또는 디아릴포스피닐기 및 아릴아민기는 각각 독립적으로, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택된 1종 이상으로 치환되거나 비치환되고, 복수 개의 치환기로 치환되는 경우 이들은 서로 동일하거나 상이할 수 있다.
본 발명의 바람직한 한 구현 예에 따르면, 상기 화학식 8 내지 화학식 10 중 어느 하나로 표시되는 화합물은 하기 화학식 C-1 내지 화학식 C-12 중 어느 하나로 표시되는 화합물일 수 있다:
상기 화학식 C-1 내지 화학식 C-12에서,
X1, X2, X3, Y1 내지 Y4 및 R2 내지 R12, R14 내지 R16 및 n 각각은 상기 화학식 8 내지 화학식 10에서 정의된 바와 같다.
본 발명의 바람직한 한 구현 예에 따르면, 상기 화학식 1로 표시되는 화합물에서 R1 내지 R12 및 Ar1 내지 Ar6
중 적어도 하나는 C1~C40의 알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되며;
상기 R1 내지 R12 및 Ar1 내지 Ar6의 알킬기, 아릴기, 헤테로아릴기 및 아릴아민기는 각각 독립적으로, 중수소, 할로겐, 시아노기, C1~C40의 알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택된 1종 이상으로 치환되거나 비치환되고, 복수 개의 치환기로 치환되는 경우 이들은 서로 동일하거나 상이할 수 있다.
본 발명의 바람직한 한 구현 예에 따르면, 상기 화학식 1로 표시되는 화합물에서, 상기 R1 내지 R12 및 Ar1 내지 Ar6
중 적어도 하나는 페닐기 또는 하기 화학식 11으로 표시되는 치환기일 수 있다.
[화학식 11]
상기 화학식 11에서,
*는 상기 화학식 1에 결합되는 부분을 의미하고;
L1은 단일결합, C6~C18의 아릴렌기 및 핵원자수 5 내지 18개의 헤테로아릴렌기로 이루어진 군에서 선택되고, 바람직하게는 단일결합, 페닐렌기, 비페닐렌기 또는 카바졸릴기일 수 있으며;
Z1 내지 Z5는 각각 독립적으로 N 또는 C(R17)이되, 상기 Z1 내지 Z5 중 적어도 하나는 N이며;
R17이 복수 개인 경우 이들은 서로 동일하거나 상이하며, 상기 R17은 각각 독립적으로 수소, 중수소, 할로겐, 시아노기, 니트로기, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C6~C60의 아릴기, 핵원자수 5 내지 40개의 헤테로아릴기, C6~C60의 아릴옥시기 C1~C40의 알킬옥시기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴아민기, C1~C40의 알킬실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴실릴기로 이루어진 군에서 선택되거나, 인접하는 기와 결합하여 축합 고리를 형성할 수 있으며;
상기 R17의 알킬기, 알케닐기, 알키닐기, 아릴기, 헤테로아릴기, 아릴옥시기, 알킬옥시기, 시클로알킬기, 헤테로시클로알킬기, 아릴아민기, 알킬실릴기, 알킬보론기, 아릴보론기, 아릴포스핀기, 모노 또는 디아릴포스피닐기 및 아릴실릴기는 각각 독립적으로 중수소, 할로겐, 시아노기, 니트로기, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C6~C60의 아릴기, 핵원자수 5 내지 40개의 헤테로아릴기, C6~C60의 아릴옥시기, C1~C40의 알킬옥시기, C6~C60의 아릴아민기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C1~C40의 알킬실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴실릴기로 이루어진 군에서 선택된 1종 이상의 치환기로 치환되거나 비치환되고, 복수 개의 치환기로 치환되는 경우, 이들은 서로 동일하거나 상이할 수 있다.
본 발명의 바람직한 한 구현 예에 따르면, 상기 화학식 11로 표시되는 치환기는 하기 화학식 A-1 내지 화학식 A-15 중 어느 하나로 표시되는 치환기일 수 있다.
상기 화학식 A-1 내지 화학식 A-15에서,
*는 상기 화학식 1에 결합되는 부분을 의미하고;
m은 0 내지 4의 정수로서, 상기 m이 0인 경우, 수소가 치환기 R18로 치환되지 않는 것을 의미하고, 상기 m이 1 내지 4의 정수인 경우, R18은 중수소, 할로겐, 시아노기, 니트로기, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 40개의 헤테로아릴기, C6~C60의 아릴옥시기 C1~C40의 알킬옥시기, C6~C60의 아릴아민기, C1~C40의 알킬실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴실릴기로 이루어진 군에서 선택되거나, 인접하는 기와 결합하여 축합 고리를 형성할 수 있고, 상기 R18이 복수 개인 경우 이들은 서로 동일하거나 상이하며;
상기 R18의 알킬기, 알케닐기, 알키닐기, 시클로알킬기, 헤테로시클로알킬기, 아릴기, 헤테로아릴기, 아릴옥시기, 알킬옥시기, 아릴아민기, 알킬실릴기, 알킬보론기, 아릴보론기, 아릴포스핀기, 모노 또는 디아릴포스피닐기 및 아릴실릴기는 각각 독립적으로 중수소, 할로겐, 시아노기, 니트로기, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C6~C60의 아릴기, 핵원자수 5 내지 40개의 헤테로아릴기, C6~C60의 아릴옥시기, C1~C40의 알킬옥시기, C6~C60의 아릴아민기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C1~C40의 알킬실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴실릴기로 이루어진 군에서 선택된 1종 이상으로 치환되거나 비치환되고, 복수 개의 치환기로 치환되는 경우, 이들은 서로 동일하거나 상이할 수 있으며;
L1 및 R17은 각각 상기 화학식 11에서 정의된 바와 같다.
본 발명의 바람직한 한 구현 예에 따르면, 상기 화학식 1로 표시되는 화합물에서, 상기 R1 내지 R12 및 Ar1 내지 Ar6
중 적어도 하나는 하기 화학식 12로 표시되는 치환기일 수 있다:
[화학식 12]
상기 화학식 12에서,
*는 상기 화학식 1에 결합되는 부분을 의미하고;
L2은 단일결합, C6~C18의 아릴렌기 및 핵원자수 5 내지 18개의 헤테로아릴렌기로 이루어진 군에서 선택되고, 바람직하게는 단일결합, 페닐렌기, 비페닐렌기 또는 카바졸릴기일 수 있으며;
R19 및 R20는 각각 독립적으로 C1~C40의 알킬기, C6~C60의 아릴기, 핵원자수 5 내지 40개의 헤테로아릴기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되거나, 상기 R19 및 R20가 서로 결합하여 축합 고리를 형성할 수 있으며;
상기 R19 및 R20의 알킬기, 아릴기, 헤테로아릴기 및 아릴아민기는 각각 독립적으로 중수소, 할로겐, 시아노기, 니트로기, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C6~C60의 아릴기, 핵원자수 5 내지 40개의 헤테로아릴기, C6~C60의 아릴옥시기, C1~C40의 알킬옥시기, C6~C60의 아릴아민기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C1~C40의 알킬실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C40의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴실릴기로 이루어진 군에서 선택된 1종 이상으로 치환되거나 비치환되고, 복수 개의 치환기로 치환되는 경우, 이들은 서로 동일하거나 상이할 수 있다.
또한, 본 발명은 (i) 양극, (ii) 음극, 및 (iii) 상기 양극과 음극 사이에 개재(介在)된 1층 이상의 유기물층을 포함하는 유기 전계 발광 소자로서, 상기 1층 이상의 유기물층 중 적어도 하나는 상기 화학식 1로 표시되는 화합물을 포함하는 것을 특징으로 하는 유기 전계 발광 소자를 제공한다.
본 발명의 바람직한 한 구현 예에 따르면, 상기 화학식 1로 표시되는 화합물을 포함하는 유기물층은 발광층, 전자 수송층, 전자 주입층, 정공 수송층, 정공 주입층, 발광 보조층 및 수명개선층으로 이루어진 군에서 선택될 수 있으며, 바람직하게는 발광층, 전자 수송층, 발광보조층, 및 수명 개선층으로 이루어진 군에서 선택될 수 있고, 보다 바람직하게는 발광층의 인광 호스트로 사용될 수 있다.
본 발명에서 "알킬"은 탄소수 1 내지 40개의 직쇄 또는 측쇄의 포화 탄화수소에서 유래되는 1가의 치환기를 의미한다. 이의 예로는 메틸, 에틸, 프로필, 이소부틸, sec-부틸, 펜틸, iso-아밀, 헥실 등을 들 수 있으나, 이에 한정되지는 않는다.
본 발명에서 "알케닐(alkenyl)"은 탄소-탄소 이중 결합을 1개 이상 가진탄소수 2 내지 40개의 직쇄 또는 측쇄의 불포화 탄화수소에서 유래되는 1가의 치환기를 의미한다. 이의 예로는 비닐(vinyl), 알릴(allyl), 이소프로펜일(isopropenyl), 2-부텐일(2-butenyl) 등을 들 수 있으나, 이에 한정되지는 않는다.
본 발명에서 "알키닐(alkynyl)"은 탄소-탄소 삼중 결합을 1개 이상 가진 탄소수 2 내지 40개의 직쇄 또는 측쇄의 불포화 탄화수소에서 유래되는 1가의 치환기를 의미한다. 이의 예로는 에티닐(ethynyl), 2-프로파닐(2-propynyl) 등을 들 수 있으나, 이에 한정되지는 않는다.
본 발명에서 "아릴"은 단독 고리 또는 2 이상의 고리가 조합된 탄소수 6 내지 60개의 방향족 탄화수소로부터 유래된 1가의 치환기를 의미한다. 또한, 2 이상의 고리가 서로 단순 부착(pendant)되거나 축합된 형태도 포함될 수 있다. 이러한 아릴의 예로는 페닐, 나프틸, 페난트릴, 안트릴 등을 들 수 있으나, 이에 한정되지는 않는다.
본 발명에서 "헤테로아릴"은 핵원자수 5 내지 60개의 모노헤테로사이클릭 또는 폴리헤테로사이클릭 방향족 탄화수소로부터 유래된 1가의 치환기를 의미한다. 이때, 고리 중 하나 이상의 탄소, 바람직하게는 1 내지 3개의 탄소가 N, O, S 또는 Se와 같은 헤테로원자로 치환된다. 또한, 2 이상의 고리가 서로 단순 부착(pendant)되거나 축합된 형태도 포함될 수 있고, 나아가 아릴기와의 축합된 형태도 포함될 수 있다. 이러한 헤테로아릴의 예로는 피리딜, 피라지닐, 피리미디닐, 피리다지닐, 트리아지닐과 같은 6-원 모노사이클릭 고리, 페녹사티에닐(phenoxathienyl), 인돌리지닐(indolizinyl), 인돌릴(indolyl), 퓨리닐(purinyl), 퀴놀릴(quinolyl), 벤조티아졸(benzothiazole), 카바졸릴(carbazolyl)과 같은 폴리사이클릭 고리 및 2-퓨라닐, N-이미다졸릴, 2-이속사졸릴, 2-피리디닐, 2-피리미디닐 등을 들 수 있으나, 이에 한정되지는 않는다.
본 발명에서 "아릴옥시"는 RO-로 표시되는 1가의 치환기로, 상기 R은 탄소수 6 내지 60개의 아릴을 의미한다. 이러한 아릴옥시의 예로는 페닐옥시, 나프틸옥시, 디페닐옥시 등을 들 수 있으나, 이에 한정되지는 않는다.
본 발명에서 "알킬옥시"는 R'O-로 표시되는 1가의 치환기로, 상기 R'는 탄소수 1 내지 40개의 알킬을 의미하며, 직쇄(linear), 측쇄(branched) 또는 사이클릭(cyclic) 구조를 포함할 수 있다. 알킬옥시의 예로는 메톡시, 에톡시, n-프로폭시, 1-프로폭시, t-부톡시, n-부톡시, 펜톡시 등을 들 수 있으나, 이에 한정되지는 않는다.
본 발명에서 "아릴아민"은 탄소수 6 내지 60개의 아릴로 치환된 아민을 의미한다.
본 발명에서 "시클로알킬"은 탄소수 3 내지 40개의 모노사이클릭 또는 폴리사이클릭 비-방향족 탄화수소로부터 유래된 1가의 치환기를 의미한다. 이러한 사이클로알킬의 예로는 사이클로프로필, 사이클로펜틸, 사이클로헥실, 노르보닐(norbornyl), 아다만틴(adamantine) 등을 들 수 있으나, 이에 한정되지는 않는다.
본 발명에서 "헤테로시클로알킬"은 핵원자수 3 내지 40개의 비-방향족 탄화수소로부터 유래된 1가의 치환기를 의미하며, 고리 중 하나 이상의 탄소, 바람직하게는 1 내지 3개의 탄소가 N, O, S 또는 Se와 같은 헤테로 원자로 치환된다. 이러한 헤테로시클로알킬의 예로는 모르폴린, 피페라진 등을 들 수 있으나, 이에 한정되지는 않는다.
본 발명에서 "알킬실릴"은 탄소수 1 내지 40개의 알킬로 치환된 실릴이고, "아릴실릴"은 탄소수 6 내지 60개의 아릴로 치환된 실릴을 의미한다.
본 발명에서 "축합고리"는 축합 지방족 고리, 축합 방향족 고리, 축합 헤테로지방족 고리, 축합 헤테로방향족 고리 또는 이들의 조합된 형태를 의미한다.
본 발명의 화학식 1로 표시되는 화합물은 열적 안정성 및 발광 특성이 우수하기 때문에 유기 전계 발광 소자의 유기물층의 재료로 사용될 수 있다. 특히, 본 발명의 화학식 1로 표시되는 화합물을 인광 호스트 재료로 사용할 경우, 종래의 호스트 재료에 비해 우수한 발광 성능, 낮은 구동 전압, 높은 발광 효율 및 장수명을 갖는 유기 전계 발광 소자를 제조할 수 있고, 나아가 성능 및 수명이 향상된 풀 칼라 디스플레이 패널도 제조할 수 있다.
본 발명은 하기 화학식 1로 표시되는 화합물을 제공한다:
[화학식 1]
상기 화학식 1에서,
R1과 R2, R2과 R3, R3과 R4, R5와 R6, R6과 R7, R7과 R8, R9과 R10, R10과 R11 및 R11과 R12 중 적어도 하나는 하기 화학식 2로 표시되는 고리와 축합되어 축합 고리를 형성하고;
하기 화학식 2로 표시되는 고리와 축합을 형성하지 않는 R1 내지 R12은 각각 독립적으로 수소, 중수소, 할로겐, 시아노기, 니트로기, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되거나, 인접하는 기와 결합하여 축합 고리를 형성할 수 있으며;
Ar1은 C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되며;
상기 R1 내지 R12 및 Ar1의 알킬기, 시클로알킬기, 헤테로시클로알킬기, 아릴기, 헤테로아릴기, 알킬옥시기, 아릴옥시기, 알킬실릴기, 아릴실릴기, 알킬보론기, 아릴보론기, 아릴포스핀기, 모노 또는 디아릴포스피닐기 및 아릴아민기는 각각 독립적으로, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택된 1종 이상으로 치환되거나 비치환되고, 복수 개의 치환기로 치환되는 경우 이들은 서로 동일하거나 상이할 수 있으며;
[화학식 2]
상기 화학식 2에서,
점선은 상기 화학식 1과 축합이 이루어지는 부분이고;
X1 및 X2는 각각 독립적으로 단일결합, O, S, N(Ar2), C(Ar3)(Ar4) 및 Si(Ar5)(Ar6)으로 구성된 군으로부터 선택되나, X1 및 X2가 모두 단일결합은 아니며, 바람직하게는 X1 및 X2 중 적어도 하나는 N(Ar2)이고;
Y1 내지 Y4은 각각 독립적으로 N 또는 C(R13)이고, 바람직하게는 Y1 내지 Y4 모두가 C(R13)이거나, 상기 Y1 내지 Y4 중 적어도 한 개가 N이며;
R13이 복수 개인 경우 이들은 서로 동일하거나 상이하며, 상기 R13은 수소, 중수소, 할로겐, 시아노기, 니트로기, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되거나, 인접하는 기와 결합하여 축합 고리를 형성할 수 있으며;
Ar2 내지 Ar6는 각각 독립적으로 C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되며;
상기 R13 및 Ar2 내지 Ar6의 알킬기, 시클로알킬기, 헤테로시클로알킬기, 아릴기, 헤테로아릴기, 알킬옥시기, 아릴옥시기, 알킬실릴기, 아릴실릴기, 알킬보론기, 아릴보론기, 아릴포스핀기, 모노 또는 디아릴포스피닐기 및 아릴아민기는 각각 독립적으로, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택된 1종 이상으로 치환되거나 비치환되고, 복수 개의 치환기로 치환되는 경우 이들은 서로 동일하거나 상이할 수 있다.
이하, 본 발명을 상세히 설명한다.
1. 신규 유기 화합물
본 발명은 신규한 유기 발광 화합물 및 이를 이용한 유기 전계 발광 소자에 관한 것으로, 보다 상세하게는 정공 주입 및 수송능과 발광능 등이 우수한 신규한 아제핀계 화합물 및 이를 하나 이상의 유기물층에 포함함으로써 낮은 구동 전압과, 높은 발광 효율 및 향상된 수명 특성을 갖는 유기 전계 발광 소자에 관한 것이다.
본 발명에서 제공하는 신규 유기 화합물은 트리벤조아제핀에 벤젠이 축합된 5원 헤테로방향족환 모이어티(moiety) 또는 벤젠이 축합된 6원 모이어티가 축합되어 기본 골격을 이루며, 바람직하게는 하기 화학식 1로 표시되는 화합물인 것을 특징으로 한다:
[화학식 1]
상기 화학식 1에서,
R1과 R2, R2과 R3, R3과 R4, R5와 R6, R6과 R7, R7과 R8, R9과 R10, R10과 R11 및 R11과 R12 중 적어도 하나는 하기 화학식 2로 표시되는 고리와 축합되어 축합 고리를 형성하고;
하기 화학식 2로 표시되는 고리와 축합을 형성하지 않는 R1 내지 R12은 각각 독립적으로 수소, 중수소, 할로겐, 시아노기, 니트로기, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되거나, 인접하는 기(예컨대, 인접한 R1 내지 R12 중 적어도 하나, 또는 R13 등과 결합하거나, 혹은 R1 과 Ar1이나 R12 와 Ar1이 결합할 수 있음.)와 결합하여 축합 고리를 형성할 수 있으며;
Ar1은 C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되며;
상기 R1 내지 R12 및 Ar1의 알킬기, 시클로알킬기, 헤테로시클로알킬기, 아릴기, 헤테로아릴기, 알킬옥시기, 아릴옥시기, 알킬실릴기, 아릴실릴기, 알킬보론기, 아릴보론기, 아릴포스핀기, 모노 또는 디아릴포스피닐기 및 아릴아민기는 각각 독립적으로, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택된 1종 이상으로 치환되거나 비치환되고, 복수 개의 치환기로 치환되는 경우 이들은 서로 동일하거나 상이할 수 있으며;
[화학식 2]
상기 화학식 2에서,
점선은 상기 화학식 1과 축합이 이루어지는 부분이고;
X1 및 X2는 각각 독립적으로 단일결합, O, S, N(Ar2), C(Ar3)(Ar4) 및 Si(Ar5)(Ar6)으로 구성된 군으로부터 선택되나, X1 및 X2가 모두 단일결합은 아니며, 바람직하게는 X1 및 X2 중 적어도 하나는 N(Ar2)이고;
Y1 내지 Y4은 각각 독립적으로 N 또는 C(R13)이고, 바람직하게는 Y1 내지 Y4 모두가 C(R13)이거나 상기 Y1 내지 Y4 중 적어도 한 개가 N이며;
R13이 복수 개인 경우 이들은 서로 동일하거나 상이하며, 상기 R13은 수소, 중수소, 할로겐, 시아노기, 니트로기, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되거나, 인접하는 기(예컨대, 인접한 R13 등)와 결합하여 축합 고리를 형성할 수 있으며;
Ar2 내지 Ar6는 각각 독립적으로 C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되며;
상기 R13 및 Ar2 내지 Ar6의 알킬기, 시클로알킬기, 헤테로시클로알킬기, 아릴기, 헤테로아릴기, 알킬옥시기, 아릴옥시기, 알킬실릴기, 아릴실릴기, 알킬보론기, 아릴보론기, 아릴포스핀기, 모노 또는 디아릴포스피닐기 및 아릴아민기는 각각 독립적으로, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택된 1종 이상으로 치환되거나 비치환되고, 복수 개의 치환기로 치환되는 경우 이들은 서로 동일하거나 상이할 수 있다.
본 발명에서 상기한 화학식 1로 표시되는 화합물은 종래 유기 전계 발광 소자용 재료[예: 4,4-디카바졸릴비페닐 (이하, 'CBP'라 함)]보다 높은 분자량을 갖기 때문에, 유리전이온도가 높아 열적 안정성이 우수할 뿐만 아니라, 캐리어 수송능 및 발광능 등이 우수하다. 따라서, 상기 화학식 1로 표시되는 화합물을 유기 전계 발광 소자가 포함할 경우, 소자의 낮은 구동 전압과 높은 발광 효율 및 장수명 등의 특성을 확보할 수 있다.
일반적으로 유기 전계 발광 소자의 인광 발광층에서, 호스트 물질은 이의 삼중항 에너지 갭이 도펀트의 삼중항 에너지 갭보다 높아야 한다. 즉, 호스트의 가장 낮은 여기 상태가 도펀트의 가장 낮은 방출 상태보다 에너지가 더 높은 경우, 인광 발광 효율이 향상될 수 있다. 본 발명에서 상기 화학식 1로 표시되는 화합물은 삼중항 에너지가 높고, 넓은 일중항 에너지 준위와 높은 삼중항 에너지 준위를 가지는 인돌 유도체가 축합되어 있는 기본 골격에 특정의 치환기가 도입됨으로써, 에너지 준위가 도펀트보다 높게 조절될 수 있어 호스트 물질로 사용될 수 있다.
또한, 본 발명의 상기 화학식 1로 표시되는 화합물은 전술한 바와 같이 높은 삼중항 에너지를 갖기 때문에, 발광층에서 생성된 엑시톤이 발광층에 인접하는 전자수송층 또는 정공수송층으로 확산되는 것을 방지할 수 있다. 따라서, 상기 화학식 1의 화합물을 이용하여 정공 수송층과 발광층 사이에 유기물층(이하, '발광 보조층'이라 함)을 형성할 경우, 상기 화합물에 의해서 엑시톤의 확산이 방지되기 때문에, 상기 제1 엑시톤 확산 방지층을 포함하지 않은 종래의 유기 전계 발광 소자와 달리, 실질적으로 발광층 내에서 발광에 기여하는 엑시톤의 수가 증가되어 소자의 발광 효율이 개선될 수 있다.
또한, 상기 화학식 1로 표시되는 화합물을 이용하여 발광층과 전자 수송층 사이에 유기물층(이하, '수명 개선층'이라 함)을 형성할 경우에도, 상기 화학식 1의 화합물에 의해 엑시톤의 확산이 방지됨으로써, 유기 전계 발광 소자의 내구성 및 안정성이 향상될 수 있고, 이로 인해 소자의 반감 수명이 효율적으로 증가될 수 있다. 이와 같이, 상기 화학식 1로 표시되는 화합물은 발광층의 호스트 이외, 발광 보조층 재료 또는 수명 개선층 재료로 사용될 수 있다.
더욱이, 본 발명에서 상기 화학식 1의 화합물은 상기와 같은 기본 골격에 도입되는 치환기의 종류에 따라 HOMO 및 LUMO 에너지 레벨을 조절할 수 있어, 넓은 밴드갭을 가질 수 있고, 높은 캐리어 수송성을 가질 수 있다. 예를 들어, 상기 화합물은 상기 기본 골격에 질소-함유 헤테로환(예컨대, 피리딘기, 피리미딘기, 트리아진기등)과 같이 전자 흡수성이 큰 전자 끌개기(EWG)가 결합될 경우, 분자 전체가 양극성(bipolar)의 특성을 갖기 때문에, 정공과 전자의 결합력을 높일 수 있다. 이와 같이, 상기 기본 골격에 EWG가 도입된 상기 화학식 1의 화합물은 우수한 캐리어 수송성 및 발광 특성이 우수하기 때문에, 유기 전계 발광 소자의 발광층 재료 이외, 전자주입/수송층 재료, 또는 수명 개선층 재료로도 사용될 수 있다.
한편, 본 발명의 상기 화학식 1의 화합물이 상기와 같은 기본 골격에 아릴아민기, 카바졸기, 터페닐기, 트리페닐렌기 등과 같이 전자 공여성이 큰 전자 주게기(EDG)가 결합될 경우, 정공의 주입 및 수송이 원활하게 이루어지기 때문에, 발광층 재료 이외, 정공주입/수송층 또는 발광 보조층 재료로도 유용하게 사용될 수 있다.
이와 같이, 본 발명에서 상기 화학식 1로 표시되는 화합물은 유기 전계 발광 소자의 발광 특성을 향상시킴과 동시에, 정공 주입/수송 능력, 전자 주입/수송 능력, 발광 효율, 구동 전압, 수명 특성 등을 향상시킬 수 있다. 따라서, 본 발명에 따른 화학식 1의 화합물은 유기 전계 발광 소자의 유기물층 재료, 바람직하게는 발광층 재료(청색, 녹색 및/또는 적색의 인광 호스트 재료), 전자 수송/주입층 재료, 정공 수송/주입층 재료, 발광보조층 재료 및 수명개선층 재료, 더 바람직하게는 발광층 재료, 전자 수송층 재료, 발광보조층 재료, 및 수명 개선층 재료로 사용될 수 있다.
또한, 본 발명의 상기 화학식 1의 화합물은 상기 기본 골격에 다양한 치환기, 특히 아릴기 및/또는 헤테로아릴기가 도입되어 화합물의 분자량이 유의적으로 증대됨으로써, 유리 전이 온도가 향상될 수 있고, 이로 인해 종래의 발광 재료(예를 들어, CBP)보다 높은 열적 안정성을 가질 수 있다.
또한, 본 발명의 상기 화학식 1로 표시되는 화합물은 유기물층의 결정화 억제에도 효과가 있다. 따라서, 본 발명에 따른 화학식 1의 화합물을 포함하는 유기 전계 발광 소자는 성능 및 수명 특성이 크게 향상될 수 있고, 이러한 유기 전계 발광 소자가 적용된 풀 칼라 유기 발광 패널도 성능이 극대화될 수 있다.
본 발명에서 상기 화학식 1로 표시되는 화합물은 R1과 R2, R2과 R3, R3과 R4, R5와 R6, R6과 R7, R7과 R8, R9과 R10, R10과 R11 및 R11과 R12 중 적어도 하나는 상기 화학식 2로 표시되는 고리와 축합되어 N, O, S, Si 중 하나 이상을 포함하는 축합 헤테로 방향족 고리 또는 축합 방향족 고리를 형성할 수 있다.
본 발명의 바람직한 한 구현 예에 따르면, 상기 화학식 1로 표시되는 화합물은 구체적으로는 하기 화학식 3 내지 화학식 7 중 어느 하나로 나타낼 수 있다.
[화학식 3]
[화학식 4]
[화학식 5]
[화학식 6]
[화학식 7]
상기 화학식 3 내지 화학식 7에 있어서,
X1, X2, Ar1, Y1 내지 Y4 및 R1 내지 R12 각각은 상기 화학식 1 및 화학식 2에서 정의된 바와 같다.
다만, 본 발명의 바람직한 한 구현 예에 따르면, 상기 화학식 3 내지 화학식 7에서 X1 및 X2 중 적어도 하나는 N(Ar1)일 수 있다.
또한, 본 발명의 바람직한 한 구현 예에 따르면, 상기 화학식 3 내지 화학식 7에서 Y1 내지 Y4은 모두 C(R13)이거나, Y1 내지 Y4 중 적어도 하나가 N일 수 있다.
한편, 본 발명의 상기 화학식 1로 표시되는 화합물에서 R1과 Ar1 및, R12와 Ar1 중 적어도 하나는 서로 결합하여 축합 방향족 고리 또는 축합 헤테로 방향족 고리를 형성할 수 있다.
보다 구체적으로, 본 발명의 바람직한 한 구현 예에 따르면, 상기 화학식 1로 표시되는 화합물에서 Ar1이 페닐이며, 상기 Ar1이 R1가 결합하여 축합 고리를 형성하는 경우, 하기 화학식 8 내지 화학식 10 중 어느 하나로 표시되는 화합물로 구체화될 수 있으나, 이에 한정하는 것은 아니다:
[화학식 8]
[화학식 9]
[화학식 10]
상기 화학식 8 내지 화학식 10에 있어서,
R2와 R3, R3과 R4, R5와 R6, R6과 R7, R7과 R8, R9과 R10, R10과 R11, R11과 R12, R2와 R15 및 R15와 R16 중 적어도 하나는 하기 화학식 2로 표시되는 고리와 축합되어 축합 고리를 형성하고;
하기 화학식 2로 표시되는 고리와 축합을 형성하지 않는 R2 내지 R12 및 R15 내지 R16는 각각 독립적으로 수소, 중수소, 할로겐, 시아노기, 니트로기, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되거나, 인접하는 기(예컨대, 인접한 R2 내지 R12 중 적어도 하나, 또는 인접한 R14 내지 R16 중 적어도 하나, 또는 인접한 R13 등)와 결합하여 축합 고리를 형성할 수 있으며;
X3은 O, S, N(Ar7), C(Ar8)(Ar9) 및 Si(Ar10)(Ar11)으로 구성된 군으로부터 선택되고, 바람직하게는 N(Ar7)이며;
Ar7 내지 Ar11은 각각 독립적으로 C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~6C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되며;
n은 0 내지 4의 정수이며;
R14는 중수소, 할로겐, 시아노기, 니트로기, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되거나, 인접하는 기(예컨대, 인접한 R2 내지 R12 중 적어도 하나, 또는 인접한 R14 내지 R16 중 적어도 하나, 또는 인접한 R13 등)와 결합하여 축합 고리를 형성할 수 있고, 상기 R14가 복수 개인 경우 이들은 서로 동일하거나 상이하며;
상기 Ar7 내지 Ar11, R2 내지 R12 및 R14 내지 R16의 알킬기, 시클로알킬기, 헤테로시클로알킬기, 아릴기, 헤테로아릴기, 알킬옥시기, 아릴옥시기, 알킬실릴기, 아릴실릴기, 알킬보론기, 아릴보론기, 아릴포스핀기, 모노 또는 디아릴포스피닐기 및 아릴아민기는 각각 독립적으로, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택된 1종 이상으로 치환되거나 비치환되고, 복수 개의 치환기로 치환되는 경우 이들은 서로 동일하거나 상이할 수 있으며;
[화학식 2]
상기 화학식 2에서,
점선은 상기 화학식 8 내지 10 중 어느 하나와 축합이 이루어지는 부분이고;
X1 및 X2는 각각 독립적으로 단일결합, O, S, N(Ar2), C(Ar3)(Ar4) 및 Si(Ar5)(Ar6)으로 구성된 군으로부터 선택되나, X1 및 X2가 모두 단일결합은 아니며, 바람직하게는 X1 및 X2 중 적어도 하나는 N(Ar2)이고;
Y1 내지 Y4은 각각 독립적으로 N 또는 C(R13)이고, 바람직하게는 Y1 내지 Y4 모두가 C(R13)이거나 상기 Y1 내지 Y4 중 적어도 한 개가 N이며;
R13이 복수 개인 경우 이들은 서로 동일하거나 상이하며, 상기 R13은 수소, 중수소, 할로겐, 시아노기, 니트로기, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되거나, 인접하는 기(예컨대, 인접한 R13 또는 R14 등)와 결합하여 축합 고리를 형성할 수 있으며;
Ar2 내지 Ar6은 각각 독립적으로 C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되며;
상기 R13 및 Ar2 내지 Ar6의 알킬기, 시클로알킬기, 헤테로시클로알킬기, 아릴기, 헤테로아릴기, 알킬옥시기, 아릴옥시기, 알킬실릴기, 아릴실릴기, 알킬보론기, 아릴보론기, 아릴포스핀기, 모노 또는 디아릴포스피닐기 및 아릴아민기는 각각 독립적으로, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택된 1종 이상으로 치환되거나 비치환되고, 복수 개의 치환기로 치환되는 경우 이들은 서로 동일하거나 상이할 수 있다.
또한, 본 발명의 바람직한 한 구현 예에 따르면, 상기 화학식 8 내지 화학식 10 중 어느 하나로 표시되는 화합물은 보다 구체적으로 하기 화학식 C-1 내지 화학식 C-12 중 어느 하나로 나타낼 수 있으나, 이에 제한되는 것은 아니다:
상기 화학식 C-1 내지 화학식 C-12에서,
X1, X2, X3, Y1 내지 Y4, R2 내지 R12, R14 내지 R16 및 n 각각은 상기 화학식 8 내지 화학식 10에서 정의된 바와 같다.
한편, 본 발명의 바람직한 한 구현 예에 따르면, 상기 화학식 1로 표시되는 화합물에서 R1 내지 R12 및 Ar1 내지 Ar6
중 적어도 하나는 C1~C40의 알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되며,
상기 R1 내지 R12 및 Ar1 내지 Ar6의 알킬기, 아릴기, 헤테로아릴기, 아릴아민기는 각각 독립적으로, 중수소, 할로겐, 시아노기, C1~C40의 알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C6~C60의 아릴아민기로 이루어진 군에서 선택된 1종 이상으로 치환되거나 비치환되고, 복수 개의 치환기로 치환되는 경우, 이들은 서로 동일하거나 상이할 수 있다.
본 발명의 바람직한 한 구현 예에 따르면, 상기 화학식 1로 표시되는 화합물에서, 상기 R1 내지 R12 및 Ar1 내지 Ar6
중 적어도 하나는 페닐기 또는 하기 화학식 11로 표시되는 치환기일 수 있다:
[화학식 11]
상기 화학식 11에서,
*는 상기 화학식 1에 결합되는 부분을 의미하고;
L1은 단일결합, C6~C18의 아릴렌기 및 핵원자수 5 내지 18개의 헤테로아릴렌기로 이루어진 군에서 선택되고, 바람직하게는 단일결합, 페닐렌기, 비페닐렌기, 또는 카바졸릴기일 수 있으며;
Z1 내지 Z5는 각각 독립적으로 N 또는 C(R17)이되, 상기 Z1 내지 Z5 중 적어도 하나는 N이며;
R17이 복수 개인 경우, 이들은 서로 동일하거나 상이하며, 상기 R17은 수소, 중수소, 할로겐, 시아노기, 니트로기, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C6~C60의 아릴기, 핵원자수 5 내지 40개의 헤테로아릴기, C6~C60의 아릴옥시기 C1~C40의 알킬옥시기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴아민기, C1~C40의 알킬실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴실릴기로 이루어진 군에서 선택되거나, 인접하는 기(예컨대, L1, 인접하는 다른 R17)와 결합하여 축합 고리를 형성할 수 있으며;
상기 R17의 알킬기, 알케닐기, 알키닐기, 아릴기, 헤테로아릴기, 아릴옥시기, 알킬옥시기, 시클로알킬기, 헤테로시클로알킬기, 아릴아민기, 알킬실릴기, 알킬보론기, 아릴보론기, 아릴포스핀기, 모노 또는 디아릴포스피닐기 및 아릴실릴기는 각각 독립적으로 중수소, 할로겐, 시아노기, 니트로기, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C6~C60의 아릴기, 핵원자수 5 내지 40개의 헤테로아릴기, C6~C60의 아릴옥시기, C1~C40의 알킬옥시기, C6~C60의 아릴아민기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C1~C40의 알킬실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴실릴기로 이루어진 군에서 선택된 1종 이상으로 치환되거나 비치환되고, 복수 개의 치환기로 치환되는 경우, 이들은 서로 동일하거나 상이할 수 있다.
본 발명의 보다 바람직한 한 구현 예에 따르면, 상기 화학식 11로 표시되는 치환기의 예로는 하기 화학식 A-1 내지 화학식 A-15 중 어느 하나로 표시되는 치환기 등이 있으나, 이에 한정되는 것은 아니다.
상기 A-1 내지 A-15에서,
*는 상기 화학식 1에 결합되는 부분을 의미하고;
m은 0 내지 4의 정수로서, 상기 m이 0인 경우, 수소가 치환기 R18로 치환되지 않는 것을 의미하고, 상기 m이 1 내지 4의 정수인 경우, R18은 중수소, 할로겐, 시아노기, 니트로기, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 40개의 헤테로아릴기, C6~C60의 아릴옥시기 C1~C40의 알킬옥시기, C6~C60의 아릴아민기, C1~C40의 알킬실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴실릴기로 이루어진 군에서 선택되거나, 인접하는 기(예컨대, L1, R17 또는 다른 R18등)와 결합하여 축합 고리를 형성할 수 있고, 상기 R18이 복수 개인 경우 이들은 서로 동일하거나 상이하며;
상기 R18의 알킬기, 알케닐기, 알키닐기, 시클로알킬기, 헤테로시클로알킬기, 아릴기, 헤테로아릴기, 아릴옥시기, 알킬옥시기, 아릴아민기, 알킬실릴기, 알킬보론기, 아릴보론기, 아릴포스핀기, 모노 또는 디아릴포스피닐기 및 아릴실릴기는 각각 독립적으로 중수소, 할로겐, 시아노기, 니트로기, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C6~C40의 아릴기, 핵원자수 5 내지 40개의 헤테로아릴기, C6~C60의 아릴옥시기, C1~C40의 알킬옥시기, C6~C40의 아릴아민기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C1~C40의 알킬실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴실릴기로 이루어진 군에서 선택된 1종 이상으로 치환되거나 비치환되고, 복수 개의 치환기로 치환되는 경우, 이들은 서로 동일하거나 상이할 수 있으며;
L1 및 R17은 각각 상기 화학식 11에서 정의된 바와 같다.
본 발명의 바람직한 한 구현 예에 따르면, 상기 화학식 1로 표시되는 화합물에서, 상기 R1 내지 R12 및 Ar1 내지 Ar6 중 적어도 하나는 하기 화학식 12로 표시되는 치환기일 수 있다.
[화학식 12]
상기 화학식 12에서,
*는 상기 화학식 1에 결합되는 부분을 의미하고;
L2는 단일결합, C6~C18의 아릴렌기 및 핵원자수 5 내지 18개의 헤테로아릴렌기로 이루어진 군에서 선택되고, 바람직하게 단일결합, 페닐렌기, 비페닐렌기 또는 카바졸릴기일 수 있으며;
R19 및 R20는 각각 독립적으로 C1~C40의 알킬기, C6~C40의 아릴기, 핵원자수 5 내지 40개의 헤테로아릴기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되거나, 상기 R19 및 R20가 결합하여 축합 고리를 형성할 수 있으며;
상기 R19 및 R20의 알킬기, 아릴기, 헤테로아릴기 및 아릴아민기는 각각 독립적으로 중수소, 할로겐, 시아노기, 니트로기, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C6~C60의 아릴기, 핵원자수 5 내지 40개의 헤테로아릴기, C6~C60의 아릴옥시기, C1~C40의 알킬옥시기, C6~C60의 아릴아민기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C1~C40의 알킬실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴실릴기로 이루어진 군에서 선택된 1종 이상으로 치환되거나 비치환되고, 복수 개의 치환기로 치환되는 경우, 이들은 서로 동일하거나 상이할 수 있다.
본 발명에서 상기 화학식 1로 표시되는 화합물은 보다 구체적으로 하기 구조로 나타낼 수 있으나, 이에 한정되는 것은 아니다:
본 발명에서 상기 화학식 1로 표시되는 화합물은 일반적인 합성방법에 따라 합성될 수 있다. 본 발명의 화합물에 대한 상세한 합성 과정은 후술하는 합성예에서 구체적으로 기술하도록 한다.
2. 유기 전계 발광 소자
한편, 본 발명의 다른 측면은 상기한 본 발명에 따른 화학식 1로 표시되는 화합물을 포함하는 유기 전계 발광 소자(유기 EL 소자)에 관한 것이다.
보다 구체적으로, 본 발명에 따른 유기 전계 발광 소자는 (i) 양극(anode), (ii) 음극(cathode) 및 (iii) 상기 양극과 음극 사이에 개재(介在)된 1층 이상의 유기물층을 포함하며, 상기 1층 이상의 유기물층 중 적어도 하나는 상기 화학식 1로 표시되는 화합물을 포함한다. 이때, 상기 화학식 1로 표시되는 화합물은 단독으로 사용되거나, 또는 2 이상이 혼합되어 사용될 수 있다.
본 발명의 일례에 따르면, 상기 1층 이상의 유기물층은 정공주입층, 정공수송층, 발광보조층, 발광층, 전자수송층 및 전자주입층 중 어느 하나 이상일 수 있고, 이 중에서 적어도 하나의 유기물층은 상기 화학식 1로 표시되는 화합물을 포함할 수 있다. 구체적으로 상기 화학식 1의 화합물을 포함하는 유기물층은 발광층, 전자 수송층, 전자 주입층, 정공 수송층, 정공 주입층, 발광 보조층 및 수명개선층으로 이루어진 군에서 선택될 수 있으며, 바람직하게는 발광층, 전자 수송층, 발광보조층, 및 수명 개선층으로 이루어진 군에서 선택될 수 있다.
본 발명의 유기 전계 발광 소자의 발광층은 호스트 재료를 포함할 수 있는데, 바람직하게는 상기 호스트 재료로서 본 발명의 화학식 1로 표시되는 화합물을 포함할 수 있다. 또한 본 발명의 유기 전계 발광 소자의 발광층은 상기 화학식 1의 화합물 이외의 화합물을 호스트로 포함할 수 있다.
이러한 본 발명의 유기 전계 발광 소자의 구조는 특별히 한정되지 않으나, 기판, 양극, 정공주입층, 정공수송층, 발광보조층, 발광층, 전자수송층 및 음극이 순차적으로 적층된 구조일 수 있다. 이때, 상기 전자수송층 위에는 전자주입층이 추가로 적층될 수 있으며, 상기한 바와 같이 정공주입층, 정공수송층, 발광보조층, 발광층, 전자수송층 및 전자주입층 중 하나 이상은 상기 화학식 1로 표시되는 화합물을 포함할 수 있다.
본 발명의 유기 전계 발광 소자의 구조는 전극과 유기물층 계면에 절연층 또는 접착층이 삽입된 구조일 수 있다.
또한, 상기 유기 전계 발광 소자는 발광층과 전자 수송층 사이에 수명 개선층 또는 전자 수송 보조층이 포함될 수 있다. 이때 상기 화학식 1로 표시되는 화합물은 수명 개선층 또는 전자 수송 보조층으로도 이용될 수 있다.
본 발명의 유기 전계 발광 소자는 상기 유기물층 중 1층 이상이 상기 화학식 1로 표시되는 화합물을 포함하는 것을 제외하고는, 당업계에 공지된 재료 및 방법으로 유기물층 및 전극을 형성하여 제조할 수 있다.
상기 유기물층은 진공 증착법이나 용액 도포법에 의하여 형성될 수 있다. 상기 용액 도포법의 예로는 스핀 코팅, 딥코팅, 닥터 블레이딩, 잉크젯 프린팅 또는 열 전사법 등이 있으나, 이에 한정되지는 않는다.
본 발명의 유기 전계 발광 소자 제조 시 사용되는 기판은 특별히 한정되지 않으나, 실리콘 웨이퍼, 석영, 유리판, 금속판, 플라스틱 필름 및 시트 등을 사용할 수 있다.
또, 양극 물질로는 바나듐, 크롬, 구리, 아연, 금과 같은 금속 또는 이들의 합금; 아연산화물, 인듐산화물, 인듐 주석 산화물(ITO), 인듐 아연 산화물(IZO)과 같은 금속 산화물; ZnO:Al 또는 SnO2:Sb와 같은 금속과 산화물의 조합; 폴리티오펜, 폴리(3-메틸티오펜), 폴리[3,4-(에틸렌-1,2-디옥시)티오펜](PEDT), 폴리피롤 또는 폴리아닐린과 같은 전도성 고분자; 및 카본블랙 등을 들 수 있으나, 이에 한정되지는 않는다.
또, 음극 물질로는 마그네슘, 칼슘, 나트륨, 칼륨, 타이타늄, 인듐, 이트륨, 리튬, 가돌리늄, 알루미늄, 은, 주석, 또는 납과 같은 금속 또는 이들의 합금; 및 LiF/Al 또는 LiO2/Al과 같은 다층 구조 물질 등을 들 수 있으나, 이에 한정되지는 않는다.
또한, 정공 주입층, 정공 수송층, 전자 주입층 및 전자 수송층은 특별히 한정되는 것은 아니며, 당 업계에 알려진 통상의 물질을 사용할 수 있다.
이하 본 발명을 실시예를 통하여 상세히 설명하면 다음과 같다. 단, 하기 실시예는 본 발명을 예시하는 것일 뿐, 본 발명이 하기 실시예에 의해 한정되는 것은 아니다.
[
준비예
1]
JJ
-
1 의
합성
<
단계1
> 2-
브로모
-3-
(2-클로로페닐)디벤조[b,e][1,4]디옥신의
합성
질소 기류 하에서 2,3-디브로모디벤조[b,e][1,4]디옥신 (25.79 g, 75.41 mmol)과 (2-클로로페닐)보론산 (14.15 g, 90.49 mmol), NaOH (9.05 g, 226.24 mmol) 및 THF/H2O(400 ml/200 ml)를 혼합한 다음, 40℃에서 Pd(PPh3)4(4.36 g, 5 mol%)를 넣고 80℃에서 12시간 동안 교반하였다.
반응 종결 후 메틸렌클로라이드로 추출한 다음, MgSO4를 넣고 여과하였다. 얻어진 유기층에서 용매를 제거한 후 컬럼 크로마토그래피 (Hexane:EA = 3:1 (v/v))로 정제하여 2-브로모-3-(2-클로로페닐)디벤조[b,e][1,4]디옥신 (20.57 g, 수율: 73%)을 얻었다.
1H-NMR: δ 6.82 (m, 2H), 6.94 (m, 2H), 7.20(s, 1H), 7.36 (m, 2H), 7.49 (s, 1H), 7.60 (d, 1H), 7.70 (d, 1H)
<
단계2
> 2-(3-
(2-클로로페닐)디벤조[b,e][1,4]디옥신
-2-일)아닐린의 합성
준비예 1의 <단계 1>에서 사용된 2,3-디브로모벤조[b,e][1,4]디옥신 대신 상기 준비예 1의 <단계 1>에서 얻은 2-브로모-3-(2-클로로페닐)디벤조[b,e][1,4]디옥신 (28.18 g, 75.41 mmol)을 사용하고 (2-클로로페닐)보론산 대신 2-(4,4,5,5-테트라메틸-1,3,2-디옥사보로란-2-일)아닐린 (19.82 g, 90.49 mmol) 을 사용하는 것을 제외하고는 상기 준비예 1의 <단계 1>과 동일한 과정을 수행하여 2-(3-(2-클로로페닐)디벤조[b,e][1,4]디옥신-2-일)아닐린을 얻었다.
1H-NMR: δ 5.29 (s, 2H), 6.82 (m, 2H), 6.94 (m, 2H), 7.28(t, 1H), 7.38 (m, 2H), 7.49 (s, 2H), 7.63 (d, 1H), 7.73 (d, 1H), 8.00 (d, 1H)
<
단계3
>
JJ
-
1 의
합성
질소 기류 하에서 2-(3-(2-클로로페닐)디벤조[b,e][1,4]디옥신-2-일)아닐린 (2.58 g, 6.7 mmol), Pd(OAc)2 (0.08 g, 0.34 mmol), P(t-Bu)3 (0.16 ml, 0.67 mmol), NaO(t-Bu) (1.29 g, 13.4 mmol) 및 톨루엔 (70 ml)을 혼합하고 110℃ 에서 5시간 동안 교반하였다. 반응이 종결된 후 톨루엔을 농축하고, 고체염을 여과한 뒤, 재결정으로 정제하여 목적 화합물인 JJ-1 (0.98 g, 수율 42%)을 얻었다.
JJ-1 의 1H-NMR: δ 6.82 (m, 2H), 6.94 (m, 2H), 7.15 (m, 3H), 7.38(m, 4H), 7.49 (s, 2H), 8.10 (d, 2H)
[
준비예
2]
JJ
-
2 의
합성
<
단계1
> 3-
브로모
-2-(2-
클로로페닐
)-9-페닐-9H-
카바졸의
합성
준비예 1의 <단계 1>에서 사용된 2,3-디브로모디벤조[b,e][1,4]디옥신 대신 3-브로모-2-요오드-9-페닐-9H-카바졸 (33.79 g, 75.41 mmol)을 사용하는 것을 제외하고는 상기 준비예 1의 <단계 1>과 동일한 과정을 수행하여 3-브로모-2-(2-클로로페닐)-9-페닐-9H-카바졸을 얻었다.
1H-NMR : δ 7.16 (t, 1H), 7.36 (m, 3H), 7.50-7.71 (m, 8H), 7.94 (d, 1H), 8.25 (s, 1H), 8.55 (d, 1H)
<
단계2
> 2-(2-(2-
클로로페닐
)-9-페닐-9H-
카바졸
-3-일)아닐린의 합성
준비예 1의 <단계 2>에서 사용된 2-브로모-3-(2-클로로페닐)디벤조[b,e][1,4]디옥신 대신 상기 준비예 2의 <단계 1>에서 얻은 3-브로모-2-(2-클로로페닐)-9-페닐-9H-카바졸 (32.63 g, 75.41 mmol)을 사용하는 것을 제외하고는 상기 준비예 1의 <단계 2>와 동일한 과정을 수행하여 2-(2-(2-클로로페닐)-9-페닐-9H-카바졸-3-일)아닐린을 얻었다.
1H-NMR : δ 5.30 (s, 2H), 6.95 (m, 2H), 7.16 (t, 1H), 7.28-7.38 (m, 5H), 7.50-7.71 (m, 7H), 7.94-7.99 (m, 3H), 8.08 (s, 1H), 8.55 (d, 1H)
<
단계3
>
JJ
-
2 의
합성
준비예 1의 <단계 3>에서 사용된 2-(3-(2-클로로페닐)디벤조[b,e][1,4]디옥신-2-일)아닐린 대신 상기 준비예 2의 <단계 2>에서 얻은 2-(2-(2-클로로페닐)-9-페닐-9H-카바졸-3-일)아닐린 (2.98 g, 6.7 mmol)을 사용하는 것을 제외하고는 상기 준비예 1의 <단계 3>과 동일한 과정을 수행하여 JJ-2 를 얻었다.
JJ-2 의 1H-NMR: δ 7.16-7.20 (m, 4H), 7.35-7.39 (m, 5H), 7.50-7.62 (m, 5H), 7.94 (m, 2H), 8.09 (m, 3H), 8.55 (d, 1H)
[
준비예
3]
JJ
-3,
JJ
-
4 의
합성
<
단계1
> 6-(2-
니트로페닐
)-9-페닐-9H-
트리벤조[b,d,f]아제핀의
합성
준비예 1의 <단계 1>에서 사용된 2,3-디브로모디벤조[b,e][1,4]디옥신 대신 6-요오드-9-페닐-9H-트리벤조[b,d,f]아제핀 (33.58 g, 75.41 mmol)을 사용하고 (2-클로로페닐)보론산 대신 (2-니트로페닐)보론산 (15.10 g, 90.49 mmol)을 사용하는 것을 제외하고는 상기 준비예 1의 <단계 1>과 동일한 과정을 수행하여 6-(2-니트로페닐)-9-페닐-9H-트리벤조[b,d,f]아제핀을 얻었다.
1H-NMR: δ 7.00-7.35 (m, 6H), 7.38 (m, 2H), 7.56-7.72 (m, 5H), 7.89-8.10 (m, 7H)
<
단계2
>
JJ
-3,
JJ
-
4 의
합성
질소 기류 하에서 상기 준비예 3의 <단계 1>에서 얻은 6-(2-니트로페닐)-9-페닐-9H-트리벤조[b,d,f]아제핀 (7.00 g, 15.91 mmol), 트리페닐포스핀 (10.43 g, 39.77 mmol) 및 1,2-디클로로벤젠 (50 ml)을 혼합한 다음, 12시간 동안 교반하였다.
반응 종료 후 1,2-디클로로벤젠을 제거하고 디클로로메탄으로 추출하였다. 얻어진 유기층에 대해 MgSO4로 물을 제거하고, 컬럼크로마토그래피 (Hexane:MC=3:1 (v/v))로 정제하여 JJ-3 (3.25 g, 수율: 50%) 및 JJ-4를 얻었다.
JJ-3의 1H-NMR: δ 7.01-7.25 (m, 7H), 7.37-7.63 (m, 7H), 7.96 (d, 2H), 8.15 (m, 2H), 8.35 (d, 1H), 11.50 (s, 1H)
JJ-4의 1H-NMR: δ 7.01-7.25 (m, 7H), 7.37-7.63 (m, 7H), 7.85 (s, 1H), 7.96 (d, 2H), 8.15 (m, 2H), 11.44 (s, 1H)
[
준비예
4]
JJ
-5,
JJ
-
6 의
합성
<
단계1
> 9-
(2-니트로페닐)디벤조[4,5:6,7]아제피노[3,2,1-jk]카바졸의
합성
준비예 3의 <단계 1>에서 사용된 6-요오드-9-페닐-9H-트리벤조[b,d,f]아제핀 대신 9-요오드디벤조[4,5:6,7]아제피노[3,2,1-jk]카바졸 (33.42 g, 75.41 mmol)을 사용하는 것을 제외하고는 상기 준비예 3의 <단계 1>과 동일한 과정을 수행하여 9-(2-니트로페닐)디벤조[4,5:6,7]아제피노[3,2,1-jk]카바졸을 얻었다.
1H-NMR: δ 7.20-7.28 (m, 2H), 7.50-7.60 (m, 3H), 7.72-7.90 (m, 5H), 8.00-8.19 (m, 6H), 8.42 (d, 2H)
<
단계2
>
JJ
-5,
JJ
-
6 의
합성
준비예 3의 <단계 2>에서 사용된 6-(2-니트로페닐)-9-페닐-9H-트리벤조[b,d,f]아제핀 대신 상기 준비예 4의 <단계 1>에서 얻은 9-(2-니트로페닐)디벤조[4,5:6,7]아제피노[3,2,1-jk]카바졸 (6.97 g, 15.91 mmol)을 사용하는 것을 제외하고는 상기 준비예 3의 <단계 2>과 동일한 과정을 수행하여 JJ-5 및 JJ-6 를 얻었다.
JJ-5의 1H-NMR: δ 7.19-7.29 (m, 4H), 7.50-7.72 (m, 5H), 8.10-8.19 (m, 6H), 8.42 (d, 2H), 11.79 (s, 1H)
JJ-6의 1H-NMR: δ 7.20-7.29 (m, 3H), 7.40 (s, 1H), 7.50-7.72 (m, 6H), 8.10-8.19 (m, 5H), 8.42 (d, 2H), 11.70 (s, 1H)
[
준비예
5]
JJ
-7,
JJ
-
8 의
합성
<
단계1
> 2-(2-
니트로페닐
)-9-페닐-9H-
트리벤조[b,d,f]아제핀의
합성
준비예 3의 <단계 1>에서 사용된 6-요오드-9-페닐-9H-트리벤조[b,d,f]아제핀 대신 2-요오드-9-페닐-9H-트리벤조[b,d,f]아제핀 (33.58 g, 75.41 mmol)을 사용하는 것을 제외하고는 상기 준비예 3의 <단계 1>과 동일한 과정을 수행하여 2-(2-니트로페닐)-9-페닐-9H-트리벤조[b,d,f]아제핀을 얻었다.
1H-NMR: δ 7.00-7.37 (m, 7H), 7.35-7.39 (m, 5H), 7.72 (t, 1H), 7.88 (t, 1H), 8.00-8.15 (m, 6H)
<
단계2
>
JJ
-7,
JJ
-
8 의
합성
준비예 3의 <단계 2>에서 사용된 6-(2-니트로페닐)-9-페닐-9H-트리벤조[b,d,f]아제핀 대신 상기 준비예 5의 <단계 1>에서 얻은 2-(2-니트로페닐)-9-페닐-9H-트리벤조[b,d,f]아제핀 (7.00 g, 15.91 mmol)을 사용하는 것을 제외하고는 상기 준비예 3의 <단계 2>과 동일한 과정을 수행하여 JJ-7 및 JJ-8 를 얻었다.
JJ-7의 1H-NMR: δ 7.00-7.37 (m, 8H), 7.35-7.50 (m, 5H), 7.63 (d, 1H), 7.93 (s, 1H), 8.09-8.19 (m, 4H), 11.60 (s, 1H)
JJ-8의 1H-NMR: δ 7.00-7.37 (m, 8H), 7.35-7.50 (m, 5H), 7.63 (d, 1H), 8.10-8.19 (m, 4H), 8.41 (d, 1H), 11.66 (s, 1H)
[
준비예
6]
JJ
-9,
JJ
-
10 의
합성
<
단계1
> 6-
(2-니트로페닐)디벤조[4,5:6,7]아제피노[3,2,1-jk]카바졸의
합성
준비예 3의 <단계 1>에서 사용된 6-요오드-9-페닐-9H-트리벤조[b,d,f]아제핀 대신 6-요오드디벤조[4,5:6,7]아제피노[3,2,1-jk]카바졸 (33.42 g, 75.41 mmol)을 사용하는 것을 제외하고는 상기 준비예 3의 <단계 1>과 동일한 과정을 수행하여 6-(2-니트로페닐)디벤조[4,5:6,7]아제피노[3,2,1-jk]카바졸을 얻었다.
1H-NMR: δ 7.06 (d, 1H), 7.25 (m, 2H), 7.39 (d, 1H), 7.50-7.72 (m, 7H), 7.90 (t, 1H), 8.00-8.19 (m, 5H), 8.44 (d, 1H)
<
단계2
>
JJ
-9,
JJ
-
10 의
합성
준비예 3의 <단계 2>에서 사용된 6-(2-니트로페닐)-9-페닐-9H-트리벤조[b,d,f]아제핀 대신 상기 준비예 6의 <단계 1>에서 얻은 6-(2-니트로페닐)디벤조[4,5:6,7]아제피노[3,2,1-jk]카바졸 (6.97 g, 15.91 mmol)을 사용하는 것을 제외하고는 상기 준비예 3의 <단계 2>과 동일한 과정을 수행하여 JJ-9 및 JJ-10 를 얻었다.
JJ-9의 1H-NMR: δ 7.20-7.70 (m, 12H), 8.10-8.20 (m, 4H), 8.42 (d, 1H), 11.69 (s, 1H)
JJ-10의 1H-NMR: δ 7.20-7.40 (m, 4H), 7.50-7.75(m, 7H), 8.10-8.20 (m, 5H), 8.42 (d, 1H), 11.79 (s, 1H)
[
준비예
7]
JJ
-11,
JJ
-
12 의
합성
<
단계1
> 5-
(2-니트로페닐)디벤조[4,5:6,7]아제피노[3,2,1-jk]카바졸의
합성
준비예 3의 <단계 1>에서 사용된 6-요오드-9-페닐-9H-트리벤조[b,d,f]아제핀 대신 5-요오드디벤조[4,5:6,7]아제피노[3,2,1-jk]카바졸 (33.42 g, 75.41 mmol)을 사용하는 것을 제외하고는 상기 준비예 3의 <단계 1>과 동일한 과정을 수행하여 5-(2-니트로페닐)디벤조[4,5:6,7]아제피노[3,2,1-jk]카바졸을 얻었다.
1H-NMR: δ 7.06 (d, 1H), 7.20-7.30 (m, 2H), 7.40 (d, 1H), 7.45-7.70 (m, 7H), 7.90 (t, 1H), 8.00-8.20 (m, 5H), 8.41 (d, 1H)
<
단계2
>
JJ
-11,
JJ
-
12 의
합성
준비예 3의 <단계 2>에서 사용된 6-(2-니트로페닐)-9-페닐-9H-트리벤조[b,d,f]아제핀 대신 상기 준비예 7의 <단계 1>에서 얻은 5-(2-니트로페닐)디벤조[4,5:6,7]아제피노[3,2,1-jk]카바졸 (6.97 g, 15.91 mmol)을 사용하는 것을 제외하고는 상기 준비예 3의 <단계 2>과 동일한 과정을 수행하여 JJ-11 및 JJ-12 를 얻었다.
JJ-11의 1H-NMR: δ 7.20-7.70 (m, 12H), 8.10-8.20 (m, 4H), 8.42 (d, 1H), 11.69 (s, 1H)
JJ-12의 1H-NMR: δ 7.20-7.40 (m, 4H), 7.50-7.75(m, 7H), 8.10-8.20 (m, 5H), 8.42 (d, 1H), 11.79 (s, 1H)
[
합성예
1] J-1의 합성
질소 기류 하에서 JJ-1 (2.34 g, 6.7 mmol), 2-(4-브로모페닐)트리페닐렌 (3.06 g, 8.0 mmol), Pd(OAc)2 (0.08 g, 0.34 mmol), P(t-Bu)3 (0.16 ml, 0.67 mmol), NaO(t-Bu) (1.29 g, 13.4 mmol) 및 톨루엔 (70 ml)을 혼합하고 110℃ 에서 5시간 동안 교반하였다. 반응이 종결된 후 톨루엔을 농축하고, 고체염을 여과한 뒤, 재결정으로 정제하여 목적 화합물인 J-1 (2.79 g, 수율 64%)을 얻었다.
Mass (이론치: 651.76, 측정치: 651 g/mol)
[
합성예
2] J-2의 합성
2-(4-브로모페닐)트리페닐렌 대신 2-클로로-4-(4-(나프탈렌-1-일)페닐)퀴나졸린 (2.93 g, 8.0 mmol)을 사용하는 것을 제외하고는 합성예 1과 동일한 과정을 수행하여 목적 화합물인 J-2 (2.77 g, 수율 61%)를 얻었다.
Mass (이론치: 679.78, 측정치: 679 g/mol)
[
합성예
3] J-3의 합성
2-(4-브로모페닐)트리페닐렌 대신 2-클로로-4,6-디페닐-1,3,5-트리아진 (2.14 g, 8.0 mmol)을 사용하는 것을 제외하고는 합성예 1과 동일한 과정을 수행하여 목적 화합물인 J-3 (2.68 g, 수율 69%)을 얻었다.
Mass (이론치: 580.65, 측정치: 580 g/mol)
[
합성예
4] J-4의 합성
2-(4-브로모페닐)트리페닐렌 대신 2-(3-브로모페닐)-4,6-디페닐-1,3,5-트리아진 (3.10 g, 8.0 mmol)을 사용하는 것을 제외하고는 합성예 1과 동일한 과정을 수행하여 목적 화합물인 J-4 (3.21 g, 수율 73%)를 얻었다.
Mass (이론치: 656.75, 측정치: 656 g/mol)
[
합성예
5] J-5의 합성
2-(4-브로모페닐)트리페닐렌 대신 2-(3'-클로로-[1,1'-비페닐]-3-일)-4,6-디페닐-1,3,5-트리아진 (3.36 g, 8.0 mmol)을 사용하는 것을 제외하고는 합성예 1과 동일한 과정을 수행하여 목적 화합물인 J-5 (3.43 g, 수율 70%)를 얻었다.
Mass (이론치: 732.84, 측정치: 732 g/mol)
[
합성예
6] J-6의 합성
JJ-1 대신 JJ-2 (2.73 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 1과 동일한 과정을 수행하여 목적 화합물인 J-6 (3.23 g, 수율 68%)을 얻었다.
Mass (이론치: 710.88, 측정치: 710 g/mol)
[
합성예
7] J-7의 합성
JJ-1 대신 JJ-2 (2.73 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 2와 동일한 과정을 수행하여 목적 화합물인 J-7 (3.01 g, 수율 61%)을 얻었다.
Mass (이론치: 738.89, 측정치: 738 g/mol)
[
합성예
8] J-8의 합성
JJ-1 대신 JJ-2 (2.73 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 3과 동일한 과정을 수행하여 목적 화합물인 J-8 (3.00 g, 수율 70%)을 얻었다.
Mass (이론치: 639.76, 측정치: 639 g/mol)
[
합성예
9] J-9의 합성
JJ-1 대신 JJ-2 (2.73 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 4와 동일한 과정을 수행하여 목적 화합물인 J-9 (3.55 g, 수율 74%)을 얻었다.
Mass (이론치: 715.86, 측정치: 715 g/mol)
[
합성예
10] J-10의 합성
JJ-1 대신 JJ-2 (2.73 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 5와 동일한 과정을 수행하여 목적 화합물인 J-10 (3.45 g, 수율 65%)을 얻었다.
Mass (이론치: 791.96, 측정치: 791 g/mol)
[
합성예
11] J-11의 합성
JJ-1 대신 JJ-3 (2.73 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 1과 동일한 과정을 수행하여 목적 화합물인 J-11 (2.95 g, 수율 62%)를 얻었다.
Mass (이론치: 710.88, 측정치: 710 g/mol)
[
합성예
12] J-12의 합성
JJ-1 대신 JJ-3 (2.73 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 2와 동일한 과정을 수행하여 목적 화합물인 J-12 (3.36 g, 수율 68%)를 얻었다.
Mass (이론치: 738.89, 측정치: 738 g/mol)
[
합성예
13] J-13의 합성
JJ-1 대신 JJ-3 (2.73 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 3과 동일한 과정을 수행하여 목적 화합물인 J-13 (2.83 g, 수율 66%)을 얻었다.
Mass (이론치: 639.76, 측정치: 639 g/mol)
[
합성예
14] J-14의 합성
JJ-1 대신 JJ-3 (2.73 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 4와 동일한 과정을 수행하여 목적 화합물인 J-14 (3.50 g, 수율 73%)를 얻었다.
Mass (이론치: 715.86, 측정치: 715 g/mol)
[
합성예
15] J-15의 합성
JJ-1 대신 JJ-3 (2.73 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 5와 동일한 과정을 수행하여 목적 화합물인 J-15 (3.76 g, 수율 71%)를 얻었다.
Mass (이론치: 791.96, 측정치: 791 g/mol)
[
합성예
16] J-16의 합성
JJ-1 대신 JJ-4 (2.73 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 1과 동일한 과정을 수행하여 목적 화합물인 J-16 (3.24 g, 수율 68%)을 얻었다.
Mass (이론치: 710.88, 측정치: 710 g/mol)
[
합성예
17] J-17의 합성
JJ-1 대신 JJ-4 (2.73 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 2와 동일한 과정을 수행하여 목적 화합물인 J-17 (3.32 g, 수율 67%)을 얻었다.
Mass (이론치: 738.89, 측정치: 738 g/mol)
[
합성예
18] J-18의 합성
JJ-1 대신 JJ-4 (2.73 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 3과 동일한 과정을 수행하여 목적 화합물인 J-18 (3.34 g, 수율 78%)을 얻었다.
Mass (이론치: 639.76, 측정치: 639 g/mol)
[
합성예
19] J-19의 합성
JJ-1 대신 JJ-4 (2.73 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 4와 동일한 과정을 수행하여 목적 화합물인 J-19 (3.40 g, 수율 71%)을 얻었다.
Mass (이론치: 715.86, 측정치: 715 g/mol)
[
합성예
20] J-20의 합성
JJ-1 대신 JJ-4 (2.73 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 5와 동일한 과정을 수행하여 목적 화합물인 J-20 (3.97 g, 수율 75%)을 얻었다.
Mass (이론치: 791.96, 측정치: 791 g/mol)
[
합성예
21] J-21의 합성
JJ-1 대신 JJ-5 (2.72 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 1과 동일한 과정을 수행하여 목적 화합물인 J-21 (3.03 g, 수율 64%)을 얻었다.
Mass (이론치: 708.86, 측정치: 708 g/mol)
[
합성예
22] J-22의 합성
JJ-1 대신 JJ-5 (2.72 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 2와 동일한 과정을 수행하여 목적 화합물인 J-22 (3.35 g, 수율 68%)를 얻었다.
Mass (이론치: 736.88, 측정치: 736 g/mol)
[
합성예
23] J-23의 합성
JJ-1 대신 JJ-5 (2.72 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 3과 동일한 과정을 수행하여 목적 화합물인 J-23 (2.65 g, 수율 62%)을 얻었다.
Mass (이론치: 637.75, 측정치: 637 g/mol)
[
합성예
24] J-24의 합성
JJ-1 대신 JJ-5 (2.72 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 4와 동일한 과정을 수행하여 목적 화합물인 J-24 (2.58 g, 수율 54%)을 얻었다.
Mass (이론치: 713.84, 측정치: 713 g/mol)
[
합성예
25] J-25의 합성
JJ-1 대신 JJ-5 (2.72 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 5와 동일한 과정을 수행하여 목적 화합물인 J-25 (3.65 g, 수율 69%)를 얻었다.
Mass (이론치: 789.94, 측정치: 789 g/mol)
[
합성예
26] J-26의 합성
JJ-1 대신 JJ-6 (2.72 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 1과 동일한 과정을 수행하여 목적 화합물인 J-26 (2.94 g, 수율 62%)을 얻었다.
Mass (이론치: 708.86, 측정치: 708 g/mol)
[
합성예
27] J-27의 합성
JJ-1 대신 JJ-6 (2.72 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 2와 동일한 과정을 수행하여 목적 화합물인 J-27 (3.55 g, 수율 72%)를 얻었다.
Mass (이론치: 736.88, 측정치: 736 g/mol)
[
합성예
28] J-28의 합성
JJ-1 대신 JJ-6 (2.72 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 3과 동일한 과정을 수행하여 목적 화합물인 J-28 (2.60 g, 수율 61%)를 얻었다.
Mass (이론치: 637.75, 측정치: 637 g/mol)
[
합성예
29] J-29의 합성
JJ-1 대신 JJ-6 (2.72 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 4와 동일한 과정을 수행하여 목적 화합물인 J-29 (3.11 g, 수율 65%)을 얻었다.
Mass (이론치: 713.84, 측정치: 713 g/mol)
[
합성예
30] J-30의 합성
JJ-1 대신 JJ-6 (2.72 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 5와 동일한 과정을 수행하여 목적 화합물인 J-30 (3.91 g, 수율 74%)을 얻었다.
Mass (이론치: 789.94, 측정치: 789 g/mol)
[
합성예
31] J-31의 합성
JJ-1 대신 JJ-7 (2.73 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 1과 동일한 과정을 수행하여 목적 화합물인 J-31 (3.72 g, 수율 78%)을 얻었다.
Mass (이론치: 710.88, 측정치: 710 g/mol)
[
합성예
32] J-32의 합성
JJ-1 대신 JJ-7 (2.73 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 2와 동일한 과정을 수행하여 목적 화합물인 J-32 (3.47 g, 수율 70%)을 얻었다.
Mass (이론치: 738.89, 측정치: 738 g/mol)
[
합성예
33] J-33의 합성
JJ-1 대신 JJ-7 (2.73 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 3과 동일한 과정을 수행하여 목적 화합물인 J-33(2.61 g, 수율 61%)을 얻었다.
Mass (이론치: 639.76, 측정치: 639 g/mol)
[
합성예
34] J-34의 합성
JJ-1 대신 JJ-7 (2.73 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 4와 동일한 과정을 수행하여 목적 화합물인 J-34 (2.92 g, 수율 61%)를 얻었다.
Mass (이론치: 715.86, 측정치: 715 g/mol)
[
합성예
35] J-35의 합성
JJ-1 대신 JJ-7 (2.73 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 5와 동일한 과정을 수행하여 목적 화합물인 J-35 (3.40 g, 수율 64%)를 얻었다.
Mass (이론치: 791.96, 측정치: 791 g/mol)
[
합성예
36] J-36의 합성
JJ-1 대신 JJ-8 (2.73 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 1과 동일한 과정을 수행하여 목적 화합물인 J-36 (3.09 g, 수율 65%)을 얻었다.
Mass (이론치: 710.88, 측정치: 710 g/mol)
[
합성예
37] J-37의 합성
JJ-1 대신 JJ-8 (2.73 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 2와 동일한 과정을 수행하여 목적 화합물인 J-37 (3.46 g, 수율 70%)를 얻었다.
Mass (이론치: 738.89, 측정치: 738 g/mol)
[
합성예
38] J-38의 합성
JJ-1 대신 JJ-8 (2.73 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 3과 동일한 과정을 수행하여 목적 화합물인 J-38 (3.13 g, 수율 73%)를 얻었다.
Mass (이론치: 639.76, 측정치: 639 g/mol)
[
합성예
39] J-39의 합성
JJ-1 대신 JJ-8 (2.73 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 4와 동일한 과정을 수행하여 목적 화합물인 J-39 (3.45 g, 수율 72%)을 얻었다.
Mass (이론치: 715.86, 측정치: 715 g/mol)
[
합성예
40] J-40의 합성
JJ-1 대신 JJ-8 (2.73 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 5와 동일한 과정을 수행하여 목적 화합물인 J-40 (4.08 g, 수율 77%)을 얻었다.
Mass (이론치: 791.96, 측정치: 791 g/mol)
[
합성예
41] J-41의 합성
JJ-1 대신 JJ-9 (2.72 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 1과 동일한 과정을 수행하여 목적 화합물인 J-41 (3.13 g, 수율 66%)을 얻었다.
Mass (이론치: 708.86, 측정치: 708 g/mol)
[
합성예
42] J-42의 합성
JJ-1 대신 JJ-9 (2.72 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 2와 동일한 과정을 수행하여 목적 화합물인 J-42 (3.21 g, 수율 65%)을 얻었다.
Mass (이론치: 736.88, 측정치: 736 g/mol)
[
합성예
43] J-43의 합성
JJ-1 대신 JJ-9 (2.72 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 3와 동일한 과정을 수행하여 목적 화합물인 J-43 (2.95 g, 수율 69%)을 얻었다.
Mass (이론치: 637.75, 측정치: 637 g/mol)
[
합성예
44] J-44의 합성
JJ-1 대신 JJ-9 (2.72 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 4와 동일한 과정을 수행하여 목적 화합물인 J-44 (2.92 g, 수율 61%)을 얻었다.
Mass (이론치: 713.84, 측정치: 713 g/mol)
[
합성예
45] J-45의 합성
JJ-1 대신 JJ-9 (2.72 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 5와 동일한 과정을 수행하여 목적 화합물인 J-45 (3.17 g, 수율 60%)를 얻었다.
Mass (이론치: 789.94, 측정치: 789 g/mol)
[
합성예
46] J-46의 합성
JJ-1 대신 JJ-10 (2.72 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 1와 동일한 과정을 수행하여 목적 화합물인 J-46 (3.32 g, 수율 70%)을 얻었다.
Mass (이론치: 708.86, 측정치: 708 g/mol)
[
합성예
47] J-47의 합성
JJ-1 대신 JJ-10 (2.72 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 2과 동일한 과정을 수행하여 목적 화합물인 J-47 (2.66 g, 수율 54%)을 얻었다.
Mass (이론치: 736.88, 측정치: 736 g/mol)
[
합성예
48] J-48의 합성
JJ-1 대신 JJ-10 (2.72 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 3과 동일한 과정을 수행하여 목적 화합물인 J-48 (3.29 g, 수율 77%)을 얻었다.
Mass (이론치: 637.75, 측정치: 637 g/mol)
[
합성예
49] J-49의 합성
JJ-1 대신 JJ-10 (2.72 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 4와 동일한 과정을 수행하여 목적 화합물인 J-49(3.15 g, 수율 66%)을 얻었다.
Mass (이론치: 713.84, 측정치: 713 g/mol)
[
합성예
50] J-50의 합성
JJ-1 대신 JJ-10 (2.72 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 5와 동일한 과정을 수행하여 목적 화합물인 J-50(3.49 g, 수율 66%)을 얻었다.
Mass (이론치: 789.94, 측정치: 789 g/mol)
[
합성예
51] J-51의 합성
JJ-1 대신 JJ-11 (2.72 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 1과 동일한 과정을 수행하여 목적 화합물인 J-51(2.61 g, 수율 55%)을 얻었다.
Mass (이론치: 708.86, 측정치: 708 g/mol)
[
합성예
52] J-52의 합성
JJ-1 대신 JJ-11 (2.72 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 2과 동일한 과정을 수행하여 목적 화합물인 J-52(3.55 g, 수율 72%)을 얻었다.
Mass (이론치: 736.88, 측정치: 736 g/mol)
[
합성예
53] J-53의 합성
JJ-1 대신 JJ-11 (2.72 g, 6.7 mmol)을 사용하는 것을 제외하고는 합성예 3과 동일한 과정을 수행하여 목적 화합물인 J-53(2.99 g, 수율 70%)을 얻었다.
Mass (이론치: 637.75, 측정치: 637 g/mol)
[
합성예
54] J-54의 합성
JJ-1 대신 JJ-11 (2.72 g, 6.7 mmol)를 사용하는 것을 제외하고는 합성예 4과 동일한 과정을 수행하여 목적 화합물인 J-54(2.39 g, 수율 50%)을 얻었다.
Mass (이론치: 713.84, 측정치: 713 g/mol)
[
합성예
55] J-55의 합성
JJ-1 대신 JJ-11 (2.72 g, 6.7 mmol)를 사용하는 것을 제외하고는 합성예 5과 동일한 과정을 수행하여 목적 화합물인 J-55(3.33 g, 수율 63%)을 얻었다.
Mass (이론치: 789.94, 측정치: 789 g/mol)
[
합성예
56] J-56의 합성
JJ-1 대신 JJ-12 (2.72 g, 6.7 mmol)를 사용하는 것을 제외하고는 합성예 1와 동일한 과정을 수행하여 목적 화합물인 J-56(2.13 g, 수율 45%)을 얻었다.
Mass (이론치: 708.86, 측정치: 708 g/mol)
[
합성예
57] J-57의 합성
JJ-1 대신 JJ-12 (2.72 g, 6.7 mmol)를 사용하는 것을 제외하고는 합성예 2과 동일한 과정을 수행하여 목적 화합물인 J-57 (2.22 g, 수율 45%)을 얻었다.
Mass (이론치: 736.88, 측정치: 736 g/mol)
[
합성예
58] J-58의 합성
JJ-1 대신 JJ-12 (2.72 g, 6.7 mmol)를 사용하는 것을 제외하고는 합성예 3과 동일한 과정을 수행하여 목적 화합물인 J-58(2.22 g, 수율 52%)을 얻었다.
Mass (이론치: 637.75, 측정치: 637 g/mol)
[
합성예
59] J-59의 합성
JJ-1 대신 JJ-12 (2.72 g, 6.7 mmol)를 사용하는 것을 제외하고는 합성예 4와 동일한 과정을 수행하여 목적 화합물인 J-59 (2.10 g, 수율 44%)을 얻었다.
Mass (이론치: 713.84, 측정치: 713 g/mol)
[
합성예
60] J-60의 합성
JJ-1 대신 JJ-12 (2.72 g, 6.7 mmol)를 사용하는 것을 제외하고는 합성예 5과 동일한 과정을 수행하여 목적 화합물인 J-60 (2.06 g, 수율 39%)을 얻었다.
Mass (이론치: 789.94, 측정치: 789 g/mol)
[
실시예
1 ~ 60] 유기 EL 소자의 제작
하기 표 1에 나타낸 바와 같이, 상기 합성예에서 합성한 J1~J60의 화합물을 통상적으로 알려진 방법으로 고순도 승화정제를 한 후 아래의 과정에 따라 녹색 유기 EL 소자를 제작하였다.
먼저, ITO (Indium tin oxide)가 1500Å 두께로 박막 코팅된 유리 기판을 증류수 초음파로 세척하였다. 증류수 세척이 끝나면 이소프로필 알코올, 아세톤, 메탄올 등의 용제로 초음파 세척을 하고 건조시킨 후 UV OZONE 세정기 (Power sonic 405, 화신테크)로 이송시킨 다음 UV를 이용하여 상기 기판을 5분간 세정하고 진공 증착기로 기판을 이송하였다.
이렇게 준비된 ITO 투명 전극 위에 m-MTDATA (60 nm)/TCTA (80 nm)/ 90% 하기 표 1의 호스트 화합물 + 10 % Ir(ppy)3 (30nm)/BCP (10 nm)/Alq3 (30 nm)/LiF (1 nm)/Al (200 nm) 순으로 적층하여 유기 EL 소자를 제작하였다.
m-MTDATA, TCTA, Ir(ppy)3, CBP 및 BCP의 구조는 하기와 같다.
[
비교예
1] 유기 EL 소자의 제작
발광층 형성시 발광 호스트 물질로서 화합물 J-1 대신 CBP를 사용하는 것을 제외하고는 실시예 1과 동일한 과정으로 유기 EL 소자를 제작하였다.
[
평가예
]
실시예 1 ~ 60 및 비교예 1에서 제작한 각각의 유기 EL 소자에 대하여 전류밀도 10 mA/㎠에서의 구동전압, 전류효율 및 발광 피크를 측정하고, 그 결과를 하기 표 1에 나타내었다.
| 샘플 | 호스트 | 구동 전압(V) | EL 피크(nm) | 전류효율(cd/A) |
| 실시예 1 | J-1 | 6.71 | 518 | 38.9 |
| 실시예 2 | J-2 | 6.65 | 518 | 41.3 |
| 실시예 3 | J-3 | 6.71 | 517 | 41.3 |
| 실시예 4 | J-4 | 6.72 | 515 | 43.1 |
| 실시예 5 | J-5 | 6.72 | 515 | 43.5 |
| 실시예 6 | J-6 | 6.73 | 518 | 41.4 |
| 실시예 7 | J-7 | 6.73 | 518 | 42.2 |
| 실시예 8 | J-8 | 6.73 | 517 | 42 |
| 실시예 9 | J-9 | 6.48 | 515 | 41.5 |
| 실시예 10 | J-10 | 6.86 | 518 | 39.2 |
| 실시예 11 | J-11 | 6.77 | 518 | 41.3 |
| 실시예 12 | J-12 | 6.66 | 517 | 39.7 |
| 실시예 13 | J-13 | 6.65 | 518 | 38.9 |
| 실시예 14 | J-14 | 6.65 | 517 | 41.3 |
| 실시예 15 | J-15 | 6.64 | 515 | 41.3 |
| 실시예 16 | J-16 | 6.64 | 518 | 41.3 |
| 실시예 17 | J-17 | 6.64 | 518 | 41.2 |
| 실시예 18 | J-18 | 6.63 | 517 | 41.2 |
| 실시예 19 | J-19 | 6.72 | 515 | 41.3 |
| 실시예 20 | J-20 | 6.73 | 517 | 41.3 |
| 실시예 21 | J-21 | 6.73 | 515 | 41.3 |
| 실시예 22 | J-22 | 6.73 | 518 | 41.2 |
| 실시예 23 | J-23 | 6.48 | 518 | 41.2 |
| 실시예 24 | J-24 | 6.86 | 517 | 41.4 |
| 실시예 25 | J-25 | 6.77 | 515 | 42.2 |
| 실시예 26 | J-26 | 6.66 | 515 | 42 |
| 실시예 27 | J-27 | 6.77 | 515 | 41.8 |
| 실시예 28 | J-28 | 6.66 | 518 | 42 |
| 실시예 29 | J-29 | 6.66 | 518 | 42.5 |
| 실시예 30 | J-30 | 6.81 | 517 | 41.3 |
| 실시예 31 | J-31 | 6.66 | 515 | 41.3 |
| 실시예 32 | J-32 | 6.81 | 518 | 41.2 |
| 실시예 33 | J-33 | 6.68 | 518 | 41.3 |
| 실시예 34 | J-34 | 6.66 | 518 | 39.7 |
| 실시예 35 | J-35 | 6.7 | 517 | 38.9 |
| 실시예 36 | J-36 | 6.7 | 515 | 41.3 |
| 실시예 37 | J-37 | 6.51 | 518 | 41.3 |
| 실시예 38 | J-38 | 6.77 | 518 | 43.1 |
| 실시예 39 | J-39 | 6.46 | 517 | 43.5 |
| 실시예 40 | J-40 | 6.81 | 515 | 41.4 |
| 실시예 41 | J-41 | 6.68 | 517 | 42.2 |
| 실시예 42 | J-42 | 6.66 | 515 | 42 |
| 실시예 43 | J-43 | 6.48 | 518 | 41.2 |
| 실시예 44 | J-44 | 6.86 | 518 | 41.2 |
| 실시예 45 | J-45 | 6.77 | 517 | 41.4 |
| 실시예 46 | J-46 | 6.66 | 515 | 42.2 |
| 실시예 47 | J-47 | 6.81 | 515 | 39.7 |
| 실시예 48 | J-48 | 6.68 | 518 | 38.9 |
| 실시예 49 | J-49 | 6.66 | 518 | 41.3 |
| 실시예 50 | J-50 | 6.7 | 517 | 41.3 |
| 실시예 51 | J-51 | 6.7 | 515 | 43.1 |
| 실시예 52 | J-52 | 6.51 | 518 | 43.5 |
| 실시예 53 | J-53 | 6.77 | 518 | 41.4 |
| 실시예 54 | J-54 | 6.46 | 518 | 42.2 |
| 실시예 55 | J-55 | 6.81 | 517 | 42 |
| 실시예 56 | J-56 | 6.68 | 515 | 41.8 |
| 실시예 57 | J-57 | 6.66 | 515 | 41.3 |
| 실시예 58 | J-58 | 6.48 | 518 | 41.2 |
| 실시예 59 | J-59 | 6.66 | 518 | 41.3 |
| 실시예 60 | J-60 | 6.81 | 517 | 39.7 |
| 비교예 1 | CBP | 6.93 | 516 | 38.2 |
상기 표 1에 나타낸 바와 같이, 본 발명에 따른 화합물(J-1 ~ J-60)을 녹색 유기 EL 소자의 발광층으로 사용하였을 경우(실시예 1-60) 종래 CBP를 사용한 녹색 유기 EL 소자(비교예1)와 비교해 볼 때, 효율 및 구동전압 면에서 우수한 성능을 나타내는 것을 알 수 있다.
본 발명은 신규한 유기 발광 화합물 및 이를 이용한 유기 전계 발광 소자에 관한 것으로, 보다 상세하게는 정공 주입 및 수송능과 발광능 등이 우수한 신규한 아제핀계 화합물 및 이를 하나 이상의 유기물층에 포함함으로써 낮은 구동 전압과, 높은 발광 효율 및 향상된 수명 특성을 갖는 유기 전계 발광 소자에 관한 것이다.
Claims (18)
- 하기 화학식 1로 표시되는 화합물:[화학식 1]상기 화학식 1에서,R1과 R2, R2과 R3, R3과 R4, R5와 R6, R6과 R7 및 R7과 R8, R9과 R10, R10과 R11 및 R11과 R12 중 적어도 하나는 하기 화학식 2로 표시되는 고리와 결합하여 축합 고리를 형성하고;하기 화학식 2로 표시되는 고리와 축합을 형성하지 않는 R1 내지 R12는 각각 독립적으로 수소, 중수소, 할로겐, 시아노기, 니트로기, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되거나, 인접하는 기와 결합하여 축합 고리를 형성하며;Ar1은 C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되며;상기 R1 내지 R12 및 Ar1의 알킬기, 시클로알킬기, 헤테로시클로알킬기, 아릴기, 헤테로아릴기, 알킬옥시기, 아릴옥시기, 알킬실릴기, 아릴실릴기, 알킬보론기, 아릴보론기, 아릴포스핀기, 모노 또는 디아릴포스피닐기 및 아릴아민기는 각각 독립적으로, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기,C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택된 1종 이상으로 치환되거나 비치환되고, 복수 개의 치환기로 치환되는 경우 이들은 서로 동일하거나 상이하며;[화학식 2]상기 화학식 2에서,점선은 상기 화학식 1과 축합이 이루어지는 부분이고;X1 및 X2는 각각 독립적으로 단일결합, O, S, N(Ar2), C(Ar3)(Ar4) 및 Si(Ar5)(Ar6)으로 구성된 군으로부터 선택되나, 상기 X1 및 X2가 모두 단일결합은 아니며;Y1 내지 Y4은 각각 독립적으로 N 또는 C(R13)이며;R13이 복수 개인 경우 이들은 서로 동일하거나 상이하며, 상기 R13은 수소, 중수소, 할로겐, 시아노기, 니트로기, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되거나, 인접하는 기와 결합하여 축합 고리를 형성하며;Ar2 내지 Ar6는 각각 독립적으로 C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~6C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되며;상기 R13 및 Ar2 내지 Ar6의 알킬기, 시클로알킬기, 헤테로시클로알킬기, 아릴기, 헤테로아릴기, 알킬옥시기, 아릴옥시기, 알킬실릴기, 아릴실릴기, 알킬보론기, 아릴보론기, 아릴포스핀기, 모노 또는 디아릴포스피닐기 및 아릴아민기는 각각 독립적으로, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택된 1종 이상으로 치환되거나 비치환되고, 복수 개의 치환기로 치환되는 경우 이들은 서로 동일하거나 상이하다.
- 제1항에 있어서,상기 X1 및 X2 중 적어도 하나는 N(Ar2)인 것을 특징으로 하는 화합물.
- 제1항에 있어서,상기 Y1 내지 Y4 모두가 C(R13)이거나 상기 Y1 내지 Y4 중 적어도 한 개가 N인 것을 특징으로 하는 화합물.
- 제1항에 있어서,상기 화학식 1로 표시되는 화합물은 하기 화학식 8 내지 화학식 10 중 어느 하나로 표시되는 화합물인 것을 특징으로 하는 화합물:[화학식 8][화학식 9][화학식 10]상기 화학식 8 내지 화학식 10에 있어서,R2와 R3, R3과 R4, R5와 R6, R6과 R7 및 R7과 R8, R9과 R10, R10과 R11, R11과 R12 및 R15와 R16 중 적어도 하나는 하기 화학식 2로 표시되는 고리와 축합되어 축합 고리를 형성하고;하기 화학식 2로 표시되는 고리와 축합을 형성하지 않는 R2 내지 R12 및 R15 내지 R16는 각각 독립적으로 수소, 중수소, 할로겐, 시아노기, 니트로기, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되거나, 인접하는 기와 결합하여 축합 고리를 형성하며;X3은 O, S, N(Ar7), C(Ar8)(Ar9) 및 Si(Ar10)(Ar11)으로 구성된 군으로부터 선택되고, 바람직하게는 N(Ar7)이며;Ar7 내지 Ar11은 각각 독립적으로 C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~6C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되며;n은 0 내지 4의 정수이며;R14는 수소, 중수소, 할로겐, 시아노기, 니트로기, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되거나, 인접하는 기와 결합하여 축합 고리를 형성하고, 상기 R14가 복수 개인 경우 이들은 서로 동일하거나 상이하며;상기 Ar7 내지 Ar11, R2 내지 R12 및 R14 내지 R16의 알킬기, 시클로알킬기, 헤테로시클로알킬기, 아릴기, 헤테로아릴기, 알킬옥시기, 아릴옥시기, 알킬실릴기, 아릴실릴기, 알킬보론기, 아릴보론기, 아릴포스핀기, 모노 또는 디아릴포스피닐기 및 아릴아민기는 각각 독립적으로, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택된 1종 이상으로 치환되거나 비치환되고, 복수 개의 치환기로 치환되는 경우 이들은 서로 동일하거나 상이하며;[화학식 2]상기 화학식 2에서,점선은 상기 화학식 8 내지 10 중 어느 하나와 축합이 이루어지는 부분이고;X1, X2 및 Y1 내지 Y4 각각은 제1항에서 정의된 바와 같다.
- 제5항에 있어서,상기 화학식 8 내지 화학식 10 중 어느 하나로 표시되는 화합물은 하기 화학식 C-1 내지 화학식 C-12 중 어느 하나로 표시되는 것을 특징으로 하는 화합물:상기 화학식 C-1 내지 화학식 C-12에서,R2 내지 R12 및 R15 내지 R16는 각각 독립적으로 수소, 중수소, 할로겐, 시아노기, 니트로기, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되거나, 인접하는 기와 결합하여 축합 고리를 형성하고;n은 0 내지 4의 정수이며;R14는 중수소, 할로겐, 시아노기, 니트로기, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되거나, 인접하는 기와 결합하여 축합 고리를 형성하고, 상기 R14가 복수 개인 경우 이들은 서로 동일하거나 상이하며;X1 및 X2는 각각 독립적으로 단일결합, O, S, N(Ar2), C(Ar3)(Ar4) 및 Si(Ar5)(Ar6)으로 구성된 군으로부터 선택되나, X1 및 X2가 모두 단일결합은 아니며;X3은 O, S, N(Ar7), C(Ar8)(Ar9) 및 Si(Ar10)(Ar11)으로 구성된 군으로부터 선택되며;Ar2 내지 Ar11은 각각 독립적으로 C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되고, 상기 Ar2 내지 Ar6 각각이 복수 개인 경우 이들은 서로 동일하거나 상이하며;Y1 내지 Y4은 각각 독립적으로 N 또는 C(R13)이며;R13이 복수 개인 경우 이들은 서로 동일하거나 상이하며, 상기 R13은 수소, 중수소, 할로겐, 시아노기, 니트로기, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되거나, 인접하는 기와 결합하여 축합 고리를 형성하며;Ar2 내지 Ar11 및 R2 내지 R16의 알킬기, 시클로알킬기, 헤테로시클로알킬기, 아릴기, 헤테로아릴기, 알킬옥시기, 아릴옥시기, 알킬실릴기, 아릴실릴기, 알킬보론기, 아릴보론기, 아릴포스핀기, 모노 또는 디아릴포스피닐기 및 아릴아민기는 각각 독립적으로, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C1~C40의 알킬옥시기, C6~C60의 아릴옥시기, C1~C40의 알킬실릴기, C6~C60의 아릴실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택된 1종 이상으로 치환되거나 비치환되고, 복수 개의 치환기로 치환되는 경우 이들은 서로 동일하거나 상이할 수 있다.
- 제1항에 있어서,R1 내지 R12 및 Ar1 내지 Ar6 중 적어도 하나는 C1~C40의 알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되며,상기 R1 내지 R12 및 Ar1 내지 Ar6의 알킬기, 아릴기, 헤테로아릴기, 아릴아민기는 각각 독립적으로, 중수소, 할로겐, 시아노기, C1~C40의 알킬기, C6~C60의 아릴기, 핵원자수 5 내지 60개의 헤테로아릴기, C6~C60의 아릴아민기로 이루어진 군에서 선택된 1종 이상으로 치환되거나 비치환되고, 복수 개의 치환기로 치환되는 경우 이들은 서로 동일하거나 상이한 것을 특징으로 하는 화합물.
- 제1항에 있어서,R1 내지 R12 및 Ar1 내지 Ar6 중 적어도 하나는 페닐기 또는 하기 화학식 11으로 표시되는 치환기인 것을 특징으로 하는 화합물:[화학식 11]상기 화학식 11에서,*는 상기 화학식 1에 결합되는 부분을 의미하고;L1은 단일결합, C6~C18의 아릴렌기 및 핵원자수 5 내지 18개의 헤테로아릴렌기로 이루어진 군에서 선택되며;Z1 내지 Z5는 서로 동일하거나 상이하고, 각각 독립적으로 N 또는 C(R17)이되, 상기 Z1 내지 Z5 중 적어도 하나는 N이며;R17이 복수 개인 경우 이들은 서로 동일하거나 상이하며, 상기 R17은 수소, 중수소, 할로겐, 시아노기, 니트로기, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C6~C60의 아릴기, 핵원자수 5 내지 40개의 헤테로아릴기, C6~C60의 아릴옥시기 C1~C40의 알킬옥시기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C40의 아릴아민기, C1~C40의 알킬실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C40의 아릴실릴기로 이루어진 군에서 선택되거나, 인접하는 기와 결합하여 축합 고리를 형성하며;상기 R17의 알킬기, 알케닐기, 알키닐기, 아릴기, 헤테로아릴기, 아릴옥시기, 알킬옥시기, 시클로알킬기, 헤테로시클로알킬기, 아릴아민기, 알킬실릴기, 알킬보론기, 아릴보론기, 아릴포스핀기, 모노 또는 디아릴포스피닐기 및 아릴실릴기는 각각 독립적으로 중수소, 할로겐, 시아노기, 니트로기, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C6~C60의 아릴기, 핵원자수 5 내지 40개의 헤테로아릴기, C6~C60의 아릴옥시기, C1~C40의 알킬옥시기, C6~C40의 아릴아민기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C1~C40의 알킬실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴실릴기로 이루어진 군에서 선택된 1종 이상으로 치환되거나 비치환되고, 복수 개의 치환기로 치환되는 경우, 이들은 서로 동일하거나 상이하다.
- 제8항에 있어서,상기 화학식 11로 표시되는 치환기는 하기 화학식 A-1 내지 화학식 A-15 중 어느 하나로 표시되는 치환기인 것을 특징으로 하는 화합물:상기 화학식 A-1 내지 화학식 A-15에서,*는 상기 화학식 1에 결합되는 부분을 의미하고;m은 0 내지 4의 정수로서, 상기 m이 0인 경우, 수소가 치환기 R18로 치환되지 않는 것을 의미하고, 상기 m이 1 내지 4의 정수인 경우, R18은 중수소, 할로겐, 시아노기, 니트로기, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C6~C60의 아릴기, 핵원자수 5 내지 40개의 헤테로아릴기, C6~C60의 아릴옥시기 C1~C40의 알킬옥시기, C6~C60의 아릴아민기, C1~C40의 알킬실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴실릴기로 이루어진 군에서 선택되거나, 인접하는 기와 결합하여 축합 고리를 형성하고, 상기 R18이 복수 개인 경우 이들은 서로 동일하거나 상이하며;상기 R18의 알킬기, 알케닐기, 알키닐기, 시클로알킬기, 헤테로시클로알킬기, 아릴기, 헤테로아릴기, 아릴옥시기, 알킬옥시기, 아릴아민기, 알킬실릴기, 알킬보론기, 아릴보론기, 아릴포스핀기, 모노 또는 디아릴포스피닐기 및 아릴실릴기는 각각 독립적으로 중수소, 할로겐, 시아노기, 니트로기, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C6~C40의 아릴기, 핵원자수 5 내지 40개의 헤테로아릴기, C6~C60의 아릴옥시기, C1~C40의 알킬옥시기, C6~C60의 아릴아민기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C1~C40의 알킬실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C60의 아릴실릴기로 이루어진 군에서 선택된 1종 이상으로 치환되거나 비치환되고, 복수 개의 치환기로 치환되는 경우, 이들은 서로 동일하거나 상이하다.
- 제8항에 있어서,L1은 단일결합, 페닐렌기, 비페닐렌기, 또는 카바졸릴기인 것을 특징으로 하는 화합물.
- 제1항에 있어서,R1 내지 R12 및 Ar1 내지 Ar6 중 적어도 하나는 하기 화학식 12로 표시되는 치환기인 것을 특징으로 하는 화합물:[화학식 12]상기 화학식 12에서,*는 상기 화학식 1에 결합되는 부분을 의미하고;L2은 단일결합, C6~C18의 아릴렌기 및 핵원자수 5 내지 18개의 헤테로아릴렌기로 이루어진 군에서 선택되며;R19 및 R20는 각각 독립적으로 C1~C40의 알킬기, C6~C40의 아릴기, 핵원자수 5 내지 40의 헤테로아릴기 및 C6~C60의 아릴아민기로 이루어진 군에서 선택되거나, 상기 R19 및 R20가 서로 결합하여 축합 고리를 형성할 수 있으며;상기 R19 및 R20의 알킬기, 아릴기, 헤테로아릴기 및 아릴아민기는 각각 독립적으로 중수소, 할로겐, 시아노기, 니트로기, C1~C40의 알킬기, C2~C40의 알케닐기, C2~C40의 알키닐기, C6~C60의 아릴기, 핵원자수 5 내지 40개의 헤테로아릴기, C6~C60의 아릴옥시기, C1~C40의 알킬옥시기, C6~C60의 아릴아민기, C3~C40의 시클로알킬기, 핵원자수 3 내지 40개의 헤테로시클로알킬기, C1~C40의 알킬실릴기, C1~C40의 알킬보론기, C6~C60의 아릴보론기, C6~C60의 아릴포스핀기, C6~C60의 모노 또는 디아릴포스피닐기 및 C6~C40의 아릴실릴기로 이루어진 군에서 선택된 1종 이상으로 치환되거나 비치환되고, 복수 개의 치환기로 치환되는 경우, 이들은 서로 동일하거나 상이하다.
- 제11항에 있어서,L2는 단일결합, 페닐렌기, 비페닐렌기, 또는 카바졸릴기인 것을 특징으로 하는 화합물.
- (i) 양극, (ii) 음극, 및 (iii) 상기 양극과 음극 사이에 개재(介在)된 1층 이상의 유기물층을 포함하는 유기 전계 발광 소자로서,상기 1층 이상의 유기물층 중에서 적어도 하나는 제1항 내지 13항 중 어느 한 항에 기재된 화학식 1로 표시되는 화합물을 포함하는 것을 특징으로 하는 유기 전계 발광 소자.
- 제13항에 있어서,상기 화학식 1로 표시되는 화합물을 포함하는 유기물층은 발광층, 발광 보조층, 정공 수송층, 정공 주입층, 전자 수송층 및 전자 주입층으로 이루어진 군에서 선택되는 유기 전계 발광 소자.
- 제15항에 있어서,상기 화학식 1로 표시되는 화합물을 포함하는 유기물층은 발광층, 정공 수송층 및 전자 수송층으로 이루어진 군에서 선택되는 유기 전계 발광 소자.
- 제16항에 있어서,상기 화학식 1로 표시되는 화합물을 포함하는 유기물층은 발광층인 것을 특징으로 하는 유기 전계 발광 소자.
- 제17항에 있어서,상기 화학식 1로 표시되는 화합물은 발광층의 인광 호스트로 사용되는 것을 특징으로 하는 유기 전계 발광 소자.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR10-2014-0190737 | 2014-12-26 | ||
| KR20140190737 | 2014-12-26 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| WO2016105165A2 true WO2016105165A2 (ko) | 2016-06-30 |
| WO2016105165A3 WO2016105165A3 (ko) | 2016-11-03 |
Family
ID=56151599
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/KR2015/014271 WO2016105165A2 (ko) | 2014-12-26 | 2015-12-24 | 유기 발광 화합물 및 이를 이용한 유기 전계 발광 소자 |
Country Status (2)
| Country | Link |
|---|---|
| KR (1) | KR102643971B1 (ko) |
| WO (1) | WO2016105165A2 (ko) |
Cited By (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN107922424A (zh) * | 2015-09-10 | 2018-04-17 | 罗门哈斯电子材料韩国有限公司 | 有机电致发光化合物和包含所述化合物的有机电致发光装置 |
| US20180134706A1 (en) * | 2016-11-17 | 2018-05-17 | Samsung Display Co., Ltd. | Heterocyclic compound and organic electroluminescence device including the same |
| WO2018110930A1 (en) * | 2016-12-14 | 2018-06-21 | Rohm And Haas Electronic Materials Korea Ltd. | Organic electroluminescent compound and organic electroluminescent device comprising the same |
| CN108864108A (zh) * | 2018-06-28 | 2018-11-23 | 宁波卢米蓝新材料有限公司 | 一种稠环化合物及其制备方法和用途 |
| CN108997347A (zh) * | 2018-06-28 | 2018-12-14 | 宁波卢米蓝新材料有限公司 | 一种稠环化合物及其制备方法和用途 |
| CN110023301A (zh) * | 2016-12-14 | 2019-07-16 | 罗门哈斯电子材料韩国有限公司 | 有机电致发光化合物和包含其的有机电致发光装置 |
| JP2019529340A (ja) * | 2016-07-27 | 2019-10-17 | ローム・アンド・ハース・エレクトロニック・マテリアルズ・コリア・リミテッド | 有機電界発光化合物およびそれを含む有機電界発光デバイス |
| CN111018855A (zh) * | 2019-12-27 | 2020-04-17 | 烟台显华化工科技有限公司 | 一类有机化合物及其应用 |
| CN111072677A (zh) * | 2019-12-27 | 2020-04-28 | 烟台显华化工科技有限公司 | 一类有机化合物及其应用 |
| JP2020527125A (ja) * | 2018-06-28 | 2020-09-03 | 寧波盧米藍新材料有限公司 | 縮合環化合物及びその製造方法と用途 |
| CN112430239A (zh) * | 2019-08-26 | 2021-03-02 | 广州华睿光电材料有限公司 | 基于七元环结构的化合物、高聚物、混合物、组合物及有机电子器件 |
| CN113272307A (zh) * | 2019-08-16 | 2021-08-17 | 株式会社Lg化学 | 新型化合物及利用其的有机发光器件 |
| CN113929691A (zh) * | 2021-11-22 | 2022-01-14 | 烟台九目化学股份有限公司 | 一种含氧杂卓并咔唑结构化合物及其应用 |
| CN115298185A (zh) * | 2020-04-16 | 2022-11-04 | 株式会社Lg化学 | 杂环化合物和包含其的有机发光元件 |
| US11706977B2 (en) | 2018-01-11 | 2023-07-18 | Samsung Electronics Co., Ltd. | Heterocyclic compound, composition including the same, and organic light-emitting device including the heterocyclic compound |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20200117591A (ko) * | 2019-04-05 | 2020-10-14 | 덕산네오룩스 주식회사 | 유기전기 소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| WO2020262865A1 (ko) * | 2019-06-24 | 2020-12-30 | 덕산네오룩스 주식회사 | 유기전기 소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| KR20220099373A (ko) * | 2021-01-06 | 2022-07-13 | 주식회사 센텀머티리얼즈 | 신규한 헤테로고리 화합물 및 이를 포함하는 유기 발광 소자 |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP4404473B2 (ja) * | 2000-12-25 | 2010-01-27 | 富士フイルム株式会社 | 新規含窒素へテロ環化合物、発光素子材料およびそれらを使用した発光素子 |
| JP2002235075A (ja) * | 2001-02-09 | 2002-08-23 | Fuji Photo Film Co Ltd | アゼピン誘導体、発光素子材料及び発光素子 |
| JP2005243394A (ja) * | 2004-02-26 | 2005-09-08 | Fuji Photo Film Co Ltd | 有機電界発光素子 |
| KR20110008619A (ko) * | 2009-07-20 | 2011-01-27 | 다우어드밴스드디스플레이머티리얼 유한회사 | 신규한 유기 발광 화합물 및 이를 채용하고 있는 유기 전계 발광 소자 |
| KR20110098293A (ko) * | 2010-02-26 | 2011-09-01 | 다우어드밴스드디스플레이머티리얼 유한회사 | 신규한 유기 발광 화합물 및 이를 포함하는 유기 발광 소자 |
| KR20120081539A (ko) * | 2011-01-11 | 2012-07-19 | (주)씨에스엘쏠라 | 유기발광화합물 및 이를 이용한 유기 광소자 |
-
2015
- 2015-12-24 WO PCT/KR2015/014271 patent/WO2016105165A2/ko active Application Filing
- 2015-12-24 KR KR1020150186353A patent/KR102643971B1/ko active IP Right Grant
Cited By (26)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN107922424A (zh) * | 2015-09-10 | 2018-04-17 | 罗门哈斯电子材料韩国有限公司 | 有机电致发光化合物和包含所述化合物的有机电致发光装置 |
| US20180223184A1 (en) * | 2015-09-10 | 2018-08-09 | Rohm And Haas Electronic Materials Korea Ltd. | Organic electroluminescent compounds and organic electroluminescent device comprising the same |
| TWI709250B (zh) * | 2015-09-10 | 2020-11-01 | 南韓商羅門哈斯電子材料韓國公司 | 有機電致發光化合物及包括其之有機電致發光裝置 |
| JP2019529340A (ja) * | 2016-07-27 | 2019-10-17 | ローム・アンド・ハース・エレクトロニック・マテリアルズ・コリア・リミテッド | 有機電界発光化合物およびそれを含む有機電界発光デバイス |
| US20180134706A1 (en) * | 2016-11-17 | 2018-05-17 | Samsung Display Co., Ltd. | Heterocyclic compound and organic electroluminescence device including the same |
| US10844059B2 (en) * | 2016-11-17 | 2020-11-24 | Samsung Display Co., Ltd. | Heterocyclic compound and organic electroluminescence device including the same |
| WO2018110930A1 (en) * | 2016-12-14 | 2018-06-21 | Rohm And Haas Electronic Materials Korea Ltd. | Organic electroluminescent compound and organic electroluminescent device comprising the same |
| CN110023301B (zh) * | 2016-12-14 | 2023-04-18 | 罗门哈斯电子材料韩国有限公司 | 有机电致发光化合物和包含其的有机电致发光装置 |
| CN110023301A (zh) * | 2016-12-14 | 2019-07-16 | 罗门哈斯电子材料韩国有限公司 | 有机电致发光化合物和包含其的有机电致发光装置 |
| US10629824B2 (en) | 2016-12-14 | 2020-04-21 | Rohm And Haas Electronic Materials Korea Ltd | Organic electroluminescent compound and organic electroluminescent device comprising the same |
| US11706977B2 (en) | 2018-01-11 | 2023-07-18 | Samsung Electronics Co., Ltd. | Heterocyclic compound, composition including the same, and organic light-emitting device including the heterocyclic compound |
| JP2020527126A (ja) * | 2018-06-28 | 2020-09-03 | 寧波盧米藍新材料有限公司 | 縮合環化合物及びその製造方法と用途 |
| CN108864108B (zh) * | 2018-06-28 | 2021-07-06 | 宁波卢米蓝新材料有限公司 | 一种稠环化合物及其制备方法和用途 |
| JP2020527125A (ja) * | 2018-06-28 | 2020-09-03 | 寧波盧米藍新材料有限公司 | 縮合環化合物及びその製造方法と用途 |
| CN108864108A (zh) * | 2018-06-28 | 2018-11-23 | 宁波卢米蓝新材料有限公司 | 一种稠环化合物及其制备方法和用途 |
| WO2020000826A1 (zh) * | 2018-06-28 | 2020-01-02 | 宁波卢米蓝新材料有限公司 | 一种稠环化合物及其制备方法和用途 |
| CN108997347A (zh) * | 2018-06-28 | 2018-12-14 | 宁波卢米蓝新材料有限公司 | 一种稠环化合物及其制备方法和用途 |
| CN113272307A (zh) * | 2019-08-16 | 2021-08-17 | 株式会社Lg化学 | 新型化合物及利用其的有机发光器件 |
| CN113272307B (zh) * | 2019-08-16 | 2023-12-19 | 株式会社Lg化学 | 化合物及利用其的有机发光器件 |
| CN112430239B (zh) * | 2019-08-26 | 2022-03-22 | 广州华睿光电材料有限公司 | 基于七元环结构的化合物、高聚物、混合物、组合物及有机电子器件 |
| CN112430239A (zh) * | 2019-08-26 | 2021-03-02 | 广州华睿光电材料有限公司 | 基于七元环结构的化合物、高聚物、混合物、组合物及有机电子器件 |
| CN111072677A (zh) * | 2019-12-27 | 2020-04-28 | 烟台显华化工科技有限公司 | 一类有机化合物及其应用 |
| CN111018855A (zh) * | 2019-12-27 | 2020-04-17 | 烟台显华化工科技有限公司 | 一类有机化合物及其应用 |
| CN115298185A (zh) * | 2020-04-16 | 2022-11-04 | 株式会社Lg化学 | 杂环化合物和包含其的有机发光元件 |
| CN113929691A (zh) * | 2021-11-22 | 2022-01-14 | 烟台九目化学股份有限公司 | 一种含氧杂卓并咔唑结构化合物及其应用 |
| CN113929691B (zh) * | 2021-11-22 | 2024-02-02 | 烟台九目化学股份有限公司 | 一种含氧杂卓并咔唑结构化合物及其应用 |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2016105165A3 (ko) | 2016-11-03 |
| KR20160079715A (ko) | 2016-07-06 |
| KR102643971B1 (ko) | 2024-03-07 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| WO2016105165A2 (ko) | 유기 발광 화합물 및 이를 이용한 유기 전계 발광 소자 | |
| WO2017188597A1 (ko) | 유기 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| WO2016089080A1 (ko) | 유기 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| WO2018110958A1 (ko) | 유기 발광 화합물 및 이를 이용한 유기 전계 발광 소자 | |
| WO2015190718A1 (ko) | 유기 전계 발광 소자 | |
| WO2020159019A1 (ko) | 유기 발광 화합물 및 이를 이용한 유기 전계 발광 소자 | |
| WO2018038400A1 (ko) | 유기 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| WO2020209679A1 (ko) | 유기 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| WO2017111439A1 (ko) | 유기 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| WO2018216921A2 (ko) | 유기 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| WO2014010810A1 (ko) | 신규 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| WO2017111544A1 (ko) | 유기 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| WO2017209488A1 (ko) | 유기 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| WO2015133804A1 (ko) | 유기 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| WO2017188596A1 (ko) | 유기 발광 화합물 및 이를 이용한 유기 전계 발광 소자 | |
| WO2017023125A1 (ko) | 유기 발광 화합물 및 이를 이용한 유기 전계 발광 소자 | |
| WO2014092354A1 (ko) | 유기 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| WO2016105123A2 (ko) | 유기 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| WO2015111943A1 (ko) | 유기 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| WO2020027463A1 (ko) | 유기 화합물 및 이를 이용한 유기 전계 발광 소자 | |
| WO2017111389A1 (ko) | 유기 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| WO2016122178A9 (ko) | 유기 발광 화합물 및 이를 이용한 유기 전계 발광 소자 | |
| WO2018186551A1 (ko) | 유기 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| WO2018117493A1 (ko) | 유기 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| WO2021010631A1 (ko) | 헤테로고리 화합물 및 이를 포함하는 유기 발광 소자 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 15873692 Country of ref document: EP Kind code of ref document: A2 |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| 32PN | Ep: public notification in the ep bulletin as address of the adressee cannot be established |
Free format text: NOTING OF LOSS OF RIGHTS PURSUANT TO RULE 112(1) EPC , EPO FORM 1205A DATED 02.10.2017 |
|
| 122 | Ep: pct application non-entry in european phase |
Ref document number: 15873692 Country of ref document: EP Kind code of ref document: A2 |