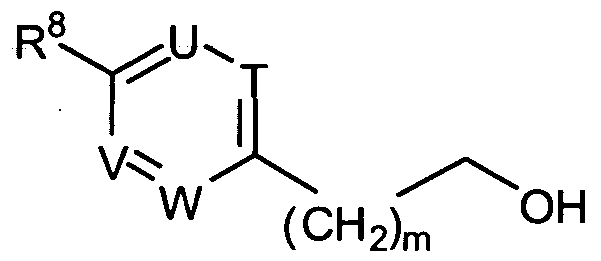
Neue Vanilloid-Rezeptor Liganden und ihre Verwendung zur Herstellung von
Arzneimitteln
Die vorliegende Erfindung betrifft neue Vanilloid-Rezeptor-Liganden, Verfahren zu ihrer Herstellung, Arzneimittel enthaltend diese Verbindungen und die Verwendung dieser Verbindungen zur Herstellung von Arzneimitteln.
Die Behandlung von Schmerz, insbesondere von neuropathischem Schmerz, hat in der Medizin große Bedeutung. Es besteht ein weltweiter Bedarf an wirksamen Schmerztherapien. Der dringende Handlungsbedarf für eine patientengerechte und zielorientierte Behandlung chronischer und nicht chronischer Schmerzzustände, wobei hierunter die erfolgreiche und zufriedenstellende Schmerzbehandlung für den Patienten zu verstehen ist, dokumentiert sich auch in der großen Anzahl von wissenschaftlichen Arbeiten, die auf dem Gebiet der angewandten Analgetik bzw. der Grundlagenforschung zur Nociception in letzter Zeit erschienen sind.
Ein geeigneter Ansatzpunkt zur Behandlung von Schmerz; insbesondere von Schmerz ausgewählt aus der Gruppe bestehend aus akutem Schmerz, chronischem Schmerz, neuropathischem Schmerz und visceralem Schmerz, besonders bevorzugt von neuropathischem Schmerz; stellt der Vanilloid-Rezeptor vom Subtyp 1 (VR1/TRPV1 ) dar, der häufig auch als Capsaicin-Rezeptor bezeichnet wird. Dieser Rezeptor wird u.a. durch Vanilloide wie z.B. Capsaicin, Hitze und Protonen stimuliert und spielt eine zentrale Rolle bei der Schmerzentstehung. Darüber hinaus ist er für eine Vielzahl weiterer physiologischer und pathophysiologischer Prozesse von Bedeutung wie beispielsweise Migräne; Depressionen; neurodegenerativen Erkrankungen; kognitiven Erkrankungen; Angstzuständen; Epilepsie; Husten; Diarrhöe; Pruritus; Entzündungen; Störungen des kardiovaskulären Systems; Störungen der Nahrungsaufnahme; Medikamentenabhängigkeit; Medikamentenmißbrauch und insbesondere Harninkontinenz.
Eine Aufgabe der vorliegenden Erfindung bestand daher darin, neue Verbindungen zur Verfügung zu stellen, die sich insbesondere als pharmakologische Wirkstoffe in Arzneimitteln eignen, vorzugsweise in Arzneimitteln zur Behandlung von Störungen
BESTÄTIGUNGSKOPIE
oder Krankheiten, die zumindest teilweise durch Vanilloid-Rezeptoren 1 (VR1/TRPV1 -Rezeptoren) vermittelt werden.
Überraschenderweise wurde nun gefunden, dass die substituierten Verbindungen der nachstehend angegebenen allgemeinen Formel I eine ausgezeichnete Affinität zum Vanilloid-Rezeptor vom Subtyp 1 (VR1/TRPV1 -Rezeptor) aufweisen und sich daher insbesondere zur Prophylaxe und/oder Behandlung von Störungen oder Krankheiten eignen, die zumindest teilweise durch Vanilloid-Rezeptoren 1 (VR1/TRPV1) vermittelt werden. Ebenfalls verfügen die substituierten Verbindungen der nachstehend angegebenen allgemeinen Formel I über eine antientzündliche Aktivität.
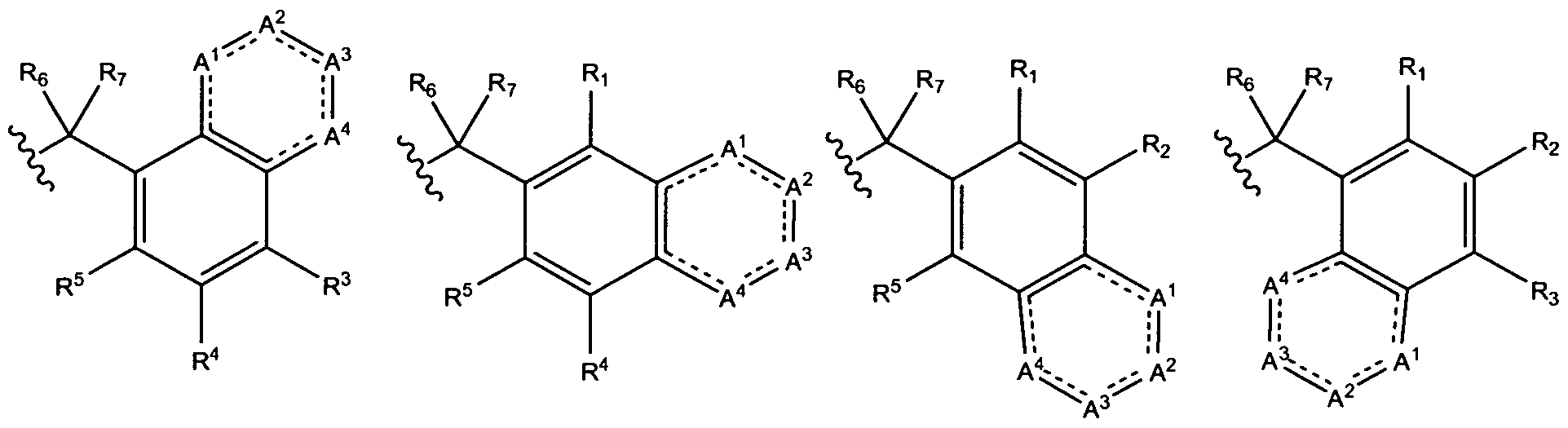
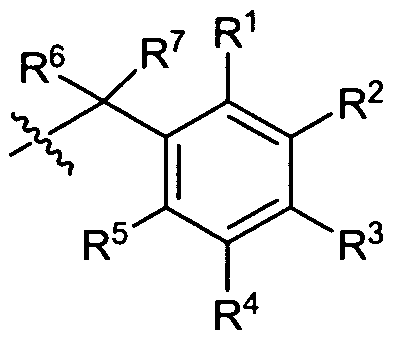
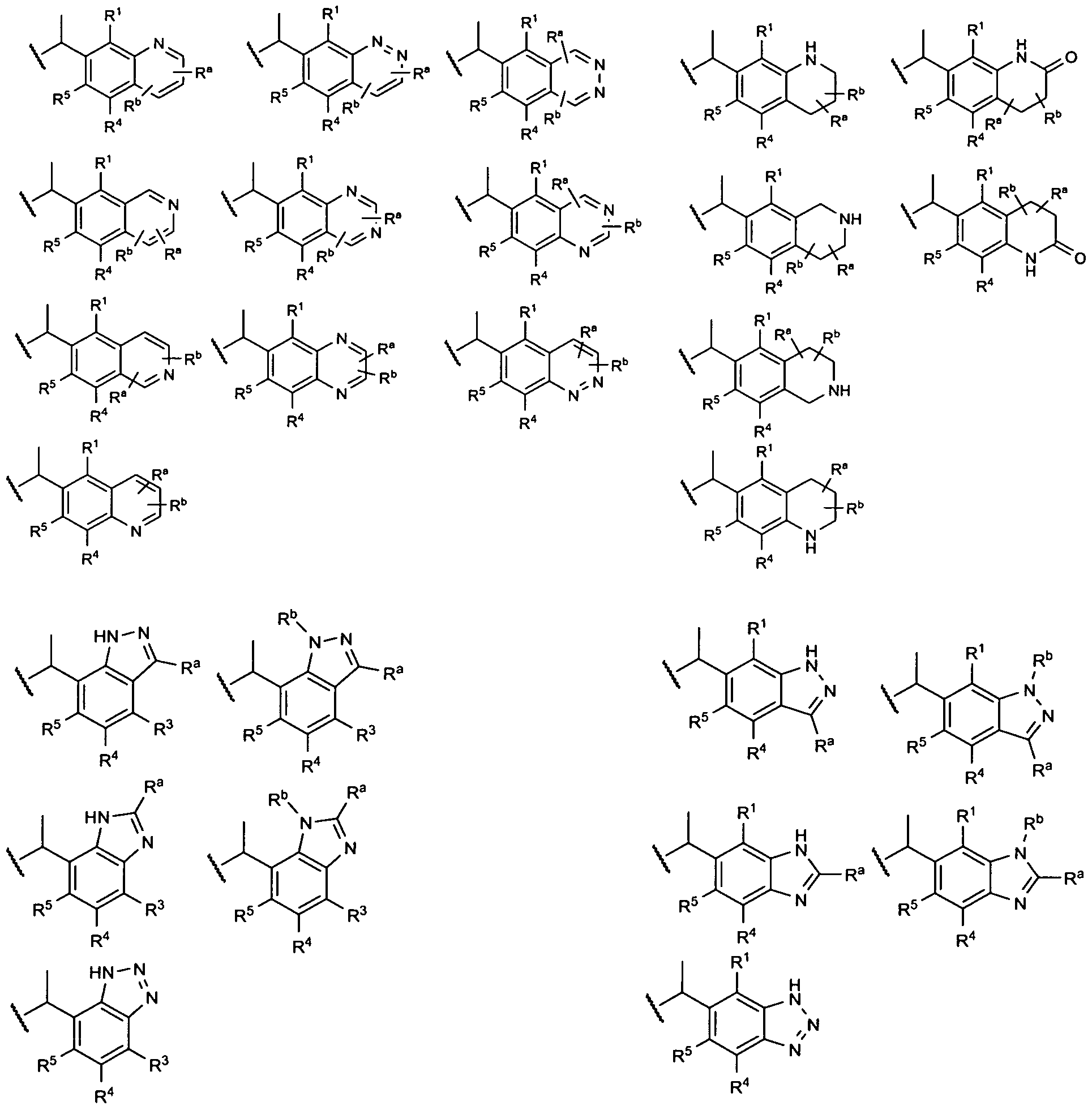
Ein Gegenstand der vorliegenden Erfindung sind daher substituierte Verbindungen der allgemeinen Formel I,
n für O, 1 , 2, 3 oder 4 steht;
R1 und R2 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CH=N-NR71-; -S-C(=S)-NH-; -O-C(=S)-NH-; -S-C(=O)-NH-; -O-C(=O)-NH-; -S-C(=S)-NR63-; -O-C(=S)-NR63-; -S-C(=O)-NR63-; -O-C(=O)- NR63-; -S-CH=N-; -S-CR29=N-; -N=CH-O-; -N=CR30-O-; -NH-C(=O)-NH-; -NH- C(=S)-NH-; -NR66-C(=O)-NR65-; -NR66-C(=S)-NR65-; -O-CH2-C(=O)-NH-; -O- CH2 -O-; -0-CH2-CH2-O-; -0-CH2-CH2-CH2-O-; -0-CH2-CH2-NH- und - CH=CH-N=CH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R2 und R3 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CR28=N-NH-; -CH=N-NR62-; -CR28=N-NR62-; -S- C(=S)-NH-; -O-C(=S)-NH-; -S-C(=O)-NH-; -O-C(=O)-NH-; -S-C(=S)-NR63-; -O- C(=S)-NR63-; -S-C(=O)-NR63-; -O-C(=O)-NR63-; -S-CH=N-; -S-CR29=N-; - N=CH-O-; -N=CR30-O-; -N=CH-NH-; -N=CH-NR64-; -NH-C(=O)-NH-; -NH- C(=S)-NH-; -NR66-C(=O)-NR65-; -NR66-C(=S)-NR65-; -N=N-NH-; -N=N-NR67-; - O-CH2-C(=O)-NH-; -0-CH2-O-; -CH2-CH2-NH-, -CH2-CH2-CH2-NH, -CH2- C(=O)-NH, -CH2-CH2-C(=O)-NH-; -0-CH2-CH2-O-; -0-CH2-CH2-CH2-O-; -N=N- CH=CH-; -N=CH-N=CH; -N=CH-CH=N-; -CH=CH-CH=N-; -CH=CH-N=CH-; - CH=N-N=CH-, -N=N-CR68=CR69-; -N=CR68-N=CR69; -N=CR68-CR69=N-; - CR68=CR69-CH=N-; -CR68=CR69-N=CR70-; -CR68=N-N=CR69- und -0-CH2- CH2-NH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R3 und R4 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CR28=N-NH-; -CH=N-NR62-; -CR28=N-NR62-; -S- C(=S)-NH-; -O-C(=S)-NH-; -S-C(=O)-NH-; -0-C(O)-NH-; -S-C(=S)-NR63-; -O- C(=S)-NR63-; -S-C(=O)-NR63-; -O-C(=O)-NR63-; -S-CH=N-; -S-CR29=N-; - N=CH-O-; -N=CR30-O-; -N=CH-NH-; -N=CH-NR64-; -NH-C(=O)-NH-; -NH- C(=S)-NH-; -NR66-C(=O)-NR65-; -NR66-C(=S)-NR65-; -N=N-NH-; -N=N-NR67-; - O-CH2-C(=O)-NH-; -0-CH2-O-; -CH2-CH2-NH-, -CH2-CH2-CH2-NH, -CH2- C(=O)-NH, -CH2-CH2-C(=O)-NH-; -0-CH2-CH2-O-; -0-CH2-CH2-CH2-O-; -N=N- CH=CH-; -N=CH-N=CH; -N=CH-CH=N-; -CH=CH-CH=N-; -CH=CH-N=CH-; - CH=N-N=CH-, -N=N-CR68=CR69-; -N=C R68- N=C R69; -N=CR68-CR69=N-; - CR68=CR69-CH=N-; -CR68=CR69-N=CR70-; -CR68=N-N=CR69- und -0-CH2- CH2-NH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R4 und R5 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CH=N-NR71-; -S-C(=S)-NH-; -O-C(=S)-NH-; -S-C(O)-NH-; -O- C(O)-NH-; -S-C(=S)-NR63-; -O-C(=S)-NR63-; -S-C(O)-NR63-; -O-C(O)- NR63-; -S-CH=N-; -S-CR29=N-; -N=CH-O-; -N=CR30-O-; -NH-C(=O)-NH-; -NH- C(=S)-NH-; -NR66-C(=O)-NR65-; -NR66-C(=S)-NR65-; -O-CH2-C(=O)-NH-; -O- CH2- O-; -0-CH2-CH2-O-; -0-CH2-CH2-CH2-O-; -0-CH2-CH2-NH- und -
CH=CH-N=CH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
bzw. R1 und R2 oder R2 und R3 oder R3 und R4 oder R4 und R5 zusammen mit den sie verbindenden Kohlenstoffatomen einen 4-, 5-, 6- oder 7-gliedrigen Ring bilden, der gesättigt, ungesättigt oder aromatisch ist, 1 , 2 oder 3 Stickstoffatome als Ringglieder aufweist und unsubstituiert oder mit 1 , 2 oder 3 Resten substituiert ist, die jeweils unabhängig voneinander ausgewählt sind aus der Gruppe bestehend aus F, Cl, Br, I, =O, -CN, -CF3, -SF5, -OH, -O-C1-5- Alkyl, -NH2, -NO2, -O-CF3, -S-CF3, -SH, -S-C1-5-Alkyl, -C1-5-Alkyl, -C(=O)-OH, - C(=O)-O-Ci-5-Alkyl, -NH-C1-5-Alkyl, -N(C1-5-Alkyl)2, -NH-S(=O)2-C1-5-Alkyl, -NH- C(=O)-O-C1-5-Alkyl, -C(=O)-H, -C(=O)-C1-5-Alkyl, -C(=O)-NH2l -C(O)-NH-C1-5- Alkyl, -C(=O)-N-(Ci-5-Alkyl)2, -O-Phenyl, -O-Benzyl, Phenyl und Benzyl, wobei jeweils der zyklische Teil der Reste -O-Phenyl, -O-Benzyl, Phenyl und Benzyl mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus F, Cl, Br, -OH, -CF3, -SF5, -CN, -NO2, -C1-5-Alkyl, - O-Ci-5-Alkyl, -O-CF3, -S-CF3, Phenyl und -O-Benzyl substituiert sein kann,
und die übrigen Reste von R1, R2, R3, R4 und R5, unabhängig voneinander, jeweils für H; F; Cl; Br; I; -SF5; -NO2; -CN; -NH2; -OH; -SH; -C(=O)-NH2; -S(=O)2-NH2; -C(=O)-NH-OH; -C(=O)-OH; -C(=O)-H; -S(=O)2-OH; -C(=NH)-NH2; -C(=NH)- NH-R9; -N=C(NH2)2; -N=C(NHR10)(NHR11); -O-P(=O)2-O-R12; -NHR13; - NR14R15; -NH-C(=O)-R13; -OR16; -SR17; -C(=O)-NHR18; -C(=O)-NR19R20; - S(=O)2-NHR21; -S(=O)2-NR22R23; -C(O)-OR24; -C(O)-R25; -S(O)-R26; - S(O)2-R27 oder für einen linearen oder verzweigten, gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten aliphatischen CI--I0 Rest stehen;
R6 für H oder für einen linearen oder verzweigten, gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten aliphatischen C-MO Rest steht;
R7 für Wasserstoff oder -OH steht;
oder R6 und R7 jeweils zusammen mit dem sie verbindenden Kohlenstoffatom als Ringglied einen gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten 3-, 4-, 5-, 6- oder 7-gliedrigen cycloaliphatischen Rest bilden;
R8 für -SF5; -0-CF3; -CF3; -0-CFH2; -O-CF2H; -CFH2; -CF2H; oder für einen unsubstituierten oder wenigstens einfach substituierten tert-Butyl-Rest steht;
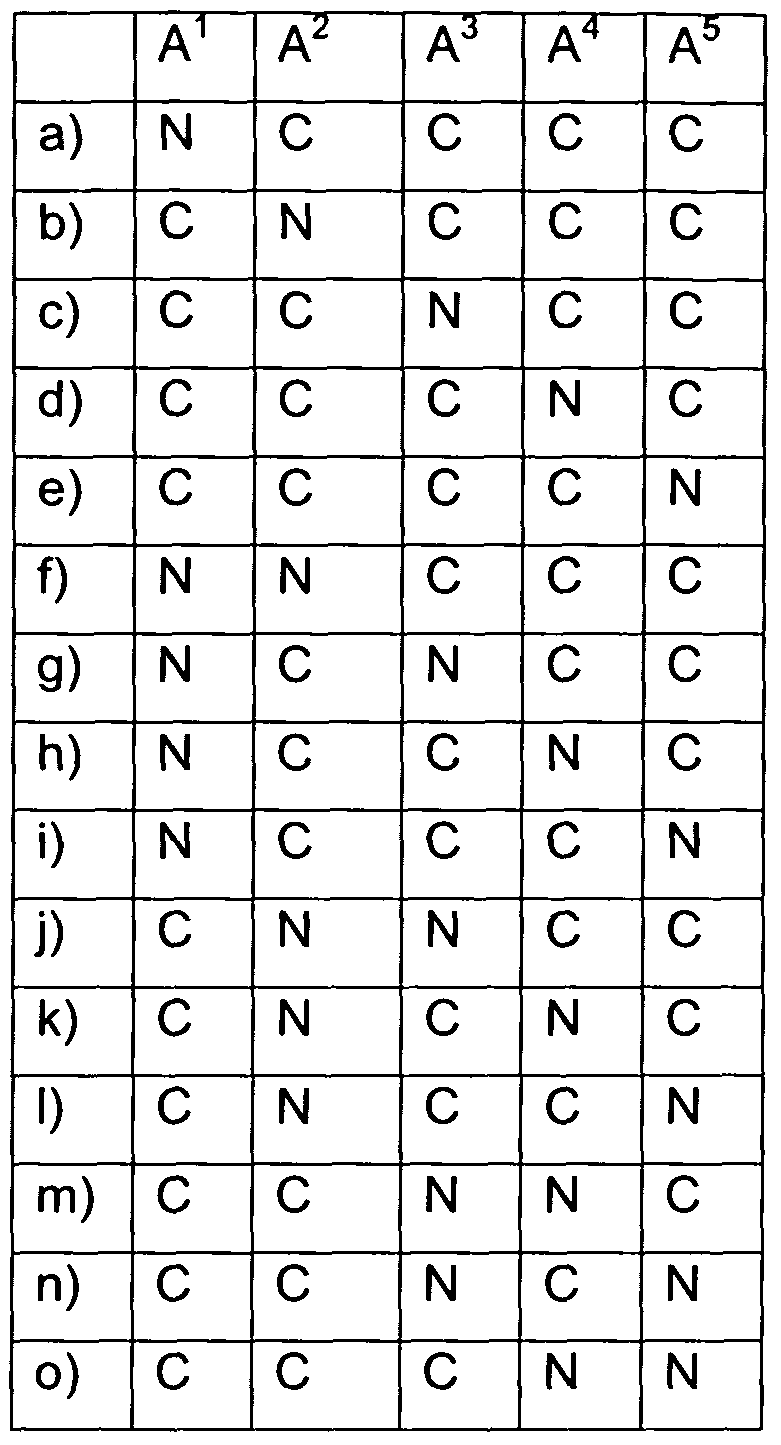
T für C-R35 und U für C-R36 und V für N und W für C-R38 oder
T für C-R35 und U für N und V für C-R37 und W für C-R38 oder
T für N und U für C-R36 und V für C-R37 und W für C-R38 oder
T für N und U für N und V für C-R37 und W für C-R38 oder
T für N und U für C-R36 und V für N und W für C-R38 oder
T für C-R35 und U für N und V für N und W für C-R38 oder
T für C-R
35 und U für C-R
36 und V für C-R
37 und W für C-R
38 steht;
, D r\
19 , r D\
21 ι D r\
22 i D r\
23 | Ri \
24 , D l \
25 ,
R26 und R27, unabhängig voneinander, jeweils
für einen linearen oder verzweigten, gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten aliphatischen C-MO Rest;
für einen ungesättigten oder gesättigten, unsubstituierten oder wenigstens einfach substituierten, ggf. wenigstens ein Heteroatom als Ringglied aufweisenden 3-, 4-, 5-, 6-, 7-, 8- oder 9-gliedrigen cycloaliphatischen Rest, der mit einem gesättigten oder ungesättigten, unsubstituierten oder
wenigstens einfach substituierten mono- oder polyzyklischen Ringsystem kondensiert und/oder über eine lineare oder verzweigte, unsubstituierte oder wenigstens einfach substituierte d-6-Alkylen-Gruppe oder 2- bis 6-gliedrige Heteroalkylen-Gruppe gebunden sein kann;
oder für einen unsubstituierten oder wenigstens einfach substituierten 5- bis 14-gliedrigen Aryl- oder Heteroaryl-Rest, der mit einem gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten mono- oder polyzyklischen Ringsystem kondensiert und/oder über eine lineare oder verzweigte, unsubstituierte oder wenigstens einfach substituierte C-ι-6-Alkylen- Gruppe oder 2- bis 6-gliedrige Heteroalkylen-Gruppe gebunden sein kann, stehen;
R28 für F; Cl; Br; I; -SF5; -NO2; -CF3; -CN; -NH2 oder für einen linearen oder verzweigten, gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten aliphatischen Ci_io Rest steht;
R29 und R30, unabhängig voneinander, jeweils für -NH-C(=O)-R31; -NH2;
-NH-S(=O)2-R32; -NH-C(=O)-O-R33; -S-R34 oder für einen linearen oder verzweigten, gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten aliphatischen Ci_io Rest stehen;
R31, R32, R33 und R34, unabhängig voneinander, jeweils für einen linearen oder verzweigten, gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten aliphatischen Ci--I0 Rest stehen;
R 35 R 36 und R 37 unabhängig voneinander, jeweils für H; F; Cl; Br; I; -SF5;
-NO2; -CF3; -CN; -NH2; -OH; -SH; -C(=O)-NH2; -S(=O)2-NH2; -C(=O)-NH-OH; - C(=O)-OH; -C(=O)-H; -S(=O)2-OH; -NHR13; -NR14R15; -NH-C(=O)-R13; -OR16; - SR17; -C(=O)-NHR18; -C(=O)-NR19R20; -S(=O)2-NHR21; -S(=O)2-NR22R23; - C(=O)-OR24; -C(=O)-R25; -S(=O)-R26; -S(=O)2-R27;
für einen linearen oder verzweigten, gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten aliphatischen Ci_io Rest;
oder für einen unsubstituierten oder wenigstens einfach substituierten 5- bis 14-gliedrigen Aryl- oder Heteroaryl-Rest, der mit einem gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten mono- oder polyzyklischen Ringsystem kondensiert und/oder über eine lineare oder verzweigte, unsubstituierte oder wenigstens einfach substituierte Ci-6-Alkylen- Gruppe oder C-2-6-Alkenylen-Gruppe oder C2-6-Alkinylen-Gruppe gebunden sein kann, steht;
für H; F; Cl; Br; I; -SF5; -NO2; -CF3; -CF2CI; -CN; -NH2; -OH; -SH; -C(=O)-NH2; -S(=O)2-NH2; -C(=O)-NH-OH; -C(=O)-OH; -C(=O)-H; -S(=O)2-OH; -NHR39; - NR40R41; -OR42; -SR43; -C(=O)-NHR44; -C(=O)-NR45R46; -S(=O)2-NHR47; - S(=O)2-NR48R49; -C(=O)-OR50; -C(=O)-R51; -S(=O)-R52; -S(=O)2-R53; -C(=NH)- NH2; -C(=NH)-NH-R54; -N=C(NH2)2; -N=C(NHR55)(NHR56);
für einen linearen oder verzweigten, gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten aliphatischen CMO Rest;
für einen ungesättigten oder gesättigten, unsubstituierten oder wenigstens einfach substituierten, ggf. wenigstens ein Heteroatom als Ringglied aufweisenden 3-, 4-, 5-, 6-, 7-, 8- oder 9-gliedrigen cycloaliphatischen Rest, der jeweils über ein Kohlenstoffatom im Ring des cycloaliphatischen Restes an das Grundgerüst gebunden ist und mit einem gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten mono- oder polyzyklischen Ringsystem kondensiert und/oder über eine lineare oder verzweigte, unsubstituierte oder wenigstens einfach substituierte C-ι.
6-Alkylen- Gruppe oder C-
2-6-Alkenylen-Gruppe oder C
2-6-Alkinylen-Gruppe gebunden sein kann;
oder für einen unsubstituierten oder wenigstens einfach substituierten 5- bis 14-gliedrigen Aryl- oder Heteroaryl-Rest, der mit einem gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten mono- oder polyzyklischen Ringsystem kondensiert und/oder über eine lineare oder verzweigte, unsubstituierte oder wenigstens einfach substituierte C-ι-
6-Alkylen- Gruppe oder C-
2-6-Alkenylen-Gruppe oder
gebunden sein kann, steht;
R39, R40, R41, R42, R43, R44, R45, R46, R47, R48, R49, R50, R51, R52, R53, R54, R55 und R56, unabhängig voneinander, jeweils
für einen linearen oder verzweigten, gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten aliphatischen C-M0 Rest;
für einen ungesättigten oder gesättigten, unsubstituierten oder wenigstens einfach substituierten, ggf. wenigstens ein Heteroatom als Ringglied aufweisenden 3-, A-, 5-, 6-, 7-, 8- oder 9-gliedrigen cycloaliphatischen Rest, der mit einem gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten mono- oder polyzyklischen Ringsystem kondensiert und/oder über eine lineare oder verzweigte, unsubstituierte oder wenigstens einfach substituierte C-ι-6-Alkylen-Gruppe oder 2- bis 6-gliedrige Heteroalkylen-Gruppe gebunden sein kann;
oder für einen unsubstituierten oder wenigstens einfach substituierten 5- bis 14-gliedrigen Aryl- oder Heteroaryl-Rest, der mit einem gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten mono- oder polyzyklischen Ringsystem kondensiert und/oder über eine lineare oder verzweigte, unsubstituierte oder wenigstens einfach substituierte d-6-Alkylen- Gruppe oder 2- bis 6-gliedrige Heteroalkylen-Gruppe gebunden sein kann, stehen;
oder
R40 und R41 jeweils zusammen mit dem sie verbindenden Stickstoffatom als
Ringglied einen gesättigten oder ungesättigten, unsubstituierten oder mit 1 , 2, 3, 4 oder 5 Resten R57 substituierten 4-, 5-, 6-, 7-, 8- oder 9-gliedrigen, ggf. wenigstens ein weiteres Heteroatom als Ringglied aufweisenden heterocycloaliphatischen Rest bilden, der mit einem gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten mono- oder polyzyklischen Ringsystem kondensiert sein kann;
R57 für -NHR58, -NR59R60 für einen linearen oder verzweigten, gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten aliphatischen Ci--I0 Rest steht;
R58, R59 und R60, unabhängig voneinander, jeweils für -C(=O)-R61; für einen linearen oder verzweigten, gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten aliphatischen C-i-io Rest
oder für einen unsubstituierten oder wenigstens einfach substituierten 5- bis 14-gliedrigen Aryl- oder Heteroaryl-Rest, der mit einem gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten mono- oder polyzyklischen Ringsystem kondensiert und/oder über eine lineare oder verzweigte, unsubstituierte oder wenigstens einfach substituierte Ci-6-Alkylen- Gruppe oder C-2-6-Alkenylen-Gruppe oder C2-6-Alkinylen-Gruppe gebunden sein kann, stehen;
R61 für einen linearen oder verzweigten, gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten aliphatischen C-MO Rest steht;
R62, R63, R64, R65, R66 und R67, unabhängig voneinander, jeweils für einen linearen oder verzweigten, gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten aliphatischen Ci-io Rest stehen;
R68, R69 und R70, unabhängig voneinander, jeweils für F, Cl, Br, I oder für einen linearen oder verzweigten, gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten aliphatischen C-MO Rest stehen;
und
R71 für einen unsubstituierten oder wenigstens einfach substituierten 5- bis 14- gliedrigen Aryl- oder Heteroaryl-Rest steht, der mit einem gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten mono- oder polyzyklischen Ringsystem kondensiert und/oder über eine lineare oder verzweigte, unsubstituierte oder wenigstens einfach substituierte d-β-Alkylen- Gruppe oder C-2-6-Alkenylen-Gruppe oder C2-6-Alkinylen-Gruppe gebunden sein kann,
jeweils ggf. in Form eines ihrer reinen Stereoisomeren, insbesondere Enantiomeren oder Diastereomeren, ihrer Racemate oder in Form einer Mischung von Stereoisomeren, insbesondere der Enantiomeren und/oder Diastereomeren, in einem beliebigen Mischungsverhältnis, oder jeweils in Form entsprechender Salze, oder jeweils in Form entsprechender Solvate;
wobei
die vorstehend genannten aliphatischen C1-I0 Reste und tert-Butyl-Reste ggf. jeweils mit 1 , 2, 3, 4, 5, 6, 7, 8 oder 9 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus F, Cl, Br, I1 -CN, -NO2, -OH, -NH2, -SH, -O(C1-5-Alkyl), -S(C1-5-Alkyl), -NH(C1-5-Alkyl), -N(C1-5-Alkyl)(C1-5-Alkyl), -C(=O)-O-C1-5-Alkyl, -O- C(=O)-Ci-5-Alkyl, -O-Phenyl, Phenyl, -OCF3 und -SCF3 substituiert sein können;
die vorstehend genannten 2- bis 6-gliedrigen Heteroalkylen-Gruppen, C1-6-Alkylen- Gruppen und C2-6-Alkenylen-Gruppen und C2-6-Alkinylen-Gruppen ggf. jeweils mit 1 , 2, 3, 4, 5, 6, 7, 8 oder 9 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus F, Cl, Br1 I, -CN, -NO2, -OH, -NH2, -SH, -O(C1-5-Alkyl), -S(C1-5- Alkyl), -NH(C1-5-Alkyl), -N(C1-5-Alkyl)(C1-5-Alkyl), -OCF3 und -SCF3 substituiert sein können;
die vorstehend genannten Heteroalkylen-Gruppen jeweils ggf. 1 , 2 oder 3 Heteroatom(e) unabhängig voneinander ausgewählt aus der Gruppe bestehend aus Sauerstoff, Schwefel und Stickstoff (NH) als Kettenglied(er) aufweisen;
die vorstehend genannten (hetero)cycloaliphatischen Reste ggf. jeweils mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus -d-6-Alkylen-OH, =CH2, -O-d-s-Alkylen-Oxetanyl, -Ci-5-Alkylen-O-Ci. 5-Alkylen-Oxetanyl>-CH2-NH-Ci-5-AlkylI -CH2-N(C1-5-Alkyl)2, -N[C(=O)-C1-5-Alkyl]- Phenyl, -CH2-O-C1-5-Alkyl, Oxo (=O), Thioxo (=S), F, Cl, Br, I, -CN, -CF3, -SF5, -OH, - O-C1-5-Alkyl, -O-C(=O)-C1-5-Alkyl, -NH2, -NO2, -0-CF3, -S-CF3, -SH, -S-Ci-5-Alkyl, -C1- 5-Alkyl, -C(=O)-C1-5-Alkyl, -C(=O)-OH, -C(=O)-O-C1-5-Alkyl, -NH-C1-5-Alkyl, -N(C1-5- Alkyl)2, -NH-Phenyl, -N(C1-5-Alkyl)-Phenyl, Cyclohexyl, Cyclopentyl, (4,5)- Dihydroisoxazolyl, Thiazolyl, (1 ,2,5)-Thiadiazolyl, Thiophenyl, Phenethyl, Piperidinyl, Pyrrolidinyl, -(CH2)-Pyridinyl, Pyridinyl, -O-Phenyl, -O-Benzyl, Phenyl und Benzyl substituiert sein können, wobei jeweils der zyklische Teil der Reste Oxetanyl, (4,5)- Dihydroisoxazolyl, Thiazolyl, (1 ,2,5)-Thiadiazolyl, Thiophenyl, Phenethyl, -N[C(=O)- C1-5-Alkyl]-Phenyl, -NH-Phenyl, -N(C1-5-Alkyl)-Phenyl, -(CH2)-Pyridinyl, Pyridinyl, -O- Phenyl, -O-Benzyl, Phenyl und Benzyl mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus F, Cl, Br, -OH, -CF3, -SF5, - CN, -NO2, -C1-5-Alkyl, -O-C1-5-Alkyl, -0-CF3, -S-CF3, Phenyl und -O-Benzyl substituiert sein kann,
und, sofern nicht anders angegeben, die vorstehend genannten (hetero)cycloaliphatischen Reste jeweils ggf. 1 , 2 oder 3 (weitere) Heteroatom(e) unabhängig voneinander ausgewählt aus der Gruppe bestehend aus Sauerstoff, Stickstoff und Schwefel aufweisen können;
die Ringe der vorstehend genannten mono- oder polyzyklischen Ringsysteme ggf. jeweils mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus Oxo (=0), Thioxo (=S), F, Cl, Br, I, -CN, -CF3, -SF5, -OH, -O-C1-5-Alkyl, -NH2, -NO2, -O-CF3l -S-CF3, -SH, -S-C1-5-Alkyl, -C1-5-Alkyl, -C(=O)-C1-5- Alkyl, -C(=O)-OH, -C(=O)-O-C1-5-Alkyl, -NH-C1-5-Alkyl, -N(C1-5-Alkyl)2, -O-Phenyl, -O- Benzyl, Phenyl und Benzyl substituiert sein können, wobei jeweils der zyklische Teil der Reste -O-Phenyl, -O-Benzyl, Phenyl und Benzyl mit 1 , 2, 3, 4 oder 5
Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus F, Cl, Br, -OH, -CF3, -SF5, -CN, -NO2, -C1-5-Alkyl, -O-C1-5-Alkyl, -O-CF3, -S-CF3, Phenyl und -O-Benzyl substituiert sein kann,
und die Ringe der vorstehend genannten mono- oder polyzyklischen Ringsysteme jeweils 5-, 6- oder 7-gliedrig sind und jeweils ggf. 1 , 2, 3, 4 oder 5 Heteroatom(e) als Ringglied(er) aufweisen können, die unabhängig voneinander aus der Gruppe bestehend aus Sauerstoff, Stickstoff und Schwefel ausgewählt sind;
und die vorstehend genannten Aryl- oder Heteroaryl-Reste ggf. jeweils mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus F, Cl, Br, I, -CN1 -CF3, -SF5, -OH, -O-C1-5-Alkyl, -NH2, -NO2, -O-CF3, - S-CF3, -SH, -S-C1-5-Alkyl, -C1-5-Alkyl, -C(=O)-OH, -C(=O)-O-C1-5-Alkyl, -NH-C1-5-Alkyl, -N(C1-5-Alkyl)2, -NH-S(=O)2-C1-5-Alkyl, -NH-C(=O)-O-C1-5-Alkyl, -C(=O)-H, -Cf=O)-C1- 5-Alkyl, -C(=O)-NH2, -C(=O)-NH-C1-5-Alkyl, -C(=O)-N-(Ci-5-Alkyl)2, -O-Phenyl, -O- Benzyl, Phenyl und Benzyl substituiert sein können, wobei jeweils der zyklische Teil der Reste -O-Phenyl, -O-Benzyl, Phenyl und Benzyl mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus F, Cl, Br, -OH, -CF3, -SF5, -CN, -NO2, -C1-5-Alkyl, -O-C1-5-Alkyl, -0-CF3, -S-CF3, Phenyl und -O-Benzyl substituiert sein kann,
und
die vorstehend genannten Heteroaryl-Reste jeweils ggf. 1 , 2, 3, 4 oder 5 Heteroatom(e) unabhängig voneinander ausgewählt aus der Gruppe bestehend aus Sauerstoff, Stickstoff und Schwefel als Ringglied(er) aufweisen.
Ein weiterer Gegenstand der vorliegenden Erfindung sind ferner substituierte Verbindungen der allgemeinen Formel I,
worin
n für 0, 1 , 2, 3 oder 4 steht;
R1 und R2 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CH=N-NR71-; -S-C(=S)-NH-; -O-C(=S)-NH-; -S-C(=O)-NH-; -O-C(=O)-NH-; -S-C(=S)-NR63-; -O-C(=S)-NR63-; -S-C(=O)-NR63-; -O-C(=O)- NR63-; -S-CH=N-; -S-CR29=N-; -N=CH-O-; -N=CR30-O-; -NH-C(=O)-NH-; -NH- C(=S)-NH-; -NR66-C(=O)-NR65-; -NR66-C(=S)-NR65-; -O-CH2-C(=O)-NH-; -O- CH2 -O-; -0-CH2-CH2-O-; -0-CH2-CH2-CH2-O-; -0-CH2-CH2-NH- und - CH=CH-N=CH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R2 und R3 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CR28=N-NH-; -CH=N-NR62-; -CR28=N-NR62-; -S- C(=S)-NH-; -O-C(=S)-NH-; -S-C(=O)-NH-; -O-C(=O)-NH-; -S-C(=S)-NR63-; -O- C(=S)-NR63-; -S-C(=O)-NR63-; -O-C(=O)-NR63-; -S-CH=N-; -S-CR29=N-; - N=CH-O-; -N=CR30-O-; -N=CH-NH-; -N=CH-NR64-; -NH-C(=O)-NH-; -NH- C(=S)-NH-; -NR66-C(=O)-NR65-; -NR66-C(=S)-NR65-; -N=N-NH-; -N=N-NR67-; - O-CH2-C(=O)-NH-; -0-CH2-O-; -CH2-CH2-NH-, -CH2-CH2-CH2-NH, -CH2- C(=O)-NH, -CH2-CH2-C(=O)-NH-; -0-CH2-CH2-O-; -0-CH2-CH2-CH2-O-; -N=N- CH=CH-; -N=CH-N=CH; -N=CH-CH=N-; -CH=CH-CH=N-; -CH=CH-N=CH-; - CH=N-N=CH-, -N=N-CR68=CR69-; -N=CR68-N=CR69; -N=CR68-CR69=N-; - CR68=CR69-CH=N-; -CR68=CR69-N=CR70-; -CR68=N-N=CR69- und -0-CH2-
CH2-NH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R3 und R4 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CR28=N-NH-; -CH=N-NR62-; -CR28=N-NR62-; -S- C(=S)-NH-; -O-C(=S)-NH-; -S-C(=O)-NH-; -O-C(=O)-NH-; -S-C(=S)-NR63-; -O- C(=S)-NR63-; -S-C(=O)-NR63-; -O-C(=O)-NR63-; -S-CH=N-; -S-CR29=N-; - N=CH-O-; -N=CR30-O-; -N=CH-NH-; -N=CH-NR64-; -NH-C(=O)-NH-; -NH- C(=S)-NH-; -NR66-C(=O)-NR65-; -NR66-C(=S)-NR65-; -N=N-NH-; -N=N-NR67-; - O-CH2-C(=O)-NH-; -0-CH2-O-; -CH2-CH2-NH-, -CH2-CH2-CH2-NH, -CH2- C(=O)-NH, -CH2-CH2-C(=O)-NH-; -0-CH2-CH2-O-; -0-CH2-CH2-CH2-O-; -N=N- CH=CH-; -N=CH-N=CH; -N=CH-CH=N-; -CH=CH-CH=N-; -CH=CH-N=CH-; - CH=N-N=CH-, -N=N-CR68=CR69-; -N=CR68-N=CR69; -N=CR68-CR69=N-; - CR68=CR69-CH=N-; -CR68=CR69-N=CR70-; -CR68=N-N=CR69- und -0-CH2- CH2-NH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R4 und R5 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CH=N-NR71-; -S-C(=S)-NH-; -O-C(=S)-NH-; -S-C(=O)-NH-; -O- C(=O)-NH-; -S-C(=S)-NR63-; -O-C(=S)-NR63-; -S-C(=O)-NR63-; -O-C(=O)- NR63-; -S-CH=N-; -S-CR29=N-; -N=CH-O-; -N=CR30-O-; -NH-C(=O)-NH-; -NH- C(=S)-NH-; -NR66-C(=O)-NR65-; -NR66-C(=S)-NR65-; -O-CH2-C(=O)-NH-; -O- CH2- O-; -0-CH2-CH2-O-; -0-CH2-CH2-CH2-O-; -0-CH2-CH2-NH- und - CH=CH-N=CH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
und die übrigen Reste von R1, R2, R3, R4 und R5, unabhängig voneinander, jeweils für H; F; Cl; Br; I; -SF5; -NO2; -CN; -NH2; -OH; -SH; -C(=O)-NH2; -S(=O)2-NH2; -C(=O)-NH-OH; -C(=O)-OH; -C(=O)-H; -S(=O)2-OH; -C(=NH)-NH2; -C(=NH)- NH-R9; -N=C(NH2)2; -N=C(NHR10)(NHR11); -O-P(=O)2-O-R12; -NHR13; - NR14R15; -NH-C(=O)-R13; -OR16; -SR17; -C(=O)-NHR18; -C(=O)-NR19R20; - S(=O)2-NHR21; -S(=O)2-NR22R23; -C(=O)-OR24; -C(=O)-R25; -S(=O)-R26; - S(=O)2-R27 oder für einen linearen oder verzweigten, gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten
aliphatischen Ci-1O Rest stehen;
R6 für H oder für einen linearen oder verzweigten, gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten aliphatischen C-MO Rest steht;
R7 für Wasserstoff oder -OH steht;
oder R6 und R7 jeweils zusammen mit dem sie verbindenden Kohlenstoffatom als Ringglied einen gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten 3-, 4-, 5-, 6- oder 7-gliedrigen cycloaliphatischen Rest bilden;
R8 für -SF5; -0-CF3; -CF3; -0-CFH2; -0-CF2H; -CFH2; -CF2H; oder für einen unsubstituierten oder wenigstens einfach substituierten tert-Butyl-Rest steht;
T für C-R35 und U für C-R36 und V für N und W für C-R38 oder
T für C-R35 und U für N und V für C-R37 und W für C-R38 oder
T für N und U für C-R36 und V für C-R37 und W für C-R38 oder
T für N und U für N und V für C-R37 und W für C-R38 oder
T für N und U für C-R36 und V für N und W für C-R38 oder
T für C-R35 und U für N und V für N und W für C-R38 oder
T für C-R35 und U für C-R36 und V für C-R37 und W für C-R38 steht;
R9 , r D\10 , Dr\1 1 , O r\12 , Dr\13 , Γ DΛ14 , D Γ\15 , RΓ\16 , Γ RΛ17 , D T\18 , R D19 , Dr\20 , D ΓΛ21 , Dr\22 , t D\23 , D r\24 , D r\25 ,
R26 und R27, unabhängig voneinander, jeweils
für einen linearen oder verzweigten, gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten aliphatischen Ci-io Rest;
für einen ungesättigten oder gesättigten, unsubstituierten oder wenigstens einfach substituierten, ggf. wenigstens ein Heteroatom als Ringglied aufweisenden 3-, 4-, 5-, 6-, 7-, 8- oder 9-gliedrigen cycloaliphatischen Rest, der mit einem gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten mono- oder polyzyklischen Ringsystem kondensiert und/oder über eine lineare oder verzweigte, unsubstituierte oder wenigstens einfach substituierte Ci-6-Alkylen-Gruppe oder 2- bis 6-gliedrige Heteroalkylen-Gruppe gebunden sein kann;
oder für einen unsubstituierten oder wenigstens einfach substituierten 5- bis 14-gliedrigen Aryl- oder Heteroaryl-Rest, der mit einem gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten mono- oder polyzyklischen Ringsystem kondensiert und/oder über eine lineare oder verzweigte, unsubstituierte oder wenigstens einfach substituierte Ci-6-Alkylen- Gruppe oder 2- bis 6-gliedrige Heteroalkylen-Gruppe gebunden sein kann, stehen;
R28 für F; Cl; Br; I; -SF5; -NO2; -CF3; -CN; -NH2 oder für einen linearen oder verzweigten, gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten aliphatischen Ci--I0 Rest steht;
R29 und R30, unabhängig voneinander, jeweils für -NH-C(=O)-R31; -NH2;
-NH-S(=O)2-R32; -NH-C(=O)-O-R33; -S-R34 oder für einen linearen oder verzweigten, gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten aliphatischen C-M0 Rest stehen;
R31, R32, R33 und R34, unabhängig voneinander, jeweils für einen linearen oder verzweigten, gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten aliphatischen Ci-10 Rest stehen;
R35, R36 und R37, unabhängig voneinander, jeweils für H; F; Cl; Br; I; -SF5;
-NO2; -CF3; -CN; -NH2; -OH; -SH; -C(=O)-NH2; -S(=O)2-NH2; -C(=O)-NH-OH; - C(=O)-OH; -C(=O)-H; -S(=O)2-OH; -NHR13; -NR14R15; -NH-C(=O)-R13; -OR16; - SR17; -C(=O)-NHR18; -C(=O)-NR19R20; -S(=O)2-NHR21; -S(=O)2-NR22R23; - C(=O)-OR24; -C(=O)-R25; -S(=O)-R26; -S(=O)2-R27;
für einen linearen oder verzweigten, gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten aliphatischen C-MO Rest;
oder für einen unsubstituierten oder wenigstens einfach substituierten 5- bis 14-gliedrigen Aryl- oder Heteroaryl-Rest, der mit einem gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten mono- oder polyzyklischen Ringsystem kondensiert und/oder über eine lineare oder verzweigte, unsubstituierte oder wenigstens einfach substituierte Ci-6-Alkylen- Gruppe oder C-2-6-Alkenylen-Gruppe oder C2-6-Alkinylen-Gruppe gebunden sein kann, steht;
R38 für H; F; Cl; Br; I; -SF5; -NO2; -CF3; -CF2CI; -CN; -NH2; -OH; -SH; -C(=O)-NH2; -S(=O)2-NH2; -C(=O)-NH-OH; -C(=O)-OH; -C(=O)-H; -S(O)2-OH; -NHR39; - NR40R41; -OR42; -SR43; -C(=O)-NHR44; -C(=O)-NR45R46; -S(=O)2-NHR47; - S(=O)2-NR48R49; -C(=O)-OR50; -C(=O)-R51; -S(=O)-R52; -S(=O)2-R53; -C(=NH)- NH2; -C(=NH)-NH-R54; -N=C(NH2)2; -N=C(NHR55)(NHR56);
für einen linearen oder verzweigten, gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten aliphatischen CM0 Rest;
für einen ungesättigten oder gesättigten, unsubstituierten oder wenigstens einfach substituierten, ggf. wenigstens ein Heteroatom als Ringglied aufweisenden 3-, 4-, 5-, 6-, 7-, 8- oder 9-gliedrigen cycloaliphatischen Rest, der jeweils über ein Kohlenstoffatom im Ring des cycloaliphatischen Restes an das Grundgerüst gebunden ist und mit einem gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten mono- oder polyzyklischen Ringsystem kondensiert und/oder über eine lineare oder verzweigte, unsubstituierte oder wenigstens einfach substituierte C-ι-6-Alkylen- Gruppe oder C-2-6-Alkenylen-Gruppe oder C2-6-Alkinylen-Gruppe gebunden sein kann;
oder für einen unsubstituierten oder wenigstens einfach substituierten 5- bis 14-gliedrigen Aryl- oder Heteroaryl-Rest, der mit einem gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten mono- oder polyzyklischen Ringsystem kondensiert und/oder über eine lineare oder verzweigte, unsubstituierte oder wenigstens einfach substituierte Ci-6-Alkylen- Gruppe oder C-2-6-Alkenylen-Gruppe oder C2-6-Alkinylen-Gruppe gebunden sein kann, steht;
R39, R40, R41, R42, R43, R44, R45, R46, R47, R48, R49, R50, R51, R52, R53, R54, R55 und R56, unabhängig voneinander, jeweils
für einen linearen oder verzweigten, gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten aliphatischen Ci.io Rest;
für einen ungesättigten oder gesättigten, unsubstituierten oder wenigstens einfach substituierten, ggf. wenigstens ein Heteroatom als Ringglied aufweisenden 3-, 4-, 5-, 6-, 7-, 8- oder 9-gliedrigen cycloaliphatischen Rest, der mit einem gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten mono- oder polyzyklischen Ringsystem kondensiert und/oder über eine lineare oder verzweigte, unsubstituierte oder wenigstens einfach substituierte Ci-6-Alkylen-Gruppe oder 2- bis 6-gliedrige
Heteroalkylen-Gruppe gebunden sein kann;
oder für einen unsubstituierten oder wenigstens einfach substituierten 5- bis 14-gliedrigen Aryl- oder Heteroaryl-Rest, der mit einem gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten mono- oder polyzyklischen Ringsystem kondensiert und/oder über eine lineare oder verzweigte, unsubstituierte oder wenigstens einfach substituierte Ci-β-Alkylen- Gruppe oder 2- bis 6-gliedrige Heteroalkylen-Gruppe gebunden sein kann, stehen;
oder
R40 und R41 jeweils zusammen mit dem sie verbindenden Stickstoffatom als
Ringglied einen gesättigten oder ungesättigten, unsubstituierten oder mit 1 , 2, 3, 4 oder 5 Resten R57 substituierten A-, 5-, 6-, 7-, 8- oder 9-gliedrigen, ggf. wenigstens ein weiteres Heteroatom als Ringglied aufweisenden heterocycloaliphatischen Rest bilden, der mit einem gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten mono- oder polyzyklischen Ringsystem kondensiert sein kann;
R57 für -NHR58, -NR59R60 für einen linearen oder verzweigten, gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten aliphatischen C-M0 Rest steht;
R58, R59 und R60, unabhängig voneinander, jeweils für -C(=O)-R61; für einen linearen oder verzweigten, gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten aliphatischen C1-10 ReSt
oder für einen unsubstituierten oder wenigstens einfach substituierten 5- bis 14-gliedrigen Aryl- oder Heteroaryl-Rest, der mit einem gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten mono- oder polyzyklischen Ringsystem kondensiert und/oder über eine lineare oder verzweigte, unsubstituierte oder wenigstens einfach substituierte Ci-6-Alkylen-
Gruppe oder C-2-6-Alkenylen-Gruppe oder C2-6-Alkinylen-Gruppe gebunden sein kann, stehen;
R61 für einen linearen oder verzweigten, gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten aliphatischen Ci-Io ReSt steht;
R62, R63, R64, R65, R66 und R67, unabhängig voneinander, jeweils für einen linearen oder verzweigten, gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten aliphatischen C-Mo Rest stehen;
R68, R69 und R70, unabhängig voneinander, jeweils für F, Cl1 Br, I oder für einen linearen oder verzweigten, gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten aliphatischen d-io Rest stehen;
und
R71 für einen unsubstituierten oder wenigstens einfach substituierten 5- bis 14- gliedrigen Aryl- oder Heteroaryl-Rest steht, der mit einem gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten mono- oder polyzyklischen Ringsystem kondensiert und/oder über eine lineare oder verzweigte, unsubstituierte oder wenigstens einfach substituierte d-β-Alkylen- Gruppe oder C-2-β-Alkenylen-Gruppe oder C2-6-Alkinylen-Gruppe gebunden sein kann,
jeweils ggf. in Form eines ihrer reinen Stereoisomeren, insbesondere Enantiomeren oder Diastereomeren, ihrer Racemate oder in Form einer Mischung von Stereoisomeren, insbesondere der Enantiomeren und/oder Diastereomeren, in einem beliebigen Mischungsverhältnis, oder jeweils in Form entsprechender Salze, oder jeweils in Form entsprechender Solvate;
wobei
die vorstehend genannten aliphatischen CMO Reste und tert-Butyl-Reste ggf. jeweils mit 1 , 2, 3, 4, 5, 6, 7, 8 oder 9 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus F1 Cl, Br, I, -CN, -NO2, -OH1 -NH2, -SH, -O(Ci-5-Alkyl), -S(C1-5-AIkVl), -NH(Ci-5-Alkyl), -N(C1-5-AIkVl)(C1-5-AIkYl), -C(=O)-O-C1-5-Alkyl, -O- C(=O)-C1-5-Alkyl, -O-Phenyl, Phenyl, -OCF3 und -SCF3 substituiert sein können;
die vorstehend genannten 2- bis 6-gliedrigen Heteroalkylen-Gruppen, C-ι-6-Alkylen- Gruppen und C2-6-Alkenylen-Gruppen und C2-6-Alkinylen-Gruppen ggf. jeweils mit 1 , 2, 3, 4, 5, 6, 7, 8 oder 9 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus F, Cl, Br1 I, -CN, -NO2, -OH, -NH2, -SH, -O(C1-5-Alkyl), -S(C1-5- Alkyl), -NH(C1-5-Alkyl), -N(C1-5-Alkyl)(C1-5-Alkyl), -OCF3 und -SCF3 substituiert sein können;
die vorstehend genannten Heteroalkylen-Gruppen jeweils ggf. 1 , 2 oder 3 Heteroatom(e) unabhängig voneinander ausgewählt aus der Gruppe bestehend aus Sauerstoff, Schwefel und Stickstoff (NH) als Kettenglied(er) aufweisen;
die vorstehend genannten (hetero)cycloaliphatischen Reste ggf. jeweils mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus -C1-6-Alkylen-OH, =CH2, -O-C1-5-Alkylen-Oxetanyl, -Cvs-Alkylen-O-Cv 5-Alkylen-Oxetanyl,-CH2-NH-C1-5-Alkyl, -CH2-N(C1-5-Alkyl)2, -N[C(=O)-C1-5-Alkyl]- Phenyl, -CH2-O-C1-5-Alkyl, Oxo (=O), Thioxo (=S), F, Cl, Br, I, -CN, -CF3, -SF5, -OH, - O-C1-5-Alkyl, -O-C(=O)-C1-5-Alkyl, -NH2, -NO2, -O-CF3l -S-CF3, -SH, -S-C1-5-Alkyl, -C1- 5-Alkyl, -C(=O)-C1-5-Alkyl, -C(=O)-OH, -C(=O)-O-C1-5-Alkyl, -NH-C1-5-Alkyl, -N(C1-5- Alkyl)2, -NH-Phenyl, -N(C1-5-Alkyl)-Phenyl, Cyclohexyl, Cyclopentyl, (4,5)- Dihydroisoxazolyl, Thiazolyl, (1 ,2,5)-Thiadiazolyl, Thiophenyl, Phenethyl, Piperidinyl, Pyrrolidinyl, -(CH2)-Pyridinyl, Pyridinyl, -O-Phenyl, -O-Benzyl, Phenyl und Benzyl substituiert sein können, wobei jeweils der zyklische Teil der Reste Oxetanyl, (4,5)- Dihydroisoxazolyl, Thiazolyl, (1 ,2,5)-Thiadiazolyl, Thiophenyl, Phenethyl, -N[C(=O)- C1-5-Alkyl]-Phenyl, -NH-Phenyl, -N(C1-5-Alkyl)-Phenyl, -(CH2)-Pyridinyl, Pyridinyl, -O- Phenyl, -O-Benzyl, Phenyl und Benzyl mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus F1 Cl1 Br, -OH, -CF3, -SF5, -
CN1 -NO2, -d-s-Alkyl, -O-C1-5-Alkyl, -O-CF3, -S-CF3, Phenyl und -O-Benzyl substituiert sein kann,
und, sofern nicht anders angegeben, die vorstehend genannten (hetero)cycloaliphatischen Reste jeweils ggf. 1 , 2 oder 3 (weitere) Heteroatom(e) unabhängig voneinander ausgewählt aus der Gruppe bestehend aus Sauerstoff, Stickstoff und Schwefel aufweisen können;
die Ringe der vorstehend genannten mono- oder polyzyklischen Ringsysteme ggf. jeweils mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus Oxo (=O), Thioxo (=S), F, Cl, Br, I1 -CN, -CF3, -SF5, -OH, -O-Ci-5-Alkyl, -NH2, -NO2, -0-CF3, -S-CF3, -SH, -S-C1-5-Alkyl, -C1-5-Alkyl, -C(=O)-C1-5- Alkyl, -C(=O)-OH, -C(=O)-O-Ci-5-Alkyl, -NH-C1-5-Alkyl, -N(C1-5-Alkyl)2, -O-Phenyl, -O- Benzyl, Phenyl und Benzyl substituiert sein können, wobei jeweils der zyklische Teil der Reste -O-Phenyl, -O-Benzyl, Phenyl und Benzyl mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus F, Cl, Br, -OH, -CF3, -SF5, -CN, -NO2, -C1-5-Alkyl, -O-C1-5-Alkyl, -0-CF3, -S-CF3, Phenyl und -O-Benzyl substituiert sein kann,
und die Ringe der vorstehend genannten mono- oder polyzyklischen Ringsysteme jeweils 5-, 6- oder 7-gliedrig sind und jeweils ggf. 1 , 2, 3, 4 oder 5 Heteroatom(e) als Ringglied(er) aufweisen können, die unabhängig voneinander aus der Gruppe bestehend aus Sauerstoff, Stickstoff und Schwefel ausgewählt sind;
und die vorstehend genannten Aryl- oder Heteroaryl-Reste ggf. jeweils mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus F, Cl, Br, I, -CN, -CF3, -SF5, -OH, -O-Ci-5-Alkyl, -NH2, -NO2, -0-CF3, - S-CF3, -SH1 -S-Ci-5-Alkyl, -Ci-5-Alkyl, -C(=O)-OH, -C(=O)-O-Ci-5-Alkyl, -NH-C1-5-Alkyl, -N(Ci-5-Alkyl)2l -NH-S(=O)2-Ci-5-Alkyl, -NH-C(=O)-O-d-5-Alkyl, -C(=O)-H, -C(=O)-C1- 5-Alkyl, -C(=O)-NH2, -C(=O)-NH-Ci-5-Alkyl, -C(=O)-N-(C1-5-Alkyl)2, -O-Phenyl, -O- Benzyl, Phenyl und Benzyl substituiert sein können, wobei jeweils der zyklische Teil der Reste -O-Phenyl, -O-Benzyl, Phenyl und Benzyl mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus
F, Cl, Br, -OH, -CF3, -SF5, -CN, -NO2, -C1-5-Alkyl, -O-Ci-5-Alkyl, -0-CF3, -S-CF3, Phenyl und -O-Benzyl substituiert sein kann,
und
die vorstehend genannten Heteroaryl-Reste jeweils ggf. 1 , 2, 3, 4 oder 5 Heteroatom(e) unabhängig voneinander ausgewählt aus der Gruppe bestehend aus Sauerstoff, Stickstoff und Schwefel als Ringglied(er) aufweisen.
Der Begriff "Heteroalkylen" bezeichnet eine Alkylen-Kette, in dem ein oder mehrere C-Atome jeweils durch ein Heteroatom unabhängig voneinander ausgewählt aus der Gruppe bestehend aus Sauerstoff, Schwefel und Stickstoff (NH) ersetzt wurden. Heteroalkylen-Gruppen können bevorzugt 1 , 2 oder 3 Heteroatom(e), besonders bevorzugt ein Heteroatom, unabhängig voneinander ausgewählt aus der Gruppe bestehend aus Sauerstoff, Schwefel und Stickstoff (NH) als Kettenglied(er) aufweisen. Heteroalkylen-Gruppen können bevorzugt 2- bis 6-gliedrig, besonders bevorzugt 2- oder 3-gliedrig, sein.
Beispielhaft seien Heteroalkylen-Gruppen wie -CH2-CH2-O-CH2-, -CH2-CH(CH3)-O- CH2-, -(CH2)-O-, -(CH2J2-O-, -(CH2)3-O-, -(CH2)4-O-, -0-(CH2)-, -O-(CH2)2-, -O-(CH2)3- , -O-(CH2)4-, -C(C2H5)(H)-O-, -0-C(C2H5)(H)-, -CH2-O-CH2-, -CH2-S-CH2-, -CH2-NH- CH2-, -CH2-NH- und -CH2-CH2-NH-CH2-CH2 genannt.
Sofern einer oder mehrere der vorstehend genannten Substituenten eine lineare oder verzweigte Ci-β-Alkylen-Gruppe aufweisen, kann diese bevorzugt ausgewählt werden aus der Gruppe bestehend aus -(CH2)-, -(CH2J2-, -C(H)(CH3)-, -(CH2)3-, - (CH2)4-, -(CH2)S-, -C(H)(C(H)(CH3)2)- und -C(C2H5)(H)-.
Gesättigte oder ungesättigte Ci.-io aliphatischen Reste können für einen Ci-io-Alkyl-, C2-io-Alkenyl- oder C2-i0-Alkinyl-Rest stehen. C2-i0-Alkenyl-Reste weisen wenigstens eine, vorzugsweise 1 , 2, 3 oder 4 C-C-Doppelbindungen und C2-1o-Alkinyl-Reste wenigstens eine, vorzugsweise 1 , 2, 3 oder 4 C-C-Dreifachbindungen auf.
Bevorzugt sind Ci.io-Alkyl-Reste ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl, n-Pentyl, 3-Methyl- but-1-yl, 2-Pentyl, 3-Pentyl, sec-Pentyl, neo-Pentyl, 4-Methyl-pent-1-yl, (3,3)- Dimethyl-but-1-yl, n-Hexyl, n-Heptyl, 2-Heptyl, 3-Heptyl, 4-Heptyl, n-Octyl, n-Nonyl, 2- Nonyl, 3-Nonyl, 4-Nonyl, 5-Nonyl und (2,6)-Dimethyl-hept-4-yl, die ggf. mit 1 , 2, 3, 4, 5, 6, 7, 8 oder 9 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus -O-Phenyl, -O-C(=O)-CH3, -O-C(=O)-C2H5, -O-C(=O)-CH(CH3)2, -O- C(=O)-C(CH3)3, -C(=O)-O-CH3, -C(=O)-O-C2H5) -C(=O)-O-CH(CH3)2, -C(=O)-O- C(CH3)3, F, Cl, Br, I1 -CN, -NO2, -OH, -NH2, -SH, -0-CH3, -0-C2H5, -O-CH(CH3)2, -O- C(CH3)3, -S-CH3, -S-C2H5, -S-CH(CH3)2, -S-C(CH3)3, -NH-CH3, -NH-C2H5, -NH- C(CHa)3, -N(CH3)2, -N(C2H5)2, -N(CH3)(C2H5), -OCF3 und -SCF3 substituiert sein können.
Ebenfalls bevorzugt sind C2-io-Alkenyl-Reste ausgewählt aus der Gruppe bestehend aus Vinyl, 1-Propenyl, 2-Propenyl, 1-Butenyl, 2-Butenyl, 3-Butenyl, 2-Methyl-propen- 1-yl, 3-Methyl-but-2-en-1-yl, (3,3)-Dimethyl-but-1-enyl, 2-Methyl-buten-2-yl, 1- Pentenyl, 2-Pentenyl, 3-Pentenyl, 4-Pentenyl, 1-Hexenyl, 1-Heptenyl und 1-Octenyl, die ggf. mit 1 , 2 oder 3 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus F, Cl, Br, I, -CN, -NO2, -OH, -NH2, -SH, -0-CH3, -0-C2H5, -O- CH(CH3)2, -O-C(CH3)3, -S-CH3, -S-C2H5, -S-CH(CH3)2, -S-C(CH3)3, -NH-CH3, -NH- C2H5, -NH-C(CH3J3, -N(CH3)2, -N(C2H5)2, -N(CH3)(C2H5), -OCF3 und -SCF3 substituiert sein können.
Weiterhin bevorzugt sind C2-i0-Alkinyl-Reste ausgewählt aus der Gruppe bestehend aus (3,3)-Dimethyl-but-1-inyl, 4-Methyl-pent-1-inyl, 1-Hexinyl, Ethinyl, 1-Propinyl, 2- Propinyl, 1-Butinyl, 2-Butinyl, 3-Butinyl, 1-Pentinyl, 2-Pentinyl, 3-Pentinyl und 4- Pentinyl, die ggf. mit 1 , 2 oder 3 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus F, Cl, Br, I, -CN, -NO2, -OH, -NH2, -SH, -0-CH3, -O- C2H5, -O-CH(CH3)2, -O-C(CH3)3, -S-CH3, -S-C2H5, -S-CH(CH3)2, -S-C(CH3)3) -NH- CH3, -NH-C2H5, -NH-C(CH3)3, -N(CH3J2, -N(C2H5)2, -N(CH3)(C2H5), -OCF3 und -SCF3 substituiert sein können.
Besonders bevorzugte ggf. substituierte C1-10 aliphatische Rest sind ausgewählt aus der Gruppe bestehend aus Methyl, -CF3, -CHF2, -CH2F1 -CF2CI, -CCI2F, -CCI3, -CBr3, -CH2-CN, -CH2-O-CH3, -CH2-O-CF3, -CH2-SF3, -CH2-NH2, -CH2-OH, -CH2-SH1 -CH2- NH-CH3, -CH2-N(CH3)2, -CH2-N(C2Hs)2, -CH2-N(CH3)(C2H5), Ethyl, -CF2-CH3, -CHF- CF2CI, -CF2-CFCI2, -CFCI-CF2CI1 -CFCI-CFCI2, -CH2-CH2-NH2. -CH2-CH2-OH1 -CH2- CH2-SH, -CH2-CH2-NH-CH3, -CH2-CH2-N(CH3)2, -CH2-CH2-N(C2Hs)2, -CH2-CH2- N(CH3)(C2H5), -CH2-CF3, -C2F5, -CH2-CCI3, -CH2-CBr3, -CH2-CH2-CN, n-Propyl, - CH2-CH2-CH2-OH, -CH2-CH2-CH2-SH1 -CH2-CH2-CH2-NH2, -CH2-CH2-CH2-NH-CH3, - CH2-CH2-CH2-N(CH3)2l -CH2-CH2-CH2-N(C2Hs)2, -CH2-CH2-CH2-N(CH3)(C2H5), -CH2- CH2-O-CH3, -CF2-CF2-CF3, -CF(CF3)2, Isopropyl, -CH2-CH2-CH2-CN, -CH2-O-CH2- CH3, -CH2-CH2-SF3, -CH2-CH2-OCF3, -CH(CH3)(O-CH3), -CH(CH3)(S-CH3), n-Butyl, - CF2-CF2-CF2-CF3, -CH2-CH2-CH2-CH2-CN, -CH2-CH2-CH2-CF3, -CH2-CH2-CH2-CH2- CF3, -CH2-O-C(=O)-CH3l -CH2-O-C(=O)-C2H5, -CH2-O-C(=O)-CH(CH3)2, -CH2-O- C(=O)-C(CH3)3l -CH2-C(=O)-O-CH3, -CH2-C(=O)-O-C2H5, -CH2-C(=O)-O-C(CH3)3, - CH2-CH2-O-CH3, -CH2-CH2-O-C2H5, -CH2-CH2-O-Phenyl, -CH2-CH2-CH2-O-CH3, sek- Butyl, Isobutyl, tert-Butyl, n-Pentyl, sec-Pentyl, neo-Pentyl, n-Hexyl, Vinyl, 1- Propenyl, 2-Propenyl, 1-Butenyl, 2-Butenyl, 3-Butenyl, 2-Methyl-buten-2-yl, (1 ,1 ,2)- Trifluor-1-butenyl, 1-Pentenyl, 2-Pentenyl, 3-Pentenyl, 4-Pentenyl, -CF=CF2, - CCI=CCI2, -CH2-CF=CF2, -CH2-CCI=CCI2, -C≡C-I, -C≡C-F und -C≡C-CI.
Sofern einer oder mehrere der vorstehend genannten Substituenten für einen (hetero)cycloaliphatischen Rest stehen, der ggf. mit einem gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten mono- oder polyzyklischen Ringsystem kondensiert sein kann, kann dieser bevorzugt ausgewählt werden aus der Gruppe bestehend aus Cyclopropyl, Cyclobutyl, Cyclopentyl, Cyclohexyl, Cycloheptyl, Cyclopentenyl, Cyclohexenyl, Cycloheptenyl, Imidazolidinyl, Tetrahydrofuranyl, Tetrahydrothiophenyl, Pyrrolidinyl, Piperidinyl, Morpholinyl, Piperazinyl, Thiomorpholinyl, Tetrahydropyranyl, Oxetanyl, (1 ,2,3,6)- Tetrahydropyridinyl, Azepanyl, Azocanyl, Diazepanyl, Dithiolanyl, (1 ,3,4,5)- Tetrahydropyrido[4,3-b]indolyl, (3,4)-Dihydro-1 H-isochinolinyl, (1 ,3,4,9)-Tetrahydro- [b]-carbolinyl und (1 ,3)-Thiazolidinyl.
Als geeignete (hetero)cycloaliphatische Reste, die unsubstituiert oder einfach oder mehrfach substituiert sein können, und mit einem mono- bzw. bizyklischem Ringsystem kondensiert sind, seien beispielhaft (4,5,6,7)-Tetrahydroisoxazolo[5,4- φyridinyl, (2,3)-Dihydro-1 H-indenyl, 3-Aza-bicyclo[3.1.1]heptyl, 3-Aza- bicyclo[3.2.1]octyl, 6-Aza-bicyclo[3.3.1]heptyl, 8-Aza-bicyclo[3.2.1]octyl, Isoindolyl, Indolyl, (1 ,2,3,4)-Tetrahydrochinolinyl, (1 ,2,3,4)-Tetrahydroisochinolinyl, (2,3)- Dihydro-1 H-isoindolyl, (1 ,2,3,4)-Tetrahydronaphthyl, (2,3)-Dihydro-benzo[1.4]dioxinyl, Benzo[1.3]dioxolyl, (1 ,4)-Benzodioxanyl, (2,3)-dihydrothieno[3,4-b][1 ,4]dioxinyl, (3,4)- Dihydro-2H-benzo[1.4]oxazinyl, Octahydro-1 H-isoindolyl und Octahydro-pyrrolo[3,4- c]pyrrolyl genannt.
(Hetero)cycloaliphatische Reste können im Sinne der vorliegenden Erfindung mit einem weiteren (hetero)cycloaliphatischen Rest über ein gemeinsames Kohlenstoffatom in beiden Ringen einen spirozyklischen Rest bilden.
Als geeignete spirozyklischer Reste seien beispielsweise ein 6-Aza-spiro[2.5]octyl- Rest, 8-Azaspiro[4.5]decyl-Rest und ein 1-Oxa-2,8-diaza-spiro[4.5]dec-2-enyl-Rest genannt.
Besonders bevorzugt können die (hetero)cycloaliphatischen Reste ggf. jeweils mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus Oxo (=0), Thioxo (=S), F, Cl, Br, I, -CN, -CF3, -SF5, -OH, -0-CH3, -O- C2H5, -O-CH(CH3)2> -O-C(CH3)3, -NH2, -NO2, -O-CF3, -S-CF3, -SH, -S-CH3, -S-C2H5, - S-CH(CH3)2, -S-C(CH3)3, Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl, n-Pentyl, -C(=O)-CH3, -C(=O)-C2H5, -C(=O)-CH(CH3)2, -C(=O)- C(CH3J3, -C(=O)-OH, -C(=O)-O-CH3, -C(=O)-O-C2H5, -C(=O)-O-CH(CH3)2, -C(=O)-O- C(CHa)3, -NH-CH3, -NH-C2H5, -NH-C(CH3)3, -N(CH3)2, -N(C2H5),, -N(CH3)(C2H5), - CH2-OH, -CH2-CH2-OH, =CH2, -CH2-O-CH2-Oxetanyl, -O-CH2-Oxetanyl, -CH2- N(CH3)2, -CH2-N(C2Hs)2, -CH2-NH-CH3, -CH2-NH-C2H5, -N-[C(=O)-C2H5]-Phenyl, -N- [C(=O)-CH3]-Phenyl, -CH2-O-CH3, -CH2-O-CH2-CH3, -NH-Phenyl, -N(CH3)-Phenyl, - N(C2H5)-Phenyl, -N(C2H5)-Phenyl, -0-CH2-CH2-CH2-CH3, (4,5)-Dihydroisoxazolyl, Thiazolyl, (1 ,2,5)-Thiadiazolyl, Thiophenyl, Phenethyl, Cyclohexyl, Cyclopentyl, Piperidinyl, Pyrrolidinyl, -O-C(=O)-CH3, -O-C(=O)-C2H5, -O-C(=O)-C(CH3)3, -(CH2)- Pyridinyl, Pyridinyl, -O-Phenyl, -O-Benzyl, Phenyl und Benzyl substituiert sein, wobei
jeweils der zyklische Teil der Reste Oxetanyl, (4,5)-Dihydroisoxazolyl, Thiazolyl, (1 ,2,5)-Thiadiazolyl, Thiophenyl, Phenethyl, -N-[C(=O)-C2H5]-Phenyl, -N-[C(=O)- CH3]-Phenyl, -NH-Phenyl, -N(CH3)-Phenyl, -N(C2H5)-Phenyl, -(CH2)-Pyridinyl, Pyridinyl, -O-Phenyl, -O-Benzyl, Phenyl und Benzyl mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus F, Cl, Br, -OH, -CF3, -SF5, -CN, -NO2, Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek- Butyl, Isobutyl, tert-Butyl, -0-CH3, -0-C2H5, -O-CH(CH3)2, -O-C(CH3)3l -0-CF3, -S- CF3, Phenyl und -O-Benzyl substituiert sein kann.
Sofern einer oder mehrere der vorstehend genannten Substituenten für einen Aryl- Rest stehen, kann dieser bevorzugt ausgewählt werden aus der Gruppe bestehend aus Phenyl und Naphthyl (1-Naphthyl und 2-Naphthyl).
Sofern einer oder mehrere der vorstehend genannten Substituenten für einen Heteroaryl-Rest stehen, kann dieser bevorzugt ausgewählt werden aus der Gruppe bestehend aus Tetrazolyl, Thiophenyl, Furanyl, Pyrrolyl, Pyrazolyl, Pyrazinyl, Pyranyl, Triazolyl, Pyridinyl, Imidazolyl, Indolyl, Isoindolyl, Benzo[b]furanyl, Benzo[b]thiophenyl, Benzoxazolyl, Benzisoxazolyl, Thiazolyl, Oxazolyl, Isoxazolyl, Pyridazinyl, Pyrazinyl, Pyrimidinyl, Indazolyl, Chinoxalinyl, Chinolinyl und Isochinolinyl.
Als geeignete Aryl- und Heteroaryl-Reste, die unsubstituiert oder einfach oder mehrfach substituiert sein können, und mit einem mono- bzw. bizyklischem Ringsystem kondensiert sind, seien beispielhaft Isoindolyl, Indolyl, (1 ,2,3,4)- Tetrahydrochinolinyl, (1 ,2,3,4)-Tetrahydroisochinolinyl, (2,3)-Dihydro-1 H-isoindolyl, (1 ,2,3,4)-Tetrahydronaphthyl, (2,3)-Dihydro-benzo[1.4]dioxinyl, (2,3)- Dihydrothieno[3,4-b][1 ,4]dioxinyl, Benzo[1.3]dioxolyl und (1 ,4)-Benzodioxanyl genannt.
Besonders bevorzugt können die Aryl- oder Heteroaryl-Reste ggf. jeweils mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus F1 Cl, Br, I, -CN, -CF3, -SF5, -OH, -0-CH3, -0-C2H5, -O-CH(CH3)2, -O- C(CH3J3, -NH2, -NO2, -O-CF3, -S-CF3, -SH, -S-CH3, -S-C2H5, -S-CH(CH3J2, -S- C(CH3)3, Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl, n-
Pentyl, -C(=O)-OH, -C(=O)-O-CH3, -C(=O)-O-C2H5, -C(=O)-O-CH(CH3)2, -C(=O)-O- C(CHa)3, -NH-CH3, -NH-C2H5, -NH-C(CH3)3, -N(CH3)2, -N(C2H5)2, -N(CH3)(C2H5), - NH-S(=O)2-CH3l -NH-S(=O2)-C2H5, -NH-S(=O)2-CH(CH3)2) -NH-C(=O)-O-CH3, -NH- C(=O)-O-C2H5> -NH-C(=O)-O-C(CH3)3, -C(=O)-H, -C(=O)-CH3, -C(=O)-C2H5, -C(=O)- CH(CHa)2, -C(=O)-C(CH3)3, -C(=O)-NH2, -C(=O)-NH-CH3, -C(=O)-NH-C2H5, -C(=O)- N(CH3)2, -C(=O)-N(C2H5)2> -O-Phenyl, -O-Benzyl, Phenyl und Benzyl substituiert sein, wobei jeweils der zyklische Teil der Reste -O-Phenyl, -O-Benzyl, Phenyl und Benzyl mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus F, Cl, Br, -OH, -CF3, -SF5, -CN, -NO2, Methyl, Ethyl, n- Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl, -0-CH3, -0-C2H5, -O- CH(CH3)2, -O-C(CH3)3, -O-CF3, -S-CF3, Phenyl und -O-Benzyl substituiert sein kann.
Sofern ein polyzyklisches Ringsystem wie beispielsweise ein bizyklisches Ringsystem vorliegt, können die verschiedenen Ringe, jeweils unabhängig voneinander, einen unterschiedlichen Sättigungsgrad aufweisen, d.h. gesättigt oder ungesättigt sein. Bevorzugt ist ein polyzyklisches Ringsystem ein bizyklisches Ringsystem.
Beispielhaft für Aryl-Reste, die mit einem mono- bzw. polyzyklischen Ringsystem kondensiert sind, seien (1 ,3)-Benzodioxolyl und (1 ,4)-Benzodioxanyl genannt.
Sofern einer oder mehrere der vorstehend genannten Substituenten ein mono- oder polyzyklisches Ringsystem aufweisen, kann dieses bevorzugt mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus Oxo (=0), Thioxo (=S), F, Cl, Br1 I, -CN, -CF3, -SF5, -OH, -0-CH3, -0-C2H5, -O- CH(CH3)2, -O-C(CH3)3, -NH2, -NO2, -0-CF3, -S-CF3, -SH, -S-CH3, -S-C2H5, -S- CH(CH3)2, -S-C(CH3)3, Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl, n-Pentyl, -C(=O)-OH, -C(=O)-O-CH3, -C(=O)-O-C2H5, -C(=O)-O-CH(CH3)2, -C(=O)-O-C(CH3)3, -NH-CH3, -NH-C2H5, -NH-C(CHa)3, -N(CH3)2, -N(C2H5)2, - N(CH3)(C2H5), -NH-C(=O)-O-CH3, -NH-C(=O)-O-C2H5, -NH-C(=O)-O-C(CH3)3, - C(=O)-H, -C(=O)-CH3, -C(=O)-C2H5, -C(=O)-CH(CH3)2, -C(=O)-C(CH3)3, -C(=O)-NH2, -C(=O)-NH-CH3, -C(=O)-NH-C2H5, -C(=O)-N(CH3)2, -C(=O)-N(C2H5)2, -O-Phenyl, -O- Benzyl, Phenyl und Benzyl substituiert sein, wobei jeweils der zyklische Teil der Reste -O-Phenyl, -O-Benzyl, Phenyl und Benzyl mit 1 , 2, 3, 4 oder 5 Substituenten
unabhängig voneinander ausgewählt aus der Gruppe bestehend aus F, Cl, Br, -OH, CF3, -SF5, -CN, -NO2, Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl, -O-CH3, -0-C2H5, -O-CH(CH3)2, -O-C(CH3)3, -0-CF3, -S-CF3, Phenyl und - O-Benzyl substituiert sein kann.
Bevorzugt sind Verbindungen der allgemeinen Formel Ia,
Ia,
worin
D für N oder CH steht;
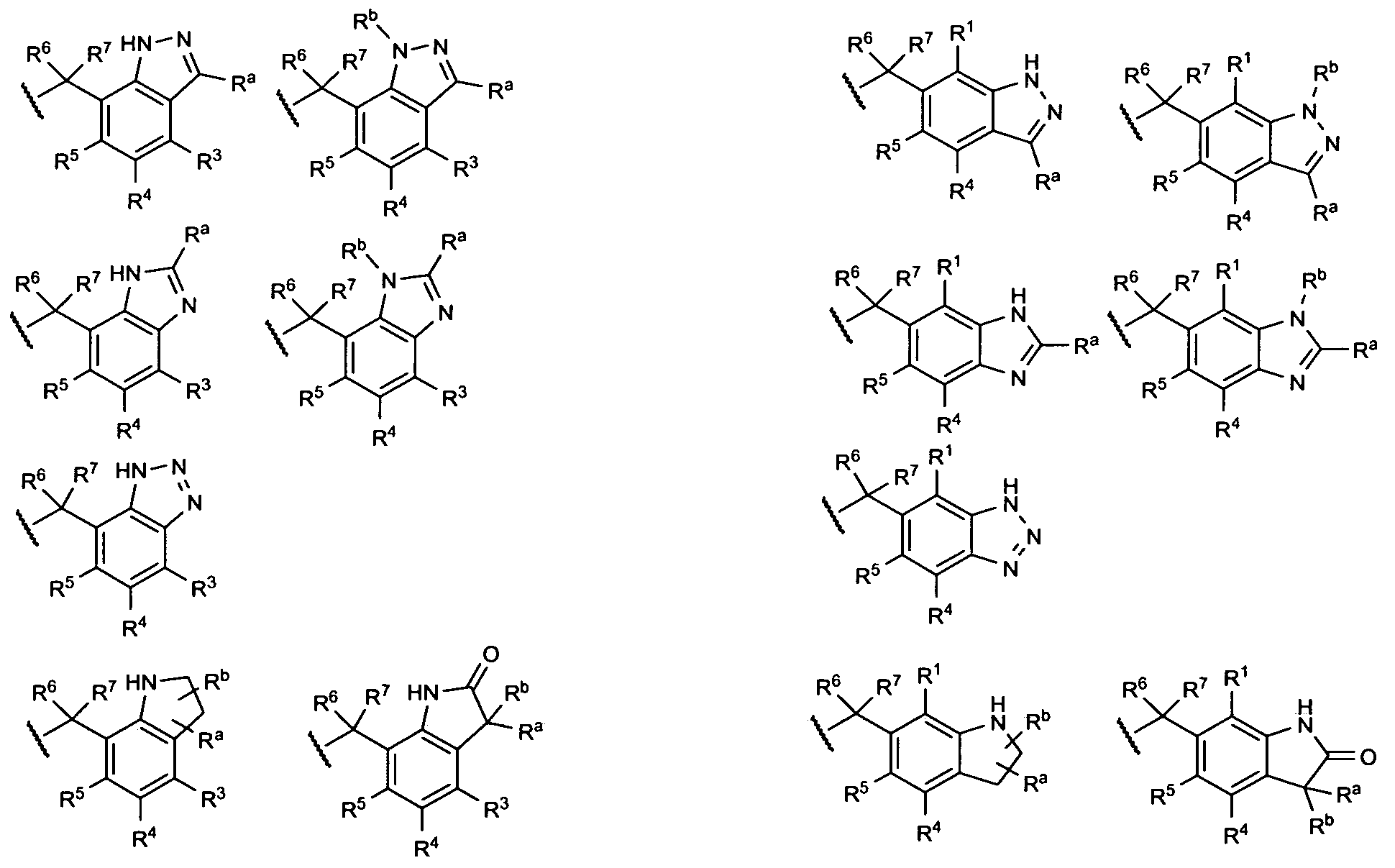
R1 und R2 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus - CH=N-NH-; -CH=N-NR71-; -S-C(=S)-NH-; -O-C(=S)-NH-; -S-C(=O)-NH-; -O-C(=O)- NH-; -S-C(=S)-NR63-; -O-C(=S)-NR63-; -S-C(=O)-NR63-; -O-C(=O)-NR63-; -S-CH=N-; - S-CR29=N-; -N=CH-O-; -N=CR30-O-; -NH-C(=O)-NH-; -NH-C(=S)-NH-; -NR66-C(=O)- NR65-; -NR66-C(=S)-NR65-; -O-CH2-C(=O)-NH-; -0-CH2-O-; -0-CH2-CH2-O-, -O-CH2- CH2-CH2-O-; -0-CH2-CH2-NH- und -CH=CH-N=CH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R2 und R3 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CR28=N-NH-; -CH=N-NR62-; -CR28=N-NR62-; -S-C(=S)-NH-; -O-C(=S)- NH-; -S-C(=O)-NH-; -O-C(=O)-NH-; -S-C(=S)-NR63-; -O-C(=S)-NR63-; -S-C(=O)-NR63- ; -O-C(=O)-NR63-; -S-CH=N-; -S-CR29=N-; -N=CH-O-; -N=CR30-O-; -N=CH-NH-; - N=CH-NR64-; -NH-C(=O)-NH-; -NH-C(=S)-NH-; -NR66-C(=O)-NR65-; -NR66-C(=S)- NR65-; -N=N-NH-; -N=N-NR67-; -O-CH2-C(=O)-NH-; -0-CH2-O-; -CH2-CH2-NH-, -CH2- CH2-CH2-NH, -CH2-C(=O)-NH, -CH2-CH2-C(=O)-NH-; -0-CH2-CH2-O-; -0-CH2-CH2- CH2-O-; -N=N-CH=CH-; -N=CH-N=CH; -N=CH-CH=N-; -CH=CH-CH=N-; -CH=CH-
N=CH-; -CH=N-N=CH- und -0-CH2-CH2-NH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R3 und R4 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CR28=N-NH-; -CH=N-NR62-; -CR28=N-NR62-; -S-C(=S)-NH-; -O-C(=S)- NH-; -S-C(=O)-NH-; -O-C(=O)-NH-; -S-C(=S)-NR63-; -O-C(=S)-NR63-; -S-C(=O)-NR63- ; -O-C(=O)-NR63-; -S-CH=N-; -S-CR29=N-; -N=CH-O-; -N=CR30-O-; -N=CH-NH-; - N=CH-NR64-; -NH-C(=O)-NH-; -NH-C(=S)-NH-; -NR66-C(=O)-NR65-; -NR66-C(=S)- NR65-; -N=N-NH-; -N=N-NR67-; -O-CH2-C(=O)-NH-; -0-CH2-O-; -CH2-CH2-NH-, -CH2- CH2-CH2-NH, -CH2-C(=O)-NH, -CH2-CH2-C(=O)-NH-; -0-CH2-CH2-O-; -0-CH2-CH2- CH2-O-; -N=N-CH=CH-; -N=CH-N=CH; -N=CH-CH=N-; -CH=CH-CH=N-; -CH=CH- N=CH-; -CH=N-N=CH- und -0-CH2-CH2-NH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R4 und R5 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CH=N-NR71-; -S-C(=S)-NH-; -O-C(=S)-NH-; -S-C(=O)-NH-; -O-C(=O)- NH-; -S-C(=S)-NR63-; -O-C(=S)-NR63-; -S-C(=O)-NR63-; -O-C(=O)-NR63-; -S-CH=N-; - S-CR29=N-; -N=CH-O-; -N=CR30-O-; -NH-C(=O)-NH-; -NH-C(=S)-NH-; -NR66-C(=O)- NR65-; -NR66-C(=S)-NR65-; -O-CH2-C(=O)-NH-; -0-CH2-O-; -0-CH2-CH2-O-, -O-CH2- CH2-CH2-O-; -0-CH2-CH2-NH- und -CH=CH-N=CH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
und die übrigen Reste von R1, R2, R3, R4 und R5, unabhängig voneinander, jeweils für H; F; Cl; Br; I; -CF3; -CN; -OR16; -SR17; oder für einen Rest ausgewählt aus der Gruppe bestehend aus Methyl, -CF3, -CHF2, -CH2F, Ethyl, n-Propyl, Isopropyl, n- Butyl, sek-Butyl, Isobutyl und tert-Butyl stehen;
R8 für -SF5; -0-CF3; -CF3; tert-Butyl oder -C(CH3)2 (CH2OH) steht;
R16 und R17, unabhängig voneinander, jeweils für einen Rest ausgewählt aus der Gruppe bestehend aus Methyl, -CF3, -CHF2, -CH2F, Ethyl, -CF2-CH3, -CH2-CF3, - C2F5, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl, n-Pentyl, 3-Pentyl, n- Heptyl, 4-Heptyl, n-Octyl, n-Nonyl, 5-Nonyl, (2,6)-Dimethyl-hept-4-yl, 3-Methyl-butyl,
n-Hexyl und (3,3)-Dimethylbutyl stehen;
R28 für F; Cl; Br; I; -CF3; -CN; -NH2 oder für einen Alkyl-Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl und n-Pentyl steht;
R29 und R30, unabhängig voneinander, jeweils für -NH-C(=O)-R31; -NH2; -NH-S(=O)2-R32; -NH-C(=O)-O-R33; -S-R34 oder für einen Alkyl-Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl und n-Pentyl stehen;
R31, R32, R33 und R34, unabhängig voneinander, jeweils für Alkyl-Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, n- Butyl, sek-Butyl, Isobutyl, tert-Butyl und n-Pentyl stehen;
R62, R63, R64, R65, R66 und R67, unabhängig voneinander, jeweils für einen Alkyl-Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, tert-Butyl, n-Butyl, sek-Butyl und Isobutyl stehen; und
R71 für einen Rest steht ausgewählt aus der Gruppe bestehend aus Phenyl, Naphthyl, Thiophenyl, Furanyl und Pyridinyl, wobei der Rest jeweils über eine -(CH2)- , -(CH2)2- oder -(CH2)3-Gruppe gebunden sein kann und/oder jeweils unsubstituiert oder ggf. mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus F, Cl, Br, I, -CN, -CF3, -SF5, -OH, -O-CH3, -0-C2H5, -O- CH(CH3)2, -O-C(CH3)3, -NH2, -NO2, -0-CF3, -S-CF3, -SH, -S-CH3, -S-C2H5, -S- CH(CH3)2, -S-C(CH3)3, Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl, -O-Phenyl, -O-Benzyl, Phenyl und Benzyl substituiert sein kann;
jeweils ggf. in Form eines ihrer reinen Stereoisomeren, insbesondere Enantiomeren oder Diastereomeren, ihrer Racemate oder in Form einer Mischung von Stereoisomeren, insbesondere der Enantiomeren und/oder Diastereomeren, in einem beliebigen Mischungsverhältnis, oder jeweils in Form entsprechender Salze, oder jeweils in Form entsprechender Solvate.
Besonders bevorzugt sind Verbindungen der allgemeinen Formel Ia,
Ia,
worin
D für N oder CH steht;
R1 und R2 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus - CH=N-NH-; -CH=N-NR71-; -S-C(=S)-NH-; -O-C(=S)-NH-; -S-C(=O)-NH-; -O-C(=O)- NH-; -S-C(=S)-NR63-; -O-C(=S)-NR63-; -S-C(=O)-NR63-; -O-C(=O)-NR63-; -S-CH=N-; - S-CR29=N-; -N=CH-O-; -N=CR30-O-; -NH-C(=O)-NH-; -NH-C(=S)-NH-; -NR66-C(=O)- NR65-; -NR66-C(=S)-NR65-; -O-CH2-C(=O)-NH-; -0-CH2-O-; -0-CH2-CH2-O-, -0-CH2- CH2-CH2-O-; -0-CH2-CH2-NH- und -CH=CH-N=CH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R2 und R3 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CR28=N-NH-; -CH=N-NR62-; -CR28=N-NR62-; -S-C(=S)-NH-; -O-C(=S)- NH-; -S-C(=O)-NH-; -O-C(=O)-NH-; -S-C(=S)-NR63-; -O-C(=S)-NR63-; -S-C(=O)-NR63- ; -O-C(=O)-NR63-; -S-CH=N-; -S-CR29=N-; -N=CH-O-; -N=CR30-O-; -N=CH-NH-; - N=CH-NR64-; -NH-C(=O)-NH-; -NH-C(=S)-NH-; -NR66-C(=O)-NR65-; -NR66-C(=S)- NR65-; -N=N-NH-; -N=N-NR67-; -O-CH2-C(=O)-NH-; -0-CH2-O-; -CH2-CH2-NH-, -CH2- CH2-CH2-NH, -CH2-C(=O)-NH, -CH2-CH2-C(=O)-NH-; -0-CH2-CH2-O-; -0-CH2-CH2- CH2-O-; -N=N-CH=CH-; -N=CH-N=CH; -N=CH-CH=N-; -CH=CH-CH=N-; -CH=CH- N=CH-; -CH=N-N=CH- und -0-CH2-CH2-NH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R3 und R4 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CR28=N-NH-; -CH=N-NR62-; -CR28=N-NR62-; -S-C(=S)-NH-; -O-C(=S)- NH-; -S-C(=O)-NH-; -O-C(=O)-NH-; -S-C(=S)-NR63-; -O-C(=S)-NR63-; -S-C(=O)-NR63- ; -O-C(=O)-NR63-; -S-CH=N-; -S-CR29=N-; -N=CH-O-; -N=CR30-O-; -N=CH-NH-; - N=CH-NR64-; -NH-C(=O)-NH-; -NH-C(=S)-NH-; -NR66-C(=O)-NR65-; -NR66-C(=S)- NR65-; -N=N-NH-; -N=N-NR67-; -O-CH2-C(=O)-NH-; -0-CH2-O-; -CH2-CH2-NH-, -CH2- CH2-CH2-NH, -CH2-C(=O)-NH, -CH2-CH2-C(=O)-NH-; -0-CH2-CH2-O-; -0-CH2-CH2- CH2-O-; -N=N-CH=CH-; -N=CH-N=CH; -N=CH-CH=N-; -CH=CH-CH=N-; -CH=CH- N=CH-; -CH=N-N=CH- und -0-CH2-CH2-NH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R4 und R5 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CH=N-NR71-; -S-C(=S)-NH-; -O-C(=S)-NH-; -S-C(=O)-NH-; -O-C(=O)- NH-; -S-C(=S)-NR63-; -O-C(=S)-NR63-; -S-C(=O)-NR63-; -O-C(=O)-NR63-; -S-CH=N-; - S-CR29=N-; -N=CH-O-; -N=CR30-O-; -NH-C(=O)-NH-; -NH-C(=S)-NH-; -NR66-C(=O)- NR65-; -NR66-C(=S)-NR65-; -O-CH2-C(=O)-NH-; -0-CH2-O-; -0-CH2-CH2-O-, -O-CH2- CH2-CH2-O-; -0-CH2-CH2-NH- und -CH=CH-N=CH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
und die übrigen Reste von R1, R2, R3, R4 und R5, unabhängig voneinander, jeweils für H; -OR16; -SR17; oder für einen Rest ausgewählt aus der Gruppe bestehend aus Methyl, -CF3, -CHF2, -CH2F, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl und tert-Butyl stehen;
R16 und R17, unabhängig voneinander, jeweils für einen Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl und n-Pentyl stehen;
R28 für F; Cl; Br oder I steht;
R29 und R30, unabhängig voneinander, jeweils für -NH-C(=O)-R31; -NH2; -NH-S(=O)2-R32; -NH-C(=O)-O-R33 oder -S-R34 stehen;
R31, R32, R33 und R34, unabhängig voneinander, jeweils für Alkyl-Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, n- Butyl, sek-Butyl, Isobutyl, tert-Butyl und n-Pentyl stehen;
und R62, R63, R64, R65, R66 und R67, unabhängig voneinander, jeweils für einen Alkyl-Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, tert-Butyl, n-Butyl, sek-Butyl und Isobutyl stehen; und
R71 für einen Rest steht ausgewählt aus der Gruppe bestehend aus Phenyl, Naphthyl, Thiophenyl, Furanyl und Pyridinyl, wobei der Rest jeweils über eine -(CH2)- , -(CH2)2- oder -(CH2)3-Gruppe gebunden sein kann und/oder jeweils unsubstituiert oder ggf. mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus F, Cl, Br, I, -CN, -CF3, -SF5, -OH1 -O-CH3, -0-C2H5, -O- CH(CH3)2, -O-C(CH3)3, -NH2, -NO2, -0-CF3, -S-CF3, -SH, -S-CH3, -S-C2H5, -S- CH(CH3)2, -S-C(CH3)3, Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl, -O-Phenyl, -O-Benzyl, Phenyl und Benzyl substituiert sein kann;
jeweils ggf. in Form eines ihrer reinen Stereoisomeren, insbesondere Enantiomeren oder Diastereomeren, ihrer Racemate oder in Form einer Mischung von Stereoisomeren, insbesondere der Enantiomeren und/oder Diastereomeren, in einem beliebigen Mischungsverhältnis, oder jeweils in Form entsprechender Salze, oder jeweils in Form entsprechender Solvate.
Ganz besonders bevorzugt sind Verbindungen der allgemeinen Formel Ia,
Ia,
worin
für N oder CH steht;
R1 und R2 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -S-CH=N-; -S-CR29=N-; -N=CH-O- und -N=CR30-O- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R2 und R3 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CR28=N-NH-; -S-C(=S)-NH-; -O-C(=S)-NH-; -S-C(=O)- NH-; -O-C(=O)-NH-; -S-CH=N-; -S-CR29=N-; -N=CH-O-; -N=CR30-O-; -N=CH-NH-; - NH-C(=O)-NH-; -NH-C(=S)-NH-; -N=N-NH-; -O-CH2-C(=O)-NH-; -0-CH2-CH2-O-; -O- CH2-CH2-CH2-O-; -N=CH-CH=N-; -CH=CH-CH=N-; -CH=CH-N=CH-; -CH=N-N=CH- und -0-CH2-CH2-NH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R3 und R4 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CR28=N-NH-; -S-C(=S)-NH-; -O-C(=S)-NH-; -S-C(=O)- NH-; -O-C(=O)-NH-; -S-CH=N-; -S-CR29=N-; -N=CH-O-; -N=CR30-O-; -N=CH-NH-; - NH-C(=O)-NH-; -NH-C(=S)-NH-; -N=N-NH-; -O-CH2-C(=O)-NH-; -0-CH2-CH2-O-; -O- CH2-CH2-CH2-O-; -N=CH-CH=N-; -CH=CH-CH=N-; -CH=CH-N=CH-; -CH=N-N=CH- und -0-CH2-CH2-NH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R4 und R5 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -S-CH=N-; -S-CR29=N-; -N=CH-O- und -N=CR30-O- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
und die übrigen Reste von R1, R2, R3, R4 und R5, unabhängig voneinander, jeweils für H; -OR16; -SR17; oder für einen Rest ausgewählt aus der Gruppe bestehend aus Methyl, -CF3, -CHF2, -CH2F, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl und tert-Butyl stehen;
R8 für -SF5; -0-CF3; -CF3; tert-Butyl oder -C(CH3)2 (CH2OH) steht;
R16 und R17, unabhängig voneinander, jeweils für einen Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl und n-Pentyl stehen;
R28 für F; Cl; Br oder I steht;
R29 für -NH-C(=O)-R31 ; -NH2; -NH-S(=O)2-R32; -NH-C(=O)-O-R33 oder -S-R34 steht;
R30 für -NH2 steht;
R31, R32, R33 und R34, unabhängig voneinander, jeweils für Alkyl-Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, n- Butyl, sek-Butyl, Isobutyl, tert-Butyl und n-Pentyl stehen; und
R71 für einen Phenyl-Rest steht, der über eine -(CH2)-, -(CH2)2- oder -(CH2)3- Gruppe gebunden sein kann und/oder jeweils unsubstituiert oder ggf. mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus F1 Cl, Br, I, -CN, -CF3, -SF5, -OH, -0-CH3, -0-C2H5, Methyl, Ethyl, n- Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl und tert-Butyl;
jeweils ggf. in Form eines ihrer reinen Stereoisomeren, insbesondere Enantiomeren oder Diastereomeren, ihrer Racemate oder in Form einer Mischung von Stereoisomeren, insbesondere der Enantiomeren und/oder Diastereomeren, in einem beliebigen Mischungsverhältnis, oder jeweils in Form entsprechender Salze, oder jeweils in Form entsprechender Solvate.
Bevorzugt sind Verbindungen der allgemeinen Formel Ib,
Ib,
worin
D für N oder CH steht;
R1 und R2 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus - CH=N-NH-; -CH=N-NR71-; -S-C(=S)-NH-; -O-C(=S)-NH-; -S-C(=O)-NH-; -O-C(=O)- NH-; -S-C(=S)-NR63-; -O-C(=S)-NR63-; -S-C(=O)-NR63-; -O-C(=O)-NR63-; -S-CH=N-; - S-CR29=N-; -N=CH-O-; -N=CR30-O-; -NH-C(=O)-NH-; -NH-C(=S)-NH-; -NR66-C(=O)- NR65-; -NR66-C(=S)-NR65-; -O-CH2-C(=O)-NH-; -0-CH2-O-; -0-CH2-CH2-O-, -O-CH2- CH2-CH2-O-; -0-CH2-CH2-NH- und -CH=CH-N=CH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R2 und R3 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CR28=N-NH-; -CH=N-NR62-; -CR28=N-NR62-; -S-C(=S)-NH-; -O-C(=S)- NH-; -S-C(=O)-NH-; -O-C(=O)-NH-; -S-C(=S)-NR63-; -O-C(=S)-NR63-; -S-C(=O)-NR63- ; -O-C(=O)-NR63-; -S-CH=N-; -S-CR29=N-; -N=CH-O-; -N=CR30-O-; -N=CH-NH-; - N=CH-NR64-; -NH-C(=O)-NH-; -NH-C(=S)-NH-; -NR66-C(=O)-NR65-; -NR66-C(=S)- NR65-; -N=N-NH-; -N=N-NR67-; -O-CH2-C(=O)-NH-; -0-CH2-O-; -CH2-CH2-NH-, -CH2- CH2-CH2-NH, -CH2-C(=O)-NH, -CH2-CH2-C(=O)-NH-; -0-CH2-CH2-O-; -0-CH2-CH2- CH2-O-; -N=N-CH=CH-; -N=CH-N=CH; -N=CH-CH=N-; -CH=CH-CH=N-; -CH=CH- N=CH-; -CH=N-N=CH- und -0-CH2-CH2-NH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R3 und R4 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CR28=N-NH-; -CH=N-NR62-; -CR28=N-NR62-; -S-C(=S)-NH-; -O-C(=S)- NH-; -S-C(=O)-NH-; -O-C(=O)-NH-; -S-C(=S)-NR63-; -O-C(=S)-NR63-; -S-C(O)-NR63- ; -O-C(=O)-NR63-; -S-CH=N-; -S-CR29=N-; -N=CH-O-; -N=CR30-O-; -N=CH-NH-; - N=CH-NR64-; -NH-C(=O)-NH-; -NH-C(=S)-NH-; -NR66-C(=O)-NR65-; -NR66-C(=S)- NR65-; -N=N-NH-; -N=N-NR67-; -O-CH2-C(=O)-NH-; -0-CH2-O-; -CH2-CH2-NH-, -CH2- CH2-CH2-NH, -CH2-C(=O)-NH, -CH2-CH2-C(=O)-NH-; -0-CH2-CH2-O-; -0-CH2-CH2- CH2-O-; -N=N-CH=CH-; -N=CH-N=CH; -N=CH-CH=N-; -CH=CH-CH=N-; -CH=CH- N=CH-; -CH=N-N=CH- und -0-CH2-CH2-NH- stehen, der in beliebiger Richtung mit dem Grundgerϋst verbunden ist,
oder R4 und R5 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CH=N-NR71-; -S-C(=S)-NH-; -O-C(=S)-NH-; -S-C(=O)-NH-; -O-C(=O)- NH-; -S-C(=S)-NR63-; -O-C(=S)-NR63-; -S-C(=O)-NR63-; -O-C(=O)-NR63-; -S-CH=N-; - S-CR29=N-; -N=CH-O-; -N=CR30-O-; -NH-C(=O)-NH-; -NH-C(=S)-NH-; -NR66-C(=O)- NR65-; -NR66-C(=S)-NR65-; -O-CH2-C(=O)-NH-; -0-CH2-O-; -0-CH2-CH2-O-, -0-CH2- CH2-CH2-O-; -0-CH2-CH2-NH- und -CH=CH-N=CH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
und die übrigen Reste von R1, R2, R3, R4 und R5, unabhängig voneinander, jeweils für H; F; Cl; Br; I; -CF3; -CN; -OR16; -SR17; oder für einen Rest ausgewählt aus der Gruppe bestehend aus Methyl, -CF3, -CHF2, -CH2F, Ethyl, n-Propyl, Isopropyl, n- Butyl, sek-Butyl, Isobutyl und tert-Butyl stehen;
R8 für -SF5; -0-CF3; -CF3; tert-Butyl oder -C(CH3)2(CH2OH) steht;
R16 und R17, unabhängig voneinander, jeweils für einen Rest ausgewählt aus der Gruppe bestehend aus Methyl, -CF3, -CHF2, -CH2F, Ethyl, -CF2-CH3, -CH2-CF3, - C2F5, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl, n-Pentyl, 3-Pentyl, n- Heptyl, 4-Heptyl, n-Octyl, n-Nonyl, 5-Nonyl, (2,6)-Dimethyl-hept-4-yl, 3-Methyl-butyl, n-Hexyl und (3,3)-Dimethylbutyl stehen;
R28 für F; Cl; Br; I; -CF3; -CN; -NH2 oder für einen Alkyl-Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl und n-Pentyl steht;
R29 und R30, unabhängig voneinander, jeweils für -NH-C(=O)-R31; -NH2; -NH-S(=O)2-R32; -NH-C(=O)-O-R33; -S-R34 oder für einen Alkyl-Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl und n-Pentyl stehen;
R31, R32, R33 und R34, unabhängig voneinander, jeweils für Alkyl-Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl und n-Pentyl stehen;
R42 für einen Rest ausgewählt aus der Gruppe bestehend aus Methyl, -CH2-O- CH3, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl, n-Pentyl, 3- Pentyl, n-Hexyl, (3,3)-Dimethylbutyl, -CH2-CH2-O-CH3, -CH2-CH2-O-C2H5 und -CH2- CH2-CH2-O-CH3 steht;
oder für einen Rest ausgewählt aus der Gruppe bestehend aus 2,3-Dihydro-1 H- indenyl, Cyclopropyl, Oxetanyl, Cyclobutyl, Cyclopentyl, Cyclohexyl, Imidazolidinyl, Tetrahydrofuranyl, Tetrahydrothiophenyl, Pyrrolidinyl, Piperidinyl, Morpholinyl, Piperazinyl, Azepanyl, Diazepanyl, Azocanyl und Thiomorpholinyl, der jeweils ggf. mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert- Butyl, n-Pentyl substituiert sein kann, steht;
R62, R63, R64, R65, R66 und R67, unabhängig voneinander, jeweils für einen Alkyl-Rest ausgewählt aus der Gruppe bestehend aus -CF3, -CH2-CF3, Methyl, Ethyl, n-Propyl, Isopropyl, tert-Butyl, n-Butyl, sek-Butyl und Isobutyl stehen; und
R71 für einen Rest steht ausgewählt aus der Gruppe bestehend aus Phenyl, Naphthyl, Thiophenyl, Furanyl und Pyridinyl, wobei der Rest jeweils über eine -(CH2)- , -(CH2)2- oder -(CH2)3-Gruppe gebunden sein kann und/oder jeweils unsubstituiert oder ggf. mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus
der Gruppe bestehend aus F, Cl, Br, I1 -CN, -CF3, -SF5, -OH, -0-CH3, -0-C2H5, -O- CH(CH3)2, -O-C(CH3)3> -NH2, -NO2, -0-CF3, -S-CF3, -SH, -S-CH3, -S-C2H5, -S- CH(CH3)2, -S-C(CH3)3, Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl, -O-Phenyl, -O-Benzyl, Phenyl und Benzyl substituiert sein kann
jeweils ggf. in Form eines ihrer reinen Stereoisomeren, insbesondere Enantiomeren oder Diastereomeren, ihrer Racemate oder in Form einer Mischung von Stereoisomeren, insbesondere der Enantiomeren und/oder Diastereomeren, in einem beliebigen Mischungsverhältnis, oder jeweils in Form entsprechender Salze, oder jeweils in Form entsprechender Solvate.
Besonders bevorzugt sind Verbindungen der allgemeinen Formel Ib,
Ib,
worin
D für N oder CH steht;
R1 und R2 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus - CH=N-NH-; -CH=N-NR71-; -S-C(=S)-NH-; -O-C(=S)-NH-; -S-C(=O)-NH-; -O-C(=O)- NH-; -S-C(=S)-NR63-; -O-C(=S)-NR63-; -S-C(=O)-NR63-; -O-C(=O)-NR63-; -S-CH=N-; ■ S-CR29=N-; -N=CH-O-; -N=CR30-O-; -NH-C(=O)-NH-; -NH-C(=S)-NH-; -NR66-C(=O)- NR65-; -NR66-C(=S)-NR65-; -O-CH2-C(=O)-NH-; -0-CH2-O-; -0-CH2-CH2-O-, -0-CH2- CH2-CH2-O-; -0-CH2-CH2-NH- und -CH=CH-N=CH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R2 und R3 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CR28=N-NH-; -CH=N-NR62-; -CR28=N-NR62-; -S-C(=S)-NH-; -O-C(=S)- NH-; -S-C(=O)-NH-; -O-C(=O)-NH-; -S-C(=S)-NR63-; -O-C(=S)-NR63-; -S-C(=O)-NR63- ; -O-C(=O)-NR63-; -S-CH=N-; -S-CR29=N-; -N=CH-O-; -N=CR30-O-; -N=CH-NH-; - N=CH-NR64-; -NH-C(=O)-NH-; -NH-C(=S)-NH-; -NR66-C(=O)-NR65-; -NR66-C(=S)- NR65-; -N=N-NH-; -N=N-NR67-; -O-CH2-C(=O)-NH-; -0-CH2-O-; -CH2-CH2-NH-, -CH2- CH2-CH2-NH, -CH2-C(=O)-NH, -CH2-CH2-C(=O)-NH-; -0-CH2-CH2-O-; -0-CH2-CH2- CH2-O-; -N=N-CH=CH-; -N=CH-N=CH; -N=CH-CH=N-; -CH=CH-CH=N-; -CH=CH- N=CH-; -CH=N-N=CH- und -0-CH2-CH2-NH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R3 und R4 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CR28=N-NH-; -CH=N-NR62-; -CR28=N-NR62-; -S-C(=S)-NH-; -O-C(=S)- NH-; -S-C(=O)-NH-; -O-C(=O)-NH-; -S-C(=S)-NR63-; -O-C(=S)-NR63-; -S-C(=O)-NR63- ; -O-C(=O)-NR63-; -S-CH=N-; -S-CR29=N-; -N=CH-O-; -N=CR30O-; -N=CH-NH-; - N=CH-NR64-; -NH-C(=O)-NH-; -NH-C(=S)-NH-; -NR66-C(=O)-NR65-; -NR66-C(=S)- NR65-; -N=N-NH-; -N=N-NR67-; -O-CH2-C(=O)-NH-; -0-CH2-O-; -CH2-CH2-NH-, -CH2- CH2-CH2-NH, -CH2-C(=O)-NH, -CH2-CH2-C(=O)-NH-; -0-CH2-CH2-O-; -0-CH2-CH2- CH2-O-; -N=N-CH=CH-; -N=CH-N=CH; -N=CH-CH=N-; -CH=CH-CH=N-; -CH=CH- N=CH-; -CH=N-N=CH- und -0-CH2-CH2-NH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R4 und R5 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CH=N-NR71-; -S-C(=S)-NH-; -O-C(=S)-NH-; -S-C(=O)-NH-; -O-C(=O)- NH-; -S-C(=S)-NR63-; -O-C(=S)-NR63-; -S-C(=O)-NR63-; -O-C(=O)-NR63-; -S-CH=N-; - S-CR29=N-; -N=CH-O-; -N=CR30-O-; -NH-C(=O)-NH-; -NH-C(=S)-NH-; -NR66-C(=O)- NR65-; -NR66-C(=S)-NR65-; -O-CH2-C(=O)-NH-; -0-CH2-O-; -0-CH2-CH2-O-, -0-CH2- CH2-CH2-O-; -0-CH2-CH2-NH- und -CH=CH-N=CH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
und die übrigen Reste von R1, R2, R3, R4 und R5, unabhängig voneinander, jeweils für H; -OR16; -SR17; oder für einen Rest ausgewählt aus der Gruppe bestehend aus Methyl, -CF3, -CHF2, -CH2F, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl und tert-Butyl stehen;
R8 für -SF5; -0-CF3; -CF3; tert-Butyl oder -C(CH3)2(CH2OH) steht;
R16 und R17, unabhängig voneinander, jeweils für einen Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl und n-Pentyl stehen;
R28 für F; Cl; Br oder I steht;
R29 und R30, unabhängig voneinander, jeweils für -NH-C(=O)-R31; -NH2; -NH-S(=O)2- R32; -NH-C(=O)-O-R33 oder -S-R34 stehen;
R31, R32, R33 und R34, unabhängig voneinander, jeweils für Alkyl-Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl und n-Pentyl stehen;
R42 für einen Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n- Propyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl, n-Pentyl, 3-Pentyl, n-Hexyl und (3,3)- Dimethylbutyl;
oder für einen Rest ausgewählt aus der Gruppe bestehend aus Cyclopropyl, Cyclobutyl, Cyclopentyl, Cyclohexyl und Cycloheptyl, der jeweils ggf. mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert- Butyl, n-Pentyl substituiert sein kann, steht;
R62, R63, R64, R65, R66 und R67, unabhängig voneinander, jeweils für einen Alkyl-Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, tert-Butyl, n-Butyl, sek-Butyl und Isobutyl stehen; und
R71 für einen Rest steht ausgewählt aus der Gruppe bestehend aus Phenyl, Naphthyl, Thiophenyl, Furanyl und Pyridinyl, wobei der Rest jeweils über eine -(CH2)- , -(CH2J2- oder -(CH2)3-Gruppe gebunden sein kann und/oder jeweils unsubstituiert oder ggf. mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus
der Gruppe bestehend aus F, Cl, Br, I, -CN, -CF3, -SF5, -OH, -0-CH3, -0-C2H5, -O- CH(CHs)2, -O-C(CH3)3, -NH2, -NO2, -O-CF3, -S-CF3, -SH, -S-CH3, -S-C2H5, -S- CH(CH3)2, -S-C(CH3)3, Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl, -O-Phenyl, -O-Benzyl, Phenyl und Benzyl substituiert sein kann
jeweils ggf. in Form eines ihrer reinen Stereoisomeren, insbesondere Enantiomeren oder Diastereomeren, ihrer Racemate oder in Form einer Mischung von Stereoisomeren, insbesondere der Enantiomeren und/oder Diastereomeren, in einem beliebigen Mischungsverhältnis, oder jeweils in Form entsprechender Salze, oder jeweils in Form entsprechender Solvate.
Ganz besonders bevorzugt sind Verbindungen der allgemeinen Formel Ib,
Ib,
worin
D für N oder CH steht;
R1 und R2 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -S-CH=N-; -S-CR29=N-; -N=CH-O- und -N=CR30-O- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R2 und R3 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CR28=N-NH-; -S-C(=S)-NH-; -O-C(=S)-NH-; -S-C(=O)- NH-; -O-C(=O)-NH-; -S-CH=N-; -S-CR29=N-; -N=CH-O-; -N=CR30-O-; -N=CH-NH-; - NH-C(=O)-NH-; -NH-C(=S)-NH-; -N=N-NH-; -O-CH2-C(=O)-NH-; -0-CH2-CH2-O-; -O- CH2-CH2-CH2-O-; -N=CH-CH=N-; -CH=CH-CH=N-; -CH=CH-N=CH-; -CH=N-N=CH-
und -0-CH2-CH2-NH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R3 und R4 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CR28=N-NH-; -S-C(=S)-NH-; -O-C(=S)-NH-; -S-C(=O)- NH-; -O-C(=O)-NH-; -S-CH=N-; -S-CR29=N-; -N=CH-O-; -N=CR30-O-; -N=CH-NH-; - NH-C(=O)-NH-; -NH-C(=S)-NH-; -N=N-NH-; -O-CH2-C(=O)-NH-; -0-CH2-CH2-O-; -O- CH2-CH2-CH2-O-; -N=CH-CH=N-; -CH=CH-CH=N-; -CH=CH-N=CH-; -CH=N-N=CH- und -0-CH2-CH2-NH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R4 und R5 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -S-CH=N-; -S-CR29=N-; -N=CH-O- und -N=CR30-O- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
und die übrigen Reste von R1, R2, R3, R4 und R5, unabhängig voneinander, jeweils für H; -OR16; -SR17; oder für einen Rest ausgewählt aus der Gruppe bestehend aus Methyl, -CF3, -CHF2, -CH2F, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl und tert-Butyl stehen;
R8 für -SF5; -0-CF3; -CF3; tert-Butyl oder -C(CH3)2 (CH2OH) steht;
R16 und R17, unabhängig voneinander, jeweils für einen Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl und n-Pentyl stehen;
R28 für F; Cl; Br oder I steht;
R29 für -NH-C(O)-R31 ; -NH2; -NH-S(=O)2-R32; -NH-C(=O)-O-R33 oder -S-R34 steht;
R30 für -NH2 steht;
R31, R32, R33 und R34, unabhängig voneinander, jeweils für Alkyl-Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, n- Butyl, sek-Butyl, Isobutyl, tert-Butyl und n-Pentyl stehen;
R ϊ42 für einen Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n- Propyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl, n-Pentyl, 3-Pentyl, n-Hexyl und (3,3)- Dimethylbutyl;
oder für einen Rest ausgewählt aus der Gruppe bestehend aus Cyclopropyl, Cyclobutyl, Cyclopentyl, Cyclohexyl und Cycloheptyl, der jeweils ggf. mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert- Butyl, n-Pentyl substituiert sein kann, steht;
j71 für einen Phenyl-Rest steht, der über eine -(CH2)-, -(CH2)2- oder -(CH2)3-
Gruppe gebunden sein kann und/oder jeweils unsubstituiert oder ggf. mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus F, Cl, Br, I, -CN, -CF3, -SF5, -OH, -O-CH3, -0-C2H5, Methyl, Ethyl, n- Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl und tert-Butyl;
jeweils ggf. in Form eines ihrer reinen Stereoisomeren, insbesondere Enantiomeren oder Diastereomeren, ihrer Racemate oder in Form einer Mischung von Stereoisomeren, insbesondere der Enantiomeren und/oder Diastereomeren, in einem beliebigen Mischungsverhältnis, oder jeweils in Form entsprechender Salze, oder jeweils in Form entsprechender Solvate.
Bevorzugt sind Verbindungen der allgemeinen Formel Ic,
Ic,
worin
D für N oder CH steht;
R1 und R2 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus - CH=N-NH-; -CH=N-NR71-; -S-C(=S)-NH-; -O-C(=S)-NH-; -S-C(=O)-NH-; -O-C(=O)- NH-; -S-C(=S)-NR63-; -O-C(=S)-NR63-; -S-C(=O)-NR63-; -O-C(=O)-NR63-; -S-CH=N-; - S-CR29=N-; -N=CH-O-; -N=CR30-O-; -NH-C(=O)-NH-; -NH-C(=S)-NH-; -NR66-C(=O)- NR65-; -NR66-C(=S)-NR65-; -O-CH2-C(=O)-NH-; -0-CH2-O-; -0-CH2-CH2-O-, -0-CH2- CH2-CH2-O-; -0-CH2-CH2-NH- und -CH=CH-N=CH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R2 und R3 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CR28=N-NH-; -CH=N-NR62-; -CR28=N-NR62-; -S-C(=S)-NH-; -O-C(=S)- NH-; -S-C(=O)-NH-; -O-C(=O)-NH-; -S-C(=S)-NR63-; -O-C(=S)-NR63-; -S-C(=O)-NR63- ; -O-C(=O)-NR63-; -S-CH=N-; -S-CR29=N-; -N=CH-O-; -N=CR30-O-; -N=CH-NH-; - N=CH-NR64-; -NH-C(=O)-NH-; -NH-C(=S)-NH-; -NR66-C(=O)-NR65-; -NR66-C(=S)- NR65-; -N=N-NH-; -N=N-NR67-; -O-CH2-C(=O)-NH-; -0-CH2-O-; -CH2-CH2-NH-, -CH2- CH2-CH2-NH, -CH2-C(=O)-NH, -CH2-CH2-C(=O)-NH-; -0-CH2-CH2-O-; -0-CH2-CH2- CH2-O-; -N=N-CH=CH-; -N=CH-N=CH; -N=CH-CH=N-; -CH=CH-CH=N-; -CH=CH- N=CH-; -CH=N-N=CH- und -0-CH2-CH2-NH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R3 und R4 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CR28=N-NH-; -CH=N-NR62-; -CR28=N-NR62-; -S-C(=S)-NH-; -O-C(=S)- NH-; -S-C(=O)-NH-; -O-C(=O)-NH-; -S-C(=S)-NR63-; -O-C(=S)-NR63-; -S-C(=O)-NR63- ; -O-C(=O)-NR63-; -S-CH=N-; -S-CR29=N-; -N=CH-O-; -N=CR30-O-; -N=CH-NH-; - N=CH-NR64-; -NH-C(=O)-NH-; -NH-C(=S)-NH-; -NR66-C(=O)-NR65-; -NR66-C(=S)- NR65-; -N=N-NH-; -N=N-NR67-; -O-CH2-C(=O)-NH-; -0-CH2-O-; -CH2-CH2-NH-, -CH2- CH2-CH2-NH, -CH2-C(=O)-NH, -CH2-CH2-C(=O)-NH-; -0-CH2-CH2-O-; -0-CH2-CH2- CH2-O-; -N=N-CH=CH-; -N=CH-N=CH; -N=CH-CH=N-; -CH=CH-CH=N-; -CH=CH- N=CH-; -CH=N-N=CH- und -0-CH2-CH2-NH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R4 und R5 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CH=N-NR71-; -S-C(=S)-NH-; -O-C(=S)-NH-; -S-C(=O)-NH-; -O-C(=O)- NH-; -S-C(=S)-NR63-; -O-C(=S)-NR63-; -S-C(=O)-NR63-; -O-C(=O)-NR63-; -S-CH=N-; - S-CR29=N-; -N=CH-O-; -N=CR30-O-; -NH-C(=O)-NH-; -NH-C(=S)-NH-; -NR66-C(=O)- NR65-; -NR66-C(=S)-NR65-; -O-CH2-C(=O)-NH-; -0-CH2-O-; -0-CH2-CH2-O-, -0-CH2- CH2-CH2-O-; -0-CH2-CH2-NH- und -CH=CH-N=CH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
und die übrigen Reste von R1, R2, R3, R4 und R5, unabhängig voneinander, jeweils für H; F; Cl; Br; I; -CF3; -CN; -OR16; -SR17; oder für einen Rest ausgewählt aus der Gruppe bestehend aus Methyl, -CF3, -CHF2, -CH2F1 Ethyl, n-Propyl, Isopropyl, n- Butyl, sek-Butyl, Isobutyl und tert-Butyl stehen;
R8 für -SF5; -0-CF3; -CF3; tert-Butyl oder -C(CH3)2(CH2OH) steht;
R16 und R17, unabhängig voneinander, jeweils für einen Rest ausgewählt aus der Gruppe bestehend aus Methyl, -CF3, -CHF2, -CH2F, Ethyl, -CF2-CH3, -CH2-CF3, - C2F5, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl, n-Pentyl, 3-Pentyl, n- Heptyl, 4-Heptyl, n-Octyl, n-Nonyl, 5-Nonyl, (2,6)-Dimethyl-hept-4-yl, 3-Methyl-butyl, n-Hexyl und (3,3)-Dimethylbutyl stehen;
R28 für F; Cl; Br; I; -CF3; -CN; -NH2 oder für einen Alkyl-Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl und n-Pentyl steht;
R29 und R30, unabhängig voneinander, jeweils für -NH-C(=O)-R31; -NH2; -NH-S(=O)2- R32; -NH-C(=O)-O-R33; -S-R34 oder für einen Alkyl-Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert- Butyl und n-Pentyl stehen;
R31, R32, R33 und R34, unabhängig voneinander, jeweils für Alkyl-Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl und n-Pentyl stehen;
R43 für einen Rest ausgewählt aus der Gruppe bestehend aus Methyl, -CH2-O- CH3, Ethyl, n-Propyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl, n-Pentyl, 3-Pentyl, n- Hexyl, (3,3)-Dimethylbutyl, -CH2-CH2-O-CH3, -CH2-CH2-O-C2H5 und -CH2-CH2-CH2- O-CH3 steht;
oder für einen Rest ausgewählt aus der Gruppe bestehend aus 2,3-Dihydro-1 H- indenyl, Cyclopropyl, Oxetanyl, Cyclobutyl, Cyclopentyl, Cyclohexyl, Imidazolidinyl, Tetrahydrofuranyl, Tetrahydrothiophenyl, Pyrrolidinyl, Piperidinyl, Morpholinyl, Piperazinyl, Azepanyl, Diazepanyl, Azocanyl und Thiomorpholinyl, der jeweils ggf. mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert- Butyl, n-Pentyl substituiert sein kann, steht;
R62, R63, R64, R65, R66 und R67, unabhängig voneinander, jeweils für einen Alkyl-Rest ausgewählt aus der Gruppe bestehend aus -CF3, -CH2-CF3, Methyl, Ethyl, n-Propyl, Isopropyl, tert-Butyl, n-Butyl, sek-Butyl und Isobutyl stehen; und
R71 für einen Rest steht ausgewählt aus der Gruppe bestehend aus Phenyl, Naphthyl, Thiophenyl, Furanyl und Pyridinyl, wobei der Rest jeweils über eine -(CH2)- , -(CH2J2- oder -(CH2)3-Gruppe gebunden sein kann und/oder jeweils unsubstituiert oder ggf. mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus F, Cl, Br, I, -CN, -CF3, -SF5, -OH, -O-CH3, -0-C2H5, -O- CH(CH3)2, -O-C(CH3)3, -NH2, -NO2, -0-CF3, -S-CF3, -SH, -S-CH3, -S-C2H5, -S- CH(CH3)2, -S-C(CH3)3, Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl, -O-Phenyl, -O-Benzyl, Phenyl und Benzyl substituiert sein kann
jeweils ggf. in Form eines ihrer reinen Stereoisomeren, insbesondere Enantiomeren oder Diastereomeren, ihrer Racemate oder in Form einer Mischung von Stereoisomeren, insbesondere der Enantiomeren und/oder Diastereomeren, in einem beliebigen Mischungsverhältnis, oder jeweils in Form entsprechender Salze, oder jeweils in Form entsprechender Solvate.
Besonders bevorzugt sind Verbindungen der allgemeinen Formel Ic,
Ic,
worin
D für N oder CH steht;
R1 und R2 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus - CH=N-NH-; -CH=N-NR71-; -S-C(=S)-NH-; -O-C(=S)-NH-; -S-C(=O)-NH-; -O-C(=O)- NH-; -S-C(=S)-NR63-; -O-C(=S)-NR63-; -S-C(=O)-NR63-; -O-C(=O)-NR63-; -S-CH=N-; - S-CR29=N-; -N=CH-O-; -N=CR30-O-; -NH-C(=O)-NH-; -NH-C(=S)-NH-; -NR66-C(=O)- NR65-; -NR66-C(=S)-NR65-; -O-CH2-C(=O)-NH-; -0-CH2-O-; -0-CH2-CH2-O-, -0-CH2- CH2-CH2-O-; -0-CH2-CH2-NH- und -CH=CH-N=CH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R2 und R3 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CR28=N-NH-; -CH=N-NR62-; -CR28=N-NR62-; -S-C(=S)-NH-; -O-C(=S)- NH-; -S-C(=O)-NH-; -O-C(=O)-NH-; -S-C(=S)-NR63-; -O-C(=S)-NR63-; -S-C(O)-NR63- ; -O-C(=O)-NR63-; -S-CH=N-; -S-CR29=N-; -N=CH-O-; -N=CR30-O-; -N=CH-NH-; - N=CH-NR64-; -NH-C(=O)-NH-; -NH-C(=S)-NH-; -NR66-C(=O)-NR65-; -NR66-C(=S)- NR65-; -N=N-NH-; -N=N-NR67-; -O-CH2-C(=O)-NH-; -0-CH2-O-; -CH2-CH2-NH-, -CH2- CH2-CH2-NH, -CH2-C(=O)-NH, -CH2-CH2-C(=O)-NH-; -0-CH2-CH2-O-; -0-CH2-CH2- CH2-O-; -N=N-CH=CH-; -N=CH-N=CH; -N=CH-CH=N-; -CH=CH-CH=N-; -CH=CH- N=CH-; -CH=N-N=CH- und -0-CH2-CH2-NH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R3 und R4 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CR28=N-NH-; -CH=N-NR62-; -CR28=N-NR62-; -S-C(=S)-NH-; -O-C(=S)- NH-; -S-C(=O)-NH-; -O-C(=O)-NH-; -S-C(=S)-NR63-; -O-C(=S)-NR63-; -S-C(=O)-NR63- ; -O-C(=O)-NR63-; -S-CH=N-; -S-CR29=N-; -N=CH-O-; -N=CR30-O-; -N=CH-NH-; - N=CH-NR64-; -NH-C(=O)-NH-; -NH-C(=S)-NH-; -NR66-C(=O)-NR65-; -NR66-C(=S)- NR65-; -N=N-NH-; -N=N-NR67-; -O-CH2-C(=O)-NH-; -0-CH2-O-; -CH2-CH2-NH-, -CH2- CH2-CH2-NH, -CH2-C(=O)-NH, -CH2-CH2-C(=O)-NH-; -0-CH2-CH2-O-; -0-CH2-CH2- CH2-O-; -N=N-CH=CH-; -N=CH-N=CH; -N=CH-CH=N-; -CH=CH-CH=N-; -CH=CH- N=CH-; -CH=N-N=CH- und -0-CH2-CH2-NH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R4 und R5 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CH=N-NR71-; -S-C(=S)-NH-; -O-C(=S)-NH-; -S-C(=O)-NH-; -O-C(=O)- NH-; -S-C(=S)-NR63-; -O-C(=S)-NR63-; -S-C(=O)-NR63-; -O-C(=O)-NR63-; -S-CH=N-; - S-CR29=N-; -N=CH-O-; -N=CR30-O-; -NH-C(=O)-NH-; -NH-C(=S)-NH-; -NR66-C(=O)- NR65-; -NR66-C(=S)-NR65-; -O-CH2-C(=O)-NH-; -0-CH2-O-; -0-CH2-CH2-O-, -O-CH2- CH2-CH2-O-; -0-CH2-CH2-NH- und -CH=CH-N=CH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
und die übrigen Reste von R1, R2, R3, R4 und R5, unabhängig voneinander, jeweils für H; -OR16; -SR17; oder für einen Rest ausgewählt aus der Gruppe bestehend aus Methyl, -CF3, -CHF2, -CH2F, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl und tert-Butyl stehen;
R8 für -SF5; -0-CF3; -CF3; tert-Butyl oder -C(CH3)2 (CH2OH) steht;
R16 und R17, unabhängig voneinander, jeweils für einen Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl und n-Pentyl stehen;
R28 für F; Cl; Br oder I steht;
R29 und R30, unabhängig voneinander, jeweils für -NH-C(=O)-R31; -NH2; -NH-S(O)2- R32; -NH-C(=O)-O-R33 oder -S-R34 stehen;
R31, R32, R33 und R34, unabhängig voneinander, jeweils für Alkyl-Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl und n-Pentyl stehen;
R43 für einen Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n- Propyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl, n-Pentyl, 3-Pentyl, n-Hexyl und (3,3)- Dimethylbutyl;
oder für einen Rest ausgewählt aus der Gruppe bestehend aus Cyclopropyl, Cyclobutyl, Cyclopentyl, Cyclohexyl und Cycloheptyl, der jeweils ggf. mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert- Butyl, n-Pentyl substituiert sein kann, steht;
R62, R63, R64, R65, R66 und R67, unabhängig voneinander, jeweils für einen Alkyl-Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, tert- Butyl, n-Butyl, sek-Butyl und Isobutyl stehen; und
R71 für einen Rest steht ausgewählt aus der Gruppe bestehend aus Phenyl, Naphthyl, Thiophenyl, Furanyl und Pyridinyl, wobei der Rest jeweils über eine -(CH2)- , -(CH2)2- oder -(CH2)3-Gruppe gebunden sein kann und/oder jeweils unsubstituiert oder ggf. mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus F, Cl, Br, I, -CN, -CF3, -SF5, -OH, -O-CH3, -0-C2H5, -O- CH(CH3)2, -O-C(CH3)3, -NH2, -NO2, -0-CF3, -S-CF3, -SH, -S-CH3, -S-C2H5, -S- CH(CH3)2, -S-C(CH3)3, Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl, -O-Phenyl, -O-Benzyl, Phenyl und Benzyl substituiert sein kann
jeweils ggf. in Form eines ihrer reinen Stereoisomeren, insbesondere Enantiomeren oder Diastereomeren, ihrer Racemate oder in Form einer Mischung von Stereoisomeren, insbesondere der Enantiomeren und/oder Diastereomeren, in einem
beliebigen Mischungsverhältnis, oder jeweils in Form entsprechender Salze, oder jeweils in Form entsprechender Solvate.
Ganz besonders bevorzugt sind Verbindungen der allgemeinen Formel Ic,
Ic,
worin
D für N oder CH steht;
R1 und R2 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -S-CH=N-; -S-CR29=N-; -N=CH-O- und -N=CR30-O- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R2 und R3 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CR28=N-NH-; -S-C(=S)-NH-; -O-C(=S)-NH-; -S-C(=O)- NH-; -O-C(=O)-NH-; -S-CH=N-; -S-CR29=N-; -N=CH-O-; -N=CR30-O-; -N=CH-NH-; - NH-C(=O)-NH-; -NH-C(=S)-NH-; -N=N-NH-; -O-CH2-C(=O)-NH-; -0-CH2-CH2-O-; -O- CH2-CH2-CH2-O-; -N=CH-CH=N-; -CH=CH-CH=N-; -CH=CH-N=CH-; -CH=N-N=CH- und -0-CH2-CH2-NH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R3 und R4 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CR28=N-NH-; -S-C(=S)-NH-; -O-C(=S)-NH-; -S-C(=O)- NH-; -O-C(=O)-NH-; -S-CH=N-; -S-CR29=N-; -N=CH-O-; -N=CR30-O-; -N=CH-NH-; - NH-C(=O)-NH-; -NH-C(=S)-NH-; -N=N-NH-; -O-CH2-C(=O)-NH-; -0-CH2-CH2-O-; -O- CH2-CH2-CH2-O-; -N=CH-CH=N-; -CH=CH-CH=N-; -CH=CH-N=CH-; -CH=N-N=CH-
und -0-CH2-CH2-NH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R4 und R5 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -S-CH=N-; -S-CR29=N-; -N=CH-O- und -N=CR30-O- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
und die übrigen Reste R1, R2, R3, R4 und R5, unabhängig voneinander, jeweils für H; -OR16; -SR17; oder für einen Rest ausgewählt aus der Gruppe bestehend aus Methyl, -CF3, -CHF2, -CH2F1 Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl und tert- Butyl stehen;
R8 für -SF5; -0-CF3; -CF3; tert-Butyl oder -C(CH3)2(CH2OH) steht;
R16 und R17, unabhängig voneinander, jeweils für einen Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl und n-Pentyl stehen;
R28 für F; Cl; Br oder I steht;
R29 für -NH-C(=O)-R31; -NH2; -NH-S(=O)2-R32; -NH-C(=O)-O-R33 oder -S-R34 steht;
R 33M0 für -NH2 steht;
R31, R32, R33 und R34, unabhängig voneinander, jeweils für Alkyl-Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, n- Butyl, sek-Butyl, Isobutyl, tert-Butyl und n-Pentyl stehen;
R43 für einen Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n- Propyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl, n-Pentyl, 3-Pentyl, n-Hexyl und (3,3)- Dimethylbutyl;
oder für einen Rest ausgewählt aus der Gruppe bestehend aus Cyclopropyl, Cyclobutyl, Cyclopentyl, Cyclohexyl und Cycloheptyl, der jeweils ggf. mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert- Butyl, n-Pentyl substituiert sein kann, steht;
und
R71 für einen Phenyl-Rest steht, der über eine -(CH2)-, -(CH2)2- oder -(CH2)3- Gruppe gebunden sein kann und/oder jeweils unsubstituiert oder ggf. mit 1, 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus F, Cl, Br, I, -CN, -CF3, -SF5, -OH, -O-CH3, -0-C2H5, Methyl, Ethyl, n- Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl und tert-Butyl;
jeweils ggf. in Form eines ihrer reinen Stereoisomeren, insbesondere Enantiomeren oder Diastereomeren, ihrer Racemate oder in Form einer Mischung von Stereoisomeren, insbesondere der Enantiomeren und/oder Diastereomeren, in einem beliebigen Mischungsverhältnis, oder jeweils in Form entsprechender Salze, oder jeweils in Form entsprechender Solvate.
Bevorzugt sind Verbindungen der allgemeinen Formel Id,
Id,
worin
D für N oder CH steht;
R1 und R2 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus - CH=N-NH-; -CH=N-NR71-; -S-C(=S)-NH-; -O-C(=S)-NH-; -S-C(O)-NH-; -O-C(=O)- NH-; -S-C(=S)-NR63-; -O-C(=S)-NR63-; -S-C(=O)-NR63-; -O-C(=O)-NR63-; -S-CH=N-; - S-CR29=N-; -N=CH-O-; -N=CR30O-; -NH-C(=O)-NH-; -NH-C(=S)-NH-; -NR66-C(=O)- NR65-; -NR66-C(=S)-NR65-; -O-CH2-C(=O)-NH-; -0-CH2-O-; -0-CH2-CH2-O-, -0-CH2- CH2-CH2-O-; -0-CH2-CH2-NH- und -CH=CH-N=CH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R2 und R3 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CR28=N-NH-; -CH=N-NR62-; -CR28=N-NR62-; -S-C(=S)-NH-; -O-C(=S)- NH-; -S-C(=O)-NH-; -O-C(=O)-NH-; -S-C(=S)-NR63-; -O-C(=S)-NR63-; -S-C(=O)-NR63- ; -O-C(=O)-NR63-; -S-CH=N-; -S-CR29=N-; -N=CH-O-; -N=CR30O-; -N=CH-NH-; - N=CH-NR64-; -NH-C(=O)-NH-; -NH-C(=S)-NH-; -NR66-C(=O)-NR65-; -NR66-C(=S)- NR65-; -N=N-NH-; -N=N-NR67-; -O-CH2-C(=O)-NH-; -0-CH2-O-; -CH2-CH2-NH-, -CH2- CH2-CH2-NH, -CH2-C(=O)-NH, -CH2-CH2-C(=O)-NH-; -0-CH2-CH2-O-; -0-CH2-CH2- CH2-O-; -N=N-CH=CH-; -N=CH-N=CH; -N=CH-CH=N-; -CH=CH-CH=N-; -CH=CH- N=CH-; -CH=N-N=CH- und -0-CH2-CH2-NH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R3 und R4 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CR28=N-NH-; -CH=N-NR62-; -CR28=N-NR62-; -S-C(=S)-NH-; -O-C(=S)- NH-; -S-C(=O)-NH-; -O-C(=O)-NH-; -S-C(=S)-NR63-; -O-C(=S)-NR63-; -S-C(O)-NR63- ; -O-C(=O)-NR63-; -S-CH=N-; -S-CR29=N-; -N=CH-O-; -N=CR30-O-; -N=CH-NH-; - N=CH-NR64-; -NH-C(=O)-NH-; -NH-C(=S)-NH-; -NR66-C(=O)-NR65-; -NR66-C(=S)- NR65-; -N=N-NH-; -N=N-NR67-; -O-CH2-C(=O)-NH-; -0-CH2-O-; -CH2-CH2-NH-, -CH2- CH2-CH2-NH, -CH2-C(=O)-NH, -CH2-CH2-C(=O)-NH-; -0-CH2-CH2-O-; -0-CH2-CH2- CH2-O-; -N=N-CH=CH-; -N=CH-N=CH; -N=CH-CH=N-; -CH=CH-CH=N-; -CH=CH- N=CH-; -CH=N-N=CH- und -0-CH2-CH2-NH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R4 und R5 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CH=N-NR71-; -S-C(=S)-NH-; -O-C(=S)-NH-; -S-C(=O)-NH-; -O-C(O)- NH-; -S-C(=S)-NR63-; -O-C(=S)-NR63-; -S-C(=O)-NR63-; -O-C(=O)-NR63-; -S-CH=N-; - S-CR29=N-; -N=CH-O-; -N=CR30-O-; -NH-C(=O)-NH-; -NH-C(=S)-NH-; -NR66-C(=O)-
NR65-; -NR66-C(=S)-NR65-; -O-CH2-C(=O)-NH-; -0-CH2-O-; -0-CH2-CH2-O-, -O-CH2- CH2-CH2-O-; -0-CH2-CH2-NH- und -CH=CH-N=CH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
und die übrigen Reste R1, R2, R3, R4 und R5, unabhängig voneinander, jeweils für H; F; Cl; Br; I; -CF3; -CN; -OR16; -SR17; oder für einen Rest ausgewählt aus der Gruppe bestehend aus Methyl, -CF3, -CHF2, -CH2F, Ethyl, n-Propyl, Isopropyl, n- Butyl, sek-Butyl, Isobutyl und tert-Butyl stehen;
R8 für -SF5; -0-CF3; -CF3; tert-Butyl oder -C(CH3)2 (CH2OH) steht;
R16 und R17, unabhängig voneinander, jeweils für einen Rest ausgewählt aus der Gruppe bestehend aus Methyl, -CF3, -CHF2, -CH2F, Ethyl, -CF2-CH3, -CH2-CF3, - C2F5, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl, n-Pentyl, 3-Pentyl, n- Heptyl, 4-Heptyl, n-Octyl, n-Nonyl, 5-Nonyl, (2,6)-Dimethyl-hept-4-yl, 3-Methyl-butyl, n-Hexyl und (3,3)-Dimethylbutyl stehen;
R28 für F; Cl; Br; I; -CF3; -CN; -NH2 oder für einen Alkyl-Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl und n-Pentyl steht;
R29 und R30, unabhängig voneinander, jeweils für -NH-C(O)-R31; -NH2; -NH-S(=O)2- R32; -NH-C(=O)-O-R33; -S-R34 oder für einen Alkyl-Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert- Butyl und n-Pentyl stehen;
R31, R32, R33 und R34, unabhängig voneinander, jeweils für Alkyl-Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl und n-Pentyl stehen;
R40 und R41, unabhängig voneinander, jeweils
für einen Rest ausgewählt aus der Gruppe bestehend aus Methyl, -CH2-O-CH3, Ethyl, n-Propyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl, n-Pentyl, 3-Pentyl, n-Hexyl, (3,3)-Dimethylbutyl, -CH2-CH2-O-CH3, -CH2-CH2-O-C2H5 und -CH2-CH2-CH2-O-CH3 stehen;
für einen Rest ausgewählt aus der Gruppe bestehend aus 2,3-Dihydro-1 H-indenyl, Cyclopropyl, Oxetanyl, Cyclobutyl, Cyclopentyl, Cyclohexyl, Imidazolidinyl, Tetrahydrofuranyl, Tetrahydrothiophenyl, Pyrrolidinyl, Piperidinyl, Morpholinyl, Piperazinyl, Azepanyl, Diazepanyl, Azocanyl und Thiomorpholinyl, der jeweils ggf. mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert- Butyl, n-Pentyl substituiert sein kann, stehen;
oder
R40 und R41 jeweils zusammen mit dem sie verbindenden Stickstoffatom als Ringglied einen Rest ausgewählt aus der Gruppe bestehend aus 3-Aza- bicyclo[3.1.1]heptyl, 6-Aza-spiro[2.5]octyl, 3-Aza-bicyclo[3.2.1]octyl, 6-Aza- bicyclo[3.3.1]heptyl, 8-Aza-bicyclo[3.2.1]octyl, 1-Oxa-2,8-diaza-spiro[4.5]dec-2-enyl, Azocanyl, Isoindolyl, Indolyl, (1 ,2,3,6)-Tetrahydropyridinyl, (4,5,6,7)- Tetrahydroisoxazolo[5,4-c]pyridinyl, Pyrrolidinyl, Piperidinyl, Piperazinyl, Morpholinyl, Azepanyl, Diazepanyl und Thiomorpholinyl bilden, dessen heterocycloaliphatischer Anteil jeweils unsubstituiert oder mit 1 , 2, 3, 4 oder 5 Resten R57 substituiert sein kann;
R57 für -NHR58, -NR59R60 oder für einen Alkyl-Rest ausgewählt aus der Gruppe bestehend aus -CF3, -CH2-CF3, Methyl, Ethyl, n-Propyl, Isopropyl, tert-Butyl, n-Butyl, sek-Butyl und Isobutyl steht;
R58, R59 und R60, unabhängig voneinander, jeweils für -C(=O)-R61; für einen Alkyl- Rest ausgewählt aus der Gruppe bestehend aus -CF3, -CH2-CF3, Methyl, Ethyl, n- Propyl, Isopropyl, tert-Butyl, n-Butyl, sek-Butyl und Isobutyl;
oder für einen Rest ausgewählt aus der Gruppe bestehend aus Phenyl und Naphthyl, wobei der Rest jeweils über eine -(CH2)-, -(CH2)2- oder -(CH2)3-Gruppe gebunden sein kann und/oder jeweils unsubstituiert oder ggf. mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus F, Cl, Br, I, - CN, -CF3, -0-CH3, -0-C2H5, -O-CH(CH3)2, -O-C(CH3)3, Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl und n-Pentyl substituiert sein kann, stehen;
R61 für einen Alkyl-Rest ausgewählt aus der Gruppe bestehend aus -CF3, -CH2- CF3, Methyl, Ethyl, n-Propyl, Isopropyl, tert-Butyl, n-Butyl, sek-Butyl und Isobutyl steht;
R62, R63, R64, R65, R66 und R67, unabhängig voneinander, jeweils für einen Alkyl-Rest ausgewählt aus der Gruppe bestehend aus -CF3, -CH2-CF3, Methyl, Ethyl, n-Propyl, Isopropyl, tert-Butyl, n-Butyl, sek-Butyl und Isobutyl stehen; und
R71 für einen Rest steht ausgewählt aus der Gruppe bestehend aus Phenyl, Naphthyl, Thiophenyl, Furanyl und Pyridinyl, wobei der Rest jeweils über eine -(CH2)- , -(CH2)2- oder -(CH2)3-Gruppe gebunden sein kann und/oder jeweils unsubstituiert oder ggf. mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus F, Cl, Br, I, -CN, -CF3, -SF5, -OH, -0-CH3, -0-C2H5, -O- CH(CHa)2, -O-C(CH3)3, -NH2, -NO2, -O-CF3, -S-CF3, -SH, -S-CH3, -S-C2H5, -S- CH(CH3)2, -S-C(CH3)3, Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl, -O-Phenyl, -O-Benzyl, Phenyl und Benzyl substituiert sein kann
jeweils ggf. in Form eines ihrer reinen Stereoisomeren, insbesondere Enantiomeren oder Diastereomeren, ihrer Racemate oder in Form einer Mischung von Stereoisomeren, insbesondere der Enantiomeren und/oder Diastereomeren, in einem beliebigen Mischungsverhältnis, oder jeweils in Form entsprechender Salze, oder jeweils in Form entsprechender Solvate.
Besonders bevorzugt sind Verbindungen der allgemeinen Formel Id,
Id,
worin
D für N oder CH steht;
R1 und R2 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus - CH=N-NH-; -CH=N-NR71-; -S-C(=S)-NH-; -O-C(=S)-NH-; -S-C(=O)-NH-; -O-C(=O)- NH-; -S-C(=S)-NR63-; -O-C(=S)-NR63-; -S-C(=O)-NR63-; -O-C(=O)-NR63-; -S-CH=N-; - S-CR29=N-; -N=CH-O-; -N=CR30-O-; -NH-C(=O)-NH-; -NH-C(=S)-NH-; -NR66-C(=O)- NR65-; -NR66-C(=S)-NR65-; -O-CH2-C(=O)-NH-; -0-CH2-O-; -0-CH2-CH2-O-, -0-CH2- CH2-CH2-O-; -0-CH2-CH2-NH- und -CH=CH-N=CH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R2 und R3 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CR28=N-NH-; -CH=N-NR62-; -CR28=N-NR62-; -S-C(=S)-NH-; -O-C(=S)- NH-; -S-C(=O)-NH-; -O-C(=O)-NH-; -S-C(=S)-NR63-; -O-C(=S)-NR63-; -S-C(=O)-NR63- ; -O-C(=O)-NR63-; -S-CH=N-; -S-CR29=N-; -N=CH-O-; -N=CR30-O-; -N=CH-NH-; - N=CH-NR64-; -NH-C(=O)-NH-; -NH-C(=S)-NH-; -NR66-C(=O)-NR65-; -NR66-C(=S)- NR65-; -N=N-NH-; -N=N-NR67-; -O-CH2-C(=O)-NH-; -0-CH2-O-; -CH2-CH2-NH-, -CH2- CH2-CH2-NH1 -CH2-C(=O)-NH, -CH2-CH2-C(=O)-NH-; -0-CH2-CH2-O-; -0-CH2-CH2- CH2-O-; -N=N-CH=CH-; -N=CH-N=CH; -N=CH-CH=N-; -CH=CH-CH=N-; -CH=CH- N=CH-; -CH=N-N=CH- und -0-CH2-CH2-NH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R3 und R4 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CR28=N-NH-; -CH=N-NR62-; -CR28=N-NR62-; -S-C(=S)-NH-; -O-C(=S)- NH-; -S-C(=O)-NH-; -O-C(=O)-NH-; -S-C(=S)-NR63-; -O-C(=S)-NR63-; -S-C(=O)-NR63- ; -O-C(=O)-NR63-; -S-CH=N-; -S-CR29=N-; -N=CH-O-; -N=CR30-O-; -N=CH-NH-; - N=CH-NR64-; -NH-C(=O)-NH-; -NH-C(=S)-NH-; -NR66-C(=O)-NR65-; -NR66-C(=S)- NR65-; -N=N-NH-; -N=N-NR67-; -O-CH2-C(=O)-NH-; -0-CH2-O-; -CH2-CH2-NH-, -CH2- CH2-CH2-NH, -CH2-C(=O)-NH, -CH2-CH2-C(=O)-NH-; -0-CH2-CH2-O-; -0-CH2-CH2- CH2-O-; -N=N-CH=CH-; -N=CH-N=CH; -N=CH-CH=N-; -CH=CH-CH=N-; -CH=CH- N=CH-; -CH=N-N=CH- und -0-CH2-CH2-NH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R4 und R5 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CH=N-NR71-; -S-C(=S)-NH-; -O-C(=S)-NH-; -S-C(=O)-NH-; -O-C(=O)- NH-; -S-C(=S)-NR63-; -O-C(=S)-NR63-; -S-C(=O)-NR63-; -O-C(=O)-NR63-; -S-CH=N-; - S-CR29=N-; -N=CH-O-; -N=CR30-O-; -NH-C(=O)-NH-; -NH-C(=S)-NH-; -NR66-C(=O)- NR65-; -NR66-C(=S)-NR65-; -O-CH2-C(=O)-NH-; -0-CH2-O-; -0-CH2-CH2-O-, -0-CH2- CH2-CH2-O-; -0-CH2-CH2-NH- und -CH=CH-N=CH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
und die übrigen Reste R1, R2, R3, R4 und R5, unabhängig voneinander, jeweils für H; -OR16; -SR17; oder für einen Rest ausgewählt aus der Gruppe bestehend aus Methyl, -CF3, -CHF2, -CH2F, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl und tert- Butyl stehen;
R8 für -SF5; -0-CF3; -CF3; tert-Butyl oder -C(CH3)2 (CH2OH) steht;
R16 und R17, unabhängig voneinander, jeweils für einen Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl und n-Pentyl stehen;
R28 für F; Cl; Br oder I steht;
R29 und R30, unabhängig voneinander, jeweils für -NH-C(O)-R31; -NH2; -NH-S(=O)2- R32; -NH-C(=O)-O-R33 oder -S-R34 stehen;
R31, R32, R33 und R34, unabhängig voneinander, jeweils für Alkyl-Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl und n-Pentyl stehen;
R40 und R41 jeweils zusammen mit dem sie verbindenden Stickstoffatom als Ringglied einen Rest ausgewählt aus der Gruppe bestehend Pyrrolidinyl, Piperidinyl, Piperazinyl, Morpholinyl und Azepanyl bilden, dessen heterocycloaliphatischer Anteil jeweils unsubstituiert oder mit 1 , 2, 3, 4 oder 5 Resten R57 substituiert sein kann;
R57 für einen Alkyl-Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, tert-Butyl, n-Butyl, sek-Butyl und Isobutyl steht;
R62, R63, R64, R65, R66 und R67, unabhängig voneinander, jeweils für einen Alkyl-Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, tert- Butyl, n-Butyl, sek-Butyl und Isobutyl stehen; und
R71 für einen Rest steht ausgewählt aus der Gruppe bestehend aus Phenyl, Naphthyl, Thiophenyl, Furanyl und Pyridinyl, wobei der Rest jeweils über eine -(CH2)- , -(CH2)2- oder -(CH2)3-Gruppe gebunden sein kann und/oder jeweils unsubstituiert oder ggf. mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus F, Cl, Br, I, -CN, -CF3, -SF5, -OH, -O-CH3, -0-C2H5, -O- CH(CHa)2, -O-C(CH3)3, -NH2, -NO2, -0-CF3, -S-CF3, -SH, -S-CH3, -S-C2H5, -S- CH(CH3)2, -S-C(CH3)3, Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl, -O-Phenyl, -O-Benzyl, Phenyl und Benzyl substituiert sein kann
jeweils ggf. in Form eines ihrer reinen Stereoisomeren, insbesondere Enantiomeren oder Diastereomeren, ihrer Racemate oder in Form einer Mischung von Stereoisomeren, insbesondere der Enantiomeren und/oder Diastereomeren, in einem beliebigen Mischungsverhältnis, oder jeweils in Form entsprechender Salze, oder jeweils in Form entsprechender Solvate.
Ganz besonders bevorzugt sind Verbindungen der allgemeinen Formel Id1
Id,
worin
D für N oder CH steht;
R1 und R2 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -S-CH=N-; -S-CR29=N-; -N=CH-O- und -N=CR30-O- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R2 und R3 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CR28=N-NH-; -S-C(=S)-NH-; -O-C(=S)-NH-; -S-C(=O)- NH-; -O-C(=O)-NH-; -S-CH=N-; -S-CR29=N-; -N=CH-O-; -N=CR30-O-; -N=CH-NH-; - NH-C(=O)-NH-; -NH-C(=S)-NH-; -N=N-NH-; -O-CH2-C(=O)-NH-; -0-CH2-CH2-O-; -O- CH2-CH2-CH2-O-; -N=CH-CH=N-; -CH=CH-CH=N-; -CH=CH-N=CH-; -CH=N-N=CH- und -0-CH2-CH2-NH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R3 und R4 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -CH=N-NH-; -CR28=N-NH-; -S-C(=S)-NH-; -O-C(=S)-NH-; -S-C(=O)- NH-; -O-C(=O)-NH-; -S-CH=N-; -S-CR29=N-; -N=CH-O-; -N=CR30-O-; -N=CH-NH-; - NH-C(=O)-NH-; -NH-C(=S)-NH-; -N=N-NH-; -O-CH2-C(=O)-NH-; -0-CH2-CH2-O-; -O- CH2-CH2-CH2-O-; -N=CH-CH=N-; -CH=CH-CH=N-; -CH=CH-N=CH-; -CH=N-N=CH- und -0-CH2-CH2-NH- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
oder R4 und R5 zusammen für einen Rest ausgewählt aus der Gruppe bestehend aus -S-CH=N-; -S-CR29=N-; -N=CH-O- und -N=CR30-O- stehen, der in beliebiger Richtung mit dem Grundgerüst verbunden ist,
und die übrigen Reste R1, R2, R3, R4 und R5, unabhängig voneinander, jeweils für H; -OR16; -SR17; oder für einen Rest ausgewählt aus der Gruppe bestehend aus Methyl, -CF3, -CHF2, -CH2F, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl und tert- Butyl stehen;
R8 für -SF5; -O-CF3; -CF3; tert-Butyl oder -C(CH3)2 (CH2OH) steht;
R16 und R17, unabhängig voneinander, jeweils für einen Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl und n-Pentyl stehen;
R28 für F; Cl; Br oder I steht;
R29 für -NH-C(=O)-R31; -NH2; -NH-S(=O)2-R32; -NH-C(=O)-O-R33 oder -S-R34 steht;
R30 für -NH2 steht;
R31, R32, R33 und R34, unabhängig voneinander, jeweils für Alkyl-Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl, tert-Butyl und n-Pentyl stehen;
R40 und R41 jeweils zusammen mit dem sie verbindenden Stickstoffatom als Ringglied einen Rest ausgewählt aus der Gruppe bestehend Pyrrolidinyl, Piperidinyl, Piperazinyl, Morpholinyl und Azepanyl bilden, dessen heterocycloaliphatischer Anteil jeweils unsubstituiert oder mit 1 , 2, 3, 4 oder 5 Resten R57 substituiert sein kann;
R57 für einen Alkyl-Rest ausgewählt aus der Gruppe bestehend aus Methyl, Ethyl, n-Propyl, Isopropyl, tert-Butyl, n-Butyl, sek-Butyl und Isobutyl steht; und
R71 für einen Phenyl-Rest steht, der über eine -(CH2)-, -(CH2)2- oder -(CH2)3- Gruppe gebunden sein kann und/oder jeweils unsubstituiert oder ggf. mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus F, Cl, Br, I, -CN1 -CF3, -SF5, -OH, -0-CH3, -0-C2H5, Methyl, Ethyl, n- Propyl, Isopropyl, n-Butyl, sek-Butyl, Isobutyl und tert-Butyl;
jeweils ggf. in Form eines ihrer reinen Stereoisomeren, insbesondere Enantiomeren oder Diastereomeren, ihrer Racemate oder in Form einer Mischung von Stereoisomeren, insbesondere der Enantiomeren und/oder Diastereomeren, in einem beliebigen Mischungsverhältnis, oder jeweils in Form entsprechender Salze, oder jeweils in Form entsprechender Solvate.
Bevorzugt sind ferner erfindungsgemäße substituierte Verbindungen der allgemeinen
Formel I, Ia, Ib, Ic und Id, worin
R1 und R2 oder R2 und R3 oder R3 und R4 oder R4 und R5 zusammen mit den sie verbindenden Kohlenstoffatomen einen 4-, 5-, 6- oder 7-gliedrigen Ring bilden, der gesättigt, ungesättigt oder aromatisch ist, 1 , 2 oder 3 Stickstoffatome als Ringglieder aufweist und unsubstituiert oder mit 1 , 2 oder 3 Resten substituiert ist, die jeweils unabhängig voneinander ausgewählt sind aus der Gruppe bestehend aus F, Cl, Br, I, -CN, =0, -CF3, -SF5, -OH, -0-Ci-5- Alkyl, -NH2, -NO2, -0-CF3, -S-CF3, -SH, -S-Ci-5-Alkyl, -C1-5-Alkyl, -C(=O)-OH, - C(=O)-O-C1-5-Alkyl, -NH-C1-5-Alkyl, -N(C1-5-Alkyl)2, -NH-S(=O)2-C1-5-Alkyl, -NH- C(=O)-O-C1-5-Alkyl, -C(=O)-H, -C(=O)-C1-5-Alkyl, -C(=O)-NH2, -C(=O)-NH-Ci-5- Alkyl, -C(=O)-N-(C1-5-Alkyl)2, -O-Phenyl, -O-Benzyl, Phenyl und Benzyl, wobei jeweils der zyklische Teil der Reste -O-Phenyl, -O-Benzyl, Phenyl und Benzyl mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus F, Cl, Br, -OH, -CF3, -SF5, -CN, -NO2, -d-5-Alkyl, - O-Ci-5-Alkyl, -0-CF3, -S-CF3, Phenyl und -O-Benzyl substituiert sein kann,
und die übrigen Reste von R1, R2, R3, R4 und R5, unabhängig voneinander, jeweils für H; F; Cl; Br; I; -SF5; -NO2; -CN; -NH2; -OH; -SH; -C(=O)-NH2; -S(=O)2-NH2; -C(=O)-NH-OH; -C(=O)-OH; -C(=O)-H; -S(=O)2-OH; -C(=NH)-NH2; -C(=NH)-
NH-R9; -N=C(NH2)2; -N=C(NHR10)(NHR11); -O-P(=O)2-O-R12; -NHR13; - NR14R15; -NH-C(=O)-R13; -OR16; -SR17; -C(=O)-NHR18; -C(=O)-NR19R20; - S(=O)2-NHR21; -S(=O)2-NR22R23; -C(=O)-OR24; -C(=O)-R25; -S(=O)-R26; - S(=O)2-R27 oder für einen linearen oder verzweigten, gesättigten oder ungesättigten, unsubstituierten oder wenigstens einfach substituierten aliphatischen C1-Io Rest stehen; und die übrigen Variablen und Substituenten jeweils eine der im Zusammenhang mit ihrer Definition genannten Bedeutungen haben,
jeweils ggf. in Form eines ihrer reinen Stereoisomeren, insbesondere Enantiomeren oder Diastereomeren, ihrer Racemate oder in Form einer Mischung von Stereoisomeren, insbesondere der Enantiomeren und/oder Diastereomeren, in einem beliebigen Mischungsverhältnis, oder jeweils in Form entsprechender Salze, oder jeweils in Form entsprechender Solvate.
Bevorzugt sind ferner erfindungsgemäße substituierte Verbindungen der allgemeinen
Formel I, Ia, Ib, Ic und Id, worin
R1 und R2 oder R2 und R3 oder R3 und R4 oder R4 und R5 zusammen mit den sie verbindenden Kohlenstoffatomen einen 4-, 5-, 6- oder 7-gliedrigen Ring bilden, der gesättigt, ungesättigt oder aromatisch ist, 1 , 2 oder 3 Stickstoffatome als Ringglieder aufweist und unsubstituiert oder mit 1 , 2 oder 3 Resten substituiert ist, die jeweils unabhängig voneinander ausgewählt sind aus der Gruppe bestehend aus F, Cl, Br, I, OH, =O, CF3, OCF3, SCF3, SF5, - O-Ci-4-Alkyl und Ci.4-Alkyl,
und die übrigen Reste von R1, R2, R3, R4 und R5, unabhängig voneinander, jeweils für H; F; Cl; Br; I; -SF5; -NO2; -CN; -NH2; -OH; -SH; -C(=O)-NH2; -S(=O)2-NH2; -C(=O)-NH-OH; -C(=O)-OH; -C(=O)-H; -S(=O)2-OH; -C(=NH)-NH2; -C(=NH)- NH-R9; -N=C(NH2)2; -N=C(NHR10)(NHR11); -O-P(=O)2-O-R12; -NHR13; - NR14R15; -NH-C(=O)-R13; -OR16; -SR17; -C(=O)-NHR18; -C(O)-NR19R20; - S(=O)2-NHR21; -S(=O)2-NR22R23; -C(=O)-OR24; -C(=O)-R25; -S(=O)-R26; - S(=O)2-R27 oder für einen linearen oder verzweigten, gesättigten oder
ungesättigten, unsubstituierten oder wenigstens einfach substituierten aliphatischen C-MO Rest stehen; und die übrigen Variablen und Substituenten jeweils eine der im Zusammenhang mit ihrer Definition genannten Bedeutungen haben,
jeweils ggf. in Form eines ihrer reinen Stereoisomeren, insbesondere Enantiomeren oder Diastereomeren, ihrer Racemate oder in Form einer Mischung von Stereoisomeren, insbesondere der Enantiomeren und/oder Diastereomeren, in einem beliebigen Mischungsverhältnis, oder jeweils in Form entsprechender Salze, oder jeweils in Form entsprechender Solvate.
Bevorzugt sind ferner erfindungsgemäße substituierte Verbindungen der allgemeinen Formel I, Ia, Ib, Ic und Id, worin die Teilstruktur
für eine der folgenden Substrukturen S-1 bis S-4 steht:
S-1 S-2 S-3 S-4
worin einer, zwei oder drei der Reste A1, A2 und A3 jeweils unabhängig voneinander für ein ggf. substituiertes Stickstoffatom stehen und die übrigen Reste jeweils unabhängig voneinander für ein ggf. substituiertes Kohlenstoffatom stehen.
Bevorzugte Bedeutungen a) bis g) für A A
1, A Λ 2
z und A
3 sind in nachfolgender Tabelle zusammengefasst, wobei N und C, je nach Position ggf. vorhandener Doppelbindungen substituiert sein können, z.B. mit -H:
Bevorzugt sind ferner erfindungsgemäße substituierte Verbindungen der allgemeinen Formel I; Ia, Ib, Ic und Id, worin die Teilstruktur
für eine der folgenden Substrukturen S-5 bis S-8 steht:
S-5 S-6 S-7 S-8
worin einer, zwei oder drei der Reste A1, A2, A3 und A4 jeweils unabhängig voneinander für ein ggf. substituiertes Stickstoffatom stehen und die übrigen Reste jeweils unabhängig voneinander für ein ggf. substituiertes Kohlenstoffatom stehen.
Bevorzugte Bedeutungen a) bis n) für A
1, A
2, A
3 und A
4 sind in nachfolgender Tabelle zusammengefasst, wobei N und C, je nach Position ggf. vorhandener Doppelbindungen substituiert sein können, z.B. mit -H:
Bevorzugt sind ferner erfindungsgemäße substituierte Verbindungen der allgemeinen Formel I1 Ia, Ib, Ic und Id, worin die Teilstruktur
für eine der folgenden Substrukturen S-9 bis S-12 steht:
S-9 S-10 S-11 S-12
worin einer, zwei oder drei der Reste A1, A2, A3, A4 und A5 jeweils unabhängig voneinander für ein ggf. substituiertes Stickstoffatom stehen und die übrigen Reste jeweils unabhängig voneinander für ein ggf. substituiertes Kohlenstoffatom stehen.
Bevorzugte Bedeutungen a) bis o) für A1, A2, A3, A4 und A5 sind in nachfolgender Tabelle zusammengefasst, wobei N und C, je nach Position ggf. vorhandener Doppelbindungen substituiert sein können, z.B. mit -H:
Bei den Substrukturen S-1 bis S-12 steht " : " jeweils für eine Einfach- oder eine
Doppelbindung. Ein Fachmann erkennt, dass in Abhängigkeit von der Position ggf. vorhandener Doppelbindungen die Anzahl der ggf. vorhandenen Wasserstoffatome oder möglichen Substituenten variiert und dass innerhalb der Ringstruktur keine Doppelbindungen unmittelbar aufeinander folgen.
Die Substrukturen S-1 bis S-12 können an den Stickstoffatmen bzw. an den Kohlenstoffatomen in den Positionen A1, A2, A3, A4 bzw. A5 aufgrund der Lage der Einfachbindungen bzw. der Lage der ggf. vorhandenen Doppelbindungen Wasserstoffatome oder andere Substituenten aufweisen.
In einer bevorzugten Ausführungsform weisen die Substrukturen S-1 bis S-12 an den Kohlenstoff- bzw. an den Stickstoffatomen in den Positionen A1, A2, A3, A4 bzw. A5 insgesamt höchstens zwei, bevorzugter insgesamt höchstens einen von Wasserstoff verschiedenen Substituenten auf, die jeweils unabhängig voneinander ausgewählt
sind aus der Gruppe bestehend aus F, Cl, Br, I1 -CN, =O, -CF3, -SF5, -OH, -0-Ci-5- Alkyl, -NH2, -NO2, -0-CF3, -S-CF3, -SH, -S-C1-5-Alkyl, -C1-5-Alkyl, -C(=O)-OH, -C(=O)- O-d-s-Alkyl, -NH-C1-5-Alkyl, -N(Ci-5-Alkyl)2, -NH-S(=O)2-C1-5-Alkyl, -NH-Ct=O)-O-C1- 5-Alkyl, -C(=O)-H, -C(=O)-C1-5-Alkyl, -C(=O)-NH2, -C(=O)-NH-C1-5-Alkyl, -C(=O)-N- (Ci-5-Alkyl)2, -O-Phenyl, -O-Benzyl, Phenyl und Benzyl, wobei jeweils der zyklische Teil der Reste -O-Phenyl, -O-Benzyl, Phenyl und Benzyl mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus F, Cl, Br, -OH, -CF3, -SF5, -CN, -NO2, -C1-5-Alkyl, -O-C1-5-Alkyl, -O-CF3, -S-CF3, Phenyl und -O-Benzyl substituiert sein kann;
vorzugsweise aus der Gruppe bestehend aus F, Cl, Br, I, OH, =0, CF3, OCF3, SCF3, SF5, -O-d-4-Alkyl und C1-4-Alkyl,
besonders bevorzugt aus der Gruppe bestehend aus F, Cl, Br, I, OH, =0, CF3, OCF3, SCF3, SF5, Methoxy, Ethoxy, Methyl, Ethyl, n-Propyl und iso-Propyl.
In einer bevorzugten Ausführungsform der Substrukturen S-1 bis S-12 ist der durch A1, A2, A3 und die ggf. vorhandenen Ringglieder A4 bzw. A5 gebildete Ring gesättigt, bis auf die Doppelbindung des anellierten Phenylrings, welcher die Substituenten R1 bis R5 trägt.
In einer anderen bevorzugten Ausführungsform der Substrukturen S-1 bis S-12 ist der durch A1, A2, A3 und die ggf. vorhandenen Ringglieder A4 bzw. A5 gebildete Ring wenigstens einfach ungesättigt, zusätzlich zu der Doppelbindung des anellierten Phenylrings, welcher die Substituenten R1 bis R5 trägt.
In einer weiteren bevorzugten Ausführungsform der Substrukturen S-1 bis S-12 ist der durch A
1, A
2, A
3 und die ggf. vorhandenen Ringglieder A
4 bzw. A
5 gebildete Ring aromatisch.
Bevorzugt sind ferner erfindungsgemäße substituierte Verbindungen der allgemeinen Formel I worin die Teilstruktur
für einen Rest steht ausgewählt aus der Gruppe bestehend aus
worin Ra und Rb, unabhängig voneinander, jeweils ausgewählt sind aus der Gruppe bestehend aus H, F, Cl, Br, I, -CN1 =O, -CF3, -SF5, -OH, -O-C1-5-Alkyl, -NH2, -NO2, - 0-CF3, -S-CF3, -SH, -S-C1-5-AIkVl, -C1-5-Alkyl, -C(=O)-OH, -C(=O)-O-C1-5-Alkyl, -NH- C1-5-Alkyl, -N(Ci-5-Alkyl)2, -NH-S(=O)2-C1-5-Alkyl, -NH-C(=O)-O-Ci-5-Alkyl, -C(=O)-H, - C(=O)-C1-5-Alkyl, -C(=O)-NH2, -C(=O)-NH-C1-5-Alkyl, -C(=O)-N-(C1-5-Alkyl)2, -O- Phenyl, -O-Benzyl, Phenyl und Benzyl, wobei jeweils der zyklische Teil der Reste -O- Phenyl, -O-Benzyl, Phenyl und Benzyl mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus F, Cl, Br, -OH, -CF3, -SF5, -
CN, -NO2, -Ci-5-Alkyl, -O-C1-5-Alkyl, -0-CF3, -S-CF3, Phenyl und -O-Benzyl substituiert sein kann; vorzugsweise aus der Gruppe bestehend aus H1 F, Cl, Br, I, OH1 =O, CF3, OCF3, SCF3, SF5, -O-d-4-Alkyl und C1-4-Alkyl,
und besonders bevorzugt aus der Gruppe bestehend aus F, Cl, Br1 I1 OH, =0, CF3, OCF3, SCF3, SF5, Methoxy, Ethoxy, Methyl, Ethyl, n-Propyl und iso-Propyl.
Bevorzugt sind ferner erfindungsgemäße substituierte Verbindungen der allgemeinen Formel I, Ia, Ib, Ic1 Id, worin die Teilstruktur
für einen Rest steht ausgewählt aus der Gruppe bestehend aus
worin Ra und Rb, unabhängig voneinander, jeweils ausgewählt sind aus der Gruppe bestehend aus H, F1 Cl1 Br, I1 -CN, =O, -CF3, -SF5, -OH, -O-C1-5-Alkyl, -NH2, -NO2, - C)-CF3, -S-CF3, -SH, -S-C1-5-AIkVl, -C1-5-Alkyl, -C(=O)-OH, -C(=O)-O-C1-5-Alkyl, -NH- d-s-Alkyl, -N(Ci-5-Alkyl)2, -NH-S(=O)2-Ci-5-Alkyl, -NH-C(=O)-O-C1-5-Alkyl, -C(=O)-H, - C(=O)-Ci-5-Alkyl, -C(=O)-NH2, -C(=O)-NH-C1-5-Alkyl, -C(=O)-N-(C1-5-Alkyl)2, -O- Phenyl, -O-Benzyl, Phenyl und Benzyl, wobei jeweils der zyklische Teil der Reste -O- Phenyl, -O-Benzyl, Phenyl und Benzyl mit 1 , 2, 3, 4 oder 5 Substituenten unabhängig voneinander ausgewählt aus der Gruppe bestehend aus F, Cl1 Br, -OH, -CF3, -SF5, - CN, -NO2, -Ci-5-Alkyl, -O-C1-5-Alkyl, -O-CF3) -S-CF3, Phenyl und -O-Benzyl substituiert sein kann; vorzugsweise aus der Gruppe bestehend aus H, F, Cl, Br, I, OH, =0, CF3, OCF3, SCF3, SF5, -O-Ci-4-Alkyl und Ci-4-Alkyl und besonders bevorzugt aus der Gruppe bestehend aus F, Cl, Br, I, OH, =0, CF3, OCF3, SCF3, SF5, Methoxy, Ethoxy, Methyl, Ethyl, n-Propyl und iso-Propyl.
Noch weiter bevorzugt sind Verbindungen der allgemeinen Formeln I, Ia, Ib, Ic und Id ausgewählt aus der Gruppe bestehend aus
[I] 2-(Benzo[d]oxazol-5-yl)-N-(4-tert-butylbenzyl)propanamid, [2] 2-(Benzo[d]oxazol-6-yl)-N-(4-tert-butylbenzyl)propanamid, [3] 2-(Benzo[d]oxazol-7-yl)-N-(4-tert-butylbenzyl)propanamid,
[4] N-(4-tert-Butylbenzyl)-2-(2-oxo-2,3-dihydro-1 H-benzo[d]imidazol-5- yl)propanamid, [5] N-(4-tert-Butylbenzyl)-2-(3-oxo-3,4-dihydro-2H-benzo[b][1 ,4]oxazin-7- yl)propanamid, [6] N-(4-tert-Butylbenzyl)-2-(3-oxo-3,4-dihydro-2H-benzo[b][1 ,4]oxazin-6- yl)propanamid,
[7] N-(4-tert-Butylbenzyl)-2-(7-methoxybenzo[d]oxazol-5-yl)propanamid, [8] 2-(Benzo[d]oxazol-4-yl)-N-(4-tert-butylbenzyl)propanamid, [9] N-(4-tert-Butylbenzyl)-2-(2,3-dihydrobenzo[b][1 ,4]dioxin-6- yl)propanamid, [10] N-(4-tert-Butylbenzyl)-2-(2-thioxo-2,3-dihydro-1 H-benzo[d]imidazol-5- yl)propanamid,
II 1] N-(4-tert-Butylbenzyl)-2-(chinoxalin-6-yl)propanamid,
[12] 2-(1 H-Benzo[d][1 ,2,3]triazol-5-yl)-N-(4-tert-butylbenzyl)propanamid, [13] 2-(1 H-Benzo[d]imidazol-5-yl)-N-((2-(4-methylpiperidin-1 -yl)-6-
(trifluormethyl)pyridin-3-yl)methyl)propanamid, [14] 2-(1 H-Benzo[d]imidazol-5-yl)-N-(4-tert-butylbenzyl)propanamid, [15] 2-(1 H-Benzo[d][1 ,2,3]triazol-5-yl)-N-((2-(4-methylpiperidin-1 -yl)-6-
(trifluormethyl)pyridin-3-yl)methyl)propanamid, [16] N-(4-tert-Butylbenzyl)-2-(2-oxo-2,3-dihydrobenzo[d]oxazol-6- yl)propanamid, [17] N-(4-tert-Butylbenzyl)-2-(2-thioxo-2,3-dihydrobenzo[d]oxazol-5- yl)propanamid,
[18] 2-(2-Aminobenzo[d]oxazol-6-yl)-N-(4-tert-butylbenzyl)propanamid, [19] N-(4-tert-Butylbenzyl)-2-(2-thioxo-2,3-dihydrobenzo[d]oxazol-6- yl)propanamid, [20] N-(4-tert-Butylbenzyl)-2-(3,4-dihydro-2H-benzo[b][1 ,4]oxazin-7- yl)propanamid,
[21] N-(4-tert-Butylbenzyl)-2-(chinolin-6-yl)propanamid,
[22] 2-(1 H-Benzo[d][1 ,2,3]triazol-5-yl)-N-((2-butoxy-6-tert-butylpyridin-3- yl)methyl)propanamid, [23] 2-(1 H-Benzo[d]imidazol-5-yl)-N-((2-butoxy-6-tert-butylpyridin-3- yl)methyl)propanamid, [24] 2-(1 H-Benzo[d][1 ,2,3]triazol-5-yl)-N-((6-tert-butyl-2-(4-methylpiperidin-1- yl)pyridin-3-yl)methyl)propanamid, [25] 2-(1 H-Benzo[d]imidazol-5-yl)-N-((6-tert-butyl-2-(4-methylpiperidin-1 - yl)pyridin-3-yl)methyl)propanamid, [26] 2-(1 H-Benzo[d][1 ,2,3]triazol-5-yl)-N-((6-tert-butyl-2-
(cyclohexylthio)pyridin-3-yl)methyl)propanamid, [27] 2-(1 H-Benzo[d]imidazol-5-yl)-N-((6-tert-butyl-2-(cyclohexylthio)pyridin-3- yl)methyl)propanamid, [28] N-((2-Butoxy-6-tert-butylpyridin-3-yl)methyl)-2-(2-oxo-2,3- dihydrobenzo[d]thiazol-6-yl)propanamid, [29] N-(2-Butoxy-6-tert-butyl-pyridin-3-ylmethyl)-2-(2-ethylsulfanyl-benzothiazol-6- yl)-propionamid, [30] N-((2-(4-Methylpiperidin-1-yl)-6-(trifluormethyl)pyridin-3-yl)methyl)-2-(2-
(methylthio)benzo[d]thiazol-6-yl)propanamid, [31] N-((2-Butoxy-6-tert-butylpyridin-3-yl)methyl)-2-hydroxy-2-(2-
(methylthio)benzo[d]thiazol-6-yl)propanamid, [32] N-((2-(4-Methylpiperidin-1-yl)-6-(trifluormethyl)pyridin-3-yl)methyl)-2-(2- thioxo-2,3-dihydrobenzo[d]thiazol-6-yl)propanamid, [33] N-((6-tert-Butyl-2-(4-methylpiperidin-1-yl)pyridin-3-yl)methyl)-2-(2- thioxo-2,3-dihydrobenzo[d]thiazol-6-yl)propanamid, [34] N-((6-tert-Butyl-2-(4-methylpiperidin-1-yl)pyridin-3-yl)methyl)-2-(2-
(methylthio)benzo[d]thiazol-6-yl)propanamid, [35] 2-(2-Aminobenzo[d]oxazol-5-yl)-N-((2-(4-methylpiperidin-1-yl)-6-
(trifluormethyOpyridin-S-yOmethyOpropanamid,
[36] 2-(2-Acetamidobenzo[d]thiazol-6-yl)-N-(4-tert-butylbenzyl)propanamid, [37] 2-(2-Acetamidobenzo[d]thiazol-6-yl)-N-((2-(4-methylpiperidin-1-yl)-6-
(trifluormethyl)pyridin-3-yl)methyl)propanamid, [38] 2-(2-Aminobenzo[d]thiazol-6-yl)-N-((2-(4-methylpiperidin-1-yl)-6-
(trifluormethyl)pyridin-3-yl)methyl)propanamid,
[39] N-((2-(4-Methylpiperidin-1-yl)-6-(trifluormethyl)pyridin-3-yl)methyl)-2-
(2-(methylsulfonamido)benzo[d]thiazol-6-yl)propanamid, [40] tert-Butyl 6-(1-((2-(4-methylpiperidin-1-yl)-6-(trifluormethyl)pyridin-3- yl)methylamino)-1-oxopropan-2-yl)benzo[d]thiazol-2-ylcarbamat, [41] 2-(2-Acetamidobenzo[d]thiazol-6-yl)-N-((2-(4-methylpiperidin-1-yl)-6-
(trifluormethyl)pyridin-3-yl)methyl)propanamid, [42] 2-(2-Acetamidobenzo[d]thiazol-5-yl)-N-((2-(4-methylpiperidin-1-yl)-6-
(trifluormethyOpyridin-S-yOmethyOpropanamid, [43] 2-(2-Acetamidobenzo[d]thiazol-4-yl)-N-((2-(4-methylpiperidin-1-yl)-6-
(trifluormethyl)pyridin-3-yl)methyl)propanamid, [44] 2-(1 H-lndazol-5-yl)-N-((2-(4-methylpiperidin-1-yl)-6-
(trifluormethyl)pyridin-3-yl)methyl)propanamid, [45] 2-(3-Fluor-1 H-indazol-5-yl)-N-((2-(4-methylpiperidin-1 -yl)-6-
(trifluormethyl)pyridin-3-yl)methyl)propanamid, [46] N-((2-Butoxy-6-tert-butylpyridin-3-yl)methyl)-2-(1 H-indazol-5- yl)propanamid, [48] N-((6-tert-Butyl-2-(cyclohexylthio)pyridin-3-yl)methyl)-2-(1 H-indazol-5- yl)propanamid [49] N-(2-Butoxy-6-tert-butyl-pyridin-3-ylmethyl)-2-(2-thioxo-2,3- dihydro-benzothiazol-6-yl)-propionamid; [50] tert-Butyl 6-(1-(4-tert-butylbenzylamino)-1-oxopropan-2- yl)benzo[d]thiazol-2-yicarbamat,
[51] 2-(2-Aminobenzo[d]thiazol-6-yl)-N-(4-tert-butylbenzyl)propanamid, [52] 2-(2-Aminobenzo[d]thiazol-6-yl)-N-((2-(4-methylpiperidin-1-yl)-6-
(trifluormethyl)pyridin-3-yl)methyl)propanamid, [53] 2-(2-Acetamidobenzo[d]thiazol-6-yl)-N-((6-tert-butyl-2-(4-methylpiperidin-1- yl)pyridin-3-yl)methyl)propanamid und [54] tert-Butyl 6-(1-((2-(4-methylpiperidin-1-yl)-6-(trifluormethyl)pyridin-3- yl)methylamino)-1-oxopropan-2-yl)benzo[d]thiazol-2-ylcarbamat; [54] tert-Butyl 6-(1 -((2-(4-methylpiperidin-1 -yl)-6-(trifluormethyl)pyridin-3- yl)methylamino)-1-oxopropan-2-yl)benzo[d]thiazol-2-ylcarbamat; [55] tert-butyl 6-(1-((6-tert-butyl-2-(4-Methylpiperidin-1-yl)pyridin-3-yl)methylamino)-
1-oxopropan-2-yl)benzo[d]thiazol-2-ylcarbamat;
[56] 2-(2-Aminobenzo[d]thiazol-6-yl)-N-((6-tert-butyl-2-(4-methylpiperidin-1- yl)pyridin-3-yl)methyl)propanamid; [57] N-(4-tert-butylbenzyl)-2-(2-(Methylsulfonamid)benzo[d]thiazol-6- yl)propanamid; [58] 2-(2,3-Dihydrobenzo[b][1 ,4]dioxin-6-yl)-N-((2-(4-methylpiperidin-1 -yl)-6-
(trifluormethyl)pyridin-3-yl)methyl)acetamid; [59] N-((2-(Cyclohexylthio)-6-(trifluormethyl)pyridin-3-yl)methyl)-2-(2,3- dihydrobenzo[b][1 ,4]dioxin-6-yl)acetamid; [60] 2-(Benzo[d][1 ,3]dioxol-5-yl)-N-((2-(4-methylpiperidin-1 -yl)-6-
(trifluormethyl)pyridin-3-yl)methyl)propanamid; [61] 2-(Benzo[d][1 ,3]dioxol-4-yl)-N-((2-(4-methylpiperidin-1-yl)-6-
(trifluormethyl)pyridin-3-yl)methyl)propanamid; [62] 2-(2,3-Dihydrobenzo[b][1 ,4]dioxin-6-yl)-N-((2-(4-methylpiperidin-1 -yl)-6-
(trifluormethyl)pyridin-3-yl)methyl)propanamid; [63] 2-(2,3-Dihydrobenzo[b][1 ,4]dioxin-5-yl)-N-((2-(4-methylpiperidin-1 -yl)-6-
(trifluormethyl)pyridin-3-yl)methyl)propanamid [64] 2-(lsochinolin-7-yl)-N-((2-(4-methylpiperidin-1-yl)-6-(trifluormethyl)pyridin-3- yl)methyl)propanamid [65] 2-(lsochinolin-6-yl)-N-((2-(4-methylpiperidin-1-yl)-6-(trifluormethyl)pyridin-3- yl)methyl)propanamid [66] N-((2-(4-Methylpiperidin-1-yl)-6-(trifluormethyl)pyridin-3-yl)methyl)-2-(chinolin-
6-yl)propanamid [67] N-((2-(4-Methylpiperidin-1-yl)-6-(trifluormethyl)pyridin-3-yl)methyl)-2-
(chinoxalin-6-yl)propanamid [68] N-((2-(4-Methylpiperidin-1-yl)-6-(trifluormethyl)pyridin-3-yl)methyl)-2-
(chinazolin-6-yl)propanamid [69] 2-(1 H-lndazol-5-yl)-N-(2-(4-methylpiperidin-1-yl)-4-
(trifluormethyl)benzyl)propanamid [70] 2-(1 H-lndazol-4-yl)-N-((2-(4-methylpiperidin-1-yl)-6-(trifluormethyl)pyridin-3- yl)methyl)propanamid [71] 2-(1 H-lndazol-6-yl)-N-((2-(4-methylpiperidin-1-yl)-6-(trifluormethyl)pyridin-3- yl)methyl)propanamid [72] 2-(1 H-lndazol-7-yl)-N-((2-(4-methylpiperidin-1-yl)-6-(trifluormethyl)pyridin-3- yl)methyl)propanamid
[73] 2-(1 -(2-Fluorphenyl)-1 H-indazol-4-yl)-N-((2-(4-methylpiperidin-1 -yl)-6-
(trifluormethyl)pyridin-3-yl)methyl)propanamid [74] 2-(lndolin-5-yl)-N-((2-(4-methylpiperidin-1-yl)-6-(trifluormethyl)pyridin-3- yl)methyl)propanamid [75] N-((2-(4-Methylpiperidin-1 -yl)-6-(trifluormethyl)pyridin-3-yl)methyl)-2-(1 ,2,3,4- tetrahydrochinolin-6-yl)propanamid [76] N-((2-(4-Methylpiperidin-1-yl)-6-(trifluormethyl)pyridin-3-yl)methyl)-2-(2- oxoindolin-5-yl)propanamid und [77] N-((2-(4-Methylpiperidin-1-yl)-6-(trifluormethyl)pyridin-3-yl)methyl)-2-(2-oxo-
1 ,2,3,4-tetrahydrochinolin-6-yl)propanamid
jeweils ggf. in Form eines ihrer reinen Stereoisomeren, insbesondere Enantiomeren oder Diastereomeren, ihrer Racemate oder in Form einer Mischung von Stereoisomeren, insbesondere der Enantiomeren und/oder Diastereomeren, in einem beliebigen Mischungsverhältnis, oder jeweils in Form entsprechender Salze, oder jeweils in Form entsprechender Solvate;
Weiterhin können erfindungsgemäße Verbindungen der allgemeinen Formeln I, Ia1 Ib, Ic und Id bevorzugt sein, die im FLIPR-Assay mit CHO K1 -Zellen, die mit dem menschlichen VR1-Gen transfiziert wurden, in einer Konzentration kleiner 2000 nM, bevorzugt kleiner 1000 nM, besonders bevorzugt kleiner 300 nM, ganz besonders bevorzugt kleiner 100 nM, noch weiter bevorzugt kleiner 75 nM, darüber hinaus bevorzugt kleiner 50 nM, am weitesten bevorzugt kleiner 10 nM, eine 50-prozentige Verdrängung von Capsaicin bewirken, dass in einer Konzentration von 100 nM vorliegt.
Dabei wird Im FLIPR-Assay der Ca2+-Einstrom mit Hilfe eines Ca2+-sensitiven Farbstoffs (Typ Fluo-4, Molecular Probes Europe BV, Leiden Niederlande) im Fluorescent Imaging Plate Reader (FLIPR, Molecular Devices, Sunnyvale, USA) quantifiziert, wie untenstehend beschrieben.
Ein weiterer Gegenstand der vorliegenden Erfindung ist ein Verfahren zur Herstellung von Verbindungen der vorstehend angegebenen allgemeinen Formel I gemäß dem wenigstens eine Verbindung der allgemeinen Formel II,
worin R8, U, T, V und W die vorstehend genannte Bedeutung haben, m für 0, 1 , 2 oder 3 steht und R für Wasserstoff oder für einen linearen oder verzweigten Ci-6- Alkyl-Rest steht, in einem Reaktionsmedium, in Gegenwart wenigstens eines Reduktionsmittels, vorzugsweise in Gegenwart wenigstens eines Reduktionsmittels ausgewählt aus der Gruppe bestehend aus Natriumhydrid, Natrium, Kaliumhydrid, Lithiumaluminiumhydrid, Natriumborhydrid und Di(isobutyl)aluminiumhydrid
zu wenigstens einer Verbindung der allgemeinen Formel III,
worin R8, U, T, V und W die vorstehend genannte Bedeutung haben und m für 0, 1 , 2 oder 3 steht, umgesetzt wird und diese ggf. gereinigt und/oder isoliert wird,
und wenigstens eine Verbindung der allgemeinen Formel III in einem Reaktionsmedium in Gegenwart von Diphenylphosphorylazid oder in Gegenwart von HN3Zu wenigstens einer Verbindung der allgemeinen Formel IV,
IV,
worin R8, U1 T, V und W die vorstehend genannte Bedeutung haben und m für 0, 1 , 2 oder 3 steht, umgesetzt wird und diese ggf. gereinigt und/oder isoliert wird,
und wenigstens eine Verbindung der allgemeinen Formel IV in einem Reaktionsmedium in Gegenwart wenigstens eines Reduktionsmittels, vorzugsweise in Gegenwart wenigstens eines Reduktionsmittels ausgewählt aus der Gruppe bestehend aus Natriumhydrid, Kaliumhydrid, Lithiumaluminiumhydrid, Natriumborhydrid und Di(isobutyl)aluminiumhydrid
oder in einem Reaktionsmedium in Gegenwart eines Katalysators, vorzugsweise in Gegenwart eines Katalysators basierend auf Platin oder Palladium, besonders bevorzugt in Gegenwart von Palladium auf Kohle, und in Gegenwart von Wasserstoff oder in Gegenwart von Hydrazin
oder in einem Reaktionsmedium in Gegenwart von Triphenylphosphin
zu wenigstens einer Verbindung der allgemeinen Formel V,
worin R8, U, T, V und W die vorstehend genannte Bedeutung haben und m für 0, 1 , 2 oder 3 steht, umgesetzt wird und diese ggf. gereinigt und/oder isoliert wird,
oder wenigstens eine Verbindung der allgemeinen Formel Vl1
VI,
worin R8, U, T, V und W die vorstehend genannte Bedeutung haben und m für 0, 1 , 2 oder 3 steht, in einem Reaktionsmedium
in Gegenwart wenigstens eines Katalysators, vorzugsweise in Gegenwart wenigstens eines Katalysators basierend auf Palladium oder Platin, besonders bevorzugt in Gegenwart von Palladium auf Kohle, unter einer Wasserstoffatmosphäre, ggf. in Gegenwart wenigstens einer Säure, vorzugsweise in Gegenwart von Salzsäure,
oder in Gegenwart wenigstens eines Reduktionsmittels ausgewählt aus der Gruppe bestehend aus BH3 #S(CH3)2, Lithiumaluminiumhydrid und Natriumborhydrid, ggf. in Gegenwart von NiC^,
zu wenigstens einer Verbindung der allgemeinen Formel V1 ggf. in Form eines entsprechenden Salzes, vorzugsweise in Form eines entsprechenden Hydrochlorids, umgesetzt wird und diese ggf. gereinigt und/oder isoliert wird,
und wenigstens eine Verbindung der allgemeinen Formel V mit wenigstens einer Verbindung der allgemeinen Formel VII,
VII,
worin R1, R2, R3, R4, R5, R6 und R7 die vorstehend genannte Bedeutung haben, in einem Reaktionsmedium, ggf. in Gegenwart wenigstens eines geeigneten Kopplungsmittels, ggf. in Gegenwart wenigstens einer Base,
oder mit wenigstens einer Verbindung der allgemeinen Formel VIII1
VIII1
worin R1, R2, R3, R4, R5, R6 und R7 die vorstehend genannte Bedeutung haben und LG für eine Abgangsgruppe, vorzugsweise für ein Chlor- oder Bromatom steht, in einem Reaktionsmedium, ggf. in Gegenwart wenigstens einer Base, zu wenigstens einer Verbindung der allgemeinen Formel I,
worin T, U, V, W, R1, R2, R3, R4, R5, R6, R7 und R8, die vorstehend genannte Bedeutung haben und n für 1 , 2, 3 oder 4 steht, umgesetzt wird und diese ggf. gereinigt und/oder isoliert wird.
Ein weiterer Gegenstand der vorliegenden Erfindung ist ein Verfahren zur Herstellung von Verbindungen der vorstehend angegebenen allgemeinen Formel gemäß dem wenigstens eine Verbindung der allgemeinen Formel X,
worin R8, U, T, V und W die vorstehend genannte Bedeutung haben, mit wenigstens einer Verbindung der allgemeinen Formel VII1
worin R
1, R
2, R
3, R
4, R
5, R
6 und R
7, die vorstehend genannte Bedeutung haben, in einem Reaktionsmedium, ggf. in Gegenwart wenigstens eines geeigneten Kopplungsmittels, ggf. in Gegenwart wenigstens einer Base,
oder mit wenigstens einer Verbindung der allgemeinen Formel VIII,
VIII,
worin R1, R2, R3, R4, R5, R6 und R7 die vorstehend genannte Bedeutung haben und LG für eine Abgangsgruppe, vorzugsweise für ein Chlor- oder Bromatom steht, in einem Reaktionsmedium, ggf. in Gegenwart wenigstens einer Base, zu wenigstens einer Verbindung der allgemeinen Formel Im,
Im,
worin T, U, V, W, R1, R2, R3, R4, R5, R6, R7 und R8 die vorstehend genannte Bedeutung haben, umgesetzt wird und diese ggf. gereinigt und/oder isoliert wird.
Die Umsetzung von Verbindungen der vorstehend angegebenen allgemeinen Formeln V bzw. X mit Carbonsäuren der vorstehend angegebenen allgemeinen Formel VII zu Verbindungen der vorstehend angegebenen allgemeinen Formeln I bzw. Im erfolgt vorzugsweise in einem Reaktionsmedium ausgewählt aus der Gruppe bestehend aus Diethylether, Tetrahydrofuran, Acetonitril, Methanol, Ethanol, (1 ,2)- Dichlorethan, Dimethylformamid, Dichlormethan und entsprechenden Mischungen, ggf. in Gegenwart wenigstens eines Kupplungsreagenzes, vorzugsweise ausgewählt
aus der Gruppe bestehend aus i-Benzotriazolyloxy-tris-(dimethylamino)- phosphonium hexafluorphosphat (BOP), Dicyclohexylcarbodiimid (DCC)1 N'-(3- Dimethylaminopropyl)-N-ethylcarbodiimid (EDCI), Diisoproylcarbodiimid, 1 ,1 '- Carbonyl-diimidazol (CDI), N-[(Dimethyamino)-1 H-1 , 2, 3-triazolo[4, 5-b]pyridino-1- ylmethylen]-N-methylmethanaminium hexafluorphosphat N-oxid (HATU), O- (Benzotriazol-1-yl)-N,N,N',N'-tetramethyluroniom hexafluorphosphat (HBTU), O- (Benzotriazol-1 -yl)-N,N, N', N'-tetramethyluronium-tetrafluorborat (TBTU), N- Hydroxybenzotriazol (HOBt) und 1-Hydroxy-7-azabenzotriazol (HOAt), ggf. in Gegenwart wenigstens einer organischen Base, vorzugsweise ausgewählt aus der Gruppe bestehend aus Triethylamin, Pyridin, Dimethylaminopyridin, N- Methylmorpholin und Diisopropylethylamin, vorzugsweise bei Temperaturen von - 700C bis 10O0C.
Alternativ erfolgt die Umsetzung von Verbindungen vorstehend angegebenen allgemeinen Formeln V bzw. X mit Carbonsäurederivaten der vorstehend angegebenen allgemeinen Formel VIII, worin LG für eine Abgangsgruppe, bevorzugt für ein Chlor- oder Bromatom, steht, zu Verbindungen der vorstehend angegebenen allgemeinen Formeln Ih bzw. Im in einem Reaktionsmedium vorzugsweise ausgewählt aus der Gruppe bestehend aus Diethylether, Tetra hydrofu ran, Acetonitril, Methanol, Ethanol, Dimethylformamid, Dichlormethan und entsprechenden Mischungen, ggf. in Gegenwart einer organischen oder anorganischen Base, vorzugsweise ausgewählt aus der Gruppe bestehend aus Triethylamin, Dimethylaminopyridin, Pyridin und Diisopropylamin, bei Temperaturen von -700C bis 100°C.
Die Verbindungen der vorstehend angegebenen Formeln II, III, IV, V, X, VI, VII und VIII sind jeweils am Markt käuflich erhältlich und können auch nach üblichen, dem Fachmann bekannten Verfahren hergestellt werden.
Die Synthese von Verbindungen der allgemeinen Formel VII kann der Druckschrift „4-(Methylsulfonylamino)phenyl analogues as vanilloid antagonist showing excellent analgesic activity and the pharmaceutical compositions comprising the same" von J. W. Lee et al. [WO 2005/003084-A1] entnommen werden. Die entsprechenden Teile der Referenz gelten hiermit als Teil der Offenbarung.
Die vorstehend beschriebenen Umsetzungen können jeweils unter den üblichen dem Fachmann geläufigen Bedingungen, beispielsweise in Hinblick auf Druck oder Reihenfolge der Zugabe der Komponenten durchgeführt werden. Ggf. kann die unter den jeweiligen Bedingungen optimale Verfahrensführung vom Fachmann durch einfache Vorversuche ermittelt werden. Die nach den vorstehend beschriebenen Umsetzungen erhaltenen Zwischen- und Endprodukte können jeweils, falls gewünscht und/oder erforderlich, nach üblichen, dem Fachmann bekannten Methoden gereinigt und/oder isoliert werden. Geeignete Reinigungsverfahren sind beispielsweise Extraktionsverfahren und chromatographische Verfahren wie Säulenchromatographie oder präparative Chromatographie. Sämtliche der vorstehend beschriebenen Verfahrensschritte sowie jeweils auch die Reinigung und/oder Isolierung von Zwischen- oder Endprodukten können teilweise oder vollständig unter einer Inertgasatmosphäre, vorzugsweise unter Stickstoffatmosphäre, durchgeführt werden.
Die erfindungsgemäßen substituierten Verbindungen der vorstehend genannten allgemeinen Formeln I, Ia, Ib, Ic und Id - im Folgenden nur als Verbindungen der allgemeinen Formel I - bezeichnet, sowie entsprechende Stereoisomere können sowohl in Form ihrer freien Basen, ihrer freien Säuren wie auch in Form entsprechender Salze, insbesondere physiologisch verträglicher Salze, isoliert werden.
Die freien Basen der jeweiligen erfindungsgemäßen substituierten Verbindungen der vorstehend genannten allgemeinen Formel I sowie entsprechender Stereoisomere; können beispielsweise durch Umsetzung mit einer anorganischen oder organischen Säure, vorzugsweise mit Salzsäure, Bromwasserstoffsäure, Schwefelsäure, Phosphorsäure, Methansulfonsäure, p-Toluolsulfonsäure, Kohlensäure, Ameisensäure, Essigsäure, Oxalsäure, Bernsteinsäure, Weinsäure, Mandelsäure, Fumarsäure, Milchsäure, Zitronensäure, Glutaminsäure oder Asparaginsäure, in die entsprechenden Salze, vorzugsweise physiologisch verträglichen Salze, überführt werden. Die freien Basen der jeweiligen substituierten Verbindungen der vorstehend genannten allgemeinen Formel I und entsprechender Stereoisomere können ebenfalls mit der freien Säure oder einem Salz eines Zuckerersatzstoffes, wie z.B.
Saccharin, Cyclamat oder Acesulfam, in die entsprechenden physiologisch verträglichen Salze überführt werden.
Entsprechend können die freien Säuren der substituierten Verbindungen der vorstehend genannten allgemeinen Formel I und entsprechender Stereoisomere durch Umsetzung mit einer geeigneten Base in die entsprechenden physiologisch verträglichen Salze überführt werden. Beispielhaft seien die Alkalimetallsalze, Erdalkalimetallsalze oder Ammoniumsalze [NHxR4-J+, worin x = 0, 1 , 2, 3 oder 4 ist und R für einen linearen oder verzweigten Ci-4-Alkyl-Rest steht, genannt.
Die erfindungsgemäßen substituierten Verbindungen der vorstehend genannten allgemeinen Formel I und entsprechender Stereoisomere können ggf., ebenso wie die entsprechenden Säuren, die entsprechenden Basen oder Salze dieser Verbindungen, nach üblichem, dem Fachmann bekannten Methoden auch in Form ihrer Solvate, vorzugsweise in Form ihrer Hydrate, erhalten werden.
Sofern die erfindungsgemäßen substituierten Verbindungen der vorstehend genannten allgemeinen Formel I nach ihrer Herstellung in Form einer Mischung ihrer Stereoisomeren, vorzugsweise in Form ihrer Racemate oder anderer Mischungen ihrer verschiedenen Enantiomeren und/oder Diastereomeren erhalten werden, können diese nach üblichen, dem Fachmann bekannten Verfahren getrennt und ggf. isoliert werden. Beispielhaft seien chromatographische Trennverfahren, insbesondere Flüssigkeitschromatographie-Verfahren unter Normaldruck oder unter erhöhtem Druck, bevorzugt MPLC- und HPLC-Verfahren, sowie Verfahren der fraktionierten Kristallisation genannt. Dabei können insbesondere einzelne Enantiomeren, z.B. mittels HPLC an chiraler stationärer Phase oder mittels Kristallisation mit chiralen Säuren, etwa (+)-Weinsäure, (-)-Weinsäure oder (+)-10- Camphersulfonsäure, gebildete diastereomere Salze voneinander getrennt werden.
Die erfindungsgemäßen substituierten Verbindungen der vorstehend genannten allgemeinen Formel I und entsprechende Stereoisomere sowie jeweils die entsprechenden Säuren, Basen, Salze und Solvate sind toxikologisch unbedenklich und eignen sich daher als pharmazeutische Wirkstoffe in Arzneimitteln.
Ein weiterer Gegenstand der vorliegenden Erfindung ist daher ein Arzneimittel enthaltend wenigstens eine erfindungsgemäße Verbindung der vorstehend angegebenen allgemeinen Formel I1 jeweils ggf. in Form eines ihrer reinen Stereoisomeren, insbesondere Enantiomeren oder Diastereomeren, ihrer Racemate oder in Form einer Mischung von Stereoisomeren, insbesondere der Enantiomeren und/oder Diastereomeren, in einem beliebigen Mischungsverhältnis, oder jeweils in Form eines entsprechenden Salzes, oder jeweils in Form eines entsprechenden Solvates, sowie ggf. einen oder mehrere pharmazeutisch verträgliche Hilfsstoffe.
Diese erfindungsgemäßen Arzneimittel eignen sich insbesondere zur Vanilloid- Rezeptor 1-(VR1/TRPV1 )-Regulation, vorzugsweise zur Vanilloid-Rezeptor 1- (VR1/TRPV1 )-Hemmung und/oder zur Vanilloid-Rezeptor 1(VR1/TRPV1 )- Stimulation.
Ebenfalls bevorzugt eignen sich die erfindungsgemäßen Arzneimittel zur Prophylaxe und/oder Behandlung von Störungen oder Krankheiten, die zumindest teilweise durch Vanilloid-Rezeptoren 1 vermittelt werden.
Bevorzugt eignet sich das erfindungsgemäße Arzneimittel zur Behandlung und/oder Prophylaxe von einer oder mehreren Erkrankungen ausgewählt aus der Gruppe bestehend aus Schmerz ausgewählt aus der Gruppe bestehend aus akutem Schmerz, chronischem Schmerz, neuropathischem Schmerz und visceralem Schmerz; Gelenkschmerz; Hyperalgesie; Allodynie; Kausalgie; Migräne; Depressionen; Nervenleiden; Nervenverletzungen; neurodegenerativen Erkrankungen, vorzugsweise ausgewählt aus der Gruppe bestehend aus Multipler Sklerose, Morbus Alzheimer, Morbus Parkinson und Morbus Huntington; kognitiven Dysfunktionen, vorzugsweise kognitiven Mangelzuständen, besonders bevorzugt Gedächtnisstörungen; Epilepsie; Atemwegserkrankungen, vorzugsweise ausgewählt aus der Gruppe bestehend aus Asthma, Bronchitis und Lungenentzündung; Husten; Harninkontinenz; einer überaktiven Blase (overactive bladder, OAB); Erkrankungen und/oder Verletzungen des Magen-Darm-Trakts; Zwölffingerdarmgeschwüren; Magengeschwüren; Reizdarmsyndrom; Schlaganfällen; Augenreizungen;
Hautreizungen; neurotischen Hauterkrankungen; allergischen Hautkrankheiten; Psiorasis; Vitiligo; Herpes Simplex; Entzündungen, vorzugsweise Entzündungen des Darmes, der Augen, der Blase, der Haut oder der Nasenschleimhaut; Diarrhöe; Pruritus; Osteoporose; Arthritis; Osteoarthritis; rheumatischen Erkrankungen; Störungen der Nahrungsaufnahme, vorzugsweise ausgewählt aus der Gruppe bestehend aus Bulimie, Kachexie, Anorexie und Fettleibigkeit; Medikamentenabhängigkeit; Medikamentenmißbrauch; Entzugserscheinungen bei Medikamentenabhängigkeit; Toleranzentwicklung gegenüber Medikamenten, vorzugsweise gegenüber natürlichen oder synthetischen Opioiden; Drogenabhängigkeit; Drogenmißbrauch; Entzugserscheinungen bei Drogenabhängigkeit; Alkoholabhängigkeit; Alkoholmissbrauch und Entzugserscheinungen bei Alkoholabhängigkeit; zur Diurese; zur Antinatriurese; zur Beeinflussung des kardiovaskulären Systems; zur Vigilanzsteigerung; zur Behandlung von Wunden und/oder Verbrennungen; zur Behandlung von durchtrennten Nerven; zur Libidosteigerung; zur Modulation der Bewegungsaktivität; zur Anxiolyse; zur Lokalanästhesie und/oder zur Hemmung unerwünschter Nebenwirkungen, vorzugsweise ausgewählt aus der Gruppe bestehend aus Hyperthermie, Bluthochdruck und Verengung der Bronchien, ausgelöst durch die Verabreichung von Vanilloid-Rezeptor 1 (VR1/TRPV1-Rezeptoren)-Agonisten, vorzugsweise ausgewählt aus der Gruppe bestehend aus Capsaicin, Resiniferatoxin, Olvanil, Arvanil, SDZ-249665, SDZ-249482, Nuvanil und Capsavanil.
Besonders bevorzugt eignet sich das erfindungsgemäße Arzneimittel zur Behandlung und/oder Prophylaxe von einer oder mehreren Erkrankungen ausgewählt aus der Gruppe bestehend aus Schmerz, vorzugsweise von Schmerz ausgewählt aus der Gruppe bestehend aus akutem Schmerz, chronischem Schmerz, neuropathischem Schmerz und visceralem Schmerz; Gelenkschmerz; Migräne; Depressionen; neurodegenerativen Erkrankungen, vorzugsweise ausgewählt aus der Gruppe bestehend aus Multipler Sklerose, Morbus Alzheimer, Morbus Parkinson und Morbus Huntington; kognitiven Dysfunktionen, vorzugsweise kognitiven Mangelzuständen, besonders bevorzugt Gedächtnisstörungen; Entzündungen, vorzugsweise Entzündungen des Darmes, der Augen, der Blase, der Haut oder der Nasenschleimhaut; Harninkontinenz; einer überaktiven Blase (overactive bladder, OAB); Medikamentenabhängigkeit; Medikamentenmißbrauch; Entzugserscheinungen
bei Medikamentenabhängigkeit; Toleranzentwicklung gegenüber Medikamenten, vorzugsweise Toleranzentwicklung gegenüber natürlichen oder synthetischen Opioiden; Drogenabhängigkeit; Drogenmißbrauch; Entzugserscheinungen bei Drogenabhängigkeit; Alkoholabhängigkeit; Alkoholmissbrauch und Entzugserscheinungen bei Alkoholabhängigkeit.
Ganz besonders bevorzugt eignet sich das erfindungsgemäße Arzneimittel zur Behandlung und/oder Prophylaxe von Schmerz, vorzugsweise von Schmerz ausgewählt aus der Gruppe bestehend aus akutem Schmerz, chronischem Schmerz, neuropathischem Schmerz und visceralem Schmerz, und/oder Harninkontinenz.
Ein weiterer Gegenstand der vorliegenden Erfindung ist die Verwendung wenigstens einer erfindungsgemäßen Verbindung sowie ggf. eines oder mehrerer pharmazeutisch verträglicher Hilfsstoffe zur Herstellung eines Arzneimittels zur Vanilloid-Rezeptor 1-(VR1/TRPV1 )-Regulation, vorzugsweise zur Vanilloid-Rezeptor 1-(VR1/TRPV1 )-Hemmung und/oder zur Vanilloid-Rezeptor 1(VR1/TRPV1 )- Stimulation.
Bevorzugt ist die Verwendung wenigstens einer erfindungsgemäßen substituierten Verbindung sowie ggf. eines oder mehrerer pharmazeutisch verträglicher Hilfsstoffe zur Herstellung eines Arzneimittels zur Prophylaxe und/oder Behandlung von Störungen oder Krankheiten, die zumindest teilweise durch Vanilloid-Rezeptoren 1 vermittelt werden.
Besonders bevorzugt ist die Verwendung wenigstens einer erfindungsgemäßen Verbindung sowie ggf. eines oder mehrerer pharmazeutisch verträglicher Hilfsstoffe zur Herstellung eines Arzneimittels zur Behandlung und/oder Prophylaxe von einer oder mehreren Erkrankungen ausgewählt aus der Gruppe bestehend aus Schmerz, vorzugsweise von Schmerz ausgewählt aus der Gruppe bestehend aus akutem Schmerz, chronischem Schmerz, neuropathischem Schmerz und visceralem Schmerz und Gelenkschmerz.
Besonders bevorzugt ist die Verwendung wenigstens einer erfindungsgemäßen Verbindung sowie ggf. eines oder mehrerer pharmazeutisch verträglicher Hilfsstoffe zur Herstellung eines Arzneimittels zur Behandlung und/oder Prophylaxe von einer oder mehreren Erkrankungen ausgewählt aus der Gruppe bestehend aus Hyperalgesie; Allodynie; Kausalgie; Migräne; Depressionen; Nervenleiden; Nervenverletzungen; neurodegenerativen Erkrankungen, vorzugsweise ausgewählt aus der Gruppe bestehend aus Multipler Sklerose, Morbus Alzheimer, Morbus Parkinson und Morbus Huntington; kognitiven Dysfunktionen, vorzugsweise kognitiven Mangelzuständen, besonders bevorzugt Gedächtnisstörungen; Epilepsie; Atemwegserkrankungen, vorzugsweise ausgewählt aus der Gruppe bestehend aus Asthma, Bronchitis und Lungenentzündung; Husten; Harninkontinenz; einer überaktiven Blase (overactive bladder, OAB); Erkrankungen und/oder Verletzungen des Magen-Darm-Trakts; Zwölffingerdarmgeschwüren; Magengeschwüren; Reizdarmsyndrom; Schlaganfällen; Augenreizungen; Hautreizungen; neurotischen Hauterkrankungen; allergischen Hautkrankheiten; Psiorasis; Vitiligo; Herpes Simplex; Entzündungen, vorzugsweise Entzündungen des Darmes, der Augen, der Blase, der Haut oder der Nasenschleimhaut; Diarrhöe; Pruritus; Osteoporose; Arthritis; Osteoarthritis; rheumatischen Erkrankungen; Störungen der Nahrungsaufnahme, vorzugsweise ausgewählt aus der Gruppe bestehend aus Bulimie, Kachexie, Anorexie und Fettleibigkeit; Medikamentenabhängigkeit; Medikamentenmißbrauch; Entzugserscheinungen bei Medikamentenabhängigkeit; Toleranzentwicklung gegenüber Medikamenten, vorzugsweise gegenüber natürlichen oder synthetischen Opioiden; Drogenabhängigkeit; Drogenmißbrauch; Entzugserscheinungen bei Drogenabhängigkeit; Alkoholabhängigkeit; Alkoholmissbrauch und Entzugserscheinungen bei Alkoholabhängigkeit; zur Diurese; zur Antinatriurese; zur Beeinflussung des kardiovaskulären Systems; zur Vigilanzsteigerung; zur Behandlung von Wunden und/oder Verbrennungen; zur Behandlung von durchtrennten Nerven; zur Libidosteigerung; zur Modulation der Bewegungsaktivität; zur Anxiolyse; zur Lokalanästhesie und/oder zur Hemmung unerwünschter Nebenwirkungen, vorzugsweise ausgewählt aus der Gruppe bestehend aus Hyperthermie, Bluthochdruck und Verengung der Bronchien, ausgelöst durch die Verabreichung von Vanilloid-Rezeptor 1 (VR1/TRPV1-Rezeptoren)-Agonisten, vorzugsweise ausgewählt aus der Gruppe bestehend aus Capsaicin, Resiniferatoxin,
Olvanil, Arvanil, SDZ-249665, SDZ-249482, Nuvanil und Capsavanil.
Ganz besonders bevorzugt ist die Verwendung wenigstens einer erfindungsgemäßen substituierten Verbindung sowie ggf. eines oder mehrerer pharmazeutisch verträglicher Hilfsstoffe zur Herstellung eines Arzneimittels zur Behandlung und/oder Prophylaxe von einer oder mehreren Erkrankungen ausgewählt aus der Gruppe bestehend aus Schmerz, vorzugsweise von Schmerz ausgewählt aus der Gruppe bestehend aus akutem Schmerz, chronischem Schmerz, neuropathischem Schmerz und visceralem Schmerz; Gelenkschmerz; Migräne; Depressionen; neurodegenerativen Erkrankungen, vorzugsweise ausgewählt aus der Gruppe bestehend aus Multipler Sklerose, Morbus Alzheimer, Morbus Parkinson und Morbus Huntington; kognitiven Dysfunktionen, vorzugsweise kognitiven Mangelzuständen, besonders bevorzugt Gedächtnisstörungen; Entzündungen, vorzugsweise Entzündungen des Darmes, der Augen, der Blase, der Haut oder der Nasenschleimhaut; Harninkontinenz; einer überaktiven Blase (overactive bladder, OAB); Medikamentenabhängigkeit; Medikamentenmißbrauch; Entzugserscheinungen bei Medikamentenabhängigkeit; Toleranzentwicklung gegenüber Medikamenten, vorzugsweise Toleranzentwicklung gegenüber natürlichen oder synthetischen Opioiden; Drogenabhängigkeit; Drogenmißbrauch; Entzugserscheinungen bei Drogenabhängigkeit; Alkoholabhängigkeit; Alkoholmissbrauch und Entzugserscheinungen bei Alkoholabhängigkeit.
Noch weiter bevorzugt ist die Verwendung wenigstens einer erfindungsgemäßen substituierten Verbindung sowie ggf. eines oder mehrerer pharmazeutisch verträglicher Hilfsstoffe zur Herstellung eines Arzneimittels zur Behandlung und/oder Prophylaxe von Schmerz, vorzugsweise ausgewählt aus der Gruppe bestehend aus akutem Schmerz, chronischem Schmerz, neuropathischem Schmerz und visceralem Schmerz, und/oder Harninkontinenz.
Das erfindungsgemäße Arzneimittel eignet sich zur Verabreichung an Erwachsene und Kinder einschließlich Kleinkindern und Säuglingen.
Das erfindungsgemäße Arzneimittel kann als flüssige, halbfeste oder feste Arzneiform, beispielsweise in Form von Injektionslösungen, Tropfen, Säften, Sirupen, Sprays, Suspensionen, Tabletten, Patches, Kapseln, Pflastern, Zäpfchen, Salben, Cremes, Lotionen, Gelen, Emulsionen, Aerosolen oder in multipartikulärer Form, beispielsweise in Form von Pellets oder Granulaten, ggf. zu Tabletten verpresst, in Kapseln abgefüllt oder in einer Flüssigkeit suspendiert, vorliegen und als solche auch verabreicht werden.
Neben wenigstens einer substituierten Verbindung der vorstehend angegebenen allgemeinen Formel I, ggf. in Form eines ihrer reinen Stereoisomeren, insbesondere Enantiomeren oder Diastereomeren, ihres Racemates oder in Form von Mischungen der Stereoisomeren, insbesondere der Enantiomeren oder Diastereomeren, in einem beliebigen Mischungsverhältnis, oder ggf. in Form eines entsprechenden Salzes oder jeweils in Form eines entsprechendes Solvates, enthält das erfindungsgemäße Arzneimittel üblicherweise weitere physiologisch verträgliche pharmazeutische Hilfsstoffe, die beispielsweise ausgewählt werden können aus der Gruppe bestehend aus Trägermaterialien, Füllstoffen, Lösungsmitteln, Verdünnungsmitteln, oberflächenaktiven Stoffen, Farbstoffen, Konservierungsstoffen, Sprengmitteln, Gleitmitteln, Schmiermitteln, Aromen und Bindemitteln.
Die Auswahl der physiologisch verträglichen Hilfsstoffe sowie die einzusetzenden Mengen derselben hängt davon ab, ob das Arzneimittel oral, subkutan, parenteral, intravenös, intraperitoneal, intradermal, intramuskulär, intranasal, buccal, rectal oder örtlich, zum Beispiel auf Infektionen an der Haut, der Schleimhäute und an den Augen, appliziert werden soll. Für die orale Applikation eignen sich bevorzugt Zubereitungen in Form von Tabletten, Dragees, Kapseln, Granulaten, Pellets, Tropfen, Säften und Sirupen, für die parenterale, topische und inhalative Applikation Lösungen, Suspensionen, leicht rekonstituierbare Trockenzubereitungen sowie Sprays. Die in dem erfindungsgemäßen Arzneimittel zum Einsatz kommenden erfindungsgemäßen substituierten Verbindungen in einem Depot in gelöster Form oder in einem Pflaster, gegebenenfalls unter Zusatz von die Hautpenetration fördernden Mitteln, sind geeignete perkutane Applikationszubereitungen. Oral oder perkutan anwendbare Zubereitungsformen können die jeweilige erfindungsgemäße substituierte Verbindung auch verzögert freisetzen.
Die Herstellung der erfindungsgemäßen Arzneimittel erfolgt mit Hilfe von üblichen, aus dem Stande der Technik bekannten Mitteln, Vorrichtungen, Methoden und Verfahren, wie sie beispielsweise in „Remington's Pharmaceutical Sciences", Herausgeber A. R. Gennaro, 17. Auflage, Mack Publishing Company, Easton, Pa, 1985, insbesondere in Teil 8, Kapitel 76 bis 93 beschrieben sind. Die entsprechende Beschreibung wird hiermit als Referenz eingeführt und gilt als Teil der Offenbarung. Die an den Patienten zu verabreichende Menge der jeweiligen erfindungsgemäßen substituierten Verbindungen der vorstehend angegebenen allgemeinen Formel I kann variieren und ist beispielsweise abhängig vom Gewicht oder Alter des Patienten sowie von der Applikationsart, der Indikation und dem Schweregrad der Erkrankung. Üblicherweise werden 0.001 bis 100 mg/kg, vorzugsweise 0.05 bis 75 mg/kg, besonders bevorzugt 0.05 bis 50 mg/kg, Körpergewicht des Patienten wenigstens einer solchen erfindungsgemäßen Verbindung appliziert.
Pharmakologische Methoden
I. Funktionelle Untersuchung am Vanilloid-Rezeptor 1 (VRI/TRPV1 -Rezeptor)
Die agonistische bzw. antagonistische Wirkung der zu untersuchenden Substanzen am Vanilloid-Rezeptor 1 (VR1/TRPV1 ) der Spezies Ratte kann mit folgendem Assay bestimmt werden. Gemäß diesem Assay wird der Ca2+-Einstrom durch den Rezeptorkanal mit Hilfe eines Ca2+-sensitiven Farbstoffs (Typ Fluo-4, Molecular Probes Europe BV, Leiden Niederlande) im Fluorescent Imaging Plate Reader (FLIPR, Molecular Devices, Sunnyvale, USA) quantifiziert.
Methode:
Komplett-Medium: 50 mL HAMS F12 Nutrient Mixture (Gibco Invitrogen GmbH,
Karlsruhe, Deutschland) mit
10 Vol-% FCS (fetal calf serum, Gibco Invitrogen GmbH, Karlsruhe, Deutschland, hitzeinaktiviert);
2mM L-Glutamin (Sigma, München, Deutschland);
1 Gew-% AA-Lösung (Antibiotika/Antimykotika-Lösung, PAA, Pasching, Österreich) und 25 ng/ml Medium NGF (2.5 S, Gibco Invitrogen GmbH, Karlsruhe, Deutschland)
Zellkultur-Platte: Poly-D-Lysin-beschichtete, schwarze 96-Loch-Platten mit klarem Boden (96 well black/clear plate, BD Biosciences, Heidelberg, Deutschland) werden zusätzlich mit Laminin (Gibco Invitrogen GmbH, Karlsruhe, Deutschland) beschichtet, indem Laminin auf eine Konzentration 100 μg/mL mit PBS (Ca-Mg-free PBS, Gibco Invitrogen GmbH, Karlsruhe, Deutschland) verdünnt wird. Es werden Aliquots mit einer Konzentration von 100 μg/mL an Laminin entnommen und bei -20 0C gelagert. Die Aliquots werden mit PBS im Verhältnis 1 :10 auf 10 μg/mL Laminin verdünnt und jeweils 50 μL der Lösung in eine Vertiefung der Zellkultur-Platte pipettiert. Die Zellkultur-Platten werden mindestens zwei Stunden bei 37 0C inkubiert, die überstehende Lösung abgesaugt und die Vertiefungen werden jeweils zweimal mit PBS gewaschen. Die beschichteten Zellkultur-Platten werden mit überstehendem PBS aufbewahrt und dieses erst direkt vor der Aufgabe der Zellen entfernt.
Präparation der Zellen:
Enthaupteten Ratten wird die Wirbelsäule entnommen und diese direkt in kalten, d. h. in einem Eisbad befindlichen, HBSS-Puffer (Hank's buffered saline Solution, Gibco Invitrogen GmbH, Karlsruhe, Deutschland) versetzt mit 1 Vol-% (Volumenprozent) einer AA-Lösung (Antibiotika/Antimykotika-Lösung, PAA, Pasching, Österreich) gelegt. Die Wirbelsäule wird längs durchtrennt und zusammen mit Fascien dem Wirbelkanal entnommen. Anschließend werden die Dorsalwurzelganglien (DRGs; dorsal root ganglia) entnommen und wiederum in kaltem HBSS-Puffer versetzt mit 1 Vol-% einer AA-Lösung aufbewahrt. Die vollständig von Blutresten und Spinalnerven befreiten DRGs werden jeweils in 500 μL kalte Collagenase Typ 2 (PAA, Pasching, Österreich) überführt und 35 Minuten bei 37 0C inkubiert. Nach Zugabe von 2.5 VoI- % Trypsin (PAA, Pasching, Österreich) wird weitere 10 Minuten bei 37 0C inkubiert. Nach der vollständigen Inkubation wird die Enzymlösung vorsichtig ab pipettiert und die zurückgebliebenen DRGs werden jeweils mit 500 μL Komplett-Medium versetzt. Die DRGs werden jeweils mehrfach suspendiert, mittels einer Spritze durch Kanülen Nr. 1 , Nr. 12 und Nr. 16 gezogen und in 50 mL Falcon-Röhrchen überführt und dieses mit Komplett-Medium auf 15 mL aufgefüllt. Der Inhalt jedes Falcon-Röhrchen wird jeweils durch einen 70 μm Falcon-Filtereinsatz filtriert und 10 Minuten bei 1200 Umdrehungen und RT zentrifugiert. Das resultierende Pellet wird jeweils in 250 μL Komplett-Medium aufgenommen und die Zellzahl ermittelt.
Die Anzahl der Zellen in der Suspension wird auf 3 mal 105 pro mL eingestellt und jeweils 150 μL dieser Suspension in eine Vertiefung der wie vorstehend beschrieben beschichteten Zellkultur-Platten gegeben. Im Brutschrank werden die Platten bei 37 0C, 5 Vol-% CO2 und 95 % relativer Luftfeuchtigkeit zwei bis drei Tage stehen gelassen.
Anschließend werden die Zellen mit 2 μM Fluo-4 und 0.01 Vol-% Pluronic F127 (Molecular Probes Europe BV, Leiden Niederlande) in HBSS-Puffer (Hank's buffered saline Solution, Gibco Invitrogen GmbH, Karlsruhe, Deutschland) für 30 min bei 37 0C beladen, 3 x mit HBSS-Puffer gewaschen und nach einer weiteren Inkubation von 15 Minuten bei RT zur Ca2+-Messung im FLIPR-Assay eingesetzt. Die Ca2+- abhängige Fluoreszenz wird dabei vor und nach Zugabe von Substanzen gemessen (λex = 488 nm, λem = 540 nm). Die Quantifizierung erfolgt durch die Messung der
höchsten Fluoreszenzintensität (FC, Fluorescence Counts) über die Zeit.
FLIPR-Assay:
Das FLIPR-Protokoll besteht aus 2 Substanzzugaben. Zunächst werden die zu testenden Verbindungen (10 μM) auf die Zellen pipettiert und der Ca2+-Einstrom mit der Kontrolle (Capsaicin 10 μM) verglichen. Daraus ergibt sich die Angabe in % Aktivierung bezogen auf das Ca2+-Signal nach Zugabe von 10 μM Capsaicin (CP). Nach 5 Minuten Inkubation werden 100 nM Capsaicin appliziert und ebenfalls der Einstrom von Ca2+ ermittelt.
Desensitisierende Agonisten und Antagonisten führen zu einer Unterdrückung des Ca2+-Einstroms. Es werden % Inhibierung im Vergleich zu der maximal erreichbaren Inhibierung mit 10 μM Capsaicin berechnet.
Es werden Dreifach-Bestimmungen (n=3) durchgeführt und diese in mindestens 3 unabhängigen Experimenten wiederholt (N=4).
Ausgehend von der prozentualen Verdrängung durch unterschiedliche Konzentrationen der zu prüfenden Verbindungen der allgemeinen Formel I wurden IC5O Hemmkonzentrationen berechnet, die eine 50-prozentige Verdrängung von Capsaicin bewirken. Durch Umrechnung mittels der Cheng-Prusoff-Beziehung wurden Kj-Werte für die Prüfsubstanzen erhalten (Cheng, Prusoff; Biochem. Pharmacol. 22, 3099-3108, 1973).
II. Funktionelle Untersuchungen am Vanilloid Rezeptor (VR1)
Die agonistische bzw. antagonistische Wirkung der zu untersuchenden Substanzen auf Vanilloid Rezeptor (VR1 ) kann auch mit dem folgenden Assay bestimmt werden. Gemäß diesem Assay wird der Ca2+-Einstrom durch den Kanal mit Hilfe eines Ca2+- sensitiven Farbstoffs (Typ Fluo-4, Molecular Probes, Europe BV, Leiden, Niederlande) im Fluorescent Imaging Plate Reader (FLIPR, Molecular Devices, Sunnyvale, USA) quantifiziert.
Methode:
Chinese Hamster Ovary Zellen (CHO K1 -Zellen, European Collection of Cell Cultures (ECACC) Großbritannien) werden stabil mit dem VR1-Gen transfiziert. Für funktionelle Untersuchungen werden diese Zellen auf Poly-D-Lysin-beschichtete, schwarze 96-Loch-Platten mit klarem Boden (BD Biosciences, Heidelberg, Deutschland) in einer Dichte von 25.000 Zellen/Loch ausplattiert. Über Nacht werden die Zellen bei 37 0C und 5 % CO2 in einem Kulturmedium (Nutrient Mixture 'am's F12, 10 Vol-% FCS (Fetal calf serum), 18 μg/ml L-Prolin) inkubiert. Am folgenden Tag werden die Zellen mit Fluo-4 (Fluo-4 2 μM, Pluronic F127 0.01 Vol-%, Molecular Probes in HBSS (Hank's buffered saline Solution), Gibco Invitrogen GmbH, Karlsruhe, Deutschland) für 30 Minuten bei 37 0C inkubiert. Anschließend werden die Platten 3-mal mit HBSS-Puffer gewaschen und nach einer weiteren Inkubation von 15 Minuten bei RT zur Ca2+-Messung im FLIPR eingesetzt. Die Ca2+-abhängige Fluoreszenz wird dabei vor und nach Zugabe der zu untersuchenden Substanzen gemessen (Wellenlänge λex=488 nm, λem= 540 nm). Die Quantifizierung erfolgt durch die Messung der höchsten Fluoreszenzintensität (FC, Fluorescence Counts) über die Zeit.
FLIPR-Assay:
Das FLIPR-Protokoll besteht aus 2 Substanzzugaben. Zunächst werden die zu testenden Substanzen (10μM) auf die Zellen pipettiert und der Ca2+-Einstrom mit der Kontrolle (Capsaicin 10 μM) verglichen (% Aktivierung bezogen auf das Ca2+-Signal nach Zugabe von 10 μM Capsaicin). Nach 5 Minuten Inkubation werden 100 nM Capsaicin appliziert und ebenfalls der Einstrom von Ca2+ ermittelt.
Desensitisierende Agonisten und Antagonisten führten zu einer Unterdrückung des Ca2+-Einstroms. Es werden % Inhibierung im Vergleich zu der maximal erreichbaren Inhibierung mit 10 μM Capsaicin berechnet.
Ausgehend von der prozentualen Verdrängung durch unterschiedliche Konzentrationen der zu prüfenden Verbindungen der allgemeinen Formel I wurden IC50 Hemmkonzentrationen berechnet, die eine 50-prozentige Verdrängung von
Capsaicin bewirken. Durch Umrechnung mittels der Cheng-Prusoff-Beziehung wurden Kj-Werte für die Prüfsubstanzen erhalten (Cheng, Prusoff; Biochem. Pharmacol. 22, 3099-3108, 1973).
IM. Formalin-Test an der Maus
Die Untersuchung zur Bestimmung der antinociceptiven Wirkung der erfindungsgemäßen Verbindungen wird im Formalin-Test an männlichen Mäusen (NMRI, 20 bis 30 g Körpergewicht, Iffa, Credo, Belgien) durchgeführt.
Im Formalin-Test werden gemäß D. Dubuisson et al., Pain 1977, 4, 161-174 die erste (frühe) Phase (0 bis 15 Minuten nach der Formalin-Injektion) und die zweite (späte) Phase (15 bis 60 Minuten nach der Formalin-Injektion) unterschieden. Die frühe Phase stellt als direkte Reaktion auf die Formalin-Injektion ein Modell für Akutschmerz dar, während die späte Phase als Modell für persistierenden (chronischen) Schmerz angesehen wird (T. J. Coderre et al., Pain 1993, 52, 259- 285). Die entsprechenden Literaturbeschreibungen werden hiermit als Referenz eingeführt und gelten als Teil der Offenbarung.
Die erfindungsgemäßen Verbindungen werden in der zweiten Phase des Formalin- Tests untersucht, um Aussagen über Substanzwirkungen auf chronisch/entzündlichen Schmerz zu erhalten.
In Abhängigkeit von der Applikationsart der erfindungsgemäßen Verbindungen wird der Applikationszeitpunkt der erfindungsgemäßen Verbindungen vor der Formalin- Injektion gewählt. Die intravenöse Applikation von 10 mg/kg Körpergewicht der Testsubstanzen erfolgt 5 Minuten vor der Formalin-Injektion. Diese erfolgt durch eine einmalige subkutane Formalin-Injektion (20 μl_, 1 %-ige wässrige Lösung) in die dorsale Seite der rechten Hinterpfote, so dass bei frei beweglichen Versuchstieren eine nociceptive Reaktion induziert wird, die sich in deutlichem Lecken und Beißen der betreffenden Pfote äußert.
Anschließend wird für einen Untersuchungszeitraum von drei Minuten in der zweiten (späten) Phase des Formalin-Tests (21 bis 24 Minuten nach der Formalin-Injektion) das nociceptive Verhalten durch Beobachtung der Tiere kontinuierlich erfasst. Die Quantifizierung des Schmerzverhaltens erfolgt durch Summation der Sekunden, in denen die Tiere in dem Untersuchungszeitraum ein Lecken und Beißen der betroffenen Pfote zeigen.
Der Vergleich erfolgt jeweils mit Kontrolltieren, die anstelle der erfindungsgemäßen Verbindungen Vehikel (0.9%-ige wässrige Natriumchlorid-Lsg.) vor Formalinapplikation erhalten. Basierend auf der Quantifizierung des Schmerzverhaltens wird die Substanzwirkung im Formalin-Test als Änderung gegen die entsprechende Kontrolle in Prozent ermittelt.
Nach Injektion von Substanzen, die im Formalin-Test antinociceptiv wirksam sind, werden die beschriebenen Verhaltensweisen der Tiere, d. h. Lecken und Beißen, reduziert bzw. aufgehoben.
IV. Untersuchung auf analgetische Wirksamkeit im Writhing-Test
Die Untersuchung der erfindungsgemäßen Verbindungen der allgemeinen Formel I auf analgetische Wirksamkeit wurde im Phenylchinon-induzierten Writhing an der Maus, modifiziert nach I. C. Hendershot und J. Forsaith (1959) J. Pharmacol. Exp. Ther. 125. 237-240 durchgeführt. Die entsprechende Literaturbeschreibung wird hiermit als Referenz eingeführt und gilt als Teil der Offenbarung.
Dazu wurden männliche NMRI-Mäuse mit einem Gewicht von 25 bis 30 g verwendet. Gruppen von 10 Tieren pro Verbindungsdosis erhielten 10 Minuten nach intravenöser Gabe der zu untersuchenden Verbindungen 0,3 ml/Maus einer 0.02%igen wässrigen Lösung von Phenylchinon (Phenylbenzochinon, Fa. Sigma, Deisenhofen, Deutschland; Herstellung der Lösung unter Zusatz von 5 Gew.-% Ethanol und Aufbewahrung im Wasserbad bei 45 C) intraperitoneal appliziert. Die Tiere wurden einzeln in Beobachtungskäfige gesetzt. Mit Hilfe eines Drucktastenzählers wurde die Anzahl der schmerzinduzierten Streckbewegungen (sogenannte Writhingreaktionen = Durchdrücken des Körpers mit Abstrecken der
Hinterextremitäten) 5 bis 20 Minuten nach der Phenylchinon-Gabe ausgezählt. Als Kontrolle wurden Tiere mit geführt, die nur physiologische Kochsalzlösung erhalten hatten. Alle Verbindungen wurden in der Standarddosierung von 10 mg/kg getestet.
V. Hypothermie Assay an der Maus
Methodenbeschreibung:
Der Hypothermie Assay wird in männlichen NMRI Mäusen (Gewicht 25-35 Gramm, Züchter IFFA CREDO, Brüssel, Belgien) durchgeführt. Die Tiere wurden unter standardisierten Bedingungen gehalten: Licht/Dunkel Rhythmus (6:00 bis 18:00 Uhr Licht-; 18:00 bis 6:00 Uhr Dunkelphase), RT 19-220C, relative Luftfeuchte 35-70%, 15 Raumluftwechsel pro Stunde, Luftbewegung < 0.2 m/sec. Die Tiere erhielten Standardfutter (ssniff R/M-Haltung, ssniff Spezialdiäten GmbH, Soest, Germany) und Leitungswasser. Wasser und Futter wurden während des Versuches entzogen. Alle Tiere wurden nur einmal im Versuch eingesetzt. Die Tiere hatten eine Eingewöhnungsphase von mindestens 5 Tagen.
Die akute Applikation von Capsaicin (VR-1 Agonist) führt zu einem Abfall der Körperkerntemperatur in Ratten und Mäusen über eine Stimulation von Wärmesensoren. Nur spezifisch wirkende VR-1 -rezeptor Antagonisten können die Capsaicin induzierte Hypothermie antagonisieren. Eine durch Morphin induzierte Hypothermie dagegen wird nicht von VR-1 Antagonisten antagonisiert. Dieses Modell ist daher geeignet, Substanzen mit VR-1 antagonistischen Eigenschaften über die Wirkung auf die Körpertemperatur zu identifizieren.
Für die Messung der Körperkerntemperatur wurde ein digitales Thermometer (Thermalert TH-5, physitemp, Clifton NJ, USA) benutzt. Der Messfühler wird dabei in das Rektum der Tiere eingeführt.
Als individueller Basiswert wird bei jedem Tier 2-mal im Abstand von ca. einer halben Stunde die Körpertemperatur gemessen. Anschließend erhält eine Gruppe von Tieren (n= 6 bis 10) eine intraperitoneale (i.p.) Applikation von Capsaicin 3mg/kg und Vehikel (Kontrollgruppe). Eine andere Gruppe von Tieren erhält die zu testende Substanz (i.v. oder p.o.) und zusätzlich Capsaicin (3mg/kg) i.p. Die Applikation der Testsubstanz erfolgt i.v. 10 min bzw. p.o. 15 Minuten vor Capsaicin. Anschließend
wird 7,5 / 15 und 30 min nach Capsaicin(i.v. + i.p.) bzw. 15 / 30 / 60 /90 /120 min (p.o. + i.p.) nach Capsaicin die Körpertemperatur gemessen. Zusätzlich wird eine Tiergruppe nur mit der Testsubstanz behandelt sowie eine Gruppe nur mit Vehikel. Die Auswertung bzw. Darstellung der Messwerte erfolgt als Mittelwert +/- S. E. M. der absoluten Werte als Grafik. Die antagonistische Wirkung wird berechnet als Prozent Reduktion der Capsaicin-induzierten Hypothermie.
VI. Neuropathischer Schmerz an der Maus
Die Untersuchung auf Wirksamkeit im neuropathischen Schmerz wurde im Bennett- Modell (chronic constriction injury; Bennett und Xie, 1988, Pain 33: 87-107) untersucht.
NMRI Mäuse mit einem Gewicht von 16-18g werden unter Ketavet-Rompun-Narkose mit drei losen Ligaturen des rechten nervus ischiaticus versehen. Die Tiere entwickeln an der vom Geschädigten Nerv innervierten Pfote eine Überempfindlichkeit, die nach einer Erholungsphase von einer Woche über etwa drei Wochen mittels einer 4°C kalten Metallplatte quantifiziert wird (Kälte-Allodynie). Die Tiere werden für einen Zeitraum von 2 min. auf dieser Platte beobachtet und die Anzahl der Wegziehreaktionen der geschädigten Pfote wird gemessen. Bezogen auf den Vorwert vor Substanzapplikation wird die Substanzwirkung über einen bestimmten Zeitraum an verschiedenen Zeitpunkten (z.B. 15, 30, 45, 60 min. nach Applikation) bestimmt und die resultierend Fläche unter der Kurve (AUC) und/oder die Hemmung der Kälte-Allodynie zu den einzelnen Messpunkten in Prozent Wirkung zur Vehikelkontrolle (AUC) bzw. zum Ausgangswert (Einzelmesspunkte) ausgedrückt. Die Gruppengröße beträgt n=10, die Signifikanz einer anti- allodynischen Wirkung (*=p<0.05) wird anhand einer Varianzanalyse mit wiederholter Messung und einer post hoc Analyse nach Bonferroni bestimmt.
Im Folgenden wird die Erfindung mit Hilfe einiger Beispiele erläutert. Diese Erläuterungen sind lediglich beispielhaft und schränken den allgemeinen Erfindungsgedanken nicht ein.
Beispiele:
Die Ausbeuten der hergestellten Verbindungen wurden nicht optimiert.
Alle Temperaturen sind unkorrigiert.
Die Angabe „Äquivalente" bedeutet Stoffmengenäquivalente, „RT" Raumtemperatur, „M" und „N" sind Konzentrationsangaben in mol/l, „aq." wäßrig, „ges." gesättigt, „Lsg." Lösung,
Weitere Abkürzungen:
AcOH Essigsäure
DCM Dichlormethan
DMF N,N-Dimethylformamid
EDCI N-Ethyl-N'-(3-dimethylaminopropyl)-carbodiimid Hydrochlorid
EE Essigsäureethylester
H2O Wasser
HOBt N-Hydroxybenzotriazol
MeOH Methanol
TEA Triethylamin
THF Tetrahydrofuran
Die eingesetzten Chemikalien und Lösungsmittel wurden kommerziell bei den herkömmlichen Anbietern (Acros, Avocado, Aldrich, Bachern, Fluka, Lancaster, Maybridge, Merck, Sigma, TCI, Oakwood etc.) bezogen oder nach den üblichen dem Fachmann bekannten Methoden synthetisiert.
Als stationäre Phase für die Säulenchromathographie wurde Kieselgel 60 (0.0-0 - 0.063 mm) der Firma E. Merck, Darmstadt, eingesetzt.
Die dünnschicht-chromatographischen Untersuchungen wurden mit HPTLC- Fertigplatten, Kieselgel 60 F 254, der Firma E. Merck, Darmstadt, durchgeführt.
Die Mischungsverhältnisse von Lösungsmitteln, Laufmitteln oder für chromatographische Untersuchungen sind stets in Volumen/Volumen angegeben.
Die Analytik erfolgte durch Massenspektroskopie und NMR.
1. Allgemeine Vorschrift zur Darstellung von Aminen der allgemeinen Formel V- A
Die Darstellung von Aminen der allgemeinen Formel V-A erfolgt wie im nachfolgenden Schema 1 dargestellt.
V\-A Vl-B V-A
Schema 1.
Stufe 1 : Darstellung von Nitrilen der allgemeinen Formel Vl-B
Methode A:
Verbindungen der allgemeinen Formel Vl-A (1 Äquivalent), worin R8, U, T und V die vorstehend genannte Bedeutung haben und m für 0, 1 , 2 oder 3 steht, werden mit einem Amin der allgemeinen Formel HNR40R41 (6 Äquivalente) 48 Stunden bei RT gerührt. Die Reaktionsmischung wird mit 1 N Salzsäure versetzt und mehrfach mit EE extrahiert. Die wässrige Phase wird mit NaCI gesättigt und anschließend wiederum mit EE extrahiert. Die vereinigten organischen Phasen werden mit 1 N Salzsäure und mit ges. aq. NaCI-Lsg. gewaschen, über MgSO4 getrocknet und das Lösungsmittel wurde im Vakuum entfernt.
Die folgende Verbindung wurde nach Methode A. hergestellt.
β'-tert-Butyl-A-methyl-S^^^-tetrahydro^H-EI^'lbipyridinyl-S'-carbonitril
1H-NMR(CDCI3) δ 7.65 (d, 1 H, J=7.9Hz, Ar), 6.70 (d, 1 H, J=8.0Hz, Ar), 4.45 (m, 2H, Piperidin), 2.98 (m, 2H, Piperidin), 1.75-1.24 (m, 5H, Piperidin), 1.29 (s, 9H, C(CHa)3), 0.98 (d, 3H1 J=5.9Hz, CHCH3)
IR 2956, 2213, 1583, 1550, 1452, 1230, 965 cm -1
Methode B:
Verbindungen der allgemeinen Formel Vl-A (1 Äquivalent), worin R8, U, T und V die vorstehend genannte Bedeutung haben und m für 0, 1 , 2 oder 3 steht, werden mit einem Amin der allgemeinen Formel HNR40R41 (2 Äquivalente) und DBU [1 ,8-Diaza- bicyclo[5.4.0]undec-7-en] (2 Äquivalente) in Acetonitril (7 ml_ pro mmol der Verbindung der Formel Vl-A) 12 Stunden bei RT gerührt. Die Reaktionsmischung wird mehrfach mit EE extrahiert. Die vereinigten organischen Phasen werden mit ges. aq. NaCI-Lsg. gewaschen, über MgSO4 getrocknet und das Lösungsmittel wurde im Vakuum entfernt. Der Rückstand wird jeweils durch Säulenchromatographie (SiO2, verschiedene Mischungen Hexan/EE) gereinigt.
Die folgenden Verbindungen wurden gemäß Methode B. hergestellt.
6-(Trifluormethyl)-2-(4-methylpiperidin-1-yl)pyridin-3-carbonitril
1H NMR (300 MHz, CDCI3) δ 7.87 (d, 1 H1 J = 7.8 Hz), 6.95 (d, 1 H1 J = 7.8 Hz), 4.53 (m, 2H)1 3.05 (m, 2 H)1 1.78 (m, 2 H)1 1.64 (m, 1 H)1 1.29 (m, 2 H), 1.00 (d, 3 H1 J = 6.6 Hz); IR (pur) 2926, 2852, 2218. 1590, 1497, 1456, 1324, 1237, 1186, 1147, 1082, 963 cm"1; MS (FAB) m/z 270 (M+H)
Stufe 2: Methode 1
Verbindungen der allgemeinen Formel Vl-B (5 mmol), worin R8, R40, R41, U, T und V die vorstehend genannte Bedeutung haben und m für 0, 1 , 2 oder 3 steht, Palladium auf Kohle (10 %, 500 mg) und konzentrierte Salzsäure (3 ml_) werden in MeOH (30 ml_) gelöst und 6 Stunden bei RT einer Wasserstoffatmosphäre ausgesetzt. Die Reaktionsmischung wird über Celite filtriert und das Filtrat wird im Vakuum eingeengt. Der Rückstand wird mittels Flashchromatographie (SiO2, EE) gereinigt.
Methode 2:
Verbindungen der allgemeinen Formel Vl-B (2 mmol), worin R8, R40, R41, U1 T und V die vorstehend genannte Bedeutung haben und m für 0, 1 , 2 oder 3 steht, werden in THF (10 mL, 10 mL) gelöst und BH3 »S(CH3)2 [2.0 M in THF, 3 mL, 3 Äquivalent] wird hinzu gegeben. Die Reaktionsmischung wird 8 Stunden zum Rückfluss erhitzt, aq. HCl (2 N) wird hinzu gegeben und die Reaktionsmischung wird erneut für 30 Minuten zum Rückfluss erhitzt. Die Reaktionsmischung wird mit aq. Natriumhydroxid-Lösung (2N) versetzt und mit EE gewaschen. Die vereinigten organischen Phasen werden mit ges. aq. NaCI-Lösung gewaschen und über Magnesiumsulfat getrocknet. Das Lösungsmittel wird im Vakuum entfernt und der Rückstand säulenchromatographisch (SiO2, verschiedene Mischung aus Dichlormethan und MeOH als Laufmittel) gereinigt.
Die folgenden Verbindungen wurden gemäß Methode 2. erhalten.
(6-(Trifluormethyl)-2-(4-methylpiperidin-1-yl)pyridin-3-yl)methanamin
1H NMR (300 MHz, CDCI3) δ 7.89 (d, 1 H, J = 7.8 Hz), 7.33 (d, 1 H, J = 7.8 Hz), 3.88 (s, 2H), 3.39 (m, 2 H), 2.83 (m, 2 H), 1.75 (m, 2 H), 1.55 (m, 1 H), 1.38 (m, 2 H), 1.00 (d, 3 H, J = 6.6 Hz); MS (FAB) m/z 274 (M+H)
C-(6'-tert-Butyl-4-methyl-3,4,5,6-tetrahydro-2H-[1,2']bipyridinyl-3
f-yl)- methylamin
1H-NMR (CDCI3) δ 7.48 (d, 1 H, J=7.7Hz, Ar), 6.90 (d, 1 H, J=7.7Hz, Ar), 3.82 (s, 2H, CH2NH2), 3.38 (m, 2H, Piperidin), 2.81 (m, 2H, Piperidin), 1.73-1.28 (m, 5H, Piperidin), 1.31 (s, 9H, C(CH3J3), 0.98 (d, 3H, J=6.4Hz, CHCH3) IR 3363, 2954, 1571 , 1451 , 1400, 1372, 1234, 960 cm'1
2. Allgemeine Vorschrift zur Darstellung von Aminen der allgemeinen Formel V-E
Die Darstellung von Aminen der allgemeinen Formel V-E erfolgt wie im nachfolgenden Schema 2 dargestellt.
Vl-A Vl-F V-E
Schema 2.
Stufe 1 :
Synthese von 2-(Cyclohexylthio)-6-(trifluormethyl)nicotinnitril
1.3 Äquivalente NaH (4.9 g, 0.124 mol) wurden unter Stickstoff-Atmosphäre in 50 ml_ DMF gelöst. Nach Zugabe von 1.2 Äquivalenten Cyclohexanthiol (14.2 ml_, 0.116 mol) wurde bei RT 1.5 h gerührt. Die entstandene Suspension wurde auf 10 0C abgekühlt und tropfenweise 1 Äquivalent 2-Chlor-6-(trifluormethyl)nicotinnitril (20 g,
0.096 mol) in 50 ml_ DMF zugefügt und 2 h bei RT gerührt. Das Reaktionsgemisch wurde mit ges. aq. NH4CI-Lsg. versetzt, mit 1 L Wasser verdünnt und mehrfach mit
EE (3 x 200 mL) extrahiert. Die vereinigten organischen Phasen wurden mit ges. aq.
NaCI-Lsg. gewaschen, über MgSO4 getrocknet und im Vakuum eingeengt. Die säulenchromatographische Reinigung (Slilicagel. 100-200 mesh, Eluent: 2 % EE in
Hexan) erbrachte 26 g (93.8 %) Produkt.
1H NMR (300 MHz, CDCI3) δ 7.94 (d ,1 H, J = 7.9 Hz), 7.34 (d, 1 H, J = 7.9 Hz), 4.00
(m, 1 H),1.90-2.14 (m, 2 H), 1.42-1.88 (m, 8 H)
IR (neat) 2930, 2854, 2232, 1643, 1573, 1447, 1334, 1245, 1186, 1149, 1107, 851 cm'1
MS (FAB ) m/z 287 (M+H)
Stufe 2:
Synthese von (2-(Cyclohexylthio)-6-(trifluormethyl)pyridin-3-yl)methanamin dihydrochlorid
Das Nitril (26 g, 0.091 mol) wurde unter Stickstoff-Atmosphäre in 600 mL THF gelöst und auf 5 0C abgekühlt. Tropfenweise wurde BH3-Dimethylsulfid (13.78 g, 0.182 mol) zugefügt und 20 h unter Rückfluß gekocht. Nach Abkühlung auf 5 0C wurde der Reaktionsansatz mit 100 mL MeOH versetzt und 15 Minuten bei RT gerührt. Dann wurde Di-tert.Butyl-dicarbonat (29.7 g, 0.136 mol) zugegeben und 30 min bei RT gerührt. Nach Entfernen des Lösungsmittels im Vakuum wurde das Rohprodukt säulenchromatographisch (Silicagel. 100-200 mesh, Eluent: 10 % EE in Hexan) gereinigt und 23.4 g (66 %) Produkt erhalten.
Das Rohprodukt wurde in 120 mL ges. HCI-Dioxan-Lsg. gelöst und 6 h bei RT gerührt. Nach Entfernen des Lösungsmittels im Vakuum wurde der Feststoff mit 10 % EE in Hexan (2 x 100 mL) gewaschen und abfiltriert. Ausbeute: 17 g (88.8 %)
1H NMR (DMSO-de, 400 MHz): δ 8.8 (s,2H), 8.05 (d,1 H), 7.76 (d,1 H), 4.01 (s, 1 H), 3.86-3.93 (m,1 H), 2.02-2.08 (m,2H), 1.71-1.74 (m,2H), 1.40-1.60 (m,6H).
3. Allgemeine Vorschrift zur Darstellung von Aminen der allgemeinen Formel V- B
Die Darstellung von Aminen der allgemeinen Formel V-B erfolgt wie im nachfolgenden Schema 3 dargestellt.
Vl-A Vl-C V-B
Schema 3.
Stufe 1 : Darstellung von Nitrilen der allgemeinen Formel Vl-C
Verbindungen der allgemeinen Formel Vl-A (1 Äquivalent), worin R8, U, T und V die vorstehend genannte Bedeutung haben und m für 0, 1 , 2 oder 3 steht, werden mit einem Alkohol der allgemeinen Formel HO-R42 (3.5 Äquivalente) und DBU [1 ,8- Diaza-bicyclo[5.4.0]undec-7-en] (3.5 Äquivalente) in Acetonitril (7 ml_ pro mmol der Verbindung der Formel Vl-A) 12 Stunden bei RT gerührt. Die Reaktionsmischung wird mehrfach mit EE extrahiert. Die vereinigten organischen Phasen werden mit ges. aq. NaCI-Lsg. gewaschen, über MgSO4 getrocknet und das Lösungsmittel wurde im Vakuum entfernt. Der Rückstand wird jeweils durch Säulenchromatographie (SiO2, verschiedene Mischungen Hexan/EE) gereinigt.
Methode 2:
Verbindungen der allgemeinen Formel Vl-C (2 mmol), worin R8, R42, U, T und V die vorstehend genannte Bedeutung haben und m für 0, 1 , 2 oder 3 steht, werden in THF (10 ml_, 10 mL) gelöst und BH3'S(CH3)2 [2.0 M in THF, 3 mL, 3 Äquivalent] wird hinzu gegeben. Die Reaktionsmischung wird 8 Stunden zum Rückfluss erhitzt, aq. HCl (2 N) wird hinzu gegeben und die Reaktionsmischung wird erneut für 30 Minuten zum Rückfluss erhitzt. Die Reaktionsmischung wird mit aq. Natriumhydroxid-Lösung (2N) versetzt und mit EE gewaschen. Die vereinigten organischen Phasen werden mit ges. aq. NaCI-Lösung gewaschen und über Magnesiumsulfat getrocknet. Das Lösungsmittel wird im Vakuum entfernt und der Rückstand säulenchromatographisch (SiO2, verschiedene Mischung aus Dichlormethan und Methanol als Laufmittel) gereinigt.
Methode 3:
Verbindungen der allgemeinen Formel Vl-C (1.5 mmol), worin R8, R42, U, T und V die vorstehend genannte Bedeutung haben und m für 0, 1 , 2 oder 3 steht, werden in Diethylether (3 ml_) gelöst und bei 0 0C wird eine Suspension von Lithiumaluminiumhydrid (3 mmol) in Ether (5 ml_) langsam zu getropft. Die Reaktionsmischung wird 4 Stunden zum Rückfluss erhitzt und bei 0 0C wird langsam Methanol und anschließend 1 N aq. NaOH-Lösung zu getropft. Die Reaktionsmischung wird mit Methanol verdünnt und über Celite filtriert. Das Lösungsmittel wird im Vakuum entfernt und der Rückstand säulenchromatographisch (SiO2, verschiedene Mischung aus Dichlormethan und Methanol als Laufmittel) gereinigt.
4. Allgemeine Vorschrift zur Darstellung von Aminen der allgemeinen Formel V- C
Die Darstellung von Aminen der allgemeinen Formel V-C erfolgt wie im nachfolgenden Schema 4 dargestellt.
Vl-A Vl-D V-C
Schema 4.
Stufe 1 : Darstellung von Nitrilen der allgemeinen Formel Vl-D
Verbindungen der allgemeinen Formel Vl-A (1 Äquivalent), worin R8, U1 T und V die vorstehend genannte Bedeutung haben und m für 0, 1 , 2 oder 3 steht, werden mit Bis(triphenylphosphin)palladium-dichlorid (7 Mol-%) und Kupfer(l)iodid (14 Mol-%) in 1-Methyl-2-pyrrolidinon (7 mL pro mmol Verbindung der allgemeinen Formel Vl-A) gelöst. Nach 10 Minuten werden das Alkin der allgemeinen Formel HC≡C-R38 (3.5 Äquivalente) und N, N-Diisopropylethylamin (2 Äquivalente) zugegeben und die
Reaktionsmischung wird 12 h bei einer Temperatur zwischen 90 und 110 0C gerührt. Die Reaktionsmischung wird über Celite filtriert und mehrfach mit EE extrahiert. Die vereinigten organischen Phasen werden mit ges. aq. NaCI-Lsg. gewaschen, über MgSO4 getrocknet und das Lösungsmittel wurde im Vakuum entfernt. Der Rückstand wird jeweils durch Säulenchromatographie (SiO2, verschiedene Mischungen Hexan/EE) gereinigt.
5. Allgemeine Vorschrift zur Darstellung von Aminen der allgemeinen Formel V- D
Die Darstellung von Aminen der allgemeinen Formel V-D erfolgt wie im nachfolgenden Schema 5 dargestellt.
R38 = Aryl, Heteroaryl, Cycloalkenyl
Vl-A Vl-E V-D
Schema 5.
Stufe 1 : Darstellung von Nitrilen der allgemeinen Formel Vl-E
Verbindungen der allgemeinen Formel Vl-A (1 Äquivalent), worin R8, U, T und V die vorstehend genannte Bedeutung haben und m für 0, 1 , 2 oder 3 steht, werden mit Palladiumdichlorid (5 mol-%) und einer Verbindung der allgemeinen Formel R38- B(OH)2 (2 Äquivalente), worin R38 für Aryl, Heteroaryl oder Cycloalkenyl steht, in einem Lösungsmittelgemisch aus Toluol/Dioxan/ 2 N aq. Natriumcarbonat-Lösung (20 mL pro 1 mmol Verbindungen der allgemeinen Formel Vl-A) gerührt. Die Reaktionsmischung wird 12 h unter Rückfluss erhitzt und über Celite filtriert. Die vereinigten organischen Phasen werden über Magnesiumsulfat getrocknet und das Lösungsmittel im Vakuum entfernt. Der Rückstand wird säulenchromatographisch (SiO2, verschiedene Lösungsmittelgemische von Hexan und EE) gereinigt.
Stufe 2: Methode 1
Verbindungen der allgemeinen Formel Vl-E (5 mmol), worin R8, R38, U, T und V die vorstehend genannte Bedeutung haben und m für 0, 1 , 2 oder 3 steht, Palladium auf Kohle (10 %, 500 mg) und konzentrierte Salzsäure (3 ml_) werden in MeOH (30 ml_) gelöst und 6 Stunden bei RT einer Wasserstoff atmosphäre ausgesetzt. Die Reaktionsmischung wird über Celite filtriert und das Filtrat wird im Vakuum eingeengt. Der Rückstand wird mittels Flashchromatographie (SiO2, EE) gereinigt.
Methode 2:
Verbindungen der allgemeinen Formel Vl-E (2 mmol), worin R8, R38, U, T und V die vorstehend genannte Bedeutung haben und m für 0, 1 , 2 oder 3 steht, werden in THF (10 ml_, 10 mL) gelöst und BH3 «S(CH3)2 [2.0 M in THF, 3 ml_, 3 Äquivalent] wird hinzu gegeben. Die Reaktionsmischung wird 8 Stunden zum Rückfluss erhitzt, aq. HCl (2 N) wird hinzu gegeben und die Reaktionsmischung wird erneut für 30 Minuten zum Rückfluss erhitzt. Die Reaktionsmischung wird mit aq. Natriumhydroxid-Lösung (2N) versetzt und mit EE gewaschen. Die vereinigten organischen Phasen werden mit ges. aq. NaCI-Lösung gewaschen und über Magnesiumsulfat getrocknet. Das Lösungsmittel wird im Vakuum entfernt und der Rückstand säulenchromatographisch (SiO2, verschiedene Mischung aus Dichlormethan und Methanol als Laufmittel) gereinigt.
6. Vorschrift zur Darstellung von Carbonsäuren der allgemeinen Formel VII
6.1 Darstellung von 2-(Benzo[d]oxazol-5-yl)propansäure
Stufe 1 : Synthese von Methyl-2-(4-hydroxy-3-nitrophenyl)acetat
Methyl-2-(4-hydroxyphenyl)acetat (2.0 g, 12.0 mmol) wurde in Essigsäure (15 ml_) gelöst und Salpetersäure (60-62%, 1.27g, 12.1 mmol) wurde bei RT hinzu gefügt. Die Reaktionsmischung wurde 30 Minuten bei RT gerührt, in Eiswasser (100 ml_) gegossen und mit EE extrahiert. Die organische Phase wurde über MgSO4 getrocknet, das Lösungsmittel im Vakuum entfernt und der Rückstand wurde mittels Säulenchromatographie (n-Hexan/EE = 4:1 ) gereinigt.
Stufe 2: Synthese von Methyl-2-(3-amino-4-hydroxyphenyl)acetat
Methyl-2-(4-hydroxy-3-nitrophenyl)acetat (2.31 g, 10.9 mmol) wurde in THF (20 ml_) und MeOH (20 mL) gelöst und 10%-ige Palladium auf Kohle (210 mg) wurde bei RT langsam hinzugegeben. Die Reaktionsmischung wurde 2 h bei 39 psi Wasserstoffdruck hydriert, über Celite filtriert und mit MeOH gewaschen. Das Lösungsmittel wurde im Vakuum entfernt und der Rückstand mittels Säulenchromatographie (n-Hexan/EE = 2:1 ) gereinigt.
Stufe 3: Synthese von Methyl-2-(benzo[d]oxazol-5-yl)acetat
Methyl-2-(3-amino-4-hydroxyphenyl)acetat (1.39 g, 7.67 mmol) wurde bei RT mit Triethylorthoformiat (10 mL) versetzt. Die Reaktionsmischung wurde 12 h zum Rückfluss erhitzt und anschließend auf RT abgekühlt. Wasser (70 mL) wurde hinzu gegeben und die Reaktionsmischung wurde mit EE extrahiert. Die vereinigten organischen Phasen wurden über MgSO4 getrocknet und filtriert. Das Lösungsmittel wurde im Vakuum entfernt und der Rückstand wurde mittels Säulenchromatographie (n-Hexan/EE = 2:1) gereinigt.
Stufe 4: Synthese von Methyl-2-(benzo[d]oxazol-5-yl)propanoat
Methyl-2-(benzo[d]oxazol-5-yl)acetat (0.90 g, 4.71 mmol) wurde in DMF (5 mL) gelöst und bei 0 0C mit Natriumhydrid (198 mg, 4.95 mmol) und Methyliodid (661 mg, 4.65 mmol) versetzt. Die Reaktionsmischung wurde 30 min bei 0 0C gerührt und anschließend 1 h bei RT. Die Reaktionsmischung wurde mit Wasser (70 mL) versetzt und mit EE extrahiert. Die vereinigten organischen Phasen wurden über MgSO4 getrocknet und filtriert. Das Lösungsmittel wurde im Vakuum entfernt und der Rückstand mittels Säulenchromatographie gereinigt (n-Hexan/EE = 4/1 ).
1H-NMR(CDCI3) δ 8.10 (s, 1 H, Ar), 7.74 (d, 1 H, J=1.7Hz, Ar), 7.54 (d, 1 H, 8.4Hz, Ar), 7.35 (dd, 1 H, J=8.6, 1.8Hz, Ar), 3.87 (q, 1 H, J=7.3Hz, CHCH3), 3.67 (s, 3H, OCH3), 1.57 (d, 3H, J=7.1 Hz, CHCH3) IR 2982, 1735, 1517, 1437, 1248, 1201 , 1170, 1067 cm"1
Stufe 5: Synthese von 2-(Benzo[d]oxazol-5-yl)propansäure
Methyl-2-(benzo[d]oxazol-5-yl)propanoat (425 mg, 2.07 mmol) wurde in THF (8 mL) und Wasser (8 mL) gelöst. LiOH*H2O (93mg, 2.21 mmol) wurde bei RT hinzu gegeben. Die Reaktionsmischung wurde 40 h bei RT gerührt, mit Wasser (25 mL) versetzt und mit Essigsäure auf einen pH-Wert von 3 eingestellt. Die Reaktionsmischung wurde mit DCM extrahiert und die vereinigten organischen Phasen wurden über MgSO4 getrocknet und filtriert. Das Lösungsmittel wurde im Vakuum entfernt und der Rückstand wurde mittels Säulenchromatographie (DCM/MeOH = 15:1 ) gereinigt.
1H-NMR (CD3OD) δ 8.46 (s, 1 H, Ar), 7.70 (d, 1 H, J=1.7Hz, Ar), 7.61 (d, 1 H, 8.0Hz, Ar), 7.42 (dd, 1 H, J=8.6, 1.8Hz, Ar), 3.87 (q, 1 H, J=7.1 Hz, CHCH3), 1.51 (d, 3H, J=7.1 Hz, CHCH3)
6.2 Darstellung von 2-(Benzo[d]oxazol-6-yl)propansäure
Die Verbindung 2-(Benzo[d]oxazol-6-yl)propansäure wurde analog zur Synthese von 2-(Benzo[d]oxazol-5-yl)propansäure (siehe 6.1 ) ausgehend von 2-(3- Hydroxyphenyl)essigsäure hergestellt.
1H-NMR (CD
3OD) δ 8.44 (s, 1 H, Ar), 7.67 (m, 2H, Ar), 7.38 (dd, 1 H
1 J=8.3, 1.5Hz, Ar), 3.88 (q, 1 H, J=7.1 Hz, CHCH
3), 1.51 (d, 3H, J=7.1 Hz, CHCH
3)
a. HNO3 AcOH, H2SO4(IOt.), EtOH, 26%; b. 10% Pd/C, H2 THF/EtOH, 85%; c. CH(OEt)3 99%; d. NaH, CH3I, DMF, 56%; e. LiOH H2O, THF/H2O, 97%
6.3 Darstellung von 2-(Benzo[d]oxazol-7-yl)propansäure
Die Verbindung 2-(Benzo[d]oxazol-7-yl)propansäure wurde analog zur Synthese von 2-(Benzo[d]oxazol-5-yl)propansäure (siehe 6.1 ) ausgehend von 2-(2- Hydroxyphenyl)essigsäure hergestellt.
a. H2SO4 (kat.), EtOH, 94%; b. HNO3 AcOH, 35%; c. 10%Pd/C, H2 THF/EtOH, 88%; d. CH(OEt)3, 96%; e. NaH, CH3I, DMF, 80%; f. UOH H2O, THF/H2O, 98%
6.4 Darstellung von 2-(7-Methoxybenzo[d]oxazol-5-yl)propansäure
Die Verbindung 2-(7-Methoxybenzo[d]oxazol-5-yl)propansäure wurde analog zur Synthese von 2-(Benzo[d]oxazol-5-yl)propansäure (siehe 6.1 ) ausgehend von Ethyl- 2-(4-hydroxy-3-methoxyphenyl)acetat hergestellt.
a. HNO3 AcOH, 48%; b. 10% Pd/C, H2 THF/EtOH, quantitativ; c. Triethylorthoformiat, 99%; d. NaH, CH3I, DMF, 52%; e. LiOH H2O,' THF/H2O, 74%
6.5 Darstellung von 2-(Benzo[d]oxazol-4-yl)propansäure
Die Verbindung 2-(Benzo[d]oxazol-4-yl)propansäure wurde analog zur Synthese von 2-(Benzo[d]oxazol-5-yl)propansäure (siehe 6.1 ) ausgehend von 2-(3- Hydroxyphenyl)essigsäure hergestellt.
1H-NMR(CD3OD) 8.42 (s, 1 H, Ar), 7.55 (dd, 1 H, J=7.9, 1.1 Hz, Ar), 7.37 (m, 2H, Ar), 4.38 (q, 1 H, J=7.1 Hz, CHCH3), 1.57 (d, 3H, J=7.4Hz, CHCH3)
a. HNO3 AcOH, H2SO4 (kat), EtOH, 14%; b. 10% Pd/C, H2 THF/EtOH, 90%; c. CH(OEt)3 90%; d. NaH, CH3I, DMF, 69%; e. LiOH H2O, THF/H2O, 67%'
6.6a. Generelle Vorschrift zur Darstellung von (Iso)chinolinpropansäuren
(vgl. Beispiele 49, 64-68)
Schritt 1 : Eine Lösung der Ausgangsverbindung (10,6 mmol) in Salzsäure (6 N, 20 ml_) wird auf 0 0C gekühlt und eine Lösung von Natriumnitrit (730 mg, 10,6 mmol) in Wasser (10 mL) tropfenweise hinzugegeben. Die daraus resultierende Lösung wird bei einer konstanten Temperatur von O0C zu einer Lösung aus Kaliumiodid (7,3 g, 44 mmol) in Wasser (15 mL) gegeben. Die Reaktionsmischung wird auf Raumtemperatur erwärmt, für drei Stunden gerührt und dann mit Essigsäureethylester extrahiert. Die vereinigten organischen Phasen werden nacheinander mit einer 10%igen Natriumthiosulfatlösung und einer gesättigten Natriumchloridlösung gewaschen, über Natriumsulfat getrocknet und unter vermindertem Druck konzentriert, um so das Jodierte Isochinolin als Feststoff zu erhalten, das ohne weitere Reinigung direkt im nächsten Schritt eingesetzt werden kann.
Schritt 2: Zu einer Mischung aus Kupfer(l)-iodid (9,5 mg, 5,0 mol%), 2-Picolinsäure (12,3 mg, 10,0 mol%), Cäsiumcarbonat (0,98 g, 3,0 mmol) und 1 ,4-Dioxan (10 ml) werden destilliertes Diethylmalonat (304 μL, 2,00 mmol) und das Aryliodid (1 ,00 mmol) gegeben und die Reaktionsmischung für 7 Stunden bei 70 0C gerührt. Dann wird die Reaktionsmischung auf Raumtemperatur erwärmt und mit Essigsäureethylester (20 mL x 3) und gesättigter Ammoniumchloridlösung (10 mL) extrahiert. Die vereinigten organischen Phasen werden über Natriumsulfat getrocknet
und unter vermindertem Druck konzentriert. Das so erhaltene Öl kann mittels Flashchromatographie an Kieselgel gereinigt werden, um das erwünschte α- Arylmalonat zu erhalten.
Schritt 3: Zu einer auf 0 0C gekühlten Lösung des α-Arylmalonates (1 mmol) in DMF (10 ml_) werden Natriumhydrid (1 ,1 mmol) und Methyliodid (1 mmol) gegeben und die Reaktionsmischung 30 Minuten bei Raumtemperatur gerührt. Anschließend kann die Reaktionsmischung bei vermindertem Druck konzentriert werden und der Rückstand unter Verwendung einer Mischung aus Hexan und Essigsäureethylester (4:1 ) als Eluent mittels Flashchromatographie an Kieselgel gereinigt werden.
Schritt 4: Eine Mischung des α-Arylmethylmalonates (1 mmol) und Natriumhydroxid (2 mmol) in 80%igem wässrigen Ethanol wird für 6 Stunden unter Rückfluss erhitzt. Die Reaktionsmischung wird mit Salzsäure (1 N) neutralisiert und anschließend mit Essigsäureethylester (20 ml_ x 3) extrahiert. Die vereinigten organischen Phasen werden unter vermindertem Druck konzentriert. Der so erhaltene Rückstand kann unter Verwendung einer Mischung aus Hexan und Essigsäureethylester (1 :1 ) mittels Flashchromatographie an Kieselgel gereinigt werden, um so die erwünschten (Iso)chinolinpropansäuren zu erhalten.
6.6b. Generelle Vorschrift zur Darstellung von (Iso)chinolinpropansäuren
a. Kalium-allyltrifluorboran, Pd(OAc)2, D-t-BPD, K2CO3, THF/H2O; b. KMnO4, NaIO4
Generelle Vorschrift für die von einem Pd(OAc)2 /D-t-BPF-Komplex katalysierte Reaktion von Arylhaliden mit Kalium-allyltrifluorboran
Analog Yamamoto, Y. et al., Chem. Lett. (2006), 35, 7, 704-705 werden in einem Kolben unter Schutzgasatmosphäre Kalium-allyltrifluorboran (2,5 mmol), Pd(OAc)2 (0,03 mmol, 3 mol%), D-t-BPF (0,036 mmol) und K2CO3 (3 mmol) vorgelegt. Nach Zugabe von THF (5 ml_) und des entsprechenden Aryl-bromids (1 mmol) wird die Reaktionsmischung 22 h unter Rückfluß gekocht. Nach Entfernung des Lösungsmittels wird der erhaltene Rückstand mittels Säulenchromatographie aufgereinigt (a).
Wie bei Kawatsura M. et al., Tetrahedron (2000), 56, 15, 2247-2258 beschrieben, kann nun das erhaltene Alken zur Propansäure verkocht werden. Hierzu wird der erhaltene Rückstand (1 mmol) in f-BuOH (18 ml_) und Wasser (45 ml_) gelöst, KMnO4 (2,5 mmol), NaIO4 (16 mmol) und K2CO3 (6,5 mmol) zugegeben und die Reaktionsmischung mit 3 N aq NaOH auf pH 8 eingestellt. Nach 2-stündigem Rühren bei Raumtemperatur wird die Mischung mit conc. HCl auf pH 1 acidifiziert und das MnO2 mit Natriumhydrogensulfit reduziert. Die Reaktionsmischung wird nun mit Ether versetzt, die Phasen getrennt und die organische Phase mit 3 N aq NaOH extrahiert. Die wässrige Phase wird mit conc. HCl angesäuert und ebenfalls mit Ether extrahiert. Die vereinigten organischen Phasen werden über MgSO4 getrocknet und im Vakuum eingeengt (b).
6.7 Darstellung von benzooxozyklischen Propion- und Essigsäuren
(vgl. Beispiele 9, 58-63)
Vorschrift Benzendioxol-propionsäure (Beispiel 60)
a NBu
4BF
4, NιBr
2bιpy, DMF, 25°C, 9% b LiOH, THF/H
2O, reflux, 12 h, 97%
Zusammen mit Ethylchlorpropionat (1 ,6 ml_, 13 mmol) wurde 4-Brom-1 ,2- (methylendioxy)benzen (2 g, 10 mmol) unter Stickstoff-Atmosphäre bei Raumtemperatur in 15 ml DMF gerührt. Zur Aktivierung wurden dann (1 ,1 g, 20 mmol) Mn, gefolgt von 2,2>-Bipyridin)nickel-(ll)-dibromid (0,26 g, 0,7 mmol) und TFA (20 mL) zugegeben. Das Reaktionsgemisch wurde 1 ,5 h bei 50 0C gerührt. Nach Abkühlung des Reaktionsgemischs wurde mit 25 mL 1 N HCl hydrolysiert, das Gemisch 3 x mit 25 mL Diethylether extrahiert, die vereinigten organischen Phasen mit 25 mL Wasser und 25 mL ges. NaCI-Lösung gewaschen, über MgSO4 getrocknet und im Vakuum eingeengt. Der hierbei entstandene Niederschlag wurde abgesaugt und mit Diethylether gewaschen. Nach Aufreinigung mittels Säulenchromatographie (n-Hexan/tert-BME = 9/1 ) konnten 0,198 g Produkt (9% d. Theorie) als weißer Feststoff erhalten werden.
Das Propionat (180 mg, 0,81 mmol) wurde in einem Gemisch aus THF (1 ,6 mL, 20 mmol) und Wasser (0,8 mL, 45 mmol) gelöst. Nach Zugabe von LiOH (0,058 g, 2,43 mmol) wurde das Reaktionsgemisch über Nacht refluxiert. Zur Aufarbeitung wurden dem Gemisch 25 mL Wasser und 25 mL Diethylether zugegeben und die entstandenen Phasen getrennt. Die wässrige Phase wurde mit HCl angesäuert und 3x mit jeweils 25 mL Dichlormethan extrahiert. Nach der Vereinigung der organischen Phasen, Trocknung über MgSO4 und Einengung im Vakuum konnte die Propionsäure in 97% Ausbeute (0,150 g) erhalten werden.
Analog der hier beschriebenen Vorgehensweise, können weitere benzooxozyklische Propansäuren dargestellt werden:
2-(Benzo[d][1 ,3]dioxol)propansäuren (i), 2-(2,3-Dihydrobenzo[b][1 ,4]dioxin)propansäuren (ii), 2-(3,4-Dihydro-2H-benzo[b][1 ,4]dioxepin)propansäuren (iii) und
Auch die entsprechenden benzooxozyklischen Essigsäuren sind mittels dieser Methode zugänglich:
2-(Benzo[d][1 ,3]dioxol)essigsäuren (i), 2-(2,3-Dihydrobenzo[b][1 ,4]dioxin)essigsäuren (ii), 2-(3,4-Dihydro-2H-benzo[b][1 ,4]dioxepin)essigsäuren (iii) und
6.8. Alternative Möglichkeiten zur Darstellung von Aryl-Propionsäuren aus Arylbromiden
a. THF, reflux, 6 h b. LiOH, THRH
2O, reflux, 12 h
Darstellung des Katalysators
Zur Darstellung des Palladium(0)-Katalysators werden zu einer einer trockenen THF- Lösung (10 ml) Pd(dppf)CI2 (110 mg, 0,15 mmol), dppf (83 mg, 0,15 mmol) und Butyllithium in Hexan (0,3 mmol) hinzugefügt. Die Reaktionsmischung wird bei Raumtemperatur 1 min gerührt und direkt in der nächsten Reaktion als Palladium- Katalysator verwendet.
Generelle Vorschrift für die Palladium-katalvsierte Reaktion von Arylhaliden mit (E)-1-
Methoxy-1 -trimethylsiloxypropan
Der frisch dargestellte Palladium(0)-Katalysator in trockenem THF (10 ml_) wird unter
Argon-Atmosphäre zu 90% TIOAc (1 ,78 g, 6 mmol) in trockenem THF (20 ml_) gegeben. Nach 5-minütigem Rühren der Reaktionsmischung bei Raumtemperatur werden das Arylhalid (3 mmol) in trockenem THF (10 ml_) und (E)-1-Methoxy-1- trimethylsiloxypropan (0,96g, 6 mmol) zugegeben und 4 - 24 h refluxiert.
Nach Entfernung des Lösungsmittels im Vakuum wird der Rückstand in Diethylether und Wasser aufgenommen und abfiltert. Das Filtrat wird mit Diethylether extrahiert, die vereinigten organischen Phasen über MgSO4 getrocknet, der Diethylether im
Vakuum entfernt und der erhaltene Rückstand säulenchromatographisch getrennt.
6.9 Alternative Vorschrift zur Darstellung von 2-(1 H-Indazol)propansäuren
(vgl. Beispiele 44-46, 48, 69-72)
a HBF
4 aq 50%, b NaNO
2 aq, 0 "C
1 c AcOK, 18-crown-6, CHCI
3 rt, d TsCI, TEA, CH
2CI
2, e Ethylchlorpropionat, NBu
4BF
4 NιBr
2bιpy DMF, rt, f TMSCI, NaI, CH
3CN, reflux
Die Darstellung von Indazol-Derivaten kann, wie im oben stehenden Schema erläutert, erfolgen. Ausgehend vom entsprechenden Brom-Methylanilin kann nach Boulouard M. et. al., Bioorganic Medicinal Chemistry Letters (2007), 17, 3177-3180 das gewünschte Brom-1-H-lndazol erhalten werden (a, b und c). Nach einer dem Fachmann bekannten Methode kann das 1 H-lndazol der Verbindung mit einer Tosylgruppe geschützt werden (d). Im folgenden kann dieses Tosyl-geschützte Brom-Indazol nach Durandetti M. et al., Tetrahedron (2007), 63, 1146-1153 mit Ethylchlorpropionat zum Indazol-propansäureester umgesetzt werden (e). Zum Erhalt der gewünschten Indazol-propansäure erfolgt die Entschützung der Propansäurefunktion und des 1-H-lndazols wie in Sabitha G. et al., Tetrahedron Letters (1999), 40, 1569-1570 beschrieben (f).
a NH
2OCH
3 1HCI, K
2CO
3, b NH
2NH
2
Ausgehend von Brom-fluorphenylethanonen beschreiben Lukin K. et al. J. Org. Chem. (2006), 71 , 21 , 8166-8172 einen alternativen Zugang zur Vorstufe der Brom- 1-H-lndazole (a, b).
6.10. Generelle Vorschrift zur Darstellung von 2-(1-Phenyl-1H- indazol)propansäuren
(vgl. Beispiel 73)
a. HOAc, H2O, 2 min, 200 °C, μwave; b. 2-Brompropansäure, Zn, I, HgCI2, Benzen; c.S, 190 °C, 1 h, Raney-Nickel; d. aq NaOH, reflux, 4 h
Die Darstellung der Phenylindazol-propansäuren kann analog zu US3657270 erfolgen (b-d). Die hierfür notwendigen Edukte, entsprechend substituierte 6,7- Dihydro-1-phenyl-indazol-4(5H)-one, können wie in Molteni V. et al., Synthesis (2002), 12, 1669-1674 beschrieben in einer Dreikomponenten-Reaktion unter Mikrowellenunterstützung erhalten werden (a).
6.11. Generelle Vorschrift zur Darstellung 2-(lndolin)propansäuren
(vgl. Beispiele 74-77)
a TsCI, TEA, CH
2CI
2; b. Ethylchlorpropionat, NBu
4BF
4, NιBr
2bιpy, DMF, rt, c TMSCI, NaI, CH
3CN, reflux
Ausgehend vom entsprechenden Brom-indolin wird nach dem Fachmann bekannter Methode eine Tosyl-Schutzgruppe eingeführt (a). Analog wie bei Durandetti M. et al., Tetrahedron (2007), 63, 1146-1153 beschrieben, wird mit Ethylchlorpropionat zum Indolin-propansäureester umgesetzt (b). Zum Erhalt der gewünschten 2-(lndolin)- propansäure wird die Verbindung wie in Sabitha G. et al., Tetrahedron Letters (1999), 40, 1569-1570 beschrieben, entschützt (c).
Analog der hier beschriebenen Vorgehensweise, können entsprechende 2-(1 H-lndol)propansäuren (i), 2-(2-Oxoindolin)propansäuren (ii), 2-(1 ,2,3,4-Tetrahydrochinolin) propansäuren (iii) und 2-(2-Oxo-1 ,2,3,4-tetrahydrochinolin)propansäuren (iv) erhalten werden.
7. Allgemeine Vorschrift zur Umsetzung von Aminen der allgemeinen Formeln V oder X mit Carbonsäuren der allgemeinen Formel VII
Methode A:
Die Säure der allgemeinen Formel VII (1 Äquivalent), das Amin der allgemeinen Formeln V oder X (1.2 Äquivalente) und EDCI (1.2 Äquivalente) werden in DMF (10 mmol Säure in 20 mL) 12 Stunden bei RT gerührt und anschließend Wasser dazugegeben. Die Reaktionsmischung wird mehrfach mit EE extrahiert, die wässrige
Phase wird mit NaCI gesättigt und anschließend wieder mit EE extrahiert. Die vereinigten organischen Phasen werden mit 1 N Salzsäure und ges. aq. NaCI-Lsg. gewaschen, über MgSO4 getrocknet und das Lösungsmittel wird im Vakuum entfernt. Der Rückstand wird mittels Flashchromatographie (Siθ2, EE/Hexan 1 :2) gereinigt.
Methode B:
Die Säure der allgemeinen Formel VII (1 Äquivalent) und das Amin der allgemeinen Formeln V oder X (1.1 Äquivalente) werden in DCM (1 mmol Säure in 6 ml_) gelöst und bei 0 0C mit EDCI (1.5 Äquivalente), HOBt (1.4 Äquivalent) und Triethylamin (3 Äquivalente) versetzt. Die Reaktionsmischung wird 20 h bei RT gerührt und mittels Säulenchromatographie (n-Hexan/EE = 2:1 ) gereinigt.
Die folgenden Beispielverbindungen wurden gemäß der vorstehend genannten Methode B erhalten.
Beispielverbindung 1: 2-Benzooxazol-5-yl-N-(4-tert-butyl-benzyl)-propionamid
1H-NMR(CDCI3) 6 8.10 (s, 1 H, Ar), 7.74 (d, 1 H, J=1.7Hz, Ar), 7.56 (d, 1 H, J=8.4Hz, Ar), 7.38 (dd, 1 H, J=8.6, 1.8Hz, Ar), 7.30 (d, 2H, J=8.4Hz, Ar), 7.09 (d, 2H, J=8.4Hz, Ar), 5.64 (bs, NH), 4.37 (m, 2H, NHCH2Ar), 3.72 (q, 1 H, J=7.1 Hz, COCH), 1.61 (d, 3H, J=7.1 Hz, CHCH3), 1.28 (s, 9H, C(CH3)3)
Synthese von Beispielverbindung 2: 2-Benzooxazol-6-yl-N-(4-tert-butyl-benzyl)-propionamid
1H-NMR(CDCI
3) δ 8.02 (d, 1 H, J=2.0Hz, Ar), 7.07 (dd, 1 H, J=8.3, 1.7Hz, Ar), 7.54 (s,
1 H, Ar), 7.25 (m, 3H, Ar), 7.04 (d, 2H, J=7.0Hz, Ar), 5.79 (bs, NH), 4.32 (m, 2H,
NHCH2Ar), 3.67 (q, 1 H, J=7.1 Hz, COCH), 1.55 (d, 3H, J=7.1 Hz, CHCH3), 1.23 (s,
9H, C(CH3)3)
IR 3296, 2963, 1649, 1518, 1479, 1434, 1247, 1067 cm 1
Masse (FAB) m/z 337 [M+H]+
Synthese von Beispielverbindung 3: 2-Benzooxazol-7-yl-N-(4-tert-butyl-benzyl)-propionamid
1H-NMR(CDCI3) δ 8.07 (s, 1 H, Ar), 7.71 (m, 1 H, Ar), 7.39-7.28 (m, 4H, Ar), 7.06 (d, 2H, J=8.4Hz, Ar), 5.74 (bs, NH), 4.38 (m, 2H, CH2NH), 4.06 (q, 1 H, J=7.1 Hz, CHCH3), 1.68 (d, 3H, J=7.1 Hz, CHCH3), 1.29 (s, 9H, C(CH3)3) Masse (FAB) m/z 337 [M+H]+
Synthese von Beispielverbindung 4:
a) 2-(4-Aminophenyl)propansäure
2-(4-nitrophenyl)propansäure im Handel erhältlich
In den Kolben wurde THF/EtOH (1 :1 , 100 ml) und anschließend 2-(4- Nitrophenyl)propansäure (10 g, 51 ,2 mmol) und 10 % Palladium-Kohle (0,87 g) bei Raumtemperatur zugegeben. Die Reaktionsmischung wurde hydriert und 1 h bei 45 psi gerührt und anschließend durch ein Kieselbett filtriert und mit EtOH gewaschen. Das Filtrat wurde unter Vakuum konzentriert. Weißer oder hellschwarzer Feststoff, Ausbeute: quantitativ.
b) 2-(4-Amino-3-nitrophenyl)propansäure
Zu einer Lösung von 2-(4-Aminophenyl)propansäure (8,45 g, 51 ,2 mmol) in AcOH (70 ml) wurde HNO3 (60 %, 5,66 g) bei Raumtemperatur zugegeben. Die Reaktionsmischung wurde 4 h unter Rückfluss gekocht und anschließend auf Raumtemperatur gekühlt. Die Mischung wurde in Eiswasser (200 ml) gegossen und mit CH2CI2 extrahiert. Die organische Schicht wurde über MgSO4 getrocknet, filtriert und unter Vakuum konzentriert.
c) Ethyl 2-(4-amino-3-nitrophenyl)propanoat
In den Kolben mit 2-(4-Amino-3-nitrophenyl)propansäure-Rückstand wurden EtOH (200 ml) und Schwefelsäure in einer Katalysatormenge (1 ml) bei Raumtemperatur zugegeben. Die Reaktionsmischung wurde 6 h unter Rückfluss gekocht und anschließend auf Raumtemperatur gekühlt. Die Mischung wurde mit H2O verdünnt und mit EtOAc extrahiert. Die organische Schicht wurde über MgSO4 getrocknet filtriert und unter Vakuum konzentriert. Hellgelbes Öl, Ausbeute: 17,4 % (zwei Schritte)
d) Ethyl 2-(3,4-diaminophenyl)propanoat
In den Kolben wurde THF/EtOH (1 :1 , 50 ml) und anschließend Ethyl 2-(4-amino-3- nitrophenyl)propanoat (2,12 g, 8,90 mmol) und 10 % Palladium-Kohle (220 mg) bei Raumtemperatur zugegeben. Die Reaktionsmischung wurde hydriert und 3 h bei 45 psi gerührt und anschließend durch ein Kieselbett filtriert und mit EtOH gewaschen. Das Filtrat wurde unter Vakuum konzentriert. Der Rückstand wurde durch Flash- Säulen-Chromatographie mit EtOAc:Hexanen (1 :4-1 :2) als Eluent an Kieselgel gereinigt. Gelbes Öl, Ausbeute: 74,5 %
e) 2-(2,3-dihydro-2-oxo-1 H-benzo[d]imidazol-5-yl)propanoat
Zu einer Lösung von Ethyl 2-(3,4-diaminophenyl)propanoat (217 mg, 1 ,04 mmol) in
CH2CI2 (4 ml) wurde 1 ,1 *-Carbonyldiimidazol (189 mg) und DBU (330 mg, in CH2CI2
(4 ml)) bei Raumtemperatur zugegeben.
Die Reaktionsmischung wurde 1 h bei Raumtemperatur gerührt. Die Mischung wurde mit H2O (20 ml) verdünnt und mit CH2CI2 extrahiert. Die organische Schicht wurde über MgSO4 getrocknet, filtriert und unter Vakuum konzentriert. Der Rückstand wurde durch Flash-Säulen-Chromatographie mit EtOAc:Hexanen (1 :4-1 :2) als Eluent an
Kieselgel gereinigt.
Hellgelber Feststoff, Ausbeute: 72,7 %
f) 2-(2,3-Dihydro-2-oxo-1 H-benzo[c/]imidazol-5-yl)propansäure
In den Kolben mit 2-(2,3-dihydro-2-oxo-1/-/-benzo[d]imidazol-5-yl)propanoat (175 mg, 0,747 mmol) wurde 90 % wässriges EtOH (5 ml) bei Raumtemperatur und zusätzlich NaOH (70 mg) zugegeben. Die Reaktionsmischung wurde 10 h bei 40 0C gerührt und anschließend auf Raumtemperatur gekühlt. Die Mischung wurde mit H2O (25 ml)
verdünnt und mit AcOH (4 ml, pH=4) angesäuert und dann mit CH2CI2 extrahiert. Die organische Schicht wurde über MgSO4 getrocknet, filtriert und unter Vakuum konzentriert. Der Rückstand wurde durch Flash-Säulen-Chromatographie mit CH2CI2:MeOH (10:1 ) als Eluent an Kieselgel gereinigt. Hellbrauner Feststoff, Ausbeute: 63,6 %
Beispiel 4 - N-(4-tert-Butyl-benzyl)-2-(2-oxo-2,3-dihydro-1H-benzoimidazol-5-yl)- propionamid
1H NMR (300 MHz, DMSO) δ 10.6-10.5 (bs, 2 H), 8.33 (bt, 1 H)1 7.34-7.22 (m, 2 H), 7.09-7.06 (m, 2 H), 6.93-6.81 (m, 3 H), 4.21-4.17 (m, 2 H), 3.60 (q, 1 H, J = 7.1 Hz), 1.34-1.24 (m, 12 H) MS (El) m/z 451 (M+H)
Synthese von Beispielverbindung 5: a) Ethyl 2-(3-hydroxyphenyl)acetat
Im Handel erhältlich
In den Kolben wurde EtOH (100 ml) und anschließend 2-(3- hydroxyphenyl)essigsäure (9,83 g, 64,6 mmol) und Schwefelsäure (Katalysatormenge) zugegeben. Die Mischung wurde 3 h unter Rückfluss gekocht und anschließend auf Raumtemperatur gekühlt. Die Mischung wurde mit H2O (100 ml) verdünnt und mit EtOAc (100 ml) extrahiert. Die organische Schicht wurde über MgSO4 getrocknet, filtriert und unter Vakuum konzentriert. Der Rückstand wurde durch Flash-Säulen-Chromatographie mit EtOAc:Hexanen (1 :4) als Eluent an Kieselgel gereinigt.
Hellgelbes Öl, Ausbeute: 94,5 %.
b) Ethyl 2-(3-methoxymethoxy)phenyl)acetat
Referenz: JACS, 100,8031 (1978)
Zu einer Lösung von Ethyl 2-(3-hydroxyphenyl)acetat (11 g, 61 mmol) in THF (100 ml) wurde NaH (2,93 g, 73,3 mmol) und MOM-CI (5,94 g, 73,3 mmol) bei O 0C zugegeben. Die Reaktionsmischung wurde 16 h bei O 0C gerührt und anschließend auf Raumtemperatur erwärmt. Die Reaktionsmischung wurde mit H2O (200 ml) verdünnt und mit EtOAc extrahiert. Die organische Schicht wurde über MgSO4 getrocknet, filtriert und unter Vakuum konzentriert. Der Rückstand wurde durch Flash-Säulen-Chromatographie mit EtOAc:Hexanen (1 :10) als Eluent an Kieselgel gereinigt. Farbloses Öl, Ausbeute: 79,7 %.
c) Ethyl 2-(3-methoxymethoxy)phenyl)propanoat
Zu einer Lösung von Ethyl 2-(3-methoxymethoxy)phenyl)acetat (8,06 g, 35,9 mmol) in DMF (50 ml) wurde NaH (1 ,74 g, 43,5 mmol) und lodmethan (6,37 g, 44,9 mmol) bei O 0C zugegeben. Die Reaktionsmischung wurde 1 h bei O 0C gerührt und anschließend mit H2O (250 ml) verdünnt und mit EtOAc extrahiert. Die organische Schicht wurde über MgSO4 getrocknet, filtriert und unter Vakuum konzentriert. Der Rückstand wurde durch Flash-Säulen-Chromatographie mit EtOAσHexanen (1 :10) als Eluent an Kieselgel gereinigt. Farbloses Öl, Ausbeute: 49,1 %.
d) Ethyl 2-(3-hydroxyphenyl)propanoat
Zu einer Lösung von Ethyl 2-(3-methoxymethoxy)phenyl)propanoat (4,17 g, 17,5 mmol) in CH2CI2 (80 ml) wurde Trifluoressigsäure (40 ml) bei O 0C zugegeben. Die Reaktionsmischung wurde 1 h bei O 0C gerührt und mit NaHCO3 (60 g) alkalisiert. Die Mischung wurde mit H2O (250 ml) allmählich verdünnt und mit CH2CI2 extrahiert.Die organische Schicht wurde über MgSO4 getrocknet, filtriert und unter Vakuum konzentriert. Der Rückstand wurde durch Flash-Säulen-Chromatographie mit EtOAc:Hexanen (1 :4) als Eluent an Kieselgel gereinigt. Farbloses Öl, Ausbeute: 74,1 %
e) Ethyl 2-(3-hydroxy-4-nitrophenyl)propanoat
Zu einer Lösung von Ethyl 2-(3-hydroxyphenyl)propanoat (2,51 g, 12,9 mmol) in Essigsäure (20 ml) wurde Salpetersäure (1 ,45 g, 13,8 mmol) in Essigsäure (2 ml) bei Raumtemperatur zugegeben. Nach 1-2 Minuten Rühren verwandelte sich das farblose Öl in das dunkelbraune Öl. Die Reaktionsmischung wurde 15 Minuten bei Raumtemperatur gerührt und anschließend in Eiswasser (100 ml) gegossen und mit EtOAc extrahiert. Die organische Schicht wurde über MgSO4 getrocknet, filtriert und unter Vakuum konzentriert. Der Rückstand wurde durch Flash-Säulen- Chromatographie mit EtOAc:Hexanen (1 :6) als Eluent an Kieselgel gereinigt. Gelber Feststoff (Schmelzpunkt 45-47 0C), Ausbeute: 30,8 %
f) Ethyl 2-(4-amino-3-hydroxyphenyl)propanoat
In den Kolben wurde THF/EtOH (1 :1 , 30 ml) und anschließend Ethyl 2-(3-hydroxy-4- nitrophenyl)propanoat (900 mg, 3,76 mmol) und 10 % Palladium-Kohle (93 mg) bei Raumtemperatur zugegeben. Die Reaktionsmischung wurde hydriert und 1 h bei 46 psi gerührt und anschließend durch ein Kieselbett filtriert und mit EtOH gewaschen. Das Filtrat wurde unter Vakuum konzentriert. Der Rückstand wurde durch Flash- Säulen-Chromatographie mit EtOAc: Hexanen (1 :2) als Eluent an Kieselgel gereinigt. Weißer Feststoff (Schmelzpunkt 119-121 0C), Ausbeute: 80,1 %
g) Ethyl 2-(4-(2-chloroacetamido)-3-hydroxyphenyl)propanoat
Zu einer Lösung von Ethyl 2-(4-amino-3-hydroxyphenyl)propanoat (101 mg, 0,483 mmol) in 4-Methyl-2-pentanon (4 ml) wurde Chloracetylchlorid (58 mg, 0,514 mmol) in 4-Methyl-2-pentanon (2 ml) bei Raumtemperatur zugegeben. Die Reaktionsmischung wurde 12 h bei 80 0C gerührt und anschließend auf Raumtemperatur gekühlt. Die Mischung wurde mit H2O verdünnt und mit EtOAc extrahiert. Die organische Schicht wurde über MgSO4 getrocknet, filtriert und unter Vakuum konzentriert. Der Rückstand wurde durch Flash-Säulen-Chromatographie mit EtOAσHexanen (1 :2) als Eluent an Kieselgel gereinigt. Hellrosa Feststoff (Schmelzpunkt 118-120 0C), Ausbeute: 90,6 %
h) Ethyl 2-(3,4-dihydro-3-oxo-2AV-benzo[ό][1 ,4]oxazin-7-yl)propanoat
Zu einer Lösung von Ethyl 2-(4-(2-chloroacetamido)-3-hydroxyphenyl)propanoat (110 mg, 0,385 mmol) in Aceton (10 ml) wurde Kaliumcarbonat (61 mg) zugegeben. Die Reaktionsmischung wurde 3 h unter Rückfluss gekocht und anschließend auf Raumtemperatur gekühlt. Die Mischung wurde mit H2O verdünnt und mit EtOAc extrahiert. Die organische Schicht wurde über MgSO4 getrocknet, filtriert und unter Vakuum konzentriert. Der Rückstand wurde durch Flash-Säulen-Chromatographie mit EtOAc:Hexanen (1 :2) als Eluent an Kieselgel gereinigt. Weißer Feststoff (Schmelzpunkt 101 0C), Ausbeute: 91 ,7 %
i) 2-(3,4-Dihydro-3-oxo-2H-benzo[/}][1 ,4]oxazin-7-yl)propansäure
Zu einer Lösung von Ethyl 2-(3,4-dihydro-3-oxo-2/-/-benzo[jb][1 ,4]oxazin-7- yl)propanoat (80 mg, 0,321 mmol) in 90 % wässrigem EtOH (5 ml) wurde NaOH (64 mg, 1 ,60 mmol) bei Raumtemperatur zugegeben. Die Reaktionsmischung wurde 12 h bei 50 °C gerührt und anschließend auf Raumtemperatur gekühlt. Die Mischung wurde mit H2O (20 ml) verdünnt und mit AcOH angesäuert und anschließend mit CH2CI2 extrahiert. Die organische Schicht wurde über MgSO4 getrocknet, filtriert und unter Vakuum konzentriert. Weißer Feststoff (Schmelzpunkt 199-201 0C), Ausbeute: 98,4 %
Beispiel 5 - N-(4-tert-Butyl-benzyl)-2-(3-oxo-3,4-dihydro-2H-benzo[1,4]oxazin-7- yl)-propionamid
1H-NMR(CDCI3) δ 9.15 (bs, NH), 7.32 (d, 2H, J=8.2Hz, Ar), 7.12 (d, 2H, J=8.2Hz, Ar), 6.93-6.78 (m, 3H, Ar), 5.79 (bs, NH), 4.58 (s, 2H1 OCH2), 4.38 (m, 2H, NHCH2), 3.50 (q, 1 H, J=7.1 Hz, COCH), 1.51 (d, 3H, J=7.1 Hz, CHCH3), 1.29 (s, 9H, C(CH3)3) IR 3284, 2962, 1700, 1645, 1517, 1417 cm 1 Masse (FAB) m/z 367 [M+H]\ 389 [M+Na]+
Synthese von Beispielverbindung 6:
a) Ethyl 2-(4-methoxymethoxy)phenylacetat
Ethyl 2-(4-hydroxyphenyl)acetat im Handel erhältlich
Zu Ethyl 2-(4-hydroxyphenyl)acetat (2,14 g, 11 ,8 mmol) in THF (20 ml) wurden Natriumhydrid (0,50 g, 12,5 mmol) und Chlormethylmethylether (1 ,00 g, 12,4 mmol) bei O 0C langsam zugegeben. Die Reaktionsmischung wurde 16 h bei Raumtemperatur gerührt. Wasser (50 ml) wurde zur Mischung zugegeben und sie wurde mit EtOAc extrahiert. Die organische Schicht wurde mit MgSO4 getrocknet. Die organische Schicht wurde filtriert und das Filtrat wurde unter Vakuum konzentriert. Der Rückstand wurde durch Säulen-Chromatographie gereinigt, wobei mit n-Hexan/EtOAc (6:1 ) eluiert wurde. Farbloses Öl, Ausbeute: 67 %
b) Ethyl 2-(4-methoxymethoxy)phenyl)propanoat
Zu Ethyl 2-(4-methoxymethoxy)phenylacetat (1 ,75 g, 7,80 mmol) in DMF (50 ml) wurden Natriumhydrid (330 mg, 8,25 mmol) und lodmethan (1 ,13 g, 7,96 mmol) bei O 0C allmählich zugegeben. Die Reaktionsmischung wurde 1 h bei O 0C gerührt. Wasser (50 ml) wurde zur Mischung zugegeben und sie wurde mit EtOAc extrahiert. Die organische Schicht wurde mit MgSO4 getrocknet. Die organische Schicht wurde filtriert und das Filtrat wurde unter Vakuum konzentriert. Der Rückstand wurde durch Säulen-Chromatographie gereinigt, wobei mit n-Hexan/EtOAc (15:1 ) eluiert wurde. Farbloses Öl, Ausbeute: 57 %
c) Ethyl 2-(4-hydroxyphenyl)propanoat
Zu einer Lösung von Ethyl 2-(4-methoxymethoxy)phenyl)propanoat (485 mg, 2,04 mmol) in Methylenchlorid (10 ml) wurde Trifluoressigsäure (5 ml) bei O 0C zugegeben. Die Mischung wurde 40 Minuten bei O 0C gerührt und anschließend wurden festes Natriumbicarbonat (7,14 g) und Wasser (100 ml) bei O 0C langsam zugegeben. Die Mischung wurde mit Methylenchlorid extrahiert. Die organische Schicht wurde mit MgSO4 getrocknet. Die organische Schicht wurde filtriert und das Filtrat wurde unter Vakuum konzentriert. Der Rückstand wurde durch Säulen- Chromatographie gereinigt, wobei mit n-Hexan/EtOAc (4:1 ) eluiert wurde. Farbloses Öl, Ausbeute: 67 %
d) Ethyl 2-(4-hydroxy-3-nitrophenyl)propanoat
Zu einer Lösung von Ethyl 2-(4-hydroxyphenyl)propanoat (275 mg, 1 ,42 mmol) in Essigsäure (2 ml) wurde Salpetersäure (60-62 %, 300 mg, 2,86 mmol) bei Raumtemperatur zugegeben. Die Reaktionsmischung wurde 1 h bei 50 0C gerührt und anschließend auf Raumtemperatur gekühlt. Die Reaktionsmischung wurde in Eiswasser (20 ml) gegossen und mit EtOAc extrahiert. Die organische Schicht wurde mit MgSO4 getrocknet und filtriert. EtOAc wurde durch Verdampfen entfernt. Der Rückstand wurde durch Säulen-Chromatographie gereinigt, wobei mit n- Hexan/EtOAc (6:1 ) eluiert wurde. Gelbes Öl, Ausbeute: 87 %
e) Ethyl 2-(3-amino-4-hydroxyphenyl)propanoat
Zu Ethyl 2-(4-hydroxy-3-nitrophenyl)propanoat (260 mg, 1 ,09 mmol) in THF (6 ml) und Ethanol (6 ml) wurde 10 % Pd/C (29 mg) allmählich bei Raumtemperatur zugegeben. Die Mischung wurde 2 h bei 43 psi hydriert und anschließend mit Kieselgur filtriert und mit EtOAc gewaschen. Das Filtrat wurde unter Vakuum konzentriert. Der Rückstand wurde durch Säulen-Chromatographie gereinigt, wobei mit n-Hexan/EtOAc (1 :1 ) eluiert wurde. Gelbes Öl, Ausbeute: 86 %
f) Ethyl 2-(3-(2-chloroacetamido)-4-hydroxyphenyl)propanoat
Zu Ethyl 2-(3-amino-4-hydroxyphenyl)propanoat (104 mg, 0,497 mmol) in 4-Methyl-2- pentanon (4 ml) wurde Chloracetylchlorid (56 mg, 0,496 mmol) bei Raumtemperatur zugegeben und die Mischung wurde 20 h bei 80 0C gerührt. Die Reaktionsmischung wurde auf Raumtemperatur gekühlt und Wasser (30 ml) wurde zugegeben. Die Mischung wurde mit EtOAc extrahiert. Die organische Schicht wurde mit MgSO4 getrocknet und filtriert. EtOAc wurde durch Verdampfen entfernt, Der Rückstand wurde durch Säulen-Chromatographie gereinigt, wobei mit n-Hexan/EtOAc (2:1 ) eluiert wurde. Weißer Feststoff (Schmelzpunkt 126-1280C), Ausbeute: 78 %
g) Ethyl 2-(3,4-dihydro-3-oxo-2/-/-benzo[6][1 ,4]oxazin-6-yl)propanoat
Zu Ethyl 2-(3-(2-chloroacetamido)-4-hydroxyphenyl)propanoat (100 mg, 0,350 mmol) in Aceton (10 ml) wurde Kaliumcarbonat (59 mg) bei Raumtemperatur zugegeben und die Mischung wurde 3 h unter Rückfluss gekocht. Die Reaktionsmischung wurde auf Raumtemperatur gekühlt und Wasser (15 ml) wurde dazu zugegeben. Die Mischung wurde mit EtOAc extrahiert. Die organische Schicht wurde mit MgSO4 getrocknet und filtriert. EtOAc wurde durch Verdampfen entfernt. Der Rückstand wurde durch Säulen-Chromatographie gereinigt, wobei mit n-Hexan/EtOAc (2:1 ) eluiert wurde. Weißer Feststoff (Schmelzpunkt 116-118 0C), Ausbeute: 92 %
h) 2-(3,4-Dihydro-3-oxo-2H-benzo[6][1 ,4]oxazin-6-yl)propansäure
Zu Ethyl 2-(3,4-dihydro-3-oxo-2H-benzo[6][1 ,4]oxazin-6-yl)propanoat (63 mg, 0,253 mmol) in 90 % wässrigem EtOH (4,5 ml) wurde Natriumhydroxid (50 mg, 1 ,25 mmol) bei Raumtemperatur zugegeben. Die Reaktionsmischung wurde 12 h bei 50 0C gerührt und anschließend auf Raumtemperatur gekühlt. Wasser (20 ml) wurde zur Mischung zugegeben und sie wurde mit Essigsäure angesäuert. Die Mischung wurde mit Methylenchlorid extrahiert. Die organische Schicht wurde mit MgSO4 getrocknet und filtriert. Das Filtrat wurde unter Vakuum konzentriert. Weißer Feststoff (Schmelzpunkt 191-193 0C ), Ausbeute: 95 %,
Beispielverbindung 6 - N-(4-tert-Butyl-benzyl)-2-(3-oxo-3,4-dihydro-2H- benzo[1,4]oxazin-6-yl)-propionamid
1H-NMR(CDCI3) δ 8.76 (bs, NH), 7.32 (d, 2H, J=8.4Hz, Ar), 7.12 (d, 2H, J=8.3Hz, Ar), 6.93-6.85 (m, 3H, Ar), 5.73 (bs, NH), 4.58 (s, 2H, OCH2), 4.38 (m, 2H, NHCH2), 3.48 (q, 1 H, J=7.1Hz, COCH), 1.51 (d, 3H, J=7.1 Hz, CHCH3), 1.29 (s, 9H, C(CH3)3) IR 2925, 2855, 1648, 1540, 1459 cnr ,ϊ-1 Masse (FAB) m/z 367 [M+H]+
Synthese von Beispielverbindung 7: N-(4-tert-Butyl-benzyl)-2-(7-methoxy-benzooxazol-5-yl)-propionamid
1H-NMR (CDCI3) δ 8.06 (s, 1 H, Ar), 7.29 (m, 3H1 Ar), 7.10 (d, 2H, J=8.1 Hz, Ar), 6.87 (s, 1 H, Ar), 5.70 (bs, NH), 4.37 (m, 2H, NHCH2Ar), 4.00 (s, 3H, OCH3), 3.69 (q, 1 H1 J=7.1 Hz, COCH), 1.60 (d, 3H, J=7.1 Hz, CHCH3), 1.28 (s, 9H, C(CH3J3) IR 3297, 2963, 1647, 1519, 1316, 1110 crrϊ1 Masse (FAB) m/z 367 [M+H]+
Beispielverbindung 8: 2-Benzooxazol-4-yl-N-(4-tert-butyl-benzyl)-propionamid
1H-NMR(CDCI3) δ 8.04 (s, 1 H, Ar), 7.51 (m, 1 H, Ar), 7.41 (m, 2H, Ar), 7.26 (d, 2H, J=8.2Hz, Ar), 7.03 (d, 2H, J=8.3Hz, Ar), 6.65 (bs, NH), 4.35 (m, 3H, NHCH2Ar & COCH), 1.68 (d, 3H, J=7.1 Hz, CHCH3), 1.29 (s, 9H, C(CH3)3) IR 3304, 2962, 1658, 1519, 1428, 1242, 1076 cm"1 Masse (FAB) m/z 337 [M+H]+
Synthese von Beispielverbindung 9:
a) Ethyl 2-(3,4-dihydroxyphenyl)acetat
In den Kolben wurde EtOH (15 ml) und anschließend 2-(3,4- dihydroxyphenyl)essigsäure (1 ,07 g, 6,36 mmol) und Schwefelsäure (Katalysatormenge) zugegeben. Die Mischung wurde 3 h unter Rückfluss gekocht und anschließend auf Raumtemperatur gekühlt.
Die Mischung wurde mit H2O (30 ml) verdünnt und mit EtOAc (30 ml)extrahiert. Die organische Schicht wurde über MgSO4 getrocknet, filtriert und unter Vakuum konzentriert. Der Rückstand wurde durch Flash-Säulen-Chromatographie mit EtOAc:Hexanen (1 :1) als Eluent an Kieselgel gereinigt. Farbloses Öl, Ausbeute: 89,8 %.
b) Ethyl 2-(2,3-dihydrobenzo[6][1 ,4]dioxin-7-yl)acetat
Zu einer Mischung von Ethyl 2-(3,4-dihydroxyphenyl)acetat (1 ,11 g, 5,66 mmol) und 1 ,2-Dibromethan (1 ,07, 5,69 mmol) in DMF (5 ml) wurde Cäsiumcarbonat (3,71g, 11 ,4 mmol) zugegeben. Die Reaktionsmischung wurde 2 h bei 80 °C gerührt und anschließend auf Raumtemperatur gekühlt. Die Mischung wurde mit H2O verdünnt und mit EtOAc extrahiert. Die organische Schicht wurde über MgSO4 getrocknet, filtriert und unter Vakuum konzentriert. Der Rückstand wurde durch Flash-Säulen- Chromatographie mit EtOAc:Hexanen (1 :4~1 :2) als Eluent an Kieselgel gereinigt. Farbloses Öl, Ausbeute: 21 ,5 %.
c) Ethyl 2-(2,3-dihydrobenzo[ö][1 ,4]dioxin-7-yl)propanoat
Zu einer Lösung von Ethyl 2-(2,3-dihydrobenzo[b][1 ,4]dioxin-7-yl)acetat (257 mg, 1 ,16 mmol) in DMF (2 ml) wurden NaH (50 mg, 1 ,25 mmol) und lodmethan (167 mg, 1 ,18 mmol) in DMF (0,5 ml) bei O 0C zugegeben. Die Reaktionsmischung wurde 1 h bei O 0C gerührt und anschließend mit H2O (20 ml) verdünnt und mit EtOAc extrahiert). Die organische Schicht wurde über MgSO4 getrocknet, filtriert und unter Vakuum konzentriert. Der Rückstand wurde durch Flash-Säulen-Chromatographie mit EtOAc:Hexanen (1 :6) als Eluent an Kieselgel gereinigt. Farbloses Öl, Ausbeute: 82,1 %.
d) 2-(2-3-Dihydrobenzo[b][1 ,4]dioxin-7-yl)propansäure
In den Kolben wurde THF/H2O (1 :1 , 4 ml) und anschließend SM (133 mg, 0,563 mmol) und NaOH (30 mg, 0,750 mmol) bei Raumtemperatur zugegeben. Die Reaktionsmischung wurde 16 h bei Raumtemperatur gerührt. Die Mischung wurde mit H2O (20 ml) verdünnt und mit Essigsäure (4 ml, pH=4) angesäuert und anschließend mit CH2CI2 extrahiert. Die organische Schicht wurde über MgSO4 getrocknet, filtriert und unter Vakuum konzentriert. Farbloses Öl, Ausbeute: quantitativ.
Beispiel 9 - N-(4-tert-Butyl-benzyl)-2-(2,3-dihydro-benzo[1,4]dioxin-6-yl)- propionamid
1H-NMR(CDCI3) δ 7.32 (d, 2H, J=8.3Hz, Ar), 7.10 (d, 2H, J=8.3Hz, Ar), 6.84-6.74 (m, 3H, Ar), 5.62 (bs, NH), 4.36 (m, 2H, NHCH2), 4.25 (s, 4H, CH2CH2), 3.49 (q, 1 H, J=7.1 Hz, COCH), 1.51 (d, 3H, J=7.1 Hz, CHCH3), 1.30 (s, 9H1 C(CH3J3) IR 3298, 2963, 1648, 1507, 1287, 1255, 1068 crr ,ϊ-1 Masse (FAB) m/z 354 [M+H]+
Synthese von Beispielverbindung 10: a) 2-(4-Aminophenyl)propansäure
2-(4-nitrophenyl)propansäure im Handel erhältlich
In den Kolben wurde THF/EtOH (1 :1 , 100 ml) und anschließend im Handel erhältlich (10 g, 51 ,2 mmol) und 10 % Palladium-Kohle (0,87 g) bei Raumtemperatur zugegeben. Die Reaktionsmischung wurde hydriert und 1 h bei 45 psi gerührt und anschließend durch ein Kieselbett filtriert und mit EtOH gewaschen. Das Filtrat wurde unter Vakuum konzentriert. Weißer oder hellschwarzer Feststoff, Ausbeute: quantitativ
b) 2-(4-Amino-3-nitrophenyl)propansäure
Zu einer Lösung von 2-(4-Aminophenyl)propansäure (8,45 g, 51 ,2 mmol) in AcOH (70 ml) wurde HNO3 (60 %, 5,66 g) bei Raumtemperatur zugegeben. Die Reaktionsmischung wurde 4 h unter Rückfluss gekocht und anschließend auf Raumtemperatur gekühlt. Die Mischung wurde in Eiswasser (200 ml) gegossen und mit CH2Cb extrahiert. Die organische Schicht wurde über MgSO4 getrocknet, filtriert und unter Vakuum konzentriert.
c) Ethyl 2-(4-amino-3-nitrophenyl)propanoat
In den Kolben mit 2-(4-Amino-3-nitrophenyl)propansäύre-Rückstand wurden EtOH (200 ml) und Schwefelsäure in einer Katalysatormenge (1 ml) bei Raumtemperatur zugegeben. Die Reaktionsmischung wurde 6 h unter Rückfluss gekocht und anschließend auf Raumtemperatur gekühlt. Die Mischung wurde mit H2O verdünnt und mit EtOAc extrahiert. Die organische Schicht wurde über MgSO4 getrocknet, filtriert und unter Vakuum konzentriert. Hellgelbes Öl, Ausbeute: 17,4 % (zwei Schritte)
d) Ethyl 2-(3,4-diaminophenyl)propanoat
In den Kolben wurde THF/EtOH (1 :1 , 50 ml) und anschließend Ethyl 2-(4-amino-3- nitrophenyl)propanoat (2,12 g, 8,90 mmol) und 10 % Palladium-Kohle (0,87 g) bei Raumtemperatur zugegeben. Die Reaktionsmischung wurde hydriert und 3 h bei 45 psi gerührt und anschließend durch ein Kieselbett filtriert und mit EtOH gewaschen. Das Filtrat wurde unter Vakuum konzentriert. Der Rückstand wurde durch Flash- Säulen-Chromatographie mit EtOAc:Hexanen (1 :4-1 :2) als Eluent an Kieselgel gereinigt. Gelbes Öl, Ausbeute: 74,5 %
e) Ethyl 2-(2,3-dihydro-2-oxo-1/-/-benzo[d]imidazol-5-yl)propanoat
Zu einer Lösung von Ethyl 2-(3,4-diaminophenyl)propanoat (222 mg, 1 ,07 mmol) in CH2CI2 (4 ml) wurde 1 ,1 *-Thiocarbonyldiimidazol (241 mg) und DBU (345 mg, in CH2CI2 (4 ml)) bei Raumtemperatur zugegeben. Die Reaktionsmischung wurde 1 h bei Raumtemperatur gerührt. Die Mischung wurde mit H2O (20 ml) verdünnt und mit CH2CI2 extrahiert. Die organische Schicht wurde über MgSO4 getrocknet, filtriert und unter Vakuum konzentriert. Der Rückstand wurde durch Flash-Säulen- Chromatographie mit EtOAc:Hexanen (1 :4-1 :2) als Eluent an Kieselgel gereinigt. Farbloses Öl, Ausbeute: 35,8 %
f) 2-(2,3-Dihydro-2-thioxo-1 H-benzo[αφmidazol-5-yl)propansäure
In den Kolben mit Ethyl 2-(2,3-dihydro-2-oxo-1/-/-benzo[cφmidazol-5-yl)propanoat (93 mg, 0,372 mmol) wurde 90 % wässriges EtOH (5 ml) bei Raumtemperatur und zusätzlich NaOH (30 mg) zugegeben. Die Reaktionsmischung wurde 10 h bei 40 0C gerührt und anschließend auf Raumtemperatur gekühlt. Die Mischung wurde mit H2O (25 ml) verdünnt und mit AcOH (3 ml, pH=4) angesäuert und anschließend mit CH2CI2 extrahiert. Die organische Schicht wurde über MgSO4 getrocknet, filtriert und unter Vakuum konzentriert. Der Rückstand wurde durch Flash-Säulen- Chromatographie mit CH2CI2:MeOH (10:1 ) als Eluent an Kieselgel gereinigt. Braunes Öl, Ausbeute: 94,3 %
Beispiel 10 - N-(4-tert-Butyl-benzyl)-2-(2-thioxo-2,3-dihydro-1H-benzoimidazol- 5-yl)-propionamid
1H NMR (300 MHz, CD3OD) δ 7.28-6.95 (m, 7 H), 4.19 (s, 2 H), 3.63 (q, 1 H, J = 7.0 Hz), 1.38 (d, 3 H, J = 7.1 Hz), 1.16 (s, 9 H) MS (El) m/z 367 (M+H)
Synthese von Beispielverbindung 11 :
a) 2-(4-Aminophenyl)propionitril
In den Kolben wurde THF/EtOH (1:1 , 70 ml) und anschließend 2-(4- Nitrophenyl)propionitril (13,2 g, 74,9 mmol) und 10 % Palladium-Kohle (1 ,07 g) bei Raumtemperatur zugegeben. Die Reaktionsmischung wurde hydriert und 30 Minuten bei 47 psi bis 28 psi gerührt und anschließend durch ein Kieselbett filtriert und mit EtOH gewaschen. Das Filtrat wurde unter Vakuum konzentriert. Der Rückstand wurde durch Flash-Säulen-Chromatographie mit EtOAc:Hexanen (1 :3) als Eluent an Kieselgel gereinigt. Gelbes Öl, Ausbeute: 94,1 %
b) Λ/-[4-(Cyanomethylmethyl)phenyl]-acetamid
Referenz: Eur. J. Med. Chem. (1975), 10, 239
Zu einer Lösung von ) 2-(4-Aminophenyl)propionitril (10,2 g, 69,8 mmol) in Pyridin (40 ml) wurde Ac2O (7,49 g, 73,4 mmol) bei Raumtemperatur zugegeben. Die Reaktionsmischung wurde 1 h unter Rückfluss gekocht und anschließend auf Raumtemperatur gekühlt und unter Vakuum zugegeben. Weißer Feststoff (Schmelzpunkt 75-77 0C)1 Ausbeute: 98,2 %
c) Λ/-[4-(Cyanomethylmethyl)-2-nitrophenyl]acetamid
Hinweis: Eur. J. Med. Chem. (1975), 10, 239
In den Kolben mit Λ/-[4-(Cyanomethylmethyl)phenyl]-acetamid (12,9 g, 68,5 mmol) wurde AC2O (35 ml) bei 5 0C. Die Mischung wurde gerührt und HNO3 (7,45 g, 70,9 mmol) bei O 0C dazu zugegeben. Diese Reaktion war stark exotherm. Die Reaktionsmischung wurde 1 h bei O 0C gerührt und zusätzlich 3 h bei Raumtemperatur gekühlt. Die Mischung wurde mit H2O verdünnt und mit EtOAc extrahiert. Die organische Schicht wurde über MgSO4 getrocknet, filtriert und unter Vakuum konzentriert. Der Rückstand wurde durch Flash-Säulen-Chromatographie mit EtOAcrHexanen (1 :2) als Eluent an Kieselgel gereinigt. Gelber Feststoff (Schmelzpunkt 84-86 0C), Ausbeute: 55,7 %
d) 2-(4-Amino-3-nitrophenyl)-propionsäure
Referenz: Eur. J. Med. Chem. (1975), 10, 239
In den Kolben mit Λ/-[4-(Cyanomethylmethyl)-2-nitrophenyl]acetamid (8,90 g, 38,2 mmol) wurde konz. HCl (25 ml) bei Raumtemperatur zugegeben. Die Reaktionsmischung wurde 5 h unter Rückfluss gekocht und anschließend auf Raumtemperatur gekühlt. Die Mischung wurde mit H2O (150 ml) verdünnt und mit CH2CI2 extrahiert. Die organische Schicht wurde über MgSO4 getrocknet, filtriert und unter Vakuum konzentriert. Der Rückstand wurde durch Flash-Säulen- Chromatographie mit CH2CI2:MeOH (20:1-10:1 ) als Eluent an Kieselgel gereinigt. Gelber Feststoff (Schmelzpunkt 118-120 0C), Ausbeute: 87,8 %
e) 2-(3,4-Diaminophenyl)propansäure
In den Kolben wurde EtOH / H2O (3,5:1 , 45 ml) und anschließend 2-(4-Amino-3- nitrophenyl)-propionsäure (5,73 g, 27,3 mmol) und 10 % Palladium-Kohle (117 mg) bei Raumtemperatur zugegeben. Die Reaktionsmischung wurde hydriert und 5 h bei 64 psi gerührt und anschließend durch ein Kieselbett filtriert und mit EtOH gewaschen. Das Filtrat wurde unter Vakuum konzentriert. Der Rückstand wurde durch Flash-Säulen-Chromatographie mit CH2CbIMeOH (10:1 ) als Eluent an Kieselgel gereinigt. Brauner Feststoff (Schmelzpunkt 142-144 0C), Ausbeute: 50,0 %
f) N-(4-tert-Butylbenzyl)-2-(3,4-diaminophenyl)-propionamid
Zu 2-(3,4-Diaminophenyl)propansäure (436 mg, 2,42 mmol) in DMF (5 ml) wurden 4- t-Butylbenzylamin (399 mg, 2,44 mmol), EDC (702 mg, 3,66 mmol), HOBt (496 mg, 3,67 mmol) und Triethylamin (617 mg, 6,10 mmol) bei O 0C zugegeben. Die Reaktionsmischung wurde 16 h bei Raumtemperatur gerührt und anschließend wurde der Mischung Wasser (50 ml) zugegeben und sie wurde mit Methylenchlorid extrahiert. Die organische Schicht wurde mit MgSO4 getrocknet und filtriert. Methylenchlorid wurde durch Verdampfen entfernt. Der Rückstand wurde durch Säulen-Chromatographie gereinigt, wobei mit CH2CI2/MeOH (20:1 ) eluiert wurde. Braunes Öl, Ausbeute: 70 %,
g) Λ/-(4-tert-Butylbenzyl)-2-(chinoxalin-6-yl)propanamid
In den Kolben mit N-(4-tert-Butylbenzyl)-2-(3,4-diaminophenyl)-propionamid (81 mg, 0,249 mmol) wurde Glyoxal (4 ml, 40 % in wässriger Lösung) bei Raumtemperatur zugegeben und zusätzlich wurde DMF (4 ml) zugegeben, weil SM in Glyoxal nicht ausreichend lösbar ist. Die Reaktionsmischung wurde 2 h unter Rückfluss gekocht und anschließend auf Raumtemperatur gekühlt. Die Mischung wurde mit H2O (25 ml) verdünnt und mit CH2CI2 extrahiert. Die organische Schicht wurde über MgSO4 getrocknet, filtriert und unter Vakuum konzentriert. Der Rückstand wurde durch Flash-Säulen-Chromatographie mit EtOAc:Hexanen (1 :1 ) als Eluent an Kieselgel gereinigt. Brauner Feststoff (Schmelzpunkt 53-55 0C), Ausbeute: 55,5 %
Beispiel 11 - N-(4-tert-Butyl-benzyl)-2-chinoxalin-6-yl-propionamid
1H NMR (300 MHz, CDCI3) δ 8.84 (m, 2 H), 8.10 (d, 1 H, J = 8.8 Hz), 7.81 (dd, 1 H, J = 8.8 Hz, 2.0 Hz), 7.30 (d, 2 H, J = 8.3 Hz), 7.11 (d, 2 H, J = 8.3 Hz), 5.68 (bt, 1 H), 4.40 (m, 2 H), 3.84 (q, 1 H, J = 7.1 Hz), 1.68 (d, 3 H1 J = 7.1 Hz), 1.28 (s, 9 H) MS (FAB) m/z 348 (M+H)
Synthese von Beispielverbindung 15:
a) 2-(4-Aminophenyl)-propionitril
In den Kolben wurde THF/EtOH (1 :1 , 70 ml) und anschließend 2-(4- Nitrophenyl)propionitril (13,2 g, 74,9 mmol) und 10 % Palladium-Kohle (1 ,07 g) bei Raumtemperatur zugegeben. Die Reaktionsmischung wurde hydriert und 30 Minuten bei 47 psi bis 28 psi gerührt und anschließend durch ein Kieselbett filtriert und mit EtOAc gewaschen. Das Filtrat wurde unter Vakuum konzentriert. Der Rückstand wurde durch Flash-Säulen-Chromatographie mit EtOAc:Hexanen (1 :3) als Eluent an Kieselgel gereinigt. Gelbes Öl, Ausbeute: 94,1 %
b) Λ/-[4-(Cyanomethylmethyl)phenyl]acetamid
Referenz: Eur. J. Med. Chem. (1975), 10, 239
Zu einer Lösung von 2-(4-Aminophenyl)-propionitril (10,2g, 69,8mmol) in Pyridin (40 ml) wurde AC2O (7,49 g, 73,4 mmol) bei Raumtemperatur zugegeben. Die Reaktionsmischung wurde 1 h unter Rückfluss gekocht, auf Raumtemperatur abgekühlt.und unter Vakuum konzentriert. Weißer Feststoff (Schmelzpunkt 75-77 0C), Ausbeute: 98,2 %
c) Λ/-[4-(Cyanomethylmethyl)-2-nitrophenyl]acetamid
Referenz: Eur. J. Med. Chem. (1975), 10, 239
In den Kolben mit Λ/-[4-(Cyanomethylmethyl)phenyl]acetamid (12,9 g, 68,5 mmol) wurde Ac2O (35 ml) bei 5 0C zugegeben. Die Mischung wurde gerührt und HNO3 (7,45 g, 70,9 mmol) bei O 0C dazu zugegeben. Diese Reaktion war stark exotherm. Die Reaktionsmischung wurde 1 h bei 0 0C gerührt und zusätzlich 3 h bei Raumtemperatur gekühlt. Die Mischung wurde mit H2O verdünnt und mit EtOAc extrahiert. Die organische Schicht wurde über MgSO4 getrocknet, filtriert und unter Vakuum konzentriert. Der Rückstand wurde durch Flash-Säulen-Chromatographie mit EtOAc:Hexanen (1 :2) als Eluent an Kieselgel gereinigt. Gelber Feststoff (Schmelzpunkt 84-86 0C), Ausbeute. 55,7 %
d) 2-(4-Amino-3-nitrophenyl)-propionsäure
Referenz: Eur. J. Med. Chem. (1975), 10, 239
In den Kolben mit Λ/-[4-(Cyanomethylmethyl)-2-nitrophenyl]acetamid (8,90 g, 38,2 mmol) wurde konz. HCl (25 ml) bei Raumtemperatur zugegeben. Die Reaktionsmischung wurde 5 h unter Rückfluss gekocht und anschließend auf Raumtemperatur gekühlt. Die Mischung wurde mit H2O (150 ml) verdünnt und mit CH2CI2 extrahiert. Die organische Schicht wurde über MgSO4 getrocknet, filtriert und unter Vakuum konzentriert. Der Rückstand wurde durch Flash-Säulen- Chromatographie mit CH2CI2:MeOH (20:1-10:1 ) als Eluent an Kieselgel gereinigt. Gelber Feststoff (Schmelzpunkt 118-120 0C), Ausbeute: 87,8 %
e) 2-(3,4-Diaminophenyl)propansäure
In den Kolben wurde EtOH / H2O (3.5:1 , 45 ml) und anschließend 2-(4-Amino-3- nitrophenyl)-propionsäure (5,73 g, 27,3 mmol) und 10 % Palladium-Kohle (117 mg) bei Raumtemperatur zugegeben. Die Reaktionsmischung wurde hydriert und 5 h bei 64 psi gerührt und anschließend durch ein Kieselbett filtriert und mit EtOH gewaschen. Das Filtrat wurde unter Vakuum konzentriert. Der Rückstand wurde durch Flash-Säulen-Chromatographie mit CH2CI2:MeOH (10:1 ) als Eluent an Kieselgel gereinigt. Brauner Feststoff (Schmelzpunkt 142-144 0C), Ausbeute: 50,0 %
f) Λ/-[4-tert-Butylbenzyl)-2-(3,4-diaminophenyl)propionamid
Zu 2-(3,4-Diaminophenyl)propansäure (436 mg, 2,42 mmol) in DMF (5 ml) wurden 4- t-Butylbenzylamin (399 mg, 2,44 mmol), EDC (702 mg, 3,66 mmol), HOBt (496 mg, 3,67 mmol) und Triethylamin (617 mg, 6,10 mmol) bei O 0C zugegeben. Die Reaktionsmischung wurde 16 h bei Raumtemperatur gerührt und anschließend wurde der Mischung Wasser (50 ml) zugegeben und sie wurde mit Methylenchlorid extrahiert. Die organische Schicht wurde mit MgSO4 getrocknet und filtriert. Methylenchlorid wurde durch Verdampfen entfernt. Der Rückstand wurde durch Säulen-Chromatographie gereinigt, wobei mit CH2CI2/MeOH (20:1 ) eluiert wurde. Braunes Öl, Ausbeute: 70 %
g) Λ/-[4-tert-butylbenzyl)-2-(1 H-benzo[c/][1 ,2,3]triazol-5-yl)propanamid
Zu Λ/-[4-tert-Butylbenzyl)-2-(3,4-diaminophenyl)propionamid (110 mg, 0,338 mmol) in 5 % wässrigem Essigsäure (3 ml) und DMF (2,5 ml) wurde Natriumnitrit (30 mg, 0,435 mmol) bei O 0C zugegeben. Die Reaktionsmischung wurde 14 h bei Raumtemperatur gerührt. Wasser (20 ml) wurde zur Mischung zugegeben und sie wurde mit Methylenchlorid extrahiert. Die organische Schicht wurde mit MgSO4 getrocknet und filtriert. Methylenchlorid wurde durch Verdampfen entfernt. Der Rückstand wurde durch Säulen-Chromatographie gereinigt, wobei mit ChfeCb/MeOH (10:1 ) eluiert wurde. Hellbrauner Feststoff (Schmelzpunkt 126-128°C), Ausbeute: quantitativ
Beispiel - 15 - 2-(1H-Benzotriazol-5-yl)-N-(4-methyl-6l-trifluormethyl-3,4J5,6- tetrahydro-2H-[1,2']bipyridinyl-3'-ylmethyl)-propionamid
1H-NMR (CDCI3) δ 7.81 (m, 2H), 7.49 (d, 1 H, J=7.7Hz), 7.35 (m, 1 H), 7.14 (d, 1 H, J=7.5Hz), 6.77 (bs, NH), 4.52 (d, 2H), 3.84 (q, 1 H, J=7.0Hz), 3.25 (m, 2H), 2.76 (m, 2H), 1.77 (m, 2H), 1.64 (d, 3H, J=7.0Hz), 1.15-1.10 (m, 2H), 0.90 (d, 3H, J=6.4Hz) IR 3295, 2921 , 1650, 1539, 1458, 1419, 1177, 1136 cm 1 Masse (FAB) m/z 447 [M+H]+ (Base), 469 [M+Na]+
Synthese von Beispielverbindung 16:
a) Ethyl 2-(3-hydroxyphenyl)acetat
2-(3-Hydroxyphenyl)essigsäure im Handel erhältlich
Zu einer Lösung von 2-(3-Hydroxyphenylessigsäure) (9,83 g, 64,6 mmol) in Ethanol (100 ml) wurde Schwefelsäure in einer Katalysatormenge zugegeben. Die Mischung wurde 3 h unter Rückfluss gekocht und anschließend auf Raumtemperatur gekühlt. Die Mischung wurde mit hfeO (100 ml) verdünnt und mit EtOAc extrahiert. Die organische Schicht wurde über MgSO4 getrocknet, filtriert und unter Vakuum konzentriert. Der Rückstand wurde durch Flash-Säulen-Chromatographie mit EtOAc:Hexanen (1 :4) als Eluent an Kieselgel gereinigt. Hellgelbes Öl, Ausbeute: 94,5 %
b)
Ethyl 2-(3-methoxymethoxy)phenyl)acetat
Zu Ethyl 2-(3-hydroxyphenyl)acetat (24 g, 80,51 mmol) in THF (100 ml) wurden Natriumhydrid (2,93 g, 73,3 mmol) und Chlormethylmethylether (5,94 g, 73,7 mmol) bei O
0C langsam zugegeben. Die Reaktionsmischung wurde 16 h bei Raumtemperatur gerührt. Wasser (200 ml) wurde zur Mischung zugegeben und sie wurde mit EtOAc extrahiert. Die organische Schicht wurde mit MgSO
4 getrocknet. Die organische Schicht wurde filtriert und das Filtrat wurde unter Vakuum konzentriert. Der Rückstand wurde durch Säulen-Chromatographie gereinigt, wobei mit n-Hexan/EtOAc (10:1 ) eluiert wurde. Farbloses Öl, Ausbeute: 79,7 %
C)
Ethyl 2-(3-methoxymethoxy)phenyl)propanoat
Zu Ethyl 2-(3-methoxymethoxy)phenyl)acetat (8,06 g, 35,9 mmol) in DMF (50 ml) wurden Natriumhydrid (1 ,74 mg, 43,5 mmol) und lodmethan (6,37 g, 44,9 mmol) bei O 0C allmählich zugegeben. Die Reaktionsmischung wurde 1 h bei O0C gerührt. Wasser (250 ml) wurde zur Mischung zugegeben und sie wurde mit EtOAc extrahiert. Die organische Schicht wurde mit MgSO4 getrocknet. Die organische Schicht wurde filtriert und das Filtrat wurde unter Vakuum konzentriert. Der Rückstand wurde durch Säulen-Chromatographie gereinigt, wobei mit n-Hexan/EtOAc (10:1 ) eluiert wurde. Farbloses Öi, Ausbeute: 49 %
Ethyl 2-(3-hydroxyphenyl)propanoat
Zu einer Lösung von Ethyl 2-(3-methoxymethoxy)phenyl)propanoat (4,17 g, 17,5 mmol) in Methylenchlorid (80 ml) wurde Trifluoressigsäure (40 ml) bei O 0C zugegeben. Die Mischung wurde 1 h bei O 0C gerührt und anschließend wurden festes Natriumbicarbonat (60 g) und Wasser (250 ml) bei O 0C dazu zugegeben. Die Mischung wurde mit Methylenchlorid extrahiert. Die organische Schicht wurde mit MgSO4 getrocknet. Die organische Schicht wurde filtriert und das Filtrat wurde unter Vakuum konzentriert. Der Rückstand wurde durch Säulen-Chromatographie gereinigt, wobei mit n-Hexan/EtOAc (4:1 ) eluiert wurde. Farbloses Öl, Ausbeute: 74 %
e)
Ethyl 2-(3-hydroxy-4-nitrophenyl)propanoat
Zu Ethyl 2-(3-hydroxyphenyl)propanoat (2,51 g, 12,9 mmol) in Essigsäure (20 ml) wurde Salpetersäure (60-62 %, 1 ,45 g, 13,8 mmol) bei Raumtemperatur zugegeben. Die Reaktionsmischung wurde 15 Minuten bei Raumtemperatur gerührt. Die Reaktionsmischung wurde in Eiswasser (100 ml) gegossen und mit EtOAc extrahiert. Die organische Schicht wurde mit MgSO4 getrocknet und filtriert. EtOAc wurde durch Verdampfen entfernt. Der Rückstand wurde durch Säulen-Chromatographie gereinigt, wobei mit n-Hexan/EtOAc (6:1) eluiert wurde. Gelber Feststoff (Schmelzpunkt 44 0C), Ausbeute: 30,8 %
f)
Ethyl 2-(4-amino-3-hydroxyphenyl)propanoat
Zu einer Lösung von Ethyl 2-(3-hydroxy-4-nitrophenyl)propanoat (900 mg, 3,76 mmol) in THF/Ethanol (1 :1 , 30 ml) wurde 10 % Pd/C (93 mg) allmählich bei Raumtemperatur zugegeben. Die Mischung wurde 1 h bei 46 psi hydriert und anschließend mit Kieselgur filtriert und mit EtOAc gewaschen. Das Filtrat wurde unter Vakuum konzentriert. Der Rückstand wurde durch Säulen-Chromatographie gereinigt, wobei mit n-Hexan/EtOAc (2:1 ) eluiert wurde. Weißer Feststoff (Schmelzpunkt 119-121
0C), Ausbeute: 80,1 %
Referenz: Heterocycles, Vol. 51 , Nr. 8, 1929-1943
Ethyl 2-(2,3-dihydro-2-oxobenzo[cfloxazol-6-yl)propanoat
Zu einer Lösung von Ethyl 2-(4-amino-3-hydroxyphenyl)propanoat (205 mg, 0,978 mmol) in DMF (5 ml) wurde Harnstoff (305 mg, 5,19 mmol) zugegeben und es wurde 5 h unter Rückfluss gekocht. Die Reaktionsmischung wurde auf Raumtemperatur gekühlt und Wasser (30 ml) wurde zugegeben. Die Mischung wurde mit konz. HCl (1 ml) angesäuert und mit EtOAc extrahiert. Die organische Schicht wurde über MgSO4 getrocknet, filtriert und unter Vakuum konzentriert. Der Rückstand wurde durch Flash-Säulen-Chromatographie mit EtOAc:Hexanen (1 :2) als Eluent an Kieselgel gereinigt. Braunes Öl, Ausbeute: 88,2 %
h)
90 % wässriges EtOH
2-(2,3-Dihydro-2-oxobenzo[c(]oxazol-6-yl)propansäure
Zu einer Lösung von Ethyl 2-(2,3-dihydro-2-oxobenzo[c(]oxazol-6-yl)propanoat (95 mg, 0,404 mmol) in 90 % wässrigem EtOH (5 ml) wurde Natriumhydroxid (82 mg, 2,05 mmol) bei Raumtemperatur zugegeben. Die Reaktionsmischung wurde 24 h bei 45 0C gerührt und auf Raumtemperatur gekühlt. Wasser (10 ml) wurde zur Mischung zugegeben und sie wurde mit Essigsäure angesäuert (pH=4). Die Mischung wurde mit Methylenchlorid extrahiert. Die organische Schicht wurde mit MgSO4 getrocknet und filtriert. Das Filtrat wurde unter Vakuum konzentriert.
Weißer Feststoff (Schmelzpunkt 169-171 0C), Ausbeute: 83,6 %,
Beispiel 16 - N-(4-tert-Butyl-benzyl)-2-(2-oxo-2,3-dihydro-benzooxazol-6-yl)- propionamid
1H-NMR(CDCI3) δ 9.46 (bs, NH), 7.32 (d, 2H, J=8.2Hz, Ar), 7.11 (m, 4H, Ar), 6.90 (d, 1 H, J=8.0Hz, Ar), 5.99 (bs, NH), 4.40 (m, 2H, NHCH2), 3.61 (q, 1 H, J=7.1 Hz, COCH), 1.54 (d, 3H, J=7.1 Hz, CHCH3), 1.28 (s, 9H, C(CH3)3) IR 3301 , 2963, 1767, 1649, 1501 , 1264, 937, 733 crr ,ϊ-1 Masse (FAB) m/z 353 [M+H]+, 375 [M+Na]+
Synthese von Beispielverbindung 17:
2-(4-Hydroxyphenyl)-propionsäure-ethylester
Zu einer Lösung von 2-(4-hydroxyphenyl)propansäure (8,60 g) in Ethanol (70 ml) wurde Schwefelsäure (10 Tropfen) zugegeben und es wurde 12 h unter Rückfluss gekocht. Die Reaktionsmischung wurde auf Raumtemperatur gekühlt. Wasser (50 ml) wurde zur Mischung zugegeben und sie wurde mit EtOAc extrahiert. Die organische Schicht wurde über Magnesiumsulfat getrocknet, filtriert und unter Vakuum konzentriert. (9,0 g, braunes Öl)
b)
2-(4-Hydroxy-3-nitrophenyl)-propionsäure-ethylester
Zu einer Lösung von 2-(4-Hydroxyphenyl)-propionsäure-ethylester (9,02 g) in Essigsäure (75 ml) wurde Salpetersäure (60 %, 5,24 g in AcOH) bei Raumtemperatur zugegeben. Die Reaktionsmischung wurde 30 Minuten bei Raumtemperatur gerührt und Wasser wurde zugegeben. Die Mischung wurde mit EtOAc extrahiert und die organische Schicht wurde über Magnesiumsulfat getrocknet, filtriert und unter Vakuum konzentriert. Der resultierende Rückstand wurde auf Kieselgel (n- Hex:EtOAc=10:1 ) chromatographiert, um das Produkt als hellgelbes Öl zu erhalten. (9,71 g)
c)
2-(3-Amino-4-hydroxyphenyl)-propionsäure-ethylester
Zu einer gerührten Lösung von 2-(4-Hydroxy-3-nitrophenyl)-propionsäure-ethylester (9,71 g) in THF (40 ml) und EtOH (40 ml) wurde 10 % Pd/C (0,89 g) bei Raumtemperatur allmählich zugegeben. Nach 0,5 h Hydrierung mit H2 Rundkolben wurde die Reaktionsmischung über Kieselgur abfiltriert und mit EtOAc gewaschen. Die organische Schicht wurde über Magnesiumsulfat getrocknet, filtriert und unter Vakuum konzentriert. Der resultierende Rückstand wurde auf Kieselgel (n- Hex:EtOAc=2:1 ) chromatographiert, um das Produkt als hellgelbes Öl zu erhalten.
d)
2-(2-Thioxo-2,3-dihydrobenzothiazol-5-yl)-propionsäure-ethylester Zu einer Lösung von 2-(3-Amino-4-hydroxyphenyl)-propionsäure-ethylester (370 mg) in DMF (2 ml) wurde Phenylchlorothionoformiat (380 mg in DMF), und DBU (540 mg, in DMF) bei Raumtemperatur zugegeben. Die Reaktionsmischung wurde 16 h bei Raumtemperatur gerührt und Wasser wurde dieser Mischung zugegeben. Die resultierende Mischung wurde mit Ethylether extrahiert. Die vereinigte organische Schicht wurde über Magnesiumsulfat getrocknet, filtriert und unter Vakuum konzentriert. Der resultierende Rückstand wurde auf Kieselgel (n-Hex:EtOAc=4:1 ) chromatographiert, um das Produkt als weißer Feststoff zu erhalten. (130 mg, 29,2
%) e)
90 % wässriges EtOH
2-(2-Thioxo-2,3-dihydrobenzooxazol-5-yl)-propionsäure
Zu einer gerührten Lösung von 2-(2-Thioxo-2,3-dihydrobenzothiazol-5-yl)- propionsäure-ethylester (124 mg) in 90 % wässrigem EtOH wurde NaOH (102 mg) bei Raumtemperatur zugegeben. Nach 20 h Rühren bei 45 0C wurde die
Reaktionsmischung auf Raumtemperatur gekühlt und mit Wasser verdünnt. Die resultierende wässrige Schicht wurde mit Essigsäure angesäuert und anschließend mit Dichlormethan extrahiert. Die vereinigte organische Schicht wurde über
Magnesiumsulfat getrocknet, filtriert und unter Vakuum konzentriert. (105 mg, 95,4
%)
Beispiel 17 - N-(4-tert-Butyl-benzyl)-2-(2-thioxo-2,3-dihydro-benzooxazol-5-yl)- propionamid
1H-NMR(CDCI3) δ 7.34-7.05 (m, 7H, Ar), 5.99 (bt, NH), 4.52 (m, 2H, NHCH2), 3.61 (q, 1H, J=7.1Hz, COCH), 1.58 (d, 3H, J=7.0Hz, CHCH3), 1.27 (s, 9H, C(CH3J3) IR 3297, 2963, 1646, 1534, 1460, 1428, 1267, 1105 cm'1 Masse (FAB) m/z 369 [M+H]+
Synthese von Beispielverbindung 18: a)
(3-Hydroxy-phenyl)-essigsäure-ethylester
Zu einer Lösung von 3-Hydroxyphenylessigsäure (15,5 g) in Ethanol (200 ml) wurde Schwefelsäure (1 ml) zugegeben und es wurde 1 h unter Rückfluß gekocht. Die Reaktionsmischung wurde auf Raumtemperatur gekühlt. Wasser (50 ml) wurde zur Mischung zugegeben und sie wurde mit EtOAc extrahiert. Die organische Schicht wurde über Magnesiumsulfat getrocknet, filtriert und unter Vakuum konzentriert. (18,2 g, braunes Öl)
(3-Methoxymethoxy-phenyl)-essigsäure-ethylester
Zu einer Lösung von (3-Hydroxy-phenyl)-essigsäure-ethylester (27,6 g) in THF wurden NaH (7,35 g) und MOM-CI (14,8 g) bei O 0C allmählich zugegeben. Nach 14 h Rühren bei derselben Temperatur wurde die Reaktionsmischung auf Raumtemperatur erwärmt. Die resultierende Mischung wurde mit Wasser verdünnt und mit EtOAc extrahiert. Die vereinigte organische Schicht wurde über Magnesiumsulfat getrocknet, filtriert und unter Vakuum konzentriert. Der resultierende Rückstand wurde auf Kieselgel (n-Hex:EtOAc=15:1 bis 10:1 ) chromatographiert, um das Produkt als farbloses Öl zu erhalten. (31 ,2 g, 90,9 %)
2-(3-Methoxymethoxy-phenyl)-propionsäure-ethylester
Zu einer gerührten Lösung von (3-Methoxymethoxy-phenyl)-essigsäure-ethylester (31 ,2 g) in DMF (200 ml) wurden Natriumhydrid (6,21 g) und lodmethan bei 0 0C allmählich zugegeben. Nach 20 h Rühren bei 0 0C wurde diese Reaktionsmischung mit Wasser gelöscht. Diese Mischung wurde mit EtOAC extrahiert und die vereinigte organische Schicht wurde über Magnesiumsulfat getrocknet, filtriert und unter Vakuum konzentriert. Der resultierende Rückstand wurde auf Kieselgel (n- Hex: EtOAc=I 0:1 ) chromatographiert, um das Produkt als farbloses Öl zu erhalten.
d)
2-(3-Hydroxy-phenyl)-propionsäure-ethylester
Zu einer gerührten Lösung von 2-(3-Methoxymethoxy-phenyl)-propionsäure- ethylester in Dichlormethan wurde TFA (150 ml) bei 0 0C zugetropft. Die Reaktionsmischung wurde 1 h bei 0 0C gerührt und festes Natriumbicarbonat (200 g) wurde sehr langsam zugegeben. Die resultierende Mischung wurde sehr langsam in Eiswasser gegossen und mit EtOAc extrahiert. Die vereinigte organische Schicht wurde über Magnesiumsulfat getrocknet, filtriert und unter Vakuum konzentriert. Der resultierende Rückstand wurde auf Kieselgel (n-Hex:EtOAc=10:1 bis 4:1 ) chromatographiert, um das Produkt als farbloses Öl zu erhalten. (19,0 g, 70,4 %, 2 Schritte)
e)
2-(3-Hydroxy-4-nitro-phenyl)-propionsäure- ethylester Zu einer Lösung von 2-(3-Hydroxy-phenyl)-propionsäure-ethylester (19,0 g) in Essigsäure (150 ml) wurde Salpetersäure (11 ,3 g) bei Raumtemperatur zugegeben. Die Reaktionsmischung wurde 1 h bei Raumtemperatur gerührt und Wasser wurde dazu zugegeben. Die Mischung wurde mit EtOAc extrahiert und die
organische Schicht wurde über Magnesiumsulfat getrocknet, filtriert und unter Vakuum konzentriert. Der resultierende Rückstand wurde auf Kieselgel (n- Hex: EtOAc= 10:1 ) chromatographiert, um das Produkt als gelber Feststoff zu erhalten. (6,08 g, 26,0 %)
f)
2-(3-Hydroxy-4-nitro-phenyl)-propionsäure
Zu einer gerührten Lösung von 2-(3-Hydroxy-4-nitro-phenyl)-propionsäure- ethylester (1 ,48 mg) in 90 % wässrigem EtOH wurde NaOH (1 ,24 mg) bei Raumtemperatur zugegeben. Nach 14 h Rühren bei 45 0C wurde die Reaktionsmischung auf Raumtemperatur gekühlt und mit Wasser verdünnt. Die resultierende wässrige Schicht wurde mit Essigsäure angesäuert und anschließend mit Dichlormethan extrahiert. Die vereinigte organische Schicht wurde über Magnesiumsulfat getrocknet, filtriert und unter Vakuum konzentriert. (1 ,30 mg, 99,5 %, gelber Feststoff)
9)
2-(4-Amino-3-hydroxy-phenyl)-propionsäure
Zu einer gerührten Lösung von 2-(3-Hydroxy-4-nitro-phenyl)-propionsäure (1 ,28 g) in THF (20 ml) und EtOH (20 ml) wurde 10 % Pd/C (0,12 g) bei Raumtemperatur allmählich zugegeben. Nach 3 h Hydrierung mit H2 Rundkolben wurde die Reaktionsmischung über Kieselgur abfiltriert und mit EtOH gewaschen. Das Filtrat wurde unter Vakuum konzentriert, um das Produkt als gelber Feststoff zu erhalten. (1 ,08 g, 98,4 %)
h)
2-(2-Amino-benzoxazol-6-yl)-propionsäure
Zu einer gerührten Lösung von 2-(4-Amino-3-hydroxy-phenyl)-propionsäure (1 ,02 g) in H20 wurde BrCN (648 mg) bei Raumtemperatur zugegeben. Nach 40 h Rühren bei Raumtemperatur wurde die Reaktionsmischung mit 30 % wässrigem NaOH auf pH 6~7 neutralisiert und 1 h gerührt, Der Feststoff wurde filtriert, mit Wasser gewaschen und unter ermäßigtem Vakuum getrocknet um das Produkt als gelber Feststoff zu erhalten. (760 mg, 65,5 %)
Beispiel 18 - 2-(2-Amino-benzooxazol-6-yl)-N-(4-tert-butyl-benzyl)-propionamid
1H-NMR(CDCI3) δ 7.32-7.28 (m, 4H, Ar), 7.12-7.07 (m, 3H, Ar), 5.61 (bt, NH), 5.01 (bs, NH2), 4.37 (m, 2H, NHCH2), 3.63 (q, 1 H, J=7.1 Hz, COCH), 1.57 (d, 3H, J=7.2Hz, CHCH3), 1.29 (s, 9H, C(CH3)3)
Synthese von Beispielverbindung 19:
2-(4-Amino-3-hydroxy -phenyl)-propionsäure-ethylester
Zu einer gerührten Lösung des Ausgangsmaterials (4,63 g) in THF (50 ml) und EtOH (50 ml) wurde 10 % Pd/C (0,42 g) bei Raumtemperatur allmählich zugegeben. Nach 2 h Hydrierung mit H2 Rundkolben wurde die Reaktionsmischung über Kieselgur abfiltriert und mit EtOH gewaschen. Das Filtrat wurde unter Vakuum konzentriert. Der
resultierende Rückstand wurde auf Kieselgel (n-Hex:EtOAc=4:1 ) chromatographiert, um das Produkt als weißer oder hellrosa Feststoff zu erhalten. (3,86 g, 95, 1 %)
2-(2-Thioxo-2,3-dihydro-benzooxazol-6-yl)-propionsäure-ethylester Zu einer Lösung von 2-(4-Amino-3-hydroxy -phenyl)-propionsäure-ethylester (570 mg) in DMF (5 ml) wurde Phenylchlorthionoformiat (563 mg in DMF), und DBU (829 mg, in DMF) bei Raumtemperatur zugegeben. Die Reaktionsmischung wurde 14 h bei Raumtemperatur gerührt und Wasser wurde dem Gemisch zugegeben. Das resultierende Gemisch wurde mit Ethylether extrahiert. Die vereinigte organische Schicht wurde über Magnesiumsulfat getrocknet, filtriert und unter Vakuum konzentriert. Der resultierende Rückstand wurde auf Kieselgel (n-Hex: EtOAc=I 0:1 bis 4:1 ) chromatographiert, um das Produkt als gelbes Öl zu erhalten. (90 mg, 13,2 %)
2-(2-Thioxo-2,3-dihydro-benzooxazol-6-yl)-propionsäure Zu einer gerührten Lösung von 2-(2-Thioxo-2,3-dihydro-benzooxazol-6-yl)- propionsäure-ethylester (76 mg) in 90 % wässrigem EtOH wurde NaOH (48 mg) bei Raumtemperatur zugegeben. Nach 16 h Rühren bei Raumtemperatur wurde die Reaktionsmischung auf Raumtemperatur gekühlt und mit Wasser verdünnt. Die resultierende wässrige Schicht wurde mit Essigsäure angesäuert und anschließend mit Dichlormethan extrahiert. Die vereinigte organische Schicht wurde über Magnesiumsulfat getrocknet, filtriert und unter Vakuum konzentriert. (58 mg, 86,0 %, brauner Feststoff)
Beispiel 19 - N-(4-tert-Butyl-benzyl)-2-(2-thioxo-2,3-dihydro-benzooxazol-6-yl)- propionamid
1H-NMR(CDCI3) δ 7.36 (d, 2H, J=8.4Hz, Ar), 7.25 (d, 1 H1 J=1.5Hz, Ar), 7.20 (d, 2H,
J=8.3Hz, Ar), 7.13 (dd, 1 H, J=8.3, 1.5Hz, Ar), 6.79 (d, 1 H1 J=8.1 Hz, Ar), 6.09 (bt,
NH), 4.47 (m, 2H, NHCH2), 3.68 (q, 1 H, J=7.1 Hz, COCH)1 1.57 (d, 3H, J=7.1 Hz,
CHCH3), 1.29 (s, 9H, C(CH3)3)
IR 3300, 2962, 1645, 1496, 1418, 1362, 1150 crr ,f-1
Masse (FAB) m/z 369 [M+H]+
Synthese von Beispielverbindung 20:
a)
2-(3,4-Dihydro-2H-benzo[1 ,4]oxazin-7-yl)-propionsäure-ethylester Zu einer gerührten Lösung des Ausgangsmaterials (2,01 g) in DMF (25 ml) wurden Kaliumcarbonat (2,68 g) und 1 ,2-Dibromethan (1 ,90 g) bei Raumtemperatur zugegeben. Nach 3 h Rühren bei 140
0C wurde die Reaktionsmischung auf Raumtemperatur gekühlt und mit EtOAc verdünnt. Das resultierende Gemisch wurde mit Wasser gewaschen und die organische Schicht wurde über Magnesiumsulfat getrocknet, filtriert und unter Vakuum konzentriert. Der resultierende Rückstand wurde auf Kieselgel (n-Hex:EtOAc=4:1 ) chromatographiert, um das Produkt als braunes Öl zu erhalten. (265 mg, 11 ,7 %)
2-(3,4-Dihydro-2H-benzo[1 ,4]oxazin-7-yl)-propionsäure Zu einer gerührten Lösung von 2-(3,4-Dihydro-2H-benzo[1 ,4]oxazin-7-yl)- propionsäure-ethylester (258 mg) in THF (3 ml) und H2O (3 ml) wurde NaOH (134 mg) bei Raumtemperatur zugegeben. Nach 20 h Rühren bei Raumtemperatur wurde die Reaktionsmischung mit AcOH (pH = 4) angesäuert und mit Wasser verdünnt. Das resultierende Gemisch wurde mit Dichlormethan extrahiert und die vereinigte organische Schicht wurde über Magnesiumsulfat getrocknet, filtriert, und unter Vakuum konzentriert. Der resultierende Rückstand wurde auf Kieselgel (CH2CI2:MeOH=15:1 ) chromatographiert, um das Produkt als braunes Öl zu erhalten. (150 mg, 65,8 %)
Beispiel 20 - N-(4-tert-Butyl-benzyl)-2-(3,4-dihydro-2H-benzo[1,4]oxazin-7-yl)- propionamid
1H-NMR(CDCI3) δ 7.31 (d, 2H, J=8.4Hz, Ar), 7.10 (d, 2H1 J=8.2Hz, Ar), 6.70 (m, 2H,
Ar), 6.55 (d, 1 H, J=7.9Hz, Ar), 5.68 (bt, NH), 4.44-4.23 (m, 4H, OCH2 & NHCH2), 3.75
(bt, NH), 3.50-3.39 (m, 3H, NHCH2 & COCH), 1.50 (d, 3H, J=7.1 Hz, CHCH3), 1.30 (s,
9H, C(CH3)3)
IR 3304, 2963, 1649, 1516, 1357, 1305 cm 1
Masse (FAB) m/z 353 [M+H]+
Synthese von Beispielverbindung 21 :
2-(4-Amino-phenyl)-propionsäure
Zu einer gerührten Lösung von 2-(4-nitrophenyl)propionsäure (2,05 g) in THF (20 ml) und EtOH (20 ml) wurde 10 % Pd/C (0,21 g) langsam bei Raumtemperatur zugegeben. Nach 2 h Hydrierung mit H2 Rundkolben wurde die Reaktionsmischung über Kieselgur abfiltriert und mit EtOH gewaschen. Das Filtrat wurde unter Vakuum konzentriert, um das Produkt als hellbrauner Feststoff zu erhalten. (1 ,75 g, quantitativ)
2-Chinolin-6-yl-propionsäure
Das Gemisch 2-(4-Amino-phenyl)-propionsäure (1 ,70 g), FeSO47H2O (0,30 g), Glycerol (4,04 g) und Schwefelsäure (2 ml) wurde 5 h unter Rückfluss gerührt. Die Reaktionsmischung wurde auf Raumtemperatur gekühlt und anschließend unter ermäßigtem Vakuum konzentriert. Die wässrige Lösung wurde mit 12/V-NaOH- Lösung behandelt. Der feste Niederschlag wurde filtriert und das Filtrat wurde mit AcOH angesäuert. Das resultierende Gemisch wurde extrahiert und die vereinigte organische Schicht wurde über Magnesiumsulfat getrocknet, filtriert und unter Vakuum konzentriert. Der resultierende Rückstand wurde auf Kieselgel (CH2CI2:MeOH=15:1 zu 10:1 ) chromatographiert, um das Produkt als brauner Feststoff zu erhalten. (0,83 g, 40,0 %)
Beispiel 21 - N-(4-tert-Butyl-benzyl)-2-chinolin-6-yl-propionamid
1H-NMR(CDCI3) δ 8.89 (dd, 1 H, J=4.2, 1.4Hz, Ar), 8.10 (m, 2H, Ar), 7.74 (d, 1 H, J=1.8Hz, Ar), 7.67 (dd, 1 H, J=8.6, 1.8Hz, Ar), 7.41 (m, 1 H1 Ar), 7.29 (d, 2H, J=8.3Hz, Ar), 7.09 (d, 2H, J=8.1 Hz, Ar), 5.74 (bt, NH)1 4.39 (m, 2H1 NHCH2), 3.77 (q, 1 H, J=7.1 Hz, COCH), 1.64 (d, 3H1 J=7.1 Hz, CHCH3), 1.28 (s, 9H, C(CH3)3)
IR 3294, 2962, 1651 , 1544, 1366, 1232, 1117 cm -1
Synthese von Beispielverbindung 22:
Beispiel -22 - 2-(1H-Benzotriazol-5-yl)-N-(2-butoxy-6-tert-butyl-pyridin-3- ylmethyl)-propionamid
1H-NMR(CDCI3) δ 7.80 (m, 2H, Ar), 7.37-7.30 (m, 2H, Ar), 6.75 (d, 1 H1 J=7.5Hz, Ar),
6.24 (bt, NH)1 4.43-4.18 (m, 4H, OCH2 & CH2NH), 3.74 (q, 1 H, J=7.1 Hz, CHCH3),
1.61-1.52 (m, 5H, CHCH3 & OCH2CH2), 1.35 (m, 2H1 CH2CH3), 1.27 (s, 9H1 C(CH3)3),
0.90 (t, 3H, J=7.4Hz, CH2CH3)
IR 3300, 2960, 1648, 1543, 1457, 1413, 1255 crr ,ϊ-1
Masse (FAB) m/z 410 [M+H]\ 432 [M+Na]+
Beispielverbindung 23:
2-(1H-Benzoimidazol-5-yl)-N-(2-butoxy-6-tert-butyl-pyridin-3-ylmethyl)- propionamid
1H-NMR(CDCI
3) δ 8.00 (s, 1 H, Ar), 7.59 (m, 2H
1 Ar), 7.30 (d, 1 H, J=7.5Hz, Ar), 7.17 (dd, 1 H, J=8.3, 1.5Hz
1 Ar), 6.73 (d, 1 H, J=7.5Hz, Ar), 6.17 (bt, NH), 4.38-4.14 (m, 4H, OCH
2 & CH
2NH)
1 3.70 (q, 1 H, J=7.1 Hz, CHCH
3), 1.58-1.47 (m, 5H
1 CHCH
3 & OCH
2CH
2), 1.38-1.25 (m, 11 H, CH
2CH
3 & C(CH
3J
3), 0.89 (t, 3H
1 J=7.3Hz, CH
2CH
3) IR 3270. 2961 , 1650, 1544, 1456, 1412, 1357, 1254 cm
"1 Masse (FAB) m/z 409 [M+H]\ 431 [M+Na]
+
Beispielverbindung 24:
2-(1H-Benzotriazol-5-yl)-N-(6l-tert-butyl-4-methyl-3,4,5,6-tetrahydro-2H-
[1,2']bipyridinyl-3'-ylmethyl)-propionamid
1H-NMR(CDCI3+CD3OD) δ 7.77 (m, 2H1 Ar), 7.37-7.26 (m, 2H1 Ar), 6.85 (d, 1 H, J=7.7Hz, Ar), 4.40 (m, 2H, CH2NH), 3.75 (q, 1 H1 J=7.0Hz, CHCH3), 3.18 (m, 2H, Piperidin), 2.72 (m, 2H, Piperidin), 1.65-1.00 (m, 5H, Piperidin), 1.60 (d, 3H, J=7.1 Hz, CHCH3), 1.27 (s, 9H, C(CH3)3), 0.88 (d, 3H, J=6.6Hz, Piperidin CH3) IR 3300, 2956, 1646, 1565, 1450, 1371 , 1234 cm"1 Masse (FAB) m/z 435 [M+H]+
Beispielverbindung 25:
2-(1H-Benzoimidazol-5-yl)-N-(6l-tert-butyl-4-methyl-3,4,5,6-tetrahydro-2H-
[1,2']bipyridinyl-3'-ylmethyl)-propionamid
1H-NMR(CDCI3) δ 8.02 (s, 1H1 Ar), 7.60 (bs, 2H, Ar), 7.26-7.19 (m, 2H, Ar), 6.83 (d, 1 H, J=7.7Hz, Ar), 6.73 (bs, NH), 4.40 (m, 2H, CH2NH), 3.71 (q, 1 H, J=6.8Hz, CHCH3), 3.18 (m, 2H1 Piperidin), 2.69 (m, 2H1 Piperidin), 1.65-1.00 (m, 5H,
Piperidin), 1.60 (d, 3H, J=7.1 Hz, CHCH3), 1.27 (s, 9H, C(CH3)3), 0.88 (d, 3H1
J=6.6Hz, Piperidin CH3)
IR 3280, 2955, 1649, 1566, 1451 , 1401 , 1371 , 1252 cm'1
Masse (FAB) m/z 434 [M+H]+
Beispielverbindung 26:
2-(1H-Benzotriazol-5-yl)-N-(6-tert-butyl-2-cyclohexylsulfanyl-pyridin-3- ylmethyl)-propionamid
1H-NMR(CDCI3) δ 7.79 (bs, 2H, Ar), 7.36-7.30 (m, 2H, Ar), 6.88 (d, 1 H, J=7.9Hz, Ar),
6.29 (bt, NH), 4.36 (m, 2H, CH2NH), 3.92 (m, 1 H, SCH), 3.78 (q, 1 H1 J=7.1 Hz,
CHCH3), 2.05-1.20 (m, 1OH, Cyclohexyl), 1.60 (d, 3H, J=7.1 Hz, CHCH3), 1.28 (s, 9H,
C(CH3)3)
IR 3278, 2929, 2854, 1649, 1553, 1450, 1370, 1203, 734 cm'1
Masse (FAB) m/z 452 [M+H]+, 474 [M+Na]+
Beispielverbindung 27:
2-(1H-Benzoimidazol-5-yl)-N-(6-tert-butyl-2-cyclohexylsulfanyl-pyridin-3- ylmethyl)-propionamid
1H-NMR(CDCI3) δ 8.03 (s, 1 H, Ar), 7.60 (bs, 2H, Ar), 7.25 (m, 2H, Ar), 6.88 (d, 1 H,
J=7.7Hz, Ar), 5.94 (bt, NH), 4.28 (m, 2H, CH2NH), 3.92 (m, 1 H, SCH), 3.72 (q, 1 H,
J=7.3Hz, CHCH3), 2.01 (m, 2H, Cyclohexyl), 1.77-1.20 (m, 8H, Cyclohexyl), 1.59 (d,
3H, J=7.1 Hz, CHCH3), 1.29 (s, 9H, C(CH3)3)
IR 3270, 2928, 2854, 1652, 1554, 1449, 733 cm 1
Masse (FAB) m/z 451 [M+H]+, 473 [M+Na]+
Synthese von Beispielverbindung 29:
n-(2-Butyloxy-6-tert-butyl-pyridin-3-ylmethyl)-2-(2-ethylsulfanyl-2,3-dihydro- benzothiazol-6-yl)-Propionamid
Zu einer gerührten Lösung von dwk-1877 (146 mg) in Aceton wurden Diethylchlorphosphat (87 mg) und Kaliumcarbonat (111 mg) bei Raumtemperatur zugegeben. Nach 14 h Rückfluss wurde die Reaktionsmischung auf RT gekühlt. Die resultierende Mischung wurde mit Wasser verdünnt und mit EtOAc extrahiert. Die vereinigte organische Schicht wurde über Magnesiumsulfat getrocknet, filtriert und unter Vakuum konzentriert. Der resultierende Rückstand wurde auf Kieselgel (n- Hex:EtOAc=4:1 bis 2:1) chromatographiert, um das Produkt als weißer Feststoff zu erhalten. (122 mg, 78,7 %)
Beispiel 29: N-(2-Butoxy-6-tert-butyl-pyridin-3-ylmethyl)-2-(2-ethylsulfanyl- benzothiazol-6-yl)-propionamid
1H-NMR(CDCI3) δ 7.80 (d, 1 H, J=8.4Hz, Ar), 7.67 (d, 1 H, J=1.7Hz, Ar), 7.34 (d, 1 H,
J=7.5Hz, Ar), 7.29 (dd, 1 H, J=8.4, 1.8Hz, Ar), 6.76 (d, 1 H1 J=7.3Hz, Ar), 5.98 (bs,
NH), 4.35-4.13 (m, 4H, OCH2 & CH2NH), 3.63 (q, 1 H, J=7.1 Hz, CHCH3), 3.35 (q, 2H,
J=7.5Hz, SCH2CH3), 1.59-1.47 (m, 8H), 1.32 (m, 2H, CH2CH3), 1.28 (s, 9H, C(CH3)3),
0.90 (t, 3H, J=7.3Hz, CH2CH3)
IR 3296, 2960, 1648, 1543, 1450, 1412, 1254, 1002 cm"1
Masse (FAB) m/z 486 [M+H]+, 508 [M+Na]+
Synthese von Beispielverbindung 30:
2-(2-Methylsulfanyl-2,3-dihydrobenzothiazol-6-yl)-N-(4-methyl-6f-trifluormethyl- 3,4,5, 6-tetrahydro-2H-[1,2']bipyridinyl-3'-ylmethyl)-propionamid
Zu einer gerührten Lösung von dwk-1891 (188 mg) in Aceton wurden Dimethylchlorphosphat (92 mg) und Kaliumcarbonat (140 mg) bei Raumtemperatur zugegeben. Nach 14 h Rückfluss wurde die Reaktionsmischung auf RT gekühlt. Die resultierende Mischung wurde mit Wasser verdünnt und mit EtOAc extrahiert. Die vereinigte organische Schicht wurde über Magnesiumsulfat getrocknet, filtriert und unter Vakuum konzentriert. Der resultierende Rückstand wurde auf Kieselgel (n- Hex:EtOAc=2:1 ) chromatographiert, um das Produkt als weißer Feststoff zu erhalten. (164 mg, 84,9 %)
Beispiel 30: 2-(2-Methylsulfanyl-benzothiazol-6-yl)-N-(4-methyl-6'-trifluormethyl- 3,4,5, 6-tetrahydro-2H-[1,2']bipyridinyl-3'-ylmethyl)-propionamid
1H-NMR(CDCI3) δ 7.82 (d, 1 H, J=8.4Hz, Ar), 7.71 (d, 1 H, J=1.7Hz, Ar), 7.43 (d, 1 H1 J=7.9Hz, Ar), 7.32 (dd, 1 H, J=8.4, 1.8Hz, Ar), 7.16 (d, 1 H, J=7.7Hz, Ar), 6.19 (bt, NH), 4.45 (m, 2H, CH2NH), 3.70 (q, 1 H, J=7.1 Hz, CHCH3), 3.25 (m, 2H, Piperidin), 2.79 (s, 3H, SCH3), 2.76 (m, 2H, Piperidin), 1.70-1.05 (m, 5H, Piperidin), 1.60 (d, 3H, J=7.1 Hz, CHCH3), 0.92 (d, 3H, J=6.6Hz, Piperidin CH3) IR 3295, 2925, 1651 , 1540, 1453, 1177, 1136 cm 1 Masse (FAB) m/z 509 [M+H]+
Synthese von Beispielverbindung 32: a)
(4-Nitrophenyl)-essigsäure-ethylester
Zur Lösung von Ausgangsmaterial (3,42 g) in Ethanol (30 ml) wurde Schwefelsäure (0,3 ml) bei Raumtemperatur zugegeben. Das Reaktionsgemisch wurde 16 h unter Rückfluss gerührt und anschließend auf Raumtemperatur gekühlt. Ethanol wurde unter ermäßigtem Vakuum konzentriert und Wasser wurde zu dem Rückstand zugegeben. Die wässrige Schicht wurde mit EtOAc extrahiert mit und die organische Schicht wurde anschließend über Magnesiumsulfat getrocknet, filtriert und unter Vakuum konzentriert. Der resultierende Rückstand wurde auf Kieselgel (n- Hex:EtOAc=4:1 ) chromatographiert, um das Produkt als weißer Feststoff zu erhalten.
b)
2-(4-Nitrophenyl)-propionsäure-ethylester
Zu einer gerührten Lösung von (4-Nitrophenyl)-essigsäure-ethylester (3,88 g) in DMF (15 ml) wurden Natriumhydrid (0,78 g) und lodmethan (1 ,21 ml) bei O 0C langsam zugegeben. Nach 14 h Rühren bei Raumtemperatur wurde dieser Reaktionsmischung mit Wasser gelöscht. Dieses Gemisch wurde mit Diethylether extrahiert und die vereinigte organische Schicht wurde über Magnesiumsulfat getrocknet, filtriert und unter Vakuum konzentriert. Der resultierende Rückstand wurde auf Kieselgel (n-Hex:EtOAc=10:1 bis 4:1 ) chromatographiert, um das Produkt als hellgelbes Öl zu erhalten. (89,1 %)
C)
2-(4-Aminophenyl)-propionsäure-ethylester
Zu einer gerührten Lösung von 2-(4-Nitrophenyl)-propionsäure-ethylester (3,67 g) in THF (40 ml) und EtOH (40 ml) wurde 10 % Pd/C (405 mg) langsam bei Raumtemperatur zugegeben. Nach 20 h Hydrierung mit H2 Rundkolben wurde die Reaktionsmischung über Kieselgur abfiltriert und mit EtOAc gewaschen. Die organische Schicht wurde über Magnesiumsulfat getrocknet, filtriert und unter Vakuum konzentriert. Der resultierende Rückstand wurde auf Kieselgel (n- Hex:EtOAc=4:1 ) chromatographiert, um das Produkt als hellgelbes Öl zu erhalten. (99,7 %)
2-(4-Amino-3-brom-phenyl)-propionsäure-ethylester
Zu einer gerührten Lösung von 2-(4-Aminophenyl)-propionsäure-ethylester (3,16 g) in Aceton und Wasser wurden OXON (10,0 g) und NaBr (6,75 g) bei Raumtemperatur zugegeben. Nach 2 min Rühren bei Raumtemperatur wurde die Reaktionsmischung mit EtOAc verdünnt und in 5 % wässrige Na2S2Oa Lösung geschüttet. Die organische Schicht wurde über Magnesiumsulfat getrocknet, filtriert und unter Vakuum konzentriert. Der resultierende Rückstand wurde auf Kieselgel (n-Hex:EtOAc=6:1 ) chromatographiert, um das Produkt als weißer Feststoff zu erhalten. (49,6 %)
Kaliumethylxanthat DMF. reflux, 14 h
2-(2-Thioxo-2,3-dihydro-benzothiazol-6-yl)-propionsäure-ethylester
Zu einer gerührten Lösung von 2-(4-Amino-3-brom-phenyl)-propionsäure-ethylester (1 ,58 g) in DMF wurde Kaliumethylxanthat (1 ,86 g) bei Raumtemperatur zugegeben. Nach 14 h Rühren unter Rückfluss wurde die Reaktionsmischung auf Raumtemperatur gekühlt und mit EtOAc verdünnt. Die organische Schicht wurde mit Wasser und Salzwasser gewaschen, über Magnesiumsulfat getrocknet und unter Vakuum konzentriert. Der resultierende Rückstand wurde auf Kieselgel (n- Hex:EtOAc=6:1 bis 4:1 ) chromatographiert, um das Produkt als gelbes Öl zu erhalten. (595 mg, 38,3 %)
2-(2-Thioxo-2,3-dihydro-benzothiazol-6-yl)-propionsäure Zu einer gerührten Lösung von 2-(2-Thioxo-2,3-dihydro-benzothiazol-6-yl)- propionsäure-ethylester (587 mg) in THF (4 ml) und H2O (4 ml) wurde NaOH (229 mg) bei Raumtemperatur zugegeben. Nach 14 h Rühren bei Raumtemperatur wurde die Reaktionsmischung mit AcOH (pH = 4) gesäuert und mit Wasser verdünnt. Das resultierende Gemisch wurde mit Dichlormethan extrahiert und die vereinigte organische Schicht wurde über Magnesiumsulfat getrocknet, filtriert, und unter Vakuum konzentriert. (511 mg, 97 %, hellgelber Feststoff)
Beispiel 32 - N-(4-Methyl-6f-trifluormethyl-3,4,5,6-tetrahydro-2H-[1,2']bipyridinyl- 3'-ylmethyl)-2-(2-thioxo-2,3-dihydro-benzothiazol-6-yl)-propionamid
1H-NMR(CDCI3) 6 7.51 (d, 1 H, J=7.9Hz, Ar), 7.41 (d, 1 H, J=1.3Hz, Ar), 7.25-7.19 (m, 2H, Ar), 7.12 (d, 1 H, J=8.4Hz, Ar), 6.42 (bt, NH), 4.51 (m, 2H, CH2NH), 3.64 (q, 1 H, J=7.1 Hz, CHCH3), 3.31 (m, 2H, Piperidin), 2.81 (m, 2H, Piperidin), 1.78-1.10 (m, 5H, Piperidin), 1.57 (d, 3H, J=7.1 Hz, CHCH3), 0.96 (d, 3H, J=6.6Hz, Piperidin CH3)
IR 3300, 2924, 1650, 1534, 1472, 1416, 1332, 1177, 1136, 1035 cm 1 Masse (FAB) m/z 495 [M+H]+
Beispielverbindung 33:
N-(6l-tert-Butyl-4-methyl-3,4,5,6-tetrahydro-2H-[1,2']bipyridinyl-3l-ylmethyl)-2-(2- thioxo-2,3-dihydro-benzothiazol-6-yl)-propionamid
1H-NMR(CDCI3) δ 7.40-7.21 (m, 3H, Ar), 7.06 (d, 1 H, J=8.4Hz, Ar), 7.05 (bs, NH),
6.90 (d, 1 H, J=7.7Hz, Ar), 4.46 (m, 2H, CH2NH), 3.61 (q, 1 H, J=7.1 Hz, CHCH3), 3.25
(m, 2H, Piperidin), 2.83-2.71 (m, 2H, Piperidin), 1.75-1.50 (m, 3H, Piperidin), 1.55 (d,
3H, J=7.1 Hz, CHCH3), 1.30 (s, 9H, C(CH3)3), 1.30-1.10 (m, 2H, Piperidin), 0.95 (d,
3H, J=6.4Hz, Piperidin CH3)
IR 3295, 2923, 1647, 1536, 1475, 1400, 1034crτϊ1
Masse (FAB) m/z 483 [M+H]+
Beispielverbindung 34:
N-(6I-tert-Butyl-4-methyl-3,4,5,6-tetrahydro-2H-[1,2l]bipyridinyl-3'-ylmethyl)-2-(2- methylsulfanyi-benzothiazol-6-yi)-propionamid
1H-NMR(CDCI3) δ 7.80 (d, 1 H, J=8.3Hz, Ar), 7.72 (s, 1 H, Ar), 7.34-7.25 (m, 2H, Ar),
6.85 (d, 1 H, J=8.0Hz, Ar), 6.68 (bt, NH), 4.40 (m, 2H, CH2NH), 3.66 (q, 1 H, J=6.8Hz,
CHCH3), 3.18 (m, 2H, Piperidin), 2.79 (s, 3H, SCH3), 2.71 (m, 2H, Piperidin), 1.65-
1.40 (m, 6H, Piperidin & CHCH3), 1.28 (s, 9H, C(CH3)3), 1.20-1.00 (m, 2H, Piperidin),
0.89 (d, 3H, J=6.4Hz, Piperidin CH3)
IR 3293, 2955, 1648, 1543, 1450, 1238, 1013 cm"1
Masse (FAB) m/z 497 [M+H]+
Synthese von Beispielverbindung 35: a)
2-(4-Hydroxy-3-nitrophenyl)-propionsäure
Zu 2-(4-Hydroxyphenyl)-propionsäure (788 mg, 1 mmol) in CH3COOH (10 ml) wurde
60 % Salpetersäure (552 mg, 1 ,11 mmol) bei Raumtemperatur zugegeben.
Das Reaktionsgemisch wurde 1 h gerührt.
Eiswasser (50 ml) wurde der Reaktionsmischung zugegeben.
Das Gemisch wurde mit Essigsäureethylester extrahiert.
Die Extrakte wurden mit Wasser gewaschen, über Magnesiumsulfat getrocknet, filtriert und unter Vakuum konzentriert.
Der Rückstand wurde durch Flash-Säulen-Chromatographie mit CH2Cl2:MeOH) gereinigt.
Hellgelber Feststoff, Ausbeute: 86,9 %. b)
2-(3-Amino-4-hydroxyphenyl)-propionsäure
Zu einer Mischung aus 2-(4-Hydroxy-3-nitrophenyl)-propionsäure (810 g, 1 mmol) in
THF (20 ml) und EtOH (20 ml) wurde 10 % Pd/C (90 mg) langsam bei
Raumtemperatur zugegeben.
Die Reaktionsmischung wurde 3 h mit H2 Rundkolben bei 45 psi hydriert.
Das Gemisch wurde über Kieselgur abfiltriert und mit EtOH gewaschen.
Das Filtrat wurde unter Vakuum konzentriert.
Hellschwarzer Feststoff, Ausbeute: 99,2 %
C)
Referenz : DE 2 324 443
2-(2-Aminobenzoxazol-5-yl)-propionsäure
Zu einem Gemisch aus 2-(3-Amino-4-hydroxyphenyl)-propionsäure (630 mg, 1 mmol) in H2O (33 ml) wurde BrCN (383 mg, 1 ,04 mmol) bei Raumtemperatur zugegeben.
Die Reaktionsmischung wurde 40 h bei Raumtemperatur gerührt.
Die Reaktionsmischung wurde auf pH 6,7 mit 40 % wässrigem NaOH neutralisiert und filtriert.
Der Feststoff wurde mit 50 % wässrigem. MeOH umkristallisiert und filtriert.
Der Feststoff wurde im Vakuum getrocknet.
Hellbrauner Feststoff, Ausbeute: 48,8 %.
Beispiel 35 - 2-(2-Amino-benzooxazol-5-yl)-N-(4-methyl-6'-trifluormethyl-3,4,5,6- tetrahydro-2H-[1,2']bipyridinyl-3'-ylmethyl)-propionamid
1H-NMR(CDCI3) δ 7.43 (d, 1 H, J=7.5Hz, Ar), 7.28-6.97 (m, 4H, Ar), 6.09 (bt, NH), 5.35 (bs, NH2), 4.43 (d, 2H, J=5.7Hz, CH2NH), 3.68 (q, 1 H1 J=7.3Hz, CHCH3), 3.26 (m, 2H, Piperidin), 2.76 (m, 2H, Piperidin), 1.72-1.45 (m, 6H, Piperidin & CHCH3), 1.14 (m, 2H, Piperidin), 0.93 (d, 3H, J=6.4Hz, CHCH3) IR 3298, 2925, 1660, 1573, 1419, 1178, 1138, 951 cm"1 Masse (FAB) m/z 462 [M+H]+
Synthese von Beispielverbindung 36:
a)
2-(4-Aminophenyl)-propionsäure (1 )
2-(4-Nitrophenylpropionitril (6,03 g) wurde konz. Salzsäure (50 ml) bei
Raumtemperatur zugegeben.
Die Reaktionsmischung wurde 14 h unter Rϋckfluss gekocht.
Das Gemisch wurde auf Raumtemperatur gekühlt.
Das Gemisch wurde mit Dichlormethan extrahiert.
Die Extrakte wurden mit Wasser gewaschen, über Magnesiumsulfat getrocknet, filtriert und unter Vakuum konzentriert.
Hellgelber Feststoff, Ausbeute: quantitativ.
b)
2-(4-Nitrophenyl)-propionsäure-ethylester (2)
Eine Mischung von 1 (6,7 g, 1 mmol) in EtOH (100 ml) wurde bei Raumtemperatur gerührt.
Eine Schwefelsäure (0,5 ml; katalytische Menge) wurde langsam dem Gemisch zugegeben.
Die Reaktionsmischung wurde 15 h unter Rückfluss gekocht.
Das Gemisch wurde mit Essigsäureethylester extrahiert.
Die Extrakte wurden mit Wasser und Salzwasser gewaschen, über Magnesiumsulfat getrocknet, filtriert und unter Vakuum konzentriert.
Der Rückstand wurde durch Flash-Säulen-Chromatographie mit (n-Hexan: EtOAc) gereinigt.
Hellgelbes Öl, Ausbeute: 88 %.
2-(4-Aminophenyl)-propionsäure-ethylester (3)
Zu einer Lösung von 2 (6,7g, 1mmol) in THF (100ml) und EtOH (100ml) wurde 10 %
Pd/C (680 mg) langsam bei Raumtemperatur zugegeben.
Die Reaktionsmischung wurde 24 h mit H2 Rundkolben bei Raumtemperatur hydriert.
Das Gemisch wurde über Kieselgur abfiltriert und mit EtOH gewaschen.
Das Filtrat wurde unter Vakuum konzentriert.
Hellgelbes Öl, Ausbeute: 54 %
Referenz: Indian Journal of Chemistry, Vol. 16B, S. 605-609
2-(2-Aminobenzothiazol-6-yl)-propionsäure-ethylester (4)
Ein Gemisch aus 3 (3,13g, 1 mmol) in CH3COOH (15ml) wurde in einem Eisbad auf -
5 gekühlt.
Ein Gemisch aus KSCN (6,36 g, 4,04 mmol) in CH3COOH (15ml) wurde dem Kolben mit 4 und CH3COOH bei -5°C in einem Eisbad zugegeben.
Eine Lösung von Brom (0,80 ml) in CH3COOH (10 ml) wurde einem gerührten
Gemisch aus 4, KSCN und CH3COOH bei -50C in einem Eisbad zugetropft.
Die Reaktionsmischung wurde 1 h bei Raumtemperatur gerührt.
Das Gemisch wurde mit Essigsäureethylester extrahiert.
Die Extrakte wurden mit Wasser und Salzwasser gewaschen, über Magnesiumsulfat getrocknet, filtriert und unter Vakuum konzentriert.
Der Rückstand wurde durch Flash-Säulen-Chromatographie (n-Hexan: EtOAc) gereinigt.
Hellgelber Feststoff.
e)
2-(2-Acethlaminobenzthiazol-6-yl)-propionsäure-ethylester (5)
Ein Gemisch aus 4 (278 mg) in Essigsäureanhydrid (4 ml) wurde 3h unter Rückfluss gekocht.
Das Gemisch wurde auf Raumtemperatur gekühlt.
Wasser (30 ml) wurde dem Gemisch zugegeben und mit Essigsäureethylester extrahiert.
Die Extrakte wurden mit Wasser und Salzwasser gewaschen, über Magnesiumsulfat getrocknet, filtriert und unter Vakuum konzentriert.
Ausbeute: 88 %.
f)
2-(2-Acetylaminobenzothiazol-6-yl)-propionsäure (6)
Ein Gemisch aus 5 (276 mg, 1 mmol) in THF (10 ml) und H2O (10 ml) wurde bei
Raumtemperatur gerührt.
Natriumhydroxid (96 mg) wurde dem Gemisch zugegeben.
Die Reaktionsmischung wurde 15 h bei Raumtemperatur gerührt.
Die Reaktionsmischung wurde mit Essigsäure auf pH 3,4 angesäuert..
Wasser wurde dem Gemisch zugegeben und mit Dichlormethan extrahiert.
Die organische Schicht wurde über Magnesiumsulfat getrocknet, filtriert und unter
Vakuum konzentriert.
Hellgelber Feststoff, Ausbeute: 99,8 %.
Beispiel 35 - 2-(2-Acetylamino-benzothiazol-6-yl)-N-(4-tert-butyl-benzyl)- propionamid
1H-NMR(CDCI3) δ 11.17 (bs, NH), 7.78-7.68 (m, 2H, Ar), 7.42-7.21 (m, 3H, Ar), 7.11 (d, 2H, J=8.2Hz, Ar), 5.75 (bt, NH), 4.39 (m, 2H, CH2NH), 3.71 (q, 1 H, J=7.1 Hz, CHCH3), 2.27 (s, 3H, COCH3), 1.61 (d, 3H, J=7.1 Hz, CHCH3), 1.28 (s, 9H, C(CH3)3) IR 3298, 2963, 1649, 1548, 1462, 1369, 1275 cm 1 Masse (FAB) m/z 410 [M+H]+, 432 [M+Na]+
Beispielverbindung 37:
2-(2-Acetylamino-benzothiazol-6-yl)-N-(4-methyl-6'-trifluormethyl-3,4,5,6- tetrahydro-2H-[1,2']bipyridinyl-3'-ylmethyl)-propionamid
1H-NMR(CDCI3) δ 7.80-7.63 (m, 2H, Ar), 7.39 (m, 2H, Ar), 7.13 (d, 1 H, J=7.5Hz, Ar), 4.43 (m, 2H, CH2NH), 3.78 (m, 1 H, CHCH3), 3.30 (m, 2H, Piperidin), 2.79 (m, 2H, Piperidin), 2.31 (s, 3H, COCH3), 1.80-1.20 (m, 8H, CHCH3 & Piperidin), 0.94 (d, 3H, J=6.2Hz, Piperidin CH3)
IR 3189, 2923, 2455, 1644, 1548, 1458, 1418, 1372, 1335, 1270, 1175, 1135 cm"1 Masse (FAB) m/z 520 [M+H]+
Synthese von Beispielverbindung 38:
a)
2-(4-Aminophenyl)-propionsäure (1 )
2-(4-Nitrophenyl)-propionitril (6,03g) wurde zu konz. Salzsäure (50 ml) bei
Raumtemperatur zugegeben.
Die Reaktionsmischung wurde 14 h unter Rückfluss gekocht.
Das Gemisch wurde auf Raumtemperatur gekühlt.
Das Gemisch wurde mit Dichlormethan extrahiert.
Die Extrakte wurden mit Wasser gewaschen, über Magnesiumsulfat getrocknet, filtriert und unter Vakuum konzentriert.
Hellweißer Feststoff, Ausbeute: 99 %.
2-(4-Aminophenyl)-propionsäure (2)
Zu einer Mischung von 1 (6,7 g, 1 mmol) in THF (100ml) und EtOH (100 ml) wurde
10 % Pd/C (680 mg) langsam bei Raumtemperatur zugegeben.
Die Reaktionsmischung wurde 24 h mit H2 Rundkolben bei Raumtemperatur hydriert.
Das Gemisch wurde über Kieselgur abfiltriert und mit EtOH gewaschen.
Das Filtrat wurde unter Vakuum konzentriert.
Hellgelber Feststoff, Ausbeute: 99,8 %
Referenz: Indian Journal of Chemistry, Vol. 16B, S. 605-609
2-(2-Aminobenzthiazol-6-yl)-propionsäure (3)
Ein Gemisch aus 2 (3,13 g, 1 mmol) in CH3COOH (15 ml) wurde in einem Eisbad auf
-5 gekühlt.
Ein Gemisch aus KSCN (6,36 g, 4,04 mmol) in CH3COOH (15 ml) wurde dem Kolben mit 4 und CH3COOH bei -5 in einem Eisbad zugegeben.
Eine Lösung von Brom (0,80 ml) in CH3COOH (10 ml) wurde einem gerührten
Gemisch aus 4, KSCN und CH3COOH bei -5 in einem Eisbad zugetropft.
Die Reaktionsmischung wurde 1 h bei Raumtemperatur gerührt. Das Gemisch wurde mit Essigsäureethylester extrahiert. Die Extrakte wurden mit Wasser und Salzwasser gewaschen, über Magnesiumsulfat getrocknet, filtriert und unter Vakuum konzentriert.
Der Rückstand wurde durch Flash-Säulen-Chromatographie (n-Hexan: EtOAc) gereinigt.
Hellgelber Feststoff.
Synthese von Beispielverbindung 39:
a)
2-(4-Aminophenyl)-propionsäure (1 )
2-(4-Nitrophenyl)-propionitril (6,03 g) wurde bei Raumtemperatur zu konz. Salzsäure
(50 ml) zugegeben.
Die Reaktionsmischung wurde 14 h unter Rückfluss gekocht.
Das Gemisch wurde auf Raumtemperatur gekühlt.
Das Gemisch wurde mit Dichlormethan extrahiert.
Die Extrakte wurden mit Wasser gewaschen, über Magnesiumsulfat getrocknet, filtriert und unter Vakuum konzentriert.
Hellgelber Feststoff, Ausbeute: quantitativ.
b)
2-(4-Nitrophenyl)-propionsäure-ethylester (2)
Eine Mischung von 1 (6,7 g, 1 mmol) in EtOH (100 ml) wurde bei Raumtemperatur gerührt.
Eine Schwefelsäure (0,5 ml; katalytische Menge) wurde langsam dem Gemisch zugegeben.
Die Reaktionsmischung wurde 15 h unter Rückfluss gekocht.
Das Gemisch wurde mit Essigsäureethylester extrahiert.
Die Extrakte wurden mit Wasser und Salzwasser gewaschen, über Magnesiumsulfat getrocknet, filtriert und unter Vakuum konzentriert.
Der Rückstand wurde durch Flash-Säulen-Chromatographie (n-Hexan:EtOAc) gereinigt.
Hellgelbes Öl, Ausbeute: 88 %.
c)
2-(4-Aminophenyl)-propionsäure-ethylester (3)
Zu einer Mischung von 2 (6,7 g, 1 mmol) in THF (100 ml) und EtOH (100 ml) wurde
10 % Pd/C (680 mg) langsam bei Raumtemperatur zugegeben.
Die Reaktionsmischung wurde 24 h mit H2 Rundkolben bei Raumtemperatur hydriert.
Das Gemisch wurde über Kieselgur abfiltriert und mit EtOH gewaschen.
Das Filtrat wurde unter Vakuum konzentriert.
Hellgelbes Öl, Ausbeute: 54 %
d)
Referenz: Indian Journal of Chemistry, Vol. 16B, S 605-609
2-(2-Aminobenzothiazol-6-yl)-propionsäure-ethylester (4)
Ein Gemisch aus 3 (3,13 g, 1 mmol) in CH3COOH (15 ml) wurde in einem Eisbad auf
-5 gekühlt.
Ein Gemisch aus KSCN (6,36 g, 4,04 mmol) in CH3COOH (15 ml) wurde dem Kolben mit 4 und CH3COOH bei -5 in einem Eisbad zugegeben.
Eine Lösung von Brom (0,80 ml) in CH3COOH (10 ml) wurde bei -5 einem gerührten
Gemisch aus 4, KSCN und CH3COOH in einem Eisbad zugetropft.
Die Reaktionsmischung wurde 1 h bei Raumtemperatur gerührt.
Das Gemisch wurde mit Essigsäureethylester extrahiert.
Die Extrakte wurden mit Wasser und Salzwasser gewaschen, über Magnesiumsulfat getrocknet, filtriert und unter Vakuum konzentriert.
Der Rückstand wurde durch Flash-Säulen-Chromatographie (n-Hexan: EtOAc) gereinigt.
Hellgelber Feststoff.
e)
2-(2-Methansulfonylamino-benzothiazol-6-yl)-propionsäure-ethylester (5)
Ein Gemisch aus 4 (347 mg, 1 mmol) in Pyridin (3 ml) wurde zu MsCI (0,13 ml, 1 ,21 mmol) bei Raumtemperatur zugegeben.
Die Reaktionsmischung wurde 14 h bei Raumtemperatur gerührt.
1 N HCl (30 ml) wurde dem Gemisch zugegeben.
Das Gemisch wurde mit Essigsäureethylester extrahiert.
Die organische Schicht wurde über Magnesiumsulfat getrocknet.
Das Filtrat wurde unter Vakuum konzentriert.
Der Rückstand wurde durch Flash-Säulen-Chromatographie (n-Hexan:EtOAc) gereinigt.
Hellgelbes Öl, Ausbeute: 35 %. f)
2-(2-Methansulfonylamino-benzothiazol-6-yl)-propionsäure (6)
Ein Gemisch aus 5 (156 mg, 1 mmol) in THF (1OmI) und H2O (10 ml) wurde bei
Raumtemperatur gerührt.
Natriumhydroxid (50 mg, 2,5 mmol) wurde dem Gemisch zugegeben.
Die Reaktionsmischung wurde 15 h bei Raumtemperatur gerührt.
Die Reaktionsmischung wurde auf pH 3~4 mit Essigsäure angesäuert.
Wasser wurde dem Gemisch zugegeben und mit Dichlormethan extrahiert.
Die organische Schicht wurde über Magnesiumsulfat getrocknet, filtriert und unter
Vakuum konzentriert.
Ausbeute: quantitativ.
Synthese von Beispielverbindung 40: a)
2-(4-Aminophenyl)-propionsäure (1 )
2-(4-Nitrophenyl)-propionitril (6,03 g) wurde konz. Salzsäure (50 ml) bei
Raumtemperatur zugegeben.
Die Reaktionsmischung wurde 14 h unter Rückfluss gekocht.
Das Gemisch wurde auf Raumtemperatur gekühlt.
Das Gemisch wurde mit Dichlormethan extrahiert.
Die Extrakte wurden mit Wasser gewaschen, über Magnesiumsulfat getrocknet, filtriert und unter Vakuum konzentriert.
Hellgelber Feststoff, Ausbeute: quantitativ.
b)
2-(4-Nitrophenyl)-propionsäure-ethylester (2)
Eine Mischung von 1 (6,7 g, 1 mmol) in EtOH (100 ml) wurde bei Raumtemperatur gerührt.
Eine Schwefelsäure (0,5 ml; katalytische Menge) wurde langsam dem Gemisch zugegeben.
Die Reaktionsmischung wurde 15 h unter Rückfluss gekocht.
Das Gemisch wurde mit Essigsäureethylester extrahiert.
Die Extrakte wurden mit Wasser und Salzwasser gewaschen, über Magnesiumsulfat getrocknet, filtriert und unter Vakuum konzentriert.
Der Rückstand wurde durch Flash-Säulen-Chromatographie (n-Hexan:EtOAc) gereinigt.
Hellgelbes Öl, Ausbeute: 88 %.
2-(4-Aminophenyl)-propionsäure-ethylester (3)
Zu einer Mischung von 2 (6,7 g, 1 mmol) in THF (100 ml) und EtOH (100 ml) wurde
10 % Pd/C (680 mg) langsam bei Raumtemperatur zugegeben.
Die Reaktionsmischung wurde 24 h mit H2 Rundkolben bei Raumtemperatur hydriert.
Das Gemisch wurde über Kieselgur abfiltriert und mit EtOH gewaschen.
Das Filtrat wurde unter Vakuum konzentriert.
Hellgelbes Öl, Ausbeute: 54 %
d)
Referenz: Indian Journal of Chemistry, Vol. 16B1 S. 605-609
2-(2-Aminobenzothiazol-6-yl)-propionsäure-ethylester (4)
Ein Gemisch aus 4 (3,13 g, 1 mmol) in CH3COOH (15 ml) wurde in einem Eisbad auf
-5 gekühlt.
Ein Gemisch aus KSCN (6,36 g, 4,04 mmol) in CH3COOH (15 ml) wurde dem Kolben mit 4 und CH3COOH bei -5 in einem Eisbad zugegeben.
Eine Lösung von Brom (0,80 ml) in CH3COOH (10 ml) wurde einem gerührten
Gemisch aus 4, KSCN und CH3COOH bei -5 in einem Eisbad zugetropft.
Die Reaktionsmischung wurde 1 h bei Raumtemperatur gerührt.
Das Gemisch wurde mit Essigsäureethylester extrahiert.
Die Extrakte wurden mit Wasser und Salzwasser gewaschen, über Magnesiumsulfat getrocknet, filtriert und unter Vakuum konzentriert.
Der Rückstand wurde durch Flash-Säulen-Chromatographie (n-Hexan:EtOAc) gereinigt.
Hellgelber Feststoff.
2-(2-tert-Butoxycarbonylamino-benzthiazol-6-yl)-propionsäure-ethylester (5)
Ein Gemisch aus 4 (793 mg, 1 mmol) in 1 ,4-Dioxan wurde Boc2O (3,5 g, 5 mmol) und
TEA (2,21 ml, 5 mmol) bei Raumtemperatur zugegeben.
Die Reaktionsmischung wurde 14 h unter Rückfluss gekocht.
Das Gemisch wurde auf Raumtemperatur gekühlt.
Wasser wurde dem Gemisch zugegeben und mit Dichlormethan extrahiert.
Die organische Schicht wurde über Magnesiumsulfat getrocknet, filtriert und unter
Vakuum konzentriert.
Der Rückstand wurde durch Flash-Säulen-Chromatographie (n-Hexan:EtOAc) gereinigt.
Hellweißer Feststoff, Ausbeute: 22 %.
f)
2-(2-tert-Butoxycarbonylamino-benzothiazol-6-yl)-propionsäure (6)
Ein Gemisch aus 5 (239 mg, 1 mmol) in THF (10 ml) und H2O (10 ml) wurde bei
Raumtemperatur gerührt.
Natriumhydroxid (68,2 mg, 2,5 mmol) wurde dem Gemisch zugegeben.
Die Reaktionsmischung wurde 15 h bei Raumtemperatur gerührt.
Die Reaktionsmischung wurde auf pH 3-4 mit Essigsäure angesäuert.
Wasser wurde dem Gemisch zugegeben und mit Dichlormethan extrahiert.
Die organische Schicht wurde über Magnesiumsulfat getrocknet, filtriert und unter
Vakuum konzentriert.
Ausbeute: quantitativ.
Synthese von Beispielverbindung 44
1 /-/-lndazol-5-ylamin 5-lod-1 H-indazol
Zu einer auf 0 0C gekühlten Lösung von 1 H-indazol-5-amin (1 ,41 g, 10,6 mmol) in 6 N HCl (20 ml) wurde eine Lösung von NaNO2 (730 mg, 10,6 mmol) in Wasser (10 ml) zugetropft. Die resultierende Lösung wurde zu einer Lösung von Kl (7,3 g, 44 mmol) in Wasser (15 ml) zugegeben und die Temperatur wurde bei 0 0C gehalten. Der Reaktionsmischung wurde erlaubt, sich auf Raumtemperatur zu erwärmen und 3 h gerührt und anschließend mit Essigsäureethylester extrahiert. Die vereinigten Schichten wurden nacheinander mit 10 % Na2S2O3 und Salzwasser gewaschen,
anschließend über Na2SO4 getrocknet und unter Vakuum konzentriert, um einen hellbraunen Feststoff (1 ,90 g, 75 %) zu erhalten, der ohne weitere Reinigung im nächsten Schritt verwendet wurde.
5-lodo-1 H-indazole 2-(1 /-/-lndazol-5-yl)-malonic acid diethyl ester
Zu CuI (9.5 mg, 5.0 mol%), 2-Picolinsäure (12.3 mg, 10.0 mol%), Cs2CO3 (0.98 g, 3.0 mmol), und Arylioidid (1.0 mmol) in 1 ,4-Dioxan (10 ml) wurden destilliiertes Diethylmalonat (304 μL, 2.00 mmol) und 5-iodo-1 H-indazole (1.00 mmol) gegeben. Nach 7 stündigem Rühren bei 70 0C, wurde die Reaktionsmischung auf Raumtemperatur abgekühlt. Die Mischung wurde mit Ethylacetat (20 ml_ * 3) und mit gesättigter wässriger NH4CI (10 ml_) extrahiert/gewaschen. Die vereinigten organischen Phasen wurden über Na2SO4, filtriert und im Vakuum eingeengt. Der ölige Rückstand wurde durch Flashchromatograpie auf Silica gel gereinigt und das gewünschte Produkt als farbloses Öl (60%) erhalten.
c)
2-(7/-/-lndazol-5-yl)-malonsäurediethylester 2-( 7H-lndazol-5-yl)-2-methyl- malonsäurediethylester
Eine gekühlte Lösung von Diethyl-2-(1 H-indazol-5-yl)malonat (1 mmol) in DMF (10 ml) wurde bei 0 0C mit NaH (1.1 mmol) und MeI (1.2 mmol) behandelt und 30 min bei Raumtemperatur gerührt. Die Reaktionsmischung wurde unter Vakuum konzentriert und der Rückstand wurde durch Flash-Säulen-Chromatographie mit EtOAc:Hexanen (1 :4) als Eluent an Kieselgel gereinigt. (65%)
d)
2-("//-/-lndazol-5-yl)-2-methyl-malonsäurediethylester 2-(7H-lndazol-5-yl)-2- Propionsäure
Ein Gemisch aus Diethyl-2-(1 H-indazol-5-yl)-2-methylmalonat (1 mmol) und NaOH (2 mmol) in 80% wässriges EtOH (10 ml) wurde 6 h unter Rϋckfluss gekocht. Das Gemisch wurde mit 1 N HCl neutralisiert. Die Reaktionsmischung wurde mit Essigsäureethylester (20 ml * 3) extrahiert und unter Vakuum konzentriert. Der Rückstand wurde durch Flash-Säulen-Chromatographie mit EtOAc:Hexanen (1 :1 ) als Eluent an Kieselgel gereinigt. 53 %
e)
Ein Gemisch aus Säure (10 mmol), Amin (12 mmol) und 1-(3-Dimethylaminopropyl)- 3-ethyl-carbodiimidhydrochlorid (12 mmol) in DMF (20 ml) wurde 12 h bei Raumtemperatur gerührt. Die Reaktionsmischung wurde mit EtOAc (50 ml) extrahiert. Die wässrige Phase wurde mit NaCI gesättigt und nochmals mit EtOAc (25 ml) extrahiert. Die vereinigten organischen Extrakte wurden mit 1 N HCl (25 ml) und Salzwasser (25 ml) gewaschen, über MgSO4 getrocknet, filtriert und unter Vakuum konzentriert. Der Rückstand wurde durch Flash-Säulen-Chromatographie mit EtOAc:Hexanen (1 :2) als Eluent an Kieselgel gereinigt. 75%, weißer Feststoff, Schmelzpunkt = 113-115 0C
Synthese von Beispielverbindung 45:
3-Fluor-1 H-indazol-5-ylamin 3-Fluor-5-iodo-1H- indazol
Gemäß allgemeinem Verfahren 56% farbloses Öl
3-Fluor-5-iodo- 1 H-indazol 2-(3-Fluor-1 H-indazol-5-yl)- malonsäurediethylester
Gemäß allgemeinem Verfahren Farbloses Öl (60%)
2-(3-Fluor-1 H-indazol-5-yl)-malonsäurediethylester 2-(3-Fluor-1 H-indazol-5- yl)-2- methyl-malonsäurediethylester
Gemäß allgemeinem Verfahren Farbloses Öl (70%)
2-(3-Fluor-1 H-indazol-5-yl)-2- 2-(3-Fluor-1 H-indazol-5-yl)- propionsäure methyl-malonsäurediethylester
Gemäß allgemeinem Verfahren Farbloses Öl (53 %)
2-(3-Fluor-1 H-indazol-5-yl)-propionsäure 2-(3-Fluor-1 H-indazol-5-yl)-Λ/-((2-(4- methylpiperidin-1 -yl)-6-
Gemäß allgemeinem Verfahren
70%, weißer Feststoff, Schmelzpunkt = 123-127 0C
Synthese von Beispieiverbindung 46:
a)
1 /-/-lndazol-5-ylamin 5-lod-1H-indazol
Zu einer auf 0 0C gekühlten Lösung von 1H-lndazol-5-amin (1 ,41 g, 10,6 mmol) in 6 N HCl (20 ml) wurde eine Lösung von NaNO2 (730 mg, 10,6 mmol) in Wasser (10 ml) zugetropft. Die resultierende Lösung wurde zu einer Lösung von Kl (7,3 g, 44 mmol) in Wasser (15 ml) zugegeben und die Temperatur wurde bei 0 0C gehalten. Der
Reaktionsmischung wurde erlaubt, sich auf Raumtemperatur zu erwärmen, 3 h gerührt und anschließend mit Essigsäureethylester extrahiert. Die vereinigten Schichten wurden nacheinander mit 10% Na2S2O3 und Salzwasser gewaschen, anschließend über Na2SO4 getrocknet und unter Vakuum konzentriert, um einen hellbraunen Feststoff (1 ,90 g, 75%) zu erhalten, der ohne weitere Reinigung im nächsten Schritt verwendet wurde. b)
5-lod-1 H-indazol 2-(1H-lndazol-5-yl)-malonsäurediethylester
Zu CuI (9,5 mg, 5,0 mol%), 2-Picolinsäure (12,3 mg, 10,0 mol%), Cs2CO3 (0,98 g, 3,0 mmol), und Aryliodid (1 ,0 mmol) in 1 ,4-Dioxan (10 ml) wurde abdestilliertes Diethylmalonat (304 μl, 2,00 mmol) und 5-lod-1 H-indazol (1 ,00 mmol) zugegeben. Nach 7 h Rühren bei 70 0C wurde die Reaktionsmischung auf RT gekühlt. Die Reaktionsmischungen wurden mit Essigsäureethylester (20 ml * 3) und gesättigtem wässrigem NH4CI (10 ml) extrahiert. Die vereinigte organische Schicht wurde über Na2SO4 getrocknet, filtriert und unter Vakuum konzentriert. Der ölige Rückstand wurde durch Flash Chromatographie an Kieselgel gereinigt, um das gewünschte Produkt in Form eines farblosen Öls zu erhalten (60%). c)
2-(1H-lndazol-5-yl)-malonsäurediethylester 2-(1 H-lndazol-5-yl)-2-methyl- malonsäurediethylester
Eine gekühlte Lösung von Diethyl-2-(1 H-indazol-5-yl)malonat (1 mmol) in DMF (10 ml) bei 0 0C wurde mit NaH (1 ,1 mmol) und MeI (1 ,2 mmol) behandelt und 30 min bei Raumtemperatur gerührt. Die Reaktionsmischung wurde unter Vakuum konzentriert
und der Rückstand wurde durch Flash-Säulen-Chromatographie an Kieselgel mit
EtOAc:Hexanen (1 :4) als Eluent gereinigt. (65%) d)
wässriges EtOH, Rückfluss, 6h 2-(1 H-lndazol-5-yl)-2-methyl- 2-(1/-/-lndazol-5-yl)-propionsäure malonsäurediethylester
Ein Gemisch aus Diethyl-2-(1 H-indazol-5-yl)-2-methylmalonat (1 mmol) und NaOH (2 mmol) in 80% wässrigem EtOH (10 ml) wurde 6 h unter Rückfluss gekocht. Die Reaktionsmischung wurde mit 1 N HCl neutralisiert. Die Reaktionsmischung wurde mit Essigsäureethylester (20 ml x 3) extrahiert und unter Vakuum konzentriert. Der Rückstand wurde durch Flash-Säulen-Chromatographie mit EtOAc:Hexanen (1 :1 ) als Eluent an Kieselgel gereinigt. 53 %
e)
2-(7H-lndazol-5-yl)-2-propionsäure N-(2-Butoxy-6-terf-butyl-pridin- 3-ylmethyl)-2- (1 H-lndazol-5-yl)- propionamid
Gemäß allgemeinem Verfahren
60%, weißer Feststoff, Schmelzpunkt = 103-107 0C
Synthese von Beispielverbindung 48
1 /-/-lndazol-5-ylamin 5-lod-1 H-indazol
Zu einer auf O 0C gekühlten Lösung von 1 H-lndazol-5-amin (1 ,41 g, 10,6 mmol) in 6 N HCl (20 ml) wurde eine Lösung von NaNO2 (730 mg, 10,6 mmol) in Wasser (10 ml) zugetropft. Die resultierende Lösung wurde zu einer Lösung von Kl (7,3 g, 44 mmol) in Wasser (15 ml) zugegeben und die Temperatur wurde bei O CC gehalten. Der Reaktionsmischung wurde erlaubt, sich auf Raumtemperatur zu erwärmen, 3 h gerührt und anschließend mit Essigsäureethylester extrahiert. Die vereinigten Schichten wurden nacheinander mit 10% Na2S2Oa und Salzwasser gewaschen, anschließend über Na2SO4 getrocknet und unter Vakuum konzentriert, um das Produkt als hellbrauner Feststoff (1 ,90 g, 75%) zu erhalten, der ohne weitere Reinigung im nächsten Schritt verwendet wurde.
b)
1 ,4-Dioxan 5-lod-1 H-indazol 2-(1 H-lndazol-5-yl)-malonsäurediethylester
Zu CuI (9,5 mg, 5,0 mol%), 2-Picolinsäuren (12,3 mg, 10,0 mol%), Cs2CO3 (0,98 g, 3,0 mmol), und Aryliodid (1 ,0 mmol) in 1 ,4-Dioxan (10 ml) wurden abdestilliertes Diethylmalonat (304 μl, 2,00 mmol) und 5-lod-1 H-indazol (1 ,00 mmol) zugegeben. Nach 7 h Rühren bei 70 0C wurde die Reaktionsmischung auf RT gekühlt. Die Reaktionsmischungen wurden mit Essigsäureethylester (20 ml * 3) und gesättigtem wässrigem NH4CI (10 ml) extrahiert. Die vereinigte organische Schicht wurde über Na2SO4 getrocknet, filtriert und unter Vakuum konzentriert. Der ölige Rückstand
wurde durch Flash-Chromatographie auf Kieselgel gereinigt, um das gewünschte
Produkt in Form eines farblosen Öls (60%) zu erhalten c)
2-(1H-lndazol-5-yl)-malonsäurediethylester 2-(1 H-lndazol-5-yl)-2-methyl- malonsäurediethylester
Eine gekühlte Lösung von Diethyl-2-(1 H-indazol-5-yl)malonat (1 mmol) in DMF (10 ml) wurde bei 0 °C mit NaH (1 ,1 mmol) und MeI (1 ,2 mmol) behandelt und 30 min bei Raumtemperatur gerührt. Die Reaktionsmischung wurde unter Vakuum konzentriert und der Rückstand wurde durch Flash-Säulen-Chromatographie an Kieselgel mit EtOAc:Hexanen (1 :4) als Eluent gereinigt.(65%)
d)
2-(1 H-lndazol-5-yl)-2-methyl- 2-(1 /-/-lndazol-5-yl)-propionsäure malonsäurediethylester
Ein Gemisch aus Diethyl-2-(1 H-indazol-5-yl)-2-methylmalonat (1 mmol) und NaOH (2 mmol) in 80% wässrigem EtOH (10 ml) wurde 6 h unter Rückfluss gekocht. Die Mischung wurde mit 1 N HCl neutralisiert. Die Reaktionsmischung wurde mit Essigsäureethylester (20 ml x 3) extrahiert und unter Vakuum konzentriert. Der Rückstand wurde durch Flash-Säulen-Chromatographie mit EtOAc:Hexanen (1 :1 ) als Eluent an Kieselgel gereinigt. 53 %
e)
2-(1H-lndazol-5-yl)-propionsäure Λ/-(6-tert-Butyl-2- zyklohexylsulfanyl-pyridin- 3-ylmethyl)-2-1 H-indazol-5-yl)- propionamid
Gemäß allgemeinem Verfahren
76%, weißer Feststoff, Schmelzpunkt = 105-108 0C
Beispielverbindung 49:
N-(2-Butoxy-6-tert-butyl-pyridin-3-ylmethyl)-2-(2-thioxo-2,3-dihydro- benzothiazol-6-yl)-propionamid
1H-NMR(CDCI3) δ 7.38 (m, 2H, Ar), 7.21-7.03 (m, 2H, Ar), 6.79 (d, 1 H, J=7.5Hz, Ar),
6.16 (bs, NH), 4.33 (m, 4H, OCH2 & CH2NH), 3.58 (q, 1 H1 J=7.1 Hz, CHCH3), 1.65
(m, 2H1 OCH2CH2), 1.52 (d, 3H, J=7.1 Hz, CHCH3), 1.40 (m, 2H, CH2CH3), 1.30 (s,
9H, C(CH3)3), 0.95 (t, 3H, J=7.3Hz, CH2CH3)
IR 2958, 1648, 1537, 1475, 1405, 1254, 1033 cm"-1
Masse (FAB) m/z 458 [M+H]+
Synthese von weiteren Beispielverbindungen
Beispielverbindung 12: 2-(1H-Benzotriazol-5-yl)-N-(4-tert-butyl-benzyl)-propionamid
1H-NMR(CDCI3) δ 7.82 (m, 2H, Ar), 7.48 (dd, 1 H, Ar), 7.26 (d, 2H, J=8.4Hz, Ar), 7.08 (d, 2H, J=8.4Hz, Ar), 4.30 (s, 2H, NHCH2), 3.87 (q, 1 H, J=7.1 Hz, CHCH3), 1.54 (d, 3H, J=7.1 Hz, CHCH3), 1.26 (s, 9H, C(CH3)3) Masse (FAB) m/z 338 [M+H]+
a. 10% Pd/C, H2 THF/EtOH, 94%; b. Ac2O, Pyridin, 98%; c. Ac2O, HNO3 56%; d. konz. HCl, 88%; e. 10% Pd/C, H2 H2O/EtOH, 50%; f. 4-t-Butylbenzylamin, EDCI, HOBt, TEA, DMF, 70%; g. NaNO2, 5% aq. AcOH, quantitativ
Beispielverbindung 13:
2-(1H-Benzoimidazol-5-yl)-N-(4-methyl-6I-trifluormethyl-3,4,5,6-tetrahydro-2H-
[1,2']bipyridinyl-3'-ylmethyl)-propionamid
2-(3,4-Diamino-phenyl)-N-(4-methyl-6'-trifluormethyl-3,4,5,6-tetrahydro-2H-
[i ^'Jbipyridinyl-S'-ylmethyO-propionamid (48mg, 0.110mmol) wurde bei RT mit
Triethylorthoformiat (2mL) versetzt. Die Reaktionsmischung wurde 2 h unter
Rückfluss erhitzt und auf RT abgekühlt. Die Reaktionsmischung wurde mit Wasser versetzt und mehrfach mit DCM extrahiert. Die vereinigten organischen Phasen wurden über MgSO4 getrocknet und filtriert. Das Lösungsmittel wurde im Vakuum entfernt und der Rückstand wurde mittels Säulenchromatographie (DCM/MeOH 10:1 ) gereinigt.
1H-NMR(CD3OD) δ 8.16 (s, 1 H), 7.61-7.56 (m, 2H), 7.39 (d, 1 H, J=7.3Hz), 7.28 (dd,
1 H1 J=8.3, 1.7Hz), 7.08 (d, 1 H, J=7.7Hz), 4.46-4.27 (m, 2H), 3.84 (q, 1 H, J=7.0Hz),
3.37-3.30 (m, 2H), 2.81-2.70 (m, 2H), 1.65 (m, 2H), 1.54 (d, 3H, J=7.0Hz), 1.52-1.45
(m, 1 H), 1.32-1.21 (m, 2H), 0.94 (d, 3H, J=6.6Hz)
IR 3310, 2921 , 1650, 1539, 1457, 1418, 1134, 759 cm"1
Masse (FAB) m/z 447 [M+H]+
Beispielverbindung 14: 2-(1H-Benzoimidazol-5-yl)-N-(4-tert-butyl-benzyl)-propionamid
Die Verbindung wurde durch Umsetzung von N-(4-tert-Butylbenzyl)-2-(3,4- diaminophenyl)propanamid mit Triethylorthoformiat analog zur Beispielverbindung 13 erhalten.
1H-NMR(CD3OD) δ 8.13 (s, 1 H), 7.61-7.53 (m, 2H), 7.29-7.24 (m, 3H), 7.06 (d, 1 H, J=8.6Hz), 4.29 (s, 2H), 3.78 (q, 1 H, J=7.1 Hz), 1.52 (d, 3H1 J=7.1 Hz), 1.25 (s, 9H) IR 3272, 2965, 1649, 1515, 1266, 1113, 756 cm'1 Masse (FAB) m/z 337 [M+H]+
Die Beispielverbindungen 61-77 und 43-49 können ebenfalls nach den hierin beschriebenen Methoden erhalten werden.
Pharmakologische Daten
Die Affinität der erfindungsgemäßen Verbindungen für den Vanilloid-Rezeptor 1 (VR1/TRPV1 -Rezeptor) wurde wie vorstehend beschrieben bestimmt (Pharmakologische Methoden I bzw. II).
Die erfindungsgemäßen Verbindungen der vorstehend angegebenen Formel I weisen eine ausgezeichnet Affinität zum VR1/TRPV1 -Rezeptor auf (Tabelle 1.).
Tabelle 1.
ne bedeutet jeweils „no effect", d. h. es wurde keine Reaktion beobachtet.
Der Wert nach dem Zeichen „@" gibt die Konzentration an, bei der die Hemmung (in Prozent) jeweils bestimmt wurde.
Die Wirkung der erfindungsgemäßen Verbindung wurde ebenfalls im Formalin-Test (Pharmakologische Methoden IM) an der Maus bestimmt.