明 細 書 炭化水素化合物、 有機電界発光素子用材料および有機電界発光 素子 技術分野
本発明は、 有機電界発光素子および該発光素子に好適に使用で きる有機電界発光素子用材料ならびに新規な炭化水素化合物に関 する。 背景技術
従来、 無機電界発光素子は、 例えば、 バックライ トなどのパネ ル型光源として使用されてきたが、 該発光素子を駆動させるには 交流の高電圧が必要である。 最近になり、 発光材料に有機材料を 用いた有機電界発光素子 (有機エレク ト口ルミネッセンス素子 : 有機 E L素子) が開発された [App l . Phys . L e t t . , l, 91 3 ( 1 987) ]。 有機電界発光素子は、 発光機能を有する化合物を含む薄膜を、 陽 極と陰極間に挟持された構造を有し、 該薄膜に電子および正孔 ( ホール) を注入して、 再結合させることにより励起子 (エキシト ン) を生成させ、 この励起子が失活する際に放出される光を利用 して発光する素子である。 有機電界発光素子は、 数 V〜数十 V程 度の直流の低電圧で、 発光が可能であり、 また蛍光性有機化合物 の種類を選択することにより種々の色 (例えば、 赤色、 青色、 緑 色) の発光が可能である。 このような特徴を有する有機電界発光 素子は、 種々の発光素子、 表示素子等への応用が期待されている しかしながら、 一般に、 発光輝度が低く、 実用上十分ではない。 発光輝度を向上させる方法として、 発光層として、 例えば、 ト
リス ( 8 —キノ リ ノラー ト) アルミニウムをホス ト化合物、 クマ リ ン誘導体、 ピラン誘導体をゲス ト化合物 (ドーパント) として 用いた有機電界発光素子が提案されている [ J . App 1. Phys . , ϋ, 361 0 (1989)]。 また、 発光層の材料として、 アントラセン誘導体を用 いた有機電界発光素子が提案されている (特開平 8 — 1 2 6 0 0 号公報、 特開平 1 1 一 1 1 1 4 5 8号公報) 。 また、 発光層のゲ ス ト化合物として、 アントラセン誘導体を用いた有機電界発光素 子が提案されている (特開平 1 0 — 3 6 8 3 2号公報、 特開平 1 0 — 2 9 4 1 7 9号公報) 。
しかしながら、 これらの発光素子も充分な発光輝度、 発光寿命 を有しているとは言い難い。
現在では、 一層高輝度、 長寿命に発光する有機電界発光素子が 望まれている。 発明の開示
本発明の目的は、 発光効率に優れ、 高輝度、 長寿命に発光する 有機電界発光素子を提供することである。 また、 該発光素子に好 適に使用できる有機電界発光素子用材料を提供することである。 さらには、 新規な炭化水素化合物を提供することである。
本発明者等は、 有機電界発光素子に関して鋭意検討した結果、 本発明を完成するに到った。
すなわち、 本発明は、
( 1 ) アントラセン環とフルオレン環が直接結合している炭化水 素化合物、
( 2 ) フルオレン環が 9位以外の位置で結合している 1項に記載 の炭化水素化合物、
( 3 ) —般式 ( 1 ) で表される炭化水素化合物、
( - (A , ) k - ( F 2) , - ( A 2)m - ( F 3) n-X 2
( 1 )
(式中、 A iおよび A 2はそれぞれ独立に、 置換または未置換の アントラセンジィル基を表し、 F 2および F 3はそれぞれ独 立に、 置換または未置換のフルオレンジィル基を表し、 ェおよ び X 2はそれぞれ独立に、 水素原子、 ハロゲン原子、 直鎖、 分岐 または環状のアルキル基、 直鎖、 分岐または環状のアルコキシ基 置換または未置換のアミノ基、 置換または未置換のァリール基、 あるいは置換または未置換ァラルキル基を表し、 j 、 mおよび n は 0 または 1 を表し、 kおよび 1 は 1 または 2 を表し、 kが 2で あるとき八ェ同士は同一でも異なるものであってもよく 、 1 が 2 であるとき F 2同士は同一でも異なるものであってもよい。 )
( 4 ) kが 1である 3項に記載の炭化水素化合物、
( 5 ) 八 丄および A 2がアン トラセン一 9 , 1 0 —ジィル基であ り、 F x、 F 2および F 3がフルオレン一 2, 7 一ジィル基である
4項に記載の炭化水素化合物、
( 6 ) j および nが 0であり、 1 が 1であり、 k + mが 2である 3項に記載の炭化水素化合物、
( 7 ) 八 および A 2がアン トラセン一 9 , 1 0 —ジィル基であ り、 F 2がフルオレン— 2, 7 —ジィル基である 6項に記載の炭 化水素化合物、
( 8 ) j + 1 + nが 2であり、 kが 1であり、 mが 0である 3項 に記載の炭化水素化合物、
( 9 ) 八 丄がアン トラセン一 9 , 1 0 —ジィル基であり 、 F x、 F 2および F 3がフルオレン一 2, 7 —ジィル基である 8項に記 載の炭化水素化合物、
( 1 0 ) j 、 mおよび nが 0であり、 kおよび 1 が 1である 3項
に記載の炭化水素化合物、
( ェ 丄 八 がアン トラセン一 9, 1 0 —ジィル基であ り、 F 2 がフルオレン一 2, 7 一ジィル基である 1 0項に記載の炭化水素 化合物、
( 1 2 ) —般式 ( 2 ) で表される炭化水素化合物、
(式中、 R 2 および R 2 2はそれぞれ独立に、 水素原子、 直鎖、 分岐または環状のアルキル基、 置換または未置換のァリール基、 あるいは置換または未置換のァラルキル基を表し、 X 2 Q 1〜X 2 2 4はそれぞれ独立に、 水素原子、 ハロゲン原子、 直鎖、 分岐ま たは環状のアルキル基、 直鎖、 分岐または環状のアルコキシ基、 置換または未置換のアミノ基、 あるいは置換または未置換のァリ 一ル基を表す。 但し、 R 2 1、 R 2 2および X s o i X s s はアン トリル基およびフルォレニル基ではない。 )
( 1 3 ) X 2。 5および X 2 4がハロゲン原子、 直鎖、 分岐または 環状のアルキル基、 直鎖、 分岐または環状のアルコキシ基、 ある いは置換または未置換のァリール基である 1 2項に記載の炭化水 素化合物、
( 1 4 ) X 2。 5および X 2 4がハロゲン原子、 直鎖、 分岐または 環状のアルキル基、 直鎖、 分岐または環状のアルコキシ基、 ある いは置換または未置換の複素環式芳香族基である 1 2項に記載の 炭化水素化合物、
( 1 5 ) X 2 0 1 X 2 0 4 X 2 0 6 X 2 0 9 X 2 1 0 X 2 1 3
X 2ェ 5および X 2 i 8が水素原子、 ハロゲン原子、 直鎖、 分岐また は環状のアルキル基、 直鎖、 分岐または環状のアルコキシ基であ る 1 2項に記載の炭化水素化合物、
( 1 6 ) 一般式 ( 3 ) で表される炭化水素化合物、
(式中、 R 3 および R 3 2はそれぞれ独立に、 水素原子、 直鎖、 分岐または環状のアルキル基、 置換または未置換のァリール基、 あるいは置換または未置換のァラルキル基を表し、 A 3ェおよび A 3 2はそれぞれ独立に置換または未置換のァリール基を表し、 Z 3 1および Z 3 2はそれぞれ独立に、 水素原子、 ハロゲン原子、 直鎖、 分岐または環状のアルキル基、 直鎖、 分岐または環状のァ ルコキシ基、 あるいは置換または未置換のァリール基を表す。 )
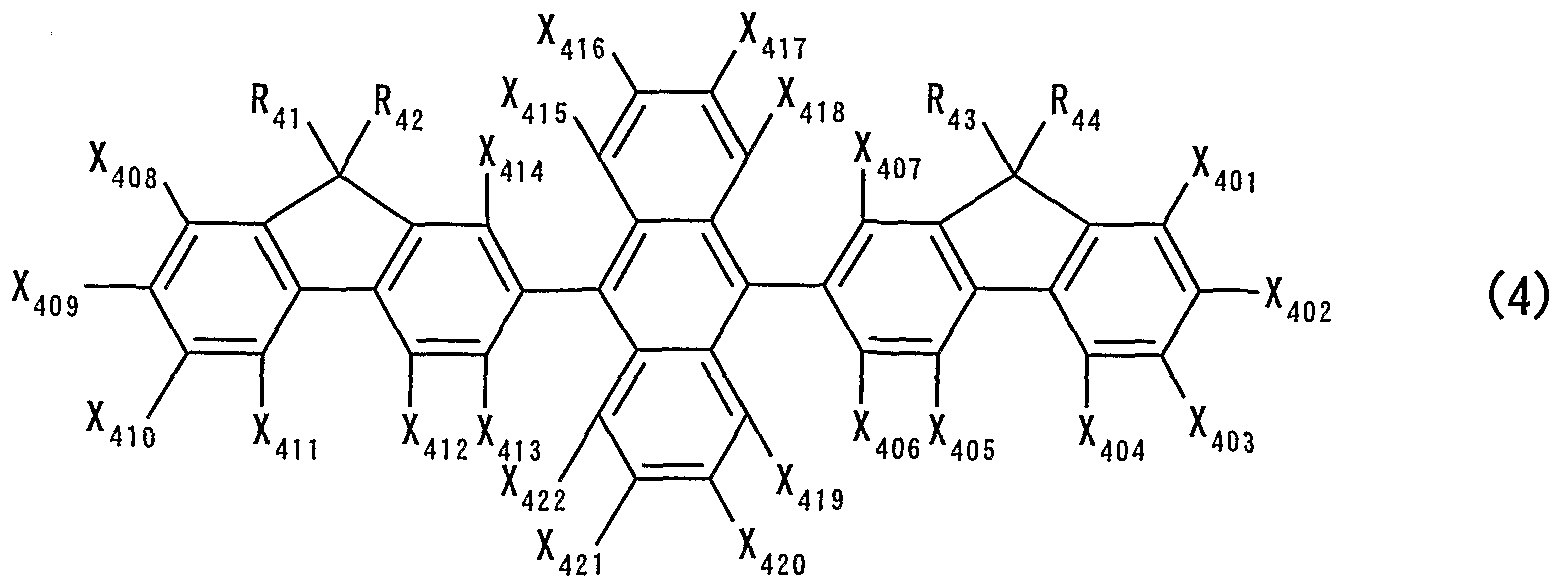
( 1 7 ) 一般式 ( 4 ) で表される炭化水素化合物、
(式中、 R R 4 4はそれぞれ独立に、 水素原子、 直鎖、 分岐 または環状のアルキル基、 置換または未置換のァリール基、 ある いは置換または未置換のァラルキル基を表し、 X 4 0 X 4 2 2は
それぞれ独立に、 水素原子、 ハロゲン原子、 直鎖、 分岐または環 状のアルキル基、 直鎖、 分岐または環状のアルコキシ基、 置換ま たは未置換のアミノ基、 あるいは置換または未置換のァリール基 を表す。 但し、 R R 44および X 4 0 X 4 2 2はアン 卜 リル 基およびフルォレニル基ではない。 )
( 1 8 ) X 4! 5 , X 4 Χ 8 , X 4 9および X 4 2 2が水素原子、 ノ\口 ゲン原子、 直鎖、 分岐または環状のアルキル基、 直鎖、 分岐また は環状のアルコキシ基である 1 7項に記載の炭化水素化合物。
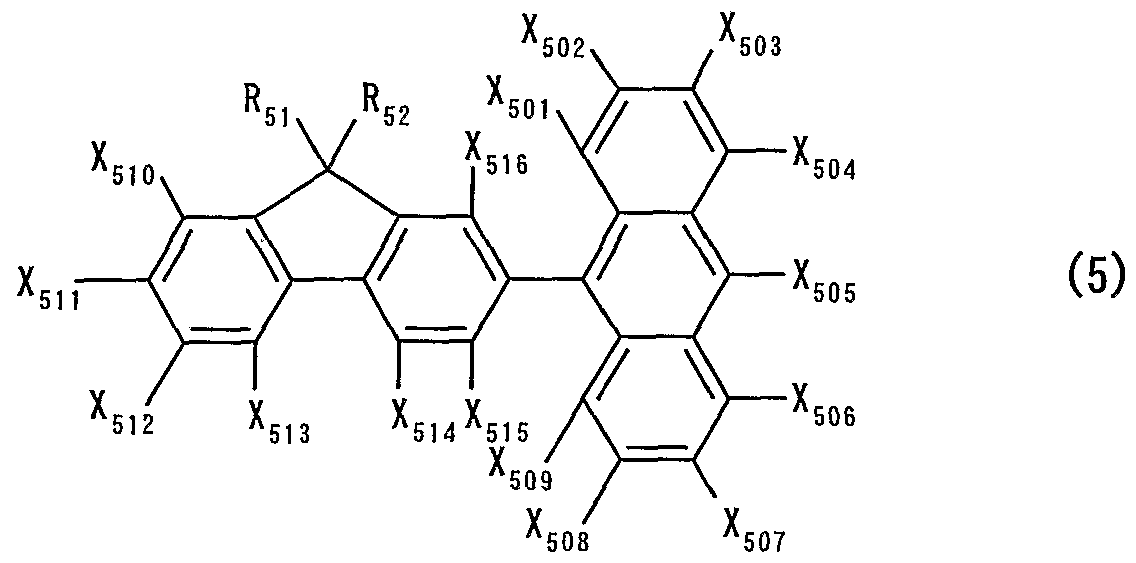
( 1 9 ) 一般式 ( 5 ) で表される炭化水素化合物、
(式中、 R 5 iおよび R 5 2はそれぞれ独立に、 水素原子、 直鎖、 分岐または環状のアルキル基、 置換または未置換のァリール基、 あるいは置換または未置換のァラルキル基を表し、 X 5 Q 1 〜 X 5 ェ 6はそれぞれ独立に、 水素原子、 ハロゲン原子、 直鎖、 分岐ま たは環状のアルキル基、 直鎖、 分岐または環状のアルコキシ基、 置換または未置換のアミノ基、 あるいは置換または未置換のァリ —ル基を表す。 但し、 R 5 1 、 R 5 2および X ^ X S はアン ト リル基およびフルォレニル基ではない。 )
( 2 0 ) X 5 Q 5が八ロゲン原子、 直鎖、 分岐または環状のアルキ ル基、 直鎖、 分岐または環状のアルコキシ基、 あるいは置換また は未置換のァリール基である 1 9項に記載の炭化水素化合物、
( 2 1 ) X 5。い X 5。 4、 X 5。 6および X 5。 9が水素原子、 ハロ ゲン原子、 直鎖、 分岐または環状のアルキル基、 直鎖、 分岐また は環状のアルコキシ基である 1 9項に記載の炭化水素化合物、
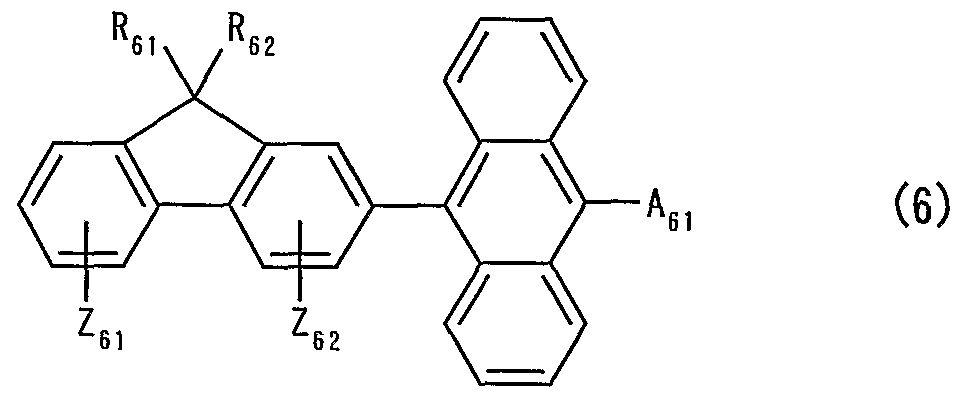
( 2 2 ) 一般式 ( 6 ) で表される炭化水素化合物、
(式中、 R 6ェおよび R 6 2はそれぞれ独立に、 水素原子、 直鎖、 分岐または環状のアルキル基、 置換または未置換のァリール基、 あるいは置換または未置換のァラルキル基を表し、 A 6 1は、 置 換または未置換のァリール基を表し、 Z 6ェおよび Z 6 2はそれぞ れ独立に、 水素原子、 ハロゲン原子、 直鎖、 分岐または環状のァ ルキル基、 直鎖、 分岐または環状のアルコキシ基、 あるいは置換 または未置換のァリール基を表す。 )
( 2 3 ) 1乃至 2 2項のいずれか 1項に記載の有機電界発光素子 用材料、
( 2 4 ) —対の電極間に、 2 3項に記載の有機電界発光素子用材 料を少なく とも一種含有する層を、 少なく とも一層挟持してなる 有機電界発光素子、
( 2 5 ) 2 3項に記載の有機電界発光素子用材料を含有する層が 発光層である 2 4項に記載の有機電界発光素子、
( 2 6 ) 2 3項に記載の有機電界発光素子用材料を含有する層が さ らに、 発光性有機金属錯体を含有することを特徴とする 2 4ま たは 2 5項に記載の有機電界発光素子、
( 2 7 ) 2 3項に記載の有機電界発光素子用材料を含有する層が
さ らに、 ト リアリールァミン誘導体を含有することを特徴とする 2 4または 2 5項に記載の有機電界発光素子、
( 2 8 ) 一対の電極間に、 さらに、 正孔注入輸送層を有する 2 4 乃至 2 7項のいずれか 1項に記載の有機電界発光素子、
( 2 9 ) 一対の電極間に、 さらに、 電子注入輸送層を有する 2 4 乃至 2 8項のいずれか 1項に記載の有機電界発光素子、 に関する ものである。 図面の簡単な説明
第 1〜 8図は、 それぞれ有機電界発光素子の概略を示す構造図 であり、 第 1 図は (A) 陽極/正孔注入輸送層 Z発光層 Z電子注 入輸送層 Z陰極型素子、 第 2図は、 (B ) 陽極/正孔注入輸送層 ノ発光層/陰極型素子、 第 3図は、 ( C ) 陽極/発光層 Z電子注 入輸送層 Z陰極型素子、 第 4図は、 (D) 陽極 Z発光層/陰極型 素子であり、 さ らには、 第 5図は、 発光層を電子注入輸送層で挟 み込んだ型の素子である (E) 陽極 Z正孔注入輸送層 Z電子注入 輸送層 Z発光層/電子注入輸送層 Z陰極型素子であり、.第 6図は (D ) 型の素子構成が発光成分を一層形態で一対の電極間に挟持 させた型の素子を包含するものであるが、 さ らには、 例えば、 ( F ) 正孔注入輸送成分、 発光成分および電子注入輸送成分を混 合させた一層形態で一対の電極間に挟持させた型の素子、 第 7図 は、 ( G) 正孔注入輸送成分および発光成分を混合させた一層形 態で一対の電極間に挟持させた型の素子、 第 8 図は、 (H) 発光 成分および電子注入輸送成分を混合させた一層形態で一対の電極 間に挟持させた型の素子である。
これらの図において、 符号は、 次の通である。
1 : 基板
2 : 陽極
3 : 正孔注入輸送層
3 a : 正孔注入輸送成分
4 • ¾¾ϋ
4 a : 発光成分
.• 雷 ¾子 j 、 < 八 7 *甲^刖 i <<S¾ )m
5 : 電子注入輸送層
5 a : 電子注入輸送成分
6 : 陰極
7 : 電源 発明を実施するための最良の形態
以下、 本発明に関して、 詳細に説明する。
本発明は、 アン トラセン環とフルオレン環が直接結合している 炭化水素化合物に関する。
本発明に係るアン トラセン環とフルオレン環が直接結合してい る炭化水素化合物 (以下、 本発明に係る化合物 Aと略記する) は 重合体を含むものではなく、 好ましくは、 分子量 2 0 0 0以下の 化合物であ り、 より好ましくは、 分子量 1 0 0 0以下の化合物で ある。
本発明に係る化合物 Aは、 好ましくは、 フルオレン環が 9位以 外の位置でアントラセン環に結合している化合物であり、 より好 ましくは、 一般式 ( 1 ) で表される化合物である。
X ( F j - (A j k - ( F 2) , - ( A 2)m - ( F 3) n-X 2
( 1 )
(式中、 八ェおよび A 2はそれぞれ独立に、 置換または未置換の アン トラセンジィル基を表し、 F 2および F 3はそれぞれ独
立に、 置換または未置換のフルオレンジィル基を表し、 およ び x 2はそれぞれ独立に、 水素原子、 八ロゲン原子、 直鎖、 分岐 または環状のアルキル基、 直鎖、 分岐または環状のアルコキシ基 置換または未置換のアミノ基、 置換または未置換のァリール基、 あるいは置換または未置換ァラルキル基を表し、 j 、 mおよび ]! は 0 または 1 を表し、 kおよび 1 は 1 または 2 を表し、 kが 2で あるとき 同士は同一でも異なるものであってもよく、 1 が 2 であるとき F 2同士は同一でも異なるものであってもよい。 ) 一般式 ( 1 ) で表される化合物において、 ェおよび X 2はそ れぞれ独立に、 水素原子、 ハロゲン原子、 直鎖、 分岐または環状 のアルキル基、 直鎖、 分岐または環状のアルコキシ基、 置換また は未置換のアミノ基、 置換または未置換のァリール基、 あるいは 置換または未置換ァラルキル基を表す。
尚、 ァリール基とは、 フエニル基、 ナフチル基などの炭素環式 芳香族基、 フリル基、 チェニル基、 ピリジル基などの複素環式芳 香族基を表す。
また、 一般式 ( 1 ) で表される化合物において、 X iおよび X 2のァミ ノ基は、 置換基を有していてもよく、 炭素数 1 〜 2 0 の アルキル基、 炭素数 3〜 2 0のァリール基、 あるいは、 炭素数 4 〜 2 0のァラルキル基などの置換基で単置換あるいはジ置換され ていてもよい。
また、 一般式 ( 1 ) で表される化合物において、 X iおよび X 2のァリール基およびァラルキル基は置換基を有していてもよく ハロゲン原子、 炭素数 1 〜 1 6 の直鎖、 分岐または環状のアルキ ル基、 炭素数 1 〜 1 6 の直鎖、 分岐または環状のアルコキシ基、 炭素数 1 〜 2 0 の N _モノ置換アミ ノ基、 炭素数 2〜 4 0の N, N —ジ置換アミノ基、 炭素数 3 〜 2 5 のァリール基、 炭素数 5 〜
1 6 のァラルキル基などの置換基で単置換あるいは多置換されて いてもよい。
X iおよび X 2は、 好ましく は、 水素原子、 ハロゲン原子、 炭 素数 1〜 1 6 の直鎖、 分岐または環状のアルキル基、 炭素数 1〜 1 6 の直鎖、 分岐または環状のアルコキシ基、 未置換のアミノ基 炭素数 1 〜 2 4の置換アミノ基、 炭素数 6〜 2 5の置換または未 置換の炭.素環式芳香族基、 炭素数 3〜 2 5 の置換または未置換の 複素環式芳香族基、 あるいは炭素数 5〜 1 6の置換または未置換 ァラルキル基であり、 より好ましく は、 水素原子、 ハロゲン原子 炭素数 1〜 1 0 の直鎖、 分岐または環状のアルキル基、 炭素数 1 〜 1 0 の直鎖、 分岐または環状のアルコキシ基、 炭素数 1〜 2 0 の置換アミノ基、 炭素数 6〜 1 2の置換または未置換の炭素環式 芳香族基、 炭素数 4〜 1 2 の置換または未置換の複素環式芳香族 基、 あるいは炭素数 7〜 1 2の置換または未置換ァラルキル基で あり、 さらに好ましくは、 水素原子、 ノ、ロゲン原子、 炭素数 1〜 8の直鎖、 分岐または環状のアルキル基、 炭素数 1 〜 8 の直鎖、 分岐または環状のアルコキシ基、 炭素数 2〜 2 0 の置換アミノ基 炭素数 6〜 1 0 の置換または未置換の炭素環式芳香族基、 炭素数 4〜 1 0の置換または未置換の複素環式芳香族基、 あるいは炭素 数 7〜 1 0 の置換または未置換ァラルキル基である。
Χ および X 2の具体例としては、 水素原子 ; フッ素原子、 塩 素原子、 臭素原子などのハロゲン原子 ; メチル基、 ェチル基、 n 一プロピル基、 イソプロピル基、 n—ブチル基、 イソブチル基、 sec—ブチル基、 tert—ブチル基、 n—ペンチル基、 イソペンチ ル基、 ネオペンチル基、 tert—ペンチル基、 シクロペンチル基、 n—へキシル基、 1 ーメチルペンチル基、 4ーメチルー 2 —ペン チル基、 3 , 3 —ジメチルブチル基、 2 —ェチルブチル基、 シク
口へキシル基、 n —ヘプチル基、 1 —メチルへキシル基、 シクロ へキシルメチル基、 4 一 t e r t—ブチルシクロへキシル基、 n —へ プチル基、 シクロへプチル基、 n—才クチル基、 シクロォクチル 基、 t e r t —ォクチル基、 1 一メチルヘプチル基、 2 —ェチルへキ シル基、 2 —プロピルペンチル基、 n —ノニル基、 2 , 2 —ジメ チルヘプチル基、 2, 6 —ジメチルー 4一へプチル基、 3 , 5 , 5 — ト リ メチルへキシル基、 n —デシル基、 n —ゥンデシル基、 1 ーメチ Jレデシ レ¾、 n — ドテシ Jレ 、 n— ト リアシリレ基、 1 一 へキシルヘプチル基、 n—テトラデシル基、 n —ペン夕デシル基 n —へキサデシル基、 n —ヘプ夕デシル基、 n —ォクタデシル基 n —エイコシル基などの直鎖、 分岐または環状のアルキル基 ; メ トキシ基、 エ トキシ基、 n —プロポキシ基、 イソプロポキシ基、 n —ブトキシ基、 イソブトキシ基、 s e c—ブトキシ基、 η _ペン チルォキシ基、 ネオペンチルォキシ基、 シクロペンチルォキシ基 η —へキシルォキシ基、 3, 3 —ジ チルブチルォキシ基、 2 — ェチルブチルォキシ基、 シクロへキシルォキシ基、 η —へプチル ォキシ基、 η 一才クチルォキシ基、 2 一ェチルへキシルォキシ基 η —ノニルォキシ基、 η —デシルォキシ基、 η —ゥンデシルォキ シ基、 η — ドデシルォキシ基、 η — ト リデシルォキシ基、 η —テ トラデシルォキシ基、 η —ペン夕デシルォキシ基、 η—へキサデ シルォキシ基、 η —へプタデシルォキシ基、 η—ォクタデシルォ キシ基、 η —エイコシルォキシ基などの直鎖、 分岐または環状の アルコキシ基 ; アミノ基、 Ν—メチルァミノ基、 Ν —ェチルアミ ノ基、 Ν— η —プチルァミノ基、 Ν —シクロへキシルァミノ基、 Ν— η —ォクチルァミノ基、 Ν— η —デシルァミノ基、 Ν —ベン ジルァミノ基、 Ν —フエニルァミノ基、 Ν— ( 3 —メチルフエ二 ル) アミ ノ基、 Ν— ( 4—メチルフエニル) アミノ基、 Ν— ( 4
— n —ブチルフエニル) アミ ノ基、 N— ( 4 — メ トキシフエ二 ル) アミ ノ基、 N— ( 3 — フルオロフェニル) アミ ノ基、 N— ( 4 一ク ロ口フエニル) アミ ノ基、 N— ( 1 —ナフチル) ァミ ノ 基、 N— ( 2 —ナフチル) アミ ノ基、 N, N—ジメチルァミ ノ基 N , N—ジェチルアミ ノ基、 N , N—ジ一 n—ブチルァミ ノ基、 N , N—ジ— n—へキシルァミ ノ基、 N, N—ジ一 n —ォクチル アミ ノ基、 N, N—ジ _ n —デシルァミ ノ基、 N, N—ジー n — ドデシルァミ ノ基、 N—メチル一 N—ェチルァミ ノ基、. N—ェチ ルー N— n —プチルァミ ノ基、 N _メチル— N—フエニルァミ ノ 基、 N— n —プチルー N—フエニルァミ ノ基、 N, N—ジフエ二 ルァミ ノ基、 N, N—ジ ( 3 —メチルフエニル) アミ ノ基、 N, N—ジ ( 4 _メチルフエニル) アミ ノ基、 N , N _ジ ( 4 ーェチ ルフエニル) アミ ノ基、 N , N—ジ ( 4 — tert—ブチルフエ二 ル) アミ ノ基、 N, N—ジ ( 4 — n —へキシルフェニル) ァミ ノ 基、 N, N—ジ ( 4 ーメ トキシフエ二ル) アミ ノ基、 N, N—ジ ( 4 一エ トキシフエニル) アミ ノ基、 N, N—ジ ( 4 — n —プチ ルォキシフエニル) アミ ノ基、 N , N—ジ ( 4 _ n —へキシルォ キシフエニル) アミ ノ基、 N, N—ジ ( 1 _ナフチル) アミ ノ基 N , N—ジ ( 2 —ナフチル) アミ ノ基、 N—フエ二ルー N— ( 3 一メチルフエニル) アミ ノ基、 N—フエニル— N— ( 4 一メチル フエニル) アミ ノ基、 N—フエ二ルー N— ( 4 一才クチルフエ二 ル) アミ ノ基、 N—フエニル一 N— ( 4 ーメ トキシフエニル) ァ ミ ノ基、 N—フエ二ルー N— ( 4 一エ トキシフエニル) アミ ノ基. N—フエ二ルー N— ( 4 一 n —へキシルォキシフエニル) ァミ ノ 基、 N—フエ二ルー N— ( 4 —フルオロフェニル) アミ ノ基、 N 一フエニル— N— ( 1 —ナフチル) アミ ノ基、 N—フエ二ルー N ― ( 2 —ナフチル) アミ ノ基、 N—フエ二ルー N— ( 4 —フエ二
ルフエ二ル) アミ ノ基などの置換または未置換のアミ ノ基 ; フエ ニル基、 4一メチルフエニル基、 3 _メチルフエニル基、 2 —メ チルフエニル基、 4一ェチルフエニル基、 3 —ェチルフエニル基 2 —ェチルフエニル基、 4 一 n—プロ ピルフエニル基、 4一イ ソ プロ ピルフエニル基、 2 —イソプロピルフエニル基、 4 一 n—ブ チルフエニル基、 4 _イ ソブチルフエニル基、 4 — s e c—ブチル フエニル基、 2 — sec—プチルフエ二ル基、 4 一 tert—ブチルフ ェニル基、 3 一 tert—ブチルフエニル基、 2 — tert—ブチルフエ エル基、 4― n—ペンチルフエ二ル基、 4一イ ソペンチルフエ二 ル基、 4一ネオペンチルフエ二ル基、 4一 tert—ペンチルフエ二 ル基、 4 一 n —へキシルフェニル基、 4 — ( 2 ' ーェチルブチ ル) フエニル基、 4 - n—ヘプチルフエニル基、 4一 n—ォクチ ルフエ二ル基、 4 一 ( 2 ' ーェチルへキシル) フエニル基、 4一 n— ノニルフエニル基、 4— n—デシルフェニル基、 4一 n—ゥ ンデシルフェニル基、 4 一 n — ドデシルフェニル基、 4 一 n —テ ト ラデシルフェニル基、 4 ー シク ロへキシルフェニル基、 4 — ( 4 ' ーメチルシク 口へキシル) フエニル基、 一 ( 4 , 一 tert ーブチルシク 口へキシル) フエニル基、 3 —シク ロへキシルフェ ニル基、 2 ーシク 口へキシルフェニル基、 2, 3 ージメチルフエ ニル基、 2 , 4—ジメチルフエニル基、 2 , 5 ージメチルフエ二 ル基、 2, 6 —ジメチルフエニル基、 3, 4ージメチルフエニル 基、 3, 5 —ジメチルフエニル基、 3, 4 , 5 — 卜 リ メチルフエ ニル基、 2 , 3 , 5 , 6 —テ トラメチルフエニル基、 2, 4—ジ ェチルフエニル基、 2 , 6 —ジェチルフエニル基、 2, 5 —ジィ ソプロピルフエニル基、 2 , 6 —ジイ ソプロピルフエニル基、 2 6 ージイソブチルフエニル基、 2 , 4 ージー t e r t—ブチルフエ二 ル基、 2, 5 —ジー tert—ブチルフエニル基、 4, 6 —ジ— tert
一プチルー 2 —メチルフエニル基、 5 — t e r t—ブチルー 2 ーメチ ルフエ二ル基、 4 一 t e —ブチル一 2, 6 —ジメチルフエニル基 1 一ナフチル基、 2 —ナフチル基、 1 , 2, 3 , 4ーテ トラヒ ド ロー 5 —ナフチル基、 1, 2 , 3 , 4 —テ トラヒ ドロー 6 —ナフ チル基、 4 —ェチルー 1 一ナフチル基、 6 — n—プチルー 2 —ナ フチル基、 5 —インダニル基、 4 —メ トキシフエニル基、 3 —メ トキシフエ二ル基、 2 —メ トキシフエ二ル基、 4 ーェ卜キシフエ ニル基、 3 —エトキシフエニル基、 2 —エ トキシフエニル基、 4 — n —プロピルォキシフエニル基、 3 — n—プロピルォキシフエ ニル基、 4 一イソプロピルォキシフエニル基、 2 一イソプロピル ォキシフエニル基、 4 - n 一ブチルォキシフエ二ル基、 4 一イソ ブチルォキシフエニル基、 2 _ s e c—ブチルォキシフエ二ル基、 4— n —ペンチルォキシフエニル基、 4 一イソべンチルォキシフ ェニル基、 2 —イソペンチルォキシフエニル基、 4 一ネオペンチ ルォキシフエニル基、 2 —ネオペンチルォキシフェニル基、 4 一 n 一へキシルォキシフエニル基、 4 一 ( 2 , —ェチルブチル) ォ キシフエニル基、 4 一 n—へプチルォキシフエ二ル基、 4 一 n— ォクチルォキシフエニル基、 4 一 n —ノニルォキシフエニリレ 、 4 — n —デシルォキシフエニル基、 4— n —ゥンデシルォキシフ ェニル基、 4— n— ドデシルォキシフエニル基、 4 一 n —テ 卜ラ デシルォキシフエニル基、 4—シクロへキシルォキシフエニル基 2 ーシクロへキシルォキシフエニル基、 2 , 3 —ジメ トキシフ X ニル基、 2 , 4—ジメ トキシフエ二ル基、 2, 5 ージメ 卜キシフ ェニル基、 3 , 4 —ジメ トキシフエ二ル基、 3 , 5 —ジメ 卜キシ フエニル基、 3, 5 —ジエトキシフエニル基、 2 ーメ トキシ一 4 一メチルフエニル基、 2 —メ トキシ一 5 —メチルフエ二ノレ基、 2 ーメチルー 4 ーメ トキシフエ二ル基、 3 —メチル一 4ーメ トキシ
フエニル基、 3 —メチル— 5 —メ トキシフエ二ル基、 2 —メ トキ シ— 1 一ナフチル基、 4 ーメ トキシー 1 一ナフチル基、 4 一 n— ブチルォキシ一 1 一ナフチル基、 5 —ェ トキシー 1 一ナフチル基 6 —メ トキシー 2 —ナフチル基、 6 —エ トキシー 2 —ナフチル基 6 一 n —ブチルォキシ一 2 —ナフチル基、 6 — n —へキシルォキ シ— 2 —ナフチル基、 7 —メ トキシ— 2 —ナフチル基、 7 — n— ブチルォキシ一 2 一ナフチル基、 4 — フエニルフエニル基、 3 一 フエニルフエニル基、 2 —フエニルフエニル基、 4 一 ( 4 , ーメ チルフエニル) フエニル基、 4― ( 3 , 一メチルフエニル) フエ ニル基、 4 一 ( 4 ' 一ェチルフエニル) フエニル基、 4— ( 4 , 一イソプロ ピルフエニル) フエニル基、 4 一 ( 4 , 一 t e r t—ブチ ルフエ二ル) フエニル基、 4 一 ( 4 , 一 n —へキシルフェニル) フエニル基、 4 ― ( 4 ' — n —才クチルフエニル) フエニル基、 4 一 ( 4 , ーメ トキシフエ二ル) フエニル基、 4 ― ( 4 , 一 n — ブチルォキシフエニル) フエニル基、 2 一 ( 2 , ーメ トキシフエ ニル) フエニル基、 4 - ( 4 , —ク ロ口フエニル) フエニル基、 3 —メチル一 4 一フエニルフエニル基、 3 —メ トキシー 4 —フエ ニルフエニル基、 9 一フエ二ルー 2 —フルォレニル基、 9 , 9 - ジフエ二ルー 2 一フルォレニル基、 9 ーメチルー 9 一フエ二ルー 2 一フルォレニル基、 9 —ェチル一 9 一フエ二ルー 2 一フルォレ ニル基、 4 _フルオロフェニル基、 3 —フルオロフェニル基、 2 一フルオロフェニル基、 4 一ク ロ口フエ二ル基、 3 —クロ口フエ ニル基、 2 —ク ロ口フエ二ル基、 4 一ブロモフエニル基、 2 —プ ロモフエニル基、 4 一 ト リ フルォロメチルフエニル基、 2, 3 — ジフルオロフェニル基、 2 , 4 —ジフルオロフェニル基、 2, 5 ージフルオロフェニル基、 2 , 6 —ジフルオロフェニル基、 3 , 4 ージフルオロフェニル基、 3, 5 —ジフルオロフェニル基、 2,
3 —ジク ロロフェニル基、 2, 4 ージク ロロフェニル基、 2, 5 ージク ロ口フエニル基、 3 , 4 —ジク ロ ロフ工ニル基、 3 , 5 — ジクロロフェニル基、 2, 5 —ジブロモフエニル基、 2 , 4 , 6 一 ト リ ク ロ 口フエニル基、 2 —フルオロ ー 4 一メチルフエニル基 2 —フルオロー 5 —メチルフエニル基、 3 —フリレオロー 2 —メチ ルフエ二ル基、 3 —フルオロー 4 —メチルフエニル基、 2 —メチ ルー 4 一フルオロフェニル基、 2 ーメチルー 5 —フルオロフェニ ル基、 3 _メチル— 4 一フルオロフェニル基、 2 —クロロー 4 — メチルフエニル基、 2 —ク ロ口— 5 —メチルフエニル基、 2 —ク ロロ一 6 —メチルフエニル基、 3 —クロ口— 4 —メチルフエニル 基、 2 —メチル— 3 _ク ロ口フエ二ル基、 2 —メチルー 4 —クロ 口フエニル基、 3 —メチルー 4 一ク ロ口フエ二ル基、 2 —ク ロ口 一 4 , 6 —ジメチルフエニル基、 2 , 4 —ジク ロ口 _ 1 一ナフチ ル基、 1, 6 —ジク ロロー 2 —ナフチル基、 2 —メ トキシ— 4 — フルオロフェニル基、 3 —メ トキシー 4 一フルオロフェニル基、 2 —フルオロー 4 —メ トキシフエ二ル基、 2 —フルオロー 4 ーェ トキシフエ二ル基、 2 —フルオロー 6 —メ トキシフエ二ル基、 3 一フルオロー 4 —メ トキシフエ二ル基、 3 —フルオロー 4 一エト キシフエニル基、 2 —ク ロ口— 4 ーメ トキシフエ二ル基、 3 —ク ロロ一 4 —メ トキシフエ二ル基、 2 —メ トキシー 5 —ク ロ口フエ ニル基、 3 —メ トキシー 4 —ク ロ口フエ二ル基、 3 —メ トキシ— 6 —ク ロ口フエ二ル基、 5 —ク ロ ロー 2 , 4 —ジメ トキシフエ二 ル基などの置換または未置換の炭素環式芳香族基 ; 4 一キノ リル 基、 3 —キノ リル基、 4 ーメチルー 2 —キノ リル基、 4 一ピリ ジ ル基、 3 — ピリ ジル基、 2 — ピリ ジル基、 4 一メチル— 2 — ピリ ジル基、 5 —メチルー 2 —ピリ ジル基、 6 —メチル— 2 — ピリ ジ ル基、 6 —フルオロー 3 —ピリ ジル基、 6 —メ トキシー 3 —ピリ
ジル基、 6 —メ トキシ— 2 —ピリジル基、 3 —フリル基、 2 —フ リル基、 3 —チェニル基、 2 —チェニル基, 4 一メチル— 3 —チ ェニル基、 5 —メチルー 2 —チェニル基、 3 —メチル— 2 —チェ ニル基、 2 —ォキサゾリル基、 2 —チアゾリル基、 2 —ベンゾォ キサゾリル基、 2 —ベンゾチアゾリル基、 2 —べンゾイミダゾリ ル基などの置換または未置換の複素環式芳香族基 ; ベンジル基、 フエネチル基、 α —メチルベンジル基、 a , a ージメチルベンジ ル基、 1 一ナフチルメチル基、 2 —ナフチルメチル基、 フルフリ ル基、 2 _メチルベンジル基、 3 一メチルベンジル基、 4 ーメチ ルベンジル基、 4 一ェチルベンジル基、 4 _イソプロピルベンジ ル基、 4 — t e r t—ブチルベンジル基、 4 一 n —へキシルベンジル 基、 4 一 n —ノエルべンジル基、 3 , 4 一ジメチルペンジル基、 3 —メ トキシベンジル基、 4ーメ トキシベンジル基、 4 一ェ卜キ シベンジル基、 4 一 n 一ブチルォキシベンジル基、 4 一 n —へキ シルォキシベンジル基、 4 - n —ノニルォキシベンジル基、 3 - フルォ口べンジル基、 4 —フルォ口べンジル基、 2 —クロ口ベン ジル基、 4 一クロ口べンジル基などの置換または未置換のァラル キル基などを挙げることができる。
一般式 ( 1 ) で表される化合物において、 Aェおよび A 2はそ れぞれ独立に、 置換または未置換のアン トラセンジィル基を表し F 1 , F 2および F 3はそれぞれ独立に、 置換または未置換のフル オレンジィル基を表す。
A! , A 2、 F 、 F 2および F 3が置換基を有する場合の置換 基としては、 例えば、 ハロゲン原子、 直鎖、 分岐または環状のァ ルキル基、 直鎖、 分岐または環状のアルコキシ基、 置換または未 置換のアミノ基、 置換または未置換のァリール基、 あるいは置換 または未置換のァラルキル基が挙げられる。
尚、 ァリール基とは、 フエニル基、 ナフチル基などの炭素環式 芳香族基、 フリル基、 チェニル基、 ピリ ジル基などの複素環式芳 香族基を表す。
A , , A 2、 F 2および F 3が置換基を有する場合の置換 基の具体例としては、 X iおよび X 2の具体例として挙げたハロ ゲン原子、 直鎖、 分岐または環状のアルキル基、 直鎖、 分岐また は環状のアルコキシ基、 置換または未置換のアミノ基、 置換また は未置換の炭素環式芳香族基、 置換または未置換の複素環式芳香 族基、 あるいは置換または未置換のァラルキル基を挙げることが できる。
および A 2は、 例えば、 置換または未置換のアントラセン 一 1 , 4 一ジィル基、 置換または未置換のアン トラセン— 1 , 5 一ジィル基、 置換または未置換のアントラセン一 1 , 8 —ジィル 基、 置換または未置換のアン トラセン一 1 , 9 一ジィル基、 置換 または未置換のアントラセン一 1 , 1 0 —ジィル基、 置換または 未置換のアントラセン— 2, 3 —ジィル基、 置換または未置換の アン トラセン一 2, 6 —ジィル基、 置換または未置換のアン トラ セン一 2 , 7 —ジィル基、 置換または未置換のアントラセン— 2 9 一ジィル基、 置換または未置換のアントラセン一 2, 1 0 —ジ ィル基、 置換または未置換のアン トラセン一 9 , 1 0 —ジィル基 であり、 好ましくは、 置換または未置換のアントラセン一 1 , 4 一ジィル基、 置換または未置換のアントラセン— 1, 5 —ジィル 基、 置換または未置換のアントラセン一 2, 6 —ジィル基、 置換 または未置換のアントラセン一 2, 7 —ジィル基、 置換または未 置換のアントラセン一 9 , 1 0 —ジィル基であり、 より好ましく は、 置換または未置換のアントラセン一 9 , 1 0 —ジィル基であ る。
F x , F 2および F 3は、 例えば、 置換または未置換のフルォレ ン— 1 , 3—ジィル基、 置換または未置換のフルオレン— 1 , 6 一ジィル基、 置換または未置換のフルオレン一 1, 7 —ジィル基 置換または未置換のフルオレン一 1 , 8—ジィル基、 置換または 未置換のフルオレン一 2, 6—ジィル基、 置換または未置換のフ ルオレン一 2 , 7—ジィル基、 置換または未置換のフルオレン— 3, 6—ジィル基であり、 好ましくは、 置換または未置換のフル オレン— 1 , 6—ジィル基、 置換または未置換のフルオレン— 1 7—ジィル基、 置換または未置換のフルオレン一 1, 8—ジィル 基、 置換または未置換のフルオレン一 2 , 6—ジィル基、 置換ま たは未置換のフルオレン一 2, 7—ジィル基、 置換または未置換 のフルオレン一 3 , 6—ジィル基であり、 より好ましくは、 置換 または未置換のフルオレン一 1 , 8—ジィル基、 置換または未置 換のフルオレン一 2 , 7—ジィル基、 置換または未置換のフルォ レン— 3, 6—ジィル基であり、 さ らに好ましくは、 置換または 未置換のフルオレン— 2, 7—ジィル基である。
一般式 ( 1 ) で表される化合物において、 j 、 mおよび nは 0 または 1 を表し、 kおよび 1 は 1または 2を表す。 好ましくは、 ① kが 1である、 ② j および nが 0であり、 1 が 1であり、 k + mが 2である、 ③ j + 1 + nが 2であり、 kが 1であり、 mが 0 である、 および④ j 、 mおよび nが 0であり、 kおよび 1が 1で ある場合を挙げることができる。
一般式 ( 1 ) で表される化合物は、 j 、 k 1 、 mおよび ηの 値により以下の構造に大別することができる
1 一 A i — F 2一入 2 ( l a )
X - — A, 一 F 2— 2 ( 1 b )
1 一 A〗 一 r 2— Α 2— Χ 2 ( 1 c )
X ,一 Α! F 2 F X ( I d )
X !一 A , A F X ( 1 e )
X !一 F A ! F A 一 ( I f )
X !一 F , A ! F F 一 ( 1 g )
X !一 F A ! A F 一 ( 1 h )
X !一 A F 2 F A 一 ( 1 i )
X 一 A A ! F A - X 2 ( Ί j )
X , - A A ! F F 一 ( I k )
X ,一 A F 2 F F 一 ( I I )
X 一 F A ! F A 一 F 一 ( 1 m)
X Λ一 F A , F F 一 A - X ( 1 n )
X 一 F A 1 A F 一 A ,一 X ( 1 o )
X F A ! A F F 2 ( 1 )
X A A , F F A - X ( 1 q )
X F A ! F F F 一 ( 1 r )
X λ - A A , F A _ F - X ( 1 s )
X 1一 A A ! F F 一 F - X 2 ( 1 t )
X F A ! A F - F 2一 2一 X ( 1 u )
X F A ! F F A 2 - F - X ( 1 v )
X - F Δ Δ 一 Δ ― F ( 1 w)
X ,一 F A ! A F ― 2 - F 一 X ( 1 x )
X 一 A A , F F 一 A 2一 F 一 X ( 1 y )
X 一 F A ! A F - F 2 - A 2一 F ( 1 z )
〔式中、 A A F F 2 F 3 X お
( 1 ) の場合と同じ意味を表す。 〕
これらの構造のうち、 好ましく は、 ( l a ) 、 ( l b ) , ( 1 c ) 、 ( I d ) , ( I f ) , ( l g ) 、 ( l i ) 、 ( 1 1 ) 、
( l m) 、 ( I n ) , ( l r ) 、 ( l v ) および ( l y ) で表さ れる構造であ り、 よ り好ましく は、 ( l a ) 、 ( l b ) , ( 1 c ) 、 ( I f ) , ( l g ) 、 ( l i ) 、 ( l m) 、 および ( 1 v ) で表される構造であり、 さ らに好ましく は、 ( l a ) 、 ( 1 b ) 、 ( 1 c ) および ( l m) で表される構造である。
さらに、 一般式 ( 1 ) で表される化合物の好ましい形態として は、 下記一般式 ( 2 ) 、 下記一般式 ( 4 ) および下記一般式
( 5 ) で表される化合物を挙げることができる。
(式中、 R 2 tおよび R 2 2はそれぞれ独立に、 水素原子、 直鎖、 分岐または環状のアルキル基、 置換または未置換のァリール基、 あるいは置換または未置換のァラルキル基を表し、 X 2 0 1 X
2 4はそれぞれ独立に、 水素原子、 ハロゲン原子、 直鎖、 分岐ま たは環状のアルキル基、 直鎖、 分岐または環状のアルコキシ基、 置換または未置換のアミ ノ基、 あるいは置換または未置換のァリ 一ル基を表す。 但し、 R
2 1、 R
2 2および X 2 0 X 2 2 4はアン ト リル基およびフルォレニル基ではない。 )
(式中、 R 4 1 R 4 4はそれぞれ独立に、 水素原子 直鎖、 分岐 または環状のアルキル基、 置換または未置換のァリール基、 ある いは置換または未置換のァラルキル基を表し、 x 4 0 1 X 4 2 2は それぞれ独立に、 水素原子、 ハロゲン原子、 直鎖、 分岐または環 状のアルキル基、 直鎖、 分岐または環状のアルコキシ基、 置換ま たは未置換のアミ ノ基、 あるいは置換または未置換のァリ一ル基 を表す。 但し、 R 4 1〜 R 4 4および X o i X s aはアン ト リル 基およびフルォレニル基ではない。 )
(式中、 R 5ェおよび R 5 2はそれぞれ独立に、 水素原子、 直鎖、 分岐または環状のアルキル基、 置換または未置換のァリール基、 あるいは置換または未置換のァラルキル基を表し、 X 5 0 1 X ェ 6はそれぞれ独立に、 水素原子、 ハロゲン原子、 直鎖、 分岐ま たは環状のアルキル基、 直鎖、 分岐または環状のアルコキシ基、 置換または未置換のアミノ基、 あるいは置換または未置換のァリ
—ル基を表す。 但し、 R 5 1 、 R 5 2および X ^ i X s はアン トリル基およびフルォレニル基ではない。 )
一般式 ( 2 ) 、 一般式 ( 4 ) および一般式 ( 5 ) で表される化 合物において、 R 2 丄 、 R 2 2 、 R 4 i〜 R 4 4、 R 5 丄および R 5 2は それぞれ独立に、 水素原子、 直鎖、 分岐または環状のアルキル基 置換または未置換のァリール基、 あるいは置換または未置換のァ ラルキル基を表す。 但し、 R 2 1 、 R 2 2 、 R 4 1 〜 R 4 4 、 R 5 1お よび R 5 2はアン トリル基およびフルォレニル基ではない。
尚、 ァリール基とは、 フエニル基、 ナフチル基などの炭素環式 芳香族基、 フリル基、 チェニル基、 ピリ ジル基などの複素環式芳 香族基を表す。
R 2 1 、 R 2 2 、 R 4 1 〜 R 4 4、 R 5 1および R 5 2は、 好ましく は 水素原子、 炭素数 1〜 1 6 の直鎖、 分岐または環状のアルキル基 炭素数 6〜 2 5 の置換または未置換の炭素環式芳香族基、 炭素数 3〜 2 5 の置換または未置換の複素環式芳香族基、 あるいは炭素 数 5〜 1 6 の置換または未置換ァラルキル基であり、 より好まし くは、 水素原子、 炭素数 1〜 1 0の直鎖、 分岐または環状のアル キル基、 炭素数 6 ~ 1 2の置換または未置換の炭素環式芳香族基 炭素数 4〜 1 2 の置換または未置換の複素環式芳香族基、 あるい は炭素数 7〜 1 2 の置換または未置換ァラルキル基であり、 さ ら に好ましく は、 水素原子、 炭素数 1 〜 8 の直鎖、 分岐または環状 のアルキル基、 炭素数 6〜 1 0 の置換または未置換の炭素環式芳 香族基、 炭素数 4〜 1 0の置換または未置換の複素環式芳香族基 あるいは炭素数?〜 1 0の置換または未置換ァラルキル基である R 2 1 、 R 2 2 、 R 4 1 〜 R 4 4 、 R 5 1および R 5 2の具体例として は、 水素原子、 または Xェおよび X 2の具体例として挙げた直鎖 分岐または環状のアルキル基、 置換または未置換の炭素環式芳香
族基、 置換または未置換の複素環式芳香族基、 あるいは置換また は未置換ァラルキル基を挙げることができる。
一般式 ( 2 ) 、 一般式 ( 4 ) および一般式 ( 5 ) で表される化 合物において、 X ^ i X ^ ^丄 〜 ^ぉょび ^ェ 〜 X 5ェ 6はそれぞれ独立に、 水素原子、 ハロゲン原子、 直鎖、 分岐 または環状のアルキル基、 直鎖、 分岐または環状のアルコキシ基 置換または未置換のアミノ基、 あるいは置換または未置換のァリ 一ル基を表す。 伹し、 X 2 () 1〜 X 2 2 4、 X^ Q i X sおよび X
5 0 1 〜 X 5 1 6はアントリル基およびフルォレニル基ではない。 尚、 ァリール基とは、 フエニル基、 ナフチル基などの炭素環式 芳香族基、 フリル基、 チェニル基、 ピリ ジル基などの複素環式芳 香族基を表す。
2。 1〜 2 2 4、 4。 1 ~ 4 2 2ぉょび入 5。 1〜 5 1 6 、 好 ましくは、 水素原子、 ハロゲン原子、 炭素数 1〜 1 6 の直鎖、 分 '岐または環状のアルキル基、 炭素数 1〜 1 6 の直鎖、 分岐または 環状のアルコキシ基、 炭素数 1 〜 2 4の置換アミ ノ基、 炭素数 6 〜 2 5 の置換または未置換の炭素環式芳香族基、 炭素数 3〜 2 5 の置換または未置換の複素環式芳香族基であり、 より好ましく は 水素原子、 ハロゲン原子、 炭素数 1 〜 1 0 の直鎖、 分岐または環 状のアルキル基、 炭素数 1〜 1 0 の直鎖、 分岐または環状のアル コキシ基、 炭素数 1〜 2 0 の置換アミノ基、 炭素数 6〜 1 2 の置 換または未置換の炭素環式芳香族基、 あるいは炭素数 4〜 1 2 の 置換または未置換の複素環式芳香族基であり、 さ らに好ましくは 水素原子、 ハロゲン原子、 炭素数 1 〜 8 の直鎖、 分岐または環状 のアルキル基、 炭素数 1〜 8 の直鎖、 分岐または環状のアルコキ シ基、 炭素数 2〜 2 0 の置換アミ ノ基、 炭素数 6〜 1 0 の置換ま たは未置換の炭素環式芳香族基、 あるいは炭素数 4〜 1 0 の置換
または未置換の複素環式芳香族基である。
X 2 0 1〜X 2 2 4、 4。 1〜∑ 4 2 2ぉょび 5。 1〜 5 1 6の具体 例としては、 水素原子、 または Xェおよび X 2の具体例として挙 げたハロゲン原子、 直鎖、 分岐または環状のアルキル基、 直鎖、 分岐または環状のアルコキシ基、 置換または未置換のアミノ基、 置換または未置換の炭素環式芳香族基、 置換または未置換の複素 環式芳香族基を挙げることができる。
一般式 ( 2 ) で表される化合物において、 好ましく は、 X 2。 5 および X 2 i 4がハロゲン原子、 直鎖、 分岐または環状のアルキル 基、 直鎖、 分岐または環状のアルコキシ基、 置換または未置換の ァリ一ル基である化合物、 および X 2 0 1、 X 2。 4、 X 2。 6、 X 2
0 9、 X 2 1 。、 X 2 1 3、 X 2 i 5および X 2 8が水素原子、 ハロゲ ン原子、 直鎖、 岐または環状のアルキル基、 直鎖、 分岐または 環状のアルコキシ基である化合物であり、 より好ましくは、 x 2 。 5および X 2 i 4がハロゲン原子、 直鎖、 分岐または環状のアル キル基、 直鎖、 分岐または環状のアルコキシ基、 置換または未置 換の複素環式芳香族基である化合物である。
一般式 ( 4 ) で表される化合物において、 好ましくは、 X 4 1 5 X 4 1 8、 X 4 9および X 4 2 2が水素原子、 ハロゲン原子、 直鎖、 分岐まだは環状のアルキル基、 直鎖、 分岐または環状のアルコキ シ基である化合物である。
一般式 ( 5 ) で表される化合物において、 好ましくは、 X 5。 5 がハロゲン原子、 直鎖、 分岐または環状のアルキル基、 直鎖、 分 岐または環状のアルコキシ基、 あるいは置換または未置換のァリ —ル基である化合物、 および X 5 0 1 、 X 5。 4、 X 5 Q 6および X 5 。 9が水素原子、 ハロゲン原子、 直鎖、 分岐または環状のアルキ ル基、 直鎖、 分岐または環状のアルコキシ基である化合物である
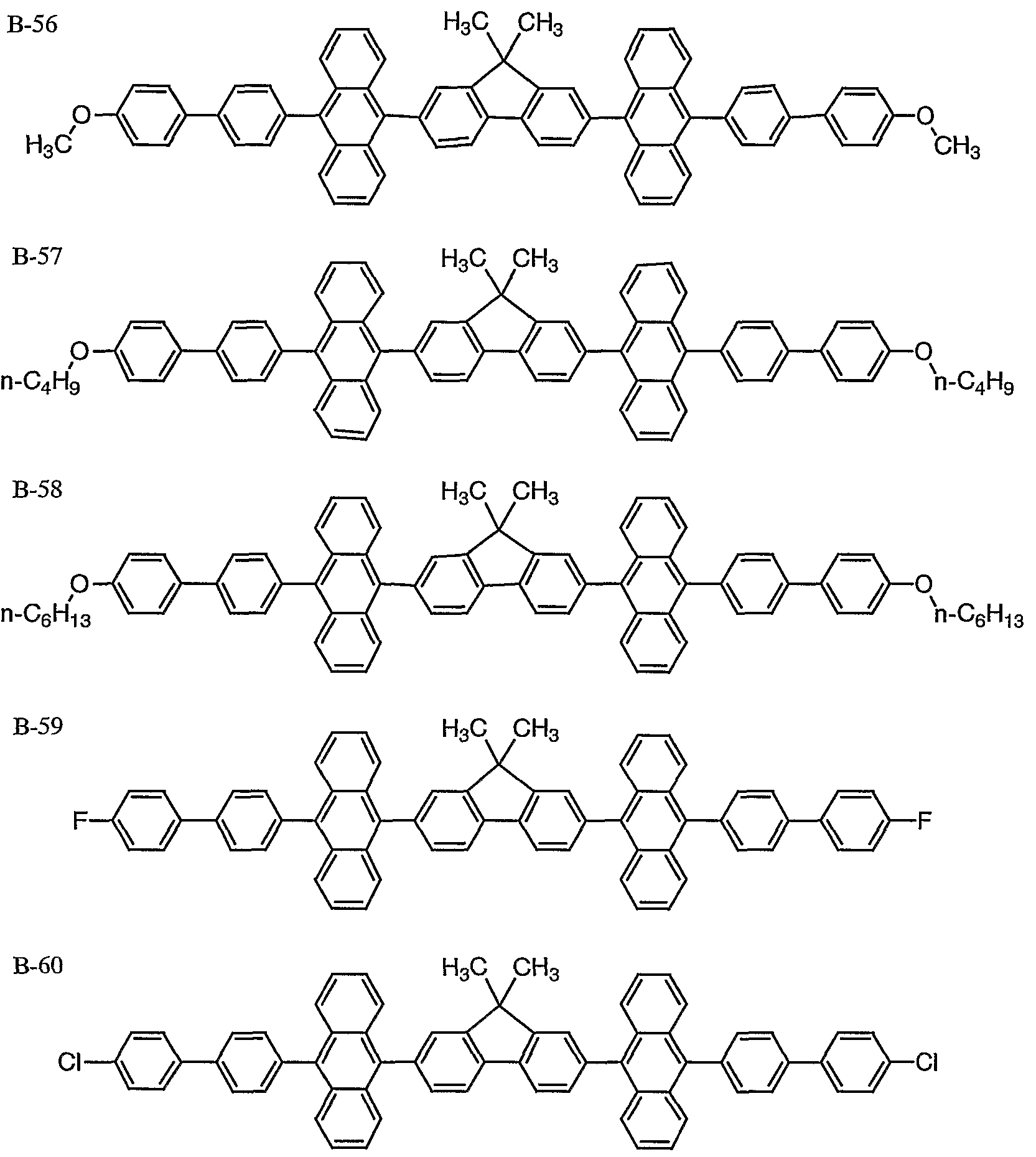
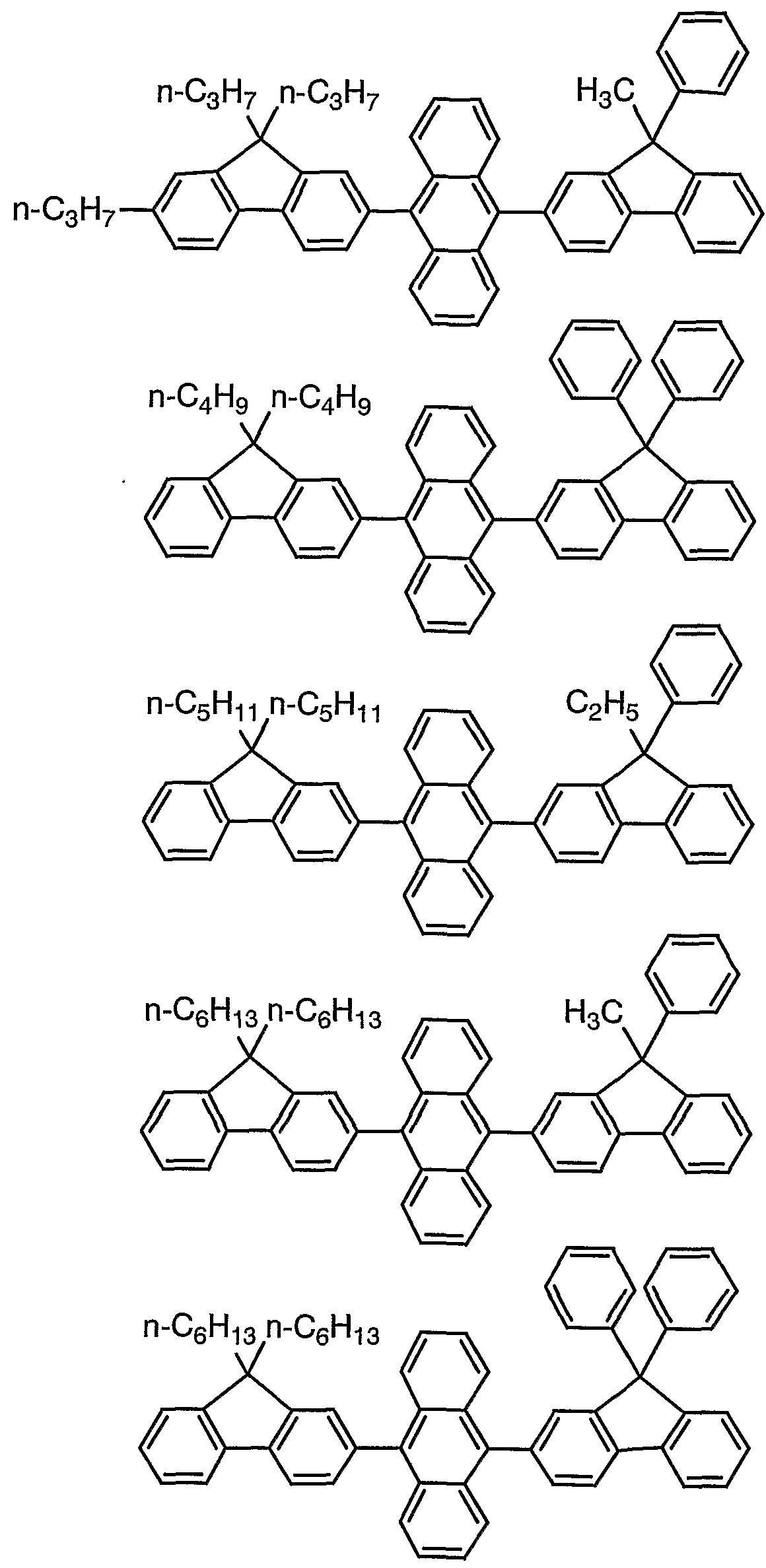
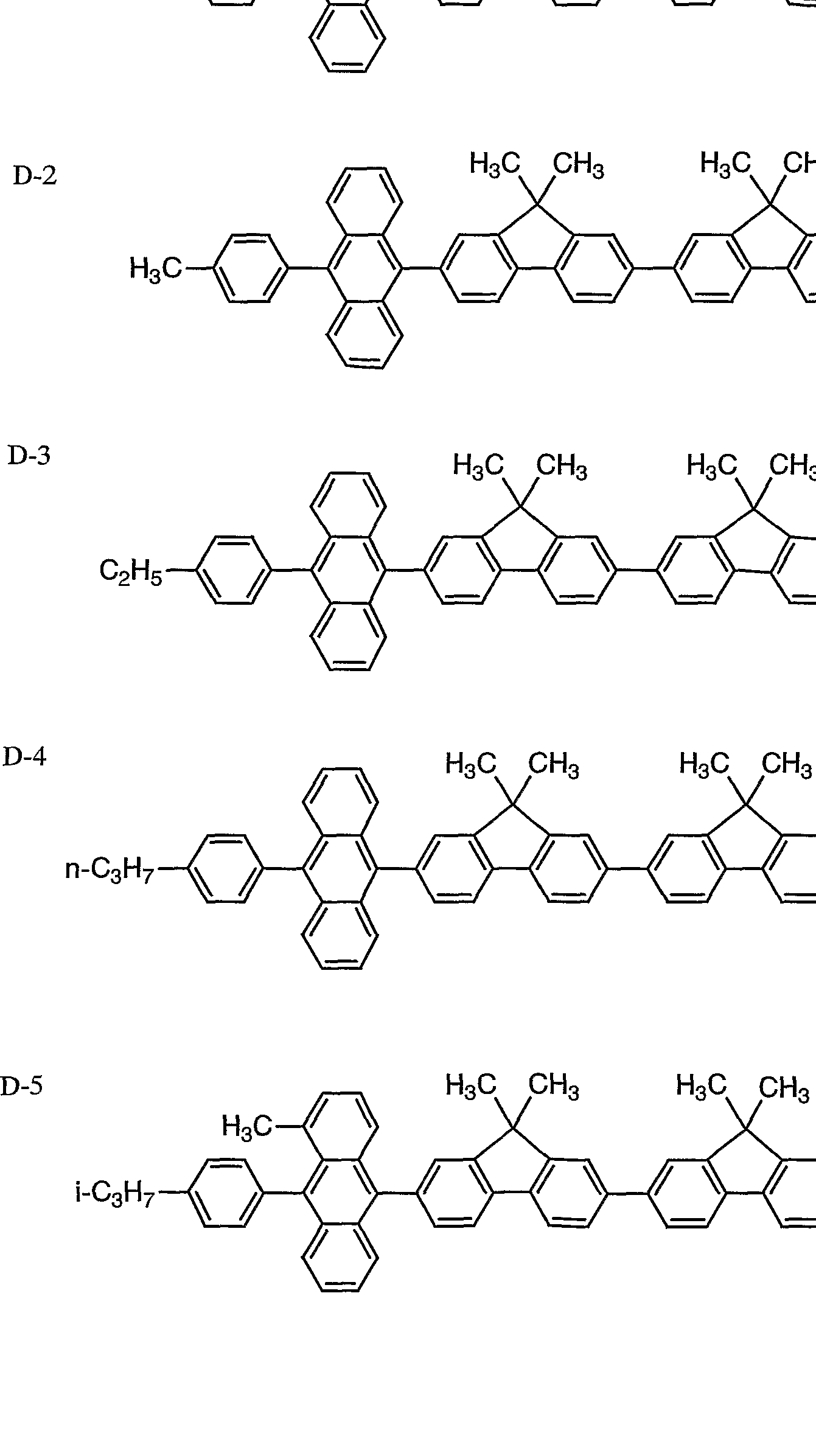
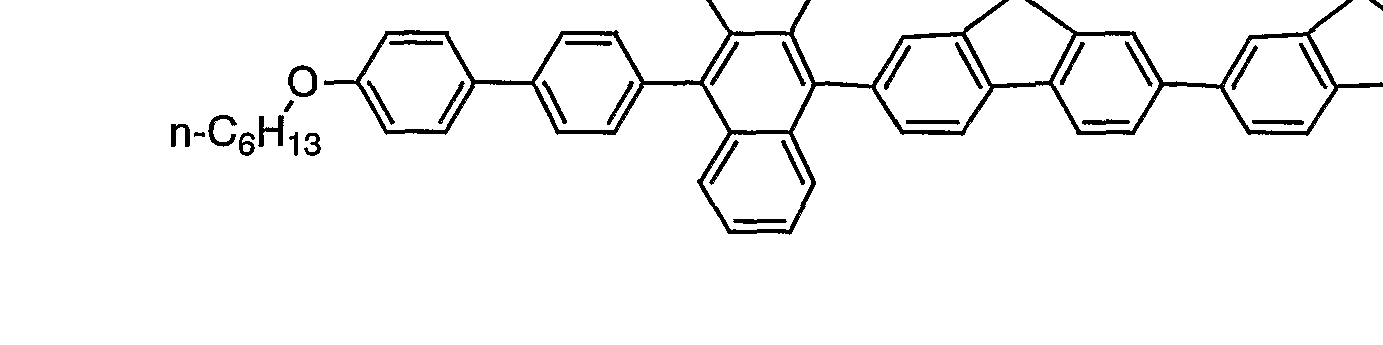
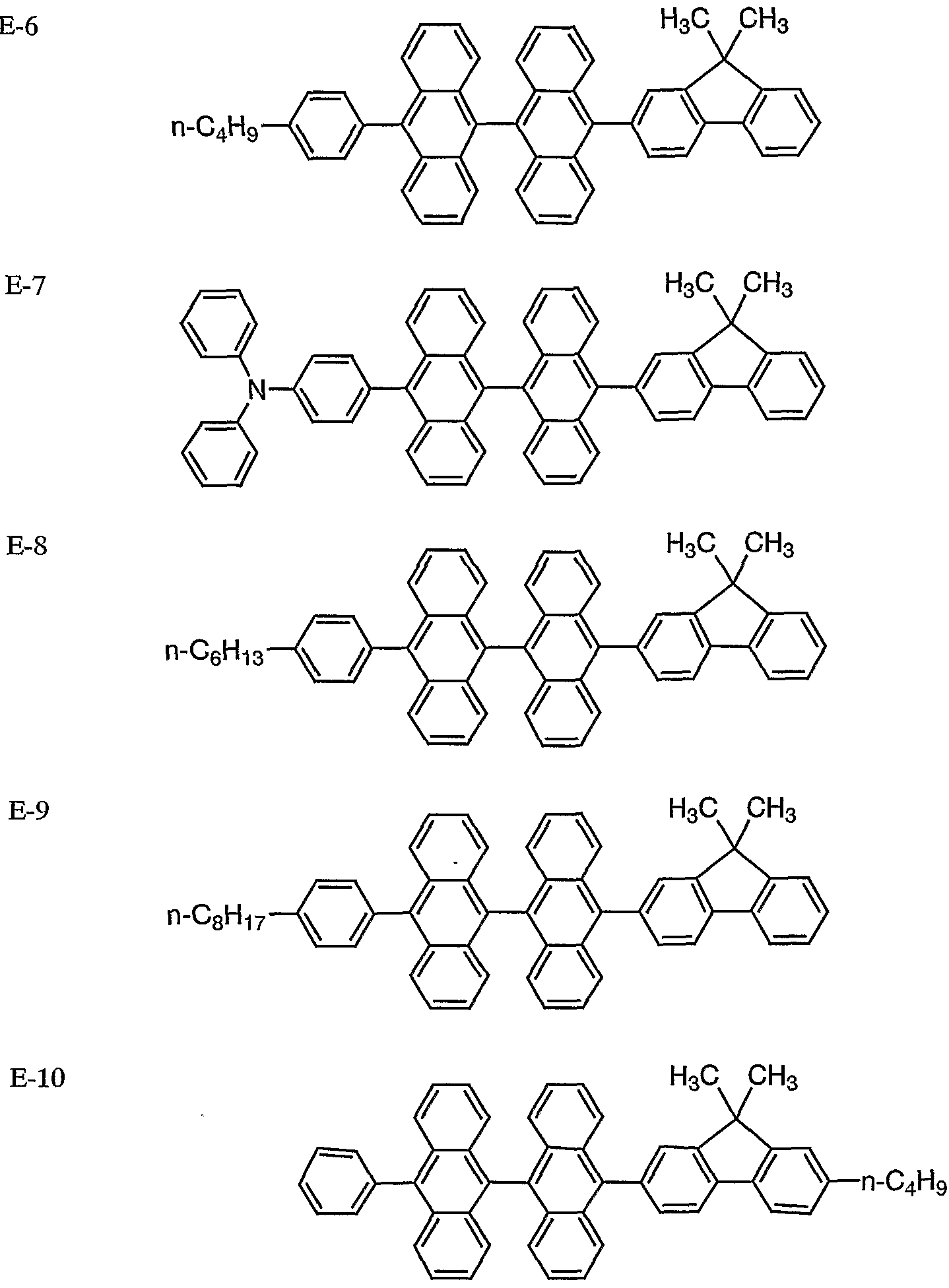
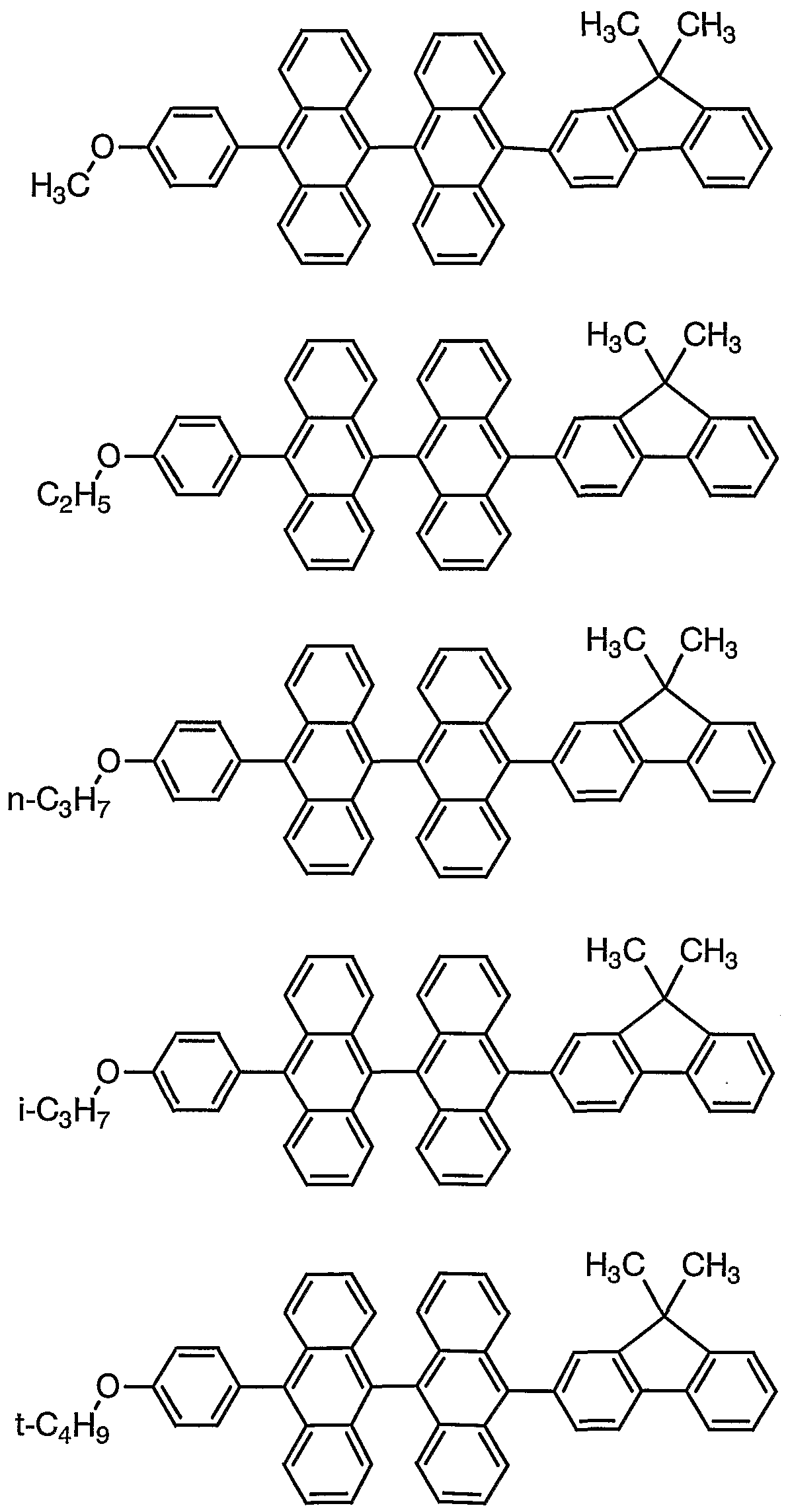
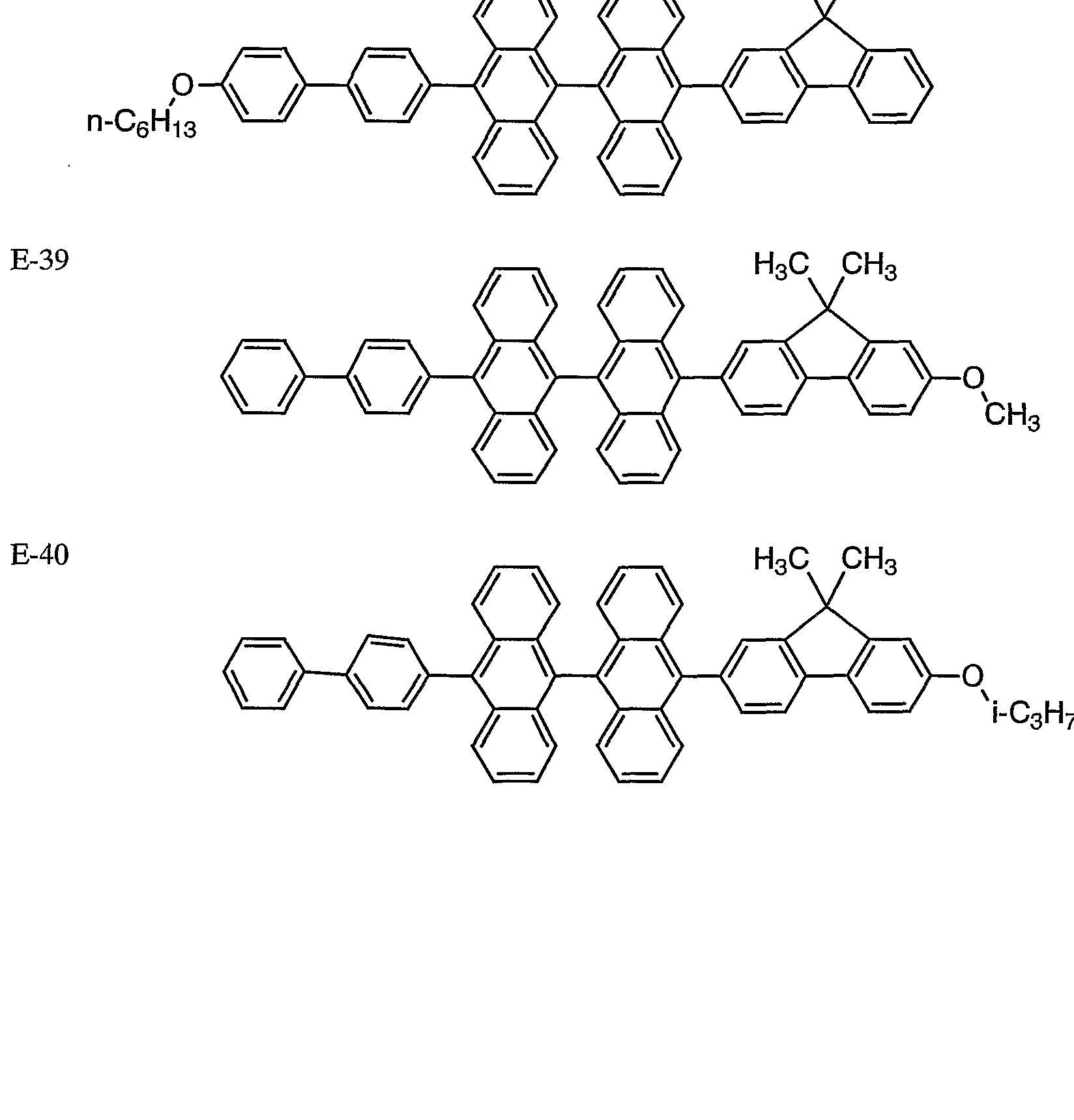
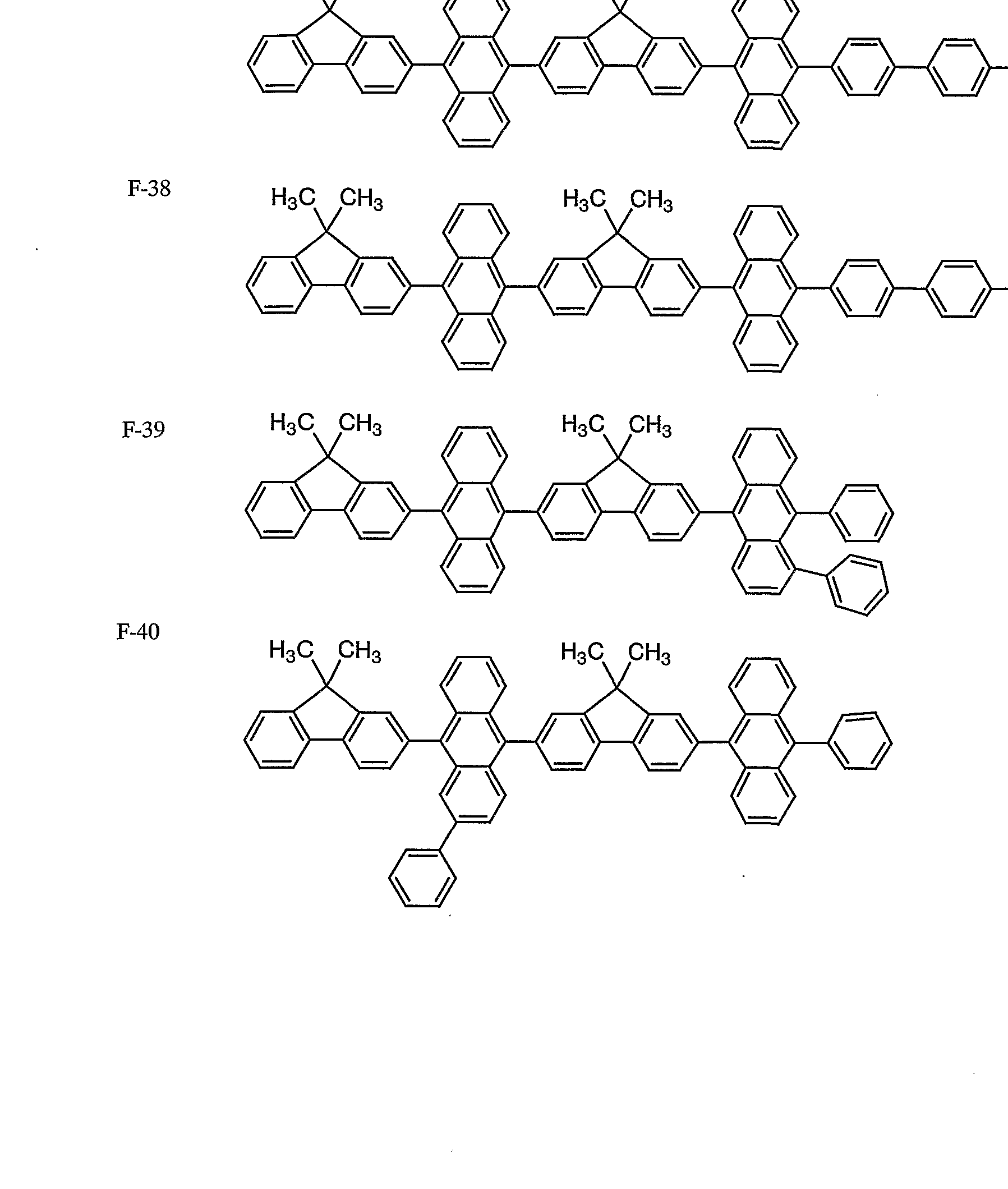
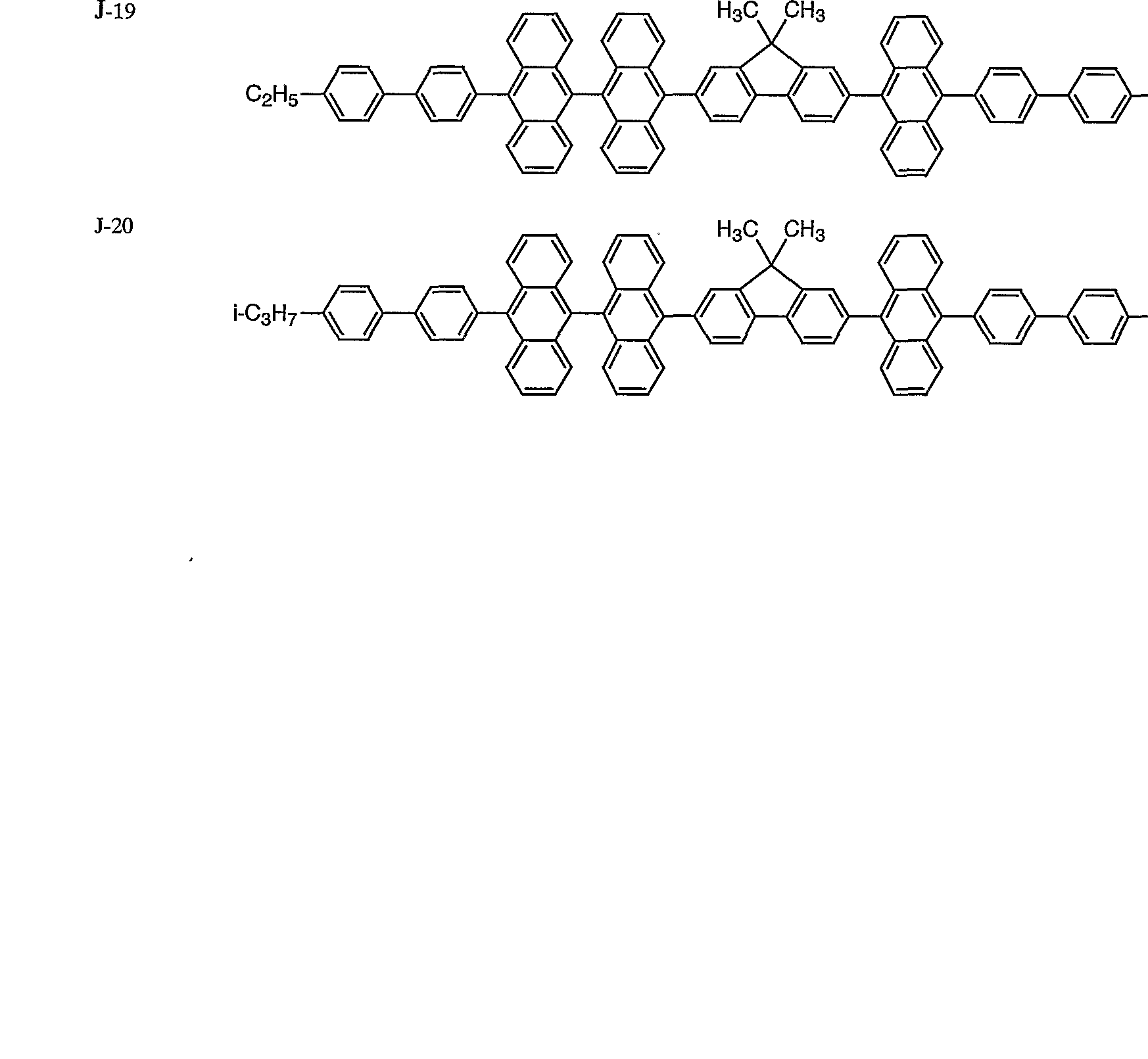
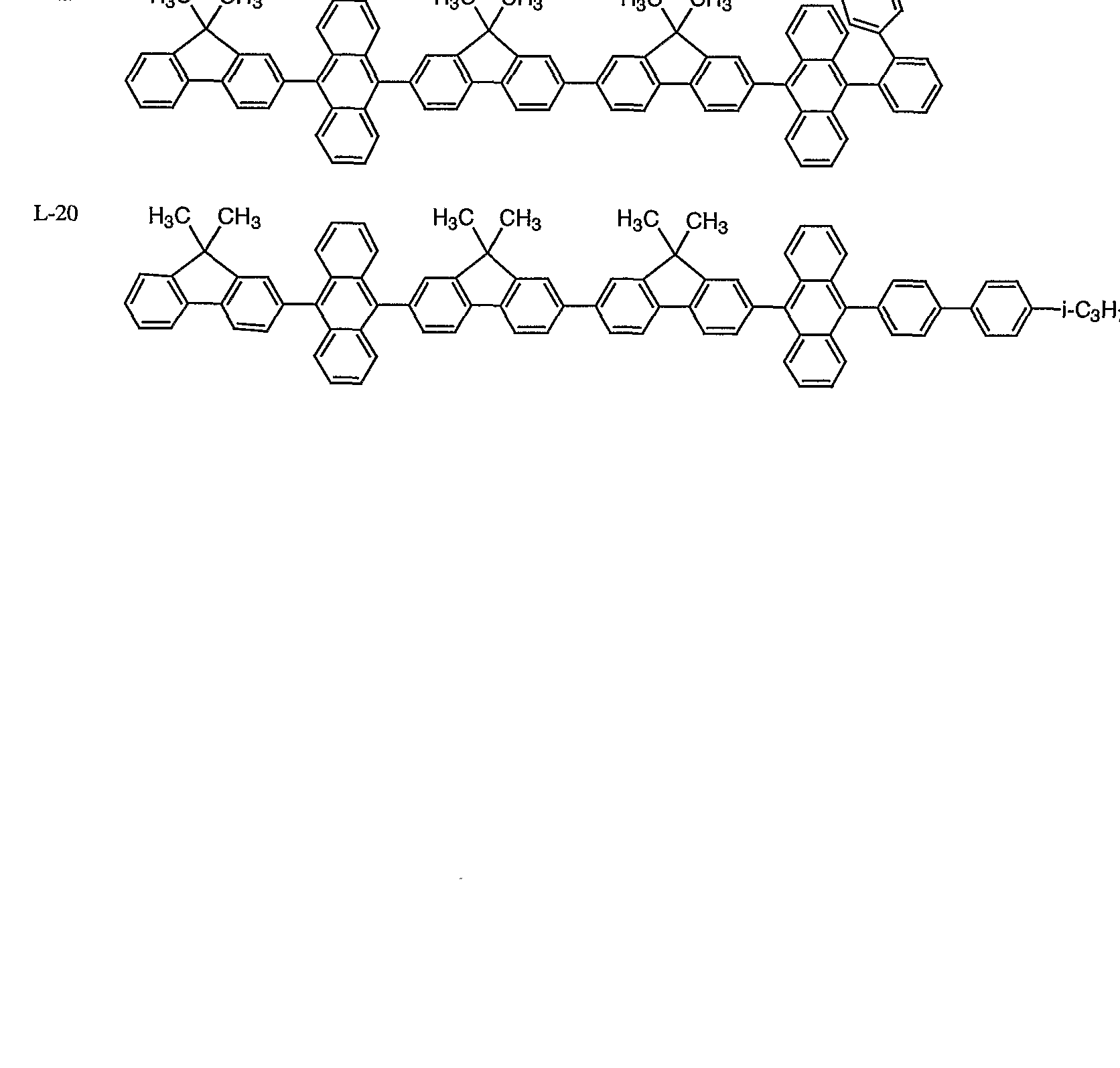
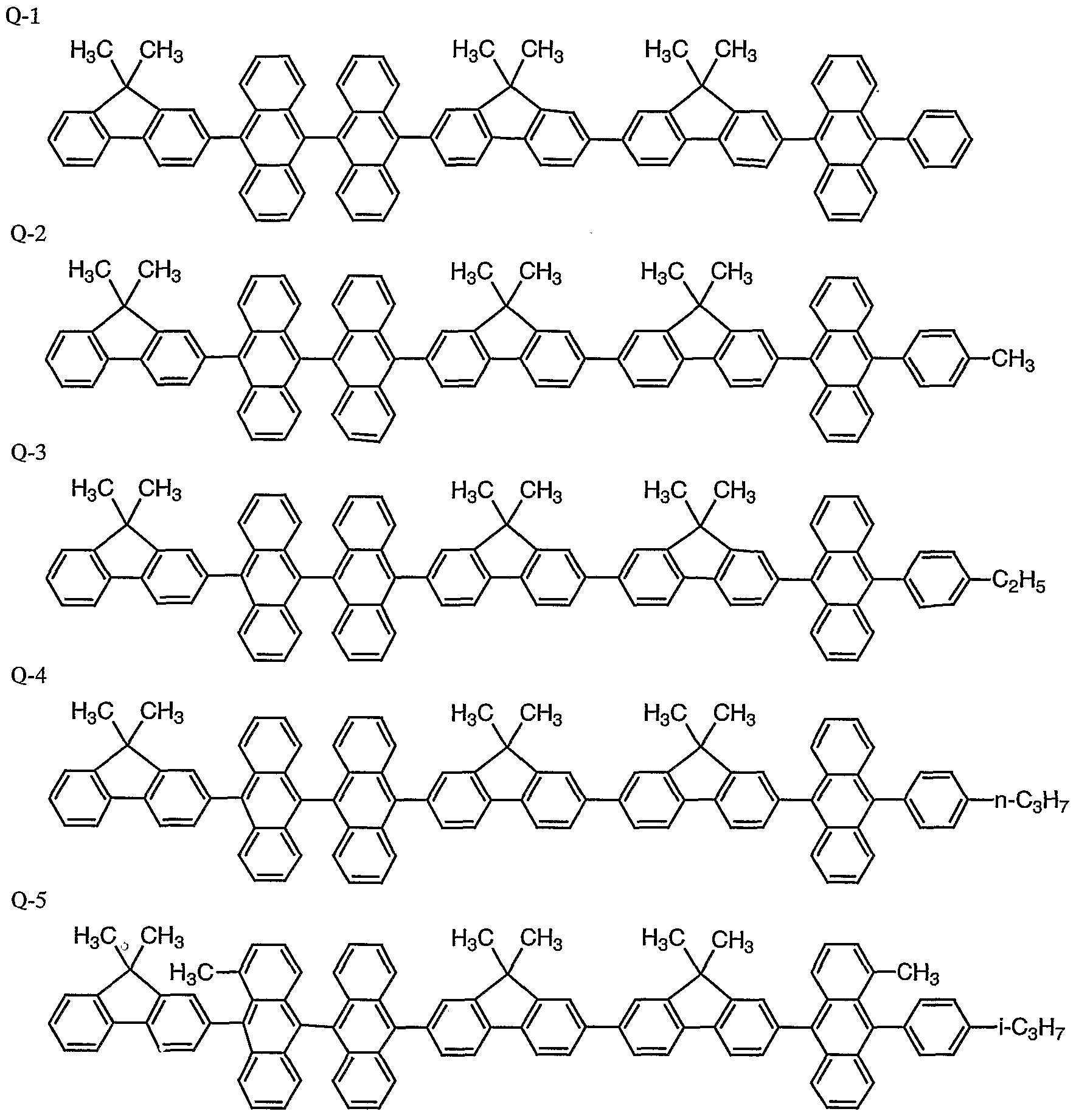
本発明に係る化合物 Aの具体例としては、 例えば、 以下の化合 物を挙げることができるが、 本発明はこれらに限定されるもので はない。
例示化合物番号
A-5 H3C CH
A-
ετ-ν
A16-
A21-
6 A2-
εΗ0 〇εΗ Ρ£-Υ
η
980df/X3d
A64-
A15-
62
df/X3d mn/zo Ο
Cd
B
ω
B
B
B
B
0269 /I0df/X3d ttZn/ZO OfA
B - 25 H3C CH3
62 B-
Β
Β
14 B-
C-10 门一 G Hg n- 4Hq
01690/T0df/X3d ζη/ζο Ο
55
C21-
0Z690/T0df/X3d ο OAV
p
2 C3-
C-40 n-C3H7 n-C3H n-C3H7 n-C3H7
麵 OAV寸:
d £-
α -
6 D-
S9
f/X3d nzn/zo OA
麵寸:
S 9
2 D--
セ ε-α
££-α
Ζ£~α
Ζ9
oa -
69 d
E12-
麵 OAV寸:
E2-
ψ
Ε
Ε
Ηε0-!
εΗ0 ΟεΗ 0ャ -3
hi
0Z690/I0df/X3d mn/zo OAV
t 1
F5,
l Fl-
18
Οί 690/10dT/X3d i" O
SH0 〇εΗ HO ΟεΗ ςζ-d
Ζ8
26 F-
p zmzo OAV
0Z690/l0dT/X3d
98
G-5 n-C6Hi3 n-C6Hi3 H3C CH3 H3C CH3
G-6 H3C CH; C2H5 C2H5 C2H5 p2H5
G-13 H3C CH3 H3C CH H3C — CH:
G-14
G - 15
G-17 H3C、 CH3 H3C CH3 H3C CH3
G-1S
G-19
G-20
elH90-u elH90-u eiH90-u eiH90-u S-H
16
/13d t nizo OAV
H-10 n-C4Hg n-C4Hg n-C6Hi3 n-C6Hi3
ΕΗ0 〇εΗ BH0 ΟεΗ
S6
0Z690/I0df/X3d ζη/ζο Ο
^6
0/T0df/X3d o OAV
H22-
96
0Z690/I0«if/X3d 0 OA
A6
0Ζ690/Ϊ0<ΙΓ/Χ3<1
86
OZ690/TOdf/X3d ζη/ζο θΛ
66
01690/1 Odf/X3d mi-ΐ/ίθ OAV
2 S
OZ690/lOdT/13d
90ΐ
Οί 690/1 Odf/X3d tun/zo OAV
901
OZ690/lOdf/X3d
Z01
OZ690/lOdf/13d ttzn/zo OAV
0Z690/T0df/X3d mn/zo OA
Πΐ
S11 d
7 K-
9Π
Κ2:-
K-30 H3C CH3 H3C CH3
K一
H3C CH3 H3G CH3
L-10 H3C CH3 H3C CH3 H3C CH3
HI
レ 24 H3C CH3 H3C CH3 H3 CHg
L-25
0l690/l0dT/I3d
εΗ0 Ο
εΗ
εΗ0 Ο
εΗ
εΗ0 Ο
εΗ 1£-Ί
0Z690/T0df/X3d ηζη/ζο Ο
2 - £Ί,
H3C CH3 H3C CH3
08ΐ
0/T0df/X3d mn/zo o/sx
H
sO-u
μΗ
90-υ "H
sO-u H
sO-u H
90-u ^H
sO-u セ -N
98ΐ
Z690/T0dT/X3d
stH90-u eiH90-u etH90-u ειμ90-υ 6H 〇-u 6Η*Ό-υ OT-N
95
εΗ〇 ΟεΗ εΗ0 ΟεΗ οτ-ο
0Z690/T0df/X3d mn/zo OA
Z690/T0df/X3d ηζη/ζο Ο
麵寸:
〇一—
0Z690/T0df/X3d mn/zo OA
6^1
0Z690/T0dT/X3d nzn/zo ojx
OS!
P-25 H3C CH3 H3C CH3
P
9-0
891
0Z690/T0df/X3d
631
0Z690/I0df/X3d mmzQ OAV
8T-0 ΐ-D
9ΐ-0
091
0Z690/I0df/X3d mxvz^ OAV
S9I
本発明に係る化合物 Aは、 好ましくは、 例示化合物番号 A— 1 〜A— 6 0、 B— 1〜 B— 6 0、 C— l 〜 C— 4 5、 F— 1 〜 F 一 4 0、 G— l〜 G— 2 5、 I 一 :! 〜 I 一 4 5、 および M— 1〜 M— 2 5で表される化合物であり、 より好ましくは、 例示化合物 番号 A— 1〜A— 6 0、 B— 1 〜 B - 6 0、 C— 1 〜 C一 4 5、 F _ 1 〜 F— 4 0、 I — :!〜 I 一 4 5、 および M— :! 〜 M— 2 5 で表される化合物であり、 さ らに好ましくは、 A— ;!〜 A— 6 0 B— 1 ~ B— 6 0、 C一 1〜 C— 4 5、 および M— 1〜Μ— 2 5 で表される化合物である。
本発明に係る化合物 Aは、 例えば、 以下の方法により製造する ことができる。 すなわち、 例えば、 ハロゲノアントラセン誘導体 を、 フルォレニルホウ酸誘導体と、 例えば、 パラジウム化合物 〔例えば、 テ 卜ラキス ( ト リ フエニルフォスフィ ン) パラジウム ビス ( ト リ フエニルフォスフィ ン) パラジウムクロライ ド〕 およ び塩基 (例えば、 炭酸ナトリ ウム、 炭酸水素ナトリ ウム、 ト リエ チルァミン) の存在下で反応させる 〔例えば、 Chem.Rev.,^ , 245 7 (1995)に記載の方法を参考にすることができる〕 ことによ り製 造することができる。
また、 本発明に係る化合物 Aは、 例えば、 アン トリルホウ酸誘 導体を、 八ロゲノフルオレン誘導体と、 例えば、 パラジウム化合 物 〔例えば、 テ 卜ラキス ( ト リ フエニルフォスフィ ン) パラジゥ ム、 ビス (ト リ フエニルフォスフィ ン) パラジウムクロライ ド〕 および塩基 (例えば、 炭酸ナト リウム、 炭酸水素ナト リ ウム、 ト リエチルァミン) の存在下で反応させる 〔例えば、 Chem.Rev. , 2457 (1995)に記載の方法を参考にすることができる〕 ことにより 製造することができる。 '
本発明に係る一般式 ( 1 ) で表わされる化合物は、 例えば、 以
下の方法により製造することができる。
すなわち、 例えば、 下記一般式 ( 7 ) で表されるホウ酸化合物 を、 下記一般式 ( 8 ) で表される化合物と、 例えば、 パラジウム 化合物 〔例えば、 テトラキス (ト リ フエニルフォスフィ ン) パラ ジゥム、 ビス (ト リ フエニルフォスフィ ン) ノ、"ラジウムクロライ ド〕 および塩基 (例えば、 炭酸ナト リウム、 炭酸水素ナト リウム ト リェチルァミン) の存在下で反応させる 〔例えば、 Chem. Rev., 2457 ( 1995)に記載の方法を参考にすることができる〕 ことに より製造することができる。
X - ( F , ) ; - ( A , ) k ~ B ( O H ) 2 ( 7 )
Y , - ( F 2) , - ( A 2)m - ( F 3) n - X 2 ( 8 )
〔上式中、 A A 2、 F 2、 F 3、 X x , X 2、 j 、 k、 1 mおよび nは、 一般式 ( 1 ) の場合と同じ意味を表し、 は八 ロゲン原子を表す〕 ' 一般式 ( 8 ) において、 はハロゲン原子を表し、 好ましく は、 塩素原子、 臭素原子、 ヨウ素原子を表す。
また、 一般式 ( 1 ) で表される化合物は、 例えば、 下記一般式 ( 9 ) で表される化合物を、 下記一般式 ( 1 0 ) で表されるホウ 酸化合物と、 例えば、 パラジウム化合物 〔例えば、 テ トラキス ( ト リ フエニルフォスフィ ン) パラジウム、 ビス (トリ フエニル フォスフィ ン) パラジウムクロライ ド〕 および塩基 (例えば、 炭 酸ナト リ ウム、 炭酸水素ナト リ ウム、 ト リェチルァミン) の存在 下で反応させる 〔例えば、 Chem. Rev. ,ϋ, 2457 (1995)に記載の方 法を参考にすることができる〕 ことにより製造することができる X , - ( F , ) j - ( A , ) k - Y 2 ( 9 )
( H O) 2 B - ( F 2) , - ( A 2)m - ( F 3) n - X 2 ( 1 0 ) 〔上式中、 A A 2、 F 2、 F 3、 X ± , X 2、 j 、 k、 1
mおよび nは、 一般式 ( 1 ) の場合と同じ意味を表し、 Y 2はハ ロゲン原子を表す〕
一般式 ( 9 ) において、 Υ 2はハロゲン原子を表し、 好ましく は、 塩素原子、 臭素原子、 ヨウ素原子を表す。
尚、 一般式 ( 7 ) および一般式 ( 1 0 ) で表される化合物は、 例えば、 一般式 ( 9 ) および一般式 ( 8 ) で表される化合物に、 例えば、 η —ブチルリチウム、 金属マグネシウムを作用させて調 整できるリチォ化合物またはグリニャール Μ薬と、 例えば、 ト リ メ トキシホウ素、 トリイソプロポキシホウ素などを反応させるこ とにより製造することができる。
また、 一般式 ( 1 ) で表される化合物のうち、 Α 1が置換また は未置換のアントラセン— 9, 1 0 —ジィル基である化合物は、 例えば、 以下の方法により製造することができる。 すなわち、 例 えば、 一般式 ( 8 ) および下記一般式 ( 1 1 ) で表される化合物 に、 例えば、 η —ブチルリチウム、 金属マグネシウムを作用させ て調整できるリチォ化合物またはグリニャール試薬と、 置換また は未置換のアン トラキノ ンを反応させて得られる化合物を、 酸 (例えば、 ヨウ化水素酸) の存在下、 脱水芳香族化することによ り、 一般式 ( 1 ) で表される化合物のうち、 A tが置換または未 置換のアン トラセン— 9, 1 0 —ジィル基であり、 kが 1 である 化合物を製造することができる。
1 - ( F , ) j - Y 3 ( 1 1 )
〔上式中、 X , , および j は、 一般式 ( 1 ) の場合と同じ 意味を表し、 Y 3はハロゲン原子を表す〕
一般式 ( 1 1 ) において、 Y 3はハロゲン原子を表し、 好まし くは、 塩素原子、 臭素原子、 ヨウ素原子を表す。
また、 同様に、 一般式 ( 8 ) および一般式 ( 1 1 ) で表される
化合物に、 例えば、 n —ブチルリチウム、 金属マグネシウムを作 用させて調整できるリチォ化合物またはグリニャール試薬と、 置 換または未置換のビアンスロンを反応させて得られる化合物を、 酸 (例えば、 ヨウ化水素酸) の存在下、 脱水芳香族化することに よ り、 一般式 ( 1 ) で表される化合物のうち、 八ェが置換または 未置換のアントラセン— 9 , 1 0 —ジィル基であり、 kが 2であ る化合物を製造することができる。
本発明に係る化合物 Aは、 場合により使用した溶媒 (例えば、 トルエンなどの芳香族炭化水素系溶媒) との溶媒和を形成した形 で製造されることがある。 本発明に係る化合物 Aはこのような溶 媒和物を包含するものであり、 勿論、 溶媒を含有しない無溶媒和 物をも包含するものである。
本発明の有機電界発光素子には、 本発明に係る化合物 Aの無溶 媒和物は勿論、 このような溶媒和物をも使用することができる。
尚、 本発明に係る化合物 Aを有機電界発光素子に使用する場合 再結晶法、 カラムクロマ トグラフィー法、 昇華精製法などの精製 方法、 あるいはこれらの方法を併用して、 純度を高めた化合物を 使用することは好ましいことである。
有機電界発光素子は、 通常、 一対の電極間に、 少なく とも一種 の発光成分を含有する発光層を、 少なく とも一層挟持してなるも のである。 発光層に使用する化合物の正孔注入および正孔輸送、 電子注入および電子輸送の各機能レベルを考慮し、 所望に応じて 正孔注入輸送成分を含有する正孔注入輸送層および Zまたは電子 注入輸送成分を含有する電子注入輸送層を設けることもできる。
例えば、 発光層に使用する化合物の正孔注入機能、 正孔輸送機 能および Zまたは電子注入機能、 電子輸送機能が良好な場合には 発光層が正孔注入輸送層および Zまたは電子注入輸送層を兼ねた
型の素子の構成とすることができる。 勿論、 場合によっては、 正 孔注入 ΐϊ送層および電子注入輸送層の両方の層を設けない型の素 子 (一層型の素子) の構成とすることもできる。
また、 正孔注入輸送層、 電子注入輸送層および発光層のそれぞ れの層は、 一層構造であっても、 また、 多層構造であってもよく 正孔注入輸送層および電子注入輸送層は、 それぞれの層において 注入機能を有する層と輸送機能を有する層を別々に設けて構成す る こともできる。
本発明の有機電界発光 子において、 本発明に係る化合物 Αは 正孔注入輸送成分、 発光成分または電子注入輸送成分に用いるこ とが好ましく、 正孔注入輸送成分または発光成分に用いることが より好ましく、 発光成分に用いることがさらに好ましい。
本発明の有機電界発光素子においては、 本発明に係る化合物 A は、 単独で使用してもよく、 あるいは複数併用してもよい。
本発明の有機電界発光素子の構成としては、 特に限定するもの ではなく、 例えば、 (A ) 陽極 Z正孔注入輸送層 Z発光層 Z電子 注入輸送層/陰極型素子 (第 1 図) 、 (B ) 陽極 Z正孔注入輸送 層 Z発光層ノ陰極型素子 (第 2 図) 、 ( C ) 陽極 Z発光層 Z電子 注入輸送層/陰極型素子 (第 3図) 、 (D ) 陽極 Z発光層 Z陰極 型素子 (第 4図) を挙げることができる。 さ らには、 発光層を電 子注入輸送層で挟み込んだ型の素子である ( E ) 陽極 Z正孔注入 輸送層 Z電子注入輸送層 Z発光層 Z電子注入輸送層 Z陰極型素子
(第 5図) とすることもできる。 (D ) 型の素子構成としては、 発光成分を一層形態で一対の電極間に挟持させた型の素子を包含 するものであるが、 さ らには、 例えば、 ( F ) 正孔注入輸送成分 発光成分および電子注入輸送成分を混合させた一層形態で一対の 電極間に挟持させた型の素子 (第 6 図) 、 ( G ) 正孔注入輸送成
分および発光成分を混合させた一層形態で一対の電極間に挟持さ せた型の素子 (第 7 図) 、 (H) 発光成分および電子注入輸送成 分を混合させた一層形態で一対の電極間に挟持させた型の素子 (第 8図) がある。
本発明の有機電界発光素子においては、 これらの素子構成に限 るものではなく、 それぞれの型の素子において、 正孔注入輸送層 発光層、 電子注入輸送層を複数層設けたりすることができる。 ま た、 それぞれの型の素子において、 正孔注入輸送層と発光層との 間に、 正孔注入輸送成分と発光成分の混合層および/または発光 層と電子注入輸送層との間に、 発光成分と電子注入輸送成分の混 合層を設けることもできる。
よ り好ま しい有機電界発光素子の構成は、 ( A ) 型素子、 ( B ) 型素子、 ( C ) 型素子、 ( E ) 型素子、 ( F ) 型素子、 ( G ) 型素子または (H) 型素子であ り、 さ らに好ましく は、 ( A) 型素子、 ( B ) 型素子、 ( C ) 型素子、 ( F ) 型素子、 ま たは (H) 型素子である。
本発明の有機電界発光素子としては、 例えば、 第 1 図に示す ( A) 陽極 Z正孔注入輸送層 Z発光層 Z電子注入輸送層 陰極型 素子について説明する。
第 1 図において、 1 は基板、 2は陽極、 3 は正孔注入輸送層、 4は発光層、 5は電子注入輸送層、 6は陰極、 7 は電源を示す。 本発明の電界発光素子は、 基板 1 に支持されていることが好ま しく、 基板としては、 特に限定するものではないが、 透明ないし 半透明であることが好ましく、 例えば、 ガラス板、 透明プラスチ ックシー ト (例えば、 ポリエステル、 ポリカーボネート、 ポリス ルフォン、 ポリ メチルメタクリ レー ト、 ポリプロピレン、 ポリエ チレンなどのシー ト) 、 半透明プラスチックシー ト、 石英、 透明
セラミ ックスあるいはこれらを組み合わせた複合シー トからなる ものを挙げることができる。 さ らに、 基板に、 例えば、 カラ一フ ィルター膜、 色変換膜、 誘電体反射膜を組み合わせて、 発光色を コントロールすることもできる。
陽極 2 としては、 比較的仕事関数の大きい金属、 合金または電 気伝導性化合物を電極物質として使用することが好ましい。
陽極に使用する電極物質としては、 例えば、 金、 白金、 銀、 銅 コバルト、 ニッケル、 パラジウム、 バナジウム、 タングステン、 酸化錫、 酸化亜鉛、 I T O (ィ ンジゥム · ティ ン · ォキサイ ド) ポリチォフェン、 ポリ ピロ一ルを挙げることができる。 これらの 電極物質は、 単独で使用してもよく、 あるいは複数併用してもよ い。
陽極は、 これらの電極物質を用いて、 例えば、 蒸着法、 スパッ 夕リ ング法などの方法により、 基板の上に形成することができる また、 陽極は一層構造であってもよく、 あるいは多層構造であつ てもよい。
陽極のシート電気抵抗は、 好ましく は、 数百 Ω Ζ口以下、 より 好ましくは、 5〜 5 0 Ω Ζ口程度に設定する。
陽極の厚みは、 使用する電極物質の材料にもよるが、 一般に、 5〜 : L O O O n m程度、 より好ましく は、 1 0〜 5 0 0 n m程度 に設定する。
正孔注入輸送層 3は、 陽極からの正孔 (ホール) の注入を容易 にする機能、 および注入された正孔を輸送する機能を有する化合 物を含有する層である。
正孔注入輸送層は、 本発明に係る化合物 Aおよび/または他の 正孔注入輸送機能を有する化合物 (例えば、 フタロシアニン誘導 体、 トリアリールメタン誘導体、 トリアリールァミン誘導体、 ォ
キサゾ一ル誘導体、 ヒ ドラゾン誘導体、 スチルベン誘導体、 ピラ ゾリ ン誘導体、 ポリシラン誘導体、 ポリ フエ二レンビニレンおよ びその誘導体、 ポリチォフェンおよびその誘導体、 ポリ — N—ビ 二ルカルバゾール誘導体) を少なく とも一種用いて形成すること ができる。
尚、 正孔注入輸送機能を有する化合物は、 単独で使用してもよ く、 あるいは複数併用してもよい。
本発明において用いる他の正孔注入輸送機能を有する化合物と しては、 ト リ ァリ一ルァミ ン誘導体 (例えば、 4, 4 ' — ビス 〔N—フエニル一 N— ( 4 " 一メチルフエニル) ァミノ〕 ビフエ ニル、 4, 4 ' —ビス 〔N—フエ二ルー N— ( 3 " —メチルフエ ニル) ァミ ノ〕 ビフエニル、 4 , 4 ' 一ビス 〔N—フエ二ルー N - ( 3 " ーメ トキシフエ二ル) ァミ ノ〕 ビフエニル、 4, 4 ' - ビス 〔N—フエ二ルー N _ ( 1 " —ナフチル) ァミノ〕 ビフエ二 ル、 3 , 3 , 一ジメチルー 4, 4 , 一ビス 〔N—フエニル一 N— ( 3 " 一メチルフエニル) ァミ ノ〕 ビフエニル、 1 , 1 — ビス 〔 4 ' ― [ N , N—ジ ( 4 " —メチルフエニル) ァミノ ] フエ二 ル〕 シクロへキサン、 9, 1 0 —ビス 〔N— ( 4 ' —メチルフエ ニル) 一 N— ( 4 " 一 n _ブチルフエニル) ァミノ〕 フエナン 卜 レン、 3, 8 —ビス (N, N—ジフエ二ルァミノ) _ 6 —フエ二 ルフエナン ト リ ジン、 4 —メチルー N , N—ビス 〔 4 " , 4 ' ' ' 一ビス [N, , N ' ージ ( 4—メチルフエニル) ァミノ ] ビフエ 二ルー 4 —ィル〕 ァニリ ン、 N, N ' —ビス 〔 4— (ジフエニル ァミ ノ) フエニル〕 一 N, N ' ージフエ二ルー 1 , 3 —ジァミ ノ ベンゼン、 N, N ' 一 ビス 〔 4 — (ジフエニルァミ ノ) フエ二 ル〕 一 N, N ' —ジフエニル— 1 , 4 —ジァミノベンゼン、 5, 5 " —ビス 〔 4 — (ビス [ 4—メチルフエニル] ァミノ) フエ二
ル〕 一 2, 2 ' : 5, , 2 " _夕一チォフェン、 1, 3, 5 — ト リス (ジフエニルァミ ノ) ベンゼン、 4, 4, , 4 " ー ト リ ス ( N—力ルバゾリィル) トリ フエニルァミン、 4 , 4 , , 4 " 一 ト リ ス 〔 Ν— ( 3 ' ' ' —メチルフエニル) — N—フエニルアミ ノ〕 ト リ フエニルァミン、 4, 4, , 4 " — トリス 〔N , N—ビ ス ( 4 ' ' '一 t e r t —プチルビフエニル— 4 " "—ィル) ァミ ノ〕 ト リ フエニルァミン、 1 , 3 , 5 — ト リス 〔N— ( 4 ' ージフエ二 ルァミ ノフエニル) 一 N —フエニルァミ ノ〕 ベンゼン) .、 ポリチ ォフェンおよびその誘導体、 ポリ一 N—ビニルカルバゾ一ル誘導 体が好ましい。
本発明に係る化合物 Aと他の正孔注入輸送機能を有する化合物 を併用する場合、 正孔注入輸送層中に占める本発明に係る化合物 Aの割合は、 好ましくは、 0 . 1〜4 0重量%程度に調製する。 発光層 4は、 正孔および電子の注入機能、 それらの輸送機能、 正孔と電子の再結合により励起子を生成させる機能を有する化合 物を含有する層である。
発光層は、 本発明に係る化合物 Aおよび Zまたは他の発光機能 を有する化合物 (例えば、 ァク リ ドン誘導体、 キナク リ ドン誘導 体、 ジケトピロ口ピロ一ル誘導体、 多環芳香族化合物 〔例えば、 Jレブレン、 アントラセン、 テ トラセン、 ピレン、 ペリ レン、 クリ セン、 デカシクレン、 コロネン、 テトラフエエルシクロペンタジ ェン、 ペン夕フエニルシクロへキサジェン、 9 , 1 0 —ジフエ二 ルアン トラセン、 9 , 1 0 —ビス (フエニルェチェル) アン 卜ラ セン、 1 , 4—ビス ( 9 , —ェチ二ルアントラセニル) ベンゼン 4, 4, 一ビス ( 9 " 一ェチニルアン トラセニル) ビフエニル〕 トリァリールァミン誘導体 〔例えば、 正孔注入輸送機能を有する 化合物として前述した化合物を挙げることができる〕 、 有機金属
錯体 〔例えば、 ト リス ( 8 —キノ リ ラー ト) アルミニウム、 ビス ( 1 0 —ベンゾ [h]キノ リ ノ ラー ト) ベリ リウム、 2 — ( 2 ' - ヒ ドロキシフエニル) ベンゾォキサゾールの亜鉛塩、 2 — ( 2 ' ーヒ ドロキシフエニル) ベンゾチアゾ一ルの亜鉛塩、 4 —ヒ ドロ キシァク リジンの亜鉛塩、 3 —ヒ ドロキシフラボンの亜鉛塩、 5 ーヒ ドロキシフラボンのベリ リウム塩、 5 —ヒ ドロキシフラボン のアルミニウム塩〕 、 スチルベン誘導体 〔例えば、 1 , 1 , 4 , 4 ーテトラフエニル一 1 , 3 一ブタジエン、 4 , 4 ' —ビス ( 2 2 —ジフエ二ルビニル) ビフエ二ル、 4, 4 ' 一ビス 〔 ( 1 , 1 2 _ ト リ フエニル) ェテニル〕 ビフエニル、 クマリ ン誘導体 〔例 えば、 クマリ ン 1 、 クマリ ン 6、 クマリ ン 7、 クマリ ン 3 0、 ク マリ ン 1 0 6、 クマリ ン 1 3 8、 クマリ ン 1 5 1 、 クマリ ン 1 5 2 、 クマリ ン 1 5 3、 クマリ ン 3 0 7、 クマリ ン 3 1 1 、 クマリ ン 3 1 4、 クマリ ン 3 3 4、 クマリ ン 3 3 8、 クマリ ン 3 4 3、 クマリ ン 5 0 0〕 、 ピラン誘導体 〔例えば、 D C M 1 、 D C M 2〕 、 ォキサゾン誘導体 〔例えば、 ナイルレツ ド〕 、 ベンゾチア ゾ一ル誘導体、 ベンゾォキサゾール誘導体、 ベンゾイミダゾ一ル 誘導体、 ピラジン誘導体、 ケィ皮酸エステル誘導体、 ポリ一 N _ ビニルカルバゾールおよびその誘導体、 ポリチォフェンおよびそ の誘導体、 ポリ フエ二レンおよびその誘導体、 ポリ フルオレンお よびその誘導体、 ポリフエ二レンビニレンおよびその誘導体、 ポ リ ビフエ二レンビニレンおよびその誘導体、 ポリターフェ二レン ビニレンおよびその誘導体、 ポリナフチレンビニレンおよびその 誘導体、 ポリチェ二レンビニレンおよびその誘導体〕 を少なく と も一種用いて形成することができる。
本発明の有機電界発光素子においては、 発光層に本発明に係る 化合物 Aを含有していることが好ましい。
本発明の有機電界発光素子においては、 発光層に本発明に係る 化合物 Aを、 単独で使用してもよく、 あるいは他の発光機能を有 する化合物と併用してもよい。
本発明に係る化合物 Aと他の発光機能を有する化合物を併用す る場合、 発光層中に占める本発明に係る化合物 Aの割合は、 好ま しくは、 0. 0 0 1〜 9 9. 9 9 9重量%程度、 より好ましくは. 0. 0 1〜 9 9. 9 9重量%程度、 さ らに好ましくは、 0. 1〜 9 9. 9重量%程度に調製する。
本発明において用いる他の発光機能を有する化合物としては、 発光性有機金属錯体が好ましい。 例えば、 ; Γ. Appl. Phys. ,ϋ, 3610 (1989)、 特開平 5 — 2 1 4 3 3 2号公報に記載のように、 発光層 をホス ト化合物とゲス ト化合物 (ドーパン ト) とより構成するこ ともできる。
本発明に係る化合物 Aは、 ホス ト化合物として用いて発光層を 形成することができ、 さ らには、 ゲス ト化合物として用いて発光 層を形成することもできる。
本発明に係る化合物 Aを、 ゲス ト化合物として用いて発光層を 形成する場合、 ホス ト化合物としては、 例えば、 前記の他の発光 機能を有する化合物を挙げることができ、 好ましくは、 発光性有 機金属錯体または前記の トリァリ一ルァミン誘導体である。
この場合、 発光性有機金属錯体またはト リァリールアミン誘導 体に対して、 本発明に係る化合物 Aを、 好ましくは、 0. 0 0 1 〜 4 0重量%程度、 よ り好ましくは、 0. 0 1 〜 3 0重量%程度. 特に好ましくは、 0. 1 〜 2 0重量%程度使用する。
本発明に係る化合物 Aと併用する発光性有機金属錯体としては. 特に限定するものではないが、 発光性有機アルミニウム錯体が好 ましく、 置換または未置換の 8 —キノ リ ノ ラー ト配位子を有する
発光性有機アルミニウム錯体がよ り好ましい。 好ましい発光性有 機金属錯体としては、 例えば、 一般式 ( a ) 〜一般式 ( c ) で表 される発光性有機アルミニウム錯体を挙げる ことができる。
( Q) a - A! ( a )
(式中、 Qは置換または未置換の 8 —キノ リ ノ ラー ト配位子を表 す)
( Q) 2 - A , - O - L ( b )
(式中、 Qは置換 8 —キノ リ ノ ラー ト配位子を表し、 O— Lはフ ェノ ラ一 ト配位子であ り、 Lはフエニル部分を含む炭素数 6〜 2 4の炭化水素基を表す)
( Q) 2 - A , - O - A , - ( Q) 2 ( c )
(式中、 Qは置換 8 —キノ リ ノ ラー ト配位子を表す)
発光性有機金属錯体の具体例としては、 例えば、 ト リス ( 8 — キノ リ ノ ラー ト) アルミニウム、 ト リス ( 4 —メチルー 8 —キノ リ ノ ラー ト) アルミニウム、 ト リス ( 5 —メチル一 8 —キノ リ ノ ラー ト) アルミニウム、 卜 リス ( 3 , 4 —ジメチルー 8 —キノ リ ノ ラ一 ト) アルミニウム、 ト リス ( 4, 5 —ジメチルー 8 —キノ リ ノ ラー ト) アルミニウム、 ト リス ( 4 , 6 —ジメチルー 8 —キ ノ リ ノ ラ一 卜) アルミニウム、 ビス ( 2 —メチルー 8 —キノ リ ノ ラー ト) (フエノ ラー ト) アルミニウム、 ビス ( 2 —メチルー 8 ーキノ リ ノ ラ一 卜) ( 2 —メチルフエノ ラ一 ト) アルミニウム、 ビス ( 2 —メチル _ 8 —キノ リ ノ ラー ト) ( 3 —メチルフエノ ラ ー ト) アルミニウム、 ビス ( 2 —メチル一 8 —キノ リ ノ ラー ト) ( 4 ーメチルフエノ ラー ト) アルミニウム、 ビス ( 2 —メチルー 8 —キノ リ ノ ラー 卜) ( 2 —フエエルフエノ ラー ト) アルミニゥ ム、 ビス ( 2 —メチルー 8 _キノ リ ノ ラー ト) ( 3 —フエエルフ エノ ラー ト) アルミニウム、 ビス ( 2 —メチル一 8 —キノ リ ノ ラ
ー ト) ( 4 —フエエルフエノ ラー ト) アルミニウム、 ビス ( 2 — メチル一 8 —キノ リ ノ ラー ト) ( 2 , 3 _ ジメチルフエノ ラ一 ト) アルミニウム、 ビス ( 2 —メチルー 8 —キノ リ ノ ラー ト) ( 2, 6 —ジメチルフエノ ラ一 ト) アルミニウム、 ビス ( 2 —メ チル一 8 —キノ リ ノ ラー ト) ( 3, 4 ージメチルフエノ ラー ト) アルミニウム、 ビス ( 2 —メチル一 8 —キノ リ ノ ラー ト) ( 3 , 5 _ジメチルフエノ ラー ト) アルミニウム、 ビス ( 2 —メチルー 8 —キノ リ ノ ラー ト) ( 3 , 5 —ジ一 tert—ブチルフエノ ラ一 ト) アルミニウム、 ビス ( 2 —メチルー 8 —キノ リ ノ ラー ト) ( 2 , 6 —ジフエニルフエノ ラー ト) アルミニウム、 ビス ( 2 — メチル _ 8 —キノ リ ノ ラ一 ト) ( 2, 4 , 6 — ト リ フエニルフエ ノ ラー ト) アルミニウム、 ビス ( 2 —メチルー 8 —キノ リ ノ ラ一 ト) ( 2, 4 , 6 — ト リ メチルフエノ ラー ト) アルミニウム、 ピ ス ( 2 —メチル一 8 —キノ リ ノ ラー ト) ( 2, 4, 5, 6 —テ ト ラメチルフエノ ラー ト) アルミニウム、 ビス ( 2 —メチルー 8 — キノ リ ノ ラー ト) ( 1 —ナフ トラ一 ト) アルミニウム、 ビス ( 2 —メチルー 8 —キノ リ ノ ラ一 ト) ( 2 —ナフ トラ一 ト) アルミ二 ゥム、 ビス ( 2 , 4 —ジメチルー 8 —キノ リ ノ ラ一 ト) ( 2 —フ ェニルフエノ ラー ト) アルミニウム、 ビス ( 2, 4 —ジメチルー 8 —キノ リ ノ ラー ト) ( 3 —フエニルフエノ ラー ト) アルミニゥ ム、 ビス ( 2, 4 ージメチル一 8 —キノ リ ノ ラー ト) ( 4 一フエ ニルフエノ ラー ト) アルミニウム、 ビス ( 2 , 4 —ジメチル一 8 一キノ リ ノ ラー ト) ( 3, 5 —ジメチルフエニルフエノ ラー ト) アルミニウム、 ビス ( 2, 4 —ジメチルー 8 —キノ リ ノ ラー ト) ( 3 , 5 —ジー tert—ブチルフエニルフエノ ラー ト) アルミニゥ ム、 ビス ( 2 —メチル一 8 —キノ リ ノ ラー ト) アルミニウム一 —ォキソービス ( 2 —メチルー 8 —キノ リ ノ ラー ト) アルミニゥ
ム、 ビス ( 2, 4 一ジメチルー 8 —キノ リ ノラー ト) アルミニゥ ム一 —ォキソ一 ビス ( 2 , 4 —ジメチルー 8 —キノ リ ノ ラー ト) アルミニウム、 ビス ( 2 —メチルー 4 一ェチル— 8 —キノ リ ノラート) アルミニウム一 —ォキソ一ビス ( 2 —メチル一 4 — ェチルー 8 —キノ リ ノラー ト) アルミニウム、 ビス ( 2 —メチル 一 4ーメ トキシー 8 —キノ リ ノラー ト) アルミニウム一 —ォキ ソ—ビス ( 2 —メチル一 4—メ トキシ一 8 —キノ リ ノ ラー ト) ァ ルミ二ゥム、 ビス ( 2 —メチル一 5 —シァノ一 8 —キノ リ ノ ラー ト) アルミニウム一 一ォキソ一ビス ( 2 —メチル— 5 —シァノ 一 8 —キノ リ ノラ一 卜) アルミニウム、 ビス ( 2 —メチル _ 5 _ ト リ フルォロメチル一 8 —キノ リ ノ ラー ト) アルミニウム— — ォキソ一ビス ( 2 —メチルー 5 _ トリ フルォロメチル一 8 —キノ リ ノ ラー ト) アルミニウムを挙げることができる。 勿論、 発光性 有機金属錯体は、 単独で使用してもよく、 あるいは複数併用して もよい。
電子注入輸送層 5 は、 陰極からの電子の注入を容易にする機能 そして注入された電子を輸送する機能を有する化合物を含有する 層である。
電子注入輸送層は、 本発明に係る化合物 Aおよび/または他の 電子注入輸送機能を有する化合物 (例えば、 有機金属錯体 〔例え ば、 ト リス ( 8 —キノ リ ノラ一 ト) アルミニウム、 ビス ( 1 0 — ベンゾ [h]キノ リ ノ ラー 卜) ベリ リ ウム、 5 — ヒ ドロキシフラボ ンのベリ リ ウム塩、 5 —ヒ ドロキシフラボンのアルミニウム塩〕 ォキサジァゾール誘導体 〔例えば、 1 , 3 —ビス [ 5 ' — ( 4 " 一 tert—ブチルフエニル) 一 1 ' , 3, , 4 ' —ォキサジァゾ一 ルー 2 ' —ィル] ベンゼン〕 、 卜 リ アゾール誘導体 〔例えば、 3 一 ( 4 ' — tert—ブチルフエニル) 一 4 一フエニル— 5 — ( 4 "
—フエニルフエニル) 一 1 , 2, 4 — トリァゾール〕 、 ト リアジ ン誘導体、 ペリ レン誘導体、 キノ リ ン誘導体、 キノキサリ ン誘導 体、 ジフエ二ルキノン誘導体、 ニトロ置換フルォレノ ン誘導体、 チォピランジオキサイ ド誘導体) を少なく とも一種用いて形成す ることができる。
尚、 電子注入輸送機能を有する化合物は、 単独で使用してもよ く、 あるいは複数併用してもよい。
本発明に係る化合物 Aと他の電子注入輸送機能を有する化合物 を併用する場合、 電子注入輸送層中に占める本発明に係る化合物 Aの割合は、 好ましくは、 0 . 1〜 4 0重量%程度に調製する。 本発明において、 本発明に係る化合物 Aと有機金属錯体 〔例えば 前記一般式 ( a ) 〜一般式 ( c ) で表される化合物〕 を併用して 電子注入輸送層を形成することは好ましい。
陰極 6 としては、 比較的仕事関数の小さい金属、 合金または電 気伝導性化合物を電極物質として使用することが好ましい。
陰極に使用する電極物質としては、 例えば、 リチウム、 リチウ ムーイ ンジウム合金、 ナト リウム、 ナト リ ウム—カリウム合金、 カルシウム、 マグネシウム、 マグネシウム一銀合金、 マグネシゥ ムーィ ンジゥム合金、 イ ンジウム、 ルテニウム、 チタニウム、 マ ンガン、 イ ッ ト リウム、 アルミニウム、 アルミニウム一リチウム 合金、 アルミニウム—カルシウム合金、 アルミニウム—マグネシ ゥム合金、 グラフアイ ト薄膜を挙げることができる。 これらの電 極物質は、 単独で使用してもよく、 あるいは、 複数併用してもよ い。
陰極は、 これらの電極物質を用いて、 蒸着法、 スパッタリ ング法 イオン化蒸着法、 イオンプレーティ ング法、 クラスターイオンビ —ム法などの方法により、 電子注入輸送層の上に形成することが
できる。
また、 陰極は一層構造であってもよく、 あるいは多層構造であ つてもよい。
尚、 陰極のシー ト電気抵抗は、 数百 Ω Ζ口以下に設定すること が好ましい。
陰極の厚みは、 使用する電極物質の材料にもよるが、 一般に、 5〜 ; L 0 0 O n m程度、 より好ましくは、 1 0〜 5 0 0 n m程度 に設定する。
尚、 有機電界発光素子の発光を効率よく取り出すために、 陽極 または陰極の少なく とも一方の電極が、 透明ないし半透明である ことが好ましく、 一般に、 発光光の透過率が 7 0 %以上となるよ うに陽極の材料、 厚みを設定することがより好ましい。
また、 本発明の有機電界発光素子においては、 その少なく とも 一層中に、 一重項酸素クェンチヤ一が含有されていてもよい。 一重項酸素クェンチヤ一としては、 特に限定するものではなく、 例えば、 ルプレン、 ニッケル錯体、 ジフエニルイソべンゾフラン が挙げられ、 特に好ましくは、 ルブレンである。
一重項酸素クェンチヤ一が含有されている層としては、 特に限 定するものではないが、 好ましく は、 発光層または正孔注入輸送 層であり、 より好ましく は、 正孔注入輸送層である。 尚、 例えば 正孔注入輸送層に一重項クェンチヤ一を含有させる場合、 正孔注 入輸送層中に均一に含有させてもよく、 正孔注入輸送層と隣接す る層 (例えば、 発光層、 発光機能を有する電子注入輸送層) の近 傍に含有させてもよい。
一重項酸素クェンチヤ一の含有量としては、 含有される層 (例 えば、 正孔注入輸送層) を構成する全体量の 0 . 0 1 〜 5 0重 量%、 好ましく は、 0 . 0 5〜 3 0重量%、 より好ましく は、 0
1 〜 2 0重量%である。
正孔注入輸送層、 発光層、 電子注入輸送層の形成方法に関して は、 特に限定するものではなく、 例えば、 真空蒸着法、 イオン化 蒸着法、 溶液塗布法 (例えば、 スピンコート法、 キャス 卜法、 デ イ ッブコー ト法、 バーコ一 ト法、 ロールコー ト法、 ラングミ ュ ァ * ブロゼッ ト法、 インクジェッ ト法) により薄膜を形成するこ とにより作成することができる。
真空蒸着法により、 各層を形成する場合、 真空蒸着の条件は、 特に限定するものではないが、 1 X 1 0 - 4 P a程度の真空下で、 5 0〜 6 0 0 °C程度のポー ト温度 (蒸着源温度) 、 一 5 0〜 3 0 0 °C程度の基板温度で、 0 . 0 0 5 〜 5 0 n m Z s e c程度の蒸 着速度で実施することが好ましい。
この場合、 正孔注入輸送層、 発光層、 電子注入輸送層などの各 層は、 真空下で、 連続して形成することにより、 諸特性に一層優 れた有機電界発光素子を製造することができる。
真空蒸着法により、 正孔注入輸送層、 発光層、 電子注入輸送層 などの各層を、 複数の化合物を用いて形成する場合、 化合物を入 れた各ポートを個別に温度制御して、 共蒸着することが好ましい 溶液塗布法により、 各層を形成する場合、 各層を形成する成分 あるいはその成分とバインダー樹脂を、 溶媒に溶解、 または分散 させて塗布液とする。
正孔注入輸送層、 発光層、 電子注入輸送層の各層に使用しうる バインダー樹脂としては、 ポリ — N —ビニルカルバゾ一ル、 ポリ ァリ レート、 ポリスチレン、 ポリエステル、 ポリ シロキサン、 ポ リ メチルァクリ レー ト、 ポリ メチルメタク リ レー ト、 ボリエーテ ル、 ポリカーボネート、 ポリアミ ド、 ポリイミ ド、 ポリアミ ドィ ミ ド、 ポリパラキシレン、 ポリエチレン、 ポリ フエ二レンォキサ
イ ド、 ポリエーテルスルフォン、 ポリア二リンおよびその誘導体 ポリチォフェンおよびその誘導体、 ポリ フエ二レンビニレンおよ びその誘導体、 ポリ フルオレンおよびその誘導体、 ポリチェニレ ンビニレンおよびその誘導体などの高分子化合物が挙げられる。 バイ ンダー樹脂は、 単独で使用してもよく、 あるいは、 複数併用 してもよい。
溶液塗布法によ り、 各層を形成する場合、 各層を形成する成分 あるいはその成分とバイ ンダー樹脂を、 適当な有機溶媒 (へキサ ン、 オクタン、 デカン、 トルエン、 キシレン、 ェチルベンゼン、 1 —メチルナフタレンなどの炭化水素系溶媒、 アセ トン、 メチル ェチルケ トン、 メチルイソブチルケ トン、 シクロへキサノンなど のケ トン系溶媒、 ジクロロメタン、 クロ口ホルム、 テトラクロ口 メタン、 ジクロロェタン、 ト リ クロロェタン、 テ 卜ラクロ口エタ ン、 クロ口ベンゼン、 ジクロロベンゼン、 クロ口 トルエンなどの 八ロゲン化炭化水素系溶媒、 酢酸ェチル、 酢酸プチル、 酢酸アミ ルなどのエステル系溶媒、 メタノール、 プロパノール、 ブタノー ル、 ペンタノ一ル、 へキサノール、 シクロへキサノール、 メチル セロソルブ、 ェチルセ口ソルブ、 エチレングリコールなどのアル コール系溶媒、 ジブチルエーテル、 テ卜ラヒ ドロフラン、 ジォキ サン、 ァニソ一ルなどのエーテル系溶媒、 N , N —ジメチルホル ムアミ ド、 N , N —ジメチルァセ トアミ ド、 1 ーメチルー 2 —ピ 口リ ドン、 1 ーメチルー 2 —イミダゾリ ジノ ン、 ジメチルスルフ オキサイ ドなどの極性溶媒) および Zまたは水に溶解、 または分 散させて塗布液とし、 各種の塗布法により、 薄膜を形成すること ができる。
尚、 分散する方法としては、 特に限定するものではないが、 ポ —ルミル、 サン ドミル、 ペイントシエ一カー、 ア トライター、 ホ
モジナイザーなどを用いて微粒子状に分散することができる。
塗布液の濃度に関しては、 特に限定するものではなく、 実施する 塗布法によ り、 所望の厚みを作成するに適した濃度範囲に設定す ることができ、 一般には、 0 . 1 〜 5 0重量%程度、 好ましく は. 1 〜 3 0重量%程度の溶液濃度である。
尚、 バイ ンダー樹脂を使用する場合、 その使用量に関しては、 特に制限するものではないが、 一般には、 各層を形成する成分に 対して (一層型の素子を形成する場合には、 各成分の総量に対し て) 、 5〜 9 9 . 9重量%程度、 好ましく は、 1 0〜 9 9 . 9重 量%程度、 より好ましくは、 1 5〜 9 0重量%程度に設定する。
正孔注入輸送層、 発光層、 電子注入輸送層の膜厚に関しては、 特に限定するものではないが、 一般に、 5 n m〜 5 m程度に設 定することが好ましい。
尚、 作製した素子に対し、 酸素や水分との接触を防止する目的 で、 保護層 (封止層) を設けたり、 また、 素子を、 パラフィ ン、 流動パラフィ ン、 シリ コンオイル、 フルォロカーボン油、 ゼオラ ィ ト含有フルォロカーボン油などの不活性物質中に封入して保護 することができる。
保護層に使用する材料としては、 例えば、 有機高分子材料 (例 えば、 フッ素化樹脂、 エポキシ樹脂、 シリ コーン樹脂、 エポキシ シリコーン樹脂、 ポリスチレン、 ポリエステル、 ボリカーボネー ト、 ポリアミ ド、 ポリイミ ド、 ポリアミ ドイミ ド、 ポリパラキシ レン、 ポリ エチレン、 ポリ フエ二レンオキサイ ド) 、 無機材料 (例えば、 ダイヤモンド薄膜、 アモルファスシリカ、 電気絶縁性 ガラス、 金属酸化物、 金属窒化物、 金属炭素化物、 金属硫化物) さ らには光硬化性樹脂を挙げることができ、 保護層に使用する材 料は、 単独で使用してもよく、 あるいは複数併用してもよい。 保
護層は、 一層構造であってもよく 、 また多層構造であってもよい また、 電極に保護層として、 例えば、 金属酸化膜 (例えば、 酸 化アルミニウム膜) 、 金属フッ化膜を設けることもできる。
また、 例えば、 陽極の表面に、 例えば、 有機リ ン化合物、 ポリ シラン、 芳香族ァミン誘導体、 フタロシアニン誘導体から成る界 面層 (中間層) を設けることもできる。
さ らに、 電極、 例えば、 陽極はその表面を、 例えば、 酸、 アン モニァ Z過酸化水素、 あるいはプラズマで処理して使用すること もできる。
本発明の有機電界発光素子は、 一般に、 直流駆動型の素子とし て使用されるが、 交流駆動型の素子としても使用することができ る。 また、 本発明の有機電界発光素子は、 セグメント型、 単純マ ト リ ックス駆動型などのパッシブ駆動型であってもよく、 T F T (薄膜トランジスタ) 型、 M I M (メタル—インスレー夕——メ タル) 型などのアクティブ駆動型であってもよい。 駆動電圧は、 一般に、 2 〜 3 0 V程度である。
本発明の有機電界発光素子は、 例えば、 パネル型光源、 各種の 発光素子、 各種の表示素子、 各種の標識、 各種のセンサーなどに 使用することができる。 実施例
以下、 製造例および実施例により、 本発明を更に詳細に説明す るが、 勿論、 本発明はこれらにより限定されるものではない。 製造例 1 例示化合物番号 A— 5の化合物の製造
9 ーブロモー 1 0 —フエ二ルアン トラセン 3 . 3 3 g 、 9 , 9 ージメチルフルオレン— 2 —ィルホウ酸 2 . 3 8 g、 炭酸ナトリ ゥム 2 . 1 2 gおよびテトラキス ( トリ フエニルフォスフィ ン)
パラジウム 0. 3 5 gをトルエン ( 1 0 0 m l ) および水 ( 5 0 m l ) 中で 5時間加熱還流した。 反応混合物より トルエンを留去 した後、 析出している固体を濾過した。 この固体をシリカゲル力 ラムクロマ トグラフィー (溶出液 : トルエン) で処理した。 トル ェンを減圧下留去した後、 残渣を トルエンとアセ トンの混合溶媒 より再結晶し、 例示化合物 A— 5 の化合物を黄色の結晶として 2 1 8 g得た。
質量分析 : m/ z = 4 4 6
元素分析 : ( C 3 5 H 2 6として)
C H
計算値 (%) 9 4. 1 3 5. 8 7
実測値 (%) 9 4. 2 0 5. 8 0
融点 2 5 0 °C以上
尚、 この化合物は、 3 0 0 、 X 1 0— 4 P aの条件下で昇華 した。
吸収極大 (トルエン中) 3 9 0 n m
製造例 2〜 6 2
製造例 1 において、 9 —ブロモー 1 0 —フエ二ルアントラセン を使用する代わり に、 種々のハロゲン化物を使用し、 9, 9 ージ メチルフルオレン一 2 —ィルホウ酸を使用する代わりに、 種々の ホウ酸誘導体を使用した以外は、 製造例 1 に記載した方法に従い 種々の化合物を製造した。
表 1〜 5 には使用したハロゲン化物、 およびホウ酸誘導体、 な らびに製造した化合物を例示化合物番号で示した。
また、 トルエン中の吸収極大 ( n m) も併せて示した。
尚、 製造された化合物は、 黄色〜橙黄色の結晶であり、 それら の化合物の融点は、 2 5 0 °C以上であった。
表 2
製造例 ハロゲン化物 ホウ酸誘導体 例示化合物 吸収極大 番号 (nm)
18 9ーブロモー 10— (4'— tert—ブチルォキシフエ二 9,9—ジメチルフルオレン一 2—ィルホウ酸 Α-45 393 ル)アントラセン
19 9ーブロモー 10— (4'—フルオロフェニル)アント 9, 9—ジメチルフルオレン一 2—ィルホウ酸 Α-47 393 ラセン
20 9一ブロモ一10—(4' _n—プロピルォキシフエ二 9,9—ジ一 η—プロピルフルオレン一 2—ィルホウ Α-53 395 ル)アントラセン 酸
21 9一プロモー 10— (6'—メ卜キシー 2'—ナフチル) 9, 9ージメチルフルオレン一 2—ィルホウ酸 Α— 55 398 アントラセン
22 9一ブロモ一10— 〔4'一(4"一 n—へキシルォキシ 9, 9ージメチルフルオレン一 2—ィルホウ酸 A-58 400 フエニル)フエニル〕 アントラセン
23 9一ブロモ一10— (9', 9'—ジメチルフルオレン一 2 9, 9-ジー η—ペンチルフルオレン一 2—ィルホウ C-8 398 '一ィル)アントラセン 酸
24 9一プロモー 10— (9'—メチル -9'—フエニルフル 9, 9ージメチルフルオレン一 2—ィルホウ酸 C-12 404 オレン一 2'—ィル)アントラセン
25 9一プロモー 10—(9',9'—ジフエニルフルオレン 9,9—ジメチルフルオレン一 2—ィルホウ酸 C-14 407 一 2' _ィル)アントラセン
26 9一プロモー 10— (9',9'ージフエニルフルオレン 9, 9—ジー η—へキシルフルオレン一 2—ィルホウ C-20 408 -2'一ィル)アントラセン 酸
27 9ーブロモー 10—フエ二ルアン卜ラセン 7 -(9',9'ージメチルフルオレン一 2'—ィル)一9, D 1 405
9—ジメチルフルオレンー2—ィルホウ酸
28 9ーブロモー 10— (4'— n—へキシルフェニル)ァ 7-(9',9'ージメチルフルオレン一 2'—ィル)ー9, D— 8 407 ン卜ラセン 9ージメチルフルオレン一 2—ィルホウ酸
29 9一プロモー 10— (4'—フエニルフエニル)アント 7-(9',9'ージメチルフルオレン一 2'—ィル)一 9, D- 16 408 ラセン 9—ジメチルフルオレン一 2—ィルホウ酸
30 9一プロモー 10_(4'—メトキシフエニル)アント 7-(9',9'—ジメチルフルオレン一 2'—ィル)一9, D— 31 398 ラセン 9ージメチルフルオレン一 2—ィルホウ酸
31 9一プロモー 10—フエ二ルアントラセン 10—(9',9'ージメチルフルオレン一2'—ィル)ァ E— 1 416 ントラセン一 9ーィルホウ酸
32 9ーブロモー 10— 〔4'— (Ν,Ν—ジフエニルァミノ) 10-(9' ,9'—ジメチルフルオレン一 2'—ィル)ァ E-7 414 ントラセン一 9ーィルホウ酸
表 3
製造例 ハロゲン化物 ホウ酸誘導体 例示化合物 吸収極大 番号 (nm)
33 9 ブロモ 10—(4'—フエニルフエニル)アント 10-(9',9'—ジメチルフルオレン 2' ィル)ァ 418 ラセン ントラセン 9—ィルホウ酸
34 9 ブロモ 10— (2' フエニルフエニル)アント 10-(9',9'—ジメチルフルオレン 2'—ィル)ァ E-18 414 ラセン ントラセン— 9ーィルホウ酸
35 9 ブロモ 10_(4'—メトキシフエ二ル)アント 10—(9' 9'—ジメチルフルオレン一 2' ィル)ァ 410 ラセン ン卜ラセン _9 Γルホゥ酸
36 9—プロモー 10— (6'ーメトキシー 2' ナフチル) 10- (9' 9'ージメチルフルオレン 2'—ィル)ァ 420 ントラセン— 9ーィルホウ酸
37 9- (7' ド一 9', 9'—ジメチルフルオレン一 2 10- (9' , 9'ージメチルフルオレン 2' ィル)ァ F-3 410 ィル) 10—(4"—ェチルフエニル)アントラセントラセン 9ーィルホウ酸
ン
38 9一(7' ョードー 9' 9'—ジメチルフルオレン一 2 10— (9' ,9'—ジメチルフルオレン 2'—ィル)ァ 412 ' レ) 10—(3" _フエニルフエ二 _Jレ)アントラ ン卜ラ ンー 9 ^ f Jレホ 酸
セン
39 9- (7'—ョード一 9', 9 ジメチルフルオレン 2 10-(9' ,9'ージメチルフルオレン一 2' ィル)ァ F-24 408 '—ィル)ー10 〔4"_(N,N—ジフエニルァミノ)フントラセン— 9—ィルホウ酸
40 2—ョードー 7—(9',9'ージメチルフルオレン一 2' 10— (9' ,9'—ジメチルフルオレン一 2'—^ fル)ァ G- 1 414 ィル) 9 9—ジメチルフルオレン ントラセン一 9—ィルホウ酸
41 2 ドー 7—(9', 9'ージメチルフルオレン一 2' 10- 〔7' N N—ジ(1 " ナフチル)ァミノ一 9',9' G— 13 414 ィル) -9, 9 ジメチルフルオレン —ジメチレフルオレン 2'—ィル〕 アントラセン
—9—ィルホウ酸
42 2 ョード _7_(9',9'—ジフエニルフルオレン一 10_(9' ,9' ジフェニルフルオレン 2' Γル) G-25 418 2'—ィル) 9, 9ージフエニルフルオレン アントラセン _9ーィルホウ酸
43 9 プロモー 10— (9' 9'ージー n ブチルフルォ 10—(9' 9'—ジメチルフルオレン一 2' ィル)ァ H-7 420 レン 2'—ィル)アントラセン ントラセン 9—ィルホウ酸
44 10—ブロモー 10'— (4" ェチルフエニル) 9, 9' 7- 〔10' _ (4" ェチルフエニル)アントラセン一 S J -3 422 ビアンスリル ィル〕 9,9—ジメチルフルオレン _2_ィルホ
ゥ酸
45 10 ブロモ 10'—(4" _エトキシフエ二ル)— 9,9 7- 〔10' _(4"—エトキシフエニル)アントラセン J-22 422 ビアンスリル 9'ーィル〕 _9 9ージメチルフルオレン 2—ィ
ルホウ酸
ト
表 4
製造例 ノ、ロケノ" f匕物 ホウ酸誘 体 例示化合物 吸収極大
口
¾· (nm)
46 10—ブロモー 10'—(4"—ェチルフエ二ル)一 9,9' 7-(9',9'—ジメチルフルオレン一 2'—ィル)一9, Κ-3 41 6 一ヒアノスリ Jレ 9—ンメナ Jレフルォレノー 2—ィルホヮ酸
47 10—プロモー 10'—(Γ—ナフチル)—9, 9'一ビア 7-(9',9'ージメチルフルオレン一 2'—ィル)一 9, 41 8 ンスリル 9ージメチルフルオレン一 2—ィルホウ酸
48 10—ブロモー 10'— (4"—フエニルフエ二ル)一 9, 9 7-(9',9'ージメチルフルオレン一 2'—ィル)一 9, Κ- 1 6 41 6 '一ビアンスリル 9—ジメチルフルオレン— 2—ィルホウ酸
49 9一(7'—ョード一 9', 9'—ジメチルフルオレン一 2 7—(10'—フエ二ルアントラセン一 9'一^ fル)一 9, L- 1 415 '—ィル)一 10— (9" , 9" -ジメチルフルォレン一 2" 9—ジメチルフルオレン— 2—ィルホウ酸
一^ Jレ)アン卜フセノ
50 9- (7'—ョ一ドー 9',9'ージメチルフルオレン一 2 7— 〔10'—(2"—フエニルフエニル)アントラセン L- 19 41 3 '一ィル)一10— (9",9"ージメチルフルオレン一 2"一 9'ーィル)ー9,9ージメチルフルオレン一 2—ィ
—ィ レ)アン卜ラセン ルホウ酸
5 1 9— (7'—ョードー 9', 9'ージメチルフルオレン一 2 7- 〔10'—(4"一エトキシフエニル)アントラセン L-32 41 3 —ィゾレ)—10— (9 ,9 —ン ナリレノリレオレン一 2 一 9 一イリレ)一 9, 9ーン テレフ Jレオレン一 2—ィ
—ィル)アントラセン ルホウ酸
52 10—ブロモー 10'—(9", 9' 'ージメチルフルオレン 7—(9',9'ージメチルフルオレン一 2'—ィル)一 9, Ν— 1 41 7 一 2—^ レ)一 9, 9一ビアノスリリレ 9—ンメナリレフ Λォレノ一2—ィ レホヮ酸
53 10—プロモー 10'—(9", 9"ージフエニルフルォレ 7- (9' , 9'ージフエニルフルオレン一 2'—ィル)一 420 ンー 2"—ィル)一 9, 9'一ビアンスリル 9, 9ージフエニルフルオレン一 2—ィルホウ酸
54 10—ブロ七一 10 ― (7 — Ν,Ν—ンノエ _Jレズ ϊノ 7— [10 ― (4 ーェナリレフェ一Jレ)アン卜フセノー 9 Ο— 3 422 -9", 9"ージメチルフルオレン一 2"一ィル)一9, 9' '一ィル〕一 9, 9ージメチルフルオレン一 2—ィルホ
—ビアンスリル
55 10—プロモー 10'—(9", 9"—ジメチルフルオレン 7- 〔10'— (2"—ナフチル)アントラセン一 9'—ィ 0— 1 5 424 一 2"—ィル)—9,9'—ビアンスリル ル〕一9,9—ジメチルフルオレン一 2—ィルホウ酸
56 10—ブロモー 10'— (9",9"—ジメチルフルオレン 7- 〔10'—(4"ーメトキシフエニル)アントラセン 0-2 1 41 2 一 2"—ィル)一9, 9'一ビアンスリル — 9'—ィル〕 一 9, 9ージメチルフルオレン一 2—ィ
ルホウ酸
57 10—フエ二ルー 10'—(7"—ョ一ドー 9", 9"ージメ 7- (10'一フエ二ルアントラセン一 9'一ィル)一9, Ρ— 1 424 チルフルオレン一 2"—ィル)一9, 9'—ビアンスリ 9ージメチルフルオレン一 2—ィルホウ酸
ル
■ζ
寸
表 5
ノヽ uヮノ 1 -w ,ノ! 1令 ¾ ΗΧ.¾ΚΧ 番号 (nm)
58 10— (4'—フエニルフエ二ル)— 10'— (7"—ョ一ド 7- 〔10'—(4"—フエニルフエニル)アントラセン P- 16 426 y , y ——ン ナリレノノレ レノ つソレ— g,y y — ίゾレ J g——ンスナソレフノレ レノー ζ—
一ビアンスリル ルホウ酸 '·
59 10— (4'—メトキシフエ二ル)一 10'— (?"—ョ一ド 7- 〔10'—(4"—メトキシフエ二ル)アントラセン P-31 426
9 , 9 ーン >ァノレノリレ^ Γレノー/! ー ノレ;一 — b —Λ)ν\ 一 9, i)—ンメナ Jレノノレオレノー 一 "1"
一ビアンスリル ルホウ酸
60 10-(9',9'ージメチルフルオレン一 2'—ィル)一 1 7— (10'—フエ二ルアントラセン一 9'—ィル)ー9, Q- 1 426 0'—(7"—ョードー 9", 9"ージメチルフルオレン一 9ージメチルフルオレン一 2—ィルホウ酸
2"—ィル)一 9, 9'一ビアンスリル
6 1 10-(9',9'ージメチルフルオレン— 2'—ィル)一 1 7- 〔10'—(4"一 n—ブチルフエニル)アントラセ Q-6 426 0' _ (7"—ョ一ドー 9", 9"ージメチルフルォレン一ン一 9'一ィル〕 一 9,9ージメチルフルオレン一 2—
2"—ィル)一 9, 9'一ビアンスリル ィルホウ酸
62 10—(9',9'—ジメチルフルオレン一 2'—ィル)一 1 7— 〔10' _(4"—メトキシフエニル)アントラセン Q— 31 424 0'一(7"—ョード -9", 9"ージメチルフルオレン—一 9'—ィル〕 一 9, 9ージメチルフルオレン一 2—ィ
2"—ィル)一 9, 9'一ビアンスリル ルホウ酸
製造例 6 3 例示化合物番号 B— 1 の化合物の製造
1 0 —フエ二ルアン トラセン一 9 ーィルホウ酸 5. 9 6 g、 2 7 —ジョー ド一 9 , 9 —ジメチルフルオレン 4. 4 6 g、 炭酸ナ トリウム 4. 2 4 gおよびテトラキス ( トリ フエニルフォスフィ ン) パラジウム 0 . 7 0 g を トルエン ( 1 0 0 m l ) および水 ( 5 0 m l ) 中で 5時間加熱還流した。 反応混合物より トルエン を留去した後、 析出している固体を濾過した。 この固体をシリカ ゲルカラムクロマ トグラフィー (溶出液 : トルエン) で処理した トルエンを減圧下留去した後、 残渣を トルエンとアセ トンの混合 溶媒よ り再結晶し、 例示化合物 B— 1 の化合物を黄色の結晶とし て 4. 8 8 g得た。
質量分析 : mZ z 6 9 8
元素分析 : ( C 5 5 H 3 8として)
C H
計算値 (%) 9 4. 5 2 5. 8
実測値 (%) 9 4. 5 6 5. 4 4
融点 2 5 0 °C以上
尚、 この化合物は、 3 0 0で X 1 0 - 4 P aの条件下で昇華 した。
吸収極大 (トルエン中) 4 2 0 n m
製造例 6 4〜 9 9
製造例 6 3 において、 1 0 —フエ二ルアントラセン— 9 ーィル ホウ酸を使用する代わりに、 種々のホウ酸誘導体を使用し、 2 , 7 —ジョー ドー 9, 9 ージメチルフルオレンを使用する代わり に 種々のジハロゲノ化合物を使用した以外は、 製造例 6 3 に記載し た方法に従い、 種々の化合物を製造した。
表 6〜表 8 には使用したホウ酸誘導体、 およびジハロゲノ化合物
ならびに製造した化合物を例示化合物番号で示した。
また、 トルエン中の吸収極大 ( n m) も併せて示した。
尚、 製造された化合物は、 黄色〜橙黄色の結晶であり、 それらの 化合物の融点は、 2 5 0 °C以上であった。
表 6
酷諸道优 』刁ヽ 1ϋ
畨 (nm)
64 1 n— (Ά'— 千)レフ τ— Jレ1)ァ、 1 ラ 、ノ一 Q—ィ 1 ώ Ρ a ∑j Δ U ルホウ酸
65 10— (9' ; ^レ) 卜ラ 1 ;レ ウ 、 ut j Ϊ R _ Q A I R 酸
66 10— (4,一: Γチ)レフて—ル)アントラセ、/— 9—ィ 2» 71—ジョ一ド一 q q—ジ チ)レフ Jレオレン A 0 0 ルホウ酸
67 10- (4*一^ f ソプロピ レフェニノレ)アントラセ 2 7—ジ 3—ド一 9 9— , チ Jレフ 1レオレ、 B— 9
9ーィルホウ酸
68 10— {4'一 [Ν,Ν—ジ(4"一メチルフエニル)アミノ〕 2, 7—ジョ一ド一 9, 9—ジメチルフルオレン B— 12 420 フエ二ル} アントラセン一 9ーィルホウ酸
69 10-(4'—η—デシルフエニル)アントラセンー9 2, 7—ジョ一ドー 9, 9一ジメチルフルォレン B— 14 422 一^ Π 1 レホゥ酸
70 10— (4'—ェチルフエニル)アントラセン一 9—ィ 2, 7—ジョ一ドー 9, 9—ジェチルフルオレン B - 17 420 ルホゥ酷
71 10— (Γ—ナフチル)アントラセン一 9—ィルホウ 2, 7—ジョ一ドー 9, 9—ジメチルフルオレン B— 19 425 酷
72 10— (4'—フエニルフエニル)アントラセン一 9— 2, 7—ジョ一ドー 9 9—ジメチルフルオレン B-21 427 ィ 1 ル>1 ゥ酸
73 10- (2'一フエニルフエニル)アントラセン一 9— 2, 7—ジョードー 9 9ージメチルフルオレン B-24 425 ィルホウ酸
74 10- {4' - 〔N—フエ二ルー N— (4 "—フエニルフエ 2, 7—ジョード一 9, 9ージメチルフルオレン B- 25 427 ニル)ァミノ〕 フエ二ル} アントラセン一 9—ィル
ホウ酸
75 10— 4'—メトキシフエ二ル) アントラセン一 9一 2,マージ 3—ドー 9, 9ージメチルフルオレン B-40 421 ィルホウ酸
76 10— (4'— n—プロピルォキシフエニル) アントラ 2, 7—ジョードー 9, 9—ジメチルフルオレン B-43 422 セン— 9—ィルホウ酸
77 10— 4'一 tert—ブチルォキシフエニル) アントラ 2 7—ジョ一ドー 9, 9ージメチルフルオレン B-45 423 セン— 9ーィルホウ酸
78 10— 4'—フルオロフェニル) アントラセン一 9一 2 7—ジョ一ドー 9, 9ージメチルフルオレン B-47 423 ィルホウ酸
表 7
製造例 ホウ酸誘導体 ジノ、ロゲノ化合物 例示化合物 吸収極大
( π m)
79 10—(4'—n—プロピルォキシフエニル)アントラ 2, 7—ジョ一ドー 9,9ージ一 η—プロピルフルォレ B— 53 425 ノ一 n - し士 ^JSfc
y つノレ ,ノ^
8 0 10— (6'—メトシキー 2'—ナフチル)アントラセン 2,7—ジョードー 9, 9—ジメチルフルオレン B-55 42 8
y ノレ ¾ ワ^
o 丄 ιυ L^t ¾ n ヽ十 ノレ 十ノノ u— レ ノ 7 ί―——ンココ^^ ~ Γ ― , y—— ;ン5スナノ 1しレ~ノ71しレ +^ rレン D U ェニル〕 アントラセン一 9ーィルホウ酸
O , ンスナノレノソレ^ 3 レン一 つノレ ワ^ Q ―
y, Λ ン5ノ口エ七マダノ t卜 «フでノ し 丄 o y O
8 3 9,9—ジ一 n—ブチルフルオレン一 2—ィルホウ酸 9, 10—ジブ口モアントラセン C一 3 400
84 9, 9—ン一 n—へキンクレス Jレオレン一 2—ィノレ ヮ 9, 10—ンフロモアノ卜フセノ し一 5 400 酸
85 7— 〔Ν,Ν—ン(4 —メチルフェール)ァ ノ〕 一 9,9 9, 10—ンブロモアノトフセン C— 25 397 —ジメチルフルオレン一 2—ィルホウ酸
86 7— LN—フエ一リレ一 — U —ナフテレ)ァ:^ノ J ― 1, 4—ンメチ Jレ— 9, 1ϋ—ンフロモアノ卜フ它ノ C— 8 d 98 9,9—ジメチルフルオレン一 2—ィルホウ酸
8 7 9—ンメテノレフノレすレノ一 —"ノレ ヮ酸 1U, 1U— 9 ——ヒ,ノスリゾレ i一丄 りに
88 10—フエ二ルアントラセン一 9—ィルホウ酸 2—ョ一 7— (7'—ョ 9',9'—ジメチルフ I一 1 422 リレオレン— Z —イノレ一g, 9——ンメァソレノノレすレノ
8 9 10—(4'一 η—プロピルフエニル)アントラセン一 2—ョ一ドー 7— (7'—ョ—ドー 9',9'—ジメチルフ 1—4 422
つ ノレ ヽ'ノ ノしレ 1レ ク ^' 一ィつ ノ Ώ [Λノ— Q 0— キノノ Ϊし"ノ 7ノ Iレ^十) Ϊ
90 10—(4' _フエニルフエニル)アントラセンー9一 2—ョ一ド一7— (7'—ョ一ド一 9',9'ージメチルフ 1 - 16 424 ィルホウ酸 ルオレン一 2'—ィル)一 9, 9—ジメチルフルオレン
9 1 10- 〔4'— (Ν,Ν—ジメチルァミノ)フエニル〕 アン 2—ョ一ド一 7— (7'—ョ一ド一 9', 9'ージメチルフ 1 -3 1 420 トラセン一 9ーィルホウ酸 ルオレン一 2'—ィル)一9, 9ージメチルフルオレン
92 10— (9',9'ージメチルフルオレン一 2'—ィル)ァ 2, 7—ジョードー 9, 9ージメチルフルオレン M- 1 428 ントラセン— 9—ィルホウ酸
93 10— (9',9'ージ一 η—ブチルフルオレン一 2'—ィ 2,7—ジョ一ドー 9,9—ジー n—ブチルフルオレン M— 3 430 ル)アントラセン一 9ーィルホウ酸
94 10—(9',9'ージ一 η—へキシルフルオレン一 2'— 2, 7—ジョ一ド一 9,9—ジ一 n—へキシルフルォレ M- 5 430 ィル)アントラセン一 9ーィルホウ酸 ン
実施例 1
厚さ 2 0 0 n mの I T O透明電極 (陽極) を有するガラス基板 を、 中性洗剤、 アセ トン、 エタノールを用いて超音波洗浄した。 その基板を窒素ガスを用いて乾燥し、 さ らに U V/オゾン洗浄し た後、 蒸着装置の基板ホルダ一に固定した後、 蒸着槽を 4 X 1 0 一4 P aに減圧した。
まず、 I T O透明電極上に、 4 , 4 ' —ビス 〔N—フエ二ルー N— ( 3 " —メチルフエニル) ァミノ〕 ビフエ二ルを蒸着速度 0 2 n m/ s e cで 7 5 n mの厚さに蒸着し、 正孔注入輸送層とし た。
次いで、 その上に、 ビス ( 2 —メチル _ 8 —キノ リ ノ ラー ト) ( 4 一フエエルフェノラ一ト) アルミニウムと例示化合物番号 A 一 5 の化合物を、 異なる蒸着源から、 蒸着速度 0 . 2 n m/ s e cで 5 0 n mの厚さに共蒸着 (重量比 1 0 0 : 0 . 5 ) し、 発光 層とした。
次に、 トリス ( 8 —キノ リ ノラート) アルミニウムを、 蒸着速 度 0 . 2 n m/ s e cで 5 0 n mの厚さに蒸着し、 電子注入輸送 層とした。
さ らにその上に、 マグネシウムと銀を 蒸着速度 0 . 2 n m/ s e cで 2 0 0 n mの厚さに共蒸着 (重 比 1 0 : 1 ) して陰極 とし、 有機電界発光素子を作製した。 尚 蒸着は、 蒸着槽の減圧 状態を保ったまま実施した。
作製した有機電界発光素子に、 乾燥雰囲気下、 1 2 Vの直流電 圧を印加したところ、 5 4 m A Z c m 2の電流が流れた。 輝度 2 4 2 0 c d Zm 2の青緑色の発光が確認された。 実施例 2〜 9 9
実施例 1 において、 発光層の形成に際して、 例示化合物 A— 5 の化合物を使用する代わり に、 例示化合物番号 A— 6 の化合物 (実施例 2 ) 、 例示化合物番号 A— 8 の化合物 (実施例 3 ) 、 例 示化合物番号 A— 9 の化合物 (実施例 4 ) 、 例示化合物番号 A— 1 1 の化合物 (実施例 5 ) 、 例示化合物番号 A— 1 3 の化合物 (実施例 6 ) 、 例示化合物番号 A— 1 4の化合物 (実施例 7 ) 、 例示化合物番号 A— 1 7 の化合物 (実施例 8 ) 、 例示化合物番号 A— 1 9 の化合物 (実施例 9 ) 、 例示化合物番号 A— 2 1 の化合 物 (実施例 1 0 ) 、 例示化合物番号 A— 2 3 の化合物 (実施例 1 1 ) 、 例示化合物番号 A - 2 5の化合物 (実施例 1 2 ) 、 例示化 合物番号 A— 2 6 の化合物 (実施例 1 3 ) 、 例示化合物番号 A—
3 5の化合物 (実施例 1 4 ) 、 例示化合物番号 A— 3 8の化合物 (実施例 1 5 ) 、 例示化合物番号 A— 4 0 の化合物 (実施例 1
6 ) 、 例示化合物番号 A— 4 3の化合物 (実施例 1 7 ) 、 例示化 合物番号 A— 4 5 の化合物 (実施例 1 8 ) 、 例示化合物番号 A—
4 7の化合物 (実施例 1 9 ) 、 例示化合物番号 A— 5 3 の化合物 (実施例 2 0 ) 、 例示化合物番号 A— 5 5 の化合物 (実施例 2
1 ) 、 例示化合物番号 A— 5 8の化合物 (実施例 2 2 ) 、 例示化 合物番号 B— 1 の化合物 (実施例 2 3 ) 、 例示化合物番号 B— 2 の化合物 (実施例 2 4 ) 、 例示化合物番号 B— 3 の化合物 (実施 例 2 5 ) 、 例示化合物番号 B— 6 の化合物 (実施例 2 6 ) 、 例示 化合物番号 B— 9 の化合物 (実施例 2 7 ) 、 例示化合物番号 B— 1 2の化合物 (実施例 2 8 ) 、 例示化合物番号 B— 1 4の化合物 (実施例 2 9 ) 、 例示化合物番号 B — 1 7 の化合物 (実施例 3 0 ) 、 例示化合物番号 B - 1 9 の化合物 (実施例 3 1 ) 、 例示化 合物番号 B— 2 1 の化合物 (実施例 3 2 ) 、 例示化合物番号 B— 2 4の化合物 (実施例 3 3 ) 、 例示化合物番号 B— 2 5の化合物
(実施例 3 4 ) 、 例示化合物番号 B — 4 0 の化合物 (実施例 3 5 ) 、 例示化合物番号 B - 4 3 の化合物 (実施例 3 6 ) 、 例示化 合物番号 B— 4 5 の化合物 (実施例 3 7 ) 、 例示化合物番号 B— 4 7 の化合物 (実施例 3 8 ) 、 例示化合物番号 B— 5 3 の化合物 (実施例 3 9 ) 、 例示化合物番号 B — 5 5 の化合物 (実施例 4 0 ) 、 例示化合物番号 B— 5 8 の化合物 (実施例 4 1 ) 、 例示化 合物番号 C一 1 の化合物 (実施例 4 2 ) 、 例示化合物番号 C一 3 の化合物 (実施例 4 3 ) 、 例示化合物番号 C一 5 の化合物 (実施 例 4 4 ) 、 例示化合物番号 C一 8の化合物 (実施例 4 5 ) 、 例示 化合物番号 C一 1 2の化合物 (実施例 4 6 ) 、 例示化合物番号 C 一 1 4の化合物 (実施例 4 7 ) 、 例示化合物番号 C一 2 0の化合 物 (実施例 4 8 ) 、 例示化合物番号 C一 2 5 の化合物 (実施例 4 9 ) 、 例示化合物番号 C— 2 8 の化合物 (実施例 5 0 ) 、 例示化 合物番号 D— 1 の化合物 (実施例 5 1 ) 、 例示化合物番号 D— 8 の化合物 (実施例 5 2 ) 、 例示化合物番号 D— 1 6の化合物 (実 施例 5 3 ) 、 例示化合物番号 D— 3 1 の化合物 (実施例 5 4 ) 、 例示化合物番号 E— 1 の化合物 (実施例 5 5 ) 、 例示化合物番号 E— 7 の化合物 (実施例 5 6 ) 、 例示化合物番号 E - 1 6 の化合 物 (実施例 5 7 ) 、 例示化合物番号 E— 1 8 の化合物 (実施例 5 8 ) 、 例示化合物番号 E - 2 1 の化合物 (実施例 5 9 ) 、 例示化 合物番号 E— 3 5 の化合物 (実施例 6 0 ) 、 例示化合物番号 F— 3 の化合物 (実施例 6 1 ) 、 例示化合物番号 F — 1 7 の化合物 (実施例 6 2 ) 、 例示化合物番号 F — 2 4の化合物 (実施例 6 3 ) 、 例示化合物番号 G - 1 の化合物 (実施例 6 4 ) 、 例示化合 物番号 G— 1 3の化合物 (実施例 6 5 ) 、 例示化合物番号 G— 2 5 の化合物 (実施例 6 6 ) 、 例示化合物番号 H— 1 の化合物 (実 施例 6 7 ) 、 例示化合物番号 H— 7 の化合物 (実施例 6 8 ) 、 例
示化合物番号 I 一 1 の化合物 (実施例 6 9 ) 、 例示化合物番号 I 一 4の化合物 (実施例 7 0 ) 、 例示化合物番号 I 一 1 6 の化合物 (実施例 7 1 ) 、 例示化合物番号 I 一 3 1 の化合物 (実施例 7 2 ) 、 例示化合物番号 J 一 3の化合物 (実施例 7 3 ) 、 例示化合 物番号 J 一 2 2 の化合物 (実施例 7 4 ) 、 例示化合物番号 K一 3 の化合物 (実施例 7 5 ) 、 例示化合物番号 K一 1 4の化合物 (実 施例 7 6 ) 、 例示化合物番号 K一 1 6の化合物 (実施例 7 7 ) 、 例示化合物番号 L一 1 の化合物 (実施例 7 8 ) 、 例示化合物番号 L一 1 9 の化合物 (実施例 7 9 ) 、 例示化合物番号 L— 3 2 の化 合物 (実施例 8 0 ) 、 例示化合物番号 M— 1 の化合物 (実施例 8 1 ) 、 例示化合物番号 M— 3 の化合物 (実施例 8 2 ) 、 例示化合 物番号 M— 5の化合物 (実施例 8 3 ) 、 例示化合物番号 M— 1 4 の化合物 (実施例 8 4 ) 、 例示化合物番号 M— 1 7 の化合物 (実 施例 8 5 ) 、 例示化合物番号 M— 2 0 の化合物 (実施例 8 6 ) 、 例示化合物番号 M - 2 2 の化合物 (実施例 8 7 ) 、 例示化合物番 号 M— 2 4の化合物 (実施例 8 8 ) 、 例示化合物番号 N— 1 の化 合物 (実施例 8 9 ) 、 例示化合物番号 N— 2 4の化合物 (実施例 9 0 ) 、 例示化合物番号〇一 3 の化合物 (実施例 9 1 ) 、 例示化 合物番号 O— 1 5 の化合物 (実施例 9 2 ) 、 例示化合物番号 O— 2 1 の化合物 (実施例 9 3 ) 、 例示化合物番号 P — 1 の化合物 (実施例 9 4 ) 、 例示化合物番号 P — 1 6 の化合物 (実施例 9 5 ) 、 例示化合物番号 P— 3 1 の化合物 (実施例 9 6 ) 、 例示化 合物番号 Q— 1 の化合物 (実施例 9 7 ) 、 例示化合物番号 Q— 6 の化合物 (実施例 9 8 ) 、 例示化合物番号 Q— 3 1 の化合物 (実 施例 9 9 ) を使用した以外は、 実施例 1 に記載の方法により有機 電界発光素子を作製した。 それぞれの素子に、 乾燥雰囲気下、 1 2 Vの直流電圧を印加したところ、 青色〜青緑色の発光が確認さ
れた。 さらにその特性を調べ、 結果を表 9〜表 1 3 に示した。 比較例 1
実施例 1 において、 発光層の形成に際して、 例示化合物番号 A 一 5 の化合物を使用せずに、 ビス ( 2 —メチル— 8 —キノ リ ノ ラ ー ト) ( 4 一フエニルフエノ ラ一 卜) アルミニウムだけを用いて 5 0 n mの厚さに蒸着し、 発光層とした以外は、 実施例 1 に記載 の方法により有機電界発光素子を作製した。 この素子に、 乾燥雰 囲気下、 1 2 Vの直流電圧を印加したところ、 青色の発光が確認 された。 さらにその特性を調べ、 結果を表 1 3 に示した。
比較例 2
実施例 1 において、 発光層の形成に際して、 例示化合物番号 A 5 の化合物を使用する代わり に、 N —メチルー 2 —メ 卜キシァ ク リ ドンを使用した以外は、 実施例 1 に記載の方法により有機電 界発光素子を作製した。 この素子に、 乾燥雰囲気下、 1 2 Vの直 流電圧を印加したところ、 青色の発光が確認された。 さ らにその 特性を調べ、 結果を表 1 3 に示した。
表 9 有機電界 輝度 亀流 度 発光素子 (c d/m2) (mA/ c m2) 実施例 2 2 3 80 54 実施例 3 2 3 6 0 55 実: «例 4 2 3 2 0 54 実施例 5 2 3 6 0 5 3 実施例 6 2440 5 6 実施例 7 2 340 56 実施例 8 2 3 3 0 5 5 実施例 9 2 3 8 0 54 実 ¾例 1 0 2 3 8 0 54 実; Sg例 1 1 2 3 5 0 56 実施例 1 2 2440 54 実施例 1 3 248 0 53 実旌例 14 2 3 9 0 5 5 実施例 1 5 2 340 54 実旃例 1 6 2 5 1 0 5 5 実旎例 1 7 2 340 5 3 実施例 1 8 242 0 56 実施例 1 9 2 340 54 実施例 2 0 242 0 54 実施例 2 1 2 340 5 5 実施例 2 2 2440 54 実施例 2 3 24 1 0 5 3 実旃例 24 2 3 5 0 5 5 実施例 2 5 2 5 1 0 5 5
有機電界 3^度 電流密] 発光素子 ( c d / m 2) (m A / c m 2) 実旃例 2 6 2 3 7 0 5 4 実旃例 2 7 2 3 2 0 5 4 実旄例 2 8 2 3 4 0 5 4 実施例 2 9 2 3 6 0 5 6 実施例 3 0 2 3 3 0 5 5 実施例 3 1 2 3 7 0 5 4 実施例 3 2 2 3 8 0 5 5 実施例 3 3 2 4 6 0 5 4 実; S6例 3 4 2 3 4 0 5 4 実施例 3 5 2 5 8 0 5 6 実施例 3 6 2 3 4 0 5 4 実施例 3 7 2 4 1 0 5 5 実施例 3 8 2 3 8 0 5 5 実施例 3 9 2 3 8 0 5 5 実 ¾例 4 0 2 4 2 0 5 4 実施例 4 1 2 4 1 0 5 3 実施例 4 2 2 3 5 0 5 5 実施例 4 3 2 3 4 0 5 6 実施例 4 4 2 3 8 0 5 5 実施例 4 5 2 5 0 0 5 6 · 実施例 4 6 2 3 6 0 5 5 実施例 4 7 2 3 4 0 5 6 実施例 4 8 2 3 2 0 5 5 実施例 4 9 2 3 3 0 5 6
有機電界 輝度 竜流 ap度 発光素子 ( c d /m2) (m A/ c m2) 実旃例 5 0 2 5 4 0 5 6 実施例 5 1 2 3 6 0 5 4 実施例 5 2 2 3 4 0 5 5 実旃例 5 3 2 3 8 0 5 4 実施例 5 4 2 3 5 0 5 6 実旃例 5 5 2 4 7 0 5 5 実施例 5 6 2 3 3 0 5 6 実施例 5 7 2 3 5 0 5 3 実旃例 5 8 2 4 6 0 5 5 実施例 5 9 2 3 4 0 5 3 実施例 6 0 2 4 2 0 5 5 実施例 6 1 2 5 3 0 5 6 実旃例 6 2 2 4 4 0 5 4 実施例 6 3 2 3 6 0 5 3 実旌例 6 4 2 3 4 0 5 5 実旌例 6 5 2 3 8 0 5 4 実 ¾例 6 6 2 4 1 0 5 6 実施例 6 7 2 3 9 0 5 5 実施例 6 8 2 3 4 0 5 6 実施例 6 9 2 3 5 0 5 4 実施例 7 0 2 3 7 0 5 5 実施例 7 1 2 4 2 0 5 6 実旃例 7 2 2 4 8 0 5 5 実施例 7 3 2 5 1 0 5 6
表 1 2 有 電界 竜流 度 究光乘子 ( c d Z m (m A/ c m i) 実施例 7 4 2 3 8 0 5 3 実施例 7 5 2 4 6 0 5 4 実旃例 6 2 3 4 0 5 5 実施例 7 7 2 4 8 0 5 5 実施例 7 8 2 3 5 0 5 4 実施例 7 9 2 3 7 0 5 5 実旃例 8 0 2 5 1 0 5 6 実施例 8 1 2 3 3 0 5 6 実施例 8 2 2 3 4 0 5 5 実施例 8 3 2 3 5 0 5 3 実施例 8 4 2 3 5 0 5 5 実施例 8 5 2 4 3 0 5 6 実; ½例 8 6 2 3 4 0 5 6 実施例 8 7 2 3 7 0 5 5 実施例 8 8 2 3 2 0 5 6 実 JS例 8 9 2 3 8 0 5 4 実施例 9 0 2 3 5 0 5 6 実施例 9 1 2 3 7 0 5 5 実施例 9 2 2 3 4 0 5 6 実旄例 9 3 2 3 5 0 5 4· 実旌例 9 4 2 3 7 0 5 5 実施例 9 5 2 4 2 0 5 6 実施例 9 6 2 4 8 0 5 5 実施例 9 7 2 5 1 0 5 6
表 1 3 有機電界 輝度 電流' ¾ί度
発光素子 (c d/m2) (mA/ c m2) 実施例 98 2460 56
実旄例 99 2 380 5 5
比較例 1 1 1 70 82
比較例 2 1 5 50 74 実施例 1 0 0
厚さ 2 0 0 n mの I T O透明電極 (陽極) を有するガラス基板 を、 中性洗剤、 アセ トン、 エタノールを用いて超音波洗浄した。 その基板を窒素ガスを用いて乾燥し、 さらに U V Zオゾン洗浄し た後、 蒸着装置の基板ホルダーに固定した後、 蒸着槽を 4 X 1 0 -4P a に減圧した。
まず、 I T O透明電極上に、 4 , 4 , , 4 " — ト リ ス 〔 N— ( 3 ' ' '—メチルフエニル) — N—フエニルァミ ノ〕 ト リ フエニル アミンを蒸着速度 0. I n mZ s e cで、 5 0 n mの厚さに蒸着 し、 第一正孔注入輸送層とした。
次いで、 4 , 4 ' , 一ビス 〔N—フエ二ルー N— ( 1 " —ナフ チル) ァミノ〕 ビフエエルと例示化合物番号 A— 5 の化合物を、 異なる蒸着源から、 蒸着速度 0 · 2 n m/ s e cで 2 0 n mの厚 さに共蒸着 (重量比 1 0 0 : 5. 0 ) し、 第二正孔注入輸送層を 兼ねた発光層とした。
次いで、 その上に、 ト リス ( 8 —キノ リ ノ ラー ト) アルミニゥ ムを、 蒸着速度 0. 2 n mZ s e c で 5 0 n mの厚さに蒸着し、 電子注入輸送層とした。
さ らにその上に、 マグネシウムと銀を、 蒸着速度 0. 2 n m/ s e cで 2 0 O n mの厚さに共蒸着 (重量比 1 0 : 1 ) して陰極 とし、 有機電界発光素子を作製した。 尚、 蒸着は、 蒸着槽の減圧 状態を保つたまま実施した。
作製した有機電界発光素子に、 乾燥雰囲気下、 1 5 Vの直流電 圧を印加したところ、 6 2 m A Z c m 2の電流が流れた。 輝度 2 6 2 0 c d /m2の青緑色の発光が確認された。
実施例 1 0 1 〜 1 6 2
実施例 1 0 0 において、 発光層の形成に際して、 例示化合物 A 一 5 の化合物を使用する代わり に、 例示化合物番号 A— 6 の化合 物 (実施例 1 0 1 ) 、 例示化合物番号 A— 8の化合物 (実施例 1 0 2 ) 、 例示化合物番号 A— 9 の化合物 (実施例 1 0 3 ) 、 例示 化合物番号 A - 1 1 の化合物 (実施例 1 0 4 ) 、 例示化合物番号 A— 1 4の化合物 (実施例 1 0 5 ) 、 例示化合物番号 A— 1 7 の 化合物 (実施例 1 0 6 ) 、 例示化合物番号 A - 1 9 の化合物 (実 施例 1 0 7 ) 、 例示化合物番号 A— 2 1 の化合物 (実施例 1 0 8 ) 、 例示化合物番号 A— 2 3 の化合物 (実施例 1 0 9 ) 、 例示 化合物番号 A - 4 0の化合物 (実施例 1 1 0 ) 、 例示化合物番号 A— 4 3 の化合物 (実施例 1 1 1 ) 、 例示化合物番号 A— 4 5の 化合物 (実施例 1 1 2 ) 、 例示化合物番号 A - 4 7 の化合物 (実 施例 1 1 3 ) 、 例示化合物番号 A _ 5 3 の化合物 (実施例 1 1 4 ) 、 例示化合物番号 A— 5 5 の化合物 (実施例 1 1 5 ) 、 例示 化合物番号 A - 5 8の化合物 (実施例 1 1 6 ) 、 例示化合物番号 B— 1 の化合物 (実施例 1 1 7 ) 、 例示化合物番号 B— 2 の化合 物 (実施例 1 1 8 ) 、 例示化合物番号 B— 6の化合物 (実施例 1 1 9 ) 、 例示化合物番号 B— 9 の化合物 (実施例 1 2 0 ) 、 例示 化合物番号 B - 1 2の化合物 (実施例 1 2 1 ) 、 例示化合物番号
B — 1 4 の化合物 (実施例 1 2 2 ) 、 例示化合物番号 B — 1 7 の 化合物 (実施例 1 2 3 ) 、 例示化合物番号 B — 1 9 の化合物 (実 施例 1 2 4 ) 、 例示化合物番号 B — 2 1 の化合物 (実施例 1 2 5 ) 、 例示化合物番号 B _ 2 5 の化合物 (実施例 1 2 6 ) 、 例示 化合物番号 B - 4 0 の化合物 (実施例 1 2 7 ) 、 例示化合物番号 B — 4 3 の化合物 (実施例 1 2 8 ) 、 例示化合物番号 B — 4 5 の 化合物 (実施例 1 2 9 ) 、 例示化合物番号 B — 4 7 の化合物 (実 施例 1 3 0 ) 、 例示化合物番号 B — 5 3 の化合物 (実施例 1 3 1 ) 、 例示化合物番号 B — 5 5 の化合物 (実施例 1 3 2 ) 、 例示 化合物番号 B - 5 8の化合物 (実施例 1 3 3 ) 、 例示化合物番号 C一 1 の化合物 (実施例 1 3 4 ) 、 例示化合物番号 C— 3 の化合 物 (実施例 1 3 5 ) 、 例示化合物番号 C一 5 の化合物 (実施例 1 3 6 ) 、 例示化合物番号 C 一 1 2 の化合物 (実施例 1 3 7 ) 、 例 示化合物番号 C一 1 4の化合物 (実施例 1 3 8 ) 、 例示化合物番 号 C一 2 0 の化合物 (実施例 1 3 9 ) 、 例示化合物番号 C一 2 5 の化合物 (実施例 1 4 0 ) 、 例示化合物番号 D— 1 の化合物 (実 施例 1 4 1 ) 、 例示化合物番号 D - 8 の化合物 (実施例 1 4 2 ) 例示化合物番号 E— 1 の化合物 (実施例 1 4 3 ) 、 例示化合物番 号 F — 3 の化合物 (実施例 1 4 4 ) 、 例示化合物番号 G _ l の化 合物 (実施例 1 4 5 ) 、 例示化合物番号 H— 1 の化合物 (実施例 1 4 6 ) 、 例示化合物番号 I 一 1 の化合物 (実施例 1 4 7 ) 、 例 示化合物番号 I 一 4の化合物 (実施例 1 4 8 ) 、 例示化合物番号 J 一 3 の化合物 (実施例 1 4 9 ) 、 例示化合物番号 K一 3 の化合 物 (実施例 1 5 0 ) 、 例示化合物番号 L一 1 の化合物 (実施例 1 5 1 ) 、 例示化合物番号 M— 1 の化合物 (実施例 1 5 2 ) 、 例示 化合物番号 M _ 3 の化合物 (実施例 1 5 3 ) 、 例示化合物番号 M 一 5 の化合物 (実施例 1 5 4 ) 、 例示化合物番号 M - 1 4の化合
物 (実施例 1 5 5 ) 、 例示化合物番号 M— 2 0 の化合物 (実施例 1 5 6 ) 、 例示化合物番号 M— 2 2 の化合物 (実施例 1 5 7 ) 、 例示化合物番号 M— 2 4の化合物 (実施例 1 5 8 ) 、 例示化合物 番号 N— 1 の化合物 (実施例 1 5 9 ) 、 例示化合物番号 O— 3 の 化合物 (実施例 1 6 0 ) 、 例示化合物番号 P— 1 の化合物 (実施 例 1 6 1 ) 、 例示化合物番号 Q— 1 の化合物 (実施例 1 6 2 ) を 使用した以外は、 実施例 1 0 0 に記載の方法により有機電界発光 素子を作製した。 それぞれの素子に、 乾燥雰囲気下、 1 5 Vの直 流電圧を印加したところ、 青色〜青緑色の発光が確認された。 さ らにその特性を調べ、 結果を表 1 4〜表 1 6に示した。
表 1 4 有機電界
発光素子 ( c a / m i) (m A / c i) 実旃例 1 0 1 2 4 5 0 5 6 実施例 1 0 2 2 4 7 0 5 4 実旃例 1 0 3 2 6 4 0 5 4 実施例 1 0 4 2 6 3 0 5 6 実施例 1 0 5 2 5 8 0 5 7 実施例 1 0 6 2 5 3 0 5 5 実施例 1 0 7 2 5 2 0 5 4 実施例 1 0 8 2 4 8 0 5 5 実旌例 1 0 9 2 5 2 0 5 7 実施例 1 1 0 2 4 8 0 5 4 実施例 1 1 1 2 5 4 0 5 5 実施例 1 1 2 2 5 9 0 5 7 実施例 1 1 3 2 4 8 0 5 7 実旃例 1 1 4 2 6 2 0 5 5 実施例 1 1 5 2 4 9 0 5 6 実施例 1 1 6 2 5 5 0 5 4 実旃例 1 1 7 2 6 4 0 6 3 実旃例 1 1 8 2 4 7 0 5 5 実施例 1 1 9 2 4 5 0 5 6 実施例 1 2 0 2 6 2 0 5 4 実施例 1 2 1 2 6 1 0 5 4 実施例 1 2 2 2 5 7 0 5 6 実施例 1 2 3 2 5 5 0 5 5 実施例 1 2 4 2 5 8 0 5 6
実施例 1 6 3
厚さ 2 0 0 nmの I T〇透明電極 (陽極) を有するガラス基板を 中性洗剤、 アセトン、 エタノールを用いて超音波洗净した。 その 基板を窒素ガスを用いて乾燥し、 さ らに UV/オゾン洗浄した後 蒸着装置の基板ホルダーに固定した後、 蒸着槽を 4 X 1 0 _4 P a に減圧した。
まず、 I T O透明電極上に、 4 , 4 ' 一ビス 〔N—フエ二ルー N— ( 3 " 一メチルフエニル) ァミ ノ〕 ビフエニルを蒸着速度 0 2 nmZ s e cで 7 5 n mの厚さに蒸着し、 正孔注入輸送層とし た。
次いで、 その上に、 ビス ( 2 —メチルー 8 —キノ リ ノ ラー ト) ( 4—フエエルフェノラ一ト) アルミニウムと例示化合物番号 A 一 6 の化合物を、 異なる蒸着源から、 蒸着速度 0. 2 nmZ s e cで 5 0 n mの厚さに共蒸着 (重量比 1 0 0 : 1 . 0 ) し、 発光 層とした。
次に、 ト リス ( 8 —キノ リ ノ ラー ト) アルミニウムを、 蒸着速 度 0. 2 n m/ s e cで 5 O n mの厚さに蒸着し、 電子注入輸送 層とした。
さ らにその上に、 マグネシウムと銀を 蒸着速度 0. 2 n / s e c で 2 0 0 n mの厚さに共蒸着 (重 比 1 0 : 1 ) して陰極 とし、 有機電界発光素子を作製した。 尚 蒸着は、 蒸着槽の減圧 状態を保ったまま実施した。
作製した有機電界発光素子に、 乾燥雰囲気下、 1 2 Vの直流電 圧を印加したところ、 5 5 m A / c m 2の電流が流れた。 輝度 2 4 4 0 c d Zm 2の青緑色の発光が確認された。
実施例 1 6 4
実施例 1 6 3 において、 発光層の形成に際して、 ビス ( 2 —メ
チルー 8 _キノ リ ノラート) ( 4一フエニルフエノラー ト) アル ミニゥムと例示化合物 A— 6 の化合物を使用する代わり に、 ビス ( 2 —メチル一 8 —キノ リ ノ ラー ト) アルミニウム一 ーオキソ 一ビス ( 2 —メチル— 8 —キノ リ ノラー ト) アルミニウムと例示 化合物番号 A— 2 1 の化合物を用いて、 5 0 n mの厚さに共蒸着 (重量比 1 0 0 : 2. 0 ) し、 発光層とした以外は、 実施例 1 6 3 に記載の方法により有機電界発光素子を作製した。
作製した有機電界発光素子に、 乾燥雰囲気下、 1 2 Vの直流電 圧を印加したところ、 5 5 m A Z c m 2の電流が流れた。 輝度 2 3 5 0 c dZm2の青緑色の発光が確認された。
実施例 1 6 5
実施例 1 6 3 において、 発光層の形成に際して、 ビス ( 2 —メ チルー 8 —キノ リ ノラート) ( 4—フエエルフエノラー ト) アル ミニゥムと例示化合物 A— 6 の化合物を使用する代わり に、 ビス ( 2 —メチルー 8 —キノ リ ノ ラー 卜) ( 4—フエエルフェノラ一 ト) アルミニウムと例示化合物番号 A— 4 0の化合物を用いて、 5 0 n mの厚さに共蒸着 (重量比 1 0 0 : 1 . 0 ) し、 発光層と した以外は、 実施例 1 6 3 に記載の方法により有機電界発光素子 を作製した。
作製した有機電界発光素子に、 乾燥雰囲気下、 1 2 Vの直流電 圧を印加したところ、 5 4 m A Z c m 2の電流が流れた。 輝度 2 3 2 0 c d /m 2の青緑色の発光が確認された。
実施例 1 6 6
実施例 1 6 3 において、 発光層の形成に際して、 ビス ( 2 —メ チルー 8 _キノ リ ノ ラー ト) ( 4一フエニルフエノ ラ一 ト) アル ミニゥムと例示化合物 A— 6 の化合物を使用する代わりに、 ト リ ス ( 8 —キノ リ ノラート) アルミニウムと例示化合物番号 B— 1
の化合物を用いて、 5 0 n mの厚さに共蒸着 (重量比 1 0 0 : 3 0 ) し、 発光層とした以外は、 実施例 1 6 3 に記載の方法により 有機電界発光素子を作製した。
作製した有機電界発光素子に、 乾燥雰囲気下、 1 2 Vの直流電 圧を印加したところ、 5 4 m A / c m 2の電流が流れた。 輝度 2 3 7 0 c dノ m 2の青緑色の発光が確認された。
実施例 1 6 7
実施例 1 6 3 において、 発光層の形成に際して、 ビス ( 2 —メ チルー 8 —キノ リ ノ ラー 卜) ( 4 —フエニルフエノ ラ一卜) アル ミニゥムと例示化合物 A— 6の化合物を使用する代わりに、 ト リ ス ( 8 —キノ リ.ノ ラー ト) アルミニウムと例示化合物番号 B— 1 2 の化合物を用いて、 5 0 n mの厚さに共蒸着 (重量比 1 0 0 : 6. 0 ) し、 発光層とした以外は、 実施例 1 6 3 に記載の方法に より有機電界発光素子を作製した。
作製した有機電界発光素子に、 乾燥雰囲気下、 1 2 Vの直流電 圧を印加したところ、 5 4 m A Z c m 2の電流が流れた。 輝度 2 3 6 0 c d / m 2の青緑色の発光が確認された。
実施例 1 6 8
実施例 1 6 3 において、 発光層の形成に際して、 ビス ( 2 —メ チル _ 8 —キノ リ ノラー ト) ( 4一フエニルフエノ ラート) アル ミニゥムと例示化合物 A— 6の化合物を使用する代わりに、 ビス ( 2 —メチルー 8 —キノ リ ノ ラー ト) アルミニウム一 i _ォキソ —ビス ( 2 —メチルー 8 —キノ リ ノラート) アルミニウムと例示 化合物番号 C 一 1 の化合物を用いて、 5 0 n mの厚さに共蒸着 (重量比 1 0 0 : 2. 0 ) し、 発光層とした以外は、 実施例 1 6 3 に記載の方法により有機電界発光素子を作製した。
作製した有機電界発光素子に、 乾燥雰囲気下、 1 2 Vの直流電
圧を印加したところ、 5 5 m A / c m 2の電流が流れた。 輝度 2 3 5 0 c dZm2の青緑色の発光が確認された。
実施例 1 6 9
実施例 1 6 3 において、 発光層の形成に際して、 ビス ( 2 —メ チル _ 8 _キノ リ ノ ラート) ( 4一フエニルフエノラート) アル ミニゥムと例示化合物 A— 6の化合物を使用する代わり に、 ト リ ス ( 8 —キノ リ ノラー ト) アルミニウムと例示化合物番号 C一 1 2 の化合物を用いて、 5 0 n mの厚さに共蒸着 (重量比 1 0 0 : 1 0. 0 ) し、 発光層とした以外は、 実施例 1 6 3 に記載の方法 により有機電界発光素子を作製した。
作製した有機電界発光素子に、 乾燥雰囲気下、 1 2 Vの直流電 圧を印加したところ、 5 5 m Aノ c m 2の電流が流れた。 輝度 2 4 4 0 c d Z m 2の青緑色の発光が確認された。
実施例 1 7 0
実施例 1 6 3 において、 発光層の形成に際して、 ビス ( 2 —メ チルー 8 —キノ リ ノ ラ一 卜) ( 4—フエエルフエノラー ト) アル ミニゥムと例示化合物 A— 6の化合物を使用する代わり に、 ビス ( 2, 4一ジメチルー 8 —キノ リ ノ ラー ト) アルミニウム一 ー 才キソ一ビス ( 2 , 4 ージメチル _ 8 _キノ リ ノ ラー ト) アルミ 二ゥムと例示化合物番号 D— 1 の化合物を用いて、 5 0 n mの厚 さに共蒸着 (重量比 1 0 0 : 1 . 0 ) し、 発光層とした以外は、 実施例 1 6 3 に記載の方法により有機電界発光素子を作製した。 作製した有機電界発光素子に、 乾燥雰囲気下、 1 2 Vの直流電圧 を印加したところ、 5 4 m A Z c m 2の電流が流れた。 輝度 2 3 2 0 c d /m 2の青緑色の発光が確認された。
実施例 1 7 1
実施例 1 6 3 において、 発光層の形成に際して、 ビス ( 2 —メ
チル一 8 —キノ リ ノ ラー ト) ( 4—フエニルフエノ ラー ト) アル ミニゥムと例示化合物 A— 6の化合物を使用する代わりに、 ビス
( 2 —メチルー 8 _キノ リ ノラート) アルミニウム— —ォキソ —ビス ( 2 —メチルー 8 —キノ リ ノ ラート) アルミニウムと例示 化合物番号 E — 1 の化合物を用いて、 5 0 n mの厚さに共蒸着
(重量比 1 0 0 : 2 . 0 ) し、 発光層とした以外は、 実施例 1 6 3 に記載の方法により有機電界発光素子を作製した。
作製した有機電界発光素子に、 乾燥雰囲気下、 1 2 Vの直流電圧 を印加したところ、 5 4 m A Z c m 2の電流が流れた。 輝度 2 3 8 0 c d / m 2の青緑色の発光が確認された。
実施例 1 7 2
実施例 1 6 3 において、 発光層の形成に際して、 ビス ( 2 —メ チル一 8 —キノ リ ノ ラー ト) ( 4 一フエニルフエノ ラー ト) アル ミニゥムと例示化合物 A— 6の化合物を使用する代わりに、 ビス ( 2 , 4—ジメチル一 8 —キノ リ ノ ラート) アルミニウム一 n 一 ォキソ一ビス ( 2, 4一ジメチルー 8 —キノ リ ノ ラー ト) アルミ 二ゥムと例示化合物番号 F— 3 の化合物を用いて、 5 0 n mの厚 さに共蒸着 (重量比 1 0 0 : 4. 0 ) し、 発光層とした以外は、 実施例 1 6 3 に記載の方法により有機電界発光素子を作製した。 作製した有機電界発光素子に、 乾燥雰囲気下、 1 2 Vの直流電圧 を印加したところ、 5 5 m A Z c m 2の電流が流れた。 輝度 2 3 4 0 c d /m2の青緑色の発光が確認された。
実施例 1 7 3
実施例 1 6 3 において、 発光層の形成に際して、 ビス ( 2 —メ チル一 8 _キノ リ ノラート) ( 4 一フエエルフエノラート) アル ミニゥムと例示化合物 A— 6 の化合物を使用する代わりに、 ト リ ス ( 8 —キノ リ ノ ラート) アルミニウムと例示化合物番号 M— 1
の化合物を用いて、 5 0 n mの厚さに共蒸着 (重量比 1 0 0 : 3 0 ) し、 発光層とした以外は、 実施例 1 6 3 に記載の方法により 有機電界発光素子を作製した。
作製した有機電界発光素子に、 乾燥雰囲気下、 1 2 Vの直流電 圧を印加したところ、 5 7 m A / c m 2の電流が流れた。 輝度 2 3 8 0 c d Zm2の青緑色の発光が確認された。
実施例 1 7 4
実施例 1 6 3 において、 発光層の形成に際して、 ビス ( 2 —メ チル _ 8 —キノ リ ノラート) ( 4 一フエニルフエノラ一 ト) アル ミニゥムと例示化合物 A— 6 の化合物を使用する代わり に、 ト リ ス ( 8 —キノ リ ノラート) アルミニウムと例示化合物番号 M— 2 0 の化合物を用いて、 5 0 n mの厚さに共蒸着 (重量比 1 0 0 : 6 . 0 ) し、 発光層とした以外は、 実施例 1 6 3 に記載の方法に より有機電界発光素子を作製した。
作製した有機電界発光素子に、 乾燥雰囲気下、 1 2 Vの直流電 圧を印加したところ、 5 8 m A / c m 2の電流が流れた。 輝度 2 3 5 0 c d /m2の青緑色の発光が確認された。
実施例 1 7 5
厚さ 2 0 0 n mの I T O透明電極 (陽極) を有するガラス基板 を、 中性洗剤、 アセ トン、 エタノールを用いて超音波洗浄した。 その基板を窒素ガスを用いて乾燥し、 さ らに U VZオゾン洗浄し た後、 蒸着装置の基板ホルダーに固定した後、 蒸着槽を 4 X 1 0 — 4 P aに減圧した。
まず、 I T O透明電極上に、 4 , 4 ' , 4 " — ト リ ス 〔 N— ( 3 ' ' '—メチルフエニル) 一 N—フエニルァミ ノ〕 ト リ フエ二 ルァミ ンを蒸着速度 0 . 1 n m/ s e cで 3 0 n mの厚さ し、 第一正孔注入輸送層とした。
次いで、 その上に、 4 , 4 , 一 ビス 〔 N — フエ二ルー N — ( 3 " —メチルフエニル) ァミノ〕 ビフエ二ルを、 蒸着速度 0 . 2 n m/ s e cで 4 5 n mの厚さに蒸着し、 第二正孔注入輸送層 とした。
次いで、 その上に、 ビス ( 2 —メチル一 8 —キノ リ ノ ラー ト) ( 4 —フエニルフエノラー トアルミニウム) と例示化合物番号 A 一 5 の化合物を、 異なる蒸着源から、 蒸着速度 0 . 2 nmZ s e c で 5 0 n mの厚さに共蒸着 (重量比 1 0 0 .· 2. 0 ) し、 発光 層とした。
次に、 ト リス ( 8 —キノ リ ノ ラー ト) アルミニウムを、 蒸着速 度 0 . 2 nmZ s e cで 5 O n mの厚さに蒸着し、 電子注入輸送 層とした。
さ らにその上に、 マグネシウムと銀を 蒸着速度 0 . 2 n m/ s e c で 2 0 O n mの厚さに共蒸着 (重 比 1 0 : 1 ) して陰極 とし、 有機電界発光素子を作製した。 尚 蒸着は、 蒸着槽の減圧 状態を保つたまま実施した。
作製した有機電界発.光素子に、 乾燥雰囲気下、 1 2 Vの直流電 圧を印加したところ、 5 6 m A Z c m 2の電流が流れた。 輝度 2 7 8 0 c d /m2の青緑色の発光が確認された。
実施例 1 7 6
実施例 1 7 5 において、 発光層の形成に際して、 ビス ( 2 —メ チル一 8 _キノ リ ノラー ト) ( 4 一フエニルフエノ ラ一 卜) アル ミニゥムと例示化合物 A— 5 の化合物を使用する代わり に、 ビス ( 2, 4 _ジメチルー 8 _キノ リ ノ ラー ト) アルミニウム一 — ォキソ一ビス ( 2 , 4 —ジメチルー 8 —キノ リ ノラー ト) アルミ 二ゥムと例示化合物番号 B — 1 の化合物を用いて、 5 0 n mの厚 さに共蒸着 (重量比 1 0 0 : 1 . 0 ) し、 発光層とした以外は、
実施例 1 Ί 5 に記載の方法により有機電界発光素子を作製した。 作製した有機電界発光素子に、 乾燥雰囲気下、 1 2 Vの直流電圧 を印加したところ、 5 5 m A Z c m 2の電流が流れた。 輝度 2 6 8 0 c d /m2の青緑色の発光が確認された。
実施例 1 7 7
実施例 1 7 5 において、 発光層の形成に際して、 ビス ( 2 —メ チル一 8 —キノ リ ノラー ト) ( 4 —フエニルフエノ ラ一 卜) アル ミニゥムと例示化合物 A— 5 の化合物を使用する代わりに、 ビス ( 2 —メチルー 8 _キノ リ ノラー ト) アルミニウム— —ォキソ 一ビス ( 2 —メチルー 8 —キノ リ ノ ラー 卜) アルミニウムと例示 化合物番号 C 一 1 の化合物を用いて、 5 0 n .mの厚さに共蒸着 (重量比 1 0 0 : 3 . 0 ) し、 発光層とした以外は、 実施例 1 7 5 に記載の方法により有機電界発光素子を作製した。
作製した有機電界発光素子に、 乾燥雰囲気下、 1 2 Vの直流電 圧を印加したところ、 5 7 m A / c m 2の電流が流れた。 輝度 2 6 5 0 c dZm2の青緑色の発光が確認された。
実施例 1 7 8
実施例 1 7 5 において、 発光層の形成に際して、 ビス ( 2 —メ チル一 8 —キノ リ ノラート) ( 4 一フエニルフエノ ラ一 ト) アル ミニゥムと例示化合物 A— 5の化合物を使用する代わりに、 トリ ス ( 8 —キノ リ ノ ラート) アルミニウムと例示化合物番号 D— 1 の化合物を用いて、 5 O n mの厚さに共蒸着 (重量比 1 0 0 : 2 0 ) し、 発光層とした以外は、 実施例 1 7 5 に記載の方法により 有機電界発光素子を作製した。
作製した有機電界発光素子に、 乾燥雰囲気下、 1 2 Vの直流電 圧を印加したところ、 5 5 m A / c m 2の電流が流れた。 輝度 2 4 2 0 c dZm2の青緑色の発光が確認された。
実施例 1 7 9
実施例 1 7 5 において、 発光層の形成に際して、 ビス ( 2 —メ チルー 8 —キノ リ ノ ラー ト) ( 4—フエニルフエノラー ト) アル ミニゥムと例示化合物 A— 5 の化合物を使用する代わり に、 ビス ( 2 —メチルー 8 —キノ リ ノ ラー ト) アルミニウム一 μ —ォキソ 一ビス ( 2 —メチルー 8 —キノ リ ノ ラー ト) アルミニウムと例示 化合物番号 F— 2 4の化合物を用いて、 5 0 n mの厚さに共蒸着 (重量比 1 0 0 : 4. 0 )' し、 発光層とした以外は、 実施例 1 7 5 に記載の方法により有機電界発光素子を作製した。
作製した有機電界発光素子に、 乾燥雰囲気下、 1 2 Vの直流電 圧を印加したところ、 5 8 m A / c m 2の電流が流れた。 輝度 2 6 0 0 c dZm2の青緑色の発光が確認された。
実施例 1 8 0
実施例 1 7 5 において、 発光層の形成に際して、 ビス ( 2 —メ チル一 8 —キノ リ ノ ラー ト) ( 4—フエニルフエノ ラート) アル ミニゥムと例示化合物 A— 5 の化合物を使用する代わりに、 ト リ ス ( 8 —キノ リノ ラート) アルミニウムと例示化合物番号 G— 1 の化合物を用いて、 5 0 n mの厚さに共蒸着 (重量比 1 0 0 : 2 0 ) し、 発光層とした以外は、 実施例 1 7 5 に記載の方法により 有機電界発光素子を作製した。
作製した有機電界発光素子に、 乾燥雰囲気下、 1 2 Vの直流電 圧を印加したところ、 5 4 m A / c m 2の電流が流れた。 輝度 2 4 8 0 c d Z m 2の青緑色の発光が確認された。
実施例 1 8 1
実施例 1 7 5 において、 発光層の形成に際して、 ビス ( 2 —メ チルー 8 —キノ リ ノ ラー ト) ( 4—フエニルフエノ ラー ト) アル ミニゥムと例示化合物 A— 5 の化合物を使用する代わりに、 ビス
( 2 , 4 _ジメチルー 8 —キノ リ ノラート) アルミニウム一 一 ォキソ一ビス ( 2 , 4 _ジメチルー 8 _キノ リ ノ ラー 卜) アルミ 二ゥムと例示化合物番号 K _ 3 の化合物を用いて、 5 0 n mの厚 さに共蒸着 (重量比 1 0 0 : 2. 0 ) し、 発光層とした以外は、 実施例 1 7 5 に記載の方法により有機電界発光素子を作製した。 作製した有機電界発光素子に、 乾燥雰囲気下、 1 2 Vの直流電庄 を印加したところ、 5 3 m A Z c m 2の電流が流れた。 輝度 2 5 1 0 c d Zm 2の青緑色の発光が確認された。
実施例 1 8 2
実施例 1 7 5 において、 発光層の形成に際して、 ビス ( 2 —メ チル _ 8 —キノ リ ノ ラー ト) ( 4 一フエエルフエノラー ト) アル ミニゥムと例示化合物 A— 5 の化合物を使用する代わり に、 ビス ( 2 , 4 一ジメチルー 8 —キノ リ ノ ラー ト) アルミニウム一 ^— ォキソ一ビス ( 2 , 4—ジメチルー 8 —キノ リ ノ ラー ト) アルミ 二ゥムと例示化合物番号 M— 1 の化合物を用いて、 5 0 n mの厚 さに共蒸着 (重量比 1 0 0 : 3. 0 ) し、 発光層とした以外は、 実施例 1 7 5 に記載の方法により有機電界発光素子を作製した。 作製した有機電界発光素子に、 乾燥雰囲気下、 1 2 Vの直流電圧 を印加したところ、 5 6 m A Z c m 2の電流が流れた。 輝度 2 5 3 0 c d / m 2の青緑色の発光が確認された。
実施例 1 8 3
厚さ 2 0 0 n mの I T O透明電極 (陽極) を有するガラス基板 を、 中性洗剤、 アセ トン、 エタノールを用いて超音波洗浄した。 その基板を窒素ガスを用いて乾燥し、 さ らに U VZオゾン洗浄し た後、 蒸着装置の基板ホルダーに固定した後、 蒸着槽を 4 X 1 0 一 4 P aに減圧した。
まず、 I T〇透明電極上に、 4, 4 ' —ビス 〔N—フエニル—
N— ( 3 " 一メチルフエニル) ァミノ〕 ビフエ二ルを蒸着速度 0 2 n mZsecで 7 5 n mの厚さに蒸着し、 正孔注入輸送層とした 次いで、 その上に、 ビス ( 2 —メチル一 8 —キノ リ ノ ラー ト) ( 4一フエニルフエノラート) アルミニウムと例示化合物番号 A _ 2 0 の化合物を、 異なる蒸着源から、 蒸着速度 0. 2 n m/ s e cで 5 0 n mの厚さに共蒸着 (重量比 1 0 0 : 2. 0 ) し、 発 光層とした。
次に、 1, 3 —ビス 〔 5 , ― ( 4 " 一 t e r t—ブチルフエニル) — 1 ' , 3 ' , 4 , 一ォキサジァゾ一ルー 2 ' —ィル〕 ベンゼン を、 蒸着速度 0. 2 n m/ s e cで 5 0 n mの厚さに蒸着し、 電 子注入輸送層とした。
さらにその上に、 マグネシウムと銀を、 蒸着速度 0. 2 n m/ s e cで 2 0 O n mの厚さに共蒸着 (重量比 1 0 : 1 ) して陰極 とし、 有機電界発光素子を作製した。 尚、 蒸着は、 蒸着槽の減圧 状態を保ったまま実施した。
作製した有機電界発光素子に、 乾燥雰囲気下、 1 2 Vの直流電 圧を印加したところ、 5 4 mA/ c m 2の電流が流れた。 輝度 2 3 2 0 c d Zm2の青緑色の発光が確認された。
実施例 1 8 4
実施例 1 8 3 において、 発光層の形成に際して、 ビス ( 2 —メ チルー 8 —キノ リ ノ ラー ト) ( 4 一フエエルフエノ ラー ト) アル ミニゥムと例示化合物 A— 2 0の化合物を使用する代わり に、 ト リス ( 8 —キノ リ ノ ラー ト) アルミニウムと例示化合物番号 E— 2 1 の化合物を用いて、 5 O n mの厚さに共蒸着 (重量比 1 0 0 : 4. 0 ) し、 発光層とした以外は、 実施例 1 8 3 に記載の方 法により有機電界発光素子を作製した。
作製した有機電界発光素子に、 乾燥雰囲気下、 1 2 Vの直流電
圧を印加したところ、 5 6 m A Z c m 2の電流が流れた。 輝度 2 4 3 0 c dZm2の青緑色の発光が確認された。
実施例 1 8 5
実施例 1 8 3において、 発光層の形成に際して、 ビス ( 2—メ チルー 8—キノ リ ノ ラ一 卜) (4一フエニルフエノ ラ一 ト) アル ミニゥムと例示化合物 A— 2 0の化合物を使用する代わりに、 ビ ス ( 2—メチルー 8—キノ リ ノラー ト) アルミニウム一 —ォキ ソ一ビス ( 2 —メチル一 8—キノ リ ノ ラー ト) アルミニウムと例 示化合物番号 L一 1の化合物を用いて、 5 0 nmの厚さに共蒸着 (重量比 1 0 0 : 3. 0 ) し、 発光層とした以外は、 実施例 1 8 3に記載の方法により有機電界発光素子を作製した。
作製した有機電界発光素子に、 乾燥雰囲気下、 1 2 Vの直流電 圧を印加したところ、 5 4 m A / c m 2の電流が流れた。 輝度 2 3 8 0 c d Z m 2の青緑色の発光が確認された。
実施例 1 8 6
厚さ 2 0 0 nmの I TO透明電極 (陽極) を有するガラス基板 を、 中性洗剤、 アセ トン、 エタノールを用いて超音波洗浄した。 その基板を窒素ガスを用いて乾燥し、 さ らに UVZオゾン洗浄し た後、 蒸着装置の基板ホルダーに固定した後、 蒸着槽を 4 X 1 0 — 4 P aに減圧した。
まず、 I T O透明電極上に、 4, 4, 一ビス 〔N—フエ二ルー N - ( 3 " —メチルフエニル) ァミ ノ〕 ビフエニルを蒸着速度 0 2 n m/ s e じ で マ 5 nmの厚さに蒸着し、 正孔注入輸送層とし た。
次いで、 その上に、 例示化合物番号 B— 1 2の化合物を、 蒸着 速度 0. 2 nmZ s e cで 5 0 nmの厚さに蒸着し、 発光層とし た。
次に、 ト リス ( 8 —キノ リ ノラー ト) アルミニウムを、 蒸着速 度 0 . 2 n m/ s e cで 5 0 n mの厚さに蒸着し、 電子注入輸送 層とした。
さ らにその上に、 マグネシウムと銀を 蒸着速度 0 . 2 n m/ s e cで 2 O O n mの厚さに共蒸着 (重 比 1 0 : 1 ) して陰極 とし、 有機電界発光素子を作製した。 尚 蒸着は、 蒸着槽の減圧 状態を保ったまま実施した。
作製した有機電界発光素子に、 乾燥雰囲気下、 1 2 Vの直流電 圧を印加したところ、 5 8 m A / c m 2の電流が流れた。 輝度 2 7 4 0 c d Zm2の青緑色の発光が確認された。
実施例 1 8 7
実施例 1 8 6 において、 発光層の形成に際して、 例示化合物 B 一 1 2 の化合物を使用する代わり に、 例示化合物番号 J — 3 の化 合物を使用した以外は、 実施例 1 8 6 に記載の方法により有機電 界発光素子を作製した。
作製した有機電界発光素子に、 乾燥雰囲気下、 1 2 Vの直流電 圧を印加したところ、 5 6 m A c m 2の電流が流れた。 輝度 2 6 6 0 c d Zm2の青緑色の発光が確認された。
実施例 1 8 8
実施例 1 8 6 において、 発光層の形成に際して、 例示化合物 B 一 1 2 の化合物を使用する代わり に、 例示化合物番号 L 一 1 の化 合物を使用した以外は、 実施例 1 8 6 に記載の方法により有機電 界発光素子を作製した。
作製した有機電界発光素子に、 乾燥雰囲気下、 1 2 Vの直流電 圧を印加したところ、 5 4 m AZ c m 2の電流が流れた。 輝度 2 4 3 0 c d /m2の青緑色の発光が確認された。
実施例 1 8 9
厚さ 2 0 0 n mの I T〇透明電極 (陽極) を有するガラス基板 を、 中性洗剤、 アセ トン、 エタノールを用いて超音波洗浄した。 その基板を窒素ガスを用いて乾燥し、 さ らに U Vノオゾン洗浄し た後、 蒸着装置の基板ホルダ一に固定した後、 蒸着槽を 4 X 1 0 -4P aに減圧した。
まず、 I T〇透明電極上に、 4 , 4 ' —ビス 〔N—フエニル一 N― ( 3 " —メチルフエニル) ァミ ノ〕 ピフヱニルを蒸着速度 0 2 nmZ s e cで 7 5 nmの厚さに蒸着し、 正孔注入輸送層とし た。
次いで、 その上に、 例示化合物番号 A— 5の化合物を、 蒸着速 度 0 . 2 n mZ s e cで 5 O n mの厚さに蒸着し、 発光層とした 次いで、 その上に、 1 , 3 —ビス 〔 5 , 一 ( 4 " 一 t e r t _ブチル フエニル) — 1 , , 3 ' , 4 ' 一ォキサジァゾ一ルー 2 , ―ィ ル〕 ベンゼンを、 蒸着速度 0 . 2 11111/ 3 6 ( で 5 0 11111の厚さ に蒸着し、 電子注入輸送層とした。
さ らにその上に、 マグネシウムと銀を 蒸着速度 0. 2 n mZ s e cで 2 0 O n mの厚さに共蒸着 (重 比 1 0 : 1 ) して陰極 とし、 有機電界発光素子を作製した。 尚 蒸着は、 蒸着槽の減圧 状態を保ったまま実施した。
作製した有機電界発光素子に、 乾燥雰囲気下、 1 4 Vの直流電 圧を印加したところ、 4 4 m A Z c m 2の電流が流れた。 輝度 1
8 2 0 c d Z m 2の青緑色の発光が確認された。
実施例 1 9 0 '
実施例 1 8 9 において、 発光層の形成に際して、 例示化合物 A — 5 の化合物を使用する代わりに、 例示化合物番号 A— 9 の化合 物を使用した以外は、 実施例 1 8 9 に記載の方法によ り有機電界 発光素子を作製した。
作製した有機電界発光素子に、 乾燥雰囲気下、 1 4 Vの直流電 圧を印加したところ、 4 4 mA/ c m2の電流が流れた。 輝度 1 8 2 0 c d /m2の青緑色の発光が確認された。
実施例 1 9 1
実施例 1 8 9 において、 発光層の形成に際して、 例示化合物 A 一 5 の化合物を使用する代わり に、 例示化合物番号 B— 5 5 の化 合物を使用した以外は、 実施例 1 8 9 に記載の方法により有機電 界発光素子を作製した。
作製した有機電界発光素子に、 乾燥雰囲気下、 1 4 Vの直流電 圧を印加したところ、 6 0 m A / c m 2の電流が流れた。 輝度 1 4 8 0 c d Z m 2の青緑色の発光が確認された。
実施例 1 9 2
厚さ 2 0 0 n mの I T O透明電極 (陽極) を有するガラス基板 を、 中性洗剤、 アセ トン、 エタノールを用いて超音波洗浄した。 その基板を窒素ガスを用いて乾燥し、 さ らに UVZオゾン洗浄し た後、 蒸着装置の基板ホルダーに固定した後、 蒸着槽を 4 X 1 0 一 4 P aに減圧した。
まず、 I T O透明電極上に、 4, 4 ' 一ビス 〔N—フエ二ルー N - ( 3 " —メチルフエニル) ァミ ノ〕 ビフエ二ルを蒸着速度 0 2 n m/ s e cで 7 5 n mの厚さに蒸着し、 正孔注入輸送層とし た。
次いで、 その上に、 ト リス ( 8 —キノ リ ノラー ト) アルミニゥ ムと例示化合物番号 A— 1 7 の化合物を、 異なる蒸着源から、 蒸 着速度 0. 2 n m/ s e cで 5 O n mの厚さに共蒸着 (重量比 1 0 0 : 1 . 0 ) し、 電子輸送層を兼ねた発光層とした。
さ らにその上に、 マグネシウムと銀を、 蒸着速度 0. 2 n m/ s e cで 2 0 O n mの厚さに共蒸着 (重量比 1 0 : 1 ) して陰極
とし、 有機電界発光素子を作製した。 尚、 蒸着は、 蒸着槽の減圧 状態を保ったまま実施した。
作製した有機電界発光素子に、 乾燥雰囲気下、 1 2 Vの直流電 圧を印加したところ、 5 3 m A Z c m 2の電流が流れた。 輝度 2 3 2 0 c dZm2の青緑色の発光が確認された。
実施例 1 9 3
実施例 1 9 2 において、 発光層の形成に際して、 ト リス ( 8 — キノ リ ノラート) アルミニウムと例示化合物 A— 1 7 の化合物を 使用する代わり に、 ト リス ( 8 —キノ リ ノラート) アルミニウム と例示化合物番号 B— 1 7 の化合物を用いて、 5 0 n mの厚さに 共蒸着 (重量比 1 0 0 : 1 . 0 ) し、 発光層とした以外は、 実施 例 1 9 2に記載の方法により有機電界発光素子を作製した。
作製した有機電界発光素子に、 乾燥雰囲気下、 1 2 Vの直流電 圧を印加したところ、 5 4 m Aノ c m 2の電流が流れた。 輝度 2 3 4 0 c d /m 2の青緑色の発光が確認された。
実施例 1 9 4
実施例 1 9 3 において、 発光層の形成に際して、 ト リス ( 8 — キノ リ ノラート) アルミニウムと例示化合物 A _ 1 7 の化合物を 使用する代わり に、 ビス ( 2 —メチルー 8 —キノ リ ノ ラー ト) ァ ルミ二ゥム一 —ォキソ一ビス ( 2 —メチルー 8 —キノ リ ノ ラー ト) アルミニウムと例示化合物番号 F— 2 4の化合物を用いて、 5 0 n mの厚さに共蒸着 (重量比 1 0 0 : 2. 0 ) し、 発光層と した以外は、 実施例 1 9 3 に記載の方法により有機電界発光素子 を作製した。
作製した有機電界発光素子に、 乾燥雰囲気下、 1 2 Vの直流電 圧を印加したところ、 5 4 m A Z c m 2の電流が流れた。 輝度 2 3 3 0 c d /m2の青緑色の発光が確認された。
実施例 1 9 5
厚さ 2 0 0 n mの I T O透明電極 (陽極) を有するガラス基板 を、 中性洗剤、 アセ トン、 エタノールを用いて超音波洗浄した。 その基板を窒素ガスを用いて乾燥し、 さ らに U VZオゾン洗浄し た後、 蒸着装置の基板ホルダ一に固定した後、 蒸着槽を 4 X 1 0 一4 P aに減圧した。
まず、 I T O透明電極上に、 例示化合物番号 A— 5 5 の化合物 を蒸着速度 0. 2 n m/ s e cで 5 5 n mの厚さに蒸着し、 発光 層とした。
次いで、 その上に、 1 , 3 —ビス 〔 5 , 一 ( 4 " — t e r t—プチ ルフエニル) 一 1 ' , 3 , , 4, 一ォキサジァゾ一ルー 2 , ーィ ル〕 ベンゼンを、 蒸着速度 0. 2 ]1 111 3 6 (:で 7 5 11 111の厚さ に蒸着し、 電子注入輸送層とした。
さらにその上に、 マグネシウムと銀を 蒸着速度 0. 2 n m/ s e cで 2 0 0 n mの厚さに共蒸着 (重 比 1 0 : 1 ) して陰極 とし、 有機電界発光素子を作製した。 尚 蒸着は、 蒸着槽の減圧 状態を保ったまま実施した。
作製した有機電界発光素子に、 乾燥雰囲気下、 1 4 Vの直流電 圧を印加したところ、 6 O mA/ c m 2の電流が流れた。 輝度 1 5 0 0 c d /m 2の青緑色の発光が確認された。
実施例 1 9 6
実施例 1 9 5 において、 発光層の形成に際して、 例示化合物 A 一 5 5 の化合物を使用する代わりに、 例示化合物番号 B— 5 5 の 化合物を使用した以外は、 実施例 1 9 5 に記載の方法により有機 電界発光素子を作製した。
作製した有機電界発光素子に、 乾燥雰囲気下、 1 4 Vの直流電 圧を印加したところ、 6 0 m A / c m 2の電流が流れた。 輝度 1
4 8 0 c d Zm2の青緑色の発光が確認された。
実施例 1 9 7
厚さ 2 0 0 n mの I T O透明電極 (陽極) を有するガラス基板 を、 中性洗剤、 アセ トン、 エタノールを用いて超音波洗浄した。 その基板を窒素ガスを用いて乾燥し、 さ らに U V Zオゾン洗浄し た。
次に、 I T O透明電極上に、 ポリ — N— ビニルカルバゾ一ル (重量平均分子量 1 5 0 0 0 0 ) 、 例示化合物番号 B - 1 2 の化 合物、 クマリ ン 6 〔 " 3 - ( 2 ' 一べンゾチアゾリル) 一 7 —ジ エチルァミ ノクマリ ン" (緑色の発光成分) 〕 、 および D C M— 1 〔" 4一 (ジシァノメチレン) 一 2 —メチルー 6 — ( 4 ' ージ メチルアミ ノスチリル) 一 4 H—ピラン" (オレンジ色の発光成 分) 〕 を、 それぞれ重量比 1 0 0 : 5 : 3 : 2 の割合で含有する 3重量%のジクロロエタン溶液を用いて、 ディ ップコート法によ り、 4 0 O n mの発光層を形成した。
次に、 この発光層を有するガラス基板を、 蒸着装置の基板ホル ダ一に固定した後、 蒸着槽を 4 X 1 0— 4 P aに減圧した。
さ らに、 発光層の上に、 3 — ( 4 ' 一 tert—ブチルフエニル) 一 4一フエニル一 5 — ( 4 " 一フエエルフェニル) 一 1 , 2 , 4 一 ト リァゾールを蒸着速度 0 . 2 11111 3 € ( で 2 0 11111の厚さ に蒸着した後、 さ らにその上に、 ト リス ( 8 —キノ リ ノラー 卜) アルミニウムを、 蒸着速度 0 . 2 11 ]11 3 6 (:で 3 0 11111の厚さ に蒸着し、 電子注入輸送層とした。
さ らにその上に、 マグネシウムと銀を、 蒸着速度 0. 2 n mZ s e cで 2 0 0 n mの厚さに共蒸着 (重量比 1 0 : 1 ) して陰極 とし、 有機電界発光素子を作製した。 作製した有機電界発光素子 に、 乾燥雰囲気下、 1 2 Vの直流電圧を印加したところ、 7 3 m
AZ c m 2の電流が流れた。 輝度 1 3 5 0 c d /m2の白色の発 光が確認された。
実施例 1 9 8〜 2 0 5
実施例 1 9 7 において、 例示化合物番号 B— 1 2の化合物を使 用する代わりに、 例示化合物番号 B— 4 3 の化合物 (実施例 1 9 8 ) 、 例示化合物番号 C一 3の化合物 (実施例 1 9 9 ) 、 例示化 合物番号 C一 5の化合物 (実施例 2 0 0 ) 、 例示化合物番号 E— 7 の化合物 (実施例 2 0 1 ) 、 例示化合物番号 E— 1 8の化合物 (実施例 2 0 2 ) 、 例示化合物番号 F— 2 4の化合物 (実施例 2 0 3 ) 、 例示化合物番号 I — 4の化合物 (実施例 2 0 4 ) 、 例示 化合物番号 M— 5 の化合物 (実施例 2 0 5 ) を使用した以外は、 実施例 1 9 7 に記載の方法により有機電界発光素子を作製した。 それぞれの素子に、 乾燥雰囲気下、 1 2 Vの直流電圧を印加した ところ、 白色の発光が観察された。 さらにその特性を調べ、 結果 を表 1 7 に示した。
表 1 7 有機電界 辉度 電流 度
発光素子 (c d/m2) (mA/ c m2) 実施例 198 1 280 76
実施例 1 99 1 250 74
実施例 200 1 240 76
実施例 20 1 1 260 75
実施例 202 1 340 75
実施例 203 1 230 73
実施例 204 1 380 7 5
実施例 205 1 260 74 実施例 2 0 6
厚さ 2 0 0 n mの I T O透明電極 (陽極) を有するガラス基板 を、 中性洗剤、 アセトン、 エタノールを用いて超音波洗浄した。 その基板を窒素ガスを用いて乾燥し、 さらに U VZオゾン洗浄し た。
次に、 I T 0透明電極上に、 ポリ 一 N—ビニルカルバゾール (重量平均分子量 1 5 0 0 0 0 ) 、 1 , 3 —ビス 〔 5 ' — ( 4 " 一 t e r t—ブチルフエニル) 一 1 ' ,' 3 , , 4 ' ーォキサジァゾ一 ルー 2 ' —ィル〕 ベンゼンおよび例示化合物番号 C一 3 の化合物 を、 それぞれ重量比 1 0 0 : 3 0 : 3 の割合で含有する 3重量% のジクロロェタン溶液を用いて、 ディ ップコート法により、 3 0 O n mの発光層を形成した。 次に、 こ の発光層を有するガラス基 板を、 蒸着装置の基板ホルダーに固定した後、 蒸着槽を 4 X 1 0 - 4 P aに減圧した。
さ らに、 発光層の上に、 マグネシウムと銀を、 蒸着速度 0. 2 11 111 / 3 6 じで 2 0 0 11 111の厚さに共蒸着 (重量比 1 0 : 1 ) し て陰極とし、 有機電界発光素子を作製した。
作製した有機電界発光素子に、 乾燥雰囲気下、 1 5 Vの直流電 圧を印加したと ころ、 6 6 m A / c m 2の電流が流れた。 輝度 1
5 2 0 c dノ m 2の青緑色の発光が確認された。
実施例 2 0 7
実施例 2 0 6 において、 発光層の形成に際して、 例示化合物番 号 C一 3の化合物を使用する代わりに、 例示化合物番号 M— 3 の 化合物を使用した以外は、 実施例 2 0 6 に記載の方法により有機 電界発光素子を作製した。
作製した有機電界発光素子に、 乾燥雰囲気下、 1 5 Vの直流電 圧を印加したところ、 6 5 mAZ c m2の電流が流れた。 輝度 1 5 4 0 c d /m2の青色の発光が確認された。
比較例 3
実施例 2 0 6 において、 発光層の形成に際して、 例示化合物番 号 C— 3の化合物を使用する代わり に、 1 , 1, 4 , 4ーテトラ フエ二ルー 1, 3 —ブタジエンを使用した以外は、 実施例 2 0 6 に記載の方法により有機電界発光素子を作製した。
作製した有機電界発光素子に、 乾燥雰囲気下、 1 5 Vの直流電 圧を印加したところ、 8 6 m A Z c m 2の電流が流れた。 輝度 7
6 0 c d Zm2の青色の発光が確認された。
実施例 2 0 8
厚さ 2 0 0 n mの I T O透明電極 (陽極) を有するガラス基板 を、 中性洗剤、 アセ トン、 エタノールを用いて超音波洗浄した。 その基板を窒素ガスを用いて乾燥し、 さらに U V/オゾン洗浄し た。
次に、 I T〇透明電極上に、 ポリカーボネー ト (重量平均分子 量 5 0 0 0 0 ) 、 4, 4 ' 一ビス 〔Ν—フエ二ルー Ν— ( 3 " ― メチルフエニル) ァミ ノ〕 ビフエ二ル、 ビス ( 2 —メチルー 8 — キノ リ ノラ一 卜) アルミニウム一 —ォキソ一ビス ( 2 —メチル — 8 —キノ リ ノ ラー ト) アルミニウムおよび例示化合物番号 Α— 5 3 の化合物を、 それぞれ重量比 1 0 0 : 4 0 : 6 0 : 1 の割合 で含有する 3重量%のジクロロェ夕ン溶液を用いて、 ディ ップコ ート法により、 3 0 0 n mの発光層を形成した。
次に、 この発光層を有するガラス基板を、 蒸着装置の基板ホル ダ一に固定した後、 蒸着槽を 4 X 1 0— 4 P aに減圧した。
さらに、 発光層の上に、 マグネシウムと銀を、 蒸着速度 0. 2 ]1 111 3 6 (;で 2 0 0 11 111の厚さに共蒸着 (重量比 1 0 : 1 ) し て陰極とし、 有機電界発光素子を作製した。
作製した有機電界発光素子に、 乾燥雰囲気下、 1 5 Vの直流電 圧を印加したところ、 6 1 m A Z c m 2の電流が流れた。 輝度 9 6 0 c d Zm2の青緑色の発光が確認された。
実施例 2 0 9
実施例 2 0 8 において、 発光層の形成に際して、 例示化合物番 号 A— 5 3 の化合物を使用する代わりに、 例示化合物番号 B— 5 3の化合物を使用した以外は、 実施例 2 0 8 に記載の方法により 有機電界発光素子を作製した。
作製した有機電界発光素子に、 乾燥雰囲気下、 1 5 Vの直流電 圧を印加したところ、 6 2 mA// c m 2の電流が流れた。 輝度 9 7 0 c d Zm2の青色の発光が確認された。
実施例 2 1 0
厚さ 2 0 0 n mの I T O透明電極 (陽極) を有するガラス基板 を、 中性洗剤、 アセ トン、 エタノールを用いて超音波洗浄した。
その基板を窒素ガスを用いて乾燥し、 さ らに UVZオゾン洗浄し た後、 蒸着装置の基板ホルダーに固定した後、 蒸着槽を 4 X 1 0 — 4 P aに減圧した。
まず、 I T O透明電極上に、 4, 4 ' 一ビス 〔N—フエニル— N— ( 1 ' 一ナフチル) ァミノ〕 ビフエニルを蒸着速度 0. 2 n 111 / 3 6 (:で 7 5 11 ]11の厚さに蒸着し、 正孔注入輸送層とした。
次いで、 その上に、 トリス ( 8 —キノ リ ノラー ト) アルミニゥ ムと例示化合物番号 A— 5 の化合物を、 異なる蒸着源から、 蒸着 速度 0. 2 n m/ s e cで 5 O n mの厚さに共蒸着 (重量比 1 0 0 : 3. 0 ) し、 発光層とした。
次に、 ト リス ( 8 —キノ リ ノラー ト) アルミニウムを、 蒸着速 度 0. 2 n m/ s e cで 5 O n mの厚さに蒸着し、 電子注入輸送 層とした。
さらにその上に、 マグネシウムと銀を、 蒸着速度 0. 2 n m/ s e c電界発光素子を作製した。 尚、 蒸着は、 蒸着槽の減圧状態 を保ったまま実施した。
作成した有機電界発光素子に、 乾燥雰囲気下、 l O mAZ c m 2の定電流密度で連続駆動させた。 初期には、 6 . 7 V、 輝度 5 2 0 c d /m 2の青緑色の発光が確認された。 輝度の半減期は 2 4 0 0時間であった。
実施例 2 1 ;! 〜 2 1 8
実施例 2 1 0 において、 例示化合物番号 A— 5の化合物を使用 する代わり に、 例示化合物番号 A— 6 の化合物 (実施例 2 1 1 ) 例示化合物番号 A— 2 3の化合物 (実施例 2 1 2 ) 、 例示化合物 番号 B— 1 の化合物 (実施例 2 1 3 ) 、 例示化合物番号 B— 3 の 化合物 (実施例 2 1 4 ) 、 例示化合物番号 B— 2 4の化合物 (実 施例 2 1 5 ) 、 例示化合物番号 C一 1 の化合物 (実施例 2 1 6 )
例示化合物番号 C一 2 8の化合物 (実施例 2 1 7 ) 、 例示化合物 番号 M— 1の化合物 (実施例 2 1 8 ) を使用した以外は、 実施例 2 1 0に記載の方法により有機電界発光素子を作製した。 それぞ れの素子に、 乾燥雰囲気下、 1 O mAZ c m2の定電流密度で連 続駆動させた。 それぞれの素子からは青色〜青緑色の発光が確認 された。 さ らにその特性を調べ、 結果を表 1 8に示じた。
比較例 4
実施例 2 1 0において、 発光層の形成に際して、 例示化合物番 号 A— 5の化合物を使用する代わり に、 9, 1 0—ジフ エ二ルァ ントラセンを使用した以外は、 実施例 2 1 0に記載の方法により 有機電界発光素子を作製した。
作製した有機電界発光素子に、 乾燥雰囲気下、 1 O mAZ c m 2の定電流密度で連続駆動させた。 素子からは青色の発光が確認 された。 さ らにその特性を調べ、 結果を表 1 8に示した。 表 1 8 有機電界 初期特性
発光素子 輝度 電圧 半減期
(c d/m2) (V) - (h r )
実施例 2 1 1 530 6. 5 2400
実施例 2 1 2 550 6. 4 2300
実施例 2 1 3 540 6. 6 2400
実施例 2 1 4 560 6. 5 2500
実施例 2 1 5 540 6. 6 2300
実施例 2 1 6 540 6. 5 2500
実施例 2 1 7 530 6. 5 2400
実施例 2 1 8 56 0 6. 4 2200
比較例 4 430 7. 2 900
産業上の利用可能性
本発明により、 発光輝度に優れ、 発光寿命の長い有機電界発光 素子を提供することが可能になった。 さ らに、 該発光素子に適し た炭化水素化合物を提供することが可能になつた。