RU2523909C2 - Конъюгаты, содержащие гидрофильные спейсеры линкеров - Google Patents
Конъюгаты, содержащие гидрофильные спейсеры линкеров Download PDFInfo
- Publication number
- RU2523909C2 RU2523909C2 RU2010102044/04A RU2010102044A RU2523909C2 RU 2523909 C2 RU2523909 C2 RU 2523909C2 RU 2010102044/04 A RU2010102044/04 A RU 2010102044/04A RU 2010102044 A RU2010102044 A RU 2010102044A RU 2523909 C2 RU2523909 C2 RU 2523909C2
- Authority
- RU
- Russia
- Prior art keywords
- linker
- compound according
- integer
- numbers
- group
- Prior art date
Links
- 0 CC(CCOC([N+]*)=C)c1ccc(C[S+])cc1 Chemical compound CC(CCOC([N+]*)=C)c1ccc(C[S+])cc1 0.000 description 8
- YVNCSQLEZHOVOJ-PMUOWJKOSA-N CC1(C)OC(C(C(OC)=O)O)[C@@H]1OC[C@@H]1OC(C)(C)OC1 Chemical compound CC1(C)OC(C(C(OC)=O)O)[C@@H]1OC[C@@H]1OC(C)(C)OC1 YVNCSQLEZHOVOJ-PMUOWJKOSA-N 0.000 description 1
- NHUJLFNOBKHVFW-ZEBHPGRWSA-N NC(NC1=O)=Nc2c1nc(CNc(cc1)ccc1C(NCCCC(N[C@@H](CCC(NC[C@@H]([C@H]([C@@H](C(O)=O)O)O)O)=O)C(N[C@@H](CCC(NC[C@@H]([C@H]([C@@H](C(O)=O)O)O)O)=O)C(N[C@@H](CCC(NC[C@@H]([C@H]([C@@H](C(O)=O)O)O)O)=O)C(NCCS)=O)=O)=O)=O)=O)cn2 Chemical compound NC(NC1=O)=Nc2c1nc(CNc(cc1)ccc1C(NCCCC(N[C@@H](CCC(NC[C@@H]([C@H]([C@@H](C(O)=O)O)O)O)=O)C(N[C@@H](CCC(NC[C@@H]([C@H]([C@@H](C(O)=O)O)O)O)=O)C(N[C@@H](CCC(NC[C@@H]([C@H]([C@@H](C(O)=O)O)O)O)=O)C(NCCS)=O)=O)=O)=O)=O)cn2 NHUJLFNOBKHVFW-ZEBHPGRWSA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K9/00—Peptides having up to 20 amino acids, containing saccharide radicals and having a fully defined sequence; Derivatives thereof
- C07K9/001—Peptides having up to 20 amino acids, containing saccharide radicals and having a fully defined sequence; Derivatives thereof the peptide sequence having less than 12 amino acids and not being part of a ring structure
- C07K9/003—Peptides being substituted by heterocyclic radicals, e.g. bleomycin, phleomycin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/54—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic compound
- A61K47/545—Heterocyclic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/56—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule
- A61K47/59—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyureas or polyurethanes
- A61K47/60—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyureas or polyurethanes the organic macromolecular compound being a polyoxyalkylene oligomer, polymer or dendrimer, e.g. PEG, PPG, PEO or polyglycerol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/62—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being a protein, peptide or polyamino acid
- A61K47/65—Peptidic linkers, binders or spacers, e.g. peptidic enzyme-labile linkers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/10—Antimycotics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P33/00—Antiparasitic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P33/00—Antiparasitic agents
- A61P33/02—Antiprotozoals, e.g. for leishmaniasis, trichomoniasis, toxoplasmosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P33/00—Antiparasitic agents
- A61P33/02—Antiprotozoals, e.g. for leishmaniasis, trichomoniasis, toxoplasmosis
- A61P33/04—Amoebicides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P33/00—Antiparasitic agents
- A61P33/10—Anthelmintics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H15/00—Compounds containing hydrocarbon or substituted hydrocarbon radicals directly attached to hetero atoms of saccharide radicals
- C07H15/20—Carbocyclic rings
- C07H15/24—Condensed ring systems having three or more rings
Abstract
Изобретение относится к конъюгатам для доставки лекарственных средств, связывающим рецепторы на клеточной поверхности, которые содержат гидрофильные спейсеры линкера. Указанные конъюгаты предназначены для визуализации, диагностики и лечения болезненных состояний, вызванных популяциями патогенных клеток. 3 н. и 35 з.п. ф-лы, 19 ил., 49 пр.
Description
ПЕРЕКРЕСТНЫЕ ССЫЛКИ НА РОДСТВЕННЫЕ ЗАЯВКИ
По настоящей заявке согласно 35 U.S.C. §119(e) испрашивается приоритет на основании предварительных заявок на патент США № 60/946092 и 61/036186, поданных 25 июня 2007 года и 13 марта 2008 года, соответственно, содержание которых включено в настоящую заявку с помощью ссылки во всей полноте.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к композициям и способам, предназначенным для применения при направленной доставке лекарственных средств. Более конкретно, изобретение направлено на конъюгаты, обеспечивающие доставку лекарственных средств за счет связывания с рецепторами на поверхности клеток и содержащие линкеры с гидрофильными спейсерами, которые предназначены для применения при лечении болезненных состояний, вызванных популяциями патогенных клеток, а также на способы и фармацевтические композиции, в которых применяются и входят такие конъюгаты.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Иммунная система млекопитающих включает средства для распознавания и устранения опухолевых клеток, других патогенных клеток, а также вторгающихся в организм внешних патогенов. Хотя обычно иммунная система создает крепкую линию обороны организма, имеется значительное количество случаев, когда раковые клетки, другие патогенные клетки или инфекционные агенты избегают иммунного ответа организма хозяина и пролиферируют или выживают, что сопровождается патогенными проявлениями в отношении организма хозяина. Были разработаны химиотерапевтические средства и радиационная терапия для устранения, например, реплицирующихся новообразований. Однако многие из существующих в настоящее время химиотерапевтических средств и видов радиационной терапии обладают нежелательными побочными эффектами, поскольку они уничтожают не только патогенные клетки, но также поражают и нормальные клетки организма хозяина, как например, клетки кроветворной системы. Нежелательные побочные эффекты упомянутых противораковых средств подчеркивают потребность в разработке новых видов лечения, селективных в отношении популяции патогенных клеток, и с уменьшенной токсичностью для нормальных клеток организма хозяина.
Исследователями разработаны терапевтические методики для поражения патогенных клеток за счет нацеливания на такие клетки цитотоксических соединений. Во многих из упомянутых методик применяются токсины, конъюгированные с антителами, которые связываются с антигенами, характерными только для патогенных клеток, или избыточно экспрессируемыми ими, в попытке минимизировать доставку токсина к нормальным клеткам. С применением этого подхода были разработаны некоторые иммунотоксины, состоящие из антител, нацеленных на конкретные антигены на патогенных клетках, где антитела были связаны с токсинами, например, рицином, экзотоксином Pseudomonas, токсином Diptheria и фактором некроза опухолей. Эти иммунотоксины нацелены на патогенные клетки, например, опухолевые клетки, несущие специфические антигены, распознаваемые антителами (Olsnes, S., Immunol. Today, 10, pp. 291-295, 1989; Melby, E.L., Cancer Res., 53(8), pp. 1755-1760, 1993; Better, M.D., PCT Publication Number WO 91/07418, published May 30, 1991).
Другой подход к нацеливанию на популяции патогенных клеток, например, раковых клеток или внешних патогенов, в организме хозяина заключается в усилении его собственной иммунной реакции против патогенных клеток во избежание необходимости введения соединений, которые могут также демонстрировать независимую токсичность в отношении хозяина. Одна из описанных стратегий иммунотерапии заключается в связывании антител, например, мультимерных антител, полученных с помощью генной инженерии, с поверхностью опухолевых клеток, так, чтобы константные области этих антител оказались на поверхности клеток, что вызывает уничтожение опухолевых клеток за счет различных процессов, опосредованных иммунной системой (De Vita, V.T., Biologic Therapy of Cancer, 2d ed., Philadelphia, Lippincott, 1995; Soulillou, J.P., U.S. Patent 5672486). Однако эти подходы осложнялись проблемами определения опухоль-специфичных антигенов. Соответственно, необходимы дополнительные соединения и способы для селективного нацеливания на популяции патогенных клеток.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Было обнаружено, что терапевтические средства, диагностические средства и средства визуализации могут быть конъюгированы с другими соединениями с целью регулирования или изменения их поведения, биораспределения, метаболизма и/или клиренса in vivo. В одном из иллюстративных вариантов осуществления настоящего изобретения описаны конъюгаты соединений, которые включают гидрофильные спейсеры линкера. В одном из аспектов описаны конъюгаты соединений, которые включают как гидрофильный спейсер линкера, так и нацеливающий лиганд. Иллюстративным примером таких конъюгатов являются описанные в заявке соединения следующей формулы
B-L-A,
где B представляет собой рецептор-связывающий лиганд, который связывается с рецептором целевой клетки, L представляет собой линкер, который включает один или несколько гидрофильных спейсеров линкера, и A представляет собой диагностическое или терапевтическое средство, или средство визуализации, которые желательно доставить к клетке.
В другом варианте осуществления в заявке описаны не связывающиеся с рецепторами не нацеленные соединения следующей формулы:
L-A,
где L представляет собой линкер, который включает один или несколько гидрофильных спейсеров линкера, и A является диагностическим или терапевтическим средством, или средством визуализации. В одном из вариантов линкер L не включает расщепляемый фрагмент, в другом варианте линкер L включает расщепляемый фрагмент. В другом варианте осуществления как минимум один из гидрофильных спейсеров линкера образован углеводами или включает как минимум один остаток углевода. В одном из вариантов углеводы образуют часть цепи линкера, связывающего фрагменты B и A. В другом варианте углеводы образуют часть боковой цепи, присоединенной к цепи линкера, связывающего фрагменты B и A.
Имеется в виду, что в каждом из описанных выше вариантов осуществления к линкерам, описанным в настоящей заявке, может быть прикреплен более чем один рецептор-связывающий лиганд B. Далее, подразумевается, что к описанным в настоящей заявке линкерам может быть присоединено более чем одно средство A. Такие мультилигандные или мультилекарственные конъюгаты также описаны в настоящей заявке, где линкеры включают гидрофильные фрагменты.
В другом варианте осуществления в заявке описаны соединения, которые снижают поглощение конъюгатов печенью и уменьшают вероятность выведения через печень. В одном из аспектов эти соединения предпочтительно выводятся в результате деятельности почек, а не печени.
Средства, обозначенные буквой A, включают терапевтические лекарственные средства, диагностические средства, средства визуализации и любые другие соединения, которые желательно или преимущественно доставляются к клеткам за счет нацеливания на клеточные рецепторы. Иллюстративные примеры лекарственных средств включают цитотоксические средства, противовоспалительные средства и т.п. Иллюстративные диагностические средства и средства визуализации включают ПЭТ средства визуализации, флуоресцентные средства визуализации, радиолиганды, средства, образующие комплексы с радиолигандами, и другие.
В различных вариантах осуществления соединений, композиций и способов, описанных в настоящей заявке, клетки, на которые можно осуществлять нацеливание терапевтических, диагностических средств и/или средств визуализации А, включают широкий круг клеток, например, не ограничиваясь перечисленными, раковые клетки, бактериальные клетки, опухолевые клетки, моноциты, активированные макрофаги, клетки-предшественники, такие как эндотелиальные клетки-предшественники, другие воспалительные клетки, атеросклеротические бляшки, инфекционные агенты и другие. Нацеливание на клетки осуществляется путем подходящего выбора лиганда B, связывающего клеточные рецепторы. Подразумевается, что селективное или специфичное нацеливание на клетки in vivo может осуществляться за счет выбора рецептора, который преимущественно или избыточно экспрессируется целевой клеткой. В качестве иллюстрации, целевая клетка преимущественно или избыточно экспрессирует рецептор витамина, например, рецепторы фолата.
В другом варианте осуществления описанные в настоящей заявке конъюгаты входят в фармацевтические композиции в количествах, эффективных для лечения заболеваний и болезненных состояний, связанных с патогенными популяциями клеток.
В другом варианте осуществления описанные в настоящей заявке конъюгаты и содержащие их фармацевтические композиции применяются в способах лечения заболеваний и болезненных состояний, связанных с патогенными популяциями клеток.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
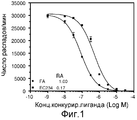
На фиг.1 показано относительное сродство к связыванию EC234, DPM для фолиевой кислоты (●) и EC0234 (■).
На фиг.2 показана активность EC0258 против клеток KB (2 ч пульс/72 ч чейз) для EC258 (●) и EC258 + избыток фолиевой кислоты (○).
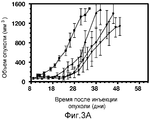
На фиг.3A показано действие EC0234 и EC0246 на опухоли M109 у мышей, контрольные животные, которым не вводили препараты (■), стандарт EC145 (TIW (три раза в неделю) 3 мкмоль/кг, 3 нед.) (●), EC0234 (TIW 3 мкмоль/кг, 3 нед.) (▼) и EC0246 (TIW 3 мкмоль/кг, 3 нед.) (▲).
На фиг.3B показано действие EC0234 и EC0246 на изменение массы тела в процентах, контрольные животные, которым не вводили препараты (■), стандарт EC145 (TIW 3 мкмоль/кг, 3 нед.) (●), EC0234 (TIW 3 мкмоль/кг, 3 нед.) (▼) и EC0246 (TIW 3 мкмоль/кг, 3 нед.) (▲); данные показывают, что во время введения препаратов не наблюдалось явной токсичности.
На фиг.4A показано влияние на объем опухоли KB у мышей EC0396 (▼), EC145 (▲) и контроля PBS (■) при дозировке 2 мкмоль/кг TIW в течение двух недель (вертикальная линия показывает последний день введения).
На фиг.4B показано влияние на изменение массы тела в процентах EC0396 (▼), EC145 (▲) и PBS контроля (■) при дозировке 2 мкмоль/кг TIW в течение двух недель (вертикальная линия показывает последний день введения); данные показывают, что во время введения препаратов не наблюдалось явной токсичности.
На фиг.5A показано влияние на объем опухоли KB EC0400 (●), EC145 (▲) и контроля PBS (■) при дозировке 2 мкмоль/кг TIW в течение двух недель (вертикальная линия показывает последний день введения).
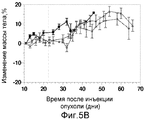
На фиг.5B показано влияние на изменение массы тела в процентах EC0400 (●), EC145 (▲) и контроля PBS (■) при дозировке 2 мкмоль/кг TIW в течение двух недель (вертикальная линия показывает последний день введения); данные показывают, что во время введения препаратов не наблюдалось явной токсичности.
На фиг. 6A показано влияние на объем опухоли EC0429 (
) и EC145 (▲) при дозировке 2 мкмоль/кг TIW в течение двух недель (вертикальная линия показывает последний день введения) по сравнению с контрольными животными, которым не вводили препараты (●), для опухолей М109 у мышей Balb/c.
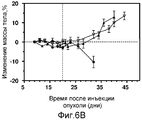
На фиг. 6B показано влияние на изменение массы тела в процентах EC0429 (
) и EC145 (▲) при дозировке 2 мкмоль/кг TIW в течение двух недель (вертикальная линия показывает последний день введения) по сравнению с контрольными животными, которым не вводили препараты (●); данные показывают, что во время введения препаратов не наблюдалось явной токсичности.
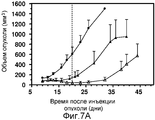
На фиг. 7A показано влияние на объем опухоли EC0434 (∆) и EC145 (▲) при дозировке 2 мкмоль/кг TIW в течение двух недель (вертикальная линия показывает последний день введения) по сравнению с контрольными животными, которым не вводили препараты (●), для s.c. опухолей М109 у мышей Balb/c.
На фиг. 7B показано влияние на изменение массы тела в процентах EC0434 (∆) и EC145 (▲) при дозировке 2 мкмоль/кг TIW в течение двух недель (вертикальная линия показывает последний день введения) по сравнению с контрольными животными, которым не вводили препараты (●); данные показывают, что во время введения препаратов не наблюдалось явной токсичности.
На фиг.8A показано влияние на объем опухоли EC0305(●), EC0436(▼) и контроля PBS (■) при дозировке 2 мкмоль/кг TIW в течение двух недель (вертикальная линия показывает последний день введения) для s.c. опухолей M109 у мышей Bulb/c.
На фиг.8B показано влияние на изменение массы тела в процентах EC0305(●), EC0436(▼) и контроля PBS (■) при дозировке 2 мкмоль/кг TIW в течение двух недель (вертикальная линия показывает последний день введения); данные показывают, что во время введения препаратов не наблюдалось явной токсичности.
На фиг.9 показано процентное изменение массы тела мышей Balb/c, имеющих s.c. опухоли M109, которым внутривенно три раза в неделю в течение одной недели вводили PBS (контрольные животные, не получавшие препаратов) (●), EC0436 (TIW 2 мкмоль/кг) (▲), EC0436 (TIW 2,5 мкмоль/кг) (▼), EC0436 (TIW 3 мкмоль/кг) (■), EC0305 (TIW 2 мкмоль/кг) (∆), EC0305 (TIW 2,5 мкмоль/кг) (
) и EC0305 (TIW 3 мкмоль/кг) (□).
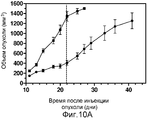
На фиг.10A показано влияние на s.c. (подкожные) опухоли KB у мышей nu/nu EC0565 при введении 3 мкмоль/кг (qdx5 в течение двух недель) (●), по сравнению с контрольными животными, получавшими PBS (■). Из этих данных можно определить значение Log Cell Kill (LCK), равное 1,2 (значения, превышающие примерно 0,7, указывают на активное противораковое соединение).
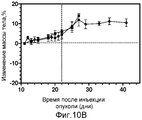
На фиг.10B показано влияние на изменение массы в процентах ЕС0565 при введении 3 мкмоль/кг (qdx5 в течение двух недель) (●), по сравнению с контрольными животными, получавшими PBS (■); данные показывают, что во время введения препаратов не наблюдалось явной токсичности.
На фиг.11 показано общее выведение DAVLBH с желчью из различных конъюгатов DAVLBH при их болюсном i.v. введении 2 мкмоль/кг в гепатобилиарной экскреции при исследовании желчных протоков канюлированных крыс. Измеренная процентная доля общей дозы в желчи составляла для EC145=8,7% (●), EC409=7,9% (♦), EC0429=8,6% (▄), EC0434=2,8% (▼). Кроме того, EC145 продемонстрировал AUC=1092 (●); последнее время отбора проб было 139 мин; и EC0434 продемонстрировал AUC=260 (▄); во все моменты времени 120, 135 и 360 минут результаты были ниже предела количественного обнаружения, т.е. <0,65 мкМ.
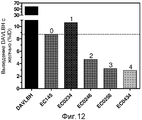
На фиг.12 показано влияние спейсеров на основе рибозы на выведение с желчью, а также результат введения в линкер производных большей длины. Числа над прямоугольниками гистограммы соответствуют количеству гидрофильных спейсеров в линкере.
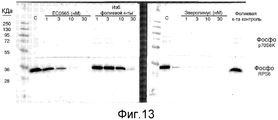
На фиг.13 показано, что EC0565 вызывает зависимое от дозы ингибирование RPS6 и p70S6K в клетках KB (1 ч пульс/4 ч чейз) при использовании экспозиции камеры 30 мин, где C=контроль (необработанные клетки); FAC=контрольный образец фолиевой кислоты (100 мкМ).
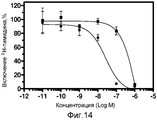
На фиг.14 показана цитотоксичность бортезомиба по сравнению с метилтиольным производным бортезомиба (EC0501). IC50 бортезомиб, 20 нМ (●), EC0501, 240 нМ (▄).
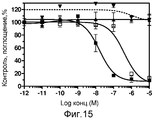
На фиг.15 показано, что гидрофильные спейсеры линкеров делают возможной специфическую активность конъюгатов моно- и бис-тио-велкейд-фолат против клеток RAW264.7. Выживаемость клеток после 5 ч пульса и 72 ч чейза (MTT); бортезомиб (■), EC0501 (□), EC0522 (▲), EC0522 плюс избыток фолиевой кислоты (
).
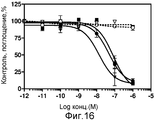
На фиг.16 показана выживаемость клеток (5 ч пульс/72 ч чейз) (XTT) после обработки EC0595 (13 нМ IC50) (▼), EC0595 плюс избыток фолиевой кислоты (
), бортезомибом (■), EC0525 (46 нМ, IC50) (●), EC0525 плюс избыток фолиевой кислоты (○).
На фиг.17 показана выживаемость клеток после 24 ч инкубирования (XTT) с бортезомибом (■), EC0587 (●), EC0587 плюс избыток фолиевой кислоты (○).
На фиг.18 показано ингибирование стимулированной LPS активности протеосомы в клетках RAW 264.7 (5 ч пульс/24 ч чейз), LPS 100 нг/мл, время реакции 30 м 20S протеосома/субстрат при действии бортезомиба (■), EC0522 (▼), EC0522 плюс избыток фолиевой кислоты (
), EC0525 (●), EC0525 плюс избыток фолиевой кислоты (○), EC0595 (♦), EC0595 плюс избыток фолиевой кислоты (□); IC50 составляет примерно 30 нМ для EC0595 и EC0525.
На фиг.19 показана активность против клеток RAW (5 ч пульс/72 ч чейз) после обработки α-амантином (■), EC0592 (IC50 3,7 нМ) (●), EC0592 плюс избыток фолиевой кислоты (○).
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В настоящей заявке описаны конъюгаты для доставки лекарственных средств, состоящие из рецептор-связывающего лиганда (B), поливалентного линкера (L), включающего один или несколько гидрофильных спейсеров, а также диагностического или терапевтического средства, или средства визуализации (A), которое желательно доставить к клетке. Связывающий лиганд (B) ковалентно присоединен к поливалентному линкеру (L), и диагностическое или терапевтическое средство, или средство визуализации (A) или его аналог или производное также ковалентно присоединено к поливалентному линкеру (L). Следует понимать, что диагностическое или терапевтическое средство или средство визуализации (A) включает его аналоги или производные, которые присоединены к линкеру (L). Поливалентный линкер (L) включает один или несколько спейсеров линкера и/или расщепляемых фрагментов, а также их комбинации в любом порядке. В одном из вариантов расщепляемые фрагменты линкера и необязательные спейсеры линкера ковалентно связаны друг с другом с образованием линкера. В другом варианте расщепляемый линкер непосредственно присоединен к средству (A), его аналогу или производному. В другом варианте расщепляемый линкер непосредственно присоединен к связывающему лиганду. В другом варианте или связывающий лиганд, или средство (A), или его аналог или производное, либо обе эти структурные единицы присоединены к расщепляемому фрагменту линкера через один или несколько спейсеров линкера. В другом варианте и связывающий лиганд, и средство (A) или его аналог или производное, присоединены к расщепляемым линкерам, каждый из которых может быть непосредственно связан с другим таким же расщепляемым линкером, или же ковалентно соединен с ним через один или несколько спейсеров линкера.
Из предыдущего описания следует понять, что расположение связывающего лиганда и средства (A), его аналога или производного, а также различных расщепляемых и необязательных спейсеров линкера может изменяться в широких пределах. В одном из аспектов связывающий лиганд и средство (A) или его аналог или производное, а также различные расщепляемые и необязательные спейсеры линкеров присоединены друг к другу через гетероатомы, например, азот, кислород, серу, фосфор, кремний и т.п. В различных вариантах гетероатомы, за исключением кислорода, могут иметь различные степени окисления, например, N(OH), S(O), S(O)2, P(O), P(O)2, P(O)3 и т.п. В других вариантах гетероатомы могут быть сгруппированы с образованием двухвалентных радикалов, как, например, в остатках гидроксиламинов, гидразинов, гидразонов, сульфонатов, фосфинатов, фосфонатов и т.п., включая радикалы формул -(NHR1NHR2)-, -SO-, -(SO2)- и -N(R3)O-, где каждый из фрагментов R1, R2 и R3 независимо выбран из водорода, алкила, арила, арилалкила, замещенного арила, замещенного арилалкила, гетероарила, замещенного гетероарила и алкоксиалкила. В другом варианте к поливалентному линкеру присоединен более чем один связывающий лиганд. В другом варианте к поливалентному линкеру присоединено более чем одно средство (A). В другом варианте к поливалентному линкеру присоединен более чем один связывающий лиганд и более чем одно средство (A).
В одном из вариантов осуществления рецептор-связывающий лиганд представляет собой лиганд, связывающий рецептор витамина, например, витамин или его аналог или производное, способное связываться с рецептором витамина. В другом варианте осуществления связывающий лиганд представляет собой витамин или его аналог или производное, присоединенное к расщепляемому линкеру, который присоединен к лекарственному средству через линкер, образованный одним или несколькими спейсерами линкера, и/или расщепляемыми фрагментами линкера, и/или гидрофильными спейсерами линкера. В одном из вариантов и лекарственное средство, и витамин или его аналог или производное могут быть присоединены к спейсерам линкеров, где упомянутые спейсеры линкеров соединены друг с другом через один или несколько расщепляемых фрагментов линкера. Кроме того, как лекарственное средство, так и витамин или его аналог или производное, могут быть присоединены к одному или нескольким расщепляемым линкерам, где расщепляемые линкеры соединены друг с другом или через спейсер линкера. Каждый из этих радикалов может быть соединен с другими через существующие или дополнительные гетероатомы, входящие в связывающий лиганд, агент A или расщепляемый, гидрофильный спейсер, или дополнительный спейсер линкера.
Сайт связывания связывающего лиганда (B) может включать рецепторы для любого связывающего лиганда (B), его производного или аналога, способного специфично связываться с рецептором, где рецептор или другой белок исключительно экспрессируется, избыточно экспрессируется или преимущественно экспрессируется популяцией патогенных клеток. Представленный на поверхности белок, который исключительно экспрессируется, избыточно экспрессируется или преимущественно экспрессируется патогенными клетками, как правило, является рецептором, который либо не присутствует на непатогенных клетках, либо присутствует в более низких концентрациях, что обеспечивает возможность селективного уничтожения, мечения или диагностирования патогенных клеток. Конъюгаты для доставки лекарственных средств, содержащие связывающий лиганд, могут обладать способностью с высоким сродством связываться с рецепторами на раковых клетках или на других типах патогенных клеток. Связывание с высоким сродством может быть присуще самому связывающему лиганду или же сродство к связыванию можно улучшить применением химически модифицированного лиганда (например, аналога или производного витамина).
Описанные в настоящем изобретении конъюгаты для доставки лекарственных средств, содержащие связывающий лиганд, могут быть получены, например, из широкого круга витаминов или рецептор-связывающих аналогов/производных витаминов, линкеров и лекарственных средств. Описанные в настоящем изобретении конъюгаты для доставки лекарственных средств, содержащие связывающий лиганд, способны к селективному нацеливанию на популяцию патогенных клеток в организме животного-хозяина благодаря преимущественной экспрессии на поверхности патогенных клеток рецептора связывающего лиганда, например, витамина, доступного для связывания с лигандом. Иллюстративные витаминные фрагменты, которые можно применять в качестве связывающих лигандов (B), включают карнитин, инозит, липоевую кислоту, пиридоксаль, аскорбиновую кислоту, никотиновую кислоту, пантотеновую кислоту, фолиевую кислоту, рибофлавин, тиамин, биотин, витамин B12, другие водорастворимые витамины, витамины группы B и жирорастворимые витамины A, D, E и K. Эти витамины и их рецептор-связывающие аналоги и производные представляют собой иллюстративные нацеливающие фрагменты, которые могут быть сшиты с лекарственным средством с помощью двухвалентного линкера (L) с получением описанного в настоящей заявке конъюгата для доставки лекарственного средства, содержащего связывающий лиганд (B). Подразумевается, что термин «витамин» включает аналоги и/или производные витаминов, если не указано иное. В качестве иллюстрации, витаминами, аналогами витаминов и производными витаминов считаются птероевая кислота, которая является производным фолата, аналоги биотина, такие как биоцитин, биотин сульфоксид, оксибиотин и другие соединения, связывающие рецептор биотина, и т.п. Следует понимать, что термин «аналоги или производные витаминов» в настоящем описании относится к витаминам, которые включают гетероатом, через который аналоги или производные витаминов ковалентно связаны с двухвалентным линкером (L).
Иллюстративные примеры витаминных фрагментов включают фолиевую кислоту, биотин, рибофлавин, тиамин, витамин B12 и рецептор-связывающие аналоги и производные этих витаминных молекул, а также другие родственные рецептор-связывающие молекулы витаминов.
В другом варианте осуществления клеточный рецептор представляет собой рецептор фолата, и нацеливающий лиганд B представляет собой лиганд, связывающий рецептор фолата. В другом варианте осуществления B представляет собой фолат, например, фолиевую кислоту или аналог или производное фолиевой кислоты, которое связывается с рецепторами фолиевой кислоты. Следует понимать, что в настоящей заявке термин «фолат» применяется в индивидуальном и обобщающем смысле для обозначения самой фолиевой кислоты и/или таких аналогов и производных фолиевой кислоты, которые способны связываться с рецепторами фолата. В другом варианте осуществления B представляет собой соединение, способное селективно или специфично связываться с рецептором фолата, например, антитело.
Иллюстративные варианты осуществления аналогов и/или производных фолатов включают фолиниевую кислоту, птерополиглутаминовую кислоту и птеридины, связывающие рецептор фолата, например, тетрагидроптерины, дигидрофолаты, тетрагидрофолаты и их деаза и дидеаза аналоги. Термины «деаза» и «дидеаза» аналоги относятся к известным в технике аналогам, в которых один или два атома азота в природной структуре фолиевой кислоты, ее аналога или производного, заменены на атомы углерода. Например, деаза аналоги включают 1-деаза, 3-деаза, 5-деаза, 8-деаза и 10-деаза аналоги фолата. Дидеаза аналоги включают, например, 1,5-дидеаза, 5,10-дидеаза, 8,10-дидеаза и 5,8-дидеаза аналоги фолата. Другие фолаты, применимые в качестве комплексообразующих лигандов, включают рецептор-связывающие аналоги фолатов аминоптерин, аметоптерин (метотрексат), N10-метилфолат, 2-деаминогидроксифолат, деаза аналоги, такие как 1-деазаметоптерин или 3-деазаметоптерин и 3',5'-дихлор-4-амино-4-дезокси-N10-метилптероилглутаминовая кислота (дихлорметотрексат). Упомянутые аналоги и/или производные фолиевой кислоты обычно именуют фолатами, что отражает их способность связываться с рецепторами фолатов, и эти лиганды в случае образования конъюгатов с экзогенными молекулами проявляют эффективность в улучшении трансмембранного транспорта, например, путем описанного в настоящей заявке опосредованного фолатами эндоцитоза. Другие подходящие связывающие лиганды, способные связывать рецепторы фолатов для инициирования опосредованного рецепторами эндоцитотического транспорта комплекса, включают антитела к рецептору фолатов. Экзогенную молекулу в комплексе с антителом к рецептору фолатов применяют для запуска трансмембранного транспорта комплекса.
Дополнительные аналоги фолиевой кислоты, которые связываются с рецепторами фолиевой кислоты, описаны в опубликованных заявках на патент США с № 2005/0227985 и 2004/0242582, содержание которых включено в настоящую заявку посредством ссылки. Иллюстративно, такие аналоги фолатов имеют следующую общую формулу:
где каждый из заместителей X и Y независимо выбран из группы, состоящей из галогена, R2, OR2, SR3 и NR4R5;
U, V и W представляют собой двухвалентные фрагменты, каждый из которых независимо выбран из группы, состоящей из -(R6a)C=, -N=, -(R6a)C(R7a)- и -N(R4a)-; фрагмент Q выбран из группы, состоящей из C и CH; фрагмент T выбран из группы, состоящей из S, O, N и -C=C-;
каждый из фрагментов A1 и A2 независимо выбран из группы, состоящей из кислорода, серы, -C(Z), -C(Z)O-, -OC(Z)-, -N(R4b)-, -C(Z)N(R4b)-, -N(R4b)C(Z)-, -OC(Z)N(R4b)-, -N(R4b)C(Z)O-, -N(R4b)C(Z)N(R5b)-, -S(O)-, -S(O)2-, -N(R4a)S(O)2-, -C(R6b)(R7b)-, -N(C≡CH)-, -N(CH2C≡CH)-, C1-C12 алкилена и C1-C12 алкиленокси, где Z представляет собой кислород или серу;
заместитель R1 выбран из группы, состоящей из водорода, галогена, C1-C12 алкила и C1-C12 алкокси; каждый из заместителей R2,R3,R4,R4a,R4b,R5,R5b,R6b и R7b независимо выбран из группы, состоящей из водорода, галогена, C1-C12 алкила, C1-C12 алкокси, C1-C12 алканоила, C1-C12 алкенила, C1-C12 алкинила, (C1-C12 алкокси)карбонила и (C1-C12 алкиламино)карбонила;
каждый из заместителей R6 и R7 независимо выбран из группы, состоящей из водорода, галогена, C1-C12 алкила и C1-C12 алкокси; или R6 и R7 совместно образуют карбонильную группу; каждый из заместителей R6a и R7a независимо выбран из группы, состоящей из водорода, галогена, C1-C12 алкила и C1-C12 алкокси; или R6a и R7a совместно образуют карбонильную группу;
L представляет собой двухвалентную группу, описанную в настоящей заявке; и
каждый из коэффициентов n, p, r, s и t независимо означает 0 или 1.
Следует понимать, что в настоящем описании термин «фолат» относится и непосредственно к фолиевой кислоте, применяемой при получении конъюгата, или, в качестве альтернативы, к аналогам или производным фолатов, которые способны связываться с рецепторами фолатов или фолиевой кислоты.
В одном из аспектов, в указанных аналогах фолатов, если s равно 1, t представляет собой 0, и если s равно 0, t означает 1. В другом аспекте в указанных аналогах фолатов оба коэффициента n и r равны 1, и линкер La представляет собой природную аминокислоту, ковалентно связанную с A2 и ее альфа-аминогруппой посредством амидной связи. Иллюстративные примеры аминокислот включают аспарагиновую кислоту, глутаминовую кислоту, лизин, цистеин и т.п.
Витамин может представлять собой фолат, который включает азот, и в этом варианте осуществления спейсерами линкера могут являться алкиленкарбонил, циклоалкиленкарбонил, карбонилалкилкарбонил, 1-алкиленсукцинимид-3-ил, 1-(карбонилалкил)сукцинимид-3-ил, где каждый из спейсеров линкера необязательно замещен заместителем X1, и спейсер линкера связан с атомом азота фолата с образованием имида или алкиламида. В этом варианте осуществления заместитель X1 может представлять собой алкил, гидроксиалкил, амино, аминоалкил, алкиламиноалкил, диалкиламиноалкил, сульфгидрилалкил, алкилтиоалкил, арил, замещенный арил, арилалкил, замещенный арилалкил, карбокси, карбоксиалкил, гуанидиноалкил, R4-карбонил, R5-карбонилалкил, R6-ациламино и R7-ациламиноалкил, где каждый из заместителей R4 и R5 независимо выбран из аминокислот, производных аминокислот и пептидов, и где каждый из заместителей R6 и R7 независимо выбран из аминокислот, производных аминокислот и пептидов.
Иллюстративные варианты осуществления аналогов и/или производных витаминов включают также аналоги и производные биотина, например, биоцитин, биотинсульфоксид, оксибиотин, а также другие соединения, связывающие рецептор биотина, и т.п. Предполагается, что аналоги и производные других витаминов, описанных в настоящей заявке, также рассматриваются в настоящем изобретении. В одном из вариантов осуществления витамины, которые могут применяться в качестве связывающего лиганда (B) в конъюгатах для доставки лекарственных средств по настоящему изобретению, включают такие лиганды, которые связываются с рецепторами витаминов, которые специфично экспрессируются на активированных макрофагах, например, рецепторами фолатов, которые связывают фолаты или их аналоги или производные, описанные в настоящей заявке.
Помимо описанных в заявке витаминов, предполагается, что другие связывающие лиганды могут быть сшиты с лекарственными средствами и линкерами, описанными и рассмотренными в настоящем изобретении, с образованием конъюгатов связывающий лиганд-линкер-лекарственное средство, способных облегчить доставку лекарственного средства к желаемой цели. Эти другие связывающие лиганды, помимо описанных витаминов и их аналогов и производных, могут применяться для образования конъюгатов для доставки лекарственных средств, способных связываться с целевыми клетками. В общем, любой связывающий лиганд (B) рецептора на клеточной поверхности может быть с успехом применен в качестве нацеливающего лиганда, к которому может быть прикреплен конъюгат линкер-лекарственное средство.
Иллюстративные примеры других лигандов, описанных в настоящей заявке, включают пептидные лиганды, выявленные в скрининг-библиотеках, пептиды, проявляющие специфичность в отношении опухолевых клеток, аптамеры, проявляющие специфичность в отношении опухолевых клеток, углеводы, проявляющие специфичность в отношении опухолевых клеток, моноклональные или поликлональные антитела, проявляющие специфичность в отношении опухолевых клеток, фрагменты антител Fab или scFv (т.е. одноцепочечные вариабельные области), например, фрагменты Fab антител, нацеленные на EphA2 или другие белки, которые специфично экспрессируются или находятся только на метастатических раковых клетках, малые органические молекулы, полученные из комбинаторных библиотек, факторы роста, такие как EGF, FGF, инсулин и инсулиноподобные факторы роста и гомологичные полипептиды, соматостатин и его аналоги, трансферрин, комплексы липопротеинов, соли желчных кислот, селектины, стероидные гормоны, Arg-Gly-Asp содержащие пептиды, ретиноиды, различные галектины, лиганды δ-опиоидного рецептора, лиганды рецептора холецитокина A, лиганды, специфичные для рецепторов ангиотензина AT1 или AT2, лиганды пероксисом пролифератор-активирующего рецептора λ, β-лактамовые антибиотики, такие как пенициллин, малые органические молекулы, в том числе противомикробные средства, а также другие молекулы, которые специфично связываются с рецепторами, преимущественно экспрессируемыми на поверхности опухолевых клеток или на инфекционных микроорганизмах, противомикробные и другие средства, структура которых разработана таким образом, чтобы они соответствовали связывающему карману конкретного рецептора на основе кристаллической структуры рецептора или других белков клеточной поверхности, связывающие лиганды опухолевых антигенов или других молекул предпочтительно экспрессируемых на поверхности опухолевых клеток, или фрагменты любых из перечисленных молекул.
Примеры опухоль-специфичных антигенов, которые могли бы служить сайтами связывания для конъюгата связывающий лиганд-лекарственное средство, включают внеклеточные эпитопы членов семейства белков эфринов, например EphA2. Экспрессия EphA2 в нормальных клетках ограничена местами соединения клеток друг с другом, но в метастатических опухолевых клетках EphA2 распределен по всей поверхности клетки. Таким образом, EphA2 на метастатических клетках мог бы быть доступен для связывания, например, с фрагментом Fab антитела, конъюгированного с лекарственным средством, в то время как указанный белок не был бы доступен для связывания с фрагментом Fab на нормальных клетках, что приведет к специфичному связыванию конъюгата связывающий лиганд-лекарственное средство с метастатическими раковыми клетками.
Линкер L включает один или несколько гидрофильных спейсеров линкера. Кроме того, в линкер L могут входить другие необязательные спейсеры линкера и/или расщепляемые линкеры. Подразумевается, что в линкер можно включать дополнительные спейсеры линкера, если для разделения связывающего лиганда B и лекарственного средства A, необходима группа заранее определенной длины. Также предполагается, что в некоторые конфигурации линкера могут быть включены расщепляемые линкеры. Например, в одном из описанных в заявке вариантов осуществления нацеленные конъюгаты лигандов могут применяться с целью доставки лекарственных средств для лечения рака или других заболеваний, в которые вовлечены патогенные клетки. В таких вариантах осуществления имеется в виду, что после доставки желательно высвобождение лекарственного средства из конъюгата. Например, в конфигурации, где нацеливающий лиганд представляет собой фолат или его аналог или производное, конъюгат может связываться с рецептором фолата. После связывания конъюгат часто подвергается процессу эндоцитоза и поступает во внутреннее пространство клетки. Клеточные механизмы могут биологически разрушить конъюгат с высвобождением «полезного груза», т.е. лекарственного средства, и фолата.
В альтернативной конфигурации нацеленный конъюгат может применяться в иммунотерапии. В этой конфигурации в состав конъюгата, как правило, не входит расщепляемый линкер. Например, конъюгаты фолатов или других соединений, связывающих рецепторы витаминов, и иммуногенов, после доставки свяжутся с соответствующим рецептором и пометят соответствующую клетку антигенным фрагментом. В другой альтернативной конфигурации нацеленный конъюгат может применяться в диагностике. В этой конфигурации расщепляемый линкер может включаться или не включаться в структуру конъюгата. Например, конъюгаты, которые включают средства визуализации, могут доставляться к целевой клетке с применением подходящего лиганда, связывающего клеточный рецептор, например, фолата или другого соединения, связывающего рецептор витамина. В одном из аспектов этот конъюгат может оставаться на поверхности клетки для получения изображения. В другом аспекте этот конъюгат может подвергаться эндоцитозу во внутренний объем клетки. В последней ситуации в структуру конъюгата может быть введен расщепляемый линкер.
Соответственно, в других аспектах описанные в настоящей заявке конъюгаты B-L-A также включают структуры, соответствующие следующим общим формулам:
B-LS-LH-A
B-LH-LS-A
B-LS-LH-LS-A
B-LR-LH-A
B-LH-LR-A
B-LR-LH-LR-A
B-LS-LR-LH-A
B-LR-LH-LS-A
B-LR-LS-LH-LR-A
B-LH-LS-LH-LR-A
где B, L и A соответствуют данным в заявке определениям и LR представляет собой расщепляемый структурный фрагмент линкера, LS представляет собой структурный фрагмент (спейсер) линкера и LH представляет собой гидрофильный структурный фрагмент линкера L. Следует понимать, что приведенные выше формулы являются только иллюстративными и что в настоящее изобретение следует включать и другие взаимные расположения гидрофильных фрагментов линкера, расщепляемых фрагментов линкера и структурных фрагментов линкера. Кроме того, следует понимать, что в изобретении рассматриваются дополнительные конъюгаты, которые включают большое число гидрофильных спейсеров линкера, и/или большое число расщепляемых фрагментов линкера, и/или большое число спейсеров линкера.
Аналогично, в других аспектах описанные в изобретении конъюгаты L-A также включают соединения, соответствующие следующим общим формулам:
LS-LH-A
LH-LS-A
LS-LH-LS-A
LR-LH-A
LH-LR-A
LR-LH-LR-A
LS-LR-LH-A
LR-LH-LS-A
LR-LS-LH-LR-A
LH-LS-LH-LR-A
где L и A соответствуют данным в заявке определениям и LR представляет собой расщепляемый структурный фрагмент линкера, LS представляет собой структурный фрагмент линкера и LH представляет собой гидрофильный структурный фрагмент линкера L. Следует понимать, что приведенные выше формулы являются только иллюстративными и что в настоящее изобретение следует включать и другие взаимные расположения гидрофильных фрагментов линкера, расщепляемых фрагментов линкера и структурных фрагментов линкера. Кроме того, следует понимать, что в изобретении рассматриваются дополнительные конъюгаты, которые включают большое число гидрофильных спейсеров линкера, и/или большое число расщепляемых фрагментов линкера, и/или большое число спейсеров линкера.
Подразумевается, что расположение и/или ориентация различных гидрофильных линкеров может быть линейного или разветвленного типа, или обоих типов. Например, гидрофильные структурные фрагменты могут образовывать каркас линкера, формирующего конъюгат фолата и лекарственного средства, средства визуализации или диагностического средства. В качестве альтернативы, гидрофильная часть линкера может быть подвешена или присоединена к основной цепи атомов, соединяющих связывающий лиганд B со средством А. В этой последней структуре гидрофильный фрагмент может находиться непосредственно рядом с основной цепью атомов или удален от нее.
В другом варианте осуществления линкер является более или менее линейным и гидрофильные группы расположены в основном последовательно, образуя в конъюгате линкер, сходный с цепью. В этом случае гидрофильные группы образуют часть или весь скелет линкера в данном линейном варианте осуществления.
В другом варианте осуществления гидрофильные группы представляют собой разветвления линкера. В этом разветвленном варианте гидрофильные группы могут быть связаны с основным скелетом или находиться на удалении от него. В каждом из этих случаев линкер имеет более сферическую или цилиндрическую форму.
В одном из вариантов линкер имеет форму щетки для мытья бутылок. В одном из аспектов скелет линкера сформирован линейной последовательностью амидов и гидрофильная часть линкера образована параллельно расположенными разветвляющими боковыми цепями, полученными, например, присоединением моносахаридов, сульфонатов и т.п., а также их производных и аналогов.
Подразумевается, что линкеры могут быть нейтральными или могут ионизоваться в определенных условиях, например, физиологических условиях, которые могут иметь место in vivo. В случае ионизируемых линкеров в выбранных условиях, линкеры могут депротонироваться с образованием отрицательного иона, или, альтернативно, протонироваться с образованием положительного иона. Имеется в виду, что может иметь место более чем один случай депротонирования или протонирования. Кроме того, предполагается, что один и тот же линкер может депротонироваться и протонироваться с образованием внутренних солей или цвиттерионных соединений.
В другом варианте осуществления гидрофильные структурные фрагменты линкеров являются нейтральными, т.е. в физиологических условиях эти линкеры не подвергаются значительному протонированию или депротонированию. В другом варианте осуществления гидрофильные фрагменты линкеров могут протонироваться, приобретая один или несколько положительных зарядов. Предполагается, что способность к протонированию зависит от условий. В одном из аспектов эти условия являются физиологическими условиями и линкер протонируется in vivo. В другом варианте осуществления структурные фрагменты включают как нейтральные области, так и области, которые могут протонироваться, приобретая один или несколько положительных зарядов. В другом варианте осуществления структурные фрагменты включают как области, которые могут депротонироваться, приобретая один или несколько отрицательных зарядов, так и области, которые могут протонироваться, приобретая один или несколько отрицательных зарядов. Подразумевается, что в последнем варианте осуществления могут образовываться цвиттерионы или внутренние соли.
В одном из аспектов области линкера, которые могут депротонироваться, приобретая отрицательный заряд, включают карбоновые кислоты, например, аспарагиновую кислоту, глутаминовую кислоту и группы карбоновых кислот с более длинными цепями, а также сложные эфиры серной кислоты, например, алкиловые эфиры серной кислоты. В другом аспекте области линкеров, которые могут протонироваться, приобретая положительный заряд, включают аминогруппы, например, полиаминоалкилены, включающие этилендиамины, пропилендиамины, бутилендиамины и т.п. и/или гетероциклы, в том числе пирролидины, пиперидины, пиперазины и другие аминогруппы, каждая из которых необязательно является замещенной. В другом варианте осуществления области линкера, которые являются нейтральными, включают полигидроксильные группы, такие как сахара, углеводы, сахариды, инозиты и т.п. и/или полиэфирные группы, например, полиооксиалкиленовые группы, в том числе полиоксиэтилены, полиоксипропилены и т.п.
В одном из вариантов осуществления описанные в настоящей заявке гидрофильные спейсеры линкеров преимущественно состоят из углерода, водорода и кислорода и имеют соотношение углерод/кислород примерно 3:1 или менее, или примерно 2:1 или менее. В одном из аспектов описанные в настоящей заявке гидрофильные фрагменты линкеров включают большое число функциональных групп простых эфиров. В другом аспекте описанные в заявке гидрофильные линкеры включают большое число гидроксильных функциональных групп. Иллюстративные примеры фрагментов, которые могут применяться для формирования таких линкеров, включают полигидроксильные соединения, например, углеводы, полиэфирные соединения, например, звенья полиэтиленгликоля, а также кислотные группы, например, группы карбоновых и алкилсерных кислот. В одном из вариантов в структуру линкера могут быть также включены олигоамидные и подобные спейсеры.
Иллюстративные примеры углеводных спейсеров включают сахаропептиды, описанные в настоящей заявке, которые объединяют в себе особенности как пептидов, так и сахаров; глюкурониды, которые могут быть введены в структуру линкера с помощью [2+3] циклизации Huisgen, известную также как «Click chemistry»; β-алкилгликозиды, например, 2-дезоксигексапиранозы (2-дезоксиглюкоза, 2-дезоксиглюкуронид и т.п.) и β-алкилманнопиранозиды. Иллюстративные примеры ПЭГ-групп включают группы с длиной, находящейся в конкретном диапазоне, от примерно 4 до примерно 20 групп ПЭГ. Иллюстративные эфиры алкилсерной кислоты также могут быть введены непосредственно в цепь при помощи «click chemistry». Иллюстративные олигоамидные фрагменты включают фрагменты EDTA и DTPA, β-аминокислоты и т.п.
В другом варианте осуществления описанный в настоящей заявке фрагмент линкера включает полиэфиры, например, линкеры следующей структуры:
где m представляет собой целое число, в каждом случае независимо выбранное из чисел от 1 до, примерно 8; p представляет собой целое число, выбранное из чисел от 1 до примерно 10; и n представляет собой целое число, в каждом случае независимо выбранное из чисел от 1 до примерно 3. В одном из аспектов m в каждом случае независимо означает целое число от 1 до примерно 3. В другом аспекте n в каждом случае равно 1. В другом аспекте p в каждом случае независимо представляет собой целое число от примерно 4 до примерно 6. Иллюстративно, в настоящей заявке рассматриваются полиэфиры полипропилена, соответствующие предыдущему описанию, и они могут быть включены в конъюгаты в качестве гидрофильных спейсеров линкера. Помимо этого, имеется в виду, что смешанные полиэфиры полиэтилена и полипропилена могут быть включены в конъюгаты в качестве гидрофильных спейсеров линкеров. Кроме того в настоящем изобретении рассматриваются циклические варианты упомянутых выше полиэфирных соединений, например те, которые включают тетрагидрофуранил, 1,3-диоксаны, 1,4-диоксаны и т.п.
В другом иллюстративном варианте осуществления гидрофильные спейсеры линкеров, описанных в настоящей заявке, включают значительное число гидроксильных функциональных групп, например, рассматриваются линкеры, которые включают моносахариды, олигосахариды, полисахариды и т.п. Следует понимать, что полигидроксилсодержащие спейсеры линкеров включают большое количество групп -(CROH)-, в которых R представляет собой водород или алкил.
В другом варианте осуществления спейсеры линкеров включают один или несколько из следующих фрагментов:
где R представляет собой H, алкил, циклоалкил или арилалкил; m представляет собой целое число от 1 до примерно 3; n представляет собой целое число от 1 до примерно 5; p является целым числом от 1 до примерно 5; и r является целым числом, выбранным из чисел от 1 до примерно 3. В одном из аспектов целое число n равно 3 или 4. В другом аспекте целое число p равно 3 или 4. В другом аспекте целое число r равно 1.
В другом варианте осуществления спейсер линкера включает одну или несколько из следующих циклических полигидроксильных групп:
где n означает целое число от 2 до примерно 5, p является целым числом от 1 до примерно 5, и r является целым числом от 1 до примерно 4. В одном из аспектов целое число n равно 3 или 4. В другом аспекте целое число p равно 3 или 4. В другом аспекте целое число r равно 2 или 3. Подразумевается, что все стереохимические формы изображенных фрагментов линкеров входят в объем настоящего изобретения. Например, в приведенных выше формулах структурный фрагмент может быть получен из рибозы, ксилозы, глюкозы, маннозы, галактозы или другого сахара, и он сохраняет пространственное расположение боковых гидроксилов и алкильных групп, присутствующих в этих молекулах. Кроме того, следует понимать, что приведенные выше формулы охватывают различные дезоксисоединения. В качестве иллюстрации, охвачены соединения следующих формул:
где n меньше или равно r, например, если r равно 2 или 3, n равно 1 или 2, или же 1, 2 или 3, соответственно.
В другом варианте осуществления спейсеры линкера включают полигидроксильные соединения следующей формулы:
где каждый из коэффициентов n и r выбран из целых чисел от 1 до примерно 3. В одном из аспектов спейсер линкера включает одно или несколько полигидроксильных соединений следующих формул:
Подразумевается, что все стереохимические формы таких фрагментов линкеров входят в объем настоящего изобретения. Например, в приведенных выше формулах структурный фрагмент может быть получен из рибозы, ксилозы, глюкозы, маннозы, галактозы или другого сахара, и он сохраняет пространственное расположение боковых гидроксилов и алкильных групп, присутствующих в этих молекулах.
В другой конфигурации описанные в настоящей заявке гидрофильные линкеры L включают полигидроксильные группы, которые находятся на определенном расстоянии от основной цепи линкера. В одном из вариантов осуществления такие углеводные группы или полигидроксильные группы соединены с основной цепью триазольной группой, образуя сшитые триазолом гидрофильные спейсеры линкера. В качестве иллюстрации, такие линкеры включают фрагменты следующих формул:
где коэффициенты n, m и r являются целыми числами и каждый из них в каждом случае независимо выбран из чисел от 1 до, примерно 5. В одном из иллюстративных аспектов m в каждом случае независимо равно 2 или 3. В другом аспекте r в каждом случае равно 1. В другом аспекте n в каждом случае равно 1. В одном из вариантов группа, связывающая полигидроксильную группу с основной цепью линкера, является другой гетероарильной группой, включая, но не ограничиваясь перечисленным, пиррол, пиразол, 1,2,4-триазол, фуран, оксазол, изоксазол, тиенил, тиазол, изотиазол, оксадиазол и т.п. Аналогично, в изобретении рассматриваются двухвалентные 6-членные циклические гетероарильные группы. Другие варианты описанных выше иллюстративных примеров гидрофильных структурных фрагментов линкеров включают оксиалкиленовые группы, например, следующих формул:
где коэффициенты n и r представляют собой целые числа и каждый из них в каждом случае выбран из чисел от 1 до примерно 5; и p представляет собой целое число от 1 до примерно 4.
В другом варианте осуществления упомянутые выше углеводные или полигидроксильные группы связаны с основной цепью амидными группами, образуя гидрофильные спейсеры линкера с амидными связями. В качестве иллюстрации, такие линкеры включают фрагменты следующих формул:
где n представляет собой целое число, выбранное из чисел от 1 до примерно 3, и m представляет собой целое число, выбранное из чисел от 1 до примерно 22. В одном из иллюстративных аспектов n равно 1 или 2. В другом иллюстративном аспекте коэффициент m выбран из чисел от примерно 6 до примерно 10, например, равен 8. В одном из вариантов группа, соединяющая полигидроксильную группу с основной цепью линкера, представляет собой другую функциональную группу, включая, но не ограничиваясь этим, группы сложных эфиров, мочевин, карбаматов, ацилгидразонов и т.п. Аналогично, изобретение охватывает циклические варианты. Другие варианты упомянутых выше иллюстративных гидрофильных спейсеров линкера включают оксиалкиленовые группы, например, имеющие следующие формулы:
где коэффициенты n и r представляют собой целые числа, и каждый из них в каждом случае независимо выбран из чисел от 1 до примерно 5; и p представляет собой целое число, выбранное из чисел от 1 до примерно 4.
В другом варианте осуществления спейсеры линкера включают один или несколько из следующих фрагментов:
где R представляет собой H, алкил, циклоалкил или арилалкил; коэффициент m является целым числом, независимо выбранным из чисел от 1 до примерно 3; n является целым числом от 1 до примерно 6, p является целым числом от 1 до примерно 5, и коэффициент r является целым числом, выбранным из чисел от 1 до примерно 3. В одном из вариантов n является целым числом, равным 3 или 4. В другом варианте p является целым числом, равным 3 или 4. В другом варианте r является целым числом, равным 1.
В другом варианте структурные фрагменты линкеров включают один или несколько из следующих фрагментов:
где коэффициент m является целым числом, независимо выбранным из чисел от 1 до примерно 3; n является целым числом от 1 до примерно 6, p является целым числом от 1 до примерно 5; и r является целым числом, выбранным из чисел от 1 до примерно 3. В одном из вариантов целое число n равно 3 или 4. В другом варианте целое число p равно 3 или 4. В другом варианте целое число r равно 1.
В другом варианте структурные фрагменты линкеров включают один или несколько из следующих фрагментов:
где коэффициент m является целым числом, независимо выбранным из чисел от 1 до примерно 3; n является целым числом от 1 до примерно 6, p является целым числом от 1 до примерно 5, и r является целым числом, выбранным из чисел от 1 до примерно 3. В одном из вариантов целое число n равно 3 или 4. В другом варианте целое число p равно 3 или 4. В другом варианте целое число r равно 1.
В другом варианте осуществления гидрофильный спейсер линкера представляет собой комбинацию структурных фрагментов основной цепи и разветвляющей боковой группы, представленную, например, следующими формулами:
где коэффициент n представляет собой целое число, в каждом случае независимо выбранное из чисел от 0 до 3. Имеется в виду, что приведенные выше формулы отображают циклические сахара с числом атомов в цикле 4, 5, 6 и даже более. Кроме того, следует понимать, что приведенная выше формула может быть модифицирована так, чтобы отображать дезоксисахара, в которых одна или несколько гидроксильных групп, имеющихся в формуле, заменены водородом, алкилом или аминогруппой. Кроме того, следует понимать, что приведенными выше формулами охвачены соответствующие карбонильные соединения, в которых одна или несколько гидроксильных групп окислены до соответствующего карбонила. Кроме того, в этом иллюстративном варианте осуществления пиранозы включают как карбоксильные, так и аминогруппы и (a) могут быть включены в основную цепь, и (b) могут обеспечить синтетические возможности для разветвления боковых цепей в разновидностях данного варианта осуществления. Любые из имеющихся гидроксильных групп могут использоваться для присоединения других химических фрагментов, в том числе дополнительных сахаров для получения соответствующих олигосахаридов. Кроме того, в изобретение входят другие разновидности данного варианта осуществления, в том числе включение пиранозы или другого сахара в основную цепь через один атом углерода, т.е. с образованием спироструктуры, через пару геминальных атомов углерода, и подобные структуры. Например, один или два конца линкера, или агент A, или связывающий лиганд B могут быть соединены с фрагментом сахара, который входит в основную цепь через положения 1,1; 1,2; 1,3; 1,4; 2,3 или другие положения.
В другом варианте осуществления описанные в настоящей заявке гидрофильные спейсеры линкеров включают и преимущественно состоят из углерода, водорода и азота и имеют соотношение углерод/азот, равное примерно 3:1 или менее, или примерно 2:1 или менее. В одном из аспектов описанные в настоящей заявке гидрофильные линкеры включают значительное число аминофункциональных групп.
В другом варианте осуществления спейсеры линкера включают одну или несколько аминогрупп следующих формул:
где n представляет собой целое число, в каждом случае независимо выбранное из чисел от 1 до примерно 3. В одном из аспектов целое число n в каждом случае независимо представляет собой 1 или 2. В другом аспекте целое число n во всех случаях представляет собой 1.
В другом варианте осуществления гидрофильный спейсер линкера представляет собой эфир серной кислоты, например, алкиловый эфир серной кислоты. В качестве иллюстрации, этот спейсер линкера отображается следующими формулами:
где n представляет собой целое число, в каждом случае независимо выбранное из чисел от 1 до примерно 3. В качестве иллюстрации, n в каждом случае независимо равен 1 или 2.
Подразумевается, что в таких линкерах, содержащих большое количество гидроксильных групп, аминогрупп, карбоксильных групп, фрагментов серной кислоты и т.п., которые включают свободные атомы водорода, связанные с гетероатомами, один или несколько из этих свободных атомов водорода могут быть защищены защитными группами, подходящими, соответственно, для гидроксила, амино и/ или кислотных групп или, в качестве альтернативы, могут быть блокированы с образованием соответствующих пролекарств, причем последние выбирают для конкретного применения, как, например, пролекарства, которые высвобождают исходное лекарственное средство в общих или конкретных физиологических условиях.
В каждый из приведенных выше иллюстративных примеров линкеров L в некоторых случаях включены также дополнительные спейсеры линкера LS и/или дополнительные расщепляемые линкеры LR. Упомянутые спейсеры линкера и расщепляемые фрагменты линкера также могут включать асимметричные атомы углерода. Далее следует понимать, что показанные в настоящем описании стереохимические конфигурации являются только иллюстративными и другие стереохимические конфигурации также входят в объем настоящего изобретения. Например, в одном из вариантов в описанные в настоящей заявке конъюгаты могут включаться соответствующие неприродные конфигурации аминокислот, такие как
где n означает целое число от 2 до примерно 5, p означает целое число от 1 до примерно 5 и r означает целое число от 1 до примерно 4, как указано выше.
Далее следует понимать, что в описанных выше вариантах осуществления незанятые положения, такие как атомы, отмеченные знаком (*), являются местами присоединения связывающего лиганда (B) или агента (A), доставку которого предполагается осуществлять. Помимо этого следует понимать, что такое присоединение любого из фрагментов B и A, или их обоих, может осуществляться непосредственно либо через промежуточный линкер. Промежуточные линкеры включают другие спейсеры линкера и/или расщепляемые фрагменты линкера. Иллюстративные примеры дополнительных спейсеров линкера и расщепляемых фрагментов линкера, которые входят в конъюгаты, описанные в настоящей заявке, приведены в заявке на патент США порядковый № 10/765335, содержание которой включено в настоящее описание с помощью ссылки.
В одном из вариантов осуществления гидрофильный спейсер линкера включает один или несколько углеводсодержащих или полигидроксилсодержащих линкеров. В другом варианте осуществления гидрофильный спейсер линкера включает как минимум три углеводсодержащих или полигидроксилсодержащих линкера. В другом варианте осуществления гидрофильный спейсер линкера включает один или несколько углеводсодержащих или полигидроксилсодержащих линкеров, а также один или несколько фрагментов аспарагиновой кислоты. В другом варианте осуществления гидрофильный спейсер линкера включает один или несколько углеводсодержащих или полигидроксилсодержащих линкеров и один или несколько фрагментов глутаминовой кислоты. В другом варианте осуществления гидрофильный спейсер линкера включает один или несколько углеводсодержащих или полигидроксилсодержащих линкеров, один или несколько фрагментов глутаминовой кислоты, один или несколько фрагментов аспарагиновой кислоты и один или несколько остатков бета-аминоаланинов. В ряде вариантов, в каждом из описанных выше вариантов осуществления гидрофильный спейсер линкера включает также один или несколько остатков цистеина. В ряде других вариантов, в каждом из описанных выше вариантов осуществления гидрофильный спейсер линкера включает также как минимум один остаток аргинина.
В другом варианте осуществления гидрофильный спейсер линкера включает один или несколько двухвалентных остатков 1,4-пиперазина, которые включены в цепь атомов, соединяющих как минимум один из связывающих лигандов с как минимум одним из агентов (A). В одном из вариантов гидрофильный спейсер линкера включает один или несколько углеводсодержащих или полигидроксилсодержащих линкеров. В другом варианте гидрофильный спейсер линкера включает один или несколько углеводсодержащих или полигидроксилсодержащих линкеров и один или несколько фрагментов аспарагиновой кислоты. В другом варианте гидрофильный спейсер линкера включает один или несколько углеводсодержащих или полигидроксилсодержащих линкеров и один или несколько фрагментов глутаминовой кислоты. В ряде вариантов, в каждом из описанных выше вариантов осуществления гидрофильный спейсер линкера включает также один или несколько остатков цистеина. В другом ряде вариантов, в каждом из описанных выше вариантов осуществления гидрофильный спейсер линкера включает также как минимум один остаток аргинина.
В другом варианте осуществления гидрофильный спейсер линкера включает один или несколько олигоамидных гидрофильных спейсеров, например, не ограничиваясь указанным, аминоэтилпиперазинилацетамид.
В другом варианте осуществления гидрофильный спейсер линкера включает один или несколько углеводсодержащих или полигидроксилсодержащих линкеров, связанных через фрагмент триазола. В другом варианте осуществления гидрофильный спейсер линкера включает один или несколько углеводсодержащих или полигидроксилсодержащих линкеров, связанных через амидный фрагмент. В еще одном варианте осуществления гидрофильный спейсер линкера включает одну или несколько групп ПЭГ и один или несколько остатков цистеина. В другом варианте осуществления, гидрофильный спейсер линкера включает один или несколько остатков производных EDTE.
В другом варианте осуществления дополнительный спейсер линкера может представлять собой 1-алкиленсукцинимид-3-ил, необязательно замещенный заместителем X1, который определен ниже, и расщепляемые фрагменты линкера могут представлять собой метилен, 1-алкоксиалкилен, 1-алкоксициклоалкилен, 1-алкоксиалкиленкарбонил, 1-алкоксициклоалкиленкарбонил, где каждый из расщепляемых фрагментов линкера необязательно замещен заместителем X2, который определен ниже, и где как спейсер линкера, так и расщепляемый фрагмент линкера связаны с другим спейсером линкера с образованием сукцинимид-1-илалкил ацеталя или кеталя.
Дополнительный спейсер линкера может представлять собой карбонил, тионокарбонил, алкилен, циклоалкилен, алкиленциклоалкил, алкиленкарбонил, циклоалкиленкарбонил, карбонилалкилкарбонил, 1-алкиленсукцинимид-3-ил, 1-(карбонилалкил)сукцинимид-3-ил, алкиленсульфоксил, сульфонилалкил, алкиленсульфоксиалкил, алкиленсульфонилалкил, карбонилтетрагидро-2H-пиранил, карбонилтетрагидрофуранил, 1-(карбонилтетрагидро-2H-пиранил)сукцинимид-3-ил и 1-(карбонилтетрагидрофуранил)сукцинимид-3-ил, где каждый из этих спейсеров линкера необязательно замещен заместителем X1, который определен ниже. В этом варианте осуществления спейсер линкера может включать дополнительные атомы азота, и спейсеры линкера могут представлять собой алкиленкарбонил, циклоалкиленкарбонил, карбонилалкилкарбонил, 1-(карбонилалкил)сукцинимид-3-ил, где каждый из этих спейсеров линкера необязательно замещен заместителем X1, который определен ниже, и этот спейсер линкера связан с атомом азота с образованием амида. В качестве альтернативы, спейсер линкера может включать дополнительный атом серы, причем спейсеры линкера могут представлять собой алкилен и циклоалкилен, где каждый из спейсеров линкера необязательно замещен карбокси, и спейсер линкера связан с серой с образованием тиолов. В другом варианте осуществления спейсер линкера может включать серу, причем спейсеры линкера могут представлять собой 1-алкиленсукцинимид-3-ил и 1-(карбонилалкил)сукцинимид-3-ил, и спейсер линкера связывается с серой с образованием сукцинимид-3-илтиола.
В вариантах осуществления, альтернативных описанным выше, дополнительный спейсер линкера может включать азот, и расщепляемый фрагмент линкера может являться двухвалентным радикалом, включая алкиленазиридин-1-ил, карбонилалкилазиридин-1-ил, сульфоксилалкилазиридин-1-ил или сульфонилалкилазиридин-1-ил, где каждый из расщепляемых линкеров необязательно замещен заместителем X2, который определен ниже. В этом альтернативном варианте осуществления спейсеры линкера могут являться карбонилом, тионокарбонилом, алкиленкарбонилом, циклоалкиленкарбонилом, карбонилалкилкарбонилом, 1-(карбонилалкил)сукцинимид-3-илом, где каждый из этих спейсеров линкера необязательно замещен заместителем X1, который определен ниже, и где спейсер линкера связан с расщепляемым линкером с образованием амида азиридина.
Заместители X1 могут представлять собой алкил, алкокси, алкоксиалкил, гидрокси, гидроксиалкил, амино, аминоалкил, алкиламиноалкил, диалкиламиноалкил, галоген, галогеналкил, сульфгидрилалкил, алкилтиоалкил, арил, замещенный арил, арилалкил, замещенный арилалкил, гетероарил, замещенный гетероарил, карбокси, карбоксиалкил, алкилкарбоксилат, алкилалканоат, гуанидиноалкил, R4-карбонил, R5-карбонилалкил, R6-ациламино и R7-ациламиноалкил, где каждый из заместителей R4 и R5 независимо выбран из аминокислот, производных аминокислот и пептидов, и где каждый из заместителей R6 и R7 независимо выбран из аминокислот, производных аминокислот и пептидов. В этом варианте осуществления спейсер линкера может включать азот, и заместитель X1, и спейсер линкера, к которому они присоединены, образуют гетероцикл.
В другом варианте осуществления расщепляемый линкер может представлять собой двухвалентный радикал, включая алкиленазиридин-1-ил, алкиленкарбонилазиридин-1-ил, карбонилалкилазиридин-1-ил, алкиленсульфоксилазиридин-1-ил, сульфоксилалкилазиридин-1-ил, сульфонилалкилазиридин-1-ил или алкиленсульфонилазиридин-1-ил, где каждый из расщепляемых линкеров необязательно замещен заместителем X2, который определен ниже.
Дополнительные иллюстративные примеры расщепляемых линкеров включают метилен, 1-алкоксиалкилен, 1-алкоксициклоалкилен, 1-алкоксиалкиленкарбонил, 1-алкоксициклоалкиленкарбонил, карбониларилкарбонил, карбонил(карбоксиарил)карбонил, карбонил(бискарбоксиарил)карбонил, галогеналкиленкарбонил, алкилен(диалкилсилил), алкилен(алкиларилсилил), алкилен(диарилсилил), (диалкилсилил)арил, (алкиларилсилил)арил, (диарилсилил)арил, оксикарбонилокси, оксикарбонилоксиалкил, сульфонилокси, оксисульфонилалкил, иминоалкилиденил, карбонилалкилидениминил, иминоциклоалкилиденил, карбонилциклоалкилидениминил, алкилентио, алкиленарилтио и карбонилалкилтио, где каждый из расщепляемых линкеров необязательно замещен заместителем X2, который определен ниже.
В предыдущем варианте осуществления расщепляемый линкер может включать кислород, и расщепляемые линкеры могут представлять собой метилен, 1-алкоксиалкилен, 1-алкоксициклоалкилен, 1-алкоксиалкиленкарбонил и 1-алкоксициклоалкиленкарбонил, где каждый из расщепляемых линкеров необязательно замещен заместителем X2, который определен ниже, и расщепляемый линкер связан с кислородом, с образованием ацеталя или кеталя. В качестве альтернативы, расщепляемый линкер может включать кислород и расщепляемый линкер может представлять собой метилен, где метилен замещен необязательно замещенным арилом, причем расщепляемый линкер связан с кислородом с образованием ацеталя или кеталя. Далее, расщепляемый линкер может включать кислород и может представлять собой сульфонилалкил, где расщепляемый линкер связан с кислородом с образованием алкилсульфоната.
В другом варианте осуществления упомянутого выше варианта расщепляемого линкера, расщепляемый линкер может включать азот, причем расщепляемый линкер может представлять собой иминоалкилиденил, карбонилалкилидениминил, иминоциклоалкилиденил и карбонилциклоалкилидениминил, где каждый из этих расщепляемых линкеров необязательно замещен заместителем X2, который определен ниже, и расщепляемый линкер связан с азотом с образованием гидразона. В альтернативной конфигурации гидразон может быть ацилирован производным карбоновой кислоты, производным ортоформиата или карбамоильным производным с образованием различных ацилгидразоновых расщепляемых линкеров.
Альтернативно, расщепляемый линкер может включать кислород, причем расщепляемые линкеры могут представлять собой алкилен(диалкилсилил), алкилен(алкиларилсилил), алкилен(диарилсилил), (диалкилсилил)арил, (алкиларилсилил)арил и (диарилсилил)арил, где каждый из расщепляемых линкеров необязательно замещен заместителем X2, который определен ниже, и расщепляемый линкер связан с кислородом с образованием силанола.
В описанном выше варианте осуществления расщепляемого линкера лекарственное средство может включать атом азота, и расщепляемый линкер может включать азот, причем расщепляемый линкер может представлять собой карбониларилкарбонил, карбонил(карбоксиарил)карбонил, карбонил(бискарбоксиарил)карбонил и расщепляемый линкер может быть связан с гетероатомом азота с образованием амида и, кроме того, связан с атомом азота лекарственного средства с образованием амида.
В описанном выше варианте осуществления расщепляемого линкера, лекарственное средство может включать атом кислорода, расщепляемый линкер может включать азот, и расщепляемые линкеры могут представлять собой карбониларилкарбонил, карбонил(карбоксиарил)карбонил, карбонил(бискарбоксиарил)карбонил и расщепляемый линкер может образовывать амид и, кроме того, связываться с атомом кислорода лекарственного средства с образованием сложного эфира.
Заместитель X2 может представлять собой алкил, алкокси, алкоксиалкил, гидрокси, гидроксиалкил, амино, аминоалкил, алкиламиноалкил, диалкиламиноалкил, галоген, галогеналкил, сульфгидрилалкил, алкилтиоалкил, арил, замещенный арил, арилалкил, замещенный арилалкил, гетероарил, замещенный гетероарил, карбокси, карбоксиалкил, алкилкарбоксилат, алкилалканоат, гуанидиноалкил, R4-карбонил, R5-карбонилалкил, R6-ациламино и R7-ациламиноалкил, где каждый из заместителей R4 и R5 независимо выбран из аминокислот, производных аминокислот и пептидов, и где каждый из заместителей R6 и R7 независимо выбран из аминокислот, производных аминокислот и пептидов. В этом варианте осуществления расщепляемый линкер может включать азот, и заместитель X2 и расщепляемый линкер могут образовать гетероцикл.
Эти гетероциклы могут являться пирролидинами, пиперидинами, оксазолидинами, изоксазолидинами, тиазолидинами, изотиазолидинами, пирролидинонами, пиперидинонами, оксазолидинонами, изоксазолидинонами, тиазолидинонами, изотиазолидинонами и сукцинимидами.
Средство А может включать атом азота, и расщепляемый линкер может представлять собой галогеналкиленкарбонил, необязательно замещенный заместителем X2, причем расщепляемый линкер связан с атомом азота лекарственного средства с образованием амида.
Средство A может включать атом кислорода, и расщепляемый линкер может представлять собой галогеналкиленкарбонил, необязательно замещенный заместителем X2, причем расщепляемый линкер связан с атомом кислорода лекарственного средства с образованием сложного эфира.
Средство A может включать атом азота, связанный двойной связью, и в этом варианте осуществления расщепляемые линкеры могут представлять собой алкиленкарбониламино и 1-(алкиленкарбониламино)сукцинимид-3-ил, причем расщепляемый линкер может быть связан с атомом азота лекарственного средства с образованием гидразона.
Средство A может включать атом серы, и в этом варианте осуществления расщепляемые линкеры могут представлять собой алкилентио и карбонилалкилтио, причем расщепляемый линкер может быть связан с атомом серы молекулы лекарственного средства с образованием дисульфида.
Средство A может представлять собой митомицин, производное митомицина или аналог митомицина и в этом варианте осуществления расщепляемые линкеры могут представлять собой карбонилалкилтио, карбонилтетрагидро-2H-пиранил, карбонилтетрагидрофуранил, 1-(карбонилтетрагидро-2H-пиранил)сукцинимид-3-ил и 1-(карбонилтетрагидрофуранил)сукцинимид-3-ил, где каждый из расщепляемых линкеров необязательно замещен заместителем X2 и где азиридиновый фрагмент митомицина связан с расщепляемым линкером, образуя ацилазиридин.
Связывающий лиганд B может представлять собой фолат, включающий атомы азота, и в этом варианте осуществления фрагменты линкеров могут представлять собой алкиленкарбонил, циклоалкиленкарбонил, карбонилалкилкарбонил, 1-алкиленсукцинимид-3-ил, 1-(карбонилалкил)сукцинимид-3-ил, где каждый из указанных спейсеров линкера необязательно замещен заместителем X1, и этот спейсер линкера связан с атомом азота фолата с образованием имида или алкиламида. В этом варианте осуществления заместитель X1 может представлять собой алкил, гидроксиалкил, амино, аминоалкил, алкиламиноалкил, диалкиламиноалкил, сульфгидрилалкил, алкилтиоалкил, арил, замещенный арил, арилалкил, замещенный арилалкил, карбокси, карбоксиалкил, гуанидиноалкил, R4-карбонил, R5-карбонилалкил, R6-ациламино и R7-ациламиноалкил, где каждый из заместителей R4 и R5 независимо выбран из аминокислот, производных аминокислот и пептидов, и где каждый из заместителей R6 и R7 независимо выбран из аминокислот, производных аминокислот и пептидов.
Термин «циклоалкилен» в настоящем описании относится к двухвалентной цепи, состоящей из атомов углерода, часть которой образует цикл, как, например, циклопроп-1,1-диилу, циклопроп-1,2-диилу, циклогекс-1,4-диилу, 3-этилциклопент-1,2-диилу, 1-метиленциклогекс-4-илу и т.п.
Термин «гетероцикл» в настоящем описании относится к одновалентной цепи, состоящей из атомов углерода и гетероатомов, где гетероатомы выбраны из азота, кислорода и серы, часть которой, включающая как минимум один гетероатом, образует цикл, такой как, азиридин, пирролидин, оксазолидин, 3-метоксипирролидин, 3-метилпиперазин и т.п.
Термин «арил» в настоящем описании относится к ароматическому моно- или полициклу, состоящему из атомов углерода, например, фенилу, нафтилу и т.п. Помимо этого, арил может также включать гетероарил.
Термин «гетероарил» в настоящем описании относится к ароматическому моно- или полициклу, состоящему из атомов углерода и как минимум одного гетероатома, выбранного из азота, кислорода и серы, например, пиридинилу, пиримидинилу, индолилу, бензоксазолилу и т.п.
Термин «необязательно замещенный» в настоящем описании относится к замене одного или нескольких атомов водорода, обычно у атома углерода, на соответствующее число заместителей, таких как галоген, гидрокси, амино, алкил- или диалкиламино, алкокси, алкилсульфонил, циано, нитро и т.п. Кроме того, два атома водорода у одного и того же атома углерода, у соседних атомов углерода или у близлежащих атомов углерода могут быть замещены двухвалентным заместителем с образованием соответствующей циклической структуры.
Термин «иминоалкилиденил» в настоящем описании относится к двухвалентному радикалу, содержащему алкилен, соответствующий данному выше определению, и атом азота, где концевой атом углерода алкилена связан двойной связью с атомом азота, что соответствует формулам -(CH)=N-, -(CH2)2(CH)=N-, -CH2C(Me)=N- и т.п.
Термин «аминокислота» в настоящей заявке относится в основном к аминоалкилкарбоксилатам, в которых алкильный радикал необязательно замещен, например, алкилом, гидроксиалкилом, сульфгидрилалкилом, аминоалкилом, карбоксиалкилом и т.п., включающим группы, соответствующие природным аминокислотам, например, серину, цистеину, метионину, аспарагиновой кислоте, глутаминовой кислоте и т.п. Следует понимать, что такие аминокислоты могут являться одним из стереоизомеров или смесью стереоизомеров, в том числе рацемическими смесями. Кроме того, термин «аминокислота» относится к бета-, гамма- и более протяженным аминокислотам, например, аминокислотам формулы:
-N(R)-(CR'R”)q-C(O)-,
где R представляет собой водород, алкил, ацил или группу, подходящую для защиты атома азота, R' и R” представляют собой водород или заместитель, каждый из которых в каждом случае выбран независимо, и q представляет собой целое число, например, 1, 2, 3, 4 или 5. В качестве иллюстрации, R' и/или R” независимо представляют собой, не ограничиваясь этим, водород или боковые цепи, встречающиеся в природных аминокислотах, например, метил, бензил, гидроксиметил, тиометил, карбоксил, карбоксиметил, гуанидинопропил и т.п., а также их производные и защищенные производные. Приведенная выше формула включает все стереоизомерные варианты. Например, аминокислоты могут быть выбраны из аспарагина, аспарагиновой кислоты, цистеина, глутаминовой кислоты, лизина, глутамина, аргинина, серина, орнитина, треонина и т.п. В другом иллюстративном аспекте интермедиата конъюгата для доставки лекарственного средства, связывающего рецептор витамина, описанного в настоящей заявке, лекарственное средство или его аналог или производное включает алкилтиольный нуклеофил.
Следует понимать, что описанные выше термины можно объединять, образуя из них названия соответствующих химических групп, как, например, термин «алкоксиалкил», относящийся к метилоксиметилу, этилоксиэтилу и т.п., «галогеналкоксиалкил», относящийся к трифторметилоксиэтилу, 1,2-дифтор-2-хлорэт-1-илоксипропилу и т.п., «арилалкил», относящийся к бензилу, фенетилу, α-метилбензилу и т.п., и других групп.
Термин «производное аминокислоты» в настоящей заявке в основном относится к необязательно замещенным аминоалкилкарбоксилатам, где аминогруппа и/или карбоксилатная группа необязательно замещены, например, алкилом, карбоксиалкилом, алкиламино и т.п., или необязательно защищены. Кроме того, необязательно замещенный промежуточный двухвалентный алкильный фрагмент может включать дополнительные группы, например, защитные группы и т.п.
Термин «пептид» в настоящем описании относится в основном к последовательностям аминокислот и/или аналогов и производных аминокислот, ковалентно связанных друг с другом амидными связями.
Термин «расщепляемый линкер» в настоящем описании относится к линкеру, который включает как минимум одну связь, которая может расщепляться в физиологических условиях (например, при определенных pH, действии кислот, при окислении или под действием ферментов). Следует понимать, что эти физиологические условия, приводящие к расщеплению связей, включают стандартные химические реакции гидролиза, которые проходят, например, при физиологических значениях pH или в результате попадания в клеточную органеллу, например, эндосому, имеющую более низкое значение pH по сравнению с pH цитоплазмы.
Расщепляемая связь или связи могут присутствовать внутри цепи расщепляемого линкера и/или с одного или двух концов расщепляемого линкера. Подразумевается, что легкость разрушения расщепляемой связи может быть отрегулирована введением в поливалентный линкер L функциональных групп или фрагментов, которые способны содействовать такому разрыву связи или облегчать его, что именуется также анхимерным содействием. Кроме того, предполагается, что в поливалентный линкер L могут быть включены дополнительные функциональные группы или фрагменты, которые способны содействовать или облегчать дополнительную фрагментацию конъюгатов рецептор-связывающий лиганд-агент после разрушения связи в расщепляемом линкере. Легкость разрушения расщепляемой связи может быть отрегулирована, например, замещениями у или вблизи от расщепляемой связи, например, введением альфа-разветвления в соседнем положении к расщепляемой дисульфидной связи, увеличением гидрофобности заместителей у кремния, во фрагменте, включающем связь кремний-кислород, которая может подвергаться гидролизу, применением гомологов заместителей в алкоксигруппах, которые образуют составную часть кеталя или ацеталя, которые могут подвергаться гидролизу и т.п.
Подразумевается, что расщепляемая связь может соединять два соседних атома в расщепляемом линкере и/или соединять другие линкеры или фрагменты V и/или D, которые описаны в настоящей заявке, с любым из или с обоими концами расщепляемого линкера. В случае, когда расщепляемая связь соединяет два соседних атома в расщепляемом линкере, после разрушения связи расщепляемый линкер распадается на два или несколько фрагментов. Напротив, в случае, если расщепляемая связь находится между расщепляемым линкером и другим фрагментом, например, дополнительным гетероатомом, дополнительным спейсером линкера, другим расщепляемым линкером, средством А, его аналогом или производным, или же связывающим лигандом B, его аналогом или производным, после разрушения связи, расщепляемый линкер отделяется от других фрагментов.
Предполагается, что каждый из дополнительных спейсеров линкера и расщепляемых фрагментов линкера является двухвалентным. Далее, необходимо понимать, что образование связи между каждым из разнообразных дополнительных спейсеров и самим расщепляемым линкером, и между различными дополнительными спейсерами и расщепляемыми линкерами и A и/или B, определенными в настоящем описании, может осуществляться по любому атому, присутствующему в различных дополнительных спейсерах или расщепляемых линкерах.
В одном из аспектов описанного в настоящей заявке конъюгата для доставки лекарственных средств, связывающего рецептор, поливалентный линкер включает дополнительный спейсер линкера и расщепляемый линкер, которые совместно образуют фрагмент 3-тиосукцинимид-1-илалкилоксиметилокси, где метил необязательно замещен алкилом или замещенным арилом.
В другом аспекте поливалентный линкер включает дополнительный спейсер линкера, и расщепляемый линкер, которые совместно образуют фрагмент 3-тиосукцинимид-1-илакилкарбонил, где карбонил формирует ацилазиридиновый фрагмент со средством A, его аналогом, или производным.
В другом аспекте поливалентный линкер включает дополнительный спейсер линкера и расщепляемый линкер, которые совместно образуют фрагмент 1-алкоксициклоалкиленокси.
В другом аспекте поливалентный линкер включает дополнительный спейсер линкера и расщепляемый линкер, которые совместно образуют фрагмент алкиленаминокарбонил(дикарбоксиларилен)карбоксилата.
В другом аспекте поливалентный линкер включает расщепляемый линкер, дополнительный спейсер линкера и расщепляемый линкер, которые совместно образуют фрагмент дитиоалкилкарбонилгидразида, где гидразид образует гидразон со средством A, его аналогом или производным.
В другом аспекте поливалентный линкер включает дополнительный спейсер линкера и расщепляемый линкер, которые совместно образуют фрагмент 3-тиосукцинимид-1-илалкилкарбонилгидразида, где гидразид образует гидразон со средством A, его аналогом или производным.
В другом аспекте поливалентный линкер включает дополнительный спейсер линкера и расщепляемый линкер, которые совместно образуют фрагмент 3-тиоалкилсульфонилалкил (дизамещенный силил)окси, где дизамещенный силил замещен алкилом или необязательно замещенным арилом.
В другом аспекте поливалентный линкер включает большое число дополнительных спейсеров линкера, выбранных из группы, состоящей из природных аминокислот и их стереоизомеров.
В другом аспекте поливалентный линкер включает расщепляемый линкер, дополнительный спейсер линкера и расщепляемый линкер, которые совместно образуют фрагмент 3-дитиоалкилоксикарбонил, где карбонил образует карбонат со средством A, его аналогом или производным.
В другом аспекте поливалентный линкер включает расщепляемый линкер, дополнительный спейсер линкера и расщепляемый линкер, которые совместно образуют фрагмент 3-дитиоарилалкилоксикарбонил, где карбонил образует карбонат со средством A, его аналогом или производным, и арил необязательно является замещенным.
В другом аспекте поливалентный линкер включает дополнительный спейсер линкера и расщепляемый линкер, которые совместно образуют фрагмент 3-тиосукцинимид-1-илалкилоксиалкилоксиалкилидена, где алкилиден образует гидразон со средством A, его аналогом или производным, каждый алкил выбран независимо, и фрагмент оксиалкилокси независимо замещен алкилом или необязательно замещенным арилом.
В другом аспекте поливалентный линкер включает расщепляемый линкер, дополнительный спейсер линкера и расщепляемый линкер, которые совместно образуют фрагмент 3-дитиоалкилоксикарбонилгидразида.
В другом аспекте поливалентный линкер включает расщепляемый линкер, дополнительный спейсер линкера и расщепляемый линкер, которые совместно образуют фрагмент 3-дитиоалкиламино, где амино образует винилог амида со средством A, его аналогом или производным.
В другом аспекте поливалентный линкер включает расщепляемый линкер, дополнительный спейсер линкера и расщепляемый линкер, которые совместно образуют фрагмент 3-дитиоалкиламино, где амино образует винилог амида со средством A, его аналогом или производным, и алкил представляет собой этил.
В другом аспекте поливалентный линкер включает расщепляемый линкер, дополнительный спейсер линкера и расщепляемый линкер, которые совместно образуют 3-дитиоалкиламинокарбонил, где карбонил образует карбамат со средством А, его аналогом или производным.
В другом аспекте поливалентный линкер включает расщепляемый линкер, дополнительный спейсер линкера и расщепляемый линкер, которые совместно образуют 3-дитиоалкиламинокарбонил, где карбонил образует карбамат со средством А, его аналогом или производным, и алкил представляет собой этил.
В другом аспекте поливалентный линкер включает расщепляемый линкер, дополнительный спейсер линкера и расщепляемый линкер, которые совместно образуют 3-дитиоарилалкилоксикарбонил, где карбонил образует карбамат или карбамоилазиридин со средством А, его аналогом или производным.
В другом варианте осуществления поливалентный линкер (L) включает дисульфидный расщепляемый линкер. В другом варианте осуществления поливалентный линкер (L) включает как минимум один расщепляемый линкер, который не является дисульфидным расщепляемым линкером.
В одном из аспектов расщепляемый фрагмент и спейсер линкера могут быть расположены таким образом, чтобы вслед за расщеплением связи в поливалентном линкере высвободившиеся функциональные группы содействовали разрыву или расщеплению дополнительных связей, что именуют также анхимерным содействием расщеплению или разрыву. Иллюстративные варианты осуществления такого поливалентного линкера или его фрагмента включают соединения, имеющие формулы:
где X представляет собой гетероатом, такой как азот, кислород или сера, или карбонильную группу; n означает целое число, выбранное из чисел от 0 до 4; в качестве иллюстрации 2; R означает водород или заместитель, в том числе заместитель, способный стабилизировать положительный заряд индуктивно или за счет резонанса с арильным циклом, например, алкокси и т.п., включая метокси; и символ (*) означает точки присоединения дополнительного структурного фрагмента, гетероатома или расщепляемых линкеров, образующих поливалентный линкер, или, с другой стороны, точки присоединения лекарственного средства, или его аналога или производного, или витамина или его аналога, или производного. В одном из вариантов осуществления n=2 и R представляет собой метокси. Предполагается, что другие заместители могут присутствовать на арильном цикле, бензильном атоме углерода, фрагменте алкановой кислоты или метиленовом мостике, включая, но не ограничиваясь этим, гидрокси, алкил, алкокси, алкилтио, галоген и т.п. Расщепление с анхимерным содействием может включать механизмы, в которые принимают участие бензилиевые промежуточные соединения, бензиновые промежуточные соединения, циклизация лактонов, оксониевые промежуточные соединения, бета-элиминирование и т.п. Далее подразумевается, что помимо фрагментации, следующей за разрывом связи в расщепляемом линкере, исходное разрушение связи в расщепляемом линкере может облегчаться механизмом анхимерного содействия.
Иллюстративные примеры промежуточного соединения, применимые при получении указанных линкеров, включают
где Xa представляет собой электрофильную группу, например, малеимид, винилсульфон, активированное производное карбоновой кислоты и т.п., Xb представляет собой NH, O или S; и каждый из коэффициентов m и n независимо выбран из целых чисел в диапазоне 0-4. В одном из вариантов каждый из коэффициентов m и n независимо выбран из целых чисел в диапазоне 0-2. Такие промежуточные соединения можно связывать с лекарственными средствами, связывающими лигандами или другими линкерами за счет нуклеофильной атаки на электрофильную группу Xa и/или за счет образования простых эфиров или производных карбоновой кислоты. В одном из вариантов осуществления бензильную гидроксильную группу превращают в соответствующее активированное бензилоксикарбонильное соединение действием фосгена или синтетического эквивалента фосгена. Такой вариант линкера может быть связан с лекарственными средствами, связывающими лигандами или другими линкерами за счет нуклеофильной атаки по активированной карбонильной группе.
Иллюстративные механизмы расщепления двухвалентных линкеров, описанных в настоящей заявке, включают следующие механизмы 1,4- и 1,6-фрагментации.
где X представляет собой экзогенный или эндогенный нуклеофил, глутатион или биологический восстанавливающий агент и т.п., и либо Z, либо Z' представляет собой витамин, его аналог или производное, или лекарственное средство, его аналог или производное, или же витамин или лекарственное средство в комбинации с другими фрагментами поливалентного линкера. Следует понимать, что хотя изображенные выше механизмы фрагментации изображены в виде синхронных механизмов, для окончательной фрагментации поливалентного линкера до показанных конечных продуктов может осуществляться любое число дискретных стадий. Например, имеется в виду, что расщепление связи может также иметь место под действием катализируемого кислотой элиминирования фрагмента карбамата, которому может оказывать анхимерное содействие стабилизация, обеспечиваемая или арильной группой у бета-атома серы или дисульфидным фрагментом, как показано в приведенных выше примерах. В этих разновидностях данного варианта осуществления расщепляемый линкер представляет собой фрагмент карбамата. В качестве альтернативы фрагментация может быть инициирована нуклеофильной атакой по дисульфидной группе, которая вызывает расщепление с образованием тиолата. Этот тиолат может по внутримолекулярному механизму замещать фрагмент карбоновой или карбаминовой кислоты с образованием соответствующего тиациклопропана. В случае поливалентного линкера, содержащего бензильный фрагмент, после иллюстративного расщепления дисульфидной связи, образующийся фенилтиолат может фрагментироваться далее с выделением фрагмента карбоновой кислоты или карбаминовой кислоты, за счет формирования резонансно-стабилизированного промежуточного соединения. В любом из этих случаев способность к расщеплению описанных в настоящей заявке иллюстративных поливалентных линкеров может быть реализована посредством любого механизма, который может соответствовать имеющимся химическим, метаболическим, физиологическим или биологическим условиям.
Другие иллюстративные механизмы расщепления связей в расщепляемом линкере включают расщепление с промежуточным образованием иона оксония по следующему механизму:
где Z представляет собой витамин, или его аналог, или производное, или лекарственное средство, его аналог или производное, или фрагмент, состоящий из витамина или лекарственного средства, в комбинации с другими фрагментами поливалентного линкера, например, фрагмент лекарственного средства или витамина, включающий один или несколько спейсеров линкера и/или других расщепляемых линкеров. Не ограничиваясь какой-либо теорией, в этом варианте осуществления кислотные катализаторы, присутствующие например, в эндосомах, могут инициировать расщепление за счет протонирования уретановой группы. Кроме того, катализируемое кислотами элиминирование карбамата ведет к выделению CO2 и азотсодержащего фрагмента, присоединенного к Z, а также образованию бензильного катиона, который может быть захвачен водой или любым другим основанием Льюиса.
Другие иллюстративные линкеры включают соединения формул:
где X представляет собой NH, CH2 или O; R представляет собой водород или заместитель, в том числе заместитель, способный стабилизировать положительный заряд, индуктивно или за счет резонанса в арильном цикле, например, алкокси и т.п., включая метокси; и символ (*) показывает точки присоединения дополнительных фрагментов, гетероатомов или расщепляемых линкеров, образующих поливалентный линкер, или, в качестве альтернативы, точки присоединения лекарственного средства, его аналога или производного, или же витамина, его аналога или производного.
Иллюстративные механизмы расщепления таких поливалентных линкеров, описанных в настоящей заявке, включают следующие механизмы 1,4- или 1,6-фрагментации, за которой следует облегчаемое анхимерным содействием отщепление ацилированного фрагмента Z' в результате циклизации при атаке гидразиновой группы.
где X представляет собой экзогенный или эндогенный нуклеофил, глутатион или биологический восстанавливающий агент и т.п., и любой из фрагментов Z или Z' представляет собой витамин, его аналог или производное, или лекарственное средство его аналог или производное, или же остаток витамина или лекарственного средства в комбинации с другой частью поливалентного линкера. Следует понимать, что хотя приведенные выше механизмы фрагментации изображены в виде синхронных механизмов, для осуществления окончательной фрагментации поливалентного линкера до показанных конечных продуктов, может осуществляться любое число дискретных стадий. Например, подразумевается, что расщепление связи может также происходить путем катализируемого кислотой элиминирования фрагмента карбамата, которое может облегчаться анхимерным содействием за счет стабилизации, обеспечиваемой или арильной группой у бета-атома серы или дисульфидным фрагментом, как показано в приведенных выше примерах. В этих разновидностях данного варианта осуществления расщепляемый линкер представляет собой фрагмент карбамата. В качестве альтернативы, фрагментация может быть инициирована нуклеофильной атакой по дисульфидной группе, которая вызывает расщепление с образованием тиолата. Этот тиолат может внутримолекулярно замещать фрагмент карбоновой кислоты или карбаминовой кислоты и образовывать соответствующий тиациклопропан. В случае поливалентного линкера, содержащего бензильный фрагмент, после иллюстративного расщепления дисульфидной связи, образующийся фенилтиолат может фрагментироваться далее с выделением фрагмента карбоновой кислоты или карбаминовой кислоты, за счет формирования резонансно-стабилизированного промежуточного соединения. В любом из этих случаев способность к расщеплению описанных в настоящей заявке иллюстративных поливалентных линкеров может быть реализована посредством любого механизма, который может соответствовать имеющимся химическим, метаболическим, физиологическим или биологическим условиям. Не ограничиваясь какой-либо теорией, в этом варианте осуществления кислотные катализаторы, присутствующие, например, в эндосомах, могут также инициировать расщепление за счет протонирования уретановой группы. Кроме того, катализируемое кислотами элиминирование карбамата ведет к выделению CO2 и азотсодержащего фрагмента, присоединенного к Z, а также образованию бензильного катиона, который может быть захвачен водой или другим основанием Льюиса, аналогично тому, как это уже было описано выше в настоящей заявке.
В одном из вариантов осуществления описанные в настоящей заявке поливалентные линкеры представляют собой соединения, имеющие следующие формулы:
где n представляет собой целое число, выбранное из чисел от 1 до примерно 4; каждый из фрагментов Ra и Rb независимо выбран из группы, состоящей из водорода и алкила, в том числе низшего алкила, например, C1-C4 алкила, который необязательно является разветвленным; или же Ra и Rb совместно с атомом углерода, к которому они присоединены, образуют карбоцикл; R представляет собой необязательно замещенную алкильную группу, необязательно замещенную ацильную группу или группу, подходящую для защиты атома азота; и знаком (*) отмечены точки присоединения лекарственного средства, витамина, средства визуализации, диагностического средства, других поливалентных линкеров или других частей конъюгата.
В другом варианте осуществления поливалентные линкеры, описанные в настоящей заявке, включают соединения следующих формул
где m представляет собой целое число, выбранное из чисел от 1 до примерно 4; R представляет собой необязательно замещенную алкильную группу, необязательно замещенную ацильную группу или подходящую защитную группу для атома азота; и знаком (*) отмечены точки присоединения лекарственного средства, витамина, средства визуализации, диагностического средства, других поливалентных линкеров или других частей конъюгата.
В другом варианте осуществления описанные в настоящей заявке поливалентные линкеры включают соединения следующих формул
где m представляет собой целое число, выбранное из чисел от 1 до примерно 4; R представляет собой необязательно замещенную алкильную группу, необязательно замещенную ацильную группу или подходящую защитную группу для атома азота; и знаком (*) отмечены точки присоединения лекарственного средства, витамина, средства визуализации, диагностического средства, других поливалентных линкеров или других частей конъюгата.
Другой иллюстративный механизм включает такое расположение расщепляемого фрагмента линкера и спейсеров линкера, что вслед за расщеплением связи в поливалентном линкере высвободившаяся функциональная группа химически содействует разрыву или расщеплению дополнительных связей, что именуют также анхимерным содействием расщеплению или разрыву. Иллюстративный вариант осуществления такого поливалентного линкера или его части включает соединения, имеющие формулу:
где X представляет собой гетероатом, например, азот, кислород или серу, n означает целое число, выбранное из 0, 1, 2 и 3, R представляет собой водород или заместитель, в том числе заместитель, способный стабилизировать положительный заряд индуктивно или за счет резонанса с участием арильного цикла, например, алкокси и т.п., и любой из символов Z или Z' означает витамин, его аналог или производное, или лекарственное средство, его аналог или производное, или остаток витамина или лекарственного средства, объединенный с другими частями поливалентного линкера. Подразумевается, что другие заместители могут присутствовать у арильного цикла, бензильного атома углерода, атома азота карбамата, фрагмента алкановой кислоты или метиленового мостика, включая, но не ограничиваясь перечисленными, гидрокси, алкил, алкокси, алкилтио, галоген и т.п. Содействие расщеплению может включать механизмы, в которые вовлечены бензилиевые промежуточные соединения, бензиновые промежуточные соединения, циклизация лактонов, оксониевые промежуточные соединения, бета-элиминирование и т.п. Далее подразумевается, что в дополнение к фрагментации, следующей за разрушением связи в расщепляемом линкере, исходное разрушение связи в расщепляемом линкере может облегчаться механизмом, включающим анхимерное содействие.
В этом варианте осуществления способная к циклизации гидроксиалкановая кислота облегчает расщепление метиленового мостика за счет образования, например, оксониевого иона, и облегчает расщепление других связей или последующую фрагментацию после разрыва связи в расщепляемом линкере. С другой стороны, катализируемое кислотой и осуществляемое с помощью иона оксония расщепление метиленового мостика может вызвать целый ряд последовательных фрагментаций упомянутого иллюстративного поливалентного линкера или его фрагмента. В качестве альтернативы, катализируемый кислотами гидролиз карбамата может облегчать бета-элиминирование гидроксиалкановой кислоты, которая способна к циклизации, и облегчает расщепление метиленового мостика за счет, например, образования оксониевого иона. Подразумевается, что другие химические механизмы разрыва или расщепления связей в метаболических, физиологических или клеточных условиях, описанных в настоящей заявке, могут инициировать такой последовательный ряд фрагментаций.
Другой иллюстративный вариант осуществления линкеров, описанных в настоящей заявке, включает расщепляемые линкеры, которые разрушаются в указанных в заявке условиях, посредством химического механизма, включающего бета-элиминирование. В одном из аспектов такие расщепляемые линкеры включают бета-тио, бета-гидрокси и бета-амино замещенные карбоновые кислоты и их производные, например, сложные эфиры, амиды, карбонаты, карбаматы и мочевины. В другом аспекте такие расщепляемые линкеры включают 2- и 4-тиоариловые сложные эфиры, карбаматы и карбонаты.
В другом варианте осуществления поливалентный линкер включает дополнительные спейсеры линкеров и расщепляемые линкеры, которые соединены с образованием поливалентного 3-тиосукцинимид-1-илалкилоксиметилоксигруппы, отображенной следующей формулой:
где n представляет собой целое число от 1 до 6; алкильная группа необязательно является замещенной, и метил необязательно замещен дополнительным алкилом или необязательно замещенной арильной группой, причем каждый из этих заместителей представлен независимо выбранной группой R. Символ (*) указывает на точки присоединения фрагмента поливалентного линкера к остальным частям конъюгата, описанного в настоящей заявке.
В другом варианте осуществления поливалентный линкер включает дополнительные спейсеры линкера и расщепляемые линкеры, соединенные таким образом, что они образуют поливалентную 3-тиосукцинимид-1-илалкилкарбонильную группу, которая отображена следующей формулой:
где n представляет собой целое число от 1 до 6, и алкильная группа необязательно является замещенной. Символы (*) указывают на точки присоединения фрагмента поливалентного линкера к остальным частям конъюгата, описанного в настоящей заявке. В другом варианте осуществления, поливалентный линкер включает структурные фрагменты и расщепляемые линкеры, которые соединены таким образом, чтобы образовалась поливалентная 3-тиоалкилсульфонилалкил(дизамещенный силил)оксигруппа, где дизамещенный силил замещен алкилом и/или необязательно замещенной арильной группой.
В другом варианте осуществления поливалентный линкер включает дополнительные спейсеры линкера и расщепляемые линкеры, соединенные таким образом, чтобы образовалась поливалентная группа дитиоалкилкарбонилгидразид или поливалентная группа 3-тиосукцинимид-1-илалкилкарбонилгидразид, которые отображены следующими формулами:
где n означает целое число от 1 до 6, алкильная группа является необязательно замещенной и гидразид образует гидразон с (B), (D) или другой частью поливалентного линкера (L). Символы (*) указывают на точки присоединения фрагмента поливалентного линкера к остальным частям конъюгата, описанного в настоящей заявке.
В другом варианте осуществления поливалентный линкер включает дополнительные спейсеры линкера и расщепляемые линкеры, соединенные таким образом, чтобы образовалась поливалентная группа 3-тиосукцинимид-1-илалкилоксиалкилоксиалкилиден, представленная следующей формулой:
где коэффициент n в каждом случае независимо выбран из целых чисел от 1 до 6, каждая алкильная группа независимо выбрана и необязательно замещена, например, алкилом и необязательно замещенным арилом, и где алкилиден образует гидразон с (B), (D) или другой частью поливалентного линкера (L). Символы (*) указывают на точки присоединения фрагмента поливалентного линкера к остальным частям конъюгата, описанного в настоящей заявке.
Другие иллюстративные дополнительные спейсеры линкера включают алкилен--амино--алкиленкарбонил, алкилен--тио--карбонилалкилсукцинимид-3-ил и т.п., что дополнительно показано следующими формулами:
где целые числа x и y равны 1, 2, 3, 4 или 5.
В другом иллюстративном варианте осуществления линкер включает одну или несколько аминокислот. В одном из вариантов линкер включает один остаток аминокислоты. В другом варианте линкер включает пептид, содержащий от 2 до примерно 50, от 2 до примерно 30 или от 2 до примерно 20 остатков аминокислот. В другом варианте линкер включает пептид, содержащий от примерно 4 до примерно 8 аминокислот. Эти аминокислоты в качестве иллюстрации выбирают из природных аминокислот или их стереоизомеров. Упомянутые аминокислоты могут также являться любыми другими аминокислотами, например, любой аминокислотой, имеющей следующую общую формулу:
-N(R)-(CR'R”)q-C(O)-,
где R представляет собой водород, алкил, ацил, или подходящую защитную группу для атома азота, R' и R” представляют собой водород или заместитель, каждый из которых в каждом из случаев выбран независимо, и коэффициент q является целым числом, таким как 1, 2, 3, 4 или 5. Иллюстративно R' и/или R” независимо представляют собой, не ограничиваясь этим, водород или группы, являющиеся боковыми цепями природных аминокислот, такие как метил, бензил, гидроксиметил, тиометил, карбоксил, карбоксиметил, гуанидинопропил и т.п., а также их производные и защищенные производные. Описанная выше формула включает все стереоизомерные варианты. Например, аминокислота может быть выбрана из аспарагина, аспарагиновой кислоты, цистеина, глутаминовой кислоты, лизина, глутамина, аргинина, серина, орнитина, треонина и т.п. В одном из вариантов расщепляемый линкер включает по меньшей мере 2 аминокислоты, выбранные из аспарагина, аспарагиновой кислоты, цистеина, глутаминовой кислоты, лизина, глутамина, аргинина, серина, орнитина и треонина. В другом варианте расщепляемый линкер включает от 2 до примерно 5 аминокислот, выбранных из аспарагина, аспарагиновой кислоты, цистеина, глутаминовой кислоты, лизина, глутамина, аргинина, серина, орнитина и треонина. В другом варианте расщепляемый линкер включает трипептид, тетрапептид, пентапептид или гексапептид, состоящий из аминокислотных остатков, выбранных из аспарагиновой кислоты, цистеина, глутаминовой кислоты, лизина, аргинина и орнитина, а также их комбинаций.
В другом иллюстративном аспекте промежуточного соединения конъюгата для доставки лекарственных средств, связывающего рецептор витамина, описанного в настоящем изобретении, лекарственное средство, его аналог или производное включает алкилтиольный нуклеофил.
Дополнительные линкеры описаны в следующих таблицах, где атом, обозначенный символом (*), является точкой присоединения дополнительного спейсера линкера или расщепляемого линкера, лекарственного средства и/или связывающего лиганда.
Описаны следующие иллюстративные структурные фрагменты линкеров.
Описаны следующие иллюстративные расщепляемые линкеры
Подразумевается, что такие гидрофильные линкеры могут изменять стабильность, метаболизм и распределение конъюгатов в тканях, в частности по сравнению с другими формами конъюгатов, как например, формами на основе пептидов, описанных в заявке на патент США № 10/765336. Например, предполагается, что в некоторых ситуациях взаимодействия углевод-белок слабее, чем взаимодействия пептид-белок. Таким образом, предполагается, что в различных вариантах осуществления, описанных в настоящем изобретении, конъюгаты могут приводить к более низкому связыванию с белками сыворотки. Эти и другие физико-химические отличия между конъюгатами, описанными в настоящей заявке, и другими, описанными ранее, могут включать улучшенное нацеливание на клеточные мишени и улучшенные, т.е. более селективные или дифференцированно селективные, профили биораспределения. Увеличенная цитотоксичность может являться естественным следствием уменьшенного связывания с белками сыворотки или же лучшего или дифференцированного биораспределения (т.е. меньшее количество лекарственного средства бесцельно тратится в нецелевых тканях организма). Это особенно справедливо в случае применения гидрофильных, но нейтральных спейсеров. Не ограничиваясь какой-либо теорией, полагают также, что гидрофильные спейсеры линкера, описанные в настоящей заявке, могут снижать токсичность, которая могла бы возникать, по крайней мере частично, из-за взаимодействий, основанных на неспецифическом связывании.
В альтернативном варианте осуществления лекарственное средство связывают с гидрофильным спейсером линкера непосредственно или через промежуточные фрагменты, для достижения такой цели, как уменьшение выведения через печень. В настоящем изобретении было обнаружено, что присоединение гидрофильных групп, независимо от того, отщепляемые они или нет, и более конкретно, гидрофильных нейтральных групп, увеличивает поступление лекарственного средства именно в почки.
Было обнаружено, что при печеночном клиренсе конъюгатов фолат-лекарственное средство, включающих дисульфидные линкеры и пептидные фрагменты, сохраняется остаточный и иногда значительный нежелательный профиль токсичности. Введение гидрофильных спейсеров, описанных в настоящей заявке, приводит к появлению тенденции поступления конъюгатов в почки. Следовательно, подразумевается, что включение таких линкеров в лекарственные конъюгаты направленного действия может снизить общее поглощение лекарственного средства печенью и, следовательно, снизить общую токсичность. Не ограничиваясь какой-либо теорией, полагают, что токсичность, выраженная в виде MTD, например конъюгатов алкалоидов барвинка, может быть вызвана неспецифическим печеночным клиренсом, ведущим к метаболизму, выделению свободного лекарственного средства, например DAVLBH, в желчь и затем в кишечник. После этого могла бы проявляться местная токсичность, а также системная токсичность (вследствие реабсорбции). Считается, что за счет введения гидрофильных линкеров в нацеленные и ненацеленные конъюгаты, описанные в настоящем изобретении, может преимущественно иметь место клиренс через почки, что позволяет снизить и/или избежать сопутствующего метаболизма в печени, который является основой токсичности. Соответственно, измерение общего выведения с желчью лекарственного компонента, например DAVLBH, из ряда конъюгатов лекарственное средство-фолат, может использоваться для прогноза того, какой из агентов был бы наименее токсичным.
Как указано выше, описанные в настоящей заявке конъюгаты могут применяться для доставки целевых средств А к клеткам селективным или специфичным образом. В одном из аспектов такой доставки можно также избежать нежелательных механизмов клиренса. Было обнаружено, что описанные в настоящем изобретении гидрофильные спейсеры линкера при их применении для получения конъюгатов рецептор-связывающих лигандов B и средств А могут уменьшать количество лекарственного средства, выводимого через печень. Далее было обнаружено, что эти гидрофильные спейсеры линкера имеют тенденцию способствовать клиренсу через мочевыводящие пути, например, почки. Далее было обнаружено, что описанные в изобретении конъюгаты проявляют более низкую токсичность, чем исходные средства А сами по себе при введении их тем же путем. Не ограничиваясь какой-либо теорией, полагают, что причиной этой более низкой токсичности является наблюдаемое уменьшение роли механизма выведения через печень и увеличение роли механизмов почечного выведения.
В другом варианте осуществления в настоящем изобретении описаны соединения, которые характеризуются уменьшенным поглощением печенью и меньшей вероятностью вывода печенью. В одном из аспектов такие соединения предпочтительно выводятся за счет почечных процессов по сравнению с печеночными процессами. Соответственно, в другом варианте осуществления в изобретении описаны не нацеленные соединения следующей формулы:
L-A,
где L является гидрофильным спейсером, и A представляет собой диагностическое или терапевтическое средство, или средство визуализации. Предполагается, что эти не нацеленные соединения, хотя они и не имеют направленного действия, вызванного применением рецептор-связывающего лиганда B, тем не менее проявляют пониженную токсичность по сравнению с исходным средством А при доставке их тем же самым путем. Эти не нацеленные соединения, как и нацеленные конъюгаты, описанные выше по тексту, включают гидрофильный спейсер L. Следовательно, агент, не достигший клетки, которую желательно подвергнуть лечению, будет выведен посредством обычных метаболических и биологических механизмов. Однако предполагается, что присутствие гидрофильного спейсера L будет направлять клиренс через почечные пути, а не через печеночные пути.
В другом варианте осуществления, в настоящем изобретении описаны мультилекарственные конъюгаты. В изобретении рассматривается несколько иллюстративных конфигураций таких мультилекарственных конъюгатов, и они включают соединения и композиции, описанные в международной публикации PCT № WO 2007/022494, содержание которой включено в настоящую заявку посредством ссылки. В качестве иллюстрации, поливалентные линкеры могут соединять рецептор-связывающий лиганд B с двумя или несколькими средствами A в ряде структурных конфигураций, включая следующие иллюстративные общие формулы, но не ограничиваясь ими:
где B представляет собой рецептор-связывающий лиганд, каждый из (L1), (L2) и (L3) является поливалентным линкером, описанным в настоящей заявке, включающим гидрофильный спейсер линкера и, необязательно, включающим один или несколько расщепляемых линкеров и/или дополнительных спейсеров линкера, и каждый из (A1), (A2) и (A3) является средством А, его аналогом или производным. Кроме того, изобретение охватывает другие варианты, включающие присутствие дополнительных средств А, их аналогов или производных, дополнительных линкеров, дополнительных конфигураций расположения каждого из (B), (L) и (A).
В одном из вариантов в описанные в настоящей заявке конъюгаты для доставки лекарственных средств входит более чем один рецептор-связывающий лиганд B, включая следующие иллюстративные общие формулы, но не ограничиваясь ими:
где каждый фрагмент B представляет собой рецептор-связывающий лиганд, каждый из (L1), (L2) и (L3) является поливалентным линкером, описанным в настоящей заявке, включающим гидрофильный спейсер линкера и, необязательно, включающим один или несколько расщепляемых линкеров и/или дополнительных спейсеров линкера, и каждый из (A1), (A2) и (A3) является средством А, его аналогом или производным. Кроме того, изобретение охватывает другие варианты, включающие присутствие дополнительных средств А, их аналогов или производных, дополнительных линкеров, дополнительных конфигураций расположения каждого из (B), (L) и (A). В одном из вариантов рецептор-связывающие лиганды B представляют собой лиганды для одного и того же рецептора, и в другом варианте рецептор-связывающие лиганды B являются лигандами для разных рецепторов.
В другом иллюстративном варианте осуществления выбирают лекарственные средства на основе активности против одной или нескольких популяций патогенных клеток с конкретным механизмом действия. Иллюстративные механизмы действия включают действие алкилирующих агентов, ингибиторов микротрубочек, в том числе тех, которые стабилизируют и/или дестабилизируют образование микротрубочек, включая средства, влияющие на бета-тубулин, ингибиторов циклин-зависимых киназ (CDK), ингибиторов топоизомеразы, ингибиторов синтеза белка, ингибиторов протеин-киназы, в том числе Ras, Raf, PKC, PI3K и подобных ингибиторов, ингибиторов транскрипции, антифолатов, блокаторов белков температурного шока и т.п.
Иллюстративные алкилирующие агенты включают, не ограничиваясь этим, митомицины CBI и т.п. Иллюстративные ингибиторы циклин-зависимой киназы (CDK) включают, не ограничиваясь перечисленными, CYC202, селициклиб, R-росковитин, AGM-1470 и т.п. Иллюстративные ингибиторы топоизомеразы включают, не ограничиваясь указанными, доксорубицин, другие антрациклины и т.п. Иллюстративные ингибиторы синтеза белка включают, не ограничиваясь этим, бруцеантин и т.п. Иллюстративные ингибиторы протеинкиназы, включающие Ras, Raf, PKC, PI3K и подобные ингибиторы, включают, не ограничиваясь этим, L-779450, R115777 и т.п. Иллюстративные ингибиторы транскрипции включают, не ограничиваясь перечисленными, α-аманатин, актиномицин и т.п. Иллюстративные антифолаты включают, не ограничиваясь этим, метотрексат и т.п. Иллюстративные блокаторы белков температурного шока включают, не ограничиваясь этим, гелданамицин и т.п.
Иллюстративные ингибиторы микротрубочек, в том числе те из них, которые стабилизируют и/или дестабилизируют образование микротрубочек, включают средства, действующие на β-тубулин, яды, разрушающие микротрубочки и т.п. Иллюстративные яды, разрушающие микротрубочки, которые связываются с выбранными рецепторами, включают, не ограничиваясь этим, ингибиторы, связывающиеся с сайтом связывания алкалоидов барвинка, такие как аренастатин, доластатин, галихондрин B, майтанзин, фомопсин A, ризоксин, устилоксин, винбластин, винкристин и т.п., стабилизаторы, связывающиеся с сайтом связывания таксола, такие как дискодермалид, эпотилон, таксол, паклитаксол, и т.п., ингибиторы, связывающиеся с сайтом связывания колхицина, такие как колхицин, комбретастатин, курацин A, подофиллотоксин, стеганацин и т.п., а также другие, связывающиеся с неустановленными сайтами, такие как криптофицин, тубулизины и т.п.
В одном из вариантов осуществления тубулизин представляет собой природный тубулизин. В другом варианте осуществления тубулизин является синтетическим или полусинтетическим тубулизином. Дополнительные разновидности тубулизина, которые могут быть включены в конъюгаты, описанные в настоящей заявке, раскрыты в международной заявке PCT № PCT/US2008/056824, содержание которой включено в настоящую заявку посредством ссылки.
В одном из вариантов осуществления конъюгата для доставки лекарственных средств, описанного в настоящем изобретении, как минимум одно из лекарственных средств представляет собой ингибитор микротрубочек, его аналог или производное. В другом варианте осуществления как минимум одно из лекарственных средств является ДНК-алкилирующим агентом. В другом варианте осуществления как минимум одно из лекарственных средств является ДНК-алкилирующим агентом, и как минимум одно из остальных лекарственных средств является ингибитором микротрубочек.
В другом варианте осуществления описанных в настоящей заявке конъюгатов для доставки лекарственных средств как минимум одно из лекарственных средств представляет собой ингибитор P-гликопротеина (PGP). В другом варианте осуществления как минимум одно из лекарственных средств, входящих в конъюгат, описанный в настоящей заявке, является ингибитором PGP, и как минимум одно из других лекарственных средств, включенных в конъюгат, является субстратом PGP. В качестве иллюстрации, в этом последнем варианте осуществления субстрат PGP представляет собой ДНК-алкилирующий агент. В отношении этого варианта осуществления подразумевается, что применение ингибитора PGP в сочетании с субстратом PGP, например ДНК-алкилирующим агентом, включая, но не ограничиваясь этим, любой из митомицинов, например, митомицин C, митомицин A и т.п., может улучшить суммарную эффективность лекарственного средства, которое в ином случае было бы субстратом PGP. В расщепляемых конъюгатах, описанных в настоящей заявке, лекарственное средство, являющееся ингибитором PGP, и лекарственное средство, являющееся субстратом PGP, совместно высвобождаются в клетку после эндоцитоза. Таким путем ингибитор PGP может улучшать общую эффективность и/или силу действия субстрата PGP. Кроме того, ингибитор PGP может уменьшать экспрессию PGP, что в свою очередь будет уменьшать выведение из патогенной клетки одного или нескольких лекарственных средств, входящих в мультилекарственный конъюгат, описанный в настоящей заявке. Подразумевается, что митомицины, их аналоги или производные, например, митомицин C, могут действовать как ингибиторы PGP или понижающие регуляторы PGP. Далее предполагается, что алкалоид барвинка, или его аналог или производное, например, аналоги и производные винбластина, могут являться субстратами PGP, которые защищены от выведения из патогенной клетки действием ингибитора или понижающего регулятора PGP.
В другом варианте осуществления описанных в изобретении конъюгатов для доставки лекарственных средств как минимум одно из лекарственных средств представляет собой алкалоид барвинка, его аналог или производное. Алкалоиды барвинка, описанные в заявке, включают всех членов семейства индол-дигидроиндольных алкалоидов барвинка, например, но не ограничиваясь указанными, виндезин, винбластин, винкристин, катарантин, виндолин, леурозин, винорелбин, имидокарб, сибутрамин, толтразурил, винбластиновую кислоту и т.п., а также их аналоги и производные.
В другом варианте осуществления в изобретении описаны способы лечения заболеваний, вызванных или проявивших себя в результате деятельности популяций патогенных клеток. Конъюгаты для доставки лекарственных средств, включающие связывающий лиганд, могут применяться для лечения болезненных состояний, характеризуемых наличием популяции патогенных клеток в организме хозяина, где члены популяции патогенных клеток имеют доступный сайт связывания связывающего лиганда (B), его аналога или производного, где указанный сайт связывания исключительно экспрессируется, избыточно экспрессируется или предпочтительно экспрессируется патогенными клетками. Селективное уничтожение патогенных клеток опосредуется связыванием фрагмента связывающего лиганда (B), входящего в конъюгат для доставки лекарственного средства, с рецептором или транспортером лиганда, или другим белком на поверхности клетки, который специфично связывает связывающий лиганд (B), его аналог или производное и который исключительно экспрессируется, избыточно экспрессируется или предпочтительно экспрессируется патогенными клетками. Присутствующий на поверхности клетки белок, который исключительно экспрессируется, избыточно экспрессируется или предпочтительно экспрессируется патогенными клетками, представляет собой рецептор, который отсутствует или присутствует в меньших концентрациях на непатогенных клетках, что обеспечивает средство для селективного уничтожения патогенных клеток.
Например, экспрессируемые на поверхности рецепторы витаминов, например высокоафинный рецептор фолатов, избыточно экспрессируются на раковых клетках. Сообщалось, что все эпителиальные формы рака яичников, молочных желез, ободочной кишки, легких, носа, гортани и мозга экспрессируют повышенные уровни рецепторов фолатов. Фактически известно, что более 90% всех опухолей яичников человека экспрессируют значительные количества этого рецептора. Соответственно, описанный в настоящей заявке конъюгат для доставки лекарственного средства, содержащий связывающий лиганд (B), может применяться для воздействия на ряд типов опухолевых клеток, а также других типов патогенных клеток, например инфекционных агентов, которые преимущественно экспрессируют рецепторы таких лигандов, как рецепторы витаминов, и, таким образом, имеют на поверхности доступные для связывания с лигандами сайты, такие как витамины, или их аналоги, или производные. В одном из аспектов, в изобретении описаны способы нацеливания конъюгатов связывающий лиганд-линкер-лекарственное средство с целью достижения максимальной селективности в отношении патогенных клеток, для их уничтожения.
Далее, в изобретении рассматривается применение комбинаций конъюгатов связывающий лиганд-линкер-лекарственное средство с целью достижения максимальной селективности в отношении патогенных клеток, для их уничтожения.
Описанные в изобретении конъюгаты для доставки лекарственного средства, включающие связывающий лиганд (B), могут применяться как для клинического лечения людей, так и в ветеринарии. Так, например, животное-хозяин, в организме которого имеется популяция патогенных клеток и которое подвергается лечению конъюгатами для доставки лекарственного средства, включающими связывающий лиганд (например, витамин), может являться человеком или, в случае применения в ветеринарии, может являться лабораторным, сельскохозяйственным, домашним или диким животным. Описанные в настоящем изобретении способы можно применять к животным-хозяевам, включая, но не ограничиваясь этим, людей, лабораторных животных, например, грызунов (например, мышей, крыс, хомяков и т.д.), кроликов, обезьян, шимпанзе, домашних животных, например, собак, кошек и кроликов, сельскохозяйственных животных, например, коров, лошадей, свиней, овец, коз, а также диких животных в неволе, например, медведей, панд, львов, тигров, леопардов, слонов, зебр, жирафов, горилл, дельфинов и китов.
Описываемые способы применимы к популяциям патогенных клеток, которые вызывают целый ряд патологий у перечисленных животных-хозяев. Термин «патогенные клетки» относится, например, к раковым клеткам, инфекционным агентам, таким как бактерии и вирусы, клеткам, инфицированным бактериями или вирусами, активированным макрофагам, способным вызывать болезненные состояния, а также любым другим типам патогенных клеток, которые исключительно экспрессируют, преимущественно экспрессируют или избыточно экспрессируют рецепторы связывающего лиганда, например, рецепторы витаминов или рецепторы, которые связывают аналоги или производные витаминов. Патогенные клетки могут также включать любые клетки, вызывающие состояние болезни, для которых лечение с помощью описанных в настоящем изобретении конъюгатов для доставки лекарственных средств, содержащих связывающий лиганд, приводит к уменьшению симптомов заболевания. Например, патогенными клетками могут являться клетки организма хозяина, которые становятся патогенными в определенных обстоятельствах, как, например, клетки иммунной системы, которые отвечают за заболевания типа «трансплантат-против-хозяина», но не являются патогенными в других ситуациях.
Так, например, популяция патогенных клеток может представлять собой популяцию раковых клеток, которые порождают новообразования, включая доброкачественные опухоли и злокачественные опухоли, или же эта популяция может не быть онкогенной. Популяция раковых клеток может возникать спонтанно или в результате такого процесса, как мутация, присутствующая в зародышевой линии животного-хозяина, или соматическая мутация, или ее появление может быть вызвано химическим, вирусным или радиационным воздействием. Описанные в изобретении способы могут применяться для лечения таких раковых заболеваний, как карциномы, саркомы, лимфомы, болезнь Ходжкина, меланомы, мезотелиомы, лимфома Беркитта, носоглоточные карциномы, лейкемии и миеломы. Популяция раковых клеток может включать, не ограничиваясь перечисленным, клетки раковых заболеваний полости рта, щитовидной железы, эндокринной системы, кожи, желудка, пищевода, гортани, поджелудочной железы, ободочной кишки, мочевого пузыря, костей, яичников, шейки матки, матки, груди, яичек, простаты, прямой кишки, почек, печени и легких.
В тех вариантах осуществления, где популяция патогенных клеток представляет собой популяцию раковых клеток, эффект от введения конъюгата представляет собой терапевтический отклик, оцениваемый по уменьшению или уничтожению опухолевой массы или по ингибированию пролиферации опухолевых клеток. В случае опухоли, уничтожение может являться уничтожением клеток первичной опухоли или клеток, которые метастазировали или находятся в процессе отделения от первичной опухоли. В изобретении описано также профилактическое лечение конъюгатом для доставки лекарственного средства, включающим связывающий лиганд (B) (в качестве связывающего лиганда применен, например, витамин), для предупреждения рецидива опухоли после ее удаления путем терапевтического подхода, который включает хирургическое удаление опухоли, радиационную терапию, химиотерапию или биологическую терапию. Профилактическое лечение может являться первичным лечением с помощью конъюгата для доставки лекарственного средства, включающего связывающий лиганд (B), например, путем введения в режиме нескольких доз в течение дня, и/или может являться дополнительным лечением или серией лечебных мероприятий с интервалом в несколько дней или месяцев, после первичного лечения. Соответственно, уничтожение любой из популяций патогенных клеток, подвергавшейся лечению с применением описанных в изобретении способов, включает уменьшение количества патогенных клеток, подавление пролиферации патогенных клеток, профилактическое лечение, которое предупреждает повторное появление патогенных клеток, или лечение патогенных клеток, которое приводит к уменьшению симптомов заболевания.
В случаях, когда необходимо уничтожить раковые клетки, способы по настоящему изобретению могут применяться в комбинации с хирургическим удалением опухоли, радиационной терапией, химиотерапией или биологическими видами лечения, например, другими формами иммунотерапии, включая, но не ограничиваясь этим, лечение моноклональными антителами, лечение иммуномодулирующими агентами, адаптивный перенос эффекторных иммунных клеток, лечение гематопоэтическими факторами роста, цитокинами и вакцинацией.
Способы лечения по настоящему изобретению применимы также к популяциям патогенных клеток, которые вызывают ряд инфекционных заболеваний. Например, эти способы применимы к таким популяциям патогенных клеток, как бактерии, грибки, в том числе дрожжи, вирусы, клетки, инфицированные вирусами, микоплазмы и паразиты. Инфекционные микроорганизмы, вызывающие заболевания, которые можно лечить описанными в изобретении конъюгатами для доставки лекарственных средств, включающими связывающий лиганд (B), представляют собой любые известные в области техники микроорганизмы, которые вызывают патогенез у животных, включая такие микроорганизмы, как грамотрицательные бактерии или грамположительные кокки или бациллы. Например, с помощью описанных в изобретении конъюгатов для доставки лекарственных средств, включающих связывающий лиганд, можно подвергать лечению заболевания, вызванные в организме хозяина бактериями рода Proteus, рода Klebsiella, рода Providencia, рода Yersinia, рода Erwinia, рода Enterobacter, рода Salmonella, рода Serratia, рода Aerobacter, рода Escherichia, рода Pseudomonas, рода Shigella, рода Vibrio, рода Aeromonas, рода Campylobacter, рода Streptococcus, рода Staphylococcus, рода Lactobacillus, рода Micrococcus, рода Moraxella, рода Bacillus, рода Clostridium, рода Corynebacterium, рода Eberthella, рода Micrococcus, рода Mycobacterium, рода Neisseria, рода Haemophilus, рода Bacteroides, рода Listeria, рода Erysipelothrix, рода Acinetobacter, рода Brucella, рода Pasteurella, рода Vibrio, рода Flavobacterium, рода Fusobacterium, рода Streptobacillus, рода Calymmatobacterium, рода Legionella, рода Treponema, рода Borrelia, рода Leptospira, рода Actinomyces, рода Nocardia, рода Rickettsia и любыми другими видами бактерий.
Особый интерес представляют бактерии, которые устойчивы к действию антибиотиков, например, устойчивые к действию антибиотиков виды Streptococcus и Staphylococcus, или бактерии, которые восприимчивы к антибиотикам, но при лечении антибиотиками вызывают рецидивирующую инфекцию, поскольку с течением времени развиваются устойчивые к антибиотику микроорганизмы. Бактерии, которые восприимчивы к антибиотикам, но вызывают рецидивирующую инфекцию при лечении антибиотиками, поскольку со временем развиваются резистентные микроорганизмы, могут подвергаться лечению с применением описанных в настоящем изобретении конъюгатов для доставки лекарственных средств, включающих связывающий лиганд (B), в отсутствие антибиотиков, или в комбинации с более низкими дозами антибиотиков по сравнению с обычно вводимыми пациентам, во избежание развития этих устойчивых к антибиотикам штаммов бактерий.
Вирусы, например, ДНК и РНК вирусы, также можно лечить описанными способами. Указанные вирусы включают, не ограничиваясь перечисленными, ДНК-вирусы, такие как вирусы папилломы, парвовирусы, аденовирусы, вирусы герпеса и вирусы осповакцины, а также РНК-вирусы, такие как аренавирусы, коронавирусы, риновирусы, респираторные синцитиальные вирусы, вирусы гриппа, пикорнавирусы, парамиксовирусы, реовирусы, ретровирусы, лентивирусы и рабдовирусы.
Способы по настоящему изобретению применимы также для лечения патологий, вызванных любыми грибками, включая дрожжи, различными видами микоплазм, паразитами или другими инфекционными микроорганизмами, которые вызывают заболевания у животных. Примеры грибков, которые могут подвергаться лечению способами и композициями по настоящему изобретению, включают грибки, которые растут в виде плесени или являются дрожжеподобными, в том числе, например, грибки, вызывающие такие заболевания, как стригущий лишай, гистоплазмоз, бластомикоз, аспергиллез, криптококкоз, споротрихоз, кокцидиоидомикоз, паракокцидиоидомикоз, мукормикоз, хромобластомикоз, дерматофитоз, прототекоз, фузариоз, питириаз, мицетому, паракокцидиоидомикоз, фаеогифомикоз, псевдоаллешериаз, споротрихоз, трихоспороз, пневмоцистные инфекции и кандидоз.
Способы по настоящему изобретению могут также применяться для лечения паразитарных инфекций, включая, но не ограничиваясь этим, инфекции, вызванные ленточными червями, например, относящимися к родам Taenia, Hymenolepsis, Diphyllothrium и Echinococcus, трематодами, например, родов Fasciolopsis, Heterophyes, Metagonimus, Clonorchis, Fasciola, Paragonimus и Schitosoma, круглыми червями, например родов Enterobius, Trichuris, Ascaris, Ancylostoma, Necator, Strongyloides, Trichinella, Wuchereria, Brugia, Loa Onchocerca и Dracunculus, амебами, например, родов Naegleria и Acanthamoeba, и простейшими, например, родов Plasmodium, Trypanosoma, Leishmania, Toxoplasma, Entamoeba, Giardia, Isospora, Cryptosporidium и Enterocytozoon.
Патогенные клетки, на которые нацелены описанные в настоящем изобретении конъюгаты для доставки лекарственных средств, включающие связывающий лиганд, могут также являться клетками, в которых находятся эндогенные патогены, например, клетками, инфицированными вирусами, микоплазмами, паразитами или бактериями, если эти клетки преимущественно экспрессируют рецепторы лиганда, например, рецепторы витамина.
В одном из вариантов осуществления конъюгаты для доставки лекарственных средств, включающие связывающие лиганды, могут быть интернализованы целевой патогенной клеткой при связывании фрагмента связывающего лиганда с рецептором, транспортером или другим белком, присутствующим на поверхности, который специфично связывается с лигандом и который преимущественно экспрессируется на патогенных клетках. Эта интернализация может осуществляться, например, путем опосредованного рецептором эндоцитоза. Если конъюгат для доставки лекарственных средств, включающий связывающий лиганд (B), содержит расщепляемый линкер, фрагмент связывающего лиганда и лекарственное средство могут разделиться внутри клетки и лекарственное средство может подействовать на свою внутриклеточную мишень.
В альтернативном варианте осуществления фрагмент связывающего лиганда конъюгата для доставки лекарственного средства может связаться с патогенной клеткой, причем лекарственное средство окажется в близком соседстве с поверхностью патогенной клетки. Затем это лекарственное средство может высвободиться за счет разрыва расщепляемого линкера, например, лекарственное средство может высвободиться под действием протеин дисульфид изомеразы, если расщепляемый линкер представляет собой дисульфидную группу. Затем лекарственное средство может быть захвачено патогенной клеткой, к которой присоединился конъюгат для доставки лекарственного средства, включающий связывающий лиганд (B), или же лекарственное средство может быть захвачено другой патогенной клеткой, находящейся в непосредственной близости к первой. В качестве альтернативы, лекарственное средство могло бы высвободиться под действием протеин дисульфид изомеразы внутри клетки, если расщепляемый линкер представляет собой дисульфидную группу. Кроме того, лекарственное средство могло бы высвободиться за счет гидролитического механизма, например, катализируемого кислотами гидролиза, который описан выше для некоторых механизмов бета-элиминирования, или за счет расщепления с анхимерным содействием, по механизму с образованием оксониевого или лактониевого иона. Выбор расщепляемого линкера или линкеров будет определять механизм, по которому лекарственное средство будет отщепляться от конъюгата. Подразумевается, что этот выбор может быть предопределен условиями, в которых будет применяться конъюгат лекарственного средства. В качестве альтернативы, конъюгаты для доставки лекарственных средств могут быть интернализованы в целевые клетки при связывании, и связывающий лиганд и лекарственное средство могут оставаться в связанном состоянии внутри клетки, причем лекарственное средство оказывает свое действие без отделения от фрагмента витамина.
В еще одном варианте осуществления, в котором связывающий лиганд представляет собой витамин, конъюгат витамин-лекарственное средство может действовать по механизму, не зависящему от клеточных рецепторов витаминов. Например, конъюгаты для доставки лекарственных средств могут связываться с растворимыми рецепторами витаминов, присутствующими в сыворотке, или с белками сыворотки, например, альбумином, что приводит к увеличению времени циркуляции конъюгатов относительно неконъюгированного лекарственного средства и к повышению активности конъюгатов в отношении популяции патогенных клеток, по сравнению с неконъюгированными лекарственными средствами.
В другом варианте осуществления, в котором линкер не содержит расщепляемого фрагмента, фрагмент витамина, входящий в конъюгат для доставки лекарственного средства, может связываться с патогенной клеткой, помещая лекарственное средство на поверхность патогенной клетки, для того чтобы сделать ее мишенью для атаки других молекул, способных связываться с лекарственным средством. В качестве альтернативы, в этом варианте осуществления конъюгат для доставки лекарственного средства может быть интернализован целевыми клетками после связывания, и фрагменты витамина и лекарственного средства могут оставаться связанными внутри клетки, причем лекарственное средство проявляет свое действие без отделения от фрагмента витамина.
В другом варианте осуществления настоящего изобретения разработан конъюгат для доставки лекарственного средства, связывающий клеточный рецептор общей формулы B-L-A, где фрагмент L соответствует приведенному в заявке описанию, и A представляет собой лекарственное средство, например, иммуноген. Иммуноген может представлять собой гаптен, например, флуоресцеин, динитрофенил и т.п. В этом варианте осуществления конъюгат для доставки лекарственного средства, связывающий рецептор витамина, связывается с поверхностью патогенной клетки и «метит» клетки иммуногеном, тем самым запуская иммунную реакцию, направленную на меченую популяцию патогенных клеток. Антитела, введенные в организм хозяина при пассивной иммунизации, или антитела, существующие в иммунной системе хозяина в рамках врожденного или приобретенного иммунитета, связываются с иммуногеном и запускают эндогенный иммунный ответ. Связывание антител с клетками, меченными конъюгатом витамин-иммуноген, приводит к комплемент-опосредованной цитотоксичности, антитело-зависимой клеточно-опосредованной цитотоксичности, опсонизации с участием антител и фагоцитозу, кластеризации рецепторов, индуцированной антителами, дающей сигнал о смерти клетки или переходе в состояние покоя, или к любому другому гуморальному или клеточному иммунному ответу, стимулированному связыванием антитела со связанным клеткой конъюгатом лиганд-иммуноген. В тех случаях, когда иммуноген может быть непосредственно распознан иммунными клетками без предварительной опсонизации антителами, может происходить прямое уничтожение патогенных клеток. Этот вариант осуществления более подробно описан в заявке на патент США № 09/822379, включенной в настоящую заявку посредством ссылки. Подразумевается, что в некоторых разновидностях данного варианта осуществления, в которых лекарственное средство представляет собой иммуноген, поливалентный линкер может включать также расщепляемые фрагменты, которые описаны выше, например, конъюгат для доставки лекарственного средства, связывающий рецептор витамина общей формулы B-L-A, где L представляет собой линкер, который включает один или несколько гидрофильных спейсеров линкера и расщепляемый линкер.
Описанные в настоящем изобретении конъюгаты для доставки лекарственных средств включают связывающий лиганд (B), поливалентный линкер (L), лекарственное средство и, необязательно, линкеры на основе гетероатомов, которые соединяют связывающий лиганд и лекарственное средство с поливалентным линкером (L). Поливалентный линкер (L) может включать спейсеры линкера, расщепляемые (т.е. разрушаемые) фрагменты линкера, а также фрагменты линкера на основе гетероатомов, или комбинации перечисленных фрагментов.
Лекарственное средство может представлять собой любую молекулу, способную модулировать или каким-либо иным образом модифицировать деятельность клетки, включая фармацевтически активные соединения. Подходящие молекулы могут включать, не ограничиваясь перечисленными, пептиды, олигопептиды, ретроинверсные олигопептиды, белки, аналоги белков, в которых как минимум одна непептидная связь заменяет пептидную связь, апопротеины, гликопротеины, ферменты, коферменты, ингибиторы ферментов, аминокислоты и их производные, рецепторы и другие мембранные белки; антигены и антитела против них; гаптены и антитела против них; гормоны, липиды, фосфолипиды, липосомы; токсины; антибиотики; аналгетики; бронхорасширяющие средства; бета-блокаторы; противомикробные средства; противогипертонические средства; сердечно-сосудистые средства, включая антиаритмические средства, сердечные гликозиды, антиангинальные средства и сосудорасширяющие средства; средства для воздействия на центральную нервную систему, включая стимуляторы, психотропные препараты, противоманиакальные средства и депрессанты; антивирусные средства; антигистаминные препараты; противораковые средства, включая химиотерапевтические средства; транквилизаторы; антидепрессанты; антагонисты H-2; противосудорожные средства; противотошнотные средства; простагландины и аналоги простагландинов; миорелаксанты; противовоспалительные средства; стимуляторы; противозастойные средства; противорвотные средства; диуретики; спазмолитические средства; антиастматические средства; средства против болезни Паркинсона; отхаркивающие средства; средства, подавляющие кашель; муколитические средства, а также минеральные и пищевые добавки.
Кроме того, лекарственное средство может быть любым лекарственным средством, известным в области техники, которое является цитотоксическим, улучшает проницаемость опухоли, ингибирует пролиферацию опухолевых клеток, способствует апоптозу, уменьшает антиапоптотическую активность в целевых клетках, применяется для лечения заболеваний, вызванных инфекционными агентами, усиливает эндогенный иммунный ответ, направленный на патогенные клетки или применяется для лечения болезненных состояний, вызванных любым типом патогенных клеток. Лекарственные средства, которые подходят для применения согласно настоящему изобретению, включают адренокортикоиды и кортикостероиды, алкилирующие агенты, антиандрогены, антиэстрогены, андрогены, акламицин и производные акламицина, эстрогены, антиметаболиты, такие как цитозина арабинозид, аналоги пурина, аналоги пиримидина, а также метотрексат, бусульфан, карбоплатин, хлорамбуцил, цисплатин и другие соединения платины, тамоксифен, таксол, паклитаксел, производные паклитаксела, Taxotere®, циклофосфамид, дауномицин, даунорубицин, доксорубицин, ризоксин, токсин Т2, растительные алкалоиды, преднизон, гидроксимочевину, тенипозид, митомицины, дискодермолиды, ингибиторы микротубулина, эпотилоны, тубулизин, циклопропилбенз[e]индолон, seco-циклопропилбенз[e]индолон, O-Ac-seco-циклопропилбенз[e]индолон, блеомицин и любые другие антибиотики, азотистые иприты, нитрозомочевины, винкристин, винбластин, его аналоги или производные, например, диацетилвинбластина моногидразид и другие алкалоиды барвинка, включая описанные в международной публикации PCT № WO 2007/022493, содержание которой включено в настоящую заявку посредством ссылки, колхицин, производные колхицина, аллоколхицин, тиоколхицин, тритилцистеин, галихондрин B, доластатины, например, доластатин 10, аманитины, например, α-аманитин, камптотекин, иринотекан и другие производные камптотекина, майтанзины, гелданамицин и производные гелданамицина, эстрамустин, нокодазол, MAP4, колцемид, воспалительные и провоспалительные агенты, пептиды и пептидомиметики, являющиеся ингибиторами передачи сигнала, а также любые другие известные в области техники лекарственные средства или токсины. Другие лекарственные средства, которые могут применяться в соответствии с настоящим изобретением, включают пенициллины, цефалоспорины, ванкомицин, эритромицин, клиндамицин, рифампин, хлорамфеникол, аминогликозидные антибиотики, гентамицин, амфотерицин B, ацикловир, трифлуридин, ганцикловир, зидовудин, амантадин, рибавирин и любые другие известные в области техники противомикробные соединения.
В другом варианте осуществления средство (А) представляет собой лекарственное средство, выбранное из алкалоидов барвинка, например, DAVLBH, криптофицина, бортезомиба, тиобортезомиба, тубулизина, аминоптерина, рапамицина, паклитаксела, доцетаксела, доксорубицина, даунорубицина, эверолимуса, α-аманатина, верукарина, дидемнина B, гелданомицина, пурваланола A, эверолимуса, испинесиба, будесонида, дазатиниба, эпотилона, майтанзина и ингибиторов тирозинкиназы, в том числе аналогов и производных перечисленных лекарственных средств. В другом варианте осуществления конъюгат включает как минимум два средства (A), выбранных из алкалоидов барвинка, например, DAVLBH, криптофицина, бортезомиба, тиобортезомиба, тубулизина, аминоптерина, рапамицина, паклитаксела, доцетаксела, доксорубицина, даунорубицина, эверолимуса, α-аманатина, верукарина, дидемнина B, гелданомицина, пурваланола A, эверолимуса, испинесиба, будесонида, дазатиниба, эпотилона, майтанзина и ингибиторов тирозинкиназы, в том числе аналогов и производных перечисленных лекарственных средств. В одном из вариантов средства (A) являются одинаковыми. В другом варианте средства (A) являются различными.
В одном из вариантов осуществления лекарственные средства, предназначенные для применения в способах, описанных в настоящей заявке, остаются стабильными в сыворотке в течение как минимум 4 часов. В другом варианте осуществления лекарственные средства имеют значение IC50 в наномолярном диапазоне, и, в другом варианте осуществления, эти лекарственные средства являются водорастворимыми. Если лекарственное средство не является водорастворимым, в поливалентный линкер (L) могут быть введены дополнительные функциональные группы для улучшения растворимости в воде. Термин «лекарственное средство» означает также любой из аналогов или производных лекарственного средства, указанного выше по тексту заявки. Следует понимать, что в соответствии с настоящим изобретением словосочетание «аналог или производное лекарственного средства» может означать лекарственное средство, которое включает гетероатом, через который аналог или производное лекарственного средства ковалентно связано с поливалентным линкером (L).
Конъюгат для доставки лекарственного средства может включать связывающий лиганд (B), двухвалентный линкер (L), лекарственное средство и, необязательно, линкеры на основе гетероатомов, для соединения рецептор-связывающего фрагмента связывающего лиганда (B) и лекарственного средства с двухвалентным линкером (L). В одном иллюстративном варианте осуществления следует понимать, что аналог или производное витамина может означать витамин, который включает гетероатом, через который аналог или производное витамина ковалентно соединено с двухвалентным линкером (L). Так, например, в этом иллюстративном варианте осуществления витамин может быть ковалентно связан с двухвалентным линкером (L) через линкер, включающий гетероатом, или же аналог или производное витамина (т.е. витамин, включающий гетероатом) может быть напрямую связано с двухвалентным линкером (L). В аналогичных иллюстративных вариантах осуществления аналог или производное лекарственного средства представляет собой лекарственное средство, и аналог или производное лекарственного средства может означать лекарственное средство, которое включает гетероатом, через который аналог или производное лекарственного средства ковалентно связано с двухвалентным линкером (L). Так, например, в этих иллюстративных аспектах лекарственное средство может быть ковалентно связано с двухвалентным линкером (L) через линкер на основе гетероатома, или же аналог или производное лекарственного средства (т.е. включающее гетероатом) может быть напрямую связано с двухвалентным линкером (L). Двухвалентный линкер (L) может включать структурные фрагменты линкера, расщепляемый (т.е. разрушаемый) фрагмент линкера и линкер на основе гетероатома, который служит для связи фрагментов линкера с расщепляемым линкером в конъюгатах, содержащих оба этих типа линкеров.
Как правило, может быть применен любой способ формирования конъюгата между двухвалентным линкером (L) и связывающим лигандом (B) или его аналогом или производным, между двухвалентным линкером (L) и лекарственным средством или его аналогом или производным, включающий введение любых промежуточных линкеров на основе гетероатомов. Кроме того, для получения двухвалентного линкера (L) может применяться любой известный в технике способ формирования конъюгата между структурным фрагментом линкера, расщепляемым фрагментом линкера и линкером на основе гетероатома. Конъюгат может быть образован непосредственным соединением любых из этих молекул, например, путем комплексообразования или через водородные, ионные или ковалентные связи. Ковалентное связывание может осуществляться, например, путем образования амидных, сложноэфирных, дисульфидных или иминосвязей между карбоксильными, альдегидными, гидроксильными, амино, сульфгидрильными или гидразогруппами.
В другом варианте осуществления двухвалентный линкер (L) включает цепь атомов, выбранных из C, N, O, S, Si и P, которые соединяют ковалентными связями связывающий лиганд (B), гидрофильные фрагменты линкера и/или средство (А). Длина этого линкера может меняться в широком диапазоне, например, от примерно 2 до примерно 100 атомов. Атомы, используемые при формировании линкера, могут соединяться друг с другом всеми подходящими с химической точки зрения путями, например, цепи атомов углерода могут представлять собой алкиленовые, алкениленовые и алкиниленовые группы и т.п.; цепи из атомов углерода и кислорода могут представлять собой простые эфиры, полиоксиалкиленовые группы или, в комбинации с карбонильными группами, представлять собой сложные эфиры, карбонаты и т.п.; цепи из атомов углерода и азота могут представлять собой амины, имины, полиамины, гидразины, гидразоны или, в комбинации с карбонильными группами, представлять собой амиды, мочевины, семикарбазиды, карбазиды и т.п.; цепи из атомов углерода, азота и кислорода могут являться алкоксиаминами, алкоксиламинами или, в комбинации с карбонильными группами, могут представлять собой уретаны, аминокислоты, ацилоксиамины, гидроксамовые кислоты и т.п. и многое другое. Кроме того, следует понимать, что атомы, образующие цепь в каждом из предыдущих иллюстративных вариантов осуществления, могут быть насыщенными или ненасыщенными, как например, радикалами, входящими в линкер, могут являться остатки алканов, алкенов, алкинов, иминов и т.п. Помимо этого, следует понимать, что атомы, образующие линкер, могут также образовывать циклы друг с другом, с формированием двухвалентных циклических структур, которые входят в линкер, включая циклоалканы, циклические простые эфиры, циклические амины, арилены, гетероарилены и т.п. в линкере.
В другом варианте осуществления в изобретении описаны фармацевтические композиции, включающие конъюгат для доставки лекарственного средства, содержащий связывающий лиганд (B), в количестве, эффективном для уничтожения популяции патогенных клеток в организме животного-хозяина, при введении одной или многих доз композиции. Конъюгаты для доставки лекарственного средства, включающие связывающий лиганд, предпочтительно вводят в организм животного-хозяина парентерально, например, внутрикожно, подкожно, внутримышечно, интраперитонеально, внутривенно или интратекально. В качестве альтернативы, конъюгат для доставки лекарственного средства, включающий связывающий лиганд, можно вводить в организм животного-хозяина другими применяемыми в медицине способами, например, перорально, причем могут применяться любые эффективные дозы и любые подходящие лекарственные формы, включая лекарственные формы с пролонгированным высвобождением.
Примеры парентеральных дозированных лекарственных форм включают водные растворы действующего агента в изотоническом солевом растворе, 5% растворе глюкозы или других хорошо известных фармацевтически приемлемых жидких носителях, таких как жидкие спирты, гликоли, сложные эфиры и амиды. Парентеральные дозированные лекарственные формы можно получать в виде восстанавливаемых лиофилизатов, включающих дозу конъюгата для доставки лекарственного средства. В одном из аспектов настоящего изобретения пациенту можно вводить любую из большого числа известных в области техники лекарственных форм с пролонгированным высвобождением, как, например, биоразрушаемые углеводные матрицы, описанные в патентах США № 4713249; 5266333 и 5417982, содержание которых включено в настоящую заявку посредством ссылки, или же, в качестве альтернативы, могут применяться насосы замедленного действия (например, осмотические насосы).
В одном из иллюстративных аспектов как минимум одна дополнительная композиция, содержащая терапевтическое действующее начало, может вводиться в организм хозяина в комбинации или в качестве вспомогательного средства к подробно описанным выше способам по настоящему изобретению, с целью улучшения уничтожения популяции патогенных клеток конъюгатом для доставки лекарственного средства, содержащим связывающий лиганд, или же можно вводить более чем один дополнительный терапевтический фактор. Этот терапевтический фактор может быть выбран из химиотерапевтических средств или других терапевтических средств, способных дополнить эффективность вводимого конъюгата, содержащего связывающий лиганд.
В одном из иллюстративных аспектов может применяться терапевтически эффективная комбинация упомянутых факторов. Например, в одном из вариантов осуществления наряду с конъюгатом для доставки лекарственного средства, содержащим связывающий лиганд, могут применяться терапевтически эффективные количества другого терапевтического фактора, находящиеся, например, в пределах от примерно 0,1 MIU/м2/доза/день до примерно 15 MIU/м2/доза/день в режиме введения нескольких доз в день, или, например, количества, находящиеся в диапазоне от примерно 0,1 MIU/м2/доза/день до примерно 7,5 MIU/м2/доза/день в режиме введения нескольких доз в день, с целью уничтожения, уменьшения количества или нейтрализации патогенных клеток в организме животного-хозяина, несущего такие клетки (MIU=миллион международных единиц; м2=приблизительная площадь поверхности тела среднестатистического человека).
В другом варианте осуществления химиотерапевтические средства, которые, например, являются цитотоксическими сами по себе или могут улучшать проницаемость опухоли, также подходят для применения в описанных способах в комбинации с конъюгатами для доставки лекарственного средства, содержащими связывающий лиганд. Такие химиотерапевтические средства включают адренокортикоиды и кортикостероиды, алкилирующие агенты, антиандрогены, антиэстрогены, андрогены, акламицин и производные акламицина, эстрогены, антиметаболиты, такие как цитозин арабинозид, аналоги пурина, аналоги пиримидина, а также метотрексат, бусульфан, карбоплатин, хлорамбуцил, цисплатин и другие соединения платины, тамоксифен, таксол, паклитаксел, производные паклитаксела, Taxotere®, циклофосфамид, дауномицин, даунорубицин, доксорубицин, ризоксин, токсин Т2, растительные алкалоиды, преднизон, гидроксимочевину, тенипозид, митомицины, дискодермолиды, ингибиторы микротубул, эпотилоны, тубулизин, циклопропилбенз[e]индолон, seco-циклопропилбенз[e]индолон, O-Ac-seco-циклопропилбенз[e]индолон, блеомицин и любые другие антибиотики, азотистые иприты, нитрозомочевины, винкристин, винбластин, его аналоги или производные, например диацетилвинбластина моногидразид, колхицин, производные колхицина, аллоколхицин, тиоколхицин, тритилцистеин, галихондрин B, доластатины, например доластатин 10, аманитины, например, α-аманитин, камптотекин, иринотекан и другие производные камптотекина, гелданамицин и производные гелданамицина, эстрамустин, нокодазол, MAP4, колцемид, воспалительные и провоспалительные агенты, пептиды и пептидомиметики, являющиеся ингибиторами передачи сигнала, а также любые другие известные в области техники лекарственные средства и токсины. Другие лекарственные средства, которые могут найти применение, включают пенициллины, цефалоспорины, ванкомицин, эритромицин, клиндамицин, рифампин, хлорамфеникол, аминогликозидные антибиотики, гентамицин, амфотерицин B, ацикловир, трифлуридин, ганцикловир, зидовудин, амантадин, рибавирин, майтанзины, их аналоги и производные, гемцитабин, а также любые другие известные в области техники противомикробные соединения.
Терапевтический фактор может вводиться в организм животного-хозяина до, после или во время введения конъюгатов для доставки лекарственного средства, содержащих связывающий лиганд, причем указанный терапевтический фактор может вводиться в виде составной части той же композиции, которая включает конъюгат для доставки лекарственного средства, содержащий связывающий лиганд, или в качестве компонента другой композиции. Может применяться любая из таких терапевтических композиций, содержащих терапевтический фактор в терапевтически эффективной дозировке.
Помимо этого, может применяться более чем один тип конъюгата для доставки лекарственного средства, содержащего связывающий лиганд. В качестве иллюстрации, животное-хозяин может, например, подвергаться лечению конъюгатами, включающими различные витамины, но одно и то же лекарственное средство, по методике, включающей совместное введение. В других вариантах осуществления животное-хозяин может подвергаться лечению конъюгатами, включающими один и тот же связывающий лиганд, соединенный с различными лекарственными средствами, или же различные связывающие лиганды, соединенные с различными лекарственными средствами. В другом иллюстративном варианте осуществления могли бы применяться конъюгаты для доставки лекарственных средств, включающие одинаковые или различные витамины и одинаковые или различные лекарственные средства, в том числе несколько витаминов и несколько лекарственных средств в качестве фрагментов одного и того же конъюгата для доставки лекарственных средств.
Общая дневная дозировка конъюгата для доставки лекарственного средства, содержащего связывающий лиганд, может значительно меняться в зависимости от состояния организма-хозяина, подвергаемого лечению болезненного состояния, молекулярной массы конъюгата, пути его введения и распределения в тканях, а также возможности совместного применения других путей лечения, например радиационной терапии. Эффективное количество, которое следует вводить пациенту, зависит от площади поверхности тела, массы пациента и оценки врачом состояния больного. В иллюстративных вариантах осуществления эффективные дозировки могут находиться в пределах, например, от приблизительно 1 нг/кг до приблизительно 1 мг/кг, от приблизительно 1 мкг/кг до приблизительно 500 мкг/кг, от приблизительно 1 мкг/кг до приблизительно 100 мкг/кг, от приблизительно 1 мкг/кг до приблизительно 50 мкг/кг и от приблизительно 1 мкг/кг до приблизительно 10 мкг/кг.
В другом иллюстративном аспекте может применяться любой эффективный режим введения конъюгатов для доставки лекарственного средства, включающих связывающий лиганд. Например, конъюгат для доставки лекарственного средства, включающий связывающий лиганд, может вводиться в виде одной дозы, или же эту дозу можно разделить и осуществлять введение в режиме нескольких доз в день. В других вариантах осуществления могут применяться прерывистые режимы введения, например, от одного до трех раз в неделю, в качестве альтернативы ежедневному введению, и считается, что такой прерывистый или периодический режим эквивалентен ежедневному введению и находится в рамках способов, описанных в настоящем изобретении. В одном из вариантов осуществления пациента подвергают лечению многократными инъекциями конъюгата для доставки лекарственных средств, содержащего связывающий лиганд, для уничтожения популяции патогенных клеток. В другом варианте осуществления пациенту проводят большое число инъекций (предпочтительно от примерно 2 до примерно 50 инъекций) конъюгата для доставки лекарственных средств, содержащего связывающий лиганд, например, с интервалами 12-72 часа или с интервалами 48-72 часа. В другом варианте осуществления пациенту проводят дополнительные инъекции конъюгата для доставки лекарственных средств, содержащего связывающий лиганд, например, через несколько дней или месяцев после первой инъекции (инъекций), причем дополнительные инъекции предотвращают рецидив болезненного состояния, вызванного патогенными клетками.
В одном из вариантов осуществления витамины, их аналоги или производные, которые могут применяться в конъюгатах для доставки лекарственных средств, содержащих связывающий лиганд, включают те витамины, которые связываются с рецепторами, которые специфически экспрессируются на активированных макрофагах, например, с рецепторами фолатов, которые связываются с фолатами, их аналогами или производными. Конъюгаты, включающие связанный фолат, могут, например, применяться для уничтожения или подавления активности активированных макрофагов, которые вызывают болезненные состояния в организме хозяина. Такие конъюгаты, нацеленные на макрофаги, при их введении пациенту, страдающему болезненным состоянием, опосредованным активированными макрофагами, концентрируют и связывают конъюгированное лекарственное средство с популяцией активированных макрофагов, уничтожая активированные макрофаги или подавляя их деятельность. Уничтожение, уменьшение количества или дезактивация популяции активированных макрофагов позволяет прекратить или уменьшить патогенез, опосредованный активированными макрофагами, характерный для болезненного состояния, подвергаемого лечению. Типичные заболевания, которые, как известно, опосредованы активированными макрофагами, включают ревматоидный артрит, язвенный колит, болезнь Крона, псориаз, остеомиелит, рассеянный склероз, атеросклероз, фиброз легких, саркоидоз, системный склероз, отторжение трансплантированного органа (GVHD) и хронические воспаления. Введение конъюгата для доставки лекарственных средств, как правило, продолжают до тех пор, пока симптомы болезненного состояния не ослабляются или не устраняются.
В качестве иллюстрации, конъюгаты для доставки лекарственных средств, содержащие связывающий лиганд, которые вводят для уничтожения активированных макрофагов или для подавления деятельности активированных макрофагов, можно вводить животному или пациенту, страдающему от болезненного состояния парентерально, например внутрикожно, подкожно, внутримышечно, интраперитонеально или внутривенно, в комбинации с фармацевтически приемлемым носителем. В другом варианте осуществления конъюгаты для доставки лекарственных средств, содержащие связывающий лиганд, можно вводить животному или пациенту с помощью других применяемых в медицине методик, и эффективные дозы могут вводиться с помощью стандартных лекарственных форм или форм с пролонгированным высвобождением. В другом аспекте описываемый способ лечения может применяться сам по себе или в комбинации с другими способами лечения, которые известны для лечения болезненных состояний, опосредованных активированными макрофагами.
Конъюгаты для доставки лекарственных средств, описанные в настоящем изобретении, можно получать известными в области техники способами синтеза. Способы синтеза выбирают в зависимости от выбора необязательных дополнительных гетероатомов или гетероатомов, которые уже присутствуют в спейсерах линкера, расщепляемых фрагментах линкера, лекарственном средстве и/или связывающем лиганде. Реакции, подходящие для образования связей, в основном описаны в Richard C. Larock, “Comprehensive Organic Transformations, a guide to functional group preparations”, VCH Publishers, Inc. New-York (1989), и в Theodora E. Green & Peter G.M. Wuts, “Protective Group in Organic Synthesis”, 2nd edition, John Wiley & Sons, Inc. New York (1991), содержание которых включено в настоящую заявку посредством ссылки. Дополнительные подробности получения функциональных групп, входящих в структуру линкера, в том числе в расщепляемые фрагменты, включая амиды и сложные эфиры, кетали и ацетали, сукцинимиды, силилоксигруппы, гидразоны, ацилгидразины, семикарбазоны, дисульфиды, карбонаты, сульфонаты и т.п., описаны в опубликованной заявке на патент США № US 2005/0002942 A1, включенной в настоящую заявку во всей полноте посредством ссылки.
Общие методики получения фолат-пептидов. Фолат-содержащий пептидильный фрагмент Pte-Glu-(AA)n-NH(CHR2)CO2H (3) получают последовательным синтезом на полимерной подложке, используя стандартные методики, например Fmoc-стратегию на чувствительной к кислотам смоле Fmoc-AA-Wang (1), как показано на схеме 1.
(a) 20% пиперидин/ДМФА; (b) Fmoc-AA-OH, PyBop, DIPEA, ДМФА; (c) Fmoc-Glu(O-t-Bu)-OH, PyBop, DIPEA, ДМФА; (d) 1.N 10-(TFA)-Pte-OH; PyBop, DIPEA, ДМСО; (e) TFAA, (CH2SH)2, i-Pr3SiH; (f) NH4OH, pH 10,3.
В этом иллюстративном варианте способа, описанного в настоящем изобретении, R1 представляет собой Fmoc, R2 представляет собой надлежащим образом защищенную боковую цепь желаемой аминокислоты и DIPEA означает диизопропилэтиламин. Применяются стандартные методики сшивания, описанные в настоящем изобретении или известные в области техники, например, с помощью PyBOP и другие, в которых сшивающий агент иллюстративно применяют в качестве активирующего реагента для гарантии эффективного сшивания. Защитные группы Fmoc удаляют после каждой стадии сшивания в стандартных условиях, например, обработкой пиперидином, фторидом тетрабутиламмония (TBAF) и т.п. Используют блоки аминокислот с соответствующей защитой, как, например, Fmoc-Glu-OtBu, N 10-TFA-Pte-OH и т.п., как показано на схеме 1 и представлено на стадии (b) соединением Fmoc-AA-OH. Так, например, AA относится к любой исходной аминокислоте, которая имеет надлежащую защиту. Следует понимать, что термин «аминокислота» в настоящем описании предназначен для наименования любого реагента, включающего как амино, так и карбоксильную группу, разделенные одним или несколькими атомами углерода, и этот термин охватывает природные альфа- и бета-аминокислоты, а также производные и аналоги этих аминокислот. В частности, в описываемом здесь синтезе фолат-пептида могут также применяться аминокислоты, имеющие боковые цепи, которые являются защищенными, как, например, защищенный серин, треонин, цистеин, аспартат и т.п. Далее в число исходных веществ для синтеза фолат-пептидов, описанных в настоящей заявке, могут входить гамма, дельта или более протяженные гомологи аминокислот. Кроме того, аналоги аминокислот, включающие гомологичные боковые цепи или структуры с другим типом разветвления, как, например, норлейцин, изовалин, β-метилтреонин, β-метилцистеин, β,β-диметилцистеин и т.п., также могут быть включены в число исходных веществ для синтеза фолат-пептидов, описанного в настоящей заявке.
Последовательность реакций сшивания (стадии (a) и (b)), в которых применяется Fmoc-AA-OH, выполняют “n” раз, получая пептид 2 на твердой подложке, где n означает целое число, которое может быть от 0 до примерно 100. После последней стадии сшивания оставшуюся группу Fmoc удаляют (стадия (a)), и пептид последовательно сшивают с глутаматным производным (стадия (c)), снимают защиту и сшивают с птероевой кислотой, защищенной TFA (стадия (d)). Затем пептид отщепляют от полимерной подложки обработкой трифторуксусной кислотой, этандитиолом и триизопропиламином (стадия (e)). Проведение реакции в этих условиях приводит к одновременному удалению защитных групп t-Bu, t-Boc и Trt, которые могут являться фрагментами боковых цепей аминокислот с соответствующей защитой. Защитную группу TFA удаляют обработкой основанием (стадия (f)), получая фолат-содержащий пептидильный фрагмент 3.
Кроме того, для получения соединений, описанных в настоящей заявке, можно применять следующий иллюстративный способ, где n представляет собой целое число от 1 до примерно 10:
Следует понимать, что хотя показанный выше способ синтеза изображен на примере выбранных соединений, а именно конкретных показанных сахаропептидов, с применением такого же или аналогичного способа могут быть получены и другие подобные соединения, путем простого выбора исходных веществ и стандартной оптимизации условий реакции.
Соединения, описанные в настоящей заявке, могут быть получены с применением стандартных методик синтетической органической химии. Кроме того, для получения описанных соединений может применяться следующий иллюстративный способ, где n представляет собой целое число от 1 до примерно 10:
Следует понимать, что хотя показанный выше способ синтеза изображен на примере выбранных соединений, а именно конкретных показанных сахаридопептидов, с применением такого же или аналогичного способа могут быть получены и другие подобные соединения, путем простого выбора исходных веществ и стандартной оптимизации условий реакции.
Кроме того, для получения соединений, описанных в настоящем изобретении, может применяться следующий иллюстративный способ.
Следует понимать, что хотя показанный выше способ синтеза изображен на примере выбранных соединений, с применением такого же или аналогичного способа могут быть получены и другие подобные соединения, путем простого выбора исходных веществ и стандартной оптимизации условий реакции.
В каждом из описанных выше способов синтеза промежуточные соединения могут быть сшиты с любыми дополнительными гидрофильными спейсерами линкера, другими спейсерами линкера, расщепляемыми линкерами или средствами A. В вариантах каждого из описанных выше способов между связывающим лигандом B и показанными гидрофильными спейсерами линкеров могут быть помещены дополнительные гидрофильные спейсеры линкеров, другие спейсеры линкеров или расщепляемые фрагменты линкеров. Кроме того, следует понимать, что размещение двухвалентных гидрофильных спейсеров линкера слева направо не является ограничивающим и, соответственно, средство A, связывающий лиганд B, дополнительные гидрофильные спейсеры линкера, другие спейсеры линкера и/или расщепляемые линкеры могут быть присоединены к любому концу гидрофильных спейсеров линкера, описанных в настоящей заявке.
ПРИМЕРЫ МЕТОДИК
Исследование относительного сродства к связыванию. Сродство соединений к рецепторам фолатов (FR) относительно сродства самих фолатов определяли в соответствии с ранее описанной методикой (Westerhof, G.R., J.H. Schornagel, et al. (1995) Mol. Pharm. 48: 459-471) с небольшими изменениями. Вкратце, FR-положительные клетки KB обильно высевали в 24-луночные планшеты для клеточных культур и давали возможность прикрепиться к стенкам в течение 18 часов. Отработанную инкубационную среду в намеченных лунках заменяли раствором RPMI, не содержащим фолатов (FFRPMI), с добавкой 100 нМ 3H-фолиевой кислоты в отсутствие и в присутствии тестируемого соединения или фолиевой кислоты в увеличивающихся концентрациях. Клетки инкубировали в течение 60 минут при 37°C и затем три раза промывали PBS, pH 7,4. Добавляли пятьсот микролитров 1% SDS в PBS, pH 7,4. Затем собирали клеточные лизаты и добавляли в отдельные пузырьки, содержавшие 5 мл сцинтилляционной смеси, после чего подсчитывали радиоактивность. Отрицательные контрольные образцы содержали только 3H-фолиевую кислоту в FFRPMI (нет конкурирующего соединения). Положительные контрольные образцы содержали фолиевую кислоту в конечной концентрации 1 мМ, и значения CPM, измеренные для этих образцов (отражающие неспецифическое связывание метки), вычитали из данных, полученных для всех образцов. Следует отметить, что значения относительного сродства определяли как величину, обратную мольному отношению соединения, требуемому для замещения 50% 3H-фолиевой кислоты, связанной рецепторами FR на клетках KB, и значение относительного сродства фолиевой кислоты к FR принимали за 1.
Ингибирование клеточного синтеза ДНК. Соединения, описанные в настоящем изобретении, оценивали с использованием анализа цитотоксичности in vitro, который прогнозирует способность лекарственного средства ингибировать рост фолат-рецептора положительных клеток KB. Соединения включали фолат, связанный с соответствующим химиотерапевтическим лекарственным средством, и их получали по методикам, описанным в настоящей заявке. Клетки KB подвергали действию конъюгатов фолат-лекарственное средство в указанных концентрациях в течение времени до 7 часов при 37°C в отсутствие или в присутствии как минимум 100-кратного избытка фолиевой кислоты. Затем клетки промывали один раз свежей культуральной средой и инкубировали в свежей культуральной среде в течение 72 часов при 37°C. Выживаемость клеток оценивали с применением анализа, основанного на включении 3H-тимидина.
Зависимая от концентрации цитотоксическая активность in vitro. Клетки обильно высевали в 24-луночные планшеты Falcon и давали им образовать почти конфлюентные монослои в течение ночи. За тридцать минут до добавления тестируемых соединений истощенную среду отсасывали из всех лунок и заменяли свежим раствором RPMI, не содержащим фолатов (FFRPMI). Следует отметить, что в намеченные лунки вводили среду, содержащую 100 мкМ фолиевую кислоту; и клетки в этих лунках использовали для определения специфичности нацеливания, поскольку цитотоксическая активность, развиваемая в присутствии избытка фолиевой кислоты (порождающего конкуренцию за связывание с FR), могла бы свидетельствовать о части общей активности, которая не связана с FR-специфичной доставкой конъюгата. После одного промывания 1 мл свежего FFRPMI, содержавшего 10% фетальную телячью сыворотку, инактивированную нагреванием, в каждую лунку добавляли 1 мл среды, содержавшей тестируемые соединения в нараставших концентрациях (4 лунки на образец) в присутствии или в отсутствие 100 мкМ свободной фолиевой кислоты (вещество, конкурирующее за сайт связывания). Обработанные клетки исследовали по методике вытеснения метки «пульс-чейз», фазу «пульс» проводили в течение 2 ч при 37°C, 4 раза промывали 0,5 мл среды и затем проводили фазу «чейз» в 1 мл свежей среды в течение времени до 70 ч. Истощенную среду отсасывали из всех лунок и заменяли свежей средой, содержавшей 5 мкКюри/мл 3H-тимидина. После следующего 2 ч инкубирования при 37°C клетки 3 раза промывали 0,5 мл PBS и затем обрабатывали ледяной 5% трихлоруксусной кислотой в количестве 0,5 мл на лунку. Через 15 минут трихлоруксусную кислоту отсасывали и солюбилизировали клеточный материал добавлением 0,5 мл 0,25N гидроксида натрия в течение 15 мин. Четыреста пятьдесят мкл каждого солюбилизированного образца переносили в сцинтилляционные пузырьки, содержавшие 3 мкл сцинтилляционной смеси Ecolume, и затем подсчитывали в счетчике сцинтилляции жидкостей. Итоговые результаты, помещенные в таблицы, выражали в виде процента включения 3H-тимидина по отношению к необработанным контрольным образцам.
Как показано на приложенных к заявке графиках, дозозависимая цитотоксичность оказалась измеряемой, и в большинстве случаев значения IC50 (концентрация лекарственного конъюгата, необходимая для уменьшения включения 3H-тимидина во вновь синтезированные молекулы ДНК на 50%) находились в нижней части наномолярного диапазона. Кроме того, значения цитотоксичности этих конъюгатов уменьшались в присутствии избытка фолиевой кислоты, указывая на то, что наблюдаемое уничтожение клеток было опосредовано связыванием с рецепторами фолата. В приведенной ниже таблице представлены данные для выбранных соединений по цитотоксичности против клеток KB и против клеток RAW264.7.
| Номер конъюгата |
Исходное лекарственное средство (средства) | Клетки KB | Клетки RAW264.7 | ||
| IC50 (нМ) | Способность конкурировать с избытком фолата | IC50 (нМ) | Способность конкурировать с избытком фолата | ||
| EC0234 | DAVLBH | 56 | Да | ||
| EC0246 | DAVLBH | Да | |||
| EC0258 | DAVLBH | 8,4 | Да | ||
| EC0262 | криптофицин | 4 | Да | ||
| EC0263 | DAVLBH | 11 | Да | ||
| EC0409 | DAVLBH | 7 | Да | ||
| EC0525 | тиобортезомиб | 68 | Да | ||
| EC0543 | тубулизин-А | 1,6 | Да | ||
| EC0551 | аминоптерин | 1 | Да | ||
| EC0552 | рапамицин | 100 | Да | ||
| EC0561 | паклитаксел | 53 | Да | ||
| EC0563 | тиобортезомиб+ рапамицин |
387 | Да | ||
| EC0582 | тиобортезомиб+ эверолимус |
51 | Да | ||
| EC0592 | α-аманатин | ~3 | Да | 5 | Да |
| EC0595 | бис-тиобортезомиб | 4 | Да | ||
| EC0598 | верукарин | 33 | Да | ||
| EC0605 | бис-верукарин | 14 | Да | ||
| EC0610 | дидемнин B | 4 | Да | ||
| EC0647 | бис-аминоптерин | 0,3 | Да | ||
Тест на активность против различных линий раковых клеток in vitro. Клетки обильно высевали в 24-луночные планшеты Falcon и давали им образовать почти конфлюентные монослои в течение ночи. За тридцать минут до добавления тестируемых соединений истощенную среду отсасывали из всех лунок и заменяли свежим раствором RPMI, не содержавшим фолатов (FFRPMI). В подгруппу намеченных лунок вводили среду, содержащую 100 мкМ фолиевую кислоту. Клетки в этих лунках использовали для определения специфичности нацеливания. Не ограничиваясь какой-либо теорией, можно предположить, что цитотоксическая активность, развиваемая тестируемыми соединениями в присутствии избытка фолиевой кислоты, т.е. когда они находятся в состоянии конкуренции за связывание с FR, соответствует тому, что часть общей активности не связана с FR-специфичной доставкой конъюгата. После одного промывания 1 мл свежего FFRPMI, содержавшего 10% фетальную телячью сыворотку, инактивированную нагреванием, в каждую лунку добавляли 1 мл среды, содержавшей тестируемые соединения в нараставших концентрациях (4 лунки на образец) в присутствии или в отсутствие 100 мкМ свободной фолиевой кислоты, что указано в результатах эксперимента. Обработанные клетки исследовали по методике вытеснения метки «пульс-чейз», где фазу «пульс» проводили в течение 2 ч при 37°C, 4 раза промывали 0,5 мл среды и затем проводили фазу «чейз» в 1 мл свежей среды в течение времени до 70 ч. Истощенную среду отсасывали из всех лунок и заменяли свежей средой, содержавшей 5 мкКюри/мл 3H-тимидина. После следующего 2 ч инкубирования при 37°C клетки 3 раза промывали 0,5 мл PBS и затем обрабатывали ледяной 5% трихлоруксусной кислотой в количестве 0,5 мл на лунку. Через 15 минут трихлоруксусную кислоту отсасывали и солюбилизировали клеточный материал добавлением 0,5 мл 0,25N гидроксида натрия в течение 15 мин. 450-мкл аликвоту каждого солюбилизированного образца переносили в сцинтилляционные пузырьки, содержавшие 3 мкл сцинтилляционной смеси Ecolume, и затем подсчитывали в счетчике сцинтилляции жидкостей. Итоговые результаты, помещенные в таблицы, выражали в виде процента включения 3H-тимидина по отношению к необработанным контрольным образцам.
Подавление роста опухоли у мышей. Мышей в возрасте от четырех до семи недель (линии Balb/c или nu/nu) приобретали у Harlan Sprague Dawley, Inc. (Indianapolis, IN). Обычная пища грызунов содержит фолиевую кислоту в высоких концентрациях (6 мг/кг за один прием пищи); соответственно использованных мышей содержали на диете, не включавшей фолатов (Harlan diet # TD00434) в течение 1 недели перед имплантацией опухоли, для достижения концентрации фолатов в сыворотке, близкой к диапазону нормальной человеческой сыворотки. С целью внесения опухолевых клеток, 1×106 клеток M109 (линия Balb/c) или 1×106 клеток KB (линия nu/nu) в 100 мкл инъецировали в подкожный слой в область середины спины. Размеры опухоли измеряли в двух перпендикулярных направлениях каждые 2-3 дня, используя штангенциркуль, и объемы опухоли рассчитывали по формуле 0,5×L×W2, где L=размер по наиболее длинной оси в мм и W=размер по оси, перпендикулярной L, в мм. Затем вычисляли величины Log уничтожения клеток (LCK) и превышение обработанных опухолей над контролем (T/C), согласно опубликованным методикам (см., например, Lee et al., “BMS-247550: a novel epothilone analog with a mode of action similar to paclitaxel but possessing superior antitumor efficacy” Clin Cancer Res 7: 1429-1437 (2001); Rose , “Taxol-based combination chemotherapy and other in vivo preclinical antitumor studies” J Natl Cancer Inst Monogr 47-53 (1993)). Каждый день готовили свежие растворы для введения в PBS и вводили через боковую хвостовую вену мышей. Введение препаратов начинали, когда подкожные опухоли приобретали средний объем в пределах 50-100 мм3 (t0), как правило, через 8 дней после введения опухолевых клеток (PTI) для опухолей KB и 11 PTI для опухолей M109.
Общая методика исследования опухоли KB. Противоопухолевую активность соединений, описанных в настоящем изобретении, при внутривенном введении (i.v.) животным - носителям опухоли, оценивали у мышей nu/nu, имевших подкожные опухоли KB. Приблизительно через 8 дней после введения 1×106 опухолевых клеток KB в подкожный слой правой подмышки (средний объем опухоли в момент t0=50-100 мм3), мышам (5 особей/группа) три раза в неделю (TIW) в течение 3 недель осуществляли i.v. инъекцию 5 мкмоль/кг конъюгата лекарственного средства или эквивалентного объема PBS (контроль), если не указано иное. Рост опухоли измеряли штангенциркулем через 2-дневные или 3-дневные промежутки в каждой группе. Объемы опухолей рассчитывали с использованием уравнения V=a×b2/2, где “a” представляет собой длину опухоли и “b” означает ширину, причем все величины выражены в миллиметрах.
Общая методика исследования опухоли M109. Противоопухолевую активность соединений, описанных в настоящем изобретении, при внутривенном введении (i.v.) животным - носителям опухоли, оценивали у мышей Balb/c, имевших подкожные опухоли M109 (сингенная карцинома легких). Приблизительно через 11 дней после введения 1×106 опухолевых клеток M109 в подкожный слой правой подмышки (средний объем опухоли в момент t0=60 мм3) мышам (5 особей/группа) три раза в неделю (TIW) в течение 3 недель осуществляли i.v. инъекцию 1500 нмоль/кг конъюгата лекарственного средства или эквивалентного объема PBS (контроль). Рост опухоли измеряли штангенциркулем через 2-дневные или 3-дневные промежутки в каждой группе. Объемы опухолей рассчитывали с использованием уравнения V=a×b2/2, где “a” представляет собой длину опухоли и “b” означает ширину, причем все величины выражены в миллиметрах.
Общая методика исследования опухолей 4T-1. Мышей в возрасте шести-семи недель (самки линии Balb/c) получали у Harlan, Inc., Indianapolis, IN. Мышей содержали на корме Harlan's, свободном от фолатов, в течение в общей сложности трех недель до начала и во время описанного эксперимента. Опухолевые клетки 4T-1, не несущие рецепторов фолатов (1×106 клеток на одно животное), вводили в подкожный слой правой подмышки животного. Приблизительно через 5 дней после введения опухолевых клеток, когда средний объем опухоли 4T-1 составлял ~100 мм3, мышам (5 особей/группа) три раза в неделю (TIW) в течение 3 недель осуществляли i.v. инъекцию 3 мкмоль/кг конъюгата лекарственного средства или эквивалентного объема PBS (контроль), если в тексте заявки не указано иное. Рост опухоли измеряли штангенциркулем через 2-дневные или 3-дневные промежутки в каждой группе. Объемы опухолей рассчитывали с использованием уравнения V=a×b2/2, где “a” представляет собой длину опухоли и “b” означает ширину, причем все величины выражены в миллиметрах.
Данные, приведенные на фиг.3A, 4A, 5A, 6A, 7A, 8A и 10A, показывают, что описанные в изобретении конъюгаты при лечении опухолей демонстрируют эффективность, которая превосходит эффективность соответствующих неконъюгированных соединений. Лечение мышей Balb/c с подкожными опухолями М109 конъюгатами EC0396 и EC145 (фиг.4A) привело к полной ремиссии у всех животных, которым вводились препараты (3/3 для EC0396 и 5/5 для EC145). Кроме того, примерно через 70 дней не наблюдали рецидивов заболевания. Аналогично, введение EC0400 (фиг.5A) привело к полной ремиссии и отсутствию рецидивов заболевания примерно через 70 дней. Лечение конъюгированными соединениями, описанными в настоящей заявке, которые включали гидрофильный спейсер линкера (например, EC0436), было более успешным по сравнению с конъюгатами, у которых не было гидрофильных спейсеров линкера (например, EC0305), что указывает на увеличение эффективности (фиг.8A). Конъюгат EC0436 привел к полной ремиссии у 5 животных из 5, при отсутствии рецидивов заболевания через 90 дней.
Определение токсичности лекарственных средств. Долговременную токсичность лекарственных препаратов оценивали путем отбора крови из пункции сердца и независимого анализа сыворотки на содержание в крови азота мочевины (BUN), креатинина, общего содержания белков, AST-SGOT, ALT-SGPT, а также стандартной гематологической клеточной панели Ani-Lytics, Inc. (Gaithersburg, MD). Кроме того, проводили гистопатологическую оценку фиксированных в формалине препаратов сердца, легких, печени, селезенки, почек, кишечника, скелетных мышц и костей (большая берцовая кость/малая берцовая кость) с привлечением сертифицированных патологов в Animal Reference Pathology Laboratories (ARUP; Salt Lake City, Utah).
Определение токсичности по измерению потери массы тела. Процентные изменения массы тела определяли у мышей (5 мышей/группа) в определенные выбранные дни после введения опухоли (PTI) по сравнению с контрольными животными и строили график. Как показано на фиг.3B, 4B, 5B, 6B, 7B, 8B и 10B, конъюгированные соединения, описанные в настоящем изобретении, демонстрировали равную или меньшую токсичность по сравнению с неконъюгированными соединениями, по данным процентной потери массы тела.
MTD app при однократном и многократном введении у мышей. Соединения, описанные в настоящей заявке, могут демонстрировать положительную взаимосвязь между количеством гидрофильных спейсеров линкера, включенных в конъюгат, и максимально переносимой дозой при однократном введении у мышей. Например, в приведенной ниже таблице помещены данные для конъюгатов винбластина, описанных в настоящей заявке, по сравнению с контрольным конъюгатом.
| Соединение | Количество гидрофильных линкеров | MTDapp для одной дозы (мкмоль/кг) |
| EC145 | 0 | 15 |
| EC0234 | 1 | 12* |
| EC0246 | 2 | <20** |
| EC0263 | 3 | >20 |
| * Доза, ограниченная растворимостью; **1/3 мышей умерло при 20 мкмоль/кг. | ||
EC0436 и конъюгат сравнительного примера EC0305 также вводили i.v. мышам Balb/c TIW в течение одной недели. Полученные значения MTD при многократном введении составляли для EC0305 (6 ммоль/кг) и для EC0436 (9 ммоль/кг). Эти данные показывают, что дозировки EC0436 могут быть на 50% выше, чем EC0305.
Связывание сывороткой. Связывание сывороткой конъюгатов фолат-DAVLBH, включающих гидрофильные спейсеры линкера, по сравнению с конъюгатом сравнительного примера EC145, у которого отсутствуют гидрофильные спейсеры линкера, при содержании соединения в сыворотке 50 мМ с 30К NMWL фильтрованием и определением результата с помощью ВЭЖХ с УФ-детектированием (n=3).
| Соединение | Сыворотка человека (% связывания) |
SD | Сыворотка мыши (% связывания) | SD |
| EC145 | 54,3 | 1,6 | 67,3 | 2,6 |
| EC0396 | 42,7 | 4,4 | 72,2 | 5,2 |
| EC0400 | 61,1 | 1,9 | 75,5 | 1,4 |
Выведение с желчью. Сравнение выведения с желчью (% ID) неконъюгированного лекарственного средства, конъюгата лекарственного средства с линкером, не содержащим гидрофильных спейсеров линкера, и конъюгатов по настоящему изобретению
| Соединение | Наличие гидрофильных фрагментов | Выведение с желчью (%ID) |
| DAVLBH | отсутствует | 58,0 |
| EC145 | отсутствует гидрофильный спейсер | 8,7 |
| EC0234 | монорибозил | 10,6 |
| EC0246 | бис-рибозил | 4,7 |
| EC0258 | три-рибозил | 3,2 |
| EC0434 | тетра-рибозил | 2,8 |
| EC0400 | моноглюкуронид | 6,3 |
| EC0423 | бис-глюкуронид | 3,9 |
| EC0409 | ПЭГ12 | 7,9 |
| EC0429 | пиперазин/Asp | 8,6 |
Результаты, показанные на фиг.11 и 13, свидетельствуют о 76% уменьшении выведения через печень конъюгата EC0434, который включает гидрофильные спейсеры линкера, описанные в настоящей заявке, по сравнению со стандартным конъюгатом EC145. Не ограничиваясь какой-либо теорией, можно предположить, что эти результаты соответствуют неспецифическому выведению через печень, и, соответственно, предполагается, что можно вводить значительно более низкие дозы тех конъюгатов, которые включают гидрофильные структурные спейсеры линкера, описанные в настоящем изобретении, по сравнению с аналогичными конъюгатами, которые не включают таких линкеров. Далее, не ограничиваясь конкретной теорией, полагают, что печеночный клиренс ведет к ограничивающей дозировку GI-связанной цитотоксичности, которая наблюдается у некоторых конъюгатов.
Вестерн-блоттинг. Данные, приведенные на фиг.13, показывают, что конъюгат EC0565 (фолат-сахар-эверолимус) может вызывать дозозависимое и специфичное поражение мишеней mTOR, расположенных далее по пути передачи сигнала (внутриклеточных мишеней для эверолимуса). Не ограничиваясь какой-либо теорией, считают, что фолат способствует доставке эверолимуса внутрь клетки, где он ингибирует mTOR, который является мишенью рапамицина у млекопитающих, и ser/thr киназу. Ингибирование последующих мишеней mTOR (P70 S6-киназы и рибосомальной S6) приводит к результатам, показанным на приведенном вестерн-блоте.
ПРИМЕРЫ СОЕДИНЕНИЙ
Пример. Метиловый эфир (3,4),(5,6)-бисацетонид-D-глюконовой кислоты. В сухой 250-мл круглодонной колбе в атмосфере аргона суспендировали δ-глюконоллактон (4,14 г, 23,24 ммоль) в смеси ацетон-метанол (50 мл). К этой суспензии добавляли диметоксипропан (17,15 мл, 139,44 ммоль) и затем каталитическое количество п-толуолсульфоновой кислоты (200 мг). Полученный раствор перемешивали при комнатной температуре в течение 16 ч. ТСХ (50% EtOAc в петролейном эфире) показала, что все исходные соединения вступили в реакцию и образовался продукт реакции. Ацетон и метанол удаляли при пониженном давлении. Остаток реакционной смеси растворяли в EtOAc и промывали водой. Органический слой промывали насыщенным раствором соли, высушивали над Na2SO4 и концентрировали досуха. Полученное вещество вносили в колонку с SiO2 и хроматографировали (30% EtOAc в петоролейном эфире), получая чистый метиловый эфир (3,4),(5,6)-бисацетонид-D-глюконовой кислоты (3,8 г, 56%) и его регио-изомер метиловый эфир (2,3),(5,6)-бисацетонид-D-глюконовой кислоты (0,71 г, 10%). Данные 1H ЯМР соответствовали необходимой структуре продукта. C13H22O7; мол. масса 290,31; точное значение массы: 290,14.
Пример. Метиловый эфир (3,4),(5,6)-бисацетонид-2-OTf-D-глюконовой кислоты. В сухой 100-мл круглодонной колбе в атмосфере аргона метиловый эфир (3,4),(5,6)-бисацетонид-D-глюконовой кислоты (3,9 г, 13,43 ммоль) растворяли в хлористом метилене (40 мл) и охлаждали до температуры -20 -25°C. К этому раствору добавляли пиридин (3,26 мл, 40,29 ммоль) и затем ангидрид трифторметансульфоновой кислоты (3,39 мл, 20,15 ммоль). Полученный белый мутный раствор перемешивали при -20°C в течение 1 ч. ТСХ (25% EtOAc в петролейном эфире) показала, что все исходные вещества вступили в реакцию и образовался продукт реакции. Реакционную смесь выливали в толченый лед и экстрагировали диэтиловым эфиром. Органический слой промывали водой, насыщенным раствором соли, высушивали над Na2SO4 и концентрировали, получая метиловый эфир (3,4),(5,6)-бисацетонид-2-OTf-D-глюконовой кислоты (5,5 г, 97%). Полученное вещество использовали в последующих синтезах без дальнейшей очистки. C14H21F3O9S; мол. масса 422,37; точное значение массы: 422,09.
Пример. Метиловый эфир (3,4),(5,6)-бисацетонид-2-дезокси-2-азидо-D-манноновой кислоты. В сухой 100-мл круглодонной колбе в атмосфере аргона растворяли метиловый эфир (3,4),(5,6)-бисацетонид-2-OTf-D-глюконовой кислоты (5,5 г, 13,02 ммоль) в ДМФА (20 мл). К этому раствору добавляли NaN3 (0,93 г, 14,32 ммоль). Полученный раствор перемешивали при комнатной температуре в течение 1 ч. ТСХ (8% EtOAc в петролейном эфире, тройное прохождение) показала, что все исходные вещества вступили в реакцию и образовался продукт реакции. ДМФА удаляли при пониженном давлении. Реакционную смесь разбавляли насыщенным раствором соли и экстрагировали EtOAc. Органический слой промывали водой, насыщенным раствором соли, высушивали над Na2SO4 и концентрировали досуха. Полученный неочищенный продукт затем помещали в колонку с SiO2 и очищали хроматографией (20% EtOAc в петролейном эфире), получая чистый метиловый эфир (3,4),(5,6)-бисацетонид-2-дезокси-2-азидо-D-манноновой кислоты (3,8 г, 93%). Данные 1H ЯМР соответствовали желаемой структуре продукта. C13H21N3O6; мол. масса 315,32; точное значение массы: 315,14.
Пример. Метиловый эфир (3,4),(5,6)-бисацетонид-2-дезокси-2-амино-D-манноновой кислоты. В сосуде Парра для гидрирования метиловый эфир (3,4),(5,6)-бисацетонид-2-дезокси-2-азидо-D-манноновой кислоты (3,5 г, 11,10 ммоль) растворяли в метаноле (170 мл). К этому раствору добавляли 10% Pd на угле (800 мг, 5% мольн.). Гидрирование осуществляли с использованием агрегата для гидрирования Парра при давлении 25 фунтов/кв.дюйм в течение 1 ч. ТСХ (10% метанол в метиленхлориде) показала, что все исходные вещества вступили в реакцию и образовался продукт реакции. Реакционную смесь фильтровали через слой целита и концентрировали досуха. Затем полученное неочищенное вещество помещали в колонку с SiO2 и очищали хроматографией (2% метанол в метиленхлориде), получая чистый метиловый эфир (3,4),(5,6)-бисацетонид-2-дезокси-2-амино-D-манноновой кислоты (2,61 г, 81%). Данные 1H ЯМР соответствовали желаемой структуре продукта. C13H23NO6S; мол. масса 289,32; точное значение массы: 289,15.
Пример. (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота. В сухой 100-мл круглодонной колбе растворяли метиловый эфир (3,4),(5,6)-бисацетонид-2-дезокси-2-амино-D-манноновой кислоты (1,24 г, 4,29 ммоль) в смеси ТГФ/MeOH (20 мл/5 мл). К этому раствору добавляли LiOH·H2O (215,8 мг, 5,14 ммоль) в воде (5 мл). Полученный светло-желтый раствор перемешивали при комнатной температуре в течение 2 ч. ТСХ (10% метанол в метиленхлориде) показала, что все исходные вещества вступили в реакцию и образовался продукт реакции. ТГФ/MeOH удаляли при пониженном давлении. Водную фазу ресуспендировали в насыщенном растворе NaHCO3 (10 мл). К этой суспензии добавляли Fmoc-Osu (1,74 г, 5,14 ммоль) в 1,4-диоксане (10 мл). Полученный гетерогенный раствор перемешивали при комнатной температуре в течение 18 ч. ТСХ (10% метанол в метиленхлориде) показала, что большая часть исходных веществ вступила в реакцию и образовался продукт реакции. Диоксан удаляли при пониженном давлении. Водный слой экстрагировали диэтиловым эфиром для удаления менее полярных примесей. После этого водный слой подкисляли до pH 6, используя 0,2N HCl и вновь экстрагировали EtOAc. EtOAc слой промывали насыщенным раствором соли, высушивали над Na2SO4 и концентрировали, получая (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновую кислоту (1,6 г, 76%). Полученное вещество использовали в последующих синтезах без дальнейшей очистки. Данные 1H ЯМР соответствовали желаемой структуре продукта. C27H31NO8; мол. масса 497,54; точное значение массы: 497,20.
Пример. EC0233 синтезировали с помощью SPPS (стандартного твердофазного пептидного синтеза) в три стадии согласно общей методике пептидного синтеза, описанной в настоящей заявке, исходя из H-Cys(4-метокситритил)-2-хлортритил-смолы и следующих SPPS реагентов:
| Реагенты | ммоль | Экв. | Мол. масса | Кол-во |
| H-Cys(4-метокситритил)-2-хлортритил-смола (содержание действующего вещества 0,56 ммоль/г) | 0,56 | 1,0 г | ||
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,7 | 1,25 | 497,54 | 0,348 г |
| Fmoc-Glu-OtBu | 1,12 | 2 | 425,5 | 0,477 г |
| N10TFA-птероевая кислота (растворяли в 10 мл ДМСО) | 0,70 | 1,25 | 408 | 0,286 г |
| DIPEA | 2,24 | 4 | 129,25 (d=0,742) | 0,390 мл |
| PyBOP | 1,12 | 2 | 520 | 0,583 г |
Стадии сочетания. В сосуд для синтеза пептидов добавляли смолу, добавляли раствор аминокислоты, DIPEA и PyBOP. Барботировали аргон в течение 1 ч и 3 раза промывали ДМФА и IPA. Перед каждой стадией сочетания для снятия защиты Fmoc применяли 20% пиперидин в ДМФА, 3×(10 мин). В указанных условиях осуществляли все три стадии сочетания. В конце промывали смолу 2% гидразином в ДМФА 3×(5 мин) для отщепления защитной группы птероевой кислоты, т.е. TFA.
Стадия отщепления. Реагент для отщепления: 92,5% (50 мл) TFA, 2,5% (1,34 мл) H2O, 2,5% (1,34 мл) триизопропилсилан, 2,5% (1,34 мл) этандитиол. Добавляли 25 мл отщепляющего реагента и барботировали аргон в течение 20 минут, высушивали и три раза промывали остатком реагента. Упаривали на роторном испарителе до остаточного объема 5 мл и осаждали этиловым эфиром. Центрифугировали и высушивали.
Стадия очистки ВЭЖХ. Колонка: Waters NovaPak C18 300×19 мм; буфер A=10 мМ ацетат аммония, pH 5; B= ACN; методика: 1% B-20% B в течение 40 мин при скорости 15 мл/мин; выход ~202 мг, 50%. C28H35N9O12S; мол. масса 721,70; точное значение массы: 721,21.
Пример. Линкер бис-сахаро-фолат EC0244. EC0244 синтезировали с помощью SPPS в пять стадий согласно общей методике пептидного синтеза, описанной в настоящей заявке, исходя из H-Cys(4-метокситритил)-2-хлортритил-смолы и следующих SPPS реагентов:
| Реагенты | ммоль | Экв. | Мол. масса | Кол-во |
| H-Cys(4-метокситритил)-2-хлортритил-смола (содержание действующего вещества 0,56 ммоль/г) | 0,56 | 1,0 г | ||
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,7 | 1,25 | 497,54 | 0,348 г |
| Fmoc-Asp(OtBu)-OH | 1,12 | 2 | 411,5 | 0,461 г |
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,7 | 1,25 | 497,54 | 0,348 г |
| Fmoc-Glu-OtBu | 1,12 | 2 | 425,5 | 0,477 г |
| N10TFA-птероевая кислота (растворяли в 10 мл ДМСО) | 0,70 | 1,25 | 408 | 0,286 г |
| DIPEA | 2,24 | 4 | 129,25 (d=0,742) | 0,390 мл |
| PyBOP | 1,12 | 2 | 520 | 0,583 г |
Стадии сочетания, стадия отщепления, реагент для отщепления и стадия очистки ВЭЖХ соответствовали описанным выше методикам; выход ~284 мг, 50%. C38H51N11O20S; мол. масса 1013,94; точное значение массы: 1013,30.
Пример. EC0257 синтезировали с помощью SPPS в шесть стадий согласно общей методике пептидного синтеза, описанной в настоящей заявке, исходя из H-Cys(4-метокситритил)-2-хлортритил-смолы и следующих SPPS реагентов:
| Реагенты | ммоль | Экв. | Мол. масса | Кол-во |
| H-Cys(4-метокситритил)-2-хлортритил-смола (содержание действующего вещества 0,56 ммоль/г) | 0,2 | 0,333 г | ||
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,25 | 1,25 | 497,54 | 0,124 г |
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,25 | 1,25 | 497,54 | 0,124 г |
| Fmoc-Asp(OtBu)-OH | 0,4 | 2 | 411,5 | 0,165 г |
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,25 | 1,25 | 497,54 | 0,124 г |
| Fmoc-Glu-OtBu | 0,4 | 2 | 425,5 | 0,170 г |
| N10TFA-птероевая кислота (растворяли в 10 мл ДМСО) | 0,25 | 1,25 | 408 | 0,119 г |
| DIPEA | 0,8 | 4 | 129,25 (d=0,742) | 0,139 мл |
| PyBOP | 0,4 | 2 | 520 | 0,208 г |
Стадии сочетания, стадия отщепления, реагент для отщепления и стадия очистки ВЭЖХ соответствовали описанным выше методикам; выход ~170 мг, 71%. C44H62N12O25S; мол. масса 1191,09; точное значение массы: 1190,37.
Пример. EC0261 синтезировали с помощью SPPS в семь стадий согласно общей методике пептидного синтеза, описанной в настоящей заявке, исходя из H-Cys(4-метокситритил)-2-хлортритил-смолы и следующих SPPS реагентов:
| Реагенты | ммоль | Экв. | Мол. масса | Кол-во |
| H-Cys(4-метокситритил)-2-хлортритил-смола (содержание действующего вещества 0,56 ммоль/г) | 0,2 | 0,333 г | ||
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,25 | 1,25 | 497,54 | 0,124 г |
| Fmoc-Asp(OtBu)-OH | 0,4 | 2 | 411,5 | 0,165 г |
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,25 | 1,25 | 497,54 | 0,124 г |
| Fmoc-Asp(OtBu)-OH | 0,4 | 2 | 411,5 | 0,165 г |
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,25 | 1,25 | 497,54 | 0,124 г |
| Fmoc-Glu-OtBu | 0,4 | 2 | 425,5 | 0,170 г |
| N10TFA-птероевая кислота (растворяли в 10 мл ДМСО) | 0,25 | 1,25 | 408 | 0,119 г |
| DIPEA | 0,8 | 4 | 129,25 (d=0,742) | 0,139 мл |
| PyBOP | 0,4 | 2 | 520 | 0,208 г |
Стадии сочетания, стадия отщепления, реагент для отщепления и стадия очистки ВЭЖХ соответствовали описанным выше методикам; выход ~170 мг, 65%. C48H67N13O28S; мол. масса 1306,18; точное значение массы: 1305,39.
Пример. Линкер тетра-сахаро-трис-Asp-фолат EC0268. EC0268 синтезировали с помощью SPPS в девять стадий согласно общей методике пептидного синтеза, описанной в настоящей заявке, исходя из H-Cys(4-метокситритил)-2-хлортритил-смолы и следующих SPPS реагентов:
| Реагенты | ммоль | Экв. | Мол. масса | Кол-во |
| H-Cys(4-метокситритил)-2-хлортритил-смола (содержание действующего вещества 0,56 ммоль/г) | 0,1 | 0,167 г | ||
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,125 | 1,25 | 497,54 | 0,062 г |
| Fmoc-Asp(OtBu)-OH | 0,2 | 2 | 411,5 | 0,082 г |
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,125 | 1,25 | 497,54 | 0,062 г |
| Fmoc-Asp(OtBu)-OH | 0,2 | 2 | 411,5 | 0,082 г |
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,125 | 1,25 | 497,54 | 0,062 г |
| Fmoc-Asp(OtBu)-OH | 0,2 | 2 | 411,5 | 0,082 г |
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,125 | 1,25 | 497,54 | 0,062 г |
| Fmoc-Glu-OtBu | 0,2 | 2 | 425,5 | 0,085 г |
| N10TFA-птероевая кислота (растворяли в 10 мл ДМСО) | 0,125 | 1,25 | 408 | 0,059 г |
| DIPEA | 0,4 | 4 | 129,25 (d=0,742) | 0,070 мл |
| PyBOP | 0,2 | 2 | 520 | 0,104 г |
Стадии сочетания, стадия отщепления, реагент для отщепления и стадия очистки ВЭЖХ соответствовали описанным выше методикам; выход ~100 мг, 63%. C94H125N19O37S2; мол. масса 2177,24; точное значение массы: 2175,79.
Следующие иллюстративные примеры можно получить по методике синтеза EC0268
Пример. Линкер тетра-сахаро-Asp-фолат EC0463. EC0463 синтезировали с помощью SPPS в семь стадий согласно общей методике пептидного синтеза, описанной в настоящей заявке, исходя из H-Cys(4-метокситритил)-2-хлортритил-смолы и следующих SPPS реагентов:
| Реагенты | ммоль | Экв. | Мол. масса | Кол-во |
| H-Cys(4-метокситритил)-2-хлортритил-смола (содержание действующего вещества 0,56 ммоль/г) | 0,1 | 0,167 г | ||
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,125 | 1,25 | 497,54 | 0,062 г |
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,125 | 1,25 | 497,54 | 0,062 г |
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,125 | 1,25 | 497,54 | 0,062 г |
| Fmoc-Asp(OtBu)-OH | 0,2 | 2 | 411,5 | 0,082 г |
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,125 | 1,25 | 497,54 | 0,062 г |
| Fmoc-Glu-OtBu | 0,2 | 2 | 425,5 | 0,085 г |
| N10TFA-птероевая кислота (растворяли в 10 мл ДМСО) | 0,125 | 1,25 | 408 | 0,059 г |
| DIPEA | 0,4 | 4 | 129,25 (d=0,742) | 0,070 мл |
| PyBOP | 0,2 | 2 | 520 | 0,104 г |
Стадии сочетания, стадия отщепления, реагент для отщепления и стадия очистки ВЭЖХ соответствовали описанным выше методикам; выход ~63 мг, 46%. C50H73N13O30S; мол. масса 1368,25; точное значение массы: 1367,43.
Пример. Линкер тетра-сахаро-бис-α-Glu-Arg-фолат EC0480. EC0480 синтезировали с помощью SPPS в девять стадий согласно общей методике пептидного синтеза, описанной в настоящей заявке, исходя из H-Cys(4-метокситритил)-2-хлортритил-смолы и следующих SPPS реагентов:
| Реагенты | ммоль | Экв. | Мол. масса | Кол-во |
| H-Cys(4-метокситритил)-2-хлортритил-смола (содержание действующего вещества 0,56 ммоль/г) | 0,2 | 0,333 г | ||
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,250 | 1,25 | 497,54 | 0,124 г |
| Fmoc-Glu(OtBu)-OH | 0,4 | 2 | 425,5 | 0,170 г |
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,250 | 1,25 | 497,54 | 0,124 г |
| Fmoc-Arg(Pbf)-OH | 0,4 | 2 | 648,78 | 0,260 г |
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,250 | 1,25 | 497,54 | 0,124 г |
| Fmoc-Glu(OtBu)-OH | 0,4 | 2 | 425,5 | 0,170 г |
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,125 | 1,25 | 497,54 | 0,124 г |
| Fmoc-Glu-OtBu | 0,4 | 2 | 425,5 | 0,170 г |
| N10TFA-птероевая кислота (растворяли в 10 мл ДМСО) | 0,250 | 1,25 | 408 | 0,119 г |
| DIPEA | 0,8 | 4 | 129,25 (d=0,742) | 0,139 мл |
| PyBOP | 0,4 | 2 | 520 | 0,208 г |
Стадии сочетания, стадия отщепления, реагент для отщепления и стадия очистки ВЭЖХ соответствовали описанным выше методикам; выход ~100 мг, 33%. C62H94N18O20S; мол. масса 1667,58; точное значение массы: 1666,59.
Пример. Линкер тетра-сахаро-бис-Asp-фолат EC0452. EC0452 синтезировали с помощью SPPS в девять стадий согласно общей методике пептидного синтеза, описанной в настоящей заявке, исходя из H-Cys(4-метокситритил)-2-хлортритил-смолы и следующих SPPS реагентов:
| Реагенты | ммоль | Экв. | Мол. масса | Кол-во |
| H-Cys(4-метокситритил)-2-хлортритил-смола (содержание действующего вещества 0,6 ммоль/г) | 0,15 | 0,250 г | ||
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,188 | 1,25 | 497,54 | 0,094 г |
| Fmoc-Asp(OtBu)-OH | 0,3 | 2 | 411,5 | 0,123 г |
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,188 | 1,25 | 497,54 | 0,094 г |
| Fmoc-4-(2-аминоэтил)-1-карбоксиметилпиперазина дигидрохлорид | 0,3 | 2 | 482,42 | 0,145 г |
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,188 | 1,25 | 497,54 | 0,094 г |
| Fmoc-Asp(OtBu)-OH | 0,3 | 2 | 411,5 | 0,123 г |
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,188 | 1,25 | 497,54 | 0,094 г |
| Fmoc-Glu-OtBu | 0,3 | 2 | 425,5 | 0,128 г |
| N10TFA-птероевая кислота (растворяли в 10 мл ДМСО) | 0,188 | 1,25 | 408 | 0,077 г |
| DIPEA | 0,6 | 4 | 129,25 (d=0,742) | 0,105 мл |
| PyBOP | 0,3 | 2 | 520 | 0,156 г |
Стадии сочетания, стадия отщепления и реагент для отщепления соответствовали описанным выше методикам; стадия очистки ВЭЖХ. Колонка: Waters NovaPak C18 300×19 мм; буфер A=10 мМ ацетат аммония, pH 5; B= ACN; методика: 1% B - 20% B в течение 40 мин при скорости 25 мл/мин; выход ~98 мг, 40%. C62H93N17O34S; мол. масса 1652,56; точное значение массы: 1651,58.
Пример. Линкер тетра-сахаро-бис-Asp-фолат EC0457. EC0457 синтезировали с помощью SPPS в восемь стадий согласно общей методике пептидного синтеза, описанной в настоящей заявке, исходя из H-Cys(4-метокситритил)-2-хлортритил-смолы и следующих SPPS реагентов:
| Реагенты | ммоль | Экв. | Мол. масса | Кол-во |
| H-Cys(4-метокситритил)-2-хлортритил-смола (содержание действующего вещества 0,6 ммоль/г) | 0,20 | 0,333 г | ||
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,25 | 1,25 | 497,54 | 0,124 г |
| Fmoc-Asp(OtBu)-OH | 0,30 | 1,5 | 411,5 | 0,123 г |
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,25 | 1,25 | 497,54 | 0,124 г |
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,25 | 1,25 | 497,54 | 0,124 г |
| Fmoc-Asp(OtBu)-OH | 0,30 | 1,5 | 411,5 | 0,123 г |
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,25 | 1,25 | 497,54 | 0,124 г |
| Fmoc-Glu-OtBu | 0,30 | 1,5 | 425,5 | 0,128 г |
| N10TFA-птероевая кислота (растворяли в 10 мл ДМСО) | 0,25 | 1,25 | 408 | 0,102 г |
| DIPEA | 2 экв. отн. амино-кислоты | 129,25 (d=0,742) | 87 мкл или 105 мкл |
|
| PyBOP | 2 экв. отн. амино-кислоты | 520 | 260 мг или 312 мг |
Стадии сочетания, стадия отщепления и реагент для отщепления соответствовали описанным выше методикам; стадия очистки ВЭЖХ. Колонка: Waters NovaPak C18 300×19 мм; буфер A=10 мМ ацетат аммония, pH 5; B= ACN; методика: 0% B-20% B в течение 40 мин при скорости 25 мл/мин; выход ~210 мг, 71%. C54H78N14O33S; мол. масса 1483,34; точное значение массы: 1482,46.
Пример. Линкер тетра-сахаро-трис-Glu-фолат EC0477. EC0477 синтезировали с помощью SPPS в девять стадий согласно общей методике пептидного синтеза, описанной в настоящей заявке, исходя из H-Cys(4-метокситритил)-2-хлортритил-смолы и следующих SPPS реагентов:
| Реагенты | ммоль | Экв. | Мол. масса | Кол-во |
| H-Cys(4-метокситритил)-2-хлортритил-смола (содержание действующего вещества 0,6 ммоль/г) | 0,20 | 0,333 г | ||
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,25 | 1,25 | 497,54 | 0,124 г |
| Fmoc-Glu(OtBu)-OH | 0,30 | 1,5 | 425,5 | 0,128 г |
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,25 | 1,25 | 497,54 | 0,124 г |
| Fmoc-Glu(OtBu)-OH | 0,30 | 1,5 | 425,5 | 0,128 г |
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,25 | 1,25 | 497,54 | 0,124 г |
| Fmoc-Glu(OtBu)-OH | 0,30 | 1,5 | 425,5 | 0,128 г |
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,25 | 1,25 | 497,54 | 0,124 г |
| Fmoc-Glu-OtBu | 0,30 | 1,5 | 425,5 | 0,128 г |
| N10TFA-птероевая кислота (растворяли в 10 мл ДМСО) | 0,25 | 1,25 | 408 | 0,102 г |
| DIPEA | 2 экв. отн. аминокислоты | 129,25 (d=0,742) | 87 мкл или 105 мкл | |
| PyBOP | 1 экв. отн. аминокислоты | 520 | 130 мг или 156 мг |
Стадии сочетания, стадия отщепления и реагент для отщепления соответствовали описанным выше методикам; стадия очистки ВЭЖХ. Колонка: Waters NovaPak C18 300×19 мм; буфер A=10 мМ ацетат аммония, pH 5; B= ACN; методика: 0% B-20% B в течение 40 мин при скорости 25 мл/мин; выход ~220 мг, 67%. C61H89N15O36S; мол. масса 1640,50; точное значение массы: 1639,53.
Пример. EC0453 синтезировали с помощью SPPS согласно общей методике пептидного синтеза, описанной в настоящей заявке, исходя из H-Cys(4-метокситритил)-2-хлортритил-смолы и следующих SPPS реагентов:
| Реагенты | ммоль | Экв. | Мол. масса |
Кол-во |
| H-Cys(4-метокситритил)-2-хлортритил-смола (содержание действующего вещества 0,56 ммоль/г) | 0,162 | 0,290 г | ||
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,203 | 1,25 | 497,54 | 0,101 г |
| Fmoc-Asp(OtBu)-OH | 0,324 | 2 | 411,5 | 0,133 г |
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,203 | 1,25 | 497,54 | 0,101 г |
| Fmoc-Asp(OtBu)-OH | 0,324 | 2 | 411,5 | 0,133 г |
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,203 | 1,25 | 497,54 | 0,101 г |
| Fmoc-Asp(OtBu)-OH | 0,324 | 2 | 411,5 | 0,133 г |
| (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновая кислота | 0,203 | 1,25 | 497,54 | 0,101 г |
| Fmoc-Glu-OtBu | 0,324 | 2 | 425,5 | 0,138 г |
| N10TFA-птероевая кислота (растворяли в 10 мл ДМСО) | 0,203 | 1,25 | 408 | 0,083 г |
| DIPEA | 2 экв. отн. аминокислоты | 129,25 (d=0,742) | 71 мкл или 85 мкл | |
| PyBOP | 1 экв. отн. аминокислоты | 520 | 211 мг или 253 мг |
Стадии сочетания. В сосуд для синтеза пептидов добавляли смолу, добавляли раствор аминокислоты, DIPEA и PyBOP. Барботировали аргон в течение 1 ч и 3 раза промывали ДМФА и IPA. Перед каждой стадией сочетания для снятия защиты Fmoc применяли 20% пиперидин в ДМФА, 3×(10 мин). В указанных условиях осуществляли все девять стадий сочетания. В конце обрабатывали смолу 2% гидразином в ДМФА 3× (5 мин) для отщепления защитной группы птероевой кислоты, т.е. TFA, промывали смолу ДМФА (3×), IPA (3×), MeOH (3×) и барботировали через смолу аргон в течение 30 мин.
Стадия отщепления. Реагент для отщепления: 92,5% TFA, 2,5% H2O, 2,5% триизопропилсилан, 2,5% этандитиол. Обрабатывали смолу отщепляющим реагентом 3 раза (15 мин, 5 мин, 5 мин) при пропускании аргона, высушивали, собирали и объединяли растворы. Упаривали на роторном испарителе до остаточного объема 5 мл и осаждали диэтиловым эфиром (35 мл). Центрифугировали, промывали диэтиловым эфиром и высушивали. Неочищенное твердое вещество очищали ВЭЖХ.
Стадия очистки ВЭЖХ. Колонка: Waters Xterra Prep MS C18 10 мкм 19×250 мм; растворитель A=10 мМ ацетат аммония, pH 5; B= ACN; методика: 5 мин 0% B до 40 мин 20% B 25 мл/мин; фракции, содержавшие продукт, собирали и подвергали лиофильной сушке, получая ~60 мг EC0453 (выход 23%). Данные 1H ЯМР и ЖХ/МС соответствовали желаемой структуре продукта.
C58H83N15O36S; мол. масса 1598,43; точное значение массы: 1597,48. C, 43,58; H, 5,23; N, 13,14; O, 36,03; S, 2,01.
Пример. (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновой кислоты-диазокетон. В сухой круглодонной 100-мл колбе растворяли (3,4),(5,6)-биацетонид-2-дезокси-2-Fmoc-амино-D-манноновую кислоту (1,0 г, 2,01 ммоль) в ТГФ (10 мл, растворение прошло не полностью) в атмосфере аргона. Реакционную смесь охлаждали до -25°C. К этому раствору добавляли NMM (0,23 мл, 2,11 ммоль) и этилхлорформиат (228,98 мг, 2,11 ммоль). Полученный раствор перемешивали при -20°C в течение 30 мин. Полученной белой суспензии давали нагреться до 0°C и добавляли раствор диазометана в эфире до появления устойчивой желтой окраски. Перемешивание продолжали, пока смесь нагревалась до комнатной температуры. После 2 ч перемешивания избыток диазометана разлагали добавлением нескольких капель уксусной кислоты при энергичном перемешивании. Полученную смесь разбавляли эфиром, промывали насыщенным водным раствором NaHCO3, насыщенным водным раствором NH4Cl, насыщенным раствором соли, высушивали над Na2SO4 и концентрировали досуха. Полученное неочищенное вещество вводили в колонку с SiO2 и очищали хроматографией (30% EtOAc в петролейном эфире), получая чистый (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновой кислоты-диазокетон (0,6 г, 57%). Данные спектроскопии 1H ЯМР соответствовали желаемой структуре продукта. C28H31N3O7; мол. масса 521,56; точное значение массы: 521,22.
Пример. (3R,4R,5S,6R)-(4,5),(6,7)-бисацетонид-3-Fmoc-аминогептановая кислота. В сухой 25-мл круглодонной колбе растворяли (3,4),(5,6)-бисацетонид-2-дезокси-2-Fmoc-амино-D-манноновой кислоты-диазокетон (0,15 г, 0,29 ммоль) в ТГФ (1,6 мл) в атмосфере аргона. К этому раствору в темноте добавляли трифторацетат серебра (6,6 мг, 0,03 ммоль) в воде (0,4 мл). Полученную смесь перемешивали при комнатной температуре в течение 16 ч. ТСХ (10% MeOH в метиленхлориде) показала, что все исходные вещества вступили в реакцию и образовался продукт реакции. Растворитель (ТГФ) удаляли при пониженном давлении, остаток разбавляли водой (значение pH составляло 3,5-4,0) и экстрагировали EtOAc. Органический слой промывали насыщенным раствором соли, высушивали над Na2SO4 и концентрировали досуха. Затем полученное неочищенное вещество вводили в колонку с SiO2 и очищали хроматографией (градиентное элюирование от 1% MeOH в метиленхлориде до 5% MeOH в метиленхлориде), получая чистую (3R,4R,5S,6R)-(4,5),(6,7)-бисацетонид-3-Fmoc-аминогептановую кислоту (0,10 г, 68%). Данные спектроскопии 1H ЯМР соответствовали желаемой структуре продукта. C28H33NO8; мол. масса 511,56; точное значение массы: 511,22.
Пример. Спейсер тетра-гомосахаро-трис-α-Glu-фолат EC0478. EC0478 синтезировали с помощью SPPS в девять стадий согласно общей методике пептидного синтеза, описанной в настоящей заявке, исходя из H-Cys(4-метокситритил)-2-хлортритил-смолы и следующих SPPS реагентов:
| Реагенты | ммоль | Экв. | Мол. масса | Кол-во |
| H-Cys(4-метокситритил)-2-хлортритил-смола (содержание действующего вещества 0,56 ммоль/г) | 0,1 | 0,167 г | ||
| Гомосахар | 0,12 | 1,2 | 511,56 | 0,061 г |
| Fmoc-Glu(OtBu)-OH | 0,2 | 2 | 425,5 | 0,085 г |
| Гомосахар | 0,12 | 1,2 | 511,56 | 0,061 г |
| Fmoc-Glu(OtBu)-OH | 0,2 | 2 | 425,5 | 0,085 г |
| Гомосахар | 0,12 | 1,2 | 511,56 | 0,061 г |
| Fmoc-Glu(OtBu)-OH | 0,2 | 2 | 425,5 | 0,085 г |
| Гомосахар | 0,12 | 1,2 | 511,56 | 0,061 г |
| Fmoc-Glu-OtBu | 0,2 | 2 | 425,5 | 0,085 г |
| N10TFA-птероевая кислота·TFA (растворяли в 10 мл ДМСО) | 0,12 | 1,2 | 408 | 0,049 г |
| DIPEA | 0,4 | 4 | 129,25 (d=0,742) | 0,070 мл |
| PyBOP | 0,2 | 2 | 520 | 0,104 г |
Стадии сочетания, стадия отщепления и реагент для отщепления соответствовали описанным выше методикам; стадия очистки ВЭЖХ. Колонка: Waters NovaPak C18 300×19 мм; буфер A=10 мМ ацетат аммония, pH 5; B=ACN; методика: 100% A в течение 5 мин, затем от 0% В до 20% B в течение 20 минут при скорости 26 мл/мин; выход ~88 мг, 52%. C65H97N15O36S; мол. масса 1696,61; точное значение массы: 1695,59.
Пример. Амид (3,4),(5,6)-бисацетонид-D-глюконовой кислоты. 20 г метилового эфира растворяли в 100 мл метанола, охлаждали при помощи смеси сухой лед/ацетон в сосуде для проведения реакций под высоким давлением, вводили в сосуд 100 мл жидкого аммиака, нагревали до комнатной температуры и нагревали при 160°C/850 фунтов/кв.дюйм в течение 2 часов. Реакционный сосуд охлаждали до комнатной температуры и сбрасывали давление. Выпаривание растворителя позволяло получить коричневатый сироп, к которому добавляли минимальное количество изопропилового спирта, чтобы получить гомогенный раствор при кипячении с обратным холодильником. Этот раствор охлаждали до -20°C и полученное при этом твердое вещество отфильтровывали, получая 8,3 г твердого вещества. Материнский раствор упаривали, к полученному остатку добавляли эфир и кипятили до образования гомогенного раствора. Затем этот раствор охлаждали до -20°C и выделившееся при этом твердое вещество отфильтровывали, получая 4,0 г продукта. Твердые продукты объединяли и перекристаллизовывали из изопропилового спирта, получая 11,2 г (59%) амида белого цвета. C12H21NO6; мол. масса 275,30; точное значение массы: 275,14.
Пример. (3,4),(5,6)-бисацетонид-1-дезокси-1-амино-D-глюцитол. В сухой 100-мл круглодонной колбе в атмосфере аргона растворяли LiAlH4 (450 мг, 11,86 ммоль) в ТГФ (10 мл) и охлаждали до 0°C. К этой суспензии очень медленно в течение 15 мин добавляли раствор амида (3,4),(5,6)-бисацетонид-D-глюконовой кислоты (1,09 г, 3,96 ммоль) в ТГФ (30 мл). Полученную смесь кипятили с обратным холодильником в течение 5 ч. ТСХ (10% MeOH в метиленхлориде) показала, что все исходные вещества вступили в реакцию и образовался продукт реакции. Реакционную смесь охлаждали до комнатной температуры и затем охлаждали до температуры ледяной бани, разбавляли диэтиловым эфиром (40 мл), медленно добавляли 0,5 мл воды, 0,5 мл 15% водного раствора NaOH и затем добавляли 1,5 мл воды. Реакционную смесь нагревали до комнатной температуры и перемешивали в течение 30 мин. Добавляли MgSO4, перемешивали еще 15 мин и фильтровали. Органический слой концентрировали досуха, получая (3,4),(5,6)-бисацетонид-1-дезокси-1-амино-D-глюцитол. Данные спектроскопии 1H ЯМР соответствовали желаемой структуре продукта. C12H23NO5; мол. масса 261,31; точное значение массы: 261,16.
Пример. EC0475. O-аллил защищенный Fmoc-Glu (2,17 г, 1 экв.), PyBOP (2,88 г, 1 экв.) и DIPEA (1,83 мл, 2 экв.) добавляли к раствору (3,4),(5,6)-бисацетонид-1-дезокси-1-амино-D-глюцитола (1,4 г, 5,3 ммоль) в сухом ДМФА (6 мл) и смесь перемешивали при КТ в атмосфере Ar в течение 2 ч. Полученный раствор разбавляли EtOAc (50 мл), промывали насыщенным раствором соли (10 мл × 3), органический слой отделяли, высушивали (MgSO4), фильтровали и концентрировали, получая остаток, который очищали колоночной флэш-хроматографией (силикагель, 60% EtOAc/петролейный эфир), получая 1,72 г (50%) защищенного аллилом EC0475 в виде твердого вещества. К раствору защищенного аллилом EC0475 (1,72 г, 2,81 ммоль) в NMM/AcOH/CHCl3 (2 мл/4 мл/74 мл) добавляли Pd(Ph3)4 (300 мг, 0,1 экв.). Полученный желтый раствор перемешивали при КТ в атмосфере Ar в течение 1 ч и затем добавляли к нему вторую порцию Pd(Ph3)4 (300 мг, 0,1 экв.). После перемешивания в течение еще 1 ч смесь промывали 1N HCl (50 мл × 3) и насыщенным раствором соли (50 мл), органический слой отделяли, высушивали (MgSO4), фильтровали и концентрировали, получая желтое пенистое твердое вещество, которое очищали хроматографией (силикагель, 1% MeOH/CHCl3 и затем 1% MeOH/CHCl3), получая 1,3 г (81%) EC0475 в виде твердого вещества. Мол. масса 612,67; точное значение массы: 612,27.
Пример. Спейсер тетра-сахароглутамат-бис-α-Glu-фолат EC0491. EC0491 синтезировали с помощью SPPS в восемь стадий согласно общей методике пептидного синтеза, описанной в настоящей заявке, исходя из H-Cys(4-метокситритил)-2-хлортритил-смолы и следующих SPPS реагентов:
| Реагенты | ммоль | Экв. | Мол. масса | Кол-во |
| H-Cys(4-метокситритил)-2-хлортритил-смола (содержание действующего вещества 0,56 ммоль/г) | 0,1 | 0,167 г | ||
| EC0475 | 0,13 | 1,3 | 612,67 | 0,080 г |
| Fmoc-Glu(OtBu)-OH | 0,2 | 2 | 425,5 | 0,085 г |
| EC0475 | 0,13 | 1,3 | 612,67 | 0,080 г |
| EC0475 | 0,13 | 1,3 | 612,67 | 0,080 г |
| Fmoc-Glu(OtBu)-OH | 0,2 | 2 | 425,5 | 0,085 г |
| EC0475 | 0,13 | 1,3 | 612,67 | 0,080 г |
| Fmoc-Glu-OtBu | 0,2 | 2 | 425,5 | 0,085 г |
| N10TFA-птероевая кислота·TFA (растворяли в 10 мл ДМСО) | 0,2 | 2 | 408 | 0,105 г |
| DIPEA | 0,4 | 4 | 129,25 (d=0,742) | 0,070 мл |
| PyBOP | 0,2 | 2 | 520 | 0,104 г |
Стадии сочетания, стадия отщепления и реагент для отщепления соответствовали описанным выше методикам; стадия очистки ВЭЖХ: Колонка: Waters NovaPak C18 300×19 мм; буфер A=10 мМ ацетат аммония, pH 5; B=ACN; методика: 100% A в течение 5 мин, затем от 0% В - 20% B в течение 20 минут при скорости 26 мл/мин; выход ~100 мг, 51%. C76H118N18O41S; мол. масса 1971,91; точное значение массы: 1970,74.
Пример. EC0479 синтезировали с помощью SPPS согласно общей методике пептидного синтеза, описанной в настоящей заявке, исходя из H-Cys(4-метокситритил)-2-хлортритил-смолы и следующих SPPS реагентов:
| Реагенты | ммоль | Экв. | Мол. масса | Кол-во |
| H-Cys(4-метокситритил)-2-хлортритил-смола (содержание действующего вещества 0,6 ммоль/г) | 0,094 | 0,16 г | ||
| EC0475 | 0,13 | 1,4 | 612,67 | 0,082 г |
| Fmoc-Glu(OtBu)-OH | 0,19 | 2,0 | 425,47 | 0,080 г |
| EC0475 | 0,13 | 1,4 | 612,67 | 0,082 г |
| Fmoc-Arg(Pbf)-OH | 0,19 | 2,0 | 648,77 | 0,12 г |
| EC0475 | 0,13 | 1,4 | 612,67 | 0,082 г |
| Fmoc-Glu(OtBu)-OH | 0,19 | 2,0 | 425,47 | 0,080 г |
| EC0475 | 0,13 | 1,4 | 612,67 | 0,082 г |
| Fmoc-Glu-OtBu | 0,19 | 2,0 | 425,47 | 0,080 г |
| N10TFA-птероевая кислота·TFA (растворяли в 10 мл ДМСО) | 0,16 | 1,7 | 408,29 | 0,066 г |
| DIPEA | 2,0 экв. АА | 41 мкл или 49 мкл |
||
| PyBOP | 1,0 экв. АА | 122 мг или 147 мг |
Стадии сочетания. В сосуд для синтеза пептидов добавляли смолу, добавляли раствор аминокислоты, DIPEA и PyBOP. Барботировали аргон в течение 1 ч и 3 раза промывали ДМФА и IPA. Перед каждой стадией сочетания аминокислот для снятия защиты Fmoc применяли 20% пиперидин в ДМФА, 3×(10 мин). В указанных условиях осуществляли все девять стадий сочетания. В конце обрабатывали смолу 2% гидразином в ДМФА 3× (5 мин) для отщепления защитной группы птероевой кислоты TFA, промывали смолу ДМФА (3×), IPA (3×), MeOH (3×) и через смолу барботировали аргон в течение 30 мин.
Стадия отщепления. Реагент для отщепления: 92,5% TFA, 2,5% H2O, 2,5% триизопропилсилан, 2,5% этандитиол. Обрабатывали смолу отщепляющим реагентом 3 раза по 15 мин при пропускании аргона, высушивали, промывали смолу расщепляющим реагентом еще один раз и объединяли раствор. Упаривали на роторном испарителе до остаточного объема 5 мл и осаждали диэтиловым эфиром (35 мл). Центрифугировали, промывали диэтиловым эфиром и высушивали. Неочищенное твердое вещество очищали ВЭЖХ.
Стадия очистки ВЭЖХ. Колонка: Waters Atlantis Prep T3 10 мкм OBD 19×250 мм; растворитель A: 10 мМ ацетат аммония, pH 5; растворитель B: ACN; методика: 5 мин 0% B до 20 мин 20% B 26 мл/мин; фракции, содержавшие продукт, собирали и подвергали лиофильной сушке, получая ~70 мг EC0479 (выход 35%). Данные 1H ЯМР и ЖХ/МС соответствовали желаемой структуре продукта.
Мол. масса 2128,10; точное значение массы: 2126,84.
EC0488. Это соединение синтезировали с помощью SPPS согласно общей методике пептидного синтеза, описанной в настоящей заявке, исходя из H-Cys(4-метокситритил)-2-хлортритил-смолы и следующих SPPS реагентов:
| Реагенты | ммоль | Экв. | Мол. масса | Кол-во |
| H-Cys(4-метокситритил)-2-хлортритил-смола (содержание действующего вещества 0,6 ммоль/г) | 0,10 | 0,17 г | ||
| EC0475 | 0,13 | 1,3 | 612,67 | 0,082 г |
| Fmoc-Glu(OtBu)-OH | 0,19 | 1,9 | 425,47 | 0,080 г |
| EC0475 | 0,13 | 1,3 | 612,67 | 0,082 г |
| Fmoc-Glu(OtBu)-OH | 0,19 | 1,9 | 425,47 | 0,080 г |
| EC0475 | 0,13 | 1,3 | 612,67 | 0,082 г |
| Fmoc-Glu-OtBu | 0,19 | 1,9 | 425,47 | 0,080 г |
| N10TFA-птероевая кислота·TFA (растворяли в 10 мл ДМСО) | 0,16 | 1,6 | 408,29 | 0,066 г |
| DIPEA | 2,0 экв. АА | |||
| PyBOP | 1,0 экв. АА |
Стадии сочетания. В сосуд для синтеза пептидов добавляли смолу, добавляли раствор аминокислоты, DIPEA и PyBOP. Барботировали аргон в течение 1 ч и 3 раза промывали ДМФА и IPA. Перед каждой стадией сочетания аминокислот для снятия защиты Fmoc применяли 20% пиперидин в ДМФА, 3×(10 мин). В указанных условиях осуществляли все девять стадий сочетания. В завершении обрабатывали смолу 2% гидразином в ДМФА 3×(5 мин) для отщепления защитной группы птероевой кислоты TFA, промывали смолу ДМФА (3×), IPA (3×), MeOH (3×) и через смолу барботировали аргон в течение 30 мин.
Стадия отщепления. Реагент для отщепления: 92,5% TFA, 2,5% H2O, 2,5% триизопропилсилан, 2,5% этандитиол. Обрабатывали смолу отщепляющим реагентом 3 раза (10 мин, 5 мин, 5 мин) при пропускании аргона, высушивали, промывали смолу отщепляющим реагентом еще один раз и объединяли растворы. Упаривали на роторном испарителе до остаточного объема 5 мл и осаждали диэтиловым эфиром (35 мл). Центрифугировали, промывали диэтиловым эфиром и высушивали. Приблизительно половину неочищенного твердого вещества очищали ВЭЖХ.
Стадия очистки ВЭЖХ. Колонка: Waters Xterra Prep MS C18 10 мкм 19×250 мм; растворитель A: 10 мМ ацетат аммония, pH 5; растворитель B: ACN; методика: 5 мин 0% B до 25 мин 20% B 26 мл/мин; фракции, содержавшие продукт, собирали и подвергали лиофильной сушке, получая ~43 мг EC0488 (выход 51%). Данные 1H ЯМР и ЖХ/МС (точное значение массы 1678,62) соответствовали желаемой структуре продукта.
Мол. масса 1679,63; точное значение массы: 1678,62.
По описанным в настоящей заявке методикам получали следующие примеры промежуточных соединений связывающий лиганд-линкер: EC0233, EC0244, EC0257 и EC0261
EC0233; C28H35N9O12S; мол. масса 721,70; точное значение массы: 721,21
EC0244; C38H51N11O20S; мол. масса 1013,94; точное значение массы: 1013,30
EC0257; C44H62N12O25S; мол. масса 1191,09; точное значение массы: 1190,37
EC0261; C48H67N13O28S; мол. масса 1306,18; точное значение массы: 1305,39
Следующие примеры иллюстративных промежуточных соединений получали, как описано в настоящей заявке.
Азид Huisgen для получения 1,2,3-триазола; (a) NaN3; (b) Ag2CO3, DCM, молекулярные сита; (c) LiOH, MeOH, H2O.
EC0501 Тиобортезомиб
EC0536 Промежуточное соединение конъюгата
EC0632 Промежуточное соединение конъюгата. C52H72N14O28S; мол. масса 1373,27; точное значение массы: 1372,44, получен из соответствующих трет-бутилзащищенных карбоксилатов.
EC0669 Промежуточное соединение конъюгата. C49H71N13O24S; мол. масса 1258,23; точное значение массы: 1257,45
Пример. Синтез сшивающего реагента EC0311. DIPEA (0,60 мл) добавляли к суспензии HOBt-OCO2-(CH2)2-SS-2-пиридин·HCl (685 мг, 91%) в безводном DCM (5,0 мл) при 0°C, перемешивали в атмосфере аргона в течение 2 минут и к полученной смеси добавляли безводный гидразин (0,10 мл). Реакционную смесь перемешивали в атмосфере аргона при 0°C в течение 10 минут и при комнатной температуре в течение еще 30 мин, фильтровали и очищали фильтрат флэш-хроматографией (силикагель, 2% MeOH в DCM), получая EC0311 в виде прозрачного густого масла (371 мг), затвердевающего при отстаивании.
Пример. Винбластин пиридинил дисульфид. 2-[(бензотриазол-1-ил-(оксикарбонилокси)этилдисульфанил)]пиридин·HCl (601 мг) и 378 мкл DIPEA последовательно добавляли к раствору дезацетил винбластин гидразида (668 мг) в 5 мл DCM при 0°C. Реакционной смеси давали нагреться до комнатной температуры и перемешивали в течение 3 часов. ТСХ (15% MeOH в DCM) продемонстрировала полное превращение исходных веществ. Полученную смесь очищали хроматографией на силикагеле (1:9 MeOH/DCM). Объединенные фракции упаривали, повторно растворяли в DCM и промывали 10% раствором Na2CO3, насыщенным раствором соли, высушивали (MgSO4) и упаривали, получая 550 мг (80%) продукта; RT ВЭЖХ 12,651 мин, чистота 91%, 1H ЯМР спектр соответствовал структуре, приписываемой продукту, МС(ESI+): 984,3, 983,3, 982,4, 492,4 491,9, 141,8. Дополнительные сведения о данной методике приведены в опубликованной заявке на патент США № US 2005/0002942 A1.
Пример. Получение гидразидов тубулизина. Показано на примере получения EC0347. N,N-диизопропилэтиламин (DIPEA, 6,1 мкл) и изобутилхлорформиат (3,0 мкл) совместно добавляли с помощью шприца к раствору тубулизина B (0,15 мг) в безводном EtOAc (2,0 мл) при -15°C. После перемешивания в течение 45 минут при -15°C в атмосфере аргона реакционную смесь охлаждали до -20°C и к ней добавляли безводный гидразин (5,0 мкл). Реакционную смесь перемешивали в атмосфере аргона при -20°C в течение 3 часов, гасили 1,0 мМ натрий-фосфатным буфером (pH 7,0, 1,0 мл) и впрыскивали в прибор для препаративной ВЭЖХ с целью очистки. Колонка: Waters Xterra Prep MS C18 10 мкм 19×250 мм; подвижная фаза A: 1,0 мМ натрий-фосфатный буфер, pH 7,0; подвижная фаза B: ацетонитрил; методика: 10% B до 80% B в течение 20 мин, скорость потока 25 мл/мин. Фракции 15,14-15,54 мин собирали и лиофилизовали, получая EC0347 в виде белого твердого вещества (2,7 мг). Приведенная выше методика применима также для получения гидразидов других тубулизинов при соответствующем выборе исходных тубулизинов.
Пример. Получение дисульфидов тубулизина (постадийный способ). Показано на примере получения EC0312. DIPEA (36 мкл) и изобутилхлорформиат (13 мкл) вместе добавляли с помощью шприца в раствор тубулизина B (82 мг) в безводном EtOAc (2,0 мл) при -15°C. После перемешивания в течение 45 мин при -15°C в атмосфере аргона к реакционной смеси добавляли раствор EC0311 в безводном EtOAc (1,0 мл). Полученный раствор перемешивали в атмосфере аргона при -15°C в течение 15 минут и при комнатной температуре в течение еще 45 минут, концентрировали и очищали остаток флэш-хроматографией (силикагель, 2-8% MeOH в DCM), получая EC0312 в виде белого твердого вещества (98 мг). Описанный выше способ применим также для получения производных других тубулизинов при соответствующем выборе исходного тубулизина.
Пример. Общая методика синтеза дисульфид-содержащих конъюгатов тубулизина. Показана на примере получения EC0312. Промежуточное соединение связывающий лиганд-линкер, содержавший тиольную группу, смешивали с деионизованной водой (приблизительно 20 мг/мл, через которую перед использованием пропускали аргон в течение 10 минут) и pH суспензии доводили добавлением насыщенного раствора NaHCO3 (через который перед использованием пропускали аргон в течение 10 минут) до значения примерно 6,9 (суспензия может переходить в раствор при увеличении значения pH). При необходимости к раствору добавляли дополнительное количество деионизованной воды (приблизительно 20-25%) и к полученному водному раствору немедленно добавляли раствор EC0312 в ТГФ (приблизительно 20 мг/мл). Реакционная смесь быстро становилась гомогенной. После перемешивания в атмосфере аргона, например, в течение 45 минут, реакционную смесь разбавляли 2,0 мМ натрий-фосфатным буфером (pH 7,0 приблизительно 150 объемных процентов) и удаляли ТГФ в вакууме. Полученную суспензию фильтровали, и фильтрат можно было очистить перпаративной ВЭЖХ (как описано в настоящей заявке). Нужную фракцию лиофилизовали для выделения конъюгатов. Описанный выше способ применим также для получения конъюгатов других тубулизинов при соответствующем выборе других исходных тубулизинов.
Сравнительный пример. Получение конъюгата винбластина EC145, в котором отсутствуют гидрофильные спейсеры линкера. Пептидильный фрагмент Pte-Glu-Asp-Arg-Asp-Asp-Cys-OH (пример 13) в ТГФ обрабатывали либо тиосульфонат-активированным винбластином, либо винбластин пиридинил дисульфидом в виде желтого раствора, полученного при растворении в 0,1 М NaHCO3 при pH>6,5 в атмосфере аргона. Лиофилизация и ВЭЖХ позволяли получить конъюгат с выходом 70%; фрагменты спектра 1H ЯМР (D2O) δ 8,67 (с, 1Н, фолиевая кислота Н-7), 7,50 (ушир.с, 1Н, VLB H-11'), 7,30-7,40 (ушир.с, 1Н, VLB H-14'), 7,35 (д, 2H, J=7,8 Гц, фолиевая кислота Н-12 и 16), 7,25 (м, 1H, VLB H-13'), 7,05 (ушир.с, 1H, VLB H-12'), 6,51 (д, 2H, J=8,7 Гц, фолиевая кислота H-13 и 15), 6,4 (c, 2H, VLB H-14 и 17), 5,7 (м, 1H, VLB олефин) 5,65 (м, 1H, VLB H-7), 5,5 (д, 1H, VLB олефин), 5,5 (м, 1H, VLB H-6), 4,15 (м, 1H, VLB H-8'), 3,82 (с, 3H, VLB C18 '-CO2CH3), 3,69 (с, 3H, VLB C16-OCH3), 2,8 (с, 3H, VLB N-CH3), 1,35 (ушир.с, 1H, VLV H-3'), 1,15 (м, 1H, VLB H-2'), 0,9 (т, 3H, J=7 Гц, VLB H-21'), 0,55 (т, 3H, J=6,9 Гц, VLB H-21); ЖХ-МС (ESI, m+H+) 1918.
Пример. EC0234 (конъюгат моно-сахаро-фолат-винбластин) включающий гидрофильный спейсер линкера. В полипропиленовой емкости для центрифугирования фолат-содержащий линкер (EC0233, 22 мг, 0,030 ммоль) растворяли в 2 мл воды и барботировали аргон в течение 10 мин. В другом сосуде барботировали аргон в течение 10 минут через 0,1N раствор NaHCO3. pH раствора линкера осторожно повышали до 6,9, используя 0,1N раствор NaHCO3. К полученному раствору медленно добавляли винбластин пиридинил дисульфид (27 мг, 0,028 ммоль) в 2 мл тетрагидрофурана (ТГФ). Полученный прозрачный раствор перемешивали в атмосфере аргона в течение 15 мин-1 ч. За ходом реакции следили с помощью аналитической ВЭЖХ (10 мМ ацетат аммония, pH=7,0 и ацетонитрил). ТГФ удаляли при пониженном давлении, водный раствор фильтровали и вводили в колонку для препаративной ВЭЖХ (колонка X-terra C18, 19×300 мм). Элюирование 1 мМ фосфатом натрия pH 7,0 и ацетонитрилом позволяло получить фракции, содержащие чистый продукт. Конъюгат винбластин-сахаро-фолат (EC0234) выделяли после лиофилизации в течение 48 ч (34 мг, 76%). Данные 1H ЯМР соответствовали желаемой структуре конъюгата фолата. C74H93N15O21S2; мол. масса 1592,75; точное значение массы: 1591,61.
Пример. EC0246 (конъюгат бис-сахаро-фолат-винбластин). В полипропиленовой емкости для центрифугирования фолат-содержащий линкер (EC0244, 30 мг, 0,030 ммоль) растворяли в 5 мл воды и барботировали аргон в течение 10 мин. В другом сосуде барботировали аргон в течение 10 минут через 0,1N раствор NaHCO3. pH раствора линкера осторожно повышали до 6,9, используя 0,1N раствор NaHCO3. К полученному раствору медленно добавляли винбластин пиридинил дисульфид (27 мг, 0,028 ммоль) в 5 мл тетрагидрофурана (ТГФ). Полученный прозрачный раствор перемешивали в атмосфере аргона в течение 15 мин-1 ч. За ходом реакции следили с помощью аналитической ВЭЖХ (10 мМ ацетат аммония, pH=7,0 и ацетонитрил). ТГФ удаляли при пониженном давлении, водный раствор фильтровали и вводили в колонку для препаративной ВЭЖХ (колонка X-terra C18, 19×300 мм). Элюирование 1 мМ фосфатом натрия pH 7,0 и ацетонитрилом позволяло получить фракции, содержащие чистый продукт. Конъюгат винбластин-бис-сахаро-фолат (EC0246) выделяли после лиофилизации в течение 48 ч (34 мг, 66%). Данные 1H ЯМР соответствовали желаемой структуре конъюгата фолата. C84H109N17O29S2; мол. масса 1884,99; точное значение массы: 1883,70.
Пример. EC0258 (конъюгат трис-сахаро-Asp-фолат-винбластин). В полипропиленовой емкости для центрифугирования фолат-содержащий линкер (EC0257, 37 мг, 0,031 ммоль) растворяли в 5 мл воды и барботировали аргон в течение 10 мин. В другом сосуде барботировали аргон в течение 10 минут через 0,1N раствор NaHCO3. pH раствора линкера осторожно повышали до 6,9, используя 0,1N раствор NaHCO3. К полученному раствору медленно добавляли винбластин пиридинил дисульфид (27,5 мг, 0,028 ммоль) в 5 мл тетрагидрофурана (ТГФ). Полученный прозрачный раствор перемешивали в атмосфере аргона в течение 15 мин-1 ч. За ходом реакции следили с помощью аналитической ВЭЖХ (10 мМ ацетат аммония, pH=7,0 и ацетонитрил). ТГФ удаляли при пониженном давлении, водный раствор фильтровали и вводили в колонку для препаративной ВЭЖХ (колонка X-terra C18, 19×300 мм). Элюирование 1 мМ фосфатом натрия pH 7,0 и ацетонитрилом позволяло получить фракции, содержащие чистый продукт. Конъюгат винбластин-трис-сахаро-Asp-фолат (EC0258) выделяли после лиофилизации в течение 48 ч (36 мг, 62%). Данные 1H ЯМР соответствовали желаемой структуре конъюгата фолата. C90H120N18O34S2; мол. масса 2062,15; точное значение массы: 2060,77.
Пример. EC0263 (конъюгат трис-сахаро-бис-Asp-фолат-винбластин). В полипропиленовой емкости для центрифугирования фолат-содержащий линкер (EC0261, 37 мг, 0,029 ммоль) растворяли в 5 мл воды и барботировали аргон в течение 10 мин. В другом сосуде барботировали аргон в течение 10 минут через 0,1N раствор NaHCO3. pH раствора линкера осторожно повышали до 6,9, используя 0,1N раствор NaHCO3. К полученному раствору медленно добавляли винбластин пиридинил дисульфид (25,5 мг, 0,026 ммоль) в 5 мл тетрагидрофурана (ТГФ). Полученный прозрачный раствор перемешивали в атмосфере аргона в течение 15 мин-1 ч. За ходом реакции следили с помощью аналитической ВЭЖХ (10 мМ ацетат аммония, pH=7,0 и ацетонитрил). ТГФ удаляли при пониженном давлении, водный раствор фильтровали и вводили в колонку для препаративной ВЭЖХ (колонка X-terra C18, 19×300 мм). Элюирование 1 мМ фосфатом натрия pH 7,0 и ацетонитрилом позволяло получить фракции, содержащие чистый продукт. Конъюгат винбластин-трис-сахаро-бис-Asp-фолат (EC0263) выделяли после лиофилизации в течение 48 ч (36 мг, 64%). Данные 1H ЯМР соответствовали желаемой структуре конъюгата фолата. C94H125N19O37S2; мол. масса 2177,24; точное значение массы: 2157,79.
Пример. EC0434 (конъюгат тетра-сахаро-трис-Asp-фолат-винбластин). В полипропиленовой емкости для центрифугирования фолат-содержащий линкер (EC0268, 20 мг, 0,012 ммоль) растворяли в 3 мл воды и барботировали аргон в течение 10 мин. В другом сосуде барботировали аргон в течение 10 минут через 0,1N раствор NaHCO3. pH раствора линкера осторожно повышали до 6,9, используя 0,1N раствор NaHCO3. К полученному раствору медленно добавляли винбластин пиридинил дисульфид (12 мг, 0,012 ммоль) в 3 мл тетрагидрофурана (ТГФ). Полученный прозрачный раствор перемешивали в атмосфере аргона в течение 15 мин-1 ч. За ходом реакции следили с помощью аналитической ВЭЖХ (10 мМ ацетат аммония, pH=7,0 и ацетонитрил). ТГФ удаляли при пониженном давлении, водный раствор фильтровали и вводили в колонку для препаративной ВЭЖХ (колонка X-terra C18, 19×300 мм). Элюирование 1 мМ фосфатом натрия pH 7,0 и ацетонитрилом позволяло получить фракции, содержащие чистый продукт. Конъюгат винбластин-тетра-сахаро-трис-Asp-фолат (EC0434) выделяли после лиофилизации в течение 48 ч (26 мг, 62%). Данные 1H ЯМР соответствовали желаемой структуре конъюгата фолата. C104H141N21O45S2; мол. масса 2469,48; точное значение массы: 2467,88.
Пример. EC0454 (конъюгат тетра-сахаро-бис-Asp-фолат-винбластин). В полипропиленовой емкости для центрифугирования фолат-содержащий линкер (EC0452, 34 мг, 0,02 ммоль) растворяли в 3 мл воды и барботировали аргон в течение 10 мин. В другом сосуде барботировали аргон в течение 10 минут через 0,1N раствор NaHCO3. pH раствора линкера осторожно повышали до 6,9, используя 0,1N раствор NaHCO3. К полученному раствору медленно добавляли винбластин пиридинил дисульфид (20 мг, 0,02 ммоль) в 3 мл тетрагидрофурана (ТГФ). Полученный прозрачный раствор перемешивали в атмосфере аргона в течение 15 мин-1 ч. За ходом реакции следили с помощью аналитической ВЭЖХ (10 мМ ацетат аммония, pH=7,0 и ацетонитрил). ТГФ удаляли при пониженном давлении, водный раствор фильтровали и вводили в колонку для препаративной ВЭЖХ (колонка X-terra C18, 19×300 мм). Элюирование 1 мМ фосфатом натрия pH 7,0 и ацетонитрилом позволяло получить фракции, содержащие чистый продукт. Конъюгат винбластин-тетра-сахаро-бис-Asp-фолат (EC0454) выделяли после лиофилизации в течение 48 ч (35 мг, 70%). Данные 1H ЯМР соответствовали желаемой структуре конъюгата фолата. C108H151N23O43S2; мол. масса 2523,62; точное значение массы: 2521,98.
Пример. EC0455 (конъюгат тетра-сахаро-бис-Asp-фолат-винбластин). В полипропиленовой емкости для центрифугирования фолат-содержащий линкер (EC0457, 20 мг, 0,013 ммоль) растворяли в 1,5 мл воды и барботировали аргон в течение 10 мин. В другом сосуде барботировали аргон в течение 10 минут через 0,1N раствор NaHCO3. pH раствора линкера осторожно повышали до 6,9, используя 0,1N раствор NaHCO3. К полученному раствору медленно добавляли винбластин пиридинил дисульфид (18 мг, 0,018 ммоль) в 1,5 мл тетрагидрофурана (ТГФ). Полученный прозрачный раствор перемешивали в атмосфере аргона в течение 30 мин. За ходом реакции следили с помощью аналитической ВЭЖХ (10 мМ ацетат аммония, pH=7,0 и ацетонитрил). ТГФ удаляли при пониженном давлении, водный раствор фильтровали и вводили в колонку для препаративной ВЭЖХ (колонка X-terra C18, 19×300 мм). Элюирование 1 мМ фосфатом натрия pH 7,0 и ацетонитрилом позволяло получить фракции, содержащие чистый продукт. Конъюгат винбластин-тетра-сахаро-бис-Asp-фолат (EC0455) выделяли после лиофилизации в течение 48 ч (19 мг, 62%). Данные 1H ЯМР соответствовали желаемой структуре конъюгата фолата. C100H136N20O42S2; мол. масса 2354,39.
Пример. EC0456. В полипропиленовой емкости для центрифугирования фолат-содержащий линкер (EC0453, 46 мг, 0,029 ммоль) растворяли в 3 мл воды, через которую барботировали аргон в течение 10 мин. В другом сосуде барботировали аргон в течение 10 минут через насыщенный раствор NaHCO3. pH раствора линкера осторожно повышали до 6,9, используя раствор NaHCO3. К полученному раствору быстро добавляли винбластин пиридинил дисульфид (32 мг, 1,1 экв.) в 3 мл тетрагидрофурана (ТГФ). Полученный прозрачный раствор перемешивали в атмосфере аргона. За ходом реакции следили с помощью аналитической ВЭЖХ (2 мМ фосфатный буфер, pH=7,0 и ацетонитрил). Через 30 мин к реакционной смеси добавляли 12 мл 2 мМ фосфатного буфера (pH 7), полученный мутный раствор фильтровали и фильтрат вводили в колонку для препаративной ВЭЖХ: колонка Waters Xterra Prep MS C18, 10 мкм 19×250 мм; растворитель A: 2 мМ фосфат натрия pH 7; растворитель B: ACN; методика: 5мин 1% B до 40 мин 80% B 25 мл/мин. Фракции, содержавшие EC0456, собирали и подвергали лиофильной сушке, получая 41,6 мг рыхлого желтого твердого вещества, содержавшего 30 мг EC0456 (выход 42%) и 11,6 натрий-фосфатной соли. Данные 1H ЯМР и ЖХ/МС соответствовали желаемой структуре продукта. C104H141N21O45S2; мол. масса 2469,48; точное значение массы: 2467,88. C, 50,58; H, 5,76; N, 11,91; O, 29,15; S 2,60.
Пример. EC0481. В полипропиленовой емкости для центрифугирования фолат-содержащий линкер (EC0479, 12 мг, 0,0058 ммоль) растворяли в 2,5 мл воды, через которую барботировали аргон в течение 10 мин. В другом сосуде барботировали аргон в течение 10 минут через насыщенный раствор NaHCO3. pH раствора линкера осторожно повышали до 6,9, используя раствор NaHCO3. К полученному раствору быстро добавляли винбластин пиридинил дисульфид (5,7 мг, 1,0 экв.) в 2,5 мл тетрагидрофурана (ТГФ). Полученный прозрачный раствор перемешивали в атмосфере аргона. За ходом реакции следили с помощью аналитической ВЭЖХ (2 мМ фосфатный буфер, pH=7,0 и ацетонитрил). Через 20 мин к реакционной смеси добавляли 12 мл 2 мМ фосфатного буфера (pH 7), полученный мутный раствор фильтровали и фильтрат вводили в колонку для препаративной ВЭЖХ: колонка Waters Atlantis Prep T3 10 мкм OBD 19×250 мм; растворитель A: 2 мМ фосфат натрия pH 7; растворитель B: ACN; методика: 5 мин 1% B до 25 мин 50% B 26 мл/мин. Фракции, содержавшие EC0481, собирали и подвергали лиофильной сушке, получая 15,5 мг рыхлого желтого твердого вещества, содержавшего 10,5 мг EC0481 (выход 60%) и 5,0 натрий-фосфатной соли. Данные 1H ЯМР и ЖХ/МС соответствовали желаемой структуре продукта. Мол. масса 2999,15; точное значение массы: 2997,24.
Пример. EC0484 (конъюгат тетра-сахаро-бис-α-Glu-Arg-фолат-винбластин). В полипропиленовой емкости для центрифугирования фолат-содержащий линкер (EC0480, 15 мг, 0,009 ммоль) растворяли в 3 мл воды и барботировали аргон в течение 10 мин. В другом сосуде барботировали аргон в течение 10 минут через 0,1N раствор NaHCO3. pH раствора линкера осторожно повышали до 6,9, используя 0,1N раствор NaHCO3. К полученному раствору медленно добавляли винбластин пиридинил дисульфид (8,8 мг, 0,009 ммоль) в 3 мл тетрагидрофурана (ТГФ). Полученный прозрачный раствор перемешивали в атмосфере аргона в течение 15 мин - 1ч. За ходом реакции следили с помощью аналитической ВЭЖХ (10 мМ ацетат аммония, pH=7,0 и ацетонитрил). ТГФ удаляли при пониженном давлении, водный раствор фильтровали и вводили в колонку для препаративной ВЭЖХ (колонка X-terra C18, 19×300 мм). Элюирование 1 мМ фосфатом натрия pH 7,0 и ацетонитрилом позволяло получить фракции, содержащие чистый продукт. Конъюгат винбластин-тетра-сахаро-бис-α-Glu-Arg-фолат (EC0484) выделяли после лиофилизации в течение 48 ч (16 мг, 70%). Данные 1H ЯМР соответствовали желаемой структуре конъюгата фолата. C108H152N24O43S2; мол. масса 2538,63; точное значение массы: 2536,99.
Пример. EC0487 (конъюгат тетра-сахаро-Asp-фолат-винбластин). В полипропиленовой емкости для центрифугирования фолат-содержащий линкер (EC0463, 21 мг, 0,015 ммоль) растворяли в 3 мл воды и барботировали аргон в течение 10 мин. В другом сосуде барботировали аргон в течение 10 минут через 0,1N раствор NaHCO3. pH раствора линкера осторожно повышали до 6,9, используя 0,1N раствор NaHCO3. К полученному раствору медленно добавляли винбластин пиридинил дисульфид (15 мг, 0,015 ммоль) в 3 мл тетрагидрофурана (ТГФ). Полученный прозрачный раствор перемешивали в атмосфере аргона в течение 15 мин - 1 ч. За ходом реакции следили с помощью аналитической ВЭЖХ (10 мМ ацетат аммония, pH=7,0 и ацетонитрил). ТГФ удаляли при пониженном давлении, водный раствор фильтровали и вводили в колонку для препаративной ВЭЖХ (колонка Atlantis, 19×300 мм). Элюирование 1 мМ фосфатом натрия pH 7,0 и ацетонитрилом позволяло получить фракции, содержащие чистый продукт. Конъюгат винбластин-тетра-сахаро-Asp-фолат (EC0487) выделяли после лиофилизации в течение 48 ч (28 мг, 84%). Данные 1H ЯМР соответствовали желаемой структуре конъюгата фолата. C96H131N19O39S2; мол. масса 2239,30; точное значение массы: 2237,83.
Пример. EC0489. В полипропиленовой емкости для центрифугирования фолат-содержащий линкер (EC0488, 26 мг, 0,015 ммоль) растворяли в 2,5 мл воды, через которую барботировали аргон в течение 10 мин. В другом сосуде барботировали аргон в течение 10 минут через насыщенный раствор NaHCO3. pH раствора линкера осторожно повышали до 6,9, используя раствор NaHCO3. К полученному раствору быстро добавляли винбластин пиридинил дисульфид (15 мг, 1,0 экв.) в 2,5 мл тетрагидрофурана (ТГФ). Полученный прозрачный раствор перемешивали в атмосфере аргона. За ходом реакции следили с помощью аналитической ВЭЖХ (2 мМ фосфатный буфер, pH=7,0 и ацетонитрил). Через 20 мин к реакционной смеси добавляли 12 мл 2 мМ фосфатного буфера (pH 7), полученный мутный раствор фильтровали и фильтрат вводили в колонку для препаративной ВЭЖХ: колонка Waters Xterra Prep MS C18 10 мкм 19×250 мм; растворитель A: 2 мМ фосфат натрия pH 7; растворитель B: ACN; методика: 5 мин 1% B до 25 мин 50% B 26 мл/мин. Фракции, содержавшие EC0489, собирали и подвергали лиофильной сушке, получая 35 мг рыхлого желтого твердого вещества, содержавшего 27,5 мг EC0489 (выход 71%) и 7,5 натрий-фосфатной соли. Данные 1H ЯМР и ЖХ/МС соответствовали желаемой структуре продукта. Мол. масса 2550,68; точное значение массы: 2549,01.
Пример. EC0490 (конъюгат тетра-гомосахаро-трис-αGlu-фолат-винбластин). В полипропиленовой емкости для центрифугирования фолат-содержащий линкер (EC0478, 22 мг, 0,013 ммоль) растворяли в 3 мл воды и барботировали аргон в течение 10 мин. В другом сосуде барботировали аргон в течение 10 минут через 0,1N раствор NaHCO3. pH раствора линкера осторожно повышали до 6,9, используя 0,1N раствор NaHCO3. К полученному раствору медленно добавляли винбластин пиридинил дисульфид (мг, ммоль) в 3 мл тетрагидрофурана (ТГФ). Полученный прозрачный раствор перемешивали в атмосфере аргона в течение 15 мин - 1ч. За ходом реакции следили с помощью аналитической ВЭЖХ (10 мМ ацетат аммония, pH=7,0 и ацетонитрил). ТГФ удаляли при пониженном давлении, водный раствор фильтровали и вводили в колонку для препаративной ВЭЖХ (колонка X-terra C18, 19×300 мм). Элюирование 1 мМ фосфатом натрия pH 7,0 и ацетонитрилом позволяло получить фракции, содержащие чистый продукт. Конъюгат винбластин-тетра-гомосахаро-трис-Glu-фолат (EC0490) выделяли после лиофилизации в течение 48 ч (15 мг, 45%). Данные 1H ЯМР соответствовали желаемой структуре конъюгата фолата. C111H155N21O45S2; мол. масса 2567,66; точное значение массы: 2565,99.
Пример. EC0492 (конъюгат тетра-гомосахаро-трис-αGlu-фолат-винбластин). В полипропиленовой емкости для центрифугирования фолат-содержащий линкер (EC0491, 26 мг, 0,013 ммоль) растворяли в 3 мл воды и барботировали аргон в течение 10 мин. В другом сосуде барботировали аргон в течение 10 минут через 0,1N раствор NaHCO3. pH раствора линкера осторожно повышали до 6,9, используя 0,1N раствор NaHCO3. К полученному раствору добавляли винбластин пиридинил дисульфид (13 мг, 0,013 ммоль) в 3 мл тетрагидрофурана (ТГФ). Полученный прозрачный раствор перемешивали в атмосфере аргона в течение 15 мин - 1ч. За ходом реакции следили с помощью аналитической ВЭЖХ (10 мМ ацетат аммония, pH=7,0 и ацетонитрил). ТГФ удаляли при пониженном давлении, водный раствор фильтровали и вводили в колонку для препаративной ВЭЖХ (колонка X-terra C18, 19×300 мм). Элюирование 1 мМ фосфатом натрия pH 7,0 и ацетонитрилом позволяло получить фракции, содержащие чистый продукт. Конъюгат винбластин-тетра-гомосахаро-трис-Glu-фолат (EC0492) выделяли после лиофилизации в течение 48 ч (22 мг, 60%). Данные 1H ЯМР соответствовали желаемой структуре конъюгата фолата. C122H176N24O50S2; мол. масса 2842,97; точное значение массы: 2841,14.
Пример. EC0493 (конъюгат тетра-сахаро-трис-Glu-фолат-винбластин). В полипропиленовой емкости для центрифугирования фолат-содержащий линкер (EC0477, 25 мг, 0,015 ммоль) растворяли в 1,5 мл воды и барботировали аргон в течение 10 мин. В другом сосуде барботировали аргон в течение 10 минут через 0,1N раствор NaHCO3. pH раствора линкера осторожно повышали до 6,9, используя 0,1N раствор NaHCO3. К полученному раствору добавляли винбластин пиридинил дисульфид (20 мг, 0,020 ммоль) в 1,5 мл тетрагидрофурана (ТГФ). Полученный прозрачный раствор перемешивали в атмосфере аргона в течение 30 мин. За ходом реакции следили с помощью аналитической ВЭЖХ (10 мМ ацетат аммония, pH=7,0 и ацетонитрил). ТГФ удаляли при пониженном давлении, водный раствор фильтровали и вводили в колонку для препаративной ВЭЖХ (колонка X-terra C18, 19×300 мм). Элюирование 1 мМ фосфатом натрия pH=7,0 и ацетонитрилом позволяло получить фракции, содержащие чистый продукт. Конъюгат винбластин-тетра-сахаро-трис-Glu-фолат (EC0493) выделяли после лиофилизации в течение 48 ч (23 мг, 61%). Данные 1H ЯМР соответствовали желаемой структуре конъюгата фолата. C107H147N21O45S2; мол. масса 2511,56; точное значение массы: 2509,93.
Пример. EC0429. Соединение этого примера, включающее гидрофильный олигоамидный спейсер, представляющий собой аминоэтилпиперазинилацетамид Asp-Asp-Cys, получали по методике, описанной в настоящей заявке.
Следующие иллюстративные примеры глюкуронид-содержащих соединений, а именно EC0400 и EC0423, где группу, включающую сахарид, иллюстративно вводили с применением “click chemistry”, также получали, как описано в настоящей заявке.
Следующие иллюстративные примеры соединений с ПЭГ-спейсером, а именно EC0367 и EC0409, также получали, как описано в настоящем изобретении.
Следующие иллюстративные примеры соединений, включающие фрагменты алкилового эфира серной кислоты, а именно EC0418 и EC0428, где фрагмент серной кислоты иллюстративно введен с помощью “click chemistry”, получали, как описано в настоящей заявке.
Следующие иллюстративные примеры дополнительных соединений, включающих олигоамидный спейсер, где олигоамид включает производное EDTE, получали, как описано в настоящей заявке.
EC0396 Конъюгат DAVLBH
Следующие иллюстративные примеры соединений, включающих β-алкилгликозиды 2-дезоксигексапиранозы, и соединений с линкером ПЭГ могут быть получены, как описано в настоящей заявке, с применением “click chemistry” для прикрепления гидрофильных групп на спейсеры линкера.
конъюгат DAVLBH, включающий β-алкил 2-дезоксиглюкозу
конъюгат DAVLBH, включающий β-алкил 2-дезоксиглюкуронид
конъюгат DAVLBH, включающий ПЭГ
конъюгат DAVLBH, включающий β-алкил маннопиранозид
Сравнительный пример конъюгата тубулизина. EC0305, не содержащий гидрофильных спейсеров в линкере. EC89 (86 мг) смешивали с деионизованной водой (4,0 мл, перед использованием барботировали аргон в течение 10 минут) и pH суспензии доводили примерно до 6,9 (суспензия переходила в раствор после повышения pH) добавлением насыщенного раствора NaHCO3 (перед использованием барботировали аргон в течение 10 минут). К раствору добавляли дополнительное количество деионизованной воды, чтобы довести общий объем до 5,0 мл, и к полученному водному раствору немедленно добавляли раствор EC0312 (97 мг) в ТГФ (5,0 мл). Реакционная смесь быстро становилась гомогенной. После перемешивания в атмосфере аргона в течение 45 минут реакционную смесь разбавляли 2,0 мМ натрий-фосфатным буфером (pH 7,0, 15 мл) и удаляли ТГФ на роторном испарителе Rotavapor. Полученную суспензию фильтровали и фильтрат вводили в препаративную колонку ВЭЖХ для очистки (колонка: Waters XTerra Prep MS C18 10 мкм 19×250 мм; подвижная фаза A: 2,0 мМ натрий-фосфатный буфер pH 7,0; подвижная фаза B: ацетонитрил; методика: 5% B до 80% B в течение 25 мин, скорость потока 25 мл/мин). Фракции 10.04-11.90 минут собирали и лиофилизовали, получая EC0305 в виде бледно-желтого рыхлого твердого вещества (117 мг).
Пример. Общая методика 2 для получения конъюгатов, включающих гидрофильный спейсер линкера (в одном сосуде). Методика показана на примере получения EC0543. DIPEA (7,8 мкл) и изобутилхлорформиат (3,1 мкл) совместно добавляли с помощью шприца в раствор тубулизина A (18 мг) в безводном EtOAc (0,50 мл) при -15°C. После перемешивания в течение 35 минут при -15°C в атмосфере аргона, к реакционной смеси добавляли раствор EC0311 (5,8 мг) в безводном EtOAc (0,50 мл). Прекращали охлаждение и реакционную смесь перемешивали в атмосфере аргона в течение еще 45 минут, концентрировали, выдерживали в вакууме и остаток растворяли в ТГФ (2,0 мл). Тем временем растворяли EC0488 (40 мг) в деионизованной воде (перед использованием барботировали аргон в течение 10 минут) и pH водного раствора доводили до 6,9 добавлением насыщенного раствора NaHCO3. К раствору EC0488 добавляли дополнительное количество деионизованной воды, чтобы получить общий объем 2,0 мл, и к полученному раствору немедленно добавляли раствор, содержащий активированный тубулизин в ТГФ. Реакционную смесь, которая быстро становилась гомогенной, перемешивали в атмосфере аргона в течение 50 минут и гасили 2,0 мМ натрий-фосфатным буфером (pH 7,0, 15 мл). Полученный мутный раствор фильтровали и фильтрат вводили в препаративную ВЭЖХ-колонку для очистки. Колонка: Waters XTerra Prep MS C18 10 мкм 19×250 мм; подвижная фаза A: 2,0 мМ натрий-фосфатный буфер pH 7,0; подвижная фаза B: ацетонитрил; методика: 1% B в течение 5 мин, затем 1% B до 60% B в течение следующих 30 мин, скорость потока=26 мл/мин. Фракции 20.75-24.50 минут собирали и лиофилизовали, получая EC0543 в виде бледно-желтого рыхлого твердого вещества (26 мг). Описанная выше методика применима также для получения конъюгатов других тубулизинов при соответствующем выборе исходного тубулизина.
Следующие дополнительные иллюстративные примеры конъюгатов тубулизина, включающих гидрофильный спейсер линкера, получали с применением методик и синтезов, описанных в настоящей заявке, исходя из тубулизина.
EC0436 конъюгат тубулизина
EC0444 конъюгат тубулизина
EC0530 конъюгат тубулизина
EC0531 конъюгат тубулизина
EC0533 конъюгат тубулизина
Приведенные ниже примеры конъюгатов также получали, как описано в настоящем изобретении.
EC0262 Конъюгат криптофицин-карбонат-CH2CH2-SS-Cys-сахаро-Asp-сахаро-Asp-сахаро-фолат. C87H115Cl2N15O38S2; мол. масса 2113,96; точное значение массы: 2111,63.
EC0278
Сравнительные примеры конъюгатов бортезомиба. Приведенные ниже сравнительные примеры конъюгатов бортезомиба (Velcade) (EC0522 и EC0587), в которых отсутствуют гидрофильные спейсеры линкера, также получали, как описано в настоящей заявке и опубликованной заявке на патент США № 2005/0002942.
EC0522 C56H69BN18O17S2 C, 50,15; H, 5,19; B, 0,81; N, 18,80; O, 20,28; S, 4,78; мол. масса 1341,20; точное значение массы: 1340,46.
EC0587 C77H90B2N20O23S4; мол. масса 1813,55; точное значение массы: 1812,56.
Следующие примеры конъюгатов бортезомиба, включающих гидрофильные спейсеры линкера, также получали, как описано в настоящем изобретении.
EC0525 Конъюгат бортезомиба (Velcade). C85H119BN20O36S2; мол. масса 2071,91; точное значение массы: 2070,76. Не ограничиваясь конкретной теорией, полагают, что в конъюгатах бортезомиба бороновая кислота и линкер могут участвовать во внутримолекулярном взаимодействии с боковыми цепями углеводов. В качестве иллюстрации, бороновая кислота образует комплексы на основе формирования сложных эфиров бороновой кислоты с одной или двумя гидроксильными группами. Такие сложноэфирные комплексы могут образовываться с вицинальными гидроксилами, а также с 1,3-гидроксилами. Подразумевается, что сложноэфирные комплексы бороновой кислоты могут формироваться в конце углеводного фрагмента или же в средней части углеводного фрагмента. Далее подразумевается, что в водном растворе сложноэфирные комплексы бороновой кислоты могут существовать в равновесии с самой бороновой кислотой.
EC0525 (гидратированный) C85H119BN20O36S2; мол. масса 2071,91; точное значение массы: 2070,76. EC0525 (координированный) C85H123BN20O38S2; мол. масса 2107,94; точное значение массы: 2106,78.
EC0595 бис-бортезомиб конъюгат. C108H145B2N25O39S4; мол. масса 2567,34; точное значение массы: 2565,92.
Сравнительный пример конъюгата α-амантина. Приведенный ниже сравнительный пример конъюгата α-амантина, в котором отсутствуют гидрофильные спейсеры линкера, также получали, как описано в настоящей заявке и опубликованной заявке на патент США № 2005/0002942.
EC0323 не вступал в конкуренцию с фолиевой кислотой и демонстрировал одинаковые значения IC50 в присутствии и в отсутствие избытка фолиевой кислоты.
Следующие примеры конъюгатов α-амантина, включающих гидрофильные спейсеры линкера, также получали, как описано в настоящей заявке.
EC0592 Конъюгат α-амантина. C107H154N26O50S3; мол. масса: 2700,71; точное значение массы: 2698,95. EC0592 продемонстрировал IC50 ~3 нМ, причем конъюгат может конкурировать с избытком фолиевой кислоты в отношении клеток KB в анализе по включению 3H-тимидина.
Приведенные ниже примеры иллюстративных конъюгатов получали, как описано в настоящей заявке.
EC0535 конъюгат гелданомицина. C95H139N19O42S2, мол. масса: 2283,35, точное значение массы: 2281,88.
EC0568 конъюгат гелданомицина. C99H146N20O44S2, мол. масса: 2384,46, точное значение массы: 2382,92.
EC0539 конъюгат, включающий лизиновый аналог аминоптерина
EC0544 конъюгат, включающий цистеиновый аналог аминоптерина. C83H116N24O37S2; C, 47,33; H, 5,55; N 15,96; O 28,11; S 3,05; мол. масса: 2106,08, точное значение массы: 2104,74.
EC0551 конъюгат аминоптерина. C86H120N24O39S2; C, 47,42; H, 5,55; N 15,43; O 28,65; S 2,94; мол. масса: 2178,14, точное значение массы: 2176,76.
EC0543 конъюгат тубулизина A. C111H167N23O45S3; C, 50,50; H, 6,38; N 12,20; O 27,27; S 3,64; мол. масса: 2639,84, m/z 2639,07 (100,0%), 2638,06 (80,8%), 2640,07 (79,6%).
EC0545 конъюгат пурваланола. C87H125ClN22O37S2; мол. масса: 2170,63, точное значение массы: 2168,77.
EC0565 конъюгат эверолимуса. C121H183N17O50S2; мол. масса: 2739,96, точное значение массы: 2738,17.
Конъюгат DAVLBH
EC0400 конъюгат DAVLBH. Получен циклизацией Huisgen из соответствующего алкина и азидоэтилуглевода; 2 экв. аскорбата Na, 1 экв. CuSO4·5H2O, ТГФ/вода (1:1); 5 экв. аскорбата Na, 2,5 экв. CuSO4·5H2O, ТГФ/вода (9:1); (10 мг). C81H100N18O24S2; C, 54,84; H, 5,68; N 14,21; O 21,65; S 3,62; мол. масса: 1773,90, точное значение массы: 1772,66.
Конъюгат DAVLBH. Получен из EC0419. C82H97N17O21S2; мол. масса: 1720,88, точное значение массы: 1719,65 (90 мг).
EC0423 конъюгат DAVLBH. Получен циклизацией Huisgen; C98H123N23O35S2; C, 52,38; H, 5,52; N 14,34; O 24,92; S 2,85; мол. масса: 2247,29, точное значение массы: 2245,80.
EC0637 конъюгат DAVLBH. C98H130N20O37S2; мол. масса: 2244,32, точное значение массы: 2242,83.
Конъюгат DAVLBH
Конъюгат DAVLBH
Конъюгат DAVLBH
EC0581 конъюгат испинесиба. C98H133ClN20O38S2; мол. масса: 2298,80, точное значение массы: 2296,82.
EC0561 конъюгат паклитаксела. C124H159N19O53S2; мол. масса: 2827,82, точное значение массы: 2825,98.
EC0594 конъюгат доцетаксела. C120H161N19O53S2; мол. масса: 2781,79, точное значение массы: 2779,99.
EC0598 конъюгат верукарина. C95H134N16O45S2; мол. масса: 2284,29, точное значение массы: 2282,81.
EC0600 конъюгат будесонида. C93H134N16O42S2; C, 50,49; H, 6,11; N, 10,13; O, 30,37; S, 2,90; мол. масса: 2212,27, точное значение массы: 2210,83.
EC0610 конъюгат дидемнина B. C125H189N23O51S2; мол. масса: 2894,09, точное значение массы: 2892,23.
EC0631 конъюгат ингибитора тирозинкиназы 4-[(3-бромфенил)амино]-6-[(2-гидроксиэтил)амино]пиридо[3,4-d]пиримидина. C83H114BrN21O37S2; мол. масса: 2141,95, точное значение массы: 2139,63.
EC0640: конъюгат 4-[(3-бромфенил)амино]-6-гидразинопиридо[3,4-d]пиримидина.
EC0663 конъюгат дазатиниба. C90H126ClN23O38S3; мол. масса: 2269,74, точное значение массы: 2267,75.
EC0593 мультилекарственное промежуточное соединение для двух лекарственных средств. C68H103N17O35S3; мол. масса: 1782,77, точное значение массы: 1781,62.
EC0613 мультилекарственное промежуточное соединение для трех лекарственных средств. C90H140N22O47S4; мол. масса: 2410,45, точное значение массы: 2408,81.
EC0542 мультилекарственное промежуточное соединение для двух лекарственных средств, с возможностью выбора селективности. C85H118N18O36S2; C, 50,24; H, 5,85; N, 12,41; O, 28,34; S, 3,16; мол. масса: 2032,08, точное значение массы: 2030,74.
EC0559 мультилекарственное промежуточное соединение для двух лекарственных средств, с возможностью выбора селективности. C90H121N19O36S3; мол. масса: 2141,22, точное значение массы: 2139,74.
EC0682 мультилекарственное промежуточное соединение для двух лекарственных средств, с возможностью выбора селективности. C95H132N20O42S2; мол. масса: 2290,30, точное значение массы: 2288,82.
EC0646 конъюгат аминоптерина и промежуточное соединение для мультилекарственного конъюгата. C106H140N26O41S3; мол. масса: 2530,59, точное значение массы: 2528,88.
EC0555 конъюгат бортезомиба (Velcade) и промежуточное соединение для мультилекарственного конъюгата. C105H139BN22O38S3; C, 52,02; H, 5,78; B, 0,45; N, 12,71; O, 25,08; S, 3,97; мол. масса: 2424,36, точное значение массы: 2422,89.
EC0606 конъюгат эверолимуса и промежуточное соединение для мультилекарственного конъюгата. C141H203N19O52S3; C, 54,76; H, 6,62; N, 8,61; O, 26,90; S, 3,11; мол. масса: 3092,42, точное значение массы: 3090,30.
EC0633 конъюгат DAVLBH и промежуточное соединение для мультилекарственного конъюгата. C131H176N24O45S3; мол. масса: 2903,13, точное значение массы: 2901,14.
EC0661 конъюгат 4-[(3-бромфенил)амино]-6-аминопиридо[3,4-d]пиримидина и промежуточное соединение для мультилекарственного конъюгата. C145H209BrN24O55S4; мол. масса: 3376,51, точное значение массы: 3373,24.
EC0679 конъюгат 4-[(3-бромфенил)амино]-6-гидразинопиридо[3,4-d]пиримидина и промежуточное соединение для мультилекарственного конъюгата. C101H131BrN24O38S3; мол. масса: 2465,36, точное значение массы: 2462,74.
EC0661 конъюгат доксорубицина и промежуточное соединение для мультилекарственного конъюгата. C115H149N19O49S3; мол. масса: 2677,71, точное значение массы: 2675,89.
EC0647 конъюгат бис-аминоптерина. C110H147N33O45S4; мол. масса: 2779,80, точное значение массы: 2777,9112, m/z: 2778,91 (100,00%), 2777,91 (74,4%), 2779,92 (62,2%).
EC0605 конъюгат бис-верукарина
EC0563 конъюгат бортезомиба и рапамицина
EC0582 конъюгат бортезомиба и эверолимуса. C147H214BN23O54S4; C, 53,40; H, 6,52; B, 0,33; N, 9,74; O, 26,13; S, 3,88; мол. масса: 3306,47, точное значение массы: 3304,37.
EC0636 конъюгат DAVLBH и эверолимуса. C173H251N25O61S4; мол. масса: 3785,23, точное значение массы: 3782,62.
EC0664 конъюгат эверолимуса и 4-[(3-бромфенил)амино]-6-аминопиридо[3,4-d]пиримидина. C145H209BrN24O55S4; мол. масса: 3376,51, точное значение массы: 3373,24.
EC0680 конъюгат эверолимуса и 4-[(3-бромфенил)амино]-6-гидразинопиридо[3,4-d]пиримидина. C143H206BrN25O54S4; мол. масса: 3347,47, точное значение массы: 3344,22.
EC0584 промежуточное соединение для возможной ненаправленной доставки. C61H91N9O31S; мол. масса: 1478,48, точное значение массы: 1477,55.
EC0634 промежуточное соединение для возможной ненаправленной доставки. C63H95N9O30S2; мол. масса: 1522,60, точное значение массы: 1521,56.
EC0586 промежуточное соединение для возможной ненаправленной доставки. C48H83N9O30S; мол. масса: 1298,28, точное значение массы: 1297,50.
EC0588 промежуточное соединение конъюгата аминоптерина для возможной ненаправленной доставки. C69H105N17O35S2; мол. масса: 1769,79, точное значение массы: 1795,64.
EC0591 промежуточное соединение конъюгата рапамицина для возможной ненаправленной доставки. C102H164N10O45S2; C, 52,93; H, 7,14; N, 6,05; O, 31,11; S, 2,77; мол. масса: 2314,57, точное значение массы: 2313,03.
Claims (38)
1. Соединение формулы
B-L-A
где В представляет собой один или несколько связывающихся с рецептором на поверхности клетки лигандов, которые связываются с рецептором на поверхности целевой клетки, L представляет собой поливалентный линкер, который включает один или несколько гидрофильных спейсеров линкера, выбранных из:
, или , или , или их сочетания;
где R в каждом случае независимо выбирают из Н, алкила, циклоалкила или арилалкила; m в каждом случае независимо представляет собой целое число от 1 до примерно 3; n1 в каждом случае независимо представляет собой целое число от 2 до примерно 6; n2 в каждом случае независимо представляет собой целое число от 1 до примерно 6; n3 в каждом случае независимо представляет собой целое число от 1 до примерно 6; р в каждом случае независимо является целым числом от 1 до примерно 5;
и А представляет собой одно или несколько диагностических, терапевтических средств или средств визуализации, которые желательно доставить к клетке.
B-L-A
где В представляет собой один или несколько связывающихся с рецептором на поверхности клетки лигандов, которые связываются с рецептором на поверхности целевой клетки, L представляет собой поливалентный линкер, который включает один или несколько гидрофильных спейсеров линкера, выбранных из:
, или , или , или их сочетания;
где R в каждом случае независимо выбирают из Н, алкила, циклоалкила или арилалкила; m в каждом случае независимо представляет собой целое число от 1 до примерно 3; n1 в каждом случае независимо представляет собой целое число от 2 до примерно 6; n2 в каждом случае независимо представляет собой целое число от 1 до примерно 6; n3 в каждом случае независимо представляет собой целое число от 1 до примерно 6; р в каждом случае независимо является целым числом от 1 до примерно 5;
и А представляет собой одно или несколько диагностических, терапевтических средств или средств визуализации, которые желательно доставить к клетке.
2. Соединение по п.1, где по меньшей мере одно средство А является терапевтическим средством.
3. Соединение по п.1, где по меньшей мере одно средство средство А представляет собой терапевтическое средство для лечения рака.
4. Соединение по п.1, где А представляет собой множество терапевтических средств для лечения рака.
5. Соединение по п.1, где связывающий лиганд В представляет собой лиганд, связывающий рецептор фолата.
6. Соединение по п.1, где связывающий лиганд В представляет собой фолат.
7. Соединение по любому из пп.1-6, в котором линкер L содержит по меньшей мере три полигидроксильные группы.
8. Соединение по любому из пп.1-6, в котором по меньшей мере один из гидрофильных спейсеров линкера образован в основном атомами углерода, водорода и кислорода и соотношение углерод/кислород составляет примерно 3:1 или менее.
9. Соединение по любому из пп.1-6, в котором по меньшей мере один из гидрофильных спейсеров линкера образован преимущественно атомами углерода, водорода и азота и соотношение углерод/азот составляет примерно 3:1 или менее.
10. Соединение по п.7, в котором линкер L дополнительно содержит один или несколько остатков аспарагиновой кислоты, один или несколько остатков глутаминовой кислоты, один или несколько остатков аргинина или один или несколько остатков аминоаланина, или их комбинацию.
11. Соединение по п.7, в котором линкер L дополнительно содержит один или несколько остатков бета-аминоаланина.
12. Соединение по п.7, в котором линкер L дополнительно содержит один или несколько двухвалентных остатков 1,4-пиперазина, где по меньшей мере часть остатков 1,4-пиперазина входит в цепь атомов, соединяющих по меньшей мере один из связывающих лигандов (В) и по меньшей мере одно из средств (А).
13. Соединение по п.7, где линкер L дополнительно содержит по меньшей мере один остаток аргинина.
14. Соединение по любому из пп.1-6, в котором линкер L дополнительно содержит один или несколько фрагментов, представляющих собой полигидроксильные группы, связанные остатками триазола.
15. Соединение по любому из пп.1-6, в котором линкер L дополнительно содержит один или несколько фрагментов, представляющих собой полигидроксильные группы, связанные амидными связями.
16. Соединение по любому из пп.1-6, где линкер L дополнительно содержит одно или несколько производных EDTA.
17. Соединение по любому из пп.1-6, в котором линкер L дополнительно содержит фрагмент формулы, выбранной из группы, состоящей из
где m представляет собой целое число, независимо выбранное в каждом случае из чисел от 1 до примерно 8; р означает целое число, выбранное в каждом случае из чисел от 1 до примерно 10; и n означает целое число, независимо выбранное в каждом случае из чисел от 1 до примерно 3.
где m представляет собой целое число, независимо выбранное в каждом случае из чисел от 1 до примерно 8; р означает целое число, выбранное в каждом случае из чисел от 1 до примерно 10; и n означает целое число, независимо выбранное в каждом случае из чисел от 1 до примерно 3.
18. Соединение по любому из пп.1-6, в котором линкер L включает одну или несколько групп формулы, выбранных из группы, состоящей из:
где m представляет собой целое число, независимо выбранное в каждом случае из чисел от 1 до примерно 3; и r означает целое число, выбранное из чисел от 1 до примерно 3.
где m представляет собой целое число, независимо выбранное в каждом случае из чисел от 1 до примерно 3; и r означает целое число, выбранное из чисел от 1 до примерно 3.
21. Соединение по любому из пп.1-6, в котором линкер L дополнительно содержит один или более фрагментов, отображаемых формулами, выбранными из группы, состоящей из
где n означает целое число, независимо выбранное в каждом случае из чисел от 2 до примерно 5; р означает целое число, выбранное из чисел от 1 до 5; и r означает целое число, независимо выбранное в каждом случае из чисел от 1 до примерно 4; при условии что n меньше или равно r+1.
где n означает целое число, независимо выбранное в каждом случае из чисел от 2 до примерно 5; р означает целое число, выбранное из чисел от 1 до 5; и r означает целое число, независимо выбранное в каждом случае из чисел от 1 до примерно 4; при условии что n меньше или равно r+1.
25. Соединение по любому из пп.1-6, в котором линкер L дополнительно содержит один или более фрагментов, отображаемых формулами, выбранными из группы, состоящей из
где n и r являются целыми числами и каждый из них в каждом случае независимо выбран из чисел от 1 до примерно 5; и р является целым числом, выбранным в каждом случае из чисел от 1 до примерно 4.
где n и r являются целыми числами и каждый из них в каждом случае независимо выбран из чисел от 1 до примерно 5; и р является целым числом, выбранным в каждом случае из чисел от 1 до примерно 4.
26. Соединение по любому из пп.1-6, в котором линкер L дополнительно содержит один или более фрагментов, отображаемых формулами, выбранными из группы, состоящей из
где n является целым числом, выбранным в каждом случае из чисел от 1 до примерно 3, и m является целым числом, выбранным из чисел от 1 до примерно 22.
где n является целым числом, выбранным в каждом случае из чисел от 1 до примерно 3, и m является целым числом, выбранным из чисел от 1 до примерно 22.
27. Соединение по любому из пп.1-6, в котором линкер L дополнительно содержит один или более фрагментов, отображаемых формулами, выбранными из группы, состоящей из
где n и r являются целыми числами и каждый из них в каждом случае независимо выбран из чисел от 1 до примерно 5; и р является целым числом, выбранным из чисел от 1 до примерно 4.
где n и r являются целыми числами и каждый из них в каждом случае независимо выбран из чисел от 1 до примерно 5; и р является целым числом, выбранным из чисел от 1 до примерно 4.
30. Соединение по любому из пп.1-6, в котором линкер L дополнительно содержит один или более фрагментов, отображаемых формулами, выбранными из группы, состоящей из
где n1 и n2 представляют собой целые числа, независимо выбранные в каждом случае из чисел от 0 до примерно 3; при условии, что n1 и n2 одновременно не равны 0; и n3 представляет собой целое число, независимо выбранное в каждом случае из чисел от 1 до примерно 3.
где n1 и n2 представляют собой целые числа, независимо выбранные в каждом случае из чисел от 0 до примерно 3; при условии, что n1 и n2 одновременно не равны 0; и n3 представляет собой целое число, независимо выбранное в каждом случае из чисел от 1 до примерно 3.
33. Соединение по любому из пп.1-6, в котором линкер L дополнительно включает один или несколько расщепляемых линкеров.
34. Соединение по любому из пп.1-6, в котором линкер L дополнительно содержит один или несколько дисульфидных расщепляемых линкеров.
37. Фармацевтическая композиция, предназначенная для направленной доставки одного или более диагностических средств, терапевтических средства или средств визуализации к клетке, которая экспрессирует или избыточно экспрессирует рецептор на поверхности клетки, содержащая терапевтически эффективное количество одного или нескольких соединений по любому из пп.1-6 и необязательно носитель, разбавитель и/или наполнитель для этих соединений или их комбинацию.
38. Применение соединения по любому из пп.1-6 или фармацевтической композиции, содержащей это соединение, для визуализации, лечения или диагностики заболевания или состояния или их комбинации, где визуализация, лечение или диагностика или их комбинация включают нацеливание на клетки, которые экспрессируют или избыточно экспрессируют рецептор на поверхности клетки, способный связываться с по меньшей мере одним связывающимся с рецептором лигандом В.
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US94609207P | 2007-06-25 | 2007-06-25 | |
| US60/946,092 | 2007-06-25 | ||
| US3618608P | 2008-03-13 | 2008-03-13 | |
| US61/036,186 | 2008-03-13 | ||
| PCT/US2008/068093 WO2009002993A1 (en) | 2007-06-25 | 2008-06-25 | Conjugates containing hydrophilic spacer linkers |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2010102044A RU2010102044A (ru) | 2011-08-20 |
| RU2523909C2 true RU2523909C2 (ru) | 2014-07-27 |
Family
ID=40186017
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2010102044/04A RU2523909C2 (ru) | 2007-06-25 | 2008-06-25 | Конъюгаты, содержащие гидрофильные спейсеры линкеров |
Country Status (12)
| Country | Link |
|---|---|
| US (5) | US9138484B2 (ru) |
| EP (2) | EP3569251A1 (ru) |
| JP (1) | JP5690589B2 (ru) |
| CN (2) | CN104383553A (ru) |
| AU (1) | AU2008268432B2 (ru) |
| BR (1) | BRPI0812970A2 (ru) |
| CA (1) | CA2690943A1 (ru) |
| ES (1) | ES2732879T3 (ru) |
| HK (1) | HK1207980A1 (ru) |
| IL (2) | IL202796A (ru) |
| RU (1) | RU2523909C2 (ru) |
| WO (1) | WO2009002993A1 (ru) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2816717C2 (ru) * | 2018-09-06 | 2024-04-03 | Сидара Терапьютикс, Инк. | Композиции и способы для лечения вирусных инфекций |
Families Citing this family (110)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2002087424A2 (en) | 2001-05-02 | 2002-11-07 | Purdue Research Foundation | Treatment and diagnosis of macrophage mediated disease |
| US8043602B2 (en) | 2002-02-07 | 2011-10-25 | Endocyte, Inc. | Folate targeted enhanced tumor and folate receptor positive tissue optical imaging technology |
| US8043603B2 (en) | 2002-02-07 | 2011-10-25 | Endocyte, Inc. | Folate targeted enhanced tumor and folate receptor positive tissue optical imaging technology |
| JP5576007B2 (ja) | 2003-01-27 | 2014-08-20 | エンドサイト・インコーポレイテッド | ビタミン受容体結合性薬剤送達結合体 |
| ES2317010T3 (es) | 2003-05-30 | 2009-04-16 | Purdue Research Foundation | Metodo de diagnostico de la arterosclerosis. |
| EP2316857A1 (en) | 2004-02-12 | 2011-05-04 | Morphotek, Inc. | Monoclonal antibodies that specifically bind to folate receptor alpha |
| US8288557B2 (en) | 2004-07-23 | 2012-10-16 | Endocyte, Inc. | Bivalent linkers and conjugates thereof |
| JP2009521206A (ja) | 2005-04-22 | 2009-06-04 | モルフォテック、インク. | 免疫エフェクター活性を有する葉酸受容体アルファ陽性細胞に内部移行する抗体 |
| JP5175723B2 (ja) | 2005-07-05 | 2013-04-03 | パーデュー・リサーチ・ファウンデーション | 単球介在性疾患を治療するための組成物の調製 |
| EP1940473A2 (en) | 2005-09-23 | 2008-07-09 | Purdue Research Foundation | Multiphoton in vivo flow cytometry method and device |
| JP2010509570A (ja) | 2006-11-03 | 2010-03-25 | パーデュー・リサーチ・ファウンデーション | エクスビボフローサイトメトリーの方法および装置 |
| WO2008098112A2 (en) | 2007-02-07 | 2008-08-14 | Purdue Research Foundation | Positron emission tomography imaging method |
| US20100104626A1 (en) | 2007-02-16 | 2010-04-29 | Endocyte, Inc. | Methods and compositions for treating and diagnosing kidney disease |
| US9555139B2 (en) | 2007-03-14 | 2017-01-31 | Endocyte, Inc. | Binding ligand linked drug delivery conjugates of tubulysins |
| EP2164525A2 (en) | 2007-05-25 | 2010-03-24 | Purdue Research Foundation | Method of imaging localized infections |
| US9138484B2 (en) | 2007-06-25 | 2015-09-22 | Endocyte, Inc. | Conjugates containing hydrophilic spacer linkers |
| US9877965B2 (en) | 2007-06-25 | 2018-01-30 | Endocyte, Inc. | Vitamin receptor drug delivery conjugates for treating inflammation |
| SI2187965T1 (sl) | 2007-08-17 | 2020-03-31 | Purdue Research Foundation Office Of Technology Commercialization | Konjugati vezalca ligand-veznika PSMA in metode za uporabo |
| US9187521B2 (en) | 2007-10-25 | 2015-11-17 | Endocyte, Inc. | Tubulysins and processes for preparing |
| NZ592255A (en) | 2008-09-17 | 2013-07-26 | Endocyte Inc | Folate receptor binding conjugates of antifolates |
| US20120022245A1 (en) * | 2008-10-17 | 2012-01-26 | Purdue Research Foundation | Folate targeting of nucleotides |
| FR2947269B1 (fr) | 2009-06-29 | 2013-01-18 | Sanofi Aventis | Nouveaux composes anticancereux |
| JP2013501224A (ja) * | 2009-07-31 | 2013-01-10 | エンドサイト,インク. | 葉酸を標的とした診断及び処置 |
| US8394922B2 (en) | 2009-08-03 | 2013-03-12 | Medarex, Inc. | Antiproliferative compounds, conjugates thereof, methods therefor, and uses thereof |
| US20120258905A1 (en) * | 2009-12-23 | 2012-10-11 | Endocyte, Inc. | Vitamin receptor drug delivery conjugates for treating inflammation |
| IL290617B2 (en) | 2010-02-24 | 2023-11-01 | Immunogen Inc | Folate receptor 1 antibodies and immunoconjugates and uses thereof |
| US9951324B2 (en) | 2010-02-25 | 2018-04-24 | Purdue Research Foundation | PSMA binding ligand-linker conjugates and methods for using |
| EP2571362A4 (en) * | 2010-05-19 | 2014-01-22 | Endocyte Inc | IMPROVED PROCESS FOR A FOLATE-TARGETED AGENT |
| CA2812543A1 (en) * | 2010-09-27 | 2012-04-12 | Endocyte, Inc. | Folate conjugates for treating inflammation of the eye |
| CN102008732B (zh) * | 2010-11-08 | 2012-10-24 | 武汉华耀生物医药有限公司 | 一种叶酸偶联抗体药物及其制备方法与应用 |
| SG190245A1 (en) | 2010-11-12 | 2013-06-28 | Endocyte Inc | Methods of treating cancer |
| TR201802659T4 (tr) | 2011-04-01 | 2018-03-21 | Immunogen Inc | Folr1 kanser terapisinin etkinliğini arttırmak için yöntemler. |
| MX2013014583A (es) | 2011-06-10 | 2014-03-31 | Mersana Therapeutics Inc | Conjugados de proteina-polimero-farmaco. |
| US9034829B1 (en) | 2011-10-27 | 2015-05-19 | Northwestern University | pH-sensitive polymer-drug conjugates for targeted delivery of therapeutics |
| WO2013126797A1 (en) | 2012-02-24 | 2013-08-29 | Purdue Research Foundation | Cholecystokinin b receptor targeting for imaging and therapy |
| US9629918B2 (en) | 2012-02-29 | 2017-04-25 | Purdue Research Foundation | Folate receptor alpha binding ligands |
| US20140080175A1 (en) | 2012-03-29 | 2014-03-20 | Endocyte, Inc. | Processes for preparing tubulysin derivatives and conjugates thereof |
| US8940742B2 (en) | 2012-04-10 | 2015-01-27 | Infinity Pharmaceuticals, Inc. | Heterocyclic compounds and uses thereof |
| US9504756B2 (en) | 2012-05-15 | 2016-11-29 | Seattle Genetics, Inc. | Self-stabilizing linker conjugates |
| CN104640572B (zh) * | 2012-05-15 | 2018-04-27 | 索伦托医疗有限公司 | 药物偶联物,偶联方法,及其用途 |
| CA3062003C (en) | 2012-05-17 | 2022-01-11 | Extend Biosciences, Inc. | Vitamin d as a targeting group for therapeutic peptides |
| DK2872157T3 (da) | 2012-07-12 | 2020-03-30 | Hangzhou Dac Biotech Co Ltd | Konjugater af cellbindende molekyler med cytotoxiske midler |
| KR20200079565A (ko) | 2012-08-31 | 2020-07-03 | 이뮤노젠 아이엔씨 | 엽산 수용체 1의 검출을 위한 진단성 검정 및 키트 |
| EP2908818A4 (en) * | 2012-10-16 | 2016-07-13 | Endocyte Inc | CONJUGATES OF DRUG DELIVERY CONTAINING ARTIFICIAL AMINO ACIDS AND METHODS OF USE |
| EP2919774A4 (en) | 2012-11-15 | 2016-11-09 | Endocyte Inc | CONJUGATES FOR THE TREATMENT OF DISEASES CAUSED BY PSMA-EXPRESSING CELLS |
| CN105849086B (zh) * | 2012-11-24 | 2018-07-31 | 杭州多禧生物科技有限公司 | 亲水性链接体及其在药物分子和细胞结合分子共轭反应上的应用 |
| US20140154702A1 (en) * | 2012-11-30 | 2014-06-05 | Endocyte, Inc. | Methods For Treating Cancer Using Combination Therapies |
| EP2928504B1 (en) | 2012-12-10 | 2019-02-20 | Mersana Therapeutics, Inc. | Protein-polymer-drug conjugates |
| EP2931316B1 (en) | 2012-12-12 | 2019-02-20 | Mersana Therapeutics, Inc. | Hydroxyl-polymer-drug-protein conjugates |
| US20150314007A1 (en) * | 2012-12-21 | 2015-11-05 | Glykos Finland Oy | Linker-payload molecule conjugates |
| DK2956173T3 (en) | 2013-02-14 | 2017-07-17 | Bristol Myers Squibb Co | TUBULYSIS RELATIONSHIPS, METHODS OF PRODUCING AND USING THEREOF |
| EP2958591A4 (en) * | 2013-02-19 | 2016-11-23 | Brigham & Womens Hospital | METHODS AND COMPOSITIONS RELATED TO THE TREATMENT OF CANCER |
| JP2016514157A (ja) * | 2013-03-14 | 2016-05-19 | アルバニー モレキュラー リサーチ, インコーポレイテッド | リガンド−治療薬コンジュゲートおよびケイ素ベースのリンカー |
| CA2921975C (en) | 2013-08-30 | 2024-02-13 | Immunogen, Inc. | Antibodies and assays for detection of folate receptor 1 |
| WO2015051241A1 (en) | 2013-10-04 | 2015-04-09 | Infinity Pharmaceuticals, Inc. | Heterocyclic compounds and uses thereof |
| NZ718430A (en) | 2013-10-04 | 2021-12-24 | Infinity Pharmaceuticals Inc | Heterocyclic compounds and uses thereof |
| KR102538993B1 (ko) | 2013-10-15 | 2023-06-02 | 씨젠 인크. | 개선된 리간드-약물 컨쥬게이트 약물동력학을 위한 peg화된 약물-링커 |
| MY194484A (en) | 2013-10-18 | 2022-11-30 | Deutsches Krebsforsch | Labeled Inhibitors of Prostate Specific Membrane Antigen (PSMA), Their use as Imaging Agents and Pharmaceutical Agents for the Treatment of Prostate Cancer |
| CN105849568B (zh) | 2013-11-14 | 2018-05-04 | 恩多塞特公司 | 用于正电子发射断层术的化合物 |
| ES2860173T3 (es) | 2013-11-19 | 2021-10-04 | Purdue Research Foundation | Método de selección de pacientes para inflamación |
| CN114262344A (zh) * | 2014-02-28 | 2022-04-01 | 杭州多禧生物科技有限公司 | 带电荷链接体及其在共轭反应上的应用 |
| CA2943075C (en) | 2014-03-19 | 2023-02-28 | Infinity Pharmaceuticals, Inc. | Heterocyclic compounds for use in the treatment of pi3k-gamma mediated disorders |
| CA2945367A1 (en) * | 2014-04-14 | 2015-10-22 | Endocyte, Inc. | Drug delivery conjugates for treating resistant cancer and for use in combination therapy |
| ES2785551T3 (es) | 2014-06-30 | 2020-10-07 | Glykos Finland Oy | Derivado de sacárido de una carga útil tóxica y sus conjugados con anticuerpos |
| WO2016054491A1 (en) | 2014-10-03 | 2016-04-07 | Infinity Pharmaceuticals, Inc. | Heterocyclic compounds and uses thereof |
| CA2964463C (en) | 2014-10-22 | 2024-02-13 | Extend Biosciences, Inc. | Therapeutic vitamin d conjugates |
| US9616109B2 (en) | 2014-10-22 | 2017-04-11 | Extend Biosciences, Inc. | Insulin vitamin D conjugates |
| US9789197B2 (en) | 2014-10-22 | 2017-10-17 | Extend Biosciences, Inc. | RNAi vitamin D conjugates |
| US10077287B2 (en) | 2014-11-10 | 2018-09-18 | Bristol-Myers Squibb Company | Tubulysin analogs and methods of making and use |
| US10188759B2 (en) | 2015-01-07 | 2019-01-29 | Endocyte, Inc. | Conjugates for imaging |
| WO2016148674A1 (en) * | 2015-03-13 | 2016-09-22 | Endocyte, Inc. | Conjugates for treating diseases |
| EP3069734A1 (en) * | 2015-03-17 | 2016-09-21 | Exiris S.r.l. | Cryptophycin-based antibody-drug conjugates with novel self-immolative linkers |
| CA2984169A1 (en) * | 2015-05-01 | 2016-11-10 | Endocyte, Inc. | Antifolate conjugates for treating inflammation |
| US10406238B2 (en) | 2015-05-11 | 2019-09-10 | Purdue Research Foundation | Ligand ionophore conjugates |
| CA2989269C (en) * | 2015-06-15 | 2020-09-22 | Robert Yongxin Zhao | Hydrophilic linkers for conjugation of a cytotoxic agent or chromophore molecule to a cell-binding molecule |
| JP6759326B2 (ja) | 2015-07-12 | 2020-09-23 | ハンジョウ ディーエーシー バイオテック シーオー.,エルティディ.Hangzhou Dac Biotech Co.,Ltd. | 細胞結合分子の共役のための架橋連結体 |
| US9839687B2 (en) | 2015-07-15 | 2017-12-12 | Suzhou M-Conj Biotech Co., Ltd. | Acetylenedicarboxyl linkers and their uses in specific conjugation of a cell-binding molecule |
| US10676487B2 (en) * | 2015-09-09 | 2020-06-09 | On Target Laboratories, LLC | Synthesis and composition of photodynamic therapeutic agents for the targeted treatment of cancer |
| KR20180058741A (ko) | 2015-09-14 | 2018-06-01 | 인피니티 파마슈티칼스, 인코포레이티드 | 이소퀴놀리논의 고체형, 그의 제조 방법, 이를 포함하는 조성물 및 이를 사용하는 방법 |
| WO2017049149A1 (en) | 2015-09-17 | 2017-03-23 | Immunogen, Inc. | Therapeutic combinations comprising anti-folr1 immunoconjugates |
| CN108367043A (zh) | 2015-12-04 | 2018-08-03 | 西雅图基因公司 | 季铵化的微管溶素化合物的缀合物 |
| US11793880B2 (en) | 2015-12-04 | 2023-10-24 | Seagen Inc. | Conjugates of quaternized tubulysin compounds |
| JP2019515880A (ja) | 2016-03-16 | 2019-06-13 | エンドサイト・インコーポレイテッドEndocyte, Inc. | 炭酸無水酵素ix阻害剤抱合体およびその使用 |
| JP7027325B2 (ja) * | 2016-03-16 | 2022-03-01 | パーデュー・リサーチ・ファウンデイション | 炭酸無水酵素ixを標的とする薬剤および方法 |
| WO2017161116A1 (en) | 2016-03-17 | 2017-09-21 | Infinity Pharmaceuticals, Inc. | Isotopologues of isoquinolinone and quinazolinone compounds and uses thereof as pi3k kinase inhibitors |
| UA125510C2 (uk) | 2016-03-25 | 2022-04-13 | Сіджен Інк. | Спосіб отримання пегильованої сполуки лікарський препарат-лінкер, де лікарським препаратом є ауристатин, та її проміжних сполук |
| EP3600430A4 (en) * | 2016-03-29 | 2020-12-30 | Endocyte, Inc. | FOLATE CONJUGATE FOR USE IN TARGETING TUMOR-ASSOCIATED MACROPHAGES |
| CN107949566B (zh) * | 2016-05-10 | 2021-09-28 | 浙江海正药业股份有限公司 | 水溶性雷帕霉素类衍生物 |
| US10919914B2 (en) | 2016-06-08 | 2021-02-16 | Infinity Pharmaceuticals, Inc. | Heterocyclic compounds and uses thereof |
| WO2017219029A2 (en) | 2016-06-17 | 2017-12-21 | Magenta Therapeutics, Inc. | Compositions and methods for the depletion of cd117+cells |
| TW201808343A (zh) | 2016-08-09 | 2018-03-16 | 美商西雅圖遺傳學公司 | 具有改善之生理化學性質之具自我穩定連接子之藥物結合物 |
| IL307357A (en) | 2016-11-08 | 2023-11-01 | Regeneron Pharma | Steroids and their protein conjugates |
| CN110099682B (zh) | 2016-11-14 | 2023-03-31 | 杭州多禧生物科技有限公司 | 偶联连接体,含有此连接体的细胞结合分子-药物偶联物及其制备和应用 |
| US10576161B2 (en) | 2017-01-20 | 2020-03-03 | Magenta Therapeutics, Inc. | Compositions and methods for the depletion of CD137+ cells |
| CN106967081A (zh) * | 2017-03-17 | 2017-07-21 | 南开大学 | 一种具有化疗增敏作用的诊疗一体化药物的合成方法 |
| EP3600443A1 (en) | 2017-03-24 | 2020-02-05 | Seattle Genetics, Inc. | Process for the preparation of glucuronide drug-linkers and intermediates thereof |
| US11491237B2 (en) | 2017-05-18 | 2022-11-08 | Regeneron Pharmaceuticals, Inc. | Cyclodextrin protein drug conjugates |
| MX2020006994A (es) * | 2018-01-08 | 2020-11-06 | Regeneron Pharma | Esteroides y conjugados de anticuerpos de los mismos. |
| US11377502B2 (en) | 2018-05-09 | 2022-07-05 | Regeneron Pharmaceuticals, Inc. | Anti-MSR1 antibodies and methods of use thereof |
| CA3130693A1 (en) | 2019-02-19 | 2020-08-27 | Ultima Genomics, Inc. | Linkers and methods for optical detection and sequencing |
| BR112021025984A2 (pt) | 2019-06-29 | 2022-04-12 | Hangzhou Dac Biotech Co Ltd | Conjugado de anticorpo-derivado de tubulisina b (análogo), composto, composição farmacêutica, e, usos do conjugado, dos compostos e das composições farmacêuticas |
| AU2020309570A1 (en) * | 2019-07-10 | 2022-02-03 | Cybrexa 2, Inc. | Peptide conjugates of cytotoxins as therapeutics |
| KR20220051332A (ko) | 2019-07-10 | 2022-04-26 | 싸이브렉사 3, 인크. | 치료제로서의 미세소관 표적화제의 펩티드 접합체 |
| CN114585623A (zh) | 2019-08-02 | 2022-06-03 | 梅尔莎纳医疗公司 | 双[N-((5-氨基甲酰基)-1H-苯并[d]咪唑-2-基)吡唑-5-甲酰胺]衍生物和相关化合物作为STING(干扰素基因刺激物)激动剂用于治疗癌症 |
| JP2022549971A (ja) | 2019-09-30 | 2022-11-29 | ザ・リージェンツ・オブ・ザ・ユニバーシティ・オブ・ミシガン | クリプトフィシン抗がん剤の生体触媒合成 |
| US11807851B1 (en) | 2020-02-18 | 2023-11-07 | Ultima Genomics, Inc. | Modified polynucleotides and uses thereof |
| CN116635083A (zh) * | 2020-12-22 | 2023-08-22 | 豪夫迈·罗氏有限公司 | 用于检测样品中的目标分析物的方法 |
| EP4337663A2 (en) * | 2021-05-14 | 2024-03-20 | Purdue Research Foundation | Small molecule-based bi-specific immune cell tethers and their use in the treatment of enveloped virus infection |
| US20230277682A1 (en) * | 2022-01-14 | 2023-09-07 | Regeneron Pharmaceuticals, Inc. | Verrucarin a derivatives and antibody drug conjugates thereof |
| WO2023156510A1 (en) * | 2022-02-18 | 2023-08-24 | F. Hoffmann-La Roche Ag | Method for detecting an analyte of interest in a sample |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2006012527A1 (en) * | 2004-07-23 | 2006-02-02 | Endocyte, Inc. | Bivalent linkers and conjugates thereof |
| RU2008110495A (ru) * | 2005-08-19 | 2009-09-27 | Эндосайт, Инк. (Us) | Конъюгаты лиганда с несколькими лекарственными средствами |
Family Cites Families (235)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2515483A (en) * | 1946-08-10 | 1950-07-18 | Merck & Co Inc | Diacylated pteroic acid and process for preparing same |
| US2816110A (en) * | 1956-11-23 | 1957-12-10 | Merck & Co Inc | Methods for the production of substituted pteridines |
| US3392173A (en) * | 1964-03-09 | 1968-07-09 | Lilly Co Eli | Novel acyl derivatives of desacetyl-vincaleukoblastine and processes for their preparation |
| US3387001A (en) * | 1964-10-19 | 1968-06-04 | Lilly Co Eli | Novel aminoacyl esters of desacetyl vincaleukoblastine |
| US3641109A (en) | 1968-09-04 | 1972-02-08 | Carl D Emerson | Alkyl and aryl esters of polyhalo-dithio alcohols |
| US3632622A (en) | 1969-04-01 | 1972-01-04 | Chevron Res | Polyhaloalkylpolythioalkyl sulfite esters |
| US4203898A (en) * | 1977-08-29 | 1980-05-20 | Eli Lilly And Company | Amide derivatives of VLB, leurosidine, leurocristine and related dimeric alkaloids |
| US4166810A (en) * | 1978-04-20 | 1979-09-04 | Eli Lilly And Company | Derivatives of 4-desacetyl VLB C-3 carboxyhydrazide |
| US4337339A (en) * | 1979-04-30 | 1982-06-29 | Baker Instruments Corp. | Process for preparation of folic acid derivatives |
| US4639456A (en) | 1980-06-10 | 1987-01-27 | Omnichem S.A. | Vinblastin-23-oyl amino acid derivatives |
| US4316885A (en) | 1980-08-25 | 1982-02-23 | Ayerst, Mckenna And Harrison, Inc. | Acyl derivatives of rapamycin |
| US4713249A (en) | 1981-11-12 | 1987-12-15 | Schroeder Ulf | Crystallized carbohydrate matrix for biologically active substances, a process of preparing said matrix, and the use thereof |
| US5140104A (en) * | 1982-03-09 | 1992-08-18 | Cytogen Corporation | Amine derivatives of folic acid analogs |
| US4687808A (en) | 1982-08-12 | 1987-08-18 | Biospecific Technologies, Inc. | Activation of biocompatible polymers with biologicals whose binding complements are pathological effectors |
| JPS59175493A (ja) | 1983-03-25 | 1984-10-04 | Kyowa Hakko Kogyo Co Ltd | マイトマイシン誘導体 |
| DE3376114D1 (en) | 1982-12-07 | 1988-05-05 | Kyowa Hakko Kogyo Kk | Mitomycin analogues |
| HUT34212A (en) | 1983-04-29 | 1985-02-28 | Omnichem Sa | Process for the production of new vindblastin conjugates |
| JPS59175493U (ja) | 1983-05-12 | 1984-11-22 | 株式会社小松製作所 | レ−ザ加工装置 |
| US4866180A (en) * | 1984-02-24 | 1989-09-12 | Bristol-Myers Company | Amino disulfide thiol exchange products |
| GB8413849D0 (en) | 1984-05-31 | 1984-07-04 | Amersham Int Plc | Nmr contrast agents |
| JPS60255789A (ja) | 1984-06-01 | 1985-12-17 | Kyowa Hakko Kogyo Co Ltd | マイトマイシン誘導体,その製造法および抗腫瘍剤 |
| US5266333A (en) | 1985-03-06 | 1993-11-30 | American Cyanamid Company | Water dispersible and water soluble carbohydrate polymer compositions for parenteral administration of growth hormone |
| US4650803A (en) | 1985-12-06 | 1987-03-17 | University Of Kansas | Prodrugs of rapamycin |
| US4801688A (en) * | 1986-05-27 | 1989-01-31 | Eli Lilly And Company | Hydrazone immunoglobulin conjugates |
| IL82579A0 (en) | 1986-05-27 | 1987-11-30 | Lilly Co Eli | Immunoglobulin conjugates |
| WO1988001622A1 (en) | 1986-08-29 | 1988-03-10 | Kyowa Hakko Kogyo Kabusiki Kaisha | Mitomycin derivatives |
| US5006652A (en) * | 1988-08-08 | 1991-04-09 | Eli Lilly And Company | Intermediates for antibody-vinca drug conjugates |
| US5094849A (en) * | 1988-08-08 | 1992-03-10 | Eli Lilly And Company | Cytotoxic antibody conjugates of hydrazide derivatized vinca analogs via simple organic linkers |
| US5688488A (en) * | 1989-04-03 | 1997-11-18 | Purdue Research Foundation | Composition and method for tumor imaging |
| US5108921A (en) * | 1989-04-03 | 1992-04-28 | Purdue Research Foundation | Method for enhanced transmembrane transport of exogenous molecules |
| WO1991007418A1 (en) | 1989-11-13 | 1991-05-30 | Xoma Corporation | Chimeric mouse-human a10 antibody with specificity to a human tumor cell antigen |
| US5627165A (en) | 1990-06-13 | 1997-05-06 | Drug Innovation & Design, Inc. | Phosphorous prodrugs and therapeutic delivery systems using same |
| US5998603A (en) * | 1994-09-29 | 1999-12-07 | Isis Pharmaceuticals, Inc. | 4'-desmethyl nucleoside analogs, and oligomers thereof |
| DE69132925T2 (de) * | 1990-08-29 | 2002-10-10 | Ct Hospitalier Regional De Nan | An stabile proteinkernstruktur gebundene proteinpolyliganden |
| US5221670A (en) | 1990-09-19 | 1993-06-22 | American Home Products Corporation | Rapamycin esters |
| US5378696A (en) | 1990-09-19 | 1995-01-03 | American Home Products Corporation | Rapamycin esters |
| US5130307A (en) | 1990-09-28 | 1992-07-14 | American Home Products Corporation | Aminoesters of rapamycin |
| US5233036A (en) | 1990-10-16 | 1993-08-03 | American Home Products Corporation | Rapamycin alkoxyesters |
| US5120842A (en) | 1991-04-01 | 1992-06-09 | American Home Products Corporation | Silyl ethers of rapamycin |
| US5100883A (en) | 1991-04-08 | 1992-03-31 | American Home Products Corporation | Fluorinated esters of rapamycin |
| US5118678A (en) | 1991-04-17 | 1992-06-02 | American Home Products Corporation | Carbamates of rapamycin |
| US5194447A (en) | 1992-02-18 | 1993-03-16 | American Home Products Corporation | Sulfonylcarbamates of rapamycin |
| US5138051A (en) | 1991-08-07 | 1992-08-11 | American Home Products Corporation | Rapamycin analogs as immunosuppressants and antifungals |
| US5118677A (en) | 1991-05-20 | 1992-06-02 | American Home Products Corporation | Amide esters of rapamycin |
| US5169851A (en) | 1991-08-07 | 1992-12-08 | American Home Products Corporation | Rapamycin analog as immunosuppressants and antifungals |
| US6335434B1 (en) * | 1998-06-16 | 2002-01-01 | Isis Pharmaceuticals, Inc., | Nucleosidic and non-nucleosidic folate conjugates |
| US5151413A (en) | 1991-11-06 | 1992-09-29 | American Home Products Corporation | Rapamycin acetals as immunosuppressant and antifungal agents |
| US5159079A (en) * | 1991-12-20 | 1992-10-27 | Eli Lilly And Company | 2-piperidones as intermediates for 5-deaza-10-oxo- and 5-deaza-10-thio-5,6,7,8-tetrahydrofolic acids |
| US6004555A (en) * | 1992-03-05 | 1999-12-21 | Board Of Regents, The University Of Texas System | Methods for the specific coagulation of vasculature |
| US6022966A (en) | 1993-11-22 | 2000-02-08 | Neorx Corporation | Pretargeting methods and compounds |
| US5302584A (en) | 1992-10-13 | 1994-04-12 | American Home Products Corporation | Carbamates of rapamycin |
| US5258389A (en) | 1992-11-09 | 1993-11-02 | Merck & Co., Inc. | O-aryl, O-alkyl, O-alkenyl and O-alkynylrapamycin derivatives |
| US5260300A (en) | 1992-11-19 | 1993-11-09 | American Home Products Corporation | Rapamycin carbonate esters as immuno-suppressant agents |
| US5583020A (en) | 1992-11-24 | 1996-12-10 | Ribozyme Pharmaceuticals, Inc. | Permeability enhancers for negatively charged polynucleotides |
| US7279561B1 (en) | 1993-04-23 | 2007-10-09 | Wyeth | Anti-rapamycin monoclonal antibodies |
| AU686629B2 (en) * | 1993-04-23 | 1998-02-12 | Wyeth | Rapamycin Conjugates and Antibodies |
| US5562907A (en) | 1993-05-14 | 1996-10-08 | Arnon; Stephen S. | Method to prevent side-effects and insensitivity to the therapeutic uses of toxins |
| US5391730A (en) | 1993-10-08 | 1995-02-21 | American Home Products Corporation | Phosphorylcarbamates of rapamycin and oxime derivatives thereof |
| US5385908A (en) | 1993-11-22 | 1995-01-31 | American Home Products Corporation | Hindered esters of rapamycin |
| US5385909A (en) | 1993-11-22 | 1995-01-31 | American Home Products Corporation | Heterocyclic esters of rapamycin |
| US5385910A (en) | 1993-11-22 | 1995-01-31 | American Home Products Corporation | Gem-distributed esters of rapamycin |
| US5389639A (en) | 1993-12-29 | 1995-02-14 | American Home Products Company | Amino alkanoic esters of rapamycin |
| US5417982A (en) | 1994-02-17 | 1995-05-23 | Modi; Pankaj | Controlled release of drugs or hormones in biodegradable polymer microspheres |
| IL112873A (en) * | 1994-03-08 | 2005-03-20 | Wyeth Corp | Rapamycin-fkbp12 binding proteins, their isolation and their use |
| US6171859B1 (en) * | 1994-03-30 | 2001-01-09 | Mitokor | Method of targeting conjugate molecules to mitochondria |
| US5362718A (en) | 1994-04-18 | 1994-11-08 | American Home Products Corporation | Rapamycin hydroxyesters |
| US5463048A (en) | 1994-06-14 | 1995-10-31 | American Home Products Corporation | Rapamycin amidino carbamates |
| US5574018A (en) | 1994-07-29 | 1996-11-12 | Amgen Inc. | Conjugates of vitamin B12 and proteins |
| US5491231A (en) | 1994-11-28 | 1996-02-13 | American Home Products Corporation | Hindered N-oxide esters of rapamycin |
| US5547668A (en) * | 1995-05-05 | 1996-08-20 | The Board Of Trustees Of The University Of Illinois | Conjugates of folate anti-effector cell antibodies |
| AUPN449295A0 (en) | 1995-07-28 | 1995-08-24 | Inner And Eastern Health Care Network, The | Radioprotectors |
| US6207157B1 (en) * | 1996-04-23 | 2001-03-27 | The United States Of America As Represented By The Department Of Health And Human Services | Conjugate vaccine for nontypeable Haemophilus influenzae |
| US6030941A (en) * | 1996-05-01 | 2000-02-29 | Avi Biopharma, Inc. | Polymer composition for delivering substances in living organisms |
| ATE365562T1 (de) * | 1996-05-03 | 2007-07-15 | Immunomedics Inc | Zielgerichtete kombinations-immuntherapie für krebs |
| DE19621133A1 (de) * | 1996-05-24 | 1997-11-27 | Boehringer Mannheim Gmbh | Bestimmungsverfahren mit oligomerisierten Rezeptoren |
| WO1998008859A1 (en) | 1996-08-27 | 1998-03-05 | University Of Utah Research Foundation | Bioconjugates and delivery of bioactive agents |
| EP0923287A4 (en) | 1996-08-30 | 2001-08-01 | Lilly Co Eli | NON-CLASSIC PYRROLO (2,3-D) PYRIMIDINE ANTIFOLATE |
| JP2001501601A (ja) | 1996-09-12 | 2001-02-06 | メルク エンド カンパニー インコーポレーテッド | 前立腺ガンの治療において有用な共役体 |
| US6056973A (en) * | 1996-10-11 | 2000-05-02 | Sequus Pharmaceuticals, Inc. | Therapeutic liposome composition and method of preparation |
| US6177404B1 (en) * | 1996-10-15 | 2001-01-23 | Merck & Co., Inc. | Conjugates useful in the treatment of benign prostatic hyperplasia |
| US6071532A (en) * | 1996-10-15 | 2000-06-06 | Emory University | Synthesis of glycophospholipid and peptide-phospholipid conjugates and uses thereof |
| US6291673B1 (en) * | 1997-10-17 | 2001-09-18 | Purdue Research Foundation | Folic acid derivatives |
| GB9723669D0 (en) * | 1997-11-07 | 1998-01-07 | Univ Aberdeen | Skin penetration enhancing components |
| US6380395B1 (en) * | 1998-04-21 | 2002-04-30 | Bristol-Myers Squibb Company | 12, 13-cyclopropane epothilone derivatives |
| US6093382A (en) * | 1998-05-16 | 2000-07-25 | Bracco Research Usa Inc. | Metal complexes derivatized with folate for use in diagnostic and therapeutic applications |
| AU4093799A (en) | 1998-05-22 | 1999-12-13 | Board Of Trustees Of The Leland Stanford Junior University | Bifunctional molecules and therapies based thereon |
| JP2000026434A (ja) | 1998-06-05 | 2000-01-25 | Zeria Pharmaceut Co Ltd | 新規1,5−ベンゾジアゼピン誘導体 |
| US6589503B1 (en) | 1998-06-20 | 2003-07-08 | Washington University | Membrane-permeant peptide complexes for medical imaging, diagnostics, and pharmaceutical therapy |
| CA2353593A1 (en) | 1998-12-18 | 2000-06-22 | Hadasit Medical Research Services & Development Ltd. | Method of administering a compound to multi-drug resistant cells |
| US6291684B1 (en) * | 1999-03-29 | 2001-09-18 | Bristol-Myers Squibb Company | Process for the preparation of aziridinyl epothilones from oxiranyl epothilones |
| US7238368B2 (en) | 1999-04-23 | 2007-07-03 | Alza Corporation | Releasable linkage and compositions containing same |
| AU769425B2 (en) | 1999-04-23 | 2004-01-29 | Alza Corporation | Conjugate having a cleavable linkage for use in a liposome |
| AUPQ014799A0 (en) * | 1999-05-04 | 1999-05-27 | Access Pharmaceuticals Australia Pty Limited | Amplification of folate-mediated targeting to tumor cells using polymers |
| AUPQ071299A0 (en) | 1999-06-02 | 1999-06-24 | Access Pharmaceuticals Australia Pty Limited | Vitamin directed dual targeting therapy |
| WO2001010468A2 (en) | 1999-08-09 | 2001-02-15 | The General Hospital Corporation | Drug-carrier complexes and methods of use thereof |
| US6822086B1 (en) | 1999-08-09 | 2004-11-23 | The General Hospital Corporation | Drug-carrier complexes and methods of use thereof |
| EP2269654A3 (en) | 1999-08-24 | 2011-04-13 | Cellgate Inc. | Enhancing drug delivery across and into epithelial tissues using oligo arginine moieties |
| US7229961B2 (en) | 1999-08-24 | 2007-06-12 | Cellgate, Inc. | Compositions and methods for enhancing drug delivery across and into ocular tissues |
| MXPA02003771A (es) | 1999-10-15 | 2005-04-28 | Mayo Foundation | Conjugados de cobalamina, utiles como agentes para obtencion de imagen y como agentes anti-tumor. |
| US7067111B1 (en) * | 1999-10-25 | 2006-06-27 | Board Of Regents, University Of Texas System | Ethylenedicysteine (EC)-drug conjugates, compositions and methods for tissue specific disease imaging |
| EP1242401B1 (en) | 1999-11-24 | 2006-12-27 | Immunogen, Inc. | Cytotoxic agents comprising taxanes and their therapeutic use |
| DE60013639T2 (de) | 1999-12-02 | 2005-02-03 | Zeria Pharmaceutical Co., Ltd. | Calciumsalze von 1,5-benzodiazepin-derivaten, verfahren zur herstellung der salze und arzneimittel, die diese enthalten |
| US7033594B2 (en) * | 2000-03-31 | 2006-04-25 | Purdue Research Foundation | Method of treatment using ligand-immunogen conjugates |
| US6670355B2 (en) * | 2000-06-16 | 2003-12-30 | Wyeth | Method of treating cardiovascular disease |
| US6290929B1 (en) | 2000-07-28 | 2001-09-18 | The Procter & Gamble Company | Cancer treatment |
| MXPA03001245A (es) * | 2000-08-11 | 2003-05-27 | Wyeth Corp | Metodo para el tratamiento del carcionma positivo para receptores de estrogeno. |
| JP2004509898A (ja) * | 2000-09-19 | 2004-04-02 | ワイス | 水溶性ラパマイシンエステル |
| US6399625B1 (en) * | 2000-09-27 | 2002-06-04 | Wyeth | 1-oxorapamycins |
| US6399626B1 (en) * | 2000-10-02 | 2002-06-04 | Wyeth | Hydroxyesters of 7-desmethylrapamycin |
| US6440991B1 (en) * | 2000-10-02 | 2002-08-27 | Wyeth | Ethers of 7-desmethlrapamycin |
| CA2429722A1 (en) * | 2000-11-28 | 2002-06-06 | Wyeth | Expression analysis of fkbp nucleic acids and polypeptides useful in the diagnosis and treatment of prostate cancer |
| US20020168737A1 (en) | 2001-01-24 | 2002-11-14 | Cornish Virginia W. | Binding and catalysis screen for high throughput determination of protein function using chemical inducers of dimerization |
| AR036993A1 (es) * | 2001-04-02 | 2004-10-20 | Wyeth Corp | Uso de agentes que modulan la interaccion entre pd-1 y sus ligandos en la submodulacion de respuestas inmunologicas |
| NZ528265A (en) * | 2001-04-02 | 2005-10-28 | Wyeth Corp | Screening of compounds which modulate PD-1 signalling by testing for compounds that modulate phosphorylation of SHP-2, ERK1 or ERK-2, and PKC-theta |
| ATE427948T1 (de) | 2001-04-24 | 2009-04-15 | Purdue Research Foundation | Folat-mimetika und deren folatrezeptorbindende konjugate |
| WO2002087424A2 (en) | 2001-05-02 | 2002-11-07 | Purdue Research Foundation | Treatment and diagnosis of macrophage mediated disease |
| US7109165B2 (en) * | 2001-05-18 | 2006-09-19 | Sirna Therapeutics, Inc. | Conjugates and compositions for cellular delivery |
| US6800653B2 (en) * | 2001-06-01 | 2004-10-05 | Bristol-Myers Squibb Compnay | Epothilone derivatives |
| US20040018203A1 (en) * | 2001-06-08 | 2004-01-29 | Ira Pastan | Pegylation of linkers improves antitumor activity and reduces toxicity of immunoconjugates |
| UA77200C2 (en) * | 2001-08-07 | 2006-11-15 | Wyeth Corp | Antineoplastic combination of cci-779 and bkb-569 |
| CN1545512A (zh) * | 2001-08-22 | 2004-11-10 | 惠氏公司 | 雷帕霉素二醛化合物 |
| CA2455308A1 (en) * | 2001-08-22 | 2003-03-06 | Wyeth | Rapamycin 29-enols |
| DE60234782D1 (de) * | 2001-09-28 | 2010-01-28 | Purdue Research Foundation | Behandlungsverfahren mit liganden-immunogenkonjugaten |
| GR1004163B (el) * | 2001-11-01 | 2003-02-21 | Πολυκυκλικα παραγωγα τροποποιησης των οπτικων ιδιοτητων και των ιδιοτητων αντοχης στο πλασμα των πολυμερων λιθογραφιας | |
| AU2002364566B2 (en) * | 2001-12-12 | 2009-03-26 | Conforma Therapeutics Corporation | Assays and implements for determining and modulating HSP90 binding activity |
| US20030194409A1 (en) * | 2002-01-17 | 2003-10-16 | Rothman James E. | Conjugate heat shock protein-binding peptides |
| US8043602B2 (en) * | 2002-02-07 | 2011-10-25 | Endocyte, Inc. | Folate targeted enhanced tumor and folate receptor positive tissue optical imaging technology |
| US7000695B2 (en) * | 2002-05-02 | 2006-02-21 | Halliburton Energy Services, Inc. | Expanding wellbore junction |
| ES2500922T3 (es) | 2002-05-06 | 2014-10-01 | Endocyte, Inc. | Agentes de formación de imágenes dirigidos al receptor de folato |
| US6596757B1 (en) * | 2002-05-14 | 2003-07-22 | Immunogen Inc. | Cytotoxic agents comprising polyethylene glycol-containing taxanes and their therapeutic use |
| CA2484640C (en) * | 2002-05-15 | 2012-01-17 | Endocyte, Inc. | Vitamin-mitomycin conjugates |
| US7776814B2 (en) | 2002-07-09 | 2010-08-17 | R&D-Biopharmaceuticals Gmbh | Tubulysin conjugates |
| US7816377B2 (en) * | 2002-07-09 | 2010-10-19 | R&D-Biopharmaceuticals Gmbh | Tubulysin analogues |
| PL374528A1 (en) | 2002-07-31 | 2005-10-31 | Schering Aktiengesellschaft | New effector conjugates, process for their production and their pharmaceutical use |
| ES2556641T3 (es) | 2002-07-31 | 2016-01-19 | Seattle Genetics, Inc. | Conjugados de fármacos y su uso para tratar cáncer, una enfermedad autoinmune o una enfermedad infecciosa |
| DE10241152A1 (de) | 2002-09-05 | 2004-03-18 | GESELLSCHAFT FüR BIOTECHNOLOGISCHE FORSCHUNG MBH (GBF) | Tubulysin-Biosynthese-Gene |
| US20040047917A1 (en) | 2002-09-06 | 2004-03-11 | Stephen Wilson | Drug delivery and targeting with vitamin B12 conjugates |
| AU2003278764C1 (en) | 2002-09-06 | 2010-09-16 | Cerulean Pharma Inc. | Cyclodextrin-based polymers for therapeutic delivery |
| WO2004032877A2 (en) * | 2002-10-10 | 2004-04-22 | Wyeth | Compositions, organisms and methodologies employing a novel human kinase |
| WO2004037210A2 (en) | 2002-10-24 | 2004-05-06 | Research Corporation Technologies | Functional mri agents for cancer imaging |
| CN1741741A (zh) * | 2002-11-21 | 2006-03-01 | 惠氏公司 | 用于治疗狼疮肾炎的组合物和方法 |
| DE10254439A1 (de) * | 2002-11-21 | 2004-06-03 | GESELLSCHAFT FüR BIOTECHNOLOGISCHE FORSCHUNG MBH (GBF) | Tubulysine, Herstellungsverfahren und Tubulysin-Mittel |
| AU2003288467A1 (en) | 2002-12-13 | 2004-07-09 | Immunomedics, Inc. | Immunoconjugates with an intracellularly-cleavable linkage |
| SI1592457T1 (sl) * | 2003-01-27 | 2012-12-31 | Endocyte, Inc. | Konjugat folat-vinblastin kot zdravilo |
| JP5576007B2 (ja) | 2003-01-27 | 2014-08-20 | エンドサイト・インコーポレイテッド | ビタミン受容体結合性薬剤送達結合体 |
| AR042938A1 (es) * | 2003-02-06 | 2005-07-06 | Wyeth Corp | Uso del cci-779 en el tratamiento de la fibrosis hepatica |
| US7482016B2 (en) | 2003-03-19 | 2009-01-27 | The J. David Gladstone Institutes | Immunogenic compositions comprising HIV-1 acetylated Tat polypeptides |
| EP2669377A3 (en) * | 2003-04-17 | 2015-10-14 | Alnylam Pharmaceuticals Inc. | Modified iRNA agents |
| EP1622646B1 (en) | 2003-05-06 | 2012-08-08 | Purdue Research Foundation | Treatment of lupus targeting the macrophages or the folate receptor |
| WO2004101803A2 (en) * | 2003-05-12 | 2004-11-25 | Wyeth Holdings Corporation | Process for producing anticancer agent ll-d45042 |
| MXPA06000407A (es) * | 2003-07-16 | 2006-03-17 | Wyeth Corp | Isomero c cci-779. |
| EP1658295B1 (en) * | 2003-08-07 | 2007-06-20 | Wyeth | Regioselective synthesis of cci-779 |
| DE602005003453T2 (de) | 2004-01-30 | 2008-09-25 | Bayer Schering Pharma Aktiengesellschaft | Neue effektor-konjugate, verfahren zu ihrer herstellung und ihre pharmazeutische verwendung |
| US7612071B2 (en) | 2004-03-12 | 2009-11-03 | Syntrix Biosystems, Inc. | Compositions and methods employing aminopterin |
| EP1737879B1 (en) | 2004-04-19 | 2012-10-10 | Archemix LLC | Aptamer-mediated intracellular delivery of therapeutic oligonucleotides |
| EP1747021B1 (en) | 2004-05-19 | 2015-09-09 | E. R. Squibb & Sons, L.L.C. | Self-immolative linkers and drug conjugates |
| WO2005115912A1 (ja) | 2004-05-25 | 2005-12-08 | Matsushita Electric Industrial Co., Ltd. | 水素生成装置及びそれを用いた燃料電池システム |
| WO2006020768A2 (en) * | 2004-08-10 | 2006-02-23 | Alnylam Pharmaceuticals, Inc. | Chemically modified oligonucleotides |
| TW200616604A (en) | 2004-08-26 | 2006-06-01 | Nicholas Piramal India Ltd | Nitric oxide releasing prodrugs containing bio-cleavable linker |
| JP2008515915A (ja) | 2004-10-07 | 2008-05-15 | エモリー ユニバーシティー | 多機能性ナノ粒子結合体およびそれらの使用 |
| US20060222653A1 (en) | 2004-11-12 | 2006-10-05 | Xencor, Inc. | Antibodies operably linked to selected chemoattractants |
| US20110166319A1 (en) | 2005-02-11 | 2011-07-07 | Immunogen, Inc. | Process for preparing purified drug conjugates |
| TW200640493A (en) | 2005-02-16 | 2006-12-01 | Insert Therapeutics Inc | Cyclodextrin-based polymers for therapeutics delivery |
| US7312217B2 (en) | 2005-03-11 | 2007-12-25 | Syntrix Biosystems, Inc. | Aminopterin dosage forms and methods for inflammatory disorders |
| EP1863816B1 (en) * | 2005-03-16 | 2014-06-25 | Endocyte, Inc. | Synthesis and purification of pteroic acid and conjugates thereof |
| RU2007139912A (ru) | 2005-03-30 | 2009-05-10 | Пердью Рисерч Фаундейшн (Us) | Способ прогнозирования течения рака на основе количественного анализа клеточного рецептора витамина фолата |
| KR20080031296A (ko) | 2005-06-20 | 2008-04-08 | 피에스엠에이 디벨롭먼트 캄파니, 엘엘씨 | Psma 항체-약물 접합체 |
| JP5175723B2 (ja) * | 2005-07-05 | 2013-04-03 | パーデュー・リサーチ・ファウンデーション | 単球介在性疾患を治療するための組成物の調製 |
| US20080280937A1 (en) * | 2005-08-19 | 2008-11-13 | Christopher Paul Leamon | Ligand Conjugates of Vinca Alkaloids, Analogs, and Derivatives |
| EP1937719A4 (en) | 2005-08-19 | 2010-11-24 | Novo Nordisk As | GLYCOPEGYLATED FACTOR VII AND FACTOR VIIA |
| DE102005039651B4 (de) * | 2005-08-22 | 2008-04-03 | Airbus Deutschland Gmbh | Illumination im Bereich von Flugzeugkabinen |
| CA2893252C (en) | 2005-08-24 | 2018-05-29 | Immunogen, Inc. | Process for preparing antibody maytansinoid conjugates |
| US20070134332A1 (en) | 2005-11-21 | 2007-06-14 | Medivas, Llc | Polymer particles for delivery of macromolecules and methods of use |
| PE20080102A1 (es) | 2006-05-25 | 2008-02-11 | Bristol Myers Squibb Co | Conjugados de analogos de aziridinil-epotilona y composiciones farmaceuticas que comprenden los mismos |
| JP2010509570A (ja) | 2006-11-03 | 2010-03-25 | パーデュー・リサーチ・ファウンデーション | エクスビボフローサイトメトリーの方法および装置 |
| US20080176958A1 (en) | 2007-01-24 | 2008-07-24 | Insert Therapeutics, Inc. | Cyclodextrin-based polymers for therapeutics delivery |
| US20100104626A1 (en) * | 2007-02-16 | 2010-04-29 | Endocyte, Inc. | Methods and compositions for treating and diagnosing kidney disease |
| CA2678427C (en) | 2007-02-16 | 2016-06-07 | Ktb Tumorforschungsgesellschaft Mbh | Dual acting prodrugs |
| US9555139B2 (en) * | 2007-03-14 | 2017-01-31 | Endocyte, Inc. | Binding ligand linked drug delivery conjugates of tubulysins |
| EP2148886B1 (en) | 2007-05-10 | 2014-02-19 | R & D Biopharmaceuticals Gmbh | Tubulysine derivatives |
| US9877965B2 (en) | 2007-06-25 | 2018-01-30 | Endocyte, Inc. | Vitamin receptor drug delivery conjugates for treating inflammation |
| US9138484B2 (en) | 2007-06-25 | 2015-09-22 | Endocyte, Inc. | Conjugates containing hydrophilic spacer linkers |
| US8476451B2 (en) | 2007-07-20 | 2013-07-02 | The Regents Of The University Of California | Tubulysin D analogues |
| SI2187965T1 (sl) | 2007-08-17 | 2020-03-31 | Purdue Research Foundation Office Of Technology Commercialization | Konjugati vezalca ligand-veznika PSMA in metode za uporabo |
| US9187521B2 (en) | 2007-10-25 | 2015-11-17 | Endocyte, Inc. | Tubulysins and processes for preparing |
| US8507455B2 (en) | 2007-12-04 | 2013-08-13 | Alnylam Pharmaceuticals, Inc. | Folate conjugates |
| DK2265283T3 (da) | 2008-03-18 | 2014-10-20 | Seattle Genetics Inc | Auristatin-lægemiddel-linker-konjugater |
| CN104524592B (zh) | 2008-04-30 | 2018-06-05 | 伊缪诺金公司 | 交联剂和它们的用途 |
| CN104258413A (zh) | 2008-04-30 | 2015-01-07 | 伊缪诺金公司 | 有效的偶联物和亲水性连接体 |
| US20100040669A1 (en) | 2008-08-12 | 2010-02-18 | Higuchi John W | Non-Invasive Ocular Delivery of Rapamycin |
| NZ592255A (en) | 2008-09-17 | 2013-07-26 | Endocyte Inc | Folate receptor binding conjugates of antifolates |
| US20100074863A1 (en) | 2008-09-17 | 2010-03-25 | Yat Sun Or | Anti-infective pyrrolidine derivatives and analogs |
| EP2174947A1 (en) | 2008-09-25 | 2010-04-14 | Universität des Saarlandes | Bioactive pre-tubulysins and use thereof |
| US20110288152A1 (en) | 2008-10-17 | 2011-11-24 | Purdue Research Foundation | Psma binding ligand-linker conjugates and methods for using |
| US20120022245A1 (en) | 2008-10-17 | 2012-01-26 | Purdue Research Foundation | Folate targeting of nucleotides |
| IT1394860B1 (it) | 2009-07-22 | 2012-07-20 | Kemotech S R L | Composti farmaceutici |
| US8394922B2 (en) | 2009-08-03 | 2013-03-12 | Medarex, Inc. | Antiproliferative compounds, conjugates thereof, methods therefor, and uses thereof |
| EP2322537A1 (en) | 2009-11-12 | 2011-05-18 | R & D Biopharmaceuticals Gmbh | Tubulin inhibitors |
| CN102648208B (zh) | 2009-11-12 | 2016-04-27 | R&D生技药品有限责任公司 | 微管蛋白抑制剂 |
| WO2011069116A1 (en) | 2009-12-04 | 2011-06-09 | Endocyte, Inc. | Binding ligand linked drug delivery conjugates of tubulysins |
| US20120258905A1 (en) | 2009-12-23 | 2012-10-11 | Endocyte, Inc. | Vitamin receptor drug delivery conjugates for treating inflammation |
| US20120322741A1 (en) | 2010-02-25 | 2012-12-20 | Purdue Research Foundation | Psma binding ligand-linker conjugates and methods for using |
| CA2793890C (en) | 2010-04-15 | 2017-08-15 | Spirogen Developments Sarl | Pyrrolobenzodiazepines and conjugates thereof |
| EP2409983A1 (en) | 2010-07-19 | 2012-01-25 | Leibniz-Institut für Pflanzenbiochemie (IPB) | Tubulysin analogues |
| JP2013535220A (ja) | 2010-08-06 | 2013-09-12 | エンドサイト,インコーポレイテッド | ツブリシンを調製するためのプロセス |
| CA2812543A1 (en) | 2010-09-27 | 2012-04-12 | Endocyte, Inc. | Folate conjugates for treating inflammation of the eye |
| SG190245A1 (en) | 2010-11-12 | 2013-06-28 | Endocyte Inc | Methods of treating cancer |
| WO2012090104A1 (en) | 2010-12-31 | 2012-07-05 | Kareus Therapeutics, Sa | Methods and compositions for designing novel conjugate therapeutics |
| SG191965A1 (en) | 2011-02-15 | 2013-08-30 | Immunogen Inc | Methods of preparation of conjugates |
| MX2013011201A (es) | 2011-03-29 | 2013-12-16 | Immunogen Inc | Proceso para la elaboracion de conjugados de mejor homogeneidad. |
| EP2691155B1 (en) | 2011-03-29 | 2018-11-14 | Immunogen, Inc. | Preparation of maytansinoid antibody conjugates by a one-step process |
| AU2012272930B2 (en) | 2011-06-21 | 2015-06-11 | Immunogen, Inc. | Novel maytansinoid derivatives with peptide linker and conjugates thereof |
| US20130224228A1 (en) | 2011-12-05 | 2013-08-29 | Igenica, Inc. | Antibody-Drug Conjugates and Related Compounds, Compositions, and Methods |
| WO2013126797A1 (en) | 2012-02-24 | 2013-08-29 | Purdue Research Foundation | Cholecystokinin b receptor targeting for imaging and therapy |
| US9629918B2 (en) | 2012-02-29 | 2017-04-25 | Purdue Research Foundation | Folate receptor alpha binding ligands |
| US20130252904A1 (en) | 2012-02-29 | 2013-09-26 | Endocyte, Inc. | Compositions and methods for treating cancer |
| US20140080175A1 (en) | 2012-03-29 | 2014-03-20 | Endocyte, Inc. | Processes for preparing tubulysin derivatives and conjugates thereof |
| CA2873112A1 (en) | 2012-05-11 | 2013-11-14 | Alexander Krantz | Site-specific labeling and targeted delivery of proteins for the treatment of cancer |
| CN104640572B (zh) | 2012-05-15 | 2018-04-27 | 索伦托医疗有限公司 | 药物偶联物,偶联方法,及其用途 |
| DK2872157T3 (da) | 2012-07-12 | 2020-03-30 | Hangzhou Dac Biotech Co Ltd | Konjugater af cellbindende molekyler med cytotoxiske midler |
| EP2708243A1 (en) | 2012-09-17 | 2014-03-19 | OntoChem GmbH | Receptor ligand linked cytotoxic molecules |
| US20140107316A1 (en) | 2012-10-16 | 2014-04-17 | Endocyte, Inc. | Drug delivery conjugates containing unnatural amino acids and methods for using |
| EP2908818A4 (en) | 2012-10-16 | 2016-07-13 | Endocyte Inc | CONJUGATES OF DRUG DELIVERY CONTAINING ARTIFICIAL AMINO ACIDS AND METHODS OF USE |
| EP2919774A4 (en) | 2012-11-15 | 2016-11-09 | Endocyte Inc | CONJUGATES FOR THE TREATMENT OF DISEASES CAUSED BY PSMA-EXPRESSING CELLS |
| CN105849086B (zh) | 2012-11-24 | 2018-07-31 | 杭州多禧生物科技有限公司 | 亲水性链接体及其在药物分子和细胞结合分子共轭反应上的应用 |
| US20140154702A1 (en) | 2012-11-30 | 2014-06-05 | Endocyte, Inc. | Methods For Treating Cancer Using Combination Therapies |
| SG11201504887TA (en) | 2012-12-21 | 2015-07-30 | Bioalliance Cv | Hydrophilic self-immolative linkers and conjugates thereof |
| DK2956173T3 (en) | 2013-02-14 | 2017-07-17 | Bristol Myers Squibb Co | TUBULYSIS RELATIONSHIPS, METHODS OF PRODUCING AND USING THEREOF |
| US20140249315A1 (en) | 2013-03-01 | 2014-09-04 | Endocyte, Inc. | Processes for preparing tubulysins |
| US9295731B2 (en) | 2013-04-01 | 2016-03-29 | Mark Quang Nguyen | Cleavable drug conjugates, compositions thereof and methods of use |
| CN104784699B (zh) | 2014-01-20 | 2019-05-03 | 博瑞生物医药(苏州)股份有限公司 | 叶酸受体结合配体-药物偶联物 |
| EP3197502A1 (en) | 2014-09-25 | 2017-08-02 | Endocyte, Inc. | Methods of treating cancer with tubulysin conjugates |
| CN106170303B (zh) | 2014-11-20 | 2019-10-25 | 法罗斯根有限公司 | 通过半胱天冬酶激活的前体药物 |
| PL3271329T3 (pl) | 2015-03-19 | 2022-01-17 | Hangzhou Dac Biotech Co., Ltd | Nowe łączniki hydrofilowe i ich koniugaty ligand-lek |
| US10975112B2 (en) | 2015-06-16 | 2021-04-13 | Hangzhou Dac Biotech Co., Ltd. | Linkers for conjugation of cell-binding molecules |
-
2008
- 2008-06-25 US US12/666,712 patent/US9138484B2/en not_active Expired - Fee Related
- 2008-06-25 AU AU2008268432A patent/AU2008268432B2/en not_active Ceased
- 2008-06-25 BR BRPI0812970A patent/BRPI0812970A2/pt not_active IP Right Cessation
- 2008-06-25 RU RU2010102044/04A patent/RU2523909C2/ru active
- 2008-06-25 EP EP19166718.7A patent/EP3569251A1/en not_active Withdrawn
- 2008-06-25 EP EP08780966.1A patent/EP2176293B1/en not_active Not-in-force
- 2008-06-25 CN CN201410643262.XA patent/CN104383553A/zh active Pending
- 2008-06-25 CA CA 2690943 patent/CA2690943A1/en not_active Abandoned
- 2008-06-25 CN CN200880104308.3A patent/CN101784565B/zh not_active Expired - Fee Related
- 2008-06-25 WO PCT/US2008/068093 patent/WO2009002993A1/en active Application Filing
- 2008-06-25 ES ES08780966T patent/ES2732879T3/es active Active
- 2008-06-25 JP JP2010515048A patent/JP5690589B2/ja not_active Expired - Fee Related
-
2009
- 2009-12-17 IL IL202796A patent/IL202796A/en active IP Right Grant
-
2013
- 2013-03-05 US US13/785,542 patent/US20140073761A1/en active Pending
-
2015
- 2015-08-07 US US14/820,777 patent/US20160168183A1/en not_active Abandoned
- 2015-09-01 IL IL240973A patent/IL240973A0/en unknown
- 2015-09-04 HK HK15108664.1A patent/HK1207980A1/xx unknown
-
2017
- 2017-02-13 US US15/431,157 patent/US10738086B2/en active Active
-
2020
- 2020-07-02 US US16/919,919 patent/US20210024581A1/en not_active Abandoned
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2006012527A1 (en) * | 2004-07-23 | 2006-02-02 | Endocyte, Inc. | Bivalent linkers and conjugates thereof |
| RU2008110495A (ru) * | 2005-08-19 | 2009-09-27 | Эндосайт, Инк. (Us) | Конъюгаты лиганда с несколькими лекарственными средствами |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2816717C2 (ru) * | 2018-09-06 | 2024-04-03 | Сидара Терапьютикс, Инк. | Композиции и способы для лечения вирусных инфекций |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2009002993A1 (en) | 2008-12-31 |
| EP2176293A4 (en) | 2016-03-02 |
| ES2732879T3 (es) | 2019-11-26 |
| EP2176293A1 (en) | 2010-04-21 |
| JP2010531363A (ja) | 2010-09-24 |
| CA2690943A1 (en) | 2008-12-31 |
| US20160168183A1 (en) | 2016-06-16 |
| EP3569251A1 (en) | 2019-11-20 |
| US9138484B2 (en) | 2015-09-22 |
| EP2176293B1 (en) | 2019-04-03 |
| IL240973A0 (en) | 2015-10-29 |
| US20100323973A1 (en) | 2010-12-23 |
| CN104383553A (zh) | 2015-03-04 |
| US20210024581A1 (en) | 2021-01-28 |
| HK1207980A1 (en) | 2016-02-19 |
| CN101784565B (zh) | 2014-12-10 |
| US20140073761A1 (en) | 2014-03-13 |
| RU2010102044A (ru) | 2011-08-20 |
| CN101784565A (zh) | 2010-07-21 |
| IL202796A0 (en) | 2011-08-01 |
| BRPI0812970A2 (pt) | 2019-09-24 |
| US10738086B2 (en) | 2020-08-11 |
| IL202796A (en) | 2015-09-24 |
| AU2008268432A1 (en) | 2008-12-31 |
| JP5690589B2 (ja) | 2015-03-25 |
| AU2008268432B2 (en) | 2015-01-15 |
| US20170151340A1 (en) | 2017-06-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2523909C2 (ru) | Конъюгаты, содержащие гидрофильные спейсеры линкеров | |
| RU2470668C2 (ru) | Конъюгаты лиганда с несколькими лекарственными средствами | |
| US20170327537A1 (en) | Binding ligand linked drug delivery conjugates of tubulysins | |
| EP2382995A2 (en) | Ligand conjugates of Vinca alkaloids, analogs and derivatives | |
| AU2013203147A1 (en) | Binding ligand linked drug delivery conjugates of tubulysins | |
| AU2016204030A1 (en) | Binding ligand linked drug delivery conjugates of tubulysins | |
| AU2013204207A1 (en) | Conjugates containing hydrophilic spacer linkers |