RU2422427C2 - Азеотропные композиции, содержащие 2,3,3,3-тетрафторпропен и фтористый водород, и их использование в способах получения 2,3,3,3-тетрафторпропена - Google Patents
Азеотропные композиции, содержащие 2,3,3,3-тетрафторпропен и фтористый водород, и их использование в способах получения 2,3,3,3-тетрафторпропена Download PDFInfo
- Publication number
- RU2422427C2 RU2422427C2 RU2008121963/04A RU2008121963A RU2422427C2 RU 2422427 C2 RU2422427 C2 RU 2422427C2 RU 2008121963/04 A RU2008121963/04 A RU 2008121963/04A RU 2008121963 A RU2008121963 A RU 2008121963A RU 2422427 C2 RU2422427 C2 RU 2422427C2
- Authority
- RU
- Russia
- Prior art keywords
- hfc
- composition
- azeotropic
- column
- distillate
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C21/00—Acyclic unsaturated compounds containing halogen atoms
- C07C21/02—Acyclic unsaturated compounds containing halogen atoms containing carbon-to-carbon double bonds
- C07C21/18—Acyclic unsaturated compounds containing halogen atoms containing carbon-to-carbon double bonds containing fluorine
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B7/00—Halogens; Halogen acids
- C01B7/19—Fluorine; Hydrogen fluoride
- C01B7/191—Hydrogen fluoride
- C01B7/195—Separation; Purification
- C01B7/196—Separation; Purification by distillation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C17/00—Preparation of halogenated hydrocarbons
- C07C17/25—Preparation of halogenated hydrocarbons by splitting-off hydrogen halides from halogenated hydrocarbons
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C17/00—Preparation of halogenated hydrocarbons
- C07C17/38—Separation; Purification; Stabilisation; Use of additives
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C17/00—Preparation of halogenated hydrocarbons
- C07C17/38—Separation; Purification; Stabilisation; Use of additives
- C07C17/383—Separation; Purification; Stabilisation; Use of additives by distillation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C17/00—Preparation of halogenated hydrocarbons
- C07C17/38—Separation; Purification; Stabilisation; Use of additives
- C07C17/383—Separation; Purification; Stabilisation; Use of additives by distillation
- C07C17/386—Separation; Purification; Stabilisation; Use of additives by distillation with auxiliary compounds
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Inorganic Chemistry (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Catalysts (AREA)
- Low-Molecular Organic Synthesis Reactions Using Catalysts (AREA)
Abstract
Изобретение относится к азеотропной или близкой к азеотропной композиции, предназначенной для получения 2,3,3,3-тетрафторпропена (HFC-1234yf), содержащей примерно от 64,6 мол.% примерно до 92,4 мол.% HFC-1234yf и примерно от 35,4 мол.% до 7,6 мол.% фтористого водорода. Также изобретение относится к способу отделения HFC-1234yf от HFC-245cb, к способу выделения HFC-1234yf из смеси, содержащей азеотропную или близкую к азеотропной композицию HFC-1234yf и фтористого водорода, к способу выделения HFC-1234yf из смеси HFC-1234yf, НРС-245 сb и фтористого водорода, к способу получения HFC-1234yf. Технический результат - получение чистого HFC-1234yf. 6 н. и 13 з.п. ф-лы, 2 ил., 11 табл.
Description
Перекрестная ссылка на родственную заявку
Настоящая заявка заявляет приоритет согласно 35 U.S.С. §119 временной заявки на патент США, серийный №60/732321 (зарегистрированной 1 ноября 2005 года), которая включается сюда в качестве ссылки во всей ее полноте.
Уровень техники
Область техники, к которой относится изобретение
Описываются азеотропные композиции, содержащие 2,3,3,3-тетрафторпропен и фтористый водород. Азеотропные композиции являются пригодными для использования в способах получения и в способах очистки 2,3,3,3-тетрафторпропена.
Описание предшествующего уровня техники
Хлорсодержащие соединения, такие как хлорфторуглероды (CFC), рассматриваются как вредные для озонового слоя Земли. Многие фторуглеводороды (HFC), используемые для замены CFC, как обнаружено, вносят вклад в глобальное потепление. По этой причине имеется необходимость в идентификации новых соединений, которые не повреждают окружающую среду, но также обладают свойствами, необходимыми для функционирования в качестве хладагентов, растворителей, чистящих агентов, пенообразующих агентов, аэрозольных пропеллентов, сред для теплопереноса, диэлектриков, агентов для гашения пламени, стерилизующих веществ и рабочих жидкостей энергетического цикла. Фторированные олефины, содержащие один или несколько атомов водорода в молекуле, рассматриваются при использовании в некоторых применениях, подобных, например, холодильной технике.
Краткая сущность изобретения
Один из аспектов относится к азеотропной или близкой к азеотропной композиции, содержащей 2,3,3,3-тетрафторпропен (HFC-1234yf, CF3CF=CH2) и фтористый водород (HF).
Дополнительный аспект относится к способу отделения HFC-1234yf от 1,1,1,2,2-пентафторпропана (HFC-245cb), включающему в себя: a) образование смеси HFC-1234yf, HFC-245cb и фтористого водорода и b) воздействие на указанную смесь стадии дистилляции, после которой образуется композиция колонного дистиллята, содержащая азеотропную или близкую к азеотропной композицию фтористого водорода и HFC-1234yf, по существу не содержащую HFC-245cb.
Дополнительный аспект относится к способу отделения HFC-1234yf от смеси, содержащей азеотропную или близкую к азеотропной композицию из HFC-1234yf и фтористого водорода, указанный способ включает в себя a) воздействие на указанную смесь первой стадии дистилляции, на которой композиция, обогащенная либо (i) фтористым водородом, либо (ii) HFC-1234yf, удаляется как первая композиция дистиллята вместе с первой композицией из нижней части колонны, обогащенной вторым из указанных компонентов (i) или (ii); и b) воздействие на указанную первую композицию дистиллята второй стадии дистилляции, осуществляемой при другом давлении, на которой компонент, обогащенный как первая композиция из нижней части колонны на стадии (а), удаляется во второй композиции дистиллята вместе со второй композицией из нижней части колонны, обогащенной тем же компонентом, который обогащается в первой композиции дистиллята.
Дополнительный аспект относится к способу очистки HFC-1234yf от смеси HFC-1234yf, HFC-245cb и фтористого водорода, указанный способ включает в себя: a) воздействие на указанную смесь первой стадии дистилляции с образованием первого дистиллята, содержащего азеотропную или близкую к азеотропной композицию, содержащую HFC-1234yf и фтористый водород, и первой композиции из нижней части колонны, содержащей HFC-245cb; b) воздействие на указанный первый дистиллят второй стадии дистилляции, из которой композиция, обогащенная либо (i) фтористым водородом, либо (ii) HFC-1234yf, удаляется как вторая композиция дистиллята, вместе с второй композицией из нижней части колонны, обогащенной вторым из указанных компонентов (i) или (ii); и c) воздействие на указанную вторую композицию дистиллята третьей стадии дистилляции, осуществляемой при давлении, ином, чем на второй стадии дистилляции, на которой компонент, обогащенный второй композицией из нижней части колонны на стадии (b), удаляется как третья композиция дистиллята вместе с третьей композицией из нижней части колонны, обогащенной таким же компонентом, который обогащается во второй композиции дистиллята.
Дополнительный аспект относится к способу получения HFC-1234yf, включающему в себя a) введение HFC-245cb в реакционную зону для дегидрофторирования с образованием продукта композиции реакции, содержащей HFC-1234yf, непрореагировавший HFC-245cb и фтористый водород; b) воздействие на указанную композицию продуктов реакции первой стадии дистилляции с образованием первой композиции дистиллята, содержащей азеотропную или близкую к азеотропной композицию, содержащую HFC-1234yf и HF, и первой композиции из нижней части колонны, содержащей HFC-245cb; c) воздействие на указанную первую композицию дистиллята второй стадии дистилляции, из которой композиция, обогащенная либо (i) фтористым водородом, либо (ii) HFC-1234yf, удаляется как вторая композиция дистиллята вместе со второй композицией из нижней части колонны, обогащенной вторым из указанных компонентов (i) или (ii); и d) воздействие на указанную вторую композицию дистиллята третьей стадии дистилляции, осуществляемой при давлении, ином, чем на второй стадии дистилляции, на которой компонент, обогащенный второй композицией из нижней части колонны на стадии (с), удаляется как третья композиция дистиллята вместе с третьей композицией из нижней части колонны, обогащенной тем же компонентом, который обогащается во второй композиции дистиллята.
Дополнительный аспект относится к способу производства CF3CF=CH2 (HFC-1234yf), включающему в себя введение CF3CF2CH3 (HFC-245cb) в зону реакции дегидрофторирования с получением реакционной смеси, содержащей CF3CF=CH2 (HFC-1234yf) и фтористый водород.
Дополнительный аспект относится к способу производства CF3CF=CH2 (HFC-1234yf), включающему в себя введение CF3CF2CH3 (HFC-245cb) в зону реакции дегидрофторирования с получением реакционной смеси, содержащей CF3CF=CH2 (HFC-1234yf) и фтористый водород.
Дополнительный аспект относится к способу производства CF3CF=CH2 (HFC-1234yf), включающему в себя введение CF3CF2CH3 (HFC-245cb) в зону реакции дегидрофторирования в присутствии катализатора с получением реакционной смеси, содержащей CF3CF=CH2 (HFC-1234yf).
Дополнительный аспект относится к способу производства CF3CF=CH2 (HFC-1234yf), включающему в себя введение CF3CF2CH3 (HFC-245cb) в зону реакции дегидрофторирования при повышенной температуре в отсутствие катализатора с получением реакционной смеси, содержащей CF3CF=CH2 (HFC-1234yf) и фтористый водород.
Краткое описание чертежей
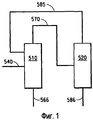
Фигура 1 представляет собой блок-схему, иллюстрирующую один из вариантов осуществления двухколонного способа азеотропной дистилляции.
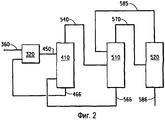
Фигура 2 представляет собой блок-схему, иллюстрирующую один из вариантов осуществления способа производства HFC-1234yf.
Подробное описание изобретения
Один из аспектов относится к композициям, содержащим 2,3,3,3-тетрафторпропен (HFC-1234yf, CF3CF=CH2, CAS reg. no. 754-12-1).
HFC-1234yf может быть получен посредством способов, известных в данной области, или как описано здесь.
Безводный фтористый водород (HF) имеет CAS reg. no. 7664-39-3 и является коммерчески доступным.
Также пригодным для использования в способах, описываемых здесь, является 1,1,1,2,2-пентафторпропан (HFC-245cb, CF3CF2CH3, CAS reg. no. 1814-88-6). HFC-245cb является коммерчески доступным или может быть получен посредством способов, известных в данной области.
Дополнительный аспект предусматривает способ производства CF3CF=CH2 (HFC-1234yf), включающий в себя введение CF3CF2CH3 (HFC-245cb) в зону реакции дегидрофторирования с получением реакционной смеси, содержащей CF3CF=CH2 (HFC-1234yf) и фтористый водород.
Дополнительный аспект предусматривает способ производства CF3CF=CH2 (HFC-1234yf), включающий в себя введение CF3CF2CH3 (HFC-245cb) в зону реакции дегидрофторирования в присутствии катализатора с получением реакционной смеси, содержащей CF3CF=CH2 (HFC-1234yf).
В этом варианте осуществления, дегидрофторирование в паровой фазе CF3CF2CH3 (HFC-245cb) в реакционной зоне может быть легко осуществлено с использованием типичных катализаторов дегидрофторирования. Как правило, настоящее дегидрофторирование может осуществляться с использованием любого катализатора дегидрофторирования, известного в данной области. Эти катализаторы включают в себя, но не ограничиваясь этим, фторид алюминия, фторированную окись алюминия, металлы на фториде алюминия, металлы на фторированной окиси алюминия; оксиды, фториды и оксифториды магния, цинка и смесей магния и цинка и/или алюминия; оксид лантана и фторированный оксид лантана; оксиды хрома, фторированные оксиды хрома и кубический трифторид хрома; углерод, уголь, промытый кислотой, активированный уголь, трехмерные материалы с углеродистой матрицей и соединения металлов на носителе угле. Соединения металлов представляют собой оксиды, фториды и оксифториды, по меньшей мере, одного металла, выбранного из группы, состоящей из натрия, калия, рубидия, цезия, иттрия, лантана, церия, празеодима, неодима, самария, хрома, железа, кобальта, родия, никеля, меди, цинка, и их смеси.
Катализаторы дегидрофторирования включают в себя, но не ограничиваясь этим, фторид алюминия, фторированную окись алюминия, металлы на фториде алюминия и металлы на фторированной окиси алюминия, как описано в патенте США № 5396000, который включается сюда в качестве ссылки. Фторированная окись алюминия и фторид алюминия могут быть получены, как описано в патенте США № 4902838, включаемом сюда в качестве ссылки. Пригодные для использования металлы включают в себя хром, магний (например, фторид магния), металлы группы VIIB (например, марганец), металлы группы IIIB (например, лантан) и цинк. При использовании такие металлы обычно присутствуют как галогениды (например, фториды), как оксиды и/или как оксигалогениды. Металлы на фториде алюминия и металлы на фторированной окиси алюминия могут быть получены с помощью процедур, как описано в патенте США № 4766260, включаемом сюда в качестве ссылки. В одном из вариантов осуществления, когда используются металлы на носителе, общее содержание металла катализатора составляет примерно от 0,1 до 20 мас.%, как правило, примерно от 0,1 до 10 мас.%. В одном из вариантов осуществления, катализаторы включают в себя катализаторы, состоящие по существу из фторида алюминия и/или фторированной окиси алюминия.
В дополнение к этому, катализаторы дегидрофторирования включают в себя, но не ограничиваясь этим, оксиды, фториды и оксифториды магния, цинка и смесей магния и цинка и/или алюминия. Пригодный для использования катализатор может быть получен, например, посредством сушки оксида магния до тех пор, пока по существу вся вода не будет удалена, например в течение примерно 18 часов примерно при 100°C. Затем высушенный материал переносится в реактор для использования. Затем температура постепенно увеличивается примерно до 400°C, в то же время поддерживая поток азота через реактор для удаления любых оставшихся следов влажности из оксида магния и реактора. Затем температуру понижают примерно до 200°C, и фторирующий агент, такой как HF, или другие испаряемые соединения, содержащие фтор, такие как SF4, СCl3F, СCl2F2, CHF3 или СCl2FСClF2, необязательно разбавленные инертным газом, таким как азот, проходит через реактор. Количество инертного газа или азота может постепенно уменьшаться до тех пор, пока только HF или другие испаряемые соединения, содержащие фтор, не будут проходить через реактор. В этот момент температура может увеличиваться примерно до 450°C и поддерживаться для преобразования оксида магния до содержания фторида, соответствующего, по меньшей мере, 40 мас.%, например, в течение 15-300 минут в зависимости от скорости потока фторирующего агента и объема катализатора. Фториды находятся в форме фторида магния или оксифторида магния; остаток катализатора представляет собой оксид магния. Специалисту в данной области понятно, что условия фторирования, такие как время и температура, могут регулироваться для получения более 40 мас.% фторидсодержащего материала.
Другая процедура, пригодная для приготовления катализатора, заключается в добавлении гидроксида аммония к раствору нитрата магния и, если он присутствует, нитрата цинка и/или нитрата алюминия. Гидроксид аммония добавляется к раствору нитрата до получения pH примерно от 9,0 до 9,5. В конце добавления раствор фильтруют, полученный твердый продукт промывают водой, сушат и медленно нагревают до 500°C, при этом он кальцинируется. Кальцинированный продукт затем обрабатывают соответствующим фторсодержащим соединением, как описано выше.
Еще одна процедура получения катализатора на основе фторида металла (то есть магния, необязательно содержащего также цинк и/или алюминий), содержащего один или несколько фторидов металла, заключается в обработке водного раствора галогенида (галогенидов) или нитрата (нитратов) металла (металлов) в деионизованной воде с помощью 48%-ного водного раствора HF при перемешивании. Перемешивание продолжают в течение ночи, и суспензию выпаривают досуха на паровой бане. Затем высушенный твердый продукт кальцинируют на воздухе при 400°C в течение примерно четырех часов, охлаждают до комнатной температуры, измельчают и просеивают с получением материала для использования при оценках катализатора.
В дополнение к этому, катализаторы дегидрофторирования включают в себя, но не ограничиваясь этим, оксид лантана и фторированный оксид лантана.
Пригодные для использования композиции фторированного оксида лантана могут быть получены любым способом, аналогичным способам, известным в данной области для получения фторированной окиси алюминия. Например, композиция катализатора может быть получена посредством фторирования оксида лантана.
Пригодные для использования композиции катализаторов могут также быть получены посредством осаждения лантана в виде гидроксида, который после этого сушат и кальцинируют с образованием оксида, эта технология хорошо известна в данной области. Затем полученный оксид может подвергаться предварительной обработке, как здесь описано.
Композиция катализатора может фторироваться до желаемого содержания фтора посредством предварительной обработки с помощью фторсодержащего соединения при повышенных температурах, например, примерно от 200°C примерно до 450°C. Предварительная обработка с помощью испаряемого фторсодержащего соединения, такого как HF, SF4, СCl3F, СCl2F3, CHF3, CHClF2 или СCl2FСClF2, может осуществляться любым удобным способом, в том числе в реакторе, который должен использоваться для осуществления реакции дегидрофторирования. Под испаряемым фторсодержащим соединением подразумевается фторсодержащее соединение, которое, когда проходит над катализатором при указанных условиях, будет фторировать катализатор до желаемой степени.
Пригодный для использования катализатор может быть получен, например, посредством сушки La2O3 до удаления по существу всей влажности, например в течение примерно 18 часов примерно при 400°C. Затем высушенный катализатор переносится в реактор, который должен использоваться. Затем температура постепенно увеличивается примерно до 400°C, в то же время поддерживая поток N2 через реактор для удаления любых оставшихся следов влажности из катализатора и реактора. Затем температура понижается примерно до 200°C, и испаряемое фторсодержащее соединение проходит через реактор. Если это необходимо, азот или другие инертные газы могут использоваться в качестве разбавителей. Содержание N2 или других инертных разбавителей может постепенно понижаться до тех пор, пока только испаряемое фторсодержащее соединение не будет проходить через реактор. В этот момент температура может увеличиваться примерно до 450°C и поддерживаться для преобразования La2O3 до содержания фтора, соответствующего, по меньшей мере, 80 мас.% LaF3, например, в течение 15-300 минут в зависимости от потока фторсодержащего соединения и объема катализатора.
Другая процедура, пригодная для получения катализатора, заключается в добавлении гидроксида аммония к раствору La(NO3)36H2O. Гидроксид аммония добавляют к раствору нитрата до получения pH примерно от 9,0 до 9,5. В конце добавления раствор фильтруют, полученный твердый продукт промывают водой и медленно нагревают примерно до 400°C, при этом он кальцинируется. Кальцинированный продукт затем обрабатывают соответствующим испаряемым фторсодержащим соединением, как описано выше.
В дополнение к этому, катализаторы дегидрофторирования включают в себя, но не ограничиваясь этим, оксиды хрома, фторированные оксиды хрома и кубический трифторид хрома. Кубический трифторид хрома может быть получен из CrF3XH2O, где X равно 3-9, предпочтительно, 4, посредством нагрева на воздухе или в инертной атмосфере (например, азота или аргона) при температуре примерно от 350°C примерно до 400°C в течение от 3 до 12 часов, предпочтительно, от 3 до 6 часов.
Кубический трифторид хрома является пригодным для использования сам по себе или вместе с другими соединениями хрома, в качестве катализатора дегидрофторирования. Необходимо отметить композиции катализаторов, содержащие хром, где, по меньшей мере, 10 мас.% хрома находится в форме кубического трифторида хрома, в частности композиции катализаторов, где, по меньшей мере, 25% хрома находится в форме кубического трифторида хрома, и в особенности композиции катализаторов, где, по меньшей мере, 60% хрома находится в форме кубического трифторида хрома. Хром, включая кубический трифторид хрома, может как наноситься на носитель, так и/или физически смешиваться с материалами, такими как углерод, фторид алюминия, фторированная окись алюминия, фторид лантана, фторид магния, фторид кальция, фторид цинка и тому подобное. Предпочтительными являются сочетания, содержащие кубический трифторид хрома в сочетании с фторидом магния и/или фторидом цинка.
В дополнение к этому, катализаторы дегидрофторирования включают в себя, но не ограничиваясь этим, активированный уголь или трехмерные материалы с углеродистой матрицей, как описано в патенте США № 6369284, включаемом сюда в качестве ссылки; или уголь или металлы, такие, например, как натрий, калий, рубидий, цезий, иттрий, лантан, церий, празеодим, неодим, самарий, хром, железо, кобальт, родий, никель, медь, цинк, и их смеси на носителе из угля, как описано в патенте США № 5268122, включаемом сюда в качестве ссылки. Уголь из любого из следующих источников является пригодным для способа по настоящему изобретению: дерево, торф, каменный уголь, оболочки кокосовых орехов, кости, лигнит, остатки на основе нефти и сахар. Коммерчески доступные угли, которые могут использоваться в настоящем изобретении, включают в себя те, которые продаются под следующими торговыми наименованиями: Barneby & Sutcliffe™, Darco™, Nucharm, Columbia JXN™, Columbia LCK™, Calgon PCB, Calgon BPL™, Westvaco™, Norit™ и Barnaby Cheny NB™.
Уголь включает в себя промытый кислотой уголь (например, уголь, который обрабатывают хлористоводородной кислотой или хлористоводородной кислотой, а затем фтористоводородной кислотой). Обработка кислотой, как правило, является достаточной для получения угля, который содержит менее чем 1000 ч./млн золы. Соответствующая обработка кислотой угля описывается в патенте США № 5136113, включаемом сюда в качестве ссылки. Уголь по настоящему изобретению также включает в себя трехмерные пористые материалы с углеродистой матрицей. Примеры являются такими, как описано в патенте США № 4978649, включаемом сюда в качестве ссылки. Необходимо отметить трехмерные материалы с углеродистой матрицей, которые получают посредством введения газообразных или парообразных углеродсодержащих соединений (например, углеводородов) в массу гранул углеродистого материала (например, сажи); разложения углеродсодержащих соединений с осаждением углерода на поверхности гранул и обработки полученного материала активирующим газом, содержащим пар, для создания пористого углеродистого материала. Таким образом формируется композитный материал углерод-углерод.
Физическая форма катализатора не является критичной и может, например, включать в себя хлопья, порошки или гранулы. В дополнение к этому, для катализаторов на носителе из угля углерод может находиться в форме порошка, гранул, хлопьев или чего-либо подобного. Хотя это и не главное, катализаторы, которые не должны фторироваться, могут обрабатываться с помощью HF перед использованием. Считается, что это преобразует некоторую часть поверхностных оксидов в оксифториды. Эта предварительная обработка может осуществляться посредством помещения катализатора в соответствующий контейнер (который может представлять собой реактор, который должен использоваться для осуществления реакции, описанной здесь), а после этого прохождения HF над высушенным катализатором, с тем чтобы частично насытить катализатор HF. Это удобно осуществлять посредством прохождения HF над катализатором в течение некоторого периода времени (например, примерно от 15 до 300 минут) при температуре, например, примерно от 200°C примерно до 450°C.
Каталитическое дегидрофторирование может быть удобным для осуществления при температуре в диапазоне, в одном из вариантов осуществления, примерно от 200°C примерно до 500°C, а в другом варианте осуществления, примерно от 300°C примерно до 450°C. Время контакта, в одном варианте осуществления, примерно от 1 примерно до 450 секунд, а в другом варианте осуществления, примерно от 10 примерно до 120 секунд.
Давление реакции может быть ниже атмосферного, атмосферным или выше атмосферного. Как правило, предпочтительным является давление вблизи атмосферного. Однако дегидрофторирование может преимущественно осуществляться при пониженном давлении (то есть при давлениях, меньших чем одна атмосфера).
Каталитическое дегидрофторирование может необязательно осуществляться в присутствии инертного газа, такого как азот, гелий или аргон. Добавление инертного газа может использоваться для увеличения степени дегидрофторирования. Необходимо отметить способы, где молярное отношение инертного газа к CF3CF2CH3 (HFC-245cb), подвергающемуся дегидрофторированию, равно примерно от 5:1 примерно до 1:1. Азот является предпочтительным инертным газом.
Дополнительный аспект предусматривает способ производства CF3CF=CH2 (HFC-1234yf), включающий в себя введение CF3CF2CH3 (HFC-245cb) в зону реакции дегидрофторирования при повышенной температуре в отсутствие катализатора с получением реакционной смеси, содержащей CF3CF=CH2 (HFC-1234yf) и фтористый водород.
В настоящем варианте осуществления дегидрофторирования, дегидрофторирование CF3CF2CH3 (HFC-245cb) может осуществляться в реакционной зоне при повышенной температуре в отсутствие катализатора, как описано во временной заявке на патент № 60/623210, зарегистрированной 29 октября 2004 года, включаемой сюда в качестве ссылки. Соответствующие температуры могут находиться в пределах между примерно 350°C и примерно 900°C, а в другом варианте осуществления, в пределах примерно между 450°C и примерно 900°C. Время пребывания газов в реакционной зоне составляет, как правило, в одном варианте осуществления, примерно от 0,5 примерно до 60 секунд, а в другом варианте осуществления, примерно от 2 секунд примерно до 20 секунд.
Давление реакции для реакции дегидрофторирования при повышенной температуре в отсутствие катализатора может быть ниже атмосферного, атмосферным или выше атмосферного. Как правило, предпочтительными являются давления вблизи атмосферного. Однако дегидрофторирование может преимущественно осуществляться при пониженном давлении (то есть при давлении, меньшем чем одна атмосфера).
Дегидрофторирование при повышенной температуре в отсутствие катализатора может необязательно осуществляться в присутствии инертного газа, такого как азот, гелий или аргон. Добавление инертного газа может использоваться для увеличения степени дегидрофторирования. Необходимо отметить способы, где молярное отношение инертного газа к CF3CF2CH3, подвергающемуся дегидрофторированию, равно примерно от 5:1 примерно до 1:1. Азот является предпочтительным инертным газом.
Реакционная зона либо для катализируемого, либо для некатализируемого дегидрофторирования может представлять собой реакционную емкость, изготовленную из никеля, железа, титана или их сплавов, как описано в патенте США № 6540933, включаемом сюда в качестве ссылки. Реакционная емкость из этих материалов (например, металлическая трубка) необязательно с насадкой из металла в соответствующей форме также может использоваться. Когда упоминаются сплавы, подразумевается никелевый сплав, содержащий примерно от 1 примерно до 99,9 мас.% никеля, сплав железа, содержащий примерно от 0,2 примерно до 99,8 мас.% железа, и сплав титана, содержащий примерно от 72 примерно до 99,8 мас.% титана. Необходимо отметить использование пустой (без насадки) реакционной емкости, изготовленной из никеля или сплавов никеля, такой как те, которые содержат примерно от 40 мас.% примерно до 80 мас.% никеля, например никелевый сплав Inconel™ 600, никелевый сплав Hastelloy™ C617 или никелевый сплав Hastelloy™ C276.
Когда они используются для насадки, металлы или сплавы металлов могут представлять собой частицы или сформированные формы, такие как перфорированные пластинки, кольца, проволока, сетка, стружки, трубки, дробь, марля или шерсть.
При рассмотрении способа дегидрофторирования HFC-245cb до HFC-1234yf и HF и выделения HFC-1234yf из такого способа неожиданно обнаружено, что гидрофторолефин HFC-1234yf образует азеотропную смесь с HF.
Один из аспектов предусматривает композицию, которая содержит HFC-1234yf и эффективное количество фтористого водорода (HF), с образованием азеотропной композиции. Под эффективным количеством подразумевается количество, которое, когда объединяется с HFC-1234yf, приводит к образованию азеотропной или близкой к азеотропной смеси. Как известно в данной области, азеотропная или близкая к азеотропной композиция представляет собой смесь двух или более различных компонентов, которые, когда они находятся в жидкой форме при данном давлении, будут кипеть при постоянной по существу температуре, эта температура может быть выше или ниже, чем температуры кипения индивидуальных компонентов, и которые будут давать композицию паров, по существу идентичную композиции жидкости, подвергающейся кипению.
Для целей настоящего описания близкая к азеотропной композиция (также обычно упоминаемая как "азеотропно-подобная композиция") означает композицию, которая ведет себя, подобно азеотропной композиции (то есть имеет постоянные характеристики кипения или тенденцию к тому, чтобы не разделяться при кипении или испарении).
Таким образом, композиция паров, образующихся во время кипения или испарения, является такой же или по существу такой же, как и композиция исходной жидкости. Следовательно, во время кипения или испарения композиция жидкости, если она вообще изменяется, изменяется только до минимальной или незначительной степени. Это должно составлять контраст с неазеотропными композициями, в которых во время кипения или испарения композиция жидкости изменяется до значительной степени.
В дополнение к этому, близкие к азеотропным композиции демонстрируют давление точки росы и давление точки образования пузырьков по существу при одинаковом давлении. То есть, так сказать, разница между давлением точки росы и давлением точки образования пузырьков при данной температуре будет представлять собой малую величину. Можно утверждать, что композиции с разницей между давлением точки росы и давлением точки образования пузырьков, равной или меньшей чем 3% (по отношению к давлению точки образования пузырьков) могут рассматриваться как близкие к азеотропным.
Соответственно основные особенности азеотропной или близкой к азеотропной композиции заключаются в том, что при данном давлении температура кипения жидкой композиции является фиксированной и что композиция паров над кипящей композицией является по существу такой же, как и для композиции кипящей жидкости (то есть не имеет место фракционирования компонентов жидкой композиции). В данной области известно также, что температура кипения и проценты массовые каждого компонента азеотропной композиции могут изменяться, когда азеотропная или близкая к азеотропной жидкая композиция подвергается кипению при различных давлениях. Таким образом, азеотропная или близкая к азеотропной композиция может определяться с точки зрения уникального соотношения, которое имеется между компонентами, или с точки зрения композиционных пределов компонентов, или с точки зрения точных массовых процентов каждого компонента композиции, отличающейся фиксированной температурой кипения при указанном давлении. В данной области также известно, что различные азеотропные композиции (включая их температуры кипения при конкретных давлениях) могут вычисляться (см., например, W. Schotte Ind. Eng. Chem. Process Des. Dev. (1980) 19, 432-439). Экспериментальная идентификация азеотропных композиций, содержащих одни и те же компоненты, может использоваться для подтверждения точности таких вычислений и/или для модификации вычислений при таких же или при иных температурах и давлениях.
Могут быть получены композиции, которые содержат азеотропные сочетания фтористого водорода с HFC-1234yf. Они включают в себя композиции, содержащие примерно от 19,3 мол.% примерно до 31,1 мол.% HF и примерно от 80,7 мол.% примерно до 68,9 мол.% HFC-1234yf (которые дают азеотропную смесь, кипящую при температуре, находящейся в пределах примерно между -20°C и примерно 80°C, и при давлении в пределах между примерно 23,2 фунт/кв.дюйм (160 кПа) и примерно 453 фунт/кв.дюйм (3123 кПа).
В дополнение к этому, также могут быть получены близкие к азеотропным композиции, содержащие HF и HFC-1234yf. Такие близкие к азеотропным композиции содержат примерно от 64,6 мол.% примерно до 92,4 мол.% HFC-1234yf и примерно от 35,4 мол.% примерно до 7,6 мол.% HF при температурах, находящихся в пределах примерно от -20°C примерно до 80°C, и при давлениях примерно от 23,2 фунт/кв.дюйм (160 кПа) и примерно 453 фунт/кв.дюйм (3123 кПа).
Необходимо понять, что не смотря на то что азеотропная или близкая к азеотропной композиция может существовать при конкретном отношении компонентов при данных температурах и давлениях, азеотропная композиция может также существовать в композициях, содержащих другие компоненты.
Могут быть получены композиции, которые состоят по существу из азеотропных сочетаний фтористого водорода с HFC-1234yf. Они включают в себя композиции, состоящие по существу из примерно от 19,3 мол.% примерно до 31,1 мол.% HF и примерно от 80,7 мол.% примерно до 68,9 мол.% HFC-1234yf (которые дают азеотропную смесь, кипящую при температуре в пределах примерно между -20°C и примерно 80°C и при давлении в пределах примерно между 23,2 фунт/кв.дюйм (160 кПа) и примерно 453 фунт/кв.дюйм (3123 кПа).
Могут также получаться близкие к азеотропным композиции, которые состоят по существу из примерно от 64,6 мол.% примерно до 92,4 мол.% HFC-1234yf и примерно от 35,4 мол.% примерно до 7,6 мол.% HF при температурах, находящихся в пределах примерно от -20°C примерно до 80°C, и при давлениях примерно от 23,2 фунт/кв.дюйм (160 кПа) и примерно 453 фунт/кв.дюйм (3123 кПа).
При атмосферном давлении температуры кипения фтористоводородной кислоты и HFC-1234yf составляют примерно 19,5°C и -28,3°C соответственно. Относительная летучесть при 67,6 фунт/кв.дюйм (466 кПа) и 9,3°C HF и HFC-1234yf, как обнаружено, составляет примерно 1,0, когда приближаются к 24,4 мол.% HF и 75,6 мол.% HFC-1234yf. Относительная летучесть при 187 фунт/кв.дюйм (1289 кПа) и 44,4°C, как обнаружено, составляет примерно 1,0, когда приближаются к 28,0 мол.% HF и 72,0 мол.% HFC-1234yf. Эти данные показывают, что использование обычных процедур дистилляции не приведет к выделению достаточно чистого соединения из-за малой величины относительной летучести соединений.
Для определения относительной летучести HF с HFC-1234yf используется так называемый метод PTx. При этой процедуре общее абсолютное давление в ячейке с известным объемом измеряют при постоянной температуре для различных известных бинарных композиций. Использование метода PTx описывается более подробно в "Phase Equilibrium in Process Design", Wiley-Interscience Publisher, 1970, written by Harold R. Null, on pages 124 to 126, полное описание которой тем самым включается сюда в качестве ссылки. Образцы пара и жидкости или пара и каждой из двух жидких фаз при таких условиях, где существуют две жидких фазы, получаются и анализируются для проверки их соответствующих композиций.
Эти измерения могут быть сведены к равновесным композициям пара и жидкости в ячейке с помощью модели уравнения для коэффициента активности, такого как уравнение Non-Random Two-Liquid (NRTL), для представления неидеальностей жидкой фазы. Использование уравнения для коэффициента активности, такого как уравнение NRTL, описывается более подробно в "The Properties of Gases and Liquids", 4th Edition, publisher McGraw Hill, written by Reid, Prausnitz and Poling, on pages 241 to 387; и в "Phase Equilibria in Chemical Engineering", published by Butterworth Publishers, 1985, written by Stanley M. Walas, pages 165 to 244; описание каждой из указанных ранее ссылок тем самым включается в качестве ссылки во всей ее полноте.
Не желая быть ограниченными любой теорией или объяснением, предполагают, что уравнение NRTL может в достаточной степени предсказать, ведут ли себя смеси HF и HFC-1234yf идеальным образом или нет, и может в достаточной степени предсказать относительные летучести компонентов в таких смесях. Таким образом, хотя HF имеет хорошую относительную летучесть по сравнению с HFC-1234yf при низких концентрациях HFC-1234yf, относительная летучесть становится примерно равной 1,0, когда приближаются к 75,6 мол.% HFC-1234yf при 9,3°C. Это сделало бы невозможным отделение HFC-1234yf от HF посредством обычной дистилляции из такой смеси. Там, где относительная летучесть приближается к 1,0, система определяется как образующая близкую к азеотропной или азеотропную композицию.
Обнаружено, что азеотропные смеси HFC-1234yf и HF образуются при различных температурах и давлениях. Азеотропные композиции могут образовываться в пределах между 23,2 фунт/кв.дюйм (160 кПа) при температуре -20°C и 453 фунт/кв.дюйм (3121 кПа) при температуре 80°C, указанные композиции состоят по существу из HFC-1234yf и HF в пределах примерно от 19,3 мол.% HF (и 80,7 мол.% HFC-1234yf) и примерно до 31,1 мол.% HF (и 68,9 мол.% HFC-1234yf). Азеотропная смесь HF и HFC-1234yf, как обнаружено, при 9,3°C и 67,6 фунт/кв.дюйм (466 кПа) состоит по существу примерно из 24,4 мол.% HF и примерно из 75,6 мол.% HFC-1234yf. Азеотропная смесь HF и HFC-1234yf, как также обнаружено, при 44,4°C и 187 фунт/кв.дюйм (1289 кПа) состоит по существу примерно из 28,0 мол.% HF и примерно из 72,0 мол.% HFC-1234yf. На основе указанных выше данных могут быть вычислены азеотропные композиции при других температурах и давлениях. Вычислено, что азеотропная композиция примерно из 19,3 мол.% HF и примерно из 80,7 мол.% HFC-1234yf может образовываться при -20°C и 23,2 фунт/кв.дюйм (160 кПа) и азеотропная композиция примерно из 31,1 мол.% HF и примерно 68,9 мол.% HFC-1234yf может образовываться при 80°C и 453 фунт/кв.дюйм (3121 кПа). Соответственно один из аспектов предусматривает азеотропную композицию, состоящую по существу из примерно от 19,3 мол.% примерно до 31,1 мол.% HF и примерно от 80,7 мол.% примерно до 68,9 мол.% HFC-1234yf, указанная композиция имеет температуру кипения примерно от -20°C при 23,2 фунт/кв.дюйм (160 кПа) примерно до 80°C при 453 фунт/кв.дюйм (3121 кПа).
Также обнаружено, что азеотропные или близкие к азеотропным композиции могут образовываться в пределах примерно между 23,2 фунт/кв.дюйм (160 кПа) и примерно 453 фунт/кв.дюйм (3121 кПа) при температурах, находящихся в пределах примерно от -20°C примерно до 80°C, указанные композиции состоят по существу из примерно от 64,6 мол.% примерно до 92,4 мол.% HFC-1234yf и примерно от 35,4 мол.% примерно до 7,6 мол.% HF.
Азеотропные и близкие к азеотропным композиции HF/HFC-1234yf являются пригодными для использования в способах получения HFC-1234yf и в способах очистки HFC-1234yf. Фактически, азеотропные и близкие к азеотропным композиции HF/HFC-1234yf могут быть пригодными для использования в любом способе, который создает композицию, содержащую HFC-1234yf и HF.
Азеотропная дистилляция может осуществляться для отделения HFC-1234yf от HFC-245cb, который представляет собой исходный материал для получения HFC-1234yf, посредством дегидрофторирования в паровой фазе. Затем двухколонная азеотропная дистилляция может использоваться для отделения получаемого при этом HF от желаемого продукта HFC-1234yf. HF может удаляться из компонентов галогенированных углеводородов в смеси продуктов с использованием, например, стандартных методик скруббинга водных растворов. Однако получение достаточных количеств продуктов скруббинга может создавать проблемы с утилизацией водных отходов. Таким образом, остается необходимость в способах, использующих HF из таких смесей продуктов.
Хотя начальная смесь, обрабатываемая в соответствии со способами, описанными здесь, может получаться из различных источников, включая, но не ограничиваясь этим, добавление HFC-1234yf к HF-содержащим композициям, преимущественное использование настоящих способов заключается в обработке смесей выходящих потоков от получения HFC-1234yf.
HFC-1234yf может быть получен посредством дегидрофторирования HFC-245cb в паровой фазе, как здесь описано ранее.
Дополнительный аспект предусматривает способ отделения HFC-1234yf от HFC-245cb, включающий в себя a) образование смеси HFC-1234yf, HFC-245cb и фтористого водорода и b) воздействие на указанную смесь стадии дистилляции с образованием композиции колонного дистиллята, содержащего азеотропную или близкую к азеотропной композицию HF и HFC-1234yf, по существу не содержащую HFC-245cb. Способ по настоящему изобретению может необязательно включать в себя дополнительное образование композиции из нижней части колонны, содержащей HFC-245cb.
Как здесь описывается, под "по существу не содержащей HFC-245cb" подразумевается, что композиция содержит меньше примерно чем 100 частей на миллион (ч./млн) (молярных), предпочтительно, меньше примерно чем 10 ч./млн и, наиболее предпочтительно, меньше примерно чем 1 ч./млн HFC-245cb.
Эта азеотропная дистилляция пользуется преимуществом низкокипящей азеотропной композиции, образованной с помощью и посредством HFC-1234yf и HF. Азеотропная композиция кипит при температуре, более низкой, чем температура кипения любого чистого компонента, и более низкой также, чем температура кипения HFC-245cb.
Как утверждалось ранее, смесь HFC-1234yf, HFC-245cb и HF может быть сформирована посредством любых практических средств. Как правило, настоящий способ является особенно пригодным для отделения HFC-1234yf из реакционной смеси, полученной посредством дегидрофторирования HFC-245cb. HF представляет собой побочный продукт, образующийся при этой реакции дегидрофторирования. Полученная реакционная смесь затем может обрабатываться посредством настоящего способа для удаления HFC-245cb. HFC-1234yf отбирают из верхней части колонны как дистиллят из дистилляционной колонны, как азеотропную или близкую к азеотропной композицию HFC-1234yf с HF. HFC-245cb может отбираться из нижней части колонны как композиция из нижней части колонны и может содержать также некоторое количество HF. Количество HF в HFC-245cb из нижней части дистилляционной колонны может изменяться примерно от 35 мол.% до менее чем 1 ч./млн (молярных) в зависимости от способа, которым осуществляется реакция дегидрофторирования Фактически, если реакция дегидрофторирования осуществляется способом, обеспечивающим 50 % преобразование HFC-245cb, и реакционная смесь, покидающая зону реакции, вводится непосредственно на стадию дистилляции, HFC-245cb, покидающий нижнюю часть способа дистилляции, будет содержать примерно 43 мол.% HF.
В одном из вариантов осуществления, работа настоящей азеотропной дистилляции включает в себя создание избытка HFC-1234yf в дистилляционной колонне. Если в колонну вводится соответствующее количество HFC-1234yf, тогда весь HF может отбираться из верхней части колонны как азеотропная композиция, содержащая HFC-1234yf и HF. Таким образом, HFC-245cb, удаляемый из нижней части колонны, по существу не будет содержать HF.
Как здесь описано, под "по существу не содержащей HF" подразумевается, что композиция содержит меньше примерно чем 100 ч./млн (молярных), предпочтительно, меньше примерно чем 10 ч./млн и, наиболее предпочтительно, меньше примерно чем 1 ч./млн HF.
На стадии дистилляции дистиллят, покидающий дистилляционную колонну из ее верхней части, содержащий HF и HFC-1234yf, может конденсироваться с использованием, например, стандартных дефлегматоров. По меньшей мере, часть этого конденсированного потока может возвращаться в верхнюю часть колонны в качестве флегмы. Отношение конденсированного материала, который возвращается в верхнюю часть дистилляционной колонны в качестве флегмы, к материалу, удаляемому в виде дистиллята, обычно упоминается как флегмовое число. Конкретные условия, которые могут использоваться для осуществления стадии дистилляции, зависят от ряда параметров, таких как диаметр дистилляционной колонны, точки введения и количества стадий разделения в колонне, среди прочего. Рабочее давление дистилляционной колонны может находиться в пределах примерно от давления 10 фунт/кв.дюйм примерно до 200 фунт/кв.дюйм (1380 кПа), как правило, примерно от 20 фунт/кв.дюйм примерно до 50 фунт/кв.дюйм. Дистилляционная колонна обычно работает при давлении примерно 25 фунт/кв.дюйм (172 кПа), при температуре нижней части примерно от -3°C и температуре верхней части примерно от -17°C. Как правило, увеличение флегмового числа приводит к увеличению чистоты потока дистиллята, но, как правило, флегмовое число находится в пределах между 1/1 и 200/1. Температура холодильника, который располагается вблизи верхней части колонны, обычно является достаточной для по существу полной конденсации дистиллята, который покидает верхнюю часть колонны, или представляет собой такую температуру, которая необходима для достижения желаемого флегмового числа посредством парциальной конденсации.
Композиция дистиллята в колонне, содержащего азеотропную или близкую к азеотропной композицию из HF и HFC-1234yf, по существу не содержащую HFC-245cb, должна обрабатываться для удаления HF и получения чистого HFC-1234yf в качестве продукта. Это может достигаться, например, посредством нейтрализации или посредством второго процесса дистилляции, как здесь описывается.
Дополнительный аспект предусматривает способ выделения HFC-1234yf из смеси, содержащей азеотропную или близкую к азеотропной композицию HFC-1234yf и HF, указанный способ включает в себя а) воздействие на указанную смесь первой стадии дистилляции, при которой композиция, обогащенная либо (i) фтористым водородом, либо (ii) HFC-1234yf, удаляется как первая композиция дистиллята вместе с первой композицией из нижней части колонны, которая обогащается вторым из указанных компонентов (i) или (ii); и b) воздействие на указанную первую композицию дистиллята второй стадии дистилляции, осуществляемой при давлении, ином, чем на первой стадии дистилляция, при которой компонент, обогащенный как первая композиция из нижней части колонны на стадии (а), удаляется как вторая композиция дистиллята вместе с композицией из нижней части колонны от второй стадии дистилляции, обогащенной таким же компонентом, который обогащается в первой композиции дистиллята.
Способ, как описано выше, имеет преимущество изменения азеотропной композиции при различных давлениях для увеличения эффективности разделения HFC-1234yf и HF. Первая стадия дистилляции может осуществляться при высоком давлении относительно второй стадии дистилляции. При высоких давлениях азеотропная смесь HF/HFC-1234yf содержит меньше HFC-1234yf. Таким образом, эта стадия дистилляции высокого давления производит избыток HFC-1234yf, который кипит при более высокой температуре, чем азеотропная смесь, и будет покидать колонну в виде фракции из нижней ее части как чистый HFC-1234yf. Затем дистиллят из первой колонны вводится на вторую стадию дистилляции, работающую при более низком давлении. При более низком давлении азеотропная смесь HF/HFC-1234yf сдвигается к более низким концентрациям HF. По этой причине на этой второй стадии дистилляции имеется избыток HF. Избыток HF, имеющий температуру кипения более высокую, чем азеотропная смесь, покидает вторую дистилляционную колонну как композиция из нижней части колонны. Настоящий способ может осуществляться таким способом, чтобы производить HFC-1234yf, по существу не содержащий HF. В дополнение к этому, настоящий способ может осуществляться таким образом, чтобы производить HF, по существу не содержащий HFC-1234yf.
Альтернативно, первая стадия дистилляции может осуществляться при низком давлении относительно второй стадии дистилляции. При более низких давлениях азеотропная смесь HF/HFC-1234yf содержит меньше HF. Таким образом, эта стадия дистилляции низкого давления производит избыток HF, который кипит при более высокой температуре, чем азеотропная смесь, и будет покидать колонну как фракция из ее нижней части, как чистый HF. Дистиллят из первой колонны затем вводится на вторую стадию дистилляции, работающую при более высоком давлении. При более высоком давлении азеотропная смесь HF/HFC-1234yf сдвигается к более низким концентрациям HFC-1234yf. По этой причине на этой второй стадии дистилляции имеется избыток HFC-1234yf. Избыток HFC-1234yf, имеющий температуру кипения, более высокую, чем азеотропная смесь, покидает вторую дистилляционную колонну как композиция из ее нижней части. Настоящий способ может осуществляться таким образом, чтобы производить HFC-1234yf, по существу не содержащий HF. В дополнение к этому, настоящий способ может осуществляться таким образом, чтобы производить HF, по существу не содержащий HFC-1234yf.
Как здесь описывается, под "по существу не содержащим HFC-1234yf" подразумевается, что композиция содержит меньше примерно чем 100 ч./млн (молярных), предпочтительно, меньше примерно чем 10 ч./млн и, наиболее предпочтительно, меньше примерно чем 1 ч./млн HFC-1234yf.
Эндотермическая реакция дегидрофторирования HFC-245cb с получением HFC-1234yf может осуществляться, например, в трубчатом реакторе с катализатором в трубах и с нагревательной средой во внешней оболочке реактора. Альтернативно, может использоваться теплоноситель, чтобы сделать возможной адиабатическую работу. Либо чистый HFC-245cb, либо чистый HFC-1234yf, которые оба получаются посредством способов дистилляции, описываемых здесь, могут рециклироваться обратно в реактор, чтобы служить в качестве теплоносителя. HFC-245cb может представлять собой предпочтительный теплоноситель, поскольку введение HFC-1234yf в реактор дегидрофторирования будет приводить к уменьшению преобразования HFC-245cb за один проход.
Как на первой, так и на второй стадии дистилляции дистиллят, покидающий верхнюю часть дистилляционной колонны, содержащий HF и HFC-1234yf, может конденсироваться с использованием, например, стандартных дефлегматоров. По меньшей мере, часть этого конденсированного потока может возвращаться в верхнюю часть колонны как флегма. Отношение конденсированного материала, который возвращается в верхнюю часть дистилляционной колонны как флегма, к материалу, удаляемому как дистиллят, обычно упоминается как флегмовое число. Конкретные условия, которые могут использоваться для осуществления стадии дистилляции по настоящему изобретению, зависят от ряда параметров, таких как диаметр дистилляционной колонны, точки ввода и количество стадий разделений в колонне, среди прочего. Рабочее давление дистилляционной колонны высокого давления (представляет ли собой колонна высокого давления первую дистилляционную колонну или вторую дистилляционную колонну) может изменяться от давления примерно 200 фунт/кв.дюйм (1380 кПа) примерно до 500 фунт/кв.дюйм (3450 кПа), обычно примерно от 250 фунт/кв.дюйм (1724 кПа) примерно до 400 фунт/кв.дюйм (2760 кПа). Первая дистилляционная колонна обычно работает при давлении примерно 365 фунт/кв.дюйм (2517 кПа) при температуре в нижней части колонны примерно 80°C и при температуре в верхней части колонны примерно 71°C. Как правило, увеличение флегмового числа приводит к увеличению чистоты потока дистиллята, но, как правило, флегмовое число находится в пределах между 0,1/1 и 100/1. Температура холодильника, который расположен вблизи верхней части колонны, обычно является достаточной для полной по существу конденсации дистиллята, который выходит из верхней части колонны, или представляет собой температуру, которая необходима для достижения желаемого флегмового числа посредством парциальной конденсации.
Рабочее давление дистилляционной колонны низкого давления (представляет ли собой колонна низкого давления первую дистилляционную колонну или вторую дистилляционную колонну) может находиться в пределах от давления примерно 5 фунт/кв.дюйм (34 кПа) примерно до 50 фунт/кв.дюйм (345 кПа), обычно примерно от 5 фунт/кв.дюйм (34 кПа) примерно до 20 фунт/кв.дюйм (138 кПа). Дистилляционная колонна низкого давления, как правило, работает при давлении примерно 25 фунт/кв.дюйм (172 кПа), при температуре нижней части колонны примерно 37°C и при температуре верхней части колонны примерно -18°C. Как правило, увеличение флегмового числа приводит к увеличению чистоты потока дистиллята, но, как правило, флегмовое число находится в пределах между 0,1/1 и 50/1. Температура холодильника, который находится вблизи верхней части колонны, обычно является достаточной для полной по существу конденсации дистиллята, который выходит из верхней части колонны, или представляет собой температуру, которая требуется для достижения желаемого флегмового числа посредством парциальной конденсации.
Фигура 1 представляет собой иллюстрацию одного из вариантов осуществления настоящего двухколонного способа дистилляции для разделения HFC-1234yf и HF. Если обращаться к Фигуре 1, смесь исходных материалов, полученная от предыдущей азеотропной дистилляции, содержащая HF и HFC-1234yf, где молярное отношение HF:HFC-1234yf составляет примерно 0,25:1 (или ниже), проходит через линию (540) в многоступенчатую дистилляционную колонну (510), работающую при температуре примерно 71°C и при давлении примерно 365 фунт/кв.дюйм (2517 кПа). Фракция из нижней части дистилляционной колонны (510), содержащая по существу чистый HFC-1234yf при температуре примерно 80°C и давлении примерно 367 фунт/кв.дюйм (2530 кПа), удаляется из нижней части колонны (510) через линию (566). Дистиллят из колонны (510), содержащий азеотропную смесь HF/HFC-1234yf (молярное отношение HF:HFC-1234yf составляет примерно 0,43:1) при температуре примерно 71°C и давлении примерно 365 фунт/кв.дюйм (2517 кПа), удаляется из верхней части колонны (510) и направляется через линию (570) в многоступенчатую дистилляционную колонну (520). Дистиллят из колонны (520), содержащий азеотропную смесь HF/HFC-1234yf (молярное отношение равно примерно 0,25:1) при температуре примерно -18°C и давлении примерно 25 фунт/кв.дюйм (172 кПа), удаляется из колонны (520) через линию (585) и рециклируется обратно в колонну (510). Фракции из нижней части колонны (520), содержащие по существу чистый HF при температуре примерно 37°C и давлении примерно 27 фунт/кв.дюйм (186 кПа), удаляются через линию (586).
Дополнительный аспект предусматривает способ выделения HFC-1234yf из смеси HFC-1234yf, HFC-245cb и HF, указанный способ включает в себя а) воздействие на указанную смесь первой стадии дистилляции с образованием первого дистиллята, содержащего азеотропную или близкую к азеотропной композицию, содержащую HFC-1234yf и HF, и первую фракцию из нижней части колонны, содержащую HFC-245cb; b) воздействие на указанный первый дистиллят второй стадии дистилляции, из которой композиция, обогащенная либо (i) фтористым водородом, либо (ii) HFC-1234yf, удаляется как вторая композиция дистиллята, вместе со второй композицией из нижней части колонны, обогащенной вторым из указанных компонентов (i) или (ii); и с) воздействие на указанную вторую композицию дистиллята третьей стадии дистилляции, осуществляемой при давлении, ином, чем на второй стадии дистилляции, на которой компонент, обогащенный во второй композиции из нижней части колонны на стадии (b), удаляется как вторая композиция дистиллята вместе с композицией из нижней части колонны из второй стадии дистилляции, обогащенной таким же компонентом, который обогащается в первой композиции дистиллята.
Дополнительный аспект предусматривает способ получения HFC-1234yf, включающий в себя а) введение HFC-245cb в реакционную зону для дегидрофторирования с образованием композиции продуктов реакции, содержащей HFC-1234yf, непрореагировавший HFC-245cb и фтористый водород; b) воздействие на указанную композицию продуктов реакции первой стадии дистилляции с образованием первой композиции дистиллята, содержащей азеотропную или близкую к азеотропной композицию, содержащую HFC-1234yf и HF, и первой композиции из нижней части колонны, содержащей HFC-245cb; c) воздействие на указанную первую композицию дистиллята второй стадии дистилляции, из которой композиция, обогащенная либо (i) фтористым водородом, либо (ii) HFC-1234yf, удаляется как вторая композиция дистиллята вместе со второй композицией из нижней части колонны, обогащенной вторым из указанных компонентов (i) или (ii); и d) воздействие на указанную вторую композицию дистиллята третьей стадии дистилляции, осуществляемой при давлении, ином, чем на второй стадии дистилляции, на которой компонент, обогащенный во второй композиции из нижней части колонны на стадии (с), удаляется как третья композиция дистиллята вместе с композицией из нижней части колонны из третьей стадии дистилляции, обогащенной таким же компонентом, который обогащается во второй композиции дистиллята. Необязательно способ может дополнительно включать в себя рециклирование, по меньшей мере, некоторой части указанной первой композиции из нижней части колонны (HFC-245cb) в указанную реакционную зону. Необязательно способ может дополнительно включать в себя рециклирование, по меньшей мере, некоторой части указанной второй композиции из нижней части колонны или указанной третьей композиции из нижней части колонны в указанную реакционную зону. Необязательно способ может дополнительно включать в себя рециклирование, по меньшей мере, некоторой части указанной второй композиции из нижней части колонны или указанной третьей композиции из нижней части колонны на указанную первую стадию дистилляции. Необязательно способ может дополнительно включать в себя извлечение, по меньшей мере, некоторой части указанного HFC-1234yf, по существу не содержащего HFC-245cb и HF.
Как здесь описывается, под "по существу не содержащим HFC-245cb и HF" подразумевается, что композиция содержит меньше примерно чем 100 ч./млн (молярных), предпочтительно, меньше примерно чем 10 ч./млн и, наиболее предпочтительно, меньше примерно чем 1 ч./млн каждого из HFC-245cb и HF.
Реакционная зона и условия для реакции дегидрофторирования описаны здесь ранее.
Фигура 2 представляет собой иллюстрацию одного из вариантов осуществления настоящего способа получения HFC-1234yf. HFC-245cb вводится через линию (360) в реактор (320). Смесь выходящего потока из реактора, содержащая HF, HFC-245cb и HFC-1234yf, покидает реактор через линию (450) и вводится в многоступенчатую дистилляционную колонну (410). Фракция из нижней части дистилляционной колонны (410), содержащая по существу чистый HFC-245cb, удаляется из нижней части колонны (410) через линию (466) и может рециклироваться обратно в реактор. Дистиллят из колонны (410), содержащий азеотропную смесь HF/HFC-1234yf, удаляется из верхней части колонны (410) и направляется через линию (540) во вторую многоступенчатую дистилляционную колонну (510). Фракция из нижней части колонны (510), которая представляет собой по существу чистый HFC-1234yf, удаляется из колонны (510) через линию (566) и может рециклироваться обратно в реактор (320) как теплоноситель. Дистиллят из колонны (510), содержащий азеотропную смесь HF/HFC-1234yf, вводится через линию (570) в третью многоступенчатую дистилляционную колонну (520). Дистиллят из колонны (520), содержащий HF/HFC-1234yf, удаляется через линию (585) и может рециклироваться во вторую дистилляционную колонну (510). Композиция из нижней части колонны (520) представляет собой по существу чистый HF и удаляется из колонны (520) через линию (586). По существу чистый продукт HF из этого способа может использоваться любым соответствующим способом, таким как введение в реактор фторирования, для получения химического соединения фтора или может нейтрализоваться для высвобождения.
Хотя это и не иллюстрируется на фигурах, понятно, что определенные части технологического оборудования могут использоваться в способах, описанных здесь, для оптимизации. Например, насосы, нагреватели или охладители могут использоваться по потребности. В качестве примера, является желательным иметь исходные материалы для дистилляционной колонны при такой же температуре, как и точка в колонне, где они вводятся. По этой причине нагрев или охлаждение технологического потока может быть необходимо для согласования температур.
Без дальнейшего пояснения, предполагается, что специалист в данной области может, используя настоящее описание, использовать описанные композиции и способы в их наиболее полной степени. Следующие далее примеры вариантов осуществления по этой причине должны рассматриваться как только лишь иллюстративные и не должны ограничивать оставшуюся часть описания каким-либо образом.
Примеры
Пример 1
Синтез HFC-1234yf посредством дегидрофторирования катализатора на основе фторированной окиси алюминия
Трубчатый реактор из Hastelloy (внешний диаметр 1,0 дюйм × внутренний диаметр 0,854 дюйма × L 9,5 дюйма) заполняют 25 см3 гамма-окиси алюминия, измельченной до 12-20 меш. Часть реактора с насадкой нагревают посредством керамического полоскового нагревателя 5 дюймов × 1 дюйм, прикрепленного снаружи реактора. Термопара, расположенная между стенкой реактора и нагревателем, измеряет температуру реактора. Катализатор сушат посредством нагрева при 200°C в течение 15 минут с продувкой азотом, а затем он взаимодействует со смесью HF/N2, нагретой до 425°C, с получением 16,7 г активированной фторированной окиси алюминия.
При температуре 350°C 10 куб.см/мин азота (1,7×10-7 м3/сек) и 15 куб.см/мин (2,5×10-7 м3/сек) HFC-245cb (CF3CF2CH3) смешиваются и протекают через реактор. Затем температуру повышают до 400°C, скорости потока поддерживают постоянными. Эффлюент для обеих температур отбирают и анализируют с помощью 19F ЯМР. В дополнение к этому, эффлюент анализируют с помощью ГХ/FID (пламенно-ионизационного детектора) для определения концентраций, как перечислено в Таблице 1.
| Таблица 1 | |||||
| Темп., °C |
Поток N2 (куб.см/мин) | Поток HFC-245cb (куб.см/мин) | Концентрации (ГХ/FID, % площади) | ||
| HFC-1234yf | HFC-245cb | Неизвестные | |||
| 350 | 10 | 15 | 84,2 | 12,8 | 3,0 |
| 400 | 10 | 15 | 91,3 | 1,9 | 6,8 |
Пример 2
Синтез HFC-1234yf с помощью углеродного катализатора
В реактор из сплава Hastelloy и никеля (внешний диаметр 1,0 дюйм × внутренний диаметр 0,854 дюйма × L 9,5 дюйма) загружают 14,5 г (25 мл) сферического (8 меш) трехмерного пористого материала с углеродистой матрицей, полученного по существу, как описано в патенте США № 4978649, включаемом сюда в качестве ссылки. Часть реактора с насадкой нагревают посредством керамического полоскового нагревателя 5 дюймов × 1 дюйм, прикрепленного снаружи реактора. Термопара, расположенная между стенкой реактора и нагревателем, измеряет температуру реактора.
При температуре 400°C 10 куб.см/мин (1,7×10-7 м3/сек) азота и 15 куб.см/мин (2,5×10-7 м3/сек) HFC-245cb (CF3CF2CH3) смешиваются и протекают через реактор с получением времени контакта 60 секунд. Затем потоки уменьшают до 5 куб.см/мин азота (8,3×10-8 м3/сек) и 7,5 куб.см/мин (1,3×10-7 м3/сек) HFC-245cb (CF3CF2CH3) с получением времени контакта 120 секунд. Эффлюент отбирают при обоих наборах условий и анализируют с помощью 19F ЯМР. В дополнение к этому, эффлюент анализируют с помощью ГХ/FID для определения концентраций, как перечислено в Таблице 2.
| Таблица 2 | |||||
| Темп., °C |
Поток N2 (куб.см/мин) | Поток HFC-245cb (куб.см/мин) | Концентрации (ГХ, % площади) | ||
| HFC-1234yf | HFC-245cb | Неизвестные | |||
| 400 | 10 | 15 | 6,0 | 93,9 | 0,1 |
| 400 | 5 | 7,5 | 22,8 | 76,4 | 0,8 |
Пример 3
Фазовые исследования смесей HF и HFC-1234yf
Фазовые исследования осуществляют для композиции, состоящей по существу из HFC-1234yf и HF, где композиция изменяется, и давления паров измеряют как при 9,3°C, так и при 44,4°C. На основе данных от фазовых исследований могут быть вычислены азеотропные композиции при других температурах и давлениях.
Таблица 3 приводит компиляцию экспериментальных и вычисленных азеотропных композиций для HF и HFC-1234yf при указанных температурах и давлениях.
| Таблица 3 | |||
| Температура, °C |
Давление, фунт/кв.дюйм (кПа) | % молярный HF | % молярный HFC-1234yf |
| -20 | 23,2 (160) | 19,3 | 80,7 |
| -18,5 | 24,7 (170) | 19,7 | 80,3 |
| 0 | 49,5 (341) | 23,0 | 77,0 |
| 9,3 | 67,6 (466) | 24,4 | 75,6 |
| 20 | 94,6 (652) | 25,7 | 74,3 |
| 40 | 167 (1151) | 27,7 | 72,3 |
| 44,4 | 187 (1289) | 28,0 | 72,0 |
| 60 | 278 (1917) | 29,5 | 70,5 |
| 70 | 354 (2441) | 30,3 | 69,7 |
| 71,2 | 365 (2517) | 30,4 | 69,6 |
| 75 | 400 (2758) | 30,7 | 69,3 |
| 80 | 453 (3123) | 31,1 | 68,9 |
Пример 4
Давления точки росы и точки образования пузырьков пара для HFC-1234yf
Давления точки росы и точки образования пузырьков пара для композиций, описанных здесь, вычисляют из измеренных и вычисленных термодинамических свойств. Диапазон вблизи азеотропии показан с помощью минимальной и максимальной концентраций HFC-1234yf (% мол.), для которых разность между давлениями точки росы и точки образования пузырьков равна или меньше 3% (по отношению к давлению точки образования пузырьков). Результаты приведены в Таблице 4.
| Таблица 4 | |||
| Температура, °C | Азеотропная композиция, % мол. HFC-1234yf | Близкие к азеотропным композиции, % мол. HFC-1234yf | |
| Минимум | Максимум | ||
| -20 | 80,7 | 75,0 | 92,4 |
| 40 | 72,4 | 66,4 | 83,4 |
| 80 | 69,0 | 64,6 | 80,6 |
Пример 5
Азеотропная дистилляция для отделения HFC-1234yf от HFC-245cb
Смесь HF, HFC-1234yf и HFC-245cb вводится в дистилляционную колонну с целью очистки HFC-1234yf. Данные в Таблице 5 получают посредством вычисления с использованием измеренных и вычисленных термодинамических свойств.
| Таблица 5 | |||
| Компонент или переменная | Исходные материалы для колонны | Фракция из верхней части колонны (дистиллят) | Фракция из нижней части колонны |
| HFC-245cb, % мол. | 33,4 | 10 ч./млн | 57,0 |
| HFC-1234yf, % мол. | 33,3 | 80,3 | 280 ч./млн |
| HF, % мол. | 33,3 | 19,7 | 43,0 |
| Темп., °C | _ | -18,5 | -6,0 |
| Давление, фунт/кв.дюйм (кПа) | - | 24,7 (170) | 26,7 (184) |
Пример 6
Азеотропная дистилляция для отделения HFC-1234yf от HFC-245cb
Смесь HF, HFC-1234yf и HFC-245cb вводится в дистилляционную колонну с целью очистки HFC-1234yf. Данные в Таблице 6 получают посредством вычисления с использованием измеренных и вычисленных термодинамических свойств.
| Таблица 6 | |||
| Компонент или переменная | Исходные материалы для колонны | Фракция из верхней части колонны (дистиллят) | Фракция из нижней части колонны |
| HFC-245cb, % мол. | 16,3 | 10 ч./млн | 100 |
| HFC-1234yf, % мол. | 67,4 | 80,5 | 50 ч./млн |
| HF, % мол. | 16,3 | 19,5 | - |
| Темп., °C | - | -17,4 | -2,7 |
| Давление, фунт/кв.дюйм (кПа) | - | 24,7 (170) | 26,7 (184) |
Пример 7
Азеотропная дистилляция для отделения HFC-1234yf от HFC-245cb
Смесь HF, HFC-1234yf и HFC-245cb вводится в дистилляционную колонну с целью очистки HFC-1234yf. Данные в Таблице 7 получают посредством вычисления с использованием измеренных и вычисленных термодинамических свойств.
| Таблица 7 | |||
| Компонент или переменная | Исходные материалы для колонны | Фракция из верхней части колонны (дистиллят) | Фракция из нижней части колонны |
| HFC-245cb, % мол. | 27,3 | 10 ч./млн | 100 |
| HFC-1234yf, % мол. | 63,6 | 87,5 | 27 ч./млн |
| HF, % мол. | 9,1 | 12,5 | - |
| Темп., °C | - | -17,2 | -2,7 |
| Давление, фунт/кв.дюйм (кПа) | - | 24,7 (170) | 26,7 (184) |
Пример 8
Азеотропная дистилляция для отделения HFC-1234yf от HFC-245cb
Смесь HF, HFC-1234yf и HFC-245cb вводится в дистилляционную колонну с целью очистки HFC-1234yf. Данные в Таблице 8 получают посредством вычисления с использованием измеренных и вычисленных термодинамических свойств.
| Таблица 8 | |||
| Компонент или переменная | Исходные материалы для колонны | Фракция из верхней части колонны (дистиллят) | Фракция из нижней части колонны |
| HFC-245cb, % мол. | 17,6 | 10 ч./млн | 100 |
| HFC-1234yf, % мол. | 76,5 | 92,9 | 47 ч./млн |
| HF, % мол. | 5,9 | 7,1 | - |
| Темп., °C | - | -17,1 | -2,7 |
| Давление, фунт/кв.дюйм (кПа) | - | 24,7 (170) | 26,7 (184) |
Пример 9
Двухколонная азеотропная дистилляция для отделения HFC-1234yf от HF
Смесь HF и HFC-1234yf вводится в способ дистилляции с целью очистки HFC-1234yf. Данные в Таблице 9 получают посредством вычисления с использованием измеренных и вычисленных термодинамических свойств. Числа вверху столбцов относятся к Фигуре 1.
| Таблица 9 | |||||
| Соединение или переменная | 540 Смесь исходных материалов | 570 Дистиллят из колонны (510) | 566 Продукт HFC-1234yf | 585 Дистиллят из колонны (520) | 586 Продукт HF |
| HF, % мол. |
19,8 | 30,0 | - | 20,0 | 100 |
| HFC-1234yf, % мол. |
80,2 | 70,0 | 100 | 80,0 | - |
| Темп., °C | - | 71,2 | 80,2 | -18,4 | 36,9 |
| Давление, фунт/кв.дюйм (кПа) | - | 364,7 (2515) |
366,7 (2528) | 24,7 (170) |
26,7 (184) |
Пример 10
Двухколонная азеотропная дистилляция для отделения HFC-1234yf от HF
Смесь HF и HFC-1234yf вводится в способ дистилляции с целью очистки HFC-1234yf. Данные в Таблице 10 получают посредством вычисления с использованием измеренных и вычисленных термодинамических свойств. Числа вверху столбцов относятся к Фигуре 1.
| Таблица 10 | |||||
| Соединение или переменная | 540 Смесь исходных материалов | 570 Дистиллят из колонны (510) | 566 Продукт HFC-1234yf | 585 Дистиллят из колонны (520) | 586 Продукт HF |
| HF, % мол. |
16,0 | 30,0 | - | 20,0 | 100 |
| HFC-1234yf, % мол. |
84,0 | 70,0 | 100 | 80,0 | - |
| Темп., °C | - | 71,2 | 80,2 | -18,4 | 36,9 |
| Давление, фунт/кв. дюйм (кПа) | - | 364,7 (2515) |
366,7 (2528) | 24,7 (170) |
26,7 (184) |
Пример 11
Двухколонная азеотропная дистилляция для отделения HFC-1234yf от HF
Смесь HF и HFC-1234yf вводится в способ дистилляции с целью очистки HFC-1234yf. Данные в Таблице 11 получают посредством вычисления с использованием измеренных и вычисленных термодинамических свойств. Числа вверху столбцов относятся к Фигуре 1.
| Таблица 11 | |||||
| Соединение или переменная | 540 Смесь исходных материалов | 570 Дистиллят из колонны (510) | 566 продукт HFC-1234yf | 585 Дистиллят из колонны (520) | 586 Продукт HF |
| HF, % молярный | 11,4 | 30,0 | - | 20,0 | 100 |
| HFC-1234yf, % молярный | 88,6 | 70,0 | 100 | 80,0 | - |
| Темп., °C | - | 71,2 | 80,2 | -18,4 | 36,9 |
| Давление, фунт/кв.дюйм (кПа) | - | 364,7 (2515) |
366,7 (2528) | 24,7 (170) |
26,7 (184) |
Claims (19)
1. Азеотропная или близкая к азеотропной композиция, предназначенная для получения 2,3,3,3-тетрафторпропена (HFC-1234yf), содержащая примерно от 64,6 мол.% примерно до 92,4 мол.% HFC-1234yf и примерно от 35,4 мол.% до 7,6 мол.% фтористого водорода.
2. Азеотропная или близкая к азеотропной композиция по п.1, содержащая примерно от 64,6 мол.% примерно до 92,4 мол.% HFC-1234yf и примерно от 35,4 мол.% примерно до 7,6 мол.% фтористого водорода, где давление паров составляет примерно от 23,2 фунт/кв.дюйм (160 кПа) примерно до 453 фунт/кв.дюйм (3123 кПа) при температуре примерно от -20°С примерно до 80°С.
3. Азеотропная композиция по п.1, содержащая примерно от 68,9 мол.% примерно до 80,7 мол.% HFC-1234yf и примерно от 31,1 мол.% примерно до 19,3 мол.% фтористого водорода, где давление паров составляет примерно от 23,2 фунт/кв.дюйм (160 кПа) примерно до 453 фунт/кв.дюйм (3123 кПа) при температуре примерно от -20°С примерно до 80°С.
4. Азеотропная или близкая к азеотропной композиция по п.1, у которой разница между давлением точки росы и давлением точки образования пузырьков, которая равна или меньше 3%, по отношению к давлению точки образования пузырьков.
5. Способ отделения HFC-1234yf от HFC-245cb, включающий в себя:
a) образование смеси HFC-1234yf, HFC-245cb и фтористого водорода и
b) воздействие на указанную смесь стадии дистилляции, от которой образуется композиция колонного дистиллята, содержащая азеотропную или близкую к азеотропной композицию из фтористого водорода и HFC-1234yf по п.1, по существу не содержащая HFC-245cb.
a) образование смеси HFC-1234yf, HFC-245cb и фтористого водорода и
b) воздействие на указанную смесь стадии дистилляции, от которой образуется композиция колонного дистиллята, содержащая азеотропную или близкую к азеотропной композицию из фтористого водорода и HFC-1234yf по п.1, по существу не содержащая HFC-245cb.
6. Способ выделения HFC-1234yf из смеси, содержащей азеотропную или близкую к азеотропной композицию HFC-1234yf и фтористого водорода по пункту 1, указанный способ включает в себя:
a) воздействие на указанную смесь первой стадии дистилляции, на которой композиция, обогащенная либо (i) фтористым водородом, либо (ii) HFC-1234yf, удаляется как первая композиция дистиллята, а из нижней части колонны выделяют первую композицию, обогащенную вторым из указанных компонентов (i) или (ii); и
b) воздействие на указанную первую композицию дистиллята второй стадии дистилляции, осуществляемой при другом давлении, при котором компонент, которым обогащена первая композиция, полученная из нижней части колонны на стадии (а), удаляется в качестве второй композиции дистиллята, а из нижней части колонны выделяют вторую композицию, обогащенную тем же компонентом, которым обогащена первая композиция дистиллята.
a) воздействие на указанную смесь первой стадии дистилляции, на которой композиция, обогащенная либо (i) фтористым водородом, либо (ii) HFC-1234yf, удаляется как первая композиция дистиллята, а из нижней части колонны выделяют первую композицию, обогащенную вторым из указанных компонентов (i) или (ii); и
b) воздействие на указанную первую композицию дистиллята второй стадии дистилляции, осуществляемой при другом давлении, при котором компонент, которым обогащена первая композиция, полученная из нижней части колонны на стадии (а), удаляется в качестве второй композиции дистиллята, а из нижней части колонны выделяют вторую композицию, обогащенную тем же компонентом, которым обогащена первая композиция дистиллята.
7. Способ выделения HFC-1234yf из смеси HFC-1234yf, HFC-245cb и фтористого водорода, указанный способ включает в себя
a) воздействие на указанную смесь первой стадии дистилляции с образованием первого дистиллята, содержащего азеотропную или близкую к азеотропной композицию по п.1, содержащую HFC-1234yf и фтористый водород, и первой композиции из нижней части колонны, содержащей HFC-245cb;
b) воздействие на указанный первый дистиллят второй стадии дистилляции, из которой композиция, обогащенная либо (i) фтористым водородом, либо (ii) HFC-1234yf, удаляется как вторая композиция дистиллята, а из нижней части колонны выделяют вторую композицию, обогащенную вторым из указанных компонентов (i) или (ii); и
с) воздействие на указанную вторую композицию дистиллята третьей стадии дистилляции, осуществляемой при давлении, ином, чем вторая стадия дистилляции, на которой компонент, которым обогащена вторая композиция, полученная из нижней части колонны на стадии (b), удаляется в качестве третьей композиции дистиллята, а из нижней части колонны выделяют третью композицию, обогащенной тем же компонентом, которым обогащена вторая композиция дистиллята.
a) воздействие на указанную смесь первой стадии дистилляции с образованием первого дистиллята, содержащего азеотропную или близкую к азеотропной композицию по п.1, содержащую HFC-1234yf и фтористый водород, и первой композиции из нижней части колонны, содержащей HFC-245cb;
b) воздействие на указанный первый дистиллят второй стадии дистилляции, из которой композиция, обогащенная либо (i) фтористым водородом, либо (ii) HFC-1234yf, удаляется как вторая композиция дистиллята, а из нижней части колонны выделяют вторую композицию, обогащенную вторым из указанных компонентов (i) или (ii); и
с) воздействие на указанную вторую композицию дистиллята третьей стадии дистилляции, осуществляемой при давлении, ином, чем вторая стадия дистилляции, на которой компонент, которым обогащена вторая композиция, полученная из нижней части колонны на стадии (b), удаляется в качестве третьей композиции дистиллята, а из нижней части колонны выделяют третью композицию, обогащенной тем же компонентом, которым обогащена вторая композиция дистиллята.
8. Способ получения HFC-1234yf, включающий в себя:
a) введение HFC-245cb в реакционную зону для дегидрофторирования с образованием композиции продукта реакции, содержащей HFC-1234yf, непрореагировавший HFC-245cb и фтористый водород;
b) воздействие на указанную композицию продуктов реакции первой стадии дистилляции с образованием первой композиции дистиллята, содержащей азеотропную или близкую к азеотропной композицию по п.1, содержащую HFC-1234yf и фтористый водород, и первой композиции из нижней части колонны, содержащей HFC-245cb;
c) воздействие на указанную первую композицию дистиллята второй стадии дистилляции, из которой композиция, обогащенная либо (i) фтористым водородом, либо (ii) HFC-1234yf, удаляется как вторая композиция дистиллята, а из нижней части колонны выделяют вторую композицию, обогащенную вторым из указанных компонентов (i) или (ii); и
d) воздействие на указанную вторую композицию дистиллята третьей стадии дистилляции, осуществляемой при давлении, ином, чем вторая стадия дистилляции, на которой компонент, которым обогащена вторая композиция, полученная из нижней части колонны на стадии (с), удаляется в качестве третьей композиции дистиллята, а из нижней части колонны выделяют третью композицию, обогащенную тем же компонентом, которым обогащена вторая композиция дистиллята.
a) введение HFC-245cb в реакционную зону для дегидрофторирования с образованием композиции продукта реакции, содержащей HFC-1234yf, непрореагировавший HFC-245cb и фтористый водород;
b) воздействие на указанную композицию продуктов реакции первой стадии дистилляции с образованием первой композиции дистиллята, содержащей азеотропную или близкую к азеотропной композицию по п.1, содержащую HFC-1234yf и фтористый водород, и первой композиции из нижней части колонны, содержащей HFC-245cb;
c) воздействие на указанную первую композицию дистиллята второй стадии дистилляции, из которой композиция, обогащенная либо (i) фтористым водородом, либо (ii) HFC-1234yf, удаляется как вторая композиция дистиллята, а из нижней части колонны выделяют вторую композицию, обогащенную вторым из указанных компонентов (i) или (ii); и
d) воздействие на указанную вторую композицию дистиллята третьей стадии дистилляции, осуществляемой при давлении, ином, чем вторая стадия дистилляции, на которой компонент, которым обогащена вторая композиция, полученная из нижней части колонны на стадии (с), удаляется в качестве третьей композиции дистиллята, а из нижней части колонны выделяют третью композицию, обогащенную тем же компонентом, которым обогащена вторая композиция дистиллята.
9. Способ по п.8, где указанная реакционная зона поддерживается при температуре, находящейся в диапазоне примерно от 200°С примерно до 500°С.
10. Способ по п.8, где указанная реакционная зона поддерживается при температуре, находящейся в диапазоне примерно от 300°С примерно до 450°С.
11. Способ по п.8, где способ осуществляют в присутствии катализатора дегидрофторирования, указанный катализатор дегидрофторирования выбирается из группы, состоящей из: фторида алюминия; фторированной окиси алюминия; металлов на фториде алюминия; металлов на фторированной окиси алюминия; оксидов, фторидов и оксифторидов магния, цинка и смесей магния и цинка и/или алюминия; оксида лантана и фторированного оксида лантана; оксидов хрома, фторированных оксидов хрома и кубического трифторида хрома; углерода, угля, промытого кислотой, активированного угля, трехмерных материалов с углеродистой матрицей и соединений металлов на носителе из угля.
12. Способ по п.11, где указанные соединения металлов на носителе из угля представляют собой соединения, по меньшей мере, одного металла, выбранного из группы, состоящей из натрия, калия, рубидия, цезия, иттрия, лантана, церия, празеодима, неодима, самария, хрома, железа, кобальта, родия, никеля, меди, цинка, и их смеси.
13. Способ по п.11, где указанные соединения металлов на носителе угле выбираются из группы, состоящей из оксидов, фторидов и оксифторидов.
14. Способ по п.11, где указанный катализатор дегидрофторирования представляет собой фторированную окись алюминия.
15. Способ по п.11, где указанный катализатор дегидрофторирования представляет собой трехмерные пористые материалы с углеродистой матрицей.
16. Способ получения СF3СF=СН2 (HFC-1234yf), включающий в себя
a) введение СF3СF2СН3 (HFC-245cb) в реакционную зону дегидрофторирования при повышенной температуре в отсутствие катализатора с получением реакционной смеси, содержащей СF3СF=СН2 (HFC-1234yf) и фтористый водород;
b) воздействие на указанную композицию продуктов реакции первой стадии дистилляции, с образованием первой композиции дистиллята, содержащей азеотропную или близкую к азеотропной композицию по п.1, содержащую HFC-1234yf и фтористый водород, и первой композиции из нижней части колонны, содержащей HFC-245cb;
c) воздействие на указанную первую композицию дистиллята второй стадии дистилляции, из которой композиция, обогащенная либо (i) фтористым водородом, либо (ii) HFC-1234yf, удаляется как вторая композиция дистиллята, а из нижней части колонны выделяют вторую композицию, обогащенную вторым из указанных компонентов (i) или (ii); и
d) воздействие на указанную вторую композицию дистиллята третьей стадии дистилляции, осуществляемой при давлении, ином, чем вторая стадия дистилляции, на которой компонент, которым обогащена вторая композиция, полученная из нижней части колонны на стадии (с), удаляется в качестве третьей композиции дистиллята, а из нижней части колонны выделяют третью композицию, обогащенную тем же компонентом, которым обогащена вторая композиция дистиллята.
a) введение СF3СF2СН3 (HFC-245cb) в реакционную зону дегидрофторирования при повышенной температуре в отсутствие катализатора с получением реакционной смеси, содержащей СF3СF=СН2 (HFC-1234yf) и фтористый водород;
b) воздействие на указанную композицию продуктов реакции первой стадии дистилляции, с образованием первой композиции дистиллята, содержащей азеотропную или близкую к азеотропной композицию по п.1, содержащую HFC-1234yf и фтористый водород, и первой композиции из нижней части колонны, содержащей HFC-245cb;
c) воздействие на указанную первую композицию дистиллята второй стадии дистилляции, из которой композиция, обогащенная либо (i) фтористым водородом, либо (ii) HFC-1234yf, удаляется как вторая композиция дистиллята, а из нижней части колонны выделяют вторую композицию, обогащенную вторым из указанных компонентов (i) или (ii); и
d) воздействие на указанную вторую композицию дистиллята третьей стадии дистилляции, осуществляемой при давлении, ином, чем вторая стадия дистилляции, на которой компонент, которым обогащена вторая композиция, полученная из нижней части колонны на стадии (с), удаляется в качестве третьей композиции дистиллята, а из нижней части колонны выделяют третью композицию, обогащенную тем же компонентом, которым обогащена вторая композиция дистиллята.
17. Способ по п.16, где указанная повышенная температура находится в пределах примерно между 350°C и примерно 900°С.
18. Способ по п.16, где указанная повышенная температура находится в пределах примерно между 450°С и примерно 900°С.
19. Способ по п.8 или 16, где указанная реакционная смесь дополнительно содержит непрореагировавший СF3СF2СН3 (HFC-245cb).
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US73232105P | 2005-11-01 | 2005-11-01 | |
| US60/732,321 | 2005-11-01 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2008121963A RU2008121963A (ru) | 2009-12-10 |
| RU2422427C2 true RU2422427C2 (ru) | 2011-06-27 |
Family
ID=37907695
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2008121963/04A RU2422427C2 (ru) | 2005-11-01 | 2006-11-01 | Азеотропные композиции, содержащие 2,3,3,3-тетрафторпропен и фтористый водород, и их использование в способах получения 2,3,3,3-тетрафторпропена |
Country Status (12)
| Country | Link |
|---|---|
| US (1) | US7476771B2 (ru) |
| EP (3) | EP1954662B1 (ru) |
| JP (1) | JP5281407B2 (ru) |
| KR (1) | KR101474026B1 (ru) |
| CN (2) | CN102603462B (ru) |
| AR (1) | AR058827A1 (ru) |
| BR (1) | BRPI0619721A2 (ru) |
| CA (1) | CA2627898A1 (ru) |
| ES (2) | ES2453159T3 (ru) |
| RU (1) | RU2422427C2 (ru) |
| UA (1) | UA95259C2 (ru) |
| WO (1) | WO2007053736A2 (ru) |
Families Citing this family (79)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9102579B2 (en) | 2004-04-29 | 2015-08-11 | Honeywell International Inc. | Method for producing fluorinated organic compounds |
| US7897823B2 (en) * | 2004-10-29 | 2011-03-01 | E. I. Du Pont De Nemours And Company | Process for production of azeotrope compositions comprising hydrofluoroolefin and hydrogen fluoride and uses of said azeotrope compositions in separation processes |
| US8766020B2 (en) * | 2008-07-31 | 2014-07-01 | Honeywell International Inc. | Process for producing 2,3,3,3-tetrafluoropropene |
| ES2530854T3 (es) * | 2005-11-03 | 2015-03-06 | Honeywell Int Inc | Método para producir compuestos orgánicos fluorados |
| KR101354492B1 (ko) * | 2006-01-03 | 2014-01-23 | 허니웰 인터내셔널 인코포레이티드 | 플루오르화 유기 화합물 제조 방법 |
| WO2007111313A1 (ja) | 2006-03-24 | 2007-10-04 | Zeon Corporation | 長尺の延伸フィルムおよびその製造方法並びに用途 |
| ES2539939T3 (es) | 2006-06-27 | 2015-07-07 | E.I. Du Pont De Nemours And Company | Procedimientos de producción de 1,2,3,3,3-pentafluoropropeno |
| US8377327B2 (en) | 2006-06-27 | 2013-02-19 | E I Du Pont De Nemours And Company | Tetrafluoropropene production processes |
| JP2009542650A (ja) | 2006-06-27 | 2009-12-03 | イー・アイ・デュポン・ドウ・ヌムール・アンド・カンパニー | テトラフルオロプロペン製造方法 |
| JP5393453B2 (ja) * | 2006-06-27 | 2014-01-22 | イー・アイ・デュポン・ドウ・ヌムール・アンド・カンパニー | テトラフルオロプロペンの製造方法 |
| EP2386533A1 (en) | 2006-07-13 | 2011-11-16 | E.I. Du Pont De Nemours And Company | Catalytic production process for making 1,3,3,3-tetrafluoropropene |
| US7803975B2 (en) * | 2006-07-13 | 2010-09-28 | E.I. Du Pont De Nemours And Company | Process for separating a fluoroolefin from HF by liquid-liquid extraction |
| GB0614927D0 (en) * | 2006-07-27 | 2006-09-06 | Ineos Fluor Holdings Ltd | Separation process |
| US8273928B2 (en) | 2006-08-24 | 2012-09-25 | E I Du Pont De Nemours And Company | Processes for separation of fluoroolefins from hydrogen fluoride by azeotropic distillation |
| US7420094B2 (en) * | 2006-09-05 | 2008-09-02 | E.I. Du Pont De Nemours And Company | Catalytic isomerization processes of 1,3,3,3-tetrafluoropropene for making 2,3,3,3-tetrafluoropropene |
| EP2129644B1 (en) | 2006-10-03 | 2020-07-01 | Mexichem Fluor S.A. de C.V. | Dehydrogenationhalogenation process for the production of c3-c6-(hydro)fluoroalkenes |
| EP4328213A3 (en) * | 2006-10-27 | 2024-04-03 | Honeywell International Inc. | A high purity 2,3,3,3-tetrafluoropropene |
| EP2091898A1 (en) * | 2006-10-31 | 2009-08-26 | E.I. Du Pont De Nemours And Company | Processes for producing 2,3,3,3-tetrafluoropropene and/or 1,2,3,3-tetrafluoropropene |
| CN101528645B (zh) | 2006-10-31 | 2013-10-30 | 纳幕尔杜邦公司 | 氟丙烷、卤代丙烯以及2-氯-3,3,3-三氟-1-丙烯与hf的共沸组合物和1,1,1,2,2-五氟丙烷与hf的共沸组合物的制备方法 |
| JP2010526982A (ja) | 2007-05-11 | 2010-08-05 | イー・アイ・デュポン・ドウ・ヌムール・アンド・カンパニー | 蒸気圧縮熱搬送システム中の熱交換方法、ならびに二列蒸発器または二列凝縮器を使用した中間熱交換器を含む蒸気圧縮熱交換システム |
| CN101687732A (zh) * | 2007-06-27 | 2010-03-31 | 阿科玛股份有限公司 | 用于制造氢氟烯烃的两步法 |
| US7884254B2 (en) * | 2007-08-08 | 2011-02-08 | Honeywell International Inc. | Dehydrochlorination of hydrochlorofluorocarbons using pre-treated activated carbon catalysts |
| US9035111B2 (en) | 2007-08-22 | 2015-05-19 | Honeywell International Inc. | Method for producing fluorinated organic compounds |
| US9079818B2 (en) | 2007-10-15 | 2015-07-14 | Honeywell International Inc. | Process for synthesis of fluorinated olefins |
| JP4849058B2 (ja) * | 2007-11-21 | 2011-12-28 | ダイキン工業株式会社 | 含フッ素オレフィンの製造方法 |
| EP2247560B1 (en) | 2008-02-21 | 2014-06-04 | E. I. du Pont de Nemours and Company | Processes for separation of 1,3,3,3-tetrafluoropropene from hydrogen fluoride by azeotropic distillation |
| KR20100138933A (ko) * | 2008-02-21 | 2010-12-31 | 이 아이 듀폰 디 네모아 앤드 캄파니 | 공비 증류에 의한 플루오르화수소로부터의 2,3,3,3-테트라플루오로프로펜의 분리 방법 |
| ES2699153T3 (es) | 2008-02-21 | 2019-02-07 | Chemours Co Fc Llc | Procedimientos para la separación de 3,3,3-trifluoropropeno y fluoruro de hidrógeno |
| EP2098499B2 (en) † | 2008-03-06 | 2017-11-22 | Honeywell International Inc. | Azeotrope-like composition of 2-chloro-3,3,3-trifluoropropene (HCFC-1233xf) and hydrogen fluoride (HF) |
| SG10201707156RA (en) | 2008-05-07 | 2017-10-30 | Du Pont | Compositions comprising 1,1,1,2,3-pentafluoropropane or 2,3,3,3- tetrafluoropropene |
| SI2634231T1 (sl) | 2008-05-07 | 2022-10-28 | The Chemours Company Fc, Llc | Sestavki |
| GB0808836D0 (en) | 2008-05-15 | 2008-06-18 | Ineos Fluor Ltd | Process |
| US8168837B2 (en) * | 2008-05-15 | 2012-05-01 | Honeywell International Inc. | Process for separating hydrogen fluoride from organic feedstocks |
| CN102076643B (zh) * | 2008-06-26 | 2014-08-06 | 阿科玛股份有限公司 | 1230xa至1234yf的催化气相氟化 |
| JP5119060B2 (ja) * | 2008-06-27 | 2013-01-16 | サンデン株式会社 | 冷凍サイクル |
| EP2326613B1 (en) * | 2008-08-26 | 2018-10-10 | Daikin Industries, Ltd. | Producing 2,3,3,3-tetrafluoropropene |
| FR2937328B1 (fr) | 2008-10-16 | 2010-11-12 | Arkema France | Procede de transfert de chaleur |
| US8008243B2 (en) * | 2008-10-31 | 2011-08-30 | Honeywell International Inc. | Azeotrope-like compositions of 1,1,2,3-tetrachloropropene and hydrogen fluoride |
| US20100119460A1 (en) * | 2008-11-11 | 2010-05-13 | Honeywell International Inc. | Azeotrope-Like Compositions Of 2,3,3,3-Tetrafluoropropene And 3,3,3-Trifluoropropene |
| EP2396293A1 (en) * | 2009-02-11 | 2011-12-21 | Arkema France | Azeotrope and azeotrope-like compositions of chlorotrifluoropropene and pentane |
| WO2010123148A1 (en) | 2009-04-23 | 2010-10-28 | Daikin Industries, Ltd. | Process for preparing 2-chloro-3,3,3-trifluoropropene |
| US8487145B2 (en) | 2009-06-03 | 2013-07-16 | E I De Pont De Nemours And Company | Catalysts and process to manufacture 2,3,3,3-tetrafluoropropene |
| WO2010141664A1 (en) | 2009-06-03 | 2010-12-09 | E. I. Du Pont De Nemours And Company | Catalysts and process to manufacture 2,3,3,3-tetrafluoropropene |
| FR2948362B1 (fr) * | 2009-07-23 | 2012-03-23 | Arkema France | Procede de preparation de composes fluores |
| FR2950066B1 (fr) * | 2009-09-11 | 2011-10-28 | Arkema France | Refrigeration basse et moyenne temperature |
| US8486293B2 (en) | 2009-10-30 | 2013-07-16 | E I Du Pont De Nemours And Company | Hydrogen fluoride-HFC-254eb azeotrope and its uses |
| JP2013510286A (ja) * | 2009-11-03 | 2013-03-21 | イー・アイ・デュポン・ドウ・ヌムール・アンド・カンパニー | フルオロオレフィン冷媒を用いるカスケード冷凍システム |
| MX2020010605A (es) | 2009-12-22 | 2022-06-14 | Du Pont | Composiciones que comprenden 2,3,3,3-tetrafluoropropeno, 1,1,2,3-tetracloropropeno, 2-cloro-3,3,3-trifluoropropeno, o 2-cloro-1,1,1,2-tetrafluoropropano. |
| MX2012009203A (es) * | 2010-02-12 | 2012-08-31 | Daikin Ind Ltd | Proceso para producir un alqueno que contiene fluor. |
| US8114308B2 (en) | 2010-03-30 | 2012-02-14 | Honeywell International Inc. | Azeotrope-like composition of 2,3-dichloro-3,3-difluoropropene (HCFO-1232xf) and hydrogen fluoride (HF) |
| US8927791B2 (en) | 2010-04-29 | 2015-01-06 | Honeywell International Inc. | Method for producing tetrafluoropropenes |
| US9492816B2 (en) | 2010-05-03 | 2016-11-15 | Arkema Inc. | Dehydrofluorination of pentafluoroalkanes to form tetrafluoroolefins |
| CN101913988B (zh) * | 2010-09-07 | 2013-09-25 | 西安近代化学研究所 | 2,3,3,3-四氟丙烯的制备方法 |
| US8741828B2 (en) * | 2011-02-23 | 2014-06-03 | Honeywell International Inc. | Azeotrope and azeotrope-like compositions useful for the production of haloolefins |
| CN102295522B (zh) * | 2011-05-27 | 2014-01-01 | 山东东岳高分子材料有限公司 | 2,3,3,3-四氟丙烯的制备方法 |
| FR2977584B1 (fr) * | 2011-07-08 | 2014-12-05 | Arkema France | Procede de separation et recuperation du 2,3,3,3-tetrafluoropropene et de l'acide fluorhydrique |
| CN104024189B (zh) * | 2011-12-28 | 2016-01-13 | 旭硝子株式会社 | 2,3,3,3-四氟丙烯的纯化方法,纯化装置及制造方法 |
| IN2014DN10381A (ru) | 2012-06-06 | 2015-08-14 | Du Pont | |
| FR3000095B1 (fr) * | 2012-12-26 | 2015-02-20 | Arkema France | Composition comprenant du 2,3,3,3-tetrafluoropropene et du 1,2-difluoroethylene |
| EP2939994B1 (en) | 2012-12-27 | 2018-07-18 | Asahi Glass Company, Limited | Method for purifying tetrafluoropropene |
| EP2970055B1 (en) | 2013-03-15 | 2018-07-25 | The Chemours Company FC, LLC | Process for the reduction of alkyne impurities in fluoroolefins |
| FR3003567B1 (fr) * | 2013-03-20 | 2015-03-06 | Arkema France | Composition comprenant hf et 3,3,3-trifluoropropene |
| FR3003569B1 (fr) * | 2013-03-20 | 2015-12-25 | Arkema France | Composition comprenant hf et 1,3,3,3-tetrafluoropropene |
| FR3003565B1 (fr) | 2013-03-20 | 2018-06-29 | Arkema France | Composition comprenant hf et 2,3,3,3-tetrafluoropropene |
| FR3003566B1 (fr) * | 2013-03-20 | 2018-07-06 | Arkema France | Composition comprenant hf et e-3,3,3-trifluoro-1-chloropropene |
| FR3015478B1 (fr) | 2013-12-19 | 2015-12-25 | Arkema France | Compositions azeotropiques a base de fluorure d'hydrogene et de z-3,3,3-trifluoro-1-chloropropene |
| JP6328589B2 (ja) | 2015-05-29 | 2018-05-23 | ダイキン工業株式会社 | 含フッ素オレフィンの製造方法 |
| GB2540427B (en) * | 2015-07-17 | 2017-07-19 | Mexichem Fluor Sa De Cv | Process for the preparation of 2,3,3,3-tetrafluoropropene (1234yf) |
| KR20160017661A (ko) | 2016-01-29 | 2016-02-16 | 한국과학기술연구원 | 헥사플루오로프로필렌으로부터 2,3,3,3-테트라플루오로프로펜과 1,3,3,3-테트라플루오로프로펜의 제조방법 |
| CN105669363A (zh) * | 2016-02-23 | 2016-06-15 | 常熟三爱富中昊化工新材料有限公司 | 一种含氟烯烃的纯化方法 |
| CN105622331A (zh) * | 2016-02-23 | 2016-06-01 | 常熟三爱富中昊化工新材料有限公司 | 一种含氟烯烃的制备方法 |
| GB201615209D0 (en) | 2016-09-07 | 2016-10-19 | Mexichem Fluor Sa De Cv | Catalyst and process using the catalyst |
| GB201615197D0 (en) | 2016-09-07 | 2016-10-19 | Mexichem Fluor Sa De Cv | Catalyst and process using the catalyst |
| FR3056222B1 (fr) | 2016-09-19 | 2020-01-10 | Arkema France | Composition a base de 1-chloro-3,3,3-trifluoropropene |
| FR3065726B1 (fr) * | 2017-04-28 | 2019-04-19 | Arkema France | Procede de production et de purification du 2,3,3,3-tetrafluoropropene. |
| JP7440409B2 (ja) | 2017-09-11 | 2024-02-28 | ザ ケマーズ カンパニー エフシー リミテッド ライアビリティ カンパニー | フッ化水素及びフルオロカーボンを含む共沸組成物 |
| FR3077572B1 (fr) | 2018-02-05 | 2021-10-08 | Arkema France | Composition azeotropique ou quasi-azeotropique ternaire comprenant hf, 2,3,3,3-tetrafluoropropene et 1,1,1,2,2,-pentafluoropropane. |
| EP3823948A1 (en) | 2018-07-18 | 2021-05-26 | The Chemours Company FC, LLC | Production of haloolefins in an adiabatic reaction zone |
| CN113624570B (zh) * | 2021-08-06 | 2023-04-28 | 清华大学 | 汽液相平衡装置及氟代烃中的hf的分析方法 |
Family Cites Families (22)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2931840A (en) * | 1958-11-25 | 1960-04-05 | Du Pont | Process for preparing 2, 3, 3, 3-tetrafluoropropene |
| US2996555A (en) * | 1959-06-25 | 1961-08-15 | Dow Chemical Co | Preparation of 2, 3, 3, 3-tetrafluoropropene |
| US4799260A (en) * | 1985-03-07 | 1989-01-17 | Dolby Laboratories Licensing Corporation | Variable matrix decoder |
| US4766260A (en) | 1987-07-07 | 1988-08-23 | E. I. Du Pont De Nemours And Company | Gas-phase fluorination process |
| JPH01207250A (ja) | 1988-02-12 | 1989-08-21 | Daikin Ind Ltd | 含フツ素オレフインの製造方法 |
| SU1706690A1 (ru) | 1988-04-19 | 1992-01-23 | Всесоюзный Научно-Исследовательский Институт Технического Углерода | Пористый углеродный материал |
| US4902838A (en) | 1988-12-28 | 1990-02-20 | E. I. Du Pont De Nemours And Company | Isomerization of saturated fluorohydrocarbons |
| US5136113A (en) | 1991-07-23 | 1992-08-04 | E. I. Du Pont De Nemours And Company | Catalytic hydrogenolysis |
| US5268122A (en) | 1991-08-28 | 1993-12-07 | E. I. Du Pont De Nemours And Company | Gem-dihydropolyfluoroalkanes and monohydropolyfluoroalkenes, processes for their production, and use of gem-dihydropolyfluoroalkanes in cleaning compositions |
| US5396000A (en) | 1993-05-24 | 1995-03-07 | E. I. Du Pont De Nemours And Company | Process for the manufacture of 1,1,1,2,3,-pentafluoropropane |
| US5396284A (en) * | 1993-08-20 | 1995-03-07 | Burle Technologies, Inc. | Motion detection system |
| JP4031052B2 (ja) | 1997-01-31 | 2008-01-09 | イー・アイ・デュポン・ドウ・ヌムール・アンド・カンパニー | ペンタフルオロプロペンの接触製造 |
| US5918481A (en) * | 1997-11-20 | 1999-07-06 | Alliedsignal Inc. | Process for separating hydrogen fluoride from fluorocarbons |
| JP2001524460A (ja) * | 1997-11-25 | 2001-12-04 | インペリアル・ケミカル・インダストリーズ・ピーエルシー | 弗素含有有機化合物の製造 |
| CA2333470C (en) | 1998-06-02 | 2008-08-26 | E.I. Du Pont De Nemours And Company | Process for the production of hexafluoropropylene from cc1f2cc1fcf3 and azeotropes of cclf2cc1fcf3 with hf |
| US7230146B2 (en) * | 2003-10-27 | 2007-06-12 | Honeywell International Inc. | Process for producing fluoropropenes |
| JP4148866B2 (ja) | 2003-09-30 | 2008-09-10 | 三洋電機株式会社 | 光ディスク装置 |
| ES2392333T3 (es) | 2004-04-16 | 2012-12-07 | Honeywell International Inc. | Composiciones de tipo azeótropo de tetrafluoropropeno y trifluoroyodometano |
| CA2564991C (en) * | 2004-04-29 | 2013-03-19 | Honeywell International Inc. | Processes for synthesis of 1,3,3,3-tetrafluoropropene and 2,3,3,3-tetrafluoropropene |
| CN1972887B (zh) * | 2004-04-29 | 2010-10-13 | 霍尼韦尔国际公司 | 1,3,3,3-四氟丙烯的合成方法 |
| US20060094911A1 (en) | 2004-10-29 | 2006-05-04 | Rao Velliyur N M | Noncatalytic manufacture of 1,1,3,3,3-pentafluoropropene from 1,1,1,3,3,3-hexafluoropropane |
| US7026520B1 (en) * | 2004-12-09 | 2006-04-11 | Honeywell International Inc. | Catalytic conversion of hydrofluoroalkanol to hydrofluoroalkene |
-
2006
- 2006-10-31 US US11/590,454 patent/US7476771B2/en active Active
- 2006-11-01 ES ES12160936.6T patent/ES2453159T3/es active Active
- 2006-11-01 EP EP06836796.0A patent/EP1954662B1/en active Active
- 2006-11-01 CN CN201210021126.8A patent/CN102603462B/zh active Active
- 2006-11-01 EP EP12160936.6A patent/EP2508499B1/en active Active
- 2006-11-01 UA UAA200806186A patent/UA95259C2/ru unknown
- 2006-11-01 JP JP2008539017A patent/JP5281407B2/ja active Active
- 2006-11-01 ES ES06836796T patent/ES2427099T3/es active Active
- 2006-11-01 AR ARP060104801A patent/AR058827A1/es not_active Application Discontinuation
- 2006-11-01 BR BRPI0619721-3A patent/BRPI0619721A2/pt not_active IP Right Cessation
- 2006-11-01 WO PCT/US2006/042771 patent/WO2007053736A2/en active Application Filing
- 2006-11-01 CA CA002627898A patent/CA2627898A1/en not_active Abandoned
- 2006-11-01 CN CN200680050042XA patent/CN101351428B/zh active Active
- 2006-11-01 EP EP12161039A patent/EP2476661A1/en not_active Withdrawn
- 2006-11-01 RU RU2008121963/04A patent/RU2422427C2/ru not_active IP Right Cessation
-
2008
- 2008-05-30 KR KR1020087013105A patent/KR101474026B1/ko active IP Right Grant
Non-Patent Citations (1)
| Title |
|---|
| MCDONIEL J.BRIDGET et al., Threshold energy and unimolecular rate constant for elimination of HF from chemically activates СF 3 СF 2 СН 3 : Effect of the СF 3 substituent on the alfa-carbon, J.FHYS.CHEM.A, vol.101, 1997, pages 1334-1337. ORKIN V.L. et al., Rate constants for the reactions of OH with HFC-245cd and some fluoroalkenes, J.FHYS.CHEM.A, vol.101, 1997, pages 9118-9124. * |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2007053736A3 (en) | 2007-08-02 |
| EP2476661A1 (en) | 2012-07-18 |
| KR20080066837A (ko) | 2008-07-16 |
| AR058827A1 (es) | 2008-02-27 |
| CN101351428B (zh) | 2012-06-27 |
| JP2009513719A (ja) | 2009-04-02 |
| CA2627898A1 (en) | 2007-05-10 |
| ES2453159T3 (es) | 2014-04-04 |
| JP5281407B2 (ja) | 2013-09-04 |
| EP1954662A2 (en) | 2008-08-13 |
| US20070100175A1 (en) | 2007-05-03 |
| KR101474026B1 (ko) | 2014-12-17 |
| RU2008121963A (ru) | 2009-12-10 |
| UA95259C2 (ru) | 2011-07-25 |
| CN102603462A (zh) | 2012-07-25 |
| CN102603462B (zh) | 2014-11-26 |
| ES2427099T3 (es) | 2013-10-28 |
| WO2007053736A2 (en) | 2007-05-10 |
| EP2508499A1 (en) | 2012-10-10 |
| CN101351428A (zh) | 2009-01-21 |
| BRPI0619721A2 (pt) | 2011-10-11 |
| EP2508499B1 (en) | 2014-01-08 |
| EP1954662B1 (en) | 2013-07-24 |
| US7476771B2 (en) | 2009-01-13 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2422427C2 (ru) | Азеотропные композиции, содержащие 2,3,3,3-тетрафторпропен и фтористый водород, и их использование в способах получения 2,3,3,3-тетрафторпропена | |
| KR101438240B1 (ko) | E-1,3,3,3-테트라플루오로프로펜 및 불화수소를 포함하는공비 조성물 및 그의 용도 | |
| JP5144525B2 (ja) | 1,1,1,2,3−ペンタフルオロプロペンおよびフッ化水素を含む共沸組成物およびその使用 | |
| KR101497709B1 (ko) | 노나플루오로펜텐 및 불화수소를 포함하는 공비 조성물 및그의 용도 | |
| JP2009513816A (ja) | トリデカフルオロ−3−ヘプテンとフッ化水素とを含む共沸組成物およびその使用 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20131102 |