KR880000062B1 - 인돌류 화합물의 제조방법 - Google Patents
인돌류 화합물의 제조방법 Download PDFInfo
- Publication number
- KR880000062B1 KR880000062B1 KR1019830003076A KR830003076A KR880000062B1 KR 880000062 B1 KR880000062 B1 KR 880000062B1 KR 1019830003076 A KR1019830003076 A KR 1019830003076A KR 830003076 A KR830003076 A KR 830003076A KR 880000062 B1 KR880000062 B1 KR 880000062B1
- Authority
- KR
- South Korea
- Prior art keywords
- catalyst
- hydroxy
- group
- hydrogen
- reaction
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/02—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom condensed with one carbocyclic ring
- C07D209/04—Indoles; Hydrogenated indoles
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/02—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom condensed with one carbocyclic ring
- C07D209/04—Indoles; Hydrogenated indoles
- C07D209/08—Indoles; Hydrogenated indoles with only hydrogen atoms or radicals containing only hydrogen and carbon atoms, directly attached to carbon atoms of the hetero ring
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Catalysts (AREA)
- Indole Compounds (AREA)
- Low-Molecular Organic Synthesis Reactions Using Catalysts (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
내용 없음.
Description
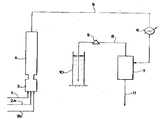
도면은 반응 설비의 개략적인 배열을 나타내는 간단한 플로우 다이아그램이다.
본 발명은 원료 물질로서 N-(β-히드록시)알킬아닐린류를 사용하여 인돌류를 제조하는 개량방법에 관한 것이다.
인돌류는 화학 산업에 원료 물질로서 공지되어 있으며 특히 최근 방향 물질과 아미노산의 합성을 위한 원료 물질로서의 인돌의 중요성이 증가하고 있다.
지금까지 인돌류를 합성적으로 얻기 위한 여러가지 시도가 행해져왔다. 그러나, 이러한 시도들은 다 단계제조 과정이 필요하고 많은 부생물이 생성되는 등의 여러가지의 문제성을 수반한다.
이와 같은 종래 기술의 방법중에서, N-(β-히드록시)알킬아닐린류의 기상 촉매 반응에 의지하는 인돌류의 제조방법이 그의 선택성의 관점에서 더 개량이 필요하며 그의 표면상에 탄소질의 침적물이 축적되는 것으로 인한 촉매의 활성이 심히 감소하는 것과 같은 문제점이 수반된다.
본 발명의 목적은 촉매의 활성감소를 막고 인돌의 개량된 선택성을 보장하면서 N-(β-히드록시)알킬아닐린의 기상 반응을 통하여 인돌을 제조하는 방법을 제공하는 것이다.
상기의 목적을 달성하기 위하여, 본 발명자들은 N-(β-히드록시)알킬아닐린류의 기상 촉매 반응에 대하여 상세히 연구를 행하였다. 그 결과 놀랍게도, 르샤트리에 - 브라운의 원칙과는 반대로, 초대기압에서 반응을 행하므로써 촉매의 활성 감소를 막을 수 있을 뿐만 아니라 목적하는 인돌의 형성을 위한 선택성을 개량할 수 있음을 발견하였다.
그러므로, 본 발명은 인돌의 하기의 제조 방법을 제공한다 :
촉매 존재하 N-(β-히드록시)알킬아닐린을 기상 촉매 반응시킴으로써 인돌을 제조하는 방법에서, 개량 방법의 특징은 초대기압에서 반응을 행하는 것이다.
본 발명에서, 예를 들어, N-(β-히드록시)에틸아닐린은 하기의 반응식에 따라 반응을 행한다 :
도면은 실시예 1에서 사용된 반응 설비의 배열의 개략을 나타내는 간단한 다이아그램이다.
본 발명에 따른 방법에서 실제로 유용한 N-(β-히드록시)알킬아닐린류는 하기식(I)으로 표시될 수 있다.
상기 식에서, R0및 R1은 각각 수소 또는 할로겐원자 또는 히드록실, 치환되지 않은 알킬, 치환된 알킬 또는 알콕시기를 의미하고, R2는 수소 또는 할로겐원자 또는 비치환된 알킬, 치환된 알킬 또는 알콕시기인데, 치환된 아미노기의 2 또는 6 위가 R0에 의하여 치환되지 않은 조건을 갖는다.
상기의 일반식(I)에서, R0는 바람직하게는 수소 또는 할로겐원자 또는 히드록실, 치환되지 않은 알킬 또는 알콕시기이고, R1및 R2는 바람직하게는 각각 수소 또는 할로겐 원자 또는 임의로 치환될 수 있는 알킬기이다. 더 바람직하게는, R0는 수소 또는 할로겐원자 또는 히드록실, 메틸 또는 메톡시기이고, R1및 R2는 각각 수소원자 또는 매틸, 에틸 또는 β-히드록시에틸기이다.
N-(β-히드록시)알킬아닐린의 특징예로서 하기의 화합물을 들 수 있다 :
N-(β-히드록시)에틸아닐린 ;
N-(β-히드록시)에틸톨루이딘 ;
N-(β-히드록시)에틸할로아닐린 ;
N-(β-히드록시)에틸히드록시아닐린 ;
N-(β-히드록시)에틸아니시딘 ;
N-(α-알킬-β-히드록시)에틸아닐린 ;
N-(α-알킬-β-히드록시)에틸톨루이딘 ;
N-(α-알킬-β-히드록시)에틸할로아닐린 ;
N-(α-알킬-β-히드록시)에틸히드록시아닐린 ;
N-(α-알킬-β-히드록시)에틸아니시딘 ;
N-(α-할로-β-히드록시)에틸아닐린 ;
N-(α-할로-β-히드록시)에틸할로아닐린 ;
N-(α-할로-β-히드록시)에틸히드록시아닐린 ;
N-(α-할로-β-히드록시)에틸아니시딘 ;
N-(α-알킬-β-히드록시)에틸아닐린 ;
N-(α-알킬-β-히드록시)에틸톨루이딘 ;
N-(α-알킬-β-히드록시)에틸할로아닐린 ;
N-(α-알킬-β-히드록시)에틸히드록시아닐린 ;
N-(α-알킬-β-히드록시)에틸아니시딘 ;
N-(α-할로-β-히드록시)에틸아닐린 ;
N-(α-할로-β-히드록시)에틸할로아닐린 ;
N-(α-할로-β-히드록시)에틸히드록시아닐린 ;
N-(α-할로-β-히드록시)에틸아니시딘 ; 등.
하기의 촉매들은 본 발명에 따른 방법에 실지로 사용될 수 있다 :
(1) Si, Al, B, Sb, Bi, Sn, Pb, Ga, Ti, In, Sr, Ca, Zr, Be, Mg, Y, Cu, Ag, Zn, Cd 및 란타나이드류(이하 "촉매 물질(1)"라 칭함)로 이루어진 군으로부터 선택된 1종 이상의 원소의 산화물 또는 수산화물, 예를 들어, Cdo, Al2O3-B2O3, SiO2-ZnO, SiO2-CaO, SiO2-In2O3, SiO2-SrO, SiO2-Cdo, SiO2-MgO, TiO2-SnO2, CdO-Bi2O3, SiO2-Y2O3, SiO2, Bi2O3-B2O, SiO2-La2O3, SiO2-Ce2O3, SiO2-ZnO-AgO, SiO-MgO-CuO 등을 함유하는 촉매
(2) Pd, Pt, Cr, Fe, Ni, Co, Zn, Mo, Cd 및 W(이하 "촉매물질(2)"라 칭함)로 이루어진 군으로부터 선택된 하나 이상의 원소의 설파이드 또는 셀레나이드, 예를 들어, PdS, PtS, CrS, FeS, NiS, CoS, ZnS, MoS2, CdS, WS2, ZnSe, CdSe 등을 함유하는 촉매 ;
(3) 무기염, 즉, Fe, Tl, Ca, Mn, Bi, Sr, Y, Al, Zn, Cd, Ni, Mg, In, Be, Co, Ga 및 란타나이드(이하 "촉매 물질(3)"이라 칭함)의 할라이드, 카르보네이트, 설패이트, 포스페이트, 피로포스페이트, 포스포몰리브데이르 또는 실리코팅스페이트, 예를 들어, 황산 제2철, 황산 탈륨; 황산 칼슘, 황산 망간, 황산 비스무스, 황산 스트론륨, 황산 이트륨, 브롬화 카드륨, 황산 알루미늄, 황산 아연, 황산 니켈, 염화 카드뮴, 황산 마그네슘, 황산 인듐, 황산 베릴륨, 황산 코발트, 황산 알루미늄 아연, 염화 마그네슘, 황산 카드뮴, 인산 카드뮴 등을 함유하는 촉매 ; 및
(4) Cu, Ag, Pt, Pd, Ni, Co, Fe, Ir, Os, Ru 및 Rh(이하 "촉매물질(4)"라칭함)로 이루어진 군으로 부터 선택된 원소 하나 이상을 함유하는 금속 촉매.
이들 촉매들은 종래 기술의 방법에 의하여 제조될 수 있다. 즉, 촉매물질(1)은 촉매-구성 원소의 수용성염을 그의 수산화물로 가수분해시킨 다음 건조 및 하소시켜 겔을 수득하거나 또는 촉매-구성 원소의 쉽게 분해될 수 있는 염을 공기중에서 열분해함으로써 제조될 수 있다.
촉매 물질(2)는 황화 나트륨 또는 셀렌화 칼륨을 촉매-구성원소의 수용성 염에 가하거나 또는 촉매-구성원소 또는 그의 염을 황화 수소 기체 또는 셀렌화 수소 기체와 접촉시킴으로써 제조될수 있다.
촉매물질(4)는 촉매-구성 원소의 염, 수산화물 또는 산화물을 수소, 포름알데히드, 포름산, 아인산, 히드라진 등과 같은 환원제로 환원시킴으로써 제조될 수 있다.
이들 촉매들은 상술한 촉매물질(1), (2), (3)및 (4)를 단독으로 또는 혼합물로서 함유한다. 이와 같은 촉매물질은 촉매상에 담지될수 있다. 종래 사용된 임의의 촉매가 사용되어도 무방하나 흔히 규조토, 부석, 티타니아, 실리카-알루미나, 알루미나, 마그네시아, 실리카켈, 활성탄, 활성 클레이, 아스베스토스 등이 사용된다. 담채-지지 촉매는 이들 담채를 졸래 공지의 기술로 상술한 촉매 물질상에 지지시킴으로써 제조될 수 있다.
담체 상에 지시될 각각의 상기 총매물질의 양에는 특별한 제한이 없다. 상기 각 촉매물질의 양은 보통 사용될 담채의 형태에 적당량, 예를 들어, 1∼50% 의존하여 지지될 수 있다.
본 발명에 따른 방법에 사용 가능한 촉매로서 황화 아연, 황화 카드뮴, 염화 마그네슘, 황산 카드뮴, 황산 아연, 황산 알루미늄, 아연, 백금, 팔라듐 또는 루테늄을 함유하는 촉매 뿐 아니라 금속으로서 구리 또는 은 또는 산화물을 함유하는촉매가 사용 가능하다.
본 발명에 사용하기에 특히 바람직한 촉매는 금속으로서 Cu 또는 Ag또는 산화물을 1∼50중량%, 바람직하게는 5∼50중량%의 양으로 그리고 SiO2를 10중량% 이상의 양으로 함유하는 촉매이다.
본 발명에 따른 방법의 반응은 기상에서 상술한 촉매 존재하 수행된다. 반응은 고정층 반응기, 유동층 반응기 또는 이동층 반응기 중에서 수행될 수 있다.
반응을 위한 원료 물질일 N-(β-히드록시)알킬아닐린은, 액체 매시 공간 속도로, 0.005∼10hr-1, 특히 0.01∼10hr-1의 범위내의 공급 속도로 충전될 수 있다. 증발기에서 미리 증기화한 후 반응기에 충전될 수 있다. 여기서, 이와 같이 증기화 된 원료 물질과 함께 캐리어 기체로서 아닐린, 증기, 수소, 일산화탄소, 메탄, 벤젠, 톨루엔, 질소, 네온 또는 아르곤 등을 함께 공급하는 것이 좋다. 이들 캐리어 기체들 중에서, 아닐린, 증기 또는 수소를 사용하는 것이 특히 바람직한데, 왜냐하면 증기 또는 수소가 촉매의 재생 싸이클을 연장하는데 효과적이며 아닐린이 목적하는 반응 생성물의 수율을 향상시키는데 효과적이기 때문이다.
반응 온도는 200∼600℃, 바람직하게는 250∼500℃의 범위이다.
여기에서 사용된 "초대기압"이란 말은 표준 대기압 이상의 압력을 의미하며 측합 상을 형성하기 위하여 여러가지 성분이 반응 대역내에 존재하도록 하지 않는다. 실질적으로 말해서, 초대기압은 바람직하게는 1.1×105Pa∼5.0×106Pa범위, 특히 바람직하게는 2.0×105Pa∼3.0×106Pa범위이다. 담체 기체가 원료 물질과 함께 공급되는 경우, 총반응압은 원료 물질의 분압과 캐리어 기체의 분압의 합계이다.
일반적으로 말해서, 반응 온도가 높은 곳에서는 반응압을 올리고 반응 온도가 낮은 곳에서는 반응압을 낮추는 것이 바람직하다. 높은 수소-활성 능력을 갖는 물질을 함유하는 촉매를 사용하고 캐리어 기체로서 수수를 사용하는 경우 수소의 분압을 1.0×106Pa 이하로 제한하는 것이 바람직하다.
본 발명에 따른 방법은 본 발명의 이 효과의 원인이 충분히 설명되지 않음에도 불구하고 각 촉매의 활성 감소를 억제하는 데 효과적이다.
본 발명은 하기의 실시예에서 설명된다.
[실시예 1 및 비고예 1]
도면에 설명된 오오토클레이브를 사용하여 실험을 행한다. 내부 직경이 20㎜인 스테인레스제 실린더형 반응기 4에 각각 직경 3㎜이고 높이가 2.5㎜인 펠릿형 촉매400cc를 채우는데, 이 촉매는 통상의 황화 카드뮴을 정제화 함으로써 수득된다. N-(β-히드록시)에틸아닐린과 아닐린의 1 : 5 몰비의 혼합물과 물을, 각각, 공급 라인 1및 공급라인 2b를 통하여 증발기 3및 실린더형 반응기 4를 내부 온도 340℃로 유지하면서 증발기 3에 80 g/hr 및 20 g/hr 로 채운다. 동시에, 수소기체를 표준조건하 측정된 50ℓ/hr로 공급 라인 2a를 통하여 채운다. 유출 기류를 반응기 4로부터 유도 해내어 라인 5을 통하여 콘데서 6으로 보내어 냉각 시킨다. 생성된 액체 축합물을 기체-액체 분리기 7중에서 기상으로부터 분리하여 라인 11을 통하여 배출시킨다. 한편, 기상을 라인 8을 통하여 운반하여 감소 밸브 9를 통과시키면서 강압시키면서 감압시킨 수밀폐된 실린더 10을 통하여 배출시킨다.
인돌의 합성 반응은 전체 반응압을 하기와 같이 변경시킴으로써 수행된다. 결과는 표 1에 나타나있다.
[표 1]
[실시예 2∼3 & 비교예 2∼3 ]
실시예 1의 방법에 따라, 단지 촉매만을 바꿈으로서 반응를 행한다. 비교 실시예에서는 상압하에서 반응을 행한다. 결과는 표 2와 같다.
[실시예 4∼ 비교예 4 ]
물유리, 질산구리, 질산 아연 및 질산 망간 수용액을 혼합한 다음 공침법에 따라 처리함으로써, 즉, 암모니아 수로 처리함으로써 그의 산화물(CuO : SiO2: ZnO : MnO)로서 측정된 40 : 20 : 30 : 10의 중량비의 Cu, Si, Zn 및 Mn 을 함유하는 침전을 얻는다. 침전을 철저히 수세한 후, 110℃에서 3시간 동안 건조 및 분쇄시켜 정제화한 다음 500℃에서 3시간 동안 불에 굽는다. 이와 같이 수득된 촉매를 사용하여 실시예 1과 같은 방법으로 실험을 행한다. 비교예에서는 상압하 반응을 행한다. 결과는 표 2와 같다.
[실시예 5∼8 & 비교예 5∼8 ]
실시예 4의 방법에 따라, 표 2에 주어진 조성을 갖는 촉매가 제조된다. 반응은 실시예 1과 동일한 방법으로 행한다. 비교예에서는 상압하 반응을 행한다. 결과는 표 2와 같다.
[실시예 9 및 비교예 9 ]
실시예 4의 방법에 따라, 표 2에 주어진 중량비의 조성을 갖는 담체가 제조된다. 이와 같이 수득된 담체를 5몰 /ℓ의 암모니아 및 0.1몰/ℓ의 아세트산은을 함유하는 수용액 중에 침지시킨 후 건조시키고, 히드라진의 3%수용액에 침지시킨 다음 건조시킨다. 이 침지 및 건조 과정을 반복하여 10중량%의 Ag이 담지된 촉매가 제조된다. 반응을 실시예 1과 같은 방법으로 행한다. 비교예에서는 상압하 반응을 수행한다. 결과는 표 2와 같다.
[실시예 10∼13 &비교예 10∼12 ]
실시예 9의 방법에 따라, 표 2에 주어진 조성을 갖는 담체상에 담지된 Cu 또는 Ag 촉매가 제조된다. 반응은 실시예 1과 같은 방법으로 수행된다. 비교예에서는 상압하 반응을 수행한다. 결과는 표 2와 같다.
[표 2]
주 :*NHEA-C : N-(β-히드록시)에틸아닐린의 전환율
**I-S : 인돌의 선택성
Claims (14)
- N-(β-히드록시)알킬아닐린을 촉매 존재하 기상 촉매 반응시킴으로써 인돌을 제조함에 있어서, 반응이 초대기압하 수행됨을 특징으로 하는 방법.
- 제 2항에 있어서, 식(I)에서 R0가 수소 또는 할로겐원자 또는 히드록실, 알킬, 또는 알콕시기이고, R1및 R2가 각각 수소 또는 할로겐원자 또는 임의로 치환 가능한 알킬기임이 특징인 방법.
- 제 2항에 있어서, 식(I)에서 R0가 수소 또는 할로겐원자 또는 히드록실, 메틸 또는 메톡시기이고, R1및 R2가 각각 수소원자 또는 메틸, 에틸 또는 β-히드록시에틸기임이 특징인 방법.
- 제 2항에 있어서, 식(I)의 화합물의 N-( β-히드록시)에틸아닐린임이 특징인 방법.
- 제 1항에 있어서, 촉매가 Si, Al, B, Sb, Bi, Su, Pb, Ga, Ti, In, Sr, Ca, Zr, Be, Mg, Y, Cu, Ag, Zn, Cd 및 란타니드로 이루어진 군으로부터 선택된 1종 이상의 원소의 산화물 또는 수산화물을 함유하는 화합물임이 특징인 방법.
- 제 1항에 있어서, 촉매가 Pd, Pt, Cr, Fe, Ni, Co, Zn, Mo, Cd 및 W로 이루어진 군으로부터 선택된 1종 이상의 원소의 황화물 또는 셀렌화물을 함유하는 촉매임이 특징인 방법.
- 제 1항에 있어서, 촉매가 Fe, T1, Ca, Mn, Bi, Sr, Y, A1, Zn, Cd, Ni, Mg, In, Be, Co, Ga 및 란타니드로 이루어진 군으로부터 선택된 1종이상의 원소의 무기염을 함유하는 촉매임이 특징인 방법.
- 제 1항에 있어서, 촉매가 Cu, Ag, Pt, Pd, Ni, Co, Fe, Ir, Os, Ru 및 Rh 로 이루어진 군으로부터 선택된 1종 이상의 원소를 함유하는 촉매임이 특징인 방법.
- 제 1항에 있어서, 반응이 200∼600℃ 범위내의 온도에서 수행됨이 특징인 방법.
- 제 1항에 있어서, 초대기압이 1.1×105Pa∼5.0×106Pa의 범위임이 특징인 방법.
- 제 1항에 있어서, N-(β-히드록시)알킬아닐린이 액체 시속 공간 속도로 0.005∼10hr-1범위내로 공급속도로 충전됨이 특징인 방법.
- 제 1항에 있어서, N-(β-히드록시)알킬아닐린이 기화된 다음, 아닐린, 증기, 수소, 일산화탄소,메탄, 벤젠, 톨루엔, 질소, 네온 및 아르곤으로 이루어진 군으로부터 선택된 캐리어 기체와 함께 반응 대역내로 공급됨이 특징인 방법.
- 제 13항에 있어서, 캐리어 기체가 아닐린임이 특징인 방법.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP117824/1982 | 1982-07-08 | ||
| JP117824 | 1982-07-08 | ||
| JP57117824A JPS5910565A (ja) | 1982-07-08 | 1982-07-08 | インド−ル類化合物の製造方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR840005423A KR840005423A (ko) | 1984-11-12 |
| KR880000062B1 true KR880000062B1 (ko) | 1988-02-22 |
Family
ID=14721151
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1019830003076A KR880000062B1 (ko) | 1982-07-08 | 1983-07-06 | 인돌류 화합물의 제조방법 |
Country Status (9)
| Country | Link |
|---|---|
| US (1) | US4916236A (ko) |
| JP (1) | JPS5910565A (ko) |
| KR (1) | KR880000062B1 (ko) |
| CA (1) | CA1194492A (ko) |
| CH (1) | CH653674A5 (ko) |
| DE (1) | DE3324092A1 (ko) |
| FR (1) | FR2529889B1 (ko) |
| GB (1) | GB2123822B (ko) |
| NL (1) | NL189195C (ko) |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2594436B1 (fr) * | 1986-02-20 | 1988-10-28 | Elf Aquitaine | Procede de preparation de l'indole |
| JPH03271217A (ja) * | 1990-03-22 | 1991-12-03 | Chon Nan Hoan | 線香 |
| US6077487A (en) * | 1997-11-05 | 2000-06-20 | Millipore Corporation | Process and apparatus of removing metal carbonyls and moisture from a gas |
| KR20080037196A (ko) * | 2006-10-25 | 2008-04-30 | 변영광 | 튜브형 화장품용기용 체크밸브의 구조 |
Family Cites Families (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE2731192C2 (de) * | 1977-07-09 | 1985-05-15 | Ernst Leitz Wetzlar Gmbh, 6330 Wetzlar | Spiegelreflexkamera mit Pentaprisma und elektronischem Entfernungsmesser |
| JPS603296B2 (ja) * | 1979-02-09 | 1985-01-26 | 三井東圧化学株式会社 | インド−ル類の製造法 |
| JPS6028818B2 (ja) * | 1979-02-13 | 1985-07-06 | 三井東圧化学株式会社 | インド−ルまたはインド−ル誘導体の製造法 |
| JPS565459A (en) * | 1979-06-27 | 1981-01-20 | Mitsui Toatsu Chem Inc | Preparation of indole |
| JPS5651451A (en) * | 1979-10-03 | 1981-05-09 | Mitsui Toatsu Chem Inc | Preparation of indole or its derivative |
| JPS5655365A (en) * | 1979-10-13 | 1981-05-15 | Mitsui Toatsu Chem Inc | Preparation of indole or indole derivative |
| JPS5661353A (en) * | 1979-10-23 | 1981-05-26 | Mitsui Toatsu Chem Inc | Preparation of indole or indole derivative |
| JPS56113761A (en) * | 1980-02-13 | 1981-09-07 | Mitsui Toatsu Chem Inc | Preparation of indole or indole derivative |
| JPS5923306B2 (ja) * | 1980-06-03 | 1984-06-01 | 三井東圧化学株式会社 | インド−ルまたはインド−ル誘導体の製造方法 |
| JPS5735564A (en) * | 1980-08-14 | 1982-02-26 | Mitsui Toatsu Chem Inc | Preparation of indole or indole derivative |
| US4376205A (en) * | 1981-04-15 | 1983-03-08 | Mitsui Toatsu Chemicals, Inc. | Process for the preparation of indoles from anilines and ethanolamines |
| US4443615A (en) * | 1981-11-10 | 1984-04-17 | Tanabe Seiyaku Co., Ltd. | Process for preparing indoles |
-
1982
- 1982-07-08 JP JP57117824A patent/JPS5910565A/ja active Granted
-
1983
- 1983-06-29 GB GB08317676A patent/GB2123822B/en not_active Expired
- 1983-07-05 DE DE3324092A patent/DE3324092A1/de active Granted
- 1983-07-06 KR KR1019830003076A patent/KR880000062B1/ko not_active IP Right Cessation
- 1983-07-07 CA CA000432038A patent/CA1194492A/en not_active Expired
- 1983-07-07 CH CH3741/83A patent/CH653674A5/de not_active IP Right Cessation
- 1983-07-07 NL NLAANVRAGE8302424,A patent/NL189195C/xx not_active IP Right Cessation
- 1983-07-08 FR FR8311450A patent/FR2529889B1/fr not_active Expired
-
1988
- 1988-11-14 US US07/270,067 patent/US4916236A/en not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| GB8317676D0 (en) | 1983-08-03 |
| FR2529889A1 (fr) | 1984-01-13 |
| NL8302424A (nl) | 1984-02-01 |
| KR840005423A (ko) | 1984-11-12 |
| CA1194492A (en) | 1985-10-01 |
| GB2123822A (en) | 1984-02-08 |
| JPS5910565A (ja) | 1984-01-20 |
| JPS6356222B2 (ko) | 1988-11-07 |
| NL189195C (nl) | 1993-02-01 |
| GB2123822B (en) | 1986-02-12 |
| US4916236A (en) | 1990-04-10 |
| DE3324092C2 (ko) | 1987-11-12 |
| FR2529889B1 (fr) | 1985-09-06 |
| CH653674A5 (de) | 1986-01-15 |
| NL189195B (nl) | 1992-09-01 |
| DE3324092A1 (de) | 1984-01-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JPS6045938B2 (ja) | シュウ酸ジエステルの水素添加触媒の製造法 | |
| JPH024448A (ja) | ルテニウムの支持された触媒、その製造方法及びその使用 | |
| KR880000062B1 (ko) | 인돌류 화합물의 제조방법 | |
| US20040087815A1 (en) | Catalyst for dehydrogenation of cyclohexanol and method for preparation thereof | |
| CA1224492A (en) | Alkylation process | |
| US4480131A (en) | Process for selective production of di- and tri-alkylamines | |
| KR920007593B1 (ko) | 메탄올의 분해방법 | |
| US4937353A (en) | Preparation process for indoles | |
| KR860001577B1 (ko) | 인돌의 개량된 제조방법 | |
| EP0180957B1 (en) | Preparation process of indoles | |
| US5026922A (en) | Process for preparing glycol aldehyde | |
| JP2002155051A (ja) | インドール類の製造方法 | |
| JPH06184066A (ja) | ジフエニルアミン類の製造方法 | |
| JPH0243738B2 (ko) | ||
| US2971984A (en) | Process for preparing butyraldehyde | |
| JPH0243736B2 (ko) | ||
| JPS61189265A (ja) | インド−ル類の製造法 | |
| JPH066573B2 (ja) | インド−ルの製造方法 | |
| JPH0432065B2 (ko) | ||
| JPH0544941B2 (ko) | ||
| JPH0544451B2 (ko) | ||
| JP2002338543A (ja) | インドール類の製造方法 | |
| JPS57193419A (en) | Selective hydrogenation of acetylene compound | |
| JPH04261165A (ja) | モルフォロンの製造法 | |
| JPH0468294B2 (ko) |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| E902 | Notification of reason for refusal | ||
| E601 | Decision to refuse application | ||
| J2X1 | Appeal (before the patent court) |
Free format text: APPEAL AGAINST DECISION TO DECLINE REFUSAL |
|
| G160 | Decision to publish patent application | ||
| E701 | Decision to grant or registration of patent right | ||
| GRNT | Written decision to grant | ||
| FPAY | Annual fee payment |
Payment date: 19960216 Year of fee payment: 9 |
|
| LAPS | Lapse due to unpaid annual fee |