KR20170140306A - 대사적으로 프로그램화된 금속 킬레이트화제 및 그의 용도 - Google Patents
대사적으로 프로그램화된 금속 킬레이트화제 및 그의 용도 Download PDFInfo
- Publication number
- KR20170140306A KR20170140306A KR1020177033736A KR20177033736A KR20170140306A KR 20170140306 A KR20170140306 A KR 20170140306A KR 1020177033736 A KR1020177033736 A KR 1020177033736A KR 20177033736 A KR20177033736 A KR 20177033736A KR 20170140306 A KR20170140306 A KR 20170140306A
- Authority
- KR
- South Korea
- Prior art keywords
- compound
- pharmaceutically acceptable
- certain embodiments
- acceptable salt
- substituted
- Prior art date
Links
- 0 CC[C@@](C)(CCC(C1)C=*C1C(C)CC1CC1)*=C* Chemical compound CC[C@@](C)(CCC(C1)C=*C1C(C)CC1CC1)*=C* 0.000 description 27
- VOOPPDTWLVCZDY-QUMQEAAQSA-N C/C(/C(O)=O)=C\C=C(/C=C)\[n]1nc(-c2ccccc2O)nc1-c1ccccc1O Chemical compound C/C(/C(O)=O)=C\C=C(/C=C)\[n]1nc(-c2ccccc2O)nc1-c1ccccc1O VOOPPDTWLVCZDY-QUMQEAAQSA-N 0.000 description 1
- RMZURDANJYUWRU-TYZXPVIJSA-N C[C@@]1(C(O)=O)N(C)C(c(c(O)c2)ccc2OCC(O)=O)SC1 Chemical compound C[C@@]1(C(O)=O)N(C)C(c(c(O)c2)ccc2OCC(O)=O)SC1 RMZURDANJYUWRU-TYZXPVIJSA-N 0.000 description 1
- JYNIJTOYUFXDEQ-BZSJEYESSA-N C[C@@]1(C(O)=O)N(C)C(c(c(O)c2)ccc2OCCOCC(O)=O)SC1 Chemical compound C[C@@]1(C(O)=O)N(C)C(c(c(O)c2)ccc2OCCOCC(O)=O)SC1 JYNIJTOYUFXDEQ-BZSJEYESSA-N 0.000 description 1
- GTPPREGWVQQLGP-BZSJEYESSA-N C[C@@]1(C(O)=O)N(C)C(c(c(O)c2)ccc2OCCOCCO)SC1 Chemical compound C[C@@]1(C(O)=O)N(C)C(c(c(O)c2)ccc2OCCOCCO)SC1 GTPPREGWVQQLGP-BZSJEYESSA-N 0.000 description 1
- NZDDFVZFKYIWKT-OAHLLOKOSA-N C[C@@]1(C(O)=O)N=C(c(c(O)c2)ccc2OCCCC(O)=O)SC1 Chemical compound C[C@@]1(C(O)=O)N=C(c(c(O)c2)ccc2OCCCC(O)=O)SC1 NZDDFVZFKYIWKT-OAHLLOKOSA-N 0.000 description 1
- OWQWNOJSWWMKMA-QGZVFWFLSA-N C[C@@]1(C(O)=O)N=C(c(c(O)c2)ccc2OCCCCCC(O)=O)SC1 Chemical compound C[C@@]1(C(O)=O)N=C(c(c(O)c2)ccc2OCCCCCC(O)=O)SC1 OWQWNOJSWWMKMA-QGZVFWFLSA-N 0.000 description 1
- WZONZWBUALMATA-QGZVFWFLSA-N C[C@@]1(C(O)=O)N=C(c(c(O)c2)ccc2OCCCCCCO)SC1 Chemical compound C[C@@]1(C(O)=O)N=C(c(c(O)c2)ccc2OCCCCCCO)SC1 WZONZWBUALMATA-QGZVFWFLSA-N 0.000 description 1
- NKDUIYSNZOPXIR-GOSISDBHSA-N C[C@@]1(C(O)=O)N=C(c(c(O)c2)ccc2OCCCCCCOC)SC1 Chemical compound C[C@@]1(C(O)=O)N=C(c(c(O)c2)ccc2OCCCCCCOC)SC1 NKDUIYSNZOPXIR-GOSISDBHSA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D277/00—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings
- C07D277/02—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings
- C07D277/08—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings having one double bond between ring members or between a ring member and a non-ring member
- C07D277/12—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings having one double bond between ring members or between a ring member and a non-ring member with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/425—Thiazoles
- A61K31/426—1,3-Thiazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P39/00—General protective or antinoxious agents
- A61P39/02—Antidotes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/06—Antianaemics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C211/00—Compounds containing amino groups bound to a carbon skeleton
- C07C211/43—Compounds containing amino groups bound to a carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings of the carbon skeleton
- C07C211/54—Compounds containing amino groups bound to a carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings of the carbon skeleton having amino groups bound to two or three six-membered aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C215/00—Compounds containing amino and hydroxy groups bound to the same carbon skeleton
- C07C215/46—Compounds containing amino and hydroxy groups bound to the same carbon skeleton having hydroxy groups bound to carbon atoms of at least one six-membered aromatic ring and amino groups bound to acyclic carbon atoms or to carbon atoms of rings other than six-membered aromatic rings of the same carbon skeleton
- C07C215/48—Compounds containing amino and hydroxy groups bound to the same carbon skeleton having hydroxy groups bound to carbon atoms of at least one six-membered aromatic ring and amino groups bound to acyclic carbon atoms or to carbon atoms of rings other than six-membered aromatic rings of the same carbon skeleton with amino groups linked to the six-membered aromatic ring, or to the condensed ring system containing that ring, by carbon chains not further substituted by hydroxy groups
- C07C215/50—Compounds containing amino and hydroxy groups bound to the same carbon skeleton having hydroxy groups bound to carbon atoms of at least one six-membered aromatic ring and amino groups bound to acyclic carbon atoms or to carbon atoms of rings other than six-membered aromatic rings of the same carbon skeleton with amino groups linked to the six-membered aromatic ring, or to the condensed ring system containing that ring, by carbon chains not further substituted by hydroxy groups with amino groups and the six-membered aromatic ring, or the condensed ring system containing that ring, bound to the same carbon atom of the carbon chain
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C229/00—Compounds containing amino and carboxyl groups bound to the same carbon skeleton
- C07C229/02—Compounds containing amino and carboxyl groups bound to the same carbon skeleton having amino and carboxyl groups bound to acyclic carbon atoms of the same carbon skeleton
- C07C229/04—Compounds containing amino and carboxyl groups bound to the same carbon skeleton having amino and carboxyl groups bound to acyclic carbon atoms of the same carbon skeleton the carbon skeleton being acyclic and saturated
- C07C229/06—Compounds containing amino and carboxyl groups bound to the same carbon skeleton having amino and carboxyl groups bound to acyclic carbon atoms of the same carbon skeleton the carbon skeleton being acyclic and saturated having only one amino and one carboxyl group bound to the carbon skeleton
- C07C229/10—Compounds containing amino and carboxyl groups bound to the same carbon skeleton having amino and carboxyl groups bound to acyclic carbon atoms of the same carbon skeleton the carbon skeleton being acyclic and saturated having only one amino and one carboxyl group bound to the carbon skeleton the nitrogen atom of the amino group being further bound to acyclic carbon atoms or to carbon atoms of rings other than six-membered aromatic rings
- C07C229/16—Compounds containing amino and carboxyl groups bound to the same carbon skeleton having amino and carboxyl groups bound to acyclic carbon atoms of the same carbon skeleton the carbon skeleton being acyclic and saturated having only one amino and one carboxyl group bound to the carbon skeleton the nitrogen atom of the amino group being further bound to acyclic carbon atoms or to carbon atoms of rings other than six-membered aromatic rings to carbon atoms of hydrocarbon radicals substituted by amino or carboxyl groups, e.g. ethylenediamine-tetra-acetic acid, iminodiacetic acids
Abstract
본 발명은 그의 친지성이고 비독성인 대사물로 생체내 전환되는 "대사적으로 프로그램화"된 금속 킬레이트화제, 예를 들어, 친지성이고 흡수되고 (예를 들어, 경구로 흡수되고), 효과적인 금속 킬레이트화제인 화학식 (I)의 화합물을 제공한다. 본 발명은 또한 "대사적으로 프로그램화"된 금속 킬레이트화제인 화학식 (II)의 화합물을 제공한다. 본 발명은 또한 본원에 기재된 화합물, 제약 조성물, 키트, 방법, 및 용도를 제공한다. 화합물, 제약 조성물, 키트, 및 방법은 질환 (예를 들어, 금속 과부하, 산화성 스트레스, 당뇨병, 간 질환, 심장 질환, 암, 방사선 손상, 신경계 또는 신경변성 장애, 프리드라이히 운동실조 (FRDA), 황반 변성, 폐쇄성 두부 손상, 과민성 장 질환, 재관류 손상, 금속 중독, 또는 감염성 질환)을 치료 또는 예방하는데 유용할 수 있다.
Description
관련 출원
본 출원은 35 U.S.C § 119(e) 하에 2015년 4월 27일에 제출된 미국 특허 가출원 U.S.S.N. 62/153,468의 우선권을 주장하며, 이는 본원에 참조로 포함된다.
정부 지원
본 발명은 미국 국립보건원 (National Institutes of Health)이 부여한 승인 번호 R37DK049108 하에 정부의 지원을 받아 이루어졌다. 정부는 본 발명에 특정 권리를 갖는다.
거의 모든 생명 형태는 미량영양소로서 철을 요구한다 (문헌 [Mladenka et al., Acta Medica. 2005, 48, 127-135]). 그러나, 저용해도의 철(III) 히드록시드 (Ksp = 1 x 10-39) (문헌 [Raymond et al., "Coordination Chemistry and Microbial Iron Transport." Acc. Chem. Res. 1979, 12, 183-190])인 생물권에서의 금속의 우세한 형태는 자연에서 복잡한 철 저장 및 수송 시스템의 개발을 요구하였다. 미생물은 저분자량의 제2철-특이적 킬레이트화제인 시데로포어를 사용하고 (문헌 [Byers et al., "Microbial Iron Transport: Iron Acquisition by Pathogenic Microorganisms." Met. Ions Biol. Syst. 1998, 35, 37-66]); 진핵생물은 철을 수송하고 저장하기 위해 단백질을 사용하는 경향이 있다 (문헌 [Gkouvatsos et al., Biochim. Biophys. Acta. 2012, 1820, (2012) 188-202; Li et al., Proc. Natl. Acad. Sci. U. S. A. 107 (2010, 107) 3505-3510; Bergeron, "Iron: A Controlling Micronutrient in Proliferative Processes." Trends Biochem. Sci. 1986, 11, 133-136; Theil et al., "Ferritin Mineralization: Ferroxidation and Beyond." J. Inorg. Biochem. 1997, 67, 30; Ponka et al., "Function and Regulation of Transferrin and Ferritin." Semin. Hematol. 1998, 35, 35-54]). 인간은 고도로 효율적인 철 관리 시스템을 진화시켰고 (문헌 [Andrews et al., Annu. Rev. Physiol. 69 (2007) 69-85]), 매일 금속 약 1 mg만을 흡수 및 배출하고; 과잉 금속의 배출에 대한 어떠한 메커니즘도 존재하지 않는다 (문헌 [Whittington et al., Review article: haemochromatosis, Aliment Pharmacol. Ther. 16 (2002) 1963-1975; Brittenham, "Disorders of Iron Metabolism: Iron Deficiency and Overload." In Hematology: Basic Principles 및 Practice; 3rd ed.; Hoffman et al., Eds.; Churchill Livingstone: New York, 2000; pp. 397-428]). 용혈성 빈혈의 치료에서 요구되는 수혈된 적혈구로부터 유래되는지 (문헌 [Peters et al., B. M. J. (2012) 344:e228. doi: 10.1136/bmj.e228; Cappellini et al., Guidelines for the Clinical Management of Thalassemia, 2nd Ed.., Thalassemia International Foundation, 2008; Olivieri et al., "Iron-Chelating Therapy and the Treatment of Thalassemia." Blood 1997, 89, 739-761; Vichinsky, "Current Issues with Blood Transfusions in Sickle Cell Disease." Semin. Hematol. 2001, 38, 14-22; Kersten et al., "Long-Term Treatment of Transfusional Iron Overload with the Oral Iron Chelator Deferiprone (L1): A Dutch Multicenter Trial." Ann. Hematol. 1996, 73, 247-252]) 또는 식이성 철의 증가된 흡수로부터 유래되는지 간에 (문헌 [[Conrad et al., "Iron Absorption and Transport." Am. J. Med. Sci. 1999, 318, 213-229; Lieu et al., "The Roles of Iron in Health and Disease." Mol. Aspects Med. 2001, 22, 1-87]), 유효한 치료 없이는, 체내 철은 계속해서 간, 심장, 췌장, 및 다른 곳에서 침착에 의해 증가한다 (철 과부하 질환) (문헌 [Lieu et al., Mol. Aspects Med. 22 (2001) 1-87]). 이는 간 질환 (문헌 [Bonkovsky et al., Clin. Liver Dis. 4 (2000) 409-429, vi-vii]), 당뇨 (문헌 [Wojcik et al., Can. J. Gastroenterol. 16 (2002) 297-302]), 증가된 암의 위험성 (문헌 [Wen et al., Cancer Res. 74 (2014) 6589-6597]), 및 종종 이들 환자의 사망 원인인 심장 질환 (문헌 [Brittenham, Disorders of iron metabolism: iron deficiency and overload, in: R. Hoffman, E. J. Benz, S. J. Shattil, B. Furie, H. J. Cohen (Eds.), Hematology: Basic Principles and Practice, 3rd Ed., Churchill Livingstone, New York, 2000, pp 397-428])으로 이어질 수 있다. 비트랜스페린-결합 혈장 철 (문헌 [Brissot et al., Biochim. Biophys. Acta. 2012, 1820, (2012) 403-410; Chua et al., Blood 104 (2004, 104,) 1519-1525; Bolli et al., Am. J. Physiol. 259 (1990, 259,) 1901-1911])은 철 과부하에 의해 발생하는 기관 손상의 원인이다.
철 과부하 질환을 갖는 환자에서, 독성은 반응성 산소 종과 철의 상호작용에서 유래한다 (문헌 [Graf et al., "Iron-Catalyzed Hydroxyl Radical Formation. Stringent Requirement for Free Iron Coordination Site." J. Biol. Chem. 1984, 259, 3620-3624; Halliwell, "Free Radicals and Antioxidants: A Personal View." Nutr. Rev. 1994, 52, 253-265; Halliwell, "Oxidative Damage, and Chelating Agents." In The Development of Iron Chelators for Clinical Use; Bergeron et al., Eds.; CRC: Boca Raton, FL, 1994; pp 33-56; Koppenol, "Kinetics and Mechanism of the Fenton Reaction: Implications for Iron Toxicity." In Iron Chelators: New Development Strategies; Badman et al., Eds.; Saratoga: Ponte Vedra Beach, FL, 2000, pp 3-10]). 예를 들어, 철(II)의 존재 하에, 내인성 H2O2는 펜톤 반응에서 매우 반응성인 종인 히드록실 라디칼 (HO·), 및 HO-로 환원된다. 히드록실 라디칼은 다양한 세포 성분과로 매우 빠르게 반응하고, DNA 및 막을 손상시킬 뿐만 아니라 발암물질을 생성하는 자유 라디칼 및 라디칼-매개 연쇄 과정을 개시할 수 있다 (문헌 [Halliwell, "Free Radicals and Antioxidants: A Personal View." Nutr. Rev. 1994, 52, 253-265); Babbs, "Oxygen Radicals in Ulcerative Colitis." Free Radical Biol. Med. 1992, 13, 169-181; Hazen et al., "Human Neutrophils Employ the Myeloperoxidase-Hydrogen Peroxide-Chloride System to Oxidize α-Amino Acids to a Family of Reactive Aldehydes. Mechanistic Studies Identifying Labile Intermediates along the Reaction Pathway." J. Biol. Chem. 1998, 273, 4997-5005]. 유리된 철(III)은 다양한 생물학적 환원제 (예를 들어, 아스코르베이트, 글로타티온)를 통해 철(II)로 다시 환원되며, 이는 문제가 있는 주기를 생성한다.
철-매개 손상은 재관류 손상 (문헌 [Millan et al., "Biological Signatures of Brain Damage Associated with High Serum Ferritin Levels in Patients with Acute Ischemic Stroke and Thrombolytic Treatment." Dis. Markers 2008, 25, 181-188]), 파킨슨병 (문헌 [Zecca et al., "Neuromelanin Can Protect Against Iron-Mediated Oxidative Damage in System Modeling Iron Overload of Brain Aging and Parkinson's Disease." J. Neurochem. 2008, 106, 1866-1875]), 프리드라이히 운동실조 (문헌 [Pietrangelo, "Iron Chelation Beyond Tranfusion Iron Overload." Am. J. Hematol. 2007, 82, 1142-1146]), 황반 변성 (문헌 [Dunaief, "Iron Induced Oxidative Damage as a Potential Factor in Age-Related Macular Degeneration: The Cogan Lecture" Invest. Ophthalmol. Vis. Sci. 2006, 47, 4660-4664]), 및 출혈성 졸중 (문헌 [Hua et al., "Long-Term Effects of Experimental Intracerebral Hemorrhage: The Role of Iron." J. Neurosurg. 2006, 104, 305-312])에서와 같이 국소적이거나, 또는 다중 기관 침범에 의해, 수혈성 철 과부화, 예를 들어, 지중해빈혈 (문헌 [Pippard, "Iron Overload 및 Iron Chelation Therapy in Thalassaemia and Sickle Cell Haemoglobinopathies." Acta. Haematol. 1987, 78, 206-211]), 겸상 적혈구 질환 (문헌 [Pippard, "Iron Overload and Iron Chelation Therapy in Thalassaemia and Sickle Cell Haemoglobinopathies." Acta. Haematol. 1987, 78, 206-211; Olivieri, "Progression of Iron Overload in Sickle Cell Disease." Semin. Hematol. 2001, 38, 57-62]), 및 골수이형성증 (문헌 [Malcovati, "Impact of Transfusion Dependency and Secondary Iron Overload on the Survival of Patients with Myelodysplastic Syndromes." Leukemia Res. 2007, 31, S2-S6])에서와 같이 전반적일 수 있다. 둘 다의 시나리오에서의 해결책은 동일하다: 킬레이트화하여 관리되지 않는 과잉의 철의 배출을 촉진한다.
철을 격리하고 신체로부터 그의 배출을 허용할 수 있는 킬레이트화제에 의한 치료가 유일하게 이용가능한 치료 접근법이다. 현재 사용 중이거나 임상적으로 평가된 바 있는 철 킬레이트화제의 일부는 데스페리옥사민 B 메실레이트 (DFO) (데스페랄; 노파르티스 파마수티칼 코포레이션(Novartis Pharmaceuticals Corporation): 뉴저지주 이스트 하노버, 2008년; www.pharma.us.novartis.com/product/pi/pdf/desferal.pdf), 1,2-디메틸-3-히드록시-4-피리디논 (디페리프론, L1) 문헌 [Hoffbrand, "Long-Term Trial of Deferiprone in 51 Transfusion-Dependent Iron Overloaded Patients." Blood 1998, 91, 295-300; Olivieri, "Long-Term Therapy with Deferiprone." Acta Haematol. 1996, 95, 37-48; Olivieri, "Long-Term Safety and Effectiveness of Iron-Chelation Therapy with Deferiprone from Thalassemia Major." N. Engl. J. Med. 1998, 339, 417-423; Richardson, "The Controversial Role of Deferiprone in the Treatment of Thalassemia." J. Lab. Clin. Med. 2001, 137, 324-329]), 및 4-[3,5-비스(2-히드록시페닐)-1,2,4-트리아졸-1-일]벤조산 (데스페라시록스, ICL670A) (문헌 [Nisbet-Brown et al., "Effectiveness and Safety of ICL670 in Iron-Loaded Patients with Thalassemia: A Randomised, Double-Blind, Placebo-Controlled, Dose-Escalation Trial." Lancet, 2003, 361, 1597-1602; Galanello et al., "Safety, Tolerability, and Pharmacokinetics of ICL670, a New Orally Active Iron-Chelating Agent in Patients with Transfusion-Dependent Iron Overload Due to β-Thalassemia." J. Clin. Pharmacol. 2003, 43, 565-572; Cappellini, "Iron-Chelating Therapy with the New Oral Agent ICL670 (Exjade)." Best Pract. Res. Clin. Haematol. 2005, 18, 289-298])을 포함한다. 이들 화합물의 각각은 결점을 갖는다. DFO는 연장된 시간 주기, 예를 들어 1일에 12시간, 1주에 5일 동안 피하로 (sc) 주입되어야 하며, 이는 심각한 환자 순응도 문제이다 (문헌 [Olivieri et al., "Iron-Chelating Therapy and the Treatment of Thalassemia." Blood 1997, 89, 739-761; Pippard, "Desferrioxamine-Induced Iron Excretion in Humans." Bailliere's Clin. Haematol. 1989, 2, 323-343; Giardina et al., "Chelation Therapy in β-Thalassemia: An Optimistic Update." Semin. Hematol. 2001, 38, 360-366]). 데스페라시록스는, 경구 활성인 한편, 환자를 음성 철 균형으로 유지시키기에 충분하게 철을 간단하게 제거하지 못한다 (문헌 [Hoffbrand, "Long-Term Trial of Deferiprone in 51 Transfusion-Dependent Iron Overloaded Patients." Blood 1998, 91, 295-300; Olivieri, "Long-Term Therapy with Deferiprone." Acta Haematol. 1996, 95, 37-48; Olivieri, "Long-Term Safety and Effectiveness of Iron-Chelation Therapy with Deferiprone from Thalassemia Major." N. Engl. J. Med. 1998, 339, 417-423; Richardson, "The Controversial Role of Deferiprone in the Treatment of Thalassemia." J. Lab. Clin. Med. 2001, 137, 324-329]). 데스페라시록스는 DFO에 대해 비열등성을 나타내지 않으며 일부 신장 독성을 포함하여 수많은 부작용과 연관된다 (문헌 [Nisbet-Brown et al., "Effectiveness and Safety of ICL670 in Iron-Loaded Patients with Thalassemia: A Randomised, Double-Blind, Placebo-Controlled, Dose-Escalation Trial." Lancet, 2003, 361, 1597-1602; Galanello et al., "Safety, Tolerability, and Pharmacokinetics of ICL670, a New Orally Active Iron-Chelating Agent in Patients with Transfusion-Dependent Iron Overload Due to β-Thalassemia." J. Clin. Pharmacol. 2003, 43, 565-572; Cappellini, "Iron-Chelating Therapy with the New Oral Agent ICL670 (Exjade)." Best Pract. Res. Clin. Haematol. 2005, 18, 289-298]).
상기 기재된 바와 같이 금속 킬레이트화제에 대한 연구에도 불구하고, 대상체의 병리학적 상태의 더 양호한 치료 및/또는 예방을 위해 보다 바람직한 특성을 갖는 금속 킬레이트화제 (균형잡힌 특성 (예를 들어, 친지성, 금속 클리어링 효율, 및 독성)을 갖는 금속 킬레이트화제)에 대한 필요가 여전히 존재한다.
본 발명은 데스페리티오신 (하기 제시된 1) 및 데스아자데스페리티오신 (하기 제시된 1a)을 기반으로 하는 데스아자데스페리티오신 유사체를 제공한다. 특정 실시양태에서, 데스아자데스페리티오신 유사체는 화학식 (I)의 화합물, 및 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 및 전구약물이다. 데스아자데스페리티오신 유사체는 금속 (예를 들어, 철 및 다른 금속)을 킬레이트화할 수 있다. 본 발명은 또한 화학식 (II)의 화합물 및 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 및 전구약물을 제공한다. 본 발명은 본원에 기재된 데스아자데스페리티오신 유사체 또는 화학식 (I) 또는 화학식 (II)의 화합물을 수반 또는 포함하는 제약 조성물, 키트, 방법, 및 용도를 제공한다. 화합물, 제약 조성물, 키트, 및 방법은 대상체, 세포, 조직, 또는 생물학적 샘플에서 금속을 킬레이트화하고, 대상체에서 질환을 치료하고, 대상체에서 질환을 예방하고, 대상체에서 바이오필름의 형성을 치료, 감소, 또는 예방하고, 대상에서 바이오필름의 형성을 감소 또는 예방하는데 유용할 수 있다. 특정 실시양태에서, 질환은 금속 과부하, 산화성 스트레스, 수혈성 철 과부하, 지중해빈혈, 원발성 혈색소증, 속발성 혈색소증, 당뇨병, 간 질환, 심장 질환, 암, 방사선 손상, 신경계 또는 신경변성 장애, 프리드라이히 운동실조 (FRDA), 황반 변성, 폐쇄성 두부 손상, 과민성 장 질환, 또는 재관류 손상이다. 특정 실시양태에서, 질환은 금속 중독이다. 특정 실시양태에서, 질환은 감염성 질환 (예를 들어, 말라리아)이다. 철은 통상적으로 미생물의 성장에 필요한 영양소이다. 철을 킬레이트화하고/거나 제거함으로써 철을 유기체에게서 박탈하는 것은 감염성 질환의 치료 및/또는 예방에 기여할 수 있다.
금속 킬레이트화제의 친지성이 금속 킬레이트화제의 금속 클리어링 효율 (MCE), 기관 분포, 및 독성 프로파일에 대해 엄청난 영향을 가질 수 있다는 것이 발견되었다. 주어진 구조적 패밀리 내에서, 전형적으로 금속 킬레이트화제가 더 친지성일수록 MCE는 더 양호하다. 그러나, 또한 제2 관계가 존재한다: 전형적으로 금속 킬레이트화제가 더 친지성일수록, 금속 킬레이트화제는 더 독성이다. 따라서, 친지성, MCE, 및 독성간의 균형이 달성되어야 한다. 유리하게는, 본원에 기재된 화합물은 적어도 본원에 기재된 화합물이 "대사적으로 프로그램화"된 금속 킬레이트화제이기 때문에, 예를 들어, 이들이 친지성이고 흡수성 (예를 들어, 경구 흡수성)이어서, 흡수되면, 유효한 금속 킬레이트화제는 친수성이고 비독성인 대사물로 전환되기 때문에 공지된 금속 킬레이트화제보다 이롭다.
한 측면에서, 본 개시내용은 화학식 (I)의 화합물 및 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 및 전구약물을 제공한다.
여기서 R1, R2, R3, R4, R5, R6, R9, Z, x, n, y, m, p, q, 및 k는 본원에 정의된 바와 같다.
예시적인 화학식 (I)의 화합물은 하기 및 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 및 전구약물을 포함하나, 이들에 제한되지는 않는다.
또 다른 측면에서, 본 개시내용은 화학식 (II)의 화합물 및 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 전구약물을 제공한다.
여기서 RC1, RC2, RC3, 및 j는 본원에 정의된 바와 같다. 또 다른 측면에서, 본원에 기재된 것은 본원에 기재된 화합물 및 임의로 제약상 허용되는 부형제를 포함하는 제약 조성물이다. 특정 실시양태에서, 본원에 기재된 제약 조성물은 유효량 (예를 들어, 치료 또는 예방 유효량)의 본원에 기재된 화합물을 포함한다. 제약 조성물은 대상체, 세포, 조직, 또는 생물학적 샘플에서 금속을 킬레이트화하고; 대상체 (예를 들어, 인간)에서 질환을 치료하고; 대상체에서 질환을 예방하고; 대상체에서 바이오필름의 형성을 치료, 감소, 또는 예방하거나; 또는 대상에서 바이오필름의 형성을 감소 또는 예방하는데 유용할 수 있다
특정 실시양태에서, 대상체는 인간이다. 특정 실시양태에서, 세포는 시험관내에 존재한다. 특정 실시양태에서, 세포는 생체내에 존재한다.
특정 실시양태에서, 본원에 기재된 화합물에 의해 킬레이트화된 금속 중 1개는 철이다. 특정 실시양태에서, 다른 금속 예컨대 알루미늄, 탈륨, 크로뮴, 마그네슘, 칼슘, 스트론튬, 니켈, 망가니즈, 코발트, 구리, 아연, 은, 나트륨, 칼륨, 카드뮴, 수은, 납, 안티모니, 몰리브데넘, 텅스텐, 란타나이드 (예를 들어, 세륨) 또는 악티나이드 (예를 들어, 우라늄)은 화합물에 의해 킬레이트화된다.
특정 실시양태에서, 질환은 금속의 킬레이트화와 연관된 질환이다. 특정 실시양태에서, 질환은 철 과부하이다. 특정 실시양태에서, 질환은 수혈성 철 과부하이다. 특정 실시양태에서, 질환은 지중해빈혈, 원발성 혈색소증, 또는 속발성 혈색소증이다. 특정 실시양태에서, 질환은 알루미늄 과부하, 란타나이드 과부하, 또는 악티나이드 과부하이다. 특정 실시양태에서, 질환은 산화성 스트레스이다. 특정 실시양태에서, 질환은 당뇨병, 간 질환, 심장 질환, 암, 또는 신경계 또는 신경변성 장애이다. 특정 실시양태에서, 질환은 방사선 손상, 프리드라이히 운동실조 (FRDA), 황반 변성, 폐쇄성 두부 손상, 과민성 장 질환, 또는 재관류 손상이다. 특정 실시양태에서, 질환은 금속 중독이다. 특정 실시양태에서, 질환은 감염성 질환이다.
또 다른 측면에서, 본원에 기재된 화합물 또는 제약 조성물을 포함하는 키트가 본원에 기재된다. 특정 실시양태에서, 키트는 추가로 화합물 또는 제약 조성물을 사용 (예를 들어, 투여)하기 위한 지침서를 포함한다.
또 다른 측면에서, 대상체에게 유효량의 본원에 기재된 화합물 또는 제약 조성물을 투여하는 것을 포함하는, 대상체에서 금속을 킬레이트화하는 방법이 본원에 제공된다.
또 다른 측면에서, 세포, 조직, 또는 생물학적 샘플을 유효량의 본원에 기재된 화합물 또는 제약 조성물과 접촉시키는 것을 포함하는, 세포, 조직, 또는 생물학적 샘플의 금속을 킬레이트화하는 방법이 본원에 제공된다.
또 다른 측면에서, 대상체에게 유효량의 본원에 기재된 화합물 또는 제약 조성물을 투여하는 것을 포함하는, 질환의 치료를 필요로 하는 대상체에서 질환을 치료하는 방법이 본원에 제공된다.
또 다른 측면에서, 대상체에게 유효량의 본원에 기재된 화합물 또는 제약 조성물을 투여하는 것을 포함하는, 질환의 예방을 필요로 하는 대상체에서 질환을 예방하는 방법이 본원에 제공된다.
또 다른 측면에서, 혈액 또는 그의 성분 (예를 들어, 적혈구)과 유효량의 본원에 기재된 화합물 또는 제약 조성물을 혼합하여 생체외 혼합물을 형성하고; 혼합물을 대상체에게 투여하는 것을 포함하는, 질환의 치료를 필요로 하는 대상체에서 질환을 치료하는 방법이 본원에 제공된다.
또 다른 측면에서, 혈액 또는 그의 성분 (예를 들어, 적혈구)과 유효량의 본원에 기재된 화합물 또는 제약 조성물을 혼합하여 혼합물을 형성하고; 대상체에게 혼합물을 투여하는 것을 포함하는, 질환의 예방을 필요로 하는 대상체의 질환을 예방하는 방법이 본원에 제공된다.
또 다른 측면에서, 본 개시내용은 유효량 (예를 들어, 치료 유효량)의 본원에 기재된 화합물 또는 제약 조성물을 바이오필름 형성의 억제를 필요로 하는 대상체에게 투여하는 것을 포함하는 바이오필름의 형성을 억제하는 방법을 제공한다. 특정 실시양태에서, 본 발명은 유효량 (예를 들어, 치료 유효량)의 본원에 기재된 화합물 또는 제약 조성물 및 항미생물제를 바이오필름의 형성 억제를 필요로 하는 대상체에게 투여하는 것을 포함하는, 바이오필름의 형성을 억제하는 방법을 제공한다. 특정 실시양태에서, 바이오필름은 박테리아, 고세균, 원충, 진균, 및 조류로 이루어진 군으로부터 선택된 1종 이상의 미생물에 의해 생성된다. 일부 실시양태에서, 바이오필름은 박테리아에 의해 생성된다. 일부 실시양태에서, 바이오필름은 그람-음성 박테리아에 의해 생성된다. 한 실시양태에서, 바이오필름은 에스. 에피더미디스(S. epidermidis), 이. 파에칼리스(E. faecalis), 이. 콜라이(E. coli), 피. 미라빌리스(P. mirabilis), 피. 아에루기노사(P. aeruginosa), 케이. 뉴모니아에(K. pneumoniae), 에스. 아우레우스(S. aureus), 이. 비리단스(S. viridans), 케이. 옥시토카(K. oxytoca), 에스. 사프로피티쿠스(S. saprophyticus), 엘. 뉴모필라(L. pneumophila), 미코박테리움 종(Mycobacterium spp.), 씨. 프레운디이(C. freundii), 에이. 히드로필라(A. hydrophila), 에프. 누클레아툼(F. nucleatum), 에이. 나에스룬디이(A. naeslundii), 피. 스투아르티이(P. stuartii), 에스. 마르세센스(S. marcescens), 또는 그의 조합에 의해 생성된다. 일부 실시양태에서, 바이오필름은 그람-양성 박테리아에 의해 생성된다.
또 다른 측면에서, 박테리아를 유효량의 본원에 기재된 화합물 또는 제약 조성물과 접촉시키는 것을 포함하는, 박테리아 세포 성장을 억제하는 방법이 본원에 제공된다.
또 다른 측면에서, 박테리아를 유효량의 본원에 기재된 화합물 또는 제약 조성물과 접촉시키는 것을 포함하는, 박테리아 과민성을 유도하는 방법이 본원에 제공된다. 과민성은 독성물질, 감염원, 또는 정상 대상체에서 전적으로 무해한 작용제에 대해 비정상적 감수성인 상태를 지칭한다.
또 다른 측면에서, 본원에 기재된 방법에 사용하기 위한 본원에 기재된 화합물 및 제약 조성물이 제공된다.
본 개시내용의 하나 이상의 실시양태의 세부사항이 본원에 제시된다. 본 개시내용의 다른 특색, 목적 및 이점은 상세한 설명, 도면, 실시예 및 청구범위로부터 명백해질 것이다.
정의
구체적 관능기 및 화학 용어의 정의는 하기에 보다 상세하게 기재된다. 본 발명의 목적상, 화학 원소는 원소 주기율표, CAS 버전, 문헌 [Handbook of Chemistry and Physics, 75th Ed.] 표지 뒷면에 따라 확인되며, 구체적 관능기는 일반적으로 본원에 기재된 바와 같이 정의된다. 추가로, 유기 화학의 일반적 원리, 뿐만 아니라 구체적 관능 모이어티 및 반응성은 문헌 [Organic Chemistry, Thomas Sorrell, University Science Books, Sausalito, 1999; Smith and March March's Advanced Organic Chemistry, 5th Edition, John Wiley & Sons, Inc., New York, 2001; Larock, Comprehensive Organic Transformations, VCH Publishers, Inc., New York, 1989; Carruthers, Some Modern Methods of Organic Synthesis, 3rd Edition, Cambridge University Press, Cambridge, 1987]에 기재되어 있다.
또한, 동일한 분자식을 갖지만 그의 원자의 결합 성질 또는 순서 또는 공간에서의 그의 원자의 배열이 상이한 화합물은 "이성질체"로 칭해진다는 것을 이해해야 한다. 공간에서의 그의 원자의 배열이 상이한 이성질체는 "입체이성질체"로 명명된다. 서로 거울상이 아닌 입체이성질체는 "부분입체이성질체"로 칭해지고, 서로 비-중첩가능한 거울상인 입체이성질체는 "거울상이성질체"로 칭해진다. 화합물이 비대칭 중심을 갖는 경우, 예를 들어, 이것이 4개의 상이한 기에 결합된 경우에, 한 쌍의 거울상이성질체가 가능하다. 거울상이성질체는 그의 비대칭 중심의 절대 배위를 특징으로 할 수 있고, 칸 및 프렐로그의 R- 및 S-순서 규칙에 의해, 또는 분자가 편광면을 회전시키는 방식에 의해 기재되고, 우선성 또는 좌선성으로서 (즉, 각각 (+) 또는 (-)-이성질체로서) 지정된다. 키랄 화합물은 개별 거울상이성질체로서 또는 그의 혼합물로서 존재할 수 있다. 동등한 비율의 거울상이성질체를 함유하는 혼합물은 "라세미 혼합물"로 불린다. 예를 들어, 본원에 기재된 화합물은 개별 거울상이성질체, 부분입체이성질체 또는 기하 이성질체 형태일 수 있거나, 또는 라세미 혼합물 및 1종 이상의 입체이성질체가 풍부한 혼합물을 포함한 입체이성질체의 혼합물 형태일 수 있다. 이성질체는 키랄 고압 액체 크로마토그래피 (HPLC) 및 키랄 염의 형성 및 결정화를 포함한, 통상의 기술자에게 공지된 방법에 의해 혼합물로부터 단리될 수 있거나; 또는 바람직한 이성질체는 비대칭 합성에 의해 제조될 수 있다. 예를 들어, 문헌 [Jacques et al., Enantiomers, Racemates 및 Resolutions (Wiley Interscience, New York, 1981); Wilen et al., Tetrahedron 33:2725 (1977); Eliel, Stereochemistry of Carbon Compounds (McGraw-Hill, NY, 1962); Wilen, Tables of Resolving Agents and Optical Resolutions p. 268 (E.L. Eliel, Ed., Univ. of Notre Dame Press, Notre Dame, IN 1972)]을 참조한다. 본 발명은 추가적으로 본원에 기재된 화합물을 실질적으로 다른 이성질체가 없는 개별 이성질체로서 및 대안적으로 다양한 이성질체의 혼합물로서 포괄한다.
이성질체/거울상이성질체가 바람직한 경우에, 일부 실시양태에서 이는 상응하는 거울상이성질체를 실질적으로 함유하지 않는 것으로서 제공될 수도 있고, 또한 "광학적으로 풍부한" 또는 "거울상이성질체적으로 풍부한" 것으로서 지칭될 수도 있다. 본원에 사용된 "광학적으로 풍부한" 및 "거울상이성질체적으로 풍부한"은 제공된 화합물이 유의하게 보다 큰 비율의 1개의 거울상이성질체로 구성됨을 의미한다. 특정 실시양태에서, 본 발명의 화합물은 적어도 약 70 중량%의 바람직한 거울상이성질체로 구성된다. 특정 실시양태에서, 본 발명의 화합물은 적어도 약 80 중량%의 바람직한 거울상이성질체로 구성된다. 특정 실시양태에서, 본 발명의 화합물은 적어도 약 90 중량%의 바람직한 거울상이성질체로 구성된다. 다른 실시양태에서, 화합물은 적어도 약 95 중량%, 98 중량% 또는 99 중량%의 바람직한 거울상이성질체로 구성된다. 바람직한 거울상이성질체는 통상의 기술자에게 공지된 임의의 방법, 예컨대 키랄 고압 액체 크로마토그래피 (HPLC) 및 키랄 염의 형성 및 결정화에 의해 라세미 혼합물로부터 단리될 수 있거나 또는 비대칭 합성에 의해 제조될 수 있다. 예를 들어, 문헌 [Jacques et al., Enantiomers, Racemates 및 Resolutions (Wiley Interscience, New York, 1981); Wilen et al., Tetrahedron 33:2725 (1977); Eliel, Stereochemistry of Carbon Compounds (McGraw-Hill, NY, 1962); Wilen, Tables of Resolving Agents 및 Optical Resolutions p. 268 (E.L. Eliel, Ed., Univ. of Notre Dame Press, Notre Dame, IN 1972)]을 참조한다.
달리 언급되지 않는 한, 본원에 도시된 구조는 또한 단지 1종 이상의 동위원소 풍부 원자의 존재만이 상이한 화합물을 포함하도록 의도된다. 예를 들어, 수소의 중수소 또는 삼중수소에 의한 대체, 또는 탄소의 13C 또는 14C에 의한 대체만이 상이한, 도시된 구조를 갖는 화합물이 본 발명의 범위 내에 있다. 이러한 화합물은, 예를 들어 분석 도구로서, 생물학적 검정에서의 프로브로서, 또는 본 발명에 따른 치료제로서 유용할 수 있다.
값의 범위가 열거되어 있는 경우에, 이는 그 범위 내의 각각의 값 및 하위-범위를 포괄하는 것으로 의도된다. 예를 들어, " C1-6"은 C1, C2, C3, C4, C5, C6, C1-6, C1-5, C1-4, C1-3, C1-2, C2-6, C2-5, C2-4, C2-3, C3-6, C3-5, C3-4, C4-6, C4-5, 및 C5-6을 포괄하는 것으로 의도된다.
용어 "정제된", "실질적으로 정제된" 및 "단리된"은 화합물이 그의 천연 상태에서 정상적으로 연관되는 유사하지 않은 다른 화합물에 결합되지 않음으로써, 화합물이 주어진 샘플 또는 조성물의 중량 기준 질량의 적어도 0.5%, 1%, 5%, 10%, 20%, 50%, 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99%, 99.5%, 99.9%를 구성하는 것인, 본 발명에 유용한 화합물을 지칭한다. 한 실시양태에서, 이들 용어는 주어진 샘플 또는 조성물의 중량 기준 질량의 적어도 95%, 98%, 99%, 또는 99.9%를 구성하는 화합물을 지칭한다.
용어 "아실"은 화학식 -C(=O)RX1, -C(=O)ORX1, -C(=O)-O-C(=O)RX1, -C(=O)SRX1, -C(=O)N(RX1)2, -C(=S)RX1, -C(=S)N(RX1)2, 및 -C(=S)S(RX1), -C(=NRX1)RX1, -C(=NRX1)ORX1, -C(=NRX1)SRX1, 및 -C(=NRX1)N(RX1)2를 갖는 기를 지칭하며, 여기서 RX1은 수소; 할로겐; 치환 또는 비치환된 히드록실; 치환 또는 비치환된 티올; 치환 또는 비치환된 아미노; 치환 또는 비치환된 아실, 시클릭 또는 비-시클릭 치환 또는 비치환된 분지형 또는 비분지형 지방족; 시클릭 또는 비-시클릭 치환 또는 비치환된 분지형 또는 비분지형 헤테로지방족; 시클릭 또는 비-시클릭 치환 또는 비치환된 분지형 또는 비분지형 알킬; 시클릭 또는 비-시클릭 치환 또는 비치환된 분지형 또는 비분지형 알케닐; 치환 또는 비치환된 알키닐; 치환 또는 비치환된 아릴, 치환 또는 비치환된 헤테로아릴, 지방족옥시, 헤테로지방족옥시, 알킬옥시, 헤테로알킬옥시, 아릴옥시, 헤테로아릴옥시, 지방족티옥시, 헤테로지방족티옥시, 알킬티옥시, 헤테로알킬티옥시, 아릴티옥시, 헤테로아릴티옥시, 모노- 또는 디- 지방족아미노, 모노- 또는 디- 헤테로지방족아미노, 모노- 또는 디- 알킬아미노, 모노- 또는 디- 헤테로알킬아미노, 모노- 또는 디- 아릴아미노, 또는 모노- 또는 디- 헤테로아릴아미노이거나; 또는 2개의 RX1 기는 함께 5- 내지 6-원 헤테로시클릭 고리를 형성한다. 예시적인 아실 기는 알데히드 (-CHO), 카르복실산 (-CO2H), 케톤, 아실 할라이드, 에스테르, 아미드, 이민, 카르보네이트, 카르바메이트 및 우레아를 포함한다. 아실 치환기는 안정한 모이어티를 형성하는 본원에 기재된 임의의 치환기 (예를 들어, 그의 각각이 추가로 치환될 수 있거나 또는 치환되지 않을 수 있는 지방족, 알킬, 알케닐, 알키닐, 헤테로지방족, 헤테로시클릭, 아릴, 헤테로아릴, 아실, 옥소, 이미노, 티오옥소, 시아노, 이소시아노, 아미노, 아지도, 니트로, 히드록실, 티올, 할로, 지방족아미노, 헤테로지방족아미노, 알킬아미노, 헤테로알킬아미노, 아릴아미노, 헤테로아릴아미노, 알킬아릴, 아릴알킬, 지방족옥시, 헤테로지방족옥시, 알킬옥시, 헤테로알킬옥시, 아릴옥시, 헤테로아릴옥시, 지방족티옥시, 헤테로지방족티옥시, 알킬티옥시, 헤테로알킬티옥시, 아릴티옥시, 헤테로아릴티옥시, 아실옥시 등)를 포함하나 이에 제한되지는 않는다.
용어 "아실옥시"는 Ri가 본원에 정의된 바와 같은 임의로 치환된 아실 기이고, 산소 모이어티가 직접적으로 모 분자에 부착되는 것인, 화학식 (-ORi)의 "치환된 히드록실"을 지칭한다.
용어 "지방족"은 1개 이상의 관능기로 임의로 치환된 포화 및 불포화 둘 다의 비방향족, 직쇄 (예를 들어, 비분지형), 분지형, 비-시클릭, 및 시클릭 (예를 들어, 카르보시클릭) 탄화수소를 포함한다. 통상의 기술자에 의해 인지되는 바와 같이, 본원에서 "지방족"은 알킬, 알케닐, 알키닐, 시클로알킬, 시클로알케닐 및 시클로알키닐 모이어티를 포함하나 이에 제한되지는 않는 것으로 의도된다. 따라서, 용어 "알킬"은 직쇄형, 분지형 및 시클릭 알킬 기를 포함한다. 유사 규정이 다른 일반적 용어, 예컨대 "알케닐", "알키닐" 등에 적용된다. 또한, 용어 "알킬", "알케닐", "알키닐" 등은 치환 및 비치환된 기 둘 다를 포괄한다. 특정 실시양태에서, "지방족"은 1 내지 20개의 탄소 원자를 갖는 지방족 기 (시클릭, 비-시클릭, 치환, 비치환, 분지형 또는 비분지형)를 나타내는데 사용된다. 지방족 기 치환기는 안정한 모이어티를 형성하는 본원에 기재된 임의의 치환기 (예를 들어, 그의 각각이 추가로 치환될 수 있거나 또는 치환되지 않을 수 있는 지방족, 알킬, 알케닐, 알키닐, 헤테로지방족, 헤테로시클릭, 아릴, 헤테로아릴, 아실, 옥소, 이미노, 티오옥소, 시아노, 이소시아노, 아미노, 아지도, 니트로, 히드록실, 티올, 할로, 지방족아미노, 헤테로지방족아미노, 알킬아미노, 헤테로알킬아미노, 아릴아미노, 헤테로아릴아미노, 알킬아릴, 아릴알킬, 지방족옥시, 헤테로지방족옥시, 알킬옥시, 헤테로알킬옥시, 아릴옥시, 헤테로아릴옥시, 지방족티옥시, 헤테로지방족티옥시, 알킬티옥시, 헤테로알킬티옥시, 아릴티옥시, 헤테로아릴티옥시, 아실옥시 등)를 포함하지만, 이에 제한되지는 않는다.
용어 "알킬"은 단일 수소 원자의 제거에 의해 1 내지 20개의 탄소 원자를 함유하는 탄화수소 모이어티로부터 유도된 포화, 직쇄 또는 분지쇄 탄화수소 라디칼을 지칭한다. 일부 실시양태에서, 본 발명에 사용된 알킬 기는 1 내지 20개의 탄소 원자를 함유한다. 또 다른 실시양태에서, 사용된 알킬 기는 1 내지 15개의 탄소 원자를 함유한다. 또 다른 실시양태에서, 사용된 알킬 기는 1 내지 10개의 탄소 원자를 함유한다. 또 다른 실시양태에서, 사용된 알킬 기는 1 내지 8개의 탄소 원자를 함유한다. 또 다른 실시양태에서, 사용된 알킬 기는 1 내지 5개의 탄소 원자를 함유한다. 알킬 라디칼의 예는 메틸 (예를 들어, 비치환된 메틸 (Me)), 에틸 (예를 들어, 비치환된 에틸 (Et)), 프로필 (예를 들어, 비치환된 프로필 (Pr)), n-프로필, 이소프로필, 부틸 (예를 들어, 비치환된 부틸 (Bu)), n-부틸, 이소-부틸, sec-부틸, sec-펜틸, 이소-펜틸, tert-부틸, n-펜틸, 네오펜틸, n-헥실, sec-헥실, n-헵틸, n-옥틸, n-데실, n-운데실, 도데실 등을 포함하지만, 이에 제한되지는 않으며, 1개 이상의 치환기를 함유할 수 있다. 알킬 기 치환기는 안정한 모이어티를 형성하는 본원에 기재된 임의의 치환기 (예를 들어, 그의 각각이 추가로 치환될 수 있거나 또는 치환되지 않을 수 있는 지방족, 알킬, 알케닐, 알키닐, 헤테로지방족, 헤테로시클릭, 아릴, 헤테로아릴, 아실, 옥소, 이미노, 티오옥소, 시아노, 이소시아노, 아미노, 아지도, 니트로, 히드록실, 티올, 할로, 지방족아미노, 헤테로지방족아미노, 알킬아미노, 헤테로알킬아미노, 아릴아미노, 헤테로아릴아미노, 알킬아릴, 아릴알킬, 지방족옥시, 헤테로지방족옥시, 알킬옥시, 헤테로알킬옥시, 아릴옥시, 헤테로아릴옥시, 지방족티옥시, 헤테로지방족티옥시, 알킬티옥시, 헤테로알킬티옥시, 아릴티옥시, 헤테로아릴티옥시, 아실옥시 등)를 포함하지만, 이에 제한되지는 않는다.
용어 "알케닐"은 단일 수소 원자의 제거에 의해 적어도 1개의 탄소-탄소 이중 결합을 갖는 직쇄 또는 분지쇄 탄화수소 모이어티로부터 유도된 1가 기를 나타낸다. 특정 실시양태에서, 본 발명에 사용된 알케닐 기는 2 내지 20개의 탄소 원자를 함유한다. 일부 실시양태에서, 본 발명에 사용된 알케닐 기는 2 내지 15개의 탄소 원자를 함유한다. 또 다른 실시양태에서, 사용된 알케닐 기는 2 내지 10개의 탄소 원자를 함유한다. 또 다른 실시양태에서, 알케닐 기는 2 내지 8개의 탄소 원자를 함유한다. 또 다른 실시양태에서, 알케닐 기는 2 내지 5개의 탄소를 함유한다. 알케닐 기는, 예를 들어 1개 이상의 치환기를 보유할 수 있는 에테닐, 프로페닐, 부테닐, 1-메틸-2-부텐-1-일 등을 포함한다. 알케닐 기 치환기는 안정한 모이어티를 형성하는 본원에 기재된 임의의 치환기 (예를 들어, 그의 각각이 추가로 치환될 수 있거나 또는 치환되지 않을 수 있는 지방족, 알킬, 알케닐, 알키닐, 헤테로지방족, 헤테로시클릭, 아릴, 헤테로아릴, 아실, 옥소, 이미노, 티오옥소, 시아노, 이소시아노, 아미노, 아지도, 니트로, 히드록실, 티올, 할로, 지방족아미노, 헤테로지방족아미노, 알킬아미노, 헤테로알킬아미노, 아릴아미노, 헤테로아릴아미노, 알킬아릴, 아릴알킬, 지방족옥시, 헤테로지방족옥시, 알킬옥시, 헤테로알킬옥시, 아릴옥시, 헤테로아릴옥시, 지방족티옥시, 헤테로지방족티옥시, 알킬티옥시, 헤테로알킬티옥시, 아릴티옥시, 헤테로아릴티옥시, 아실옥시 등)를 포함하지만, 이에 제한되지는 않는다.
용어 "알키닐"은 단일 수소 원자의 제거에 의해 적어도 1개의 탄소-탄소 삼중 결합을 갖는 직쇄 또는 분지쇄 탄화수소로부터 유도된 1가 기를 지칭한다. 특정 실시양태에서, 본 발명에 사용된 알키닐 기는 2 내지 20개의 탄소 원자를 함유한다. 일부 실시양태에서, 본 발명에 사용된 알키닐 기는 2 내지 15개의 탄소 원자를 함유한다. 또 다른 실시양태에서, 사용된 알키닐 기는 2 내지 10개의 탄소 원자를 함유한다. 또 다른 실시양태에서, 알키닐 기는 2 내지 8개의 탄소 원자를 함유한다. 또 다른 실시양태에서, 알키닐 기는 2 내지 5개의 탄소 원자를 함유한다. 대표적인 알키닐 기는 1개 이상의 치환기를 보유할 수 있는 에티닐, 2-프로피닐 (프로파르길), 1-프로피닐 등을 포함하지만, 이에 제한되지는 않는다. 알키닐 기 치환기는 안정한 모이어티를 형성하는 본원에 기재된 임의의 치환기 (예를 들어, 그의 각각이 추가로 치환될 수 있거나 또는 치환되지 않을 수 있는 지방족, 알킬, 알케닐, 알키닐, 헤테로지방족, 헤테로시클릭, 아릴, 헤테로아릴, 아실, 옥소, 이미노, 티오옥소, 시아노, 이소시아노, 아미노, 아지도, 니트로, 히드록실, 티올, 할로, 지방족아미노, 헤테로지방족아미노, 알킬아미노, 헤테로알킬아미노, 아릴아미노, 헤테로아릴아미노, 알킬아릴, 아릴알킬, 지방족옥시, 헤테로지방족옥시, 알킬옥시, 헤테로알킬옥시, 아릴옥시, 헤테로아릴옥시, 지방족티옥시, 헤테로지방족티옥시, 알킬티옥시, 헤테로알킬티옥시, 아릴티옥시, 헤테로아릴티옥시, 아실옥시 등)를 포함하지만, 이에 제한되지는 않는다.
예시적인 탄소 원자 치환기는 할로겐, -CN, -NO2, -N3, -SO2H, -SO3H, -OH, -ORaa, -ON(Rbb)2, -N(Rbb)2, -N(Rbb)3 +X-, -N(ORcc)Rbb, -SH, -SRaa, -SSRcc, -C(=O)Raa, -CO2H, -CHO, -C(ORcc)2, -CO2Raa, -OC(=O)Raa, -OCO2Raa, -C(=O)N(Rbb)2, -OC(=O)N(Rbb)2, -NRbbC(=O)Raa, -NRbbCO2Raa, -NRbbC(=O)N(Rbb)2, -C(=NRbb)Raa, -C(=NRbb)ORaa, -OC(=NRbb)Raa, -OC(=NRbb)ORaa, -C(=NRbb)N(Rbb)2, -OC(=NRbb)N(Rbb)2, -NRbbC(=NRbb)N(Rbb)2, -C(=O)NRbbSO2Raa, -NRbbSO2Raa, -SO2N(Rbb)2, -SO2Raa, -SO2ORaa, -OSO2Raa, -S(=O)Raa, -OS(=O)Raa, -Si(Raa)3, -OSi(Raa)3 -C(=S)N(Rbb)2, -C(=O)SRaa, -C(=S)SRaa, -SC(=S)SRaa, -SC(=O)SRaa, -OC(=O)SRaa, -SC(=O)ORaa, -SC(=O)Raa, -P(=O)(Raa)2, -P(=O)(ORcc)2, -OP(=O)(Raa)2, -OP(=O)(ORcc)2, -P(=O)(N(Rbb)2)2, -OP(=O)(N(Rbb)2)2, -NRbbP(=O)(Raa)2, -NRbbP(=O)(ORcc)2, -NRbbP(=O)(N(Rbb)2)2, -P(Rcc)2, -P(ORcc)2, -P(Rcc)3 +X-, -P(ORcc)3 +X-, -P(Rcc)4, -P(ORcc)4, -OP(Rcc)2, -OP(Rcc)3 +X-, -OP(ORcc)2, -OP(ORcc)3 +X-, -OP(Rcc)4, -OP(ORcc)4, -B(Raa)2, -B(ORcc)2, -BRaa(ORcc), C1-10 알킬, C1-10 퍼할로알킬, C2-10 알케닐, C2-10 알키닐, 헤테로C1-10 알킬, 헤테로C2-10 알케닐, 헤테로C2-10 알키닐, C3-10 카르보시클릴, 3-14원 헤테로시클릴, C6-14 아릴, 및 5-14원 헤테로아릴을 포함하나 이에 제한되지는 않으며, 여기서 각각의 알킬, 알케닐, 알키닐, 헤테로알킬, 헤테로알케닐, 헤테로알키닐, 카르보시클릴, 헤테로시클릴, 아릴, 및 헤테로아릴은 독립적으로 0, 1, 2, 3, 4, 또는 5개의 Rdd 기로 치환되고; 여기서 X-는 반대이온이거나;
또는 탄소 원자 상의 2개의 같은자리 수소는 기 =O, =S, =NN(Rbb)2, =NNRbbC(=O)Raa, =NNRbbC(=O)ORaa, =NNRbbS(=O)2Raa, =NRbb, 또는 =NORcc로 치환되고;
각 경우의 Raa는 독립적으로 C1-10 알킬, C1-10 퍼할로알킬, C2-10 알케닐, C2-10 알키닐, 헤테로C1-10 알킬, 헤테로C2-10알케닐, 헤테로C2-10알키닐, C3-10 카르보시클릴, 3-14원 헤테로시클릴, C6-14 아릴, 및 5-14원 헤테로아릴로부터 선택되거나, 또는 2개의 Raa 기는 연결되어 3-14원 헤테로시클릴 또는 5-14원 헤테로아릴 고리를 형성하며, 여기서 각각의 알킬, 알케닐, 알키닐, 헤테로알킬, 헤테로알케닐, 헤테로알키닐, 카르보시클릴, 헤테로시클릴, 아릴, 및 헤테로아릴은 독립적으로 0, 1, 2, 3, 4, 또는 5개의 Rdd이기로 치환되고;
각 경우의 Rbb는 독립적으로 수소, -OH, -ORaa, -N(Rcc)2, -CN, -C(=O)Raa, -C(=O)N(Rcc)2, -CO2Raa, -SO2Raa, -C(=NRcc)ORaa, -C(=NRcc)N(Rcc)2, -SO2N(Rcc)2, -SO2Rcc, -SO2ORcc, -SORaa, -C(=S)N(Rcc)2, -C(=O)SRcc, -C(=S)SRcc, -P(=O)(Raa)2, -P(=O)(ORcc)2, -P(=O)(N(Rcc)2)2, C1-10 알킬, C1-10 퍼할로알킬, C2-10 알케닐, C2-10 알키닐, 헤테로C1-10알킬, 헤테로C2-10알케닐, 헤테로C2-10알키닐, C3-10 카르보시클릴, 3-14원 헤테로시클릴, C6-14 아릴, 및 5-14원 헤테로아릴로부터 선택되거나, 또는 2개의 Rbb 기는 연결되어 3-14원 헤테로시클릴 또는 5-14원 헤테로아릴 고리를 형성하며, 여기서 각각의 알킬, 알케닐, 알키닐, 헤테로알킬, 헤테로알케닐, 헤테로알키닐, 카르보시클릴, 헤테로시클릴, 아릴, 및 헤테로아릴은 독립적으로 0, 1, 2, 3, 4 또는 5개의 Rdd 기로 치환되고; 여기서 X-는 반대이온이고;
각 경우의 Rcc는 독립적으로 수소, C1-10 알킬, C1-10 퍼할로알킬, C2-10알케닐, C2-10 알키닐, 헤테로C1-10 알킬, 헤테로C2-10 알케닐, 헤테로C2-10 알키닐, C3-10 카르보시클릴, 3-14원 헤테로시클릴, C6-14 아릴 및 5-14원 헤테로아릴로부터 선택되거나, 또는 2개의 Rcc 기는 연결되어 3-14원 헤테로시클릴 또는 5-14원 헤테로아릴 고리를 형성하며, 여기서 각각의 알킬, 알케닐, 알키닐, 헤테로알킬, 헤테로알케닐, 헤테로알키닐, 카르보시클릴, 헤테로시클릴, 아릴, 및 헤테로아릴은 독립적으로 0, 1, 2, 3, 4 또는 5개의 Rdd 기로 치환되고;
각 경우의 Rdd는 독립적으로 할로겐, -CN, -NO2, -N3, -SO2H, -SO3H, -OH, -ORee, -ON(Rff)2, -N(Rff)2, -N(Rff)3 +X-, -N(ORee)Rff, -SH, -SRee, -SSRee, -C(=O)Ree, -CO2H, -CO2Ree, -OC(=O)Ree, -OCO2Ree, -C(=O)N(Rff)2, -OC(=O)N(Rff)2, -NRffC(=O)Ree, -NRffCO2Ree, -NRffC(=O)N(Rff)2, -C(=NRff)ORee, -OC(=NRff)Ree, -OC(=NRff)ORee, -C(=NRff)N(Rff)2, -OC(=NRff)N(Rff)2, -NRffC(=NRff)N(Rff)2, -NRffSO2Ree, -SO2N(Rff)2, -SO2Ree, -SO2ORee, -OSO2Ree, -S(=O)Ree, -Si(Ree)3, -OSi(Ree)3, -C(=S)N(Rff)2, -C(=O)SRee, -C(=S)SRee, -SC(=S)SRee, -P(=O)(ORee)2, -P(=O)(Ree)2, -OP(=O)(Ree)2, -OP(=O)(ORee)2, C1-6 알킬, C1-6 퍼할로알킬, C2-6 알케닐, C2-6 알키닐, 헤테로C1-6알킬, 헤테로C2-6알케닐, 헤테로C2-6알키닐, C3-10 카르보시클릴, 3-10원 헤테로시클릴, C6-10 아릴, 5-10원 헤테로아릴로부터 선택되며, 여기서 각각의 알킬, 알케닐, 알키닐, 헤테로알킬, 헤테로알케닐, 헤테로알키닐, 카르보시클릴, 헤테로시클릴, 아릴, 및 헤테로아릴은 독립적으로 0, 1, 2, 3, 4 또는 5개의 Rgg 기로 치환되거나, 또는 2개의 같은자리 Rdd 치환기는 연결되어 =O 또는 =S를 형성할 수 있고; 여기서 X-는 반대이온이고;
각 경우의 Ree는 독립적으로 C1-6 알킬, C1-6 퍼할로알킬, C2-6 알케닐, C2-6 알키닐, 헤테로C1-6 알킬, 헤테로C2-6알케닐, 헤테로C2-6 알키닐, C3-10 카르보시클릴, C6-10 아릴, 3-10원 헤테로시클릴, 및 3-10원 헤테로아릴로부터 선택되며, 여기서 각각의 알킬, 알케닐, 알키닐, 헤테로알킬, 헤테로알케닐, 헤테로알키닐, 카르보시클릴, 헤테로시클릴, 아릴, 및 헤테로아릴은 독립적으로 0, 1, 2, 3, 4 또는 5개의 Rgg 기로 치환되고;
각 경우의 Rff는 독립적으로 수소, C1-6 알킬, C1-6 퍼할로알킬, C2-6 알케닐, C2-6 알키닐, 헤테로C1 - 6알킬, 헤테로C2 - 6알케닐, 헤테로C2 - 6알키닐, C3-10 카르보시클릴, 3-10원 헤테로시클릴, C6-10 아릴 및 5-10원 헤테로아릴로부터 선택되거나, 또는 2개의 Rff 기는 연결되어 3-10원 헤테로시클릴 또는 5-10원 헤테로아릴 고리를 형성하며, 여기서 각각의 알킬, 알케닐, 알키닐, 헤테로알킬, 헤테로알케닐, 헤테로알키닐, 카르보시클릴, 헤테로시클릴, 아릴, 및 헤테로아릴은 독립적으로 0, 1, 2, 3, 4 또는 5개의 Rgg 기로 치환되고;
각 경우의 Rgg는, 독립적으로, 할로겐, -CN, -NO2, -N3, -SO2H, -SO3H, -OH, -OC1-6 알킬, -ON(C1-6 알킬)2, -N(C1-6 알킬)2, -N(C1-6 알킬)3 +X-, -NH(C1-6 알킬)2 +X-, -NH2(C1-6 알킬) +X-, -NH3 +X-, -N(OC1-6 알킬)(C1-6 알킬), -N(OH)(C1-6 알킬), -NH(OH), -SH, -SC1-6 알킬, -SS(C1-6 알킬), -C(=O)(C1-6 알킬), -CO2H, -CO2(C1-6 알킬), -OC(=O)(C1-6 알킬), -OCO2(C1-6 알킬), -C(=O)NH2, -C(=O)N(C1-6 알킬)2, -OC(=O)NH(C1-6 알킬), -NHC(=O)( C1-6 알킬), -N(C1-6 알킬)C(=O)( C1-6 알킬), -NHCO2(C1-6 알킬), -NHC(=O)N(C1-6 알킬)2, -NHC(=O)NH(C1-6 알킬), -NHC(=O)NH2, -C(=NH)O(C1-6 알킬), -OC(=NH)(C1-6 알킬), -OC(=NH)OC1-6 알킬, -C(=NH)N(C1-6 알킬)2, -C(=NH)NH(C1-6 알킬), -C(=NH)NH2, -OC(=NH)N(C1-6 알킬)2, -OC(NH)NH(C1-6 알킬), -OC(NH)NH2, -NHC(NH)N(C1-6 알킬)2, -NHC(=NH)NH2, -NHSO2(C1-6 알킬), -SO2N(C1-6 알킬)2, -SO2NH(C1-6 알킬), -SO2NH2, -SO2C1-6 알킬, -SO2OC1-6 알킬, -OSO2C1-6 알킬, -SOC1-6 알킬, -Si(C1-6 알킬)3, -OSi(C1-6 알킬)3 -C(=S)N(C1-6 알킬)2, C(=S)NH(C1-6 알킬), C(=S)NH2, -C(=O)S(C1-6 알킬), -C(=S)SC1-6 알킬, -SC(=S)SC1-6 알킬, -P(=O)(OC1-6 알킬)2, -P(=O)(C1-6 알킬)2, -OP(=O)(C1-6 알킬)2, -OP(=O)(OC1-6 알킬)2, C1-6 알킬, C1-6 퍼할로알킬, C2-6 알케닐, C2-6 알키닐, 헤테로C1-6알킬, 헤테로C2-6알케닐, 헤테로C2-6알키닐, C3-10 카르보시클릴, C6-10 아릴, 3-10원 헤테로시클릴, 5-10원 헤테로아릴이거나; 또는 2개의 같은자리 Rgg 치환기는 결합하여 =O 또는 =S를 형성할 수 있고; 여기서 X-는 반대이온이다.
용어 "아미노"는 화학식 (-NH2)의 기를 지칭한다. "치환된 아미노"는 일-치환된 아민 (-NHRh) 또는 이치환된 아민 (-NRh 2)을 지칭하며, 여기서 Rh 치환기는 안정한 모이어티를 형성하는 본원에 기재된 바와 같은 임의의 치환기 (예를 들어, 그의 각각이 추가로 치환될 수 있거나 또는 치환되지 않을 수 있는 적합한 아미노 보호기; 지방족, 알킬, 알케닐, 알키닐, 헤테로지방족, 헤테로시클릭, 아릴, 헤테로아릴, 아실, 아미노, 니트로, 히드록실, 티올, 할로, 지방족아미노, 헤테로지방족아미노, 알킬아미노, 헤테로알킬아미노, 아릴아미노, 헤테로아릴아미노, 알킬아릴, 아릴알킬, 지방족옥시, 헤테로지방족옥시, 알킬옥시, 헤테로알킬옥시, 아릴옥시, 헤테로아릴옥시, 지방족티옥시, 헤테로지방족티옥시, 알킬티옥시, 헤테로알킬티옥시, 아릴티옥시, 헤테로아릴티옥시, 아실옥시 등)이다. 특정 실시양태에서, 이치환된 아미노 기 (-NRh 2)의 Rh 치환기는 5- 내지 6-원 헤테로시클릭 고리를 형성한다.
용어 "알콕시"는 Ri가 본원에 정의된 바와 같은 임의로 치환된 알킬 기이고, 산소 모이어티가 직접적으로 모 분자에 부착되는 것인, 화학식 (-ORi)의 "치환된 히드록실"을 지칭한다.
용어 "알킬티옥시"는 Rr이 본원에 정의된 바와 같은 임의로 치환된 알킬 기이고, 황 모이어티가 직접적으로 모 분자에 부착되는 것인, 화학식 (-SRr)의 "치환된 티올"을 지칭한다.
용어 "알킬아미노"는 Rh가 독립적으로 수소 또는 본원에 정의된 바와 같은 임의로 치환된 알킬 기이고, 질소 모이어티가 직접적으로 모 분자에 부착되는 것인, 화학식 (-NRh 2)의 "치환된 아미노"를 지칭한다.
용어 "아릴"은 모든 고리 원자가 탄소이고, 치환 또는 비치환될 수 있는, 3 내지 20개의 고리 원자를 갖는 안정한 방향족 모노- 또는 폴리시클릭 고리계를 지칭한다. 본 발명의 특정 실시양태에서, "아릴"은 페닐, 비페닐, 나프틸 등을 포함하지만 이에 제한되지는 않으며, 1개 이상의 치환기를 보유할 수 있는, 1, 2 또는 3개의 방향족 고리를 갖는 모노, 비 또는 트리시클릭 C4-C20 방향족 고리계를 지칭한다. 아릴 치환기는 안정한 모이어티를 형성하는 본원에 기재된 임의의 치환기 (예를 들어, 그의 각각이 추가로 치환될 수 있거나 또는 치환되지 않을 수 있는 지방족, 알킬, 알케닐, 알키닐, 헤테로지방족, 헤테로시클릭, 아릴, 헤테로아릴, 아실, 옥소, 이미노, 티오옥소, 시아노, 이소시아노, 아미노, 아지도, 니트로, 히드록실, 티올, 할로, 지방족아미노, 헤테로지방족아미노, 알킬아미노, 헤테로알킬아미노, 아릴아미노, 헤테로아릴아미노, 알킬아릴, 아릴알킬, 지방족옥시, 헤테로지방족옥시, 알킬옥시, 헤테로알킬옥시, 아릴옥시, 헤테로아릴옥시, 지방족티옥시, 헤테로지방족티옥시, 알킬티옥시, 헤테로알킬티옥시, 아릴티옥시, 헤테로아릴티옥시, 아실옥시 등)를 포함하지만, 이에 제한되지는 않는다.
용어 "아릴알킬"은 아릴 치환된 알킬 기를 지칭하며, 여기서 용어 "아릴" 및 "알킬"은 본원에 정의되고, 아릴 기는 알킬 기에 부착되고, 이는 다시 모 분자에 부착된다. 예시적인 아릴알킬 기는 벤질 및 페네틸이다.
용어 "아릴옥시"는 Ri가 본원에 정의된 바와 같은 임의로 치환된 아릴 기이고, 산소 모이어티가 직접적으로 모 분자에 부착되는 것인, 화학식 (-ORi)의 "치환된 히드록실"을 지칭한다.
용어 "아릴아미노"는 Rh가 독립적으로 수소 또는 본원에 정의된 바와 같은 임의로 치환된 아릴 기이고, 질소 모이어티가 직접적으로 모 분자에 부착되는 것인, 화학식 (-NRh 2)의 "치환된 아미노"를 지칭한다.
용어 "아릴티옥시"는 Rr이 본원에 정의된 바와 같은 임의로 치환된 아릴 기이고, 황 모이어티가 직접적으로 모 분자에 부착되는 것인, 화학식 (-SRr)의 "치환된 티올"을 지칭한다.
본원에 사용된 용어 "할로" 및 "할로겐"은 플루오린 (플루오로, -F), 염소 (클로로, -Cl), 브로민 (브로모, -Br), 및 아이오딘 (아이오도, -I)으로부터 선택된 원자를 지칭한다.
용어 "헤테로지방족"은 1개 이상의 관능기로 임의로 치환된, 포화 및 불포화 둘 다의, 비방향족, 직쇄 (즉, 비분지형), 분지형, 비-시클릭, 시클릭 (예를 들어, 헤테로시클릭) 또는 폴리시클릭 탄화수소를 포함하고, 예를 들어 탄소 원자 대신에 1개 이상의 산소, 황, 질소, 인, 또는 규소 원자를 함유하는, 본원에 정의된 바와 같은 지방족 모이어티를 지칭한다. 특정 실시양태에서, 헤테로지방족 모이어티는 그 위의 1개 이상의 수소 원자가 독립적으로 1개 이상의 치환기로 대체됨으로써 치환된다. 통상의 기술자에게 인지되는 바와 같이, "헤테로지방족"은 헤테로알킬, 헤테로알케닐, 헤테로알키닐, 헤테로시클로알킬, 헤테로시클로알케닐 및 헤테로시클로알키닐 모이어티를 포함하지만 이에 제한되지는 않도록 본원에서 의도된다. 따라서, 용어 "헤테로지방족"은 용어 "헤테로알킬", "헤테로알케닐", "헤테로알키닐" 등을 포함한다. 또한, 용어 "헤테로알킬", "헤테로알케닐", "헤테로알키닐" 등은 치환 및 비치환된 기 둘 다를 포괄한다. 특정 실시양태에서, "헤테로지방족"은 1-20개의 탄소 원자를 갖는 헤테로지방족 기 (시클릭, 비-시클릭, 치환된, 비치환된, 분지형 또는 비분지형)를 나타내는데 사용된다. 헤테로지방족 기 치환기는 안정한 모이어티를 형성하는 본원에 기재된 임의의 치환기 (예를 들어, 그의 각각이 추가로 치환될 수 있거나 또는 치환되지 않을 수 있는 지방족, 알킬, 알케닐, 알키닐, 헤테로지방족, 헤테로시클릭, 아릴, 헤테로아릴, 아실, 술피닐, 술포닐, 옥소, 이미노, 티오옥소, 시아노, 이소시아노, 아미노, 아지도, 니트로, 히드록실, 티올, 할로, 지방족아미노, 헤테로지방족아미노, 알킬아미노, 헤테로알킬아미노, 아릴아미노, 헤테로아릴아미노, 알킬아릴, 아릴알킬, 지방족옥시, 헤테로지방족옥시, 알킬옥시, 헤테로알킬옥시, 아릴옥시, 헤테로아릴옥시, 지방족티옥시, 헤테로지방족티옥시, 알킬티옥시, 헤테로알킬티옥시, 아릴티옥시, 헤테로아릴티옥시, 아실옥시 등)를 포함하지만, 이에 제한되지는 않는다.
용어 "헤테로알킬"은, 예를 들어 탄소 원자 대신에 1개 이상의 산소, 황, 질소, 인, 또는 규소 원자를 함유하는, 본원에 정의된 바와 같은 알킬 모이어티를 지칭한다.
용어 "헤테로알케닐"은, 예를 들어 탄소 원자 대신에 1개 이상의 산소, 황, 질소, 인, 또는 규소 원자를 함유하는, 본원에 정의된 바와 같은 알케닐 모이어티를 지칭한다.
용어 "헤테로알키닐"은, 예를 들어 탄소 원자 대신에 1개 이상의 산소, 황, 질소, 인, 또는 규소 원자를 함유하는, 본원에 정의된 바와 같은 알키닐 모이어티를 지칭한다.
용어 "헤테로알킬아미노"는 Rh가 독립적으로 수소 또는 본원에 정의된 바와 같은 임의로 치환된 헤테로알킬 기이고, 질소 모이어티가 직접적으로 모 분자에 부착되는 것인, 화학식 (-NRh 2)의 "치환된 아미노"를 지칭한다.
용어 "헤테로알킬옥시"는 Ri가 본원에 정의된 바와 같은 임의로 치환된 헤테로알킬 기이고, 산소 모이어티가 직접적으로 모 분자에 부착되는 것인, 화학식 (-ORi)의 "치환된 히드록실"을 지칭한다.
용어 "헤테로알킬티옥시"는 Rr이 본원에 정의된 바와 같은 임의로 치환된 헤테로알킬 기이고, 황 모이어티가 직접적으로 모 분자에 부착되는 것인, 화학식 (-SRr)의 "치환된 티올"을 지칭한다.
용어 "카르보시클릴" 또는 "카르보시클릭"은 비-방향족 고리계에 3 내지 14개의 고리 탄소 원자 및 0개의 헤테로원자를 갖는 비-방향족 시클릭 탄화수소 기 ("C3-14 카르보시클릴")의 라디칼을 지칭한다. 일부 실시양태에서, 카르보시클릴 기는 3 내지 10개의 고리 탄소 원자를 갖는다 ("C3-10 카르보시클릴"). 일부 실시양태에서, 카르보시클릴 기는 3 내지 8개의 고리 탄소 원자를 갖는다 ("C3-8 카르보시클릴"). 일부 실시양태에서, 카르보시클릴 기는 3 내지 7개의 고리 탄소 원자 ("C3-7 카르보시클릴")를 갖는다. 일부 실시양태에서, 카르보시클릴 기는 3 내지 6개의 고리 탄소 원자를 갖는다 ("C3-6 카르보시클릴"). 일부 실시양태에서, 카르보시클릴 기는 4 내지 6개의 고리 탄소 원자 ("C4-6 카르보시클릴")를 갖는다. 일부 실시양태에서, 카르보시클릴 기는 5 내지 6개의 고리 탄소 원자 ("C5-6 카르보시클릴")를 갖는다. 일부 실시양태에서, 카르보시클릴 기는 5 내지 10개의 고리 탄소 원자를 갖는다 ("C5-10 카르보시클릴"). 예시적인 C3-6 카르보시클릴 기는, 비제한적으로, 시클로프로필 (C3), 시클로프로페닐 (C3), 시클로부틸 (C4), 시클로부테닐 (C4), 시클로펜틸 (C5), 시클로펜테닐 (C5), 시클로헥실 (C6), 시클로헥세닐 (C6), 시클로헥사디에닐 (C6) 등을 포함한다. 예시적인 C3-8 카르보시클릴 기는, 비제한적으로, 상기 언급된 C3-6 카르보시클릴 기, 뿐만 아니라 시클로헵틸 (C7), 시클로헵테닐 (C7), 시클로헵타디에닐 (C7), 시클로헵타트리에닐 (C7), 시클로옥틸 (C8), 시클로옥테닐 (C8), 비시클로[2.2.1]헵타닐 (C7), 비시클로[2.2.2]옥타닐 (C8) 등을 포함한다. 예시적인 C3-10 카르보시클릴 기는, 비제한적으로, 상기 언급된 C3-8 카르보시클릴 기, 뿐만 아니라 시클로노닐 (C9), 시클로노네닐 (C9), 시클로데실 (C10), 시클로데세닐 (C10), 옥타히드로-1H-인데닐 (C9), 데카히드로나프탈레닐 (C10), 스피로[4.5]데카닐 (C10) 등을 포함한다. 상기 예들이 예시하는 바와 같이, 특정 실시양태에서, 카르보시클릴 기는 모노시클릭 ("모노시클릭 카르보시클릴")이거나 또는 폴리시클릭 (예를 들어, 융합, 가교 또는 스피로 고리계, 예컨대 비시클릭 계 ("비시클릭 카르보시클릴") 또는 트리시클릭 계 ("트리시클릭 카르보시클릴")을 함유함)이고, 포화될 수 있거나 또는 1개 이상의 탄소-탄소 이중 결합 또는 삼중 결합을 함유할 수 있다. "카르보시클릴"은 또한 상기 정의된 바와 같은 카르보시클릴 고리가 1개 이상의 아릴 또는 헤테로아릴 기와 융합되고, 여기서 부착 지점은 카르보시클릴 고리 상에 있는 것인 고리계를 포함하고, 이러한 경우에 탄소의 수는 카르보시클릭 고리계 내의 탄소의 수를 계속해서 지정한다. 달리 명시되지 않는 한, 각 경우의 카르보시클릴 기는 독립적으로 비치환되거나 ("비치환된 카르보시클릴") 또는 1개 이상의 치환기로 치환된다 ("치환된 카르보시클릴"). 특정 실시양태에서, 카르보시클릴기는 비치환된 C3-14 카르보시클릴이다. 특정 실시양태에서, 카르보시클릴기는 치환된 C3-14 카르보시클릴이다.
일부 실시양태에서, "카르보시클릴"은 3 내지 14개의 탄소 원자를 갖는 모노시클릭 포화 카르보시클릴 기이다 ("C3-14 시클로알킬"). 일부 실시양태에서, 시클로알킬 기는 3 내지 10개의 탄소 원자를 갖는다 ("C3-10 시클로알킬"). 일부 실시양태에서, 시클로알킬 기는 3 내지 8개의 고리 탄소 원자를 갖는다 ("C3-8 시클로알킬"). 일부 실시양태에서, 시클로알킬 기는 3 내지 6개의 고리 탄소 원자를 갖는다 ("C3-6 시클로알킬"). 일부 실시양태에서, 시클로알킬 기는 4 내지 6개의 고리 탄소 원자 ("C4-6 시클로알킬")를 갖는다. 일부 실시양태에서, 시클로알킬 기는 5 내지 6개의 고리 탄소 원자를 갖는다 ("C5-6 시클로알킬"). 일부 실시양태에서, 시클로알킬 기는 5 내지 10개의 고리 탄소 원자를 갖는다 ("C5-10 시클로알킬"). C5-6 시클로알킬 기의 예는 시클로펜틸 (C5) 및 시클로헥실 (C5)을 포함한다. C3-6 시클로알킬 기의 예는 상기 언급된 C5-6 시클로알킬 기, 뿐만 아니라 시클로프로필 (C3) 및 시클로부틸 (C4)을 포함한다. C3-8 시클로알킬 기의 예는 상기 언급된 C3-6 시클로알킬 기, 뿐만 아니라 시클로헵틸 (C7) 및 시클로옥틸 (C8)을 포함한다. 달리 명시되지 않는 한, 각 경우의 시클로알킬 기는 독립적으로 비치환되거나 ("비치환된 시클로알킬") 또는 1개 이상의 치환기로 치환된다 ("치환된 시클로알킬"). 특정 실시양태에서, 시클로알킬기는 비치환된 C3-14 시클로알킬이다. 특정 실시양태에서, 시클로알킬기는 치환된 C3-14 시클로알킬이다.
용어 "헤테로시클릭", "헤테로사이클" 또는 "헤테로시클릴"은 시클릭 헤테로지방족 기를 지칭한다. 헤테로시클릭 기는 3 내지 8개 원자 크기의 단일 고리를 포함하는, 부분적으로 불포화되거나 또는 완전히 포화된 비-방향족 3- 내지 12-원 고리계, 및 비-방향족 고리에 융합된 5- 또는 6-원 방향족 아릴 또는 헤테로아릴 기를 포함할 수 있는 비- 및 트리시클릭 고리계를 지칭한다. 이들 헤테로시클릭 고리는 산소, 황 및 질소로부터 독립적으로 선택된 1 내지 3개의 헤테로원자를 갖는 것을 포함하고, 여기서 질소 및 황 헤테로원자는 임의로 산화될 수 있고, 질소 헤테로원자는 임의로 4급화될 수 있다. 특정 실시양태에서, 용어 헤테로시클릭은 적어도 1개의 고리 원자가 O, S 및 N (여기서, 질소 및 황 헤테로원자는 임의로 산화될 수 있음)으로부터 선택된 헤테로원자이고, 나머지 고리 원자가 탄소이고, 라디칼이 임의의 고리 원자를 통해 분자의 나머지 부분과 연결되는 것인, 비-방향족 5-, 6-, 또는 7-원 고리 또는 폴리시클릭 기를 지칭한다. 헤테로시클릴 기는 산소, 황 및 질소로부터 독립적으로 선택된 1 내지 3개의 헤테로원자를 갖는 융합된 5-, 6-, 또는 7-원 고리를 포함하는 비- 또는 트리-시클릭 기를 포함하지만 이에 제한되지는 않으며, 여기서 (i) 각각의 5-원 고리는 0 내지 2개의 이중 결합을 갖고, 각각의 6-원 고리는 0 내지 2개의 이중 결합을 가지며, 각각의 7-원 고리는 0 내지 3개의 이중 결합을 갖고, (ii) 질소 및 황 헤테로원자는 임의로 산화될 수 있고, (iii) 질소 헤테로원자는 임의로 4급화될 수 있고, (iv) 임의의 상기 헤테로시클릭 고리는 아릴 또는 헤테로아릴 고리에 융합될 수 있다. 예시적인 헤테로사이클은 1개 이상의 치환기를 보유할 수 있는 아자시클로프로파닐, 아자시클로부타닐, 1,3-디아자티디닐, 피페리디닐, 피페라지닐, 아조카닐, 티아라닐, 티에타닐, 테트라히드로티오페닐, 디티올라닐, 티아시클로헥사닐, 옥시라닐, 옥세타닐, 테트라히드로푸라닐, 테트라히드로퓨라닐, 디옥사닐, 옥사티올라닐, 모르폴리닐, 티옥사닐, 테트라히드로나프틸 등을 포함한다. 치환기는 안정한 모이어티를 형성하는 본원에 기재된 임의의 치환기 (예를 들어, 그의 각각이 추가로 치환될 수 있거나 또는 치환되지 않을 수 있는 지방족, 알킬, 알케닐, 알키닐, 헤테로지방족, 헤테로시클릭, 아릴, 헤테로아릴, 아실, 술피닐, 술포닐, 옥소, 이미노, 티오옥소, 시아노, 이소시아노, 아미노, 아지도, 니트로, 히드록실, 티올, 할로, 지방족아미노, 헤테로지방족아미노, 알킬아미노, 헤테로알킬아미노, 아릴아미노, 헤테로아릴아미노, 알킬아릴, 아릴알킬, 지방족옥시, 헤테로지방족옥시, 알킬옥시, 헤테로알킬옥시, 아릴옥시, 헤테로아릴옥시, 지방족티옥시, 헤테로지방족티옥시, 알킬티옥시, 헤테로알킬티옥시, 아릴티옥시, 헤테로아릴티옥시, 아실옥시 등)를 포함하지만, 이에 제한되지는 않는다.
용어 "헤테로아릴"은 3-20개의 고리 원자를 갖고, 이들 중 1개의 고리 원자가 S, O 및 N으로부터 선택되고; 0, 1, 또는 2개의 고리 원자가 독립적으로 S, O 및 N으로부터 선택된 추가의 헤테로원자이고; 나머지 고리 원자가 탄소이고, 라디칼이 임의의 고리 원자를 통해 분자의 나머지 부분과 연결되는 것인, 안정한 방향족 모노- 또는 폴리시클릭 고리계를 지칭한다. 예시적인 헤테로아릴은 1개 이상의 치환기를 보유할 수 있는 피롤릴, 피라졸릴, 이미다졸릴, 피리디닐 (피리딜), 피리미디닐, 피라지닐, 피리다지닐, 트리아지닐, 테트라지닐, 피롤리지닐, 인돌릴, 퀴놀리닐, 이소퀴놀리닐, 벤조이미다졸릴, 인다졸릴, 퀴놀리닐, 이소퀴놀리닐, 퀴놀리지닐, 신놀리닐, 퀴나졸리닐, 프탈라지닐, 나프티리디닐, 퀴녹살리닐, 티오페닐, 티아나프테닐, 푸라닐, 벤조푸라닐, 벤조티아졸릴, 티아졸리닐, 이소티아졸릴, 티아디아졸리닐, 옥사졸릴, 이속사졸릴, 옥사디아지올릴, 옥사디아지올릴 등을 포함하지만, 이에 제한되지는 않는다. 헤테로아릴 치환기는 안정한 모이어티를 형성하는 본원에 기재된 임의의 치환기 (예를 들어, 그의 각각이 추가로 치환될 수 있거나 또는 치환되지 않을 수 있는 지방족, 알킬, 알케닐, 알키닐, 헤테로지방족, 헤테로시클릭, 아릴, 헤테로아릴, 아실, 술피닐, 술포닐, 옥소, 이미노, 티오옥소, 시아노, 이소시아노, 아미노, 아지도, 니트로, 히드록실, 티올, 할로, 지방족아미노, 헤테로지방족아미노, 알킬아미노, 헤테로알킬아미노, 아릴아미노, 헤테로아릴아미노, 알킬아릴, 아릴알킬, 지방족옥시, 헤테로지방족옥시, 알킬옥시, 헤테로알킬옥시, 아릴옥시, 헤테로아릴옥시, 지방족티옥시, 헤테로지방족티옥시, 알킬티옥시, 헤테로알킬티옥시, 아릴티옥시, 헤테로아릴티옥시, 아실옥시 등)를 포함하지만, 이에 제한되지는 않는다.
용어 "헤테로아릴아미노"는 Rh가 독립적으로 수소 또는 본원에 정의된 바와 같은 임의로 치환된 헤테로아릴 기이고, 질소 모이어티가 직접적으로 모 분자에 부착되는 것인, (-NRh 2)의 "치환된 아미노"를 지칭한다.
용어 "헤테로아릴옥시"는 Ri가 본원에 정의된 바와 같은 임의로 치환된 헤테로아릴 기이고, 산소 모이어티가 직접적으로 모 분자에 부착되는 것인, 화학식 (-ORi)의 "치환된 히드록실"을 지칭한다.
용어 "헤테로아릴티옥시"는 Rr이 본원에 정의된 바와 같은 임의로 치환된 헤테로아릴 기이고, 황 모이어티가 직접적으로 모 분자에 부착되는 것인, 화학식 (-SRr)의 "치환된 티올"을 지칭한다.
용어 "히드록시" 또는 "히드록실"은 기 -OH를 지칭한다. 더 나아가, 용어 "치환된 히드록실" 또는 "치환된 히드록실"은 모 분자에 직접적으로 부착된 산소 원자가 수소 이외의 기로 치환된 것인 히드록실 기를 지칭하고, -ORaa, -ON(Rbb)2, -OC(=O)SRaa, -OC(=O)Raa, -OCO2Raa, -OC(=O)N(Rbb)2, -OC(=NRbb)Raa, -OC(=NRbb)ORaa, -OC(=NRbb)N(Rbb)2, -OS(=O)Raa, -OSO2Raa, -OSi(Raa)3, -OP(Rcc)2, -OP(Rcc)3 +X-, -OP(ORcc)2, -OP(ORcc)3 +X-, -OP(=O)(Raa)2, -OP(=O)(ORcc)2, 및 -OP(=O)(N(Rbb))2 (여기서, X-, Raa, Rbb, 및 Rcc는 본원에 정의된 바와 같음)로부터 선택된 기를 포함한다.
용어 "이미노"는 화학식 (=NRr)의 기를 지칭하며, 여기서 Rr은 수소 또는 안정한 모이어티를 생성하는 본원에 기재된 바와 같은 임의의 치환기 (예를 들어, 그의 각각이 추가로 치환될 수 있거나 또는 치환되지 않을 수 있는 적합한 아미노 보호기; 지방족, 알킬, 알케닐, 알키닐, 헤테로지방족, 헤테로시클릭, 아릴, 헤테로아릴, 아실, 아미노, 히드록실, 알킬아릴, 아릴알킬 등)에 상응한다. 특정 실시양태에서, 이미노는 Rr이 수소인 =NH를 지칭한다.
용어 "니트로"는 화학식 (-NO2)의 기를 지칭한다.
용어 "옥소"는 화학식 (=O)의 기를 지칭한다.
"보호기"는 관련 기술분야에 널리 공지되어 있고, 문헌 [Greene's Protective Groups in Organic Synthesis, P. G. M. Wuts and T. W. Greene, 4th edition, Wiley-Interscience, 2006]에 상세히 기재된 것을 포함하며, 그의 전문은 본원에 참조로 포함된다.
질소 원자는 원자가가 허용하는 바에 따라 치환 또는 비치환될 수 있고, 1급, 2급, 3급 및 4급 질소 원자를 포함한다. 예시적인 질소 원자 치환기는 수소, -OH, -ORaa, -N(Rcc)2, -CN, -C(=O)Raa, -C(=O)N(Rcc)2, -CO2Raa, -SO2Raa, -C(=NRbb)Raa, -C(=NRcc)ORaa, -C(=NRcc)N(Rcc)2, -SO2N(Rcc)2, -SO2Rcc, -SO2ORcc, -SORaa, -C(=S)N(Rcc)2, -C(=O)SRcc, -C(=S)SRcc, -P(=O)(ORcc)2, -P(=O)(Raa)2, -P(=O)(N(Rcc)2)2, C1-10 알킬, C1-10 퍼할로알킬, C2-10 알케닐, C2-10 알키닐, 헤테로C1-10알킬, 헤테로C2-10알케닐, 헤테로C2-10알키닐, C3-10 카르보시클릴, 3-14원 헤테로시클릴, C6-14 아릴, 및 5-14원 헤테로아릴을 포함하나 이에 제한되지는 않거나, 또는 N 원자에 부착된 2개의 Rcc 기는 연결되어 3-14원 헤테로시클릴 또는 5-14원 헤테로아릴 고리를 형성하며, 여기서 각각의 알킬, 알케닐, 알키닐, 헤테로알킬, 헤테로알케닐, 헤테로알키닐, 카르보시클릴, 헤테로시클릴, 아릴, 및 헤테로아릴은 독립적으로 0, 1, 2, 3, 4 또는 5개의 Rdd 기로 치환되고, 여기서 Raa, Rbb, Rcc, 및 Rdd은 상기 정의된 바와 같다.
특정 실시양태에서, 질소 원자 상에 존재하는 치환기는 질소 보호기 (본원에서 "아미노 보호기"라고도 지칭함)이다. 질소 보호기는 -OH, -ORaa, -N(Rcc)2, -C(=O)Raa, -C(=O)N(Rcc)2, -CO2Raa, -SO2Raa, -C(=NRcc)Raa, -C(=NRcc)ORaa, -C(=NRcc)N(Rcc)2, -SO2N(Rcc)2, -SO2Rcc, -SO2ORcc, -SORaa, -C(=S)N(Rcc)2, -C(=O)SRcc, -C(=S)SRcc, C1-10 알킬 (예를 들어, 아르알킬, 헤테로아르알킬), C2-10 알케닐, C2-10 알키닐, 헤테로C1-10 알킬, 헤테로C2-10 알케닐, 헤테로C2-10 알키닐, C3-10 카르보시클릴, 3-14원 헤테로시클릴, C6-14 아릴, 및 5-14원 헤테로아릴 기를 포함하지만 이에 제한되는 것은 아니며, 여기서 각각의 알킬, 알케닐, 알키닐, 헤테로알킬, 헤테로알케닐, 헤테로알키닐, 카르보시클릴, 헤테로시클릴, 아르알킬, 아릴 및 헤테로아릴은 독립적으로 0, 1, 2, 3, 4 또는 5개의 Rdd 기로 치환되고, 여기서 Raa, Rbb, Rcc 및 Rdd는 본원에 정의된 바와 같다. 질소 보호기는 관련 기술분야에 널리 공지되어 있고, 본원에 참조로 포함되는 문헌 [Protecting Groups in Organic Synthesis, T. W. Greene and P. G. M. Wuts, 3rd edition, John Wiley & Sons, 1999]에 상세하게 기재된 것을 포함한다.
예를 들어, 질소 보호기, 예컨대 아미드 기 (예를 들어, -C(=O)Raa)는 포름아미드, 아세트아미드, 클로로아세트아미드, 트리클로로아세트아미드, 트리플루오로아세트아미드, 페닐아세트아미드, 3-페닐프로판아미드, 피콜린아미드, 3-피리딜카르복스아미드, N-벤조일페닐알라닐 유도체, 벤즈아미드, p-페닐벤즈아미드, o-니트로페닐아세트아미드, o-니트로페녹시아세트아미드, 아세토아세트아미드, (N'-디티오벤질옥시아실아미노)아세트아미드, 3-(p-히드록시페닐)프로판아미드, 3-(o-니트로페닐)프로판아미드, 2-메틸-2-(o-니트로페녹시)프로판아미드, 2-메틸-2-(o-페닐아조페녹시)프로판아미드, 4-클로로부탄아미드, 3-메틸-3-니트로부탄아미드, o-니트로신나미드, N-아세틸메티오닌 유도체, o-니트로벤즈아미드, 및 o-(벤조일옥시메틸)벤즈아미드를 포함하나 이에 제한되지는 않는다.
질소 보호기, 예컨대 카르바메이트 기 (예를 들어, -C(=O)ORaa)는 메틸 카르바메이트, 에틸 카르바메이트, 9-플루오레닐메틸 카르바메이트 (Fmoc), 9-(2-술포)플루오레닐메틸 카르바메이트, 9-(2,7-디브로모)플루오로에닐메틸 카르바메이트, 2,7-디-t-부틸-[9-(10,10-디옥소-10,10,10,10-테트라히드로티오크산틸)]메틸 카르바메이트 (DBD-Tmoc), 4-메톡시페나실 카르바메이트 (Phenoc), 2,2,2-트리클로로에틸 카르바메이트 (Troc), 2-트리메틸실릴에틸 카르바메이트 (Teoc), 2-페닐에틸 카르바메이트 (hZ), 1-(1-아다만틸)-1-메틸에틸 카르바메이트 (Adpoc), 1,1-디메틸-2-할로에틸 카르바메이트, 1,1-디메틸-2,2-디브로모에틸 카르바메이트 (DB-t-BOC), 1,1-디메틸-2,2,2-트리클로로에틸 카르바메이트 (TCBOC), 1-메틸-1-(4-비페닐릴)에틸 카르바메이트 (Bpoc), 1-(3,5-디-t-부틸페닐)-1-메틸에틸 카르바메이트 (t-Bumeoc), 2-(2'- 및 4'-피리딜)에틸 카르바메이트 (Pyoc), 2-(N,N-디시클로헥실카르복스아미도)에틸 카르바메이트, t-부틸 카르바메이트 (BOC 또는 Boc), 1-아다만틸 카르바메이트 (Adoc), 비닐 카르바메이트 (Voc), 알릴 카르바메이트 (Alloc), 1-이소프로필알릴 카르바메이트 (Ipaoc), 신나밀 카르바메이트 (Coc), 4-니트로신나밀 카르바메이트 (Noc), 8-퀴놀릴 카르바메이트, N-히드록시피페리디닐 카르바메이트, 알킬디티오 카르바메이트, 벤질 카르바메이트 (Cbz), p-메톡시벤질 카르바메이트 (Moz), p-니트로벤질 카르바메이트, p-브로모벤질 카르바메이트, p-클로로벤질 카르바메이트, 2,4-디클로로벤질 카르바메이트, 4-메틸술피닐벤질 카르바메이트 (Msz), 9-안트릴메틸 카르바메이트, 디페닐메틸 카르바메이트, 2-메틸티오에틸 카르바메이트, 2-메틸술포닐에틸 카르바메이트, 2-(p-톨루엔술포닐)에틸 카르바메이트, [2-(1,3-디티아닐)]메틸 카르바메이트 (Dmoc), 4-메틸티오페닐 카르바메이트 (Mtpc), 2,4-디메틸티오페닐 카르바메이트 (Bmpc), 2-포스포니오에틸 카르바메이트 (Peoc), 2-트리페닐포스포니오이소프로필 카르바메이트 (Ppoc), 1,1-디메틸-2-시아노에틸 카르바메이트, m-클로로-p-아실옥시벤질 카르바메이트, p-(디히드록시보릴)벤질 카르바메이트, 5-벤즈이속사졸릴메틸 카르바메이트, 2-(트리플루오로메틸)-6-크로모닐메틸 카르바메이트 (Tcroc), m-니트로페닐 카르바메이트, 3,5-디메톡시벤질 카르바메이트, o-니트로벤질 카르바메이트, 3,4-디메톡시-6-니트로벤질 카르바메이트, 페닐(o-니트로페닐)메틸 카르바메이트, t-아밀 카르바메이트, S-벤질 티오카르바메이트, p-시아노벤질 카르바메이트, 시클로부틸 카르바메이트, 시클로헥실 카르바메이트, 시클로펜틸 카르바메이트, 시클로프로필메틸 카르바메이트, p-데실옥시벤질 카르바메이트, 2,2-디메톡시아실비닐 카르바메이트, o-(N,N-디메틸카르복스아미도)벤질 카르바메이트, 1,1-디메틸-3-(N,N-디메틸카르복스아미도)프로필 카르바메이트, 1,1-디메틸프로피닐 카르바메이트, 디(2-피리딜)메틸 카르바메이트, 2-푸라닐메틸 카르바메이트, 2-아이오도에틸 카르바메이트, 이소보르닐 카르바메이트, 이소부틸 카르바메이트, 이소니코티닐 카르바메이트, p-(p'-메톡시페닐아조)벤질 카르바메이트, 1-메틸시클로부틸 카르바메이트, 1-메틸시클로헥실 카르바메이트, 1-메틸-1-시클로프로필메틸 카르바메이트, 1-메틸-1-(3,5-디메톡시페닐)에틸 카르바메이트, 1-메틸-1-(p-페닐아조페닐)에틸 카르바메이트, 1-메틸-1-페닐에틸 카르바메이트, 1-메틸-1-(4-피리딜)에틸 카르바메이트, 페닐 카르바메이트, p-(페닐아조)벤질 카르바메이트, 2,4,6-트리-t-부틸페닐 카르바메이트, 4-(트리메틸암모늄)벤질 카르바메이트, 및 2,4,6-트리메틸벤질 카르바메이트를 포함하나 이에 제한되지는 않는다.
질소 보호기, 예컨대 술폰아미드 기 (예를 들어, -S(=O)2Raa)는 p-톨루엔술폰아미드 (Ts), 벤젠술폰아미드, 2,3,6-트리메틸-4-메톡시벤젠술폰아미드 (Mtr), 2,4,6-트리메톡시벤젠술폰아미드 (Mtb), 2,6-디메틸-4-메톡시벤젠술폰아미드 (Pme), 2,3,5,6-테트라메틸-4-메톡시벤젠술폰아미드 (Mte), 4-메톡시벤젠술폰아미드 (Mbs), 2,4,6-트리메틸벤젠술폰아미드 (Mts), 2,6-디메톡시-4-메틸벤젠술폰아미드 (iMds), 2,2,5,7,8-펜타메틸크로만-6-술폰아미드 (Pmc), 메탄술폰아미드 (Ms), β-트리메틸실릴에탄술폰아미드 (SES), 9-안트라센술폰아미드, 4-(4',8'-디메톡시나프틸메틸)벤젠술폰아미드 (DNMBS), 벤질술폰아미드, 트리플루오로메틸술폰아미드, 및 페나실술폰아미드를 포함하나 이에 제한되지는 않는다.
다른 질소 보호기는 페노티아지닐-(10)-아실 유도체, N'-p-톨루엔술포닐아미노아실 유도체, N'-페닐아미노티오아실 유도체, N-벤조일페닐알라닐 유도체, N-아세틸메티오닌 유도체, 4,5-디페닐-3-옥사졸린-2-온, N-프탈이미드, N-디티아숙신이미드 (Dts), N-2,3-디페닐말레이미드, N-2,5-디메틸피롤, N-1,1,4,4-테트라메틸디실릴아자시클로펜탄 부가물 (STABASE), 5-치환된 1,3-디메틸-1,3,5-트리아자시클로헥산-2-온, 5-치환된 1,3-디벤질-1,3,5-트리아자시클로헥산-2-온, 1-치환된 3,5-디니트로-4-피리돈, N-메틸아민, N-알릴아민, N-[2-(트리메틸실릴)에톡시]메틸아민 (SEM), N-3-아세톡시프로필아민, N-(1-이소프로필-4-니트로-2-옥소-3-프롤린-3-일)아민, 4급 암모늄 염, N-벤질아민, N-디(4-메톡시페닐)메틸아민, N-5-디벤조수베릴아민, N-트리페닐메틸아민 (Tr), N-[(4-메톡시페닐)디페닐메틸]아민 (MMTr), N-9-페닐플루오레닐아민 (PhF), N-2,7-디클로로-9-플루오레닐메틸렌아민, N-페로세닐메틸아미노 (Fcm), N-2-피콜릴아미노 N'-옥시드, N-1,1-디메틸티오메틸렌아민, N-벤질리덴아민, N-p-메톡시벤질리덴아민, N-디페닐메틸렌아민, N-[(2-피리딜)메시틸]메틸렌아민, N-(N',N'-디메틸아미노메틸렌)아민, N,N'-이소프로필리덴디아민, N-p-니트로벤질리덴아민, N-살리실리덴아민, N-5-클로로살리실리덴아민, N-(5-클로로-2-히드록시페닐)페닐메틸렌아민, N-시클로헥실리덴아민, N-(5,5-디메틸-3-옥소-1-시클로헥세닐)아민, N-보란 유도체, N-디페닐보린산 유도체, N-[페닐(펜타아실크로뮴- 또는 텅스텐)아실]아민, N-구리 킬레이트, N-아연 킬레이트, N-니트로아민, N-니트로소아민, 아민 N-옥시드, 디페닐포스핀아미드 (Dpp), 디메틸티오포스핀아미드 (Mpt), 디페닐티오포스핀아미드 (Ppt), 디알킬 포스포르아미데이트, 디벤질 포스포르아미데이트, 디페닐 포스포르아미데이트, 벤젠술펜아미드, o-니트로벤젠술펜아미드 (Nps), 2,4-디니트로벤젠술펜아미드, 펜타클로로벤젠술펜아미드, 2-니트로-4-메톡시벤젠술펜아미드, 트리페닐메틸술펜아미드, 및 3-니트로피리딘술펜아미드 (Npys)를 포함하나 이에 제한되지는 않는다.
특정 실시양태에서, 산소 원자 상에 존재하는 치환기는 산소 보호기 (본원에서 "히드록실 보호기"라고도 지칭함)이다. 산소 보호기는 -Raa, -N(Rbb)2, -C(=O)SRaa, -C(=O)Raa, -CO2Raa, -C(=O)N(Rbb)2, -C(=NRbb)Raa, -C(=NRbb)ORaa, -C(=NRbb)N(Rbb)2, -S(=O)Raa, -SO2Raa, -Si(Raa)3, -P(Rcc)2, -P(Rcc)3 +X-, -P(ORcc)2, -P(ORcc)3 +X-, -P(=O)(Raa)2, -P(=O)(ORcc)2, 및 -P(=O)(N(Rbb) 2)2를 포함하나 이에 제한되지는 않으며, 여기서 X-, Raa, Rbb, 및 Rcc는 본원에 정의된 바와 같다. 산소 보호기는 관련 기술분야에 널리 공지되어 있고, 본원에 참조로 포함되는 문헌 [Protecting Groups in Organic Synthesis, T. W. Greene and P. G. M. Wuts, 3rd edition, John Wiley & Sons, 1999]에 상세하게 기재된 것을 포함한다.
산소 보호기의 예는 메틸, 메톡실메틸 (MOM), 메틸티오메틸 (MTM), t-부틸티오메틸, (페닐디메틸실릴)메톡시메틸 (SMOM), 벤질옥시메틸 (BOM), p-메톡시벤질옥시메틸 (PMBM), (4-메톡시페녹시)메틸 (p-AOM), 구아이아콜메틸 (GUM), t-부톡시메틸, 4-펜테닐옥시메틸 (POM), 실록시메틸, 2-메톡시에톡시메틸 (MEM), 2,2,2-트리클로로에톡시메틸, 비스(2-클로로에톡시)메틸, 2-(트리메틸실릴)에톡시메틸 (SEMOR), 테트라히드로피라닐 (THP), 3-브로모테트라히드로피라닐, 테트라히드로티오피라닐, 1-메톡시시클로헥실, 4-메톡시테트라히드로피라닐 (MTHP), 4-메톡시테트라히드로티오피라닐, 4-메톡시테트라히드로티오피라닐 S,S-디옥시드, 1-[(2-클로로-4-메틸)페닐]-4-메톡시피페리딘-4-일 (CTMP), 1,4-디옥산-2-일, 테트라히드로푸라닐, 테트라히드로티오푸라닐, 2,3,3a,4,5,6,7,7a-옥타히드로-7,8,8-트리메틸-4,7-메타노벤조푸란-2-일, 1-에톡시에틸, 1-(2-클로로에톡시)에틸, 1-메틸-1-메톡시에틸, 1-메틸-1-벤질옥시에틸, 1-메틸-1-벤질옥시-2-플루오로에틸, 2,2,2-트리클로로에틸, 2-트리메틸실릴에틸, 2-(페닐셀레닐)에틸, t-부틸, 알릴, p-클로로페닐, p-메톡시페닐, 2,4-디니트로페닐, 벤질 (Bn), p-메톡시벤질, 3,4-디메톡시벤질, o-니트로벤질, p-니트로벤질, p-할로벤질, 2,6-디클로로벤질, p-시아노벤질, p-페닐벤질, 2-피콜릴, 4-피콜릴, 3-메틸-2-피콜릴 N-옥시도, 디페닐메틸, p,p'-디니트로벤즈히드릴, 5-디벤조수베릴, 트리페닐메틸, α-나프틸디페닐메틸, p-메톡시페닐디페닐메틸, 디(p-메톡시페닐)페닐메틸, 트리(p-메톡시페닐)메틸, 4-(4'-브로모페나실옥시페닐)디페닐메틸, 4,4',4"-트리스(4,5-디클로로프탈이미도페닐)메틸, 4,4',4"-트리스(레불리노일옥시페닐)메틸, 4,4',4"-트리스(벤조일옥시페닐)메틸, 3-(이미다졸-1-일)비스(4',4"-디메톡시페닐)메틸, 1,1-비스(4-메톡시페닐)-1'-피레닐메틸, 9-안트릴, 9-(9-페닐)크산테닐, 9-(9-페닐-10-옥소)안트릴, 1,3-벤조디티올란-2-일, 벤즈이소티아졸릴 S,S-디옥시도, 트리메틸실릴 (TMS), 트리에틸실릴 (TES), 트리이소프로필실릴 (TIPS), 디메틸이소프로필실릴 (IPDMS), 디에틸이소프로필실릴 (DEIPS), 디메틸테실실릴, t-부틸디메틸실릴 (TBDMS), t-부틸디페닐실릴 (TBDPS), 트리벤질실릴, 트리-p-크실릴실릴, 트리페닐실릴, 디페닐메틸실릴 (DPMS), t-부틸메톡시페닐실릴 (TBMPS), 포르메이트, 벤조포르메이트, 아세테이트, 클로로아세테이트, 디클로로아세테이트, 트리클로로아세테이트, 트리플루오로아세테이트, 메톡시아세테이트, 트리페닐메톡시아세테이트, 페녹시아세테이트, p-클로로페녹시아세테이트, 3-페닐프로피오네이트, 4-옥소펜타노에이트 (레불리네이트), 4,4-(에틸렌디티오)펜타노에이트 (레불리노일디티오아세탈), 피발로에이트, 아다만토에이트, 크로토네이트, 4-메톡시크로토네이트, 벤조에이트, p-페닐벤조에이트, 2,4,6-트리메틸벤조에이트 (메시토에이트), 메틸 카르보네이트, 9-플루오레닐메틸 카르보네이트 (Fmoc), 에틸 카르보네이트, 2,2,2-트리클로로에틸 카르보네이트 (Troc), 2-(트리메틸실릴)에틸 카르보네이트 (TMSEC), 2-(페닐술포닐) 에틸 카르보네이트 (Psec), 2-(트리페닐포스포니오) 에틸 카르보네이트 (Peoc), 이소부틸 카르보네이트, 비닐 카르보네이트, 알릴 카르보네이트, t-부틸 카르보네이트 (BOC 또는 Boc), p-니트로페닐 카르보네이트, 벤질 카르보네이트, p-메톡시벤질 카르보네이트, 3,4-디메톡시벤질 카르보네이트, o-니트로벤질 카르보네이트, p-니트로벤질 카르보네이트, S-벤질 티오카르보네이트, 4-에톡시-1-나프틸 카르보네이트, 메틸 디티오카르보네이트, 2-아이오도벤조에이트, 4-아지도부티레이트, 4-니트로-4-메틸펜타노에이트, o-(디브로모메틸)벤조에이트, 2-포르밀벤젠술포네이트, 2-(메틸티오메톡시)에틸, 4-(메틸티오메톡시)부티레이트, 2-(메틸티오메톡시메틸)벤조에이트, 2,6-디클로로-4-메틸페녹시아세테이트, 2,6-디클로로-4-(1,1,3,3-테트라메틸부틸)페녹시아세테이트, 2,4-비스(1,1-디메틸프로필)페녹시아세테이트, 클로로디페닐아세테이트, 이소부티레이트, 모노숙시노에이트, (E)-2-메틸-2-부테노에이트, o-(메톡시카르보닐)벤조에이트, α-나프토에이트, 니트레이트, 알킬 N,N,N',N'-테트라메틸포스포로디아미데이트, 알킬 N-페닐카르바메이트, 보레이트, 디메틸포스피노티오일, 알킬 2,4-디니트로페닐술페네이트, 술페이트, 메탄술포네이트 (메실레이트), 벤질술포네이트, 및 토실레이트 (Ts)를 포함하나 이에 제한되지는 않는다.
특정 실시양태에서, 황 원자 상에 존재하는 치환기는 황 보호기 ("티올 보호기"라고도 지칭함)이다. 황 보호기는, -Raa, -N(Rbb)2, -C(=O)SRaa, -C(=O)Raa, -CO2Raa, -C(=O)N(Rbb)2, -C(=NRbb)Raa, -C(=NRbb)ORaa, -C(=NRbb)N(Rbb)2, -S(=O)Raa, -SO2Raa, -Si(Raa)3, -P(Rcc)2, -P(Rcc)3 +X-, -P(ORcc)2, -P(ORcc)3 +X-, -P(=O)(Raa)2, -P(=O)(ORcc)2, 및 -P(=O)(N(Rbb) 2)2를 포함하나 이에 제한되지는 않으며, 여기서 Raa, Rbb, 및 Rcc는 본원에 정의된 바와 같다. 황 보호기는 관련 기술분야에 널리 공지되어 있고, 본원에 참조로 포함되는 문헌 [Protecting Groups in Organic Synthesis, T. W. Greene and P. G. M. Wuts, 3rd edition, John Wiley & Sons, 1999]에 상세하게 기재된 것을 포함한다.
"반대이온" 또는 "음이온성 반대이온"은 전자 중성을 유지하기 위해 양으로 하전된 기와 회합된 음으로 하전된 기이다. 음이온성 반대이온은 1가 (즉, 1개의 형식적 음전하를 포함함)일 수 있다. 음이온성 반대이온은 또한 다가 (즉, 1개 초과의 형식적 음전하를 포함함), 예컨대 2가 또는 3가일 수 있다. 예시적인 반대이온은 할라이드 이온 (예를 들어, F-, Cl-, Br-, I-), NO3 -, ClO4 -, OH-, H2PO4 -, HCO3 - , HSO4 -, 술포네이트 이온 (예를 들어, 메탄술포네이트, 트리플루오로메탄술포네이트, p-톨루엔술포네이트, 벤젠술포네이트, 10-캄포르 술포네이트, 나프탈렌-2-술포네이트, 나프탈렌-1-술폰산-5-술포네이트, 에탄-1-술폰산-2-술포네이트 등), 카르복실레이트 이온 (예를 들어, 아세테이트, 프로파노에이트, 벤조에이트, 글리세레이트, 락테이트, 타르트레이트, 글리콜레이트, 글루코네이트 등), BF4 -, PF4 -, PF6 -, AsF6 -, SbF6 -, B[3,5-(CF3)2C6H3]4]-, B(C6F5)4 -, BPh4 -, Al(OC(CF3)3)4 -, 및 카르보란 음이온 (예를 들어, CB11H12 - 또는 (HCB11Me5Br6)-)을 포함한다. 다가일 수 있는 예시적인 반대이온은 CO3 2-, HPO4 2-, PO4 3- , B4O7 2-, SO4 2-, S2O3 2-, 카르복실레이트 음이온 (예를 들어, 타르트레이트, 시트레이트, 푸마레이트, 말레에이트, 말레이트, 말로네이트, 글루코네이트, 숙시네이트, 글루타레이트, 아디페이트, 피멜레이트, 수베레이트, 아젤레이트, 세바케이트, 살리실레이트, 프탈레이트, 아스파르테이트, 글루타메이트 등), 및 카르보란을 포함한다.
용어 "탄수화물" 또는 "사카라이드"는 다가 알콜의 알데히드 또는 케톤 유도체를 지칭한다. 탄수화물은 상대적으로 소분자(예를 들어, 당) 뿐만 아니라 거대분자 또는 중합체 물질 (예를 들어, 전분, 글리코겐, 및 셀룰로스 폴리사카라이드)을 갖는 화합물을 포함한다. 용어 "당"은 모노사카라이드, 디사카라이드, 또는 폴리사카라이드를 지칭한다. 모노사카라이드는 그들이 더 작은 탄수화물로 가수분해될 수 없다는 점에서 가장 단순한 탄수화물이다. 대부분의 모노사카라이드는 화학식 CyH2yOy (예를 들어, C6H12O6 (헥소스 예컨대 글루코스))로 나타내어질 수 있고, 여기서 y는 3 이상의 정수이다. 상기 기재된 화학식으로 나타내어지지 않는 특정 다가 알콜은 또한 모노사카라이드라고 생각될 수 있다. 예를 들어, 데옥시리보스는 화학식 C5H10O4이고, 모노사카라이드이다. 모노사카라이드는 통상적으로 5 또는 6개의 탄소 원자로 구성되고, 각각 펜토스 및 헥소스를 지칭한다. 모노사카라이드가 알데히드를 함유하면 이는 알도스를 지칭하고; 이것이 케톤을 함유하면, 이는 케토스를 지칭한다. 모노사카라이드는 또한 알도스 또는 케토스 형태로 3, 4, 또는 7개의 탄소 원자로 이루어질 수 있고, 각각 트리오스, 테트로스, 및 헵토스를 지칭한다. 글리세르알데히드 및 디히드록시아세톤은 각각 알도트리오스 및 케토트리오스 당으로 여겨진다. 알도테트로스 당의 예는 에리트로스 및 트레오스를 포함하고; 케토테트로스 당은 에리트룰로스를 포함한다. 알도펜토스 당은 리보스, 아라비노스, 크실로스, 및 릭소스를 포함하고; 케토펜토스 당은 리불로스, 아라불로스, 크실룰로스, 및 릭술로스를 포함한다. 알도헥소스 당의 예는 글루코스 (예를 들어, 덱스트로스), 만노스, 갈락토스, 알로스, 알트로스, 탈로스, 굴로스, 및 이도스를 포함하고; 케토헥소스 당은 프룩토스, 프시코스, 소르보스, 및 타가토스를 포함한다. 케토헵토스 당은 세도헵툴로스를 포함한다. 최초 및 최종 탄소는 예외로 하고, 모노사카라이드의 각각의 탄소 원자가 히드록실 기 (-OH)를 보유하는 것은, 비대칭이며, 탄소 원자를 2개의 가능한 배위 (R 또는 S)를 갖는 입체중심을 생성시킨다. 비대칭 때문에, 수많은 이성질체는 임의의 주어진 모노사카라이드 화학식에 대해 존재할 수 있다. 알도헥소스 d-글루코스는, 예를 들어, 화학식 C6H12O6을 갖고, 그의 6개의 탄소 원자 중 2개를 제외하고 모두가 입체생성이며, d-글루코스를 16개 (즉, 24)의 가능한 입체이성질체 중 1종을 생성시킨다. D 또는 L의 할당은 카르보닐 기에서 가장 멀리 떨어진 비대칭 탄소의 배향에 따라 구성된다: 표준 피셔 투영도에서 히드록실 기가 오른편에 있으면 분자는 D 당이고, 다르게는 이는 L 당이다. 직쇄 모노사카라이드의 알데히드 또는 케톤 기는 상이한 탄소 원자에서 가역적으로 히드록실 기와 반응하여 헤미아세탈 또는 헤미케탈을 형성하며, 2개의 탄소 원자간의 산소 가교에 의해 헤테로시클릭 고리를 형성할 것이다. 5 및 6개의 원자를 갖는 고리는 각각 푸라노스 및 피라노스 형태로 칭하고, 직쇄 형태를 갖는 평형으로 존재한다. 직쇄 형태에서 시클릭 형태로의 전환 동안, 아노머 탄소로 칭하는 카르보닐 산소를 포함하는 탄소 원자는 2개의 가능한 배위를 갖는 입체생성 중심이 된다: 산소 원자는 고리의 평면 위 또는 아래의 위치를 취할 수 있다. 생성된 가능한 입체이성질체의 쌍은 아노머로 칭한다. α 아노머에서, 아노머 탄소의 -OH 치환기는 -CH2OH 측분지로부터 고리의 반대측 (트랜스)에 놓일 수 있다. -CH2OH 치환기 및 아노머 히드록실이 고리의 평면의 동일한 측 (시스)에 있는 대안적 형태는, β 아노머로 칭한다. 2개 이상의 결합된 모노사카라이드 단위를 포함하는 탄수화물은 각각 디사카라이드 또는 폴리사카라이드 (예를 들어, 트리사카라이드)로 칭한다. 2개 이상의 모노사카라이드 단위는, 1개의 모노사카라이드로부터 수소 원자의 상실 및 또 다른 것으로부터 히드록실 기의 상실에 기인하는, 탈수 반응을 통해 형성된 글리코시드 연결로 공지된 공유 결합에 의해 함께 결합하였다. 예시적인 디사카라이드는 수크로스, 락툴로스, 락토스, 말토스, 이소말토스, 트레할로스, 셀로비오스, 크실로비오스, 라미나리비오스, 겐티오비오스, 만노비오스, 멜리비오스, 니게로스, 및 루티노스를 포함하나 이에 제한되지는 않는다. 예시적인 트리사카라이드는 이소말토트리오스, 니게로트리오스, 말토트리오스, 멜레지토스, 말토트리울로스, 라피노스, 및 케스토스를 포함하나 이에 제한되지는 않는다. 용어 탄수화물은 또한 본원에 기재된 탄수화물의 다른 천연 또는 합성 입체이성질체를 포함한다.
용어 "제약상 허용되는 염"은 타당한 의학적 판단의 범주 내에서 과도한 독성, 자극, 알레르기 반응 등이 없이 인간 및 다른 동물의 조직과 접촉시켜 사용하기에 적합하고 합리적인 이익/위험 비에 부합하는 그러한 염을 지칭한다. 제약상 허용되는 염은 관련 기술분야에 널리 공지되어 있다. 예를 들어, 베르게(Berge) 등은 본원에 참조로 포함된 문헌 [J. Pharmaceutical Sciences, 1977, 66, 1-19]에서 제약상 허용되는 염을 상세하게 기재한다. 본 발명의 화합물의 제약상 허용되는 염은 적합한 무기 및 유기 산 및 염기로부터 유래된 것을 포함한다. 염은 화합물의 최종 단리 및 정제 동안 제조할 수 있거나, 또는 유리 염기 형태의 적절한 화합물을 적합한 산과 반응시킴으로써 별도로 제조할 수 있다. 대표적인 산 부가염은 아세테이트, 아디페이트, 알기네이트, L-아스코르베이트, 아스파르테이트, 벤조에이트, 벤젠술포네이트 (베실레이트), 비술페이트, 부티레이트, 캄포레이트, 캄포술포네이트, 시트레이트, 디글루코네이트, 포르메이트, 푸마레이트, 겐티세이트, 글루타레이트, 글리세로포스페이트, 글리콜레이트, 헤미술페이트, 헵타노에이트, 헥사노에이트, 히푸레이트, 히드로클로라이드, 히드로브로마이드, 히드로아이오다이드, 2-히드록시에탄술포네이트 (이세티오네이트), 락테이트, 말레에이트, 말로네이트, DL-만델레이트, 메시틸렌술포네이트, 메탄술포네이트, 나프틸렌술포네이트, 니코티네이트, 2-나프탈렌술포네이트, 옥살레이트, 파모에이트, 펙티네이트, 퍼술페이트, 3-페닐프로피오네이트, 포스포네이트, 피크레이트, 피발레이트, 프로피오네이트, 피로글루타메이트, 숙시네이트, 술포네이트, 타르트레이트, L-타르트레이트, 트리클로로아세테이트, 트리플루오로아세테이트, 포스페이트, 글루타메이트, 비카르보네이트, 파라-톨루엔술포네이트 (p-토실레이트), 및 운데카노에이트를 포함한다. 또한, 본 발명의 화합물 내의 염기성 기는 메틸, 에틸, 프로필, 및 부틸 클로라이드, 브로마이드 및 아이오다이드; 디메틸, 디에틸, 디부틸 및 디아밀 술페이트; 데실, 라우릴, 미리스틸, 및 스테릴 클로라이드, 브로마이드, 및 아이오다이드; 및 벤질 및 페네틸 브로마이드를 사용하여 4급화될 수 있다. 제약상 허용되는 염을 형성하는데 사용될 수 있는 산의 예는 무기산 예컨대 염산, 브로민화수소산, 황산, 및 인산; 및 유기산, 예컨대 옥살산, 말레산, 숙신산, 및 시트르산을 포함한다. "염기성 부가염"은 적절한 염기, 알칼리 금속, 알칼리 토금속, 및 4급 아민 염을 포함하는 이들 염에서 유도된 염을 지칭한다. 따라서, 본 발명은 본원에 개시된 화합물의 나트륨, 칼륨, 마그네슘, 및 칼슘 염 등을 고려한다. 염기성 부가염은 화합물의 최종 단리 및 정제 동안 종종 카르복시 기를 적합한 염기 예컨대 금속 양이온의 수산화물, 탄산염, 또는 중탄산염과 또는 암모니아 또는 유기 1급, 2급, 또는 3급 아민과 반응시킴으로써 제조될 수 있다. 치료상 허용되는 염의 양이온은 리튬, 나트륨 (예를 들어, NaOH를 사용하는 것에 의함), 칼륨 (예를 들어, KOH를 사용하는 것에 의함), 칼슘 (예를 들어, Ca(OH)2를 사용하는 것에 의함), 마그네슘 (예를 들어, Mg(OH)2 및 마그네슘 아세테이트를 사용하는 것에 의함), 아연 (예를 들어, Zn(OH)2 및 아세트산아연을 사용하는 것에 의함), 및 알루미늄, 뿐만 아니라 비독성 4급 아민 양이온 예컨대 암모늄, 테트라메틸암모늄, 테트라에틸암모늄, 메틸아민, 디메틸아민, 트리메틸아민, 트리에틸아민, 디에틸아민, 에틸아민, 트리부틸아민, 피리딘, N,N-디메틸아닐린, N-메틸피페리딘, N-메틸모르폴린, 디시클로헥실아민, 프로카인, 디벤질아민, N,N-디벤질페네틸아민, 1-에페나민, 및 N,N-디벤질에틸렌디아민을 포함한다. 염기 부가염의 형성에 유용한 다른 대표적인 유기 아민은 에틸렌디아민, 에탄올아민, 디에탄올아민, 피페리딘, 피페라진, 콜린 히드록시드, 히드록시에틸 모르폴린, 히드록시에틸 피롤리돈, 이미다졸, n-메틸-d-글루카민, N,N'-디벤질에틸렌디아민, N,N'-디에틸에탄올아민, N,N'-디메틸에탄올아민, 트리에탄올아민, 및 트로메타민을 포함한다. 염기성 아미노산 (예를 들어, 1-글리신 및 1-아르기닌) 및 중성 pH에서 쯔비터이온성일 수 있는 아미노산 (예를 들어, 베타인 (N,N,N-트리메틸글리신))이 또한 고려된다.
용어 "호변이성질체" 또는 "호변이성질체적"은 수소 원자의 적어도 1회의 형식적 이동 및 원자가에서의 적어도 1회의 변화 (예를 들어, 단일 결합에서 이중 결합, 삼중 결합에서 단일 결합, 또는 그 반대의 경우)로부터 생성된 2종 이상의 상호전환성 화합물을 지칭한다. 호변이성질체의 정확한 비는 온도, 용매 및 pH를 비롯한 몇몇 인자에 따라 달라진다. 호변이성질체화 (즉, 호변이성질체 쌍을 제공하는 반응)는 산 또는 염기에 의해 촉매화된다. 예시적인 호변이성질체화는 케토에서 엔올로, 아미드에서 이미드로, 락탐에서 락팀으로, 엔아민에서 이민으로, 및 엔아민에서 (상이한 엔아민)으로의 호변이성질체화를 포함한다.
용어 "다형체"는 화합물 (또는 그의 염, 수화물 또는 용매화물)의 결정질 형태를 지칭한다. 모든 다형체는 동일한 원소 조성을 갖는다. 상이한 결정질 형태는 통상적으로 상이한 x선 회절 패턴, 적외선 스펙트럼, 융점, 밀도, 경도, 결정 형상, 광학적 및 전기적 특성, 안정성, 및 용해도를 갖는다. 재결정화 용매, 결정화 속도, 저장 온도, 및 다른 인자는 1종의 결정 형태를 우세하게 할 수 있다. 화합물의 다양한 다형체는 상이한 조건 하의 결정화에 의해 제조될 수 있다.
용어 "용매화물"은 통상적으로 가용매분해 반응에 의해 용매와 회합된 화합물 또는 그의 염의 형태를 지칭한다. 이러한 물리적 회합은 수소 결합을 포함할 수 있다. 통상적인 용매는 물, 메탄올, 에탄올, 아세트산, DMSO, THF, 디에틸 에테르 등을 포함한다. 본 발명의 화합물은 예를 들어 결정질 형태로 제조될 수 있으며, 용매화될 수 있다. 적합한 용매화물은 제약상 허용되는 용매화물을 포함하고, 추가로 화학량론적 용매화물 및 비-화학량론적 용매화물 둘 다를 포함한다. 특정 경우에, 예를 들어 1종 이상의 용매 분자가 결정질 고체의 결정 격자에 혼입되는 경우에, 용매화물은 단리될 수 있을 것이다. "용매화물"은 용액-상 및 단리가능한 용매화물 둘 다를 포괄한다. 대표적인 용매화물은 수화물, 에탄올레이트, 및 메탄올레이트를 포함한다.
용어 "수화물"은 물과 회합된 화합물을 지칭한다. 전형적으로, 화합물의 수화물에 함유된 물 분자의 수는 수화물 내 화합물 분자의 수에 대한 명확한 비로 존재한다. 따라서, 화합물의 수화물은, 예를 들어 화학식 R·xH2O (여기서 R은 화합물이고, x는 0초과의 수임)에 의해 나타내어질 수 있다. 주어진 화합물은, 예를 들어 1수화물 (x는 1임), 저급 수화물 (x는 0초과 1 미만의 수임, 예를 들어 반수화물 (R·0.5H2O)), 및 다중수화물 (x는 1초과의 수임, 예를 들어 2수화물 (R·2H2O) 및 6수화물 (R·6H2O))을 포함한 1종 초과의 유형의 수화물을 형성할 수 있다.
용어 "대상체"는 임의의 동물을 지칭한다. 특정 실시양태에서, 대상체는 포유동물이다. 특정 실시양태에서, 대상체는 인간 (예를 들어, 인간, 여자, 또는 어린이)이다. 인간은 어느 하나의 성별을 가질 수 있고, 임의의 발달 단계에 있을 수 있다. 특정 실시양태에서, 대상체는 치료할 상태 또는 질환으로 진단된 바 있다. 다른 실시양태에서, 대상체는 상태 또는 질환이 발병할 위험이 있다. 특정 실시양태에서, 대상체는 실험 동물 (예를 들어, 마우스, 래트, 개, 돼지, 또는 영장류)이다. 실험 동물은 유전자 조작될 수 있다. 특정 실시양태에서, 대상체는 가축 (예를 들어, 개, 고양이, 새, 말, 소, 염소, 양)이다.
용어 "투여하다", "투여하는" 또는 "투여"는 본 발명의 화합물, 또는 그의 제약 조성물을 이식, 흡수, 섭취, 주입, 흡입 또는 달리 도입하는 것을 지칭한다.
용어 "치료", "치료하다" 및 "치료하는"은 본원에 기재된 "병리학적 상태" (예를 들어, 질환, 장애 또는 상태, 또는 그의 하나 이상의 징후 또는 증상)를 역전시키거나, 완화시키거나, 그의 발병을 지연시키거나, 또는 그의 진행을 억제하는 것을 지칭한다. 일부 실시양태에서, 치료는 하나 이상의 징후 또는 증상이 발병하였거나 또는 관찰된 후에 투여될 수 있다. 다른 실시양태에서, 치료는 질환 또는 상태의 징후 또는 증상의 부재 하에 투여될 수 있다. 예를 들어, 치료는 (예를 들어, 증상의 병력에 비추어 및/또는 유전적 또는 다른 감수성 요인에 비추어) 증상의 발병 이전에 감수성 개체에게 투여될 수 있다. 또한, 예를 들어 증상이 해소된 후에 치료를 계속하여 재발을 지연 또는 예방할 수도 있다.
용어 "상태", "병리학적 상태", "질환" 및 "장애"는 상호교환가능하게 사용된다.
본 발명의 화합물 또는 그의 제약 조성물의 "유효량"은 원하는 생물학적 반응, 예를 들어 상태를 치료를 도출하기에 충분한 양을 지칭한다. 통상의 기술자들에 의해 인지될 것과 같이, 본 발명의 화합물의 유효량은 목적하는 생물학적 목적, 화합물의 약동학, 치료되는 상태, 투여 모드, 및 대상체의 연령 및 건강과 같은 인자에 따라 달라질 수 있다. 특정 실시양태에서, 유효량은 치료 유효량이다. 특정 실시양태에서, 유효량은 예방적 치료이다. 특정 실시양태에서, 유효량은 단일 용량의 본원에 기재된 화합물의 양이다. 특정 실시양태에서, 유효량은 다중 용량의 본원에 기재된 화합물의 합한 양이다.
본 발명의 화합물 또는 그의 제약 조성물의 "치료 유효량"은 상태, 예를 들어 철 과부하의 치료에서 치료적 이익을 제공하거나, 상태와 연관된 1종 이상의 증상을 지연 또는 최소화하기에 충분한 양이다. 화합물의 치료 유효량은 상태의 치료에서 치료 이익을 제공하는, 단독의 또는 다른 요법과 조합된 치료제의 양을 의미한다. 용어 "치료 유효량"은 전반적인 요법을 개선시키거나, 상태의 증상 또는 원인을 감소 또는 회피시키고/거나, 또 다른 치료제의 치료 효능을 증진시키는 양을 포괄할 수 있다. 특정 실시양태에서, 치료 유효량은 본원에 기재된 금속을 킬레이트화하기 위해 충분한 양이다. 특정 실시양태에서, 치료 유효량은 본원에 기재된 병리학적 상태를 처리하기 위해 충분한 양이다. 특정 실시양태에서, 치료 유효량은 본원에 기재된 금속을 킬레이트화하고 본원에 기재된 병리학적 상태를 치료하기에 충분한 양이다.
본 발명의 화합물의 "예방 유효량"은 상태, 예를 들어, 철 과부하 또는 상태와 연관된 1종 이상의 증상을 예방하거나 그의 재발을 방지하기에 충분한 양이다. 화합물의 예방 유효량은 상태의 예방에서 예방 이익을 제공하는, 단독의 또는 다른 작용제와 조합된 치료제의 양을 의미한다. 용어 "예방 유효량"은 전반적인 예방을 개선시키거나 또 다른 예방제의 예방 효능을 증진시키는 양을 포괄할 수 있다. 특정 실시양태에서, 예방 유효량은 본원에 기재된 금속을 킬레이트화하기에 충분한 양이다. 특정 실시양태에서, 예방 유효량은 본원에 기재된 병리학적 상태를 예방하기에 충분한 양이다. 특정 실시양태에서, 예방 유효량은 본원에 기재된 금속을 킬레이트화하고 본원에 기재된 병리학적 상태를 예방하기에 충분한 양이다.
용어 "생물학적 샘플"은 조직 샘플 (예컨대 조직 절편 및 조직의 바늘 생검); 세포 샘플 (예를 들어, 세포학적 도말 (예컨대 Pap 또는 혈액 도말) 또는 미세절제에 의해 수득된 세포의 샘플); 전체 유기체의 샘플 (예컨대 효모 또는 박테리아의 샘플); 또는 세포 분획물, 단편 또는 소기관 (예컨대 세포를 용해시키고 그의 성분을 원심분리 또는 다른 것에 의해 분리시켜 수득된 것)을 포함한 임의의 샘플을 지칭한다. 생물학적 샘플의 다른 예는 혈액, 혈청, 소변, 정액, 분변물, 뇌척수액, 간질액, 점액, 눈물, 땀, 고름, 생검 조직 (예를 들어, 수술적 생검 또는 바늘 생검에 의해 수득된 것), 유두 흡인물, 유액, 질액, 타액, 스왑 (예컨대, 협측 스왑), 또는 제1 생물학적 샘플로부터 유래된 생체분자를 함유하는 임의의 물질을 포함한다.
"킬레이트화", "킬레이트화하는", "격리", 또는 "격리하는"은 여러자리 (다중-결합) 화합물 및 단일 중심 원자 간의 2개 이상의 분리된 배위 결합의 형성 또는 존재이다. 여러자리 화합물은 전형적으로 유기 화합물이고 "킬레이트화제 (chelator)", "킬레이트화제 (chelant)", "킬레이트화제 (chelating agent)", "격리제 (sequestrator)", "격리제 (sequestering agent)", 또는 "리간드"로 지칭한다. 중심 원자는 통상적으로 금속 원자 또는 금속 이온 (예를 들어, 본원에 기재된 금속 원자 또는 금속 이온, 예컨대 철 (예를 들어, Fe(III)), Al(III), 크로뮴 (예를 들어, Cr(III) 또는 Cr(VI)), 및 우라늄 (예를 들어, U(VI)) 등)이다. 킬레이트화제는 배위 결합을 통해 중심 원자와 안정한 착물을 형성하고, 중심 원자를 비활성화시켜, 중심 원자가 다른 분자 또는 원자와 반응할 가능성이 적을 수 있다.
용어 "금속-클리어링 효율" 또는 "MCE"은 신체 또는 그의 기관 또는 부분 중 하나로부터 금속 원자 또는 금속 이온 (예를 들어, 본원에 기재된 금속 원자 또는 금속 이온, 예컨대 철 (예를 들어, Fe(III)), Al(III), 크로뮴 (예를 들어, Cr(III) 또는 Cr(VI)), 및 우라늄 (예를 들어, U(VI))을 클리어링함에 있어 주어진 농도의 킬레이트화제의 효능을 지칭한다. 따라서 효과성은 시간 단위에서 표적 시스템 (예를 들어, 전신, 기관, 또는 조직)으로부터 제거된 금속 원자 또는 금속 이온의 수량에 관련된다. 금속 원자 또는 금속 이온의 킬레이트화제는 3가지의 임상 상황의 1가지 이상에 요구된다: (1) 금속 원자 또는 금속 이온의 섭취 또는 주입으로부터의 급성 금속 독성을 위해; (2) 수혈 또는 과잉의 금속 흡수에 대한 부차적인 전체 체내 금속을 감소시키기 위해; 및 (3) 전체 체내 금속이 만족하게 감소되었고 단지 1일 식이성 금속이 배출될 필요가 있은 후 금속 균형의 유지를 위해. 따라서, 실용적 용어로, 수혈에 대한 부차적인 만성 금속 과부하의 경우, 0.3-0.5 mg/kg/일 (즉, 1일당 대상체의 kg 체중당 mg 철)은 배출될 필요가 있다. 유지 치료의 경우, 0.25-1 mg/kg/일이 충분하다. 다른 범위가 또한 가능하다. 특정 실시양태에서, 금속-클리어링 효율은 철-클리어링 효율 또는 "ICE"이다. 특정 실시양태에서, 금속-클리어링 효율은 알루미늄-클리어링 효율이다. 특정 실시양태에서, 금속-클리어링 효율은 크로뮴-클리어링 효율이다. 특정 실시양태에서, 금속-클리어링 효율은 우라늄-클리어링 효율이다.
용어 "국소 철 과부하"는 조직 또는 기관에서의 관리되지 않는 철의 축적을 포함하는 임의의 질환 또는 상태를 지칭한다. 국소 철 과부하는 전형적으로 대상체의 전신 미만을 포함하지만, 하나 초과의 기관 또는 조직을 포함할 수 있다. 임의의 조직 또는 기관에서의 관리되지 않는 철은 전형적으로 바람직하지 않고, 본 발명의 치료의 초점이 될 수 있다. 치료는 조직 또는 기관으로부터 가능한 한 많은 철을 제거하는 것을 포함할 수도 있고, 과량의 철을 제거하는 것만을 포함할 수도 있다. 국소 철 과부하와 연관된 질환 및 상태의 예는 황반 변성, IBD, 재관류 손상, 출혈성 졸중을 비롯한 졸중, 및 폐쇄성 두부 손상을 포함하지만 이에 제한되지는 않으며; 임의의 국소 철 과부하 질환 또는 상태가 본원에 기재된 바와 같이 치료할 수 있다. 특정 실시양태에서, 용어 "국소 철 과부하"는 전신 철 과부하와 연관된 질환 또는 상태 (예를 들어, 장기적 수혈 요법, 유전성 혈색소증 등과 연관된 전신 철 과부하)를 포함하지 않는다. 국소 철 과부하의 치료는 유효량의 본 발명의 화합물, 또는 그의 제약 조성물의 전신 또는 국부 투여일 수 있다.
용어 "반응성 산소 종" 또는 "ROS"는 산소의 불완전한 환원에 의해 형성된 분자 또는 이온을 지칭한다. 반응성 산소 종은 슈퍼옥시드 음이온 (O2 ·-), 퍼옥시드, 예컨대 과산화수소 (H2O2), 히드록실 라디칼 (HO·) 및 차아염소산 (HClO)을 포함한다. 이들 분자는 전형적으로 화학적으로 반응성이다. 반응성 산소 종은 임의의 수의 메카니즘에 의해 (예를 들어, 효소적으로, 이온화 방사선에 의해, 산소와 금속의 반응에 의해) 형성될 수 있다. 특정 실시양태에서, 반응성 산소 종은 철 이온, 예컨대 Fe+2에 의한 산소의 환원에 의해 형성된다.
"원발성 혈색소증"은 조직 손상을 생성하는 과잉의 철 축적을 특징으로 하는 유전 장애이다. 징후는 전신 증상, 간 장애, 심근병증, 당뇨병, 발기 기능장애, 및 관절병증을 포함한다. 보통 전체 체내 철 함량은 여성 약 2.5 g 및 남성 3.5 g이다. 증상은 철 축적이 과잉이 될 때까지 지연될 수 있기 때문에, 혈색소증은 전체 체내 철 함량이 >10 g이거나, 또는 종종 수회 초과일 때까지 인지되지 않을 수 있다. 여성에서, 월경 (및 때때로 임신 및 분만)으로 인해 철 손실이 철 축적을 상쇄하는 경향이 있기 때문에, 임상 징후는 폐경기 전에 드물다. 철 과부하에 대한 1가지 메카니즘은 조직에서 철의 만성 침착을 유발하는 위장관으로부터의 상승된 철 흡수이다. 헵시딘인 간-유래 펩티드는 철 흡수를 위한 중요한 제어 메커니즘이다. 헵시딘은, 정상적인 HFE 유전자와 함께, 정상인에서 과잉의 철 흡수 및 저장을 방지한다. 원발성 혈색소증을 갖는 대상체의 조직 손상은, 조직에서의 철 침착이 이들의 형성을 촉매화하는 경우, 생성된 반응성 자유 히드록실 라디칼로부터 유래할 수 있다. 다른 메카니즘은 특정한 기관에 영향을 미칠 수 있다 (예를 들어, 피부 과다색소침착은 상승된 멜라닌 뿐만 아니라 철 축적으로부터 유래할 수 있음).
"속발성 혈색소증"은 철 과부하, 또는 수혈, 또는 둘 다를 유발하는 또 다른 질환의 결과로서 획득된 상태이며, 전형적으로 증가된 간 및 전체 체내 철 함량 및 명백한 간문맥의 간경변증을 특징으로 한다. 속발성 혈색소증은 통상적으로 적혈구생성 (예를 들어, 지중해빈혈, 겸상 적혈구성 빈혈, X-연관 철적혈모구성 빈혈, 피루베이트 키나제 결핍, 유전성 구상적혈구증, 및 선천성 적혈구생성이상 빈혈 (CDA))의 장애 및 수혈에 의한 이들 질환의 치료에 기인한다. 수혈된 적혈구가 대식세포에 의해 손상된 후, 헴에서 유리된 철은 체내에 (예를 들어, 간, 심장, 또는 피부에) 축적된다.
"당뇨병" 또는 "당뇨병"은 혈액에서 글루코스의 수준이 높은 대사 장애이다. 당뇨병은 인슐린 (혈액 글루코스를 제어하기 위한 췌장에 의해 생산된 호르몬)의 불충분한 양 또는 대상체에서 인슐린에 대한 저항성, 또는 둘 다에 기인할 수 있다. 당뇨병은 3가지의 주요 유형이 있다: 유형 1, 유형 2, 및 임신성 당뇨병. 제1형 당뇨병은 통상적으로 소아 및 청소년에서 진단되고, 이전에 소아 당뇨병으로서 공지되었다. 제1형 당뇨병에서, 신체는 인슐린을 생산하지 않고, 이에 의해 췌장의 도세포의 파괴의 결과일 수 있다. 제2형 당뇨병, 또는 비-인슐린-의존성 당뇨병 (NIDDM) 또는 성인-발병 당뇨병은, 당뇨병의 가장 흔한 형태이다. 제2형 당뇨병은 인슐린 저항성 및 상대적인 인슐린 결핍의 맥락에서 높은 혈액 글루코스를 특징으로 한다. 이는 절대적 인슐린 결핍이 있는 제1형 당뇨병과 상반된다. 비만은 비만에 유전적으로 걸리기 쉬운 대상체에서 제2형 당뇨병의 주요한 원인 중 하나로 여겨진다. 임신성 당뇨병은 임신 전에 당뇨병을 앓지 않는 여성에서 임신 동안 발달한 높은 혈액 글루코스를 특징으로 한다. 임신성 당뇨병은 인슐린에 대한 신체의 반응을 방해할 수 있는 다양한 임신 호르몬에 기인할 수 있다.
용어 "폐쇄성 두부 손상"은 두개골에 침투하지 않은 두부에 대한 임의의 손상를 지칭한다. 폐쇄성 두부 손상은 추락, 폭발, 교통 사고를 비롯한 사고, 폭행으로부터 발생할 수 있다. 폐쇄성 두부 손상은 출혈 또는 뇌 종창을 유발할 수 있으며, 이는 두개 내압 항진을 초래하고, 이는 다시 영구적 뇌 손상 또는 심지어 사망을 유발할 수 있다. 다양한 유형의 폐쇄성 두부 손상은 뇌진탕, 뇌 좌상, 미만성 축삭 손상 및 혈종을 포함한다.
"지중해빈혈"은 지중해 지역에서 시작된 유전된 상염색체 열성 혈액 장애의 군이다. 지중해빈혈을 갖는 대상체에서, 돌연변이 또는 결실일 수 있는 유전적 결함은 헤모글로빈을 구성하는 글로빈 쇄 중 1종이 감소된 비율로 합성되거나 또는 전혀 합성되지 않게 한다. 이는 비정상 헤모글로빈 분자의 형성을 유발하고, 따라서 빈혈의 원인이 된다. 지중해빈혈의 2가지 주요 유형이 있다: 알파 및 베타 지중해빈혈. 알파 지중해빈혈은 유전자 또는 알파 글로빈 단백질과 관련된 유전자가 상실 또는 변경 (즉, 돌연변이)된 경우 발생한다. 베타 지중해빈혈은 유사한 유전자 결함이 베타 글로빈 단백질의 생산에 영향을 미치는 경우 발생한다. 각각의 알파 및 베타 지중해빈혈은 2가지 형태를 포함한다: 중증성 지중해빈혈 및 경증성 지중해빈혈. 베타 중증성 지중해빈혈은 또한 쿨리 (Cooley) 빈혈 또는 지중해 빈혈을 지칭한다.
"프리드라이히 운동실조" 또는 "FRDA"은 근육 약화, 언어 문제, 및 심장 질환을 포함하는 증상을 일으키는 대상체의 신경계에 대한 점진적 손상을 유발하는 유전성 질환이다. 프리드라이히 운동실조를 갖는 대상체에서, 척수 및 말초 신경은 악화하고 더 얇아진다. 균형 및 운동을 조정하는 뇌의 일부인 소뇌는 또한 더 적은 정도로 악화한다. 이 손상은 어색하고 불안정한 운동 및 손상된 감각 기능을 일으킨다. 프리드라이히 운동실조는 또한 심장 및 척추에서의 문제를 유발하고, 상태를 갖는 일부 대상체는 당뇨병을 발병시킨다. 그러나, 이 장애는 통상적으로 인지 기능, 예컨대 사고 및 추론에 영향을 미치지는 않는다. 프리드라이히 운동실조는 FXN으로 표지된 유전자에서 돌여변이의 결과일 수 있는 결함에 기인한다. 이 장애는 열성이며, 이는 각 부모로부터 1개씩 받은 유전자의 2개의 결함 복제를 물려받은 사람에게서만 발생하는 것을 의미한다.
"황반 변성"은 대상체의 망막에 영향을 미치는 질환이다. 망막은 눈의 뒤쪽을 라이닝하는 얇은 조직이다. 망막의 감광 세포는 광을 전기 자극으로 전환시키는 역할을 하고, 이는 이어서 해석을 위해 시신경을 통해 뇌로 보내진다. 망막의 중심에 황반이 있다. 황반은 가장 높은 농도의 원추라고 불리는 감광 세포를 함유하고, 이는 날카롭고, 상세하고, 중심의 시각을 담당한다. 황반 변성에서, 황반 영역에서의 세포는 사멸하기 시작하고, 이는 맹점 및 왜곡된 시각을 생성한다. 황반 변성은 60세가 넘는 연령의 인간에서 시각 상실의 주요 원인이다. 황반 변성의 2가지 형태가 존재한다: 건조 및 습윤 황반 변성. 대상체가 둘 다의 형태를 앓고 이것은 눈의 1개 또는 둘 다에 영향을 미치고, 질환이 서서히 또는 급속히 진행하게 하는 것이 가능하다. 건조 황반 변성은 황반 변성의 가장 흔한 유형이고, 이에 의해 황반의 감광성 세포는 서서히 나빠진다. 드루젠이라고 불리는 황색 참착물 (대사로부터의 세포외 폐기물)은 망막 색소 상피 (RPE) 층 및 브루크 막 사이의 망막 하에 형성하고 축적하며, 이는 망막을 지지한다. 시간이 지나서, 드루젠은 망막의 저하 및 RPE의 사멸과 연관되어, 광수용체 세포는 깨끗하고 표준의 시각의 흐림 또는 점 상실을 일으킨다. 이 과정은 임의의 통증을 유발하지 않는다. 질환의 조기 단계에서, 대상체는 흐린 시각을 다소 인지할 수 있다. 그러나, 점점 더 많은 세포가 사멸함에 따라, 중심 시각은 악화된다. 건성 황반 변성은 질환의 습윤 형태로 변하지 않으면서 시각의 상실을 진전시키고 유발한다. 그러나, 또한 조기 단계 건조 형태가 황반 변성의 습윤 형태로 변하는 것은 가능하다. 습윤 황반 변성은 비정상 혈관이 RPE 및 광수용체 세포가 사멸함에 따라 황반 뒤에서 성장할 때 발생한다. 브루크 막은 나빠지기 시작하고, 통상적으로 드루젠 침착물, 및 신규 혈관이 성장한다. 이들 혈관은 매우 취약하고 유체 및 혈액을 누출시킬 수 있다. 황반의 반흔형성 및 심각한 손상이 발생할 수 있다. 표준의 시각은 단기간에 변형되거나 잃게 될 수 있다.
용어 "신생물" 및 "종양"은 본원에서 상호교환가능하게 사용되고, 덩어리의 성장이 정상 조직의 성장을 능가하며 그와 조화롭지 못한 비정상적 조직 덩어리를 지칭한다. 신생물 또는 종양은 하기 특징에 따라 "양성" 또는 "악성"일 수 있다: 세포 분화의 정도 (형태 및 기능성을 포함함), 성장 속도, 국부 침습, 및 전이. "양성 신생물"은 일반적으로 잘 구별되고, 악성 신생물보다 특징적으로 더 느린 성장을 가지며, 원래 부위에 국재화되어 남아있다. 추가로, 양성 신생물은 원위 부위로의 침윤, 침습 또는 전이 능력을 갖지 않는다. 예시적인 양성 신생물은 지방종, 연골종, 선종, 연성섬유종, 노인성 혈관종, 지루성 각화증, 흑색점, 및 피지 증식증을 포함하나 이에 제한되지는 않는다. 일부 경우에서, 특정 "양성" 종양은 나중에 악성 신생물을 일으킬 수 있으며, 이는 종양의 신생물성 세포의 하위집단에서 추가의 유전적 변화로부터 유발될 수 있고, 이들 종양은 "전암성 신생물"로 지칭된다. 예시적인 전암성 신생물은 기형종이다. 대조적으로, "악성 신생물"은 일반적으로 불량하게 분화 "역형성"되고, 특징적으로 진행성 침윤, 침습 및 주위 조직의 파괴를 동반하는 빠른 성장을 한다. 추가로, 악성 신생물은 일반적으로 원위 부위로 전이하는 능력을 갖는다. 용어 "전이", "전이성" 또는 "전이하다"는 원발성 또는 원래 종양으로부터 또 다른 기관 또는 조직으로의 암성 세포의 확산 또는 이동을 지칭하고, 전형적으로 속발성 "전이성" 종양이 위치하는 기관 또는 조직의 것이 아닌 원발성 또는 원래 종양의 조직 유형의 "속발성 종양" 또는 "속발성 세포 덩어리"의 존재에 의해 확인가능하다. 예를 들어, 골로 이동한 전립선암은 전이된 전립선암이라 불리고, 골 조직에서 성장하는 암성 전립선암 세포를 포함한다.
용어 "암"은 제어할 수 없게 증식하고 정상 신체 조직을 침윤 및 파괴할 수 있는 능력을 갖는 비정상적 세포의 발생을 특징으로 하는 질환의 부류를 지칭한다. 예를 들어, 문헌 [Stedman's Medical Dictionary, 25th ed.; Hensyl ed.; Williams & Wilkins: Philadelphia, 1990]을 참조한다. 예시적인 암은 혈액 악성종양을 포함하나 이에 제한되지는 않는다. 혈액계 악성종양은 혈액, 골수 및/또는 림프절에 영향을 미치는 암이다. 예시적인 혈액 악성종양은 백혈병, 예컨대 급성 림프구성 백혈병 (ALL) (예를 들어, B-세포 ALL, T-세포 ALL), 급성 골수구성 백혈병 (AML) (예를 들어, B-세포 AML, T-세포 AML), 만성 골수구성 백혈병 (CML) (예를 들어, B-세포 CML, T-세포 CML), 및 만성 림프구성 백혈병 (CLL) (예를 들어, B-세포 CLL, T-세포 CLL)); 림프종, 예컨대 호지킨 림프종 (HL) (예를 들어, B-세포 HL, T-세포 HL) 및 비-호지킨 림프종 (NHL) (예를 들어, B-세포 NHL, 예컨대 미만성 대세포 림프종 (DLCL) (예를 들어, 미만성 대 B-세포 림프종 (DLBCL, 예를 들어, 활성화된 B-세포 (ABC) DLBCL (ABC-DLBCL))), 여포성 림프종, 만성 림프구성 백혈병/소림프구성 림프종 (CLL/SLL), 외투 세포 림프종 (MCL), 변연부 B-세포 림프종 (예를 들어, 점막-연관 림프성 조직 (MALT) 림프종, 결절성 변연부 B-세포 림프종, 비장 변연부 B-세포 림프종), 원발성 종격 B-세포 림프종, 버킷 림프종, 발덴스트롬 마크로글로불린혈증 (WM, 림프형질세포성 림프종), 모발상 세포 백혈병 (HCL), 면역모세포성 대세포 림프종, 전구체 B-림프모구성 림프종, 중추 신경계 (CNS) 림프종 (예를 들어, 원발성 CNS 림프종 및 속발성 CNS 림프종); 및 T-세포 NHL, 예컨대 전구체 T-림프모구성 림프종/백혈병, 말초 T-세포 림프종 (PTCL) (예를 들어, 피부 T-세포 림프종 (CTCL) (예를 들어, 균상 식육종, 세자리 증후군), 혈관면역모세포성 T-세포 림프종, 림프절외 자연 킬러 T-세포 림프종, 장병증 유형 T-세포 림프종, 피하 지방층염-유사 T-세포 림프종, 및 역형성 대세포 림프종); 면역 특권 부위의 림프종 (예를 들어, 뇌 림프종, 안구 림프종, 태반 림프종, 태아 림프종, 고환 림프종); 상기 기재된 바와 같은 1종 이상의 백혈병/림프종의 혼합물; 골수이형성증; 및 다발성 골수종 (MM)을 포함하나 이에 제한되지는 않는다. 추가의 예시적인 암은 폐암 (예를 들어, 기관지원성 암종, 소세포 폐암 (SCLC), 비-소세포 폐암 (NSCLC), 폐의 선암종); 신장암 (예를 들어, 신모세포종, 일명 윌름스 종양, 신세포 암종); 청신경종; 선암종; 부신암; 항문암; 혈관육종 (예를 들어, 림프관육종, 림프관내피육종, 혈관육종); 충수암; 양성 모노클로날 감마글로불린병증; 담도암 (예를 들어, 담관암종); 방광암; 유방암 (예를 들어, 유방의 선암종, 유방의 유두상 암종, 유방암, 유방의 수질성 암종); 뇌암 (예를 들어, 수막종, 교모세포종, 신경교종 (예를 들어, 성상세포종, 핍지교종), 수모세포종); 기관지 암; 카르시노이드 종양; 자궁경부암 (예를 들어, 자궁경부 선암종); 융모막암종; 척삭종; 두개인두종; 결장직장암 (예를 들어, 결장암, 직장암, 결장직장 선암종); 결합 조직 암; 상피 암종; 상의세포종; 내피육종 (예를 들어, 카포시 육종, 다발성 특발성 출혈성 육종); 자궁내막암 (예를 들어, 자궁암, 자궁 육종); 식도암 (예를 들어, 식도의 선암종, 바렛 선암종); 유잉 육종; 안구암 (예를 들어, 안내 흑색종, 망막모세포종); 가족성 과다호산구증가증; 담낭암; 위암 (예를 들어, 위 선암종); 위장 기질 종양 (GIST); 배세포 암; 두경부 암 (예를 들어, 두경부 편평 세포 암종, 구강암 (예를 들어, 경구 편평 세포 암종), 인후암 (예를 들어, 후두암, 인두암, 비인두암, 구인두암)); 중쇄 질환 (예를 들어, 알파 쇄 질환, 감마 쇄 질환, 뮤 쇄 질환; 혈관모세포종; 하인두암; 염증성 근섬유모세포성 종양; 면역세포성 아밀로이드증; 간암 (예를 들어, 간세포성암 (HCC), 악성 간세포암); 평활근육종 (LMS); 비만세포증 (예를 들어, 전신 비만세포증); 근육 암; 골수이형성 증후군 (MDS); 중피종; 골수증식성 장애 (MPD) (예를 들어, 진성 다혈구혈증 (PV), 본태성 혈소판증가증 (ET), 원인불명 골수 화생 (AMM) 일명 골수섬유증 (MF), 만성 특발성 골수섬유증, 만성 골수구성 백혈병 (CML), 만성 호중구성 백혈병 (CNL), 과다호산구성 증후군 (HES)); 신경모세포종; 신경섬유종 (예를 들어, 신경섬유종증 (NF) 유형 1 또는 유형 2, 슈반세포종증); 신경내분비 암 (예를 들어, 위장췌장 신경내분비 종양 (GEP-NET), 카르시노이드 종양); 골육종 (예를 들어, 골암); 난소암 (예를 들어, 낭선암종, 난소 배아성 암종, 난소 선암종); 유두상 선암종; 췌장암 (예를 들어, 췌장 선암종, 관내 유두상 점액성 신생물 (IPMN), 도세포 종양); 음경암 (예를 들어, 음경 및 음낭의 파제트 질환); 송과체종; 원시 신경외배엽 종양 (PNT); 형질 세포 신생물; 부신생물성 증후군; 상피내 신생물; 전립선암 (예를 들어, 전립선 선암종); 직장암; 횡문근육종; 타액선암; 피부암 (예를 들어, 편평 세포 암종 (SCC), 각화극세포종 (KA), 흑색종, 기저 세포 암종 (BCC)); 소장 암 (예를 들어, 충수암); 연부 조직 육종 (예를 들어, 악성 섬유성 조직구종 (MFH), 지방육종, 악성 말초 신경초 종양 (MPNST), 연골육종, 섬유육종, 점액육종); 피지선 암종; 소장암; 한선 암종; 활막종; 고환암 (예를 들어, 정상피종, 고환 배아성 암종); 갑상선암 (예를 들어, 갑상선의 유두상 암종, 유두상 갑상선 암종 (PTC), 수질성 갑상선암); 요도암; 질암; 및 외음부암 (예를 들어, 외음부의 파제트 질환)을 포함하나 이에 제한되지는 않는다.
"전신생물성 질환"은 양성 또는 악성 신생물의 형성에 선행하는 질환이다. 전암성 병변은 전형적으로 악성 신생물 전에 형성한다. 전신생물성 질환은 광피부염, x선 피부염, 타르 피부염, 비소 피부염, 루푸스 피부염, 노인성 각화증, 파제트병, 콘딜롬, 화상 반흔, 매독성 반흔, 누공 반흔, 하퇴 궤양 반흔, 만성 궤양, 정맥류성 궤양, 골 누공, 직장루, 바렛 식도, 위 궤양, 위염, 담석증, 외음 위축증 색소모반, 보언 피부병, 색소성 건피증, 홍색비후증, 백색판증, 골의 파제트병, 외골종, 외연골종, 섬유성 골염, 골성사자면, 신경섬유종증, 폴립증, 포상 기태, 선종양 과형성 및 결정성 갑상샘종를 포함하나 이에 제한되지는 않는다.
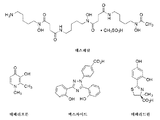
도 1은 인간에서 임상적으로 평가된 일부 철 킬레이트화제의 구조를 도시한다.
도 2a-2b는 래트 간에서 화합물 2 및 4-7의 조직 대사/분포를 도시한다. 래트 (군 당 n = 3)에 300 μmol/kg의 용량으로 피하로 화합물을 제공하였다. 화합물 (y-축)의 농도 데이터는 간의 nmol/g 습윤 중량으로서 나타내어진다. "투여 화합물": 투여된 화합물.
도 3은 먼저 알콜 (대사물 I)로, 이어서 카르복실산 (대사물 II)으로 산화되는, 글리코디아진의 메틸 에테르의 탈알킬화를 도시한다.
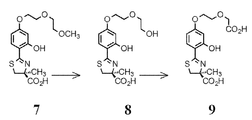
도 4는 화합물 8 및 9로의 화합물 7의 추정 대사, 및 화합물 7 내지 9의 친지성 (log Papp)을 도시한다.
도 5a는 래트 혈장, 간, 신장, 심장, 및 췌장에서 화합물 7 및 8의 조직 대사/분포를 도시한다. 도 5b는 래트 혈장에서 화합물 7 및 8의 조직 대사/분포를 도시한다. 도 5c는 래트 간에서 화합물 7 및 8의 조직 대사/분포를 도시한다. 도 5d는 래트 신장에서 화합물 7 및 8의 조직 대사/분포를 도시한다. 도 5e는 래트 심장에서 화합물 7 및 8의 조직 대사/분포를 도시한다. 도 5f는 래트 췌장에서 화합물 7 및 8의 조직 대사/분포를 도시한다. 래트 (군 당 n = 3)에 300 μmol/kg의 용량으로 피하로 화합물을 제공하였다. 화합물의 농도 데이터 (y-축)는 기관 (예를 들어, 간, 신장, 심장, 췌장)의 nmol/g 습윤 중량으로서, 또는 μM (혈장)으로서 나타내어진다. "투여 화합물": 투여된 화합물.
도 6은 화합물 12 내지 14로의 화합물 11의 추정 대사, 및 화합물 11 내지 14의 친지성 (log Papp)를 도시한다.
도 7a는 래트 심장에서 화합물 11의 조직 대사/분포를 도시한다. 도 7b는 래트 혈장에서 화합물 11의 조직 대사/분포를 도시한다. 도 7c는 래트 간에서 화합물 11의 조직 대사/분포를 도시한다. 도 7d는 래트 신장에서 화합물 11의 조직 대사/분포를 도시한다. 도 7e는 래트 췌장에서 화합물 11의 조직 대사/분포를 도시한다. 래트 (군 당 n = 3)에 300 μmol/kg의 용량으로 피하로 화합물 11을 제공하였다. 화합물 11의 농도 데이터 (y-축)는 기관 (예를 들어, 간, 신장, 심장, 췌장)의 nmol/g 습윤 중량으로서, 또는 μM (혈장)으로서 나타내어진다. "투여 화합물": 투여된 화합물.
도 8은 화합물 11의 경구 흡수의 개략적 표현, 및 화합물 12 내지 14로의 화합물 11의 빠른 대사이다. 화합물 11은 매우 친지성이고, 화합물 12 내지 14는 친수성이다.
도 2a-2b는 래트 간에서 화합물 2 및 4-7의 조직 대사/분포를 도시한다. 래트 (군 당 n = 3)에 300 μmol/kg의 용량으로 피하로 화합물을 제공하였다. 화합물 (y-축)의 농도 데이터는 간의 nmol/g 습윤 중량으로서 나타내어진다. "투여 화합물": 투여된 화합물.
도 3은 먼저 알콜 (대사물 I)로, 이어서 카르복실산 (대사물 II)으로 산화되는, 글리코디아진의 메틸 에테르의 탈알킬화를 도시한다.
도 4는 화합물 8 및 9로의 화합물 7의 추정 대사, 및 화합물 7 내지 9의 친지성 (log Papp)을 도시한다.
도 5a는 래트 혈장, 간, 신장, 심장, 및 췌장에서 화합물 7 및 8의 조직 대사/분포를 도시한다. 도 5b는 래트 혈장에서 화합물 7 및 8의 조직 대사/분포를 도시한다. 도 5c는 래트 간에서 화합물 7 및 8의 조직 대사/분포를 도시한다. 도 5d는 래트 신장에서 화합물 7 및 8의 조직 대사/분포를 도시한다. 도 5e는 래트 심장에서 화합물 7 및 8의 조직 대사/분포를 도시한다. 도 5f는 래트 췌장에서 화합물 7 및 8의 조직 대사/분포를 도시한다. 래트 (군 당 n = 3)에 300 μmol/kg의 용량으로 피하로 화합물을 제공하였다. 화합물의 농도 데이터 (y-축)는 기관 (예를 들어, 간, 신장, 심장, 췌장)의 nmol/g 습윤 중량으로서, 또는 μM (혈장)으로서 나타내어진다. "투여 화합물": 투여된 화합물.
도 6은 화합물 12 내지 14로의 화합물 11의 추정 대사, 및 화합물 11 내지 14의 친지성 (log Papp)를 도시한다.
도 7a는 래트 심장에서 화합물 11의 조직 대사/분포를 도시한다. 도 7b는 래트 혈장에서 화합물 11의 조직 대사/분포를 도시한다. 도 7c는 래트 간에서 화합물 11의 조직 대사/분포를 도시한다. 도 7d는 래트 신장에서 화합물 11의 조직 대사/분포를 도시한다. 도 7e는 래트 췌장에서 화합물 11의 조직 대사/분포를 도시한다. 래트 (군 당 n = 3)에 300 μmol/kg의 용량으로 피하로 화합물 11을 제공하였다. 화합물 11의 농도 데이터 (y-축)는 기관 (예를 들어, 간, 신장, 심장, 췌장)의 nmol/g 습윤 중량으로서, 또는 μM (혈장)으로서 나타내어진다. "투여 화합물": 투여된 화합물.
도 8은 화합물 11의 경구 흡수의 개략적 표현, 및 화합물 12 내지 14로의 화합물 11의 빠른 대사이다. 화합물 11은 매우 친지성이고, 화합물 12 내지 14는 친수성이다.
한 측면에서, 본 발명은 화학식 (I)의 화합물, 및 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 및 그의 전구약물을 제공한다. 데스아자데스페리티오신 유사체는 금속 (예를 들어, 철 및 다른 금속)을 킬레이트화할 수 있다. 본 발명은 또한 본원에 기재된 데스아자데스페리티오신 유사체를 수반하거나 포함하는 제약 조성물, 키트, 방법, 및 용도를 제공한다. 또 다른 측면에서, 본 발명은 하기 화학식 (II)의 화합물, 및 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 및 전구약물을 제공한다. 본 발명은 또한 본원에 기재된 화학식 (I) 또는 화학식 (II)의 화합물을 수반하거나 포함하는 제약 조성물, 키트, 방법, 및 용도를 제공한다. 화합물, 제약 조성물, 키트, 및 방법은 대상체, 세포, 조직, 또는 생물학적 샘플에서 금속을 킬레이화하는데 유용할 수 있다. 화합물, 제약 조성물, 키트, 및 방법은 또한 대상체에서 질환을 치료하거나, 대상체에서 질환을 예방하거나, 대상체에서 바이오필름의 형성을 치료, 감소, 또는 방지하거나, 또는 대상에서 바이오필름의 형성을 감소 또는 방지하는데 유용할 수 있다. 특정 실시양태에서, 질환은 금속 과부하, 산화성 스트레스, 수혈성 철 과부하, 지중해빈혈, 원발성 혈색소증, 속발성 혈색소증, 당뇨병, 간 질환, 심장 질환, 암, 방사선 손상, 신경계 또는 신경변성 장애, 프리드라이히 운동실조 (FRDA), 황반 변성, 폐쇄성 두부 손상, 과민성 장 질환, 또는 재관류 손상이다. 특정 실시양태에서, 질환은 금속 중독이다. 특정 실시양태에서, 질환은 감염성 질환 (예를 들어, 말라리아)이다.
화합물
데스페리티오신 (DFT) 1은 스트렙토미세스 안티비오티쿠스(Streptomyces antibioticus)로부터 단리된 천연 생성물 철 킬레이트화제이다 (Naegeli et al., "Metabolites of Microorganisms. Part 193. Ferrithiocin." Helv. Chim. Acta 1980, 63, 1400-1406). 이는 4 x 1029 M-1의 누적 형성 상수를 갖는 Fe(III)와의 2:1 착물을 형성한다 (Hahn et al., "Coordination Chemistry of Microbial Iron Transport. 42. Structural and Spectroscopic Characterization of Diastereomeric Cr(III) and Co(III) Complexes of Desferriferrithiocin." J. Am. Chem. Soc. 1990, 112, 1854-1860; Anderegg et al., "Metal Complex Formation of a New Siderophore Desferrithiocin and of Three Related Ligands." J. Chem. Soc., Chem. Commun. 1990, 1194-1196). 화합물이 래트 (문헌 [Bergeron et al., "Evaluation of Desferrithiocin and Its Synthetic Analogs as Orally Effective Iron Chelators." J. Med. Chem. 1991, 34, 2072-2078]) 및 영장류 (문헌 [Bergeron et al., "A Comparative Evaluation of Iron Clearance Models." Ann. N.Y. Acad. Sci. 1990, 612, 378-393; Wolfe et al., "A Non-Human Primate Model for the Study of Oral Iron Chelators." Br. J. Haematol. 1989, 72, 456-461])에게 경구로 (po) 투여되는 경우, 탁월한 탈철화제라는 것이 제시되었지만, 이는 래트에서 심각한 신독성을 일으켰다 (Bergeron et al., "A Comparative Study of the Iron-Clearing Properties of Desferrithiocin Analogs with Desferrioxamine B in a Cebus Monkey Model." Blood 1993, 81, 2166-2173). 그러나, 화합물의 경구 활성은 경구 활성이면서 안전한 DFT 유사체를 확인하는 것을 목표로 하는 DFT 집중 SAR 연구에 박차를 가했다 (Bergeron et al., "Effects of C-4 Stereochemistry and C-4' Hydroxylation on the Iron Clearing Efficiency and Toxicity of Desferrithiocin Analogs." J. Med. Chem. 1999, 42, 2432-2440; Bergeron et al., "Methoxylation of Desazadesferrithiocin Analogs: Enhanced Iron Clearing Efficiency." J. Med. Chem. 2003, 46, 1470-1477; Bergeron et al., "Desazadesmethyldesferrithiocin Analogs as Orally Effective Iron Chelators." J. Med. Chem. 1999, 42, 95-108). 생물계에서 금속을 효과적으로 킬레이트화하거나 제거하는 다양한 데스아자데스페리티오신 유사체가 개발되었다. 국제 PCT 출원 공개, 1997년 10월 9일에 공개된 WO 1997/036885; 2000년 3월 30일에 공개된 WO 2000/016763; 2000년 3월 9일에 공개된 WO 2000/012493; 2004년 3월 4일에 공개된 WO 2004/017959; 2005년 4월 21일에 공개된 WO 2005/034949; 2005년 3월 17일에 공개된 WO 2005/023310; 2006년 10월 12일에 공개된 WO 2006/107626; 2008년 10월 30일에 공개된 WO 2008/130395; 2008년 9월 25일에 공개된 WO 2008/115433; 2011년 3월 10일에 공개된 WO 2011/028255; 2013년 6월 20일에 공개된 WO 2013/090750; 및 2013년 6월 20일에 공개된 WO 2013/090766을 참조하며; 그의 각각은 본원에 참조로 포함된다. 또한 미국 특허 번호 US 5,840,739; US 6,864,270; US 7,144,904; US 7,879,886; 미국 재발행 39,132; US 6,083,966; US 6,521,652; US 6,525,080; US 6,559,315; US 8,278,458; 및 US 8,324,397을 참조하고; 그의 각각은 본원에 참조로 포함된다. 또한 미국 특허 출원 공개, US 2004/044220, US 2004/132789, US 2005/234113, US 2008/255081, US 2006/211746, US 2006/211773, US 2008/096974, US 2013/030028, US 2010/137346, US 2013/210870, 및 US 2012/184586을 참조하고, 그의 각각은 본원에 참조로 포함된다.
1의 피리딘 질소의 제거는 1a, 데스아자데스페리티오신 (DADFT) 계의 모 화합물을 제공하였다 (Bergeron et al., "Desazadesmethyldesferrithiocin Analogs as Orally Effective Iron Chelators." J. Med. Chem. 1999, 42, 95-108). 흥미롭게도 1a는 명백히 신독성이지 않았지만, 이는 심각한 위장 (GI) 문제를 유도하였다 (Bergeron et al., "A Comparative Study of the Iron-Clearing Properties of Desferrithiocin Analogs with Desferrioxamine B in a Cebus Monkey Model." Blood 1993, 81, 2166-2173; Bergeron et al., "Effects of C-4 Stereochemistry and C-4' Hydroxylation on the Iron Clearing Efficiency and Toxicity of Desferrithiocin Analogs." J. Med. Chem. 1999, 42, 2432-2440; Bergeron et al., "Desazadesmethyldesferrithiocin Analogs as Orally Effective Iron Chelators." J. Med. Chem. 1999, 42, 95-108). 그의 GI 독성에도 불구하고, 화합물의 탁월한 철-클리어링 효율 (ICE) 및 신독성의 부재는 이 약물작용발생단에 근거한 SAR 연구를 추가로 유도하였다. 이는 DADFT 유사체의 친지성 (옥탄올 층에서의 분획의 log로서 나타내어지는 옥탄올과 물의 분배, logPapp) (문헌 [Sangster, Octanol-Water Partition Coefficients: Fundamentals and Physical Chemistry; John Wiley and Sons: West Sussex, England, 1997; Vol. 2])이 화합물의 ICE, 기관 분포, 및 독성 프로파일에 대한 엄청난 결과를 가질 수 있다는 발견으로 이어진다 (Bergeron et al., "Effects of C-4 Stereochemistry and C-4' Hydroxylation on the Iron Clearing Efficiency and Toxicity of Desferrithiocin Analogs." J. Med. Chem. 1999, 42, 2432-2440; Bergeron et al., "Iron Chelators and Therapeutic Uses." In: Abraham, ed. Burger's Medicinal Chemistry. 6th. Wiley; New York: 2003. pp. 479-561; Bergeron et al., "Desferrithiocin Analogs and Nephrotoxicity." J. Med. Chem. 2008, 51, 5993-6004). 데스페리티오신 유사체는 철 또는 다른 금속을 킬레이트화 및 제거한다고 보고된 바 있다. 국제 PCT 출원 공개, 1997년 10월 9일에 공개된 WO 1997/036885; 2000년 3월 30일에 공개된 WO 2000/016763; 2000년 3월 9일에 공개된 WO 2000/012493; 및 2004년 3월 4일에 공개된 WO 2004/017959를 참조하고; 그의 각각이 본원에 참조로 포함된다. 또한 미국 특허 번호, US 5,840,739; US 6,864,270; US 7,144,904; US 7,879,886을 참조하고; 미국 재발행 39,132; US 6,083,966; US 6,521,652; US 6,525,080; 및 US 6,559,315를 참조하고; 그의 각각이 본원에 참조로 포함된다. 또한 미국 특허 출원 공개, US 2004/044220, US 2004/132789, US 2005/234113, 및 US 2008/255081을 참조하고, 그의 각각이 본원에 참조로 포함된다.
과잉의 철과 연관된 독성은 반응성 산소 종, 예를 들어 내인성 과산화수소 (H2O2)와의 그의 상호작용으로부터 유도된다.20-22 Fe(II)의 존재에서, H2O2는 히드록실 라디칼 (HO·) 및 HO-로 환원되고, 방법은 펜톤 반응 (하기 제시됨)으로서 공지된다. 히드록실 라디칼은 다양한 세포 성분과 매우 빨리 반응하고 DNA 및 막을 손상시킬 뿐만 아니라 발암물질을 생성하는 라디칼-매개 연쇄 과정을 개시할 수 있다.23 펜톤 반응의 주기적 성질은 잠재적 위험을 더한다. 이 반응에서 유리된 Fe(III)가 다양한 생물학적 환원제, 예를 들어, 아스코르베이트 또는 글루타티온을 통해 다시 Fe(II)로 전환된다.
중증성 지중해빈혈 또는 다른 수혈-의존성 불응성 빈혈을 갖는 환자의 대다수에서, 철을 격리할 수 있고 신체로부터 그의 배출을 허용할 수 있는 킬레이트화제에 의한 치료는 유일하게 이용가능한 치료 옵션이다. 현재 선택 (도 1)은 데스페리옥사민 B (DFO)의 메실레이트24 염인 데스페랄, 1,2-디메틸-3-히드록시피리딘-4-온 (디페리프론, L1),25,26 및 4-[3,5-비스(2-히드록시페닐)-1,2,4-트리아졸-1-일]벤조산 (데페라시록스, ICL670A)27,28을 포함한다. 각각은 결점29 및 일부 경우에, 심각한 독성 문제를 갖는다. 스트렙토미세스 필로수스(Streptomyces pilosus),30 시데로포어에 의해 생산된 헥사코오디네이트 히드록사메이트 철 킬레이트화제인 DFO는 경구 활성이 아니고, 최적으로 긴 시간 주기에 걸쳐 연속적 주입에 의해 피하로 (sc) 투여되며,31 이는 환자 순응도 문제를 나타낸다. 디페리프론은, 경구 활성이지만, 환자를 음성 철 균형으로 유지시키기에 충분하게 철을 제거하지 못하고, 무과립구증과 연관되었다 (페리프록스(Ferriprox) 처방 정보, 아포텍스 인크.(Apotex Inc.), 캐나다 온타리오주 토론토, 2015년 4월; www.ferriprox.com/us/pdf/ferriprox_full_pi.pdf). 노파르티스의 약물 데페라시록스는 DFO에 대해 비열등성을 제시하지 못했고, 수많은 심각한 부작용과 연관되고, 불행하게도, 한정적 치료 윈도우를 가지고 있었다.28,33 허용가능한 독성 프로파일을 갖는 효율적인 경구 활성 철 킬레이트화제에 대한 본 발명자들의 추적은 데스페리티오신, (S)-4,5-디히드로-2-(3-히드록시-2-피리디닐)-4-메틸-4-티아졸카르복실산 (DFT, 1, 표 1)로 시작하였다. DFT는 Fe(III)과 안정한 2:1 착물을 형성하는 스트렙토미세스 안티바이오티쿠스(Streptomyces antibiotics)34에 의해 배출된 세자리 시데로포어34,35이고; 누적 형성 상수는 4 x 1029이다.35 설치류36 및 영장류37-39에서의 DFT에 의한 초기 동물 시험은 경구 활성이고 철을 제거하는 것에서 고도로 효율적인 것으로 나타났다. 그의 철 클리어링 효율 (ICE)는 설치류36에서 5.5 ± 3.2% 및 영장류38에서 16.1 ± 8.5%였다 (Bergeron et al., Ann N.Y. Acad. Sci. 612 (1990, 612,) 378-393; Wolfe et al., Br. J. Hematol. 72 (1989, 72,) 456-461) (표 1). ICE는 (리간드-유도 철 배출량/이론적 철 배출량) x 100로서 계산되고, %로 표현된다. 그러나, DFT는 래트에서 허용되지 않은 신장 독성을 가지고 있다.40,41 그럼에도 불구하고, 리간드의 주목할 만한 경구 생체이용률 및 ICE는 DFT-유도 신독성을 개선시키는 것을 목적으로 하는 성공적인 구조-활성 연구를 유도하였다.37 ,42-45 (S)-4,5-디히드로-2-(2-히드록시페닐)-4-메틸-4-티아졸카르복실산 (데스아자데스페리티오신, DADFT)을 제공하는 데스페리티오신 방향족 질소의 제거, 및 4'-방향족에서 (S)-2-(2,4-디히드록시페닐)-4,5-디히드로-4-메틸-4-티아졸카르복실산37 [(S)-4'-(HO)-DADFT, 데페리트린, 2]를 수득하거나, 또는 3'-방향족에서 (S)-2-(2,3-디히드록시페닐)-4,5-디히드로-4-메틸-4-티아졸카르복실산37 [(S)-3'-(OH)-DADFT, 3]을 수득하기 위한 히드록실의 도입은, 우수한 ICE 값 (표 1) 및 독성에서의 주목할 만한 감소를 갖는 킬레이트화제로 이어진다는 것으로 결과가 밝혀졌다. 데페리트린 (2, 도 1)은 겐자임에 의해 인간 임상 시험에 진입하였다. 킬레이트화제 2는 환자에게 최대 12주 동안 5, 10, 또는 15 mg/kg/일의 용량으로 1일 1회 (s.i.d) 내약성이 우수하고,46 철 클리어런스 수준은 필수적인 450 μg/kg/d에 근접하였다.47 그러나, 약물이 12.5 mg/kg (25 mg/kg/일)의 용량으로 1일 2회 (b.i.d) 제공된 경우, 허용되지 않은 신장 독성, 예를 들어 혈액 중 우레아 질소 (BUN) 및 혈청 크레아티닌 (SCr)의 증가가 단지 4-5주의 치료 후에 3명의 환자에서 관찰되었고, 연구를 종료하였다.48 그럼에도 불구하고, 결과는 그의 독성을 개선하기 위한 시도에 있어서 본 발명자들이 데페리트린을 개량시키게 하기에 충분히 매력적이었다.
2의 재설계는 리간드 2 및 3 둘 다가 설치류 및 영장류에서 경구 활성 철 킬레이트화제인 것, 및 2의 4'-(OH)를 메틸화하여, (S)-4,5-디히드로-2-(2-히드록시-4-메톡시페닐)-4-메틸-4-티아졸카르복실산43 [(S)-4'-(CH3O)-DADFT, 4]을 제공하는 경우, ICE 및 친지성 (log Papp) 둘 다에서 주목할 만한 향상이 있다는 관찰에 기초하였다 (표 1). log Papp 데이터는 옥탄올 층에서 나타난 킬레이트화제의 분획의 log로서 표현되고; "진탕 플라스크" 직접적 방법을 사용하여 트리스 완충제, pH 7.4에서 측정이 행해졌다.49 log Papp이 더 음성일수록 옥탄올 상 중의 킬레이트화제는 더 적고, 친지성이 더 작다. 불행하게도, 4의 ICE의 증가는 독성의 증가를 수반하면서 나타났다.50 따라서, 증진된 친지성에 의한 ICE의 증가 및 독성 간의 까다로운 균형을 이해하고 이용할 필요가 있다. 폴리에테르 단편을 2의 4'-(OH)에 도입하여 (S)-4,5-디히드로-2-[2-히드록시-4-(3,6,9-트리옥사데실옥시)페닐]-4-메틸-4-티아졸카르복실산50 [(S)-4'-(HO)-DADFT-PE, 5]을 제조하거나, 또는 3의 3'-(OH)에 도입하여 (S)-4,5-디히드로-2-[2-히드록시-3-(3,6,9-트리옥사데실옥시)페닐]-4-메틸-4-티아졸카르복실산51 [(S)-3'-(HO)-DADFT-PE, 6]을 수득하는 것은 덜 친지성, 예를 들어 더 낮은 log Papp, 주목할 만한 효율적인 철 킬레이트화제로 이어지는 것으로 결정되었다 (표 1). 데페리트린과 달리, 킬레이트화제가 b.i.d.로 투여되는 경우라도, 5 또는 6에 의해 보여지는 신장 독성은 전혀 없었다. 50-52
리간드 6의 마그네슘 염 (SPD602, 데페리타졸 마그네슘, CAS # 1173092-59-5)이 샤이어 (Shire)에 의해 임상 시험에서 평가되었다.53,54 6은 오일이기 때문에, 그의 나트륨 염은 흡습성이고, 투여 형태 문제는 마그네슘 염에 대한 그의 선택을 유도할 수 있었다. 653,54의 마그네슘 염에 의해 관찰된 위장 (GI) 및 다른 부작용이 마그네슘 자체에서 유래하는지의 여부에 대해 추측하는 것은 흥미롭다.55-57 6에 의한 본 발명자들의 모든 연구는 일나트륨 염에 의해 수행되었다.41,51,52,58 마그네슘 염이 환자에서 얼마나 잘 수행할 것인지는 지켜보아야 한다.
주목이 필요한 (S)-3'-(HO)-DADFT-PE (6)의 2가지 특성이 있었다. 모 약물은 오일이고, 래트의 용량 반응 곡선은 매우 빨리 정체하였다. 예를 들어, 6을 담관-캐뉼라삽입된 래트에 150 μmol/kg의 용량으로 경구로 (po) 제공한 경우, 약물은 철 0.782 ± 0.121 mg/kg을 제외시키고; ICE는 18.7 ± 2.9%이었다.45,58 그러나, 킬레이트화제의 용량이 추가로 300 μmol/kg로 증가된 경우, 배출된 철의 양, 0.887 ± 0.367 mg/kg은 150 μmol/kg (p > 0.05)의 약물에 의해 유도된 오차 내에 있고, ICE는 10.6 ± 4.4%이었다.45,58 따라서, 6에 의해 유도된 탈철화는 상당히 적은 용량 범위에 걸쳐 포화가능하였다. 추가의 구조 활성 관계 (SAR) 연구를 수행하여 보다 우수한 물리화학적 특성을 갖는 킬레이트화제, 예를 들어 광범위의 용량에 걸쳐 그의 ICE를 유지한 고체를 찾았다. 응답은 (S)-4'-(HO)-DADFT-PE (5)의 단순한 구조 변경에 딸려올 것이다: 3,6,9-트리옥사데실옥시 폴리에테르 모이어티를 3,6-디옥사헵틸옥시 관능으로 치환하여, (S)-4,5-디히드로-2-[2-히드록시-4-(3,6-디옥사헵틸옥시)페닐]-4-메틸-4-티아졸카르복실산58,59 [(S)-4'-(HO)-DADFT-norPE, 7]을 제공하였다. 산 7 (표 1) 및 그의 에스테르 전구체59 둘 다는 결정질 고체이고, 설치류 및 영장류 둘 다에 대해 캡슐로 매우 효과적으로 제공될 수 있다. 리간드 7은 설치류 및 영장류에서 탁월한 ICE 특성 (~26%)를 갖는다. 이는 또한 설치류에서 6보다 더욱더 우수한 용량 반응을 갖는다.58
b.i.d. 데페리트린에 의한 문제 때문에, 7에서 가장 우려되는 독성 문제는 신장 근위 세관 손상과 관련되었다. 신장 기능에 대한 (S)-4'-(HO)-DADFT-norPE의 영향에 집중된 일련의 내약성 연구를 수행하였다.58 약물을 28일 동안 s.i.d. (56.9, 113.8, 또는 170.7 μmol/kg/일); 10일 동안 s.i.d. (384 μmol/ kg/일), 및 b.i.d.로 237 μmol/kg/용량 (474 μmol/kg/일) x 7일로 경구로 래트에게 제공하였다.58 희생시키기 바로 전에 혈액을 수집하고 동물의 혈액 우레아 질소 (BUN) 및 혈청 크레아티닌 (SCr)의 결정을 포함하여, 온혈구 카운트 (CBC) 및 혈청 화학 분석을 하였다. 어떠한 약물-관련 이상도 발견되지 않았고, 래트의 BUN 및 SCr 수준은 정상 범위내에 있었다.59 게다가, 비뇨기 신장 손상 분자-1 (Kim-1)60,61 배출에 대한 약물의 효과의 평가를 결정하였다. Kim-1은 근위 세관의 상피 세포에 위치한 유형 1 막횡단 단백질이다.60,61 Kim-1의 엑토도메인은 신독성제 또는 허혈에 대한 노출 후 매우 초기에 소변으로 방출되고; BUN 또는 SCr의 증가는 혈청에서 검출된 것보다 더욱더 빠르게 나타난다.62,63 최대 28일 동안 래트에 대한 7의 투여는 요 중 Kim-1 배출에서 어떠한 증가도 도출하지 않았다.58 확장 조직을 조직병리 분석하였고; 어떠한 약물-관련 이상도 확인되지 않았다. 이러한 SAR 성공은 얼마나 최적으로 친지성, ICE, 및 리간드 독성 간의 관계를 추가로 도출하는 지에 대한 보다 면밀한 관찰을 위한 단계를 설정한다. 설계 전략은 어떻게 킬레이트화제의 치환기가 잠재적으로 대사되는 지에 대해 무겁게 따져볼 것이다.
한 부류의 화합물로서의 DFT 및 DADFT 유사체는 금속 킬레이트화제로서 유망하게 보이지만, 대상체에서 병리학적 상태의 더 우수한 치료 및/또는 예방에 대해 안전하고 효과적인 화합물을 제공하려는 목적을 위해, 작업을 행하여 이들 화합물의 물리화학적, 약동학적, 약역학적, 및/또는 독성학적 특성, 예컨대 흡수, 분배, 금속-클리어링 효율, 및 독성을 향상시킬 수 있다.
본 개시내용의 한 측면은 화학식 (I)의 화합물 및 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 및 전구약물에 관한 것이다:
여기서
각 경우의 R'는 독립적으로 수소, 치환 또는 비치환된 알킬 또는 산소 보호기이고;
각 경우의 n은 독립적으로 1 내지 8의 정수이고;
각 경우의 x는 독립적으로 0 내지 8의 정수이고;
각 경우의 m은 독립적으로 1 내지 8의 정수이고;
각 경우의 y는 독립적으로 0 내지 8의 정수이고;
각 경우의 p는 독립적으로 1 내지 10의 정수이고;
각 경우의 R2는 독립적으로 -CH2OR2a, -CH2OH, -C(=O)OH, 또는 -C(=O)OR2a이고, 여기서 각 경우의 R2a는 독립적으로 치환 또는 비치환된 알킬 또는 산소 보호기이고;
각 경우의 R3은 독립적으로 할로겐, 치환 또는 비치환된 알킬 또는 -OR8이고, 여기서 각 경우의 R8은 독립적으로 수소, 치환 또는 비치환된 알킬, 치환 또는 비치환된 아실, 산소 보호기, 이고;
k는 0, 1, 2, 3, 또는 4이고;
R4는 수소 또는 치환 또는 비치환된 알킬이고;
R5는 수소 또는 치환 또는 비치환된 알킬이고;
R6은 수소 또는 치환 또는 비치환된 알킬이고;
Z는 -O- 또는 -S-이고;
화학식 (I)은 페닐 고리의 2'-위치에 치환기 -O-R1을 포함한다. 특정 실시양태에서, R1은 H이다. 특정 실시양태에서, R1은 치환 또는 비치환된 알킬 (예를 들어, 치환 또는 비치환된 C1-6 알킬)이다. 특정 실시양태에서, R1은 Me이다. 특정 실시양태에서, R1은 Et, Pr, Bu, 비치환된 펜틸, 또는 비치환된 헥실이다. 특정 실시양태에서, R1은 치환된 메틸 (예를 들어, -CF3, 또는 Bn), 치환된 에틸 (예를 들어, 퍼플루오로에틸), 치환된 프로필 (예를 들어, 퍼플루오로프로필), 치환된 부틸 (예를 들어, 퍼플루오로부틸), 치환된 펜틸 (예를 들어, 퍼플루오로펜틸), 또는 치환된 헥실 (예를 들어, 퍼플루오로헥실)이다. 특정 실시양태에서, R1은 치환 또는 비치환된 아실이다. 특정 실시양태에서, R1은 -C(=O)Ra이고, 임의로 여기서 Ra는 치환 또는 비치환된 C1-6 알킬 (예를 들어, Me)이다. 특정 실시양태에서, R1은 -C(=O)ORa이고, 임의로 여기서 Ra는 H, 치환 또는 비치환된 C1-6 알킬 (예를 들어, Me), 또는 산소 보호기 (예를 들어, 실릴, TBDPS, TBDMS, TIPS, TES, TMS, MOM, THP, t-Bu, Bn, 알릴, 아세틸, 피발로일, 또는 벤조일)이다. 특정 실시양태에서, R1은 -C(=O)N(Ra)2이고, 임의로 여기서 각 경우의 Ra는 독립적으로 H, 치환 또는 비치환된 C1-6 알킬 (예를 들어, Me), 또는 질소 보호기 (예를 들어, Bn, Boc, Cbz, Fmoc, 트리플루오로아세틸, 트리페닐메틸, 아세틸, 또는 Ts)이다. 특정 실시양태에서, R1은 산소 보호기 (예를 들어, 실릴, TBDPS, TBDMS, TIPS, TES, TMS, MOM, THP, t-Bu, Bn, 알릴, 아세틸, 피발로일, 또는 벤조일)이다. 특정 실시양태에서, R1은 이다. 특정 실시양태에서, R1은 이다. 특정 실시양태에서, R1은 이다. 특정 실시양태에서, R1은 이다. 특정 실시양태에서, R1은 화학식: 이다. 특정 실시양태에서, -O-R1은 화학식:
이다. 특정 실시양태에서, -O-R1은 화학식:
이다. 특정 실시양태에서, -O-R1은 화학식:
이다. 특정 실시양태에서, -O-R1은 화학식:
이다. 특정 실시양태에서, -O-R1은 화학식:
특정 실시양태에서, -O-R1은 화학식:
이다. 특정 실시양태에서, -O-R1은 화학식:
이다. 특정 실시양태에서, -O-R1은 화학식:
이다. 특정 실시양태에서, -O-R1은 화학식:
이다. 특정 실시양태에서, -O-R1은 화학식:
화학식 (I)은 1개 이상의 경우의 치환기 R'를 포함할 수 있다. 화학식 (I)이 2개 이상의 경우의 R'을 포함하는 경우, 임의의 2개 경우의 Ra는 독립적으로 서로 동일하거나 상이할 수 있다. 특정 실시양태에서, 적어도 1개 경우의 R'는 H이다. 특정 실시양태에서, 각 경우의 R'는 H이다. 특정 실시양태에서, 적어도 1개 경우의 R'는 치환 또는 비치환된 알킬 (예를 들어, 치환 또는 비치환된 C1-6 알킬)이다. 특정 실시양태에서, 적어도 1개 경우의 R'는 Me이다. 특정 실시양태에서, 적어도 1개 경우의 R'는 Et, Pr, Bu, 비치환된 펜틸, 또는 비치환된 헥실이다. 특정 실시양태에서, 적어도 1개 경우의 R'는 메틸 (예를 들어, -CF3, 또는 Bn), 치환된 에틸 (예를 들어, 퍼플루오로에틸), 치환된 프로필 (예를 들어, 퍼플루오로프로필), 치환된 부틸 (예를 들어, 퍼플루오로부틸), 치환된 펜틸 (예를 들어, 퍼플루오로펜틸), 또는 치환된 헥실 (예를 들어, 퍼플루오로헥실)이다. 특정 실시양태에서, 적어도 1개 경우의 R'는 산소 보호기 (예를 들어, 아실, 실릴, TBDPS, TBDMS, TIPS, TES, TMS, MOM, THP, t-Bu, Bn, 알릴, 아세틸, 피발로일, 또는 벤조일)이다.
화학식 (I)은 페닐 고리의 3', 4', 5', 또는 6'-위치에서 모이어티 를 포함할 수 있다. 특정 실시양태에서, q는 0이다. 특정 실시양태에서, q는 1이다. 화학식 (I)이 2개 이상의 경우의 n을 포함하는 경우, 임의의 2개 경우의 n은 독립적으로 서로 동일하거나 상이할 수 있다. 특정 실시양태에서, 적어도 1개 경우의 n은 1이다. 특정 실시양태에서, 적어도 1개 경우의 n은 2이다. 특정 실시양태에서, 각 경우의 n은 2이다. 특정 실시양태에서, 적어도 1개 경우의 n은 3, 4, 5, 6, 7, 또는 8이다.
화학식 (I)이 2개 이상의 경우의 x를 포함하는 경우, 임의의 2개 경우의 x는 독립적으로 서로 동일하거나 상이할 수 있다. 특정 실시양태에서, 적어도 1개 경우의 x는 0이다. 특정 실시양태에서, 적어도 1개 경우의 x는 1이다. 특정 실시양태에서, 적어도 1개 경우의 x는 2이다. 특정 실시양태에서, 각 경우의 x는 2이다. 특정 실시양태에서, 적어도 1개 경우의 x는 3이다. 특정 실시양태에서, 적어도 1개 경우의 x는 4이다. 특정 실시양태에서, 적어도 1개 경우의 x는 5, 6, 7, 또는 8이다.
화학식 (I)이 2개 이상의 경우의 m을 포함하는 경우, 임의의 2개 경우의 m은 독립적으로 서로 동일하거나 상이할 수 있다. 특정 실시양태에서, 적어도 1개 경우의 m은 1이다. 특정 실시양태에서, 적어도 1개 경우의 m은 2이다. 특정 실시양태에서, 각 경우의 m은 2이다. 특정 실시양태에서 적어도 1개 경우의 m은 3, 4, 5, 6, 7, 또는 8이다.
화학식 (I)이 2개 이상의 경우의 y를 포함하는 경우, 임의의 2개 경우의 y는 독립적으로 서로 동일하거나 상이할 수 있다. 특정 실시양태에서, 적어도 1개 경우의 y는 0이다. 특정 실시양태에서, 적어도 1개 경우의 y는 1이다. 특정 실시양태에서, 적어도 1개 경우의 y는 2이다. 특정 실시양태에서, 적어도 1개 경우의 y는 3이다. 특정 실시양태에서, 적어도 1개 경우의 y는 4이다. 특정 실시양태에서, 적어도 1개 경우의 y는 5, 6, 7, 또는 8이다.
특정 실시양태에서, 각각의 x 및 y는 0이다. 특정 실시양태에서, 각 경우의 x는 1, 2, 3, 또는 4이고; 각 경우의 n은 2이고; 각 경우의 y는 0이다. 특정 실시양태에서, 각 경우의 x는 1이고; 각 경우의 n은 2이고; 각 경우의 y는 0이다. 특정 실시양태에서, 각 경우의 x는 2이고; 각 경우의 n은 2이고; 각 경우의 y는 0이다. 특정 실시양태에서, 각 경우의 x는 3이고; 각 경우의 n은 2이고; 각 경우의 y는 0이다. 특정 실시양태에서, 각 경우의 x는 4이고; 각 경우의 n은 2이고; 각 경우의 y는 0이다.
화학식 (I)이 2개 이상의 경우의 p를 포함하는 경우, 임의의 2개 경우의 p는 독립적으로 서로 동일하거나 상이할 수 있다. 특정 실시양태에서, 적어도 1개 경우의 p는 1이다. 특정 실시양태에서, 적어도 1개 경우의 p는 2이다. 특정 실시양태에서, 적어도 1개 경우의 p는 3이다. 특정 실시양태에서, 적어도 1개 경우의 p는 4이다. 특정 실시양태에서, 적어도 1개 경우의 p는 5이다. 특정 실시양태에서, 적어도 1개 경우의 p는 6, 7, 8, 9, 또는 10이다.
특정 실시양태에서, 각각의 x 및 y는 0이고; 적어도 1개 경우의 p는 1, 2, 3, 4, 또는 5이다. 특정 실시양태에서, 각 경우의 x는 1, 2, 3, 또는 4이고; 각 경우의 n은 2이고; 각 경우의 y는 0이고; 적어도 1개 경우의 p는 1, 2, 3, 4, 또는 5이다. 특정 실시양태에서, 각 경우의 x는 1이고; 각 경우의 n은 2이고; 각 경우의 y는 0이고; 적어도 1개 경우의 p는 1, 2, 3, 4, 또는 5이다. 특정 실시양태에서, 각 경우의 x는 2이고; 각 경우의 n은 2이고; 각 경우의 y는 0이고; 적어도 1개 경우의 p는 1, 2, 3, 4, 또는 5이다. 특정 실시양태에서, 각 경우의 x는 3이고; 각 경우의 n은 2이고; 각 경우의 y는 0이고; 적어도 1개 경우의 p는 1, 2, 3, 4, 또는 5이다. 특정 실시양태에서, 각 경우의 x는 4이고; 각 경우의 n은 2이고; 각 경우의 y는 0이고; 적어도 1개 경우의 p는 1, 2, 3, 4, 또는 5이다.
특정 실시양태에서, 적어도 1개의 모이어티 는 페닐 고리의 3'-위치에 있다. 특정 실시양태에서, 적어도 1개의 모이어티 는 페닐 고리의 4'-위치에 있다. 특정 실시양태에서, 적어도 1개의 모이어티 는 페닐 고리의 5'-위치에 있다. 특정 실시양태에서, 적어도 1개의 모이어티 는 페닐 고리의 6'-위치에 있다. 특정 실시양태에서, 페닐 고리의 3', 4', 5', 또는 6'-위치의 모이어티 는 화학식:
화학식 (I)이 2개 이상의 경우의 R2를 포함하는 경우, 임의의 2개 경우의 R2는 독립적으로 서로 동일하거나 상이할 수 있다. 특정 실시양태에서, 적어도 1개 경우의 R2는 -CH2OR2a이다. 특정 실시양태에서, 적어도 1개 경우의 R2는 -CH2OR2a이고, 여기서 R2a는 치환 또는 비치환된 알킬 (예를 들어, 치환 또는 비치환된 C1-6 알킬)이다. 특정 실시양태에서, 적어도 1개 경우의 R2는 -CH2OMe이다. 특정 실시양태에서, 적어도 1개 경우의 R2는 -CH2OEt, -CH2OPr, -CH2OBu, -CH2O(치환된 펜틸), 또는 -CH2O(비치환된 헥실)이다. 특정 실시양태에서, 적어도 1개 경우의 R2는 -CH2O(치환된 메틸) (예를 들어, -CH2OCF3 또는 -CH2OBn), -CH2O(치환된 에틸) (예를 들어, -CH2O(퍼플루오로에틸)), -CH2O(치환된 프로필) (예를 들어, -CH2O(퍼플루오로프로필)), -CH2O(치환된 부틸) (예를 들어, -CH2O(퍼플루오로부틸)), -CH2O(치환된 펜틸) (예를 들어, -CH2O(퍼플루오로펜틸)), 또는 -CH2O(치환된 헥실) (예를 들어, -CH2O(퍼플루오로헥실))이다. 특정 실시양태에서, 적어도 1개 경우의 R2는 -CH2OR2a이고, 여기서 R2a는 산소 보호기 (예를 들어, 아실, 실릴, TBDPS, TBDMS, TIPS, TES, TMS, MOM, THP, t-Bu, Bn, 알릴, 아세틸, 피발로일, 또는 벤조일)이다.
특정 실시양태에서, 적어도 1개 경우의 R2는 -CH2OH이다
특정 실시양태에서, 적어도 1개 경우의 R2는 -C(=O)OH이다.
특정 실시양태에서, 적어도 1개 경우의 R2는 -C(=O)OR2a이다. 특정 실시양태에서, 적어도 1개 경우의 R2는 -C(=O)OR2a이고, 여기서 R2a는 치환 또는 비치환된 알킬 (예를 들어, 치환 또는 비치환된 C1-6 알킬)이다. 특정 실시양태에서, 적어도 1개 경우의 R2는 -C(=O)OMe이다. 특정 실시양태에서, 적어도 1개 경우의 R2는 -C(=O)OEt, -C(=O)OPr, -C(=O)OBu, -C(=O)O(비치환된 펜틸), 또는 -C(=O)O(비치환된 헥실)이다. 특정 실시양태에서, 적어도 1개 경우의 R2는 -C(=O)O(치환된 메틸) (예를 들어, -C(=O)OCF3 또는 -C(=O)OBn), -C(=O)O(치환된 에틸) (예를 들어, -C(=O)O(퍼플루오로에틸)), -C(=O)O(치환된 프로필) (예를 들어, -C(=O)O(퍼플루오로프로필)), -C(=O)O(치환된 부틸) (예를 들어, -C(=O)O(퍼플루오로부틸)), -C(=O)O(치환된 펜틸) (예를 들어, -C(=O)O(퍼플루오로펜틸)), 또는 -C(=O)O(치환된 헥실) (예를 들어, -C(=O)O(퍼플루오로헥실))이다. 특정 실시양태에서, 적어도 1개 경우의 R2는 -C(=O)OR2a이고, 여기서 R2a는 산소 보호기 (예를 들어, 아실, 실릴, TBDPS, TBDMS, TIPS, TES, TMS, MOM, THP, t-Bu, Bn, 알릴, 아세틸, 피발로일, 또는 벤조일)이다.
화학식 (I)은 페닐 고리의 3', 4', 5', 및/또는 6'-위치에 1개 이상의 치환기 R3을 포함할 수 있다. 화학식 (I)이 2개 이상의 경우의 R3을 포함하는 경우, 임의의 2개 경우의 R3은 독립적으로 서로 동일하거나 상이할 수 있다.
특정 실시양태에서, 적어도 1개 경우의 R3은 할로겐 (예를 들어, F, Cl, Br, 또는 I)이다. 특정 실시양태에서, 적어도 1개 경우의 R3은 치환 또는 비치환된 알킬 (예를 들어, 치환 또는 비치환된 C1-6 알킬)이다. 특정 실시양태에서, 적어도 1개 경우의 R3은 Me이다. 특정 실시양태에서, 적어도 1개 경우의 R3은 Et, Pr, Bu, 비치환된 펜틸, 또는 비치환된 헥실이다. 특정 실시양태에서, 적어도 1개 경우의 R3은 치환된 메틸 (예를 들어, -CF3, 또는 Bn), 치환된 에틸 (예를 들어, 퍼플루오로에틸), 치환된 프로필 (예를 들어, 퍼플루오로프로필), 치환된 부틸 (예를 들어, 퍼플루오로부틸), 치환된 펜틸 (예를 들어, 퍼플루오로펜틸), 또는 치환된 헥실 (예를 들어, 퍼플루오로헥실)이다. 특정 실시양태에서, 적어도 1개 경우의 R3은 -OR8이다. 특정 실시양태에서, 적어도 1개 경우의 R3은 -OH이다. 특정 실시양태에서, 어떠한 경우의 R3도 -OH가 아니다.
특정 실시양태에서, 적어도 1개 경우의 R3은 -OR8이고, 여기서 R8이 치환 또는 비치환된 알킬 (예를 들어, 치환 또는 비치환된 C1-6 알킬)이다. 특정 실시양태에서, 적어도 1개 경우의 R3은 -OMe이다. 특정 실시양태에서, 어떠한 경우의 R3도 -OMe이 아니다. 특정 실시양태에서, 적어도 1개 경우의 R3은 -OEt, -OPr, -OBu, -O(비치환된 펜틸), 또는 -O(비치환된 헥실)이다. 특정 실시양태에서, 적어도 1개 경우의 R3은 -O(치환된 메틸) (예를 들어, -OCF3 또는 -OBn), -O(치환된 에틸) (예를 들어, -O(퍼플루오로에틸)), -O(치환된 프로필) (예를 들어, -O(퍼플루오로프로필)), -O(치환된 부틸) (예를 들어, -O(퍼플루오로부틸)), -O(치환된 펜틸) (예를 들어, -O(퍼플루오로펜틸)), 또는 -O(치환된 헥실) (예를 들어, -O(퍼플루오로헥실))이다. 특정 실시양태에서, 적어도 1개 경우의 R3은 치환 또는 비치환된 아실이다. 특정 실시양태에서, 적어도 1개 경우의 R3은 -C(=O)Ra이고, 임의로 여기서 Ra는 치환 또는 비치환된 C1-6 알킬 (예를 들어, Me)이다. 특정 실시양태에서, 적어도 1개 경우의 R3은 -C(=O)ORa이고, 임의로 여기서 Ra는 H, 치환 또는 비치환된 C1-6 알킬 (예를 들어, Me), 또는 산소 보호기 (예를 들어, 실릴, TBDPS, TBDMS, TIPS, TES, TMS, MOM, THP, t-Bu, Bn, 알릴, 아세틸, 피발로일, 또는 벤조일)이다. 특정 실시양태에서, 적어도 1개 경우의 R3은 -C(=O)N(Ra)2이고, 임의로 여기서 각 경우의 Ra는 독립적으로 H, 치환 또는 비치환된 C1-6 알킬 (예를 들어, Me), 또는 질소 보호기 (예를 들어, Bn, Boc, Cbz, Fmoc, 트리플루오로아세틸, 트리페닐메틸, 아세틸, 또는 Ts)이다. 특정 실시양태에서, 적어도 1개 경우의 R3은 -OR8이고, 여기서 R8은 산소 보호기 (예를 들어, 실릴, TBDPS, TBDMS, TIPS, TES, TMS, MOM, THP, t-Bu, Bn, 알릴, 아세틸, 피발로일, 또는 벤조일)이다. 특정 실시양태에서, 적어도 1개 경우의 R3은 -OR8이고, 여기서 R8은 이다. 특정 실시양태에서, 적어도 1개 경우의 R3은 -OR8이고, 여기서 R8은 이다. 특정 실시양태에서, 적어도 1개 경우의 R3은 -OR8이고, 여기서 R8은 이다. 특정 실시양태에서, 적어도 1개 경우의 R3은 -OR8이고, 여기서 R8은 이다.
특정 실시양태에서, k는 0이다. 특정 실시양태에서, k는 1이다. 특정 실시양태에서, k는 2이다. 특정 실시양태에서, k는 3이다. 특정 실시양태에서, k는 4이다.
화학식 (I)은 티아졸리닐 고리의 5-위치에 치환기 R4를 포함한다. 특정 실시양태에서, R4는 H이다. 특정 실시양태에서, R4는 치환 또는 비치환된 알킬 (예를 들어, 치환 또는 비치환된 C1-6 알킬)이다. 특정 실시양태에서, R4는 Me이다. 특정 실시양태에서, R4는 Et, Pr, Bu, 비치환된 펜틸, 또는 비치환된 헥실이다. 특정 실시양태에서, R4는 치환된 메틸 (예를 들어, -CF3, 또는 Bn), 치환된 에틸 (예를 들어, 퍼플루오로에틸), 치환된 프로필 (예를 들어, 퍼플루오로프로필), 치환된 부틸 (예를 들어, 퍼플루오로부틸), 치환된 펜틸 (예를 들어, 퍼플루오로펜틸), 또는 치환된 헥실 (예를 들어, 퍼플루오로헥실)이다.
화학식 (I)은 티아졸리닐 고리의 5-위치에 치환기 R5를 포함한다. 특정 실시양태에서, R5는 H이다. 특정 실시양태에서, R5는 치환 또는 비치환된 알킬 (예를 들어, 치환 또는 비치환된 C1-6 알킬)이다. 특정 실시양태에서, R5는 Me이다. 특정 실시양태에서, R5는 Et, Pr, Bu, 비치환된 펜틸, 또는 비치환된 헥실이다. 특정 실시양태에서, R5는 치환된 메틸 (예를 들어, -CF3, 또는 Bn), 치환된 에틸 (예를 들어, 퍼플루오로에틸), 치환된 프로필 (예를 들어, 퍼플루오로프로필), 치환된 부틸 (예를 들어, 퍼플루오로부틸), 치환된 펜틸 (예를 들어, 퍼플루오로펜틸), 또는 치환된 헥실 (예를 들어, 퍼플루오로헥실)이다.
특정 실시양태에서, 각각의 R4 및 R5는 수소이다. 특정 실시양태에서, 각각의 R4 및 R5는 독립적으로 치환 또는 비치환된 알킬 (예를 들어, 치환 또는 비치환된 C1-6 알킬)이다. 특정 실시양태에서, 각각의 R4 및 R5는 Me이다.
화학식 (I)은 티아졸리닐 고리의 4-위치에 치환기 R6을 포함한다. 특정 실시양태에서, R6은 H이다. 특정 실시양태에서, R6은 치환 또는 비치환된 알킬 (예를 들어, 치환 또는 비치환된 C1-6 알킬)이다. 특정 실시양태에서, R6은 Me이다. 특정 실시양태에서, R6은 Et, Pr, Bu, 비치환된 펜틸, 또는 비치환된 헥실이다. 특정 실시양태에서, R6은 치환된 메틸 (예를 들어, -CF3, 또는 Bn), 치환된 에틸 (예를 들어, 퍼플루오로에틸), 치환된 프로필 (예를 들어, 퍼플루오로프로필), 치환된 부틸 (예를 들어, 퍼플루오로부틸), 치환된 펜틸 (예를 들어, 퍼플루오로펜틸), 또는 치환된 헥실 (예를 들어, 퍼플루오로헥실)이다.
특정 실시양태에서, 각각의 R4 및 R5는 수소이고 R6은 치환 또는 비치환된 알킬 (예를 들어, 치환 또는 비치환된 C1-6 알킬)이다. 특정 실시양태에서, 각각의 R4 및 R5는 수소이고, R6은 Me이다.
특정 실시양태에서, Z는 -O-이다. 특정 실시양태에서, Z는 -S-이다.
특정 실시양태에서, R9는 H이다. 특정 실시양태에서, R9는 치환 또는 비치환된 알킬 (예를 들어, 치환 또는 비치환된 C1-6 알킬)이다. 특정 실시양태에서, R9는 Me이다. 특정 실시양태에서, R9는 Et, Pr, Bu, 비치환된 펜틸, 또는 비치환된 헥실이다. 특정 실시양태에서, R9는 치환된 메틸 (예를 들어, -CF3, 또는 Bn), 치환된 에틸 (예를 들어, 퍼플루오로에틸), 치환된 프로필 (예를 들어, 퍼플루오로프로필), 치환된 부틸 (예를 들어, 퍼플루오로부틸), 치환된 펜틸 (예를 들어, 퍼플루오로펜틸), 또는 치환된 헥실 (예를 들어, 퍼플루오로헥실)이다. 특정 실시양태에서, R9는 이다. 특정 실시양태에서, R9는 이다. 특정 실시양태에서, R9는 이다. 특정 실시양태에서, R9는 이다. 특정 실시양태에서, R9는 산소 원자에 부착된 경우 산소 보호기 (예를 들어, 실릴, TBDPS, TBDMS, TIPS, TES, TMS, MOM, THP, t-Bu, Bn, 알릴, 아세틸, 피발로일, 또는 벤조일)이다. 특정 실시양태에서, R9는 황 원자에 부착된 경우 황 보호기 (예를 들어, 아세트아미도메틸, t-Bu, 3-니트로-2-피리딘 술페닐, 2-피리딘-술페닐, 또는 트리페닐메틸)이다.
특정 실시양태에서, -Z-R9는 -OH이다. 특정 실시양태에서, -Z-R9는 -O(비치환된 C1-6 알킬)이다.
화학식 (I)은 티아졸리닐 고리의 4-위치에 키랄 탄소 원자 ("*"로 표지된 탄소 원자)를 포함한다. 특정 실시양태에서, "*"로 표지된 탄소 원자는 S 배위이다. 특정 실시양태에서, "*"로 표지된 탄소 원자는 R 배위이다.
특정 실시양태에서, 페닐 고리의 3', 4', 5', 또는 6'-위치의 모이어티 는 화학식: 이 아니다. 특정 실시양태에서, 페닐 고리의 3', 4', 5', 또는 6'-위치의 모이어티 가 화학식: 인 경우, R2a는 Me가 아니다. 특정 실시양태에서, 페닐 고리의 3', 4', 5', 또는 6'-위치의 모이어티 가 화학식: 인 경우, R2a는 치환 또는 비치환된 메틸이 아니다. 특정 실시양태에서, 페닐 고리의 3', 4', 5', 또는 6'-위치의 모이어티 가 화학식: 인 경우, R2a는 비치환된 C1-6 알킬이 아니다. 특정 실시양태에서, 각 경우의 x가 1, 2, 3, 또는 4이고, 각 경우의 n이 2이고, 각 경우의 y가 0인 경우, 각 경우의 R2는 -CH2OH, -C(=O)OH, 또는 -C(=O)OR2a이다. 특정 실시양태에서, 페닐 고리의 4'-위치가 모이어티 로 치환되는 경우, R2는 -CH2OR2a, -C(=O)OH, 또는 -C(=O)OR2a이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이고, 여기서 x는 1, 2, 3, 4, 5, 6, 7, 또는 8이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이고, 여기서 x는 1, 2, 3, 4, 5, 6, 7, 또는 8이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이고, 여기서 x는 1, 2, 3, 4, 5, 6, 7, 또는 8이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이고, 여기서 x는 1, 2, 3, 4, 5, 6, 7, 또는 8이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이고, 여기서 x는 1, 2, 3, 4, 5, 6, 7, 또는 8이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이고, 여기서 x는 1, 2, 3, 4, 5, 6, 7, 또는 8이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이고, 여기서 x는 1, 2, 3, 4, 5, 6, 7, 또는 8이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이고, 여기서 x는 1, 2, 3, 4, 5, 6, 7, 또는 8이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이고, 여기서 x는 1, 2, 3, 4, 5, 6, 7, 또는 8이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이고, 여기서 x는 1, 2, 3, 4, 5, 6, 7, 또는 8이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이고, 여기서 x는 1, 2, 3, 4, 5, 6, 7, 또는 8이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이고, 여기서 x는 1, 2, 3, 4, 5, 6, 7, 또는 8이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이고, 여기서 x는 1, 2, 3, 4, 5, 6, 7, 또는 8이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이고, 여기서 x는 1, 2, 3, 4, 5, 6, 7, 또는 8이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이고, 여기서 x는 1, 2, 3, 4, 5, 6, 7, 또는 8이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이고, 여기서 x는 1, 2, 3, 4, 5, 6, 7, 또는 8이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이고, 여기서 x는 1, 2, 3, 4, 5, 6, 7, 또는 8이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이고, 여기서 x는 1, 2, 3, 4, 5, 6, 7, 또는 8이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
특정 실시양태에서, 화학식 (I)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
화학식 (I)의 예시적인 화합물은 다음을 포함하나 이에 제한되지는 않는다:
및 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체 및 전구약물.
화학식 (I)의 추가의 예시적인 화합물은 다음을 포함하나 이에 제한되지는 않는다:
및 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체 및 전구약물.
화학식 (I)의 추가의 예시적인 화합물은 다음을 포함하나 이에 제한되지는 않는다:
및 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체 및 전구약물.
화학식 (I)의 추가의 예시적인 화합물은 다음을 포함하나 이에 제한되지는 않는다:
및 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체 및 전구약물.
화학식 (I)의 추가의 예시적인 화합물은 다음을 포함하나 이에 제한되지는 않는다:
및 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체 및 전구약물.
본 발명의 화합물은 다양한 염 형태로 제공될 수 있다. 특정 실시양태에서, 본 발명의 화합물은 알칼리 금속 염으로서 제공된다. 특정 실시양태에서, 본 발명의 화합물은 알칼리 토금속 염으로서 제공된다. 특정 실시양태에서, 본원에 기재된 화합물이 1개 이상의 -C(=O)OH 또는 -C(=O)SH 모이어티 (예를 들어, -Z-R9가 -OH 또는 -SH이고, R2가 -C(=O)OH임)를 포함하는 경우, 화합물은 염기에 의해 카르복실레이트 염 또는 티오카르복실레이트 염으로서 제공될 수 있다. 특정 실시양태에서, 염기는 베타인, 콜린 히드록시드, 디에탄올아민, 디에틸아민, 에탄올아민, 히드록시에틸모르폴린, 4-(2-히드록시에틸 모르폴린), 1-(2-히드록시에틸 피롤리딘), 1-(2-히드록시에틸)-피페리딘, 히드록시에틸 피롤리딘, 이미다존, 리신 (예를 들어, L-리신), 아르기닌 (예를 들어, L-아르기닌), 히스티딘 (예를 들어, L-히스티딘), N-메틸-D-글루카민 (NMG), N,N'-디벤질-에틸렌디아민, N,N'-디에틸-에탄올아민, 트리에탄올아민, 트로메타민, Ca(OH)2, Mg(OH)2, 마그네슘 아세테이트, LiOH, KOH, 칼륨 2-에틸헥사노에이트, NaOH, 아세트산나트륨, 나트륨 2-에틸헥사노에이트, Zn(OH)2, 아세트산아연, Zn(OH)2 및 Mg(OH)2의 혼합물, 또는 피페라진이다. 특정 실시양태에서, 본원에 기재된 염은 리튬 염 (예를 들어, 모노-리튬 염 또는 디-리튬 염)이다. 특정 실시양태에서, 본원에 기재된 염은 나트륨 염 (예를 들어, 모노-나트륨 염 또는 디-나트륨 염)이다. 특정 실시양태에서, 본원에 기재된 염은 칼륨 염 (예를 들어, 모노-칼륨 염 또는 디-칼륨 염)이다. 특정 실시양태에서, 본원에 기재된 염은 아연 염 (예를 들어, 헤미-아연 염 또는 모노-아연 염)이다. 특정 실시양태에서, 본원에 기재된 염은 마그네슘 염 (예를 들어, 헤미-마그네슘 염 또는 모노-마그네슘 염)이다. 특정 실시양태에서, 본원에 기재된 염은 칼슘 염 (예를 들어, 헤미-칼슘 염 또는 모노-칼슘 염)이다.
본원에 기재된 염에서 양이온 (예를 들어, Li+, Na+, K+, Mg2+, Mg(OH)+, Ca2+, Ca(OH)+, Zn2+, 또는 Zn(OH)+) 및 음이온 (예를 들어, 1개 이상의 -C(=O)OH 또는 -C(=O)SH 모이어티를 포함하는 본원에 기재된 화합물 (예를 들어, -Z-R9가 -OH 또는 -SH이고, R2가 -C(=O)OH)임)은 1:1 몰비로 결합할 수 있다. 염에서 양이온 및 음이온의 형식 전하의 합이 약 0인 한, 다른 몰비 (예를 들어, 1:1.5, 1:2, 1:3, 및 2:1 (양이온 : 음이온))가 또한 가능하다.
화학식 (I)의 추가의 예시적인 화합물은 다음을 포함하나 이에 제한되지는 않는다:
및 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체 및 전구약물.
화학식 (I)의 추가의 예시적인 화합물은 다음을 포함하나 이에 제한되지는 않는다:
및 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체 및 전구약물.
화학식 (I)의 추가의 예시적인 화합물은 다음을 포함하나 이에 제한되지는 않는다:
및 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체 및 전구약물.
화학식 (I)의 추가의 예시적인 화합물은 다음을 포함하나 이에 제한되지는 않는다:
및 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체 및 전구약물.
화학식 (I)의 추가의 예시적인 화합물은 다음을 포함하나 이에 제한되지는 않는다:
및 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체 및 전구약물.
화학식 (I)의 추가의 예시적인 화합물은 다음을 포함하나 이에 제한되지는 않는다:
및 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체 및 전구약물.
특정 실시양태에서, 본원에 기재된 화합물은 화학식 (I)의 화합물, 또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다. 특정 실시양태에서, 본원에 기재된 화합물은 화학식 (I)의 화합물, 또는 그의 제약상 허용되는 염 또는 입체이성질체이다. 특정 실시양태에서, 본원에 기재된 화합물은 화학식 (I)의 화합물, 또는 그의 제약상 허용되는 염이다.
본 개시내용의 또 다른 측면은 화학식 (II)의 화합물 또는 그의 제약상 허용되는 염에 관한 것이다:
여기서
각 경우의 RC1은 독립적으로 -(CH2)hORA1, 또는 -(CH2)hC(=O)ORA1이고, 여기서 각 경우의 RA1은 독립적으로 수소, 치환 또는 비치환된 알킬, 또는 산소 보호기이며, 단 RC1이 -(CH2)hC(=O)ORA1인 경우 h는 0이 아니고, RA1은 수소가 아니며;
각 경우의 RC2는 독립적으로 수소, 할로겐, 치환 또는 비치환된 C1-6 알킬, -CN, -NO2, -ORX, 또는 -N(RY)2이고;
각 경우의 RC3은 독립적으로 수소, 알킬, 또는 산소 보호기이고;
RX는 수소, 치환 또는 비치환된 C1-6 알킬, 또는 산소 보호기이고;
각 경우의 RY는 독립적으로 수소, 치환 또는 비치환된 C1-6 알킬, 질소 보호기이거나, 또는 임의로 2개의 RY가 개입 원자와 함께 치환 또는 비치환된 헤테로시클릴 또는 치환 또는 비치환된 헤테로아릴을 형성하고;
각 경우의 h는 독립적으로 0, 1, 2, 3, 4, 5, 6, 7, 또는 8이고;
각 경우의 j는 독립적으로 0, 1, 2, 3, 또는 4이다.
화학식 (II)는 1개 이상의 경우의 치환기 RC1을 포함한다. 특정 실시양태에서, 적어도 1개 경우의 RC1은 화학식: -(CH2)hORA1이고, 여기서 각 경우의 RA1은 독립적으로 수소, 치환 또는 비치환된 알킬 또는 산소 보호기이다. 특정 실시양태에서, 적어도 1개 경우의 RC1은 -(CH2)hOH이고, 여기서 h는 0, 1, 2, 3, 4, 5, 6, 7, 또는 8이다. 특정 실시양태에서, h는 0이다. 특정 실시양태에서, h는 1이다. 특정 실시양태에서, h는 2이다. 특정 실시양태에서, h는 3이다. 특정 실시양태에서, h는 4이다. 특정 실시양태에서, h는 5이다. 특정 실시양태에서, h는 6이다. 특정 실시양태에서, h는 7이다. 특정 실시양태에서, h는 8이다. 특정 실시양태에서, 적어도 1개 경우의 RC1은 -OH이다. 특정 실시양태에서, RA1은 수소이다. 특정 실시양태에서, RA1은 치환 또는 비치환된 C1-6 알킬 (예를 들어, 메틸 또는 에틸)이다. 특정 실시양태에서, 적어도 1개 경우의 RA1은 메틸이다. 특정 실시양태에서, 적어도 1개 경우의 RA1은 치환된 메틸 (예를 들어, -CF3, -CH2OH, 또는 Bn)이다. 특정 실시양태에서, 적어도 1개 경우의 RA1은 비치환된 에틸, 치환된 에틸 (예를 들어, 퍼플루오로에틸), 비치환된 프로필 (예를 들어, n-Pr 또는 i-Pr), 치환된 프로필 (예를 들어, 퍼플루오로프로필), 비치환된 부틸, 또는 치환된 부틸 (예를 들어, 퍼플루오로부틸)이다. 특정 실시양태에서, 적어도 1개 경우의 RC1은 -OMe 또는 -OEt이다. 특정 실시양태에서, RA1은 산소 보호기 (예를 들어, 실릴, TBDPS, TBDMS, TIPS, TES, TMS, MOM, THP, t-Bu, Bn, 알릴, 아세틸, 피발로일, 또는 벤조일)이다. 특정 실시양태에서, 적어도 1개 경우의 RC1은 화학식: -(CH2)hC(=O)ORA1이고, 여기서 각 경우의 RA1은 독립적으로 수소, 치환 또는 비치환된 알킬, 또는 산소 보호기이며, 단 RC1이 -(CH2)hC(=O)ORA1인 경우 h는 0이 아니고, RA1은 수소가 아니다. 특정 실시양태에서, 적어도 1개 경우의 RA1은 -(CH2)C(=O)ORA1 (예를 들어, -(CH2)C(=O)OH, -(CH2)C(=O)O(치환 또는 비치환된 C1-6 알킬) (예를 들어, -OMe, -OCF3, -OEt, -OPr, -OBu, 또는 -OBn), 또는 -(CH2)C(=O)O(치환 또는 비치환된 페닐) (예를 들어, -(CH2)C(=O)OPh))이다. 특정 실시양태에서, 적어도 1개 경우의 RC1은 -(CH2)C(=O)OMe이다. 특정 실시양태에서, 적어도 1개 경우의 RC1은 -(CH2)C(=O)OEt이다.
화학식 (II)는 1개 이상의 경우의 치환기 RC2를 포함한다. 특정 실시양태에서, j는 0이다. 특정 실시양태에서, j는 1이다. 특정 실시양태에서, j는 2이다. 특정 실시양태에서, j는 3이다. 특정 실시양태에서, j는 4이다. 특정 실시양태에서, 적어도 1개 경우의 RC2는 수소이다. 특정 실시양태에서, 적어도 1개 경우의 RC2는 할로겐 (예를 들어, F, Cl, Br, 또는 I)이다. 특정 실시양태에서, 적어도 1개 경우의 RC2는 F이다. 특정 실시양태에서, 적어도 1개 경우의 RC2는 Cl이다. 특정 실시양태에서, 적어도 1개 경우의 RC2는 치환 또는 비치환된 C1-6 알킬이다. 특정 실시양태에서, 적어도 1개 경우의 RC2는 메틸이다. 특정 실시양태에서, 적어도 1개 경우의 RC2는 치환된 메틸 (예를 들어, -CF3, -CH2OH, 또는 Bn)이다. 특정 실시양태에서, 적어도 1개 경우의 RC2는 비치환된 에틸, 치환된 에틸 (예를 들어, 퍼플루오로에틸), 비치환된 프로필 (예를 들어, n-Pr 또는 i-Pr), 치환된 프로필 (예를 들어, 퍼플루오로프로필), 비치환된 부틸, 또는 치환된 부틸 (예를 들어, 퍼플루오로부틸)이다. 특정 실시양태에서, 적어도 1개 경우의 RC2는 -CN이다. 특정 실시양태에서, 적어도 1개 경우의 RC2는 -NO2이다. 특정 실시양태에서, 적어도 1개 경우의 RC2는 -ORX (예를 들어, -OH, -O(치환 또는 비치환된 C1-6 알킬) (예를 들어, -OMe, -OCF3, -OEt, -OPr, -OBu, 또는 -OBn), 또는 -O(치환 또는 비치환된 페닐) (예를 들어, -OPh))이고, 여기서 RX는 수소, 치환 또는 비치환된 C1-6 알킬, 또는 산소 보호기이다. 특정 실시양태에서, 적어도 1개 경우의 RC2는 -OH이다. 특정 실시양태에서, 적어도 1개 경우의 RC2는 -OMe이다. 특정 실시양태에서, 적어도 1개 경우의 RC2는 -OEt이다. 특정 실시양태에서, 적어도 1개 경우의 RC2는 -N(RY)2 (예를 들어, -NH2, -NH(치환 또는 비치환된 C1-6 알킬) (예를 들어, -NHMe), 또는 -N(치환 또는 비치환된 C1-6 알킬)-(치환 또는 비치환된 C1-6 알킬) (예를 들어, -NMe2))이고, 여기서 각 경우의 RY는 독립적으로 수소, 치환 또는 비치환된 C1-6 알킬, 질소 보호기이거나, 또는 임의로 2개의 RY가 개입 원자와 함께 치환 또는 비치환된 헤테로시클릴 또는 치환 또는 비치환된 헤테로아릴을 형성한다. 특정 실시양태에서, 적어도 1개 경우의 RC2는 -NMe2이다. 특정 실시양태에서, 적어도 1개 경우의 RC2는 -NEt2이다. 특정 실시양태에서, 2개의 경우의 RY는 개입 원자와 함께 헤테로시클릭 고리에 0, 1, 또는 2개의 이중 결합을 포함하는 치환 또는 비치환된 5- 내지 14-원 모노시클릭 또는 비시클릭 헤테로시클릭 고리를 형성하고, 여기서 헤테로시클릭 고리의 1, 2, 또는 3개의 원자는 독립적으로 질소, 산소, 또는 황이다.
화학식 (II)는 1개 이상의 경우의 치환기 RC3을 포함한다. 특정 실시양태에서, 적어도 1개 경우의 RC3은 수소이다. 특정 실시양태에서, 적어도 1개 경우의 RC3은 치환 또는 비치환된 알킬이다. 특정 실시양태에서, 적어도 1개 경우의 RC3은 치환 또는 비치환된 C1-6 알킬이다. 특정 실시양태에서, 적어도 1개 경우의 RC3은 Me이다. 특정 실시양태에서, 적어도 1개 경우의 RC3은 치환된 메틸 (예를 들어, -CF3, -CH2OH, 또는 Bn)이다. 특정 실시양태에서, 적어도 1개 경우의 RC3은 Et, 치환된 에틸 (예를 들어, 퍼플루오로에틸), Pr (예를 들어, n-Pr 또는 i-Pr), 치환된 프로필 (예를 들어, 퍼플루오로프로필), Bu, 또는 치환된 부틸 (예를 들어, 퍼플루오로부틸)이다. 특정 실시양태에서, 적어도 1개 경우의 RC3은 산소 보호기 (예를 들어, 실릴, TBDPS, TBDMS, TIPS, TES, TMS, MOM, THP, t-Bu, Bn, 알릴, 아세틸, 피발로일, 또는 벤조일)이다.
특정 실시양태에서, 화학식 (II)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
특정 실시양태에서, 화학식 (II)의 화합물은 화학식:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다.
화학식 (II)의 예시적인 화합물은 다음을 포함하나 이에 제한되지는 않는다:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물.
화학식 (II)의 예시적인 화합물은 다음을 을 포함하나 이에 제한되지는 않는다:
또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물.
특정 실시양태에서, 본원에 기재된 화합물은 화학식 (II)의 화합물, 또는 그의 제약상 허용되는 염, 용매화물, 수화물, 다형체, 공-결정, 호변이성질체, 입체이성질체, 동위원소 표지된 유도체, 또는 전구약물이다. 특정 실시양태에서, 본원에 기재된 화합물은 화학식 (II)의 화합물, 또는 그의 제약상 허용되는 염 또는 입체이성질체이다. 특정 실시양태에서, 본원에 기재된 화합물은 화학식 (II)의 화합물, 또는 그의 제약상 허용되는 염이다.
제약 조성물, 키트 및 투여
본 발명은 본 발명의 화합물, 및 임의로 제약상 허용되는 부형제를 포함하는 제약 조성물을 제공한다. 제약 조성물은 대상체, 세포, 조직, 또는 생물학적 샘플에서 금속 (예를 들어, 철 또는 또 다른 금속)을 킬레이트화하고, 그의 대상체에서의 질환을 치료하고, 질환의 예방을 필요로 하는 대상체에서 질환을 예방하고, 대상체에서 바이오필름의 형성을 치료, 감소, 또는 방지하거나, 대상에서 바이오필름의 형성을 감소 또는 방지하는데 유용할 수 있다. 특정 실시양태에서, 본 발명의 화합물은 화학식 (I)의 화합물, 또는 그의 제약상 허용되는 염이다. 특정 실시양태에서, 본 발명의 화합물은 화학식 (II)의 화합물, 또는 그의 제약상 허용되는 염이다. 특정 실시양태에서, 본 발명의 화합물은 제약 조성물 중에 유효량으로 제공된다. 특정 실시양태에서, 유효량은 치료 유효량이다. 특정 실시양태에서, 유효량은 예방 유효량이다.
본원에 기재된 제약 조성물은 약리학 기술분야에 공지된 임의의 방법에 의해 제조될 수 있다. 일반적으로, 이러한 정제용 방법은 본 발명의 화합물 (즉, "활성 성분")을 담체 또는 부형제, 및/또는 1종 이상의 다른 보조 성분과 회합하도록 한 다음, 필요한 경우에 및/또는 바람직한 경우에, 생성물을 목적하는 단일- 또는 다중-용량 단위로 성형 및/또는 포장하는 단계를 포함한다.
제약 조성물은 단일 단위 용량으로서 및/또는 복수의 단일 단위 용량으로서 벌크로 제조, 포장 및/또는 판매될 수 있다. "단위 용량"은 미리 결정된 양의 활성 성분을 포함하는 제약 조성물의 개별적 양이다. 활성 성분의 양은 일반적으로 대상체에게 투여될 활성 성분의 투여량 및/또는 이러한 투여량의 편리한 분획, 예컨대 예를 들어 이러한 투여량의 1/2 또는 1/3과 동일하다.
본 발명의 제약 조성물 중의 활성 성분, 제약상 허용되는 부형제, 및/또는 임의의 추가의 성분의 상대량은 치료할 대상체의 정체성, 크기, 및/또는 상태에 따라 및 추가로 조성물이 투여되는 경로에 따라 달라질 것이다. 예로서, 조성물은 0.1% 내지 100% (w/w) 활성 성분을 포함할 수 있다.
제공된 제약 조성물의 제조에 사용되는 제약상 허용되는 부형제는 불활성 희석제, 분산제 및/또는 과립화제, 표면 활성제 및/또는 유화제, 붕해제, 결합제, 보존제, 완충제, 윤활제 및/또는 오일을 포함한다. 부형제, 예컨대 코코아 버터 및 좌제 왁스, 착색제, 코팅제, 감미제, 향미제 및 퍼퓸제가 또한 조성물 중에 존재할 수 있다.
예시적인 희석제는 탄산칼슘, 탄산나트륨, 인산칼슘, 인산이칼슘, 황산칼슘, 인산수소칼슘, 인산나트륨 락토스, 수크로스, 셀룰로스, 미세결정질 셀룰로스, 카올린, 만니톨, 소르비톨, 이노시톨, 염화나트륨, 건조 전분, 옥수수 전분, 분말화 당, 및 그의 혼합물을 포함한다.
예시적인 과립화제 및/또는 분산제는 감자 전분, 옥수수 전분, 타피오카 전분, 소듐 스타치 글리콜레이트, 점토, 알긴산, 구아 검, 시트러스 펄프, 한천, 벤토나이트, 셀룰로스 및 목재 제품, 천연 스폰지, 양이온-교환 수지, 탄산칼슘, 실리케이트, 탄산나트륨, 가교 폴리(비닐-피롤리돈) (크로스포비돈), 소듐 카르복시메틸 전분 (소듐 스타치 글리콜레이트), 카르복시메틸 셀룰로스, 가교 소듐 카르복시메틸 셀룰로스 (크로스카르멜로스), 메틸셀룰로스, 예비젤라틴화 전분 (전분 1500), 미세결정질 전분, 수불용성 전분, 칼슘 카르복시메틸 셀룰로스, 규산알루미늄마그네슘 (비검), 소듐 라우릴 술페이트, 4급 암모늄 화합물, 및 그의 혼합물을 포함한다.
예시적인 표면 활성제 및/또는 유화제는 천연 유화제 (예를 들어, 아카시아, 한천, 알긴산, 알긴산나트륨, 트라가칸트, 콘드룩스, 콜레스테롤, 크산탄, 펙틴, 젤라틴, 난황, 카세인, 양모 지방, 콜레스테롤, 왁스, 및 레시틴), 콜로이드성 점토 (예를 들어, 벤토나이트 (규산알루미늄) 및 비검 (규산알루미늄마그네슘)), 장쇄 아미노산 유도체, 고분자량 알콜 (예를 들어, 스테아릴 알콜, 세틸 알콜, 올레일 알콜, 트리아세틴 모노스테아레이트, 에틸렌 글리콜 디스테아레이트, 글리세릴 모노스테아레이트, 및 프로필렌 글리콜 모노스테아레이트, 폴리비닐 알콜), 카르보머 (예를 들어, 카르복시 폴리메틸렌, 폴리아크릴산, 아크릴산 중합체, 및 카르복시비닐 중합체), 카라기난, 셀룰로스 유도체 (예를 들어, 카르복시메틸셀룰로스 소듐, 분말화 셀룰로스, 히드록시메틸 셀룰로스, 히드록시프로필 셀룰로스, 히드록시프로필 메틸셀룰로스, 메틸셀룰로스), 소르비탄 지방산 에스테르 (예를 들어, 폴리옥시에틸렌 소르비탄 모노라우레이트 (트윈(Tween) 20), 폴리옥시에틸렌 소르비탄 (트윈 60), 폴리옥시에틸렌 소르비탄 모노올레에이트 (트윈 80), 소르비탄 모노팔미테이트 (스팬(Span) 40), 소르비탄 모노스테아레이트 (스팬 60), 소르비탄 트리스테아레이트 (스팬 65), 글리세릴 모노올레에이트, 소르비탄 모노올레에이트 (스팬 80)), 폴리옥시에틸렌 에스테르 (예를 들어, 폴리옥시에틸렌 모노스테아레이트 (미르즈(Myrj) 45), 폴리옥시에틸렌 수소화 피마자 오일, 폴리에톡실화 피마자 오일, 폴리옥시메틸렌 스테아레이트, 및 솔루톨), 수크로스 지방산 에스테르, 폴리에틸렌 글리콜 지방산 에스테르 (예를 들어, 크레모포르(Cremophor)™), 폴리옥시에틸렌 에테르, (예를 들어, 폴리옥시에틸렌 라우릴 에테르 (브리즈(Brij) 30)), 폴리(비닐-피롤리돈), 디에틸렌 글리콜 모노라우레이트, 트리에탄올아민 올레에이트, 올레산나트륨, 올레산칼륨, 에틸 올레에이트, 올레산, 에틸 라우레이트, 소듐 라우릴 술페이트, 플루로닉(Pluronic) F-68, 폴록사머(Poloxamer) 188, 세트리모늄 브로마이드, 세틸피리디늄 클로라이드, 벤즈알코늄 클로라이드, 도큐세이트 소듐, 및/또는 그의 혼합물을 포함한다.
예시적인 결합제는 전분 (예를 들어, 옥수수 전분 및 전분 페이스트), 젤라틴, 당 (예를 들어, 수크로스, 글루코스, 덱스트로스, 덱스트린, 당밀, 락토스, 락티톨, 만니톨 등), 천연 및 합성 검 (예를 들어, 아카시아, 알긴산나트륨, 아이리쉬 모스의 추출물, 판워 검, 가티 검, 이사폴 허스크의 점액, 카르복시메틸셀룰로스, 메틸셀룰로스, 에틸셀룰로스, 히드록시에틸셀룰로스, 히드록시프로필 셀룰로스, 히드록시프로필 메틸셀룰로스, 미세결정질 셀룰로스, 셀룰로스 아세테이트, 폴리(비닐-피롤리돈), 규산알루미늄마그네슘 (비검), 및 라치 아라보갈락탄), 알기네이트, 폴리에틸렌 옥시드, 폴리에틸렌 글리콜, 무기 칼슘 염, 규산, 폴리메타크릴레이트, 왁스, 물, 알콜, 및/또는 그의 혼합물을 포함한다.
예시적인 보존제는 항산화제, 킬레이트화제, 항미생물 보존제, 항진균 보존제, 알콜 보존제, 산성 보존제, 및 다른 보존제를 포함한다.
예시적인 항산화제는 알파 토코페롤, 아스코르브산, 아스코르빌 팔미테이트, 부틸화 히드록시아니솔, 부틸화 히드록시톨루엔, 모노티오글리세롤, 메타중아황산칼륨, 프로피온산, 프로필 갈레이트, 아스코르브산나트륨, 중아황산나트륨, 메타중아황산나트륨, 및 아황산나트륨을 포함한다.
예시적인 킬레이트화제는 에틸렌디아민테트라아세트산 (EDTA) 및 그의 염 및 수화물 (예를 들어, 에데트산나트륨, 에데트산이나트륨, 에데트산삼나트륨, 에데트산이나트륨 칼슘, 에데트산 이칼륨 등), 시트르산 및 그의 염 및 수화물 (예를 들어, 시트르산 1수화물), 푸마르산 및 그의 염 및 수화물, 말산 및 그의 염 및 수화물, 인산 및 그의 염 및 수화물, 및 타르타르산 및 그의 염 및 수화물을 포함한다. 예시적인 항미생물 보존제는 벤즈알코늄 클로라이드, 벤제토늄 클로라이드, 벤질 알콜, 브로노폴, 세트리미드, 세틸피리디늄 클로라이드, 클로르헥시딘, 클로로부탄올, 클로로크레졸, 클로로크실레놀, 크레졸, 에틸 알콜, 글리세린, 헥세티딘, 이미드우레아, 페놀, 페녹시에탄올, 페닐에틸 알콜, 질산페닐제2수은, 프로필렌 글리콜, 및 티메로살을 포함한다.
예시적인 항진균 보존제는 부틸 파라벤, 메틸 파라벤, 에틸 파라벤, 프로필 파라벤, 벤조산, 히드록시벤조산, 벤조산칼륨, 소르브산칼륨, 벤조산나트륨, 프로피온산나트륨, 및 소르브산을 포함한다.
예시적인 알콜 보존제는 에탄올, 폴리에틸렌 글리콜, 페놀, 페놀계 화합물, 비스페놀, 클로로부탄올, 히드록시벤조에이트, 및 페닐에틸 알콜을 포함한다.
예시적인 산성 보존제는 비타민 A, 비타민 C, 비타민 E, 베타-카로틴, 시트르산, 아세트산, 데히드로아세트산, 아스코르브산, 소르브산, 및 피트산을 포함한다.
다른 보존제는 토코페롤, 토코페롤 아세테이트, 데테르옥심 메실레이트, 세트리미드, 부틸화 히드록시아니솔 (BHA), 부틸화 히드록시톨루엔 (BHT), 에틸렌디아민, 소듐 라우릴 술페이트 (SLS), 나트륨 라우릴 에테르 술페이트 (SLES), 중아황산나트륨, 메타중아황산나트륨, 아황산칼륨, 메타중아황산칼륨, 글리단트 플러스(Glydant Plus), 페노닙(Phenonip), 메틸파라벤, 저몰(Germall) 115, 게르마벤(Germaben) II, 네올론(Neolone), 카톤(Kathon) 및 에욱실(Euxyl)을 포함한다. 특정 실시양태에서, 보존제는 항산화제이다. 다른 실시양태에서, 보존제는 킬레이트화제이다.
예시적인 완충제는 시트레이트 완충제 용액, 아세테이트 완충제 용액, 포스페이트 완충제 용액, 염화암모늄, 탄산칼슘, 염화칼슘, 시트르산칼슘, 글루비온산칼슘, 글루셉트산칼슘, 글루콘산칼슘, D-글루콘산, 글리세로인산칼슘, 락트산칼슘, 프로판산, 레불린산칼슘, 펜탄산, 이염기성 인산칼슘, 인산, 삼염기성 인산칼슘, 수산화인산칼슘, 아세트산칼륨, 염화칼륨, 글루콘산칼륨, 칼륨 혼합물, 이염기성 인산칼륨, 일염기성 인산칼륨, 인산칼륨 혼합물, 아세트산나트륨, 중탄산나트륨, 염화나트륨, 시트르산나트륨, 락트산나트륨, 이염기성 인산나트륨, 일염기성 인산나트륨, 인산나트륨 혼합물, 트로메타민, 수산화마그네슘, 수산화알루미늄, 알긴산, 발열원 무함유 물, 등장성 염수, 링거액, 에틸 알콜, 및 그의 혼합물을 포함한다.
예시적인 윤활제는 스테아르산마그네슘, 스테아르산칼슘, 스테아르산, 실리카, 활석, 맥아, 글리세릴 베하네이트, 수소화 식물성 오일, 폴리에틸렌 글리콜, 벤조산나트륨, 아세트산나트륨, 염화나트륨, 류신, 마그네슘 라우릴 술페이트, 소듐 라우릴 술페이트, 및 그의 혼합물을 포함한다.
예시적인 천연 오일은 아몬드, 살구 커넬, 아보카도, 바바수, 베르가모트, 블랙 커런트 종자, 보리지, 케이드, 카모마일, 카놀라, 캐러웨이, 카르나우바, 피마자, 시나몬, 코코아 버터, 코코넛, 대구 간, 커피, 옥수수, 목화 종자, 에뮤, 유칼립투스, 달맞이꽃, 어류, 아마씨, 게라니올, 고드, 포도씨, 헤이즐넛, 히솝, 이소프로필 미리스테이트, 호호바, 쿠쿠이 넛, 라반딘, 라벤더, 레몬, 리트세아 쿠베바, 마카데미아 넛, 아욱, 망고씨, 메도우폼씨, 밍크, 넛멕, 올리브, 오렌지, 오렌지 라피, 팜, 팜핵, 복숭아 커넬, 땅콩, 양귀비씨, 호박씨, 평지씨, 쌀겨, 로즈마리, 홍화, 샌달우드, 사스쿠아나, 세이보리, 산자나무, 참깨, 시어 버터, 실리콘, 대두, 해바라기, 티트리, 엉겅퀴, 츠바키, 베티버, 호두, 및 밀 배아 오일을 포함한다. 예시적인 합성 오일은 부틸 스테아레이트, 카프릴산 트리글리세리드, 카프르산 트리글리세리드, 시클로메티콘, 디에틸 세바케이트, 디메티콘 360, 이소프로필 미리스테이트, 미네랄 오일, 옥틸도데칸올, 올레일 알콜, 실리콘 오일, 및 그의 혼합물을 포함하나 이에 제한되지는 않는다.
경구 및 비경구 투여를 위한 액체 투여 형태는 제약상 허용되는 에멀젼, 마이크로에멀젼, 용액, 현탁액, 시럽 및 엘릭시르를 포함한다. 활성 성분 뿐만 아니라, 액체 투여 형태는 관련 기술분야에서 통상적으로 사용되는 불활성 희석제, 예컨대, 예를 들어 물 또는 다른 용매, 가용화제 및 유화제, 예컨대 에틸 알콜, 이소프로필 알콜, 에틸 카르보네이트, 에틸 아세테이트, 벤질 알콜, 벤질 벤조에이트, 프로필렌 글리콜, 1,3-부틸렌 글리콜, 디메틸포름아미드, 오일 (예를 들어, 목화씨, 땅콩, 옥수수, 배아, 올리브, 피마자 및 참깨 오일), 글리세롤, 테트라히드로푸르푸릴 알콜, 폴리에틸렌 글리콜 및 소르비탄의 지방산 에스테르, 및 그의 혼합물을 포함할 수 있다. 불활성 희석제 이외에도, 경구 조성물은 아주반트, 예컨대 습윤제, 유화제 및 현탁화제, 감미제, 향미제, 및 퍼퓸제를 포함할 수 있다. 비경구 투여를 위한 특정 실시양태에서, 본 발명의 접합체는 가용화제, 예컨대 크레모포르™, 알콜, 오일, 변형 오일, 글리콜, 폴리소르베이트, 시클로덱스트린, 중합체 및 그의 혼합물과 혼합된다.
주사가능한 제제, 예를 들어 멸균 주사가능한 수성 또는 유질 현탁액은 관련 기술분야에 공지된 바에 따라 적합한 분산제 또는 습윤제 및 현탁화제를 사용하여 제제화될 수 있다. 멸균 주사가능한 제제는 또한 예를 들어 1,3-부탄디올 중의 용액으로서 비독성의 비경구로 허용되는 희석제 또는 용매 중의 멸균 주사가능한 용액, 현탁액 또는 에멀젼일 수 있다. 사용될 수 있는 허용되는 비히클 및 용매 중에는 물, 링거액, U.S.P. 및 등장성 염화나트륨 용액이 있다. 또한, 멸균 고정 오일은 통상적으로 용매 또는 현탁 매질로서 사용된다. 이러한 목적을 위해 합성 모노- 또는 디글리세리드를 포함한 임의의 무자극 고정 오일이 사용될 수 있다. 추가로, 지방산 예컨대 올레산은 주사가능한 제제에 사용된다.
주사가능한 제제는, 예를 들어 박테리아-잔류 필터를 통한 여과에 의해, 또는 사용 전에 멸균수 또는 다른 멸균 주사가능한 매질 중에 용해되거나 또는 분산될 수 있는 멸균 고체 조성물 형태로 멸균제를 혼입함으로써 멸균될 수 있다.
약물의 효과를 연장시키기 위해, 피하 또는 근육내 주사로부터의 약물의 흡수를 늦추는 것이 종종 바람직하다. 이는 불량한 수용해도를 갖는 결정질 또는 무정형 물질의 액체 현탁액의 사용에 의해 달성될 수 있다. 이어서, 약물의 흡수 속도는 그의 용해 속도에 따라 달라지며, 이는 또한 결정 크기 및 결정질 형태에 따라 달라질 수 있다. 대안적으로, 비경구로 투여된 약물 형태의 지연된 흡수는 약물을 오일 비히클 중에 용해 또는 현탁시킴으로써 달성된다.
직장 또는 질 투여를 위한 조성물은 전형적으로 본 발명의 접합체를, 주위 온도에서는 고체이지만 체온에서는 액체이고 따라서 직장 또는 질강에서 용융되어 활성 성분을 방출하는 적합한 비-자극성 부형제 또는 담체, 예컨대 코코아 버터, 폴리에틸렌 글리콜 또는 좌제 왁스와 혼합하여 제조될 수 있는 좌제이다.
본원에 개시된 화합물, 또는 그의 제약상 허용되는 염, 호변이성질체, 입체이성질체, 용매화물, 수화물, 또는 다형체가 있는 그대로 투여되는 것이 가능할 수 있으며, 그들을 제약 제제 또는 투여로서 제공하는 것이 가능하다. 경구 투여를 위한 고체 투여 형태는 캡슐, 정제, 환제, 분말, 및 과립을 포함한다. 이러한 고체 투여 형태에서, 활성 성분은 적어도 1종의 불활성, 제약상 허용되는 부형제 또는 담체 예컨대 시트르산나트륨 또는 인산이칼슘 및/또는 (a) 충전제 또는 증량제 예컨대 전분, 락토스, 수크로스, 글루코스, 만니톨, 및 규산; (b) 결합제 예컨대, 예를 들어, 카르복시메틸셀룰로스, 알기네이트, 젤라틴, 폴리비닐피롤리디논, 수크로스, 및 아카시아; (c) 함습제 예컨대 글리세롤; (d) 붕해제 예컨대 한천, 탄산칼슘, 감자 또는 타피오카 전분, 알긴산, 특정 실리케이트, 및 탄산나트륨; (e) 용해 지연제 예컨대 파라핀; (f) 흡수 촉진제 예컨대 4급 암모늄 화합물; (g) 습윤제 예컨대, 예를 들어, 세틸 알콜 및 글리세롤 모노스테아레이트; (h) 흡수제 예컨대 카올린 및 벤토나이트 점토, 및 (i) 윤활제 예컨대 활석, 스테아르산칼슘, 스테아르산마그네슘, 고체 폴리에틸렌 글리콜, 소듐 라우릴 술페이트, 및 그의 혼합물을 포함한다. 캡슐, 정제 및 환제의 경우에, 투여 형태는 완충제를 포함할 수 있다.
유사한 유형의 고체 조성물은 부형제, 예컨대 락토스 또는 유당, 뿐만 아니라 고분자량 폴리에틸렌 글리콜 등을 사용하여 연질 및 경질-충전된 젤라틴 캡슐에서 충전제로서 사용될 수 있다. 정제, 당의정, 캡슐, 환제 및 과립의 고체 투여 형태는 코팅 및 쉘 예컨대 장용 코팅 및 제약 제제화 기술분야에 널리 공지된 다른 코팅에 의해 제조될 수 있다. 이들은 임의로 불투명화제를 포함할 수 있고, 장관의 특정 부분에서 임의로는 지연된 방식으로 활성 성분(들)만을 방출하거나 또는 활성 성분(들)을 우선적으로 방출하는 조성물일 수 있다. 사용될 수 있는 포매 조성물의 예는 중합체 물질 및 왁스를 포함한다. 유사한 유형의 고체 조성물은 부형제, 예컨대 락토스 또는 유당, 뿐만 아니라 고분자량 폴리에틸렌 글리콜 등을 사용하여 연질 및 경질-충전된 젤라틴 캡슐에서 충전제로서 사용될 수 있다.
활성 성분은 상기 언급된 바와 같은 하나 이상의 부형제와 함께 마이크로캡슐화된 형태일 수 있다. 정제, 당의정, 캡슐, 환제 및 과립의 고체 투여 형태는 코팅 및 쉘 예컨대 장용 코팅, 방출 제어 코팅 및 제약 제제화 기술분야에 널리 공지된 다른 코팅에 의해 제조될 수 있다. 이러한 고체 투여 형태에서 활성 성분은 적어도 1종의 불활성 희석제, 예컨대 수크로스, 락토스 또는 전분과 혼합될 수 있다. 이러한 투여 형태는, 통상적인 실시에서와 같이, 불활성 희석제 이외의 추가의 물질, 예를 들어 타정 윤활제 및 다른 타정 보조제, 예컨대 스테아르산마그네슘 및 미세결정질 셀룰로스를 포함할 수 있다. 캡슐, 정제 및 환제의 경우에, 투여 형태는 완충제를 포함할 수 있다. 이들은 임의로 불투명화제를 포함할 수 있고, 장관의 특정 부분에서 임의로는 지연된 방식으로 활성 성분(들)만을 방출하거나 또는 활성 성분(들)을 우선적으로 방출하는 조성물일 수 있다. 사용될 수 있는 포매 조성물의 예는 중합체 물질 및 왁스를 포함한다.
본 발명의 화합물의 국소 및/또는 경피 투여를 위한 투여 형태는 연고, 페이스트, 크림, 로션, 겔, 분말, 용액, 스프레이, 흡입제 및/또는 패치를 포함할 수 있다. 일반적으로, 활성 성분은 멸균 조건 하에 제약상 허용되는 담체 또는 부형제 및/또는 요구될 수 있는 경우에 임의의 필요한 보존제 및/또는 완충제와 혼합된다. 추가로, 본 발명은 활성 성분의 신체로의 제어된 전달을 제공하는 부가의 이점을 종종 갖는 경피 패치의 사용을 고려한다. 이러한 투여 형태는, 예를 들어 활성 성분을 적절한 매질 중에 용해 및/또는 분배함으로써 제조될 수 있다. 대안적으로 또는 추가로, 속도는 속도 제어 막을 제공하고/거나 활성 성분을 중합체 매트릭스 및/또는 겔 중에 분산시킴으로써 제어될 수 있다.
본원에 기재된 피내 제약 조성물을 전달하는데 사용하기에 적합한 장치는 짧은 바늘 장치를 포함한다. 피내 조성물은 피부 내로의 바늘의 유효 침투 길이를 제한하는 장치에 의해 투여될 수 있다. 대안적으로 또는 추가로, 통상적인 시린지가 피내 투여의 전형적 망투 방법에 사용될 수 있다. 각질층을 뚫고 진피에 도달하는 제트를 생성하는 액체 제트 분사기를 통해 및/또는 바늘을 통해 액체 제제를 진피에 전달하는 제트 주사 장치가 적합하다. 압축 기체를 사용하여 피부의 외부 층을 통해 진피까지 분말 형태의 화합물을 가속시키는 탄도 분말/입자 전달 장치가 적합하다.
국소 투여에 적합한 제제는 액체 및/또는 반 액체 제제, 예컨대 도찰제, 로션, 수중유 및/또는 유중수 에멀젼, 예컨대 크림, 연고 및/또는 페이스트, 및/또는 용액 및/또는 현탁액을 포함하나 이에 제한되지는 않는다. 국소적으로 투여가능한 제제는, 예를 들어 약 1% 내지 약 10% (w/w)의 활성 성분을 포함할 수 있지만, 활성 성분의 농도는 용매 중 활성 성분의 용해도 한계만큼 높을 수 있다. 국소 투여를 위한 제제는 본원에 기재된 추가의 성분 중 1종 이상을 추가로 포함할 수 있다.
저비등 추진제는 일반적으로 대기압에서 65℉ 미만의 비점을 갖는 액체 추진제를 포함한다. 일반적으로, 추진제는 조성물의 50 내지 99.9% (w/w)를 구성할 수 있고, 활성 성분은 조성물의 0.1 내지 20% (w/w)를 구성할 수 있다. 추진제는 추가의 성분, 예컨대 액체 비-이온성 및/또는 고체 음이온성 계면활성제 및/또는 고체 희석제 (이는 활성 성분을 포함하는 입자와 동일한 정도의 입자 크기를 가질 수 있음)를 추가로 포함할 수 있다.
폐 전달을 위해 제제화된 본 발명의 제약 조성물은 용액 및/또는 현탁액의 액적 형태로 활성 성분을 제공할 수 있다. 이러한 제제는 활성 성분을 포함하는, 임의로 멸균된 수성 및/또는 묽은 알콜성 용액 및/또는 현탁액으로서 제조, 포장 및/또는 판매될 수 있고, 편리하게는 임의의 연무화 및/또는 분무화 장치를 사용하여 투여될 수 있다. 이러한 제제는 향미제, 예컨대 사카린 소듐, 휘발성 오일, 완충제, 표면 활성제, 및/또는 보존제, 예컨대 메틸히드록시벤조에이트를 포함하나 이에 제한되지는 않는 1종 이상의 추가의 성분을 추가로 포함할 수 있다. 이러한 투여 경로로 제공되는 액적은 약 0.1 내지 약 200 나노미터 범위의 평균 직경을 가질 수 있다.
폐 전달에 유용한 것으로 본원에 기재된 제제는 본 발명의 제약 조성물의 비강내 전달에 유용하다. 비강내 투여에 적합한 또 다른 제제는, 활성 성분을 포함하고 약 0.2 내지 500 마이크로미터의 평균 입자를 갖는 조대 분말이다. 이러한 제제는 비공에 근접하게 놓인 분말 용기로부터 비도를 통한 신속한 흡입에 의해 투여된다.
비강 투여에 적합한 제제는 예를 들어 약 0.1% (w/w)만큼 적게 및 100% (w/w)만큼 많은 활성 성분을 포함할 수 있으며, 본원에 기재된 하나 이상의 추가의 성분을 포함할 수 있다. 본 발명의 제약 조성물은 협측 투여를 위한 제제로 제조, 포장 및/또는 판매될 수 있다. 이러한 제제는, 예를 들어 통상적인 방법을 사용하여 제조된 정제 및/또는 로젠지 형태일 수 있고, 예를 들어 0.1 내지 20% (w/w)의 활성 성분을 함유할 수 있으며, 나머지는 경구로 용해가능한 및/또는 분해가능한 조성물 및 임의로 본원에 기재된 추가의 성분 중 1종 이상을 포함한다. 대안적으로, 협측 투여를 위한 제제는 활성 성분을 포함하는 분말 및/또는 에어로졸화 및/또는 분무화 용액 및/또는 현탁액을 포함할 수 있다. 이러한 분말화, 에어로졸화 및/또는 에어로졸화 제제는 분산되는 경우에, 약 0.1 내지 약 200 나노미터 범위의 평균 입자 및/또는 액적 크기를 가질 수 있고, 본원에 기재된 추가의 성분 중 1종 이상을 추가로 포함할 수 있다.
본 발명의 제약 조성물은 안과적 투여를 위한 제제로 제조, 포장, 및/또는 판매될 수 있다. 이러한 제제는, 예를 들어 수성 또는 유성 액체 담체 또는 부형제 중 활성 성분의 0.1-1.0% (w/w) 용액 및/또는 현탁액을 포함하는 점안제 형태일 수 있다. 이러한 점안제는 완충제, 염 및/또는 본원에 기재된 다른 추가의 성분 중 1종 이상을 추가로 포함할 수 있다. 다른 유용한 안과적으로 투여가능한 제제는 미세결정질 형태 및/또는 리포솜 제제로 활성 성분을 포함하는 것을 포함한다. 점이제 및/또는 점안제는 본 발명의 범위 내에 포함되는 것으로서 고려된다.
본원에 제공된 제약 조성물의 설명은 주로 인간에 대한 투여에 적합한 제약 조성물에 관한 것이지만, 이러한 조성물은 일반적으로 모든 종류의 동물에 대한 투여에도 적합함을 통상의 기술자는 이해할 것이다. 인간에 대한 투여에 적합한 제약 조성물을 변형시켜 조성물을 다양한 동물에 대한 투여에 적합하게 하는 것은 잘 이해되어 있고, 통상의 숙련된 수의학 약리학자는 이러한 변형을 통상의 실험으로 설계 및/또는 수행할 수 있다.
본원에 제공된 화합물은 전형적으로 투여의 용이성 및 투여량의 균일성을 위해 투여 단위 형태로 제제화된다. 그러나, 본원에 기재된 조성물의 총 1일 용법은 타당한 의학적 판단의 범주 내에서 의사에 의해 결정될 것임이 이해될 것이다. 임의의 특정한 대상체 또는 유기체에 대한 구체적인 치료상 유효한 용량 수준은 치료할 질환 및 장애의 중증도; 사용되는 특정 활성 성분의 활성; 사용되는 특정 조성물; 대상체의 연령, 체중, 전반적 건강, 성별 및 식이; 투여 시간, 투여 경로, 및 사용되는 특정 활성 성분의 배출 속도; 치료 지속기간; 사용되는 특정 활성 성분과 조합하여 또는 동시에 사용되는 약물; 및 의학 기술분야에 널리 공지된 유사 요인을 포함한 다양한 요인에 좌우될 것이다.
본원에 제공된 화합물 및 조성물은 경장 (예를 들어, 경구), 비경구, 정맥내, 근육내, 동맥내, 수질내, 척수강내, 피하, 뇌실내, 경피, 피내, 직장, 질내, 복강내, 국소 (분말, 연고, 크림 및/또는 점적제에 의해서와 같이), 점막, 비강, 협측, 설하를 포함한 임의의 경로에 의해; 기관내 점적주입, 기관지 점적주입 및/또는 흡입에 의해; 및/또는 경구 스프레이, 비강 스프레이 및/또는 에어로졸로서 투여될 수 있다. 구체적으로 고려되는 경로는 경구 투여, 정맥내 투여 (예를 들어, 전신 정맥내 주사), 혈액 및/또는 림프 공급을 통한 국한성 투여, 및/또는 이환 부위로의 직접 투여이다. 본 발명의 화합물 및 조성물은 또한 생체외 혈액과 혼합될 수 있고 생성된 혼합물은 대상체에게 (예를 들어, 정맥내로) 투여될 수 있다. 일반적으로, 가장 적절한 투여 경로는 작용제의 성질 (예를 들어, 위장관 환경에서의 그의 안정성) 및/또는 대상체의 상태 (예를 들어, 대상체가 경구 투여를 허용할 수 있는지의 여부)를 비롯한 다양한 인자에 좌우될 것이다.
유효량을 달성하기 위해 요구되는 화합물의 정확한 양은, 예를 들어 대상체의 종, 연령 및 일반적 상태, 부작용 또는 장애의 중증도, 특정한 화합물의 정체, 투여 방식 등에 따라 대상체마다 달라질 것이다. 유효량은 단일 용량 (예를 들어, 단일 경구 용량) 또는 다중 용량 (예를 들어, 다중 경구 용량) 내에 포함될 수 있다. 특정 실시양태에서, 다중 용량이 대상체에게 투여되거나 조직 또는 세포에 적용되는 경우에, 다중 용량 중 임의의 2회 용량은 상이하거나 실질적으로 동일한 양의 본원에 기재된 화합물을 포함한다. 특정 실시양태에서, 다중 용량이 대상체에게 투여되거나 조직 또는 세포에 적용되는 경우에, 다중 용량이 대상체에게 투여되거나 다중 용량이 조직 또는 세포에 적용되는 빈도는 1일 3회 용량, 1일 2회 용량, 1일 1회 용량, 격일 1회 용량, 3일마다 1회 용량, 매주 1회 용량, 2주마다 1회 용량, 3주마다 1회 용량, 또는 4주마다 1회 용량이다. 특정 실시양태에서, 다중 용량이 대상체에게 투여되거나 다중 용량이 조직 또는 세포에 적용되는 빈도는 1일에 1회 용량이다. 특정 실시양태에서, 다중 용량이 대상체에게 투여되거나 다중 용량이 조직 또는 세포에 적용되는 빈도는 1일에 2회 용량이다. 특정 실시양태에서, 다중 용량이 대상체에게 투여되거나 다중 용량이 조직 또는 세포에 적용되는 빈도는 1일에 3회 용량이다. 특정 실시양태에서, 다중 용량이 대상체에게 투여되거나 조직 또는 세포에 적용되는 경우에, 다중 용량의 최초 용량 및 최종 용량 사이의 지속기간은 1일, 2일, 4일, 1주, 2주, 3주, 1개월, 2개월, 3개월, 4개월, 6개월, 9개월, 1년, 2년, 3년, 4년, 5년, 7년, 10년, 15년, 20년 또는 대상체, 조직 또는 세포의 수명이다. 특정 실시양태에서, 다중 용량의 최초 용량과 최종 용량 사이의 지속기간은 3개월, 6개월, 또는 1년이다. 특정 실시양태에서, 다중 용량의 최초 용량과 최종 용량 사이의 지속기간은 대상체, 조직 또는 세포의 수명이다. 특정 실시양태에서, 본원에 기재된 용량 (예를 들어, 단일 용량, 또는 다중 용량 중 임의의 용량)은 독립적으로 본원에 기재된 화합물 0.1 μg 내지 1 μg, 0.001 mg 내지 0.01 mg, 0.01 mg 내지 0.1 mg, 0.1 mg 내지 1 mg, 1 mg 내지 3 mg, 3 mg 내지 10 mg, 10 mg 내지 30 mg, 30 mg 내지 100 mg, 100 mg 내지 300 mg, 300 mg 내지 1,000 mg, 또는 1 g 내지 10 g을 포함한다. 특정 실시양태에서, 본원에 기재된 용량은 독립적으로 본원에 기재된 화합물 1 mg 내지 3 mg을 포함한다. 특정 실시양태에서, 본원에 기재된 용량은 독립적으로 본원에 기재된 화합물 3 mg 내지 10 mg을 포함한다. 특정 실시양태에서, 본원에 기재된 용량은 독립적으로 본원에 기재된 화합물 10 mg 내지 30 mg을 포함한다. 특정 실시양태에서, 본원에 기재된 용량은 독립적으로 본원에 기재된 화합물 30 mg 내지 100 mg을 포함한다.
본원에 기재된 바와 같은 용량 범위는 제공되는 제약 조성물의 성인에 대한 투여 지침을 제공하는 것으로 인지될 것이다. 예를 들어, 유아 또는 청소년에게 투여되는 양은 의료 진료의 또는 통상의 기술자에 의해 결정될 수 있고, 성인에게 투여되는 양보다 더 적거나 그와 동일할 수 있다. 특정 실시양태에서, 본원에 기재된 용량은 체중이 70 kg인 성인 인간에 대한 용량이다.
본원에 기재된 화합물 또는 조성물은 1종 이상의 추가의 제약 작용제 (예를 들어, 치료적 및/또는 예방적 활성제)와 조합하여 투여될 수 있다. 화합물 또는 조성물은 그의 활성 (예를 들어, 질환의 치료를 필요로 하는 대상체에서 질환을 치료하고/거나, 질환의 예방을 필요로 하는 대상체에서 질환을 예방하고/거나, 질환의 발병 위험의 감소를 필요로 하는 대상체에서 질환을 발병할 위험을 감소시키고/거나, 대상체 또는 세포에서 단백질 키나제의 활성을 억제하는 활성 (예를 들어, 효력 및 효능))을 개선하고/거나, 생체이용률을 개선시키고/거나, 안전성을 개선시키고/거나, 약물 내성을 감소시키고/거나, 대사를 감소 및/또는 변형시키고/거나, 배출을 억제하고/거나, 대상체 또는 세포에서 분포를 변형시키는 추가의 제약 작용제와 조합되어 투여될 수 있다. 사용된 요법이 동일한 장애에 대해 목적하는 효과를 달성할 수 있고/거나, 상이한 효과를 달성할 수 있음이 또한 인지될 것이다. 특정 실시양태에서, 본원에 기재된 화합물 및 추가의 제약 작용제를 포함하는 본원에 기재된 제약 조성물은, 화합물 및 추가의 제약 작용제 중 하나를 포함하나 둘 다를 포함하는 것은 아닌 제약 조성물에서는 부재하는 상승작용적 효과를 나타낸다.
화합물 또는 조성물은 1종 이상의 추가의 제약 작용제 전에, 또는 후속으로 공동으로 투여될 수 있으며, 이는 화합물 또는 조성물과 상이하고, 예를 들어 조합 요법으로서 유용할 수 있다. 제약 작용제는 치료 활성제를 포함한다. 제약 작용제는 또한 예방 활성제를 포함한다. 제약 작용제는 유기 소분자, 예컨대 약물 화합물 (예를 들어, 미국 연방 규정집 (CFR)에서 제공된 바와 같이 미국 식품 의약품국에 의해 인간 또는 수의학적 사용을 위해 승인된 화합물), 펩티드, 단백질, 탄수화물, 모노사카라이드, 올리고사카라이드, 폴리사카라이드, 핵단백질, 뮤코단백질, 지단백질, 합성 폴리펩티드 또는 단백질, 단백질에 연결된 소분자, 당단백질, 스테로이드, 핵산, DNA, RNA, 뉴클레오티드, 뉴클레오시드, 올리고뉴클레오티드, 안티센스 올리고뉴클레오티드, 지질, 호르몬, 비타민, 및 세포를 포함한다. 특정 실시양태에서, 추가의 제약 작용제는 질환 (예를 들어, 증식성 질환, 혈액 질환, 신경계 질환, 통증성 상태, 정신 장애, 또는 대사 장애)를 치료 및/또는 예방하는데 유용한 제약 작용제이다. 각각의 추가의 제약 작용제는 그 제약 작용제에 대해 결정된 용량 및/또는 시간 스케줄로 투여될 수 있다. 추가의 제약 작용제는 또한 서로 함께 및/또는 본원에 기재된 화합물 또는 조성물과 함께 단일 용량으로 투여될 수 있거나 또는 상이한 용량으로 개별적으로 투여될 수 있다. 요법에 사용하기 위한 특정한 조합은 본원에 기재된 화합물과 추가의 제약 작용제(들)와의 상용성 및/또는 달성하려는 목적 치료 및/또는 예방 효과를 고려할 것이다. 일반적으로, 추가의 제약 작용제(들)는 이들이 개별적으로 이용되는 경우의 수준을 초과하지 않는 수준에서 조합되어 이용되는 것으로 예상된다. 일부 실시양태에서, 조합에 이용되는 수준은 개별적으로 이용되는 수준보다 더 낮을 것이다.
추가의 제약 작용제는 항증식제, 항암제, 항혈관신생제, 항염증제, 면역억제제, 항박테리아제, 항바이러스제, 심혈관제, 콜레스테롤-강하제, 항당뇨병제, 항알레르기제, 피임제 및 통증-완화제를 포함하나 이에 제한되지는 않는다. 특정 실시양태에서, 추가의 제약 작용제는 항증식제이다. 특정 실시양태에서, 추가의 제약 작용제는 항암제이다. 특정 실시양태에서, 추가의 제약 작용제는 항바이러스제이다. 특정 실시양태에서, 추가의 제약 작용제는 단백질 키나제의 결합제 또는 억제제이다. 특정 실시양태에서, 추가의 제약 작용제는 후성적 또는 전사 조정제 (예를 들어, DNA 메틸트랜스퍼라제 억제제, 히스톤 데아세틸라제 억제제 (HDAC 억제제), 리신 메틸트랜스퍼라제 억제제), 항유사분열 약물 (예를 들어, 탁산 및 빈카 알칼로이드), 호르몬 수용체 조정제 (예를 들어, 에스트로겐 수용체 조정제 및 안드로겐 수용체 조정제), 세포 신호전달 경로 억제제 (예를 들어, 티로신 키나제 억제제), 단백질 안정성 조정제 (예를 들어, 프로테아솜 억제제), Hsp90 억제제, 글루코코르티코이드, 모든-트랜스 레티노산, 및 분화를 촉진하는 다른 작용제로 이루어진 군으로부터 선택된다. 특정 실시양태에서, 추가의 제약 작용제는 철 킬레이트화제 (예를 들어, 데스페리옥사민 (DFO, DFX, 데페록사민, 데페록사민 메실레이트, 데스페리옥사민 B, 데스페랄(Desferal)®), 데페라시록스 (엑스자이드(Exjade)®), 디페리프론 (L1, 페리프록스(Ferriprox)®) 또는 페라렉스(Feralex)-G)이다. 특정 실시양태에서, 본원에 기재된 화합물 또는 제약 조성물은 수술, 방사선 요법, 이식 (예를 들어, 줄기 세포 이식, 골수 이식), 면역요법, 및 화학요법을 포함하나 이에 제한되지는 않는 항암 요법과 조합되어 투여될 수 있다.
또한, 본 발명은 키트 (예를 들어, 제약 팩)를 포괄한다. 키트는 본 발명의 화합물 또는 제약 조성물 및 제1 용기 (예를 들어, 바이알, 앰플, 병, 시린지 및/또는 분배기 패키지, 또는 다른 적합한 용기)를 포함할 수 있다. 일부 실시양태에서, 키트는, 예를 들어 본 발명의 화합물 또는 제약 조성물의 희석 또는 현탁을 위한 제약 부형제를 포함하는 제2 용기를 추가로 포함한다. 일부 실시양태에서, 제1 용기 및 제2 용기에 제공된 본 발명의 화합물 또는 제약 조성물은 조합되어 하나의 단위 투여 형태를 형성한다.
키트는 대상체, 세포, 조직, 또는 생물학적 샘플에서 금속 (예를 들어, 철 또는 또 다른 금속)을 킬레이트화하고, 그의 대상체에서 질환을 치료하고, 질환의 예방을 필요로 하는 대상체에서 질환을 예방하고, 대상체에서 바이오필름의 형성을 치료, 감소, 또는 방지하거나, 또는 대상에서 바이오필름의 형성을 감소 또는 방지하는데 유용할 수 있다. 특정 실시양태에서, 키트는 본원에 기재된 화합물 또는 제약 조성물을 포함하고 (예를 들어, 제1 용기에서); 화합물 또는 제약 조성물의 사용에 대한 지침서 (예를 들어, 대상체에게 화합물 또는 제약 조성물을 투여하기 위한 지침서, 세포, 조직, 또는 생물학적 샘플을 화합물 또는 제약 조성물과 접촉시키기 위한 지침서)를 포함한다. 본원에 기재된 키트는 또한 규제 기관 예컨대 미국 식품 의약품국 (FDA)에서 요구하는 바와 같은 정보를 포함할 수 있다. 특정 실시양태에서, 키트에 포함된 정보는 처방 정보이다. 특정 실시양태에서, 키트 및 지침서는 대상체, 세포, 조직, 또는 생물학적 샘플에서 금속 (예를 들어, 철 또는 또 다른 금속)을 킬레이트화하는 것을 제공한다. 특정 실시양태에서, 키트 및 지침서는 질환의 치료를 필요로 하는 대상체에서 질환을 치료하는 것을 제공한다. 특정 실시양태에서, 키트 및 지침서는 질환의 예방을 필요로 하는 대상체에서 질환을 예방하는 것을 제공한다. 특정 실시양태에서, 키트 및 지침서는 대상체에서 바이오필름의 형성을 치료, 감소, 또는 방지하는 것을 제공한다. 특정 실시양태에서, 키트 및 지침서는 대상에서 바이오필름의 형성을 감소 또는 방지하는 것을 제공한다. 본원에 기재된 키트는 본원에 기재된 1종 이상의 추가의 제약 작용제를 개별 조성물로서 포함할 수 있다.
치료 방법 및 용도
화학식 (I) 또는 화학식 (II)의 화합물, 및 본원에 기재된 제약 조성물은 대상체, 세포, 조직, 또는 생물학적 샘플에서 금속 (예를 들어, 철 또는 또 다른 금속)을 킬레이트화하거나, 질환의 치료를 필요로 하는 대상체에서 질환을 치료하거나, 질환의 예방을 필요로 하는 대상체에서 질환을 예방하거나, 대상체에서 바이오필름의 형성을 치료, 감소, 또는 방지하거나, 또는 대상에서 바이오필름의 형성을 감소 또는 방지하는데 유용할 수 있다.
본 발명의 화합물은 금속 킬레이트화제라고 여겨진다. 화합물은 적어도 본원에 기재된 화합물이 "대사적으로 프로그램화"된 금속 킬레이트화제, 예를 들어 친수성이고 비독성인 그의 대응물로 빨리 전환되는 (예를 들어, 생체내 전환되는), 친지성, 흡수성 (예를 들어, 경구로 흡수성)의 효과적인 금속 킬레이트화제이기 때문에 공지된 금속 킬레이트화제보다 이롭다. 친수성 화합물 (예를 들어, 2개 이상 카르복실 기를 포함한 화학식 (I) 또는 화학식 (II)의 화합물)은 전형적으로 세포 막을 용이하게 통과할 수 없고/거나, 불량하게 흡수성 (예를 들어, 경구로 흡수성)이다. 친지성 화합물 (예를 들어, 0개 또는 1개의 카르복실 기를 포함한 화학식 (I) 또는 화학식 (II)의 화합물)은 전형적으로 세포 막을 용이하게 통과할 수 있고/거나, 흡수성 (예를 들어, 경구로 흡수성)이다. 더욱이, 친지성 화합물은 전형적으로 친수성 화합물보다 금속을 킬레이트화하는데 더 효과적이다. 그러나, 친지성 화합물 전형적으로 친수성 화합물보다 더 독성이다. 따라서, 친수성 화합물을 "대사적으로 프로그램화"하는 것, 예를 들어, 친수성 화합물을, 세포 막을 용이하게 통과할 수 있고, 이어서 대사적으로 친수성 화합물로 다시 전환되는 친지성 화합물로 구조적으로 변형시키는 것에 의해, 흡수성의, 효과적이고, 비독성인 것과 같은 균형잡힌 특성을 갖는 금속 킬레이트화제가 달성된다.
특정 실시양태에서, 금속은 철 (예를 들어, Fe(II) 또는 Fe(III))이다. 특정 실시양태에서, 금속은 철이 아니다. 특정 실시양태에서, 금속은 알루미늄, 탈륨 (예를 들어, Tl(I) 또는 Tl(III)), 크로뮴 (예를 들어, Cr(III) 또는 Cr(VI)), 마그네슘, 칼슘, 스트론튬, 니켈 (예를 들어, Ni(II)), 망가니즈 (예를 들어, Mn(II)), 코발트 (예를 들어, Co(II) 또는 Co(III)), 구리 (예를 들어, Cu(I) 또는 Cu(II)), 아연, 은 (예를 들어, Ag(I)), 나트륨, 칼륨, 카드뮴 (예를 들어, Cd(II)), 수은 (예를 들어, Hg(I) 또는 Hg(II)), 납 (예를 들어, Pb(II) 또는 Pb(IV)), 안티모니 (예를 들어, Sb(III) 또는 Sb(V)), 몰리브데넘 (예를 들어, Mo(III) 또는 Mo(VI)), 텅스텐 (예를 들어, W(VI)), 란타나이드 (예를 들어, 세륨, 예컨대 Ce(III) 또는 Ce(IV)), 또는 악티나이드 (예를 들어, 우라늄, 예컨대 U(VI))이다. 특정 실시양태에서, 금속은 3가 금속 (예를 들어, Fe(III) 또는 알루미늄)이다. 특정 실시양태에서, 3가 금속은 Tl(III), Cr(III), Co(III), Sb(III), Mo(III), 또는 Ce(III)이다. 특정 실시양태에서, 금속은 1가 금속 (예를 들어, Tl(I), Cu(I), Ag(I), Na(I), K(I), 또는 Hg(I))이다. 특정 실시양태에서, 금속은 2가 금속 (예를 들어, Fe(II), Mg(II), Ca(II), Sr(II), Ni(II), Mn(II), Co(II), Cu(II), Zn(II), Cd(II), Hg(II), 또는 Pb(II))이다. 특정 실시양태에서, 금속은 4가 금속 (예를 들어, Pb(IV) 또는 Ce(IV))이다. 특정 실시양태에서, 금속은 5가 금속 (예를 들어, Sb(V))이다. 특정 실시양태에서, 금속은 6가 금속 (예를 들어, Cr(VI), Mo(VI), W(VI), 또는 U(VI))이다.
또 다른 측면에서, 대상체에게 유효량 (예를 들어, 치료 유효량)의 본원에 기재된 화합물 또는 제약 조성물을 투여하는 것을 포함하는, 대상체에서 금속 (예를 들어, 철 또는 또 다른 금속)을 킬레이트화하는 방법이 본원에 제공된다.
또 다른 측면에서, 세포, 조직, 또는 생물학적 샘플을 유효량의 본원에 기재된 화합물 또는 제약 조성물과 접촉시키는 것을 포함하는, 세포, 조직, 또는 생물학적 샘플에서 금속 (예를 들어, 철 또는 또 다른 금속)을 킬레이트화하는 방법이 본원에 제공된다.
또 다른 측면에서, 대상체에게 유효량 (예를 들어, 치료 유효량)의 본원에 기재된 화합물 또는 제약 조성물을 투여하는 것을 포함하는, 질환의 치료를 필요로 하는 대상체에서 질환을 치료하는 방법이 본원에 제공된다.
또 다른 측면에서, 대상체에게 유효량 (예를 들어, 예방 유효량)의 본원에 기재된 화합물 또는 제약 조성물을 투여하는 것을 포함하는, 질환의 예방을 필요로 하는 대상체에서 질환을 예방하는 방법이 본원에 제공된다
또 다른 측면에서, 혈액 또는 그의 성분 (예를 들어, 적혈구)과 유효량 (예를 들어, 치료 유효량)의 본원에 기재된 화합물 또는 제약 조성물을 혼합하여 혼합물을 형성하고; 대상체에게 혼합물을 투여하는 것을 포함하는, 질환의 치료를 필요로 하는 대상체에서 질환을 치료하는 방법이 본원에 제공된다.
또 다른 측면에서, 혈액 또는 그의 성분 (예를 들어, 적혈구)과 유효량 (예를 들어, 예방 유효량)의 본원에 기재된 화합물 또는 제약 조성물을 혼합하여 혼합물을 형성하고; 대상체에게 혼합물을 투여하는 것을 포함하는, 질환의 예방을 필요로 하는 대상체에서 질환을 예방하는 방법이 본원에 제공된다.
혈액은 전혈 또는 전혈의 1종 이상의 성분을 포함하는 유체 (예를 들어, 적혈구, 백혈구, 혈장, 응고 인자, 및 혈소판)일 수 있다. 특정 실시양태에서, 혼합물은 대상체에게 정맥내로 투여된다.
또 다른 측면에서, 본원에 기재된 방법 (예를 들어, 대상체, 세포, 조직, 또는 생물학적 샘플에서 금속 (예를 들어, 철 또는 또 다른 금속)을 킬레이트화하는 방법, 그의 대상체에서 질환을 치료하는 방법, 또는 질환의 예방을 필요로 하는 대상체에서 질환을 예방하는 방법)에 사용하기 위한 본원에 기재된 화합물이 제공된다.
또 다른 측면에서, 본원에 기재된 방법 (예를 들어, 대상체, 세포, 조직, 또는 생물학적 샘플에서 금속 (예를 들어, 철 또는 또 다른 금속)을 킬레이트화하는 방법, 그의 대상체에서 질환을 치료하는 방법, 질환의 예방을 필요로 하는 대상체에서 질환을 예방하는 방법)에 사용하기 위한 본원에 기재된 제약 조성물이 제공된다.
본 발명은 다양한 질환의 발병기전에 대한 인식으로부터 유래한다. 특정 실시양태에서, 질환은 산화성 스트레스, 수혈성 철 과부하, 지중해빈혈, 원발성 혈색소증, 속발성 혈색소증, 당뇨병, 간 질환, 심장 질환, 암, 방사선 손상, 신경계 또는 신경변성 장애, 프리드라이히 운동실조 (FRDA), 황반 변성, 폐쇄성 두부 손상, 과민성 장 질환, 또는 재관류 손상이다. 이들 질환은 자유 철 및 슈퍼옥시드 음이온, 과산화수소, 차아염소산, 및 히드록실 라디칼을 포함하는 반응성 산소 종 (ROS)의 생성, 및 다른 장수하는 자유 라디칼을 포함한다. 이러한 라디칼은 이제 이들 질환에 중요한 기여자라고 인식된다. 자유 철은 반응성 산소 종의 형성에 기여한다고 공지되어 있다. 예를 들어, 생물계에서 Fe+2 이온은 펜톤 반응을 통해 산소 종과 반응하여 고도로 반응성인 히드록실 라디칼을 생성한다. 히드록실 라디칼은 대부분의 유기 종, 예컨대 핵산, 단백질, 및 지질과 확산-제어 속도로 반응하는, 매우 효과적인 산화제이다. 또한, 슈퍼옥시드 음이온 또는 생물학적 환원제 (예를 들어, 아스코르브산)는 생성된 Fe+3 이온을 연속되는 퍼옥시드 환원 동안 Fe+2로 다시 환원시킬 수 있고, 따라서 이는 문제가 있는 주기이다.
따라서, 출혈 및/또는 염증 반응을 유발하는 질환은 반응성 산소 종이 Fe+2 이온과 접촉하여 고도로 반응성이고 해로운 히드록실 라디칼을 생성할 가능성을 포함한다. 즉, 적혈구로부터 방출된 철은 염증 세포 예컨대 호중구에 의해 생성된 산소 종과 반응하여 세포 및 조직 손상을 야기하는 히드록실 라디칼을 생성한다. 따라서, 해결책은 관리되지 않는 철의 킬레이트화 및 제거이다.
특정 실시양태에서, 대상체는 포유동물이다. 특정 실시양태에서, 대상체는 인간이다. 특정 실시양태에서, 대상체는 집동물, 예컨대 개, 고양이, 소, 돼지, 말, 양, 또는 염소이다. 특정 실시양태에서, 대상체는 반려 동물, 예컨대 개 또는 고양이이다. 특정 실시양태에서, 대상체는 가축 동물, 예컨대 소, 돼지, 말, 양 또는 염소이다. 특정 실시양태에서, 대상체는 동물원 동물이다. 또 다른 실시양태, 대상체는 실험 동물 예컨대 설치류 또는 비-인간 영장류이다. 특정 실시양태에서, 대상체는 낭성 섬유증으로 진단된다. 특정 실시양태에서, 대상체는 면역손상된 것이다.
특정 실시양태에서, 세포는 시험관내에 존재한다. 특정 실시양태에서, 세포는 생체내에 존재한다.
특정 실시양태에서, 세포는 혈액 세포이다. 특정 실시양태에서, 세포는 간 세포, 폐 세포 또는 비장 세포이다. 특정 실시양태에서, 세포는 암 세포이다.
특정 실시양태에서, 조직은 표적 조직 (예를 들어, 심장, 폐, 간, 췌장, 신장, 뇌, 또는 비장)이다.
특정 실시양태에서, 본원에 기재된 방법에 의해 치료 또는 예방되는 질환은 감염성 질환이다. 감염성 질환은 전형적으로 대상체 ("숙주")의 세포 ("숙주 세포")로 미생물 병원체 (예를 들어, 바이러스, 박테리아, 기생충 (예를 들어, 원충 및 다세포 기생충), 및 진균)에 의해 유발된다. 철은 산화제 뿐만 아니라 많은 미생물을 위한 영양소이다. 생존 및 복제하기 위해, 미생물 병원체는 그의 숙주로부터 철을 획득하여야 한다. 매우 병독성인 미생물 균주는 통상적으로 그의 숙주로부터 철을 획득하기 위한 강력한 메카니즘을 소유한다. 철을 병원성 미생물에게서 박탈하는 것은 그의 활성을 억제할 수 있고 미생물로 인한 감염성 질환의 치료 및/또는 예방에 유용할 수 있다. 특정 실시양태에서, 감염성 질환은 금속의 킬레이트화 또는 격리에 대해 반응성이다. 특정 실시양태에서, 본 발명의 화합물, 제약 조성물, 및 방법에 의해 치료 및/또는 예방되는 질환은 바이러스 감염이다. 특정 실시양태에서, 질환은 박테리아 감염이다. 특정 실시양태에서, 박테리아 감염은 그람-양성 박테리아에 의해 유발된다. 예시적인 그람-양성 박테리아는 스타필로코쿠스 속(Staphylococcus), 스트렙토코쿠스(Streptococcus), 미크로코쿠스(Micrococcus), 펩토코쿠스(Peptococcus), 펩토스트렙토코쿠스(Peptostreptococcus), 엔테로코쿠스(Enterococcus), 바실루스(Bacillus), 클로스트리디움(Clostridium), 락토바실루스(Lactobacillus), 리스테리아(Listeria), 에리시펠로트릭스(Erysipelothrix), 프로피오니박테리움(Propionibacterium), 유박테리움(Eubacterium), 및 코리네박테리움(Corynebacterium)의 종을 포함하나 이에 제한되지는 않는다. 특정 실시양태에서, 그람-양성 박테리아는 피르미쿠테스(Firmicutes) 문의 박테리아이다. 특정 실시양태에서, 박테리아는 피르미쿠테스(Firmicutes) 문 및 엔테로코쿠스(Enterococcus) 속의 구성원이고, 즉, 박테리아 감염은 엔테로코쿠스(Enterococcus) 감염이다. 예시적인 엔테로코쿠스(Enterococci) 박테리아는 이. 아비움(E. avium), 이. 두란스(E. durans), 이. 파에칼리스(E. faecalis), 이. 파에시움(E. faecium), 이. 갈리나룸(E. gallinarum), 이. 솔리타리우스(E. solitarius), 이. 카셀리플라부스(E. casseliflavus), 및 이. 라피노수스(E. raffinosus)를 포함하나 이에 제한되지는 않는다. 특정 실시양태에서, 엔테로코쿠스 감염은 이. 파에칼리스(E. faecalis) 감염이다. 특정 실시양태에서, 엔테로코쿠스 감염은 이. 파에시움(E. faecium) 감염이다. 특정 실시양태에서, 박테리아는 피르미쿠테스(Firmicutes) 문 및 스타필로코쿠스(Staphylococcus) 속의 구성원이고, 즉, 박테리아 감염은 스타필로코쿠스(Staphylococcus) 감염이다. 예시적인 스타필로코쿠스(Staphylococci) 박테리아는 에스. 아를레타에(S. arlettae), 에스. 아우레우스(S. aureus), 에스. 아우리쿨라리스(S. auricularis), 에스. 카피티스(S. capitis), 에스. 카프라에(S. caprae), 에스. 카르노우스(S. carnous), 에스. 크로모제네스(S. chromogenes), 에스. 코히이(S. cohii), 에스. 콘디멘티(S. condimenti), 에스. 크로세올리티쿠스(S. croceolyticus), 에스. 델피니(S. delphini), 에스. 데브리에세이(S. devriesei), 에스. 에피더미스(S. epidermis), 에스. 에쿠오룸(S. equorum), 에스. 펠리스(S. felis), 에스. 플루오에티이(S. fluroettii), 에스. 갈리나룸(S. gallinarum), 에스. 헤몰리티쿠스(S. haemolyticus), 에스. 호미니스(S. hominis), 에스. 하이이쿠스(S. hyicus), 에스. 인테르메디우스(S. intermedius), 에스. 클로오시이(S. kloosii), 에스. 레에이(S. leei), 에스. 레누스(S. lenus), 에스. 루그두네시스(S. lugdunesis), 에스. 루트라에(S. lutrae), 에스. 리티칸스(S. lyticans), 에스. 마실리엔시스(S. massiliensis), 에스. 미크로티(S. microti), 에스. 무스카에(S. muscae), 에스. 네팔렌시스(S. nepalensis), 에스. 파스테우리(S. pasteuri), 에스. 펜텐코페리(S. penttenkoferi), 에스. 피스시페르멘탄스(S. piscifermentans), 에스. 수도인테르메디우스(S. psuedointermedius), 에스. 수도루그덴시스(S. psudolugdensis), 에스. 풀베레리(S. pulvereri), 에스. 로스트리(S. rostri), 에스. 사카롤리티쿠스(S. saccharolyticus), 에스. 사프로피티쿠스(S. saprophyticus), 에스. 슐라이페리(S. schleiferi), 에스. 시우리(S. sciuri), 에스. 시미아에(S. simiae), 에스. 시물란스(S. simulans), 에스. 스테파노비시이(S. stepanovicii), 에스. 숙시누스(S. succinus), 에스. 비툴리누스(S. vitulinus), 에스. 와르네리(S. warneri), 및 에스. 크실로수스(S. xylosus)이다. 특정 실시양태에서, 스타필로코쿠스(Staphylococcus) 감염은 에스. 아우레우스(S. aureus) 감염이다. 특정 실시양태에서, 스타필로코쿠스(Staphylococcus) 감염은 에스. 에피더미스(S. epidermis) 감염이다. 특정 실시양태에서, 그람-양성 박테리아는 스타필로코쿠스 아우레우스(Staphylococcus aureus), 스타필로코쿠스 아우리쿨라리스(Staphylococcus auricularis), 스타필로코쿠스 카피티스(Staphylococcus capitis), 스타필로코쿠스 코니이(Staphylococcus cohnii), 스타필로코쿠스 에피더미디스(Staphylococcus epidermidis), 스타필로코쿠스 헤몰리티쿠스(Staphylococcus haemolyticus), 스타필로코쿠스 호미니스(Staphylococcus hominis), 스타필로코쿠스 루그다넨시스(Staphylococcus lugdanensis), 스타필로코쿠스 사카롤리티쿠스(Staphylococcus saccharolyticus), 스타필로코쿠스 사프로피티쿠스(Staphylococcus saprophyticus), 스타필로코쿠스 슐라이페리(Staphylococcus schleiferi), 스타필로코쿠스 시밀란스(Staphylococcus similans), 스타필로코쿠스 워네리(Staphylococcus warneri), 스타필로코쿠스 크실로수스(Staphylococcus xylosus), 스트렙토코쿠스 아갈락티아에(Streptococcus agalactiae), 스트렙토코쿠스 안지노수스(Streptococcus anginosus), 스트렙토코쿠스 보비스(Streptococcus bovis), 스트렙토코쿠스 카니스(Streptococcus canis), 스트렙토코쿠스 에쿠이(Streptococcus equi), 스트렙토코쿠스 밀레리(Streptococcus milleri), 스트렙토코쿠스 미티오르(Streptococcus mitior), 스트렙토코쿠스 뮤탄스(Streptococcus mutans), 스트렙토코쿠스 뉴모니아에(Streptococcus pneumoniae), 스트렙토코쿠스 피오게네스(Streptococcus pyogenes), 스트렙토코쿠스 살리바리우스(Streptococcus salivarius), 스트렙토코쿠스 산구이스(Streptococcus sanguis), 바실루스 안트라시스(Bacillus anthracis), 클로스트리디움 보툴리눔(Clostridium botulinum), 클로스트리디움 페르프린겐스(Clostridium perfringens), 클로스트리디움 테타니(Clostridium tetani), 코리네박테리움 디프테리아에(Corynebacterium diphtheriae), 코리네박테리움 제이케이움(Corynebacterium jeikeium), 엔테로코쿠스 파에칼리스(Enterococcus faecalis), 엔테로코쿠스 파에시움(Enterococcus faecium), 에리시펠로트릭스 루시오파티아에(Erysipelothrix rhusiopathiae), 가르드네렐라 바기날리스(Gardnerella vaginalis), 게멜라 모르빌로룸(Gemella morbillorum), 미코박테리움 아브세수스(Mycobacterium abcessus), 미코박테리움 켈로나에(Mycobacterium chelonae), 미코박테리움 포르투이툼(Mycobacterium fortuitum), 미코박테리움 하에모필리움(Mycobacterium haemophilium), 미코박테리움 칸사시이(Mycobacterium kansasii), 미코박테리움 레프라에(Mycobacterium leprae), 미코박테리움 마리눔(Mycobacterium marinum), 미코박테리움 스크로풀라세움(Mycobacterium scrofulaceum), 미코박테리움 스메그마티스(Mycobacterium smegmatis), 미코박테리움 테라에(Mycobacterium terrae), 미코박테리움 투베르쿨로시스(Mycobacterium tuberculosis), 미코박테리움 울세란스(Mycobacterium ulcerans), 및 펩토코수스 니거(Peptococcus niger)로 이루어진 군으로부터 선택된다.
특정 실시양태에서, 박테리아 감염은 그람-음성 박테리아에 의해 유발된 감염이다. 예시적인 그람-음성 박테리아는 에스케르키아 콜라이(Escherchia coli), 카울로박터 크레센투스(Caulobacter crescentus), 슈도모나스(Pseudomonas), 아그로박테리움 투메파시엔스(Agrobacterium tumefaciens), 브란하멜라 카타랄리스(Branhamella catarrhalis), 시트로박터 디베르수스(Citrobacter diversus), 엔테로박터 아에로게네스(Enterobacter aerogenes), 클레브시엘라 뉴모니아에(Klebsiella pneumoniae), 프로테우스 미라빌리스(Proteus mirabilis), 살모넬라 티피무리움(Salmonella typhimurium), 네이세리아 메닌기티디스(Neisseria meningitidis), 세라티아 마르세센스(Serratia marcescens), 시겔라 손네이(Shigella sonnei), 네이세리아 고노레아에(Neisseria gonorrhoeae), 아시네토박터 바우만니이(Acinetobacter baumannii), 살모넬라 엔테리디티스(Salmonella enteriditis), 푸소박테리움 누클레아툼(Fusobacterium nucleatum), 베일로넬라 파르불라(Veillonella parvula), 박테로이데스 포르시투스(Bacteroides forsythus), 악티노바실루스 악티노미세템코미탄스(Actinobacillus actinomycetemcomitans), 아그레가티박터 악티노미세템코미탄스(Aggregatibacter actinomycetemcomitans), 포르피로모나스 긴기발리스(Porphyromonas gingivalis), 헬리코박터 필로리(Helicobacter pylori), 프란시셀라 툴라렌시스(Francisella tularensis), 예르시니아 페스티스(Yersinia pestis), 모르가넬라 모르가니이(Morganella morganii), 에드워드시엘라 타르다(Edwardsiella tarda), 및 헤모필루스 인플루엔자에(Haemophilus influenzae)를 포함하나 이에 제한되지는 않는다. 특정 실시양태에서, 그람-음성 박테리아 종은 슈도모나스(Pseudomonas)이다. 특정 실시양태에서, 그람-음성 박테리아 종은 슈도모나스 아에루기노사(Pseudomonas aeruginosa)이다.
특정 실시양태에서, 박테리아 감염은 만성 박테리아 감염이다. "만성 박테리아 감염"은 장기 지속기간 또는 빈번한 재발을 갖는 박테리아 감염이다. 예를 들어, 만성 중이 감염, 또는 중이염은, 유스타키오관이 알레르기, 다중 감염, 귀 외상, 또는 아데노이드의 종창으로 인해 반복적으로 차단되게 되는 경우 발생할 수 있다. "장기 지속기간"의 정의는 특별한 감염에 따라 달라질 것이다. 예를 들어, 만성 중이 감염의 경우에, 이는 수주 내지 수개월 지속할 수 있다. 예시적인 만성 박테리아 감염은 요로 감염 (예를 들어, 에스케리키아 콜라이(Escherichia coli) 및/또는 스타필로코쿠스 사프로피티쿠스(Staphylococcus saprophyticus)로 인한 요로 감염), 위염 (예를 들어, 헬리코박터 필로리(Helicobacter pylori)로 인한 위염), 호흡기 감염 (예를 들어, 낭성 섬유증 및 슈도모나스 아에우로기노사(Pseudomonas aeuroginosa)로 인한 호흡기 감염을 갖는 환자가 고통받는 호흡기 감염), 방광염 (예를 들어, 에스케리키아 콜라이(Escherichia coli)로 인한 방광염), 신우신염 (예를 들어, 프로테우스 스피시스(Proteus Species), 에스케리키아 콜라이(Escherichia coli) 및/또는 슈도모나스(Pseudomonas) 종으로 인한 신우신염), 골수염 (예를 들어, 스타필로코쿠스 아우레우스(Staphylococcus aureus) 및/또는 에스케리키아 콜라이(Escherichia coli)로 인한 골수염), 박테리아혈증, 피부 감염, 장미증, 여드름, 만성 상처 감염, 감염성 신장 결석 (예를 들어, 프로테우스 미라빌리스(Proteus mirabilis)로 인한 감염성 신장 결석), 박테리아 심내막염, 및 부비동 감염을 포함하나 이에 제한되지는 않는다.
특정 실시양태에서, 박테리아 감염은 1종 이상의 항생제에 내성인 유기체에 의해 유발된다. 특정 실시양태에서, 박테리아 감염은 페니실린에 내성인 유기체에 의해 유발된다. 특정 실시양태에서, 박테리아 감염은 반코마이신 (VR)에 내성인 유기체에 의해 유발된다. 특정 실시양태에서, 박테리아 감염은 반코마이신-저항성 이. 파에칼리스(E. faecalis)에 의해 유발된다. 특정 실시양태에서, 박테리아 감염은 반코마이신-내성 이. 파에시움(E. faecium)에 의해 유발된다. 특정 실시양태에서, 박테리아 감염은 반코마이신-내성 스타필로코쿠스 아우레우스(Staphylococcus aureus) (VRSA)에 의해 유발된다. 특정 실시양태에서, 박테리아 감염은 반코마이신-내성 엔테로코쿠스(Enterococci) (VRE)에 의해 유발된다. 특정 실시양태에서, 박테리아 감염은 메티실린-내성 (MR) 유기체에 의해 유발된다. 특정 실시양태에서, 박테리아 감염은 메티실린-내성 에스. 아우레우스(S. aureus) (MRSA)에 의해 유발된다. 특정 실시양태에서, 박테리아 감염은 메티실린-내성 스타필로코쿠스 에피더미디스(Staphylococcus epidermidis) (MRSE)에 의해 유발된다. 특정 실시양태에서, 박테리아 감염은 페니실린-내성 스트렙토코쿠스 뉴모니아(Streptococcus pneumonia)에 의해 유발된다. 특정 실시양태에서, 박테리아 감염은 퀴놀론-내성 스타필로코쿠스 아우레우스(Staphylococcus aureus) (QRSA)에 의해 유발된다. 특정 실시양태에서, 박테리아 감염은 다중-약물 내성 미코박테리움 투베르쿨로시스(Mycobacterium tuberculosis)에 의해 유발된다.
일부 실시양태에서, 박테리아 감염은 요로 감염, 위염, 호흡기 감염, 방광염, 신우신염, 골수염, 박테리아혈증, 피부 감염, 장미증, 여드름, 만성 상처 감염, 감염성 신장 결석, 박테리아 심내막염, 및 부비동 감염으로 이루어진 군으로부터 선택된 1종 이상의 감염이다. 특정 실시양태에서, 감염성 질환은 폐렴, 요로 감염, 합병성 복부내 감염, 또는 합병성 피부/피부 구조 감염이다. 특정 실시양태에서, 감염성 질환은 병원내 폐렴, 지역사회-획득 폐렴, 요로 감염, 합병성 복부내 감염, 합병성 피부/피부 구조 감염, 낭성 섬유증의 감염성 악화, 패혈증 또는 유비저이다. 특정 실시양태에서, 박테리아 감염은 호흡기 감염이다. 특정 실시양태에서, 박테리아 감염은 상기도 감염이다. 특정 실시양태에서, 박테리아 감염은 폐렴이다. 특정 실시양태에서, 박테리아 감염은 기관지염이다. 특정 실시양태에서, 질환은 기생충 감염이다. 특정 실시양태에서, 질환은 원충 감염이다. 특정 실시양태에서, 질환은 말라리아이다. 말라리아는 전형적으로 종 피. 팔시파룸(P. falciparum), 피. 말라리아에(P. malariae), 피. 오발레(P. ovale), 피. 비박스(P. vivax), 및 피. 노울레시(P. knowlesi)를 포함하나 이에 제한되지는 않는 플라스모디움(Plasmodium) (정단복합체충문)의 기생충에 의해 유발된다. 특정 실시양태에서, 질환은 다세포-기생충 감염이다. 특정 실시양태에서, 질환은 진균 감염이다.
특정 실시양태에서, 본원에 기재된 방법에 의해 치료 또는 예방되는 질환은 금속 과부하이다. 자유 금속 (예를 들어, 3가 금속, 예컨대 철(III) 또는 알루미늄)의 양은, 예컨대 금속 방출로 이어지는 금속 저장 시스템에서의 금속에 대한 불충분한 저장 용량 또는 이상이 있는 경우, 대상체 (예를 들어, 혈청 또는 세포)에서 상승될 수 있다. 특정 실시양태에서, 금속 과부하는 철 과부하 (예를 들어, Fe(III) 과부하 또는 Fe (II) 과부하)이다.
철 과부하 상태 또는 질환은 전반적 철 과부하 또는 국소 철 과부하를 특징으로 할 수 있다. 전반적 철 과부하 상태는 다중 조직에서 철의 과잉 또는 유기체의 도처에 위치된 과잉의 철을 일반적으로 포함한다. 전반적 철 과부하 상태는, 예를 들어 식이 철 또는 혈액 수혈로부터, 대상체에 의한 철의 과잉 흡수, 철의 과잉의 저장 및/또는 유지에 의해 발생한다. 전반적 철 과부하 상태는 있는 원발성 혈색소증이고, 이는 전형적으로 유전 장애이다. 제2 전반적 철 과부하 상태는 속발성 혈색소증이고, 이는 전형적으로 다중 (만성) 혈액 수혈을 받는 것의 결과이다. 혈액 수혈은 종종 지중해빈혈 또는 겸상 적혈구성 빈혈을 앓는 대상체를 위해요구된다. 식이 철 과부하의 유형은 반투 (Bantu) 철침착증을 지칭하고, 이는 높은 철 함량을 갖는 수제 맥주의 섭취와 연관된다. 특정 실시양태에서, 본원에 기재된 방법에 의해 치료 및/또는 예방된 질환은 전반적 철 과부하이다. 특정 실시양태에서, 질환은 국소 철 과부하이다. 특정 실시양태에서, 질환은 원발성 혈색소증이다. 특정 실시양태에서, 질환은 속발성 혈색소증이다. 특정 실시양태에서, 질환은 반투 철침착증이다.
국소 철 과부하 상태에서, 과잉의 철은 하나 또는 몇몇 세포 유형 또는 조직 또는 특정 기관에 한정된다. 대안적으로, 과잉의 철과 연관된 증상은 별개 기관, 예컨대 심장, 폐, 간, 췌장, 신장, 또는 뇌로 한정된다. 국소 철 과부하가 신경계 또는 신경변성 장애 예컨대 파킨슨병, 알츠하이머병, 헌팅턴병, 페리틴신경병증, 근위축성 측삭 경화증, 및 다발성 경화증으로 이어질 수 있다고 여겨진다. 금속 킬레이트화에서 이득을 보는 질환은 종종 대상체의 조직에서 금속의 침착과 연관된다. 침착은 전반적으로 또는 국소적으로 발생할 수 있다. 특정 실시양태에서, 질환은 신경계 또는 신경변성 장애이다. 특정 실시양태에서, 질환은 파킨슨병, 알츠하이머병, 헌팅턴병, 페리틴신경병증, 근위축성 측삭 경화증, 또는 다발성 경화증이다.
인간은 이들이 1일 철 약 1 mg을 흡수 및 배출하는 고도로 효율적인 철 관리 시스템을 갖지만, 과잉의 금속의 배출에 대한 도관은 존재하지 않는다. 지중해빈혈과 같은 수혈-의존성 빈혈은, 간, 심장, 췌장, 및 (i) 간경변증으로 진행할 수 있는 간 질환 (문헌 [Angelucci et al., "Hepatic Iron Concentration and Total Body Iron Stores in Thalassemia Major." N. Engl. J. Med. 2000, 343, 327-331; Bonkovsky et al., "Iron-Induced Liver Injury." Clin. Liver Dis. 2000, 4, 409-429; Peitrangelo, "Mechanism of Iron Toxicity." Adv. Exp. Med. Biol. 2002, 509, 19-43]), (ii) 췌장 베타-세포 분비에서의 철-유도된 감소 및 간 인슐린 저항성에서의 증가 둘 다와 관련된 당뇨병 (문헌 [Cario et al., "Insulin Sensitivity 및 β-Cell Secretion in Thalassemia Major with Secondary Haemochromatosis: Assessment by Oral Glucose Tolerance Test." Eur. J. Pediatr. 2004, 162, 139-146; Wojcik et al., "Natural History of C282Y Homozygotes for Haemochromatosis." Can. J. Gastroenterol. 2002, 16, 297-302]), 및 (iii) 심장 질환을 일으키는 다른 곳에서 철의 축적을 야기한다. 상대적인 과잉의 철은 심장 질환의 증가된 위험과 연관되었다. 심부전은 여전히 중증성 빈혈 및 수혈성 철 과부하의 관련 형태의 주요 사망 원인이다 (Brittenham, "Disorders of Iron Metabolism: Iron Deficiency and Overload." In: Hoffman et al., editors. Hematology: Basic Principles and Practice. 3. Churchill Livingstone; New York: 2000. pp. 397-428; Brittenham et al., "Efficacy of Deferoxamine in Preventing Complications of Iron Overload in Patients with Thalassemia Major." N. Engl. J. Med. 1994, 331, 567-573; Zurlo et al., "Survival and Causes of Death in Thalassemia Major." Lancet. 1989, 2, 27-30). 혈청 페리틴 수준, 염증성 바이오마커 예컨대 C-반응성 단백질 및 인터류킨-1 사이의 강한 상관관계가 있고, 사망은 말초 동맥 질환을 갖는 환자의 하위세트이며; 정맥절개술 및 철 킬레이트화는 그 위험을 완화하는데 사용되었다. 철 킬레이트화제에 의한 치료는 철 저장을 감소시키고, 혈청 페리틴을 감소시키고, 잠재적으로 심장 질환 및 졸중의 발생률을 감소시킬 것이다. 특정 실시양태에서, 본원에 기재된 방법에 의해 치료 및/또는 예방되는 질환은 수혈성 철 과부하이다. 특정 실시양태에서, 질환은 수혈-의존성 빈혈이다. 특정 실시양태에서, 질환은 지중해빈혈이다. 특정 실시양태에서, 질환은 간 질환 (예를 들어, B형 간염, C형 간염, 및 간 경변증), 심장 질환 (예를 들어, 심근병증, 관상동맥 심장 질환, 염증성 심장 질환, 허혈성 심장 질환, 심장 판막 질환, 고혈압 심장 질환, 및 아테롬성동맥경화증), 또는 췌장 질환이다. 특정 실시양태에서, 질환은 당뇨병이다.
더욱이, 본 발명의 화합물, 제약 조성물 및 방법은 금속은 철이 아닌 금속 과부하의 치료 및/또는 예방에 유용할 수 있다. 특정 실시양태에서, 금속 과부하는 알루미늄 과부하, 크로뮴 과부하, 마그네슘 과부하, 칼슘 과부하, 스트론튬 과부하, 니켈 과부하, 망가니즈 과부하, 코발트 과부하, 구리 과부하, 아연 과부하, 은 과부하, 나트륨 과부하, 칼륨 과부하, 카드뮴 과부하, 수은 과부하, 납 과부하, 몰리브데넘 과부하, 텅스텐 과부하, 또는 악티나이드 과부하 (예를 들어, 우라늄 과부하)이다. 특정 실시양태에서, 금속 과부하는 3가 금속 과부하이다. 특정 실시양태에서, 금속 과부하는 알루미늄 과부하이다. 특정 실시양태에서, 3가 금속 과부하는 Cr(III) 과부하, Mo(III) 과부하 또는 Co(III) 과부하이다. 특정 실시양태에서, 금속 과부하는 1가 금속 과부하 (예를 들어, Cu(I) 과부하, Ag(I) 과부하, Na(I) 과부하, K(I) 과부하, 또는 Hg(I) 과부하)이다. 특정 실시양태에서, 금속 과부하는 2가 금속 과부하 (예를 들어, Mg(II) 과부하, Ca(II) 과부하, Sr(II) 과부하, Ni(II) 과부하, Mn(II) 과부하, Co(II) 과부하, Cu(II) 과부하, Zn(II) 과부하, Cd(II) 과부하, Hg(II) 과부하, 또는 Pb(II) 과부하)이다. 특정 실시양태에서, 금속 과부하는 4가 금속 과부하 (예를 들어, Pb(IV) 과부하)이다. 특정 실시양태에서, 금속 과부하는 5가 금속 과부하이다. 특정 실시양태에서, 금속 과부하는 6가 금속 과부하 (예를 들어, Cr(VI) 과부하, Mo(VI) 과부하, W(VI) 과부하, 또는 U(VI) 과부하)이다.
특정 실시양태에서, 본원에 기재된 방법에 의해 치료 또는 예방된 질환은 금속 중독이다. 금속 중독은 대상체에 금속 독성에 의해 유발될 수 있다. 예를 들어, 내인성 기능을 거의 또는 전혀 갖지 않은 금속은 대상체의 체내로의 이들의 통로를 찾고 손상을 일으킨다. 중금속 이온 예컨대 Hg(II)는 금속단백질에서 이온 예컨대 Zn(II)를 대체하고 이들을 불활성으로 하여, 환자의 사망 또는 출생 결함으로 끝날 수 있는 중증의 급성 또는 만성 독성을 일으킨다. 보다 더 현저하게, 란타나이드 (예를 들어, 세륨) 및 악티나이드 (예를 들어, 우라늄) 계의 방사성 동위원소는 구강, 공기, 또는 피부 접촉에 의해 이들에 노출된 개체에 대한 심각한 질병의 원인이 될 수 있다. 이러한 노출은 핵쓰레기로 구성된 핵 폭탄 또는 "더티 밤"의 폭굉 뿐만 아니라, 원자력 발전 시설의 파괴로부터 기인할 수 있다. 특정 실시양태에서, 금속 중독은 철 중독, 알루미늄 중독, 탈륨 중독, 크로뮴 중독, 마그네슘 중독, 칼슘 중독, 스트론튬 중독, 니켈 중독, 망가니즈 중독, 코발트 중독, 구리 중독, 아연 중독, 은 중독, 나트륨 중독, 칼륨 중독, 카드뮴 중독, 수은 중독, 납 중독, 안티모니 중독, 몰리브데넘 중독, 텅스텐 중독, 란타나이드 중독 (예를 들어, 세륨 중독), 또는 악티나이드 중독 (예를 들어, 우라늄 중독)이다. 특정 실시양태에서, 금속 중독은 철 중독 (예를 들어, Fe(II) 중독 또는 Fe(III) 중독)이다. 특정 실시양태에서, 금속 중독은 알루미늄 중독이다. 특정 실시양태에서, 금속 중독은 3가 금속 중독 (예를 들어, Fe(III) 중독, Al(III) 중독, Tl(III) 중독, Cr(III) 중독, Co(III) 중독, Sb(III) 중독, Mo(III) 중독, 또는 Ce(III) 중독)이다. 특정 실시양태에서, 금속 중독은 1가 금속 중독 (예를 들어, Tl(I) 중독, Cu(I) 중독, Ag(I) 중독, Na(I) 중독, K(I) 중독, 또는 Hg(I) 중독)이다. 특정 실시양태에서, 금속 중독은 2가 금속 중독 (예를 들어, Fe(II) 중독, Mg(II) 중독, Ca(II) 중독, Sr(II) 중독, Ni(II) 중독, Mn(II) 중독, Co(II) 중독, Cu(II) 중독, Zn(II) 중독, Cd(II) 중독, Hg(II) 중독, 또는 Pb(II) 중독)이다. 특정 실시양태에서, 금속 중독은 4가 금속 중독 (예를 들어, Pb(IV) 또는 Ce(IV) 중독)이다. 특정 실시양태에서, 금속 중독은 5가 금속 중독 (예를 들어, Sb(V) 중독)이다. 특정 실시양태에서, 금속 중독은 6가 금속 중독 (예를 들어, Cr(VI) 중독, Mo(VI) 중독, W(VI) 중독, 또는 U(VI) 중독)이다.
특정 실시양태에서, 본원에 기재된 방법에 의해 치료 또는 예방된 질환은 산화성 스트레스이다. 산화성 스트레스를 앓고, 따라서 산화성 스트레스 감소를 필요로 하는 대상체에서, 대상체의 적혈구로부터 방출된 철은 염증 세포 예컨대 호중구에 의해 생성된 산소 종과 반응하여 세포 및 조직 손상을 일으키는 히드록실 라디칼을 생성할 수 있다. 관리되지 않는 철의 킬레이트화 및 제거는 이들의 해로운 반응을 방지 또는 방해하고, 따라서, 산화성 스트레스를 감소시킬 수 있다. 산화성 스트레스 감소를 필요로 하는 대상체는 1개 이상의 하기 조건을 가질 수 있다: 환원제의 감소된 수준, 반응성 산소 종의 증가된 수준, 항산화제 효소의 돌연변이 또는 감소된 수준 (예를 들어, Cu/Zn 슈퍼옥시드 디스뮤타제, Mn 슈퍼옥시드 디스뮤타제, 글루타티온 리덕타제, 글루타티온 퍼옥시다제, 티오레독신, 티오레독신 퍼옥시다제, DT-디아포라제), 금속-결합 단백질의 돌연변이 또는 감소된 수준 (예를 들어, 트랜스페린, 페리틴, 세룰로플라스민, 알부민, 메탈로티오네인), 슈퍼옥시드를 생산할 수 있는 돌연변이 또는 과민성 효소 (예를 들어, 산화질소 신타제, NADPH 옥시다제, 크산틴 옥시다제, NADH 옥시다제, 알데히드 옥시다제, 디히드로오로테이트 데히드로게나제, 시토크롬 c 옥시다제), 및 방사선 손상. 환원제, 반응성 산소 종, 및 단백질의 상승된 또는 감소된 수준은 건강한 사람에서 전형적으로 확인되는 이러한 물질의 양과 관련된다고 결정된다. 산화성 스트레스 감소를 필요로 하는 대상체는 허혈성 에피소드를 앓을 수 있다. 허혈성 에피소드는 예컨대 동맥 협소화 또는 붕괴로부터 혈액 공급의 기계적 폐쇄가 있는 경우 발생할 수 있다. 협심증 및 심근경색을 일으킬 수 있는 심근 허혈은, 통상적으로 관상 동맥 질환으로 인해, 심근에 혈액의 부적당한 순환으로부터 발생한다. 24시간 내에 분해한 뇌의 허혈성 에피소드는 일과성 허혈 발작을 지칭한다. 장기 지속되는 허혈성 에피소드인 졸중은 돌이킬 수 없는 뇌 손상을 포함하며, 증상의 유형 및 중증도는 그의 혈액 순환으로의 접근이 손상된 뇌 조직의 위치 및 정도에 따라 달라진다. 허혈성 에피소드를 앓는 위험이 있는 대상체는 전형적으로 아테롬성동맥경화증, 혈관의 다른 장애, 혈전에 대한 혈액의 증가된 경향, 또는 심장 질환을 앓는다.
산화성 스트레스 감소를 필요로하는 대상체는 염증을 앓을 수 있다. 염증은 물리적 화학적, 또는 생물학적 작용제에 의해 유발된 손상 또는 비정상적 자극에 대한 반응에서 혈관 및 인접한 조직에서 일어나는 세포학적 및 화학적 반응의 복합으로 구성되는 기본적인 병리학적 과정이다. 염증성 장애는 연장된 기간 (예를 들어, 만성 염증) 동안 지속되거나 또는 조직을 손상시키는 염증을 특징으로 한다. 이러한 염증성 장애는 광범위한 다양한 조직, 예컨대 기도, 관절, 장, 및 연부 조직에 영향을 미칠 수 있다. 본 발명의 화합물 또는 제약 조성물은 이들 질환을 치료하는데 사용될 수 있다. 임의의 이론에 얽매이는 것을 원하지는 않지만, 본 발명의 화합물은 그의 능력을 끌어내어 다양한 메카니즘을 통해 산화성 스트레스를 감소시킨다고 여겨진다. 1개의 메카니즘에서, 화합물은 금속, 특히 산화환원-활성 금속 (예를 들어, 철)을 결합하고, 금속의 모든 배위 부위를 충전한다. 모든 금속 배위 부위가 충전되면, 산화 및/또는 환원제는 금속과 상호작용하는 능력이 감소되고 산화환원 순환을 일으킨다고 여겨진다. 또 다른 메카니즘에서, 화합물은 특정 산화 상태에서 금속을 안정화시켜, 산화환원 순환을 겪을 가능성이 더 적다. 또 다른 메카니즘에서, 화합물 자체는 항산화제 활성 (예를 들어, 자유 라디칼 스캐빈징, 반응성 산소 또는 질소 종의 스캐빈징)을 갖는다. 데스페리티오신 및 데스아자데스페리티오신, 및 그의 유도체 및 유사체는, 2004년 3월 4일에 공개되고 이제는 포기된 미국 출원 공개 번호 2004/0044220; 2004년 7월 8일에 공개되고 이제는 포기된 미국 출원 공개 번호 2004/0132789; 2004년 3월 4일에 공개된 국제 PCT 출원 공개 번호 WO 2004/017959; 2005년 10월 20일에 공개되고 이제는 포기된 미국 출원 공개 번호 2005/0234113; 2008년 10월 16일에 공개되고 이제는 포기된 미국 출원 공개 번호 2008/0255081; 2003년 12월 25일에 공개되고 이제는 포기된 미국 출원 공개 번호 2003/0236417; 2011년 12월 16일 제출된 미국 특허 출원, U.S.S.N. 61/576,920; 2011년 12월 16일 제출된 미국 특허 출원, U.S.S.N. 61/576,913; 및 미국 특허 번호 6,083,966, 6,559,315, 6,525,080, 6,521,652, 7,126,004, 7,531,563, 및 8,008,502에 기재되고; 그의 각각이 본원에 참조로 포함된 바와 같이, 본질적 항산화제 활성을 갖는다는 것이 공지되어 있다. 본 발명의 화합물은 이들 질환을 치료하는데 사용될 수 있다. 특정 실시양태에서, 본원에 기재된 방법에 의해 치료 또는 예방되는 질환은 산화성 스트레스이다. 특정 실시양태에서, 산화성 스트레스는 본원에 기재된 방법만큼 감소된다. 특정 실시양태에서, 질환은 방사선 손상이다. 특정 실시양태에서, 질환은 염증이다.
특정 실시양태에서, 본원에 기재된 방법에 의해 치료 또는 예방되는 질환은 황반 변성이다. 특정한 이론에 얽매이는 것을 원하지는 않지만, 본원에 기재된 화합물 및 제약 조성물은 눈에 들어갈 수 있다. 예를 들어, 2011년 12월 16일 제출된 미국 특허 출원, U.S.S.N. 61/576,920; 2011년 12월 16일 제출된 미국 특허 출원, U.S.S.N. 61/576,913, 2013년 6월 20일에 공개된 국제 PCT 출원 공개 번호 WO 2013/090750; 및 2013년 6월 20일에 공개된 국제 PCT 출원 공개 번호 WO 2013/090766을 참조한다. 이어서, 본 발명의 화합물은 눈으로부터 철을 킬레이트화하고 제거할 수 있어, 이에 따라 Fe+2이 반응성 산소 종을 생성하는 것을 방지한다. 철의 국부 축적은 황반 변성에 기여하는 것으로 여겨진다. 따라서, 눈 (망막을 포함함)으로부터의 철의 제거는 황반 변성을 방지하고 치료할 수 있다. 황반 변성의 치료에서, 본원에 기재된 화합물 또는 제약 조성물은 전신으로 또는 안구로 투여될 수 있다. 특정 실시양태에서, 화합물 또는 제약 조성물은 경구로 투여된다. 다른 실시양태에서, 화합물 또는 제약 조성물은 점안제 또는 안구 투여에 적합한 연고를 사용하여 눈에 투여된다.
특정 실시양태에서, 본원에 기재된 방법에 의해 치료 또는 예방된 질환은 두부 손상, 예컨대 뇌 또는 중추 신경계의 다른 부분에 출혈하는 것을 포함한다. 임의의 특정한 이론에 의해 얽매이는 것을 원하지는 않지만, 본 발명의 화합물 및 제약 조성물은 두부 손상으로부터 발생하는 혈액의 적혈구로부터의 철을 킬레이트화함으로써, 철 이온이 반응성 산소 종을 생성하는 것을 방지하는 것으로 여겨진다. 혈관계가 손상된 중추 신경계로의 출혈을 초래하는 두부 손상의 경우에, 사용되는 화합물은 혈액 뇌 장벽을 가로지르는 능력을 갖거나 또는 갖지 않을 수 있다. 특정 실시양태에서, 대상체에서 두부 손상을 치료하는데 사용되는 화합물은 혈액 뇌 장벽을 가로지를 수 있다. 다른 실시양태에서, 화합물은 혈액 뇌 장벽을 가로지를 수 없다. 본 발명의 특정 화합물은 전신 투여 (경구로 및 피하로) 후에 CSF에서 발견되었다.
두부 손상은 다양한 형태로 나타나고, 다양한 원인으로부터 발생한다. 특정 실시양태에서, 손상은 두개골에 침투한 두부에 대한 손상이다. 다른 실시양태에서, 두부 손상은 두개골에 침투한 폐쇄성 두부 손상이다. 폐쇄성 두부 손상은 교통 사고를 비롯한 사고, 추락, 및 폭행을 비롯한 다양한 원인으로부터 발생한다. 폐쇄성 두부 손상의 유형은 뇌진탕, 뇌 좌상, 미만성 축삭 손상, 및 혈종을 포함한다. 특정 실시양태에서, 폐쇄성 두부 손상은 뇌의 혈관 외부의 혈액을 발생시키는 폐쇄성 두부 손상이다. 출혈로부터의 철의 국소 축적은 폐쇄성 두부 손상과 연관된 후유증에 기여하는 것으로 여겨진다. 뇌로부터 철의 클리어런스를 보조함으로써 출혈의 영향을 최소화한다. 폐쇄성 두부 손상의 치료 또는 예방에서, 본원에 기재된 화합물 또는 제약 조성물은 전신으로, 예를 들어 비경구로 (예를 들어, 정맥내로) 또는 경구로 투여될 수 있다.
반응성 산소 종은 염증성 장 질환 (IBD)의 발병기전에 연관되었다. 문헌 [Grisham et al., "Neutophil-mediated mucosal injury. Role of reactive oxygen metabolites." Dig. Dis. Sci. 33:6S-15S, 1988; Allgayer "Clinical relevance of oxygen radicals in inflammatory bowel disease-facts and fashion." Klin. Wochenschr. 69:1001-1003, 1991; Ymamada et al. "Role of neutrophil-derived oxidants in the pathogenesis of intestinal inflammation." Klin. Wocheschr. 69:988-944, 1991; Babbs, "Oxygen radicals in ulcerative colitis." Free Radic. Biol. Med. 13:169-181, 1992]. 본 발명은 IBD의 치료 또는 예방에 대해 제공한다. DFO, 철 킬레이트화제는 래트, IBD의 동물 모델에서 아세트산-유도 결장염을 예방하는 것으로 발견되었다. 예를 들어, 2011년 12월 16일 제출된 미국 특허 출원, U.S.S.N. 61/576,920; 2011년 12월 16일 제출된 미국 특허 출원, U.S.S.N. 61/576,913; 문헌 [Bergeron et al., "Prevention of Acetic Acid-Induced Colitis by Desferrithiocin Analgos in a Rat Model." Digestive Diseases and Sciences, 48(2):399-407, February 2003]을 참조한다. 본원에 기재된 화합물 및 제약 조성물은 IBD를 갖는 대상체에서 보여지는 조직 손상 및 염증의 원인이 될 수 있는 반응성 산소 종 또는 보다 오래 존속하는 다른 안정한 라디칼의 생성을 방지하거나 또는 제거한다고 여겨진다. 본 발명에 유용한 화합물의 또 다른 가능한 작용의 메카니즘은 세포 손상을 야기하는 반응성 산소 종, 예컨대 히드록실 라디칼 및 과산화수소의 생성에 기여할 수 있는 금속, 예컨대 철의 킬레이트화이다. 본 발명은 또한 IBD로 진단된 대상체를 치료하는데 유용할 수 있다. 치료는 대상체를 장기간 치료하는데 사용될 수 있거나 또는 IBD가 격발한 대상체를 치료하는데 사용될 수 있다. 특정 실시양태에서, 본원에 기재된 화합물 또는 제약 조성물에 의한 치료는 장, 특히 장 점막에서 반응성 산소 종의 감소된 수준으로 이어진다. IBD의 치료에서, 화합물 또는 제약 조성물은 전신으로, 예를 들어, 비경구로 (예를 들어, 정맥내로), 경구로, 또는 직장으로 투여될 수 있다.
특정 실시양태에서, 본원에 기재된 방법에 의해 치료 또는 예방된 질환은 졸중이다. 본 발명의 치료는 전형적으로 졸중으로부터의 보다 양호하고/거나 보다 빠른 회복을 유발한다. 치료할 졸중은 허혈성 졸중 또는 출혈성 졸중일 수 있다. 허혈성 졸중의 치료에서, 본 발명에 기재된 화합물 또는 제약 조성물은 영향받은 뇌의 부분으로의 혈액 공급이 복구된 후의 재관류 손상에 기인한 손상을 예방하거나 또는 최소화하기 위해 대상체에게 투여된다. 화합물 및 제약 조성물은 반응성 산소 종 생성의 원인이 되는 철을 킬레이트화하고/거나 이러한 라디칼 종이 발생할 때 이것을 켄칭함으로써 반응성 산소 종의 생성을 방지하는 것으로 여겨진다. 출혈성 졸중에서, 화합물 및 제약 조성물은 유사한 메카니즘에 의해 작용하는 것으로 여겨지지만, 아마도 뇌에서 혈액으로부터 철을 격리시키는 것이 본 발명의 치료가 작용하는 우세한 메커니즘이다. 화합물 또는 제약 조성물의 작용의 메커니즘은 두부 손상의 치료에서와 유사하다. 치료에 사용되는 화합물은 혈액 뇌 장벽을 가로지르는 능력을 가질 수 있다. 특정 실시양태에서, 대상체가 허혈성 졸중으로 진단되었을 때, 치료에 사용되는 화합물은 혈액 뇌 장벽을 통과할 수 있다.
게다가, 본 발명은 대상체가 졸중을 앓는 것으로 진단된 후에 대상체를 치료하는데 유용할 수 있거나, 또는 졸중을 앓기 쉬운 대상체에게 화합물 또는 그의 제약 조성물을 투여하여 졸중의 영향을 예방하거나 또는 최소화할 수 있다. 특정 실시양태에서, 화합물 또는 제약 조성물은 대상체가 졸중을 앓는 것으로 진단된 후에 가능한 한 빨리 투여된다. 특정 실시양태에서, 화합물은 졸중이 여전히 발생하고 있는 대상체에게 투여된다. 특정 실시양태에서, 화합물 또는 제약 조성물은 졸중의 병력을 갖거나, 또는 대상체의 근본적인 의학적 상태 때문에 졸중을 앓기 쉬운 대상체에게 투여된다. 졸중의 치료에서 화합물 또는 제약 조성물은 전신으로, 예를 들어 비경구 (예를 들어, 정맥내로) 또는 경구로 투여될 수 있다.
특정 실시양태에서, 본원에 기재된 방법에 의해 치료 또는 예방된 질환은 재관류 손상이다. 재관류 손상은 혈액 공급이 손상된 신체의 임의의 영역에서 발생할 수 있다. 특정 실시양태에서, 치료할 재관류 손상은 심장에서 발생한다. 다른 실시양태에서, 재관류 손상은, 예를 들어 졸중과 관련하여 상기 논의된 바와 같이 뇌에서 발생한다. 본 발명의 치료는 영향받은 기관 또는 조직에 대한 혈액 공급이 복구될 때 재관류 손상을 최소화한다. 재관류 손상의 치료 및/또는 예방에서, 본원에 기재된 화합물 또는 제약 조성물은 조직 또는 기관의 허혈을 앓고 있는 대상체에게 투여된다. 어떠한 특정한 이론에 얽매이는 것을 원하지는 않지만, 화합물 또는 제약 조성물은 반응성 산소 종 생성의 원인이 되는 철을 킬레이트화하고/거나 이러한 라디칼 종이 발생할 때 이것을 켄칭함으로써 반응성 산소 종의 생성을 방지하는 것으로 여겨진다.
본 발명은 대상체가 특정한 기관 또는 조직의 허혈로 진단된 후에 대상체를 치료하는데 유용할 수 있다. 특정 실시양태에서, 본원에 기재된 화합물 또는 제약 조성물은 대상체가 허혈로 진단된 후에 가능한 한 빨리 투여된다. 특정 실시양태에서, 화합물 또는 제약 조성물은 허혈의 위험이 있는 대상체에게 투여된다. 특정 실시양태에서, 화합물 또는 제약 조성물은 기관 또는 조직의 허혈을 유발할 수 있는 절차 (예를 들어, 심장 수술)를 곧 겪을 대상체에게 투여된다. 특정 실시양태에서, 화합물 또는 제약 조성물은 이식된 기관에서 재관류 손상을 예방하는데 사용된다. 특정 실시양태에서, 화합물 또는 제약 조성물은 기증을 위해 제조되는 단리된 기관을 관류시키는데 사용된다. 재관류 손상의 예방 또는 치료에서, 화합물 또는 제약 조성물은 전신으로, 예를 들어 비경구 (예를 들어 정맥내로) 또는 경구로 투여될 수 있다. 특정 실시양태에서, 화합물 또는 제약 조성물은 허혈을 앓고 있는 기관 또는 조직으로 국부 투여된다.
특정 실시양태에서, 본원에 기재된 방법에 의해 치료 또는 예방되는 질환은 신생물성 질환 또는 전신생물성 상태이다. 특정 실시양태에서, 질환은 양성 신생물성 질환이다. 특정 실시양태에서, 질환은 암이다. 특정 실시양태에서, 질환은 전신생물성 질환이다.
1종 이상의 기관, 조직, 종양, 또는 그의 조합을 영상화 또는 검사하는 것은 대상체에게 본원에 기재된 화합물 또는 제약 조성물의 금속 염이 투여된 후에 수행될 수 있다. 영상화 및 검사 방법은 진단에 사용되는 다양한 기기 기술, 예컨대 x선 방법 (CT 스캔 및 종래 x선 영상을 포함함), 자기성 영상화 (자기 공명 영상화, 전자 상자성 공명 영상화) 및 방사화학물질 방법을 포함하도록 의도된다. 전형적으로, 영상화 또는 검사에 사용된 금속 염은 조영제로서 기능한다. 따라서, 한 실시양태에서 본 발명의 화합물의 금속 착물 또는 금속 염은 예를 들어 1종 이상의 기관, 예를 들어 위장관을 영상화 또는 검사하는데 조영제로서 사용될 수 있다. 조영제로서 기능할 수 있는 금속은 가돌리늄, 철, 망가니즈, 크로뮴, 디스프로슘, 테크네튬, 스칸듐, 바륨, 알루미늄 및 홀뮴, 바람직하게는 3가 양이온을 포함한다. 방사성 금속 염은 241Am, 51Cr, 60Co, 57Co, 58Co, 64Cu, 153Gd, 67Ga, 198Au, 113mIn, 111ln, 59Fe, 55Fe, 197Hg, 203Hg, 99mTc, 201T1, 및 169Yb를 포함하는 동위원소로부터, 다시 바람직하게는 금속이 3가의 양이온으로서 존재하는 경우에 제조될 수 있다.
또 다른 측면에서, 본 개시내용은 치료 유효량의 본원에 기재된 화합물 또는 제약 조성물을 바이오필름의 치료 또는 방지를 필요로 하는 대상체에게 투여하는 것을 포함하는, 바이오필름 형성을 치료 또는 방지하는 방법을 제공한다. 특정 실시양태에서, 바이오필름 형성을 치료 또는 방지하는 방법은 상처를 치료, 세척, 또는 소독하는 것이다. 특정 실시양태에서, 상처는 만성 상처, 급성 상처, 수술 상처, 수술 부위, 제2 또는 제3도 화상, 정체 궤양, 열대성 병변, 욕창, 심한 자상 또는 찰과상이다.
또 다른 측면에서, 본 개시내용은 대상과 유효량의 본원에 기재된 화합물 또는 제약 조성물을 접촉시키는 것을 포함하는 바이오필름 형성을 감소 또는 방지하는 방법을 제공한다. 특정 실시양태에서, 제공된 방법은 대상에서 바이오필름을 억제, 감소, 또는 제거한다. 특정 실시양태에서, 제공된 방법은 대상의 표면에서 바이오필름을 억제 또는 제거한다. 특정 실시양태에서, 표면은 단단하고 강성인 표면이다. 특정 실시양태에서, 표면은 배수관, 광택제 세라믹, 도자기, 유리, 금속, 목재, 크롬, 플라스틱, 비닐, 및 포르미카로 이루어진 군으로부터 선택된다. 특정 실시양태에서, 표면은 연질 가요성 표면이다. 특정 실시양태에서, 표면은 샤워 커튼 및 라이너, 실내장식재, 세탁물, 및 카펫천으로 이루어진 군으로부터 선택된다. 특정 실시양태에서, 표면은 음식물 제조 표면, 예컨대 주방 카운터, 도마, 싱크, 스토브, 냉장고 표면, 또는 스폰지 상이다. 특정 실시양태에서, 표면은 욕실 표면 예컨대 변기, 싱크, 욕조, 샤워실, 또는 배수구이다. 특정 실시양태에서, 표면은 의료 장치 표면이다.
일부 실시양태에서, 본원에 기재된 화합물 또는 제약 조성물과 대상의 접촉은 와이핑, 스폰징, 또는 소킹, 또는, 세탁 수단에 의해 수행된다.
일부 실시양태에서, 제공된 방법은 세치제, 구강세정제, 치아 우식, 여드름 치료, 콘택트 렌즈의 세척 및 소독의 처리를 위한 화합물, 및 인공 심장 판막 또는 고관절과 같이 영구적인 의학적으로 이식된 장치, 및 유치 카테터, 박동조율기, 및 외과용 핀과 같은 비영구적인 것들로서 바이오필름을 방지 또는 제거한다. 일부 실시양태에서, 제공된 방법은 대상체의 박테리아 감염를 포함하는 상황에서, 예를 들어 화상 환자를 위한 국소 드레싱에서 바이오필름을 방지 또는 제거한다. 이러한 상황의 예는 표재성 상처의 피. 아에루기노사(P. aeruginosa)에 의한 감염 예컨대 화상 환자 또는 낭성 섬유증을 갖는 대상체의 폐에서 확인되는 것이다. 일부 실시양태에서, 제공된 방법은 집적 회로, 회로 기판, 또는 다른 전자 또는 마이크로전자 장치를 제조하는 방법에서 바이오필름의 발생을 제어 또는 방지한다.
특정 실시양태에서, 박테리아는 시험관내 화합물 또는 제약 조성물과 접촉된다. 특정 실시양태에서, 박테리아는 생체내 화합물 또는 제약 조성물과 접촉된다. 특정 실시양태에서, 박테리아는 후속적으로 항생제와 접촉된다.
일부 실시양태에서, 화합물 또는 제약 조성물은 1종 이상의 추가의 제약 작용제 (예를 들어, 살생물제, 예를 들어, 항미생물제, 예를 들어, 항생제)에 의해 투여된다.
실시예
본원에 기재된 발명이 보다 완전하게 이해될 수 있도록 하기 위해, 하기 실시예를 제시한다. 본 출원에 기재된 합성 및 생물학적 실시예는 본원에 제공된 화합물, 제약 조성물 및 방법을 예시하기 위해 제공되며, 어떠한 방식으로도 그의 범주를 제한하는 것으로 해석되어서는 안 된다.
화합물의 설계
설계 개념은 킬레이트화제에 그의 위장 흡수를 촉진할 친지성 단편을 고정하는 것이다. 흡수되면, 이는 친수성이며 비독성인 대응물로 빠르게 전환되어야 한다. 따라서, 현재 킬레이트화제의 대사 프로파일은 미래 설계 전략을 위한 구조적 경계 조건을 설정할 것이다. (S)-4'-(CH3O)-DADFT (4)를 사용한 초기 대사 연구 (리간드를 래트에 피하로 300 μmol/kg의 용량으로 제공하는 것)는, 이것이 간에서 탈메틸화되어 (문헌 [Kem et al., Mol. Pharmacol. 65 (2004) 56-67], (S)-4'-(HO)-DADFT (2, 도 2)를 생산하는 것을 나타냈다.42 약물 노출 후 2시간에, 약 30%의 (S)-4'-(CH3O)-DADFT (4)가 탈메틸화되어 2가 되고, 대사물은 8-시간 시점에 걸쳐 상당히 높은 수준으로 유지된다 (도 2). 이러한 관찰은 폴리에테르 (S)-4'-(HO)-DADFT-PE (5) 및 (S)-3'-(HO)-DADFT-PE (6)의 유사한 평가를 장려하였다. 예를 들어, 5가 임의의 상당량으로 2로 전환된 경우, 신장 독성이 장기간 노출에 걸쳐 예측될 수 있기 때문에 이로써 b.i.d.로 제공되지 못하도록 된다. b.i.d.로 제공된 경우에도 5 및 6의 독성이 없다는 것은 2로의 절단이 부재하거나 또는 매우 보통이었음을 시사한다. 따라서, 킬레이트화제 5 및 6를 래트에게 300 μmol/kg의 용량으로 피하로 제공하였다. 평가된 조직은 혈장, 간, 신장, 심장, 및 췌장을 포함하였다. 임의의 4'- 또는 3'-폴리에테르 절단이 제공된 기관은 오직 간이었다 (도 2). 2시간에, 5의 2%가 2로 전환되고, 6의 2.6%가 상응하는 3으로 대사되었다. 대사물은 4 및 8시간 시점에 검출되지 않았다.45
7을 래트에게 5 및 6에 대해 기재된 바와 같은 동일한 시험 프로토콜 하에서 피하로 제공한 경우, 2로의 절단은 존재하지 않았다 (도 2). 그러나, 폴리에테르 단편이 첨부된 다른 약물, 예를 들어, 글리코디아진을 사용한 연구를 기반으로 하여64-68, 7의 말단 메틸이 절단되는지 아닌지를 결정할 필요가 있었다.
글리코디아진 (도 3)의 경우, 메틸 에테르가 알콜 (대사물 I)로 탈알킬화되고 (문헌 [Platzer et al., Europ. J. Clin. Pharmacol. 14 (1978) 293-299]), 이는 카르복실산 (대사물 II)으로 산화되었다. 7에서도 마찬가지였다면, 예를 들어, 이는 우선 상응하는 알콜 (S)-4,5-디히드로-2-[2-히드록시-4-(5-히드록시-3-옥사펜틸옥시)페닐]-4-메틸-4-티아졸카르복실산 [(S)-4'-(HO)-DADFT-PEA, 8]로 유도된 다음, 이어서 산 (S)-4,5-디히드로-2-[2-히드록시-4-(4-카르복시-3-옥사부틸옥시)페닐]-4-메틸-4-티아졸카르복실산 [(S)-4'-(HO)-DADFT-PEAA, 9]으로 유도되었을 것이다 (도 4). 이들 대사 산물 둘 다는 매우 친수성일 것으로 예상될 것이다. 이러한 친수성의 증가는, 이전 연구를 기반으로 하여, 추가로 리간드 독성을 최소화하는 것으로 예상될 것이다.37,43,45 실제로 이러한 탈메틸화-산화 시나리오가 7에 의해 발생하면, 이는 "대사적으로 프로그램화"된 철 킬레이트화제, 예를 들어, 친수성이고 가능하게는 비독성인 대사물로 빠르게 전환되는 고도로 친지성이고 경구로 흡수가능한 리간드에 대한 신규 접근법을 지지할 수 있다.
(S)-4'-(HO)-DADFT-norPE (7)의 2가지의 추정 대사물인 알콜 (S)-4'-(HO)-DADFT-PEA (8) 및 카르복실산 (S)-4'-(HO)-DADFT-PEAA (9)를 조립하였다. 이들 2가지의 합성 킬레이트화제는 본 발명자들로 하여금 모 킬레이트화제 7로 치료된 동물의 기관에서 7의 그의 대사물로의 잠재적인 전환을 추적하는 분석적 고압 액체 크로마토그래피 (HPLC) 방법을 개발하도록 하였다. 게다가, 킬레이트화제를 래트 및 영장류에게 경구로 및/또는 피하로 제공한 경우, 8 및 9의 친지성 (log Papp) 및 ICE 값을 평가하는 기회를 제공하였다.
화합물의 제조
본원에 제공된 화합물은 하기 일반적 방법 및 절차를 사용하여 용이하게 입수가능한 출발 물질로부터 제조될 수 있다. 전형적인 또는 바람직한 공정 조건 (예를 들어, 반응 온도, 시간, 반응물의 몰비, 용매, 압력 등)이 주어진 경우에, 달리 언급되지 않는 한, 다른 공정 조건이 또한 사용될 수 있다. 최적 반응 조건은 사용되는 특정한 반응물 또는 용매에 따라 달라질 수 있지만, 이러한 조건은 관련 기술분야의 통상의 기술자에 의해 상용 최적화 절차에 의해 결정될 수 있다.
실시예 1 내지 2에 사용된 예시적인 물질 및 방법은 하기 제시한다. 시약은 알드리치 케미칼 코.(Aldrich Chemical Co.) (위스콘신주 밀워키)로부터 구입하였다. 피셔 옵티마 등급 용매를 상용적으로 사용하였다. DMF는 4 Å 분자체 상에서 건조시켰다. 탄산칼륨은 화염 활성화하여, 드라이어라이트 상에서 데시케이터에서 냉각시켰다. 반응은 질소 분위기 하에 수행하고, 유기 추출물을 황산나트륨에 의해 건조시키고 여과하였다. 실리사이클 인크.(SiliCycle, Inc.) (캐나다 퀘벡주 퀘벡 시티)로부터의 실리카 겔 40-63을 칼럼 크로마토그래피에 사용하였다. 3 N HCl에 15분 동안 미리 담그고, 증류수 및 증류된 EtOH로 세척하고, 오븐-건조된 유리제품을 8-14의 단리 동안 사용하였다. 융점은 비보정하였다. 광회전을 퍼킨-엘머 341 편광계에서 589 nm (나트륨 D 선) 및 20℃에서 구동하고, c는 용액 100 mL 당 화합물 g의 농도이다 (CHCl3은 나타내지 않음). NMR 스펙트럼은 400 MHz (1H) 또는 100 MHz (13C)에서 획득되었다. 1H 스펙트럼에서 화학적 이동 (δ)은 유기 용매 (CDCl3은 나타내지 않음)의 경우 테트라메틸실란 또는 D2O의 경우 나트륨 3-(트리메틸실릴)프로피오네이트-2,2,3,3-d4로부터의 백만분율 다운필드로 제공된다. 13C 스펙트럼에 대한 화학적 이동 (δ)는 D2O 중 CH3OH (δ 49.50), 또는 CDCl3 (δ 77.16) (나타내지 않음) 또는 DMSO-d6 (δ 39.52) 중 잔류 용매 공명을 참조한 백만분율로 제공된다. 기준 피크는 ESI-FTICR 질량 스펙트럼에 대해 보고된다. 원소 분석은 애틀랜틱 마이크로랩스(Atlantic Microlabs) (조지아주 노크로스)에 의해 수행하였고, 계산 값의 ±0.4% 내에 있었다. 모든 화합물의 순도는 원소 분석으로 확인하였다. 게다가, 8-14의 순도는 HPLC 분석에 의해 ≥95%였다.
실시예 1. 화합물 8 및 9의 합성
알콜 8 및 카르복실산 9의 조립 (반응식 1)은 4'-히드록실52에서 데페리트린 에틸 에스테르 (15)의 알킬화에 의해 시작하였다. 구체적으로, 15와 DMF 중 2-(2-클로로에톡시)에탄올 (16), K2CO3 및 KI와의 100℃에서의 반응은 알콜 에스테르 17을 62% 수율로 제공하였다. CH3OH 중 50% NaOH에 의한 17의 처리는 알콜 8을 97% 수율로 유도하였다. 상기 조건 하에서 에틸 2-클로로에톡시아세테이트(18)69를 사용한 15의 알킬화는 디에스테르 19를 35% 수율로 생성하였다. 19의 비누화에 의해 이산 9를 98% 수율로 그의 일나트륨 염으로서 수득하였다.
반응식 1. (S)-4,5-디히드로-2-[2-히드록시-4-(5-히드록시-3-옥사펜틸옥시)페닐]-4-메틸-4-티아졸카르복실산 (8) 및 (S)-4,5-디히드로-2-[2-히드록시-4-(4-카르복시-3-옥사부틸옥시)페닐]-4-메틸-4-티아졸카르복실산 (9)의 합성a
a시약 및 조건: (a) K2CO3 (2.0 당량), KI, DMF, 100℃, 1일, 62%; (b) K2CO3 (2.1 당량), NaI, DMF, 95℃, 22시간, 35%; (c) 50% NaOH (수성), CH3OH, 97% (8), 98% (9, 그의 일나트륨 염으로서).
에틸 (S)-4,5-디히드로-2-[2-히드록시-4-(5-히드록시-3-옥사펜틸옥시)페닐]-4-메틸-4-티아졸카르복실레이트 (17). 탄산칼륨 (2.76 g, 20.0 mmol) 및 KI (200 mg, 1.2 mmol)를 DMF (100 mL) 중 15 (문헌 [Bergeron et al., J. Med. Chem. 48 (2005) 4120-4137]) (2.81 g, 10 mmol)의 혼합물에 첨가하였다. DMF (10 mL) 중 16 (1.24 g, 10 mmol)의 용액을 반응 혼합물에 첨가하고, 이를 100℃에서 24시간 동안 가열하였다. 실온으로 냉각시킨 후, H2O (100 mL)를 첨가한 후, 이어서 EtOAc (2 x 100 mL)로 추출하였다. 유기 층을 합하고, H2O (100 mL) 및 6 M NaCl (100 mL)로 세척하고, 용매를 진공 하에 제거하였다. 30% EtOAc/CH2Cl2을 사용한 칼럼 크로마토그래피에 의해 2.30 g의 17 (62%)을 점성 오일로서 수득하였다: [α] +48.0° (c 0.15).
1H NMR δ 12.70 (br s, 1H), 7.30 (d, J = 8.8 Hz, 1H), 6.50 (d, J = 2.4 Hz, 1H), 6.47 (dd, J = 8.8, 2.4 Hz, 1H), 4.24 (dq, J = 7.6, 1.6 Hz, 2H), 4.15-4.17 (m, 2H), 3.83-3.88 (m, 3H), 3.76-3.79 (m, 2H), 3.66-3.69 (m, 2H), 3.20 (d, J = 10.8 Hz, 1H), 1.66 (s, 3H), 1.3 (t, J = 7.2 Hz, 3H). 13C NMR δ 172.96, 170.92, 162.95, 161.32, 131.87, 110.14, 107.39, 101.51, 83.25, 72.73, 69.54, 67.61, 62.05, 61.89, 39.98, 24.61,14.23. C17H24NO6S에 대한 HRMS m/z 계산치, 370.1319 (M + H); 실측치, 370.1323. C17H23NO6S에 대한 분석 계산치: C, 55.27; H, 6.28; N, 3.79. 실측치: C, 54.99; H, 6.24; N, 3.75.
에틸 (S)-4,5-디히드로-2-[2-히드록시-4-[(4-에톡시카르보닐)-3-옥사부틸옥시]페닐]-4-메틸-4-티아졸카르복실레이트 (19). 아이오딘화나트륨 (0.5527 g, 3.69 mmol) 및 K2CO3 (5.1304 g, 37.12 mmol)을 DMF (46 mL) 중 15 (5.08 g, 18.1 mmol) 및 1869 (3.31 g, 19.9 mmol)에 첨가하고, 반응 혼합물을 95℃에서 22시간 동안 가열하였다. 혼합물을 냉각시키고, 여과하고, 아세톤 (100 mL, 2 x 50 mL)으로 고체를 세척하였다. 용매를 진공 하에서 제거하고, 농축물을 1:1 0.5 N HCl/6 M NaCl (120 mL)로 처리한 후, 이어서 EtOAc (100 mL, 2 x 50 mL)로 추출하였다. 유기 층을 합하고, 1% NaHSO3 (75 mL), H2O (75 mL) 및 6 M NaCl (55 mL)로 세척하고, 용매를 회전 증발에 의해 제거하였다. 8.4:25:66.5의 EtOAc/석유 에테르/CH2Cl2를 사용하는 플래쉬 칼럼 크로마토그래피에 의해 2.574 g의 19 (35%)를 황색 오일로서 수득하였다: [α] +41.0° (c 0.68).
1H NMR δ 12.70 (s, 1H), 7.29 (d, J = 8.6 Hz, 1H), 6.50 (d, J = 2.3 Hz, 1H), 6.47 (dd, J = 8.8, 2.5 Hz, 1H), 4.17-4.28 (m + s, 8H), 3.92-3.97 (m, 2H), 3.84 (d, J = 11.3 Hz, 1H), 3.20 (d, J = 11.3 Hz, 1H), 1.66 (s, 3H), 1.298 (t, J = 7.2 Hz, 3H), 1.290 (t, J = 7.0 Hz, 3H). 13C NMR δ 172.96, 170.92, 170.42, 162.88, 161.29, 131.84, 110.13, 107.34, 101.52, 83.25, 69.94, 69.02, 67.71, 62.05, 61.10, 39.97, 24.60, 14.33,14.22. C19H26NO7S에 대한 HRMS m/z 계산치, 412.1424 (M + H); 실측치, 412.1440. C19H25NO7S에 대한 분석 계산치: C, 55.46; H, 6.12; N, 3.40. 실측치: C, 55.66; H, 6.21; N, 3.44.
(S)-4,5-디히드로-2-[2-히드록시-4-(5-히드록시-3-옥사펜틸옥시)페닐]-4-메틸-4-티아졸카르복실산 (8). CH3OH (25 mL) 중 50% (w/w) NaOH (3.0 mL, 57 mmol)의 용액을 0℃에서 CH3OH (50 mL) 중 17 (2.0 g, 5.4 mmol)의 용액에 천천히 첨가하였다. 반응 혼합물을 실온에서 16시간 동안 교반하고, 대부분의 용매를 감압 하에 제거하였다. 잔류물을 묽은 NaCl (50 mL) 중에 용해시키고, Et2O (2 x 30 mL)로 추출하였다. 수성 층을 얼음 상에서 냉각시키고, 차가운 6 N HCl에 의해 pH = 2로 산성화시키고, EtOAc (8 x 30 mL)로 추출하였다. 합한 EtOAc 층을 진공 하에 농축시켜 1.78 g의 8 (97%)을 황색 오일로서 수득하였다: [α] +25.3° (c 0.88).
1H NMR δ 7.9 (br s, 1H), 7.21 (d, J = 8.8 Hz, 1H), 6.50 (d, J = 2.4 Hz, 1H), 6.47 (dd, J = 8.8, 2.4 Hz, 1H), 4.15-4.19 (m, 2H), 3.74-3.92 (m, 5H), 3.65-3.70 (m, 2H), 3.20 (d, J = 10.8 Hz, 1H), 1.68 (s, 3H). 13C NMR δ 176.29, 171.96, 163.02, 161.32, 131.97, 109.79, 107.69, 101.49, 82.68, 72.57, 69.19, 67.56, 61.78, 39.78, 24.61. C15H20NO6S에 대한 HRMS m/z 계산치, 342.1006 (M + H), C15H19NNaO6S, 364.0825 (M + Na); 실측치, 342.1014, 364.0826. C15H19NO6S에 대한 분석 계산치: C, 52.78; H, 5.61; N, 4.10. 실측치: C, 52.93; H, 5.83; N, 4.02.
(S)-4,5-디히드로-2-[2-히드록시-4-(4-카르복시-3-옥사부틸옥시)페닐]-4-메틸-4-티아졸카르복실산 (9). CH3OH (30 mL) 중 50% (w/w) NaOH (2.88 mL, 55.1 mmol)의 용액을 CH3OH (62 mL) 중 19 (2.27 g, 5.52 mmol)의 혼합물에 5 분에 걸쳐 0℃에서 첨가하였다. 반응 혼합물을 실온에서 17시간 동안 교반하고, 대부분의 용매를 회전 증발에 의해 제거하였다. 잔류물을 3 M NaCl (70 mL) 중에 용해시키고, Et2O (3 x 40 mL)로 추출하였다. 수성 층을 얼음 상에서 냉각시키고, 차가운 2 N HCl (30 mL)로 처리하고, EtOAc (100 mL, 4 x 50 mL)로 추출하였다. 유기 층을 합하고, 6 M NaCl (80 mL)로 세척하고, 회전 증발에 의해 농축시켰다. 잔류물을 H2O (43 mL) 및 0.1050 N NaOH (52.76 mL, 5.540 mmol)와 합하고, 증기 조에서 가열하고, 핫 석션 여과하고, H2O (18 mL)로 세척하였다. 여과물을 H2O (34 mL)로 희석하고, 동결건조시켰다. 고체를 72℃에서 고 진공 하에서 건조하여, 그의 나트륨 염 (98%)으로서 2.05 g의 9를 무정형 황색 고체로서 수득하였다: [α] +124.3° (c 0.73, H2O).
1H NMR (D2O) δ 7.57 (d, J = 9.0 Hz, 1H), 6.61 (dd, J = 9.0, 2.3 Hz, 1H), 6.52 (d, J = 2.3 Hz, 1H), 4.26-4.30 (m, 2H), 4.06 (s, 2H), 3.90-3.95 (m, 3H), 3.53 (d, J = 11.7 Hz, 1H), 1.74 (s, 3H). 13C NMR (D2O) δ 178.94, 177.92, 177.62, 166.41, 162.21, 134.11, 109.15, 107.12, 102.09, 78.41, 70.23, 69.43, 68.45, 39.67, 23.98. C15H15NNaO7S에 대한 HRMS m/z 계산치, 376.0472 (M - H), C15H16NO7S, 354.0653 (M - Na); 실측치, 376.0479, 354.0663. 샘플 (1.00 g)을 EtOH (수성)으로부터 재결정화하여 0.631 g의 9 (Na 염)를 생성하였다. C15H16NNaO7S에 대한 분석 계산치: C, 47.75; H, 4.27; N, 3.71. 실측치: C, 47.82; H, 4.43; N, 3.75.
실시예 2. 데페리트린 헥사메틸렌 메틸 에테르 (S)-4'-(HO)-DADFT-HXME (10), 상응하는 알콜 유사체 (S)-4'-(HO)-DADFT-HXA (11), 및 그의 추정 대사물 12, 13 및 14의 합성
메틸 에테르-함유 킬레이트화제 10의 합성은 63℃에서 DMF 중 25% NaOCH3 (1 당량)을 사용하는 것에 의해 1,6-디아이오도헥산 (20)으로부터 먼저 6-아이오도-1-메톡시헥산 (21)70을 28% 수율로 생성하는 것을 요구한다 (반응식 2). 62℃에서 DMF 중 K2CO3을 사용하여 데페리트린 에틸 에스테르 (15)와 21의 알킬화에 의해, 중간체 22를 59% 수율로 생성하였다. 에스테르 22의 알칼리 절단은 (S)-4'-(HO)-DADFT-HXME (10)를 97% 수율로 제공하였다. 알콜 11의 합성은 먼저 70℃에서 DMF 중 K2CO3을 사용하는 데페리트린의 에스테르 (15)와 6-아이오도헥실 아세테이트 (23)71의 알킬화에 의해, 디에스테르 24를 53% 수율로 제공하는 것을 포함하였다 (반응식 2). 24의 알칼리 가수분해는 최종 생성물 11을 91%의 재결정화된 수율로 제공하였다.
알콜 11 (12-14)의 예상되는 대사물의 합성은 폴리에테르 산 9와 유사한 방법론을 따랐다 (반응식 3). DADFT 에스테르 15를 K2CO3 및 촉매 아이오다이드 염의 존재 하에 DMF 중 3개의 ω-브로모알카노에이트 (25, 26, 또는 27) 중 1개와 선택적으로 알킬화하였다. 상응하는 디에스테르 28, 29, 및 30을 61, 72, 및 66% 수율로 수득하였다. 다시 한번, 이들 디에스테르를 CH3OH 중 50% NaOH에서 절단하여, 요구된 산 12, 13, 및 14를 각각 99, 90, 및 98% 수율로 생성하였다.
반응식 2. (S)-4,5-디히드로-2-[2-히드록시-4-(6-메톡시헥실옥시)페닐]-4-메틸-4-티아졸카르복실산 (10) 및 (S)-4,5-디히드로-2-[2-히드록시-4-(6-히드록시헥실옥시)페닐]-4-메틸-4-티아졸카르복실산 (11)의 합성a
a시약 및 조건: (a) 25% NaOCH3 (1.0 당량), DMF, 63℃, 17시간, 28%; (b) K2CO3 (2.0 당량), DMF, 62℃, 22시간, 59%; (c) 50% NaOH (수성), CH3OH, 97% (10) (d) K2CO3 (1.9 당량), DMF, 70℃, 18시간, 53%; (c) 50% NaOH (수성), CH3OH, 91% (11).
1-아이오도-6-메톡시헥산 (21). 소듐 메톡시드 (25 wt%, 5.5 mL, 24.1 mmol)를 20분에 걸쳐 DMF (10 mL) 중 20 (4.0 mL, 24.3 mmol)에 시린지로 첨가하였다. 반응 용액을 63℃에서 17시간 동안 가열하였다. 0℃로 냉각시킨 후, 반응 용액을 3:1의 차가운 0.5 N HCl/ 6 M NaCl (200 mL)로 처리하고, EtOAc (2 x 150 mL, 50 mL)로 추출하였다. 유기 추출물을 1% NaHSO3 (150 mL), H2O (2 x 150 mL) 및 6 M NaCl (100 mL)로 세척하고, 용매를 회전 증발에 의해 제거하였다. 4%에 이어서 6% EtOAc/석유 에테르를 사용하는 액체 플래쉬 칼럼 크로마토그래피에 의해 1.61 g의 2170 (28%)을 액체로서 수득하였다.
1H NMR δ 3.37 (t, J = 6.4 Hz, 2H), 3.33 (s, 3H), 3.19 (t, J = 7.0 Hz, 2H), 1.83 (오중선, J = 7.1 Hz, 2H), 1.54-1.62 (m, 2H), 1.33-1.46 (m, 4H). 13C NMR δ 72.78, 58.72, 33.58, 30.46, 29.57, 25.26, 7.25. C7H19INO에 대한 HRMS m/z 계산치, 260.0506 (M + NH4); 실측치, 260.0515. C7H15IO에 대한 분석 계산치: C, 34.73; H, 6.25. 실측치: C, 34.44; H, 6.19.
에틸 (S)-4,5-디히드로-2-[2-히드록시-4-(6-메톡시헥실옥시)페닐]-4-메틸-4-티아졸카르복실레이트 (22). 탄산칼륨 (1.81 g, 13.1 mmol)을 DMF (32 mL) 중 15 (1.77 g, 6.29 mmol) 및 21 (1.56 g, 6.44 mmol)에 첨가하고, 반응 혼합물을 62℃에서 22시간 동안 가열하였다. 빙조에서 냉각시킨 후, 차가운 0.5 N HCl (100 mL)을 첨가한 후, 이어서 EtOAc (120 mL, 2 x 50 mL)로 추출하였다. 유기 층을 합하고, 1% NaHSO3 (100 mL), H2O (3 x 100 mL) 및 6 M NaCl (80 mL)로 세척하고, 용매를 회전 증발에 의해 제거하였다. 10% EtOAc/석유 에테르에 이어서 1:3:6 EtOAc/석유 에테르/CH2Cl2를 사용하는 플래쉬 칼럼 크로마토그래피에 의해 1.47 g의 22 (59%)를 점성 황색 오일로서 수득하였다: [α] +43.3° (c 0.72).
1H NMR δ 12.68 (s, 1H), 7.28 (d, J = 8.6 Hz, 1H), 6.47 (d, J = 2.3 Hz, 1H), 6.43 (dd, J = 8.8, 2.5 Hz, 1H), 4.18-4.29 (m, 2H), 3.97 (t, J = 6.6 Hz, 2H), 3.83 (d, J = 11.3 Hz, 1H), 3.38 (t, J = 6.4 Hz, 2H), 3.34 (s, 3H), 3.19 (d, J = 11.3 Hz, 1H), 1.75-1.83 (m, 2H), 1.65 (s, 3H), 1.56-1.64 (m, 2H), 1.37-1.53 (m, 4H), 1.30 (t, J = 7.0 Hz, 3H). 13C NMR δ 173.02, 170.92, 163.50, 161.34, 131.77, 109.71, 107.40, 101.36, 83.23, 72.86, 68.19, 62.02, 58.70, 39.96, 29.69, 29.14, 26.03, 25.99, 24.61,14.22. C20H30NO5S에 대한 HRMS m/z 계산치, 396.1839 (M + H); 실측치, 396.1858. C20H29NO5S에 대한 분석 계산치: C, 60.74; H, 7.39; N, 3.54. 실측치: C, 60.59; H, 7.29; N, 3.60.
에틸 (S)-4,5-디히드로-2-[2-히드록시-4-(6-아세톡시헥실옥시)페닐]-4-메틸-4-티아졸카르복실레이트 (24). 탄산칼륨 (3.42 g, 24.8 mmol)을 DMF (60 mL) 중 15 (3.255 g, 11.57 mmol) 및 23 [75] (3.44 g, 12.7 mmol)에 첨가하고, 혼합물을 70℃에서 21시간 동안 가열하였다. 0℃로 냉각시킨 후, 차가운 0.5 M HCl (150 mL)을 첨가한 후, 이어서 EtOAc (150 mL, 2 x 80 mL)로 추출하였다. 유기 층을 합하고, 1% NaHSO3 (150 mL), H2O (3 x 150 mL) 및 6 M NaCl (100 mL)로 세척하고, 용매를 회전 증발에 의해 제거하였다. 1:3:6 EtOAc/석유 에테르/CH2Cl2를 사용하는 플래쉬 칼럼 크로마토그래피에 의해 2.60 g의 24 (53%)를 백색 고체로서 수득하였다: mp 58.5-60℃, [α] +40.1° (c 0.98).
1H NMR δ 12.69 (s, 1H), 7.29 (d, J = 9.0 Hz, 1H), 6.47 (d, J = 2.3 Hz, 1H), 6.43 (dd, J = 8.8, 2.5 Hz, 1H), 4.20-4.28 (m, 2H), 4.07 (t, J = 6.6 Hz, 2H), 3.97 (t, J = 6.4 Hz, 2H), 3.84 (d, J = 11.3 Hz, 1H), 3.19 (d, J = 11.3 Hz, 1H), 2.05 (s, 3H), 1.76-1.84 (m, 2H), 1.62-1.70 (m, 2H), 1.66 (s, 3H), 1.38-1.54 (m, 4H), 1.30 (t, J = 7.0 Hz, 3H). 13C NMR δ 173.01, 171.39, 170.93, 163.45, 161.36, 131.79, 109.76, 107.40, 101.35, 83.23, 68.10, 64.58, 62.03, 39.98, 29.07, 28.66, 25.84, 25.83, 24.62, 21.16, 14.23. C21H30NO6S에 대한 HRMS m/z 계산치, 424.1788 (M + H); 실측치, 424.1798. C21H29NO6S에 대한 분석 계산치: C, 59.56; H, 6.90; N, 3.31. 실측치: C, 59.71; H, 6.81; N, 3.33.
(S)-4,5-디히드로-2-[2-히드록시-4-(6-메톡시헥실옥시)페닐]-4-메틸-4-티아졸카르복실산 (10). CH3OH (40 mL) 중 50% (w/w) NaOH (1.87 mL, 35.8 mmol)의 용액을 0℃에서 CH3OH (80 mL) 중 22 (1.41 g, 3.56 mmol)의 용액에 4 분에 걸쳐 첨가하였다. 반응 혼합물을 실온에서 15시간 동안 교반하고, 대부분의 용매를 감압 하에 제거하였다. 잔류물을 2 M NaCl (120 mL) 중에 희석하고, Et2O (3 x 50 mL)로 추출하였다. 수성 층을 얼음 상에서 냉각시키고, 차가운 2 N HCl (30 mL)로 산성화시키고, EtOAc (100 mL, 3 x 50 mL)로 추출하였다. 합한 EtOAc 추출물을 6 M NaCl (60 mL)로 세척하고, 진공 하에 농축시켜 1.275 g의 10 (97%)을 왁스상 연황갈색 고체로서 수득하였다: mp 68-68.5℃, [α] +48.8° (c 0.80, DMF).
1H NMR (DMSO-d6) δ 13.17 (s, 1H), 12.74 (s, 1H), 7.31 (d, J = 8.6 Hz, 1H), 6.52 (dd, J = 2.3, 8.6 Hz, 1H), 6.50 (d, J = 2.3 Hz, 1H), 4.00 (t, J = 6.6 Hz, 2H), 3.79 (d, J = 11.3 Hz, 1H), 3.36 (d, J = 11.3 Hz, 1H), 3.30 (t, J = 6.4 Hz, 2H), 3.21 (s, 3H), 1.66-1.74 (m, 2H), 1.58 (s, 3H), 1.47-1.54 (m, 2H),1.29-1.45 (m, 4H). 13C NMR (DMSO-d6) δ 173.73, 170.03, 162.96, 160.49, 131.57, 108.97, 107.27, 101.13, 82.45, 71.82, 67.80, 57.79, 28.97, 28.47, 25.42, 25.28, 24.11. C18H26NO5S에 대한 HRMS m/z 계산치, 368.1526 (M + H); 실측치, 368.1540. C18H25NO5S에 대한 분석 계산치: C, 58.84; H, 6.86; N, 3.81. 실측치: C, 58.55; H, 6.81; N, 3.80.
(S)-4,5-디히드로-2-[2-히드록시-4-(6-히드록시헥실옥시)페닐]-4-메틸-4-티아졸카르복실산 (11). CH3OH (95 mL) 중 50% (w/w) NaOH (3.12 mL, 59.7 mmol)의 용액을 CH3OH (100 mL) 중 24 (2.53 g, 5.97 mmol)의 혼합물에 0℃에서 32 분에 걸쳐 첨가하였다. 반응 혼합물을 실온에서 1일 동안 교반하고, 대부분의 용매를 감압 하에서 제거하였다. 잔류물을 2 M NaCl (150 mL)로 처리하고, Et2O (3 x 50 mL)로 추출하였다. 수성 층을 얼음 상에서 냉각시키고, 차가운 2 N HCl (50 mL)로 처리하고, EtOAc (2 x 100 mL, 50 mL)로 추출하였다. 유기 층을 합하고, 6 M NaCl (65 mL)로 세척하고, 회전 증발에 의해 농축시켰다. 잔류물을 EtOAc/헥산으로부터 재결정화하였다. 고체를 수집하고, 고진공 하에 58℃에서 건조시켜, 1.917 g의 11 (91%)을 연황색 결정으로서 수득하였다: mp 116-116.5℃, [α] +50.1° (c 0.83, DMF).
1H NMR (DMSO-d6) δ 13.20 (s, 1H), 12.73 (s, 1H), 7.32 (d, J = 9.0 Hz, 1H), 6.52 (dd, J = 8.6, 2.3 Hz, 1H), 6.50 (d, J = 2.3 Hz, 1H), 4.35 (br s, 1H), 4.00 (t, J = 6.4 Hz, 2H), 3.79 (d, J = 11.3 Hz, 1H), 3.36-3.42 (m, 2H), 3.36 (d, J = 11.3 Hz, 1H), 1.66-1.75 (m, 2H), 1.58 (s, 3H), 1.29-1.48 (m, 6H). 13C NMR (DMSO-d6) δ 173.76, 170.04, 162.97, 160.50, 131.59, 108.97, 107.28, 101.13, 82.45, 67.85, 60.64, 32.48, 28.56, 25.35, 25.27, 24.12. C17H24NO5S에 대한 HRMS m/z 계산치, 354.1370 (M + H); 실측치, 354.1384. C17H23NO5S에 대한 분석 계산치: C, 57.77; H, 6.56; N, 3.96. 실측치: C, 57.94; H, 6.50; N, 3.93.
반응식 3. (S)-4,5-디히드로-2-[2-히드록시-4-(5-카르복시펜틸옥시)페닐]-4-메틸-4-티아졸카르복실산 (12), (S)-4,5-디히드로-2-[2-히드록시-4-(3-카르복시프로필옥시)페닐]-4-메틸-4-티아졸카르복실산 (13), 및 (S)-4,5-디히드로-2-[2-히드록시-4-(카르복시메톡시)페닐]-4-메틸-4-티아졸카르복실산 (14)의 합성a
a시약 및 조건: (a) K2CO3 (1.3 당량), NaI, DMF, 65℃, 5일, 61% (28); K2CO3 (1.3 당량), NaI, DMF, 100℃, 2일, 72% (29); K2CO3 (2.1 당량), NaI, DMF, 70℃, 20시간, 66% (30); (b) 50% NaOH (수성), CH3OH, 99% (12), 90% (13), 98% (14).
에틸 (S)-4,5-디히드로-2-[2-히드록시-4-[5-(에톡시카르보닐)펜틸옥시]페닐]-4-메틸-4-티아졸카르복실레이트 (28). 탄산칼륨 (3.19 g, 23.1 mmol), NaI (0.351 g, 2.34 mmol), 및 DMF (25 mL) 중 25 (4.46 g, 20.0 mmol)의 용액을 DMF (100 mL) 중 15 (5.0 g, 17.8 mmol)의 용액에 첨가하였다. 반응 혼합물을 65℃에서 5일 동안 가열하였다. 실온으로 냉각시킨 후, 용매를 회전 증발에 의해 제거하였다. 잔류물을 차가운 0.5 M HCl (200 mL)로 처리하고, EtOAc (150 mL, 2 x 50 mL)로 추출하였다. 유기 추출물을 1% NaHSO3 (100 mL), H2O (100 mL), 6 M NaCl (50 mL)로 세척하고, 용매를 진공 하에 제거하였다. 30% EtOAc/석유 에테르를 사용하는 칼럼 크로마토그래피에 의해 4.586 g의 28 (61%)을 회백색 고체로서 수득하였다: mp 61-62℃, [α] +40.94° (c 0.171).
1H NMR δ 12.68 (s, 1H), 7.28 (d, J = 8.4 Hz, 1H), 6.47 (d, J = 2.4 Hz, 1H), 6.42 (dd, J = 8.8, 2.4 Hz, 1H), 4.24 (dq, J = 7.2, 2.0 Hz, 2H), 4.13 (q, J = 7.2 Hz, 2H), 3.97 (t, J = 6.4 Hz, 2H), 3.84 (d, J = 11.2 Hz, 1H), 3.19 (d, J = 11.2 Hz, 1H), 2.33 (t, J = 7.6 Hz, 2H), 1.77-1.84 (m, 2H), 1.67-1.73 (m, 2H), 1.66 (s, 3H), 1.46-1.54 (m, 2H), 1.30 (t, J = 7.2 Hz, 3H), 1.26 (t, J = 7.2 Hz, 3H). 13C NMR δ 173.70, 172.96, 170.88, 163.38, 161.31, 131.75, 109.73, 107.32, 101.33, 83.20, 67.93, 61.99, 60.37, 39.93, 34.31, 28.85, 25.68, 24.78, 24.58, 14.36, 14.20. C21H30NO6S에 대한 HRMS m/z 계산치, 424.1788 (M + H); 실측치, 424.1784. C21H29NO6S에 대한 분석 계산치: C, 59.56; H, 6.90; N, 3.31. 실측치: C, 59.69; H, 6.78; N, 3.24.
에틸 (S)-4,5-디히드로-2-[2-히드록시-4-[3-(에톡시카르보닐)프로필옥시]페닐]-4-메틸-4-티아졸카르복실레이트 (29). 탄산칼륨 (4.41 g, 32.0 mmol) 및 NaI (182 mg, 1.2 mmol)를 DMF (150 mL) 중 15 (6.90 g, 24.5 mmol) 및 26 (5.27 g, 27.0 mmol)의 혼합물에 첨가하였다. 반응 혼합물을 실온에서 6시간 동안 교반한 다음, 100℃에서 48시간 동안 가열하였다. 실온으로 냉각시킨 후, 용매를 고진공 하에 회전 증발에 의해 제거하고, 잔류물을 0.2 M HCl/6 M NaCl (50 mL)로 처리한 후, 이어서 EtOAc (4 x 30 mL)로 추출하였다. 유기 추출물을 1% NaHSO3 (150 ml), H2O (150 mL) 및 6 M NaCl (150 mL)로 세척하고, 용매를 진공 하에 제거하였다. 30% EtOAc/CH2Cl2를 사용하는 칼럼 크로마토그래피에 의해 6.94 g의 29 (72%)를 담황색 점성 오일로서 수득하였다: [α] +44.35° (c 0.372).
1H NMR δ 12.65 (s, 1H), 7.28 (d, J = 8.4 Hz, 1H), 6.47 (d, J = 2.4 Hz, 1H), 6.42 (dd, J = 8.8, 2.0 Hz, 1H), 4.24 (dq, J = 7.2, 1.6 Hz, 2H), 4.15 (q, J = 7.6 Hz, 2H), 4.03 (t, J = 6.4 Hz, 2H), 3.84 (d, J = 11.2 Hz, 1H), 3.19 (d, J = 11.2 Hz, 1H), 2.51 (t, J = 7.6 Hz, 2H), 2.11 (오중선, J = 6.2 Hz, 2H), 1.66 (s, 3H), 1.30 (t, J = 7.6 Hz, 3H), 1.26 (t, J = 7.2 Hz, 3H). 13C NMR δ 173.21, 172.98, 170.90, 163.15, 161.32, 131.81, 109.91, 107.24, 101.44, 83.23, 67.02, 62.02, 60.63, 39.96, 30.84, 24.60, 24.55, 14.35, 14.22. C19H26NO6S에 대한 HRMS m/z 계산치, 396.1475 (M + H); 실측치, 396.1475. C19H25NO6S에 대한 분석 계산치: C, 57.71; H, 6.37; N, 3.54. 실측치: C, 57.72; H, 6.23; N, 3.52.
에틸 (S)-4,5-디히드로-2-[2-히드록시-4-(에톡시카르보닐메톡시)페닐]-4-메틸-4-티아졸카르복실레이트 (30). 탄산칼륨 (5.29 g, 38.3 mmol) 및 NaI (0.498 g, 3.32 mmol)를 DMF (75 mL) 중 15 (5.035 g, 17.90 mmol)에 첨가하였다. 혼합물을 수분 동안 교반하고, 27 (2.2 mL, 19.8 mmol)을 도입하고, 내용물을 70℃에서 3.5일 동안 가열하였다. 0℃로 냉각시킨 후, 차가운 0.5 M HCl (200 mL)을 첨가한 후, 이어서 EtOAc (200 mL, 2 x 100 mL)로 추출하였다. 유기 층을 합하고, 1% NaHSO3 (200 mL), H2O (2 x 200 mL) 및 6 M NaCl (130 mL)으로 세척하고, 용매를 진공 하에 제거하였다. 1% EtOAc/CH2Cl2에 이어서 6% 아세톤/CH2Cl2를 사용하는 플래쉬 칼럼 크로마토그래피에 의해 4.37 g의 30 (66%)을 점성 황색 오일로서 수득하였다: [α] +45.1° (c 0.88).
1H NMR δ 12.73 (s, 1H), 7.32 (d, J = 8.6 Hz, 1H), 6.50 (d, J = 2.7 Hz, 1H), 6.47 (dd, J = 6.8, 2.5 Hz, 1H), 4.63 (s, 2H), 4.20-4.31 (m, 4H), 3.84 (d, J = 11.3 Hz, 1H), 3.20 (d, J = 11.3 Hz, 1H), 1.66 (s, 3H), 1.305 (t, J = 7.2 Hz, 3H), 1.298 (t, J = 7.0 Hz, 3H). 13C NMR δ 172.89, 170.92, 168.39, 161.91, 161.29, 132.00, 110.74, 107.18, 101.71, 83.28, 65.27, 62.07, 61.68, 40.00, 24.59, 14.28, 14.22. C17H22NO6S에 대한 HRMS m/z 계산치, 368.1162 (M + H); 실측치, 368.1172. C17H21NO6S에 대한 분석 계산치: C, 55.57; H, 5.76; N, 3.81. 실측치: C, 55.72; H, 5.72; N, 3.82.
(S)-4,5-디히드로-2-[2-히드록시-4-(5-카르복시펜틸옥시)페닐]-4-메틸-4-티아졸카르복실산 (12). CH3OH (50 mL) 중 50% (w/w) NaOH (5.00 mL, 95.6 mmol)의 용액을 CH3OH (120 mL) 중 28 (4.434 g, 10.47 mmol)의 혼합물에 0℃에서 7 분에 걸쳐 첨가하였다. 반응 혼합물을 실온에서 2일 동안 교반하고, 대부분의 용매를 감압 하에 제거하였다. 잔류물을 3 M NaCl (110 mL) 중에 용해시키고, Et2O (2 x 100 mL)로 추출하였다. 수성 층을 얼음 상에서 냉각시키고, 차가운 2 N HCl (54 mL)로 처리하고, EtOAc (150 mL, 2 x 60 mL)로 추출하였다. 유기 층을 합하고, 6 M NaCl (100 mL)로 세척하고, 회전 증발에 의해 농축시켰다. 잔류물을 고진공 하에 57℃에서 16시간 동안 건조시켜 3.80 g의 12 (99%)를 담색 결정으로서 수득하였다: mp 153.5-155℃, [α] +47.5° (c 0.76, DMF).
1H NMR (DMSO-d6) δ 12.72 (s, 2H), 7.31 (d, J = 8.6 Hz, 1H), 6.52 (dd, J = 8.6, 2.3 Hz, 1H), 6.49 (d, J = 2.3 Hz, 1H), 4.00 (t, J = 6.4 Hz, 2H), 3.79 (d, J = 11.3 Hz, 1H), 3.36 (d, J = 11.3 Hz, 1H), 2.23 (t, J = 7.2 Hz, 2H), 1.66-1.75 (m, 2H), 1.58 (s, 3H), 1.51-1.60 (m, 2H), 1.36-1.45 (m, 2H). 13C NMR (DMSO-d6) δ 174.46, 173.76, 170.05, 162.96, 160.50, 131.60, 108.98, 107.29, 101.16, 82.46, 67.76, 33.61, 28.26, 25.08, 24.25, 24.12. C17H22NO6S에 대한 HRMS m/z 계산치, 368.1162 (M + H); 실측치, 368.1169. C17H21NO6S에 대한 분석 계산치: C, 55.57; H, 5.76; N, 3.81. 실측치: C, 55.58; H, 5.79; N, 3.78.
(S)-4,5-디히드로-2-[2-히드록시-4-(3-카르복시프로필옥시)페닐]-4-메틸-4-티아졸카르복실산 (13). CH3OH (100 mL) 중 50% (w/w) NaOH (6.34 mL, 0.121 mol)의 용액을 CH3OH (50 mL) 중 29 (6.56 g, 16.6 mmol)의 용액에 0℃에서 적가하였다. 반응 혼합물을 실온에서 36시간 동안 교반하고, 대부분의 용매를 감압 하에 제거하였다. 잔류물을 묽은 NaCl (150 mL) 중에 용해시키고, Et2O (2 x 100 mL)로 세척하였다. 수성 층을 0℃로 냉각시키고, 6 N HCl에 의해 pH = 2로 산성화시켰다. 고체를 여과하고, 차가운 물로 세척하였다. 뜨거운 CH3OH 및 EtOAc 중에서의 결정화에 의해 5.06 g의 13 (90%)을 백색 고체로서 수득하였다: mp 202-204℃, [α] +22.1° (c 0.086, CH3OH).
1H NMR (DMSO-d6) δ 7.32 (d, J = 8.4 Hz, 1H), 6.53 (dd, J = 8.4, 2.0 Hz, 1H), 6.50 (d, J = 2.4 Hz, 1H), 4.03 (t, J = 6.4 Hz, 2H), 3.79 (d, J = 11.2 Hz, 1H), 3.35 (d, J = 11.2 Hz, 1H), 2.38 (t, J = 7.2 Hz, 2H), 1.93 (오중선, J = 7.2 Hz, 2H), 1.57 (s, 3H). 13C NMR (DMSO-d6) δ 177.42, 177.11, 173.34, 166.13, 163.85, 135.00, 112.48, 110.60, 104.58, 85.86, 70.38, 33.42, 27.51, 27.43. C15H18NO6S에 대한 HRMS m/z 계산치, 340.0849 (M + H); 실측치, 340.0849. C15H17NO6S에 대한 분석 계산치: C, 53.09; H, 5.05; N, 4.13. 실측치: C, 52.81; H, 5.17; N, 4.09.
(S)-4,5-디히드로-2-[2-히드록시-4-(카르복시메톡시)페닐]-4-메틸-4-티아졸카르복실산 (14). CH3OH (75 mL) 중 50% (w/w) NaOH (5.60 mL, 0.107 mol)의 용액을 CH3OH (120 mL) 중 30 (4.32 g, 11.76 mmol)의 용액에 0℃에서 10분에 걸쳐 첨가하였다. 반응 혼합물을 실온에서 2일 동안 교반하고, 대부분의 용매를 감압 하에 제거하였다. 잔류물을 H2O (120 mL) 중에 용해시키고, Et2O (2 x 100 mL)로 추출하였다. 수성 층을 얼음 상에서 냉각시키고, 2 N HCl (60 mL)로 처리하고, EtOAc (150 mL, 2 x 100 mL)로 추출하였다. 유기 층을 합하고, 6 M NaCl (100 mL)로 세척하고, 회전 증발에 의해 농축시켰다. 잔류물을 고진공 하에 건조시켜 3.589 g의 14 (98%)를 연황색 고체로서 수득하였다: mp 206-206.5℃ (dec), [α] +56.3° (c 0.76, DMF).
1H NMR (DMSO-d6) δ 13.14 (s, 2H), 12.75 (s, 1H), 7.34 (d, J = 8.6 Hz, 1H), 6.53 (dd, J = 8.6, 2.3 Hz, 1H), 6.47 (d, J = 2.3 Hz, 1H), 4.75 (s, 2H), 3.79 (d, J = 11.3 Hz, 1H), 3.37 (d, J = 11.3 Hz, 1H), 1.58 (s, 3H). 13C NMR (DMSO-d6) δ 173.71, 170.04, 169.72, 161.94, 160.33, 131.62, 109.52, 107.17, 101.46, 82.47, 64.57, 39.34, 24.09. C13H14NO6S에 대한 HRMS m/z 계산치, 312.0536 (M + H); 실측치, 312.0546. C13H13NO6S에 대한 분석 계산치: C, 50.16; H, 4.21; N, 4.50. 실측치: C, 50.06; H, 4.38; N, 4.41.
화합물의 생물학적 검정
실시예 3 내지 10에 사용된 예시적인 물질 및 방법은 하기에 제시된다.
물질. 수컷 검은머리카푸친 원숭이는 월드 와이드 프라이메이츠(World Wide Primates) (플로리다주 마이애미)로부터 입수하였다. 수컷 스프라그-돌리 래트는 하를란 스프라그-돌리(Harlan Sprague-Dawley) (인디아나주 인디애나폴리스)로부터 입수하였다. 초순수 염은 존슨 매티 일렉트로닉스(Johnson Matthey Electronics) (영국 로이스톤)로부터 입수하였다. 모든 혈액학 및 생화학적 연구는 안테크 다이어그노스틱스(Antech Diagnostics) (플로리다주 탐파)에 의해 실행되었다. 조직병리학적 분석은 플로리다 베트 패쓰(Florida Vet Path) (플로리다주 부쉬넬)에 의해 수행되었다. 원자 흡수 (AA) 측정은 퍼킨-엘머 모델 5100 PC (코네티컷주 노워크) 상에서 이루어졌다.
생물학적 방법. 모든 동물 실험 치료 프로토콜은 플로리다 대학의 기관 동물 실험 윤리 위원회(University of Florida's Institutional Animal Care and Use Committee)에 의해 검토 및 승인되었다.
비 철-과부하된 래트의 담관의 캐뉼라삽입. 캐뉼라삽입은 이전에 기재되었다. 38,40 담즙 샘플을 최대 48시간 동안 3시간 간격으로 수컷 스프라그-돌리 래트 (400-450 g)로부터 수집하였다. 소변 샘플(들)을 24시간 간격으로 취하였다. 샘플 수집 및 취급은 이전에 기재된 것과 같다.38,40
검은머리카푸친 원숭이의 철 부하. 원숭이 (3.5-6.5 kg)는 체중 kg 당 철 약 500 mg을 제공하도록 앞선 간행물에서 명시된 바와 같이 정맥내 철 덱스트란으로 철 과부하되었고; 혈청 트랜스페린 철 포화도는 70 내지 80%로 상승하였다.38,40 철-킬레이트화제를 평가하는 실험에 임의의 동물을 사용하기 전에 적어도 20의 반감기, 60일이 경과하였다.
영장류 분변 및 소변 샘플. 분변 및 소변 샘플을 24시간 간격으로 수집하고, 이전에 기재된 바와 같이 처리하였다.38,40,74 간단히, 수집을 시험 약물의 투여전 4일에 시작하고, 약물을 제공한 후 추가의 5일 동안 계속하였다. 철 농도를 다른 간행물에 제시된 화염 흡수 분광분석법에 의해 결정하였다.38,40
약물 제조 및 투여. 철 클리어링 실험에서, 래트에 300 μmol/kg의 용량으로 8-14를 경구로 제공하였다. 리간드 9 및 12-14를 또한 동일한 용량으로 피하로 제공하였다. 영장류에 75 μmol/kg의 용량으로 8-9 및 11-14를 경구로 제공하였다. 리간드 9 및 12-14를 또한 동일한 용량으로 피하로 제공하였다. 킬레이트화제를 그의 일나트륨 염 (증류수 중 유리 산의 현탁액에 1 당량의 NaOH의 추가에 의해 제조함)으로서 투여하였다.
킬레이트화제 철 클리어링 효율 (ICE)의 계산. 용어 "ICE"는 킬레이트화제에 의해 유발된 철 배출의 양의 측정으로서 사용된다. 백분율로 표현된 ICE는 (리간드-유도 철 배출량/이론적 철 배출량) x 100으로서 계산된다. 예시하기 위해, Fe(III)과의 1:1 착물을 형성하는 헥사덴테이트 킬레이트화제인 DFO 1 mmol의 투여 후의 이론적 철 배출량은 철 1 mg-원자이다. 킬레이트화제의 이론적 철 배출량은 2:1의 리간드:철 착물을 기초로 하여 생성되었다. 래트 및 원숭이에서의 효율은 다른 경우에 설정된 바와 같이 계산하였다.37 데이터를 평균 ± 평균의 표준 오차로서 제시하고; p-값을 일측 스튜던트 t-검정 (여기서, 불균등 분산이 상정됨)을 통해 작성하며, <0.05의 p-값을 유의한 것으로 간주하였다. 9 및 12-14가 경구 및 피하로 제공된 원숭이에 대한 p-값은 일측 대응표본 스튜던트 t-검정을 통해 작성하고; <0.05의 p-값을 유의한 것으로 간주하였다.
설치류로부터의 킬레이트화제 조직 분포 샘플 수집. 수컷 스프라그-돌리 래트 (250-350 g)에 300 μmol/kg의 용량으로 상기 기재된 바와 같이 제조된 8 및 11의 일나트륨 염을 단일 피하로 주사하였다. 투여한 후 0.5, 1, 2, 4 및 8시간째에 (시점당 n = 3마리의 래트), 동물을 CO2 기체에 노출시켜 안락사시켰다. 심장 천자를 통해 시트르산나트륨을 함유하는 바큐테이너 내로 혈액을 획득하였다. 혈액을 원심분리하고, 분석을 위해 혈장을 분리하였다. 간, 신장, 심장, 및 췌장을 동물로부터 제거하고 동결시켰다.
조직 분석 방법. 8로 치료된 동물의 조직 샘플을 HPLC 분석을 위해 비 1:1 (w/v)로 H2O에서 이들을 균질화함으로써 제조하였다. 이어서, 세정액으로서, 비 1:3 (w/v)의 CH3OH를 첨가하고, 혼합물을 30분 동안 -20℃에서 저장하였다. 이 균질물을 원심분리하였다. 상청액을 H2O로 희석하고, 볼텍싱시키고, 0.2 μm 막으로 여과하였다. 분석용 분리를 이전에 기재된 바와 같이 310 nm에서의 UV 검출에 의해 슈펠코 디스커버리 RP 아미드 C16 HPLC 시스템에서 수행하였다.44,75 이동상 및 크로마토그래피 조건은 하기와 같았다: 용매 A, 5% CH3CN/95% 완충제 (25 mM KH2PO4 + 2.5 mM 1-옥탄술폰산, pH 3.0); 용매 B 60% CH3CN/40% 완충제.
11로 치료된 동물의 조직 샘플을 HPLC 분석을 위해 비 1:3 (w/v)으로 0.5 N HClO4에서 이들을 균질화함으로써 제조하였다. 이어서, 세정으로서, 비 1:3 (w/v)의 CH3OH를 첨가하고, 혼합물을 30분 동안 -20℃에서 저장하였다. 이 균질물을 원심분리하였다. 상청액을 95% 완충제 (25 mM KH2PO4, pH 3.0)/5% CH3CN으로 희석하고, 볼텍싱시키고, 0.2 μm 막으로 여과하였다. 분석용 분리를 이전에 기재된 바와 같이 310 nm에서의 UV 검출에 의해 슈펠코 아센티스 익스프레스 RP-아미드 HPLC 시스템에서 수행하였다 [47,80]. 이동상 및 크로마토그래피 조건은 8에 대해서와 같다.
리간드 농도를 시마즈 등급-VP 7.4 소프트웨어를 사용하여 비가중 최소-사각 선형 회귀에 의해 보정 곡선에 대해 보정된 피크 면적으로부터 계산하였다. 방법은 0.25 μM의 검출 한계를 가지며, 1-1000 μM의 범위에 걸쳐 재현가능하고 선형이었다. 조직 분포 데이터는 평균으로서 제공되고; p-값은 일측 스튜던트 t-검정 (여기서, 불균등 분산이 상정됨)을 통해 작성하며; <0.05의 p-값을 유의한 것으로 간주하였다.
래트에서 (S)-4'-(HO)-DADFT-HXA (11)의 독성 평가. 리간드 11에 대한 10-일 독성 시험을 설치류에서 수행하였다. 수컷 스프라그-돌리 래트 (n=5, 375-400 g)에 384 μmol/kg/일의 용량으로 10 일 동안 경구로 1일 1회로 그의 일나트륨 염으로서 투여되는 약물을 제공하였다. 이 용량은 그의 나트륨 염으로서의 DFT (1) 100 mg/kg/일과 동등하다는 것에 유의한다. 래트를 개별적 대사 케이지에 격납하고, 매일 칭량하였다. 기준선 (제0일) 소변 샘플을 수집하고, 그의 Kim-1 함량에 대해 평가하였다 (문헌 [Bergeron et al., J. Med. Chem. 57 (2014) 9259-9291; Bergeron et al., Biometals 24 (2011) 239-258]); 각각의 동물은 그 자신의 대조군으로서의 역할을 하였다. 냉각된 소변을 이전에 기재된 것과 같이 24-시간 간격으로 대사 케이지에서 수집하여 (문헌 [Bergeron et al., Biometals 24 (2011) 239-258]), Kim-1 수준을 결정하게 하였다. 래트는 밤새 단식하고, 아침에 맨 먼저 킬레이트화제를 제공받았다. 설치류에 ~3시간 후 약물을 공급하고, 밤새 단식하기 전에 ~5시간 동안 음식에 접근시켰다. 동물을 약물 후 1일에 안락사시켰다 (제11일). 일상적 CBC 및 혈청 화학의 성능을 위해 혈액을 수집하였다 (문헌 [Bergeron et al., Blood 79 (1992) 1882-1890]). 광범위한 조직 (문헌 [Bergeron et al., J. Med. Chem. 42 (1999) 2432-2440])을 수집하고, 조직병리학적 분석을 위해 외부의 실험실에 제출하였다. 추가의 연령-정합 래트를 CBC 및 혈청 화학 및 조직병리학에 대해 비치료된 대조군으로서 제공하였다. 소변을 이들 동물에서 전혀 수집하지 않았다. 정상 철 저장을 갖는 래트에 대해 연구를 수행하였다.
실시예 3. (S)-4'-(HO)-DADFT-norPE (7)의 조직 분포/대사
상기 기재된 바와 같이, 7을 300 μmol/kg의 용량으로 래트에게 피하로 제공한 경우, 2로의 절단은 전혀 없었다 (도 2). 8 또는 9의 존재에 대한 HPLC를 통한추가의 분석을 조직에 적용한 경우, 상응하는 알콜 8로의 7의 말단 메틸의 절단이 발생하였다 (도 5). 그러나, 카르복실산 9는 검출되지 않았고, 이는 아마도 8로의 모체 7의 대사의 정도가 매우 작기 때문이다. 산 9로의 알콜 8의 전환이 효율적으로 일어날 수 있음을 확증하기 위해, 설치류에 합성 알콜 8을 300 μmol/kg의 용량으로 피하로 제공하였다. 래트를 약물 후 0.5, 1, 2, 4, 및 8시간에서 안락사시켰다. 동물의 혈장, 간, 신장, 심장 및 췌장을 제거하고, 8 및 그의 추정 대사물 9의 존재에 대해 평가하였다. 나타난 9로의 8의 산화의 정도 및 속도는 놀라웠다 (도 5). 약물 후 0.5시간에서의 혈장에서, 8의 거의 60%가 9로 전환되었다. 투여 후 2시간에서, 약물의 88%는 대사물 형태로 있다. 모체 8 및 대사물 9 모두 8시간 시점에 확인되지 않았다. 유사한 이야기가 간에서 나타났다 (도 5). 약물 후 0.5시간에서, 약물 (모체 + 대사물)의 단지 53%가 모체 8 형태로 있다. 1시간에서, 대사물 9는 전체의 59%를 차지한다. 모체 대 대사물 비는 2 및 4시간 시점에 유사하다. 8시간에서, 매우 소량의 모 알콜 8이 남아 있고, 대사물 9는 전혀 남아있지 않았다. 신장, 심장 및 췌장은 또한 9로의 8의 유사 및 유의한 전환을 입증하였다 (도 5).
실시예 4. 비-철-과부하된 담관 캐뉼라삽입 설치류에서 2 및 7-9의 킬레이트화제-유도 철 클리어런스
화합물 2 및 7 (표 2)의 ICE 값은 이력이 있고, 비교 목적을 위해 포함하였다. 킬레이트화제를 래트에게 300 μmol/kg의 용량으로 경구로 제공하고; 9를 또한 동일한 용량으로 피하로 제공하였다. 화합물 2 (log Papp = -1.05)는 1.1 ± 0.8%의 ICE로 최소로 유효한 리간드였다.50 유사체 7 (log Papp = -0.89)은 26.7 ± 4.7%의 ICE로 가장 유효하였다.59 7의 2가지 추정 대사물인 리간드 8 (log Papp = -0.53) 및 9 (log Papp = -1.63)는 경구로 제공된 경우 모 약물 7보다 현저하게 덜 활성이었다. 8의 ICE는 15.4 ± 5.6% (p < 0.02)인 반면, 9의 ICE는 또한 6.2 ± 1.7% (p < 0.005)이었다. 리간드 9가 매우 친수성 (log Papp = -1.63)이기 때문에, 경구 투여 시의 활성의 결여는 그의 불량한 경구 흡수 때문인 것으로 보인다. 실제로, 9를 래트에게 300 μmol/kg의 용량으로 피하로 제공한 경우, 그의 ICE는 약물을 경구로 투여했을 때의 거의 2배인 11.3 ± 3.4%였다 (p < 0.05).
표 1. 래트 및 검은머리카푸친 영장류에게 제공된 철 킬레이트화제의 철 클리어링 효율 및 상기 화합물의 log Papp
a데이터를 옥탄올 층에서 나타난 킬레이트화제의 분획의 로그 (log Papp)로 표현하고; 측정을 "진탕 플라스크" 직접 방법을 사용하여, 트리스 완충제, pH 7.4에서 행하였다. b설치류에서, n= 3 (7), 4 (3-6), 5 (1), 6 (DFO) 또는 8 (2). 약물을 150 (데스페랄 및 1) 또는 300 μmol/kg (2-7)의 용량으로 표에 나타낸 바와 같이 경구로 (po) 또는 피하로 (sc) 제공하였다. 약물을 40% 크레모포르 RH-40/물 (DFO 및 1), 증류수 (5)에 용해시키거나, 캡슐로 투여 (7)하거나, 또는 증류수 중 유리 산의 현탁액에 NaOH 1 당량의 첨가에 의해 제조된 그의 일나트륨 염으로서 제공 (2-4, 6)하였다. 각각의 화합물의 효율을 치료된 동물의 철 배출량으부터 동물의 대조군의 철 배출량을 뺌으로써 계산하였다. 이어서, 이 수를 이론 배출량으로 나누고; 결과를 백분율로 표현하였다. cICE는 48시간 샘플 수집 기간을 기반으로 한다. 담즙 및 소변으로 배출된 철의 상대적인 백분율은 괄호 안에 있다. d영장류에서, n= 3 (6), 4 (캡슐d 중 1, 3-5, 7), 5 (DFO) 또는 7 (그의 일나트륨 염e으로서 2, 7). 킬레이트화제를 75 (7) 또는 150 μmol/kg (DFO, 1-6)의 용량으로 경구로 또는 피하로 제공하였다. 리간드를 40% 크레모포르 RH-40/물 (1, 3, 4), 증류수 (DFO, 5)에 용해시키거나, 캡슐로 투여 (7d)하거나, 또는 증류수 중 유리 산의 현탁액에 NaOH 1 당량의 첨가에 의해 제조된 그의 일나트륨 염으로서 제공 (2, 6, 7 f)하였다. ICE는 약물 전 4일 동안의 철 배출량을 평균내고, 약물의 투여 후 2-일의 철 클리어런스로부터 이들 값을 빼고, 이어서 이론 배출량으로 나눔으로써 계산하였고; 결과는 백분율로 나타낸다. 분변 및 소변에서 배출된 철의 상대적인 백분율은 괄호 안에 있다.
표 2. 래트 및 검은머리카푸친 영장류에게 제공된 철 킬레이트화제의 철 클리어링 효율 및 상기 화합물의 Log Papp
a데이터는 옥탄올 층에서 나타난 킬레이트화제의 분획의 로그 (log Papp)로 표현하고; 측정을 "진탕 플라스크" 직접 방법을 사용하여, 트리스 완충제, pH 7.4에서 행하였다.
b설치류에서, 약물을 300 μmol/kg의 용량으로 경구로 (po) 또는 피하로 (sc) 제공하였다. 약물을 캡슐로 투여 (7)하거나, 또는 증류수 중 유리 산의 현탁액에 NaOH 1 당량의 첨가에 의해 제조된 그의 일나트륨 염으로서 제공 (2, 8-14)하였다. 각각의 화합물의 효율을 처리된 동물의 철 배출량으로부터 동물 대조군의 철 배출량을 뺌으로써 계산하였다. 이어서, 이 수를 이론 배출량으로 나누고; 결과는 백분율로 표현하였다.
cICE는 48시간 샘플 수집 기간을 기반으로 한다. 담즙 및 소변으로 배출된 철의 상대적인 백분율은 괄호 안에 있다.
d영장류에서, 킬레이트화제를 75 μmol/kg (7-9, 11-14) 또는 150 μmol/kg (2)의 용량으로 경구로 또는 피하로 제공하였다.
약물을 캡슐로 투여 (2e)하거나, 또는 증류수 중 유리 산의 현탁액에 NaOH 1 당량의 첨가에 의해 제조된 그의 일나트륨 염으로서 제공 (2f)하였다. 효율은 약물 전 4일 동안의 철 배출량을 평균내고, 약물의 투여 후 2-일의 철 클리어런스로부터 이들 수를 빼고, 이어서 이론 배출량으로 나눔으로써 계산하였고; 결과는 백분율로 표현하였다. 분변 및 소변으로 배출된 철의 상대적인 백분율은 괄호 안에 있다.
g성능 비 (PR)는 평균 ICE영장류/ICE설치류로서 정의한다.
실시예 5. 철-과부하된 영장류에서 2 및 7-9의 킬레이트화제-유도 철 클리어런스
영장류 철 클리어런스 데이터를 표 2에 제공한다. 화합물 2 및 7에 대한 ICE 값은 이력이 있고, 비교 목적을 위해 포함하였다. 킬레이트화제를 원숭이에게 75 (7-9) 또는 150 μmol/kg (2)의 용량으로 경구로 제공하고; 9를 또한 영장류에게 75 μmol/kg의 용량으로 피하로 제공하였다. 리간드 2의 ICE는 16.8 ± 7.2% 였다.50 래트에 의해서 마찬가지로, 화합물 7은 캡슐로 경구로 제공할 때 26.3 ± 9.9%의 ICE를 갖고, 그의 일나트륨 염으로서 경구로 투여할 때 28.7 ± 12.4%의 ICE를 갖는 가장 유효한 철 탈조합제였다.59 7의 추정 대사물인 8은 7보다 더 친지성 (log Papp = -0.53 대 -0.89)이지만, 그의 ICE는 9.8 ± 3.4%로 더 낮았다 (p < 0.003, 표 2). 경구로 제공된 9의 ICE는 보다 더 낮아서, 단지 1.7 ± 1.4%였다. 약물을 경구로 제공하였던 동일한 군의 원숭이에게 9를 피하로 투여한 경우, ICE는 10-배 초과만큼 17.4 ± 9.7% (p < 0.03)로 증가하였다. 이는, 9와 같이 고도로 하전된 리간드 (log Papp = -1.63)는 이가 장 점막을 횡단하도록 하지 않지만, 친수성 대사 전구체는 그렇게 한다는 아이디어와 관련이 있다.
실시예 6. 대사적으로 프로그램화된 철 킬레이트화제
따라서, 대사적으로 프로그램화된 철 킬레이트화제의 설계는 알콜 8이 카르복실산 9로 매우 효율적으로 산화된다는 관찰 (도 4 및 5)로부터 유래된다. 이의 모든 것에 대한 필연적 결과는 모 폴리에테르 (S)-4'-(HO)-DADFT-norPE (7)의 3,6-디옥사헵틸 기를 장쇄 알콜로 대체한 것이 우수한 경구 흡수를 갖는 매우 친지성인 킬레이트화제를 제공한다는 것이다. 흡수되면, 리간드는 그의 덜 친지성이고 덜 독성인 산 대응물로 대사될 수 있다. 이 대사 프로그램화는, 증진된 킬레이트화제 친지성과 ICE 사이에 나타나는 민감한 균형을 이용하고, 친지성에서의 증가와 통상적으로 연관되는 독성에서의 수반되는 증가를 개선하는 혁신적인 방법을 나타낸다.
따라서, (S)-4'-(HO)-DADFT 플랫폼에 기반을 둔 5개의 상이한 리간드를 조립하였다 (반응식 2 및 3): 1) 7의 헥사메틸렌 유사체, (S)-4,5-디히드로-2-[2-히드록시-4-(6-메톡시헥실옥시)페닐]-4-메틸-4-티아졸카르복실산 [S)-4'-(HO)-DADFT-HXME, 10]; 2) 10의 상응하는 알콜, (S)-4,5-디히드로-2-[2-히드록시-4-(6-히드록시헥실옥시)페닐]-4-메틸-4-티아졸카르복실산 [(S)-4'-(HO)-DADFT-HXA, 11]; 3) 11의 추정 제1 대사물, (S)-4,5-디히드로-2-[2-히드록시-4-(5-카르복시펜틸옥시)페닐]-4-메틸-4-티아졸카르복실산 [(S)-4'-(5-카르복시펜틸옥시)-DADFT, 12]; 4) 11의 β-산화 생성물, (S)-4,5-디히드로-2-[2-히드록시-4-(3-카복시프로필옥시)페닐]-4-메틸-4-티아졸카르복실산 [(S)-4'-(3-카복시프로필옥시)-DADFT, 13], 및 5) 11의 제2 β-산화 생성물, (S)-4,5-디히드로-2-[2-히드록시-4-(카르복시메톡시)페닐]-4-메틸-4-티아졸카르복실산 [(S)-4'-(카르복시메톡시)-DADFT, 14]. 모 알콜 11의 그의 추정 대사물 12-14로의 전환 (도 6)을, 300 μmol/kg의 용량으로 피하로 11이 제공된 래트에서 평가하였다. 또한, 리간드를 래트 및 영장류에서 그의 log Papp 및 그의 ICE에 대해 평가하였다 (표 2).
실시예 7. (S)-4'-(HO)-DADFT-HXA (11)의 조직 분포/대사: 대사적으로 프로그램화된 리간드
알콜 11의 그의 추정 대사물 12-14로의 전환 (도 6)이 생체내에서 일어나는 것을 입증하기 위해서, 래트에 300 μmol/kg의 용량으로 피하로 모 알콜 11을 제공하였다. 래트를 약물 후 0.5, 1, 2, 4 및 8시간에 안락사시켰다. 11→ 12-14의 전환을 동물의 혈장, 간, 신장, 심장 및 췌장에서 평가하였다. 11→ 12-14의 유의한 전환은 시험된 모든 조직에서 확인되었다 (도 7). 펼쳐진 11→ 12-14의 대사의 정도 및 속도는 놀라웠다. 킬레이트화제 11 및 그의 대사물은 약물 후 0.5시간에 혈장 중 400 μM의 농도를 달성한다. 이 조직 농도는 4-노르폴리에테르 7에 의해 보여진 것과 매우 유사하다 (도 5). 그러나, 7에 의해, 모체는 전체 약물 농도의 95%를 나타내는 반면, 그의 대사물 (8)은 전체 약물의 단지 5%를 차지하였다. 0.5시간에서의 혈장 중 11의 경우에서, 전체 (모체 + 대사물)의 단지 22%가 모체 11의 형태로 있었다 (도 7). 제1 β-산화 생성물 13은 전체의 62%를 차지하는 한편, 제2 β-산화 생성물 14는 전체의 16%를 나타냈다. 모체 11 대 그의 대사물 13 및 14의 비는 1 및 2시간 시점에서 유사하였다. 투여 후 4시간이 되었을 때, 모체 11은 더 이상 검출가능하지 않았고, 대사물 13 및 14 각각이 전체의 50%를 차지하였다. 투여 후 8시간에, 전체 혈장 약물 농도는 23 μM로 감소하였다. 대사물 13이 이 양의 65%를 차지한 한편, 나머지는 대사물 14의 형태로 있었다. 알콜 11의 제1 산화 생성물인 디카르복실산 12는 혈장에서 전혀 검출되지 않았다.
11→ 12-14의 유의한 전환이 또한 간에서 발생하였다 (도 7). 흥미롭게도, 모체 11은 임의의 시점에 간에서 확인되지 않았다. 그러나, 혈장과 달리, 알콜 11의 소량의 제1 산화 생성물인 디카르복실산 12를 약물 후 0.5 및 1시간에 간에서 확인하였다. 0.5시간에, 12는 전체 약물 (모체 + 대사물)의 11%를 나타내고; 제1 β-산화 생성물 13이 전체의 71%를 차지하는 한편, 제2 β-산화 생성물 14는 전체의 18%를 나타냈다. 투여 후 1시간에서, 간에서의 대사물 12 및 13의 농도는 각각 전체의 2% 및 59%로 감소한 반면, 14의 비율은 39%로 증가하였다 (도 7). 리간드 12는 투여 후 간 2, 4, 또는 8시간에 간에서 검출되지 않았다. 대사물 13은 2시간에서 전체 약물 (대사물)의 66%, 및 4시간에서 전체의 70%를 차지하였다. 투여 후 8시간이 되었을 때, 13은 간에 전혀 남지 않고, 단지 미량의 14만 검출되었다.
모 약물 11을 약물 후 0.5시간에 미량으로 신장에서 확인하고, 카르복실산 12를 약물 후 0.5 및 1시간에 확인하였다. 제1 β-산화 생성물인 대사물 13은 신장에서 매우 높은 수준 (0.5 및 1시간에 ~300 nmol/g 습윤 중량)을 달성하지만, 약물 후 8시간에 검출가능하지 않다. 제2 β-산화 생성물인 대사물 14 또한 0.5, 1 및 2시간에 신장에서 높은 수준 (각각 156, 201, 및 161 nmol/g 습윤 중량)에 도달하였지만, 8시간에서 단지 5 nmol/g 습윤 중량으로 감소하였다.
모 약물 11을 약물 후 0.5시간에 26 nmol/g 습윤 중량으로 심장에서 확인하였다. 디카르복실산 12는 임의의 시점에 심장 조직에서 확인되지 않았다. 심장에서 대사물 13의 농도는 약물 후 0.5 및 1시간에 ~46 nmol/g 습윤 중량이었지만, 이후 시점에서는 확인되지 않았다. 대사물 14를 투여 후 0.5 및 1시간에 각각 17 및 23 nmol/g 습윤 중량으로 확인하였지만, 2-8시간 시점에는 확인되지 않았다 (도 7).
췌장에서, 약물 후 0.5시간에 오직 모체 11이 < 5 nmol/g 습윤 중량으로 확인되었다. 대사물 12는 임의의 시점에 확인되지 않았다. 리간드 13은 0.5 및 1시간 샘플에서 각각 19 및 23 nmol/g 습윤 중량으로 존재하였다 (도 7). 미량의 14를 투여 후 0.5, 1 및 2시간에서 확인하였다. 리간드 11-14는 약물 후 4 또는 8시간에 췌장에서 검출되지 않았다.
실시예 8. 비-철-과부하된 담관 캐뉼라삽입 설치류에서 10-14의 킬레이트화제-유도 철 클리어런스
리간드 10-14를 래트에게 300 μmol/kg의 용량으로 경구로 투여하고; 12-14를 동물에게 동일한 용량으로 피하로 제공하였다. 래트에서 평가된 제1 킬레이트화제는 11의 메틸 에테르 유사체인 10이었다. 리간드 10은 매우 친지성 (log Papp = 0.95)이고, 또한 매우 독성이다. 이를 담관 캐뉼라삽입 래트에게 경구로 제공한 경우, 동물 중 1마리는 약물 후 약 22시간에 사망하였다. 남아있는 설치류를 그의 급속한 악화 상태로 인해 투여 후 24시간에 안락사시켰다. 본 발명자들은 2의 4'-부톡시 유사체 (log Papp = 1.02)인 (S)-2-(4-부톡시-2-히드록시페닐)-4,5-디히드로-4-티아졸카르복실산의 경우에 이러한 동일한 시나리오 (사망이 24시간 내에 일어남)를 확인하였다.72 그럼에도 불구하고, 10은 매우 활성인 탈조합제였다. 10으로 치료된 래트에 대한 기준선 철 배출량은 철 5 μg/kg이었다. 약물-유도 철 배출은, 약물 후 6시간에 철 300 μg/kg로 피크였고, 설치류를 투여 후 24시간 이내에 안락사시킬 때 여전히 철 80 μg/kg이었다. 약물의 ICE는 15.8 ± 3.7%였고 (표 2), 분명히 동물이 더 많이 생존하였을 것이다. 10의 ICE는 설치류에 의해 확인된 명백한 독성으로 인해 영장류에서는 평가하지 않았다. 10의 ICE 및 독성은 분자의 친지성에 따랐다. 그 다음, O-탈메틸화된, 10의 대사적으로 불안정성 유사체인 11을 평가하였다.
알칸올, 예를 들어, 6-(HO) 헥실 단편을 15의 4'-(HO) 위치에 고정하여 11을 유발하였다 (반응식 2). 이는 10보다 덜 친지성 (log Papp = 0.21)이며 덜 독성인 리간드를 생성하였다. 킬레이트화제 11을 래트에게 300 μmol/kg의 용량으로 경구로 제공하였다. 약물은 잘 흡수되었고, 9.9 ± 0.8%의 ICE을 가지며, 임의의 명백한 독성을 나타내지 않았다. 상기 기재된 바와 같이, 리간드 11을 래트에게 피하로 제공한 경우, 이는 상응하는 친수성 대사물인 카르복실산 (12, log Papp = -1.90)64,66으로 빠르게 전환되었으며, 산 13 log Papp = -2.21 및 산 14 log Papp = -1.98로 β-산화73되었다 (도 6). 12-14의 ICE를 300 μmol/kg의 용량으로 경구 및 피하로 약물을 제공한 설치류에서 결정하였다. 추정 제1 대사물인 12의 경구 ICE는 11의 것과 유사하고, 8.8 ± 1.8% (p > 0.05)였다. 그러나, 13 및 14의 경구 ICE는 11보다 현저히 더 적고, 각각 3.7 ± 1.7% (p < 0.001) 및 2.6 ± 1.6% (p < 0.005)였다. 12 및 13을 래트에 피하로 제공한 경우, 그의 ICE는 약물을 경구로 투여할 때의 오차 내에 있었다 (표 2). 대조적으로, 피하로 제공된 14의 ICE (6.0 ± 1.9%)는 약물을 경구로 제공한 경우 (2.6 ± 1.6%, p < 0.05)의 2배 초과였다.
실시예 9. 철-과부하된 영장류에서 11-14의 킬레이트화제-유도 철 클리어런스
리간드 11을 영장류에게 75 μmol/kg의 용량으로 경구로 투여하고; 12-14를 동일한 용량으로 경구 및 피하로 제공하였다. 6-(HO)-헥실 단편이 2의 4'-(HO) 위치에 고정된 리간드 11은 매우 친지성이었다 (log Papp = 0.21). 원숭이에게 제공된 이 화합물의 ICE는 21.9 ± 3.6%였다 (표 2). 11의 보다 더 친수성인 대사물인 12-14의 ICE는 모두 모체보다 현저하게 적었다. 알콜 11의 제1 산화 생성물인 디카르복실산 12 (log Papp = -1.90)는 이를 경구로 제공한 경우 (p < 0.01) 영장류에서 10.6 ± 4.0%의 ICE를 가졌다. 제1 및 제2 β-산화 생성물인 13 (log Papp = -2.21) 및 14 (log Papp = -1.98)는 또한 이들을 경구로 투여한 경우 11보다 유의하게 덜 효과적이었다 (각각 5.4 ± 1.5% (p < 0.005) 및 3.0 ± 2.7% (p < 0.002)). 다시, 경구로 투여된 12-14의 효능의 실질적인 감소의 이유는 그들의 전하로 인한 디카르복실산의 불량한 GI 흡수에 기인할 가능성이 있었다: 이들은 생리학적 pH에서 이음이온이다. 이를 확인하기 위해서, 리간드 12-14를 영장류에게 피하로 제공하였다. 각 경우에, 약물을 경구로 제공한 동일한 동물은 또한 피하로 킬레이트화제를 제공받았다.
원숭이에서 12의 경구 ICE는 10.6 ± 4.0%였고; 리간드를 피하로 제공한 경우 ICE는 18.8 ± 8.7%로 증가하였지만, 증가는 유의하지 않았다 (p = 0.06). 13의 ICE는 영장류에서, 이를 경구로 투여한 경우 5.4 ± 1.5%에서 이를 피하로 투여한 경우 18.1 ± 7.5%로 유의하게 증가하였다 (p < 0.03). 최종적으로, 이를 경구로 제공한 경우 영장류에서 제2 β-산화 생성물 14의 ICE는 3.0 ± 2.7%였다. 동일한 동물에게 피하로 제공한 경우, ICE는 15.9 ± 4.3%로 현저하게 증가하였다 (p < 0.001). 따라서, 리간드 전하, log Papp의 중요성은 영장류 모델에서 훨씬 더 중요한 역할을 맡는다.
실시예 10. ICE 관찰
여러 일반화를 표 2로부터 유도할 수 있다. 성능 비 (PR), ICE영장류/ICE설치류는, 8 및 9는 (경구) 영장류에서보다 래트에서 철 제외에 보다 효과적이지만, 나머지 리간드 11-14는 영장류에서 철 클리어런스에 있어 효과적이거나 보다 양호함을 나타낸다. 설치류에서, 9 및 14는 피하로 투여하는 경우, 이들을 경구로 투여한 경우의 대략 2배만큼 효과적이었다. 영장류에서 9, 13, 및 14의 피하 대 경구 ICE에서의 극적인 차이가 또한 있었다: 그의 피하의 경우의 ICE는 각각 10.2, 3.4 및 5.3배 더 높았다. 12의 ICE는 또한 피하로 투여시 증가하지만, 증가는 현저하지 않았다 (p = 0.06).
실시예 11. (S)-4'-(HO)-DADFT-HXA (11), 대사적으로 프로그램화된 킬레이트화제의 독성학 프로파일.
대사적으로 프로그램화된 철 킬레이트화제의 개발의 배후의 개념은 경구로 잘 흡수될 것이며, 탁월한 ICE 특성을 나타내고, 잠재적 독성을 최소화하기 위해 덜 친지성으로 빠르게 대사되어야 하지만 여전히 활성인 탈철화제로 빠르게 대사되야만 하는 매우 친지성인 약물의 투여를 근거로 한다. 예를 들어, 비-대사가능한 말단 메틸 에테르를 갖는 데페리트린 유사체 10 (표 2)은 담관 캐뉼라삽입 래트에서 매우 친지성이었고, 효과적인 철 클리어링 작용제였다. 불행하게도, 상기 킬레이트화제는 매우 독성이었다. 반대로, 또한 친지성인, 상응하는 탈메틸화된 화합물인 알콜 11은 설치류 및 영장류에서 탁월한 ICE 특성을 가졌고, 임의의 명백한 독성을 나타내지 않았다. 상기 기재된 바와 같이, 리간드 11은 잘 흡수되었고, 조직 분포/대사 연구에서, 상응하는 친수성 산 12, 13, 및 14로 빠르게 전환되는 것으로 나타났다 (도 6).
11의 10-일 독성 시험을 수컷 스프라그-돌리 래트에서 수행하였다. 동물을 개별적 대사 케이지에 격납하였다. 리간드 11을 384 μmol/kg/일의 용량으로 10일 동안 1일 1회 위관영양법에 의해 경구로 제공하였다. 이 용량은 그의 나트륨 염으로서의 DFT (1) 100 mg/kg/일과 동일한 것임에 유의한다. 소변을 24-시간 간격으로 대사 케이지에서 수집하고, 그의 Kim-1 함량에 대해 평가하였다. 연구를 정상 철 저장을 갖는 래트에서 수행하고; 각각의 동물은 그 자신의 대조군으로서의 역할을 하였다. 추가의 연령-매칭된 래트는 CBC 및 혈청 화학 평가 및 조직병리학에 대한 비처리된 대조군으로서의 역할을 하였다.
11로 치료된 모든 래트는 약물에 대한 노출에 대해 생존하였다. 동물은 연구의 초기에 밝고 빈틈없고 반응성이었고, 실험의 과정에 걸쳐 그와 같이 유지하였다. 설치류의 기준선 비뇨기 Kim-1 배출은 < 20 ng/kg/24시간이었고, 킬레이트화제에 대한 10-일 노출 동안 임의의 시간에 이 수준을 초과하지 않았다. 래트를 약물 후 24시간에 희생시켰다. 혈액을 일상 CBC 및 혈청 화학 분석을 위해 제출하였다. 치료된 래트의 BUN, 20 ± 4 mg/dl은 비치료된 대조군의 BUN, 21 ± 2 mg/dl의 오차 내에 있었다 (p > 0.05). 또한, 둘 다의 군에 대한 SCr은 0.5 ± 0.1 mg/dl (p > 0.05)였다. 이들 값이 이 종을 위한 정상 범위 내에 잘 있다는 것에 유의한다: BUN의 경우 9-30 mg/dl 및 SCr의 경우 0.4-1.0 mg/dl (안테크 다이어그노스틱스 (2015년), 2015년 4월 접속한 www.antechdiagnostics.com). 광범위한 조직 (25/래트)을 조직병리학의 평가를 위해 외부 실험실에 제공하였다. 병리학자는 임의의 약물-관련 이상을 확인하지 못했다.
미루어 볼 때, 이들 결과는 매우 효과적인 탈철화제인 대사적으로 프로그램화된 리간드를 성공적으로 설계할 수 있음을 입증한다. 예상되는 바와 같이, 이 경우에 모 친지성 알콜 11은 잘 흡수되었고, 집합적으로 인식가능한 독성이 거의 없는 내지는 전혀 없는 탁월한 ICE를 갖는 친지성 리간드로 빠르게 대사되었다.
결론
수많은 주목할 만한 결과가 (S)-4'-(HO)-DADFT-norPE (7)의 대사 연구로부터도출되었다. 첫째로, 리간드 7은 2를 생성하기 위한 4'-(HO)에서의 대사 절단을 지속하지 않는다 (도 2). 그러나, 불명확하게 남아있는 것은 7의 폴리에테르 단편 상의 말단 메틸이 대사적으로 불안정성인지의 여부이다. 이것이 그러한 경우라면, 이는 아마 우선 상응하는 알콜 8로 전환된 다음, 카르복실산 9로 전환될 것이다 (도 4). 이들 대사 산물 둘 다는 매우 친수성인 것으로 예상될 것이다. 이전 연구를 기반으로, 친수성에서의 이러한 증가는 리간드 독성을 최소로 할 것으로 추가로 예상할 수 있었다.37,43,45 실제로 이러한 탈메틸화-산화 시나리오가 7에 의해 발생하면, 이는 "대사적으로 프로그램화"된 철 킬레이트화제, 예를 들어 경구로 잘 흡수될 것이지만, 이어서 친수성이며 비독성인 리간드로 빠르게 대사될 것인 고도로 친지성인 킬레이트화제에 대한 신규 접근법을 지지할 수 있다.
7, 8 및 9의 추정 대사물을 조립하였다. 알콜 8은 4'-(HO)에 고정된 3-옥사-5-히드록시펜틸 단편을 갖고; 산 9는 4'-(HO) 상에 3-옥사-4-카르복시부틸 기를 갖는다. 이들 2개의 합성 킬레이트화제는 본 발명자들로 하여금 7의 잠재적 대사를 추적하는 분석용 HPLC 방법을 개발하도록 하였다. 피하로 7로 치료된 래트의 조직을 8 또는 9의 존재에 대한 HPLC를 통한 추가의 분석 처리한 경우, 상응하는 알콜 8로의 7의 말단 메틸의 절단이 발생하였다 (도 5). 그러나, 카르복실산 9는 검출되지 않았고, 이는 아마도 모체 7의 8로의 대사의 정도가 매우 작았기 때문일 것이다. 그러나, 합성 알콜 8을 래트에 피하로 제공한 경우, 이는 매우 효율적으로 산 9로 전환되었다.
설치류에 300 μmol/kg의 용량으로 피하로 합성 알콜 8을 투여하였다. 실제로, 알콜 8은 매우 빠르게 9로 산화되었다 (도 5).
설치류 및 영장류에 경구로 제공한 경우, 7의 합성 대사물인 알콜 8 또는 산 9 중 어떠한 것도 모 리간드만큼 높은 ICE를 갖지 않았다. 경구로 제공한 산 9는 특히 비효과적이었다. 그러나, 피하로 제공한 경우, 9의 ICE는 설치류에서 2배가 되었고, 영장류에서 동일한 원숭이에게 경구로 제공한 경우보다 10배 더 높았다 (표 2). 이는 고도로 하전된 리간드는 이것이 장 점막을 가로지르지 않는다는 아이디어와 관련이 있다. 집합적으로 미루어보아, 데이터는 2의 4'-(HO)에 친지성 알콜 단편을 고정하는 것이, 친지성이며 경구로 흡수되고, 친수성 산 대사물로 빠르게 전환되는 킬레이트를 제공할 것임을 시사하였다.
초기에, 6-메톡시헥실 기를 2의 4'-(HO)에 첨부하여 메틸 에테르 10을 제공하였다. 이 리간드는 매우 친지성 (log Papp = 0.95)이었고, 래트에서 15.8 ± 3.7%의 ICE을 가졌으며, 매우 독성이었다. 본 발명자들은 이전에 2의 4'-부톡시 유사체 (log Papp = 1.02)의 경우 이 시나리오를 확인한 바 있었으며, 사망이 24시간 내에 발생하였다.72 그럼에도 불구하고, 이 리간드는 이러한 구조적 패밀리에 대한 친지성/독성 관계의 상부 경계를 확인하는 역할을 하였다.
후속적으로, 대사가능한 6-히드록시헥실 기를 2의 4'-(HO)에 고정하여 알콜 11을 제공하였다 (표 2). 리간드 11은 여전히 매우 친지성 (log Papp = 0.21)이지만, 이는 명백한 독성의 어떠한 신호도 도출하지 않았다. 예상된 바와 같이, 11의 각각의 대사물 (12, 13, 및 14)은 매우 친수성이며, 모체의 경우 log Papp = 0.21에서, 산 12의 경우 -1.90, 산 13의 경우 -2.21, 및 산 14의 경우 -1.98로 이동한다 (도 6). 래트에 피하로 제공한 경우, 11은 상응하는 산 (12)으로, β-산화에 의해 산 13 및 최종적으로 산 14로 매우 빠르게 전환된다 (도 7).
래트에서 리간드 11의 경구 ICE는 9.9 ± 0.8%이다. 12의 경구 ICE는 유사한 반면, 13 및 14의 경구 ICE는 유의하게 더 작았다. 영장류에서, 모체 11의 경구 ICE는 21.9 ± 3.6%였다. 친수성 대사물 12-14의 경구 ICE는 모 알콜 11보다 원숭이에서 모두 유의하게 더 작았다 (표 2). 다시, 이는, 고도로 하전된 리간드는 이것이 장 점막을 가로지르지 않는다는 아이디어와 관련이 있다. 이를 확인하기 위해, 리간드 12-14를 설치류 및 영장류에 피하로 제공하였다. 래트에서, 12 및 13의 피하로의 ICE는 그의 경구 값의 오차 내에 있지만, 14의 피하로의 것은 약물을 경구로 제공한 경우보다 현저하게 더 컸다. 원숭이에서, 12의 피하로의 ICE는 경구 투여에 대해 증가하였지만, 증가는 유의하지 않았다. 대조적으로, 13 및 14의 피하로의 ICE는 약물을 동일한 동물에게 경구로 제공한 경우보다 각각 3.4 및 5.3배 더 컸다 (표 2). 가장 주목할만한 발견은 설치류에게 384 μmol/kg/일의 용량으로 10일 동안 1일 1회 제공한 경우 리간드 11에 의한 독성의 결여였다. 10 및 11 사이의 독성 차이는 현저했다. 이는 친지성 모 킬레이트화제가 친수성, 비독성 탈철화 대사물로 빠르게 전환된다는 아이디어를 입증한다. 따라서, "대사적으로 프로그램화"된 킬레이트화제, 예를 들어 그의 친수성 대응물로 빠르게 전환되는, 고도로 친지성, 경구 흡수성의, 효과적인 분자를 개발하는 개념은 실제로 매우 효과적인 철 킬레이트화제의 신뢰할 수 있는 접근법이다. 도 8은 이 연구에서 확립된 개념을 설명한다.
참고문헌
등가물 및 범주
청구범위에서, 단수표현은, 달리 나타내거나 또는 다르게는 문맥으로부터 명백하게 나타내지 않는 한, 하나 또는 하나 초과를 의미할 수 있다. 군의 1종 이상의 구성원 사이에 "또는"을 포함하는 청구범위 또는 상세한 설명은, 달리 나타내거나 또는 다르게는 문맥으로부터 명백하게 나타내지 않는 한, 군 구성원 중 하나, 하나 초과, 또는 모두가 주어진 생성물 또는 방법에 존재하거나, 그에 사용되거나, 또는 달리 관련되는 경우에 충족되는 것으로 간주된다. 본 발명은 군의 정확히 하나의 구성원이 주어진 생성물 또는 방법에 존재하거나, 그에 사용되거나, 또는 달리 관련되는 실시양태를 포함한다. 본 발명은, 군 구성원 중 하나 초과, 또는 모두가 주어진 생성물 또는 방법에 존재하거나, 그에 사용되거나, 또는 달리 관련되는 실시양태를 포함한다.
추가로, 본 발명은 열거된 청구범위 중 1개 이상으로부터의 1개 이상의 제한, 요소, 항목 및 서술적 용어가 또 다른 청구항에 도입되는 모든 변형, 조합 및 순열을 포괄한다. 예를 들어, 또 다른 청구항에 종속항인 임의의 청구항은 동일한 기반의 청구항에 종속항인 임의의 다른 청구항에서 발견된 1개 이상의 제한을 포함하도록 변형될 수 있다. 요소가, 예를 들어 마쿠쉬 군 포맷의 목록으로서 제시되는 경우에, 요소의 각 하위군이 또한 개시되고, 임의의 요소(들)가 군으로부터 제거될 수 있다. 일반적으로, 본 발명 또는 본 발명의 측면이 특정한 요소 및/또는 특색을 포함하는 것으로 지칭되는 경우에, 본 발명 또는 본 발명의 측면의 특정 실시양태는 이러한 요소 및/또는 특색으로 이루어지거나 또는 본질적으로 이루어진다는 것이 이해되어야 한다. 단순성의 목적상, 이들 실시양태는 본원에 구체적으로 제시되지 않았다. 또한 용어 "포함하는" 및 "함유하는"은 개방적이고 추가의 요소 또는 단계의 포함을 허용하는 것으로 의도됨을 주목한다. 범위가 제공된 경우에, 종점이 포함된다. 추가로, 달리 나타내지 않는 한 또는 문맥 및 통상의 기술자의 이해로부터 달리 명백하지 않는 한, 범위로서 표현된 값은 본 발명의 상이한 실시양태에서 언급된 범위 내의 임의의 구체적 값 또는 하위-범위를, 문맥이 달리 명백하게 지시하지 않는 한 범위의 하한치 단위의 1/10까지 가정할 수 있다.
본원은 다양한 허여 특허, 공개 특허 출원, 학술지 및 기타 공개물을 인용하며, 이들 모두는 본원에 참조로 포함된다. 임의의 포함된 참고문헌과 본 명세서 사이에 충돌이 존재하는 경우에, 본 명세서가 우선할 것이다. 추가로, 선행 기술에 속하는 본 발명의 임의의 특정한 실시양태는 청구범위 중 어느 하나 이상으로부터 명시적으로 제외될 수 있다. 이러한 실시양태는 통상의 기술자에게 공지된 것으로 여겨지기 때문에, 이들은 제외가 본원에서 명시적으로 제시되지 않더라도 제외될 수 있다. 본 발명의 임의의 특정한 실시양태는 선행 기술의 존재와 관련이 있는지 여부와 관계 없이, 임의의 이유로, 임의의 청구범위로부터 제외될 수 있다.
통상의 기술자는 상용을 초과하지 않는 실험을 사용하여, 본원에 기재된 구체적 실시양태에 대한 많은 등가물을 인식하거나 또는 확인할 수 있을 것이다. 본원에 기재된 본 실시양태의 범주는 상기 상세한 설명으로 제한되는 것으로 의도되지 않으며, 오히려 첨부된 청구범위에 제시된 바와 같다. 통상의 기술자는 이러한 기재에 대한 다양한 변화 및 변형이 하기 청구범위에 정의된 바와 같이, 본 발명의 취지 또는 범주를 벗어나지 않고 이루어질 수 있음을 인지할 것이다.
Claims (115)
- 화학식 (I)의 화합물 또는 그의 제약상 허용되는 염.
여기서
R1은 수소, 치환 또는 비치환된 알킬, 치환 또는 비치환된 아실, 산소 보호기, 이고;
각 경우의 R'는 독립적으로 수소, 치환 또는 비치환된 알킬, 또는 산소 보호기이고;
각 경우의 n은 독립적으로 1 내지 8의 정수이고,
각 경우의 x는 독립적으로 0 내지 8의 정수이고;
각 경우의 m은 독립적으로 1 내지 8의 정수이고;
각 경우의 y는 독립적으로 0 내지 8의 정수이고;
각 경우의 p는 독립적으로 1 내지 10의 정수이고;
q는 0 또는 1이며, 단 q가 0인 경우, R1은 화학식: 이고;
각 경우의 R2는 독립적으로 -CH2OR2a, -CH2OH, -C(=O)OH, 또는 -C(=O)OR2a이고, 여기서 각 경우의 R2a는 독립적으로 치환 또는 비치환된 알킬 또는 산소 보호기이고;
각 경우의 R3은 독립적으로 할로겐, 치환 또는 비치환된 알킬, 또는 -OR8이고, 여기서 각 경우의 R8은 독립적으로 수소, 치환 또는 비치환된 알킬, 치환 또는 비치환된 아실, 산소 보호기, 이고;
k는 0, 1, 2, 3, 또는 4이고;
R4는 수소 또는 치환 또는 비치환된 알킬이고;
R5는 수소 또는 치환 또는 비치환된 알킬이고;
R6은 수소 또는 치환 또는 비치환된 알킬이고;
Z는 -O- 또는 -S-이고;
R9는 수소, 치환 또는 비치환된 알킬, , 산소 원자에 부착된 경우 산소 보호기 또는 황 원자에 부착된 경우 황 보호기이고;
단 페닐 고리의 3', 4', 5', 또는 6'-위치에서의 모이어티 는 화학식 이 아니다. - 제1항에 있어서, 각 경우의 x가 1, 2, 3, 또는 4이고, 각 경우의 n이 2이고, 각 경우의 y가 0인 경우, 각 경우의 R2는 -CH2OH, -C(=O)OH, 또는 -C(=O)OR2a인 화합물.
- 제5항에 있어서, 하기 화학식의 화합물 또는 그의 제약상 허용되는 염.
- 제1항 내지 제44항 중 어느 한 항에 있어서, R1이 수소인 화합물.
- 제1항 내지 제3항, 제5항 내지 제9항, 및 제27항 내지 제46항 중 어느 한 항에 있어서, 각각의 x 및 y가 0인 화합물.
- 제1항 내지 제3항, 제5항 내지 제9항, 및 제18항 내지 제46항 중 어느 한 항에 있어서, 각 경우의 x가 1, 2, 3, 또는 4이고; 각 경우의 n이 2이고; 각 경우의 y가 0인 화합물.
- 제1항 내지 제48항 중 어느 한 항에 있어서, 적어도 1개 경우의 p가 1, 2, 3, 4, 또는 5인 화합물.
- 제1항 내지 제3항, 제5항, 제18항, 제27항, 제36항, 및 제45항 내지 제49항 중 어느 한 항에 있어서, 적어도 1개 경우의 R2가 -CH2OR2a인 화합물.
- 제50항에 있어서, 적어도 1개 경우의 R2가 -CH2OMe인 화합물.
- 제1항 내지 제3항, 제5항, 제18항, 제27항, 제36항, 및 제45항 내지 제49항 중 어느 한 항에 있어서, 적어도 1개 경우의 R2가 -CH2OH인 화합물.
- 제1항 내지 제3항, 제5항, 제18항, 제27항, 제36항, 및 제45항 내지 제49항 중 어느 한 항에 있어서, 적어도 1개 경우의 R2가 -C(=O)OH인 화합물.
- 제1항 내지 제3항, 제5항, 제18항, 제27항, 제36항 및 제45항 내지 제49항 중 어느 한 항에 있어서, 적어도 1개 경우의 R2가 -C(=O)OR2a인 화합물.
- 제1항, 제4항, 및 제46항 내지 제54항 중 어느 한 항에 있어서, q가 0인 화합물.
- 제1항 내지 제4항 및 제45항 내지 제54항 중 어느 한 항에 있어서, q가 1인 화합물
- 제1항 내지 제56항 중 어느 한 항에 있어서, k가 0인 화합물.
- 제1항 내지 제57항 중 어느 한 항에 있어서, 각각의 R4 및 R5가 수소인 화합물.
- 제1항 내지 제57항 중 어느 한 항에 있어서, 각각의 R4 및 R5가 독립적으로 치환 또는 비치환된 C1-6 알킬인 화합물.
- 제59항에 있어서, 각각의 R4 및 R5가 Me인 화합물.
- 제1항 내지 제60항 중 어느 한 항에 있어서, R6이 수소인 화합물.
- 제1항 내지 제60항 중 어느 한 항에 있어서, R6이 치환 또는 비치환된 C1-6 알킬인 화합물.
- 제62항에 있어서, R6이 Me인 화합물.
- 제1항 내지 제63항 중 어느 한 항에 있어서, Z가 -O-인 화합물.
- 제1항 내지 제63항 중 어느 한 항에 있어서, Z가 -S-인 화합물.
- 제1항 내지 제65항 중 어느 한 항에 있어서, R9가 수소인 화합물.
- 제1항 내지 제65항 중 어느 한 항에 있어서, R9가 치환 또는 비치환된 C1-6 알킬인 화합물.
- 제1항 내지 제67항 중 어느 한 항에 있어서, "*"로 표지된 탄소 원자가 S 배위인 화합물.
- 제1항 내지 제67항 중 어느 한 항에 있어서, "*"로 표지된 탄소 원자가 R 배위인 화합물.
- 제1항 내지 제70항 중 어느 한 항에 있어서, 제약상 허용되는 염이 제약상 허용되는 알칼리 금속 또는 알칼리 토금속 염인 화합물.
- 제1항 내지 제71항 중 어느 한 항에 있어서, 제약상 허용되는 염이 제약상 허용되는, 나트륨 염, 칼륨 염 또는 마그네슘 염인 화합물.
- 화학식 (II)의 화합물 또는 그의 제약상 허용되는 염.
여기서
각 경우의 RC1은 독립적으로 -(CH2)hORA1, 또는 -(CH2)hC(=O)ORA1이고, 여기서 각 경우의 RA1은 독립적으로 수소, 치환 또는 비치환된 알킬 또는 산소 보호기이며, 단 RC1이 -(CH2)hC(=O)ORA1인 경우 h가 0이 아니고 RA1은 수소가 아니고;
각 경우의 RC2는 독립적으로 수소, 할로겐, 치환 또는 비치환된 C1-6 알킬, -CN, -NO2, -ORX, 또는 -N(RY)2이고;
각 경우의 RC3은 독립적으로 수소, 알킬, 또는 산소 보호기이고;
RX는 수소, 치환 또는 비치환된 C1-6 알킬, 또는 산소 보호기이고;
각 경우의 RY는 독립적으로 수소, 치환 또는 비치환된 C1-6 알킬, 질소 보호기이거나, 또는 임의로 2개의 RY가 개재 원자와 함께 치환 또는 비치환된 헤테로시클릴 또는 치환 또는 비치환된 헤테로아릴을 형성하고;
각 경우의 h는 독립적으로 0, 1, 2, 3, 4, 5, 6, 7, 또는 8이고;
각 경우의 j는 독립적으로 0, 1, 2, 3, 또는 4이다. - 제73항 내지 제75항 중 어느 한 항에 있어서, 적어도 1개 경우의 RC1이 -(CH2)hOH이고, 여기서
h는 0, 1, 2, 3, 4, 5, 6, 7, 또는 8인 화합물. - 제73항 내지 제76항 중 어느 한 항에 있어서, 적어도 1개 경우의 RC1이 -OH인 화합물.
- 제73항 내지 제75항 중 어느 한 항에 있어서, 적어도 1개 경우의 RC1이 -(CH2)hORA1이고, 여기서
h는 0, 1, 2, 3, 4, 5, 6, 7, 또는 8이고;
RA1은 수소, 치환 또는 비치환된 C1-6 알킬, 또는 산소 보호기인 화합물. - 제73항 내지 제75항 중 어느 한 항에 있어서, 적어도 1개 경우의 RC1이 -OMe 또는 -OEt인 화합물.
- 제73항 내지 제75항 중 어느 한 항에 있어서, 적어도 1개 경우의 RC1이 -(CH2)hC(=O)ORA1이고, 여기서
h는 0, 1, 2, 3, 4, 5, 6, 7, 또는 8이고;
RA1은 수소, 치환 또는 비치환된 C1-6 알킬, 또는 산소 보호기인 화합물. - 제73항 내지 제75항, 및 제80항 중 어느 한 항에 있어서, 적어도 1개 경우의 RC1이 -(CH2)C(=O)OMe 또는 -(CH2)C(=O)OEt인 화합물.
- 제73항 내지 제81항 중 어느 한 항에 있어서, 적어도 1개 경우의 RC2가 수소인 화합물.
- 제73항 내지 제81항 중 어느 한 항에 있어서, 적어도 1개 경우의 RC2가 할로겐, 또는 치환 또는 비치환된 C1-6 알킬인 화합물.
- 제73항 내지 제81항, 및 제83항 중 어느 한 항에 있어서, 적어도 1개 경우의 RC2가 메틸 또는 에틸인 화합물.
- 제73항 내지 제81항 중 어느 한 항에 있어서, 적어도 1개 경우의 RC2가 -CN 또는 -NO2인 화합물.
- 제73항 내지 제81항 중 어느 한 항에 있어서, 적어도 1개 경우의 RC2가 -ORX 또는 -N(RY)2이고; 여기서
RX는 수소, 치환 또는 비치환된 C1-6 알킬, 또는 산소 보호기이고;
각 경우의 RY는 독립적으로 수소, 치환 또는 비치환된 C1-6 알킬, 또는 질소 보호기이거나, 또는 임의로 2개의 RY는 개재 원자와 함께 치환 또는 비치환된 헤테로시클릴 또는 치환 또는 비치환된 헤테로아릴을 형성하는 것인 화합물. - 제73항 내지 제81항, 및 제86항 중 어느 한 항에 있어서, 적어도 1개 경우의 RC2가 -OH인 화합물.
- 제73항 내지 제81항, 및 제86항 중 어느 한 항에 있어서, 적어도 1개 경우의 RC2가 -OMe 또는 -OEt인 화합물.
- 제73항 내지 제81항, 및 제86항 중 어느 한 항에 있어서, 적어도 1개 경우의 RC2가 -NMe2 또는 -NEt2인 화합물.
- 제73항 내지 제81항, 및 제86항 중 어느 한 항에 있어서, 2개 경우의 RC2가 개입 원자와 함께 헤테로시클릭 고리에 0, 1, 또는 2개의 이중 결합을 포함하는 치환 또는 비치환된, 5- 내지 14-원 모노시클릭 또는 비시클릭 헤테로시클릭 고리를 형성하고, 여기서 헤테로시클릭 고리의 1, 2, 또는 3개의 원자는 독립적으로 질소, 산소, 또는 황인 화합물.
- 제73항 내지 제90항 중 어느 한 항에 있어서, 각 경우의 j가 독립적으로 1, 2, 3, 또는 4인 화합물.
- 제73항 내지 제91항 중 어느 한 항에 있어서, 적어도 1개 경우의 RC3이 수소인 화합물.
- 제73항 내지 제91항 중 어느 한 항에 있어서, 적어도 1개 경우의 RC3이 메틸, 에틸, 또는 프로필인 화합물.
- 제1항 내지 제95항 중 어느 한 항에 기재된 화합물 및 임의로 제약상 허용되는 부형제를 포함하는 제약 조성물.
- 제1항 내지 제96항 중 어느 한 항에 있어서, 추가의 제약 작용제를 추가로 포함하는 것인 제약 조성물.
- 대상체에게 유효량의 제1항 내지 제95항 중 어느 한 항에 기재된 화합물 또는 제96항 또는 제97항에 기재된 제약 조성물을 투여하는 것을 포함하는, 질환의 치료를 필요로 하는 대상체에서 질환을 치료하는 방법이며, 여기서 질환은 철 과부하, 알루미늄 과부하, 란타나이드 과부하, 악티나이드 과부하, 산화성 스트레스, 수혈성 철 과부하, 지중해빈혈, 원발성 혈색소증, 속발성 혈색소증, 당뇨병, 간 질환, 심장 질환, 암, 방사선 손상, 신경계 또는 신경변성 장애, 프리드라이히 운동실조 (FRDA), 황반 변성, 폐쇄성 두부 손상, 과민성 장 질환, 재관류 손상, 감염성 질환, 또는 금속 중독인 방법.
- 유효량의 제1항 내지 제95항 중 어느 한 항에 기재된 화합물 또는 제96항 또는 제97항에 기재된 제약 조성물을 혈액과 혼합하여 혼합물을 제조하고;
혼합물을 대상체에게 투여하는 것을 포함하는, 질환의 치료를 필요로 하는 대상체에서 질환을 치료하는 방법이며,
여기서 질환은 철 과부하, 알루미늄 과부하, 란타나이드 과부하, 악티나이드 과부하, 산화성 스트레스, 수혈성 철 과부하, 지중해빈혈, 원발성 혈색소증, 속발성 혈색소증, 당뇨병, 간 질환, 심장 질환, 암, 방사선 손상, 신경계 또는 신경변성 장애, 프리드라이히 운동실조 (FRDA), 황반 변성, 폐쇄성 두부 손상, 과민성 장 질환, 재관류 손상, 감염성 질환, 또는 금속 중독인 방법. - 제98항 또는 제99항에 있어서, 질환이 철 과부하인 방법.
- 제98항 또는 제99항에 있어서, 질환이 알루미늄 과부하, 란타나이드 과부하, 또는 악티나이드 과부하인 방법.
- 제98항 또는 제99항에 있어서, 질환이 산화성 스트레스인 방법.
- 제98항 또는 제99항에 있어서, 질환이 수혈성 철 과부하인 방법.
- 제98항 또는 제99항에 있어서, 질환이 지중해빈혈, 원발성 혈색소증, 또는 속발성 혈색소증인 방법.
- 제98항 또는 제99항에 있어서, 질환이 방사선 손상인 방법.
- 제98항 또는 제99항에 있어서, 질환이 프리드라이히 운동실조 (FRDA)인 방법.
- 제98항 또는 제99항에 있어서, 질환이 당뇨병, 간 질환, 심장 질환, 암, 신경계 또는 신경변성 장애, 황반 변성, 폐쇄성 두부 손상, 과민성 장 질환, 또는 재관류 손상인 방법.
- 제98항 또는 제99항에 있어서, 질환이 감염성 질환인 방법.
- 제98항 내지 제99항, 및 제108항 중 어느 한 항에 있어서, 감염성 질환이 박테리아 감염인 방법.
- 제98항 내지 제99항, 및 제108항 중 어느 한 항에 있어서, 감염성 질환이 말라리아인 방법.
- 제98항 또는 제99항에 있어서, 질환이 금속 중독인 방법.
- 제98항 내지 제99항, 및 제108항 중 어느 한 항에 있어서, 금속 중독이 철 중독인 방법.
- 바이오필름 형성의 감소를 필요로 하는 대상체에게 유효량의 제1항 내지 제95항 중 어느 한 항에 기재된 화합물 또는 제96항 또는 제97항에 기재된 제약 조성물을 투여하는 것을 포함하는, 상기 대상체에서 바이오필름의 형성을 감소시키는 방법.
- 제98항 내지 제113항 중 어느 한 항에 있어서, 대상체가 인간인 방법.
- 제1항 내지 제95항 중 어느 한 항에 기재된 화합물 또는 제96항 또는 제97항에 기재된 제약 조성물; 및
화합물 또는 제약 조성물의 사용에 대한 지침서
를 포함하는 키트.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201562153468P | 2015-04-27 | 2015-04-27 | |
| US62/153,468 | 2015-04-27 | ||
| PCT/US2016/029587 WO2016176343A1 (en) | 2015-04-27 | 2016-04-27 | Metabolically programmed metal chelators and uses thereof |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20170140306A true KR20170140306A (ko) | 2017-12-20 |
Family
ID=57199470
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020177033736A KR20170140306A (ko) | 2015-04-27 | 2016-04-27 | 대사적으로 프로그램화된 금속 킬레이트화제 및 그의 용도 |
Country Status (10)
| Country | Link |
|---|---|
| US (1) | US10570104B2 (ko) |
| EP (1) | EP3288557A4 (ko) |
| JP (1) | JP2018515475A (ko) |
| KR (1) | KR20170140306A (ko) |
| CN (1) | CN107708693A (ko) |
| AU (1) | AU2016255770A1 (ko) |
| CA (1) | CA2984250A1 (ko) |
| HK (1) | HK1250216A1 (ko) |
| IL (1) | IL255279A0 (ko) |
| WO (1) | WO2016176343A1 (ko) |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ES2761200T3 (es) | 2011-12-16 | 2020-05-19 | Univ Florida | Usos de análogos de 4'-desferritiocina |
| US11541105B2 (en) | 2018-06-01 | 2023-01-03 | The Research Foundation For The State University Of New York | Compositions and methods for disrupting biofilm formation and maintenance |
| CN112542306B (zh) * | 2020-12-17 | 2022-12-30 | 华东理工大学 | 一种基于一价金属离子的强顺磁性材料、其制备方法及应用 |
| CN112960780B (zh) * | 2021-03-03 | 2023-02-03 | 龙江环保集团股份有限公司 | 一种生物膜载体的预处理方法及生物法污水处理工艺 |
Family Cites Families (98)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3274207A (en) | 1966-09-20 | Processes for preparing thiazole carboxylic acids | ||
| US39132A (en) | 1863-07-07 | Improved clod-crusher and harrow | ||
| US3809754A (en) | 1968-12-31 | 1974-05-07 | Medial De Toledo & Cie | Method of treating diseases of the mucous membrane using compounds of a thiazolidine carboxylic acid and pharmaceutical preparations thereof |
| US3882110A (en) | 1969-06-11 | 1975-05-06 | Roussel Uclaf | Novel 2-alkyl-5-thiazole-carboxylic acid derivatives |
| FR2062210A5 (ko) | 1969-09-17 | 1971-06-25 | Godo Shusei Kk | |
| FR2062120A5 (ko) | 1969-10-10 | 1971-06-25 | Messier Fa | |
| FR2141526B1 (ko) | 1971-06-14 | 1975-05-30 | Roussel Uclaf | |
| DE2245560A1 (de) | 1972-09-16 | 1974-03-21 | Basf Ag | Verfahren zur herstellung von 4alkoxycarbonyl-2-thiazolinen |
| AU528115B2 (en) | 1978-04-08 | 1983-04-14 | Santen Pharmaceutical Co. Ltd. | Antihypertensive 4-thiazolidine/carboxylic acids |
| CS205217B1 (cs) | 1979-04-05 | 1981-05-29 | Zdenek Vitamvas | Dozimetr ionizujícího záření |
| US4270537A (en) | 1979-11-19 | 1981-06-02 | Romaine Richard A | Automatic hypodermic syringe |
| DE3002989A1 (de) | 1980-01-29 | 1981-07-30 | Hoechst Ag, 6000 Frankfurt | Hydroxyphenyl-thiazol, -thiazolin und -thiazolidin-carbonsaeuren, verfahren zu ihrer herstellung und ihre verwendung zur beeinflussung des kollagenstoffwechsels |
| DE3170401D1 (en) | 1980-07-28 | 1985-06-13 | Ciba Geigy Ag | Triazoline derivatives and processes for their preparation |
| JPS5758682A (en) | 1980-07-28 | 1982-04-08 | Ciba Geigy Ag | Thiazoline derivatives, manufacture and medicinal composition containing same |
| JPS5772975A (en) | 1980-10-24 | 1982-05-07 | Kureha Chem Ind Co Ltd | 2-substituted phenylthiazole derviative, and medicine for peptic ulcer containing said derivative as active component |
| US4367233A (en) | 1981-10-02 | 1983-01-04 | American Home Products Corporation | Inhibitors of mammalian collagenase |
| EP0226591B1 (en) | 1984-12-18 | 1992-09-23 | Clark Pharmaceutical Development, Ltd. | Anti-tumor compositions containing the reaction product of a cytotoxic aldehyde with penicillamine and their use for the manufacture of medicaments |
| US4596556A (en) | 1985-03-25 | 1986-06-24 | Bioject, Inc. | Hypodermic injection apparatus |
| HU200177B (en) | 1985-06-18 | 1990-04-28 | Biogal Gyogyszergyar | Process for producing thiazolidinecarboxylic acids and pharmaceutical compositions comprising such compounds |
| US4736060A (en) | 1985-08-06 | 1988-04-05 | Nippon Rikagakuyakuhin Co., Ltd. | Method for optical resolution of DL-cysteine and (R,S)-1-(1-naphthyl) ethylamine |
| EP0214933A3 (de) | 1985-09-03 | 1989-05-24 | Ciba-Geigy Ag | Kombinationspräparate zur Behandlung von Malaria |
| EP0214101A3 (de) | 1985-09-03 | 1989-05-31 | Ciba-Geigy Ag | Verwendung von Eisen(III)-Chelatoren vom Typ Desferrioxamin B und Desferriferrithiocin zur Behandlung von Malaria |
| JPS62142168A (ja) | 1985-10-16 | 1987-06-25 | Mitsubishi Chem Ind Ltd | チアゾ−ル誘導体及びそれを有効成分とするロイコトリエンきつ抗剤 |
| DE3621540A1 (de) | 1986-06-27 | 1988-01-07 | Basf Ag | Chinolinderivate, verfahren zu ihrer herstellung, diese enthaltende mikrobizide und ihre verwendung zur bekaempfung von bakterien und pilzen |
| CA1283827C (en) | 1986-12-18 | 1991-05-07 | Giorgio Cirelli | Appliance for injection of liquid formulations |
| GB8704027D0 (en) | 1987-02-20 | 1987-03-25 | Owen Mumford Ltd | Syringe needle combination |
| US4940460A (en) | 1987-06-19 | 1990-07-10 | Bioject, Inc. | Patient-fillable and non-invasive hypodermic injection device assembly |
| US4790824A (en) | 1987-06-19 | 1988-12-13 | Bioject, Inc. | Non-invasive hypodermic injection device |
| US4941880A (en) | 1987-06-19 | 1990-07-17 | Bioject, Inc. | Pre-filled ampule and non-invasive hypodermic injection device assembly |
| DE3735757A1 (de) | 1987-10-22 | 1989-05-03 | Degussa | Optisch aktive salze aus einem substituierten thiazolidin-4-carboxylat und 3-chlor-2-hydroxypropyltrimethylammonium, deren herstellung und verwendung |
| ES2047149T3 (es) | 1988-01-20 | 1994-02-16 | Ciba Geigy Ag | Procedimiento para la obtencion de compuestos complejos. |
| US5339163A (en) | 1988-03-16 | 1994-08-16 | Canon Kabushiki Kaisha | Automatic exposure control device using plural image plane detection areas |
| FR2638359A1 (fr) | 1988-11-03 | 1990-05-04 | Tino Dalto | Guide de seringue avec reglage de la profondeur de penetration de l'aiguille dans la peau |
| US5182402A (en) | 1988-11-07 | 1993-01-26 | Imperial Chemical Industries Plc | Herbicidal compositions |
| GB8826035D0 (en) | 1988-11-07 | 1988-12-14 | Ici Plc | Herbicidal compositions |
| US5106992A (en) | 1989-07-28 | 1992-04-21 | E. R. Squibb & Sons, Inc. | 3,5-dihydroxypentanoic acid derivatives useful as antihypercholesterolemic agents and method for preparing same |
| US5312335A (en) | 1989-11-09 | 1994-05-17 | Bioject Inc. | Needleless hypodermic injection device |
| US5064413A (en) | 1989-11-09 | 1991-11-12 | Bioject, Inc. | Needleless hypodermic injection device |
| US5190521A (en) | 1990-08-22 | 1993-03-02 | Tecnol Medical Products, Inc. | Apparatus and method for raising a skin wheal and anesthetizing skin |
| NL9001955A (nl) | 1990-09-05 | 1992-04-01 | Cedona Pharm Bv | Nieuwe thiazolidinederivaten. |
| US5393777A (en) | 1990-11-15 | 1995-02-28 | State Of Oregon Acting By And Through The State Board Of Higher Education On Behalf Of Oregon Health Sciences University | Deferration using anguibactin siderophore |
| DK0934937T3 (da) | 1990-11-30 | 2002-04-02 | Otsuka Pharma Co Ltd | Azolderivater som superoxidradikalinhibitor |
| HU218942B (hu) | 1990-11-30 | 2001-01-29 | Teijin Ltd. | 2-Fenil-tiazol-származékok, az ezeket tartalmazó gyógyászati készítmények, valamint eljárás a vegyületek előállítására |
| US5527288A (en) | 1990-12-13 | 1996-06-18 | Elan Medical Technologies Limited | Intradermal drug delivery device and method for intradermal delivery of drugs |
| FR2677021B1 (fr) | 1991-05-31 | 1993-10-01 | Upsa Laboratoires | Nouveaux derives de thiazole antagonistes des recepteurs a l'angiotensine ii; leurs procedes de preparation, compositions pharmaceutiques les contenant. |
| GB9118204D0 (en) | 1991-08-23 | 1991-10-09 | Weston Terence E | Needle-less injector |
| SE9102652D0 (sv) | 1991-09-13 | 1991-09-13 | Kabi Pharmacia Ab | Injection needle arrangement |
| US5328483A (en) | 1992-02-27 | 1994-07-12 | Jacoby Richard M | Intradermal injection device with medication and needle guard |
| US5383851A (en) | 1992-07-24 | 1995-01-24 | Bioject Inc. | Needleless hypodermic injection device |
| US5569189A (en) | 1992-09-28 | 1996-10-29 | Equidyne Systems, Inc. | hypodermic jet injector |
| US5334144A (en) | 1992-10-30 | 1994-08-02 | Becton, Dickinson And Company | Single use disposable needleless injector |
| US5840739A (en) | 1992-11-16 | 1998-11-24 | University Of Florida Research Foundation, Inc. | Thiazoline acid derivatives |
| WO1994011367A1 (en) | 1992-11-16 | 1994-05-26 | University Of Florida Research Foundation Inc. | 2-(pyrid-2'-yl)-2-thiazoline-4(s)-carboxylic acid derivatives |
| DE4301356A1 (de) | 1993-01-20 | 1994-07-21 | Basf Ag | Verfahren zur Herstellung von 2-Alkyl-4-fluormethyl-thiazolcarbonsäure-alkylestern |
| WO1995024176A1 (en) | 1994-03-07 | 1995-09-14 | Bioject, Inc. | Ampule filling device |
| US5466220A (en) | 1994-03-08 | 1995-11-14 | Bioject, Inc. | Drug vial mixing and transfer device |
| US5599302A (en) | 1995-01-09 | 1997-02-04 | Medi-Ject Corporation | Medical injection system and method, gas spring thereof and launching device using gas spring |
| US5730723A (en) | 1995-10-10 | 1998-03-24 | Visionary Medical Products Corporation, Inc. | Gas pressured needle-less injection device and method |
| US5893397A (en) | 1996-01-12 | 1999-04-13 | Bioject Inc. | Medication vial/syringe liquid-transfer apparatus |
| GB9607549D0 (en) | 1996-04-11 | 1996-06-12 | Weston Medical Ltd | Spring-powered dispensing device |
| FR2749583B1 (fr) | 1996-06-07 | 1998-08-21 | Lipha | Nouveaux derives de thiazolidine -2,4- dione substitues, leurs procedes d'obtention et les compositions pharmaceutiques en renfermant |
| US20020049316A1 (en) | 1997-04-29 | 2002-04-25 | Halbert Stacie Marie | Protease inhibitors |
| US5993412A (en) | 1997-05-19 | 1999-11-30 | Bioject, Inc. | Injection apparatus |
| US6373912B1 (en) | 1997-06-16 | 2002-04-16 | Legerity, Inc. | Phase-locked loop arrangement with fast lock mode |
| IT1298087B1 (it) | 1998-01-08 | 1999-12-20 | Fiderm S R L | Dispositivo per il controllo della profondita' di penetrazione di un ago, in particolare applicabile ad una siringa per iniezioni |
| MA26618A1 (fr) | 1998-04-09 | 2004-12-20 | Smithkline Beecham Corp | Composes et compositions pharmaceutiques pour le traitement du paludisme |
| US6147070A (en) | 1998-06-05 | 2000-11-14 | Facchini; Francesco | Methods and compositions for controlling iron stores to treat and cure disease states |
| US6083966A (en) | 1998-08-31 | 2000-07-04 | University Of Florida | Thiazoline acid derivatives |
| US6159983A (en) | 1998-09-18 | 2000-12-12 | University Of Florida | Method and composition for treatment of inflammatory bowel disease |
| EP1143951A3 (en) | 1998-09-21 | 2002-02-06 | University Of Florida Research Foundation, Inc. | Antimalarial agents |
| US6251927B1 (en) | 1999-04-20 | 2001-06-26 | Medinox, Inc. | Methods for treatment of sickle cell anemia |
| DE19948434A1 (de) | 1999-10-08 | 2001-06-07 | Gruenenthal Gmbh | Substanzbibliothek enthaltend bicyclische Imidazo-5-amine und/oder bicyclische Imidazo-3-amine |
| US7160855B2 (en) | 2002-03-14 | 2007-01-09 | Children's Hospital & Research Center At Oakland | Enhancement of iron chelation therapy |
| US20040044220A1 (en) | 2002-08-22 | 2004-03-04 | University Of Florida | Antioxidant and radical scavenging activity of synthetic analogs of desferrithiocin |
| WO2004017959A2 (en) | 2002-08-22 | 2004-03-04 | University Of Florida | Antioxidant and radical scavenging activity of synthetic analogs of desferrithiocin |
| WO2005023310A2 (en) | 2003-09-09 | 2005-03-17 | University Of Florida Research Foundation, Inc. | Polyamine-metal chelator conjugates |
| AU2003270473A1 (en) | 2003-09-09 | 2005-04-27 | University Of Florida | Desferrithiocin derivatives and their use as iron chelators |
| AU2005306772A1 (en) | 2004-11-19 | 2006-05-26 | Shiva Biomedical, Llc | Methods of treating erythropoietin-resistance |
| EP1866296B1 (en) | 2005-04-04 | 2016-11-02 | University of Florida Research Foundation, Inc. | Desferrithiocin polyether analogues |
| US20080194518A1 (en) | 2005-12-23 | 2008-08-14 | MOOKERJEE Pradip | Antimicrobial Compositions |
| CN101129381B (zh) | 2006-08-25 | 2012-02-01 | 天津和美生物技术有限公司 | 含β-内酰胺类抗生素和离子螯合剂的抗生素复方 |
| WO2008130395A2 (en) | 2006-12-12 | 2008-10-30 | University Of Florida | Desferrithiocin analogue actinide decorporation agents |
| NZ579994A (en) | 2007-03-15 | 2011-09-30 | Univ Florida | Desferrithiocin polyether analogues useful in the treatment of pathological conditions responsive to chelation or sequestration of trivalent metal |
| FR2922210A1 (fr) | 2007-10-11 | 2009-04-17 | Univ Louis Pasteur Etablisseme | Nouveaux composes, preparation et utilisations |
| WO2009140215A2 (en) * | 2008-05-11 | 2009-11-19 | Geraghty, Erin | Method for treating drug-resistant bacterial and other infections with clioquinol, phanquinone, and related compounds |
| US20110189260A1 (en) * | 2008-05-30 | 2011-08-04 | University Of Cincinnati | Use of zinc chelators to inhibit biofilm formation |
| KR20110039347A (ko) * | 2008-07-14 | 2011-04-15 | 페로킨 바이오사이언시스 인코포레이티드 | 금속 킬레이트화제로서의 데스아자데스페리티오신 폴리에테르 유사체의 신규한 염 및 다형체 |
| BR112012001761A2 (pt) | 2009-07-27 | 2017-05-09 | Ferrokin Bioscience Inc | composto de formula i, composto farmacêutica e método de tratamento de uma condição mediada por metal em um indivduo |
| US20120184586A1 (en) * | 2009-08-25 | 2012-07-19 | University Of Florida Research Foundation, Inc. | Desferrithiocin polyether analogues and uses thereof |
| CA2780756A1 (en) * | 2009-11-23 | 2011-05-26 | Prothera, Inc. | Compositions and methods comprising serratia peptidase for inhibition and treatment of biofilms related to certain conditions |
| NZ603774A (en) * | 2010-05-04 | 2014-11-28 | Ferrokin Biosciences Inc | Desazadesferrothiocin analogues as metal chelation agents |
| WO2012027794A2 (en) | 2010-09-01 | 2012-03-08 | The Mental Health Research Institute Of Victoria | Method of treatment and agents useful for same |
| TW201338777A (zh) | 2011-12-09 | 2013-10-01 | Ferrokin Biosciences Inc | 用於治療金屬過載之經口調配物 |
| US20140323534A1 (en) | 2011-12-16 | 2014-10-30 | University Of Florida Research Foundation, Inc. | Uses of 3'-desferrithiocin analogs |
| ES2761200T3 (es) | 2011-12-16 | 2020-05-19 | Univ Florida | Usos de análogos de 4'-desferritiocina |
| WO2014027355A2 (en) * | 2012-08-15 | 2014-02-20 | Yissum Research Development Company Of The Hebrew University Of Jerusalem Ltd. | Cytotoxic titanium and vanadium complexes |
| WO2014134701A1 (en) | 2013-03-07 | 2014-09-12 | Kane Biotech Inc. | Antimicrobial-antibiofilm compositions and methods of use thereof |
| EP3071201A4 (en) | 2013-11-22 | 2017-04-26 | University of Florida Research Foundation, Inc. | Desferrithiocin analogs and uses thereof |
-
2016
- 2016-04-27 CA CA2984250A patent/CA2984250A1/en not_active Abandoned
- 2016-04-27 CN CN201680037700.5A patent/CN107708693A/zh active Pending
- 2016-04-27 KR KR1020177033736A patent/KR20170140306A/ko unknown
- 2016-04-27 EP EP16787077.3A patent/EP3288557A4/en not_active Withdrawn
- 2016-04-27 WO PCT/US2016/029587 patent/WO2016176343A1/en active Application Filing
- 2016-04-27 AU AU2016255770A patent/AU2016255770A1/en not_active Abandoned
- 2016-04-27 US US15/569,750 patent/US10570104B2/en active Active
- 2016-04-27 JP JP2017556738A patent/JP2018515475A/ja active Pending
-
2017
- 2017-10-26 IL IL255279A patent/IL255279A0/en unknown
-
2018
- 2018-07-26 HK HK18109714.6A patent/HK1250216A1/zh unknown
Also Published As
| Publication number | Publication date |
|---|---|
| AU2016255770A1 (en) | 2017-11-16 |
| WO2016176343A1 (en) | 2016-11-03 |
| IL255279A0 (en) | 2017-12-31 |
| EP3288557A4 (en) | 2018-11-07 |
| EP3288557A1 (en) | 2018-03-07 |
| CN107708693A (zh) | 2018-02-16 |
| CA2984250A1 (en) | 2016-11-03 |
| US10570104B2 (en) | 2020-02-25 |
| HK1250216A1 (zh) | 2018-12-07 |
| JP2018515475A (ja) | 2018-06-14 |
| US20180140581A1 (en) | 2018-05-24 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6838966B2 (ja) | デスフェリチオシン類似体およびその使用 | |
| JP7260521B2 (ja) | タウタンパク質分解の化合物 | |
| JP7308146B2 (ja) | インターロイキン1受容体関連キナーゼの阻害剤およびその使用 | |
| KR20170140306A (ko) | 대사적으로 프로그램화된 금속 킬레이트화제 및 그의 용도 | |
| CA2824317C (en) | Uses of certain f-series prostaglandin analogs for treating diabetes and dyslipidemia | |
| JP6987399B2 (ja) | 4’−デスフェリチオシン類似体の使用 | |
| JP2013500342A (ja) | 金属キレート化剤としてのデサザデスフェロチオシンポリエーテルアナログのプロドラッグ | |
| WO2016154051A1 (en) | Combination therapy for treating infections diseases | |
| JPH0566385B2 (ko) | ||
| CA2728636A1 (en) | Salts and polymorphs of desazadesferrithiocin polyether analogues as metal chelation agents | |
| JP2013525495A (ja) | 金属キレート化剤としてのデスアザデスフェリチオシン類似体 | |
| JP2014520897A (ja) | 一酸化ルテニウム放出分子およびその使用 | |
| CN112566894A (zh) | D-氨基酸氧化酶(daao)的有效抑制剂及其用途 | |
| US20210206713A1 (en) | Compounds and methods for the treatment of neurodegenerative diseases | |
| JP2018184414A (ja) | 新規フラボノイド化合物およびその使用 | |
| JP2000509375A (ja) | 眼炎症の処置における使用のためのニトロン化合物を含む組成物 | |
| WO2016154547A1 (en) | Use of metal chelators in managing infectious diseases | |
| AU2009225298A1 (en) | Novel Bismuth(III) NSAID Compounds and Method for their Use | |
| JP2022516745A (ja) | Dot1l分解剤およびその使用 | |
| JP7449283B2 (ja) | ビアリール誘導体 | |
| JP2005075834A (ja) | 神経変性疾患の処置 | |
| WO2015077652A1 (en) | Desazadesferrithiocin analogs and uses thereof | |
| JP6082643B2 (ja) | 低酸素性細胞放射線増感剤 | |
| WO2014089482A1 (en) | Polymorph forms of desazadesferrithiocin analogs | |
| WO2020081723A1 (en) | Carbon monoxide prodrugs for the treatment of medical disorders |