KR20170056532A - 개선된 색가를 갖는 적색 산화철 안료 - Google Patents
개선된 색가를 갖는 적색 산화철 안료 Download PDFInfo
- Publication number
- KR20170056532A KR20170056532A KR1020177006434A KR20177006434A KR20170056532A KR 20170056532 A KR20170056532 A KR 20170056532A KR 1020177006434 A KR1020177006434 A KR 1020177006434A KR 20177006434 A KR20177006434 A KR 20177006434A KR 20170056532 A KR20170056532 A KR 20170056532A
- Authority
- KR
- South Korea
- Prior art keywords
- iron
- hematite
- pigment
- reaction
- less
- Prior art date
Links
Images
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B82—NANOTECHNOLOGY
- B82Y—SPECIFIC USES OR APPLICATIONS OF NANOSTRUCTURES; MEASUREMENT OR ANALYSIS OF NANOSTRUCTURES; MANUFACTURE OR TREATMENT OF NANOSTRUCTURES
- B82Y30/00—Nanotechnology for materials or surface science, e.g. nanocomposites
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B82—NANOTECHNOLOGY
- B82Y—SPECIFIC USES OR APPLICATIONS OF NANOSTRUCTURES; MEASUREMENT OR ANALYSIS OF NANOSTRUCTURES; MANUFACTURE OR TREATMENT OF NANOSTRUCTURES
- B82Y40/00—Manufacture or treatment of nanostructures
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01G—COMPOUNDS CONTAINING METALS NOT COVERED BY SUBCLASSES C01D OR C01F
- C01G49/00—Compounds of iron
- C01G49/02—Oxides; Hydroxides
- C01G49/06—Ferric oxide (Fe2O3)
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K3/00—Use of inorganic substances as compounding ingredients
- C08K3/01—Use of inorganic substances as compounding ingredients characterized by their specific function
- C08K3/013—Fillers, pigments or reinforcing additives
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K3/00—Use of inorganic substances as compounding ingredients
- C08K3/18—Oxygen-containing compounds, e.g. metal carbonyls
- C08K3/20—Oxides; Hydroxides
- C08K3/22—Oxides; Hydroxides of metals
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09C—TREATMENT OF INORGANIC MATERIALS, OTHER THAN FIBROUS FILLERS, TO ENHANCE THEIR PIGMENTING OR FILLING PROPERTIES ; PREPARATION OF CARBON BLACK ; PREPARATION OF INORGANIC MATERIALS WHICH ARE NO SINGLE CHEMICAL COMPOUNDS AND WHICH ARE MAINLY USED AS PIGMENTS OR FILLERS
- C09C1/00—Treatment of specific inorganic materials other than fibrous fillers; Preparation of carbon black
- C09C1/22—Compounds of iron
- C09C1/24—Oxides of iron
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09C—TREATMENT OF INORGANIC MATERIALS, OTHER THAN FIBROUS FILLERS, TO ENHANCE THEIR PIGMENTING OR FILLING PROPERTIES ; PREPARATION OF CARBON BLACK ; PREPARATION OF INORGANIC MATERIALS WHICH ARE NO SINGLE CHEMICAL COMPOUNDS AND WHICH ARE MAINLY USED AS PIGMENTS OR FILLERS
- C09C3/00—Treatment in general of inorganic materials, other than fibrous fillers, to enhance their pigmenting or filling properties
- C09C3/06—Treatment with inorganic compounds
- C09C3/063—Coating
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09D—COATING COMPOSITIONS, e.g. PAINTS, VARNISHES OR LACQUERS; FILLING PASTES; CHEMICAL PAINT OR INK REMOVERS; INKS; CORRECTING FLUIDS; WOODSTAINS; PASTES OR SOLIDS FOR COLOURING OR PRINTING; USE OF MATERIALS THEREFOR
- C09D1/00—Coating compositions, e.g. paints, varnishes or lacquers, based on inorganic substances
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09D—COATING COMPOSITIONS, e.g. PAINTS, VARNISHES OR LACQUERS; FILLING PASTES; CHEMICAL PAINT OR INK REMOVERS; INKS; CORRECTING FLUIDS; WOODSTAINS; PASTES OR SOLIDS FOR COLOURING OR PRINTING; USE OF MATERIALS THEREFOR
- C09D7/00—Features of coating compositions, not provided for in group C09D5/00; Processes for incorporating ingredients in coating compositions
-
- C09D7/1216—
-
- C09D7/1225—
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09D—COATING COMPOSITIONS, e.g. PAINTS, VARNISHES OR LACQUERS; FILLING PASTES; CHEMICAL PAINT OR INK REMOVERS; INKS; CORRECTING FLUIDS; WOODSTAINS; PASTES OR SOLIDS FOR COLOURING OR PRINTING; USE OF MATERIALS THEREFOR
- C09D7/00—Features of coating compositions, not provided for in group C09D5/00; Processes for incorporating ingredients in coating compositions
- C09D7/40—Additives
- C09D7/60—Additives non-macromolecular
- C09D7/61—Additives non-macromolecular inorganic
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09D—COATING COMPOSITIONS, e.g. PAINTS, VARNISHES OR LACQUERS; FILLING PASTES; CHEMICAL PAINT OR INK REMOVERS; INKS; CORRECTING FLUIDS; WOODSTAINS; PASTES OR SOLIDS FOR COLOURING OR PRINTING; USE OF MATERIALS THEREFOR
- C09D7/00—Features of coating compositions, not provided for in group C09D5/00; Processes for incorporating ingredients in coating compositions
- C09D7/40—Additives
- C09D7/60—Additives non-macromolecular
- C09D7/61—Additives non-macromolecular inorganic
- C09D7/62—Additives non-macromolecular inorganic modified by treatment with other compounds
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2004/00—Particle morphology
- C01P2004/60—Particles characterised by their size
- C01P2004/62—Submicrometer sized, i.e. from 0.1-1 micrometer
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2004/00—Particle morphology
- C01P2004/60—Particles characterised by their size
- C01P2004/64—Nanometer sized, i.e. from 1-100 nanometer
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2004/00—Particle morphology
- C01P2004/80—Particles consisting of a mixture of two or more inorganic phases
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2004/00—Particle morphology
- C01P2004/80—Particles consisting of a mixture of two or more inorganic phases
- C01P2004/82—Particles consisting of a mixture of two or more inorganic phases two phases having the same anion, e.g. both oxidic phases
- C01P2004/84—Particles consisting of a mixture of two or more inorganic phases two phases having the same anion, e.g. both oxidic phases one phase coated with the other
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2006/00—Physical properties of inorganic compounds
- C01P2006/12—Surface area
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2006/00—Physical properties of inorganic compounds
- C01P2006/19—Oil-absorption capacity, e.g. DBP values
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2006/00—Physical properties of inorganic compounds
- C01P2006/22—Rheological behaviour as dispersion, e.g. viscosity, sedimentation stability
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2006/00—Physical properties of inorganic compounds
- C01P2006/60—Optical properties, e.g. expressed in CIELAB-values
- C01P2006/63—Optical properties, e.g. expressed in CIELAB-values a* (red-green axis)
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2006/00—Physical properties of inorganic compounds
- C01P2006/80—Compositional purity
- C01P2006/82—Compositional purity water content
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K3/00—Use of inorganic substances as compounding ingredients
- C08K3/18—Oxygen-containing compounds, e.g. metal carbonyls
- C08K3/20—Oxides; Hydroxides
- C08K3/22—Oxides; Hydroxides of metals
- C08K2003/2265—Oxides; Hydroxides of metals of iron
- C08K2003/2272—Ferric oxide (Fe2O3)
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K2201/00—Specific properties of additives
- C08K2201/002—Physical properties
- C08K2201/005—Additives being defined by their particle size in general
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Inorganic Chemistry (AREA)
- Materials Engineering (AREA)
- Life Sciences & Earth Sciences (AREA)
- Wood Science & Technology (AREA)
- Nanotechnology (AREA)
- Polymers & Plastics (AREA)
- Medicinal Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Health & Medical Sciences (AREA)
- Physics & Mathematics (AREA)
- Condensed Matter Physics & Semiconductors (AREA)
- General Physics & Mathematics (AREA)
- Crystallography & Structural Chemistry (AREA)
- Manufacturing & Machinery (AREA)
- Composite Materials (AREA)
- Compounds Of Iron (AREA)
- Pigments, Carbon Blacks, Or Wood Stains (AREA)
- Paints Or Removers (AREA)
Abstract
본 발명은 개선된 색가를 갖는 적색 산화철 안료, 질산염을 사용하는 페니만 공정 (질산염 공정 또는 직접 적색 공정이라고도 함)에 따른 상기 개선된 적색 산화철 안료의 제조 방법, 및 상기 안료의 제조 장치에 관한 것이다.
Description
본 발명은 개선된 색가(color value)를 갖는 산화철 적색 안료, 질산염을 사용하는 페니만 적색 공정(Penniman red process) (질산염 공정 또는 직접 적색 공정(direct red process)이라고도 함)에 의한 상기 개선된 산화철 적색 안료의 제조 방법, 및 그의 제조 장치에 관한 것이다.
산화철은 수많은 산업 분야에서 사용된다. 따라서, 산화철은 예를 들어 세라믹, 건설 자재, 플라스틱, 페인트, 표면 코팅 및 종이에 착색 안료로서 사용되고, 다양한 촉매 또는 지지체 재료를 위한 기재로서 기능을 하며, 오염물질을 흡착 또는 흡수할 수 있다. 자성 산화철은 자기 기록 매체, 토너, 자성유체(ferrofluid)에 또는 의료 용도로, 예를 들어 자기 공명 단층촬영용 조영제로 사용된다.
산화철은 철 염의 침전, 가수분해 및 분해 반응에 의해 수득가능하다 (Ullmann's Encyclopedia of Industrial Chemistry, VCH Weinheim 2006, Chapter 3.1.1. Iron Oxide Pigments, pp. 61-67). 라우스(Laux), 코페라스(Copperas), 침전, 하소 및 페니만 적색 공정이 산업적으로 가장 중요하였다.
그러나, α-Fe2O3 변형체에 상응하는 미분 헤마타이트의 수성 제법은 상당히 더 복잡하다. 숙성 단계의 사용 및 핵으로서의 마그헤마이트 변형체 γ-Fe2O3, 또는 레피도크로사이트 γ-FeOOH의 미분 산화철의 첨가로 헤마타이트가 또한 직접 수성 침전에 의해 제조될 수 있도록 한다 [US 5,421,878; EP0645437A; WO 2009/100767A].
산화철 적색 안료의 또 다른 제조 방법은 질산염 공정 또는 직접 적색 공정이라고도 하는, 페니만 적색 공정이다 (US 1,327,061; US 1,368,748; US 2,937,927; EP 1106577A: US 6,503,315). 이 경우에, 산화철 안료는 철 금속을 용해시키고 철 염 및 산화철 핵의 첨가로 산화시킴으로써 제조된다. 그에 따라, 문헌 [SHEN, Qing; SUN, Fengzhi; Wujiyan Gongye 1997, (6), 5 - 6 (CH), Wujiyan Gongye Bianjib, (CA 128:218378n)]에 묽은 질산이 승온에서 철에 대하여 작용하는 공정이 개시되어 있다. 이로써 헤마타이트 핵 현탁액이 형성된다. 상기 현탁액은 그 자체가 공지된 방식으로 조성되어 적색 안료의 현탁액을 제공하고, 안료가 필요에 따라 통상의 방식으로 상기 현탁액으로부터 단리된다. 그러나, 상기 공정으로 제조된 적색 안료는 상업용 130 표준물의 색 포화도와 유사한 비교적 낮은 색 포화도를 가지므로, 주로 건설 산업에서 사용된다. 130 표준물은 산화철 안료의 색 측정을 위해 통상적으로 사용되는 기준 표준물 베이페록스(Bayferrox)? 130 (독일에 소재하는 란세스 도이치란트 게엠베하(LANXESS Deutschland GmbH)의 제품)에 상응한다.
EP 1106577A에는 승온에서 철에 묽은 질산을 작용시켜 핵, 즉 100 nm 이하의 입자 크기를 갖는 미분 산화철을 제조하는 것을 포함하는, 페니만 적색 공정의 변형예가 개시되어 있다. 철과 질산의 반응은 복잡한 반응이고, 실험 조건에 따라 철의 부동태화로 인한 반응 중단 또는 용해된 질산철을 형성하는 철의 용해를 유도할 수 있다. 이들 두 반응 경로 모두 바람직하지 않고, 따라서 미분 헤마타이트의 제조는 제한된 실험 조건 하에서만 성공적이다. EP 1106577A에는 미분 헤마타이트를 제조하기 위한 그러한 조건이 기재되어 있다. 이 경우에, 철을 90 내지 99℃ 범위의 온도에서 묽은 질산과 반응시킨다.
WO 2013/045608에는 핵, 즉 100 nm 이하의 입자 크기를 갖는 미분 헤마타이트를 제조하는 반응 단계가 개선된, 산화철 적색 안료의 제조 방법이 기재되어 있다.
선행기술에 따른 질산염 공정에서, 철 또는 철과 물의 혼합물이 일반적으로 초기에 충전된다. 그 후에, 헤마타이트 핵 현탁액이 일반적으로 적어도 철에 첨가되고, 후속적으로 질산철 (II) 용액이 혼합물에 첨가된다. 반응은 일반적으로 반응 혼합물의 온도가, 전형적으로 70 내지 99℃로 증가한 후, 및 산소-함유 기체의 도입이 시작된 후에 시작된다.
산화철 적색 안료의 색 강도를 측정하기 위한 오랫동안 인정되어 온 시험 방법이 있는데, 여기서는 산화철 적색 안료로 착색된 콘크리트 시험 시편 또는 표면 코팅 시스템과 같은 매체의 색이 측정된다. 표면 코팅 시스템에서의 산화철 적색 안료의 색을 측정하기 위한 표준 파라미터로서 CIELAB 색 공간의 파라미터가 확립되었다. 그의 기본 방법이 표준 DIN EN ISO 11664-4 "측색법 - 파트 4: CIE 1976 L*a*b* 색 공간" (Beuth publishers, 2011-07 edition)에 서술되어 있다. 이러한 3차원 색 공간에서의 각각의 인지가능한 색은 L* (명도), a* (적색-녹색 값) 및 b* (황색-청색 값) 좌표를 갖는 색 위치에 의해 정의된다. 반대색 이론에 따르면, 녹색과 적색이 a* 축을 따라 서로 반대 편에 위치하고, 황색-청색의 색이 b* 축을 따라 서로 반대 편에 위치한다. a* 값이 보다 큰 양수일수록, 보다 강한 색조의 적색이 보인다. 반대로, a* 값이 보다 큰 음수일수록, 보다 강한 색조의 녹색이 보인다. 황색-청색의 반대색은 a* 축과 직각으로 교차하는 b* 축을 따라서 상황이 유사하다. b* 값이 보다 큰 양수일수록, 보다 강한 색조의 황색이 보인다. 반대로, b* 값이 보다 큰 음수일수록, 보다 강한 색조의 청색이 보인다. L* 축은 a* 및 b* 좌표에 의해 형성된 평면에 대하여 수직이고 명도를 나타낸다. L* 축은 또한 무채색(neutral gray) 축이라고도 한다. 이것은 흑색 (L=0) 및 백색 (L=100) 종점을 포함한다. 이러한 파라미터 외에도, 색 포화도 C* (채도, 색도 또는 색 강도라고도 함)가 또한 종종 기록된다. 이 값은 a* 및 b* 값으로부터 직접 유도되며 a* 및 b*의 제곱의 합계의 제곱근이다. a*, b*, L* 및 C*는 무차원 값이다. 그러나, CIELAB 단위의 차원이 본 명세서에서 일반적으로 사용된다.
산화철 적색 안료의 색 측정에 있어서, 요변성 장유성 알키드 수지를 이용하는 시험 (DIN EN ISO 11664-4:2011-07 및 DIN EN ISO 787-25:2007에 따라, 이들의 변형법으로서, 63 중량% 대신에 64 중량%의 오일 함량 및 상이한 요변성을 갖는 장유성 알키드 수지가 사용됨. 자세한 내용이 실시예 및 방법 섹션에서 제공되었음)에 의한 측정이 특히 유용한 것으로 밝혀졌다. 이 시험은 본 발명에 따라 표면 코팅 시험이라고도 지칭될 것이다. 알키드 수지는 건조되지 않는다는 장점이 있다. 따라서, 페이스트가 측정 전에 먼저 건조되어야 하는 경우보다 더 신속히 측정이 수행될 수 있다. 이 시험 방법에 대한 더욱 자세한 내용이 실시예 및 방법 섹션에서 제공되었다. 이 시험은 또한 산업용으로 제조되는 적색 안료, 예를 들어 란세스 도이치란트 게엠베하 제품을 특정하는데도 사용된다. 이 경우에, 안료 산업에서 일반적인 것처럼, a*, b* 및 L*의 절대 값 뿐만 아니라, Δa*, Δb* 및 ΔL*의 차이 값이 또한 기록된다. 이러한 차이 값은 측정되는 샘플에 대한 값을 기준 표준물과 비교함으로써 결정되고 값 (샘플) - 값 (기준물)의 차이를 나타낸다. 기준 표준물 자체가 다시 서로 비교되고 고유의 배치 번호를 가지므로, a*, b* 및 L*의 절대 값의 비교 뿐만 아니라, 원래의 기준 샘플이 더 이상 이용가능하지 않을 때에도 샘플과 상이한 세대의 기준 표준물 사이에 직접적인 비교가 항상 가능하다. 비교용 측정을 위한 추가 파라미터는 색차 ΔE*이다. 이것은 Δa*, Δb* 및 ΔL*의 차이 값으로부터 결정되며 Δa*, Δb* 및 ΔL*의 제곱의 합계의 제곱근이다.
표면 코팅 시험을 수행하는 2가지 변형예가 있는데, 즉 풀 쉐이드(full shade) 측정 및 리덕션(reduction) 측정이 있다. 풀 쉐이드 측정에서는, 안료가 표준법에서 한정된 표준 조건 하에 투명한 페이스트에 분산된다. 그 후에, 착색된 페이스트의 색가가 결정된다. 리덕션 측정에서는, 안료 대 이산화티타늄의 비율이 1:5를 달성하도록, 금홍석 변형체의 이산화티타늄이 페이스트에 첨가된다. 리덕션은 색을 연하게 하는 백색 안료의 존재 하에서도 안료의 색 강도 및 색 순도 평가를 가능하게 한다.
특히, 풀 쉐이드에서 29 내지 30.5 CIELAB 단위의 a* 값을 갖는 표면 코팅 산업용 높은 색 순도의 산화철 적색 안료가 코페라스, 침전 및 페니만 적색 공정에 의해 제조가능하다. 풀 쉐이드 표면 코팅 시험에서, 이들은 특정 적색 및 황색 캐스트에 의해 구분되고 색 포화도 C*가 40.0 CIELAB 단위 이하이다. 그러나, 리덕션에 의해서는, 즉 상기에 기재된 이산화티타늄과의 혼합물에서는, 적색 캐스트의 상당한 감소, 즉 보다 낮은 a* 값을 나타낸다. 그러나, 사용 관점에서 보면, 풀 쉐이드 및 이산화티타늄과의 혼합물로서의 리덕션 모두에서 매우 강한 적색 캐스트를 갖는 산화철 적색 안료가 이용가능한 것이 특히 유리할 것이다. 풀 쉐이드 및 리덕션에서 적색 캐스트의 거동을 기술하기 위한 특히 매우 적합한 파라미터로서, 풀 쉐이드 및 리덕션으로부터의 a* 값의 합계가 그에 따라 정의된다. 이 파라미터와 관련하여 다양한 시판 제품을 비교하면, a* (풀 쉐이드)와 a* (리덕션)의 합계가 58.0 CIELAB 단위보다 상당히 낮은 것으로 확인된다.
하기 표 1은 다양한 시판 안료의 풀 쉐이드 및 리덕션 표면 코팅 시험에서의 색가를 기록한다.
<표 1> 선행기술에 따른 산화철 적색 안료의 색가
1) 록우드 피그먼츠 엔에이, 인크.(Rockwood Pigments NA, Inc.)의 코페라스? 공정에 의해 제조된 코페라스? 안료
2) 록우드 피그먼츠 엔에이, 인크.의 침전 공정에 의해 제조된 페록시드(Ferroxide)™ 안료
3) 란세스 도이치란트 게엠베하의 라우스 공정에 의해 하소 단계를 통해 제조된 안료
4) 이싱 유싱 인더스트리 앤드 트레이딩 캄파니(Yixing Yuxing Industry and Trading Company)의 페니만 적색 공정에 의해 제조된 안료
5) 침전 공정에 의해 제조된 안료. 실시예는 DE 4235947A의 실시예 3 및 4와 유사한 방식으로 제조되고 그의 색가가 풀 쉐이드 및 리덕션 표면 코팅 시험으로 측정되었음
산화철 적색 안료의 추가 요건은 가용성 염화물의 매우 낮은 함량이다. 강철-보강 콘크리트 (카테고리 2, EN12878)에 산화철 적색 안료를 사용하는 경우에 매우 낮은 염화물 함량이 바람직한데, 그 이유는 염화물에 의해 부식이 초래되기 때문이다. 유럽 표준 DIN EN12878에 따르면 안료 중에 0.1 중량%의 최고 염화물 농도가 규정되어 있다. 염화물 함량은 이온 크로마토그래피에 의해 결정된다.
따라서, 본 발명의 목적은 콘크리트, 플라스틱, 페인트 및 바니시와 같은 매체의 착색에 있어서 동일한 적색 색조를 달성하는 데에 선행기술의 안료에 대한 경우보다 소량이 필요하거나, 또는 선행기술에 따른 안료로서 그의 동량을 사용하여 착색이 수행될 때보다 더 강한 색조가 달성되고, 이러한 특성이 매체의 철저한 착색의 경우 및 또한 보다 연한 안료, 예컨대 백색 안료에 의한 희석 시의 약한 착색으로 나타나는, 산화철 적색 안료를 제공하는 것이다. 또한, 이러한 안료의 단순한 제조 방법을 제공하는 것을 목적으로 한다.
본 발명은 풀 쉐이드 및 리덕션 표면 코팅 시험 (표면 코팅 시험의 정확한 기재내용은 실시예 및 방법을 참조함)에서 a* 값의 합계가 적어도 58.0 CIELAB 단위이고, 바람직하게는 58.5 CIELAB 단위를 초과하고, 특히 바람직하게는 59.0 CIELAB 단위를 초과하는 산화철 적색 안료, 그의 제조 방법, 및 또한 콘크리트, 플라스틱, 페인트 및 바니시의 착색에 있어서의 그의 용도를 제공한다.
추가 실시양태는 풀 쉐이드 및 리덕션 표면 코팅 시험에서 a* 값의 합계가 58.0 내지 61.0 CIELAB 단위, 바람직하게는 58.0 내지 60.0 CIELAB 단위, 보다 바람직하게는 58.5 내지 61.0 CIELAB 단위, 보다 바람직하게는 58.5 내지 60.0 CIELAB 단위, 특히 바람직하게는 59.0 내지 61.0 CIELAB 단위, 보다 특히 바람직하게는 59.0 내지 60.0 CIELAB 단위인 산화철 적색 안료를 포함한다.
추가 실시양태는 풀 쉐이드 및 리덕션 표면 코팅 시험에서 a* 값의 합계가 58.0 내지 61.0 CIELAB 단위, 바람직하게는 58.0 내지 60.0 CIELAB 단위, 보다 바람직하게는 58.5 내지 61.0 CIELAB 단위, 보다 바람직하게는 58.5 내지 60.0 CIELAB 단위, 특히 바람직하게는 59.0 내지 61.0 CIELAB 단위, 보다 특히 바람직하게는 59.0 내지 60.0 CIELAB 단위인 본 발명에 따른 안료, 및 또한 바람직하게는 오일, 왁스, 지방산 또는 지방산 염이 함유된 유기 코팅, 및/또는 바람직하게는 알칼리 금속 및 알칼리 토금속 또는 Mg, Zn, Al, La, Y, Zr, Sn 및/또는 Ca의 무기 염, 예컨대 탄산염, 산화물 또는 수산화물이 함유된 무기 코팅 또는 각각의 경우에 해당되지 않는 것을 포함한다.
바람직한 실시양태에서, 본 발명의 산화철 적색 안료는 α-Fe2O3 변형체를 갖는다. 추가로 바람직한 실시양태에서, 본 발명의 산화철 적색 안료는 0.1 내지 0.3 ㎛의 입자 크기를 포함하고, 본 발명의 산화철 적색 안료의 적어도 80 중량%가 0.1 내지 0.3 ㎛의 입자 크기를 갖는 것이 특히 바람직하다. 추가로 바람직한 실시양태에서, 본 발명의 산화철 적색 안료는 DIN EN ISO 787-5: 1995에 따라 측정된, 15 내지 26, 바람직하게는 15 내지 24의 오일 가를 갖는다. 추가로 바람직한 실시양태에서, 본 발명의 산화철 적색 안료는 1.0 중량% 이상, 바람직하게는 1.0 내지 5.0 중량%의 물 함량을 갖는다. 물은 특히 바람직하게는 결정수로서 존재한다. 추가로 바람직한 실시양태에서, 본 발명의 산화철 적색 안료는 0.001 내지 0.1 중량%의 염화물 함량을 갖는다. 본 발명의 목적상, 염화물 함량은 고체 중 염화물의 총 함량이다.
특히 바람직한 실시양태에서, 본 발명의 산화철 적색 안료는 헤마타이트 변형체 (α-Fe2O3)를 가지고, 0.1 내지 0.3 ㎛의 입자 크기를 포함하며, 매우 특히 바람직하게는 본 발명의 산화철 적색 안료의 적어도 80 중량%가 0.1 내지 0.3 ㎛의 입자 크기를 가지고, DIN EN ISO 787-5: 1995에 따라 측정된, 17 내지 26, 바람직하게는 19 내지 24의 오일 가를 가지며, 1.0 중량% 이상, 바람직하게는 1.0 내지 5.0 중량%의 물 함량을 갖는다.
바람직한 실시양태에서, 본 발명의 산화철 적색 안료는 또한 페이스트의 형태로, 예를 들어 안료 범용 페이스트의 형태로 존재할 때, 뉴턴(Newtonian) 유동 거동을 갖는다.
뉴턴 유동 거동은 전단 속도에 대한 페이스트 점도의 특별한 의존성에 의해 정의된다. 점도는 유체, 예를 들어 안료 페이스트의 점성 거동의 척도로서 정의되며, Pa·s 단위를 갖는다. 점도가 낮을수록, 유체가 보다 묽다. 전단 속도는 유변학, 즉 재료의 변형 및 유동 거동을 연구하는 학문의 개념이고, 유변학적 측정에서 샘플에 적용되는 기계적 응력의 척도로서 정의된다. 전단 속도는 또한 전단 구배라고도 한다. 전단 속도는 시간의 역수, 일반적으로는 1/s 단위를 갖는다. 이상적인 뉴턴 유동 거동을 갖는 유체의 경우에, 그의 점도는 점도가 측정되는 전단 속도와 무관하다. 본 발명의 목적상, 안료 페이스트의 점도는 원뿔 평판 점도계 (미국에 소재하는 브룩필드 엔지니어링 래보러토리즈, 인크.(Brookfield Engineering Laboratories, Inc.)의 Rheo3000)를 사용하여 500/s 내지 2000/s의 전단 속도에서 측정된다. 본 발명에 따르면, 500/s, 1000/s, 1500/s 및 2000/s의 전단 속도에서 측정된 각각의 점도 값이 500/s, 1000/s, 1500/s 및 2000/s의 전단 속도에서의 측정 값의 산술 평균과 10% 이하, 바람직하게는 5% 이하의 편차가 있을 때 뉴턴 유동 거동의 기준이 충족된다. 전단 속도에서 측정되어, 예를 들어 점도가 최고 측정가능한 점도보다 크면, 본 발명에 따른 뉴턴 유동 거동의 기준이 충족되지 않는다. 본 발명에 따르면, 상이한 전단 속도에서의 점도 측정은 20℃에서 수행된다. 본 발명에 따른 측정을 위해 사용되는 안료 페이스트는 중량% 단위로 하기 조성을 갖는 통상의 범용 페이스트이다:
PEG 200
10.0
물
14.7
Byk 044
2.0
디스퍼byk(Disperbyk) 102
2.0
벤톤(Bentone) SD 2
1.0
디스퍼byk 185
8.8
안료
61.5
여기서 사용된 성분은 하기와 같다:
PEG 200: 폴리에틸렌 글리콜 200, 독일에 소재하는 머크 카게아아(Merck KGaA)
Byk 044: 수성 인쇄 잉크 및 중복인쇄 바니시용 실리콘-함유 소포제, 독일에 소재하는 BYK 케미 게엠베하(BYK Chemie GmbH)
디스퍼byk 102: 무용매 습윤화 및 분산 첨가제, 독일에 소재하는 BYK 케미 게엠베하
벤톤 SD 2: 유변학적 첨가제, 미국에 소재하는 엘리멘티스 스페셜티즈(Elementis Specialities)
디스퍼byk 185: 무용매 습윤화 및 분산 첨가제, 독일에 소재하는 BYK 케미 게엠베하
페이스트는 고속 혼합기에서 4500 rpm으로 30분 동안 모든 성분을 서로 혼합함으로써 제조된다.
본 발명의 목적상, 이 시험을 페이스트 점도 시험이라 지칭한다.
이 실시양태에서, 본 발명의 산화철 적색 안료는 풀 쉐이드 및 리덕션 표면 코팅 시험에서 적어도 58.0 CIELAB 단위, 바람직하게는 58.5 CIELAB 단위 초과, 특히 바람직하게는 59.0 CIELAB 단위 초과의 a* 값의 합계를 가지고, 또한 페이스트 점도 시험에서 500/s, 1000/s, 1500/s 및 2000/s의 전단 속도에서 측정된 각각의 점도 값이 500/s, 1000/s, 1500/s 및 2000/s의 전단 속도에서의 측정 값의 산술 평균과 10% 이하, 바람직하게는 5% 이하의 편차가 있는 뉴턴 유동 거동을 나타낸다.
추가 실시양태에서, 본 발명의 산화철 적색 안료는 풀 쉐이드 및 리덕션 표면 코팅 시험에서 58.0 내지 61.0 CIELAB 단위, 바람직하게는 58.0 내지 60.0 CIELAB 단위, 보다 바람직하게는 58.5 내지 61.0 CIELAB 단위, 보다 바람직하게는 58.5 내지 60.0 CIELAB 단위, 특히 바람직하게는 59.0 내지 61.0 CIELAB 단위, 보다 특히 바람직하게는 59.0 내지 60.0의 a* 값의 합계를 가지고, 또한 페이스트 점도 시험에서 500/s, 1000/s, 1500/s 및 2000/s의 전단 속도에서 측정된 각각의 점도 값이 500/s, 1000/s, 1500/s 및 2000/s의 전단 속도에서의 측정 값의 산술 평균과 10% 이하, 바람직하게는 5% 이하의 편차가 있는 뉴턴 유동 거동을 나타낸다.
특히 바람직한 실시양태에서, 본 발명의 안료는 풀 쉐이드 및 리덕션 표면 코팅 시험에서 적어도 58.0 CIELAB 단위, 바람직하게는 58.5 CIELAB 단위 초과, 특히 바람직하게는 59.0 CIELAB 단위 초과의 a* 값의 합계를 가지고, 또한 페이스트 점도 시험에서 500/s, 1000/s, 1500/s 및 2000/s의 전단 속도에서 0.300 내지 0.400 Pa·s의 점도를 갖는다.
추가로 특히 바람직한 실시양태에서, 본 발명의 안료는 풀 쉐이드 및 리덕션 표면 코팅 시험에서 58.0 내지 61.0 CIELAB 단위, 바람직하게는 58.0 내지 60.0 CIELAB 단위, 보다 바람직하게는 58.5 내지 61.0 CIELAB 단위, 보다 바람직하게는 58.5 내지 60.0 CIELAB 단위, 특히 바람직하게는 59.0 내지 61.0 CIELAB 단위, 보다 특히 바람직하게는 59.0 내지 60.0, 특히 바람직하게는 59.0 CIELAB 단위 초과의 a* 값의 합계를 가지고, 또한 페이스트 점도 시험에서 500/s, 1000/s, 1500/s 및 2000/s의 전단 속도에서 0.300 내지 0.400 Pa·s의 점도를 갖는다.
본 발명은 또한 본 발명의 산화철 적색 안료의 제조 방법을 제공한다. 본 발명의 산화철 적색 안료는 바람직하게는 철을 수성 헤마타이트 핵 현탁액 및 철 (II) 염 용액, 바람직하게는 질산철 (II) 용액과, 적어도 1종의 산소-함유 기체의 존재 하에 반응시킴으로써, 즉 페니만 적색 공정에 의해 제조된다. 추가로 바람직한 실시양태에서, 본 발명의 산화철 적색 안료는 600℃ 초과의 온도에서의 하소 단계를 제외한 공정에 의해 제조된다.
추가 실시양태에서, 본 발명의 방법은 적어도 철, 100 nm 이하의 입자 크기 및 40 m2/g 내지 150 m2/g의 BET 비표면적 (DIN 66131에 따라 측정됨)을 갖는 헤마타이트 핵을 함유하는 헤마타이트 핵 현탁액 및 질산철 (II) 용액을, 적어도 1종의 산소-함유 기체의 존재 하에 70 내지 99℃의 온도에서 반응시키는 것을 포함하고,
반응이 산소-함유 기체의 도입 중에 pH 2.2 내지 pH 4.0, 바람직하게는 pH 2.2 내지 pH 3.0의 pH 범위에서 진행되어 헤마타이트 안료 현탁액을 제조하는 것을 특징으로 한다.
바람직한 실시양태에서, 반응은 적어도 산소-함유 기체의 도입 중 처음 40시간에, 바람직하게는 기체의 도입 중 처음 40시간의 80%가 넘게, pH 2.2 내지 pH 4.0, 바람직하게는 pH 2.2 내지 pH 3.0의 pH 범위에서 진행된다.
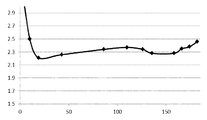
놀랍게도, 반응 현탁액의 pH는 산소-함유 기체 이외에도 기체성 질소를 반응 혼합물에, 바람직하게는 액체 상에 도입함으로써 조절가능하다. 이는 전체 반응 시간 동안에, 예를 들어 상이한 부피/반응 시간 (h)으로, 또는 바람직하게는 반응 혼합물의 pH가 2.2 미만으로 떨어질 때만 수행될 수 있다. 본 발명에 따르면, 기체성 질소는 0 내지 10 부피%의 산소, 바람직하게는 0 내지 1 부피%의 산소를 함유한다. 본 발명에 따르면, 산소-함유 기체는 15 내지 100 부피%의 산소를 함유한다. 산소-함유 기체와 기체성 질소의 총 부피를 기준으로 한 산소 함량이 0 내지 15 부피%, 바람직하게는 0 내지 10 부피%이도록 하는 양의 기체성 질소가 반응 혼합물에 도입되는 것이 바람직하다. 이 경우에, 기체성 질소의 도입은 산소-함유 기체의 도입이 계속되거나 또는 중단되지만, 도입되는 산소-함유 기체와 기체성 질소의 부피 합계가 적어도 1 m3의 기체 부피/배치 부피 (m3)/시간이도록 하는 방식으로 수행될 수 있다. 기체성 질소의 반응 혼합물에의 도입은 반응 혼합물의 pH가 급속히 증가하도록 하여, 반응 혼합물의 pH가 pH 2.2 내지 pH 4.0, 바람직하게는 pH 2.2 내지 pH 3.0의 범위 내에서 유지될 수 있다. 본 발명에 따르면, 질소의 도입은 pH 4.0 초과, 바람직하게는 pH 3.0 초과의 pH 상한에 도달한 후에 다시 중지되며, 단지 pH 2.2 미만의 pH 하한에 도달한 후에 재시작된다. 도 1은 본 발명에 따른 방법의 pH 프로파일을 도시한다. x 축은 반응 시간을 나타내고 y 축은 반응 혼합물의 pH를 나타낸다.
이와 달리, 기체성 질소의 추가 도입 없이 0.2 기체 부피/배치 부피 (m3)/시간 미만으로 도입되는 산소-함유 기체의 부피를 감소시키는 것은 잠시동안만 pH의 증가를 초래하지만, 반응 혼합물에 존재하는 철의 부동태화 때문에 후속적으로 1시간 이내에 pH 1.7 이하로 pH의 급격한 감소를 초래한다. 철의 부동태화는 철 표면 상의 폐쇄적인 수산화철 및 산화철 침착물의 형성에 의해 발생한다. 그에 따라 철이 표면 상의 폐쇄적인 산화철/수산화철 층에 의해 완전히 코팅된다. 이는 바람직하지 않은 조기 중단을 초래하고 결국에는 불완전한 반응에 이른다.
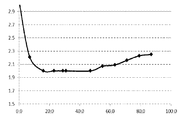
선행기술에 따른 페니만 적색 공정의 전형적인 반응의 pH 프로파일이 도 2에 도시되어 있다.
x 축을 반응 시간을 나타내고 y 축은 반응 혼합물의 pH를 나타낸다. 반응 혼합물의 pH는 보통 2.5 이상이고 산성 질산철 (II) 용액과 산성 헤마타이트 핵 현탁액의 혼합에 의해 한정된다. 승온에서, 전형적으로 70 내지 99℃에서 기체의 도입이 시작된 후에, pH는 약 20시간 이내에 2.1 미만으로 떨어지고, 후속적으로 또 다른 40시간의 기간에 걸쳐서 2.1 내지 2.3의 pH로 다시 증가한다. 이러한 pH 프로파일을 갖는 반응은 풀 쉐이드 및 리덕션에서 57.5 이하의 a* 값의 합계를 갖는 헤마타이트 안료를 제공한다.
한 실시양태에서, 반응은 헤마타이트 안료가 표면 코팅 시험에서 바람직한 색조를 가질 때까지, 즉 풀 쉐이드 및 리덕션에서 적절한 a* 값을 가질 때까지 계속된다. a* 값은 적어도 1종의 산소-함유 기체의 존재 하에 70 내지 99℃의 온도에서의 반응 동안에 보통 증가한다. 이러한 이유로, 샘플을 반응 중 상이한 시점에 수집하여 표면 코팅 시험에 의해 분석한다. 표면 코팅 시험은 보통 1시간 이내에 수행될 수 있다. 그 시간 이내에, 반응 혼합물 중 헤마타이트의 색가는 다시 약간 변화할 수 있다. 그러나, 경험을 토대로 고도로 재현 진행되는 본 발명의 방법에 따른 산업적 제조의 경우에는, 관련 기술분야의 통상의 기술자가 반응의 최적의 중지 시점을 결정할 수 있을 것이다.
추가 실시양태에서, 본 발명의 방법은 통상의 방법에 의해 헤마타이트 안료 현탁액으로부터 헤마타이트 안료를 분리하는 것을 포함한다.
철, 헤마타이트 핵 현탁액 및 질산철 (II) 용액의 적어도 1종의 산소-함유 기체 존재 하의 70 내지 99℃의 온도에서의 반응을 또한 안료 조성이라 한다.
본 발명의 방법에 의해 제조된 산화철 적색 안료는 헤마타이트 변형체 (α-Fe2O3)를 가지므로, 본 발명의 명세서에서 헤마타이트 안료라고도 지칭된다.
한 실시양태에서, 본 발명의 방법에 따른 안료 조성은 도 3에 도시된 반응기에서 수행된다.
본 발명은 추가로 본 발명의 방법을 수행하기에 적합한 장치를 포함한다. 이러한 장치는 도 3을 참조하여 하기에서 더욱 자세히 기재된다.
도 3은 본 발명에 따른 장치를 도시한다.
도 3에서, 부호는 하기 의미를 갖는다:
A
산소-함유 기체
Fe
철
AQ-Fe(NO3)2
질산철 (II) 용액
S-Fe2O3
헤마타이트 핵 현탁액
PAQ- Fe2O3
헤마타이트 안료 현탁액
H2O
물
NOX
산화질소-함유 스트림 (헤마타이트 안료 현탁액의 제조로부터의 오프가스)
1
헤마타이트 안료 현탁액 제조 반응기
11
반응 용기
12
철을 위한 지지체
13
기체 도입 유닛
111
질산철 (II) 용액, 헤마타이트 핵 현탁액 유입구
112
NOX 유출구
113
헤마타이트 안료 현탁액 유출구
114
액체 상 유출구
115
액체 상 유입구
2
교반 디바이스
21
구동기
22
구동기와 교반기 사이의 연결부
23
교반기
31
펌프
41
pH 전극
반응기(1)는 전형적으로 출발 재료에 대하여 내성인 재료로 제조된 1개 이상의 반응 용기를 포함한다. 단일 반응 용기는 예를 들어, 접지되어 있는 벽돌-라이닝 또는 타일 용기일 수 있다. 반응기는 또한 예를 들어, 유리, 질산-내성 플라스틱, 예컨대 폴리테트라플루오로에틸렌 (PTFE), 강철, 예를 들어 에나멜 처리 강철, 플라스틱-코팅 또는 페인팅 강철, 재료 번호 1.44.01의 스테인리스 강철로 제조된 용기를 포함한다. 반응 용기는 개방형 또는 폐쇄형일 수 있다. 본 발명의 바람직한 실시양태에서, 반응 용기는 폐쇄형이다. 반응 용기는 전형적으로 0 내지 150℃ 범위의 온도 및 0.05 MPa 내지 1.5 MPa의 압력용으로 설계된다.
반응기(1)의 바람직한 실시양태가 도 1에 도시되어 있다. 반응기(1)는 적어도 반응 용기(11), 철을 위한 지지체(12), 적어도 1종의 산소-함유 기체(A)를 위한 기체 도입 유닛(13), 적어도 질산철 (II) 용액 및 헤마타이트 핵 현탁액을 위한 유입구(111), 산화질소-함유 스트림(NOX)을 위한 유출구(112), 헤마타이트 안료 현탁액을 위한 유출구(113), 액체 상 유출구(114), 액체 상 유입구(115), 구동기(21), 구동기와 교반기 사이의 연결부(22), 교반기 (23)를 포함하는 교반 디바이스(2), 펌프(31) 및 pH 전극(41)을 갖는다. 유출구(114), 유입구(115) 및 펌프(31)는 액체 상이 반응 용기(11)로부터 도관을 통해 순환하여 다시 반응 용기(11)로 들어갈 수 있도록 도관을 통해 서로 연결된다.
반응기(1)의 추가로 바람직한 실시양태는 적어도 반응 용기(11), 철을 위한 지지체(12), 적어도 1종의 산소-함유 기체(A)를 위한 기체 도입 유닛(13), 적어도 질산철 (II) 용액 및 헤마타이트 핵 현탁액을 위한 유입구(111), 산화질소-함유 스트림(NOX)을 위한 유출구(112), 및 헤마타이트 안료 현탁액을 위한 유출구(113), 및 임의로 pH 전극(41)을 갖는다.
반응기(1)의 추가로 바람직한 실시양태는 적어도 반응 용기(11), 철을 위한 지지체(12), 적어도 1종의 산소-함유 기체(A)를 위한 기체 도입 유닛(13), 적어도 질산철 (II) 용액 및 헤마타이트 핵 현탁액을 위한 유입구(111), 산화질소-함유 스트림(NOX)을 위한 유출구(112), 헤마타이트 안료 현탁액을 위한 유출구(113), 구동기(21), 구동기와 교반기 사이의 연결부(22), 교반기(23)를 포함하는 교반 디바이스(2), 및 임의로 pH 전극(41)을 갖는다.
반응기(1)의 추가로 바람직한 실시양태는 적어도 반응 용기(11), 철을 위한 지지체(12), 적어도 1종의 산소-함유 기체(A)를 위한 기체 도입 유닛(13), 적어도 질산철 (II) 용액 및 헤마타이트 핵 현탁액을 위한 유입구(111), 산화질소-함유 스트림(NOX)을 위한 유출구(112), 헤마타이트 안료 현탁액을 위한 유출구(113), 액체 상 유출구(114), 액체 상 유입구(115), 펌프(31), 및 임의로 pH 전극(41)을 갖는다.
본 발명의 방법은 하기에서 더욱 자세히 기재된다.
도면은 하기를 기재한다:
도 1: 본 발명의 방법에 따른 반응의 pH 프로파일. 시간 (h)이 x 축에 플롯팅되고, 반응 혼합물의 pH가 y 축에 플롯팅된다.
도 2: 선행기술에 따른 질산염 공정의 pH 프로파일. 시간 (h)이 x 축에 플롯팅되고, 반응 혼합물의 pH가 y 축에 플롯팅된다.
도 3: 본 발명의 방법을 수행하기 위한 반응기(1)
도 4: 교반 디바이스(2)
도 1: 본 발명의 방법에 따른 반응의 pH 프로파일. 시간 (h)이 x 축에 플롯팅되고, 반응 혼합물의 pH가 y 축에 플롯팅된다.
도 2: 선행기술에 따른 질산염 공정의 pH 프로파일. 시간 (h)이 x 축에 플롯팅되고, 반응 혼합물의 pH가 y 축에 플롯팅된다.
도 3: 본 발명의 방법을 수행하기 위한 반응기(1)
도 4: 교반 디바이스(2)
여기서 본 발명의 범주는 상기 및 하기에서 언급된 바와 같이 바람직한 범위로 특정된 일반 범위 또는 성분, 값의 범위 또는 공정 파라미터의 모든 바람직하고 가능한 조합을 포함함을 주목할 수 있다.
본 발명의 방법에 사용되는 수성 헤마타이트 핵 현탁액 및 그 중에 존재하는 헤마타이트 핵은 선행기술로부터 공지되어 있다. 상기 대상에 대해서는 선행기술의 개시내용을 참조한다. 물-함유 헤마타이트 핵 현탁액 중에 존재하는 헤마타이트 핵은 100 nm 이하의 입자 크기 및 40 m2/g 내지 150 m2/g의 BET 비표면적 (DIN 66131에 따라 측정됨)을 갖는 핵을 포함한다. 헤마타이트 핵의 적어도 90%가 100 nm 이하, 특히 바람직하게는 30 nm 내지 90 nm의 입자 크기를 가질 때 입자 크기의 기준이 충족된다. 본 발명의 방법에 사용되는 수성 헤마타이트 핵 현탁액은 전형적으로 원형, 타원형 또는 6각형의 입자 형상을 갖는 헤마타이트 핵을 포함한다. 미분 헤마타이트는 전형적으로 높은 순도를 갖는다. 헤마타이트 핵 현탁액의 제조에 사용되는 철 스크랩에 존재하는 이종 금속은 일반적으로 다양한 농도의 망가니즈, 크로뮴, 알루미늄, 구리, 니켈, 코발트 및/또는 티타늄이고, 이들은 또한 산화물 또는 옥시수산화물로서 침전되고 질산과의 반응 중에 미분 헤마타이트에 혼입될 수 있다. 물-함유 헤마타이트 핵 현탁액 중에 존재하는 헤마타이트 핵은 전형적으로 0.1 내지 0.7 중량%, 바람직하게는 0.4 내지 0.6 중량%의 망가니즈 함량을 갖는다. 강하게 착색되는 적색 산화철 안료는 이러한 품질의 핵을 사용하여 제조될 수 있다.
본 발명의 방법에 사용되는 질산철 (II) 용액은 선행기술로부터 공지되어 있다. 상기 대상에 대해서는 선행기술의 개시내용을 참조한다. 상기 질산철 (II) 용액은 전형적으로 50 내지 150 g/l의 Fe(NO3)2 농도 (무수 물질을 기준으로 한 Fe(NO3)2로서 기록됨)를 갖는다. Fe(NO3)2 이외에도, 질산철 (II) 용액은 0 내지 50 g/l의 양으로 Fe(NO3)3를 또한 함유할 수 있다. 그러나, 매우 소량의 Fe(NO3)3가 유리하다.
철로서, 와이어, 시트, 네일(nail), 과립 또는 조대 선삭분(turning) 형태의 철이 보통 본 발명의 방법에 사용된다. 개별 조각은 임의의 형상을 가질 수 있으며 보통 약 0.1 밀리미터 내지 약 10 mm의 두께 (예를 들어, 와이어의 직경으로서 또는 시트의 두께로서 측정됨)를 가질 수 있다. 방법에 사용되는 와이어 번들 또는 시트의 크기는 보통 실현가능성에 따라 달라진다. 따라서, 반응기는 이러한 출발 재료를 어렵지 않게 충전할 수 있어야 하고, 이는 일반적으로 맨홀을 통해 실시된다. 이러한 철은 특히 금속 가공 산업에서 스크랩으로서 또는 부산물로서 제조되고, 예를 들어 스탬핑(stamping) 시트가 있다.
본 발명의 방법에 사용되는 철은 일반적으로 >90 중량%의 철 함량을 갖는다. 이러한 철에 존재하는 불순물은 보통 이종 금속, 예컨대 망가니즈, 크로뮴, 규소, 니켈, 구리 및 다른 원소이다. 그러나, 보다 높은 순도를 갖는 철이 또한 단점 없이 사용될 수 있다. 철은 전형적으로 본 발명에 따라서 반응이 시작될 때 반응 혼합물의 부피를 기준으로 20 내지 150 g/l의 양으로 사용된다. 추가로 바람직한 실시양태에서, 바람직하게는 스탬핑 시트 또는 와이어 형태의 철이 철 지지체 상에 그의 면적에 걸쳐서 2000 kg/m3 미만, 특히 바람직하게는 1000 kg/m3 미만의 바람직한 벌크 밀도로 분배된다. 벌크 밀도는 예를 들어, 적어도 1종의 철 등급의 시트의 굽힘 및/또는 철의 표적 조준에 의해 달성될 수 있다. 이는 전형적으로 철 지지체 아래에서의 산소-함유 기체의 축적 없이, 철 지지체 아래에서 송풍되는 산소-함유 기체의 90 부피%가 넘게 철 지지체를 통과하도록 한다.
철 지지체, 예를 들어 지지체(12)는 가능한 철 지지체에 존재하는 개구를 통해 현탁액과 기체의 교환을 이룬다. 철 지지체의 전형적인 실시양태는 체판, 다공판 또는 그물망일 수 있다. 한 실시양태에서, 개구의 누가 면적 대 총 지지체 면적의 비율은 0.1 내지 0.9, 바람직하게는 0.1 내지 0.3이다. 현탁액의 교환을 위해 요구되는 구멍 또는 개구는 전형적으로 철 지지체를 통한 철의 낙하가 거의 방지되도록 선택된다. 철 지지체, 예를 들어 지지체(12)는 반응기의 내경, 예를 들어 반응 용기(11)의 내경의 직경에 상응할 수 있거나 또는 그 보다 작을 수 있다. 후자의 경우에, 철의 낙하를 방지하기 위해 바람직하게는 철 지지체 디바이스의 측면에 벽이 설치된다. 이러한 벽은 현탁액에 대하여 투과성인, 예를 들어 그물망으로서 구성될 수 있거나, 또는 현탁액에 대하여 불투과성이고, 예를 들어 상단이 개방된 튜브 또는 입방형의 형상을 가질 수 있다.
본 발명에 따르면, 방법을 수행하기 위해 철의 총량이 반응에서 반응한 철 양의 100 내지 140 중량%, 바람직하게는 100 내지 120 중량%의 양으로 초기에 충전된다. 반응에서 반응한 철의 양은 반응 전후에 칭량된 철 양의 차이에 의해 결정된다.
선행기술에 따른 하나의 변형예에서는, 특정 양의 철이 초기에 충전되고, 그 후에 추가 철이 상당한 초과량으로 전체 반응 시간에 걸쳐서 나누어 첨가되며, 전형적으로는 반응에서 반응한 철의 총량의 150 내지 200 중량%가 사용된다. 이러한 방식으로, 반응 혼합물의 pH가 증가할 수 있지만, 생성 안료의 색 특성은 개선이 달성될 수 없다.
바람직한 실시양태에서, 헤마타이트 핵 현탁액 및/또는 질산철 (II) 용액 및/또는 헤마타이트 안료 현탁액의 제조 방법에서 저염수가 물로서 사용된다. 단순하게, 전도도가 염 부하의 척도로서 고려될 수 있다. 본 발명의 목적상, 저염수는 20 μS/cm 이하, 바람직하게는 10 μS/cm 이하, 특히 바람직하게는 5 μS/cm 이하의 전도도를 갖는다. 다가 음이온, 예컨대 공정수에 흔히 존재하는 인산염, 규산염, 황산염 및 탄산염은 산화철 안료에 대하여 응집 효과를 가져 반응 중에도 산화철 안료의 응집을 초래하고 반응기의 바닥에 침강물로서 침적시킨다. 이러한 효과를 피하기 위해, 저염수, 예를 들어 탈이온수 (DI 수), 증류수 또는 역삼투수가 바람직하게 사용된다. 추가적으로, 헤마타이트 안료의 색가가 이로써 개선된다. 특히 바람직한 실시양태에서, 헤마타이트 핵 현탁액 및 질산철 (II) 용액 및 헤마타이트 안료 현탁액의 제조 방법에서 저염수가 물로서 사용된다. 안료의 색가가 이로써 다시 개선될 수 있다.
본 발명의 방법에서, 적어도 1종의 산소-함유 기체 존재 하의 적어도 철, 헤마타이트 핵 현탁액 및 질산철 (II) 용액의 반응은 70 내지 99℃의 온도에서 수행된다.
적어도 1종의 산소-함유 기체는 바람직하게는 공기, 산소, 주위 온도를 초과하여 가열된 공기 또는 증기 풍부화 공기로부터 선택된다.
본 발명의 방법에서, 적어도 철, 헤마타이트 핵 현탁액 및 질산철 (II) 용액의 반응은, 적어도 반응 중에 존재하는 액체 상이 기계식 및/또는 유압식 혼합에 의해, 또는 이들에 의한 혼합 없이 혼합됨으로써 수행된다. 현탁된 헤마타이트가 액체 상에 존재하므로, 기계식 및/또는 유압식 혼합은 임의로 바람직하게는 액체 상에 현탁된 헤마타이트가 액체 상에 균일하게 분산되어 존재하고 액체 상의 하부에 축적되지 않도록 하는 방식으로 수행된다.
본 발명의 목적상, 기계식 혼합은 적합한 디바이스에 의한 액체 상의 혼합이다. 본 발명에 따르면, 액체 상은 그 중에 현탁되어 있는 고체, 예를 들어 헤마타이트 핵 또는 헤마타이트 안료 및 또한 또 다른 고체, 예컨대 철 입자를 또한 함유한다. 기계식 혼합을 위한 적합한 디바이스는 교반 디바이스, 예를 들어 축 방향 교반기, 반경 방향 교반기 및 접선 방향 교반기를 포함한다. 교반 디바이스, 예컨대 도 1의 교반 디바이스(2)는 적어도 1개의 교반기, 예컨대 도 1의 교반기(23), 예를 들어 액체 상의 유동을 발생시키는 프로펠러, 나선체 또는 블레이드를 갖는다. 교반 디바이스는 또한 전형적으로 구동기, 예컨대 도 1의 구동기(21), 예를 들어 모터, 및 교반기와 구동기 사이의 연결부(22), 예를 들어 샤프트 또는 자기 커플링을 갖는다. 교반기 유형에 따라, 유동은 반경 방향으로, 즉 교반기 축에 대하여 직각으로, 또는 축 방향으로, 즉 교반기 축에 대하여 평행하게, 또는 이들이 혼합되어 발생한다. 예를 들어, 블레이드 교반기는 바람직하게는 반경 방향 유동을 발생시키고, 경사 블레이드 교반기 및 프로펠러 교반기는 축 방향 유동을 발생시킨다. 축 방향 유동은 상향 또는 하향일 수 있다. 본 발명의 목적상, 축 방향으로 아래에서부터 철 위로 상향 이동하는 액체 상의 기계식 혼합이 바람직하다. 이는 철 조각 사이의 공극에 존재하는 액체 상이 또한 철 조각 사이의 공극 밖에 존재하는 액체 상과 혼합되도록 보장한다. 적어도 1개의 교반기가 철의 아래 및/또는 위에 바람직하게 위치한다. 축 방향 교반기, 특히 바람직하게는 경사 블레이드 교반기 또는 프로펠러 교반기가 또한 교반기로서 바람직하다.
한 실시양태에서, 반경 방향으로 작동하는 교반기의 경우에 배플이 반응 용기(1)의 내부 벽 상에 추가로 존재한다. 액체 상의 동방향 회전 및 그에 따른 와류 발생이 이로써 방지된다.
기계식 혼합 정도는 교반기, 예를 들어 교반기(23)의 외주 속도에 의해 한정된다. 교반기의 직경에 의해 형성된 원의 원주를 따라 측정된, 바람직한 원주 속도는 0.5 - 15 m/s이다. 본 발명에 따르면, 교반기의 동력 투입으로부터 유도가능한, 액체 상으로의 동력 입력은 배치 부피 1 m3 당 0.1 내지 5 kW, 바람직하게는 배치 부피 1 m3 당 0.4 내지 3 Kw이다. 교반기 직경 대 반응기 내경의 비율은 바람직하게는 0.1 내지 0.9이다. 액체 상으로의 동력 입력은 교반기의 동력 투입 x 교반기의 효율 (%)에 의해 주어진다. 본 발명의 방법에 사용되는 교반기의 전형적인 효율은 70 내지 90%의 범위이다. 본 발명의 목적상, 1 내지 15 m/s의 원주 속도 및 배치 부피 1 m3 당 적어도 0.4 kW의 동력 입력이 특히 바람직하다.
추가 실시양태에서, 유출구, 예를 들어 유출구(114)에서 반응기로부터 액체 상을 수집하고 그 액체 상을 다시 유입구, 예를 들어 유입구(115)로 상이한 위치에서 반응기로 공급하는 펌프, 예를 들어 펌프(31)에 의한 유압식 혼합이 수행된다. 유동이 유입구와 유출구 및 또한 전체 반응 혼합물에서 발생한다. 유압식 혼합은 유출구, 예를 들어 유출구(114)에서 반응기로부터 액체 상을 수집하고 그 액체 상을 다시 유입구, 예를 들어 유입구(115)로 상이한 위치에서 반응기로 공급하는 펌프, 예를 들어 펌프(31)에 의해 수행된다. 그에 따라 유동이 유입구와 유출구 및 또한 전체 반응 혼합물에서 발생한다. 본 발명의 목적상, 0.1 내지 20 배치 부피/시간의 펌핑되는 순환 부피가 바람직하다. 예를 들어, 30 m3의 배치 부피에서 5 배치 부피/시간의 값으로 펌핑되는 순환 부피는 150 m3/시간이다. 추가 실시양태에서, 유입구, 예를 들어 유입구(115)에서 적어도 0.05 m/s, 바람직하게는 적어도 0.06 내지 15 m/s의 유동 속도를 발생시키는 펌핑 순환 부피가 바람직하다. 이 경우에, 유동 속도는 반응기 내부의 반응 혼합물로의 유동의 펌핑에 의해 액체 상이 순환하는 도관으로 전환되는 유입구에서 직접적으로 측정된다. 추가 실시양태에서, 유동은 유입구, 예를 들어 유입구(115)로부터 철 지지체, 예를 들어 철 지지체(12) 위로, 바람직하게는 철 지지체 아래에서 철 지지체 위로 2 m 미만, 바람직하게는 1 m 미만의 거리를 이동한다. 추가 실시양태에서, 유입구, 예를 들어 유입구(115)는 파이프로서 또는 2유체 분무기로서 또는 노즐로서 구성된다.
본 발명의 방법의 바람직한 실시양태에서, 적어도 철, 헤마타이트 핵 현탁액 및 질산철 (II) 용액의 반응은 적어도 1종의 산소-함유 기체를 6 m3 이하의 기체 부피/배치 부피(m3)/시간, 바람직하게는 0.2 내지 6 m3의 기체 부피/배치 부피(m3)/시간, 특히 바람직하게는 0.2 내지 5 m3의 기체 부피/배치 부피(m3)/시간, 매우 특히 바람직하게는 0.2 내지 3 m3의 기체 부피/배치 부피(m3)/시간의 기체 도입 부피로 도입하면서 수행된다.
추가 실시양태에서, 적어도 1종의 산소-함유 기체의 도입은 기계식 혼합 없이, 또한 유압식 혼합 없이 수행된다. 이 경우에, 예를 들어 7 내지 10 m3/시간/배치 부피 (m3)의 기체 도입 부피에서는, 산소-함유 기체의 도입만으로 반응 혼합물의 강력한 혼합이 초래되고, 그 결과 반응 혼합물의 표면에서 액체의 엄격한 비등과 유사한 강력한 대류 및 강력한 기포 형성이 반응 혼합물에서 발생한다.
본 발명에 따르면, 반응 혼합물은 모든 출발 재료 및 그로부터 형성된 고체, 액체 및 기체성 생성물을 포함한다. 산화질소-함유 스트림(NOX)이 또한 반응 중에 형성된다. 바람직한 실시양태에서, 산화질소-함유 스트림(NOX)은, 예를 들어 반응기(1)의 유출구(112)를 통해 반응기로부터 방출된다. 본 발명에 따르면, 배치 부피는 반응 중 특정 시점에 반응 용기, 예를 들어 반응기(1)에 존재하는 반응 혼합물의 액체 및 고체 구성성분의 총 부피로서 정의된다. 배치 부피는 예를 들어 반응 중 임의의 시점에, 반응이 수행되는 반응기의 충전 수준 표시기를 통해 결정될 수 있다.
적어도 1종의 산소-함유 기체의 도입은 바람직하게는 적어도 1종의 산소-함유 기체를 철 지지체, 예를 들어 지지체(12) 아래에 있는 반응 혼합물의 액체 상으로 도입함으로써 수행된다. 기체의 도입은 바람직하게는 반응 혼합물 내에 위치하는 기체 도입 유닛, 예를 들어 기체 도입 유닛(13), 예를 들어 분사 링, 노즐, (2-)유체 분무기 또는 구멍이 있는 파이프 링을 사용하여 수행된다. 상기 목적을 위해, 적어도 1종의 산소-함유 기체는 반응 혼합물의 액체 컬럼의 정수압에 대응하는 충분한 압력을 가져야 한다. 본 발명에 따르면, 반응 혼합물의 pH가 2.2 미만으로 떨어질 때, 기체성 질소가 예를 들어 기체 도입 유닛(13) 또는 또 다른 디바이스를 통해 반응 혼합물에 도입된다. 기체성 질소의 반응 혼합물에의 도입은 pH가 다시 pH 2.2 내지 pH 4.0, 바람직하게는 pH 2.2 내지 pH 3.0의 범위가 되면 중지된다. 반응 혼합물의 pH는 반응 혼합물의 주기적인 샘플링에 의해 또는 반응 용기 내에 위치하는 pH 측정 프로브, 예를 들어 pH 프로브(41)에 의해 결정될 수 있다. pH 프로브(41)는 반응 혼합물 내에 완전히 담겨 있도록 설치된다.
본 발명의 방법 동안에, 안료가 액체 상에 존재하는 헤마타이트 핵 상에서 조성되어 헤마타이트 안료 현탁액을 제조하는데, 그의 색가, 바람직하게는 표면 코팅 시험의 a* 및 b* 값이 안료 조성 중에 변화하는 입자 크기 및/또는 형태학 때문에 반응 동안에 변화한다. 본 발명의 방법이 중지되는 시점은 헤마타이트 안료 현탁액 중에 존재하는 헤마타이트 안료의 색가를 측정함으로써 결정된다. 본 발명의 방법은 헤마타이트 안료가 표면 코팅 시험에서 적어도 58.0 CIELAB 단위, 바람직하게는 58.5 CIELAB 단위 초과, 특히 바람직하게는 59.0 CIELAB 단위 초과의 풀 쉐이드 및 리덕션 표면 코팅 시험의 요구되는 a* 값 합계를 가질 때 중지된다. 수행되는 표면 코팅 시험의 포괄적인 기재내용은 실시예 및 방법 섹션에서 확인될 수 있다. 이는 기체의 도입을 중지함과 동시에, 임의로 반응 혼합물을 70℃ 미만의 온도로 냉각시킴으로써 실시된다. 본 발명에 따른 반응의 전형적인 반응 시간은 바람직한 색조에 따라 10 내지 150시간이다.
바람직한 실시양태에서, 본 발명에 따른 반응 후에 헤마타이트 안료는 통상적인 방법에 의해, 바람직하게는 여과 및/또는 침강 및/또는 원심분리에 의해 헤마타이트 현탁액으로부터 분리된다. 분리 후에 수득된 여과 케이크의 세척 및 여과 케이크의 후속 건조가 또한 바람직하게 수행된다. 특히 바람직하게는 상이한 그물망 개구를 사용하고 또한 그물망 개구를 감소시키면서, 하나 이상의 체질 단계가 또한 헤마타이트 안료를 헤마타이트 안료 현탁액으로부터 분리하기 전에 바람직하게 수행된다. 이는 이종 물체, 예를 들어 금속 조각이 헤마타이트 안료 현탁액으로부터 분리되는 장점을 가지며; 그렇지 않으면 이들 이종 물체는 헤마타이트 안료를 오염시킬 것이다.
헤마타이트 안료 현탁액으로부터의 헤마타이트 안료의 분리는 관련 기술분야의 통상의 기술자에게 공지된 모든 방법, 예를 들어 침강 후에 이어지는 수성 상의 제거 또는 필터 프레스, 예를 들어 막 필터 프레스에 의한 여과를 사용하여 수행될 수 있다.
본 발명의 방법의 바람직한 실시양태에서, 적어도 1종의 황산염, 예를 들어 황산철 (II) 및/또는 알칼리 금속 또는 알칼리 토금속 황산염, 바람직하게는 황산철 (II) 및/또는 황산나트륨이 체질 중에 또는 체질 전에 또한/또는 안료의 분리 중에 또는 안료의 분리 전에 헤마타이트 안료 현탁액에 첨가될 수 있다. 이는 헤마타이트 안료 현탁액으로부터의 헤마타이트 안료의 침강이 가속되는 장점을 갖는다. 이는 헤마타이트 안료의 후속 단리를 더욱 용이하게 한다.
임의로, 이러한 방식으로 분리된 침강물 또는 여과 케이크의 적어도 1번의 세척이 후속적으로 수행된다. 분리 및/또는 세척 후에는 임의로 생성된 헤마타이트 안료를, 예를 들어 필터 건조기, 벨트 건조기, 혼련 건조기, 스핀-플래시 건조기, 건조 오븐 또는 분무 건조기를 사용하여 건조시키는 것이 이어진다. 건조는 바람직하게는 벨트 건조기, 평판 건조기, 혼련 건조기 및/또는 분무 건조기를 사용하여 수행된다.
놀랍게도, 이전에는 달성하지 못했던 색 품질을 가지며 또한 세라믹, 건설 자재, 플라스틱, 페인트, 바니시 및 종이와 같은 매체의 우수한 착색을 위해 요구되는 모든 추가적인 특성을 갖는 산화철 적색 안료가 본 발명의 방법에 의해 수득된다. 특정 실시양태에서, 본 발명의 산화철 적색 안료는 안료 페이스트 형태에서 뉴턴 유동 거동을 추가적으로 갖는다. 이는 페이스트 및 표면 코팅 생성에서 안료의 가공성을 단순화한다. 또한, 본 발명의 산화철 적색 안료는 본 발명의 안료의 색 강도와 가장 근접한 코페라스 안료보다 단순한 방법으로 제조가능하다.
본 발명은 또한 본 발명의 산화철 적색 안료의 페인트, 바니시, 코팅, 건설 자재, 플라스틱 또는 종이 산업 제품의 착색, 식품, 소부 에나멜(baking enamel) 또는 코일 코팅, 모래 과립(sand granule), 규회 벽돌, 에나멜, 세라믹 글레이즈, 아스팔트 또는 바크 멀치(bark mulch)의 착색, 또는 제약 산업 제품, 바람직하게는 정제의 착색에 있어서의 용도, 또는 흡착제, 센서, 촉매로서의 용도, 또는 배터리 또는 어큐뮬레이터, 전극 내 구성요소로서의 용도, 또는 다른 산화철 또는 철 화학물질의 제조를 위한 원료로서의 용도를 제공한다.
본 발명은 또한 본 발명의 산화철 적색 안료를 사용하여, 페인트, 바니시, 코팅, 건설 자재, 플라스틱 또는 종이 산업의 제품, 식품, 소부 에나멜 또는 코일 코팅, 모래 과립, 규회 벽돌, 에나멜, 세라믹 글레이즈, 아스팔트 또는 바크 멀치, 또는 제약 산업의 제품, 바람직하게는 정제를 착색하는 방법을 제공하고, 여기서 착색은 그 자체가 공지된 방법을 사용하여 수행된다.
본 발명은 또한 본 발명의 산화철 적색 안료를 함유하는, 페인트, 바니시, 코팅, 건설 자재, 플라스틱 또는 종이 산업의 제품, 식품, 소부 에나멜 또는 코일 코팅, 모래 과립, 규회 벽돌, 에나멜, 세라믹 글레이즈, 아스팔트 또는 바크 멀치, 또는 제약 산업의 제품, 바람직하게는 정제를 제공한다.
실시예
및 방법:
철 (II) 및 철 (III)의 적정 결정:
질산철 (II)의 함량은 염산으로 산성화된 샘플 용액의 황산세륨 (III)을 사용하는 전위차 적정에 의해 철 (II) 함량을 측정함으로써 간접적으로 결정될 수 있었다.
pH 측정:
pH 측정은 닉(Knick), 메모센스(MemoSens), SE533X/2-NMSN을 사용하여 닉 측정 기구인 프로토스(Protos) MS3400-160에 의해 수행되었다. 측정 전에 pH 4.65 및 pH 9.23의 완충 용액을 사용하여 보정을 수행하였다 (DIN 19267). 85℃의 교반 반응 용기 내에서 pH 측정을 수행하였다.
염화물 함량의 측정:
염화물 함량은 이온 크로마토그래피에 의해 결정되었다.
사용되는 철 등급:
0.8 mm의 두께를 가지며 2500 ppm 이하의 망가니즈, 150 mg 이하의 크로뮴, 0.07% 이하의 탄소, 500 ppm 이하의 알루미늄, 400 ppm 이하의 티타늄 및 250 ppm 이하의 구리를 함유하는 철 스탬핑 시트가 사용되었다.
DI
수 (
탈이온수
):
사용되는 저염수 (DI 수)는 4 μS/cm의 전도도를 가졌다. 이온 농도가 전도도 값으로부터 유도될 수 있었다. WTW의 기구를 사용하여 전기화학 내성 측정법으로 측정을 수행하였다. DI 수의 대체물로서, 전도도가 상기에 언급된 명세에 상응하는 한, 예를 들어 증류수 또는 역삼투 플랜트로부터의 정제수를 사용하는 것이 또한 가능하였다.
색 시험:
요변성 장유성 알키드 수지를 이용하여 풀 쉐이드 및 리덕션 색가, 및 또한 리덕션 색 강도를 시험하였다 (DIN EN ISO 11664-4:2011-07 및 DIN EN ISO 787-25:2007의 방법에 기반함). 무기 착색 안료의 색가를 시험하기 위해, 안료를 불건성 장유성 알키드 수지를 기재로 하는 결합제 페이스트에 분산시켰다. 안료 첨가된 페이스트를 페이스트 평판에 페인팅한 후에, 측색법으로 기준 안료와 비교하여 평가하였다.
1.
작업 기구
-
평판 색 연화기 (PCTM), 평판 직경 240 mm*
-
정밀 저울:
감도 0.001 g (풀 쉐이드)
감도 0.0001 g (리덕션)
-
d/8°의 측정 기하학을 갖는 스펙트럼 색 측정 기구
-
탄성의, 고 연마 블레이드를 갖는 팔레트 나이프 (블레이드 길이: 약 100 mm, 폭: 약 20 mm)
-
DIN EN ISO 787-25:2007에 따른 페이스트 평판 및 닥터 블레이드
2.
보조제
2.1
풀 쉐이드
투명한 시험 페이스트 (DIN EN ISO 787-25:2007에 기반한 방법에 의해 제조된 요변성 장유성 알키드 수지)는 95 중량%의 알키드 수지 (독일에 소재하는 볼리-케미 게엠베하(Worlee-Chemie GmbH)의 볼리키드(WorleeKyd) P151) 및 요변제로서의 5 중량%의 루보틱스(Luvotix) HAT (독일에 소재하는 레만 앤트 포스 앤트 코. 카게(Lehmann & Voss & Co. KG))를 함유하였다. 여기서, 루보틱스를 70-75℃로 예열된 알키드 수지에 넣어 교반하고, 그 후에 전체 요변제가 용해될 때까지 95℃에서 교반하였다. 냉각된 페이스트를 최종적으로 3롤 밀 상에서 기포가 제거될 때까지 압연시켰다.
2.2
리덕션
-
백색 시험 페이스트 (60 중량%의 투명한 시험 페이스트 + 40 중량%의 이산화티타늄 (독일에 소재하는 자흐트레벤 피그먼트 게엠베하(Sachtleben Pigment GmbH)의 R-KB-2))
-
화이트 스피릿(white spirit) 및 기구 세정을 위한 세정포 (2.1 및 2.2에 적용가능함)
3.
절차
3.1
풀 쉐이드 색가 시험
5.00 g의 투명한 시험 페이스트를 평판 색 연화기 (PCTM)의 하부에 도포하였다. 시험할 안료 2.6 g을 색 연화기의 하단 평판의 중간점 바깥쪽에서 완전히 습윤화될 때까지 무압력으로 팔레트 나이프에 의해 "투명한 시험 페이스트"와 예비혼합하였다. 이 혼합물을 후속적으로 3 x 25 회전을 사용하여 분산시켰다. 25 회전 후에 매번, 밀링되고 있는 재료를 팔레트 나이프에 의해 상단 평판으로부터 수집하고 하단 평판에서 밀링되고 있는 재료와 다시 혼합하여 중간점 바깥쪽에 도말하였다. 전체 분산 작업 동안에 색 연화기에 전면 브라킷(bracket)에 대하여 추가 2.5 kg의 중량을 로딩하였다. 마감 제조된 페이스트를 팔레트 나이프에 의해 혼합하여 측정을 위해 페이스트 평판으로 옮겼다. 측정을 위해, 페이스트 평판 상의 초과량의 페이스트를 페이스트 닥터 블레이드로 약한 압력 하에 긁어내었다. 1분의 휴지 시간 후에, 색가의 측정을 즉각적으로 수행하였다.
3.2
리덕션 색가 시험
5.00 g의 "백색 시험 페이스트"를 색 연화기 (PCTM)의 하부에 도입하였다. 안료 대 이산화티타늄의 질량비가 1:5가 되도록, 시험할 안료 0.400 g을 칭량하여 첨가하였다. 각각의 안료를 색 연화기의 하단 평판의 중간점 바깥쪽에서 완전히 습윤화될 때까지 무압력으로 팔레트 나이프에 의해 결합제와 예비혼합하였다. 이 혼합물을 후속적으로 5 x 25 회전을 사용하여 분산시켰다. 25 회전 후에 매번, 모터가 운전되는 동안에, 밀링되고 있는 재료를 팔레트 나이프에 의해 상단 평판으로부터 수집하고 하단 평판에서 밀링되고 있는 재료와 다시 혼합하여 중간점 바깥쪽에 도말하였다. 전체 분산 작업 동안에 색 연화기에 전면 브라킷에 대하여 추가 2.5 kg의 중량을 로딩하였다. 마감 제조된 페이스트를 팔레트 나이프에 의해 혼합하여 측정을 위해 페이스트 평판으로 옮겼다. 측정을 위해, 페이스트 평판 상의 초과량의 페이스트를 페이스트 닥터 블레이드로 약한 압력 하에 긁어내었다. 1분의 휴지 시간 후에, 색가의 측정을 즉각적으로 수행하였다.
상관성 확인을 통해 등가의 분산이 사용된 설정 및 방법에서 가능한 것으로 보장될 때, 다른 분산 장치, 예컨대 마이크로디스멤브레이터(Mikrodismembrator) S (사토리우스(Sartorius)) 또는 2-플래닛 원심분리기 (이축 원심분리기 또는 와동 혼합기)가 사용될 수 있다.
4.
평가
측색법에 의한 평가를 하기 표준법에 따라 수행하였다:
DIN EN ISO 11664-4 (2011-07). 대략 균일한 CIELAB 색 공간에서의 색가 및 색차의 측색법에 의한 결정
DIN 5033 파트 7 색 측정, 체색의 측정 조건; 포인트 2.1.1 하에 한정된 빛의 유형 C; 포인트 3.2.3 하에 한정된 d/8°의 측정 기하학
EN ISO 787-25: 2007 안료 및 충전제의 일반 시험 방법 - 파트 25: 풀 쉐이드 시스템에서 백색, 흑색 및 착색 안료의 색 비교; 측색법 (ISO 787-25:2007).
헤마타이트
핵 현탁액의 제조
핵의 제조
약 1 mm의 두께를 갖는 37 kg의 철 시트를 체판 (그물망 개구: 약 10 mm), 분사 링 (반응기 바닥에 위치), 펌핑 순환 및 경사 블레이드 교반기가 장치된 1 m3 반응기에 넣었다. 분사 링 및 교반기는 체판 아래에 설치되고, 펌프 순환의 유출구는 철 층 측방에, 또한 펌프 순환의 유입구는 반응기의 바닥에 설치되었다. 철 시트를 체판 위에 균일하게 분배하였다. 그 후에, 423 kg의 DI 수를 도입하고 120 rpm으로 교반하였다 (3.2 m/s, 경사 블레이드 교반기, 50 cm의 직경, 동력 입력은 배치 부피 1 m3 당 0.6 kW였음). 철의 초기 충전물을 물이 완전히 덮었다. 혼합물을 90℃로 가열하고, 25 중량% 강도의 질산 97 kg을 60분의 기간에 걸쳐서 후속 계량 첨가하였다. <2.0의 pH에 도달할 때까지 반응을 수행하였다. 이를 위해 8시간이 필요하였다. 수득된 헤마타이트 핵 현탁액을 이어서 주위 온도로 냉각시키고 용기에 분배하였다. 이어서, 용기에서 핵을 완전히 교반한 후에 필요한 양의 헤마타이트 핵 농도를 취하여 페니만 조성을 위해 사용하였다. 헤마타이트 핵 농도 (Fe2O3)는 130 g/l였다.
질산철
(II) 용액의 제조
약 1 mm의 두께를 갖는 62 kg의 철 시트를 체판 (그물망 개구: 약 10 mm), 분사 링 (반응기 바닥에 위치), 펌프 순환 및 경사 블레이드 교반기가 장치된 1 m3 반응기에 넣었다. 분사 링 및 교반기는 체판 아래에 설치되고, 펌프 순환의 유출구는 철 층 측방에, 또한 펌프 순환의 유입구는 반응기의 바닥에 설치되었다. 철 시트를 체판 위에 균일하게 분배하였다. 그 후에, 423 kg의 DI 수를 도입하고 120 rpm으로 교반하였다 (3.2 m/s, 경사 블레이드 교반기, 50 cm의 직경, 동력 입력은 배치 부피 1 m3 당 0.6 kW였음). 25 중량% 강도의 질산 277 kg을 200분의 기간에 걸쳐서 계량 첨가하였다. 5.0의 pH에 도달할 때까지 반응을 수행하였다. 이를 위해 15시간이 필요하였다. 수득된 질산철 (II) 용액을 이어서 주위 온도로 냉각시키고 용기에 분배하였다. 24시간의 침강 시간 후에, 상단에 있는 상 (투명한 상)을 황색/갈색 침강물로부터 분리한 다음, 페니만 조성에 사용하였다. 질산철 (II) 농도 120 g/l였다.
실시예
1
약 1 mm의 두께를 갖는 55 kg의 철 시트를 체판 (그물망 개구: 약 10 mm), 분사 링 (반응기 바닥에 위치), 펌핑 순환 및 경사 블레이드 교반기가 장치된 1 m3 반응기에 넣었다. 분사 링 및 교반기는 체판 아래에 설치되고, 펌프 순환의 유출구는 철 층 측방에, 또한 펌프 순환의 유입구는 반응기의 바닥에 설치되었다. 철 시트를 체판 위에 균일하게 분배하였다. 그 후에, 510 리터의 부피가 수득되고 질산철 (II)의 농도 (무수 질산철로서 계산됨)가 62 g/l이도록 하는 양으로 DI 수 및 질산철 (II)을 첨가하였다. 혼합물을 전체 반응 시간 동안에 교반기에 의해 혼합하였다 (80 rpm, 2.1 m/s, 경사 블레이드 교반기, 50 cm의 직경, 동력 입력은 배치 부피 1 m3 당 0.31 kW였음). 질산철 (II) 용액을 첨가한지 1시간 후에, 130 g/l의 농도 (Fe2O3)를 갖는 헤마타이트 핵 현탁액 161 리터를 첨가하고 혼합물을 85℃로 가열하였다. 85℃에서의 1시간 후에, 800 l/h의 공기 분사를 시작하였다. 또한, 반응 pH를 2.2-2.4의 범위에서 유지하기 위해 필요에 따라 2 m3/h의 질소를 분사 링을 통해 도입하였다 (pH 2.2에서 질소 분사 스위치를 켜고 pH 2.4에서 다시 스위치를 끔).
각각의 경우에 현탁액 샘플 1 리터를 반응 중에 4시간 간격으로 수집하였고, 이들을 석션 필터로 여과하여 DI 수로 세척하였다. 여과물이 <1000 μS/cm의 전도도를 가질 때까지 세척 작업을 계속하였다. 그 후에, 여과 케이크를 80℃에서 5 중량% 미만의 잔류 수분 함량까지 건조시키고, 표면 코팅 시스템에서 색을 측정하였다 (색 시험의 정확한 기재내용은 방법을 참조함). 바람직한 색 공간이 달성된 후에, 반응 혼합물을 황산철 (II) (206 g/l의 FeSO4를 함유하는 29 리터)과 혼합하고, 이어서 필터 프레스로 여과하고, 수득된 헤마타이트 안료를 여과물의 전도도가 <1000 μS/cm일 때까지 DI 수로 세척하였다. 그 후에, 헤마타이트 안료를 80℃에서 5 중량% 미만의 잔류 수분 함량까지 건조시켰다. 건조된 여과 케이크를 이어서 파쇄기에 의해 기계적으로 분쇄하였다. 이러한 방식으로 분말 형태의 헤마타이트 안료가 81.0 kg의 수율로 수득되었다. 총 반응 시간은 185시간이었다. 상기에 기재된 방법의 기재내용에 따라 색 시험을 수행하였다. 건조된 안료의 염화물 함량은 0.006 중량%인 것으로 확인되었다. 페이스트 점도 시험에서 점도는 하기와 같았다: 0.358 Pa·s (500/s), 0.341 Pa·s (1000/s), 0.337 Pa·s (1500/s) 및 0.344 Pa·s (2000/s).
실시예
2 (
비교예
)
약 1 mm의 두께를 갖는 55 kg의 철 시트를 체판 (그물망 개구: 약 10 mm), 분사 링 (반응기 바닥에 위치), 펌프 순환 및 경사 블레이드 교반기가 장치된 1 m3 반응기에 넣었다. 분사 링 및 교반기는 체판 아래에 설치되고, 펌프 순환의 유출구는 철 층 측방에, 또한 펌프 순환의 유입구는 반응기의 바닥에 설치되었다. 철 시트를 체판 위에 균일하게 분배하였다. 그 후에, 510 리터의 부피가 수득되고 질산철 (II)의 농도 (무수 질산철로서 계산됨)가 62 g/l이도록 하는 양으로 DI 수 및 질산철 (II)을 첨가하였다. 혼합물을 전체 반응 시간 동안에 교반기에 의해 혼합하였다 (80 rpm, 2.1 m/s, 경사 블레이드 교반기, 50 cm의 직경, 동력 입력은 배치 부피 1 m3 당 0.31 kW였음). 질산철 (II) 용액을 첨가한지 1시간 후에, 130 g/l의 농도 (Fe2O3)를 갖는 헤마타이트 핵 현탁액 161 리터를 첨가하고 혼합물을 85℃로 가열하였다. 85℃에서의 1시간 후에, 800 l/h의 공기 분사를 시작하였다. 반응 pH가 도 1에 도시되어 있다. 현탁액 샘플 1 리터를 반응 중에 4시간 간격으로 수집하였고, 이들을 석션 필터로 여과하여 DI 수로 세척하였다. 여과물이 <1000 μS/cm의 전도도를 가질 때까지 세척 작업을 수행하였다. 그 후에, 여과 케이크를 80℃에서 5 중량% 미만의 잔류 수분 함량까지 건조시키고, 표면 코팅 시스템에서 색을 측정하였다 (색 시험의 정확한 기재내용은 방법을 참조함). 바람직한 색 공간이 달성된 후에, 반응 혼합물을 황산철 (II) (206 g/l의 FeSO4를 함유하는 29 리터)과 혼합하고, 이어서 필터 프레스로 여과하고, 수득된 헤마타이트 안료를 여과물의 전도도가 <1000 μS/cm일 때까지 DI 수로 세척하였다. 그 후에, 헤마타이트 안료를 80℃에서 5 중량% 미만의 잔류 수분 함량까지 건조시켰다. 건조된 여과 케이크를 이어서 파쇄기에 의해 기계적으로 분쇄하였다. 이러한 방식으로 분말 형태의 헤마타이트 안료가 76.0 kg의 수율로 수득되었다. 총 반응 시간은 96시간이었다. 표면 코팅 시험에서, 풀 쉐이드 a* 값은 29.5 CIELAB 단위로 측정되었고 리덕션 a*는 25.1 CIELAB 단위로 측정되었다. 따라서 a* 값의 합계는 54.6 CIELAB 단위였다. 표면 코팅 시험을 상기에 기재된 방법 기재내용에 따라 수행하였다.
<표 2> 표면 코팅 시험에서의 실시예의 색가
<표 3> 내부 기준 표준물과 R1599D 유형 안료의 비교 값
Claims (18)
- 표면 코팅 시험에서 풀 쉐이드 및 리덕션 a* 값의 합계가 58.0 내지 61.0 CIELAB 단위, 바람직하게는 58.0 내지 60.0 CIELAB 단위, 보다 바람직하게는 58.5 내지 61.0 CIELAB 단위, 보다 바람직하게는 58.5 내지 60.0 CIELAB 단위, 특히 바람직하게는 59.0 내지 61.0 CIELAB 단위, 보다 특히 바람직하게는 59.0 내지 60.0인 것을 특징으로 하는 헤마타이트 안료.
- 제1항에 있어서, α-Fe2O3 변형체를 포함하는 헤마타이트 안료.
- 제1항 또는 제2항에 있어서, 바람직하게는 오일, 왁스, 지방산 또는 지방산 염이 함유된 유기 코팅, 및/또는 바람직하게는 알칼리 금속 및 알칼리 토금속 또는 Mg, Zn, Al, La, Y, Zr, Sn 및/또는 Ca의 탄산염, 산화물 또는 수산화물이 함유된 무기 코팅을 포함하는 헤마타이트 안료.
- 제1항 내지 제3항 중 어느 한 항에 있어서, 유기 코팅 또는 무기 코팅을 어느 것도 포함하지 않는 헤마타이트 안료.
- 제1항 내지 제4항 중 어느 한 항에 있어서, 0.1 내지 0.3 ㎛의 입자 크기를 갖는 헤마타이트 안료.
- 제5항에 있어서, 0.1 내지 0.3 ㎛의 입자 크기를 가지며, 여기서 헤마타이트 안료의 적어도 80 중량%가 0.1 내지 0.3 ㎛의 입자 크기를 갖는 것인 헤마타이트 안료.
- 제1항 내지 제6항 중 어느 한 항에 있어서, 1.0 중량% 이상의 물 함량을 갖는 헤마타이트 안료.
- 제1항 내지 제7항 중 어느 한 항에 있어서, 페이스트 점도 시험에서 500/s, 1000/s, 1500/s 및 2000/s의 전단 속도에서 측정된 각각의 점도 값이 500/s, 1000/s, 1500/s 및 2000/s의 전단 속도에서의 측정 값의 산술 평균과 10% 이하, 바람직하게는 5% 이하의 편차가 있는 뉴턴 유동 거동을 갖는 것을 특징으로 하는 헤마타이트 안료.
- 제1항 내지 제8항 중 어느 한 항에 있어서, 페이스트 점도 시험에서 500/s, 1000/s, 1500/s 및 2000/s의 전단 속도에서 0.300 내지 0.400 Pa·s의 점도를 갖는 것을 특징으로 하는 헤마타이트 안료.
- 제1항 내지 제9항 중 어느 한 항에 있어서, 적어도 1종의 산소-함유 기체 존재 하의 철과 수성 헤마타이트 핵 현탁액 및 철 (II) 염 용액, 바람직하게는 질산철 (II) 용액의 반응에 의해 제조된 헤마타이트 안료.
- 철, 100 nm 이하의 입자 크기 및 40 m2/g 내지 150 m2/g의 BET 비표면적 (DIN 66131에 따라 측정됨)을 갖는 헤마타이트 핵을 함유하는 헤마타이트 핵 현탁액 및 질산철 (II) 용액을, 적어도 1종의 산소-함유 기체의 존재 하에 70 내지 99℃의 온도에서 반응시키는 것을 포함하고, 반응이 산소-함유 기체의 도입 중에 pH 2.2 내지 pH 4.0, 바람직하게는 pH 2.2 내지 pH 3.0의 pH 범위에서 진행되어 헤마타이트 안료 현탁액을 제조하는 것을 특징으로 하는, 헤마타이트 안료의 제조 방법.
- 제11항에 있어서, 반응이 적어도 산소-함유 기체의 도입 중 처음 40시간에, 바람직하게는 기체의 도입 중 처음 40시간의 80%가 넘게, pH 2.2 내지 pH 4.0, 바람직하게는 pH 2.2 내지 pH 3.0의 pH 범위에서 진행되는 것을 특징으로 하는, 헤마타이트 안료의 제조 방법.
- 제11항 또는 제12항에 있어서, 반응 혼합물의 pH가 2.2 미만일 때, 기체성 질소를 반응 혼합물에 추가로 도입하는 것을 특징으로 하는, 헤마타이트 안료의 제조 방법.
- 철, 100 nm 이하의 입자 크기 및 40 m2/g 내지 150 m2/g의 BET 비표면적 (DIN 66131에 따라 측정됨)을 갖는 헤마타이트 핵을 함유하는 헤마타이트 핵 현탁액 및 질산철 (II) 용액을, 적어도 1종의 산소-함유 기체의 존재 하에 70 내지 99℃의 온도에서 반응시키는 것을 포함하고, 반응이 15 내지 100 부피%의 산소 함량을 바람직하게 갖는 산소-함유 기체의 도입 중에 pH 2.2 내지 pH 4.0, 바람직하게는 pH 2.2 내지 pH 3.0의 pH 범위에서 진행되어 헤마타이트 안료 현탁액을 제조하고, 반응 혼합물의 pH가 2.2 미만이라면, 바람직하게는 0 내지 10 부피%의 산소, 특히 바람직하게는 0 내지 1 부피%의 산소를 함유하는 기체성 질소를 도입하는 것을 특징으로 하는, 헤마타이트 안료의 제조 방법.
- 제11항 내지 제14항 중 어느 한 항에 있어서, 철이 철과 물의 혼합물로서 사용되고, 물이 20 μS/cm 이하, 바람직하게는 10 μS/cm 이하, 특히 바람직하게는 5 μS/cm 이하의 전도도를 갖는 것을 특징으로 하는, 헤마타이트 안료의 제조 방법.
- 제1항 내지 제10항 중 어느 한 항의 헤마타이트 안료 또는 제11항 내지 제15항 중 어느 한 항의 방법에 의해 제조된 헤마타이트 안료의, 페인트, 바니시, 코팅, 건설 자재, 플라스틱 또는 종이 산업 제품의 착색을 위한, 식품, 소부 에나멜 또는 코일 코팅, 모래 과립, 규회 벽돌, 에나멜, 세라믹 글레이즈, 아스팔트 또는 바크 멀치의 착색을 위한, 또는 제약 산업 제품, 바람직하게는 정제의 착색을 위한 용도, 또는 흡착제, 센서, 촉매로서의 용도, 또는 배터리 또는 어큐뮬레이터, 전극 내 구성요소로서의 용도, 또는 다른 산화철 또는 철 화학물질의 제조를 위한 원료로서의 용도.
- 제1항 내지 제10항 중 어느 한 항의 헤마타이트 안료 또는 제11항 내지 제15항 중 어느 한 항의 방법에 의해 제조된 헤마타이트 안료를 사용하여, 공지된 방법 그 자체에 의해 착색을 수행하는 페인트, 바니시, 코팅, 건설 자재, 플라스틱 또는 종이 산업의 제품, 식품, 소부 에나멜 또는 코일 코팅, 모래 과립, 규회 벽돌, 에나멜, 세라믹 글레이즈, 아스팔트 또는 바크 멀치, 또는 제약 산업의 제품, 바람직하게는 정제를 착색하는 방법.
- 제1항 내지 제10항 중 어느 한 항의 헤마타이트 안료를 함유하는, 페인트, 바니시, 코팅, 건설 자재, 플라스틱 또는 종이 산업의 제품, 식품, 소부 에나멜 또는 코일 코팅, 모래 과립, 규회 벽돌, 에나멜, 세라믹 글레이즈, 아스팔트 또는 바크 멀치, 또는 제약 산업의 제품, 바람직하게는 정제.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP14184507.3 | 2014-09-11 | ||
| EP14184507 | 2014-09-11 | ||
| PCT/EP2015/070745 WO2016038152A1 (de) | 2014-09-11 | 2015-09-10 | Eisenoxid-rot-pigmente mit verbesserten farbwerten |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20170056532A true KR20170056532A (ko) | 2017-05-23 |
| KR102470829B1 KR102470829B1 (ko) | 2022-11-28 |
Family
ID=51542187
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020177006434A KR102470829B1 (ko) | 2014-09-11 | 2015-09-10 | 헤마타이트 안료 및 그의 제조 방법 |
Country Status (17)
| Country | Link |
|---|---|
| US (1) | US10563066B2 (ko) |
| EP (1) | EP3191409B1 (ko) |
| JP (1) | JP6440830B2 (ko) |
| KR (1) | KR102470829B1 (ko) |
| CN (1) | CN106715336B (ko) |
| AU (1) | AU2015314215B2 (ko) |
| BR (1) | BR112017004876B1 (ko) |
| CA (1) | CA2960836A1 (ko) |
| CO (1) | CO2017002374A2 (ko) |
| DK (1) | DK3191409T3 (ko) |
| ES (1) | ES2718045T3 (ko) |
| MX (1) | MX2017003203A (ko) |
| PL (1) | PL3191409T3 (ko) |
| RU (1) | RU2701032C2 (ko) |
| TR (1) | TR201905873T4 (ko) |
| WO (1) | WO2016038152A1 (ko) |
| ZA (1) | ZA201702513B (ko) |
Families Citing this family (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10221326B2 (en) | 2013-11-08 | 2019-03-05 | Lanxess Deutschland Gmbh | Production of red iron oxide pigment |
| DK3189010T3 (da) | 2014-09-05 | 2019-08-26 | Lanxess Deutschland Gmbh | Fremstilling af rødt jernoxidpigment |
| TR201905873T4 (tr) | 2014-09-11 | 2019-05-21 | Lanxess Deutschland Gmbh | Geliştirilmiş renk değerlerine sahip kırmızı demir oksit pigmentleri. |
| EP3216764A1 (de) | 2016-03-09 | 2017-09-13 | LANXESS Deutschland GmbH | Herstellung von eisenoxid-rot-pigmenten |
| EP3216765A1 (de) * | 2016-03-09 | 2017-09-13 | LANXESS Deutschland GmbH | Herstellung von eisenoxid-rot-pigment |
| PL3219763T3 (pl) * | 2016-03-16 | 2019-05-31 | Lanxess Deutschland Gmbh | Zastosowanie czerwonych pigmentów tlenku żelaza w preparatach wodnych |
| EP3381984A1 (de) | 2017-03-31 | 2018-10-03 | LANXESS Deutschland GmbH | Al-haltige eisenoxidpigmente |
| BR112019020265A2 (pt) | 2017-03-31 | 2020-04-22 | Lanxess Deutschland Gmbh | pigmentos de óxido de ferro contendo al |
| EP3597602A1 (en) | 2018-07-18 | 2020-01-22 | LANXESS Deutschland GmbH | Hematite pigments |
| EP4201999A1 (de) | 2021-12-21 | 2023-06-28 | LANXESS Deutschland GmbH | Verfahren zur herstellung von eisenoxidpigmenten |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6179908B1 (en) * | 1997-10-20 | 2001-01-30 | Bayer Ag | Iron oxide red pigments, process for the production of iron oxide red pigments and use thereof |
| EP1239480A2 (en) * | 2001-03-07 | 2002-09-11 | Pioneer Corporation | Information reproduction apparatus and method for erasing program data |
| JP2003201122A (ja) * | 2001-09-13 | 2003-07-15 | Toda Kogyo Corp | 粒状ヘマタイト粒子粉末の製造法 |
| WO2014091008A1 (de) * | 2012-12-13 | 2014-06-19 | Lanxess Deutschland Gmbh | Beschichtete pigmente zur einfärbung von pvc |
Family Cites Families (37)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US1327061A (en) | 1917-06-20 | 1920-01-06 | West Coast Kalsomine Company | Process of manufacturing iron compounds |
| US1368748A (en) | 1920-01-05 | 1921-02-15 | Nat Ferrite Company | Process of manufacturing iron compounds and product |
| US2937927A (en) | 1956-11-13 | 1960-05-24 | C K Williams & Co | Production of red oxide of iron pigments |
| DE2249274A1 (de) * | 1972-10-07 | 1974-04-18 | Bayer Ag | Herstellung von gefaelltem rotem eisen(iii)-oxid |
| JPS5594968A (en) * | 1979-01-11 | 1980-07-18 | Sanyo Shikiso Kk | Preparing red iron oxide pigment |
| DE3107117A1 (de) | 1981-02-26 | 1982-09-09 | Kali-Chemie Ag, 3000 Hannover | "verfarhen zur atrennung von no(pfeil abwaerts)x(pfeil abwaerts)-gas" |
| JPS57209834A (en) * | 1981-06-22 | 1982-12-23 | Mitsui Toatsu Chem Inc | Preparation of goethite |
| DE3500470A1 (de) | 1985-01-09 | 1986-07-10 | Bayer Ag, 5090 Leverkusen | Verfahren zur herstellung heller farbreiner eisenoxidrotpigmente |
| JPS6320367A (ja) | 1986-07-11 | 1988-01-28 | Ube Ind Ltd | 赤色複合顔料 |
| SU1458368A1 (ru) | 1987-01-26 | 1989-02-15 | Предприятие П/Я Г-4855 | Способ получени зародышей красного железоокисного пигмента |
| CN1054088A (zh) | 1990-03-17 | 1991-08-28 | 浑江市青沟天然铁红厂 | 利用赤铁矿石生产天然铁红 |
| RU2047556C1 (ru) | 1992-03-13 | 1995-11-10 | Пуртов Анатолий Иванович | Способ получения индивидуальных и сложных оксидов металлов |
| DE4235944A1 (de) * | 1992-10-23 | 1994-04-28 | Bayer Ag | Farbreine Eisenoxid-Direktrotpigmente, Verfahren zu ihrer Herstellung sowie deren Verwendung |
| DE4235947A1 (de) | 1992-10-23 | 1994-04-28 | Bayer Ag | Farbreine Eisenoxid-Direktrotpigmente, Verfahren zu ihrer Herstellung sowie deren Verwendung |
| US5421878A (en) | 1992-10-23 | 1995-06-06 | Bayer Ag | Pure-colored iron oxide direct red pigments, a process for their production and their use |
| EP0645437B1 (de) | 1993-09-23 | 1997-03-19 | Bayer Ag | Farbreine Eisenoxid-Direktrotpigmente, Verfahren zu ihrer Herstellung sowie deren Verwendung |
| DE19533715A1 (de) | 1995-09-12 | 1997-03-13 | Basf Ag | Verfahren zum Entfernen von Stickstoffoxiden aus einem diese enthaltenden Gasstrom |
| JP2001084571A (ja) * | 1999-09-16 | 2001-03-30 | Sony Corp | 磁気記録媒体 |
| DE19958168A1 (de) | 1999-12-02 | 2001-06-07 | Bayer Ag | Verfahren zur Herstellung von Eisenoxidpigmenten |
| CN1406873A (zh) * | 2001-09-13 | 2003-04-02 | 户田工业株式会社 | 粒状赤铁矿微粒的制造方法 |
| US20030170163A1 (en) | 2002-03-07 | 2003-09-11 | Banerjee Pritish Chandra | Synthethic process of manufacturing micronised pure magnetic grade ferric oxide Fe2O3 |
| ITMI20020567A1 (it) | 2002-03-18 | 2003-09-18 | Sud Chemie S R L | Processo per la preparazione di ossidi di ferro |
| ES2553798T3 (es) | 2003-09-03 | 2015-12-11 | Lanxess Deutschland Gmbh | Procedimiento para la producción de pigmentos amarillos de óxido de hierro con CaCO3 como agente de precipitación |
| US7604793B2 (en) | 2004-04-29 | 2009-10-20 | Metalox International | Iron oxide precipitation from acidic iron salt solutions |
| DE102004024013A1 (de) | 2004-05-14 | 2005-12-01 | Bayer Chemicals Ag | Farbreine, gut dispergierbare Eisenoxidrotpigmente mit hoher Mahlstabilität |
| CN1318518C (zh) | 2005-05-27 | 2007-05-30 | 华南理工大学 | 硫酸晶种混酸法氧化铁红制备方法 |
| WO2009100767A1 (en) | 2008-02-15 | 2009-08-20 | Rockwood Italia Spa | Process for producing red iron oxide |
| KR100957855B1 (ko) | 2008-03-31 | 2010-05-14 | (주) 휴브글로벌 | 질산제이철의 제조방법 |
| KR101026361B1 (ko) * | 2008-07-03 | 2011-04-05 | 씨큐브 주식회사 | 판상 산화철 제조방법, 그로부터 제조된 판상 산화철 및판상 산화철 안료 |
| IN2014DN01801A (ko) | 2011-09-30 | 2015-05-15 | Lanxess Deutschland Gmbh | |
| JP5951303B2 (ja) | 2012-03-22 | 2016-07-13 | 日鉄鉱業株式会社 | 硝酸第二鉄水溶液及び亜硝酸ナトリウムの製造方法 |
| CN102976413B (zh) * | 2012-10-29 | 2014-06-25 | 中国有色集团(广西)平桂飞碟股份有限公司 | 一种二步氧化生产氧化铁红颜料的方法 |
| US10221326B2 (en) | 2013-11-08 | 2019-03-05 | Lanxess Deutschland Gmbh | Production of red iron oxide pigment |
| FR3020310B1 (fr) | 2014-04-25 | 2016-04-15 | Michelin & Cie | Pneumatique comportant des epaisseurs de melanges caoutchouteux reduites et des elements de renforcement d'armature de carcasse gaines |
| DK3189010T3 (da) | 2014-09-05 | 2019-08-26 | Lanxess Deutschland Gmbh | Fremstilling af rødt jernoxidpigment |
| CN106795007B (zh) * | 2014-09-05 | 2018-10-30 | 朗盛德国有限责任公司 | 氧化铁(iii)颜料的制备 |
| TR201905873T4 (tr) | 2014-09-11 | 2019-05-21 | Lanxess Deutschland Gmbh | Geliştirilmiş renk değerlerine sahip kırmızı demir oksit pigmentleri. |
-
2015
- 2015-09-10 TR TR2019/05873T patent/TR201905873T4/tr unknown
- 2015-09-10 US US15/510,312 patent/US10563066B2/en active Active
- 2015-09-10 WO PCT/EP2015/070745 patent/WO2016038152A1/de active Application Filing
- 2015-09-10 ES ES15763878T patent/ES2718045T3/es active Active
- 2015-09-10 PL PL15763878T patent/PL3191409T3/pl unknown
- 2015-09-10 JP JP2017513773A patent/JP6440830B2/ja active Active
- 2015-09-10 CA CA2960836A patent/CA2960836A1/en not_active Abandoned
- 2015-09-10 MX MX2017003203A patent/MX2017003203A/es unknown
- 2015-09-10 DK DK15763878.4T patent/DK3191409T3/da active
- 2015-09-10 AU AU2015314215A patent/AU2015314215B2/en active Active
- 2015-09-10 KR KR1020177006434A patent/KR102470829B1/ko active IP Right Grant
- 2015-09-10 CN CN201580048472.7A patent/CN106715336B/zh active Active
- 2015-09-10 EP EP15763878.4A patent/EP3191409B1/de active Active
- 2015-09-10 RU RU2017112052A patent/RU2701032C2/ru active
- 2015-09-10 BR BR112017004876-0A patent/BR112017004876B1/pt active IP Right Grant
-
2017
- 2017-03-10 CO CONC2017/0002374A patent/CO2017002374A2/es unknown
- 2017-04-10 ZA ZA2017/02513A patent/ZA201702513B/en unknown
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6179908B1 (en) * | 1997-10-20 | 2001-01-30 | Bayer Ag | Iron oxide red pigments, process for the production of iron oxide red pigments and use thereof |
| EP1239480A2 (en) * | 2001-03-07 | 2002-09-11 | Pioneer Corporation | Information reproduction apparatus and method for erasing program data |
| JP2003201122A (ja) * | 2001-09-13 | 2003-07-15 | Toda Kogyo Corp | 粒状ヘマタイト粒子粉末の製造法 |
| WO2014091008A1 (de) * | 2012-12-13 | 2014-06-19 | Lanxess Deutschland Gmbh | Beschichtete pigmente zur einfärbung von pvc |
Also Published As
| Publication number | Publication date |
|---|---|
| AU2015314215A1 (en) | 2017-03-30 |
| BR112017004876A2 (pt) | 2017-12-12 |
| US10563066B2 (en) | 2020-02-18 |
| EP3191409B1 (de) | 2019-01-30 |
| CA2960836A1 (en) | 2016-03-17 |
| WO2016038152A1 (de) | 2016-03-17 |
| ZA201702513B (en) | 2019-07-31 |
| RU2017112052A3 (ko) | 2019-03-15 |
| RU2701032C2 (ru) | 2019-09-24 |
| BR112017004876B1 (pt) | 2022-11-16 |
| MX2017003203A (es) | 2017-07-20 |
| DK3191409T3 (da) | 2019-05-06 |
| CN106715336A (zh) | 2017-05-24 |
| EP3191409A1 (de) | 2017-07-19 |
| CN106715336B (zh) | 2019-05-10 |
| AU2015314215B2 (en) | 2018-02-22 |
| JP6440830B2 (ja) | 2018-12-19 |
| US20170253745A1 (en) | 2017-09-07 |
| RU2017112052A (ru) | 2018-10-11 |
| TR201905873T4 (tr) | 2019-05-21 |
| JP2017530080A (ja) | 2017-10-12 |
| PL3191409T3 (pl) | 2019-07-31 |
| ES2718045T3 (es) | 2019-06-27 |
| CO2017002374A2 (es) | 2017-06-20 |
| KR102470829B1 (ko) | 2022-11-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR102470829B1 (ko) | 헤마타이트 안료 및 그의 제조 방법 | |
| JP6374601B2 (ja) | 赤色酸化鉄顔料の製造 | |
| JP6735737B2 (ja) | 酸化鉄赤色顔料の製造 | |
| JP2017201039A (ja) | 改良された黄色酸化鉄顔料 | |
| KR102331662B1 (ko) | 수성 제제에서의 적색 산화철 안료의 용도 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| E902 | Notification of reason for refusal | ||
| AMND | Amendment | ||
| E601 | Decision to refuse application | ||
| AMND | Amendment | ||
| X701 | Decision to grant (after re-examination) | ||
| GRNT | Written decision to grant |