KR20090051140A - 새로운 유기 발광 소자 재료 및 이를 이용한 유기 발광 소자 - Google Patents
새로운 유기 발광 소자 재료 및 이를 이용한 유기 발광 소자 Download PDFInfo
- Publication number
- KR20090051140A KR20090051140A KR1020080110471A KR20080110471A KR20090051140A KR 20090051140 A KR20090051140 A KR 20090051140A KR 1020080110471 A KR1020080110471 A KR 1020080110471A KR 20080110471 A KR20080110471 A KR 20080110471A KR 20090051140 A KR20090051140 A KR 20090051140A
- Authority
- KR
- South Korea
- Prior art keywords
- group
- formula
- substituted
- compound
- unsubstituted
- Prior art date
Links
- 150000001875 compounds Chemical class 0.000 title claims abstract description 126
- 239000011368 organic material Substances 0.000 claims abstract description 31
- 238000002347 injection Methods 0.000 claims abstract description 20
- 239000007924 injection Substances 0.000 claims abstract description 20
- 230000005525 hole transport Effects 0.000 claims abstract description 14
- YLQBMQCUIZJEEH-UHFFFAOYSA-N Furan Chemical group C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 claims description 42
- 239000000126 substance Substances 0.000 claims description 33
- 125000001424 substituent group Chemical group 0.000 claims description 32
- 125000000217 alkyl group Chemical group 0.000 claims description 24
- 125000003118 aryl group Chemical group 0.000 claims description 22
- 125000000623 heterocyclic group Chemical group 0.000 claims description 22
- 125000003545 alkoxy group Chemical group 0.000 claims description 21
- 125000003342 alkenyl group Chemical group 0.000 claims description 15
- 125000005018 aryl alkenyl group Chemical group 0.000 claims description 14
- 125000003710 aryl alkyl group Chemical group 0.000 claims description 14
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 claims description 12
- 125000002560 nitrile group Chemical group 0.000 claims description 12
- 229910052736 halogen Inorganic materials 0.000 claims description 10
- 125000005843 halogen group Chemical group 0.000 claims description 10
- 150000002367 halogens Chemical group 0.000 claims description 10
- 125000005264 aryl amine group Chemical group 0.000 claims description 9
- 238000000034 method Methods 0.000 claims description 8
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 claims description 8
- 125000000524 functional group Chemical group 0.000 claims description 7
- 125000003277 amino group Chemical group 0.000 claims description 6
- 150000002825 nitriles Chemical group 0.000 claims description 6
- YJTKZCDBKVTVBY-UHFFFAOYSA-N 1,3-Diphenylbenzene Chemical group C1=CC=CC=C1C1=CC=CC(C=2C=CC=CC=2)=C1 YJTKZCDBKVTVBY-UHFFFAOYSA-N 0.000 claims description 5
- PJANXHGTPQOBST-VAWYXSNFSA-N Stilbene Natural products C=1C=CC=CC=1/C=C/C1=CC=CC=C1 PJANXHGTPQOBST-VAWYXSNFSA-N 0.000 claims description 5
- 125000002178 anthracenyl group Chemical group C1(=CC=CC2=CC3=CC=CC=C3C=C12)* 0.000 claims description 5
- 125000006267 biphenyl group Chemical group 0.000 claims description 5
- 125000004432 carbon atom Chemical group C* 0.000 claims description 5
- 125000001624 naphthyl group Chemical group 0.000 claims description 5
- 229910052757 nitrogen Inorganic materials 0.000 claims description 5
- 125000001792 phenanthrenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3C=CC12)* 0.000 claims description 5
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 5
- 125000001725 pyrenyl group Chemical group 0.000 claims description 5
- PJANXHGTPQOBST-UHFFFAOYSA-N stilbene Chemical compound C=1C=CC=CC=1C=CC1=CC=CC=C1 PJANXHGTPQOBST-UHFFFAOYSA-N 0.000 claims description 5
- 235000021286 stilbenes Nutrition 0.000 claims description 5
- YTPLMLYBLZKORZ-UHFFFAOYSA-N Thiophene Chemical group C=1C=CSC=1 YTPLMLYBLZKORZ-UHFFFAOYSA-N 0.000 claims description 4
- 125000005842 heteroatom Chemical group 0.000 claims description 4
- 229910052760 oxygen Inorganic materials 0.000 claims description 4
- FZWLAAWBMGSTSO-UHFFFAOYSA-N Thiazole Chemical group C1=CSC=N1 FZWLAAWBMGSTSO-UHFFFAOYSA-N 0.000 claims description 3
- 125000000732 arylene group Chemical group 0.000 claims description 3
- 229910052739 hydrogen Inorganic materials 0.000 claims description 3
- 239000001257 hydrogen Substances 0.000 claims description 3
- 125000002883 imidazolyl group Chemical group 0.000 claims description 3
- WCPAKWJPBJAGKN-UHFFFAOYSA-N oxadiazole Chemical group C1=CON=N1 WCPAKWJPBJAGKN-UHFFFAOYSA-N 0.000 claims description 3
- 125000002971 oxazolyl group Chemical group 0.000 claims description 3
- 125000003373 pyrazinyl group Chemical group 0.000 claims description 3
- 125000004076 pyridyl group Chemical group 0.000 claims description 3
- 125000000168 pyrrolyl group Chemical group 0.000 claims description 3
- 125000001425 triazolyl group Chemical group 0.000 claims description 3
- 125000001931 aliphatic group Chemical group 0.000 claims description 2
- 150000004982 aromatic amines Chemical class 0.000 claims description 2
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 2
- 125000002080 perylenyl group Chemical group C1(=CC=C2C=CC=C3C4=CC=CC5=CC=CC(C1=C23)=C45)* 0.000 claims description 2
- 125000000843 phenylene group Chemical group C1(=C(C=CC=C1)*)* 0.000 claims description 2
- 229910052717 sulfur Inorganic materials 0.000 claims description 2
- 229920001187 thermosetting polymer Polymers 0.000 claims 6
- 239000000463 material Substances 0.000 abstract description 41
- UJOBWOGCFQCDNV-UHFFFAOYSA-N Carbazole Natural products C1=CC=C2C3=CC=CC=C3NC2=C1 UJOBWOGCFQCDNV-UHFFFAOYSA-N 0.000 abstract description 9
- -1 carbazole compound Chemical class 0.000 abstract description 4
- 150000002894 organic compounds Chemical class 0.000 abstract description 2
- 238000002360 preparation method Methods 0.000 description 120
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 80
- 239000010410 layer Substances 0.000 description 49
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 48
- 238000006243 chemical reaction Methods 0.000 description 37
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 31
- 229940126062 Compound A Drugs 0.000 description 26
- NLDMNSXOCDLTTB-UHFFFAOYSA-N Heterophylliin A Natural products O1C2COC(=O)C3=CC(O)=C(O)C(O)=C3C3=C(O)C(O)=C(O)C=C3C(=O)OC2C(OC(=O)C=2C=C(O)C(O)=C(O)C=2)C(O)C1OC(=O)C1=CC(O)=C(O)C(O)=C1 NLDMNSXOCDLTTB-UHFFFAOYSA-N 0.000 description 26
- 239000012044 organic layer Substances 0.000 description 25
- NFHFRUOZVGFOOS-UHFFFAOYSA-N palladium;triphenylphosphane Chemical compound [Pd].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 NFHFRUOZVGFOOS-UHFFFAOYSA-N 0.000 description 23
- 238000004821 distillation Methods 0.000 description 22
- 238000003756 stirring Methods 0.000 description 22
- 238000001953 recrystallisation Methods 0.000 description 19
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 19
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 18
- MFRIHAYPQRLWNB-UHFFFAOYSA-N sodium tert-butoxide Chemical compound [Na+].CC(C)(C)[O-] MFRIHAYPQRLWNB-UHFFFAOYSA-N 0.000 description 17
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 16
- PCLIMKBDDGJMGD-UHFFFAOYSA-N N-bromosuccinimide Chemical compound BrN1C(=O)CCC1=O PCLIMKBDDGJMGD-UHFFFAOYSA-N 0.000 description 14
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 14
- 239000007787 solid Substances 0.000 description 13
- 239000000243 solution Substances 0.000 description 13
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 11
- 239000008096 xylene Substances 0.000 description 11
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 10
- 239000007864 aqueous solution Substances 0.000 description 10
- 239000012153 distilled water Substances 0.000 description 10
- 230000005684 electric field Effects 0.000 description 10
- AFCARXCZXQIEQB-UHFFFAOYSA-N N-[3-oxo-3-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)propyl]-2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidine-5-carboxamide Chemical compound O=C(CCNC(=O)C=1C=NC(=NC=1)NCC1=CC(=CC=C1)OC(F)(F)F)N1CC2=C(CC1)NN=N2 AFCARXCZXQIEQB-UHFFFAOYSA-N 0.000 description 7
- 229910000027 potassium carbonate Inorganic materials 0.000 description 7
- LVTJOONKWUXEFR-FZRMHRINSA-N protoneodioscin Natural products O(C[C@@H](CC[C@]1(O)[C@H](C)[C@@H]2[C@]3(C)[C@H]([C@H]4[C@@H]([C@]5(C)C(=CC4)C[C@@H](O[C@@H]4[C@H](O[C@H]6[C@@H](O)[C@@H](O)[C@@H](O)[C@H](C)O6)[C@@H](O)[C@H](O[C@H]6[C@@H](O)[C@@H](O)[C@@H](O)[C@H](C)O6)[C@H](CO)O4)CC5)CC3)C[C@@H]2O1)C)[C@H]1[C@H](O)[C@H](O)[C@H](O)[C@@H](CO)O1 LVTJOONKWUXEFR-FZRMHRINSA-N 0.000 description 7
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 6
- 230000002378 acidificating effect Effects 0.000 description 6
- 150000004945 aromatic hydrocarbons Chemical group 0.000 description 6
- 239000004927 clay Substances 0.000 description 6
- JNGZXGGOCLZBFB-IVCQMTBJSA-N compound E Chemical compound N([C@@H](C)C(=O)N[C@@H]1C(N(C)C2=CC=CC=C2C(C=2C=CC=CC=2)=N1)=O)C(=O)CC1=CC(F)=CC(F)=C1 JNGZXGGOCLZBFB-IVCQMTBJSA-N 0.000 description 6
- 238000000151 deposition Methods 0.000 description 6
- 239000000758 substrate Substances 0.000 description 6
- 238000000576 coating method Methods 0.000 description 5
- 238000001914 filtration Methods 0.000 description 5
- 238000004768 lowest unoccupied molecular orbital Methods 0.000 description 5
- TYJJADVDDVDEDZ-UHFFFAOYSA-M potassium hydrogencarbonate Chemical compound [K+].OC([O-])=O TYJJADVDDVDEDZ-UHFFFAOYSA-M 0.000 description 5
- 239000002904 solvent Substances 0.000 description 5
- ZGNPLWZYVAFUNZ-UHFFFAOYSA-N tert-butylphosphane Chemical compound CC(C)(C)P ZGNPLWZYVAFUNZ-UHFFFAOYSA-N 0.000 description 5
- CAYQIZIAYYNFCS-UHFFFAOYSA-N (4-chlorophenyl)boronic acid Chemical compound OB(O)C1=CC=C(Cl)C=C1 CAYQIZIAYYNFCS-UHFFFAOYSA-N 0.000 description 4
- JAUCIDPGGHZXRP-UHFFFAOYSA-N 4-phenyl-n-(4-phenylphenyl)aniline Chemical compound C=1C=C(C=2C=CC=CC=2)C=CC=1NC(C=C1)=CC=C1C1=CC=CC=C1 JAUCIDPGGHZXRP-UHFFFAOYSA-N 0.000 description 4
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 4
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 4
- MZRVEZGGRBJDDB-UHFFFAOYSA-N N-Butyllithium Chemical compound [Li]CCCC MZRVEZGGRBJDDB-UHFFFAOYSA-N 0.000 description 4
- 238000004519 manufacturing process Methods 0.000 description 4
- MXQOYLRVSVOCQT-UHFFFAOYSA-N palladium;tritert-butylphosphane Chemical compound [Pd].CC(C)(C)P(C(C)(C)C)C(C)(C)C.CC(C)(C)P(C(C)(C)C)C(C)(C)C MXQOYLRVSVOCQT-UHFFFAOYSA-N 0.000 description 4
- HXITXNWTGFUOAU-UHFFFAOYSA-N phenylboronic acid Chemical compound OB(O)C1=CC=CC=C1 HXITXNWTGFUOAU-UHFFFAOYSA-N 0.000 description 4
- 238000000746 purification Methods 0.000 description 4
- YJLUBHOZZTYQIP-UHFFFAOYSA-N 2-[5-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]-1,3,4-oxadiazol-2-yl]-1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethanone Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)C1=NN=C(O1)CC(=O)N1CC2=C(CC1)NN=N2 YJLUBHOZZTYQIP-UHFFFAOYSA-N 0.000 description 3
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 3
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- XQVWYOYUZDUNRW-UHFFFAOYSA-N N-Phenyl-1-naphthylamine Chemical compound C=1C=CC2=CC=CC=C2C=1NC1=CC=CC=C1 XQVWYOYUZDUNRW-UHFFFAOYSA-N 0.000 description 3
- 230000021615 conjugation Effects 0.000 description 3
- 230000008021 deposition Effects 0.000 description 3
- 238000004770 highest occupied molecular orbital Methods 0.000 description 3
- PQXKHYXIUOZZFA-UHFFFAOYSA-M lithium fluoride Chemical compound [Li+].[F-] PQXKHYXIUOZZFA-UHFFFAOYSA-M 0.000 description 3
- 239000000203 mixture Substances 0.000 description 3
- 238000005406 washing Methods 0.000 description 3
- OHVLMTFVQDZYHP-UHFFFAOYSA-N 1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)-2-[4-[2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidin-5-yl]piperazin-1-yl]ethanone Chemical compound N1N=NC=2CN(CCC=21)C(CN1CCN(CC1)C=1C=NC(=NC=1)NCC1=CC(=CC=C1)OC(F)(F)F)=O OHVLMTFVQDZYHP-UHFFFAOYSA-N 0.000 description 2
- HMUNWXXNJPVALC-UHFFFAOYSA-N 1-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]piperazin-1-yl]-2-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethanone Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)N1CCN(CC1)C(CN1CC2=C(CC1)NN=N2)=O HMUNWXXNJPVALC-UHFFFAOYSA-N 0.000 description 2
- VZSRBBMJRBPUNF-UHFFFAOYSA-N 2-(2,3-dihydro-1H-inden-2-ylamino)-N-[3-oxo-3-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)propyl]pyrimidine-5-carboxamide Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)C(=O)NCCC(N1CC2=C(CC1)NN=N2)=O VZSRBBMJRBPUNF-UHFFFAOYSA-N 0.000 description 2
- SXAMGRAIZSSWIH-UHFFFAOYSA-N 2-[3-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]-1,2,4-oxadiazol-5-yl]-1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethanone Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)C1=NOC(=N1)CC(=O)N1CC2=C(CC1)NN=N2 SXAMGRAIZSSWIH-UHFFFAOYSA-N 0.000 description 2
- WZFUQSJFWNHZHM-UHFFFAOYSA-N 2-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]piperazin-1-yl]-1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethanone Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)N1CCN(CC1)CC(=O)N1CC2=C(CC1)NN=N2 WZFUQSJFWNHZHM-UHFFFAOYSA-N 0.000 description 2
- IHCCLXNEEPMSIO-UHFFFAOYSA-N 2-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]piperidin-1-yl]-1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethanone Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)C1CCN(CC1)CC(=O)N1CC2=C(CC1)NN=N2 IHCCLXNEEPMSIO-UHFFFAOYSA-N 0.000 description 2
- ZRPAUEVGEGEPFQ-UHFFFAOYSA-N 2-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]pyrazol-1-yl]-1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethanone Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)C=1C=NN(C=1)CC(=O)N1CC2=C(CC1)NN=N2 ZRPAUEVGEGEPFQ-UHFFFAOYSA-N 0.000 description 2
- JVKRKMWZYMKVTQ-UHFFFAOYSA-N 2-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]pyrazol-1-yl]-N-(2-oxo-3H-1,3-benzoxazol-6-yl)acetamide Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)C=1C=NN(C=1)CC(=O)NC1=CC2=C(NC(O2)=O)C=C1 JVKRKMWZYMKVTQ-UHFFFAOYSA-N 0.000 description 2
- YLZOPXRUQYQQID-UHFFFAOYSA-N 3-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)-1-[4-[2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidin-5-yl]piperazin-1-yl]propan-1-one Chemical compound N1N=NC=2CN(CCC=21)CCC(=O)N1CCN(CC1)C=1C=NC(=NC=1)NCC1=CC(=CC=C1)OC(F)(F)F YLZOPXRUQYQQID-UHFFFAOYSA-N 0.000 description 2
- MKYBYDHXWVHEJW-UHFFFAOYSA-N N-[1-oxo-1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)propan-2-yl]-2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidine-5-carboxamide Chemical compound O=C(C(C)NC(=O)C=1C=NC(=NC=1)NCC1=CC(=CC=C1)OC(F)(F)F)N1CC2=C(CC1)NN=N2 MKYBYDHXWVHEJW-UHFFFAOYSA-N 0.000 description 2
- NIPNSKYNPDTRPC-UHFFFAOYSA-N N-[2-oxo-2-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethyl]-2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidine-5-carboxamide Chemical compound O=C(CNC(=O)C=1C=NC(=NC=1)NCC1=CC(=CC=C1)OC(F)(F)F)N1CC2=C(CC1)NN=N2 NIPNSKYNPDTRPC-UHFFFAOYSA-N 0.000 description 2
- 229910052782 aluminium Inorganic materials 0.000 description 2
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 2
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 2
- 239000011248 coating agent Substances 0.000 description 2
- 239000003599 detergent Substances 0.000 description 2
- 239000010408 film Substances 0.000 description 2
- 230000009477 glass transition Effects 0.000 description 2
- 229910052751 metal Inorganic materials 0.000 description 2
- 239000002184 metal Substances 0.000 description 2
- 230000003647 oxidation Effects 0.000 description 2
- 238000007254 oxidation reaction Methods 0.000 description 2
- 239000001301 oxygen Substances 0.000 description 2
- 239000003208 petroleum Substances 0.000 description 2
- 238000005240 physical vapour deposition Methods 0.000 description 2
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 2
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 2
- WRECIMRULFAWHA-UHFFFAOYSA-N trimethyl borate Chemical compound COB(OC)OC WRECIMRULFAWHA-UHFFFAOYSA-N 0.000 description 2
- 238000001771 vacuum deposition Methods 0.000 description 2
- NAWXUBYGYWOOIX-SFHVURJKSA-N (2s)-2-[[4-[2-(2,4-diaminoquinazolin-6-yl)ethyl]benzoyl]amino]-4-methylidenepentanedioic acid Chemical compound C1=CC2=NC(N)=NC(N)=C2C=C1CCC1=CC=C(C(=O)N[C@@H](CC(=C)C(O)=O)C(O)=O)C=C1 NAWXUBYGYWOOIX-SFHVURJKSA-N 0.000 description 1
- KZEVSDGEBAJOTK-UHFFFAOYSA-N 1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)-2-[5-[2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidin-5-yl]-1,3,4-oxadiazol-2-yl]ethanone Chemical compound N1N=NC=2CN(CCC=21)C(CC=1OC(=NN=1)C=1C=NC(=NC=1)NCC1=CC(=CC=C1)OC(F)(F)F)=O KZEVSDGEBAJOTK-UHFFFAOYSA-N 0.000 description 1
- CTPUUDQIXKUAMO-UHFFFAOYSA-N 1-bromo-3-iodobenzene Chemical compound BrC1=CC=CC(I)=C1 CTPUUDQIXKUAMO-UHFFFAOYSA-N 0.000 description 1
- UCCUXODGPMAHRL-UHFFFAOYSA-N 1-bromo-4-iodobenzene Chemical compound BrC1=CC=C(I)C=C1 UCCUXODGPMAHRL-UHFFFAOYSA-N 0.000 description 1
- GWQSENYKCGJTRI-UHFFFAOYSA-N 1-chloro-4-iodobenzene Chemical compound ClC1=CC=C(I)C=C1 GWQSENYKCGJTRI-UHFFFAOYSA-N 0.000 description 1
- LDXJRKWFNNFDSA-UHFFFAOYSA-N 2-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)-1-[4-[2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidin-5-yl]piperazin-1-yl]ethanone Chemical compound C1CN(CC2=NNN=C21)CC(=O)N3CCN(CC3)C4=CN=C(N=C4)NCC5=CC(=CC=C5)OC(F)(F)F LDXJRKWFNNFDSA-UHFFFAOYSA-N 0.000 description 1
- TUCRZHGAIRVWTI-UHFFFAOYSA-N 2-bromothiophene Chemical compound BrC1=CC=CS1 TUCRZHGAIRVWTI-UHFFFAOYSA-N 0.000 description 1
- DMEVMYSQZPJFOK-UHFFFAOYSA-N 3,4,5,6,9,10-hexazatetracyclo[12.4.0.02,7.08,13]octadeca-1(18),2(7),3,5,8(13),9,11,14,16-nonaene Chemical group N1=NN=C2C3=CC=CC=C3C3=CC=NN=C3C2=N1 DMEVMYSQZPJFOK-UHFFFAOYSA-N 0.000 description 1
- CONKBQPVFMXDOV-QHCPKHFHSA-N 6-[(5S)-5-[[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]piperazin-1-yl]methyl]-2-oxo-1,3-oxazolidin-3-yl]-3H-1,3-benzoxazol-2-one Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)N1CCN(CC1)C[C@H]1CN(C(O1)=O)C1=CC2=C(NC(O2)=O)C=C1 CONKBQPVFMXDOV-QHCPKHFHSA-N 0.000 description 1
- ZOXJGFHDIHLPTG-UHFFFAOYSA-N Boron Chemical group [B] ZOXJGFHDIHLPTG-UHFFFAOYSA-N 0.000 description 1
- ILEFZGNFDZBUEC-UHFFFAOYSA-N C(CCC)C(CCCP)(CCCC)CCCC Chemical compound C(CCC)C(CCCP)(CCCC)CCCC ILEFZGNFDZBUEC-UHFFFAOYSA-N 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical group [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- YZCKVEUIGOORGS-OUBTZVSYSA-N Deuterium Chemical compound [2H] YZCKVEUIGOORGS-OUBTZVSYSA-N 0.000 description 1
- FXHOOIRPVKKKFG-UHFFFAOYSA-N N,N-Dimethylacetamide Chemical compound CN(C)C(C)=O FXHOOIRPVKKKFG-UHFFFAOYSA-N 0.000 description 1
- 229920000144 PEDOT:PSS Polymers 0.000 description 1
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical group [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 1
- 150000001338 aliphatic hydrocarbons Chemical class 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 125000004122 cyclic group Chemical group 0.000 description 1
- 229910052805 deuterium Inorganic materials 0.000 description 1
- 238000003618 dip coating Methods 0.000 description 1
- 238000001704 evaporation Methods 0.000 description 1
- 230000008020 evaporation Effects 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 150000008282 halocarbons Chemical group 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 229930195733 hydrocarbon Natural products 0.000 description 1
- 150000002430 hydrocarbons Chemical group 0.000 description 1
- 150000002431 hydrogen Chemical class 0.000 description 1
- AMGQUBHHOARCQH-UHFFFAOYSA-N indium;oxotin Chemical compound [In].[Sn]=O AMGQUBHHOARCQH-UHFFFAOYSA-N 0.000 description 1
- 238000007641 inkjet printing Methods 0.000 description 1
- 229910044991 metal oxide Inorganic materials 0.000 description 1
- 150000004706 metal oxides Chemical class 0.000 description 1
- 150000002739 metals Chemical class 0.000 description 1
- IBHBKWKFFTZAHE-UHFFFAOYSA-N n-[4-[4-(n-naphthalen-1-ylanilino)phenyl]phenyl]-n-phenylnaphthalen-1-amine Chemical group C1=CC=CC=C1N(C=1C2=CC=CC=C2C=CC=1)C1=CC=C(C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C3=CC=CC=C3C=CC=2)C=C1 IBHBKWKFFTZAHE-UHFFFAOYSA-N 0.000 description 1
- 229960005235 piperonyl butoxide Drugs 0.000 description 1
- 125000002943 quinolinyl group Chemical group N1=C(C=CC2=CC=CC=C12)* 0.000 description 1
- 239000011541 reaction mixture Substances 0.000 description 1
- 238000010992 reflux Methods 0.000 description 1
- 238000007650 screen-printing Methods 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 239000002356 single layer Substances 0.000 description 1
- 238000004528 spin coating Methods 0.000 description 1
- 239000007921 spray Substances 0.000 description 1
- 238000004544 sputter deposition Methods 0.000 description 1
- 239000010409 thin film Substances 0.000 description 1
- BZHGXQBPJUHVFW-UHFFFAOYSA-N toluene;tritert-butylphosphane Chemical compound CC1=CC=CC=C1.CC(C)(C)P(C(C)(C)C)C(C)(C)C BZHGXQBPJUHVFW-UHFFFAOYSA-N 0.000 description 1
- XZZNDPSIHUTMOC-UHFFFAOYSA-N triphenyl phosphate Chemical compound C=1C=CC=CC=1OP(OC=1C=CC=CC=1)(=O)OC1=CC=CC=C1 XZZNDPSIHUTMOC-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/56—Ring systems containing three or more rings
- C07D209/80—[b, c]- or [b, d]-condensed
- C07D209/82—Carbazoles; Hydrogenated carbazoles
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings
- C07D409/10—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/06—Luminescent, e.g. electroluminescent, chemiluminescent materials containing organic luminescent materials
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/631—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine
- H10K85/636—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine comprising heteroaromatic hydrocarbons as substituents on the nitrogen atom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6572—Polycyclic condensed heteroaromatic hydrocarbons comprising only nitrogen in the heteroaromatic polycondensed ring system, e.g. phenanthroline or carbazole
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1007—Non-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1011—Condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1014—Carbocyclic compounds bridged by heteroatoms, e.g. N, P, Si or B
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1029—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1092—Heterocyclic compounds characterised by ligands containing sulfur as the only heteroatom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/14—Carrier transporting layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/17—Carrier injection layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/17—Carrier injection layers
- H10K50/171—Electron injection layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/655—Aromatic compounds comprising a hetero atom comprising only sulfur as heteroatom
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Electroluminescent Light Sources (AREA)
- Plural Heterocyclic Compounds (AREA)
- Indole Compounds (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
본 발명은 유기 발광 소자의 수명, 효율, 전기 화학적 안정성 및 열적 안정성을 크게 향상시킬 수 있는 신규 화합물, 및 상기 화합물이 유기화합물 층에 함유되어 있는 유기 발광 소자를 제공한다.
유기 발광 소자, 유기물층, 정공주입물질, 정공수송물질, 발광물질, 카바졸 화합물, 아릴아민 화합물
Description
본 발명은 유기 발광 소자의 수명, 효율, 전기 화학적 안정성 및 열적 안정성을 크게 향상시킬 수 있는 신규 화합물이 유기화합물 층에 함유되어 있는 유기 발광 소자에 관한 것이다. 본 출원은 2007년 11월 18일에 한국 특허청에 제출된 한국특허출원 제10-2007-0113852호의 출원일의 이익을 주장하며, 그 내용 전부는 본 명세서에 포함된다.
유기 발광 현상은 특정 유기 분자의 내부 프로세스에 의하여 전류가 가시광으로 전환되는 예의 하나이다. 유기 발광 현상의 원리는 다음과 같다. 양극과 음극 사이에 유기물 층을 위치시켰을 때 두 전극 사이에 전압을 걸어주게 되면 음극과 양극으로부터 각각 전자와 정공이 유기물 층으로 주입된다. 유기물 층으로 주입된 전자와 정공은 재결합하여 엑시톤(exciton)을 형성하고, 이 엑시톤이 다시 바닥 상태로 떨어지면서 빛이 나게 된다. 이러한 원리를 이용하는 유기 발광소자는 일반적으로 음극과 양극 및 그 사이에 위치한 유기물층, 예컨대 정공주입층, 정공수송층, 발광층, 전자수송층을 포함하는 유기물 층으로 구성될 수 있다.
유기 발광 소자에서 사용되는 물질로는 순수 유기 물질 또는 유기 물질과 금속이 착물을 이루는 착화합물이 대부분을 차지하고 있으며, 용도에 따라 정공주입 물질, 정공수송 물질, 발광 물질, 전자수송 물질, 전자주입 물질 등으로 구분될 수 있다. 여기서, 정공주입 물질이나 정공수송 물질로는 p-타입의 성질을 가지는 유기 물질, 즉 쉽게 산화가 되고 산화시에 전기화학적으로 안정한 상태를 가지는 유기물이 주로 사용되고 있다. 한편, 전자주입 물질이나 전자수송 물질로는 n-타입 성질을 가지는 유기 물질, 즉 쉽게 환원이 되고 환원시에 전기화학적으로 안정한 상태를 가지는 유기물이 주로 사용되고 있다. 발광층 물질로는 p-타입 성질과 n-타입 성질을 동시에 가진 물질, 즉 산화와 환원 상태에서 모두 안정한 형태를 갖는 물질이 바람직하며, 엑시톤이 형성되었을 때 이를 빛으로 전환하는 발광 효율이 높은 물질이 바람직하다.
위에서 언급한 외에, 유기 발광 소자에서 사용되는 물질은 다음과 같은 성질을 추가적으로 갖는 것이 바람직하다.
첫째로 유기 발광 소자에서 사용되는 물질은 열적 안정성이 우수한 것이 바람직하다. 유기 발광 소자 내에서는 전하들의 이동에 의한 줄열(joule heating)이 발생하기 때문이다. 현재 정공수송층 물질로 주로 사용되는 NPB는 유리 전이 온도가 100 ℃ 이하의 값을 가지므로, 높은 전류를 필요로 하는 유기 발광 소자에서는 사용하기 힘든 문제가 있다.
둘째로 저전압 구동 가능한 고효율의 유기 발광 소자를 얻기 위해서는 유기 발광 소자 내로 주입된 정공 또는 전자들이 원활하게 발광층으로 전달되는 동시에, 주입된 정공과 전자들이 발광층 밖으로 빠져나가지 않도록 하여야 한다. 이를 위해서 유기 발광 소자에 사용되는 물질은 적절한 밴드갭(band gap)과 HOMO 또는 LUMO 에너지 준위를 가져야 한다. 현재 용액 도포법에 의해 제조되는 유기 발광 소자에서 정공수송 물질로 사용되는 PEDOT:PSS의 경우, 발광층 물질로 사용되는 유기물의 LUMO 에너지 준위에 비하여 LUMO 에너지 준위가 낮기 때문에 고효율 장수명의 유기 발광 소자 제조에 어려움이 있다.
이외에도 유기 발광 소자에서 사용되는 물질은 화학적 안정성, 전하이동도, 전극이나 인접한 층과의 계면 특성 등이 우수하여야 한다. 즉, 유기 발광소자에서 사용되는 물질은 수분이나 산소에 의한 물질의 변형이 적어야 한다. 또한, 적절한 정공 또는 전자 이동도를 가짐으로써 유기 발광 소자의 발광층에서 정공과 전자의 밀도가 균형을 이루도록 하여 엑시톤 형성을 극대화할 수 있어야 한다. 그리고, 소자의 안정성을 위해 금속 또는 금속 산화물을 포함한 전극과의 계면을 좋게 할 수 있어야 한다.
따라서, 당 기술 분야에서는 상기와 같은 요건을 갖춘 유기물의 개발이 요구되고 있다.
이에 본 발명자들은 유기 발광 소자에서 사용 가능한 물질에 요구되는 조건, 예컨대 적절한 에너지 준위, 전기 화학적 안정성 및 열적 안정성 등을 만족시킬 수 있으며, 치환기에 따라 유기 발광 소자에서 요구되는 다양한 역할을 할 수 있는 화학 구조를 갖는 헤테로 화합물 유도체를 포함하는 유기 발광 소자를 제공하는 것을 목적으로 한다.
본 발명은 하기 화학식 1의 화합물을 제공한다.
또한, 본 발명은 제 1 전극, 발광층, 1층 이상의 유기물층 및 제 2 전극을 적층된 형태로 포함하는 유기 발광 소자에 있어서, 상기 유기물층 중 1층 이상이 하기 화학식 1의 화합물, 또는 이 화합물에 열 경화성 또는 광경화성 작용기가 도입된 화합물을 포함하는 것인 유기 발광 소자를 제공한다.
[화학식 1]
상기 화학식 1에 있어서,
X는 -(A)m-(B)n 이고,
Y는 -(B)p 이고,
Ar은 니트로, 니트릴, 할로겐, 알킬기, 알콕시기 및 아미노기로 이루어진 군으로부터 선택되는 1개 이상의 치환기로 치환 또는 비치환된 탄소수 6 내지 40의 아릴렌기; 또는 니트로, 니트릴, 할로겐, 알킬기, 알콕시기 및 아미노기로 이루어진 군으로부터 선택되는 1개 이상의 치환기로 치환 또는 비치환된 2가 헤테로고리기이며,
A는 할로겐기, 알킬기, 알케닐기 알콕시기, 치환 또는 비치환된 아릴아민기, 치환 또는 비치환된 아릴기, 치환 또는 비치환된 아릴알킬기, 치환 또는 비치환된 아릴알케닐기, 치환 또는 비치환된 헤테로 고리기, 니트릴기 및 아세틸렌기로 이루어진 군에서 선택된 1개 이상의 치환기로 치환 또는 비치환된 아릴기이고,
B는 할로겐기, 알킬기, 알케닐기 알콕시기, 치환 또는 비치환된 아릴아민기, 치환 또는 비치환된 아릴기, 치환 또는 비치환된 아릴알킬기, 치환 또는 비치환된 아릴알케닐기, 치환 또는 비치환된 헤테로 고리기, 니트릴기 및 아세틸렌기로 이루어진 군에서 선택된 1개 이상의 치환기로 치환 또는 비치환된 아릴아민기; 또는 할로겐기, 알킬기, 알케닐기 알콕시기, 치환 또는 비치환된 아릴아민기, 치환 또는 비치환된 아릴기, 치환 또는 비치환된 아릴알킬기, 치환 또는 비치환된 아릴알케닐기, 치환 또는 비치환된 헤테로 고리기, 니트릴기 및 아세틸렌기로 이루어진 군에서 선택된 1개 이상의 치환기로 치환 또는 비치환되고 이종원자로 O, N 또는 S를 포함하는 헤테로 고리기이고,
m 및 n은 각각 1 내지 10 및 0 내지 10인 정수이고, p는 1 내지 10의 정수이고,
R1 내지 R7은 각각 독립적으로 수소; 할로겐기, 알킬기, 알케닐기, 알콕시기, 치환 또는 비치환된 아릴기, 치환 또는 비치환된 아릴알킬기, 치환 또는 비치환된 아릴알케닐기, 치환 또는 비치환된 헤테로 고리기, 니트릴기 및 아세틸렌기로 이루어진 군에서 선택된 1개 이상의 치환기로 치환 또는 비치환된 알킬기; 할로겐기, 알킬기, 알케닐기, 알콕시기, 치환 또는 비치환된 아릴기, 치환 또는 비치환된 아릴알킬기, 치환 또는 비치환된 아릴알케닐기, 치환 또는 비치환된 헤테로 고리기, 니트릴기 및 아세틸렌기로 이루어진 군에서 선택된 1개 이상의 치환기로 치환 또는 비치환된 알콕시기; 할로겐기, 알킬기, 알케닐기 알콕시기, 치환 또는 비치환된 아릴기, 치환 또는 비치환된 아릴알킬기, 치환 또는 비치환된 아릴알케닐기, 치환 또는 비치환된 헤테로 고리기, 니트릴기 및 아세틸렌기로 이루어진 군에서 선택된 1개 이상의 치환기로 치환 또는 비치환된 아릴기; 알킬기, 알케닐기 치환 또는 비치환된 아릴기, 치환 또는 비치환된 아릴알킬기, 치환 또는 비치환된 아릴알케닐기로 이루어진 군에서 선택된 1개 이상의 치환기로 치환된 아미노기; 니트로기; 및 할로겐기로 이루어진 군에서 선택되며, 여기서 이들은 서로 인접하는 기와 지방족 또는 헤테로의 축합 고리를 형성할 수 있다.
본 발명의 화합물은 유기 발광 소자에서 유기물층 물질, 특히 정공주입 물질 및/또는 정공수송 물질로 사용될 수 있으며, 이 화합물을 유기 발광 소자에 사용하는 경우 소자의 구동전압을 낮추고, 광효율을 향상시키며, 화합물의 열적 안정성에 의하여 소자의 수명 특성을 향상시킬 수 있다.
상기 화학식 1의 치환기를 상세히 설명하면 다음과 같다.
상기 화학식 1의 R1 내지 R7 중 알킬기, 알콕시기, 알케닐기는 탄소수는 특별히 한정되지 않으나 1-20인 것이 바람직하다.
화합물 중에 포함되어 있는 알킬기의 길이는 화합물의 공액 길이에는 영향을 미치지 않고, 다만 부수적으로 화합물의 유기 발광 소자에의 적용 방법, 예컨대 진공증착법 또는 용액도포법의 적용에 영향을 미칠 수 있다.
상기 화학식 1의 R1 내지 R7 중 아릴기의 예로는 페닐기, 비페닐기, 터페닐기, 스틸벤 등의 단환식 방향족 및 나프틸기, 안트라세닐기, 페나트렌기, 파이레닐기, 페릴레닐기등의 다환식 방향족환등이 있으나, 이들에만 한정되는 것은 아니다.
상기 화학식 1의 R1 내지 R7 중 헤테로 고리기의 예로는 티오펜기, 퓨란기, 피롤기, 이미다졸기, 티아졸기, 옥사졸기, 옥사디아졸기, 트리아졸기, 피리딜기, 피라다진기, 퀴놀리닐기, 이소퀴톨린기, 아크리딜기 등이 있으나, 이들에만 한정되는 것은 아니다.
화학식 1의 A는 아릴기로서 바람직하게는, 페닐기, 비페닐기, 터페닐기, 스틸벤 등의 단환식 방향족 및 나프틸기, 안트라세닐기, 페나트렌기, 파이레닐기, 페릴레닐기 등의 다환식 방향족환이 있으나, 이들에만 한정되는 것은 아니다.
화학식 1의 B가 헤테로고리인 경우 바람직하게는 티오펜기, 퓨란기, 피롤기, 이미다졸기, 티아졸기, 옥사졸기, 옥사디아졸기, 트리아졸기, 피리딜기, 피라다진기, 퀴놀리닐기, 이소퀴톨린기, 아크리딜기 등이 있으나, 이들에만 한정되는 것은 아니다.
상기 화학식 1로 표시되는 화합물은 바람직하게는 하기 화학식 2 내지 화학식 3 중 하나로 표시되는 화합물일 수 있다.
[화학식 2] [화학식 3]
상기 화학식에서 Ar'는 각각 독립적으로 페닐기, 비페닐기, 터페닐기, 스틸벤, 나프틸기, 안트라세닐기, 페나트렌기, 파이레닐기 및 페릴레닐기로 이루어진 군에서 선택되고, Ar, Y 및 R1 내지 R8은 각각 상기 화학식 1의 Ar, Y 및 R1 내지 R7에 대한 정의와 같다.
또한, 상기 화학식 1로 표시되는 화합물은 바람직하게는 하기 화학식 2-1 내지 화학식 3-1 중 하나로 표시되는 화합물일 수 있다.
[화학식 2-1] [화학식 3-1]
여기서 Ar, Y 및 R1 내지 R8은 각각 상기 화학식 1의 Ar, Y 및 R1 내지 R7에 대한 정의와 같다.
또한, 상기 화학식 1로 표시되는 화합물은 바람직하게는 하기 화학식 2-2 내지 화학식 3-3 중 하나로 표시되는 화합물일 수 있다.
[화학식 2-2] [화학식 3-2]
여기서 Ar, Y 및 R1 내지 R8은 각각 상기 화학식 1의 Ar, Y 및 R1 내지 R7에 대한 정의와 같다.
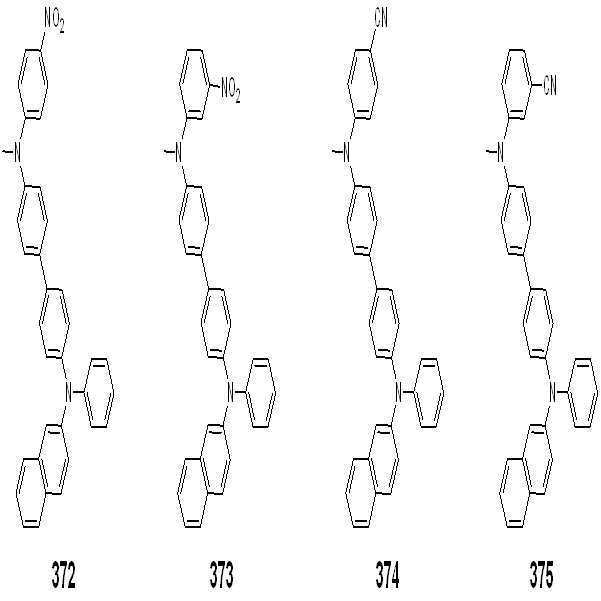
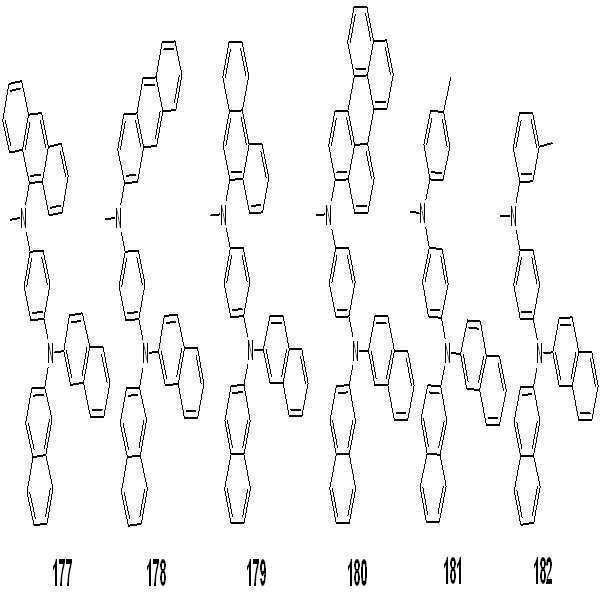
또한, 아릴아민인 경우, 바람직하게는 하기의 기가 있으나 이들에만 한정되는 것은 아니다.
상기 Ar은 바람직하게는 페닐렌일 수 있다.
화학식 1의 화합물은 바람직하게는 하기 화학식 4 내지 화학식 12로 표시되 는 화합물일 수 있다.
[화학식 4]
[화학식 5]
[화학식 6]
[화학식 7]
[화학식 8]
[화학식 9]
[화학식 10]
[화학식 11]
[화학식 12]
[화학식 13]
[화학식 14]
[화학식 15]
상기 화학식 1의 화합물은 상기 화학식 1에 표시된 코어 구조, 즉 카바졸의 R5 및 R6 사이의 탄소 위치에 아릴렌이 치환된 구조를 코어 구조로 하여 각각 독립적으로 각각, 수소, 중수소; 탄소수 1-20의 지방족 탄화수소; 방향족 탄화수소; 니트로, 니트릴, 할로겐, 알킬기, 알콕시기, 아미노기, 방향족 탄화수소 및 헤테로 고리기로 이루어진 군으로부터 선택되는 1개 이상의 치환기로 치환된 방항족 탄화수소; 방향족 탄화수소로 치환된 실리콘기; 헤테로고리기; 니트로, 니트릴, 할로겐, 알킬기, 알콕시기, 아미노기, 방향족 탄화수소 및 헤테로 고리기로 이루어진 군으로부터 선택되는 1개 이상의 치환기로 치환된 헤테로고리기; 탄소수 1-20의 탄화수소 또는 탄소수 6-20의 방향족 탄화수소로 치환된 티오펜기; 또는 방향족 탄화수소로 치환된 붕소기 구조가 융합된 코어 구조에 다양한 치환체를 도입함으로써 유기 발광 소자에서 사용되는 유기물층으로 사용되기에 적합한 특성을 가질 수 있다.
화합물의 컨쥬게이션 길이와 에너지 밴드갭은 밀접한 관계가 있다. 구체적으 로, 화합물의 컨쥬게이션 길이가 길수록 에너지 밴드갭이 작아진다. 전술한 바와 같이, 상기 화학식 1의 화합물의 코어는 제한된 컨쥬게이션을 포함하고 있으므로, 이는 에너지 밴드 갭이 큰 성질을 갖는다.
본 발명에서는 상기와 같이 에너지 밴드 갭이 큰 코어 구조의 R1 내지 R7, X 및 Y 위치에 다양한 치환기를 도입함으로써 다양한 에너지 밴드 갭을 갖는 화합물을 합성할 수 있다. 통상 에너지 밴드 갭이 큰 코어 구조에 치환기를 도입하여 에너지 밴드 갭을 조절하는 것은 용이하나, 코어 구조가 에너지 밴드 갭이 작은 경우에는 치환기를 도입하여 에너지 밴드 갭을 크게 조절하기 어렵다. 또한, 본 발명에서는 상기와 같은 구조의 코어 구조의 R1 내지 R7, X 및 Y 위치에 다양한 치환기를 도입함으로써 화합물의 HOMO 및 LUMO 에너지 준위도 조절할 수 있다.
또한, 상기와 같은 구조의 코어 구조에 다양한 치환기를 도입함으로써 도입된 치환기의 고유 특성을 갖는 화합물을 합성할 수 있다. 예컨대, 유기발광소자 제조시 사용되는 정공주입층 물질, 정공수송응 물질, 발광층 물질, 및 전자 수송층 물질에 줄 사용되는 치환기를 상기 코억어 구조에 도입함으로써 각 유기물층에서 요구하는 조건들을 충족시키는 물질을 합성할 수 있다.
상기 화학식 1의 화합물은 코어 구조에 아릴 아민 구조를 포함하고 있으므로, 유기 발광 소자에서 정공주입 및/또는 정공수송 물질로서의 적절한 에너지 준위를 가질 수 있다. 본 발명에서는 상기 화학식 1의 화합물 중 치환기에 따라 적절한 에너지 준위를 갖는 화합물을 선택하여 유기 발광 소자에 사용함으로써 구동 전압이 낮고 광효율이 높은 소자를 구현할 수 있다.
또한, 상기 코어구조에 다양한 치환기를 도입함으로써 에너지 밴드 갭을 미세하게 조절이 가능하게 하며, 한편으로 유기물사이에서의 계면에서의 특성을 향상되게 하며 물질의 용도를 다양하게 할 수 있다.
또한, 치환기 B에 포함된 아민 수를 조절 함으로써 HOMO, LUMO 에너지 준위 및 에너지 밴드 갭을 미세하게 조절 가능하며, 한편으로 유기물사이에서의 계면에서의 특성을 향상되게 하며 물질의 용도를 다양하게 할 수 있다.
한편, 상기 화학식 1의 화합물은 유리 전이 온도(Tg)가 높아 열적 안정성이 우수하다. 이러한 열적 안정성의 증가는 소자에 구동 안정성을 제공하는 중요한 요인이 된다.
또한, 상기 화학식 1의 화합물은 유기 발광 소자의 제조시 진공 증착법 뿐만 아니라 용액 도포법에 의하여 유기물층으로 형성될 수 있다. 여기서, 용액 도포법이라 함은 스핀코팅, 딥코팅, 잉크젯프린팅, 스크린 프린팅, 스프레이법, 롤 코팅 등을 의미하지만, 이들만으로 한정되는 것은 아니다.
본 발명의 유기 발광 소자는 유기물층 중 1층 이상이 본 발명의 화합물, 즉 상기 화학식 1의 화합물을 포함하는 것을 제외하고는 당 기술분야에 알려져 있는 재료와 방법으로 제조될 수 있다.
본 발명의 유기 발광 소자의 유기물층은 단층 구조로 이루어질 수도 있으나, 2층 이상의 유기물층이 적층된 다층 구조로 이루어질 수 있다. 예컨대, 본 발명의 유기 발광 소자는 유기물층으로서 정공주입층, 정공수송층, 발광층, 전자수송층, 전자주입층 등을 포함하는 구조를 가질 수 있다. 그러나, 유기 발광 소자의 구조는 이에 한정되지 않고 더 적은 수의 유기물층을 포함할 수 있다.
그리고, 본 발명의 유기 발광 소자는 예컨대 기판 상에 제1 전극, 유기물층 및 제2 전극을 순차적으로 적층시킴으로써 제조할 수 있다. 이 때 스퍼터링법(sputtering)이나 전자빔 증발법(e-beam evaporation)과 같은 PVD(Physical Vapor Deposition) 방법 등을 이용할 수 있으나, 이들 방법에만 한정되는 것은 아니다.
상기 화학식 1의 화합물의 제조 방법은 이하의 제조예에서 구체적으로 설명한다. 그러나, 하기 제조예 및 실험예는 본 발명을 예시하기 위한 것이며, 본 발명의 범위가 이들에 의하여 한정되는 것은 아니다.
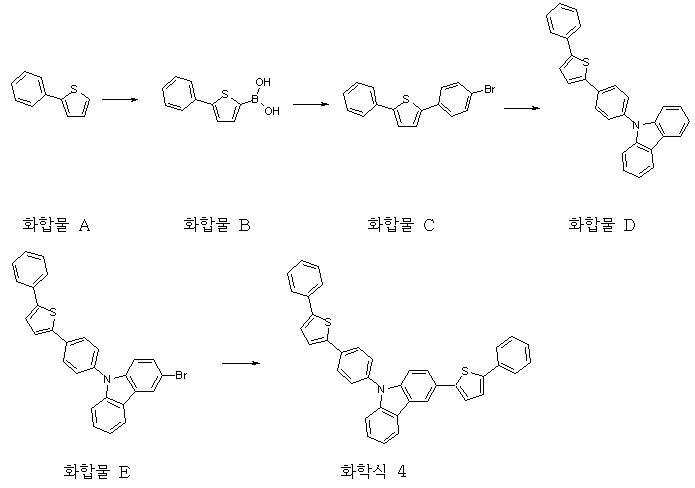
< 제조예 1> 화학식 4로 표시되는 화합물의 제조
<제조예 1-1> 화합물 A의 제조
2-브로모티오펜(20 g, 122.7 mmol)과 페닐보론산(18 g, 147.6 mmol)을 테트 라하이드로퓨란(300 mL)에 녹이고, 4N 탄산칼륨수용액(130 mL)과 테트라키스(트리페닐포스핀)팔라듐(0)(2.9 g, 2.5 mmol)을 넣고 교반하면서 가열하였다. 반응 종료 후 유기층을 분리하여 무수 황산마그네슘으로 건조하였다. 감압 증류 후 헥산으로 재결정하여 화합물 A(14.6 g, 수율 74 %; [M+H]+ = 161)를 얻었다.
<제조예 1-2> 화합물 B의 제조
상기 제조예 1-1에서 제조한 화합물 A(18 g, 112.3 mmol)를 무수 테트라하이드로퓨란에 녹이고, -78℃에서 n-부틸리튬 2.5M 헥산용액(49.4 mL, 123.5 mmol)을 넣고 1시간 동안 교반하였다. 트리메틸보레이트(15.1 g, 145.3 mmol)를 넣고 1시간 동안 교반한 후 2N 염산 수용액(80 mL)를 넣고 상온으로 승온시켰다. 유기층을 분리하여 무수 황산마그네슘으로 건조하였다. 감압 증류 후 헥산으로 재결정하여 화합물 B(15.2 g, 수율 66 %; [M+H]+ = 205)를 얻었다.
<제조예 1-3> 화합물 C의 제조
상기 제조예 1-2에서 제조한 화합물 B(15 g, 73.5 mmol)와 4-브로모-1-아이오도벤젠(20.8 g, 73.5 mmol)을 테트라하이드로퓨란(250 mL)에 녹이고, 4N 탄산칼륨수용액(75 mL)과 테트라키스(트리페닐포스핀)팔라듐(0)(1.7 g, 1.5 mmol)을 넣고 교반하면서 가열하였다. 반응 종료 후 유기층을 분리하여 무수 황산마그네슘으로 건조하였다. 감압 증류 후 에탄올로 재결정하여 화합물 C(14.8 g, 수율 64 %; [M+H]+ = 316)를 얻었다.
<제조예 1-4> 화합물 D의 제조
상기 제조예 1-3에서 제조한 화합물 C(14 g, 44.4 mmol)와 카바졸(7.5 g, 44.9 mmol), 나트륨 터셔리부톡사이드(5.5 g, 57.2 mmol), 비스(트리 터셔리부틸포스핀)팔라듐(0)(0.23 g, 0.45 mmol)을 자일렌(300 mL)에 현탁시킨 후 교반하면서 환류시켰다. 반응 종료 후 상온으로 온도를 낮춘 후 생성된 고체를 여과하였다. 물과 에탄올로 순차적으로 씻어 주어 화합물 D(14.7 g, 수율 82 %; [M+H]+ = 402)를 얻었다.
<제조예 1-5> 화합물 E의 제조
상기 제조예 1-4에서 제조한 화합물 D(14 g, 34.9 mmol)를 클로로포름(300 mL)에 녹이고, N-브로모숙신이미드(6.3 g, 35.4 mmol)를 넣고 상온에서 교반하였다. 반응 종료 후 물을 붓고 유기층을 분리하여 무수 황산마그네슘으로 건조하였다. 감압 증류 후 테트라하이드로퓨란과 에탄올로 재결정하여 화합물 E(14.3 g, 수율 85 %; [M+H]+ = 481)를 얻었다.
<제조예 1-6> 화학식 4의 제조
상기 제조예 1-5에서 제조한 화합물 E(13 g, 27 mmol)와 제조예 1-2에서 제조한 화합물 B(5.5 g, 27 mmol)를 테트라하이드로퓨란(200 mL)에 녹이고, 4N 탄산칼륨수용액(30 mL)과 테트라키스(트리페닐포스핀)팔라듐(0)(0.62 g, 0.54 mmol)을 넣고 교반하면서 가열하였다. 반응 종료 후 유기층을 분리하여 무수 황산마그네슘으로 건조하였다. 감압 증류 후 테트라하이드로퓨란과 에탄올로 재결정하여 화학식 4(10.7 g, 수율 71 %; [M+H]+ = 560)를 얻었다.
< 제조예 2> 화학식 5로 표시되는 화합물의 제조
<제조예 2-1> 화합물 A의 제조
상기 제조예 1-5의 화합물 E(10 g, 20.8 mmol)와 페닐보론산(2.7 g, 22.1 mmol)을 테트라하이드로퓨란(300 mL)에 녹이고, 4N 탄산칼륨수용액(25 mL)과 테트라키스(트리페닐포스핀)팔라듐(0)(0.49 g, 0.42 mmol)을 넣고 교반하면서 가열하였다. 반응 종료 후 유기층을 분리하여 무수 황산마그네슘으로 건조하였다. 감압 증류 후 테트라하이드로퓨란과 헥산으로 재결정하여 화합물 A(8.2 g, 수율 83 %; [M+H]+ = 478)를 얻었다.
<제조예 2-2> 화합물 B의 제조
상기 제조예 2-1에서 제조한 화합물 A(8 g, 16.7 mmol)를 클로로포름(200 mL)에 녹이고, N-브로모숙신이미드(3 g, 16.9 mmol)를 넣고 상온에서 교반하였다. 반응 종료 후 물을 붓고 생성된 고체를 여과하였다. 물과 에탄올로 순차적으로 씻어 주어 화합물 B(8.2 g, 수율 88 %; [M+H]+ = 557)를 얻었다.
<제조예 2-3> 화학식 5의 제조
상기 제조예 2-2에서 제조한 화합물 B(5 g, 9 mmol)와 제조예 1-2에서 제조한 화합물 B(1.9 g, 9.3 mmol)를 테트라하이드로퓨란(150 mL)에 녹이고, 4N 탄산칼륨수용액(12 mL)과 테트라키스(트리페닐포스핀)팔라듐(0)(0.2 g, 0.18 mmol)을 넣고 교반하면서 가열하였다. 반응 종료 후 유기층을 분리하여 무수 황산마그네슘으로 건조하였다. 감압 증류 후 테트라하이드로퓨란과 에탄올로 재결정하여 화학식 5(3.9 g, 수율 68 %; [M+H]+ = 636)를 얻었다.
< 제조예 3> 화학식 6으로 표시되는 화합물의 제조
<제조예 3-1> 화합물 A의 제조
상기 제조예 1-3에서 제조한 화합물 C(10 g, 31.7 mmol)를 무수 테트라하이드로퓨란에 녹이고, -78℃에서 n-부틸리튬 2.5M 헥산용액(13.8 mL, 34.5 mmol)을 넣고 1시간 동안 교반하였다. 트리메틸보레이트(4.3 g, 41.4 mmol)를 넣고 1시간 동안 교반한 후 2N 염산 수용액(20 mL)을 넣고 상온으로 승온시켰다. 유기층을 분리하여 무수 황산마그네슘으로 건조하였다. 감압 증류 후 헥산으로 재결정하여 화합물 A(5.4 g, 수율 61 %; [M+H]+ = 281)를 얻었다.
<제조예 3-2> 화학식 6의 제조
상기 제조예 3-1에서 제조한 화합물 A(5 g, 17.8 mmol)와 제조예 1-5에서 제조한 화합물 E(8.5 g, 17.7 mmol)를 테트라하이드로퓨란(150 mL)에 녹이고, 4N 탄산칼륨수용액(20 mL)과 테트라키스(트리페닐포스핀)팔라듐(0)(0.42 g, 0.36 mmol)을 넣고 교반하면서 가열하였다. 반응 종료 후 유기층을 분리하여 무수 황산마그네슘으로 건조하였다. 감압 증류 후 테트라하이드로퓨란과 에탄올로 재결정하여 화학식 6(8.2 g, 수율 73 %; [M+H]+ = 636)을 얻었다.
< 제조예 4> 화학식 7로 표시되는 화합물의 제조
<제조예 4-1> 화합물 A의 제조
상기 제조예 1-2에서 제조한 화합물 B(15 g, 73.5 mmol)와 3-브로모-1-아이오도벤젠(20.8 g, 73.5 mmol)을 테트라하이드로퓨란(180 mL)에 녹이고, 4N 탄산칼륨수용액(75 mL)과 테트라키스(트리페닐포스핀)팔라듐(0)(1.7 g, 1.5 mmol)을 넣고 교반하면서 가열하였다. 반응 종료 후 유기층을 분리하여 무수 황산마그네슘으로 건조하였다. 감압 증류 후 테트라하이드로퓨란/헥산 = 1/10의 용매로 컬럼 정제하 여 화합물 A(14.4 g, 수율 62 %; [M+H]+ = 316)를 얻었다.
<제조예 4-2> 화합물 B의 제조
상기 제조예 4-1에서 제조한 화합물 A(14 g, 44.4 mmol)와 카바졸(7.5 g, 44.9 mmol), 나트륨 터셔리부톡사이드(5.5 g, 57.2 mmol), 비스(트리 터셔리부틸포스핀)팔라듐(0)(0.23 g, 0.45 mmol)을 자일렌(300 mL)에 현탁시킨 후 교반하면서 환류시켰다. 반응 종료 후 상온으로 온도를 낮춘 후 생성된 고체를 여과하였다. 물과 에탄올로 순차적으로 씻어 주어 화합물 B(15.1 g, 수율 85 %; [M+H]+ = 402)를 얻었다.
<제조예 4-3> 화합물 C의 제조
상기 제조예 4-2에서 제조한 화합물 B(15 g, 37.4 mmol)를 클로로포름(300 mL)에 녹이고, N-브로모숙신이미드(6.7 g, 37.6 mmol)를 넣고 상온에서 교반하였다. 반응 종료 후 물을 붓고 유기층을 분리하여 무수 황산마그네슘으로 건조하였다. 감압 증류 후 테트라하이드로퓨란과 에탄올로 재결정하여 화합물 C(14.2 g, 수율 79 %; [M+H]+ = 481)를 얻었다.
<제조예 4-4> 화합물 D의 제조
상기 제조예 4-3에서 제조한 화합물 C(13 g, 27 mmol)와 4-클로로페닐보론산(4.3 g, 27.5 mmol)을 테트라하이드로퓨란(300 mL)에 녹이고, 4N 탄산칼륨수용액(33 mL)과 테트라키스(트리페닐포스핀)팔라듐(0)(0.62 g, 0.54 mmol)을 넣고 교반하면서 가열하였다. 반응 종료 후 유기층을 분리하여 무수 황산마그네슘으로 건 조하였다. 감압 증류 후 테트라하이드로퓨란과 에탄올로 재결정하여 화합물 D(9.5g, 수율 69 %; [M+H]+ = 512)를 얻었다.
<제조예 4-5> 화학식 7의 제조
상기 제조예 4-4에서 제조한 화합물 D(8 g, 15.6 mmol)와 N-페닐-1-나프틸아민(3.8 g, 17.3 mmol), 나트륨 터셔리부톡사이드(2 g, 20.8 mmol), 비스(트리 터셔리부틸포스핀)팔라듐(0)(0.08 g, 0.16 mmol)을 자일렌(300 mL)에 현탁시킨 후 교반하면서 환류시켰다. 반응 종료 후 상온으로 온도를 낮춘 후 산성백토를 넣고 교반하였다. 여과 후 감압 증류하고, 테트라하이드로퓨란/헥산 = 1/7의 용매로 컬럼 정제하여 화학식 7(6.4 g, 수율 59 %; [M+H]+ = 695)을 얻었다.
< 제조예 5> 화학식 8로 표시되는 화합물의 제조
<제조예 5-1> 화학식 8의 제조
상기 제조예 4-4에서 제조한 화합물 D(8 g, 15.6 mmol)와 비스(4-비페닐일)아민(5.5 g, 17.1 mmol), 나트륨 터셔리부톡사이드(2 g, 20.8 mmol), 비스(트리 터셔리부틸포스핀)팔라듐(0)(0.08 g, 0.16 mmol)을 자일렌(250 mL)에 현탁시킨 후 교반하면서 환류시켰다. 반응 종료 후 상온으로 온도를 낮춘 후 산성백토를 넣고 교 반하였다. 여과 후 감압 증류하고, 테트라하이드로퓨란과 에탄올로 재결정하여 화학식 8(7.8 g, 수율 63 %; [M+H]+ = 797)을 얻었다.
< 제조예 6> 화학식 9로 표시되는 화합물의 제조
<제조예 6-1> 화합물 A의 제조
상기 제조예 1-5에서 제조한 화합물 E(10 g, 20.8 mmol)와 4-클로로페닐보론산(3.6 g, 23 mmol)을 테트라하이드로퓨란(250 mL)에 녹이고, 4N 탄산칼륨수용액(22 mL)과 테트라키스(트리페닐포스핀)팔라듐(0)(0.49 g, 0.42 mmol)을 넣고 교반하면서 가열하였다. 반응 종료 후 유기층을 분리하여 무수 황산마그네슘으로 건조하였다. 감압 증류 후 테트라하이드로퓨란과 에탄올로 재결정하여 화합물 A(7 g, 수율 66 %; [M+H]+ = 512)를 얻었다.
<제조예 6-2> 화학식 9의 제조
상기 제조예 6-1에서 제조한 화합물 A(5 g, 9.7 mmol)와 비스(4-비페닐일)아민(3.4 g, 10.6 mmol), 나트륨 터셔리부톡사이드(1.2 g, 12.6 mmol), 비스(트리 터셔리부틸포스핀)팔라듐(0)(0.05 g, 0.1 mmol)을 자일렌(150 mL)에 현탁시킨 후 교 반하면서 환류시켰다. 반응 종료 후 상온으로 온도를 낮춘 후 생성된 고체를 여과하였다. 여과된 고체를 클로로포름에 녹인 후 산성백토를 넣고 교반하였다. 여과 후 감압 증류하고, 테트라하이드로퓨란과 에탄올로 재결정하여 화학식 9(5.2 g, 수율 67 %; [M+H]+ = 797)를 얻었다.
< 제조예 7> 화학식 10으로 표시되는 화합물의 제조
<제조예 7-1> 화합물 A의 제조
상기 제조예 4-4에서 제조한 화합물 D(10 g, 19.5 mmol)를 클로로포름(300 mL)에 녹이고, N-브로모숙신이미드(3.7 g, 20.8 mmol)를 넣고 상온에서 교반하였다. 반응 종료 후 물을 붓고 유기층을 분리하여 무수 황산마그네슘으로 건조하였다. 감압 증류 후 테트라하이드로퓨란과 에탄올로 재결정하여 화합물 A(8.9 g, 수율 77 %; [M+H]+ = 591)를 얻었다.
<제조예 7-2> 화합물 B의 제조
상기 제조예 7-1에서 제조한 화합물 A(8 g, 13.5 mmol)와 4-클로로페닐보론산(2.3 g, 14.7 mmol)을 테트라하이드로퓨란(200 mL)에 녹이고, 4N 탄산칼륨수용 액(15 mL)과 테트라키스(트리페닐포스핀)팔라듐(0)(0.31 g, 0.27 mmol)을 넣고 교반하면서 가열하였다. 반응 종료 후 생성된 고체를 여과하였다. 여과된 고체를 테트라하이드로퓨란과 에탄올로 재결정하여 화합물 B(5.2 g, 수율 65 %; [M+H]+ = 588)를 얻었다.
<제조예 7-3> 화학식 10의 제조
상기 제조예 7-2에서 제조한 화합물 B(5 g, 8.5 mmol)와 비스(4-비페닐일)아민(3 g, 9.3 mmol), 나트륨 터셔리부톡사이드(1.1 g, 11.4 mmol), 비스(트리 터셔리부틸포스핀)팔라듐(0)(0.05 g, 0.1 mmol)을 자일렌(150 mL)에 현탁시킨 후 교반하면서 환류시켰다. 반응 종료 후 상온으로 온도를 낮춘 후 산성백토를 넣고 교반하였다. 여과 후 감압 증류하고, 테트라하이드로퓨란과 에탄올로 재결정하여 화학식 10(4.5 g, 수율 61 %; [M+H]+ = 873)을 얻었다.
< 제조예 8> 화학식 11로 표시되는 화합물의 제조
<제조예 8-1> 화합물 A의 제조
상기 제조예 6-1에서 제조한 화합물 A(10 g, 19.5 mmol)를 클로로포름(300 mL)에 녹이고, N-브로모숙신이미드(3.7 g, 20.8 mmol)를 넣고 상온에서 교반하였다. 반응 종료 후 물을 붓고 유기층을 분리하여 무수 황산마그네슘으로 건조하였다. 감압 증류 후 테트라하이드로퓨란과 에탄올로 재결정하여 화합물 A(9.4 g, 수율 82 %; [M+H]+ = 591)를 얻었다.
<제조예 8-2> 화합물 B의 제조
상기 제조예 8-1에서 제조한 화합물 A(8 g, 13.5 mmol)와 제조예 1-2에서 제조한 화합물 B(3 g, 14.7 mmol)를 테트라하이드로퓨란(150 mL)에 녹이고, 4N 탄산칼륨수용액(15 mL)과 테트라키스(트리페닐포스핀)팔라듐(0)(0.31 g, 0.27 mmol)을 넣고 교반하면서 가열하였다. 반응 종료 후 생성된 고체를 여과하였다. 여과된 고체를 테트라하이드로퓨란과 에탄올로 재결정하여 화합물 B(6.2 g, 수율 69 %; [M+H]+ = 670)를 얻었다.
<제조예 8-3> 화학식 11의 제조
상기 제조예 8-2에서 제조한 화합물 B(6 g, 9 mmol)와 N-페닐-1-나프틸아민(2.1 g, 9.6 mmol), 나트륨 터셔리부톡사이드(1.1 g, 11.7 mmol), 비스(트리 터셔리부틸포스핀)팔라듐(0)(0.05 g, 0.1 mmol)을 자일렌(100 mL)에 현탁시킨 후 교반하면서 환류시켰다. 반응 종료 후 상온으로 온도를 낮춘 후 산성백토를 넣고 교반하였다. 여과 후 감압 증류하고, 테트라하이드로퓨란/헥산 = 1/6의 용매로 컬럼 정제하여 화학식 11(3.8 g, 수율 49 %; [M+H]+ = 853)을 얻었다.
< 제조예 9> 화학식 12로 표시되는 화합물의 제조
<제조예 9-1> 화합물 A의 제조
상기 제조예 4-4에서 제조한 화합물 D(10 g, 19.5 mmol)를 클로로포름(300 mL)에 녹이고, N-브로모숙신이미드(3.7 g, 20.8 mmol)를 넣고 상온에서 교반하였다. 반응 종료 후 물을 붓고 유기층을 분리하여 무수 황산마그네슘으로 건조하였다. 감압 증류 후 테트라하이드로퓨란과 에탄올로 재결정하여 화합물 A(9.1 g, 수율 79 %; [M+H]+ = 591)를 얻었다.
<제조예 9-2> 화합물 B의 제조
상기 제조예 9-1에서 제조한 화합물 A(9 g, 15.2 mmol)와 제조예 1-2에서 제조한 화합물 B(3.4 g, 16.7 mmol)를 테트라하이드로퓨란(150 mL)에 녹이고, 4N 탄산칼륨수용액(18 mL)과 테트라키스(트리페닐포스핀)팔라듐(0)(0.35 g, 0.3 mmol)을 넣고 교반하면서 가열하였다. 반응 종료 후 생성된 고체를 여과하였다. 여과된 고체를 테트라하이드로퓨란과 에탄올로 재결정하여 화합물 B(7.3 g, 수율 72 %; [M+H]+ = 670)를 얻었다.
<제조예 9-3> 화학식 12의 제조
상기 제조예 9-2에서 제조한 화합물 B(6 g, 9 mmol)와 비스(4-비페닐일)아민(3 g, 9.3 mmol), 나트륨 터셔리부톡사이드(1.1 g, 11.4 mmol), 비스(트리 터셔리부틸포스핀)팔라듐(0)(0.05 g, 0.1 mmol)을 자일렌(150 mL)에 현탁시킨 후 교반하면서 환류시켰다. 반응 종료 후 상온으로 온도를 낮춘 후 생성된 고체를 여과하였다. 여과된 고체를 클로로포름에 녹이고 산성백토를 넣고 교반한 후 여과하였다. 감압 증류 후 테트라하이드로퓨란과 에탄올로 재결정하여 화학식 12(5.6 g, 수율 65 %; [M+H]+ = 955)를 얻었다.
< 제조예 10> 화학식 13의 제조
상기 제조예 6의 화합물 A(4 g, 7.8 mmol) 및 아민 화합물(3.17 g, 8.2 mmol)을 자일렌 150 ml에 용해시키고, 나트륨-터셔리-부톡사이드(1.9 g, 19.5 mmol), Pd[P(t-Bu)3]2 20 mg(0.06 mmol)을 첨가한 후, 5 시간 동안 질소 기류 하에서 환류하였다.
반응 용액에 증류수를 넣고 반응을 종료시키고 유기층을 추출하였다. 노르말 -헥산/테트라하이드로퓨란 = 10/1 용매로 컬럼 분리한 후, 석유에테르에 교반한 뒤 진공 건조하여 화학식 13(3.4 g, 수율 50%)을 얻었다. MS: [M+H]+ = 861
< 제조예 11> 화학식 14의 제조
(1) 화학식 A의 제조
카바졸(17.5 g, 104.8 mmol)을 다이메틸아세트아마이드(100mL)에 녹이고, 4-클로로아이오도벤젠(25 g, 104.8mmol), Cu(13.3 g, 209.6mmol), K2CO3(43.5 g, 314.4 mmol)을 넣고 12시간 동안 환류시켰다.
반응 용액을 여과한 후 농축시키고 EtOH로 재결정하여 화학식 A(24.8g, 수율 85 %)를 얻었다. MS: [M+H]+ = 278
(2) 화학식 B 의 제조
상기 (1) 단계에서 제조한 화학식 A(24.8 g, 89.3 mmol)를 클로로포름(200mL)에 녹이고, N-브로모 숙신이미드(15.9 g, 89.3 mmol)를 첨가한 후, 5시간 상온에서 교반하였다.
반응 용액에 증류수를 넣고 종료시키고 유기층을 추출하였다. 반응액을 농축 시킨 후 정제과정 없이 다음 반응을 진행하였다. MS: [M+H]+ = 357
(3) 화학식 C 의 제조
상기 (2) 단계에서 제조한 화학식 B(31.7 g, 89 mmol)와 4-클로로벤젠 보론산(15.3 g, 97.9 mmol)을 THF(150 mL)에 녹인 후, Pd(PPh3)4(2.1 g, 1.78 mmol)과 K2CO3 /H20수용액(6 g/100mL, 356 mmol)을 넣고, 24시간 동안 환류시켰다.
반응 용액에 증류수를 넣고 종료시키고 유기층을 추출하였다. 반응액을 농축시키고, 노르말-헥산/테트라하이드로퓨란 = 10/1 용매로 컬럼 분리한 후, EtOH에 교반한 뒤 여과한 후 진공 건조하여 화학식 C(8.9 g, 수율 26 %)를 얻었다. MS: [M+H]+ = 388
(4) 화학식 14의 제조
상기 (3) 단계에서 제조한 화학식 C(4.9 g, 12.6 mmol), N-페닐-1-나프틸아민(6.9 g, 31.5 mmol)을 자일렌 150 ml에 용해시키고, 나트륨-터셔리-부톡사이드(3 g , 31.5 mmol), 비스디벤질리덴아세톤팔라듐(0)(0.28 g, 0.5 mmol), 50wt% 트리-터셔리-부틸포스핀 톨루엔 용액(0.24ml, 0.5 mmol)을 첨가한 후, 5 시간 동안 질소 기류 하에서 환류하였다.
반응 용액에 증류수를 넣고 반응을 종료시키고 유기 층을 추출하였다. 노르말-헥산/테트라하이드로퓨란 = 10/1 용매로 컬럼 분리한 후, EtOH에 교반한 뒤 여과한 후 진공 건조하여 화학식 14(1.8 g, 수율 19 %)를 얻었다. MS: [M+H]+ = 754
< 제조예 12> 화학식 15의 제조
상기 제조예 11의 (3) 단계에서 제조한 화학식 C(4 g, 10.3 mmol) 및 비스디페닐아민(8.28 g, 25.8 mmol)을 자일렌 150 ml에 용해시키고, 나트륨-터셔리-부톡사이드(2.47 g, 25.8 mmol), Pd[P(t-Bu)3]2(0.2 g, 0.4 mmol)을 첨가한 후, 5 시간 동안 질소 기류 하에서 환류하였다.
반응 용액에 증류수를 넣고 반응을 종료시키고 유기 층을 추출하였다. 노르말-헥산/테트라하이드로퓨란 = 10/1 용매로 컬럼 분리한 후, 석유에테르에 교반한 뒤 진공 건조하여 화학식 15(6.9 g, 수율 70 %)를 얻었다. MS: [M+H]+ = 958
<
실험예
1>
ITO(indium tin oxide)가 1500 Å의 두께로 박막 코팅된 유리 기판을 세제를 녹인 증류수에 넣고 초음파로 세척하였다. 이때, 세제로는 피셔사(Fischer Co.) 제품을 사용하였으며, 증류수로는 밀리포어사(Millipore Co.) 제품의 필터(Filter)로 2 차로 걸러진 증류수를 사용하였다. ITO를 30 분간 세척한 후 증류수로 2 회 반복하여 초음파 세척을 10 분간 진행하였다. 증류수 세척이 끝난 후, 이소프로필알콜, 아세톤, 메탄올의 용제로 초음파 세척을 하고 건조시킨 후 플라즈마 세정기로 수송시켰다. 또한, 산소 플라즈마를 이용하여 상기 기판을 5 분간 세정한 후 진공 증착기로 기판을 수송시켰다.
이렇게 준비된 ITO 투명 전극 위에 하기 화학식의 헥사니트릴 헥사아자트리페닐렌(hexanitrile hexaazatriphenylene; HAT)를 500 Å의 두께로 열 진공 증착하여 정공주입층을 형성하였다.
[HAT]
상기 정공주입층 위에 제조예 1에서 제조된 화학식 4의 화합물을 400 Å의 두께로 열 진공 증착하여 정공수송층을 형성하였다.
이어서, 상기 정공수송층 위에 막 두께 300 Å으로 아래와 같은 GH와 GD를 20:1의 막 두께비로 진공증착하여 발광층을 형성하였다.
[GH] [GD]
상기 발광층 위에 아래와 같은 전자 수송 물질을 200 Å의 두께로 진공 증착하여 전자주입 및 수송층을 형성하였다.
[전자 수송 물질]
상기 전자주입 및 수송층 위에 순차적으로 12 Å 두께로 리튬 플루라이드(LiF)와 2000 Å 두께로 알루미늄을 증착하여 음극을 형성하였다.
상기의 과정에서 유기물의 증착속도는 0.4~0.7 Å/sec를 유지하였고, 음극의 리튬플루오라이드는 0.3 Å/sec, 알루미늄은 2 Å/sec의 증착 속도를 유지하였으며, 증착시 진공도는 2 × 10-7 ~ 5 × 10-8 torr를 유지하였다.
상기에서 제조된 유기발광소자에 4.8 V의 순방향 전계를 가한 결과, 50 mA/㎠의 전류밀도에서 색좌표가 (0.32, 0.66)인 녹색 빛이 26 cd/A로 관찰되었고, 90% 휘도까지의 수명은 180시간이었다.
<
실험예
2>
실험예 1에서 화학식 4의 화합물 대신 화학식 5의 화합물을 사용한 것 이외에는 똑같이 하고 유기 EL 소자를 제작했다.
상기에서 제조된 유기발광소자에 4.7 V의 순방향 전계를 가한 결과, 50 mA/ ㎠의 전류밀도에서 색좌표가 (0.33, 0.64)인 녹색 빛이 27 cd/A로 관찰되었고, 90% 휘도까지의 수명은 200시간이었다.
<
실험예
3>
실험예 1에서 화학식 4의 화합물 대신 화학식 6의 화합물을 사용한 것 이외에는 똑같이 하고 유기 EL 소자를 제작했다.
상기에서 제조된 유기발광소자에 4.8 V의 순방향 전계를 가한 결과, 50 mA/㎠의 전류밀도에서 색좌표가 (0.33, 0.65)인 녹색 빛이 29 cd/A로 관찰되었고, 90% 휘도까지의 수명은 210시간이었다.
<
실험예
4>
실험예 1에서 화학식 4의 화합물 대신 화학식 7의 화합물을 사용한 것 이외에는 똑같이 하고 유기 EL 소자를 제작했다.
상기에서 제조된 유기발광소자에 4.6 V의 순방향 전계를 가한 결과, 50 mA/㎠의 전류밀도에서 색좌표가 (0.32, 0.65)인 녹색 빛이 28 cd/A로 관찰되었고, 90% 휘도까지의 수명은 190시간이었다.
<
실험예
5>
실험예 1에서 화학식 4의 화합물 대신 화학식 8의 화합물을 사용한 것 이외에는 똑같이 하고 유기 EL 소자를 제작했다.
상기에서 제조된 유기발광소자에 4.7 V의 순방향 전계를 가한 결과, 50 mA/㎠의 전류밀도에서 색좌표가 (0.32, 0.64)인 녹색 빛이 30 cd/A로 관찰되었고, 90% 휘도까지의 수명은 250시간이었다.
<
실험예
6>
실험예 1에서 화학식 4의 화합물 대신 화학식 9의 화합물을 사용한 것 이외에는 똑같이 하고 유기 EL 소자를 제작했다.
상기에서 제조된 유기발광소자에 4.6 V의 순방향 전계를 가한 결과, 50 mA/㎠의 전류밀도에서 색좌표가 (0.31, 0.65)인 녹색 빛이 29 cd/A로 관찰되었고, 90% 휘도까지의 수명은 240시간이었다.
<
실험예
7>
실험예 1에서 화학식 4의 화합물 대신 화학식 10의 화합물을 사용한 것 이외에는 똑같이 하고 유기 EL 소자를 제작했다.
상기에서 제조된 유기발광소자에 4.5 V의 순방향 전계를 가한 결과, 50 mA/㎠의 전류밀도에서 색좌표가 (0.32, 0.65)인 녹색 빛이 31 cd/A로 관찰되었고, 90% 휘도까지의 수명은 270시간이었다.
<
실험예
8>
실험예 1에서 화학식 4의 화합물 대신 화학식 11의 화합물을 사용한 것 이외에는 똑같이 하고 유기 EL 소자를 제작했다.
상기에서 제조된 유기발광소자에 4.4 V의 순방향 전계를 가한 결과, 50 mA/㎠의 전류밀도에서 색좌표가 (0.32, 0.66)인 녹색 빛이 31 cd/A로 관찰되었고, 90% 휘도까지의 수명은 270시간이었다.
<
실험예
9>
실험예 1에서 화학식 4의 화합물 대신 화학식 12의 화합물을 사용한 것 이외 에는 똑같이 하고 유기 EL 소자를 제작했다.
상기에서 제조된 유기발광소자에 4.4 V의 순방향 전계를 가한 결과, 50 mA/㎠의 전류밀도에서 색좌표가 (0.33, 0.65)인 녹색 빛이 32 cd/A로 관찰되었고, 90% 휘도까지의 수명은 280시간이었다.
<
비교예
1>
실험예 1에서 화학식 4의 화합물 대신 하기 화학식의 4,4'-비스[N-(1-나프틸)-N-페닐아미노]비페닐(NPB)을 사용한 것 이외에는 똑같이 하고 유기 EL 소자를 제작했다.
[NPB]
상기에서 제조된 유기발광소자에 4.6 V의 순방향 전계를 가한 결과, 50 mA/㎠의 전류밀도에서 색좌표가 (0.32, 0.64)인 녹색 빛이 26 cd/A로 관찰되었고, 90% 휘도까지의 수명은 140시간이었다.
도 1은 기판 (1), 양극 (2), 발광층 (3), 음극 (4)으로 이루어진 유기 발광 소자의 예를 도시한 것이다.
도 2는 기판(1), 양극 (2), 정공주입층 (5), 정공수송층 (6), 발광층 (7), 전자수송층 (8) 및 음극 (4)으로 이루어진 유기 발광 소자의 예를 도시한 것이다.
Claims (15)
- 하기 화학식 1의 화합물.[화학식 1]상기 화학식 1에 있어서,X는 -(A)m-(B)n 이고Y는 -(B)p 이고Ar은 니트로, 니트릴, 할로겐, 알킬기, 알콕시기 및 아미노기로 이루어진 군으로부터 선택되는 1개 이상의 치환기로 치환 또는 비치환된 탄소수 6 내지 40의 아릴렌기; 또는 니트로, 니트릴, 할로겐, 알킬기, 알콕시기 및 아미노기로 이루어진 군으로부터 선택되는 1개 이상의 치환기로 치환 또는 비치환된 2가 헤테로고리기이며,A는 할로겐기, 알킬기, 알케닐기 알콕시기, 치환 또는 비치환된 아릴아민기, 치환 또는 비치환된 아릴기, 치환 또는 비치환된 아릴알킬기, 치환 또는 비치환된 아릴알케닐기, 치환 또는 비치환된 헤테로 고리기, 니트릴기 및 아세틸렌기로 이루 어진 군에서 선택된 1개 이상의 치환기로 치환 또는 비치환된 아릴기이고,B는 할로겐기, 알킬기, 알케닐기 알콕시기, 치환 또는 비치환된 아릴아민기, 치환 또는 비치환된 아릴기, 치환 또는 비치환된 아릴알킬기, 치환 또는 비치환된 아릴알케닐기, 치환 또는 비치환된 헤테로 고리기, 니트릴기 및 아세틸렌기로 이루어진 군에서 선택된 1개 이상의 치환기로 치환 또는 비치환된 아릴아민기; 또는 할로겐기, 알킬기, 알케닐기 알콕시기, 치환 또는 비치환된 아릴아민기, 치환 또는 비치환된 아릴기, 치환 또는 비치환된 아릴알킬기, 치환 또는 비치환된 아릴알케닐기, 치환 또는 비치환된 헤테로 고리기, 니트릴기 및 아세틸렌기로 이루어진 군에서 선택된 1개 이상의 치환기로 치환 또는 비치환되고 이종원자로 O, N 또는 S를 포함하는 헤테로 고리기이고,m 및 n은 각각 1 내지 10 및 0 내지 10인 정수이고, p는 1 내지 10의 정수이고,R1 내지 R7은 각각 독립적으로 수소; 할로겐기, 알킬기, 알케닐기, 알콕시기, 치환 또는 비치환된 아릴기, 치환 또는 비치환된 아릴알킬기, 치환 또는 비치환된 아릴알케닐기, 치환 또는 비치환된 헤테로 고리기, 니트릴기 및 아세틸렌기로 이루어진 군에서 선택된 1개 이상의 치환기로 치환 또는 비치환된 알킬기; 할로겐기, 알킬기, 알케닐기, 알콕시기, 치환 또는 비치환된 아릴기, 치환 또는 비치환된 아릴알킬기, 치환 또는 비치환된 아릴알케닐기, 치환 또는 비치환된 헤테로 고리기, 니트릴기 및 아세틸렌기로 이루어진 군에서 선택된 1개 이상의 치환기로 치환 또는 비치환된 알콕시기; 할로겐기, 알킬기, 알케닐기 알콕시기, 치환 또는 비치환 된 아릴기, 치환 또는 비치환된 아릴알킬기, 치환 또는 비치환된 아릴알케닐기, 치환 또는 비치환된 헤테로 고리기, 니트릴기 및 아세틸렌기로 이루어진 군에서 선택된 1개 이상의 치환기로 치환 또는 비치환된 아릴기; 알킬기, 알케닐기 치환 또는 비치환된 아릴기, 치환 또는 비치환된 아릴알킬기, 치환 또는 비치환된 아릴알케닐기로 이루어진 군에서 선택된 1개 이상의 치환기로 치환된 아미노기; 니트로기; 및 할로겐기로 이루어진 군에서 선택되며, 여기서 이들은 서로 인접하는 기와 지방족 또는 헤테로의 축합 고리를 형성할 수 있다.
- 청구항 1에 있어서, 상기 화학식 1의 A는 페닐기, 비페닐기, 터페닐기, 스틸벤, 나프틸기, 안트라세닐기, 페나트렌기, 파이레닐기 및 페릴레닐기로 이루어진 군에서 선택되는 것인 화학식 1의 화합물.
- 청구항 1에 있어서, 상기 화학식1의 B가 헤테로고리인 경우 티오펜기, 퓨란기, 피롤기, 이미다졸기, 티아졸기, 옥사졸기, 옥사디아졸기, 트리아졸기, 피리딜기, 피라다진기, 퀴놀리닐기, 이소퀴톨린기 및 아크리딜기로 이루어진 군에서 선택되는 것인 화학식 1의 화합물.
- 청구항 1에 있어서, 상기 화학식 1의 Ar은 페닐렌인 것인 화학식 1의 화합물.
- 제1 전극, 발광층을 비롯한 1층 이상으로 이루어진 유기물층 및 제2 전극을 순차적으로 적층된 형태로 포함하는 유기 발광 소자에 있어서, 상기 유기물층 중 1층 이상이 청구항 1의 화학식 1의 화합물, 또는 이 화합물에 열경화성 또는 광경화성 작용기가 도입된 화합물을 포함하는 것인 유기 발광 소자.
- 청구항 10에 있어서, 유기물층은 정공수송층을 포함하고, 이 정공수송층이 상기 화학식 1의 화합물 또는 이 화합물에 열 경화성 또는 광경화성 작용기가 도입된 화합물을 포함하는 것인 유기 발광 소자.
- 청구항 10에 있어서, 유기물층은 정공주입층을 포함하고, 이 정공주입층이 상기 화학식 1의 화합물 또는 이 화합물에 열 경화성 또는 광경화성 작용기가 도입된 화합물을 포함하는 것인 유기 발광 소자.
- 청구항 10에 있어서, 유기물층은 정공주입과 정공수송을 동시에 하는 층을 포함하고, 이 층이 상기 화학식 1의 화합물인 또는 이 화합물에 열 경화성 또는 광경화성 작용기가 도입된 화합물을 포함하는 것인 유기 발광 소자.
- 청구항 10에 있어서, 유기물층은 전자 주입 및 전자수송층을 포함하고, 이 전자주입 또는 전자수송층이 상기 화학식 1의 화합물, 또는 이 화합물에 열 경화성 또는 광경화성 작용기가 도입된 화합물을 포함하는 것인 유기 발광 소자.
- 청구항 10에 있어서, 발광층이 상기 화학식 1의 화합물, 또는 이 화합물에 열 경화성 또는 광경화성 작용기가 도입된 화합물을 포함하는 것인 유기 발광 소자.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR20070113852 | 2007-11-08 | ||
| KR1020070113852 | 2007-11-18 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20090051140A true KR20090051140A (ko) | 2009-05-21 |
Family
ID=40625953
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020080073238A KR20090048299A (ko) | 2007-11-08 | 2008-07-25 | 새로운 유기 발광 소자 재료 및 이를 이용한 유기 발광소자 |
| KR1020080110472A KR101127264B1 (ko) | 2007-11-08 | 2008-11-07 | 새로운 유기 발광 소자 재료 및 이를 이용한 유기 발광 소자 |
| KR1020080110471A KR20090051140A (ko) | 2007-11-08 | 2008-11-07 | 새로운 유기 발광 소자 재료 및 이를 이용한 유기 발광 소자 |
Family Applications Before (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020080073238A KR20090048299A (ko) | 2007-11-08 | 2008-07-25 | 새로운 유기 발광 소자 재료 및 이를 이용한 유기 발광소자 |
| KR1020080110472A KR101127264B1 (ko) | 2007-11-08 | 2008-11-07 | 새로운 유기 발광 소자 재료 및 이를 이용한 유기 발광 소자 |
Country Status (7)
| Country | Link |
|---|---|
| US (2) | US8968884B2 (ko) |
| EP (2) | EP2215182B1 (ko) |
| JP (3) | JP5562862B2 (ko) |
| KR (3) | KR20090048299A (ko) |
| CN (2) | CN101896574B (ko) |
| TW (2) | TWI403503B (ko) |
| WO (1) | WO2009061156A1 (ko) |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2011055932A2 (ko) * | 2009-11-05 | 2011-05-12 | 덕산하이메탈(주) | 유기화합물 및 이를 이용한 유기전기소자, 그 단말 |
| WO2012177006A2 (ko) * | 2011-06-22 | 2012-12-27 | 덕산하이메탈(주) | 유기전기소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| US8890126B2 (en) | 2010-04-23 | 2014-11-18 | Cheil Industries, Inc. | Compound for optoelectronic device, organic light emitting diode including the same, and display including the organic light emitting diode |
| US9102616B2 (en) | 2009-11-05 | 2015-08-11 | Duk San Neolux Co., Ltd. | Organic compound, organic electronic device using same, and terminal for same |
Families Citing this family (54)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20090048299A (ko) * | 2007-11-08 | 2009-05-13 | 주식회사 엘지화학 | 새로운 유기 발광 소자 재료 및 이를 이용한 유기 발광소자 |
| KR102340209B1 (ko) * | 2007-12-03 | 2021-12-17 | 가부시키가이샤 한도오따이 에네루기 켄큐쇼 | 카바졸 유도체, 및 카바졸 유도체를 사용하는 발광 소자, 발광 장치 및 전자 기기 |
| CN102224150B (zh) | 2008-11-25 | 2015-08-12 | 出光兴产株式会社 | 芳香族胺衍生物以及有机电致发光元件 |
| EP2399906A4 (en) | 2009-02-18 | 2012-08-29 | Idemitsu Kosan Co | AROMATIC AMINE DERIVATIVE AND ORGANIC ELECTROLUMINESCENT ELEMENT |
| KR20100106014A (ko) * | 2009-03-23 | 2010-10-01 | 다우어드밴스드디스플레이머티리얼 유한회사 | 신규한 유기 발광 화합물 및 이를 포함하고 있는 유기 전계발광 소자 |
| JP2010254671A (ja) | 2009-03-31 | 2010-11-11 | Semiconductor Energy Lab Co Ltd | カルバゾール誘導体、発光素子用材料、発光素子、発光装置、電子機器、及び照明装置 |
| US8877356B2 (en) | 2009-07-22 | 2014-11-04 | Global Oled Technology Llc | OLED device with stabilized yellow light-emitting layer |
| JP5617202B2 (ja) * | 2009-07-24 | 2014-11-05 | 三菱化学株式会社 | 有機化合物、電荷輸送材料、有機電界発光素子用組成物、有機電界発光素子、有機elディスプレイ及び有機el照明 |
| JP5672858B2 (ja) * | 2009-08-27 | 2015-02-18 | 三菱化学株式会社 | 電荷輸送材料、電荷輸送膜用組成物、有機電界発光素子、有機elディスプレイ及び有機el照明 |
| KR101137385B1 (ko) * | 2009-08-28 | 2012-04-20 | 삼성모바일디스플레이주식회사 | 헤테로아릴아민 화합물 및 이를 이용한 유기 발광 소자 |
| WO2011024451A1 (ja) * | 2009-08-28 | 2011-03-03 | 保土谷化学工業株式会社 | カルバゾール環構造を有する化合物および有機エレクトロルミネッセンス素子 |
| KR101127579B1 (ko) * | 2009-08-28 | 2012-03-23 | 삼성모바일디스플레이주식회사 | 헤테로아릴아민 화합물 및 이를 이용한 유기 발광 소자 |
| KR101007516B1 (ko) * | 2010-04-23 | 2011-01-14 | 주식회사 이엘엠 | 유기 전기 발광 조성물 및 이를 포함하는 유기 전기 발광 소자 |
| EP2421064B1 (en) | 2010-08-18 | 2018-07-04 | Cheil Industries Inc. | Compound for organic optoelectronic device, organic light emmiting diode including the same and display including the light emmiting diode |
| JP5623996B2 (ja) | 2010-09-21 | 2014-11-12 | 株式会社半導体エネルギー研究所 | カルバゾール誘導体 |
| JP5872861B2 (ja) | 2010-11-30 | 2016-03-01 | 株式会社半導体エネルギー研究所 | カルバゾール化合物 |
| TW201238113A (en) * | 2011-02-10 | 2012-09-16 | Du Pont | Process and materials for making contained layers and devices made with same |
| CN103430344B (zh) * | 2011-03-14 | 2016-03-23 | 东丽株式会社 | 发光元件材料及发光元件 |
| KR101298483B1 (ko) * | 2011-04-01 | 2013-08-21 | 덕산하이메탈(주) | 화합물 및 이를 이용한 유기전기소자, 그 전자장치 |
| EP2816025B1 (en) | 2012-02-10 | 2018-12-26 | Idemitsu Kosan Co., Ltd | Aromatic amine derivative, organic electroluminescent element and electronic device |
| KR101932563B1 (ko) | 2012-06-27 | 2018-12-28 | 삼성디스플레이 주식회사 | 다층 구조의 정공수송층을 포함하는 유기 발광 소자 및 이를 포함하는 유기 발광 표시 장치 |
| KR102169273B1 (ko) * | 2012-07-26 | 2020-10-23 | 주식회사 동진쎄미켐 | 아크리딘 유도체를 포함하는 유기발광 화합물 및 이를 포함하는 유기발광소자 |
| KR20190000390A (ko) * | 2012-08-03 | 2019-01-02 | 가부시키가이샤 한도오따이 에네루기 켄큐쇼 | 발광 소자, 발광 장치, 전자 장치 및 조명 장치 |
| KR101415730B1 (ko) * | 2012-08-07 | 2014-07-04 | (주)위델소재 | 방향족 화합물 유도체 및 이를 이용한 유기전계 발광소자 |
| KR101483933B1 (ko) * | 2012-10-17 | 2015-01-19 | 롬엔드하스전자재료코리아유한회사 | 신규한 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| KR102086546B1 (ko) * | 2012-10-19 | 2020-03-10 | 삼성디스플레이 주식회사 | 화합물 및 이를 포함한 유기 발광 소자 |
| CN104837834B (zh) * | 2012-12-07 | 2018-04-03 | 出光兴产株式会社 | 芳香族胺衍生物和有机电致发光元件 |
| KR102026645B1 (ko) * | 2013-02-07 | 2019-09-30 | 덕산네오룩스 주식회사 | 유기전기 소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| KR102065656B1 (ko) * | 2013-02-19 | 2020-01-13 | 덕산네오룩스 주식회사 | 유기전기 소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| KR102120891B1 (ko) * | 2013-02-22 | 2020-06-10 | 삼성디스플레이 주식회사 | 헤테로고리 화합물 및 이를 포함한 유기 발광 소자 |
| KR101979651B1 (ko) * | 2013-04-01 | 2019-05-17 | 덕산네오룩스 주식회사 | 유기전기 소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| KR102223672B1 (ko) | 2013-08-19 | 2021-03-08 | 삼성디스플레이 주식회사 | 아민계 화합물 및 이를 포함한 유기 발광 소자 |
| JP2015122459A (ja) * | 2013-12-25 | 2015-07-02 | 三星ディスプレイ株式會社Samsung Display Co.,Ltd. | 有機el素子 |
| KR102253438B1 (ko) | 2014-03-26 | 2021-05-20 | 삼성디스플레이 주식회사 | 아민계 화합물 및 이를 포함한 유기 발광 소자 |
| WO2016006629A1 (ja) * | 2014-07-09 | 2016-01-14 | 保土谷化学工業株式会社 | 有機エレクトロルミネッセンス素子 |
| WO2016026122A1 (en) * | 2014-08-21 | 2016-02-25 | Dow Global Technologies Llc | Benzocyclobutenes derived compositions, and electronic devices containing the same |
| US11158811B2 (en) * | 2014-12-05 | 2021-10-26 | Hodogaya Chemical Co., Ltd. | Organic electroluminescent device |
| JP6446254B2 (ja) | 2014-12-15 | 2018-12-26 | 三星ディスプレイ株式會社Samsung Display Co.,Ltd. | カルバゾール化合物、有機エレクトロルミネッセンス素子用材料、および有機エレクトロルミネッセンス素子 |
| CN107112425B (zh) * | 2014-12-24 | 2019-05-17 | 保土谷化学工业株式会社 | 有机电致发光器件 |
| WO2016107459A1 (en) | 2014-12-29 | 2016-07-07 | Dow Global Technologies Llc | Compositions with 2, 3-disubstituted indoles as charge transport materials, and display devices fabricated therefrom |
| EP3244463B1 (en) * | 2015-01-08 | 2020-07-22 | Hodogaya Chemical Co., Ltd. | Organic electroluminescent device |
| WO2016111301A1 (ja) * | 2015-01-08 | 2016-07-14 | 保土谷化学工業株式会社 | 有機エレクトロルミネッセンス素子 |
| US10566540B2 (en) * | 2015-02-03 | 2020-02-18 | Hodogaya Chemical Co., Ltd. | Organic electroluminescent device |
| JP6282614B2 (ja) * | 2015-06-22 | 2018-02-21 | ユニバーサル ディスプレイ コーポレイション | 溶液加工可能な、ドープされたトリアリールアミン正孔注入材料 |
| KR102359879B1 (ko) | 2015-06-25 | 2022-02-10 | 덕산네오룩스 주식회사 | 유기전기 소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| US20210210691A1 (en) * | 2015-12-24 | 2021-07-08 | Dow Global Technologies Llc | Polymeric layer and organic electronic device comprising same. |
| WO2017118238A1 (zh) * | 2016-01-07 | 2017-07-13 | 广州华睿光电材料有限公司 | 氘代三芳胺衍生物及其在电子器件中的应用 |
| KR101850424B1 (ko) | 2016-11-11 | 2018-04-20 | 한국과학기술연구원 | 조직접착용 포스파젠계 고분자, 이의 제조방법 및 용도 |
| CN108417724A (zh) * | 2018-03-15 | 2018-08-17 | 京东方科技集团股份有限公司 | 发光二极管显示器及其制备方法 |
| KR102654810B1 (ko) * | 2018-10-30 | 2024-04-03 | 주식회사 엘지화학 | 신규한 화합물 및 이를 이용한 유기발광 소자 |
| KR102418662B1 (ko) | 2019-01-14 | 2022-07-08 | 주식회사 엘지화학 | 유기 발광 소자 |
| CN114516859A (zh) * | 2020-11-18 | 2022-05-20 | 北京鼎材科技有限公司 | 一种化合物及其应用 |
| CN112876406A (zh) * | 2021-01-15 | 2021-06-01 | 安徽秀朗新材料科技有限公司 | 氘代咔唑类化合物及其制备方法、光电材料及药物 |
| CN115353483B (zh) * | 2022-07-06 | 2024-04-09 | 南京高光半导体材料有限公司 | 一种含有双咔唑结构的化合物及有机电致发光器件 |
Family Cites Families (22)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP3649302B2 (ja) | 1996-05-23 | 2005-05-18 | 出光興産株式会社 | 有機電界発光素子 |
| US6660410B2 (en) * | 2000-03-27 | 2003-12-09 | Idemitsu Kosan Co., Ltd. | Organic electroluminescence element |
| US6579630B2 (en) | 2000-12-07 | 2003-06-17 | Canon Kabushiki Kaisha | Deuterated semiconducting organic compounds used for opto-electronic devices |
| JP2003133075A (ja) * | 2001-07-25 | 2003-05-09 | Toray Ind Inc | 発光素子 |
| US20030170423A1 (en) * | 2002-01-25 | 2003-09-11 | Fuji Photo Film Co., Ltd. | Method of producing pattern member, apparatus of producing pattern member, and pattern member |
| JP4316387B2 (ja) | 2002-03-22 | 2009-08-19 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子用材料及びそれを用いた有機エレクトロルミネッセンス素子 |
| CN100366703C (zh) | 2002-03-22 | 2008-02-06 | 出光兴产株式会社 | 用于有机电致发光器件的材料以及使用该材料的有机电致发光器件 |
| JP4336537B2 (ja) | 2003-07-31 | 2009-09-30 | キヤノン株式会社 | 有機発光素子 |
| KR20050118098A (ko) | 2004-03-19 | 2005-12-15 | 주식회사 엘지화학 | 새로운 정공 주입 또는 수송용 물질 및 이를 이용한 유기발광 소자 |
| EP1725632B1 (en) * | 2004-03-19 | 2014-04-30 | LG Chem, Ltd. | Organic electroluminescence devices comprising new materials for injecting holes |
| KR100573137B1 (ko) | 2004-04-02 | 2006-04-24 | 삼성에스디아이 주식회사 | 플루오렌계 화합물 및 이를 이용한 유기 전계 발광 소자 |
| KR100669716B1 (ko) | 2004-07-14 | 2007-01-16 | 삼성에스디아이 주식회사 | 페닐카르바졸 화합물 및 이를 이용한 유기 전계 발광 소자 |
| US8188315B2 (en) * | 2004-04-02 | 2012-05-29 | Samsung Mobile Display Co., Ltd. | Organic light emitting device and flat panel display device comprising the same |
| EP1805140B1 (en) | 2004-10-19 | 2016-08-31 | Semiconductor Energy Laboratory Co., Ltd. | Carbazole derivative, and light emitting element and light emitting device using the carbazole derivative |
| WO2007002789A2 (en) * | 2005-06-29 | 2007-01-04 | Teknovus, Inc. | Accommodating different clock frequencies in an ethernet passive optical network |
| KR100806812B1 (ko) * | 2005-07-25 | 2008-02-25 | 엘지.필립스 엘시디 주식회사 | 유기 el 소자 및 그 제조방법 |
| KR101359412B1 (ko) * | 2005-08-31 | 2014-02-27 | 가부시키가이샤 한도오따이 에네루기 켄큐쇼 | 카르바졸 유도체, 발광소자용 재료, 발광소자, 발광 장치 및 전자기기 |
| JP2007110097A (ja) | 2005-09-14 | 2007-04-26 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子、有機エレクトロルミネッセンス素子の製造方法、表示装置及び照明装置 |
| WO2008029729A1 (fr) | 2006-09-08 | 2008-03-13 | Konica Minolta Holdings, Inc. | Dispositif électroluminescent organique, dispositif d'éclairage et affichage utilisant un tel dispositif |
| JP4830750B2 (ja) | 2006-09-21 | 2011-12-07 | 東レ株式会社 | 発光素子材料および発光素子 |
| KR101347519B1 (ko) | 2006-11-24 | 2014-01-03 | 이데미쓰 고산 가부시키가이샤 | 방향족 아민 유도체 및 그것을 이용한 유기 전기발광 소자 |
| KR20090048299A (ko) * | 2007-11-08 | 2009-05-13 | 주식회사 엘지화학 | 새로운 유기 발광 소자 재료 및 이를 이용한 유기 발광소자 |
-
2008
- 2008-07-25 KR KR1020080073238A patent/KR20090048299A/ko active Search and Examination
- 2008-11-07 JP JP2010533010A patent/JP5562862B2/ja active Active
- 2008-11-07 US US12/741,996 patent/US8968884B2/en active Active
- 2008-11-07 WO PCT/KR2008/006588 patent/WO2009061156A1/en active Application Filing
- 2008-11-07 CN CN200880119858.2A patent/CN101896574B/zh active Active
- 2008-11-07 JP JP2010533011A patent/JP5566898B2/ja active Active
- 2008-11-07 CN CN200880115350.5A patent/CN101855315B/zh active Active
- 2008-11-07 TW TW097142998A patent/TWI403503B/zh active
- 2008-11-07 KR KR1020080110472A patent/KR101127264B1/ko active IP Right Grant
- 2008-11-07 KR KR1020080110471A patent/KR20090051140A/ko not_active Application Discontinuation
- 2008-11-07 EP EP08847358.2A patent/EP2215182B1/en active Active
- 2008-11-07 EP EP08847615.5A patent/EP2215183B1/en active Active
- 2008-11-07 US US12/742,069 patent/US8395143B2/en active Active
- 2008-11-07 TW TW097143000A patent/TWI388647B/zh active
-
2014
- 2014-04-08 JP JP2014079343A patent/JP2014169297A/ja active Pending
Cited By (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2011055932A2 (ko) * | 2009-11-05 | 2011-05-12 | 덕산하이메탈(주) | 유기화합물 및 이를 이용한 유기전기소자, 그 단말 |
| WO2011055932A3 (ko) * | 2009-11-05 | 2011-10-27 | 덕산하이메탈(주) | 유기화합물 및 이를 이용한 유기전기소자, 그 단말 |
| US9102616B2 (en) | 2009-11-05 | 2015-08-11 | Duk San Neolux Co., Ltd. | Organic compound, organic electronic device using same, and terminal for same |
| US8890126B2 (en) | 2010-04-23 | 2014-11-18 | Cheil Industries, Inc. | Compound for optoelectronic device, organic light emitting diode including the same, and display including the organic light emitting diode |
| WO2012177006A2 (ko) * | 2011-06-22 | 2012-12-27 | 덕산하이메탈(주) | 유기전기소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| WO2012177006A3 (ko) * | 2011-06-22 | 2013-02-21 | 덕산하이메탈(주) | 유기전기소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
Also Published As
| Publication number | Publication date |
|---|---|
| TW200927878A (en) | 2009-07-01 |
| KR20090048299A (ko) | 2009-05-13 |
| EP2215183B1 (en) | 2013-12-25 |
| US8395143B2 (en) | 2013-03-12 |
| CN101855315A (zh) | 2010-10-06 |
| EP2215183A4 (en) | 2011-11-09 |
| KR101127264B1 (ko) | 2012-03-29 |
| CN101896574B (zh) | 2014-08-20 |
| US20100244008A1 (en) | 2010-09-30 |
| JP5566898B2 (ja) | 2014-08-06 |
| TWI388647B (zh) | 2013-03-11 |
| CN101855315B (zh) | 2014-04-30 |
| JP2011503055A (ja) | 2011-01-27 |
| KR20090051141A (ko) | 2009-05-21 |
| WO2009061156A1 (en) | 2009-05-14 |
| EP2215183A1 (en) | 2010-08-11 |
| JP2011503056A (ja) | 2011-01-27 |
| JP5562862B2 (ja) | 2014-07-30 |
| EP2215182B1 (en) | 2014-01-08 |
| US8968884B2 (en) | 2015-03-03 |
| TW200927730A (en) | 2009-07-01 |
| CN101896574A (zh) | 2010-11-24 |
| JP2014169297A (ja) | 2014-09-18 |
| US20110127495A1 (en) | 2011-06-02 |
| TWI403503B (zh) | 2013-08-01 |
| EP2215182A1 (en) | 2010-08-11 |
| EP2215182A4 (en) | 2011-08-24 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101127264B1 (ko) | 새로운 유기 발광 소자 재료 및 이를 이용한 유기 발광 소자 | |
| KR100775738B1 (ko) | 새로운 유기 발광 소자 재료 및 이를 이용한 유기 발광소자(10) | |
| KR101350581B1 (ko) | 새로운 화합물 및 이를 이용한 유기 발광 소자 | |
| JP5836487B2 (ja) | 有機発光素子材料およびこれを利用した有機発光素子 | |
| KR101565200B1 (ko) | 신규한 화합물 및 이를 이용한 유기 발광 소자 | |
| KR100645052B1 (ko) | 새로운 유기 발광 소자 재료 및 이를 이용한 유기 발광소자(3) | |
| KR20120112277A (ko) | 새로운 유기 발광 소자 재료 및 이를 이용한 유기 발광 소자 | |
| KR101356953B1 (ko) | 카바졸 유도체 및 이를 이용한 유기 발광 소자 | |
| KR101306531B1 (ko) | 새로운 유기 발광 소자 재료 및 이를 이용한 유기 발광 소자 | |
| KR100925323B1 (ko) | 신규한 화합물 및 이를 이용한 유기 발광 소자 | |
| JP4642772B2 (ja) | 有機発光素子の有機物層に使用可能な新規化合物 | |
| KR20140018166A (ko) | 새로운 유기 발광 소자 재료 및 이를 이용한 유기 발광 소자 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| E902 | Notification of reason for refusal | ||
| E601 | Decision to refuse application |