KR101426125B1 - 암 세포의 전이 예방을 위한 화합물, 조성물 및 방법 - Google Patents
암 세포의 전이 예방을 위한 화합물, 조성물 및 방법 Download PDFInfo
- Publication number
- KR101426125B1 KR101426125B1 KR1020117018742A KR20117018742A KR101426125B1 KR 101426125 B1 KR101426125 B1 KR 101426125B1 KR 1020117018742 A KR1020117018742 A KR 1020117018742A KR 20117018742 A KR20117018742 A KR 20117018742A KR 101426125 B1 KR101426125 B1 KR 101426125B1
- Authority
- KR
- South Korea
- Prior art keywords
- cancer
- delete delete
- cell
- tumor
- ethyl
- Prior art date
Links
- 0 CC(C)(*)OC(NC*C(N[C@](*)Cc(cc1)ccc1NS(O)(=O)=O)=O)=O Chemical compound CC(C)(*)OC(NC*C(N[C@](*)Cc(cc1)ccc1NS(O)(=O)=O)=O)=O 0.000 description 12
- OFNQMGQYBXWJSG-UHFFFAOYSA-N C=Nc1ccc(CC2(CC2)c2c[s]c(-c3ccc[s]3)n2)cc1 Chemical compound C=Nc1ccc(CC2(CC2)c2c[s]c(-c3ccc[s]3)n2)cc1 OFNQMGQYBXWJSG-UHFFFAOYSA-N 0.000 description 1
- YOEJXAZZPHIMBK-UHFFFAOYSA-N CCC1=CSC(C(Cc(cc2)ccc2[IH]C(C)S(=O)=O)NC(Cc2cc(C=O)c(C=O)cc2)=O)=[I]1 Chemical compound CCC1=CSC(C(Cc(cc2)ccc2[IH]C(C)S(=O)=O)NC(Cc2cc(C=O)c(C=O)cc2)=O)=[I]1 YOEJXAZZPHIMBK-UHFFFAOYSA-N 0.000 description 1
- GWFIEMVBGDEDSC-IBGZPJMESA-N CCc1c[o]c([C@H](Cc(cc2)ccc2N)NC(Cc2ccccc2)=O)n1 Chemical compound CCc1c[o]c([C@H](Cc(cc2)ccc2N)NC(Cc2ccccc2)=O)n1 GWFIEMVBGDEDSC-IBGZPJMESA-N 0.000 description 1
- DFMNJBSBPRRYMI-PKTZIBPZSA-N CCc1c[s]c([C@H](Cc(cc2)ccc2NS(O)(=O)=O)NC([C@@H](Cc2ccccc2)NC(OC(C)(C)C)=O)=O)n1 Chemical compound CCc1c[s]c([C@H](Cc(cc2)ccc2NS(O)(=O)=O)NC([C@@H](Cc2ccccc2)NC(OC(C)(C)C)=O)=O)n1 DFMNJBSBPRRYMI-PKTZIBPZSA-N 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/425—Thiazoles
- A61K31/426—1,3-Thiazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/095—Sulfur, selenium, or tellurium compounds, e.g. thiols
- A61K31/10—Sulfides; Sulfoxides; Sulfones
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/335—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin
- A61K31/337—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin having four-membered rings, e.g. taxol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/415—1,2-Diazoles
- A61K31/4155—1,2-Diazoles non condensed and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/4192—1,2,3-Triazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/425—Thiazoles
- A61K31/427—Thiazoles not condensed and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/425—Thiazoles
- A61K31/428—Thiazoles condensed with carbocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/433—Thidiazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/4353—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems
- A61K31/4375—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems the heterocyclic ring system containing a six-membered ring having nitrogen as a ring heteroatom, e.g. quinolizines, naphthyridines, berberine, vincamine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4427—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems
- A61K31/4439—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems containing a five-membered ring with nitrogen as a ring hetero atom, e.g. omeprazole
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/4965—Non-condensed pyrazines
- A61K31/497—Non-condensed pyrazines containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/506—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim not condensed and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/517—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim ortho- or peri-condensed with carbocyclic ring systems, e.g. quinazoline, perimidine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
- A61K31/5375—1,4-Oxazines, e.g. morpholine
- A61K31/538—1,4-Oxazines, e.g. morpholine ortho- or peri-condensed with carbocyclic ring systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/65—Tetracyclines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7042—Compounds having saccharide radicals and heterocyclic rings
- A61K31/7052—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides
- A61K31/706—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom
- A61K31/7064—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom containing condensed or non-condensed pyrimidines
- A61K31/7068—Compounds having saccharide radicals and heterocyclic rings having nitrogen as a ring hetero atom, e.g. nucleosides, nucleotides containing six-membered rings with nitrogen as a ring hetero atom containing condensed or non-condensed pyrimidines having oxo groups directly attached to the pyrimidine ring, e.g. cytidine, cytidylic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/19—Cytokines; Lymphokines; Interferons
- A61K38/20—Interleukins [IL]
- A61K38/2013—IL-2
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
- A61K39/39533—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals
- A61K39/39558—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals against tumor tissues, cells, antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/04—Antineoplastic agents specific for metastasis
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D277/00—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings
- C07D277/02—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings
- C07D277/20—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D277/22—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to ring carbon atoms
- C07D277/28—Radicals substituted by nitrogen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D277/00—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings
- C07D277/60—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings condensed with carbocyclic rings or ring systems
- C07D277/62—Benzothiazoles
- C07D277/64—Benzothiazoles with only hydrocarbon or substituted hydrocarbon radicals attached in position 2
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/04—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing three or more hetero rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/425—Thiazoles
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- General Health & Medical Sciences (AREA)
- Epidemiology (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Immunology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Oncology (AREA)
- Gastroenterology & Hepatology (AREA)
- Zoology (AREA)
- Molecular Biology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Biomedical Technology (AREA)
- Mycology (AREA)
- Microbiology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Plural Heterocyclic Compounds (AREA)
- Thiazole And Isothizaole Compounds (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Abstract
암 세포의 전이를 예방하기 위한 방법이 개시된다. 개시된 화합물은 종양 또는 암 세포의 기타 유형의 전파를 방지하기 위해 이용될 수 있다.
Description
본 출원은 2009 년 6 월 6 일자로 출원된 임시 출원 일련 번호 61/223,260 의 이권을 청구하며, 그 전체 개시 내용은 본 출원에 참고문헌으로 포함된다.
분야
암 종양의 전이를 예방하고/하거나 종양 성장을 감소시킬 수 있는 화합물이 개시된다. 악성 종양의 전이를 예방하고 종양 성장을 감소시키기 위한 조성물, 특히 약제학적 조성물이 또한 개시된다. 암 치료에서의 사용을 위한 병용 치료요법 조성물도 또한 상기 조성물에 포함된다. 또한, 암 종양 및 기타 암 세포의 전이를 예방하는 방법도 또한 개시된다. 이와 같이, 개시된 화합물은 암을 갖고 있거나 또는 암으로 진단받은 대상체에서의 암 성장의 예방을 보조하기 위해 이용될 수 있다.
암의 가장 놀랄만한 측면들 중 하나는 전파 또는 전이하는 그의 능력이다. 최초에는, 암 세포는 함께 무리지어 하나 이상의 종양을 형성하는 것으로 발견된다. 원발 종양의 형성 후, 암 세포는 본래 종양으로부터 떨어져 나와 신체의 여타 영역으로 이동하는 능력을 얻을 수 있다. 간에서 취해지고 종양을 형성하는 폐암 세포는 여전히 폐암 세포이다. 따라서, 전이하는 암의 한가지 특별한 형태의 경향성은 암의 유형을 포함하는 수많은 요인에 좌우되나; 세포가 전이 과정을 시작하는 방법에 있어서의 전반적인 과정은 아직 완전하게 이해되지 않고 있다.
단일 집락 종양을 전이 기회 획득 전 발견한다면, 환자 생존의 예측값이 더 높아질 것이다. 이는, 종양이 방사선 또는 화학요법에 의해 유효하게 절제 또는 제거될 수 있기 때문이다. 따라서, 종양 성장 및 종양 세포의 전이 사이에는 차이가 있다; 종양 성장이 종양 세포 전이를 항상 유도하는 것은 아니다. 그러나, 전이된 암은, 그것이 신체를 통해 전파된 정도를 때때로 알 수 없기 때문에, 치료하기가 어렵다.
전이를 위해서는, 암 세포는 그의 종양으로부터 떨어져 나와 순환계 또는 림프계에 침입해야 한다. 유리된 세포는 이어 이들 자체를 확립하게 될 새로운 위치로 수송된다. 신체는 그의 세포가 본래 위치로부터 떨어져 나온 후에는 생존하는 것을 막는 자연적인 방위체계를 갖고 있긴 하지만, 일부 암 세포는 이러한 방위체계를 극복하는 능력을 갖고 있다. 따라서, 전이가 중단되거나 또는 현저하게 감소된 경우, 암의 정도는 측정될 수 있으며, 후속하여 치료될 수 있다. 마찬가지로, 종양을 절제하거나 또는 방사선/화학요법이 사용되는 암 치료요법에 대한 후속 치료는 전이방지제에 대한 환자의 치료일 것이다. 암 세포 전이 예방 방법에 대한 필요성 체감은 오래되었다.
원발 종양의 성장은 또한 치료에 대한 도전과제를 제시한다. 원발 종양의 성장이 억제되지 않고 진행된다면, 최초의 종양은 1 차적인 부위 및 부근 조직에서 장기 기능에 악영향을 끼치는 크기로 성장할 수 있다. 원발 종양의 성장이 제어되지 않는다면, 원발 종양의 전이는 또한 더욱더 그러할 것이다. 종양 성장을 감속 또는 예방할 방법이 필요하다.
개요
암 세포의 전이를 예방할 화합물, 조성물 및 방법이 개시된다. 추가로, 개시된 화합물을 하나 이상의 암 치료 약물 또는 여타 화학요법제와 병용하는 병용 치료요법 조성물을 포함하는, 암 치료에 사용될 수 있는 화합물, 조성물 및 방법이 개시된다.
추가적인 장점은 하기의 상세한 설명에 일부 제시될 것이며, 일부는 상세한 설명으로부터 자명하거나, 또는 하기 설명된 국면의 실시에 의해 습득될 수 있을 것이다. 하기 기재된 장점들은 첨부된 특허청구범위에서 특별히 지적된 구성요소 및 조합을 수단으로 하여 구현 및 수득될 수 있을 것이다. 상기 포괄적인 기재내용 및 하기의 상세한 설명 모두 단지 예시적이며 설명을 위한 것이고, 제한하려는 의미는 없다는 점이 이해되어야 한다.
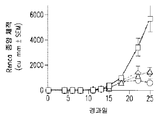
도 1 은 마우스에서의 신장 세포 암 종양 (Renca) 의 종양 체적이 몇 배 증가했는지 보여주는 그래프를 도시한다; 비히클 대조군 (□); 1 일 2 회 100,000 IU/투여량의 IL-2 (◇); 1 일 2 회 40 mg/kg 의 D91 (△); 1 일 2 회, 100,000 IU/투여량의 IL-2 및 40 mg/kg 의 D91 (○).
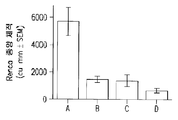
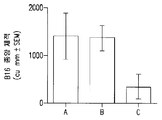
도 2 는 제 25 일째 마우스에서의 신장 세포 암 종양 (Renca) 부피의 히스토그램을 도시한다; 비히클 대조군 (A); 1 일 2 회 40 mg/kg 의 D91 (B); 1 일 2 회 100,000 IU/투여량의 IL-2 (C); 1 일 2 회 100,000 IU/투여량의 IL-2 및 40 mg/kg 의 D91 (D).
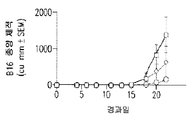
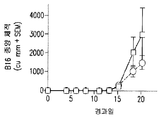
도 3 은 마우스에서의 B16 흑색종 종양의 종양 체적이 몇 배 증가했는지 보여주는 그래프를 도시한다; 비히클 대조군 (□); 1 일 2 회 300,000 IU/투여량의 IL-2 (◇); 1 일 2 회 300,000 IU/투여량의 IL-2 및 40 mg/kg 의 D91 (○).
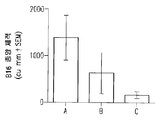
도 4 는 제 22 일째 마우스에서의 B16 흑색종 종양 체적의 히스토그램을 도시한다; 비히클 대조군 (A); 1 일 2 회 300,000 IU/투여량의 IL-2 (B); 1 일 2 회 300,000 IU/투여량의 IL-2 및 40 mg/kg 의 D91 (C).
도 5 는 B16 흑색종 종양이 있는 마우스의 체중의 그래프를 도시한다; 비히클 대조군 (□); 1 일 2 회 100,000 IU/투여량의 IL-2 (◇); 1 일 2 회 300,000 IU/투여량의 IL-2 (△); 1 일 2 회 100,000 IU/투여량의 IL-2 및 40 mg/kg 의 D91 (○); 및 1 일 2 회 300,000 IU/투여량의 IL-2 및 40 mg/kg 의 D91 (■).
도 6 은 마우스에서의 B16 흑색종 종양의 종양 체적이 몇 배 증가했는지 보여주는 그래프를 도시한다; 비히클 대조군 (□); 1 일 2 회 100,000 IU/투여량의 IL-2 (◇); 및 1 일 2 회 100,000 IU/투여량의 IL-2 및 40 mg/kg 의 D91 (○).
도 7 은 제 22 일째 마우스에서의 B16 흑색종 종양 체적의 히스토그램을 도시한다; 비히클 대조군 (A); 1 일 2 회 100,000 IU/투여량의 IL-2 (B); 및 1 일 2 회 100,000 IU/투여량의 IL-2 및 40 mg/kg 의 D91 (C).
도 8 은 마우스에서의 B16 흑색종 종양의 종양 체적이 몇 배 증가했는지 보여주는 그래프를 도시한다; 비히클 대조군 (□); 및 1 일 2 회 40 mg/kg 의 D91 (○).
도 9 는 NCr nu/nu 마우스에 정위이식된 췌장 종양의 크기를 도시한다: 비히클 대조군 (◇); 100 mg/kg 겜시타빈 (gemcitabine), i.p.주 2 회 (X); 150 mg/kg 겜시타빈, i.p.주 2 회 (□); 20 mg/kg D91 1 일 2 회 (○); 100 mg/kg 겜시타빈, i.p.주 2 회 및 20 mg/kg D91 1 일 2 회 (*); 및 150 mg/kg 겜시타빈, i.p.주 2 회 및 20 mg/kg D91 1 일 2 회 (△).
상세한 설명
본 명세서 및 후속하는 특허청구범위에서, 하기의 의미를 갖는 것으로 정의되는 다수 용어를 참조한다:
모든 백분율, 비율 및 분율은 달리 명시하지 않으면 중량 기준이다.
모든 온도는 달리 명시하지 않으면 섭씨 온도 (℃) 이다.
"약제학적으로 허용되는" 은 생물학적으로 또는 그 외적으로 바람직하지 않은 것이 아닌 물질을 의미하며, 즉 해당 물질이 임상적으로 허용되지 않는 생물학적 유효성을 야기한다거나 그것이 포함되는 약제학적 조성물의 임의의 여타 구성요소들과 불리한 방식으로 상호작용하지 않으면서 관련 활성 화합물들과 함께 개체에게 투여될 수 있다.
본 명세서 및 본 명세서의 특허청구범위를 통틀어, 용어 "포함하다" 및 상기 용어의 여타 활용 형태, 예컨대 "포함함" 은, 이에 제한되지 않으나, 포함을 의미하며, 예를 들어 여타 첨가물, 구성요소, 정수 또는 단계를 배제하려는 의도의 것은 아니다.
본 명세서 및 본 명세서의 특허청구범위에서 사용된 바와 같이, 대표 단수는 해당 문맥에서 명확히 달리 언급하지 않으면, 복수 언급을 포함한다. 따라서, "조성물" 의 언급은 두가지 이상의 해당 조성물의 혼합물을 포함하며, "페닐술팜산" 의 언급은 주가지 이상의 해당 페닐술팜산의 혼합물을 포함하며, "화합물" 의 언급은 두가지 이상의 해당 화합물의 혼합물 등을 포함한다.
"선택적인" 또는 "선택적으로" 는 후속하여 기재되는 사건 또는 환경이 일어날 수도 있고, 일어나지 않을 수도 있으며, 상기 기재는 해당 사건 또는 환경이 발생하는 경우 및 발생하지 않는 경우를 포함한다.
범위는 "약" 한가지 특정 값부터 및/또는 "약" 또다른 특정 값까지로 본원에서 표현될 수 있다. 상기 범위를 표현할 경우, 또다른 국면은 한 특정 값으로부터 및/또는 다른 특정 값까지를 포함한다. 유사하게, 값들이 선행사 "약" 의 이용으로 근사값으로 표현되는 경우, 해당 특별한 값들은 또다른 국면을 형성하는 것으로 이해될 것이다. 추가로, 각 범위의 종점들은 서로 독립적으로 여타 종점에 대해 전부 유의하다는 점이 이해될 것이다. 또한, 본원에 개시된 수많은 값들이 있으며, 각각의 상기 값은 또한 그 값 자체에 추가하여 약" 해당 특별 값과 같이 본원에 개시됨을 이해해야 한다. 예를 들어, 값 "10" 이 개시된 경우, "약 10" 이 또한 개시된다. 하나의 값이 개시된 경우, 해당 값의 "미만 또는 동등", "해당 값 초과 또는 동등" 및 값들 사이의 가능한 범위들이 또한 당업자가 적절하게 이해할 수 있게 개시된다는 점이 이해될 것이다. 예를 들어, 값 "10" 이 개시된 경우, "10 이하" 뿐만 아니라 "10 이상" 이 또한 개시된다. 출원 데이터를 통틀어, 수많은 상이한 포맷의 것이 제공되며, 상기 데이터는 종점 및 출발점을 나타내고, 데이터 지점들의 임의의 조합을 범위 내에 포함한다. 예를 들어, 특정 데이터 지점 "10" 내지 특정 데이터 지점 "15" 가 개시된 경우, 10 및 15 초과, 그 이상, 그 미만, 그 이하, 및 동등한 값 뿐만 아니라 10 내지 15 도 개시된 것으로 간주된다. 두 특정 단위 사이의 각 단위가 또한 개시된다는 것이 이해된다. 예를 들어, 10 내지 15 가 개시된 경우, 11, 12, 13 및 14 가 또한 개시된다.
본원에 사용된 바와 같이, 용어 "관리하다", "관리함" 및 "관리" 는 질환 또는 질환들의 치료를 결과로 제공하지 않는 예방 또는 치료제의 투여로 환자가 얻게 되는 이익을 지칭한다. 특정 구현예에서, 대상체는 질환을 "관리" 하여 질환 또는 질환들의 진행 또는 악화를 예방하고자 하나 이상의 예방 또는 치료제를 투여받는다.
본원에 사용된 바와 같이, 용어 "예방하다", "예방함" 및 "예방" 은, 예방제의 투여로 인해 대상체에서 질환 또는 장애를 방지 또는 회피하거나 또는 장애의 하나 이상의 병후의 재발 또는 안착을 지연시키는 방법을 지칭한다.
본원에 사용된 바와 같이, 용어 "병용" 은 하나 이상의 예방 및/또는 치료제의 이용을 지칭한다. 용어 "병용" 의 이용은 장애, 예를 들어 과다증식성 세포 장애, 특히 암이 있는 대상체에 예방 및/또는 치료제를 투여하는 순서를 제한하지 않는다. 첫번째 예방 또는 치료제는, 장애가 있었거나, 있거나 또는 그렇게 되기 쉬운 대상체에 두번째 예방 또는 치료제를 투여하기 이전에 (예를 들어, 1 분, 5 분, 15 분, 30 분, 45 분, 1 시간, 2 시간, 4 시간, 6 시간, 12 시간, 24 시간, 48 시간, 72 시간, 96 시간, 1 주, 2 주, 3 주, 4 주, 5 주, 6 주, 8 주 또는 12 주 이전), 그와 동시에, 또는 그에 후속하여 (예를 들어, 1 분, 5 분, 15 분, 30 분, 45 분, 1 시간, 2 시간, 4 시간, 6 시간, 12 시간, 24 시간, 48 시간, 72 시간, 96 시간, 1 주, 2 주, 3 주, 4 주, 5 주, 6 주, 8 주 또는 12 주 후) 투여될 수 있다. 예방제 또는 치료제는 본 개시의 약제가 여타 약제와 함께 작용하여 다르게 투여되는 것보다 증대된 이익을 제공하도록 순서대로 시간 간격을 두고 대상체에 투여된다. 임의의 추가적인 예방 또는 치료제가 여타 추가적인 예방 또는 치료제와 임의의 순서로 투여될 수 있다.
본원에 사용된 바와 같이, 용어 "투여하다" 는 화합물의 투여를 기재하기 위해 사용되는 경우, 화합물의 단독 투여량 또는 다중 투여량을 의미한다.
본원에 사용된 바와 같이, 용어 "암 치료" 는, 이에 제한되지 않으나 화학요법 및 방사요법을 포함하는 당업계에 공지된 임의의 암 치료법을 의미한다.
본원에 사용된 바와 같이, "종양 세포" 는 악성 종양을 포함하여 종양으로부터 유도되는 세포 및 시험관내에서 불멸화된 세포를 전부 의미한다. "정상" 세포는 비정상적 증식을 보이지 않는 정상적인 성장 특징을 가진 세포를 지칭한다.
본원에 사용된 바와 같이, 용어 "암이 있는 것으로 밝혀진 개인" 및 "암 환자" 는 호환하여 사용되며, 암이 있는 것으로 진단된 개인을 지칭하는 것을 의미한다. 암이 있는 개인을 밝혀내기 위한 수많은 공지된 수단이 있다. 일부 구현예에서, 암 진단은 PET 영상기법을 이용해 하거나 확인한다. 본 개시의 일부 구현예는 암이 있는 개인을 밝혀내는 단계를 포함한다.
본원에 사용된 바와 같이, 용어 "치료 유효량" 은 병후를 완화 또는 예방하거나, 종양 크기를 줄이거나, 또는 치료하는 환자의 수명을 연장시키기 위해 유효한 활성제 또는 활성제 배합물의 양을 지칭하는 것을 의미한다. 치료 유효량의 결정은 특히 본원에 개시된 상세한 개시 내용의 맥락에서, 당업자의 재량에 따른다.
본원에 사용된 바와 같이, 용어 "억제하다" 또는 "억제" 는 활성에 있어서의 통계적으로 유의하고 측정가능한 감소, 바람직하게는 대조군 대비 약 10% 이상의 감소, 더욱 바람직하게는 약 50% 이상의 감소, 더욱더 바람직하게는 약 80% 이상의 감소를 지칭한다.
본원에 사용된 바와 같이, 용어 "증가하다" 또는 "강화" 는 활성에 있어서의 통계적으로 유의하고 측정가능한 증가, 바람직하게는 대조군 대비 약 10% 이상의 증가, 더욱 바람직하게는 약 50% 이상의 증가, 더욱더 바람직하게는 약 80% 이상의 증가를 지칭한다.
용어 "예방하다" 또는 "예방" 은 상태, 예컨대 국지적 재발 (예를 들어, 통증), 질환, 예컨대 암, 복합 증후군, 예컨대 심부전 또는 임의의 기타 의학적 상태와 관련하여 사용될 때, 당업계에서는 널리 이해되고 있으며, 조성물을 투여받지 않은 대상체에 비해 대상체에서 의학적 상태의 병후들의 빈도를 감소시키거나 또는 그의 안착을 지연시키는 조성물의 투여를 포함한다. 따라서, 암 예방은, 예를 들어 통계적으로 및/또는 임상적으로 유의한 양에 의한 미치료 대조군 집단에 비해 예방 치료를 받은 환자의 집단에서 검출가능한 암 성장 개체수 감소 및/또는 미치료 대조군 집단에 비해 치료 집단에서 검출가능한 암 성장의 출현 지연을 포함한다. 감염 예방에는, 예를 들어 미치료 대조군 집단에 비해 치료 집단에서의 감염 진단 횟수 감소 및/또는 미치료 대조군 집단에 비해 치료 집단에서의 감염 병후 안착의 지연을 포함한다. 통증 예방에는, 예를 들어 미치료 대조군 집단 대비 치료 집단에서의 대상체가 경험하는 통증 감각 확대의 감소 또는 대안적으로 그의 지연을 포함한다.
용어 "치료", "치료함", "치료하다" 등은 원하는 약학적 및/또는 생리학적 유효성을 수득하는 것을 지칭한다. 유효성은 질환 또는 그의 병후를 완전히 또는 부분적으로 예방함에 있는 예방에 있을 수 있고/있거나 질환에 대한 부분적 또는 완전한 치료 측면에서의 치료 및/또는 질환에 부여가능한 부정적 영향력에 있을 수 있다.
"치료" 는, 본원에 사용된 바와 같이, 포유류, 특히 인간에서의 질환의 임의의 치료를 포괄하며, 하기를 포함한다: (a) 해당 질환 체질이나, 그것을 가진 것으로 아직 진단되지는 않은 대상체에서 질환이 발병하는 것을 예방함; (b) 질환을 억제함, 즉 그의 발생을 정지시킴; 및 (c) 질환을 완화함, 즉 질환의 퇴행을 야기함 및/또는 하나 이상의 질환 병후를 완화함. "치료" 는 또한, 심지어는 질환 또는 상태가 부재할 때에도, 약학적 유효성을 제공하기 위한 약제의 전달을 포함하는 것을 의미한다. 예를 들어, "치료" 는 대상체에서의 증강되거나 또는 바람직한 유효성 (예를 들어, 병원 부담의 감소, 대상체의 생리학적 파라미터에서의 유익한 증가, 질환 병후의 감소 등) 을 제공할 수 있는 수용체 조절제의 전달을 포함한다.
본 출원을 통틀어, 다양한 출판물이 언급된다. 상기 출판물은 그의 전체가 본원에 참고문헌으로 포함되어, 본 출원이 관련된 당업계의 현황을 더욱 완전하게 기재한다. 개시된 참고문헌들은 또한, 해당 참고문헌을 필요로 하는 문장에서 논의되는 곳에 포함된 자료에 대해 본원에 참고문헌으로 개별적으로 분명히 포함된다.
하기의 화학 체계는 본 개시내용의 범위를 기술하고 실현가능케 하며, 본 개시내용의 화합물을 포함하는 단위체를 특정하여 지시하고 명백하게 청구하기 위해 본 명세서를 통틀어 사용되나, 달리 특정하여 정의되지 않는 한, 본원에 사용된 해당 용어들은 당업자의 것과 동일하다. 용어 "히드로카르빌" 은 임의의 탄소 원자-기재 단위체 (유기 분자) 를 뜻하며, 상기 단위체는 무기 원자 함유 염, 특히 카르복실레이트 염, 4 차 암모늄 염을 포함하는하나 이상의 유기 관능기를 선택적으로 포함한다. 광의의 의미에서, 용어 "히드로카르빌" 은 히드로카르빌 단위체를 고리형 및 비-고리형 클래스로 분류하기 위해 사용되는 용어의 클래스 "비고리형 히드로카르빌" 및 "고리형 히드로카르빌" 의 것이다.
하기 정의와 관련하여, "고리형 히드로카르빌" 단위체는 고리 내에 오직 탄소 원자만을 포함 (즉, 카르보고리형 및 아릴 고리) 할 수 있거나, 또는 고리 내에 하나 이상의 헤테로원자를 포함 (즉, 복소환 및 헤테로아릴 고리) 할 수 있다. "카르보고리형" 고리에 대해, 고리 내 최소 탄소 원자 갯수는 3 개이다; 시클로프로필. "아릴" 고리에 대해, 고리 내 최소 탄소 원자 갯수는 6 개이다; 페닐. "복소환" 고리에 대해, 고리 내 최소 탄소 원자 갯수는 1 개이다; 디아지리닐. 에틸렌 옥시드는 2 개의 탄소 원자를 포함하며, C2 복소환이다. "헤테로아릴" 고리에 대해, 고리 내 최소 탄소 원자 갯수는 1 개이다; 1,2,3,4-테트라졸릴. 하기는 본원에 사용된 용어 "비고리형 히드로카르빌" 및 "고리형 히드로카르빌" 의 비제한적 설명이다.
A. 치환 및 비치환 비고리형 히드로카르빌:
본 개시내용의 목적을 위해, 용어 "치환 및 비치환 비고리형 히드로카르빌" 은 3 가지 단위체 카테고리를 포함한다:
1) 선형 또는 분지형 알킬, 그의 비제한적 예시에는, 메틸 (C1), 에틸 (C2), n-프로필 (C3), 이소-프로필 (C3), n-부틸 (C4), sec-부틸 (C4), 이소-부틸 (C4), tert-부틸 (C4) 등이 포함됨; 치환 선형 또는 분지형 알킬, 그의 비제한적 예시에는, 히드록시메틸 (C1), 클로로메틸 (C1), 트리플루오로메틸 (C1), 아미노메틸 (C1), 1-클로로에틸 (C2), 2-히드록시에틸 (C2), 1,2-디플루오로에틸 (C2), 3-카르복시프로필 (C3) 등이 포함됨.
2) 선형 또는 분지형 알케닐, 그의 비제한적 예시에는 에테닐 (C2), 3-프로페닐 (C3), 1-프로페닐 (또한, 2-메틸에테닐) (C3), 이소프로페닐 (또한, 2-메틸에텐-2-일) (C3), 부텐-4-일 (C4) 등이 포함됨; 치환 선형 또는 분지형 알케닐, 그의 비제한적 예시에는 2-클로로에테닐 (또한, 2-클로로비닐) (C2), 4-히드록시부텐-1-일 (C4), 7-히드록시-7-메틸옥트-4-엔-2-일 (C8), 7-히드록시-7-메틸옥트-3,5-디엔-2-일 (C9), 등이 포함됨.
3) 선형 또는 분지형 알키닐, 그의 비제한적 예시에는 에티닐 (C2), 프로프-2-이닐 (또한, 프로파르길) (C3), 프로핀-1-일 (C3), 및 2-메틸-헥스-4-인-1-일 (C7) 이 포함됨; 치환 선형 또는 분지형 알키닐, 그의 비제한적 예시에는 5-히드록시-5-메틸헥스-3-이닐 (C7), 6-히드록시-6-메틸헵트-3-인-2-일 (C8), 5-히드록시-5-에틸헵트-3-이닐 (C9) 등이 포함됨.
B. 치환 및 비치환 고리형 히드로카르빌:
본 개시내용의 목적을 위해, 용어 "치환 및 비치환 고리형 히드로카르빌" 은 5 가지 단위체 카테고리를 포함한다:
1) 용어 "카르보고리형" 은 "3 내지 20 개의 탄소 원자를 포함하는 고리로서, 상기 고리가 포함하는 원자들은 탄소 원자로 한정되고, 추가로 각 고리는 하나 이상의 수소 원자를 대체할 수 있는 하나 이상의 잔기로 독립적으로 치환될 수 있는 고리" 로 정의된다. 하기는 하기의 단위체 카테고리를 포함하는 "치환 및 비치환 카르보고리형 고리" 의 비제한적 예시이다:
i) 단일 치환 또는 비치환 탄화수소 고리를 가진 카르보고리형 고리, 그의 비제한적 예시에는 시클로프로필 (C3), 2-메틸-시클로프로필 (C3), 시클로프로페닐 (C3), 시클로부틸 (C4), 2,3-디히드록시시클로부틸 (C4), 시클로부테닐 (C4), 시클로펜틸 (C5), 시클로펜테닐 (C5), 시클로펜타디에닐 (C5), 시클로헥실 (C6), 시클로헥세닐 (C6), 시클로헵틸 (C7), 시클로옥타닐 (C8), 2,5-디메틸시클로펜틸 (C5), 3,5-디클로로시클로헥실 (C6), 4-히드록시시클로헥실 (C6), 및 3,3,5-트리메틸시클로헥스-1-일 (C6) 이 포함됨.
ii) 2 개 이상의 치환 또는 비치환 융합 탄화수소 고리를 가진 카르보고리형 고리, 그의 예시에는 옥타히드로펜타레닐 (C8), 옥타히드로-1H-인데닐 (C9), 3a,4,5,6,7,7a-헥사히드로-3H-인덴-4-일 (C9), 데카히드로아줄레닐 (C10) 이 포함됨.
iii) 치환 또는 비치환 비고리형 탄화수소인 카르보고리형 고리, 그의 예시에는 비시클로-[2.1.1]헥사닐, 비시클로[2.2.1]헵타닐, 비시클로[3.1.1]헵타닐, 1,3-디메틸[2.2.1]헵탄-2-일, 비시클로[2.2.2]옥타닐, 및 비시클로[3.3.3]운데카닐이 포함됨.
2) 용어 "아릴" 은 "하나 이상의 페닐 또는 나프틸 고리를 포함하는 단위체로서, 여기서 헤테로아릴이나 복소환 고리가 전혀 페닐 또는 나프틸 고리에 융합되어 있지 않고, 추가로 각 고리는 하나 이상의 수소 원자를 대체할 수 있는 하나 이상의 잔기로 독립적으로 치환될 수 있는 단위체" 로 정의된다. 하기는 하기 단위체 카테고리를 포함하는 "치환 및 비치환 아릴 고리" 의 비제한적 예시이다:
i) C6 또는 C10 치환 또는 비치환 아릴 고리; 치환 또는 비치환인 페닐 및 나프틸 고리, 그의 비제한적 예시에는 페닐 (C6), 나프틸렌-1-일 (C10), 나프틸렌-2-일 (C10), 4-플루오로페닐 (C6), 2-히드록시페닐 (C6), 3-메틸페닐 (C6), 2-아미노-4-플루오로페닐 (C6), 2-(N,N-디에틸아미노)페닐 (C6), 2-시아노페닐 (C6), 2,6-디-tert-부틸페닐 (C6), 3-메톡시페닐 (C6), 8-히드록시나프틸렌-2-일 (C10), 4,5-디메톡시나프틸렌-1-일 (C10), 및 6-시아노-나프틸렌-1-일 (C10) 이 포함됨.
ii) C8 내지 C2O 고리 시스템을 수득하기 위해 1 또는 2 개의 포화 고리에 융합된 C6 또는 C10 아릴 고리, 그의 비제한적 예시에는 비시클로[4.2.0]옥타-1,3,5-트리에닐 (C8), 및 인다닐 (C9) 이 포함됨.
3) 용어 "복소환" 및/또는 "헤테로싸이클" 은 "3 내지 20 개의 원자를 가진 하나 이상의 고리를 포함하는 단위체로서, 여기서 하나 이상의 고리 내의 하나 이상의 원자는 질소 (N), 산소 (O), 또는 황 (S) 으로부터 선택되는 헤테로원자, 또는 N, O, 및 S 의 혼합물이고, 여기서 추가로 헤테로원자를 포함하는 고리는 또한 방향족 고리가 아닌 단위체" 로 정의된다. 하기는 하기의 단위체 카테고리를 포함하는 "치환 및 비치환 복소환 고리" 의 비제한적 예시이다:
i) 하나 이상의 헤테로원자를 포함하는 단일 고리를 가진 복소환 단위체, 그의 예시에는 디아지리닐 (C1), 아지리디닐 (C2), 우라졸릴 (C2), 아제티디닐 (C3), 피라졸리디닐 (C3), 이미다졸리디닐 (C3), 옥사졸리디닐 (C3), 이속사졸리닐 (C3), 티아졸리디닐 (C3), 이소티아졸리닐 (C3), 옥사티아졸리디니노닐 (C3), 옥사졸리디노닐 (C3), 히단토이닐 (C3), 테트라히드로푸라닐 (C4), 피롤리디닐 (C4), 모르폴리닐 (C4), 피페라지닐 (C4), 피페리디닐 (C4), 디히드로피라닐 (C5), 테트라히드로피라닐 (C5), 피페리딘-2-오닐 (발레로락탐) (C5), 2,3,4,5-테트라히드로-1H-아제피닐 (C6), 2,3-디히드로-1H-인돌 (C8), 및 1,2,3,4-테트라히드로퀴놀린 (C9) 이 포함된다.
ii) 복소환 고리인 2 개 이상의 고리를 가진 복소환 단위체, 그의 비제한적 예시에는 헥사히드로-1H-피롤리지닐 (C7), 3a,4,5,6,7,7a-헥사히드로-1H-벤조[d]이미다졸릴 (C7), 3a,4,5,6,7,7a-헥사히드로-1H-인돌릴 (C8), 1,2,3,4-테트라히드로퀴놀리닐 (C9), 및 데카히드로-1H-시클로옥타[b]피롤릴 (C10) 이 포함된다.
4) 용어 "헤테로아릴" 은 "5 내지 20 개의 원자를 포함하는 하나 이상의 고리를 포함하고, 여기서 하나 이상의 고리 내의 하나 이상의 원자가 질소 (N), 산소 (O), 또는 황 (S) 으로부터 선택되는 헤테로원자, 또는 N, O 및 S 의 혼합물이고, 여기서 추가로 헤테로원자를 포함하는 하나 이상의 고리가 방향족 고리인 것" 으로 정의된다. 하기는 하기의 단위체 카테고리를 포함하는 "치환 및 비치환 복소환 고리" 의 비제한적 예시이다:
i) 단일 고리를 포함하는 헤테로아릴 고리, 그의 비제한적 예시에는 1,2,3,4-테트라졸릴 (C1), [1,2,3]트리아졸릴 (C2), [1,2,4]트리아졸릴 (C2), 트리아지닐 (C3), 티아졸릴 (C3), 1H-이미다졸릴 (C3), 옥사졸릴 (C3), 이속사졸릴 (C3), 이소티아졸릴 (C3), 푸라닐 (C4), 티오페닐 (C4), 피리미디닐 (C4), 2-페닐피리미디닐 (C4), 피리디닐 (C5), 3-메틸피리디닐 (C5) 및 4-디메틸아미노피리디닐 (C5) 이 포함된다.
ii) 2 개 이상의 고리들 중 하나가 헤테로아릴 고리인 2 개 이상의 융합된 고리를 포함하는 헤테로아릴 고리, 그의 비제한적 예시에는 하기의 것이 포함된다: 7H-푸리닐 (C5), 9H-푸리닐 (C5), 6-아미노-9H-푸리닐 (C5), 5H-피롤로[3,2-b]피리미디닐 (C6), 7H-피롤로[2,3-d]피리미디닐 (C6), 피리도[2,3-b]피리미디닐 (C7), 2-페닐벤조[d]티아졸릴 (C7), 1H-인돌릴 (C8), 4,5,6,7-테트라히드로-1H-인돌릴 (C8), 퀴녹살리닐 (C8), 5-메틸퀴녹살리닐 (C8), 퀴나졸리닐 (C8), 퀴놀리닐 (C8), 8-히드록시-퀴놀리닐 (C8), 및 이소퀴놀리닐 (C9).
5) C1-C6 알킬렌 단위체를 거쳐 분자의 또다른 잔기 단위체 또는 코어에 연결된 C1-C6 구속 고리형 히드로카르빌 단위체 (카르보고리형 단위체, C6 또는 C10 아릴 단위체, 복소환 단위체 또는 헤테로아릴 단위체임). 구속 고리형 히드로카르빌 단위체의 비제한적 예시에는 하기 화학식을 가진 벤질 C1-(C6) 이 포함된다:
식 중, Ra 은 선택적으로는 수소에 대한 하나 이상의 독립적으로 선택된 치환기이다. 추가 예시에는 아릴 단위체, 특히 (2-히드록시페닐)헥실 C6-(C6); 나프탈렌-2-일메틸 C1-(C10), 4-플루오로벤질 C1-(C6), 2-(3-히드록시페닐)에틸 C2- (C6), 및 치환 및 비치환 C3-C1O 알킬렌카르보고리형 단위체, 예를 들어 시클로프로필메틸 C1-(C3), 시클로펜틸에틸 C2-(C5), 시클로헥실메틸 C1-(C6) 이 포함된다. 상기 카테고리에는 치환 및 비치환 C1-C10 알킬렌-헤테로아릴 단위체, 예를 들어 하기 화학식을 가진 2-피콜릴 C1-(C6) 단위체가 포함된다:
식 중, Ra 는 상기 정의된 바와 동일하다. 추가로, C1-C12 구속 고리형 히드로카르빌 단위체에는 C1-C10 알킬렌복소환 단위체 및 알킬렌-헤테로아릴 단위체가 포함되며, 그의 비제한적 예시에는 아지리디닐메틸 C1-(C2) 및 옥사졸-2-일메틸 C1-(C3) 이 포함된다.
본 개시내용의 목적을 위해, 카르보고리형 고리는 C3 내지 C20 의 것이며; 아릴 고리는 C6 또는 C10 의 것이며; 복소환 고리는 C1 내지 C9 의 것이며; 헤테로아릴 고리는 C1 내지 C9 의 것이다.
본 개시내용의 목적을 위해, 본 개시내용을 정의함에 있어서 일관성을 제공하기 위해, 단일 헤테로원자를 포함하는 융합된 고리 단위체 및 스피로고리형 고리, 비고리형 고리 등은, 당업계에서 대안적인 특징들을 가질 수도 있지만, 본원에서 헤테로원자 포함 고리에 해당하는 고리형 패밀리에 포함되는 것으로 본원에서 특징지어지고 지칭될 것이다. 예를 들어, 하기 화학식을 가진 1,2,3,4-테트라히드로퀴놀린은:
본 개시내용의 목적을 위해, 복소환 단위체로 간주된다.
하기 화학식을 가진 6,7-디히드로-tert-시클로펜타피리미딘은:
본 개시내용의 목적을 위해, 헤테로아릴 단위체로 간주된다. 융합된 고리 단위체가 포화된 고리 (복소환 고리) 및 아릴 고리 (헤테로아릴 고리) 의 두가지 모두에서 헤테로원자를 포함하는 경우, 아릴 고리가 주된 것이고, 본 개시내용을 설명하는 목적을 위해 고리가 결정되는 카테고리 타입을 결정할 것이다. 예를 들어, 하기 화학식을 가진 1,2,3,4-테트라히드로-[1,8]나프트피리딘은:
본 개시내용의 목적을 위해 헤테로아릴 단위체로 간주된다.
용어 "치환" 이 본 명세서 전체에 사용된다. 용어 "치환" 은 "치환 단위체 또는 잔기가 히드로카르빌 단위체 또는 잔기로서, 비고리형이든 고리형이든, 하기 본원에서 정의되는 치환기 또는 여러 치환기들로 대체되는 하나 이상의 수소 원자를 갖는 단위체 또는 잔기" 로 본원에서 기술되는 단위체에 적용된다. 수소 원자를 치환하는 경우 단위체는 히드로카르빌 잔기의 1 개 수소, 2 개 수소 또는 3 개 수소를 한 번에 대체할 수 있다. 추가로, 상기 치환기들은 2 개의 근접하는 탄소 상의 2 개의 수소 원자를 대체하여 상기 치환기, 신규 잔기 또는 단위체를 형성할 수 있다. 예를 들어, 단일 수소 대체를 필요로 하는 치환 단위체에는 수소, 히드록실 등이 포함된다. 2 개 수소 원자 대체에는 카르보닐, 옥시미노 등이 포함된다. 근접 탄소 원자로부터의 2 개 수소 원자 대체에는 에폭시 등이 포함된다. 3 개 수소 대체에는 시아노 등이 포함된다. 용어 치환은 히드로카르빌 잔기, 특히 방향족 고리, 알킬 사슬이 치환기에 의해 대체되는 하나 이상의 수소 원자를 가질 수 있음을 표시하기 위해 본 명세서 전체에서 사용된다. 잔기가 "치환" 으로 기재되는 경우, 임의의 갯수의 수소 원자가 대체될 수 있다. 예를 들어, 4-히드록시페닐은 "치환 방향족 카르보고리형 고리 (아릴 고리)" 이고, (N,N-디메틸-5-아미노)옥타닐은 "치환 C8 선형 알킬 단위체" 이고, 3-구아니디노프로필은 "치환 C3 선형 알킬 단위체" 이고, 2-카르복시피리디닐은 "치환 헤테로아릴 단위체" 이다.
하기는 카르보고리형, 아릴, 복소환 또는 헤테로아릴 단위체 상의 수소 원자를 치환할 수 있는 단위체의 비제한적 예시이다:
i) C1-C12 선형, 분지형 또는 고리형 알킬, 알케닐 및 알키닐; 메틸 (C1), 에틸 (C2), 에테닐 (C2), 에티닐 (C2), n-프로필 (C3), 이소-프로필 (C3), 시클로프로필 (C3), 3-프로페닐 (C3), 1-프로페닐 (또한, 2-메틸에테닐) (C3), 이소프로페닐 (또한, 2-메틸에텐-2-일) (C3), 프로프-2-이닐 (또한, 프로파르길) (C3), 프로핀-1-일 (C3), n-부틸 (C4), sec-부틸 (C4), 이소-부틸 (C4), tert-부틸 (C4), 시클로부틸 (C4), 부텐-4-일 (C4), 시클로펜틸 (C5), 시클로헥실 (C6);
ii) 치환 또는 비치환 C6 또는 C10 아릴; 예를 들어, 페닐, 나프틸 (또한, 본원에서 나프틸렌-1-일 (C10) 또는 나프틸렌-2-일 (C10) 로도 언급함);
iii) 치환 또는 비치환 C6 또는 C10 알킬렌아릴; 예를 들어, 벤질, 2-페닐에틸, 나프틸렌-2-일메틸;
iv) 치환 또는 비치환 C1-C9 복소환 고리; 하기 본원에 기재된 바와 같음;
v) 치환 또는 비치환 C1-C9 헤테로아릴 고리; 하기 본원에 기재된 바와 같음;
vi) -(CR102aR102b)aOR101; 예를 들어, -OH, -CH2OH, -OCH3, -CH2OCH3, -OCH2CH3, -CH2OCH2CH3, -OCH2CH2CH3 및 -CH2OCH2CH2CH3;
vii) -(CR102aR102b)aC(O)R101; 예를 들어, -COCH3, -CH2COCH3, -COCH2CH3, -CH2COCH2CH3, -COCH2CH2CH3, 및 -CH2COCH2CH2CH3;
viii) -(CR102aR102b)aC(O)OR101; 예를 들어, -CO2CH3, -CH2CO2CH3, -CO2CH2CH3, -CH2CO2CH2CH3, -CO2CH2CH2CH3, 및 -CH2CO2CH2CH2CH3;
ix) -(CR102aR102b)aC(O)N(R101)2; 예를 들어, -CONH2, -CH2CONH2, -CONHCH3, -CH2CONHCH3, -CON(CH3)2, 및 -CH2CON(CH3)2;
x) -(CR102aR102b)aN(R101)2; 예를 들어, -NH2, -CH2NH2, -NHCH3, -CH2NHCH3, -N(CH3)2, 및 -CH2N(CH3)2;
xi) 할로겐; -F, -Cl, -Br 및 -I;
xii) -(CR102aR102b)aCN;
xiii) -(CR102aR102b)aNO2;
xiv) -CHjXk; 식 중, X 는 할로겐이고, 지수 j 는 0 내지 2 의 정수이고, j + k = 3 임; 예를 들어, -CH2F, -CHF2, -CF3, -CCl3, 또는 -CBr3;
xv) -(CR102aR102b)aSR101; -SH, -CH2SH, -SCH3, -CH2SCH3, -SC6H5 및 -CH2SC6H5;
xvi) -(CR102aR102b)aSO2R101; 예를 들어, -SO2H, -CH2SO2H, -SO2CH3, -CH2SO2CH3, -SO2C6H5, 및 -CH2SO2C6H5; 및
xvii) -(CR102aR102b)aSO3R101; 예를 들어, -SO3H, -CH2SO3H, -SO3CH3, -CH2SO3CH3, -SO3C6H5, 및 -CH2SO3C6H5;
식 중, 각 R101 은 독립적으로 수소, 치환 또는 비치환 C1-C6 선형, 분지형 또는 고리형 알킬, 페닐, 벤질, 복소환, 또는 헤테로아릴이거나; 또는 2 개의 R101 단위체는 함께 취해져 3 내지 7 개의 원자를 포함하는 고리를 형성하고; R102a 및 R102b 는 각각 독립적으로 수소 또는 C1-C4 선형 또는 분지형 알킬이고; 지수 "a" 는 O 내지 4 이다.
본 개시내용의 목적을 위해, 용어 "화합물", "유사체" 및 "대상 화합물" 은 서로 동등하게 표시되며, 본 명세서 전체에서 호환되어 사용된다. 개시된 화합물에는 모든 거울상이성질체 형태, 부분입체이성질체 형태, 염 등이 포함된다.
본원에 개시된 화합물에는 모든 염 형태, 예를 들어 염기성 기, 특히 아민의 염 뿐 아니라 산성 기, 특히 카르복실산의 염이 포함된다. 하기는 양성자화된 염기성 기와 함께 염을 형성할 수 있는 비제한적 예시이다. 하기는 양성자화된 염기성 기와의 염을 형성할 수 있음 음이온의 비제한적 예시이다: 클로라이드, 브로마이드, 요오다이드, 설페이트, 비설페이트, 카르보네이트, 비카르보네이트, 포스페이트, 포르메이트, 아세테이트, 프로피오네이트, 부티레이트, 피루베이트, 락테이트, 옥살레이트, 말로네이트, 말레에이트, 숙시네이트, 타르트레이트, 푸마레이트, 시트레이트, 등. 하기는 산성 기의 염을 형성할 수 있는 양이온의 비제한적 예시이다: 암모늄, 나트륨, 리튬, 칼륨, 칼슘, 마그네슘, 비스무트, 라이신 등.
개시된 화합물은 화학식 (I) 을 갖는다:
식 중, 아미노 단위체를 가진 탄소 원자는 하기 화학식에 나타낸 바와 같은 (S) 입체화학을 갖는다:
R 및 Z 를 포함하는 단위체는 임의의 배치를 가진 단위체를 포함할 수 있고, 마찬가지로 개시된 화합물들은 단일 거울상이성질체, 부분입체이성질체 쌍 또는 이들의 조합일 수 있다. 추가로, 화합물들은 염 또는 수화물로 단리될 수 있다. 염의 경우, 화합물들은 1 개 초과의 양이온 또는 음이온을 포함할 수 있다. 수화물의 경우, 임의의 갯수의 물 분자, 또는 그의 분획 부분 (예를 들어, 유사체 각 몰에 대해 존재하는 1 개 미만의 물 분자) 이 존재할 수 있다.
R 단위체
R 은 하기 화학식을 가진 치환 또는 비치환 티아졸릴 단위체이다:
R2, R3 및 R4 는 매우 다양한 비-탄소 원자 포함 단위체 (예를 들어, 수소, 히드록실, 아미노, 할로겐, 니트로 등) 또는 유기 치환 단위체, 예컨대 본원에 기재된 바와 같은 치환 및 비치환 비고리형 히드로카르빌 및 고리형 히드로카르빌 단위체로부터 독립적으로 선택될 수 있는 치환기이다. 단위체를 포함하는 탄소는 1 내지 12 개의 탄소 원자, 또는 1 내지 10 개의 탄소 원자, 또는 1 내지 6 개의 탄소 원자를 포함할 수 있다.
화학식 (I) 의 화합물의 예시에는 R 단위체가 하기 화학식을 가진 티아졸-2-일 단위체인 화합물이 포함된다:
식 중, R2 및 R3 은 각각 독립적으로 하기로부터 선택되거나:
i) 수소;
ii) 치환 또는 비치환 C1-C6 선형, 분지형 또는 고리형 알킬;
iii) 치환 또는 비치환 C2-C6 선형, 분지형 또는 고리형 알케닐;
iv) 치환 또는 비치환 C2-C6 선형 또는 분지형 알키닐;
v) 치환 또는 비치환 C6 또는 C10 아릴;
vi) 치환 또는 비치환 C1-C8 헤테로아릴;
vii) 치환 또는 비치환 C1-C8 복소환; 또는
viii) R2 및 R3 가 함께 취해져 5 내지 7 개의 원자를 가진 포화 또는 불포화 고리를 형성할 수 있고; 여기서, 1 내지 3 개의 원자는 선택적으로는 산소, 질소 및 황으로부터 선택되는 헤테로원자일 수 있다.
하기는 R2 및 R3 단위체 상의 하나 이상의 수소 원자를 치환할 수 있는 단위체의 비제한적 예시이다. 하기 치환기 및 본원에 기재되지 않은 여타의 것이 각각 독립적으로 선택된다:
i) C1-C12 선형, 분지형 또는 고리형 알킬, 알케닐 및 알키닐; 메틸 (C1), 에틸 (C2), 에테닐 (C2), 에티닐 (C2), n-프로필 (C3), 이소-프로필 (C3), 시클로프로필 (C3), 3-프로페닐 (C3), 1-프로페닐 (또한, 2-메틸에테닐) (C3), 이소프로페닐 (또한, 2-메틸에텐-2-일) (C3), 프로프-2-이닐 (또한, 프로파르길) (C3), 프로핀-1-일 (C3), n-부틸 (C4), sec-부틸 (C4), 이소-부틸 (C4), tert-부틸 (C4), 시클로부틸 (C4), 부텐-4-일 (C4), 시클로펜틸 (C5), 시클로헥실 (C6);
ii) 치환 또는 비치환 C6 또는 C10 아릴; 예를 들어, 페닐, 나프틸 (또한, 본원에서는 나프틸렌-1-일 (C10) 또는 나프틸렌-2-일 (C10) 로도 언급됨);
iii) 치환 또는 비치환 C6 또는 C10 알킬렌아릴; 예를 들어, 벤질, 2-페닐에틸, 나프틸렌-2-일메틸;
iv) 치환 또는 비치환 C1-C8 복소환 고리; 본원에 기재된 바와 같음;
v) 치환 또는 비치환 C1-C8 헤테로아릴 고리; 본원에 기재된 바와 같음;
vi) -(CR21aR21b)pOR20; 예를 들어, -OH, -CH2OH, -OCH3, -CH2OCH3, -OCH2CH3, -CH2OCH2CH3, -OCH2CH2CH3, 및 -CH2OCH2CH2CH3;
vii) -(CR21aR21b)pC(O)R20; 예를 들어, -COCH3, -CH2COCH3, -COCH2CH3, -CH2COCH2CH3, -COCH2CH2CH3, 및 -CH2COCH2CH2CH3;
viii) -(CR21aR21b)pC(O)OR20; 예를 들어, -CO2CH3, -CH2CO2CH3, -CO2CH2CH3, -CH2CO2CH2CH3, -CO2CH2CH2CH3, 및 -CH2CO2CH2CH2CH3;
x) -(CR21aR21b)pC(O)N(R20)2; 예를 들어, -CONH2, -CH2CONH2, -CONHCH3, -CH2CONHCH3, -CON(CH3)2, 및 -CH2CON(CH3)2;
x) -(CR21aR21b)pN(R20)2; 예를 들어, -NH2, -CH2NH2, -NHCH3, -CH2NHCH3, -N(CH3)2, 및 -CH2N(CH3)2;
xi) 할로겐; -F, -Cl, -Br 및 -I;
xii) -(CR21aR21b)pCN;
xiii) -(CR21aR21b)pNO2;
xiv) -(CHj'Xk')hCHjXk; 식 중, X 는 할로겐이고, 지수 j 는 O 내지 2 의 정수이고, j + k = 3 이고, 지수 j' 는 O 내지 2 의 정수이고, j' + k' = 2 이고, 지수 h 는 O 내지 6 이고; 예를 들어, -CH2F, -CHF2, -CF3, -CH2CF3, -CHFCF3, -CCl3, 또는 -CBr3;
xv) -(CR21aR21b)pSR20; -SH, -CH2SH, -SCH3, -CH2SCH3, -SC6H5, 및 -CH2SC6H5;
xvi) -(CR21aR21b)pSO2R20; 예를 들어, -SO2H, -CH2SO2H, -SO2CH3, -CH2SO2CH3, -SO2C6H5, 및 -CH2SO2C6H5; 및
xvii) -(CR21aR21b)pSO3R20; 예를 들어, -SO3H, -CH2SO3H, -SO3CH3, -CH2SO3CH3, -SO3C6H5, 및 -CH2SO3C6H5;
[식 중, 각 R20 은 독립적으로 수소, 치환 또는 비치환 C1-C4 선형, 분지형 또는 고리형 알킬, 페닐, 벤질, 복소환, 또는 헤테로아릴이거나; 또는 2 개의 R20 단위체가 함께 취해져 3 내지 7 개의 원자를 포함하는 고리를 형성할 수 있고; R21a 및 R21b 는 각각 독립적으로 수소 또는 C1-C4 선형 또는 분지형 알킬이고; 지수 p 는 0 내지 4 임].
화학식 (I) 의 화합물의 예시에는 하기 화학식을 가진 R 단위체가 포함된다:
[식 중, R3 은 수소이고, R2 는 메틸 (C1), 에틸 (C2), n-프로필 (C3), 이소- 프로필 (C3), n-부틸 (C4), sec-부틸 (C4), 이소-부틸 (C4), tert-부틸 (C4), n-펜틸 (C5), 1-메틸부틸 (C5), 2-메틸부틸 (C5), 3-메틸부틸 (C5), 시클로프로필 (C3), n-헥실 (C6), 4- 메틸펜틸 (C6), 및 시클로헥실 (C6) 로부터 선택되는 단위체임].
화학식 (I) 의 화합물의 또다른 예시에는 하기 화학식을 가진 R 단위체가 포함된다:
[식 중, R2 는 메틸 (C1), 에틸 (C2), n-프로필 (C3), 이소-프로필 (C3), n-부틸 (C4), sec-부틸 (C4), 이소-부틸 (C4), 및 tert-부틸 (C4) 로부터 선택되는 단위체이고; R3 은 메틸 (C1) 또는 에틸 (C2) 로부터 선택되는 단위체임]. R 의 상기 국면의 비제한적 예시에는 4,5-디메틸티아졸-2-일, 4-에틸-5-메틸티아졸-2-일, 4-메틸-5-에틸티아졸-2-일, 및 4,5-디에틸티아졸-2-일이 포함된다.
화학식 (I) 의 화합물의 추가 예시에는 R3 이 수소이고, R2 가 치환 알킬 단위체인 R 단위체가 포함되며, 상기 치환기는 하기로부터 선택된다:
i) 할로겐: -F, -Cl, -Br 및 -I;
ii) -N(R11)2; 및
iii) -OR11;
[식 중, 각 R11 은 독립적으로 수소 또는 C1-C4 선형 또는 분지형 알킬임]. R 단위체 상의 R2 또는 R3 수소 원자를 치환할 수 있는 단위체의 비제한적 예시에는 -CH2F, -CHF2, -CF3, -CH2CF3, -CH2CH2CF3, -CH2Cl, -CH2OH, -CH2OCH3, -CH2CH2OH, -CH2CH2OCH3, -CH2NH2, -CH2NHCH3, -CH2N(CH3)2, 및 -CH2NH(CH2CH3) 가 포함된다.
R 단위체 상의 R2 또는 R3 수소 원자를 치환할 수 있는 단위체의 추가적인 비제한적 예시에는 2,2-디플루오로시클로프로필, 2-메톡시시클로헥실 및 4-클로로시클로헥실이 포함된다.
화학식 (I) 의 화합물의 추가 예시, R 단위체에는 R3 가 수소이고, R2 가 페닐 또는 치환 페닐인 단위체가 포함되며, 여기서 R2 단위체의 비제한적 예시에는 페닐, 3,4-디메틸페닐, 4-tert-부틸페닐, 4-시클로프로필페닐, 4-디에틸아미노페닐, 4-(트리플루오로메틸)페닐, 4-메톡시페닐, 4-(디플루오로메톡시)페닐, 4-(트리플루오로메톡시)페닐, 3-클로로페닐, 4-클로로페닐 및 3,4-디클로로페닐이 포함되며, 이것이 R 의 정의에 포함되는 경우, 하기의 R 단위체 4-페닐티아졸-2-일, 3,4-디메틸페닐티아졸-2-일, 4-tert-부틸페닐티아졸-2-일, 4-시클로프로필페닐티아졸-2-일, 4-디에틸아미노페닐티아졸-2-일, 4-(트리플루오로메틸)페닐티아졸-2-일, 4-메톡시페닐티아졸-2-일, 4-(디플루오로메톡시)페닐티아졸-2-일, 4-(트리플루오로메톡시)페닐티아졸-2-일, 3-클로로페닐티아졸-2-일, 4-클로로페닐티아졸-2-일 및 3,4-디클로로페닐티아졸-2-일을 제공한다.
화학식 (I) 의 화합물의 추가 예시에는 R 단위체로서, R2 가 수소, 메틸, 에틸, n-프로필, 및 이소-프로필로부터 선택되고, R3 가 페닐 또는 치환 페닐인 것이 포함된다. R 단위체의 첫번째 카테고리의 제 5 국면에 따른 R 단위체의 비제한적 예시에는 4-메틸-5-페닐티아졸-2-일 및 4-에틸-5-페닐티아졸-2-일이 포함된다.
화학식 (I) 의 화합물의 또다른 추가 예시에는, R 단위체로서 R3 이 수소이고, R2 가 1,2,3,4-테트라졸-1-일, 1,2,3,4-테트라졸-5-일, [1,2,3]트리아졸-4-일, [1,2,3]트리아졸-5-일, [1,2,4]트리아졸-4-일, [1,2,4]트리아졸-5-일, 이미다졸-2-일, 이미다졸-4-일, 피롤-2-일, 피롤-3-일, 옥사졸-2-일, 옥사졸-4-일, 옥사졸-5-일, 이속사졸-3-일, 이속사졸-4-일, 이속사졸-5-일, [1,2,4]옥사디아졸-3-일, [1,2,4]옥사디아졸-5-일, [1,3,4]옥사디아졸-2-일, 푸란-2-일, 푸란-3-일, 티오펜-2-일, 티오펜-3-일, 이소티아졸-3-일, 이소티아졸-4-일, 이소티아졸-5-일, 티아졸-2-일, 티아졸-4-일, 티아졸-5-일, [1,2,4]티아디아졸-3-일, [1,2,4]티아디아졸-5-일, 및 [1,3,4]티아디아졸-2-일로부터 선택되는 치환 또는 비치환 헤테로아릴 단위체인 단위체가 포함된다.
화학식 (I) 의 화합물의 추가적인 비제한적 예시에는 R 단위체로서, R2 이 치환 또는 비치환 티오펜-2-일, 예를 들어 티오펜-2-일, 5-클로로티오펜-2-일 및 5-메틸티오펜-2-일인 단위체가 포함된다.
화학식 (I) 의 화합물의 추가적인 예시에는 R 단위체로서, R2 이 치환 또는 비치환 티오펜-3-일, 예를 들어 티오펜-3-일, 5-클로로티오펜-3-일 및 5-메틸티오펜-3-일인 단위체가 포함된다.
화학식 (I) 의 화합물의 또다른 예시에는 R 단위체로서, R2 및 R3 가 함께 취해져 5 내지 7 개의 원자를 가진 포화 또는 불포화 고리를 형성하는 R 단위체가 포함된다. R 단위체의 첫번째 카테고리의 여섯번째 국면의 비제한적 예시에는 5,6-디히드로-4H-시클로펜타[d]티아졸-2-일 및 4,5,6,7-테트라히드로벤조[d]티아졸-2-일이 포함된다.
화학식 (I) 의 화합물의 추가 예시에는 하기 화학식을 가진 티아졸-4-일 단위체인 R 단위체가 포함된다:
[식 중, R4 는 하기로부터 선택되는 단위체임:
i) 수소;
ii) 치환 또는 비치환 C1-C6 선형, 분지형 또는 고리형 알킬;
iii) 치환 또는 비치환 C2-C6 선형, 분지형 또는 고리형 알케닐;
iv) 치환 또는 비치환 C2-C6 선형 또는 분지형 알키닐;
v) 치환 또는 비치환 C6 또는 C10 아릴;
vi) 치환 또는 비치환 C1-C9 헤테로아릴; 또는
vii) 치환 또는 비치환 C1-C9 복소환].
하기는 R4 단위체 상에서 1 개 이상의 수소 원자를 치환할 수 있는 단위체의 비제한적 예시이다. 하기 치환기들 및 여기에 기재되지 않은 기타의 것은 각각 독립적으로 하기로부터 선택된다:
i) C1-C12 선형, 분지형 또는 고리형 알킬, 알케닐, 및 알키닐; 메틸 (C1), 에틸 (C2), 에테닐 (C2), 에티닐 (C2), n-프로필 (C3), 이소-프로필 (C3), 시클로프로필 (C3), 3-프로페닐 (C3), 1-프로페닐 (또한, 2-메틸에테닐) (C3), 이소프로페닐 (또한, 2-메틸에텐-2-일) (C3), 프로프-2-이닐 (또한, 프로파르길) (C3), 프로핀-1-일 (C3), n-부틸 (C4), sec-부틸 (C4), 이소-부틸 (C4), tert-부틸 (C4), 시클로부틸 (C4), 부텐-4-일 (C4), 시클로펜틸 (C5), 시클로헥실 (C6);
ii) 치환 또는 비치환 C6 또는 C10 아릴; 예를 들어, 페닐, 나프틸 (또한, 본원에서는 나프틸렌-1-일 (C10) 또는나프틸렌-2-일 (C10) 로도 언급함);
iii) 치환 또는 비치환 C6 또는 C10 알킬렌아릴; 예를 들어, 벤질, 2-페닐에틸, 나프틸렌-2-일메틸;
iv) 치환 또는 비치환 C1-C9 복소환 고리; 하기 본원에 기재된 바와 같음;
v) 치환 또는 비치환 C1-C9 헤테로아릴 고리; 하기 본원에 기재된 바와 같음;
vi) -(CR21aR21b)pOR20; 예를 들어, -OH, -CH2OH, -OCH3, -CH2OCH3, -OCH2CH3, -CH2OCH2CH3, -OCH2CH2CH3, 및-CH2OCH2CH2CH3;
vii) -(CR21aR21b)pC(O)R20; 예를 들어, -COCH3, -CH2COCH3, -COCH2CH3, -CH2COCH2CH3, -COCH2CH2CH3, 및 -CH2COCH2CH2CH3;
viii) -(CR21aR21b)pC(O)OR20; 예를 들어, -CO2CH3, -CH2CO2CH3, -CO2CH2CH3, -CH2CO2CH2CH3, -CO2CH2CH2CH3, 및 -CH2CO2CH2CH2CH3;
xi) -(CR21aR21b)pC(O)N(R20)2; 예를 들어, -CONH2, -CH2CONH2, -CONHCH3, -CH2CONHCH3, -CON(CH3)2, 및 -CH2CON(CH3)2;
x) -(CR21aR21b)pN(R20)2; 예를 들어, -NH2, -CH2NH2, -NHCH3, -CH2NHCH3, -N(CH3)2, 및 -CH2N(CH3)2;
xi) 할로겐; -F, -Cl, -Br, 및 -I;
xii) -(CR21aR21b)pCN;
xiii) -(CR21aR21b)pNO2;
xiv) -(CHj'Xk')hCHjXk; 여기서, X 는 할로겐이고, 지수 j 는 0 내지 2 의 정수이고, j + k = 3 이고, 지수 j' 는 O 내지 2 의 정수이고, j' + k' = 2 이고, 지수 h 는 O 내지 6 임; 예를 들어, -CH2F, -CHF2, -CF3, -CH2CF3, -CHFCF3, -CCl3, 또는 -CBr3;
xv) -(CR21aR21b)pSR20; -SH, -CH2SH, -SCH3, -CH2SCH3, -SC6H5, 및 -CH2SC6H5;
xvi) -(CR21aR21b)pSO2R20; 예를 들어, -SO2H, -CH2SO2H, -SO2CH3, -CH2SO2CH3, -SO2C6H5, 및 -CH2SO2C6H5; 및
xvii) -(CR21aR21b)pSO3R20; 예를 들어, -SO3H, -CH2SO3H, -SO3CH3, -CH2SO3CH3, -SO3C6H5, 및 -CH2SO3C6H5;
[식 중, 각 R20 는 독립적으로 수소, 치환 또는 비치환 C1-C4 선형, 분지형 또는 고리형 알킬, 페닐, 벤질, 복소환, 또는 헤테로아릴이거나; 또는 2 개의 R 단위체가 함께 취해져 3 내지 7 개의 원자를 포함하는 고리를 형성하고; R21a 및 R21b 는 각각 독립적으로 수소 또는 C1-C4 선형 또는 분지형 알킬이고; 지수 p 는 0 내지 4 임].
화학식 (I) 의 화합물의 예시에는 R4 가 수소인 R 단위체가 포함된다.
화학식 (I) 의 화합물의 추가 예시에는 R4 가 메틸 (C1), 에틸 (C2), n-프로필 (C3), 이소-프로필 (C3), n-부틸 (C4), sec-부틸 (C4), 이소-부틸 (C4), 및 tert-부틸 (C4) 로부터 선택되는 단위체인 R 단위체가 포함된다. R 의 상기 국면의 비제한적 예시에는 2-메틸티아졸-4-일, 2-에틸티아졸-4-일, 2-(n-프로필)티아졸-4-일, 및 2-(이소-프로필)티아졸-4-일이 포함된다.
화학식 (I) 의 화합물의 추가 예시에는 R 단위체로서, R4 가 치환 또는 비치환 페닐인, 그의 비제한적 예시에 페닐, 2-플루오로페닐, 2-클로로페닐, 2-메틸페닐, 2-메톡시페닐, 3-플루오로페닐, 3-클로로페닐, 3-메틸페닐, 3-메톡시페닐, 4-플루오로페닐, 4-클로로페닐, 4-메틸페닐, 및 4-메톡시페닐이 포함되는 R 단위체가 포함된다.
화학식 (I) 의 화합물의 추가 예시에는 R 단위체로서, R4 가 치환 또는 비치환 헤테로아릴인, 그의 비제한적 예시에 티오펜-2-일, 티오펜-3-일, 티아졸-2-일, 티아졸-4-일, 티아졸-5-일, 2,5-디메틸티아졸-4-일, 2,4-디메틸티아졸-5-일, 4-에틸티아졸-2-일, 옥사졸-2-일, 옥사졸-4-일, 옥사졸-5-일, 및 3-메틸-1,2,4-옥사디아졸-5-일이 포함되는 R 단위체가 포함된다.
5-원 고리 R 단위체의 또다른 예시에는 하기 화학식을 가진 치환 또는 비치환 이미다졸릴 단위체가 포함된다:
이미다졸릴 R 단위체의 한가지 예시에는 하기 화학식을 가진 이미다졸-2-일 단위체가 포함된다:
식 중, R2 및 R3 은 각각 독립적으로 하기로부터 선택됨:
i) 수소;
ii) 치환 또는 비치환 C1-C6 선형, 분지형 또는 고리형 알킬;
iii) 치환 또는 비치환 C2-C6 선형, 분지형 또는 고리형 알케닐;
iv) 치환 또는 비치환 C2-C6 선형 또는 분지형 알키닐;
v) 치환 또는 비치환 C6 또는 C10 아릴;
vi) 치환 또는 비치환 C1-C8 헤테로아릴;
vii) 치환 또는 비치환 C1-C8 복소환; 또는
viii) R2 및 R3 이 함께 취해져 5 내지 7 개의 원자를 가진 포화 또는 불포화 고리를 형성하고; 여기서, 1 내지 3 개의 원자는 임의로 산소, 질소 및 황으로부터 선택되는 헤테로원자일 수 있음.
하기는 R2 및 R3 단위체 상에서 하나 이상의 수소 원자를 치환할 수 있는 단위체의 비제한적 예시이다. 하기 치환기 및 본원에 기재되지 않은 것이 각각 독립적으로 선택된다:
i) C1-C12 선형, 분지형 또는 고리형 알킬, 알케닐, 및 알키닐; 메틸 (C1), 에틸 (C2), 에테닐 (C2), 에티닐 (C2), n-프로필 (C3), 이소-프로필 (C3), 시클로프로필 (C3), 3-프로페닐 (C3), 1-프로페닐 (또한, 2-메틸에테닐) (C3), 이소프로페닐 (또한, 2-메틸에텐-2-일) (C3), 프로프-2-이닐 (또한, 프로파르길) (C3), 프로핀-1-일 (C3), n-부틸 (C4), sec-부틸 (C4), 이소-부틸 (C4), tert-부틸 (C4), 시클로부틸 (C4), 부텐-4-일 (C4), 시클로펜틸 (C5), 시클로헥실 (C6);
ii) 치환 또는 비치환 C6 또는 C10 아릴; 예를 들어, 페닐, 나프틸 (또한, 본원에서는 나프틸렌-1-일 (C10) 또는 나프틸렌-2-일 (C10) 로도 언급함);
iii) 치환 또는 비치환 C6 또는 C10 알킬렌아릴; 예를 들어, 벤질, 2-페닐에틸, 나프틸렌-2-일메틸;
iv) 치환 또는 비치환 C1-C9 복소환 고리; 본원에 기재된 바와 같음;
v) 치환 또는 비치환 C1-C9 헤테로아릴 고리; 본원에 기재된 바와 같음;
vi) -(CR21aR21b)zOR20; 예를 들어, -OH, -CH2OH, -OCH3, -CH2OCH3, -OCH2CH3, -CH2OCH2CH3, -OCH2CH2CH3, 및 -CH2OCH2CH2CH3;
vii) -(CR21aR21b)zC(O)R20; 예를 들어, -COCH3, -CH2COCH3, -COCH2CH3, -CH2COCH2CH3, -COCH2CH2CH3, 및 -CH2COCH2CH2CH3;
viii) -(CR21aR21b)zC(O)OR20; 예를 들어, -CO2CH3, -CH2CO2CH3, -CO2CH2CH3, -CH2CO2CH2CH3, -CO2CH2CH2CH3, 및 -CH2CO2CH2CH2CH3;
xii) -(CR21aR21b)zC(O)N(R20)2; 예를 들어, -CONH2, -CH2CONH2, -CONHCH3, -CH2CONHCH3, -CON(CH3)2, 및 -CH2CON(CH3)2;
x) -(CR21aR21b)zN(R20)2; 예를 들어, -NH2, -CH2NH2, -NHCH3, -CH2NHCH3, -N(CH3)2, 및 -CH2N(CH3)2;
xi) 할로겐; -F, -Cl, -Br, 및 -I;
xii) -(CR21aR21b)zCN;
xiii) -(CR21aR21b)zNO2;
xiv) -(CHj'Xk')hCHjXk; 여기서, X 는 할로겐이고, 지수 j 는 0 내지 2 의 정수이고, j + k = 3 이고, 지수 j' 는 0 내지 2 의 정수이고, j' + k' = 2 이고, 지수 h 는 0 내지 6 이고; 예를 들어, -CH2F, -CHF2, -CF3, -CH2CF3, -CHFCF3, -CCl3, 또는 -CBr3;
xv) -(CR21aR21b)zSR20; -SH, -CH2SH, -SCH3, -CH2SCH3, -SC6H5, 및 -CH2SC6H5;
xvi) -(CR21aR21b)zSO2R20; 예를 들어, -SO2H, -CH2SO2H, -SO2CH3, -CH2SO2CH3, -SO2C6H5, 및 -CH2SO2C6H5; 및
xvii) -(CR21aR21b)zSO3R20; 예를 들어, -SO3H, -CH2SO3H, -SO3CH3, -CH2SO3CH3, -SO3C6H5, 및 -CH2SO3C6H5;
[식 중, 각 R20 은 독립적으로 수소, 치환 또는 비치환 C1-C4 선형, 분지형 또는 고리형 알킬, 페닐, 벤질, 복소환, 또는 헤테로아릴이거나; 또는 2 개의 R20 단위체가 함께 취해져 3 내지 7 개의 원자를 포함하는 고리를 형성하고; R21a 및 R21b 이 각각 독립적으로 수소 또는 C1-C4 선형 또는 분지형 알킬이고; 지수 p 가 0 내지 4 임].
R 단위체의 한 예시에는 R 단위체가 하기 화학식을 갖는 화합물이 포함된다:
식 중, R3 은 수소이고, R2 는 메틸 (C1), 에틸 (C2), n-프로필 (C3), 이소- 프로필 (C3), n-부틸 (C4), sec-부틸 (C4), 이소-부틸 (C4), 및 tert-부틸 (C4) 로부터 선택되는 단위체이다.
R 단위체의 또다른 예시에는 R2 가 메틸 (C1), 에틸 (C2), n-프로필 (C3), 이소-프로필 (C3), n-부틸 (C4), sec-부틸 (C4), 이소-부틸 (C4), 및 tert-부틸 (C4) 로부터 선택되는 단위체이고; R3 가 메틸 (C1) 또는 에틸 (C2) 로부터 선택되는 단위체인 화합물이 포함된다. R 의 상기 국면의 비제한적 예시에는 4,5-디메틸이미다졸-2-일, 4-에틸-5-메틸이미다졸-2-일, 4-메틸-5-에틸이미다졸-2-일 및 4,5-디에틸이미다졸-2-일이 포함된다.
R 단위체의 예시에는 R3 이 수소이고, R2 가 하기로부터 선택되는 치환기로 치환된 알킬 단위체인 화합물이 포함된다:
i) 할로겐: -F, -Cl, -Br 및 -I;
ii) -N(R11)2; 및
iii) -OR11;
[식 중, 각 R11 는 독립적으로 수소 또는 C1-C4 선형 또는 분지형 알킬임].
R 의 상기 구현예를 포함하는 단위체의 비제한적 예시에는 하기가 포함된다: -CH2F, -CHF2, -CF3, -CH2CF3, -CH2Cl, -CH2OH, -CH2OCH3, -CH2CH2OH, -CH2CH2OCH3, - CH2NH2, -CH2NHCH3, -CH2N(CH3)2, 및 -CH2NH(CH2CH3).
R 단위체의 또다른 예시에는 R3 이 수소이고, R2 가 페닐인 단위체가 포함된다.
R 단위체의 또다른 예시에는 R3 이 수소이고, R2 가 1,2,3,4-테트라졸-1-일, 1,2,3,4-테트라졸-5-일, [1,2,3]트리아졸-4-일, [1,2,3]트리아졸-5-일, [1,2,4]트리아졸-4-일, [1,2,4]트리아졸-5-일, 이미다졸-2-일, 이미다졸-4-일, 피롤-2-일, 피롤-3-일, 옥사졸-2-일, 옥사졸-4-일, 옥사졸-5-일, 이속사졸-3-일, 이속사졸-4-일, 이속사졸-5-일, [1,2,4]옥사디아졸-3-일, [1,2,4]옥사디아졸-5-일, [1,3,4]옥사디아졸-2-일, 푸란-2-일, 푸란-3-일, 티오펜-2-일, 티오펜-3-일, 이소티아졸-3-일, 이소티아졸-4-일, 이소티아졸-5-일, 티아졸-2-일, 티아졸-4-일, 티아졸-5-일, [1,2,4]티아디아졸-3-일, [1,2,4]티아디아졸-5-일, 및 [1,3,4]티아디아졸-2-일로부터 선택되는 헤테로아릴 단위체인 단위체가 포함된다.
Z 단위체
Z 는 하기 화학식을 가진 단위체이다:
R1 은 하기로부터 선택된다:
i) 수소;
ii) 히드록실;
iii) 아미노;
iv) 치환 또는 비치환 C1-C6 선형, 분지형 또는 고리형 알킬;
v) 치환 또는 비치환 C1-C6 선형, 분지형 또는 고리형 알콕시;
vi) 치환 또는 비치환 C6 또는 C10 아릴;
vii) 치환 또는 비치환 C1-C9 복소환 고리; 또는
viii) 치환 또는 비치환 C1-C9 헤테로아릴 고리.
하기는 R1 단위체 상의 하나 이상의 수소 원자를 치환할 수 있는 단위체의 비제한적 예시이다. 하기 치환기 및 본원에 기재되지 않은 여타의 것이 각각 독립적으로 선택된다:
i) C1-C12 선형, 분지형 또는 고리형 알킬, 알케닐, 및 알키닐; 메틸 (C1), 에틸 (C2), 에테닐 (C2), 에티닐 (C2), n-프로필 (C3), 이소-프로필 (C3), 시클로프로필 (C3), 3-프로페닐 (C3), 1-프로페닐 (또한, 2-메틸에테닐) (C3), 이소프로페닐 (또한, 2-메틸에텐-2-일) (C3), 프로프-2-이닐 (또한, 프로파르길) (C3), 프로핀-1-일 (C3), n-부틸 (C4), sec-부틸 (C4), 이소-부틸 (C4), tert-부틸 (C4), 시클로부틸 (C4), 부텐-4-일 (C4), 시클로펜틸 (C5), 시클로헥실 (C6);
ii) 치환 또는 비치환 C6 또는 C10 아릴; 예를 들어, 페닐, 나프틸 (또한, 본원에서 나프틸렌-1-일 (C10) 또는 나프틸렌-2-일 (C10) 로도 언급됨);
iii) 치환 또는 비치환 C6 또는 C10 알킬렌아릴; 예를 들어, 벤질, 2-페닐에틸, 나프틸렌-2-일메틸;
iv) 치환 또는 비치환 C1-C9 복소환 고리; 본원에 기재된 바와 같음;
v) 치환 또는 비치환 C1-C9 헤테로아릴 고리; 본원에 기재된 바와 같음;
vi) -(CR31aR31b)qOR30; 예를 들어, -OH, -CH2OH, -OCH3, -CH2OCH3, -OCH2CH3, -CH2OCH2CH3, -OCH2CH2CH3, 및 -CH2OCH2CH2CH3;
vii) -(CR31aR31b)qC(O)R30; 예를 들어, -COCH3, -CH2COCH3, -COCH2CH3, -CH2COCH2CH3, -COCH2CH2CH3, 및 -CH2COCH2CH2CH3;
viii) -(CR31aR31b)qC(O)OR30; 예를 들어, -CO2CH3, -CH2CO2CH3, -CO2CH2CH3, -CH2CO2CH2CH3, -CO2CH2CH2CH3, 및 -CH2CO2CH2CH2CH3;
xiii) -(CR31aR31b)qC(O)N(R30)2; 예를 들어, -CONH2, -CH2CONH2, -CONHCH3, -CH2CONHCH3, -CON(CH3)2, 및 -CH2CON(CH3)2;
x) -(CR31aR31b)qN(R30)2; 예를 들어, -NH2, -CH2NH2, -NHCH3, -CH2NHCH3, -N(CH3)2, 및 -CH2N(CH3)2;
xi) 할로겐; -F, -Cl, -Br 및 -I;
xii) -(CR31aR31b)qCN;
xiii) -(CR31aR31b)qNO2;
xiv) -(CHj'Xk')hCHjXk; 여기서, X 는 할로겐이고, 지수 j 는 0 내지 2 의 정수이고, j + k = 3 이고, 지수 j' 는 0 내지 2 의 정수이고, j' + k' = 2 이고, 지수 h 는 O 내지 6 임; 예를 들어, -CH2F, -CHF2, -CF3, -CH2CF3, -CHFCF3, -CCl3, 또는 -CBr3;
xv) -(CR31aR31b)qSR30; -SH, -CH2SH, -SCH3, -CH2SCH3, -SC6H5, 및 CH2SC6H5;
xvi) -(CR31aR31b)qSO2R30; 예를 들어, -SO2H, -CH2SO2H, -SO2CH3, CH2SO2CH3, -SO2C6H5, 및 -CH2SO2C6H5; 및
xvii) -(CR31aR31b)qSO3R30; 예를 들어, -SO3H, -CH2SO3H, -SO3CH3, CH2SO3CH3, -SO3C6H5 및 -CH2SO3C6H5;
[식 중, 각 R30 은 독립적으로 수소, 치환 또는 비치환 C1-C6 선형, 분지형 또는 고리형 알킬, 페닐, 벤질, 복소환, 또는 헤테로아릴이거나; 또는 2 개의 R30 단위체는 함께 취해져 3 내지 7 개의 원자를 포함하는 고리를 형성할 수 있고; R31a 및 R31b 는 각각 독립적으로 수소 또는 C1-C4 선형 또는 분지형 알킬이고; 지수 q 는 O 내지 4 임.
R1 단위체의 한 예시에는 치환 또는 비치환 페닐 (C6 아릴) 단위체로서, 각 치환기가 하기로부터 독립적으로 선택되고: 할로겐, C1-C4 선형, 분지형 알킬 또는 고리형 알킬, -OR11, -CN, -N(R11)2-CO2R11, -C(O)N(R11)2, -NR11C(O)R11, -NO2 및 - SO2R11; 각 R11 이 수소; 치환 또는 비치환 C1-C4 선형, 분지형, 고리형 알킬, 알케닐, 또는 알키닐; 치환 또는 비치환 페닐 또는 벤질이거나; 또는 2 개의 R11 단위체가 함께 취해져 3 내지 7 개의 원자를 포함하는 고리를 형성할 수 있는 단위체가 포함된다.
R1 단위체의 또다른 예시에는 페닐, 2-플루오로페닐, 3-플루오로페닐, 4-플루오로페닐, 2,3-디플루오로페닐, 3,4-디플루오로페닐, 3,5-디플루오로페닐, 2-클로로페닐, 3-클로로페닐, 4-클로로페닐, 2,3-디클로로페닐, 3,4-디클로로페닐, 3,5-디클로로페닐, 2-히드록시페닐, 3-히드록시페닐, 4-히드록시페닐, 2-메톡시페닐, 3-메톡시페닐, 4-메톡시페닐, 2,3-디메톡시페닐, 3,4-디메톡시페닐 및 3,5-디메톡시페닐로부터 선택되는 치환 C6 아릴 단위체가 포함된다.
R1 단위체의 또다른 예시에는 2,4-디플루오로페닐, 2,5-디플루오로페닐, 2,6-디플루오로페닐, 2,3,4-트리플루오로페닐, 2,3,5-트리플루오로페닐, 2,3,6-트리플루오로페닐, 2,4,5-트리플루오로페닐, 2,4,6-트리플루오로페닐, 2,4-디클로로페닐, 2,5-디클로로페닐, 2,6-디클로로페닐, 3,4-디클로로페닐, 2,3,4-트리클로로페닐, 2,3,5-트리클로로페닐, 2,3,6-트리클로로페닐, 2,4,5-트리클로로페닐, 3,4,5-트리클로로페닐 및 2,4,6-트리클로로페닐로부터 선택되는 치환 또는 비치환 C6 아릴 단위체가 포함된다.
R1 단위체의 또다른 추가 예시에는 2-메틸페닐, 3-메틸페닐, 4-메틸페닐, 2,3-디메틸페닐, 2,4-디메틸페닐, 2,5-디메틸페닐, 2,6-디메틸페닐, 3,4-디메틸페닐, 2,3,4-트리메틸페닐, 2,3,5-트리메틸페닐, 2,3,6-트리메틸페닐, 2,4,5-트리메틸페닐, 2,4,6-트리메틸페닐, 2-에틸페닐, 3-에틸페닐, 4-에틸페닐, 2,3-디에틸페닐, 2,4-디에틸페닐, 2,5-디에틸페닐, 2,6-디에틸페닐, 3,4-디에틸페닐, 2,3,4-트리에틸페닐, 2,3,5-트리에틸페닐, 2,3,6-트리에틸페닐, 2,4,5-트리에틸페닐, 2,4,6-트리에틸페닐, 2-이소프로필페닐, 3-이소프로필페닐, 및 4-이소프로필페닐로부터 선택되는 치환 C6 아릴 단위체가 포함된다.
R1 단위체의 또다른 추가 예시에는 2-아미노페닐, 2-(N-메틸아미노)페닐, 2-(N,N-디메틸아미노)페닐, 2-(N-에틸아미노)페닐, 2-(N,N-디에틸아미노)페닐, 3-아미노페닐, 3-(N-메틸아미노)페닐, 3-(N,N-디메틸아미노)페닐, 3-(N-에틸아미노)페닐, 3-(N,N-디에틸아미노)페닐, 4-아미노페닐, 4-(N-메틸아미노)페닐, 4-(N,N-디메틸아미노)페닐, 4-(N-에틸아미노)페닐, 및 4-(N,N-디에틸아미노)페닐로부터 선택되는 치환 C6 아릴 단위체가 포함된다.
R1 은 헤테로아릴 단위체를 포함할 수 있다. 헤테로아릴 단위체의 비제한적 예시에는 하기가 포함된다:
R1 헤테로아릴 단위체는 치환 또는 비치환일 수 있다. 수소를 치환할 수 있는 단위체의 비제한적 예시에는 하기로부터 선택되는 단위체가 포함된다:
i) C1-C6 선형, 분지형 및 고리형 알킬;
ii) 치환 또는 비치환 페닐 및 벤질;
iii) 치환 또는 비치환 C1-C8 헤테로아릴;
iv) -C(O)R9; 및
v) -NHC(O)R9;
여기서, R9 는 C1-C6 선형 및 분지형 알킬; C1-C6 선형 및 분지형 알콕시; 또는 -NHCH2C(O)R10 이고; R10 은 수소, 메틸, 에틸 및 tert-부틸로부터 선택된다.
R1 의 한 예시는 메틸, 에틸, n-프로필, 이소-프로필, n-부틸, 이소-부틸, sec-부틸, 및 tert-부틸로부터 선택되는 알킬 단위체로 치환된 단위체에 관한 것이다.
R1 의 또다른 예시에는 치환 또는 비치환 페닐 및 벤질로 치환된 단위체로서, 페닐 및 벤질 치환기가 하기의 하나 이상으로부터 선택되는 단위체가 포함된다:
i) 할로겐;
ii) C1-C3 알킬;
iii) C1-C3 알콕시;
iv) -CO2R11; 및
v) -NHCOR16;
[식 중, R11 및 R16 은 각각 독립적으로 수소, 메틸 또는 에틸임].
R1 의 또다른 예시는 화학식 -C(O)R9 을 가진 카르복시 단위체로 치환된 페닐 및 벤질 단위체로서; R9 가 메틸, 메톡시, 에틸 및 에톡시로부터 선택되는 단위체가 포함된다.
R1 의 추가 예시에는 화학식 -NHC(O)R9 을 가진 아미드 단위체로 치환된 페닐 및 벤질 단위체로서; R9 가 메틸, 메톡시, 에틸, 에톡시, tert-부틸 및 tert-부톡시로부터 선택되는 단위체가 포함된다.
R1 의 추가 예시에는 하나 이상의 플루오로 또는 클로로 단위체로 치환된 페닐 및 벤질 단위체가 포함된다.
L 단위체
L 은 지수 n 이 1 일 때 존재하나, 지수 n 이 0 일 때는 부재하는 연결 단위체이다. L 단위체는 하기 화학식을 갖는다:
-[Q]y[C(R5aR5b)]x[Q1]z[C(R6aR6b)]w-
식 중, Q 및 Q1 은 각각 독립적으로 하기의 것이다:
i) -C(O)-;
ii) -NH-;
iii) -C(O)NH-;
iv) -NHC(O)-;
v) -NHC(O)NH-;
vi) -NHC(O)O-;
vii) -C(O)O-;
viii) -C(O)NHC(O)-;
ix) -0-;
x) -S-;
xi) -SO2-;
xii) -C(=NH)-;
xiii) -C(=NH)NH-;
xiv) -NHC(=NH)-; 또는
xv) -NHC(=NH)NH-.
지수 y 가 1 인 경우, Q 는 존재한다. 지수 y 가 O 인 경우, Q 는 부재한다. 지수 z 이 1 인 경우, Q1 은 존재한다. 지수 z 이 0 인 경우, Q1 는 부재한다.
R5a 및 R5b 는 각각 독립적으로 하기이다:
i) 수소;
ii) 히드록시;
iii) 할로겐;
iv) C1-C6 치환 또는 비치환 선형 또는 분지형 알킬; 또는
v) 하기 화학식을 가진 단위체:
-[C(R7aR7b)]tR8
식 중, R7a 및 R7b 은 각각 독립적으로 하기이다:
i) 수소; 또는
ii) 치환 또는 비치환 C1-C6 선형, 분지형 또는 고리형 알킬.
R8 은 하기의 것이다:
i) 수소;
ii) 치환 또는 비치환 C1-C6 선형, 분지형 또는 고리형 알킬;
iii) 치환 또는 비치환 C6 또는 C10 아릴;
iv) 치환 또는 비치환 C1-C9 헤테로아릴; 또는
v) 치환 또는 비치환 C1-C9 복소환.
R6a 및 R6b 은 각각 독립적으로 하기이다:
i) 수소; 또는
ii) C1-C4 선형 또는 분지형 알킬.
지수 t, w 및 x 는 각각 독립적으로 0 내지 4 이다.
하기는 R5a, R5b, R7a, R7b 및 R8 단위체 상에서 하나 이상의 수소 원자를 치환할 수 있는 단위체의 비제한적 예시이다. 하기 치환기 및 본원에 기재되지 않은 여타의 것이 각각 독립적으로 선택된다:
i) C1-C12 선형, 분지형 또는 고리형 알킬, 알케닐, 및 알키닐; 메틸 (C1), 에틸 (C2), 에테닐 (C2), 에티닐 (C2), n-프로필 (C3), 이소-프로필 (C3), 시클로프로필 (C3), 3-프로페닐 (C3), 1-프로페닐 (또한, 2-메틸에테닐) (C3), 이소프로페닐 (또한, 2-메틸에텐-2-일) (C3), 프로프-2-이닐 (또한, 프로파르길) (C3), 프로핀-1-일 (C3), n-부틸 (C4), sec-부틸 (C4), 이소-부틸 (C4), tert-부틸 (C4), 시클로부틸 (C4), 부텐-4-일 (C4), 시클로펜틸 (C5), 시클로헥실 (C6);
ii) 치환 또는 비치환 C6 또는 C10 아릴; 예를 들어, 페닐, 나프틸 (또한, 본원에서 나프틸렌-1-일 (C10) 또는 나프틸렌-2-일 (C10) 로도 언급됨);
iii) 치환 또는 비치환 C6 또는 C10 알킬렌아릴; 예를 들어, 벤질, 2-페닐에틸, 나프틸렌-2-일메틸;
iv) 치환 또는 비치환 C1-C8 복소환 고리; 하기 본원에 기재된 바와 같음;
v) 치환 또는 비치환 C1-C9 헤테로아릴 고리; 본원에 기재된 바와 같음;
vi) -(CR41aR41b)rOR40; 예를 들어, -OH, -CH2OH, -OCH3, -CH2OCH3, -OCH2CH3, -CH2OCH2CH3, -OCH2CH2CH3, 및 -CH2OCH2CH2CH3;
vii) -(CR41aR41b)rC(O)R40; 예를 들어, -COCH3, -CH2COCH3, -COCH2CH3, -CH2COCH2CH3, -COCH2CH2CH3, 및 -CH2COCH2CH2CH3;
viii) -(CR41aR41b)rC(O)OR40; 예를 들어, -CO2CH3, -CH2CO2CH3, -CO2CH2CH3, -CH2CO2CH2CH3, -CO2CH2CH2CH3, 및 -CH2CO2CH2CH2CH3;
xiv) -(CR41aR41b)rC(O)N(R40)2; 예를 들어, -CONH2, -CH2CONH2, -CONHCH3, -CH2CONHCH3, -CON(CH3)2, 및 -CH2CON(CH3)2;
x) -(CR41aR41b)rN(R40)2; 예를 들어, -NH2, -CH2NH2, -NHCH3, -CH2NHCH3, -N(CH3)2, 및 -CH2N(CH3)2;
xi) 할로겐; -F, -Cl, -Br, 및 -I;
xii) -(CR41aR41b)rCN;
xiii) -(CR41aR41b)rNO2;
xiv) -(CHj'Xk')hCHjXk; 여기서, X 는 할로겐이고, 지수 j 는 0 내지 2 의 정수이고, j + k = 3 이고, 지수 j' 은 0 내지 2 의 정수이고, j' + k' = 2 이고, 지수 h 는 O 내지 6 임; 예를 들어, -CH2F, -CHF2, -CF3, -CH2CF3, -CHFCF3, -CCl3, 또는 -CBr3;
xv) -(CR41aR41b)rSR40; -SH, -CH2SH, -SCH3, -CH2SCH3, -SC6H5, 및 -CH2SC6H5;
xvi) -(CR41aR41b)rSO2R40; 예를 들어, -SO2H, -CH2SO2H, -SO2CH3, -CH2SO2CH3, -SO2C6H5, 및 -CH2SO2C6H5; 및
xvii) -(CR41aR41b)rSO3R40; 예를 들어, -SO3H, -CH2SO3H, -SO2CH3, -CH2SO2CH3, -SO2C6H5, 및 -CH2SO2C6H5;
식 중, 각 R40 는 독립적으로 수소, 치환 또는 비치환 C1-C6 선형, 분지형 또는 고리형 알킬, 페닐, 벤질, 복소환, 또는 헤테로아릴이거나; 또는 2 개의 R40 단위체는 함께 취해져 3 내지 7 개의 원소를 포함하는 고리를 형성하고; R41a 및 R41b 는 각각 독립적으로 수소 또는 C1-C4 선형 또는 분지형 알킬이고; 지수 r 은 0 내지 4 이다.
L 단위체의 한 국면은 하기 화학식을 가진 단위체에 관한 것이다:
-C(O)[C(R5aR5b)]xNHC(O)-
식 중, R5a 는 수소, 치환 또는 비치환 C1-C4 알킬, 치환 또는 비치환 페닐, 및 치환 또는 비치환 헤테로아릴이고; 지수 x 는 1 또는 2 이다. 한 구현예는 하기 화학식을 가진 연결 단위체에 관한 것이다:
i) -C(O)[C(R5aH)]NHC(O)O-;
ii) -C(O)[C(R5aH)][CH2]NHC(O)O-;
iii) -C(O)[CH2][C(R5aH)]NHC(0)0-;
iv) -C(O)[C(R5aH)]NHC(O)-;
v) -C(O)[C(R5aH)] [CH2]NHC(O)-; 또는
vi) -C(O)[CH2] [C(R5aH)]NHC(0)-;
식 중, R5a 는 하기이다:
i) 수소;
ii) 메틸;
iii) 에틸;
iv) 이소프로필;
v) 페닐;
vi) 벤질;
vii) 4-히드록시벤질;
viii) 히드록시메틸; 또는
ix) 1-히드록시 에틸.
지수 x 가 1 인 경우, 상기 구현예는 L 단위체의 하기의 비제한적 예시를 제공한다:
지수 x 가 2 인 경우, 상기 구현예는 L 단위체의 하기의 비제한적 예시를 제공한다:
L 단위체의 또다른 예시에는 Q 가 -C(O)- 이고, 지수 x 및 z 가 0 이고, w 가 1 또는 2 이고, 첫번째 R6a 단위체가 페닐, 2-플루오로페닐, 3-플루오로페닐, 4-플루오로페닐, 2,3-디플루오로페닐, 3,4-디플루오로페닐, 3,5-디플루오로페닐, 2-클로로페닐, 3-클로로페닐, 4-클로로페닐, 2,3-디클로로페닐, 3,4-디클로로페닐, 3,5-디클로로페닐, 2-히드록시페닐, 3-히드록시페닐, 4-히드록시페닐, 2-메톡시페닐, 3-메톡시페닐, 4-메톡시페닐, 2,3-디메톡시페닐, 3,4-디메톡시페닐 및 3,5-디메톡시페닐로부터 선택되고; 두번째 R6a 단위체가 수소이고, R6b 단위체가 수소인 단위체가 포함된다. 예를 들어, 하기 화학식을 가진 연결 단위체:
L 의 상기 구현예의 추가 예시에는 상기 본원에 기재한 바와 같은 치환 또는 비치환 헤테로아릴 단위체인 상기 본원에 제시한 바와 같은 첫번째 R6a 단위체가 포함된다.
L 의 상기 구현예의 추가 예시에는 하기 화학식을 가진 단위체가 포함된다:
-C(O)[C(R6aR6b)]w-;
식 중, R6a 및 R6b 는 수소이고, 지수 w 는 1 또는 2 이고; 상기 단위체는 하기로부터 선택된다:
i) -C(O)CH2-; 및
ii) -C(O)CH2CH2-.
L 단위체의 추가 예시에는 하기 화학식을 가진 단위체가 포함된다:
-C(O)[C(R5aR5b)]xC(O)-;
식 중, R5a 및 R5b 는 수소이고, 지수 x 는 1 또는 2 이고; 상기 단위체는 하기로부터 선택된다:
i) -C(O)CH2C(O)-; 및
ii) -C(O)CH2CH2C(O)-.
L 단위체의 또다른 예시에는 하기 화학식을 가진 단위체가 포함된다:
-C(O)NH[C(R5aR5b)]x-;
식 중, R5a 및 R5b 는 수소이고, 지수 w 은 O, 1 또는 2 이고; 상기 단위체는 하기로부터 선택된다:
i) -C(O)NH-;
ii) -C(O)NHCH2-; 및
iii) -C(O)NHCH2CH2-.
L 단위체의 또다른 예시에는 하기 화학식을 가진 단위체가 포함된다:
-SO2[C(R6aR6b)]w-;
식 중, R8a 및 R8b 는 수소 또는 메틸이고, 지수 w 는 0, 1 또는 2 이고; 상기 단위체는 하기로부터 선택된다:
i) -SO2-;
ii) -SO2CH2-; 및
iii) -SO2CH2CH2-.
도 2 는 제 25 일째 마우스에서의 신장 세포 암 종양 (Renca) 부피의 히스토그램을 도시한다; 비히클 대조군 (A); 1 일 2 회 40 mg/kg 의 D91 (B); 1 일 2 회 100,000 IU/투여량의 IL-2 (C); 1 일 2 회 100,000 IU/투여량의 IL-2 및 40 mg/kg 의 D91 (D).
도 3 은 마우스에서의 B16 흑색종 종양의 종양 체적이 몇 배 증가했는지 보여주는 그래프를 도시한다; 비히클 대조군 (□); 1 일 2 회 300,000 IU/투여량의 IL-2 (◇); 1 일 2 회 300,000 IU/투여량의 IL-2 및 40 mg/kg 의 D91 (○).
도 4 는 제 22 일째 마우스에서의 B16 흑색종 종양 체적의 히스토그램을 도시한다; 비히클 대조군 (A); 1 일 2 회 300,000 IU/투여량의 IL-2 (B); 1 일 2 회 300,000 IU/투여량의 IL-2 및 40 mg/kg 의 D91 (C).
도 5 는 B16 흑색종 종양이 있는 마우스의 체중의 그래프를 도시한다; 비히클 대조군 (□); 1 일 2 회 100,000 IU/투여량의 IL-2 (◇); 1 일 2 회 300,000 IU/투여량의 IL-2 (△); 1 일 2 회 100,000 IU/투여량의 IL-2 및 40 mg/kg 의 D91 (○); 및 1 일 2 회 300,000 IU/투여량의 IL-2 및 40 mg/kg 의 D91 (■).
도 6 은 마우스에서의 B16 흑색종 종양의 종양 체적이 몇 배 증가했는지 보여주는 그래프를 도시한다; 비히클 대조군 (□); 1 일 2 회 100,000 IU/투여량의 IL-2 (◇); 및 1 일 2 회 100,000 IU/투여량의 IL-2 및 40 mg/kg 의 D91 (○).
도 7 은 제 22 일째 마우스에서의 B16 흑색종 종양 체적의 히스토그램을 도시한다; 비히클 대조군 (A); 1 일 2 회 100,000 IU/투여량의 IL-2 (B); 및 1 일 2 회 100,000 IU/투여량의 IL-2 및 40 mg/kg 의 D91 (C).
도 8 은 마우스에서의 B16 흑색종 종양의 종양 체적이 몇 배 증가했는지 보여주는 그래프를 도시한다; 비히클 대조군 (□); 및 1 일 2 회 40 mg/kg 의 D91 (○).
도 9 는 NCr nu/nu 마우스에 정위이식된 췌장 종양의 크기를 도시한다: 비히클 대조군 (◇); 100 mg/kg 겜시타빈 (gemcitabine), i.p.주 2 회 (X); 150 mg/kg 겜시타빈, i.p.주 2 회 (□); 20 mg/kg D91 1 일 2 회 (○); 100 mg/kg 겜시타빈, i.p.주 2 회 및 20 mg/kg D91 1 일 2 회 (*); 및 150 mg/kg 겜시타빈, i.p.주 2 회 및 20 mg/kg D91 1 일 2 회 (△).
상세한 설명
본 명세서 및 후속하는 특허청구범위에서, 하기의 의미를 갖는 것으로 정의되는 다수 용어를 참조한다:
모든 백분율, 비율 및 분율은 달리 명시하지 않으면 중량 기준이다.
모든 온도는 달리 명시하지 않으면 섭씨 온도 (℃) 이다.
"약제학적으로 허용되는" 은 생물학적으로 또는 그 외적으로 바람직하지 않은 것이 아닌 물질을 의미하며, 즉 해당 물질이 임상적으로 허용되지 않는 생물학적 유효성을 야기한다거나 그것이 포함되는 약제학적 조성물의 임의의 여타 구성요소들과 불리한 방식으로 상호작용하지 않으면서 관련 활성 화합물들과 함께 개체에게 투여될 수 있다.
본 명세서 및 본 명세서의 특허청구범위를 통틀어, 용어 "포함하다" 및 상기 용어의 여타 활용 형태, 예컨대 "포함함" 은, 이에 제한되지 않으나, 포함을 의미하며, 예를 들어 여타 첨가물, 구성요소, 정수 또는 단계를 배제하려는 의도의 것은 아니다.
본 명세서 및 본 명세서의 특허청구범위에서 사용된 바와 같이, 대표 단수는 해당 문맥에서 명확히 달리 언급하지 않으면, 복수 언급을 포함한다. 따라서, "조성물" 의 언급은 두가지 이상의 해당 조성물의 혼합물을 포함하며, "페닐술팜산" 의 언급은 주가지 이상의 해당 페닐술팜산의 혼합물을 포함하며, "화합물" 의 언급은 두가지 이상의 해당 화합물의 혼합물 등을 포함한다.
"선택적인" 또는 "선택적으로" 는 후속하여 기재되는 사건 또는 환경이 일어날 수도 있고, 일어나지 않을 수도 있으며, 상기 기재는 해당 사건 또는 환경이 발생하는 경우 및 발생하지 않는 경우를 포함한다.
범위는 "약" 한가지 특정 값부터 및/또는 "약" 또다른 특정 값까지로 본원에서 표현될 수 있다. 상기 범위를 표현할 경우, 또다른 국면은 한 특정 값으로부터 및/또는 다른 특정 값까지를 포함한다. 유사하게, 값들이 선행사 "약" 의 이용으로 근사값으로 표현되는 경우, 해당 특별한 값들은 또다른 국면을 형성하는 것으로 이해될 것이다. 추가로, 각 범위의 종점들은 서로 독립적으로 여타 종점에 대해 전부 유의하다는 점이 이해될 것이다. 또한, 본원에 개시된 수많은 값들이 있으며, 각각의 상기 값은 또한 그 값 자체에 추가하여 약" 해당 특별 값과 같이 본원에 개시됨을 이해해야 한다. 예를 들어, 값 "10" 이 개시된 경우, "약 10" 이 또한 개시된다. 하나의 값이 개시된 경우, 해당 값의 "미만 또는 동등", "해당 값 초과 또는 동등" 및 값들 사이의 가능한 범위들이 또한 당업자가 적절하게 이해할 수 있게 개시된다는 점이 이해될 것이다. 예를 들어, 값 "10" 이 개시된 경우, "10 이하" 뿐만 아니라 "10 이상" 이 또한 개시된다. 출원 데이터를 통틀어, 수많은 상이한 포맷의 것이 제공되며, 상기 데이터는 종점 및 출발점을 나타내고, 데이터 지점들의 임의의 조합을 범위 내에 포함한다. 예를 들어, 특정 데이터 지점 "10" 내지 특정 데이터 지점 "15" 가 개시된 경우, 10 및 15 초과, 그 이상, 그 미만, 그 이하, 및 동등한 값 뿐만 아니라 10 내지 15 도 개시된 것으로 간주된다. 두 특정 단위 사이의 각 단위가 또한 개시된다는 것이 이해된다. 예를 들어, 10 내지 15 가 개시된 경우, 11, 12, 13 및 14 가 또한 개시된다.
본원에 사용된 바와 같이, 용어 "관리하다", "관리함" 및 "관리" 는 질환 또는 질환들의 치료를 결과로 제공하지 않는 예방 또는 치료제의 투여로 환자가 얻게 되는 이익을 지칭한다. 특정 구현예에서, 대상체는 질환을 "관리" 하여 질환 또는 질환들의 진행 또는 악화를 예방하고자 하나 이상의 예방 또는 치료제를 투여받는다.
본원에 사용된 바와 같이, 용어 "예방하다", "예방함" 및 "예방" 은, 예방제의 투여로 인해 대상체에서 질환 또는 장애를 방지 또는 회피하거나 또는 장애의 하나 이상의 병후의 재발 또는 안착을 지연시키는 방법을 지칭한다.
본원에 사용된 바와 같이, 용어 "병용" 은 하나 이상의 예방 및/또는 치료제의 이용을 지칭한다. 용어 "병용" 의 이용은 장애, 예를 들어 과다증식성 세포 장애, 특히 암이 있는 대상체에 예방 및/또는 치료제를 투여하는 순서를 제한하지 않는다. 첫번째 예방 또는 치료제는, 장애가 있었거나, 있거나 또는 그렇게 되기 쉬운 대상체에 두번째 예방 또는 치료제를 투여하기 이전에 (예를 들어, 1 분, 5 분, 15 분, 30 분, 45 분, 1 시간, 2 시간, 4 시간, 6 시간, 12 시간, 24 시간, 48 시간, 72 시간, 96 시간, 1 주, 2 주, 3 주, 4 주, 5 주, 6 주, 8 주 또는 12 주 이전), 그와 동시에, 또는 그에 후속하여 (예를 들어, 1 분, 5 분, 15 분, 30 분, 45 분, 1 시간, 2 시간, 4 시간, 6 시간, 12 시간, 24 시간, 48 시간, 72 시간, 96 시간, 1 주, 2 주, 3 주, 4 주, 5 주, 6 주, 8 주 또는 12 주 후) 투여될 수 있다. 예방제 또는 치료제는 본 개시의 약제가 여타 약제와 함께 작용하여 다르게 투여되는 것보다 증대된 이익을 제공하도록 순서대로 시간 간격을 두고 대상체에 투여된다. 임의의 추가적인 예방 또는 치료제가 여타 추가적인 예방 또는 치료제와 임의의 순서로 투여될 수 있다.
본원에 사용된 바와 같이, 용어 "투여하다" 는 화합물의 투여를 기재하기 위해 사용되는 경우, 화합물의 단독 투여량 또는 다중 투여량을 의미한다.
본원에 사용된 바와 같이, 용어 "암 치료" 는, 이에 제한되지 않으나 화학요법 및 방사요법을 포함하는 당업계에 공지된 임의의 암 치료법을 의미한다.
본원에 사용된 바와 같이, "종양 세포" 는 악성 종양을 포함하여 종양으로부터 유도되는 세포 및 시험관내에서 불멸화된 세포를 전부 의미한다. "정상" 세포는 비정상적 증식을 보이지 않는 정상적인 성장 특징을 가진 세포를 지칭한다.
본원에 사용된 바와 같이, 용어 "암이 있는 것으로 밝혀진 개인" 및 "암 환자" 는 호환하여 사용되며, 암이 있는 것으로 진단된 개인을 지칭하는 것을 의미한다. 암이 있는 개인을 밝혀내기 위한 수많은 공지된 수단이 있다. 일부 구현예에서, 암 진단은 PET 영상기법을 이용해 하거나 확인한다. 본 개시의 일부 구현예는 암이 있는 개인을 밝혀내는 단계를 포함한다.
본원에 사용된 바와 같이, 용어 "치료 유효량" 은 병후를 완화 또는 예방하거나, 종양 크기를 줄이거나, 또는 치료하는 환자의 수명을 연장시키기 위해 유효한 활성제 또는 활성제 배합물의 양을 지칭하는 것을 의미한다. 치료 유효량의 결정은 특히 본원에 개시된 상세한 개시 내용의 맥락에서, 당업자의 재량에 따른다.
본원에 사용된 바와 같이, 용어 "억제하다" 또는 "억제" 는 활성에 있어서의 통계적으로 유의하고 측정가능한 감소, 바람직하게는 대조군 대비 약 10% 이상의 감소, 더욱 바람직하게는 약 50% 이상의 감소, 더욱더 바람직하게는 약 80% 이상의 감소를 지칭한다.
본원에 사용된 바와 같이, 용어 "증가하다" 또는 "강화" 는 활성에 있어서의 통계적으로 유의하고 측정가능한 증가, 바람직하게는 대조군 대비 약 10% 이상의 증가, 더욱 바람직하게는 약 50% 이상의 증가, 더욱더 바람직하게는 약 80% 이상의 증가를 지칭한다.
용어 "예방하다" 또는 "예방" 은 상태, 예컨대 국지적 재발 (예를 들어, 통증), 질환, 예컨대 암, 복합 증후군, 예컨대 심부전 또는 임의의 기타 의학적 상태와 관련하여 사용될 때, 당업계에서는 널리 이해되고 있으며, 조성물을 투여받지 않은 대상체에 비해 대상체에서 의학적 상태의 병후들의 빈도를 감소시키거나 또는 그의 안착을 지연시키는 조성물의 투여를 포함한다. 따라서, 암 예방은, 예를 들어 통계적으로 및/또는 임상적으로 유의한 양에 의한 미치료 대조군 집단에 비해 예방 치료를 받은 환자의 집단에서 검출가능한 암 성장 개체수 감소 및/또는 미치료 대조군 집단에 비해 치료 집단에서 검출가능한 암 성장의 출현 지연을 포함한다. 감염 예방에는, 예를 들어 미치료 대조군 집단에 비해 치료 집단에서의 감염 진단 횟수 감소 및/또는 미치료 대조군 집단에 비해 치료 집단에서의 감염 병후 안착의 지연을 포함한다. 통증 예방에는, 예를 들어 미치료 대조군 집단 대비 치료 집단에서의 대상체가 경험하는 통증 감각 확대의 감소 또는 대안적으로 그의 지연을 포함한다.
용어 "치료", "치료함", "치료하다" 등은 원하는 약학적 및/또는 생리학적 유효성을 수득하는 것을 지칭한다. 유효성은 질환 또는 그의 병후를 완전히 또는 부분적으로 예방함에 있는 예방에 있을 수 있고/있거나 질환에 대한 부분적 또는 완전한 치료 측면에서의 치료 및/또는 질환에 부여가능한 부정적 영향력에 있을 수 있다.
"치료" 는, 본원에 사용된 바와 같이, 포유류, 특히 인간에서의 질환의 임의의 치료를 포괄하며, 하기를 포함한다: (a) 해당 질환 체질이나, 그것을 가진 것으로 아직 진단되지는 않은 대상체에서 질환이 발병하는 것을 예방함; (b) 질환을 억제함, 즉 그의 발생을 정지시킴; 및 (c) 질환을 완화함, 즉 질환의 퇴행을 야기함 및/또는 하나 이상의 질환 병후를 완화함. "치료" 는 또한, 심지어는 질환 또는 상태가 부재할 때에도, 약학적 유효성을 제공하기 위한 약제의 전달을 포함하는 것을 의미한다. 예를 들어, "치료" 는 대상체에서의 증강되거나 또는 바람직한 유효성 (예를 들어, 병원 부담의 감소, 대상체의 생리학적 파라미터에서의 유익한 증가, 질환 병후의 감소 등) 을 제공할 수 있는 수용체 조절제의 전달을 포함한다.
본 출원을 통틀어, 다양한 출판물이 언급된다. 상기 출판물은 그의 전체가 본원에 참고문헌으로 포함되어, 본 출원이 관련된 당업계의 현황을 더욱 완전하게 기재한다. 개시된 참고문헌들은 또한, 해당 참고문헌을 필요로 하는 문장에서 논의되는 곳에 포함된 자료에 대해 본원에 참고문헌으로 개별적으로 분명히 포함된다.
하기의 화학 체계는 본 개시내용의 범위를 기술하고 실현가능케 하며, 본 개시내용의 화합물을 포함하는 단위체를 특정하여 지시하고 명백하게 청구하기 위해 본 명세서를 통틀어 사용되나, 달리 특정하여 정의되지 않는 한, 본원에 사용된 해당 용어들은 당업자의 것과 동일하다. 용어 "히드로카르빌" 은 임의의 탄소 원자-기재 단위체 (유기 분자) 를 뜻하며, 상기 단위체는 무기 원자 함유 염, 특히 카르복실레이트 염, 4 차 암모늄 염을 포함하는하나 이상의 유기 관능기를 선택적으로 포함한다. 광의의 의미에서, 용어 "히드로카르빌" 은 히드로카르빌 단위체를 고리형 및 비-고리형 클래스로 분류하기 위해 사용되는 용어의 클래스 "비고리형 히드로카르빌" 및 "고리형 히드로카르빌" 의 것이다.
하기 정의와 관련하여, "고리형 히드로카르빌" 단위체는 고리 내에 오직 탄소 원자만을 포함 (즉, 카르보고리형 및 아릴 고리) 할 수 있거나, 또는 고리 내에 하나 이상의 헤테로원자를 포함 (즉, 복소환 및 헤테로아릴 고리) 할 수 있다. "카르보고리형" 고리에 대해, 고리 내 최소 탄소 원자 갯수는 3 개이다; 시클로프로필. "아릴" 고리에 대해, 고리 내 최소 탄소 원자 갯수는 6 개이다; 페닐. "복소환" 고리에 대해, 고리 내 최소 탄소 원자 갯수는 1 개이다; 디아지리닐. 에틸렌 옥시드는 2 개의 탄소 원자를 포함하며, C2 복소환이다. "헤테로아릴" 고리에 대해, 고리 내 최소 탄소 원자 갯수는 1 개이다; 1,2,3,4-테트라졸릴. 하기는 본원에 사용된 용어 "비고리형 히드로카르빌" 및 "고리형 히드로카르빌" 의 비제한적 설명이다.
A. 치환 및 비치환 비고리형 히드로카르빌:
본 개시내용의 목적을 위해, 용어 "치환 및 비치환 비고리형 히드로카르빌" 은 3 가지 단위체 카테고리를 포함한다:
1) 선형 또는 분지형 알킬, 그의 비제한적 예시에는, 메틸 (C1), 에틸 (C2), n-프로필 (C3), 이소-프로필 (C3), n-부틸 (C4), sec-부틸 (C4), 이소-부틸 (C4), tert-부틸 (C4) 등이 포함됨; 치환 선형 또는 분지형 알킬, 그의 비제한적 예시에는, 히드록시메틸 (C1), 클로로메틸 (C1), 트리플루오로메틸 (C1), 아미노메틸 (C1), 1-클로로에틸 (C2), 2-히드록시에틸 (C2), 1,2-디플루오로에틸 (C2), 3-카르복시프로필 (C3) 등이 포함됨.
2) 선형 또는 분지형 알케닐, 그의 비제한적 예시에는 에테닐 (C2), 3-프로페닐 (C3), 1-프로페닐 (또한, 2-메틸에테닐) (C3), 이소프로페닐 (또한, 2-메틸에텐-2-일) (C3), 부텐-4-일 (C4) 등이 포함됨; 치환 선형 또는 분지형 알케닐, 그의 비제한적 예시에는 2-클로로에테닐 (또한, 2-클로로비닐) (C2), 4-히드록시부텐-1-일 (C4), 7-히드록시-7-메틸옥트-4-엔-2-일 (C8), 7-히드록시-7-메틸옥트-3,5-디엔-2-일 (C9), 등이 포함됨.
3) 선형 또는 분지형 알키닐, 그의 비제한적 예시에는 에티닐 (C2), 프로프-2-이닐 (또한, 프로파르길) (C3), 프로핀-1-일 (C3), 및 2-메틸-헥스-4-인-1-일 (C7) 이 포함됨; 치환 선형 또는 분지형 알키닐, 그의 비제한적 예시에는 5-히드록시-5-메틸헥스-3-이닐 (C7), 6-히드록시-6-메틸헵트-3-인-2-일 (C8), 5-히드록시-5-에틸헵트-3-이닐 (C9) 등이 포함됨.
B. 치환 및 비치환 고리형 히드로카르빌:
본 개시내용의 목적을 위해, 용어 "치환 및 비치환 고리형 히드로카르빌" 은 5 가지 단위체 카테고리를 포함한다:
1) 용어 "카르보고리형" 은 "3 내지 20 개의 탄소 원자를 포함하는 고리로서, 상기 고리가 포함하는 원자들은 탄소 원자로 한정되고, 추가로 각 고리는 하나 이상의 수소 원자를 대체할 수 있는 하나 이상의 잔기로 독립적으로 치환될 수 있는 고리" 로 정의된다. 하기는 하기의 단위체 카테고리를 포함하는 "치환 및 비치환 카르보고리형 고리" 의 비제한적 예시이다:
i) 단일 치환 또는 비치환 탄화수소 고리를 가진 카르보고리형 고리, 그의 비제한적 예시에는 시클로프로필 (C3), 2-메틸-시클로프로필 (C3), 시클로프로페닐 (C3), 시클로부틸 (C4), 2,3-디히드록시시클로부틸 (C4), 시클로부테닐 (C4), 시클로펜틸 (C5), 시클로펜테닐 (C5), 시클로펜타디에닐 (C5), 시클로헥실 (C6), 시클로헥세닐 (C6), 시클로헵틸 (C7), 시클로옥타닐 (C8), 2,5-디메틸시클로펜틸 (C5), 3,5-디클로로시클로헥실 (C6), 4-히드록시시클로헥실 (C6), 및 3,3,5-트리메틸시클로헥스-1-일 (C6) 이 포함됨.
ii) 2 개 이상의 치환 또는 비치환 융합 탄화수소 고리를 가진 카르보고리형 고리, 그의 예시에는 옥타히드로펜타레닐 (C8), 옥타히드로-1H-인데닐 (C9), 3a,4,5,6,7,7a-헥사히드로-3H-인덴-4-일 (C9), 데카히드로아줄레닐 (C10) 이 포함됨.
iii) 치환 또는 비치환 비고리형 탄화수소인 카르보고리형 고리, 그의 예시에는 비시클로-[2.1.1]헥사닐, 비시클로[2.2.1]헵타닐, 비시클로[3.1.1]헵타닐, 1,3-디메틸[2.2.1]헵탄-2-일, 비시클로[2.2.2]옥타닐, 및 비시클로[3.3.3]운데카닐이 포함됨.
2) 용어 "아릴" 은 "하나 이상의 페닐 또는 나프틸 고리를 포함하는 단위체로서, 여기서 헤테로아릴이나 복소환 고리가 전혀 페닐 또는 나프틸 고리에 융합되어 있지 않고, 추가로 각 고리는 하나 이상의 수소 원자를 대체할 수 있는 하나 이상의 잔기로 독립적으로 치환될 수 있는 단위체" 로 정의된다. 하기는 하기 단위체 카테고리를 포함하는 "치환 및 비치환 아릴 고리" 의 비제한적 예시이다:
i) C6 또는 C10 치환 또는 비치환 아릴 고리; 치환 또는 비치환인 페닐 및 나프틸 고리, 그의 비제한적 예시에는 페닐 (C6), 나프틸렌-1-일 (C10), 나프틸렌-2-일 (C10), 4-플루오로페닐 (C6), 2-히드록시페닐 (C6), 3-메틸페닐 (C6), 2-아미노-4-플루오로페닐 (C6), 2-(N,N-디에틸아미노)페닐 (C6), 2-시아노페닐 (C6), 2,6-디-tert-부틸페닐 (C6), 3-메톡시페닐 (C6), 8-히드록시나프틸렌-2-일 (C10), 4,5-디메톡시나프틸렌-1-일 (C10), 및 6-시아노-나프틸렌-1-일 (C10) 이 포함됨.
ii) C8 내지 C2O 고리 시스템을 수득하기 위해 1 또는 2 개의 포화 고리에 융합된 C6 또는 C10 아릴 고리, 그의 비제한적 예시에는 비시클로[4.2.0]옥타-1,3,5-트리에닐 (C8), 및 인다닐 (C9) 이 포함됨.
3) 용어 "복소환" 및/또는 "헤테로싸이클" 은 "3 내지 20 개의 원자를 가진 하나 이상의 고리를 포함하는 단위체로서, 여기서 하나 이상의 고리 내의 하나 이상의 원자는 질소 (N), 산소 (O), 또는 황 (S) 으로부터 선택되는 헤테로원자, 또는 N, O, 및 S 의 혼합물이고, 여기서 추가로 헤테로원자를 포함하는 고리는 또한 방향족 고리가 아닌 단위체" 로 정의된다. 하기는 하기의 단위체 카테고리를 포함하는 "치환 및 비치환 복소환 고리" 의 비제한적 예시이다:
i) 하나 이상의 헤테로원자를 포함하는 단일 고리를 가진 복소환 단위체, 그의 예시에는 디아지리닐 (C1), 아지리디닐 (C2), 우라졸릴 (C2), 아제티디닐 (C3), 피라졸리디닐 (C3), 이미다졸리디닐 (C3), 옥사졸리디닐 (C3), 이속사졸리닐 (C3), 티아졸리디닐 (C3), 이소티아졸리닐 (C3), 옥사티아졸리디니노닐 (C3), 옥사졸리디노닐 (C3), 히단토이닐 (C3), 테트라히드로푸라닐 (C4), 피롤리디닐 (C4), 모르폴리닐 (C4), 피페라지닐 (C4), 피페리디닐 (C4), 디히드로피라닐 (C5), 테트라히드로피라닐 (C5), 피페리딘-2-오닐 (발레로락탐) (C5), 2,3,4,5-테트라히드로-1H-아제피닐 (C6), 2,3-디히드로-1H-인돌 (C8), 및 1,2,3,4-테트라히드로퀴놀린 (C9) 이 포함된다.
ii) 복소환 고리인 2 개 이상의 고리를 가진 복소환 단위체, 그의 비제한적 예시에는 헥사히드로-1H-피롤리지닐 (C7), 3a,4,5,6,7,7a-헥사히드로-1H-벤조[d]이미다졸릴 (C7), 3a,4,5,6,7,7a-헥사히드로-1H-인돌릴 (C8), 1,2,3,4-테트라히드로퀴놀리닐 (C9), 및 데카히드로-1H-시클로옥타[b]피롤릴 (C10) 이 포함된다.
4) 용어 "헤테로아릴" 은 "5 내지 20 개의 원자를 포함하는 하나 이상의 고리를 포함하고, 여기서 하나 이상의 고리 내의 하나 이상의 원자가 질소 (N), 산소 (O), 또는 황 (S) 으로부터 선택되는 헤테로원자, 또는 N, O 및 S 의 혼합물이고, 여기서 추가로 헤테로원자를 포함하는 하나 이상의 고리가 방향족 고리인 것" 으로 정의된다. 하기는 하기의 단위체 카테고리를 포함하는 "치환 및 비치환 복소환 고리" 의 비제한적 예시이다:
i) 단일 고리를 포함하는 헤테로아릴 고리, 그의 비제한적 예시에는 1,2,3,4-테트라졸릴 (C1), [1,2,3]트리아졸릴 (C2), [1,2,4]트리아졸릴 (C2), 트리아지닐 (C3), 티아졸릴 (C3), 1H-이미다졸릴 (C3), 옥사졸릴 (C3), 이속사졸릴 (C3), 이소티아졸릴 (C3), 푸라닐 (C4), 티오페닐 (C4), 피리미디닐 (C4), 2-페닐피리미디닐 (C4), 피리디닐 (C5), 3-메틸피리디닐 (C5) 및 4-디메틸아미노피리디닐 (C5) 이 포함된다.
ii) 2 개 이상의 고리들 중 하나가 헤테로아릴 고리인 2 개 이상의 융합된 고리를 포함하는 헤테로아릴 고리, 그의 비제한적 예시에는 하기의 것이 포함된다: 7H-푸리닐 (C5), 9H-푸리닐 (C5), 6-아미노-9H-푸리닐 (C5), 5H-피롤로[3,2-b]피리미디닐 (C6), 7H-피롤로[2,3-d]피리미디닐 (C6), 피리도[2,3-b]피리미디닐 (C7), 2-페닐벤조[d]티아졸릴 (C7), 1H-인돌릴 (C8), 4,5,6,7-테트라히드로-1H-인돌릴 (C8), 퀴녹살리닐 (C8), 5-메틸퀴녹살리닐 (C8), 퀴나졸리닐 (C8), 퀴놀리닐 (C8), 8-히드록시-퀴놀리닐 (C8), 및 이소퀴놀리닐 (C9).
5) C1-C6 알킬렌 단위체를 거쳐 분자의 또다른 잔기 단위체 또는 코어에 연결된 C1-C6 구속 고리형 히드로카르빌 단위체 (카르보고리형 단위체, C6 또는 C10 아릴 단위체, 복소환 단위체 또는 헤테로아릴 단위체임). 구속 고리형 히드로카르빌 단위체의 비제한적 예시에는 하기 화학식을 가진 벤질 C1-(C6) 이 포함된다:
식 중, Ra 은 선택적으로는 수소에 대한 하나 이상의 독립적으로 선택된 치환기이다. 추가 예시에는 아릴 단위체, 특히 (2-히드록시페닐)헥실 C6-(C6); 나프탈렌-2-일메틸 C1-(C10), 4-플루오로벤질 C1-(C6), 2-(3-히드록시페닐)에틸 C2- (C6), 및 치환 및 비치환 C3-C1O 알킬렌카르보고리형 단위체, 예를 들어 시클로프로필메틸 C1-(C3), 시클로펜틸에틸 C2-(C5), 시클로헥실메틸 C1-(C6) 이 포함된다. 상기 카테고리에는 치환 및 비치환 C1-C10 알킬렌-헤테로아릴 단위체, 예를 들어 하기 화학식을 가진 2-피콜릴 C1-(C6) 단위체가 포함된다:
식 중, Ra 는 상기 정의된 바와 동일하다. 추가로, C1-C12 구속 고리형 히드로카르빌 단위체에는 C1-C10 알킬렌복소환 단위체 및 알킬렌-헤테로아릴 단위체가 포함되며, 그의 비제한적 예시에는 아지리디닐메틸 C1-(C2) 및 옥사졸-2-일메틸 C1-(C3) 이 포함된다.
본 개시내용의 목적을 위해, 카르보고리형 고리는 C3 내지 C20 의 것이며; 아릴 고리는 C6 또는 C10 의 것이며; 복소환 고리는 C1 내지 C9 의 것이며; 헤테로아릴 고리는 C1 내지 C9 의 것이다.
본 개시내용의 목적을 위해, 본 개시내용을 정의함에 있어서 일관성을 제공하기 위해, 단일 헤테로원자를 포함하는 융합된 고리 단위체 및 스피로고리형 고리, 비고리형 고리 등은, 당업계에서 대안적인 특징들을 가질 수도 있지만, 본원에서 헤테로원자 포함 고리에 해당하는 고리형 패밀리에 포함되는 것으로 본원에서 특징지어지고 지칭될 것이다. 예를 들어, 하기 화학식을 가진 1,2,3,4-테트라히드로퀴놀린은:
본 개시내용의 목적을 위해, 복소환 단위체로 간주된다.
하기 화학식을 가진 6,7-디히드로-tert-시클로펜타피리미딘은:
본 개시내용의 목적을 위해, 헤테로아릴 단위체로 간주된다. 융합된 고리 단위체가 포화된 고리 (복소환 고리) 및 아릴 고리 (헤테로아릴 고리) 의 두가지 모두에서 헤테로원자를 포함하는 경우, 아릴 고리가 주된 것이고, 본 개시내용을 설명하는 목적을 위해 고리가 결정되는 카테고리 타입을 결정할 것이다. 예를 들어, 하기 화학식을 가진 1,2,3,4-테트라히드로-[1,8]나프트피리딘은:
본 개시내용의 목적을 위해 헤테로아릴 단위체로 간주된다.
용어 "치환" 이 본 명세서 전체에 사용된다. 용어 "치환" 은 "치환 단위체 또는 잔기가 히드로카르빌 단위체 또는 잔기로서, 비고리형이든 고리형이든, 하기 본원에서 정의되는 치환기 또는 여러 치환기들로 대체되는 하나 이상의 수소 원자를 갖는 단위체 또는 잔기" 로 본원에서 기술되는 단위체에 적용된다. 수소 원자를 치환하는 경우 단위체는 히드로카르빌 잔기의 1 개 수소, 2 개 수소 또는 3 개 수소를 한 번에 대체할 수 있다. 추가로, 상기 치환기들은 2 개의 근접하는 탄소 상의 2 개의 수소 원자를 대체하여 상기 치환기, 신규 잔기 또는 단위체를 형성할 수 있다. 예를 들어, 단일 수소 대체를 필요로 하는 치환 단위체에는 수소, 히드록실 등이 포함된다. 2 개 수소 원자 대체에는 카르보닐, 옥시미노 등이 포함된다. 근접 탄소 원자로부터의 2 개 수소 원자 대체에는 에폭시 등이 포함된다. 3 개 수소 대체에는 시아노 등이 포함된다. 용어 치환은 히드로카르빌 잔기, 특히 방향족 고리, 알킬 사슬이 치환기에 의해 대체되는 하나 이상의 수소 원자를 가질 수 있음을 표시하기 위해 본 명세서 전체에서 사용된다. 잔기가 "치환" 으로 기재되는 경우, 임의의 갯수의 수소 원자가 대체될 수 있다. 예를 들어, 4-히드록시페닐은 "치환 방향족 카르보고리형 고리 (아릴 고리)" 이고, (N,N-디메틸-5-아미노)옥타닐은 "치환 C8 선형 알킬 단위체" 이고, 3-구아니디노프로필은 "치환 C3 선형 알킬 단위체" 이고, 2-카르복시피리디닐은 "치환 헤테로아릴 단위체" 이다.
하기는 카르보고리형, 아릴, 복소환 또는 헤테로아릴 단위체 상의 수소 원자를 치환할 수 있는 단위체의 비제한적 예시이다:
i) C1-C12 선형, 분지형 또는 고리형 알킬, 알케닐 및 알키닐; 메틸 (C1), 에틸 (C2), 에테닐 (C2), 에티닐 (C2), n-프로필 (C3), 이소-프로필 (C3), 시클로프로필 (C3), 3-프로페닐 (C3), 1-프로페닐 (또한, 2-메틸에테닐) (C3), 이소프로페닐 (또한, 2-메틸에텐-2-일) (C3), 프로프-2-이닐 (또한, 프로파르길) (C3), 프로핀-1-일 (C3), n-부틸 (C4), sec-부틸 (C4), 이소-부틸 (C4), tert-부틸 (C4), 시클로부틸 (C4), 부텐-4-일 (C4), 시클로펜틸 (C5), 시클로헥실 (C6);
ii) 치환 또는 비치환 C6 또는 C10 아릴; 예를 들어, 페닐, 나프틸 (또한, 본원에서 나프틸렌-1-일 (C10) 또는 나프틸렌-2-일 (C10) 로도 언급함);
iii) 치환 또는 비치환 C6 또는 C10 알킬렌아릴; 예를 들어, 벤질, 2-페닐에틸, 나프틸렌-2-일메틸;
iv) 치환 또는 비치환 C1-C9 복소환 고리; 하기 본원에 기재된 바와 같음;
v) 치환 또는 비치환 C1-C9 헤테로아릴 고리; 하기 본원에 기재된 바와 같음;
vi) -(CR102aR102b)aOR101; 예를 들어, -OH, -CH2OH, -OCH3, -CH2OCH3, -OCH2CH3, -CH2OCH2CH3, -OCH2CH2CH3 및 -CH2OCH2CH2CH3;
vii) -(CR102aR102b)aC(O)R101; 예를 들어, -COCH3, -CH2COCH3, -COCH2CH3, -CH2COCH2CH3, -COCH2CH2CH3, 및 -CH2COCH2CH2CH3;
viii) -(CR102aR102b)aC(O)OR101; 예를 들어, -CO2CH3, -CH2CO2CH3, -CO2CH2CH3, -CH2CO2CH2CH3, -CO2CH2CH2CH3, 및 -CH2CO2CH2CH2CH3;
ix) -(CR102aR102b)aC(O)N(R101)2; 예를 들어, -CONH2, -CH2CONH2, -CONHCH3, -CH2CONHCH3, -CON(CH3)2, 및 -CH2CON(CH3)2;
x) -(CR102aR102b)aN(R101)2; 예를 들어, -NH2, -CH2NH2, -NHCH3, -CH2NHCH3, -N(CH3)2, 및 -CH2N(CH3)2;
xi) 할로겐; -F, -Cl, -Br 및 -I;
xii) -(CR102aR102b)aCN;
xiii) -(CR102aR102b)aNO2;
xiv) -CHjXk; 식 중, X 는 할로겐이고, 지수 j 는 0 내지 2 의 정수이고, j + k = 3 임; 예를 들어, -CH2F, -CHF2, -CF3, -CCl3, 또는 -CBr3;
xv) -(CR102aR102b)aSR101; -SH, -CH2SH, -SCH3, -CH2SCH3, -SC6H5 및 -CH2SC6H5;
xvi) -(CR102aR102b)aSO2R101; 예를 들어, -SO2H, -CH2SO2H, -SO2CH3, -CH2SO2CH3, -SO2C6H5, 및 -CH2SO2C6H5; 및
xvii) -(CR102aR102b)aSO3R101; 예를 들어, -SO3H, -CH2SO3H, -SO3CH3, -CH2SO3CH3, -SO3C6H5, 및 -CH2SO3C6H5;
식 중, 각 R101 은 독립적으로 수소, 치환 또는 비치환 C1-C6 선형, 분지형 또는 고리형 알킬, 페닐, 벤질, 복소환, 또는 헤테로아릴이거나; 또는 2 개의 R101 단위체는 함께 취해져 3 내지 7 개의 원자를 포함하는 고리를 형성하고; R102a 및 R102b 는 각각 독립적으로 수소 또는 C1-C4 선형 또는 분지형 알킬이고; 지수 "a" 는 O 내지 4 이다.
본 개시내용의 목적을 위해, 용어 "화합물", "유사체" 및 "대상 화합물" 은 서로 동등하게 표시되며, 본 명세서 전체에서 호환되어 사용된다. 개시된 화합물에는 모든 거울상이성질체 형태, 부분입체이성질체 형태, 염 등이 포함된다.
본원에 개시된 화합물에는 모든 염 형태, 예를 들어 염기성 기, 특히 아민의 염 뿐 아니라 산성 기, 특히 카르복실산의 염이 포함된다. 하기는 양성자화된 염기성 기와 함께 염을 형성할 수 있는 비제한적 예시이다. 하기는 양성자화된 염기성 기와의 염을 형성할 수 있음 음이온의 비제한적 예시이다: 클로라이드, 브로마이드, 요오다이드, 설페이트, 비설페이트, 카르보네이트, 비카르보네이트, 포스페이트, 포르메이트, 아세테이트, 프로피오네이트, 부티레이트, 피루베이트, 락테이트, 옥살레이트, 말로네이트, 말레에이트, 숙시네이트, 타르트레이트, 푸마레이트, 시트레이트, 등. 하기는 산성 기의 염을 형성할 수 있는 양이온의 비제한적 예시이다: 암모늄, 나트륨, 리튬, 칼륨, 칼슘, 마그네슘, 비스무트, 라이신 등.
개시된 화합물은 화학식 (I) 을 갖는다:
식 중, 아미노 단위체를 가진 탄소 원자는 하기 화학식에 나타낸 바와 같은 (S) 입체화학을 갖는다:
R 및 Z 를 포함하는 단위체는 임의의 배치를 가진 단위체를 포함할 수 있고, 마찬가지로 개시된 화합물들은 단일 거울상이성질체, 부분입체이성질체 쌍 또는 이들의 조합일 수 있다. 추가로, 화합물들은 염 또는 수화물로 단리될 수 있다. 염의 경우, 화합물들은 1 개 초과의 양이온 또는 음이온을 포함할 수 있다. 수화물의 경우, 임의의 갯수의 물 분자, 또는 그의 분획 부분 (예를 들어, 유사체 각 몰에 대해 존재하는 1 개 미만의 물 분자) 이 존재할 수 있다.
R 단위체
R 은 하기 화학식을 가진 치환 또는 비치환 티아졸릴 단위체이다:
R2, R3 및 R4 는 매우 다양한 비-탄소 원자 포함 단위체 (예를 들어, 수소, 히드록실, 아미노, 할로겐, 니트로 등) 또는 유기 치환 단위체, 예컨대 본원에 기재된 바와 같은 치환 및 비치환 비고리형 히드로카르빌 및 고리형 히드로카르빌 단위체로부터 독립적으로 선택될 수 있는 치환기이다. 단위체를 포함하는 탄소는 1 내지 12 개의 탄소 원자, 또는 1 내지 10 개의 탄소 원자, 또는 1 내지 6 개의 탄소 원자를 포함할 수 있다.
화학식 (I) 의 화합물의 예시에는 R 단위체가 하기 화학식을 가진 티아졸-2-일 단위체인 화합물이 포함된다:
식 중, R2 및 R3 은 각각 독립적으로 하기로부터 선택되거나:
i) 수소;
ii) 치환 또는 비치환 C1-C6 선형, 분지형 또는 고리형 알킬;
iii) 치환 또는 비치환 C2-C6 선형, 분지형 또는 고리형 알케닐;
iv) 치환 또는 비치환 C2-C6 선형 또는 분지형 알키닐;
v) 치환 또는 비치환 C6 또는 C10 아릴;
vi) 치환 또는 비치환 C1-C8 헤테로아릴;
vii) 치환 또는 비치환 C1-C8 복소환; 또는
viii) R2 및 R3 가 함께 취해져 5 내지 7 개의 원자를 가진 포화 또는 불포화 고리를 형성할 수 있고; 여기서, 1 내지 3 개의 원자는 선택적으로는 산소, 질소 및 황으로부터 선택되는 헤테로원자일 수 있다.
하기는 R2 및 R3 단위체 상의 하나 이상의 수소 원자를 치환할 수 있는 단위체의 비제한적 예시이다. 하기 치환기 및 본원에 기재되지 않은 여타의 것이 각각 독립적으로 선택된다:
i) C1-C12 선형, 분지형 또는 고리형 알킬, 알케닐 및 알키닐; 메틸 (C1), 에틸 (C2), 에테닐 (C2), 에티닐 (C2), n-프로필 (C3), 이소-프로필 (C3), 시클로프로필 (C3), 3-프로페닐 (C3), 1-프로페닐 (또한, 2-메틸에테닐) (C3), 이소프로페닐 (또한, 2-메틸에텐-2-일) (C3), 프로프-2-이닐 (또한, 프로파르길) (C3), 프로핀-1-일 (C3), n-부틸 (C4), sec-부틸 (C4), 이소-부틸 (C4), tert-부틸 (C4), 시클로부틸 (C4), 부텐-4-일 (C4), 시클로펜틸 (C5), 시클로헥실 (C6);
ii) 치환 또는 비치환 C6 또는 C10 아릴; 예를 들어, 페닐, 나프틸 (또한, 본원에서는 나프틸렌-1-일 (C10) 또는 나프틸렌-2-일 (C10) 로도 언급됨);
iii) 치환 또는 비치환 C6 또는 C10 알킬렌아릴; 예를 들어, 벤질, 2-페닐에틸, 나프틸렌-2-일메틸;
iv) 치환 또는 비치환 C1-C8 복소환 고리; 본원에 기재된 바와 같음;
v) 치환 또는 비치환 C1-C8 헤테로아릴 고리; 본원에 기재된 바와 같음;
vi) -(CR21aR21b)pOR20; 예를 들어, -OH, -CH2OH, -OCH3, -CH2OCH3, -OCH2CH3, -CH2OCH2CH3, -OCH2CH2CH3, 및 -CH2OCH2CH2CH3;
vii) -(CR21aR21b)pC(O)R20; 예를 들어, -COCH3, -CH2COCH3, -COCH2CH3, -CH2COCH2CH3, -COCH2CH2CH3, 및 -CH2COCH2CH2CH3;
viii) -(CR21aR21b)pC(O)OR20; 예를 들어, -CO2CH3, -CH2CO2CH3, -CO2CH2CH3, -CH2CO2CH2CH3, -CO2CH2CH2CH3, 및 -CH2CO2CH2CH2CH3;
x) -(CR21aR21b)pC(O)N(R20)2; 예를 들어, -CONH2, -CH2CONH2, -CONHCH3, -CH2CONHCH3, -CON(CH3)2, 및 -CH2CON(CH3)2;
x) -(CR21aR21b)pN(R20)2; 예를 들어, -NH2, -CH2NH2, -NHCH3, -CH2NHCH3, -N(CH3)2, 및 -CH2N(CH3)2;
xi) 할로겐; -F, -Cl, -Br 및 -I;
xii) -(CR21aR21b)pCN;
xiii) -(CR21aR21b)pNO2;
xiv) -(CHj'Xk')hCHjXk; 식 중, X 는 할로겐이고, 지수 j 는 O 내지 2 의 정수이고, j + k = 3 이고, 지수 j' 는 O 내지 2 의 정수이고, j' + k' = 2 이고, 지수 h 는 O 내지 6 이고; 예를 들어, -CH2F, -CHF2, -CF3, -CH2CF3, -CHFCF3, -CCl3, 또는 -CBr3;
xv) -(CR21aR21b)pSR20; -SH, -CH2SH, -SCH3, -CH2SCH3, -SC6H5, 및 -CH2SC6H5;
xvi) -(CR21aR21b)pSO2R20; 예를 들어, -SO2H, -CH2SO2H, -SO2CH3, -CH2SO2CH3, -SO2C6H5, 및 -CH2SO2C6H5; 및
xvii) -(CR21aR21b)pSO3R20; 예를 들어, -SO3H, -CH2SO3H, -SO3CH3, -CH2SO3CH3, -SO3C6H5, 및 -CH2SO3C6H5;
[식 중, 각 R20 은 독립적으로 수소, 치환 또는 비치환 C1-C4 선형, 분지형 또는 고리형 알킬, 페닐, 벤질, 복소환, 또는 헤테로아릴이거나; 또는 2 개의 R20 단위체가 함께 취해져 3 내지 7 개의 원자를 포함하는 고리를 형성할 수 있고; R21a 및 R21b 는 각각 독립적으로 수소 또는 C1-C4 선형 또는 분지형 알킬이고; 지수 p 는 0 내지 4 임].
화학식 (I) 의 화합물의 예시에는 하기 화학식을 가진 R 단위체가 포함된다:
[식 중, R3 은 수소이고, R2 는 메틸 (C1), 에틸 (C2), n-프로필 (C3), 이소- 프로필 (C3), n-부틸 (C4), sec-부틸 (C4), 이소-부틸 (C4), tert-부틸 (C4), n-펜틸 (C5), 1-메틸부틸 (C5), 2-메틸부틸 (C5), 3-메틸부틸 (C5), 시클로프로필 (C3), n-헥실 (C6), 4- 메틸펜틸 (C6), 및 시클로헥실 (C6) 로부터 선택되는 단위체임].
화학식 (I) 의 화합물의 또다른 예시에는 하기 화학식을 가진 R 단위체가 포함된다:
[식 중, R2 는 메틸 (C1), 에틸 (C2), n-프로필 (C3), 이소-프로필 (C3), n-부틸 (C4), sec-부틸 (C4), 이소-부틸 (C4), 및 tert-부틸 (C4) 로부터 선택되는 단위체이고; R3 은 메틸 (C1) 또는 에틸 (C2) 로부터 선택되는 단위체임]. R 의 상기 국면의 비제한적 예시에는 4,5-디메틸티아졸-2-일, 4-에틸-5-메틸티아졸-2-일, 4-메틸-5-에틸티아졸-2-일, 및 4,5-디에틸티아졸-2-일이 포함된다.
화학식 (I) 의 화합물의 추가 예시에는 R3 이 수소이고, R2 가 치환 알킬 단위체인 R 단위체가 포함되며, 상기 치환기는 하기로부터 선택된다:
i) 할로겐: -F, -Cl, -Br 및 -I;
ii) -N(R11)2; 및
iii) -OR11;
[식 중, 각 R11 은 독립적으로 수소 또는 C1-C4 선형 또는 분지형 알킬임]. R 단위체 상의 R2 또는 R3 수소 원자를 치환할 수 있는 단위체의 비제한적 예시에는 -CH2F, -CHF2, -CF3, -CH2CF3, -CH2CH2CF3, -CH2Cl, -CH2OH, -CH2OCH3, -CH2CH2OH, -CH2CH2OCH3, -CH2NH2, -CH2NHCH3, -CH2N(CH3)2, 및 -CH2NH(CH2CH3) 가 포함된다.
R 단위체 상의 R2 또는 R3 수소 원자를 치환할 수 있는 단위체의 추가적인 비제한적 예시에는 2,2-디플루오로시클로프로필, 2-메톡시시클로헥실 및 4-클로로시클로헥실이 포함된다.
화학식 (I) 의 화합물의 추가 예시, R 단위체에는 R3 가 수소이고, R2 가 페닐 또는 치환 페닐인 단위체가 포함되며, 여기서 R2 단위체의 비제한적 예시에는 페닐, 3,4-디메틸페닐, 4-tert-부틸페닐, 4-시클로프로필페닐, 4-디에틸아미노페닐, 4-(트리플루오로메틸)페닐, 4-메톡시페닐, 4-(디플루오로메톡시)페닐, 4-(트리플루오로메톡시)페닐, 3-클로로페닐, 4-클로로페닐 및 3,4-디클로로페닐이 포함되며, 이것이 R 의 정의에 포함되는 경우, 하기의 R 단위체 4-페닐티아졸-2-일, 3,4-디메틸페닐티아졸-2-일, 4-tert-부틸페닐티아졸-2-일, 4-시클로프로필페닐티아졸-2-일, 4-디에틸아미노페닐티아졸-2-일, 4-(트리플루오로메틸)페닐티아졸-2-일, 4-메톡시페닐티아졸-2-일, 4-(디플루오로메톡시)페닐티아졸-2-일, 4-(트리플루오로메톡시)페닐티아졸-2-일, 3-클로로페닐티아졸-2-일, 4-클로로페닐티아졸-2-일 및 3,4-디클로로페닐티아졸-2-일을 제공한다.
화학식 (I) 의 화합물의 추가 예시에는 R 단위체로서, R2 가 수소, 메틸, 에틸, n-프로필, 및 이소-프로필로부터 선택되고, R3 가 페닐 또는 치환 페닐인 것이 포함된다. R 단위체의 첫번째 카테고리의 제 5 국면에 따른 R 단위체의 비제한적 예시에는 4-메틸-5-페닐티아졸-2-일 및 4-에틸-5-페닐티아졸-2-일이 포함된다.
화학식 (I) 의 화합물의 또다른 추가 예시에는, R 단위체로서 R3 이 수소이고, R2 가 1,2,3,4-테트라졸-1-일, 1,2,3,4-테트라졸-5-일, [1,2,3]트리아졸-4-일, [1,2,3]트리아졸-5-일, [1,2,4]트리아졸-4-일, [1,2,4]트리아졸-5-일, 이미다졸-2-일, 이미다졸-4-일, 피롤-2-일, 피롤-3-일, 옥사졸-2-일, 옥사졸-4-일, 옥사졸-5-일, 이속사졸-3-일, 이속사졸-4-일, 이속사졸-5-일, [1,2,4]옥사디아졸-3-일, [1,2,4]옥사디아졸-5-일, [1,3,4]옥사디아졸-2-일, 푸란-2-일, 푸란-3-일, 티오펜-2-일, 티오펜-3-일, 이소티아졸-3-일, 이소티아졸-4-일, 이소티아졸-5-일, 티아졸-2-일, 티아졸-4-일, 티아졸-5-일, [1,2,4]티아디아졸-3-일, [1,2,4]티아디아졸-5-일, 및 [1,3,4]티아디아졸-2-일로부터 선택되는 치환 또는 비치환 헤테로아릴 단위체인 단위체가 포함된다.
화학식 (I) 의 화합물의 추가적인 비제한적 예시에는 R 단위체로서, R2 이 치환 또는 비치환 티오펜-2-일, 예를 들어 티오펜-2-일, 5-클로로티오펜-2-일 및 5-메틸티오펜-2-일인 단위체가 포함된다.
화학식 (I) 의 화합물의 추가적인 예시에는 R 단위체로서, R2 이 치환 또는 비치환 티오펜-3-일, 예를 들어 티오펜-3-일, 5-클로로티오펜-3-일 및 5-메틸티오펜-3-일인 단위체가 포함된다.
화학식 (I) 의 화합물의 또다른 예시에는 R 단위체로서, R2 및 R3 가 함께 취해져 5 내지 7 개의 원자를 가진 포화 또는 불포화 고리를 형성하는 R 단위체가 포함된다. R 단위체의 첫번째 카테고리의 여섯번째 국면의 비제한적 예시에는 5,6-디히드로-4H-시클로펜타[d]티아졸-2-일 및 4,5,6,7-테트라히드로벤조[d]티아졸-2-일이 포함된다.
화학식 (I) 의 화합물의 추가 예시에는 하기 화학식을 가진 티아졸-4-일 단위체인 R 단위체가 포함된다:
[식 중, R4 는 하기로부터 선택되는 단위체임:
i) 수소;
ii) 치환 또는 비치환 C1-C6 선형, 분지형 또는 고리형 알킬;
iii) 치환 또는 비치환 C2-C6 선형, 분지형 또는 고리형 알케닐;
iv) 치환 또는 비치환 C2-C6 선형 또는 분지형 알키닐;
v) 치환 또는 비치환 C6 또는 C10 아릴;
vi) 치환 또는 비치환 C1-C9 헤테로아릴; 또는
vii) 치환 또는 비치환 C1-C9 복소환].
하기는 R4 단위체 상에서 1 개 이상의 수소 원자를 치환할 수 있는 단위체의 비제한적 예시이다. 하기 치환기들 및 여기에 기재되지 않은 기타의 것은 각각 독립적으로 하기로부터 선택된다:
i) C1-C12 선형, 분지형 또는 고리형 알킬, 알케닐, 및 알키닐; 메틸 (C1), 에틸 (C2), 에테닐 (C2), 에티닐 (C2), n-프로필 (C3), 이소-프로필 (C3), 시클로프로필 (C3), 3-프로페닐 (C3), 1-프로페닐 (또한, 2-메틸에테닐) (C3), 이소프로페닐 (또한, 2-메틸에텐-2-일) (C3), 프로프-2-이닐 (또한, 프로파르길) (C3), 프로핀-1-일 (C3), n-부틸 (C4), sec-부틸 (C4), 이소-부틸 (C4), tert-부틸 (C4), 시클로부틸 (C4), 부텐-4-일 (C4), 시클로펜틸 (C5), 시클로헥실 (C6);
ii) 치환 또는 비치환 C6 또는 C10 아릴; 예를 들어, 페닐, 나프틸 (또한, 본원에서는 나프틸렌-1-일 (C10) 또는나프틸렌-2-일 (C10) 로도 언급함);
iii) 치환 또는 비치환 C6 또는 C10 알킬렌아릴; 예를 들어, 벤질, 2-페닐에틸, 나프틸렌-2-일메틸;
iv) 치환 또는 비치환 C1-C9 복소환 고리; 하기 본원에 기재된 바와 같음;
v) 치환 또는 비치환 C1-C9 헤테로아릴 고리; 하기 본원에 기재된 바와 같음;
vi) -(CR21aR21b)pOR20; 예를 들어, -OH, -CH2OH, -OCH3, -CH2OCH3, -OCH2CH3, -CH2OCH2CH3, -OCH2CH2CH3, 및-CH2OCH2CH2CH3;
vii) -(CR21aR21b)pC(O)R20; 예를 들어, -COCH3, -CH2COCH3, -COCH2CH3, -CH2COCH2CH3, -COCH2CH2CH3, 및 -CH2COCH2CH2CH3;
viii) -(CR21aR21b)pC(O)OR20; 예를 들어, -CO2CH3, -CH2CO2CH3, -CO2CH2CH3, -CH2CO2CH2CH3, -CO2CH2CH2CH3, 및 -CH2CO2CH2CH2CH3;
xi) -(CR21aR21b)pC(O)N(R20)2; 예를 들어, -CONH2, -CH2CONH2, -CONHCH3, -CH2CONHCH3, -CON(CH3)2, 및 -CH2CON(CH3)2;
x) -(CR21aR21b)pN(R20)2; 예를 들어, -NH2, -CH2NH2, -NHCH3, -CH2NHCH3, -N(CH3)2, 및 -CH2N(CH3)2;
xi) 할로겐; -F, -Cl, -Br, 및 -I;
xii) -(CR21aR21b)pCN;
xiii) -(CR21aR21b)pNO2;
xiv) -(CHj'Xk')hCHjXk; 여기서, X 는 할로겐이고, 지수 j 는 0 내지 2 의 정수이고, j + k = 3 이고, 지수 j' 는 O 내지 2 의 정수이고, j' + k' = 2 이고, 지수 h 는 O 내지 6 임; 예를 들어, -CH2F, -CHF2, -CF3, -CH2CF3, -CHFCF3, -CCl3, 또는 -CBr3;
xv) -(CR21aR21b)pSR20; -SH, -CH2SH, -SCH3, -CH2SCH3, -SC6H5, 및 -CH2SC6H5;
xvi) -(CR21aR21b)pSO2R20; 예를 들어, -SO2H, -CH2SO2H, -SO2CH3, -CH2SO2CH3, -SO2C6H5, 및 -CH2SO2C6H5; 및
xvii) -(CR21aR21b)pSO3R20; 예를 들어, -SO3H, -CH2SO3H, -SO3CH3, -CH2SO3CH3, -SO3C6H5, 및 -CH2SO3C6H5;
[식 중, 각 R20 는 독립적으로 수소, 치환 또는 비치환 C1-C4 선형, 분지형 또는 고리형 알킬, 페닐, 벤질, 복소환, 또는 헤테로아릴이거나; 또는 2 개의 R 단위체가 함께 취해져 3 내지 7 개의 원자를 포함하는 고리를 형성하고; R21a 및 R21b 는 각각 독립적으로 수소 또는 C1-C4 선형 또는 분지형 알킬이고; 지수 p 는 0 내지 4 임].
화학식 (I) 의 화합물의 예시에는 R4 가 수소인 R 단위체가 포함된다.
화학식 (I) 의 화합물의 추가 예시에는 R4 가 메틸 (C1), 에틸 (C2), n-프로필 (C3), 이소-프로필 (C3), n-부틸 (C4), sec-부틸 (C4), 이소-부틸 (C4), 및 tert-부틸 (C4) 로부터 선택되는 단위체인 R 단위체가 포함된다. R 의 상기 국면의 비제한적 예시에는 2-메틸티아졸-4-일, 2-에틸티아졸-4-일, 2-(n-프로필)티아졸-4-일, 및 2-(이소-프로필)티아졸-4-일이 포함된다.
화학식 (I) 의 화합물의 추가 예시에는 R 단위체로서, R4 가 치환 또는 비치환 페닐인, 그의 비제한적 예시에 페닐, 2-플루오로페닐, 2-클로로페닐, 2-메틸페닐, 2-메톡시페닐, 3-플루오로페닐, 3-클로로페닐, 3-메틸페닐, 3-메톡시페닐, 4-플루오로페닐, 4-클로로페닐, 4-메틸페닐, 및 4-메톡시페닐이 포함되는 R 단위체가 포함된다.
화학식 (I) 의 화합물의 추가 예시에는 R 단위체로서, R4 가 치환 또는 비치환 헤테로아릴인, 그의 비제한적 예시에 티오펜-2-일, 티오펜-3-일, 티아졸-2-일, 티아졸-4-일, 티아졸-5-일, 2,5-디메틸티아졸-4-일, 2,4-디메틸티아졸-5-일, 4-에틸티아졸-2-일, 옥사졸-2-일, 옥사졸-4-일, 옥사졸-5-일, 및 3-메틸-1,2,4-옥사디아졸-5-일이 포함되는 R 단위체가 포함된다.
5-원 고리 R 단위체의 또다른 예시에는 하기 화학식을 가진 치환 또는 비치환 이미다졸릴 단위체가 포함된다:
이미다졸릴 R 단위체의 한가지 예시에는 하기 화학식을 가진 이미다졸-2-일 단위체가 포함된다:
식 중, R2 및 R3 은 각각 독립적으로 하기로부터 선택됨:
i) 수소;
ii) 치환 또는 비치환 C1-C6 선형, 분지형 또는 고리형 알킬;
iii) 치환 또는 비치환 C2-C6 선형, 분지형 또는 고리형 알케닐;
iv) 치환 또는 비치환 C2-C6 선형 또는 분지형 알키닐;
v) 치환 또는 비치환 C6 또는 C10 아릴;
vi) 치환 또는 비치환 C1-C8 헤테로아릴;
vii) 치환 또는 비치환 C1-C8 복소환; 또는
viii) R2 및 R3 이 함께 취해져 5 내지 7 개의 원자를 가진 포화 또는 불포화 고리를 형성하고; 여기서, 1 내지 3 개의 원자는 임의로 산소, 질소 및 황으로부터 선택되는 헤테로원자일 수 있음.
하기는 R2 및 R3 단위체 상에서 하나 이상의 수소 원자를 치환할 수 있는 단위체의 비제한적 예시이다. 하기 치환기 및 본원에 기재되지 않은 것이 각각 독립적으로 선택된다:
i) C1-C12 선형, 분지형 또는 고리형 알킬, 알케닐, 및 알키닐; 메틸 (C1), 에틸 (C2), 에테닐 (C2), 에티닐 (C2), n-프로필 (C3), 이소-프로필 (C3), 시클로프로필 (C3), 3-프로페닐 (C3), 1-프로페닐 (또한, 2-메틸에테닐) (C3), 이소프로페닐 (또한, 2-메틸에텐-2-일) (C3), 프로프-2-이닐 (또한, 프로파르길) (C3), 프로핀-1-일 (C3), n-부틸 (C4), sec-부틸 (C4), 이소-부틸 (C4), tert-부틸 (C4), 시클로부틸 (C4), 부텐-4-일 (C4), 시클로펜틸 (C5), 시클로헥실 (C6);
ii) 치환 또는 비치환 C6 또는 C10 아릴; 예를 들어, 페닐, 나프틸 (또한, 본원에서는 나프틸렌-1-일 (C10) 또는 나프틸렌-2-일 (C10) 로도 언급함);
iii) 치환 또는 비치환 C6 또는 C10 알킬렌아릴; 예를 들어, 벤질, 2-페닐에틸, 나프틸렌-2-일메틸;
iv) 치환 또는 비치환 C1-C9 복소환 고리; 본원에 기재된 바와 같음;
v) 치환 또는 비치환 C1-C9 헤테로아릴 고리; 본원에 기재된 바와 같음;
vi) -(CR21aR21b)zOR20; 예를 들어, -OH, -CH2OH, -OCH3, -CH2OCH3, -OCH2CH3, -CH2OCH2CH3, -OCH2CH2CH3, 및 -CH2OCH2CH2CH3;
vii) -(CR21aR21b)zC(O)R20; 예를 들어, -COCH3, -CH2COCH3, -COCH2CH3, -CH2COCH2CH3, -COCH2CH2CH3, 및 -CH2COCH2CH2CH3;
viii) -(CR21aR21b)zC(O)OR20; 예를 들어, -CO2CH3, -CH2CO2CH3, -CO2CH2CH3, -CH2CO2CH2CH3, -CO2CH2CH2CH3, 및 -CH2CO2CH2CH2CH3;
xii) -(CR21aR21b)zC(O)N(R20)2; 예를 들어, -CONH2, -CH2CONH2, -CONHCH3, -CH2CONHCH3, -CON(CH3)2, 및 -CH2CON(CH3)2;
x) -(CR21aR21b)zN(R20)2; 예를 들어, -NH2, -CH2NH2, -NHCH3, -CH2NHCH3, -N(CH3)2, 및 -CH2N(CH3)2;
xi) 할로겐; -F, -Cl, -Br, 및 -I;
xii) -(CR21aR21b)zCN;
xiii) -(CR21aR21b)zNO2;
xiv) -(CHj'Xk')hCHjXk; 여기서, X 는 할로겐이고, 지수 j 는 0 내지 2 의 정수이고, j + k = 3 이고, 지수 j' 는 0 내지 2 의 정수이고, j' + k' = 2 이고, 지수 h 는 0 내지 6 이고; 예를 들어, -CH2F, -CHF2, -CF3, -CH2CF3, -CHFCF3, -CCl3, 또는 -CBr3;
xv) -(CR21aR21b)zSR20; -SH, -CH2SH, -SCH3, -CH2SCH3, -SC6H5, 및 -CH2SC6H5;
xvi) -(CR21aR21b)zSO2R20; 예를 들어, -SO2H, -CH2SO2H, -SO2CH3, -CH2SO2CH3, -SO2C6H5, 및 -CH2SO2C6H5; 및
xvii) -(CR21aR21b)zSO3R20; 예를 들어, -SO3H, -CH2SO3H, -SO3CH3, -CH2SO3CH3, -SO3C6H5, 및 -CH2SO3C6H5;
[식 중, 각 R20 은 독립적으로 수소, 치환 또는 비치환 C1-C4 선형, 분지형 또는 고리형 알킬, 페닐, 벤질, 복소환, 또는 헤테로아릴이거나; 또는 2 개의 R20 단위체가 함께 취해져 3 내지 7 개의 원자를 포함하는 고리를 형성하고; R21a 및 R21b 이 각각 독립적으로 수소 또는 C1-C4 선형 또는 분지형 알킬이고; 지수 p 가 0 내지 4 임].
R 단위체의 한 예시에는 R 단위체가 하기 화학식을 갖는 화합물이 포함된다:
식 중, R3 은 수소이고, R2 는 메틸 (C1), 에틸 (C2), n-프로필 (C3), 이소- 프로필 (C3), n-부틸 (C4), sec-부틸 (C4), 이소-부틸 (C4), 및 tert-부틸 (C4) 로부터 선택되는 단위체이다.
R 단위체의 또다른 예시에는 R2 가 메틸 (C1), 에틸 (C2), n-프로필 (C3), 이소-프로필 (C3), n-부틸 (C4), sec-부틸 (C4), 이소-부틸 (C4), 및 tert-부틸 (C4) 로부터 선택되는 단위체이고; R3 가 메틸 (C1) 또는 에틸 (C2) 로부터 선택되는 단위체인 화합물이 포함된다. R 의 상기 국면의 비제한적 예시에는 4,5-디메틸이미다졸-2-일, 4-에틸-5-메틸이미다졸-2-일, 4-메틸-5-에틸이미다졸-2-일 및 4,5-디에틸이미다졸-2-일이 포함된다.
R 단위체의 예시에는 R3 이 수소이고, R2 가 하기로부터 선택되는 치환기로 치환된 알킬 단위체인 화합물이 포함된다:
i) 할로겐: -F, -Cl, -Br 및 -I;
ii) -N(R11)2; 및
iii) -OR11;
[식 중, 각 R11 는 독립적으로 수소 또는 C1-C4 선형 또는 분지형 알킬임].
R 의 상기 구현예를 포함하는 단위체의 비제한적 예시에는 하기가 포함된다: -CH2F, -CHF2, -CF3, -CH2CF3, -CH2Cl, -CH2OH, -CH2OCH3, -CH2CH2OH, -CH2CH2OCH3, - CH2NH2, -CH2NHCH3, -CH2N(CH3)2, 및 -CH2NH(CH2CH3).
R 단위체의 또다른 예시에는 R3 이 수소이고, R2 가 페닐인 단위체가 포함된다.
R 단위체의 또다른 예시에는 R3 이 수소이고, R2 가 1,2,3,4-테트라졸-1-일, 1,2,3,4-테트라졸-5-일, [1,2,3]트리아졸-4-일, [1,2,3]트리아졸-5-일, [1,2,4]트리아졸-4-일, [1,2,4]트리아졸-5-일, 이미다졸-2-일, 이미다졸-4-일, 피롤-2-일, 피롤-3-일, 옥사졸-2-일, 옥사졸-4-일, 옥사졸-5-일, 이속사졸-3-일, 이속사졸-4-일, 이속사졸-5-일, [1,2,4]옥사디아졸-3-일, [1,2,4]옥사디아졸-5-일, [1,3,4]옥사디아졸-2-일, 푸란-2-일, 푸란-3-일, 티오펜-2-일, 티오펜-3-일, 이소티아졸-3-일, 이소티아졸-4-일, 이소티아졸-5-일, 티아졸-2-일, 티아졸-4-일, 티아졸-5-일, [1,2,4]티아디아졸-3-일, [1,2,4]티아디아졸-5-일, 및 [1,3,4]티아디아졸-2-일로부터 선택되는 헤테로아릴 단위체인 단위체가 포함된다.
Z 단위체
Z 는 하기 화학식을 가진 단위체이다:
R1 은 하기로부터 선택된다:
i) 수소;
ii) 히드록실;
iii) 아미노;
iv) 치환 또는 비치환 C1-C6 선형, 분지형 또는 고리형 알킬;
v) 치환 또는 비치환 C1-C6 선형, 분지형 또는 고리형 알콕시;
vi) 치환 또는 비치환 C6 또는 C10 아릴;
vii) 치환 또는 비치환 C1-C9 복소환 고리; 또는
viii) 치환 또는 비치환 C1-C9 헤테로아릴 고리.
하기는 R1 단위체 상의 하나 이상의 수소 원자를 치환할 수 있는 단위체의 비제한적 예시이다. 하기 치환기 및 본원에 기재되지 않은 여타의 것이 각각 독립적으로 선택된다:
i) C1-C12 선형, 분지형 또는 고리형 알킬, 알케닐, 및 알키닐; 메틸 (C1), 에틸 (C2), 에테닐 (C2), 에티닐 (C2), n-프로필 (C3), 이소-프로필 (C3), 시클로프로필 (C3), 3-프로페닐 (C3), 1-프로페닐 (또한, 2-메틸에테닐) (C3), 이소프로페닐 (또한, 2-메틸에텐-2-일) (C3), 프로프-2-이닐 (또한, 프로파르길) (C3), 프로핀-1-일 (C3), n-부틸 (C4), sec-부틸 (C4), 이소-부틸 (C4), tert-부틸 (C4), 시클로부틸 (C4), 부텐-4-일 (C4), 시클로펜틸 (C5), 시클로헥실 (C6);
ii) 치환 또는 비치환 C6 또는 C10 아릴; 예를 들어, 페닐, 나프틸 (또한, 본원에서 나프틸렌-1-일 (C10) 또는 나프틸렌-2-일 (C10) 로도 언급됨);
iii) 치환 또는 비치환 C6 또는 C10 알킬렌아릴; 예를 들어, 벤질, 2-페닐에틸, 나프틸렌-2-일메틸;
iv) 치환 또는 비치환 C1-C9 복소환 고리; 본원에 기재된 바와 같음;
v) 치환 또는 비치환 C1-C9 헤테로아릴 고리; 본원에 기재된 바와 같음;
vi) -(CR31aR31b)qOR30; 예를 들어, -OH, -CH2OH, -OCH3, -CH2OCH3, -OCH2CH3, -CH2OCH2CH3, -OCH2CH2CH3, 및 -CH2OCH2CH2CH3;
vii) -(CR31aR31b)qC(O)R30; 예를 들어, -COCH3, -CH2COCH3, -COCH2CH3, -CH2COCH2CH3, -COCH2CH2CH3, 및 -CH2COCH2CH2CH3;
viii) -(CR31aR31b)qC(O)OR30; 예를 들어, -CO2CH3, -CH2CO2CH3, -CO2CH2CH3, -CH2CO2CH2CH3, -CO2CH2CH2CH3, 및 -CH2CO2CH2CH2CH3;
xiii) -(CR31aR31b)qC(O)N(R30)2; 예를 들어, -CONH2, -CH2CONH2, -CONHCH3, -CH2CONHCH3, -CON(CH3)2, 및 -CH2CON(CH3)2;
x) -(CR31aR31b)qN(R30)2; 예를 들어, -NH2, -CH2NH2, -NHCH3, -CH2NHCH3, -N(CH3)2, 및 -CH2N(CH3)2;
xi) 할로겐; -F, -Cl, -Br 및 -I;
xii) -(CR31aR31b)qCN;
xiii) -(CR31aR31b)qNO2;
xiv) -(CHj'Xk')hCHjXk; 여기서, X 는 할로겐이고, 지수 j 는 0 내지 2 의 정수이고, j + k = 3 이고, 지수 j' 는 0 내지 2 의 정수이고, j' + k' = 2 이고, 지수 h 는 O 내지 6 임; 예를 들어, -CH2F, -CHF2, -CF3, -CH2CF3, -CHFCF3, -CCl3, 또는 -CBr3;
xv) -(CR31aR31b)qSR30; -SH, -CH2SH, -SCH3, -CH2SCH3, -SC6H5, 및 CH2SC6H5;
xvi) -(CR31aR31b)qSO2R30; 예를 들어, -SO2H, -CH2SO2H, -SO2CH3, CH2SO2CH3, -SO2C6H5, 및 -CH2SO2C6H5; 및
xvii) -(CR31aR31b)qSO3R30; 예를 들어, -SO3H, -CH2SO3H, -SO3CH3, CH2SO3CH3, -SO3C6H5 및 -CH2SO3C6H5;
[식 중, 각 R30 은 독립적으로 수소, 치환 또는 비치환 C1-C6 선형, 분지형 또는 고리형 알킬, 페닐, 벤질, 복소환, 또는 헤테로아릴이거나; 또는 2 개의 R30 단위체는 함께 취해져 3 내지 7 개의 원자를 포함하는 고리를 형성할 수 있고; R31a 및 R31b 는 각각 독립적으로 수소 또는 C1-C4 선형 또는 분지형 알킬이고; 지수 q 는 O 내지 4 임.
R1 단위체의 한 예시에는 치환 또는 비치환 페닐 (C6 아릴) 단위체로서, 각 치환기가 하기로부터 독립적으로 선택되고: 할로겐, C1-C4 선형, 분지형 알킬 또는 고리형 알킬, -OR11, -CN, -N(R11)2-CO2R11, -C(O)N(R11)2, -NR11C(O)R11, -NO2 및 - SO2R11; 각 R11 이 수소; 치환 또는 비치환 C1-C4 선형, 분지형, 고리형 알킬, 알케닐, 또는 알키닐; 치환 또는 비치환 페닐 또는 벤질이거나; 또는 2 개의 R11 단위체가 함께 취해져 3 내지 7 개의 원자를 포함하는 고리를 형성할 수 있는 단위체가 포함된다.
R1 단위체의 또다른 예시에는 페닐, 2-플루오로페닐, 3-플루오로페닐, 4-플루오로페닐, 2,3-디플루오로페닐, 3,4-디플루오로페닐, 3,5-디플루오로페닐, 2-클로로페닐, 3-클로로페닐, 4-클로로페닐, 2,3-디클로로페닐, 3,4-디클로로페닐, 3,5-디클로로페닐, 2-히드록시페닐, 3-히드록시페닐, 4-히드록시페닐, 2-메톡시페닐, 3-메톡시페닐, 4-메톡시페닐, 2,3-디메톡시페닐, 3,4-디메톡시페닐 및 3,5-디메톡시페닐로부터 선택되는 치환 C6 아릴 단위체가 포함된다.
R1 단위체의 또다른 예시에는 2,4-디플루오로페닐, 2,5-디플루오로페닐, 2,6-디플루오로페닐, 2,3,4-트리플루오로페닐, 2,3,5-트리플루오로페닐, 2,3,6-트리플루오로페닐, 2,4,5-트리플루오로페닐, 2,4,6-트리플루오로페닐, 2,4-디클로로페닐, 2,5-디클로로페닐, 2,6-디클로로페닐, 3,4-디클로로페닐, 2,3,4-트리클로로페닐, 2,3,5-트리클로로페닐, 2,3,6-트리클로로페닐, 2,4,5-트리클로로페닐, 3,4,5-트리클로로페닐 및 2,4,6-트리클로로페닐로부터 선택되는 치환 또는 비치환 C6 아릴 단위체가 포함된다.
R1 단위체의 또다른 추가 예시에는 2-메틸페닐, 3-메틸페닐, 4-메틸페닐, 2,3-디메틸페닐, 2,4-디메틸페닐, 2,5-디메틸페닐, 2,6-디메틸페닐, 3,4-디메틸페닐, 2,3,4-트리메틸페닐, 2,3,5-트리메틸페닐, 2,3,6-트리메틸페닐, 2,4,5-트리메틸페닐, 2,4,6-트리메틸페닐, 2-에틸페닐, 3-에틸페닐, 4-에틸페닐, 2,3-디에틸페닐, 2,4-디에틸페닐, 2,5-디에틸페닐, 2,6-디에틸페닐, 3,4-디에틸페닐, 2,3,4-트리에틸페닐, 2,3,5-트리에틸페닐, 2,3,6-트리에틸페닐, 2,4,5-트리에틸페닐, 2,4,6-트리에틸페닐, 2-이소프로필페닐, 3-이소프로필페닐, 및 4-이소프로필페닐로부터 선택되는 치환 C6 아릴 단위체가 포함된다.
R1 단위체의 또다른 추가 예시에는 2-아미노페닐, 2-(N-메틸아미노)페닐, 2-(N,N-디메틸아미노)페닐, 2-(N-에틸아미노)페닐, 2-(N,N-디에틸아미노)페닐, 3-아미노페닐, 3-(N-메틸아미노)페닐, 3-(N,N-디메틸아미노)페닐, 3-(N-에틸아미노)페닐, 3-(N,N-디에틸아미노)페닐, 4-아미노페닐, 4-(N-메틸아미노)페닐, 4-(N,N-디메틸아미노)페닐, 4-(N-에틸아미노)페닐, 및 4-(N,N-디에틸아미노)페닐로부터 선택되는 치환 C6 아릴 단위체가 포함된다.
R1 은 헤테로아릴 단위체를 포함할 수 있다. 헤테로아릴 단위체의 비제한적 예시에는 하기가 포함된다:
R1 헤테로아릴 단위체는 치환 또는 비치환일 수 있다. 수소를 치환할 수 있는 단위체의 비제한적 예시에는 하기로부터 선택되는 단위체가 포함된다:
i) C1-C6 선형, 분지형 및 고리형 알킬;
ii) 치환 또는 비치환 페닐 및 벤질;
iii) 치환 또는 비치환 C1-C8 헤테로아릴;
iv) -C(O)R9; 및
v) -NHC(O)R9;
여기서, R9 는 C1-C6 선형 및 분지형 알킬; C1-C6 선형 및 분지형 알콕시; 또는 -NHCH2C(O)R10 이고; R10 은 수소, 메틸, 에틸 및 tert-부틸로부터 선택된다.
R1 의 한 예시는 메틸, 에틸, n-프로필, 이소-프로필, n-부틸, 이소-부틸, sec-부틸, 및 tert-부틸로부터 선택되는 알킬 단위체로 치환된 단위체에 관한 것이다.
R1 의 또다른 예시에는 치환 또는 비치환 페닐 및 벤질로 치환된 단위체로서, 페닐 및 벤질 치환기가 하기의 하나 이상으로부터 선택되는 단위체가 포함된다:
i) 할로겐;
ii) C1-C3 알킬;
iii) C1-C3 알콕시;
iv) -CO2R11; 및
v) -NHCOR16;
[식 중, R11 및 R16 은 각각 독립적으로 수소, 메틸 또는 에틸임].
R1 의 또다른 예시는 화학식 -C(O)R9 을 가진 카르복시 단위체로 치환된 페닐 및 벤질 단위체로서; R9 가 메틸, 메톡시, 에틸 및 에톡시로부터 선택되는 단위체가 포함된다.
R1 의 추가 예시에는 화학식 -NHC(O)R9 을 가진 아미드 단위체로 치환된 페닐 및 벤질 단위체로서; R9 가 메틸, 메톡시, 에틸, 에톡시, tert-부틸 및 tert-부톡시로부터 선택되는 단위체가 포함된다.
R1 의 추가 예시에는 하나 이상의 플루오로 또는 클로로 단위체로 치환된 페닐 및 벤질 단위체가 포함된다.
L 단위체
L 은 지수 n 이 1 일 때 존재하나, 지수 n 이 0 일 때는 부재하는 연결 단위체이다. L 단위체는 하기 화학식을 갖는다:
-[Q]y[C(R5aR5b)]x[Q1]z[C(R6aR6b)]w-
식 중, Q 및 Q1 은 각각 독립적으로 하기의 것이다:
i) -C(O)-;
ii) -NH-;
iii) -C(O)NH-;
iv) -NHC(O)-;
v) -NHC(O)NH-;
vi) -NHC(O)O-;
vii) -C(O)O-;
viii) -C(O)NHC(O)-;
ix) -0-;
x) -S-;
xi) -SO2-;
xii) -C(=NH)-;
xiii) -C(=NH)NH-;
xiv) -NHC(=NH)-; 또는
xv) -NHC(=NH)NH-.
지수 y 가 1 인 경우, Q 는 존재한다. 지수 y 가 O 인 경우, Q 는 부재한다. 지수 z 이 1 인 경우, Q1 은 존재한다. 지수 z 이 0 인 경우, Q1 는 부재한다.
R5a 및 R5b 는 각각 독립적으로 하기이다:
i) 수소;
ii) 히드록시;
iii) 할로겐;
iv) C1-C6 치환 또는 비치환 선형 또는 분지형 알킬; 또는
v) 하기 화학식을 가진 단위체:
-[C(R7aR7b)]tR8
식 중, R7a 및 R7b 은 각각 독립적으로 하기이다:
i) 수소; 또는
ii) 치환 또는 비치환 C1-C6 선형, 분지형 또는 고리형 알킬.
R8 은 하기의 것이다:
i) 수소;
ii) 치환 또는 비치환 C1-C6 선형, 분지형 또는 고리형 알킬;
iii) 치환 또는 비치환 C6 또는 C10 아릴;
iv) 치환 또는 비치환 C1-C9 헤테로아릴; 또는
v) 치환 또는 비치환 C1-C9 복소환.
R6a 및 R6b 은 각각 독립적으로 하기이다:
i) 수소; 또는
ii) C1-C4 선형 또는 분지형 알킬.
지수 t, w 및 x 는 각각 독립적으로 0 내지 4 이다.
하기는 R5a, R5b, R7a, R7b 및 R8 단위체 상에서 하나 이상의 수소 원자를 치환할 수 있는 단위체의 비제한적 예시이다. 하기 치환기 및 본원에 기재되지 않은 여타의 것이 각각 독립적으로 선택된다:
i) C1-C12 선형, 분지형 또는 고리형 알킬, 알케닐, 및 알키닐; 메틸 (C1), 에틸 (C2), 에테닐 (C2), 에티닐 (C2), n-프로필 (C3), 이소-프로필 (C3), 시클로프로필 (C3), 3-프로페닐 (C3), 1-프로페닐 (또한, 2-메틸에테닐) (C3), 이소프로페닐 (또한, 2-메틸에텐-2-일) (C3), 프로프-2-이닐 (또한, 프로파르길) (C3), 프로핀-1-일 (C3), n-부틸 (C4), sec-부틸 (C4), 이소-부틸 (C4), tert-부틸 (C4), 시클로부틸 (C4), 부텐-4-일 (C4), 시클로펜틸 (C5), 시클로헥실 (C6);
ii) 치환 또는 비치환 C6 또는 C10 아릴; 예를 들어, 페닐, 나프틸 (또한, 본원에서 나프틸렌-1-일 (C10) 또는 나프틸렌-2-일 (C10) 로도 언급됨);
iii) 치환 또는 비치환 C6 또는 C10 알킬렌아릴; 예를 들어, 벤질, 2-페닐에틸, 나프틸렌-2-일메틸;
iv) 치환 또는 비치환 C1-C8 복소환 고리; 하기 본원에 기재된 바와 같음;
v) 치환 또는 비치환 C1-C9 헤테로아릴 고리; 본원에 기재된 바와 같음;
vi) -(CR41aR41b)rOR40; 예를 들어, -OH, -CH2OH, -OCH3, -CH2OCH3, -OCH2CH3, -CH2OCH2CH3, -OCH2CH2CH3, 및 -CH2OCH2CH2CH3;
vii) -(CR41aR41b)rC(O)R40; 예를 들어, -COCH3, -CH2COCH3, -COCH2CH3, -CH2COCH2CH3, -COCH2CH2CH3, 및 -CH2COCH2CH2CH3;
viii) -(CR41aR41b)rC(O)OR40; 예를 들어, -CO2CH3, -CH2CO2CH3, -CO2CH2CH3, -CH2CO2CH2CH3, -CO2CH2CH2CH3, 및 -CH2CO2CH2CH2CH3;
xiv) -(CR41aR41b)rC(O)N(R40)2; 예를 들어, -CONH2, -CH2CONH2, -CONHCH3, -CH2CONHCH3, -CON(CH3)2, 및 -CH2CON(CH3)2;
x) -(CR41aR41b)rN(R40)2; 예를 들어, -NH2, -CH2NH2, -NHCH3, -CH2NHCH3, -N(CH3)2, 및 -CH2N(CH3)2;
xi) 할로겐; -F, -Cl, -Br, 및 -I;
xii) -(CR41aR41b)rCN;
xiii) -(CR41aR41b)rNO2;
xiv) -(CHj'Xk')hCHjXk; 여기서, X 는 할로겐이고, 지수 j 는 0 내지 2 의 정수이고, j + k = 3 이고, 지수 j' 은 0 내지 2 의 정수이고, j' + k' = 2 이고, 지수 h 는 O 내지 6 임; 예를 들어, -CH2F, -CHF2, -CF3, -CH2CF3, -CHFCF3, -CCl3, 또는 -CBr3;
xv) -(CR41aR41b)rSR40; -SH, -CH2SH, -SCH3, -CH2SCH3, -SC6H5, 및 -CH2SC6H5;
xvi) -(CR41aR41b)rSO2R40; 예를 들어, -SO2H, -CH2SO2H, -SO2CH3, -CH2SO2CH3, -SO2C6H5, 및 -CH2SO2C6H5; 및
xvii) -(CR41aR41b)rSO3R40; 예를 들어, -SO3H, -CH2SO3H, -SO2CH3, -CH2SO2CH3, -SO2C6H5, 및 -CH2SO2C6H5;
식 중, 각 R40 는 독립적으로 수소, 치환 또는 비치환 C1-C6 선형, 분지형 또는 고리형 알킬, 페닐, 벤질, 복소환, 또는 헤테로아릴이거나; 또는 2 개의 R40 단위체는 함께 취해져 3 내지 7 개의 원소를 포함하는 고리를 형성하고; R41a 및 R41b 는 각각 독립적으로 수소 또는 C1-C4 선형 또는 분지형 알킬이고; 지수 r 은 0 내지 4 이다.
L 단위체의 한 국면은 하기 화학식을 가진 단위체에 관한 것이다:
-C(O)[C(R5aR5b)]xNHC(O)-
식 중, R5a 는 수소, 치환 또는 비치환 C1-C4 알킬, 치환 또는 비치환 페닐, 및 치환 또는 비치환 헤테로아릴이고; 지수 x 는 1 또는 2 이다. 한 구현예는 하기 화학식을 가진 연결 단위체에 관한 것이다:
i) -C(O)[C(R5aH)]NHC(O)O-;
ii) -C(O)[C(R5aH)][CH2]NHC(O)O-;
iii) -C(O)[CH2][C(R5aH)]NHC(0)0-;
iv) -C(O)[C(R5aH)]NHC(O)-;
v) -C(O)[C(R5aH)] [CH2]NHC(O)-; 또는
vi) -C(O)[CH2] [C(R5aH)]NHC(0)-;
식 중, R5a 는 하기이다:
i) 수소;
ii) 메틸;
iii) 에틸;
iv) 이소프로필;
v) 페닐;
vi) 벤질;
vii) 4-히드록시벤질;
viii) 히드록시메틸; 또는
ix) 1-히드록시 에틸.
지수 x 가 1 인 경우, 상기 구현예는 L 단위체의 하기의 비제한적 예시를 제공한다:
지수 x 가 2 인 경우, 상기 구현예는 L 단위체의 하기의 비제한적 예시를 제공한다:
L 단위체의 또다른 예시에는 Q 가 -C(O)- 이고, 지수 x 및 z 가 0 이고, w 가 1 또는 2 이고, 첫번째 R6a 단위체가 페닐, 2-플루오로페닐, 3-플루오로페닐, 4-플루오로페닐, 2,3-디플루오로페닐, 3,4-디플루오로페닐, 3,5-디플루오로페닐, 2-클로로페닐, 3-클로로페닐, 4-클로로페닐, 2,3-디클로로페닐, 3,4-디클로로페닐, 3,5-디클로로페닐, 2-히드록시페닐, 3-히드록시페닐, 4-히드록시페닐, 2-메톡시페닐, 3-메톡시페닐, 4-메톡시페닐, 2,3-디메톡시페닐, 3,4-디메톡시페닐 및 3,5-디메톡시페닐로부터 선택되고; 두번째 R6a 단위체가 수소이고, R6b 단위체가 수소인 단위체가 포함된다. 예를 들어, 하기 화학식을 가진 연결 단위체:
L 의 상기 구현예의 추가 예시에는 상기 본원에 기재한 바와 같은 치환 또는 비치환 헤테로아릴 단위체인 상기 본원에 제시한 바와 같은 첫번째 R6a 단위체가 포함된다.
L 의 상기 구현예의 추가 예시에는 하기 화학식을 가진 단위체가 포함된다:
-C(O)[C(R6aR6b)]w-;
식 중, R6a 및 R6b 는 수소이고, 지수 w 는 1 또는 2 이고; 상기 단위체는 하기로부터 선택된다:
i) -C(O)CH2-; 및
ii) -C(O)CH2CH2-.
L 단위체의 추가 예시에는 하기 화학식을 가진 단위체가 포함된다:
-C(O)[C(R5aR5b)]xC(O)-;
식 중, R5a 및 R5b 는 수소이고, 지수 x 는 1 또는 2 이고; 상기 단위체는 하기로부터 선택된다:
i) -C(O)CH2C(O)-; 및
ii) -C(O)CH2CH2C(O)-.
L 단위체의 또다른 예시에는 하기 화학식을 가진 단위체가 포함된다:
-C(O)NH[C(R5aR5b)]x-;
식 중, R5a 및 R5b 는 수소이고, 지수 w 은 O, 1 또는 2 이고; 상기 단위체는 하기로부터 선택된다:
i) -C(O)NH-;
ii) -C(O)NHCH2-; 및
iii) -C(O)NHCH2CH2-.
L 단위체의 또다른 예시에는 하기 화학식을 가진 단위체가 포함된다:
-SO2[C(R6aR6b)]w-;
식 중, R8a 및 R8b 는 수소 또는 메틸이고, 지수 w 는 0, 1 또는 2 이고; 상기 단위체는 하기로부터 선택된다:
i) -SO2-;
ii) -SO2CH2-; 및
iii) -SO2CH2CH2-.
혈관 누출 제어 (
Vascular
Leakage
Control
)
개시된 화합물들 (유사체) 는 제형자로 하여금 본원에 명시되어 예시하지 않은 유사체의 제조에 대해 납득할 합성 전략을 적용하도록 보조하기 위해 몇가지 카테고리로 정리한다. 카테고리에 대한 정리는 본원에 기재된 실체의 임의의 조성물에 대한 증가되거나 또는 감소된 효능을 의미하지 않는다.
개시된 화합물로 본원에 기재된 것에는 모든 약제학적으로 허용되는 염 형태가 포함된다. 하기 화학식을 가진 화합물:
은 염, 예를 들어 술팜산의 염을 형성할 수 있다:
상기 화합물은 또한 쯔비터성 이온, 예를 들어:
강산의 염, 예를 들어:
로 존재할 수 있다.
본 개시내용의 카테고리 I 의 첫번째 국면은 R 이 하기 화학식을 가진 치환 또는 비치환 티아졸-2-일 단위체인 화합물에 관한 것이고:
그의 한 구현예는 하기 화학식을 가진 억제제에 관한 것이다:
식 중, R 단위체는 티아졸-2-일 단위체로서, 치환된 경우 R2 및 R3 단위체로 치환된 것이다. R 및 R5a 단위체는 표 I 에 추가로 기재되어 있다.
본 개시내용의 카테고리 I 의 제 1 국면에 속하는 화합물은 하기 본원에 제공되는 반응식 I 에 개괄하고 실시예 1 에 기재한 과정으로 제조될 수 있다.
반응식 I
시약 및 조건: (a)(i) (이소-부틸)OCOCl, NMM, DMF; 0℃, 20 분.
(ii) NH3; 30 분 동안 0℃.
시약 및 조건: (b) 로손 시약 (Lawesson's reagent), THF; rt, 3 시간
시약 및 조건: (c) CH3CN; 환류, 3 시간
시약 및 조건: (d) Boc-Phe, EDCI, HOBt, DIPEA, DMF; rt, 18 시간
시약 및 조건: (e) (i) H2:Pd/C, MeOH; (ii) SO3-피리딘, NH4OH; rt, 2 시간
실시예
1
4-{(S)-2-[(S)-2-(
tert
-
부톡시카르보닐아미노
)-3-
페닐프로판아미도
]-2-(4-
에
틸티아졸-2-일)에틸}
페닐술팜산
(5) 의 제조
[1-(S)-카르바모일-2-(4-니트로페닐)에틸-카르밤산 tert-부틸 에스테르 (1) 의 제조: 2-(S)-tert-부톡시카르보닐아미노-3-(4-니트로페닐)-프로피온산 및 N-메틸모르폴린 (1.1 mL, 9.65 mmol) 의 DMF (10 mL) 중 0℃ 용액에 이소-부틸 클로로포르메이트 (1.25 mL, 9.65 mmol) 를 적가했다. 상기 혼합물을 0℃ 에서 20 분 동안 교반한 후, NH3 (g) 를 반응 혼합물에 30 분 동안 0℃ 에서 통과시켰다. 반응 혼합물을 농축하고, 잔사를 EtOAc 에 용해시키고, 5% 시트르산, 물, 5% NaHCO3, 물 및 식염수로 순차적으로 세척하고, 건조시키고 (Na2SO4), 여과하고 진공에서 잔사로 농축하고, EtO Ac/석유 에테르의 혼합물로 분쇄하여 2.2 g (74%) 의 원하는 생성물을 백색 고체로 수득했다.
[2-(4-니트로페닐)-1-(S)-티오카르바모일에틸]카르밤산 tert-부틸 에스테르 (2) 의 제조: [1-(S)-카르바모일-2-(4-니트로페닐)에틸-카르밤산 tert-부틸 에스테르 (1) (0.400 g, 1.29 mmol) 의 THF (10 mL) 중 용액에 로손 시약 (0.262 g, 0.65 mmol) 을 첨가했다. 반응 혼합물을 3 시간 동안 교반하고 잔사로 농축해, 이를 실리카 상에서 정제하여 0.350 g (83%) 의 원하는 생성물을 수득했다.
1-(S)-(4-에틸티아졸-2-일)-2-(4-니트로페닐)에틸 아민 (3) 의 제조: [2-(4-니트로페닐)-1-(5)-티오카르바모일에틸]-카르밤산 tert-부틸 에스테르, 2, (0.245 g, 0.753 mmol), 1-브로모-2-부타논 (0.125 g, 0.828 mmol) 의 CH3CN (5 mL) 중 혼합물을 3 시간 동안 환류시켰다. 반응 혼합물을 실온으로 냉각시키고, 디에틸 에테르를 상기 용액에 첨가하고 형성된 석출물을 여과로 제거했다. 고체를 진공 하에 건조시켜 0.242 g (90% 수율) 의 원하는 생성물을 수득했다. ESI+ MS 278 (M+1).
{1-[1-(4-에틸티아졸-2-일)-2-(4-니트로페닐)에틸카르바모일]-2-페닐에틸} 카르밤산 tert-부틸 에스테르 (4) 의 제조: 1-(S)-(4-에틸티아졸-2-일)-2-(4-니트로페닐)에틸 아민 히드로브로마이드, 3, (0.393 g, 1.1 mmol), (S)-(2-tert-부톡시카르보닐아미노)-3-페닐프로피온산 (0.220 g, 0.828 mmol) 및 1-히드록시벤조트리아졸 (HOBt) (0.127 g, 0.828 mmol) 의 DMF (10 mL) 중 용액에 0℃ 에서 1-(3-디메틸아미노프로필)-3-에틸카르보디이미드 (EDCI) (0.159 g, 0.828 mmol) 에 이어 디이소프로필아민 (0.204 g, 1.58 mmol) 을 첨가했다. 혼합물을 0℃ 에서 30 분, 이어서 실온에서 밤새 교반했다. 반응 혼합물을 물로 희석하고, EtOAc 로 추출했다. 조합한 유기상을 1 N 수성 HCl, 5 % 수성 NaHCO3, 물 및 식염수로 세척하고, Na2SO4 상에서 건조시켰다. 용매를 진공에서 제거하여 0.345 g 의 원하는 생성물을 수득하여, 추가 정제없이 사용했다. LC/MS ESI+ 525 (M+1).
4-{(S)-2-[(S)-2-(tert-부톡시카르보닐아미노)-3-페닐프로판아미도]-2-(4-에틸티아졸-2-일)에틸}페닐술팜산 암모늄 염 (5) 의 제조: {1-[1-(4-에틸티아졸-2-일)-2-(4-니트로페닐)에틸카르바모일]-2-페닐에틸} 카르밤산 tert-부틸 에스테르, 4, (0.345 g) 를 MeOH (4 mL) 에 용해시켰다. 촉매량의 Pd/C (10% w/w) 를 첨가하고, 혼합물을 수소 분위기 하에 2 시간 동안 교반했다. 반응 혼합물을 CELITE™ 의 층을 통해 여과하고, 용매를 감압 하에 제거했다. 미정제 생성물을 피리딘 (12 mL) 에 용해시키고, SO3-피리딘 (0.314 g) 을 첨가했다. 반응물을 실온에서 5 분 동안 교반한 후, NH4OH 의 7% 용액 (50 mL) 을 첨가했다. 이어서, 혼합물을 농축하고, 결과로서 수득한 잔사를 역상 크로마토그래피로 정제하여 0.222 g 의 원하는 생성물을 암모늄 염으로 수득했다.
개시된 억제제는 또한 유리산으로 단리될 수 있다. 상기 과정의 비제한적 예시는 하기 실시예 4 에 기재되어 있다.
하기는 본 개시내용의 카테고리 I 의 첫번째 국면의 상기 구현예에 속하는 화합물의 비제한적 예시이다.
4-{(S)-2-[(R)-2-(tert-부톡시카르보닐아미노)-3-페닐프로판아미도]-2-(4-에틸티아졸-2-일)에틸}페닐술팜산: 1H NMR (CD3OD ): δ 7.22-7.02 (m, 10H), 5.39 (s, 1H), 4.34 (s, 1H), 3.24-2.68 (m, 6H), 1.37 (s, 9H), 1.30 (t, 3H, J=7.5 Hz).
카테고리 I 의 상기 국면의 또다른 구현예는 하기 화학식을 가진 억제제에 관한 것이다:
식 중, R 단위체 및 R5a 단위체는 표 II 에서 추가로 기재된다.
본 구현예의 화합물은 단계 (d) 에서 적당한 Boc-β-아미노산을 (S)-(2-tert-부톡시카르보닐아미노)-3-페닐프로피온산에 대해 치환함으로써 상기 반응식 I 에서 개요하고 실시예 1 에서 기재한 과정에 따라 제조될 수 있다.
하기는 상기 구현예에 따른 화합물의 비제한적 예시이다.
{1-[1-(4-에틸티아졸-2-일)-(S)-2-(4-술포아미노페닐)에틸카르바모일]-(S)-2-페닐에틸}메틸 카르밤산 tert-부틸 에스테르:
1H NMR (300 MHz, MeOH-d4) δ 8.36 (d, J = 8.1 Hz, 1H), 7.04-7.22 (m, 9H), 5.45 (s, 1H), 3.01-3.26 (m, 2H), 2.60-2.88 (m, 4H), 2.33 (s, 3H), 1.30 (s, 9H).
{1-[1-(4-페닐티아졸-2-일)-(S)-2-(4-술포아미노페닐)에틸카르바모일]-(S)-2-페닐에틸}메틸 카르밤산 tert-부틸 에스테르: 1H NMR (300 MHz, MeOH-d4) δ 8.20 (d, J = 8.1 Hz, 1H), 7.96-7.99 (m, 2H), 7.48-7.52 (m, 3H), 7.00-7.23(m, 7H), 6.89 (s, 1H), 5.28 (q, J = 7.5 Hz, 1H), 4.33 (t, J= 6.6 Hz, 1H), 3.09-3.26 (m, 2H), 3.34 (dd, J= 13.2 and 8.4 Hz, IH), 2.82 (dd, J= 13.2 and 8.4 Hz, IH), 1.38 (s, 9H).
본 개시내용의 카테고리 I 의 제 2 국면은 하기 화학식을 가진 R 이 치환 또는 비치환 티아졸-4-일인 화합물에 관한 것이며:
그의 한 국면은 하기 화학식을 가진 억제제에 관한 것이다:
식 중, R 단위체 및 R5a 단위체는 표 III 에서 추가로 기재된다.
본 개시내용의 카테고리 I 의 제 2 국면에 속하는 화합물들은 하기 본원의 반응식 II 에서 개요하고 실시예 2 에서 기재되는 과정으로 제조될 수 있다.
반응식 II
시약 및 조건: (a)(i) (이소-부틸)OCOCl, Et3N, THF; 0℃, 20 분.
(ii) CH2N2; 실온에서 3 시간.
시약 및 조건: (b) 48% HBr, THF; 0℃, 1.5 시간
시약 및 조건: (c)(i) 티오벤즈아미드, CH3CN; 환류, 2 시간
(ii) Boc-Phe, HOBt, DIPEA, DMF; rt, 18 시간
시약 및 조건: (d) (i) H2:Pd/C, MeOH; (ii) SO3-피리딘, NH4OH; rt, 12시간
실시예
2
4-{(S)-2-(S)-2-(
tert
-
부톡시카르보닐아미노
)-3-
페닐프로판아미도
-2-(2-
페닐티아졸
-4-일)}
페닐술팜산
(9)
(S)-[3-디아조-1-(4-니트로벤질)-2-옥소-프로필]-카르밤산 tert-부틸 에스테르 (6) 의 제조: 2-(S)-tert-부톡시카르보닐아미노-3-(4-니트로페닐)-프로피온산 (1.20 g, 4.0 mmol) 의 THF (20 mL) 중 0℃ 용액에 트리에틸아민 (0.61 mL, 4.4 mmol) 에 이어 이소-부틸 클로로포르메이트 (0.57 mL, 4.4 mmol) 를 적가했다. 반응 혼합물을 0℃ 에서 20 분 동안 교반하고 여과했다. 여과액을 디아조메탄 (약 16 mmol) 의 에테르 용액으로 0℃ 에서 처리했다. 반응 혼합물을 실온에서 3 시간 동안 교반한 후, 진공에서 농축했다. 결과로서 수득한 잔사를 EtOAc 에 용해시키고, 물 및 식염수로 순차적으로 세척하고, 건조시키고 (Na2SO4), 여과하고 농축했다. 잔사를 실리카 (헥산/EtOAc 2:1) 상에서 건조시켜 1.1 g (82% 수율) 의 원하는 생성물을 연황색 고체로 수득했다.
(S)-tert-부틸 4-브로모-1-(4-니트로페닐)-3-옥소부탄-2-일카르바메이트 (7) 의 제조: (S)-[3-디아조-1-(4-니트로벤질)-2-옥소-프로필]-카르밤산 tert-부틸 에스테르, 6, (0.350 g, 1.04 mmol) 의 THF (5 mL) 중 0℃ 용액에 48% aq. HBr (0.14 mL, 1.25 mmol) 를 적가했다. 반응 혼합물을 0℃ 에서 1.5 시간 동안 교반한 후, 반응물을 0℃ 에서 포화 Na2CO3 로 켄칭했다. 혼합물을 EtOAc (3x 25 mL) 로 추출하고, 조합한 유기 추출물 식염수로 세척하고, 건조시키고 (Na2SO4), 여과하고, 농축하여 0.400 g 의 생성물을 수득해, 추가 정제없이 후속 단계에서 사용했다.
tert-부틸 (S)-1-(S)-2-(4-니트로페닐)-1-(2-페닐티아졸-4-일)에틸아미노-1-옥소-3-페닐프로판-2-일카르바메이트 (8) 의 제조: 티오벤즈아미드 (0.117 g, 0.85 mmol) 및 (S)-tert-부틸 4-브로모-1-(4-니트로페닐)-3-옥소부탄-2-일카르바메이트, 7, (0.300 g, 0.77 mmol) 의 CH3CN (4 mL) 중 혼합물을 2 시간 동안 환류시켰다. 반응 혼합물을 실온으로 냉각시키고, 디에틸 에테르를 첨가해 중간체 2-(니트로페닐)-(S)-1-(4-페닐티아졸-2-일)에틸아민을 석출시키고, 이를 여과에 의해 히드로브로마이드 염으로 단리했다. 상기 히드로브로마이드 염을 디이소프로필에틸아민 (0.42 mL, 2.31 mmol), 1-히드록시벤조트리아졸 (0.118 g, 0.79 mmol) 및 (5)-(2-tert-부톡시카르보닐-아미노)-3-페닐프로피온산 (0.212 g, 0.80 mmol) 과 함께 DMF (3 mL) 에 용해시켰다. 혼합물을 0℃ 에서 30 분, 이어서 실온에서 밤새 교반했다. 반응 혼합물을 물로 희석하고, EtOAc 로 추출했다. 조합한 유기상을 1 N 수성 HCl, 5 % 수성 NaHCO3, 물 및 식염수로 세척하고, Na2SO4 상에서 건조시켰다. 용매를 진공에서 제거하여 0.395 g (90 % 수율) 의 원하는 생성물을 수득하여, 추가 정제없이 사용했다. LC/MS ESI+ 573 (M+1).
4-{(S)-2-(S)-2-(tert-부톡시카르보닐)-3-페닐프로판아미도-2-(2-페닐티아졸-4-일)}페닐술팜산 (9) 의 제조: tert-부틸 (S)-1-(S)-2-(4-니트로페닐)-1-(2-페닐티아졸-4-일)에틸아미노-1-옥소-3-페닐프로판-2-일카르바메이트, 8, (0.360 g) 를 MeOH (4 mL) 에 용해시켰다. 촉매량의 Pd/C (10% w/w) 를 첨가하고, 혼합물을 수소 분위기 하에 12 시간 동안 교반했다. 반응 혼합물을 CELITE™ 의 층을 통해 여과하고, 용매를 감압 하에 제거했다. 미정제 생성물을 피리딘 (12 mL) 에 용해시키고, SO3-피리딘 (0.296 g) 으로 처리했다. 반응물을 실온에서 5 분 동안 교반하고, 이후 NH4OH 의 7% 용액 (10 mL) 을 첨가했다. 이어서, 혼합물을 농축하고, 결과로서 수득한 잔사를 역상 크로마토그래피로 정제하여 0.050 g 의 원하는 생성물을 암모늄 염으로 수득했다.
본 개시내용의 카테고리 II 의 첫번째 국면은 R 이 하기 화학식을 가진 치환 또는 비치환 티아졸-4-일 단위체인 화합물에 관한 것이며:
그의 한 국면은 하기 화학식을 가진 억제제에 관한 것이다:
식 중, R 단위체는 티아졸-4-일 단위체이고, 치환된 경우, R4 단위체로 치환된다. R 및 R5a 단위체는 표 IV 에 추가로 기재한다.
본 개시내용의 카테고리 II 의 두번째 국면에 속하는 화합물들은 반응식 III 에서 개요하고 하기 본원의 실시예 3 에 기재된 과정으로 제조될 수 있다.
반응식
III
시약 및 조건: (a)(i) 프로판티오아미드, CH3CN; 환류, 2 시간
(ii) Boc-Phe, HOBt, DIPEA, DMF; rt, 18 시간
시약 및 조건: (b) (i) H2:Pd/C, MeOH; (ii) SO3-피리딘, NH4OH; rt, 18 시간
실시예
3
4-{(S)-2-[(S)-2-(
메톡시카르보닐아미노
)-3-
페닐프로판아미도
]-2-(2-
에틸티
아졸-4-일)에틸}
페닐술팜산
(13)
메틸 (S)-1-[(S)-1-(2-에틸티아졸-4-일)-2-(4-니트로페닐)-에틸]아미노-1-옥소-3-페닐프로판-2-일카르바메이트 (12) 의 제조: 프로판티오아미드 (69 mg, 0.78 mmol) 및 (S)-tert-부틸 4-브로모-1-(4-니트로페닐)-3-옥소부탄-2-일카르바메이트, 7, (0.300 g, 0.77 mmol) 의 CH3CN (4 mL) 중 혼합물을 2 시간 동안 환류시켰다. 반응 혼합물을 실온으로 냉각시키고, 디에틸 에테르를 첨가하여 중간체 2-(니트로페닐)-(S)-1-(4-에틸티아졸-2-일)에틸아민을 석출시켜, 여과로 히드로브로마이드 염으로 단리했다. 상기 히드로브로마이드 염을 디이소프로필에틸아민 (0.38 mL, 2.13 mmol), 1-히드록시벤조트리아졸 (107 mg, 0.71 mmol) 및 (S)-(2-메톡시카르보닐-아미노)-3-페닐프로피온산 (175 mg, 0.78 mmol) 과 함께 DMF (8 mL) 에 용해시켰다. 혼합물을 0℃ 에서 30 분, 이어서 실온에서 밤새 교반했다. 반응 혼합물을 물로 희석하고, EtOAc 로 추출했다. 조합한 유기상을 1 N 수성 HCl, 5 % 수성 NaHCO3, 물 및 식염수로 세척하고, Na2SO4 상에서 건조시켰다. 용매를 진공에서 제거하여 0.30Og (81% 수율) 의 원하는 생성물을 수득하여, 추가 정제없이 사용했다. LC/MS ESI+MS 483 (M+1).
4-((S)-2-((S)-2-(메톡시카르보닐아미노)-3-페닐프로판아미도)-2-(2-에틸티아졸-4-일)에틸)페닐술팜산 암모늄 염 (13) 의 제조: tert-부틸 (S)-1-(S)-2-(4- 니트로페닐)-1-(2-에틸티아졸-4-일)에틸아미노-1-옥소-3-페닐프로판-2-일카르바메이트, 12, (0.30Og) 를 MeOH (4 mL) 에 용해시켰다. 촉매량의 Pd/C (10% w/w) 를 첨가하고, 혼합물을 수소 분위기 하에 18 시간 동안 교반했다. 반응 혼합물을 CELITE™ 의 층을 통해 여과하고, 용매를 감압 하에 제거했다. 미정제 생성물을 피리딘 (12 mL) 에 용해시키고, SO3-피리딘 (223 mg, 1.40 mmol) 으로 처리했다. 반응물을 실온에서 5 분 동안 교반한 후, NH4OH 의 7% 용액 (12 mL) 을 첨가했다. 이어서, 혼합물을 농축하고, 결과로서 수득한 잔사를 역상 크로마토그래피로 정제하여 25 mg 의 원하는 생성물을 암모늄 염으로 수득했다.
본 개시내용의 프로세스의 또다른 반복에서, 본 개시내용을 포함하는 화합물 13 뿐만 아니라 또다른 유사체가 하기 본원에 기재되는 과정을 채택함으로써 유리 산으로 단리될 수 있다.
시약 및 조건: (a) H2:Pd/C, MeOH; rt, 40 시간
시약 및 조건: (b) SO3-피리딘, CH3CN; 가열, 45 분.
실시예
4
4-((S)-2-((S)-2-(
메톡시카르보닐아미노
)-3-
페닐프로판아미도
)-2-(2-
에틸티
아졸-4-일)에틸)
페닐술팜산
[
유리 산
형태] (13)
{1-[2-(S)-(4-(S)-아미노페닐)-1-(2-에틸티아졸-4-일)에틸-카르바모일]-2-페닐에틸}-카르밤산메틸 에스테르 (12a) 의 제조: Parr 수소첨가 용기에 tert-부틸 (S)-1-(S)-2-(4-니트로페닐)-1-(2-에틸티아졸-4-일)에틸아미노-1-옥소-3-페닐프로판-2-일카르바메이트, 12, (18.05 g, 37.4 mmol, 1.0 eq) 및 고체로서의 Pd/C (C 상의 10% Pd, 50% 습도, Degussa-type E101 NE/W, 2.68 g, 15 wt %) 를 충전시켰다. MeOH (270 mL, 15 mL/g) 를 첨가하여 현탁액을 제공했다. 용기를 Parr 수소첨가 기구 상에 설치했다. 용기는 N2 (3 x 20 psi) 를 이용해 충전/진공 일소 프로세스에 적용해 불활성으로 만든 후, H2 (3 x 40 psi) 를 이용해 동일 과정을 진행했다. 용기를 H2 로 충전하고, 용기를 40 psi H2 하에 약 40 hr 동안 진탕시켰다. 용기를 진공으로 탈기시키고, 대기를 N2 (5 x 20 psi) 로 일소했다. 일 분취물을 여과하고 HPLC 로 분석으로 완전한 변환을 확인했다. 현탁액을 셀라이트의 패드로 여과하여 촉매를 제거하고, 균질 황색 여과액을 회전 증발기로 농축하여 16.06 g (95% 수율) 의 원하는 생성물을 갈색 고체로 수득하여, 추가 정제없이 사용했다.
4-((S)-2-((S)-2-(메톡시카르보닐)-3-페닐프로판아미도)-2-(2-에틸티아졸-4-일)에틸)페닐술팜산 (13) 의 제조: 100 mL RBF 를 상기 본원에 기재한 단계에서 제조한 {1-[2-(S)-(4-(S)-아미노페닐)-1-(2-에틸티아졸-4-일)에틸-카르바모일]-2-페닐에틸}-카르밤산메틸 에스테르, 12a, (10.36 g, 22.9 mmol, 1.0 eq) 로 충전했다. 아세토니트릴 (50 mL, 5 mL/g) 을 첨가하고, 황색 현탁액을 실온에서 교반했다. 제 2 의 3-목 500 mL RBF 를 SO3·pyr (5.13 g, 32.2 mmol, 1.4 eq) 및 아세토니트릴 (50 mL 5 mL/g) 로 충전시키고, 백색 현탁액을 실온에서 교반했다. 두 현탁액을 {1-[2-(S)-(4-(S)-아미노페닐)-1-(2-에틸티아졸-4-일)에틸-카르바모일]-2-페닐에틸}-카르밤산메틸 에스테르를 포함하는 반응 용액의 색상이 적색-오렌지로 변할 때까지 약하게 가열했다 (약 44℃). 용액을 포함하는 상기 기질을 SO3· pyr 의 교반 현탁액에 35℃ 에서 한번에 부었다. 결과로서 수득한 탁한 혼합물 (39℃) 을 세게 교반하면서, 실온으로 서서히 냉각되도록 했다. 45 분 동안 교반 후, HPLC 로 반응 완결을 결정했다. H2O (200 mL, 20 mL/g) 를 오렌지색 현탁액에 첨가하여 pH 가 약 2.4 인 황색-오렌지 균질 용액을 제공했다. 진한 H3PO4 을 12 분에 걸쳐 서서히 첨가하여 pH 를 약 1.4 로 낮췄다. 상기 pH 조정 동안, 오프-화이트 석출물이 형성되고, 용액을 실온에서 1 시간 동안 교반했다. 현탁액을 여과하고, 필터 케이크 (filter cake) 를 여과액으로 세척했다. 상기 필터 케이트를 필터 상에서 대기에서 건조시켜 10.89 g (89 % 수율) 의 원하는 생성물을 갈색 고체로 수득했다.
하기는 본 개시내용의 카테고리 II 의 제 2 국면의 추가적인 비제한적 예시이다.
4-{(S)-2-[(S)-2-(메톡시카르보닐아미노)-3-페닐프로판아미도]-2-(2-메틸티아졸-4-일)에틸}페닐술팜산:
4-{(S)-2-(2-에틸티아졸-4-일)-2-[(S)-2-(메톡시카르보닐아미노)-3-페닐프로판-아미도]에틸}페닐술팜산:
4-{(S)-2-(2-이소프로필티아졸-4-일)-2-[(S)-2-(메톡시카르보닐아미노)-3-페닐프로판-아미도]에틸}페닐술팜산:
4-{(S)-2-(2-시클로프로필티아졸-4-일)-2-[(S)-2-(메톡시카르보닐아미노)-3- 페닐프로판아미도]에틸}페닐술팜산:
4-{(S)-2-{2-[(4-클로로페닐술포닐)메틸]티아졸-4-일}-2-[(S)-2-(메톡시-카르보닐아미노)-3-페닐프로판아미도]에틸}페닐술팜산:
4-{(S)-2-[2-(tert-부틸술포닐메틸)티아졸-4-일]-2-[(S)-2-(메톡시카르보닐아미노)-3-페닐프로판아미도]에틸}페닐술팜산:
4-{(S)-2-[(S)-2-(메톡시카르보닐아미노)-3-페닐프로피온아미도]-2-(2-페닐티아졸-4-일)에틸}페닐술팜산:
4-{(S)-2-[(S)-2-(메톡시카르보닐아미노)-3-페닐프로판아미도]-2-[2-(티오펜-2-일)티아졸-4-일]에틸}페닐술팜산:
4-{(S)-2-[2-(3-클로로티오펜-2-일)티아졸-4-일]-2-[(S)-2-(메톡시카르보닐아미노)-3- 페닐프로판아미도]에틸}페닐술팜산:
4-{(S)-2-[(S)-2-(메톡시카르보닐아미노)-3-페닐프로판아미도]-2-[2-(3-메틸티오펜-2-일)티아졸-4-일]에틸}페닐술팜산:
4-{[(S)-2-(2-(푸란-2-일)티아졸-4-일]-2-[(S)-2-(메톡시카르보닐아미노)-3- 페닐프로판아미도]에틸}페닐술팜산:
4-{(S)-2-[(S)-2-(메톡시카르보닐아미노)-3-페닐프로판아미도]-2-[2-(2-메틸티아졸- 4-일)티아졸-4일]에틸}페닐술팜산:
4-{(S)-2-[(S)-2-(메톡시카르보닐아미노)-3-페닐프로판아미도]-2-[(2-피라진-2-일)티아졸-4-일]에틸}페닐술팜산:
4-{(S)-2-[(S)-2-(메톡시카르보닐아미노)-3-페닐프로판아미도]-2-[2-(6-메틸피리딘-3-일)티아졸-4-일]에틸}페닐술팜산:
본 개시내용의 카테고리 III 은 하기 화학식을 가진 R 이 치환 또는 비치환 티아졸-2-일인 화합물에 관한 것이다:
그의 한 구현예는 하기 화학식을 가진 억제제이다:
식 중, R 단위체는 티아졸-2-일 단위체이고, 치환된 경우, R2 및 R3 단위체로 치환되고,
R 및 R5a 단위체는 표 V 에 추가로 기재된다.
본 개시내용의 카테고리 III 에 속하는 화합물들은 하기 본원에서 반응식 IV 에 개요되고 실시예 5 에 기재된 과정으로 제조될 수 있다.
반응식 IV
시약 및 조건: (a) Ac-Phe, EDCI, HOBt, DIPEA, DMF; rt, 18 시간
시약 및 조건: (b) (i) H2:Pd/C, MeOH; (ii) SO3-피리딘, NH4OH.
실시예
5
4-[(S)-2-((S)-2-
아세트아미도
-3-
페닐프로판아미도
)-2-(4-
에틸티아졸
-2-일)에틸]
페닐술팜산
(15)
(S)-2-아세트아미도-N-[(S)-1-(4-에틸티아졸-2-일)-2-(4-니트로페닐)-에틸]-3- 페닐프로판아미드 (14) 의 제조: 1-(S)-(4-에틸티아졸-2-일)-2-(4-니트로페닐)에틸 아민 히드로브로마이드, 3, (0.343 g, 0.957 mmol), N-아세틸-L-페닐알라닌 (0.218 g), 1-히드록시벤조트리아졸 (HOBt) (0.161 g), 디이소프로필-에틸아민 (0.26 g) 의 DMF (10 mL) 중 용액에 0°에서, 1-(3-디메틸아미노프로필)-3-에틸카르보디이미드 (EDCI) (0.201 g) 를 첨가했다. 혼합물을 0℃ 에서 30 분, 이어서 실온에서 밤새 교반했다. 반응 혼합물을 물로 희석하고, EtOAc 로 추출했다. 조합한 유기상을 1 N 수성 HCl, 5 % 수성 NaHCO3, 물 및 식염수로 세척하고, Na2SO4 상에서 건조시켰다. 용매를 진공에서 제거하여 0.313 g (70 % 수율) 의 원하는 생성물을 수득하여, 추가 정제없이 사용했다. LC/MS ESI+ 467 (M+ 1).
4-((S)-2-((S)-2-아세트아미도-3-페닐프로판아미도)-2-(4-에틸티아졸-2-일)에틸)페닐술팜산 (15) 의 제조: (S)-2-아세트아미도-N-[(S)-1-(4-에틸티아졸-2-일)-2-(4-니트로페닐)에틸]-3-페닐프로판아미드, 14, (0.313 g) 를 MeOH (4 mL) 에 용해시켰따. 촉매량의 Pd/C (10% w/w) 를 첨가하고, 혼합물을 수소 분위기 하에 2 시간 동안 교반했다. 반응 혼합물을 CELITE™ 의 층을 통해 여과하고, 용매를 감압 하에 제거했다. 미정제 생성물을 피리딘 (12 mL) 에 용해시키고, SO3-피리딘 (0.320 g) 으로 처리했다. 반응물을 실온에서 5 분 동안 교반한 후, NH4OH 의 7% 용액 (30 mL) 을 첨가했다. 이어서, 혼합물을 농축하고, 결과로서 수득한 잔사를 역상 크로마토그래피로 정제해 0.215 g 의 원하는 생성물을 암모늄 염으로 수득했다.
하기는 본 개시내용의 카테고리 III 에 속하는 화합물들의 추가적인 비제한적 예시이다.
4-[(S)-2-((S)-2-아세트아미도-3-페닐프로판아미도)-2-(4-tert-부틸티아졸-2-일)에틸]페닐술팜산:
4-{(S)-2-((S)-2-아세트아미도-3-페닐프로판아미도)-2-[4-(티오펜-3-일)티아졸-2-일]에틸)페닐술팜산:
본 개시내용의 카테고리 IV 의 제 1 국면은 하기 화학식을 가진 R 이 치환 또는 비치환 티아졸-2-일 단위체인 화합물에 관한 것이다:
그의 한 구현예는 하기 화학식을 가진 억제제에 관한 것이다:
[식 중, R 단위체 및 R5a 단위체는 표 VI 에 추가로 기재됨].
본 개시내용의 카테고리 IV 에 속하는 화합물들은 하기 본원의 반응식 V 에 개요되고 실시예 6 에 기재한 과정으로 제조될 수 있다.
반응식 V
시약 및 조건: (a) Boc-Val; EDCI, HOBt, DIPEA, DMF; rt, 18 시간
시약 및 조건: (b) (i) H2:Pd/C, MeOH; (ii) SO3-피리딘, NH4OH, rt, 2 시간.
실시예
6
4-{(S)-2-[(S)-2-(
tert
-
부톡시카르보닐아미노
)-3-
메틸부탄아미도
]-2-(4-
에틸티아졸
-2-일)에틸}
페닐술팜산
(17)
tert-부틸 (S)-1-[(S)-(4-에틸티아졸-2-일)-2-(4-니트로페닐)에틸아미노]-3-메틸-1-옥소부탄-2-일카르바메이트 (16) 의 제조: 1-(S)-(4-에틸티아졸-2-일)-2-(4-니트로페닐)에틸 아민 히드로브로마이드, 3, (0.200 g, 0.558 mmol), (S)-(2-tert-부톡시카르보닐아미노)-3-메틸부티르산 (0.133 g) 및 1-히드록시벤조트리아졸 (HOBt) (0.094 g) 의 DMF (5 mL) 중 용액에 0°에서 1-(3-디메틸아미노프로필)-3-에틸카르보디이미드 (EDCI) (0.118 g) 에 이어 디이소프로필아민 (0.151 g) 을 첨가했다. 혼합물을 0℃ 에서 30 분, 이어서 실온에서 밤새 교반했다. 반응 혼합물을 물로 희석하고, EtOAc 로 추출했다. 조합한 유기상을 1 N 수성 HCl, 5 % 수성 NaHCO3, 물 및 식염수로 세척하고, Na2SO4 상에서 건조시켰다. 용매를 진공에서 제거하여 0.219 g (82% 수율) 의 원하는 생성물을 수득하여, 추가 정제없이 사용했다. LC/MS ESI+ 477 (M+1).
4-{(S)-2-[(S)-2-(tert-부톡시카르보닐아미노)-3-메틸부탄아미도]-2-(4-에틸티아졸-2-일)에틸}페닐술팜산 (17) 의 제조: tert-부틸 (S)-1-[(S)-(4-에틸티아졸-2-일)-2-(4-니트로페닐)에틸아미노]-3-메틸-1-옥소부탄-2-일카르바메이트, 16, (0.219 g) 를 MeOH (4 mL) 에 용해시켰다. 촉매량의 Pd/C (10% w/w) 를 첨가하고, 혼합물을 수소 분위기 하에 2 시간 동안 교반했다. 반응 혼합물을 CELITE™ 의 층을 통해 여과하고, 용매를 감압 하에 제거했다. 미정제 생성물을 피리딘 (5 mL) 에 용해시키고, SO3-피리딘 (0.146 g) 으로 처리했다. 반응물을 실온에서 5 분 동안 교반한 후, NH4OH 의 7% 용액 (30 mL) 을 첨가했다. 이어서, 혼합물을 농축하고, 결과로서 수득한 잔사를 역상 크로마토그래피로 정제하여 0.148 g 의 원하는 생성물을 암모늄 염으로 수득했다.
하기는 본 개시내용의 카테고리 IV 의 제 2 국면의 추가적인 비제한적 예시이다.
(S)-4-{2-[2-(tert-부톡시카르보닐)아세트아미드]-2-(4-에틸티아졸-2-일)에틸}-페닐술팜산:
4-{(S)-2-[(S)-2-(tert-부톡시카르보닐아미노)-4-메틸펜탄아미도]-2-(4-에틸티아졸-2-일)에틸}페닐술팜산:
4-{(S)-2-[(S)-2-(tert-부톡시카르보닐아미노)-4-메틸펜탄아미도]-2-[2-(티오펜-2-일)티아졸-4-일]에틸}페닐술팜산:
(S)-4-{2-[2-(tert-부톡시카르보닐)아세트아미드]-2-(4-에틸티아졸-2-일)에틸}-페닐술팜산:
카테고리 IV 의 추가 구현예는 하기 화학식을 가진 억제제이다:
[식 중, R 단위체 및 R5a 단위체는 표 VII 에 추가로 기재된다].
카테고리 IV 의 구현예에 속하는 화합물들은 해당하는 메틸카르바메이트를 Boc-보호 시약으로 치환하여 반응식 V 에 개요하고 실시예 6 에 기재된 과정에 따라 제조될 수 있다. 하기는 상기 구현예의 비제한적 예시이다.
4-{(S)-2-(4-에틸티아졸-2-일)-2-[(S)-2-(메톡시카르보닐)-4-메틸펜탄-아미도]에틸}페닐술팜산:
(S)-4-{2-(4-에틸티아졸-2-일)-2-[2-(메톡시카르보닐)아세트아미도]에틸}페닐-술팜산:
4-{(S)-2-(4-에틸티아졸-2-일)-2-[(S)-2-(메톡시카르보닐)-3-메틸부탄아미도]-에틸}페닐술팜산:
4-{(S)-2-[(S)-2-(메톡시카르보닐)-4-메틸펜탄아미도]-2-[2-(티오펜-2-일)티아졸-4-일]에틸}페닐술팜산:
본 개시내용의 카테고리 IV 는 하기 화학식을 가진 화합물에 관한 것이다:
[식 중, R 은 치환 또는 비치환 티오펜-2-일 또는 티오펜-4-일 단위체이고, R2 의 비제한적 예시는 표 VIII 에 추가로 기재되어 있음].
본 개시내용의 카테고리 IV 에 속하는 화합물들은 하기 본원의 반응식 VI 에 개요하고 실시예 7 에 기재한 과정으로 제조될 수 있다.
반응식 VI
시약 및 조건: (a)(i) CH3CN; 환류, 1.5 시간
(ii) Boc2O, 피리딘, CH2Cl2; rt, 2시간
시약 및 조건: (b)(i) H2:Pd/C, MeOH; 환류
(ii) SO3-피리딘, NH4OH; rt, 12 시간
실시예
7
[1-(S)-(
페닐티아졸
-2-일)-2-(4-
술포아미노페닐
)에틸]-
카르밤산
tert
-부틸 에스테르 (19)
[2-(4-니트로페닐)-1-(S)-(4-페닐티아졸-2-일)에틸]-카르밤산 tert-부틸 에스테르 (18) 의 제조: [2-(4-니트로페닐)-1-(S)-티오카르바모일에틸]-카르밤산 tert-부틸 에스테르, 2, (0.343 g, 1.05 mmol), 2-브로모아세토페논 (0.231 g, 1.15 mmol) 의 CH3CN (5 mL) 중 혼합물을 1.5 시간 동안 환류시켰다. 용매를 감압 하에 제거하고, 잔사를 CH2Cl2 에 재용해시킨 후, 피리딘 (0.24 mL, 3.0 mmol) 및 Boc2O (0.24 mL, 1.1 mmol) 를 첨가했다. 반응물을 2 시간 동안 교반하고, 디에틸 에테르를 용액에 첨가하고, 형성된 석출물을 여과로 제거했다. 유기층을 건조시키고 (Na2SO4), 여과하고, 농축하여 잔사를 실리카 상에서 정제하여 0.176 g (39%) 의 원하는 생성물을 수득했다 ESI+ MS 426 (M+ 1).
[1-(S)-(페닐티아졸-2-일)-2-(4-술포아미노페닐)에틸]-카르밤산 tert-부틸 에스테르 (19) 의 제조: [2-(4-니트로페닐)-1-(S)-(4-페닐티아졸-2-일)에틸]-카르밤산 tert-부틸 에스테르, 18, (0.176 g, 0.41 mmol) 를 MeOH (4 mL) 에 용해시켰다. 촉매량의 Pd/C (10% w/w) 를 첨가하고, 혼합물을 수소 분위기 하에 12 시간 동안 교반했다. 반응 혼합물을 CELITE™ 의 층을 통해 여과하고, 용매를 감압 하에 제거했다. 미정제 생성물을 피리딘 (12 mL) 에 용해시키고, SO3-피리딘 (0.195 g, 1.23 mmol) 로 처리했다. 반응물을 실온에서 5 분 동안 교반한 후, NH4OH 의 7% 용액 (10 mL) 을 첨가했다. 이어서, 혼합물을 농축하고, 결과로서 수득한 잔사를 역상 크로마토그래피로 정제하여 0.080 g 의 원하는 생성물을 암모늄 염으로 수득했다.
하기는 본 개시내용의 카테고리 VI 의 추가적인 비제한적 실시예이다.
(S)-4-(2-(4-메틸티아졸-2-일)-2-피발라미도에틸)페닐술팜산:
S-4-(2-(4-에틸티아졸-2-일)-2-피발라미도에틸)페닐술팜산:
(S)-4-(2-(4-(히드록시메틸)티아졸-2-일)-2-피발라미도에틸)페닐술팜산:
(S)-4-(2-(4-(에톡시카르보닐)티아졸-2-일)-2-피발라미도에틸)페닐술팜산:
(S)-4-(2-(4-페닐티아졸-2-일)-2-피발라미도에틸)페닐술팜산:
4-((S)-2-(4-(3-메톡시페닐)티아졸-2-일)-2-피발라미도에틸)페닐술팜산:
4-((S)-2-(4-(2,4-디메톡시페닐)티아졸-2-일)-2-피발라미도에틸)페닐술팜산:
(S)-4-(2-(4-벤질티아졸-2-일)-2-피발라미도에틸)페닐술팜산
(S)-4-(2-피발아미도-2-(4-(티오펜-2-일메틸)티아졸-2-일)에틸)페닐술팜산:
(S)-4-(2-(4-(3-메톡시벤질)티아졸-2-일)-2-피발라미도에틸)페닐술팜산:
4-((S)-2-(4-(2,3-디히드로벤조[b][1,4]디옥신-6-일)티아졸-2-일)-2-피발라미도에틸)-페닐술팜산:
(S)-4-(2-(5-메틸-4-페닐티아졸-2-일)-2-피발라미도에틸)페닐술팜산:
(S)-4-(2-(4-(비펜-4-일)티아졸-2-일)-2-피발라미도에틸)페닐술팜산:
(S)-4-(2-tert-부톡시카르보닐-2-(2-메틸티아졸-4-일)-페닐술팜산
(S)-4-(2-(tert-부톡시카르보닐)-2-(4-프로필티아졸-2-일)에틸)-페닐 술팜산:
(S)-4-(2-(tert-부톡시카르보닐)-2-(4-tert-부틸티아졸-2-일)에틸)-페닐 술팜산:
(S)-4-(2-(tert-부톡시카르보닐아미노)-2-(4-(메톡시메틸)티아졸-2-일)에틸)-페닐 술팜산:
(S)-4-(2-tert-부톡시카르보닐아미노)-2-(4-(2-히드록시메틸)티아졸-2-일)에틸)페닐술팜산:
(S)-4-(2-tert-부톡시카르보닐아미노)-2-(4-(2-에톡시-2-옥소에틸)-티아졸-2-일)-에틸)페닐술팜산:
(S)-4-(2-(tert-부톡시카르보닐아미노)-2-(4-(2-메톡시-2-옥소에틸)티아졸-2-일)에틸)페닐술팜산:
(S)-4-(2-(tert-부톡시카르보닐아미노)-2-(2-(피발로일옥시)티아졸-4-일)에틸)페닐술팜산:
(S)-4-(2-(tert-부톡시카르보닐아미노)-2-(5-페닐티아졸-2-일)에틸)-페닐 술팜산:
4-((S)-2-(tert-부톡시카르보닐아미노)-2-(4-(3-(트리플루오로메틸)페닐)티아졸-2-일)에틸)-페닐 술팜산:
(S)-4-(2-(tert-부톡시카르보닐아미노)-2-(4-페닐티아졸-2-일)에틸)-페닐 술팜산:
(S,S)-2-(2-{2-[2-tert-부톡시카르보닐아미노-2-(4-술포아미노페닐)에틸]티아졸-4-일}아세틸아미도)-3-페닐프로피온산 메틸 에스테르:
(S)-[1-{1-옥소-4-[2-(1-페닐-1H-테트라졸-5-술포닐)에틸]-1H-1λ4-티아졸-2-일}-2-(4-술파미노-페닐)-에틸]-카르밤산 tert-부틸 에스테르:
4-((S)-2-(tert-부톡시카르보닐아미노)-2-(4-(티오펜-3-일)티아졸-2-일)에틸)페닐 술팜산:
(S)-4-(2-(벤조[d]티아졸-2-일아미노)-2-(tert-부톡시카르보닐)에틸)페닐술팜산:
(S)-4-(2-tert-부톡시카르보닐아미노)-2-(2-메틸티아졸-4-일)-페닐술팜산:
본 개시내용의 카테고리 V 의 제 1 국면은 하기 화학식을 가진 2-(티아졸-2-일) 화합물에 관한 것이다:
식 중, R1, R2, R3 및 L 은 하기 본원의 표 IX 에 추가로 정의되어 있다.
본 개시내용의 카테고리 V 의 제 1 국면에 속하는 화합물들은 하기 본원의 반응식 VII 에 개요되고 실시예 8 에 기재된 과정으로 제조될 수 있다.
반응식 VII
시약 및 조건: (a) C6H4CO2H, EDCI, HOBt, DIPEA, DMF; rt, 18 시간
시약 및 조건: (b) (i) H2:Pd/C, MeOH; (ii) SO3-피리딘, NH4OH, rt, 18 시간
실시예
8
{4-[2-(S)-(4-
에틸티아졸
-2-일)-2-(2-
페닐아세틸아미도
)에틸]
페닐
}
술팜산
(21)
N-[1-(4-에틸티아졸-2-일)-2-(4-니트로페닐)에틸]-2-페닐-아세트아미드 (20) 의 제조: 1-(S)-(4-에틸티아졸-2-일)-2-(4-니트로페닐)에틸 아민 히드로브로마이드, 3, (0.393 g, 1.1 mmol), 페닐아세트산 (0.190 g, 1.4 mmol) 및 1-히드록시벤조트리아졸 (HOBt) (0.094 g, 0.70 mmol) 의 DMF (10 mL) 중 용액에 0°에서, 1-(3-디메틸아미노프로필)-3-에틸카르보디이미드 (EDCI) (0.268g, 1.4 mmol) 에 이어 트리에틸아민 (0.60 mL, 4.2mmol) 을 첨가했다. 혼합물을 0℃ 에서 30 분, 이어서 실온에서 밤새 교반했다. 반응 혼합물을 물로 희석하고, EtOAc 로 추출했다. 조합한 유기상을 1 N 수성 HCl, 5 % 수성 NaHCO3, 물 및 식염수로 세척하고, Na2SO4 상에서 건조시켰다. 용매를 진공에서 제거하여 0.260 g (60 % 수율) 의 원하는 생성물을 수득하여, 추가 정제없이 사용했다. ESI+ MS 396 (M+ 1).
{4-[2-(S)-(4-에틸티아졸-2-일)-2-(2-페닐아세틸아미도)에틸]-페닐}술팜산 (21) 의 제조: N-[1-(4-에틸티아졸-2-일)-2-(4-니트로페닐)에틸]-2-페닐-아세트아미드, 20, (0.260 g) 를 MeOH (4 mL) 에 용해시켰다. 촉매량의 Pd/C (10% w/w) 를 첨가하고, 혼합물을 수소 분위기 하에 18 시간 동안 교반했다. 반응 혼합물 CELITE™ 의 층을 통해 여과하고, 용매를 감압 하에 제거했다. 미정제 생성물을 피리딘 (12 mL) 에 용해시키고, SO3-피리딘 (0.177 g, 1.23) 를 첨가했다. 반응물을 실온에서 5 분 동안 교반한 후, NH4OH 의 7% 용액 (10 mL) 을 첨가했다. 이어서, 혼합물을 농축하고, 결과로서 수득한 잔사를 역상 크로마토그래피로 정제하여 0.136 g 의 원하는 생성물을 암모늄 염으로 수득했다.
하기는 본 개시내용의 카테고리 V 의 제 1 국면의 비제한적 예시이다.
(S)-4-(2-(4-에틸티아졸-2-일)-2-(2-(2-플루오로페닐)아세트아미도)에틸)페닐술팜산:
(S)-4-(2-(4-에틸티아졸-2-일)-2-(2-(3-플루오로페닐)아세트아미도)에틸)페닐술팜산:
(S)-4-(2-(2-(2,3-디플루오로페닐)아세트아미도)-2-(4-에틸티아졸-2-일)에틸)페닐-술팜산:
(S)-4-(2-(2-(3,4-디플루오로페닐)아세트아미도)-2-(4-에틸티아졸-2-일)에틸)페닐-술팜산:
(S)-4-(2-(2-(2-클로로페닐)아세트아미도)-2-(4-에틸티아졸-2-일)에틸)페닐술팜산:
(S)-4-(2-(2-(3-클로로페닐)아세트아미도)-2-(4-에틸티아졸-2-일)에틸)페닐술팜산:
(S)-4-(2-(4-에틸티아졸-2-일)-2-(2-(3-히드록시페닐)아세트아미도)에틸)페닐-술팜산:
(S)-4-(2-(4-에틸티아졸-2-일)-2-(2-(2-메톡시페닐)아세트아미도)에틸)페닐-술팜산:
(S)-4-{2-(4-에틸티아졸-2-일)-2-[2-(3-메톡시페닐)아세트아미도]에틸}-페닐술팜산:
(S)-4-(2-(4-에틸티아졸-2-일)-2-(3-페닐프로판아미도)에틸)페닐술팜산:
(S)-4-(2-(2-(3,4-디메톡시페닐)아세트아미도)-2-(4-에틸티아졸-2-일)에틸)-페닐술팜산:
(S)-4-(2-(2-(2,3-디메톡시페닐)아세트아미도)-2-(4-에틸티아졸-2-일)에틸)-페닐술팜산:
(S)-4-(2-(3-(3-클로로페닐)프로판아미도)-2-(4-에틸티아졸-2-일)에틸)페닐-술팜산:
(S)-4-(2-(4-에틸티아졸-2-일)-2-(3-(2-메톡시페닐)프로판아미도)에틸)페닐-술팜산:
(S)-4-(2-(4-에틸티아졸-2-일)-2-(3-(3-메톡시페닐)프로판아미도)에틸)페닐-술팜산:
(S)-4-(2-(4-에틸티아졸-2-일)-2-(3-(4-메톡시페닐)프로판아미도)에틸)페닐-술팜산:
(S)-4-{2-[2-(4-에틸-2,3-디옥소피페라진-1-일)아세트아미도]-2-(4-에틸티아졸-2-일)에틸}페닐술팜산:
(S)-4-{2-(4-에틸티아졸-2-일)-2-[2-(5-메틸-2,4-디옥소-3,4-디히드로피리미딘-1(2H)-일)아세트아미도]에틸}페닐술팜산:
(S)-4-[2-(벤조[d][1,3]디옥솔-5-카르복사미도)-2-(4-에틸티아졸-2-일)에틸]-페닐술팜산:
(S)-4-{2-[2-(2,5-디메틸티아졸-4-일)아세트아미도]-2-(4-에틸티아졸-2-일)에틸}-페닐술팜산:
(S)-4-{2-[2-(2,4-디메틸티아졸-5-일)아세트아미도]-2-(4-메틸티아졸-2-일)에틸}-페닐술팜산:
(S)-4-{2-(4-에틸티아졸-2-일)-2-[3-(티아졸-2-일)프로판아미도]에틸}페닐술팜산:
(S)-4-{2-(4-에틸티아졸-2-일)-2-[2-(4-에틸티아졸-2-일)아세트아미도]에틸}페닐-술팜산:
본 개시내용의 카테고리 V 의 제 2 국면은 하기 화학식을 가진 2-(티아졸-4-일) 화합물에 관한 것이다:
[식 중, R1, R4 및 L 은 하기 본원의 표 X 에 추가로 정의되어 있음].
본 개시내용의 카테고리 I 의 제 2 국면에 속하는 화합물들은 하기 본원의 반응식 II 에 개요하고 실시예 9 에 기재한 과정으로 제조될 수 있다.
반응식 VIII
시약 및 조건: (a) CH3CN; 환류 5 시간
시약 및 조건: (b) (3-Cl)C6H4CO2H, EDCI, HOBt, DIPEA, DMF; rt, 18 시간
시약 및 조건: (c) (i) H2:Pd/C, MeOH; (ii) SO3-피리딘, NH4OH, rt, 18 시간
실시예
9
4-((S)-2-(2-(3-
클로로페닐
)
아세트아미도
)-2-(2-(티오펜-2-일)티아졸-4-일)에틸)
페닐술팜산
(23)
(S)-2-(4-니트로페닐)-1-[(티오펜-2-일)티아졸-4-일]에탄아민 히드로브로마이드 염 (22) 의 제조: (S)-tert-부틸 4-브로모-1-(4-니트로페닐)-3-옥소부탄-2-일카르바메이트, 7, (7.74 g, 20 mmol) 및 티오펜-2-카르보티오산 아미드 (3.14 g, 22 mmol) 의 CH3CN (200 mL) 중 혼합물을 5 시간 동안 환류시켰다. 반응 혼합물을 실온으로 냉각시키고, 디에틸 에테르 (50 mL) 를 용액에 첨가했다. 형성된 석출물을 여과로 수집했다. 고체를 진공 하에 건조시켜 7.14 g (87 % 수율) 의 원하는 생성물을 수득했다. ESI+ MS 332 (M+1).
2-(3-클로로페닐)-N-{(S)-2-(4-니트로페닐)-1-[2-(티오펜-2-일)티아졸-4-일]에틸}아세트아미드 (23) 의 제조: 2-(4-니트로페닐)-1-(2-티오펜2-일티아졸-4-일)에틸아민, 22, (0.41 g, 1 mmol) 3-클로로페닐아세트산 (0.17O g, 1 mmol) 및 1- 히드록시벤조트리아졸 (HOBt) (0.07O g, 0.50 mmol) 의 DMF (5 mL) 중 용액에 0°에서, 1-(3-디메틸아미노프로필)-3-에틸카르보디이미드 (EDCI) (0.19O g, 1 mmol) 에 이어 트리에틸아민 (0.42 mL, 3 mmol) 을 첨가했다. 혼합물을 0℃ 에서 30 분, 이어서 실온에서 밤새 교반했다. 반응 혼합물을 물로 희석하고, EtOAc 로 추출했다. 조합한 유기상을 1 N 수성 HCl, 5 % 수성 NaHCO3, 물 및 식염수로 세척하고, Na2SO4 상에서 건조시켰다. 용매를 진공에서 제거하여 0.290 g (60 % 수율) 의 원하는 생성물을 수득하여, 추가 정제없이 사용했다. ESI-MS 482 (M-I).
{4-[2-(3-클로로페닐)아세틸아미노]-2-(2-티오펜-2-일티아졸-4-일)에틸]페닐} 술팜산 (24) 의 제조: 2-(3-클로로페닐)-N-{(S)-2-(4-니트로페닐)-1-[2-(티오펜2-일)티아졸-4-일]에틸}아세트아미드, 23, (0.290 g) 를 MeOH (4 mL) 에 용해시켰다. 촉매량의 Pd/C (10% w/w) 를 첨가하고, 혼합물을 수소 분위기 하에 18 시간 동안 교반했다. 반응 혼합물을 CELITE™ 의 층을 통해 여과하고, 용매를 감압 하에 제거했다. 미정제 생성물을 피리딘 (12 mL) 에 용해시키고, SO3-피리딘 (0.157 g) 를 처리했다. 반응물을 실온에서 5 분 동안 교반한 후, NH4OH 의 7% 용액을 첨가했다. 이어서, 혼합물을 농축하고, 결과로서 수득한 잔사를 역상 크로마토그래피로 정제하여 0.078 g 의 원하는 생성물을 암모늄 염으로 수득했다.
1H NMR (CD3OD) δ 7.61 (d, 1H, J = 3.6Hz), 7.58 (d, 1H, J = 5.1Hz), 7.41-7.35 (m, 1H), 7.28-7.22 (m, 2H), 7.18-6.98 (m, 6H), 5.33 (t, 1H, J = 6.6Hz), 3.70 (d, 2H, J = 3.9Hz), 3.23 (IH, A of ABX, J = 6.6, 13.8Hz), 3.07 (1H, B of ABX, J = 8.1, 13.5Hz).
하기는 본 개시내용의 카테고리 V 의 제 2 국면에 속하는 화합물들의 비제한적 예시이다.
4-((S)-2-(2-(3-메톡시페닐)아세트아미도)-2-(2-(티오펜2-일)티아졸-4-일)에틸)-페닐술팜산:
4-{(S)-2-(3-페닐프로판아미도)-2-[2-(티오펜2-일)티아졸-4-일]에틸}-페닐술팜산:
4-{(S)-2-(3-(3-클로로페닐)프로판아미도)-2-[2-(티오펜2-일)티아졸-4-일]에틸}페닐술팜산:
4-{(S)-2-[2-(3-플루오로페닐)아세트아미도]-2-[2-(티오펜-2-일)티아졸-4-일]에틸}페닐술팜산:
(S)-4-{2-[2-(3-메틸-1,2,4-옥사디아졸-5-일)아세트아미도]-2-(2-페닐티아졸-4-일)에틸}페닐술팜산:
4-{(S)-2-[2-(4-에틸-2,3-디옥소피페라진-1-일)아세트아미도]-2-[2-(티오펜-2-일)티아졸-4-일]에틸}페닐술팜산:
본 개시내용의 카테고리 V 의 제 3 국면은 하기 화학식을 가진 화합물에 관한 것이다:
[식 중, 연결 단위체 L 은 페닐 단위체를 포함하며, 상기 연결기는 하기 화학식을 갖는다:
[식 중, R1 은 수소이고, R6a 은 페닐이고, R5a 은 페닐 또는 치환 페닐이며, 단위체 R2, R3 및 R5a 의 비제한적 예시는 표 XI 에 하기 본원에 추가로 예시됨].
본 개시내용의 카테고리 V 에 속하는 화합물들을 하기 본원의 반응식 IX 에 개요하고 실시예 10 에 기재하는 과정으로 제조할 수 있다.
반응식 IX
시약 및 조건: (a) 디페닐프로피온산, EDCI, HOBt, TEA, DMF;
0℃ 내지 rt, 18 시간
시약 및 조건: (b) (i) H2:Pd/C, MeOH; (ii) SO3-피리딘, NH4OH; rt, 18 시간
실시예
10
(S)-4-(2-(2,3-
디페닐프로판아미도
)-2-(4-
에틸티아졸
-2-일)에틸)-
페닐술팜산
(26)
(S)-N-[1-(4-에틸티아졸-2-일)-2-(4-니트로페닐)에틸]-2,3-디페닐-프로판아미드 (25) 의 제조: 1-(S)-(4-에틸티아졸-2-일)-2-(4-니트로페닐)에틸 아민 히드로브로마이드, 3, (0.95 g, 2.65 mmol), 디페닐프로피온산 (0.60 g, 2.65 mmol) 및 1-히드록시벤조트리아졸 (HOBt) (0.180 g, 1.33 mmol) 의 DMF (10 mL) 중 용액에 0°에서, 1-(3-디메틸아미노프로필)-3-에틸카르보디이미드 (EDCI) (0.502 g, 2.62 mmol) 에 이어 트리에틸아민 (1.1 mL, 7.95 mmol) 을 첨가했다. 혼합물을 0℃ 에서 30 분, 이어서 실온에서 밤새 교반했다. 반응 혼합물을 물로 희석하고, EtOAc 로 추출했다. 조합한 유기상을 1 N 수성 HCl, 5 % 수성 NaHCO3, 물 및 식염수로 세척하고, Na2SO4 상에서 건조시켰다. 용매를 진공에서 제거하여 0.903 g (70% 수율) 의 원하는 생성물을 수득하여, 추가 정제없이 사용했다.
(S)-4-(2-(2,3-디페닐프로판아미도)-2-(4-에틸티아졸-2-일)에틸)페닐술팜산 (26) 의 제조: (S)-N-[1-(4-에틸티아졸-2-일)-2-(4-니트로페닐)에틸]-2,3-디페닐-프로판아미드, 25, (0.903 g) 를 MeOH (10 mL) 에 용해시켰다. 촉매량의 Pd/C (10% w/w) 를 첨가하고, 혼합물을 수소 분위기 하에 18 시간 동안 교반했다. 반응 혼합물을 CELITE™ 의 층을 통해 여과하고, 용매를 감압 하에 제거했다. 미정제 생성물을 피리딘 (30 mL) 에 용해시키고, SO3-피리딘 (0.621 g) 으로 처리했다. 반응물을 실온에서 5 분 동안 교반한 후, NH4OH 의 7% 용액을 첨가했다. 이어서, 혼합물을 농축하고, 결과로서 수득한 잔사를 역상 크로마토그래피로 정제하여 0.415 g 의 원하는 생성물을 암모늄 염으로 수득했다.
카테고리 V 의 제 3 국면을 포함하는 Z 단위체의 다수의 전구체는 쉽게 입수가능하지 않다. 하기의 과정은 본 개시내용에 따라 상이한 R5a 단위체를 제공하기 위해 사용될 수 있는 과정의 예시를 설명한다. 반응식 X 에 개요되고 실시예 11 에 기재된 과정을 이용하여, 당업자는 기약없는 실험없이도 본 개시 내용에 속하는 R5a 단위체를 수득하기 위해 변형을 행할 수 있다.
반응식 X
시약 및 조건: (a) 벤질 브로마이드, LDA, THF;
0℃ 내지 rt 18 시간
시약 및 조건: (b) NaOH, THF/MeOH; rt, 18 시간
실시예
11
2-(2-
메톡시페닐
)-3-
페닐프로판산
(28)
메틸 2-(2-메톡시페닐)-3-페닐프로파노에이트 (27) 의 제조: 50O mL 둥근바닥 플라스크에 메틸 2-(2-메톡시페닐)아세테이트 (8.496 g, 47 mmol, 1 eq) 및 THF (20O mL) 를 충전했다. 균질 혼합물을 빙욕에서 0℃ 로 냉각시켰다. 리튬 디이소프로필 아미드 (23.5 mL 의, 헵탄/THF 중 2.0M 용액) 를 첨가하고, 온도를 3℃ 미만으로 유지했다. 반응물을 45 분 동안 상기 강하된 온도에서 교반했다. 벤질 브로마이드 (5.6mL, 47mmol, 1 eq) 를 적가했다. 반응물을 실온으로 점차 승온되도록 하고, 18 시간 동안 교반했다. 반응물을 1 N HCl 로 켄칭하고, 동량의 EtOAc 로 3 회 추출했다. 조합된 추출물을 H2O 및 식염수로 세척하고, Na2SO4 상에서 건조시키고, 여과하고 농축했다. 잔사를 실리카 상에서 정제하여 4.433 g (35%) 의 원하는 화합물을 수득했다. ESI+ MS 293 (M+Na).
2-(2-메톡시페닐)-3-페닐프로판산 (28) 의 제조: 메틸 2-(2-메톡시페닐)-3-페닐프로파노에이트 (4.433g, 16 mmol, 1 eq) 을 THF 및 메탄올의 1:1 (v:v) 혼합물 100 mL 에 용해시켰다. 나트륨 히드록시드 (3.28 g, 82 mmol, 5 eq) 를 첨가하고, 반응 혼합물을 실온에서 18 시간 동안 교반했다. 이어서, 반응물을 H2O 에 붓고, pH 를 1 N HCl 의 첨가를 통해 2 로 조정했다. 백색 석출물이 형성되어 여과로 제거했다. 결과로서 수득한 용액을 3 부의 디에틸 에테르로 추출했다. 추출물을 모으고, H2O 및 식염수로 세척하고, Na2SO4 상에서 건조시키고, 여과하고, 진공에서 농축했다. 결과로서 수득한 잔사를 실리카 상에서 정제하여 2.107 g (51%) 의 원하는 화합물을 수득했다. ESI-MS 255 (M-1), 211 (M-CO2H).
중간체 28 의 제조는 카테고리 V 의 제 3 국면에 따라 하기 화합물을 제조하기 위해 반응식 IX 에 개요하고 실시예 10 에 기재한 과정에 따라 수행될 수 있다.
(S)-4-{2-(4-에틸티아졸-2-일)-2-[2-(2-메톡시페닐)-3-페닐프로판아미도]-에틸}페닐술팜산:
하기는 본 개시내용의 카테고리 I 의 제 3 국면에 따른 화합물들의 추가적인 비제한적 예시이다.
(S)-4-{2-(4-에틸티아졸-2-일)-2-[2-(3-플루오로페닐)-3-페닐프로판아미도]-에틸}페닐술팜산:
(S)-4-{2-(4-에틸티아졸-2-일)-2-[2-(3-메톡시페닐)-3-페닐프로판아미도]-에틸}페닐술팜산:
본 개시내용의 카테고리 V 의 제 4 국면은 하기 화학식을 가진 화합물들에 관한 것이다:
[식 중, 연결 단위체 L 은 페닐 단위체를 포함하고, 상기 연결기는 하기 화학식을 갖고:
-C(O)[(CR5aH)][(CR6aH]-
R1 은 수소이고, R6a 은 페닐이고, R5a 는 치환 또는 비치환 헤테로아릴이고, 단위체 R2, R3 및 R5a 는 표 XII 에서 하기 본원에서 추가로 예시됨].
본 개시내용의 카테고리 V 의 제 4 국면에 속하는 화합물들은 하기 본원의 반응식 V 에서 개요하고 실시예 5 에 기재한 과정으로 제조될 수 있다.
반응식 XI
시약 및 조건 (a) 2-벤질-3-에톡시-3-옥소프로판산, EDCI, HOBt, DIPEA, DMF; rt, 18 시간
시약 및 조건: (b) CH3C(=NOH)NH2, K2CO3, 톨루엔; 환류, 18 hr
시약 및 조건: (c) (i) 주석 (II) 클로라이드, EtOH; (ii) SO3-피리딘, NH4OH; rt, 18 시간
실시예
12
4-{(S)-2-(4-
에틸티아졸
-2-일)-2-[2-(3-
메틸
-1,2,4-
옥사디아졸
-5-일)-3-
페
닐프로판아미도]에틸}
페닐술팜산
(31)
에틸-2-벤질-3-[(S)-1-(4-에틸티아졸-2-일)-2-(4-니트로페닐)-에틸아미노]-3-옥소프로파노에이트 (29) 의 제조: 1-(S)-(4-에틸티아졸-2-일)-2-(4-니트로페닐)에틸 아민 히드로브로마이드, 3, (0.406 g, 1.13 mmol), 2-벤질-3-에톡시-3-옥소프로판산 (0.277 g) 및 1-히드록시벤조트리아졸 (HOBt) (0.191 g, 1.41 mmol) 의 DMF (10 mL) 중 용액에 0°에서, 1-(3-디메틸아미노프로필)-3-에틸카르보디이미드 (EDCI) (0.240 g, 1.25 mmol) 에 이어 디이소프로필에틸아민 (DIPEA) (0.306 g) 을 첨가했다. 혼합물을 0℃ 에서 30 분, 이어서 실온에서 밤새 교반했다. 반응 혼합물을 물로 희석하고, EtOAc 로 추출했다. 조합한 유기상을 1 N 수성 HCl, 5% 수성 NaHCO3, 물 및 식염수로 세척하고, Na2SO4 상에서 건조시켰다. 용매를 진공에서 제거하여 0.169 g (31 % 수율) 의 원하는 생성물을 수득하여, 추가 정제없이 사용했다.
N-[(S)-1-(4-에틸티아졸-2-일)-2-(4-니트로페닐)에틸]-2-(3-메틸-1,2,4-옥사디아졸-5-일)-3-페닐프로판아미드 (30) 의 제조: 에틸 2-벤질-3-((S)-1-(4-에틸티아졸-2-일)-2-(4-니트로페닐)에틸아미노)-3-옥소프로파노에이트를 톨루엔 (5 mL) 에 용해시키고, 환류될 때까지 가열했다. 칼륨 카르보네이트 (80 mg) 및 아세트아미드 옥심 (43 mg) 을 첨가하고, 80 mg 칼륨 카르보네이트 및 43 mg 아세트아미드 옥심을 환류시 처리했다. 반응 혼합물을 실온으로 냉각시키고,, 여과하고 농축했다. 잔사를 실리카 상에서 크로마토그래피하여 0.221 g (94%) 의 원하는 생성물을 황색 오일로 수득했다.
4-{(S)-2-(4-에틸티아졸-2-일)-2-[2-(3-메틸-1,2,4-옥사디아졸-5-일)-3-페닐프로판아미도]에틸}페닐술팜산 (31) 의 제조: N-[(S)-1-(4-에틸티아졸-2-일)-2-(4- 니트로페닐)에틸]-2-(3-메틸-1,2,4-옥사디아졸-5-일)-3-페닐프로판아미드, 30, (0.221 g) 및 주석 (II) 클로라이드 (507 mg, 2.2 mmol) 를 EtOH (25 mL) 에 용해시키고, 상기 용액을 4 시간 동안 환류시켰다. 용매를 진공에서 제거하고, 결과로서 수득한 잔사를 EtOAc 에 용해시켰다. NaHCO3 의 포화 용액 (50 mL) 을 첨가하고, 상기 용액을 1 시간 동안 교반했다. 유기층을 분리하고, 수층을 EtOAc 로 2 회 추출했다. 조합한 유기층을 건조시키고 (Na2SO4), 여과하고 잔사로 농축하여, 그것을 피리딘 (0.143 g) 에 용해시키고, SO3-피리딘 (0.143 g) 으로 처리했다. 반응물을 실온에서 5 분 동안 교반한 후, NH4OH 의 7% 용액을 첨가했다. 이어서, 혼합물을 농축하고, 결과로서 수득한 잔사를 역상 크로마토그래피로 정제하여 0.071g 의 원하는 생성물을 암모늄 염으로 수득했다.
본 개시내용의 카테고리 VI 은 하기 화학식을 가진 2-(티아졸-2-일) 화합물들에 관한 것이다:
식 중, R1, R2, R3 및 L 은 하기 표 XIII 에서 본원에서 추가로 정의된다.
본 개시내용의 카테고리 VI 에 속하는 화합물들은 하기 본원의 반응식 XII 에 개요하고 실시예 13 에 기재한 과정으로 제조될 수 있다.
반응식 VI
시약 및 조건: (a) 3-벤조일프로피온산, SOCl2, N-메틸 이미다졸, CH2Cl2; rt, 18 시간
시약 및 조건: (b) (i) H2:Pd/C, MeOH; (ii) SO3-피리딘, NH4OH.
실시예 13
(S)-4-[2-(4-에틸티아졸-2-일)-2-(4-옥소-4-페닐부탄아미도)에틸]-페닐술팜산 (33)
(S)-N-[1-(4-에틸티아졸-2-일)-2-(4-니트로페닐)에틸]-4-옥소-4-페닐부탄아미드 (32) 의 제조: 3-벤조일프로피온산 (0.250 g) 을 CH2Cl2 (5 mL) 에 용해시키고, N-메틸 이미다졸 (0.333 mL) 을 첨가하고, 결과로서 수득한 용액을 0℃ 로 냉각시킨 후, 티오닐 클로라이드 (0.320 g) 의 CH2Cl2 (2 mL) 중 용액을 적가했다. 0.5 시간 후, (S)-1-(4-에틸티아졸-2-일)-2-(4-니트로페닐)에탄아민, 3, (0.388 g) 을 첨가했다. 반응물을 18 시간 동안 실온에서 교반하고, 이어서 진공에서 농축했다. 결과로서 수득한 잔사를 EtOAc 에 용해시키고, 1N HCl 및 식염수로 세척했다. 상기 용액을 Na2SO4 상에서 건조시키고, 여과하고, 농축하여, 미정제 물질을 실리카 상에서 정제하여 0.415 g 의 원하는 생성물을 수득했다.
(S)-4-[2-(4-에틸티아졸-2-일)-2-(4-옥소-4-페닐부탄아미도)-에틸]페닐술팜산 (33) 의 제조: (S)-N-[1-(4-에틸티아졸-2-일)-2-(4-니트로페닐)에틸]-2,3-디페닐-프로판아미드, 32, (0.2 g) 를 MeOH (15 mL) 에 용해시켰다. 촉매량의 Pd/C (10% w/w) 를 첨가하고, 혼합물을 수소 분위기 하에 18 시간 동안 교반했다. 반응 혼합물을 CELITE™ 의 층을 통해 여과하고, 용매를 감압 하에 제거했다. 미정제 생성물을 피리딘 (5 mL) 에 용해시키고, SO3-피리딘 (0.153 g) 으로 처리했다. 반응물을 실온에서 5 분 동안 교반한 후, NH4OH 의 7% 용액을 첨가했다. 이어서, 혼합물을 농축하고, 결과로서 수득한 잔사를 역상 크로마토그래피로 정제하여 0.090 g 의 원하는 생성물을 암모늄 염으로 수득했다.
하기는 본 개시내용의 카테고리 II 에 속하는 화합물들의 비제한적 예시이다. 하기 화학식의 중간체 니트로 화합물은 반응식 I 의 중간체 4 에 대해 상기 본원에 기재한 조건 하에 적당한 4-옥소-카르복실산을 중간체 3 과 커플링시켜 제조할 수 있다.
(S)-4-(2-(4-에틸티아졸-2-일)-2-(5-메틸-4-옥소헥산아미도)에틸)페닐술팜산:
(S)-4-{2-[4-(3,4-디히드로-2H-벤조[b][1,4]디옥세핀-7-일)-4-옥소부탄아미도]-2-(4-에틸티아졸-2-일)에틸}페닐술팜산:
(S)-4-{2-[4-(2,3-디메톡시페닐)-4-옥소부탄아미도]-2-(4-에틸티아졸-2-일)에틸}페닐술팜산:
(S)-4-{2-(4-에틸티아졸-2-일)-2-[4-옥소-4-(피리딘-2-일)부탄아미도]에틸}-페닐술팜산:
(S)-4-{2-[4-(2,3-디히드로벤조[b][1,4]디옥신-6-일)-4-옥소부탄아미도]-2-(4-에틸티아졸-2-일)에틸}페닐술팜산:
(S)-4-[2-(4-tert-부톡시-4-옥소부탄아미도)-2-(4-에틸티아졸-2-일)에틸]페닐술팜산:
(S)-4-[2-(4-에톡시-4-옥소부탄아미도)-2-(4-에틸티아졸-2-일)에틸]페닐술팜산:
본 개시내용의 카테고리 VII 의 제 1 국면은 하기 화학식을 가진 2-(티아졸-2-일) 화합물들에 관한 것이다:
[식 중, R1, R2 및 R3 의 비제한적 예시는 표 XIV 의 하기 본원에 추가로 기재되어 있음].
본 개시내용의 카테고리 VII 에 속하는 화합물들은 하기 본원의 반응식 VIII 에 개요되고 실시예 14 에 기재된 과정으로 제조될 수 있다.
반응식 XIII
시약 및 조건: (a) 벤질 이소시아네이트, TEA, CH2Cl2; rt, 18 시간
시약 및 조건: (b) (i) H2:Pd/C, MeOH; (ii) SO3-피리딘, NH4OH.
실시예
14
(S)-4-(2-(3-
벤질우레이도
)-2-(4-
에틸티아졸
-2-일)에틸)
페닐술팜산
(35)
(S)-1-벤질-3-[1-(4-에틸티아졸-2-일)-2-(4-니트로페닐)에틸]우레아 (34) 의 제조: 1-(S)-(4-에틸티아졸-2-일)-2-(4-니트로페닐)에틸 아민 히드로브로마이드, 3, (0.360 g, 1 mmol) 및 Et3N (0.42 mL, 3 mmol) 의 10 mL CH2Cl2 중 용액에 벤질 이소시아네이트 (0.12 mL, 1 mmol) 를 첨가했다. 상기 혼합물을 실온에서 18 시간 동안 교반했다. 생성물을 여과로 단리하여 0.425 g (96% 수율) 의 원하는 생성물을 수득하여, 추가 정제없이 사용했다.
(S)-4-(2-(3-벤질우레이도)-2-(4-에틸티아졸-2-일)에틸)페닐술팜산 (35) 의 제조: (S)-1-벤질-3-[1-(4-에틸티아졸-2-일)-2-(4-니트로페닐)에틸]우레아, 34, (0.425 g) 를 MeOH (4 mL) 에 용해시켰다. 촉매량의 Pd/C (10% w/w) 를 첨가하고, 혼합물을 수소 분위기 하에 18 시간 동안 교반했다. 반응 혼합물을 CELITE™ 의 층을 통해 여과하고, 용매를 감압 하에 제거했다. 미정제 생성물을 피리딘 (12 mL) 에 용해시키고, SO3-피리딘 (0.220 g) 을 처리했다. 반응물을 실온에서 6 분 동안 교반한 후, NH4OH 의 7% 용액을 첨가했다. 이어서, 혼합물을 농축하고, 결과로서 수득한 잔사를 역상 크로마토그래피로 정제하여 0.143 g 의 원하는 생성물을 암모늄 염으로 수득했다.
하기는 본 개시내용의 카테고리 VII 의 제 1 국면에 속하는 화합물들의 비제한적 예시이다.
4-{[(S)-2-(2-에틸티아졸-4-일)-2-(3-(R)-메톡시-1-옥소-3-페닐프로판-2-일)우레이도]에틸}페닐술팜산:
본 개시내용의 카테고리 VII 의 제 2 국면은 하기 화학식을 가진 2-(티아졸-4-일) 화합물들에 관한 것이다:
[식 중, R1 및 R4 의 비제한적 예시는 표 XV 에서 하기 본원에 추가로 기재됨].
본 개시내용의 카테고리 VII 의 제 2 국면에 속하는 화합물들은 하기 본원의 반응식 XIV 에 개요되고 실시예 14 에 기재된 과정으로 제조될 수 있다.
반응식 XIV
시약 및 조건 (a) 벤질 이소시아네이트, TEA, CH2Cl2; rt, 18 시간
시약 및 조건: (b) (i) H2:Pd/C, MeOH; (ii) SO3-피리딘, NH4OH.
실시예
15
4-{(S)-2-(3-
벤질우레이도
)-2-[2-(티오펜-2-일)티아졸-4-일]에틸}-
페닐술팜산
(37)
1-벤질-3-{(S)-2-(4-니트로페닐)-1-[2-(티오펜-2-일)티아졸-4-일]에틸}우레아 (36) 의 제조: (S)-2-(4-니트로페닐)-1-[(2-티오펜-2-일)티아졸-4-일)에탄아민 히드로브로마이드 염, 8, 및 Et3N (0.42 mL, 3 mmol) 의 10 mL DCM 중 용액에 벤질 이소시아네이트 (0.12 mL, 1 mmol) 를 첨가했다. 상기 혼합물을 실온에서 18 시간 동안 교반했다. 생성물을 여과로 단리하여 0.445 g (96% 수율) 의 원하는 생성물을 수득하여, 추가 정제없이 사용했다.
4-{(S)-2-(3-벤질우레이도)-2-[2-(티오펜-2-일)티아졸-4-일]에틸}페닐술팜산 (37) 의 제조: 1-벤질-3-{(S)-2-(4-니트로페닐)-1-[2-(티오펜-2-일)티아졸-4-일]에틸}우레아, 36, (0.445 g) 를 MeOH (10 mL) 및 CH2Cl2 (5 mL) 에 용해시켰다. 촉매량의 Pd/C (10% w/w) 를 첨가하고, 혼합물을 수소 분위기 하에 18 시간 동안 교반했다. 반응 혼합물을 CELITE™ 의 층을 통해 여과하고, 용매를 감압 하에 제거했다. 미정제 생성물을 피리딘 (12 mL) 에 용해시키고, SO3-피리딘 (0.110 g) 으로 처리했다. 반응물을 실온에서 5 분 동안 교반한 후, NH4OH 의 7% 용액을 첨가했다. 이어서, 혼합물을 농축하고, 결과로서 수득한 잔사를 역상 크로마토그래피로 정제하여 0.080 g 의 원하는 생성물을 암모늄 염으로 수득했다.
본 개시내용의 카테고리 VIII 은 하기 화학식을 가진 2-(티아졸-4-일) 화합물들에 관한 것이다:
[식 중, R1, R4 및 L 은 하기 본원의 표 XVI 에서 본원에서 추가로 정의됨].
본 개시내용의 카테고리 VIII 에 속하는 화합물들은 하기 본원의 반응식 XV 에서 개요하고 실시예 16 에 기재한 과정으로 제조될 수 있다.
반응식 XV
시약 및 조건: (a) C6H4CH2SO2Cl, DIPEA, CH2Cl2; 0℃ 내지 rt, 14 시간
시약 및 조건: (b) (i) H2:Pd/C, MeOH; (ii) SO3-피리딘, NH4OH.
실시예
16
{4-(S)-[2-
페닐메탄술포닐아미노
-2-(2-티오펜-2-
일티아졸
-4-일)에틸]
페닐
} 술팜산 (39)
(S)-N-{2-(4-니트로페닐)-1-[2-(티오펜-2-일)티아졸-4-일] 에틸}-1-페닐메탄술폰아미드 (38) 의 제조: 2-(4-니트로페닐)-1-(2-티오펜2-일티아졸-4-일)에틸아민, 8, (330 mg, 0.80 mmol) 의 CH2Cl2 (6 mL) 중 현탁액에 0℃ 에서 디이소프로필에틸아민 (0.30 mL, 1.6 mmol) 에 이어 페닐메탄술포닐 클로라이드 (167 mg, 0.88 mmol) 를 첨가했다. 반응 혼합물을 실온에서 14 시간 동안 교반했다. 혼합물을 CH2Cl2 로 희석하고, 포화 NaHCO3 에 이어 식염수로 세척하고, 건조시키고 (Na2SO4), 여과하고 진공에서 농축시켰다. 결과로서 수득한 잔사를 실리카 상에서 정제시켜 210 mg 의 원하는 생성물을 백색 고체로 수득했다.
{4-(S)-[2-페닐메탄술포닐아미노-2-(2-티오펜-2-일티아졸-4-일)에틸]페닐} 술팜산 (39) 의 제조: (S)-N-{2-(4-니트로페닐)-1-[2-(티오펜-2-일)티아졸-4-일] 에틸}-1-페닐메탄술폰아미드, 38, (210 mg, 0.41 mmol) 를 MeOH (4 mL) 에 용해시켰다. 촉매량의 Pd/C (10% w/w) 를 첨가하고, 혼합물을 수소 분위기 하에 18 시간 동안 교반했다. 반응 혼합물을 CELITE™ 의 층을 통해 여과하고, 용매를 감압 하에 제거했다. 미정제 생성물을 피리딘 (12 mL) 에 용해시키고, SO3-피리딘 (197 mg, 1.23 mmol) 으로 처리했다. 반응물을 실온에서 5 분 동안 교반한 후, NH4OH 의 7% 용액을 첨가했다. 이어서, 혼합물을 농축하고, 결과로서 수득한 잔사를 역상 크로마토그래피로 정제하여 0.060 g 의 원하는 생성물을 암모늄 염으로 수득했다.
반응식 XV 의 단계 (a) 에 사용하기 위한 중간체는 반응식 XVI 에서 하기 본원에 개요하고 실시예 17 에 기재한 과정으로 편리하게 제조할 수 있다.
반응식 XVI
시약 및 조건: (a) Na2SO3, H2O; 200℃ 에서 마이크로파, 20 분.
시약 및 조건: (b) PCl5, POCl3; 50℃, 3 시간.
실시예
17
(2-
메틸티아졸
-4-일)
메탄술포닐
클로라이드 (41)
나트륨 (2-메틸티아졸-4-일)메탄술포네이트 (40) 의 제조: 4-클로로메틸-2- 메틸티아졸 (250 mg, 1.69 mmol) 을 H2O (2 mL) 에 용해시키고, 아황산나트륨 (224 mg, 1.78 mmol) 으로 처리했다. 반응 혼합물을 200℃ 에서 20 분 동안의 마이크로파 조사에 적용했다. 반응 혼합물을 H2O (30 mL) 로 희석하고, EtOAc (2 x 25 mL) 로 세척했다. 수층을 농축하여 0.368g 의 원하는 생성물을 황색 고체로 수득했다. LC/MS ESI+ 194 (M+1, 유리 산).
(2-메틸티아졸-4-일)메탄술포닐 클로라이드 (41) 의 제조: 나트륨 (2-메틸티아졸-4-일)메탄술포네이트, 40, (357 mg, 1.66 mmol) 을 포스포러스 옥시클로라이드 (6 mL) 에 용해시키고, 포스포러스 펜타클로라이드 (345 mg, 1.66 mmol) 로 처리했다. 반응 혼합물을 50℃ 에서 3 시간 동안 교반한 후, 실온으로 냉각되도록 했다. 용매를 감압 하에 제거하고, 잔사를 CH2Cl2 (40 mL) 에 재용해시키고, 포화 NaHCO3 및 식염수로 세척했다. 유기층을 MgSO4 상에서 건조시키고, 여과하고, 용매를 진공에서 제거하여 0.095 g 의 원하는 생성물을 브라운 오일로 수득했다. LC/MS ESI+ 211 (M+1). 반응식 IX 에 따라 수행해 중간체들을 충분한 순도로 수득하여, 추가 정제가 필요없었다.
4-{(S)-2-[(2-메틸티아졸-4-일)메틸술폰아미도]-2-[2-(티오펜-2-일)티아졸-4-일]에틸}페닐술팜산:
하기는 본 개시내용의 카테고리 VIII 에 속하는 화합물들의 비제한적 예시이다.
{4-(S)-[2-페닐메탄술포닐아미노-2-(2-에틸티아졸-4-일)에틸]페닐}-술팜산:
{4-(S)-[2-(3-메톡시페닐)메탄술포닐아미노-2-(2-에틸티아졸-4-일)에틸]페닐} 술팜산:
(S)-4-{[1-(2-에틸티아졸-4-일)-2-(4-술포아미노페닐)에틸술파모일]메틸}-벤조산 메틸 에스테르:
(S)-4-[2-(2-에틸티아졸-4-일)-2-(1-메틸-1H-이미다졸-4-술폰아미도)에틸]-페닐술팜산:
4-{(S)-2-[2-(티오펜-2-일)티아졸-4-일]-2-(2,2,2-트리플루오로에틸술폰아미도)-에틸}페닐술팜산:
{4-(S)-[2-(페닐에탄술포닐아미노)-2-(2티오펜-2-일티아졸-4-일)에틸]-페닐} 술팜산:
{4-(S)-[3-(페닐프로판술포닐아미노)-2-(2티오펜-2-일티아졸-4-일)에틸]-페닐} 술팜산:
(S)-{4-[2-(4-메틸-3,4-디히드로-2H-벤조[1,4]옥사진-7-술포닐아미노)-2-(2-티오펜- 2-일티아졸-4-일)에틸]페닐} 술팜산:
4-{(S)-2-(4-아세트아미도페닐술폰아미도)-2-[2-(티오펜-2-일)티아졸-4-일]에틸}페닐술팜산:
본 개시내용의 카테고리 IX 의 제 1 국면은 하기 화학식을 가진 화합물들에 관한 것이다:
[식 중, R1 은 치환 또는 비치환 헤테로아릴이고, R4 는 C1-C6 선형, 분지형 또는 고리형 알킬이며, 이들은 표 XVII 에서 하기 본원에 추가로 기재됨].
R1 에 대한 치환 또는 비치환 티아졸-4-일 단위체를 포함하는 카테고리 IX 의 제 1 국면에 따른 화합물들은 반응식 XVII 에 개요되고 실시예 18 에서 하기에 기재된 과정으로 제조될 수 있다.
반응식 XVII
시약 및 조건: (a) CH3CN, 환류; 24 시간
시약 및 조건: (b) 티오포스겐, CaCO3, CCl4, H2O; rt, 18 시간
시약 및 조건: (c) KOtBu, THF; rt, 2시간
시약 및 조건: (d) (i) SnCl2-2H2O, EtOH; 환류, 4 시간 (ii) SO3-피리딘, NH4OH.
실시예 18
(S)-4-(2-(2-페닐티아졸-4-일)2-(4-(메톡시카르보닐)티아졸-5-일아미노)에틸)페닐술팜산 (45)
(S)-2-(4-니트로페닐)-1-(2-페닐티아졸-4-일)에탄아민 히드로브로마이드 염 (42) 의 제조: (S)-tert-부틸 4-브로모-1-(4-니트로페닐)-3-옥소부탄-2-일카르바메이트, 7, (1.62 g, 4.17 mmol) 및 티오벤즈아미드 (0.63 g, 4.60 mmol) 의 CH3CN (5 mL) 중 혼합물을 24 시간 동안 환류시켰다. 반응 혼합물을 실온으로 냉각시키고, 디에틸 에테르 (50 mL) 를 용액에 첨가했다. 형성된 석출물을 여과로 수집했다. 고체를 진공에서 건조시켜 1.2 g (67% 수율) 의 원하는 생성물을 수득했다. LC/MS ESI+ 326 (M+ 1).
(S)-4-(1-이소티오시아나토-2-(4-니트로페닐)에틸)-2-페닐티아졸 (43) 의 제조: (S)-2-(4-니트로페닐)-1-(2-페닐티아졸-4-일)에탄아민 히드로브로마이드 염, 42, (726 mg, 1.79 mmol) 및 CaCO3 (716 mg, 7.16 mmol) 의 H2O (2 mL) 중 용액에 CCl4 (3 mL) 에 이어 티오포스겐 (0.28 mL, 3.58 mmol) 을 첨가했다. 반응물을 실온에서 18 시간 동안 교반시킨 후, CH2Cl2 및 물로 희석했다. 층들을 분리하고, 수층을 CH2Cl2 로 추출했다. 조합한 유기층을 식염수로 세척하고, 건조시키고 (Na2SO4), 진공에서 농축하여 잔사를 수득해 실리카 상에서 정제하여 (CH2Cl2) 480 mg (73 %) 의 원하는 생성물을 황색 고체로 수득했다.
(S)-메틸 5-[1-(2-페닐티아졸-4-일)-2-(4-니트로페닐)-에틸아미노]티아졸-4-카르복실레이트 (44) 의 제조: 칼륨 tert-부톡시드 (89 mg, 0.75 mmol) 의 THF (3 mL) 중 현탁액에 메틸 이소시아노아세테이트 (65 μL, 0.68 mmol) 에 이어 (S)-2-페닐-4-(1-이소티오시아나토-2-(4-니트로페닐)에틸)티아졸, 43, (250 mg, 0.68 mmol) 을 첨가했다. 반응 혼합물을 실온에서 2 시간 동안 교반한 후, 포화 NaHCO3 에 부었다. 혼합물을 EtOAc (3x 25 mL) 로 추출하고, 조합한 유기층을 식염수로 세척하고, 건조시키고 (Na2SO4), 진공에서 농축했다. 미정제 잔사를 실리카 상에서 정제하여 323 mg (약 100% 수율) 의 원하는 생성물을 연황색 고체로 수득했다.
(S)-4-(2-(2-페닐티아졸-4-일)2-(4-(메톡시카르보닐)티아졸-5-일아미노)에틸)페닐술팜산 (45) 의 제조: (S)-메틸 5-[1-(2-페닐티아졸-4-일)-2-(4-니트로페닐)-에틸아미노]티아졸-4-카르복실레이트, 44, (323 mg, 0.68 mmol) 및 주석 (II) 클로라이드 (612 mg, 2.72 mmol) 를 EtOH 에 용해시키고, 상기 용액을 환류시켰다. 용매를 진공에서 제거하고, 결과로서 수득한 잔사를 EtOAc 에 용해시켰다. NaHCO3 의 포화 용액을 첨가하고, 상기 용액을 1 시간 동안 교반했다. 유기층을 분리하고, 수층을 EtOAc 로 2 회 추출했다. 조합한 유기층을 건조시키고 (Na2SO4), 여과하고, 농축하여 잔사를 피리딘 (10 mL) 에 용해시키고, SO3-피리딘 (130 mg, 0.82 mmol) 으로 처리했다. 반응물을 실온에서 5 분 동안 교반한 후, NH4OH 의 7% 용액을 첨가했다. 이어서, 혼합물을 농축하고, 결과로서 수득한 잔사를 역상 크로마토그래피로 정제하여 0.071 g 의 원하는 생성물을 암모늄 염으로 수득했다.
R1 에 대한 치환 또는 비치환 티아졸-2-일 단위체를 포함하는 카테고리 IX 의 제 1 국면에 따른 화합물들은 반응식 XVIII 에 개요하고 실시예 19 에서 하기 본원에 기재한 과정으로 제조될 수 있다. 중간체 46 은 시클로프로판-카르보티오산 아미드를 티오펜-2-카르보티오산 아미드에 대해 치환해 반응식 II 및 실시예 2 에 따라 제조할 수 있다.
반응식 XVIII
시약 및 조건: (a) 티오포스겐, CaCO3, CCl4/H2O; rt, 18 시간
시약 및 조건: (b) CH3CN, 환류, 24 시간
시약 및 조건: (c) (i) H2:Pd/C, MeOH; (ii) SO3-피리딘, NH4OH.
실시예
19
4-{(S)-2-(2-
시클로프로필티아졸
-4-일)-2-[4-(3-
메톡시페닐
)티아졸-2-
일아미노
]에틸}
페닐술팜산
(50)
(S)-1-(1-(2-시클로프로필티아졸-4-일)-2-(4-니트로페닐)에틸)-티오우레아 (47) 의 제조: (S)-1-(2-시클로프로필티아졸-4-일)-2-(4-니트로페닐)에탄-아민 히드로브로마이드 히드로브로마이드 염, 32, (4.04 g, 10.9 mmol) 및 CaCO3 (2.18 g, 21.8 mmol) 의 CCl4/물 (25 mL/20 mL) 중 용액에 티오포스겐 (1.5 g, 13.1 mmol) 을 첨가했다. 반응물을 실온에서 18 시간 동안 교반한 후, CH2Cl2 및 물로 희석했다. 층들을 분리하고, 수층을 CH2Cl2 로 추출했다. 조합한 유기층을 식염수로 세척하고, 건조시키고 (Na2SO4), 진공에서 농축하고, 잔사를 후속하여 암모니아 (1,4-디옥산 중 0.5M, 120 mL) 로 처리하고, 실리카 상에서 정제하여 2.90 g 의 원하는 생성물을 적갈색 고체로 수득했다. LC/MS ESI-347 (M-1).
(S)-4-(3-메톡시벤질)-N-(1-(2-시클로프로필티아졸-4-일)-2-(4-니트로페닐)에틸)티아졸-2-아민 (48) 의 제조: (S)-1-(1-(2-시클로프로필티아졸-4-일)-2-(4- 니트로페닐)에틸)-티오우레아, 47, (350 mg, 1.00 mmol) 및 2-브로모-3'-메톡시-아세토페논 (253 mg, 1.10 mmol) 을 3 mL CH3CN 에서 조합하여 24 시간 동안 환류시까지 가열했다. 혼합물을 농축하고 크로마토그래피하여 0.172 g 의 생성물을 황색 고체로 수득했다. LC/MS ESI+ 479 (M+1).
4-{(S)-2-(2-시클로프로필티아졸-4-일)-2-[4-(3-메톡시페닐)-티아졸-2-일아미노]에틸}페닐술팜산 (49) 의 제조: (S)-4-(3-메톡시벤질)-N-(1-(2-시클로프로필티아졸-4-일)-2-(4-니트로페닐)에틸)티아졸-2-아민, 48, (0.172 g) 을 10 mL MeOH 에 용해시켰다. 촉매량의 Pd/C (10% w/w) 를 첨가하고, 혼합물을 수소 분위기 하에 18 시간 동안 교반했다. 반응 혼합물을 CELITE™ 의 층을 통해 여과하고, 용매를 감압 하에 제거했다. 미정제 생성물을 5 mL 피리딘에 용해시키고, SO3-피리딘 (114 mg) 을 처리했다. 반응물을 실온에서 5 분 동안 교반한 후, 10 mL 의, NH4OH 의 7% 용액을 첨가했다. 이어서, 혼합물을 농축하고, 결과로서 수득한 잔사를 역상 크로마토그래피로 정제하여 0.033 g 의 원하는 생성물을 암모늄 염으로 수득했다.
하기는 카테고리 IX 의 제 1 국면에 속하는 화합물들의 비제한적 예시이다.
(S)-4-(2-(4-((2-메톡시-2-옥소에틸)카르바모일)티아졸-5-일아미노)2-(2-에틸티아졸-4-일)에틸)페닐술팜산:
(S)-4-(2-{5-[1-N-(2-메톡시-2-옥소에틸카르바모일)-1-H-인돌-3-일]옥사졸-2-일아미노}-2-(2-메틸티아졸-4-일)에틸)페닐술팜산:
4-((S)-2-(5-(2-메톡시페닐)옥사졸-2-일아미노)-2-(2-메틸티아졸-4-일)에틸)페닐술팜산:
4-((S)-2-(5-((S)-1-(tert-부톡시카르보닐)-2-페닐에틸)옥사졸-2-일아미노)-2-(2-메틸티아졸-4-일)에틸)페닐술팜산:
(S)-{4-{2-[5-(4-메톡시카르보닐)페닐]옥사졸-2-일아미노}-2-(2-메틸티아졸-4-일)에틸}페닐술팜산:
(S)-4-(2-(5-(3-메톡시벤질)옥사졸-2-일아미노)-2-(2-메틸티아졸-4-일)에틸)페닐술팜산:
(S)-4-(2-(2-메틸티아졸-4-일)2-(5-페닐옥사졸-2-일아미노)에틸)페닐술팜산:
4-((S)-2-(2-시클로프로필티아졸-4-일)-2-(4-(3-메톡시페닐)티아졸-2-일아미노)에틸)페닐술팜산:
(S)-4-(2-(2-시클로프로필티아졸-4-일)-2-(4-(4-플루오로페닐)티아졸-2-일아미노)에틸)페닐술팜산:
4-((S)-2-(2-시클로프로필티아졸-4-일)-2-(4-(2-메톡시페닐)티아졸-2-일아미노)에틸)페닐술팜산:
4-((S)-2-(2-시클로프로필티아졸-4-일)-2-(4-(2,4-디플루오로페닐)티아졸-2-일아미노)에틸)페닐술팜산:
(S)-4-(2-(4-(3-메톡시벤질)티아졸-2-일아미노)-2-(2-시클로프로필티아졸-4-일)에틸)페닐술팜산:
(S)-{5-[1-(2-에틸티아졸-4-일)-2-(4-술포아미노페닐)에틸아미노]-2-메틸-2H-[1,2,4]트리아졸-3-일}카르밤산메틸 에스테르:
본 개시내용의 카테고리 V 의 제 2 국면은 하기 화학식을 가진 화합물들에 관한 것이다:
[식 중, R1 은 치환 또는 비치환 헤테로아릴이고, R4 는 치환 또는 비치환 페닐 및 치환 또는 비치환 헤테로아릴이고, 이들은 표 XVIII 에서 하기 본원에 추가로 기재됨].
R1 에 대한 치환 또는 비치환 티아졸-4-일 단위체를 포함하는 카테고리 IX 의 제 2 국면에 따른 화합물들은 반응식 XIX, XX 및 XXI 에서 개요되고, 실시예 20, 21 및 22 에서 하기 본원에 기재된 과정으로 제조될 수 있다.
반응식 XIX
시약 및 조건: (a)(i) (이소-부틸)OCOCl, Et3N, THF; 0℃, 20 분.
(ii) CH2N2; 0℃ 내지 실온에서 3 시간.
시약 및 조건: (b) 48% HBr, THF; 0℃, 1.5 시간
시약 및 조건: (c) CH3CN; 환류 2 시간.
시약 및 조건: (d) 티오포스겐, CaCO3, CCl4, H2O; rt, 18 시간
시약 및 조건: (e)(i) CH3C(O)NHNH2, EtOH; 환류, 2 시간
(ii) POCl3, rt 18 시간; 50℃ 2 시간
시약 및 조건: (f) (i) H2:Pd/C, MeOH; (ii) SO3-피리딘, NH4OH.
실시예 20
(S)-4-(2-(5-
메틸
-1,3,4-
티아디아졸
-2-
일아미노
)-2-(2-
페닐티아졸
-4-일)에틸)
페닐술팜산
(55)
[3-디아조-1-(4-니트로벤질)-2-옥소-프로필]-카르밤산 tert-부틸 에스테르 (50) 의 제조: 2-(5)-tert-부톡시카르보닐아미노-3-(4-니트로페닐)-프로피온산 (1.20 g, 4.0 mmol) 의 THF (20 mL) 중 0℃ 용액에 트리에틸아민 (0.61 mL, 4.4 mmol) 에 이어 이소-부틸 클로로포르메이트 (0.57 mL, 4.4 mmol) 를 적가했다. 반응 혼합물을 0℃ 에서 20 분간 교반한 후 여과했다. 여과액을 디아조메탄 (~16 mmol) 의 에테르 용액으로 0℃ 에서 처리했다. 반응 혼합물을 실온에서 3 시간 동안 교반하고 농축했다. 잔사를 EtOAc 에 용해시키고, 물 및 식염수로 순차적으로 세척하고, 건조시키고 (Na2SO4), 여과하고, 진공에서 농축했다. 결과로서 수득한 잔사를 실리카 상에서 정제하여 (헥산/EtOAc 2:1), 1.1 g (82% 수율) 의 원하는 생성물을 연황색 고체로 수득했다.
[3-브로모-1-(4-니트로-벤질)-2-옥소-프로필]-카르밤산 tert-부틸 에스테르 (51) 의 제조: [3-디아조-1-(4-니트로벤질)-2-옥소-프로필]-카르밤산 tert-부틸 에스테르, 50, (0.350 g, 1.04 mmol) 의 THF (5 mL) 중 0℃ 용액에 48% aq. HBr (0.14 mL, 1.25 mmol) 를 첨가했다. 반응 혼합물을 0℃ 에서 1.5 시간 동안 교반하고, 포화 수성 Na2CO3 로 0℃ 에서 켄칭했다. 혼합물을 EtOAc (3 x 25 mL) 로 추출하고, 조합한 유기 추출물을 식염수로 세척하고, 건조시키고 (Na2SO4), 여과하고, 진공에서 농축하여 0.400 g 의 원하는 생성물을 수득해, 추가 정제없이 후속 단계에서 사용했다.
(S)-2-(4-니트로페닐)-1-(2-페닐티아졸-4-일)에탄아민 히드로브로마이드 염 (52) 의 제조: [3-브로모-1-(4-니트로-벤질)-2-옥소-프로필]-카르밤산 tert-부틸 에스테르, 51, (1.62 g, 4.17 mmol) 및 벤조티오아미드 (0.630 g, 4.59 mmol) 의 CH3CN (5 mL) 중 혼합물을 24 시간 동안 환류시켰다. 반응 혼합물을 실온으로 냉각시키고, 디에틸 에테르 (50 mL) 를 상기 용액에 첨가하고, 형성된 석출물을 여과로 수집했다. 고체를 진공 하에 건조시켜 1.059 g (63%) 의 원하는 생성물을 수득했다. ESI+MS 326 (M+1).
(S)-4-[1-이소티오시아나토-2-(4-니트로페닐)-에틸]-2-페닐티아졸 (53) 의 제조: (S)-2-(4-니트로페닐)-1-(2-페닐티아졸-4-일)에탄아민 히드로브로마이드 염, 52, (2.03g, 5 mmol) 및 CaCO3 (1 g, 10 mmol) 의 CCl4/물 (10:7.5 mL) 중 용액에 티오포스겐 (0.46 mL, 6 mmol) 을 첨가했다. 반응물을 실온에서 18 시간 동안 교반한 후, CH2Cl2 및 물로 세척했다. 층들을 분리하고, 수층을 CH2Cl2 로 추출했다. 조합한 유기층을 식염수로 세척하고, 건조시키고 (Na2SO4), 진공에서 농축하여 잔사를 수득해 실리카 상에서 정제하여 (CH2Cl2), 1.71 g (93% 수율) 의 원하는 생성물을 수득했다. ESI+ MS 368 (M+1).
(S)-5-메틸-N-[2-(4-니트로페닐)-1-(2-페닐티아졸-4-일)에틸]-1,3,4-티아디아졸-2-아민 (54) 의 제조: (S)-4-[1-이소티오시아나토-2-(4-니트로페닐)-에틸]-2-페닐티아졸, 53, (332 mg, 0.876 mmol) 및 아세트 히드라지드 (65 mg, 0.876 mmol) 의 EtOH (5 mL) 중 용액을 2 시간 동안 환류시켰다. 용매를 감압 하에 제거하고, 잔사를 POCl3 (3 mL) 에 용해시키고, 결과로서 수득한 용액을 실온에서 18 시간 동안 교반한 후, 용액을 50℃ 로 2 시간 동안 교반했다. 용매를 진공에서 제거하고, 잔사를 EtOAc (40 mL) 에 용해시키고, pH 가 약 8 에 머무를 때까지 결과로서 수득한 용액을 1 N NaOH 로 처리했다. 상기 용액을 EtOAc 로 처리했다. 조합한 수층을 EtOAc 로 세척하고, 유기층을 조합하고, 식염수로 세척하고, MgSO4 상에서 건조시키고, 여과하고, 진공에서 농축하여 0.345 g (93% 수율) 의 원하는 생성물을 황색 고체로 수득했다.
(S)-4-[2-(5-메틸-1,3,4-티아디아졸-2-일아미노)-2-(2-페닐티아졸-4-일)에틸]페닐술팜산 (55) 의 제조: (S)-5-메틸-N-[2-(4-니트로페닐)-1-(2-페닐티아졸-4-일)에틸]-1,3,4-티아디아졸-2-아민, 54, (0.404 g, 0.954 mmol) 을 MeOH (5 mL) 에 용해시켰다. Pd/C (50 mg, 10% w/w) 를 첨가하고, 반응이 완결된 것으로 판단될 때까지 혼합물을 수소 분위기 하에 교반했다. 반응 혼합물을 CELITE™ 의 층을 통해 여과하고, 용매를 감압 하에 제거했다. 미정제 생성물을 피리딘 (4 mL) 에 용해시키고, SO3-피리딘 (0.304 g, 1.91 mmol) 를 처리했다. 반응물을 실온에서 5 분 동안 교반한 후, NH4OH 의 7% 용액 (50 mL) 을 첨가했다. 이어서, 혼합물을 농축하고, 결과로서 수득한 잔사를 역상 예비 HPLC 로 정제하여 0.052 g (11% 수율) 의 원하는 생성물을 암모늄 염으로 수득했다.
반응식 XX
시약 및 조건: (a) 티오포스겐, CaCO3, CCl4/H2O; rt, 18 시간
시약 및 조건: (b) CH3CN, 환류, 5 시간
시약 및 조건: (c) (i) H2:Pd/C, MeOH; (ii) SO3-피리딘, NH4OH; rt, 18 시간
실시예
21
4-{(S)-2-[4-(2-
메톡시페닐
)티아졸-2-
일아미노
)-2-[2-(티오펜-2-일)티아졸-4-일]에틸}
페닐술팜산
(58)
(S)-1-[1-(티오펜-2-일티아졸-4-일)-2-(4-니트로페닐)에틸]-티오우레아 (56) 의 제조: (S)-2-(4-니트로페닐)-1-(티오펜-2-일티아졸-4-일)에탄아민 히드로브로마이드 염, 8, (1.23 g, 2.98 mmol) 및 CaCO3 (0.597 g, 5.96 mmol) 의 CCl4/물 (10 mL/5 mL) 중 용액에 티오포스겐 (0.412g, 3.58 mmol) 을 첨가했다. 반응물을 실온에서 18 시간 동안 교반한 후, CH2Cl2 및 물로 희석했다. 층들을 분리하고, 수층을 CH2Cl2 로 추출했다. 조합한 유기층을 식염수로 세척하고, 건조시키고 (Na2SO4), 진공에서 농축하여 잔사를 후속하여 디옥산 중 암모니아 (1,4- 디옥산 중 0.5 M, 29.4 mL, 14.7 mmol) 로 처리하고, 실리카 상에서 정제하여 0.490 g 의 원하는 생성물을 적갈색 고체로 수득했다. ESI+ MS 399 (M+ 1).
4-(2-메톡시페닐)-N-{(S)-2-(4-니트로페닐)-1-[2-(티오펜-2-일)티아졸-4-일]에틸}티아졸-2-아민 (57) 의 제조: (S)-1-[1-(티오펜-2-일티아졸-4-일)-2-(4-니트로페닐)에틸]-티오우레아, 56, (265 mg, 0.679 mmol) 를 브로모-2'-메톡시아세토페논 (171 mg, 0.746 mmol) 으로 처리하여 0.221 g 의 생성물을 황색 고체로 수득했다. ESI+ MS 521 (M+1).
4-{(S)-2-[4-(2-메톡시페닐)티아졸-2-일아미노)-2-[2-(티오펜-2-일)티아졸-4-일]에틸}페닐술팜산 (58) 의 제조: 4-(2-메톡시페닐)-N-{(S)-2-(4-니트로페닐)- 1-[2-(티오펜-2-일)티아졸-4-일]에틸}티아졸-2-아민, 57, (0.229 g) 을 12 mL MeOH 에 용해시켰다. 촉매량의 Pd/C (10% w/w) 을 첨가하고, 혼합물을 수소 분위기 하에 18 시간 동안 교반했다. 반응 혼합물을 CELITE™ 의 층을 통해 여과하고, 용매를 감압 하에 제거했다. 미정제 생성물을 6 mL 피리딘에 용해시키고, SO3-피리딘 (140 mg) 으로 처리했다. 반응물을 실온에서 5 분 동안 교반한 후, 10 mL 의, NH4OH 의 7% 용액을 첨가했다. 이어서, 혼합물을 농축하고, 결과로서 수득한 잔사를 역상 크로마토그래피로 정제하여 0.033g 의 원하는 생성물을 암모늄 염으로 수득했다.
R1 에 대한 치환 또는 비치환 옥사졸-2-일 단위츨 포함하는 카테고리 IX 의 제 2 국면에 따른 화합물들을 반응식 XXI 에 개요하고, 실시예 22 에서 하기 본원에 기재한 과정으로 제조할 수 있다. 중간체 39 는 반응식 XVII 및 실시예 18 에 따라 제조할 수 있다.
반응식 XXI
시약 및 조건: (a) 1-아지도-1-(3-메톡시페닐)에타논, PPh3, 디옥산, 90℃ 20 분.
시약 및 조건: (b) (i) H2:Pd/C, MeOH; (ii) SO3-피리딘, NH4OH; rt, 18 시간
실시예
22
4-{(S)-2-[5-(3-
메톡시페닐
)
옥사졸
-2-
일아미노
]-2-(2-
페닐티아졸
-4-일)에틸}페닐술팜산 (61)
[5-(3-메톡시페닐)옥사졸-2-일]-[2-(4-니트로페닐)-1-(2-페닐티아졸-4-일)에틸아민 (60) 의 제조: (S)-4-(이소티오시아나토-2-(4-니트로페닐)에틸)-2-페닐티아졸, 53, (300 mg, 0.81 mmol), 1-아지도-1-(3-메톡시페닐)에타논 (382 mg, 2.0 mmol) 및 PPh3 (0.8 g, 중합체 결합, 약 3 mmol/g) 의 디옥산 (6 mL) 중 혼합물을 90℃ 에서 20 분 동안 가열했다. 반응 용액을 실온으로 냉각시키고, 용매를 진공에서 제거하고, 결과로서 수득한 잔사를 실리카 상에서 정제하여 300 mg (74% 수율) 의 원하는 생성물을 황색 고체로 수득했다.
4-{(S)-2-[5-(3-메톡시페닐)옥사졸-2-일아미노]-2-(2-페닐티아졸-4-일)에틸}페닐술팜산 (61) 의 제조: [5-(3-메톡시페닐)옥사졸-2-일]-[2-(4-니트로페닐)-l-(2-페닐티아졸-4-일) 에틸]아민, 60, (300 mg, 0.60 mmol) 을 MeOH (15 mL) 에 용해시켰다. 촉매량의 Pd/C (10% w/w) 를 첨가하고, 혼합물을 수소 분위기 하에 18 시간 동안 교반했다. 반응 혼합물을 CELITE™ 의 층을 통해 여과하고, 용매를 감압 하에 제거했다. 미정제 생성물을 피리딘 (10 mL) 에 용해시키고, SO3-피리딘 (190 mg, 1.2 mmol) 을 처리했다. 반응물을 실온에서 5 분 동안 교반한 후, NH4OH 의 7% 용액을 첨가했다. 이어서, 혼합물을 농축하고, 결과로서 수득한 잔사를 역상 크로마토그래피로 정제하여 0.042 g 의 원하는 생성물을 암모늄 염으로 수득했다.
하기는 본 개시내용의 카테고리 IX 의 제 2 국면의 비제한적 예시이다.
(S)-4-(2-(5-페닐-1,3,4-티아디아졸-2-일아미노)-2-(2-페닐티아졸-4-일)에틸)-페닐술팜산:
4-((S)-2-(5-프로필-1,3,4-티아디아졸-2-일아미노)-2-(2-(티오펜-2-일)티아졸-4-일)에틸)페닐술팜산:
4-((S)-2-(5-벤질-1,3,4-티아디아졸-2-일아미노)-2-(2-(티오펜-2-일)티아졸-4-일)에틸)페닐술팜산:
4-((S)-2-(5-(나프탈렌-1-일메틸)-1,3,4-티아디아졸-2-일아미노)-2-(2-(티오펜-2-일)티아졸-4-일)에틸)페닐술팜산:
4-((S)-2-(5-((메톡시카르보닐)메틸)-1,3,4-티아디아졸-2-일아미노)-2-(2-(티오펜-2-일)티아졸-4-일)에틸)페닐술팜산:
4-((S)-2-(5-((2-메틸티아졸-4-일)메틸)-1,3,4-티아디아졸-2-일아미노)-2-(2-(티오펜-2-일)티아졸-4-일)에틸)페닐술팜산:
4-{(S)-2-[4-(2,4-디플루오로페닐)티아졸-2-일아미노]-2-[2-(티오펜-2-일)티아졸-4-일]에틸}페닐술팜산:
(S)-4-{2-[4-(에톡시카르보닐)티아졸-2-일아미노]-2-(2-페닐티아졸-4-일)에틸}페닐술팜산:
(S)-4-{2-[4-(2-에톡시-2-옥소에틸)티아졸-2-일아미노]-2-(2-페닐티아졸-4-일)에틸}페닐술팜산:
(S)-4-{2-[4-(4-아세트아미도페닐)티아졸-2-일아미노]-2-(2-페닐티아졸-4-일)에틸}페닐술팜산:
(S)-4-[2-(4-페닐티아졸-2-일아미노)-2-(2-페닐티아졸-4-일)에틸]페닐술팜산:
(S)-4-{2-[4-(4-(메톡시카르보닐)페닐)티아졸-2-일아미노]-2-(2-페닐티아졸-4-일)에틸}페닐술팜산:
4-{(S)-2-[4-(에톡시카르보닐)티아졸-2-일아미노]-2-[2-(티오펜-2-일)티아졸-4-일]에틸}페닐술팜산:
(S)-4-[2-(4-(메톡시카르보닐)티아졸-5-일아미노)-2-(2-페닐티아졸-4-일)에틸]페닐술팜산:
(S)-4-[2-(5-페닐옥사졸-2-일아미노)-2-(2-페닐티아졸-4-일)에틸]-페닐술팜산:
(S)-4-{2-[5-(4-아세트아미도페닐)옥사졸-2-일아미노]-2-(2-페닐티아졸-4-일)에틸}페닐술팜산:
4-((S)-2-(5-(2,4-디플루오로페닐)옥사졸-2-일아미노)-2-(2-페닐티아졸-4-일)에틸)페닐술팜산:
4-{(S)-2-[5-(3-메톡시페닐)옥사졸-2-일아미노]-2-[(2-티오펜-2-일)티아졸-4-일]에틸}페닐술팜산:
(S)-4-[2-(4,6-디메틸피리미딘-2-일아미노)-2-(2-메틸티아졸-4-일)에틸]페닐술팜산:
(S)-4-[2-(4-히드록시-6-메틸피리미딘-2-일아미노)-2-(2-메틸티아졸-4-일)에틸]페닐술팜산:
본 개시내용의 카테고리 X 의 제 1 국면은 하기 화학식을 가진 화합물들에 관한 것이다:
[식 중, R1 은 헤테로아릴이고, R4 는 표 XIX 에 본원에서 추가로 기재됨].
카테고리 X 의 제 1 국면에 따른 화합물들은 반응식 XXII 에 개요되고, 실시예 23 에서 하기 기재된 과정으로 제조될 수 있다.
반응식 XXII
시약 및 조건: (a) CH3CN; 환류 2 시간.
시약 및 조건: (b) (3-Cl)C6H4CO2H, EDCI, HOBt, DIPEA, DMF; rt, 18 시간
시약 및 조건: (c) (i) H2:Pd/C, MeOH; (ii) SO3-피리딘, NH4OH, rt, 18 시간
실시예
23
4-((S)-2-(2-(3-
클로로페닐
)
아세트아미도
)-2-(2-(티오펜-2-일)
옥사졸
-4-일)에틸)
페닐술팜산
(64)
(S)-2-(4-니트로페닐)-1-[(티오펜-2-일)옥사졸-4-일]에탄아민 히드로브로마이드 염 (62) 의 제조: (S)-tert-부틸 4-브로모-1-(4-니트로페닐)-3-옥소부탄-2-일카르바메이트, 7, (38.7 g, 100 mmol), 및 티오펜-2-카르복사미드 (14 g, 110 mmol) (Alfa Aesar 로부터 입수가능) 의 CH3CN (500 mL) 중 혼합물을 5 시간 동안 환류시켰다. 반응 혼합물을 실온으로 냉각시키고, 디에틸 에테르 (200 mL) 를 용액에 첨가했다. 형성된 석출물을 여과로 수집했다. 고체를 진공 하에 건조시켜 원하는 생성물을 수득하여, 정제없이 후속 단계에서 사용할 수 있다.
2-(3-클로로페닐)-N-{(S)-2-(4-니트로페닐)-1-[2-(티오펜-2-일)옥사졸-4-일]에틸}아세트아미드 (63) 의 제조: (S)-2-(4-니트로페닐)-1-[(티오펜-2-일)옥사졸-4-일]에탄아민 HBr, 47, (3.15 g, 10 mmol), 3-클로로페닐-아세트산 (1.70 g, 10 mmol) 및 1-히드록시벤조트리아졸 (HOBt) (0.7Og, 5.0 mmol) 의 DMF (50 mL) 중 용액에 0℃ 에서 1-(3-디메틸아미노프로필)-3-에틸카르보디이미드 (EDCI) (1.90 g, 10 mmol) 에 이어 트리에틸아민 (4.2 mL, 30 mmol) 을 첨가했다. 혼합물을 0℃ 에서 30 분, 이어서 실온에서 밤새 교반했다. 반응 혼합물을 물로 희석하고, EtOAc 로 추출했다. 조합한 유기상을 1 N 수성 HCl, 5 % 수성 NaHCO3, 물 및 식염수로 세척하고, Na2SO4 상에서 건조시켰다. 용매를 진공에서 제거하여 원하는 생성물을 추가 정제없이 사용했다.
-((S)-2-(2-(3-클로로페닐)아세트아미도)-2-(2-(티오펜-2-일)옥사졸-4-일)에틸)페닐술팜산 (64) 의 제조: 2-(3-클로로페닐)-N-{(S)-2-(4-니트로페닐)-1-[2-(티오펜- 2-일)옥사졸-4-일]에틸}아세트아미드, 63, (3 g) 를 MeOH (4 mL) 에 용해시켰다. 촉매량의 Pd/C (10% w/w) 를 첨가하고, 혼합물을 수소 분위기 하에 18 시간 동안 교반했다. 반응 혼합물을 CELITE™ 의 층을 통해 여과하고, 용매를 감압 하에 제거했다. 미정제 생성물을 피리딘 (12 mL) 에 용해시키고, SO3-피리딘 (0.157 g) 으로 처리했다. 반응물을 실온에서 5 분 동안 교반한 후, NH4OH 의 7% 용액을 첨가했다. 이어서, 혼합물을 농축하고, 결과로서 수득한 잔사를 역상 크로마토그래피로 정제하여 원하는 생성물을 암모늄 염으로 제공했다.
본 개시내용의 카테고리 X 의 제 2 국면은 하기 화학식을 가진 화합물들에 관한 것이다:
[식 중, R1 은 아릴이고, R2 및 R3 은 표 XX 에서 하기 본원에 추가로 기재됨].
카테고리 X 의 제 2 국면에 따른 화합물들은 반응식 XXIII 에서 개요하고 실시예 24 에서 하기 기재한 과정으로 제조할 수 있다.
반응식 XXIII
시약 및 조건: (a) CH3CN; 환류, 2 시간
시약 및 조건: (b) C6H4CO2H, EDCI, HOBt, DIPEA, DMF; rt, 18 시간
시약 및 조건: (c) (i) H2:Pd/C, MeOH; (ii) SO3-피리딘, NH4OH, rt, 18 시간
실시예
24
{4-[2-(S)-(4-
에틸옥사졸
-2-일)-2-
페닐아세틸아미노에틸
]-
페닐
}
술팜산
(67)
(S)-1-(4-에틸옥사졸-2-일)-2-(4-니트로페닐)에탄아민 (65) 의 제조: [1-(S)-카르바모일-2-(4-니트로페닐)에틸-카르밤산 tert-부틸 에스테르, 1, (10 g, 32.3 mmol) 및 1-브로모-2-부타논 (90%, 4.1 mL, 36 mmol) 의 CH3CN (500 mL) 중 혼한물을 18 시간 동안 환류시켰다. 반응 혼합물을 실온으로 냉각시키고, 디에틸 에테르를 용액에 첨가하고, 형성된 석출물을 여과로 제거하고, 추가 정제없이 사용했다.
N-[1-(4-에틸옥사졸-2-일)-2-(4-니트로페닐)에틸]-2-페닐-아세트아미드 (66) 의 제조: (S)-1-(4-에틸옥사졸-2-일)-2-(4-니트로페닐)에탄아민, 65, (2.9 g, 11 mmol), 페닐아세트산 (1.90 g, 14 mmol) 및 1-히드록시벤조트리아졸 (HOBt) (0.94 g, 7.0 mmol) 의 DMF (100 mL) 중 용액에 0℃ 에서, 1-(3-디메틸아미노-프로필)-3-에틸카르보디이미드 (EDCI) (2.68g, 14 mmol) 에 이어 트리에틸아민 (6.0 mL, 42 mmol) 을 첨가했다. 혼합물을 0℃ 에서 30 분, 이어서 실온에서 밤새 교반했다. 반응 혼합물을 물로 희석하고, EtOAc 로 추출했다. 조합한 유기상을 1 N 수성 HCl, 5 % 수성 NaHCO3, 물 및 식염수로 세척하고, Na2SO4 상에서 건조시켰다. 용매를 진공에서 제거하여, 원하는 생성물을 수득해 추가 정제없이 사용했다.
{4-[2-(S)-(4-에틸옥사졸-2-일)-2-페닐아세틸아미노에틸]-페닐}술팜산 (67) 의 제조: N-[1-(4-에틸옥사졸-2-일)-2-(4-니트로페닐)에틸]-2-페닐-아세트아미드, 66, (0.260 g) 를 MeOH (4 mL) 에 용해시켰다. 촉매량의 Pd/C (10% w/w) 를 첨가하고, 혼합물을 수소 분위기 하에 18 시간 동안 교반했다. 반응 혼합물을 CELITE™ 의 층을 통해 여과하고, 용매를 감압 하에 제거했다. 미정제 생성물을 피리딘 (12 mL) 에 용해시키고, SO3-피리딘 (0.177 g, 1.23) 으로 처리했다. 반응물을 실온에서 5 분 동안 교반한 후, NH4OH 의 7% 용액 (10 mL) 을 첨가했다. 이어서, 혼합물을 농축하고, 결과로서 수득한 잔사를 역상 크로마토그래피로 정제하여 암모늄 염으로서의 원하는 생성물을 수득했다.
방법
개시된 화합물들은 인간 및 동물에서 종양 전이를 예방, 약화, 최소화, 제어 및/또는 완화시키기 위해 이용할 수 있다. 개시된 화합물들은 또한 원발 종양 성장 속도를 둔화시키기 위해 이용될 수 있다. 개시된 화합물들은 치료가 필요한 대상체에게 투여되는 경우, 암 세포의 전파를 정지시키기 위해 사용될 수 있다. 이와 같이, 본원에 개시된 화합물들은 하나 이상의 약물 또는 여타 약제학적 제제와의 병용 요법의 일부로서 투여될 수 있다. 병용 요법의 일부로서 사용되는 경우, 전이의 감소 및 원발 종양 성장에서의 감소는 환자 치료에 사용되는 임의의 약제학적 또는 약물 요법의 더욱 유효하고 효율적인 이용을 가능케 한다. 추가로, 개시된 화합물에 의한 전이의 제어는 대상체에게 한 지점에 질병이 집중되도록 하는 더 큰 능력을 부여한다.
악성 종양 및 기타 암종 세포의 전이 방지 방법 뿐만 아니라 종양 성장 속도 감소 방법이 본원에 개시된다. 상기 방법은 유효량의 하나 이상의 개시된 화합물들을 악성 종양 또는 암종 세포가 있는 것으로 진단된 대상체 또는 종양 또는 암종 세포를 가진 대상체에게 투여하는 것을 포함한다.
추가로, 악성 종양 또는 여타 암종 세포의 전이를 방지하고, 종양 성장 속도를 완화하기 위한 의약 제조를 위한 개시된 화합물들의 용도가 개시된다.
하기는 개시된 방법 및 조성물로 치료될 수 있는 암의 비제한적 예시이다: 급성 림프구성 백혈병 (Acute Lymphoblastic); 급성 골수성 백혈병 (Acute Myeloid Leukemia); 부신피질암 (Adrenocortical Carcinoma); 소아 부신피질암 (Adrenocortical Carcinoma, Childhood); 충수암 (Appendix Cancer); 기저세포 암종 (Basal Cell Carcinoma); 간외 담도암 (Bile Duct Cancer, Extrahepatic); 방광암 (Bladder Cancer); 골암 (Bone Cancer); 골육종 (Osteosarcoma) 및 악성 섬유성 조직구종 (Malignant Fibrous Histiocytoma); 소아 뇌간교종 (Brain Stem Glioma, Childhood); 성인 뇌종양 (Brain Tumor, Adult); 뇌종양 (Brain Tumor), 소아 뇌간교종; 뇌종양, 소아 중추신경계 비정형 기형/횡문근양 종양 (Central Nervous System Atypical Teratoid/Rhabdoid Tumor, Childhood); 중추 신경계 배아종 (Central Nervous System Embryonal Tumors); 소뇌별아교세포종 (Cerebellar Astrocytoma); 소뇌별아교세포종 (Cerebral Astrocytoma)/악성 교종 (Malignant Glioma); 두개인두종 (Craniopharyngioma); 뇌실막모세포종 (Ependymoblastoma); 뇌실막종 (Ependymoma); 속질모세포종 (Medulloblastoma); 속질상피종 (Medulloepithelioma); 등도분화의 송과 실질세포 종양 (Pineal Parenchymal Tumors of Intermediate Differentiation); 천막위 원시 신경외배엽종양 (Supratentorial Primitive Neuroectodermal Tumors) 및 송과체모세포종 (Pineoblastoma); 시각경로 및 시상하부 신경아교종 (Visual Pathway and Hypothalamic Glioma); 뇌 및 척추 종양 (Brain and Spinal Cord Tumors); 유방암 (Breast Cancer); 기관지내 종양 (Bronchial Tumors); 버킷 림프종 (Burkitt Lymphoma); 유암종 (Carcinoid Tumor); 위장관 유암종 (Carcinoid Tumor, Gastrointestinal); 중추신경계 비정형 기형/횡문근양 종양 (Central Nervous System Atypical Teratoid/Rhabdoid Tumor); 중추 신경계 배아종 (Central Nervous System Embryonal Tumors); 중추신경계 림프종 (Central Nervous System Lymphoma); 소뇌별아교세포종 (Cerebellar Astrocytoma); 소아 소뇌별아교세포종/악성 교종 (Cerebral Astrocytoma/Malignant Glioma, Childhood); 자궁경부암 (Cervical Cancer); 소아 척삭종 (Chordoma, Childhood); 만성 림프성 백혈병 (Chronic Lymphocytic Leukemia); 만성 골수성 백혈병 (Chronic Myelogenous Leukemia); 만성 골수 증식 질환 (Chronic Myeloproliferative Disorders); 대장암 (Colon Cancer); 직장암 (Colorectal Cancer); 두개인두종 (Craniopharyngioma); 피부 T-세포 림프종 (Cutaneous T-Cell Lymphoma); 식도암 (Esophageal Cancer); 종양의 유잉 패밀리 (Ewing Family of Tumors); 고환외 배세포종 (Extragonadal Germ Cell Tumor); 간외 담도암 (Extrahepatic Bile Duct Cancer); 안암으로서, 안구내 흑색종 (Eye Cancer, Intraocular Melanoma); 안암으로서, 망막모세포종 (Eye Cancer, Retinoblastoma); 담낭암 (Gallbladder Cancer); 위암 (Gastric (Stomach) Cancer); 위장관 악성 종양 (Gastrointestinal Carcinoid Tumor); 위장관 기질종양 (Gastrointestinal Stromal Tumor (GIST)); 두개외 생식세포 종양 (Germ Cell Tumor, Extracranial); 고환외 생식 세포 종양 (Germ Cell Tumor, Extragonadal); 난소 생식 세포 종양 (Germ Cell Tumor, Ovarian); 임신성 융모성 종양 (Gestational Trophoblastic Tumor); 신경아교종 (Glioma); 소아 뇌간 신경아교종 (Glioma, Childhood Brain Stem); 신경아교종으로서의, 소아 뇌 별아교세포종 (Glioma, Childhood Cerebral Astrocytoma), 신경아교종으로서의, 소아 시각경로 및 시상하부 신경아교종 (Glioma, Childhood Visual Pathway and Hypothalamic), 털세포 백혈병 (Hairy Cell Leukemia); 두경부암 (Head and Neck Cancer); 간암 (hepatocellular (Liver) Cancer); 랑게르한스 세포의 조직구증 (Histiocytosis, Langerhans Cell); 호지킨 림프종 (Hodgkin Lymphoma); http://www.cancer.gov/cancertopics/typcs/hodgkinslymphoma/피열후두개 암 (Hypopharyngeal Cancer); 시상하부 및 시각경로 신경아교종 (Hypothalamic and Visual Pathway Glioma); 안구내 흑색종 (Intraocular Melanoma); 췌도 세포종 (Islet Cell Tumors); 신장암 (Kidney (Renal Cell) Cancer); 랑게르한스 세포 조직구증 (Langerhans Cell Histiocytosis); 후두암 (Laryngeal Cancer); 급성 림프모구 백혈병 (Leukemia, Acute Lymphoblastic); 급성 골수성 백혈병 (Leukemia, Acute Myeloid); 만성 림프구성 백혈병 (Leukemia, Chronic Lymphocytic); 만성 골수성 백혈병 (Leukemia, Chronic Myelogenous); 털세포 백혈병 (Leukemia, Hairy Cell); 구순 및 구강암 (Lip and Oral Cavity Cancer); 간암 (Liver Cancer); 비소세포 폐암 (Lung Cancer, Non-Small Cell); 소세포 폐암 (Lung Cancer, Small Cell); AIDS 관련 림프종 (Lymphoma, AIDS-Related); 버킷 림프종 (Lymphoma, Burkitt); 피부 T-세포 림프종 (Lymphoma, Cutaneous T-Cell); 호지킨 림프종 (Lymphoma, Hodgkin); 비-호지킨 림프종 (Lymphoma, Non-Hodgkin); 원발성 중추 신경계 림프종 (Lymphoma, Primary Central Nervous System); 왈덴스트롬 마크로불린혈증 (Macroglobulinemia, Waldenstrom); 뼈의 악성 섬유조직구종 (Malignant Fibrous Histiocytoma of Bone) 및 골육종 (Osteosarcoma); 수모세포종 (Medulloblastoma); 흑색종 (Melanoma); 안내 흑색종 (Melanoma, Intraocular (눈)); 메르켈 세포 암 (Merkel Cell Carcinoma); 중피종 (Mesothelioma); 잠복 원발성의 전이성 편평상피 경부암 (Metastatic Squamous Neck Cancer with Occult Primary); 구강암 (Mouth Cancer); 소아의 다발성 내분비 샘종증 증후군 (Multiple Endocrine Neoplasia Syndrome, (Childhood)); 다발 골수종 (Multiple Myeloma)/형질 세포 종양 (Plasma Cell Neoplasm); 균상 식육종 (Mycosis Fungoides); 골수형성이상 증후군 (Myelodysplastic Syndromes); 골수형성이상/골수증식 질환 (Myelodysplastic/Myeloproliferative Diseases); 만성 골수성 백혈병 (Myelogenous Leukemia, Chronic); 성인 급성 골수성 백혈병 (Myeloid Leukemia, Adult Acute); 소아 급성 골수성 백혈병 (Myeloid Leukemia, Childhood Acute); 다발성 골수종 (Myeloma, Multiple); 만성 골수증식 질환 (Myeloproliferative Disorders, Chronic); 비강 및 부비동 암 (Nasal Cavity and Paranasal Sinus Cancer); 비인두암 (Nasopharyngeal Cancer); 신경모세포종 (Neuroblastoma); 비소세포폐암 (Non-Small Cell Lung Cancer); 구강암 (Oral Cancer); 구강암 (Oral Cavity Cancer); 입인두암 (Oropharyngeal Cancer); 뼈육종 (Osteosarcoma) 및 뼈의 악성 섬유 조직구종 (Malignant Fibrous Histiocytoma of Bone); 난소암 (Ovarian Cancer); 상피성 난소암 (Ovarian Epithelial Cancer); 난소 생식 세포 종양 (Ovarian Germ Cell Tumor); 난소 저악성 잠재성 종양 (Ovarian Low Malignant Potential Tumor); 췌장암 (Pancreatic Cancer); 췌장암으로서, 췌도 세포 종양 (Pancreatic Cancer, Islet Cell Tumors); 유두종증 (Papillomatosis); 부갑상선암 (Parathyroid Cancer); 음경암 (Penile Cancer); 인두암 (Pharyngeal Cancer); 크롬친화세포종 (Pheochromocytoma); 등도분화의 송과 실질세포 종양 (Pineal Parenchymal Tumors of Intermediate Differentiation); 송과체모세포종 (Pineoblastoma) 및 천막위 원시 신경외배엽종양 (Supratentorial Primitive Neuroectodermal Tumors); 하수체 종양 (Pituitary Tumor); 형질 세포 종양 (Plasma Cell Neoplasm)/다발 골수종 (Multiple Myeloma); 흉막폐아세포종 (Pleuropulmonary Blastoma); 원발성 중추신경계 림프종 (Primary Central Nervous System Lymphoma); 전립선암 (Prostate Cancer); 직장암 (Rectal Cancer); 신장암 (Renal Cell (Kidney) Cancer); 신우 및 요관 이행세포암 (Renal Pelvis and Ureter, Transitional Cell Cancer); 15 번 염색체 상의 NUT 유전자와 관련된 기 도 암종 (Respiratory Tract Carcinoma Involving the NUT Gene on Chromosome 15); 망막모세포종 (Retinoblastoma); 횡문근육종 (Rhabdomyosarcoma); 침샘암 (Salivary Gland Cancer); 종양의 유잉 패밀리의 육종 (Sarcoma, Ewing Family of Tumors); 카포시 육종 (Sarcoma, Kaposi); 연조직 육종 (Sarcoma, Soft Tissue); 요관 육종 (Sarcoma, Uterine); 세자리 증후군 (Sezary Syndrome); 피부암 (비흑색종) (Skin Cancer (Nonmelanoma)); 피부암 (흑색종) (Skin Cancer (Melanoma)); 메르켈 세포 피부 암종 (Skin Carcinoma, Merkel Cell); 소세포 폐암 (Small Cell Lung Cancer); 소장암 (Small Intestine Cancer); 연조직 육종 (Soft Tissue Sarcoma), 편평세포 암종 (Squamous Cell Carcinoma), 잠복 원발성의 전이성 편평상피 경부암 (Squamous Neck Cancer with Occult Primary, Metastatic); 위암 (Stomach (Gastric) Cancer); 천막위 원시 신경외배엽종양 (Supratentorial Primitive Neuroectodermal Tumors); 피부 T-세포 림프종 (T-Cell Lymphoma, Cutaneous); 고환암 (Testicular Cancer); 인후두암 (Throat Cancer); 가슴샘종 (Thymoma) 및 흉선 암종 (Thymic Carcinoma); 갑상선암 (Thyroid Cancer); 신우 및 요관 이행세포암 (Transitional Cell Cancer of the Renal Pelvis and Ureter); 임신성 융모 종양 (Trophoblastic Tumor, Gestational); 요도암 (Urethral Cancer); 자궁내막 자궁암 (Uterine Cancer, Endometrial); 자궁 육종 (Uterine Sarcoma); 질암 (Vaginal Cancer); 외음부암 (Vulvar Cancer); 왈덴스트룀 마크로글로불린혈증 (Waldenstrom Macroglobulinemia) 또는 윌름 종양 (Wilms Tumor).
생체내 항-전이 연구 5 내지 6 주령의 총 50 마리 NCr nu/nu 수컷 마우스를 하기 생체내 시험을 위해 선별했다. NCr nu/nu 수컷 마우스에서 피하에서 H460-GFP 인간 종양 세포를 성장시킨 후, 결과로서 수득한 종양을 수합했다. 수합에 후속하여, 본 연구의 수용자 NCr nu/nu 마우스가 외과적 동종 이식 (SOI) 에 의해 이식된 종양 분절을 갖도록 했다. 각 동물은 이소푸란으로 마취시키고, 수술 부위를 요오드 및 알콜로 멸균시켰다. 길이가 약 1.5 cm 인 대각선 절개를 외과용 가위를 이용해 마우스의 좌측 흉벽에 가했다. 늑간 절개는 3 번째 및 4 번째 갈비뼈 사이에 가하고, 폐를 노출시켰다. 2 개 편의 H460-GFP 종양 절편을 8-0 외과용 나일론 봉합사를 이용해 폐의 표면에 이식했다. 흉벽을 6-0 실크 봉합사를 이용해 닫았다. 폐를 25 G 11A 바늘이 있는 3 cc 주사기를 이용한 흉내 천공으로 재팽창시켜, 흉강 내 남아있는 공기를 빼 냈다. 흉벽을 6-0 외과용 실크 봉합사를 이용해 닫았다. 상기 기술한 모든 수술 과정은 HEPA 여과 층류후드 하에 7 배 확대 현미경 (Olympus) 을 이용해 수행했다.
처리한 마우스를 각각 10 마리씩 무리지어 포함하는 5 개 군으로 나누었다. 군 I (대조군) 에는 15 일 동안 1 일 2 회 100 μL 약물 비히클을 제공했다. 군 II 에는 15 mg/kg 의 택솔을 정맥내로 제 6, 9, 12 및 15 일째에 제공했다. 군 III 에는 15 mg/kg 의 택솔을 정맥내로 제 6, 9, 12 및 15 일째에, 15 mg/kg 의 4-{(S)-2-[(S)-2-(메톡시카르보닐아미노)-3-페닐-프로판아미도]-2-[2-(티오펜-2-일)티아졸-4-일]에틸}페닐술팜산, D91, (시험 화합물) 을 제 3 내지 15 일째에 1 일 2 회 제공했다. 군 IV 에는 10 mg/kg 의 택솔을 정맥내로 제 6, 9, 12 및 15 일째에, 15 mg/kg 의 시험 화합물을 제 3 내지 15 일째에 매일 2 회씩 제공했다. 군 V 에는 15 mg/kg 의 시험 화합물을 제 3 내지 15 일째에 1 일 2 회 제공했다. 모든 동물들은 제 28 일째에 희생시켰다.
각 동물은 종격 림프절의 GFP 개방 영상을 통해 원발 종양 및 전이에 대해 주 2 회 체크했다. 임의의 여타 장기에서 전이가 발견되지 않았다. 연구 종료 전에 대조군으로부터의 6 마리 마우스가 폐사했으나, 종양 및/또는 세포 전이에 대해서는 평가했다. 표 XXI 는 하기에서 생체내 전이 연구의 결과를 요약한다.
생체내에서의
항암 연구
B16 흑색종
흑색종에 대한 치료로서의 개시된 화합물들의 유효성을 연구했다. C57BL/6 마우스 (6-8 주령, 암컷, Taconic Farm) 에 B16 흑색종 세포 (5 x 104 세포/부위, s.c) 를 접종했다. 접종 4 일 후, 마우스 (5 마리/군) 에 비히클 대조군 (bid, i.p.), 낮은 투여량의 IL-2 (100,000 IU/마우스, bid, i.p.), 높은 투여량의 IL-2 (300,000 IU/마우스, bid, i.p.), 또는 D91 와의 조합물 (40 mg/kg, bid, s.c, IL-2 보다 30 분 먼저 투여) 을 처리 (5 일/주, M-F) 했다. 종양 체적을 기록했다. 별도 실험에서, B16 흑색종 세포를 유사하게 접종한 마우스에 비히클 대조군 (bid, i.p.), IL-2 (300,000 IU/마우스, bid, i.p.), 높은 투여량의 D91 (40 mg/kg, bid, s.c), 낮은 투여량의 D91 (10 mg/kg, bid, s.c.) 또는 IL-2 (300,000 IU/마우스, bid, i.p.) 과 낮은 투여량의 D91 (10 mg/kg, bid, s.c, IL-2 보다 30 분 먼저 투여) 의 조합물을 처리했다 (5 일/주, M-F). 종양 체적을 기록했다.
도 3 에 도시한 바와 같이, 높은 투여량의 IL-2 (◇) 는 대조군 (□) 에 비해 예상한 바와 같이 감소된 종양 체적을 나타냈으나, 높은 투여량의 D91 (○) 와 조합한 높은 투여량의 IL-2 를 이용한 치료는 높은 투여량의 IL-2 만을 처리한 것 (◇) 에 비해 현저하게 종양 체적을 감소시켰다.
도 4 는 대조군 (A), 높은 투여량의 IL-2 (B), 및 높은 투여량의 IL-2/높은 투여량의 D91 (C) 를 제공받은 동물의 종양 체적을 나타내는 히스토그램이다. 도 5 에 도시한 데이터는 연구 동안 동물 체중 증가가 각 군에서 일정했으며, 치료법 선택으로 인한 임의의 유효성은 나타내지 않음을 나타낸다.
도 6 에 도시한 바와 같이, 높은 투여량의 D91 (○) 와 병용된 낮은 투여량의 IL-2 를 이용한 처리는 대조군 (□) 에 비해 종양 체적을 현저히 감소시키는 한편, 낮은 투여량의 IL-2 (◇) 만으로는 제 22 일째 연구 종료시 측정가능한 종양 체적 감소를 나타내지 않았다. 도 7 은 대조군 (A), 낮은 투여량의 IL-2 (B), 및 낮은 투여량의 IL-2/높은 투여량의 D91 (C) 를 제공받은 동물의 종양 체적을 나타내는 히스토그램이다. 도 8 은 B16 흑색종 종양 체적에 대한 40 mg/kg b.i.d. D91 (○) 대 비히클 대조군 (□) 의 처리 유효성을 보여준다.
신장 세포
암종
신장 세포 암종에 대한 치료법으로서의 개시된 화합물들의 유효성을 연구했다. Balb/c 마우스 (6-8 주령, 암컷, Taconic Farm) 에 Renca 신장 암 세포 (5 x 105 세포/부위) 를 접종했다. 접종 4 일 후, 마우스를 4 개의 군 (4 마리 마우스/군) 으로 무작위로 나누어, 비히클 대조군 (bid, i.p.), IL-2 (100,000 IU/마우스, bid, i.p.), D91 (40 mg/kg, bid, s.c, IL-2 보다 30 분 앞서 투여) 또는 조합물을 처리했다 (5 일/주, M-F).
도 1 및 도 2 에 도시한 바와 같이, 4-{(S)-2-[(S)-2-(메톡시카르보닐아미노)-3-페닐-프로판아미도]-2-[2-(티오펜-2-일)티아졸-4-일]에틸}페닐술팜산, D91 은 신장 종양 성장을 현저히 감소시키고, 종양 체적 감소에 있어 IL-2 만큼 유효했다. 추가로, D91 및 IL-2 의 조합은 종양 체적을 더 감소시켰다.
췌장 암
췌장 암은 췌장의 악성 신생물이다. 미국에서는 매년, 약 42,000 명이 이를 진단받아, 그 질병으로 인해 35,000 명이 사망한다 ("Pancreatic Cancer - National Cancer Institute. U.S. National Institutes of Health" (2009)). 예후는 비교적 안 좋으나, 개선된 바 있다; 3 년 생존율이 현재 약 30% 이나, 진단받은 이들 중 5% 미만만이 진단 5 년 후에 여전히 생존한다. 완전한 차도는 여전히 거의 희박하다 (Ghaneh P et al., (August 2007). "Biology and management of pancreatic cancer". Gut 56 (8): 1134-52).
췌장암 치료로서의 개시된 화합물들의 유효성을 조사했다. 5-6 주령의 60 마리 NCr nu/nu 수컷에, 원 동물로부터 수합한 MiaPaCa-2-RFP 종양 절편을 외과적 동종 이식 (SOI) 으로 이식했다. 상기 동물들을 이소플루란으로 마취하고, 수술 영역을 요오드 및 알콜을 멸균시켰다. 약 1.5 cm 길이의 절개를 외과용 가위를 이용해 누드 마우스의 좌측 상복부에 가했다. 췌장을 노출시키고, 이식 부위의 캡슐을 벗겨낸 후, 2 ㎣ 의 2 개 편의 MiaPaCa-2-RFP 종양 절편을 8-0 외과용 봉합사 (나일론) 을 이용해 마우스 췌장에 이식했다. 복부는 6-0 외과용 봉합사 (실크) 로 닫았다. 상기 기재한 수술의 모든 과정은 HEPA 여과 층류후드 하에 7 배 확대 현미경 (Olympus) 을 이용해 수행했다.
동물의 약물처리는 종양 이식 3 일 후 시작했다. 높은 투여량의 겜시타빈은 150 mg/kg 였다. 낮은 투여량의 겜시타빈은 100 mg/kg 였다. D91 는 20 mg/kg 로 제공했다. 겜시타빈은 i.p.로 제공했고, D91 는 s.c.로 제공했다.
동물들은 표 XXII 에 나타낸 바와 같이 각각 동물 10 마리씩 하기의 군으로 나누었다. 표 XXII 에 나타낸 바와 같이, D91 는 1 일 2 회 투여한 반면, 겜시타빈은 주 2 회 투여했다.
도 9 에 도시한 바와 같이, 20 mg/kg 로 제공한 D91 은 제 28 일째 췌장 종양 체적에 있어서 현저한 감소를 나타냈다 (○). 추가로, 낮은 투여량의 겜시타빈 및 20 mg/kg D91 (*) 의 조합은 낮은 투여량의 겜시타빈 (X) 또는 D91 단독 (○) 보다 종양 체적에 있어서 더 큰 감소를 나타냈다.
암종이 있는 대상체에게 유효량의 하나 이상의 개시된 화합물을 투여하는 것을 포함하는, 대상체에서의 암종의 치료 방법이 본원에 개시된다.
대상체에게 유효량의 하나 이상의 개시된 화합물을 투여하는 것을 포함하는, 암으로 진단된 대상체의 치료 방법이 또한 본원에 개시된다.
암이 있는 대상체에게 하기를 함유하는 조성물을 투여하는 것을 포함하는, 대상체에서의 암종 치료 방법이 본원에서 추가로 개시된다:
a) 유효량의 하나 이상의 개시된 화합물; 및
b) 유효량의 항암 약물.
암종을 가진 대상체에게 하기를 함유하는 조성물을 투여하는 것을 포함하는, 대상체에서의 암종 치료 방법이 또한 추가로 개시된다:
a) 유효량의 하나 이상의 개시된 화합물; 및
b) 종양 성장을 억제하는 유효량의 화합물.
또한, 암으로 진단받은 대상체에게 하기를 함유하는 조성물을 투여하는 것을 포함하는, 암으로 진단받은 대상체의 치료 방법이 추가로 개시된다:
a) 유효량의 하나 이상의 개시된 화합물; 및
b) 유효량의 항암 약물.
또한, 암으로 진단받은 대상체에게 하기를 함유하는 조성물을 투여하는 것을 포함하는, 암으로 진단받은 대상체의 치료 방법이 또한 제공된다:
a) 유효량의 하나 이상의 개시된 화합물; 및
b) 종양 성장을 억제하는 유효량의 화합물.
조성물
본원에서는 대상체에서의 암 세포의 전이를 예방하기 위해 사용될 수 있는 조성물로서, 유효량의 하나 이상의 본원에 개시된 화합물을 함유하는 조성물이 개시된다. 추가로, 본원에서는 인간 또는 여타 포유류에서의 종양 치료에 사용될 수 있는 조성물이 개시된다.
한 국면은 하기를 함유하는 조성물에 관한 것이다:
a) 유효량의 하나 이상의 본원에 개시된 화합물; 및
b) 하나 이상의 약제학적으로 허용되는 성분.
또다른 국면은 하기를 함유하는 조성물에 관한 것이다:
a) 유효량의 하나 이상의 본원에 개시된 화합물; 및
b) 유효량의 하나 이상의 화학치료제;
여기서, 개시된 화합물 및 화학치료제는 함께 또는 임의의 순서로 투여될 수 있음.
한 구현예는 하기를 함유하는 조성물에 관한 것이다:
a) 유효량의 하나 이상의 본원에 개시된 화합물; 및
b) 유효량의 택솔;
여기서, 개시된 화합물 및 택솔은 함께 또는 임의의 순서로 투여될 수 있음.
또다른 구현예는 하기를 함유하는 조성물에 관한 것이다:
a) 유효량의 하나 이상의 본원에 개시된 화합물; 및
b) 유효량의 겜시타빈;
여기서, 개시된 화합물 및 겜시타빈은 함께 또는 임의의 순서로 투여될 수 있음.
추가 구현예는 하기를 함유하는 조성물에 관한 것이다:
a) 유효량의 하나 이상의 본원에 개시된 화합물; 및
b) 유효량의 엘로티닙;
여기서, 개시된 화합물 및 엘로티닙은 함께 또는 임의의 순서로 투여될 수 있음.
또다른 구현예는 하기를 함유하는 조성물에 관한 것이다:
a) 유효량의 하나 이상의 본원에 개시된 화합물; 및
b) 유효량의 독실;
여기서, 개시된 화합물 및 독실은 함께 또는 임의의 순서로 투여될 수 있음.
또다른 구현예는 하기를 함유하는 조성물에 관한 것이다:
a) 유효량의 하나 이상의 본원에 개시된 화합물; 및
b) 유효량의 이리노르테칸;
여기서, 개시된 화합물 및 이리노르테칸은 함께 또는 임의의 순서로 투여될 수 있음.
또다른 구현예는 하기를 함유하는 조성물에 관한 것이다:
a) 유효량의 하나 이상의 본원에 개시된 화합물; 및
b) 유효량의 베바시주마브;
여기서, 개시된 화합물 및 베바시주마브는 함께 또는 임의의 순서로 투여될 수 있음.
"화학치료제" 또는 "화학치료 화합물" 은 암 치료에 유용한 화학물 화합물이다. 본원에 개시된 것과 병용하여 사용될 수 있는 화학치료 암 약제에는, 이에 제한되지 않으나, 유사분열 억제제 (mitotic inhibitors) (빈카 알칼로이드 (vinca alkaloid)) 가 포함된다. 여기에는, 빈크리스틴 (vincristine), 빈블라스틴 (vinblastine), 빈데신 (vindesine) 및 Navelbine™ (비노렐빈-5'-노르안히드로블라스틴 (vinorelbin-5'-noranhydroblastine)) 이 포함된다. 또다른 구현예에서, 화학치료 암 약제에는 토포이소머라아제 I 억제제, 예컨대 캄토테신 (camptothecin) 화합물이 포함된다. 본원에 사용된 바와 같이, "캄토테신 화합물" 에는 Camptosar™ (irinotecan HCL), Hycamtin™ (topotecan HCL) 및 캄토테신 및 그의 유사체로부터 유도된 여타 화합물이 포함된다. 본 개시내용의 방법 및 조성물에 사용될 수 있는 화학요법 암 약제의 또다른 카테고리는 포도필로톡신 (podophyllotoxin) 유도체, 예컨대 에토포시드 (etoposide), 테니포시드 (teniposide) 및 미토포다지드 (mitopodozide) 이다. 본 개시내용은 추가로 알킬화제로 공지된 여타 화학요법 암 약제가 포함되며, 이는 종양 세포 내 유전자 물질을 알킬화시킨다. 여기에는, 이에 제한됨없이, 시스플라틴 (cisplatin), 시클로포스파미드 (cyclophosphamide), 질소 머스타드 (nitrogen mustard), 트리메틸렌 티오포스포르아미드, 카르무스틴 (carmustine), 부술판 (busulfan), 클로람부실 (chlorambucil), 벨루스틴 (belustine), 우라실 머스타드 (uracil mustard), 클로마파진 (chlomaphazin) 및 다카르바진 (dacarbazine) 이 포함된다. 본 개시내용은 화학치료제로서의 항대사약물을 포함한다. 그러한 유형의 약제의 예시에는, 싸이토신 아라비노사이드 (cytosine arabinoside), 플루오로우라실 (fluorouracil), 메토트렉세이트 (methotrexate), 메르캅토퓨린 (mercaptopurine), 아자티오프림 (azathioprime), 및 프로카르바진 (procarbazine) 이 포함된다. 본 개시내용의 방법 및 조성물에 사용될 수 있는 화학치료 암 약제의 추가적인 카테고리에는 항생제가 포함된다. 예시에는, 이에 제한되지 않으나, 독소루비신 (doxorubicin), 블레오마이신 (bleomycin), 닥티노마이신 (dactinomycin), 다우노루비신 (daunorubicin), 미트라마이신 (mithramycin), 미토마이신 (mitomycin), 미토마이신 C (mytomycin C) 및 다우노마이신 (daunomycin) 이 포함된다. 상기 화합물에 대해 시판되어 입수가능한 수많은 리포좀 제형물이 있다. 본 개시내용은 추가로, 이에 제한되지 않으나, 항종양 항체, 다카르바진 (dacarbazine), 아자싸이티딘 (azacytidine), 암사크린 (amsacrine), 멜팔란 (melphalan), 이포스파미드 (ifosfamide) 및 미톡사트론 (mitoxantrone) 을 포함하는 여타 화학치료 암 약제를 포함한다.
본원에 개시된 화합물들은 단독으로, 또는 세포독성/항신생물제 및 항혈관형성제를 포함하는 여타 항종양 약제와 조합되어 투여될 수 있다.
세포독성/항신생물 약제는 암 세포를 공격 및 사멸시키는 약제로서 정의된다. 일부 세포독성/항신생물제는 알킬화제이며, 이는 종양 세포 내 유전자 물질을 알킬화시키며, 예를 들어 시스플라틴 (cis-platin), 시클로포스파미드 (cyclophosphamide), 질소 머스타드 (nitrogen mustard), 트리메틸렌 티오포스포르아미드, 카르무스틴 (carmustine), 부술판 (busulfan), 클로르암부실 (chlorambucil), 벨루스틴 (belustine), 우라실 머스타드 (uracil mustard), 클로마파진 (chlomaphazin) 및 다카바진 (dacabazine) 이 있다. 여타 세포독성/항신생물제는 종양 세포에 대한 항대사약물이며, 예를 들어 싸이토신 아라비노시드 (cytosine arabinoside), 플루오로우라실 (fluorouracil), 메토트렉세이트 (methotrexate), 메르캅토퓨린 (mercaptopurine), 아자티오프림 (azathioprime), 및 프로카르바진 (procarbazine) 이 있다. 여타 세포독성/항신생물제는 항생제이며, 예를 들어 독소루비신 (doxorubicin), 블레오마이신 (bleomycin), 닥티노마이신 (dactinomycin), 다우노루비신 (daunorubicin), 미트라마이신 (mithramycin), 미토마이신 (mitomycin), 미토마이신 C (mytomycin C) 및 다우노마이신 (daunomycin) 이 있다. 상기 화합물들에 대해 시판되어 입수가능한 수많은 리포좀 제형물이 있다. 또다른 세포독성/항신생물제는 유사분열 억제제 (빈카 알칼로이드 (vinca alkaloid)) 이다. 여기에는, 빈크리스틴 (vincristine), 빈블라스틴 (vinblastine) 및 에토포사이드 (etoposide) 가 포함된다. 다양한 세포독성/항신생물제에는 택솔 (taxol) 및 그의 유도체, L-아스파라기나아제, 항종양 항체, 다카르바진 (dacarbazine), 아자싸이티딘 (azacytidine), 암사크린 (amsacrine), 멜팔란 (melphalan), VM-26, 이포스파미드 (ifosfamide), 미톡산트론 (mitoxantrone) 및 빈데신 (vindesine) 이 포함된다.
항혈관형성제는 당업계에 널리 공지되어 있다. 본 개시내용의 방법 및 조성물에 사용하기에 적합한 항혈관형성제에는 항-VEGF 항체가 포함되며, 여기에는 인간화 및 키메라성 항체, 항-VEGF 아프타머 (aptamer) 및 안티센스 올리고뉴클레오티드가 포함된다. 여타 공지된 혈관형성 억제제에는 안지오스타틴 (angiostatin), 엔도스타틴 (endostatin), 인터페론, 인터류킨 1 (α 및 β 포함), 인터류킨 12, 레티노산, 및 메탈로프로테이나제-1 및 -2 의 조직 억제제가 포함된다. (TIMP-I 및 -2). 토포이소머라아제, 예컨대 라족산 (razoxane), 항혈관형성 활성이 있는 토포이소머라아제 II 억제제를 포함하는 소형 분자들이 또한 이용될 수 있다.
개시된 화합물과 병용하여 사용될 수 있는 여타 항암제에는, 이에 제한되지 않으나 하기의 것이 포함된다: 아시비신 (acivicin); 아클라루비신 (aclarubicin), 아코다졸 히드로클로라이드 (acodazole hydrochloride; 아크로닌 (acronine), 아도젤레신 (adozelesin); 알데스류킨 (aldesleukin); 알트레타민 (altretamine), 암보마이신 (ambomycin); 아메탄트론 아세테이트 (ametantrone acetate); 아미노글루테티마이드 (aminoglutethimide); 암사크린 (amsacrine); 아나스트로졸 (anastrozole); 안트라마이신 (anthramycin); 아스파라기나아제 (asparaginase); 아스페름 (asperlm); 아자싸이티딘 (azacitidine); 아제테파 (azetepa); 아조토마이신 (azotomycin); 바티마스타트 (batimastat); 벤조데파 (benzodepa); 비칼루타마이드 (bicalutamide); 비산트렌 히드로클로라이드 (bisantrene hydrochloride); 비스나파이드 디메실레이트 (bisnafide dimesylate); 비젤레신 (bizelesin); 블레오마이신 설페이트 (bleomycin sulfate); 브레퀴나르 소듐 (brequinar sodium); 브로피리민 (bropirimine); 부술판 (busulfan); 칵티노마이신 (cactinomycin); 칼루스테론 (calusterone); 카라세마이드 (caracemide); 카르베티메르 (carbetimer), 카르보플라틴 (carboplatin); 카르무스틴 (carmustine); 카루비신 히드로클로라이드 (carubicin hydro클로라이드); 카르젤레신 (carzelesin); 세데핀골 (cedefingol); 클로람부실 (chlorambucil); 시롤레마이신 (cirolemycin); 시스플라틴 (cisplatin); 클라드리빈 (cladribine); 크리스나톨 메실레이트 (crisnatol mesylate); 시클로포스파마이드 (cyclophosphamide); 시타라빈 (cytarabine), 다카르바진 (dacarbazine); 닥티노마이신 (dactinomycin); 다우노루비신 히드로클로라이드 (daunorubicin hydrochloride); 데시타빈 (decitabine); 덱소르마플라틴 (dexormaplatin); 데자구아닌 (dezaguanine); 데자구아닌 메실레이트 (dezaguanine mesylate); 디아지쿠온 (diaziquone); 도세탁셀 (docetaxel); 독소루비신 (doxorubicin); 독소루비신 히드로클로라이드 (doxorubicin hydrochloride); 드롤록시펜 (droloxifene); 드롤록시펜 시트레이트; 드로모스타놀론 프로피오네이트 (dromostanolone propionate); 두아조마이신 (duazomycin); 에다트렉세이트 (edatrexate); 에플로르니틴 히드로클로라이드 (eflornithine hydrochloride); 엘라사미트루신 (elsamitrucin); 엔로플라틴 (enloplatin); 엔프로메이트 (enpromate); 에피프로피딘 (epipropidine); 에피루비신 히드로클로라이드 (epirubicin hydrochloride); 에르불로졸 (erbulozole); 에소루비신 히드로클로라이드 (esorubicin hydrochloride); 에스트라무스틴 (estramustine); 에스트라부스틴 포스페이트 소듐 (estramustine phosphate sodium); 에타니다졸 (etanidazole); 에토포사이드 (etoposide); 에토포사이드 포스페이트 (etoposide phosphate); 에토프린 (etoprine); 파드로졸 히드로클로라이드 (fadrozole hydrochloride); 파자라빈 (fazarabine); 펜레티나이드 (fenretinide); 플록수리딘 (floxuridine); 플루다라빈 포스페이트 (fludarabine phosphate); 플루오로우라실 (fluorouracil); 플루오로시타빈 (flurocitabine); 포스퀴돈 (fosquidone); 포스트리에신 소듐 (fostriecin sodium); 겜시타빈 (gemcitabine), 겜시타빈 히드로클로라이드; 히드록시우레아; 이다루비신 히드로클로라이드 (idarubicin hydrochloride); 이포스파미드 (ifosfamide); 일모포신 (ilmofosine); 인터류킨 II (재조합 인터류킨 II 또는 rIL2 포함), 인터페론 알파-2a; 인터페론 알파-2b; 인터페론 알파-n1, 인터페론 알파-n3; 인터페론 베타-1a; 인터페론 감마-1b; 이프로플라틴 (iproplatin); 이리노테칸 히드로클로라이드 (irinotecan hydrochloride); 란레오타이드 아세테이트 (lanreotide acetate); 레트로졸 (letrozole); 류프롤라이드 아세테이트 (leuprolide acetate); 리아로졸 히드로클로라이드 (liarozole hydrochloride); 로메트렉솔 소듐 (lometrexol sodium); 로무스틴 (lomustine); 록속산트론 히드로클로라이드 (losoxantrone hydrochloride); 마소프로콜 (masoprocol); 메이탄신 (maytansine); 메클로레타민 히드로클로라이드 (mechlorethamine hydrochloride); 메게스트롤 아세테이트 (megestrol acetate); 멜렌게스트롤 아세테이트 (melengestrol acetate); 멜팔란 (melphalan); 메노가릴 (menogaril); 메르캅토퓨린 (mercaptopurine); 메토트렉세이트 (methotrexate); 메토트렉세이트 소듐 (methotrexate sodium); 메토프린 (metoprine); 메투레데파 (meturedepa); 미틴도마이드 (mitindomide); 미토카르신 (mitocarcin); 미토크로민 (mitocromin); 미토길린 (mitogillin); 미토말신 (mitomalcin); 미토마이신 (mitomycin), 미토스페르 (mitosper); 미토탄 (mitotane), 미톡산트론 히드로클로라이드 (mitoxantrone hydro클로라이드); 미코페놀산 (mycophenolic acid); 노코다졸 (nocodazole); 노갈라마이신 (nogalamycin), 오르마플라틴 (ormaplatin); 옥시수란 (oxisuran); 파클리탁셀 (paclitaxel); 페가스파르가아제 (pegaspargase); 펠리오마이신 (peliomycin); 펜타무스틴 (pentamustine); 페플레오마이신 설페이트 (peplomycin sulfate); 페르포스파미드 (perfosfamide), 피포브로만 (pipobroman), 피포술판 (piposulfan), 피록산트론 히드로클로라이드 (piroxantrone hydrochloride); 플리카마이신 (plicamycin); 플로메스탄 (plomestane); 포르피메르 소듐 (porfimer sodium); 포르피로마이신 (porfiromycin); 프레드니무스틴 (prednimustine); 프로카르바진 히드로클로라이드 (procarbazine hydrochloride); 푸로마이신 (puromycin); 푸로마이신 히드로클로라이드; 피라조푸린 (pyrazofurin); 리보프린 (riboprine); 로글리티마이드 (rogletimide); 사핀골 (safingol); 사핀골 히드로클로라이드; 세무스틴 (semustine); 심트라젠 (simtrazene); 스파르포세이트 소듐 (sparfosate sodium); 스파르소마이신 (sparsomycin); 스피로게르마늄 히드로클로라이드 (spirogermanium hydrochloride); 스피로무스틴 (spiromustine); 스피로플라틴 (spiroplatin); 스트렙토니그린 (streptonigrin); 스트렙토조신 (streptozocin); 술포레누르 (sulofenur); 탈리소마이신 (talisomycin); 테코갈란 소듐 (tecogalan sodium), 테가푸르 (tegafur); 텔록산트론 히드로클로라이드 (teloxantrone hydrochloride); 테모포르핀 (temoporfin); 테니포사이드 (teniposide); 테록시론 (teroxirone); 테스톨락톤 (testolactone); 티아미프린 (thiamiprine); 티오구아닌 (thioguanine); 티오테파 (thiotepa); 티아조푸린 (tiazofurin); 티라파자민 (tirapazamine); 토레미펜 시트레이트 (toremifene citrate); 트레스톨론 아세테이트 (trestolone acetate); 트리시리빈 포스페이트 (triciribine phosphate); 트리메트렉세이트 (trimetrexate); 트리메트렉세이트 글루쿠로네이트; 트리프토렐린 (triptorelin), 투불로졸 히드로클로라이드 (tubulozole hydrochloride), 우라실 머스타드 (uracil mustard), 우레데파 (uredepa), 바프레오타이드 (vapreotide), 베르테포르핀 (verteporfin), 빈블라스틴 설페이트 (vinblastine sulfate), 빈크리스틴 설페이트 (vincristine sulfate); 빈데신 (vindesine); 빈데신 설페이트 (vindesine sulfate), 빈네피딘 설페이트 (vinepidine sulfate); 빈글리시네이트 설페이트 (vinglycinate sulfate); 빈류로신 설페이트 (vinleurosine sulfate); 비노렐빈 타르트레이트 (vinorelbine tartrate); 빈로시딘 설페이트 (vinrosidine sulfate), 빈졸리딘 설페이트 (vinzolidine sulfate), 보로졸 (vorozole); 제니플라틴 (zeniplatin); 지노스타틴 (zinostatin); 조루비신 히드로클로라이드 (zorubicin hydrochloride), 20-epi-l,25 디히드록시비타민 D3; 5-에티닐우라실, 아비라테론 (abiraterone); 아클라루비신 (aclarubicin), 아실풀벤 (acylfulvene), 아데시페놀 (adecypenol); 아도젤레신 (adozelesin); 알데슬류킨 (aldesleukin), ALL-TK 안타고니스트; 알트레타민 (altretamine); 암바무스틴 (ambamustine); 아미독스 (아미도x); 아미포스틴 (amifostine); 아미노레불린산 (aminolevulinic acid); 암루비신 (amrubicin); 암사크린 (amsacrine); 아나그렐라이드 (anagrelide); 아나스트로졸 (anastrozole); 안드로그라폴라이드 (andrographolide); 혈관형성 억제제; 안타고니스트 D; 안타고니스트 G; 안타렐릭스 (antarelix); 항-등쪽 형태형성 단백질-1 (anti-dorsalizing morphogenetic protein-1); 안티안드로겐 (antiandrogen), 전립선 암종 (prostatic carcinoma), 안티에스트로겐 (antiestrogen); 안티네오플라스톤 (antineoplaston), 안티센스 올리고뉴클레오티드 (antisense oligonucleotides), 아피디콜린 글리시네이트 (aphidicolin glycinate); 아폽토시스 유전자 조절제, 아폽토시스 조절제, 아푸린산 (apurinic acid); ara-CDP-DL-PTBA, 아르기닌 디아미나아제 (arginine deaminase); 아술라크린 (asulacrine); 아타메스탄 (atamestane), 아트리무스틴 (atrimustine); 악시나스타틴 1 (axinastatin 1); 악시나스타틴 2; 악시나스타틴 3, 아자세트론 (azasetron), 아자톡신 (azatoxin), 아자타이로신 (azatyrosine), 바카틴 III 유도체 (baccatin III derivatives), 발라놀 (balanol), 바티마스타트 (batimastat), BCR/ABL 안타고니스트; 벤조클로린 (benzochlorin), 벤조일스타우로스포린 (benzoylstaurosporine), 베타 락탐 유도체; 베타-알레틴 (beta-alethine); 베타클라마이신 B (betaclamycin B); 베툴린산 (betulinic acid); bFGF 억제제; 비칼루타마이드 (bicalutamide); 비산트렌 (bisantrene), 비스아지리디닐스페르민 (bisaziridinylspermine); 비스나파이드 (bisnafide), 비스트라텐 A (bistratene A); 비젤레신 (bizelesin), 브레플레이트 (breflate); 브로피리민 (bropiromine); 부도티탄 (budotitane); 부티오닌 술폭시민 (buthionine sulfoximine); 칼시포트리오 (calcipotriol); 칼포스틴 C (calphostin C); 캄토테신 유도체 (camptothecin derivatives), 카나르폭스 (canarypox) IL-2; 카페시타빈 (capecitabine); 카르복사마이드-아미드-트리아졸 (carboxamide-amino-triazol); 카르복시아미도트리아졸 (carboxyamidotriazol); CaRest M3; CARN 700, 연골 유도성 억제제, 카르젤레신 (carzelesin), 카제인 키아나제 억제제 (ICOS), 카스타노스페르민 (castanospermine); 세크로핀 B (cecropin B), 세트로렐릭스 (cetrorelix); 클로르린 (chlorlns); 클로로퀴녹살린 술폰아미드 (chloroquinoxaline sulfonamide), 시카프로스트 (cicaprost); 시스-포르피린 (cis-porphyrin), 클라드리빈 (cladribine); 클로미펜 유사체 (clomifene analogues), 클로트리마졸 (clotrimazole), 콜리스마이신 A (collismycin A), 콜리스마이신 B (collismycin B), 콤브레타스타틴 A4 (combretastatin A4); 콤브레타스타틴 유사체; 코나게닌 (conagenin); 크람베시딘 (crambescidin) 816, 크리스나톨 (crisnatol); 크립토피신 8 (cryptophycin 8), 크립토피신 A 유도체; 쿠라신A (curacin A); 시클로펜타트라퀴논 (cyclopentanthraquinones), 시클로플라탐 (cycloplatam), 시페마이신 (cypemycin), 시타라빈 옥포스페이트 (cytarabine ocfosfate), 세포가수분해 인자 (cytolytic factor), 싸이토스타틴 (cytostatin), 다클릭시마브 (dacliximab), 데시타빈 (decitabine), 디히드로디데민 B (dehydrodidemnin B); 데슬로렐린 (deslorelin); 덱사메타손 (dexamethasone), 덱시포스파마이드 (dexifosfamide), 덱스라족산 (dexrazoxane); 덱스베라파밀 (dexverapamil); 디아지쿠온 (diaziquone); 디뎀닌 B (didemnin B); 디독스 (didox), 디에틸노르스페르민 (디에틸norspermine), 디히드로-5-아자싸이티딘; 디히드로택솔 (dihydrotaxol), 9-; 디옥사마이신 (dioxamycin), 디페닐스피로무스틴 (diphenyl spiromustine); 도세탁셀 (docetaxel), 도코사놀 (docosanol); 돌라세트론 (dolasetron); 독시플루리딘 (doxifluridine), 드롤록시펜 (droloxifene); 드로나비놀 (dronabinol), 두오카르마이신 SA (duocarmycin SA); 에브셀렌 (ebselen); 에코무스틴 (ecomustine); 에델포신 (edelfosine), 에드레콜로마브 (edrecolomab), 에플로르니틴 (eflornithine), 엘레멘 (elemene); 에미테푸르 (emitefur); 에피루비신 (epirubicin), 에피리스테라이드 (epristeride), 에스트라무스틴 유사체 (estramustine analogue), 에스트로겐 아고니스트 (estrogen agonist), 에스트로겐 안타고니스트 (estrogen antagonist); 에타니다졸 (etanidazole); 에토포사이드 포스페이트 (etoposide phosphate); 엑세메스탄 (exemestane); 파드로졸 (fadrozole); 파자라빈 (fazarabine), 펜레트마이드 (fenretmide), 필그라스팀 (filgrastim), 피나스테라이드 (finasteride); 플라보피리돌 (flavopiridol); 플레젤라스틴 (flezelastine); 플루아스테론 (fluasterone); 플루다라빈 (fludarabine), 플루오로다우노루니신 히드로클로라이드 (fluorodaunorunicin hydrochloride), 포르페니멕스 (forfenimex), 포르메스탄 (formestane), 포스트리에신 (fostriecin), 포테무스틴 (fotemustine); 가돌리늄 텍사피린 (gadolinium texaphyrin); 갈륨 니트레이트 (gallium nitrate); 갈로시타빈 (galocitabine); 가니렐릭스 (ganirelix), 젤라티나아제 억제제 (gelatinase inhibitors); 겜시타빈 (gemcitabine); 글루타티온 억제제; 헵술팜 (hepsulfam); 헤레굴린 (heregulin); 헥사메틸렌 비스아세트아미드 (hexamethylene bisacetamide); 히페리신 (hypericin), 이바드론산 (ibandronic acid); 이다루비신 (idarubicin), 이독시펜 (idoxifene); 이드라만톤 (idramantone); 일모포신 (ilmofosine), 일로마스타트 (ilomastat), 이미다졸크리돈 (imidazoacridone); 이미퀴모드 (imiquimod); 면역자극 펩티드; 인슐린형 성장 인자-1 수용체 억제제; 인터페론 아고니스트; 인터페론; 인터류킨; 요벤구안 (iobenguane); 요오독소루비신 (iododoxorubicin); 이포메아놀 (ipomeanol), 4-; 이로플락트 (iroplact); 이르소글라딘 (irsogladine); 이소벤가졸 (isobengazole); 이소호모할리콘드린 B (isohomohalicondrin B); 이타세트론 (itasetron); 자스플라키놀라이드 (jasplakinolide); 카할랄라이드 F (kahalalide F); 라멜라린-N 트리아세테이트 (lamellarin-N triacetate), 란레오타이드 (lanreotide); 레이나마이신 (leinamycin); 레노그라스틴 (lenograstine), 렌티난 설페이트 (lentinan sulfate), 렙톨스타틴 (leptolstatin); 레트로졸 (letrozole); 백혈병 억제 인자; 백혈구 알파 인터페론; 류프롤라이드 + 에스트로겐 + 프로게스테론; 류프로렐린 (leuprorelin); 레바미솔 (levamisole); 리아로졸 (liarozole), 선형 폴리아민 유사체; 친유성 이당류 펩티드; 친유성 백금 화합물; 리소클린아미드 7 (lissoclinamide 7); 로바플라틴 (lobaplatin), 롬브리신 (lombricine), 로메트렉솔 (lometrexol); 로니다민 (lonidamine); 로속산트론 (losoxantrone), 로바스타틴 (lovastatin), 록소리빈 (loxoribine), 루르토테칸 (lurtotecan), 루테튬 텍사피린 (lutetium texaphyrin), 리소필린 (lysofylline), 분해 펩티드 (lytic peptides); 마이탄신 (maitansine); 만노스타틴 A (mannostatin A), 마리마스타트 (marimastat); 마소프로콜 (masoprocol); 마스핀 (maspin), 마트릴리신 억제제 (matrilysin inhibitors); 매트릭스 메탈로프로테이나제 억제제 (matrix metalloproteinase inhibitors), 메노가릴 (menogaril); 메르바론 (merbarone); 메테렐린 (meterelin); 메티오니나아제 (methioninase), 메토클로프라마이드 (metoclopramide) 및 미토구아존 (mitoguazone); 미토락톨 (mitolactol); 미토마이신 유사체 (mitomycin analogues); 미토나파이드 (mitonafide); 미토톡신 섬유아세포 성장 인자-사포린 (mitotoxin fibroblast growth factor-saporin); 미톡산트론 (mitoxantrone); 모파로텐 (mofarotene); 몰그라모스팀 (molgramostim); 모노클로날 항체, 인간 코리오닉 고나도트로핀 (human chorionic gonadotrophin); 모노포스포릴 지질 A (monophosphoryl lipid A) + 미요박테리움 세포벽 sk (myobacterium cell wall sk), 모피다몰 (mopidamol), 다중 약물 내성 유전자 억제제, 다중 종양 억제자 1-기반 요법; 머스타드 항암제 (mustard anticancer agent); 미카페록시드 B (mycaperoxide B), 미코박테리아 세포벽 추출물; 미리아포론 (myriaporone); N-아세틸디날란 (N-아세틸dinaline), N-치환 벤즈아미드, 나파렐린 (nafarelin), 나그레스팁 (nagrestip), 날록손 (naloxone) + 펜타조신 (pentazocine), 나파빈 (napavin), 나프테르핀 (naphterpin), 나르토그라스팀 (nartograstim); 네다플라틴 (nedaplatin); 네모루비신 (nemorubicin); 네리드론산 (neridronic acid); 중성 엔도펩티다아제 (neutral endopeptidase), 니룰타마이드 (nilutamide), 니사마이신 (nisamycin); 산화질소 조절제, 니트록시드 산화방지제, 니트룰린 (nitrullyn), 06-벤질구아닌, 옥트레오타이드 (octreotide), 오키세논 (okicenone); 올리고뉴클레오티드; 오나프리스톤 (onapristone); 온단세트론 (ondansetron), 온단세트론; 오라신 (oracin); 경구용 사이토카인 유도체 (oral cytokine inducer), 오르마플라틴 (ormaplatin); 오사테론 (osaterone); 옥살리플라틴 (oxaliplatin); 옥사우로마이신 (oxaunomycin), 파클리탁셀 (paclitaxel), 파클리탁셀 유사체; 파클리탁셀 유도체; 팔라우아민 (palauamine), 팔미토일리족신 (palmitoylrhizoxin); 파미드론산 (pamidronic acid); 파낙실트리올 (panaxytriol); 파노미펜 (panomifene); 바라박틴 (parabactin); 파젤리프틴 (pazelliptine); 페가스파르가아제 (pegaspargase); 펠데신 (peldesine); 펜토산 폴리설페이트 소듐 (pentosan polysulfate sodium), 펜토스타틴 (pentostatin), 펜트로졸 (pentrozole), 퍼플루브론 (perflubron), 퍼포스파미드 (perfosfamide), 페릴릴 알콜 (perillyl alcohol), 페나즈모마이신 (phenazmomycin), 페닐아세테이트, 포스파타아제 억제제; 피시바닐 (picibanil); 필로카르핀 히드로클로라이드 (pilocarpine hydrochloride); 피라루비신 (pirarubicin), 피리트렉심 (piritrexim); 플라세틴 A (placetin A), 플라세틴 B; 플라스미노겐 활성화제 억제제 (plasminogen activator inhibitor); 백금 착물, 백금 화합물; 백금-트리아민 착물, 포르피메르 소듐 (porfimer sodium); 포르피로마아신 (porfiromycin); 프레드니손 (prednisone), 프로필 비스-아크리돈 (propyl bis-acridone); 프로스타글란딘 12 (prostaglandin 12); 프로테아좀 억제제; 단백질 A-기반 면역 조절제; 단백질 키나아제 C 억제제; 단백질 키나아제 C 억제제, 미크로알칼 (microalgal); 단백질 타이로신 포스파타아제 억제제; 퓨린 뉴클레오시드 포스포릴라아제 억제제; 푸르푸린 (purpurin); 피라졸로아크리딘 (pyrazoloacridine); 피리독실화 헤모글로빈 폴리옥시에틸렌 콘쥬게이트 (pyridoxylated hemoglobin polyoxyethylene conjugate); raf 안타고니스트; 랄티트렉스드 (raltitrexed); 라모세트론 (ramosetron); ras 파르네실 단백질 트랜스퍼라아제 억제제; ras 억제제; ras-GAP 억제제; 디메틸화된 레텔리프틴 (retelliptine demethylated); 레늄 Re 186 에티드로네이트 (etidronate); 리족신 (rhizoxin); 리보자임; RII 레틴아미드 (retinamide); 로글레티마이드 (rogletimide); 로히투킨 (rohitukine); 로무르타이드 (romurtide); 로퀴니멕스 (roquinimex); 루비기논 B1 (rubiginone B1); 루복실 (ruboxyl); 사핀골 (safingol); 삼토핀 (samtopin); SarCNU; 사르코피톨 A (sarcophytol A); 사르그라모스팀 (sargramostim); Sdi 1 모방체; 세무스틴 (semustine); 세네센스 유도성 억제제 1 (senescence derived inhibitor 1); 센스 올리고뉴클레오티드; 신호 전달 억제제; 신호 전달 조절제; 단일 사슬 항원 결합 단백질; 시조피란 (sizofiran); 소보족산 (sobuzoxane); 소듐 보로카프테이트 (sodium borocaptate); 소듐 페닐 아세테이트; 솔베롤 (solverol); 소마토메딘 (somatomedin) 결합 단백질, 소네르민 (sonermin); 스파르포스산 (sparfosic acid); 스피카마이신 D (spicamycin D); 스피로무스틴 (spiromustine); 스플레노펜틴 (splenopentin); 스포기스타틴 1 (spongistatin 1); 스쿠알라민 (squalamine); 줄기 세포 억제제; 줄기 세포 분열 억제제; 스티피아미드 (stipiamide); 스토멜리신 (stromelysin) 억제제; 술피노신 (sulfinosine); 수퍼액티브 혈관작용성 소장 펩티드 안타고니스트 (superactive vasoactive intestinal peptide antagonist); 수라디스타 (suradista); 수라민 (suramin); 스와인소닌 (swainsonine), 합성 글리코사미노글리칸; 탈리무스틴 (tallimustine); 타목시펜 메티오다이드 (tamoxifen methiodide); 타우로무스틴 (tauromustine); 타자로텐 (tazarotene); 테코갈란 소듐 (tecogalan sodium); 테가푸르 (tegafur); 텔루라피릴륨 (tellurapyrylium); 텔로머라아제 억제제; 테모포르핀 (temoporfin); 테모졸로마이드 (temozolomide); 템포사이드 (temposide); 테트라클로로데카옥시드; 테트라조민 (tetrazomine), 탈리블라스틴 (thaliblastine); 티오코랄린 (thiocoraline); 트롬보포이에틴 (thrombopoietin); 트롬보포이에틴 모방체; 티말파신 (thymalfasin); 티모포이에틴 수용체 아고니스트; 티모트리난 (thymotrinan); 흉선 자극 호르몬; 주석 에틸 에티오푸르푸린 (tin ethyl etiopurpurin); 티라파자민 (tirapazamine), 티타노오센 비클로라이드 (titanocene bichloride); 탑센틴 (topsentin), 토레미펜 (toremifene); 토티포텐트 줄기 세포 인자 (totipotent stem cell factor); 번역 억제제 (translation inhibitors); 트레티노인 (tretinoin); 트리아세틸우리딘 (triacetyluridine); 트리시리빈 (triciribine); 트리메트렉세이트 (trimetrexate); 트리프토렐린 (triptorelin); 트로피세트론 (tropisetron); 투로스테라이드 (turosteride); 타이로신 키나아제 억제제; 티르포스틴 (tyrphostin); UBC 억제제, 우베니멕스 (ubenimex), 우로제니탈 사이너스-유도성 성장 저해 인자 (urogenital sinus-derived growth inhibitory factor), 우로키나아제 수용체 안타고니스트 (urokinase receptor antagonists); 바프레타이드 (vapreotide); 바리올린 B (variolin B); 벡터 시스템, 적혈구 유전자 요법 (erythrocyte gene therapy); 벨라레솔 (velaresol); 베라민 (veramine), 베르딘스 (verdins); 베르테포핀 (verteporfin); 비노렐빈 (vinorelbine); 빈잘틴 (vinxaltine); 비탁신 (vitaxin); 보로졸 (vorozole); 자노테론 (zanoterone); 제니플라틴 (zeniplatin); 질라스코르브 (zilascorb); 및 지노스타틴 스티말머 ( zinostatin stimalamer). 한 구현예에서, 항암 약물은 5-플루오로우라실, 택솔 또는 류코보린이다.
본원에 사용된 용어 "유효량" 은 "원하는 또는 치료 결과를 달성하기 위해 투여량 및 필요한 기간 동안 유효한 하나 이상의 페닐술팜산의 양" 을 의미한다. 유효량은 당업계에 공지된 인자들, 예컨대 치료한 인간 또는 동물의 질병 상태, 연령, 성별 및 체중에 따라 가변적일 수 있다.
특정 투여 계획이 본원에서 실시예에서 기재될 수 있지만, 당업자라면 투여 계획이 최적의 치료 응답성 제공을 위해 변경될 수 있다는 점을 감안할 것이다. 따라서, 정확한 "유효량" 을 설명하는 것을 가능하지 않다. 예를 들어, 수 최 나눈 투여량을 매일 투여할 수 있거나, 또는 치료 상황의 긴급성에 의해 표시된 것에서 비율에 맞게 투여량을 감소시킬 수 있다. 추가로, 본 개시내용의 조성물은 치료량 달성에 필요한 만큼 빈번하게 투여될 수 있다.
본 개시내용의 특정 구현예가 설명 및 기술되었지만, 당업자에게는 다양한 여타 변경 및 개질이 본 개시내용의 진의 및 범위를 벗어나지 않고도 가능하다는 것이 자명할 것이다. 따라서, 첨부된 특허청구범위는 본 개시내용의 범위 내에 있는 모든 그러한 변화 및 개질을 전부 청구하는 것을 의도로 한다.
Claims (54)
- 삭제
- 삭제
- 제 4 항에 있어서, 화학치료제가 택솔, IL-2, 겜시타빈, 엘로티닙, 독실, 이리노르테칸 및 베바시주마브로부터 선택되는 의약.
- 제 1 항, 제 2 항, 제 4 항 및 제 6 항 중 어느 한 항에 있어서, 암이 하기로부터 선택되는 의약:
급성 림프구성 백혈병 (Acute Lymphoblastic); 급성 골수성 백혈병 (Acute Myeloid Leukemia); 부신피질암 (Adrenocortical Carcinoma); 소아 부신피질암 (Adrenocortical Carcinoma, Childhood); 충수암 (Appendix Cancer); 기저세포 암종 (Basal Cell Carcinoma); 간외 담도암 (Bile Duct Cancer, Extrahepatic); 방광암 (Bladder Cancer); 골암 (Bone Cancer); 골육종 (Osteosarcoma) 및 악성 섬유성 조직구종 (Malignant Fibrous Histiocytoma); 소아 뇌간교종 (Brain Stem Glioma, Childhood); 성인 뇌종양 (Brain Tumor, Adult); 뇌종양 (Brain Tumor), 소아 뇌간교종; 뇌종양, 소아 중추신경계 비정형 기형/횡문근양 종양 (Central Nervous System Atypical Teratoid/Rhabdoid Tumor, Childhood); 중추 신경계 배아종 (Central Nervous System Embryonal Tumors); 소뇌별아교세포종 (Cerebellar Astrocytoma); 소뇌별아교세포종 (Cerebral Astrocytoma)/악성 교종 (Malignant Glioma); 두개인두종 (Craniopharyngioma); 뇌실막모세포종 (Ependymoblastoma); 뇌실막종 (Ependymoma); 속질모세포종 (Medulloblastoma); 속질상피종 (Medulloepithelioma); 등도분화의 송과 실질세포 종양 (Pineal Parenchymal Tumors of Intermediate Differentiation); 천막위 원시 신경외배엽종양 (Supratentorial Primitive Neuroectodermal Tumors) 및 송과체모세포종 (Pineoblastoma); 시각경로 및 시상하부 신경아교종 (Visual Pathway and Hypothalamic Glioma); 뇌 및 척추 종양 (Brain and Spinal Cord Tumors); 유방암 (Breast Cancer); 기관지내 종양 (Bronchial Tumors); 버킷 림프종 (Burkitt Lymphoma); 유암종 (Carcinoid Tumor); 위장관 유암종 (Carcinoid Tumor, Gastrointestinal); 중추신경계 비정형 기형/횡문근양 종양 (Central Nervous System Atypical Teratoid/Rhabdoid Tumor); 중추 신경계 배아종 (Central Nervous System Embryonal Tumors); 중추신경계 림프종 (Central Nervous System Lymphoma); 소뇌별아교세포종 (Cerebellar Astrocytoma); 소아 소뇌별아교세포종/악성 교종 (Cerebral Astrocytoma/Malignant Glioma, Childhood); 자궁경부암 (Cervical Cancer); 소아 척삭종 (Chordoma, Childhood); 만성 림프성 백혈병 (Chronic Lymphocytic Leukemia); 만성 골수성 백혈병 (Chronic Myelogenous Leukemia); 만성 골수 증식 질환 (Chronic Myeloproliferative Disorders); 대장암 (Colon Cancer); 직장암 (Colorectal Cancer); 두개인두종 (Craniopharyngioma); 피부 T-세포 림프종 (Cutaneous T-Cell Lymphoma); 식도암 (Esophageal Cancer); 종양의 유잉 패밀리 (Ewing Family of Tumors); 고환외 배세포종 (Extragonadal Germ Cell Tumor); 간외 담도암 (Extrahepatic Bile Duct Cancer); 안암으로서, 안구내 흑색종 (Eye Cancer, Intraocular Melanoma); 안암으로서, 망막모세포종 (Eye Cancer, Retinoblastoma); 담낭암 (Gallbladder Cancer); 위암 (Gastric (Stomach) Cancer); 위장관 악성 종양 (Gastrointestinal Carcinoid Tumor); 위장관 기질종양 (Gastrointestinal Stromal Tumor (GIST)); 두개외 생식세포 종양 (Germ Cell Tumor, Extracranial); 고환외 생식 세포 종양 (Germ Cell Tumor, Extragonadal); 난소 생식 세포 종양 (Germ Cell Tumor, Ovarian); 임신성 융모성 종양 (Gestational Trophoblastic Tumor); 신경아교종 (Glioma); 소아 뇌간 신경아교종 (Glioma, Childhood Brain Stem); 신경아교종으로서의, 소아 뇌 별아교세포종 (Glioma, Childhood Cerebral Astrocytoma), 신경아교종으로서의, 소아 시각경로 및 시상하부 신경아교종 (Glioma, Childhood Visual Pathway and Hypothalamic), 털세포 백혈병 (Hairy Cell Leukemia); 두경부암 (Head and Neck Cancer); 간암 (hepatocellular (Liver) Cancer); 랑게르한스 세포의 조직구증 (Histiocytosis, Langerhans Cell); 호지킨 림프종 (Hodgkin Lymphoma); 피열후두개 암 (Hypopharyngeal Cancer); 시상하부 및 시각경로 신경아교종 (Hypothalamic and Visual Pathway Glioma); 안구내 흑색종 (Intraocular Melanoma); 췌도 세포종 (Islet Cell Tumors); 신장암 (Kidney (Renal Cell) Cancer); 랑게르한스 세포 조직구증 (Langerhans Cell Histiocytosis); 후두암 (Laryngeal Cancer); 급성 림프모구 백혈병 (Leukemia, Acute Lymphoblastic); 급성 골수성 백혈병 (Leukemia, Acute Myeloid); 만성 림프구성 백혈병 (Leukemia, Chronic Lymphocytic); 만성 골수성 백혈병 (Leukemia, Chronic Myelogenous); 털세포 백혈병 (Leukemia, Hairy Cell); 구순 및 구강암 (Lip and Oral Cavity Cancer); 간암 (Liver Cancer); 비소세포 폐암 (Lung Cancer, Non-Small Cell); 소세포 폐암 (Lung Cancer, Small Cell); AIDS 관련 림프종 (Lymphoma, AIDS-Related); 버킷 림프종 (Lymphoma, Burkitt); 피부 T-세포 림프종 (Lymphoma, Cutaneous T-Cell); 호지킨 림프종 (Lymphoma, Hodgkin); 비-호지킨 림프종 (Lymphoma, Non-Hodgkin); 원발성 중추 신경계 림프종 (Lymphoma, Primary Central Nervous System); 왈덴스트롬 마크로불린혈증 (Macroglobulinemia, Waldenstrom); 뼈의 악성 섬유조직구종 (Malignant Fibrous Histiocytoma of Bone) 및 골육종 (Osteosarcoma); 수모세포종 (Medulloblastoma); 흑색종 (Melanoma); 안내 흑색종 (Melanoma, Intraocular (눈)); 메르켈 세포 암 (Merkel Cell Carcinoma); 중피종 (Mesothelioma); 잠복 원발성의 전이성 편평상피 경부암 (Metastatic Squamous Neck Cancer with Occult Primary); 구강암 (Mouth Cancer); 소아의 다발성 내분비 샘종증 증후군 (Multiple Endocrine Neoplasia Syndrome, (Childhood)); 다발 골수종 (Multiple Myeloma)/형질 세포 종양 (Plasma Cell Neoplasm); 균상 식육종 (Mycosis Fungoides); 골수형성이상 증후군 (Myelodysplastic Syndromes); 골수형성이상/골수증식 질환 (Myelodysplastic/Myeloproliferative Diseases); 만성 골수성 백혈병 (Myelogenous Leukemia, Chronic); 성인 급성 골수성 백혈병 (Myeloid Leukemia, Adult Acute); 소아 급성 골수성 백혈병 (Myeloid Leukemia, Childhood Acute); 다발성 골수종 (Myeloma, Multiple); 만성 골수증식 질환 (Myeloproliferative Disorders, Chronic); 비강 및 부비동 암 (Nasal Cavity and Paranasal Sinus Cancer); 비인두암 (Nasopharyngeal Cancer); 신경모세포종 (Neuroblastoma); 비소세포폐암 (Non-Small Cell Lung Cancer); 구강암 (Oral Cancer); 구강암 (Oral Cavity Cancer); 입인두암 (Oropharyngeal Cancer); 뼈육종 (Osteosarcoma) 및 뼈의 악성 섬유 조직구종 (Malignant Fibrous Histiocytoma of Bone); 난소암 (Ovarian Cancer); 상피성 난소암 (Ovarian Epithelial Cancer); 난소 생식 세포 종양 (Ovarian Germ Cell Tumor); 난소 저악성 잠재성 종양 (Ovarian Low Malignant Potential Tumor); 췌장암 (Pancreatic Cancer); 췌장암으로서, 췌도 세포 종양 (Pancreatic Cancer, Islet Cell Tumors); 유두종증 (Papillomatosis); 부갑상선암 (Parathyroid Cancer); 음경암 (Penile Cancer); 인두암 (Pharyngeal Cancer); 크롬친화세포종 (Pheochromocytoma); 등도분화의 송과 실질세포 종양 (Pineal Parenchymal Tumors of Intermediate Differentiation); 송과체모세포종 (Pineoblastoma) 및 천막위 원시 신경외배엽종양 (Supratentorial Primitive Neuroectodermal Tumors); 하수체 종양 (Pituitary Tumor); 형질 세포 종양 (Plasma Cell Neoplasm)/다발 골수종 (Multiple Myeloma); 흉막폐아세포종 (Pleuropulmonary Blastoma); 원발성 중추신경계 림프종 (Primary Central Nervous System Lymphoma); 전립선암 (Prostate Cancer); 직장암 (Rectal Cancer); 신장암 (Renal Cell (Kidney) Cancer); 신우 및 요관 이행세포암 (Renal Pelvis and Ureter, Transitional Cell Cancer); 15 번 염색체 상의 NUT 유전자와 관련된 기 도 암종 (Respiratory Tract Carcinoma Involving the NUT Gene on Chromosome 15); 망막모세포종 (Retinoblastoma); 횡문근육종 (Rhabdomyosarcoma); 침샘암 (Salivary Gland Cancer); 종양의 유잉 패밀리의 육종 (Sarcoma, Ewing Family of Tumors); 카포시 육종 (Sarcoma, Kaposi); 연조직 육종 (Sarcoma, Soft Tissue); 요관 육종 (Sarcoma, Uterine); 세자리 증후군 (Sezary Syndrome); 피부암 (비흑색종) (Skin Cancer (Nonmelanoma)); 피부암 (흑색종) (Skin Cancer (Melanoma)); 메르켈 세포 피부 암종 (Skin Carcinoma, Merkel Cell); 소세포 폐암 (Small Cell Lung Cancer); 소장암 (Small Intestine Cancer); 연조직 육종 (Soft Tissue Sarcoma), 편평세포 암종 (Squamous Cell Carcinoma), 잠복 원발성의 전이성 편평상피 경부암 (Squamous Neck Cancer with Occult Primary, Metastatic); 위암 (Stomach (Gastric) Cancer); 천막위 원시 신경외배엽종양 (Supratentorial Primitive Neuroectodermal Tumors); 피부 T-세포 림프종 (T-Cell Lymphoma, Cutaneous); 고환암 (Testicular Cancer); 인후두암 (Throat Cancer); 가슴샘종 (Thymoma) 및 흉선 암종 (Thymic Carcinoma); 갑상선암 (Thyroid Cancer); 신우 및 요관 이행세포암 (Transitional Cell Cancer of the Renal Pelvis and Ureter); 임신성 융모 종양 (Trophoblastic Tumor, Gestational); 요도암 (Urethral Cancer); 자궁내막 자궁암 (Uterine Cancer, Endometrial); 자궁 육종 (Uterine Sarcoma); 질암 (Vaginal Cancer); 외음부암 (Vulvar Cancer); 왈덴스트룀 마크로글로불린혈증 (Waldenstrom Macroglobulinemia) 또는 윌름 종양 (Wilms Tumor). - 제 1 항, 제 2 항, 제 4 항 및 제 6 항 중 어느 한 항에 있어서, 화합물이 암모늄, 나트륨, 리튬, 칼륨, 칼슘, 마그네슘, 비스무트 및 라이신으로부터 선택되는 양이온의 염의 형태인 의약.
- 제 9 항에 있어서, 화학치료제가 택솔, IL-2, 겜시타빈, 엘로티닙, 독실, 이리노르테칸 및 베바시주마브로부터 선택되는 조성물.
- 제 9 항에 있어서, 상기 화합물이 암모늄, 나트륨, 리튬, 칼륨, 칼슘, 마그네슘, 비스무트 및 라이신으로부터 선택되는 양이온의 염의 형태인 조성물.
- 제 9 항 내지 제 11 항 중 어느 한 항에 있어서, 상기 암이 신장암, 폐암, 악성 흑색종 또는 췌장암인 조성물.
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US22326009P | 2009-07-06 | 2009-07-06 | |
| US61/223,260 | 2009-07-06 | ||
| PCT/US2010/020822 WO2011005330A1 (en) | 2009-07-06 | 2010-01-12 | Compounds, compositions, and methods for preventing metastasis of cancer cells |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20110114655A KR20110114655A (ko) | 2011-10-19 |
| KR101426125B1 true KR101426125B1 (ko) | 2014-08-06 |
Family
ID=43429466
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020117018742A KR101426125B1 (ko) | 2009-07-06 | 2010-01-12 | 암 세포의 전이 예방을 위한 화합물, 조성물 및 방법 |
Country Status (21)
| Country | Link |
|---|---|
| US (4) | US8569348B2 (ko) |
| EP (2) | EP3556367A1 (ko) |
| JP (5) | JP5536113B2 (ko) |
| KR (1) | KR101426125B1 (ko) |
| CN (3) | CN103976998A (ko) |
| AU (1) | AU2010271105C1 (ko) |
| BR (1) | BRPI1006897A2 (ko) |
| CA (1) | CA2748765C (ko) |
| DK (1) | DK2451279T3 (ko) |
| ES (1) | ES2726946T3 (ko) |
| IL (2) | IL214048A (ko) |
| MX (1) | MX2011007420A (ko) |
| MY (1) | MY160399A (ko) |
| NZ (1) | NZ594537A (ko) |
| PL (1) | PL2451279T3 (ko) |
| PT (1) | PT2451279T (ko) |
| RU (1) | RU2519123C2 (ko) |
| SG (2) | SG10201505672TA (ko) |
| TR (1) | TR201907783T4 (ko) |
| WO (1) | WO2011005330A1 (ko) |
| ZA (1) | ZA201105678B (ko) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20210035426A (ko) | 2019-09-24 | 2021-04-01 | 충북대학교 산학협력단 | N-아릴-2-[(6-부틸-1,3-디메틸-2,4-디옥소-1,2,3,4-테트라하이드로피리도[2,3-d]피리미딘-5-일)설페닐]아세트아마이드를 유효성분으로 함유하는 종양의 예방 및 치료용 조성물 |
Families Citing this family (57)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| NZ571300A (en) | 2006-04-07 | 2011-12-22 | Warner Chilcott Co Llc | Antibodies that bind human protein tyrosine phosphatase beta (HPTPBeta) and uses thereof |
| US8846685B2 (en) | 2006-06-27 | 2014-09-30 | Aerpio Therapeutics Inc. | Human protein tyrosine phosphatase inhibitors and methods of use |
| US7589212B2 (en) | 2006-06-27 | 2009-09-15 | Procter & Gamble Company | Human protein tyrosine phosphatase inhibitors and methods of use |
| US7622593B2 (en) | 2006-06-27 | 2009-11-24 | The Procter & Gamble Company | Human protein tyrosine phosphatase inhibitors and methods of use |
| US7795444B2 (en) | 2006-06-27 | 2010-09-14 | Warner Chilcott Company | Human protein tyrosine phosphatase inhibitors and methods of use |
| US9096555B2 (en) | 2009-01-12 | 2015-08-04 | Aerpio Therapeutics, Inc. | Methods for treating vascular leak syndrome |
| US8883832B2 (en) | 2009-07-06 | 2014-11-11 | Aerpio Therapeutics Inc. | Compounds, compositions, and methods for preventing metastasis of cancer cells |
| DK2451279T3 (da) | 2009-07-06 | 2019-05-20 | Aerpio Therapeutics Inc | Benzosulfonamid derivater forbindelser deraf og deres brug til at forhindre metastaser af cancerceller |
| WO2011057112A1 (en) | 2009-11-06 | 2011-05-12 | Akebia Therapeutics Inc. | Methods for increasing the stabilization of hypoxia inducible factor-1 alpha |
| MY176514A (en) * | 2010-10-07 | 2020-08-12 | Aerpio Therapeutics Inc | Compositions and methods for treating ocular edema, neovascularization and related diseases |
| CN104039351A (zh) | 2011-10-13 | 2014-09-10 | 阿尔皮奥治疗学股份有限公司 | 用于治疗血管渗漏综合征和癌症的方法 |
| ES2774972T3 (es) | 2011-10-13 | 2020-07-23 | Aerpio Therapeutics Inc | Tratamiento de enfermedades oculares |
| HUE055562T2 (hu) | 2011-11-23 | 2021-11-29 | Therapeuticsmd Inc | Természetes kombinációjú hormon helyettesítõ kiszerelések, és terápiák ezekkel |
| US9301920B2 (en) | 2012-06-18 | 2016-04-05 | Therapeuticsmd, Inc. | Natural combination hormone replacement formulations and therapies |
| US10806740B2 (en) | 2012-06-18 | 2020-10-20 | Therapeuticsmd, Inc. | Natural combination hormone replacement formulations and therapies |
| US20130338122A1 (en) | 2012-06-18 | 2013-12-19 | Therapeuticsmd, Inc. | Transdermal hormone replacement therapies |
| US10806697B2 (en) | 2012-12-21 | 2020-10-20 | Therapeuticsmd, Inc. | Vaginal inserted estradiol pharmaceutical compositions and methods |
| US20150196640A1 (en) | 2012-06-18 | 2015-07-16 | Therapeuticsmd, Inc. | Progesterone formulations having a desirable pk profile |
| US10471072B2 (en) | 2012-12-21 | 2019-11-12 | Therapeuticsmd, Inc. | Vaginal inserted estradiol pharmaceutical compositions and methods |
| US10568891B2 (en) | 2012-12-21 | 2020-02-25 | Therapeuticsmd, Inc. | Vaginal inserted estradiol pharmaceutical compositions and methods |
| US9180091B2 (en) | 2012-12-21 | 2015-11-10 | Therapeuticsmd, Inc. | Soluble estradiol capsule for vaginal insertion |
| US11246875B2 (en) | 2012-12-21 | 2022-02-15 | Therapeuticsmd, Inc. | Vaginal inserted estradiol pharmaceutical compositions and methods |
| US11266661B2 (en) | 2012-12-21 | 2022-03-08 | Therapeuticsmd, Inc. | Vaginal inserted estradiol pharmaceutical compositions and methods |
| US10537581B2 (en) | 2012-12-21 | 2020-01-21 | Therapeuticsmd, Inc. | Vaginal inserted estradiol pharmaceutical compositions and methods |
| US20150050277A1 (en) | 2013-03-15 | 2015-02-19 | Aerpio Therapeutics Inc. | Compositions and methods for treating ocular diseases |
| US9440963B2 (en) * | 2013-03-15 | 2016-09-13 | Aerpio Therapeutics, Inc. | Compositions, formulations and methods for treating ocular diseases |
| WO2015013565A1 (en) * | 2013-07-25 | 2015-01-29 | Nemucore Medical Innovations, Inc. | Platinum derivatives for hydrophobic formulations |
| US9902767B2 (en) | 2013-07-29 | 2018-02-27 | Samsung Electronics Co., Ltd. | Method of blocking vascular leakage using an anti-ANG2 antibody |
| KR102196450B1 (ko) | 2013-09-17 | 2020-12-30 | 삼성전자주식회사 | Tie2와 결합을 유도하는 항 Ang2 항체를 포함하는 항암제 |
| EP3107542B1 (en) | 2014-02-19 | 2019-05-01 | Aerpio Therapeutics, Inc. | Process for preparing n-benzyl-3-hydroxy-4-substituted-pyridin-2-(1h)-ones |
| US9994560B2 (en) | 2014-03-14 | 2018-06-12 | Aerpio Therapeutics, Inc. | HPTP-β inhibitors |
| RU2016143081A (ru) | 2014-05-22 | 2018-06-26 | Терапьютиксмд, Инк. | Натуральные комбинированные гормонозаместительные составы и терапии |
| WO2016022813A1 (en) | 2014-08-07 | 2016-02-11 | Aerpio Therapeutics, Inc. | Combination of immunotherapies with activators of tie-2 |
| CN104551003B (zh) * | 2014-12-30 | 2016-08-24 | 燕山大学 | 一种以醋酸兰瑞肽为模板制备纳米铂螺旋杆的方法 |
| CN106138019A (zh) * | 2015-03-25 | 2016-11-23 | 中国科学院大连化学物理研究所 | Gpr35受体激动剂及其应用 |
| US10722527B2 (en) | 2015-04-10 | 2020-07-28 | Capsugel Belgium Nv | Abiraterone acetate lipid formulations |
| EP3101007A1 (en) * | 2015-06-05 | 2016-12-07 | Lead Pharma Cel Models IP B.V. | Ror gamma (rory) modulators |
| EP3101005A1 (en) * | 2015-06-05 | 2016-12-07 | Lead Pharma Cel Models IP B.V. | Ror gamma (rory) modulators |
| US10328087B2 (en) | 2015-07-23 | 2019-06-25 | Therapeuticsmd, Inc. | Formulations for solubilizing hormones |
| CN108290057A (zh) | 2015-09-23 | 2018-07-17 | 爱尔皮奥治疗有限公司 | 用tie-2的激活剂治疗眼内压的方法 |
| TW201711566A (zh) * | 2015-09-28 | 2017-04-01 | 拜耳作物科學公司 | 製備n-(1,3,4-㗁二唑-2-基)芳基甲醯胺之方法 |
| US10286077B2 (en) | 2016-04-01 | 2019-05-14 | Therapeuticsmd, Inc. | Steroid hormone compositions in medium chain oils |
| KR20180126582A (ko) | 2016-04-01 | 2018-11-27 | 쎄러퓨틱스엠디, 인코퍼레이티드 | 스테로이드 호르몬 약제학적 조성물 |
| CN105796830A (zh) * | 2016-04-19 | 2016-07-27 | 王刚 | 一种治疗鼻旁窦支气管综合征的中药 |
| US10253094B2 (en) | 2016-07-20 | 2019-04-09 | Aerpio Therapeutics, Inc. | Antibodies that target human protein tyrosine phosphatase-beta (HPTP-beta) and methods of use thereof to treat ocular conditions |
| KR102011366B1 (ko) * | 2016-11-17 | 2019-10-14 | 연세대학교 산학협력단 | 암 전이 억제제의 스크리닝 방법 |
| US11299467B2 (en) | 2017-07-21 | 2022-04-12 | Antabio Sas | Chemical compounds |
| US20190262321A1 (en) * | 2018-02-26 | 2019-08-29 | Aerpio Therapeutics, Inc. | Methods of treating diabetic nephropathy using hptpb inhibitors |
| KR102087044B1 (ko) * | 2018-04-30 | 2020-03-10 | 인하대학교 산학협력단 | Mmp-10 또는 이를 코딩하는 유전자의 발현을 억제하는 제제를 포함하는 암 전이 억제용 조성물 |
| US10894824B2 (en) | 2018-09-24 | 2021-01-19 | Aerpio Pharmaceuticals, Inc. | Multispecific antibodies that target HPTP-β (VE-PTP) and VEGF |
| CN109453195B (zh) * | 2018-11-29 | 2021-04-20 | 湖南补天药业股份有限公司 | 一种用于抑制肿瘤细胞的药物组合物 |
| WO2020223209A1 (en) | 2019-04-29 | 2020-11-05 | Aerpio Pharmaceuticals, Inc. | Tie-2 activators targeting the schlemm's canal |
| GB2589400A (en) | 2019-06-24 | 2021-06-02 | Aerpio Pharmaceuticals Inc | Formulations of tie-2 activators and methods of use thereof |
| CA3156225A1 (en) | 2019-10-29 | 2021-05-06 | EyePoint Pharmaceuticals, Inc. | Small molecule activators of tie-2 |
| CN111184726A (zh) * | 2020-02-25 | 2020-05-22 | 沈阳药科大学 | β-内酰胺类化合物的应用 |
| EP4164690A1 (en) * | 2020-06-16 | 2023-04-19 | Amy Ripka | Small molecule ve-ptp inhibitors |
| CN114456143B (zh) * | 2022-02-23 | 2023-08-15 | 北京丰帆生物医药科技有限公司 | 一种uPA的抑制剂及其制备方法和应用 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2008002570A2 (en) * | 2006-06-27 | 2008-01-03 | The Procter & Gamble Company | Human protein tyrosine phosphatase inhibitors and methods of use |
| WO2008002571A2 (en) * | 2006-06-27 | 2008-01-03 | The Procter & Gamble Company | Human protein tyrosine phosphatase inhibitors and methods of use |
| WO2008002569A2 (en) * | 2006-06-27 | 2008-01-03 | The Procter & Gamble Company | Human protein tyrosine phosphatase inhibitors and methods of use |
Family Cites Families (91)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4673641A (en) | 1982-12-16 | 1987-06-16 | Molecular Genetics Research And Development Limited Partnership | Co-aggregate purification of proteins |
| US5530101A (en) | 1988-12-28 | 1996-06-25 | Protein Design Labs, Inc. | Humanized immunoglobulins |
| ATE222291T1 (de) | 1992-03-13 | 2002-08-15 | Organon Teknika Bv | Epstein-barr-virus verwandte peptide und nukleinsäuresegmenten |
| US5770565A (en) | 1994-04-13 | 1998-06-23 | La Jolla Cancer Research Center | Peptides for reducing or inhibiting bone resorption |
| US5688781A (en) | 1994-08-19 | 1997-11-18 | Bristol-Myers Squibb Company | Method for treating vascular leak syndrome |
| DK0833934T4 (da) | 1995-06-15 | 2012-11-19 | Crucell Holland Bv | Pakningssystemer til human rekombinant adenovirus til anvendelse ved genterapi |
| US20030040463A1 (en) | 1996-04-05 | 2003-02-27 | Wiegand Stanley J. | TIE-2 ligands, methods of making and uses thereof |
| WO1998018914A1 (en) | 1996-10-31 | 1998-05-07 | Duke University | Soluble tie2 receptor |
| JPH11225351A (ja) | 1998-02-04 | 1999-08-17 | Matsushita Electric Ind Co Ltd | ページャー機能を備える無線通信装置のメッセージ消去方法および装置 |
| US5919813C1 (en) | 1998-03-13 | 2002-01-29 | Univ Johns Hopkins Med | Use of a protein tyrosine kinase pathway inhibitor in the treatment of diabetic retinopathy |
| US5980929A (en) | 1998-03-13 | 1999-11-09 | Johns Hopkins University, School Of Medicine | Use of a protein tyrosine kinase pathway inhibitor in the treatment of retinal ischmemia or ocular inflammation |
| AR022303A1 (es) | 1999-01-22 | 2002-09-04 | Lundbeck & Co As H | Derivados de piperidina, tetrahidropiridina y piperazina, su preparacion y utilizacion |
| RU2236251C2 (ru) * | 1999-02-12 | 2004-09-20 | Дзе Скриппс Рисерч Инститьют | Способы лечения опухолей и метастазов с использованием комбинации антиангиогенной терапии и иммунотерапии |
| US6455035B1 (en) | 1999-03-26 | 2002-09-24 | Regeneron Pharmaceuticals, Inc. | Angiopoietins and methods of use thereof |
| DE60003011T2 (de) | 1999-03-26 | 2004-04-08 | Regeneron Pharmaceuticals, Inc. | Modulierung der gefässepermeabilität mittels tie2 rezeptoraktivatoren |
| EP1046715A1 (en) | 1999-04-23 | 2000-10-25 | Max-Planck-Gesellschaft zur Förderung der Wissenschaften e.V. | Interaction of vascular-endothelial protein-tyrosine phosphatase with the angiopoietin receptor tie-2 |
| AU5062500A (en) | 1999-04-26 | 2000-11-10 | Amersham Pharmacia Biotech Ab | Primers for identifying typing or classifying nucleic acids |
| US6342221B1 (en) | 1999-04-28 | 2002-01-29 | Board Of Regents, The University Of Texas System | Antibody conjugate compositions for selectively inhibiting VEGF |
| AU5147700A (en) | 1999-05-19 | 2000-12-05 | Amgen, Inc. | Crystal of a lymphocyte kinase-ligand complex and methods of use |
| ATE309207T1 (de) | 1999-08-27 | 2005-11-15 | Sugen Inc | Phosphat-mimetika sowie behandlungsmethoden unter verwendung von phosphatase-inhibitoren |
| US6589758B1 (en) | 2000-05-19 | 2003-07-08 | Amgen Inc. | Crystal of a kinase-ligand complex and methods of use |
| IL152794A0 (en) | 2000-06-23 | 2003-06-24 | Schering Ag | Combinations and compositions which interfere with vegf/vegf and angiopoietin/tie receptor function and their use |
| CZ2003788A3 (cs) | 2000-09-27 | 2003-08-13 | The Procter & Gamble Company | Ligandy melanokortinového receptoru |
| US7052695B2 (en) | 2001-10-25 | 2006-05-30 | Regeneron Pharmaceuticals, Inc. | Angiopoietins and methods of treating hypertension |
| AU2003229627A1 (en) | 2002-04-08 | 2003-10-20 | Max-Planck-Gesellschaft Zur | Ve-ptp as regulator of ve-cadherin mediated processes or disorders |
| RU2376029C2 (ru) | 2002-04-25 | 2009-12-20 | Юниверсити Оф Коннектикут Хелт Сентер | Применение белков теплового шока для улучшения терапевтического эффекта невакцинного лечебного воздействия |
| US7507568B2 (en) | 2002-09-25 | 2009-03-24 | The Proctor & Gamble Company | Three dimensional coordinates of HPTPbeta |
| US7226755B1 (en) | 2002-09-25 | 2007-06-05 | The Procter & Gamble Company | HPTPbeta as a target in treatment of angiogenesis mediated disorders |
| US6930117B2 (en) | 2002-11-09 | 2005-08-16 | The Procter & Gamble Company | N-alkyl-4-methyleneamino-3-hydroxy-2-pyridones |
| US6946479B2 (en) | 2002-11-09 | 2005-09-20 | The Procter & Gamble Company | N-sulfonyl-4-methyleneamino-3-hydroxy-2-pyridones |
| US20050154011A1 (en) | 2003-02-20 | 2005-07-14 | The Procter & Gamble Company | Tetrahydroisoquinolnyl sulfamic acids |
| AR046510A1 (es) | 2003-07-25 | 2005-12-14 | Regeneron Pharma | Composicion de un antagonista de vegf y un agente anti-proliferativo |
| US20050158320A1 (en) * | 2003-11-12 | 2005-07-21 | Nichols M. J. | Combinations for the treatment of proliferative diseases |
| US8298532B2 (en) | 2004-01-16 | 2012-10-30 | Regeneron Pharmaceuticals, Inc. | Fusion polypeptides capable of activating receptors |
| ME02221B (me) | 2004-03-15 | 2016-02-20 | Janssen Pharmaceutica Nv | Postupak za proizvodnju intermedijara jedinjenja korisnih kao modulatori opioidnih receptora |
| US7771742B2 (en) | 2004-04-30 | 2010-08-10 | Allergan, Inc. | Sustained release intraocular implants containing tyrosine kinase inhibitors and related methods |
| SI1771474T1 (sl) | 2004-07-20 | 2010-06-30 | Genentech Inc | Inhibitorji angiopoetinu podobnega proteina kombinacije in njihova uporaba |
| US7691365B2 (en) | 2004-09-28 | 2010-04-06 | Aprogen, Inc. | Methods of using chimeric coiled coil molecule to treat ischemic disease |
| CN105085678B (zh) | 2004-12-21 | 2019-05-07 | 阿斯利康公司 | 血管生成素-2的抗体及其应用 |
| WO2006116458A2 (en) * | 2005-04-26 | 2006-11-02 | Coley Pharmaceutical Gmbh | Modified oligoribonucleotide analogs with enhances immunostimulatory activity |
| JO2787B1 (en) | 2005-04-27 | 2014-03-15 | امجين إنك, | Alternative amide derivatives and methods of use |
| US7893040B2 (en) | 2005-07-22 | 2011-02-22 | Oculis Ehf | Cyclodextrin nanotechnology for ophthalmic drug delivery |
| US20070154482A1 (en) | 2005-09-12 | 2007-07-05 | Beth Israel Deaconess Medical Center | Methods and compositions for the treatment and diagnosis of diseases characterized by vascular leak, hypotension, or a procoagulant state |
| CA2633211A1 (en) | 2005-12-15 | 2007-06-21 | Astrazeneca Ab | Combination of angiopoietin-2 antagonist and of vegf-a, kdr and/or flt1 antagonist for treating cancer |
| US7588924B2 (en) | 2006-03-07 | 2009-09-15 | Procter & Gamble Company | Crystal of hypoxia inducible factor 1 alpha prolyl hydroxylase |
| NZ571300A (en) | 2006-04-07 | 2011-12-22 | Warner Chilcott Co Llc | Antibodies that bind human protein tyrosine phosphatase beta (HPTPBeta) and uses thereof |
| US20130023542A1 (en) | 2006-06-27 | 2013-01-24 | Aerpio Therapeutics Inc. | Human protein tyrosine phosphatase inhibitors and methods of use |
| US8846685B2 (en) | 2006-06-27 | 2014-09-30 | Aerpio Therapeutics Inc. | Human protein tyrosine phosphatase inhibitors and methods of use |
| DK2076290T3 (en) | 2006-10-27 | 2017-01-23 | Sunnybrook Health Sciences Center | MULTIMERIC TIE 2 AGONISTS AND APPLICATIONS THEREOF IN STIMULATING ANGIOGENESIS |
| US8642067B2 (en) | 2007-04-02 | 2014-02-04 | Allergen, Inc. | Methods and compositions for intraocular administration to treat ocular conditions |
| US11078262B2 (en) | 2007-04-30 | 2021-08-03 | Allergan, Inc. | High viscosity macromolecular compositions for treating ocular conditions |
| WO2009105774A2 (en) | 2008-02-21 | 2009-08-27 | Sequoia Pharmaceuticals, Inc. | Amino acid inhibitors of cytochrome p450 |
| US9096555B2 (en) | 2009-01-12 | 2015-08-04 | Aerpio Therapeutics, Inc. | Methods for treating vascular leak syndrome |
| SG172312A1 (en) * | 2009-01-12 | 2011-07-28 | Akebia Therapeutics Inc | Methods for treating vascular leak syndrome |
| ES2508290T3 (es) | 2009-03-03 | 2014-10-16 | Alcon Research, Ltd. | Composición farmacéutica para la administracón de compuestos de inhibición del receptor de tirosina cinasa (RTKI) al ojo |
| WO2010101971A1 (en) | 2009-03-03 | 2010-09-10 | Alcon Research, Ltd. | Pharmaceutical composition for delivery of receptor tyrosine kinase inhibiting (rtki) compounds to the eye |
| US8883832B2 (en) | 2009-07-06 | 2014-11-11 | Aerpio Therapeutics Inc. | Compounds, compositions, and methods for preventing metastasis of cancer cells |
| DK2451279T3 (da) | 2009-07-06 | 2019-05-20 | Aerpio Therapeutics Inc | Benzosulfonamid derivater forbindelser deraf og deres brug til at forhindre metastaser af cancerceller |
| WO2011057112A1 (en) | 2009-11-06 | 2011-05-12 | Akebia Therapeutics Inc. | Methods for increasing the stabilization of hypoxia inducible factor-1 alpha |
| ES2877629T3 (es) | 2010-07-12 | 2021-11-17 | Immunogenesis Inc | Administración de profármacos activados por hipoxia y agentes antiangiogénicos para el tratamiento del cáncer |
| MY176514A (en) | 2010-10-07 | 2020-08-12 | Aerpio Therapeutics Inc | Compositions and methods for treating ocular edema, neovascularization and related diseases |
| KR20140009278A (ko) | 2010-12-02 | 2014-01-22 | 마루젠세이야쿠 가부시키가이샤 | Tie2 활성화제, 혈관내피증식인자(VEGF) 억제제, 혈관신생 억제제, 혈관 성숙화제, 혈관 정상화제, 혈관 안정화제 및 약제학적 조성물 |
| CN104039351A (zh) | 2011-10-13 | 2014-09-10 | 阿尔皮奥治疗学股份有限公司 | 用于治疗血管渗漏综合征和癌症的方法 |
| ES2774972T3 (es) | 2011-10-13 | 2020-07-23 | Aerpio Therapeutics Inc | Tratamiento de enfermedades oculares |
| US20130190324A1 (en) | 2011-12-23 | 2013-07-25 | The Regents Of The University Of Colorado, A Body Corporate | Topical ocular drug delivery |
| WO2013155512A2 (en) | 2012-04-13 | 2013-10-17 | The Johns Hopkins University | Treatment of ischemic retinopathies |
| DK2880167T3 (en) | 2012-07-31 | 2018-07-30 | Univ Texas | METHODS AND COMPOSITIONS FOR IN VIVO-INDUCTION OF PANCREAS BETA CELL CREATION |
| RU2673881C2 (ru) | 2012-10-11 | 2018-12-03 | Асцендис Фарма Офтальмолоджи Дивижн А/С | Vegf-нейтрализующие пролекарства для лечения офтальмологических заболеваний |
| SG11201503637SA (en) | 2012-11-08 | 2015-06-29 | Clearside Biomedical Inc | Methods and devices for the treatment of ocular diseases in human subjects |
| EP2922572A1 (en) | 2012-11-23 | 2015-09-30 | AB Science | Use of small molecule inhibitors/activators in combination with (deoxy)nucleoside or (deoxy)nucleotide analogs for treatment of cancer and hematological malignancies or viral infections |
| US20150050277A1 (en) | 2013-03-15 | 2015-02-19 | Aerpio Therapeutics Inc. | Compositions and methods for treating ocular diseases |
| US9440963B2 (en) | 2013-03-15 | 2016-09-13 | Aerpio Therapeutics, Inc. | Compositions, formulations and methods for treating ocular diseases |
| WO2014165963A1 (en) | 2013-04-11 | 2014-10-16 | Sunnybrook Research Institute | Methods, uses and compositions of tie2 agonists |
| US20160130321A1 (en) | 2013-06-20 | 2016-05-12 | Gabriela Burian | Use of a vegf antagonist in treating macular edema |
| JP2016522249A (ja) | 2013-06-20 | 2016-07-28 | ノバルティス アーゲー | 脈絡膜血管新生の治療におけるvegfアンタゴニストの使用 |
| US20160151410A1 (en) | 2013-07-02 | 2016-06-02 | The Trustees Of Columbia University In The City Of New York | Clearance of bioactive lipids from membrane structures by cyclodextrins |
| US20160159893A1 (en) | 2013-07-11 | 2016-06-09 | Gabriela Burian | Use of a VEGF Antagonist in Treating Retinopathy of Prematurity |
| CN105377891A (zh) | 2013-07-11 | 2016-03-02 | 诺华股份有限公司 | Vegf拮抗剂在治疗儿童患者的脉络膜视网膜新生血管和通透性疾病中的应用 |
| US9902767B2 (en) | 2013-07-29 | 2018-02-27 | Samsung Electronics Co., Ltd. | Method of blocking vascular leakage using an anti-ANG2 antibody |
| US10617755B2 (en) | 2013-08-30 | 2020-04-14 | Genentech, Inc. | Combination therapy for the treatment of glioblastoma |
| TR201905773T4 (tr) | 2013-10-01 | 2019-05-21 | Sphingotec Gmbh | Bir majör advers kardiyak olayla karşılaşma riskinin tahmin edilmesi için bir usul. |
| LT3062811T (lt) | 2013-11-01 | 2019-05-10 | Regeneron Pharmaceuticals, Inc. | Intervencijos angiopoietino pagrindu cerebrinės maliarijos gydymui |
| EP3107542B1 (en) | 2014-02-19 | 2019-05-01 | Aerpio Therapeutics, Inc. | Process for preparing n-benzyl-3-hydroxy-4-substituted-pyridin-2-(1h)-ones |
| US9994560B2 (en) | 2014-03-14 | 2018-06-12 | Aerpio Therapeutics, Inc. | HPTP-β inhibitors |
| JP2015199733A (ja) | 2014-04-04 | 2015-11-12 | 国立大学法人東北大学 | 眼圧降下剤 |
| US9719135B2 (en) | 2014-07-03 | 2017-08-01 | Mannin Research Inc. | Conditional angiopoietin-1/angiopoietin-2 double knock-out mice with defective ocular drainage system |
| WO2016022813A1 (en) | 2014-08-07 | 2016-02-11 | Aerpio Therapeutics, Inc. | Combination of immunotherapies with activators of tie-2 |
| US20160082129A1 (en) | 2014-09-24 | 2016-03-24 | Aerpio Therapeutics, Inc. | VE-PTP Extracellular Domain Antibodies Delivered by a Gene Therapy Vector |
| TWI806150B (zh) | 2014-11-07 | 2023-06-21 | 瑞士商諾華公司 | 穩定的含有高濃度抗vegf抗體之蛋白質溶液調配物 |
| US20160144025A1 (en) | 2014-11-25 | 2016-05-26 | Regeneron Pharmaceuticals, Inc. | Methods and formulations for treating vascular eye diseases |
| CN108290057A (zh) | 2015-09-23 | 2018-07-17 | 爱尔皮奥治疗有限公司 | 用tie-2的激活剂治疗眼内压的方法 |
-
2010
- 2010-01-12 DK DK10797461.0T patent/DK2451279T3/da active
- 2010-01-12 CN CN201410144271.4A patent/CN103976998A/zh active Pending
- 2010-01-12 JP JP2011554058A patent/JP5536113B2/ja active Active
- 2010-01-12 AU AU2010271105A patent/AU2010271105C1/en not_active Ceased
- 2010-01-12 WO PCT/US2010/020822 patent/WO2011005330A1/en active Application Filing
- 2010-01-12 CN CN201510713404.XA patent/CN105412094A/zh active Pending
- 2010-01-12 PT PT10797461T patent/PT2451279T/pt unknown
- 2010-01-12 SG SG10201505672TA patent/SG10201505672TA/en unknown
- 2010-01-12 BR BRPI1006897A patent/BRPI1006897A2/pt not_active Application Discontinuation
- 2010-01-12 PL PL10797461T patent/PL2451279T3/pl unknown
- 2010-01-12 NZ NZ594537A patent/NZ594537A/en not_active IP Right Cessation
- 2010-01-12 TR TR2019/07783T patent/TR201907783T4/tr unknown
- 2010-01-12 EP EP19159755.8A patent/EP3556367A1/en not_active Withdrawn
- 2010-01-12 US US12/677,550 patent/US8569348B2/en active Active
- 2010-01-12 SG SG2011045648A patent/SG172313A1/en unknown
- 2010-01-12 MY MYPI2011003556A patent/MY160399A/en unknown
- 2010-01-12 EP EP10797461.0A patent/EP2451279B1/en active Active
- 2010-01-12 RU RU2011133835/15A patent/RU2519123C2/ru not_active IP Right Cessation
- 2010-01-12 ES ES10797461T patent/ES2726946T3/es active Active
- 2010-01-12 CN CN2010800121928A patent/CN102365024A/zh active Pending
- 2010-01-12 CA CA2748765A patent/CA2748765C/en not_active Expired - Fee Related
- 2010-01-12 KR KR1020117018742A patent/KR101426125B1/ko active IP Right Grant
- 2010-01-12 MX MX2011007420A patent/MX2011007420A/es active IP Right Grant
-
2011
- 2011-07-12 IL IL214048A patent/IL214048A/en not_active IP Right Cessation
- 2011-08-02 ZA ZA2011/05678A patent/ZA201105678B/en unknown
-
2014
- 2014-03-11 JP JP2014048238A patent/JP2014139208A/ja active Pending
- 2014-05-08 US US14/272,689 patent/US9174950B2/en active Active
-
2015
- 2015-09-16 JP JP2015183047A patent/JP2016006118A/ja active Pending
- 2015-09-24 US US14/864,462 patent/US9949956B2/en active Active
-
2016
- 2016-10-26 IL IL248514A patent/IL248514A0/en unknown
-
2017
- 2017-04-14 JP JP2017080657A patent/JP6505153B2/ja active Active
-
2018
- 2018-03-06 US US15/913,392 patent/US20190076405A1/en not_active Abandoned
-
2019
- 2019-03-26 JP JP2019058234A patent/JP2019089866A/ja not_active Withdrawn
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2008002570A2 (en) * | 2006-06-27 | 2008-01-03 | The Procter & Gamble Company | Human protein tyrosine phosphatase inhibitors and methods of use |
| WO2008002571A2 (en) * | 2006-06-27 | 2008-01-03 | The Procter & Gamble Company | Human protein tyrosine phosphatase inhibitors and methods of use |
| WO2008002569A2 (en) * | 2006-06-27 | 2008-01-03 | The Procter & Gamble Company | Human protein tyrosine phosphatase inhibitors and methods of use |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20210035426A (ko) | 2019-09-24 | 2021-04-01 | 충북대학교 산학협력단 | N-아릴-2-[(6-부틸-1,3-디메틸-2,4-디옥소-1,2,3,4-테트라하이드로피리도[2,3-d]피리미딘-5-일)설페닐]아세트아마이드를 유효성분으로 함유하는 종양의 예방 및 치료용 조성물 |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101426125B1 (ko) | 암 세포의 전이 예방을 위한 화합물, 조성물 및 방법 | |
| US8883832B2 (en) | Compounds, compositions, and methods for preventing metastasis of cancer cells | |
| EP2429292B1 (en) | Compounds and compositions comprising cdk inhibitors and their use in the treatment of cancer | |
| DK2592072T3 (en) | Human protein tyrosine phosphatase inhibitors and their use | |
| KR101495950B1 (ko) | 혈관 누수 증후군 치료 방법 | |
| US20080004267A1 (en) | Human protein tyrosine phosphatase inhibitors and methods of use | |
| US7179827B2 (en) | Thiazoles and methods of their use |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| N231 | Notification of change of applicant | ||
| E902 | Notification of reason for refusal | ||
| E902 | Notification of reason for refusal | ||
| E701 | Decision to grant or registration of patent right | ||
| GRNT | Written decision to grant | ||
| FPAY | Annual fee payment |
Payment date: 20170713 Year of fee payment: 4 |
|
| FPAY | Annual fee payment |
Payment date: 20180713 Year of fee payment: 5 |