JP7621625B2 - 全分子量分布のヒアルロン酸ナトリウム及びその調製方法と応用 - Google Patents
全分子量分布のヒアルロン酸ナトリウム及びその調製方法と応用 Download PDFInfo
- Publication number
- JP7621625B2 JP7621625B2 JP2023568598A JP2023568598A JP7621625B2 JP 7621625 B2 JP7621625 B2 JP 7621625B2 JP 2023568598 A JP2023568598 A JP 2023568598A JP 2023568598 A JP2023568598 A JP 2023568598A JP 7621625 B2 JP7621625 B2 JP 7621625B2
- Authority
- JP
- Japan
- Prior art keywords
- sodium hyaluronate
- molecular weight
- solution
- preparing
- minutes
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08B—POLYSACCHARIDES; DERIVATIVES THEREOF
- C08B37/00—Preparation of polysaccharides not provided for in groups C08B1/00 - C08B35/00; Derivatives thereof
- C08B37/006—Heteroglycans, i.e. polysaccharides having more than one sugar residue in the main chain in either alternating or less regular sequence; Gellans; Succinoglycans; Arabinogalactans; Tragacanth or gum tragacanth or traganth from Astragalus; Gum Karaya from Sterculia urens; Gum Ghatti from Anogeissus latifolia; Derivatives thereof
- C08B37/0063—Glycosaminoglycans or mucopolysaccharides, e.g. keratan sulfate; Derivatives thereof, e.g. fucoidan
- C08B37/0072—Hyaluronic acid, i.e. HA or hyaluronan; Derivatives thereof, e.g. crosslinked hyaluronic acid (hylan) or hyaluronates
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES, NOT OTHERWISE PROVIDED FOR; PREPARATION OR TREATMENT THEREOF
- A23L29/00—Foods or foodstuffs containing additives; Preparation or treatment thereof
- A23L29/03—Organic compounds
- A23L29/035—Organic compounds containing oxygen as heteroatom
- A23L29/04—Fatty acids or derivatives
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES, NOT OTHERWISE PROVIDED FOR; PREPARATION OR TREATMENT THEREOF
- A23L29/00—Foods or foodstuffs containing additives; Preparation or treatment thereof
- A23L29/03—Organic compounds
- A23L29/045—Organic compounds containing nitrogen as heteroatom
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES, NOT OTHERWISE PROVIDED FOR; PREPARATION OR TREATMENT THEREOF
- A23L33/00—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof
- A23L33/10—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof using additives
- A23L33/125—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof using additives containing carbohydrate syrups; containing sugars; containing sugar alcohols; containing starch hydrolysates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/715—Polysaccharides, i.e. having more than five saccharide radicals attached to each other by glycosidic linkages; Derivatives thereof, e.g. ethers, esters
- A61K31/726—Glycosaminoglycans, i.e. mucopolysaccharides
- A61K31/728—Hyaluronic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/72—Cosmetics or similar toiletry preparations characterised by the composition containing organic macromolecular compounds
- A61K8/73—Polysaccharides
- A61K8/735—Mucopolysaccharides, e.g. hyaluronic acid; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q19/00—Preparations for care of the skin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q19/00—Preparations for care of the skin
- A61Q19/08—Anti-ageing preparations
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D15/00—Separating processes involving the treatment of liquids with solid sorbents; Apparatus therefor
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D61/00—Processes of separation using semi-permeable membranes, e.g. dialysis, osmosis or ultrafiltration; Apparatus, accessories or auxiliary operations specially adapted therefor
- B01D61/02—Reverse osmosis; Hyperfiltration ; Nanofiltration
- B01D61/027—Nanofiltration
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D61/00—Processes of separation using semi-permeable membranes, e.g. dialysis, osmosis or ultrafiltration; Apparatus, accessories or auxiliary operations specially adapted therefor
- B01D61/02—Reverse osmosis; Hyperfiltration ; Nanofiltration
- B01D61/04—Feed pretreatment
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D69/00—Semi-permeable membranes for separation processes or apparatus characterised by their form, structure or properties; Manufacturing processes specially adapted therefor
- B01D69/02—Semi-permeable membranes for separation processes or apparatus characterised by their form, structure or properties; Manufacturing processes specially adapted therefor characterised by their properties
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L5/00—Compositions of polysaccharides or of their derivatives not provided for in groups C08L1/00 or C08L3/00
- C08L5/08—Chitin; Chondroitin sulfate; Hyaluronic acid; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23V—INDEXING SCHEME RELATING TO FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES AND LACTIC OR PROPIONIC ACID BACTERIA USED IN FOODSTUFFS OR FOOD PREPARATION
- A23V2002/00—Food compositions, function of food ingredients or processes for food or foodstuffs
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D2311/00—Details relating to membrane separation process operations and control
- B01D2311/04—Specific process operations in the feed stream; Feed pretreatment
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D2311/00—Details relating to membrane separation process operations and control
- B01D2311/26—Further operations combined with membrane separation processes
- B01D2311/2626—Absorption or adsorption
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D2311/00—Details relating to membrane separation process operations and control
- B01D2311/26—Further operations combined with membrane separation processes
- B01D2311/2699—Drying
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D2325/00—Details relating to properties of membranes
- B01D2325/34—Molecular weight or degree of polymerisation
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Animal Behavior & Ethology (AREA)
- Medicinal Chemistry (AREA)
- Organic Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Dermatology (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Molecular Biology (AREA)
- Polymers & Plastics (AREA)
- Water Supply & Treatment (AREA)
- Epidemiology (AREA)
- Nanotechnology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Pain & Pain Management (AREA)
- Birds (AREA)
- Biochemistry (AREA)
- Materials Engineering (AREA)
- Rheumatology (AREA)
- Nutrition Science (AREA)
- Food Science & Technology (AREA)
- Analytical Chemistry (AREA)
- Mycology (AREA)
- Gerontology & Geriatric Medicine (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Polysaccharides And Polysaccharide Derivatives (AREA)
- Cosmetics (AREA)
- Coloring Foods And Improving Nutritive Qualities (AREA)
- Medicinal Preparation (AREA)
Description
ステップ1)であって、ヒアルロン酸ナトリウム固体原料に対して過酸化水素水噴霧及び紫外線照射処理を行い、ヒアルロン酸ナトリウム分解材料を得る。
ステップ2)であって、上記ヒアルロン酸ナトリウム分解材料を水に溶解し、NaOH溶液でpHをアルカリ性に調整することで、ヒアルロン酸ナトリウムのアルカリ性溶液を得る。
ステップ3)であって、上記ヒアルロン酸ナトリウムのアルカリ溶液に対して超音波処理を行う。
ステップ4)であって、上記ヒアルロン酸ナトリウム固体原料を、0.1%~1%(w/v)の濃度を有するヒアルロン酸ナトリウム溶液に調製し、20%~60%(v/v)の添加割合で、ステップ3)で得られた超音波処理後のヒアルロン酸ナトリウムのアルカリ性溶液と均一に混合する。
ステップ5)であって、それぞれ珪藻土と活性炭を用いて吸着処理を行い、且つナノ濾過膜を用いて濾過濃縮し、乾燥した後に上記全分子量分布のヒアルロン酸ナトリウムを得る。
好ましくは、上記ヒアルロン酸ナトリウムにおけるエンドトキシン含有量は<0.01EUであり、タンパク質含有量は<0.01%である。
好ましくは、上記ヒアルロン酸ナトリウムは、280nmでOD値<0.01であり、260nmでOD値<0.01である。
1、本発明の提供する調製方法は迅速に、効率的に全分子量分布のヒアルロン酸ナトリウムを調製して得ることができ、調製されたヒアルロン酸ナトリウムは均一性に優れ、安定性が高く、各分子量のヒアルロン酸ナトリウムの効能優位性を十分に利用することができ、分子量分散係数Mw/Mnは5以上である。
2、本発明の提供する全分子量ヒアルロン酸ナトリウムの調製方法は、同時に紫外線照射分解、超音波-アルカリ分解処理、珪藻土濾過、活性炭吸着及びナノ膜濾過を融合し、得られたヒアルロン酸ナトリウムのエンドトキシン含有量<0.01EU、タンパク質含有量<0.01%、280nmでOD値<0.01、260nmでOD値<0.01であり、より高い生体適合性を有し、より高い品質レベルに達することができ、ヒアルロン酸ナトリウムが皮膚保湿、細胞保護、経口などの方面における応用効果を向上させることに有利である。
3、本発明の提供する全分子量ヒアルロン酸ナトリウムの調製方法は、紫外線照射分解、超音波分解を高粘度ヒアルロン酸溶液の濾過前に置き、高粘度溶液の濾過の難易度を大幅に低下させ、調製効率及び収率を向上させ、不純物の除去効率を向上させる。
4、本発明の提供する全分子量ヒアルロン酸ナトリウムの調製方法は、得られた高品質全分子量分布ヒアルロン酸ナトリウムは、優れたスマート補水保湿、抗炎症及び細胞保護等の活性を備える。
該実施例は全分子量分布ヒアルロン酸ナトリウムの調製方法を提供し、具体的には以下のステップを含む:
ステップ1)であって、分子量が100万の食品グレードのヒアルロン酸ナトリウム原料1kgを取り、ヒアルロン酸ナトリウム原料の表面に1%の過酸化水素水50mLを均一に噴霧し、300μW/cm2の線量で紫外線照射を60分間行う。
ステップ2)であって、紫外線照射後のヒアルロン酸ナトリウム材料を水に溶解し、濃度が1%(w/v)であり、室温で撹拌し、完全に溶解させる。
ステップ3)であって、2%のNaOH溶液を用いてpHを10に調整し、10kHzの超音波下で15分間超音波処理する。
ステップ4)であって、濃度1%(w/v)の100万ヒアルロン酸ナトリウム溶液を調製し、添加割合60%(v/v)で上記処理後のヒアルロン酸ナトリウムのアルカリ性溶液と混合する。
ステップ5)であって、0.1%の珪藻土を用い、45℃で攪拌し、30分間吸着処理し、濾過する。
ステップ6)であって、2%の希塩酸溶液でpHを5.0に調整した後、0.1%の活性炭を用いて45℃で攪拌し、30分間吸着処理し、濾過する。
ステップ7)であって、ナノ濾過膜システムを用いて濾過液を濃縮し、そのうちナノ濾過膜の分画分子量が300Daであり、操作圧力が15barであり、温度を40℃に制御し、ナノ濾過濃縮液を得て、それを噴霧乾燥し、高品質の全分子量分布ヒアルロン酸ナトリウムのサンプルを得る。
該実施例は全分子量分布ヒアルロン酸ナトリウムの調製方法を提供し、具体的には以下のステップを含む:
ステップ1)であって、分子量が120万の食品グレードのヒアルロン酸ナトリウム原料1kgを取り、ヒアルロン酸ナトリウム原料の表面に3%の過酸化水素水80mLを均一に噴霧し、600μW/cm2の線量で紫外線照射を60分間行う。
ステップ2)であって、紫外線照射後のヒアルロン酸ナトリウム材料を水に溶解し、濃度が3%(w/v)であり、室温で撹拌し、完全に溶解させる。
ステップ3)であって、5%のNaOH溶液を用いてpHを12に調整し、30kHzの超音波下で30分間超音波処理する。
ステップ4)であって、濃度0.8%(w/v)の120万ヒアルロン酸ナトリウム溶液を調製し、添加割合40%(v/v)で上記処理後のヒアルロン酸ナトリウムのアルカリ性溶液と混合する。
ステップ5)であって、0.2%の珪藻土を用い、50℃で攪拌し、40分間吸着処理し、濾過する。
ステップ6)であって、2%の希硫酸溶液でpHを5.0に調整した後、0.3%の活性炭を用いて50℃で攪拌し、50分間吸着処理し、濾過する。
ステップ7)であって、ナノ濾過膜システムを用いて濾過液を濃縮し、そのうちナノ濾過膜の分画分子量が250Daであり、操作圧力が20barであり、温度を50℃に制御し、ナノ濾過濃縮液を得て、それを噴霧乾燥し、高品質の全分子量分布ヒアルロン酸ナトリウムのサンプルを得る。
該実施例は全分子量分布ヒアルロン酸ナトリウムの調製方法を提供し、具体的には以下のステップを含む:
ステップ1)であって、分子量が120万の化粧品グレードのヒアルロン酸ナトリウム原料1kgを取り、ヒアルロン酸ナトリウム原料の表面に5%の過酸化水素水80mLを均一に噴霧し、900μW/cm2の線量で紫外線照射を60分間行う。
ステップ2)であって、紫外線照射後のヒアルロン酸ナトリウム材料を水に溶解し、濃度が5%(w/v)であり、室温で撹拌し、完全に溶解させる。
ステップ3)であって、5%(w/v)のNaOH溶液を用いてpHを12に調整し、60kHzの超音波下で60分間超音波処理する。
ステップ4)であって、濃度0.6%(w/v)の120万の高分子量ヒアルロン酸ナトリウム溶液を調製し、添加割合40%(v/v)で上記処理後のヒアルロン酸ナトリウムのアルカリ性溶液と混合する。
ステップ5)であって、0.4%の珪藻土を用い、55℃で攪拌し、40分間吸着処理し、濾過する。
ステップ6)であって、2%の希硫酸溶液でpHを5.0に調整した後、0.3%の活性炭を用いて55℃で攪拌し、50分間吸着処理し、濾過する。
ステップ7)であって、ナノ濾過膜システムを用いて濾過液を濃縮し、そのうちナノ濾過膜の分画分子量が200Daであり、操作圧力が30barであり、温度を50℃に制御し、ナノ濾過濃縮液を得て、それを噴霧乾燥し、高品質の全分子量分布ヒアルロン酸ナトリウムのサンプルを得る。
該実施例は全分子量分布ヒアルロン酸ナトリウムの調製方法を提供し、具体的には以下のステップを含む:
ステップ1)であって、分子量が140万の化粧品グレードのヒアルロン酸ナトリウム原料1kgを取り、ヒアルロン酸ナトリウム原料の表面に5%の過酸化水素水100mLを均一に噴霧し、1200μW/cm2の線量で紫外線照射を60分間行う。
ステップ2)であって、紫外線照射後のヒアルロン酸ナトリウム材料を水に溶解し、濃度が5%(w/v)であり、室温で撹拌し、完全に溶解させる。
ステップ3)であって、6%(w/v)のNaOH溶液を用いてpHを12に調整し、90kHzの超音波下で60分間超音波処理する。
ステップ4)であって、濃度0.3%(w/v)の140万の高分子量ヒアルロン酸ナトリウム溶液を調製し、添加割合30%(v/v)で上記処理後のヒアルロン酸ナトリウムのアルカリ性溶液と混合する。
ステップ5)であって、0.6%の珪藻土を用い、55℃で攪拌し、60分間吸着処理し、濾過する。
ステップ6)であって、2%の希硫酸溶液でpHを5.0に調整した後、0.4%の活性炭を用いて55℃で攪拌し、60分間吸着処理し、濾過する。
ステップ7):であって、ナノ濾過膜システムを用いて濾過液を濃縮し、そのうちナノ濾過膜の分画分子量が200Daであり、操作圧力が30barであり、温度を50℃に制御し、ナノ濾過濃縮液を得て、それを噴霧乾燥し、高品質の全分子量分布ヒアルロン酸ナトリウムのサンプルを得る。
該実施例は全分子量分布ヒアルロン酸ナトリウムの調製方法を提供し、具体的には以下のステップを含む:
ステップ1)であって、分子量が150万の化粧品グレードのヒアルロン酸ナトリウム原料1kgを取り、ヒアルロン酸ナトリウム原料の表面に5%の過酸化水素水100mLを均一に噴霧し、1500μW/cm2の線量で紫外線照射を60分間行う。
ステップ2)であって、紫外線照射後のヒアルロン酸ナトリウム材料を水に溶解し、濃度が3%(w/v)であり、室温で撹拌し、完全に溶解させる。
ステップ3)であって、5%のNaOH溶液を用いてpHを12に調整し、90kHzの超音波下で60分間超音波処理する。
ステップ4)であって、濃度0.3%(w/v)の150万の高分子量ヒアルロン酸ナトリウム溶液を調製し、添加割合20%(v/v)で上記処理後のヒアルロン酸アルカリ性溶液と混合する。
ステップ5)であって、0.8%の珪藻土を用い、55℃で攪拌し、30分間吸着処理し、濾過する。
ステップ6)であって、2%の希硫酸溶液でpHを5.0に調整した後、0.6%の活性炭を用いて55℃で攪拌し、30分間吸着処理し、濾過する。
ステップ7):であって、ナノ濾過膜システムを用いて濾過液を濃縮し、そのうちナノ濾過膜の分画分子量が300Daであり、操作圧力が30barであり、温度を50℃に制御し、ナノ濾過濃縮液を得て、それを噴霧乾燥し、高品質の全分子量分布ヒアルロン酸ナトリウムのサンプルを得る。
該実施例は全分子量分布ヒアルロン酸ナトリウムの調製方法を提供し、具体的には以下のステップを含む:
ステップ1)であって、分子量が200万の化粧品グレードのヒアルロン酸ナトリウム原料1kgを取り、ヒアルロン酸ナトリウム原料の表面に5%の過酸化水素水100mLを均一に噴霧し、1500μW/cm2の線量で紫外線照射を60分間行う。
ステップ2)であって、紫外線照射後のヒアルロン酸ナトリウム材料を水に溶解し、濃度が1%(w/v)であり、室温で撹拌し、完全に溶解させる。
ステップ3)であって、5%のNaOH溶液を用いてpHを12に調整し、100kHzの超音波下で60分間超音波処理する。
ステップ4)であって、濃度0.1%(w/v)の200万の高分子量ヒアルロン酸ナトリウム溶液を調製し、添加割合30%(v/v)で上記処理後のヒアルロン酸ナトリウムのアルカリ性溶液と混合する。
ステップ5)であって、1%の珪藻土を用い、55℃で攪拌し、50分間吸着処理し、濾過する。
ステップ6)であって、2%の希硫酸溶液でpHを5.0に調整した後、1%の活性炭を用いて55℃で攪拌し、50分間吸着処理し、濾過する。
ステップ7):であって、ナノ濾過膜システムを用いて濾過液を濃縮し、そのうちナノ濾過膜の分画分子量が300Daであり、操作圧力が30barであり、温度を50℃に制御し、ナノ濾過濃縮液を得て、それを噴霧乾燥し、高品質の全分子量分布ヒアルロン酸ナトリウムのサンプルを得る。
該比較例はある商品化された市販のヒアルロン酸ナトリウム1号(化粧品グレード、125万の重量平均分子量)を選択する。
該比較例はある商品化された市販のヒアルロン酸ナトリウム2号(化粧品グレード、10万の重量平均分子量)を選択する。
該比較例は実施例1の調製方法とほぼ同じであり、相違点は、ステップ1)において1%の過酸化水素水50mLのみを均一に散布し、紫外線照射を行わず、且つ活性炭で吸着した後にナノ濾過膜システムを使用した濾過液を濾過濃縮しないことである。
該比較例は実施例1の調製方法とほぼ同じであり、相違点は、ステップ1)において300μW/cm2線量を採用して60分間紫外線照射を行うのみで、過酸化水素水処理を使用せず、且つ活性炭を採用して吸着した後に、ナノ濾過膜システムを使用した濾液に対する濾過濃縮を行わないことである。
この比較例は、200万の重量平均分子量を有する高分子量ヒアルロン酸ナトリウム、100万の重量平均分子量を有するヒアルロン酸ナトリウム、30万の重量平均分子量を有する低分子量ヒアルロン酸ナトリウム、及び1万未満の重量平均分子量を有するオリゴヒアルロン酸ナトリウムを、単独でそれぞれ1:1:1:1の質量比で60分間混合撹拌し、ヒアルロン酸ナトリウムのサンプルを得る。
上記実施例1~6及び比較例3~5で得られた異なるヒアルロン酸ナトリウムに対して異なる位置のサンプリングを行い、均一性及び安定性を測定し、25℃でNDJ-1型回転粘度計3号回転子を用い、それぞれ1%の異なるヒアルロン酸ナトリウム溶液に対して60r/分で粘度を測定する。各サンプルをそれぞれ調製後4℃で保存し、6ヶ月後にサンプリングして粘度を測定する。結果は表1に示すように、実施例1~6で得られたヒアルロン酸ナトリウムは外観が均一で、安定性に優れる。比較例3及び比較例4で得られたヒアルロン酸ナトリウムは外観が比較的均一であるが、安定性がやや悪く、且つ粘度が比較的大きく、濾過効率が低く、且つナノ濾過膜システムを用いて濾過することが困難であり、比較例5で得られたヒアルロン酸ナトリウムは均一性及び安定性がいずれも悪い。
[表1]
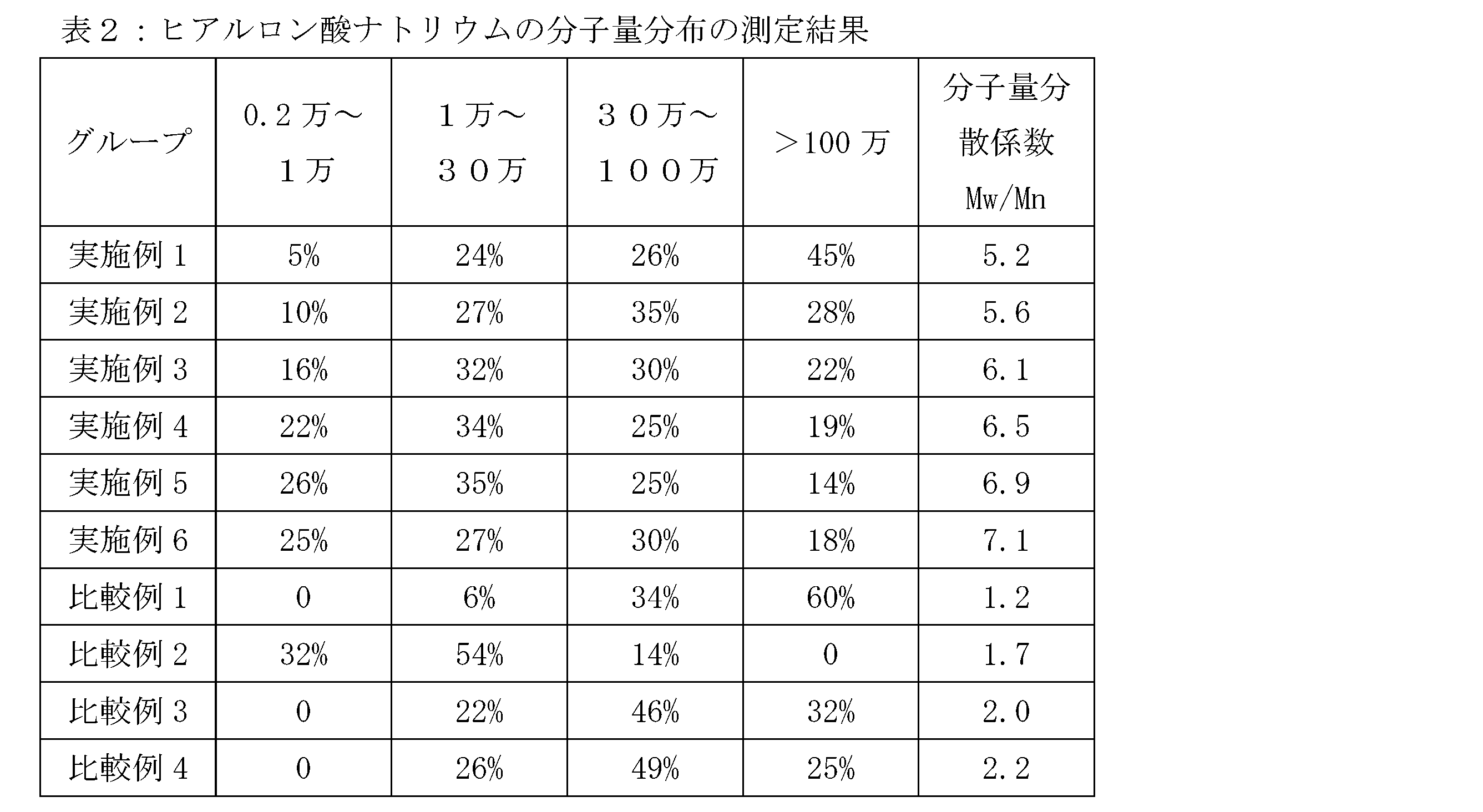
上記実施例と比較例で得られたヒアルロン酸ナトリウムのサンプルの分子量分布を測定すると、重量平均分子量Mwがそれぞれ0.2万~1万、1万~30万、30万~100万、>100万の範囲にあるヒアルロン酸ナトリウム分子の割合が表2のようになる。
[表2]
表2のデータから、実施例1~6で得られたヒアルロン酸ナトリウム原料は、市販の異なる分子量規格のヒアルロン酸ナトリウムと比較して分子量分布の幅が広く、分子量分散係数Mw/Mnが5以上であることが分かる。比較例3と比較例4では分子量分布範囲が狭く、分子量分散係数が2.5以下であることから、紫外線照射や過酸化水素水処理の単独使用では効果が期待できないことが分かる。
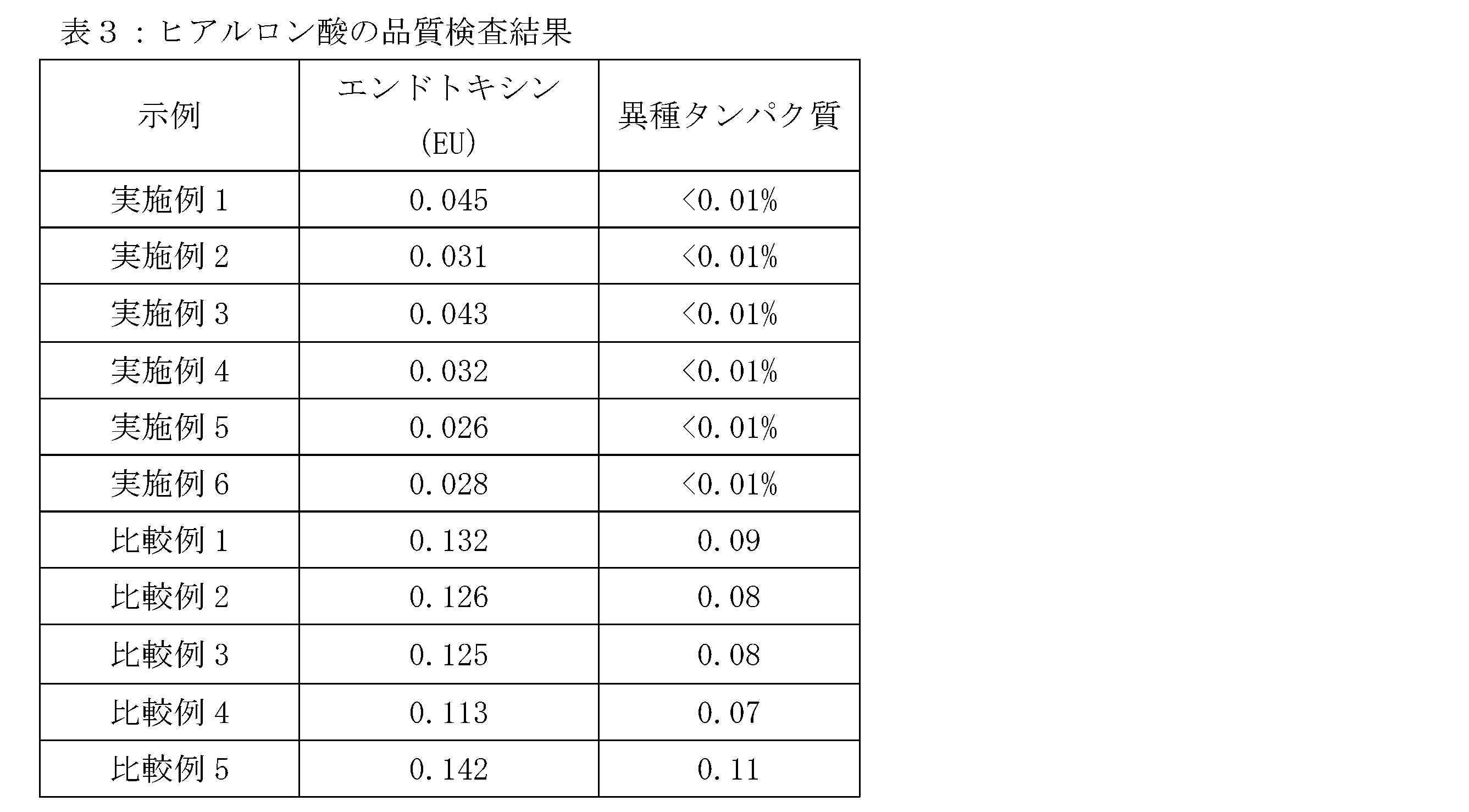
上記実施例1~6で調製したヒアルロン酸ナトリウムのエンドトキシンと異種タンパク質について、それぞれリムルス試薬検出法、Folinフェノール法を用いて測定した結果を表3に示す。
[表3]
表3の結果から、実施例1~6の調製方法で得られたヒアルロン酸は、エンドトキシン含有量が0.01EU未満、タンパク質含有量が0.01%未満であり、280nmでのOD値が0.01未満、260nmでのOD値が0.01未満であり、生体適合性が高く、品質レベルが高いことが分かる。
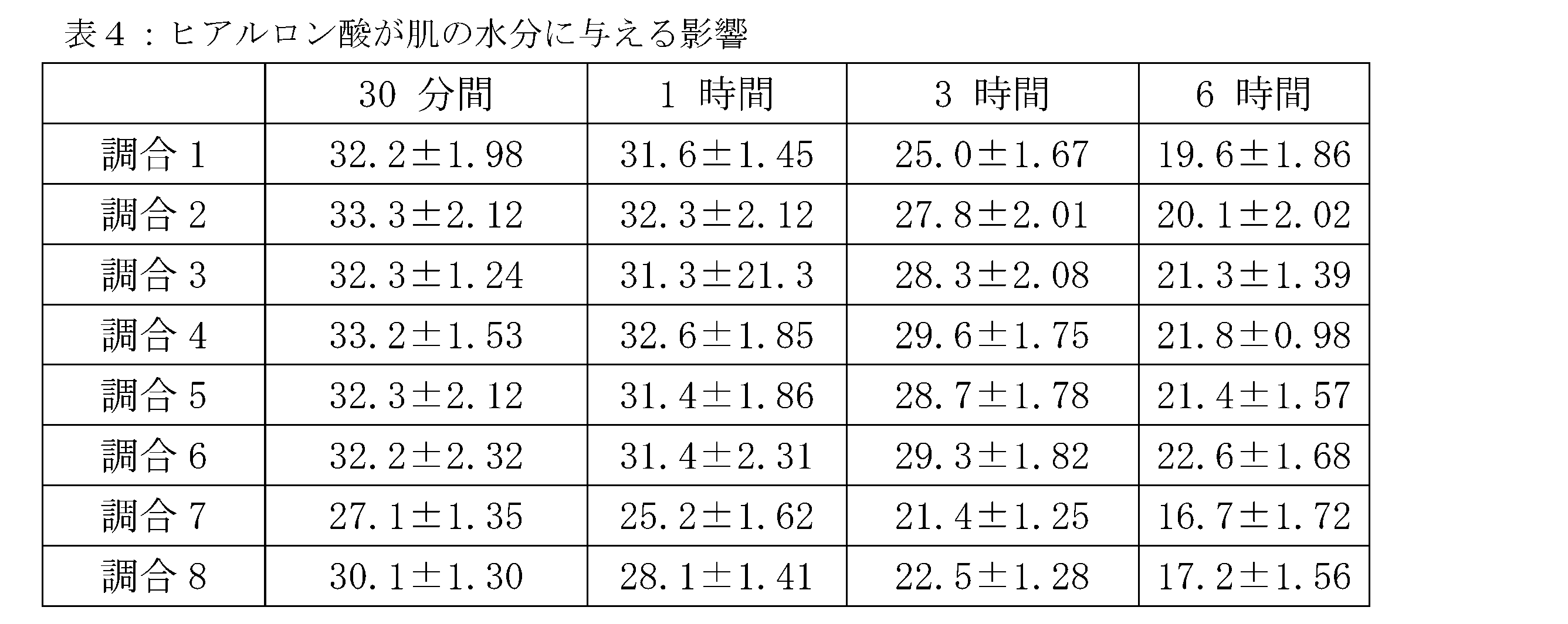
有効な受験希望者45名を選択し、年齢は20~55歳で、2~3日前の受験部位にはどの製品(化粧品や外用薬品などが含まれる)も使用できない。試験前に、被験者は両手の前腕の内側を統一的に清潔にし、4×4cmの試験エリアに印をつけ、調合1~8サンプル(それぞれ実施例1~6の全分子量ヒアルロン酸ナトリウム1%、調合7の市販120万ヒアルロン酸ナトリウム1%、調合8の比較例5ヒアルロン酸ナトリウム1%、調合中の残りの成分はグリセリン2%、ブタンジオール2%)を左右の腕に均一に塗布しランダムに分布し、使用量は3mg/cm2であり、皮膚水分測定器で製品塗布前及び塗布後30分間、1時間、3時間、6時間の時の被検皮膚エリアの水分量を測定し、各エリアごとに平行に5回測定し、平均値を測定値とする。同一被験者の測定は同一の測定者が完成し、すべての被験者は、測定前後に、温度と湿度が一定の室内空間に居る。皮膚水分増加量(%)=(塗布後水分量?塗布前水分量)/塗布前水分量×100%である。
[表4]
表4の結果から、本発明により調製された全分子量ヒアルロン酸ナトリウムは、優れた保湿性を有し、市販のヒアルロン酸ナトリウム製品よりも優れており、化粧品に使用することにより優れた保湿効果を発揮することが分かった。
インターロイキンIL-1βによりヒト不死化上皮細胞(HaCaT)の炎症反応を誘導することをモデルとして、本発明により調製された全分子量分布のヒアルロン酸ナトリウムが抗炎症効果を有することを検証する。
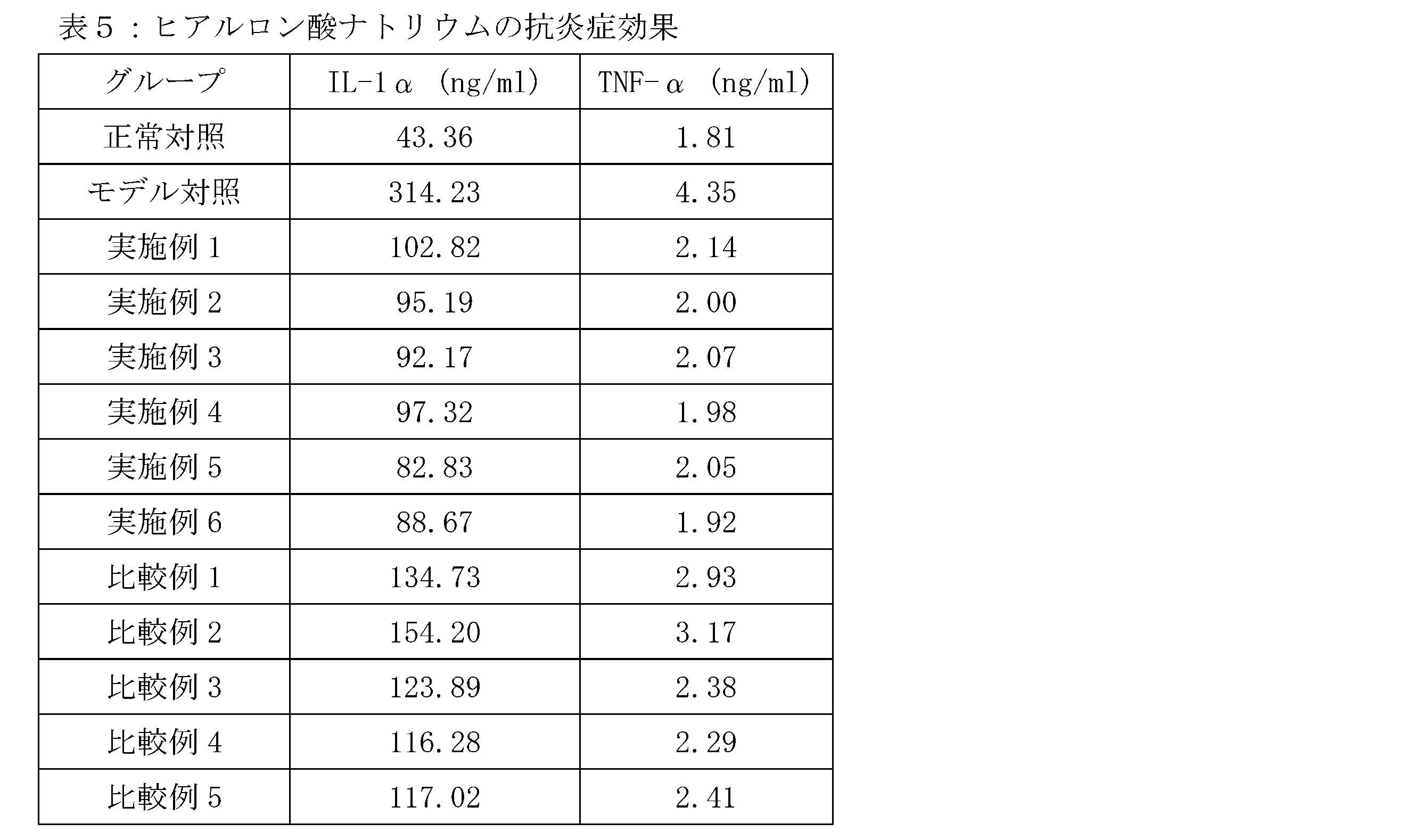
ヒト不死化上皮細胞(HaCaT)を96孔プレートに、5×103cells/mLで、1孔あたり100μLで接種し、1群あたり6個の複数孔を設け、24時間培養後、10ng/mLのインターロイキンIL-1β、20mg/mLの本発明の全分子量ヒアルロン酸ナトリウム(実施例1~6)、及び比較例ヒアルロン酸ナトリウム(比較例1~5)を含む培地を交換し、IL-1及びヒアルロン酸ナトリウムを加えない細胞を正常対照群とし、IL-1βのみを加えヒアルロン酸ナトリウムを加えない細胞をモデル対照群とし、24時間培養を続けた後、ELISAキットを用いてインターロイキンIL-1α及び腫瘍壊死因子TNF-αの発現レベルを測定する。
[表5]
表5のデータから、異なる実施例と比較例のヒアルロン酸は、細胞のIL-1α及びTNF-αの発現レベルを低下させ、いずれも一定の抗炎症効果を示しているが、本発明のプロセスで調製された全分子量分布ヒアルロン酸ナトリウムは比較例の通常のヒアルロン酸ナトリウムよりも優れた抗炎症効果を示していることが分かる。
ラウリル硫酸ナトリウム(SDS)で皮膚モデル損傷を誘導することをモデルとし、本発明で調製した全分子量分布ヒアルロン酸ナトリウムの抗細胞損傷及び細胞修復効果を検証する。
EpiSkin皮膚モデルを12孔プレートに移して培養し、24時間培養後に、0.5%(v/v)SDSを含む培地を交換し、2時間インキュベートした後、1孔当たり1%(w/v)の本発明の全分子量ヒアルロン酸ナトリウム(実施例1~6)、及び比較例ヒアルロン酸ナトリウム(比較例1~5)を含む同量培地を直接添加し、培地のヒアルロン酸ナトリウム含有最終濃度を0.5%(w/v)とし、SDS及びヒアルロン酸ナトリウムを添加しない細胞を正常対照群とし、SDSのみ添加しヒアルロン酸ナトリウムを添加しない細胞をモデル対照群とし、24時間培養を続けた後、皮膚組織モデルを取り出し、MTT法で酵素マーカーを用いて570nmにおける吸光度値を測定し、組織細胞の活性は次の式で計算する:
組織細胞活性(%)=Ap(t)/An×100%
ここで、Ap(t)は陽性対照群又は実験群の吸光度値である。Anは陰性対照群の吸光度値であり、結果は次の表のようになる。
[表6]
表6のデータから、本発明により調製された全分子量分布ヒアルロン酸ナトリウムは、SDSによって誘導されるEpiSkin皮膚モデルの損傷を強く抑制し、損傷した細胞の修復を効果的に促進することが明らかになった。本発明の方法により調製された全分子量分布ヒアルロン酸ナトリウムは、比較例の通常のヒアルロン酸ナトリウムと比較して、細胞修復促進効果が高い。
Claims (9)
- ヒアルロン酸ナトリウムの調製方法であって、
前記方法は、
ヒアルロン酸ナトリウム固体原料に対して過酸化水素水噴霧及び紫外線照射処理を行い、キログラム当たりの前記ヒアルロン酸ナトリウム固体原料は、質量濃度1%~5%の過酸化水素水50~100ミリリットルを噴霧し、紫外照射線量が300~1500μW/cm2であり、照射時間が50~70分であり、ヒアルロン酸ナトリウム分解材料を得る、ステップ1)と、
前記ヒアルロン酸ナトリウム分解材料を水に溶解し、NaOH溶液でpHをアルカリ性に調整することで、ヒアルロン酸ナトリウムのアルカリ性溶液を得る、ステップ2)と、
前記ヒアルロン酸ナトリウムのアルカリ溶液に対して超音波処理を行う、ステップ3)と、
前記ヒアルロン酸ナトリウム固体原料を、0.1%~1%(w/v)の濃度を有するヒアルロン酸ナトリウム溶液に調製し、20%~60%(v/v)の添加割合で、ステップ3)で得られた超音波処理後のヒアルロン酸ナトリウムのアルカリ性溶液と均一に混合する、ステップ4)と、
それぞれ珪藻土と活性炭を用いて吸着処理を行い、且つナノ濾過膜を用いて濾過濃縮し、乾燥した後に、重量平均分子量範囲は0.2万~150万であり、分子量分散係数Mw/Mnは5以上であるヒアルロン酸ナトリウムを得る、ステップ5)とを含む、ことを特徴とするヒアルロン酸ナトリウムの調製方法。 - 前記ヒアルロン酸ナトリウム固体原料の分子量は、100万~200万である、ことを特徴とする請求項1に記載のヒアルロン酸ナトリウムの調製方法。
- 前記ヒアルロン酸ナトリウム固体原料は、化粧品グレードのヒアルロン酸ナトリウム、食品グレードのヒアルロン酸ナトリウム、医薬グレードのヒアルロン酸ナトリウムのうちの一つ又は複数から選択される、ことを特徴とする請求項2に記載のヒアルロン酸ナトリウムの調製方法。
- 前記ステップ2)において、前記ヒアルロン酸ナトリウム分解材料を水に溶解した後の体積濃度は1%~10%(w/v)であり、及び/又は、
NaOH溶液でpHを10~12に調整する、ことを特徴とする請求項1に記載のヒアルロン酸ナトリウムの調製方法。 - 前記ステップ3)において、超音波処理の周波数は10~100kHzであり、時間は15~180分である、ことを特徴とする請求項1に記載のヒアルロン酸ナトリウムの調製方法。
- 前記ステップ5)において、
珪藻土を採用する吸着処理のステップは、以下の含み、
前記ヒアルロン酸ナトリウムのアルカリ溶液の質量に基づき、0.1%~1%(w/v)の珪藻土を加え、45~80℃で撹拌して30~60分間吸着し、濾過し、及び/又は、
活性炭を採用する吸着処理のステップは、以下を含み、
希酸溶液でpHを6~7に調整し、前記ヒアルロン酸ナトリウム溶液の質量に基づく0.1%~1%(w/v)の活性炭を加え、45~80℃で撹拌して30~60分間吸着し、濾過し、前記希酸溶液は、希塩酸溶液、希硫酸溶液、希酢酸溶液、希次亜塩素酸溶液のうちの一種又は多種から選択される、ことを特徴とする請求項1に記載のヒアルロン酸ナトリウムの調製方法。 - 前記ステップ5)において、前記ナノ濾過膜の分画分子量は200-300Daであり、操作圧力を15-30barに制御し、温度を30~50℃に制御する、ことを特徴とする請求項1に記載のヒアルロン酸ナトリウムの調製方法。
- 前記ステップ5における前記ヒアルロン酸ナトリウムのエンドトキシン含有量は<0.01EUであり、タンパク質含有量は<0.01%であり、
前記ステップ5における前記ヒアルロン酸ナトリウムは、280nmでOD値<0.01であり、260nmでOD値<0.01である、ことを特徴とする請求項1~7のいずれか一項に記載のヒアルロン酸ナトリウムの調製方法。 - 請求項1~7のいずれか一項に記載の調製方法で調製されたヒアルロン酸ナトリウムの医薬用、食品用及び/又は化粧品用の保湿剤、潤滑剤、抗炎症剤及び/又は細胞修復剤の調製における使用。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN202110874694.1 | 2021-07-30 | ||
| CN202110874694.1A CN113512134B (zh) | 2021-07-30 | 2021-07-30 | 一种全分子量分布的透明质酸钠及其制备方法和应用 |
| PCT/CN2022/109329 WO2023006108A1 (zh) | 2021-07-30 | 2022-07-31 | 一种全分子量分布的透明质酸钠及其制备方法和应用 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2024522452A JP2024522452A (ja) | 2024-06-21 |
| JP7621625B2 true JP7621625B2 (ja) | 2025-01-27 |
Family
ID=78068930
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2023568598A Active JP7621625B2 (ja) | 2021-07-30 | 2022-07-31 | 全分子量分布のヒアルロン酸ナトリウム及びその調製方法と応用 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US11976139B2 (ja) |
| EP (1) | EP4386013B1 (ja) |
| JP (1) | JP7621625B2 (ja) |
| CN (1) | CN113512134B (ja) |
| AU (1) | AU2022317614B2 (ja) |
| WO (1) | WO2023006108A1 (ja) |
Families Citing this family (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN113512134B (zh) | 2021-07-30 | 2022-05-20 | 梅晔生物医药股份有限公司 | 一种全分子量分布的透明质酸钠及其制备方法和应用 |
| CN116656012B (zh) * | 2022-02-18 | 2024-08-09 | 广东粤港澳大湾区国家纳米科技创新研究院 | 一种水溶性富勒烯复合物及其制备方法和应用 |
| CN116650355B (zh) * | 2022-02-18 | 2025-11-07 | 广州广纳慧川科技有限公司 | 一种透明质酸钠-富勒烯5d复合物及其制备方法和应用 |
| KR102762718B1 (ko) * | 2022-02-23 | 2025-02-06 | 주식회사 스카이테라퓨틱스 | 고분자 히알루론산의 구조체, 이의 제조방법 및 이를 포함하는 화장료 조성물 |
| CN116987327B (zh) * | 2022-04-25 | 2024-08-20 | 广东粤港澳大湾区国家纳米科技创新研究院 | 一种碳纳米材料-透明质酸钠复合物及其制备方法 |
| CN115558040B (zh) * | 2022-09-30 | 2024-01-23 | 华熙生物科技股份有限公司 | 一种无防腐剂添加的透明质酸或其盐的生产方法 |
| CN115998640B (zh) * | 2022-10-31 | 2023-08-22 | 梅晔生物医药股份有限公司 | 一种抗糖组合物、精华液以及生产方法 |
| CN115670968B (zh) * | 2022-10-31 | 2023-08-25 | 梅晔生物医药股份有限公司 | 一种具有抗炎舒敏作用的组合物、日化品 |
| CN115501127B (zh) * | 2022-11-01 | 2023-08-18 | 梅晔生物医药股份有限公司 | 一种抗炎舒敏组合物、日化品 |
| CN116715786A (zh) * | 2023-05-15 | 2023-09-08 | 仁恒智研新材料科技(广东)有限公司 | 一种低动力粘度的线性透明质酸钠的制备方法 |
| CN117771123A (zh) * | 2023-11-30 | 2024-03-29 | 梅晔生物医药股份有限公司 | 一种保湿促渗组合物及其应用、日化品 |
| CN118924640A (zh) * | 2024-07-31 | 2024-11-12 | 广东诗妃化妆品有限公司 | 一种祛痘组合物及其制备方法、应用、日化品 |
| CN119015486B (zh) * | 2024-08-19 | 2025-06-27 | 珠海市雅莎医疗器械有限公司 | 一种医用透明质酸钠凝胶敷料及其制备方法 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2000502141A (ja) | 1995-12-20 | 2000-02-22 | フィディア アドヴァンスド バイオポリマーズ ソシエタ ア レスポンサビリタ リミタータ | 低い多分散指数を有するヒアルロン酸分画の調製方法 |
| JP2004250592A (ja) | 2003-02-20 | 2004-09-09 | Seikagaku Kogyo Co Ltd | 紫外線照射による低分子化グリコサミノグリカンの製造方法 |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| IT1402382B1 (it) * | 2010-09-09 | 2013-09-04 | Ibsa Inst Biochimique Sa | Complessi cooperativi ibridi di acido ialuronico |
| CN104059166A (zh) * | 2013-03-21 | 2014-09-24 | 上海昊海生物科技股份有限公司 | 一种从透明质酸发酵液制备寡聚透明质酸的方法 |
| CN108484796B (zh) * | 2018-05-08 | 2021-02-05 | 山东焦点福瑞达生物股份有限公司 | 一种低分子透明质酸钠制备工艺 |
| CN108992369B (zh) * | 2018-07-02 | 2021-07-30 | 山东天晟生物科技有限公司 | 一种透明质酸、其制备方法和用途 |
| CN110423291B (zh) * | 2019-09-06 | 2020-06-16 | 焦点生物医药有限公司 | 一种速溶透明质酸钠制备方法 |
| US11058640B1 (en) * | 2020-04-07 | 2021-07-13 | Amc Group, Llc | Hyaluronate compositions and soft tissue fillers |
| CN112076127B (zh) | 2020-09-28 | 2023-02-03 | 广东丸美生物技术股份有限公司 | 抗氧化剂及其原料制备方法、保湿剂及其原料制备方法 |
| CN112553273B (zh) * | 2020-12-26 | 2022-12-09 | 河北华曙新合药业有限公司 | 一种超小分子量透明质酸钠的制备工艺 |
| CN112920289A (zh) | 2021-02-03 | 2021-06-08 | 华南理工大学 | 一种海藻多糖的降解方法 |
| CN113512134B (zh) | 2021-07-30 | 2022-05-20 | 梅晔生物医药股份有限公司 | 一种全分子量分布的透明质酸钠及其制备方法和应用 |
-
2021
- 2021-07-30 CN CN202110874694.1A patent/CN113512134B/zh active Active
-
2022
- 2022-07-31 JP JP2023568598A patent/JP7621625B2/ja active Active
- 2022-07-31 US US18/038,777 patent/US11976139B2/en active Active
- 2022-07-31 AU AU2022317614A patent/AU2022317614B2/en active Active
- 2022-07-31 WO PCT/CN2022/109329 patent/WO2023006108A1/zh not_active Ceased
- 2022-07-31 EP EP22848712.0A patent/EP4386013B1/en active Active
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2000502141A (ja) | 1995-12-20 | 2000-02-22 | フィディア アドヴァンスド バイオポリマーズ ソシエタ ア レスポンサビリタ リミタータ | 低い多分散指数を有するヒアルロン酸分画の調製方法 |
| JP2004250592A (ja) | 2003-02-20 | 2004-09-09 | Seikagaku Kogyo Co Ltd | 紫外線照射による低分子化グリコサミノグリカンの製造方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| US11976139B2 (en) | 2024-05-07 |
| EP4386013A1 (en) | 2024-06-19 |
| CN113512134B (zh) | 2022-05-20 |
| EP4386013B1 (en) | 2026-03-18 |
| AU2022317614B2 (en) | 2024-08-22 |
| AU2022317614A1 (en) | 2024-08-15 |
| EP4386013A4 (en) | 2025-03-26 |
| WO2023006108A1 (zh) | 2023-02-02 |
| US20240002551A1 (en) | 2024-01-04 |
| CN113512134A (zh) | 2021-10-19 |
| JP2024522452A (ja) | 2024-06-21 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7621625B2 (ja) | 全分子量分布のヒアルロン酸ナトリウム及びその調製方法と応用 | |
| JP5976537B2 (ja) | 新規な充填剤としての粘弾性ゲル | |
| EP1753787B1 (en) | Method of covalently linking hyaluronan and chitosan | |
| CN111040048A (zh) | 一种超低分子量透明质酸及其制备方法 | |
| JP2004536624A (ja) | 不飽和ガス雰囲気中での固体照射により得られる新規なバイオポリマー | |
| JP2024115499A (ja) | 皮膚の鎮静・修復用の組換えコラーゲンおよびその使用 | |
| CN110655662B (zh) | 一种橄榄苦苷交联制备透明质酸钠凝胶的方法及透明质酸钠凝胶 | |
| WO2007131424A1 (fr) | Procédé de préparation de compositions de protéoglycane et de collagène à faible poids moléculaire, produits résultants et utilisations de ceux-ci | |
| US20250320275A1 (en) | Method for preparing undenatured collagen type ii for alleviating joint pain | |
| CN105985994B (zh) | 一种无盐无有机溶剂纯化技术制备透明质酸钠的方法 | |
| CN116808309B (zh) | 一种胶原蛋白壳聚糖复合支架及其制备方法及应用 | |
| CN119930801B (zh) | 一种高热稳定性的仿生胶原蛋白、化妆品、药物、组织工程材料或医疗器械及其制备方法和用途 | |
| CN120859882A (zh) | 修复组合物及其用途 | |
| CN115215948B (zh) | 一种低分子的乙酰透明质酸脱羧肌肽衍生物、制备方法及应用 | |
| CN116179629A (zh) | 不饱和透明质酸钠二糖的制备方法 | |
| CN119564533B (zh) | 一种透皮吸收纳米羊胎盘胶原及其制备方法和应用 | |
| CN119015486B (zh) | 一种医用透明质酸钠凝胶敷料及其制备方法 | |
| CN112251483A (zh) | 一种小分子透明质酸钠的生产方法 | |
| CN119954940B (zh) | 一种透明、高热稳定性的仿生胶原蛋白、化妆品、药物、组织工程材料或医疗器械及其制备方法和用途 | |
| CN113559015B (zh) | 一种可应用于化妆品的生物活性低分子量汉生胶及其用途 | |
| CN118178261B (zh) | 透明质酸在制备促进角蛋白ck15生成的制剂中的应用 | |
| CN110698700B (zh) | 一种单宁交联制备透明质酸钠凝胶的方法及透明质酸钠凝胶 | |
| CN102803298B (zh) | 透明质酸的提纯方法 | |
| CN121628996A (zh) | 一种修护头皮和强韧头发的透明质酸钠发酵滤液及其制备方法与应用 | |
| CN119838056A (zh) | 一种负载美洲大蠊糖蛋白微球的可注射凝胶 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240208 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20231227 |
|
| A871 | Explanation of circumstances concerning accelerated examination |
Free format text: JAPANESE INTERMEDIATE CODE: A871 Effective date: 20240208 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240730 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20241028 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20241224 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20250106 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7621625 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |