定義
本発明がより容易に理解されるために、いくつかの用語を最初に以下で定義する。以下の用語及び他の用語についての追加の定義は、本明細書全体を通して説明される。
本明細書及び添付の特許請求の範囲で使用される場合、単数形「a」、「an」及び「the」は、文脈上特に明確に指示されない限り、複数の指示対象を含む。
特に明記されていないか又は文脈から明らかでない限り、本明細書で使用される場合、「又は」という用語は包括的であると理解され、「又は」と「及び」の両方を包含する。
本明細書で使用される「例えば」及び「すなわち」という用語は、単に例示の目的で使用され、限定を意図されず、明細書で明示的に列挙された項目のみを指すと解釈されるべきではない。
「1つ以上の」、「少なくとも1つの」、「複数の」等の用語は、少なくとも1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19 20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98、99、100、101、102、103、104、105、106、107、108、109、110、111、112、113、114、115、116、117、118、119、120、121、122、123、124、125、126、127、128、129、130、131、132、133、134、135、136、137、138、139、140、141、142、143、144、145、146、147、148、149又は150、200、300、400、500、600、700、800、900、1000、2000、3000、4000、5000又はこれ以上、及びこの間の任意の数を含むがこれらに限定されないと理解される。
逆に、「以下」という用語は、記述される値よりも小さい各々の値を含む。例えば、「100ヌクレオチド以下」は、100、99、98、97、96、95、94、93、92、91、90、89、88、87、86、85、84、83、82、81、80、79、78、77、76、75、74、73、72、71、70、69、68、67、66、65、64、63、62、61、60、59、58、57、56、55、54、53、52、51、50、49、48、47、46、45、44、43、42、41、40、39、38、37、36、35、34、33、32、31、30、29、28、27、26、25、24、23、22、21、20、19、18、17、16、15、14、13、12、11、10、9、8、7、6、5、4、3、2、1及び0個のヌクレオチドを含む。
「複数」、「少なくとも2つ」、「2つ以上」、「少なくとも2番目」等の用語は、少なくとも2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19 20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98、99、100、101、102、103、104、105、106、107、108、109、110、111、112、113、114、115、116、117、118、119、120、121、122、123、124、125、126、127、128、129、130、131、132、133、134、135、136、137、138、139、140、141、142、143、144、145、146、147、148、149又は150、200、300、400、500、600、700、800、900、1000、2000、3000、4000、5000又はこれ以上、及びこの間の任意の数を含むがこれらに限定されないと理解される。
本明細書を通して、「含む(comprising)」という語又は「含む(comprises)」若しくは「含むこと(comprising)」などの変形は、記述される要素、整数若しくは工程、又は要素、整数又は若しくは工程の群を包含することを意味するが、任意の他の要素、整数若しくは工程、又は要素、整数若しくは工程の群を排除することを意味しないことが理解される。
特に明記されていないか又は文脈から明らかでない限り、本明細書で使用される場合、「約」という用語は、当技術分野における通常の許容範囲内、例えば平均の2標準偏差以内であると理解される。「約」は、記述される値の10%、9%、8%、7%、6%、5%、4%、3%、2%、1%、0.5%、0.1%、0.05%、0.01%又は0.001%以内であると理解することができる。文脈から特に明らかでない限り、本明細書で提供されるすべての数値は、「約」という用語によって修飾される。
表面は、細胞壁、細胞エンベロープ、形質膜若しくは細胞被膜の外面;細胞壁、細胞エンベロープ、形質膜若しくは細胞被膜の内面であり得るか;又は細胞壁、細胞エンベロープ、形質膜若しくは細胞被膜内に存在し得る。表面は、繊毛(cilium)、線毛(pilus)及びべん毛を含むがこれらに限定されない、細胞外に突出している細胞の構造体を含み得る。表面は、細胞小器官を含み得る。表面は、膜貫通タンパク質、細胞壁タンパク質、細胞外タンパク質、細胞内タンパク質、細胞外関連多糖、細胞内関連多糖、細胞外脂質、細胞内脂質、膜脂質、細胞壁脂質、タンパク質、多糖及び/又は細胞エンベロープに不可欠であるか若しくは関連する脂質を含み得る。表面は、核酸を含み得る。
表面は、シグナル伝達剤が結合又は会合する生体分子を含み得る。例示的な生体分子には、ペプチドグリカン、ムレイン、マンノプロテイン、ポーリン、β-グルカン、キチン、糖タンパク質、多糖、リポ多糖、リポオリゴ糖、リポタンパク質、内毒素、リポテイコ酸、テイコ酸、脂質A、炭水化物結合ドメイン、流出ポンプ、他の細胞壁及び/又は細胞膜関連タンパク質、他のアニオン性リン脂質、並びにこれらの組み合わせが含まれる。
増殖は、微生物の増殖におけるように、数の増殖、長さの増加、体積の増加、並びに/又は微生物の核酸及び/若しくはタンパク質含量の増加を含む。
対照は、微生物が感受性でない抗菌剤を含み得る。例として、アッセイがグラム陽性菌の感受性を決定するために使用される場合は、対照(及び試験インキュベーション)は、グラム陰性菌を標的とする1つ以上の抗菌剤を含み得、アッセイが真核微生物の感受性を決定するために使用される場合は、対照(及び試験インキュベーション)は、1つ以上の抗菌抗微生物剤を含み得る。
対照は、他の点では同一条件であるが、抗菌剤を含まない条件下又は微生物が感受性でない1つ以上の抗菌剤を含む条件下で微生物から測定された陽性対照であり得る。
対照は、他の点では同一条件であるが、栄養素を含まない条件下で微生物から測定され得る。
対照は、他の点では同一条件であるが、微生物の増殖を阻害することが公知の1つ以上の毒素を含む条件下で微生物から測定され得る。
対照は、歴史的な(historic)対照であり得る。ここで、試験インキュベーションは、対照インキュベーションが行われた後に実施され得る。
又は、対照は、試験インキュベーションを含むカートリッジとは別個のカートリッジ内で実施され得る。
「処理される」とは、生物学的試料から微生物を単離する工程、生物学的試料から得られる微生物の濃度を増加させる工程、及び/又は、例えば微生物の増殖を促進する条件下で微生物を培養することによって、生物学的試料から得られる微生物の数を増加させる工程を意味する。
本発明の化合物は、本明細書で一般的に記載される化合物を含み、本明細書で開示されるクラス、サブクラス及び種によってさらに説明される。本明細書で使用される場合、特に指示されない限り、以下の定義が適用される。本発明の目的のために、化学元素は、元素の周期表、CAS版、Handbook of Chemistry and Physics、第75版に従って同定される。さらに、有機化学の一般原則は、「Organic Chemistry」,Thomas Sorrell,University Science Books,Sausalito:1999及び「March’s Advanced Organic Chemistry」,5th Ed.,Ed.:Smith,M.B.and March,J.,John Wiley&Sons,New York:2001に記載されており、これらの内容全体が参照により本明細書に組み込まれる。
本明細書で使用される「複素環」、「ヘテロシクリル」又は「複素環式」という用語は、1つ以上の環員が独立して選択されるヘテロ原子である非芳香族、単環式、二環式又は三環式環系を意味する。いくつかの実施形態では、「複素環」、「ヘテロシクリル」又は「複素環式」基は、1つ以上の環員が酸素、硫黄、窒素又はリンから独立して選択されるヘテロ原子である3~14個の環員を有し、系の各環は3~7個の環員を含む。
「ヘテロ原子」という用語は、酸素、硫黄、窒素、リン及びケイ素(窒素、硫黄、リン又はケイ素の任意の酸化形態、任意の塩基性窒素の四級化形態又は複素環式環の置換可能な窒素、例えばN(3,4-ジヒドロ-2H-ピロリルにおけるような)、NH(ピロリジニルにおけるような)又はNR+(N置換ピロリジニルにおけるような)を含む)の1つ以上を指す。
本明細書で使用される「アルコキシ」又は「チオアルキル」という用語は、先に定義されたような、酸素原子を介して(「アルコキシ」)又は硫黄原子を介して(「チオアルキル」)結合されたアルキル基を指す。
「ハロアルキル」、「ハロアルケニル」、「ハロ脂肪族」及び「ハロアルコキシ」という用語は、場合によって、1つ以上のハロゲン原子で置換されたアルキル、アルケニル又はアルコキシを意味する。この用語は、-CF3及び-CF2CF3などのペルフルオロアルキル基を含む。
「ハロゲン」、「ハロ」及び「ハル」は、F、Cl、Br又はIを意味する。
単独又はより大きな部分、例えば「アラルキル」、「アラルコキシ」又は「アリールオキシアルキル」の一部として使用される「アリール」及び「アル」という用語は、1~3個の芳香環を含む任意に置換されたC6-14の芳香族炭化水素部分を指す。例えば、アリール基は、C6-10アリール基(すなわちフェニル及びナフチル)である。アリール基には、任意に置換されたフェニル、ナフチル又はアントラセニルが含まれるが、これらに限定されない。本明細書で使用される「アリール」及び「アル」という用語はまた、アリール環が1つ以上の脂環式環に縮合して、テトラヒドロナフチル、インデニル又はインダニル環などの任意に置換された環状構造を形成する基も含む。「アリール」という用語は、「アリール基」、「アリール環」及び「芳香環」という用語と交換可能に使用され得る。
本発明の化合物は、治療のための遊離形態で、又は適切な場合は、薬学的に許容される塩として存在し得る。
本明細書で使用される場合、「芳香族」という用語は、以下及び本明細書で一般的に記述されるアリール及びヘテロアリール基を含む。
本明細書で使用される「脂肪族」又は「脂肪族基」という用語は、完全に飽和しているか又は1つ以上の不飽和単位を含む任意に置換された直鎖又は分岐C1-12炭化水素を意味する。例えば、適切な脂肪族基には、任意に置換された直鎖又は分岐アルキル、アルケニル及びアルキニル基が含まれる。特に指定されない限り、様々な実施形態において、脂肪族基は、1~12、1~10、1~8、1~6、1~4、1~3又は1~2個の炭素原子を有する。いくつかの実施形態では、本明細書に記載の「脂肪族」基が2価であり得ることは当業者に明らかである。
単独で又はより大きな部分の一部として使用される「アルキル」という用語は、1~12、1~10、1~8、1~6、1~4、1~3又は1~2個の炭素原子を有する、飽和の、任意に置換された直鎖又は分岐鎖炭化水素基を指す。
単独で又はより大きな部分の一部として使用される「アルケニル」という用語は、少なくとも1つの二重結合を有し、2~12、2~10、2~8、2~6、2~4又は2~3個の炭素原子を有する任意に置換された直鎖又は分岐鎖炭化水素基を指す。
単独で又はより大きな部分の一部として使用される「アルキニル」という用語は、少なくとも1つの三重結合を有し、2~12、2~10、2~8、2~6、2~4又は2~3個の炭素原子を有する任意に置換された直鎖又は分岐鎖炭化水素基を指す。
特に明記されない限り、本明細書に示される構造はまた、構造のすべての異性体(例えばエナンチオマー、ジアステレオマー及び幾何(又は立体配座))形態、例えば各不斉中心のR及びS立体配置、(Z)及び(E)二重結合異性体、並びに(Z)及び(E)立体配座異性体を含むことが意図されている。したがって、本発明の化合物の単一立体化学異性体並びにエナンチオマー、ジアステレオマー及び幾何(又は立体配座)混合物は、本発明の範囲内である。特に明記されない限り、本発明の化合物のすべての互変異性体は、本発明の範囲内である。さらに、特に明記されない限り、本明細書に示される構造は、1つ以上の同位体濃縮原子が存在することにおいてのみ異なる化合物を含むことも意図されている。例えば、重水素又はトリチウムによる水素の置換、又は13C若しくは14C濃縮炭素による炭素の置換が存在する本発明の構造を有する化合物は、本発明の範囲内である。このような化合物は、非限定的な例として、生物学的アッセイにおける分析ツール又はプローブとして有用である:
開示される化合物が少なくとも1つのキラル中心を有する場合、本発明は、対応する光学異性体を含まない阻害剤の1つのエナンチオマー、阻害剤のラセミ混合物及び対応する光学異性体と比較して1つのエナンチオマーが濃縮された混合物を包含することが理解されるべきである。混合物が、光学異性体と比較して1つのエナンチオマーが濃縮されている場合、混合物は、例えば少なくとも50%、75%、90%、95%、99%又は99.5%のエナンチオマー過剰率を含む。
特に定義されない限り、本明細書で使用されるすべての技術及び学術用語は、本出願が属する技術分野の当業者によって一般的に理解され、本出願が属する技術分野で一般的に使用されるのと同じ意味を有し、このような技術は、全体が参照により本明細書に組み込まれる。紛争の場合は、定義を含む本明細書が支配する。
発明の詳細な説明
本発明は、微生物感染の抗生物質感受性の迅速な決定を可能にする。本発明は、一部には、12時間未満、具体的には4時間未満で、正確で迅速な抗菌剤感受性試験(AST)の決定を提供する非特異的な表面結合アッセイの驚くべき発見に基づく。本発明(「高速AST」)は、Clinical Laboratory Standards Institute(CLSI)の参照法を用いて、複数の抗菌剤を用いて複数の微生物に関して試験した場合に得られた結果と一致する、正確な結果を提供する;しかしながら、本発明は、結果を得るのにCLSI法よりも有意に短い時間しかかからない。さらに、本発明は、1つ以上の抗菌剤に耐性である臨床的に関連する微生物株に対する抗菌剤のMICと、抗菌剤に感受性である同じ微生物株に対する抗菌剤のMICとを正確に区別する。さらに、本発明は、特異的ではなく非特異的に(例えば化学的に保存された基又は微生物上の生化学的に保存された結合部位を介して)微生物に結合するシグナル伝達剤(例えばユウロピウム化合物)を含み得、これにより本発明の一般化を任意の微生物に拡大し、特定の感染性微生物を最初に同定する必要なしに適切な処置を開始することを可能にする。また、本発明は、例えば微生物の希薄な培養物から、又は患者の生物学的試料を介して、微生物がより低い濃度で迅速に検出され得るシグナル増幅を可能にする。さらに、本発明は、化学的部分としてユウロピウム製剤を使用することができ、これにより本発明の方法のダイナミックレンジを拡大し、様々な微生物試料からのより正確な測定を可能にする。最後に、本発明は既存の機器と互換性があり、これにより現在の臨床検査室での迅速な採用を可能にする。したがって、本発明は、標準的な方法と比較して大幅に低減された量の時間と費用で、患者に適切な治療レジメン、すなわち特定の抗菌剤を特定の投与量で提供することができる。したがって、本発明は、患者の転帰を改善し、病院の費用を低減し、抗菌剤耐性微生物のさらなる進化を減少させるのに役立つ;したがって、本発明は、AST分野における重要なブレイクスルーである。
本発明の態様は、微生物表面を化学的に増幅することにより、正確で低コストの表現型AST結果を提供する。この新規アプローチは、現在使用されている方法に比べて2つの主要な進歩を提供する:1)当業者に周知のように、糸状増殖状態に関する現在のプラットフォームの限界を克服する、相対表面積を決定することによる微生物増殖の定量化;及び2)標準的な光学検出装置を用いて1×103~1×108CFU/ml範囲の最適感受性での微生物増幅。
本明細書で(例えば実施例において)開示されるように、本発明は、6種全部(エンテロコッカス・フェシウム(Enterococcus faecium)、スタフィロコッカス・アウレウス(Staphylococcus aureus)、クレブシエラ・ニューモニエ(Klebsiella pneumoniae)、アシネトバクター・バウマニ(Acinetobacter baumannii)、シュードモナス・アエルギノーサ(Pseudomonas aeruginosa)及びエンテロバクター属(Enterobacter)種)(「ESKAPE」)の病原体を含む広範囲の微生物種について、ゴールドスタンダードと同等の結果を提供することが示されている。本発明の一般性ゆえに、新しい微生物種株及び診断試験に容易に及び安価に適合させることができるという点で本発明は柔軟性がある。
本発明は、8時間未満、好ましくは5時間未満で、標準的な微生物コロニー単離物から又は直接陽性血液試料から、低コストの表現型ASTを提供する。これは、標準的な臨床微生物学研究室の同じシフトでの表現型AST結果を可能にする。以下の実施例は、微生物表面の化学的増幅が、4時間未満で正確な最小阻害濃度(MIC)及びブレークポイントコールを生じることを実証する。これは、現在の待機時間を20時間以上短縮し、現在FDA治験に近づいている直接陽性血液培養MALDI-TOF同定、並びに既にFDAクリアランスを取得した直接陽性血液培養マルチプレックスPCR同定プラットフォームに匹敵する。この設計は、本発明(「高速AST」プラットフォーム)が従来の速度対コストのトレードオフを打破することを可能にする。本発明は、標準的なマイクロプレート形式(例えば6、12、24、48、96、384又は1536ウェルを有する)及び従来の光検出器の両方と適合性である。
速度と精度を備えた、侵入する病原体の同定及び抗菌剤感受性試験(AST)は、最も有効な治療薬の時宜を得た投与を可能にする。このような治療は、感染を改善し、入院患者の滞在期間を短縮し、患者が、抗菌剤耐性の世界的蔓延をもたらす広域スペクトルの抗菌剤を投与される時間を低減する。対照的に、微生物の同定及び感受性結果についての現在受け入れられている30時間以上の待機時間は、広域スペクトル抗菌剤の過剰使用及び患者の必要以上に長い入院を余儀なくさせる。この理由から、Presidential Advisory Council on Combating Antibiotic-Resistant Bacteriaは、最近、抗生物質耐性菌の検出のための迅速な診断の開発と使用をその主要目標の1つとした。
より迅速で正確なAST決定を生じる本発明は、患者1人当たり2,000ドルを超える実際の費用便益を提供し得る。これらの価値ポイントには、より容易に定量化できる点(入院期間の短縮及び高額な治療の低減)並びにより無形で価値を測るのが難しい点(患者の死亡率及び抗菌薬適正使用の改善による社会的影響)が含まれる。規制機関が、より厳密な抗菌薬適正使用支援プログラムを採用していない病院にコストを負担させることを始めたため、抗菌薬適正使用支援の価値のような、これらの無形の価値の一部がより定量化されるようになり得る。2014年9月にカリフォルニア州上院法案第1311号が署名されて法律として成立し連邦政府及び専門機関によって制定されたガイドラインに従って、抗菌薬適正使用支援方針を採用し実施すること、及び適正使用支援に関連する特定の訓練を受けた少なくとも1名の医師又は薬剤師を含む、医師が監督する多専門分野にわたる抗菌薬適正使用支援委員会を設置することが、病院にさらに要求された。2016年6月に、Centers for Medicare and Medicaid Systems(CMS)は、今後2年間に経済的インセンティブが導入されることを期待する多くの産業専門家と共に、病院における抗菌薬適正使用支援を促進するという提案された役割を使用した。本発明は、より良い抗菌薬適正使用支援という政府及び医療産業の目標を前進させる。
本発明の態様の一般化された工程を図1に示す。図1の画像は、異なる工程段階を含む態様を示す;しかしながら、本発明の態様は自動化され得る。
図2A~図2Dは、本発明の態様の特徴を示す。図2Aは、3つの代表的な病原体に対する検出感度範囲を示す。点線はゼロ濃度のシグナルレベルを示す。図2Bは、本発明で使用し得る「Crocodile」(Titertek-Berthold)自動高速ASTプロトタイププラットフォームを示す。図2Cは、カチオン性ナノ標識及びポリマーと相互作用するアニオン性細菌を示す概略図である。生じる中性錯体の溶解度低下は、磁気ビーズの結合を可能にする。図2Dは、高増殖対照及び「frozen-in-time(FIT)」対照と比較した静菌性(クリンダマイシン)及び殺菌性(ペニシリン)抗菌剤の結果を示す、SensiTitre(R)グラム陽性パネル(GPALL3F)を用いたS.アウレウス(S.aureus)についてのデータを示す。
当業者に公知のように、ASTプラットフォームは、試験される各抗菌剤について最小阻害濃度(MIC)結果及び/又は定性的感受性結果(QSR)をもたらし得る。MICは、微生物増殖を阻害し、医師に投薬情報を提供する抗菌剤の最小濃度であることが一般的に知られている。QSRも医師に同様の投薬情報を提供し得るが、数値としてのMICは提供しないことがある。ASTアッセイは、主として、得られた各生物学的試料について複数の抗菌剤を並行して試験するように構成されている。MIC又はQSRの結果を得るためには、各抗菌剤について希釈系列が必要である。したがって、CLSIによる「微量液体希釈法」と呼ばれる液体ベースのASTでは、アッセイは、異なる濃度の異なる抗菌剤の並行試験を可能にする、カートリッジ及び/又はマイクロプレートで一般的に実施される。
AST測定結果を得るため長い時間は、医師に不完全な情報を与えることになる。これらの長い時間は、しばしば、抗菌効果又は死滅動態の速度の同定を妨げる。この追加情報は、治療情報を与えるために重要であり得る。治療開始後6時間以上(一般に12時間以上)まで決定されない現在のASTは、多くの場合、抗菌効果の速度の差を識別する能力を失う:微生物を直ちに死滅させる抗菌剤は、4時間以内に死滅させたものと12時間後に死滅させたものとが同じに見える。
表1は、2時間のインキュベーション後の細菌の数への種々の処理の効果を推定する。30分の倍加時間を仮定すると、未処理対照は16倍増加するはずである。MICより上の「強力な」抗菌剤(例えば細菌に対して効果を有するものと定義される)による処理群は、微生物の最小限の増殖及び、殺菌性抗菌剤の場合は、微生物の死滅をもたらすはずである。したがって、出発濃度よりも少ない細菌が予想される。MIC未満の「強力な」抗菌剤による処理群は、抗菌剤なしの対照と同等又はこれより少ない微生物増殖をもたらすはずである。この場合細菌を死滅させるのに2時間以上を要するものと定義される(例えば静菌性抗菌剤の場合のように)、遅効性抗菌剤は、出発濃度と16倍増加との間でシグナルを生じる。
5x105CFU/mlの細菌の出発濃度は、微量液体希釈技術についての、Marie B.Coyleを調整編集者とするアメリカ微生物学会のManual of Antimicrobial Susceptibility Testing(C)2005に示されている。各ウェルは約100μLを含むので、1ウェルにつき約5×104個の細菌が存在する。標準的な蛍光色素は、約0.1nM濃度で定量可能になり始め、これは約1.2×1010分子に相当する。したがって、30分の倍加時間の細菌が2時間後に可視であるためには、個々の細菌を1.5×104の蛍光分子で標識しなければならない。蛍光バックグラウンドや非特異的結合などの実際的な考慮事項は、この数を数桁増加させ得る。標準的な光検出器との互換性を可能にするために、より低濃度で検出可能なシグナルを生成する化学及び/又は生化学増幅剤を使用することが有利であり得る。
理論に拘束されることを望むものではないが、本発明は、一部には、微量液体希釈法の原理に基づく。評価する培養物を、最も好ましくは1~10×105CFU/mlに希釈し、MICが抗菌剤の適切なパネルについて決定できるように、異なる濃度の異なる抗菌剤を含むウェルに導入する。次いで、細菌を増殖させるために、プレートを適切な温度、最も好ましくは31~37℃のインキュベータに、適切な条件下で、最も好ましくは好気的条件下で、導入する。この時間に、微生物は増殖することができる。
ブイヨンは、カチオン調整ミューラーヒントンブロスであってもよく、溶解ウマ血液などの微生物増殖のため及び/又は高塩化ナトリウム濃度などの抗菌効果を測定するために有利であることが当業者に公知である追加の補助剤を含有してもよい。この増殖期間中、マイクロプレートを撹拌してもよく、これは、各ウェル中の栄養素及び/若しくはガス交換及び/若しくは抗菌剤を分散させるため、並びに/又はバイオフィルム形成を減少させるために有利であり得る。
AST開始の0~8時間(最も好ましくは0~4時間)以内に、公知の量のシグナル伝達剤を各ウェルに添加する。試薬(シグナル発生剤を含む)の添加は、自動化された機器若しくは半自動化された機器によって実施してもよく、又は手動で実施してもよい。
シグナル伝達剤(「粘着性amp」と称され得る)は、微生物に結合することができる部分(例えば微生物表面に結合する抗体及び/若しくはレクチン、荷電した部分及び/又は微生物表面に非特異的に結合する機能性部分)並びにシグナルを提供する又はシグナルの生成に寄与することができる化学的部分(例えば酵素ケミルミノフォア及びランタニドキレート)を含む。例示的な酵素には、ホースラディッシュペルオキシダーゼ、アルカリホスファターゼ、アセチルコリンエステラーゼ、グルコースオキシダーゼ、β-D-ガラクトシダーゼ、β-ラクタマーゼ及びこれらの組み合わせが含まれる。
本明細書で使用される場合、シグナル発生剤は、1つ以上の「微生物受容体」に結合した1つ以上の化学的部分(すなわち「シグナル発生剤」)を含み得る。シグナル発生剤には、1つ以上の触媒(酵素、金属酸化物ナノ粒子、有機金属触媒、シグナル増幅用に設計されたナノ粒子(本出願が優先権を主張し、これらの全体が参照により本明細書に組み込まれる米国仮特許出願に記載されているものなど)、シグナル生成要素を含むバクテリオファージ、フルオロフォア(有機フルオロフォア、ユウロピウム若しくはルテニウム(II)、レニウム(I)、パラジウム(II)、白金(II)含有有機金属を含む)、及び/又は比色色素(例えば有機「染料」を含む)が含まれるが、これらに限定されない。ナノ粒子、デンドリマー並びに/又は酵素、フルオロフォア及び/若しくは有機金属分子を有する他のナノスケール構造体などの、上記の組み合わせを使用し得る。
シグナル伝達剤を微生物に接触させる前に、シグナル伝達剤が微生物に最初に接触する間に、又はシグナル伝達剤が微生物に接触した後に、化学的部分をシグナル伝達剤に結合させ得る。
微生物を含むAST希釈液にシグナル伝達剤を添加する場合、シグナル伝達剤受容体(例えば微生物に特異的又は非特異的に結合することができる部分)は、微生物表面と会合する。したがって、例えば無傷の微生物が多いほど、これらの細菌と会合するより多数のシグナル伝達剤が溶液中に存在する。この結果として、無傷の細菌の数と、無傷の細菌によって結合されないものによって定義される、溶液中に「遊離」しているシグナル伝達剤の数との間には、逆の相関がある。例えば抗菌剤処理に応答して微生物が溶解する場合、遊離シグナル伝達剤は可溶性微生物成分に結合し得ることに留意されたい。
微生物表面と会合する及び/又は微生物表面にインターカレートするシグナル伝達剤の数は、微生物の表面積に比例する。微生物の表面積は真に耐性の微生物と強く関連する。特に、MIC及びサブMIC未満の濃度の抗菌剤に応答して膨潤又は伸長する微生物(例えばフィラメント形成細菌)の場合、代謝及び/又は体積同定は、6時間未満のものと定義される、「迅速な」ASTの時点について誤った感受性プロフィールを与えることが公知である。この制限を克服するために、本発明は、微生物表面積(体積ではなく)を測定可能なシグナル、最も好ましくは光シグナルに変換する。本発明の方法は、6時間未満で微生物の耐性プロフィールを正確に決定することができる。
微生物と会合した及び/又は微生物にインターカレートしたシグナル伝達剤を遊離シグナル伝達剤から分離するために、1つ以上の分離及び/又は競合的結合工程を実施することが必要であり得る。このような工程には、遠心分離(例えばg力>500×gで)、ろ過(例えば0.45ミクロン以下、好ましくは0.2ミクロン以下の細孔を有するフィルタによって)、電気泳動及び/又は磁気捕捉が含まれるが、これらに限定されない;このような工程は当業者に周知である。
シグナル伝達剤の結合を促進する及び/又はバックグラウンドを低減するために、シグナル伝達剤を添加する前に、インキュベーションの間微生物が懸濁されていた液体から微生物を分離することがさらに有利であり得る。このような分離には、遠心分離、ろ過、電気泳動及び/又は磁気捕捉が含まれ得るが、これらに限定されない。
これらのデータを処理群にわたって比較すると、現在使用されているAST測定と同様の工程を用いて、微生物の耐性プロフィールを決定し得る。さらに、これらのデータは、抗菌効果の速度又は死滅動態の決定を可能にし得る。
シグナル伝達剤は、ASTインキュベーション期間全体にわたって存在するように、微生物及び/又は抗菌剤と共に添加され得る。この合計時間は、24時間までであり得るが、好ましくは8時間以内、より好ましくは5時間以内である。又は、シグナル伝達剤は、所定のインキュベーション期間後に微生物及び抗菌剤に添加され得る。この期間は、24時間までであり得るが、好ましくは8時間以内、より好ましくは4時間以内である。
シグナル伝達剤は、壁及び/又は膜を含む微生物表面と会合する及び/又は微生物表面にインターカレートするように設計される。会合のために設計されたシグナル伝達剤は、1つ以上の抗体、レクチン、他のタンパク質、1つ以上の荷電した化学基を有する小分子、1つ以上の機能的化学基を有する小分子、ファージ、糖タンパク質、ペプチド、アプタマー、荷電小分子、固定電荷を有する小分子、荷電ポリマー、固定電荷を有する荷電ポリマー、疎水性小分子、荷電ペプチド、固定電荷を有する荷電ペプチド、交互の親水性領域と疎水性領域を有するペプチド、及び/又は有機金属錯体であってもよく若しくは有機金属錯体でなくてもよい小分子配位子を含むがこれらに限定されない結合部分を含む。微生物会合のために設計された分子は、当業者に周知である。シグナル伝達剤は、微生物に結合したままでもよく、及び/又はインターナライズされてもよく、したがってすべての会合が含まれる。インターカレーションのために設計されたシグナル伝達剤は、疎水性小分子、疎水性ペプチド、及び/又は交互の疎水性領域と親水性領域を有するペプチドを含み得るが、これらに限定されない。微生物のインターカレーションのために設計された分子は、当業者に周知である。シグナル伝達剤は、さらに、1つ以上の種類の微生物に特異的であり得る。シグナル伝達剤は複数の受容体を有し得る。これらは、結合を強化し得る及び/又は細菌を「凝集させる」のにさらに役立ち得る、2つ以上の微生物への同時結合を可能にし得る。シグナル伝達剤の添加の前に又は添加と同時に、溶液のpHを調整することが有利であり得る。これは、微生物とシグナル伝達剤との間の電荷-電荷相互作用を増強するために有益であり得る。微生物のアニオン電荷は、溶液のpHを中性より上(より塩基性)に滴定することによって増加させ得る。したがって、1以上の固定されたカチオン電荷を有する部分を利用することが有益であり得る。
シグナル伝達剤が、微生物に特異的に結合し得るか(例えば微生物種又は微生物株に特異的に結合する抗体)、又は微生物に非特異的に結合し得る(例えば一般的な共有結合又は非共有結合の形成及び当技術分野で公知の別の非特異的化学会合によって)ことは注目すべきである。
シグナル伝達剤は、天然の微生物表面に結合することが好ましい。
又は、シグナル伝達剤と会合することができる化学物質及び/又は生化学物質を、インキュベーション中に化学物質及び/又は生化学物質が微生物に取り込まれるように、増殖の間微生物が懸濁される液体に添加し得る。これは、微生物とのシグナル伝達剤の会合を増強するのに役立ち得る。代替実施形態では、シグナル伝達剤自体が、インキュベーションの間微生物が懸濁される液体中に存在してもよく、増殖中に微生物に取り込まれてもよい。
好ましくは、シグナル伝達剤は、それぞれの無傷微生物からのシグナルが、各微生物と会合したシグナル伝達剤の数を超えて増幅され得るように、増幅シグナル発生剤を含む。例えば、酵素ホースラディッシュペルオキシダーゼ(HRP)は、シグナルを>1×104倍増幅できることが公知である。したがって、100個のHRP分子が各微生物表面に結合している場合、106の増幅が達成され得る。これは、さもなければ区別できない微生物濃度の識別を可能にすることにより、AST測定が行われ得る速度を増加させ得る。ユウロピウム製剤の使用は、同様にシグナル増幅を提供する。
又は、シグナル伝達剤は、細胞膜などの疎水性領域へのインターカレーションの際に蛍光発光を大きく増加させるように設計された「膜色素」として当業者に公知の光学色素前駆体を含み得る。これらのシグナル伝達剤を用いて設計されたアッセイは、光学的に容易に測定されるのに十分なシグナルを生成するために、微生物をより小さな体積に濃縮し、平面に近づけることを必要とし得る。干渉種は、近赤外フルオロフォアの使用を必要とし得る。
可能性のある分離技術には、ろ過(例えば0.45ミクロン以下、好ましくは0.2ミクロン以下の細孔を有するフィルタによって)、遠心分離(例えばg力>500xg)、電気泳動、誘電泳動及び磁気捕捉が含まれるが、これらに限定されない。これらの技術は、フィルタに固着し、遠心分離機でペレット化され、並びに/又は電気泳動的及び/若しくは磁気的に分離される、微生物と会合したシグナル伝達剤を、溶液中に遊離しているシグナル伝達剤から分離するために使用される。遊離シグナル伝達剤は、フィルタを通過し(「ろ液」)、遠心分離又は磁気分離後に溶液中に残存し(「上清」)、及び/又は電気泳動的に別々に泳動する。遠心分離は、標準、密度勾配又は分画遠心分離であり得る。磁気分離は、微生物と会合又は結合するように特異的に標的化された1つ以上の磁性粒子の添加を必要とし得る。これらは、シグナル伝達剤の添加の前に又は同時に添加され得る。
このような分離技術はまた、抗菌剤処理に応答して形態を変化させ、測定を混乱させ得る微生物をも単離し得る。このような微生物の一例は、抗菌剤処理に応答して最初に伸長する糸状菌である。この増殖形態は当業者に公知である。本明細書に記載の分離技術を使用して、アッセイから糸状菌を単離し、除外することは、得られる結果の精度を高める。
微生物の分離は、微生物種との粒子の会合によって増強され得る。例えば、磁気分離の場合、磁気ビーズは微生物と(特異的又は非特異的に)会合し得る。磁気ビーズ表面上に存在する部分は、微生物の、シグナル伝達剤と同じ表面(若しくはこの生体分子)又は異なる表面(若しくはこの生体分子)に結合し得る。磁気ビーズは、シグナル伝達剤と同じ及び/又は異なる部分を有し得る。例えば、シグナル伝達剤がE.コリ(E.coli)に結合する抗体を含む場合、磁気ビーズは同じ抗体で官能基化され得る。他の例では、シグナル伝達剤は、微生物に結合するモチーフを含み得、磁気ビーズは、微生物に非特異的に結合するように官能基化される。
磁気ビーズと会合した1つ以上の結合部分は、シグナル伝達剤と会合した化学的部分又はシグナル伝達剤の化学的部分と同一であってもよく又は異なっていてもよい。
磁気ビーズと会合した1つ以上の結合部分は、微生物とシグナル伝達剤の結合の前、結合と同時、又は結合後に微生物に結合し得る。
磁気ビーズと会合した1つ以上の結合部分は、微生物を沈殿させる1つ以上のポリマーと会合し得る。微生物を沈殿させる1つ以上のポリマーは、カチオン性であり得る。微生物を沈殿させる1つ以上のポリマーは、ポリ(エチレングリコール)であり得る。
磁気ビーズは、当業者に公知のように、20nm~20ミクロンのサイズ範囲であり得る。
分離後、微生物分離後に残存するシグナル伝達剤の数及び/又は微生物分離中に除去されたシグナル伝達剤(「遊離」シグナル伝達剤)の数を測定するための1つ以上のアッセイを実施し得る。遊離シグナル伝達剤のアッセイを実施すると、微生物濃度に反比例するシグナルが得られる。この場合、微生物と会合するシグナル伝達剤は、微生物によって結合され得るか又はインターナライズされ得る。又は、微生物と会合したシグナル伝達剤についてアッセイを実施し得る。この場合、微生物が特異的に溶解されない限り、結合シグナル伝達剤のみがシグナルに寄与する。
分離効率を最大にするために、すなわち残存する遊離シグナル伝達剤の数を最小限に抑えるために、1回以上の洗浄工程を実施し得る。これらは、ろ過、磁気捕捉若しくは電気泳動の場合のように連続的あってもよく、及び/又は遠心分離若しくは磁気捕捉の場合のように不連続的であってもよい。
代替実施形態では、シグナル伝達剤は洗浄を必要としないと考えられる。これは、「膜色素」シグナル伝達剤を使用する場合に当てはまり得る。微生物膜にインターカレートされていない分子は、インターカレートされた種よりも有意に低い光学活性を有するので、したがって洗浄を必要としないと考えられる。
シグナル伝達剤を微生物に添加する前に、1回以上の洗浄を実施し得る。これらの洗浄は、例えば、インキュベーションの間微生物が懸濁された液体中に存在する干渉種を除去し得る。
実施形態では、洗浄は実施しない。
シグナルの展開は、「展開液」の添加を必要とし得る。触媒を含むシグナル伝達剤の場合、展開液は、光学的及び/又は電気的に活性なシグナル伝達分子に変換され得る1つ以上のシグナル前駆体を含み得る。ナノ粒子内などの、カプセル化された分子を含むシグナル伝達剤の場合、展開液は、カプセル化された種を放出するための1つ以上の試薬を含み得る。展開液の添加後の所定の時間に、比色及び/又は電気化学的シグナルを測定し得る。このようなシグナルには、吸光度、蛍光、時間分解蛍光、化学発光、電気化学発光、電流測定、ボルタンメトリ、インピーダンス及び/又はインピーダンス分光法が含まれるが、これらに限定されない。次に、現在のASTプロトコルと同様に、データを比較してAST及びMICを決定し得る。
実施形態では、シグナルレベルを決定することは、無傷の微生物と会合したシグナルレベルを測定することを含む。代替的又は追加的に、シグナルレベルを決定することは、無傷の微生物に会合していないシグナルレベルを測定することを含む。
これらの工程は、培養物、継代培養物、陽性血液培養物、試料から直接実施され得る。微生物を濃縮する及び/又は潜在的な干渉種を除去する処理は、ASTの前又はシグナル伝達剤の添加前に実施し得る。
シグナル伝達剤はまた、勾配拡散などのAST測定のためのプレートベースの方法と共に使用し得る。これらは、微生物をプレートに添加するのと同時に又は設定されたインキュベーション期間後に添加し得る。これらの場合、光及び/又は電気シグナルについての空間情報が重要である。このアプローチでは、空間情報を保持するために、無傷の微生物に結合したシグナル伝達剤のアッセイが好ましいと考えられる。この場合、遊離シグナル伝達剤を除去するために、展開液の添加前に1回以上の洗浄工程を実施し得る。
実施形態では、洗浄は実施しない。
又は、シグナル伝達剤は、細菌によって取り込まれるように設計することができ、これは、例えばバクテリオファージの使用によって達成され得る。このような方法では、遊離シグナル伝達剤についてのアッセイを実施する。
又は、ニトロセルロース紙で標準的であるようなブロット転写アプローチを用いて細菌又は遊離シグナル伝達剤を転写し、次いで、ブロットした紙に関して空間アッセイを実施し得る。
シグナル伝達剤が結合の際にシグナルを生成する場合、分離工程は必要ないと考えられる。又は、シグナル伝達剤が結合の際に特定の展開液成分に感受性又は耐性になる場合は、分離工程を含まない方法を達成し得る。
最終的なMIC及び/又はQSR出力データは、本明細書に記載のアッセイによって生成されたデータから直接ユーザーによって解釈され得る。又は、これらのデータは、MIC及び/又はQSRを生成するための1つ以上のアルゴリズムによって処理されてもよい。報告されたMIC及び/又はQSR値は、本明細書に記載されるアッセイの1つ以上から導かれ得るか、又は代謝色素指示薬アッセイ、pH指示薬アッセイ、核酸アッセイ及びATPアッセイを含むがこれらに限定されない、微生物増殖についての1つ以上の公知のアッセイと共に、本明細書に記載されるアッセイの1つ以上から導かれ得る。
本発明の方法
本発明の一態様は、微生物の抗菌剤感受性を決定するための方法である。この方法は、微生物の増殖を促進する条件下で、抗菌剤及び微生物の表面に結合することができるシグナル伝達剤の存在下に微生物の液体懸濁液をインキュベートする工程、シグナル伝達剤によって結合された微生物を非結合シグナル伝達剤から分離する工程、並びに1つ以上の対照と比較して微生物に関連するシグナルレベルを決定し、これにより微生物の抗菌剤感受性を決定する工程を含む。
本発明の別の態様は、微生物の抗菌剤感受性を決定するための方法である。この方法は、微生物の増殖を促進する条件下で抗菌剤の存在下に微生物の液体懸濁液をインキュベートする工程、微生物の表面に結合することができるシグナル伝達剤を添加する工程、シグナル伝達剤によって結合された微生物を非結合シグナル伝達剤から分離する工程、1つ以上の対照と比較して微生物に関連するシグナルレベルを決定し、これにより微生物の抗菌剤感受性を決定する工程を含む。実施形態では、シグナル伝達剤の添加は、インキュベーション工程の前若しくは工程の間に行われるか、又はインキュベーション工程の後にシグナル伝達剤の添加が行われる。
本発明の別の態様は、微生物の抗菌剤感受性を決定するための方法である。この方法は、微生物の増殖を促進する条件下で、1つ以上の抗菌剤をそれぞれ含有する複数のチャンバを含むカートリッジ内で微生物の液体懸濁液をインキュベートする工程、微生物の表面に結合することができるシグナル伝達剤を複数のチャンバに添加する工程、非結合シグナル伝達剤を除去する工程、及び1つ以上の対照と比較して複数のチャンバにおけるシグナルレベルを決定し、これにより1つ以上の抗菌剤に対する微生物の感受性を決定する工程を含む。実施形態では、カートリッジは、抗菌剤を含まない又は微生物が感受性でない1つ以上の抗菌剤を含まない1つ以上の対照チャンバ(例えば少なくとも2、4、6、8、12、24、48、96、192、384、1536又はこれ以上のチャンバ)をさらに含む。
上記の態様の実施形態では、微生物の表面への結合は非特異的であり、例えば非共有結合相互作用を含み、共有結合を形成することによる。
上記態様の実施形態では、シグナル伝達剤は、微生物の表面に結合することができる化学基及び/又は生化学基を含んでもよく、表面は、膜、壁、タンパク質、細胞小器官、糖類、脂質、細胞エンベロープ及び/又は核酸の1つ以上を含む。
上記態様の実施形態では、シグナル伝達剤は、微生物の表面の生体分子に結合することができる化学基及び/又は生化学基を含んでもよく、表面生体分子は、ペプチドグリカン、ムレイン、マンノプロテイン、ポーリン、β-グルカン、キチン、糖タンパク質、多糖、リポ多糖、リポオリゴ糖、リポタンパク質、内毒素、リポテイコ酸、テイコ酸、脂質A、炭水化物結合ドメイン、流出ポンプ、他の細胞壁及び/又は細胞膜関連タンパク質、他のアニオン性リン脂質、並びにこれらの組み合わせから選択される。
上記態様の実施形態では、シグナル伝達剤は、シグナル増幅剤及び微生物の表面に非特異的に結合することができる1つ以上の化学的部分を含み得る。
本発明の別の態様は、微生物の抗菌剤感受性を決定するための方法である。この方法は、微生物の増殖を促進する条件下で抗菌剤及びシグナル増幅剤と微生物の表面に非特異的に結合することができる1つ以上の化学的部分とを含むシグナル伝達剤の存在下にて微生物をインキュベートすること、シグナル伝達剤によって結合された微生物を非結合シグナル伝達剤から分離すること、並びに1つ以上の対照と比較して微生物に関連するシグナルレベルを決定し、これにより微生物の抗菌剤感受性を決定することを含む。
本発明の別の態様は、微生物の抗菌剤感受性を決定するための方法である。この方法は、微生物の増殖を促進する条件下で抗菌剤の存在下にて微生物をインキュベートすること、シグナル増幅剤と微生物の表面に非特異的に結合することができる1つ以上の化学的部分とを含むシグナル伝達剤を添加すること、シグナル伝達剤によって結合された微生物を非結合シグナル伝達剤から分離すること、及び1つ以上の対照と比較して微生物に関連するシグナルレベルを決定し、これにより微生物の抗菌剤感受性を決定することを含む。実施形態では、シグナル伝達剤は、インキュベーション工程の開始前、開始時又は工程の間、好ましくはインキュベーション工程の間に生じる。実施形態では、微生物を液体懸濁液中でインキュベートする。
上記態様の実施形態では、液体懸濁液は、生物学的試料から増殖させた微生物単離物を液体培地に接種することによって調製し得る。
上記態様の実施形態では、微生物の液体懸濁液は、未処理生物学的試料、例えば培養工程を経ていない未処理生物学的試料から調製し得る。
上記態様の実施形態では、微生物の液体懸濁液は、培養又は処理された生物学的試料から調製され得る。
上記態様の実施形態では、生物学的試料は、血液、脳脊髄液、尿、便、膣試料、痰、気管支肺胞洗浄液、咽喉、鼻/創傷スワブ、及びこれらの組み合わせから選択される。
上記態様の実施形態では、この方法は、インキュベーション前又はインキュベーション中に固体表面上で微生物を捕捉する工程を含まない。
上記態様の実施形態では、この方法は、インキュベーション工程中又は工程後に固体表面上で微生物を増殖させる工程を含まない。
上記態様の実施形態では、インキュベーションは、微生物の液体懸濁液を撹拌することを含み得る。
上記態様の実施形態では、微生物の液体懸濁液は、インキュベーションの間、機械、超音波及び/又は磁気撹拌によって連続的又は不連続的に撹拌され得る。
上記態様の実施形態では、インキュベーションは31~37℃で行われる。本発明と現在使用されているASTシステムとの比較
本発明は、一部には現在使用されているAST法よりも有意に短い時間で正確なAST結果を提供するため、現在使用されているAST法より優れている。
現在臨床で使用されている3つの自動ASTシステムは、BioMerieuxのVitek2、Beckman DickinsonのPhoenix及びBeckman-CoulterのMicroScanである。現在使用されているASTシステムと本発明における工程の比較を図3に示す。本発明で述べる方法は、少なくとも2つの様式で実施され得る。最初の様式は標準的な分離株用であり、現在の検査室のワークフローに変更はない。2番目は、陽性血液培養物から直接の様式である。
標準的な単離物処理に関して、本発明は既存の臨床検査室ワークフローと適合性であり、したがって変更を必要としない。図3の「工程8」に示すように、コロニー単離(工程6)及び微生物濃度の標準化(工程7)後に現在の感受性(AST)試験を実施する。このワークフローでは、本発明は現在のシステムを「工程8」で置き換える。本発明によるAST結果は、医療従事者のシフト内(<5時間)に入手可能であるので、有用性は、患者が最適化された治療を受ける(工程9)速度を実際上最大1日まで高め得る。自動化は、「工程7」及び、潜在的に、ワークフローのさらなる工程を含むように設計され得る。このような自動化は当業者に公知である。図3は、血液試料についてのワークフローを示すことに留意されたい。尿やスワブなどの多くの試料タイプは、プレートに直接画線接種し得る(工程4)。この場合、工程6でグラム染色を実施し得る。
血液検査のために、現在使用されているASTシステムは、得られた血液培養物が検出可能に陽性になること(10時間以上かかる)、続いて継代培養工程(少なくとも12時間)、次いでAST試験(最低8時間を要する)を必要とする:これは、病原体に応じて合計48時間を要し、しばしば実際には3日以上かかる。ほとんどのワークフローでは、生物の同定は継代培養工程後に行われ、ますます質量分析によって実施されるようになりつつある。臨床医又は薬剤師が適切な標的化抗菌剤を処方するためには同定とAST結果の両方が必要であるので、AST結果へのこの遅延は、広域スペクトル抗菌剤の治療期間を直接延長する。さらに、待機は、しばしば、多くの臨床微生物学研究室で一般的なワンシフト操作によってさらに延長される。
又は、本発明は、陽性血液培養物から直接使用され得る。採血及びインキュベーション/培養の標準的な工程1及び工程2の後、培養物が陽性であれば、培養物の瓶は直ちに微生物単離(工程3)へと移動し、次いで自動化システム(工程4)に進む。本発明は完全に自動化することができ、技術者は、微生物希釈液を含む標準カートリッジをシステムに装填し、次いで4時間の「高速AST」法を開始するだけでよい。次いで、検査技師は、最小阻害濃度(「MIC」)のASTについて同じ標準的な表現型結果を受け取る。しかし、合理化された方法は、ASTの時間を理論的には24時間以上、潜在的には実際上2日間短縮し、検査室のワークフローを簡略化する。
現在使用されているASTシステムは、Clinical Laboratory Standards Institute(CLSI)の微量液体希釈法の変形を実施する。細菌を複数のウェルに並行して接種する。各々のウェルは、公知濃度の1つの(又はこれ以上の)抗菌剤及び栄養ブロスを含む。細菌が対数増殖期にあることを確実にするためにウェルに5×105CFU/mlで接種する。これは抗菌剤に対する正確な応答を検出するために重要である。次いで、微生物検出を視覚的に実施する。
表現型AST試験の緩やかな速度は、一部には、検出可能な光シグナルを生成するために微生物増殖に依存することによる。細菌は、約1×108CFU/mlの濃度より低い光学密度測定によっては定量化することができないので、CLSI出発濃度は最低8倍の倍加時間では目に見えない。最も緩やかに増殖するウェルにおける微生物増殖を全く増殖しないウェルから識別することは最小阻害濃度(MIC)の決定にとって極めて重要であるので、有意により長い時間が必要である。当業者に公知のように、いくつかの既存のプラットフォームは、インキュベーションの間微生物が懸濁される液体中に代謝プローブを含めることによってこれらの増殖の問題を克服する。しかし、これらのプローブを含めると、糸状増殖などの増殖形態を見逃すことがあり、結果の精度に影響を及ぼし得る。
AST特異的な工程が開始された後、現在使用されているASTシステムは、依然として、典型的には単純な高感受性細菌の結果を報告するのに8時間以上を要し、複雑な耐性プロフィール又は緩やかな増殖動態を有する病原体については10時間以上を要する;図4参照。
さらに、現在使用されている自動化ASTシステムには、6時間未満で正確な結果を報告するのを妨げる2つの欠点:1)非常に重大なエラーである、真に耐性の菌株に対する不正確な「感受性」コール;及び2)重大なエラーである、真に感受性の菌株に対する不正確な「耐性」コール、がある。実際に、これらの問題により、BioMerieux及びBDは、Vitek2(R)及びPhoenix(R)について当初の4時間という速度の謳い文句を改訂することが必要になった。
非常に重大なエラーの存在は、抗菌剤耐性を達成する際に微生物が消費する代謝エネルギーによって部分的に説明される。耐性微生物は、抗菌剤に応答してエネルギー消費を変化させることがあり、MIC付近の代謝プローブの結果を混乱させ得る。これらはまた、増殖培地中の酸化還元指示薬などの添加剤の存在によっても生じ得る。重大なエラーの頻発は、主として特定の細菌の糸状増殖に起因する。この増殖形式は、グラム陰性菌における、特にβ-ラクタムなどの細胞壁作用性抗菌剤に対する共通の抗菌剤応答である。糸状菌は自らの内部の内容物を複製し続けるが、分離はしない。したがって、再び、代謝プローブは誤ったMIC付近の結果を与えることになる。糸状菌の除去は、AST法の重大なエラーを有意に減少させることが示された。
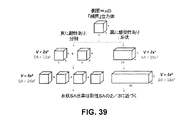
本発明で使用される相対微生物表面積の測定は、ASTの代謝プローブの落とし穴を克服する。第一に、相対的表面積は代謝活性のシフトによって交絡されないので、高速ASTは迅速で正確な耐性コールを可能にする。第二に、表面積測定は過剰な耐性コールを防止する。現在使用されているASTシステムの代謝プローブで得られる体積測定とは対照的に、表面積測定は、真の耐性と糸状増殖との間の正確な区別を可能にする。図39の概略図に示されるように、耐性及び感受性糸状菌の体積は区別することが困難である。しかし、分離の欠如は、真に耐性の細菌のものよりも有意に低い糸状表面積を生じる。したがって、各細菌の表面積を増幅することにより、本発明は、E.コリ(E.coli)試料について4時間のβ-ラクタム(アンピシリン)MICを正確にコールすることができる(以下の実施例参照)。図39に示すように、伸長と「真の」耐性との間の表面積の差は2/3に近く、これは増幅されたシグナルで検出され得る。
患者
本明細書で使用される場合、「患者」という用語(交換可能に「宿主」又は「被験体」とも称される)は、本明細書で論じられるような生物学的試料又は標本の1つ以上の供給源として働くことができる任意の宿主を指す。特定の態様では、ドナーは、任意の動物種(及び好ましくは、ヒトなどの哺乳動物種)を表すことが意図されている、脊椎動物である。特定の実施形態では、「患者」とは、家畜、牧畜又は移住動物又は鳥類、外来種又は動物学的標本、並びにコンパニオン動物、ペット及び獣医師の世話を受けている任意の動物を含むがこれらに限定されない、ヒト及び非ヒト霊長動物、鳥類、爬虫類、両生類、ウシ、イヌ、ヤギ、キャビティ、カラス、エピン、ウマ、ネコ、ヤギ、ラピン、ウサギ、オオカミ、ヒツジ、ブタ、ラシン、キツネ等を含むがこれらに限定されない任意の動物宿主を指す。
生物学的試料
生物学的試料は、微生物、例えば細菌及び真菌細胞を含む任意の試料である。
典型的な生物学的試料には、全血、血漿、血清、痰、尿、便、白血球、赤血球、軟膜、涙、粘液、唾液、精液、膣液、リンパ液、羊水、脊髄又は脳脊髄液、腹膜滲出液、胸水、滲出液、穿刺液、上皮スミア、生検材料、骨髄試料、嚢胞又は膿瘍からの液体、滑液、硝子体液又は房水、眼洗浄又は吸引液、気管支肺胞洗浄液、気管支洗浄液又は肺洗浄液、肺吸引液、並びに肝臓、脾臓、腎臓、肺、腸、脳、心臓、筋肉、膵臓等を含むがこれらに限定されない器官及び組織、スワブ(創傷スワブ、口腔スワブ、咽喉スワブ、膣スワブ、尿道スワブ、子宮頸部スワブ、直腸スワブ、病変スワブ、膿瘍スワブ、鼻咽頭スワブ等を含むがこれらに限定されない)、並びにこれらの任意の組み合わせが含まれるが、これらに限定されない。また、細菌培養物又は細菌単離物、真菌培養物又は真菌単離物も含まれる。当業者はまた、上記の例示的な生物学的試料のいずれかから得られた単離物、抽出物又は物質も本発明の範囲内であることを理解する。
生物学的試料から得られた微生物は、当技術分野において日常的に行われるように培養され得るか、さもなければ処理され得る。
例示的微生物
本明細書で使用される場合、感染は、微生物起源の任意の感染性因子、例えば細菌、真菌細胞、古細菌及び原生動物を含むことが意図されている。好ましい例では、感染因子は細菌、例えばグラム陽性菌、グラム陰性菌及び非定型細菌である。「抗菌剤耐性微生物」という用語は、1つ以上の異なる抗菌剤、すなわち抗菌薬、抗真菌薬、抗古細菌薬及び抗原生動物薬に耐性である微生物(例えば細菌、真菌、古細菌及び原生動物)である。
微生物(例えば微生物の液体懸濁液)は、1つの株の微生物を含み得る。微生物は、1つの種の微生物を含み得る。微生物は、2つ以上の株の微生物を含み得る。微生物は、1つの目の微生物を含み得る。微生物は、1つの綱の微生物を含み得る。微生物は、1つの科の微生物を含み得る。微生物は、1つの界の微生物を含み得る。
微生物(例えば微生物の液体懸濁液)は、2つ以上の株の微生物を含み得る。微生物は、2つ以上の種の微生物を含み得る。微生物は、2つ以上の属の微生物を含み得る。微生物は、2つ以上の目の微生物を含み得る。微生物は、2つ以上の綱の微生物を含み得る。微生物は、2つ以上の科の微生物を含み得る。微生物は、2つ以上の界の微生物を含み得る。
微生物は細菌であり得る。細菌の例には、アセトバクター・アウランティウス(Acetobacter aurantius)、アシネトバクター・ビチューメン(Acinetobacter bitumen)、アシネトバクター属種(Acinetobacter spp.)、アクチノミセス・イスラエリ(Actinomyces israelii)、アクチノミセス属種(Actinomyces spp.)、アエロコッカス属種(Aerococcus spp.)、アグロバクテリウム・ラジオバクター(Agrobacterium radiobacter)、アグロバクテリウム・ツメファシエンス(Agrobacterium tumefaciens)、アナプラズマ(Anaplasma)、アナプラズマ・ファゴサイトフィルム(Anaplasma phagocytophilum)、アゾリゾビウム・カウリノダンス(Azorhizobium caulinodans)、アゾトバクター・ビネランディ(Azotobacter vinelandii)、バチルス(Bacillus)、バチルス・アントラシス(Bacillus anthracis)、バチルス・ブレビス(Bacillus brevis)、バチルス・セレウス(Bacillus cereus)、バチルス・フシフォルミス(Bacillus fusiformis)、バチルス・リケニフォルミス(Bacillus licheniformis)、バチルス・メガテリウム(Bacillus megaterium)、バチルス・マイコイデス(Bacillus mycoides)、バチルス属種(Bacillus spp.)、バチルス・ステアロサーモフィルス(Bacillus stearothermophilus)、バチルス・サブチリス(Bacillus subtilis)、バチルス・チューリンゲンシス(Bacillus thuringiensis)、バクテロイデス(Bacteroides)、バクテロイデス・フラギリス(Bacteroides fragilis)、バクテロイデス・ギンギバリス(Bacteroides gingivalis)、バクテロイデス・メラニノゲニカス(Bacteroides melaninogenicus)(プレボテラ・メラニノゲニカ(Prevotella melaninogenica)としても公知である)、バルトネラ(Bartonella)、バルトネラ・ヘンセレ(Bartonella henselae)、バルトネラ・クインターナ(Bartonella quintana)、バルトネラ属種(Bartonella spp.)、ボルデテラ(Bordetella)、ボルデテラ・ブロンキセプチカ(Bordetella bronchiseptica)、ボルデテラ・パータシス(Bordetella pertussis)、ボルデテラ属種(Bordetella spp.)、ボレリア・ブルグドルフェリ(Borrelia burgdorferi)、ブルセラ(Brucella)、ブルセラ・アボルタス(Brucella abortus)、ブルセラ・メリテンシス(Brucella melitensis)、ブルセラ属種(Brucella spp.)、ブルセラ・スイス(Brucella suis)、バークホルデリア(Burkholderia)、バークホルデリア・セパシア(Burkholderia cepacia)、バークホルデリア・マレイ(Burkholderia mallei)、バークホルデリア・シュードマレイ(Burkholderia pseudomallei)、カリマトバクテリウム・グラヌロマティス(Calymmatobacterium granulomatis)、カンピロバクター(Campylobacter)、カンピロバクター・コリ(Campylobacter coli)、カンピロバクター・フェタス(Campylobacter fetus)、カンピロバクター・ジェジュニ(Campylobacter jejuni)、カンピロバクター・ピロリ(Campylobacter pylori)、カンピロバクター属種(Campylobacter spp.)、クラミジア(Chlamydia)、クラミジア属種(Chlamydia spp.)、クラミジア・トラコマチス(Chlamydia trachomatis)、クラミドフィラ(Chlamydophila)、クラミドフィラ・ニューモニエ(Chlamydophila pneumoniae)(以前はクラミジア・ニューモニエ(Chlamydia pneumoniae)と呼ばれていた)、クラミドフィラ・シタッシ(Chlamydophila psittaci)(以前はクラミジア・シタッシ(Chlamydia psittaci)と呼ばれていた)、クラミドフィラ属種(Chlamydophila spp.)、クロストリジウム(Clostridium)、クロストリジウム・ボツリナム(Clostridium botulinum)、クロストリジウム・ディフィシル(Clostridium difficile)、クロストリジウム・パーフリンゲンス(Clostridium perfringens)(以前はクロストリジウム・ウェルチ(Clostridium welchii)と呼ばれていた)、クロストリジウム属種(Clostridium spp.)、クロストリジウム・テタニ(Clostridium tetani)、コリネバクテリウム(Corynebacterium)、コリネバクテリウム・ジフテリアエ(Corynebacterium diphtheriae)、コリネバクテリウム・フシフォルメ(Corynebacterium fusiforme)、コリネバクテリウム属種(Corynebacterium spp.)、コキセラ・ブルネッチ(Coxiella burnetii)、エールリヒア・シャフェエンシス(Ehrlichia chaffeensis)、エールリヒア属種(Ehrlichia spp.)、エンテロバクター・クロアカエ(Enterobacter cloacae)、エンテロバクター属種(Enterobacter spp.)、エンテロコッカス(Enterococcus)、エンテロコッカス・アビウム(Enterococcus avium)、エンテロコッカス・デュランス(Enterococcus durans)、エンテロコッカス・フェカリス(Enterococcus faecalis)、エンテロコッカス・フェシウム(Enterococcus faecium)、エンテロコッカス・ガリナルム(Enterococcus galllinarum)、エンテロコッカス・マロラツス(Enterococcus maloratus)、エンテロコッカス属種(Enterococcus spp.)、エシェリキア・コリ(Escherichia coli)、フランシセラ属種(Francisella spp.)、フランシセラ・ツラレンシス(Francisella tularensis)、フソバクテリウム・ヌクレアタム(Fusobacterium nucleatum)、ガルドネレラ属種(Gardenerella spp.)、ガルドネレラ・バギナリス(Gardnerella vaginalis)、ヘモフィルス属種(Haemophilius spp.)、ヘモフィルス(Haemophilus)、ヘモフィルス・デュクレイ(Haemophilus ducreyi)、ヘモフィルス・インフルエンザ(Haemophilus influenzae)、ヘモフィルス・パラインフルエンザ(Haemophilus parainfluenzae)、ヘモフィルス・パータシス(Haemophilus pertussis)、ヘモフィルス・バギナリス(Haemophilus vaginalis)、ヘリコバクター・ピロリ(Helicobacter pylori)、ヘリコバクター属種(Helicobacter spp.)、クレブシエラ・ニューモニエ(Klebsiella pneumoniae)、クレブシエラ属種(Klebsiella spp.)、ラクトバチルス(Lactobacillus)、ラクトバチルス・アシドフィルス(Lactobacillus acidophilus)、ラクトバチルス・ブルガリカス(Lactobacillus bulgaricus)、ラクトバチルス・カゼイ(Lactobacillus casei)、ラクトバチルス属種(Lactobacillus spp.)、ラクトコッカス・ラクチス(Lactococcus lactis)、レジオネラ・ニューモフィラ(Legionella pneumophila)、レジオネラ属種(Legionella spp.)、レプトスピラ属種(Leptospira spp.)、リステリア・モノサイトゲネシス(Listeria monocytogenes)、リステリア属種(Listeria spp.)、メタノバクテリウム・エキストロクエンス(Methanobacterium extroquens)、ミクロバクテリウム・マルチフォルム(Microbacterium multiforme)、ミクロコッカス・ルテウス(Micrococcus luteus)、モラクセラ・カタラリス(Moraxella catarrhalis)、マイコバクテリウム(Mycobacterium)、マイコバクテリウム・アビウム(Mycobacterium avium)、マイコバクテリウム・ボビス(Mycobacterium bovis)、マイコバクテリウム・ジフテリアエ(Mycobacterium diphtheriae)、マイコバクテリウム・イントラセルラーレ(Mycobacterium intracellulare)、マイコバクテリウム・レプラエ(Mycobacterium leprae)、マイコバクテリウム・レプラムリウム(Mycobacterium lepraemurium)、マイコバクテリウム・フレイ(Mycobacterium phlei)、マイコバクテリウム・スメグマチス(Mycobacterium smegmatis)、マイコバクテリウム属種(Mycobacterium spp.)、マイコバクテリウム・ツベルクローシス(Mycobacterium tuberculosis)、マイコプラズマ(Mycoplasma)、マイコプラズマ・ファーメンタンス(Mycoplasma fermentans)、マイコプラズマ・ゲニタリウム(Mycoplasma genitalium)、マイコプラズマ・ホミニス(Mycoplasma hominis)、マイコプラズマ・ペネトランス(Mycoplasma penetrans)、マイコプラズマ・ニューモニエ(Mycoplasma pneumoniae)、マイコバクテリア属種(Mycoplasma spp.)、ナイセリア(Neisseria)、ナイセリア・ゴノレア(Neisseria gonorrhoeae)、ナイセリア・メニンギチジス(Neisseria meningitidis)、ナイセリア属種(Neisseria spp.)、ノカルジア属種(Nocardia spp.)、パスツレラ(Pasteurella)、パスツレラ・ムルトシダ(Pasteurella multocida)、パスツレラ属種(Pasteurella spp.)、パスツレラ・ツラレンシス(Pasteurella tularensis)、ペプトストレプトコッカス(Peptostreptococcus)、ポルフィロッモナス・ギンギバリス(Porphyromonas gingivalis)、プレボテラ・メラニノゲニカ(Prevotella melaninogenica)(以前はバクテロイデス・メラニノゲニカス(Bacteroides melaninogenicus)と呼ばれていた)、プロテウス属種(Proteus spp.)、シ
ュードモナス・アエルギノーサ(Pseudomonas aeruginosa)、シュードモナス属種(Pseudomonas spp.)、リゾビウム・ラジオバクター(Rhizobium radiobacter)、リケッチア(Rickettsia)、リケッチア・プロワツェキイ(Rickettsia prowazekii)、リケッチア・シタッシ(Rickettsia psittaci)、リケッチア・クインターナ(Rickettsia quintana)、リケッチア・リケッチイ(Rickettsia rickettsii)、リケッチア属種(Rickettsia spp.)、リケッチア・トラコマエ(Rickettsia trachomae)、ロシャリメア(Rochalimaea)、ロシャリメア・ヘンセラ(Rochalimaea henselae)、ロシャリメア・クインターナ(Rochalimaea quintana)、ロシア・デントカリオーサ(Rothia dentocariosa)、サルモネラ(Salmonella)、サルモネラ・エンテリティディス(Salmonella enteritidis)、サルモネラ属種(Salmonella spp.)、サルモネラ・ティフィ(Salmonella typhi)、サルモネラ・ティフィムリウム(Salmonella typhimurium)、セラチア・マルセッセンス(Serratia marcescens)、シゲラ・ディセンテリアエ(Shigella dysenteriae)、シゲラ属種(Shigella spp.)、スピリルム・ボルタンス(Spirillum volutans)、スタフィロコッカス(Staphylococcus)、スタフィロコッカス・アウレウス(Staphylococcus aureus)、スタフィロコッカス・エピデルミディス(Staphylococcus epidermidis)、スタフィロコッカス属種(Staphylococcus spp.)、ステノトロフォモナス・マルトフィラ(Stenotrophomonas maltophilia)、ステノトロフォモナス属種(Stenotrophomonas spp.)、ストレプトコッカス(Streptococcus)、ストレプトコッカス・アガラクチア(Streptococcus agalactiae)、ストレプトコッカス・アビウム(Streptococcus avium)、ストレプトコッカス・ボビス(Streptococcus bovis)、ストレプトコッカス。クリセツス(Streptococcus cricetus)、ストレプトコッカス・フェシウム(Streptococcus faceium)、ストレプトコッカス・フェカリス(Streptococcus faecalis)、ストレプトコッカス・フェラス(Streptococcus ferus)、ストレプトコッカス・ガリナルム(Streptococcus gallinarum)、ストレプトコッカス・ラティス(Streptococcus lactis)、ストレプトコッカス・ミティオール(Streptococcus mitior)、ストレプトコッカス・ミティス(Streptococcus mitis)、ストレプトコッカス・ミュータンス(Streptococcus mutans)、ストレプトコッカス・オラリス(Streptococcus oralis)、ストレプトコッカス・ニューモニエ(Streptococcus pneumoniae)、ストレプトコッカス・ピオゲネス(Streptococcus pyogenes)、ストレプトコッカス・ラッタス(Streptococcus rattus)、ストレプトコッカス・サリバリウス(Streptococcus salivarius)、ストレプトコッカス・サンギス(Streptococcus sanguis)、ストレプトコッカス・ソブリヌス(Streptococcus sobrinus)、ストレプトコッカス属種(Streptococcus spp.)、トレポネーマ(Treponema)、トレポネーマ・デンティコーラ(Treponema denticola)、トレポネーマ・パリダム(Treponema pallidum)、トレポネーマ属種(Treponema spp.)、ウレアプラズマ属種(Ureaplasma spp.)、ビブリオ(Vibrio)、ビブリオ・コレラ(Vibrio cholerae)、ビブリオ・コンマ(Vibrio comma)、ビブリオ・パラヘモリチカス(Vibrio parahaemolyticus)、ビブリオ属種(Vibrio spp.)、ビブリオ・バルニフィカス(Vibrio vulnificus)、ストレプトコッカス・ヴィリダンス(viridans streptococci)、ウォールバキア(Wolbachia)、エルシニア(Yersinia)、エルシニア・エンテロコリチカ(Yersinia enterocolitica)、エルシニア・ペスティス(Yersinia pestis)、エルシニア・シュードツベルクローシス(Yersinia pseudotuberculosis)及びエルシニア属種(Yersinia spp.)が含まれるが、これらに限定されない。
微生物は真菌であってもよい。真菌の例には、アスペルギルス属種(Aspergillus spp.)、ブラストミセス属種(Blastomyces spp.)、カンジダ属種(Candida spp.)、クラドスポリウム属(Cladosporium)、コクシジオイデス属種(Coccidioides spp.)、クリプトコッカス属種(Cryptococcus spp.)、エキセロヒラム属(Exserohilum)、フザリウム属(fusarium)、ヒストプラスマ属種(Histoplasma spp.)、イサチェンキア属種(Issatchenkia spp.)、ムコールミセテス(mucormycetes)、ニューモシスティス属種(Pneumocystis spp.)、白癬、セドスポリウム(scedosporium)、スポロトリクス属(Sporothrix)及びスタキボトリス属種(Stachybotrys spp.)が含まれるが、これらに限定されない。
微生物は原生動物であってもよい。原生動物の例には、エンタモエバ・ヒストリチカ(Entamoeba histolytica)、プラスモジウム属種(Plasmodium spp.)、ジアルジア・ランブリア(Giardia lamblia)及びトリパノソーマ・ブルセイ(Trypanosoma brucei)が含まれ、これらに限定されない。
例示的な抗菌剤
微生物が細菌である場合、例示的な抗菌剤には、アミカシン、アミノグリコシド、アミノグリコシドアモキシシリン、アミノグリコシド類、アモキシシリン、アモキシシリン/クラブランネート、アンピシリン、アンピシリン/スルバクタム、抗毒素、アルスフェナミン、アジスロマイシン、アズロシリン、アズトレオナム、β-ラクタム、バシトラシン、カプレオマイシン、カルバペネム、カルベニシリン、セファクロール、セフラドキシル、セファレキシン、セファロチン、セファロチン、セファマンドール、セファゾリン、セフジニル、セフジトレン、セフェピム、セフィキシム、セフォペラゾン、セフォタキシム、セフォキシチン、セフポドキシム、セフプロジル、セフタロリン、セフタロリンフォサミル、セフタジジム、セフチブテン、セフチゾキシム、セフトビプロール、セフトリアキソン、セフロキシム、セファロスポリン、クロラムフェニコール、クロラムフェニコール(Bs)、シプロフロキサシン、クラリスロマイシン、クリンダマイシン、クロファジミン、クロキサシリン、コリスチン、コトリモキサゾール、シクロセリン、ダルババンシン、ダプソン、ダプトマイシン、デメクロサイクリン、ジクロキサシリン、ジリスロマイシン、ドリペネム、ドキシサイクリン、エノキサシン、エルタペネム、エリスロマイシン、エタンブトール、エタンブトール(Bs)、エチオナミド、フルクロキサシリン、フルオロキノロン、フルオロキノロン類、ホスホマイシン、フラゾリドン、フシジン酸、ガチフロキサシン、ゲルダナマイシン、ゲミフロキサシン、ゲンタマイシン、グレパフロキサシン、ハービマイシン、イミペネム/シラスタチン、イソニアジド、カナマイシン、レボフロキサシン、リンコマイシン、リネゾリド、ロメフロキサシン、ロラカルベフ、マクロライド系抗生物質、マフェニド、メロペネム、メチシリン、メトロニダゾール、メズロシリン、ミノサイクリン、モキシフロキサシン、ムピロシン、ナフシリン、ナフシリン、ナリジクス酸、ネオマイシン、ネチルミシン、ニトロフラントイン(Bs)、ノルフロキサシン、オフロキサシン、オリタバンシン、オキサシリン、オキシテトラサイクリン、パロモマイシン、ペニシリン、ペニシリンG、ペニシリンV、ピペラシリン、ピペラシリン/タゾバクタム、プラテンシマイシン、ポミキシンB、ポシゾリド、ピラジナミド、キヌプリスチン/ダルフォプリスチン、ラデゾリド、ラキシバクマブ、リファブチン、リファンピシン、リファンピン、リファペンチン、リファキシミン、ロキシスロマイシン、シルバースルファジアジン、スパルフロキサシン、スペクチノマイシン、スペクチノマイシン(Bs)、スピラマイシン、ストレプトグラミン類、ストレプトマイシン、スルバクタム、スルファアセトアミド、スルファジアジン、スルファジメトキシン、スルファメチゾール、スルファメトキサゾール、スルファニルイミド、スルファサラジン、スルファイソオキサゾール、スルホンアミドクリソイジン、テジゾリド、テイコプラニン、テイキソバクチン、テラバンシン、テリスロマイシン、テマフロキサシン、テモシリン、テトラサイクリン、チアンフェニコール、チカルシリン、チカルシリン/クラブランネート、チカルシリン/クラブラン酸、チゲサイクリン、チゲサイクリン(Bs)、チニダゾール、TMP/SMX、トブラマイシン、トレゾリド、トリメトプリム(Bs)、トリメトプリム-スルファメトキサゾール、トロレアンドマイシン、トロバフロキサシン、バンコマイシン及びこれらのジェネリック医薬品又はこれらの変種が含まれる。
微生物との相互作用が微生物表面上の負電荷に影響を及ぼし、微生物表面上の負電荷によって影響を受ける抗菌剤には、以下が含まれる:細胞表面に結合すると、脂質膜成分と架橋するMg2+イオンを置換し、これによって外膜を破壊し、薬剤吸収を増強するポリカチオン性アミノグリコシド;やはり微生物細胞への結合が膜の負電荷に依存性であるため膜の負電荷を減少させることによって突然変異及びプラスミド媒介性耐性が生じるカチオン性ポリミキシン(コリスチン及びポリミキシンB);並びに宿主の自然免疫応答のカチオン性抗菌ペプチドに類似し、膜破壊の作用機構のためにCa2+及びホスファチジルグリセロールを必要とするリポペプチドであって、やはり耐性が細胞表面電荷の変化を含み得る、ダプトマイシン。
微生物が真菌である場合、例示的な抗菌剤には、5-フルオロシトシン、アバファンジン、アルバコナゾール、アリルアミン、アムホテリシンB、アンコボン、アニドゥラファンギン、アゾール、ペルーバルサム、安息香酸、ビフォナゾール、ブトコナゾール、カンジシジン、カスポファンギン、シクロピロクス、クロトリマゾール、クレセンバ、クリスタルバイオレット、ジフルカン、エキノカンジン、エコナゾール、エフィナコナゾール、エポキシコナゾール、フェンチコナゾール、フィリピン、フルコナゾール、フルシトシン、グリフルビンV、グリセオフルビン、グリス-PEG、ハロプロギン、ハマイシン、イミダゾール、イサブコナゾール、イサブコナゾニウム、イソコナゾール、イトラコナゾール、ケトコナゾール、ラミシール、ルリコナゾール、ミカファンギン、ミコナゾール、ナタマイシン、ノキサフィル、ナイスタチン、オモコナゾール、オンメル、オラビグ、オキシコナゾール、ポサコナゾール、プロピコナゾール、ラブコナゾール、リモシジン、セルタコナゾール、スポラノックス、スルコナゾール、テルビナフィン、テルコナゾール、チアゾール、チオカルバメート抗真菌剤、チコナゾール、トルナフテート、トリアゾール、ウンデシレン酸、ブイフェンド、ボリコナゾール及びこれらのジェネリック医薬品又はこれらの変種が含まれる。
微生物が原生動物である場合、例示的な抗菌剤には、8-アミノキノリン、アセタール、アメーバゾア(amoebozoa)に対する作用薬、アイラントン、アモジアキン、アムホテリシンB、アムプロリウム、抗トリコモナス薬、アプラスモマイシン、アルスチノール、アルテリン酸、アルテメテル、アルテメテル/ルメファントリン、アルテミシニン、アルテモチル、アルテロラン、アルテスネート、アルテスネート/アモジアキン、アトバコン、アトバコン/プログアニル、アザニダゾール、アジスロマイシン、ベンズニダゾール、ブロキシキノリン、ブパルバコン、カルバルゾン、カルニダゾール、アセトキノン、アズバキノン、アズニダゾール、アジスロマイシン、ベンズイミダゾール、ブロキシキノリン、ブパルバコン、カルバゾーネ、カルニダゾール、キニオホン、クロロキン、クロルプログアニル、クロルプログアニル/ダプソン、クロルプログアニル/ダプソン/アルテスネート、クロルキナルドール、クロムアルベオレート駆虫薬、キンコナ、シパルガミン、クラズリル、クレファミド、クリオキノール、抗コクシジウム薬、コジネオプシン、コトリファジド、クリプトレピン、シクログアニル、デヒドロエメチン、ジフェタルゾン、ジヒドロアルテミシニン、ジロキサニド、ジミナゼン、ジスルフィラム、ドキシサイクリン、エフロルニチン、ELQ-300、エメチン、エトファミド、エクスカバタ(Excavata)駆虫薬、フマギリン、フラゾリドン、グリコビアルゾール、GNF6702、ハロファントリン、ヒドロキシクロロキン、イミドカーブ、イプロニダゾール、ジェスイット(Jesuit)の樹皮、KAF156、ルメファントリン、マヅラミシン、メフロキン、メガゾール、アンチモン酸メグルミン、メラルソプロル、メパクリン、メトロニダゾール、ミルテフォシン、ニイロレニンB、ニカルバジン、ニフルチモックス、ニモラゾール、ニタルソン、ニチジン、ニトロフラル、オリバシン、オルニダゾール、オロイジン、パマキン、パロモマイシン、ペンタミジン、五価アンチモン薬、ファンキノン、フェナミジン、ピペラキン、プリマキン、プログアニル、プロジェクト523、プロペニダゾール、ピリメタミン、ピロナリジン、キンファミド、キニン、ロニダゾール、スケジューラ・ロマーナ、SCYX-7158、セクニダゾール、セマピモド、スチボグルコン酸ナトリウム、スピロインドロン、スルファドキシン、スルファドキシン-ピリメタミン、スルファレン、スラミン、タフェノキン、テクロザン、テノニトロゾール、チルブロキノール、チニダゾール、トリメトレキセート、抗トリパノソーマ薬、ワールブルグのチンキ剤、及びこれらのジェネリック医薬品又はこれらの変種が含まれる。
抗菌剤は、本明細書で列挙した薬剤と同様の機構によって作用する薬剤であり得る。
当技術分野で公知の他の抗菌剤を、本発明において使用し得る。
液体懸濁液
微生物の液体懸濁液は、機械、超音波及び/又は磁気撹拌を用いて撹拌され得る。機械撹拌の例には、振とう又は揺動並びに/又は撹拌棒、撹拌パドル、撹拌翼及び/若しくは撹拌プロペラ若しくは羽根車の使用が含まれる。
微生物の分離は、遠心分離(例えばg力>500×g)、磁気分離、ろ過(例えば0.45ミクロン以下、好ましくは0.2ミクロン以下の細孔を有するフィルタによって)、電気泳動、誘電泳動、沈殿、凝集又はこれらの任意の組み合わせによって実施される。
液体は、カチオン調整ミューラーヒントンブロスなどの増殖培地を含み得る。この培地は、微生物の増殖及び安定性を促進するための当業者に公知の1つ以上の添加剤を含み得る。種々の抗菌剤に加えて、種々の試験ウェルは、特定の抗菌剤についてのAST精度を改善することが公知である1つ以上の添加剤を含み得る。例えば、オキサシリンを含む試験物に追加の塩化ナトリウムを添加してもよく、ダプトマイシンを含む試験物に追加のカルシウムを添加してもよい。
カートリッジ
カートリッジの種類は限定されない。カートリッジは、微生物の液体懸濁液を保持し、増殖させることができる容器である。カートリッジの非限定的な例には、培養フラスコ、培養皿、ペトリ皿、バイオアッセイ皿、培養管、試験管、微量遠心管、瓶、マイクロウェルプレート、マルチウェルプレート、マイクロタイタープレート、マイクロプレートが含まれる。カートリッジは、1つのチャンバを含み得る。カートリッジは複数のチャンバを含んでもよく、各々のチャンバは、液体懸濁液を別の空間から物理的に隔離して保持することができる空間であり、チャンバの一例は、マルチウェルプレートのウェルである。カートリッジは、1、2、3、4、5、6、7、8、9、10、11、12、24、48、96、192、384、1536又はこれ以上のチャンバ及びこの間の任意の数のチャンバを含み得る。
光学装置
シグナルを検出することができる多くの様々な特徴を有する任意の光学装置(例えば顕微鏡、マイクロプレートリーダー)は、本発明において有用である。例えば、広域スペクトルランプ(例えばキセノン)、狭域スペクトルランプ、レーザー、LED、多光子、共焦点又は全反射照明を励起のために使用することができる。カメラ(単一若しくは複数)、単一のフォトダイオード若しくはフォトダイオードのアレイ(1D若しくは2D)、アバランシェフォトダイオード、CMOS若しくはCCDセンサ、固体光電子増倍管(例えばシリコン光電子増倍管)、及び/又はフィルタ若しくは回折格子に基づくスペクトル分解(1つ以上のスペクトル分解された発光波長)を有する光電子増倍管(単一又は複数)が検出側で可能である。
キット
本発明において本明細書で使用される「キット」及び「システム」という用語は、複数のシグナル伝達剤と1つ以上の他の種類の要素又は成分(例えば他の種類の生化学試薬、シグナル検出試薬、対照(すなわち陽性及び陰性対照、例えば化学的に感受性/耐性の微生物)、分離手段(例えばフィルタ及び磁気ビーズ)、容器、商業的販売目的のパッケージングなどのパッケージ、微生物懸濁液を培養、処理又は含有することができる基質/カートリッジ、電子ハードウェア部品、及び非一時的なプロセッサ可読媒体に記録されたソフトウェア)との組み合わせなどの事物を指すことが意図されている。
本発明の別の態様は、微生物の抗菌剤感受性を決定するためのキットである。このキットは、関心対象の無傷の微生物の表面に結合することができるシグナル伝達剤、微生物を含む試料をインキュベートするための溶液、及びシグナル伝達剤からシグナルを生成するための1つ以上の試薬を含む。
実施形態では、シグナル伝達剤は、関心対象の無傷の微生物に直接又は間接的に結合することができる1つ以上の結合部分と会合している。
実施形態では、1つ以上の結合部分は、抗体、レクチン、天然及び/若しくは合成ペプチド、合成及び/若しくは天然リガンド、合成及び/若しくは天然ポリマー、合成及び/若しくは天然糖ポリマー、炭水化物結合タンパク質及び/若しくはポリマー、糖タンパク質結合タンパク質及び/若しくはポリマー、荷電小分子、他のタンパク質、バクテリオファージ並びに/又はアプタマーから選択される。
実施形態では、1つ以上の結合部分は、ポリクローナル及び/又はモノクローナル抗体であり得る。
実施形態では、1つ以上の結合部分は、合成及び/又は天然リガンド及び/又はペプチドであり得る。リガンド及び/又はペプチドは、ビス(亜鉛-ジピコリルアミン)、TATペプチド、セリンプロテアーゼ、カテリシジン、カチオン性デキストリン、カチオン性シクロデキストリン、サリチル酸、リジン及びこれらの組み合わせから選択され得る。
実施形態では、1つ以上の結合部分は、合成及び/又は天然ポリマー及び/又は糖ポリマーであり得る。天然及び/又は合成ポリマーは、アミロペクチン、ポリ(N-[3-(ジメチルアミノ)プロピル]メタクリルアミド)、ポリ(エチレンイミン)、ポリ-L-リジン、ポリ[2-(N,N-ジメチルアミノ)エチルメタクリレート]及びこれらの組み合わせであり得る。天然及び/又は合成ポリマー及び/又は糖ポリマーは、キトサン、ゼラチン、デキストラン、トレハロース、セルロース、マンノース、カチオン性デキストラン及びシクロデキストラン、又はコブロックポリマー、グラフトポリマー及び交互ポリマーを含むがこれらに限定されない、これらの組み合わせを含むがこれらに限定されない部分を含み得る。
実施形態では、1つ以上の結合部分は、マンノース結合レクチン、他のレクチン、アネキシン及びこれらの組み合わせから選択される糖タンパク質を含み得る。
実施形態では、1つ以上の結合部分は、2つ以上の結合部分を含み得る。
実施形態では、1つ以上の結合部分は、微生物表面上に存在する1つ以上の生体分子に直接又は間接的に結合し得る。例示的な生体分子には、ペプチドグリカン、ムレイン、マンノプロテイン、ポーリン、β-グルカン、キチン、糖タンパク質、多糖、リポ多糖、リポオリゴ糖、リポタンパク質、内毒素、リポテイコ酸、テイコ酸、脂質A、炭水化物結合ドメイン、流出ポンプ、他の細胞壁及び/又は細胞膜関連タンパク質、他のアニオン性リン脂質、並びにこれらの組み合わせが含まれる。
実施形態では、結合部分はナノ粒子である。
実施形態では、結合部分はバクテリオファージである。
実施形態では、1つ以上の結合部分は、1つ以上の生体分子に特異的に結合し得る。
実施形態では、1つ以上の結合部分は、1つ以上の種特異的生体分子に結合し得る。
実施形態では、1つ以上の結合部分は、例えば非共有結合相互作用によって及び共有結合を形成することによって、非特異的に微生物に結合し得る。
実施形態では、キットは、上清から微生物を磁気的に分離する磁気ビーズをさらに含む。
実施形態では、磁気ビーズは、微生物に結合する1つ以上の結合部分と会合している。磁気ビーズと会合している1つ以上の結合部分は、シグナル伝達剤と会合しているものと同一であってもよい。磁気ビーズに会合している1つ以上の結合部分は、シグナル伝達剤に会合しているものとは異なっていてもよい。
実施形態では、磁気ビーズは、20nm~20ミクロンの範囲の直径を有する。
実施形態では、キットは、結合部分と微生物との間の結合を増強するための1つ以上のイオン又は小分子をさらに含む。
実施形態では、溶液は<0.15Mの塩を含む。
実施形態では、キットは、微生物結合剤をさらに含み、結合部分は、微生物結合剤を介して間接的に微生物に結合する。結合部分は、ストレプトアビジン、ニュートラアビジン又はアビジンにコンジュゲートしていてもよく、微生物結合剤はビオチン化されていてもよい。結合部分は、種特異的Fcドメインに結合する抗体であってもよく、微生物結合剤は、種特異的Fcドメインを有する微生物に結合することができる抗体であってもよい。
実施形態では、シグナル伝達剤は、ケミルミノフォア、触媒又は酵素の1つ以上を含み得る。酵素は、ホースラディッシュペルオキシダーゼ、アルカリホスファターゼ、アセチルコリンエステラーゼ、グルコースオキシダーゼ、β-D-ガラクトシダーゼ、β-ラクタマーゼ及びこれらの組み合わせの少なくとも1つであり得る。触媒は、有機金属化合物であり得る。
実施形態では、シグナル伝達剤はナノ粒子の形態で提供され、例えば、シグナル伝達剤はナノ粒子内に封入される。ナノ粒子は解離性であり得、これは、金属酸化物を含んでもよく、金属酸化物は、酸化鉄、酸化セシウム及び/又は酸化セリウムであってもよく又はこれらを含んでもよい。
実施形態では、シグナルレベルを決定する前に、0回、1回又は2回の洗浄を実施する。
実施形態では、シグナル伝達剤の添加の前に0回、1回又は2回の洗浄を実施する。
実施形態では、キットは、測定可能なシグナルを生成するための展開剤試薬をさらに含む。
実施形態では、1つ以上の試薬は、触媒反応のための試薬及び触媒反応を停止させる試薬を含む。
実施形態では、キットは、シグナル、例えば光及び/又は電気シグナルを測定するための装置をさらに含む。光学測定は、蛍光、時間分解蛍光、吸収及び/又は発光であり得る。
実施形態では、キットは、マルチウェルプレート、例えば24ウェル、96ウェル、192ウェル又は384ウェルプレートをさらに含む。
実施形態では、キットは、本明細書に開示される方法を実施するのにキットを使用するための説明書をさらに含む。キットは、本明細書に記載の1つ以上の方法の前又は後に行われる工程を実施するための説明書をさらに含み得る。
一実施形態では、本明細書に記載の1つ以上の方法を実施するために必要な試薬又は本明細書に記載の1つ以上の方法の前又は後の工程を実施するために必要な試薬を含むキットが提供される。
治療法
本明細書で使用される場合、「治療する」、「治療すること」、「治療」等の用語は、これに関連する障害及び/又は症状を軽減又は改善することを指す。除外されるわけではないが、障害又は状態を治療することは、これに関連する障害、状態又は症状が完全に排除されることを必要としないことが理解される。治療することは、医療専門家又は診断学者が所望の作用経過又は治療レジメン、例えば処方について被験体にアドバイスすることを含み得る。
本明細書で使用される場合、「予防する」、「予防すること」、「予防」、「予防的処置」等の用語は、障害又は状態を有していないが、発症する危険性がある又は発症しやすい被験体において障害又は状態を発症する可能性を低減することを指す。
「治療する方法」という用語は、管理する方法を含み、感染性微生物又は感染に関連して使用される場合は、感染性微生物の有害な作用からの改善、排除、軽減、予防又は他の緩和若しくは管理を含む。
本明細書で使用される場合、「薬物」、「薬剤」、「治療薬」、「活性剤」、「治療化合物」、「組成物」又は「化合物」という用語は、交換可能に使用され、疾患、疾病、状態又は身体機能の障害を治療又は予防するために使用できる任意の化学的実体、薬剤、薬物、生物学的製剤、植物製剤等を指す。薬剤は、公知の治療化合物及び潜在的な治療化合物の両方を含み得る。薬剤は、当業者に公知のスクリーニングを用いてスクリーニングすることによって治療的であると決定され得る。「公知の治療化合物」、「薬物」又は「薬剤」は、このような治療において有効であることが示されている(例えば動物試験又はヒトへの投与に関する事前の経験を通して)治療化合物を指す。「治療レジメン」は、本明細書で開示される「薬物」、「薬剤」、「治療薬」、「活性剤」、「治療化合物」、「組成物」若しくは「化合物」を含む治療及び/又は被験体による行動変容を含む治療及び/又は外科的手段を含む治療に関する。
抗菌剤、例えば抗生物質は、微生物を死滅させるか又は微生物の増殖を阻害することができる作用物質である。
シグナル伝達剤及び化学的結合
実施形態では、本発明は、微生物の表面に結合することができるシグナル伝達剤を特徴とする。実施形態では、前記結合は非特異的である。実施形態では、前記結合は特異的である。
実施形態では、シグナル伝達剤は、本明細書に記載の方法のインキュベーション工程の間存在する。実施形態では、シグナル伝達剤は、本明細書に記載の方法のインキュベーション工程の後に存在する。
実施形態では、結合は、共有結合の形成を含む。実施形態では、シグナル伝達剤は微生物の表面に結合することができ、前記結合は、共有結合の形成を含む。実施形態では、本明細書に記載の方法は、微生物表面上の基と本明細書に記載のシグナル伝達剤との間での共有結合の形成(例えば本明細書に記載の求電子性基又は求核性基などの反応性基を介して)をもたらす。実施形態では、シグナル伝達剤は、微生物の表面への共有結合を形成している。
実施形態では、結合は、非共有結合相互作用の形成を含む。実施形態では、シグナル伝達剤は微生物の表面に結合することができ、前記結合は、非共有結合相互作用の形成を含む。実施形態では、本明細書に記載の方法は、微生物表面上の基と本明細書に記載のシグナル伝達剤との間での非共有結合相互作用の形成(例えば本明細書に記載の求電子性基又は求核性基などの反応性基を介して)をもたらす。実施形態では、シグナル伝達剤は、微生物の表面と非共有結合相互作用を形成している。
実施形態では、非共有結合相互作用は、イオン性相互作用、イオン-イオン相互作用、双極子-双極子相互作用、イオン-双極子相互作用、静電的相互作用、ロンドン分散、ファンデルワールス相互作用、水素結合、π-π相互作用、疎水性相互作用又はこれらの任意の組み合わせを含む。実施形態では、非共有結合相互作用は、イオン性相互作用、イオン-イオン相互作用、双極子-双極子相互作用、イオン-双極子相互作用、静電的相互作用、ロンドン分散、ファンデルワールス相互作用、水素結合、π-π相互作用、疎水性相互作用又はこれらの任意の組み合わせである。
実施形態では、非共有結合相互作用は、イオン性相互作用、ファンデルワールス相互作用、疎水性相互作用、π-π相互作用若しくは水素結合、又はこれらの任意の組み合わせを含む。実施形態では、非共有結合相互作用は、イオン性相互作用、ファンデルワールス相互作用、水素結合若しくはπ-π相互作用、又はこれらの任意の組み合わせを含む。
実施形態では、微生物の表面に結合することができるシグナル伝達剤は、微生物の膜、壁、タンパク質、細胞小器官、サッカリド、脂質、細胞エンベロープ若しくは核酸、又はこれらの任意の組み合わせに結合することができる基(例えば化学基又は生化学基)を含む。実施形態では、微生物の表面に結合することができるシグナル伝達剤は、微生物の膜、壁、タンパク質、細胞小器官、サッカリド、脂質、細胞エンベロープ若しくは核酸、又はこれらの任意の組み合わせに結合することができる化学基(例えば求核性基又は求電子性基)を含む。実施形態では、微生物の表面に結合することができるシグナル伝達剤は、微生物の膜、壁、タンパク質、細胞小器官、サッカリド、脂質、細胞エンベロープ若しくは核酸、又はこれらの任意の組み合わせに結合することができる生化学基を含む。
実施形態では、表面は、シグナル伝達剤が結合又は会合する生体分子を含み得る。例示的な生体分子には、ペプチドグリカン、ムレイン、マンノプロテイン、ポーリン、β-グルカン、キチン、糖タンパク質、多糖、リポ多糖、リポオリゴ糖、リポタンパク質、内毒素、リポテイコ酸、テイコ酸、脂質A、炭水化物結合ドメイン、流出ポンプ、他の細胞壁及び/又は細胞膜関連タンパク質、他のアニオン性リン脂質、並びにこれらの組み合わせが含まれる。
実施形態では、微生物の表面に結合することができるシグナル伝達剤は、微生物の膜、壁、タンパク質、細胞小器官、サッカリド、脂質、細胞エンベロープ若しくは核酸、又はこれらの任意の組み合わせに結合することができる生化学基を含む。
実施形態では、微生物の表面に結合することができるシグナル伝達剤は、微生物の膜、壁、タンパク質、細胞小器官、サッカリド、脂質、細胞エンベロープ若しくは核酸、又はこれらの任意の組み合わせに結合することができる化学基(例えば求核性又は求電子性官能基)を含む。実施形態では、前記化学基は、求核性官能基である。実施形態では、前記化学基は、求電子性官能基である。
実施形態では、シグナル伝達剤は、生化学的シグナル伝達剤である。実施形態では、生化学的シグナル伝達剤は、抗体、リガンド、タンパク質、アプタマー、ss-DNA、ss-RNA又はss-PNAなどの生体分子を含む。
実施形態では、シグナル伝達剤は、化学的シグナル伝達剤である。実施形態では、化学的シグナル伝達剤は、化学化合物(例えば合成化学化合物)である。実施形態では、化学的シグナル伝達剤は、抗体、リガンド、タンパク質、アプタマー、ss-DNA、ss-RNA又はss-PNAなどの生体分子を含まない。
実施形態では、微生物の表面に結合することができるシグナル伝達剤は、
リンカー基L;及び
増幅基(例えば化学又は生化学増幅剤である増幅基104)
を含む。
実施形態では、増幅基は、化学又は生化学増幅剤である増幅基104である。実施形態では、増幅基104は化学増幅剤である。実施形態では、増幅基104は生化学増幅剤である。
実施形態では、シグナル伝達剤は化学化合物である。実施形態では、化学化合物は、本明細書に記載のもののような化学増幅基を含む。
実施形態では、リンカー基Lは、抗体の保存された(Fc)領域を含む。
実施形態では、リンカー基Lは、増幅基(例えば化学又は生化学増幅剤である増幅基104)と共有結合を形成することができる。
実施形態では、リンカー基Lは、シグナル増幅基(例えば化学又は生化学増幅剤である増幅基104)と共有結合を形成する。
実施形態では、リンカー基Lは、増幅基(例えば化学又は生化学増幅剤である増幅基104)に対して1つ以上の非共有結合相互作用を形成することができる。
実施形態では、リンカー基Lは、増幅基(例えば化学又は生化学増幅剤である増幅基104)に対して1つ以上の非共有結合相互作用を形成する。
実施形態では、リンカー基Lは、微生物表面に結合することができる基(例えば化学基又は生化学基)を含む。実施形態では、リンカー基Lは、微生物表面に結合する基(例えば化学基又は生化学基)を含む。
実施形態では、リンカー基Lは、微生物の表面と共有結合を形成することができる基(例えば化学基又は生化学基)を含む。実施形態では、リンカー基Lは、微生物の表面と共有結合を形成する基(例えば化学基又は生化学基)を含む。
実施形態では、リンカー基Lは、微生物の表面と1つ以上の非共有結合相互作用を形成することができる基(例えば化学基又は生化学基)を含む。実施形態では、リンカー基Lは、微生物の表面と1つ以上の非共有結合相互作用を形成する基(例えば化学基又は生化学基)を含む。
実施形態では、リンカー基Lは化学的部分101を含み、前記化学的部分は、微生物の表面と非共有結合相互作用を形成することができる。実施形態では、リンカー基Lは化学的部分101を含み、前記化学的部分は、微生物の表面と共有結合を形成することができる。実施形態では、リンカー基Lは化学的部分101を含み、前記化学的部分は、微生物の表面と非共有結合相互作用を形成する。実施形態では、リンカー基Lは化学的部分101を含み、前記化学的部分は、微生物の表面と共有結合を形成する。
実施形態では、リンカー基Lは、スペーサー部分102を含む。実施形態では、スペーサー部分102は、化学的部分101及び/又は化学的部分103に共有結合している。実施形態では、スペーサー部分102は、化学的部分101に共有結合している。実施形態では、スペーサー部分102は、化学的部分103に共有結合している。実施形態では、スペーサー部分102は、化学的部分101及び化学的部分103に共有結合している。実施形態では、スペーサー部分102は、化学的部分101及び/又は化学的部分103と非共有結合相互作用を形成する。実施形態では、スペーサー部分102は、化学的部分101と非共有結合相互作用を形成する。実施形態では、スペーサー部分102は、化学的部分103と非共有結合相互作用を形成する。実施形態では、スペーサー部分102は、化学的部分101及び化学的部分103と非共有結合相互作用を形成する。
実施形態では、リンカー基Lは化学的部分103を含み、前記化学的部分は、増幅基(例えば化学又は生化学増幅剤である増幅基104)と共有結合を形成することができる。実施形態では、リンカー基Lは化学的部分103を含み、前記化学的部分は、増幅基(例えば化学又は生化学増幅剤である増幅基104)と共有結合を形成している。実施形態では、リンカー基Lは化学的部分103を含み、前記化学的部分は、増幅基(例えば化学又は生化学増幅剤である増幅基104)と非共有結合相互作用を形成することができる。実施形態では、リンカー基Lは化学的部分103を含み、前記化学的部分は、増幅基(例えば化学又は生化学増幅剤である増幅基104)と非共有結合相互作用を形成している。
実施形態では、シグナル伝達剤は、
微生物の表面と共有結合又は非共有結合相互作用を形成することができる化学的部分101、
化学的部分101及び化学的部分103に共有結合しているスペーサー部分102、並びに
化学又は生化学増幅剤である増幅基104と共有結合を形成している又は形成することができる化学的部分103
を含むリンカー基Lを含む化学化合物である。
実施形態では、シグナル伝達剤は、
微生物の表面と共有結合又は非共有結合相互作用を形成することができる化学的部分101、
化学的部分101及び化学的部分103に共有結合しているスペーサー部分102、並びに
化学又は生化学増幅剤である増幅基104と非共有結合相互作用を形成している又は形成することができる化学的部分103
を含むリンカー基Lを含む化学化合物である。
実施形態では、リンカー基は、1つの化学的部分101を含む。実施形態では、リンカー基は、2つ以上の化学的部分101(例えばリンカー基は1、2、3、4、5又は6個の化学的部分101を含む)を含む。
実施形態では、リンカー基は、1つのスペーサー部分102を含む。実施形態では、リンカー基は、2つ以上のスペーサー部分102(例えばリンカー基は1、2、3、4、5又は6個のスペーサー部分102を含む)を含む。
実施形態では、リンカー基は、1つの化学的部分103を含む。実施形態では、リンカー基は、2つ以上の化学的部分103(例えばリンカー基は1、2、3、4、5又は6個の化学的部分103を含む)を含む。
実施形態では、リンカー基は、1つの化学的部分101、1つのスペーサー部分102及び1つの化学的部分103を含む。実施形態では、リンカー基は、1つの化学的部分101、1つのスペーサー部分102及び1つの化学的部分103からなる。
実施形態では、リンカー基は、部分構造(I):
-101-102-103-、(I)
[ここで、
「101」は化学的部分101を表し、
「102」はスペーサー部分102を表し;及び
「103」は化学的部分103を表す]
の構造を有する。
実施形態では、化学的部分101は、微生物の表面と共有結合を形成することができる。
実施形態では、化学的部分101は、カップリングを促進する1つ以上の作用物質(本明細書ではカップリング剤とも称される)の存在下で微生物の表面と共有結合を形成することができる。
実施形態では、カップリングを促進する作用物質には、グルタルアルデヒド、ホルムアルデヒド、パラホルムアルデヒド、1-エチル-3-(3-ジメチルアミノプロピル)カルボジイミド(EDC)、N,N’-ジシクロヘキシルカルボジイミド(DCC)、N-シクロヘキシル-N’-(2-モルホリノエチル)カルボジイミド-メチル-p-トルエンスルホネート(CMC)、ジイソプロピルカルボジイミド(DIC)、(1-[ビス(ジメチルアミノ)メチレン]-1H-1,2,3-トリアゾロ[4,5-b]ピリジニウム3-オキシドヘキサフルオロホスフェート(HATU)、ウッドワード試薬、N,N’-カルボニルジイミダゾール、N-ヒドロキシスクシンイミド(NHS)若しくはN-ヒドロキシスルホスクシンイミド(スルホ-NHS)、又はこれらの任意の組み合わせが含まれる。
実施形態では、カップリングを促進する作用物質には、アルデヒド、アクリレート、アミド、イミド、無水物、クロロトリアジン、エポキシド、イソシアネート、イソチオシアネート、有機酸、モノマー、ポリマー、シラン若しくはシリケート、又はこれらの任意の組み合わせが含まれる。
実施形態では、カップリングを促進する作用物質には、カルボジイミド、ホスホニウム塩若しくはアンモニウム塩、又はこれらの任意の組み合わせが含まれる。
実施形態では、カップリングを促進する作用物質には、グルタルアルデヒド、N-(3-ジメチルアミノプロピル)-N’-エチルカーボネート(EDC)、(1-[ビス(ジメチルアミノ)メチレン]-1H-1,2,3-トリアゾロ[4,5-b]ピリジニウム3-オキシドヘキサフルオロホスフェート)(HATU)、(O-ベンゾトリアゾール-1-イル-N,N,N,N-テトラメチルウロニウムヘキサフルオロホスフェート)(HBTU)、N-ヒドロキシスクシンイミド(NHS)、N,N’-ジシクロヘキシルカルボジイミド(DCC)、ジイソプロピルカルボジイミド(DIC)、ヒドロキシ-3,4-ジヒドロ-4-オキソ-1,2,3-ベンゾトリアジン(HOOBt)、ヒドロキシベンゾトリアゾール(HOBT)、1-ヒドロキシ-7-アザベンゾトリアゾール(HOAt)、(N-3-ジメチルアミノプロピル)-N’-エチルカルボジイミド(EDAC)、4-(N,N-ジメチルアミノ)ピリジン(DMAP)、ベンゾトリアゾール-1-イルオキシ-トリス(ジメチルアミノ)-ホスホニウムヘキサフルオロホスフェート(BOP)、ベンゾトリアゾール-1-イルオキシ-トリピロリジノホスホニウムヘキサフルオロホスフェート(PyBOP)、ブロモ-トリピロリジノホスホニウムヘキサフルオロホスフェート(PyBrOP)、7-アザ-ベンゾトリアゾール-1-イルオキシ-トリピロリジノホスホニウムヘキサフルオロホスフェート(PyAOP)、エチルシアノ(ヒドロキシイミノ)アセタート-O2)-トリ-(1-ピロリジニル)-ホスホニウムヘキサフルオロホスフェート(PyOxim)、3-(ジエトキシ-ホスホリルオキシ)-1,2,3-ベンゾ[d]トリアジン-4(3H)-オン(DEPBT)、2-(6-クロロ-1H-ベンゾトリアゾール-1-イル)-N,N,N’,N’-テトラメチルアミニウムヘキサフルオロホスフェート(HCTU)、N-[(5-クロロ-1H-ベンゾトリアゾール-1-イル)-ジメチルアミノ-モルホリノ]-ウロニウムヘキサフルオロホスフェートN-オキシド(HDMC)、1-[1-(シアノ-2-エトキシ-2-オキソエチリデンアミノオキシ)-ジメチルアミノ-モルホリノ]-ウロニウムヘキサフルオロホスフェート(COMU)、2-(1-オキシ-ピリジン-2-イル)-1,1,3,3-テトラメチルイソチオウロニウムテトラフルオロボレート(TOTT)、テトラメチルフルオロホルムアミジニウムヘキサフルオロホスフェート(TFFH)、N-エトキシカルボニル-2-エトキシ-1,2-ジヒドロキノリン(EEDQ)、2-プロパンホスホン酸無水物(PPA)、トリホスゲン、1,1’-カルボニルジイミダゾール(CDI)、[(6-ニトロベンゾトリアゾール-1-イル)オキシ]トリス(ピロリジノ)ホスホニウムヘキサフルオロホスフェート(PyNOP)、[[6-(トリフルオロメチル)ベンゾトリアゾール-1-イル]オキシ]トリス(ピロリジノ)ホスホニウムヘキサフルオロホスフェート(PyFOP)、[[4-ニトロ-6-(トリフルオロメチル)ベンゾトリアゾール-1-イル]オキシ]トリス(ピロリジノ)ホスホニウムヘキサフルオロホスフェート(PyNFOP)、[(6-ニトロベンゾトリアゾール-1-イル)オキシ]トリス(ジメチルアミノ)ホスホニウムヘキサフルオロホスフェート(NOP)、1-β-ナフタレンスルホニルオキシベンゾトリアゾール(NSBt)、1-β-ナフタレンスルホニルオキシ-6-ニトロベンゾトリアゾール(N-NSBt)、テトラメチルフルオロホルムアミジニウムヘキサフルオロホスフェート(TFFH)、ビス(テトラメチレン)フルオロホルムアミジニウムヘキサフルオロホスフェート(BTFFH)、1,3-ジメチル-2-フルオロ-4,5-ジヒドロ-1H-イミダゾリウムヘキサフルオロホスフェート(DFIH)、塩化シアヌル(CC)若しくは2,4-ジクロロ-6-メトキシ-1,3,5-トリアジン(DCMT)、及び2-クロロ-4,6-ジメトキシ-1,3,5-トリアジン(CDMT)、又はこれらの任意の組み合わせが含まれる。
実施形態では、カップリングを促進する作用物質には、EDC、HATU、HBTU、NHS、DCC、HOBT若しくはPyBOP、又はこれらの任意の組み合わせが含まれる。
実施形態では、カップリングを促進する作用物質には、EDC、DCC、CMC、DIC若しくはHATU、又はこれらの任意の組み合わせが含まれる。
実施形態では、カップリングを促進する作用物質には、グルタルアルデヒド、ホルムアルデヒド若しくはパラホルムアルデヒド、又はこれらの任意の組み合わせが含まれる。
実施形態では、化学的部分101は、微生物の表面と非共有結合的相互作用(例えば本明細書に記載される任意の非共有結合相互作用)を形成することができる。実施形態では、非共有結合相互作用は、イオン性、イオン-イオン、双極子-双極子、イオン-双極子、静電的、ロンドン分散、ファンデルワールス、水素結合若しくはπ-π相互作用、又はこれらの任意の組み合わせを含む。
実施形態では、化学的部分101は、微生物の表面と非共有結合相互作用を形成することができ、前記非共有結合相互作用は、イオン性相互作用、ファンデルワールス相互作用、疎水性相互作用、π-π相互作用若しくは水素結合、又はこれらの任意の組み合わせを含む。
実施形態では、化学的部分101は、求核性官能基を含む。実施形態では、化学的部分101は、求核性官能基から形成される基を含む。
実施形態では、求核性官能基は、アミノ、アミド、ヒドラジノ、ヒドロキシアミノ、ヒドロキシ又はチオである。実施形態では、求核性官能基は、アミノ、ヒドラジノ、ヒドロキシアミノ又はチオである。実施形態では、求核性官能基は、アミノ、ヒドラジノ、ヒドロキシアミノ、ヒドロキシ又はチオを含む。実施形態では、求核性官能基は、カルボキサミド、N-ヒドロキシカルボキサミド、カルボキシルヒドラジド又はグアニジノである。
実施形態では、求核性官能基は、-NH2、-NHNH2、-CONHOH、-CONHNH2、-ONH2、-OH又は-SHである。実施形態では、求核性官能基は、-NH2、-NHNH2、-CONHNH2又は-ONH2である。
実施形態では、化学的部分101は、求電子性官能基を含む。
実施形態では、化学的部分101は、求電子性官能基から形成される基を含む。
実施形態では、求電子性官能基は、アルデヒド、ケトン、カルボン酸、カルボン酸エステル、カルボン酸ハロゲン化物(例えば塩化アセチル)又はカルボン酸無水物(例えば無水酢酸)を含む。
実施形態では、求電子性官能基は、アルデヒド、α-ハロケトン、マレイミド、スクシンイミド、ヒドロキシスクシンイミド、イソチオシアネート、イソシアネート、アシルアジド、塩化スルホニル、トシレートエステル、グリオキサール、エポキシド、オキシラン、カーボネート、イミドエステル、無水物、フルオロフェニルエステル、ヒドロキシメチルホスフィン誘導体、カーボネート、ハロアセチル、クロロトリアジン、ハロアセチル、ハロゲン化アルキル、アジリジン又はアクリロイル誘導体を含む。実施形態では、求電子性官能基は、アルデヒド、α-ハロケトン、マレイミド、スクシンイミド、ヒドロキシスクシンイミド、イソチオシアネート、イソシアネート、アシルアジド、塩化スルホニル、トシレートエステル、グリオキサール、エポキシド、オキシラン、カーボネート、イミドエステル、無水物、フルオロフェニルエステル、ヒドロキシメチルホスフィン誘導体、カーボネート、ハロアセチル、クロロトリアジン、ハロアセチル、ハロゲン化アルキル、アジリジン又はアクリロイル誘導体である。
実施形態では、求電子性官能基は、アルデヒド、α-ハロケトン、マレイミド、スクシンイミド又はヒドロキシスクシンイミド基を含む。
実施形態では、求電子性官能基は、-CHO、-C(O)CH2I、
実施形態では、求電子性官能基は、-CHO、-C(O)CH2I、
実施形態では、化学的部分101は、アルキル、アルケニル、アルキニル、フェニル、ヘテロアリール、ハロアルキル、ヒドロキシ、カルボニル、ハロゲン化アシル、アルコキシカルボニルオキシ、カルボキシ、ハロケトン、アルコキシ、アルコキシオール(ヘミアセタール又はヘミケタール)、ジアルコキシ(例えばケタール又はアセタール)、トリアルコキシ(オルトエーテル)、カルバモイル、アミノ、アンモニオ、イミノ、イミド、スクシンアミド、マレイミド、ヒドロキシスクシンアミド、ビオチン、D-ビオチン、アジド、アゾ、シアネート、イソシアナト、ニトロキシ、シアノ、イソシアノ、ニトロソオキシ、ニトロ、ニトロソ、オキシム、スルファニル、スルフィニル、スルホニル、スルフィノ、スルホ、チオシアナト、イソチオシアナト、チオイル、ホスフェート又はボロネートである基を含む。
実施形態では、スペーサー部分102は疎水性である。実施形態では、スペーサー部分102は親水性である。
実施形態では、スペーサー部分102はペプチド性(例えばペプチド結合に由来する)である。
実施形態では、スペーサー部分102は無機結合を含む。実施形態では、スペーサー部分102は、有機結合を含む。実施形態では、スペーサー部分102は、有機結合のみを含む。
実施形態では、スペーサー部分102はオリゴマー性である。実施形態では、スペーサー部分102はポリマー性である。実施形態では、スペーサー部分102は、メチレン(-CH2-)、エチレングリコール(-CH2CH2O-)、イミノエチレン(-CH2CH2NH-)、ビニルアルコール(-CH2CHOH-)x、乳酸(-CH(CH3)-C(O)-O-)、アクリル酸(-CH2CH2(CO2H)-)、メタクリル酸(-CH2C(CH3)(CO2H)-)又はメチルメタクリレート(-CH2C(CH3)(CO2CH3)-)のセグメント(例えば1~約300、1~約200、1~約100、1~約50、1~約25若しくは1~約10又は1、2、3、4、5、6、7、8、9若しくは10個のセグメント)を含む。
実施形態では、スペーサー部分102は、
実施形態では、n、m、p及びqは、独立して、1~約300(例えば1~約200、1~約100、1~約50、1~約25又は1~約10)の整数である。実施形態では、n、m、p及びqの各々は、独立して、1、2、3、4、5、6、7、8、9又は10である。
実施形態では、スペーサー部分102は、
を含む。実施形態では、R’は、独立して、水素又はC
1-C
12アルキル、C
2-C
12アルケニル若しくはC
2-C
12アルキニルである基である。実施形態では、oは、1~約300(例えば1~約200、1~約100、1~約50、1~約25又は1~約10)の整数である。実施形態では、oは、独立して、1、2、3、4、5、6、7、8、9又は10である。
実施形態では、スペーサー部分102は、
を含む。実施形態では、Rは、独立して、水素又はC
1-C
12アルキル、C
2-C
12アルケニル若しくはC
2-C
12アルキニルである基である。実施形態では、rは、1~約300(例えば1~約200、1~約100、1~約50、1~約25又は1~約10)の整数である。実施形態では、rは、独立して、1、2、3、4、5、6、7、8、9又は10である。
実施形態では、スペーサー部分102は、
を含む。実施形態では、Rは、独立して、水素又はC
1-C
12アルキル、C
2-C
12アルケニル若しくはC
2-C
12アルキニルである基である。いくつかの実施形態では、sは、1~約300(例えば1~約200、1~約100、1~約50、1~約25又は1~約10)の整数である。実施形態では、sは、独立して、1、2、3、4、5、6、7、8、9又は10である。
実施形態では、スペーサー部分102は、
を含む。実施形態では、tは、1~約300(例えば1~約200、1~約100、1~約50、1~約25又は1~約10)の整数である。実施形態では、tは、独立して、1、2、3、4、5、6、7、8、9又は10である。
実施形態では、スペーサー部分102は、
実施形態では、スペーサー部分102は、アルキル、アルコキシ、エステル、アクリル、アミノ、ヒドロキシル若しくはアシルヒドラジン官能基、又はこれらの任意の組み合わせを含む反復基を含むポリマーである。
実施形態では、スペーサー部分102は、
であり、ここで、n、m、p及びqは、本明細書で定義される通りである。
実施形態では、n、m、o、p、q、r、s又はtの各々は、独立して、1~100、10~90、10~80、10~70、10~60、10~50、10~40、10~30、10~20又は1~10の整数である。
実施形態では、化学的部分103は、求核性官能基である基を含む。
実施形態では、化学的部分103は、求核性官能基から形成される基を含む。
実施形態では、求核性官能基は、アミノ、アミド、ヒドラジノ、ヒドロキシアミノ、ヒドロキシ又はチオである。実施形態では、求核性官能基は、アミノ、ヒドラジノ、ヒドロキシアミノ又はチオである。
実施形態では、求核性官能基は、アミノ、ヒドラジノ、ヒドロキシアミノ、ヒドロキシ又はチオを含む。実施形態では、求核性官能基は、カルボキサミド、N-ヒドロキシカルボキサミド、カルボキシルヒドラジド又はグアニジノである。
実施形態では、求核性官能基は、-NH2、-NHNH2、-CONHOH、-CONHNH2、-ONH2、-OH又は-SHである。実施形態では、求核性官能基は、-NH2、-NHNH2、-CONHNH2又は-ONH2である。
実施形態では、化学的部分103は、求電子性官能基である基を含む。
実施形態では、化学的部分103は、求電子性官能基から形成される基を含む。
実施形態では、求電子性官能基は、アルデヒド、ケトン、カルボン酸、カルボン酸エステル、カルボン酸ハロゲン化物(例えば塩化アセチル)又はカルボン酸無水物(例えば無水酢酸)を含む。
実施形態では、求電子性官能基は、アルデヒド、α-ハロケトン、マレイミド、スクシンイミド、ヒドロキシスクシンイミド、イソチオシアネート、イソシアネート、アシルアジド、塩化スルホニル、トシレートエステル、グリオキサール、エポキシド、オキシラン、カーボネート、イミドエステル、無水物、フルオロフェニルエステル、ヒドロキシメチルホスフィン誘導体、カーボネート、ハロアセチル、クロロトリアジン、ハロアセチル、ハロゲン化アルキル、アジリジン又はアクリロイル誘導体を含む。実施形態では、求電子性官能基は、アルデヒド、α-ハロケトン、マレイミド、スクシンイミド、ヒドロキシスクシンイミド、イソチオシアネート、イソシアネート、アシルアジド、塩化スルホニル、トシレートエステル、グリオキサール、エポキシド、オキシラン、カーボネート、イミドエステル、無水物、フルオロフェニルエステル、ヒドロキシメチルホスフィン誘導体、カーボネート、ハロアセチル、クロロトリアジン、ハロアセチル、ハロゲン化アルキル、アジリジン又はアクリロイル誘導体である。
実施形態では、求電子性官能基は、アルデヒド、α-ハロケトン、マレイミド、スクシンイミド又はヒドロキシスクシンイミド基を含む。
実施形態では、求電子性官能基は、-CHO、-C(O)CH2I、
実施形態では、求電子性官能基は、-CHO、-C(O)CH2I、
実施形態では、化学的部分103は、カルボニル、アルケニル、アルキニル、ヒドロキシル、アミノ、チオール、マレイミド、スクシンイミド、ヒドロキシスクシンイミド、ビオチニル、無水物、クロロトリアジン、エポキシド、イソシアネート又はイソチオシアネートである化学構造を含む。実施形態では、カルボニル、アルケニル、アルキニル、ヒドロキシル、アミノ、チオール、マレイミド、スクシンイミド、ヒドロキシスクシンイミド、ビオチニル、無水物、クロロトリアジン、エポキシド、イソシアネート又はイソチオシアネートである前記基は、増幅基(例えば増幅基104)と共有結合を形成することができる。実施形態では、カルボニル、アルケニル、アルキニル、ヒドロキシル、アミノ、チオール、マレイミド、スクシンイミド、ヒドロキシスクシンイミド、ビオチニル、無水物、クロロトリアジン、エポキシド、イソシアネート又はイソチオシアネートである前記基は、増幅基(例えば増幅基104)と非共有結合相互作用を形成することができる。
実施形態では、化学的部分103は、カルボニル、アルケニル、アルキニル、ヒドロキシル、アミノ、チオール、マレイミド、スクシンイミド、ヒドロキシスクシンイミド、ビオチニル、無水物、クロロトリアジン、エポキシド、イソシアネート又はイソチオシアネートである基を含む化学構造から形成される。実施形態では、カルボニル、アルケニル、アルキニル、ヒドロキシル、アミノ、チオール、マレイミド、スクシンイミド、ヒドロキシスクシンイミド、ビオチニル、無水物、クロロトリアジン、エポキシド、イソシアネート又はイソチオシアネートである前記基は、増幅基(例えば増幅基104)と共有結合を形成している。実施形態では、カルボニル、アルケニル、アルキニル、ヒドロキシル、アミノ、チオール、マレイミド、スクシンイミド、ヒドロキシスクシンイミド、ビオチニル、無水物、クロロトリアジン、エポキシド、イソシアネート又はイソチオシアネートである前記基は、増幅基(例えば増幅基104)と非共有結合相互作用を形成している。
実施形態では、化学的部分103は、カルボニル、アルケニル、アルキニル、ヒドロキシル、アミノ、チオール、マレイミド、スクシンイミド、ヒドロキシスクシンイミド又はビオチニルである基を含む。
実施形態では、化学的部分103は、カルボニル、アルケニル、アルキニル、ヒドロキシル、アミノ、チオール、マレイミド、スクシンイミド、ヒドロキシスクシンイミド又はビオチニル官能基を含む。
実施形態では、化学的部分103は、
実施形態では、化学的部分103は、カルボニル、アルケニル、アルキニル、ヒドロキシル、アミノ、チオール、マレイミド、スクシンイミド、ヒドロキシスクシンイミド又はビオチニル官能基である基を含む化学構造から形成される基を含む。
実施形態では、リンカー基Lは、部分構造(II):
[ここで、
Xは、化学的部分101(例えば本明細書に記載の任意の化学的部分101)を表し、
Rは、スペーサー部分102(例えば本明細書に記載の任意のスペーサー部分102)を表し、
Yは、化学的部分103(例えば本明細書に記載の任意の化学的部分103)を表し、並びに
j及びkの各々は、独立して、0~100の整数である]
の構造を有する。
実施形態では、Xは、
実施例では、Rは、
であり、ここで、n、m、o、p、q、r、s又はtの各々は、本明細書に記載の通り(例えば1~約300の整数)である。
実施形態では、Yは、
実施形態では、Xは微生物の表面と共有結合を形成することができる。実施形態では、Xは微生物の表面と共有結合を形成する。
実施形態では、Xは、微生物の表面と1つ以上の非共有結合相互作用を形成することができる。実施形態では、Xは、微生物の表面と1つ以上の非共有結合相互作用を形成する。
実施形態では、Yは、増幅基104(例えば化学又は生化学増幅剤)と共有結合を形成することができる。実施形態では、Yは、増幅基104(例えば化学又は生化学増幅剤)などの増幅基と共有結合を形成する。
実施形態では、Yは、増幅基104(例えば化学又は生化学増幅剤)に対して1つ以上の非共有結合相互作用を形成することができる。実施形態では、Yは、増幅基104(例えば化学又は生化学増幅剤)などの増幅基に対して1つ以上の非共有結合相互作用を形成する。
実施形態では、リンカー基Lは、
WGA-ビオチン、ポリミキシンB-ビオチン、モノクローナル抗体、ポリクローナル抗体、ビオチン化モノクローナル抗体、ビオチン化ポリクローナル抗体、ユウロピウムキレート-抗体、ホースラディッシュペルオキシダーゼ結合抗体、並びに抗体変異体(例えばFab:抗原結合フラグメント(一方の腕);F(ab’)2:ヒンジ領域を含む抗原結合フラグメント(両方の腕);Fab’:ヒンジ領域を含む抗原結合フラグメント(一方の腕);scFv:一本鎖可変フラグメント;di-scFv:二量体一本鎖可変フラグメント;sdAb:単一ドメイン抗体;二重特異性モノクローナル抗体;三官能性抗体及びBiTE:二重特異性T細胞誘導体)である。
例示的な増幅基には、例えば国際公開WO2016/015027号及び国際出願PCT/US16/42589号に記載されているものが含まれ、これらの各々は全体が参照により本明細書に組み込まれる。
実施形態では、増幅基(例えば増幅基104)は、触媒、フルオロフォア又は比色色素を含む。実施形態では、増幅基(例えば増幅基104)は、触媒、フルオロフォア又は比色色素である。
実施形態では、増幅基(例えば増幅基104)は、酵素、触媒又はナノ粒子を含む。実施形態では、増幅基(例えば増幅基104)は、酵素、触媒又はナノ粒子である。
実施形態では、化学増幅基は、触媒、フルオロフォア、ナノ粒子又は比色色素を含む。実施形態では、化学増幅基は、触媒、フルオロフォア、ナノ粒子又は比色色素である。
実施形態では、増幅基(例えば増幅基104)は触媒を含む。実施形態では、増幅基(例えば増幅基104)は触媒である。
実施形態では、増幅基(例えば増幅基104)はフルオロフォアを含む。実施形態では、増幅基(例えば増幅基104)はフルオロフォアである。例示的なフルオロフォアには、全体が参照により本明細書に組み込まれる、国際出願PCT/US16/42589号の表1に記載されているものが含まれる。
実施形態では、増幅基(例えば増幅基104)は比色色素を含む。実施形態では、増幅基(例えば増幅基104)は比色色素である。
実施形態では、増幅基(例えば増幅基104)は酵素を含む。実施形態では、増幅基(例えば増幅基104)は酵素である。
実施形態では、増幅基(例えば増幅基104)はナノ粒子を含む。実施形態では、増幅基(例えば増幅基104)はナノ粒子である。
実施形態では、増幅基(例えば増幅基104)はランタニドを含む。
実施形態では、増幅基(例えば増幅基104)は、ユウロピウム、ストロンチウム、テルビウム、サマリウム又はジスプロシウムであるランタニドを含む。実施形態では、増幅基(例えば増幅基104)は、ユウロピウム、ストロンチウム、テルビウム、サマリウム及びジスプロシウムからなる群より選択されるランタニドを含む。
実施形態では、増幅基(例えば増幅基104)は有機フルオロフォアを含む。
実施形態では、増幅基(例えば増幅基104)は、配位錯体であるフルオロフォアを含む。
実施形態では、増幅基(例えば増幅基104)はユウロピウム配位錯体を含む。実施形態では、配位錯体はユウロピウム配位錯体である。実施形態では、増幅基(例えば増幅基104)はルテニウム配位錯体を含む。実施形態では、配位錯体はルテニウム配位錯体である。実施形態では、増幅基(例えば増幅基104)はレニウム配位錯体を含む。実施形態では、配位錯体はレニウム配位錯体である。実施形態では、増幅基(例えば増幅基104)はパラジウム配位錯体を含む。実施形態では、配位錯体はパラジウム配位錯体である。実施形態では、増幅基(例えば増幅基104)は白金配位錯体を含む。実施形態では、配位錯体は白金配位錯体である。
実施形態では、増幅基(例えば増幅基104)は、ケミルミノフォア、量子ドット、酵素、鉄配位触媒、ユウロピウム配位錯体、ルテニウム配位錯体、レニウム配位錯体、パラジウム配位錯体、白金配位錯体、サマリウム配位錯体、テルビウム配位錯体又はジスプロシウム配位錯体を含む。
実施形態では、増幅基(例えば増幅基104)はケミルミノフォアを含む。実施形態では、増幅基(例えば増幅基104)は量子ドットを含む。実施形態では、増幅基(例えば増幅基104)は酵素を含む。実施形態では、増幅基(例えば増幅基104)は鉄配位触媒を含む。実施形態では、増幅基(例えば増幅基104)はユウロピウム配位錯体を含む。実施形態では、増幅基(例えば増幅基104)はルテニウム配位錯体を含む。実施形態では、増幅基(例えば増幅基104)はレニウム配位錯体を含む。実施形態では、増幅基(例えば増幅基104)はパラジウム配位錯体を含む。実施形態では、増幅基(例えば増幅基104)は白金配位錯体を含む。実施形態では、増幅基(例えば増幅基104)はサマリウム配位錯体を含む。実施形態では、増幅基(例えば増幅基104)はテルビウム配位錯体を含む。実施形態では、増幅基(例えば増幅基104)はジスプロシウム配位錯体を含む。
実施形態では、増幅基104は、
実施形態では、増幅基104は、
実施形態では、増幅基104は、触媒又は酵素である。実施形態では、増幅基は、ホースラディッシュペルオキシダーゼ、アルカリホスファターゼ、アセチルコリンエステラーゼ、グルコースオキシダーゼ、β-D-ガラクトシダーゼ又はβ-ラクタマーゼである。
実施形態では、増幅基104はホースラディッシュペルオキシダーゼである。
実施形態では、増幅基104は、フルオロフォア又は比色色素である。
適切なフルオロフォア及び比色色素は当業者に周知であり、The Molecular Probes(R)Handbook:A Guide to Fluorescent Probes and Labeling Technologies,11th Ed.(2010)及びGomes,Fernandes,and Lima J.Biochem.Biophys.Methods 65(2005)pp 45-80に記載されており、これらは全体が参照により本明細書に組み込まれる。例示的なフルオロフォアには、例えば国際公開WO2016/015027号及び国際出願PCT/US16/42589号に記載されているものも含まれ、これらの各々は全体が参照により本明細書に組み込まれる。
適切なフルオロフォア又は比色色素の例には、臭化エチジウム、ヨウ化プロピジウム、SYTOXグリーン、フェナントリジン、アクリジン、インドール、イミダゾール、シアニン、TOTO、TO-PRO、SYTO、5-カルボキシ-2,7-ジクロロフルオレセイン、5-カルボキシフルオレセイン(5-FAM)、5-カルボキシナフトフルオレセイン、5-カルボキシテトラメチルローダミン(5-TAMRA)、5-FAM(5-カルボキシフルオレセイン)、5-HAT(ヒドロキシトリプタミン)、5-ROX(カルボキシ-X-ローダミン、6-カルボキシローダミン6G、7-アミノ-4-メチルクマリン、7-アミノアクチノマイシンD(7-AAD)、7-ヒドロキシ-4-メチルクマリン、9-アミノ-6-クロロ-2-メトキシアクリジン、ACMA(9-アミノ-6-クロロ-2-メトキシアクリジン)、アクリジン、アレクサフルオル、アリザリン、アロフィコシアニン(APC)、AMCA(アミノメチルクマリン)、ボディピー、カルボキシ-X-ローダミン、カテコールアミン、フルオレセイン(FITC)、ヒドロキシクマリン、リサミンローダミン、モノブロモビマン、オレゴングリーン、フィコエリトリン、SYTO、チアジカルボシアニン(DiSC3)、チオフラビン、X-ローダミンC又はテトラメチルローダミンイソチオシアネートが含まれるが、これらに限定されない。
実施形態では、増幅基104は、有機金属化合物、遷移金属錯体又は配位錯体である。例示的な例は、EP0180492、EP0321353、EP0539435、EP0539477、EP0569496、EP139675、EP64484、US4,283,382、US4,565,790、US4,719,182、US4,735,907、US4,808,541、US4,927,923、US5,162,508、US5,220,012、US5,324,825、US5,346,996、US5,373,093、US5,432,101、US5,457,185、US5,512,493、US5,527,684、US5,534,622、US5,627,074、US5,696,240、US6,100,394、US6,340,744、US6,524,727、US6,717,354、US7,067,320、US7,364,597、US7,393,599、US7,456,023、US7,465,747、US7,625,930、US7,854,919、US7,910,088、US7,955,859、US7,968,904、US8,007,926、US8,012,609、US8,017,254、US8,018,145、US8,048,659、US8,067,100、US8,129,897、US8,174,001、US8,183,586、US8,193,174、US8,221,719、US8,288,763、US8,362,691、US8,383,249、US8,492,783、US8,632,753、US8,663,603、US8,722,881、US8,754,206、US8,890,402、US8,969,862、US9,012,034、US9,056,138、US9,118,028、US9,133,205、US9,187,690、US9,193,746、US9,312,496、US9,337,432、US9,343,685、US9,391,288及びUS9,537,107に記載されているが、これらに限定されず、これらは全体が参照により本明細書に組み込まれる。例示的な有機金属化合物、遷移金属錯体又は配位錯体には、例えば国際公開WO2016/015027号及び国際出願PCT/US16/42589号に記載されているものも含まれ、これらの各々は全体が参照により本明細書に組み込まれる。
実施形態では、増幅基104はランタニド配位錯体である。
実施形態では、ランタニド配位錯体は、ランタニド(例えばEu又はTb)と四座配位子との間の錯体である。
実施形態では、ランタニド配位錯体は、ランタニド(例えばEu又はTb)とクリプテート配位子との間の錯体である。
実施形態では、増幅基104は、ランタン(La)、セリウム(Ce)、プラセオジム(Pr)、ネオジム(Pm)、サマリウム(Sm)、ユウロピウム(Eu)、ガドリニウム(Gd)、テルビウム(Tb)、ジスプロシウム(Dy)、ホルミウム(Ho)、エルビウム(Er)、ツリウム(Tm)、イッテルビウム(Yb)、ルテチウム(Lu)、ルテニウム(Ru)、ロジウム(Rh)、パラジウム(Pd)、オスミウム(Os)、イリジウム(Ir)又は白金(Pt)の配位錯体である。
実施形態では、増幅基104は、原子番号57のランタンから原子番号71のルテチウムまでの15元素の群(ランタニド)と、原子番号21のスカンジウム及び原子番号39のイットリウムの2つの追加元素とからなる17元素を集合的に指す、希土類金属の配位錯体である。希土類金属の具体的な例には、ユウロピウム、テルビウム、ランタン、セリウム、プラセオジム、ネオジム、プロメチウム、サマリウム、ガドリニウム、ジスプロシウム、ホルミウム、エルビウム、ツリウム、イッテルビウム、ルテチウム、スカンジウム及びイットリウムが含まれ、ユウロピウム及びテルビウムが好ましく、ユウロピウムがより好ましい。
実施形態では、増幅基104は、ランタニド(例えばユウロピウム又はテルビウム)とジエチレントリアミン四酢酸又はクリプテート配位子との配位錯体である。
実施形態では、増幅基104は、ランタニド(例えばユウロピウム又はテルビウム)とジエチレントリアミン四酢酸との配位錯体である。
実施形態では、増幅基104は、ランタニド(例えばユウロピウム又はテルビウム)とクリプテート配位子との配位錯体である。
実施形態では、シグナル伝達剤(例えば化学的シグナル伝達剤)は、
実施形態では、シグナル伝達剤は、造影剤を形成するために1つ以上の常磁性金属キレートを含み得る。好ましい常磁性金属イオンは、原子番号21~29、42、44又は57~83を有する。これには、1つ、より好ましくは5つ以上の不対電子及び少なくとも1.7ボーア磁子の磁気モーメントを有する遷移金属又はランタニド系列のイオンが含まれる。好ましい常磁性金属には、クロム(III)、マンガン(II)、マンガン(III)、鉄(II)、鉄(III)、コバルト(II)、ニッケル(II)、銅(II)、プラセオジム(III)、ネオジム(III)、サマリウム(III)、ガドリニウム(III)、テルビウム(III)、ジスプロシウム(III)、ホルミウム(III)、エルビウム(III)、ユウロピウム(III)及びイッテルビウム(III)が含まれる。さらに、本発明のシグナル伝達剤は、1つ以上の超常磁性粒子も含み得る。
実施形態では、シグナル伝達剤は、蛍光化合物と共に又は蛍光化合物の一部として金属錯体に含まれる1つ以上の金属を含み得る:金属錯体には、中心金属としてAl、Zn、Be等;Tb、Eu若しくはDyなどの希土類金属;又はPt若しくはIrなどの遷移金属を有し、配位子としてオキサジアゾール、チアジアゾール、フェニルピリジン、フェニルベンゾイミダゾール若しくはキノリン構造を有する金属錯体、例えばアルミニウムキノリノール錯体、ベンゾキノリノールベリリウム錯体、ベンゾオキサゾール亜鉛錯体、ベンゾチアゾール亜鉛錯体、アゾメチル亜鉛錯体、ポルフィリン亜鉛錯体及びユウロピウム錯体などが含まれる。
実施形態では、シグナル伝達剤は、高いルミネセンス量子効率及び長いルミネセンス減衰時間(>100ナノ秒)を特徴とする発光団(供与体)を含み得る。好ましい発光団は、パラジウム、ロジウム、白金、ルテニウム、オスミウム、希土類(特にユウロピウム及びランタン)のカチオン性有機金属錯体である。これらの有機金属錯体の有機部分は、例えばポルフィリン、ビピリジル、フェナントロリン又は他の複素環式化合物の群からの配位子で構成され得る。
実施形態では、微生物表面に結合することができるシグナル伝達剤は、抗体(例えばモノクローナル若しくはポリクローナル抗体)、修飾抗体(例えばビオチン化モノクローナル抗体、ビオチン化ポリクローナル抗体、ユウロピウムキレート抗体、ホースラディッシュペルオキシダーゼ結合抗体)、抗体変異体(例えばFab:抗原結合フラグメント(一方の腕);F(ab’)2:ヒンジ領域を含む抗原結合フラグメント(両方の腕);Fab’:ヒンジ領域を含む抗原結合フラグメント(一方の腕);scFv:一本鎖可変フラグメント;di-scFv:二量体一本鎖可変フラグメント;sdAb:単一ドメイン抗体;二重特異性モノクローナル抗体;三官能性抗体及びBiTE:二重特異性T細胞誘導体)、WGA-ビオチン、ポリミキシンB-ビオチン、レクチン、天然ペプチド、合成ペプチド、合成及び/若しくは天然リガンド、合成及び/若しくは天然ポリマー、合成及び/若しくは天然糖ポリマー、炭水化物結合タンパク質及び/若しくはポリマー、糖タンパク質結合タンパク質及び/若しくはポリマー、荷電小分子、他のタンパク質、バクテリオファージ並びに/又はアプタマーを含む。
本明細書で使用される場合、「抗体」という用語は、任意の本明細書に記載される種類の抗体、修飾抗体若しくは抗体フラグメント、又は当技術分野で公知の種類の抗体、修飾抗体若しくは抗体フラグメントを指す。したがって、「抗体を含むシグナル伝達剤」は、例として、未修飾モノクローナル抗体、Fabフラグメント及び三官能性抗体を含むシグナル伝達剤を含む。
実施形態では、微生物表面に結合することができるシグナル伝達剤は、ランタニド配位錯体、ビオチン、抗体及び/又は酵素を含む。
実施形態では、微生物表面に結合することができるシグナル伝達剤は、抗体、レクチン、天然ペプチド、合成ペプチド、合成及び/若しくは天然リガンド、合成及び/若しくは天然ポリマー、合成及び/若しくは天然糖ポリマー、炭水化物結合タンパク質及び/若しくはポリマー、糖タンパク質結合タンパク質及び/若しくはポリマー、荷電小分子、他のタンパク質、バクテリオファージ並びに/又はアプタマーを含む構造を含む又は前記構造から形成される。
実施形態では、微生物表面に結合することができるシグナル伝達剤は、ランタニド配位錯体及び/又は酵素とストレプトアビジン及び/又は抗体及び/又はアプタマーを含む増幅基104を含む。
実施形態では、微生物表面に結合することができるシグナル伝達剤は、ポリクローナル及び/又はモノクローナル抗体を含む結合部分を含む。
実施形態では、微生物表面に結合することができるシグナル伝達剤は、修飾抗体を含む結合部分を含む。例示的な修飾抗体には、ビオチン化モノクローナル抗体、ビオチン化ポリクローナル抗体、ユウロピウムキレート-抗体及びホースラディッシュペルオキシダーゼ結合抗体が含まれる。
実施形態では、微生物表面に結合することができるシグナル伝達剤は、抗体変異体を含む結合部分を含む。例示的な抗体変異体には、Fab:抗原結合フラグメント(一方の腕);F(ab’)2:ヒンジ領域を含む抗原結合フラグメント(両方の腕);Fab’:ヒンジ領域を含む抗原結合フラグメント(一方の腕);scFv:一本鎖可変フラグメント;di-scFv:二量体一本鎖可変フラグメント;sdAb:単一ドメイン抗体;二重特異性モノクローナル抗体;三官能性抗体及びBiTE:二重特異性T細胞誘導体が含まれる。
実施形態では、微生物表面に結合することができるシグナル伝達剤は、WGA-ビオチン又はポリミキシンB-ビオチンを含む。
実施形態では、微生物表面に結合することができるシグナル伝達剤は、合成及び/又は天然リガンド及び/又はペプチドを含む結合部分を含む。
実施形態では、リガンド及び/又はペプチドは、ビス(亜鉛-ジピコリルアミン)、TATペプチド、セリンプロテアーゼ、カテリシジン、カチオン性デキストリン、カチオン性シクロデキストリン、サリチル酸、リジン及びこれらの組み合わせから選択される。
実施形態では、微生物表面に結合することができるシグナル伝達剤は、合成及び/又は天然ポリマー及び/又は糖ポリマーを含む結合部分を含む。
実施形態では、天然及び/又は合成ポリマーは、直鎖又は分岐であり、アミロペクチン、ポリ(N-[3-(ジメチルアミノ)プロピル]メタクリルアミド)、ポリ(エチレンイミン)、ポリ-L-リジン、ポリ[2-(N,N-ジメチルアミノ)エチルメタクリレート]及びこれらの組み合わせから選択される。
実施形態では、天然及び/又は合成ポリマー及び/又は糖ポリマーは、キトサン、ゼラチン、デキストラン、トレハロース、セルロース、マンノース、カチオン性デキストラン及びシクロデキストラン、第四級アミン、ピリジニウムトリブロミド、ヒスチジン、リジン、システイン、アルギニン、スルホニウム、ホスホニウム、又はコブロックポリマー、グラフトポリマー及び交互ポリマーを含むがこれらに限定されない、これらの組み合わせを含むがこれらに限定されない部分を含む。
実施形態では、微生物表面に結合することができるシグナル伝達剤は、マンノース結合レクチン、他のレクチン、アネキシン及びこれらの組み合わせから選択される糖タンパク質を含む結合部分を含む。
実施形態では、微生物表面に結合することができるシグナル伝達剤は、
抗体;及び
ユウロピウム配位錯体
を含む。
実施形態では、微生物表面に結合することができるシグナル伝達剤は、NH2-PEG-ビオチン(2K)、NH2-PEG-ビオチン(4K)、スルホ-NHS-ビオチン、WGA-ビオチン又はポリミキシンB-ビオチンを含むリンカー基Lを含む。
実施形態では、微生物表面に結合することができるシグナル伝達剤は、
実施形態では、微生物表面に結合することができるシグナル伝達剤は、
以下の実施例において及び本明細書及び図面を通して開示されるように、本発明は、少なくとも:
・12の細菌種の75株(グラム陰性桿菌によるβ-ラクタムを含む)について重大な/非常に重大なエラーを伴わずに、ここで開示される方法とCLSI標準法との間で>89.9%のMIC一致(±1希釈);
・直接陽性血液培養についてのここで開示される方法とCLSI標準血液培養試料処理との間で同等のMIC;
・グラム陽性及び陰性種の2×103CFU/mlまでの検出;
・シグナル伝達剤による微生物の非特異的結合;
・ユウロピウム製剤の使用;
・データ出力を伴う半自動化装置の使用
を提供する。
本発明に関連するさらなる教示は、EP139675;EP64484;US2013/0217063;US2014/0278136;US2014/0323340;US2014/0363817;US2015/0064703;US2015/0337351;US2016/0010138;US3,798,320;US4,565,790;US4,647,536;US4,808,541;US4,927,923;US5,457,185;US5,489,401;US5,512,493;US5,527,684;US5,627,074;US5,665,554;US5,695,946;US6,284,470;US6,385,272;US6,844,028;US7,341,841;US7,629,029;US7,868,144;US8,178,602;US8,895,255;PCT/US2016/042589;及びWO/2016015027の1つ以上に記載されており、これらの各々は全体が参照により本明細書に組み込まれる。
上記の態様及び実施形態のいずれもが、以下の実施例を含む、図面、発明の概要及び/又は詳細な説明に開示されている任意の他の態様又は実施形態と組み合わせることができる。
本明細書に記載されているものと類似又は同等の方法及び材料を本発明の実施又は試験において使用することができるが、適切な方法及び材料を以下で述べる。本明細書で言及されるすべての公表文献、特許出願、特許及び他の参考文献は、これらの全体が参照により本明細書に組み込まれる。本明細書で引用される参考文献は、特許請求される本発明の先行技術であるとは認められない。さらに、材料、方法及び実施例は例示に過ぎず、限定を意図するものではない。
[実施例1]
本発明は、抗菌剤の最小阻害濃度(MIC)の迅速で正確な決定を提供する。
この実施例では、スタフィロコッカス・アウレウス(Staphylococcus aureus)又はシュードモナス・アエルギノーサ(Pseudomonas aeruginosa)に対する抗菌剤の最小阻害濃度(MIC)を迅速に決定するための本発明を、S.アウレウス(S.aureus)又はP.アエルギノーサ(P.aeruginosa)の一晩のインキュベーションを必要とする標準的な方法と比較した。
スタフィロコッカス・アウレウス(Staphylococcus aureus)(ATCC 29213株)の培養物を、ミューラーヒントン(MH)ブロスを用いて激しく振とうしながら37℃で一晩増殖させた。同時に、2つの滅菌96ウェルマイクロプレートを、32μg/ml~0.125μg/mlのクリンダマイシンの段階希釈液及びクリンダマイシンなしの対照を用いて、すべてMHブロス中で調製した。次いで、一晩培養物からのS.アウレウス(S.aureus)濃度を、600nmでの光学密度読み取りのためにマクファーランド標準技術を用いて5×105CFU/mlに設定した。本明細書で開示される発明(例えば「高速AST」技術)を使用して抗菌剤の感受性を決定するために、調製した抗菌剤希釈液を、各ウェルがそれぞれ200μLを含むマイクロプレートに接種し、37℃で3.5時間インキュベートするか、又はOD600対照については37℃で一晩(>12時間)インキュベートした。「高速AST」マイクロプレートを振とうインキュベータから4時間後に取り出し、ポリクローナルウサギ抗S.アウレウス(S.aureus)抗体(Fitzgerald Industries International,Inc.)のホースラディッシュペルオキシダーゼ(HRP)コンジュゲートを各ウェルに添加した。次いで、結合を可能にするためにプレートを室温で20分間振とうし、この後、残存する無傷の細菌をペレット化するために、マイクロプレートを4,000×gで遠心分離した。次いで、MHブロスを吸引し、滅菌ブロスを合計3回の洗浄のために添加した。最後の吸引の後、3,3’,5,5’-テトラメチルベンジジン(TMB)及び過酸化水素(ThermoFisher)からなる安定化された展開溶液を添加し、マイクロプレートリーダー(Vmax、Molecular Devices)を用いて650nm及び450nmでの光学密度を10分間観測した。一晩のインキュベーション後、OD600対照のマイクロプレートをインキュベータから取り出し、600nmでの光学密度を直接読み取った(Vmax、Molecular Devices)。最後に、図5に示すように、データからCLSI標準法によってMICを決定した。両方の技術によって決定されたMICは同じである:0.125μg/ml。
同様に、シュードモナス・アエルギノーサ(Pseudomonas aeruginosa)(ATCC株27853)の培養物を、MHブロスを用いて激しく振とうしながら37℃で一晩増殖させた。同時に、2つの滅菌96ウェルマイクロプレートを、32μg/ml~0.125μg/mlのセフタジジムの段階希釈液及びセフタジジムなしの対照を用いて、すべてMHブロス中で調製した。次いで、一晩培養物からのP.アエルギノーサ(P.aeruginosa)濃度を、600nmでの光学密度読み取りのためにマクファーランド標準技術を用いて5×105CFU/mlに設定した。本明細書で開示される発明を使用して抗菌剤の感受性を決定するために、調製した抗菌剤希釈液を、各ウェルがそれぞれ200μLを含むマイクロプレートに接種し、37℃で3.5時間インキュベートするか、又はOD600対照については37℃で一晩(>12時間)インキュベートした。「高速AST」マイクロプレートを振とうインキュベータから4時間後に取り出し、ポリクローナルウサギ抗P.アエルギノーサ(P.aeruginosa)抗体(Abcam)のホースラディッシュペルオキシダーゼ(HRP)コンジュゲートの溶液を各ウェルに添加した。次いで、結合を可能にするためにプレートを室温で20分間振とうし、この後、残存する無傷の細菌をペレット化するために、マイクロプレートを4,000×gで遠心分離した。次いで、MHブロスを吸引し、滅菌ブロスを合計3回の洗浄のために添加した。最後の吸引の後、3,3’,5,5’-TMB及び過酸化水素(ThermoFisher)からなる安定化された展開溶液を添加し、マイクロプレートリーダー(Vmax、Molecular Devices)を用いて650nm及び450nmでの光学密度を10分間観測した。図6に示すデータは、検出溶液とのインキュベーションの開始後5分の時点から描画されている。一晩のインキュベーション後、OD600対照のマイクロプレートをインキュベータから取り出し、600nmでの光学密度を直接読み取った(Vmax、Molecular Devices)。最後に、図6に示すように、データからCLSI標準法によってMICを決定した。両方の技術によって決定されたMICは同じである:4μg/ml。
MICを決定する上での本発明の正確さは、データの下方領域の勾配(図5及び図6)が本発明と一晩の培養物とでほぼ同一であることで明らかに実証される。
これらのデータは、本発明が、細菌培養物の一晩のインキュベーションを必要とする標準的な方法と少なくとも同程度に正確な抗菌剤のMICを正確に決定できることを示す。
[実施例2]
本発明は、抗菌剤耐性細菌に対する抗菌剤の最小阻害濃度(MIC)の迅速で正確な決定を提供する。
この実施例では、本発明を使用して、それぞれ抗菌剤耐性であるP.アエルギノーサ(P.aeruginosa)、S.アウレウス(S.aureus)及びE.コリ(E.coli)株に対するMICを、抗菌剤感受性であるP.アエルギノーサ(P.aeruginosa)、S.アウレウス(S.aureus)及びE.コリ(E.coli)株に対するMICと比較した。
感受性P.アエルギノーサ(P.aeruginosa)株、ATCC 27853のMICを実施例1で述べたように決定したが、重要な違いは、イミペネムを抗菌剤として使用した(32μg/ml~0.125μg/mlの段階希釈を使用した)ことであった。耐性P.アエルギノーサ(P.aeruginosa)株、ATCC BAA-2108のMICも同様に決定した。両方の菌株に同じ96ウェルマイクロプレートを使用し、48ウェルを各々の菌株に割り当てた。この実験を3回繰り返して同様の結果を得、得られたデータを図7に示す。感受性株に対するMICは2μg/mlであり、耐性株のMICは32μg/mlである。
S.アウレウス(S.aureus)については、抗菌剤としてメチシリンを使用し、耐性株ATCC 43300を使用したことを除き、実施例1で上述したのと同じ手順を使用した。E.コリ(E.coli)については、E.コリ(E.coli)感受性(25922)株及び耐性(35218)株を使用し、抗菌剤としてアンピシリンを使用し、及びシグナル伝達剤が細菌に結合することを可能にする化学的部分としてポリクローナルウサギ抗E.コリ(E.coli)抗体(Abcam)のHRPコンジュゲートを使用したことを除き、P.アエルギノーサ(P.aeruginosa)について上述したのと同じ手順を用いた。検出溶液との5分間のインキュベーション後の「高速AST」値をOD600の一晩対照と比較し、データを図8にまとめている。
これらのデータは、本発明が、抗菌剤に耐性である細菌株及び抗菌剤に感受性である同じ細菌の株について、抗菌剤のMICを正確に区別できることを示す。
[実施例3]
本発明は、標準法に必要とされるよりも200倍濃縮されていない微生物濃度で検出可能なシグナルを提供する。
この実施例では、本発明において検出可能なシグナルを提供するのに必要な微生物濃度を、S.アウレウス(S.aureus)の一晩のインキュベーションを必要とする標準的な方法と比較した。
S.アウレウス(S.aureus)を実施例1で述べたように一晩培養した。一晩コロニーの段階希釈を96ウェルマイクロプレート中で行い、吸光度を600nmで読み取った。これらの値をマクファーランド標準と比較して、細菌濃度をCFU/mlとして得た。曲線の定量化可能な領域を図9に示す(OD600);実験を3回繰り返し、同様の結果を得た。同様の希釈系列のS.アウレウス(S.aureus)を、実施例2で述べたように、S.アウレウス(S.aureus)特異的シグナル伝達剤で20分間処理した。実施例2の手順に従って、微生物を遠心分離し、3回洗浄して、検出溶液を添加した。
図9において、得られた吸光度を、マクファーランド標準法で決定したS.アウレウス(S.aureus)濃度と比較して示す。「高速AST」シグナルは、矢印で示すように、Clinical Laboratory Standards Institute(CLSI)の標準AST実験の出発細菌濃度(すなわち5×105CFU/ml)から可視である。対照的に、光シグナルは~108CFU/mlまで正確な定量化ができない。
これらのデータは、本発明が、標準的な方法に必要とされる濃度よりも200倍低い微生物培養濃度で、検出可能で利用可能なシグナルを提供できることを示す。
[実施例4]
本発明は、病原菌の複数の種及び株にわたってCLSI参照法から得られるものと同様のMIC値を、CLSI法に必要な時間よりも有意に短い時間で提供する。
この実施例では、複数の病原性細菌に対する抗菌剤のMICを迅速に決定するための本発明を、Clinical Laboratory Standards Institute(CLSI)の方法と比較した。
図10に示すように、3.5時間のインキュベーション後に6つの細菌のMIC決定を得たが、CLSI AST参照法の決定は、16時間のインキュベーション後(アンピシリン処理培養物の場合)又は24時間のインキュベーション後(オキサシリン処理培養物の場合)に得られた。薬剤、シグナル伝達剤/化学的部分(「抗体-HRPコンジュゲート」)及び細菌株を図11に列挙する。シグナル伝達剤/化学的部分に関して、S.エピデルミディス(S.epidermidis)試験には小麦胚芽凝集素(WGA)HRPコンジュゲートを使用し、「高速AST」アッセイは上記実施例2の手順に従う。すべての臨床単離物は同定されていない試料であり、使用前に少なくとも2回継代培養した。以下の細菌種:E.コリ(E.coli)、S.アウレウス(S.aureus)、P.アエルギノーサ(P.aeruginosa)、K.pneumoniae(K.ニューモニエ)、E.フェカリス(E.faecalis)、コアグラーゼ陰性スタフィロコッカス属(Staphylococci)、P.ミラビリス(P.mirabilis)、E.フェシウム(E.faecium)、E.クロカエ(E.clocae)及びA.バウマニ(A.baumannii)を含むがこれらに限定されない、合計87の個々の試料を試験した。この実施例で試験した細菌種(P.ミラビリス(P.mirabilis)を除く)が、合わせると、多くの臨床検査室で陽性血液培養物の>90%を占めることは注目に値する。したがって、本発明は、ヒト感染症に対する明らかな臨床的関連性を有する。本発明とCLSI法との間でMIC値は極めて類似しているが、本発明は3時間半のインキュベーションを必要とし、一方CLSI法は16時間又は24時間のインキュベーションを必要とする。
これらのデータは、本発明が、少なくともCLSI法と同程度に正確な抗菌剤のMICを正確に決定することができるが、MICを決定するのに有意に短い時間しか要さないことを示す;したがって、本発明は、患者に適切な治療レジメン、すなわち特定の抗菌剤及び特定の投与量が提供されるまでの時間を大幅に短縮する。
[実施例5]
S.アウレウス(S.aureus)及びK.ニューモニエ(K.pneumoniae)試料に関して、広範囲の抗菌剤にわたって、本発明はCLSI参照法から得られたものと同様のMIC値を有意に短い時間で提供する。
この実施例では、S.アウレウス(S.aureus)(グラム陽性細菌)又はK.pneumoniae(K.ニューモニエ)(グラム陰性菌)を処理する場合に、本発明を用いて複数の抗菌剤のMICを迅速に決定し、CLSI法によって得られたMIC値と比較した。
実施例2で上述した本発明の方法において、市販の全面乾燥抗菌プレートSensiTitre(R)(ThermoFisher)を使用し、4時間目に細菌生存率を評価した。代表的なS.アウレウス(S.aureus)及びK.pneumoniae(K.ニューモニエ)の結果を図12A~図12Cに示す。S.アウレウス(S.aureus)に関するエリスロマイシン実験並びにK.pneumoniae(K.ニューモニエ)に関するテトラサイクリン及びイミペネム実験を除き、本発明の「高速AST」から得られたMIC値とCLSI法で得られた結果との間には優れた一致があった;しかし、FDAによれば、本発明とCLSI結果との間の食い違いは「軽微なエラー」である;図12C参照。
これらのデータは、本発明が、2つの異なる細菌種について、少なくともCLSI法と同程度に正確な複数の抗菌剤のMICを正確に決定することができるが、MICを決定するのに有意に短い時間しか要さないことを示す;したがって、本発明は、患者に適切な治療レジメン、すなわち特定の抗菌剤及び特定の投与量が提供されるまでの時間を大幅に短縮する。
[実施例6]
本発明は、複数のS.アウレウス(S.aureus)及びE.コリ(E.coli)臨床株を使用し多種多様な抗菌剤にわたってCLSI参照法から得られたものと同様のMIC値を、有意に短い時間で提供する。
この実施例では、S.アウレウス(S.aureus)(グラム陽性細菌)又はE.コリ(E.coli)(グラム陰性菌)を処理する場合に、本発明を用いて複数の抗菌剤のMICを迅速に決定し、CLSI法によって得られたMIC値と比較した。
実施例5におけるように、これらの実験を行うためにSensititre(R)プレート(ThermoFisher)を使用した。ThermoFisherの指示に従って、接種物50μLを各ウェルに添加したことを除き、実施例2で述べたのと同じ手順を使用した。CLSI参照法を24時間(オキサシリン及びバンコマイシン)並びに18時間(レボフロキサシン)実施し、本発明(「高速AST」法)を用いたすべての実験は4時間(3時間半のインキュベーションを含む)で実施した。結果を図13A~図13C及び図14A~図14Dに示す。図13A~図13C及び図14A~図14Dの黒い線は、各抗菌剤についてのCLSIのブレークポイントを示す。基本的一致「EA」及び明確な一致「CA」は、FDAにより、「自動ASTシステムのためのクラスIIガイダンス資料(Class II Guidance Document for Automated AST Systems)」の中で定義されている。さらに、結果の一貫性を判定するために、S.アウレウス(S.aureus)の1つの臨床種について、上述したように複数の「高速AST」アッセイ及びCLSI標準参照アッセイを1ヶ月間にわたって実施した;図15参照。
これらのデータは、本発明(「高速AST」手順)が、S.アウレウス(S.aureus)及びE.コリ(E.coli)臨床株に関して複数の抗菌剤で試験した場合、CLSI参照法と一致する結果を提供するが、MICを決定するのに有意に短い時間しか要さないことを示す;したがって、本発明は、患者に適切な治療レジメン、すなわち特定の抗菌剤及び特定の投与量が提供されるまでの時間を大幅に短縮する。
[実施例7]
本発明は、抗菌剤耐性細菌に対する複数の抗菌剤のMICの迅速で正確な決定を提供する。
この実施例では、本発明を用いて、抗菌剤耐性であるE.コリ(E.coli)株に対する複数の抗菌剤のMICを、抗菌剤感受性であるE.コリ(E.coli)株のMICと比較した。
エシェリキア・コリ(Escherichia coli)(QC株、ATCC 25922)及び臨床耐性E.コリ(E.coli)(「臨床」)の両方を、ミューラーヒントン(MH)ブロス中標準的な滅菌条件下で、振とうしながら37℃で一晩培養した。次いで、一晩培養物からのE.コリ(E.coli)濃度を、600nmでの光学濃度の読み取りのためにマクファーランド標準技術を用いて5×105CFU/mlに設定した。同時に、2つの滅菌96ウェルマイクロプレートを、指定の抗菌剤(下記参照)及び抗菌剤なし(生理食塩水)対照の段階希釈液を用いて、すべてMHブロス中で調製した。本発明(「高速AST」技術)を用いた測定のために、調製した抗菌剤希釈液を、各ウェルがそれぞれ200μLを含むマイクロプレートに接種し、37℃で3時間45分間インキュベートした。「高速AST」マイクロプレートを振とうインキュベータから3時間45分後に取り出し、ペレット化するために2500gで2.5分間遠心分離した。次いで、MHブロスを吸引し、両方のマイクロプレートの各ウェルに水100μLを添加した。次に、化学的部分(ここではユウロピウム-クリプテート製剤)10μLを各ウェルに添加し(20ng/ウェルになるように)、5%グルタルアルデヒド(シグナル伝達剤として)10μLを各ウェルに添加した。次いで、2つのマイクロプレートを300rpmで30分間振とうした。この後、両方のプレートを2500gで2.5分間遠心分離してペレット化した。溶液を吸引し、PBS-トゥイーン200μLの洗浄液を各ウェルに添加し、続いて遠心分離してペレット化した。溶液の吸引後、PBS-トゥイーン200μLの2回目の同じ洗浄を実施し、続いて最終的な遠心分離を行ってペレット化した。次いで、BioTek H1プレートリーダーで時間分解蛍光を用いてプレートを読み取った。この工程を、以下の抗菌製剤を用いて実施した:8μg/ml~0.12μg/mlの希釈濃度のイミペネム(図16);32μg/ml~0.25μg/mlの希釈濃度のアンピシリン(図17);32μg/ml~0.03μg/mlの希釈濃度のセフタジジム(図18);16μg/ml~0.06μg/mlの希釈濃度のゲンタマイシン(図19);8μg/ml~0.06μg/mlの希釈濃度のレボフロキサシン(図20);32μg/ml~0.5μg/mlの希釈濃度のトリメトプリム/スルファメトキサゾール(SXT)(図21);4μg/ml~0.015μg/mlの希釈濃度のシプロフロキサシン(図22)及び64μg/ml~0.12μg/mlの希釈濃度のセトリアキソン(図23)。
図16~図23に見られるように、エシェリキア・コリ(Escherichia coli)(QC株、ATCC 25922)及び臨床耐性E.コリ(E.coli)(「臨床」)は、イミペネム、セフタジジム、ゲンタマイシン、レボフロキサシン、シプロフロキサシン及びセトリアキソンについては同様のMICを有していたが、アンピシリン及びトリメトプリム/スルファメトキサゾール(SXT)に関しては、2つの株は類似しないMICを有していた。したがって、このデータは、臨床耐性E.コリ(E.coli)株が、アンピシリン及びトリメトプリム/スルファメトキサゾール(SXT)に対して耐性であることを示す。したがって、患者がこの株(又は類似の株)による感染を呈する場合、アンピシリン及びトリメトプリム/スルファメトキサゾール(SXT)は投与すべきではない;代わりに、イミペネム、セフタジジム、ゲンタマイシン、レボフロキサシン、シプロフロキサシン及びセトリアキソンを投与すべきである。
これらのデータは、本発明が、1つ以上の抗菌剤に耐性である細菌の臨床的に関連する株に対する抗菌剤のMICと、抗菌剤に感受性である同じ細菌の株に対する抗菌剤のMICとを正確に区別できることを示す;したがって、本発明は、標準的な方法と比較して大幅に短縮された時間量で、患者に適切な治療レジメン、すなわち特定の抗菌剤及び特定の投与量を提供することができる。
[実施例8]
本発明は、抗菌剤感受性細菌に対する複数の抗菌剤のMICの迅速で正確な決定を提供する。
この実施例では、本発明を用いて、抗菌剤感受性であるS.アウレウス(S.aureus)株に対する複数の抗菌剤のMICを決定した。
S.アウレウス(S.aureus)(QC株29213)を、ミューラーヒントン(MH)ブロス中、標準的な滅菌条件下で振とうしながら37℃で一晩培養した。次いで、一晩培養物からのS.アウレウス(S.aureus)濃度を、600nmでの光学密度読み取りのためにマクファーランド標準技術を用いて5×105CFU/mlに設定した。同時に、2つの滅菌96ウェルマイクロプレートを、指定の抗菌剤(下記参照)及び抗菌剤なし(生理食塩水)対照の段階希釈液を用いて、すべてMHブロス中で調製した。
本発明(「高速AST」技術)を用いた測定のために、調製した抗菌剤希釈液を、各ウェルがそれぞれ100μLを含むマイクロプレートに接種し、37℃で3時間45分間インキュベートした。「高速AST」マイクロプレートを振とうインキュベータから3時間45分後に取り出し、ペレット化するために2500xgで2.5分間遠心分離した。次いで、MHブロスを吸引し、25mM PBS 100μLを両方のマイクロプレートの各ウェルに添加した。次に、化学的部分(ここではユウロピウム-クリプテート製剤)10μLを各ウェルに添加し(20ng/ウェルになるように)、0.005%グルタルアルデヒド(シグナル伝達剤として)10μLを各ウェルに添加した。次いで、2つのマイクロプレートを300rpmで30分間振とうした。この後、両方のプレートを2500xgで2.5分間遠心分離してペレット化した。溶液を吸引し、PBS-トゥイーン200μLの洗浄液を各ウェルに添加し、続いて遠心分離してペレット化した。溶液の吸引後、PBS-トゥイーン200μLの2回目の同じ洗浄を実施し、続いて最終的な遠心分離を行ってペレット化した。PBS-トゥイーン200μLを各ウェルに添加した。次いで、BioTek H1プレートリーダーで時間分解蛍光を用いてプレートを読み取った。この工程を、以下の抗菌製剤を用いて実施した:32μg/ml~0.25μg/mlの希釈濃度のバンコマイシン(図24);8μg/ml~0.0625μg/mlの希釈濃度のペニシリン(図25)及び16μg/ml~0.0125μg/mlの希釈濃度のテイコプラニン(図26)。
図24~図26に見られるように、S.アウレウス(S.aureus)(QC株29213)に関して、本発明は、標準的なCLSI参照方法から得られたものと同様のMICを決定した:バンコマイシン:0.5~2μg/ml;ペニシリン:0.25~2μg/ml及びテイコプラニン:0.25~1μg/ml。
これらのデータは、本発明が複数の抗菌剤のMICを正確に決定できることを示す;したがって、本発明は、標準的な方法と比較して大幅に短縮された時間量で、患者に適切な治療レジメン、すなわち特定の抗菌剤及び特定の投与量を提供することができる。
[実施例9]
本発明は、継代培養及び一晩増殖インキュベーションを必要とせずに、血液培養試料から直接、抗菌剤のMICの迅速で正確な決定を提供する。
この実施例では、血液培養試料から直接、抗菌剤のMICを迅速に決定するために本発明を使用した。
E.コリ(E.coli)、S.アウレウス(S.aureus)及びK.ニューモニエ(K.pneumoniae)の各々について1つの臨床試料を得た。単離物を寒天斜面上で輸送し、継代培養して、-80℃で保存した。試料を冷凍庫から取り出し、室温に温め、5%ヒツジ血液トリプシン大豆寒天(TSA)ペトリ皿(ThermoFisher)上に画線接種した。ペトリ皿を35℃のインキュベータに一晩入れた。単一コロニーを採取し、画線接種工程を新しいプレート上で繰り返し、続いて2回目の35℃での一晩インキュベーションを行った。合計3~5コロニーを採取し、滅菌生理食塩水(Hardy Diagnostics)1mL中に分散させ、600nmでの光学密度測定(Molecular Devices M2)によって濃度を決定した。試料を、蓋付きフラスコにおいて、滅菌カチオン調整ミューラーヒントンブロス(MHB、Hardy Diagnostics)40mL中で2CFU/mlに2段階で希釈した。
BD BACTEC(R)血液培養システムの性能を模倣するために、フラスコを35℃で一晩振とうインキュベータに入れた。フラスコを10時間後に4℃に置き、この時点でE.コリ(E.coli)の濃度は~1×108CFU/mlであると測定された。これは、BD BACTEC及びbioMerieux BacT/Alertなどの市販の血液培養システムが陽性血液培養物と記録するのに近い濃度である。10時間のインキュベーション時間は、血液培養試料を5%ヒツジ血液TSAペトリ皿上に画線接種し、これらを35℃で一晩インキュベートして、コロニー数を測定することによって決定した。
この「陽性」血液培養物をTSAプレート上に画線接種し、35℃で一晩インキュベートすることによって継代培養「対照」試料を採取した。次いで、先に述べたように、標準的なCLSI微量液体希釈参照法を実施した。
次いで、SepsiTyper(Bruker Daltonics)プロトコルに従って、遠心分離に基づく分離を行った。簡単に述べると、溶解緩衝液(Bruker Daltonics)1mLを、1×108CFU/mlのE.コリ(E.coli)を含むMHBブロス5mLに添加した。混合物を6つの微量遠心管に分取し、10秒間ボルテックスして、次いで13,000rpmで2分間遠心した。上清を取り出して廃棄し、洗浄緩衝液(Bruker)1mLを各々の管に添加して、管を13,000rpmで1分間遠心分離した。再び上清を取り出して廃棄した。各ペレットを、ピペットを上下させることによって滅菌生理食塩水500μLに再懸濁した。溶液を混合し、Promega Bactitre-Glo(TM)細菌細胞生存率キットを用いて細菌濃度を測定した。
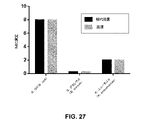
試料を約5×105CFU/mlの濃度でMHBに希釈した。次に、「高速AST」アッセイ(実施例2で述べたように)を実施し、MIC測定を比較した。臨床試料に関する「高速AST」法は、継代培養を必要とする標準的な方法と同様のMIC値を提供した;図27及び図28参照。
これらのデータは、本発明(「高速AST」手順)が臨床試料に直接使用された場合、一晩増殖の前に継代培養工程を必要とする標準的なMIC決定方法と一致する結果を提供することを示す;したがって、本発明は、患者に適切な治療レジメン、すなわち特定の抗菌剤及び特定の投与量が提供されるまでの時間を大幅に短縮する。
[実施例10]
ユウロピウムにコンジュゲートしたストレプトアビジンは、グラム陽性菌に特異的に結合するビオチン化小麦胚芽凝集素に結合する。
この実施例では、ユウロピウムを、グラム陽性菌に特異的に結合する小麦胚芽凝集素を含むシグナル伝達剤中の化学的部分として使用した。
細菌(S.アウレウス(S.aureus))を、pH6のMES緩衝液中、1×105~1×109の範囲の濃度で96ウェルプレートに接種した。細菌を含む各ウェル及び対応する対照ウェルに、ビオチン化小麦胚芽凝集素(Sigma)2μgを添加し、選択したレポーターによるウェル内の細菌の外側の標識化を促進するために、反応溶液を15分間インキュベートした。次いで、市販のストレプトアビジン-ユウロピウム(例えばPerkin-Elmerからの)を0.4μg/mlのウェル当たり最終濃度になるように添加した。さらに15分間インキュベートした後、上清中の非結合レポーターを残しつつプレートの底部の細菌をペレット化するために、Thermo Scientific Heraeus Multifuge X3を使用して2500xgの速度で2.5分間遠心分離した。次いで、洗浄緩衝液を添加する前に、BioTek Multiflo Xプレート洗浄機を用いてプレートを吸引し、上清及び未反応のレポーターを除去した。未反応レポーターを完全に除去するために、この洗浄手順をさらに2回繰り返した。最後に、吸引したウェルに、読み取り緩衝液を添加した後、デルフィア増強溶液を添加した。次いで、プレートを15分間インキュベートしてユウロピウムを増強させた後、図29に示すように、BioTek H1プレートリーダーで時間分解蛍光を用いてユウロピウムを測定した。
これらのデータは、シグナル伝達剤中の化学的部分としてのユウロピウムの使用が、溶液中の細菌濃度を正確に定量化できることを示す。
[実施例11]
ユウロピウムにコンジュゲートしたストレプトアビジンは、グラム陰性菌に特異的に結合するビオチン化ポリミキシンBに結合する。
この実施例では、ユウロピウムを、グラム陰性菌に特異的に結合するポリミキシンBを含むシグナル伝達剤中の化学的部分として使用した。
細菌(E.コリ(E.coli))を、pH6のMES緩衝液中、1×105~1×109の範囲の濃度で96ウェルプレートに接種した。細菌を含む各ウェル及び対応する対照ウェルに、ビオチン化ポリミキシン(Hycult Biosciences)を最終希釈1:200になるように添加し、選択したレポーターによるウェル内の細菌の外側の標識化を促進するために、反応溶液を15分間インキュベートした。次いで、市販のストレプトアビジン-ユウロピウム(例えばPerkin-Elmerからの)を0.4μg/mlのウェル当たり最終濃度になるように添加した。さらに15分間インキュベートした後、上清中の非結合レポーターを残しつつプレートの底部の細菌をペレット化するために、Thermo Scientific Heraeus Multifuge X3を使用して2500xgの速度で2.5分間遠心分離した。次いで、洗浄緩衝液を添加する前に、BioTek Multiflo Xプレート洗浄機を用いてプレートを吸引し、上清及び未反応のレポーターを除去した。未反応レポーターを完全に除去するために、この洗浄手順をさらに2回繰り返した。最後に、吸引したウェルに、読み取り緩衝液を添加した後、デルフィア増強溶液を添加した。次いで、プレートを15分間インキュベートしてユウロピウムを増強させた後、図30に示すように、BioTek H1プレートリーダーで時間分解蛍光を用いてユウロピウムを測定した。
これらのデータは、シグナル伝達剤中の化学的部分としてのユウロピウムの使用が、溶液中の細菌濃度を正確に定量化できることを示す。
[実施例12]
ユウロピウム検出器は、より大きなシグナル範囲のMICデータ、したがって、より正確なMICデータを提供する。
この実施例は、シグナル伝達剤中の化学的部分(細菌に特異的に結合する抗体を含む)として、ユウロピウムとHRPのMICを正確に決定する能力を比較した。
カチオン調整ミューラーヒントンブロスと適切な抗菌剤希釈液を含む96ウェルプレートを用いて、コロニーを生理食塩水に希釈して0.5のマクファーランド値に達するように細菌を調製し、これを分光光度計を用いて検証した。これを生理食塩水で1:20に希釈し、接種物10μlを各ウェルに添加した。細菌抗菌剤試験プレートを、150rpmで振とうしながら35℃で3時間45分間インキュベートした。このインキュベーション後、カチオン性磁気ビーズ及び抗S.アウレウス(S.aureus)抗体(ホースラディッシュペルオキシダーゼ又はユウロピウムのいずれかにコンジュゲートさせた;Cisbio Assaysによって実施されたカスタムコンジュゲーション)を各ウェルに添加し、20分間インキュベートした。自動プレート洗浄機を用いて磁気ビーズを捕捉し、各ウェルの内容物をPBS-トゥイーン20(0.1%)で3回洗浄した。次いで、時間分解蛍光(ユウロピウム)を用いてウェルを直接画像化するか、又はTMBを添加し、15分間インキュベートした後、1M硫酸の添加によって反応を停止させ、450nmでの吸光度を各ウェルについて測定した。
図31に示すように、化学的部分としてユウロピウムを使用することにより、HRPを化学的部分として用いて測定したMICよりも正確にSXTのMICが決定された。
これらのデータは、シグナル伝達剤中の化学的部分としてのユウロピウムの使用が、抗菌剤のMICを正確に決定できることを示す。
[実施例13]
細菌を非特異的に標識するユウロピウム製剤の実施形態は、細菌を検出し、細菌濃度を定量化するのに有効である。
この実施例では、ユウロピウム製剤は細菌に非特異的に結合する。
細菌(E.コリ(E.coli))を、pH6のMES緩衝液(ユウロピウムクリプテート-ジアミン)又はpH7.5のHEPES(ユウロピウムN1-アミノ)中、1e5~1e9の範囲の濃度で96ウェルプレートに接種した。細菌を含む各ウェル及び対応する対照ウェルに、ユウロピウムクリプテート-ジアミン(化合物(3);Cisbio)又はユウロピウムN1-アミノ(化合物(6);PerkinElmer)を66ng/ウェルで添加し、次いでEDC/NHS(0.1及び0.3mg/ml)又はグルタルアルデヒド(0.5%最終濃度)を指示通りに添加した。
選択したレポーターによるウェル内の細菌の外側の標識化を促進するために、反応溶液を30分間インキュベートした。次いで、上清中の非結合レポーターを残しつつプレートの底部の細菌をペレット化するために、Thermo Scientific Heraeus Multifuge X3を使用して2500xgの速度で2.5分間遠心分離した。次いで、洗浄緩衝液を添加する前に、BioTek Multiflo Xプレート洗浄機を用いてプレートを吸引し、上清及び未反応のレポーターを除去した。未反応のレポーターを完全に除去するために、この洗浄手順をさらに1回(Eu-クリプテート-ジアミン)又は2回(ユウロピウムN1-アミノ)繰り返した。ユウロピウム-クリプテート-ジアミンを含むウェルを読み取り緩衝液中で再構成し、図32に示すように、、BioTek H1プレートリーダーで時間分解蛍光を用いて読み取った。最後に、ユウロピウムN1-アミノで処理した吸引ウェルに、読み取り緩衝液を添加した後、デルフィア増強溶液を添加した。次いで、プレートを15分間インキュベートしてユウロピウムを増強させた後、図32に示すように、BioTek H1プレートリーダーで時間分解蛍光を用いてユウロピウムを測定した。
これらのデータは、ユウロピウム製剤が、細菌に非特異的に結合する場合、溶液中の細菌濃度を正確に定量化できることを示す。
[実施例14]
ユウロピウムは、細菌濃度を定量化する場合、細菌を非特異的に標識するためにイソチオシアネートを介してアミンに又はNH2を介してカルボン酸に結合することができる。
この実施例では、ユウロピウム製剤は細菌に非特異的に結合する。
クレブシエラ・ニューモニエ(Klebsiella pneumoniae)又はE.コリ(E.coli)を、pH6のMES緩衝液(ユウロピウムクリプテート-ジアミン;化合物(3))又はpH7.5のHEPES(ユウロピウムITC;化合物(4))中1×105~1×109の範囲の濃度で96ウェルプレートに接種した。細菌を含む各ウェル及び対応する対照ウェルに、ユウロピウムクリプテート-ジアミン(Cisbio)又はユウロピウムITC(PerkinElmer)を66ng/ウェルで添加し、次にユウロピウムクリプテートを含むウェルにEDC/NHS(0.1及び0.3mg/ml)を添加した。
選択したレポーターによるウェル内の細菌の外側の標識化を促進するために、反応溶液を30分間インキュベートした。次いで、上清中の非結合レポーターを残しつつプレートの底部の細菌をペレット化するために、Thermo Scientific Heraeus Multifuge X3を使用して2500xgの速度で2.5分間遠心分離した。次いで、洗浄緩衝液を添加する前に、BioTek Multiflo Xプレート洗浄機を用いてプレートを吸引し、上清及び未反応のレポーターを除去した。未反応のレポーターを完全に除去するために、この洗浄手順をさらに1回(ユウロピウムクリプテート-ジアミン)又は2回(PerkinElmer)繰り返した。ユウロピウムクリプテート-ジアミンを含むウェルを読み取り緩衝液中で再構成し、図33に示すように、BioTek H1プレートリーダーで時間分解蛍光を用いて読み取った。最後に、Eu-N1で処理した吸引ウェルに、読み取り緩衝液を添加した後、デルフィア増強溶液を添加した。次いで、プレートを15分間インキュベートしてユウロピウムを増強させた後、図33に示すように、BioTek H1プレートリーダーで時間分解蛍光を用いてユウロピウムを測定した。
これらのデータは、ユウロピウム製剤が、細菌に非特異的に結合する場合、溶液中の細菌濃度を正確に定量化できることを示す。
[実施例15]
グルタルアルデヒドは、ユウロピウム-クリプテートを細菌表面に非特異的に連結するために使用することができる。
この実施例では、ユウロピウム製剤は、グルタルアルデヒドを含む細菌に非特異的に結合する。
クレブシエラ・ニューモニエ(Klebsiella pneumoniae)、E.コリ(E.coli)又はスタフィロコッカス・アウレウス(Staph aureus)を、pH6のMES緩衝液中1×105~1×109の範囲の濃度で96ウェルプレートに接種した。細菌を含む各ウェル及び対応する対照ウェルに、ユウロピウムクリプテート-ジアミン(化合物(3);Cisbio)を66ng/ウェルで添加し、次いでユウロピウムクリプテートを含むウェルにグルタルアルデヒドの5%溶液を添加した。
選択したレポーターによるウェル内の細菌の外側の標識化を促進するために、反応溶液を30分間インキュベートした。次いで、上清中の非結合レポーターを残しつつプレートの底部の細菌をペレット化するために、Thermo Scientific Heraeus Multifuge X3を使用して2500xgの速度で2.5分間遠心分離した。次いで、洗浄緩衝液を添加する前に、BioTek Multiflo Xプレート洗浄機を用いてプレートを吸引し、上清及び未反応のレポーターを除去した。未反応のレポーターを完全に除去するためにこの洗浄手順を1回繰り返しした。ユウロピウムクリプテート-ジアミンを含むウェルを読み取り緩衝液中で再構成し、図34に示すように、BioTek H1プレートリーダーで時間分解蛍光を用いて読み取った。
これらのデータは、ユウロピウム製剤が、細菌に非特異的に結合する場合、溶液中の細菌濃度を正確に定量化できることを示す。
[実施例16]
EDC/NHSは、ユウロピウム-クリプテートを細菌表面に非特異的に結合するために使用できる。
この実施例では、ユウロピウム製剤は、EDC/NHSを含む細菌に非特異的に結合する。
クレブシエラ・ニューモニエ(Klebsiella pneumoniae)又はE.コリ(E.coli)を、pH6のMES緩衝液中1×105~1×109の範囲の濃度で96ウェルプレートに接種した。細菌を含む各ウェル及び対応する対照ウェルに、ユウロピウムクリプテート-ジアミン(化合物(3);Cisbio)を66ng/ウェルで添加し、次いでユウロピウムクリプテートを含むウェルにEDC/NHS(0.1及び0.3mg/ml)を添加した。
選択したレポーターによるウェル内の細菌の外側の標識化を促進するために、反応溶液を30分間インキュベートした。次いで、上清中の非結合レポーターを残しつつプレートの底部の細菌をペレット化するために、Thermo Scientific Heraeus Multifuge X3を使用して2500xgの速度で2.5分間遠心分離した。次いで、洗浄緩衝液を添加する前に、BioTek Multiflo Xプレート洗浄機を用いてプレートを吸引し、上清及び未反応のレポーターを除去した。未反応のレポーターを完全に除去するためにこの洗浄手順を1回繰り返しした。ユウロピウムクリプテート-ジアミンを含むウェルを読み取り緩衝液中で再構成し、図35に示すように、BioTek H1プレートリーダーで時間分解蛍光を用いて読み取った。
これらのデータは、ユウロピウム製剤が、細菌に非特異的に結合する場合、溶液中の細菌濃度を正確に定量化できることを示す。
[実施例17]
非特異的にクリプテート標識した細菌へのグルタルアルデヒド洗浄サイクルの影響。
この実施例では、グルタルアルデヒドを含む種々の洗浄を用いてユウロピウム製剤を細菌に非特異的に結合させる。
E.コリ(E.coli)又はS.アウレウス(S.aureus)を、pH6のMES緩衝液中1×105~1×109の範囲の濃度で96ウェルプレートに接種した。細菌を含む各ウェル及び対応する対照ウェルに、ユウロピウムクリプテート-ジアミン(化合物(3);Cisbio)を66ng/ウェルで添加し、次いでユウロピウムクリプテートを含むウェルにグルタルアルデヒドの5%溶液を添加した。
選択したレポーターによるウェル内の細菌の外側の標識化を促進するために、反応溶液を30分間インキュベートした。次いで、上清中の非結合レポーターを残しつつプレートの底部の細菌をペレット化するために、Thermo Scientific Heraeus Multifuge X3を使用して2500xgの速度で2.5分間遠心分離した。次いで、洗浄緩衝液を添加する前に、BioTek Multiflo Xプレート洗浄機を用いてプレートを吸引し、上清及び未反応のレポーターを除去した。複数の洗浄が全体的なデータ品質に及ぼす影響を調べるために、この洗浄手順を2回繰り返した。ユウロピウムクリプテート-ジアミンを含むウェルを読み取り緩衝液中で再構成し、図36A~図36Cに示すように、BioTek H1プレートリーダーで時間分解蛍光を用いて読み取った。
これらのデータは、ユウロピウム製剤を、グルタルアルデヒドを含む種々の洗浄を用いて細菌に非特異的に結合させ得ることを示す。
[実施例18]
NH2-PEG-ビオチンとこれに続くストレプトアビジン-ユウロピウム(Eu-SAv)を用いた2段階標識化工程は、細菌を非特異的に標識することができる。
この実施例では、2段階工程を用いてユウロピウム製剤を細菌に非特異的に結合させる。
E.コリ(E.coli)を、pH6のMES緩衝液中1×105~1×109の範囲の濃度で96ウェルプレートに接種した。細菌を含む各ウェル及び対応する対照ウェルに、アミン-PEG-ビオチン(Laysan Bio)を1mg/ウェルで添加し、次にアミン-PEG-ビオチンを含むウェルにEDC/NHS(0.1及び0.3mg/ml)を添加した。ビオチン種によるウェル内の細菌の外側の官能基化を促進するために、反応溶液を15分間インキュベートした。各反応ウェルに、ストレプトアビジン-ユウロピウム(Eu-SAv)(PerkinElmer)を400ng/ウェルで添加した。ビオチンとストレプトアビジンとの間の結合を促進するために、反応溶液を15分間インキュベートした。次いで、上清中の非結合レポーターを残しつつプレートの底部の細菌をペレット化するために、Thermo Scientific Heraeus Multifuge X3を使用して2500xgの速度で2.5分間遠心分離した。次いで、洗浄緩衝液を添加する前に、BioTek Multiflo Xプレート洗浄機を用いてプレートを吸引し、上清及び未反応のレポーターを除去した。複数の洗浄が全体的なデータ品質に及ぼす影響を調べるために、この洗浄手順を2回繰り返した。Eu-SAvを含むウェルを読み取り緩衝液中で再構成し、図37に示すように、BioTek H1プレートリーダーで時間分解蛍光を用いて読み取った。
これらのデータは、ユウロピウム製剤を、NH2-PEG-ビオチンとこれに続くEu-SAvを含む2段階工程を用いて細菌に非特異的に結合させ得ることを示す。
[実施例19]
NHS-LC-LC-ビオチンとこれに続くEu-SAvによる2段階細菌標識化工程は、細菌を非特異的に標識することができる。
この実施例では、別の2段階工程を用いてユウロピウム製剤を細菌に非特異的に結合させる。
E.コリ(E.coli)を、pH6のMES緩衝液中1×105~1×109の範囲の濃度で96ウェルプレートに接種した。細菌を含む各ウェル及び対応する対照ウェルに、アミン-LC-LC-ビオチン(Thermo-Fisher)を1mg/ウェルで添加し、次にアミン-PEG-ビオチンを含むウェルにEDC/NHS(0.1及び0.3mg/ml)を添加した。ビオチン種によるウェル内の細菌の外側の官能基化を促進するために、反応溶液を15分間インキュベートした。各反応ウェルに、ストレプトアビジン-ユウロピウム(Perkin-Elmer)を400ng/ウェルで添加した。ビオチンとストレプトアビジンとの間の結合を促進するために、反応溶液を15分間インキュベートした。次いで、上清中の非結合レポーターを残しつつプレートの底部の細菌をペレット化するために、Thermo Scientific Heraeus Multifuge X3を使用して2500xgの速度で2.5分間遠心分離した。次いで、洗浄緩衝液を添加する前に、BioTek Multiflo Xプレート洗浄機を用いてプレートを吸引し、上清及び未反応のレポーターを除去した。複数の洗浄が全体的なデータ品質に及ぼす影響を調べるために、この洗浄手順を2回繰り返した。ユウロピウムクリプテート-ジアミンを含むウェルを読み取り緩衝液中で再構成し、図38に示すように、BioTek H1プレートリーダーで時間分解蛍光を用いて読み取った。
これらのデータは、ユウロピウム製剤を、NHS-LC-LC-ビオチンとこれに続くEu-SAvを含む2段階工程を用いて細菌に非特異的に結合させ得ることを示す。
[実施例20]
糸状菌を、>0.2ミクロン~<10ミクロンのサイズ範囲の細孔を有するフィルタシステムを用いて溶液から単離することができる;これにより、より正確な化学的感受性データが提供される。
この実施例は、抗菌剤処理に応答して糸状増殖を受けた細菌を排除するためのろ過を用いた実施形態を示す。
特に、グラム陰性桿菌は、細胞壁作用性抗菌剤(β-ラクタムなど)の亜阻害濃度に応答して糸状増殖を最初に受ける。これらは最終的には阻害されるが、代謝的「体積」アプローチは、糸状増殖を受けた細菌から抗菌剤耐性細菌を区別することは極めて困難である。考慮されない場合、このような糸状増殖は、細菌を実際よりも耐性であると不適切に同定する。「体積」アプローチを用いて抗菌剤耐性を決定することの難しさは図39に認められる。
これを避けるために、一実施形態では、インキュベーション期間の最後に、各微量液体希釈液を、1つ以上の所定の細孔径を含むフィルタに充填する(図40参照)。細孔径は、複数の「正常」細菌がフィルタを通過することができるように選択されるが、特定の長さよりも大きい糸状菌は捕捉される。細孔径は、>0.2ミクロン及び<10ミクロンであり得る。
このフィルタは、96、384又は1586ウェルプレートなどの並行試料処理用に設計し得る。図40に示すように、AST工程の間にフィルタを適用し得る。
この実施例は、基本的に体積測定である従来の代謝アプローチとは対照的に、表面積によって無傷の細菌の存在を決定する迅速なASTプラットフォームを設計することの重要な利点をさらに示す。
[実施例21]
蛍光ナノ粒子を含むシグナル伝達剤を調製し、使用するための方法。
この実施例では、蛍光ナノ粒子を含むシグナル伝達剤を調製し、使用する方法を述べる。
最初に、透明ガラスシンチレーションバイアルにフルオレセインジラウレート(FL-DL)20mgを秤量し、エタノール1000mgを添加した。次いで、ボルテックスによってFL-DLをバイアル中で溶解した。この後、DSPE-PEG-2k-アミン(Laysan Bio)10mgをこの混合物に添加し、ボルテックスによって溶解した。別途に、脱イオン水40gをビーカーに秤量し、撹拌棒を加えた。次いで、ビーカーをマグネチックスターラ上に置き、200RPMで撹拌した。次に、エタノール溶液をビーカーに滴下し、この後の溶液をMicrofluidicsホモジナイザーに導入して、6000psiで1回処理した。次いで、得られた混合物に脱イオン水200gを添加し、タンジェンシャルフローフィルトレーション(TFF)を用いてナノ粒子を精製し、20mLまで約12倍濃縮して、次いでガラスシンチレーションバイアルに収集した。この収集したナノ粒子製剤を0.2μmフィルタでろ過し、ナノ粒子のサイズ及び濃度を、平均サイズ読み取り102nmでNanoSight(Malvern)によって決定した。
フルオロフォア含有ナノ粒子を、正に荷電した小分子で官能基化し、本発明に有用なシグナル伝達剤を形成した。
エシェリキア・コリ(Escherichia coli)(ATCC11303)及びアンピシリン耐性E.コリ(E.coli)(ATCC39936)の両方を、LBブロス中、標準的な滅菌条件下に37℃で培養した。600nmでの吸光度(マクファーランド)を測定することによって濃度を決定し、5×105CFU/mlの濃度を希釈によって設定した。次いで、アンピシリンを滅菌水に秤量し、滅菌3mL微量遠心管に適切な濃度で添加した。これらのアンピシリンで被覆された滅菌微量遠心管に、細菌及び8×108ナノ粒子/mlの濃度のナノ粒子の両方を添加した。次いで、管に蓋をして、連続振とうしながら37℃で1.5時間置いた後、これらを開放し、それぞれ0.2μmフィルタに通した。次に、各ろ液100μLを96ウェルプレートのウェルに添加し、展開溶液(エタノール中5%テトラメチルアンモニウムヒドロキシド)150μLを各ウェルに添加した。5分後、プレートを、SpectraMax M2マイクロプレートリーダー(Molecular Devices)において490nm励起/530nm発光で読み取った。
図41は、上記で調製したナノ粒子を含むシグナル伝達剤を用いたアッセイの結果を示す。ここで、エシェリキア・コリ(Escherichia coli)及びアンピシリン耐性E.コリ(E.coli)を、MICより十分高い濃度である100μg/mlのアンピシリンで処理した及びアンピシリンなしで処理した。無傷の細菌を0.2μmフィルタでのろ過によって除去した後、無傷の細菌と結合していない遊離シグナル伝達剤のアッセイを実施した。アンピシリンを含まない対照群は、アンピシリンで処理したアンピシリン耐性E.コリ(E.coli)群と同様に、低い蛍光シグナルを示す。MICより上のアンピシリンで処理したE.コリ(E.coli)は、蛍光の有意の増加を示し、この抗菌剤の有効性を示す。
図42は、様々なアンピシリン濃度についてのE.コリ(E.coli)のアッセイの結果を示す。アンピシリン濃度がMICより下の約15μg/mlである場合、蛍光シグナルは低く、この値で上昇し、この範囲内の抗菌剤の有効性を示す。
[実施例22]
本発明は、無傷の細菌を単離するために磁気ビーズを用いて実施することができる。
この実施例では、無傷の細菌に結合することができる作用物質と結合した磁気ビーズを用いて、無傷の細菌を溶液から単離する。
E.コリ(E.coli)に反応性の磁気ビーズを、製造者の指示(ThermoFisher)に従ってN-ヒドロキシスクシンイミジルエステル活性化1ミクロン磁気ビーズから調製した。簡単に述べると、供給されたビーズを磁気的に捕捉し、保存溶液を吸引した。次いで、ビーズを氷冷0.1M塩酸で洗浄し、続いてポリクローナルヤギ抗リポ多糖(LPS)抗体(Antibodies-Online Inc.)を添加した。反応物を2時間振とうし、最初の30分間は、製造者の指示に従って5分ごとにボルテックスした。次いでビーズを十分に洗浄し、使用時まで4℃でリン酸緩衝生理食塩水(pH 7.4)中に保存した。
シグナル伝達剤は、微生物に結合することができる部分(例えばE.コリ(E.coli)に結合する抗体)及びシグナルを提供する又はシグナルの生成に寄与することができる化学的部分(例えばホースラディッシュペルオキシダーゼ(HRP))を含む。
抗LPS磁気ビーズ及び抗E.コリ(E.coli)シグナル伝達剤を、MHブロス中のE.コリ(E.coli)のマクファーランド標準測定希釈系列に同時に添加した。反応を20分間進行させ、続いて96ウェルマイクロプレート磁気スタンド(V&P Scientific)で磁気ビーズを捕捉した。ウェルを3回洗浄し、続いて実施例1で述べた検出溶液を添加した。450nm及び650nmでの光学密度を10分間読み取った。5分目の値を図43にプロットする。
次いで、シグナル伝達剤及び官能基化磁気ビーズの添加によって実施例1の手順を使用した。しかし、ここでは、S.アウレウス(S.aureus)株はATCC12600であり、3つの抗菌剤:セフタジジム、オキサシリン及びバンコマイシンを使用した。
インキュベーション期間後、0.5μmサイズの固定カチオン電荷を有する磁気ビーズ(ChemiCell Fluidmag)をシグナル伝達剤と同時に添加した。ホウ酸塩緩衝液50μLの添加によってpHを~8.4に調整した。マイクロプレートをオービタルシェーカーで20分間撹拌した。次いで、マイクロプレートを、24個のネオジムN52磁性物質を含む磁気捕捉プレート上に置いた。次いで、MHブロスを吸引し、0.1%トゥイーン20を含むPBSを添加して合計3回洗浄した。最後の吸引後、3,3’,5,5’-テトラメチルベンジジン(TMB)及び過酸化水素(ThermoFisher)からなる安定化された展開溶液を添加し、650nm及び450nmでの光学密度をマイクロプレートリーダー(Vmax、Molecular Devices)で10分間観測した。図44に示すデータは、検出溶液とのインキュベーションの開始後5分の時点から描画されている。予想されたように、細菌細胞の溶解を引き起こす抗菌剤の量が増加すると、無傷の細菌の数が減少する。
これらのデータは、官能基化された磁性粒子が、無傷の細菌を捕捉することができ、抗菌剤処理後に無傷細菌の定量化を可能にし得る(シグナル伝達剤に結合した場合)ことを示す。このような磁気捕捉を、本発明における使用のために無傷の細菌を収集するために、他の分離技術と共に又は他の分離技術の代わりに使用し得る。
[実施例23]
官能基化された磁気ビーズによる無傷細菌の単離と比較した場合、細菌溶液の遠心分離は無傷細菌のより正確な計数を提供する。
この実施例では、官能基化磁気ビーズを用いて無傷の細菌を単離する方法(実施例21+に記載)を、遠心分離を用いて無傷の細菌を単離する方法と比較する。
官能基化された磁気ビーズを用いた無傷細菌の捕捉を上述したように実施した。遠心分離データのために、2500×gで2.5分間の遠心分離、手作業での吸引及びPBS-トゥイーンの添加の工程によって細菌を3回洗浄した。磁気ビーズは、遠心分離洗浄には使用しなかった。細菌を様々な濃度のバンコマイシン(「VAN」)で処理した。
図45は、遠心分離が、官能基化された磁気ビーズによる単離よりもはるかに高く、より正確な細菌数及びMICを提供することを示す。
これらのデータは、無傷の細菌を単離するための細菌培養物の遠心分離が、官能基化された磁性粒子を用いる方法よりも優れていることを示す。遠心分離を用いた単離を、本発明における使用のために無傷の細菌を収集するために、他の分離技術(例えば磁気単離)と共に又は他の分離技術の代わりに使用し得る。
[実施例24]
TAMLナノ粒子増幅剤による化学増幅は、標準的な光学検出装置を用いて1×103~1×108CFU/mlの範囲で、最適感受性でのシグナル伝達を可能にする。
この実施例では、テトラアミノ有機金属配位子(TAML(R))触媒を含むシグナル伝達剤を調製し、使用する方法を述べる。
薬物送達からの最先端のナノ粒子製剤技術及び環境に優しい化学からの小分子触媒に適合する、独自のナノ粒子増幅剤を用いて化学増幅が可能となる。各々の「ナノ標識」は、特定の配位子で官能基化されたポリマーシェルによって保護された>6×104の高密度に充填された鉄含有テトラアミノ有機金属配位子(TAML(R))触媒を含む(図46)。各TAML分子は、ゴールドスタンダードのイムノアッセイ酵素標識であるホースラディッシュペルオキシダーゼのモル活性の5倍以内のモル活性を有する(図46B)。特異的結合後、ナノ標識は、内容物を溶液中に放出するように化学的に誘発され、光シグナルの均一な触媒作用を可能にする。結合事象当たりの高い数の触媒は、標準的な酵素イムノアッセイに比べてわずか200個の無傷細菌の定量化(図46A)及び100倍の感受性増強(図46C)を可能にする。新しい検出技術の開発の必要性を取り除くことに加えて、標準的な光学的検出は、SensiTitreプレートなどの標準的な乾燥抗菌パネルマイクロプレートとの適合性を可能にする。