JP7009356B2 - ハンチンチンmRNAをターゲティングするオリゴヌクレオチド化合物 - Google Patents
ハンチンチンmRNAをターゲティングするオリゴヌクレオチド化合物 Download PDFInfo
- Publication number
- JP7009356B2 JP7009356B2 JP2018502624A JP2018502624A JP7009356B2 JP 7009356 B2 JP7009356 B2 JP 7009356B2 JP 2018502624 A JP2018502624 A JP 2018502624A JP 2018502624 A JP2018502624 A JP 2018502624A JP 7009356 B2 JP7009356 B2 JP 7009356B2
- Authority
- JP
- Japan
- Prior art keywords
- rna
- nucleotides
- seq
- gene
- rna molecule
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 0 COC1C(OC(*)N)=C(C=CP(O)(O)=O)O[C@]1N(C=CC(N1)=O)C1=O Chemical compound COC1C(OC(*)N)=C(C=CP(O)(O)=O)O[C@]1N(C=CC(N1)=O)C1=O 0.000 description 6
- JRZONRPMOSGDHY-UHFFFAOYSA-N CC(C)P(NCCCOCCOCCOCCOCC(COP(C(C)C)(O)=O)O)(O)=O Chemical compound CC(C)P(NCCCOCCOCCOCCOCC(COP(C(C)C)(O)=O)O)(O)=O JRZONRPMOSGDHY-UHFFFAOYSA-N 0.000 description 1
- VTVAFTBJHCAOQM-UHFFFAOYSA-N CCP(NCCCOCCOCCOCCOCC(COP(CC)(O)=O)O)(O)=O Chemical compound CCP(NCCCOCCOCCOCCOCC(COP(CC)(O)=O)O)(O)=O VTVAFTBJHCAOQM-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/113—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7088—Compounds having three or more nucleosides or nucleotides
- A61K31/713—Double-stranded nucleic acids or oligonucleotides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0085—Brain, e.g. brain implants; Spinal cord
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/10—Type of nucleic acid
- C12N2310/14—Type of nucleic acid interfering N.A.
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/31—Chemical structure of the backbone
- C12N2310/315—Phosphorothioates
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/32—Chemical structure of the sugar
- C12N2310/321—2'-O-R Modification
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/32—Chemical structure of the sugar
- C12N2310/322—2'-R Modification
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/34—Spatial arrangement of the modifications
- C12N2310/343—Spatial arrangement of the modifications having patterns, e.g. ==--==--==--
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/34—Spatial arrangement of the modifications
- C12N2310/344—Position-specific modifications, e.g. on every purine, at the 3'-end
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/34—Spatial arrangement of the modifications
- C12N2310/346—Spatial arrangement of the modifications having a combination of backbone and sugar modifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/35—Nature of the modification
- C12N2310/351—Conjugate
- C12N2310/3515—Lipophilic moiety, e.g. cholesterol
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/35—Nature of the modification
- C12N2310/351—Conjugate
- C12N2310/3517—Marker; Tag
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/35—Nature of the modification
- C12N2310/351—Conjugate
- C12N2310/3519—Fusion with another nucleic acid
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/50—Physical structure
- C12N2310/52—Physical structure branched
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2320/00—Applications; Uses
- C12N2320/10—Applications; Uses in screening processes
- C12N2320/11—Applications; Uses in screening processes for the determination of target sites, i.e. of active nucleic acids
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2320/00—Applications; Uses
- C12N2320/30—Special therapeutic applications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2320/00—Applications; Uses
- C12N2320/30—Special therapeutic applications
- C12N2320/32—Special delivery means, e.g. tissue-specific
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2320/00—Applications; Uses
- C12N2320/50—Methods for regulating/modulating their activity
- C12N2320/51—Methods for regulating/modulating their activity modulating the chemical stability, e.g. nuclease-resistance
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Chemical & Material Sciences (AREA)
- Genetics & Genomics (AREA)
- Biomedical Technology (AREA)
- Molecular Biology (AREA)
- General Health & Medical Sciences (AREA)
- Organic Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Pharmacology & Pharmacy (AREA)
- General Engineering & Computer Science (AREA)
- Animal Behavior & Ethology (AREA)
- Medicinal Chemistry (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Biochemistry (AREA)
- Biotechnology (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Epidemiology (AREA)
- Plant Pathology (AREA)
- Microbiology (AREA)
- Biophysics (AREA)
- Physics & Mathematics (AREA)
- Psychology (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Saccharide Compounds (AREA)
Description
本出願は、2016年1月31日出願の米国仮特許出願番号62/289,274号および2015年4月3日出願の米国仮特許出願番号62/142,731号に基づく優先権を主張し、これらの出願の全内容を、引用によりここに包含させる。
本発明は、国立衛生研究所(NIH)により与えられる認可番号NS038194およびTR000888のもとに政府援助を受けて実施された。政府は、本発明に一定の権利を有する。
本発明は、ハンチントン病の処置のための新規ハンチンチン標的および新規オリゴヌクレオチドに関する。
ハンチントン病、パーキンソン病およびアルツハイマー病を含む神経障害は、主要なまだ満たされていない医療上の必要性を代表する。一部の症例では、これらの疾患は一遺伝子性であり、オリゴヌクレオチド治療介入、例えば、RNA干渉(RNAi)の理想的な標的となる。RNAiは、細胞機序を再プログラムし、標的mRNAをオン・デマンドで発現停止および分解させるのに使用できる、短二本鎖RNA断片を含む基本メカニズムである。このテクノロジーは臨床的に進歩しており、ヒトの機能遺伝学の分野に大改革をもたらしている。
従って、ここに提供するのは、新規ハンチンチン標的配列である。新規ハンチンチン標的配列を標的とする新規RNA分子(例えば、siRNA)も提供される。該新規RNA分子(例えば、siRNA)は、効能および効力を、インビトロでの一次ニューロンおよびインビボでの単回低用量注射後のマウス脳の両方で示す。
本発明の前記のおよび他の特性および利点は、添付する図面と組み合わせて解説する、下記の説明的態様の詳細な説明からより完全に理解される。特許または出願書類は、カラーで提出した少なくとも一枚の図を含む。カラー図面を含むこの特許または特許出願公報は、請求と必要な費用の支払いにより、役所から提供される。
新規ハンチンチン標的配列が提供される。本発明の新規ハンチンチン標的配列を標的とする新規siRNAも提供される。
ポリグルタミン障害は、一般的遺伝子突然変により特徴付けられる疾患または障害の一群である。特に、本疾患または障害は、コード化タンパク質における、拡張した一続きのグルタミン残基を生じさせる、トリヌクレオチドCAGの拡張反復により特徴付けられる。ポリグルタミン障害は、疾患が神経細胞の進行性変性により特徴付けられる点で類似する。それらの類似性にも関わらず、ポリグルタミン障害は種々の染色体で生じ、故に、DNAの全く異なるセグメントで生じる。ポリグルタミン障害の例は、ハンチントン病、歯状核赤核淡蒼球ルイ体萎縮症、球脊髄性筋萎縮症、脊髄小脳失調症1型、脊髄小脳失調症2型、脊髄小脳失調症3型、脊髄小脳失調症6型および脊髄小脳失調症7型を含む。
ある態様において、本発明のRNAサイレンシング剤は、ハンチントン病の処置のための変異体ヒトハンチンチンタンパク質(htt)における多型(例えば一塩基多型)を標的とするよう設計される。
ハンチントン病と関連する疾患遺伝子は、ハンチンチンまたは(htt)と呼ばれる。ハンチンチン座位は大きく、180kbに及び、67エクソンからなる。ハンチンチン遺伝子は広範に発現され、正常発達に必要である。種々の胎児および成体組織において種々の相対的豊富さを示す、2つの選択的ポリアデニル化形態として発現される。大きなトランスクリプトは約13.7kbであり、主に成体および胎児脳で発現され、約10.3kbの小トランスクリプトはより広範に発現される。2つのトランスクリプトは、その3’非翻訳領域が異なる(Lin et al., 1993)。両メッセージは、3144アミノ酸を含む348キロダルトンタンパク質をコードすると予測される。ハンチントン病に至る遺伝的欠陥は、mRNAに新規性質を付与するかまたはタンパク質の機能を変えると考えられる。
ある態様において、siRNAは、次のように設計される。まず、標的遺伝子(例えば、htt遺伝子)、例えば、図8に示す標的配列の1以上の部分、例えば、標的遺伝子の5’非翻訳領域から10150、10146および/または10125を選択する。これらの部位でのmRNAの開裂は、対応する変異体タンパク質の翻訳を排除するはずである。センス鎖を、標的配列に基づき設計した(図8参照)。好ましくは、該部分(および対応するセンス鎖)は、約19~25ヌクレオチド、例えば、19、20、21、22、23、24または25ヌクレオチド含む。より好ましくは、該部分(および対応するセンス鎖)は、21、22または23ヌクレオチド含む。しかしながら、当業者は、19未満のヌクレオチドまたは25を超えるヌクレオチドの長さを有するsiRNAも、RNAiの介在に機能できることを認識する。従って、このような長さのsiRNAも、RNAiに介在する能力を保持する限り、本発明の範囲内である。長いRNAi剤は、ある哺乳動物細胞においてインターフェロンまたはPKR応答を惹起することが示されており、これは望ましくない可能性がある。好ましくは、本発明のRNAi剤はPKR応答を惹起しない(すなわち、十分に短い長さである)。しかしながら、長いRNAi剤は、例えば、PRK応答を産生できない細胞型またはPKR応答が代替的に手段により下方制御または減弱されている状況では有用であり得る。
本発明は、例えば、上記のとおりに設計された、siRNA分子を含む。本発明のsiRNA分子は化学的に合成できまたはインビトロでDNA鋳型からまたはインビボで例えば、shRNAからまたはインビトロ転写dsRNA鋳型を20、21または23bp二本鎖RNA介在RNAiのプールに開裂するための組み換えヒトダイサー(DICER)酵素の使用により、転写され得る。siRNA分子を、当分野で知られる任意の方法を使用して設計できる。
本発明は、抗ハンチンチンRNAサイレンシング剤(例えば、siRNAおよびshRNA)、該RNAサイレンシング剤を製造する方法およびハンチンチンタンパク質(例えば、変異体ハンチンチンタンパク質)のRNAサイレンシングのための該改善されたRNAサイレンシング剤(またはその一部)の使用のための方法(例えば、研究および/または治療方法)に関する。RNAサイレンシング剤はアンチセンス鎖(またはその一部)を含み、ここで、アンチセンス鎖は、RNA介在サイレンシング機序(例えばRNAi)に介在するのに十分な相補性をヘテロ接合一塩基多型に対して有する。
X-A(-L-B-L-A)j(-S-B-S-A)r(-S-B)t-OR
〔式中、Xは5’リン酸基であり;Aは、各々独立して2’-メトキシ-リボヌクレオチドであり;Bは、各々独立して2’-フルオロ-リボヌクレオチドであり;Lは、各々独立してホスホジエステルまたはホスホロチオエートリンカーであり;Sはホスホロチオエートリンカーでわり;Rは水素およびキャッピング基(例えば、アセチルのようなアシル)から選択され;jは4、5、6または7であり;rは2または3であり;tは0または1である。〕
を有するオリゴヌクレオチドである。
C-L-B(-S-A-S-B)m’(-P-A-P-B)n’(-P-A-S-B)q’(-S-A)r’(-S-B)t’-OR
〔式中、Cは疎水性分子であり;Aは各々独立して2’-メトキシ-リボヌクレオチドであり;Bは、各々独立して2’-フルオロ-リボヌクレオチドであり;Lはエチレングリコール、ホスホジエステルおよびホスホロチオエートの0~4反復単位からなる群から選択される1以上の部分を含むリンカーであり;Sはホスホロチオエートリンカーであり;Pはホスホジエステルリンカーであり;Rは水素およびキャッピング基(例えば、アセチルのようなアシル)から選択され;m’は0または1であり;n’は4、5または6であり;q’は0または1であり;r’は0または1であり;t’は0または1である。〕
を有する。
本発明のsiRNA分子は、センス鎖および相補的アンチセンス鎖からなる二本鎖であり、アンチセンス鎖は、htt mRNAに対してRNAiに介在するのに十分な相補性を有する。好ましくは、siRNA分子は約10~50以上のヌクレオチドの長さであり、すなわち、各鎖は10~50ヌクレオチド(またはヌクレオチドアナログ)を含む。より好ましくは、siRNA分子は各鎖で約16~30、例えば、16、17、18、19、20、21、22、23、24、25、26、27、28、29または30ヌクレオチドの長さを有し、ここで、鎖の一方は、標的領域に十分に相補性である。好ましくは、これらの鎖を、これらの鎖をアニールしたとき、二本鎖の一端または両端に1、2または3残基のオーバーハングが生じるように、鎖の末端に整列しない(すなわち、相補的塩基が反対の鎖に存在しない)少なくとも1、2または3塩基があるように、整列させる。好ましくは、siRNA分子は約10~50以上のヌクレオチドの長さを有し、すなわち、各鎖は10~50ヌクレオチド(またはヌクレオチドアナログ)含む。より好ましくは、siRNA分は、各鎖約16~30、例えば、16、17、18、19、20、21、22、23、24、25、26、27、28、29または30ヌクレオチドの長さを有し、ここで、鎖の一方は標的配列に実質的に相補性であり、他方の鎖は、第一鎖と同一または実質的に同一である。
本発明のsiRNA様分子は、RNAiまたは翻訳抑制により遺伝子サイレンシングを指示するためにmRNAの標的配列と“十分に相補的”である配列を有する(すなわち、配列を有する鎖を有する)。siRNA様分子はsiRNA分子に準じて設計されるが、センス鎖と標的RNAの間の配列同一性の程度はmiRNAとその標的の間で観察されるものに近似する。一般に、miRNA配列と対応する標的遺伝子配列の間の配列同一性の程度が下がるに連れて、RNAiではなく翻訳抑制により転写後遺伝子サイレンシングに介在する傾向が高まる。それ故に、代替的態様において、標的遺伝子の翻訳抑制による転写後遺伝子サイレンシングが望まれるとき、miRNA配列は、標的遺伝子配列と部分的相補性を有する。ある態様において、miRNA配列は、標的mRNAに分散している1以上の短配列(相補性部位)と部分的相補性を有する(例えば標的mRNAの3’-UTR内)(Hutvagner and Zamore, Science, 2002; Zeng et al., Mol. Cell, 2002; Zeng et al., RNA, 2003; Doench et al., Genes & Dev., 2003)。翻訳抑制の機序が協調的であるとき、複数相補性部位(例えば、2、3、4、5または6)がある態様において標的とされ得る。
ある特徴的態様において、本発明は、増強された選択性でhtt標的配列のRNAサイレンシングに介在できるshRNAを提供する。siRNAとは対照的に、shRNAはマイクロRNA(miRNA)の天然前駆体を模倣し、遺伝子サイレンシング経路の最初の部分で介入する。この理由のため、shRNAは、天然遺伝子サイレンシング経路全体を通して供給されることにより、遺伝子サイレンシングにより効率的に介在すると考えられる。
他の態様において、本発明のRNAサイレンシング剤は、miRNAの細胞間動員に有用な二機能性オリゴヌクレオチドテザーを含む。動物細胞は、転写後または翻訳後レベルで遺伝子発現を制御できる約22ヌクレオチドの非コーディングRNAである様々なmiRNAを発現する。miRNAをRISCに結合させ、それを標的mRNAに動員することにより、二機能性オリゴヌクレオチドテザーは、例えば、動脈硬化過程に関与する、遺伝子の発現を抑制できる。オリゴヌクレオチドテザーの使用は、特定の遺伝子の発現抑制のための、既存の技術を超えるいくつかの利点を提供する。第一に、ここに記載する方法は、内在性分子(しばしば豊富に存在する)、miRNAのRNAサイレンシングへの介在を可能とする。従って、ここに記載する方法は、RNAサイレンシングの介在に外来分子(例えば、siRNA)を導入する必要性をなくす。第二に、RNAサイレンシング剤、および、特に、連結部分(例えば、2’-O-メチルオリゴヌクレオチドのようなオリゴヌクレオチド)は、安定であり、かつヌクレアーゼ活性に抵抗性であるように製造できる。その結果、本発明のテザーは直接送達のために設計でき、細胞内で所望の薬剤を製造するよう設計された前駆体分子またはプラスミドの間接的送達(例えばウイルス)の必要性を取り除く。第三に、テザーおよびその各部分は、特異的mRNA部位および特異的miRNAと適合するように設計され得る。設計は細胞および遺伝子産物特異的であり得る。第四に、ここに開示する方法は、mRNAをインタクトとし、当業者が細胞それら自体の機序を使用して短パルスでタンパク質合成を遮断することを可能とする。その結果、RNAサイレンシングのこれらの方法は、高度に制御可能である。
ある例示的態様において、遺伝子発現(すなわち、htt遺伝子発現)は、htt遺伝子発現を効果的に阻害または減少させるために2以上の利用可能な3’末端の存在を可能にする、5’末端を経て連結した2以上の一本鎖アンチセンスオリゴヌクレオチドを含むオリゴヌクレオチドベースの化合物を使用して調節できる。このような連結オリゴヌクレオチドはまた遺伝子サイレンシングオリゴヌクレオチド(GSO)として知られている(例えば、その全体を全ての目的のために本明細書に引用により包含させる、Idera Pharmaceuticals, Incに譲渡されたUS8,431,544参照)。
本発明のある側面において、上記の本発明のRNAサイレンシング剤(またはその任意の部分)は、該薬剤の活性がさらに改善されるように修飾し得る。例えば、上記セクションIIのRNAサイレンシング剤を、下記修飾のいずれかで修飾し得る。修飾は、一部、さらなる標的識別増強、薬剤の安定性増強(例えば、分解阻止)、細胞の取り込み促進、標的効率増強、(例えば、標的への)結合における有効性改善、薬剤に対する患者耐容性改善および/または毒性軽減に役立つ。
ある態様において、本発明のRNAサイレンシング剤を、単一ヌクレオチド標的識別を増強するために、不安定化ヌクレオチドで置換し得る(2007年1月25日出願の米国出願11/698,689号および2006年1月25日出願の米国仮出願60/762,225号参照、これら両者は引用により本明細書に包含させる)。このような修飾は、標的mRNA(例えば機能獲得型変異体mRNA)に対するRNAサイレンシング剤の特異性に明らかに影響することなく、非標的mRNA(例えば野生型mRNA)に対するRNAサイレンシング剤の特異性を排除するのに十分であり得る。
ある態様において、本発明のRNAサイレンシング剤を、非対称設計規則により、介在RNAiにおける有効性および特異性の増強を促進するように変改し得る(米国特許8,309,704号、7,750,144号、8,304,530号、8,329,892号および8,309,705号参照)。このような変改は、アンチセンス鎖が優先的に標的mRNAの開裂または翻訳抑制をガイドし、それにより、標的開裂およびサイレンシングの効率を増加または改善するように、センス鎖のために、siRNAのアンチセンス鎖(例えば、本発明の方法を使用して設計されたsiRNAまたはshRNAから産生されたsiRNA)のRISCへのエントリーを促進する。好ましくは、RNAサイレンシング剤の非対称性は、RNAサイレンシング剤のアンチセンス鎖5’末端(AS 5’)とセンス鎖3’末端(S 3’)の間の塩基対強度を、該RNAサイレンシング剤のアンチセンス鎖3’末端(AS 3’)とセンス鎖5’末端(S ’5)の間の結合強度または塩基対強度に比して低減させることにより増強される。
本発明のRNAサイレンシング剤を、血清または細胞培養用増殖培地における安定性を改善するために修飾できる。安定性を増強するために、3’残基を分解に対して安定化でき、例えば、それらをプリンヌクレオチド、特にアデノシンまたはグアノシンヌクレオチドからなるように選択し得る。あるいは、ピリミジンヌクレオチドの修飾アナログによる置換、例えば、ウリジンの2’-デオキシチミジンによる置換は耐容性であり、RNA干渉の効率に影響しない。
他の態様において、RNAサイレンシング剤を、例えば、標的細胞(例えば、神経細胞)による細胞の取り込みを増強するために、化学的部分で修飾し得る。それ故に、本発明は、他の部分(例えばペプチドのような非核酸部分)、有機化合物(例えば、色素)などとコンジュゲートしたまたはコンジュゲートしていない(例えば、3’末端で)RNAサイレンシング剤を含む。コンジュゲーションは、当分野で知られる方法により、例えば、Lambert et al., Drug Deliv. Rev.: 47(1), 99-112 (2001)(ポリアルキルシアノアクリレート(PACA)ナノ粒子に充填された核酸を記載する);Fattal et al., J. Control Release 53(1-3):137-43 (1998)(ナノ粒子に結合した核酸を記載する);Schwab et al., Ann. Oncol. 5 Suppl. 4:55-8 (1994)(挿入剤、疎水性基、ポリカチオンまたはPACAナノ粒子に連結された核酸を記載する);およびGodard et al., Eur. J. Biochem. 232(2):404-10 (1995)(ナノ粒子に連結された核酸を記載する)の方法を使用して、達成できる。
他の物を、本発明のRNAサイレンシング剤にテザーできる。リガンドを、例えば、安定性、標的核酸とのハイブリダイゼーション熱力学、特定の組織または細胞型へのターゲティングまたは、例えば、エンドサイトーシス依存的または非依存的機序による細胞透過性の改善のためにRNAサイレンシング剤にテザーする。リガンドおよび関連する修飾は、配列特異性を増加し、結果として標的外ターゲティングを減少させ得る。テザーリガンドは、介入物として機能できる1以上の修飾塩基または糖を含み得る。これらは、好ましくは、RNAサイレンシング剤/標的二本鎖の隆起におけるような、内部領域に位置する。介入物は芳香族、例えば、多環式芳香族またはヘテロ環式芳香族化合物であり得る。多環式介入物は、スタッキング能を有することができ、2、3または4縮合環を有する系を含み得る。ここに記載する普遍的塩基は、リガンド上に挿入され得る。ある態様において、リガンドは、標的核酸の開裂により標的遺伝子阻害に寄与する開裂基を含み得る。開裂基は、例えば、ブレオマイシン(例えば、ブレオマイシン-A5、ブレオマイシン-A2またはブレオマイシン-B2)、ピレン、フェナントロリン(例えば、O-フェナントロリン)、ポリアミン、トリペプチド(例えば、lys-tyr-lysトリペプチド)または金属イオンキレート基であり得る。金属イオンキレート基は、例えば、Lu(III)またはEU(III)大環状複合体、Zn(II)2,9-ジメチルフェナントロリン誘導体、Cu(II)テルピリジンまたはアクリジンを含み得て、これは、Lu(III)のような遊離金属イオンにより隆起の部位での標的RNAの選択的開裂を促進できる。ある態様において、ペプチドリガンドを、例えば、隆起領域での、標的RNAの開裂促進のためにRNAサイレンシング剤にテザーできる。例えば、1,8-ジメチル-1,3,6,8,10,13-ヘキサアザシクロテトラデカン(シクラム)を、ペプチドにコンジュゲートさせて(例えば、アミノ酸誘導体により)、標的RNA開裂を促進できる。テザーリガンドは、RNAサイレンシング剤のハイブリダイゼーション性質改善または配列特異性改善をもたらし得る、アミノグリコシドリガンドであり得る。アミノグリコシドの例は、グリコシル化ポリリシン、ガラクトース化ポリリシン、ネオマイシンB、トブラマイシン、カナマイシンAおよびアミノグリコシドのアクリジンコンジュゲート、例えばNeo-N-アクリジン、Neo-S-アクリジン、Neo-C-アクリジン、Tobra-N-アクリジンおよびKanaA-N-アクリジンを含む。アクリジンアナログの使用は配列特異性を増加させ得る。例えば、ネオマイシンBは、DNAと比較してRNAに高親和性を有するが、低配列特異性である。アクリジンアナログ、neo-5-アクリジンは、HIV Rev応答配列(RRE)に対して増加した親和性を有する。ある態様において、アミノグリコシドリガンドのグアニジンアナログ(グアニジノグリコシド)を、RNAサイレンシング剤にテザーする。グアニジノグリコシドにおいて、アミノ酸のアミン基をグアニジン基に交換する。グアニジンアナログの結合は、RNAサイレンシング剤の細胞透過性を増加させる。テザーリガンドは、ポリアルギニンペプチド、ペプトイドまたはペプチド模倣体であってよく、これは、オリゴヌクレオチド剤の細胞の取り込みを増強できる。
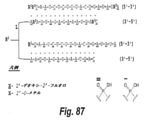
ある側面において、ここに提供されるのは、図81に示す式の化合物またはその薬学的に許容される塩であり、ここで、
R1は
R3は、各々独立して、図82に示すヌクレオチド間リンカーからなる群から選択され;
Lは、2部分を連結するリンカーであり、ここで、リンカーは、エチレングリコール鎖、アルキル鎖、ペプチド、RNA、DNA、
R1は
R3は、各々独立して、図82に示すヌクレオチド間リンカーからなる群から選択され;
Lは、2部分を連結するリンカーであり、ここで、リンカーは、エチレングリコール鎖、アルキル鎖、ペプチド、RNA、DNA、
Bは2以上のリンカー間の分岐点であり、ここで、分岐点はグリコール、アミノ酸または任意の多価有機種からなる群から選択される。
R3は、各々独立して、図82に示すヌクレオチド間リンカーからなる群から選択され;
Lは、2部分を連結するリンカーであり、ここで、リンカーは、エチレングリコール鎖、アルキル鎖、ペプチド、RNA、DNA、
Bは2以上のリンカー間の分岐点であり、ここで、分岐点はグリコール、アミノ酸またはあらゆる多価有機種からなる群から選択される。
R1は
R3は、各々独立して、図82に示すヌクレオチド間リンカーからなる群から選択され;
Lは、2部分を連結するリンカーであり、ここで、リンカーは、エチレングリコール鎖、アルキル鎖、ペプチド、RNA、DNA、
R2は、アルキル鎖(例えば、C1-6、C1-10、C1-20、C1-30またはC1-40)、ビタミン、リガンド、ペプチド、生理活性コンジュゲート(スフィンゴ糖脂質、多不飽和脂肪酸、セコステロイド、ステロイドホルモンまたはステロール脂質を含むが、これらに限定されない)、
R1は
R3は、各々独立して、図82に示すヌクレオチド間リンカーからなる群から選択され;
R2は、アルキル鎖(例えば、C1-6、C1-10、C1-20、C1-30またはC1-40)、ビタミン、リガンド、ペプチド、生理活性コンジュゲート(スフィンゴ糖脂質、多不飽和脂肪酸、セコステロイド、ステロイドホルモンまたはステロール脂質を含むが、これらに限定されない)、
本発明のRNAサイレンシング剤を、細胞(例えば、神経系細胞)に直接導入できる(すなわち、細胞内)、または細胞外に、空洞、間質性空間、生物の循環に、経口的に導入しまたは核酸含有溶液に細胞または生物を浸すことにより導入し得る。血管または血管外循環、血液またはリンパ系および脳脊髄液は、核酸を導入し得る部位である。
ある例示的態様において、組み換えアデノ随伴ウイルス(rAAV)およびその関連ベクターを使用して、1以上のsiRNAを細胞、例えば、神経系細胞(例えば、脳細胞)に送達できる。AAVは、多くの細胞型への感染が可能であるが、感染効率は、カプシドタンパク質の配列により決定される血清型により変わる。いくつかの天然AAV血清型が同定されており、血清型1~9が組み換えAAVに最も一般的に使用されている。AAV-2が最も広く研究され、公開されている血清型である。AAV-DJ系は、血清型AAV-DJおよびAAV-DJ/8を含む。これらの血清型を、インビトロで(AAV-DJ)および種々の細胞および組織においてインビボで(AAV-DJ/8)、改善された形質導入効率を有するハイブリッドカプシドを備えたAAVを産生するための複数AAV血清型のDNAシャッフリングにより作製した。
本発明は、全体または一部が、機能獲得型変異体タンパク質が原因の、疾患または障害のリスクにある(または疑われる)対象における予防および治療両方の方法を提供する。ある態様において、疾患または障害は、トリヌクレオチド反復疾患または障害である。他の態様において、疾患または障害は、ポリグルタミン障害である。好ましい態様において、疾患または障害は、ハンチンチンの発現と関連する障害であり、ハンチンチンの変改、特にCAG反復コピー数の増幅が、臨床的顕在化がハンチントン病患者に見られるものを含むように、ハンチンチン遺伝子(構造または機能)またはハンチンチンタンパク質(構造または機能または発現)の欠損をもたらす。
本発明は、下記のとおり予防および/または治療処置のための上記薬剤の使用に関する。従って、本発明のモジュレーター(例えば、RNAi剤)を、投与に適する医薬組成物に組み込み得る。このような組成物は、一般に核酸分子、タンパク質、抗体または調節化合物および薬学的に許容される担体を含む。ここで使用する用語“薬学的に許容される担体”は、医薬投与と適合する任意かつ全ての溶媒、分散媒体、コーティング、抗細菌および抗真菌剤、等張および吸収遅延剤などを含む。薬学的活性物質のためのこのような媒体および薬剤の使用は当分野で周知である。何らかの慣用の媒体または薬剤が活性化合物と非適合性でない限り、組成物におけるその使用が企図される。補助的活性化合物も組成物に組み込み得る。
ある他の側面において、本発明は、RNAサイレンシング剤、例えば、二本鎖RNAサイレンシング剤またはsRNA剤の医薬製剤を含む適当な容器を含むキットを提供する(例えば、sRNA剤に処理され得る前駆体、例えば、大型RNAサイレンシング剤またはRNAサイレンシング剤、例えば、二本鎖RNAサイレンシング剤またはsRNA剤またはその前駆体をコードするDNA)。ある態様において、医薬製剤の個々の成分を一容器に提供し得る。あるいは、医薬製剤の成分を2以上の容器、例えば、RNAサイレンシング剤製剤用の一容器および担体化合物の少なくとも一つの他の容器に別々に提供するのが望ましいことがある。キットを、一つの箱における1以上の容器のような多くの配置で包装し得る。異なる成分を、例えば、キットに備わった指示書に従い組み合わせ得る。成分を、ここに記載する方法で組み合わせて、例えば、医薬組成物を製造し、投与できる。キットはまた送達デバイスも含み得る。
インビボで良好な有効性および分布ならびにインビトロで一次ニューロンにおけるノックダウンの両方を提供する可能性を有する疎水性に修飾されたASO-siRNAハイブリッドを探索した。ハンチンチン遺伝子をmRNAノックダウンの標的として使用した。ハンチントン病は一遺伝子性であり(Mangiarini, L. et al. Exon 1 of the HTT gene with an expanded CAG repeat is sufficient to cause a progressive neurological phenotype in transgenic mice. Cell 87, 493-506 (1996))、疾患病理に至る多数の細胞の機序を有し(Zuccato, C., Valenza, M. & Cattaneo, E. Molecular Mechanisms and Potential Therapeutical Targets in Huntington's Disease. Physiological Reviews 90, 905-981 (2010))、将来的オリゴヌクレオチド治療の可能性の優れた候補となる。
hsiRNAは非対称化合物であり、短二本鎖領域(15塩基対)および一本鎖完全ホスホロチオエート化テイルを有する。これらの化合物における全ピリミジンは2’-フルオロおよび2’-O-メチル修飾され(安定化する)、パッセンジャー鎖の3’末端はTEG-コレステロールにコンジュゲートされた(図1A、図8)13。コレステロールコンジュゲートは迅速な膜結合を可能とし、一方一本鎖ホスホロチオエート化テイルは、慣用のアンチセンスオリゴヌクレオチドにより使用されるものに類似する機序による細胞内部移行に必要であった。Cy3標識hsiRNAの一次皮質ニューロンへの添加は、即時の(数分以内)細胞結合をもたらした(図1B)。興味深いことに、取り込みがまず優先的にデンドライトで観察され、続いて細胞体に再局在化した(図9)。取り込みは、皿の全細胞で均一であり、効率的内部移行が確認された。
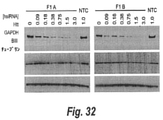
ハンチンチンmRNAをターゲティングする一団の94hsiRNA化合物(図8)を設計し、合成した。これらの配列は遺伝子にわたっており、GC含量、特異性および低シード相補性(compliment)頻度の評価(Anderson, E. M. et al. Experimental validation of the importance of seed complement frequency to siRNA specificity. RNA 14, 853-861 (2008))、miRNAシード含有配列の除去および熱力学バイアスの試験(Khvorova, A., Reynolds, A. & Jayasena, S. D. Functional siRNAs and miRNAs Exhibit Strand Bias. Cell 115, 209-216 (2003); Schwarz, D. S. et al. Asymmetry in the Assembly of the RNAi Enzyme Complex. Cell 115, 199-208 (2003))を含み、標準的siRNA設計パラメータに適合するように選択した(Birmingham, A. et al. A protocol for designing siRNAs with high functionality and specificity. Nat Protoc 2, 2068-2078 (2007))。50%を超える塩基が化学修飾され、インビボ安定性および免疫応答の最小化を提供した(Judge, A., Bola, G., Lee, A. & MacLachlan, I. Design of Noninflammatory Synthetic siRNA Mediating Potent Gene Silencing in Vivo. Molecular Therapy 13, 494-505 (2006))。修飾は、さらなる制限を配列空間に付し、ヒット率を低減した。ハンチンチンmRNA発現への影響を、QUANTIGENEアッセイによりHeLa細胞における1.5μM hsiRNA(受動的取り込み、製剤せず)暴露72時間後に測定し(図2)、7%の配列が70%を超えるサイレンシングを示した。機能的標的部位は、3’UTRの遠位部分を例外として遺伝子中に広がり、後にHeLa細胞における短httアイソフォームの優先的発現により説明された(Li, S. H. et al. Huntington's disease gene (IT15))。IC50値が、活性および異種間保存の一次スクリーンに基づき選択された16活性配列で同定された(図10)。IC50値は、受動的取り込みで90~766nM(製剤せず)および脂質介在取り込みで4~91pMの範囲であった(図8)。完全化学的最適化活性化合物は容易に同定され、はるかに小さいライブラリーが他の遺伝子の将来的スクリーニングに十分であるが、hit率は標的毎に異なる可能性がある。10150位をターゲティングするhsiRNA(HTT10150(すなわち、5’CAGUAAAGAGAUUAA 3’(配列番号1)))をさらなる試験に使用した。hsiRNA化学的骨格がHTT10150の有効性および効力に負に影響しないことを確実にするために、修飾および非修飾型の化合物を受動的および脂質介在サイレンシングアッセイの両方で試験した(図3)。予想通り、修飾配列のみが受動的取り込みによる細胞送達およびHttサイレンシングに成功し(IC50=82.2nM)、一方修飾および非修飾化合物両者は、脂質介在送達で類似IC50値を示し(それぞれ4pMおよび13pM)、hsiRNA骨格修飾がRNA誘発サイレンシング複合体(RISC)充填を妨害しないことを示唆した。
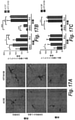
HTT10150を、FVBNマウスから単離した一次ニューロンにおけるmRNAサイレンシングについてさらに試験した。有効性を、皮質ニューロンに単純非製剤化化合物添加72時間および1週間後見られ(図4A)、最大サイレンシング(70%)は1.25μM濃度で見られた。HTT10150はまた一次線条体ニューロンで類似サイレンシングを示した(図4B)。タンパク質レベルを1週間後ウェスタンブロットで測定し(図14)、1.25μMの化合物で処置後タンパク質が85%減少するmRNAデータを確認した(図4C)。ALAMARBLUEアッセイで測定したハウスキーピング遺伝子(PPIB、GAPDH)および全体的細胞生存能(図11Bおよび14)はこれらの濃度で影響されなかった。他の実験において、細胞生存能へのわずかな影響が3μMで観察された。
RNAは、インビトロで種々のタイプのニューロンにより効率的に内在化される。選択hsiRNA、HTT10150を、さらにインビボで脳における遺伝子発現をサイレンシングする可能性について評価した。インビボ投与によるHTT10150の分布プロファイルを確認するために、12.5μgのCy3標識hsiRNA(配列について図8参照)を線条体内注射し、24時間後、脳を潅流し、切片化し、オリゴヌクレオチド分布を蛍光顕微鏡(ライカDM5500 - DFC365FX)で可視化した。同時に処理した人工CSF注入サンプルを、背景組織落射蛍光の対照のために設定した顕微鏡的造影設定のために使用した。
HTT10150有効性をインビボで決定するために、野生型FVBNマウスを、3~25μg(0.1~0.9mg/kg)の化合物の単回注射により線条体内投与し、mRNAサイレンシングを注射部位の同側性および対側性の両方で試験した。8動物を処置群あたり投与し、3の個々のパンチをmRNAおよびタンパク質定量化のために線条体の各側からとった。ハンチンチン発現レベルをQUANTIGENEアッセイで測定し、ハウスキーピング遺伝子に対して正規化した(オンライン方法に詳述)。
非修飾、ネイキッドsiRNAのコレステロール修飾が、siRNA脳分布改善のために先に使用されており、高用量での毒性は可能性限界と同定された。脳に対する非特異的化学関連効果の程度を評価するために、線条体における中型有棘ニューロンのドーパミン受容体発現の確立されたマーカーであり、神経細胞生存能を表すDARPP32発現を試験した。さらに、免疫応答を誘発する可能性を、hsiRNA注射によるミクログリア活性化の評価により実施した。
持続性サイレンシングが、21日間末期分化ニューロンで達成された(図24)。サイレンシングプラトーがRNAi(細胞質)で観察されたが、RNaseH(主に核)化合物で観察されなかった(図25)。観察されたプラトーは、htt遺伝子に特異的であった。htt mRNAの約60%が核に局在化した(図26)。
本研究は、一次細胞への送達のための疎水性に修飾されたsiRNAの使用が、神経細胞経路および神経障害の機能試験およびゲノム試験を可能にするための価値あるツールであることを示す。
細胞培養
HeLa細胞を、10%胎児ウシ血清(Gibco)および100U/mLペニシリン/ストレプトマイシン(Invitrogen)添加DMEM(Corning Cellgro)に播種し、37℃および5%CO2で増殖させた。細胞は15継代まで2~5日に分け、その後廃棄した。
細胞を、96ウェル組織培養処置プレートにおいて6%FBS添加DMEM中、10,000細胞/ウェルで播種した。hsiRNAをOptiMEM(Gibco)で2×最終濃度まで希釈し、50μL希釈hsiRNAを50μLの細胞に3%FBS最終まで添加した。細胞を、72時間、37℃および5%CO2でインキュベートした。
細胞を、96ウェル組織培養処置プレートにおいて、6%FBS添加DMEM中10,000細胞/ウェルで播種した。hsiRNAを、OptiMEMで4×最終濃度に希釈した。LIPOFECTAMINE RNAIMAX Transfection Reagent(Invitrogen #13778150)を4×最終濃度に希釈した(最終=0.3μL/25μL/ウェル)。RNAIMAXおよびhsiRNAを1:1で混合し、50μLを、50μLの細胞に3%FBS最終について添加した。細胞を、72時間、37℃および5%CO2でインキュベートした。
一次皮質ニューロンをWT(FVBN)マウスのE15.5マウス胚から得た。妊娠雌をアバチン(250mg/体重kg)IP注射で麻酔し、次いで頚椎脱臼させた。胚を除き、氷冷DMEM/F12媒体(Invitrogen)含有ペトリ皿に移した。脳を除き、髄膜を注意深く離した。皮質を単離し、予め温めたパパイン溶液含有1.5mlチューブに25分、37℃および5%CO2で移し、組織を溶解した。パパイン溶液を次のとおり調製した:パパイン(Worthington #54N15251)を2mL HibernateE(Brainbits)および1mL EBSS(Worthington)に溶解した。別に、DNase(Worthington #54M15168)を0.5mL HibernateEに再懸濁した。次いで、0.25mLの再懸濁DNaseを再懸濁パパインに最終溶液のために移した。25分インキュベーション後、パパイン溶液を除き、2.5%FBS添加1mL NbActiv4(Brainbits)を組織に添加した。次いで皮質を、熱加工、ガラスパスツールピペットを上下することにより解離させた。皮質ニューロンを計数し、1×106細胞/mlでプレーティングした。生存細胞造影試験のために、培養プレートをポリL-リシン(Sigma #P4707)でプレコートし、2×105細胞を、各皿のガラス中心に添加した。サイレンシングアッセイのために、ニューロンを、ポリL-リシンプレコート96ウェルプレート(BD BIOCOAT #356515)に1×105細胞/ウェルで播種した。一夜、37℃および5%CO2でインキュベーション後、非神経細胞の増殖を阻止するための有糸分裂阻害剤、0.484μL/mLの5’UtP(Sigma #U6625)および0.2402μL/mLの5’FdU(Sigma #F3503)添加等体積のNbActiv4(Brainbits)を神経細胞培養に添加した。培地の体積の半分を、ニューロンをsiRNAで処置するまで48時間毎に変えた(有糸分裂阻害剤含有新NbActiv4)。細胞が処置されたら、培地を除かず、添加だけした。全てのこの後の培地添加は有糸分裂阻害剤を含んだ。
mRNAをQUANTIGENE 2.0アッセイ(Affymetrix #QS0011)を使用して定量化した。細胞を250μL希釈溶解混合物(Affymetrix #13228)、1部溶解混合物、2部H2Oと、0.167μg/μLプロテイナーゼK(Affymetrix #QS0103)で30分、55℃で溶解した。細胞ライセートを徹底的に混合し、40μL(約8000細胞)のライセートを、プロテイナーゼKなしの40μLのさらなる希釈溶解混合物と共に捕捉プレートに添加した。プローブセットをAffymetrixプロトコールに特定のとおり希釈した。HeLa細胞について、20μLのヒトHTTまたはPPIBプローブセット(Affymetrix #SA-50339, #SA-10003)を100μL最終体積まで適切なウェルに添加した。一次ニューロンについて、20μLのマウスHTTまたはPPIBプローブセット(Affymetrix #SB-14150, #SB-10002)を使用した。
生存細胞hsiRNA取り込みをモニターするために、一次ニューロンの製造について上記のとおり細胞を35mmガラス底皿あたり2×105細胞で播種した。造影前に、細胞核を、製造業者により示されるとおり、NUCBLUE(Life Technologies #R37605によるMolecular Probes)を使用して無フェノールレッドNbActiv4で染色した。造影を無フェノールレッドNbActiv4で実施した。細胞を0.5μMのCy3標識hsiRNAで処置し、生存細胞造影を経時的に実施した。全生存細胞共焦点画像をツァイス共焦点顕微鏡で獲得し、画像をImageJ(1.47v)ソフトウェアを使用して処理した。
分布試験について、脳に1nmol(12.5μg)のCy3標識hsiRNAを注射した。24時間後、マウスを屠殺し、脳を取り出し、DERC Morphology Core at UMASS Medical Schoolに送り、パラフィンに包埋させ、4μm切片にスライスし、ガラススライドにマウントした。切片をキシレン中で2回8分脱パラフィン化した。次いで切片を連続エタノール希釈(100%、95%、80%)で各4分再水和し、次いで2回、2分、PBSで洗浄した。NueN染色について、スライドを、5分、抗原回収緩衝液で沸騰させ、次いで室温で20分静置し、続いてPBSで5分洗浄した。次いでスライドを5%正常ヤギ血清でPBS+0.05%Tween20で1時間遮断し、PBS+0.05%Tween20で1回、5分洗浄した。一次抗体(PBS+0.05%Tween20中1:1000希釈)をスライドに1時間インキュベーションのために添加し、続いて3回PBS+0.05%Tween20で5分洗浄した。二次抗体(PBS+0.05%Tween20中1:1000希釈)をスライドに暗所での30分インキュベーションのために添加し、続いて3回PBS+0.05%Tween20で5分洗浄した。次いで、スライドをDAPI(Life Technologies #D3571のMolecular Probes)で染色し、250ng/mLにPBSで1分希釈し、続いて3回、PBSで1分洗浄した。マウンティング媒体およびカバーグラスをスライドに適用し、一夜乾燥させて、記載する拡大率でライカDM5500 - DFC365FX顕微鏡で造影した。
野生型(FVBN)マウスは、定位的配置で右線条体(協調(ブレグマに相対的)は1.0mm前側、2.0mm側面および3.0mm腹側)のマイクロ注射を受けた。動物を、1.2%アバチンで注射前に深く麻酔した。毒性(DARPP32)および有効性の両方の試験について、マウスはPBSまたは人工脳脊髄液(2μL/線条体、N=8マウス)、12.5μgのNTC hsiRNA(2μLの500μM原液/線条体、N=8マウス)、25μgのHTT10150 hsiRNA(2μLの1mM原液/線条体、N=8マウス)、12.5μgのHTT10150 hsiRNA(2μLの500μM原液/線条体、計N=16マウス、2回の異なる日に8マウスの2セット)、6.3μgのHTT10150 hsiRNA(2μLの250μM原液/線条体、N=8マウス)または3.1μgのHTT10150 hsiRNA(2μLの125μM原液/線条体、N=8マウス)を注射され、5日後屠殺された。脳を取り出し、3個の300μm冠状切片を製造した。1個の2mmパンチを各切片の側あたり(注射および非注射)取得し、RNAlater(Ambion #AM7020)で24時間、4℃に置いた。各パンチを、QUANTIGENEアッセイ解析のための独立したサンプルとして処理した。全動物手順は、the University of Massachusetts Medical School Institutional Animal Care and Use Committee(IACUC, protocol number A-2411)により承認された。
データ分析を、GraphPad Prism 6 version 6.04ソフトウェア(GraphPad Software, Inc., San Diego, CA)を使用して実施した。濃度依存的曲線IC50について、曲線をlog(阻害剤)対応答-可変傾斜(4パラメータ)を使用して適合させた。曲線の底を0以上に設定し、曲線上部を100以下に設定した。各独立したマウス実験について、全データが対照の比率として表されるように、各用量でのノックダウンレベルをPBSまたは人工CSF群の非注射部位である対照群の平均に対して正規化した。インビボデータを複数比較についてボンフェローニ補正を伴うクラスカル・ワリス検定(一元配置ANOVA)を使用して分析した。全比較における差異は、0.05未満のP値で有意とみなした。
細胞を、96ウェル組織培養処置プレートで6%FBS(Gibco)添加DMEM(Gibco)中、10,000細胞/ウェルで播種した。HsiRNAをOptiMEM(Gibco)で2×最終濃度に希釈し、50μL希釈hsiRNAを、50μLの細胞に3%FBS最終について添加した。細胞を、72時間、37Cおよび5%CO2でインキュベートした。
細胞を、96ウェル組織培養処置プレートで6%FBS(Gibco)含有DMEM(Gibco)中、10,000細胞/ウェルで播種した。HsiRNAを、OptiMEM(Gibco)で4×最終濃度に希釈した。LIPOFECTAMINE RNAIMAX Transfection Reagent(Invitrogen CAT#13778150)を4×最終濃度に希釈した(最終=0.3μL/25μL/ウェル)。RNAIMAXおよびhsiRNAを1:1で混合し、50μLを50μLの細胞に3%FBS最終のために添加した。細胞を72時間、37Cおよび5%CO2でインキュベートした。
mRNAを、QUANTIGENE 2.0アッセイ(Affymetrix QS0011)を使用して定量化した。細胞を250μL希釈溶解混合物、1部溶解混合物、2部H2Oと、0.167μg/μLプロテイナーゼK(Affymetrix QS0103)で30分、55℃で溶解した。細胞ライセートを徹底的に混合し、40μL(~8000細胞)のライセートをプロテイナーゼKを含まない40μLのさらなる希釈溶解混合物と共に捕捉プレートに添加した。組織を、5mg組織パンチについて、2μg/μLプロテイナーゼK含有300μLの均質化緩衝液(Affymetrix)を使用して同様に処置した。次いで組織を、96ウェルプレート形式でQaigen TissueLyzerで均質化し、40μLを捕捉プレートに添加した。プローブセットをAffymetrixプロトコールに特定されるように希釈し、20μLのHTTまたはPPIBプローブ(Affymetrix:SA-50339, SA-10003)を捕捉プレートの各ウェルに最終体積100μLまで添加した。シグナルを製造プロトコールに従い増幅させた。発光をVeritas LuminometeまたはTecan M 1000で検出した。
生存細胞取り込みモニタリングについて、細胞を35mmガラス底皿あたり2×105細胞密度で播種し、一夜増殖させた。造影前に、細胞小器官を、特記しない限り、Life Technologiesから購入した染色試薬を使用してHBSS(Gibco)において染色した:細胞核、小胞体およびリソソームを、製造業者の指示どおり、NUCBLUE LIVE READYPROBE、ER-TRACKER Green(Bodipy FL Glibenclamide)およびLYSOTRACKER Deep Red試薬を使用して、各々染色した。造影を、フェノールレッドなしの非補足DMEMで実施した(Invitrogen)。細胞を0.5μMのCy3標識hsiRNAで処置し、生存細胞造影を経時的に実施した。
全共焦点画像を、60x Plan/APOオイルレンズおよびCoolsnap HQ2カメラ(Roper)を備えたTE-200E2倒立顕微鏡(Nikon)にマウントしたCSU10B Spinning Disk Confocal System scan head(Solamere Technology Group)で獲得した。画像をImageJ(1.47v)ソフトウェアを使用して処理した。hsiRNAを伴わないまたは伴うニューロン数をImageJソフトウェアを使用して計数した。脳切片画像を、1μmのz軸スペーシングで獲得した。
FM-hsiRNAは、部分的安定化hsiRNAより10倍低用量で脳および脊髄における改善された保持および蓄積ならびに最大サイレンシングを示すが、それらは注射部位近辺に大部分保持された(図102;Chol-hsiRNA)。hsiRNAの限定的な分布が、コレステロールコンジュゲートの強い疎水性によるものであり、hsiRNAの脂質に富むミエリンおよび有髄構造への優先的結合に起因し、そしてhsiRNAコンジュゲートの疎水性の微調整が脊髄および脳にわたる分布を改善するとの仮説を立てた。この考えを試験するために、活性神経細胞輸送ができる一団の天然に存在する疎水性分子をスクリーニングし、(i)向神経活性ステロイド、すなわち、GABA(Lan NC, Gee KW. Neuroactive steroid actions at the GABAA receptor. Hormones and behavior. 1994; 28:537-44. PMID: 7729823)を含む、血液脳関門を通過でき、多様な開口型イオンチャネルおよび神経細胞発現受容体に結合する(Rupprecht R. Neuroactive steroids: mechanisms of action and neuropsychopharmacological properties. Psychoneuroendocrinology. 2003; 28:139-68. PMID: 12510009)内在性ステロイド;(ii)神経細胞可塑性および修復に重要なガングリオシド神経保護糖脂質(Aureli M, Mauri L, Ciampa MG, Prinetti A, Toffano G, Secchieri C, Sonnino S. GM1 Ganglioside: Past Studies and Future Potential. Molecular neurobiology. 2015. PMID: 25762012);および(iii)食欲、疼痛、気分および記憶に関与する受容体により認識されるエンドカンナビノイド様長鎖多不飽和脂肪酸神経調節性脂質((Dyall SC. Long-chain omega-3 fatty acids and the brain: a review of the independent and shared effects of EPA, DPA and DHA. Frontiers in aging neuroscience. 2015; 7:52. PMID: 25954194; PMCID: PMC4404917; Janssen CI, Kiliaan AJ. Long-chain polyunsaturated fatty acids (LCPUFA) from genesis to senescence: the influence of LCPUFA on neural development, aging, and neurodegeneration. Progress in lipid research. 2014; 53:1-17. PMID: 24334113; Figueroa JD, De Leon M. Neurorestorative targets of dietary long-chain omega-3 fatty acids in neurological injury. Molecular neurobiology. 2014; 50:197-213. PMID: 24740740; PMCID: PMC4183712)を含めた。
部分的に修飾されたhsiRNAは短効果持続時間を示し、全身曝露を示さなかった(図35A~C)。代謝安定化をさらに探索した(図36)。完全代謝安定化は、hsiRNAのRISCエントリーを妨害しなかった(図37)。完全代謝安定化hsiRNA(FM-hsiRNA)は局所送達および分布を増大し、長時間の効果持続を可能とした(図38、39A~B、91、110および111;用語“ヌクレオシド”)。
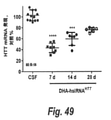
DHA-hsiRNAの広い治療指数に鼓舞され、DHAおよび関連コンジュゲートをより詳細に調べた。循環DHAは大部分リソホスファチジルコリンエステルとして存在し、これは、特異的輸送体Mfsd2aにより血液脳関門を通して能動的に輸送される唯一の形態である(Nguyen LN, Ma D, Shui G, Wong P, Cazenave-Gassiot A, Zhang X, Wenk MR, Goh EL, Silver DL. Mfsd2a is a transporter for the essential omega-3 fatty acid docosahexaenoic acid. Nature. 2014; 509:503-6. PMID: 24828044)。
分枝オリゴヌクレオチドは、新規オリゴヌクレオチド治療剤群を代表する。2~8オリゴヌクレオチドを、疎水性リンカーを介して一体として結合させ、2~3オリゴヌクレオチドを一体として結合させるのが好ましかった。実質的化学的安定化が一般に使用された(少なくとも40%塩基修飾、完全修飾が好ましい。2~20の一本鎖ホスホロチオエート化テイルを一般に使用した(8~10が好ましい))。
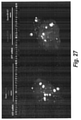
ジ-hsiRNAのニューロンへの、特に注射部位遠位への優先的送達は励みとなった。Cy3-ジ-hsiRNAを線条体内注射したマウスにおいて(図95C)、我々は、皮質の全NeuN陽性細胞(ニューロン)でジ-hsiRNAを検出したが、他の非神経細胞型(例えば、膠細胞)では検出しなかった。この観察の一つの解釈は、ジ-hsiRNAが遠位ニューロンまで軸索に沿って優先的に輸送されることである。なぜ分枝オリゴヌクレオチドが分布にこのような深い効果を有するのか?hsiRNAが受容体と弱く結合し、第二の独立した結合事象が内部移行を促進する、協調的結合の役割が仮説立てられた(Alves ID, Ciano KA, Boguslavski V, Varga E, Salamon Z, Yamamura HI, Hruby VJ, Tollin G. Selectivity, cooperativity, and reciprocity in the interactions between the delta-opioid receptor, its ligands, and G-proteins. The Journal of biological chemistry. 2004; 279:44673-82. PMID: 15317820)。hsiRNAの共有結合による協調的結合は、細胞の取り込み率および結果として組織保持を劇的に増強するはずである。この仮説および他の仮説を試験し、ジ-hsiRNAの詳細な構造-活性相関試験を実施する。
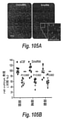
上述のデータで説明するとおり、CSF注入後CNS組織における広い分布および強力な遺伝子サイレンシングを支持する、2つの新規な、化学的に異なる群の治療siRNA、PC-DHA-hsiRNAおよびジ-hsiRNAが設計されている。ジ-hsiRNAは有望であるように見えるが、現在安全性および治療指数のデータが足りない。PC-DHA-hsiRNAは、広い治療可能性を有する(図103)。CNS適応症についての臨床治験におけるアンチセンスオリゴヌクレオチドが狭い治療指数を有するため、これは重要である。
オリゴヌクレオチド合成
HsiRNAおよびジ-hsiRNAを合成し(0.2g、+/-Cy3)、完全代謝的安定hsiRNAとしてHPLC精製し(末端ホスフェートアナログとして5’-E-VPを含む)、続いてマススペクトロメトリーにより特徴付けする。多種多様なリンカーがスクリーニングされており、PC-DHAおよびジ-hsiRNAコンジュゲーションの最適骨格が同定されている。官能化支持体を図93および94に示すとおり合成する。次の化合物を使用する:HTT-10150(HD)およびPPIB-437(ハウスキーピング対照)。数字は、ガイド鎖の5’ヌクレオチドにより標的されるヒトmRNAの位置を示す。全化合物は、先に、最適化バイオインフォマティクスパラメータを使用して、同定(Birmingham A, Anderson E, Sullivan K, Reynolds A, Boese Q, Leake D, Karpilow J, Khvorova A. A protocol for designing siRNAs with high functionality and specificity. Nature protocols. 2007; 2:2068-78. PMID: 17853862)および詳細な実験スクリーニングされている。各siRNAは、対応するヒト、マウスおよびサルmRNAを標的およびサイレンシングし、これは、将来的臨床開発を単純化する。
数投与経路を比較し、CSFを経るボーラス注入(ICVおよびIT注入)が、最良の程度の化合物保持およびCNS組織における分布を支持することが決定された。これらの経路を経るCSF送達は、臨床的に許容される投与経路である“脊椎穿刺”に類似する。組織保持および有効性のサイド・バイ・サイドの比較を、等用量がボーラス注射または1週間の期間にわたるALZETポンプによる送達で実施した。顕著に良好な組織保持および有効性が、ASOで報告されたデータに一致して、ボーラス注射で観察された(Rigo F, Chun SJ, Norris DA, Hung G, Lee S, Matson J, Fey RA, Gaus H, Hua Y, Grundy JS, Krainer AR, Henry SP, Bennett CF. Pharmacology of a central nervous system delivered 2'-O-methoxyethyl-modified survival of motor neuron splicing oligonucleotide in mice and nonhuman primates. The Journal of pharmacology and experimental therapeutics. 2014; 350:46-55. PMID: 24784568; PMCID: PMC4056267)。科学的理論に縛られることを意図しないが、ポンプ投与を超えるボーラス投与の良好な成績は、オリゴヌクレオチド取り込み機序と関係する。例えば、非増殖性オリゴヌクレオチドシンクは、ポンプ注入よりボーラスで速く飽和し、それにより過剰なオリゴヌクレオチドがより容易に輸送されることを可能にする。
パイロット試験において、200μg DHA-hsiRNAおよびジ-hsiRNAが線条体内注射の安全用量として確立され(DHAのデータは図103Bおよび103Cに示す)、150μgが髄腔内注射の安全用量として確立され、400μgが脳室内注射の安全用量として確立された。これらのレベルから開始して、用量を動物が何らかの毒性徴候を示すかまたはPC-DHA-hsiRNAについて約20mMおよびジ-hsiRNAについて約50mMである薬物溶解度限度に達するまで、2倍増分で増加させる。注射3週間後(オリゴヌクレオチド毒性を見るのに必要な最適時間)、脳組織を採取し、ニューロンの数および生存能を神経細胞マーカーNeuNおよびDARPP-32での染色により評価する(Mullen RJ, Buck CR, Smith AM. NeuN, a neuronal specific nuclear protein in vertebrates. Development (Cambridge, England). 1992; 116:201-11. PMID: 1483388; Weyer A, Schilling K. Developmental and cell type-specific expression of the neuronal marker NeuN in the murine cerebellum. Journal of neuroscience research. 2003; 73:400-9. PMID: 12868073; Ouimet CC, Miller PE, Hemmings HC, Jr., Walaas SI, Greengard P. DARPP-32, a dopamine- and adenosine 3':5'-monophosphate-regulated phosphoprotein enriched in dopamine-innervated brain regions. III. Immunocytochemical localization. The Journal of neuroscience : the official journal of the Society for Neuroscience. 1984; 4:111-24. PMID: 6319625)。ミクログリア活性化(天然免疫活性化)もIBA1での染色により評価する(Judge AD, Bola G, Lee AC, MacLachlan I. Design of noninflammatory synthetic siRNA mediating potent gene silencing in vivo. Molecular therapy : the journal of the American Society of Gene Therapy. 2006; 13:494-505. PMID: 16343994; Marques JT, Williams BR. Activation of the mammalian immune system by siRNAs. Nature biotechnology. 2005; 23:1399-405. PMID: 16273073)。化合物が、可逆性、短期炎症性応答を誘発するかを試験するために、マウスに最大耐性用量を注射し、膠細胞活性化を投与6時間後に試験する。この研究の完成は、ここに記載する新規2群の治療hsiRNAの最大耐性用量に対するデータを作成する。
CSFおよび血液におけるRNA滞在時間を決定する。マウスにおける反復CSF採取は実行不可能であり、それ故にCSFクリアランス試験を、用量を適宜調節した、ラットを使用して実施する。10μlのCSFを、動物の重複群を使用して、PC-DHA-およびジ-hsiRNA投与1時間、6時間、12時間および24時間および1週間後に採取する。同様に、20μLの血液を、注射5分および30分および1時間、4時間、12時間、24時間、48時間、72時間および96時間後に採る。短時間の反復採血と関連する懸念を最小化し、厳密なデータを得るために必要な動物数を最小化するために、頸静脈カテーテル法を使用する。
用量応答試験を実施し、顕著なオリゴヌクレオチド蓄積を示す脳の領域におけるサイレンシングの最適用量を決定する。実験は、図103、104および105に示すものに準じて実施する。3mmパンチ生検試料をPC-DHAおよびジ-hsiRNAの用量を増加させながら注入したマウスの脳および脊柱から採取し、HTTまたは対照mRNAのレベルをQUANTIGENE(登録商標)アッセイを使用して測定する。
大部分の神経変性障害および疾患モデルは、症状の発症遅延を示す(例えば、マウスにおいて3~9ヶ月)。1回の注入からのサイレンシング期間および何回の注射が6~9ヶ月のサイレンシング支持に必要であるかを決定しなければならない。一般に、非分裂細胞におけるsiRNA誘発サイレンシングは月単位(1ヶ月または数ヶ月)で続くと予測される。充填RISC複合体の半減期は数週間であり(Whitehead KA, Langer R, Anderson DG. Knocking down barriers: advances in siRNA delivery. Nature reviews Drug discovery. 2009; 8:129-38. PMID: 19180106)、細胞あたり1,000未満の充填RISC分子がサイレンシング誘発に十分である(Stalder L, Heusermann W, Sokol L, Trojer D, Wirz J, Hean J, Fritzsche A, Aeschimann F, Pfanzagl V, Basselet P, Weiler J, Hintersteiner M, Morrissey DV, Meisner-Kober NC. The rough endoplasmatic reticulum is a central nucleation site of siRNA-mediated RNA silencing. The EMBO journal. 2013; 32:1115-27. PMID: 23511973; PMCID: 3630355; Pei Y, Hancock PJ, Zhang H, Bartz R, Cherrin C, Innocent N, Pomerantz CJ, Seitzer J, Koser ML, Abrams MT, Xu Y, Kuklin NA, Burke PA, Sachs AB, Sepp-Lorenzino L, Barnett SF. Quantitative evaluation of siRNA delivery in vivo. Rna. 2010; 16:2553-63. PMID: 20940339; PMCID: 2995415)。
二分岐hsiRNAは、等用量のリンカー結合単一siRNAと比較してCNS組織における顕著に増強された保持および分布を示しており、共有結合したsiRNAの協調的結合または受容体二量体化が細胞の取り込みを駆動することを示す(図95C)。示差的取り込みを、TESM顕微鏡(時間分解落射蛍光構造顕微鏡)およびマススペクトロメトリーの組み合わせにより可視化および特徴付けする。
遺伝子治療アプローチ(すなわち、永続的遺伝子サイレンシング)は現在神経変性障害の処置について考慮されており、したがって1~6ヶ月のサイレンシング期間は比較的安全であると考えられる。それにも関わらず、サイレンシングを戻す“解毒薬が安全性に関する懸念である。“解毒薬”はまたインビボでの遺伝子機能の研究の大きなツールであり、関連する表現型を産生するためにどの程度の時間が遺伝子の下方制御に必要があるかの試験を可能とする。
神経変性障害の処置用アンチセンスオリゴヌクレオチドは、臨床的に進んだ開発段階にある(Evers MM, Toonen LJ, van Roon-Mom WM. Antisense oligonucleotides in therapy for neurodegenerative disorders. Advanced drug delivery reviews. 2015. PMID: 25797014; Kordasiewicz HB, Stanek LM, Wancewicz EV, Mazur C, McAlonis MM, Pytel KA, Artates JW, Weiss A, Cheng SH, Shihabuddin LS, Hung G, Bennett CF, Cleveland DW. Sustained therapeutic reversal of Huntington's disease by transient repression of huntingtin synthesis. Neuron. 2012; 74:1031-44. PMID: 22726834; PMCID: PMC3383626)。IONIS-HTTRxは、Ionisに独占的な2.5世代アンチセンス化学であり、学界で一般に利用可能ではない。
ここに示すデータ(図92、103、104および105)は、PC-DHA-およびジ-hsiRNA化合物が、脊髄、線条体および皮質における標的に1ヶ月~3ヶ月効果持続期間で到達するのに十分であることを示し、これは、インビボ機能的ゲノム研究に十分である。これ単独で、顕著な達成であるが、このテクノロジープラットホームのヒト治療に向けた将来的翻訳は、他のレベルの複雑さを示す。テクノロジー翻訳前に、我々は、(i)最も広い可能な治療指数および(ii)大きな脳への送達を支持する分布の増強のために、この化合物を最適化する。
PC-DHA構造に2個の必須成分がある。ホスファチジルコリンおよびDHA(図92における構造参照)である。ここに記載する合成アプローチ(図93および94)は、これらの化合物を独立して変えることを可能とする。オリゴヌクレオチドコンジュゲートの構造機能相関に関する情報は文献にはほとんどまたは全く存在せず、むしろポリマー構造および脂質化合物がどのように脂質-粒子形成に影響するかを記載する多くの情報が存在する48。試験は、脂質の長さが製剤の全体的有効性に大きく影響することを示す。
ジ-hsiRNA化合物における二つのhsiRNAは、非対称性に結合されている:一方はホスフェート結合および他方はホスホロアミデート結合による(図93、94および103A)。ホスホロアミデート結合が必要であるか否かを確立するために、hsiRNAが両方ともホスフェートを経てリンカーに連結した二分岐化合物が現在試験中である(図93および94に基づく修飾合成スキーム)。ホスホロアミデート結合が必須でないことを示すことは、多数の前駆体が購入可能であるため、構造活性相関試験を単純化する。それにも関わらず、ホスホアミド結合の必要性は、ホスホアミドが酸性条件ではるかに不安定であり、エンドソームからの化合物遊離を促進すると予測されるため、興味深い。
組織培養実験を使用して、安全性およびRISC複合体への効率的侵入を確認する。次いで、各化合物を、ここで記載するように確立された最小有効量および最大耐性用量でICV注射する。低濃度で有効であるおよび/または高濃度で非毒性である化合物を、詳細な試験のために選択する。最後に、大きな脳(例えば、ヒツジ)中の分布に最も有望な化合物を評価する。ヒツジモデルは、AAV-httベクターの分布の評価のために設計されている。ここに記載するPNAアッセイを使用して、ボーラスICV注入後のヒツジ脳の種々の領域からの生検サンプルにおける化合物のレベルを測定する。
ハンチントン病動物モデルにおけるhsiRNA HTT10150の新規コンジュゲートの評価
Httのための機能亢進性、FM-hsiRNAであるHTT-10150をここで記載する。その研究室で現在飼育されている複数HD動物モデル(Chang R, Liu X, Li S, Li XJ. Transgenic animal models for study of the pathogenesis of Huntington's disease and therapy. Drug design, development and therapy. 2015; 9:2179-88. PMID: 25931812; PMCID: PMC4404937)は、YAC128(Hodgson JG, Agopyan N, Gutekunst CA, Leavitt BR, LePiane F, Singaraja R, Smith DJ, Bissada N, McCutcheon K, Nasir J, Jamot L, Li XJ, Stevens ME, Rosemond E, Roder JC, Phillips AG, Rubin EM, Hersch SM, Hayden MR. A YAC mouse model for Huntington's disease with full-length mutant huntingtin, cytoplasmic toxicity, and selective striatal neurodegeneration. Neuron. 1999; 23:181-92. PMID: 10402204)、BACHD(Hult S, Soylu R, Bjorklund T, Belgardt BF, Mauer J, Bruning JC, Kirik D, Petersen A. Mutant huntingtin causes metabolic imbalance by disruption of hypothalamic neurocircuits. Cell metabolism. 2011;13:428-39. PMID: 21459327; Hult Lundh S, Nilsson N, Soylu R, Kirik D, Petersen A. Hypothalamic expression of mutant huntingtin contributes to the development of depressive-like behavior in the BAC transgenic mouse model of Huntington's disease. Human molecular genetics. 2013; 22:3485-97. PMID: 23697793; Gray M, Shirasaki DI, Cepeda C, Andre VM, Wilburn B, Lu XH, Tao J, Yamazaki I, Li SH, Sun YE, Li XJ, Levine MS, Yang XW. Full-length human mutant huntingtin with a stable polyglutamine repeat can elicit progressive and selective neuropathogenesis in BACHD mice. The Journal of neuroscience : the official journal of the Society for Neuroscience. 2008; 28:6182-95. PMID: 18550760; PMCID: PMC2630800)および最近確立されたQ140を含むアレルシリーズ(Website:chdifoundation.org)を含み、使用される。
本明細書を通して引用され得る引用文献(文献、特許、特許出願およびウェブサイトを含む)を、引用文献がここに引用される限り、その全体を、あらゆる目的のために、ここに明示的に包含させる。特に断らない限り、本開示は、当分野で周知の免疫学、分子生物学および細胞生物学の慣用の技術を使用する。
Atwell et al. J. Mol. Biol. 1997, 270: 26-35;
Ausubel et al. (eds.), CURRENT PROTOCOLS IN MOLECULAR BIOLOGY, John Wiley &Sons, NY (1993);
Ausubel, F.M. et al. eds., SHORT PROTOCOLS IN MOLECULAR BIOLOGY (4th Ed. 1999) John Wiley & Sons, NY. (ISBN 0-471-32938-X);
CONTROLLED DRUG BIOAVAILABILITY, DRUG PRODUCT DESIGN AND PERFORMANCE, Smolen and Ball (eds.), Wiley, New York (1984);
Giege, R. and Ducruix, A. Barrett, CRYSTALLIZATION OF NUCLEIC ACIDS AND PROTEINS, a Practical Approach, 2nd ea., pp. 20 1-16, Oxford University Press, New York, New York, (1999);
Goodson, in MEDICAL APPLICATIONS OF CONTROLLED RELEASE, vol. 2, pp. 115-138 (1984);
Hammerling, et al., in: MONOCLONAL ANTIBODIES AND T-CELL HYBRIDOMAS 563-681 (Elsevier, N.Y., 1981;
Harlow et al. , ANTIBODIES: A LABORATORY MANUAL, (Cold Spring Harbor Laboratory Press, 2nd ed. 1988);
Kabat et al., SEQUENCES OF PROTEINS OF IMMUNOLOGICAL INTEREST (National Institutes of Health, Bethesda, Md. (1987) and (1991);
Kabat, E.A., et al. (1991) SEQUENCES OF PROTEINS OF IMMUNOLOGICAL INTEREST, Fifth Edition, U.S. Department of Health and Human Services, NIH Publication No. 91-3242;
Kontermann and Dubel eds., ANTIBODY ENGINEERING (2001) Springer-Verlag. New York. 790 pp. (ISBN 3-540-41354-5).
Kriegler, Gene Transfer and Expression, A Laboratory Manual, Stockton Press, NY (1990);
Lu and Weiner eds., CLONING AND EXPRESSION VECTORS FOR GENE FUNCTION ANALYSIS (2001) BioTechniques Press. Westborough, MA. 298 pp. (ISBN 1-881299-21-X).
MEDICAL APPLICATIONS OF CONTROLLED RELEASE, Langer and Wise (eds.), CRC Pres., Boca Raton, Fla. (1974);
Old, R.W. & S.B. Primrose, PRINCIPLES OF GENE MANIPULATION: AN INTRODUCTION TO GENETIC ENGINEERING (3d Ed. 1985) Blackwell Scientific Publications, Boston. Studies in Microbiology; V.2:409 pp. (ISBN 0-632-01318-4).
Sambrook, J. et al. eds., MOLECULAR CLONING: A LABORATORY MANUAL (2d Ed. 1989) Cold Spring Harbor Laboratory Press, NY. Vols. 1-3. (ISBN 0-87969-309-6).
SUSTAINED AND CONTROLLED RELEASE DRUG DELIVERY SYSTEMS, J.R. Robinson, ed., Marcel Dekker, Inc., New York, 1978
Winnacker, E.L. FROM GENES TO CLONES: INTRODUCTION TO GENE TECHNOLOGY (1987) VCH Publishers, NY (translated by Horst Ibelgaufts). 634 pp. (ISBN 0-89573-614-4)
本開示は、その精神または必須特徴から逸脱することなく、他の特定の形態に具現化され得る。前記態様は、それ故に、全てに関して、開示を限定するのではなく、説明的と見なされる。本開示の範囲は、それゆえに、前の記載ではなく、添付する特許請求の範囲により示され、特許請求の範囲の均等の意義および範囲内に入る全ての変化は、それ故に、ここに包含されることが意図される。
Claims (24)
- 生物におけるハンチンチン(HTT)遺伝子の発現を阻害することにおける治療的使用のための、5’CAGUAAAGAGAUUAA 3’(配列番号1)、5’AUAUCAGUAAAGAGA 3’(配列番号2)または5’CUCAGGAUUUAAAAU 3’(配列番号3)に対する完全相補性を含む、15~35塩基長であるRNA分子。
- 該RNA分子が一本鎖(ss)RNAまたは二本鎖(ds)RNAである、請求項1に記載の治療的使用のためのRNA分子であって、該RNA分子が、HTT遺伝子短mRNAの3’非翻訳領域(UTR)を標的とし、該RNA分子が、
2’-デオキシ-2’-フルオロ修飾ヌクレオチド、2’-デオキシ修飾ヌクレオチド、ロックドヌクレオチド、脱塩基ヌクレオチド、2’-アミノ修飾ヌクレオチド、2’-アルキル修飾ヌクレオチド、モルホリノヌクレオチド、ホスホロアミデート、非天然塩基含有ヌクレオチド、2’-O-メチル修飾ヌクレオチド、5’ホスホロチオエート基を含むヌクレオチド、およびコレステリル誘導体またはドデカン酸ビスデシルアミド基に結合した末端ヌクレオチドからなる群から選択される、少なくとも一つの修飾ヌクレオチドを含むdsRNA
を含む、RNA分子。 - 請求項2に記載のRNA分子および薬学的に許容される担体を含む、生物におけるハンチンチン(HTT)遺伝子の発現を阻害することにおける治療的使用のための医薬組成物。
- 5’末端、3’末端を含み、標的に対する相補性を有し、ここで、
(1)RNA分子は交互の2’-メトキシ-リボヌクレオチドおよび2’-フルオロ-リボヌクレオチドを含み;
(2)5’末端から2位および14位のヌクレオチドは2’-メトキシ-リボヌクレオチドではなく;
(3)ヌクレオチドはホスホジエステル結合またはホスホロチオエート結合により結合し;そして
(4)3’末端から1~6位または3’末端から1~7位のヌクレオチドはホスホロチオエート結合により隣接ヌクレオチドと結合する、
請求項1に記載の治療的使用のためのRNA分子。 - 5’末端、3’末端および標的に対する相補性を有し、第一オリゴヌクレオチドおよび第二オリゴヌクレオチドを含み、ここで、
(1)第一オリゴヌクレオチドは配列番号1に示す配列を含み;
(2)第一オリゴヌクレオチドの一部は第二オリゴヌクレオチドの一部と相補的であり;
(3)第二オリゴヌクレオチドは交互の2’-メトキシ-リボヌクレオチドおよび2’-フルオロ-リボヌクレオチドを含み;
(4)第二オリゴヌクレオチドの3’末端から2位および14位のヌクレオチドは2’-メトキシ-リボヌクレオチドであり、そして
(5)第二オリゴヌクレオチドのヌクレオチドはホスホジエステル結合またはホスホロチオエート結合により結合する、
請求項2に記載のRNA分子。 - 以下:
第二オリゴヌクレオチドが第二オリゴヌクレオチドの3’末端で疎水性分子と結合する、ここで第二オリゴヌクレオチドと疎水性分子の結合がポリエチレングリコールまたはトリエチレングリコールを含む;
第二オリゴヌクレオチドの3’末端から1位および2位のヌクレオチドが隣接ヌクレオチドにホスホロチオエート結合により結合する;および
第二オリゴヌクレオチドの3’末端から1位および2位のヌクレオチドおよび第二オリゴヌクレオチドの5’末端から1位および2位のヌクレオチドが隣接リボヌクレオチドにホスホロチオエート結合により結合する、
の1つ以上を含む、請求項5に記載のRNA分子。 - (a)細胞に請求項2に記載のRNA分子をインビトロで導入し;そして
(b)工程(a)で産生した細胞を、HTT遺伝子のmRNAトランスクリプトを分解させるのに十分な時間維持し、それにより、細胞におけるHTT遺伝子の発現を阻害する
ことを含む、細胞におけるHTT遺伝子の発現をインビトロで阻害する方法。 - 請求項2に記載のRNA分子がdsRNAであって、
以下:
該dsRNAが患者の脳に投与される;
該dsRNAが線条体内注入により投与される;
請求項2に記載のdsRNAの脳への投与が、線条体におけるHTT遺伝子mRNAの減少を引き起こす;および
請求項2に記載のdsRNAの脳への投与が、皮質におけるHTT遺伝子mRNAの減少を引き起こす、
の1つ以上を含む、請求項2に記載の治療的使用のためのRNA分子。 - 細胞におけるHTT遺伝子の発現を阻害することにおける治療的使用のためのベクターであって、5’CAGUAAAGAGAUUAA 3’(配列番号1)、5’AUAUCAGUAAAGAGA 3’(配列番号2)または5’CUCAGGAUUUAAAAU 3’(配列番号3)に完全相補性であるRNA分子をコードするヌクレオチド配列に操作可能に結合した制御配列を含み、ここで、該RNA分子が10~35塩基長であり、該RNA分子が、該HTT遺伝子を発現する細胞と接触したとき、該HTT遺伝子の発現を少なくとも20%阻害する、ベクター。
- 該RNA分子が、ssRNAである;または
該RNA分子が、dsRNAであり、30~35塩基対長である、請求項9に記載のベクターであって、該dsRNAが、センス鎖およびアンチセンス鎖を含み、ここで、アンチセンス鎖が5’CAGUAAAGAGAUUAA 3’(配列番号1)、5’AUAUCAGUAAAGAGA 3’(配列番号2)または5’CUCAGGAUUUAAAAU 3’(配列番号3)に対する完全相補性を含む、
ベクター。 - 請求項10に記載のベクターを含む、細胞。
- 生物におけるハンチンチン(HTT)遺伝子の発現を阻害することにおける治療的使用のための、5’CAGUAAAGAGAUUAA 3’(配列番号1)、5’AUAUCAGUAAAGAGA 3’(配列番号2)または5’CUCAGGAUUUAAAAU 3’(配列番号3)に対する完全相補性を含む、15~35塩基長であるRNA分子であって、HTT mRNAを標的とし、少なくとも一つの修飾ヌクレオチドを含む、RNA分子。
- 該修飾ヌクレオチドがホスファチジルコリン誘導体に結合した末端ヌクレオチドである、請求項12に記載のRNA分子。
- 2RNA分子を含む二分岐RNA化合物であって、各RNA分子が、(i)独立して15~35塩基長であり、および(ii)5’CAGUAAAGAGAUUAA 3’(配列番号1)、5’AUAUCAGUAAAGAGA 3’(配列番号2)または5’CUCAGGAUUUAAAAU 3’(配列番号3)に対する完全相補性を含み、ここで2RNA分子がリンカー、スペーサーおよび分岐点から独立して選択される1以上の部分により、互いに結合する、二分岐RNA化合物。
- 該RNA分子がアンチセンスオリゴヌクレオチドまたはGAPMER分子である、請求項1に記載のRNA分子。
- ヒトにおけるHTT遺伝子の発現を阻害することにおける使用のための、請求項1、2、4-6、8および12-15のいずれか一項に記載のRNA分子。
- ヒトにおけるHTT遺伝子の発現を阻害することにおける使用のための、請求項3に記載の医薬組成物。
- ハンチントン病を処置または管理するための医薬組成物であって、治療有効量の請求項2に記載のRNA分子を含む、医薬組成物。
- 5’CAGUAAAGAGAUUAA 3’(配列番号1)に対する完全相補性を含む、請求項1に記載の治療的使用のためのRNA分子。
- 5’AUAUCAGUAAAGAGA 3’(配列番号2)に対する完全相補性を含む、請求項1に記載の治療的使用のためのRNA分子。
- 5’CUCAGGAUUUAAAAU 3’(配列番号3)に対する完全相補性を含む、請求項1に記載の治療的使用のためのRNA分子。
- 各RNA分子が、5’CAGUAAAGAGAUUAA 3’(配列番号1)に対する完全相補性を含む、請求項14に記載の二分岐RNA化合物。
- 各RNA分子が、5’AUAUCAGUAAAGAGA 3’(配列番号2)に対する完全相補性を含む、請求項14に記載の二分岐RNA化合物。
- 各RNA分子が、5’CUCAGGAUUUAAAAU 3’(配列番号3)に対する完全相補性を含む、請求項14に記載の二分岐RNA化合物。
Priority Applications (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2022003057A JP2022064900A (ja) | 2015-04-03 | 2022-01-12 | ハンチンチンmRNAをターゲティングするオリゴヌクレオチド化合物 |
| JP2022003059A JP7504482B2 (ja) | 2015-04-03 | 2022-01-12 | ハンチンチンmRNAをターゲティングするオリゴヌクレオチド化合物 |
| JP2023206985A JP2024028909A (ja) | 2015-04-03 | 2023-12-07 | ハンチンチンmRNAをターゲティングするオリゴヌクレオチド化合物 |
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201562142731P | 2015-04-03 | 2015-04-03 | |
| US62/142,731 | 2015-04-03 | ||
| US201662289274P | 2016-01-31 | 2016-01-31 | |
| US62/289,274 | 2016-01-31 | ||
| PCT/US2016/025722 WO2016161374A1 (en) | 2015-04-03 | 2016-04-01 | Oligonucleotide compounds for targeting huntingtin mrna |
Related Child Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022003059A Division JP7504482B2 (ja) | 2015-04-03 | 2022-01-12 | ハンチンチンmRNAをターゲティングするオリゴヌクレオチド化合物 |
| JP2022003057A Division JP2022064900A (ja) | 2015-04-03 | 2022-01-12 | ハンチンチンmRNAをターゲティングするオリゴヌクレオチド化合物 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2018516091A JP2018516091A (ja) | 2018-06-21 |
| JP2018516091A5 JP2018516091A5 (ja) | 2019-03-07 |
| JP7009356B2 true JP7009356B2 (ja) | 2022-01-25 |
Family
ID=55752785
Family Applications (4)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018502624A Active JP7009356B2 (ja) | 2015-04-03 | 2016-04-01 | ハンチンチンmRNAをターゲティングするオリゴヌクレオチド化合物 |
| JP2022003057A Pending JP2022064900A (ja) | 2015-04-03 | 2022-01-12 | ハンチンチンmRNAをターゲティングするオリゴヌクレオチド化合物 |
| JP2022003059A Active JP7504482B2 (ja) | 2015-04-03 | 2022-01-12 | ハンチンチンmRNAをターゲティングするオリゴヌクレオチド化合物 |
| JP2023206985A Pending JP2024028909A (ja) | 2015-04-03 | 2023-12-07 | ハンチンチンmRNAをターゲティングするオリゴヌクレオチド化合物 |
Family Applications After (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022003057A Pending JP2022064900A (ja) | 2015-04-03 | 2022-01-12 | ハンチンチンmRNAをターゲティングするオリゴヌクレオチド化合物 |
| JP2022003059A Active JP7504482B2 (ja) | 2015-04-03 | 2022-01-12 | ハンチンチンmRNAをターゲティングするオリゴヌクレオチド化合物 |
| JP2023206985A Pending JP2024028909A (ja) | 2015-04-03 | 2023-12-07 | ハンチンチンmRNAをターゲティングするオリゴヌクレオチド化合物 |
Country Status (17)
| Country | Link |
|---|---|
| US (5) | US9809817B2 (ja) |
| EP (2) | EP3766973A1 (ja) |
| JP (4) | JP7009356B2 (ja) |
| CN (2) | CN116004624A (ja) |
| AU (3) | AU2016244027B2 (ja) |
| CA (1) | CA2980337A1 (ja) |
| CY (1) | CY1123289T1 (ja) |
| DK (1) | DK3277814T3 (ja) |
| ES (1) | ES2808750T3 (ja) |
| HR (1) | HRP20201200T1 (ja) |
| HU (1) | HUE050441T2 (ja) |
| LT (1) | LT3277814T (ja) |
| PL (1) | PL3277814T3 (ja) |
| PT (1) | PT3277814T (ja) |
| RS (1) | RS60762B1 (ja) |
| SI (1) | SI3277814T1 (ja) |
| WO (1) | WO2016161374A1 (ja) |
Families Citing this family (71)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2009102427A2 (en) | 2008-02-11 | 2009-08-20 | Rxi Pharmaceuticals Corp. | Modified rnai polynucleotides and uses thereof |
| EP2949752B1 (en) | 2008-09-22 | 2017-12-20 | RXi Pharmaceuticals Corporation | Reduced size self-delivering rnai compounds |
| WO2010059226A2 (en) | 2008-11-19 | 2010-05-27 | Rxi Pharmaceuticals Corporation | Inhibition of map4k4 through rnai |
| CN102282155B (zh) | 2008-12-02 | 2017-06-09 | 日本波涛生命科学公司 | 磷原子修饰的核酸的合成方法 |
| WO2010078536A1 (en) | 2009-01-05 | 2010-07-08 | Rxi Pharmaceuticals Corporation | Inhibition of pcsk9 through rnai |
| US9745574B2 (en) | 2009-02-04 | 2017-08-29 | Rxi Pharmaceuticals Corporation | RNA duplexes with single stranded phosphorothioate nucleotide regions for additional functionality |
| US9744183B2 (en) | 2009-07-06 | 2017-08-29 | Wave Life Sciences Ltd. | Nucleic acid prodrugs and methods of use thereof |
| CN106074591B (zh) | 2010-03-24 | 2020-01-14 | 菲奥医药公司 | 眼部症候中的rna干扰 |
| RU2615143C2 (ru) | 2010-03-24 | 2017-04-04 | Адвирна | Самодоставляющие PHKi соединения уменьшенного размера |
| CN110042099A (zh) | 2010-03-24 | 2019-07-23 | 菲奥医药公司 | 皮肤与纤维化症候中的rna干扰 |
| DK2620428T3 (da) | 2010-09-24 | 2019-07-01 | Wave Life Sciences Ltd | Asymmetrisk hjælpegruppe |
| DK2734208T3 (en) | 2011-07-19 | 2017-06-19 | Wave Life Sciences Ltd | PROCEDURES FOR SYNTHESIS OF FUNCTIONALIZED NUCLEIC ACIDS |
| EP2872485B1 (en) | 2012-07-13 | 2020-12-16 | Wave Life Sciences Ltd. | Asymmetric auxiliary group |
| RU2015104762A (ru) | 2012-07-13 | 2018-08-31 | Уэйв Лайф Сайенсес Лтд. | Хиральный контроль |
| CN104684923B (zh) | 2012-07-13 | 2018-09-28 | 株式会社新日本科学 | 手性核酸佐剂 |
| CN106061488B (zh) | 2013-12-02 | 2021-04-09 | 菲奥医药公司 | 癌症的免疫治疗 |
| US10322173B2 (en) | 2014-01-15 | 2019-06-18 | Shin Nippon Biomedical Laboratories, Ltd. | Chiral nucleic acid adjuvant having anti-allergic activity, and anti-allergic agent |
| WO2015108048A1 (ja) | 2014-01-15 | 2015-07-23 | 株式会社新日本科学 | 抗腫瘍作用を有するキラル核酸アジュバンド及び抗腫瘍剤 |
| JPWO2015108047A1 (ja) | 2014-01-15 | 2017-03-23 | 株式会社新日本科学 | 免疫誘導活性を有するキラル核酸アジュバンド及び免疫誘導活性剤 |
| PT3094728T (pt) | 2014-01-16 | 2022-05-19 | Wave Life Sciences Ltd | Desenho quiral |
| US11279934B2 (en) | 2014-04-28 | 2022-03-22 | Phio Pharmaceuticals Corp. | Methods for treating cancer using nucleic acids targeting MDM2 or MYCN |
| US10900039B2 (en) | 2014-09-05 | 2021-01-26 | Phio Pharmaceuticals Corp. | Methods for treating aging and skin disorders using nucleic acids targeting Tyr or MMP1 |
| MX2017006216A (es) | 2014-11-14 | 2018-08-29 | Voyager Therapeutics Inc | Composiciones y métodos para tratar la esclerosis lateral amiotrófica (ela). |
| SG11201703419UA (en) | 2014-11-14 | 2017-05-30 | Voyager Therapeutics Inc | Modulatory polynucleotides |
| SI3277814T1 (sl) | 2015-04-03 | 2020-12-31 | University Of Massachusetts | Oligonukleotidne spojine za ciljanja MRNA huntingtina |
| SI3277815T1 (sl) | 2015-04-03 | 2022-01-31 | University Of Massachusetts | Ologonukleotidne spojine za zdravljenje preeklampsije in drugih angiogeneznih motenj |
| EP3862005A1 (en) | 2015-07-06 | 2021-08-11 | Phio Pharmaceuticals Corp. | Nucleic acid molecules targeting superoxide dismutase 1 (sod1) |
| WO2017007825A1 (en) | 2015-07-06 | 2017-01-12 | Rxi Pharmaceuticals Corporation | Methods for treating neurological disorders using a synergistic small molecule and nucleic acids therapeutic approach |
| MA43072A (fr) | 2015-07-22 | 2018-05-30 | Wave Life Sciences Ltd | Compositions d'oligonucléotides et procédés associés |
| US10633653B2 (en) | 2015-08-14 | 2020-04-28 | University Of Massachusetts | Bioactive conjugates for oligonucleotide delivery |
| EP3365446A4 (en) | 2015-10-19 | 2019-06-26 | Phio Pharmaceuticals Corp. | SELF ADMINISTRATION-REDUCED SIZE NUCLEIC ACID COMPOUNDS TARGETING LONGS NON-CODING LONGS |
| EP3408391A4 (en) * | 2016-01-31 | 2019-08-28 | University of Massachusetts | BRANCHED OLIGONUCLEOTIDES |
| MA45270A (fr) | 2016-05-04 | 2017-11-09 | Wave Life Sciences Ltd | Compositions d'oligonucléotides et procédés associés |
| SG11201809643UA (en) | 2016-05-18 | 2018-12-28 | Voyager Therapeutics Inc | Compositions and methods of treating huntington's disease |
| KR102392236B1 (ko) | 2016-05-18 | 2022-05-03 | 보이저 테라퓨틱스, 인크. | 조절성 폴리뉴클레오티드 |
| US11299733B2 (en) | 2016-07-15 | 2022-04-12 | University Of Massachusetts | Process of delivering small RNAs to sperm |
| CA3033368A1 (en) | 2016-08-12 | 2018-02-15 | University Of Massachusetts | Conjugated oligonucleotides |
| US10457940B2 (en) | 2016-09-22 | 2019-10-29 | University Of Massachusetts | AAV treatment of Huntington's disease |
| CN110121558B (zh) * | 2016-11-28 | 2023-06-13 | 日商那帕洁制药股份有限公司 | 化学修饰siRNA |
| DK3607069T3 (da) * | 2017-04-05 | 2022-11-21 | Silence Therapeutics Gmbh | Produkter og sammensætninger |
| CA3061652A1 (en) | 2017-05-05 | 2018-11-08 | Voyager Therapeutics, Inc. | Compositions and methods of treating amyotrophic lateral sclerosis (als) |
| EP3619308A4 (en) | 2017-05-05 | 2021-01-27 | Voyager Therapeutics, Inc. | COMPOSITIONS AND METHODS OF TREATMENT FOR HUNTINGTON'S MORBUS |
| JP2020524485A (ja) | 2017-06-02 | 2020-08-20 | ウェイブ ライフ サイエンシズ リミテッドWave Life Sciences Ltd. | オリゴヌクレオチド組成物及びその使用方法 |
| CN111050806A (zh) * | 2017-06-02 | 2020-04-21 | 波涛生命科学有限公司 | 寡核苷酸组合物及其使用方法 |
| JP7406793B2 (ja) | 2017-06-23 | 2023-12-28 | ユニバーシティー オブ マサチューセッツ | 2テイル自己デリバリー型siRNAおよび関連方法 |
| CA3077213A1 (en) | 2017-10-04 | 2019-04-11 | Avidity Biosciences, Inc. | Nucleic acid-polypeptide compositions and uses thereof |
| JP7502991B2 (ja) | 2017-10-16 | 2024-06-19 | ボイジャー セラピューティクス インコーポレイテッド | 筋萎縮性側索硬化症(als)の治療 |
| WO2019079242A1 (en) | 2017-10-16 | 2019-04-25 | Voyager Therapeutics, Inc. | TREATMENT OF AMYOTROPHIC LATERAL SCLEROSIS (ALS) |
| MA51583A (fr) * | 2018-01-04 | 2020-11-11 | Avidity Biosciences Inc | Molécules d'acide nucléique hétéroduplex et leurs utilisations |
| JP2021513903A (ja) * | 2018-02-21 | 2021-06-03 | アルキオーネ・ライフサイエンシズ・インコーポレイテッドAlcyone Lifesciences, Inc. | 流体送達システムおよび方法 |
| WO2019181946A1 (ja) * | 2018-03-19 | 2019-09-26 | 国立大学法人東京医科歯科大学 | 毒性が軽減した核酸 |
| EP3781677A4 (en) | 2018-04-16 | 2022-01-19 | University of Massachusetts | COMPOSITIONS AND METHODS FOR IMPROVED GENE EDITTING |
| SG11202101288TA (en) * | 2018-08-10 | 2021-03-30 | Univ Massachusetts | Modified oligonucleotides targeting snps |
| US11279930B2 (en) | 2018-08-23 | 2022-03-22 | University Of Massachusetts | O-methyl rich fully stabilized oligonucleotides |
| EP3911747A4 (en) | 2019-01-18 | 2023-05-24 | University Of Massachusetts | DYNAMIC PHARMACOKINETICS-MODIFYING ANCHORS |
| WO2020185651A2 (en) * | 2019-03-08 | 2020-09-17 | Rutgers, The State University Of New Jersey | Compositions and methods for treating huntington's disease |
| US11820985B2 (en) * | 2019-03-26 | 2023-11-21 | University Of Massachusetts | Modified oligonucleotides with increased stability |
| EP3966328A4 (en) * | 2019-05-06 | 2023-10-18 | University Of Massachusetts | ANTI-C9ORF72 OLIGONUCLEOTIDES AND RELATED METHODS |
| US12006499B2 (en) | 2019-06-06 | 2024-06-11 | Avidity Biosciences, Inc. | Una amidites and uses thereof |
| CA3142283A1 (en) | 2019-06-06 | 2020-12-10 | Avidity Biosciences, Inc. | Nucleic acid-polypeptide compositions and uses thereof |
| EP3983077A4 (en) * | 2019-06-17 | 2023-12-20 | Alnylam Pharmaceuticals, Inc. | DELIVERY OF OLIGONUCLEOTIDES TO THE STRIATUM |
| US20220348912A1 (en) | 2019-06-20 | 2022-11-03 | University Of Massachusetts | Compositions and methods for improved gene editing |
| JP2022547790A (ja) | 2019-08-09 | 2022-11-16 | ユニバーシティー オブ マサチューセッツ | Snpを標的とする化学修飾オリゴヌクレオチド |
| US20210108200A1 (en) * | 2019-09-16 | 2021-04-15 | University Of Massachusetts | BRANCHED LIPID CONJUGATES OF siRNA FOR SPECIFIC TISSUE DELIVERY |
| TW202132567A (zh) * | 2019-11-01 | 2021-09-01 | 美商阿尼拉製藥公司 | 亨汀頓蛋白(HTT)iRNA劑組成物及其使用方法 |
| AU2021260581A1 (en) * | 2020-04-20 | 2022-11-24 | University Of Massachusetts | Oligonucleotides for MSH3 modulation |
| US20220090069A1 (en) * | 2020-08-03 | 2022-03-24 | University Of Massachusetts | Oligonucleotides for htt-1a modulation |
| MX2023011466A (es) | 2021-03-29 | 2024-02-01 | Alnylam Pharmaceuticals Inc | Composiciones de agentes de ácido ribonucleico de interferencia (arni) de huntingtina (htt) y métodos de uso de estas. |
| BR112023026862A2 (pt) | 2021-06-23 | 2024-03-05 | Beth Israel Deaconess Medical Ct Inc | Compostos de oligonucleotídeos anti-flt1 otimizados para tratamento de pré-eclâmpsia e outros distúrbios angiogênicos |
| WO2023114959A2 (en) * | 2021-12-17 | 2023-06-22 | University Of Massachusetts | Oligonucleotides for mlh1 modulation |
| WO2024073595A2 (en) * | 2022-09-28 | 2024-04-04 | Atalanta Therapeutics, Inc. | Compositions and methods for treatment of huntington's disease |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2009504782A (ja) | 2005-08-18 | 2009-02-05 | アルナイラム ファーマシューティカルズ インコーポレイテッド | 神経疾患を治療するための方法および組成物 |
| WO2012005898A2 (en) | 2010-06-15 | 2012-01-12 | Alnylam Pharmaceuticals, Inc. | Chinese hamster ovary (cho) cell transcriptome, corresponding sirnas and uses thereof |
Family Cites Families (63)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4522811A (en) | 1982-07-08 | 1985-06-11 | Syntex (U.S.A.) Inc. | Serial injection of muramyldipeptides and liposomes enhances the anti-infective activity of muramyldipeptides |
| US5328470A (en) | 1989-03-31 | 1994-07-12 | The Regents Of The University Of Michigan | Treatment of diseases by site-specific instillation of cells or site-specific transformation of cells and kits therefor |
| ES2113371T3 (es) | 1989-11-16 | 1998-05-01 | Univ Duke | Transformacion de celulas epidermicas de tejidos animales con la ayuda de particulas. |
| US5252479A (en) * | 1991-11-08 | 1993-10-12 | Research Corporation Technologies, Inc. | Safe vector for gene therapy |
| US5587308A (en) * | 1992-06-02 | 1996-12-24 | The United States Of America As Represented By The Department Of Health & Human Services | Modified adeno-associated virus vector capable of expression from a novel promoter |
| US5858988A (en) | 1993-02-24 | 1999-01-12 | Wang; Jui H. | Poly-substituted-phenyl-oligoribo nucleotides having enhanced stability and membrane permeability and methods of use |
| US6291438B1 (en) | 1993-02-24 | 2001-09-18 | Jui H. Wang | Antiviral anticancer poly-substituted phenyl derivatized oligoribonucleotides and methods for their use |
| TW360548B (en) | 1993-04-08 | 1999-06-11 | Powderject Res Ltd | Products for therapeutic use |
| AU5545596A (en) | 1995-04-28 | 1996-11-18 | Medtronic, Inc. | Intraparenchymal infusion catheter system |
| US5684143A (en) | 1996-02-21 | 1997-11-04 | Lynx Therapeutics, Inc. | Oligo-2'-fluoronucleotide N3'->P5' phosphoramidates |
| US5735814A (en) | 1996-04-30 | 1998-04-07 | Medtronic, Inc. | Techniques of treating neurodegenerative disorders by brain infusion |
| US5898031A (en) | 1996-06-06 | 1999-04-27 | Isis Pharmaceuticals, Inc. | Oligoribonucleotides for cleaving RNA |
| WO2005121370A2 (en) | 2004-06-03 | 2005-12-22 | Isis Pharmaceuticals, Inc. | Oligomeric compounds that facilitate risc loading |
| US6177403B1 (en) | 1996-10-21 | 2001-01-23 | The Trustees Of The University Of Pennsylvania | Compositions, methods, and apparatus for delivery of a macromolecular assembly to an extravascular tissue of an animal |
| US6042820A (en) | 1996-12-20 | 2000-03-28 | Connaught Laboratories Limited | Biodegradable copolymer containing α-hydroxy acid and α-amino acid units |
| US6472375B1 (en) | 1998-04-16 | 2002-10-29 | John Wayne Cancer Institute | DNA vaccine and methods for its use |
| WO2002081628A2 (en) | 2001-04-05 | 2002-10-17 | Ribozyme Pharmaceuticals, Incorporated | Modulation of gene expression associated with inflammation proliferation and neurite outgrowth, using nucleic acid based technologies |
| EP2385123B1 (en) | 2001-09-28 | 2018-04-25 | Max-Planck-Gesellschaft zur Förderung der Wissenschaften e.V. | Microrna molecules |
| US20050096284A1 (en) | 2002-02-20 | 2005-05-05 | Sirna Therapeutics, Inc. | RNA interference mediated treatment of polyglutamine (polyQ) repeat expansion diseases using short interfering nucleic acid (siNA) |
| US7858367B2 (en) | 2002-04-30 | 2010-12-28 | Duke University | Viral vectors and methods for producing and using the same |
| EA200500232A1 (ru) | 2002-07-19 | 2005-12-29 | Бет Изрейэл Диконисс Медикал Сентер | Способы диагностики и лечения преэклампсии или эклампсии |
| AU2003287502B2 (en) | 2002-11-05 | 2010-12-09 | Isis Pharmaceuticals, Inc. | Compositions comprising alternating 2'-modified nucleosides for use in gene modulation |
| DK2284266T3 (da) * | 2002-11-14 | 2014-01-13 | Thermo Fisher Scient Biosciences Inc | sIRNA-MOLEKYLE MOD TP53 |
| US7250496B2 (en) * | 2002-11-14 | 2007-07-31 | Rosetta Genomics Ltd. | Bioinformatically detectable group of novel regulatory genes and uses thereof |
| EP3502252B1 (en) | 2003-06-02 | 2023-04-05 | University of Massachusetts | Methods and compositions for controlling efficacy of rna silencing |
| US7750144B2 (en) | 2003-06-02 | 2010-07-06 | University Of Massachusetts | Methods and compositions for enhancing the efficacy and specificity of RNA silencing |
| ATE485394T1 (de) | 2003-06-02 | 2010-11-15 | Univ Massachusetts | Verfahren und zusammensetzungen zur verbesserung der wirksamkeit und spezifität von fnai |
| WO2008005562A2 (en) | 2006-07-07 | 2008-01-10 | University Of Massachusetts | Rna silencing compositions and methods for the treatment of huntington's disease |
| JP5059411B2 (ja) | 2003-12-19 | 2012-10-24 | ノバルティス バクシンズ アンド ダイアグノスティックス,インコーポレーテッド | 短鎖干渉rnaの細胞トランスフェクティング処方物、関連する組成物および作製方法ならびに使用 |
| WO2005077333A2 (en) | 2004-02-10 | 2005-08-25 | University Of Florida Research Foundation, Inc. | Gel-based delivery of recombinant adeno-associated virus vectors |
| WO2005089224A2 (en) | 2004-03-12 | 2005-09-29 | Alnylam Pharmaceuticals, Inc. | iRNA AGENTS TARGETING VEGF |
| CA2564616C (en) | 2004-04-20 | 2016-08-30 | Nastech Pharmaceutical Company Inc. | Methods and compositions for enhancing delivery of double-stranded rna or a double-stranded hybrid nucleic acid to regulate gene expression in mammalian cells |
| JPWO2005116204A1 (ja) * | 2004-05-11 | 2008-06-19 | 株式会社アルファジェン | Rna干渉を生じさせるポリヌクレオチド、および、これを用いた遺伝子発現抑制方法 |
| AU2005316476A1 (en) | 2004-12-15 | 2006-06-22 | University Of Florida Research Foundation, Inc. | Chimeric vectors |
| CA2627025A1 (en) * | 2005-10-28 | 2007-05-03 | Alnylam Pharmaceuticals, Inc. | Compositions and methods for inhibiting expression of huntingtin gene |
| US20070259827A1 (en) | 2006-01-25 | 2007-11-08 | University Of Massachusetts | Compositions and methods for enhancing discriminatory RNA interference |
| US9198981B2 (en) | 2006-02-01 | 2015-12-01 | The University Of Kentucky | Modulation of angiogenesis |
| JPWO2007094218A1 (ja) | 2006-02-16 | 2009-07-02 | 国立大学法人岐阜大学 | 修飾オリゴヌクレオチド |
| US20090306178A1 (en) | 2006-03-27 | 2009-12-10 | Balkrishen Bhat | Conjugated double strand compositions for use in gene modulation |
| US20080039415A1 (en) | 2006-08-11 | 2008-02-14 | Gregory Robert Stewart | Retrograde transport of sirna and therapeutic uses to treat neurologic disorders |
| WO2008154482A2 (en) | 2007-06-08 | 2008-12-18 | Sirnaomics, Inc. | Sirna compositions and methods of use in treatment of ocular diseases |
| CN101199858A (zh) | 2007-10-18 | 2008-06-18 | 广州拓谱基因技术有限公司 | 治疗眼科疾病的多靶点小干扰rna鸡尾酒制剂及制备方法 |
| TW200927177A (en) | 2007-10-24 | 2009-07-01 | Nat Inst Of Advanced Ind Scien | Lipid-modified double-stranded RNA having potent RNA interference effect |
| US20110081362A1 (en) | 2008-01-31 | 2011-04-07 | The Brigham And Women's Hospital, Inc. | Treatment of cancer |
| US9217155B2 (en) | 2008-05-28 | 2015-12-22 | University Of Massachusetts | Isolation of novel AAV'S and uses thereof |
| EP2949752B1 (en) | 2008-09-22 | 2017-12-20 | RXi Pharmaceuticals Corporation | Reduced size self-delivering rnai compounds |
| US8734809B2 (en) | 2009-05-28 | 2014-05-27 | University Of Massachusetts | AAV's and uses thereof |
| HUE026020T2 (en) | 2009-08-27 | 2016-05-30 | Idera Pharmaceuticals Inc | Preparation for inhibiting gene expression and its uses |
| RU2615143C2 (ru) | 2010-03-24 | 2017-04-04 | Адвирна | Самодоставляющие PHKi соединения уменьшенного размера |
| SG10201604479YA (en) * | 2011-03-03 | 2016-07-28 | Quark Pharmaceuticals Inc | Oligonucleotide Modulators Of The Toll-Like Receptor Pathway |
| WO2012177906A1 (en) * | 2011-06-21 | 2012-12-27 | Alnylam Pharmaceuticals, Inc. | Assays and methods for determining activity of a therapeutic agent in a subject |
| WO2013165816A2 (en) | 2012-05-02 | 2013-11-07 | Merck Sharp & Dohme Corp. | SHORT INTERFERING NUCLEIC ACID (siNA) COMPOSITIONS |
| JP6139671B2 (ja) | 2012-05-22 | 2017-05-31 | オリックス ファーマシューティカルズ インコーポレイテッドOlix Pharmaceuticals Inc. | 細胞内貫通能を持ってrna干渉を誘導する核酸分子およびその用途 |
| BR112015000236A2 (pt) | 2012-07-10 | 2017-06-27 | Baseclick Gmbh | moléculas de ácidos nucleicos modificadas por anandamida |
| WO2014043544A1 (en) | 2012-09-14 | 2014-03-20 | Rana Therapeutics, Inc. | Multimeric oligonucleotide compounds |
| EP2920304B1 (en) | 2012-11-15 | 2019-03-06 | Roche Innovation Center Copenhagen A/S | Oligonucleotide conjugates |
| EP3132044B1 (en) | 2014-04-18 | 2020-04-08 | University of Massachusetts | Exosomal loading using hydrophobically modified oligonucleotides |
| SI3277814T1 (sl) | 2015-04-03 | 2020-12-31 | University Of Massachusetts | Oligonukleotidne spojine za ciljanja MRNA huntingtina |
| US20160319278A1 (en) | 2015-04-03 | 2016-11-03 | University Of Massachusetts | Fully stabilized asymmetric sirna |
| SI3277815T1 (sl) | 2015-04-03 | 2022-01-31 | University Of Massachusetts | Ologonukleotidne spojine za zdravljenje preeklampsije in drugih angiogeneznih motenj |
| MA43072A (fr) | 2015-07-22 | 2018-05-30 | Wave Life Sciences Ltd | Compositions d'oligonucléotides et procédés associés |
| US10633653B2 (en) | 2015-08-14 | 2020-04-28 | University Of Massachusetts | Bioactive conjugates for oligonucleotide delivery |
| EP3408391A4 (en) | 2016-01-31 | 2019-08-28 | University of Massachusetts | BRANCHED OLIGONUCLEOTIDES |
-
2016
- 2016-04-01 SI SI201630878T patent/SI3277814T1/sl unknown
- 2016-04-01 LT LTEP16716412.8T patent/LT3277814T/lt unknown
- 2016-04-01 EP EP20164108.1A patent/EP3766973A1/en active Pending
- 2016-04-01 CN CN202211430603.6A patent/CN116004624A/zh active Pending
- 2016-04-01 CN CN201680031524.4A patent/CN107980062B/zh active Active
- 2016-04-01 DK DK16716412.8T patent/DK3277814T3/da active
- 2016-04-01 US US15/089,319 patent/US9809817B2/en active Active
- 2016-04-01 HU HUE16716412A patent/HUE050441T2/hu unknown
- 2016-04-01 PT PT167164128T patent/PT3277814T/pt unknown
- 2016-04-01 WO PCT/US2016/025722 patent/WO2016161374A1/en active Application Filing
- 2016-04-01 PL PL16716412T patent/PL3277814T3/pl unknown
- 2016-04-01 CA CA2980337A patent/CA2980337A1/en active Pending
- 2016-04-01 EP EP16716412.8A patent/EP3277814B1/en active Active
- 2016-04-01 ES ES16716412T patent/ES2808750T3/es active Active
- 2016-04-01 RS RS20200929A patent/RS60762B1/sr unknown
- 2016-04-01 AU AU2016244027A patent/AU2016244027B2/en active Active
- 2016-04-01 JP JP2018502624A patent/JP7009356B2/ja active Active
-
2017
- 2017-09-06 US US15/697,120 patent/US10435688B2/en active Active
-
2019
- 2019-01-31 US US16/263,200 patent/US10774327B2/en active Active
-
2020
- 2020-03-06 US US16/811,580 patent/US11230713B2/en active Active
- 2020-07-31 HR HRP20201200TT patent/HRP20201200T1/hr unknown
- 2020-08-24 CY CY20201100791T patent/CY1123289T1/el unknown
-
2021
- 2021-11-29 US US17/536,647 patent/US20220251554A1/en active Pending
-
2022
- 2022-01-12 JP JP2022003057A patent/JP2022064900A/ja active Pending
- 2022-01-12 JP JP2022003059A patent/JP7504482B2/ja active Active
- 2022-06-30 AU AU2022204719A patent/AU2022204719A1/en active Pending
- 2022-06-30 AU AU2022204722A patent/AU2022204722A1/en active Pending
-
2023
- 2023-12-07 JP JP2023206985A patent/JP2024028909A/ja active Pending
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2009504782A (ja) | 2005-08-18 | 2009-02-05 | アルナイラム ファーマシューティカルズ インコーポレイテッド | 神経疾患を治療するための方法および組成物 |
| WO2012005898A2 (en) | 2010-06-15 | 2012-01-12 | Alnylam Pharmaceuticals, Inc. | Chinese hamster ovary (cho) cell transcriptome, corresponding sirnas and uses thereof |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7504482B2 (ja) | ハンチンチンmRNAをターゲティングするオリゴヌクレオチド化合物 | |
| US20240132892A1 (en) | OLIGONUCLEOTIDE-BASED MODULATION OF C9orf72 | |
| US20200362341A1 (en) | Oligonucleotides for tissue specific apoe modulation | |
| JP2018517429A (ja) | 十分に安定化された非対称sirna | |
| WO2008005562A2 (en) | Rna silencing compositions and methods for the treatment of huntington's disease | |
| JP2022528840A (ja) | 安定性が増加した修飾オリゴヌクレオチド | |
| TW202315943A (zh) | 用於治療子癇前症及其它血管新生病症的最佳化抗flt1寡核苷酸化合物 | |
| KR20230002327A (ko) | Snca 조절을 위한 올리고뉴클레오티드 | |
| EP4110913A2 (en) | Oligonucleotides for prnp modulation | |
| US20230392146A1 (en) | Oligonucleotides for app modulation |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20180227 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20190124 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20190124 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20191024 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20191112 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20200210 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200410 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20200915 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20201214 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20210601 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20210831 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20210908 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20211028 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20211201 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20211214 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20220112 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7009356 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |