JP6861630B2 - Il−4rアンタゴニストの投与により鼻ポリープを伴う慢性副鼻腔炎を処置する方法 - Google Patents
Il−4rアンタゴニストの投与により鼻ポリープを伴う慢性副鼻腔炎を処置する方法 Download PDFInfo
- Publication number
- JP6861630B2 JP6861630B2 JP2017525897A JP2017525897A JP6861630B2 JP 6861630 B2 JP6861630 B2 JP 6861630B2 JP 2017525897 A JP2017525897 A JP 2017525897A JP 2017525897 A JP2017525897 A JP 2017525897A JP 6861630 B2 JP6861630 B2 JP 6861630B2
- Authority
- JP
- Japan
- Prior art keywords
- nasal
- antigen
- antibody
- binding fragment
- administration
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2866—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against receptors for cytokines, lymphokines, interferons
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/56—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids
- A61K31/57—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids substituted in position 17 beta by a chain of two carbon atoms, e.g. pregnane or progesterone
- A61K31/573—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids substituted in position 17 beta by a chain of two carbon atoms, e.g. pregnane or progesterone substituted in position 21, e.g. cortisone, dexamethasone, prednisone or aldosterone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/56—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids
- A61K31/58—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids containing heterocyclic rings, e.g. danazol, stanozolol, pancuronium or digitogenin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
- A61K39/39533—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals
- A61K39/3955—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals against proteinaceous materials, e.g. enzymes, hormones, lymphokines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0043—Nose
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/02—Nasal agents, e.g. decongestants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/08—Antiallergic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
- C07K14/715—Receptors; Cell surface antigens; Cell surface determinants for cytokines; for lymphokines; for interferons
- C07K14/7155—Receptors; Cell surface antigens; Cell surface determinants for cytokines; for lymphokines; for interferons for interleukins [IL]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/48—Other medical applications
- A61B5/4848—Monitoring or testing the effects of treatment, e.g. of medication
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/54—Medicinal preparations containing antigens or antibodies characterised by the route of administration
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/545—Medicinal preparations containing antigens or antibodies characterised by the dose, timing or administration schedule
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/21—Immunoglobulins specific features characterized by taxonomic origin from primates, e.g. man
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Animal Behavior & Ethology (AREA)
- Organic Chemistry (AREA)
- Immunology (AREA)
- Pharmacology & Pharmacy (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Pulmonology (AREA)
- Epidemiology (AREA)
- Molecular Biology (AREA)
- Biophysics (AREA)
- Genetics & Genomics (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Biochemistry (AREA)
- Otolaryngology (AREA)
- Endocrinology (AREA)
- Mycology (AREA)
- Microbiology (AREA)
- Transplantation (AREA)
- Surgery (AREA)
- Physics & Mathematics (AREA)
- Medical Informatics (AREA)
- Heart & Thoracic Surgery (AREA)
- Biomedical Technology (AREA)
- Pathology (AREA)
- Hematology (AREA)
- Diabetes (AREA)
- Cell Biology (AREA)
- Zoology (AREA)
- Toxicology (AREA)
- Gastroenterology & Hepatology (AREA)
Description
本出願は、2014年11月14日に出願された米国特許仮出願第62/080,092号、2014年11月24日に出願された米国特許仮出願第62/083,821号、2015年5月8日に出願された米国特許仮出願第62/158,832号、および2015年7月31日に出願された米国特許仮出願第62/199,305号、ならびに2015年10月14日に出願された欧州出願第15306632.9号の利益を主張し、それらの各々は、参照によってそれらの全体が本明細書に組み入れられる。
特定の態様において、本発明は、鼻ポリープ/鼻茸を伴う慢性副鼻腔炎(CSwNP)を処置する方法を提供する。他の態様において、本発明は、鼻ポリープ/鼻茸を伴わない慢性副鼻腔炎を処置する方法を提供する。本明細書で使用される場合、「慢性副鼻腔炎」(「CS」)は、限定されないが、鼻閉塞、嗅覚の低下もしくは喪失、前部および/もしくは後部鼻漏、顔面痛ならびに/または頭痛およびその帰結を含む、多くの場合何年にもわたる、特異的症状の任意の組合せを特徴とする、副鼻腔の炎症状態を指す。正式な診断は、副鼻腔コンピューター断層撮影(CT)スキャンおよび/または副鼻腔内視鏡検査に基づいて行われる。内視鏡評価に基づいて、CSは、鼻ポリープ/鼻茸を伴うCS(CSwNP)、または鼻ポリープ/鼻茸を伴わないCSとして臨床的に分類することができる。
本発明は、それを必要とする対象において1つまたはそれ以上の鼻ポリープに関連するパラメーターを改善する方法であって、インターロイキン−4受容体(IL−4R)アンタゴニストを含む医薬組成物を対象に投与する工程を含む、方法を含む。別の言葉で表現すると、本発明は、それを必要とする対象における1つまたはそれ以上の鼻ポリープに関連するパラメーターを改善するのに使用するための、インターロイキン−4受容体(IL−4R)アンタゴニストを含む医薬組成物を含む。例えば、IL−4R受容体アンタゴニストは患者において内視鏡的鼻ポリープスコア(NPS)を低下させることができる。0の鼻ポリープスコアはポリープの存在がないことを示す。1のNPSは中鼻甲介の下縁の下に到達しない中鼻道における小さいポリープの存在を示す。3のNPSは、下鼻甲介の下縁に到達する大きなポリープまたは中鼻甲介までの中間のポリープを示す。4のNPSは下鼻腔の完全な閉塞を引き起こす大きなポリープを示す(以下の表15を参照のこと)。最大スコアは8である(鼻腔ごとに4ポイント)。IL−4Rアンタゴニストによる処置はNPSを約1〜約8ポイント減少させることができる。例えば、IL−4Rアンタゴニストによる処置は、NPSを約1ポイントもしくはそれ以上、約2ポイントもしくはそれ以上、または約3ポイントもしくはそれ以上減少させることができる。いくつかの実施形態において、IL−4Rアンタゴニストによる処置は、NPSを約1ポイントもしくはその割合;2ポイントもしくはその割合;3ポイントもしくはその割合;4ポイントもしくはその割合;5ポイントもしくはその割合;6ポイントもしくはその割合;7ポイントもしくはその割合;または8ポイントもしくはその割合減少させることができる。
一実施形態において、インターロイキン−4受容体(IL−4R)アンタゴニストを含む治療組成物を、それを必要とする対象は投与される。本明細書で使用される場合、「IL−4Rアンタゴニスト」は、IL−4Rに結合するかまたはIL−4Rと相互作用し、IL−4Rがin vitroまたはin vivoで細胞上に発現された場合にIL−4Rの通常の生物学的シグナル伝達機能を阻害する任意の薬剤である。IL−4Rアンタゴニストのカテゴリーの非限定的な例には、小分子IL−4Rアンタゴニスト、ペプチドベースのIL−4Rアンタゴニスト(例えば、「ペプチボディ(peptibody)」分子)、およびヒトIL−4Rに特異的に結合する抗体または抗体の抗原結合断片が含まれる。
本発明は、IL−4Rアンタゴニストを患者に投与する工程であって、IL−4Rアンタゴニストは医薬組成物内に含有される、工程を含む方法を含む。本発明において特徴付けられる医薬組成物は、適切な担体、賦形剤および適切な移送、送達、耐性などをもたらす他の薬剤と共に製剤化される。複数の適切な製剤は、全ての薬剤師に公知の処方集に見出すことができる:Remington’s Pharmaceutical Sciences、Mack Publishing Company、Easton、PA。これらの製剤には、例えば、粉剤、ペースト剤、軟膏、ゼリー、ワックス、オイル、脂質、脂質(カチオン性またはアニオン性)含有小胞(LIPOFECTIN(商標)など)、DNAコンジュゲート、無水吸収ペースト、水中油および油中水エマルション、カーボワックスエマルション(様々な分子量のポリエチレングリコール)、半固形ゲルおよびカーボワックスを含有する半固形混合物が含まれる。Powellら「Compendium of excipients for parenteral formulations」PDA(1998)J Pharm Sci Technol 52:238〜311も参照されたい。
本明細書において特徴付けられる方法に従って対象に投与されるIL−4Rアンタゴニスト(例えば、抗IL−4R抗体またはその抗原結合断片)の量は、一般的に治療有効量である。本明細書で使用される場合、「治療有効量」という語句は、鼻ポリープに関連する1つもしくはそれ以上の症状の検出可能な改善を生じるIL−4Rアンタゴニストの用量、または鼻ポリープもしくは鼻ポリープに関連する状態の進行を阻害、予防、軽減または遅延させるIL−4Rアンタゴニストの用量を意味する。抗IL−4R抗体の場合、治療有効量は、約0.05mg〜約600mg、例えば、約0.05mg、約0.1mg、約1.0mg、約1.5mg、約2.0mg、約10mg、約20mg、約30mg、約40mg、約50mg、約60mg、約70mg、約80mg、約90mg、約100mg、約110mg、約120mg、約130mg、約140mg、約150mg、約160mg、約170mg、約180mg、約190mg、約200mg、約210mg、約220mg、約230mg、約240mg、約250mg、約260mg、約270mg、約280mg、約290mg、約300mg、約310mg、約320mg、約330mg、約340mg、約350mg、約360mg、約370mg、約380mg、約390mg、約400mg、約410mg、約420mg、約430mg、約440mg、約450mg、約460mg、約470mg、約480mg、約490mg、約500mg、約510mg、約520mg、約530mg、約540mg、約550mg、約560mg、約570mg、約580mg、約590mgまたは約600mgの抗IL−4R抗体または抗原結合断片であってもよい。例えば、治療有効量は、抗IL−4R抗体または抗原結合断片約0.1mg〜約590mg、または約1.0mg〜約580mg、または約1.5mg〜約570mg、または約2.0mg〜約570mg、または約10mg〜約560mg、または約20mg〜約550mg、または約30mg〜約540mg、または約40mg〜約530mg、または約50mg〜約520mg、または約60mg〜約510mg、または約70mg〜約500mg、または約80mg〜約490mg、または約90mg〜約480mg、または約100mg〜約470mg、または約110mg〜約460mg、または約120mg〜約450mg、または約130mg〜約440mg、または約140mg〜約430mg、または約150mg〜約420mg、または約160mg〜約410mg、または約170mg〜約400mg、または約180mg〜約390mg、または約190mg〜約380mg、または約200mg〜約380mg、または約210mg〜約370mg、または約220mg〜約360mg、または約230mg〜約350mg、または約240mg〜約340mg、または約250mg〜約330mg、または約260mg〜約320mg、または約270mg〜約310mg、または約280mg〜約300mg、または約290mg〜約300mgであってもよい。
特定の実施形態による方法は、1つまたはそれ以上のさらなる治療剤をIL−4Rアンタゴニストと組み合わせて対象に投与する工程を含む。言い換えると、特定の実施形態は、対象の治療に使用するためにIL−4Rアンタゴニストと組み合わせて1つまたはそれ以上のさらなる治療剤を含む。本明細書において使用される場合、「と組み合わせて」という表現は、さらなる治療剤を、IL−4Rアンタゴニストを含む医薬組成物の前、後または同時に投与することを意味する。例えば、IL−4Rアンタゴニストを含む医薬組成物の「前」に投与される場合、さらなる治療剤は、IL−4Rアンタゴニストを含む医薬組成物の投与の約72時間、約60時間、約48時間、約36時間、約24時間、約12時間、約10時間、約8時間、約6時間、約4時間、約2時間、約1時間、約30分、約15分または約10分前に投与される。IL−4Rアンタゴニストを含む医薬組成物の「後」に投与される場合、さらなる治療剤は、IL−4Rアンタゴニストを含む医薬組成物の投与の約10分、約15分、約30分、約1時間、約2時間、約4時間、約6時間、約8時間、約10時間、約12時間、約24時間、約36時間、約48時間、約60時間または約72時間後に投与される。IL−4Rアンタゴニストを含む医薬組成物と「同時」の投与は、さらなる治療剤が、IL−4Rアンタゴニストを含む医薬組成物の投与の5分未満以内(前、後、または同時)に別々の剤形で対象に投与されるか、またはさらなる治療剤およびIL−4Rアンタゴニストの両方を含む単一の配合投薬製剤として対象に投与されることを意味する。
特定の実施形態によれば、IL−4Rアンタゴニストの複数回用量は規定された時間経過にわたって対象に投与される。その方法は、例えば、IL−4Rアンタゴニストの複数回用量を対象に連続投与する工程を含む。本明細書で使用される場合、「連続投与する」とは、IL−4Rアンタゴニストの各用量が、異なる時点、例えば、所定の間隔(例えば、時間、日、週または月)だけ隔てた異なる日に対象に投与されることを意味する。本発明は、IL−4Rアンタゴニストの単回初期用量、続いてIL−4Rアンタゴニストの1回またはそれ以上の二次用量、場合により続いてIL−4Rアンタゴニストの1回またはそれ以上の三次用量を患者に連続投与する工程を含む方法を含む。
本発明において特徴付けられる方法は、IL−4Rアンタゴニストを含む治療組成物を、それを必要とする対象に投与する工程を含む。本明細書で使用される場合、「それを必要とする対象」との表現は、(i)鼻茸、(ii)鼻ポリープを伴う慢性副鼻腔炎、(iii)アレルギー性もしくは非アレルギー性鼻炎、または(iv)アレルギー性もしくは非アレルギー性鼻副鼻腔炎の1つまたはそれ以上の症状または適応症を示すヒトまたは非ヒト動物、あるいはこれらの状態の1つと診断された対象を意味する。例えば、一実施形態において、それを必要とする対象は、両側性鼻ポリープ、および各々の鼻孔について少なくとも2のスコアで、両方の鼻孔について少なくとも4から最大8の鼻ポリープスコアを有する。特定の実施形態において、ポリープは中鼻道にある。特定の実施形態において、鼻ポリープの存在は内視鏡検査によって確認される。いくつかの実施形態において、対象はまた、CTスキャンなどの方法によって確認される、両側性粘膜疾患を有する。本明細書で使用される場合、「両側性粘膜疾患」は、鼻腔、例えば、上顎鼻腔の粘膜内層の感染である。いくつかの実施形態において、両側性鼻茸(例えば、各々の鼻孔について少なくとも2のスコアで、両方の鼻孔について少なくとも4から最大8の鼻ポリープスコア)は、INCSが少なくとも6週間、少なくとも7週間、少なくとも8週間またはそれ以上の間、投与された場合などの、吸入コルチコステロイド(INCS)の処置レジメン後でさえも持続する。
A.研究目的および概要
無作為化、プラセボ対照、二重盲検、並行群研究を、吸入コルチコステロイド(ICS)および長時間作用性ベータ2アゴニスト(LABA)治療により部分的に管理された/管理されなかった持続性の中程度から重度の好酸球性喘息を有する患者に、300mgのデュピルマブ(「mAb1」)またはプラセボのいずれかを12週間、週に1回皮下投与して行った。デュピルマブは配列番号1の重鎖可変領域および配列番号2の軽鎖可変領域を有する抗IL−4R抗体である。特定の例示的な実施形態において、デュピルマブは、配列番号9の重鎖配列および配列番号10の軽鎖配列を含む。デュピルマブは米国特許第7,608,693号に記載されている。
フルチカゾン/サルメテロール組合せ治療
− Advair(登録商標)Diskus−ドライパウダー吸入器(DPI):250/50μg BIDもしくは500/50μg BID;もしくは
− Advair(登録商標)HFA−定量吸入器(MDI):230/42μg BIDもしくは460/42μg BID;または
ブデソニド/ホルモテロール組合せ治療(Symbicort(登録商標)160/9μg BIDまたは320/9μg BID);または
モメタゾン/ホルモテロール組合せ治療(Dulera(登録商標)200/10μg BIDまたは400/10μg BID)。
患者は、300mg mAb1(またはプラセボ)の付加型治療または処置を開始した後4週間、BID フルチカゾン/サルメテロールバックグラウンド治療を継続したままであった。無作為化の4週後に、患者を、BID フルチカゾン/サルメテロール組合せ治療から等価ICS用量のフルチカゾン単独療法(250ugもしくは500μg BIDのFLOVENT(登録商標)Diskus−DPI製剤;または220μgもしくは440μg BIDのFLOVENT(登録商標)HFA−MDI製剤のいずれかを含む)に切り替えた。LABA成分(すなわち、サルメテロール)を中断した。その後の来診時に、患者が喘息増悪(以下に定義される通り)についての基準をいずれも満たしていなかった場合には、6週目に開始して、フルチカゾン用量を約50%低下させた。喘息増悪が発生しなかった場合には、ICS休薬を表1に記載されるスケジュールに従って進めた。
治験医薬品:デュピルマブまたは合致するプラセボ。製剤:SC注射用の滅菌デュピルマブ150mg/mL溶液を5mLガラスバイアルで提供した。各バイアルは2mLの引きぬき可能体積を含んでいた。滅菌プラセボを、完全に同じように合致するガラス製の5mLバイアルで提供した。投与経路:皮下(SC)注射。用量レジメン:D1にデュピルマブ600mg SC(負荷用量)、その後15週間にわたって毎週300mg SC注射。D1にプラセボSC負荷用量、その後15週間にわたって毎週SC注射。
この研究の主要評価項目は、以下のいずれかにより定義される喘息の増悪の発生であった:(1)連続した2日間、朝の最大呼気流量(PEF)におけるベースラインからの30%もしくはそれ以上の低下;または(2)連続した2日間、24時間で(ベースラインと比較して)アルブテロールもしくはレブアルブテロールの6回またはそれ以上のさらなる発作治療薬パフ;または(3)(a)全身(経口および/または非経口)ステロイド処置、もしくは(b)研究からの中断前に受けていた最後の用量のICSの4倍以上の増加、もしくは(c)入院を必要とする、治験責任医師により決定された喘息の悪化。
有害事象および重篤な有害事象をモニタリングすることにより、安全性を研究全体を通じて評価した。
喘息増悪を経験した患者の比率の一次分析のために、ロジスティック回帰モデルを使用して、SAR群をプラセボと比較した。このモデルは、処置および層別因子の項(先行するICS/LABA組合せ治療用量)を含んでいた。一次分析を修正包括解析(modified intent−to−treat)(mITT)集団に基づいて行い、これは少なくとも1回の用量のmAb1を投与された全ての無作為化された患者を含んでいた。層別カイ二乗検定もまた、一次分析を裏付けるために使用した。
研究の処置段階を完了したか、または中断した全104人の無作為化した患者(491人からスクリーニングされた)で観察された結果を以下にまとめる。全ての無作為化した患者を、研究処置に曝露し、mITT集団に含めた。ベースライン特徴は群間で同様であった。人口統計および臨床特徴も2つの群間で同様であった(表3)。上に示したように、患者を週に1回の300mg皮下mAb1またはプラセボのいずれかで処置した。研究処置期間を、それぞれmAb1およびプラセボ患者の86.5%および67.3%が完了した。中止の最も一般的な原因は効能の欠如であり、これはmAb1(1.9%)よりもプラセボ(21.2%)でより頻繁であった。
プラセボおよびmAb1処置群における喘息増悪の発生率を表4に示す。
肺機能パラメーター(FEV1、AM PEFおよびPM PEF)、喘息症状ベースの評価項目(ACQスコア、夜間覚醒)、およびアルブテロール使用を、各患者について各来診時に評価した。さらに、SNOT−22スコアをベースラインおよび処置の終わりに評価した。全てのパラメーターについて、ベースラインおよび12週(LOCF)の平均値を、処置群間の平均差異と共に(SNOT−22についてのANOVAモデル)表7にまとめる。表7において、「プラセボに対する差異」と標示される列は、プラセボ処置群におけるそのパラメーターについて観察された変化と比較して、パラメーターの値において観察された変化を考慮した、ベースラインからのプラセボ補正値を示す。
mAb1は一般的に安全であり、良好な耐容性を示した。処置により発現した有害事象(TEAE)が、40人(76.9%)のプラセボにより処置した患者および42人(80.8%)のmAb1により処置した患者によって同様に報告された(表10)。TEAEは非特異的であり、一般的には軽度から中程度の強度であり、大部分は研究の終わりまでに回復した。以下のTEAEの増加した報告がプラセボと比較してmAb1について観察された:注射部位反応が15人(28.8%)のmAb1患者および5人(9.6%)のプラセボ患者によって報告された;鼻咽頭炎が7人(13.5%)のmAb1患者および2人(3.8%)のプラセボ患者によって報告された;頭痛が6人(11.5%)のmAb1患者および3人(5.85)のプラセボ患者によって報告され、悪心が4人(7.7%)のmAb1患者および1人(1.9%)のプラセボ患者によって報告された。
肺機能および他の喘息管理パラメーターについて有意な改善が観察された。バックグラウンド治療休薬にもかかわらず、効能が早期に、持続して観察された。好酸球増加症を有する持続性の中程度から重度の喘息患者における喘息増悪の発生率の主要評価項目における約87%の相対的減少(p<0.0001)が、プラセボ(44.2%)と比較して、週に1回の300mgのmAb1での12週間の処置後に観察された(5.8%)。表7に示されるように、プラセボと比較して処置での臨床上意味のある統計的に有意な(多重度調整無し)改善が、肺機能パラメーター(FEV1、PEF AM)、喘息症状スコア(ACQ)およびアルブテロール使用において観察された。有益な傾向がPEF PM(p=0.0567)および夜間覚醒(p=0.0518)について観察された。統計的に有意な(多重度調整なし)改善がSNOT−22スコアについても観察された。積極的処置群内で、ベースラインに対する持続した改善が、LABAおよびICSの休薬にもかかわらず、全てのパラメーターについての研究の過程の間に観察された。mAb1は一般的に安全であり、良好な耐容性を示した。
バイオマーカー分析を、mAb1の臨床試験に参加した対象(上記の実施例1を参照のこと)から得たサンプルで行った。特に、胸腺および活性化ケモカイン(TARC;CCL17)、免疫グロブリンE(IgE)、エオタキシン−3、ペリオスチン、癌胎児抗原(CEA)、YKL−40および血中好酸球のようなTH2炎症に関連する血清/血漿バイオマーカーを、ベースラインおよび研究処置の開始後の異なる時点での患者由来のサンプルにおいて測定した。これらのバイオマーカーのベースラインレベルを、処置応答についての潜在的な予測値について評価した。さらに、呼気NO濃度(FeNO)ならびに誘発痰中好酸球および好中球を、気管支炎症のバイオマーカーとして測定した。呼気一酸化窒素評価を肺活量測定の前および少なくとも1時間の絶食後にNIOX機器(Aerocrine AB、Solna、Sweden)を使用して行った。バイオマーカーを、混合モデルを使用して分析し、モデルから誘導された最小二乗平均を以下に報告する。
これらの結果は、mAb1が、成人喘息患者において、Th2炎症(TARC、エオタキシン−3およびIgE)および気管支炎症(FeNO)に関連する血清バイオマーカーを有意に減少させたということを示す。FeNO低下とFEV1改善との間の相関は、IL−4/IL−13媒介性抗炎症活性と中程度から重度の管理されていない喘息における肺機能の改善との間の関係を示唆する。
A.研究目的および概要
実施例1に記載されるSNOT−22試験に対するmAb1の陽性効果は、抗IL−4R抗体もまた、鼻ポリープを伴う慢性副鼻腔炎を処置するのに有効であり得ることを示唆した。さらに、鼻ポリープは最も一般的には好酸球性/TH2により駆動され、mAb1はTh2炎症に関連するバイオマーカーを顕著に低下させた(実施例2を参照のこと)。したがって、鼻ポリープを伴う慢性副鼻腔炎に対するmAb1の治療効果を試験するために臨床試験を設計した。
治験薬:様々な濃度の滅菌mAb1を5mLガラスバイアルで提供した。各バイアルは2mLの引きぬき可能体積を含んでいた:150mg/mL溶液(300mg用量/2mL)。滅菌プラセボを、完全に同じように合致するガラス製の5mLバイアルで提供し、各バイアルは2mLの送達可能体積を含んでいた。
この研究の主要評価項目は両側性内視鏡的鼻ポリープスコアにおける16週でのベースラインからの変化である(表15を参照のこと)。
事前に設定した一次分析を16週間の処置期間の終了時に行った。効能の分析は、研究処置を受けたことのいかんを問わず、無作為化された全ての患者と事前に定義した、包括解析(ITT)集団を使用して行った。安全性の分析は、投与した処置の量を問わず、研究対象薬物に曝露される全ての無作為化された患者と事前に定義した、安全性集団を使用して行った。
人口統計学およびベースライン臨床特徴は、2つ群間で同様であった(表51)。16週間の処置期間を、それぞれ、プラセボ患者30人のうちの23人、およびデュピルマブ患者30人のうちの28人が完了した。プラセボ群において、患者7人のうち5人は、1つまたはそれ以上の有害事象のため、および7人のうち2人は、効能の欠如のため、研究を早期に中止した。デュピルマブ群において、患者30人のうち2人は、両方の有害事象のため処置期間を完了しなかった。
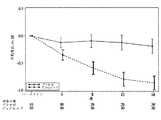
SNOT−22は、研究中、患者によって生活の質に対する鼻副鼻腔炎の影響を評価するために使用された。スコアが高いほど悪い疾患を示し;全最大スコアは110であった。結果は、16週においてデュピルマブに有利な有意差を実証した;16週におけるベースラインからのLS平均(SE)変化は、プラセボ群では−9.17(2.96)およびデュピルマブ群では−27.28(2.71)であり、その結果、LS平均差は−18.11(95%CI、−25.62〜−10.60、p<0.0001)となった(表22)。SNOT−22スコアに対するデュピルマブの効果は、4週から16週まで観察された(図5)。
ベースライン特徴は、群間で同様であった。NPSの最小二乗(LS)平均変化は、プラセボ/モメタゾン群で−0.30であり、デュピルマブ/モメタゾン群で−1.85であった(LS平均差(95%CI)−1.55;p=0.0009)。デュピルマブに有利な有意な変化は、Lund−Mackay CTスコア(差−8.84;p<0.0001)、罹病した上顎洞容積のパーセント(差−32.24;p<0.0001)、SNOT−22(差−18.1;p<0.0001)、嗅覚、および他の全ての副次的評価項目についても観察された。喘息を有する患者(n=16)に関して、デュピルマブは、予測FEV1%を向上させ(7.2%増加、p=0.04)、喘息管理を改善した(ACQ5の1.1単位低下;p<0.0001)。注射部位反応、頭痛および上咽頭炎は、デュピルマブに関して報告頻度が最も高かった有害事象であった。
併存する喘息を有する患者のサブセットにおいて、デュピルマブでの処置は、肺機能(図22A)および喘息管理(図22B)の改善に関連しており、FEV1(%)の処置群間LS平均差は7.2%(95%CI、0.4〜13.9、p=0.04)であり、ACQ−5の減少は、プラセボ群では0.3(0.3)単位およびデュピルマブ群では1.4(0.4)単位であり、結果としてACQスコアのLS平均差は−1.1単位(95%CI、−1.5〜−0.6、p<0.0001)になった。加えて、このサブグループにおいて、ベースラインから16週の間の両側性内視鏡的鼻ポリープスコアの平均変化は、プラセボ群では0.3(0.9)およびデュピルマブ群では−2.4(2.0)であり、その結果、LS平均差は、デュピルマブに有利な−2.3(95%CI、−3.4〜−1.2、p=0.0002)になった。喘息を有する患者は、デュピルマブ/MFNSを用いてUPSIT、SNOT−22、および詰まりの症状の改善も経験した(表55)。
有害事象は、プラセボ群の患者30人のうちの25人、およびデュピルマブ群の30人のうちの29人によって報告された(表37)。注射部位反応(ISR)、頭痛、および上咽頭炎は、全研究集団にわたって最も高頻度の有害事象であり、ISRは、デュピルマブ処置に関してより高頻度に見られた。これらの事象は、一般に、非特異的であり、軽度から中等度の強度であった。
Claims (15)
- それを必要とする対象の鼻ポリープを伴う慢性鼻副鼻腔炎(CRSwNP)の治療に使用するための、インターロイキン−4受容体(IL−4R)に特異的に結合する抗体またはその抗原結合断片を含む医薬組成物であって、
抗体またはその抗原結合断片は、配列番号6、7および8の軽鎖CDR配列と、配列番号3、4および5の重鎖CDR配列とを含み、
医薬組成物は、300mgの用量で14日に1回(Q2W)投与されるものである、
前記医薬組成物。 - 対象は、各鼻腔に存在する2つまたはそれ以上の鼻ポリープを含む、合計少なくとも5つの鼻ポリープを有する;
対象は、重症の両側性鼻ポリープを伴う慢性副鼻腔炎を有する;
対象は、鼻ポリープを伴う 難治性慢性鼻副鼻腔炎(CRS)を有する;
対象は、さらに、アレルギー性鼻炎、喘息、アスピリン過敏症および非ステロイド性抗炎症薬(NSAID)過敏症からなる群から選択される1つまたはそれ以上の状態をさらに有する;
対象は、鼻ポリープおよび慢性鼻副鼻腔炎の一方または両方のための手術を受けたことがある;
最初の機能的内視鏡下副鼻腔手術(FESS)が指示されるか、修正手術が指示されるか、または手術が禁忌となる;
抗体またはその抗原結合断片は、経口コルチコステロイド、全身性コルチコステロイドによる治療の必要性を減少させ、および/または鼻ポリープ手術の必要性を減少させる;
医薬組成物は、鼻ポリープスコア(NPS)を、約10%〜約50%、約20%〜約40%、または約25%〜約30%減少させるのに使用するためのものである;
医薬組成物は、日中(AM)に、夜(PM)に、またはAMとPMの両方に発生する、
嗅覚の喪失、鼻水、後部鼻漏および鼻最大吸気流量のうちの1つまたはそれ以上を改善させるのに使用するためのものである;
抗体またはその抗原結合断片の投与は、皮下的に行われる;および/または
抗体またはその抗原結合断片の投与は、注射器、場合により充填済みの注射器または自動注射器で行われる;
請求項1に記載の医薬組成物。 - 抗体またはその抗原結合断片は、配列番号1のアミノ酸配列を有するHCVRと配列番号2のアミノ酸配列を有するLCVRとを含む;
抗体またはその抗原結合断片は、配列番号9の重鎖配列と配列番号10の軽鎖配列とを含む;および/または
抗体は、デュピルマブである;
請求項1又は2に記載の医薬組成物。 - 医薬組成物は、さらに、鼻詰まり/閉塞(NC)の重症度、内視鏡鼻ポリープスコア(NPS)、コンピュータ断層撮影(CT)スキャン副鼻腔混濁、総症状スコア(TSS)、22項目副鼻腔評価試験(SNOT−22)スコア、嗅覚の喪失、鼻水、後部鼻漏および鼻最大吸気流量(NPIF)からなる群から選択される1つまたはそれ以上の鼻茸に関連するパラメーターを改善するのに使用するためのものである;
医薬組成物は、さらに、血清IgEレベル、血漿エオタキシン−3レベル、ならびに血清胸腺および活性化調節ケモカイン(TARC)レベルのうちの1つまたはそれ以上を減少させるのに使用するためのものである;および/または
医薬組成物は、さらに、対象の鼻汁における総IgEレベル、エオタキシン−3レベルおよび好酸球陽イオンタンパク質(ECP)レベルのうちの1つまたはそれ以上を減少させるのに使用するためのものである;
請求項1〜3のいずれか1項に記載の医薬組成物。 - それを必要とする対象の鼻ポリープを伴う慢性鼻副鼻腔炎(CRSwNP)の治療に使用するための、IL−4Rに特異的に結合する抗体またはその抗原結合断片を含む医薬組成物であって、
抗体またはその抗原結合断片は、鼻ポリープスコア(NPS)が決定された対象への投与のためのものであり;
医薬組成物は、1またはそれ以上の維持容量のICSを受けた対象に投与されるものであり、
抗体またはその抗原結合断片は300mgの用量で14日に1回(Q2W)投与されるものであり;ならびに
抗体またはその抗原結合断片は、配列番号6、7および8の軽鎖CDR配列と、配列番号3、4および5の重鎖CDR配列とを含む、
前記医薬組成物。 - 対象は、重症の両側性鼻ポリープを伴う慢性副鼻腔炎を有する;
対象は、鼻ポリープを伴う難治性慢性鼻副鼻腔炎(CRS)を有する、
対象は、投与前に、各鼻腔に存在する2つまたはそれ以上の鼻ポリープを含む、合計少なくとも5つの鼻ポリープを有する;
抗体またはその抗原結合断片は、鼻ポリープスコア(NPS)を、約10%〜約50%、約20%〜約40%、または約25%〜約30%減少させるのに使用するためのものである;
対象はさらに、アレルギー性鼻炎、喘息、アスピリン過敏症およびNSAID過敏症からなる群から選択される1つまたはそれ以上の状態をさらに有する;
対象は、鼻ポリープおよび慢性鼻副鼻腔炎の一方または両方のための手術を受けたこと
がある;
最初の機能的内視鏡下副鼻腔手術(FESS)が指示されるか、修正手術が指示されるか、または手術が禁忌となる;
ICSは、フランカルボン酸モメタゾンの鼻内噴霧(MFNS)、場合により、MFNS約100mgが対象の各鼻孔に1日1回または2回投与されるものである;および/または
医薬組成物の投与は、注射器、場合により充填済み注射器による皮下または静脈内送達、または、ペン型または自動注入送達デバイスによる皮下送達で行われるものである、
請求項5に記載の医薬組成物。 - 抗体またはその抗原結合断片は、配列番号1のアミノ酸配列を有するHCVRと配列番号2のアミノ酸配列を有するLCVRとを含む;
抗体またはその抗原結合断片は、配列番号9の重鎖配列と配列番号10の軽鎖配列とを含む;および/または
抗体は、デュピルマブである;
請求項5または6に記載の医薬組成物。 - 抗体またはその抗原結合断片は、さらに、鼻詰まり/閉塞(NC)の重症度、内視鏡鼻ポリープスコア(NPS)、コンピュータ断層撮影(CT)スキャン副鼻腔混濁、総症状スコア(TSS)、22項目副鼻腔評価試験(SNOT−22)スコア、嗅覚の喪失、鼻水、後部鼻漏およびNPIFからなる群から選択される1つまたはそれ以上の鼻茸に関連するパラメーターを改善するのに使用するためのものである;
抗体またはその抗原結合断片は、経口コルチコステロイド、全身性コルチコステロイドによる治療の必要性を減少させ、および/または鼻ポリープ手術の必要性を減少させるのに使用されるためのものである;
抗体またはその抗原結合断片は、AMに、PMに、またはAMとPMの両方に発生する、嗅覚の喪失、鼻水、後部鼻漏および鼻最大吸気流量のうちの1つまたはそれ以上を改善させるのに使用するためのものである;
抗体またはその抗原結合断片は、血清IgEレベル、血漿エオタキシン−3レベル、ならびに血清TARCレベルのうちの1つまたはそれ以上を減少させるのに使用するためのものである;および/または
抗体またはその抗原結合断片は、対象の鼻汁における総IgEレベル、エオタキシン−3レベルおよびECPレベルのうちの1つまたはそれ以上を減少させるのに使用するためのものである、
請求項5〜7のいずれか1項に記載の医薬組成物。 - それを必要とする対象の鼻ポリープを伴う慢性鼻副鼻腔炎(CRSwNP)の治療に使用するための、インターロイキン−4レセプター(IL−4R)に特異的に結合する抗体またはその抗原結合断片を含む医薬組成物であって、
抗体またはその抗原結合断片は、鼻ポリープスコア(NPS)が決定された対象への投与のためのものであり;
抗体またはその抗原結合断片は、ICSの1回またはそれ以上の維持用量を受けた対象への投与のためのものであり;
抗体またはその抗原結合断片は、300mgの用量で14日に1回(Q2W)投与されるものであり;
抗体またはその抗原結合断片は、配列番号6、7および8の軽鎖CDR配列と、配列番号3、4および5の重鎖CDR配列とを含み;ならびに
該ICSが、該抗体またはその抗原結合断片の投与期間中の投与のためのものである、前記医薬組成物。 - 対象は、投与前に各鼻腔に存在する2つまたはそれ以上の鼻ポリープを含む、合計少なくとも5つの鼻ポリープを有する;
対象は、両側性鼻ポリープを有する;
対象は、鼻ポリープを伴う難治性慢性鼻副鼻腔炎(CRS)を有する;
抗体またはその抗原結合断片は、鼻ポリープスコア(NPS)を、約10%〜約50%、約20%〜約40%、または約25%〜約30%減少させるのに使用するためのものである;
対象はさらに、アレルギー性鼻炎、喘息、アスピリン過敏症およびNSAID過敏症からなる群から選択される1つまたはそれ以上の状態をさらに有する;
対象は、鼻ポリープおよび慢性鼻副鼻腔炎の一方または両方のための手術を受けたことがある;
最初の機能的内視鏡下副鼻腔手術(FESS)が指示されるか、修正手術が指示されるか、または手術が禁忌となる;
抗体またはその抗原結合断片の投与は、皮下的に行われる;
抗体またはその抗原結合断片の投与は、注射器、場合により充填済みの注射器または自動注射器で行われる;および/または
ICSは、フランカルボン酸モメタゾンの鼻内噴霧(MFNS)であり、場合により、MFNSは、対象の各鼻孔に約100mgの用量での1日1回または2回投与のためのものである;
請求項9に記載の医薬組成物。 - 抗体またはその抗原結合断片は、配列番号1のアミノ酸配列を有するHCVRと配列番号2のアミノ酸配列を有するLCVRとを含む;
抗体またはその抗原結合断片は、配列番号9の重鎖配列と配列番号10の軽鎖配列とを含む;および/または
抗体は、デュピルマブである;
請求項9または10に記載の医薬組成物。 - 抗体またはその抗原結合断片は、さらに、鼻詰まり/閉塞(NC)の重症度、内視鏡鼻ポリープスコア(NPS)、コンピュータ断層撮影(CT)スキャン副鼻腔混濁、総症状スコア(TSS)、22項目副鼻腔評価試験(SNOT−22)スコア、嗅覚の喪失、鼻水、後部鼻漏およびNPIFからなる群から選択される1つまたはそれ以上の鼻茸に関連するパラメーターを改善するのに使用するためのものである;
抗体またはその抗原結合断片は、経口コルチコステロイド、全身性コルチコステロイドによる治療の必要性を減少させ、および/または鼻ポリープ手術の必要性を減少させるのに使用されるためのものである;
抗体またはその抗原結合断片は、AMに、PMに、またはAMとPMの両方に発生する、嗅覚の喪失、鼻水、後部鼻漏および鼻最大吸気流量のうちの1つまたはそれ以上を改善させるのに使用するためのものである;
抗体またはその抗原結合断片は、血清IgEレベル、血漿エオタキシン−3レベル、ならびに血清TARCレベルのうちの1つまたはそれ以上を減少させるのに使用するためのものである;および/または
抗体またはその抗原結合断片は、対象の鼻汁における総IgEレベル、エオタキシン−3レベルおよびECPレベルのうちの1つまたはそれ以上を減少させるのに使用するためのものである;
請求項9〜11のいずれか1項に記載の医薬組成物。 - それを必要とする対象の、鼻ポリープを伴う慢性鼻副鼻腔炎(CRSwNP)を治療するのに使用するための、および1つまたはそれ以上のさらなる鼻茸に関連するパラメーターを改善するのに使用するための、インターロイキン−4受容体(IL−4R)に特異的
に結合する抗体またはその抗原結合断片を含む医薬組成物であって;
抗体またはその抗原結合断片は、鼻ポリープスコア(NPS)が決定された対象への投与のためのものであり;
抗体またはその抗原結合断片は、1つまたはそれ以上のさらなる鼻茸に関連するパラメーターのレベルが決定された対象への投与のためのものであり;
抗体またはその抗原結合断片は、ICSの1回またはそれ以上の維持用量を受けた対象への投与のためのものであり;
抗体またはその抗原結合断片は、300mgの用量で14日に1回(Q2W)投与されるものであり;
抗体またはその抗原結合断片は、配列番号6、7および8の軽鎖CDR配列と、配列番号3、4および5の重鎖CDR配列とを含み;ならびに
ICSが、該抗体またはその抗原結合断片の投与期間中の投与のためのものであり、
場合により、
1つまたはそれ以上の鼻茸に関連するパラメーターは、嗅覚の喪失、鼻水、後部鼻漏およびNPIFからなる群から選択され、
対象は、鼻ポリープを伴う難治性慢性鼻副鼻腔炎(CRS)を有し、および/または
対象は、重症の両側性鼻ポリープを伴う慢性副鼻腔炎を有する;
前記医薬組成物。 - 対象は、両側性鼻ポリープを有する;
医薬組成物は、対象の鼻ポリープスコア(NPS)を約10%〜約50%、約20%〜約40%、または約25%〜約30%減少させるのに使用するためのものである;
対象は喘息を有し、場合により肺機能および喘息管理の一方または両方が改善される;
対象は喘息を有さない;
医薬組成物は、内視鏡検査評価項目、X線検査評価項目および臨床評価項目からなる群から選択される1つまたはそれ以上の鼻茸評価項目を改善するのに使用するためのものである;
抗体またはその抗原結合断片の投与は、皮下的に行われる;および/または
抗体またはその抗原結合断片の投与は、注射器、場合により充填済みの注射器または自動注射器で行われる、
請求項1に記載の医薬組成物。 - それを必要とする対象の鼻ポリープを伴う難治性慢性鼻副鼻腔炎(CRSwNP)の治療に使用するための、インターロイキン−4受容体(IL−4R)に特異的に結合する抗体またはその抗原結合断片を含む医薬組成物であって、
抗体またはその抗原結合断片は、配列番号6、7および8の軽鎖CDR配列と、配列番号3、4および5の重鎖CDR配列とを含み;
300mgの用量で14日に1回(Q2W)投与されるものである、
前記医薬組成物。
Applications Claiming Priority (11)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201462080092P | 2014-11-14 | 2014-11-14 | |
| US62/080,092 | 2014-11-14 | ||
| US201462083821P | 2014-11-24 | 2014-11-24 | |
| US62/083,821 | 2014-11-24 | ||
| US201562158832P | 2015-05-08 | 2015-05-08 | |
| US62/158,832 | 2015-05-08 | ||
| US201562199305P | 2015-07-31 | 2015-07-31 | |
| US62/199,305 | 2015-07-31 | ||
| EP15306632 | 2015-10-14 | ||
| EP15306632.9 | 2015-10-14 | ||
| PCT/US2015/060540 WO2016077675A1 (en) | 2014-11-14 | 2015-11-13 | Methods for treating chronic sinusitis with nasal polyps by administering an il-4r antagonist |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021001858A Division JP7216122B2 (ja) | 2014-11-14 | 2021-01-08 | Il-4rアンタゴニストの投与により鼻ポリープを伴う慢性副鼻腔炎を処置する方法 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2017535547A JP2017535547A (ja) | 2017-11-30 |
| JP2017535547A5 JP2017535547A5 (ja) | 2018-12-20 |
| JP6861630B2 true JP6861630B2 (ja) | 2021-04-21 |
Family
ID=54330704
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2017525897A Active JP6861630B2 (ja) | 2014-11-14 | 2015-11-13 | Il−4rアンタゴニストの投与により鼻ポリープを伴う慢性副鼻腔炎を処置する方法 |
| JP2023005585A Pending JP2023052458A (ja) | 2014-11-14 | 2023-01-18 | Il-4rアンタゴニストの投与により鼻ポリープを伴う慢性副鼻腔炎を処置する方法 |
| JP2025003986A Pending JP2025063155A (ja) | 2014-11-14 | 2025-01-10 | Il-4rアンタゴニストの投与により鼻ポリープを伴う慢性副鼻腔炎を処置する方法 |
Family Applications After (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2023005585A Pending JP2023052458A (ja) | 2014-11-14 | 2023-01-18 | Il-4rアンタゴニストの投与により鼻ポリープを伴う慢性副鼻腔炎を処置する方法 |
| JP2025003986A Pending JP2025063155A (ja) | 2014-11-14 | 2025-01-10 | Il-4rアンタゴニストの投与により鼻ポリープを伴う慢性副鼻腔炎を処置する方法 |
Country Status (11)
| Country | Link |
|---|---|
| US (3) | US10066017B2 (ja) |
| EP (1) | EP3218412A1 (ja) |
| JP (3) | JP6861630B2 (ja) |
| KR (2) | KR20230158131A (ja) |
| CN (1) | CN107206073A (ja) |
| AU (3) | AU2015346150B2 (ja) |
| CA (2) | CA3246946A1 (ja) |
| IL (4) | IL294554B2 (ja) |
| MX (2) | MX2017006286A (ja) |
| RU (1) | RU2734490C2 (ja) |
| WO (1) | WO2016077675A1 (ja) |
Families Citing this family (30)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7608693B2 (en) | 2006-10-02 | 2009-10-27 | Regeneron Pharmaceuticals, Inc. | High affinity human antibodies to human IL-4 receptor |
| WO2014031610A1 (en) | 2012-08-21 | 2014-02-27 | Sanofi | Methods for treating or preventing asthma by administering an il-4r antagonist |
| HRP20181227T1 (hr) | 2012-09-07 | 2018-10-05 | Regeneron Pharmaceuticals, Inc. | Metode za liječenje atopijskog dermatitisa primjenom antagonista il-4r |
| TWI755763B (zh) * | 2013-06-04 | 2022-02-21 | 美商再生元醫藥公司 | 藉由投與il-4r抑制劑以治療過敏及增強過敏原-特異之免疫療法的方法 |
| TWI634900B (zh) | 2013-07-11 | 2018-09-11 | 再生元醫藥公司 | 藉由投與il-4r抑制劑治療嗜酸性食道炎的方法 |
| IL315136A (en) | 2014-02-21 | 2024-10-01 | Sanofi Biotechnology | Methods for treating or preventing asthma by administering an il-4rantagonist |
| RU2704999C2 (ru) | 2014-02-28 | 2019-11-01 | Ридженерон Фармасьютикалз, Инк. | Способ лечения кожной инфекции путем введения антагониста il-4r |
| PT3613432T (pt) | 2014-05-07 | 2025-10-29 | Regeneron Pharma | Métodos para tratar a polipose nasal através da administração de um antagonista de il-4r |
| US10066017B2 (en) | 2014-11-14 | 2018-09-04 | Sanofi Biotechnology | Methods for treating chronic sinusitis with nasal polyps by administering an IL-4R antagonist |
| CN109789196B (zh) * | 2016-09-01 | 2024-03-19 | 瑞泽恩制药公司 | 用于通过施用il-4r拮抗剂来预防或治疗变态反应的方法 |
| MX2019012171A (es) * | 2017-04-13 | 2019-11-25 | Regeneron Pharma | Tratamiento e inhibicion de enfermedades pulmonares inflamatorias en pacientes que tienen alelos de riesgo en los genes que codifican la il33 e il1rl1. |
| WO2019018441A1 (en) * | 2017-07-17 | 2019-01-24 | Massachusetts Institute Of Technology | ATLAS OF HEAVY AND ILLUMINATED HEAVY BARRIER TISSUE CELLS |
| WO2019028367A1 (en) | 2017-08-04 | 2019-02-07 | Regeneron Pharmaceuticals, Inc. | METHODS OF TREATING ESOPHAGITIS WITH ACTIVE EOSINOPHILES |
| PT3515465T (pt) | 2017-08-18 | 2024-03-04 | Regeneron Pharma | Métodos para o tratamento de uma dermatite atópica grave mediante a administração de um inibidor de il-4r |
| PL3703818T3 (pl) * | 2017-10-30 | 2024-03-25 | Sanofi Biotechnology | Antagonista IL-4R do zastosowania w sposobie leczenia lub zapobiegania astmie |
| RU2667819C1 (ru) * | 2017-12-20 | 2018-09-24 | Владимир Викторович Сунцов | Способ аэрозольной терапии риносинуситов |
| US20210361693A1 (en) * | 2018-02-09 | 2021-11-25 | Empirico Inc. | Process to inhibit or eliminate eosinophilic diseases of the airway and related conditions |
| EP3793597A1 (en) | 2018-05-13 | 2021-03-24 | Regeneron Pharmaceuticals, Inc. | Methods for treating atopic dermatitis by administering an il-4r inhibitor |
| IL316308A (en) | 2018-07-10 | 2024-12-01 | Regeneron Pharma | Modifying binding molecules to minimize pre-existing interactions |
| CN111494625B (zh) | 2018-12-25 | 2022-06-21 | 江苏荃信生物医药股份有限公司 | 用于治疗il-4和/或il-13介导的信号转导相关的疾病的药物组合物 |
| US11116778B2 (en) | 2019-01-15 | 2021-09-14 | Empirico Inc. | Prodrugs of ALOX-15 inhibitors and methods of using the same |
| MA55372A (fr) | 2019-03-21 | 2022-01-26 | Regeneron Pharma | Combinaison d'inhibiteurs de la voie il-4/il-13 et d'ablation de plasmocytes pour traiter une allergie |
| JP7592064B2 (ja) | 2019-07-16 | 2024-11-29 | サノフィ・バイオテクノロジー | Il-4rアンタゴニストを投与することにより喘息を治療するまたは予防するための方法 |
| CN114173819A (zh) | 2019-08-05 | 2022-03-11 | 瑞泽恩制药公司 | 通过施用il-4r拮抗剂治疗过敏和增强过敏原特异性免疫疗法的方法 |
| AU2020326713A1 (en) | 2019-08-05 | 2022-02-17 | Regeneron Pharmaceuticals, Inc. | Methods for treating atopic dermatitis by administering an il-4r antagonist |
| EP4073810A1 (en) | 2019-12-09 | 2022-10-19 | Sanofi Biotechnology | Methods for treating digitally-identified il-4/il-13 related disorders |
| EP3992974A1 (en) * | 2020-11-02 | 2022-05-04 | Sanofi Biotechnology | Methods for treating digitally-identified il-4/il-13 related disorders |
| KR20240038841A (ko) * | 2022-09-16 | 2024-03-26 | 연세대학교 산학협력단 | 신규한 인간 인터류킨-4 수용체 결합 나노바디 및 이의 용도 |
| CN116819076A (zh) * | 2023-05-26 | 2023-09-29 | 首都医科大学附属北京同仁医院 | 一种预测或评估抗IL-4Rα单抗在治疗慢性鼻窦炎伴鼻息肉中疗效的生物标志物、应用和方法 |
| EP4623903A1 (en) | 2024-03-28 | 2025-10-01 | Fresenius Kabi Deutschland GmbH | Pharmaceutical composition comprising dupilumab |
Family Cites Families (82)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB8808015D0 (en) | 1988-04-06 | 1988-05-05 | Ritter M A | Chemical compounds |
| AU643427B2 (en) | 1988-10-31 | 1993-11-18 | Immunex Corporation | Interleukin-4 receptors |
| AU665763B2 (en) | 1991-05-03 | 1996-01-18 | Seragen, Inc. | Interleukin receptor targeted molecules for treatment of inflammatory arthritis |
| JP3315427B2 (ja) | 1992-03-05 | 2002-08-19 | 大日本除蟲菊株式会社 | 皮膚炎治療剤 |
| US5714146A (en) | 1992-08-26 | 1998-02-03 | Board Of Regents Of The University Of Washington | IL-4 bone therapy |
| EP0604693A1 (en) | 1992-12-29 | 1994-07-06 | Schering-Plough | Monoclonal antibodies against the human interleukin-4 receptor and hybridomas producing the same |
| RU2162711C2 (ru) | 1993-09-07 | 2001-02-10 | Смитклайн Бичам Корпорейшн | Рекомбинантные il4-антитела, используемые для лечения нарушений, связанных с действием il4 |
| US6664227B1 (en) * | 1996-03-01 | 2003-12-16 | Genetics Institute, Llc | Treatment of fibrosis by antagonism of IL-13 and IL-13 receptor chains |
| ES2259478T3 (es) | 1998-09-18 | 2006-10-01 | Dynavax Technologies Corporation | Metodos para tratar trastornos asociados con la ige y composiciones para este uso. |
| US6927044B2 (en) | 1998-09-25 | 2005-08-09 | Regeneron Pharmaceuticals, Inc. | IL-1 receptor based cytokine traps |
| DE16192152T1 (de) | 2000-05-26 | 2020-08-06 | Immunex Corporation | Verwendung von interleukin-4 rezeptor (il-4r) antikörpern und zusammensetzungen davon |
| US7879328B2 (en) | 2000-06-16 | 2011-02-01 | Human Genome Sciences, Inc. | Antibodies that immunospecifically bind to B lymphocyte stimulator |
| DE60130466T2 (de) | 2000-07-26 | 2008-06-12 | Hououdou Co. Ltd. | Antipruritische zusammensetzungen und die wundheilung fördernde zusammensetzungen |
| US6596541B2 (en) | 2000-10-31 | 2003-07-22 | Regeneron Pharmaceuticals, Inc. | Methods of modifying eukaryotic cells |
| EP1229034B1 (en) | 2001-01-31 | 2005-04-13 | Pfizer Products Inc. | Nicotinamide derivatives and their mimetics as inhibitors of PDE4 isozymes |
| US8178098B2 (en) | 2001-04-03 | 2012-05-15 | National Jewish Health | Method to inhibit airway hyperresponsiveness using aerosolized T cell receptor antibodies |
| US20030103938A1 (en) | 2001-05-09 | 2003-06-05 | Alk-Abello A/S | Pharmaceutical compositions for preventing or treating Th1 and Th2 cell related diseases by modulating the Th1/Th2 ratio |
| EP1390067A1 (en) | 2001-05-11 | 2004-02-25 | Novartis AG | Compositions for use in treating ige-associated disorders |
| CA2447795A1 (en) | 2001-05-23 | 2002-11-28 | Duotol Ab | Suppression of allergic reactions by transdermal administration of allergens in conjunction with or conjugated to toxin subunits or fragments thereof |
| DK1461300T3 (da) | 2001-11-30 | 2011-10-24 | Biogen Idec Inc | Antistoffer mod kemotaktiske monocytproteiner |
| CN1326879C (zh) | 2002-03-29 | 2007-07-18 | 先灵公司 | 人源抗白细胞介素5单克隆抗体及其制备方法和包含这些抗体的组合物 |
| MXPA05005528A (es) | 2002-11-26 | 2006-04-05 | Alk Abello As | Producto farmaceutico de alergeno. |
| ES2575547T3 (es) | 2003-02-01 | 2016-06-29 | Tanox, Inc. | Anticuerpos anti-IgE de humano de alta afinidad |
| US7923209B2 (en) | 2003-03-14 | 2011-04-12 | Anergis, S.A. | Allergen peptide fragments and use thereof |
| GEP20104991B (en) | 2003-11-07 | 2010-05-25 | Immunex Corp | Antibodies that bind interleukin-4 receptor |
| AU2004309373A1 (en) | 2003-12-22 | 2005-07-14 | Amgen Inc. | Methods for identifying functional antibodies |
| CA2554596A1 (en) | 2004-02-27 | 2005-09-15 | Regeneron Pharmaceuticals, Inc. | Il-4/il-13 specific polypetides and therapeutic uses thereof |
| US20090098142A1 (en) | 2004-06-09 | 2009-04-16 | Kasaian Marion T | Methods and compositions for treating and monitoring treatment of IL-13-associated disorders |
| TWI307630B (en) | 2004-07-01 | 2009-03-21 | Glaxo Group Ltd | Immunoglobulins |
| JP5234445B2 (ja) | 2004-10-05 | 2013-07-10 | 源一郎 杣 | 薬剤 |
| WO2006083390A2 (en) | 2004-12-07 | 2006-08-10 | Children's Hospital Medical Center | Eotaxin-3 in eosinophilic esophagitis |
| TW200902555A (en) | 2005-01-03 | 2009-01-16 | Hoffmann La Roche | Antibodies against IL-13 receptor alpha 1 and uses thereof |
| US8679545B2 (en) | 2005-11-12 | 2014-03-25 | The Regents Of The University Of California | Topical corticosteroids for the treatment of inflammatory diseases of the gastrointestinal tract |
| US8324192B2 (en) | 2005-11-12 | 2012-12-04 | The Regents Of The University Of California | Viscous budesonide for the treatment of inflammatory diseases of the gastrointestinal tract |
| JP2009523460A (ja) | 2006-01-24 | 2009-06-25 | ドマンティス リミテッド | Il−4および/またはil−13に結合するリガンド |
| RS52176B (sr) | 2006-06-02 | 2012-08-31 | Regeneron Pharmaceuticals Inc. | Antitela visokog afiniteta prema humanom il-6 receptoru |
| JP4221018B2 (ja) | 2006-08-31 | 2009-02-12 | トヨタ自動車株式会社 | 頭部保護エアバッグ装置 |
| WO2008054606A2 (en) | 2006-10-02 | 2008-05-08 | Regeneron Pharmaceuticals, Inc. | High affinity human antibodies to human il-4 receptor |
| US7608693B2 (en) | 2006-10-02 | 2009-10-27 | Regeneron Pharmaceuticals, Inc. | High affinity human antibodies to human IL-4 receptor |
| WO2008073627A2 (en) | 2006-11-03 | 2008-06-19 | Alba Therapeutics Corporation | Method of diagnosing and treating asthma |
| WO2008116165A2 (en) | 2007-03-21 | 2008-09-25 | Next Safety, Inc. | Methods and systems of delivering medication via inhalation |
| EP2022507A1 (en) | 2007-08-07 | 2009-02-11 | Universität Hamburg | Antibody compositions specific for lgE, lgG4 and lgA epitopes as tools for the design of hypoallergenic molecules for specific immunotherapy |
| US20090062168A1 (en) | 2007-08-27 | 2009-03-05 | Joseph Timar | Process for making a two-cycle gasoline engine lubricant |
| EP2050764A1 (en) | 2007-10-15 | 2009-04-22 | sanofi-aventis | Novel polyvalent bispecific antibody format and uses thereof |
| WO2009061819A1 (en) | 2007-11-05 | 2009-05-14 | The Regents Of The University Of Colorado | Minimally-invasive measurement of esophageal inflammation |
| RU2490278C2 (ru) * | 2007-12-21 | 2013-08-20 | Медиммун Лимитед | ЭЛЕМЕНТ, СВЯЗЫВАЮЩИЙСЯ С α-РЕЦЕПТОРОМ ИНТЕРЛЕЙКИНА-4 (IL-4Rα)-173 |
| US8092804B2 (en) | 2007-12-21 | 2012-01-10 | Medimmune Limited | Binding members for interleukin-4 receptor alpha (IL-4Rα)-173 |
| DE202008006598U1 (de) | 2008-04-11 | 2008-10-02 | Alk-Abelló A/S | Allergie-Impfstoff-Formulierung zur mucosalen Verabreichung |
| US20090264392A1 (en) | 2008-04-21 | 2009-10-22 | Meritage Pharma, Inc. | Treating eosinophilic esophagitis |
| EP2376656A4 (en) | 2008-12-01 | 2012-05-16 | Cincinnati Children S Hospital Medical Ct | METHOD AND DETERMINATION OF THE EFFECTIVENESS OF A GLUCOCORTICOID TREATMENT OF EOSINOPHILIAN ESOPHAGITIS |
| EP2414520A2 (en) * | 2009-03-31 | 2012-02-08 | Altair Therapeutics, Inc. | Methods of modulating an immune response to a viral infection |
| US8497528B2 (en) | 2010-05-06 | 2013-07-30 | Taiwan Semiconductor Manufacturing Company, Ltd. | Method for fabricating a strained structure |
| RU2403071C1 (ru) * | 2009-09-03 | 2010-11-10 | Логина Наталия Алексеевна | Способ лечения хронических рецидивирующих воспалительных заболеваний слизистой носа и околоносовых пазух методом эндоназальной аутолимфоцитотерапии |
| AU2010291171B2 (en) | 2009-09-07 | 2015-10-29 | Dbv Technologies | Method of treating eosinophilic esophagitis |
| US8993347B2 (en) | 2009-12-17 | 2015-03-31 | Cornell University | Methods for detecting antibodies in mucosal samples and device for sampling mucosal material |
| US20120240930A1 (en) | 2010-03-16 | 2012-09-27 | Dan Allan Robert Kristensson | Treatment of Asthma, Allergic Rhinitis and Improvement of Quality of Sleep by Temperature Controlled Laminar Airflow Treatment |
| WO2011163614A2 (en) | 2010-06-24 | 2011-12-29 | Meritage Pharma, Inc. | Methods of treatment for esophageal inflammation |
| UA111731C2 (uk) | 2010-10-06 | 2016-06-10 | Рідженерон Фармасьютікалз, Інк. | Стабілізована композиція, яка містить антитіло до рецептора інтерлейкіну-4 (іl-4r), варіанти |
| PL2624865T3 (pl) | 2010-10-06 | 2018-11-30 | Regeneron Pharmaceuticals, Inc. | Stabilizowane preparaty zawierające przeciwciała przeciwko receptorowi interleukiny-4 (IL-4R) |
| CA2824043A1 (en) | 2011-01-06 | 2012-07-12 | Marc E. Rothenberg | Esophageal cytokine expression profiles in eosinophilic esophagitis |
| US20130052190A1 (en) | 2011-02-22 | 2013-02-28 | Oxagen Limited | CRTH2 Antagonists for Treatment of Eosinophilic Diseases and Conditions |
| AU2012272858B2 (en) | 2011-06-21 | 2017-03-09 | Children's Hospital Medical Center | Diagnostic methods for eosinophilic esophagitis |
| CN103974706A (zh) | 2011-10-06 | 2014-08-06 | N·V·努特里奇亚 | 嗜酸细胞性食管炎的治疗 |
| KR20140097217A (ko) | 2011-11-01 | 2014-08-06 | 메디뮨 엘엘씨 | 급성 천식 악화의 빈도 및 중증도를 감소시키는 방법 |
| SG11201402796SA (en) | 2011-12-16 | 2014-06-27 | Atopix Therapeutics Ltd | Combination of crth2 antagonist and a proton pump inhibitor for the treatment of eosinophilic esophagitis |
| WO2013155010A1 (en) | 2012-04-09 | 2013-10-17 | Children's Hospital Medical Center | Non-invasive biomarkers for eosinophilic esophagitis |
| EP2677838B1 (en) | 2012-06-18 | 2017-12-06 | Whirlpool Corporation | Microwave heating apparatus |
| WO2014031610A1 (en) | 2012-08-21 | 2014-02-27 | Sanofi | Methods for treating or preventing asthma by administering an il-4r antagonist |
| HRP20181227T1 (hr) * | 2012-09-07 | 2018-10-05 | Regeneron Pharmaceuticals, Inc. | Metode za liječenje atopijskog dermatitisa primjenom antagonista il-4r |
| WO2014059178A1 (en) | 2012-10-10 | 2014-04-17 | Rhode Island Hospital | Differential expression of novel protein markers for the diagnosis and treatment of eosinophilic esophagitis |
| TWI755763B (zh) | 2013-06-04 | 2022-02-21 | 美商再生元醫藥公司 | 藉由投與il-4r抑制劑以治療過敏及增強過敏原-特異之免疫療法的方法 |
| TWI634900B (zh) | 2013-07-11 | 2018-09-11 | 再生元醫藥公司 | 藉由投與il-4r抑制劑治療嗜酸性食道炎的方法 |
| IL315136A (en) | 2014-02-21 | 2024-10-01 | Sanofi Biotechnology | Methods for treating or preventing asthma by administering an il-4rantagonist |
| RU2704999C2 (ru) | 2014-02-28 | 2019-11-01 | Ридженерон Фармасьютикалз, Инк. | Способ лечения кожной инфекции путем введения антагониста il-4r |
| PT3613432T (pt) | 2014-05-07 | 2025-10-29 | Regeneron Pharma | Métodos para tratar a polipose nasal através da administração de um antagonista de il-4r |
| IL285483B (en) * | 2014-11-14 | 2022-08-01 | Regeneron Pharma | Methods for the treatment of chronic sinusitis with nasal polyps by adding an il-4r antagonist |
| US10066017B2 (en) | 2014-11-14 | 2018-09-04 | Sanofi Biotechnology | Methods for treating chronic sinusitis with nasal polyps by administering an IL-4R antagonist |
| MA44238B1 (fr) | 2016-02-19 | 2024-07-31 | Regeneron Pharmaceuticals, Inc. | Procédés d'augmentation de l'efficacité d'un vaccin par administration d'un antagoniste d'il-4r |
| CN109789196B (zh) | 2016-09-01 | 2024-03-19 | 瑞泽恩制药公司 | 用于通过施用il-4r拮抗剂来预防或治疗变态反应的方法 |
| WO2019028367A1 (en) | 2017-08-04 | 2019-02-07 | Regeneron Pharmaceuticals, Inc. | METHODS OF TREATING ESOPHAGITIS WITH ACTIVE EOSINOPHILES |
| PT3515465T (pt) | 2017-08-18 | 2024-03-04 | Regeneron Pharma | Métodos para o tratamento de uma dermatite atópica grave mediante a administração de um inibidor de il-4r |
| PL3703818T3 (pl) | 2017-10-30 | 2024-03-25 | Sanofi Biotechnology | Antagonista IL-4R do zastosowania w sposobie leczenia lub zapobiegania astmie |
-
2015
- 2015-11-13 US US14/940,431 patent/US10066017B2/en active Active
- 2015-11-13 KR KR1020237038116A patent/KR20230158131A/ko not_active Ceased
- 2015-11-13 AU AU2015346150A patent/AU2015346150B2/en active Active
- 2015-11-13 CN CN201580073344.8A patent/CN107206073A/zh active Pending
- 2015-11-13 KR KR1020177015962A patent/KR20170081262A/ko not_active Ceased
- 2015-11-13 CA CA3246946A patent/CA3246946A1/en active Pending
- 2015-11-13 EP EP15804646.6A patent/EP3218412A1/en active Pending
- 2015-11-13 CA CA2967602A patent/CA2967602C/en active Active
- 2015-11-13 WO PCT/US2015/060540 patent/WO2016077675A1/en not_active Ceased
- 2015-11-13 IL IL294554A patent/IL294554B2/en unknown
- 2015-11-13 JP JP2017525897A patent/JP6861630B2/ja active Active
- 2015-11-13 RU RU2017120437A patent/RU2734490C2/ru active
- 2015-11-13 MX MX2017006286A patent/MX2017006286A/es unknown
-
2017
- 2017-05-11 IL IL252228A patent/IL252228B/en active IP Right Grant
- 2017-05-12 MX MX2023000079A patent/MX2023000079A/es unknown
-
2018
- 2018-07-18 US US16/038,925 patent/US11214621B2/en active Active
-
2021
- 2021-11-15 AU AU2021269269A patent/AU2021269269A1/en not_active Abandoned
- 2021-11-23 US US17/534,106 patent/US20220204631A1/en active Pending
-
2023
- 2023-01-18 JP JP2023005585A patent/JP2023052458A/ja active Pending
- 2023-05-31 IL IL303337A patent/IL303337B2/en unknown
-
2025
- 2025-01-10 JP JP2025003986A patent/JP2025063155A/ja active Pending
- 2025-02-14 AU AU2025201031A patent/AU2025201031A1/en active Pending
- 2025-09-15 IL IL323384A patent/IL323384A/en unknown
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6861630B2 (ja) | Il−4rアンタゴニストの投与により鼻ポリープを伴う慢性副鼻腔炎を処置する方法 | |
| AU2022201336B2 (en) | Methods for treating nasal polyposis by administering an IL-4R antagonist | |
| JP6898421B2 (ja) | Il−4rアンタゴニストの投与により鼻茸を処置する方法 | |
| JP7216122B2 (ja) | Il-4rアンタゴニストの投与により鼻ポリープを伴う慢性副鼻腔炎を処置する方法 | |
| HK40023224A (en) | Methods for treating nasal polyposis by administering an il-4r antagonist | |
| HK1222567B (en) | Methods for treating nasal polyposis by administering an il-4r antagonist |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20181112 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20181112 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20191015 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20200115 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200316 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20200421 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20200908 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210108 |
|
| C60 | Trial request (containing other claim documents, opposition documents) |
Free format text: JAPANESE INTERMEDIATE CODE: C60 Effective date: 20210108 |
|
| C11 | Written invitation by the commissioner to file amendments |
Free format text: JAPANESE INTERMEDIATE CODE: C11 Effective date: 20210119 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20210201 |
|
| C21 | Notice of transfer of a case for reconsideration by examiners before appeal proceedings |
Free format text: JAPANESE INTERMEDIATE CODE: C21 Effective date: 20210202 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20210309 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20210330 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6861630 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |