JP6783797B2 - 抗がん融合ポリペプチド - Google Patents
抗がん融合ポリペプチド Download PDFInfo
- Publication number
- JP6783797B2 JP6783797B2 JP2017557310A JP2017557310A JP6783797B2 JP 6783797 B2 JP6783797 B2 JP 6783797B2 JP 2017557310 A JP2017557310 A JP 2017557310A JP 2017557310 A JP2017557310 A JP 2017557310A JP 6783797 B2 JP6783797 B2 JP 6783797B2
- Authority
- JP
- Japan
- Prior art keywords
- ser
- lys
- arg
- asp
- leu
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 108090000765 processed proteins & peptides Proteins 0.000 title claims description 386
- 102000004196 processed proteins & peptides Human genes 0.000 title claims description 373
- 229920001184 polypeptide Polymers 0.000 title claims description 370
- 230000004927 fusion Effects 0.000 title claims description 299
- 230000001093 anti-cancer Effects 0.000 title 1
- 101000851370 Homo sapiens Tumor necrosis factor receptor superfamily member 9 Proteins 0.000 claims description 203
- 102100036856 Tumor necrosis factor receptor superfamily member 9 Human genes 0.000 claims description 196
- 101001012157 Homo sapiens Receptor tyrosine-protein kinase erbB-2 Proteins 0.000 claims description 171
- 102100030086 Receptor tyrosine-protein kinase erbB-2 Human genes 0.000 claims description 167
- 102000019298 Lipocalin Human genes 0.000 claims description 118
- 108050006654 Lipocalin Proteins 0.000 claims description 118
- 125000003275 alpha amino acid group Chemical group 0.000 claims description 93
- 230000027455 binding Effects 0.000 claims description 88
- 206010028980 Neoplasm Diseases 0.000 claims description 81
- 210000001744 T-lymphocyte Anatomy 0.000 claims description 79
- 210000004881 tumor cell Anatomy 0.000 claims description 53
- 108010002350 Interleukin-2 Proteins 0.000 claims description 44
- 108060003951 Immunoglobulin Proteins 0.000 claims description 43
- 102000018358 immunoglobulin Human genes 0.000 claims description 43
- 150000007523 nucleic acids Chemical class 0.000 claims description 39
- 125000000539 amino acid group Chemical group 0.000 claims description 37
- 102000039446 nucleic acids Human genes 0.000 claims description 36
- 108020004707 nucleic acids Proteins 0.000 claims description 36
- 239000000203 mixture Substances 0.000 claims description 29
- 101000946124 Homo sapiens Lipocalin-1 Proteins 0.000 claims description 26
- 230000004913 activation Effects 0.000 claims description 24
- 230000035772 mutation Effects 0.000 claims description 22
- 210000004899 c-terminal region Anatomy 0.000 claims description 21
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 claims description 18
- 239000002773 nucleotide Substances 0.000 claims description 16
- 125000003729 nucleotide group Chemical group 0.000 claims description 16
- 239000012634 fragment Substances 0.000 claims description 14
- 102100037850 Interferon gamma Human genes 0.000 claims description 13
- 108010074328 Interferon-gamma Proteins 0.000 claims description 13
- 229960000575 trastuzumab Drugs 0.000 claims description 13
- 230000001939 inductive effect Effects 0.000 claims description 12
- 101001023833 Homo sapiens Neutrophil gelatinase-associated lipocalin Proteins 0.000 claims description 11
- 102000047202 human LCN2 Human genes 0.000 claims description 11
- 210000000822 natural killer cell Anatomy 0.000 claims description 11
- 230000005867 T cell response Effects 0.000 claims description 10
- 239000000427 antigen Substances 0.000 claims description 10
- 108091007433 antigens Proteins 0.000 claims description 10
- 102000036639 antigens Human genes 0.000 claims description 10
- 201000011510 cancer Diseases 0.000 claims description 9
- 230000035755 proliferation Effects 0.000 claims description 9
- 230000007783 downstream signaling Effects 0.000 claims description 8
- 238000004519 manufacturing process Methods 0.000 claims description 7
- 230000006052 T cell proliferation Effects 0.000 claims description 6
- 229960002087 pertuzumab Drugs 0.000 claims description 5
- 101150029707 ERBB2 gene Proteins 0.000 claims description 3
- 230000036755 cellular response Effects 0.000 claims description 2
- 230000002265 prevention Effects 0.000 claims description 2
- 238000011084 recovery Methods 0.000 claims 1
- 238000002560 therapeutic procedure Methods 0.000 claims 1
- 210000004027 cell Anatomy 0.000 description 139
- 241000282414 Homo sapiens Species 0.000 description 71
- 235000001014 amino acid Nutrition 0.000 description 62
- 241000699670 Mus sp. Species 0.000 description 54
- 238000000034 method Methods 0.000 description 49
- 210000003819 peripheral blood mononuclear cell Anatomy 0.000 description 49
- 229940024606 amino acid Drugs 0.000 description 47
- 238000002474 experimental method Methods 0.000 description 47
- 150000001413 amino acids Chemical class 0.000 description 45
- 102000000588 Interleukin-2 Human genes 0.000 description 43
- 238000006467 substitution reaction Methods 0.000 description 41
- 108090000623 proteins and genes Proteins 0.000 description 40
- 238000011282 treatment Methods 0.000 description 40
- 102000004169 proteins and genes Human genes 0.000 description 36
- 108010057281 Lipocalin 1 Proteins 0.000 description 35
- 230000000694 effects Effects 0.000 description 34
- 235000018102 proteins Nutrition 0.000 description 34
- 102100034724 Lipocalin-1 Human genes 0.000 description 29
- 238000003556 assay Methods 0.000 description 29
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 28
- 239000002953 phosphate buffered saline Substances 0.000 description 28
- 238000012360 testing method Methods 0.000 description 28
- 102100037422 Receptor-type tyrosine-protein phosphatase C Human genes 0.000 description 27
- 101000738771 Homo sapiens Receptor-type tyrosine-protein phosphatase C Proteins 0.000 description 25
- 230000006044 T cell activation Effects 0.000 description 24
- 230000008685 targeting Effects 0.000 description 23
- 230000004614 tumor growth Effects 0.000 description 23
- 102100034922 T-cell surface glycoprotein CD8 alpha chain Human genes 0.000 description 21
- 230000014509 gene expression Effects 0.000 description 21
- 210000004698 lymphocyte Anatomy 0.000 description 18
- 230000004044 response Effects 0.000 description 18
- 239000006228 supernatant Substances 0.000 description 17
- 239000000872 buffer Substances 0.000 description 16
- 239000003446 ligand Substances 0.000 description 16
- 238000004458 analytical method Methods 0.000 description 15
- 230000001419 dependent effect Effects 0.000 description 15
- 230000001965 increasing effect Effects 0.000 description 15
- 239000013642 negative control Substances 0.000 description 15
- 239000000523 sample Substances 0.000 description 14
- 239000000126 substance Substances 0.000 description 14
- 102000017420 CD3 protein, epsilon/gamma/delta subunit Human genes 0.000 description 13
- 238000002965 ELISA Methods 0.000 description 13
- 238000012286 ELISA Assay Methods 0.000 description 13
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 12
- 238000012217 deletion Methods 0.000 description 12
- 230000037430 deletion Effects 0.000 description 12
- 238000001542 size-exclusion chromatography Methods 0.000 description 12
- 108020004414 DNA Proteins 0.000 description 11
- 108010073807 IgG Receptors Proteins 0.000 description 11
- 102000009490 IgG Receptors Human genes 0.000 description 11
- 241000699666 Mus <mouse, genus> Species 0.000 description 11
- 230000015572 biosynthetic process Effects 0.000 description 11
- 230000034994 death Effects 0.000 description 11
- 231100000517 death Toxicity 0.000 description 11
- 239000001963 growth medium Substances 0.000 description 11
- 230000036470 plasma concentration Effects 0.000 description 11
- 238000005406 washing Methods 0.000 description 11
- 102000002627 4-1BB Ligand Human genes 0.000 description 10
- 108010082808 4-1BB Ligand Proteins 0.000 description 10
- 241001465754 Metazoa Species 0.000 description 10
- 238000005516 engineering process Methods 0.000 description 10
- 238000000338 in vitro Methods 0.000 description 10
- 238000001727 in vivo Methods 0.000 description 10
- 238000011534 incubation Methods 0.000 description 10
- 238000004020 luminiscence type Methods 0.000 description 10
- 230000004048 modification Effects 0.000 description 10
- 238000012986 modification Methods 0.000 description 10
- 238000002703 mutagenesis Methods 0.000 description 10
- 231100000350 mutagenesis Toxicity 0.000 description 10
- 230000037361 pathway Effects 0.000 description 10
- 238000011002 quantification Methods 0.000 description 10
- 238000002198 surface plasmon resonance spectroscopy Methods 0.000 description 10
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 9
- 102100026122 High affinity immunoglobulin gamma Fc receptor I Human genes 0.000 description 9
- 101000913074 Homo sapiens High affinity immunoglobulin gamma Fc receptor I Proteins 0.000 description 9
- 101000917858 Homo sapiens Low affinity immunoglobulin gamma Fc region receptor III-A Proteins 0.000 description 9
- 102100029193 Low affinity immunoglobulin gamma Fc region receptor III-A Human genes 0.000 description 9
- 238000007792 addition Methods 0.000 description 9
- 239000012298 atmosphere Substances 0.000 description 9
- 125000000151 cysteine group Chemical group N[C@@H](CS)C(=O)* 0.000 description 9
- 239000003814 drug Substances 0.000 description 9
- 239000012636 effector Substances 0.000 description 9
- 210000003171 tumor-infiltrating lymphocyte Anatomy 0.000 description 9
- YBJHBAHKTGYVGT-ZKWXMUAHSA-N (+)-Biotin Chemical compound N1C(=O)N[C@@H]2[C@H](CCCCC(=O)O)SC[C@@H]21 YBJHBAHKTGYVGT-ZKWXMUAHSA-N 0.000 description 8
- BKAYIFDRRZZKNF-VIFPVBQESA-N N-acetylcarnosine Chemical compound CC(=O)NCCC(=O)N[C@H](C(O)=O)CC1=CN=CN1 BKAYIFDRRZZKNF-VIFPVBQESA-N 0.000 description 8
- 238000001514 detection method Methods 0.000 description 8
- 230000006870 function Effects 0.000 description 8
- 238000011577 humanized mouse model Methods 0.000 description 8
- 230000005764 inhibitory process Effects 0.000 description 8
- 238000003780 insertion Methods 0.000 description 8
- 230000037431 insertion Effects 0.000 description 8
- 238000003118 sandwich ELISA Methods 0.000 description 8
- 239000013598 vector Substances 0.000 description 8
- 241000282567 Macaca fascicularis Species 0.000 description 7
- 229940079593 drug Drugs 0.000 description 7
- 102000050327 human TNFRSF9 Human genes 0.000 description 7
- 230000002055 immunohistochemical effect Effects 0.000 description 7
- 230000006698 induction Effects 0.000 description 7
- 108010045069 keyhole-limpet hemocyanin Proteins 0.000 description 7
- 239000000463 material Substances 0.000 description 7
- 239000013641 positive control Substances 0.000 description 7
- 101001002657 Homo sapiens Interleukin-2 Proteins 0.000 description 6
- 102000003752 Lipocalin 1 Human genes 0.000 description 6
- 230000009471 action Effects 0.000 description 6
- CKLJMWTZIZZHCS-REOHCLBHSA-N aspartic acid group Chemical group N[C@@H](CC(=O)O)C(=O)O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 6
- 239000005018 casein Substances 0.000 description 6
- BECPQYXYKAMYBN-UHFFFAOYSA-N casein, tech. Chemical compound NCCCCC(C(O)=O)N=C(O)C(CC(O)=O)N=C(O)C(CCC(O)=N)N=C(O)C(CC(C)C)N=C(O)C(CCC(O)=O)N=C(O)C(CC(O)=O)N=C(O)C(CCC(O)=O)N=C(O)C(C(C)O)N=C(O)C(CCC(O)=N)N=C(O)C(CCC(O)=N)N=C(O)C(CCC(O)=N)N=C(O)C(CCC(O)=O)N=C(O)C(CCC(O)=O)N=C(O)C(COP(O)(O)=O)N=C(O)C(CCC(O)=N)N=C(O)C(N)CC1=CC=CC=C1 BECPQYXYKAMYBN-UHFFFAOYSA-N 0.000 description 6
- 235000021240 caseins Nutrition 0.000 description 6
- 239000003795 chemical substances by application Substances 0.000 description 6
- 210000003162 effector t lymphocyte Anatomy 0.000 description 6
- 229940072221 immunoglobulins Drugs 0.000 description 6
- 239000007788 liquid Substances 0.000 description 6
- 238000005259 measurement Methods 0.000 description 6
- 239000002609 medium Substances 0.000 description 6
- 229910052757 nitrogen Inorganic materials 0.000 description 6
- 239000004033 plastic Substances 0.000 description 6
- 230000002829 reductive effect Effects 0.000 description 6
- 210000002966 serum Anatomy 0.000 description 6
- 210000001519 tissue Anatomy 0.000 description 6
- WOVKYSAHUYNSMH-RRKCRQDMSA-N 5-bromodeoxyuridine Chemical compound C1[C@H](O)[C@@H](CO)O[C@H]1N1C(=O)NC(=O)C(Br)=C1 WOVKYSAHUYNSMH-RRKCRQDMSA-N 0.000 description 5
- 102000014914 Carrier Proteins Human genes 0.000 description 5
- 102000004127 Cytokines Human genes 0.000 description 5
- 108090000695 Cytokines Proteins 0.000 description 5
- 241000124008 Mammalia Species 0.000 description 5
- 108091028043 Nucleic acid sequence Proteins 0.000 description 5
- 229920001213 Polysorbate 20 Polymers 0.000 description 5
- 230000006399 behavior Effects 0.000 description 5
- 230000008901 benefit Effects 0.000 description 5
- 108091008324 binding proteins Proteins 0.000 description 5
- 210000004369 blood Anatomy 0.000 description 5
- 239000008280 blood Substances 0.000 description 5
- 210000002889 endothelial cell Anatomy 0.000 description 5
- 108020001507 fusion proteins Proteins 0.000 description 5
- 102000037865 fusion proteins Human genes 0.000 description 5
- 230000012010 growth Effects 0.000 description 5
- 239000007924 injection Substances 0.000 description 5
- 238000002347 injection Methods 0.000 description 5
- 239000003287 lymphocyte surface marker Substances 0.000 description 5
- 210000005259 peripheral blood Anatomy 0.000 description 5
- 239000011886 peripheral blood Substances 0.000 description 5
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 5
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 5
- 230000011664 signaling Effects 0.000 description 5
- 239000000243 solution Substances 0.000 description 5
- 241000894007 species Species 0.000 description 5
- 238000010186 staining Methods 0.000 description 5
- 238000013519 translation Methods 0.000 description 5
- MTCFGRXMJLQNBG-REOHCLBHSA-N (2S)-2-Amino-3-hydroxypropansäure Chemical compound OC[C@H](N)C(O)=O MTCFGRXMJLQNBG-REOHCLBHSA-N 0.000 description 4
- LMDZBCPBFSXMTL-UHFFFAOYSA-N 1-ethyl-3-(3-dimethylaminopropyl)carbodiimide Chemical compound CCN=C=NCCCN(C)C LMDZBCPBFSXMTL-UHFFFAOYSA-N 0.000 description 4
- HSTOKWSFWGCZMH-UHFFFAOYSA-N 3,3'-diaminobenzidine Chemical compound C1=C(N)C(N)=CC=C1C1=CC=C(N)C(N)=C1 HSTOKWSFWGCZMH-UHFFFAOYSA-N 0.000 description 4
- 108010088751 Albumins Proteins 0.000 description 4
- 102000009027 Albumins Human genes 0.000 description 4
- 241000894006 Bacteria Species 0.000 description 4
- 108020004705 Codon Proteins 0.000 description 4
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 4
- 241000588724 Escherichia coli Species 0.000 description 4
- 102000009109 Fc receptors Human genes 0.000 description 4
- 108010087819 Fc receptors Proteins 0.000 description 4
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 4
- NWIBSHFKIJFRCO-WUDYKRTCSA-N Mytomycin Chemical compound C1N2C(C(C(C)=C(N)C3=O)=O)=C3[C@@H](COC(N)=O)[C@@]2(OC)[C@@H]2[C@H]1N2 NWIBSHFKIJFRCO-WUDYKRTCSA-N 0.000 description 4
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 4
- 108010090804 Streptavidin Proteins 0.000 description 4
- 108091008874 T cell receptors Proteins 0.000 description 4
- 230000003213 activating effect Effects 0.000 description 4
- 235000003704 aspartic acid Nutrition 0.000 description 4
- 230000001580 bacterial effect Effects 0.000 description 4
- OQFSQFPPLPISGP-UHFFFAOYSA-N beta-carboxyaspartic acid Natural products OC(=O)C(N)C(C(O)=O)C(O)=O OQFSQFPPLPISGP-UHFFFAOYSA-N 0.000 description 4
- 229960002685 biotin Drugs 0.000 description 4
- 235000020958 biotin Nutrition 0.000 description 4
- 239000011616 biotin Substances 0.000 description 4
- 230000000903 blocking effect Effects 0.000 description 4
- 239000006285 cell suspension Substances 0.000 description 4
- 238000010367 cloning Methods 0.000 description 4
- 238000011161 development Methods 0.000 description 4
- 230000018109 developmental process Effects 0.000 description 4
- 201000010099 disease Diseases 0.000 description 4
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 4
- 238000010494 dissociation reaction Methods 0.000 description 4
- 230000005593 dissociations Effects 0.000 description 4
- 239000007789 gas Substances 0.000 description 4
- 102000051957 human ERBB2 Human genes 0.000 description 4
- 230000005847 immunogenicity Effects 0.000 description 4
- 230000001976 improved effect Effects 0.000 description 4
- 230000002401 inhibitory effect Effects 0.000 description 4
- 239000000047 product Substances 0.000 description 4
- 238000000746 purification Methods 0.000 description 4
- 230000008929 regeneration Effects 0.000 description 4
- 238000011069 regeneration method Methods 0.000 description 4
- 230000001105 regulatory effect Effects 0.000 description 4
- 125000003607 serino group Chemical group [H]N([H])[C@]([H])(C(=O)[*])C(O[H])([H])[H] 0.000 description 4
- 230000000638 stimulation Effects 0.000 description 4
- 238000003786 synthesis reaction Methods 0.000 description 4
- 238000013518 transcription Methods 0.000 description 4
- 230000035897 transcription Effects 0.000 description 4
- 210000003462 vein Anatomy 0.000 description 4
- 230000003442 weekly effect Effects 0.000 description 4
- 206010006187 Breast cancer Diseases 0.000 description 3
- 208000026310 Breast neoplasm Diseases 0.000 description 3
- 241000283707 Capra Species 0.000 description 3
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 description 3
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 3
- 241000282412 Homo Species 0.000 description 3
- -1 Jun Proteins 0.000 description 3
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 3
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 3
- ROHFNLRQFUQHCH-YFKPBYRVSA-N L-leucine Chemical compound CC(C)C[C@H](N)C(O)=O ROHFNLRQFUQHCH-YFKPBYRVSA-N 0.000 description 3
- COLNVLDHVKWLRT-QMMMGPOBSA-N L-phenylalanine Chemical compound OC(=O)[C@@H](N)CC1=CC=CC=C1 COLNVLDHVKWLRT-QMMMGPOBSA-N 0.000 description 3
- AYFVYJQAPQTCCC-GBXIJSLDSA-N L-threonine Chemical compound C[C@@H](O)[C@H](N)C(O)=O AYFVYJQAPQTCCC-GBXIJSLDSA-N 0.000 description 3
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 description 3
- 239000012980 RPMI-1640 medium Substances 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 102000016266 T-Cell Antigen Receptors Human genes 0.000 description 3
- 108010076089 accutase Proteins 0.000 description 3
- 230000000259 anti-tumor effect Effects 0.000 description 3
- 238000004113 cell culture Methods 0.000 description 3
- 230000004663 cell proliferation Effects 0.000 description 3
- 239000003153 chemical reaction reagent Substances 0.000 description 3
- 230000002860 competitive effect Effects 0.000 description 3
- 230000009918 complex formation Effects 0.000 description 3
- 150000001875 compounds Chemical class 0.000 description 3
- 239000012228 culture supernatant Substances 0.000 description 3
- 235000018417 cysteine Nutrition 0.000 description 3
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Natural products SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 description 3
- 230000007423 decrease Effects 0.000 description 3
- 239000003085 diluting agent Substances 0.000 description 3
- 230000008030 elimination Effects 0.000 description 3
- 238000003379 elimination reaction Methods 0.000 description 3
- 210000003527 eukaryotic cell Anatomy 0.000 description 3
- 238000001943 fluorescence-activated cell sorting Methods 0.000 description 3
- 238000010353 genetic engineering Methods 0.000 description 3
- 235000013922 glutamic acid Nutrition 0.000 description 3
- 239000004220 glutamic acid Substances 0.000 description 3
- 230000013595 glycosylation Effects 0.000 description 3
- 238000006206 glycosylation reaction Methods 0.000 description 3
- 229940022353 herceptin Drugs 0.000 description 3
- 210000000987 immune system Anatomy 0.000 description 3
- 230000008595 infiltration Effects 0.000 description 3
- 238000001764 infiltration Methods 0.000 description 3
- 230000000977 initiatory effect Effects 0.000 description 3
- 230000003993 interaction Effects 0.000 description 3
- 239000003550 marker Substances 0.000 description 3
- 230000001404 mediated effect Effects 0.000 description 3
- 238000010172 mouse model Methods 0.000 description 3
- 230000001590 oxidative effect Effects 0.000 description 3
- 239000012146 running buffer Substances 0.000 description 3
- 230000009870 specific binding Effects 0.000 description 3
- 238000010561 standard procedure Methods 0.000 description 3
- 229960005322 streptomycin Drugs 0.000 description 3
- 239000000758 substrate Substances 0.000 description 3
- 230000001225 therapeutic effect Effects 0.000 description 3
- 238000004448 titration Methods 0.000 description 3
- 238000002054 transplantation Methods 0.000 description 3
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 2
- HZAXFHJVJLSVMW-UHFFFAOYSA-N 2-Aminoethan-1-ol Chemical compound NCCO HZAXFHJVJLSVMW-UHFFFAOYSA-N 0.000 description 2
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 2
- CDEURGJCGCHYFH-DJLDLDEBSA-N 5-ethynyl-2'-deoxyuridine Chemical compound C1[C@H](O)[C@@H](CO)O[C@H]1N1C(=O)NC(=O)C(C#C)=C1 CDEURGJCGCHYFH-DJLDLDEBSA-N 0.000 description 2
- 239000004475 Arginine Substances 0.000 description 2
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 2
- 102000053602 DNA Human genes 0.000 description 2
- YCAGGFXSFQFVQL-UHFFFAOYSA-N Endothion Chemical compound COC1=COC(CSP(=O)(OC)OC)=CC1=O YCAGGFXSFQFVQL-UHFFFAOYSA-N 0.000 description 2
- 239000007995 HEPES buffer Substances 0.000 description 2
- 102100026120 IgG receptor FcRn large subunit p51 Human genes 0.000 description 2
- 102000006496 Immunoglobulin Heavy Chains Human genes 0.000 description 2
- 108010019476 Immunoglobulin Heavy Chains Proteins 0.000 description 2
- QNAYBMKLOCPYGJ-REOHCLBHSA-N L-alanine Chemical compound C[C@H](N)C(O)=O QNAYBMKLOCPYGJ-REOHCLBHSA-N 0.000 description 2
- AGPKZVBTJJNPAG-WHFBIAKZSA-N L-isoleucine Chemical compound CC[C@H](C)[C@H](N)C(O)=O AGPKZVBTJJNPAG-WHFBIAKZSA-N 0.000 description 2
- FFEARJCKVFRZRR-BYPYZUCNSA-N L-methionine Chemical compound CSCC[C@H](N)C(O)=O FFEARJCKVFRZRR-BYPYZUCNSA-N 0.000 description 2
- QIVBCDIJIAJPQS-VIFPVBQESA-N L-tryptophane Chemical compound C1=CC=C2C(C[C@H](N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-VIFPVBQESA-N 0.000 description 2
- KZSNJWFQEVHDMF-BYPYZUCNSA-N L-valine Chemical compound CC(C)[C@H](N)C(O)=O KZSNJWFQEVHDMF-BYPYZUCNSA-N 0.000 description 2
- 101150055061 LCN2 gene Proteins 0.000 description 2
- ROHFNLRQFUQHCH-UHFFFAOYSA-N Leucine Natural products CC(C)CC(N)C(O)=O ROHFNLRQFUQHCH-UHFFFAOYSA-N 0.000 description 2
- 239000004472 Lysine Substances 0.000 description 2
- 102000003945 NF-kappa B Human genes 0.000 description 2
- 108010057466 NF-kappa B Proteins 0.000 description 2
- 108700020796 Oncogene Proteins 0.000 description 2
- 230000010799 Receptor Interactions Effects 0.000 description 2
- 101710138747 Receptor-type tyrosine-protein phosphatase C Proteins 0.000 description 2
- VBKBDLMWICBSCY-IMJSIDKUSA-N Ser-Asp Chemical compound OC[C@H](N)C(=O)N[C@H](C(O)=O)CC(O)=O VBKBDLMWICBSCY-IMJSIDKUSA-N 0.000 description 2
- MTCFGRXMJLQNBG-UHFFFAOYSA-N Serine Natural products OCC(N)C(O)=O MTCFGRXMJLQNBG-UHFFFAOYSA-N 0.000 description 2
- AYFVYJQAPQTCCC-UHFFFAOYSA-N Threonine Natural products CC(O)C(N)C(O)=O AYFVYJQAPQTCCC-UHFFFAOYSA-N 0.000 description 2
- 239000004473 Threonine Substances 0.000 description 2
- QIVBCDIJIAJPQS-UHFFFAOYSA-N Tryptophan Natural products C1=CC=C2C(CC(N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-UHFFFAOYSA-N 0.000 description 2
- 108060008683 Tumor Necrosis Factor Receptor Proteins 0.000 description 2
- 101710165434 Tumor necrosis factor receptor superfamily member 9 Proteins 0.000 description 2
- KZSNJWFQEVHDMF-UHFFFAOYSA-N Valine Natural products CC(C)C(N)C(O)=O KZSNJWFQEVHDMF-UHFFFAOYSA-N 0.000 description 2
- 230000001133 acceleration Effects 0.000 description 2
- 230000006786 activation induced cell death Effects 0.000 description 2
- 235000004279 alanine Nutrition 0.000 description 2
- 230000006229 amino acid addition Effects 0.000 description 2
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 2
- 239000012911 assay medium Substances 0.000 description 2
- 210000003719 b-lymphocyte Anatomy 0.000 description 2
- 239000011230 binding agent Substances 0.000 description 2
- 230000008827 biological function Effects 0.000 description 2
- 239000012472 biological sample Substances 0.000 description 2
- 230000037396 body weight Effects 0.000 description 2
- 230000010261 cell growth Effects 0.000 description 2
- 238000005119 centrifugation Methods 0.000 description 2
- 210000004978 chinese hamster ovary cell Anatomy 0.000 description 2
- 239000002299 complementary DNA Substances 0.000 description 2
- 238000004590 computer program Methods 0.000 description 2
- 239000012468 concentrated sample Substances 0.000 description 2
- 230000003750 conditioning effect Effects 0.000 description 2
- 210000000172 cytosol Anatomy 0.000 description 2
- 210000004443 dendritic cell Anatomy 0.000 description 2
- 238000009826 distribution Methods 0.000 description 2
- 230000009977 dual effect Effects 0.000 description 2
- 230000002708 enhancing effect Effects 0.000 description 2
- 210000003743 erythrocyte Anatomy 0.000 description 2
- 238000011156 evaluation Methods 0.000 description 2
- 239000012091 fetal bovine serum Substances 0.000 description 2
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 description 2
- 238000011532 immunohistochemical staining Methods 0.000 description 2
- 230000004073 interleukin-2 production Effects 0.000 description 2
- 208000030776 invasive breast carcinoma Diseases 0.000 description 2
- AGPKZVBTJJNPAG-UHFFFAOYSA-N isoleucine Natural products CCC(C)C(N)C(O)=O AGPKZVBTJJNPAG-UHFFFAOYSA-N 0.000 description 2
- 229960000310 isoleucine Drugs 0.000 description 2
- 238000000111 isothermal titration calorimetry Methods 0.000 description 2
- 239000012139 lysis buffer Substances 0.000 description 2
- 210000004962 mammalian cell Anatomy 0.000 description 2
- 108010082117 matrigel Proteins 0.000 description 2
- 239000011159 matrix material Substances 0.000 description 2
- 229930182817 methionine Natural products 0.000 description 2
- 229960004857 mitomycin Drugs 0.000 description 2
- 210000001616 monocyte Anatomy 0.000 description 2
- 108010068617 neonatal Fc receptor Proteins 0.000 description 2
- 239000012188 paraffin wax Substances 0.000 description 2
- 230000003285 pharmacodynamic effect Effects 0.000 description 2
- COLNVLDHVKWLRT-UHFFFAOYSA-N phenylalanine Natural products OC(=O)C(N)CC1=CC=CC=C1 COLNVLDHVKWLRT-UHFFFAOYSA-N 0.000 description 2
- 230000000770 proinflammatory effect Effects 0.000 description 2
- 108020001580 protein domains Proteins 0.000 description 2
- 238000002708 random mutagenesis Methods 0.000 description 2
- 102000005962 receptors Human genes 0.000 description 2
- 108020003175 receptors Proteins 0.000 description 2
- 239000012925 reference material Substances 0.000 description 2
- 230000000284 resting effect Effects 0.000 description 2
- 230000028327 secretion Effects 0.000 description 2
- 239000011780 sodium chloride Substances 0.000 description 2
- 239000007790 solid phase Substances 0.000 description 2
- 239000004094 surface-active agent Substances 0.000 description 2
- 230000002195 synergetic effect Effects 0.000 description 2
- 231100000419 toxicity Toxicity 0.000 description 2
- 230000001988 toxicity Effects 0.000 description 2
- 230000005030 transcription termination Effects 0.000 description 2
- 238000001890 transfection Methods 0.000 description 2
- 238000011830 transgenic mouse model Methods 0.000 description 2
- 102000003298 tumor necrosis factor receptor Human genes 0.000 description 2
- OUYCCCASQSFEME-UHFFFAOYSA-N tyrosine Natural products OC(=O)C(N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-UHFFFAOYSA-N 0.000 description 2
- 239000004474 valine Substances 0.000 description 2
- DTLVBHCSSNJCMJ-UHFFFAOYSA-N (2,5-dioxopyrrolidin-1-yl) 3-[2-[2-[2-[2-[5-(2-oxo-1,3,3a,4,6,6a-hexahydrothieno[3,4-d]imidazol-4-yl)pentanoylamino]ethoxy]ethoxy]ethoxy]ethoxy]propanoate Chemical compound S1CC2NC(=O)NC2C1CCCCC(=O)NCCOCCOCCOCCOCCC(=O)ON1C(=O)CCC1=O DTLVBHCSSNJCMJ-UHFFFAOYSA-N 0.000 description 1
- MZOFCQQQCNRIBI-VMXHOPILSA-N (3s)-4-[[(2s)-1-[[(2s)-1-[[(1s)-1-carboxy-2-hydroxyethyl]amino]-4-methyl-1-oxopentan-2-yl]amino]-5-(diaminomethylideneamino)-1-oxopentan-2-yl]amino]-3-[[2-[[(2s)-2,6-diaminohexanoyl]amino]acetyl]amino]-4-oxobutanoic acid Chemical compound OC[C@@H](C(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H](CC(O)=O)NC(=O)CNC(=O)[C@@H](N)CCCCN MZOFCQQQCNRIBI-VMXHOPILSA-N 0.000 description 1
- UKAUYVFTDYCKQA-UHFFFAOYSA-N -2-Amino-4-hydroxybutanoic acid Natural products OC(=O)C(N)CCO UKAUYVFTDYCKQA-UHFFFAOYSA-N 0.000 description 1
- GOJUJUVQIVIZAV-UHFFFAOYSA-N 2-amino-4,6-dichloropyrimidine-5-carbaldehyde Chemical group NC1=NC(Cl)=C(C=O)C(Cl)=N1 GOJUJUVQIVIZAV-UHFFFAOYSA-N 0.000 description 1
- FVFVNNKYKYZTJU-UHFFFAOYSA-N 6-chloro-1,3,5-triazine-2,4-diamine Chemical group NC1=NC(N)=NC(Cl)=N1 FVFVNNKYKYZTJU-UHFFFAOYSA-N 0.000 description 1
- 241001316595 Acris Species 0.000 description 1
- 102100034540 Adenomatous polyposis coli protein Human genes 0.000 description 1
- 206010002091 Anaesthesia Diseases 0.000 description 1
- 244000063299 Bacillus subtilis Species 0.000 description 1
- 235000014469 Bacillus subtilis Nutrition 0.000 description 1
- 241000283690 Bos taurus Species 0.000 description 1
- 125000001433 C-terminal amino-acid group Chemical group 0.000 description 1
- 101100026251 Caenorhabditis elegans atf-2 gene Proteins 0.000 description 1
- 101100421200 Caenorhabditis elegans sep-1 gene Proteins 0.000 description 1
- 101100314454 Caenorhabditis elegans tra-1 gene Proteins 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- 231100000023 Cell-mediated cytotoxicity Toxicity 0.000 description 1
- 206010057250 Cell-mediated cytotoxicity Diseases 0.000 description 1
- 241000282693 Cercopithecidae Species 0.000 description 1
- 108010019670 Chimeric Antigen Receptors Proteins 0.000 description 1
- 108091026890 Coding region Proteins 0.000 description 1
- 208000003322 Coinfection Diseases 0.000 description 1
- 101100077740 Cyprinus carpio map2k2 gene Proteins 0.000 description 1
- 241000238557 Decapoda Species 0.000 description 1
- 229920002307 Dextran Polymers 0.000 description 1
- 102000001301 EGF receptor Human genes 0.000 description 1
- 238000008157 ELISA kit Methods 0.000 description 1
- 102100034789 Epididymal-specific lipocalin-6 Human genes 0.000 description 1
- 241000283086 Equidae Species 0.000 description 1
- 241000206602 Eukaryota Species 0.000 description 1
- 108700024394 Exon Proteins 0.000 description 1
- 241000282326 Felis catus Species 0.000 description 1
- 241000192125 Firmicutes Species 0.000 description 1
- 102000013382 Gelatinases Human genes 0.000 description 1
- 108010026132 Gelatinases Proteins 0.000 description 1
- 108700039691 Genetic Promoter Regions Proteins 0.000 description 1
- 102000006395 Globulins Human genes 0.000 description 1
- 108010044091 Globulins Proteins 0.000 description 1
- 239000004471 Glycine Substances 0.000 description 1
- 102100032558 Glypican-2 Human genes 0.000 description 1
- 208000009329 Graft vs Host Disease Diseases 0.000 description 1
- 241000238631 Hexapoda Species 0.000 description 1
- 101000924577 Homo sapiens Adenomatous polyposis coli protein Proteins 0.000 description 1
- 101000851181 Homo sapiens Epidermal growth factor receptor Proteins 0.000 description 1
- 101000945886 Homo sapiens Epididymal-specific lipocalin-6 Proteins 0.000 description 1
- 101000605055 Homo sapiens Epididymal-specific lipocalin-8 Proteins 0.000 description 1
- 101001014664 Homo sapiens Glypican-2 Proteins 0.000 description 1
- 101001052490 Homo sapiens Mitogen-activated protein kinase 3 Proteins 0.000 description 1
- 101001052477 Homo sapiens Mitogen-activated protein kinase 4 Proteins 0.000 description 1
- 101000950669 Homo sapiens Mitogen-activated protein kinase 9 Proteins 0.000 description 1
- 101000763579 Homo sapiens Toll-like receptor 1 Proteins 0.000 description 1
- LCWXJXMHJVIJFK-UHFFFAOYSA-N Hydroxylysine Natural products NCC(O)CC(N)CC(O)=O LCWXJXMHJVIJFK-UHFFFAOYSA-N 0.000 description 1
- PMMYEEVYMWASQN-DMTCNVIQSA-N Hydroxyproline Chemical compound O[C@H]1CN[C@H](C(O)=O)C1 PMMYEEVYMWASQN-DMTCNVIQSA-N 0.000 description 1
- 206010061598 Immunodeficiency Diseases 0.000 description 1
- 102000013463 Immunoglobulin Light Chains Human genes 0.000 description 1
- 108010065825 Immunoglobulin Light Chains Proteins 0.000 description 1
- 108091029795 Intergenic region Proteins 0.000 description 1
- 108091092195 Intron Proteins 0.000 description 1
- PIWKPBJCKXDKJR-UHFFFAOYSA-N Isoflurane Chemical compound FC(F)OC(Cl)C(F)(F)F PIWKPBJCKXDKJR-UHFFFAOYSA-N 0.000 description 1
- 108010055717 JNK Mitogen-Activated Protein Kinases Proteins 0.000 description 1
- 102000019145 JUN kinase activity proteins Human genes 0.000 description 1
- 241000235058 Komagataella pastoris Species 0.000 description 1
- SNDPXSYFESPGGJ-BYPYZUCNSA-N L-2-aminopentanoic acid Chemical compound CCC[C@H](N)C(O)=O SNDPXSYFESPGGJ-BYPYZUCNSA-N 0.000 description 1
- AHLPHDHHMVZTML-BYPYZUCNSA-N L-Ornithine Chemical compound NCCC[C@H](N)C(O)=O AHLPHDHHMVZTML-BYPYZUCNSA-N 0.000 description 1
- RHGKLRLOHDJJDR-BYPYZUCNSA-N L-citrulline Chemical compound NC(=O)NCCC[C@H]([NH3+])C([O-])=O RHGKLRLOHDJJDR-BYPYZUCNSA-N 0.000 description 1
- UKAUYVFTDYCKQA-VKHMYHEASA-N L-homoserine Chemical compound OC(=O)[C@@H](N)CCO UKAUYVFTDYCKQA-VKHMYHEASA-N 0.000 description 1
- SNDPXSYFESPGGJ-UHFFFAOYSA-N L-norVal-OH Natural products CCCC(N)C(O)=O SNDPXSYFESPGGJ-UHFFFAOYSA-N 0.000 description 1
- 102000013519 Lipocalin-2 Human genes 0.000 description 1
- 108010051335 Lipocalin-2 Proteins 0.000 description 1
- 108060001084 Luciferase Proteins 0.000 description 1
- 239000005089 Luciferase Substances 0.000 description 1
- YEIYAQQKADPIBJ-GARJFASQSA-N Lys-Asp-Pro Chemical compound C1C[C@@H](N(C1)C(=O)[C@H](CC(=O)O)NC(=O)[C@H](CCCCN)N)C(=O)O YEIYAQQKADPIBJ-GARJFASQSA-N 0.000 description 1
- 102100024192 Mitogen-activated protein kinase 3 Human genes 0.000 description 1
- 102100024189 Mitogen-activated protein kinase 4 Human genes 0.000 description 1
- 102100037809 Mitogen-activated protein kinase 9 Human genes 0.000 description 1
- 102100033127 Mitogen-activated protein kinase kinase kinase 5 Human genes 0.000 description 1
- 101710164337 Mitogen-activated protein kinase kinase kinase 5 Proteins 0.000 description 1
- 241000699660 Mus musculus Species 0.000 description 1
- NQTADLQHYWFPDB-UHFFFAOYSA-N N-Hydroxysuccinimide Chemical compound ON1C(=O)CCC1=O NQTADLQHYWFPDB-UHFFFAOYSA-N 0.000 description 1
- 125000001429 N-terminal alpha-amino-acid group Chemical group 0.000 description 1
- RHGKLRLOHDJJDR-UHFFFAOYSA-N Ndelta-carbamoyl-DL-ornithine Natural products OC(=O)C(N)CCCNC(N)=O RHGKLRLOHDJJDR-UHFFFAOYSA-N 0.000 description 1
- 108091005461 Nucleic proteins Proteins 0.000 description 1
- AHLPHDHHMVZTML-UHFFFAOYSA-N Orn-delta-NH2 Natural products NCCCC(N)C(O)=O AHLPHDHHMVZTML-UHFFFAOYSA-N 0.000 description 1
- UTJLXEIPEHZYQJ-UHFFFAOYSA-N Ornithine Natural products OC(=O)C(C)CCCN UTJLXEIPEHZYQJ-UHFFFAOYSA-N 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- 108091000080 Phosphotransferase Proteins 0.000 description 1
- 108010029485 Protein Isoforms Proteins 0.000 description 1
- 102000001708 Protein Isoforms Human genes 0.000 description 1
- 102000001253 Protein Kinase Human genes 0.000 description 1
- 108010076504 Protein Sorting Signals Proteins 0.000 description 1
- 241000508269 Psidium Species 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- 108020004511 Recombinant DNA Proteins 0.000 description 1
- 206010070308 Refractory cancer Diseases 0.000 description 1
- 108700005075 Regulator Genes Proteins 0.000 description 1
- 108700008625 Reporter Genes Proteins 0.000 description 1
- 240000004808 Saccharomyces cerevisiae Species 0.000 description 1
- 235000014680 Saccharomyces cerevisiae Nutrition 0.000 description 1
- 208000005718 Stomach Neoplasms Diseases 0.000 description 1
- 238000000692 Student's t-test Methods 0.000 description 1
- 241000282887 Suidae Species 0.000 description 1
- 239000012505 Superdex™ Substances 0.000 description 1
- 108700026226 TATA Box Proteins 0.000 description 1
- 102000004398 TNF receptor-associated factor 1 Human genes 0.000 description 1
- 108090000920 TNF receptor-associated factor 1 Proteins 0.000 description 1
- 108091023040 Transcription factor Proteins 0.000 description 1
- 102000040945 Transcription factor Human genes 0.000 description 1
- 108060008682 Tumor Necrosis Factor Proteins 0.000 description 1
- 102000000852 Tumor Necrosis Factor-alpha Human genes 0.000 description 1
- 241000251539 Vertebrata <Metazoa> Species 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 230000002730 additional effect Effects 0.000 description 1
- 230000004520 agglutination Effects 0.000 description 1
- 230000002776 aggregation Effects 0.000 description 1
- 238000004220 aggregation Methods 0.000 description 1
- 230000003321 amplification Effects 0.000 description 1
- 230000037005 anaesthesia Effects 0.000 description 1
- 230000008485 antagonism Effects 0.000 description 1
- 230000005809 anti-tumor immunity Effects 0.000 description 1
- 229930193936 anticarin Natural products 0.000 description 1
- 239000002246 antineoplastic agent Substances 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 125000000637 arginyl group Chemical group N[C@@H](CCCNC(N)=N)C(=O)* 0.000 description 1
- 210000004507 artificial chromosome Anatomy 0.000 description 1
- 238000002869 basic local alignment search tool Methods 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 230000002146 bilateral effect Effects 0.000 description 1
- 238000010170 biological method Methods 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 229960000074 biopharmaceutical Drugs 0.000 description 1
- 210000004204 blood vessel Anatomy 0.000 description 1
- 239000007853 buffer solution Substances 0.000 description 1
- 238000002619 cancer immunotherapy Methods 0.000 description 1
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 1
- 238000006555 catalytic reaction Methods 0.000 description 1
- 230000020411 cell activation Effects 0.000 description 1
- 239000006143 cell culture medium Substances 0.000 description 1
- 230000030833 cell death Effects 0.000 description 1
- 230000003915 cell function Effects 0.000 description 1
- 238000002659 cell therapy Methods 0.000 description 1
- 230000005890 cell-mediated cytotoxicity Effects 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 238000007385 chemical modification Methods 0.000 description 1
- 238000002512 chemotherapy Methods 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- 235000013477 citrulline Nutrition 0.000 description 1
- 229960002173 citrulline Drugs 0.000 description 1
- 238000003776 cleavage reaction Methods 0.000 description 1
- 239000013599 cloning vector Substances 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 230000000295 complement effect Effects 0.000 description 1
- 230000001276 controlling effect Effects 0.000 description 1
- 239000007822 coupling agent Substances 0.000 description 1
- 238000004132 cross linking Methods 0.000 description 1
- 238000013211 curve analysis Methods 0.000 description 1
- 210000000805 cytoplasm Anatomy 0.000 description 1
- YSMODUONRAFBET-UHFFFAOYSA-N delta-DL-hydroxylysine Natural products NCC(O)CCC(N)C(O)=O YSMODUONRAFBET-UHFFFAOYSA-N 0.000 description 1
- 238000011033 desalting Methods 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 238000002405 diagnostic procedure Methods 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- PMMYEEVYMWASQN-UHFFFAOYSA-N dl-hydroxyproline Natural products OC1C[NH2+]C(C([O-])=O)C1 PMMYEEVYMWASQN-UHFFFAOYSA-N 0.000 description 1
- 231100000673 dose–response relationship Toxicity 0.000 description 1
- 210000002472 endoplasmic reticulum Anatomy 0.000 description 1
- 239000003623 enhancer Substances 0.000 description 1
- YSMODUONRAFBET-UHNVWZDZSA-N erythro-5-hydroxy-L-lysine Chemical compound NC[C@H](O)CC[C@H](N)C(O)=O YSMODUONRAFBET-UHNVWZDZSA-N 0.000 description 1
- 230000000763 evoking effect Effects 0.000 description 1
- 239000013604 expression vector Substances 0.000 description 1
- 210000003608 fece Anatomy 0.000 description 1
- 230000005714 functional activity Effects 0.000 description 1
- 206010017758 gastric cancer Diseases 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- WHUUTDBJXJRKMK-VKHMYHEASA-L glutamate group Chemical group N[C@@H](CCC(=O)[O-])C(=O)[O-] WHUUTDBJXJRKMK-VKHMYHEASA-L 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 208000024908 graft versus host disease Diseases 0.000 description 1
- 229960002897 heparin Drugs 0.000 description 1
- 229920000669 heparin Polymers 0.000 description 1
- 244000144980 herd Species 0.000 description 1
- 125000000487 histidyl group Chemical group [H]N([H])C(C(=O)O*)C([H])([H])C1=C([H])N([H])C([H])=N1 0.000 description 1
- QJHBJHUKURJDLG-UHFFFAOYSA-N hydroxy-L-lysine Natural products NCCCCC(NO)C(O)=O QJHBJHUKURJDLG-UHFFFAOYSA-N 0.000 description 1
- 229960002591 hydroxyproline Drugs 0.000 description 1
- 230000028993 immune response Effects 0.000 description 1
- 230000036039 immunity Effects 0.000 description 1
- 238000003018 immunoassay Methods 0.000 description 1
- 230000009851 immunogenic response Effects 0.000 description 1
- 239000002955 immunomodulating agent Substances 0.000 description 1
- 229940121354 immunomodulator Drugs 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 210000003000 inclusion body Anatomy 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 229960003130 interferon gamma Drugs 0.000 description 1
- 230000003834 intracellular effect Effects 0.000 description 1
- 239000007928 intraperitoneal injection Substances 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 229960002725 isoflurane Drugs 0.000 description 1
- 230000002147 killing effect Effects 0.000 description 1
- 238000002372 labelling Methods 0.000 description 1
- 210000000265 leukocyte Anatomy 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 239000007791 liquid phase Substances 0.000 description 1
- 244000144972 livestock Species 0.000 description 1
- 210000000207 lymphocyte subset Anatomy 0.000 description 1
- 125000003588 lysine group Chemical group [H]N([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])(N([H])[H])C(*)=O 0.000 description 1
- 230000001320 lysogenic effect Effects 0.000 description 1
- 238000012423 maintenance Methods 0.000 description 1
- 201000001441 melanoma Diseases 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 230000001394 metastastic effect Effects 0.000 description 1
- 206010061289 metastatic neoplasm Diseases 0.000 description 1
- 238000010369 molecular cloning Methods 0.000 description 1
- 238000000302 molecular modelling Methods 0.000 description 1
- 239000000178 monomer Substances 0.000 description 1
- 231100000219 mutagenic Toxicity 0.000 description 1
- 230000003505 mutagenic effect Effects 0.000 description 1
- 210000000581 natural killer T-cell Anatomy 0.000 description 1
- 230000017095 negative regulation of cell growth Effects 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 210000000440 neutrophil Anatomy 0.000 description 1
- 230000005937 nuclear translocation Effects 0.000 description 1
- 238000003199 nucleic acid amplification method Methods 0.000 description 1
- 229960003104 ornithine Drugs 0.000 description 1
- 230000002018 overexpression Effects 0.000 description 1
- 102000002574 p38 Mitogen-Activated Protein Kinases Human genes 0.000 description 1
- 108010068338 p38 Mitogen-Activated Protein Kinases Proteins 0.000 description 1
- 239000006174 pH buffer Substances 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 230000002093 peripheral effect Effects 0.000 description 1
- 210000001322 periplasm Anatomy 0.000 description 1
- 102000013415 peroxidase activity proteins Human genes 0.000 description 1
- 108040007629 peroxidase activity proteins Proteins 0.000 description 1
- 230000002688 persistence Effects 0.000 description 1
- 210000001539 phagocyte Anatomy 0.000 description 1
- 239000008194 pharmaceutical composition Substances 0.000 description 1
- 239000000546 pharmaceutical excipient Substances 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- 102000020233 phosphotransferase Human genes 0.000 description 1
- 230000000704 physical effect Effects 0.000 description 1
- 230000004962 physiological condition Effects 0.000 description 1
- 239000013612 plasmid Substances 0.000 description 1
- 230000008488 polyadenylation Effects 0.000 description 1
- 229920001515 polyalkylene glycol Polymers 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 150000003141 primary amines Chemical class 0.000 description 1
- 210000001236 prokaryotic cell Anatomy 0.000 description 1
- 230000002062 proliferating effect Effects 0.000 description 1
- 125000001500 prolyl group Chemical group [H]N1C([H])(C(=O)[*])C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 108060006633 protein kinase Proteins 0.000 description 1
- 230000012743 protein tagging Effects 0.000 description 1
- 239000011541 reaction mixture Substances 0.000 description 1
- 230000007115 recruitment Effects 0.000 description 1
- 239000013558 reference substance Substances 0.000 description 1
- 208000016691 refractory malignant neoplasm Diseases 0.000 description 1
- 230000010076 replication Effects 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 108091008146 restriction endonucleases Proteins 0.000 description 1
- 230000000717 retained effect Effects 0.000 description 1
- 238000005070 sampling Methods 0.000 description 1
- 230000007017 scission Effects 0.000 description 1
- 210000000582 semen Anatomy 0.000 description 1
- 230000003393 splenic effect Effects 0.000 description 1
- 230000002269 spontaneous effect Effects 0.000 description 1
- 230000006641 stabilisation Effects 0.000 description 1
- 238000013112 stability test Methods 0.000 description 1
- 238000011105 stabilization Methods 0.000 description 1
- 238000007447 staining method Methods 0.000 description 1
- 201000011549 stomach cancer Diseases 0.000 description 1
- 230000001629 suppression Effects 0.000 description 1
- 230000004083 survival effect Effects 0.000 description 1
- 208000024891 symptom Diseases 0.000 description 1
- 238000001308 synthesis method Methods 0.000 description 1
- 238000007910 systemic administration Methods 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- 229940124597 therapeutic agent Drugs 0.000 description 1
- 230000009258 tissue cross reactivity Effects 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- FGMPLJWBKKVCDB-UHFFFAOYSA-N trans-L-hydroxy-proline Natural products ON1CCCC1C(O)=O FGMPLJWBKKVCDB-UHFFFAOYSA-N 0.000 description 1
- 230000002103 transcriptional effect Effects 0.000 description 1
- 230000009466 transformation Effects 0.000 description 1
- 230000009261 transgenic effect Effects 0.000 description 1
- 230000032258 transport Effects 0.000 description 1
- 230000001960 triggered effect Effects 0.000 description 1
- 125000000430 tryptophan group Chemical group [H]N([H])C(C(=O)O*)C([H])([H])C1=C([H])N([H])C2=C([H])C([H])=C([H])C([H])=C12 0.000 description 1
- 241000701447 unidentified baculovirus Species 0.000 description 1
- 229950005972 urelumab Drugs 0.000 description 1
- 210000002700 urine Anatomy 0.000 description 1
- 230000003612 virological effect Effects 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
- 238000005303 weighing Methods 0.000 description 1
- 238000001262 western blot Methods 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2878—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the NGF-receptor/TNF-receptor superfamily, e.g. CD27, CD30, CD40, CD95
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/46—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates
- C07K14/47—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates from mammals
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/32—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against translation products of oncogenes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/52—Constant or Fc region; Isotype
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/73—Inducing cell death, e.g. apoptosis, necrosis or inhibition of cell proliferation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2318/00—Antibody mimetics or scaffolds
- C07K2318/20—Antigen-binding scaffold molecules wherein the scaffold is not an immunoglobulin variable region or antibody mimetics
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/70—Fusion polypeptide containing domain for protein-protein interaction
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Immunology (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Molecular Biology (AREA)
- Genetics & Genomics (AREA)
- Zoology (AREA)
- Toxicology (AREA)
- Gastroenterology & Hepatology (AREA)
- Oncology (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Microbiology (AREA)
- Mycology (AREA)
- Epidemiology (AREA)
- Peptides Or Proteins (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
Description
HER2/neuはヒト上皮成長因子受容体ファミリーのメンバーである。このがん遺伝子の増幅または過剰発現は、侵攻性が高い一定タイプの乳がんを含むさまざまな腫瘍の発生および進行に重要な役割を果たすことが示されている。HER2/neuは、腫瘍細胞上に、健常組織と比較してはるかに高い細胞表面密度で、著しく差次的に発現することが示されている。
(a)CD137に対する結合特異性、および
(b)HER2/neuに対する結合特異性
を有する融合ペプチドによってCD137と腫瘍抗原HER2/neuとに同時に会合する新規なアプローチを提供する。
以下の一覧では、本明細書の全体を通して使用される用語、語句、および略号を定義する。本明細書に列挙して定義する用語はいずれも、すべての文法形式を包含するものとする。
[本発明1001]
CD137にもHer2にも結合する能力を有する融合ポリペプチドであって、少なくとも2つのサブユニットを任意の順序で含み、第1サブユニットは完全長免疫グロブリンまたはその抗原結合ドメインを含み、この第1結合ドメインはHER2に対する結合特異性を有し、かつ第2サブユニットはCD137に対する結合特異性を有するリポカリンムテインを含む、融合ポリペプチド。
[本発明1002]
融合ポリペプチドに含まれるCD137に特異的なリポカリンムテインと融合ポリペプチドとを本質的に実施例3に記載するようにELISAアッセイにおいて測定した場合に、融合ポリペプチドに含まれるCD137に特異的なリポカリンムテインのEC50値と、少なくともほぼ同じかそれより優れたEC50値で、CD137に結合する能力を有する、本発明1001の融合ポリペプチド。
[本発明1003]
本質的に実施例3に記載するようにELISAアッセイにおいて測定した場合に、少なくとも約1nMのEC50値でCD137に結合する能力を有する、本発明1001の融合ポリペプチド。
[本発明1004]
融合ポリペプチドに含まれるHER2/neuに特異的な免疫グロブリンと融合ポリペプチドとを本質的に実施例2に記載するようにELISAアッセイにおいて測定した場合に、当該融合ポリペプチドに含まれるHER2/neuに特異的な免疫グロブリンのEC50値に匹敵するEC50値で、HER2/neuに結合する能力を有する、本発明1001の融合ポリペプチド。
[本発明1005]
本質的に実施例2に記載するようにELISAアッセイにおいて測定した場合に、少なくとも約1nMのEC50値でHER2/neuに結合する能力を有する、本発明1001の融合ポリペプチド。
[本発明1006]
本質的に実施例4に記載するELISAアッセイにおいて測定した場合に、CD137およびHER2/neuに同時に結合する能力を有する、本発明1001の融合ポリペプチド。
[本発明1007]
本質的に実施例4に記載するELISAアッセイにおいて測定した場合に、少なくとも約4nMのEC50値でCD137およびHER2/neuに同時に結合する能力を有する、本発明1001の融合ポリペプチド。
[本発明1008]
本質的に実施例5に記載する機能的T細胞活性化アッセイにおいてT細胞応答を共刺激する能力を有する、本発明1001の融合ポリペプチド。
[本発明1009]
本質的に実施例5に記載する機能的T細胞活性化アッセイにおいて、IL-2分泌およびT細胞増殖を誘発することができる、本発明1001の融合ポリペプチド。
[本発明1010]
本質的に実施例5に記載する機能的T細胞活性化アッセイにおいて、T細胞活性化の成功をもたらす、本発明1001の融合ポリペプチド。
[本発明1011]
前記ムテインが、成熟ヒト涙液リポカリンの直鎖ポリペプチド配列(SEQ ID NO:18)の配列位置5、26〜31、33〜34、42、46、52、56、58、60〜61、65、71、85、94、101、104〜106、108、111、114、121、133、148、150および153に少なくとも1つの変異アミノ酸残基を含む、本発明1001〜1010のいずれかの融合ポリペプチド。
[本発明1012]
前記ムテインのアミノ酸配列が、成熟ヒト涙液リポカリンの直鎖ポリペプチド配列(SEQ ID NO:18)との比較において以下の変異アミノ酸残基:
のうちの少なくとも1つを含む、本発明1011の融合ポリペプチド。
[本発明1013]
前記ムテインのアミノ酸配列が以下の組のアミノ酸置換:
のうちの1つを含む、本発明1011〜1012のいずれかの融合ポリペプチド。
[本発明1014]
前記ムテインのアミノ酸配列が、SEQ ID NO:32〜38からなる群またはそのフラグメントもしくは変異体からなる群より選択されるアミノ酸配列を含む、本発明1011〜1013のいずれかの融合ポリペプチド。
[本発明1015]
前記ムテインのアミノ酸配列が、SEQ ID NO:32〜38からなる群より選択されるアミノ酸配列に対して少なくとも85%の配列同一性を有する、本発明1011〜1013のいずれかの融合ポリペプチド。
[本発明1016]
前記ムテインが、成熟hNGALの直鎖ポリペプチド配列(SEQ ID NO:17)の配列位置28、36、40〜41、49、52、65、68、70、72〜73、77、79、81、83、87、94、96、100、103、106、125、127、132および134に少なくとも1つの変異アミノ酸残基を含む、本発明1001〜1010のいずれかの融合ポリペプチド。
[本発明1017]
前記ムテインのアミノ酸配列が、成熟hNGALの直鎖ポリペプチド配列(SEQ ID NO:17)との比較において、以下の変異アミノ酸残基:
のうちの少なくとも1つを含む、本発明1016の融合ポリペプチド。
[本発明1018]
前記ムテインのアミノ酸配列が、以下の組のアミノ酸置換:
のうちの1つを含む、本発明1016〜1017のいずれかの融合ポリペプチド。
[本発明1019]
前記ムテインのアミノ酸配列が、SEQ ID NO:2および39〜46からなる群またはそのフラグメントもしくは変異体からなる群より選択されるアミノ酸配列を含む、本発明1016〜1018のいずれかの融合ポリペプチド。
[本発明1020]
前記ムテインのアミノ酸配列が、SEQ ID NO:2および39〜46からなる群より選択されるアミノ酸配列に対して少なくとも85%の配列同一性を有する、本発明1016〜1018のいずれかの融合ポリペプチド。
[本発明1021]
1つのサブユニットが、本質的に図1に記載するように、ペプチド結合を介して別のサブユニットに連結されうる、本発明1001〜1020のいずれかの融合ポリペプチド。
[本発明1022]
第1サブユニットと第2結合ドメインとが、第2サブユニットのリポカリンムテインのN末と第1サブユニットの免疫グロブリンの重鎖定常領域(CH)のC末との間のペプチド結合を介して連結されている、本発明1001〜1020のいずれかの融合ポリペプチド。
[本発明1023]
第3サブユニットが、第3サブユニットのリポカリンムテインのN末と第1サブユニットの免疫グロブリンの軽鎖定常領域(CL)のC末との間でペプチド結合を介して第1サブユニットに連結されている、本発明1001〜1020のいずれかの融合ポリペプチド。
[本発明1024]
ペプチド結合が、構造化されていない(G4S)3リンカーである、本発明1021〜1023のいずれかの融合ポリペプチド。
[本発明1025]
SEQ ID NO:19に示すアミノ酸を含む、本発明1001〜1024のいずれかの融合ポリペプチド。
[本発明1026]
リポカリンムテインがSEQ ID NO:2に示すアミノ酸を含む、本発明1001〜1025のいずれかの融合ポリペプチド。
[本発明1027]
免疫グロブリンがモノクローナル抗体である、本発明1001〜1025のいずれかの融合ポリペプチド。
[本発明1028]
モノクローナル抗体がトラスツズマブまたはペルツズマブである、本発明1001〜1025のいずれかの融合ポリペプチド。
[本発明1029]
モノクローナル抗体がSEQ ID NO:3および4によって与えられる重鎖および軽鎖を有する、本発明1001〜1025のいずれかの融合ポリペプチド。
[本発明1030]
モノクローナル抗体がIgG4バックボーンを有する、本発明1001〜1025のいずれかの融合ポリペプチド。
[本発明1031]
IgG4バックボーンが、S228P、N297A、F234A、およびL235Aからなる群より選択される突然変異のうちのいずれか1つを有する、本発明1030の融合ポリペプチド。
[本発明1032]
SEQ ID NO:5および6に示すアミノ酸、SEQ ID NO:7および8に示すアミノ酸、またはSEQ ID NO:9および10に示すアミノ酸、またはSEQ ID NO:11および12に示すアミノ酸、またはSEQ ID NO:13および14に示すアミノ酸、またはSEQ ID NO:15および16に示すアミノ酸を含む、本発明1001〜1010のいずれかの融合ポリペプチド。
[本発明1033]
本発明1001〜1032のいずれかのポリペプチドをコードするヌクレオチド配列を含む核酸分子。
[本発明1034]
核酸分子の発現を可能にする制御配列に機能的に連結されている、本発明1033の核酸分子。
[本発明1035]
ベクター中またはファージミドベクター中に含まれている、本発明1033または1034の核酸分子。
[本発明1036]
本発明1034〜1035のいずれかの核酸分子を含有する宿主細胞。
[本発明1037]
本発明1001〜1232のいずれかの融合ポリペプチドを生産する方法であって、融合ポリペプチドが、ムテインをコードする核酸から出発して、遺伝子工学的方法を使って生産される、方法。
[本発明1038]
融合ポリペプチドが細菌宿主細胞または真核宿主細胞中で生産され、かつ、この宿主生物またはその培養物から単離される、本発明1037の方法。
[本発明1039]
CD137の下流シグナリング経路を活性化し、同時にHER2/neu陽性腫瘍細胞に会合(engage)するための、本発明1001〜1032のいずれかの融合ポリペプチドまたはそのような融合ポリペプチドを含む組成物の使用。
[本発明1040]
CD137の下流シグナリング経路を活性化し、同時にHER2/neu陽性腫瘍細胞に会合するための、本発明1001〜1032のいずれかの融合ポリペプチドまたはそのような融合ポリペプチドを含む組成物の使用。
[本発明1041]
CD137の下流シグナリング経路を活性化し、同時にHER2/neu陽性腫瘍細胞に会合する方法であって、本発明1001〜1032のいずれかの融合ポリペプチドまたはそのような融合ポリペプチドを含む組成物を適用する工程を含む、方法。
[本発明1042]
T細胞を共刺激し、同時にHER2/neu陽性腫瘍細胞に会合する方法であって、本発明1001〜1032のいずれかの融合ポリペプチドまたはそのような融合ポリペプチドを含む組成物を適用する工程を含む、方法。
[本発明1043]
Tリンパ球増殖を誘発し、同時にHER2/neu陽性腫瘍細胞に会合する方法であって、本発明1001〜1032のいずれかの融合ポリペプチドまたはそのような融合ポリペプチドを含む組成物を適用する工程を含む、方法。
[本発明1044]
T細胞でのCD137クラスター化および活性化をHER2/neu陽性腫瘍細胞へ方向づける方法であって、本発明1001〜1032のいずれかの融合ポリペプチドまたはそのような融合ポリペプチドを含む組成物を適用する工程を含む、方法。
[本発明1045]
HER2/neu陽性腫瘍細胞の近傍において局所的T細胞応答を誘発する方法であって、本発明1001〜1032のいずれかの融合ポリペプチドまたはそのような融合ポリペプチドを含む組成物を適用する工程を含む、方法。
[本発明1046]
HER2/neu陽性腫瘍細胞の近傍において局所的NK細胞応答を誘発する方法であって、本発明1001〜1032のいずれかの融合ポリペプチドまたはそのような融合ポリペプチドを含む組成物を適用する工程を含む、方法。
[本発明1047]
HER2/neu陽性腫瘍細胞の近傍においてT細胞によるIL-2および/またはIFNガンマの生産を誘発する方法であって、本発明1001〜1032のいずれかの融合ポリペプチドまたはそのような融合ポリペプチドを含む組成物を適用する工程を含む、方法。
いくつかの態様において、融合ポリペプチドは、任意の順序で、少なくとも2つのサブユニット、すなわちHER2/neuに特異的な完全長免疫グロブリンまたはその抗原結合ドメインを含む第1サブユニットと、CD137に特異的なリポカリンムテインを含む第2サブユニットとを含有する。
いくつかの態様では、融合ポリペプチドに関して、第1結合ドメインは、HER2/neuに特異的な完全長免疫グロブリンまたはその抗原結合ドメインを含む。免疫グロブリンは、例えばIgG1またはIgG4でありうる。さらなる態様において、免疫グロブリンは、HER2/neuに対するモノクローナル抗体である。そのような免疫グロブリンの具体例をいくつか挙げると、トラスツズマブ(商品名Herclon、Herceptin)およびペルツズマブ(2C4とも呼ばれる、商品名Perjeta)がある。
本明細書にいう「リポカリン」は、複数(好ましくは4つ)のループにより一端においてペアワイズに接続されることで結合ポケットを規定している複数(好ましくは8つ)のβストランドを含む円柱状のβプリーツシート超二次構造領域を有する、重量が約18〜20kDAの単量体型タンパク質と定義される。サイズ、形状、および化学的特徴が異なる標的を収容する能力をそれぞれが有するリポカリンファミリーメンバー間に、さまざまな異なる結合様式を生じさせるのは、他の点では剛直なリポカリンスキャフォールドにおけるループの多様性である(例えばFlower, D.R.(1996),前掲; Flower, D.R. et al.(2000),前掲、またはSkerra, A.(2000)Biochim. Biophys. Acta 1482, 337-3に概説されている)。事実、リポカリンタンパク質ファミリーは、広範なリガンドに結合するように、自然に進化しており、それらが共有する全体的配列保存のレベルは異常に低い(多くの場合、配列同一性は20%未満である)にもかかわらず、高度に保存された全体的フォールディングパターンを保っている。さまざまなリポカリンにおける位置間の対応は当業者には周知である。例えば米国特許第7,250,297号を参照されたい。
一局面において、本開示は、CD137結合性ヒト涙液リポカリンムテインを提供する。
のうちの1つまたは複数を含む。いくつかの態様において、本開示によるTlcムテインは、成熟ヒト涙液リポカリンのこれらの配列位置における変異アミノ酸残基を、2つ以上、例えば3、4、5、6、7、8、9、10、11、12個、さらにはそれ以上、例えば13、14、15、16、17、18、19、20、21、22、23、24、25、26個、またはすべて含む。
のうちの1つまたは複数を含む。
いくつかの態様において、本開示の融合ポリペプチドは、CD137およびHER2の二重ターゲティングによる相乗効果をもたらしうる。例えば、エクスビボアッセイおよびマウスモデルにおいて証明されるとおり、NK細胞のCD137刺激は、NK細胞の機能および活性を強化することによって、トラスツズマブの活性を増進する(Kohrt, H. et al, J Clin Invest. 2012 Mar; 122(3):1066-75)。
実施例1:融合ポリペプチドの発現および分析
HER2およびCD137に同時に会合するために、本発明者らは、SEQ ID NO:3および4によって与えられる重鎖および軽鎖を有する抗体を、構造化されていない(G4S)3リンカー(SEQ ID NO:19)を介してSEQ ID NO:2のリポカリンムテインに融合することにより、いくつかの代表的な抗体-リポカリンムテイン融合ポリペプチドを作製した。設計した複数の異なるフォーマットを図1に示す。そのような融合ポリペプチド(SEQ ID NO:9および10、SEQ ID NO:11および12、SEQ ID NO:13および14、SEQ ID NO:15および16)を、SEQ ID NO:2のリポカリンムテインを、インビトロおよびインビボでのIgG4半抗体交換を最小限に抑えるためのS228P突然変異(Silva 2015参照)ならびにFc-ガンマ受容体相互作用を低減するためのF234AおよびL235A突然変異(Alegre 1992)を含有する工学的に操作されたIgG4バックボーンを有する突然変異させた抗体の変異体の4つの末部のうちのいずれか1つに融合することによって作製した。さらにまた、本発明者らは、SEQ ID NO:9および10の融合ポリペプチドとの比較において、天然のグリコシル化モチーフを除去するために抗体重鎖中に追加のN297A突然変異を有する(Bolt 1993参照)、SEQ ID NO:7および8の融合ポリペプチドを作製した。この除去は、潜在的に、Fc-ガンマ受容体との相互作用をさらに低減しうる。加えて、本発明者らは、IgG1バックグラウンドを持つSEQ ID NO:3および4の抗体の重鎖のC末へのSEQ ID NO:2のリポカリンムテインの直接融合物であり、それゆえにIgG1抗体の元来のFc-ガンマ相互作用を保っている、SEQ ID NO:5および6の融合ポリペプチドを作製した。
本発明者らは、ELISAアッセイを使って、組換えHER2(Sino Biological)に対する融合タンパク質の親和性を決定した。標的をPBS(5μg/mL)に溶解し、マイクロタイタープレートに4℃で終夜コーティングした。各インキュベーション工程後に、0.05%(v/v)Tween 20を補足したPBS(PBS-T)80μLで、プレートを5回洗浄した。プレートを、PBS中の2%BSA(w/v)により、室温で1時間ブロッキングした後、洗浄した。ベンチマーク抗体(SEQ ID NO:3および4、トラスツズマブ、すなわちHerceptin(登録商標)、Roche Diagnostics)または融合ポリペプチドをさまざまな濃度でウェルに加え、室温で1時間インキュベートした後、洗浄工程を行った。PBS-T中の1:5000希釈抗ヒトIgG Fc-HRP(#109-035-098、Jackson Laboratory)と共にインキュベーションした後、結合している試験対象の作用物質を検出した。追加洗浄工程後に、蛍光原性HRP基質(QuantaBlu、Thermo)を各ウェルに加え、蛍光マイクロプレートリーダーを使って蛍光強度を検出した。
本発明者らは、ELISAアッセイを使って、組換えCD137-Fc融合物(#838-4B-100、R&D Systems)に対する融合ポリペプチドおよびSEQ ID NO:2の陽性対照リポカリンムテインの親和性を決定した。標的をPBS(5μg/mL)に溶解し、マイクロタイタープレートに4℃で終夜コーティングした。各インキュベーション工程後に、80μLのPBS-Tで、プレートを5回洗浄した。プレートを、PBS中の2%BSA(w/v)により、室温で1時間ブロッキングした後、洗浄した。単量体型のCD137特異的リポカリンムテイン(SEQ ID NO:2)または融合ポリペプチドをさまざまな濃度でウェルに加え、室温で1時間インキュベートした後、洗浄工程を行った。PBS-T中の1:1000希釈抗hNGAL抗体(HRPにコンジュゲートされているもの)と共に室温で1時間インキュベーションした後、結合している試験対象の作用物質を検出した。追加洗浄工程後に、蛍光原性HRP基質(QuantaBlu、Thermo)を各ウェルに加え、蛍光マイクロプレートリーダーを使って蛍光強度を検出した。
HER2およびCD137への融合ポリペプチドの同時結合を証明するために、二重結合ELISAフォーマットを使用した。PBS中の組換えHER2(Sino Biological)(5μg/mL)をマイクロタイタープレートに4℃で終夜コーティングした。Biotek ELx405 select CW洗浄機を使って、各インキュベーション工程後に、0.05%(v/v)Tween 20を補足したPBS(PBS-T)80μLで、プレートを5回洗浄した。プレートを、PBS中の2%BSA(w/v)により、室温で1時間ブロッキングした後、再び洗浄した。融合ポリペプチドをさまざまな濃度でウェルに加え、室温で1時間インキュベートした後、洗浄工程を行った。次に、ビオチン化ヒトCD137-Fcを、PBS-T中1μg/mLの定濃度で1時間加えた。洗浄後にExtravidin-HRP(Sigma-Adrich、PBS-T中に1:5000)をウェルに1時間加えた。追加洗浄工程後に、蛍光原性HRP基質(QuantaBlu、Thermo)を各ウェルに加え、蛍光マイクロプレートリーダーを使って蛍光強度を検出した。
本発明者らは、T細胞活性化アッセイを使って、T細胞応答を共刺激するSEQ ID NO:15および16の融合ポリペプチドの能力を評価した。この目的のために、SEQ ID NO:15および16の融合ポリペプチドを、さまざまな濃度で、抗ヒトCD3抗体(OKT3、eBioscience)と一緒にプラスチック製ディッシュにコーティングし、次に精製T細胞をその被覆表面上でインキュベートした。本発明者らは、読み出し情報として、3日間のインキュベーション後のT細胞増殖の継続を、4時間BrdUパルスを使って評価し、上清のインターロイキン2(IL-2))レベルを測定した。以下にこの実験を詳細に説明する。
本発明者らは、標的細胞依存的T細胞活性化アッセイを使って、CD137およびHER2を同時に結合する能力を有するSEQ ID NO:9および10、SEQ ID NO:11および12、SEQ ID NO:13および14、ならびにSEQ ID NO:15および16の融合ポリペプチドの、HER2陽性細胞株上に固定化された場合のT細胞応答共刺激能力を評価した。本発明者らは、陰性対照として、SEQ ID NO:3および4の単一特異性HER2結合抗体を使用した。さらなる対照として、HER2陽性細胞に結合している二重特異性コンストラクトSEQ ID NO:9および10、SEQ ID NO:11および12、SEQ ID NO:13および14、ならびにSEQ ID NO:15および16を追い出すために、過剰量のSEQ ID NO:3および4の単一特異性HER2結合抗体の存在下で、実験を行った。この実験では、抗ヒトCD3抗体(OKT3、eBioscience)をプラスチック製培養ディッシュにコーティングした後、HER2陽性SKBR3細胞をそのディッシュ上で終夜培養した。翌日、精製T細胞を、さまざまな濃度の、SEQ ID NO:9および10、SEQ ID NO:11および12、SEQ ID NO:13および14、ならびにSEQ ID NO:15および16の融合ポリペプチド、またはSEQ ID NO:3および4の対照抗体の存在下、被覆表面上でインキュベートした。本発明者らは、読み出し情報として、上清インターロイキン2(IL-2)およびインターフェロン-γ(IFN-γ)のレベルを測定した。以下にこの実験を詳述する。
Fc-ガンマ受容体hFcγRI/CD64(R&D Systems)およびhFcγRIIIA/CD16a(R&D Systems)に対する、工学的に操作されたIgG4に基づくバックボーンを持つポリペプチド融合物(SEQ ID NO:9および10、SEQ ID NO:11および12、SEQ ID NO:13および14、ならびにSEQ ID NO:15および16)の結合親和性を測定するために、表面プラズモン共鳴(SPR)に基づくアッセイを使用した。SEQ ID NO:3および4を、IgG1バックボーンを持つ単一特異性抗体の対照とした。SEQ ID NO:5および6を、IgG1に基づくポリペプチド融合物の対照とした。このSPR親和性アッセイでは、ポリペプチド融合物をビオチン化し、ビオチンCAPtureキット(Biotin CAPture Kit)(GE Healthcare)を使ってセンサーチップCAP上に捕捉した。センサーチップCAPをssDNAオリゴでプレ固定化処理(pre-immobilize)した。無希釈のビオチンCAPture試薬(相補的ssDNAオリゴとコンジュゲートされたストレプトアビジン)を、2μL/分の流速で300秒、適用した。次に10μg/mLのビオチン化ポリペプチド融合物を、5μL/分の流速で300秒、適用した。SEQ ID NO:3および4、ならびにポリペプチド融合物は、EZ-Link(登録商標)NHS-PEG4-ビオチン(Thermo Scientific)と共に室温で2時間インキュベートすることによってビオチン化した。反応混合物をZeba(商標)スピン脱塩プレート(Thermo Scientific)にローディングすることにより、反応しなかった過剰のビオチン試薬を除去した。リファレンスチャネルにはビオチンCAPture試薬だけをローディングした。
工学的に操作されたIgG4に基づくバックボーンを持つポリペプチド融合物(SEQ ID NO:9および10、SEQ ID NO:11および12、SEQ ID NO:13および14、ならびにSEQ ID NO:15および16)の、新生児型Fc受容体(FcRn、Sino Biologicals、#CT009-H08H)に対する結合親和性を測定するために、表面プラズモン共鳴(SPR)に基づくアッセイを使用した。SEQ ID NO:3および4を、IgG1バックボーンを持つ単一特異性抗体の対照とした。SEQ ID NO:5および6を、IgG1に基づくポリペプチド融合物の対照とした。このSPR親和性アッセイでは、FcRnをCM5センサーチップ(GE Healthcare)上に製造者の説明書に従って共有結合で固定化した。簡単に述べると、デキストランマトリックスのカルボキシル基を、1-エチル-3-(3-ジメチルアミノプロピル)-カルボジイミド(EDC)およびN-ヒドロキシスクシンイミド(NHS)で活性化した後、FcRnタンパク質の1級アミンを、シグナルが約200RUに達するまで表面上のNHSエステルと反応させた。最後に、表面を横切るように1Mエタノールアミンの溶液を通すことによって、未反応のNHSエステルをブロッキングした。固定化手順中の流速は常に10μl/分とした。
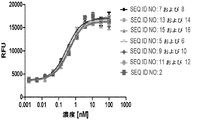
本発明者らは、標的細胞依存的T細胞活性化アッセイを使って、SEQ ID NO:9および10の融合ポリペプチドの、T細胞応答を共刺激する能力を、標的細胞のHER2発現レベルの関数として評価した。この目的のために、本発明者らは、HER2高発現SKBR3細胞およびHER2高発現BT474細胞を、健常HER2発現細胞と類似するレベルでHER2を発現する細胞HepG2およびMCF7と共に使用した。比較のために、本発明者らは、SEQ ID NO:47および48、ならびにSEQ ID NO:49および50のリファレンス抗CD137モノクローナル抗体の挙動を調べた。陰性対照として、本発明者らはSEQ ID NO:3および4の単一特異性HER2結合抗体を使用した。さらにもう1つの陰性対照として、試験物の添加なしでこの実験を実行した(「媒体対照」)。この実験では、抗ヒトCD3抗体(OKT3、eBioscience)をプラスチック製培養ディッシュにコーティングしてから、そのディッシュ上でSKBR3、BT474、HepG2またはMCF7細胞を別々に終夜培養した。翌日、精製T細胞を、さまざまな濃度のSEQ ID NO:9および10の融合ポリペプチド、リファレンス抗体SEQ ID NO:47および48ならびにSEQ ID NO:49および50、SEQ ID NO:3および4の対照抗体の存在下で、または試験物を添加することなく、被覆表面上でインキュベートした。本発明者らは、読み出し情報として、上清インターロイキン2(IL-2)レベルを測定した。以下にこの実験を詳述する。
SEQ ID NO:9および10、SEQ ID NO:11および12、SEQ ID NO:13および14、ならびにSEQ ID NO:15および16によって規定される融合ポリペプチドの安定性を調べるために、本発明者らは、試料を、およそ20mg/mL(21〜23mg/mLの範囲)の濃度において、pH7.4のPBS中、40℃で、4週間インキュベートする実験を使用した。比較のために、本発明者らは、SEQ ID NO:3および4によって規定されるポリペプチドの同一条件下での挙動を調べた。試料を5mg/mL前後の濃度から20mg/mL前後の濃度まで遠心分離フィルタ(Ultracel-3K、Amicon)を使って濃縮し、この濃縮試料の一部をリファレンス物質として-20℃で保存した。次に、0.5mLチューブ(PCR-PT、Sarstedt)中の濃縮試料0.1mLを、インキュベータ(Memmert)中、40℃で、4週間保存した。次に、試料の保全性および単量体含量を調べるために、0.150mL/分の流速で、Agilent 1200シリーズGPC2システムでのSuperdex200 Increaseカラム分析用サイズ排除クロマトグラフィー(SEC)に付した。20μgの試料をカラムに適用した。連続的フロースルー中の相対的タンパク質濃度を波長280nmにおける吸収によって検出した。
SEQ ID NO:9および10、SEQ ID NO:11および12、SEQ ID NO:13および14、ならびにSEQ ID NO:15および16によって規定される融合ポリペプチドの薬物動態と、参照用のSEQ ID NO:3および4の薬物動態との分析を、マウスにおいて行った。およそ5週齢の雄CD-1マウス(1時点あたり3匹; Charles River Laboratories, Research Models and Services, Germany GmbH)の尾静脈に10mg/kgの用量で融合ポリペプチドを注射した。試験物は5mL/kgの体積を使ってボーラスとして投与した。5分、1時間、2時間、4時間、8時間、24時間、48時間、4日、8日、14日および20日の時点において、マウスから血漿試料を得た。各動物および各時点について少なくとも100μLのLi-ヘパリン血漿が得られるように、十分な全血(イソフルラン麻酔下で採血)を収集した。薬物レベルは、標的HER2およびCD137によって完全な二重特異性コンストラクトを検出するサンドイッチELISAを使って決定した。トラスツズマブの血漿中レベルは、標的HER2およびヒトFcによるサンドイッチELISAを使って決定した。Prism GraphPad 5ソフトウェアを使用し、2コンパートメントモデルを使って、データを当てはめた。
SEQ ID NO:9および10、SEQ ID NO:11および12、SEQ ID NO:13および14、ならびにSEQ ID NO:15および16によって規定される融合ポリペプチドの薬物動態と、参照用のSEQ ID NO:3および4の薬物動態との分析を、カニクイザルにおいて行った。雄カニクイザルに、用量3mg/kgの試験物を、60分かけて静脈内注入した。15分、2時間、4時間、8時間、24時間、48時間、3日、4日、5日、6日、7日、9日、11日、14日、18日、および24日の時点において、カニクイザルから血漿試料を得た。薬物レベルは、標的HER2およびCD137によって完全な二重特異性コンストラクトを検出するサンドイッチELISAを使って決定した。トラスツズマブの血漿中レベルは、標的HER2およびヒトFcによるサンドイッチELISAを使って決定した。Prism GraphPad 5ソフトウェアを使用し、2コンパートメントモデルを使って、データを当てはめた。
人間における抗薬物抗体形成のリスクを調べるために、二重特異性融合ポリペプチドSEQ ID NO:9および10、SEQ ID NO:11および12、SEQ ID NO:13および14、SEQ ID NO:15および16、ならびに参照用のSEQ ID NO:3および4、SEQ ID NO:3および4の対照抗体、そして陽性対照キーホールリンペットヘモシアニン(KLH)のインビトロT細胞免疫原性評価を行った。この実験を行うために、世界人口における分布を反映するHLAアロタイプをカバーするように選択された32人のドナーのPBMCを融解し、洗浄し、1ウェルあたり3×105細胞の密度で96ウェルプレート上に播種した。アッセイ培地に希釈した試験物を、30μg/mLの濃度で細胞に加えた。ブランクとしてはアッセイ培地のみを使用し、キーホールリンペットヘモシアニン(KLH)をナイーブ陽性対照として使用した。PBMCを、湿潤雰囲気中、37℃および5%CO2で、7日間インキュベートした。7日目に、PBMCを表面表現型CD3+およびCD4+マーカーについて標識すると共に、DNAに取り込まれたEdU(5-エチニル-2'デオキシウリジン)(細胞増殖マーカーとして使用)について標識した。Guava easyCyte 8HTフローサイトメーターを使ってCD3+CD4+EdU+増殖細胞のパーセンテージを測定し、GuavaSoft InCyteソフトウェアを使って分析した。
インビボマウスモデルにおけるSEQ ID NO:9および10、SEQ ID NO:11および12、SEQ ID NO:13および14、ならびにSEQ ID NO:32および33の活性を調べるために、本発明者らは、ヒトSK-OV-3腫瘍およびヒトPBMCが移植された免疫不全NOGマウス(Taconic、NOD/Shi-scid/IL-2Rγnull)を使用した。
本発明者らは、標的細胞に基づくレポーターアッセイを使って、CD137およびHER2に同時に結合する能力を有するSEQ ID NO:9および10の融合ポリペプチドの、標的細胞のHER2状態に依存してCD137経路を活性化する能力を評価した。この目的のために、本発明者らは、NF-κB-luc2P/4-1BB Jurkat細胞(Promega、CS196002)(これは、CD137を過剰発現するように工学的に操作されており、NF-κBルシフェラーゼレポーター遺伝子を保因している)と混合されたHER2高発現性NCI-N87胃がん細胞を使用した。比較のために本発明者らは、SEQ ID NO:32および33ならびにSEQ ID NO:34および35のリファレンス抗CD137モノクローナル抗体の挙動を調べた。本発明者らは、陰性対照として、SEQ ID NO:3および4の単一特異性HER2結合抗体を使用した。さらなる対照として、本発明者らは、SEQ ID NO:9および10の融合ポリペプチド、SEQ ID NO:32および33ならびにSEQ ID NO:34および35の抗CD137モノクローナル抗体、そしてSEQ ID NO:3および4の単一特異性HER2結合抗体について、NCI-N87細胞非存在下でのCD137経路活性化も評価した。最後に、試験物の添加なしでも、この実験を実行した(「媒体対照」)。NCI-N87細胞のみの存在下で測定されるバックグラウンドシグナルを、NF-κB-luc2P/4-1BB Jurkat細胞が加えられていないウェルで評価した。この実験では、NCI-N87細胞をディッシュ上で終夜培養した。翌日、新たに融解したNF-κB-luc2P/4-1BB Jurkat細胞(Promega、CS196002)を、被覆表面上、さまざまな濃度のSEQ ID NO:9および10の融合ポリペプチド、リファレンス抗体SEQ ID NO:32および33ならびにSEQ ID NO:34および35、SEQ ID NO:3および4の対照抗体の存在下、または試験物の添加なしで、6時間インキュベートした。本発明者らは、読み出し情報として、Bio-Glo(商標)緩衝液(Promega、G7940)の添加によって誘発されるJurkatレポーター細胞上のルミネセンスを測定した。以下にこの実験を詳述する。
実施例14と類似するプロトコールで、HER2陽性腫瘍細胞(SKOV-3)を移植した免疫無防備状態のマウスにヒトPBMCを注射し、3週間にわたって、100μg/週または20μg/週のSEQ ID NO:9および10、抗CD137抗体SEQ ID NO:32および33、または媒体とPBMCである対照(「PBMCのみ」)、PBMCなしの媒体である対照(「PBMCなし」)、もしくはアイソタイプ対照とPBMCである対照で処置した。具体的には、NOGマウスにSK-OV-3細胞を皮下(s.c.)注射し、腫瘍を平均で120mm3まで成長させてから、処置群にランダムに割り当てた。1つの処置群につき10匹とした。マウスの尾静脈に新鮮ヒトPBMCを静脈内(i.v.)移植し、1時間後に処置を開始した。マウスには、SEQ ID NO:9および10またはSEQ ID NO:32および33または対照の処置(20μgまたは100μg)を、週3回、腹腔内(i.p.)に施行した。腫瘍成長を週に2回記録した。処置後20日目に2匹のマウスから腫瘍を収穫し、ヒトT細胞の浸潤を、ヒトリンパ球マーカーCD45に関する染色による免疫組織化学検査によって評価した。
SEQ ID NO:9および10の安全性を評価するために、実験16のマウスのマウス血液試料からPBMCを単離した。これらの試料を、PBMC移植後の19日目に採取し、ヒト表面マーカーCD45、CD3およびCD8に関するマルチカラーFACSによって分析した。末梢血を10mlの1×赤血球溶解緩衝液(0.15M NH4Cl、10mM KHCO3、0.1mM EDTA)に再懸濁し、15mlチューブ中、室温で1〜3分、溶解した。細胞を300×g、4℃で10分、遠心分離し、10mlのFC緩衝液(PBS中の2%ウシ胎児血清、pH7.4)で1回洗浄し、200μlのFC緩衝液に再懸濁した。細胞を5×105細胞/ウェルの密度で96ウェルプレートに移した。プレートを400×g、4℃で3分遠心分離することによって細胞をペレット化し、上清を除去した。Fc-ブロック抗体(2.4G2抗体(0.5mg/ml、#553142-BD Bioscience)を緩衝液に1:100希釈したもの、10μl/ウェル)を各ウェルに加え、プレートを室温で15分インキュベートした。次に、ヒト標的hCD45(Life Technologies)、hCD3およびhCD8(どちらもBD Bioscience)に対する特異的抗体を加え(0.5〜1μg/試料)、プレートを遮光して4℃で30分インキュベートした。さらに1回の洗浄工程(プレートを400×g、4℃で3分、遠心分離)後、Attune Focusingサイトメーター(青色(488nm)/紫色(405nm)のレーザー構成)で分析するために、細胞を200μlのFC緩衝液に再懸濁した。フローサイトメトリーデータはFlowJoデータ分析ソフトウェアで分析した。
インビボマウスモデルにおけるSEQ ID NO:9および10の活性を調べるために、本発明者らは、ヒトSK-OV-3腫瘍およびヒトPBMCが移植された免疫不全NOGマウス(Taconic、NOD/Shi-scid/IL-2Rγnull)を使用した。受容体HER2およびCD137の単一特異性ターゲティングの効果と二重特異性ターゲティングの効果とを対比して評価するために、単一特異性CD137ターゲティング抗体SEQ ID NO:32および33ならびに単一特異性HER2ターゲティングコンストラクト(IgG4バックボーン)SEQ ID NO:51および52を並行して調べた。
実施例18に記載のインビボ試験のフォローアップ分析において、9つの試験群のそれぞれのうち、5匹または6匹の腫瘍担持マウスから、試験終了時または倫理的屠殺時に腫瘍を切除し、ヒトリンパ球マーカーCD45に関する染色による免疫組織化学検査によって、ヒトT細胞の浸潤について評価した。この目的のために、腫瘍をホルマリン固定し、パラフィンに包埋し、抗ヒトCD45抗体を用いる免疫組織化学検査用に処理した。CD45陽性細胞は、3,3'-ジアミノベンジジン(DAB)染色によって同定した。グレースケール画像中のDAB陽性を明確に視覚化することができるように、画像のコントラストおよび輝度をデジタルに調整した。
SEQ ID NO:9および10の作用様式をさらに解明し、その安全性を評価するために、実験18のマウスの血液試料から、PBMCを単離した。これらの試料は、試験終了時のマウス屠殺後または倫理的屠殺後の最終採血によって採取し、ヒト表面マーカーCD45およびCD8についてマルチカラーFACSによって分析した。末梢血を10mlの1×赤血球溶解緩衝液(0.15M NH4Cl, 10mM KHCO3、0.1mM EDTA)に再懸濁し、15mlチューブ中、室温で1〜3分、溶解した。細胞を300×g、4℃で10分、遠心分離し、10mlのFC緩衝液(PBS中の2%ウシ胎児血清、pH7.4)で1回洗浄し、200μlのFC緩衝液に再懸濁した。細胞を5×105細胞/ウェルの密度で96ウェルプレートに移した。プレートを400×g、4℃で3分遠心分離することによって細胞をペレット化し、上清を除去した。Fc-ブロック抗体(2.4G2抗体(0.5mg/ml、#553142-BD Bioscience)を緩衝液に1:100希釈したもの、10μl/ウェル)を各ウェルに加え、プレートを室温で15分インキュベートした。次に、ヒト標的hCD45(Life Technologies)およびhCD8(BD Bioscience)に対する特異的抗体を加え(0.5〜1μg/試料)、プレートを遮光して4℃で30分インキュベートした。さらに1回の洗浄工程(プレートを400×g、4℃で3分、遠心分離)後、Attune Focusingサイトメーター(青色(488nm)/紫色(405nm)レーザー構成)で分析するために、細胞を200μlのFC緩衝液に再懸濁した。フローサイトメトリーデータはFlowJoデータ分析ソフトウェアで分析した。
Claims (36)
- CD137にもHer2/neuにも結合する能力を有する融合ポリペプチドであって、少なくとも2つのサブユニットを任意の順序で含み、第1サブユニットは完全長免疫グロブリンまたはその抗原結合ドメインを含み、この第1結合ドメインはHER2/neuに対する結合特異性を有し、かつ第2サブユニットはCD137に対する結合特異性を有するリポカリンムテインを含み、該リポカリンムテインのアミノ酸配列が、SEQ ID NO:2、32〜38、および39〜46からなる群より選択されるアミノ酸配列に対して少なくとも90%の配列同一性を有する、融合ポリペプチド。
- 4nM以下のEC50値でCD137およびHER2/neuに同時に結合する能力を有する、請求項1記載の融合ポリペプチド。
- T細胞応答を共刺激する能力を有し、かつ/またはT細胞増殖を誘発する能力を有する、請求項1または2記載の融合ポリペプチド。
- 前記ムテインが、成熟ヒト涙液リポカリンの直鎖ポリペプチド配列(SEQ ID NO:18)の配列位置5、26〜31、33〜34、42、46、52、56、58、60〜61、65、71、85、94、101、104〜106、108、111、114、121、133、148、150および153に少なくとも1つの変異アミノ酸残基を含む、請求項1〜3のいずれか一項記載の融合ポリペプチド。
- 前記リポカリンムテインのアミノ酸配列が、成熟ヒト涙液リポカリンの直鎖ポリペプチド配列(SEQ ID NO:18)との比較において以下の変異アミノ酸残基:
Ala 5 → ValまたはThr, Arg 26 → Glu, Glu 27 → Gly, Phe 28 → Cys, Pro 29 → Arg, Glu 30 → Pro, Met 31 → Trp, Leu 33 → Ile, Glu 34 → Phe, Thr 42 → Ser, Gly 46 → Asp, Lys 52 → Glu, Leu 56 → Ala, Ser 58 → Asp, Arg 60 → Pro, Cys 61 → Ala, Lys 65 → ArgまたはAsn, Thr 71 → Ala, Val 85 → Asp, Lys 94 → ArgまたはGlu, Cys 101 → Ser, Glu 104 → Val, Leu 105 → Cys, His 106 → Asp, Lys 108 → Ser, Arg 111 → Pro, Lys 114 → Trp, Lys 121 → Glu, Ala 133 → Thr, Arg 148 → Ser, Ser 150 → IleおよびCys 153 → Ser
のうちの少なくとも1つを含む、請求項4記載の融合ポリペプチド。 - 前記ムテインのアミノ酸配列が、成熟ヒト涙液リポカリンの直鎖ポリペプチド配列(SEQ ID NO:18)との比較において、以下の変異アミノ酸残基の組:
(a)Arg 26 → Glu, Glu 27 → Gly, Phe 28 → Cys, Pro 29 → Arg, Glu 30 → Pro, Met 31 → Trp, Leu 33 → Ile, Glu 34 → Phe, Leu 56 → Ala, Ser 58 → Asp, Arg 60 → Pro, Cys 61 → Ala, Cys 101 → Ser, Glu 104 → Val, Leu 105 → Cys, His 106 → Asp, Lys 108 → Ser, Arg 111 → Pro, Lys 114 → Trpおよび Cys 153 → Ser;
(b)Ala 5 → Thr, Arg 26 → Glu, Glu 27 → Gly, Phe 28 → Cys, Pro 29 → Arg, Glu 30 → Pro, Met 31 → Trp, Leu 33 → Ile, Glu 34 → Phe, Leu 56 → Ala, Ser 58 → Asp, Arg 60 → Pro, Cys 61 → Ala, Lys 65 → Arg, Val 85 → Asp, Cys 101 → Ser, Glu 104 → Val, Leu 105 → Cys, His 106 → Asp, Lys 108 → Ser, Arg 111 → Pro, Lys 114 → Trp, Lys 121 → Glu, Ala 133 → ThrおよびCys 153 → Ser;
(c)Arg 26 → Glu, Glu 27 → Gly, Phe 28 → Cys, Pro 29 → Arg, Glu 30 → Pro, Met 31 → Trp, Leu 33 → Ile, Glu 34 → Phe, Leu 56 → Ala, Ser 58 → Asp, Arg 60 → Pro, Cys 61 → Ala, Lys 65 → Asn, Lys 94 → Arg, Cys 101 → Ser, Glu 104 → Val, Leu 105 → Cys, His 106 → Asp, Lys 108 → Ser, Arg 111 → Pro, Lys 114 → Trp, Lys 121 → Glu, Ala 133 → Thrおよび Cys 153 → Ser;
(d)Ala 5 → Val, Arg 26 → Glu, Glu 27 → Gly, Phe 28 → Cys, Pro 29 → Arg, Glu 30 → Pro, Met 31 → Trp, Leu 33 → Ile, Glu 34 → Phe, Leu 56 → Ala, Ser 58 → Asp, Arg 60 → Pro, Cys 61 → Ala, Lys 65 → Arg, Lys 94 → Glu, Cys 101 → Ser, Glu 104 → Val, Leu 105 → Cys, His 106 → Asp, Lys 108 → Ser, Arg 111 → Pro, Lys 114 → Trp, Lys 121 → Glu, Ala 133 → ThrおよびCys 153 → Ser;
(e)Arg 26 → Glu, Glu 27 → Gly, Phe 28 → Cys, Pro 29 → Arg, Glu 30 → Pro, Met 31 → Trp, Leu 33 → Ile, Glu 34 → Phe, Thr 42 → Ser, Leu 56 → Ala, Ser 58 → Asp, Arg 60 → Pro, Cys 61 → Ala, Cys 101 → Ser, Glu 104 → Val, Leu 105 → Cys, His 106 → Asp, Lys 108 → Ser, Arg 111 → Pro, Lys 114 → Trp, Ser 150 → IleおよびCys 153 → Ser;
(f)Arg 26 → Glu, Glu 27 → Gly, Phe 28 → Cys, Pro 29 → Arg, Glu 30 → Pro, Met 31 → Trp, Leu 33 → Ile, Glu 34 → Phe, Lys 52 → Glu, Leu 56 → Ala, Ser 58 → Asp, Arg 60 → Pro, Cys 61 → Ala, Thr 71 → Ala, Cys 101 → Ser, Glu 104 → Val, Leu 105 → Cys, His 106 → Asp, Lys 108 → Ser, Arg 111 → Pro, Lys 114 → Trp, Ala 133 → Thr, Arg 148 → Ser, Ser 150 → IleおよびCys 153 → Ser; または
(g)Ala 5 → Thr, Arg 26 → Glu, Glu 27 → Gly, Phe 28 → Cys, Pro 29 → Arg, Glu 30 → Pro, Met 31 → Trp, Leu 33 → Ile, Glu 34 → Phe, Gly 46 → Asp, Leu 56 → Ala, Ser 58 → Asp, Arg 60 → Pro, Cys 61 → Ala, Thr 71 → Ala, Cys 101 → Ser, Glu 104 → Val, Leu 105 → Cys, His 106 → Asp, Lys 108 → Ser, Arg 111 → Pro, Lys 114 → Trp, Ser 150 → IleおよびCys 153 → Ser
のうちの1つを含む、請求項4または5記載の融合ポリペプチド。 - 前記リポカリンムテインのアミノ酸配列が、SEQ ID NO:32〜38からなる群より選択されるアミノ酸配列に対して少なくとも95%の配列同一性を有するか、または
SEQ ID NO:32〜38からなる群より選択されるアミノ酸配列またはそのフラグメントのアミノ酸配列を含む、
請求項4〜6のいずれか一項記載の融合ポリペプチド。 - 前記リポカリンムテインが、成熟ヒトリポカリン2(hNGAL)の直鎖ポリペプチド配列(SEQ ID NO:17)の配列位置28、36、40〜41、49、52、65、68、70、72〜73、77、79、81、83、87、94、96、100、103、106、125、127、132および134に少なくとも1つの変異アミノ酸残基を含む、請求項1〜3のいずれか一項記載の融合ポリペプチド。
- 前記リポカリンムテインのアミノ酸配列が、成熟hNGALの直鎖ポリペプチド配列(SEQ ID NO:17)との比較において、以下の変異アミノ酸残基:
Gln 28 → His, Leu 36 → Gln, Ala 40 → Ile, Ile 41 → ArgまたはLys, Gln 49 → Val, Ile, His, SerまたはAsn, Tyr 52 → Met, Asn 65 → Asp, Ser 68 → Met, AlaまたはGly, Leu 70 → Ala, Lys, SerまたはThr, Arg 72 → Asp, Lys 73 → Asp, Asp 77 → Met, Arg, ThrまたはAsn, Trp 79 → AlaまたはAsp, Arg 81 → Met, TrpまたはSer, Phe 83 → Leu, Cys 87 → Ser, Leu 94 → Phe, Asn 96 → Lys, Tyr 100 → Phe, Leu 103 → His, Tyr 106 → Ser, Lys 125 → Phe, Ser 127 → Phe, Tyr 132 → GluおよびLys 134 → Tyr
のうちの少なくとも1つを含む、請求項8記載の融合ポリペプチド。 - 前記リポカリンムテインのアミノ酸配列が、成熟hNGALの直鎖ポリペプチド配列(SEQ ID NO:17)との比較において、以下の変異アミノ酸残基の組:
(a)Gln 28 → His, Leu 36 → Gln, Ala 40 → Ile, Ile 41 → Lys, Gln 49 → Asn, Tyr 52 → Met, Ser 68 → Gly, Leu 70 → Thr, Arg 72 → Asp, Lys 73 → Asp, Asp 77 → Thr, Trp 79 → Ala, Arg 81 → Ser, Cys 87 → Ser, Asn 96 → Lys, Tyr 100 → Phe, Leu 103 → His, Tyr 106 → Ser, Lys 125 → Phe, Ser 127 → Phe, Tyr 132 → GluおよびLys 134 → Tyr;
(b)Gln 28 → His, Leu 36 → Gln, Ala 40 → Ile, Ile 41 → Arg, Gln 49 → Ile, Tyr 52 → Met, Asn 65 → Asp, Ser 68 → Met, Leu 70 → Lys, Arg 72 → Asp, Lys 73 → Asp, Asp 77 → Met, Trp 79 → Asp, Arg 81 → Trp, Cys 87 → Ser, Asn 96 → Lys, Tyr 100 → Phe, Leu 103 → His, Tyr 106 → Ser, Lys 125 → Phe, Ser 127 → Phe, Tyr 132 → GluおよびLys 134 → Tyr;
(c)Gln 28 → His, Leu 36 → Gln, Ala 40 → Ile, Ile 41 → Arg, Gln 49 → Asn, Tyr 52 → Met, Asn 65 → Asp, Ser 68 → Ala, Leu 70 → Ala, Arg 72 → Asp, Lys 73 → Asp, Asp 77 → Thr, Trp 79 → Asp, Arg 81 → Trp, Cys 87 → Ser, Asn 96 → Lys, Tyr 100 → Phe, Leu 103 → His, Tyr 106 → Ser, Lys 125 → Phe, Ser 127 → Phe, Tyr 132 → GluおよびLys 134 → Tyr;
(d)Gln 28 → His, Leu 36 → Gln, Ala 40 → Ile, Ile 41 → Lys, Gln 49 → Asn, Tyr 52 → Met, Asn 65 → Asp, Ser 68 → Ala, Leu 70 → Ala, Arg 72 → Asp, Lys 73 → Asp, Asp 77 → Thr, Trp 79 → Asp, Arg 81 → Trp, Cys 87 → Ser, Asn 96 → Lys, Tyr 100 → Phe, Leu 103 → His, Tyr 106 → Ser, Lys 125 → Phe, Ser 127 → Phe, Tyr 132 → GluおよびLys 134 → Tyr;
(e)Gln 28 → His, Leu 36 → Gln, Ala 40 → Ile, Ile 41 → Lys, Gln 49 → Ser, Tyr 52 → Met, Asn 65 → Asp, Ser 68 → Gly, Leu 70 → Ser, Arg 72 → Asp, Lys 73 → Asp, Asp 77 → Thr, Trp 79 → Ala, Arg 81 → Met, Cys 87 → Ser, Asn 96 → Lys, Tyr 100 → Phe, Leu 103 → His, Tyr 106 → Ser, Lys 125 → Phe, Ser 127 → Phe, Tyr 132 → GluおよびLys 134 → Tyr;
(f)Gln 28 → His, Leu 36 → Gln, Ala 40 → Ile, Ile 41 → Lys, Gln 49 → Val, Tyr 52 → Met, Asn 65 → Asp, Ser 68 → Gly, Leu 70 → Thr, Arg 72 → Asp, Lys 73 → Asp, Asp 77 → Arg, Trp 79 → Asp, Arg 81 → Ser, Cys 87 → Ser, Leu 94 → Phe, Asn 96 → Lys, Tyr 100 → Phe, Leu 103 → His, Tyr 106 → Ser, Lys 125 → Phe, Ser 127 → Phe, Tyr 132 → GluおよびLys 134 → Tyr;
(g)Gln 28 → His, Leu 36 → Gln, Ala 40 → Ile, Ile 41 → Arg, Gln 49 → His, Tyr 52 → Met, Asn 65 → Asp, Ser 68 → Gly, Leu 70 → Thr, Arg 72 → Asp, Lys 73 → Asp, Asp 77 → Thr, Trp 79 → Ala, Arg 81 → Ser, Cys 87 → Ser, Asn 96 → Lys, Tyr 100 → Phe, Leu 103 → His, Tyr 106 → Ser, Lys 125 → Phe, Ser 127 → Phe, Tyr 132 → GluおよびLys 134 → Tyr;
(h)Gln 28 → His, Leu 36 → Gln, Ala 40 → Ile, Ile 41 → Lys, Gln 49 → Asn, Tyr 52 → Met, Asn 65 → Asp, Ser 68 → Gly, Leu 70 → Thr, Arg 72 → Asp, Lys 73 → Asp, Asp 77 → Thr, Trp 79 → Ala, Arg 81 → Ser, Phe 83 → Leu, Cys 87 → Ser, Leu 94 → Phe, Asn 96 → Lys, Tyr 100 → Phe, Leu 103 → His, Tyr 106 → Ser, Lys 125 → Phe, Ser 127 → Phe, Tyr 132 → GluおよびLys 134 → Tyr;または
(i)Gln 28 → His, Leu 36 → Gln, Ala 40 → Ile, Ile 41 → Arg, Gln 49 → Ser, Tyr 52 → Met, Asn 65 → Asp, Ser 68 → Ala, Leu 70 → Thr, Arg 72 → Asp, Lys 73 → Asp, Asp 77 → Asn, Trp 79 → Ala, Arg 81 → Ser, Cys 87 → Ser, Asn 96 → Lys, Tyr 100 → Phe, Leu 103 → His, Tyr 106 → Ser, Lys 125 → Phe, Ser 127 → Phe, Tyr 132 → GluおよびLys 134 → Tyr
のうちの1つを含む、請求項8または9記載の融合ポリペプチド。 - 前記ムテインのアミノ酸配列が、SEQ ID NO:2および39〜46からなる群より選択されるアミノ酸配列に対して少なくとも95%の配列同一性を有する、請求項8〜10のいずれか一項記載の融合ポリペプチド。
- 前記ムテインのアミノ酸配列が、SEQ ID NO:2および39〜46からなる群より選択されるアミノ酸配列またはそのフラグメントのアミノ酸配列を含む、請求項8〜10のいずれか一項記載の融合ポリペプチド。
- 第1サブユニットと第2サブユニットとが、第2サブユニットのリポカリンムテインのN末と第1サブユニットの免疫グロブリンの重鎖定常領域(CH)のC末との間のペプチドリンカーを介して連結されている、請求項1〜12のいずれか一項記載の融合ポリペプチド。
- 第3サブユニットが、第3サブユニットのリポカリンムテインのN末と第1サブユニットの免疫グロブリンの軽鎖定常領域(CL)のC末との間でペプチドリンカーを介して第1サブユニットに連結されている、請求項1〜13のいずれか一項記載の融合ポリペプチド。
- SEQ ID NO:19に示すアミノ酸配列を含む、請求項1〜14のいずれか一項記載の融合ポリペプチド。
- リポカリンムテインがSEQ ID NO:2に示すアミノ酸配列を含む、請求項1〜15のいずれか一項記載の融合ポリペプチド。
- 免疫グロブリンがトラスツズマブまたはペルツズマブである、請求項1〜15のいずれか一項記載の融合ポリペプチド。
- 免疫グロブリンがSEQ ID NO:3および4によって与えられる重鎖および軽鎖を有する、請求項1〜15のいずれか一項記載の融合ポリペプチド。
- 免疫グロブリンがIgG4バックボーンを有する、請求項1〜15のいずれか一項記載の融合ポリペプチド。
- IgG4バックボーンが、S228P、N297A、F234A、およびL235Aからなる群より選択される突然変異のうちのいずれか1つを有する、請求項19記載の融合ポリペプチド。
- SEQ ID NO:5および6に示すアミノ酸配列を含む、請求項1〜3のいずれか一項記載の融合ポリペプチド。
- SEQ ID NO:7および8に示すアミノ酸配列を含む、請求項1〜3のいずれか一項記載の融合ポリペプチド。
- SEQ ID NO:9および10に示すアミノ酸配列を含む、請求項1〜3のいずれか一項記載の融合ポリペプチド。
- SEQ ID NO:11および12に示すアミノ酸配列を含む、請求項1〜3のいずれか一項記載の融合ポリペプチド。
- SEQ ID NO:13および14に示すアミノ酸配列を含む、請求項1〜3のいずれか一項記載の融合ポリペプチド。
- SEQ ID NO:15および16に示すアミノ酸配列を含む、請求項1〜3のいずれか一項記載の融合ポリペプチド。
- 請求項1〜26のいずれか一項記載のポリペプチドをコードするヌクレオチド配列を含む核酸分子。
- 請求項1〜26のいずれか一項記載の融合ポリペプチドを生産する方法であって、融合ポリペプチドが、ムテインをコードする核酸から出発して生産される、方法。
- CD137の下流シグナリング経路を活性化し、同時にHER2/neu陽性腫瘍細胞に会合(engage)するのに使用するための、請求項1〜26のいずれか一項記載の融合ポリペプチドまたはそのような融合ポリペプチドを含む組成物。
- T細胞を共刺激し、同時にHER2/neu陽性腫瘍細胞に会合するのに使用するための、請求項1〜26のいずれか一項記載の融合ポリペプチドまたはそのような融合ポリペプチドを含む組成物。
- Tリンパ球増殖を誘発し、同時にHER2/neu陽性腫瘍細胞に会合するのに使用するための、請求項1〜26のいずれか一項記載の融合ポリペプチドまたはそのような融合ポリペプチドを含む組成物。
- CD137クラスター化誘発性の活性化T細胞をHER2/neu陽性腫瘍細胞へ方向づけるのに使用するための、請求項1〜26のいずれか一項記載の融合ポリペプチドまたはそのような融合ポリペプチドを含む組成物。
- HER2/neu陽性腫瘍細胞の近傍において局所的T細胞応答を誘発するのに使用するための、請求項1〜26のいずれか一項記載の融合ポリペプチドまたはそのような融合ポリペプチドを含む組成物。
- HER2/neu陽性腫瘍細胞の近傍において局所的ナチュラルキラー細胞応答を誘発するのに使用するための、請求項1〜26のいずれか一項記載の融合ポリペプチドまたはそのような融合ポリペプチドを含む組成物。
- HER2/neu陽性腫瘍細胞の近傍においてT細胞によるIL-2および/またはIFNガンマの生産を誘発するのに使用するための、請求項1〜26のいずれか一項記載の融合ポリペプチドまたはそのような融合ポリペプチドを含む組成物。
- HER2/ner陽性がんの防止、回復、または治療に使用するための、請求項1〜26のいずれか一項記載の融合ポリペプチドまたはそのような融合ポリペプチドを含む組成物。
Applications Claiming Priority (13)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP15166179.0 | 2015-05-04 | ||
| EP15166179 | 2015-05-04 | ||
| EP15167917.2 | 2015-05-18 | ||
| EP15167917 | 2015-05-18 | ||
| EP15002702 | 2015-09-17 | ||
| EP15002702.7 | 2015-09-17 | ||
| EP15192870 | 2015-11-04 | ||
| EP15192870.2 | 2015-11-04 | ||
| EP16150705.8 | 2016-01-11 | ||
| EP16150705 | 2016-01-11 | ||
| EP16000862.9 | 2016-04-15 | ||
| EP16000862 | 2016-04-15 | ||
| PCT/EP2016/060041 WO2016177802A1 (en) | 2015-05-04 | 2016-05-04 | Anti-cancer fusion polypeptide |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2018515085A JP2018515085A (ja) | 2018-06-14 |
| JP2018515085A5 JP2018515085A5 (ja) | 2019-06-06 |
| JP6783797B2 true JP6783797B2 (ja) | 2020-11-11 |
Family
ID=55948826
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2017557310A Active JP6783797B2 (ja) | 2015-05-04 | 2016-05-04 | 抗がん融合ポリペプチド |
Country Status (14)
| Country | Link |
|---|---|
| US (2) | US10865250B2 (ja) |
| EP (2) | EP3292148B1 (ja) |
| JP (1) | JP6783797B2 (ja) |
| KR (1) | KR20170138574A (ja) |
| CN (2) | CN107636014B (ja) |
| AU (1) | AU2016258977C1 (ja) |
| BR (1) | BR112017020434A2 (ja) |
| CA (1) | CA2980840A1 (ja) |
| HK (1) | HK1249526A1 (ja) |
| MX (1) | MX2017014083A (ja) |
| RU (1) | RU2727165C2 (ja) |
| SG (1) | SG11201708334RA (ja) |
| WO (1) | WO2016177802A1 (ja) |
| ZA (1) | ZA201705961B (ja) |
Families Citing this family (37)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2936611A1 (en) * | 2014-01-13 | 2015-07-16 | Pieris Pharmaceuticals Gmbh | Multi-specific polypeptide useful for localized tumor immunomodulation |
| NZ736560A (en) * | 2015-05-04 | 2021-12-24 | Pieris Pharmaceuticals Gmbh | Proteins specific for cd137 |
| EP4219535A1 (en) | 2015-05-18 | 2023-08-02 | Pieris Pharmaceuticals GmbH | Anti-cancer fusion polypeptide |
| AR106188A1 (es) | 2015-10-01 | 2017-12-20 | Hoffmann La Roche | Anticuerpos anti-cd19 humano humanizados y métodos de utilización |
| WO2017220555A1 (en) | 2016-06-20 | 2017-12-28 | F-Star Beta Limited | Lag -3 binding members |
| CA3027612A1 (en) | 2016-06-20 | 2017-12-28 | F-Star Delta Limited | Binding molecules binding pd-l1 and lag-3 |
| GB201612520D0 (en) | 2016-07-19 | 2016-08-31 | F-Star Beta Ltd | Binding molecules |
| CR20190309A (es) * | 2017-01-03 | 2019-08-21 | Hoffmann La Roche | Moleculas de unión de3 antígeno biespecíficas que comprenden el clon 20h4.9 anti-4-1bb |
| GB201700345D0 (en) * | 2017-01-09 | 2017-02-22 | F-Star Beta Ltd | Conditional agonists of immune responses |
| WO2018134279A1 (en) * | 2017-01-18 | 2018-07-26 | Pieris Pharmaceuticals Gmbh | Novel fusion polypeptides specific for lag-3 and pd-1 |
| EP3585431A4 (en) * | 2017-02-24 | 2020-12-16 | MacroGenics, Inc. | BISPECIFIC BINDING MOLECULES CAPABLE OF BINDING TO CD137 AND TUMOR ANTIGENS, AND THEIR USES |
| MY202336A (en) | 2017-07-11 | 2024-04-24 | Compass Therapeutics Llc | Agonist antibodies that bind human cd137 and uses thereof |
| US11718679B2 (en) | 2017-10-31 | 2023-08-08 | Compass Therapeutics Llc | CD137 antibodies and PD-1 antagonists and uses thereof |
| CN118667027A (zh) * | 2017-11-13 | 2024-09-20 | 克雷森多生物制剂有限公司 | 结合至cd137和psma的分子 |
| WO2019100052A2 (en) | 2017-11-20 | 2019-05-23 | Compass Therapeutics Llc | Cd137 antibodies and tumor antigen-targeting antibodies and uses thereof |
| US11548948B2 (en) | 2017-12-19 | 2023-01-10 | F-Star Therapeutics Limited | FC binding fragments comprising a PD-L1 antigen-binding site |
| TWI841551B (zh) * | 2018-03-13 | 2024-05-11 | 瑞士商赫孚孟拉羅股份公司 | 使用靶向4-1bb (cd137)之促效劑的組合療法 |
| TW202003462A (zh) | 2018-03-26 | 2020-01-16 | 德商4Sc製藥公司 | 用於癌症療法的包括hdac抑制劑和cd137激動劑之組合 |
| CR20200459A (es) * | 2018-04-13 | 2020-11-11 | Hoffmann La Roche | Moléculas de unión a antígeno dirigidas a her2 que comprendan 4-1bbl |
| GB201811404D0 (en) | 2018-07-12 | 2018-08-29 | F Star Beta Ltd | Anti-CD137 Antibodies |
| US20220049007A1 (en) | 2018-07-12 | 2022-02-17 | F-Star Beta Limited | Antibody molecules that bind pd-l1 and cd137 |
| GB201811408D0 (en) | 2018-07-12 | 2018-08-29 | F Star Beta Ltd | CD137 Binding Molecules |
| CA3100119A1 (en) * | 2018-07-31 | 2020-02-06 | Pieris Pharmaceuticals Gmbh | Fusion protein specific for cd137 and pd-l1 |
| KR20210052468A (ko) * | 2018-08-27 | 2021-05-10 | 피어이스 파마슈티컬즈 게엠베하 | Cd137/her2 이중특이적 제제 및 pd-1 축 억제제를 포함하는 조합물 치료요법 및 이의 용도 |
| MA55069A (fr) * | 2019-02-26 | 2022-01-05 | Pieris Pharmaceuticals Gmbh | Nouvelles protéines de fusion spécifique à cd137 et gpc3 |
| JP2022526367A (ja) * | 2019-03-29 | 2022-05-24 | ピエリス ファーマシューティカルズ ゲーエムベーハー | リポカリンムテインの吸入投与 |
| JP7301155B2 (ja) * | 2019-04-12 | 2023-06-30 | エフ・ホフマン-ラ・ロシュ・アクチェンゲゼルシャフト | リポカリンムテインを含む二重特異性抗原結合分子 |
| BR112022001336A8 (pt) * | 2019-07-26 | 2023-02-07 | Abl Bio Inc | Anticorpo biespecífico anti-her2/anti-4-1bb e uso do mesmo |
| EP4054718A1 (en) | 2019-11-04 | 2022-09-14 | Pieris Pharmaceuticals GmbH | Her2/4-1bb bispecific fusion proteins for the treatment of cancer |
| EP4110826A4 (en) * | 2020-02-28 | 2024-08-14 | Shanghai Henlius Biotech Inc | ANTI-CD137 CONSTRUCTS, MULTISPECIFIC ANTIBODIES AND THEIR USES |
| WO2022029496A1 (en) * | 2020-08-07 | 2022-02-10 | Eutilex Co., Ltd. | Anti-her2 / anti-4-1bb bispecific antibodies and uses thereof |
| EP4213946A1 (en) | 2020-09-18 | 2023-07-26 | Pieris Pharmaceuticals GmbH | Biomarker methods and uses |
| KR20220107968A (ko) * | 2021-01-25 | 2022-08-02 | 주식회사유한양행 | 항-4-1bb/항-her2 이중특이적 항체의 정제방법 |
| CA3211591A1 (en) | 2021-03-23 | 2022-09-29 | Markus Zettl | Her2/4-1bb bispecific fusion proteins for the treatment of cancer |
| WO2022200478A1 (en) | 2021-03-24 | 2022-09-29 | Pieris Pharmaceuticals Gmbh | Tumor treatment with a 4-1bb/her2-bispecific agent and a her2-targeted tyrosine kinase inhibitor |
| WO2023180523A1 (en) | 2022-03-24 | 2023-09-28 | Pieris Pharmaceuticals Gmbh | Process for purifying fusion proteins |
| WO2024085166A1 (ja) * | 2022-10-19 | 2024-04-25 | アステラス製薬株式会社 | がん治療におけるpd-1シグナル阻害剤との組み合わせによる抗cldn4-抗cd137二重特異性抗体の使用 |
Family Cites Families (53)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4376110A (en) | 1980-08-04 | 1983-03-08 | Hybritech, Incorporated | Immunometric assays using monoclonal antibodies |
| ATE76311T1 (de) | 1986-08-19 | 1992-06-15 | Genentech Inc | Einrichtung und dispersion zum intrapulmonalen eingeben von polypeptidwuchsstoffen und zytokinen. |
| JPH01215289A (ja) | 1988-02-22 | 1989-08-29 | Toa Nenryo Kogyo Kk | 遺伝子組換えによる正常ヒト血清アルブミンaの製造方法 |
| FR2649991B2 (fr) | 1988-08-05 | 1994-03-04 | Rhone Poulenc Sante | Utilisation de derives stables du plasmide pkd1 pour l'expression et la secretion de proteines heterologues dans les levures du genre kluyveromyces |
| US5728553A (en) | 1992-09-23 | 1998-03-17 | Delta Biotechnology Limited | High purity albumin and method of producing |
| ES2245780T3 (es) | 1994-05-18 | 2006-01-16 | Nektar Therapeutics | Metodos y composiciones para la formulacion de interferones como un polvo seco. |
| DE4417598A1 (de) | 1994-05-19 | 1995-12-14 | Max Planck Gesellschaft | Verwendung des Tetracyclinpromotors zur stringent regulierten Produktion von rekombinanten Proteinen in prokaryontischen Zellen |
| AU5132096A (en) | 1995-01-30 | 1996-08-21 | Terrapin Technologies, Inc. | Glubodies - multiplicities of proteins capable of binding a variety of small molecules |
| US5908621A (en) | 1995-11-02 | 1999-06-01 | Schering Corporation | Polyethylene glycol modified interferon therapy |
| US6620413B1 (en) | 1995-12-27 | 2003-09-16 | Genentech, Inc. | OB protein-polymer chimeras |
| DE19641876B4 (de) | 1996-10-10 | 2011-09-29 | Iba Gmbh | Streptavidinmuteine |
| WO1998016873A1 (fr) | 1996-10-14 | 1998-04-23 | Firm Forsat Ltd. | Procede de preparation de dispersions a base de composants chromogenes |
| US20030171551A1 (en) | 1997-01-31 | 2003-09-11 | Joseph D. Rosenblatt | Chimeric antibody fusion proteins for the recruitment and stimulation of an antitumor immune response |
| WO1999007740A2 (en) | 1997-08-06 | 1999-02-18 | Zymogenetics, Inc. | Lipocalin homologs |
| US20140080177A1 (en) | 1997-09-26 | 2014-03-20 | Pieris Ag | Anticalins |
| DE19742706B4 (de) | 1997-09-26 | 2013-07-25 | Pieris Proteolab Ag | Lipocalinmuteine |
| GB9722131D0 (en) | 1997-10-20 | 1997-12-17 | Medical Res Council | Method |
| CA2233725A1 (en) | 1998-03-31 | 1999-09-30 | Hemosol Inc. | Hemoglobin-hydroxyethyl starch complexes |
| PL192364B1 (pl) | 1998-06-08 | 2006-10-31 | Hoffmann La Roche | Zastosowanie koniugatu PEG-IFN-α 2A w połączeniu z rybawiryną |
| US6403564B1 (en) | 1998-10-16 | 2002-06-11 | Schering Corporation | Ribavirin-interferon alfa combination therapy for eradicating detectable HCV-RNA in patients having chronic hepatitis C infection |
| CA2343917A1 (en) | 1998-10-19 | 2000-04-27 | Ariad Gene Therapeutics, Inc. | Materials and methods involving conditional retention domains |
| DE19926068C1 (de) | 1999-06-08 | 2001-01-11 | Arne Skerra | Muteine des Bilin-Bindungsproteins |
| CA2440582A1 (en) | 2001-03-09 | 2002-10-03 | Dyax Corp. | Serum albumin binding moieties |
| WO2003029462A1 (en) | 2001-09-27 | 2003-04-10 | Pieris Proteolab Ag | Muteins of human neutrophil gelatinase-associated lipocalin and related proteins |
| CA2464690A1 (en) | 2001-09-27 | 2003-04-10 | Pieris Proteolab Ag | Muteins of apolipoprotein d |
| AU2003264100A1 (en) | 2003-08-25 | 2005-03-10 | Pieris Proteolab Ag | Muteins of a bilin-binding protein with affinity for a given target |
| AU2003275958A1 (en) | 2003-08-25 | 2005-03-10 | Pieris Proteolab Ag | Muteins of tear lipocalin |
| US7288638B2 (en) | 2003-10-10 | 2007-10-30 | Bristol-Myers Squibb Company | Fully human antibodies against human 4-1BB |
| JP2007284351A (ja) | 2004-07-27 | 2007-11-01 | Osaka Bioscience Institute | アミロイド蛋白質の凝集を抑制する物質とその作用 |
| US7892827B2 (en) | 2004-11-26 | 2011-02-22 | Pieris Ag | Compound with affinity for the cytotoxic T lymphocyte-associated antigen (CTLA-4) |
| WO2007038619A2 (en) | 2005-09-27 | 2007-04-05 | Amunix, Inc. | Proteinaceous pharmaceuticals and uses thereof |
| EP2046820B1 (en) * | 2006-08-01 | 2010-10-20 | Pieris AG | Muteins of tear lipocalin and methods for obtaining the same |
| EP2235053A1 (en) | 2007-10-19 | 2010-10-06 | Abbott Laboratories | Glycosylated mammalian ngal and use thereof |
| GB2468232B (en) | 2007-11-30 | 2012-10-24 | Glaxo Group Ltd | Antigen-bindng constructs |
| EP2262531A1 (en) | 2008-03-08 | 2010-12-22 | Immungene, Inc. | Engineered fusion molecules immunotherapy in cancer and inflammatory diseases |
| AU2009264214B2 (en) * | 2008-06-24 | 2013-06-06 | Technische Universitaet Muenchen | Muteins of hNGAL and related proteins with affinity for a given target |
| WO2010097394A1 (en) | 2009-02-24 | 2010-09-02 | Glaxo Group Limited | Multivalent and/or multispecific rankl-binding constructs |
| BRPI1013807A2 (pt) | 2009-05-28 | 2019-09-24 | Glaxo Group Ltd | composição, uso de uma composição, antagonista, sequência de polinucleotídeo, célula hospedeira recombinante transformada ou transfectada, método para a produção de uma composição, método para prevenir ou tratar um paciente, molécula de ligação de antígeno de marcação dual, e, proteína de ligação de antígeno. |
| IN2012DN00407A (ja) | 2009-08-05 | 2015-08-21 | Pieris Ag | |
| EP3660510A3 (en) | 2009-12-07 | 2020-07-08 | Pieris Pharmaceuticals GmbH | Muteins of human lipocalin 2 (lcn2, hngal) with affinity for a given target |
| DK2542590T4 (da) * | 2010-03-05 | 2020-07-13 | Univ Johns Hopkins | Sammensætninger og fremgangsmåde til målrettede immunomodulatoriske antistof-fer og fusionproteiner |
| CN103154023B (zh) | 2010-08-16 | 2017-04-05 | 皮里斯制药有限公司 | 铁调素的结合蛋白 |
| JP6100694B2 (ja) | 2010-11-15 | 2017-03-22 | ピエリス ファーマシューティカルズ ゲーエムベーハー | グリピカン−3(gpc3)に対して親和性を有するヒトリポカリン2の突然変異タンパク質 |
| EP2646552B1 (en) | 2010-12-02 | 2017-07-05 | Pieris Pharmaceuticals GmbH | Muteins of human lipocalin 2 with affinity for ctla-4 |
| PT3489254T (pt) * | 2012-04-30 | 2022-12-30 | Biocon Ltd | Proteínas de fusão direcionadas/imunomoduladoras e seus métodos de fabrico |
| CA2936611A1 (en) | 2014-01-13 | 2015-07-16 | Pieris Pharmaceuticals Gmbh | Multi-specific polypeptide useful for localized tumor immunomodulation |
| EA037654B1 (ru) * | 2014-12-30 | 2021-04-27 | Селджин Корпорейшн | Анти-cd47-антитела и их применения |
| US11382963B2 (en) | 2015-01-12 | 2022-07-12 | Pieris Pharmaceuticals Gmbh | Engineered T cells and uses therefor |
| EP3250586B1 (en) | 2015-01-28 | 2021-10-27 | Pieris Pharmaceuticals GmbH | Novel proteins specific for angiogenesis |
| WO2016131804A1 (en) | 2015-02-18 | 2016-08-25 | Sanofi | Novel proteins specific for pyoverdine and pyochelin |
| NZ736560A (en) | 2015-05-04 | 2021-12-24 | Pieris Pharmaceuticals Gmbh | Proteins specific for cd137 |
| BR112017020961A2 (pt) | 2015-05-18 | 2018-07-10 | Pieris Pharmaceuticals Gmbh | muteína, molécula de ácido nucleico, célula hospedeira, método de produção de uma muteína e método de ligação |
| TW201725212A (zh) | 2015-12-10 | 2017-07-16 | 第一三共股份有限公司 | 特異性於降鈣素基因相關胜肽的新穎蛋白 |
-
2016
- 2016-05-04 SG SG11201708334RA patent/SG11201708334RA/en unknown
- 2016-05-04 RU RU2017135596A patent/RU2727165C2/ru active
- 2016-05-04 CN CN201680025273.9A patent/CN107636014B/zh active Active
- 2016-05-04 KR KR1020177034820A patent/KR20170138574A/ko not_active Application Discontinuation
- 2016-05-04 CN CN202111366682.4A patent/CN114316067A/zh active Pending
- 2016-05-04 US US15/571,561 patent/US10865250B2/en active Active
- 2016-05-04 WO PCT/EP2016/060041 patent/WO2016177802A1/en active Application Filing
- 2016-05-04 BR BR112017020434A patent/BR112017020434A2/pt active Search and Examination
- 2016-05-04 EP EP16721154.9A patent/EP3292148B1/en active Active
- 2016-05-04 AU AU2016258977A patent/AU2016258977C1/en active Active
- 2016-05-04 EP EP24151494.2A patent/EP4378962A3/en active Pending
- 2016-05-04 CA CA2980840A patent/CA2980840A1/en active Pending
- 2016-05-04 JP JP2017557310A patent/JP6783797B2/ja active Active
- 2016-05-04 MX MX2017014083A patent/MX2017014083A/es unknown
-
2017
- 2017-09-01 ZA ZA2017/05961A patent/ZA201705961B/en unknown
-
2018
- 2018-06-22 HK HK18107992.3A patent/HK1249526A1/zh unknown
-
2020
- 2020-11-12 US US17/096,750 patent/US20210198380A1/en active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| CN114316067A (zh) | 2022-04-12 |
| EP4378962A2 (en) | 2024-06-05 |
| EP3292148A1 (en) | 2018-03-14 |
| AU2016258977A1 (en) | 2017-11-30 |
| AU2016258977C1 (en) | 2022-07-14 |
| JP2018515085A (ja) | 2018-06-14 |
| CA2980840A1 (en) | 2016-11-10 |
| MX2017014083A (es) | 2018-11-09 |
| SG11201708334RA (en) | 2017-11-29 |
| RU2727165C2 (ru) | 2020-07-21 |
| US20210198380A1 (en) | 2021-07-01 |
| ZA201705961B (en) | 2023-12-20 |
| EP3292148B1 (en) | 2024-01-24 |
| BR112017020434A2 (pt) | 2018-06-26 |
| KR20170138574A (ko) | 2017-12-15 |
| HK1249526A1 (zh) | 2018-11-02 |
| CN107636014A (zh) | 2018-01-26 |
| WO2016177802A1 (en) | 2016-11-10 |
| RU2017135596A3 (ja) | 2019-09-16 |
| RU2017135596A (ru) | 2019-06-04 |
| EP4378962A3 (en) | 2024-07-31 |
| AU2016258977B2 (en) | 2022-03-17 |
| CN107636014B (zh) | 2021-12-07 |
| US20190010248A1 (en) | 2019-01-10 |
| US10865250B2 (en) | 2020-12-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6783797B2 (ja) | 抗がん融合ポリペプチド | |
| US11919931B2 (en) | Anti-cancer fusion polypeptide capable of binding both CD137 and glypican-3 (GPC3) | |
| JP6041799B2 (ja) | Trailr2特異的多量体足場 | |
| TW202126683A (zh) | T細胞調節多肽及其使用方法 | |
| JP7303391B2 (ja) | バイアス型il2ムテイン、方法、および組成物 | |
| JP2023511274A (ja) | Il2オルソログおよび使用法 | |
| JP2023510870A (ja) | Icd statシグナル伝達が改変されたcd122 | |
| US20230366884A1 (en) | Biomarker methods and uses | |
| WO2024064713A1 (en) | Novel fusion protein specific for cd137 and cd228 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20171106 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20190424 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20190424 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20200427 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200716 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20201014 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20201022 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6783797 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| S531 | Written request for registration of change of domicile |
Free format text: JAPANESE INTERMEDIATE CODE: R313531 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |