JP6781989B2 - 微粒子検出システム及び微粒子検出プログラム - Google Patents
微粒子検出システム及び微粒子検出プログラム Download PDFInfo
- Publication number
- JP6781989B2 JP6781989B2 JP2017514177A JP2017514177A JP6781989B2 JP 6781989 B2 JP6781989 B2 JP 6781989B2 JP 2017514177 A JP2017514177 A JP 2017514177A JP 2017514177 A JP2017514177 A JP 2017514177A JP 6781989 B2 JP6781989 B2 JP 6781989B2
- Authority
- JP
- Japan
- Prior art keywords
- fine particles
- unit
- zeta potential
- particle
- flow path
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 239000010419 fine particle Substances 0.000 title claims description 266
- 238000001514 detection method Methods 0.000 title claims description 110
- 239000002245 particle Substances 0.000 claims description 293
- 210000001808 exosome Anatomy 0.000 claims description 153
- 238000005286 illumination Methods 0.000 claims description 122
- 238000011156 evaluation Methods 0.000 claims description 67
- 239000012530 fluid Substances 0.000 claims description 51
- 210000002472 endoplasmic reticulum Anatomy 0.000 claims description 39
- 238000003860 storage Methods 0.000 claims description 37
- 239000000126 substance Substances 0.000 claims description 36
- 230000003287 optical effect Effects 0.000 claims description 34
- 238000004364 calculation method Methods 0.000 claims description 31
- 230000009870 specific binding Effects 0.000 claims description 23
- 238000009434 installation Methods 0.000 claims description 20
- 238000009826 distribution Methods 0.000 claims description 17
- 230000008859 change Effects 0.000 claims description 16
- 238000003384 imaging method Methods 0.000 claims description 12
- 230000005653 Brownian motion process Effects 0.000 claims description 4
- 238000005537 brownian motion Methods 0.000 claims description 4
- 230000001678 irradiating effect Effects 0.000 claims description 4
- 238000006243 chemical reaction Methods 0.000 claims description 2
- 238000004458 analytical method Methods 0.000 description 23
- 238000001962 electrophoresis Methods 0.000 description 18
- 230000009471 action Effects 0.000 description 17
- 238000010586 diagram Methods 0.000 description 16
- 239000000463 material Substances 0.000 description 16
- 210000004027 cell Anatomy 0.000 description 15
- 238000000034 method Methods 0.000 description 15
- 230000005012 migration Effects 0.000 description 12
- 238000013508 migration Methods 0.000 description 12
- 239000000523 sample Substances 0.000 description 12
- 239000012488 sample solution Substances 0.000 description 12
- 230000027455 binding Effects 0.000 description 10
- 230000004907 flux Effects 0.000 description 10
- 230000033001 locomotion Effects 0.000 description 9
- 230000008569 process Effects 0.000 description 9
- 230000000704 physical effect Effects 0.000 description 8
- 108090000623 proteins and genes Proteins 0.000 description 8
- 201000010099 disease Diseases 0.000 description 7
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 7
- 238000002372 labelling Methods 0.000 description 7
- 102000004169 proteins and genes Human genes 0.000 description 7
- 230000004520 agglutination Effects 0.000 description 6
- 230000005684 electric field Effects 0.000 description 6
- 230000006870 function Effects 0.000 description 6
- 108091023037 Aptamer Proteins 0.000 description 5
- 230000002776 aggregation Effects 0.000 description 5
- 238000004220 aggregation Methods 0.000 description 5
- 230000005540 biological transmission Effects 0.000 description 5
- 239000007853 buffer solution Substances 0.000 description 5
- 230000007423 decrease Effects 0.000 description 5
- 230000007246 mechanism Effects 0.000 description 5
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 4
- 239000000427 antigen Substances 0.000 description 4
- 108091007433 antigens Proteins 0.000 description 4
- 102000036639 antigens Human genes 0.000 description 4
- 210000004369 blood Anatomy 0.000 description 4
- 239000008280 blood Substances 0.000 description 4
- 230000003247 decreasing effect Effects 0.000 description 4
- 239000003446 ligand Substances 0.000 description 4
- 229910052751 metal Inorganic materials 0.000 description 4
- 239000002184 metal Substances 0.000 description 4
- 230000036961 partial effect Effects 0.000 description 4
- 238000003825 pressing Methods 0.000 description 4
- 238000012545 processing Methods 0.000 description 4
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 3
- 230000005856 abnormality Effects 0.000 description 3
- 230000002411 adverse Effects 0.000 description 3
- 238000005516 engineering process Methods 0.000 description 3
- 239000000284 extract Substances 0.000 description 3
- 150000002632 lipids Chemical class 0.000 description 3
- 239000007788 liquid Substances 0.000 description 3
- 238000005259 measurement Methods 0.000 description 3
- 239000012528 membrane Substances 0.000 description 3
- 108090000765 processed proteins & peptides Proteins 0.000 description 3
- 239000000243 solution Substances 0.000 description 3
- 229920001059 synthetic polymer Polymers 0.000 description 3
- 210000002700 urine Anatomy 0.000 description 3
- YBJHBAHKTGYVGT-ZKWXMUAHSA-N (+)-Biotin Chemical compound N1C(=O)N[C@@H]2[C@H](CCCCC(=O)O)SC[C@@H]21 YBJHBAHKTGYVGT-ZKWXMUAHSA-N 0.000 description 2
- 241000894006 Bacteria Species 0.000 description 2
- 102100027221 CD81 antigen Human genes 0.000 description 2
- 102100037904 CD9 antigen Human genes 0.000 description 2
- 101000914479 Homo sapiens CD81 antigen Proteins 0.000 description 2
- UQSXHKLRYXJYBZ-UHFFFAOYSA-N Iron oxide Chemical compound [Fe]=O UQSXHKLRYXJYBZ-UHFFFAOYSA-N 0.000 description 2
- 206010028980 Neoplasm Diseases 0.000 description 2
- PXHVJJICTQNCMI-UHFFFAOYSA-N Nickel Chemical compound [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 2
- 108010079855 Peptide Aptamers Proteins 0.000 description 2
- 108700031126 Tetraspanins Proteins 0.000 description 2
- 102000043977 Tetraspanins Human genes 0.000 description 2
- 241000700605 Viruses Species 0.000 description 2
- 230000001640 apoptogenic effect Effects 0.000 description 2
- 239000011324 bead Substances 0.000 description 2
- 201000011510 cancer Diseases 0.000 description 2
- 210000000170 cell membrane Anatomy 0.000 description 2
- 238000004891 communication Methods 0.000 description 2
- 239000000470 constituent Substances 0.000 description 2
- 238000003745 diagnosis Methods 0.000 description 2
- 239000004205 dimethyl polysiloxane Substances 0.000 description 2
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 2
- 238000012377 drug delivery Methods 0.000 description 2
- 230000008030 elimination Effects 0.000 description 2
- 238000003379 elimination reaction Methods 0.000 description 2
- RWSXRVCMGQZWBV-WDSKDSINSA-N glutathione Chemical compound OC(=O)[C@@H](N)CCC(=O)N[C@@H](CS)C(=O)NCC(O)=O RWSXRVCMGQZWBV-WDSKDSINSA-N 0.000 description 2
- 229910052742 iron Inorganic materials 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 150000002739 metals Chemical class 0.000 description 2
- 239000000693 micelle Substances 0.000 description 2
- 108091008104 nucleic acid aptamers Proteins 0.000 description 2
- 239000002953 phosphate buffered saline Substances 0.000 description 2
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 2
- 229920000435 poly(dimethylsiloxane) Polymers 0.000 description 2
- 229920000642 polymer Polymers 0.000 description 2
- 108020003175 receptors Proteins 0.000 description 2
- 102000005962 receptors Human genes 0.000 description 2
- 230000002829 reductive effect Effects 0.000 description 2
- 210000003296 saliva Anatomy 0.000 description 2
- 230000003248 secreting effect Effects 0.000 description 2
- 230000028327 secretion Effects 0.000 description 2
- 239000000725 suspension Substances 0.000 description 2
- 108090001008 Avidin Proteins 0.000 description 1
- 102100025222 CD63 antigen Human genes 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- 108091006027 G proteins Proteins 0.000 description 1
- 102000030782 GTP binding Human genes 0.000 description 1
- 108091000058 GTP-Binding Proteins 0.000 description 1
- 108010024636 Glutathione Proteins 0.000 description 1
- 102000005720 Glutathione transferase Human genes 0.000 description 1
- 108010070675 Glutathione transferase Proteins 0.000 description 1
- 229930186217 Glycolipid Natural products 0.000 description 1
- 102000012215 HSC70 Heat-Shock Proteins Human genes 0.000 description 1
- 108010036652 HSC70 Heat-Shock Proteins Proteins 0.000 description 1
- 101000934368 Homo sapiens CD63 antigen Proteins 0.000 description 1
- 101000738354 Homo sapiens CD9 antigen Proteins 0.000 description 1
- 102000015696 Interleukins Human genes 0.000 description 1
- 108010063738 Interleukins Proteins 0.000 description 1
- 108010052285 Membrane Proteins Proteins 0.000 description 1
- 108010006519 Molecular Chaperones Proteins 0.000 description 1
- 208000008589 Obesity Diseases 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 239000004793 Polystyrene Substances 0.000 description 1
- 108020004459 Small interfering RNA Proteins 0.000 description 1
- 108010090804 Streptavidin Proteins 0.000 description 1
- 210000001744 T-lymphocyte Anatomy 0.000 description 1
- 230000002159 abnormal effect Effects 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 210000004381 amniotic fluid Anatomy 0.000 description 1
- 210000003719 b-lymphocyte Anatomy 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 238000001574 biopsy Methods 0.000 description 1
- 229960002685 biotin Drugs 0.000 description 1
- 235000020958 biotin Nutrition 0.000 description 1
- 239000011616 biotin Substances 0.000 description 1
- 210000001124 body fluid Anatomy 0.000 description 1
- 239000010839 body fluid Substances 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 239000012930 cell culture fluid Substances 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- 239000012228 culture supernatant Substances 0.000 description 1
- 210000004443 dendritic cell Anatomy 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 206010012601 diabetes mellitus Diseases 0.000 description 1
- 239000003937 drug carrier Substances 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 229920001971 elastomer Polymers 0.000 description 1
- 239000000806 elastomer Substances 0.000 description 1
- 210000001163 endosome Anatomy 0.000 description 1
- 210000000416 exudates and transudate Anatomy 0.000 description 1
- 239000007850 fluorescent dye Substances 0.000 description 1
- 230000004927 fusion Effects 0.000 description 1
- 238000010353 genetic engineering Methods 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 229960003180 glutathione Drugs 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 239000010931 gold Substances 0.000 description 1
- 229910052737 gold Inorganic materials 0.000 description 1
- 235000020256 human milk Nutrition 0.000 description 1
- 210000004251 human milk Anatomy 0.000 description 1
- 230000002706 hydrostatic effect Effects 0.000 description 1
- 238000011900 installation process Methods 0.000 description 1
- 230000010354 integration Effects 0.000 description 1
- 230000002452 interceptive effect Effects 0.000 description 1
- 238000010030 laminating Methods 0.000 description 1
- 239000004816 latex Substances 0.000 description 1
- 229920000126 latex Polymers 0.000 description 1
- 230000005389 magnetism Effects 0.000 description 1
- 230000003211 malignant effect Effects 0.000 description 1
- 108091070501 miRNA Proteins 0.000 description 1
- 239000002679 microRNA Substances 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004770 neurodegeneration Effects 0.000 description 1
- 208000015122 neurodegenerative disease Diseases 0.000 description 1
- 108010087904 neutravidin Proteins 0.000 description 1
- 229910052759 nickel Inorganic materials 0.000 description 1
- 108020004707 nucleic acids Proteins 0.000 description 1
- 102000039446 nucleic acids Human genes 0.000 description 1
- 150000007523 nucleic acids Chemical class 0.000 description 1
- 235000020824 obesity Nutrition 0.000 description 1
- 239000011146 organic particle Substances 0.000 description 1
- 230000002093 peripheral effect Effects 0.000 description 1
- 239000008055 phosphate buffer solution Substances 0.000 description 1
- 229910052697 platinum Inorganic materials 0.000 description 1
- 230000010287 polarization Effects 0.000 description 1
- -1 polydimethylsiloxane Polymers 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 229920002223 polystyrene Polymers 0.000 description 1
- 102000004196 processed proteins & peptides Human genes 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 239000004065 semiconductor Substances 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 210000002966 serum Anatomy 0.000 description 1
- 239000000377 silicon dioxide Substances 0.000 description 1
- 229920002379 silicone rubber Polymers 0.000 description 1
- 239000004945 silicone rubber Substances 0.000 description 1
- 210000001082 somatic cell Anatomy 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 210000004881 tumor cell Anatomy 0.000 description 1
- 238000000108 ultra-filtration Methods 0.000 description 1
- 238000005199 ultracentrifugation Methods 0.000 description 1
- 239000013603 viral vector Substances 0.000 description 1
- 229910052727 yttrium Inorganic materials 0.000 description 1
- 238000000733 zeta-potential measurement Methods 0.000 description 1
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume, or surface-area of porous materials
- G01N15/10—Investigating individual particles
- G01N15/14—Electro-optical investigation, e.g. flow cytometers
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume, or surface-area of porous materials
- G01N15/10—Investigating individual particles
- G01N15/14—Electro-optical investigation, e.g. flow cytometers
- G01N15/1429—Electro-optical investigation, e.g. flow cytometers using an analyser being characterised by its signal processing
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume, or surface-area of porous materials
- G01N15/02—Investigating particle size or size distribution
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume, or surface-area of porous materials
- G01N15/02—Investigating particle size or size distribution
- G01N15/0205—Investigating particle size or size distribution by optical means, e.g. by light scattering, diffraction, holography or imaging
- G01N15/0227—Investigating particle size or size distribution by optical means, e.g. by light scattering, diffraction, holography or imaging using imaging, e.g. a projected image of suspension; using holography
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume, or surface-area of porous materials
- G01N15/10—Investigating individual particles
- G01N15/14—Electro-optical investigation, e.g. flow cytometers
- G01N15/1484—Electro-optical investigation, e.g. flow cytometers microstructural devices
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N27/00—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means
- G01N27/26—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means by investigating electrochemical variables; by using electrolysis or electrophoresis
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume, or surface-area of porous materials
- G01N2015/0042—Investigating dispersion of solids
- G01N2015/0053—Investigating dispersion of solids in liquids, e.g. trouble
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume, or surface-area of porous materials
- G01N15/10—Investigating individual particles
- G01N2015/1006—Investigating individual particles for cytology
-
- G01N2015/1027—
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume, or surface-area of porous materials
- G01N15/10—Investigating individual particles
- G01N15/14—Electro-optical investigation, e.g. flow cytometers
- G01N2015/1486—Counting the particles
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume, or surface-area of porous materials
- G01N15/10—Investigating individual particles
- G01N15/14—Electro-optical investigation, e.g. flow cytometers
- G01N2015/1493—Particle size
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Immunology (AREA)
- Biochemistry (AREA)
- Analytical Chemistry (AREA)
- Physics & Mathematics (AREA)
- General Health & Medical Sciences (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Dispersion Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Molecular Biology (AREA)
- Biomedical Technology (AREA)
- Urology & Nephrology (AREA)
- Hematology (AREA)
- Signal Processing (AREA)
- Biotechnology (AREA)
- Cell Biology (AREA)
- Electrochemistry (AREA)
- Microbiology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Food Science & Technology (AREA)
- Medicinal Chemistry (AREA)
- Investigating Or Analysing Materials By Optical Means (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
Description
本願は、2015年4月21日に,日本に出願された特願2015−087021号に基づき優先権を主張し,その内容をここに援用する。
本発明は、媒質中に存在する細胞外小胞体などの微粒子のゼータ電位と、微粒子径との相関を判定することができる微粒子検出システム及び微粒子検出プログラムを提供する。
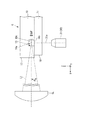
図1は、実施形態に係る粒子検出システム1の概略的な平面図である。図2は、実施形態に係る粒子検出装置100の概略的な正面図である。
本実施形態における流体デバイスCは、一例として、検体を分析する際に用いられる電気泳動分析チップである。検体となる微粒子としては、細胞、細菌、ウィルス、細胞外小胞体(細胞外ベシクル)、合成高分子、無機物、若しくは金属を基材とする微粒子、磁性微粒子、高分子ミセル構造を有する微粒子等が挙げられる。合成高分子を基材とする微粒子としては、例えばポリスチレン等のラテックス粒子が挙げられる。無機物を基材とする微粒子としては、例えばシリカ粒子が挙げられる。金属を基材とする微粒子としては、例えば鉄製ビーズが挙げられる。磁性微粒子としては、例えば鉄、酸化鉄、ニッケル等を含む磁性を有するビーズが挙げられる。合成高分子、無機物、若しくは金属を基材とする微粒子、及び磁性微粒子のいずれも、ペプチド、タンパク質、細胞、各種化合物等で表面を修飾された粒子を含む。
本実施形態では、電気泳動分析チップとして、細胞外小胞体を分析するための細胞外小胞体分析チップを用いる場合について説明する。本明細書において、細胞外小胞体とは、エクソソーム(エキソソーム)、アポトーシス小体、マイクロベシクル等を含む、脂質小胞を意味するものとする。細胞外小胞体の大きさは直径30nmから1μm程度である。細胞外小胞体は、細胞の分泌物であり、その表面に分泌源の細胞由来のタンパク質を発現している。
以下に、エクソソームを分析する場合を例として、本実施形態に係る細胞外小胞体分析チップ(電気泳動分析チップ)について説明する。
エクソソームは、直径30〜200nm程度の脂質小胞であり、エンドソームと細胞膜との融合体として、腫瘍細胞、樹状細胞、T細胞、B細胞等、種々の細胞から、血液、尿、唾液等の体液中に分泌される。
生体内に存在する癌細胞等の異常細胞は、その細胞膜に特有のタンパク質を発現している。エクソソームは細胞の分泌物であり、その表面に分泌源の細胞由来のタンパク質を発現している。
細胞外小胞体分析チップを用いたエクソソームの分析は、一例として次のようにして行うことができる。まず、検出対象のエクソソームを精製する。次に、エクソソームと特異的結合物質とを接触させる。ここで、特異的結合物質とは、エクソソームの表面に存在する分子に特異的に結合することができる物質を意味し、詳細は後述する。次に、細胞外小胞体分析チップを用いて、エクソソームのゼータ電位を計測し、分析を行う。本分析は、エクソソームに限らず、広く細胞外小胞体一般の分析にも適用できる。
特異的結合物質としては、例えば、抗体、改変抗体、アプタマー、リガンド分子等が挙げられる。抗体としては、IgG、IgA、IgD、IgE、IgM等が挙げられる。IgGとしては、IgG1、IgG2、IgG3、IgG4等が挙げられる。IgAとしては、IgA1、IgA2等が挙げられる。IgMとしては、IgM1、IgM2等が挙げられる。改変抗体としては、Fab、F(ab’)2、scFv等が挙げられる。アプタマーとしては、ペプチドアプタマー、核酸アプタマー等が挙げられる。リガンド分子としては、エクソソームの表面に存在する検出対象分子が、レセプタータンパク質である場合の、当該レセプタータンパク質のリガンド等が挙げられる。例えば、エクソソームの表面に存在する分子がインターロイキンである場合、リガンド分子としてはGタンパク質等が挙げられる。
本分析の各工程について説明する。まず、エクソソームを含有する試料から該エクソソームを精製する。試料としては、目的に応じて、血液、尿、母乳、気管支肺胞洗浄液、羊水、悪性滲出液、唾液、細胞培養液等が挙げられる。中でも、血液及び尿からは、エクソソームを精製しやすい。
次に、エクソソームと特異的結合物質(抗体、アプタマー等)とを接触させる。エクソソームの表面に検出対象の分子が存在した場合、特異的結合物質−エクソソーム複合体が形成される。特異的結合物質を適切に選択することにより、例えば、癌、肥満、糖尿病、神経変性疾患等の疾患に関連する異常を検出することができる。また、例えば人工的に膜表面にあるペプチドやタンパク質を発現させたエクソソームに対し、そのペプチドやタンパク質に対して特異的に結合する特異的結合物質を用いるなど、機能を改変したエクソソームを評価することもできる。
一例として、特異的結合物質として抗体を使用した場合について説明する。エクソソームと抗体とを反応させた後、抗体と反応させたエクソソームのゼータ電位を計測する。ゼータ電位とは、溶液中の微粒子の表面電荷である。例えば、エクソソームが負に帯電しているのに対し、抗体は正に帯電している。このため、抗体−エクソソーム複合体のゼータ電位は、エクソソーム単独のゼータ電位と比較して正にシフトしている。したがって、抗体と反応させたエクソソームのゼータ電位を測定することによって、エクソソームの膜表面における抗原の発現を検出することができる。これは、抗体に限らず、正に帯電した特異的結合物質でも同様である。
エクソソームの粒子径dは、一例として、細胞外小胞体分析チップのマイクロ流路内で、エクソソームの電気泳動を行い、エクソソームの電気泳動速度Sを光学的に測定し、測定されたエクソソームの電気泳動速度Sに基づいて、以下の式(2)に示すアインシュタイン・ストークスの式を用いて算出することができる。
図3は、実施形態に係る細胞外小胞体分析チップの基本構造を示す斜視図である。図4は、図3におけるII−II線断面図である。細胞外小胞体分析チップCHは、第1リザーバ110と、第2リザーバ120と、第1リザーバ110と第2リザーバ120とを接続する泳動流路150と、基材160とを備えている。泳動流路150は、例えば、ミリ流路やマイクロ流路である。泳動流路150は、一例として、幅200μm、高さ400μm、長さ10mm程度の大きさである。泳動流路150の断面は矩形でなくてもよく、例えば、円、楕円、多角形、又はトンネル形状としてもよい。泳動流路150は、細胞外小胞体、あるいは、細胞外小胞体の表面に存在する生体分子に特異的に結合する特異的結合物質と細胞外小胞体とが相互作用してなる、特異的結合物質−細胞外小胞体複合体(一例として、抗体−エクソソーム複合体)を電気泳動するものである。特異的結合物質の一例として、抗体、アプタマー、またはこれらの組み合わせからなるものが挙げられる。アプタマーは例えば、核酸アプタマー、ペプチドアプタマーなどである。特異的結合物質が認識する分子としては、例えば抗原、膜タンパク質、核酸、糖鎖、糖脂質等が挙げられる。
図5は、実施形態に係るステージ部STの設置面STaに流体デバイスCが設置された平面図である。図6は、実施形態に係る流体デバイスCをxz平面で部分的に断面した部分断面図である。図7は、図6におけるA−A線断面図である。
この場合、流体デバイスCの積層構造は二層構造となっている。また、例えば、このような流体デバイスCの積層構造は、リザーバ部材10と、底板11とを互いに貼りあわせて形成される。
複数のレーンをレーンごとに順番に分析してもよく、また、複数の検出系によって同時に分析してもよい。なお、複数のレーン2は高さ方向(z方向)に配列されていてもよい。
この場合、溶液は長さ方向(x方向)から注入されてもよく、y方向から注入されてもよい。照射光源は例えば複数あって、それぞれの光源が対応する高さのレーン2を流れる微粒子を照射する。また、少なくとも一つの照射光源から照射方向を変えることでレーン2を流れる微粒子を照射してもよい。
照明光L1は、上述した直交面と交差する方向に延びる光軸に沿って流体デバイスCに照射される。本実施形態では、照明光L1の光軸は、x方向と平行である。本実施形態の照明光L1は、x方向に延びる光軸に沿って流体デバイスCに照射される。
この場合、流路13の位置が異なるチップを用いた場合であっても、流路13内に収光点が位置するように調整することが可能である。また、収光点と流路13の中心とがほぼ一致するように調整してもよく、検出部の中心部と収光点とがほぼ一致するように調整してもよい。
図9は、実施形態に係る調整部CLおよび流体デバイスCの部分詳細図である。調整部CLは、一例として、シリンドリカルレンズで構成される。調整部CLは、照明光L1のz方向の幅が流路13の内部において最小となり、且つ、流路13の照射光入射側の側面16aの位置における照明光L1の通過領域が側面16a内に限定されるように収束する収束角度に調整している。調整部CLは、照明光L1のz方向の幅が流路13の内部において最小となり、且つ、流路13の照射光入射側の側面16aの位置における照明光L1の照射領域が側面16a内に集光するような収束角度に照明光L1を調整している。また、調整部CLは、流路13の照射光射出側の側面16bの位置における照明光L1(照射光束)の通過領域が側面16b内に限定されるように収束する収束角度に調整している。
調整部CLは、流路13の照射光射出側の側面16bの位置における照明光L1(照射光束)の照射領域が側面16b内に集光するような収束角度に照明光L1を調整している。
また、調整部CLは、リザーバ部材10の端面17の位置における照明光L1の照射領域が端面17内に収束する収束角度に調整している。さらに、調整部CLは、照明光L1が流路13内の検出領域において収束点が存在するような収束角に調整している。
例えば、流路13の検出領域において検出部30の焦点深度外の照明光L1の照明光束は焦点深度内の照明光束よりも少なくなるような収束角を有する。なお、例えば、上述の直交面は、リザーバ部材10の端面17、流路13の照射光入射側の側面16a、又は流路13の照射光射出側の側面16bを含む。
n2sinα3=n3sinα4
α1+β1=δ1
α2+β1=δ2
α3+β2=δ2
α4+β2=δ3
α1:自由空間からリザーバ部材10の端面17への照明光L1の入射角
α2:端面17からリザーバ部材10内の照明光L1の出射角
α3:リザーバ部材10内から流路13の壁面16aへの照明光L1の入射角
α4:壁面16aから流路13内部への照明光L1の出射角
β1:端面17の傾斜角
β2:壁面16aの傾斜角
δ1:自由空間においての照明光L1の焦点面Fからの仰角
δ2:リザーバ部材10内においての照明光L1の焦点面Fからの仰角
δ3:流路13内においての照明光L1の焦点面Fからの仰角
n1:自由空間媒質の屈折率
n2:リザーバ部材10材質の屈折率
n3:流路13内の媒質の屈折率
であり、
入射角・出射角:端面17および壁面16aへの垂線からの角度
傾斜角:焦点面Fの垂線からの角度
仰角:焦点面Fからの角度
としている。また、符号は全て反時計回り方向を正とする。
図5に示すように、ステージ部STは、流体デバイスCが設置される設置面STaを備える。設置面STaは、xy平面と平行の面である。設置面STaは、y方向に間隔をあけて配置されている。設置面STaは、流路デバイスCのレーン2が設けられていないy方向の両端部を−Z側から支持する。流体デバイスCは、レーン2が配される領域が検出部30による−Z側からの観察に支障を来すことなく設置面STaに支持される。また、流体デバイスCにおけるレーン2に照射されるまでの照明光L1の光路にステージ部STが存在しないため、流体デバイスCに入射する照明光L1の一部がステージ部STに入射して、後述する粒子検出に悪影響を及ぼすことを抑制できる。
送信部40は、撮像部32で撮像された画像情報を制御装置5へ送信する。
粒子検出装置100の動作は、設置工程、導入工程、照射工程、検出工程を含む。
設置工程は、流体デバイスCをステージ部STの設置面STaに設置する工程である。
具体的には、図5に示したように、押し付けコマ52により流体デバイスCを対角方向に押し付けることにより、流体デバイスCは、固定ピン51a、51bに押し付けられ、流路13(レーン2)がy方向と平行になるように、ステージ部STに位置決めされた状態で設置面STaに設置される。
試料が流路13に導入されたら、制御装置5はステージ駆動部60を駆動して、検出対象となるレーン2が照明光L1の光路および検出部30の検出軸31a上に位置させる。
検出対象となるレーン2が検出位置に移動すると、制御装置5は、電源部BTを制御して電極18A及び電極18Bに電界を印加させ、エクソソームを流路13に沿って電気泳動させる力を付与する。一例として、制御装置5は、約50V/cmの電界強度の電圧を約10秒間印加する。エクソソームの移動方向は、y方向と平行である。
照明光L1を照射する照射部20および調整部CLは、y方向の幅が一定で、上述した式(3)〜式(8)を満足する収束角θでz方向に収束するシートビーム状の照明光L1を照射する。照明光L1の最小ビーム厚(z方向のビーム幅)は、一例として、10μmである。照明光L1の最小ビーム厚(z方向のビーム幅)方向は、図7および図9のz方向またはz方向と平行な方向である。照明光L1の最小ビーム厚(z方向のビーム幅)方向は、入射面(端面17および側面16a)における照明光L1の光軸方向及び流路方向とは異なる方向であり、該光軸方向及び流路方向と直交する方向である。流路方向は、流路13が延在する方向である。流路方向は、流路13を流体が流れる方向である。
照射された照明光L1は、流体デバイスCの一方の端面(照明光入射側端面)17、流路13の側面(照明光入射側側面)16a、流路13の内部、流路13の側面(照明光射出側側面)16b、流体デバイスCの他方の端面(照明光射出側端面)27(図5参照)を順次通過する。照明光L1は、エクソソームの移動方向と直交する方向に照射される。
照射された照明光L1は、図9に示すように、流路13の内部においてz方向の幅が最小となるように収束し、且つ、流路13の側面16aの位置における照射光束の通過領域が側面16a内に限定されるように収束する。さらに、照射された照明光L1は、流路13の照明光射出側の側面16bの位置における照射光束の通過領域が側面16a内に限定されるように収束する。照明光L1は、側面16aの位置における照射領域が側面16a内に集光し、側面16bの位置における照射領域が側面16b内に集光するような収束角に調整されている。また、照射された照明光L1は、流路13における検出部30の検出領域において収束点が存在する。
制御装置5は、粒子検出システム1を統括的に制御する。制御装置5は、ステージ駆動部60を介してステージ部STおよび流体デバイスCの移動を制御する。制御装置5は、電源部(印加部)BTを制御して、電極18A、18Bに流路13に沿った方向の電界を印加させる。また、制御装置5は、粒子検出装置100が撮像した画像を処理することにより、種々の判定を行う。この制御装置5の構成の詳細について、図11から図16を参照して説明する。
ゼータ電位判定部503は、上述の式(1)に基づいてゼータ電位ζを判定する。なお、この一例では、サンプル溶液の誘電率ε及びサンプル溶液の粘性係数ηは、予め記憶部520に記憶されている。ゼータ電位判定部503は、記憶部520に記憶されているサンプル溶液の誘電率ε及びサンプル溶液の粘性係数ηと、識別部502によるトラッキング結果から求めた微粒子の移動速度とに基づいて、微粒子のゼータ電位ζを判定する。
このように、本実施形態によれば、媒質中に存在する微粒子の状態の相関を判定することができる。
エクソソームの特徴として、粒径が直径30〜200nm程度の微粒子であること、そしてまた、構成因子としてシャペロン分子であるHsc70、Hsc90やテトラスパニン(CD9, CD63, CD81)が特異的に存在していることが挙げられる。
この場合、記憶部520には、粒子径のしきい値Thdが、基準範囲情報として記憶されている。また、記憶部520には、ゼータ電位のしきい値Thζが、基準範囲情報として記憶されている。これらの場合、記憶部520を基準記憶部と言い換えてもよい。このしきい値Thd、及びしきい値Thζの一例を図14に示す。
具体的には、この一例の場合、記憶部520には、粒子径のしきい値Thdとして、100nmが記憶されている。また、記憶部520には、ゼータ電位のしきい値Thζとして、−6mVが記憶されている。状態判定部506は、粒子相関リストLS2に記憶されている粒子相関情報PCのうち、粒子径dが、しきい値Thd以下である微粒子であり、かつ、ゼータ電位ζがしきい値Thζ以下である微粒子を、エクソソームであると判定する。一方、状態判定部506は、粒子相関リストLS2に記憶されている粒子相関情報PCのうち、粒子径dが、しきい値Thdを超える微粒子や、ゼータ電位ζが、しきい値Thζを超える微粒子を、エクソソームでないと判定する。
また、直径が200nmよりも大きい範囲には、単一のエクソソームが含まれていない場合がある。この場合には、粒子径のしきい値Thd(200nm)は、微粒子が単一のエクソソームであるか否かを判定するための一要素として、利用することができる。
また、直径が200nmよりも大きい範囲には、単一のエクソソームが複数個凝集した微粒子が含まれている場合がある。この場合には、粒子径のしきい値Thd(200nm)は、微粒子が単一のエクソソームであるか、凝集したエクソソームであるかを判定するための一要素として、利用することができる。
このように、基準記憶部において記憶される基準値となるしきい値を、微粒子の状態の判定のための要因として用いることができる。
ここで、粒子径dが200nm以下の微粒子をエクソソームであると判定する場合を一例にして説明する。粒子径判定部504は、抗体−エクソソーム複合体を直径が200nmを超える微粒子であると判定することがある。このため、状態判定部506が粒子径dのみによって判定した場合には、抗体−エクソソーム複合体の粒子径dが、エクソソームであるか否かの粒子径dのしきい値Thdを超えるため、抗体−エクソソーム複合体がエクソソームではないと判定される場合がある。そこで、状態判定部506は、粒子径dが200nm以下の微粒子をエクソソームであると判定するとともに、粒子径dが200nmを超える微粒子であっても、ゼータ電位ζがしきい値Thζ以下である場合には、その微粒子をエクソソームであると判定する。つまり、状態判定部506は、粒子径dのしきい値Thdとゼータ電位ζのしきい値Thζとを組み合わせて、微粒子がエクソソームであるか否かを判定する。
つまり、エクソソームに対して抗体を作用させることによるゼータ電位ζ及び粒子径dの、それぞれの変化に基づいて、微粒子がエクソソームであるか否かを判定することができる。
本実施形態の粒子検出システム1は、ゼータ電位ζ及び粒子径dに基づく、上述のような評価条件を様々に組み合わせて、微粒子の評価を行うことができる利点を有する。
次に、図15を参照して、制御装置5の動作について説明する。
図15は、本実施形態の制御装置5の動作の一例を示す図である。ここでは、粒子検出装置100が、所定の時間間隔によって側方散乱光の画像を撮像する場合について説明する。
相関部505は、関連付けした結果を示す粒子相関リストLS2を生成し、生成した粒子相関リストLS2を記憶部520に記憶させる。相関部505は、すべての微粒子について関連付けが終了していないと判定した場合(ステップS80;NO)には、処理をステップS40に戻す。相関部505は、すべての微粒子について関連付けが終了したと判定した場合(ステップS80;YES)には、処理をステップS90に進める。
評価部507は、微粒子に対して物質を作用させる前の粒子径及びゼータ電位の分布と、作用させた後の粒子径及びゼータ電位の分布とを比較評価することができる。具体例として、微粒子がヒト繊維肉芽腫由来のエクソソームである場合に、評価部507は、このエクソソームに抗CD81抗体を作用させた場合の粒子径及びゼータ電位の分布を評価する。この具体例の場合、相関部505は、抗CD81抗体を作用させる前のエクソソームについて、ゼータ電位ζと、粒子径dとを関連付けて、粒子相関リストLS2−1を生成する。次に、相関部505は、抗CD81抗体を作用させた後のエクソソームについて、ゼータ電位ζと、粒子径dとを関連付けて、粒子相関リストLS2−2を生成する。評価部507は、抗CD81抗体を作用させる前のエクソソームについての粒子相関リストLS2−1と、抗CD81抗体を作用させた後のエクソソームについての粒子相関リストLS2−2とに基づいて、図15に示すように、粒子径及びゼータ電位の分布を出力する。
これまで、粒子径及びゼータ電位の評価のしきい値は、予め定められているとして説明した。評価部507は、微粒子の状態に基づいて、評価のしきい値を算出する構成であってもよい。具体例として、評価部507が、物質を作用させる前のエクソソームの状態に基づいて、評価のしきい値を算出し、この算出したしきい値に基づいて、物質を作用させた後のエクソソームについて評価する場合について、図17から図19を参照して説明する。
計数部508は、基準範囲情報が示す粒子径のしきい値Thd及びゼータ電位のしきい値Thζによって区分される領域毎に、当該領域に含まれる細胞外小胞体の数を計数する。ここで、領域の一例には、図14を参照して説明した、領域DM1〜領域DM4がある。
比率算出部509は、計数部508が計数する細胞外小胞体の数の、領域間の比率を算出する。具体的には、比率算出部509は、計数部508が計数した細胞外小胞体の数を100%とした場合の、各領域内の細胞外小胞体の数の割合を、領域毎に算出する。
変化率算出部510は、物質を作用させる前の細胞外小胞体の比率と、物質を作用させた後の細胞外小胞体の比率との変化率を、領域毎に算出する。例えば、変化率算出部510は、抗CD81抗体を作用させる前のエクソソームの領域毎の比率と、抗CD81抗体を作用させた後のエクソソームの領域毎の比率との間の変化率を、領域毎に算出する。
粒子径判定部504は、抗体作用前のエクソソームについて、粒子径dを判定する。評価部507は、粒子径判定部504が判定した粒子径dの平均値を算出する(ステップS110)。この一例では、評価部507は、平均粒径を120nmとして算出する。評価部507は、算出した平均粒径120nmを、粒子径のしきい値Thdとして、記憶部520に記憶させる(ステップS120)。図19に、評価部507が算出したしきい値Thdの一例を示す。
ゼータ電位判定部503は、抗体作用前のエクソソームについて、ゼータ電位ζを判定する。評価部507は、ゼータ電位判定部503が判定したゼータ電位ζの平均値を算出する(ステップS130)。この一例では、評価部507は、平均ゼータ電位を−(マイナス)13mVとして算出する。評価部507は、算出した平均ゼータ電位−13mVを、粒子径のしきい値Thζとして、記憶部520に記憶させる(ステップS140)。図19に、評価部507が算出したしきい値Thζの一例を示す。
ステップS110からステップS140の処理によって、記憶部520にしきい値が記憶される。
次に、比率算出部509は、計数部508が計数したエクソソームの粒子数に基づいて、領域間の粒子数の比率を算出する。具体的には、図20に示すように、比率算出部509は、領域DM1〜領域DM4の粒子数の比率を、28%、31%、19%、22%と算出する。
評価部507は、算出された変化率と、予め求められている変化率の傾向との比較により、微粒子の状態を評価する。
評価部507は、抗体の作用前後における各領域の粒子数の増減について、次に示すような傾向に基づいて、微粒子の状態を評価してもよい。すなわち、領域DM1について、粒子数の増加要因には、凝集発生があり、減少要因には、抗体結合、及び凝集発生がある。また、領域DM2について、粒子数の増加要因には、凝集解消があり、減少要因には、抗体結合、及び凝集発生がある。また、領域DM3について、粒子数の増加要因には、抗体結合があり、減少要因には、凝集発生がある。また、領域DM4について、粒子数の増加要因には、抗体結合及び凝集発生があり、減少要因には、凝集解消がある。
また、評価部507は、抗体結合によって予測される各領域の粒子数の増減について、次に示すような傾向に基づいて、微粒子の状態を評価してもよい。すなわち、領域DM1について、抗体作用の結果、粒子が領域DM4に移行する。この場合、想定される機構は、抗体結合である。また、領域DM2について、抗体作用の結果、粒子数が減少する。この場合、想定される機構は、抗体結合及び凝集発生である。また、領域DM3について、抗体作用の結果、粒子が領域DM4に移行する。この場合、想定される機構は、抗体結合及び凝集発生である。また、領域DM4について、抗体作用の結果、粒子数が増加する。
この場合、想定される機構は、抗体結合及び凝集発生である。
また、粒子検出システム1は、複数のレーンを備えているため、レーンごとに微粒子の種類及び抗体の種類を変えることができる。具体例を図21から図23に示す。
図21は、本実施形態の複数のレーンにそれぞれ種類が異なる抗体を添加する場合の一例を示す模式図である。
図22は、本実施形態の疾患の判定パネルの一例を示す表である。
図23は、本実施形態の疾患の診断及び指導パネルの一例を示す表である。
これら図21から図23に示すように、評価部507は、レーンごとに異なる抗体を添加し、それぞれのレーンにおける微粒子の状態を評価することもできる。すなわち、粒子検出システム1によれば、目的の疾患の診断に最適な抗体の組合せを任意に選択して検査することができる。また、粒子検出システム1によれば、複数レーンを同時に評価することができるため、単一のレーンによって評価する場合に比べて、評価時間を短縮することができる。
評価部507は、微粒子の物性評価を行うこともできる。具体例として、評価部507が、機能を改変したエクソソームの物性評価を行う場合について、図24から図26を参照して説明する。
図25は、本実施形態の演算部500による微粒子の物性評価の動作の一例を示す図である。
評価部507は、記憶部520から、粒子径dの下限しきい値Thd1及び上限しきい値Thd2と、ゼータ電位ζの下限しきい値Thζ1及び上限しきい値Thζ2とを読み出す(ステップS210)。
評価部507は、ステップS210において読み出した各しきい値に基づいて、ゲート領域を示す情報を、ディスプレイ(不図示)に表示する(図24のゲート領域Gを参照)(ステップS220)。
次に、ゼータ電位判定部503は、評価対象の微粒子のゼータ電位ζを判定する。また、粒子径判定部504は、評価対象の微粒子の粒子径dを判定する(ステップS230)。この具体例において、評価対象の微粒子とは、機能改変されたエクソソームである。
次に、相関部505は、ステップS230において判定されたゼータ電位ζと、粒子径dとを、微粒子毎に関連付けする(ステップS240)。また、相関部505は、関連付けしたゼータ電位ζと、粒子径dとを、微粒子毎にディスプレイ(不図示)に表示する。
計数部508は、ゲート領域G内に存在する微粒子の粒子数を計数する(ステップS250)。また、計数部508は、ゲート領域G外に存在する微粒子の粒子数を計数する(ステップS260)。
比率算出部509は、計数部508が計数した粒子数に基づいて、ゲート領域G内の粒子数と、ゲート領域G外の粒子数との比率を算出して(ステップS270)、処理を終了する。
図26は、本実施形態の評価部507による評価の一例を示す図である。同図に示すように、評価部507は、ゲート領域G内に存在する粒子が比較的多い場合に、適合と判定し、ゲート領域G内に存在する粒子が比較的少ない場合に、不適合と判定する。つまり、評価部507は、ゲート領域G内の粒子数と、ゲート領域G外の粒子数に基づいて、評価対象の微粒子の適合性を判定する。
上述の評価部507によれば、機能改変したエクソソームが、上述のドラッグデリバリシステムに適合するものであるか否かについて、評価することができる。
以上説明したように、本実施形態に係る粒子検出システム1は、微粒子の粒子径と、ゼータ電位とを、微粒子毎に求めるとともに、求めた粒子径とゼータ電位とを相関づける。
これにより、粒子検出システム1によれば、粒子径又はゼータ電位のいずれか一方だけでは判定が困難であった微粒子の状態を判定することができる。
また、本実施形態に係る粒子検出システム1は、照明光をレーン2の側面から入射させることにより、微粒子から生ずる散乱光を精度よく検出することができる。これにより、粒子検出システム1によれば、微粒子の粒子径やゼータ電位を精度よく判定することができる。したがって、粒子検出システム1によれば、微粒子の状態を精度よく判定することができる。
また、半導体技術の進歩によりLSIに代替する集積回路化の技術が出現した場合、当該技術による集積回路を用いてもよい。
Claims (20)
- 微粒子を含む試料が移動可能な流路を備えた流体デバイスが設置されうる設置面を有するステージ部と、
前記流路を移動する前記微粒子の粒子径を判定する粒子径判定部と、
前記流路を移動する前記微粒子のゼータ電位を判定するゼータ電位判定部と、
前記粒子径判定部が判定した前記微粒子毎の前記粒子径と、前記ゼータ電位判定部が判定した前記微粒子毎の前記ゼータ電位とを、前記微粒子毎に関連付けする相関部と、
前記粒子径の基準範囲と、前記ゼータ電位の基準範囲とをそれぞれ示す基準範囲情報を記憶する基準記憶部と、
前記相関部が前記微粒子毎に前記粒子径と前記ゼータ電位とを関連付けて得た相関情報と、前記基準記憶部が記憶する前記基準範囲情報とに基づいて、前記微粒子の種類又は状態の少なくとも一方を判定する状態判定部と、
を備える微粒子検出システム。 - 前記流路に照明光を照射する照射部と、
前記照明光の照射により生ずる散乱光を撮像する撮像部と、
前記撮像部が撮像した画像に基づいて、前記画像に含まれる前記微粒子を前記微粒子毎に識別する識別部と、
を更に備え、
前記粒子径判定部と前記ゼータ電位判定部は、それぞれ、前記識別部が識別した前記微粒子毎に、前記粒子径と前記ゼータ電位とを判定する、請求項1に記載の微粒子検出システム。 - 前記状態判定部は、前記基準範囲情報が示す前記粒子径の基準範囲及び前記ゼータ電位の基準範囲によって区分される少なくとも1つの領域について、当該領域に含まれる前記微粒子の種類又は状態のうち少なくとも一方を判定する、
請求項2に記載の微粒子検出システム。 - 前記基準範囲情報が示す前記粒子径のしきい値及び前記ゼータ電位のしきい値によって区分される領域毎に、当該領域に含まれる前記微粒子の数を計数する計数部
を更に備える請求項3に記載の微粒子検出システム。 - 前記計数部が計数する前記微粒子の数の、前記領域間の比率を算出する比率算出部と、
ある物質と反応させる前の前記微粒子について、前記比率算出部が算出する前記領域間の前記微粒子の数の比率と、前記物質と反応させた後の前記微粒子について、前記比率算出部が算出する前記領域間の前記微粒子の数の比率との変化率を算出する変化率算出部と
を更に備える請求項4に記載の微粒子検出システム。 - 前記微粒子は、表面の生体分子と別の物質が結合した複合体を含み、
前記状態判定部は、
前記相関情報と前記基準範囲情報とに基づいて、前記複合体の種類を特定する
請求項2から請求項5のいずれか一項に記載の微粒子検出システム。 - 前記微粒子はエクソソームであって、
前記状態判定部は、特定した前記複合体の種類に基づいて、前記エクソソームの表面に特異的に結合した特異的結合物質を検出する
請求項6に記載の微粒子検出システム。 - 前記状態判定部は、複数の前記微粒子について、前記微粒子毎の前記粒子径及び前記ゼータ電位に関する分布を出力する
請求項2から請求項7のいずれか一項に記載の微粒子検出システム。 - 前記状態判定部の判定に基づいて前記微粒子の種類又は状態の少なくとも一方の分布を評価する評価部
を更に備える請求項2から請求項8のいずれか一項に記載の微粒子検出システム。 - 前記基準範囲情報は、前記状態判定部の判定に用いられる前記微粒子の状態の前記分布毎に予め記憶される
請求項8または請求項9に記載の微粒子検出システム。 - 前記基準範囲情報は、表面の生体分子に物質が結合していない複数の前記微粒子の前記粒子径及び前記ゼータ電位の分布に基づいて定められる
請求項2から請求項10のいずれか一項に記載の微粒子検出システム。 - 前記粒子径判定部は、
前記識別部が識別した前記微粒子のブラウン運動に基づいて前記粒子径を判定する
請求項2から請求項11のいずれか一項に記載の微粒子検出システム。 - 前記ゼータ電位判定部は、
前記識別部が識別した前記微粒子の移動速度に基づいて前記ゼータ電位を判定する
請求項2から請求項12のいずれか一項に記載の微粒子検出システム。 - 前記照射部は、前記設置面と直交し前記流路と平行な面と交差する第1方向に平行な光軸に沿って前記流路に照明光を照射し、
前記流路の内部において、前記照明光の前記第1方向と直交する第2方向の幅が最小となり、かつ、前記流路の照射光入射側の側面の位置における照射領域が前記側面内に収まるように前記照明光を収束させる調整部
を更に備える請求項2から請求項13のいずれか一項に記載の微粒子検出システム。 - 前記微粒子は、別の物質が結合していない又は結合している、エクソソーム又は細胞外小胞体である
請求項2から請求項14のいずれか一項に記載の微粒子検出システム。 - 前記識別部は、識別した前記微粒子毎に、固有の微粒子識別子を付与し、
前記相関部は、前記粒子径判定部が粒子径を判定した前記微粒子に対して付与された前記微粒子識別子と、前記ゼータ電位判定部がゼータ電位を判定した前記微粒子に対して付与された前記微粒子識別子との一致に基づいて、前記微粒子毎の前記粒子径と、前記ゼータ電位判定部が判定した前記微粒子毎の前記ゼータ電位とを、前記微粒子毎に関連付けする
請求項2から請求項14のいずれか一項に記載の微粒子検出システム。 - 微粒子を含む試料を移動可能な流路を備えた流体デバイスが設置されうる設置面を有するステージ部を備えるコンピュータに、
前記流路を移動する前記微粒子の粒子径を判定する粒子径判定ステップと、
前記流路を移動する前記微粒子のゼータ電位を判定するゼータ電位判定ステップと、
前記微粒子の前記粒子径と前記ゼータ電位とを、前記微粒子毎に関連付けする相関ステップと、
前記粒子径のしきい値と前記ゼータ電位のしきい値とに基づいて区分される領域を表示するステップと、
前記微粒子毎に前記粒子径と前記ゼータ電位との分布を表示するステップと、
を実行させるための微粒子検出プログラム。 - 前記粒子径のしきい値及び前記ゼータ電位のしきい値によって区分される領域のうち、特定の当該領域に含まれる前記微粒子の数を計数する計数ステップ
を更に実行させる請求項17に記載の微粒子検出プログラム。 - 前記流路に照明光を照射する照射ステップと、
前記照明光の照射により生ずる散乱光を撮像する撮像ステップと、
前記撮像ステップにおいて撮像された画像に基づいて、前記画像に含まれる前記微粒子を前記微粒子毎に識別する識別ステップと、
を更に実行させ、
前記粒子径判定ステップと前記ゼータ電位判定ステップは、それぞれ、前記識別ステップで識別された前記微粒子毎に、前記粒子径と前記ゼータ電位とを判定する、
請求項18に記載の微粒子検出プログラム。 - 前記照射ステップは、前記設置面と直交し前記流路と平行な面と交差する第1方向に平行な光軸に沿って前記流路に照明光を照射し、
前記流路の内部において、前記照明光の前記第1方向と直交する第2方向の幅が最小となり、かつ、前記流路の照射光入射側の側面の位置における照射領域が前記側面内に収まるように前記照明光を調整する、
請求項19に記載の微粒子検出プログラム。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2015087021 | 2015-04-21 | ||
| JP2015087021 | 2015-04-21 | ||
| PCT/JP2016/062591 WO2016171198A1 (ja) | 2015-04-21 | 2016-04-21 | 微粒子検出システム及び微粒子検出プログラム |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPWO2016171198A1 JPWO2016171198A1 (ja) | 2018-03-22 |
| JP6781989B2 true JP6781989B2 (ja) | 2020-11-11 |
Family
ID=57143119
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2017514177A Active JP6781989B2 (ja) | 2015-04-21 | 2016-04-21 | 微粒子検出システム及び微粒子検出プログラム |
Country Status (3)
| Country | Link |
|---|---|
| US (1) | US10295454B2 (ja) |
| JP (1) | JP6781989B2 (ja) |
| WO (1) | WO2016171198A1 (ja) |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE102016013236B4 (de) * | 2016-11-07 | 2020-07-16 | Particle Metrix Gmbh | Vorrichtung und Verfahren zum Messen der Konzentration, der Größe und des Zetapotentials von Nanopartikeln in Flüssigkeiten im Streulichtmodus und im Fluoreszenzmodus |
| US20180128733A1 (en) * | 2016-11-07 | 2018-05-10 | Applied Materials, Inc. | Methods and apparatus for detection and analysis of nanoparticles from semiconductor chamber parts |
| JP6596636B2 (ja) * | 2016-12-06 | 2019-10-30 | 国立研究開発法人産業技術総合研究所 | 流速分布計測方法及び粒径計測方法 |
| JP6814474B2 (ja) * | 2017-02-28 | 2021-01-20 | 国立大学法人 東京大学 | 電気泳動分析チップおよび電気泳動分析装置 |
| US10514331B1 (en) * | 2019-03-23 | 2019-12-24 | Horiba Instruments Incorporated | Method for determining the size of nanoparticles in a colloid |
| JP7356891B2 (ja) * | 2019-06-12 | 2023-10-05 | 株式会社堀場製作所 | 粒子分析装置及び粒子分析方法 |
| US11665929B2 (en) * | 2019-06-13 | 2023-05-30 | Intel Corporation | Micro light-emitting diode displays with improved power efficiency |
| JP7421968B2 (ja) * | 2020-03-17 | 2024-01-25 | リオン株式会社 | 粒子測定装置及び粒子測定方法 |
| US20220067953A1 (en) * | 2020-09-02 | 2022-03-03 | International Business Machines Corporation | Reflection-based monoscopic depth perception |
Family Cites Families (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2832117B2 (ja) * | 1991-11-29 | 1998-12-02 | キヤノン株式会社 | サンプル測定デバイス及びサンプル測定システム |
| DE60109616T2 (de) * | 2000-06-12 | 2006-05-11 | Sysmex Corp. | Immunoassay und immunoassayvorrichtung |
| JP4812393B2 (ja) * | 2005-03-04 | 2011-11-09 | 株式会社日立ハイテクノロジーズ | 蛍光分子計測システム |
| JP4411440B2 (ja) * | 2006-06-02 | 2010-02-10 | 国立大学法人 筑波大学 | 粒子特性計測装置および粒子特性計測方法 |
| JP4982697B2 (ja) * | 2007-04-12 | 2012-07-25 | 興和株式会社 | 粒子計測装置 |
| JP2009229103A (ja) | 2008-03-19 | 2009-10-08 | Toshiba Corp | 金属コロイドの定量方法 |
| US20120135054A1 (en) * | 2009-06-29 | 2012-05-31 | Cornell University | Poly (Ester Ether Amide)s and Uses Thereof |
| US20120264948A1 (en) * | 2009-12-30 | 2012-10-18 | Cargill, Incorporated | Membrane separation and purification of monatin |
| JP2011149793A (ja) * | 2010-01-21 | 2011-08-04 | Ihi Corp | ゼータ電位測定装置 |
| WO2013056113A1 (en) * | 2011-10-13 | 2013-04-18 | The Johns Hopkins University | Nanocomposites of gold and polymers |
| JP6230027B2 (ja) * | 2012-08-24 | 2017-11-15 | 国立大学法人 東京大学 | エキソソームの分析方法、エキソソーム分析装置、抗体−エキソソーム複合体、及びエキソソーム電気泳動チップ |
| US10022334B2 (en) * | 2013-12-23 | 2018-07-17 | The Brigham and Women's Hostpital, Inc. | Cationic materials and formulations for drug delivery |
| WO2015108023A1 (ja) * | 2014-01-17 | 2015-07-23 | 株式会社ニコン | 微粒子分析装置、観察装置、微粒子分析プログラムおよび微粒子分析方法 |
| AT515577B1 (de) * | 2014-03-12 | 2018-06-15 | Anton Paar Gmbh | Gemeinsamer Strahlungspfad zum Ermitteln von Partikel-information durch Direktbildauswertung und durch Differenzbildanalyse |
| JPWO2016063912A1 (ja) * | 2014-10-24 | 2017-08-03 | 国立大学法人 東京大学 | 粒子検出方法、粒子検出装置および粒子検出システム |
| US9561286B2 (en) * | 2015-03-06 | 2017-02-07 | The Board Of Trustees Of The University Of Illinois | Sterically stabilized cationic nanocarrier, kits and method of use |
| EP3939571A1 (en) * | 2015-05-21 | 2022-01-19 | Ohio State Innovation Foundation | Benzene-1,3,5-tricarboxamide derivatives and uses thereof |
-
2016
- 2016-04-21 WO PCT/JP2016/062591 patent/WO2016171198A1/ja active Application Filing
- 2016-04-21 JP JP2017514177A patent/JP6781989B2/ja active Active
-
2017
- 2017-10-17 US US15/786,450 patent/US10295454B2/en not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| US20180100793A1 (en) | 2018-04-12 |
| US10295454B2 (en) | 2019-05-21 |
| JPWO2016171198A1 (ja) | 2018-03-22 |
| WO2016171198A1 (ja) | 2016-10-27 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6781989B2 (ja) | 微粒子検出システム及び微粒子検出プログラム | |
| US9952215B2 (en) | Exosome analysis method, exosome analysis apparatus, antibody-exosome complex, and exosome electrophoresis chip | |
| Chia et al. | Advances in exosome quantification techniques | |
| Daaboul et al. | Digital detection of exosomes by interferometric imaging | |
| Akagi et al. | On-chip immunoelectrophoresis of extracellular vesicles released from human breast cancer cells | |
| Yoshioka et al. | Ultra-sensitive liquid biopsy of circulating extracellular vesicles using ExoScreen | |
| US10768141B2 (en) | Isoelectric focusing arrays and methods of use thereof | |
| AU2015307593B2 (en) | Particle imaging apparatus and particle imaging method | |
| JP2020531863A (ja) | 粒子分離システムおよび方法 | |
| WO2015029979A1 (ja) | エキソソームの分析方法、エキソソーム分析チップ、及びエキソソーム分析装置 | |
| US20170242020A1 (en) | Subcellular Western Blotting of Single Cells | |
| US20200055048A1 (en) | Optofluidic device and method for detecting circulating tumour cells | |
| JPWO2014129292A1 (ja) | 生体分析デバイスおよび生体分子分析装置 | |
| US10113948B2 (en) | Particle detection method, particle detection device and particle detection system | |
| Kwon et al. | Methods to analyze extracellular vesicles at single particle level | |
| JP2020204604A (ja) | 粒子分析装置及び粒子分析方法 | |
| US20190369046A1 (en) | Electrophoretic analysis chip and electrophoretic analysis apparatus | |
| JP2017129425A (ja) | 抗癌剤の評価方法 | |
| WO2015163194A1 (ja) | 細胞外小胞体分析チップ、細胞外小胞体分析方法、細胞外小胞体分析装置 | |
| JPWO2018198470A1 (ja) | 撮像対象分析用装置、流路構造、撮像用部材、撮像方法、及び撮像対象分析用システム | |
| JP6482774B2 (ja) | 生体分析用のデバイス、分析装置および分析方法 | |
| US10852272B2 (en) | Devices and methods using pore size modulation for detecting analytes in a fluid sample | |
| JP5943002B2 (ja) | 細胞検出方法および細胞検出システム | |
| Tan | Investigating Physicochemical Principles for Sample Preparation and Detection From Single-cell Immunoblots | |
| WO2021099545A1 (en) | Nanoparticle tracking analysis as a biomarker tool in autoimmune diseases |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20171117 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20190418 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20190418 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20200623 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200821 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20200908 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20201008 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6781989 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| S111 | Request for change of ownership or part of ownership |
Free format text: JAPANESE INTERMEDIATE CODE: R313117 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| S531 | Written request for registration of change of domicile |
Free format text: JAPANESE INTERMEDIATE CODE: R313531 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |