JP6234224B2 - 血栓溶解及び抗凝固特性を有するタンパク質融合構築物 - Google Patents
血栓溶解及び抗凝固特性を有するタンパク質融合構築物 Download PDFInfo
- Publication number
- JP6234224B2 JP6234224B2 JP2013522316A JP2013522316A JP6234224B2 JP 6234224 B2 JP6234224 B2 JP 6234224B2 JP 2013522316 A JP2013522316 A JP 2013522316A JP 2013522316 A JP2013522316 A JP 2013522316A JP 6234224 B2 JP6234224 B2 JP 6234224B2
- Authority
- JP
- Japan
- Prior art keywords
- egf
- construct
- egf4
- chimeric protein
- domain
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 230000002537 thrombolytic effect Effects 0.000 title claims description 66
- 239000003146 anticoagulant agent Substances 0.000 title claims description 62
- 230000002429 anti-coagulating effect Effects 0.000 title description 2
- 230000012743 protein tagging Effects 0.000 title description 2
- 108090000623 proteins and genes Proteins 0.000 claims description 254
- 108090000190 Thrombin Proteins 0.000 claims description 153
- 229960004072 thrombin Drugs 0.000 claims description 153
- 102000004169 proteins and genes Human genes 0.000 claims description 116
- 235000018102 proteins Nutrition 0.000 claims description 114
- 108020001507 fusion proteins Proteins 0.000 claims description 104
- 102000037865 fusion proteins Human genes 0.000 claims description 104
- 108010023197 Streptokinase Proteins 0.000 claims description 66
- 229960005202 streptokinase Drugs 0.000 claims description 65
- 230000014509 gene expression Effects 0.000 claims description 62
- 230000033885 plasminogen activation Effects 0.000 claims description 60
- 230000000694 effects Effects 0.000 claims description 53
- 108010079274 Thrombomodulin Proteins 0.000 claims description 45
- 210000004027 cell Anatomy 0.000 claims description 44
- 239000004019 antithrombin Substances 0.000 claims description 33
- 241000235058 Komagataella pastoris Species 0.000 claims description 28
- 239000013598 vector Substances 0.000 claims description 27
- 230000005764 inhibitory process Effects 0.000 claims description 25
- 235000004279 alanine Nutrition 0.000 claims description 24
- KZSNJWFQEVHDMF-UHFFFAOYSA-N Valine Natural products CC(C)C(N)C(O)=O KZSNJWFQEVHDMF-UHFFFAOYSA-N 0.000 claims description 23
- 239000004474 valine Substances 0.000 claims description 23
- 108060008539 Transglutaminase Proteins 0.000 claims description 20
- 229910052757 nitrogen Inorganic materials 0.000 claims description 20
- 102000003601 transglutaminase Human genes 0.000 claims description 20
- QNAYBMKLOCPYGJ-REOHCLBHSA-N L-alanine Chemical group C[C@H](N)C(O)=O QNAYBMKLOCPYGJ-REOHCLBHSA-N 0.000 claims description 19
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Chemical group OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 claims description 19
- 125000003275 alpha amino acid group Chemical group 0.000 claims description 18
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical group OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 claims description 17
- 239000008194 pharmaceutical composition Substances 0.000 claims description 16
- 150000007523 nucleic acids Chemical class 0.000 claims description 14
- 230000001580 bacterial effect Effects 0.000 claims description 12
- 230000010005 growth-factor like effect Effects 0.000 claims description 9
- 210000004102 animal cell Anatomy 0.000 claims description 6
- 125000002987 valine group Chemical group [H]N([H])C([H])(C(*)=O)C([H])(C([H])([H])[H])C([H])([H])[H] 0.000 claims description 6
- 238000004132 cross linking Methods 0.000 claims description 5
- 108020004707 nucleic acids Proteins 0.000 claims description 5
- 102000039446 nucleic acids Human genes 0.000 claims description 5
- 210000005253 yeast cell Anatomy 0.000 claims description 5
- 239000003937 drug carrier Substances 0.000 claims description 2
- 102000012607 Thrombomodulin Human genes 0.000 claims 3
- 239000013615 primer Substances 0.000 description 162
- 108090000373 Tissue Plasminogen Activator Proteins 0.000 description 144
- 102000003978 Tissue Plasminogen Activator Human genes 0.000 description 142
- 229960000187 tissue plasminogen activator Drugs 0.000 description 140
- 230000004927 fusion Effects 0.000 description 126
- 238000000034 method Methods 0.000 description 105
- 102100033237 Pro-epidermal growth factor Human genes 0.000 description 91
- 101710145796 Staphylokinase Proteins 0.000 description 50
- 238000004925 denaturation Methods 0.000 description 50
- 230000036425 denaturation Effects 0.000 description 50
- 239000012634 fragment Substances 0.000 description 48
- 108010088842 Fibrinolysin Proteins 0.000 description 47
- 229940012957 plasmin Drugs 0.000 description 47
- 239000000047 product Substances 0.000 description 47
- 230000004913 activation Effects 0.000 description 46
- 238000013461 design Methods 0.000 description 46
- 108020004414 DNA Proteins 0.000 description 44
- 238000006243 chemical reaction Methods 0.000 description 43
- 102100026966 Thrombomodulin Human genes 0.000 description 41
- 235000001014 amino acid Nutrition 0.000 description 40
- 108090000765 processed proteins & peptides Proteins 0.000 description 40
- 102000013566 Plasminogen Human genes 0.000 description 37
- 108010051456 Plasminogen Proteins 0.000 description 37
- 101800004937 Protein C Proteins 0.000 description 37
- 102000017975 Protein C Human genes 0.000 description 37
- 101800001700 Saposin-D Proteins 0.000 description 37
- 229960000856 protein c Drugs 0.000 description 37
- 239000003527 fibrinolytic agent Substances 0.000 description 36
- 230000000875 corresponding effect Effects 0.000 description 34
- 229940024606 amino acid Drugs 0.000 description 33
- 229920001184 polypeptide Polymers 0.000 description 33
- 102000004196 processed proteins & peptides Human genes 0.000 description 33
- 238000000137 annealing Methods 0.000 description 32
- 239000000499 gel Substances 0.000 description 32
- 229960000103 thrombolytic agent Drugs 0.000 description 32
- 238000011144 upstream manufacturing Methods 0.000 description 31
- 108010073385 Fibrin Proteins 0.000 description 30
- 102000009123 Fibrin Human genes 0.000 description 30
- BWGVNKXGVNDBDI-UHFFFAOYSA-N Fibrin monomer Chemical compound CNC(=O)CNC(=O)CN BWGVNKXGVNDBDI-UHFFFAOYSA-N 0.000 description 30
- 229950003499 fibrin Drugs 0.000 description 30
- 150000001413 amino acids Chemical class 0.000 description 28
- 238000003556 assay Methods 0.000 description 28
- 239000002773 nucleotide Substances 0.000 description 28
- 125000003729 nucleotide group Chemical group 0.000 description 28
- 101150084418 EGF gene Proteins 0.000 description 27
- 230000003321 amplification Effects 0.000 description 27
- 238000003199 nucleic acid amplification method Methods 0.000 description 27
- 239000013612 plasmid Substances 0.000 description 27
- 108091008146 restriction endonucleases Proteins 0.000 description 26
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 24
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 22
- 238000010276 construction Methods 0.000 description 22
- 239000000203 mixture Substances 0.000 description 22
- 230000003647 oxidation Effects 0.000 description 22
- 238000007254 oxidation reaction Methods 0.000 description 22
- 238000004519 manufacturing process Methods 0.000 description 21
- 230000037361 pathway Effects 0.000 description 20
- 108020004705 Codon Proteins 0.000 description 19
- 241000588724 Escherichia coli Species 0.000 description 19
- 208000007536 Thrombosis Diseases 0.000 description 18
- 238000010367 cloning Methods 0.000 description 18
- 108090000790 Enzymes Proteins 0.000 description 17
- 102000004190 Enzymes Human genes 0.000 description 17
- 210000004899 c-terminal region Anatomy 0.000 description 17
- 229940088598 enzyme Drugs 0.000 description 17
- 230000035772 mutation Effects 0.000 description 17
- 239000000243 solution Substances 0.000 description 17
- KZSNJWFQEVHDMF-BYPYZUCNSA-N L-valine Chemical compound CC(C)[C@H](N)C(O)=O KZSNJWFQEVHDMF-BYPYZUCNSA-N 0.000 description 16
- 238000010586 diagram Methods 0.000 description 16
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 15
- 239000007983 Tris buffer Substances 0.000 description 15
- 230000035602 clotting Effects 0.000 description 15
- 230000009089 cytolysis Effects 0.000 description 15
- 238000003780 insertion Methods 0.000 description 15
- 230000037431 insertion Effects 0.000 description 15
- 108091028043 Nucleic acid sequence Proteins 0.000 description 14
- 108700026244 Open Reading Frames Proteins 0.000 description 14
- 230000015572 biosynthetic process Effects 0.000 description 14
- 239000003814 drug Substances 0.000 description 14
- 239000002609 medium Substances 0.000 description 14
- 235000006109 methionine Nutrition 0.000 description 14
- 238000000746 purification Methods 0.000 description 14
- 150000001651 triphenylamine derivatives Chemical class 0.000 description 14
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 14
- 108091026890 Coding region Proteins 0.000 description 13
- 240000004808 Saccharomyces cerevisiae Species 0.000 description 13
- 229940079593 drug Drugs 0.000 description 13
- 230000006870 function Effects 0.000 description 13
- 229930182817 methionine Natural products 0.000 description 13
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 12
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 12
- 241000124008 Mammalia Species 0.000 description 12
- 230000003197 catalytic effect Effects 0.000 description 12
- 238000001976 enzyme digestion Methods 0.000 description 12
- 239000011780 sodium chloride Substances 0.000 description 12
- 238000006467 substitution reaction Methods 0.000 description 12
- 102000001938 Plasminogen Activators Human genes 0.000 description 11
- 108010001014 Plasminogen Activators Proteins 0.000 description 11
- 238000007792 addition Methods 0.000 description 11
- 239000000306 component Substances 0.000 description 11
- 238000002360 preparation method Methods 0.000 description 11
- 239000006228 supernatant Substances 0.000 description 11
- 206010038563 Reocclusion Diseases 0.000 description 10
- 210000003000 inclusion body Anatomy 0.000 description 10
- 229940127126 plasminogen activator Drugs 0.000 description 10
- 206010053567 Coagulopathies Diseases 0.000 description 9
- FFEARJCKVFRZRR-BYPYZUCNSA-N L-methionine Chemical compound CSCC[C@H](N)C(O)=O FFEARJCKVFRZRR-BYPYZUCNSA-N 0.000 description 9
- 241000235648 Pichia Species 0.000 description 9
- 230000001419 dependent effect Effects 0.000 description 9
- 238000007429 general method Methods 0.000 description 9
- 230000010354 integration Effects 0.000 description 9
- 125000001360 methionine group Chemical group N[C@@H](CCSC)C(=O)* 0.000 description 9
- 239000000651 prodrug Substances 0.000 description 9
- 229940002612 prodrug Drugs 0.000 description 9
- 238000002560 therapeutic procedure Methods 0.000 description 9
- 108010076504 Protein Sorting Signals Proteins 0.000 description 8
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Chemical compound NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 description 8
- 108090000435 Urokinase-type plasminogen activator Proteins 0.000 description 8
- 125000000539 amino acid group Chemical group 0.000 description 8
- 210000004204 blood vessel Anatomy 0.000 description 8
- 239000000872 buffer Substances 0.000 description 8
- 238000004587 chromatography analysis Methods 0.000 description 8
- 238000012217 deletion Methods 0.000 description 8
- 230000037430 deletion Effects 0.000 description 8
- 238000001727 in vivo Methods 0.000 description 8
- 238000012163 sequencing technique Methods 0.000 description 8
- 238000001712 DNA sequencing Methods 0.000 description 7
- 239000004471 Glycine Substances 0.000 description 7
- KDXKERNSBIXSRK-YFKPBYRVSA-N L-lysine Chemical compound NCCCC[C@H](N)C(O)=O KDXKERNSBIXSRK-YFKPBYRVSA-N 0.000 description 7
- 101150060587 SK gene Proteins 0.000 description 7
- 102000003990 Urokinase-type plasminogen activator Human genes 0.000 description 7
- 208000027418 Wounds and injury Diseases 0.000 description 7
- 239000011543 agarose gel Substances 0.000 description 7
- 239000007864 aqueous solution Substances 0.000 description 7
- 230000008901 benefit Effects 0.000 description 7
- 210000004369 blood Anatomy 0.000 description 7
- 239000008280 blood Substances 0.000 description 7
- 230000015271 coagulation Effects 0.000 description 7
- 238000005345 coagulation Methods 0.000 description 7
- 230000006378 damage Effects 0.000 description 7
- 230000029087 digestion Effects 0.000 description 7
- 238000000605 extraction Methods 0.000 description 7
- 230000001965 increasing effect Effects 0.000 description 7
- 208000014674 injury Diseases 0.000 description 7
- 230000007246 mechanism Effects 0.000 description 7
- 230000001404 mediated effect Effects 0.000 description 7
- 238000007857 nested PCR Methods 0.000 description 7
- 230000036961 partial effect Effects 0.000 description 7
- 230000008569 process Effects 0.000 description 7
- 229960005356 urokinase Drugs 0.000 description 7
- 229920000936 Agarose Polymers 0.000 description 6
- 108010025188 Alcohol oxidase Proteins 0.000 description 6
- 239000001888 Peptone Substances 0.000 description 6
- 108010080698 Peptones Proteins 0.000 description 6
- 102100029477 Vitamin K-dependent protein C Human genes 0.000 description 6
- 101710193900 Vitamin K-dependent protein C Proteins 0.000 description 6
- 230000010100 anticoagulation Effects 0.000 description 6
- 229940041514 candida albicans extract Drugs 0.000 description 6
- 239000005018 casein Substances 0.000 description 6
- BECPQYXYKAMYBN-UHFFFAOYSA-N casein, tech. Chemical compound NCCCCC(C(O)=O)N=C(O)C(CC(O)=O)N=C(O)C(CCC(O)=N)N=C(O)C(CC(C)C)N=C(O)C(CCC(O)=O)N=C(O)C(CC(O)=O)N=C(O)C(CCC(O)=O)N=C(O)C(C(C)O)N=C(O)C(CCC(O)=N)N=C(O)C(CCC(O)=N)N=C(O)C(CCC(O)=N)N=C(O)C(CCC(O)=O)N=C(O)C(CCC(O)=O)N=C(O)C(COP(O)(O)=O)N=C(O)C(CCC(O)=N)N=C(O)C(N)CC1=CC=CC=C1 BECPQYXYKAMYBN-UHFFFAOYSA-N 0.000 description 6
- 235000021240 caseins Nutrition 0.000 description 6
- 239000003795 chemical substances by application Substances 0.000 description 6
- 238000003776 cleavage reaction Methods 0.000 description 6
- WQPDUTSPKFMPDP-OUMQNGNKSA-N hirudin Chemical compound C([C@@H](C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC=1C=CC(OS(O)(=O)=O)=CC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(O)=O)NC(=O)[C@H](CC(O)=O)NC(=O)CNC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CCCCN)NC(=O)[C@H]1N(CCC1)C(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)CNC(=O)[C@@H](NC(=O)[C@@H](NC(=O)[C@H]1NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CCC(O)=O)NC(=O)CNC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)CNC(=O)[C@H](CC(C)C)NC(=O)[C@H]([C@@H](C)CC)NC(=O)[C@@H]2CSSC[C@@H](C(=O)N[C@@H](CCC(O)=O)C(=O)NCC(=O)N[C@@H](CO)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@H](C(=O)N[C@H](C(NCC(=O)N[C@@H](CCC(N)=O)C(=O)NCC(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCCCN)C(=O)N2)=O)CSSC1)C(C)C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H]1NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)CNC(=O)[C@H](CO)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@@H](NC(=O)[C@H](CC=2C=CC(O)=CC=2)NC(=O)[C@@H](NC(=O)[C@@H](N)C(C)C)C(C)C)[C@@H](C)O)CSSC1)C(C)C)[C@@H](C)O)[C@@H](C)O)C1=CC=CC=C1 WQPDUTSPKFMPDP-OUMQNGNKSA-N 0.000 description 6
- 238000001990 intravenous administration Methods 0.000 description 6
- 230000001575 pathological effect Effects 0.000 description 6
- 239000008188 pellet Substances 0.000 description 6
- 235000019319 peptone Nutrition 0.000 description 6
- 230000007017 scission Effects 0.000 description 6
- 238000012216 screening Methods 0.000 description 6
- 239000012138 yeast extract Substances 0.000 description 6
- 239000004475 Arginine Substances 0.000 description 5
- HTTJABKRGRZYRN-UHFFFAOYSA-N Heparin Chemical compound OC1C(NC(=O)C)C(O)OC(COS(O)(=O)=O)C1OC1C(OS(O)(=O)=O)C(O)C(OC2C(C(OS(O)(=O)=O)C(OC3C(C(O)C(O)C(O3)C(O)=O)OS(O)(=O)=O)C(CO)O2)NS(O)(=O)=O)C(C(O)=O)O1 HTTJABKRGRZYRN-UHFFFAOYSA-N 0.000 description 5
- 108010007267 Hirudins Proteins 0.000 description 5
- 102000007625 Hirudins Human genes 0.000 description 5
- DCXYFEDJOCDNAF-REOHCLBHSA-N L-asparagine Chemical compound OC(=O)[C@@H](N)CC(N)=O DCXYFEDJOCDNAF-REOHCLBHSA-N 0.000 description 5
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 5
- 108091005804 Peptidases Proteins 0.000 description 5
- 102000035195 Peptidases Human genes 0.000 description 5
- 239000004365 Protease Substances 0.000 description 5
- 230000009471 action Effects 0.000 description 5
- 230000003213 activating effect Effects 0.000 description 5
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 5
- 239000003593 chromogenic compound Substances 0.000 description 5
- 150000001875 compounds Chemical class 0.000 description 5
- 238000002651 drug therapy Methods 0.000 description 5
- 101150012763 endA gene Proteins 0.000 description 5
- 239000013604 expression vector Substances 0.000 description 5
- 238000009472 formulation Methods 0.000 description 5
- 229960002897 heparin Drugs 0.000 description 5
- 229920000669 heparin Polymers 0.000 description 5
- 229940006607 hirudin Drugs 0.000 description 5
- 238000011068 loading method Methods 0.000 description 5
- 239000012528 membrane Substances 0.000 description 5
- 239000000825 pharmaceutical preparation Substances 0.000 description 5
- 239000008057 potassium phosphate buffer Substances 0.000 description 5
- 239000003805 procoagulant Substances 0.000 description 5
- -1 proline amino acid Chemical class 0.000 description 5
- 101150079601 recA gene Proteins 0.000 description 5
- 238000002741 site-directed mutagenesis Methods 0.000 description 5
- 238000003786 synthesis reaction Methods 0.000 description 5
- 238000012795 verification Methods 0.000 description 5
- DCXYFEDJOCDNAF-UHFFFAOYSA-N Asparagine Natural products OC(=O)C(N)CC(N)=O DCXYFEDJOCDNAF-UHFFFAOYSA-N 0.000 description 4
- 241000894006 Bacteria Species 0.000 description 4
- 108010014172 Factor V Proteins 0.000 description 4
- 208000032843 Hemorrhage Diseases 0.000 description 4
- 101000605403 Homo sapiens Plasminogen Proteins 0.000 description 4
- 101000763314 Homo sapiens Thrombomodulin Proteins 0.000 description 4
- 239000004472 Lysine Substances 0.000 description 4
- 101150076271 SAK gene Proteins 0.000 description 4
- 108010000499 Thromboplastin Proteins 0.000 description 4
- 102000002262 Thromboplastin Human genes 0.000 description 4
- 239000004480 active ingredient Substances 0.000 description 4
- 125000003295 alanine group Chemical group N[C@@H](C)C(=O)* 0.000 description 4
- 230000002785 anti-thrombosis Effects 0.000 description 4
- 229940127219 anticoagulant drug Drugs 0.000 description 4
- 238000013459 approach Methods 0.000 description 4
- 235000009582 asparagine Nutrition 0.000 description 4
- 229960001230 asparagine Drugs 0.000 description 4
- 208000034158 bleeding Diseases 0.000 description 4
- 230000000740 bleeding effect Effects 0.000 description 4
- 239000004202 carbamide Substances 0.000 description 4
- 238000005119 centrifugation Methods 0.000 description 4
- 230000008859 change Effects 0.000 description 4
- 238000007819 clotting time assay Methods 0.000 description 4
- 230000003111 delayed effect Effects 0.000 description 4
- 239000006167 equilibration buffer Substances 0.000 description 4
- 229960000301 factor viii Drugs 0.000 description 4
- 230000003480 fibrinolytic effect Effects 0.000 description 4
- XOXYHGOIRWABTC-UHFFFAOYSA-N gentisin Chemical compound C1=C(O)C=C2C(=O)C3=C(O)C=C(OC)C=C3OC2=C1 XOXYHGOIRWABTC-UHFFFAOYSA-N 0.000 description 4
- 102000051206 human THBD Human genes 0.000 description 4
- 230000007062 hydrolysis Effects 0.000 description 4
- 238000006460 hydrolysis reaction Methods 0.000 description 4
- 230000002209 hydrophobic effect Effects 0.000 description 4
- 238000011534 incubation Methods 0.000 description 4
- 230000002401 inhibitory effect Effects 0.000 description 4
- 238000004255 ion exchange chromatography Methods 0.000 description 4
- BPHPUYQFMNQIOC-NXRLNHOXSA-N isopropyl beta-D-thiogalactopyranoside Chemical compound CC(C)S[C@@H]1O[C@H](CO)[C@H](O)[C@H](O)[C@H]1O BPHPUYQFMNQIOC-NXRLNHOXSA-N 0.000 description 4
- 235000020183 skimmed milk Nutrition 0.000 description 4
- 238000002415 sodium dodecyl sulfate polyacrylamide gel electrophoresis Methods 0.000 description 4
- 239000003381 stabilizer Substances 0.000 description 4
- 239000000126 substance Substances 0.000 description 4
- 230000001225 therapeutic effect Effects 0.000 description 4
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 4
- 238000001262 western blot Methods 0.000 description 4
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 3
- 208000024172 Cardiovascular disease Diseases 0.000 description 3
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- 108010054218 Factor VIII Proteins 0.000 description 3
- 102000001690 Factor VIII Human genes 0.000 description 3
- 108010061932 Factor VIIIa Proteins 0.000 description 3
- 108010074105 Factor Va Proteins 0.000 description 3
- 108010024636 Glutathione Proteins 0.000 description 3
- 108010053070 Glutathione Disulfide Proteins 0.000 description 3
- 108091034117 Oligonucleotide Proteins 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- 108020004511 Recombinant DNA Proteins 0.000 description 3
- 102000007056 Recombinant Fusion Proteins Human genes 0.000 description 3
- 108010008281 Recombinant Fusion Proteins Proteins 0.000 description 3
- 229920002684 Sepharose Polymers 0.000 description 3
- 108700005078 Synthetic Genes Proteins 0.000 description 3
- 101710137500 T7 RNA polymerase Proteins 0.000 description 3
- 229940122388 Thrombin inhibitor Drugs 0.000 description 3
- 239000013504 Triton X-100 Substances 0.000 description 3
- 229920004890 Triton X-100 Polymers 0.000 description 3
- 238000002835 absorbance Methods 0.000 description 3
- 239000012190 activator Substances 0.000 description 3
- 229960000723 ampicillin Drugs 0.000 description 3
- AVKUERGKIZMTKX-NJBDSQKTSA-N ampicillin Chemical compound C1([C@@H](N)C(=O)N[C@H]2[C@H]3SC([C@@H](N3C2=O)C(O)=O)(C)C)=CC=CC=C1 AVKUERGKIZMTKX-NJBDSQKTSA-N 0.000 description 3
- 239000011324 bead Substances 0.000 description 3
- 230000023555 blood coagulation Effects 0.000 description 3
- 238000012512 characterization method Methods 0.000 description 3
- 238000001514 detection method Methods 0.000 description 3
- 239000003085 diluting agent Substances 0.000 description 3
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 3
- 231100000673 dose–response relationship Toxicity 0.000 description 3
- 238000004520 electroporation Methods 0.000 description 3
- 230000002255 enzymatic effect Effects 0.000 description 3
- 239000013613 expression plasmid Substances 0.000 description 3
- 230000002068 genetic effect Effects 0.000 description 3
- RWSXRVCMGQZWBV-WDSKDSINSA-N glutathione Chemical compound OC(=O)[C@@H](N)CCC(=O)N[C@@H](CS)C(=O)NCC(O)=O RWSXRVCMGQZWBV-WDSKDSINSA-N 0.000 description 3
- YPZRWBKMTBYPTK-BJDJZHNGSA-N glutathione disulfide Chemical compound OC(=O)[C@@H](N)CCC(=O)N[C@H](C(=O)NCC(O)=O)CSSC[C@@H](C(=O)NCC(O)=O)NC(=O)CC[C@H](N)C(O)=O YPZRWBKMTBYPTK-BJDJZHNGSA-N 0.000 description 3
- 230000001976 improved effect Effects 0.000 description 3
- 238000010348 incorporation Methods 0.000 description 3
- 239000003112 inhibitor Substances 0.000 description 3
- 235000018977 lysine Nutrition 0.000 description 3
- 230000004048 modification Effects 0.000 description 3
- 238000012986 modification Methods 0.000 description 3
- 208000010125 myocardial infarction Diseases 0.000 description 3
- 210000004897 n-terminal region Anatomy 0.000 description 3
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 3
- 239000002953 phosphate buffered saline Substances 0.000 description 3
- 239000007787 solid Substances 0.000 description 3
- 239000000758 substrate Substances 0.000 description 3
- 239000000725 suspension Substances 0.000 description 3
- 239000003868 thrombin inhibitor Substances 0.000 description 3
- 210000001519 tissue Anatomy 0.000 description 3
- 230000009466 transformation Effects 0.000 description 3
- 230000001052 transient effect Effects 0.000 description 3
- 230000014616 translation Effects 0.000 description 3
- 238000005406 washing Methods 0.000 description 3
- MTCFGRXMJLQNBG-REOHCLBHSA-N (2S)-2-Amino-3-hydroxypropansäure Chemical compound OC[C@H](N)C(O)=O MTCFGRXMJLQNBG-REOHCLBHSA-N 0.000 description 2
- RDEIXVOBVLKYNT-VQBXQJRRSA-N (2r,3r,4r,5r)-2-[(1s,2s,3r,4s,6r)-4,6-diamino-3-[(2r,3r,6s)-3-amino-6-(1-aminoethyl)oxan-2-yl]oxy-2-hydroxycyclohexyl]oxy-5-methyl-4-(methylamino)oxane-3,5-diol;(2r,3r,4r,5r)-2-[(1s,2s,3r,4s,6r)-4,6-diamino-3-[(2r,3r,6s)-3-amino-6-(aminomethyl)oxan-2-yl]o Chemical compound OS(O)(=O)=O.O1C[C@@](O)(C)[C@H](NC)[C@@H](O)[C@H]1O[C@@H]1[C@@H](O)[C@H](O[C@@H]2[C@@H](CC[C@@H](CN)O2)N)[C@@H](N)C[C@H]1N.O1C[C@@](O)(C)[C@H](NC)[C@@H](O)[C@H]1O[C@@H]1[C@@H](O)[C@H](O[C@@H]2[C@@H](CC[C@H](O2)C(C)N)N)[C@@H](N)C[C@H]1N.O1[C@H](C(C)NC)CC[C@@H](N)[C@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](NC)[C@@](C)(O)CO2)O)[C@H](N)C[C@@H]1N RDEIXVOBVLKYNT-VQBXQJRRSA-N 0.000 description 2
- PUMZXCBVHLCWQG-UHFFFAOYSA-N 1-(4-Hydroxyphenyl)-2-aminoethanol hydrochloride Chemical compound [Cl-].[NH3+]CC(O)C1=CC=C(O)C=C1 PUMZXCBVHLCWQG-UHFFFAOYSA-N 0.000 description 2
- FJKROLUGYXJWQN-UHFFFAOYSA-N 4-hydroxybenzoic acid Chemical compound OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 2
- SLXKOJJOQWFEFD-UHFFFAOYSA-N 6-aminohexanoic acid Chemical compound NCCCCCC(O)=O SLXKOJJOQWFEFD-UHFFFAOYSA-N 0.000 description 2
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 2
- 229920002271 DEAE-Sepharose Polymers 0.000 description 2
- 108010014303 DNA-directed DNA polymerase Proteins 0.000 description 2
- 102000016928 DNA-directed DNA polymerase Human genes 0.000 description 2
- 102000010911 Enzyme Precursors Human genes 0.000 description 2
- 108010062466 Enzyme Precursors Proteins 0.000 description 2
- 241000672609 Escherichia coli BL21 Species 0.000 description 2
- 108010074864 Factor XI Proteins 0.000 description 2
- 108010080865 Factor XII Proteins 0.000 description 2
- 102000000429 Factor XII Human genes 0.000 description 2
- 108010049003 Fibrinogen Proteins 0.000 description 2
- 102000008946 Fibrinogen Human genes 0.000 description 2
- 241000233866 Fungi Species 0.000 description 2
- 108010000487 High-Molecular-Weight Kininogen Proteins 0.000 description 2
- 241000282412 Homo Species 0.000 description 2
- 102000008100 Human Serum Albumin Human genes 0.000 description 2
- 108091006905 Human Serum Albumin Proteins 0.000 description 2
- 102100035792 Kininogen-1 Human genes 0.000 description 2
- ODKSFYDXXFIFQN-BYPYZUCNSA-N L-arginine Chemical compound OC(=O)[C@@H](N)CCCN=C(N)N ODKSFYDXXFIFQN-BYPYZUCNSA-N 0.000 description 2
- ODKSFYDXXFIFQN-BYPYZUCNSA-P L-argininium(2+) Chemical compound NC(=[NH2+])NCCC[C@H]([NH3+])C(O)=O ODKSFYDXXFIFQN-BYPYZUCNSA-P 0.000 description 2
- 125000000174 L-prolyl group Chemical group [H]N1C([H])([H])C([H])([H])C([H])([H])[C@@]1([H])C(*)=O 0.000 description 2
- 229930195725 Mannitol Natural products 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- 229920001213 Polysorbate 20 Polymers 0.000 description 2
- 108010022999 Serine Proteases Proteins 0.000 description 2
- 102000012479 Serine Proteases Human genes 0.000 description 2
- 102000008847 Serpin Human genes 0.000 description 2
- 108050000761 Serpin Proteins 0.000 description 2
- VMHLLURERBWHNL-UHFFFAOYSA-M Sodium acetate Chemical compound [Na+].CC([O-])=O VMHLLURERBWHNL-UHFFFAOYSA-M 0.000 description 2
- DBMJMQXJHONAFJ-UHFFFAOYSA-M Sodium laurylsulphate Chemical compound [Na+].CCCCCCCCCCCCOS([O-])(=O)=O DBMJMQXJHONAFJ-UHFFFAOYSA-M 0.000 description 2
- AYFVYJQAPQTCCC-UHFFFAOYSA-N Threonine Natural products CC(O)C(N)C(O)=O AYFVYJQAPQTCCC-UHFFFAOYSA-N 0.000 description 2
- 239000004473 Threonine Substances 0.000 description 2
- YJQCOFNZVFGCAF-UHFFFAOYSA-N Tunicamycin II Natural products O1C(CC(O)C2C(C(O)C(O2)N2C(NC(=O)C=C2)=O)O)C(O)C(O)C(NC(=O)C=CCCCCCCCCC(C)C)C1OC1OC(CO)C(O)C(O)C1NC(C)=O YJQCOFNZVFGCAF-UHFFFAOYSA-N 0.000 description 2
- SXEHKFHPFVVDIR-UHFFFAOYSA-N [4-(4-hydrazinylphenyl)phenyl]hydrazine Chemical compound C1=CC(NN)=CC=C1C1=CC=C(NN)C=C1 SXEHKFHPFVVDIR-UHFFFAOYSA-N 0.000 description 2
- MZVQCMJNVPIDEA-UHFFFAOYSA-N [CH2]CN(CC)CC Chemical compound [CH2]CN(CC)CC MZVQCMJNVPIDEA-UHFFFAOYSA-N 0.000 description 2
- 238000001042 affinity chromatography Methods 0.000 description 2
- 239000002506 anticoagulant protein Substances 0.000 description 2
- 230000009286 beneficial effect Effects 0.000 description 2
- 230000004071 biological effect Effects 0.000 description 2
- 230000017531 blood circulation Effects 0.000 description 2
- 239000003114 blood coagulation factor Substances 0.000 description 2
- 229960000182 blood factors Drugs 0.000 description 2
- 238000006664 bond formation reaction Methods 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 230000004087 circulation Effects 0.000 description 2
- 239000002299 complementary DNA Substances 0.000 description 2
- 238000010790 dilution Methods 0.000 description 2
- 239000012895 dilution Substances 0.000 description 2
- 208000035475 disorder Diseases 0.000 description 2
- 238000005516 engineering process Methods 0.000 description 2
- 238000002474 experimental method Methods 0.000 description 2
- 238000000855 fermentation Methods 0.000 description 2
- 230000004151 fermentation Effects 0.000 description 2
- 229940012952 fibrinogen Drugs 0.000 description 2
- 230000013595 glycosylation Effects 0.000 description 2
- 238000006206 glycosylation reaction Methods 0.000 description 2
- 125000003630 glycyl group Chemical group [H]N([H])C([H])([H])C(*)=O 0.000 description 2
- XKUKSGPZAADMRA-UHFFFAOYSA-N glycyl-glycyl-glycine Chemical compound NCC(=O)NCC(=O)NCC(O)=O XKUKSGPZAADMRA-UHFFFAOYSA-N 0.000 description 2
- 230000023597 hemostasis Effects 0.000 description 2
- 230000002439 hemostatic effect Effects 0.000 description 2
- 238000004191 hydrophobic interaction chromatography Methods 0.000 description 2
- 239000012535 impurity Substances 0.000 description 2
- 238000011065 in-situ storage Methods 0.000 description 2
- 230000002779 inactivation Effects 0.000 description 2
- 230000006698 induction Effects 0.000 description 2
- 238000001802 infusion Methods 0.000 description 2
- 230000000977 initiatory effect Effects 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- 230000003993 interaction Effects 0.000 description 2
- 238000010253 intravenous injection Methods 0.000 description 2
- 238000002955 isolation Methods 0.000 description 2
- 239000000594 mannitol Substances 0.000 description 2
- 235000010355 mannitol Nutrition 0.000 description 2
- 239000000463 material Substances 0.000 description 2
- 239000011159 matrix material Substances 0.000 description 2
- 239000012092 media component Substances 0.000 description 2
- 238000002483 medication Methods 0.000 description 2
- 108020004999 messenger RNA Proteins 0.000 description 2
- 229960001576 octopamine Drugs 0.000 description 2
- 239000000546 pharmaceutical excipient Substances 0.000 description 2
- 239000008363 phosphate buffer Substances 0.000 description 2
- 238000003752 polymerase chain reaction Methods 0.000 description 2
- 108091033319 polynucleotide Proteins 0.000 description 2
- 102000040430 polynucleotide Human genes 0.000 description 2
- 239000002157 polynucleotide Substances 0.000 description 2
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 2
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 2
- 239000002243 precursor Substances 0.000 description 2
- 239000003755 preservative agent Substances 0.000 description 2
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 2
- 230000002947 procoagulating effect Effects 0.000 description 2
- 230000001737 promoting effect Effects 0.000 description 2
- 230000002797 proteolythic effect Effects 0.000 description 2
- 239000011541 reaction mixture Substances 0.000 description 2
- 102000005962 receptors Human genes 0.000 description 2
- 108020003175 receptors Proteins 0.000 description 2
- 230000002829 reductive effect Effects 0.000 description 2
- 230000008439 repair process Effects 0.000 description 2
- 150000003839 salts Chemical class 0.000 description 2
- 239000003001 serine protease inhibitor Substances 0.000 description 2
- 239000001632 sodium acetate Substances 0.000 description 2
- 235000017281 sodium acetate Nutrition 0.000 description 2
- 239000002904 solvent Substances 0.000 description 2
- 230000000638 stimulation Effects 0.000 description 2
- 238000003860 storage Methods 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- 230000001732 thrombotic effect Effects 0.000 description 2
- 101150010939 tpa gene Proteins 0.000 description 2
- 238000013519 translation Methods 0.000 description 2
- LWIHDJKSTIGBAC-UHFFFAOYSA-K tripotassium phosphate Chemical compound [K+].[K+].[K+].[O-]P([O-])([O-])=O LWIHDJKSTIGBAC-UHFFFAOYSA-K 0.000 description 2
- ZHSGGJXRNHWHRS-VIDYELAYSA-N tunicamycin Chemical compound O([C@H]1[C@@H]([C@H]([C@@H](O)[C@@H](CC(O)[C@@H]2[C@H]([C@@H](O)[C@@H](O2)N2C(NC(=O)C=C2)=O)O)O1)O)NC(=O)/C=C/CC(C)C)[C@H]1O[C@H](CO)[C@@H](O)[C@H](O)[C@H]1NC(C)=O ZHSGGJXRNHWHRS-VIDYELAYSA-N 0.000 description 2
- MEYZYGMYMLNUHJ-UHFFFAOYSA-N tunicamycin Natural products CC(C)CCCCCCCCCC=CC(=O)NC1C(O)C(O)C(CC(O)C2OC(C(O)C2O)N3C=CC(=O)NC3=O)OC1OC4OC(CO)C(O)C(O)C4NC(=O)C MEYZYGMYMLNUHJ-UHFFFAOYSA-N 0.000 description 2
- 230000002792 vascular Effects 0.000 description 2
- 210000005166 vasculature Anatomy 0.000 description 2
- QIJRTFXNRTXDIP-UHFFFAOYSA-N (1-carboxy-2-sulfanylethyl)azanium;chloride;hydrate Chemical compound O.Cl.SCC(N)C(O)=O QIJRTFXNRTXDIP-UHFFFAOYSA-N 0.000 description 1
- SBKVPJHMSUXZTA-MEJXFZFPSA-N (2S)-2-[[(2S)-2-[[(2S)-1-[(2S)-5-amino-2-[[2-[[(2S)-1-[(2S)-6-amino-2-[[(2S)-2-[[(2S)-5-amino-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-amino-3-(1H-indol-3-yl)propanoyl]amino]-3-(1H-imidazol-4-yl)propanoyl]amino]-3-(1H-indol-3-yl)propanoyl]amino]-4-methylpentanoyl]amino]-5-oxopentanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]pyrrolidine-2-carbonyl]amino]acetyl]amino]-5-oxopentanoyl]pyrrolidine-2-carbonyl]amino]-4-methylsulfanylbutanoyl]amino]-3-(4-hydroxyphenyl)propanoic acid Chemical group C([C@@H](C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCCN)C(=O)N1CCC[C@H]1C(=O)NCC(=O)N[C@@H](CCC(N)=O)C(=O)N1CCC[C@H]1C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(O)=O)NC(=O)[C@@H](N)CC=1C2=CC=CC=C2NC=1)C1=CNC=N1 SBKVPJHMSUXZTA-MEJXFZFPSA-N 0.000 description 1
- JWICNZAGYSIBAR-LEEGLKINSA-N (4s)-4-[[2-[[(2s)-2-[[(2s)-2-[[(2s)-2-aminopropanoyl]amino]-3-carboxypropanoyl]amino]-3-hydroxypropanoyl]amino]acetyl]amino]-5-[[2-[[(2s)-3-carboxy-1-[[(2s)-1-[[1-[[(2s)-1-[[(2s)-4-carboxy-1-[[2-[[2-[[2-[[(2s)-1-[[(1s)-1-carboxy-4-(diaminomethylideneamino Chemical compound NC(N)=NCCC[C@@H](C(O)=O)NC(=O)[C@H](C(C)C)NC(=O)CNC(=O)CNC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C)NC(=O)C(CC(C)C)NC(=O)[C@@H](NC(=O)[C@H](CC(O)=O)NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)CNC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](C)N)CC1=CC=CC=C1 JWICNZAGYSIBAR-LEEGLKINSA-N 0.000 description 1
- IIZPXYDJLKNOIY-JXPKJXOSSA-N 1-palmitoyl-2-arachidonoyl-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCC\C=C/C\C=C/C\C=C/C\C=C/CCCCC IIZPXYDJLKNOIY-JXPKJXOSSA-N 0.000 description 1
- KIUMMUBSPKGMOY-UHFFFAOYSA-N 3,3'-Dithiobis(6-nitrobenzoic acid) Chemical compound C1=C([N+]([O-])=O)C(C(=O)O)=CC(SSC=2C=C(C(=CC=2)[N+]([O-])=O)C(O)=O)=C1 KIUMMUBSPKGMOY-UHFFFAOYSA-N 0.000 description 1
- 229940090248 4-hydroxybenzoic acid Drugs 0.000 description 1
- 229920001817 Agar Polymers 0.000 description 1
- 108010088751 Albumins Proteins 0.000 description 1
- 102000009027 Albumins Human genes 0.000 description 1
- 102100036826 Aldehyde oxidase Human genes 0.000 description 1
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 1
- IYMAXBFPHPZYIK-BQBZGAKWSA-N Arg-Gly-Asp Chemical compound NC(N)=NCCC[C@H](N)C(=O)NCC(=O)N[C@@H](CC(O)=O)C(O)=O IYMAXBFPHPZYIK-BQBZGAKWSA-N 0.000 description 1
- BSYNRYMUTXBXSQ-UHFFFAOYSA-N Aspirin Chemical compound CC(=O)OC1=CC=CC=C1C(O)=O BSYNRYMUTXBXSQ-UHFFFAOYSA-N 0.000 description 1
- 102000015081 Blood Coagulation Factors Human genes 0.000 description 1
- 108010039209 Blood Coagulation Factors Proteins 0.000 description 1
- 238000009010 Bradford assay Methods 0.000 description 1
- 241001631457 Cannula Species 0.000 description 1
- 102100023804 Coagulation factor VII Human genes 0.000 description 1
- 102220489870 Cofilin-1_H46A_mutation Human genes 0.000 description 1
- 241000699802 Cricetulus griseus Species 0.000 description 1
- 102000012410 DNA Ligases Human genes 0.000 description 1
- 108010061982 DNA Ligases Proteins 0.000 description 1
- 230000004544 DNA amplification Effects 0.000 description 1
- 239000003155 DNA primer Substances 0.000 description 1
- 230000006820 DNA synthesis Effects 0.000 description 1
- 206010051055 Deep vein thrombosis Diseases 0.000 description 1
- 102000012545 EGF-like domains Human genes 0.000 description 1
- 108050002150 EGF-like domains Proteins 0.000 description 1
- 208000005189 Embolism Diseases 0.000 description 1
- 241000196324 Embryophyta Species 0.000 description 1
- 241000701867 Enterobacteria phage T7 Species 0.000 description 1
- 241001198387 Escherichia coli BL21(DE3) Species 0.000 description 1
- 108010023321 Factor VII Proteins 0.000 description 1
- 108010071289 Factor XIII Proteins 0.000 description 1
- 108010074860 Factor Xa Proteins 0.000 description 1
- 101800000974 Fibrinopeptide A Proteins 0.000 description 1
- 102400000525 Fibrinopeptide A Human genes 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 102000003886 Glycoproteins Human genes 0.000 description 1
- 108090000288 Glycoproteins Proteins 0.000 description 1
- 101710121996 Hexon protein p72 Proteins 0.000 description 1
- 101000928314 Homo sapiens Aldehyde oxidase Proteins 0.000 description 1
- 101500025419 Homo sapiens Epidermal growth factor Proteins 0.000 description 1
- 108090000144 Human Proteins Proteins 0.000 description 1
- 102000003839 Human Proteins Human genes 0.000 description 1
- 206010061218 Inflammation Diseases 0.000 description 1
- 206010048620 Intracardiac thrombus Diseases 0.000 description 1
- 208000032382 Ischaemic stroke Diseases 0.000 description 1
- 235000019766 L-Lysine Nutrition 0.000 description 1
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 1
- AGPKZVBTJJNPAG-WHFBIAKZSA-N L-isoleucine Chemical compound CC[C@H](C)[C@H](N)C(O)=O AGPKZVBTJJNPAG-WHFBIAKZSA-N 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- 108090001030 Lipoproteins Proteins 0.000 description 1
- 102000004895 Lipoproteins Human genes 0.000 description 1
- 239000006142 Luria-Bertani Agar Substances 0.000 description 1
- 101710125418 Major capsid protein Proteins 0.000 description 1
- 108010038049 Mating Factor Proteins 0.000 description 1
- 125000000729 N-terminal amino-acid group Chemical group 0.000 description 1
- 101800000135 N-terminal protein Proteins 0.000 description 1
- 239000000020 Nitrocellulose Substances 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 101800001452 P1 proteinase Proteins 0.000 description 1
- 238000012408 PCR amplification Methods 0.000 description 1
- 235000019483 Peanut oil Nutrition 0.000 description 1
- 108010033276 Peptide Fragments Proteins 0.000 description 1
- 102000007079 Peptide Fragments Human genes 0.000 description 1
- 108010002747 Pfu DNA polymerase Proteins 0.000 description 1
- 102000004160 Phosphoric Monoester Hydrolases Human genes 0.000 description 1
- 108090000608 Phosphoric Monoester Hydrolases Proteins 0.000 description 1
- 108091000080 Phosphotransferase Proteins 0.000 description 1
- 108090000113 Plasma Kallikrein Proteins 0.000 description 1
- ONIBWKKTOPOVIA-UHFFFAOYSA-N Proline Natural products OC(=O)C1CCCN1 ONIBWKKTOPOVIA-UHFFFAOYSA-N 0.000 description 1
- 101710111620 Protein C activator Proteins 0.000 description 1
- 229940096437 Protein S Drugs 0.000 description 1
- 108010066124 Protein S Proteins 0.000 description 1
- 108010094028 Prothrombin Proteins 0.000 description 1
- 102100027378 Prothrombin Human genes 0.000 description 1
- 241000283984 Rodentia Species 0.000 description 1
- 241000264435 Streptococcus dysgalactiae subsp. equisimilis Species 0.000 description 1
- 208000006011 Stroke Diseases 0.000 description 1
- 108010039185 Tenecteplase Proteins 0.000 description 1
- 102100031358 Urokinase-type plasminogen activator Human genes 0.000 description 1
- 208000024248 Vascular System injury Diseases 0.000 description 1
- 208000012339 Vascular injury Diseases 0.000 description 1
- 206010047249 Venous thrombosis Diseases 0.000 description 1
- 241000251539 Vertebrata <Metazoa> Species 0.000 description 1
- 102100028885 Vitamin K-dependent protein S Human genes 0.000 description 1
- 230000002159 abnormal effect Effects 0.000 description 1
- 230000001133 acceleration Effects 0.000 description 1
- 229960001138 acetylsalicylic acid Drugs 0.000 description 1
- 238000003916 acid precipitation Methods 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 230000002730 additional effect Effects 0.000 description 1
- 238000012382 advanced drug delivery Methods 0.000 description 1
- 238000013019 agitation Methods 0.000 description 1
- 229940050528 albumin Drugs 0.000 description 1
- 125000001931 aliphatic group Chemical group 0.000 description 1
- 102000003801 alpha-2-Antiplasmin Human genes 0.000 description 1
- 108090000183 alpha-2-Antiplasmin Proteins 0.000 description 1
- 229960002684 aminocaproic acid Drugs 0.000 description 1
- 238000012801 analytical assay Methods 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 229940127217 antithrombotic drug Drugs 0.000 description 1
- 108010072041 arginyl-glycyl-aspartic acid Proteins 0.000 description 1
- 210000001367 artery Anatomy 0.000 description 1
- 125000003118 aryl group Chemical group 0.000 description 1
- 235000003704 aspartic acid Nutrition 0.000 description 1
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 1
- OQFSQFPPLPISGP-UHFFFAOYSA-N beta-carboxyaspartic acid Natural products OC(=O)C(N)C(C(O)=O)C(O)=O OQFSQFPPLPISGP-UHFFFAOYSA-N 0.000 description 1
- 238000002306 biochemical method Methods 0.000 description 1
- 230000003115 biocidal effect Effects 0.000 description 1
- 239000003130 blood coagulation factor inhibitor Substances 0.000 description 1
- 239000012503 blood component Substances 0.000 description 1
- 230000036770 blood supply Effects 0.000 description 1
- 239000007853 buffer solution Substances 0.000 description 1
- 239000002775 capsule Substances 0.000 description 1
- 230000000747 cardiac effect Effects 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 238000010523 cascade reaction Methods 0.000 description 1
- 238000004113 cell culture Methods 0.000 description 1
- 230000005779 cell damage Effects 0.000 description 1
- 208000037887 cell injury Diseases 0.000 description 1
- 238000011260 co-administration Methods 0.000 description 1
- 230000004186 co-expression Effects 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 238000002648 combination therapy Methods 0.000 description 1
- 230000021615 conjugation Effects 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 230000002596 correlated effect Effects 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 230000008025 crystallization Effects 0.000 description 1
- 238000012258 culturing Methods 0.000 description 1
- 238000005520 cutting process Methods 0.000 description 1
- ATDGTVJJHBUTRL-UHFFFAOYSA-N cyanogen bromide Chemical compound BrC#N ATDGTVJJHBUTRL-UHFFFAOYSA-N 0.000 description 1
- 125000000151 cysteine group Chemical group N[C@@H](CS)C(=O)* 0.000 description 1
- 229960001305 cysteine hydrochloride Drugs 0.000 description 1
- 210000000805 cytoplasm Anatomy 0.000 description 1
- 230000034994 death Effects 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 239000008121 dextrose Substances 0.000 description 1
- 238000000502 dialysis Methods 0.000 description 1
- 235000005911 diet Nutrition 0.000 description 1
- 230000037213 diet Effects 0.000 description 1
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 1
- 230000008034 disappearance Effects 0.000 description 1
- 201000010099 disease Diseases 0.000 description 1
- PXEDJBXQKAGXNJ-QTNFYWBSSA-L disodium L-glutamate Chemical compound [Na+].[Na+].[O-]C(=O)[C@@H](N)CCC([O-])=O PXEDJBXQKAGXNJ-QTNFYWBSSA-L 0.000 description 1
- 239000002552 dosage form Substances 0.000 description 1
- 238000009510 drug design Methods 0.000 description 1
- 238000009509 drug development Methods 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- 238000001962 electrophoresis Methods 0.000 description 1
- 238000010828 elution Methods 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 210000002889 endothelial cell Anatomy 0.000 description 1
- 210000002919 epithelial cell Anatomy 0.000 description 1
- 230000008508 epithelial proliferation Effects 0.000 description 1
- 210000000981 epithelium Anatomy 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- 238000012869 ethanol precipitation Methods 0.000 description 1
- BEFDCLMNVWHSGT-UHFFFAOYSA-N ethenylcyclopentane Chemical compound C=CC1CCCC1 BEFDCLMNVWHSGT-UHFFFAOYSA-N 0.000 description 1
- 230000006624 extrinsic pathway Effects 0.000 description 1
- 229940012413 factor vii Drugs 0.000 description 1
- 229940012444 factor xiii Drugs 0.000 description 1
- 230000008713 feedback mechanism Effects 0.000 description 1
- 230000020764 fibrinolysis Effects 0.000 description 1
- 239000000796 flavoring agent Substances 0.000 description 1
- 239000007850 fluorescent dye Substances 0.000 description 1
- 235000013355 food flavoring agent Nutrition 0.000 description 1
- 238000004108 freeze drying Methods 0.000 description 1
- 238000002825 functional assay Methods 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 238000012215 gene cloning Methods 0.000 description 1
- 238000010353 genetic engineering Methods 0.000 description 1
- 229960001031 glucose Drugs 0.000 description 1
- 125000000404 glutamine group Chemical group N[C@@H](CCC(N)=O)C(=O)* 0.000 description 1
- 108010067216 glycyl-glycyl-glycine Proteins 0.000 description 1
- 238000013537 high throughput screening Methods 0.000 description 1
- HNDVDQJCIGZPNO-UHFFFAOYSA-N histidine Natural products OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 description 1
- 238000002744 homologous recombination Methods 0.000 description 1
- 230000006801 homologous recombination Effects 0.000 description 1
- 229940116978 human epidermal growth factor Drugs 0.000 description 1
- 230000004047 hyperresponsiveness Effects 0.000 description 1
- 230000028993 immune response Effects 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 230000001939 inductive effect Effects 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- 239000003999 initiator Substances 0.000 description 1
- 239000002054 inoculum Substances 0.000 description 1
- 230000003834 intracellular effect Effects 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000010255 intramuscular injection Methods 0.000 description 1
- 239000007927 intramuscular injection Substances 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- 230000006623 intrinsic pathway Effects 0.000 description 1
- 238000005342 ion exchange Methods 0.000 description 1
- 208000028867 ischemia Diseases 0.000 description 1
- 229960000310 isoleucine Drugs 0.000 description 1
- AGPKZVBTJJNPAG-UHFFFAOYSA-N isoleucine Natural products CCC(C)C(N)C(O)=O AGPKZVBTJJNPAG-UHFFFAOYSA-N 0.000 description 1
- 229930027917 kanamycin Natural products 0.000 description 1
- 229960000318 kanamycin Drugs 0.000 description 1
- SBUJHOSQTJFQJX-NOAMYHISSA-N kanamycin Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CN)O[C@@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](N)[C@H](O)[C@@H](CO)O2)O)[C@H](N)C[C@@H]1N SBUJHOSQTJFQJX-NOAMYHISSA-N 0.000 description 1
- 229930182823 kanamycin A Natural products 0.000 description 1
- 238000012933 kinetic analysis Methods 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 229960001375 lactose Drugs 0.000 description 1
- 239000000787 lecithin Substances 0.000 description 1
- 229940067606 lecithin Drugs 0.000 description 1
- 235000010445 lecithin Nutrition 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 238000012417 linear regression Methods 0.000 description 1
- 239000002502 liposome Substances 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 238000012044 lysine affinity chromatography Methods 0.000 description 1
- 125000003588 lysine group Chemical group [H]N([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])(N([H])[H])C(*)=O 0.000 description 1
- 230000002934 lysing effect Effects 0.000 description 1
- 230000014759 maintenance of location Effects 0.000 description 1
- 229960001855 mannitol Drugs 0.000 description 1
- 239000003550 marker Substances 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 230000010534 mechanism of action Effects 0.000 description 1
- 230000004089 microcirculation Effects 0.000 description 1
- 238000010369 molecular cloning Methods 0.000 description 1
- 238000003032 molecular docking Methods 0.000 description 1
- 238000012544 monitoring process Methods 0.000 description 1
- 235000013923 monosodium glutamate Nutrition 0.000 description 1
- 230000000869 mutational effect Effects 0.000 description 1
- 208000031225 myocardial ischemia Diseases 0.000 description 1
- 230000014508 negative regulation of coagulation Effects 0.000 description 1
- GVUGOAYIVIDWIO-UFWWTJHBSA-N nepidermin Chemical compound C([C@@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)NCC(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CS)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(O)=O)NC(=O)CNC(=O)[C@@H](NC(=O)[C@@H](NC(=O)[C@H](CS)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CS)NC(=O)[C@H](C)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](C)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CCSC)NC(=O)[C@H](CS)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CS)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)CNC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CC(C)C)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CS)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC(N)=O)C(C)C)[C@@H](C)CC)C(C)C)C(C)C)C1=CC=C(O)C=C1 GVUGOAYIVIDWIO-UFWWTJHBSA-N 0.000 description 1
- 229920001220 nitrocellulos Polymers 0.000 description 1
- 231100000252 nontoxic Toxicity 0.000 description 1
- 230000003000 nontoxic effect Effects 0.000 description 1
- 230000000414 obstructive effect Effects 0.000 description 1
- 238000005580 one pot reaction Methods 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- 210000000056 organ Anatomy 0.000 description 1
- 210000001672 ovary Anatomy 0.000 description 1
- 238000007500 overflow downdraw method Methods 0.000 description 1
- 230000001590 oxidative effect Effects 0.000 description 1
- 239000006179 pH buffering agent Substances 0.000 description 1
- 238000007911 parenteral administration Methods 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 230000008506 pathogenesis Effects 0.000 description 1
- 239000000312 peanut oil Substances 0.000 description 1
- 230000002572 peristaltic effect Effects 0.000 description 1
- 238000001050 pharmacotherapy Methods 0.000 description 1
- 239000012071 phase Substances 0.000 description 1
- 102000020233 phosphotransferase Human genes 0.000 description 1
- 230000035790 physiological processes and functions Effects 0.000 description 1
- 239000002504 physiological saline solution Substances 0.000 description 1
- 239000013600 plasmid vector Substances 0.000 description 1
- 229920002401 polyacrylamide Polymers 0.000 description 1
- 239000013641 positive control Substances 0.000 description 1
- 229910000160 potassium phosphate Inorganic materials 0.000 description 1
- 235000011009 potassium phosphates Nutrition 0.000 description 1
- 230000003389 potentiating effect Effects 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 230000000644 propagated effect Effects 0.000 description 1
- 238000000734 protein sequencing Methods 0.000 description 1
- 230000006337 proteolytic cleavage Effects 0.000 description 1
- 229940039716 prothrombin Drugs 0.000 description 1
- 238000013139 quantization Methods 0.000 description 1
- 230000007420 reactivation Effects 0.000 description 1
- 238000010188 recombinant method Methods 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 238000000518 rheometry Methods 0.000 description 1
- 239000012723 sample buffer Substances 0.000 description 1
- 238000007480 sanger sequencing Methods 0.000 description 1
- 238000007789 sealing Methods 0.000 description 1
- 230000028327 secretion Effects 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 210000002966 serum Anatomy 0.000 description 1
- 239000008159 sesame oil Substances 0.000 description 1
- 235000011803 sesame oil Nutrition 0.000 description 1
- WXMKPNITSTVMEF-UHFFFAOYSA-M sodium benzoate Chemical compound [Na+].[O-]C(=O)C1=CC=CC=C1 WXMKPNITSTVMEF-UHFFFAOYSA-M 0.000 description 1
- 239000004299 sodium benzoate Substances 0.000 description 1
- 235000010234 sodium benzoate Nutrition 0.000 description 1
- BEOOHQFXGBMRKU-UHFFFAOYSA-N sodium cyanoborohydride Chemical compound [Na+].[B-]C#N BEOOHQFXGBMRKU-UHFFFAOYSA-N 0.000 description 1
- 229940073490 sodium glutamate Drugs 0.000 description 1
- 238000010532 solid phase synthesis reaction Methods 0.000 description 1
- 238000000527 sonication Methods 0.000 description 1
- 239000004334 sorbic acid Substances 0.000 description 1
- 235000010199 sorbic acid Nutrition 0.000 description 1
- 229940075582 sorbic acid Drugs 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 238000002798 spectrophotometry method Methods 0.000 description 1
- 230000002269 spontaneous effect Effects 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 239000008174 sterile solution Substances 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 238000010254 subcutaneous injection Methods 0.000 description 1
- 239000007929 subcutaneous injection Substances 0.000 description 1
- 239000000829 suppository Substances 0.000 description 1
- 230000001629 suppression Effects 0.000 description 1
- 238000001356 surgical procedure Methods 0.000 description 1
- 230000004083 survival effect Effects 0.000 description 1
- 239000000375 suspending agent Substances 0.000 description 1
- 208000011580 syndromic disease Diseases 0.000 description 1
- 230000001839 systemic circulation Effects 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- 229960000216 tenecteplase Drugs 0.000 description 1
- 229940124597 therapeutic agent Drugs 0.000 description 1
- 201000005665 thrombophilia Diseases 0.000 description 1
- 230000036962 time dependent Effects 0.000 description 1
- 238000011200 topical administration Methods 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 230000032258 transport Effects 0.000 description 1
- YNJBWRMUSHSURL-UHFFFAOYSA-N trichloroacetic acid Chemical compound OC(=O)C(Cl)(Cl)Cl YNJBWRMUSHSURL-UHFFFAOYSA-N 0.000 description 1
- VBEQCZHXXJYVRD-GACYYNSASA-N uroanthelone Chemical compound C([C@@H](C(=O)N[C@H](C(=O)N[C@@H](CS)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CS)C(=O)N[C@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)NCC(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H](CO)C(=O)NCC(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CS)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(O)=O)C(C)C)[C@@H](C)O)NC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@@H](NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H](CCSC)NC(=O)[C@H](CS)NC(=O)[C@@H](NC(=O)CNC(=O)CNC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CS)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)CNC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CS)NC(=O)CNC(=O)[C@H]1N(CCC1)C(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC(N)=O)C(C)C)[C@@H](C)CC)C1=CC=C(O)C=C1 VBEQCZHXXJYVRD-GACYYNSASA-N 0.000 description 1
- 210000003462 vein Anatomy 0.000 description 1
- 230000034365 zymogen activation Effects 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/14—Hydrolases (3)
- C12N9/48—Hydrolases (3) acting on peptide bonds (3.4)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K19/00—Hybrid peptides, i.e. peptides covalently bound to nucleic acids, or non-covalently bound protein-protein complexes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/164—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from bacteria
- A61K38/166—Streptokinase
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/1703—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates
- A61K38/1709—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates from mammals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/43—Enzymes; Proenzymes; Derivatives thereof
- A61K38/54—Mixtures of enzymes or proenzymes covered by more than a single one of groups A61K38/44 - A61K38/46 or A61K38/51 - A61K38/53
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/02—Antithrombotic agents; Anticoagulants; Platelet aggregation inhibitors
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/195—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from bacteria
- C07K14/315—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from bacteria from Streptococcus (G), e.g. Enterococci
- C07K14/3153—Streptokinase
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/745—Blood coagulation or fibrinolysis factors
- C07K14/7455—Thrombomodulin
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/14—Hydrolases (3)
- C12N9/48—Hydrolases (3) acting on peptide bonds (3.4)
- C12N9/50—Proteinases, e.g. Endopeptidases (3.4.21-3.4.25)
- C12N9/52—Proteinases, e.g. Endopeptidases (3.4.21-3.4.25) derived from bacteria or Archaea
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/14—Hydrolases (3)
- C12N9/48—Hydrolases (3) acting on peptide bonds (3.4)
- C12N9/50—Proteinases, e.g. Endopeptidases (3.4.21-3.4.25)
- C12N9/64—Proteinases, e.g. Endopeptidases (3.4.21-3.4.25) derived from animal tissue
- C12N9/6421—Proteinases, e.g. Endopeptidases (3.4.21-3.4.25) derived from animal tissue from mammals
- C12N9/6424—Serine endopeptidases (3.4.21)
- C12N9/6456—Plasminogen activators
- C12N9/6459—Plasminogen activators t-plasminogen activator (3.4.21.68), i.e. tPA
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/96—Stabilising an enzyme by forming an adduct or a composition; Forming enzyme conjugates
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Y—ENZYMES
- C12Y304/00—Hydrolases acting on peptide bonds, i.e. peptidases (3.4)
- C12Y304/21—Serine endopeptidases (3.4.21)
- C12Y304/21069—Protein C activated (3.4.21.69)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02A—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE
- Y02A50/00—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE in human health protection, e.g. against extreme weather
- Y02A50/30—Against vector-borne diseases, e.g. mosquito-borne, fly-borne, tick-borne or waterborne diseases whose impact is exacerbated by climate change
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Genetics & Genomics (AREA)
- Zoology (AREA)
- Biochemistry (AREA)
- Wood Science & Technology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Molecular Biology (AREA)
- Gastroenterology & Hepatology (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- General Engineering & Computer Science (AREA)
- Biomedical Technology (AREA)
- Immunology (AREA)
- Epidemiology (AREA)
- Biotechnology (AREA)
- Microbiology (AREA)
- Biophysics (AREA)
- Hematology (AREA)
- Toxicology (AREA)
- Marine Sciences & Fisheries (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Diabetes (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Peptides Or Proteins (AREA)
- Enzymes And Modification Thereof (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
Description
脂肪族、非極性:G A P I L V
極性、無荷電:C S T M N Q
極性、荷電:D E K R 芳香族H F W Y
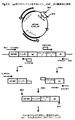
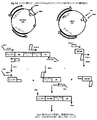
遺伝子構築物:
EGF4、5、6ドメイン配列は、酵母ピチア・パストリス(Pichia pastoris)における最適な発現のために商業的にカスタム合成(GeneScript Inc、米国)されたヒトトロンボモジュリンcDNAのものであった。合成遺伝子セグメントを正しい順序でライゲーションし、細菌プラスミドでクローニングした。一方のトロンボモジュリンのEGF4、5、6ドメインと血栓溶解剤(例えば、SAK、SK又はtPA(又はこれらの誘導体/変異体))との融合構築物を本質的に、(a)化学的手法を用いたカスタム遺伝子合成と、(b)適切なプラスミドから特異的に設計したプライマーを使用して選択された遺伝子セグメントを得るための定評のあるPCR技術の使用(以下の実施例で用いた方法を参照のこと)とを組み合わせ、続いてPCRで得られた遺伝子セグメントブロックを単離し、これらをオーバーラップエクステンションPCR等の特殊なPCR法を用いてインフレームで「融合」することによって行った。一般に、通常のPCRは、適切な高処理能力の熱安定性DNAポリメラーゼ(Fermantas Inc.又はStratagene Inc.のPfu DNAポリメラーゼ)又は高フィデリティpfuターボ(Stratagene Inc.)酵素を使用して行われた。ハイブリッドDNA構築物を、タンパク質の同時発現のないルーチンのプラスミドサブクローニングのための適切な大腸菌株XL−Blue及びT7 RNA Polプロモーター下でのタンパク質発現のための株BL21(DE3)株(Novagen Inc.、マディソン、WI、米国から調達)への形質変換によりT7 RNAポリメラーゼプロモーターをベースとした発現ベクターpET23−dにおいてクローニング/発現させ、またベクターpPIC−9Kにインフレームα交配因子シグナル配列を有するメタノール誘導性プロモーター下で酵母(ピチア・パストリス)において発現させ、GS115細胞を発現に使用した(Invitrogen Life Technologies、カリフォルニア、米国)。様々な制限エンドヌクレアーゼ、T4 DNAリガーゼ及び他のDNA修飾酵素をNew England Biolabs(ビバリー、MA)から入手した。オリゴヌクレオチドプライマーは、Biobasic,Inc.(カナダ)から入手した。DNAの精製及びPCR増幅産物のアガロースゲルからの抽出を、Qiagen GmbH(ドイツ)から入手可能なキットを使用して行った。蛍光色素を使用した自動DNAシーケンシングを、16本のキャピラリのApplied Biosystems 3130xlジェネティックアナライザで行った。Glu−プラスミノーゲンはRoche Diagnostics GmbH(ペンツベルク、ドイツ)から購入するか、アフィニティクロマトグラフィによりヒト血漿から精製した(Deutsch and Mertz、1970)。ヒトタンパク質C、トロンビン、ヒルジンはCalbiochem(米国)から購入し、ウサギの標準トロンボモジュリン及び組み換えトロンボモジュリンを両方共、American Diagnostica Inc.(米国)から購入した。N末端気相アミノ酸シーケンシングを、Applied Biosystemsシーケンサーモデル491を使用して行った。ウロキナーゼ、EACA、シアノ水素化ホウ素ナトリウム及びL−リジンをSigma Chemical Co.(セントルイス、米国)から購入した。フェニルアガロース6XL及びDEAEセファロース(ファストフロー)をGE−Amersham(ウプサラ、スウェーデン)から調達し、Ni−NTAビーズをQiagenから調達した。他の試薬は全て入手可能な範囲で最高の分析グレードであった。
1.組み換えDNA融合方法:
まとめて組み換えDNA技術と称される様々な方法は分子生物学の分野で今や周知である。幾つかの技法、標準的なプロトコル及びこれらの変形は幾つかの参考文献、例えばSambrook et al.,Molecular Cloning:A laboratory Manual(IInd edition,Cold Spring Harbor Press,New York.,1989;McPherson,M.J.,Quirke,P.,and Taylor,G.R.,[Ed.]PCR:A practical approach.,IRL Press,Oxford.,1991).に詳しく記載されている。しかしながら、幾つかの変更が融合構築物の設計で必要であり、発行された文献から異なる刊行物を特定の用途に合わせて引用する。本発明において、発明者は2個の遺伝子を融合させたが、Hoら(Ho,Hunt et al.1989)及びMehta及びSingh(Mehta and Singh 1999)のオーバーラップエクステンションPCRとして知られる方法に頼った。2Kbまでの小さい構築物の増幅には、pfu DNAポリメラーゼ(Fermentas Inc.、米国)を使用し、点変異構築用に高フィデリティのポリメラーゼ作用が必要とされるより長いPCRには、pfuターボ(Stratagene)を長さ6〜7Kbのフラグメント増幅の増幅及び部位特異的変異誘発に使用した(Wang and Malcolm 1999)。
制限酵素切断及びライゲーション用の酵素は、New England Biolabs(米国)から入手し、Fermantas Inc.の「消化が速い」制限酵素を製造者のプロトコルに従って使用した。ほぼ全てのキメラ融合構築物例について述べるように、ライゲーションは、XhoI(四塩基カッター)及びNotI(六塩基カッター)で消化されたベクターとインサートとの間で行われ、定方向クローニングの機会を最大にした。
反応用のライゲーション混合物をXL 1Bコンピテント細胞に電気穿孔した(Sharma and Schimke 1996)。QiagenのMidi prepキットで指示に従って調製した多量のDNA。Midi調製の最終ステップにおいて、DNAを高塩分濃度で溶出させ、ここで発明者はpH5の0.3Mの酢酸ナトリウムを最終濃度で使用し、70%のエタノールを消化反応を妨害し得る余分な塩の除去に使用した(Sambrook et al.,1989)。この工程により、発明者は50〜60μgのDNAを得て、DNAはBg1 II酵素を使用した直線化ステップに供され、消化後、再度酢酸ナトリウム及びエタノール沈殿ステップに供され、最後に乾燥させたペレットを7〜8μlのオートクレーブした塩非含有水に溶解させ、1〜3μg/μlのDNAが得られた。ここで7〜10μgのDNAをピチア・パストリスのHis−GS115細胞のエレクトロコンピテント細胞における形質転換に使用し、最後にMD培地上に蒔き、His+形質転換体だけがプレート上で成長した。プラスミドpPIC−9kは、AOX1プロモーターを使用した相同組み換えを通じて所望の遺伝子のマルチコピー挿入が可能となるような形で設計される(Ramchuran,Mateus et al.,2005)。マルチコピーターゲット遺伝子挿入は、細菌カナマイシン耐性遺伝子(Tn903)を介し、抗生物質濃度の上昇に伴うゲンチシン(genticin)耐性個体群をモニタすることによってモニタすることができる。ピチアはそのままでゲンチシン耐性0.25mg/mlに耐えるが、0.5mg/ml及び4mg/mlは1〜2コピー及び7〜12コピー挿入をそれぞれ示す。ゲンチシン耐性は所望の遺伝子の複数挿入と直接の相関関係にある。遺伝子量効果により、所望の遺伝子産物の分泌量の多さはより多い挿入数に対応すると推論することができる(Norden,Agemark et al.2011)。
EGF−SAK、SAK−EGF等の一部の構築物を、pET23−d下で発現させ、キメラタンパク質は宿主である大腸菌Bl 21−DE3細胞において封入体の形態で蓄積した。封入体が形成された場合は、最大量の過剰発現タンパク質が得られた(Misawa and Kumagai 1999;Zhang,Xu et al.2009)。大腸菌BL21 DE3細胞をキメラ融合タンパク質の封入体の産生に使用し、一晩増殖させたBL21 DE3細胞培養物からの25mlのLB(ルリアベルターニ)を一次接種材料として使用し、500mlのLB(二次培養物)培地に移した。OD600が一旦0.6〜0.8に達したら、タンパク質生成を1mMのIPTGの助けを借りて誘導した。誘導後、細胞を振盪条件下で6時間にわたって40℃で維持した。6時間のインキュベーション後、細胞を6000rpmでの10分間にわたる4℃での遠心分離により収穫した。最後に、収穫した細胞を50mMのtris、100mMのNaCl及び1mMのEDTA溶液で洗浄して細胞塊から培地成分を除去した。洗浄後、細胞を最終OD60035〜40まで洗浄液に懸濁させた。この希釈で、細胞をプローブタイプのソニケーターでの超音波処理に供し、30秒のオン/オフサイクルを45分間にわたって行った。溶解サイクルの完了後、細胞ペレットを12,000rpmでの15分間にわたる遠心分離により収穫した。得られたペレットを2回、100mMのNaCl、50mMのTris Cl(pH7.4)、1mMのEDTA、0.1%のTriton X−100及び2Mの尿素含有溶液で洗浄した。再度、これらの封入体を溶液に再懸濁させ、12000rpmでの15分間にわたる遠心分離により収穫した。収穫したペレットを2回、100mMのNaCl、50mMのTris Cl(pH7.4)及び1mMのEDTA溶液で洗浄すると、Triton X−100が除去された。最後に、ペレットを8Mの尿素(20mMのTris Cl中で調製、pH7.4)及び1mMのDTTに2時間にわたって再懸濁させた。この溶液中の溶解した封入体の殆どが、12000rpmでの20分間にわたる遠視分離によりペレットから分離し、最終的な上清は最大量のキメラ融合タンパク質を含有していた。ここで、このタンパク質画分をリフォールディングのために供し、最高0.2mg/mlまで希釈し、以下の条件下でリフォールドした:50mMのNaCl、50mMのTris−Cl、2%のグリセロール中の2Mの尿素、酸化/還元グルタチオンモル比1.5:0.5、ごく軽く撹拌しながら4℃で36時間。このリフォールディングステップの完了後、混合物を20mMのTris Cl(pH7.6)及び50mMの尿素に対して48時間にわたって透析し、透析した反応混合物を疎水及びイオン交換クロマトグラフィを用いたタンデムクロマトグラフィによる精製に供した。ジスルフィド結合形成を、ジスルフィド結合形成及びリフォールディングの直接的な指標であるDTNB反応によりモニタした(Riener,Kada et al.2002)。最後に、精製したタンパク質を様々な活性アッセイに供した。
融合構築物においては、予備レベルにおいて、プラスミノーゲン活性化をこの方法でスクリーニングし、5%(w/v)のスキムミルクを15mMのNaCl及び50mMのTrisを1%のアガロースと共に含有している水中で沸騰させる。冷却後、約200〜400μgのプラスミノーゲンをこの混合物に添加し、スクリーニング対象であるコロニー/クローンの入ったLBアンピシリン含有プレートにオーバーレイした(Malke and Ferretti 1984)。プラスミノーゲン活性化能を有する全ての融合組み換えタンパク質は、1〜2時間から最高18時間にわたるインキュベーション後、カゼインを分解し、白色の背景に対して見えやすいクリアランス領域を生じさせるプラスミンの生成に起因する加水分解領域から容易に検出された。
ゲンチシン耐性マーカーを使用してより多いコピー数を含有する形質転換体を選択した後、最良のプロデューサークローンの実際のスクリーニングに供した。この方法では、一次培養物は2.5mlのBMGY培地(1%酵母抽出物、2%ペプトン、1Xグリセロール、1Xアミノ酸非含有酵母ニトロゲンベース及び100mMリン酸カリウム緩衝液pH5.5)において、30℃で16〜18時間にわたって培養した。一旦光学密度(OD600)が最高3〜4単位に達したら、7.5mlのBMMY培地(1%酵母抽出物、2%ペプトン、1Xメタノール、1Xアミノ酸非含有酵母ニトロゲンベース及び100mMリン酸カリウム緩衝液pH5.5)を添加することによって培養物を誘導した。これらの培養物を、組み換え産物の産生のために最終の0.5v/v%メタノールで5日間にわたって更に誘導すると、組み換え融合タンパク質が強力なメタノール誘導性プロモーターの影響下で産生された。
プラスミノーゲン活性化能を有する細胞外分泌産物及び関心の対象である所望のバンドはこの方法により検出され、10〜12.5%SDS−pageゲルを非還元サンプルバッファー中で行った。完了後、余分なドデシル硫酸ナトリウムを2.5%のTriton X−100溶液中での洗浄により除去した。次に、このゲルを2〜3回、50mMのTris(pH7.4)ですすいだ。この洗浄したゲルをスキムミルクアガロース及びプラスミノーゲン含有固形物面(寒天ゲル)上に置いた。5〜7時間にわたるインキュベーション後、加水分解領域が広がって目に見えるようになり、分解されたタンパク質におけるプラスミノーゲン活性化能を表している。
所望のタンパク質の検出は、ウェスタンブロット法の助けを借りて行われた。ピチア・パストリス細胞からの細胞外媒体に分泌された全ての融合構築物を6000rpmでの遠心分離により分離し、上清を所望の産物の同定のために取り出した。上清をウェスタンブロット法のためにそのままで直接取り出した。あるいはまず5KDa又は10KDaのカットオフ範囲のコンセントレーター(Amicon)で濃縮した。あるいは、トリクロロ酢酸沈殿に供し、アセトンで洗浄し、10〜12.5%SDSポリアクリルアミドゲル上に置いた。タンパク質を、25mMのトリス、175mMのグリシン及び20%のメタノールを含有する転写バッファーの助けを借りてニトロセルロース膜上で転写した。膜上でのゲルブロッティングを250mAで35分間にわたって行った。ブロットした膜を10%のスキムミルクで一晩、4℃で浸漬させ、あるいは37℃で2時間にわたってインキュベートした。このブロットを更に0.1%のTween−20を含有するリン酸緩衝食塩水で3回洗浄し、これにより余分なスキムミルクが除去された。その後、ブロットを一次抗体又はポリセラ(polysera)に推奨される希釈で1時間にわたって浸し、Tween−20含有PBSで3回洗浄した。更に、このブロットをHRPコンジュゲート二次抗体でインキュベートし、続いてPBS洗浄を3回行った。最後に、ブロットをDAB(ジアミノベンジジン)溶液の添加により現像した。
EGF4、5、6との様々な組織プラスミノーゲン活性化因子融合構築物は、リジン残基への親和性で知られるクリングルドメインを含有する(McCance,Menhart et al.1994;Ye,Rahman et al.2001)。この方法においては、組織プラスミノーゲン活性化因子融合ポリペプチドを有する、ピチア・パストリス発酵から得られた上清をリン酸緩衝液(pH7.5)に対して3〜4時間にわたって透析し、リン酸緩衝液で事前に平衡化したリジン/セファロースカラム(Amersham Biosciences、ウプサラ、スウェーデンから購入)に約0.5ml/分のゆっくりとした流速で装填した。装填完了後、カラムを再度4〜5ベッド体積のリン酸緩衝液で洗浄すると、最終的にタンパク質が0.3Mのε−アミノカプロン酸及び100mMのNaCl溶液に溶出された(Qiu,Swartz et al.1998)。
トロンビンカップリングを、上述の手順により臭化シアン活性化ビーズで行った(Salem,Maruyama et al.1984)。ここで、異なる精製ステップで得られたタンパク質を最終的に、カラムが50mMのTris Cl(pH7.4)で平衡化されたトロンビンアフィニティに供し、約0.5ml/分のゆっくりとした流速での装填に使用した50mMのTris Cl(pH7.4)に対して透析した。装填完了後、カラムを同じ緩衝液で洗浄した。最後に、NaClの勾配を上昇させることによってタンパク質を溶出させた(Salem,Maruyama et al.1984)。次に、異なるタンパク質画分をタンパク質C活性化能について試験した。
EGF−SK、EGF−tPA及びEGF−SAKの異なる融合遺伝子構築物の精製を異なるクロマトグラフィ法で行い、疎水及びイオン交換クロマトグラフィを異なる融合ポリペプチドの頻回の精製に用いた(Goyal,Sahoo et al.2007)。疎水クロマトグラフィにおいては、平均粒径100〜300μM直径のフェニルセファロース(Amersham Biosciences、ウプサラ、スウェーデン)6%架橋ビーズをカラムの準備に使用した。単純なXK16/20カラム(Amersham Biosciences、ウプサラ、スウェーデン)を蠕動ポンプの助けを借りてパックし、約25mlのフェニルセファロースベッドを形成し、4〜5ベッド体積の0.3MのNaCl及び50mMのTrisで平衡化し、ピチア・パストリス発酵中に得られた、所望の融合構築物を含有する隣接する上清を平衡化緩衝液と同じ緩衝強度及び塩の組成物に透析により維持した。平衡化された上清をパックされたカラムに流速40ml/時間で装填し、上清の装填完了後、4〜5ベッド体積の平衡化緩衝液を通して培地成分及び非特異的に結合した不純物を除去すると、最終的に所望の融合ポリペプチドが水に溶出した。溶出したタンパク質を2回目の精製に供し(以下を参照のこと)、プラスミノーゲン活性化及びトロンビン阻害及びタンパク質C活性化アッセイについて試験した。
このクロマトグラフィ手順においては、DEAEセファロース(登録商標)ファストフローをXK16/20カラム(Amersham Biosciences、ウプサラ、スウェーデン)にパックし、概して、製造者の説明書に従い、殆どの場合、20mlの膨潤マトリックスをパッキングに使用した。このカラムを20mMのTris Cl緩衝液(pH7.4)で平衡化し、ピチア・パストリスから得られた上清を、20mMのTris Cl緩衝液(pH7.4)に対して十分に透析した後、平衡化したカラムに装填し(別々に実行)、あるいは疎水性相互作用クロマトグラフィによる精製後(上記)、またそのイオン強度を平衡化緩衝液と同じに維持したまま、それぞれのカラムに装填した。装填完了後、各カラムを4〜5ベッド体積の平衡化緩衝液で洗浄し、この洗浄は非特異的に又は緩く結合した不純物及びポリペプチドの除去に役立つ。タンパク質の溶出を、1MのNaClの上昇勾配を5ベッド体積のマトリックスにかけて行った。タンパク質量子化(quantization)をブラッドフォード法の助けを借りて行い(Bradford 1976)、BSAの標準曲線と比較した。最後に、精製したタンパク質を20KDaのカットオフ値のコンセントレーター(Amicon)で濃縮し、様々な分析及び機能アッセイに使用した。
全てのキメラ融合ポリペプチド構築物は血栓溶解成分(SK、SAK、tPA)を含有した為、これらの構築物のプラスミノーゲン活性化能をプラスミン用の発色性ペプチド基質からの色素の放出によって測定した。ストレプトキナーゼ及び全ての融合構築物の一段階アッセイを2μMのヒトプラスミノーゲン、50mMのTris、0.05%のBSA及び5mMの発色基質を使用する条件下で行い、発色基質の放出を時間の関数として分光光度的にモニタする。次に非線形回帰を行い、吸光度と時間2との間のプロットは直線方程式に従った。ストレプトキナーゼは速やかにプラスミノーゲンのプラスミンへの変換を開始し、また事実上、活性化における遅延を示さないが、一部の融合構築物の場合、プラスミノーゲンをプラスミンに活性化するのに長い時間がかかる。これはプラスミノーゲンのプラスミンへの酵素前駆体活性化(経路I)がアクティブではなく、微量のプラスミンが活性複合体を形成することを示した。このことは、微量(ナノモル)の外部プラスミンの段階的な添加によりラグタイムが段階的に短くなった時、確認された。組織プラスミノーゲン活性化因子によるプラスミノーゲン活性化の場合は、迅速且つ単純な分光光度法に従い、単純な発色ペプチド(H−D−Val−Leu−Lys−pNA、S−2251、Chromogenix Inc.から購入)を、組織プラスミノーゲン活性化因子の作用によって形成されるプラスミンの検出に使用した(Verheijen,Mullaart et al.1982)。この方法を、フィブリン及び組織プラスミノーゲン活性化の存在下での強化されたプラスミノーゲン活性化の検証にも用いた(van Zonneveld,Veerman et al.1986)。この活性化アッセイにおいては、2μMのプラスミノーゲン、0.05MのTris Cl(pH7.2)、100mMのNaCl、0.05%及び0.5mMのS−2251とインキュベートした異なる精製量のタンパク質を可溶性フィブリン(American Diagnostics、米国から購入)の存在下及び不在下及びフィブリンなしで使用した。1分の間隔で最高2時間にわたって405でモニタした吸光度。
異なるキメラ構築物の存在下でのトロンビン誘導血餅形成への作用を観察するために、異なるトロンビン濃度の標準曲線を作成し、6.6IUのトロンビンでの20秒の凝固時間を得た。次に、同量のトロンビンを構築物の濃度を上昇させながらインキュベートすることによって凝固時間がコントロールの2倍になる濃度を測定した(Lougheed,Bowman et al.1995)。
組織プラスミノーゲン活性化因子、スタフィロキナーゼ及びストレプトキナーゼの異なる融合構築物を用量依存的にトロンビン介在タンパク質C活性化アッセイに供した。このアッセイでは、異なる量のタンパク質(nMレンジ)を10nMのトロンビンと、50mMのTris−Cl、5mMのCaCl2及び0.05%のBSAの存在下、37℃で20分間にわたってインキュベートした。その後、0.5μMのタンパク質Cをウェルに添加し、20分間にわたって25℃でインキュベートした。その後、0.5mMのヒルジンを添加することによってトロンビンを阻害し、インキュベーションを5分間にわたって25℃で継続し、次に発色基質を0.5mMの最終濃度で添加し、着色されたpNAの放出を405nmで上で詳述したように時間に対してモニタした(Eisenberg,Miletich et al.1988;Ewald and Eisenberg 1995;Lougheed,Bowman et al.1995;Meininger,Hunter et al.1995;Dahlback and Villoutreix 2005)。
ストレプトキナーゼとEGF4、5、6ドメインとの様々な融合遺伝子の調製:
(i)SKコード化オープンリーディングフレーム(ORF)の上流にインフレームで融合したEGFドメインの発現のためのハイブリッド遺伝子構築物:
EGF−SKタンパク質融合をコードしている二本鎖(ds)DNAブロック(EGF4、5、6コード化配列をインフレームでSK ORFのN末端コード化側に融合させた)を、プライマーN_EGF_SK Fp1及びN_EGF_SK Rp2(プライマーの配列に関しては表1を参照のこと)を使用して構築した。細菌発現ベクターpET23−d_SKの設計及び構築はNihalaniら(1998)により記載されている。構築は、pBR322におけるストレプトコッカス・エクイシミリス(Streptococcus equisimilis)、H46AからのSK遺伝子のクローニングを伴い(Pratap et al.,1996)、ファージT7主要カプシドタンパク質からの高効率リボソーム結合部位を含有する発現ベクターであるpET−23dへのサブクローニング(Studier and Moffatt,1986)及び二次構造体形成の傾向を最小限に抑えるための遺伝子の5’端の更なる修飾が続いた。pET23−d_SK構築物から発現したストレプトキナーゼはMet−SKである。更なる詳細は米国特許第7163817号明細書に記載される。この構築物を、SK遺伝子増幅のためのテンプレートとして使用した(DNA SEQ ID 1、対応するタンパク質SEQ ID 112)。
SK_EGF Fp1(上流)及びSK_EGF Rp2(下流)プライマー(プライマー配列については表1を参照のこと)セットを使用することによって、SKに対応するヌクレオチド配列(DNA SEQ ID 1、対応するタンパク質SEQ ID 114)をpET23−d−SKプラスミドをテンプレートとして使用して増幅した(「実施例で用いた一般的な方法」を参照のこと)。プライマーSK_EGF FplはXhoI制限部位をその5’端に含有し、SK_EGF Rp2はその5’端にSK配列を最高1149bpまで含有し、三重グリシン(Gly−Gly−Gly)コード化セグメント及びトランスグルタミナーゼ認識コード化配列が続き、最後にEGF4、5、6の4番ドメインをコードする5’端とオーバーラップする配列で終了している。得られる遺伝子ブロックは同じXhoI制限部位をその5’端を含有し、下流(3’端)は4番ドメインのためのオーバーラップヌクレオチド配列を含有する。第2のPCRにおいて、SK_EGF Fp3及びSK_EGF Rp4(プライマー配列については表1を参照のこと)のプライマーセットを、テンプレートとしてのpET23−d_EGF4、5、6(EGF4、5、6のための合成カスタムメイド遺伝子を含有する)からのEGF4、5、6ドメインの増幅に使用した。プライマーSK_EGF_Fp3はSKの下流配列、最高1149bpを含有し、三重グリシンコドンセグメント、トランスグルタミナーゼ認識部位コード化配列がその5’端に向って続いた。もう一方のプライマー、すなわちSK_EGF_Rp4は、その5’端にEGF4、5、6の6番ドメインの端部の部分配列及びNotI制限部位を含有した。PCR後、このプライマーセットを使用して得られた遺伝子ブロック2はその5’端に(SKの上流1149番bp、続いて三重グリシンコード化及びトランスグルタミナーゼ認識コード化配列を含有し、他方、その3’端にNotI制限部位を含有してpET23−dベクターへのクローニングを促進する。PCR条件は以下の通りであった:95℃での5分間にわたる完全変性、次に28サイクルの:95℃での45秒間、45℃での45秒間にわたるプライマーのアニーリング及び72℃での1分間、最後に72℃での10分間にわたる伸長により部分長PCR産物を完了させる。
ハイブリッド遺伝子構築物を得るための、EGF4、5、6の配列を翻訳的にインフレームなやり方でSKの配列内に散在させた「ドメイン間SK」−EGF構築物の構築も設計し、次に適切なプライマーを使用して形成した(プライマーの配列については表1を参照のこと)。EGF配列を、ドメイン間フレキシブルセグメント(Wang et al.,1998;Yadav&Sahni,2009)をコードしているSK遺伝子の領域、すなわち一方でαドメインとβドメインとの間、あるいは他方でβドメインとγドメインとの間に挿入した。これを目的として、SKのα−ドメインをコードしているDNAの増幅を最初に行い、プライマーセットIDα.Fp1及びIDα Rp2を使用した(配列の詳細については、表1を参照のこと)。プライマーIDα.Fp1はXhoI制限部位をその5’端に含有し、他方、プライマーIDα Rp 2はEGFの4番ドメインのためのオーバーラップ配列をその5’端に含有する。この反応のために、以下のPCR条件を用いた:95℃での5分間にわたるホットスタート、完全変性、続く28サイクルの95℃での45秒間にわたる変性、45℃での45秒間にわたるアニーリング、72℃での1.5分間にわたる伸長及び最後に不完全なPCR産物を完成させるための72℃での10分間にわたる「伸長セグメント」。EGF4、5、6をコードしているDNAブロックも別々にプライマーセットID EGF Fp3及びID EGF Rp4(これらのプライマーの配列については表1を参照のこと)を使用して増幅した。このプライマーセットを使用して、EGF4、5、6配列をコードしているDNAブロックを得て、5’端に向かう上流配列はSKのα−ドメインの下流配列と部分的にオーバーラップした。同様に、このブロックの3’端はSKβ−ドメインの上流配列とオーバーラップしている配列を含有した。SKのβ及びγドメインの両方をコードしている第3のPCRブロックを、プライマーセットID βFp5及びID γRp6(これらのプライマーの配列については表1を参照のこと)を使用してPCRにより得た。この反応に関しては、以下のPCR条件を用いた:95℃での5分間にわたるホットスタート、完全変性、続く95℃での45秒間にわたる変性、45℃での45秒間にわたるアニーリング、72℃での1.5分間にわたる伸長(全部で28サイクル)及び72℃での10分間にわたる最終伸長による不完全なPCR産物の完全増幅。5’端がEGFの6番ドメインの下流配列と相同となるようにID βFp5プライマーを設計し、下流プライマーID γRp6は終止コドン、それに続くNotI制限部位を含有した。3個の遺伝子ブロック全てをアガロースゲルからゲル精製キット(Qiagen)の助けを借りて精製し、ワンポットスプライスオーバーラップエクステンション反応に供して1つの隣接遺伝子産物を得て、遺伝子セグメントの順序は以下の通りであった:SKα−EGF4、5、6−SKβ−SKγ。単純なPCR反応において3個のセグメント全てを1:1:1のモル比で添加し、最初の10サイクルはプライマーなしで行い、次の18サイクルをそれぞれ最終濃度0.6μMのIDαFp1及びIDγRp6を添加して行うことによって3フラグメントSOE中間体を更に増幅した。この反応のために、以下のPCR条件を用いた:95℃での5分間にわたるホットスタート、完全変性、それに続く(各サイクルにおいて)95℃での45秒間にわたる変性、45℃での45秒間にわたるアニーリング、72℃での3分間にわたる伸長及び72℃での10分間にわたる最終伸長による不完全なPCR産物の完成。最終PCR産物をゲル精製し、XhoI及びNotI制限酵素で消化した(図1G及び図2Dを参照のこと)。このハイブリッド遺伝子構築物を次にpET23−dベクターにライゲーションし、大腸菌XL1B(recA-及びendA-)コンピテント細胞に形質転換させ、DNAはタンパク質発現を起こすことなく増殖でき(宿主が必要とするファージコード化RNAポリメラーゼを提供しなかった為)、これをいわゆるジデオキシチェーンターミネーション法でのサンガーの自動シーケンシングに供した(DNA SEQ ID3、対応するタンパク質SEQ ID 116)。結果によりハイブリッド遺伝子構築物が完全に検証された。その後、ハイブリッド遺伝子カセットをpET23−dドメイン間SK_EGFプラスミドから、XhoI及びNotI酵素での消化により単離した。このカセットを次にα−分泌シグナル配列の上流且つインフレームでpPIC−9Kにライゲーションし、ピチア・パストリス(GS115)に形質転換させ、クローニングし、前回のようにプラスミノーゲン活性化についての機能性スクリーニングにより選択し、発現は、方法のセクションで詳述しているように、宿主ゲノムにおける組み込み後、メタノール誘導後、ベクターのアルコールオキシダーゼプロモーターの影響下にあった。
SKコード化配列がインフレームで融合したEGF4、5、6ドメインによって両側でフランキングされている別の構築物も、pET23−d N_EGF_SKプラスミド構築物をとり(上のサブセクションi及びiiを参照のこと)、これをXhoI及びAflII(pET23−d N_EGF_SK構築物に特有の部位)による消化に供することによって構築され、同じ処理をpET23−d−SK_EGF構築物にも行って、両方の消化産物がアガロースゲル上で分離した。N_EGF_SK構築物から得られたXhoI及びAfl−IIセグメントをSK_EGF消化の大きいほうのフラグメントにライゲーションするとN_EGF_SK_EGF(DNA SEQ ID 7、対応するタンパク質SEQ ID 115)がpET23−dベクター中に得られた(図1C及び図2Cを参照のこと)。このプラスミドからの発現カセットをXhoI及びNotI消化により単離し(この構築物は前回のようにまずDNAシーケンシングにより検証される)、EGF−SK−EGFハイブリッドカセットの上流でα−分泌シグナル配列とインフレームでpPIC−9Kにライゲーションし、前回のように、宿主ゲノムにおける組み込み後、機能的スクリーニング後(以下を参照のこと)、アルコールオキシダーゼプロモーターの制御下、ピチア・パストリスにおいて発現させた。
N_EGF_SK、SK_EGF及びN_EGF_SK_EGFポリペプチドにおいて、それぞれEGF4、5、6ドメインの41番アミノ酸残基又はSK_EGFの434番アミノ酸残基並びにN_EGF_SK_EGFの41番及び434番アミノ酸位置に存在するメチオニン残基は、EGF4、5、6ドメインの一部として、その酸化傾向で知られており、これらのドメインの抗トロンビン活性、特にはタンパク質C活性化機能を妨げる。このため、このことに留意しつつ、様々なSK−EGF融合/遺伝子融合セグメントの設計において、発明者はこのメチオニンをバリン/アラニン/グルタミンアミノ酸残基に遺伝子レベルで置き換えた。この目標は、前回のように、高フィデリティ酵素pfuターボDNAポリメラーゼ(Stratagene)の使用及び適切なプライマーを使用した異なるテンプレートにおける部位特異的変異の導入によって達成された(Wang and Malcolm 1999)。これらの構築物を形成するために、3セットのプライマーを設計し、これらのプライマーがバリン、アラニン又はグルタミンを別々に異なる構築物に遺伝子構築物のEGF4、5、6ドメイン/セグメントの本来のMet残基の位置に組み込むことを可能にする。プライマーセットを以下のように命名した。
i.M rep V Fp及びM rep V Rp(プライマーの配列については表1を参照のこと)
ii. M rep A Fp及びM rep A Rp(プライマーの配列については表1を参照のこと)
iii.M rep Q Fp及びM rep Q Rp(プライマーの配列については表1を参照のこと)
この構築物において、最終的な目的はSKのN末端領域での5個のアミノ酸の除去であった。これらの5個のアミノ酸をコードするヌクレオチドを、PCRプライマーΔSK_EGF Fp1及びΔSK_EGF Rp2(これらのプライマーの配列については表1を参照のこと)の助けを借り、pET23−d_SK_GGG_TG_EGF(酸化耐性。EGF4、5、6セグメントのmet41番をバリンで置き換えた。上記を参照のこと)をテンプレートとして使用して除去した。プライマーΔSK_EGF Fp1はXhoI制限部位及び16番塩基対から始まるSKのオーバーラップ配列をその5'端に含有する。ΔSK_EGF Rp2はEGF4、5、6の6番ドメインの配列及びNotI部位をその5'端に含有する。PCRサイクルをこの反応に以下のようにして用いた:95℃での5分間にわたる完全変性、次の28サイクル:95℃での45秒間にわたる変性、55℃での45秒間にわたるアニーリング、72℃での3分間にわたる伸長及び72℃での10分間にわたる最終伸長による不完全なPCR産物の完全増幅。最終PCR産物をゲル溶出させ、XhoI及びNotI酵素で消化し、pET23−dベクターにライゲーションし、完全且つ正しいオープンリーディングフレームの検証のためにシーケンシングした。最後に、ΔSK_EGF(図1Dを参照のこと)カセットをpPIC−9Kにおいてライゲーションし、上述したような標準化手順でその発現についてチェックした。
N_EGF_SKの発現、精製及びプラスミノーゲン活性化の動態解析から(プラスミノーゲン活性化が遅れることを証明した)、未変性/無修飾SKとは異なり、この構築物は直接、ヒトプラスミノーゲンを活性化できなかったが、事前に生成されたプラスミンの存在を必要としたことが明らかであった。これによって自動的にこのような構築物における血餅特異的な活性化の利点がもたらされる。これは生体内の血餅はプラスミンを多く含有するが、プラスミンは全身循環においては迅速に不活性化されるからである。同様に、フィブリン塊もトロンビンを多く含有する。このため、発明者は構築物中の適切な部位を変異させて構築物をトロンビン活性化可能にもした。これを行うために、発明者はトロンビン切断可能部位によりEGF及びSKのドメイン間接合領域を変異させ、この結果、プラスミノーゲン活性化におけるトロンビン切断可能活性化スウィッチが得られる。このことは漸増的に少量のトロンビンを添加し、(上述した同様のプラスミン富化実験の場合と同様に)、N末端EGF4、5、6融合SK構築物のプラスミノーゲン活性化におけるラグの段階的な減少を観察することによって一段階アッセイでモニタすることができる。第XI因子のトロンビン切断可能配列をEGF及びSK遺伝子構築物の接合部に導入した。これはオーバーラップエクステンションPCRで達成され、オーバーラップ配列及びトロンビン切断可能アミノ酸コード化ヌクレオチドを含有するジャンクションプライマーを使用した。最初のPCR反応において、プライマーN_EGF_TCS Fp1及びN_EGF_TCS Rp2(これらのプライマーの配列については表1を参照のこと)をEGF4、5、6ドメインの増幅に使用した。プライマーN_EGF_TCS Fp1はXhoI制限部位及びEGFの4番ドメインの配列をその5'端に含有し、他方、N_EGF_TCS Rp2はEGFの6番ドメインの配列、それに続くトロンビン切断可能部位コード化配列及びそれに続くSKの上流部を含有する。PCR条件は以下の通りであった:95℃での5分間にわたる変性、次の28サイクルにおいて95℃での45秒間にわたる変性、50℃での45秒間にわたるアニーリング、72℃での1分間にわたる伸長及び72℃での10分間にわたる最終伸長による不完全なPCRフラグメントの完成。この反応によって得られたPCRブロックはXhoI制限部位をその5'端に含有し、トロンビン切断可能コード化ヌクレオチド配列及びSKのオーバーラップ部を3'端に含有する。次のPCR反応において、TCS_SK Fp3及びSK Rp4(これらのプライマーの配列については表1を参照のこと)を使用し、上流プライマー(TCS_SK Fp3)は6番ドメインの配列、EGF4、5、6のオーバーラップ部、トロンビン切断可能コード化ヌクレオチド配列及びSKコード化ヌクレオチド配列を5'から3'の順序で含有する。他方、SK Rp4はNotI切断可能部位をその5'端に含有する。PCR条件は以下の通りであった:95℃での5分間にわたる変性、次の28サイクルにおいて95℃での45秒間にわたる変性、50℃での45秒間にわたるアニーリング、72℃での1分間にわたる伸長及び72℃での10分間にわたる最終伸長による部分長娘フラグメントの合成の完了。得られたPCRブロックは6番ドメインのオーバーラップ配列及びトロンビン切断可能コード化ヌクレオチドを上流に含有するはずであり、下流においてはNotI制限部位を含有するはずである。両方のPCRブロックをゲル精製し、1:1のモル比でシングルポット反応において混合し、エンドプライマーTCS Fp1及びSK Rp6により増幅すると、必要とするN_EGF_TCS_SK PCRブロックが得られ(図1Eを参照のこと)(TCS:トロンビン切断可能配列)、これをゲル精製し、XhoI及びNotI酵素で消化し、最後に同様に消化したpET23−dに標準的な手順でライゲーションした。この構築物配列を、大腸菌XL Blueにおけるサブクローニング後、オープンリーディングフレームについて検証した。これにより、EGF4、5、6及びSKの接合部に以下のアミノ酸配列を有する第XI因子トロンビン切断可能部位が遺伝子中に創り出されたことが証明された:Ile−Lys−Pro−Arg−Ile−Val−Gly。この配列において、トロンビン特異性はアルギニンとイソロイシンとの接合部での切断につながり、トロンビンの作用後、1つのアミノ酸がSKのN末端から除去された。また第2のアミノ酸がバリンに変更され得る(未変性のSKにおいて、N末端残基はIle−Ala−Gly−である)。その後、N_EGF_TCS_SKカセットをpPIC−9Kにライゲーションし、その発現をピチア・パストリスで行った。トロンビンでの処理後、トロンビン切断が精製構築物において本当であると確かに判明し、N末端タンパク質シーケンシングにより確認された。
これを目的として、β−ドメインの増幅をプライマーID αβFp1及びID αβRp2(これらのプライマーの配列については表1を参照のこと)を利用し、pET23−d_SKをテンプレートとして使用して行った。プライマーID αβFp1はXhoI制限部位をその5'端に含有し、他方、ID αβRp2はSKのβドメインの下流配列及びEGF4、5、6の4番ドメインの部分オーバーラップ配列を含有する。これらのプライマーセットで得られたPCRブロックはXhoI制限部位を上流配列に含有し、下流にはβ−ドメインの末端配列及びEGFの4番ドメインのオーバーラップ配列を含有する。次のステップにおいて、EGF4、5、6をコードするPCRブロック2をIDE4Fp3及びIDE6Rp4(これらのプライマーの配列については表1を参照のこと)プライマーセットを使用して単離した。プライマーIDE4Fp3はSKのβ−ドメインの下流配列をその5'端に含有し、IDE6Rp4はγドメイン上流オーバーラップ配列をその5'端に含有する。これらのプライマーセットで得られたPCRブロック2は下流β−ドメインのオーバーラップ配列を5'端に含有し、他方の端はγドメインの上流配列を含有する。この増幅のためのPCR条件は以下の通りである:95℃での5分間にわたる完全変性、次の27サイクル:95℃での45秒間、45℃での45秒間にわたるアニーリング、72℃での1分間にわたる伸長及び72℃での10分間にわたる最終伸長。次のステップにおいて、SKのγドメインをID γFp5及びID γRp6(これらのプライマーの配列については表1を参照のこと)プライマーセットを使用して単離した。ID γFp5’の5'端がEGF4、5、6の6番ドメインの相同下流配列を含有するようにプライマーID γFp5を設計し、ID γRp6は終止コドンとそれに続くNotI制限部位を含有する。以下のpcrスキームをブロック3の増幅に用いた:95℃での5分間にわたるホットスタート、95℃での45秒間にわたる変性、47℃での45秒間にわたるアニーリング及び72℃での1.5分間にわたる伸長。全部で28サイクルを行い、72℃での10分間にわたる最終伸長により不完全な増幅産物を完成させた。得られた全てのPCR産物をゲル抽出キット(Qiagen)によりゲル精製し、A260により分光光度的に定量化した。最終pcr反応において、3個の遺伝子ブロックの全てをシングルポットでスプライスオーバーラップエクステンション反応に供して1個の隣接遺伝子ブロックを得て、得られた構築物の順序は以下:SKα−SKβ−EGF4、5、6−SKγであり、3個のpcr産物の全てが1:1:1のモル比でポリメラーゼ連鎖反応において混合され、最初の10サイクルはプライマーなしで行われ、次の18サイクルは最終濃度0.6μMのIDαβFp1及びIDγRp6プライマーを添加して行われ、3フラグメント中間体完全遺伝子ブロックを増幅した。PCR条件は以下の通りであった:95℃での5分間にわたるホットスタート、95℃での45秒間にわたる変性(donaturation)、45℃での45秒間にわたるアニーリング、72℃での3分間にわたる伸長。全部で28サイクルを行い、最初の10サイクルをプライマーなしで行い、最終増幅を72℃で10分間にわたって行った。最終的に得られた遺伝子ブロックはXhoI部位をその5'端に含有し、NotI部位をその3'端に含有する。この遺伝子ブロックをXhoI及びNotI酵素で消化し、pET23−d及びpPIC9Kにクローニングした。その発現、精製及びキャラクタリゼーションをピチア・パストリスにおいてチェックした。この遺伝子ブロックはEGF4、5、6ドメインをSKのβ及びγドメインの間に含有する(DNA SEQ ID 5、対応するタンパク質SEQ ID 129;図1H及び図2Eを参照のこと)。
EGF−SK構築物におけるEGF4、5、6ドメインの4番のドメインの始まり又は前にトランスグルタミナーゼ認識配列を組み込むために、プライマーTG_N_EGF_Fp1及びAfl II Rp2(プライマーの詳細な配列については表1を参照のこと)を設計し、TG Fp1はXhoI制限部位及び第XIII血液因子トランスグルタミナーゼ認識アミノ酸配列をコードするヌクレオチド配列をその上流領域に含有し、プライマーAfl II Rp2はAfl II制限消化部位を含有するその領域のヌクレオチド配列を含有する(SKの165〜170番ヌクレオチドはこのプライマーの中心に位置するAfl II制限部位を含有する)。これらのプライマーから、PCRにより、発明者はXhoI制限部位、トランスグルタミナーゼ認識コード化ヌクレオチド及びEGF4、5、6の4番ドメインの配列を含有する遺伝子ブロックを得て、このブロックの下流部はAfl II制限部位を含有する。この遺伝子ブロック(酸化耐性及びトロンビン切断可能配列含有)をゲルから抽出した。プラスミドpET23−dN_EGF_TCS_SK及びpET23−dN_EGF_TCS_SK_EGFをXhoI及びAfl IIで消化した。この結果、両方のプラスミド構築物からXhoI及びAfl II遺伝子ブロック及び大小の部位が得られた。消化された遺伝子ブロックを構築物の大きいほうの部位とライゲーションし、大腸菌XL Blueに形質転換させてTG_N_EGF_TCS_SK及びTG_N_EGF_TCS_SK_EGF含有プラスミドが得られた(図1Fを参照のこと)。これらを、正しいオープンリーディングフレーム、すなわち上述のEGF−SK構築物との関連でトランスグルタミナーゼコード化配列の存在についてシーケンシングし、検証した。両方のカセットを次にピチア・パストリスにおいてライゲーションし、これらの構築物の発現についてチェックした(「実施例で用いた方法」を参照のこと)。
様々なEGF−SKハイブリッドポリペプチドの発現及び機能的キャラクタリゼーション
実施例1に記載の異なる遺伝子ブロック、例えばN_EGF−SK、SK−EGF及びN_EGF_SK_EGF並びに別種のドメイン間融合構築物、例えばドメイン間EGF_αβSK、ドメイン間EGF_βγSK、切断ΔSK_EGF並びにN_EGF_SK、SK_EGF及びN_EGF_SK_EGFの酸化耐性形態(トランスグルタミナーゼ及びトロンビン切断部位等が組み込まれ、また全て発現ベクターpPIC−9Kにおいてクローニングされ、またそれぞれの遺伝子融合体の配列から期待される発現した機能的に活性なハイブリッド遺伝子産物に関して検証した)を次に比較的多量の培養物からその更なるキャラクタリゼーションに先立って単離した。実施例1に記載したように、ピチアクローンを最初にルーチンでカゼインオーバーレイ法によりプラスミノーゲン活性化能について試験し、幾つかの(それぞれ10〜20)陽性のものを次にBMGY、BMMY培地(BMGY=1%酵母抽出物、2%ペプトン、1Xグリセロール、1Xアミノ酸非含有酵母ニトロゲンベース及び100mMリン酸カリウム緩衝液pH5.5、BMMY=1%酵母抽出物、2%ペプトン、1Xメタノール、1Xアミノ酸非含有酵母ニトロゲンベース及び100mMリン酸カリウム緩衝液pH5.5)上で成長させ、次に「方法」で前述したようにメタノールで誘導し、細胞非含有上清をカゼインオーバーレイアッセイ(再確認のために)及びペプチド発色基質の存在下でのプラスミノーゲン活性化(分光光度)アッセイに使用した。比較的高いプロデューサーであると判明したものを次に1リットルレベルで成長させ、タンパク質を疎水性相互作用(例えば、フェニル−アガロース)及びイオン交換(DEAE−アガロース)クロマトグラフィのタンデムで精製した(詳細は「実施例で用いた一般的な方法」のセクションに記載)。これら2種類の精製方法で得られたハイブリッドSK−EGFポリペプチドは概してSDS−PAGEで90〜95%純粋であった。精製された全ての構築物をプラスミノーゲン活性化能(ヒトプラスミノーゲンを使用した一段階アッセイ)について試験し、凝固時間を測定するためにトロンビン阻害アッセイを行い、タンパク質C活性化について発色アッセイを行った(「実施例で用いた方法」を参照のこと)。SK_EGF及び酸化耐性SK_EGFはSKと極めて似た、ただし活性化動態における2〜3分多いラグを伴ったPG活性化動態を示したが、N_EGF_SK並びに酸化耐性N_EGF_SK、N_EGF_TCS_SK及びTG_N_EGF_SKの場合、活性化におけるラグはかなり大きく(20〜25分)、その後、プラスミノーゲン活性化動態は未変性のSK様であった。これは構築物によるPGの初期活性化が遅延したが、無修飾のSKの場合は事実上、即時であることを示唆した。しかしながら、一旦SK構築物が活性化されると、ラグの後ではあるが、完全なプラスミノーゲン活性化特性を示した。若干大きいラグ(30〜35分)が双極性EGF融合タンパク質、すなわちN_EGF_SK_EGF、酸化耐性N_EGF_SK_EGF、N_EGF_TCS_SK_EGF及びそのバリアントTG_N_EGF_TCS_SK_EGFにおいて見られた。しかしながら、上述したように、ラグの消失後、タンパク質1ミリグラムあたりのプラスミノーゲン活性化率(比活性)は無修飾のSKのものと同様であった。N_EGF_SK、N_EGF_SK_EGF及び同様の種類の構築物におけるラグの理由は酵素前駆体の自己活性化機構の喪失であると判明した(Bajaj and Castellino 1977;Boxrud,Verhamme et al.2004;Aneja,Datt et al.2009)。このことは、少量の(ナノモル量)プラスミンを反応アッセイに若干添加することによるラグの漸進的な喪失があったという観察結果により証明された。加えて、これらの構築物の事前に生成されたプラスミン複合体をアッセイで使用した場合はラグがなく、これはSKで観察された即時のプラスミノーゲン活性化機構のかわりに、ラグのある融合構築物が今はプラスミンと複合体を一旦形成しさえすればプラスミノーゲン活性化可能であることをはっきりと示唆している。同様のプラスミン依存性活性化が、ドメイン間αβEGF_SK構築物においても見られた。しかしながら、活性化後、その総比活性は無修飾のストレプトキナーゼのものの40〜50%にすぎないことが判明した。特筆すべきことに、EGF4、5、6セグメントがSKのβ及びγドメインの接合部に置かれた他方のドメイン間構築物の場合、精製されたタンパク質は無修飾のSKと比較して5%未満のプラスミノーゲン活性を示した。このことは、EGFのSKとの融合が自動的に機能性となるわけではなく、正しく設計したものだけがそうなることをはっきりと示している。正しく設計されたものは、プラスミノーゲン活性化、トロンビン阻害等についての、高スループットスクリーニングシステムに簡単に適合させ得るプレート/分光光度アッセイを利用してスクリーニング(設計が実験に基づいて又は構造的な仮定により行われた時)することによって選択することができる。このため、設計されたSKの部位特異的置換、欠失又はドメイン付加変異体あるいはストレプトキナーゼの天然のバリアントを使用し、ここで採用するアプローチにより同様のSK−EGFタンパク質を得ることができる。
様々なEGF4、5、6及びTPAハイブリッド遺伝子をコードするDNAの構築:
コード化tpA(SEQ ID 9、対応するタンパク質SEQ ID 120)及びインフレームで融合したEGF4、5、6をコードしているDNAの別のセグメント(SEQ ID 8、対応するタンパク質SEQ ID 111)にインフレームで融合したEGF4、5、6配列をコードしているDNAセグメント(SEQ ID 2、対応するタンパク質SEQ ID 111)を化学的に合成、精製及びpUC19においてクローニングした。シーケンシングにかけることによってその妥当性(SEQ ID 8、対応するタンパク質SEQ ID 111)を証明した。この構築物をEGF−tpA−EGF(SEQ ID 10、対応するタンパク質SEQ ID 121)と称する。EGF4、5、6ドメイン遺伝子コード化セグメントがtPAのN末端部位で融合した(SEQ ID 11、対応するタンパク質SEQ ID122)又はtpAのC末端で融合した(SEQ ID 12、対応するタンパク質SEQ ID 123)この遺伝子構築物に加えて。tPAコード化配列をまずプライマーtPAFp1及びtPARp2プライマーで増幅した(プライマー配列については表2を参照のこと)。この反応で用いたPCR条件は以下の通りである:95℃での5分間にわたるホットスタート、完全変性、95℃での45秒間にわたる変性、55℃での45秒間にわたるアニーリング、72℃での4分間にわたる伸長(全部で28サイクル)及び72℃での10分間にわたる最終伸長による不完全なPCR産物の完全増幅。このため、この反応に使用したプライマーtPAFp1はXhoI制限部位をその5'端に含有し、tPARp2はNotI制限部位を含有する。得られたPCR産物をXhoI及びNotI制限酵素で消化し、pET23−dにライゲーションした。この工程で形成された最終構築物をpET23−d tPAと称し(図2Fを参照のこと)、シーケンシングによりtPAオープンリーディングフレームを検証した。N末端(N_EGF_tPA)及びC末端(tPA_EGF)融合体を形成するために、単純な制限酵素消化及びライゲーションスキームに従った。両方の構築物を1つのステップで形成するために、pET23−d tPA及びpUC−19_N_EGF_tPA_EGFを共に特有のカッターであるXhoI及びBSrGIで切断した。これにより小さいフラグメント及び大きいフラグメントが得られた。小さいフラグメントのpUC−19_N_EGF_tPA_EGF消化物はN_EGF_tPA配列を含有し、pET23−d_tPAの大きいフラグメントにライゲーションされ、このステップによりN_EGF_tPA(DNA SEQ ID 11、対応するタンパク質SEQ ID 122)構築物が得られた。tPA_EGF(DNA SEQ ID 12、対応するタンパク質SEQ ID 123)構築物は、pUC−19_N_EGF_tPA_EGFの大きいフラグメントとpET23−d_tPAの小さいフラグメントとのライゲーションにより形成され、この構築についてtPA_EGF(図1Jを参照のこと)が得られた。N_EGF_tPA(図1Kを参照のこと)及びtPA_EGF(図2Gを参照のこと)をXhoI及びNotI制限酵素で消化し、単離したインサートフラグメントをpPIC−9Kにライゲーションし、構築物はα−分泌シグナル配列にインフレームで置かれた。全てのこれらの構築物を、ピチア・パストリス(GS115)においてベクター内に置かれたメタノール誘導性プロモーターの影響下で宿主ゲノムへの組み込み後に発現させた。
組織プラスミノーゲン活性化因子とヒトトロンボモジュリンのEGF4、5、6ドメインとの様々なハイブリッド遺伝子の構築
(i)ドメイン間EGF4、5、6−tPA構築物の構築
組織プラスミノーゲン活性化因子は異なるドメインを以下の順序:N末端ペプチド−フィンガードメイン−EGF様ドメイン−クリングル1−クリングル2−触媒ドメインで含有する。新規な非天然のハイブリッド設計を遺伝子レベルで構築し、tPAの内因性EGFドメインをトロンボモジュリンのEGF4、5、6ドメインで置き換えた。これらの構築物を他のハイブリッド遺伝子の産生に関して上で用いたオーバーラップエクステンションPCR戦略により形成した。
この構築物を形成するために、pET23−d_tPA(SEQ ID 9、対応するタンパク質SEQ ID 120)を、内因性egfコード化領域が187bpから297bpまでの基準として使用した。第1のステップにおいて、フィンガードメインコード化DNAを以下のプライマー:Fin Fp1及びFin Rp2(これらのプライマーの配列については表2を参照のこと)を使用して単離し、上流プライマーはXhoI制限部位をその5'末端に含有し、他方、第2プライマーは、EGF4、5、6ドメインの4番ドメインのためのオーバーラップ配列と共にフィンガードメインをコードする下流配列を含有する。PCR条件は以下の通りであった:95℃での5分間にわたる完全変性、続く次の28サイクル:95℃での45秒間、48℃での45秒間にわたるアニーリング、72℃での1分間にわたる伸長及び72℃での10分間にわたる最終伸長。第2のPCRにおいて、EGF4、5、6ドメインセグメントを増幅し、EGF Fp3及びEGF Rp4(これらのプライマーの配列については表2を参照のこと)プライマーセットを使用した。プライマーEGF Fp3はEGFのフィンガードメインの下流配列及びEGFの4番ドメインを含有し、他方、下流プライマーEGF Rp4はクリングル1のオーバーラップ配列をその5'末端に含有する。PCR条件は以下の通りであった:95℃での5分間にわたる完全変性、続く次の28サイクル:95℃での45秒間、48℃での45秒間にわたるアニーリング、72℃での1分間にわたる伸長、最後に72℃での10分間にわたる伸長セグメントで終了。このプライマーセットで得られた遺伝子ブロックはフィンガードメイン配列を5'末端に、またその3'端にクリングル1のオーバーラップ配列を含有する。第3のPCR反応において、クリングル1を触媒ドメインの最後までコードしている配列を、K1 Fp5及びCD Rp6(これらのプライマーの配列については表2を参照のこと)プライマーセットの使用により選択的に増幅した。プライマーK1 Fp1はEGF4、5、6の6番ドメインのオーバーラップ配列をその5'末端に含有し、プライマーCD Rp6は終止コドン及びNotI制限部位を5'端に含有する。PCR条件は以下の通りであった:95℃での5分間にわたる完全変性、続く次の28サイクル:95℃での45秒間、48℃での45秒間にわたるアニーリング、72℃での3分間にわたる伸長及び72℃での10分間にわたる最終伸長による全ての部分長フラグメントの合成完了。この反応で得られた遺伝子ブロックはEGF6番ドメインオーバーラップ配列を5'末端に、また触媒ドメインコード化配列、終止コドン及びNotI部位をその3'端に含有する。3個のPCR産物の全てをゲル精製し、シングルポットSOEに供することによって完全ハイブリッド遺伝子構築物を増幅し、アセンブリの順序は以下の通りであった:フィンガードメイン−EGF4、5、6ドメイン−クリングル1−クリングル2及びtPA(図1Q及び図2Jを参照のこと)。触媒ドメイン。これをFin Fp1及びCD Rp6(これらのプライマーの配列については表2を参照のこと)プライマーセットを使用して行った。最終PCR条件は以下の通りであった:95℃での5分間にわたる完全変性、次の28サイクル:95℃での45秒間、48℃での45秒間にわたるアニーリング、72℃での4分間にわたる伸長及び72℃での10分間にわたる最終伸長(単一セグメント)。この遺伝子ブロックを、上述したように、ゲル抽出で精製し、XhoI及びNotI酵素で消化し、同様に消化及び精製したpET23−dベクターとライゲーションし、大腸菌XL Blueにクローニングした。幾つかのランダムに選択したクローンを、完全インサート/遺伝子ブロックについてサンガー法によるシーケンシングに供し、tPAのものへのEGF4、5、6ドメインの正しいインフレームでの組み込みを検証した(DNA SEQ ID 13、対応するタンパク質SEQ ID 124)。この遺伝子ブロックを次に、前回のようにpPIC−9Kベクターに移し、ピチア・パストリスへとクローニングし、「実施例で用いた一般的な方法」に記載したように高レベルのプラスミノーゲン活性化因子活性についてスクリーニングした。
この構築物を形成するために、3つの異なるPCRを別々に行い、得られた遺伝子ブロックはオーバーラップ配列を各遺伝子ブロックの末端に含有し、次にこれらをシングルポットSOE反応で増幅して以下のハイブリッド構築物:tPAフィンガードメイン−EGF4、5、6−tPAクリングル2−tPA触媒(セリンプロテアーゼ)ドメイン(図1R及び図2Hを参照のこと)を形成した。この構築物を形成するために、pET23−d_tPA(SEQ ID 9、対応するタンパク質SEQ ID 120)を内因性egf及びクリングル1コード化ヌクレオチド領域が187bpから564bpまでのテンプレートして使用した。第1のステップにおいて、フィンガードメインコード化セグメントを以下のプライマー:Fg Fp1及びFg Rp2(これらのプライマーの配列については表2を参照のこと)を使用して単離し、上流プライマーはXhoI制限部位を5'末端に含有し、他方、第2プライマーはフィンガードメインの下流配列及びEGF4、5、6ドメインの4番ドメインのオーバーラップ配列を含有する。PCR条件は以下の通りである:95℃での5分間にわたる完全変性、次の28サイクル:95℃での45秒間、48℃での45秒間にわたるアニーリング、72℃での1分間にわたる伸長及び72℃での10分間にわたる最終伸長。第2のPCRにおいて、EGF4、5、6ドメインをプライマーEFI Fp3及びEFI Rp4(これらのプライマーの配列については表2を参照のこと)で増幅した。プライマーEFI Fp3はフィンガードメインの下流配列及びEGFの4番ドメインを含有し、他方、下流プライマーはクリングル2のオーバーラップ配列をその5'末端に含有した。PCR条件は以下の通りであった:95℃での5分間にわたる完全変性、次の28サイクル:95℃での45秒間、48℃での45秒間にわたるアニーリング、72℃での1分間にわたる伸長及び72℃での10分間にわたる最終伸長。このプライマーセットで得られた遺伝子ブロックはフィンガードメイン配列を5'末端に含有し、クリングル2のオーバーラップ配列をその3'端に含有した。第3のPCR反応において、クリングル2からtPA触媒ドメインへの配列を、K2 Fp5及びK2 CD Rp6(これらのプライマーの配列については表2を参照のこと)の2個のプライマーのセットを使用して増幅した。プライマーK2 Fp5はEGF4、5、6の6番ドメインのオーバーラップ配列をその5'末端に含有し、プライマーK2 CD Rp6は終止コドン及びNotI制限部位を5'端に含有する。PCR条件は以下の通りであった:95℃での5分間にわたる完全変性による「ホットスタート」、次の28サイクル:95℃での45秒間、48℃での45秒間にわたるアニーリング、72℃での3分間にわたる伸長及び72℃での10分間にわたる最終伸長。この反応で得られた遺伝子ブロックは6番ドメインオーバーラップ配列をその5'末端に、また触媒ドメインコード化配列、続く終止コドン及びNotI部位をその3'端に含有した。3個のPCR産物の全てをゲル精製し、Fg Fp1及びK2CD Rp6プライマーセット(これらのプライマーの配列については表2を参照のこと)によるシングルポットSOE反応に供して増幅して完全ハイブリッド遺伝子構築物を得て、様々なタンパク質コード化セグメントのアセンブリの順序は以下の通りであった(最終的にクローニング後にDNAシーケンシングにより確認された):フィンガードメイン−EGF4、5、6ドメイン−クリングル2及び触媒ドメイン(DNA SEQ ID 14、対応するタンパク質SEQ ID 126)。最終PCR条件は以下の通りであった:95℃での5分間にわたる完全変性、次の28サイクル:95℃での45秒間、48℃での45秒間にわたるアニーリング、72℃での4分間にわたる伸長及び72℃での10分間にわたる最終伸長。この遺伝子ブロックをゲル抽出により精製し、XhoI及びNotI酵素で消化し、pET23−dベクターとライゲーションし、大腸菌XL Blueにおいてクローニングし、完全遺伝子ブロックを次にシーケンシングし、部分切断tPA遺伝子へのEGF4、5、6ドメインの正しいインフレーム組み込みについて検証した。上述したように、この最終ハイブリッド遺伝子ブロックをpPIC−9Kベクターに移し、ピチア・パストリスにおけるそのORF発現を標準化手順を用いてチェックした。
これらの構築物を、事前に形成したpET23−dN_EGF_tPA(SEQ ID 11、対応するタンパク質SEQ ID 121)及びpET23−d_tPA_EGF(SEQ ID 12、対応するタンパク質SEQ ID 123)をテンプレートとして使用して調製した。両方の構築物において、内因性egf及びクリングル1ドメインをオーバーラップPCRスキームの助けを借りて除去した。tPAの内因性egf及びクリングル1ドメインをN_EGF_tPA構築物から除去するために(図1Nを参照のこと)、2セットのプライマーを設計した。第1のプライマーセットN_EtPA Fp1及びN_EtPA Rp2(これらのプライマーの配列については表2を参照のこと)をEGF4、5、6ドメイン及びtPAフィンガードメインの隣接ヌクレオチド配列の増幅に使用した。この場合、上流プライマーはEGFの4番ドメイン配列及びXhoI制限部位をその5'端に含有し、プライマーN_EtPA Rp2はtPAクリングル2のオーバーラップ配列を含有した。第2のプライマーセット、すなわちEK2 CD Fp3及びK2 CD Rp4(これらのプライマーの配列については表2を参照のこと)をtPAのクリングル2及び触媒ドメインの増幅に使用した。プライマーEK2 CD Fp3はフィンガードメインの下流オーバーラップ配列を5'端に含有し、もう一方のプライマーはtPA触媒ドメインの下流配列及びNotI制限部位を含有する(PCR条件:95℃での5分間にわたるホットスタート、28サイクルの95℃での45秒間、52℃での45秒間、72℃での2分間及び72℃での10分間にわたる最終伸長)。この反応で得られた遺伝子ブロックはtPAフィンガードメインオーバーラップ配列をその5'端に、NotI制限部位をその3'端に含有した。両方のPCR産物をゲル精製し、完全遺伝子ブロックの構築に供し、内因性egf及びクリングル1をプライマーN_EtPA Fp1及びK2 CD Rp4(これらのプライマーの配列については表2を参照のこと)プライマーセットの助けを借りて欠失させた。得られた遺伝子ブロックを精製し、XhoI及びNotI制限酵素で消化し、pET23−dベクターにライゲーションし、大腸菌においてサブクローニングし、tPA(DNA SEQ ID 15、対応するタンパク質SEQ ID 126;図2.I)コード化遺伝子ブロックからのegf及びクリングル1の除去後の正しいインフレーム接合についてDNAシーケンシングした。遺伝子ブロックの正しいオープンリーディングフレームについてシーケンシングによる検証後、このカセットをpPIC−9Kにライゲーションし、前回のようにピチアに形質転換させ、活性についてスクリーニングし、細胞外発現についてチェックした。同様のやり方で、内因性egf及びクリングル1を構築物tPA_EGF中のtPAコード化遺伝子ブロックから欠失させた(図1P及び図2Hを参照のこと)。ここで、pET23−d−tPA_EGFプラスミドDNAを切断tPAヌクレオチド配列増幅用のテンプレートとして使用した。フィンガードメインの増幅にフィンガーFp1及びフィンガーRp2のプライマーセットを使用し(これらのプライマーの配列については表2を参照のこと)、フィンガーFp1プライマーはXhoI制限部位をその5'端に含有し、もう一方のプライマーフィンガーRp2はフィンガードメインの下流配列及びtPAのクリングル2のオーバーラップ配列を含有した。PCR条件は以下の通りであった:95℃での5分間にわたる完全変性、続く30サイクルの:95℃での45秒間にわたる変性、44℃での45秒間にわたるアニーリング、72℃での1分間にわたる伸長及び72℃での10分間にわたる最終伸長による終了。これによりtPAフィンガードメインオーバーラップ配列、続くXhoI制限部位をその5'端に含有する遺伝子ブロックが得られ、その3'端はクリングル2オ−バーラップ配列を含有した。第2のプライマーセットをクリングル2触媒コード化ドメイン及びEGF4、5、6ドメインの増幅に使用した。第1のプライマーK2 CD Fp3(これらのプライマーの配列については表2を参照のこと)はtPAフィンガードメインの下流端及びクリングル2の小部分までのオーバーラップ配列を含有した。他方、第2のプライマーEGF Rp4(これらのプライマーの配列については表2を参照のこと)はEGFの下流配列及びNotI制限部位を含有した。PCR条件は以下の通りであった:95℃での5分間にわたる完全変性、30サイクルの:95℃での45秒間にわたる変性、44℃での45秒間にわたるアニーリング、72℃での1分間にわたる伸長及び72℃での10分間にわたる最終伸長。両方の遺伝子ブロックをゲルから精製し、プライマーフィンガーFp1及びEGF Rp4(これらのプライマーの配列については表2を参照のこと)の存在下でのオーバーラップエクステンション反応に供し、この反応から得られたPCR産物をゲル精製し、前回のようにpET23−d(DNA SEQ ID 16、対応するタンパク質SEQ ID 127)に大腸菌においてライゲーションし、シーケンシングして完全遺伝子ブロックを検証した。最後に、この遺伝子ブロックをpPIC−9Kにライゲーションし、上述したように発現及び機能的特性のスクリーニングのためにピチア・パストリスに形質転換させた。
上述のEGF4、5、6及びtPAの異なる融合構築物において、以下のアミノ酸変更を行った:スレオニン115番アミノ酸をアスパラギン(T115N)に変更し、アスパラギン129番アミノ酸をグルタミン(N129Q)に変更し、tPA308〜311のKHRRコード化領域を、4重アラニン変異列(KHRR(308−311)AAAA)で置き換えた(DNA SEQ ID 20、対応するタンパク質SEQ ID 128)。これらの変異により追加のフィブリン特異性が得られる分子に付与され、生体内でのtPAの半減期が上昇することが知られている(Keytt et al.,1994)。これらの変異を導入するために、発明者は部位特異的変異誘発アプローチ(「実施例で用いた方法」を参照のこと)を用いて、これらの変更を酸化耐性(EGF4、5、6ドメインの129番メチオニンをバリン/アラニン/グルタミンに置き換えた)遺伝子テンプレートにも組み込んだ。以下のプライマーを部位特異的変異誘発に使用した:1.T115 N Fp及びT115 N Rp(これらのプライマーの配列については表2を参照のこと)、2.N129 Q Fp及びN129 Q Rp(これらのプライマーの配列については表2を参照のこと)。
スタフィロキナーゼとトロンボモジュリンドメインEGF4、5、6とのハイブリッド遺伝子の構築:
SAK_EGF及びEGF_SAKコード化ハイブリッド遺伝子ブロックの構築
EGF−SAK融合体の構築のために、EGF4、5、6PCRブロックをN_EGF_SAK Fp1及びN_EGF_SAK Rp2プライマーセット(これらのプライマーの配列については表3を参照のこと)の助けを借りて単離し、pET23−d_EGF4、5、6(Seq ID 2、対応するタンパク質SEQ ID 111)をテンプレートとして使用した。ここでN_EGF_SAK Fp1はXhoI制限部位をその5'端に含有し、N_EGF_SAK Rp2はSAKヌクレオチドのオーバーラップ配列を5'端に含有した。PCR条件は以下の通りであった:第1の(ホットスタート)サイクルにおける95℃での5分間にわたる完全変性、次の28サイクル:95℃での45秒間にわたる変性、50℃での45秒間にわたるアニーリング、72℃での1分間にわたる伸長及び72℃での10分間にわたる最終ステップによる不完全なPCR産物の完成。PCR産物はXhoI制限部位をその5'端に含有し、3'端はSAKのオーバーラップ配列を含有した。第2のステップにおいて、SAK PCRブロックをN_EGF_SAK Fp3及びN_EGF_SAK Rp4プライマーセットの助けを借りて増幅し、pGMEX_SAK(SEQ ID 17、対応するタンパク質SEQ ID 130)構築物をテンプレートとして使用した。この反応において、プライマーN_EGF_SAK Fp3はEGF4、5、6の6番ドメインの下流オーバーラップ配列を含有し、N_EGF_SAK Rp4は終止コドンとそれに続くNotI制限部位を含有した。PCR条件は以下の通りであった:95℃での5分間にわたる1サイクルの完全変性、続く28サイクルの95℃での45秒間にわたる変性、50℃での45秒間にわたるアニーリング、72℃での1分間にわたる伸長及び72℃での10分間にわたる最終ステップによる不完全なPCR産物の完成。これによって6番EGFドメインオーバーラップ配列を5'端に有する遺伝子ブロックが得られ、3'端は終止コドンとそれに続くNotI制限部位を含有した。両方のPCR産物をゲル精製キットの助けを借り得てゲル抽出及び精製し、ハイブリッド遺伝子中間体(オーバーラップエクステンションで得られる)増幅に使用するN_EGF_SAK上流Fp1及びN_EGF_SAK Rp4下流プライマーとモル比1:1でシングルSOE PCR反応において混合した。この結果、N_EGF_SAK(DNA SEQ ID 18、対応するタンパク質SEQ ID 118)配列を含有する隣接遺伝子フラグメントが得られた。この遺伝子ブロックを次にXhoI及びNotIで消化し、pPIC−9Kベクターに移した。DNAシーケンシングによりEGF_SAK(図1Tを参照のこと)構築物で期待されるインフレーム融合及び他の変異の不在を検証した。この構築物をピチア・パストリスのGS115株に形質転換させ、前回のように、宿主ゲノムへの組み込み後、アルコールオキシダーゼプロモーターの影響下での発現についてチェックした。
上記のN_EGF_SAK及びSAK_EGF DNA構築物をまた、IPTG誘導性lacプロモーターの影響下で発現させた。これらの構築物を作製するために、pPIC−9K_N_EGF_SAK及びpPIC−9K_SAK_EGFプラスミドをテンプレートとして使用した。
N_EGF_SAK遺伝子ブロックをまずBac Fp1及びBac Rp2プライマーの助けを借り、pPIC−9K_N_EGF_SAKをテンプレートとして使用して増幅した。Bac Fp1プライマーはNcoI部位をその5'端に、必要するAUGコドンを遺伝子ブロックの最初に配置するのを支援するために、またイニシエーターMet残基コード化コドンをmRNAに配置するために含有した。プライマーBac Rp2はXhoI制限部位を含有し、6ヒスチジンアミノ酸コード化ヌクレオチドを転写したmRNAの端部に遺伝子産物の検出及びその精製に役立つ終止コドンの前にインフレームで導入することを促進した。この遺伝子ブロックをゲルから単離し、NcoI及びXhoI制限酵素で消化し、最後にT7プロモーターをベースとしたpET23−dベクターとライゲーションし、大腸菌に形質転換させた。特有であるこれらの2つの部位は、T7 RNAポリメラーゼプロモーターの影響下でのハイブリッド遺伝子構築物の挿入に役立つ(Studier and Moffatt,1986)。この構築物pET23−d_N_EGF_SAKをXL1B細胞に形質転換させ(recA-及びendA-)、プラスミドは増殖し、シーケンシングにかけられた。ここでこのプラスミドをBL21(DE3)細胞(発現宿主)に移し、T7 RNAポリメラーゼの誘導をIPTGにより行い、封入体として細胞内形態で発現させた(発現条件、封入体の単離及びリフォールディングプロトコルに関しては「実施例で用いた方法」を参照のこと)。最後に、リフォールディングしたタンパク質をクロマトグラフィにより高精製形態で得て、活性アッセイに供した。
SAK_EGF構築物をSAK_EGF Fp1及びSAK_EGF Rp2プライマーの助けを借りて調製し、pPIC−9K_SAK_EGFを増幅のためのテンプレートに使用した。プライマーSAK_bac Fp1はNcoI制限部位を5'端に含有し、AUGコドンの導入を支援した。他方、SAK_bac Rp2はXhoI制限部位を含有し、6ヒスチジンアミノ酸コード化ヌクレオチドの意図したSAK_EGF遺伝子構築物の下流端の終止コドンに先立っての導入を促進した。PCR条件は以下の通りであった:第1サイクルにおける95℃での5分間にわたる完全変性、次の28サイクル:95℃での45秒間にわたる変性、50℃での45秒間にわたるアニーリング、72℃での1.5分間にわたる伸長及び72℃での10分間にわたる最終ステップによる部分長PCR産物の完成。得られた遺伝子ブロックはNcoI部位をその上流端に含有し、XhoI部位はその下流端に存在し、ゲル抽出により精製し、pET23−dベクターにライゲーションした。このライゲーション産物を電気穿孔法により大腸菌XL1B細胞に形質転換し(recA-及びendA-)、得られたプラスミドを正しいオープンリーディングフレームの検証のためにシーケンシングした。プラスミドの増殖はXL1B細胞で行われたが、ハイブリッド遺伝子産物の発現のために、プラスミドを大腸菌BL21(DE3)細胞(Novagen Inc.)に形質転換した。最後に、タンパク質をIPTGの存在下で発現させ、封入体が形成され、これらを単離し、「実施例で用いた方法」で詳述したように酸化/還元グルタチオンの存在下でリフォールディングし、上記のEGF_SAK構築物についてのプラスミノーゲン活性化因子及びトロンビン阻害活性アッセイに供した。
トロンビン切断可能配列を、N末端融合構築物においてEGFとSAKとの接合部で導入した。この構築物に関し、プラスミドpET−23−dにおけるEGF_SAK DNAをEGF及びSAKの増幅ためのテンプレートとして使用した。トロンビン切断可能プライマーを設計した。EGF増幅のために、指定のE4 Fp1及びE6 Rp2(これらのプライマーの配列については表3の番号13、14を参照のこと)プライマーを使用した。E4 Fp1プライマーはXhoI制限部位及びEGF4、5、6ドメインの上流配列をその5'端に含有し、他方、E6 Rp2はEGF4、5、6の下流配列及びトロンビン切断可能ヌクレオチド配列をその5'端に含有する。以下のPCR条件を増幅に用いた:95℃での完全変性、続く次の28サイクル:95℃での45秒間、45℃での45秒間のアニーリング、72℃での1分間にわたる伸長及び最後に72℃での更に10分間にわたる伸長。このPCR反応で得られた遺伝子ブロックはEGFの4番ドメインをインフレームでコードしている配列をその5'端に含有し、その3'端はEGF4、5、6の下流配列及びトロンビン切断可能配列を含有する。第2のPCR反応において、SAK遺伝子ブロックをTCS SAK Fp3及びTCS SAK Rp4(これらのプライマーの配列については表3、すなわち配列番号15、16を参照のこと)の助けを借りて増幅した。TCS SAK Fp3はトロンビン切断可能配列及びSAKヌクレオチドの上流配列を含有する。同様に、他方のプライマーTCS SAK Rp4はSAKの下流配列及び終止コドン、それに続くNotI制限部位を含有する。得られる増幅された遺伝子ブロックはトロンビン切断可能ヌクレオチド配列をその5'端に、また終止コドン及びNotI部位をその3'端に含有する。以下のPCR条件をSAK遺伝子ブロックの増幅に用いた:95℃での完全変性、続く以下の通りの次の28サイクル:95℃での45秒間にわたる変性、45℃での45秒間にわたるアニーリング、72℃での1分間にわたる伸長及び72℃での更に10分間にわたる最終伸長。両方のPCR産物をゲル溶出させ、E4 Fp1及びTCS_SAK Rp4(これらのプライマーの配列については表3、すなわち表の配列番号13及び16番を参照のこと)の助けを借りた、EGF_TCS_SAK遺伝子ブロックの増幅のための一般的なオーバーラップエクステンションPCR反応に以下の条件下で供した:95℃での完全変性、続く95℃での45秒間にわたる変性、45℃での45秒間にわたるアニーリング、72℃での2分間にわたる伸長(28サイクル)及び72℃での更に10分間にわたる最終伸長。得られた遺伝子ブロックはXhoI制限部位をその5'端に、またNotI部位をその3'端に含有した。このPCR産物をXhoI及びNotI酵素で消化し、pET23−dにおけるクローニングに続くトロンビン切断可能配列の正しいインフレーム挿入についてシーケンシングした後、pPIC−9Kにライゲーションした。
TPA−EGF及びSAK−EGF融合構築物の生物学的活性:
EGFとtPAとの異なるハイブリッド遺伝子構築物(化学的に合成した(N_EGF_tPA_EGF)ハイブリッドtPA融合構築物(EGF4、5、6を挿入してtPAの内因性ドメイン、すなわちegf及びクリングル1を置き換えた)、内的欠失型のtPAとEGFとの融合体(内因性egf及びクリングル1が欠失し、EGF4、5、6はN又はC末端(at either N and C terminii)で融合)及び上記の構築物の酸化耐性バリアント)を、本質的に上述したようにpPIC−9Kベクターのα−分泌シグナル配列の上流でインフレームでクローニングした。各構築物を制限エンドヌクレアーゼにより別々にチェックし、またDNAシーケンシングにより検証した。これらの構築物全てを個々にピチア・パストリス(GS115)に電気穿孔法により移した(「実施例で用いた一般的な方法」のセクションを参照のこと)。個々のクローンをBMGY及びBMMY培地
(BMGY=1%酵母抽出物、2%ペプトン、1Xグリセロール、1Xアミノ酸非含有酵母ニトロゲンベース及び100mMリン酸カリウム緩衝液pH5.5、BMMY=1%酵母抽出物、2%ペプトン、1Xメタノール、1Xアミノ酸非含有酵母ニトロゲンベース及び100mMリン酸カリウム緩衝液pH5.5)上で5日間にわたって、メタノールで誘導しながら成長させ、上清をカゼインオーバーレイ法によりプラスミノーゲン活性化能について試験した(「実施例で用いた方法」のセクションを参照のこと)。これとは別に、各陽性クローンの上清をプラスミノーゲン活性化について一段階アッセイにおいて試験した。次に、各高活性クローンを1リットルレベルで成長させ、各タンパク質中のtPAポリペプチドの存在をウェスタンブロット法により検証し、リジン親和性及びイオン交換クロマトグラフィが続いた(詳細なプロトコルについては「実施例で用いた方法」を参照のこと)。クロマトグラフィにより得られた異なる融合構築物は、SDS−PAGEにより92〜95%純粋であった。これらの精製されたタンパク質をプラスミノーゲン活性化アッセイに供した。精製された各タンパク質の比活性はピチア由来の未変性の組織プラスミノーゲン活性化因子と極めて似ていた。しかしながら、フィンガー、egf、クリングル1及びクリングル2ドメインを欠失させてEGF4、5、6ドメインに置き換えた構築物はカゼインオーバーレイ法では比較的弱い加水分解領域を示し、また概して、プラスミノーゲン及び発色基質を使用した定量的マイクロタイタープレートをベースとしたアッセイでは比較的低いプラスミノーゲン活性化因子活性を示した。更に、内的に欠失した構築物における可溶性フィブリンの存在下で見られる活性における刺激の程度は、EGFの融合がtPAの末端であったtPA/tPA変異体と比較してはるかに低かった。tPA変異体(アスパラギンに変更となったスレオニン115番アミノ酸(T115N)、グルタミンに変更となったアスパラギン129番アミノ酸(N129Q)及びtPAのKHRRコード化領域、すなわち4重アラニン変異列に置き換えられた残基308〜311(KHRR(308〜311→AAAA、上の実施例を参照のこと))を含有)の場合、プラスミノーゲン活性化因子活性は「基礎」活性及び可溶性フィブリンの存在下でのその刺激の両方の観点で未変性様であった。同時に、この構築物は、トロンビン阻害及びタンパク質C活性化の明確に定義されたアッセイにおいて最も高いトロンビン阻害特性を示した(「実施例で用いた方法」のセクションを参照のこと)。対照的に、凝固時間アッセイでチェックするトロンビン阻害(高マイクロモル濃度にのぼる未変性のtPAの存在又は不在下のフィブリン網形成)は本質的に緩衝液のコントロールと比較して変化せず、ナノモル濃度の、上記の「四重アラニン」変異体あるいはEGF4、5、6をtPAに異なる場所に内的に又は端部で組み込むこんだことを含めた異なる精製キメラ構築物の添加により凝固時間が用量依存的に著しく増加した。凝固における観察された増加は、いずれかの端部で融合したEGFドメインと比較してN_EGF_tPA_EGF構築物においてより顕著であった。このタイプの作用はトロンビン介在タンパク質C活性化アッセイでも観察され、N_EGF_tPA_EGにより産生されたタンパク質Cの量は1つのEGF4、5、6ドメインを含有するtPA融合構築物及び内的に融合したEGF−tPA構築物より概して2〜4倍高かった。別の結果では、EGF−tPA融合体のEGF部位にメチオニン置換がある酸化耐性形態をそのトロンビン介在タンパク質C活性化能について比較した場合、メチオニンをバリンで置き換えた酸化耐性形態は常に15〜20%高いタンパク質C活性化を示した。
本発明は、当該分野で使用されている抗トロンビン血栓溶解剤より有利である。組織プラスミノーゲン活性化因子のクリングル、アルギニン(R)、グリシン(G)及びアスパラギン酸(D)を含有するペプチド配列並びにヒルジンの抗トロンビン部をスタフィロキナーゼのC末端に導入して抗トロンビン血栓溶解剤を作ろうとの試みがこれまでなされてきて、これはこの形態のスタフィロキナーゼが、「RGDペプチド」、tPA由来クリングルによるフィブリン親和性上昇及び早期の一時的に生成されるトロンビンの阻害を通じて抗トロンビン特性を付与するトロンビン不活性化ヒルジン部による血小板阻害に役立つということを前提としている(Szemraj,Walkowiak et al.2005)。血栓溶解後の再閉塞問題に対抗するために、組織因子及び第VII因子を阻害する組み換えリポタンパク質関連凝固阻害因子(LACI)を通じた試みもなされた(Haskel,Torr et al.1991)。これは組織因子との不活性複合体の形成に役立つが、一時的な血餅に結合したトロンビンを妨害することはできない。
本発明のまた別の態様は、以下のとおりであってもよい。
〔1〕キメラタンパク質構築物であって、
ストレプトキナーゼ、組織プラスミノーゲン活性化因子、スタフィロキナーゼ、ウロキナーゼ並びにこれらの誘導体及び類似体から成る群から選択される血栓溶解タンパク質に融合したトロンボモジュリンの4、5及び6上皮増殖因子様ドメイン(EGF4、5、6)を含むことを特徴とするキメラタンパク質構築物。
〔2〕前記トロンボモジュリンEGF4、5、6ドメインが、前記血栓溶解タンパク質又はその誘導体若しくは類似体に、前記血栓溶解タンパク質又はその誘導体若しくは類似体のN末端、C末端又はN及びCの両方の末端で融合する、前記〔1〕に記載のキメラタンパク質構築物。
〔3〕前記血栓溶解タンパク質が1つ以上のアミノ酸置換、挿入、欠失又は切断を有するストレプトキナーゼを含み、また前記構築物がプラスミノーゲン活性化、トロンビン阻害及び抗凝固タンパク質C経路活性化活性を有する、前記〔1〕に記載のキメラタンパク質構築物。
〔4〕前記トロンボモジュリンEGF4、5、6ドメインが前記ストレプトキナーゼのアルファドメインとベータドメインとの間又はベータドメインとガンマドメインとの間、あるいはストレプトキナーゼ誘導体又は類似体のアルファドメインとベータドメインとの間又はベータドメインとガンマドメインとの間で融合し、前記ストレプトキナーゼ誘導体又は類似体が1つ以上の変異、付加、挿入又は切断を含み、また前記構築物がプラスミノーゲンを活性化し、トロンビンを阻害し、抗凝固タンパク質C経路を活性化する、前記〔1〕に記載のキメラタンパク質構築物。
〔5〕前記EGF4、5、6ドメインがストレプトキナーゼ又はストレプトキナーゼ誘導体若しくは類似体に、ストレプトキナーゼN末端、ストレプトキナーゼC末端、N及びCの両方のストレプトキナーゼ末端又はストレプトキナーゼのドメイン間位置から選択される1つ以上の位置にてインフレームで融合する、前記〔2〕に記載のキメラタンパク質構築物。
〔6〕前記ストレプトキナーゼ誘導体が残基5〜383又は5〜414に及ぶ、前記〔5〕に記載のキメラタンパク質構築物。
〔7〕前記ストレプトキナーゼ誘導体が残基16〜383に及ぶ、前記〔6〕に記載のキメラタンパク質構築物。
〔8〕前記EGF4、5、6ドメインがストレプトキナーゼN末端、ストレプトキナーゼC末端又はN及びCの両方のストレプトキナーゼ末端から選択される1つ以上の位置にてインフレームで融合し、前記EGF4、5、6ドメインのMet41がバリン、アラニン又はグルタミンに置き換えられ、あるいはC末端Met435がバリン、アラニン又はグルタミンに置き換えられ、あるいは同時N及びC末端融合構築物において、Met41及びMet435が独立してバリン、アラニン又はグルタミンに置き換えられる、前記〔2〕に記載のキメラタンパク質構築物。
〔9〕トランスグルタミナーゼ認識配列を更に含む、前記〔1〕に記載のキメラタンパク質構築物。
〔10〕前記EGF4、5、6ドメインと前記血栓溶解タンパク質又はその誘導体若しくは類似体との接合部に1つ以上のトロンビン切断可能配列を更に含む、前記〔1〕に記載のキメラタンパク質構築物。
〔11〕哺乳動物において血栓症を治療する方法であって、
治療を必要とする該哺乳動物に治療有効量の前記〔1〕〜〔10〕のいずれかに記載のキメラタンパク質構築物を投与することを含むことを特徴とする方法。
〔12〕キメラタンパク質構築物であって、
組織プラスミノーゲン活性化因子(tPA)誘導体、類似体又はフラグメントに、前記tPA誘導体、類似体又はフラグメントのN末端で融合、前記tPA誘導体、類似体又はフラグメントのC末端で融合、前記tPA誘導体、類似体又はフラグメントの両方の末端で融合、あるいは前記tPA誘導体、類似体又はフラグメント内で内的に融合したトロンボモジュリンのEGF4、5、6ドメインを含むことを特徴とするキメラタンパク質構築物。
〔13〕前記EGF4、5、6ドメインと前記tPA誘導体、類似体又はフラグメントとの融合が1つ以上のリンカーフラグメントを更に含む、前記〔12〕に記載のキメラタンパク質構築物。
〔14〕前記1つ以上のリンカーフラグメントが構築物の柔軟性を促進する1つ以上のアミノ酸を含む、前記〔13〕に記載のキメラタンパク質構築物。
〔15〕前記tPA誘導体、類似体又はフラグメントが1つ以上の変異、付加、挿入又は切断を含み、前記tPA誘導体、類似体又はフラグメントがプラスミノーゲンを活性化し、トロンビンを阻害し、抗凝固タンパク質Cを活性化させる、前記〔12〕に記載のキメラタンパク質構築物。
〔16〕1つ以上のトロンボモジュリンEGF4、5、6ドメインに融合した組織プラスミノーゲン活性化因子(tPA)のフラグメント又はその切断若しくは修飾形態を含むため、tPAのEGFドメインが前記1つ以上のトロンボモジュリンEGF4、5、6ドメインに置き換えられ、また抗トロンビン及びプラスミノーゲン活性化の両方の活性を有する、前記〔12〕に記載のキメラタンパク質構築物。
〔17〕1つ以上のトロンボモジュリンEGF4、5、6ドメインに融合した組織プラスミノーゲン活性化因子(tPA)のフラグメント又はその切断若しくは修飾形態を含むため、tPAのクリングル1及びEGFドメインが前記1つ以上のトロンボモジュリンEGF4、5、6ドメインに置き換えられ、また抗トロンビン及びプラスミノーゲン活性化の両方の活性を有する、前記〔12〕に記載のキメラタンパク質構築物。
〔18〕前記tPA EGFドメイン及びクリングル1ドメインが前記tPAフラグメントのN末端又はC末端で1つ以上のトロンボモジュリンEGF4、5、6ドメインに置き換えられる、前記〔17〕に記載のキメラタンパク質構築物。
〔19〕1つ以上のリンカーフラグメントを前記tPAフラグメント又はその切断若しくは修飾形態と前記トロンボモジュリンEGF4、5、6ドメインとの間に更に含み、前記リンカーフラグメントが、構築物がトロンビン阻害、タンパク質C活性化及びプラスミノーゲン活性化能を有するように構築物の柔軟性を促進するアミノ酸残基を含む、前記〔17〕又は〔18〕のいずれかに記載のキメラタンパク質構築物。
〔20〕前記EGF4、5、6成分のメチオニン41がアラニン、バリン又はグルタミンに置き換えられる、前記〔17〕〜〔19〕のいずれかに記載のキメラタンパク質構築物。
〔21〕キメラタンパク質構築物であって、
スタフィロキナーゼ(SAK)のN末端側又はC末端側の端にインフレームで融合したトロンボモジュリンのEGF4、5、6ドメインを含むことを特徴とするキメラタンパク質構築物。
〔22〕前記トロンボモジュリンEGF4、5、6ドメインのメチオニン41がアラニン、バリン又はグルタミンに置き換えられる、前記〔21〕に記載のキメラタンパク質構築物。
〔23〕トロンビン切断可能配列を前記SAKと前記EGF4、5、6ドメイン領域との間に更に含む、前記〔21〕又は〔22〕のいずれかに記載のキメラタンパク質構築物。
〔24〕トランスグルタミナーゼ架橋配列を更に含む、前記〔22〕〜〔23〕のいずれかに記載のキメラタンパク質構築物。
〔25〕水溶液又は生理食塩水に可溶性である、前記〔1〕〜〔10〕又は〔12〕〜〔24〕のいずれかに記載のキメラタンパク質構築物。
〔26〕トロンビンを阻害する方法であって、
前記〔1〕〜〔10〕又は〔12〕〜〔24〕のいずれかに記載のキメラタンパク質構築物の使用を含むことを特徴とする方法。
〔27〕タンパク質Cを活性化する方法であって、
前記〔1〕〜〔10〕又は〔12〕〜〔24〕のいずれかに記載のキメラタンパク質構築物の使用を含むことを特徴とする方法。
〔28〕抗トロンビン及びプラスミノーゲン活性化の両方をもたらす方法であって、
前記〔1〕〜〔10〕又は〔12〕〜〔24〕のいずれかに記載のキメラタンパク質構築物の使用を含むことを特徴とする方法。
〔29〕医薬製剤であって、
薬学的有効量の前記〔1〕〜〔10〕又は〔12〕〜〔24〕のいずれかに記載のキメラタンパク質構築物を含むことを特徴とする医薬製剤。
〔30〕哺乳動物における血栓溶解の方法であって、
それを必要とする該哺乳動物に治療有効量の前記〔1〕〜〔10〕又は〔12〕〜〔24〕のいずれかに記載のキメラタンパク質構築物をそれを必要とする患者に投与することを含むことを特徴とする方法。
〔31〕細菌系における発現によって調製される、前記〔1〕〜〔10〕又は〔12〕〜〔24〕のいずれかに記載のキメラ構築物。
〔32〕真核生物系における発現によって調製される、前記〔1〕〜〔10〕又は〔12〕〜〔24〕のいずれかに記載のキメラ構築物。
〔33〕前記真核生物発現系が、動物細胞、ピチア・パストリス及び真菌から成る群から選択される、前記〔32〕に記載のキメラ構築物。
〔34〕細胞外媒体に分泌される、前記〔33〕に記載のキメラタンパク質構築物。
〔35〕1つ以上のアミノ酸が、Gly、Asn、Pro、Ser、Gln、Arg及びLysから成る群から選択される、前記〔13〕に記載のキメラタンパク質構築物。
〔36〕核酸配列であって、
前記〔1〕〜〔10〕、〔12〕〜〔25〕又は31〜35のいずれかに記載のキメラタンパク質構築物をコードしていることを特徴とする核酸配列。
〔37〕ベクターであって、
前記〔36〕に記載の核酸配列を含むことを特徴とするベクター。
〔38〕宿主細胞であって、
前記〔37〕に記載のベクターを含むことを特徴とする宿主細胞。
〔39〕宿主細胞発現系における前記タンパク質をコードしている核酸配列の発現によって調製される、前記〔1〕〜〔10〕、〔12〕〜〔25〕又は31〜35のいずれかに記載のキメラタンパク質構築物。
〔40〕前記〔1〕〜〔10〕及び〔12〕〜〔25〕又は31〜35のいずれかに記載のキメラタンパク質構築物を調製する方法であって、
宿主細胞発現系における該タンパク質をコードしている核酸配列の発現によることを特徴とする方法。
〔41〕前記宿主細胞発現系が真核生物発現系である、前記〔40〕に記載の方法。
〔42〕前記宿主細胞発現系が細菌発現系である、前記〔41〕に記載の方法。
〔43〕前記細菌が大腸菌である、前記〔42〕に記載の方法。
〔44〕前記真核生物発現系が動物細胞又は酵母細胞である、前記〔43〕に記載の方法。
〔45〕前記酵母がピチア・パストリスである、前記〔44〕に記載の方法。
〔46〕前記キメラタンパク質構築物が前記宿主細胞から細胞外媒体に分泌される、前記〔40〕〜〔45〕のいずれかに記載の方法。
Seq ID 1=SK
Seq ID 2=EGF
Seq Id 3=ドメイン間SK_EGF
アルファ/ベータ間
Seq ID 4=N_EGF_SK
SEQ ID 5=ドメイン間ベータ/ガンマ
SEQ ID 6=SK_EGF
SEQ ID 7=N_EGF_SK_EGF
SEQ ID 8=EGF456人工
SEQ ID 9=人工合成TPA
SEQ ID 10=N_EGF_TPA_EGF
SEQ ID 11=N_EGF_TPA
SEQ ID 12=TPA_EGF
SEQ ID 13=ID EGF TPA(egf欠失)
SEQ ID 14=ID EGF TPA(egf、K1欠失)
SEQ ID 15=N_EGF(egf、k1欠失)
SEQ ID 16=TPA_EGF(egf、k1欠失)
SEQ ID 17=SAK
SEQ ID 18=N_EGF_SAK
SEQ ID 19=SAK_EGF
SEQ ID 20=tPAのバリアント
(テネクテプラーゼ)
Claims (20)
- キメラタンパク質構築物であって、
ストレプトキナーゼ、及び、前記ストレプトキナーゼの無修飾のタンパク質に対して少なくとも90%の配列同一性を有するストレプトキナーゼ相同体から成る群から選択される血栓溶解タンパク質に融合したトロンボモジュリンの4、5及び6上皮増殖因子様ドメイン(EGF4、5、6)を含み、
前記トロンボモジュリンの4、5、6上皮増殖因子様ドメインが、前記血栓溶解タンパク質に、前記血栓溶解タンパク質のN末端、C末端又はN及びCの両方の末端で融合している
ことを特徴とするキメラタンパク質構築物。 - 前記血栓溶解タンパク質が、ストレプトキナーゼ又は前記ストレプトキナーゼの無修飾のタンパク質に対して少なくとも95%の配列同一性を有するストレプトキナーゼ相同体である、請求項1に記載のキメラタンパク質構築物。
- 前記血栓溶解タンパク質が、配列番号112のアミノ酸配列に対して少なくとも90%の配列同一性を有するアミノ酸配列を含む、請求項1に記載のキメラタンパク質構築物。
- 前記ストレプトキナーゼ相同体が、配列番号112の残基5〜383又は残基5〜414又は残基16〜383に及ぶ、請求項1に記載のキメラタンパク質構築物。
- 前記構築物のトロンボモジュリンの4、5及び6上皮増殖因子様ドメインが、配列番号111のアミノ酸配列に対して少なくとも90%の配列同一性を有する配列を含み、
前記配列番号111の前記EGF4、5、6ドメインのMet41の1つ以上がバリン、アラニン又はグルタミンに置き換えられており、
前記キメラタンパク質構築物が、抗トロンビン活性及びプラスミノーゲン活性化活性を示す、
請求項1に記載のキメラタンパク質構築物。 - 少なくとも1つのトランスグルタミナーゼ認識可能架橋配列を更に含む、請求項2に記載のキメラタンパク質構築物。
- 前記EGF4、5、6ドメインとストレプトキナーゼ又はストレプトキナーゼ相同体との接合部に1つ以上のトロンビン切断可能配列を更に含む、請求項2に記載のキメラタンパク質構築物。
- 細菌系又は真核生物系における発現により調製される、請求項1に記載のキメラタンパク質構築物。
- 前記真核生物系が、動物細胞系及び酵母細胞系からなる群より選択される、請求項8に記載のキメラタンパク質構築物。
- 前記キメラタンパク質構築物が、細胞外媒体に分泌される、請求項9に記載のキメラタンパク質構築物。
- 請求項1に記載のキメラタンパク質構築物をコードしている、核酸分子。
- 請求項11に記載の核酸分子を含む、ベクター。
- 請求項12に記載のベクターを含む、宿主細胞。
- 宿主細胞発現系における請求項11に記載の核酸分子の発現によって調製される、請求項1に記載のキメラタンパク質構築物。
- 前記構築物をコードしている核酸分子が、配列番号3、4、5、6又は7から選択される、請求項1に記載のキメラタンパク質構築物。
- 前記酵母細胞がピチア・パストリス(Pichia pastoris)である、請求項9に記載のキメラタンパク質構築物。
- 薬学的担体と共に、薬学的有効量の請求項1に記載のキメラタンパク質構築物を含む、医薬製剤。
- 請求項1に記載のキメラタンパク質構築物を含む、トロンビン阻害に使用するための医薬組成物。
- 請求項1に記載のキメラタンパク質構築物を含む、抗トロンビン及びプラスミノーゲン活性化に使用するための医薬組成物。
- 請求項1に記載のキメラタンパク質構築物を含む、血栓溶解に使用するための医薬組成物。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| IN1845/DEL/2010 | 2010-08-05 | ||
| IN1845DE2010 | 2010-08-05 | ||
| PCT/IB2011/001825 WO2012017310A2 (en) | 2010-08-05 | 2011-08-05 | Protein fusion constructs possessing thrombolytic and anticoagulant properties |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2013535211A JP2013535211A (ja) | 2013-09-12 |
| JP2013535211A5 JP2013535211A5 (ja) | 2014-09-18 |
| JP6234224B2 true JP6234224B2 (ja) | 2017-11-22 |
Family
ID=45559872
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013522316A Active JP6234224B2 (ja) | 2010-08-05 | 2011-08-05 | 血栓溶解及び抗凝固特性を有するタンパク質融合構築物 |
Country Status (13)
| Country | Link |
|---|---|
| US (1) | US9150844B2 (ja) |
| EP (1) | EP2600891B1 (ja) |
| JP (1) | JP6234224B2 (ja) |
| KR (1) | KR20130099027A (ja) |
| CN (1) | CN103179982A (ja) |
| AR (1) | AR082588A1 (ja) |
| AU (1) | AU2011287360A1 (ja) |
| BR (1) | BR112013002739A2 (ja) |
| CA (1) | CA2807749C (ja) |
| CL (1) | CL2011001887A1 (ja) |
| MX (1) | MX2013001385A (ja) |
| WO (1) | WO2012017310A2 (ja) |
| ZA (1) | ZA201301032B (ja) |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| IN2015MN00047A (ja) * | 2012-07-05 | 2015-10-16 | Hadasit Med Res Service | |
| BR102017005783A2 (pt) * | 2017-03-21 | 2018-10-02 | Fund Butantan | processo de obtenção de esculptina e seus fragmentos, esculptina recombinante e seus usos |
| WO2024060167A1 (zh) * | 2022-09-23 | 2024-03-28 | 庄伟哲 | 靶向整合素αIIbβ3的含组织纤维溶酶原活化剂或其变异体的融合蛋白质及其应用 |
Family Cites Families (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE3853100T2 (de) * | 1987-06-04 | 1995-08-03 | Zymogenetics Inc | Gewebs-Plasminogen-Aktivator-Analoge mit modifizierten Wachstumsfaktordomänen. |
| DK299087D0 (da) * | 1987-06-12 | 1987-06-12 | Novo Industri As | Proteins and derivatives thereof |
| KR940009084B1 (ko) * | 1988-05-18 | 1994-09-29 | 체크 포인트 시스템스, 인코오퍼레이티드 | 자기 및 공명회로 검출용 안테나 시스템 |
| WO1990010081A1 (en) * | 1989-02-17 | 1990-09-07 | Codon | Soluble analogs of thrombomodulin |
| US5256770A (en) * | 1990-04-09 | 1993-10-26 | Schering Ag | Oxidation resistant thrombomodulin analogs |
| US5466668A (en) | 1989-04-28 | 1995-11-14 | Schering Aktiengesellschaft | Superior thrombomodulin analogs for pharmaceutical use |
| GB8927722D0 (en) * | 1989-12-07 | 1990-02-07 | British Bio Technology | Proteins and nucleic acids |
| CA2065409C (en) | 1990-06-27 | 2002-05-14 | Mochida Pharmaceutical Co., Ltd. | Anticoagulant polypeptides |
| WO1994016085A2 (en) * | 1992-12-30 | 1994-07-21 | Zymogenetics, Inc. | Hybrid proteins having cross-linking and tissue-binding activities |
| DE4442665A1 (de) | 1994-11-30 | 1996-06-05 | Gruenenthal Gmbh | Chimäre Proteine mit fibrinolytischen und thrombinhemmenden Eigenschaften |
| IN190822B (ja) | 1998-12-24 | 2003-08-23 | Council Scient Ind Res | |
| AU2001258230A1 (en) * | 2000-05-10 | 2001-11-20 | Novo-Nordisk A/S | Pharmaceutical composition comprising a factor viia and a tfpi inhibitor |
| US6632791B1 (en) | 2000-06-21 | 2003-10-14 | Schering Aktiengesellschaft | Thrombomodulin analogs for pharmaceutical use |
| KR101013697B1 (ko) | 2002-05-01 | 2011-02-10 | 바이엘 쉐링 파마 악티엔게젤샤프트 | 항응고제로서의 조직 인자 표적화된 신규 트롬보모둘린융합 단백질 |
| CN1480466A (zh) * | 2002-09-03 | 2004-03-10 | �й������ž�����ҽѧ��ѧԺ����ҽ | 一类溶栓抗凝双功能融合蛋白及应用 |
| WO2005059142A1 (en) * | 2003-12-18 | 2005-06-30 | Werner Seeger | Novel chimeric plasminogen activators and their pharmaceutical use |
| JP4897792B2 (ja) | 2005-04-20 | 2012-03-14 | ビロメッド カンパニー, リミテッド | 融合タンパク質の分離のための組成物および方法 |
| AR071169A1 (es) | 2008-03-31 | 2010-06-02 | Council Scient Ind Res | Variantes de la estreptoquinasa que contienen cisteina y sus formas covalentemente modificadas |
-
2011
- 2011-08-05 CA CA2807749A patent/CA2807749C/en active Active
- 2011-08-05 CL CL2011001887A patent/CL2011001887A1/es unknown
- 2011-08-05 JP JP2013522316A patent/JP6234224B2/ja active Active
- 2011-08-05 AR ARP110102867A patent/AR082588A1/es not_active Application Discontinuation
- 2011-08-05 WO PCT/IB2011/001825 patent/WO2012017310A2/en active Application Filing
- 2011-08-05 AU AU2011287360A patent/AU2011287360A1/en not_active Abandoned
- 2011-08-05 BR BR112013002739A patent/BR112013002739A2/pt not_active IP Right Cessation
- 2011-08-05 US US13/814,412 patent/US9150844B2/en active Active
- 2011-08-05 EP EP11814173.8A patent/EP2600891B1/en not_active Not-in-force
- 2011-08-05 CN CN2011800482916A patent/CN103179982A/zh active Pending
- 2011-08-05 KR KR1020137005514A patent/KR20130099027A/ko not_active Application Discontinuation
- 2011-08-05 MX MX2013001385A patent/MX2013001385A/es not_active Application Discontinuation
-
2013
- 2013-02-07 ZA ZA2013/01032A patent/ZA201301032B/en unknown
Also Published As
| Publication number | Publication date |
|---|---|
| BR112013002739A2 (pt) | 2019-09-24 |
| CL2011001887A1 (es) | 2012-02-03 |
| AU2011287360A1 (en) | 2013-02-21 |
| CA2807749A1 (en) | 2012-02-09 |
| ZA201301032B (en) | 2014-04-30 |
| CN103179982A (zh) | 2013-06-26 |
| KR20130099027A (ko) | 2013-09-05 |
| EP2600891A4 (en) | 2014-01-01 |
| MX2013001385A (es) | 2013-07-15 |
| EP2600891B1 (en) | 2018-01-17 |
| AR082588A1 (es) | 2012-12-19 |
| US9150844B2 (en) | 2015-10-06 |
| US20130136731A1 (en) | 2013-05-30 |
| WO2012017310A3 (en) | 2012-07-19 |
| JP2013535211A (ja) | 2013-09-12 |
| EP2600891A2 (en) | 2013-06-12 |
| CA2807749C (en) | 2023-02-28 |
| WO2012017310A2 (en) | 2012-02-09 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP0191606B1 (en) | Vectors and methods for expression of human protein c activity | |
| US5759542A (en) | Compositions and methods for the delivery of drugs by platelets for the treatment of cardiovascular and other diseases | |
| AU666104B2 (en) | Recombinant agents affecting thrombosis | |
| US5632986A (en) | Phospholipid-targeted thrombolytic agents | |
| JP4355924B2 (ja) | トロンビン切断性キメラタンパク質 | |
| EP0200451B1 (en) | Protease resistant urokinase composition, its production and use | |
| NO175066B (no) | DNA-konstruksjon, plasmid og fremgangsmåte for ekspresjon av faktor VII og IX aktiviteter i pattedyrceller | |
| EP0538459A1 (en) | Phospholipid-targeted thrombolytic agents | |
| US7163817B2 (en) | Clot-specific streptokinase proteins possessing altered plasminogen activation characteristics and a process for their preparation | |
| JP6234224B2 (ja) | 血栓溶解及び抗凝固特性を有するタンパク質融合構築物 | |
| US7223583B2 (en) | Antithrombotic thrombin variants | |
| JPH0193535A (ja) | 線溶活性増強剤 | |
| JP2006516113A5 (ja) | ||
| NZ237244A (en) | Cloning and production of human von willebrand factor analogues and compositions thereof | |
| JPH08507200A (ja) | 昆虫類の唾液からのトロンビン阻害剤 | |
| JPH05506354A (ja) | 端が切り取られた軽鎖を有する活性プロテインc | |
| JP2942578B2 (ja) | 新しい結合特性を有する超酸化物不均化酵素類縁体 | |
| TW201306861A (zh) | 具有血栓溶解與抗凝血劑特性之蛋白質融合構造 | |
| AU6629194A (en) | Novel polypeptide having factor xa inhibitory activity | |
| JPH08510903A (ja) | 蛭ヒルド・メディシナリスの組換えxa因子インヒビターの作製 | |
| JP3153236B2 (ja) | 端が切り取られた軽鎖を有する組換えプロテインc | |
| JP2518832B2 (ja) | 変形された組織プラスミノ−ゲンアクチベ−タ− | |
| JPH0571228B2 (ja) | ||
| IE62206B1 (en) | Protease resistant urolinase composition, its production and use | |
| JP2002234899A (ja) | 血栓症に作用する組換え薬剤 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20140804 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20140804 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20150819 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20151118 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20151218 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20160119 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20160218 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20160704 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20161003 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20161028 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20170104 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20170524 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20170823 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20170925 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20171024 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6234224 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |