JP5824523B2 - 電気化学ルミネセンス検出における信号増強化合物 - Google Patents
電気化学ルミネセンス検出における信号増強化合物 Download PDFInfo
- Publication number
- JP5824523B2 JP5824523B2 JP2013535387A JP2013535387A JP5824523B2 JP 5824523 B2 JP5824523 B2 JP 5824523B2 JP 2013535387 A JP2013535387 A JP 2013535387A JP 2013535387 A JP2013535387 A JP 2013535387A JP 5824523 B2 JP5824523 B2 JP 5824523B2
- Authority
- JP
- Japan
- Prior art keywords
- ecl
- reagent
- reagent composition
- group
- analyte
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/75—Systems in which material is subjected to a chemical reaction, the progress or the result of the reaction being investigated
- G01N21/76—Chemiluminescence; Bioluminescence
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D499/00—Heterocyclic compounds containing 4-thia-1-azabicyclo [3.2.0] heptane ring systems, i.e. compounds containing a ring system of the formula:, e.g. penicillins, penems; Such ring systems being further condensed, e.g. 2,3-condensed with an oxygen-, nitrogen- or sulfur-containing hetero ring
- C07D499/04—Preparation
- C07D499/10—Modification of an amino radical directly attached in position 6
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/66—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light electrically excited, e.g. electroluminescence
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L3/00—Containers or dishes for laboratory use, e.g. laboratory glassware; Droppers
- B01L3/50—Containers for the purpose of retaining a material to be analysed, e.g. test tubes
- B01L3/502—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures
- B01L3/5027—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip
- B01L3/502715—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip characterised by interfacing components, e.g. fluidic, electrical, optical or mechanical interfaces
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L3/00—Containers or dishes for laboratory use, e.g. laboratory glassware; Droppers
- B01L3/50—Containers for the purpose of retaining a material to be analysed, e.g. test tubes
- B01L3/502—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures
- B01L3/5027—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip
- B01L3/502761—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip specially adapted for handling suspended solids or molecules independently from the bulk fluid flow, e.g. for trapping or sorting beads, for physically stretching molecules
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/52—Use of compounds or compositions for colorimetric, spectrophotometric or fluorometric investigation, e.g. use of reagent paper and including single- and multilayer analytical elements
Description
本発明はまた、i)式Iおよび式IIのカルボン酸アミドの群から選択される化合物ならびにii)少なくとも1種類の共反応体を含む、ECL測定用の試薬組成物に関する。
定義:
本明細書中で用いる以下の用語はそれぞれ、このセクションにおけるものと関連する意味をもつ。
“カルボン酸アミド”およびそれらの化学構造を表1に挙げる。
本発明による“被検体特異的試薬(analyte specific reagent)”(ASR)という用語は、被検体を特異的に結合する能力を備えた分子または生体分子(たとえば、タンパク質または抗体)であると理解すべきである。“被検体特異的試薬”(ASR)は、生物検体中の個々の化学物質を同定し、その量を測定するために使用できる生体分子のクラスである。ASRは、たとえば抗体(ポリクローナル抗体およびモノクローナル抗体の両方)、特異的受容体タンパク質、リガンド、核酸配列、およびこれらに類する試薬であって、検体中の物質と特異的に結合または化学反応させることにより生物検体中の個々の化学物質またはリガンドを同定および定量するための診断用途に使用することを意図したものである。簡単に言えば、被検体特異的試薬はアッセイの活性成分である。ASRは、被検体を結合する親和性および特異性に関する両方の基準を満たすであろう。
“検出”には、直接的および間接的な検出を含めたいずれかの検出手段が含まれる。用語“検出”は、被検体の定量および定性の両方の測定(本明細書中では被検体の測定)を含む最も広い意味で用いられる。1観点において、本明細書に記載する検出方法は、試料中の目的とする被検体の存在のみを同定するために用いられる。他の観点において、この方法は、試料中の目的とする被検体の量を定量するために使用できる。
科学の分野で“測定すること”/“測定”は、量の大きさ、たとえば長さまたは質量を、測定単位、たとえばメートルまたはキログラムに関して推定または決定するプロセスである。測定すること/測定は、それに対比して他のものを評価できる基準点を用いる。測定という用語は、測定プロセスから得られた特定の結果(測定値)を表わすためにも使用できる。それは比較のための基礎である。測定信号または測定値を濃度に相関させるための材料および方法を当業者は承知している。
1態様において、本発明は、試料中の被検体を電気化学ルミネセンス検出により測定するための、下記の段階を含む方法に関する:a)試料を、電気化学ルミネセント基で標識した検出試薬と共にインキュベートする、b)被検体を結合した標識付き検出試薬と被検体を含まない標識付き検出試薬を分離する、c)分離した標識付き検出試薬を、下記を含む試薬組成物と共にインキュベートする:i)少なくとも1種類の共反応体、ならびにii)式Iおよび式IIのカルボン酸アミドの群から選択される少なくとも1種類の化合物
本発明の1観点は、本発明の試薬組成物に基づく改善されたECL方法、特に低い検出限界を特徴とするECL方法に関する。この試薬組成物は意外にも、特異的信号を増強しかつバックグラウンド信号を低下させる。より詳細には、本発明の方法は、ECL標識の不存在下でのバックグラウンド電気化学ルミネセンスを低下させることによって、低い検出レベルで改善された感度をもたらす。
ある態様において、本方法に用いるカルボン酸アミドは、アセトアミド、2−フルオロアセトアミド、2−クロロアセトアミド、プロパンアミド、2−クロロプロパンアミド、3−クロロプロパンアミド、ブタンアミドおよび2−クロロブタンアミドからなる群から選択される。
好ましい態様において、本方法に用いるカルボン酸アミドは、アセトアミド、プロパンアミドおよびブタンアミドからなる群から選択される。
本発明の1観点は、試薬混合物および試薬組成物の有効保存、たとえば長期貯蔵の要望を満たす。適切な保存剤はECL信号発生に対して影響をもたないか、あるいは理想的な場合にはECL信号発生にプラスの影響をもつべきである。
ある態様において、試料中の被検体を電気化学ルミネセンス検出により測定するための方法は、試薬組成物がさらに塩類および消泡剤を含むことを特徴とする。
電気化学ルミネセンスによる検出方法を実施するための装置は、実施例のセクション(実施例1、2または3)に述べてあり、あるいはEP 1 892 524 (A1)に記載されている。さらに、そのような装置は測定ユニットおよび/または液体容器の温度を制御する手段も含むことができる。測定ユニットは、その中で電気化学ルミネセンスを測定するセルであると理解される。液体容器は貯蔵容器であってもよいが、供給デバイス、たとえば測定に際して測定ユニットに収容される試薬溶液用のチューブであってもよい。
本発明のある観点は、ECL信号発生のための、信号対ノイズ比を高める改善された試薬組成物に関する。より具体的には、本発明の試薬組成物は、ECL標識の不存在下でのバックグラウンド電気化学ルミネセンスを低下させることによって、低い検出レベルでの改善された感度をもたらす。意外にも、カルボン酸アミドのような化合物を含む試薬組成物は、これらの化合物を用いない一般的な検査試薬より低いバックグラウンドルミネセンスを放射する。これは特に、信号対バックグラウンド比(=信号対ノイズ比)の増大によって感度が大幅に改善される低い検出レベルにおける利点である。この改善された試薬組成物は、ECLを発生させるための方法を支持するカルボン酸アミドおよび他の化合物の群からの化合物を含む。意外にも本発明者らは、本発明による試薬組成物を用いて電気化学ルミネセンス検出を実施すると、ECL検出の信号対ノイズ比が10%〜60%改善されることを見出した。
前記のように、本発明のある観点は、ECL信号発生に対して影響をもたないかあるいはプラスの影響をもつ有効な保存剤の添加という要望を満たす。細菌および真菌の増殖を効果的に制御する適切な無機化合物であるホウ酸および/またはボレートが同定された。意外にも本発明者らは、ECL測定用の試薬組成物中に存在するホウ酸および/またはボレートがECL信号発生にマイナスの影響をもたないことを見出した。保存剤としてホウ酸および/またはボレートを含む試薬組成物がECL信号発生プロセスにプラスの効果、すなわち特異的信号の増強効果をもつことが、意外にも見出された。さらに、それらの高い活性、および安全性妨害または環境事項に関連する問題が軽度であることは有利である。ホウ酸またはボレートは、試薬組成物中に一般に用いられる他の幾つかの保存剤と異なり、ハロゲンを含まず、またホルムアルデヒドを放出しない。ECL信号発生に際してホウ酸を存在させた結果を、実施例のセクション、たとえば実施例2に示す。
ある態様において、本発明は、i)少なくとも1種類の共反応体、およびiii)保存剤であるボレートを含む、ECL測定用の試薬組成物に関する。
本発明の他の観点は、試料、検査特異的試薬および/または検査試薬の必要体積が少なくなることによる経費削減に関する。より低い試薬体積に対する信号損失は、本発明による有利な試薬組成物の使用によって補償できる。
試薬混合物:
ECLを測定するために、本発明による試薬組成物を追加化合物と混合して試薬混合物を調製することができる。ある態様において、本発明は、ECL測定用の試薬組成物を含むECL測定用の試薬混合物であって、下記を含む試薬混合物に関する:i)式Iおよび式IIのカルボン酸アミドの群から選択される化合物、ii)少なくとも1種類の共反応体、iii)試験すべき試料、ならびにiv)電気化学ルミネセント基で標識した少なくとも1種類の検出試薬。
使用:
本発明のある観点は、電気化学ルミネセンス検出方法を実施するための、本発明の改良された試薬組成物および/または改良された試薬混合物の使用に関する。
本発明の1観点は、1以上の容器内に本発明の試薬組成物の1以上の成分を含むキットに関する。これらの成分を、場合により追加試薬と組み合わせて、本発明の試薬組成物を調製することができる。キットは、ある態様において、追加のアッセイ関連構成要素、たとえばECL標識、ECL標識したアッセイ試薬、希釈剤、洗浄溶液、タンパク質変性試薬、酵素、結合試薬、アッセイプレート、使い捨て用品なども含むことができる。
ある態様において、本発明は、下記を含むECL測定用の試薬組成物を含む、ECL測定用キットに関する:i)式Iおよび式IIのカルボン酸アミドの群から選択される化合物、ならびにii)少なくとも1種類の共反応体。
カルボン酸アミドを含むアッセイ緩衝液(試薬組成物)を用いるECL測定
Roche Elecsys(登録商標)2010デバイスを用い、以下に述べるアッセイに利用できるプロトコルを用いてECL測定を実施した。
180mMトリプロピルアミン(TPA)
0.1%ポリドカノール
300mMリン酸緩衝液
KOH/H3PO4を用いて最終pHをpH6.8に調整した。アッセイ緩衝液もブランク値として用いた。
同様な実験で、遊離標識の信号を測定した。遊離標識値は、遊離ECL標識を含有する溶液が微粒子(アッセイ緩衝液中10nMのRuBpy)の不存在下で発生する信号を表わす。この値を、いずれかの追加化合物を含まないアッセイ緩衝液に対比して%で表3に示す。このアッセイ方式は、均一測定または均一アッセイ方式としても知られる。100%を超える値は、選択したカルボン酸アミドを指示した濃度で添加することによって増強したECL信号の指標となる。結果を表3に示す。
さらに、ビーズを含む簡略化アッセイを用いた値を測定した。この人為的アッセイは、高い特異的信号を得るためのRuBpy標識微粒子を含むアッセイである。このアッセイ方式は、不均一測定または不均一アッセイ方式としても知られる。この人為的アッセイの特異的信号と、追加化合物を含む前記のアッセイ緩衝液を用いたバックグラウンド信号(アッセイ緩衝液バックグラウンド)との差を、△人為的アッセイとして、追加化合物を含まないアッセイ緩衝液に対する%で示す。100%を超える値は、選択したカルボン酸アミドを指示した濃度で添加することにより増強したECL信号の指標となる。結果を表4に示す。
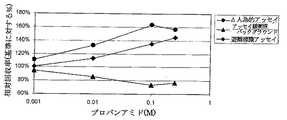
図1に、表2、3および4に示すプロパンアミドについての結果を含むグラフを提示する。図2に、表2、3および4に示す2−クロロアセトアミドについての結果を含むグラフを提示する。図3に、表2、3および4に示すブタンアミドについての結果を含むグラフを提示する。図4に、表2、3および4に示すアセトアミドについての結果を含むグラフを提示する。
信号増強性保存剤としてのホウ酸
Roche Elecsys(登録商標)2010デバイスを用い、以下に述べるアッセイに推奨されるプロトコルを用いてECL測定を実施した。
180mMトリプロピルアミン(TPA)
0.1%ポリドカノール
0.1% Oxaban A
300mMリン酸緩衝液
このアッセイ緩衝液に漸増量のホウ酸を指示に従って添加した。KOH/H3PO4を用いて最終pHをpH6.8に調整した。
特に下記の測定を実施した:
実施例3
プロパンアミドおよびホウ酸を含有するアッセイ緩衝液がElecsys(登録商標)アッセイの検出下限に及ぼす効果
幾つかの市販インビトロ診断アッセイ(HBeAg:Roche注文No.:11820583,Anti−TSHR:Roche注文No.:04388780,TNThs:Roche注文No.:05092744)についての検出下限を測定して、2種類のアッセイ緩衝液調製物を比較した。
180mM TPA,0.1%ポリドカノール,300mMリン酸緩衝液,0.1% Oxaban A
アッセイ緩衝液B:
180mM TPA,0.1 %ポリドカノール,50mMプロパンアミド,300mMリン酸緩衝液,1%ホウ酸
KOH/H3PO4を用いて、両方のアッセイ緩衝液AおよびBの最終pHをpH6.8に調整した。
Claims (16)
- 試料中の被検体を電気化学ルミネセンス検出により測定するための、下記の段階を含む方法:
a)試料を、電気化学ルミネセント基で標識した検出試薬と共にインキュベートする、
b)被検体を結合した標識付き検出試薬と被検体を含まない標識付き検出試薬を分離する、
c)分離した被検体を結合した標識付き検出試薬を、下記を含む試薬組成物と共にインキュベートする:
i)少なくとも1種類のECL共反応体、ならびに
ii)式Iおよび式IIのカルボン酸アミドの群から選択される少なくとも1種類の化合物
e)電気化学ルミネセンス(ECL)信号を測定し、これにより被検体を測定する。 - ECLを用いる試料中の被検体の測定を水溶液中で実施することを特徴とする、請求項1に記載の方法。
- カルボン酸アミドが、アセトアミド、2−フルオロアセトアミド、2−クロロアセトアミド、プロパンアミド、2−クロロプロパンアミド、3−クロロプロパンアミド、ブタンアミドおよび2−クロロブタンアミドからなる群から選択されることを特徴とする、請求項1または2に記載の方法。
- 試薬組成物が0.01M〜0.25Mの濃度のカルボン酸アミドを含むことを特徴とする、請求項1〜3のいずれか1項に記載の方法。
- 段階1c)の試薬組成物が保存剤を含むことを特徴とする、請求項1〜4のいずれか1項に記載の方法。
- 段階1c)の試薬組成物が0.1%〜5%の濃度の保存剤を含むことを特徴とする、請求項5に記載の方法。
- 段階1c)の試薬組成物がホウ酸およびボレートからなる群から選択される保存剤を含むことを特徴とする、請求項5または6に記載の方法。
- 段階1c)の試薬組成物が界面活性剤および緩衝剤を含むことを特徴とする、請求項1〜7のいずれか1項に記載の方法。
- 段階1c)の試薬組成物が、さらに塩類および/または消泡剤を含むことを特徴とする、請求項8に記載の方法。
- 第三級アミンがトリプロピルアミン(TPA)である、請求項10に記載の試薬組成物。
- 試薬組成物が、さらにホウ酸およびボレートからなる群から選択される保存剤を含むことを特徴とする、請求項10または請求項11に記載の試薬組成物。
- 請求項10〜12のいずれか1項に記載の試薬組成物、試験すべき試料、および電気化学ルミネセント基で標識した少なくとも1種類の検出試薬を含む、ECL測定用の試薬混合物。
- ECLの測定における、請求項10〜12のいずれか1項に記載の試薬組成物の使用。
- 請求項10〜12のいずれか1項に記載の試薬組成物を含む、ECL測定のためのキット。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP10188716.4 | 2010-10-25 | ||
| EP10188716 | 2010-10-25 | ||
| EP10192106.2 | 2010-11-22 | ||
| EP10192106 | 2010-11-22 | ||
| PCT/EP2011/068540 WO2012055815A1 (en) | 2010-10-25 | 2011-10-24 | Use of signal enhancing compounds in electrochemiluminescence detection |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2013542436A JP2013542436A (ja) | 2013-11-21 |
| JP2013542436A5 JP2013542436A5 (ja) | 2014-07-03 |
| JP5824523B2 true JP5824523B2 (ja) | 2015-11-25 |
Family
ID=44860372
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013535387A Active JP5824523B2 (ja) | 2010-10-25 | 2011-10-24 | 電気化学ルミネセンス検出における信号増強化合物 |
Country Status (16)
| Country | Link |
|---|---|
| US (1) | US9341575B2 (ja) |
| EP (1) | EP2633289B1 (ja) |
| JP (1) | JP5824523B2 (ja) |
| KR (1) | KR101789356B1 (ja) |
| CN (1) | CN103443614B (ja) |
| AU (1) | AU2011322704B2 (ja) |
| BR (1) | BR112013007614B1 (ja) |
| CA (1) | CA2813089C (ja) |
| DK (1) | DK2633289T3 (ja) |
| ES (1) | ES2581553T3 (ja) |
| HK (1) | HK1188826A1 (ja) |
| HU (1) | HUE029030T2 (ja) |
| MX (1) | MX336940B (ja) |
| PL (1) | PL2633289T3 (ja) |
| SG (1) | SG189113A1 (ja) |
| WO (1) | WO2012055815A1 (ja) |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN106153953A (zh) * | 2015-04-03 | 2016-11-23 | 盐城拜明生物技术有限公司 | 一种用于检测血清样品中叶酸含量的叶酸释放剂 |
| CN108698047B (zh) | 2016-03-11 | 2022-04-01 | 豪夫迈·罗氏有限公司 | 电化学发光检测中的支链胺 |
| CN106124753B (zh) * | 2016-07-08 | 2018-03-06 | 广州东林生物科技有限公司 | 电化学发光缓冲液及清洗液 |
| CN108375571B (zh) * | 2018-02-05 | 2019-11-26 | 苏州长光华医生物医学工程有限公司 | 一种用于化学发光免疫检测的磁颗粒试剂及试剂盒 |
| CN113366313A (zh) * | 2019-01-03 | 2021-09-07 | 中尺度技术有限责任公司 | 实施分析测量的组合物及方法 |
| CN114375391A (zh) * | 2019-07-31 | 2022-04-19 | 株式会社日立高新技术 | 生物分子分析方法和生物分子分析装置 |
| CN115494232B (zh) * | 2022-10-31 | 2023-10-27 | 江苏三联生物工程股份有限公司 | 4,4-二甲基噁唑啉在制备含辣根过氧化物酶的试剂中的应用 |
Family Cites Families (60)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| NL178647C (nl) * | 1974-03-08 | 1986-05-01 | Duphar Int Res | Werkwijze ter bereiding van een de plantengroei bevorderende vloeibare samenstelling. |
| US4554088A (en) | 1983-05-12 | 1985-11-19 | Advanced Magnetics Inc. | Magnetic particles for use in separations |
| US4695393A (en) | 1983-05-12 | 1987-09-22 | Advanced Magnetics Inc. | Magnetic particles for use in separations |
| US4628037A (en) | 1983-05-12 | 1986-12-09 | Advanced Magnetics, Inc. | Binding assays employing magnetic particles |
| US4698302A (en) | 1983-05-12 | 1987-10-06 | Advanced Magnetics, Inc. | Enzymatic reactions using magnetic particles |
| US5310687A (en) * | 1984-10-31 | 1994-05-10 | Igen, Inc. | Luminescent metal chelate labels and means for detection |
| US5147806A (en) | 1988-04-29 | 1992-09-15 | Igen, Inc. | Method and apparatus for conducting electrochemiluminescence measurements |
| US5591581A (en) | 1986-04-30 | 1997-01-07 | Igen, Inc. | Electrochemiluminescent rhenium moieties and methods for their use |
| US6165729A (en) | 1986-04-30 | 2000-12-26 | Hyperion Catalysis International, Inc. | Electrochemiluminescent reaction utilizing amine-derived reductant |
| US6316607B1 (en) | 1986-04-30 | 2001-11-13 | Igen International, Inc. | Electrochemiluminescent assays |
| US4965392A (en) | 1987-03-26 | 1990-10-23 | Neorx Corporation | Chelating compounds for metal-radionuclide labeled proteins |
| US5935779A (en) | 1988-11-03 | 1999-08-10 | Igen International Inc. | Methods for improved particle electrochemiluminescence assay |
| US5202238A (en) | 1987-10-27 | 1993-04-13 | Oncogen | Production of chimeric antibodies by homologous recombination |
| US5204244A (en) | 1987-10-27 | 1993-04-20 | Oncogen | Production of chimeric antibodies by homologous recombination |
| US5308754A (en) | 1988-03-21 | 1994-05-03 | Kankare Jouko J | Electrogenerated luminescence in solution |
| US5093268A (en) | 1988-04-28 | 1992-03-03 | Igen, Inc. | Apparatus for conducting a plurality of simultaneous measurements of electrochemiluminescent phenomena |
| US5779976A (en) * | 1988-11-03 | 1998-07-14 | Igen International, Inc. | Apparatus for improved luminescence assays |
| US5705402A (en) | 1988-11-03 | 1998-01-06 | Igen International, Inc. | Method and apparatus for magnetic microparticulate based luminescence assay including plurality of magnets |
| CA2002083C (en) | 1988-11-03 | 2001-01-09 | Haresh P. Shah | Enhanced electrochemiluminescence |
| US5324457A (en) | 1989-10-02 | 1994-06-28 | Board Of Regents, The University Of Tx System | Devices and methods for generating electrogenerated chemiluminescence |
| JPH0534345A (ja) | 1991-02-19 | 1993-02-09 | Tdk Corp | 化学発光を利用する抗原・抗体の測定方法 |
| ZA929351B (en) | 1991-12-11 | 1993-06-04 | Igen Inc | Electrochemiluminescent label for DNA assays. |
| JP3541047B2 (ja) * | 1993-02-18 | 2004-07-07 | 日本化薬株式会社 | バイオリアクターの防腐剤および測定法 |
| DE4401577A1 (de) * | 1993-05-03 | 1994-11-10 | Boehringer Mannheim Gmbh | Elektrochemilumineszenzverfahren |
| EP0697106B1 (de) * | 1993-05-03 | 1997-04-02 | Roche Diagnostics GmbH | Elektrochemilumineszenzverfahren |
| US5466416A (en) | 1993-05-14 | 1995-11-14 | Ghaed; Ali | Apparatus and methods for carrying out electrochemiluminescence test measurements |
| NZ291154A (en) | 1994-07-25 | 1997-11-24 | Boehringer Mannheim Gmbh | Di- or trivalent rare earth or transition metal complexes having three ligands, each of which has at least two nitrogen-containing heterocycles and complexed through nitrogen, and at least one reactive group bound to the ligard(s) |
| US5786141A (en) | 1994-08-26 | 1998-07-28 | Bard; Allen J. | Electrogenerated chemiluminescence labels for analysis and/or referencing |
| US5866434A (en) | 1994-12-08 | 1999-02-02 | Meso Scale Technology | Graphitic nanotubes in luminescence assays |
| US5643713A (en) | 1995-06-07 | 1997-07-01 | Liang; Pam | Electrochemiluminescent monitoring of compounds |
| US5641623A (en) | 1995-01-04 | 1997-06-24 | Martin; Mark T. | Electrochemiluminescence assay |
| US20010003647A1 (en) | 1995-06-07 | 2001-06-14 | Ji Sun | Coreatant-including electrochemiluminescent compounds, methods, systems and kits utilizing same |
| US6140045A (en) | 1995-03-10 | 2000-10-31 | Meso Scale Technologies | Multi-array, multi-specific electrochemiluminescence testing |
| US6066448A (en) | 1995-03-10 | 2000-05-23 | Meso Sclae Technologies, Llc. | Multi-array, multi-specific electrochemiluminescence testing |
| US6207369B1 (en) | 1995-03-10 | 2001-03-27 | Meso Scale Technologies, Llc | Multi-array, multi-specific electrochemiluminescence testing |
| US6319670B1 (en) | 1995-05-09 | 2001-11-20 | Meso Scale Technology Llp | Methods and apparatus for improved luminescence assays using microparticles |
| US5679519A (en) | 1995-05-09 | 1997-10-21 | Oprandy; John J. | Multi-label complex for enhanced sensitivity in electrochemiluminescence assay |
| US6099760A (en) | 1995-06-07 | 2000-08-08 | Igen, Inc. | Hydrogen peroxide based ECL |
| GB9606850D0 (en) | 1996-04-01 | 1996-06-05 | Univ Liverpool | An assay system and novel labelled compounds for use therwith |
| FI970593A (fi) * | 1997-02-12 | 1998-08-13 | Sakari Mikael Kulmala | Pinnoitettujen johteiden käyttö analyyttisiin tarkoituksiin |
| FR2764381A1 (fr) | 1997-06-09 | 1998-12-11 | Univ De Neuchatel | Detecteur electrochimioluminescent |
| US6413783B1 (en) | 1997-09-18 | 2002-07-02 | Meso Scale Technologies, Llc | Assay sonication apparatus and methodology |
| DE19803528A1 (de) | 1998-01-30 | 1999-08-05 | Roche Diagnostics Gmbh | Verfahren zur Analyse einer Probe mittels eines Elektrochemolumineszenz-Bindungsreaktion-Tests |
| US6200531B1 (en) | 1998-05-11 | 2001-03-13 | Igen International, Inc. | Apparatus for carrying out electrochemiluminescence test measurements |
| EP0962773A1 (en) | 1998-06-03 | 1999-12-08 | Mark Howard Jones | Electrochemical based assay processes instrument and labels |
| GB9815042D0 (en) | 1998-07-10 | 1998-09-09 | Imperial College | Detector |
| US6136268A (en) | 1999-08-17 | 2000-10-24 | Orion Diagnostica | Method for luminescence measurements |
| US6994971B1 (en) * | 1999-10-08 | 2006-02-07 | University Of Utah Research Foundation | Particle analysis assay for biomolecular quantification |
| US7897404B2 (en) | 2000-09-29 | 2011-03-01 | Roche Diagnostics Operations, Inc. | Conjugates of defined stoichiometry |
| DK1412487T3 (da) | 2001-07-30 | 2010-08-30 | Meso Scale Technologies Llc | Assayelektroder der har immobiliserede lipid/proteinlag og fremgangsmåder til at fremstille og anvende disse |
| AU2002324947B2 (en) * | 2001-09-10 | 2007-11-15 | Meso Scale Technologies, Llc. | Assay buffer, compositions containing the same, and methods of using the same |
| CN102620959B (zh) * | 2002-12-26 | 2015-12-16 | 梅索磅秤技术有限公司 | 检定盒及其使用方法 |
| US20060275841A1 (en) * | 2004-12-20 | 2006-12-07 | Martin Blankfard | Assay method and apparatus with reduced sample matrix effects |
| FI119894B (fi) * | 2005-03-30 | 2009-04-30 | Labmaster Oy | Elektrokemiluminesenssiin perustuva analyysimenetelmä ja siinä käytettävä laite |
| US20070116600A1 (en) * | 2005-06-23 | 2007-05-24 | Kochar Manish S | Detection device and methods associated therewith |
| CN102841195B (zh) * | 2005-12-21 | 2016-02-03 | 梅索斯卡莱科技公司 | 具有分析试剂的分析模块及其制备和使用方法 |
| ATE530895T1 (de) | 2006-08-25 | 2011-11-15 | Hoffmann La Roche | Zelle zur durchführung elektrochemilumineszenter messungen |
| CN101246125A (zh) * | 2008-03-14 | 2008-08-20 | 华南师范大学 | 基于纳米/微米粒子放大信号的非pcr扩增的快速检测转基因产品的电化学发光方法 |
| JP2010237020A (ja) * | 2009-03-31 | 2010-10-21 | Japan Aerospace Exploration Agency | 生体分子検出装置及び生体分子検出方法 |
| FI20100246A (fi) * | 2010-06-11 | 2011-12-12 | Sakari Kulmala | Menetelmät ja laitteet luminesenssin tuottamiseksi integroiduista elektrodisiruista katodisten ja bipolaaristen pulssien avulla |
-
2011
- 2011-10-24 CA CA2813089A patent/CA2813089C/en active Active
- 2011-10-24 KR KR1020137009849A patent/KR101789356B1/ko active IP Right Grant
- 2011-10-24 MX MX2013004230A patent/MX336940B/es active IP Right Grant
- 2011-10-24 HU HUE11774051A patent/HUE029030T2/en unknown
- 2011-10-24 ES ES11774051.4T patent/ES2581553T3/es active Active
- 2011-10-24 DK DK11774051.4T patent/DK2633289T3/en active
- 2011-10-24 BR BR112013007614-3A patent/BR112013007614B1/pt active IP Right Grant
- 2011-10-24 WO PCT/EP2011/068540 patent/WO2012055815A1/en active Application Filing
- 2011-10-24 AU AU2011322704A patent/AU2011322704B2/en active Active
- 2011-10-24 EP EP11774051.4A patent/EP2633289B1/en active Active
- 2011-10-24 PL PL11774051.4T patent/PL2633289T3/pl unknown
- 2011-10-24 SG SG2013022553A patent/SG189113A1/en unknown
- 2011-10-24 JP JP2013535387A patent/JP5824523B2/ja active Active
- 2011-10-24 CN CN201180062441.9A patent/CN103443614B/zh active Active
-
2013
- 2013-03-15 US US13/844,778 patent/US9341575B2/en active Active
-
2014
- 2014-02-26 HK HK14101834.2A patent/HK1188826A1/xx unknown
Also Published As
| Publication number | Publication date |
|---|---|
| HUE029030T2 (en) | 2017-01-30 |
| BR112013007614A2 (pt) | 2018-05-02 |
| CN103443614B (zh) | 2015-07-22 |
| KR101789356B1 (ko) | 2017-10-23 |
| CN103443614A (zh) | 2013-12-11 |
| ES2581553T3 (es) | 2016-09-06 |
| CA2813089A1 (en) | 2012-05-03 |
| CA2813089C (en) | 2018-02-20 |
| WO2012055815A1 (en) | 2012-05-03 |
| EP2633289A1 (en) | 2013-09-04 |
| BR112013007614B1 (pt) | 2020-12-29 |
| HK1188826A1 (en) | 2014-05-16 |
| US20130224758A1 (en) | 2013-08-29 |
| US9341575B2 (en) | 2016-05-17 |
| AU2011322704A1 (en) | 2013-03-21 |
| DK2633289T3 (en) | 2016-06-06 |
| JP2013542436A (ja) | 2013-11-21 |
| EP2633289B1 (en) | 2016-04-20 |
| AU2011322704B2 (en) | 2014-12-11 |
| PL2633289T3 (pl) | 2016-12-30 |
| MX336940B (es) | 2016-02-08 |
| KR20140012940A (ko) | 2014-02-04 |
| SG189113A1 (en) | 2013-05-31 |
| MX2013004230A (es) | 2013-05-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5824523B2 (ja) | 電気化学ルミネセンス検出における信号増強化合物 | |
| US20240044804A9 (en) | Branched-chain amines in electrochemiluminescence detection | |
| CN100420947C (zh) | 用单一捕获剂定量检测特异性分析物的方法及其试剂盒 | |
| Debad et al. | Clinical and biological applications of ECL | |
| CN108333344A (zh) | 高灵敏度的化学发光免疫分析试剂盒及其制备方法和应用 | |
| EP2639584A1 (en) | Real time diagnostic assays using an evanescence biosensor | |
| CN101718779A (zh) | 检测人血清铜蓝蛋白的免疫纳米金同步散射光谱试剂盒及其使用方法 | |
| CN1963512A (zh) | 乙肝病毒的化学发光定性定量检测方法 | |
| EP0812920A1 (en) | Use of porphyrins in instrumental detection methods | |
| KR101928333B1 (ko) | 복수개의 금속 나노 태그를 이용한 복수개의 타겟의 동시 분석 방법 | |
| JPH0750032B2 (ja) | 溶液中での電気発生のルミネセンスに基づく分析方法 | |
| US5677192A (en) | Electrochemiluminescence assay | |
| CN101504410A (zh) | 用于蛋白悬浮芯片检测的血清样品处理制剂 | |
| JP2021505906A (ja) | HBsAgの定量検出のためのキット及び方法 | |
| CN108872609A (zh) | 一种用于检测犬细小病毒抗体的时间分辨荧光免疫试剂盒 | |
| US20230384297A1 (en) | Electrothermal flow-enhanced electrochemical magneto-immunosensor | |
| JPH04262258A (ja) | 細胞atpの免疫特異性的および生物発光的検定法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20140516 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20140516 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20141226 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20150127 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20150423 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20150911 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20151009 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5824523 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |