JP5701601B2 - 糖尿病前症、心血管疾患及びその他のメタボリックシンドローム関連障害のバイオマーカー並びにその使用方法 - Google Patents
糖尿病前症、心血管疾患及びその他のメタボリックシンドローム関連障害のバイオマーカー並びにその使用方法 Download PDFInfo
- Publication number
- JP5701601B2 JP5701601B2 JP2010517019A JP2010517019A JP5701601B2 JP 5701601 B2 JP5701601 B2 JP 5701601B2 JP 2010517019 A JP2010517019 A JP 2010517019A JP 2010517019 A JP2010517019 A JP 2010517019A JP 5701601 B2 JP5701601 B2 JP 5701601B2
- Authority
- JP
- Japan
- Prior art keywords
- biomarkers
- level
- diabetes
- subject
- acid
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 239000000090 biomarker Substances 0.000 title claims description 546
- 238000000034 method Methods 0.000 title claims description 172
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 title description 203
- 201000009104 prediabetes syndrome Diseases 0.000 title description 132
- 206010018429 Glucose tolerance impaired Diseases 0.000 title description 123
- 208000001145 Metabolic Syndrome Diseases 0.000 title description 106
- 201000000690 abdominal obesity-metabolic syndrome Diseases 0.000 title description 106
- 208000001280 Prediabetic State Diseases 0.000 title description 101
- 208000024172 Cardiovascular disease Diseases 0.000 title description 17
- 208000001072 type 2 diabetes mellitus Diseases 0.000 claims description 292
- 206010022489 Insulin Resistance Diseases 0.000 claims description 270
- 239000000523 sample Substances 0.000 claims description 128
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 claims description 102
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 claims description 101
- 239000008103 glucose Substances 0.000 claims description 100
- 239000012472 biological sample Substances 0.000 claims description 55
- 102000004877 Insulin Human genes 0.000 claims description 50
- 108090001061 Insulin Proteins 0.000 claims description 50
- 229940125396 insulin Drugs 0.000 claims description 50
- 235000000346 sugar Nutrition 0.000 claims description 30
- 238000012545 processing Methods 0.000 claims description 28
- WQZGKKKJIJFFOK-QTVWNMPRSA-N D-mannopyranose Chemical compound OC[C@H]1OC(O)[C@@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-QTVWNMPRSA-N 0.000 claims description 9
- GHOKWGTUZJEAQD-ZETCQYMHSA-N (D)-(+)-Pantothenic acid Chemical compound OCC(C)(C)[C@@H](O)C(=O)NCCC(O)=O GHOKWGTUZJEAQD-ZETCQYMHSA-N 0.000 claims description 6
- KPGXRSRHYNQIFN-UHFFFAOYSA-N 2-oxoglutaric acid Chemical compound OC(=O)CCC(=O)C(O)=O KPGXRSRHYNQIFN-UHFFFAOYSA-N 0.000 claims description 6
- COLNVLDHVKWLRT-QMMMGPOBSA-N L-phenylalanine Chemical compound OC(=O)[C@@H](N)CC1=CC=CC=C1 COLNVLDHVKWLRT-QMMMGPOBSA-N 0.000 claims description 6
- 235000021588 free fatty acids Nutrition 0.000 claims description 6
- COLNVLDHVKWLRT-UHFFFAOYSA-N phenylalanine Natural products OC(=O)C(N)CC1=CC=CC=C1 COLNVLDHVKWLRT-UHFFFAOYSA-N 0.000 claims description 6
- LRFVTYWOQMYALW-UHFFFAOYSA-N 9H-xanthine Chemical compound O=C1NC(=O)NC2=C1NC=N2 LRFVTYWOQMYALW-UHFFFAOYSA-N 0.000 claims description 5
- QHKABHOOEWYVLI-UHFFFAOYSA-N 3-methyl-2-oxobutanoic acid Chemical compound CC(C)C(=O)C(O)=O QHKABHOOEWYVLI-UHFFFAOYSA-N 0.000 claims description 4
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 claims description 4
- 230000037396 body weight Effects 0.000 claims description 4
- OUYCCCASQSFEME-UHFFFAOYSA-N tyrosine Natural products OC(=O)C(N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-UHFFFAOYSA-N 0.000 claims description 4
- 102000011690 Adiponectin Human genes 0.000 claims description 3
- 108010076365 Adiponectin Proteins 0.000 claims description 3
- YNXLOPYTAAFMTN-SBUIBGKBSA-N C([C@H](N)C(=O)N1CCC[C@H]1C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CCCCN)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C)C(=O)N1[C@@H](CCC1)C(=O)NCC(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](CO)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H](C)C(=O)N[C@@H](CO)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1NC=NC=1)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(N)=O)C1=CC=C(O)C=C1 Chemical compound C([C@H](N)C(=O)N1CCC[C@H]1C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CCCCN)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C)C(=O)N1[C@@H](CCC1)C(=O)NCC(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](CO)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H](C)C(=O)N[C@@H](CO)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1NC=NC=1)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(N)=O)C1=CC=C(O)C=C1 YNXLOPYTAAFMTN-SBUIBGKBSA-N 0.000 claims description 3
- GHOKWGTUZJEAQD-UHFFFAOYSA-N Chick antidermatitis factor Natural products OCC(C)(C)C(O)C(=O)NCCC(O)=O GHOKWGTUZJEAQD-UHFFFAOYSA-N 0.000 claims description 3
- 108010088847 Peptide YY Proteins 0.000 claims description 3
- 102100029909 Peptide YY Human genes 0.000 claims description 3
- 108010076181 Proinsulin Proteins 0.000 claims description 3
- HWXBTNAVRSUOJR-UHFFFAOYSA-N alpha-hydroxyglutaric acid Natural products OC(=O)C(O)CCC(O)=O HWXBTNAVRSUOJR-UHFFFAOYSA-N 0.000 claims description 3
- 229940009533 alpha-ketoglutaric acid Drugs 0.000 claims description 3
- 229940055726 pantothenic acid Drugs 0.000 claims description 3
- 235000019161 pantothenic acid Nutrition 0.000 claims description 3
- 239000011713 pantothenic acid Substances 0.000 claims description 3
- VOUAQYXWVJDEQY-QENPJCQMSA-N 33017-11-7 Chemical compound OC(=O)CC[C@H](N)C(=O)N[C@@H](C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](C(C)C)C(=O)NCC(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)NCC(=O)NCC(=O)NCC(=O)N1CCC[C@H]1C(=O)NCC(=O)N[C@@H](C)C(=O)NCC(=O)N[C@@H](CO)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)N1[C@H](C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(O)=O)C(=O)NCC(=O)N[C@@H](CO)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(O)=O)CCC1 VOUAQYXWVJDEQY-QENPJCQMSA-N 0.000 claims description 2
- 108010075254 C-Peptide Proteins 0.000 claims description 2
- 102000001554 Hemoglobins Human genes 0.000 claims description 2
- 108010054147 Hemoglobins Proteins 0.000 claims description 2
- 108010028554 LDL Cholesterol Proteins 0.000 claims description 2
- 238000008214 LDL Cholesterol Methods 0.000 claims description 2
- 239000008777 Glycerylphosphorylcholine Substances 0.000 claims 6
- WWNNZCOKKKDOPX-UHFFFAOYSA-N N-methylnicotinate Chemical compound C[N+]1=CC=CC(C([O-])=O)=C1 WWNNZCOKKKDOPX-UHFFFAOYSA-N 0.000 claims 6
- SUHOQUVVVLNYQR-MRVPVSSYSA-N choline alfoscerate Chemical compound C[N+](C)(C)CCOP([O-])(=O)OC[C@H](O)CO SUHOQUVVVLNYQR-MRVPVSSYSA-N 0.000 claims 6
- 229960004956 glycerylphosphorylcholine Drugs 0.000 claims 5
- WHBMMWSBFZVSSR-UHFFFAOYSA-N 3-hydroxybutyric acid Chemical compound CC(O)CC(O)=O WHBMMWSBFZVSSR-UHFFFAOYSA-N 0.000 claims 4
- XMIIGOLPHOKFCH-UHFFFAOYSA-N 3-phenylpropionic acid Chemical compound OC(=O)CCC1=CC=CC=C1 XMIIGOLPHOKFCH-UHFFFAOYSA-N 0.000 claims 4
- BKAJNAXTPSGJCU-UHFFFAOYSA-N 4-methyl-2-oxopentanoic acid Chemical compound CC(C)CC(=O)C(O)=O BKAJNAXTPSGJCU-UHFFFAOYSA-N 0.000 claims 4
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 claims 4
- CVSVTCORWBXHQV-UHFFFAOYSA-N creatine Chemical compound NC(=[NH2+])N(C)CC([O-])=O CVSVTCORWBXHQV-UHFFFAOYSA-N 0.000 claims 4
- WRIDQFICGBMAFQ-UHFFFAOYSA-N (E)-8-Octadecenoic acid Natural products CCCCCCCCCC=CCCCCCCC(O)=O WRIDQFICGBMAFQ-UHFFFAOYSA-N 0.000 claims 3
- AFENDNXGAFYKQO-VKHMYHEASA-N (S)-2-hydroxybutyric acid Chemical compound CC[C@H](O)C(O)=O AFENDNXGAFYKQO-VKHMYHEASA-N 0.000 claims 3
- LQJBNNIYVWPHFW-UHFFFAOYSA-N 20:1omega9c fatty acid Natural products CCCCCCCCCCC=CCCCCCCCC(O)=O LQJBNNIYVWPHFW-UHFFFAOYSA-N 0.000 claims 3
- QSBYPNXLFMSGKH-UHFFFAOYSA-N 9-Heptadecensaeure Natural products CCCCCCCC=CCCCCCCCC(O)=O QSBYPNXLFMSGKH-UHFFFAOYSA-N 0.000 claims 3
- ZQPPMHVWECSIRJ-UHFFFAOYSA-N Oleic acid Natural products CCCCCCCCC=CCCCCCCCC(O)=O ZQPPMHVWECSIRJ-UHFFFAOYSA-N 0.000 claims 3
- 239000005642 Oleic acid Substances 0.000 claims 3
- QXJSBBXBKPUZAA-UHFFFAOYSA-N isooleic acid Natural products CCCCCCCC=CCCCCCCCCC(O)=O QXJSBBXBKPUZAA-UHFFFAOYSA-N 0.000 claims 3
- ZQPPMHVWECSIRJ-KTKRTIGZSA-N oleic acid Chemical compound CCCCCCCC\C=C/CCCCCCCC(O)=O ZQPPMHVWECSIRJ-KTKRTIGZSA-N 0.000 claims 3
- MTCFGRXMJLQNBG-REOHCLBHSA-N (2S)-2-Amino-3-hydroxypropansäure Chemical compound OC[C@H](N)C(O)=O MTCFGRXMJLQNBG-REOHCLBHSA-N 0.000 claims 2
- FPRKGXIOSIUDSE-SYACGTDESA-N (2z,4z,6z,8z)-docosa-2,4,6,8-tetraenoic acid Chemical compound CCCCCCCCCCCCC\C=C/C=C\C=C/C=C\C(O)=O FPRKGXIOSIUDSE-SYACGTDESA-N 0.000 claims 2
- MVJLYXCJBPXRCY-UHFFFAOYSA-N 2-methylbutyl propanoate Chemical compound CCC(C)COC(=O)CC MVJLYXCJBPXRCY-UHFFFAOYSA-N 0.000 claims 2
- 239000001142 4-methyl-2-oxopentanoic acid Substances 0.000 claims 2
- 235000021292 Docosatetraenoic acid Nutrition 0.000 claims 2
- 239000004471 Glycine Substances 0.000 claims 2
- AGPKZVBTJJNPAG-WHFBIAKZSA-N L-isoleucine Chemical compound CC[C@H](C)[C@H](N)C(O)=O AGPKZVBTJJNPAG-WHFBIAKZSA-N 0.000 claims 2
- ROHFNLRQFUQHCH-YFKPBYRVSA-N L-leucine Chemical compound CC(C)C[C@H](N)C(O)=O ROHFNLRQFUQHCH-YFKPBYRVSA-N 0.000 claims 2
- ROHFNLRQFUQHCH-UHFFFAOYSA-N Leucine Natural products CC(C)CC(N)C(O)=O ROHFNLRQFUQHCH-UHFFFAOYSA-N 0.000 claims 2
- MTCFGRXMJLQNBG-UHFFFAOYSA-N Serine Natural products OCC(N)C(O)=O MTCFGRXMJLQNBG-UHFFFAOYSA-N 0.000 claims 2
- 229960003624 creatine Drugs 0.000 claims 2
- 239000006046 creatine Substances 0.000 claims 2
- AGPKZVBTJJNPAG-UHFFFAOYSA-N isoleucine Natural products CCC(C)C(N)C(O)=O AGPKZVBTJJNPAG-UHFFFAOYSA-N 0.000 claims 2
- 229960000310 isoleucine Drugs 0.000 claims 2
- 229940041290 mannose Drugs 0.000 claims 2
- 125000002811 oleoyl group Chemical group O=C([*])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])/C([H])=C([H])\C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 claims 2
- 229940075420 xanthine Drugs 0.000 claims 2
- 108010023302 HDL Cholesterol Proteins 0.000 claims 1
- KZSNJWFQEVHDMF-BYPYZUCNSA-N L-valine Chemical compound CC(C)[C@H](N)C(O)=O KZSNJWFQEVHDMF-BYPYZUCNSA-N 0.000 claims 1
- KZSNJWFQEVHDMF-UHFFFAOYSA-N Valine Natural products CC(C)C(N)C(O)=O KZSNJWFQEVHDMF-UHFFFAOYSA-N 0.000 claims 1
- 125000005645 linoleyl group Chemical group 0.000 claims 1
- 125000001117 oleyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])/C([H])=C([H])\C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 claims 1
- 239000004474 valine Substances 0.000 claims 1
- 201000010099 disease Diseases 0.000 description 182
- 239000002207 metabolite Substances 0.000 description 102
- 150000001875 compounds Chemical class 0.000 description 91
- 201000001320 Atherosclerosis Diseases 0.000 description 82
- 210000002381 plasma Anatomy 0.000 description 68
- 238000011282 treatment Methods 0.000 description 67
- 206010012601 diabetes mellitus Diseases 0.000 description 54
- 208000031229 Cardiomyopathies Diseases 0.000 description 48
- 238000004458 analytical method Methods 0.000 description 48
- 239000000203 mixture Substances 0.000 description 45
- 208000002705 Glucose Intolerance Diseases 0.000 description 36
- 238000007637 random forest analysis Methods 0.000 description 36
- 206010056370 Congestive cardiomyopathy Diseases 0.000 description 34
- 201000010046 Dilated cardiomyopathy Diseases 0.000 description 34
- 210000004369 blood Anatomy 0.000 description 33
- 239000008280 blood Substances 0.000 description 33
- 238000012360 testing method Methods 0.000 description 32
- 208000008589 Obesity Diseases 0.000 description 27
- 210000004027 cell Anatomy 0.000 description 25
- 235000020824 obesity Nutrition 0.000 description 25
- 238000003745 diagnosis Methods 0.000 description 24
- 238000012544 monitoring process Methods 0.000 description 22
- 230000004044 response Effects 0.000 description 22
- 238000004422 calculation algorithm Methods 0.000 description 21
- 208000035475 disorder Diseases 0.000 description 20
- 238000005259 measurement Methods 0.000 description 20
- HVYWMOMLDIMFJA-DPAQBDIFSA-N cholesterol Chemical compound C1C=C2C[C@@H](O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H]([C@H](C)CCCC(C)C)[C@@]1(C)CC2 HVYWMOMLDIMFJA-DPAQBDIFSA-N 0.000 description 18
- 239000003814 drug Substances 0.000 description 18
- 241000282414 Homo sapiens Species 0.000 description 17
- 230000002596 correlated effect Effects 0.000 description 16
- 235000018102 proteins Nutrition 0.000 description 15
- 108090000623 proteins and genes Proteins 0.000 description 15
- 102000004169 proteins and genes Human genes 0.000 description 15
- 208000011580 syndromic disease Diseases 0.000 description 15
- 241000699670 Mus sp. Species 0.000 description 14
- 238000007619 statistical method Methods 0.000 description 14
- 239000000126 substance Substances 0.000 description 14
- 230000007423 decrease Effects 0.000 description 13
- 239000003596 drug target Substances 0.000 description 13
- 210000002966 serum Anatomy 0.000 description 13
- 238000011161 development Methods 0.000 description 12
- 230000000694 effects Effects 0.000 description 12
- 150000003384 small molecules Chemical class 0.000 description 12
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 11
- 230000008238 biochemical pathway Effects 0.000 description 11
- 230000003247 decreasing effect Effects 0.000 description 11
- 239000000543 intermediate Substances 0.000 description 11
- 238000007410 oral glucose tolerance test Methods 0.000 description 11
- 229940079593 drug Drugs 0.000 description 10
- 230000001771 impaired effect Effects 0.000 description 10
- WGNAKZGUSRVWRH-UHFFFAOYSA-N p-cresol sulfate Chemical compound CC1=CC=C(OS(O)(=O)=O)C=C1 WGNAKZGUSRVWRH-UHFFFAOYSA-N 0.000 description 10
- 238000000692 Student's t-test Methods 0.000 description 9
- 230000008859 change Effects 0.000 description 9
- 239000003550 marker Substances 0.000 description 9
- 208000030159 metabolic disease Diseases 0.000 description 9
- 230000002503 metabolic effect Effects 0.000 description 9
- 230000037361 pathway Effects 0.000 description 9
- 230000002829 reductive effect Effects 0.000 description 9
- 238000012216 screening Methods 0.000 description 9
- 238000000638 solvent extraction Methods 0.000 description 9
- 238000012353 t test Methods 0.000 description 9
- 230000005856 abnormality Effects 0.000 description 8
- 210000000577 adipose tissue Anatomy 0.000 description 8
- 238000003556 assay Methods 0.000 description 8
- 238000005192 partition Methods 0.000 description 8
- 230000036470 plasma concentration Effects 0.000 description 8
- 238000000611 regression analysis Methods 0.000 description 8
- 208000024891 symptom Diseases 0.000 description 8
- 210000001519 tissue Anatomy 0.000 description 8
- RGHNJXZEOKUKBD-SQOUGZDYSA-N Gluconic acid Natural products OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C(O)=O RGHNJXZEOKUKBD-SQOUGZDYSA-N 0.000 description 7
- 150000002500 ions Chemical class 0.000 description 7
- 210000004185 liver Anatomy 0.000 description 7
- 230000001019 normoglycemic effect Effects 0.000 description 7
- 241000894007 species Species 0.000 description 7
- 238000012549 training Methods 0.000 description 7
- 206010060378 Hyperinsulinaemia Diseases 0.000 description 6
- 230000002159 abnormal effect Effects 0.000 description 6
- 210000000709 aorta Anatomy 0.000 description 6
- 230000003143 atherosclerotic effect Effects 0.000 description 6
- 235000012000 cholesterol Nutrition 0.000 description 6
- 230000000875 corresponding effect Effects 0.000 description 6
- 210000002216 heart Anatomy 0.000 description 6
- 210000005003 heart tissue Anatomy 0.000 description 6
- 230000003451 hyperinsulinaemic effect Effects 0.000 description 6
- 201000008980 hyperinsulinism Diseases 0.000 description 6
- 238000001802 infusion Methods 0.000 description 6
- 238000002705 metabolomic analysis Methods 0.000 description 6
- NILQLFBWTXNUOE-UHFFFAOYSA-N 1-aminocyclopentanecarboxylic acid Chemical compound OC(=O)C1(N)CCCC1 NILQLFBWTXNUOE-UHFFFAOYSA-N 0.000 description 5
- 206010020772 Hypertension Diseases 0.000 description 5
- 230000009471 action Effects 0.000 description 5
- 238000009534 blood test Methods 0.000 description 5
- 238000002290 gas chromatography-mass spectrometry Methods 0.000 description 5
- 238000004895 liquid chromatography mass spectrometry Methods 0.000 description 5
- XZWYZXLIPXDOLR-UHFFFAOYSA-N metformin Chemical compound CN(C)C(=N)NC(N)=N XZWYZXLIPXDOLR-UHFFFAOYSA-N 0.000 description 5
- 229960003105 metformin Drugs 0.000 description 5
- 230000003285 pharmacodynamic effect Effects 0.000 description 5
- 230000000291 postprandial effect Effects 0.000 description 5
- 230000002265 prevention Effects 0.000 description 5
- 238000011160 research Methods 0.000 description 5
- 230000035945 sensitivity Effects 0.000 description 5
- 238000011830 transgenic mouse model Methods 0.000 description 5
- RGHNJXZEOKUKBD-UHFFFAOYSA-N D-gluconic acid Natural products OCC(O)C(O)C(O)C(O)C(O)=O RGHNJXZEOKUKBD-UHFFFAOYSA-N 0.000 description 4
- 206010061818 Disease progression Diseases 0.000 description 4
- IAJILQKETJEXLJ-UHFFFAOYSA-N Galacturonsaeure Natural products O=CC(O)C(O)C(O)C(O)C(O)=O IAJILQKETJEXLJ-UHFFFAOYSA-N 0.000 description 4
- 241000699666 Mus <mouse, genus> Species 0.000 description 4
- OKJIRPAQVSHGFK-UHFFFAOYSA-N N-acetylglycine Chemical compound CC(=O)NCC(O)=O OKJIRPAQVSHGFK-UHFFFAOYSA-N 0.000 description 4
- 150000001720 carbohydrates Chemical class 0.000 description 4
- 238000012512 characterization method Methods 0.000 description 4
- 238000003066 decision tree Methods 0.000 description 4
- 230000001419 dependent effect Effects 0.000 description 4
- 230000005750 disease progression Effects 0.000 description 4
- 230000006870 function Effects 0.000 description 4
- 239000000174 gluconic acid Substances 0.000 description 4
- 229950006191 gluconic acid Drugs 0.000 description 4
- 235000012208 gluconic acid Nutrition 0.000 description 4
- 230000004190 glucose uptake Effects 0.000 description 4
- CDAISMWEOUEBRE-GPIVLXJGSA-N inositol Chemical compound O[C@H]1[C@H](O)[C@@H](O)[C@H](O)[C@H](O)[C@@H]1O CDAISMWEOUEBRE-GPIVLXJGSA-N 0.000 description 4
- 229960000367 inositol Drugs 0.000 description 4
- 230000003914 insulin secretion Effects 0.000 description 4
- 238000012417 linear regression Methods 0.000 description 4
- 239000011159 matrix material Substances 0.000 description 4
- -1 metabolite-6346 Substances 0.000 description 4
- 229960005190 phenylalanine Drugs 0.000 description 4
- CDAISMWEOUEBRE-UHFFFAOYSA-N scyllo-inosotol Natural products OC1C(O)C(O)C(O)C(O)C1O CDAISMWEOUEBRE-UHFFFAOYSA-N 0.000 description 4
- 229940124597 therapeutic agent Drugs 0.000 description 4
- 230000001225 therapeutic effect Effects 0.000 description 4
- 230000004584 weight gain Effects 0.000 description 4
- 235000019786 weight gain Nutrition 0.000 description 4
- MPCAJMNYNOGXPB-SLPGGIOYSA-N 1,5-anhydro-D-glucitol Chemical compound OC[C@H]1OC[C@H](O)[C@@H](O)[C@@H]1O MPCAJMNYNOGXPB-SLPGGIOYSA-N 0.000 description 3
- RGDVNLHBCKWZDA-XLPZGREQSA-N 2'-deoxy-5-methyl-5'-cytidylic acid Chemical compound O=C1N=C(N)C(C)=CN1[C@@H]1O[C@H](COP(O)(O)=O)[C@@H](O)C1 RGDVNLHBCKWZDA-XLPZGREQSA-N 0.000 description 3
- BRMWTNUJHUMWMS-UHFFFAOYSA-N 3-Methylhistidine Natural products CN1C=NC(CC(N)C(O)=O)=C1 BRMWTNUJHUMWMS-UHFFFAOYSA-N 0.000 description 3
- WQZGKKKJIJFFOK-IVMDWMLBSA-N D-allopyranose Chemical compound OC[C@H]1OC(O)[C@H](O)[C@H](O)[C@@H]1O WQZGKKKJIJFFOK-IVMDWMLBSA-N 0.000 description 3
- WQZGKKKJIJFFOK-RSVSWTKNSA-N D-altro-hexose Chemical compound OC[C@H]1OC(O)[C@@H](O)[C@H](O)[C@@H]1O WQZGKKKJIJFFOK-RSVSWTKNSA-N 0.000 description 3
- 238000002965 ELISA Methods 0.000 description 3
- 108090000790 Enzymes Proteins 0.000 description 3
- 102000004190 Enzymes Human genes 0.000 description 3
- 229930091371 Fructose Natural products 0.000 description 3
- RFSUNEUAIZKAJO-ARQDHWQXSA-N Fructose Chemical compound OC[C@H]1O[C@](O)(CO)[C@@H](O)[C@@H]1O RFSUNEUAIZKAJO-ARQDHWQXSA-N 0.000 description 3
- 239000005715 Fructose Substances 0.000 description 3
- SQUHHTBVTRBESD-UHFFFAOYSA-N Hexa-Ac-myo-Inositol Natural products CC(=O)OC1C(OC(C)=O)C(OC(C)=O)C(OC(C)=O)C(OC(C)=O)C1OC(C)=O SQUHHTBVTRBESD-UHFFFAOYSA-N 0.000 description 3
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 3
- 241000699660 Mus musculus Species 0.000 description 3
- JDHILDINMRGULE-LURJTMIESA-N N(pros)-methyl-L-histidine Chemical compound CN1C=NC=C1C[C@H](N)C(O)=O JDHILDINMRGULE-LURJTMIESA-N 0.000 description 3
- 206010033307 Overweight Diseases 0.000 description 3
- LEHOTFFKMJEONL-UHFFFAOYSA-N Uric Acid Chemical compound N1C(=O)NC(=O)C2=C1NC(=O)N2 LEHOTFFKMJEONL-UHFFFAOYSA-N 0.000 description 3
- 238000001790 Welch's t-test Methods 0.000 description 3
- 238000009825 accumulation Methods 0.000 description 3
- WQZGKKKJIJFFOK-PHYPRBDBSA-N alpha-D-galactose Chemical compound OC[C@H]1O[C@H](O)[C@H](O)[C@@H](O)[C@H]1O WQZGKKKJIJFFOK-PHYPRBDBSA-N 0.000 description 3
- LKDRXBCSQODPBY-BGPJRJDNSA-N alpha-L-sorbopyranose Chemical compound OC[C@@]1(O)OC[C@H](O)[C@@H](O)[C@@H]1O LKDRXBCSQODPBY-BGPJRJDNSA-N 0.000 description 3
- 239000003472 antidiabetic agent Substances 0.000 description 3
- 229960000074 biopharmaceutical Drugs 0.000 description 3
- 238000010224 classification analysis Methods 0.000 description 3
- 208000029078 coronary artery disease Diseases 0.000 description 3
- 238000001514 detection method Methods 0.000 description 3
- 238000002405 diagnostic procedure Methods 0.000 description 3
- 238000002474 experimental method Methods 0.000 description 3
- 229930182830 galactose Natural products 0.000 description 3
- 230000002641 glycemic effect Effects 0.000 description 3
- 210000005228 liver tissue Anatomy 0.000 description 3
- 229920002521 macromolecule Polymers 0.000 description 3
- HEBKCHPVOIAQTA-UHFFFAOYSA-N meso ribitol Natural products OCC(O)C(O)C(O)CO HEBKCHPVOIAQTA-UHFFFAOYSA-N 0.000 description 3
- 230000001431 metabolomic effect Effects 0.000 description 3
- 238000010172 mouse model Methods 0.000 description 3
- 210000000056 organ Anatomy 0.000 description 3
- 210000000496 pancreas Anatomy 0.000 description 3
- HXEACLLIILLPRG-UHFFFAOYSA-N pipecolic acid Chemical compound OC(=O)C1CCCCN1 HXEACLLIILLPRG-UHFFFAOYSA-N 0.000 description 3
- UFTFJSFQGQCHQW-UHFFFAOYSA-N triformin Chemical compound O=COCC(OC=O)COC=O UFTFJSFQGQCHQW-UHFFFAOYSA-N 0.000 description 3
- BJEPYKJPYRNKOW-REOHCLBHSA-N (S)-malic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O BJEPYKJPYRNKOW-REOHCLBHSA-N 0.000 description 2
- QHZLMUACJMDIAE-UHFFFAOYSA-N 1-monopalmitoylglycerol Chemical compound CCCCCCCCCCCCCCCC(=O)OCC(O)CO QHZLMUACJMDIAE-UHFFFAOYSA-N 0.000 description 2
- VBUYCZFBVCCYFD-NUNKFHFFSA-N 2-dehydro-L-idonic acid Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)C(=O)C(O)=O VBUYCZFBVCCYFD-NUNKFHFFSA-N 0.000 description 2
- IZSRJDGCGRAUAR-MROZADKFSA-N 5-dehydro-D-gluconic acid Chemical compound OCC(=O)[C@@H](O)[C@H](O)[C@@H](O)C(O)=O IZSRJDGCGRAUAR-MROZADKFSA-N 0.000 description 2
- VBUYCZFBVCCYFD-UHFFFAOYSA-N D-arabino-2-Hexulosonic acid Natural products OCC(O)C(O)C(O)C(=O)C(O)=O VBUYCZFBVCCYFD-UHFFFAOYSA-N 0.000 description 2
- RGHNJXZEOKUKBD-MGCNEYSASA-N D-galactonic acid Chemical compound OC[C@@H](O)[C@H](O)[C@H](O)[C@@H](O)C(O)=O RGHNJXZEOKUKBD-MGCNEYSASA-N 0.000 description 2
- SHZGCJCMOBCMKK-UHFFFAOYSA-N D-mannomethylose Natural products CC1OC(O)C(O)C(O)C1O SHZGCJCMOBCMKK-UHFFFAOYSA-N 0.000 description 2
- 208000032928 Dyslipidaemia Diseases 0.000 description 2
- 108010049003 Fibrinogen Proteins 0.000 description 2
- 102000008946 Fibrinogen Human genes 0.000 description 2
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 description 2
- 208000031773 Insulin resistance syndrome Diseases 0.000 description 2
- 229940122355 Insulin sensitizer Drugs 0.000 description 2
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 2
- WQZGKKKJIJFFOK-QRXFDPRISA-N L-gulose Chemical compound OC[C@@H]1OC(O)[C@@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-QRXFDPRISA-N 0.000 description 2
- PNNNRSAQSRJVSB-UHFFFAOYSA-N L-rhamnose Natural products CC(O)C(O)C(O)C(O)C=O PNNNRSAQSRJVSB-UHFFFAOYSA-N 0.000 description 2
- 108010007622 LDL Lipoproteins Proteins 0.000 description 2
- 102000007330 LDL Lipoproteins Human genes 0.000 description 2
- 208000017170 Lipid metabolism disease Diseases 0.000 description 2
- 238000000585 Mann–Whitney U test Methods 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- 102000000536 PPAR gamma Human genes 0.000 description 2
- 108010016731 PPAR gamma Proteins 0.000 description 2
- YASAKCUCGLMORW-UHFFFAOYSA-N Rosiglitazone Chemical group C=1C=CC=NC=1N(C)CCOC(C=C1)=CC=C1CC1SC(=O)NC1=O YASAKCUCGLMORW-UHFFFAOYSA-N 0.000 description 2
- TVWHNULVHGKJHS-UHFFFAOYSA-N Uric acid Natural products N1C(=O)NC(=O)C2NC(=O)NC21 TVWHNULVHGKJHS-UHFFFAOYSA-N 0.000 description 2
- PYMYPHUHKUWMLA-LMVFSUKVSA-N aldehydo-D-ribose Chemical compound OC[C@@H](O)[C@@H](O)[C@@H](O)C=O PYMYPHUHKUWMLA-LMVFSUKVSA-N 0.000 description 2
- MBMBGCFOFBJSGT-KUBAVDMBSA-N all-cis-docosa-4,7,10,13,16,19-hexaenoic acid Chemical compound CC\C=C/C\C=C/C\C=C/C\C=C/C\C=C/C\C=C/CCC(O)=O MBMBGCFOFBJSGT-KUBAVDMBSA-N 0.000 description 2
- AEMOLEFTQBMNLQ-WAXACMCWSA-N alpha-D-glucuronic acid Chemical compound O[C@H]1O[C@H](C(O)=O)[C@@H](O)[C@H](O)[C@H]1O AEMOLEFTQBMNLQ-WAXACMCWSA-N 0.000 description 2
- BJEPYKJPYRNKOW-UHFFFAOYSA-N alpha-hydroxysuccinic acid Natural products OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 2
- 229940024606 amino acid Drugs 0.000 description 2
- 235000001014 amino acid Nutrition 0.000 description 2
- 150000001413 amino acids Chemical class 0.000 description 2
- 230000003178 anti-diabetic effect Effects 0.000 description 2
- 238000013459 approach Methods 0.000 description 2
- 210000000227 basophil cell of anterior lobe of hypophysis Anatomy 0.000 description 2
- SRBFZHDQGSBBOR-UHFFFAOYSA-N beta-D-Pyranose-Lyxose Natural products OC1COC(O)C(O)C1O SRBFZHDQGSBBOR-UHFFFAOYSA-N 0.000 description 2
- 239000012620 biological material Substances 0.000 description 2
- 230000001413 cellular effect Effects 0.000 description 2
- 238000004587 chromatography analysis Methods 0.000 description 2
- 238000002591 computed tomography Methods 0.000 description 2
- 238000010219 correlation analysis Methods 0.000 description 2
- 238000002790 cross-validation Methods 0.000 description 2
- 230000006378 damage Effects 0.000 description 2
- 239000000104 diagnostic biomarker Substances 0.000 description 2
- 235000020805 dietary restrictions Nutrition 0.000 description 2
- 230000004069 differentiation Effects 0.000 description 2
- 238000002592 echocardiography Methods 0.000 description 2
- 229940012952 fibrinogen Drugs 0.000 description 2
- 238000004817 gas chromatography Methods 0.000 description 2
- 235000013922 glutamic acid Nutrition 0.000 description 2
- 239000004220 glutamic acid Substances 0.000 description 2
- 150000004676 glycans Chemical class 0.000 description 2
- 230000036541 health Effects 0.000 description 2
- 208000019622 heart disease Diseases 0.000 description 2
- 238000004128 high performance liquid chromatography Methods 0.000 description 2
- JYGXADMDTFJGBT-VWUMJDOOSA-N hydrocortisone Chemical compound O=C1CC[C@]2(C)[C@H]3[C@@H](O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 JYGXADMDTFJGBT-VWUMJDOOSA-N 0.000 description 2
- ROBFUDYVXSDBQM-UHFFFAOYSA-N hydroxymalonic acid Chemical compound OC(=O)C(O)C(O)=O ROBFUDYVXSDBQM-UHFFFAOYSA-N 0.000 description 2
- 201000001421 hyperglycemia Diseases 0.000 description 2
- 238000000338 in vitro Methods 0.000 description 2
- 238000001727 in vivo Methods 0.000 description 2
- 150000002632 lipids Chemical class 0.000 description 2
- 238000004811 liquid chromatography Methods 0.000 description 2
- 230000007774 longterm Effects 0.000 description 2
- 230000014759 maintenance of location Effects 0.000 description 2
- 235000011090 malic acid Nutrition 0.000 description 2
- 239000001630 malic acid Substances 0.000 description 2
- 229940099690 malic acid Drugs 0.000 description 2
- 238000004949 mass spectrometry Methods 0.000 description 2
- 230000004060 metabolic process Effects 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 210000003205 muscle Anatomy 0.000 description 2
- 208000010125 myocardial infarction Diseases 0.000 description 2
- 235000016709 nutrition Nutrition 0.000 description 2
- 230000035764 nutrition Effects 0.000 description 2
- GLDOVTGHNKAZLK-UHFFFAOYSA-N octadecan-1-ol Chemical compound CCCCCCCCCCCCCCCCCCO GLDOVTGHNKAZLK-UHFFFAOYSA-N 0.000 description 2
- 230000000737 periodic effect Effects 0.000 description 2
- HYAFETHFCAUJAY-UHFFFAOYSA-N pioglitazone Chemical compound N1=CC(CC)=CC=C1CCOC(C=C1)=CC=C1CC1C(=O)NC(=O)S1 HYAFETHFCAUJAY-UHFFFAOYSA-N 0.000 description 2
- 229920001282 polysaccharide Polymers 0.000 description 2
- 239000005017 polysaccharide Substances 0.000 description 2
- 238000002203 pretreatment Methods 0.000 description 2
- 238000003908 quality control method Methods 0.000 description 2
- 238000005070 sampling Methods 0.000 description 2
- 238000013517 stratification Methods 0.000 description 2
- 150000008163 sugars Chemical class 0.000 description 2
- 238000004885 tandem mass spectrometry Methods 0.000 description 2
- 230000009466 transformation Effects 0.000 description 2
- 230000009261 transgenic effect Effects 0.000 description 2
- 150000003626 triacylglycerols Chemical class 0.000 description 2
- 229960004441 tyrosine Drugs 0.000 description 2
- 229940116269 uric acid Drugs 0.000 description 2
- REWYJJRDEOKNBQ-UHFFFAOYSA-N valine betaine Chemical compound CC(C)C(C([O-])=O)[N+](C)(C)C REWYJJRDEOKNBQ-UHFFFAOYSA-N 0.000 description 2
- 208000019553 vascular disease Diseases 0.000 description 2
- 230000002861 ventricular Effects 0.000 description 2
- 238000012795 verification Methods 0.000 description 2
- 230000004580 weight loss Effects 0.000 description 2
- 208000016261 weight loss Diseases 0.000 description 2
- GVJHHUAWPYXKBD-IEOSBIPESA-N α-tocopherol Chemical compound OC1=C(C)C(C)=C2O[C@@](CCC[C@H](C)CCC[C@H](C)CCCC(C)C)(C)CCC2=C1C GVJHHUAWPYXKBD-IEOSBIPESA-N 0.000 description 2
- XUFXOAAUWZOOIT-SXARVLRPSA-N (2R,3R,4R,5S,6R)-5-[[(2R,3R,4R,5S,6R)-5-[[(2R,3R,4S,5S,6R)-3,4-dihydroxy-6-methyl-5-[[(1S,4R,5S,6S)-4,5,6-trihydroxy-3-(hydroxymethyl)-1-cyclohex-2-enyl]amino]-2-oxanyl]oxy]-3,4-dihydroxy-6-(hydroxymethyl)-2-oxanyl]oxy]-6-(hydroxymethyl)oxane-2,3,4-triol Chemical compound O([C@H]1O[C@H](CO)[C@H]([C@@H]([C@H]1O)O)O[C@H]1O[C@@H]([C@H]([C@H](O)[C@H]1O)N[C@@H]1[C@@H]([C@@H](O)[C@H](O)C(CO)=C1)O)C)[C@@H]1[C@@H](CO)O[C@@H](O)[C@H](O)[C@H]1O XUFXOAAUWZOOIT-SXARVLRPSA-N 0.000 description 1
- FUFLCEKSBBHCMO-UHFFFAOYSA-N 11-dehydrocorticosterone Natural products O=C1CCC2(C)C3C(=O)CC(C)(C(CC4)C(=O)CO)C4C3CCC2=C1 FUFLCEKSBBHCMO-UHFFFAOYSA-N 0.000 description 1
- GCKMFJBGXUYNAG-UHFFFAOYSA-N 17alpha-methyltestosterone Natural products C1CC2=CC(=O)CCC2(C)C2C1C1CCC(C)(O)C1(C)CC2 GCKMFJBGXUYNAG-UHFFFAOYSA-N 0.000 description 1
- UXFQFBNBSPQBJW-UHFFFAOYSA-N 2-amino-2-methylpropane-1,3-diol Chemical compound OCC(N)(C)CO UXFQFBNBSPQBJW-UHFFFAOYSA-N 0.000 description 1
- SJZRECIVHVDYJC-UHFFFAOYSA-N 4-hydroxybutyric acid Chemical compound OCCCC(O)=O SJZRECIVHVDYJC-UHFFFAOYSA-N 0.000 description 1
- YPMOAQISONSSNL-UHFFFAOYSA-N 8-hydroxyoctyl 2-methylprop-2-enoate Chemical compound CC(=C)C(=O)OCCCCCCCCO YPMOAQISONSSNL-UHFFFAOYSA-N 0.000 description 1
- 208000004611 Abdominal Obesity Diseases 0.000 description 1
- PQSUYGKTWSAVDQ-ZVIOFETBSA-N Aldosterone Chemical compound C([C@@]1([C@@H](C(=O)CO)CC[C@H]1[C@@H]1CC2)C=O)[C@H](O)[C@@H]1[C@]1(C)C2=CC(=O)CC1 PQSUYGKTWSAVDQ-ZVIOFETBSA-N 0.000 description 1
- PQSUYGKTWSAVDQ-UHFFFAOYSA-N Aldosterone Natural products C1CC2C3CCC(C(=O)CO)C3(C=O)CC(O)C2C2(C)C1=CC(=O)CC2 PQSUYGKTWSAVDQ-UHFFFAOYSA-N 0.000 description 1
- 206010002383 Angina Pectoris Diseases 0.000 description 1
- 102100040214 Apolipoprotein(a) Human genes 0.000 description 1
- 200000000007 Arterial disease Diseases 0.000 description 1
- 241000283690 Bos taurus Species 0.000 description 1
- 108010074051 C-Reactive Protein Proteins 0.000 description 1
- 102100032752 C-reactive protein Human genes 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- 208000014882 Carotid artery disease Diseases 0.000 description 1
- 206010065941 Central obesity Diseases 0.000 description 1
- 241000282693 Cercopithecidae Species 0.000 description 1
- 208000017667 Chronic Disease Diseases 0.000 description 1
- MFYSYFVPBJMHGN-ZPOLXVRWSA-N Cortisone Chemical compound O=C1CC[C@]2(C)[C@H]3C(=O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 MFYSYFVPBJMHGN-ZPOLXVRWSA-N 0.000 description 1
- MFYSYFVPBJMHGN-UHFFFAOYSA-N Cortisone Natural products O=C1CCC2(C)C3C(=O)CC(C)(C(CC4)(O)C(=O)CO)C4C3CCC2=C1 MFYSYFVPBJMHGN-UHFFFAOYSA-N 0.000 description 1
- CKLJMWTZIZZHCS-UHFFFAOYSA-N D-OH-Asp Natural products OC(=O)C(N)CC(O)=O CKLJMWTZIZZHCS-UHFFFAOYSA-N 0.000 description 1
- ODBLHEXUDAPZAU-ZAFYKAAXSA-N D-threo-isocitric acid Chemical compound OC(=O)[C@H](O)[C@@H](C(O)=O)CC(O)=O ODBLHEXUDAPZAU-ZAFYKAAXSA-N 0.000 description 1
- ZAQJHHRNXZUBTE-WUJLRWPWSA-N D-xylulose Chemical compound OC[C@@H](O)[C@H](O)C(=O)CO ZAQJHHRNXZUBTE-WUJLRWPWSA-N 0.000 description 1
- 206010051055 Deep vein thrombosis Diseases 0.000 description 1
- MQIUGAXCHLFZKX-UHFFFAOYSA-N Di-n-octyl phthalate Natural products CCCCCCCCOC(=O)C1=CC=CC=C1C(=O)OCCCCCCCC MQIUGAXCHLFZKX-UHFFFAOYSA-N 0.000 description 1
- 208000016546 Distal 16p11.2 microdeletion syndrome Diseases 0.000 description 1
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 1
- 241000283086 Equidae Species 0.000 description 1
- UNXHWFMMPAWVPI-UHFFFAOYSA-N Erythritol Natural products OCC(O)C(O)CO UNXHWFMMPAWVPI-UHFFFAOYSA-N 0.000 description 1
- 239000004386 Erythritol Substances 0.000 description 1
- 241000282326 Felis catus Species 0.000 description 1
- 206010019280 Heart failures Diseases 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 206010022491 Insulin resistant diabetes Diseases 0.000 description 1
- ODBLHEXUDAPZAU-FONMRSAGSA-N Isocitric acid Natural products OC(=O)[C@@H](O)[C@H](C(O)=O)CC(O)=O ODBLHEXUDAPZAU-FONMRSAGSA-N 0.000 description 1
- CKLJMWTZIZZHCS-UWTATZPHSA-N L-Aspartic acid Natural products OC(=O)[C@H](N)CC(O)=O CKLJMWTZIZZHCS-UWTATZPHSA-N 0.000 description 1
- SHZGCJCMOBCMKK-PQMKYFCFSA-N L-Fucose Natural products C[C@H]1O[C@H](O)[C@@H](O)[C@@H](O)[C@@H]1O SHZGCJCMOBCMKK-PQMKYFCFSA-N 0.000 description 1
- MYFMARDICOWMQP-UHFFFAOYSA-N L-L-gamma-Glutamylleucine Natural products CC(C)CC(C(O)=O)NC(=O)CCC(N)C(O)=O MYFMARDICOWMQP-UHFFFAOYSA-N 0.000 description 1
- HEBKCHPVOIAQTA-IMJSIDKUSA-N L-arabinitol Chemical compound OC[C@H](O)C(O)[C@@H](O)CO HEBKCHPVOIAQTA-IMJSIDKUSA-N 0.000 description 1
- SHZGCJCMOBCMKK-DHVFOXMCSA-N L-fucopyranose Chemical compound C[C@@H]1OC(O)[C@@H](O)[C@H](O)[C@@H]1O SHZGCJCMOBCMKK-DHVFOXMCSA-N 0.000 description 1
- FFFHZYDWPBMWHY-VKHMYHEASA-N L-homocysteine Chemical compound OC(=O)[C@@H](N)CCS FFFHZYDWPBMWHY-VKHMYHEASA-N 0.000 description 1
- 108010033266 Lipoprotein(a) Proteins 0.000 description 1
- 239000004472 Lysine Substances 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- GCKMFJBGXUYNAG-HLXURNFRSA-N Methyltestosterone Chemical compound C1CC2=CC(=O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@](C)(O)[C@@]1(C)CC2 GCKMFJBGXUYNAG-HLXURNFRSA-N 0.000 description 1
- 208000003430 Mitral Valve Prolapse Diseases 0.000 description 1
- 206010027727 Mitral valve incompetence Diseases 0.000 description 1
- FSVCELGFZIQNCK-UHFFFAOYSA-N N,N-bis(2-hydroxyethyl)glycine Chemical compound OCCN(CCO)CC(O)=O FSVCELGFZIQNCK-UHFFFAOYSA-N 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 208000018262 Peripheral vascular disease Diseases 0.000 description 1
- 108010022233 Plasminogen Activator Inhibitor 1 Proteins 0.000 description 1
- 102100039418 Plasminogen activator inhibitor 1 Human genes 0.000 description 1
- 208000006396 Pulmonary artery stenosis Diseases 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- 206010038748 Restrictive cardiomyopathy Diseases 0.000 description 1
- 208000034189 Sclerosis Diseases 0.000 description 1
- 235000021355 Stearic acid Nutrition 0.000 description 1
- 241000282887 Suidae Species 0.000 description 1
- 208000037063 Thinness Diseases 0.000 description 1
- FNYLWPVRPXGIIP-UHFFFAOYSA-N Triamterene Chemical compound NC1=NC2=NC(N)=NC(N)=C2N=C1C1=CC=CC=C1 FNYLWPVRPXGIIP-UHFFFAOYSA-N 0.000 description 1
- 206010047249 Venous thrombosis Diseases 0.000 description 1
- TVXBFESIOXBWNM-UHFFFAOYSA-N Xylitol Natural products OCCC(O)C(O)C(O)CCO TVXBFESIOXBWNM-UHFFFAOYSA-N 0.000 description 1
- 210000001015 abdomen Anatomy 0.000 description 1
- 210000000579 abdominal fat Anatomy 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 229960002632 acarbose Drugs 0.000 description 1
- XUFXOAAUWZOOIT-UHFFFAOYSA-N acarviostatin I01 Natural products OC1C(O)C(NC2C(C(O)C(O)C(CO)=C2)O)C(C)OC1OC(C(C1O)O)C(CO)OC1OC1C(CO)OC(O)C(O)C1O XUFXOAAUWZOOIT-UHFFFAOYSA-N 0.000 description 1
- 210000001789 adipocyte Anatomy 0.000 description 1
- 230000001800 adrenalinergic effect Effects 0.000 description 1
- IAJILQKETJEXLJ-RSJOWCBRSA-N aldehydo-D-galacturonic acid Chemical compound O=C[C@H](O)[C@@H](O)[C@@H](O)[C@H](O)C(O)=O IAJILQKETJEXLJ-RSJOWCBRSA-N 0.000 description 1
- PYMYPHUHKUWMLA-UOWFLXDJSA-N aldehydo-D-lyxose Chemical compound OC[C@@H](O)[C@H](O)[C@H](O)C=O PYMYPHUHKUWMLA-UOWFLXDJSA-N 0.000 description 1
- PNNNRSAQSRJVSB-BXKVDMCESA-N aldehydo-L-rhamnose Chemical compound C[C@H](O)[C@H](O)[C@@H](O)[C@@H](O)C=O PNNNRSAQSRJVSB-BXKVDMCESA-N 0.000 description 1
- PYMYPHUHKUWMLA-WISUUJSJSA-N aldehydo-L-xylose Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)C=O PYMYPHUHKUWMLA-WISUUJSJSA-N 0.000 description 1
- 229930195726 aldehydo-L-xylose Natural products 0.000 description 1
- 229960002478 aldosterone Drugs 0.000 description 1
- 229940087168 alpha tocopherol Drugs 0.000 description 1
- 230000001195 anabolic effect Effects 0.000 description 1
- 239000003098 androgen Substances 0.000 description 1
- 238000002583 angiography Methods 0.000 description 1
- 238000010171 animal model Methods 0.000 description 1
- 210000003423 ankle Anatomy 0.000 description 1
- 229940127003 anti-diabetic drug Drugs 0.000 description 1
- 210000002376 aorta thoracic Anatomy 0.000 description 1
- PYMYPHUHKUWMLA-WDCZJNDASA-N arabinose Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)C=O PYMYPHUHKUWMLA-WDCZJNDASA-N 0.000 description 1
- PYMYPHUHKUWMLA-UHFFFAOYSA-N arabinose Natural products OCC(O)C(O)C(O)C=O PYMYPHUHKUWMLA-UHFFFAOYSA-N 0.000 description 1
- 206010003119 arrhythmia Diseases 0.000 description 1
- 230000006793 arrhythmia Effects 0.000 description 1
- 230000003126 arrythmogenic effect Effects 0.000 description 1
- 210000001367 artery Anatomy 0.000 description 1
- 230000001174 ascending effect Effects 0.000 description 1
- 229960005261 aspartic acid Drugs 0.000 description 1
- 238000011948 assay development Methods 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- AEMOLEFTQBMNLQ-UHFFFAOYSA-N beta-D-galactopyranuronic acid Natural products OC1OC(C(O)=O)C(O)C(O)C1O AEMOLEFTQBMNLQ-UHFFFAOYSA-N 0.000 description 1
- 239000007998 bicine buffer Substances 0.000 description 1
- 238000010256 biochemical assay Methods 0.000 description 1
- 230000001851 biosynthetic effect Effects 0.000 description 1
- 230000006696 biosynthetic metabolic pathway Effects 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- BJQHLKABXJIVAM-UHFFFAOYSA-N bis(2-ethylhexyl) phthalate Chemical compound CCCCC(CC)COC(=O)C1=CC=CC=C1C(=O)OCC(CC)CCCC BJQHLKABXJIVAM-UHFFFAOYSA-N 0.000 description 1
- 230000036772 blood pressure Effects 0.000 description 1
- 238000010241 blood sampling Methods 0.000 description 1
- 210000004204 blood vessel Anatomy 0.000 description 1
- 238000004364 calculation method Methods 0.000 description 1
- 230000001925 catabolic effect Effects 0.000 description 1
- 230000015556 catabolic process Effects 0.000 description 1
- 238000004113 cell culture Methods 0.000 description 1
- 230000019522 cellular metabolic process Effects 0.000 description 1
- 230000033077 cellular process Effects 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 238000003759 clinical diagnosis Methods 0.000 description 1
- 230000015271 coagulation Effects 0.000 description 1
- 238000005345 coagulation Methods 0.000 description 1
- 208000012696 congenital leptin deficiency Diseases 0.000 description 1
- 238000010276 construction Methods 0.000 description 1
- 229960004544 cortisone Drugs 0.000 description 1
- 238000009223 counseling Methods 0.000 description 1
- 230000009260 cross reactivity Effects 0.000 description 1
- 238000007821 culture assay Methods 0.000 description 1
- 210000000805 cytoplasm Anatomy 0.000 description 1
- GVJHHUAWPYXKBD-UHFFFAOYSA-N d-alpha-tocopherol Natural products OC1=C(C)C(C)=C2OC(CCCC(C)CCCC(C)CCCC(C)C)(C)CCC2=C1C GVJHHUAWPYXKBD-UHFFFAOYSA-N 0.000 description 1
- 230000007812 deficiency Effects 0.000 description 1
- 230000006735 deficit Effects 0.000 description 1
- CZWCKYRVOZZJNM-USOAJAOKSA-N dehydroepiandrosterone sulfate Chemical compound C1[C@@H](OS(O)(=O)=O)CC[C@]2(C)[C@H]3CC[C@](C)(C(CC4)=O)[C@@H]4[C@@H]3CC=C21 CZWCKYRVOZZJNM-USOAJAOKSA-N 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 235000014113 dietary fatty acids Nutrition 0.000 description 1
- 235000001434 dietary modification Nutrition 0.000 description 1
- ZBCBWPMODOFKDW-UHFFFAOYSA-N diethanolamine Chemical compound OCCNCCO ZBCBWPMODOFKDW-UHFFFAOYSA-N 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 229940090949 docosahexaenoic acid Drugs 0.000 description 1
- 235000020669 docosahexaenoic acid Nutrition 0.000 description 1
- 238000002651 drug therapy Methods 0.000 description 1
- 230000008482 dysregulation Effects 0.000 description 1
- 230000002526 effect on cardiovascular system Effects 0.000 description 1
- 238000002565 electrocardiography Methods 0.000 description 1
- 238000007824 enzymatic assay Methods 0.000 description 1
- 238000006911 enzymatic reaction Methods 0.000 description 1
- UNXHWFMMPAWVPI-ZXZARUISSA-N erythritol Chemical compound OC[C@H](O)[C@H](O)CO UNXHWFMMPAWVPI-ZXZARUISSA-N 0.000 description 1
- 229940009714 erythritol Drugs 0.000 description 1
- 235000019414 erythritol Nutrition 0.000 description 1
- 230000001610 euglycemic effect Effects 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 229930195729 fatty acid Natural products 0.000 description 1
- 239000000194 fatty acid Substances 0.000 description 1
- 150000004665 fatty acids Chemical class 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- 235000013305 food Nutrition 0.000 description 1
- 230000037406 food intake Effects 0.000 description 1
- 150000004675 formic acid derivatives Chemical class 0.000 description 1
- MYFMARDICOWMQP-YUMQZZPRSA-N gamma-Glu-Leu Chemical compound CC(C)C[C@@H](C(O)=O)NC(=O)CC[C@H](N)C(O)=O MYFMARDICOWMQP-YUMQZZPRSA-N 0.000 description 1
- 108010064169 gamma-glutamyl-leucine Proteins 0.000 description 1
- 238000001415 gene therapy Methods 0.000 description 1
- 238000007429 general method Methods 0.000 description 1
- 230000009229 glucose formation Effects 0.000 description 1
- 230000004153 glucose metabolism Effects 0.000 description 1
- 238000007446 glucose tolerance test Methods 0.000 description 1
- 229960002989 glutamic acid Drugs 0.000 description 1
- 230000036252 glycation Effects 0.000 description 1
- 230000002394 glycogenic effect Effects 0.000 description 1
- 230000005802 health problem Effects 0.000 description 1
- 230000013632 homeostatic process Effects 0.000 description 1
- 229940088597 hormone Drugs 0.000 description 1
- 239000005556 hormone Substances 0.000 description 1
- 229960000890 hydrocortisone Drugs 0.000 description 1
- 206010020871 hypertrophic cardiomyopathy Diseases 0.000 description 1
- NBZBKCUXIYYUSX-UHFFFAOYSA-N iminodiacetic acid Chemical compound OC(=O)CNCC(O)=O NBZBKCUXIYYUSX-UHFFFAOYSA-N 0.000 description 1
- 238000003018 immunoassay Methods 0.000 description 1
- 230000000984 immunochemical effect Effects 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 238000005462 in vivo assay Methods 0.000 description 1
- 230000005764 inhibitory process Effects 0.000 description 1
- 230000000977 initiatory effect Effects 0.000 description 1
- 238000002608 intravascular ultrasound Methods 0.000 description 1
- 210000003734 kidney Anatomy 0.000 description 1
- 150000002605 large molecules Chemical class 0.000 description 1
- 230000003902 lesion Effects 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 210000004072 lung Anatomy 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 238000013178 mathematical model Methods 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 230000004066 metabolic change Effects 0.000 description 1
- 229960001566 methyltestosterone Drugs 0.000 description 1
- 210000003470 mitochondria Anatomy 0.000 description 1
- 208000001022 morbid obesity Diseases 0.000 description 1
- 210000000663 muscle cell Anatomy 0.000 description 1
- 230000035772 mutation Effects 0.000 description 1
- 210000004165 myocardium Anatomy 0.000 description 1
- 102000039446 nucleic acids Human genes 0.000 description 1
- 108020004707 nucleic acids Proteins 0.000 description 1
- 150000007523 nucleic acids Chemical class 0.000 description 1
- 239000002773 nucleotide Substances 0.000 description 1
- 125000003729 nucleotide group Chemical group 0.000 description 1
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 1
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 1
- 210000003463 organelle Anatomy 0.000 description 1
- 238000012261 overproduction Methods 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 230000004203 pancreatic function Effects 0.000 description 1
- 230000036961 partial effect Effects 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 230000008506 pathogenesis Effects 0.000 description 1
- 230000007170 pathology Effects 0.000 description 1
- 230000001991 pathophysiological effect Effects 0.000 description 1
- CWEFIMQKSZFZNY-UHFFFAOYSA-N pentyl 2-[4-[[4-[4-[[4-[[4-(pentoxycarbonylamino)phenyl]methyl]phenyl]carbamoyloxy]butoxycarbonylamino]phenyl]methyl]phenyl]acetate Chemical compound C1=CC(CC(=O)OCCCCC)=CC=C1CC(C=C1)=CC=C1NC(=O)OCCCCOC(=O)NC(C=C1)=CC=C1CC1=CC=C(NC(=O)OCCCCC)C=C1 CWEFIMQKSZFZNY-UHFFFAOYSA-N 0.000 description 1
- 230000002093 peripheral effect Effects 0.000 description 1
- 235000008729 phenylalanine Nutrition 0.000 description 1
- 230000035790 physiological processes and functions Effects 0.000 description 1
- 229960005095 pioglitazone Drugs 0.000 description 1
- 230000003449 preventive effect Effects 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 239000000092 prognostic biomarker Substances 0.000 description 1
- 230000000750 progressive effect Effects 0.000 description 1
- 230000000770 proinflammatory effect Effects 0.000 description 1
- 230000000069 prophylactic effect Effects 0.000 description 1
- 230000003331 prothrombotic effect Effects 0.000 description 1
- 238000011002 quantification Methods 0.000 description 1
- 230000000306 recurrent effect Effects 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- HEBKCHPVOIAQTA-ZXFHETKHSA-N ribitol Chemical compound OC[C@H](O)[C@H](O)[C@H](O)CO HEBKCHPVOIAQTA-ZXFHETKHSA-N 0.000 description 1
- 229960004586 rosiglitazone Drugs 0.000 description 1
- 238000007423 screening assay Methods 0.000 description 1
- 238000010187 selection method Methods 0.000 description 1
- 230000011664 signaling Effects 0.000 description 1
- 210000002027 skeletal muscle Anatomy 0.000 description 1
- 239000000243 solution Substances 0.000 description 1
- 238000011425 standardization method Methods 0.000 description 1
- 150000003431 steroids Chemical class 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- 229940065721 systemic for obstructive airway disease xanthines Drugs 0.000 description 1
- 229940124598 therapeutic candidate Drugs 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- CBDKQYKMCICBOF-UHFFFAOYSA-N thiazoline Chemical compound C1CN=CS1 CBDKQYKMCICBOF-UHFFFAOYSA-N 0.000 description 1
- ODBLHEXUDAPZAU-UHFFFAOYSA-N threo-D-isocitric acid Natural products OC(=O)C(O)C(C(O)=O)CC(O)=O ODBLHEXUDAPZAU-UHFFFAOYSA-N 0.000 description 1
- 238000004448 titration Methods 0.000 description 1
- 229960000984 tocofersolan Drugs 0.000 description 1
- 229930003799 tocopherol Natural products 0.000 description 1
- 235000010384 tocopherol Nutrition 0.000 description 1
- 239000011732 tocopherol Substances 0.000 description 1
- 229960001295 tocopherol Drugs 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- 238000000844 transformation Methods 0.000 description 1
- 238000012301 transgenic model Methods 0.000 description 1
- 230000032258 transport Effects 0.000 description 1
- 230000004102 tricarboxylic acid cycle Effects 0.000 description 1
- 229960001641 troglitazone Drugs 0.000 description 1
- GXPHKUHSUJUWKP-UHFFFAOYSA-N troglitazone Chemical group C1CC=2C(C)=C(O)C(C)=C(C)C=2OC1(C)COC(C=C1)=CC=C1CC1SC(=O)NC1=O GXPHKUHSUJUWKP-UHFFFAOYSA-N 0.000 description 1
- GXPHKUHSUJUWKP-NTKDMRAZSA-N troglitazone Natural products C([C@@]1(OC=2C(C)=C(C(=C(C)C=2CC1)O)C)C)OC(C=C1)=CC=C1C[C@H]1SC(=O)NC1=O GXPHKUHSUJUWKP-NTKDMRAZSA-N 0.000 description 1
- 235000002374 tyrosine Nutrition 0.000 description 1
- 206010048828 underweight Diseases 0.000 description 1
- 238000011144 upstream manufacturing Methods 0.000 description 1
- 210000002700 urine Anatomy 0.000 description 1
- 208000037997 venous disease Diseases 0.000 description 1
- 239000000811 xylitol Substances 0.000 description 1
- 235000010447 xylitol Nutrition 0.000 description 1
- HEBKCHPVOIAQTA-SCDXWVJYSA-N xylitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)CO HEBKCHPVOIAQTA-SCDXWVJYSA-N 0.000 description 1
- 229960002675 xylitol Drugs 0.000 description 1
- 235000004835 α-tocopherol Nutrition 0.000 description 1
- 239000002076 α-tocopherol Substances 0.000 description 1
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/5308—Immunoassay; Biospecific binding assay; Materials therefor for analytes not provided for elsewhere, e.g. nucleic acids, uric acid, worms, mites
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/04—Anorexiants; Antiobesity agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/483—Physical analysis of biological material
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/483—Physical analysis of biological material
- G01N33/487—Physical analysis of biological material of liquid biological material
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/5005—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells
- G01N33/5091—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing the pathological state of an organism
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
- G01N33/6893—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids related to diseases not provided for elsewhere
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/04—Endocrine or metabolic disorders
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/04—Endocrine or metabolic disorders
- G01N2800/042—Disorders of carbohydrate metabolism, e.g. diabetes, glucose metabolism
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/04—Endocrine or metabolic disorders
- G01N2800/044—Hyperlipemia or hypolipemia, e.g. dyslipidaemia, obesity
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/32—Cardiovascular disorders
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/50—Determining the risk of developing a disease
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/52—Predicting or monitoring the response to treatment, e.g. for selection of therapy based on assay results in personalised medicine; Prognosis
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/56—Staging of a disease; Further complications associated with the disease
Description
本出願は、その全文が参照として本明細書に組み込まれる2007年7月17日に出願された米国仮出願第60/950,286号及び2008年3月18日に出願された米国仮出願第61/037,628号の利益を主張する。
「バイオマーカー」とは、第2の表現型を有する(例えば、疾患を有さない)対象又は対象の群から得た生体試料と比較して、第1の表現型を有する(例えば、疾患を有する)対象又は対象の群から得た生体試料で異なった形で存在する(例えば、増加しているか、減少している)化合物、好ましくは、代謝産物を意味する。バイオマーカーは、任意のレベルで異なった形で存在し得るが、通常、少なくとも5%、少なくとも10%、少なくとも15%、少なくとも20%、少なくとも25%、少なくとも30%、少なくとも35%、少なくとも40%、少なくとも45%、少なくとも50%、少なくとも55%、少なくとも60%、少なくとも65%、少なくとも70%、少なくとも75%、少なくとも80%、少なくとも85%、少なくとも90%、少なくとも95%、少なくとも100%、少なくとも110%、少なくとも120%、少なくとも130%、少なくとも140%、少なくとも150%或いはそれ以上増加しているレベルで存在するか、又は、通常、少なくとも5%、少なくとも10%、少なくとも15%、少なくとも20%、少なくとも25%、少なくとも30%、少なくとも35%、少なくとも40%、少なくとも45%、少なくとも50%、少なくとも55%、少なくとも60%、少なくとも65%、少なくとも70%、少なくとも75%、少なくとも80%、少なくとも85%、少なくとも90%、少なくとも95%又は100%(即ち、存在しない)減少したレベルで存在する。バイオマーカーは、統計上有意であるレベルで(例えば、ウエルチt検定又はウィルコクソン順位和検定のいずれかを用いて決定される、0.05未満のp値及び/又は0.10未満のq値)異なった形で存在することが好ましい。或いは、バイオマーカーは、糖尿病前症又は特定のレベルの糖尿病前症との相関を示す。相関の可能性の範囲は、陰性(−)1から陽性(+)1の間である。陰性(−)1の結果とは、完全に陰性の相関を意味し、陽性(+)1は、完全に陽性の相関を意味し、0は、全く相関がないことを意味する。「実質的に陽性の相関」とは、障害と、又は臨床測定値(例えば、Rd)と+0.25〜+1.0の相関を有するバイオマーカーを指すのに対し、「実質的に陰性の相関」とは、所与の障害又は臨床測定値との−0.25〜−1.0の相関を指す。「相当に陽性の相関」とは、所与の障害又は臨床測定値(例えば、Rd)と、+0.5〜+1.0の相関を有するバイオマーカーを指すのに対し、「相当に陰性の相関」とは、所与の障害又は臨床測定値と−0.5〜−1.0の障害に対する相関を指す。
本明細書に記載されるバイオマーカーは、メタボロミクスプロファイリング技術を用いて発見した。このようなメタボロミクスプロファイリング技術は、以下に示される実施例において、並びに、その全内容が参照として本明細書に組み込まれる、米国特許第7,005,255号及び同7,329,489号及び米国特許出願第11/357,732号(公開番号第2007/0026389号)、同11/301,077号(公開番号第2006/0134676号)、同11/301,078号(公開番号第2006/0134677号)、同11/301,079号(公開番号第2006/0134678号)及び同11/405,033号(公開番号US2007/0072203)においてより詳細に記載されている。
本明細書に記載されるバイオマーカーは、対象が、インスリン抵抗性、糖尿病前症、2型糖尿病、メタボリックシンドローム、アテローム性動脈硬化症又は心筋症などの疾患又は状態を有するかどうかを診断するために、又は診断において補助するために使用できる。例えば、対象がインスリン抵抗性を有するかどうかを診断すること又は診断において補助することにおいて使用するためのバイオマーカーとして、表4、5、6、7、8、9A、9B、27、28、29及びそれらの組合せにおいて同定されるもののうち1種又は複数が挙げられる。一実施形態では、これらのバイオマーカーとして、表4、5、6、7、8、9A、9B、27、28及びそれらの組合せにおいて同定されるもののうち1種又は複数が挙げられる。別の実施形態では、バイオマーカーの組合せとして、表4、5、6、7、8、9A、9B、27、28及び/又は29において同定される1種又は複数のバイオマーカーと組み合わせた2−ヒドロキシ酪酸などのものが挙げられる。
本明細書におけるバイオマーカーの同定によって、対象におけるそれぞれの疾患又は状態(例えば、糖尿病前症、メタボリックシンドローム、アテローム性動脈硬化症、心筋症、インスリン抵抗性など)の進行/退縮をモニタリングすることが可能となる。対象における糖尿病前症、2型糖尿病、メタボリックシンドローム、アテローム性動脈硬化症及び心筋症などの疾患又は状態の進行/退縮をモニタリングする方法は、(1)対象から得た第1の生体試料を分析して、第1の時点で対象から得られた第1の試料中の、表4、5、6、7、8、9A、9B、14、15、16、17、21、22、23、25、26、27、28及びそれらの組合せから選択されるそれぞれの疾患又は状態の1種又は複数のバイオマーカーのレベルを決定するステップと、(2)対象から得た第2の生体試料を分析して、1種又は複数のバイオマーカー、第2の時点で対象から得られた第2の試料のレベルを決定するステップと、(3)第1の試料中の1種又は複数のバイオマーカーのレベルを、第2の試料中の1種又は複数のバイオマーカーのレベルと比較して、対象における疾患又は状態の進行/退縮をモニタリングするステップとを含む。本方法の結果は、対象における疾患又は状態の経過(即ち、変化があるとすれば、進行又は退縮)を示す。
本明細書において同定されるバイオマーカーを、対象が、糖尿病前症、2型糖尿病、メタボリックシンドローム、アテローム性動脈硬化症又は心筋症などの疾患又は状態の何らかの症状を示していないかどうかの決定において用いてもよい。バイオマーカーはまた、例えば、対象が、インスリン抵抗性の発生の素因があるかどうかを決定するために使用してもよい。糖尿病前症、2型糖尿病、メタボリックシンドローム、アテローム性動脈硬化症又は心筋症などの特定の疾患又は状態の症状が全くない対象が、特定の疾患又は状態の発症の素因があるかどうかを決定するこのような方法は、(1)対象から得た生体試料を分析して、試料中の、それぞれの表(例えば、表4、5、6、7、8、9A、9B、14、15、16、17、21、22、23、25、26及びそれらの組合せ)中に列挙される1種又は複数のバイオマーカーのレベルを決定するステップと、(2)試料中の1種又は複数のバイオマーカーのレベルを、1種又は複数のバイオマーカーの疾患若しくは状態陽性及び/又は疾患若しくは状態陰性参照レベルと比較して、対象がそれぞれの疾患又は状態の発症の素因があるかどうかを決定するステップとを含む。例えば、インスリン抵抗性のバイオマーカーの同定によって、インスリン抵抗性の症状のない対象が、インスリン抵抗性の発症の素因があるかどうかを決定することが可能となる。インスリン抵抗性の症状がない対象が、インスリン抵抗性の発症の素因があるかどうかを決定する方法は、(1)対象から得た生体試料を分析して、試料中の、表4、5、6、7、8、9A及び9B及びそれらの組合せ中に列挙される1種又は複数のバイオマーカーのレベルを決定するステップと、(2)試料中の1種又は複数のバイオマーカーのレベルを、1種又は複数のバイオマーカーのインスリン抵抗性陽性及び/又はインスリン抵抗性陰性参照レベルと比較して、対象がインスリン抵抗性の発症の素因があるかどうかを決定するステップとを含む。この方法の結果は、対象が疾患又は状態の発症の素因があるかどうかの臨床的判断において有用なその他の方法(又はその結果)とともに用いてもよい。
また、提供されるバイオマーカーによって、インスリン抵抗性、糖尿病前症、2型糖尿病、メタボリックシンドローム、アテローム性動脈硬化症又は心筋症などの疾患又は状態を治療するための組成物の有効性の評価が可能となる。例えば、インスリン抵抗性のバイオマーカーの同定によってまた、インスリン抵抗性を治療するための組成物の有効性の評価並びにインスリン抵抗性を治療するための2種以上の組成物の相対有効性の評価も可能となる。このような評価は、例えば、疾患又は状態を治療するための組成物の有効性研究に、並びにリード選択に用いてもよい。
また、提供されるバイオマーカーによって、糖尿病前症、2型糖尿病、メタボリックシンドローム、アテローム性動脈硬化症又は心筋症などの疾患又は状態を治療するための組成物が有効である対象(即ち、患者が治療に応答する)の同定が可能となる。例えば、インスリン抵抗性のバイオマーカーの同定によってまた、インスリン抵抗性を治療するための組成物に対する対象応答の評価並びにインスリン抵抗性を治療するための2種以上の組成物に対する相対的な患者応答の評価も可能となる。このような評価を、例えば、特定の対象の疾患又は状態を治療するための組成物の選択に用いてもよい。
本明細書に提供されるバイオマーカーによってまた、糖尿病前症、2型糖尿病、メタボリックシンドローム、アテローム性動脈硬化症及び心筋症などの疾病又は状態と関連しているバイオマーカーの調節(疾患又は状態の治療において有用であり得る)における活性について組成物をスクリーニングすることが可能となる。このような方法は、それぞれの表中に列挙されるそれぞれのバイオマーカーから選択される1種又は複数のバイオマーカーのレベルの調節における活性について、試験化合物をアッセイすることを含む。このようなスクリーニングアッセイは、in vitro及び/又はin vivoで実施でき、試験組成物の存在下で、このようなバイオマーカーの調節をアッセイするのに有用な、当技術分野で公知の任意の形、例えば、細胞培養アッセイ、器官培養アッセイ及びin vivoアッセイ(例えば、動物モデルを用いるアッセイ)などであり得る。例えば、インスリン抵抗性のバイオマーカーの同定によって、インスリン抵抗性と関連しているバイオマーカーの調節(インスリン抵抗性の治療において有用であり得る)における活性について組成物をスクリーニングすることが可能となる。インスリン抵抗性の治療にとって有用な組成物をスクリーニングする方法は、表4、5、6、7、8、9A、9B、27及び/又は28中の1種又は複数のバイオマーカーのレベルの調節における活性について、試験組成物をアッセイすることを含む。この例では、インスリン抵抗性が論じられているが、上記で示される1種又は複数のそれぞれのバイオマーカーを用い、この方法に従って、糖尿病前症、2型糖尿病、メタボリックシンドローム、アテローム性動脈硬化症及び心筋症などのその他の疾患及び状態も、診断され得る、又は診断されるのを補助され得る。
本開示内容はまた、表4、5、6、7、8、9A、9B、14、15、16、17、21、22、23、25、26、27及び/又は28に列挙されるバイオマーカーを用いて、インスリン抵抗性、糖尿病前症、2型糖尿病、メタボリックシンドローム、アテローム性動脈硬化症及び心筋症などの疾患又は状態の可能性ある薬物標的を同定する方法を提供する。糖尿病前症、2型糖尿病、メタボリックシンドローム、アテローム性動脈硬化症及び心筋症などの疾患又は状態の可能性ある薬物標的を同定する方法は、(1)それぞれの表(表4、5、6、7、8、9A、9B、14、15、16、17、21、22、23、25、26、27及び/又は28)から選択される、メタボリックシンドローム関連代謝障害の1種又は複数のバイオマーカーと関連している1種又は複数の生化学経路を同定するステップと、(2)1種又は複数の同定された生化学経路のうち少なくとも1種に影響を及ぼすタンパク質(例えば、酵素)を同定し、このタンパク質が疾患又は状態の可能性ある薬物標的であるステップとを含む。例えば、インスリン抵抗性のバイオマーカーの同定によって、インスリン抵抗性の可能性ある薬物標的の同定も可能となる。インスリン抵抗性の可能性ある薬物標的を同定する方法は、(1)表4、5、6、7、8、9A、9B、27及び/又は28から選択される、インスリン抵抗性の1種又は複数のバイオマーカーと関連している1種又は複数の生化学経路を同定するステップと、(2)1種又は複数の同定された生化学経路のうち少なくとも1種に影響を及ぼすタンパク質(例えば、酵素)を同定し、タンパク質がインスリン抵抗性の可能性ある薬物標的であるステップとを含む。この例では、インスリン抵抗性が論じられているが、上記で示される1種又は複数のそれぞれのバイオマーカーを用い、この方法に従って、2型糖尿病、メタボリックシンドローム、アテローム性動脈硬化症及び心筋症などのその他の疾患又は状態も、診断され得る、又は診断されるのを補助され得る。
別の態様では、糖尿病前症、2型糖尿病、メタボリックシンドローム、アテローム性動脈硬化症及び心筋症などの疾患又は状態を治療する方法が提供される。この方法は、概して、糖尿病前症、2型糖尿病、メタボリックシンドローム、アテローム性動脈硬化症及び心筋症などの疾患又は状態を有する対象を、疾患又は状態を有していない健常な対象と比較して、疾患又は状態を有する対象では低下している、1種又は複数のバイオマーカーの有効量を用いて治療することを含む。投与され得るバイオマーカーは、その疾患又は状態を有していない対象と比較して、疾患又は状態の状況では減少している、表4、5、6、7、8、9A、9B、14、15、16、17、21、22、23、25、26、27、28及び/又は29中の1種又は複数のバイオマーカーを含み得る。このようなバイオマーカーは、バイオマーカー化合物の同定(即ち、化合物名)に基づいて単離できる。現在名前のない代謝産物であるバイオマーカーは、以下の実施例(例えば、表29)に列挙されるバイオマーカーの分析的特性決定に基づいて単離できる。いくつかの実施形態では、投与されるバイオマーカーは、メタボリックシンドローム関連代謝障害において減少しており、ウエルチt検定又はウィルコクソン順位和検定を用いることによって求められる、0.05未満のp値若しくは0.10未満のq値、又は0.05未満のp値及び0.10未満のq値の両方を有する、表4、5、6、7、8、9A、9B、14、15、16、17、21、22、23、25、26、27、28及び/又は29中に列挙される1種又は複数のバイオマーカーである。その他の実施形態では、投与されるバイオマーカーは、疾患又は状態において減少しており、疾患又は状態と正相関又は逆相関のいずれかを有する、表4、5、6、7、8、9A、9B、14、15、16、17、21、22、23、25、26、27、28及び/又は29中に列挙される1種又は複数のバイオマーカーである。一実施形態では、バイオマーカーは、疾患又は状態と、それぞれ≧+0.5又は≦−0.5いずれかの正相関又は逆相関を有する。その他の実施形態では、投与されるバイオマーカーは、疾患又は状態において、少なくとも5%、少なくとも10%、少なくとも15%、少なくとも20%、少なくとも25%、少なくとも30%、少なくとも35%、少なくとも40%、少なくとも45%、少なくとも50%、少なくとも55%、少なくとも60%、少なくとも65%、少なくとも70%、少なくとも75%、少なくとも80%、少なくとも85%、少なくとも90%、少なくとも95%又は100%(即ち、存在しない)減少している、表4、5、6、7、8、9A、9B、14、15、16、17、21、22、23、25、26、27、28及び/又は29中に列挙される1種又は複数のバイオマーカーである。一実施例では、インスリン抵抗性のバイオマーカーの同定によってまた、インスリン抵抗性の治療が可能となる。例えば、インスリン抵抗性を有する対象を治療するために、インスリン抵抗性を有さない健常対象と比較してインスリン抵抗性を有する対象では低下している、1種又は複数のインスリン抵抗性バイオマーカーの有効量を、対象に投与してもよい。投与してもよいバイオマーカーは、インスリン抵抗性を有する対象では減少している、表4、5、6、7、8、9A、9B、27、28及び/又は29中の1種又は複数のバイオマーカーを含み得る。この例では、インスリン抵抗性が論じられているが、上記で示される1種又は複数のそれぞれのバイオマーカーを用い、この方法に従って、2型糖尿病、メタボリックシンドローム、アテローム性動脈硬化症及び心筋症などのその他の疾患又は状態も治療できる。
別の態様では、特定の疾患又は状態の本明細書に開示されるバイオマーカーの少なくとも一部はまた、その他の疾患又は状態のバイオマーカーでもあり得る。例えば、インスリン抵抗性バイオマーカーの少なくとも一部は、その他の疾患又は状態(例えば、メタボリックシンドローム)について本明細書に記載される方法において使用できるということが考えられる。即ち、インスリン抵抗性に関して本明細書に記載される方法を、2型糖尿病、メタボリックシンドローム、アテローム性動脈硬化症又は心筋症などの疾患又は状態の診断(又は診断における補助)、このような疾患又は状態の進行/退縮をモニタリングする方法、このような疾患又は状態を治療するための組成物の有効性を評価する方法、このような疾患又は状態と関連しているバイオマーカーの調節における活性について組成物をスクリーニングする方法、このような疾患及び状態のための可能性ある薬物標的を同定する方法、このような疾患及び状態を治療する方法のために用いてもよい。このような方法は、インスリン抵抗性に関して本明細書に記載されるように実施できる。
本明細書に開示されるバイオマーカーを用いるその他の方法も企図される。例えば、米国特許第7,005,255号及び米国特許出願第11/357,732号、同10/695,265号(公開番号第2005/0014132号)、同11/301,077号(公開番号第2006/0134676号)、同11/301,078号(公開番号第2006/0134677号)、同11/301,079号(公開番号第2006/0134678号)及び同11/405,033号に記載される方法は、本明細書に開示される1種又は複数のバイオマーカーを含む小分子プロフィールを用いて実施してもよい。
A.代謝プロフィールの同定
各試料を分析して、数百種の代謝産物の濃度を決定した。GC−MS(ガスクロマトグラフィー−質量分析)及びLC−MS(液体クロマトグラフィー質量分析)などの分析技術を用いて代謝産物を分析した。複数のアリコートを同時に、並行して分析し、適当な品質管理(QC)後、各分析から得られた情報を再結合させた。どの試料も、数千の特徴に従って特性決定し、最終的に、数百種の化学種になった。用いた技術は、新規の、化学的に名前のない化合物を同定できた。
データを、いくつかの統計的手法を用いて分析し、限定できる集団間(例えば、インスリン抵抗性及び対照、インスリン抵抗性及び寛解、寛解及び対照)を区別するのに有用な、限定できる集団又は亜集団において異なるレベルで存在する分子(既知の、名前のついた代謝産物又は名前のない代謝産物のいずれか)(例えば、対照生体試料と比較した、又はインスリン抵抗性からの寛解にある患者と比較したメタボリックシンドローム生体試料のバイオマーカー)を同定した。限定できる集団又は亜集団中のその他の分子(既知の、名前のついた代謝産物又は名前のない代謝産物のいずれか)も同定した。
糖尿病前症のバイオマーカー
2A:糖処理と相関するバイオマーカーの同定
あるアルゴリズムにおいて使用されると、糖処理速度(即ち、Rd)と相関するバイオマーカーの組合せを発見した。さらに、バイオマーカーの最初のパネルを、15〜30種の候補代謝産物を含む標的とされるアッセイの開発のために縮小してもよい。インスリン抵抗性を予測するアルゴリズムを開発した。
表1 研究1コホートの性別及び処理
表2 研究1コホートの治療及び採取時間
表3 コホート説明、研究2
略語
Rd:糖処理速度
NGT:正常耐糖能(OGTT、<140mg/dL又は<7.8mmol/L)
IFG:空腹時血糖異常(空腹時血漿グルコース、100〜125mg/dL又は5.6〜6.9mmol/L)
IGT:耐糖能異常(OGTT、140〜199mg/dL又は7.8〜11.0mmol/L)
(1)ヒト対象の種々の群から採取した血液試料を分析して、試料中の代謝産物のレベルを決定するステップと、次いで、(2)結果を統計的に分析して、対象の群中に異なった形で存在した代謝産物及び糖処理速度、インスリン感受性の指標と相関する代謝産物を決定するステップとによって、バイオマーカーを発見した。
表4 Rdとのバイオマーカー相関性
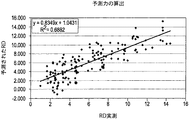
完全5倍交差検定回帰を含む50反復のランダムフォレスト解析(研究1について、この解析は、ベースラインデータ、n=111のみを含んでいたが、研究2については、すべての試料を含めた、n=402)を以下のとおりに実施した:
代謝産物の数が約30又はそれ以上に達する時は、平均R二乗値は、常に高いままであり、対応するエラーは、一貫して低いままであり(図1及び2)、このことは、約30種の代謝産物は、Rdと相関させるアルゴリズムを構築するのに十分であり得るが、また、7種未満の代謝産物の組合せに基づいてRdと相関させるためのアルゴリズムを構築することが可能であり得ることを示唆する。結果として、上位30〜50の交差検定された化合物を回帰分析のために選択した。
モデリング実験に基づいて、代謝産物の数が、7以上に達する時は、平均R二乗値は、常に高いままであり、対応するエラーは一貫して低いままであり(図3及び4)、このことは、7種の代謝産物の組合せは、Rdと相関させるアルゴリズムを構築するのに十分であり得るが、また、7種未満の代謝産物の組合せに基づいてRdと相関させるアルゴリズムを構築することも可能であり得ることを示唆する。
上記のランダムフォレスト解析からの交差検定された変数のみを、LASSO回帰に用い、Rdを予測するための変数の最良の組合せを選んだ。LASSO回帰のために、交差検定された変数の最も適当な変換も検討した。
表5 非変換データを用いるLASSO回帰
注記:**同重体56は、分離され得る、DL−ピペコリン酸及び1−アミノ−1−シクロペンタンカルボン酸を含む。
表6 変換データを用いるLASSO回帰
注記:**同重体56は、DL−ピペコリン酸及び1−アミノ−1−シクロペンタンカルボン酸を含む。
表7 非変換データを用いるLASSO回帰
研究2において、ランダムフォレスト及びLasso回帰によってRdを予測するためのモデルの構築において重要と同定された化合物が、表4に列挙されている。次いで、交差検定された化合物を、臨床測定値とともに(例えば、空腹時インスリン、空腹時プロインスリン、空腹時遊離脂肪酸(FFA)、空腹時C−ペプチド、HDLコレステロール、LDLコレステロール、空腹時血漿グルコース、アディポネクチン、BMI、PYYなど)回帰分析のために選択した。次いで、各々回帰法及び一変量相関/線形回帰法モデルを用いて、個々のものの各々のRdを予測し、次いで、これを用いて、グルコース利用のレベルに従って個々のものを、正常、インスリンの障害又はインスリン抵抗性と分類した。90パーセントの対象から得た試料を用いて、モデルを構築し、残りの10パーセントの対象から得た試料を用いて、モデルの予測力を試験した。これらの分析において、Rdを予測するために有用であるバイオマーカー化合物及びRdと正相関又は逆相関するバイオマーカー化合物を同定した。これらのマーカーは、インスリン抵抗性を予測するために有用である。バイオマーカー化合物のすべては、回帰モデルの各々において統計的に有意である(p<0.05)。
表8 糖処理速度(Rd)によって決定されるようなインスリン抵抗性を予測する代謝産物バイオマーカー及びモデル
略語:BMI、肥満度指数;FFA、遊離脂肪酸;FPG、空腹時血漿グルコース
表9A及び9Bに示されるように、多数のバイオマーカー化合物が相関した。表9Aは、研究1において同定されたバイオマーカーのペアワイズ相関分析を含み、表9Bは、研究2において同定されたバイオマーカーのペアワイズ相関分析を含む。相関する化合物は、回帰モデルでは互いに排反することが多く、従って、上記の表8に示されるような同様の予測力を有していた異なるモデルにおいて使用することができる(即ち、相関する化合物のために置換することができる)。特定のバイオマーカーは、その他のバイオマーカーよりもアッセイ開発に従い得るので、この態様は、特異的バイオマーカーを標的とする生化学アッセイを開発する場合に有用である。
表9A 研究1における相関バイオマーカー
表9B 研究2における相関バイオマーカー
バイオマーカーパネル及びアルゴリズムは、2型糖尿病の主要因であるインスリン抵抗性(IR)を評価する。結果は、対象のインスリン抵抗性のレベルを表す「IRスコア(商標)」として示される。IRスコアは、正常耐糖能(NGT)から増大するレベル(低、中、高)の耐糖能異常(IGT)に及ぶ。IRスコア(商標)によって、医師が患者を耐糖能の範囲、正常から高に入れることが可能になる。例えば、25のIRスコア(商標)は患者を低IGTカテゴリーに入れ、他方、80のIRスコア(商標)は、患者を高IGTカテゴリーに入れる。
表10:IRスコア
新規コホートを用いて本発明において発見されたバイオマーカーを試験するために、高インスリン血症正常血糖(HI)クランプによって測定されるようなインスリン感受性(IS)及びインスリン抵抗性(IR)と相関するさらなる生化学的バイオマーカーを発見するために別の研究を実施する(表11)。以下の研究デザインを用いて、NGT、IGT、IFG IGT/IFG及び糖尿病の対象から集めたベースライン空腹時EDTA血漿試料(合計=250)を分析する。
表11:研究対象の概要
略語
NGT:正常グルコース耐性(OGTT、<140mg/dL又は<7.8mmol/L)
IGT:耐糖能異常(OGTT、140〜199mg/dL又は7.8〜11.0mmol/L)
IFG:空腹時血糖異常(空腹時血漿グルコース、100〜125mg/dL又は5.6〜6.9mmol/L)
IGT/IFG:IGT及び/又はIFG
T2D:II型糖尿病(OGTT、≧200mg/dL又は≧11.1mmol/L)
メタボリックシンドローム関連障害のバイオマーカー
3A:メタボリックシンドロームのバイオマーカー
(1)種々の群の対象から得た血漿及び血清試料を分析して、試料中の代謝産物のレベルを決定するステップと、(2)結果を統計的に分析して、2群において異なった形で存在していた代謝産物を決定するステップとによってバイオマーカーを発見した。
表12及び13において以下で列挙されるように、メタボリックシンドロームの対象及び対照(健常)対象から得た試料間で異なった形で存在するバイオマーカーを発見した。
表12 血漿におけるメタボリックシンドロームの代謝産物バイオマーカー
表13 血清におけるメタボリックシンドロームの代謝産物バイオマーカー
(1)アテローム性動脈硬化症の対象及び健常対象から取り出した血漿、大動脈及び肝臓試料を分析して、試料中の代謝産物のレベルを決定するステップと、次いで、(2)結果を統計的に分析して、2群において異なった形で存在する代謝産物を決定するステップとによって、バイオマーカーを発見した。
表14、15及び16において以下で列挙されるように、LDb(アテローム性動脈硬化性の)対象及びC57BL/6(健常)対象から得た試料間で異なった形で存在するバイオマーカーを発見した。
表14 血漿におけるアテローム性動脈硬化症の代謝産物バイオマーカー
[1]同重体71は、コンデュリトール−β−エポキシド−3−デオキシグルコソンを含む
[2]同重体56は、DL−ピペコリン酸−1−アミノ−1−シクロペンタンカルボン酸を含む
[3]同重体59は、N−6−トリメチル−L−リシン−H−ホモarg−OHを含む
[4]同重体21は、γ−アミノブチリル−L−ヒスチジン−L−アンセリンを含む
[5]同重体6は、バリン−ベタインを含む
[6]同重体1は、マンノース、フルクトース、グルコース、ガラクトース、α−L−ソルボピラノース、イノシトール、D−アロース、D−アルトロース、D−プシコン(psicone)、L−グロース、アロイノシトールを含む
表15 大動脈におけるアテローム性動脈硬化症の代謝産物バイオマーカー
[1]おそらくはギ酸塩二量体のCl−付加物
[2]同重体19は、1,5−無水−D−グルシトール、2’−デオキシ−D−ガラクトース、2’−デオキシ−D−グルコース、L−フコース、L−ラムノースを含む
[3]同重体4は、グルコン酸、DL−アラビノース、D−リボース、L−キシロース、DL−リキソース、D−キシルロース、ガラクトン酸を含む
[4]同重体58は、ビシン、2−メチルアミノメチル−タルトロン酸を含む
[5]同重体6は、バリン−ベタインを含む
[6]同重体13は、5−ケト−D−グルコン酸、2−ケト−L−グロン酸、D−グルクロン酸、D−ガラクツロン酸を含む
[7]同重体1は、マンノース、フルクトース、グルコース、ガラクトース、α−L−ソルボピラノース、イノシトール、D−アロース、D−アルトロース、D−プシコン(psicone)、L−グロース、アロイノシトールを含む
[8]同重体22は、グルタミン酸−O−アセチル−L−セリンを含む
[9]同重体10は、グルタミン−H−β−ala−gly−OH−1−メチルグアニン−H−Gly−Sar−OH−リシンを含む
[10]同重体71は、コンデュリトール−β−エポキシド−3−デオキシグルコソンを含む
表16 肝臓におけるアテローム性動脈硬化症の代謝産物バイオマーカー
[1]同重体56は、DL−ピペコリン酸−1−アミノ−1−シクロペンタンカルボン酸を含む
[2]5−メチル−デオキシシチジン一リン酸の可能性
[3]同重体24は、L−アラビトール、アドニトール、キシリトールを含む
[4]同重体1は、マンノース、フルクトース、グルコース、ガラクトース、α−L−ソルボピラノース、イノシトール、D−アロース、D−アルトロース、D−プシコン(psicone)、L−グロース、アロイノシトールを含む
表17 血漿中の、アテローム性動脈硬化症対象(LDb)及び健常対照対象(C57BL/6マウス)をエラーなく区別するアテローム性動脈硬化症バイオマーカー
表18 血漿におけるアテローム性動脈硬化症のランダムフォレスト混同行列
表19 大動脈組織におけるアテローム性動脈硬化症のランダムフォレスト混同行列
表20 肝臓におけるアテローム性動脈硬化症のランダムフォレスト混同行列
(1)種々の群のマウス対象から得た心組織試料(表21)又は血漿試料(表22)を分析して、試料中の代謝産物のレベルを決定するステップと、次いで、(2)結果を統計的に分析して、2群において異なった形で存在していた代謝産物を決定するステップとによって、バイオマーカーを発見した。これらの対象は、ヒトDCMの動物(マウス)モデルを提供した。
表21及び22において以下で列挙されるように、拡張型心筋症対象及び健常対象から採取した、心組織及び血漿試料それぞれの間で異なった形で存在していたバイオマーカーを発見した。
表21 心組織における拡張型心筋症(DCM)の代謝産物バイオマーカー
[1]同重体56は、DL−ピペコリン酸、1−アミノ−1−シクロペンタンカルボン酸を含む。
[2]メチルテストステロン及びその他の可能性。
[3]イソロビニン(isolobinine)又は4−アミノエストラ−1,3,5(10)−トリエン−3,17β−ジオールの可能性。
[4]スタキドリンの可能性。
[5]同重体−52は、イミノ二酢酸、L−アスパラギン酸を含む。
[6]尿酸のCl付加物の可能性。
[7]同重体13は、5−ケト−D−グルコン酸、2−ケト−L−グロン酸、D−グルクロン酸,D(+)−ガラクツロン酸を含む。
[8]同重体48は、セリン−2,2−アミノ−2−メチル−1,3−プロパンジオール,ジエタノールアミンを含む。
表22 血漿における、拡張型心筋症(DCM)の代謝産物バイオマーカー
表23において以下で列挙されるように、拡張型心筋症対象及び健常対象から採取した血漿試料間で異なった形で存在していたバイオマーカーを発見した。
表23 DCMのバイオマーカー
表24 DCM及び健常対象のランダムフォレスト分類
(1)種々の群のヒト対象から取り出した血液試料を分析し、試料中の代謝産物のレベルを決定するステップと、次いで、(2)結果を統計的に分析して、2群において異なった形で存在していた代謝産物を決定するステップとによって、バイオマーカーを発見した。
表26において以下で列挙されるように、肥満対象及び痩せた対象から得た試料間で異なった形で存在していたバイオマーカーを発見した。
表26 痩せた対象と比較して肥満において異なった形で存在する代謝産物バイオマーカー
バイオマーカー代謝産物を、単独及び/又はメタボリックシンドロームの臨床的尺度(例えば、BMI、Rd)と組み合わせて用い、インスリン感受性(Rd)及びメタボリックシンドロームを予測する能力を試験するためにモデルを開発した。分析に使用した血漿試料は、種々の速度の糖処理(Rd)を有する対象に由来するものであった。
治療応答バイオマーカー
「ノンレスポンダー」であった(即ち、ベースライン及び治療の12週後間でRdがほとんど、又は全く変化しない(<15%))対象及び治療に応答した対象(即ち「レスポンダー」)を比較することによって、治療に対する応答を予測するバイオマーカーを同定した。対象を、治療レスポンダー又はノンレスポンダーと予測したバイオマーカーは、ベースラインのみでの化合物レベルに基づいていた。レスポンダーは、35%以上のRd変化を有するか、又は15%以上のRd変化を有する対象のいずれかと定義された。データは、ノンレスポンダーを両クラスのレスポンダーと比較することによって分析した。次いで、両分析(即ち、15%を下回るRd変化を有するノンレスポンダー対35%を上回るRd変化を有するレスポンダー、15%を下回るRd変化を有するノンレスポンダー対15%を上回るRd変化を有するレスポンダー)を合わせ、2種の分析のいずれかで<0.1のp値を有するバイオマーカーを同定した。バイオマーカーは、表27に列挙されている。治療前のバイオマーカー測定値は、チアゾリンジンジオン(TZD)応答を予測し、従って、これを用いて、TZD薬で治療のための患者を選択できる。実験は、その他の治療薬(例えば、メトホルミンなど)などの、インスリン感受性、糖尿病前症及び糖尿病コントロールのためのその他の治療、減量、栄養摂取及びその他のライフスタイル改善を予測するバイオマーカーを評価するよう計画されている。この群の予測的バイオマーカーは、個別医療にとって極めて価値のあるツールを提供する。
表27 治療のレスポンダー又はノンレスポンダーを分類するためのバイオマーカー
表28 治療応答の薬力学的バイオマーカー
名前のないバイオマーカー化合物の分析的特性決定
以下の表29は、上記の表に列挙される名前のない代謝産物各々の分析的特徴を含む。この表は、列挙される代謝産物各々について、上記の分析法を用いて得られた保持時間(RT)、保持指数(RI)、質量、定量質量及び極性を含む。「質量」とは、化合物の定量に用いた親イオンのC12同位体の質量を指す。「極性」とは、正(+)又は負(−)のいずれかである定量イオンの極性を示す。
表29 バイオマーカー代謝産物の分析的特徴
Claims (5)
- 対象における糖処理速度を予測する方法であって、対象から得た生体試料を分析して、試料中のリノリルLPCのレベル及びインスリン抵抗性に関する1種又は複数のさらなるバイオマーカーのレベルを決定するステップであって、1種又は複数のさらなるバイオマーカーが、2−ヒドロキシ酪酸、オレイン酸、グリシン、トリゴネリン(N−メチルニコチネート)、ヒドロケイ皮酸、パントテン酸、クレアチン、キサンチン、マンノース、3−ヒドロキシ酪酸、α−ケトグルタル酸、3−メチル−2−オキソ酪酸、3−メチル−2−オキソ吉草酸、4−メチル−2−オキソペンタン酸、イソロイシン、ロイシン、フェニルアラニン、セリン、チロシン、オレオイルLPC、グリセロホスホリルコリン(GPC)、ドコサテトラエン酸及びバリンからなる群から選択されるステップと、試料中のリノリルLPCのレベル及び1種又は複数のさらなるバイオマーカーのレベルを、リノリルLPC及び1種又は複数のさらなるバイオマーカーの糖処理参照レベルと比較して、対象における糖処理速度を予測するステップとを含む方法。
- 1種又は複数のさらなるバイオマーカーが、2−ヒドロキシ酪酸と、オレイン酸、グリシン、トリゴネリン(N−メチルニコチネート)、ヒドロケイ皮酸、パントテン酸、クレアチン、キサンチン、マンノース、3−ヒドロキシ酪酸、α−ケトグルタル酸、3−メチル−2−オキソ酪酸、3−メチル−2−オキソ吉草酸、4−メチル−2−オキソペンタン酸、イソロイシン、ロイシン、フェニルアラニン、セリン、チロシン、オレオイルLPC、グリセロホスホリルコリン(GPC)、ドコサテトラエン酸及びバリンからなる群から選択される1種又は複数のバイオマーカーとを組み合わせて含む、請求項1に記載の方法。
- 予測糖処理速度を用いて、対象のインスリン感受性のレベルを決定する、請求項1に記載の方法。
- 1種又は複数のさらなるバイオマーカーが、2−ヒドロキシ酪酸、オレイルLPC、オレイン酸及びグリセロリン酸コリン(GPC)からなる群から選択される、請求項1に記載の方法。
- 空腹時血漿インスリン、空腹時血漿グルコース、空腹時血漿プロインスリン、空腹時遊離脂肪酸、HDL−コレステロール、LDL−コレステロール、C−ペプチド、アディポネクチン、ペプチドYY、ヘモグロビンA1C、ウエスト周囲、体重又は肥満度指数の対象の測定値を決定するステップをさらに含む、請求項1に記載の方法。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US95028607P | 2007-07-17 | 2007-07-17 | |
| US60/950,286 | 2007-07-17 | ||
| US3762808P | 2008-03-18 | 2008-03-18 | |
| US61/037,628 | 2008-03-18 | ||
| PCT/US2008/008756 WO2009014639A2 (en) | 2007-07-17 | 2008-07-17 | Biomarkers for pre-diabetes, cardiovascular diseases, and other metabolic-syndrome related disorders and methods using the same |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2014218116A Division JP5876918B2 (ja) | 2007-07-17 | 2014-10-27 | 糖尿病前症、心血管疾患及びその他のメタボリックシンドローム関連障害のバイオマーカー並びにその使用方法 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2010537157A JP2010537157A (ja) | 2010-12-02 |
| JP2010537157A5 JP2010537157A5 (ja) | 2011-10-27 |
| JP5701601B2 true JP5701601B2 (ja) | 2015-04-15 |
Family
ID=40282019
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2010517019A Active JP5701601B2 (ja) | 2007-07-17 | 2008-07-17 | 糖尿病前症、心血管疾患及びその他のメタボリックシンドローム関連障害のバイオマーカー並びにその使用方法 |
| JP2014218116A Active JP5876918B2 (ja) | 2007-07-17 | 2014-10-27 | 糖尿病前症、心血管疾患及びその他のメタボリックシンドローム関連障害のバイオマーカー並びにその使用方法 |
| JP2015236454A Pending JP2016102797A (ja) | 2007-07-17 | 2015-12-03 | 糖尿病前症、心血管疾患及びその他のメタボリックシンドローム関連障害のバイオマーカー並びにその使用方法 |
Family Applications After (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2014218116A Active JP5876918B2 (ja) | 2007-07-17 | 2014-10-27 | 糖尿病前症、心血管疾患及びその他のメタボリックシンドローム関連障害のバイオマーカー並びにその使用方法 |
| JP2015236454A Pending JP2016102797A (ja) | 2007-07-17 | 2015-12-03 | 糖尿病前症、心血管疾患及びその他のメタボリックシンドローム関連障害のバイオマーカー並びにその使用方法 |
Country Status (10)
| Country | Link |
|---|---|
| US (5) | US8187830B2 (ja) |
| EP (1) | EP2164977B1 (ja) |
| JP (3) | JP5701601B2 (ja) |
| AU (1) | AU2008279778B2 (ja) |
| BR (1) | BRPI0815095B1 (ja) |
| CA (1) | CA2690541A1 (ja) |
| ES (1) | ES2443540T3 (ja) |
| HK (1) | HK1142636A1 (ja) |
| MX (2) | MX2010000414A (ja) |
| WO (1) | WO2009014639A2 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016102797A (ja) * | 2007-07-17 | 2016-06-02 | メタボロン インコーポレイテッド | 糖尿病前症、心血管疾患及びその他のメタボリックシンドローム関連障害のバイオマーカー並びにその使用方法 |
Families Citing this family (118)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2647197A1 (en) * | 2006-03-24 | 2007-10-04 | Metanomics Gmbh | Means and method for predicting diabetes |
| JPWO2008015929A1 (ja) * | 2006-08-04 | 2009-12-24 | 味の素株式会社 | メタボリック・シンドロームの評価方法、メタボリック・シンドローム評価装置、メタボリック・シンドローム評価方法、メタボリック・シンドローム評価システム、メタボリック・シンドローム評価プログラムおよび記録媒体、ならびにメタボリック・シンドロームの予防・改善物質の探索方法 |
| US9867530B2 (en) | 2006-08-14 | 2018-01-16 | Volcano Corporation | Telescopic side port catheter device with imaging system and method for accessing side branch occlusions |
| JPWO2009001862A1 (ja) * | 2007-06-25 | 2010-08-26 | 味の素株式会社 | 内臓脂肪蓄積の評価方法 |
| WO2009009802A1 (en) | 2007-07-12 | 2009-01-15 | Volcano Corporation | Oct-ivus catheter for concurrent luminal imaging |
| US9596993B2 (en) | 2007-07-12 | 2017-03-21 | Volcano Corporation | Automatic calibration systems and methods of use |
| JP5524835B2 (ja) | 2007-07-12 | 2014-06-18 | ヴォルカノ コーポレイション | 生体内撮像用カテーテル |
| WO2009054350A1 (ja) * | 2007-10-25 | 2009-04-30 | Ajinomoto Co., Inc. | 耐糖能異常の評価方法 |
| EP2546649B1 (en) * | 2007-11-02 | 2015-02-25 | Metabolon Inc. | Biomarkers for fatty liver disease and methods using the same |
| SG10201704689XA (en) | 2008-01-18 | 2017-07-28 | Harvard College | Methods of detecting signatures of disease or conditions in bodily fluids |
| CN102066943A (zh) * | 2008-04-09 | 2011-05-18 | B.R.A.H.M.S有限公司 | 用于预测受损峰值耗氧量的内皮素1原 |
| US20100222315A1 (en) * | 2008-09-24 | 2010-09-02 | Harbor BioSciencs, Inc. | Patient populations and treatment methods |
| WO2010047767A2 (en) * | 2008-10-20 | 2010-04-29 | Liposcience, Inc. | Lipoprotein insulin resistance indexes and related methods, systems and computer programs for generating same |
| EP2405806A4 (en) | 2009-03-10 | 2014-01-22 | Univ Duke | PREDICTION OF CORONARY DISEASE AND THE RISK OF CARDIOVASCULAR EVENTS |
| CN102449161A (zh) * | 2009-03-31 | 2012-05-09 | 梅塔博隆公司 | 与胰岛素抵抗有关的生物标记和使用该生物标记的方法 |
| AU2010247750B2 (en) | 2009-05-11 | 2016-09-22 | Berg Llc | Methods for treatment of metabolic disorders using epimetabolic shifters, multidimensional intracellular molecules, or environmental influencers |
| US20110059861A1 (en) * | 2009-09-08 | 2011-03-10 | Nodality, Inc. | Analysis of cell networks |
| JP5787339B2 (ja) * | 2009-12-28 | 2015-09-30 | 学校法人福岡大学 | 糖尿病前症の検査方法 |
| JP2013522652A (ja) * | 2010-03-23 | 2013-06-13 | パーデュー・リサーチ・ファウンデーション | 代謝物プロファイリングを用いた再発乳癌の早期検出 |
| KR101873193B1 (ko) | 2010-06-08 | 2018-07-02 | 아사히 그룹 홀딩스 가부시키가이샤 | 지질 대사 개선제 |
| MX2013000917A (es) | 2010-07-23 | 2013-07-05 | Harvard College | Metodos para detectar las enfermedades o condiciones usando celulas fagociticas. |
| WO2012012717A1 (en) | 2010-07-23 | 2012-01-26 | President And Fellows Of Harvard College | Methods of detecting prenatal or pregnancy-related diseases or conditions |
| EP2596116A4 (en) | 2010-07-23 | 2014-03-19 | Harvard College | METHODS FOR DETECTION OF AUTOIMMUNE OR IMMUNE-RELATED DISEASES / PATHOLOGIES |
| AU2011280996B2 (en) | 2010-07-23 | 2017-03-30 | President And Fellows Of Harvard College | Methods for detecting signatures of disease or conditions in bodily fluids |
| EP2596349B1 (en) | 2010-07-23 | 2017-12-13 | President and Fellows of Harvard College | Methods of detecting cardiovascular diseases or conditions |
| WO2012013667A1 (en) * | 2010-07-30 | 2012-02-02 | Technische Universität Graz | Analyses of analytes by mass spectrometry with values in at least 3 dimensions |
| WO2012058298A1 (en) * | 2010-10-26 | 2012-05-03 | Mayo Foundation For Medical Education And Research | Biomarkers of reduced insulin action |
| AU2011346553A1 (en) * | 2010-12-23 | 2013-07-11 | Metanomics Health Gmbh | Means and method for predicting diabetes |
| US11141063B2 (en) | 2010-12-23 | 2021-10-12 | Philips Image Guided Therapy Corporation | Integrated system architectures and methods of use |
| US11040140B2 (en) | 2010-12-31 | 2021-06-22 | Philips Image Guided Therapy Corporation | Deep vein thrombosis therapeutic methods |
| WO2012116074A1 (en) * | 2011-02-22 | 2012-08-30 | Mayo Foundation For Medical Education And Research | Biomarkers of insulin sensitivity |
| JP6092844B2 (ja) | 2011-04-04 | 2017-03-08 | バーグ エルエルシー | 中枢神経系腫瘍の治療方法 |
| WO2013002381A1 (ja) | 2011-06-30 | 2013-01-03 | 味の素株式会社 | 脂肪性肝疾患の評価方法、脂肪性肝疾患評価装置、脂肪性肝疾患評価方法、脂肪性肝疾患評価プログラム、脂肪性肝疾患評価システム、情報通信端末装置、および脂肪性肝疾患の予防・改善物質の探索方法 |
| CA2841915A1 (en) * | 2011-07-28 | 2013-01-31 | Metanomics Gmbh | Means and methods for diagnosing and monitoring heart failure in a subject |
| WO2013033592A1 (en) | 2011-08-31 | 2013-03-07 | Volcano Corporation | Optical-electrical rotary joint and methods of use |
| EP2756095A4 (en) * | 2011-09-14 | 2015-07-22 | Metabolon Inc | BIOMARKERS RELATED TO INSULIN RESISTANCE AND METHOD OF USE THEREOF |
| WO2013122469A2 (en) * | 2012-02-17 | 2013-08-22 | Rijksuniversiteit Groningen | Prediction of the efficacy of a medicament on renal or cardiovascular clinical outcomes |
| EP2642294A1 (en) * | 2012-03-22 | 2013-09-25 | Nestec S.A. | Phenylacetylglutamine as biomarker for healthy ageing |
| EP2642297A1 (en) * | 2012-03-22 | 2013-09-25 | Nestec S.A. | Hydroxy-sphingomyelin 22:1 as biomarker for healthy ageing |
| EP2642296A1 (en) * | 2012-03-22 | 2013-09-25 | Nestec S.A. | p-Cresol sulphate as biomarker for healthy ageing |
| EP2642293A1 (en) | 2012-03-22 | 2013-09-25 | Nestec S.A. | 9-oxo-octadecadienoic acid (9-oxo-HODE)as as biomarker for healthy ageing |
| EP2642295A1 (en) | 2012-03-22 | 2013-09-25 | Nestec S.A. | 1-O-alkyl-2-acylglycerophosphocholine (PC-O) 40:1 as biomarker for healthy ageing |
| US20150153353A1 (en) * | 2012-06-05 | 2015-06-04 | Nestec Sa | Methods for diagnosing chronic valvular disease |
| US9361429B2 (en) | 2012-06-08 | 2016-06-07 | Liposcience, Inc. | Multi-parameter diabetes risk evaluations |
| US9928345B2 (en) | 2012-06-08 | 2018-03-27 | Liposciences, Inc. | Multiple-marker risk parameters predictive of conversion to diabetes |
| CA2876731A1 (en) | 2012-06-15 | 2013-12-19 | Harry Stylli | Methods of detecting diseases or conditions |
| SG11201408383SA (en) | 2012-06-15 | 2015-01-29 | Harry Stylli | Methods of detecting diseases or conditions using circulating diseased cells |
| EP2867669B1 (en) | 2012-06-27 | 2016-12-21 | Metanomics Health GmbH | Methods for identifying diabetes drugs |
| DK2883058T3 (en) * | 2012-08-13 | 2018-03-26 | Helmholtz Zentrum Muenchen Deutsches Forschungszentrum Gesundheit & Umwelt Gmbh | Biomarkers for type 2 diabetes |
| US20140324460A1 (en) * | 2012-09-26 | 2014-10-30 | Health Diagnostic Laboratory, Inc. | Method for determining and managing total cardiodiabetes risk |
| JP2015532536A (ja) | 2012-10-05 | 2015-11-09 | デイビッド ウェルフォード, | 光を増幅するためのシステムおよび方法 |
| US9324141B2 (en) | 2012-10-05 | 2016-04-26 | Volcano Corporation | Removal of A-scan streaking artifact |
| US9858668B2 (en) | 2012-10-05 | 2018-01-02 | Volcano Corporation | Guidewire artifact removal in images |
| US11272845B2 (en) | 2012-10-05 | 2022-03-15 | Philips Image Guided Therapy Corporation | System and method for instant and automatic border detection |
| US10070827B2 (en) | 2012-10-05 | 2018-09-11 | Volcano Corporation | Automatic image playback |
| US9307926B2 (en) | 2012-10-05 | 2016-04-12 | Volcano Corporation | Automatic stent detection |
| US9292918B2 (en) | 2012-10-05 | 2016-03-22 | Volcano Corporation | Methods and systems for transforming luminal images |
| US10568586B2 (en) | 2012-10-05 | 2020-02-25 | Volcano Corporation | Systems for indicating parameters in an imaging data set and methods of use |
| US9286673B2 (en) | 2012-10-05 | 2016-03-15 | Volcano Corporation | Systems for correcting distortions in a medical image and methods of use thereof |
| US9367965B2 (en) | 2012-10-05 | 2016-06-14 | Volcano Corporation | Systems and methods for generating images of tissue |
| US9840734B2 (en) | 2012-10-22 | 2017-12-12 | Raindance Technologies, Inc. | Methods for analyzing DNA |
| WO2014093374A1 (en) | 2012-12-13 | 2014-06-19 | Volcano Corporation | Devices, systems, and methods for targeted cannulation |
| US10939826B2 (en) | 2012-12-20 | 2021-03-09 | Philips Image Guided Therapy Corporation | Aspirating and removing biological material |
| US11406498B2 (en) | 2012-12-20 | 2022-08-09 | Philips Image Guided Therapy Corporation | Implant delivery system and implants |
| CA2895502A1 (en) | 2012-12-20 | 2014-06-26 | Jeremy Stigall | Smooth transition catheters |
| US10942022B2 (en) | 2012-12-20 | 2021-03-09 | Philips Image Guided Therapy Corporation | Manual calibration of imaging system |
| JP2016506276A (ja) | 2012-12-20 | 2016-03-03 | ジェレミー スティガール, | 血管内画像の位置の特定 |
| EP2934310A4 (en) | 2012-12-20 | 2016-10-12 | Nathaniel J Kemp | RECONFIGURABLE OPTICAL COHERENCE TOMOGRAPHY SYSTEM BETWEEN DIFFERENT IMAGING MODES |
| US9486143B2 (en) | 2012-12-21 | 2016-11-08 | Volcano Corporation | Intravascular forward imaging device |
| US10191220B2 (en) | 2012-12-21 | 2019-01-29 | Volcano Corporation | Power-efficient optical circuit |
| US10413317B2 (en) | 2012-12-21 | 2019-09-17 | Volcano Corporation | System and method for catheter steering and operation |
| US10058284B2 (en) | 2012-12-21 | 2018-08-28 | Volcano Corporation | Simultaneous imaging, monitoring, and therapy |
| US10993694B2 (en) | 2012-12-21 | 2021-05-04 | Philips Image Guided Therapy Corporation | Rotational ultrasound imaging catheter with extended catheter body telescope |
| US9612105B2 (en) | 2012-12-21 | 2017-04-04 | Volcano Corporation | Polarization sensitive optical coherence tomography system |
| EP2936426B1 (en) | 2012-12-21 | 2021-10-13 | Jason Spencer | System and method for graphical processing of medical data |
| WO2014099760A1 (en) | 2012-12-21 | 2014-06-26 | Mai Jerome | Ultrasound imaging with variable line density |
| CA2895940A1 (en) | 2012-12-21 | 2014-06-26 | Andrew Hancock | System and method for multipath processing of image signals |
| US9383263B2 (en) | 2012-12-21 | 2016-07-05 | Volcano Corporation | Systems and methods for narrowing a wavelength emission of light |
| CN105393117A (zh) | 2013-01-31 | 2016-03-09 | 凯普里昂蛋白质组学公司 | 2型糖尿病生物标志物及其用途 |
| JP6404834B2 (ja) * | 2013-01-31 | 2018-10-17 | メタボロン,インコーポレイテッド | インスリン抵抗性の進行に関連するバイオマーカー及びこれを使用する方法 |
| WO2014125443A1 (en) * | 2013-02-14 | 2014-08-21 | Metanomics Health Gmbh | Means and methods for assessing the quality of a biological sample |
| WO2014138555A1 (en) | 2013-03-07 | 2014-09-12 | Bernhard Sturm | Multimodal segmentation in intravascular images |
| US10226597B2 (en) | 2013-03-07 | 2019-03-12 | Volcano Corporation | Guidewire with centering mechanism |
| EP4202441A3 (en) | 2013-03-09 | 2023-07-26 | Immunis.AI, Inc. | Gene expression profile in macrophages for the diagnosis of cancer |
| EP3385717A3 (en) | 2013-03-09 | 2018-10-24 | Harry Stylli | Methods of detecting prostate cancer |
| US10638939B2 (en) | 2013-03-12 | 2020-05-05 | Philips Image Guided Therapy Corporation | Systems and methods for diagnosing coronary microvascular disease |
| US11154313B2 (en) | 2013-03-12 | 2021-10-26 | The Volcano Corporation | Vibrating guidewire torquer and methods of use |
| US11026591B2 (en) | 2013-03-13 | 2021-06-08 | Philips Image Guided Therapy Corporation | Intravascular pressure sensor calibration |
| EP2967488B1 (en) | 2013-03-13 | 2021-06-16 | Jinhyoung Park | System for producing an image from a rotational intravascular ultrasound device |
| US20140278121A1 (en) * | 2013-03-13 | 2014-09-18 | Robust for Life, Inc. | Systems and methods for network-based calculation and reporting of metabolic risk |
| US9301687B2 (en) | 2013-03-13 | 2016-04-05 | Volcano Corporation | System and method for OCT depth calibration |
| WO2014152365A2 (en) | 2013-03-14 | 2014-09-25 | Volcano Corporation | Filters with echogenic characteristics |
| US10219887B2 (en) | 2013-03-14 | 2019-03-05 | Volcano Corporation | Filters with echogenic characteristics |
| US10292677B2 (en) | 2013-03-14 | 2019-05-21 | Volcano Corporation | Endoluminal filter having enhanced echogenic properties |
| SG11201508272YA (en) | 2013-04-08 | 2015-11-27 | Berg Llc | Treatment of cancer using coenzyme q10 combination therapies |
| US10475536B2 (en) | 2013-07-18 | 2019-11-12 | True Health Ip Llc | Method of determination of risk of 2 hour blood glucose equal to or greater than 140 mg/dL |
| EA034143B1 (ru) | 2013-09-04 | 2020-01-09 | Берг Ллк | Способы лечения рака непрерывной инфузией кофермента q10 |
| GB2524230A (en) * | 2014-02-14 | 2015-09-23 | Asda Stores Ltd | Transaction processing system and transaction processing method |
| EP4075139A1 (en) | 2014-09-11 | 2022-10-19 | Harry Stylli | Methods of detecting prostate cancer |
| JP6401297B2 (ja) * | 2014-12-25 | 2018-10-10 | 株式会社日立製作所 | インスリン分泌能分析装置、当該装置を備えるインスリン分泌能分析システム及びインスリン分泌能分析方法 |
| HUE047951T2 (hu) * | 2015-01-09 | 2020-05-28 | Global Genomics Group Llc | Vér alapú biomarkerek atheroszklerotikus koszorúsér betegség diagnosztizálására |
| WO2016149220A1 (en) | 2015-03-13 | 2016-09-22 | Duke University | Compositions and methods for metabolic profiling in subjects with heart failure with preserved ejection fraction |
| JP6051258B2 (ja) * | 2015-04-15 | 2016-12-27 | ライオン株式会社 | 脂質異常症への罹患しやすさを試験する方法 |
| KR101795689B1 (ko) * | 2015-04-30 | 2017-11-30 | 경희대학교 산학협력단 | 혈관 협착 질환 진단용 마커 및 이의 용도 |
| WO2018094204A1 (en) * | 2016-11-17 | 2018-05-24 | Arivale, Inc. | Determining relationships between risks for biological conditions and dynamic analytes |
| US11881311B1 (en) | 2017-02-17 | 2024-01-23 | BioAge Labs, Inc. | Survival prediction using metabolomic profiles |
| JP2018141728A (ja) * | 2017-02-28 | 2018-09-13 | トヨタ自動車株式会社 | 生活習慣病の診断方法 |
| AU2018371776A1 (en) * | 2017-11-22 | 2020-05-28 | Mayo Foundation For Medical Education And Research | Methods and materials for assessing and treating obesity |
| US20200041496A1 (en) * | 2018-08-01 | 2020-02-06 | Joshua Health Care LLC | Methods for Identifying and Treating Mammalian Subjects with Insulin Resistance |
| JP7189537B2 (ja) * | 2019-06-27 | 2022-12-14 | サンスター株式会社 | 血液試料の酸化hdl量の反映値を測定する工程を含む、測定方法 |
| EP3997980A4 (en) * | 2019-07-08 | 2023-06-21 | Shimadzu Corporation | TRANSPLANT ORGAN FUNCTIONAL EVALUATION METHOD, TRANSPLANT ORGAN FUNCTIONAL EVALUATION PROGRAM AND TRANSPLANT ORGAN FUNCTIONAL EVALUATION DEVICE |
| EP4100541A1 (en) * | 2020-02-05 | 2022-12-14 | The Cleveland Clinic Foundation | Disease detection and treatment based on phenylacetyl glutamine levels |
| CN113866284B (zh) * | 2020-06-30 | 2023-09-05 | 上海脉示生物技术有限公司 | 一组用于心力衰竭诊断的肠道微生物代谢标志物及其应用 |
| CN112684064B (zh) * | 2020-12-08 | 2022-05-17 | 安徽农业大学 | 用于筛选抗应激胁迫肉羊的血清代谢标志物及其应用 |
| CN113325117B (zh) * | 2021-06-25 | 2022-07-15 | 中国医学科学院北京协和医院 | 一组生物标记物在制备预测静脉内平滑肌瘤病进展的试剂盒中的应用 |
| WO2023097510A1 (zh) * | 2021-11-30 | 2023-06-08 | 江苏品生医疗科技集团有限公司 | 预测受试者患有糖尿病的可能性的标记物及其应用 |
| WO2023147522A1 (en) * | 2022-01-28 | 2023-08-03 | GATC Health Corp | Biomarkers for early detection of diabetes |
| CN114965733B (zh) * | 2022-04-07 | 2023-12-01 | 中国人民解放军总医院第一医学中心 | 结直肠进展期腺瘤诊断代谢标志物组合及其应用 |
Family Cites Families (33)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5367052A (en) * | 1987-04-27 | 1994-11-22 | Amylin Pharmaceuticals, Inc. | Amylin peptides |
| CA2218488A1 (en) | 1996-02-20 | 1997-08-28 | Kyowa Hakko Kogyo Co., Ltd. | Method for quantitative determination of 1,5-anhydroglucitol |
| JP2938048B1 (ja) * | 1998-06-30 | 1999-08-23 | 技術研究組合医療福祉機器研究所 | 代謝機能測定装置 |
| US6140067A (en) | 1999-04-30 | 2000-10-31 | Mitokor | Indicators of altered mitochondrial function in predictive methods for determining risk of type 2 diabetes mellitus |
| JP3975279B2 (ja) * | 1999-11-01 | 2007-09-12 | 旭化成ファーマ株式会社 | 糖尿病予備群の検査方法 |
| JP2003530130A (ja) | 2000-04-14 | 2003-10-14 | メタボロン インコーポレイテッド | メタボロミクスを使用した薬物発見、疾患の処置、及び診断のための方法 |
| US7329489B2 (en) | 2000-04-14 | 2008-02-12 | Matabolon, Inc. | Methods for drug discovery, disease treatment, and diagnosis using metabolomics |
| NZ524519A (en) * | 2000-08-07 | 2004-09-24 | Ranbaxy Signature Llc | Liquid formulation of metformin |
| WO2002098355A2 (en) * | 2001-06-01 | 2002-12-12 | Clingenix, Inc. | Methods and reagents for diagnosis and treatment of insulin resistance and related conditions |
| US7425545B2 (en) | 2001-07-25 | 2008-09-16 | Isis Pharmaceuticals, Inc. | Modulation of C-reactive protein expression |
| JP4100673B2 (ja) * | 2001-12-07 | 2008-06-11 | 日本化薬株式会社 | 肝糖放出の検査方法 |
| JP2003204800A (ja) * | 2002-01-15 | 2003-07-22 | Sumitomo Pharmaceut Co Ltd | 糖代謝異常疾患マーカーおよびその利用 |
| US20040101874A1 (en) | 2002-04-12 | 2004-05-27 | Mitokor Inc. | Targets for therapeutic intervention identified in the mitochondrial proteome |
| AU2003246644A1 (en) * | 2002-07-08 | 2004-01-23 | Genova, Ltd. | Secreted peptides |
| JP2005006645A (ja) * | 2003-05-22 | 2005-01-13 | Sumitomo Chemical Co Ltd | インスリン応答性の評価方法 |
| WO2005094200A2 (en) * | 2003-06-20 | 2005-10-13 | University Of Florida | Biomarkers for differentiating between type 2 and type 2 diabetes |
| US7345142B2 (en) * | 2004-01-27 | 2008-03-18 | Compugen Ltd. | Nucleotide and amino acid sequences, and assays and methods of use thereof for diagnosis of cardiac disease |
| JP4547173B2 (ja) * | 2004-03-17 | 2010-09-22 | シスメックス株式会社 | 糖尿病診療支援システム |
| JP4533042B2 (ja) * | 2004-08-25 | 2010-08-25 | 裕 笹川 | 糖尿病および糖代謝異常を判断する方法 |
| US20080261317A1 (en) * | 2004-09-07 | 2008-10-23 | Fifer Michael A | Methods of Detecting Myocardial Ischemia and Myocardial Infarction |
| JP4522222B2 (ja) * | 2004-10-22 | 2010-08-11 | 扶桑薬品工業株式会社 | 血中脂肪酸濃度測定による心疾患の早期診断方法 |
| WO2006063733A1 (en) * | 2004-12-14 | 2006-06-22 | F.Hoffmann-La Roche Ag | Cd99 as target/marker for insulin resistance |
| US20070026458A1 (en) * | 2004-12-17 | 2007-02-01 | Entelos, Inc. | Assessing insulin resistance using biomarkers |
| WO2006073195A1 (ja) * | 2005-01-07 | 2006-07-13 | Biomarker Science Co., Ltd | 糖尿病の予知・診断方法および糖尿病予知・診断用キット |
| FR2890079B1 (fr) * | 2005-08-26 | 2007-11-30 | Alain Rambach | Detection des salmonelles lactose + |
| AU2006294565A1 (en) * | 2005-09-30 | 2007-04-05 | Perlegen Sciences, Inc. | Methods and compositions for screening and treatment of disorders of blood glucose regulation |
| AU2006302031A1 (en) * | 2005-10-11 | 2007-04-19 | Tethys Bioscience, Inc. | Diabetes-associated markers and methods of use thereof |
| JP2007127423A (ja) * | 2005-10-31 | 2007-05-24 | Toray Ind Inc | 3−ヒドロキシ酪酸の測定方法およびキット |
| CA2647197A1 (en) * | 2006-03-24 | 2007-10-04 | Metanomics Gmbh | Means and method for predicting diabetes |
| EP2293077B1 (en) * | 2007-03-26 | 2014-05-14 | BG Medicine, Inc. | Methods for detecting coronary artery disease |
| MX2010000414A (es) * | 2007-07-17 | 2010-04-01 | Metabolon Inc | Biomarcadores para prediabetes, enfermedades cardiovasculares y otros trastornos relacionados con sindrome metabolico, y metodos de uso de los mismos. |
| CN102449161A (zh) * | 2009-03-31 | 2012-05-09 | 梅塔博隆公司 | 与胰岛素抵抗有关的生物标记和使用该生物标记的方法 |
| AU2011346553A1 (en) * | 2010-12-23 | 2013-07-11 | Metanomics Health Gmbh | Means and method for predicting diabetes |
-
2008
- 2008-07-17 MX MX2010000414A patent/MX2010000414A/es active IP Right Grant
- 2008-07-17 US US12/218,980 patent/US8187830B2/en active Active
- 2008-07-17 AU AU2008279778A patent/AU2008279778B2/en active Active
- 2008-07-17 MX MX2013008169A patent/MX341954B/es unknown
- 2008-07-17 EP EP08780229.4A patent/EP2164977B1/en active Active
- 2008-07-17 BR BRPI0815095-8A patent/BRPI0815095B1/pt active IP Right Grant
- 2008-07-17 WO PCT/US2008/008756 patent/WO2009014639A2/en active Search and Examination
- 2008-07-17 JP JP2010517019A patent/JP5701601B2/ja active Active
- 2008-07-17 CA CA2690541A patent/CA2690541A1/en not_active Abandoned
- 2008-07-17 ES ES08780229.4T patent/ES2443540T3/es active Active
-
2010
- 2010-09-21 HK HK10109028.5A patent/HK1142636A1/xx unknown
-
2012
- 2012-04-27 US US13/457,620 patent/US8546098B2/en active Active
-
2013
- 2013-08-14 US US13/966,475 patent/US8809008B2/en active Active
-
2014
- 2014-07-07 US US14/324,689 patent/US9250225B2/en active Active
- 2014-10-27 JP JP2014218116A patent/JP5876918B2/ja active Active
-
2015
- 2015-12-03 JP JP2015236454A patent/JP2016102797A/ja active Pending
- 2015-12-21 US US14/975,988 patent/US10175233B2/en active Active
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016102797A (ja) * | 2007-07-17 | 2016-06-02 | メタボロン インコーポレイテッド | 糖尿病前症、心血管疾患及びその他のメタボリックシンドローム関連障害のバイオマーカー並びにその使用方法 |
| US10175233B2 (en) | 2007-07-17 | 2019-01-08 | Metabolon, Inc. | Biomarkers for cardiovascular diseases and methods using the same |
Also Published As
| Publication number | Publication date |
|---|---|
| US20090155826A1 (en) | 2009-06-18 |
| AU2008279778A1 (en) | 2009-01-29 |
| US8546098B2 (en) | 2013-10-01 |
| AU2008279778B2 (en) | 2014-09-18 |
| US20130338031A1 (en) | 2013-12-19 |
| EP2164977A4 (en) | 2011-07-27 |
| MX341954B (es) | 2016-09-08 |
| US20160178620A1 (en) | 2016-06-23 |
| BRPI0815095A2 (pt) | 2017-05-09 |
| EP2164977B1 (en) | 2013-10-30 |
| ES2443540T3 (es) | 2014-02-19 |
| WO2009014639A2 (en) | 2009-01-29 |
| US8809008B2 (en) | 2014-08-19 |
| WO2009014639A3 (en) | 2009-03-19 |
| EP2164977A2 (en) | 2010-03-24 |
| US20150005195A1 (en) | 2015-01-01 |
| BRPI0815095B1 (pt) | 2021-04-13 |
| HK1142636A1 (en) | 2010-12-10 |
| US10175233B2 (en) | 2019-01-08 |
| JP5876918B2 (ja) | 2016-03-02 |
| MX2010000414A (es) | 2010-04-01 |
| JP2016102797A (ja) | 2016-06-02 |
| JP2015064362A (ja) | 2015-04-09 |
| JP2010537157A (ja) | 2010-12-02 |
| US20120208215A1 (en) | 2012-08-16 |
| CA2690541A1 (en) | 2009-01-29 |
| US8187830B2 (en) | 2012-05-29 |
| US9250225B2 (en) | 2016-02-02 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5876918B2 (ja) | 糖尿病前症、心血管疾患及びその他のメタボリックシンドローム関連障害のバイオマーカー並びにその使用方法 | |
| JP6404834B2 (ja) | インスリン抵抗性の進行に関連するバイオマーカー及びこれを使用する方法 | |
| US20120122981A1 (en) | Biomarkers Related to Insulin Resistance and Methods using the Same | |
| Klein et al. | Decreased plasma levels of select very long chain ceramide species are associated with the development of nephropathy in type 1 diabetes | |
| JP6158186B2 (ja) | インスリン抵抗性に関連するバイオマーカーおよびそれを使用する方法 | |
| TW201802471A (zh) | 用於診斷冠狀動脈粥樣硬化症之以血液為主的生物標記 | |
| US10475536B2 (en) | Method of determination of risk of 2 hour blood glucose equal to or greater than 140 mg/dL | |
| AU2014216035B2 (en) | Method for Determining Insulin Sensitivity with Biomarkers | |
| AU2016206265A1 (en) | Method for Determining Insulin Sensitivity with Biomarkers | |
| Grau et al. | Lipidomic Profiling in Clinical Practice Using LC-MS Check for updates |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110715 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20110715 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110804 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130723 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20131023 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20140627 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20141027 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20141028 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20141119 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20150210 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20150218 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5701601 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |