JP5572157B2 - Nos阻害活性を有するベンゾオキサジン類、ベンゾチアジン類、および関係化合物 - Google Patents
Nos阻害活性を有するベンゾオキサジン類、ベンゾチアジン類、および関係化合物 Download PDFInfo
- Publication number
- JP5572157B2 JP5572157B2 JP2011515041A JP2011515041A JP5572157B2 JP 5572157 B2 JP5572157 B2 JP 5572157B2 JP 2011515041 A JP2011515041 A JP 2011515041A JP 2011515041 A JP2011515041 A JP 2011515041A JP 5572157 B2 JP5572157 B2 JP 5572157B2
- Authority
- JP
- Japan
- Prior art keywords
- carbon atoms
- optionally substituted
- alkyl
- group
- alkaryl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 0 C1Nc2ccccc2*1 Chemical compound C1Nc2ccccc2*1 0.000 description 5
- KVJVXERVBNBTLK-UHFFFAOYSA-N CCN(CC)CCN1c(ccc(NC(c2ccc[s]2)=N)c2)c2SCC1 Chemical compound CCN(CC)CCN1c(ccc(NC(c2ccc[s]2)=N)c2)c2SCC1 KVJVXERVBNBTLK-UHFFFAOYSA-N 0.000 description 2
- ROUYFJUVMYHXFJ-UHFFFAOYSA-N CC(C)(C)OC(N(CC1)CCC1=O)=O Chemical compound CC(C)(C)OC(N(CC1)CCC1=O)=O ROUYFJUVMYHXFJ-UHFFFAOYSA-N 0.000 description 1
- YMDNODNLFSHHCV-UHFFFAOYSA-N CCN(CC)CCCl Chemical compound CCN(CC)CCCl YMDNODNLFSHHCV-UHFFFAOYSA-N 0.000 description 1
- GVFWAVKNJJSSHM-UHFFFAOYSA-N CCN(CC)CCN1c(ccc(N)c2)c2SCC1 Chemical compound CCN(CC)CCN1c(ccc(N)c2)c2SCC1 GVFWAVKNJJSSHM-UHFFFAOYSA-N 0.000 description 1
- OGYJREJPTXNVJN-UHFFFAOYSA-N CCN(CC)CCN1c(ccc([N+]([O-])=O)c2)c2SCC1 Chemical compound CCN(CC)CCN1c(ccc([N+]([O-])=O)c2)c2SCC1 OGYJREJPTXNVJN-UHFFFAOYSA-N 0.000 description 1
- OLTLUEQWMQJCNC-UHFFFAOYSA-N CN(C)CCN1c(ccc(N)c2)c2OCC1=O Chemical compound CN(C)CCN1c(ccc(N)c2)c2OCC1=O OLTLUEQWMQJCNC-UHFFFAOYSA-N 0.000 description 1
- CRJHJFJTZNXGPF-UHFFFAOYSA-N CN(C)CCN1c(ccc(NC(c2ccc[s]2)=N)c2)c2OCC1=O Chemical compound CN(C)CCN1c(ccc(NC(c2ccc[s]2)=N)c2)c2OCC1=O CRJHJFJTZNXGPF-UHFFFAOYSA-N 0.000 description 1
- BEZSHGLTJKYZBW-UHFFFAOYSA-N CN(C)CCN1c(ccc([N+]([O-])=O)c2)c2OCC1=O Chemical compound CN(C)CCN1c(ccc([N+]([O-])=O)c2)c2OCC1=O BEZSHGLTJKYZBW-UHFFFAOYSA-N 0.000 description 1
- LYWNQLCSOFZLOR-UHFFFAOYSA-N Nc(c(F)c1)cc([N+]([O-])=O)c1F Chemical compound Nc(c(F)c1)cc([N+]([O-])=O)c1F LYWNQLCSOFZLOR-UHFFFAOYSA-N 0.000 description 1
- YWXLKZLOQSJCJN-UHFFFAOYSA-N Nc(c(SCCO)c1)cc([N+]([O-])=O)c1F Chemical compound Nc(c(SCCO)c1)cc([N+]([O-])=O)c1F YWXLKZLOQSJCJN-UHFFFAOYSA-N 0.000 description 1
- YVGHCFMAEHXPBH-UHFFFAOYSA-N [O-][N+](c(cc1OC2)ccc1NC2=O)=O Chemical compound [O-][N+](c(cc1OC2)ccc1NC2=O)=O YVGHCFMAEHXPBH-UHFFFAOYSA-N 0.000 description 1
- LCOAYUPAESYAHF-UHFFFAOYSA-N [O-][N+](c1ccc2NCCSc2c1)=O Chemical compound [O-][N+](c1ccc2NCCSc2c1)=O LCOAYUPAESYAHF-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing three or more hetero rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
- A61K31/5375—1,4-Oxazines, e.g. morpholine
- A61K31/538—1,4-Oxazines, e.g. morpholine ortho- or peri-condensed with carbocyclic ring systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/54—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one sulfur as the ring hetero atoms, e.g. sulthiame
- A61K31/5415—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one sulfur as the ring hetero atoms, e.g. sulthiame ortho- or peri-condensed with carbocyclic ring systems, e.g. phenothiazine, chlorpromazine, piroxicam
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/02—Drugs for disorders of the nervous system for peripheral neuropathies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/04—Centrally acting analgesics, e.g. opioids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/06—Antimigraine agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/08—Antiepileptics; Anticonvulsants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
- A61P25/16—Anti-Parkinson drugs
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/18—Antipsychotics, i.e. neuroleptics; Drugs for mania or schizophrenia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/22—Anxiolytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/24—Antidepressants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/30—Drugs for disorders of the nervous system for treating abuse or dependence
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02A—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE
- Y02A50/00—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE in human health protection, e.g. against extreme weather
- Y02A50/30—Against vector-borne diseases, e.g. mosquito-borne, fly-borne, tick-borne or waterborne diseases whose impact is exacerbated by climate change
Description
QはO-(CHR6)1-3またはS-(CHR6)1-3であり;
R1およびそれぞれのR6は、独立して、H、任意に置換されたC1-6アルキル、任意に置換されたC1-4アルカリール、任意に置換されたC1-4アルクヘテロシクリル、任意に置換されたC2-9ヘテロシクリル、任意に置換されたC3-8シクロアルキル、任意に置換されたC1-4アルクシクロアルキルまたは-(CR1AR1B)nNR1CR1Dであり;
R1AおよびR1Bは、独立して、H、ヒドロキシ、ハロ(例えば、フルオロ)、任意に置換されたC1-6アルキル、任意に置換されたC1-6アルコキシ、任意に置換されたC1-4アルクシクロアルキル、任意に置換されたC1-4アルカリール、任意に置換されたC1-4アルクヘテロシクリル、任意に置換されたC1-4アルクヘテロアリール、任意に置換されたC3-8シクロアルキル、または任意に置換されたC2-9ヘテロシクリルであるか、またはR1AおよびR1Bは一緒に=Oを形成し;
R1CおよびR1Dは、独立して、H、ヒドロキシ、任意に置換されたC1-6アルキル、任意に置換されたC1-6アルコキシ、任意に置換されたC1-4アルクシクロアルキル、任意に置換されたC1-4アルカリール、任意に置換されたC1-4アルクヘテロシクリル、任意に置換されたC1-4アルクヘテロアリール、任意に置換されたC3-8シクロアルキル、任意に置換されたC2-9ヘテロシクリル、もしくはN-保護基であるか、またはR1CおよびR1Dは一緒に任意に置換されたC2-9ヘテロシクリルもしくはN-保護基を形成し;
nは整数1〜6であり;
R2およびR3のそれぞれは、独立して、H、hal、任意に置換されたC1-6アルキル、任意に置換されたC6-10アリール、任意に置換されたC1-6アルカリール、任意に置換されたC2-9ヘテロシクリル、ヒドロキシ、任意に置換されたC1-6アルコキシ、任意に置換されたC1-6チオアルコキシ、(CH2)r2NHC(NH)R2A、または(CH2)r2NHC(S)NHR2A、または任意に置換されたC1-4アルクヘテロシクリルであり、
ここで、r2は整数0〜2であり、R2Aは任意に置換されたC1-6アルキル、任意に置換されたC6-10アリール、任意に置換されたC1-4アルカリール、任意に置換されたC2-9ヘテロシクリル、任意に置換されたC1-4アルクヘテロシクリル、任意に置換されたC1-6チオアルコキシ、任意に置換されたC1-4チオアルカリール、任意に置換されたアリーロイル、任意に置換されたC1-4チオアルクヘテロシクリル、または任意に置換されたアミノであり;
R4およびR5のそれぞれは独立してH、hal、(CH2)r2NHC(NH)R2A、または(CH2)r2NHC(S)NHR2Aであり;
ここで、Y1およびY2はそれぞれHであるかまたはY1およびY2は一緒に=Oであるか、またはY1およびY2は独立してH、任意に置換されたC1-6アルキル、任意に置換されたC6-10アリール、任意に置換されたC1-6アルカリール、任意に置換されたC2-9ヘテロシクリル、ヒドロキシ、任意に置換されたC1-6アルコキシ、任意に置換されたC1-6チオアルコキシ、または任意に置換されたC1-4アルクヘテロシクリルであり;
ここで、R2、R3、R4、およびR5のうちの1つだけは(CH2)r2NHC(NH)R2Aまたは(CH2)r2NHC(S)NHR2Aである]
を有する化合物またはその製薬上許容される塩またはプロドラッグを特徴とする。
X1、X2、X4、およびX5のそれぞれは独立してO、S、NR7、N、またはCR8から選択され;X3はNまたはCから選択され;
R7はH、任意に置換されたC1-6アルキル、またはN-保護基であり;
R8はH、hal、任意に置換されたC1-6アルキル、ヒドロキシ、任意に置換されたC1-6アルコキシ、または任意に置換されたC1-6チオアルコキシであり、
ここで、X1、X2、X4、およびX5の少なくとも1つはCR8でない。特に、R2Aは式:
本発明はまた、式(I)の化合物、またはその製薬上許容される塩またはプロドラッグ、および製薬上許容される賦形剤を含む医薬組成物を特徴とする。
「アシル」または「アルカノイル」という用語は、本明細書において互換的に使用されるが、本明細書に記載されているようなカルボニル基を介して親分子基に結合している本明細書に記載されているようなアルキル基または水素を表し、ホルミル、アセチル、プロピオニル、ブタノイルなどによって例示される。例示的な非置換アシル基は、2〜7個の炭素を含む。
「アミノアルキル」という用語は、本明細書で使用する場合、アミノ基で置換されている本明細書に記載されているようなアルキル基を表す。
式中、
F'は、-CH2-、-CH2O-および-O-からなる群から選択され、G'は、-C(O)-および-(C(R')(R''))V-(式中、R'およびR''の各々は、独立に、水素または1〜4個の炭素原子のアルキルからなる群から選択され、vは、1〜3である)からなる群から選択され、1,3-ベンゾジオキソリル、1,4-ベンゾジオキサニルなどの基を含む。本明細書において記載される複素環基のいずれかは、(1)1〜6個の炭素原子のアルカノイル;(2)1〜6個の炭素原子のアルキル;(3)1〜6個の炭素原子のアルコキシ;(4)アルコキシアルキル(アルキルおよびアルキレン基は、独立に、1〜6個の炭素原子のアルキルおよびアルキレン基である);(5)1〜6個の炭素原子のアルキルスルフィニル;(6)アルキルスルフィニルアルキル(アルキルおよびアルキレン基は、独立に、1〜6個の炭素原子のアルキルおよびアルキレン基である);(7)1〜6個の炭素原子のアルキルスルホニル;(8)アルキルスルホニルアルキル(アルキルおよびアルキレン基は、独立に、1〜6個の炭素原子のアルキルおよびアルキレン基である);(9)アリール;(10)アミノ;(11)1〜6個の炭素原子のアミノアルキル;(12)ヘテロアリール;(13)アルカリール(アルキレン基は、1〜6個の炭素原子のアルキレン基である);(14)アリーロイル;(15)アジド;(16)1〜6個の炭素原子のアジドアルキル;(17)カルボキシアルデヒド;(18)(カルボキシアルデヒド)アルキル(アルキレン基は、1〜6個の炭素原子のアルキレン基である);(19)3〜8個の炭素原子のシクロアルキル;(20)アルクシクロアルキル(シクロアルキル基は、3〜8個の炭素原子のシクロアルキル基であり、アルキレン基は、1〜10個の炭素原子のアルキレン基である);(21)ハロ;(22)1〜6個の炭素原子のハロアルキル;(23)ヘテロシクリル;(24)(ヘテロシクリル)オキシ;(25)(ヘテロシクリル)オイル;(26)ヒドロキシ;(27)1〜6個の炭素原子のヒドロキシアルキル;(28)ニトロ;(29)1〜6個の炭素原子のニトロアルキル;(30)N-保護アミノ;(31)N-保護アミノアルキル(アルキレン基は、1〜6個の炭素原子のアルキレン基である);(32)オキソ;(33)1〜6個の炭素原子のチオアルコキシ;(34)チオアルコキシアルキル(アルキルおよびアルキレン基は、独立に、1〜6個の炭素原子のアルキルおよびアルキレン基である);(35)-(CH2)qCO2RA(qは、0〜4の整数であり、RAは、(a)アルキル、(b)アリール、(c)アルカリール、および(d)水素(アルキレン基は、1〜6個の炭素原子のアルキレン基である)からなる群から選択される);(36)-(CH2)qCONRBRC(qは、0〜4の整数であり、RBおよびRCは、(a)水素、(b)アルキル、(c)アリール、および(d)アルカリール(アルキレン基は、1〜6個の炭素原子のアルキレン基である)からなる群から独立に選択される);(37)-(CH2)qSO2RD(qは、0〜4の整数であり、RDは、(a)アルキル、(b)アリール、および(c)アルカリール(アルキレン基は、1〜6個の炭素原子のアルキレン基である)からなる群から選択される);(38)-(CH2)qSO2NRERF(qは、0〜4の整数であり、REおよびRFの各々は、独立に、(a)水素、(b)アルキル、(c)アリール、および(d)アルカリール(アルキレン基は、1〜6個の炭素原子のアルキレン基である)からなる群から選択される);(39)-(CH2)qNRGRH(qは、0〜4の整数であり、RGおよびRHの各々は、独立に、(a)水素;(b)N-保護基;(c)1〜6個の炭素原子のアルキル;(d)2〜6個の炭素原子のアルケニル;(e)2〜6個の炭素原子のアルキニル;(f)アリール;(g)アルカリール(アルキレン基は、1〜6個の炭素原子のアルキレン基である);(h)3〜8個の炭素原子のシクロアルキル;および(i)アルクシクロアルキル(シクロアルキル基は、3〜8個の炭素原子のシクロアルキル基であり、アルキレン基は、1〜10個の炭素原子のアルキレン基である)からなる群から選択され、一実施形態では、2つの基は、カルボニル基またはスルホニル基を介して窒素原子に結合していない);(40)チオール;(41)ペルフルオロアルキル;(42)ペルフルオロアルコキシ;(43)アリールオキシ;(44)シクロアルコキシ;(45)シクロアルキルアルコキシ;および(46)アリールアルコキシからなる群から独立に選択される、1個、2個、3個、4個または5個の置換基で任意選択で置換されている場合がある。
本発明の化合物は、当技術分野で確立されているものと類似のプロセスにより、例えば、スキーム1〜5に示した反応順序により調製することができる。一般スキームで用いた番号系は、本明細書または請求の範囲の随所で使用されているものと必ずしも対応しない。
本発明は、単独または他の治療物質と組み合わせた治療方法における使用、NOS活性、例えば、nNOSを阻害するための組成物におけるそれらの使用、診断アッセイにおけるそれらの使用、および研究道具としてのそれらの使用を含めた、本発明の化合物についての全ての使用を特徴とする。
NO放出剤である少量のニトログリセリンが激しい頭痛をもたらすというAsciano Sobrero(1847)による最初の観察は、片頭痛の一酸化窒素仮説を導く(Olesenら、Cephalagia、15:94〜100、1995)。片頭痛の治療において臨床的に使用されるスマトリプタンなどのセロトニン作動性5HT1D/1Bアゴニストは、片頭痛発作の間の滑沢脳(lissencephalic)および皺脳(gycencephalic)における皮質拡延性抑制(NOの広範囲に及ぶ放出をもたらす過程である)を防止することが知られている。実際に、ラットにおけるニトログリセリンの注入後に、スマトリプタンは人為的に増強した皮質のNOレベルを変更することが示された(Readら、Brain Res.847:1〜8、1999;同書、870(1〜2):44〜53、2000)。片頭痛についてのヒト無作為二重盲検臨床試験において、L-NG塩酸メチルアルギニン(L-NMMA、NOS阻害剤)の単回のi.v.投与後に67%の反応率が観察された。中大脳動脈において経頭蓋ドップラーによって決定する速度について作用が観察されなかったため、作用はeNOSを介する単純な血管収縮によるものではなかった(Lassenら、Lancet349:401〜402、1997)。最近の急性片頭痛を治療する適応臨床試験設計において、5〜180mgの用量の選択的iNOS阻害剤GW274150の投与は、治療後2時間に疼痛が無くなる被験者の比率で表して、プラセボと異ならなかった。片頭痛予防の臨床試験において評価した同じ化合物(毎日120mg、12週間)も、片頭痛発作の頻度を低減するのに無効であった(Hoye et al. Cephalalgia, 2009, 29, 132)。しかしながら、NOスカベンジャーであるヒドロキシコバラミンを使用したオープンパイロット試験において、50%の片頭痛発作頻度の減少が患者の53%において観察され、片頭痛発作の全持続時間の減少もまた観察された(van der Kuyら、Cephalgia22(7):513〜519、2002)。臨床試験の結果は、iNOSまたはeNOSは片頭痛頭痛の発生に有意な役割を果たさないことを示唆し、むしろnNOSが片頭痛頭痛に重要なイソ型であることを示している。本発明の化合物(例えば、式(I)の化合物、例えば、(1)〜(33)の化合物)も片頭痛予防用に使用することができる。
臨床試験によって、患者の75%もが片頭痛発作の間に皮膚アロディニア(誇張された皮膚感受性)を発生し、片頭痛の間のその発生は、トリプタン5HT1B/1Dアゴニストの抗片頭痛作用に対して有害であることが示された(Bursteinら、Ann.Neurol.47:614〜624、2000;Bursteinら、Brain、123:1703〜1709、2000)。スマトリプタンなどのトリプタンの早期投与は、片頭痛の痛みを終わらせることができる一方、スマトリプタン後期介入は、すでにアロディニアと関係がある片頭痛患者において片頭痛の痛みを終わらせること、または過度の皮膚感受性を逆転させることができない(Bursteinら、Ann.Neurol.DOI:10.1002/ana.10785、2003;BursteinおよびJakubowski、Ann.Neurol.、55:27〜36、2004)。末梢および中枢感作の発生は、片頭痛の臨床症状と相関する。片頭痛患者において、頭痛の開始後5〜20分で拍動が起こり、一方20〜120分で皮膚アロディニアが始まる(Bursteinら、Brain、123:1703〜1709、2000)。ラットにおいて、髄膜侵害受容器の実験的に誘発された末梢感作は、硬膜に炎症性スープ(inflammatory soup)(I.S.)を施した後5〜20分以内に起こり(LevyおよびStrassman、J.Physiol、538:483〜493、2002)、一方では、三叉神経血管ニューロンの中枢感作は、I.S.投与後20〜120分に発生する(Bursteinら、J.Neurophysiol.79:964〜982、1998)。スマトリプタンなどの抗片頭痛薬トリプタンの早期または後期投与が中枢感作の発生に与える類似する作用は、ラットにおいて示されてきた(BursteinおよびJakubowski、上記を参照されたい)。したがって、後期ではなく早期のスマトリプタンは、中枢三叉神経血管ニューロンにおいて見出されるI.S.が誘発する自発運動の長期に亘る増加を防止する(片頭痛強度の臨床的相関)。さらに、ラットにおけるスマトリプタン後期介入は、眼窩周囲皮膚における機械的刺激に対するI.S.が誘発するニューロン感受性を防止せず、熱に対する閾値を減少させなかった(眼窩周囲領域における機械的および熱アロディニアを有する患者の臨床的相関)。対照的に、早期スマトリプタンは、I.S.が熱および機械的過敏性の両方を誘発することを防止した。中枢感作の発生後、スマトリプタンの後期介入は、硬膜の受容野の拡大を逆行させ、硬膜の陥入に対する感受性が増加し(かがむことによって悪化する痛みの拍動の臨床的相関)、一方、早期介入はその発生を防止する。
NOは、末梢神経系(Aleyら、J.Neurosci.1:7008〜7014、1998)および中枢神経系(MellerおよびGebhart、Pain52:127〜136、1993)における感覚伝達の一因となる。実験上の実質的な証拠は、末梢からの長引く侵害受容によって生じた中枢感作が、CNSにおいてニューロンの興奮性を増加させ、NOS活性化およびNO合成の増加に起因する、または関連することを示す(Bendtsen、Cephalagia20:486〜508、2000;WoolfおよびSalter、Science288:1765〜1769、2000)。NO供与体であるグリセリルトリニトレートの実験的注入は、患者において頭痛を誘発することが示された。二重盲検試験において、L-NMMA(NOS阻害剤)を投与されている慢性緊張型頭痛を有する患者では、頭痛強度が有意に減少した(AshinaおよびBendtsen、J.Headache Pain2:21〜24、2001;Ashinaら、Lancet243(9149):287〜9、1999)。したがって、本発明のNOS阻害剤は、慢性緊張型頭痛の治療において有用である可能性がある。
ヒトにおいて、NOは皮内注射で疼痛を惹起し(HolthusenおよびArndt、Neurosci.Lett.165:71〜74、1994)、したがって疼痛におけるNOの直接の関与が示される。さらに、NOS阻害剤は、通常条件下で侵害受容伝達に対しての作用が殆どまたは全くない(MellerおよびGebhart、Pain52:127〜136、1993)。NOは、末梢、脊髄および脊髄上位レベルでの侵害受容情報の伝達および調節に関与している(Duarteら、Eur.J.Pharmacol.217:225〜227、1992;Haleyら、Neuroscience31:251〜258、1992)。CNSにおける病変または機能不全は、中枢痛として知られる慢性疼痛症状の発生をもたらすことがあり、自発痛、痛覚過敏、ならびに機械的および冷感アロディニアが含まれる(Pagni、Textbook of Pain、Churchill Livingstone、Edinburgh、1989、634〜655頁;Tasker In:The Management of Pain、264〜283頁、JJ.Bonica(編)、LeaおよびFebiger、Philadelphia、PA、1990;Casey、Pain and Central Nervous System Disease:The Central Pain Syndromes、1〜11頁、K.L.Casey(編)、Raven Press、New York、1991)。NOS阻害剤である7-NIおよびL-NAMEの全身投与(i.p.)は、脊髄損傷を有するラットにおいて慢性アロディニア様症状を軽減することが示された(HaoおよびXu、Pain66:313〜319、1996)。7-NIの作用は、有意な鎮静作用と関係がなく、L-アルギニン(NO前駆体)によって逆転した。熱痛覚過敏の維持は、腰髄における一酸化窒素によって媒介されると考えられ、L-NAMEなどの一酸化窒素シンターゼ阻害剤または可溶性グアニル酸シクラーゼ阻害剤メチレンブルーのくも膜下腔内投与によって遮断することができる(Neuroscience50(l):7〜10、1992)。
内因性ポリアミン代謝物であるアグマチンは、NOS阻害剤およびN-メチル-D-アスパラギン酸(NMDA)チャネルアンタゴニストの両方である、アルギニンの代謝物である。アグマチンは、神経因性疼痛の脊髄神経結紮(SNL)モデル、並びに糖尿病性ニューロパチーのストレプトゾトシンモデルの両方において有効である(Karadagら、Neurosci.Lett.339(l):88〜90、2003)。したがって、例えば、式Iの化合物などのNOS阻害活性を有する化合物、NOS阻害剤とNMDAアンタゴニストとの組合せは、糖尿病性ニューロパチーおよび他の神経因性疼痛状態の治療に有効であるはずである。
周知の薬理学的道具であるLPSは、多くの組織において炎症を誘発し、静脈内に投与された場合全ての脳領域におけるNFKBを活性化させる。それはまた、線条体に局所注射された場合、炎症誘発性遺伝子を活性化させる(Sternら、J.Neuroimmunology、109:245〜260、2000)。最近、NMDA受容体アンタゴニストMK801および脳選択的nNOS阻害剤7-NIの両方は、脳におけるNFKB活性化を減少させ、したがって神経炎症におけるグルタミン酸およびNO経路が果たす明らかな役割を明らかにすることが示された(Glezerら、Neuropharmacology45(8):1120〜1129、2003)。したがって、単独またはNMDAアンタゴニストと組み合わせた本発明の化合物の投与は、神経炎症から起こる疾患の治療において有効であるはずである。
脳虚血におけるNOの役割は、虚血過程の進展段階によって、およびNOを産生する細胞コンパートメントによって、保護的または破壊的であることがある(Dalkaraら、Brain Pathology4:49、1994)。eNOSにより産生されたNOは、血管拡張薬として作用し、患部への血流を改善することによって有益である可能性がある(Huangら、J.Cereb.Blood Flow Metab.16:981、1996)一方、nNOSにより産生されたNOは、虚血性ペナンブラの初期の代謝悪化の一因となり、より大きな梗塞をもたらす(Haraら、J.Cereb.Blood Flow Metab.16:605、1996)。虚血の間に起こる代謝異常およびそれに続く再灌流は、中枢神経系のいくつかを含めたいくつかの細胞型においてiNOSを活性化するいくつかのサイトカインの発現および放出をもたらす。NOは、iNOSによって細胞毒性レベルで生じることがあり、iNOSのレベルの増加は、ペナンブラにおける進行性組織損傷の一因となり、より大きな梗塞をもたらす(Parmentierら、Br.J.Pharmacol.127:546、1999)。iNOSの阻害は、ラットにおける脳虚血性損傷を改善することが示された(Am.J.Physiol.268:R286、1995)。
脳損傷および認知機能障害は、いまだ冠動脈バイパス手術(CABG)を受けた患者の主要な合併症である(Rochら、N.Eng.J.Med.335:1857〜1864、1996;Shawら、Q.J.Med.58:59〜68、1986)。手術後のこの脳障害は、手術前の脳微小塞栓による虚血の結果である。NMDAアンタゴニストであるレマセミドの無作為化試験において、患者は、欠損の減少に加えて学習能力における手術後の有意で全体的な改善を示した(Arrowsmithら、Stroke29:2357〜2362、1998)。グルタミン酸の過剰な放出およびカルシウム流入によって生じる興奮毒性の関与を考慮すると、本発明の化合物などの神経保護剤またはNMDAアンタゴニストは、単独または(上記のように)組み合わせて、CABG後に神経学的結果を改善させる有益な作用を有する可能性があることが期待されている。
HIV-I感染症は、認知症を生じさせることがある。HIV-Iコートタンパク質gp-120は、低ピコモルレベルで大脳皮質初代培養においてニューロンを殺し、外部のグルタミン酸およびカルシウムを必要とする(Dawsonら、90(8):3256〜3259、1993)。この毒性は、神経保護剤、例えば、本発明の化合物を、単独でまたは他の治療剤(例えば、(上記のような)NMDAアンタゴニストなど)と組み合わせて投与することによって軽減することができる。
心原性ショック(CS)は、NOおよび炎症性サイトカインのレベルの増加と一致する急性心筋梗塞の患者の主要な死因である。高レベルのNOおよびペルオキシナイトライトは、心筋の収縮性に対する直接の阻害、心筋におけるミトコンドリア呼吸の抑制、グルコース代謝の変化、カテコールアミン反応性の減少、および全身的血管拡張の誘発を含めた多くの作用を有する(Hochman、Circulation107:2998、2003)。持続ショックを有する11人の患者の臨床試験において、NOS阻害剤L-NMMAの投与は、30日間まで尿量および血圧および72%の生存率の増加をもたらした(Cotterら、Circulation101:1258〜1361、2000)。30名の患者の無作為化試験において、L-NAMEが患者の死亡率を67%から27%に減少させたことが報告された(Cotterら、Eur.Heart.J.24(14):1287〜95、2003)。同様に、単独または他の治療剤と組み合わせた本発明の化合物の投与は、心原性ショックの治療において有用である可能性がある。
強制水泳試験(FST)におけるラットおよびマウスの最近の研究は、NOS阻害剤がマウスにおいて抗うつ作用を有し(Harkinら、Eur.J.Pharm.372:207〜213、1999)、それらの作用がセロトニン依存性機序によって媒介されることを示す(Harkinら、Neuropharmacology44(5):6l6〜623、1993)。7-NIは、ラット十字迷路試験において抗不安作用を示し(Yildizら、Pharmacology、Biochemistry and Behavior65:199〜202、2000)、一方では選択的nNOS阻害剤TRIMは、抑うつのFSTモデルおよび明暗コンパートメント試験における不安の両方において有効である(Volkeら、Behavioral Brain Research140(1〜2):141〜7、2003)。患っている個人への単独または他の治療剤(例えば、抗うつ剤など)と組み合わせた本発明の化合物の投与は、不安または抑うつの治療において有用である可能性がある。
自然発症高血圧(SHR)ラットおよびNaples低興奮性(NHE)ラットにおける環境刺激に対する非選択的注意(NSA)は、注意欠陥多動性障害(ADHD)の動物モデルとして使用されてきた(Aspideら、Behav.Brain Res.95(l):23〜33、1998)。これらの遺伝子改変動物は、正常な動物において観察されるよりもより短期間の立ち上がりエピソードの増加を示す。L-NAMEの10mg/kgの単回注射は、立ち上がり期間の増加をもたらした。同様に、ニューロンにより選択的な7-NINAを使用して、急速投与(i.p.)後に立ち上がり期間の増加が観察された一方、単回の持続放出用量または多回の持続放出用量(DMSO中s.c.)は反対の作用を生じた。したがって、本発明の化合物の投与は、ADHDの治療において有用である可能性がある。
フェンシクリジン(PCP)は、ヒトおよび哺乳動物において行動の副作用(精神病を有する患者において観察されるものと一致する)を生じさせる非競合的NMDAチャネル遮断剤である。精神病の2種の動物モデルにおいて、nNOS選択的阻害剤AR-R17477は、PCP誘発性の移動運動の亢進および聴覚性驚愕反応(acoustic response startle)の前パルス阻害におけるPCP誘発性の欠損を拮抗させた(Johanssonら、Pharmacol.Toxicol.84(5):226〜33、1999)。これらの結果は、精神病におけるnNOSの関与を示唆している。したがって、患っている個人への本発明の化合物の投与は、これもしくは関連した疾患または障害の治療に有用である可能性がある。
頭部外傷を有する患者における神経障害のメカニズムは、脳卒中のメカニズムに匹敵し、過剰なグルタミン酸放出からの興奮毒性カルシウム流入、ミトコンドリア機能不全および炎症からの酸化ストレスおよびフリーラジカル生成に関連する(Drug & Market Development9(3):60〜63、1998)。7-NIおよび3-ブロモ-7-ニトロインダゾールなどの一酸化窒素シンターゼ(NOS)阻害剤で処置した動物は、実験的外傷性脳損傷(TBI)後の神経脱落において改善を示した(Mesengeら、J.Neurotrauma、13:209〜14、1996)。患っている個人への本発明の化合物の投与はまた、頭部外傷における神経障害の治療に有用である可能性がある。
低体温心停止(HCA)は、脳が血流妨害の期間中の損傷に対して感受性である場合、心臓手術の間に虚血性損傷から保護するために使用される技術である。HCAの間の補助剤として様々な神経保護剤が使用されてきており、HCAの間に一酸化窒素産生を減少させることは、神経機能の改善をもたらすことが予測される。これは、グルタミン酸興奮毒性がHCA誘発性神経障害において役割を果たし(Redmondら、J.Thorac.Cardiovasc.Surg.107:776〜87、1994;Redmondら、Ann.Thorac.Surg.59:579〜84、1995)、NOがグルタミン酸興奮毒性を媒介する(DawsonおよびSnyder、J.Neurosci.14:5147〜59、1994)ことを示した従前の研究に基づいている。18℃で2時間のHCAを受けた32匹のイヌの研究において、ニューロンNOS阻害剤は、脳のNO産生を減少させ、ニューロン壊死を有意に減少させることが示され、対照と比較して優れた神経機能をもたらした(Tsengら、Ann.Thorac.Surg.67:65〜71、1999)。本発明の化合物の投与は、患者を心臓手術の間の虚血性損傷から保護するために有用である可能性がある。
ミトコンドリア機能不全、グルタミン酸興奮毒性、およびフリーラジカル誘発性酸化損傷は、筋萎縮性側索硬化症(ALS)、パーキンソン病(PD)、アルツハイマー病(AD)、およびハンチントン舞踏病(HD)を含めた多くの神経変性疾患の根底にある病因であると思われ(Schulzら、Mol.Cell.Biochem.174(1〜2):193〜197、1997;Beal、Ann.Neurol.38:357〜366、1995)、NOは、これらのメカニズムにおける主要なメディエーターである。例えば、Dawsonらによって、PNAS88(14):6368〜6371、1991において、7-NIおよびL-NAMEなどのNOS阻害剤は、N-メチル-D-アスパラギン酸および関連する興奮性アミノ酸によって誘発される神経毒性を防止することが示された。
研究によって、NOは、パーキンソン病の一般的に使用される動物モデルである1-メチル-4-フェニル-1,2,3,6-テトラヒドロピリジン(MPTP)神経毒性において重要な役割を果たすことがまた示された(Matthewsら、Neurobiology of Disease4:114〜121、1997)。MPTPは、MAO-BによりMPP+に変換され、ドーパミン輸送体によってドーパミン含有ニューロンのミトコンドリアに急速に取り込まれ、続いてnNOSが活性化され、神経細胞死がもたらされる。nNOS遺伝子欠損変異マウス(eNOS遺伝子欠損ではない)において、線条体へのMPP+注射後、黒質における病変が減少した。非特異的阻害剤L-NAMEがそうであったように(T.S.Smithら、Neuroreport1994、5、2598〜2600)、霊長類研究において、7-NIは、MPTP曝露後に著明な神経保護および抗パーキンソン病作用を及ぼす(Hantrayeら、Nature Med.2:1017〜1021、1996)。これらの結果は、適切な用量のNOS阻害剤(例えば、本発明の化合物など)の投与が、パーキンソン病の治療において有益である可能性があることを示唆する。
ADの病理は、活性化ミクログリアおよびアストロサイトにより浸潤されるβ-アミロイド斑と関連する。培養されたラットミクログリアがβ-アミロイドに曝された場合、特にγ-インターフェロンの存在下で、ミクログリアにおける一酸化窒素の顕著な放出がある(Goodwinら、Brain Research692(1〜2):207〜14、1995)。皮質ニューロン培養物において、一酸化窒素シンターゼ阻害剤による処理は、ヒトβ-アミロイドによって誘発された毒性に対して神経保護を提供する(Resinkら、Neurosci.Abstr.21:1010、1995)。神経変性障害における興奮毒性のグルタミン酸仮説と一致して、弱いNMDAアンタゴニストであるアマンタジンは、PD患者の平均余命を増加させる(Uittiら、Neurology46(6):1551〜6、1996)。脳血管型またはアルツハイマー型認知症を有する患者の予備的なプラセボ対照試験において、NMDAアンタゴニストであるメマンチンは、改良された全般臨床改善度および老人患者についての行動評価尺度スコアと関連があった(WinbladおよびPoritis、Int.J.Geriatr.Psychiatry14:135〜46、1999)。これらの結果は、適切な用量のNOS阻害剤(例えば、本発明の化合物など)の投与が、ADの治療において有益である可能性があることを示唆する。
筋萎縮性側索硬化症(ALS)は、選択的運動神経細胞死によって特徴付けられる致命的な神経変性疾患である。ALSの病因は、グルタミン酸輸送体によるグルタミン酸の不十分な排除であり、脊髄運動ニューロンにおけるCa2+透過性AMPA受容体の特異的分布がグルタミン酸誘発性神経毒性を示すことを、蓄積された証拠は示唆する。nNOS免疫反応性の増加が、ALS患者の脊髄(Sasakiら、Acta Neuropathol.(Berl)101(4):351〜7、2001)およびグリア細胞(Anneserら、Exp.Neurol.171(2):418〜21、2001)において見出され、これはNOをALSの病因における重要な要因として結びつける。これらの結果は、適切な用量のNOS阻害剤(例えば、本発明の化合物など)の投与が、ALSの治療において有益である可能性があることを示唆する。
Httタンパク質における突然変異から生じるハンチントン舞踏病(HD)の病因は、興奮毒性、酸化ストレスおよびアポトーシスと関連し、それらの全てにおいて、過剰なNOが明確な役割を有する(Petersonら、Exp.Neurol.157:1〜18、1999)。酸化損傷は、エネルギー代謝における欠陥の主要な結果の1つであり、興奮毒およびミトコンドリア阻害剤の注射後のHDモデルにおいて存在する(A.Petersenら、Exp.Neurol.157:1〜18、1999)。このミトコンドリア機能不全は、HDにおける選択的および進行性神経細胞脱落と関連する(Brownら、Ann.Neurol.41:646〜653、1997)。NOは、ミトコンドリアの呼吸鎖複合体IVを直接障害することができる(Calabreseら、Neurochem.Res.25:1215〜41、2000)。線条体中型有棘ニューロンは、HDにおける運動機能障害の発生のための第1標的であるように思われる。これらのニューロン上のNMDA受容体の過剰リン酸化および活性化は、運動機能障害の発生に関与しているようである。NMDAアンタゴニストであるアマンタジンは、HDにおいて舞踏病様ジスキネジアを改善することが臨床的に示された(Verhagen Metmanら、Neurology59:694〜699、2002)。NMDA媒介による神経毒性におけるnNOSの役割を鑑みて、nNOS阻害剤、特にnNOS/NMDAの混合とのnNOS阻害剤、またはnNOSおよびNMDA活性を有する薬物の組合せもまた、HDの作用および/または進行の改善において有用であろうことが期待される。例えば、ラットを7-ニトロインダゾールによって前処理することによって、マロネートの定位固定注射によって誘発される線条体病変(ハンチントン舞踏病に似た状態をもたらす傷害である)を軽減する(Hobbsら、Ann.Rev.Pharm.Tox.39:191〜220、1999)。ヒト変異型htt exon1(116のCAG反復)を発現しているHDのR6/1トランスジェニックマウスモデルにおいて、11週、19週および35週においてマウスは脂質過酸化の進行性増加を示し、11週では、スーパーオキシドジスムターゼ(SOD)は野生型(WT)マウスと同様正常レベルであり、19週では最大レベルであり、これはWTマウスにおいて観察されるものを超え、疾患の悪化の初期に相当し、最後に、35週では、WTマウスにおいて観察されるものより低いレベルに低下する(Perez-Sevrianoら、Brain Res.951:36〜42、2002)。SOD活性の増加は、代償性神経保護メカニズムに起因し、35週での低下したレベルは、保護メカニズムの障害に相当する。SODのレベルと同時に、カルシウム依存性NOSのレベルは、WTおよびR6/1マウスの両方において11週のマウスについて同じであったが、WT対照マウスと比較して19週では有意に上昇し、35週では低下した。nNOS発現のレベルはまた、19週で対照と比較して劇的に上昇したが、35週で対照と比較して有意に低下した。eNOS発現のレベルにおいて有意差は観察されず、疾患の進行の間にiNOSタンパク質を検出することはできなかった。体重減少、足を握り締める挙動、ならびに水平および上下移動の増加によって測定される疾患の進行的な形質発現は、NOS活性およびnNOS発現の変化と一致する。最後に、R6/2トランスジェニックHDマウスおよびWTマウスの両方へのL-NAME投与の作用は、対照と同様に10mg/kg用量で握り締める挙動のレベルの改善を示し、これは最も高用量の500mg/kgで悪化した(Deckelら、Brain Res.919(l):70〜81、2001)。HDマウスにおける体重増加の改善はまた、10mg/kgの用量で有意であったが、高用量レベルのL-NAMEでは対照と比較して減少した。これらの結果は、適切な用量のNOS阻害剤(例えば、本発明の化合物など)の投与が、HDの治療において有益である可能性があることを示す。
MSは、サイトカインおよび他の炎症メディエーターが関与するCNSの炎症性脱髄性疾患である。多くの研究は、NOおよびその反応性誘導体ペルオキシナイトライトがMSの病因に関与していることを示唆する(Acarら、J.Neurol.250(5):588〜92、2003;Calabreseら、Neurochem.Res.28(9):1321〜8、2003)。MSのモデルである実験的自己免疫性脳脊髄炎(EAE)において、nNOSレベルはEAEラットの脊髄において僅かに増加し、7-ニトロインダゾールによる処置は、EAE麻痺の発症の有意な遅延をもたらす(Shin、J.Vet.Sci.2(3):195〜9、2001)。これらの結果は、適切な用量のNOS阻害剤(例えば、本発明の化合物など)の投与が、MSの治療において有益である可能性があることを示唆する。
メタンフェタミンは、ドーパミン神経終末をin vivoで破壊することにより神経毒性である。メタンフェタミン誘発性神経毒性は、in vitro(Shengら、Ann.N.Y.Acad.Sci.801:174〜186、1996)およびin vivo動物モデル(Itzhakら、Neuroreport11(13):2943〜6、2000)において、NOS阻害剤による治療によって軽減することができることが示されてきた。同様に、nNOS選択的阻害剤であるAR-17477ARは、マウスにおいて5mg/kg(s.c)で、マウス脳におけるニューロフィラメントタンパク質NF68のメタンフェタミンが誘発する損失を防止することができ、線条体ドーパミンおよびホモバニリン酸(HVA)の損失を防止することができた(Sanchezら、J.Neurochem.85(2):515〜524、2003)。これらの結果は、適切な用量のNOS阻害剤(例えば、本発明の化合物など)の投与が、メタンフェタミン誘発性神経毒性の治療において有益である可能性があることを示唆する。
薬物誘発性報酬および依存の過程における重要なステップは、中脳辺縁系ドーパミンニューロンからのドーパミン放出の制御である。コカインの慢性服用は、ドーパミンのシナプスレベルを制御する重要なタンパク質であるドーパミン輸送体(DAT)の発現を変化させる。
動物は確実に静脈内に刺激薬を自己投与し、ドーパミンはそれらの強化効果において重大な意味を持つことを、研究は示してきた。最近、NO含有ニューロンは、線条体および腹側被蓋野の領域においてドーパミンと共に共存し、NOは刺激薬により惹起されたドーパミン(DA)放出を調節できることが示された。ドーパミンD1受容体アンタゴニストの投与は、NOS活性のマーカーである線条体のNADPH-ジアフォラーゼ染色のレベルを減少させ、一方、D2アンタゴニストは、反対の作用を生じさせる。NOS基質であるL-アルギニンはまた、DA放出の強力なモジュレーターである。また、多数のNO産生剤は、DA流出を増加させ、またはin vitroおよびin vivoの両方で再取込みを阻害する。L-NAMEは、自己投与の量を減らすことによって、および連続的なコカイン注射の間の反応間時間を増加させることによって、コカイン強化を有意に変化させることが示された(PudiakおよびBozarth、Soc.Neurosci.Abs.22:703、1996)。これは、本発明の化合物によるNOS阻害が、コカイン嗜癖の治療において有用である可能性があることを示す。
成体および幼児期の動物のオピオイド依存におけるNMDAおよびNO経路の両方の役割を支持する多くの証拠がある。モルヒネ硫酸塩を注射された成体または幼児期のげっ歯類は、ナルトレキソンによる沈殿後、行動離脱が発生した。ナルトレキソン開始後の離脱症状は、7-NIまたはL-NAMEなどのNOS阻害剤の投与によって減少させることができる(ZhuおよびBarr、Psychopharmacology150(3):325〜336、2000)。関連した研究では、よりnNOS選択的な阻害剤7-NIは、より選択的でない化合物より、咀嚼、唾液分泌および生殖作用を含めたモルヒネ誘発性離脱症状をより軽減することが示された(Vaupelら、Psychopharmacology(Berl.)118(4):361〜8、1995)。これは、本発明の化合物によるNOS阻害が、モルヒネ/オピオイド誘発性耐性および離脱症状の治療において有用である可能性があることを示す。
アルコール依存に影響を与える要因の中で、エタノールの作用に対する耐性は、それがアルコール飲料の過剰な飲用を促進することから、重要な構成要素である(LeおよびKiianmaa、Psychopharmacology(Berl.)94:479〜183、1988)。ラットを用いた研究において、運動失調および低体温に対するエタノール耐性は急速に発生し、脳内エタノール濃度を変化させることなく、7-NIのi.c.v.投与によって阻止することができる(WazlawikおよびMorato、Brain Res.Bull57(2):165〜70、2002)。他の研究では、L-NAMEによるNOS阻害(Rezvaniら、Pharmacol.Biochem.Behav.50:265〜270、1995)またはnNOSアンチセンスのi.c.v.注射によるNOS阻害(Naassilaら、Pharmacol.Biochem.Behav.67:629〜36、2000)は、これらの動物におけるエタノール消費を減少させた。これは、本発明の化合物によるNOS阻害が、エタノール耐性および依存の治療において有用であることがある可能性を示す。
7-NIとカルバマゼピンなどの特定の抗痙攣剤との同時投与は、回転ロッド(roto-rod)動作を変化させない濃度で、ラットの扁桃体キンドリング発作に対して相乗的保護作用を示す(Borowiczら、Epilepsia41(9:112〜8、2000)。したがって、例えば、本発明の化合物などのNOS阻害剤は、単独でまたは他の治療剤(例えば、抗てんかん剤など)と組み合わせて、てんかんまたは同様の障害の治療において有用である可能性がある。本発明の組合せにおいて有用な抗てんかん剤の例には、カルバマゼピン、ガバペンチン、ラモトリジン、オクスカルバゼピン、フェニロイン、トピラメート、およびバルプロエートが挙げられる。
NO副産物の尿中排泄は、ストレプトゾトシン処理後に糖尿病ラットにおいて増加し、NO合成の増加が、糖尿病性糸球体過剰濾過に関与していることが示唆されてきた。ニューロンアイソフォームnNOSは、腎臓のヘンレ係蹄および緻密斑において発現し、7-NIを使用したこのアイソフォームの阻害は、腎臓の細動脈圧または腎臓の血流に影響を与えることなく糸球体濾過を減少させる(Sigmonら、Gen.Pharmacol.34(2):95〜100、2000)。非選択的NOS阻害剤であるL-NAMEおよびnNOS選択的7-NIの両方は、糖尿病動物において腎臓の過剰濾過を正常化する(Itoら、J.Lab Clin.Med.138(3):177〜185、2001)。したがって、本発明の化合物の投与は、糖尿病性腎症の治療において有用である可能性がある。
薬物乱用頭痛(MOH)は、複合鎮痛剤、オピオイド、バルビツレート、アスピリン、NSAID、カフェインおよびトリプタンの過剰使用と関連し、これらのタイプの薬物の有用性を限定する一般的な問題である(DienerおよびLimmroth、Medication-overuse headache:a worldwide problem、Lancet Neurol.2004:3、475〜483)。1ヵ月当たり15日間を超えて存在する場合、一般に頭痛と定義される(頭痛分類委員会、The International Classification of Headache Disorders(第2版)。Cephalalgia2004:24(追補1);9〜160)。片頭痛または緊張型頭痛のための患者の急性期治療によって、頭痛悪化、毎日の頭痛の発生の危険性が高まり、または急性薬物が過剰に摂取された場合、治療に対して不応性となる場合があることは十分な資料の裏付けがある(Zeebergら、Cephalalgia2006:26、1192〜1198)。MOH患者は一般に、薬物を乱用している一方、予防的薬物投与に反応しない。現在、MOHに最適な治療法は薬物を中断することであるが、これは悪心、嘔吐および睡眠障害などの離脱症状を伴うことが多い。2ヵ月間薬物を中断したMOHを患っている片頭痛または緊張型頭痛患者では、頭痛頻度が減少する(45%)一方、多くの患者で、離脱後に変化がない(48%)か、または頭痛が悪化した(Zeebergら、Cephalalgia2006:26、1192〜1198)。したがって、MOHを患っている患者について未だ対処されていない大きな必要性が存在する。
nNOSは、小腸における総NOSの90%超を構成する。iNOSは恒常的に存在するが、それは総NOS活性の10%未満を占め、eNOSは本質的に腸において検出不可能である(Qu XWら、Type I nitric oxide synthase(NOS)is the predominant NOS in rat small intestine.Regulation by platelet-activating factor.Biochim Biophys Acta、1999;1451:211〜217)。腸におけるnNOSの主要な機能は、神経系のNANC成分におけるニューロンのシグナル伝達を介した消化管の運動性の制御であると考えられている。NOは、下部食道、幽門、オッディ括約筋、および肛門における括約筋の筋緊張を制御する。NOはまた、胃底の調節反射および腸の蠕動反射を制御する。NOS阻害剤は、胃内容物排出および結腸通過を遅らせることが知られている(T.Takahashi J.Gastroenterol、2003;38(5):421〜30)。したがって、nNOS阻害剤は、胃内容物排出の遅延または結腸通過の緩徐化から恩恵を受けるGI障害において治療剤である場合がある。ダンピング症候群は、食物が胃からあまりにも急速に空にされ、小腸において栄養素の効率的な吸収が可能となるように適切に準備されていない未消化の食物が小腸に満ちる障害であり、胃切除術後に観察されることが多い。したがって、本発明の化合物の投与は、ダンピング症候群などの消化器障害の治療において有用である可能性がある。本研究の化合物を使用して他の刺激性腸症候群を治療することもできる。
内臓痛は疼痛の最も普通の疼痛であり、治療すべき疼痛の最も難しい形態の一つである。内臓痛は体性痛と異なり、一般的に身体の内腔または器官に起因する疼痛として記載され、次の5つの重要な臨床的かつ感覚的特徴を有する:(1)全ての内臓器官から惹起されるものでない(例えば、肝、腎、肺臓);(2)常に内臓傷害と連結するものでない(例えば、小腸の切断は疼痛を惹起しない);(3)散在性でない;(4)他の部位に関係する;および(5)他の自律性および運動反射に関係しうる(例えば、吐き気、腎仙痛由来の低背筋肉伸長)(Lancet 353、2145-48,1999)。いくつかの理論が内臓痛の機構に対して提案されている。第1の理論では、内臓は別々のクラスの神経細胞により神経支配されており、一つは自律調節に関わり、他は疼痛などの感覚現象に関わる。第2の理論は、低頻度の活性化(通常調節シグナル)でまたは高頻度の活性化(強い疼痛により誘導されるシグナル)で活性化される単独の均一なクラスの感覚受容体を示唆する。しかし、研究は、内臓が2つのクラスの侵害性感覚受容体:高い閾値(ほとんど、心、静脈、肺、気道、食道、胆汁系、小腸、大腸、尿管、膀胱、および子宮に見出され、侵害性刺激により活性化される機械的受容体である)ならびに非侵害性および侵害性刺激に応答する低い閾値強度(心、食道、大腸、膀胱、および精巣)をコードする受容体により神経支配されることを示す。さらに他の理論は、通常は刺激に対して不応答であって、炎症中は活性化または感作化しうる求心性繊維成分(サイレント侵害受容体)を示唆する(Trends Neurosci.15, 374-78, 1992)。感作化されると、これらの侵害受容体は、通常内部器官で起こって脊髄への収束性入力に高い関門を生じる非侵害性刺激に対しても応答し、続いて末梢神経入力の効果を増幅する中枢神経機構をトリガーする。
上記の製剤に加えて、1種または複数の本発明の化合物は、他の治療剤と組み合わせて使用することができる。例えば、1種または複数の本発明の化合物は、他のNOS阻害剤と合わせることができる。この目的のために有用な例示的阻害剤には、これらだけに限定されないが、米国特許第6,235,747号、米国特許第7,141,595号および米国特許第7,375,219号、米国特許出願第09/127,158号、同第09/325,480号、同第09/403,177号、同第09/802,086号、同第09/826,132号、同第09/740,385号、同第09/381,887号、同第10/476,958号、同第10/483,140号、同第10/484,960号、同第10/678,369号、同第10/819,853号、同第10/938,891号、同第11/436,393号、同第11/787,167号、同第12/054,083号および同第12/272,656号;国際公開第WO97/36871号、同第WO98/24766号、同第WO98/34919号、同第WO99/10339号、同第WO99/11620号、および同第WO99/62883号において記載されたものが挙げられる。
神経損傷は、神経因性疼痛として知られる異常な疼痛状態をもたらすことがある。臨床症状のいくつかには、触覚アロディニア(通常は非侵害性の機械的刺激に対する侵害受容反応)、痛覚過敏(通常の疼痛性刺激に対する疼痛強度の増大)、および自発痛が挙げられる。ラットにおける脊髄神経結紮(SNL)は、ヒト患者において観察される臨床症状と類似した、自発痛、アロディニア、および痛覚過敏を生じさせる神経因性疼痛の動物モデルである(KimおよびChung、Pain50:355〜363、1992;Seltzer、Neurosciences7:211〜219、1995)。
多くの抗うつ剤が、神経因性疼痛(McQuayら、Pain68:217〜227、1996)および片頭痛(Tomkinsら、Am.J.Med.111:54〜63、2001)の治療のために使用され、セロトニン作動性またはノルアドレナリン作動性系を介して作用する。NOは、これらの系の神経調節物質としての役割を果たす(GarthwaiteおよびBoulton、Annu.Rev.Physiol.57:683、1995)。7-NIは、NA輸送体を介してニコチン性アセチルコリン受容体アゴニストDMPPによってノルアドレナリン(NA)の放出を増強することが示された(Kissら、Neuroscience Lett.215:115〜118、1996)。パロキセチン、チアネプチン、およびイミプラミンなどの抗うつ剤の局所投与は、海馬NOのレベルを減少させることが示された(Wegenerら、Brain Res.959:128〜134、2003)。抗うつ剤が疼痛および抑うつを治療するのに有効であるメカニズムにNOが重要であり、nNOS阻害剤と抗うつ剤との組合せ、例えば上記の組合せは、より良好な治療をもたらすと思われる。
NO供与体であるグリセリルトリニトレート(GTN)の投与は、正常な個人において即時型頭痛を誘発し、片頭痛患者において4〜6時間の潜伏期を伴う遅延型片頭痛発作をもたらす(Iversenら、Pain38:17〜24、1989)。片頭痛発作を有する患者において、頸動脈における強力な血管拡張剤であるCGRP(カルシトニン遺伝子関連ペプチド)のレベルは、片頭痛発作の開始および消失と相関する(Durham、Curr Opin Investig Drugs5(7):731〜5、2004)。5HT1B、5HT1D、および5HT1F受容体において親和性を有する抗片頭痛薬であるスマトリプタンは、GTN誘発性即時型頭痛を減少させ、同時に大脳動脈および脳以外の動脈を収縮させる(IversenおよびOlesen、Cephalagia、13(Suppl13):186、1993)。抗片頭痛薬リザトリプタンはまた、片頭痛の痛みの減少の後にCGRPの血漿レベルを減少させる(Stepienら、Neurol.Neurochir.Pol.37(5):1013〜23、2003)。したがって、NOおよびCGRPの両方は、片頭痛の原因として意味付けられてきた。セロトニン5HT1B/1Dアゴニストは、脳皮質切片におけるNMDA受容体誘起性NOシグナル伝達を遮断することが示された(Strosznajderら、Cephalalgia、19(10):859、1999)。これらの結果は、上記のそれらの組合せなどの、本発明の化合物と選択的もしくは非選択的5HT1B/1D/1FアゴニストまたはCGRPアンタゴニストとの組合せが、片頭痛の治療に有用であろうことを示唆する。
本発明の化合物は好ましくは、in vivo投与に適した生物学的に適合した形態でヒト対象への投与のための医薬組成物に製剤される。したがって、他の態様では、本発明は、適切な希釈剤、担体、または賦形剤と混合した本発明の化合物を含む医薬組成物を提供する。
本発明の化合物は、NOSのニューロンアイソフォーム(nNOS)の選択的阻害を示すことが見出された。当業者は、例えば、実施例34ならびに本明細書において下記に記載されている方法を使用することによって、化合物のiNOSおよび/またはeNOSよりもnNOSを優先的に阻害するそれらの効力について調べることできる。
7-ニトロ-3,4-ジヒドロ-2H-ベンゾ[b][1,4]オキサジン(300mg、1.665mmol)のDMF(10mL)中の溶液を、NaH(213mg,5.33mmol、鉱油中の60重量%)で0℃にて処理し、明るいオレンジ色の懸濁液を得た。混合物を10分間攪拌した。2-クロロエチル-ピロリジン塩酸塩(566mg、3.33mmol)を次いで加えると、反応液は明赤色の懸濁液に変わった。その反応液を90℃に1時間加熱し、次いで室温まで冷却した。混合物を次いで水(20ml)で希釈し、分液漏斗に移し、EtOAc(2×15mL)中に抽出した。組合わせた有機層をブライン(3×5mL)で洗浄し、乾燥し(Na2SO4)、濾過し、そして濃縮した。残留物をシリカゲル上のフラッシュクロマトグラフィで、CH2Cl2、次いで5:95(MeOH中の2M NH3):CH2Cl2を用いて処理し、固体(330mg,72%)を得た。1H-NMR (DMSO-d6) δ 7.75 (dd, J = 2.7, 9.3 Hz, 1H), 7.47 (d, J = 2.7 Hz, 1H), 6.80 (d, J = 9.0 Hz, 1H), 4.18 (t, J = 4.2 Hz, 2H), 3.58-3.55 (m, 4H), 2.63 (t, J = 6.9 Hz, 2H), 2.58-2.48 (m, 4H), 1.70-1.63 (m, 4H); ESI-MS (m/z, %): 278 (MH+, 100), 98 (20)。
N,N-ジメチル-2-(7-ニトロ-2H-ベンゾ[b][1,4]オキサジン-4(3H)-イル)エタンアミン(210mg、0.836mmol)およびPd-C(10%wt、89mg、0.084mmol)の乾燥EtOH(15mL)中の懸濁液を水素ガスでパージした。反応液を室温で3時間水素雰囲気(風船圧)下で攪拌した。反応混合物を次いでセライトパッドを通して濾過し、EtOH(15mL)で洗浄した。淡紫色の濾液を濃縮して粗4-(2-(ジメチルアミノ)エチル)-3,4-ジヒドロ-2H-ベンゾ[b][1,4]オキサジン-7-アミンを得た。この粗4-(2-(ジメチルアミノ)エチル)-3,4-ジヒドロ-2H-ベンゾ[b][1,4]オキサジン-7-アミン(185mg、0.836mmol)の乾燥EtOH(10mL)中の溶液をメチルチオフェン-2-カルビミドチオエートヨウ化水素酸塩(477mg、1.672mmol)で処理し、一晩室温にて攪拌した。反応液を飽和NaHCO3溶液(50mL)で希釈し、生成物をCH2Cl2(3×25mL)中に抽出した。組合わせた有機層を乾燥し(Na2SO4)、濃縮した。残留物をシリカゲル上のフラッシュクロマトグラフィで、2:98 MeOH:CH2Cl2、次いで5:95 (MeOH中の2M NH3):CH2Cl2を用いて処理して黄色の固体(150 mg、54%)を得た。1H-NMR (DMSO-d6) δ 7.69 (dd, J = 3.6, 0.9 Hz, 1H), 7.56 (dd, J = 5.1, 0.9 Hz, 1H), 7.07 (dd, J = 5.1, 3.9 Hz, 1H), 6.64 (d, J = 8.4 Hz, 1H), 6.35-6.26 (m, 4H), 4.14 (t, J = 3.9 Hz, 2H), 3.33-3.29 (m, 4H), 2.42 (t, J = 6.9 Hz, 2H), 2.19 (s, 6H); ESI-MS (m/z, %): 331 (MH+, 100), 260 (25);C17H23N4OS(MH+)について計算したESI-HRMS:331.1587、測定値:331.1594;HPLC純度:99.0%(面積による)を得た。
2-アミノ-5-ニトロベンゼンチオール(1.72g、10.11mmol)のテトラヒドロフラン(10mL)中の攪拌溶液に、炭酸水素ナトリウム(2.80g、33.4mmol)を水溶液(40.0mL)として加えた。この暗赤色の溶液に2-クロロアセチルクロリド(0.885mL、11.12mmol)を加えた。得られる淡赤色に転じた混合物を次いで室温にて一晩攪拌した。その混合物を次いで水で希釈し、ジクロロメタンで3回抽出した。組合わせた有機層を乾燥し、濾過し、濃縮し、次いでジクロロメタン中の10%酢酸エチルでクロマトグラフィ処理をして所望の生成物(1.02g、48.0%)を得た。1H NMR (DMSO-d6) δ 11.17 (s, 1H), 8.24 (d, J = 2.7 Hz, 1H), 8.07 (dd, J = 9.0, 2.7 Hz, 1H), 7.13 (d, J = 9.0 Hz, 1H), 3.60 (s, 2H); MS-EI: (m/z, %) 210 (M+, 100), 181 (40), 131 (46)。
4-(2-(ジメチルアミノ)エチル)-7-ニトロ-2H-ベンゾ[b][1,4]チアジン-3(4H)-オン(730mg、2.59mmol)のアルゴン雰囲気下のテトラヒドロフラン(3mL)中の攪拌溶液にボラン(THF中の1M;7.784mL、7.78mmol)を加えた。得られる混合物を一晩室温で攪拌すると、黄色の沈降部を生じた。その混合物を60℃に一寸加熱して固体を解体させた。反応液を次いで0℃に冷却し、メタノールでクエンチした(徐々に泡立ちが止まるまで)。混合物を次いで濃縮し、MeOH(15mL)および1M HCl(5 mL)に再溶解し、そして60℃にて30分間加熱した。クエンチした混合物を次いで水および炭酸ナトリウムで希釈し、次いでジクロロメタン(3×)で抽出した。組合わせた有機層を乾燥し、濾過し、濃縮し、次いで酢酸エチル中でクロマトグラフィ処理して黄色の固体と所望の錯体をボラン錯体として得て、これをその後の反応に直接使用した。
オーブンで乾燥しアルゴンでパージした、磁性攪拌バーを備えた丸底フラスコにtert-ブチルメチル(2-(6-ニトロ-2H-ベンゾ[b][1,4]オキサジン-4(3H)-イル)エチル)カルバメート(0.13g、0.385mmol)、EtOH(10mL)を加えた。この時点で、攪拌を開始した。10%Pd-C(0.041g、0.039mmol)を加え、フラスコを真空で吸引し、材料を、本明細書に記載した標準条件下で水素化処理をした。2.5時間後、混合物をセライトのパッドを通して濾過し、エタノールで洗浄した。空気に曝露すると徐々に暗色化した淡桃色の溶液を〜10mLの体積に濃縮して表題化合物を得て、これを次のステップに直ぐ使用した。小部分を濃縮乾固して分析に用いた。1H NMR (DMSO-d6) δ 6.34 (d, 1H, J = 8.3 Hz), 6.03-5.95 (m, 1H), 5.75 (dd, 1H, J = 8.3, 2.3 Hz), 4.35 (m, 2H), 3.98 (t, 2H, J = 4.1 Hz), 3.30-3.15 (m, 6H), 2.81 (s, 3H), 1.38, 1.30 (2 × s, 9H); ESI-MS (m/z, %): 308 (MH+, 90), 252 (100)。
6-ニトロベンゾ[d]チアゾール(5g、27.7mmol)のエタノール(45mL)中の懸濁液に、ヒドラジン水和物(8.10mL、166mmol)を加えた。得られる混合物(暗赤色)を一晩室温にて攪拌した。混合物を次いで徐々に注意深く3M HCl水溶液(50mL)を加えることにより酸性化した。この混合物をさらに水(50mL)で希釈し、得られる黄色/オレンジ色の沈降物をジクロロメタン(3×)で抽出した。組合わせた有機層を乾燥し、濾過し、濃縮してオレンジ色の固体(4.62g、98%)を得た。1H NMR (DMSO-d6) δ 8.12-8.09 (m, 1H), 7.88-7.85 (m, 1H), 6.75-6.71 (m, 1H), 6.28 (brs, 2H); ESI-MS (m/z, %): 170 (MH+, 100)。
4-(2-(ジメチルアミノ)エチル)-3,4-ジヒドロ-2H-ベンゾ[b][1,4]チアジン-7-アミン(0.888g、3.74mmol)およびメチルチオフェン-2-カルビミドチオエートヨウ化水素酸塩(2.134g、7.48mmol)の乾燥エタノール(15mL)中の懸濁液を、室温にて一晩(16時間)攪拌した。溶媒を蒸発させ、残留物を飽和NaHCO3溶液(50mL)とCH2Cl2(25mL)の間で分配した。20分間の攪拌後、混合物を分液漏斗に移し、有機層を取り出した。水層をCH2Cl2(2×25mL)中に抽出した。組合わせた有機層を乾燥し(Na2SO4)、濾過し、濃縮した。残留物をカラムクロマトグラフィ(CH2Cl2、次いで5:95 (MeOH中の2MNH3):CH2Cl2)で、シリカゲルを用いて処理して表題生成物12を固体(0.44g、33.9%)として得た。1H-NMR (DMSO-d6) δ 7.69 (d, J = 3.3 Hz, 1H), 7.56 (d, J = 5.1 Hz, 1H), 7.07 (dd, J = 4.8, 3.9 Hz, 1H), 6.66 (d, J = 8.7 Hz, 1H), 6.52-6.46 (m, 2H), 6.32 (brs, 2H), 3.56-3.52 (m, 2H), 3.36-3.32 (m, 2H), 3.03-3.00 (m, 2H), 2.41 (t, J = 7.2 Hz, 2H), 2.19 (s, 6H); ESI-MS (m/z, %): 347 (MH+, 100), 276 (84%)。
N-(4-(2-(ジメチルアミノ)エチル)-3,4-ジヒドロ-2H-ベンゾ[b][1,4]チアジン-7-イル)チオフェン-2-カルボキシミドアミド(0.44g、1.270mmol)の乾燥エタノール(10mL)中の溶液を塩酸(エーテル中の1M;6.35mL、6.35mmol)で処理し、室温にて1時間攪拌した。沈降物を単離し、エーテルで洗浄して黄緑色の粉末を得た。粉末を減圧下で乾燥した(0.46 g、86%)。1H-NMR (DMSO-d6) δ 11.25 (brs, 2H), 9.69 (brs, 1H), 8.69 (brs, 1H), 8.15-8.13 (m, 2H), 7.37-7.37 (m, 1H), 7.07-7.01 (m, 3H), 3.82-3.77 (m, 2H), 3.70-3.60 (m, 2H), 3.25-3.21 (m, 2H), 3.15-3.10 (m, 2H), 2.80 (d, J = 3.6 Hz, 6H); ESI-MS (m/z, %): 347 (MH+, フリー塩基, 100); C17H23N4S2 (MH+、フリー塩基)について計算したESI-HRMS: 347.1358、測定値:347.1343; HPLC 純度:97%(面積による)。
4-(2-(1-メチルピロリジン-2-イル)エチル)-3,4-ジヒドロ-2H-ベンゾ[b][1,4]チアジン-7-アミン(0.7g、2.52mmol)およびメチルチオフェン-2-カルビミドチオエートヨウ化水素酸塩(1.439g、5.05mmol)の乾燥エタノール(15mL)中の懸濁液を、室温にて一晩(16時間)アルゴン雰囲気下で攪拌した。この時点で溶媒を蒸発させ、残留物を飽和NaHCO3溶液(50mL)とジクロロメタン(25mL)の間で分配した。混合物を分液漏斗に移し、有機層を取り除いた。水層をジクロロメタン(2×25mL)中に抽出した。組合わせた有機層を乾燥し(Na2SO4)、濾過し、濃縮した。残留物をシリカゲルのカラムクロマトグラフィ(溶出液の順序:2:98 メタノール:ジクロロメタン、5:95 メタノール:ジクロロメタン、および5:95(メタノール中の2Mアンモニア):ジクロロメタン)で処理して化合物13を黄色のシロップ(0.48g、49%)として得た。1H-NMR (DMSO-d6) δ 7.69 (brd, J = 2.7 Hz, 1H), 7.57 (brd, J = 4.5 Hz, 1H), 7.07 (dd, J = 3.9, 4.8 Hz, 1H), 6.52 (dd, J = 1.8, 8.1 Hz, 2H), 6.47 (brd, J = 1.8 Hz, 1H), 6.38 (brs, 2H), 3.51-3.47 (m, 2H), 3.28-3.22 (m, 2H), 3.05-3.02 (m, 2H), 2.99-2.93 (m, 1H), 2.24 (s, 3H), 2.12-2.06 (m, 2H), 1.94-1.87 (m, 2H), 1.68-1.63 (m, 2H), 1.51-1.42 (m, 2H); ESI-MS (m/z, %): 387 (MH+, 90), 276 (100), 194 (50)。
4-(2-(ピペリジン-1-イル)エチル)-3,4-ジヒドロ-2H-ベンゾ[b][1,4]チアジン-7-アミン(0.90g、3.24mmol)とメチルチオフェン-2-カルビミドチオエートヨウ化水素酸塩(1.85g、6.49mmol)の懸濁液を室温にて一晩(16時間)アルゴン雰囲気下で攪拌した。反応液を濃縮し、残留物を飽和炭酸水素ナトリウム溶液(50mL)とジクロロメタン(25mL)の間で分配した。1時間攪拌後、混合物を分液漏斗中に注いだ。有機層を取り除いて、水層をジクロロメタン(2×20mL)中に抽出した。組合わせた有機層を乾燥し(Na2SO4)、濾過し、濃縮した。残留物をシリカゲルのカラムクロマトグラフィ(2:98〜5:95 MeOH:CH2Cl2次いで5:95(MeOH中の2MNH3):CH2Cl2)で処理して化合物14を黄色の固体(0.288g、23%)として得た。1H-NMR (DMSO-d6) δ 7.69 (d, J = 3.3 Hz, 1H), 7.57 (d, J = 4.5 Hz, 1H), 7.09-7.06 (m, 1H), 6.67 (d, J = 8.7 Hz, 1H), 6.52-6.47 (m, 2H), 6.39 (brs, 2H), 3.56-3.53 (m, 2H), 3.39-3.33 (m, 2H), 3.03-3.01 (m, 2H), 2.45-2.39 (m, 6H), 1.49-1.48 (m, 4H), 1.39-1.38 (m, 2H); ESI-MS (m/z, %): 387 (MH+, 77), 276 (46), 194 (100)。
N-(4-(2-(ピペリジン-1-イル)エチル)-3,4-ジヒドロ-2H-ベンゾ[b][1,4]チアジン-7-イル)チオフェン-2-カルボキシミドアミド(0.288g、0.745mmol)の無水メタノール(8mL)中の溶液を、塩酸(エーテル中の1M;3.72mL、3.72mmol)で処理した。反応液を室温にて0.5時間攪拌し、次いで濃縮してオレンジ色の固体(0.34g、99%)を得た。1H-NMR (DMSO-d6) δ 11.21 (brs, 1H), 11.16 (brs, 1H), 9.67 (brs, 1H), 8.69 (brs, 1H), 8.15 (brd, J = 4.8 Hz, 1H), 8.11 (brd, J = 3.0 Hz, 1H), 7.38-7.35 (m, 1H), 7.11-6.98 (m, 3H), 3.89-3.84 (m, 2H), 3.68-3.64 (m, 2H), 3.45-3.42 (m, 2H), 3.22-3.15 (m, 2H), 3.12-3.09 (m, 2H), 2.89-2.88 (m, 2H), 1.87-1.71 (m, 5H), 1.42-1.38 (m, 1H); ESI-MS (m/z, %):387 (MH+、フリー塩基, 100), 194 (23); C20H27N4S2 (MH+、フリー塩基)について計算したESI-HRMS:387.1671、測定値:337.1657;HPLC純度:99%(面積による)。
N,N-ジエチル-2-(7-ニトロ-2H-ベンゾ[b][1,4]チアジン-4(3H)-イル)エタンアミン(1.109g、3.76mmol)のMeOH(30mL)中の攪拌溶液に、ラネーニッケル(水中のスラリー;〜0.1g、3.76mmol)、次いでヒドラジン水和物(1.828mL、37.6mmol)を加えた。混合物を予熱した油浴に浸漬し、30分間還流した。溶液を室温に冷却し、セライトを通して濾過し、MeOHで洗浄した。粗材料をシリカプラグ[3.5%(MeOH中の2MNH3):CH2Cl2]を通して濾過した。溶媒を蒸発させて生成物を暗褐色の油(1.07g、定量)として得た。1H NMR (CDCl3) δ 6.58 (d, J = 8.7 Hz, 1H), 6.45 (d, J = 2.7 Hz, 1H), 6.40 (dd, J = 2.7, 8.7 Hz, 1H), 3.53-3.50 (m, 2H), 3.30 (m, 4H), 3.03-2.99 (m, 2H), 1.03 (t, J = 7.2 Hz, 6H); ESI-MS (m/z, %): 268, 266 (MH+, 100), 100 (52)。
2-クロロアセチルクロリド(4.08mL、50.9mmol)を、7-ニトロ-3,4-ジヒドロ-2H-ベンゾ[b][1,4]チアジン(5g、25.5mmol)をトルエン(30mL)中に含有する溶液に滴状で加えた。混合物を110℃にて20分間還流した。混合物を飽和炭酸水素ナトリウム溶液(100mL)でクエンチした。混合物を分液漏斗に移し、EtOAcで抽出した(4×100mL)。粗材料をシリカゲルのパッドを通して濾過し、EtOAcで洗浄した。濾液を濃縮して黄褐色の固体を得た。1H-NMR (DMSO-d6) δ 8.12 (d, J = 2.7 Hz, 1H), 7.94 (dd, J = 2.7, 9.0 Hz, 1H), 7.72 (d, J = 9.0 Hz, 1H), 4.63 (s, 2H), 3.96 (t, J = 5.1 Hz, 2H), 3.32 (t, J = 5.4 Hz, 2H、溶媒ピークと重複); ESI-MS (m/z, %): 273 (MH+, 100), 295 (40)。
2-クロロ-1-(7-ニトロ-2H-ベンゾ[b][1,4]チアジン-4(3H)-イル)エタノン(1.0g,3.67mmol)のTHF(20mL)中の溶液を、1,4-ジオキサン(4.58mL、18.33mmol)中の4M HClで処理し、次いで2-アミノエタノール(2.207mL、36.7mmol)の水溶液(4mL)を徐々に加えた。暗色の溶液を室温にて24時間攪拌した。混合物をEtOAc(50mL)および飽和炭酸水素ナトリウム(100mL)で希釈し、次いで20分間攪拌した。内容物を分液漏斗中に注ぎ、有機層を分離し、乾燥し(Na2SO4)、濾過し、濃縮して暗黄色の残留物を得た。この残留物をシリカゲルのクロマトグラフィで5:95 MeOH:CH2Cl2、次いで5:95 (MeOH中の2MNH3):CH2Cl2を用いて処理して黄色残留物(320mg、29.4%)を得た。1H-NMR (CDCl3) δ 8.14 (d, J = 2.7 Hz, 1H), 7.95 (dd, J = 2.7, 9.0 Hz, 1H), 7.37 (d, J = 9.0 Hz, 1H), 4.02 (t, J = 5.1 Hz, 2H), 3.61 (t, J = 5.1 Hz, 2H), 3.57 (s, 2H), 3.28 (t, J = 5.4 Hz, 2H), 2.77 (t, J = 4.8 Hz, 2H); ESI-MS (m/z, %): 298 (MH+, 100%)。
tert-ブチル2-ヒドロキシエチル(2-(7-ニトロ-2H-ベンゾ[b][1,4]チアジン-4(3H)-イル)-2-オキソエチル)カルバメート(250mg、0.629mmol)のTHF(10mL)中の溶液を0℃に冷却し、次いでTHF(1M)(6.29mL、6.29mmol)中のボランで処理した。得られる明黄色の溶液を室温に加温させ、次いでこの温度で2.5 日間攪拌した。その混合物を0℃に冷却し、反応を次いでMeOH(最初は滴状で加えて;合計20mL)で注意深くクエンチした。冷却浴を取り除いて、黄色溶液を20分間攪拌し次いで濃縮した。オレンジ色の残留物をMeOH(50mL)に溶解し、濃縮乾固した。この残留物をEtOAc(20mL)に溶解し、シリカゲルを通して濾過した。シリカパッドをEtOAc(100mL)で溶出した。濾液を濃縮してオレンジ色の残留物を得て、これを減圧下で4時間乾燥した(230mg、95%)。1H-NMR (CDCl3) δ 7.97 (brs, 1H), 7.87 (brd, J = 8.7 Hz, 1H), 6.85-6.71 (m, 1H), 3.81 (brs, 5H), 3.61 (brs, 2H), 4.54-3.31 (m, 4H), 3.02 (overlapping t, 2H), 1.47 (brs, 9H); ESI-MS (m/z, %): 406 (M+Na, 60), 384 (MH+, 10), 328 (60), 284 (100)。
tert-ブチル2-ヒドロキシエチル(2-(7-ニトロ-2H-ベンゾ[b][1,4]チアジン-4(3H)-イル)エチル)カルバメート(220mg、0.574mmol)をアルゴン下で含有する丸底フラスコにパラジウム炭素(10%wt;61.0mg、0.057mmol)を装入した。混合物をアルゴンでパージした後、EtOH (20 mL)を加えた。得られる懸濁液をポンプを用いて真空に吸引し、水素を風船を経由して系内に導入した。混合物を、水素で満たした風船のもとで3時間攪拌した。水素風船を取外し、メチルチオフェン-2-カルビミドチオエートヨウ化水素酸塩(327mg、1.147mmol)を反応液に加えた。懸濁液を室温にて17時間(一晩)攪拌した。この後、混合物をセライトのパッドを通して濾過し、次いでこれをMeOH(10mL)で漱いだ。濾液を濃縮し、残留物を飽和炭酸水素ナトリウム溶液(50mL)とCH2Cl2(100mL)の間で分配した。混合物を分液漏斗に移し、抽出した。抽出後、有機層を分離し、乾燥し(Na2SO4)、濾過し、濃縮して暗色の残留物を得た。この残留物をシリカゲルのフラッシュクロマトグラフィ(2:98 MeOH/CH2Cl2、次いで3.5:96.5 (MeOH中の2M NH3):CH2Cl2)で処理して黄色の固体(140mg、52.7%)を得た。1H-NMR (DMSO-d6) δ 7.69 (brd, J = 3.0 Hz, 1H), 7.57 (d, J = 5.1 Hz, 1H), 7.07 (dd, J = 3.9, 4.8 Hz, 1H), 6.82-6.75 (m, 1H), 6.53-6.42 (m, 2H), 6.32 (brs, 2H), 4.73 (t, J = 5.4 Hz, 1H), 3.54 (brs, 2H), 3.50-3.42 (m, 2H), 3.38 (brs, 4H, overlp with 溶媒 peak), 3.27-3.19 (m, 2H), 3.08-2.96 (m, 2H), 1.41 (brs, 9H); ESI-MS (m/z, %): 463 (MH+, 100), 398 (60); HPLC 純度: 96.4% a/a。
tert-ブチル2-(メチル(2-(7-ニトロ-2H-ベンゾ[b][1,4]チアジン-4(3H)-イル)エチル)アミノ)アセテート(925mg、2.52mmol)を含有する丸底フラスコをアルゴンでパージし、次いでパラジウム炭素(10%wt;268mg、0.252mmol)を装入した。この混合物にEtOH(40mL)を加えた。得られる懸濁液をポンプを用いて真空吸引し、水素を系内に風船を経由して導入した。混合物を水素で満たした風船下で3時間攪拌した。風船を取外し、アルゴンを懸濁液を通して10分間バブリングした。混合物をセライトのパッドを通して濾過し、セライトパッドをメタノール(20mL)で漱いだ。濾液を濃縮し、残留物を減圧下で乾燥して表題化合物(850mg、定量)を得た。1H-NMR (CDCl3) δ 6.59 (d, J = 8.7 Hz, 1H), 6.45 (d, J = 2.4 Hz, 1H), 6.40 (dd, J = 2.7, 8.4 Hz, 1H), 3.54-3.45 (m, 2H), 3.33 (t, J = 7.2 Hz, 2H), 3.27 (brs, 2H), 3.20 (s, 2H), 3.04-2.98 (m, 2H), 2.71 (t, J = 7.5 Hz, 2H), 2.42 (s, 3H), 1.46 (s, 9H); ESI-MS (m/z, %): 338 (MH+, 95), 282 (100)。
THF(17.18mL、17.18mmol)中の1Mボランを(S)-tert-ブチル1-(2-(7-ニトロ-2H-ベンゾ[b][1,4]チアジン-4(3H)-イル)-2-オキソエチル)ピロリジン-2-カルボキシレート(1.4g、3.44mmol)に加え、得られる黄色溶液を室温にて一晩(17時間)攪拌した。黄色溶液を0℃に冷却し、MeOH(10 mL)で注意深くクエンチした。溶液を濃縮し、MeOH(50mL)に溶解し、再び濃縮して暗黄色の残留物を得た。この残留物をシリカゲルクロマトグラフィでBiotage精製系(カラム:シリサイクル(Silicycle)80g;勾配:10カラム体積にわたって20:80 EtOAc:ヘキサン〜60:40 EtOAc:ヘキサン;流量:45mL/min;採集波長:254nm)を用いて処理した。黄色残留物(550mg、40.7%)を得た。1H-NMR (CDCl3) δ 7.96 (d, J = 2.7 Hz, 1H), 7.87 (dd, J = 2.7, 9.3 Hz, 1H), 6.68 (d, J = 9.3 Hz, 1H), 3.86-3.82 (m, 2H), 3.57 (t, J = 7.5 Hz, 2H), 3.24-3.10 (m, 2H), 3.05-2.96 (m, 3H), 2.75-2.63 (m, 1H), 2.52-2.41 (m, 1H), 2.15-2.04 (m, 1H), 1.97-1.78 (m, 3H), 1.44 (s, 9H); ESI-MS (m/z, %): 394 (MH+, 25), 338 (100)。
(S)-tert-ブチル1-(2-(7-ニトロ-2H-ベンゾ[b][1,4]チアジン-4(3H)-イル)エチル)ピロリジン-2-カルボキシレート(525mg、1.334mmol)を含有する丸底フラスコをアルゴンでパージした。このフラスコにパラジウム炭素(10%wt;142mg、0.133mmol)を装入し、次いでEtOH(25mL)を装入した。得られる 懸濁液をポンプを用いて真空に吸引し、水素を風船を経由して導入した。混合物を水素で満たした風船の雰囲気下で2時間攪拌した。この時点で、水素風船を取外し、メチルチオフェン-2-カルビミドチオエートヨウ化水素酸塩(761mg、2.67mmol)を混合物に加えた。懸濁液を室温にて17時間(一晩)攪拌した。この時点で、混合物をセライトのパッドを通して濾過し、パッドをMeOH(20mL)で漱いだ。濾液を濃縮し、残留物を飽和炭酸水素ナトリウム溶液(50mL)とCH2Cl2(100mL)の間で分配した。混合物を分離漏斗に移し、抽出した。抽出後、有機層を分離し、乾燥し(Na2SO4)、濾過し、濃縮して暗色の残留物を得た。この残留物をシリカゲルのフラッシュクロマトグラフィで、2:98 MeOH:CH2Cl2、次いで3.5:96.5 (MeOH中の2M NH3):CH2Cl2を用いて処理して黄緑色の残留物(398mg、63.1%)を得た。1H-NMR (CDCl3) δ 7.39 (dd, J = 1.2, 5.1 Hz, 1H), 7.37 (dd, J = 1.2, 3.9 Hz, 1H), 7.05 (dd, J = 3.6, 4.8 Hz, 1H), 6.73 (brd, J = 5.1 Hz, 1H), 6.71 (brs, 1H), 6.65 (dd, J = 2.1, 8.7 Hz, 1H), 4.86 (brs, 2H), 3.63-3.60 (m, 2H), 3.44 (t, J = 7.5 Hz, 2H), 3.25-3.19 (m, 1H), 3.11 (brdd, J = 5.4, 8.4 Hz, 1H), 3.04-2.94 (m, 3H), 2.71-2.59 (m, 1H), 2.45 (brdd, J = 7.8, 16.2 Hz, 1H), 2.13-1.99 (m, 1H), 1.97-1.74 (m, 3H), 1.45 (s, 9H); ESI-MS (m/z, %): 473 (MH+, 90), 417 (85), 276 (100); HPLC 純度: 99.6% a/a。
(S)-tert-ブチル1-(2-(7-(チオフェン-2-カルボキシミドアミド)-2H-ベンゾ[b][1,4]チアジン-4(3H)-イル)エチル)ピロリジン-2-カルボキシレート(200mg、0.423mmol)のCH2Cl2(5mL)中の溶液をアニソール(0.092mL、0.846mmol)で処理した。反応液を0℃に冷却し、次いでトリフルオロ酢酸(2.76mL、25.4mmol)を加えた。混合物を0℃にて2時間攪拌し、次いで濃縮乾固した。この残留物に、ジオキサン(3.17mL、12.69mmol)中の4M HClを加え、得られる懸濁液を20分間攪拌した。この混合物をEt2O(10mL)で希釈し、1時間攪拌した。固体を濾過し、Et2O(10mL)で洗浄し、次いで減圧下で乾燥した。その固体を3N HCl(4.0mL、12.00mmol)に溶解し、50℃にて1時間加熱した。黄色の溶液を濃縮し、減圧下で乾燥して化合物18を黄色の固体(200mg、97%)として得た。1H-NMR (CD3OD) δ 7.98-7.94 (m, 2H), 7.28 (dd, J = 4.2, 4.8 Hz, 1H), 7.05-7.01 (m, 2H), 6.92 (d, J = 8.7 Hz, 1H), 4.42 (dd, J = 7.8, 9.0 Hz, 1H), 3.85-3.56 (m, 6H), 3.48-3.29 (m, 2H), 3.13-3.03 (m, 2H), 2.62-2.47 (m, 1H), 2.26-2.10 (m, 2H), 2.08-1.92 (m, 1H); ESI-MS (m/z, %): 417 (MH+、フリー塩基, 100);C20H25N4O2S2(MH+、フリー塩基)について計算したESI-HRMS:417.1419、測定値:417.1399;HPLC純度:99.5%a/a;光学回転:25[α]589=-27.0°、c=0.52(MeOH中)。
N-(4-(2-(ジメチルアミノ)エチル)-3,4-ジヒドロ-2H-ベンゾ[b][1,4]チアジン-7-イル)フラン-2-カルボキシミドアミド(0.166g、0.504mmol)をMeOH(2mL)に溶解した。エーテル(2.52mL、2.52mmol)中の1M HClをこの溶液に室温にて加え、反応液を5分間アルゴン雰囲気下で攪拌した。混合物を濃縮して淡黄色の固体(0.18g、93%)を得た。1H NMR (DMSO-d6) δ 11.36 (s, 1H), 11.25 (brs, 1H), 9.68 (s, 1H), 8.69 (s, 1H), 8.23 (s, 1H), 7.91 (d, J = 2.7 Hz, 1H), 7.07-6.96 (m, 3H), 6.90 (d, J = 1.8 Hz, 1H), 3.82-3.77 (m, 2H), 3.67-3.63 (m, 2H), 3.25-3.22 (m, 2H), 3.12-3.09 (m, 2H), 2.80 (s, 3H), 2.78 (s, 3H); ESI-MS (m/z, %): 333, 331 (MH+、フリー塩基, 100), 260, 262 (57);C17H23N4OS(MH+、フリー塩基)について計算したHRMS:計算値:331.1587、測定値:331.1589;HPLC純度:98%(面積による)。
実施例8に報じた手順に従って調製した。
4-(3-(ジメチルアミノ)プロピル)-3,4-ジヒドロ-2H-ベンゾ[b][1,4]チアジン-7-アミン(0.22g、0.875mmol)の乾燥エタノール(10mL)中の溶液を、メチルチオフェン-2-カルビミドチオエートヨウ化水素酸塩(0.499g、1.750mmol)で室温にて処理し、得られる混合物を一晩室温にて攪拌した(18時間)。反応液を飽和NaHCO3溶液(25mL)で希釈し、生成物をCH2Cl2(3×20mL)中に抽出した。組合わせたCH2Cl2層をブラインで洗浄し(15mL)、そして乾燥した(Na2SO4)。溶媒を蒸発させ、粗材料をシリカゲルのカラムクロマトグラフィ(5:95 (MeOH中の2MNH3):CH2Cl2)により精製して表題生成物22(0.27g、86%)を固体として得た。1H NMR (DMSO-d6) δ 7.68 (d, 1H, J = 3.0 Hz), 7.56 (d, 1H, J = 5.1 Hz), 7.06 (dd, 1H, J = 3.9, 4.8 Hz), 6.69 (d, 1H, J = 8.7 Hz), 6.52-6.45 (m, 2H), 6.33 (brs, 2H), 3.51-3.48 (m, 2H), 3.25 (t, 2H, J = 7.2 Hz), 3.04-3.01 (m, 2H), 2.25 (t, 2H, J = 6.9 Hz), 2.14 (s, 6H), 1.70-1.61 (m, 2H);ESI-MS(m/z、%):361(MH+、93)、276(100);HPLC純度:98.23%(面積による)。
N-(4-(3-(ジメチルアミノ)プロピル)-3,4-ジヒドロ-2H-ベンゾ[b][1,4]チアジン-7-イル)チオフェン-2-カルボキシミドアミド(0.16g、0.444mmol)の乾燥メタノール(5mL)中の溶液を、塩化水素(エーテル中の1M溶液;1.331mL、1.331mmol)で室温にて処理した。混合物を15分間攪拌し、溶媒を蒸発させ、残留物を高真空下で乾燥して表題生成物(0.19g、99%)を固体として得た。1H NMR (DMSO-d6) δ 11.22 (s, 1H), 10.91 (brs, 1H), 9.67 (s, 1H), 8.69 (s, 1H), 8.15-8.11 (m, 2H), 7.36 (t, 1H, J = 4.5 Hz), 7.04-6.88 (m, 3H), 3.64-3.61 (m, 2H), 3.41 (t, 2H, J = 6.9 Hz), 3.14-3.02 (m, 4H), 2.72 (d, 6H, J = 4.8 Hz), 2.06-1.98 (m, 2H); ESI-MS (m/z, %): 361 (MH+、フリー塩基, 91), 276 (100);C18H25N4S2(MH+、フリー塩基)について計算したESI-HRMS、計算値:361.1515、測定値:361.1515;HPLC純度:98.15%(面積による)。
tert-ブチルメチル(3-(7-ニトロ-2H-ベンゾ[b][1,4]チアジン-4(3H)-イル)プロピル)カルバメート(0.6g、1.633mmol)の乾燥メタノール(10mL)中の懸濁液を室温にてラネーニッケル(0.1g、1.633mmol)、次いでヒドラジン水和物(0.595mL、16.33mmol)で処理した。得られる混合物を10分間、予熱した油浴で還流した。反応液を次いで室温にし、セライトのパッドを通して濾過し、そしてメタノール(3×10mL)で洗浄した。組合わせたメタノール層を蒸発させ、粗材料をシリカゲルのフラッシュカラムクロマトグラフィ(5:95 (MeOH中の2M NH3):CH2Cl2)により精製して表題生成物(0.55g、定量)を褐色のシロップとして得た。1H NMR (DMSO-d6) δ 6.46 (d, 1H, J = 9.6 Hz), 6.25-6.21 (m, 2H), 4.44 (s, 2H), 3.32-3.28 (m, 2H), 3.19 (t, 2H, J = 6.9 Hz), 3.04 (t, 2H, J = 7.2 Hz), 3.00-2.97 (m, 2H), 2.77 (s, 3H), 1.74-1.62 (m, 2H), 1.38 (s, 9H); ESI-MS (m/z, %): 338 (MH+, 100), 337 (96), 282 (54)。
トリフェニルホスフィン(1.81g、6.93mmol)およびイミダゾール(1.887mL、13.86mmol)のTHF(15mL)中の攪拌溶液に、0℃にてヨウ素(1.759g、6.93mmol)を加えた。5分間攪拌後、2-(2-アミノ-4-ニトロフェニルチオ)エタノール(990mg、4.62mmol)をTHF(5mL)中の溶液として加えた。得られる混合物を0℃にて1時間攪拌し、次いで酢酸エチルで希釈し、そして水(3×)およびブラインで洗浄した。有機相を乾燥し、濾過し、濃縮し、次いでクロマトグラフィ(4:1 ヘキサン:酢酸エチル)で処理し、所望の化合物をオレンジ色の固体(1.18g、79%)として得た。1H NMR (DMSO-d6) δ 7.55 (d, J = 2.4 Hz, 1H), 7.45 (d, J = 8.4 Hz, 1H), 7.34 (dd, J = 8.4, 2.4 Hz, 1H), 5.89 (brs, 2H), 3.38-3.26 (m, 4H); EI-MS (m/z, %): 324 (M+, 46), 196 (81), 154 (100), 126 (95)。
tert-ブチル2-(6-アミノ-2H-ベンゾ[b][1,4]チアジン-4(3H)-イル)エチル(エチル)カルバメート(800mg、2.371mmol)のエタノール(8mL)中の攪拌溶液に、メチルチオフェン-2-カルビミドチオエートヨウ化水素酸塩(1.014g、3.56mmol)を加えた。得られる混合物を室温にて3時間攪拌した。混合物を次いで酢酸エチルで希釈し、そして飽和炭酸ナトリウム(3×)で洗浄した。有機相を乾燥し、濾過し、濃縮し、次いでクロマトグラフィ(1:1 ヘキサン:酢酸エチル)で処理して所望の生成物(415mg、39.2%)を得た。1H NMR (DMSO-d6) δ 7.70 (d, J = 3.0 Hz, 1H), 7.58 (d, J = 2.4 Hz, 1H), 7.49-7.44 (m, 1H), 7.07 (t, J = 4.4 Hz, 1H), 6.84 (d, J = 7.8 Hz, 1H), 6.35-6.26 (m, 2H), 6.08 (d, J = 7.5 Hz, 1H), 3.64-3.49 (m, 2H), 3.45-3.25 (m, 4H), 3.24-3.12 (m, 2H), 3.01-2.85 (m, 2H), 1.39-1.29 (m, 9H), 1.02 (t, J = 6.9 Hz, 3H); ESI-MS (m/z, %): 447 (MH+, 100)。
N-(4-(2-(エチルアミノ)エチル)-3,4-ジヒドロ-2H-ベンゾ[b][1,4]チアジン-6-イル)チオフェン-2-カルボキシミドアミド(131mg、0.378mmol)のメタノール(2mL)中の溶液に、塩化水素(ジエチルエーテル中の1M;1.134mL、1.134mmol)を加えた。得られる混合物を真空で濃縮してオレンジ色の固体(159mg、100%)を得た。1H NMR (DMSO-d6) δ 11.43 (s, 1H), 9.72 (s, 1H), 9.22 (brs, 2H), 8.73 (s, 1H), 8.18-8.12 (m, 2H), 7.38-7.34 (m, 1H), 7.14-7.05 (m, 2H), 6.64-6.60 (m, 1H), 3.70-3.61 (m, 4H), 3.16-3.02 (m, 4H), 2.99-2.88 (m, 2H), 1.21 (t, J = 7.2 Hz, 3H);(C17H23N4S2、MH+、フリー塩基)について計算したHRMS:計算値:347.1358、測定値:347.1346;HPLC純度:97%(面積による)。
N,N-ジメチル-2-(6-ニトロ-2H-ベンゾ[b][1,4]チアジン-4(3H)-イル)エタンアミン(75mg、0.281mmol)およびパラジウム10重量%担持活性炭(29.9mg、0.028mmol)のエタノール(5mL)中の懸濁液を室温にて水素雰囲気(風船圧)下で90分間攪拌した。この間に、反応液の黄色は消えた。この混合物に、次いでメチルチオフェン-2-カルビミドチオエートヨウ化水素酸塩(160mg、0.561mmol)を加え、得られる懸濁液を一晩室温にて攪拌した。混合物を次いでジクロロメタンで希釈し、濾過してパラジウムを除去した。有機濾液をさらに水および飽和炭酸ナトリウム(1:1)で希釈した。有機層を分離し、水層を再びジクロロメタンで抽出した。組合わせた有機相を乾燥し、濾過し、濃縮し、次いでクロマトグラフィ(1:19 (メタノール中の2M NH3):酢酸エチル)で処理して所望の生成物27(61mg、62.8%)を得た。1H NMR (DMSO-d6) δ 7.71 (d, J = 3.3 Hz, 1H), 7.58 (d, J = 5.1 Hz, 1H), 7.10-7.06 (m, 1H), 6.83 (d, J = 8.1 Hz, 1H), 6.37 (brs, 2H), 6.17 (s, 1H), 6.08 (d, J = 7.8 Hz, 1H), 3.63-3.58 (m, 2H), 3.39-3.32 (m, 2H), 3.01-2.96 (m, 2H), 2.42 (t, J = 6.9 Hz, 2H), 2.10 (s, 6H); ESI-MS (m/z, %): 347 (MH+, 100), 276 (74);C17H23N4S2(MH+)について計算したESI-HRMS、計算値:347.1358、測定値:347.1349;HPLC純度:95%(面積による)。
tert-ブチルメチル(2-(6-(チオフェン-2-カルボキシミドアミド)-2H-ベンゾ[b][1,4]チアジン-4(3H)-イル)エチル)カルバメート(415mg、0.959mmol)のメタノール(4mL)中の攪拌溶液に、3N HCl溶液(3.198mL、9.59mmol)を加えた。得られる混合物を次いで90℃にて1時間攪拌した。その混合物を次いで室温に冷却し、水で希釈し、3N水酸化ナトリウムでpH12に塩基性化し、そしてジクロロメタン(3×)で抽出した。組合わせた有機相を乾燥し、濾過し、濃縮し次いでクロマトグラフィ(1:9 (メタノール中の2M NH3):酢酸エチル)で処理して所望の生成物28(165mg、51.7%)を得た。1H NMR (DMSO-d6) δ 7.71 (d, J = 3.0 Hz, 1H), 7.58 (d, J = 5.1 Hz, 1H), 7.10-7.06 (m, 1H), 6.82 (d, J = 8.1 Hz, 1H), 6.34 (brs, 2H), 6.22 (s, 1H), 6.07 (d, J = 8.1 Hz, 1H), 3.62-3.57 (m, 2H), 3.32 (t, J = 6.8 Hz, 2H), 3.01-2.97 (m, 2H), 2.64 (t, J = 6.8 Hz, 1H), 2.29 (s, 3H). ESI-MS (m/z, %): 333 (MH+, 100), 276 (71);C16H21N4S2(MH+)について計算したESI-HRMS、計算値:333.1202、測定値:333.1207;HPLC純度:97%(面積による)。
N-(4-(2-(メチルアミノ)エチル)-3,4-ジヒドロ-2H-ベンゾ[b][1,4]チアジン-6-イル)チオフェン-2-カルボキシミドアミド(158mg、0.475mmol)のメタノール(3mL)中の溶液に、塩化水素(ジエチルエーテル中の1M;1.426mL、1.426mmol)を加えた。得られる混合物を真空で濃縮して黄色固体(192mg、100%)を得た。1H NMR (DMSO-d6) δ 11.47 (s, 1H), 9.76 (s, 1H), 9.31-9.19 (m, 2H), 8.74 (s, 1H), 8.20-8.11 (m, 2H), 7.39-7.33 (m, 1H), 7.11 (d, J = 8.1 Hz, 1H), 7.04 (s, 1H), 6.62 (d, J = 7.8 Hz, 1H), 3.71-3.61 (m, 4H), 3.18-3.04 (m, 4H), 2.58-2.52 (m, 3H);HRMS(C16H21N4S2、MH+、フリー塩基):計算値:333.1202、測定値:333.1207;HPLC純度:97%(面積による)。
tert-ブチル4-(2-クロロ-5-ニトロフェニルアミノ)ピペリジン-1-カルボキシレート(1.25g、3.51mmol)のDMF(10mL)中の攪拌溶液に順に、炭酸カリウム(0.971g、7.03mmol)および2-メルカプトエタノール(0.493mL、7.03mmol)を加えた。得られる混合物を60℃にて1時間攪拌し、その後、TLC分析(2:3 酢酸エチル:ヘキサン)は反応が完了したことを示した。混合物を次いで酢酸エチルで希釈し、順に水および飽和炭酸ナトリウム(3×)で洗浄した。有機相を乾燥し、濾過し、濃縮し、次いでクロマトグラフィ(2:3 酢酸エチル:ヘキサン)で処理して所望の生成物(1.202g、86%)をオレンジ色の泡状物として得た。1H NMR (DMSO-d6) δ 7.51 (d, J = 8.4 Hz, 1H), 7.43-7.37 (m, 2H), 5.40 (d, J = 8.1 Hz, 1H), 5.06 (t, J = 5.4 Hz, 1H), 3.95-3.86 (m, 2H), 3.75-3.60 (m, 1H), 3.59-3.50 (m, 2H), 3.01-2.85 (m, 4H), 1.94-1.83 (m, 2H), 1.49-1.29 (m, 11H); ESI-MS (m/z, %): 420 (M+Na, 22), 342 (100)。
tert-ブチル3-(2H-ベンゾ[b][1,4]チアジン-4(3H)-イル)ピロリジン-1-カルボキシレート(0.41g、1.302mmol)のDMF(5mL)中の溶液を0℃に冷却し、DMF(5mL)中のN-ブロモスクシンイミド(0.17g、0.977mmol)を滴状で用いて15分間処理した。反応液を0℃に保ち、1時間この温度で攪拌した。この時点に、DMF(1mL)中のN-ブロモスクシンイミド(0.023g、0.130mmol)を滴状で反応液に加え、これを次いで1時間0℃にて攪拌した。溶液を再びDMF(1mL)中のN-ブロモスクシンイミド(0.023g、0.130mmol)で処理し、1時間0℃にて攪拌した。溶液を水(100mL)で希釈し、EtOAc(2×100mL)で抽出した。水相を1回EtOAc(50mL)で洗浄した。有機溶液を組合わせて、水(100mL)およびブライン(50mL)で洗浄し、そして乾燥した(Na2SO4)。粗材料をシリカパッドを通して濾過し(20%EtOAc/ヘキサン)、濃縮して透明な油(0.47g、90%)を得た。1H NMR (CDCl3) δ 7.18 (d, J = 2.4 Hz, 1H), 7.07 (d, J = 8.7 Hz, 1H), 6.62 (d, J = 8.7 Hz, 1H), 4.34-4.28 (m, 1H), 3.71-3.23 (m, 6H), 3.03-3.04 (m, 2H), 2.19-1.95 (m, 2H), 1.47 (s, 9H); ESI-MS (m/z, %): 423, 421 (M+Na, 8), 401, 399 (MH+, 2), 343, 345 (100)。
実施例18に報じた手順に従って調製した。
tert-ブチルエチル(2-(7-ニトロ-2H-ベンゾ[b][1,4]チアジン-4(3H)-イル)-2-オキソエチル)カルバメート(0.8g、2.097mmol)の無水テトラヒドロフラン(5mL)中の溶液をボラン-THF錯体(THF中の1M;6.29mL、6.29mmol)で処理し、室温にて3時間攪拌した。反応液をメタノール(10mL)を滴状で用いてクエンチし、次いで濃縮した。粗残留物をメタノール(25mL)で希釈し、10分間還流した。混合物を次いで濃縮し、残留物をシリカゲルのカラムクロマトグラフィ(1:9〜3:7 EtOAc:CH2Cl2)で処理して黄色シロップ(0.493g、64%)を得た。1H-NMR (DMSO-d6) δ 7.85-7.78 (m, 2H), 6.94-6.85 (m, 1H), 3.76-3.79 (m, 2H), 3.62-3.57 (m, 2H), 3.37- 3.33 (m, 2H), 3.22-3.19 (m, 2H), 3.08-3.04 (m, 2H), 1.35 and 1.30 (2 × brs, 9H), 1.03 (t, J = 6.9 Hz, 3H). ESI-MS (m/z, %):390 (M+Na, 67%), 368 (MH+, 17%), 312 (83%), 268 (100%)。
tert-ブチルエチル(2-(7-(チオフェン-2-カルボキシミドアミド)-2H-ベンゾ[b][1,4]チアジン-4(3H)-イル)エチル)カルバメート(0.4g、0.896mmol)のメタノール(10mL)中の溶液を3NHCl(3.88mL、11.64mmol)で処理し、還流にて1.5時間攪拌した。混合物を室温にて冷却し、水(20mL)で希釈し、1N NaOHで塩基性化した。生成物をジクロロメタン(2×25mL)中に抽出した。組合わせた有機層を乾燥し(Na2SO4)、そして濃縮した。粗材料をシリカゲルのクロマトグラフィ(5:95 (MeOH中の2M NH3):CH2Cl2)で処理して黄色固体(0.142g、45.8%)を得た。1H-NMR (DMSO-d6) δ 7.69 (dd, J = 0.9, 3.6 Hz, 1H), 7.56 (d, J = 5.1 Hz, 1H), 7.07 (dd, J = 3.6, 4.8 Hz, 1H), 6.72 (d, J = 8.7 Hz, 1H), 6.49 (dd, J = 2.1, 8.4 Hz, 1H), 6.45 (d, J = 2.1 Hz, 1H), 6.31 (brs, 2H), 3.55 -3.51 (m, 2H), 3.30-3.24 (m, 2H), 3.04-3.00 (m, 2H), 2.62 (t, J = 6.9 Hz, 2H), 2.56 (q, J = 7.2 Hz, 2H), 1.01 (t, J = 7.2 Hz, 3H); ESI-MS (m/z, %): 347 (MH+, 75%), 276 (100%); HPLC 純度: 99.5% (面積による)。
N-(4-(2-(エチルアミノ)エチル)-3,4-ジヒドロ-2H-ベンゾ[b][1,4]チアジン-7-イル)チオフェン-2-カルボキシミドアミド(0.142g、0.410mmol)の乾燥メタノール(5mL)中の溶液を塩酸(エーテル中の1M;2.049mL、2.049mmol)で処理し、室温にて1時間攪拌した。反応液を次いで濃縮して黄色固体を得た。1H-NMR (DMSO-d6) δ 11.22 (brs, 1H) 9.68 (brs, 1H), 9.32 (brs, 2H), 8.69 (brs, 1H), 8.15-8.11 (m, 2H), 7.36 (pseudo t, J = 7.2 Hz, 1H), 7.06-6.99 (m, 3H), 3.70-3.60 (overlap with 溶媒 peak, m, 4H), 3.12-3.02 (m, 4H), 3.02-2.93 (m, 2H), 1.23 (t, J = 7.2 Hz, 3H)。
ヒトiNOSアッセイを本明細書に記載した2つのプロトコルのどちらか1つにより行なった:
プロトコル1:
組換えヒト誘導型NOS(iNOS)は、バキュロウイルスに感染したSf9細胞(ALEXIS)において産生した。放射測定法において、NOシンターゼ活性を、[3H]L-アルギニンから[3H]L-シトルリンへの変換を測定することによって決定した。iNOSを測定するために、10μLの酵素を、1mM CaCl2、1mM EDTA、1mM ジチオスレイトール、1μM FMN、1μM FAD、10μM テトラヒドロビオプテリン、120μM NADPH、および100nM CaMを含有する100μLの100mM HEPES、pH=7.4に加えた。
試薬と材料:
酵素:一酸化窒素シンターゼ(誘導型、ヒト組換え)iNOS II、カタログ番号 ALX-201-060、Axxora LLC、CA 92121、USA;
L-NMMA:NG-モノメチル-L-アルギニン二塩酸塩、カタログ番号M7033、Sigma Aldrich;
反応バッファー:50mM トリス-HCl(pH 7.4)、カタログ番号93313、Sigma-AldrichCo.、St.Louis、MO;6μM テトラヒドロビオプテリン二塩酸塩(BH4)、カタログ番号T4425、Sigma;2μM フラビンアデニンジヌクレオチド(FAD)、カタログ番号 F6625、Sigma;2μM フラビンアデニンモノヌクレオチド(FMN)、カタログ番号 F8399、Sigma;
停止バッファー:50mM N-2-ヒドロキシエチルピペラジン-N’-2-エタンスルホン酸(HEPES)(pH5.5)、H7523、Sigma;および
5mM エチレンジアミン四酢酸(EDTA)、カタログ番号 EDS、Sigma;
NADPH:10mM トリス-HCl(pH7.4)中に調製した12mM、カタログ番号 N7505、Sigma;
カルモジュリン:1mM、カタログ番号 P2277、Sigma;
[3H]-L-アルギニン:1μCi/反応、40-70 Ci/mmol、カタログ番号 TRK-698、Amersham Biosciences;
L-アルギニン:2.5μM(最終アッセイ濃度)、カタログ番号 A5131、Sigma;
平衡化した樹脂:HEPESバッファー(pH5.5)中のAG-50WX8樹脂、カタログ番号1421441、Bio-Rad Laboratories Ltd.;
スピンカップ:カタログ番号 C8163、Fisher Scientific;
Microbeta:Wallac Microbeta Trilux、Perkin Elmer;
液シンチレーション液:Optiphase Supermix、カタログ番号 1200-439、Perkin Elmer;
インキュベーター:Lab-Line Enviro Shaker;
微量遠心分離機:Mikro 20。
研究の日に、各化合物の一次ストック溶液を蒸留水で6mMの最終濃度となるように調製した。IC50値を決定するために、11種の試験化合物濃度を3倍連続希釈液として調製した。試験化合物はiNOSアッセイにおいて1000μM〜0.0169μMの濃度で試験した。試験化合物または阻害剤のビヒクル(蒸留水)をブランク対照として用いた。非特異的活性については、100μML-NMMAを対照として平行して試験した。
10μLの試験化合物、参照阻害剤、または対照(ビヒクルまたはL-NMMA)溶液;
25μLの反応バッファー(50mM トリス-HCl、6μM BH4、2μM FMN、2μM FAD);
5μLの10mM NADPH溶液;
5μLの蒸留水;
5μLの1μM カルモジュリン;および
5μLの0.0024μg/μL iNOS。
試薬と材料
酵素:一酸化窒素シンターゼ(神経細胞、ヒト組換え)nNOS I、カタログ番号 ALX-201-068、Axxora LLC、CA 92121、USA;
一酸化窒素シンターゼ(内皮,ヒト組換え)eNOS III、カタログ番号 ALX-201- 070、Axxora LLC;
L-NMMA:NG-モノメチル-L-アルギニン 1/04/05、カタログ番号 A17933、Novabiochem;
L-NAME:NG-ニトロ-L-アルギニンメチルエステル、カタログ番号 N5751、Aldrich;
2X反応バッファー:50mMトリス-HCl(pH7.4)、カタログ番号93313、Sigma-Aldrich Co.、St. Louis、MO;6μM テトラヒドロビオプテリン(BH4)、カタログ番号 T4425、Sigma;2μM フラビンアデニンジヌクレオチド(FAD)、カタログ番号 F6625、Sigma;2μM フラビンアデニンモノヌクレオチド(FMN)、カタログ番号 F8399、Sigma;
停止バッファー:50mM N-2-ヒドロキシエチルピペラジン-N’-2-エタンスルホン酸(HEPES)(pH 5.5)、H7523、Sigma、および5mM エチレンジアミン四酢酸(EDTA)、カタログ番号 EDS、Sigma;
NADPH:試験日に新しく調製した10 mM、カタログ番号N7505、Sigma;
塩化カルシウム:6mM、カタログ番号 21107、Sigma;
カルモジュリン:1mM、カタログ番号 P2277、Sigma;
[3H]-L-アルギニン:1μCi/反応、40-70 Ci/mmol、カタログ番号 TRK-698、Amersham Biosciences;
L-アルギニン:2.5μM(最終アッセイ濃度)、カタログ番号 A5131、Sigma;
平衡化した樹脂:HEPESバッファー(pH5.5)中のAG-50WX8樹脂、カタログ番号1421441、Bio-Rad Laboratories Ltd.;
スピンカップとホルダー:カタログ番号 C8163、Fisher Scientific;
液シンチレーションカウンター:Tri-Carb 2000CA/LL、Canberra Packard Canada;
液シンチレーション液:カタログ番号6012239、Ultima Gold、Perkin-Elmer Life および Analytical Sciences、MA;
CO2インキュベーター:Lab-Line Enviro Shaker;
微量遠心分離機:Mikro 20;
ボルテックスミキサー:Mini Vortex mixer、IKA。
試験化合物の6mMの濃度の一次ストック溶液を2〜5mg粉末から調製した。各試験化合物の一次ストック溶液は、研究の日に蒸留水で新しく調製し、6mMの最終濃度となるようにした。IC50値を決定するために、12種の試験化合物濃度を3倍連続希釈液として調製した。使用した試験化合物の濃度範囲は、nNOSについて0.001〜300μM、およびeNOSについて0.003〜1000μMであった。試験化合物または阻害剤のビヒクルをブランク対照として用いた。非特異的活性用には100μML-NMMAを用いた。L-NAMEのIC50濃度を用いる試験は対照と平行して実施した。
10μLの試験化合物、阻害剤または対照(ビヒクルまたはL-NMMA)溶液;
25μLの反応バッファー{25mMトリス-HCl、0.6μMBH4、0.2μMFMN、0.2μMFAD};
5μLの10mM NADPH溶液{1mM}(10mMトリス-HCl(pH7.4)で新しく調製した);
5μLの6mM CaCl2{600μM};
5μLの1mM カルモジュリン{100μM};および
5μLの0.02μg/μL nNOSまたは0.12μg/μL eNOS。
Xは試験化合物または阻害剤濃度の対数値である。
慢性狭窄傷害を含む神経傷害に関わるいくつかの神経因性疼痛の動物モデルが記載されており、これらとしては、CCIまたはBennettモデル(例えば、Bennett and Xie, Pain, 33: 87-107, 1988;Vissers et al. Pharmacol. Biochem. Behav. 84: 479-486, 2006を参照)、脊髄神経結紮(SNLまたはChungモデル;例えば、Kim ら Neurosci. Lett. 199: 158-60、1995を参照)、およびSeltzerモデル(Seltzer et al. Pain 43: 205-18, 1990)が挙げられる。これらのモデルは、薬物間でヒトにおける実証された活性とこれらのモデルの薬理学的活性について良い相関を示す(Kontinen and Meert, In: Dostrovsky J., Carr D.B., Kotzenburg M., editors. 10th World Congress on Pain, 2003, 24. San Diego, California: IASP Press, 489-98)。概して、これらの動物モデルは行動応答、例えば、機械的閾値の低下、機械的痛覚過敏、化学機能亢進、温熱痛覚過敏および冷感アロディニアに変化を示す(Dowdell et al. Pharmacol. Biochem. Behavior 80: 93-108, 2005)。
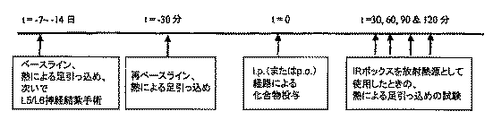
神経因性疼痛のためのChung脊髄神経結紮SNLモデルアッセイの実験計画を、図1および2に示す。KimおよびChung(Kim and Chung, Pain 50:355-363, 1992)に記載の方法に従って、神経結紮損傷を行った。この技法は、触覚アロディニア、温熱痛覚過敏、および冒された足の保護を含む神経因性知覚異常の徴候を生じさせる。ラットをハロタンによって麻酔し、L4からS2領域に亘る脊椎を露出させた。L5およびL6脊髄神経を露出させ、注意深く単離し、DRGに対して末梢側を4-0絹縫合糸でしっかりと結紮した。恒常性の安定を確認した後、傷を縫合し、動物を個々のケージ内で回復させた。偽手術ラットを、L5/L6脊髄神経を結紮しないことを除けば同様の方法で作製した。運動障害の徴候を示したラットは安楽死させた。外科的介入に続く回復期後、ラットは、痛み刺激、および通常では無痛の刺激に対して増強された感受性を示す。
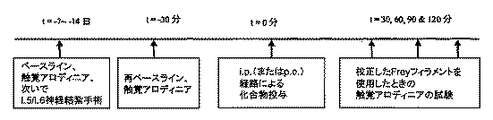
炎症性スープ(IS)または化学刺激のラットの硬膜トップへの施用は、中枢感作の発症および顔面領域ならびに動物の後足における機械的アロディニアの発現を誘発することが実証されている。これらの特性は頭痛の間に、とりわけ、治療が遅れて、中枢感作の発症が起こった時に、片頭痛でしばしばみられる特徴を模倣している(Burstein et al., Ann. Neurol. 47:614-624, 2000; Burstein et al., Brain, 123:1703-1709, 2000)。化合物(8)を片頭痛の硬膜炎症モデルにおいて先に記載の手順(WO2007/120830またはUS-2008-0031822-A1)に従って試験した。IS投与のほぼ30分前に、校正したvon Freyフィラメントの後足への適用により触覚アロディニアを測定してベースライン足引っ込め閾値を記録した。IS投与投与のほぼ15分前に、水中の試験化合物を経口胃管栄養法(1mL/kg)により3mg/kg経口(p.o.)の用量で投与した。触覚アロディニアの測定値をIS投与後6時間まで1時間間隔で記録した。化合物8(3mg/kg p.o.)の抗アロディニア効果を図5に示した。
0.1mLの3%カラゲナン懸濁液を、軽く麻酔したラットの後足の取って代わる側にs.c.注射することにより、炎症を誘導した。典型的には、顕著な炎症および浮腫が注入の3時間以内に現れた。このカラゲナンモデルは2つの成分をもつ炎症性疼痛のモデルであり:注入後直ぐ起こる第1成分は、有痛刺激(この場合、化学物質のカラゲナン)に対する急性侵害性応答の情報を与える。また、第2の神経因性成分も存在し、これは数時間後に発生して神経因性疼痛で見られる痛覚過敏およびアロディニア成分に因る神経細胞活性の型である。多くの確証は、NOとその酵素群が脊髄レベルで炎症性痛覚過敏の中枢機構に関わること、および末梢炎症が脊髄におけるnNOS発現をアップレギュレートしかつiNOS発現を誘導しうることを示している(Guhring et al., J. Neurosci. 20:6714-6720, 2000; Wu et al., Exp. Brain Res. 118:457-465, 1998;およびWu et al., Pain 94:47-58, 2001)。さらに、動物におけるiNOSノックアウト研究は、nNOSがカラゲナン炎症性疼痛の二次成分の発生と維持に必須である一方、iNOSは温熱痛覚過敏の後期に十分であるが必須でないことを示す(Tao et al., Neuroscience 120:847-854, 2003)。図6は、カラゲナン注射および化合物(8)の投与後のラットの同側の足における機械的アロディニアの逆転を示す。図7は、温熱刺激に対する足引っ込め潜伏時間により測定したi.p.投与後の化合物によるラットの同側の足における温熱痛覚過敏の逆転(後期)を示す。
現在好ましい実施例であると考えられるものを参照して本発明を説明してきたが、本発明は開示した実施例に限定されないことを理解すべきである。それとは反対に、本発明は、添付の特許請求の精神および範囲内に含まれる様々な修正形態および同様の組合せを包含することを意図する。
いくつかの実施形態を以下に示す。
項1
式:
Qは-O-(CHR 6 ) 1-3 または-S-(CHR 6 ) 1-3 -であり;
R 1 およびそれぞれのR 6 は、独立して、H、任意に置換されたC 1-6 アルキル、任意に置換されたC 1-4 アルカリール、任意に置換されたC 1-4 アルクヘテロシクリル、任意に置換されたC 2-9 ヘテロシクリル、任意に置換されたC 3-8 シクロアルキル、任意に置換されたC 1-4 アルクシクロアルキルまたは-(CR 1A R 1B ) n NR 1C R 1D であり;
R 1A およびR 1B は、独立して、H、ヒドロキシ、ハロ、任意に置換されたC 1-6 アルキル、任意に置換されたC 1-6 アルコキシ、任意に置換されたC 1-4 アルクシクロアルキル、任意に置換されたC 1-4 アルカリール、任意に置換されたC 1-4 アルクヘテロシクリル、任意に置換されたC 1-4 アルクヘテロアリール、任意に置換されたC 3-8 シクロアルキル、または任意に置換されたC 2-9 ヘテロシクリルであるか、またはR 1A およびR 1B は一緒に=Oを形成し;
R 1C およびR 1D は、独立して、H、任意に置換されたC 1-6 アルキル、任意に置換されたC 1-6 アルコキシ、任意に置換されたC 1-4 アルクシクロアルキル、任意に置換されたC 1-4 アルカリール、任意に置換されたC 1-4 アルクヘテロシクリル、任意に置換されたC 1-4 アルクヘテロアリール、任意に置換されたC 3-8 シクロアルキル、任意に置換されたC 2-9 ヘテロシクリル、もしくはN-保護基であるか、またはR 1C およびR 1D は一緒に任意に置換されたC 2-9 ヘテロシクリルもしくはN-保護基を形成し;
nは整数1〜6であり;
R 2 およびR 3 のそれぞれは、独立して、H、hal、任意に置換されたC 1-6 アルキル、任意に置換されたC 6-10 アリール、任意に置換されたC 1-6 アルカリール、任意に置換されたC 2-9 ヘテロシクリル、ヒドロキシ、任意に置換されたC 1-6 アルコキシ、任意に置換されたC 1-6 チオアルコキシ、(CH 2 ) r2 NHC(NH)R 2A 、または(CH 2 ) r2 NHC(S)NHR 2A 、または任意に置換されたC 1-4 アルクヘテロシクリルであり、
ここで、r2は整数0〜2であり、R 2A は任意に置換されたC 1-6 アルキル、任意に置換されたC 6-10 アリール、任意に置換されたC 1-4 アルカリール、任意に置換されたC 2-9 ヘテロシクリル、任意に置換されたC 1-4 アルクヘテロシクリル、任意に置換されたC 1-6 チオアルコキシ、任意に置換されたC 1-4 チオアルカリール、任意に置換されたアリーロイル、任意に置換されたC 1-4 チオアルクヘテロシクリル、または任意に置換されたアミノであり;
R 4 およびR 5 のそれぞれは独立してH、hal、(CH 2 ) r2 NHC(NH)R 2A 、または(CH 2 ) r2 NHC(S)NHR 2A であり;
ここで、Y 1 およびY 2 はそれぞれHであるかまたはY 1 およびY 2 は一緒に=Oであるか、またはY 1 およびY 2 は独立してH、任意に置換されたC 1-6 アルキル、任意に置換されたC 6-10 アリール、任意に置換されたC 1-6 アルカリール、任意に置換されたC 2-9 ヘテロシクリル、ヒドロキシ、任意に置換されたC 1-6 アルコキシ、任意に置換されたC 1-6 チオアルコキシ、または任意に置換されたC 1-4 アルクヘテロシクリルであり;
ここで、R 2 、R 3 、R 4 、およびR 5 のうちの1つだけは(CH 2 ) r2 NHC(NH)R 2A または(CH 2 ) r2 NHC(S)NHR 2A である]
を有する化合物またはその製薬上許容される塩またはプロドラッグ。
項2
QはO-(CHR 6 ) 1-2 またはS-(CHR 6 ) 1-2 であり;R 1 およびそれぞれのR 6 は、独立して、H、任意に置換されたC 1-6 アルキル、任意に置換されたC 1-4 アルカリール、任意に置換されたC 1-4 アルクヘテロシクリル、または任意に置換されたC 2-9 ヘテロシクリルである、項1に記載の化合物。
項3
R 2 、R 3 、R 4 、またはR 5 は式:
項4
R 2A は式:
X 1 、X 2 、X 4 、およびX 5 のそれぞれは独立してO、S、NR 7 、N、またはCR 8 から選択され;
X 3 はNまたはCから選択され;
R 7 はH、任意に置換されたC 1-6 アルキルであり;
R 8 はH、hal、任意に置換されたC 1-6 アルキル、ヒドロキシ、任意に置換されたC 1-6 アルコキシ、または任意に置換されたC 1-6 チオアルコキシであり、
ここで、X 1 、X 2 、X 4 、およびX 5 の少なくとも1つはCR 8 でない、項3に記載の化合物。
項5
R 2A は式:
X 1 およびX 2 のそれぞれは独立してO、S、NH、N、またはCHから選択され;
ここでX 1 およびX 2 の少なくとも1つはCHでない、項4に記載の化合物。
項6
項7
項8
Y 1 およびY 2 はそれぞれHであり、かつQはO-CHR 6 である、項1に記載の化合物。
項9
Y 1 およびY 2 はそれぞれHであり、かつQはS-CHR 6 である、項1に記載の化合物。
項10
Y 1 およびY 2 は一緒に=Oであり、かつQはO-CHR 6 である、項1に記載の化合物。
項11
Y 1 およびY 2 は一緒に=Oであり、かつQはS-CHR 6 である、項1に記載の化合物。
項12
Y 1 およびY 2 は一緒に=Oであり、かつQはO-(CHR 6 ) 2 である、項1に記載の化合物。
項13
Y 1 およびY 2 はそれぞれHであり、かつQはS-(CHR 6 ) 2 である、項1に記載の化合物。
項14
Y 1 およびY 2 は一緒に=Oであり、かつQはS-(CHR 6 ) 2 である、項1に記載の化合物。
項15
Y 1 およびY 2 はそれぞれHであり、かつQはO-(CHR 6 ) 2 である、項1に記載の化合物。
項16
Y 1 およびY 2 は一緒に=Oであり、かつQはO-(CHR 6 ) 3 である、項1に記載の化合物。
項17
Y 1 およびY 2 はそれぞれHであり、かつQはS-(CHR 6 ) 3 である、項1に記載の化合物。
項18
Y 1 およびY 2 は一緒に=Oであり、かつQはS-(CHR 6 ) 3 である、項1に記載の化合物。
項19
Y 1 およびY 2 はそれぞれHであり、かつQはO-(CHR 6 ) 3 である、項1に記載の化合物。
項20
R 1 が任意に置換されたC 1-6 アルキル、任意に置換されたC 2-9 ヘテロシクリル、または任意に置換されたC 1-4 アルクヘテロシクリルである、項1〜19に記載の化合物。
項21
R 1 が任意に置換されたアミノC 1-6 アルキルである、項20に記載の化合物。
項22
R 1 が任意に置換されたC 1-4 アルクヘテロシクリルであり、前記ヘテロシクリルが5または6員の環状アミンである、項20に記載の化合物。
項23
前記環状アミンがカルボン酸、C 1-6 エステル、またはアミドで置換されている、項26に記載の化合物。
項24
R 1 が任意に置換されたC 2-9 ヘテロシクリルである、項20に記載の化合物。
項25
前記ヘテロシクリルが任意に置換されたピロリジニルまたは任意に置換されたピペリジニルである、項24に記載の化合物。
項26
R 1 が
項27
R 9 がHである、項26に記載の化合物。
項28
R 1 が任意に置換されたC 3 -C 8 シクロアルキルまたは-(CR 1A R 1B ) n NR 1C R 1D である、項1および項3〜19のいずれか1項に記載の化合物。
項29
R 1 が-(CR 1A R 1B ) n NR 1C R 1D である、項28に記載の化合物。
項30
R 1A およびR 1B がそれぞれHであり、かつnが2または3である、項29に記載の化合物。
項31
NR 1C がHでありかつNR 1D が-CH 3 、-CH 2 CH 3 、-(CH 2 ) 2 OH、または-CH 2 CO 2 Hである、項29に記載の化合物。
項32
R 1 が-CH 2 CH 2 N(CH 3 ) 2 または-CH 2 CH 2 NHCH 3 である、項29に記載の化合物。
項33
前記C 3 -C 8 シクロアルキルがアミノにより置換されている、項28に記載の化合物。
項34
R 4 またはR 5 の1つがHまたはFである、項1〜33のいずれか1項に記載の化合物。
項35
前記化合物が次の化合物:
項36
前記化合物が次の化合物:
項37
前記化合物が次の化合物:
項38
項1〜37のいずれか1項に記載の化合物、またはその製薬上許容される塩もしくはプロドラッグ、および製薬上許容される賦形剤を含むものである医薬組成物。
項39
一酸化窒素シンターゼ(NOS)の作用により引き起こされる哺乳動物における症状を治療または予防する方法であって、項1〜37のいずれか1項に記載の化合物、またはその製薬上許容される塩もしくはプロドラッグの有効量を前記哺乳動物に投与するステップを含むものである前記方法。
項40
前記哺乳動物がヒトである、項39に記載の方法。
項41
前記症状が頭痛、神経因性疼痛、慢性炎症性疼痛、内臓疼痛、神経炎症、薬物誘発性痛覚過敏および/またはアロディニア、急性疼痛、慢性疼痛、骨癌疼痛;化学物質依存症または嗜癖、CNS障害、神経変性疾患または神経傷害、心血管関連症状、または消化器障害である、項39に記載の方法。
項42
前記頭痛が片頭痛頭痛(前兆を伴うまたは伴わない)、慢性緊張型頭痛(CTTH)、アロディニアを伴う片頭痛、薬物乱用頭痛、群発性頭痛、慢性頭痛、または変容性片頭痛である、項41に記載の方法。
項43
前記頭痛が中枢感作の根底をなす機構に伴う頭痛である、項41に記載の方法。
項44
前記慢性疼痛が中枢感作の成分を有する、項41に記載の方法。
項45
前記慢性疼痛が神経因性疼痛である、項44に記載の方法。
項46
前記神経因性疼痛がAIDS関連有痛性ニューロパチー、中枢性卒中後痛(CPSP)、糖尿病性ニューロパチー、化学療法誘発性神経因性疼痛、帯状疱疹後神経痛、または三叉神経の神経痛である、項45に記載の方法。
項47
前記神経因性疼痛が帯状疱疹後神経痛である、項43に記載の方法。
項48
前記慢性炎症性疼痛が骨関節炎、慢性関節リウマチ、強直性脊椎炎、乾癬性関節炎、未分化脊椎関節症、または反応性関節炎から生じる、項41に記載の方法。
項49
前記薬物誘発性痛覚過敏またはアロディニアがオピオイド誘発性痛覚過敏/アロディニアまたはトリプタン(5-HT 1D/1B アゴニスト)誘発性痛覚過敏またはアロディニアである、項41に記載の方法。
項50
前記化学療法誘発性神経因性疼痛がパクリタキセル、シスプラチン、またはドキソルビシンにより誘発される、項41に記載の方法。
項51
前記化学物質依存症または嗜癖が薬物嗜癖、コカイン嗜癖、ニコチン嗜癖、メタンフェタミン誘発性神経毒性、エタノール耐性、依存、または離脱、あるいはモルヒネ/オピオイド誘発性耐性、依存、痛覚過敏、または離脱である、項41に記載の方法。
項52
前記CNS障害が癲癇、不安、うつ病、注意欠陥機能亢進障害(ADHD)、精神病、または認知症である、項41に記載の方法。
項53
前記神経変性疾患または神経傷害が急性脊椎損傷、AIDS関連認知症、パーキンソン病、アルツハイマー病、筋萎縮性側索硬化症(ALS)、ハンチントン舞踏病、多発性硬化症、神経毒性、または頭部外傷である、項41に記載の方法。
項54
前記心血管関連症状が脳卒中、冠動脈バイパス移植(CABG)関連神経障害、低体温心停止(HCA)、卒中後痛、心原性ショック、再灌流傷害、または血管性認知症である、項41に記載の方法。
項55
前記消化器障害が回腸造瘻術に関連する下痢、またはダンピング症候群である、項41に記載の方法。
項56
前記症状が内臓疼痛である、項41に記載の方法。
項57
前記症状が脳卒中、再灌流傷害、神経変性、頭部外傷、CABG、アロディニアを伴う片頭痛、中枢性卒中後痛(CPSP)、モルヒネ/オピオイド誘導性痛覚過敏または慢性疼痛である、項41に記載の方法。
項58
前記哺乳動物にさらにオピオイドを投与するステップを含む、項39に記載の方法。
項59
前記オピオイドが、アルフェンタニル、ブトルファノール 、ブプレノルフィン、デキストロモラミド、デゾシン、デキストロプロポキシフェン、コデイン、ジヒドロコデイン、ジフェノキシレート、エトルフィン、フェンタニル、ヒドロコドン、ヒドロモルフォン、ケトベミドン、ロペラミド、レボルファノール、レボメタドン、メペリジン、メプタジノール、メタドン、モルヒネ、モルヒネ-6-グルクロニド、ナルブフィン、ナロキソン、オキシコドン、オキシモルフォン、ペンタゾシン、ペチジン、ピリトラミド、プロポキシフェン、レミフェンタニル、スルフェンタニル、チリジン、またはトラマドールである、項58に記載の方法。
項60
前記哺乳動物にさらに抗うつ薬を投与するステップを含む、項39に記載の方法。
項61
前記抗うつ薬が選択的なセロトニン再取込み阻害剤、ノルエピネフリン再取込み阻害剤、デュアルセロトニン/ノルエピネフリン再取込み阻害剤、モノアミンオキシダーゼ阻害剤、可逆的モノアミンオキシダーゼA型阻害剤、または三環系である、項60に記載の方法。
項62
前記選択的セロトニン再取込み阻害剤がシタロプラム、エスシタロプラム、フルオキセチン、フルボキサミン、パロキセチン、またはセルトラリンである、項61に記載の方法。
項63
前記ノルエピネフリン再取込み阻害剤がアミトリプチリン、アトモキセチン、ブプロピオン、デスメチルアミトリプチリン、クロミプラミン、ドキセピン、イミプラミン、イミプラミンオキシド、トリミプラミン;アジナゾラム、アミルトリプチルイノキシド、アモキサピン、デシプラミン、マプロチリン、ノルトリプチリン、プロトリプチリン、アミネプチン、ブトリプチリン、デメキシプチリン、ジベンゼピン、ジメタクリン、ドチエピン、フルアシジン、イプリンドール、ロフェプラミン、メリトラセン、メタプラミン、ノルクロミプラミン、ノキシプチリン、オピプラモール、ペルラピン、ピゾチリン、プロピゼピン、キヌプラミン、レボキセチン、チアネプチン、またはトモキセチンである、項61に記載の方法。
項64
前記デュアルセロトニン/ノルエピネフリン再取込み阻害剤がデュロキセチン、ミルナシプラン、ミルタザピン、ネファゾドン、ベンラファキシン、またはデスベンラファキシンである、項61に記載の方法。
項65
前記モノアミンオキシダーゼ阻害剤がアミフラミン、イプロニアジド、イソカルボキサジド、M-3-PPC(Draxis)、モクロベミド、パルギリン、フェネルジン、トラニルシプロミン、またはバノキセリンである、項61に記載の方法。
項66
前記可逆的モノアミンオキシダーゼA型阻害剤がバジナプリン、ベフロキサトン、ブロファロミン、シモキサトン、またはクロルジリンである、項61に記載の方法。
項67
前記三環系がアミトリプチリン、クロミプラミン、デシプラミン、ドキセピン、イミプラミン、マプロチリン、ノルトリプチリン、プロトリプチリン、またはトリミプラミンである、項61に記載の方法。
項68
前記抗うつ薬がアジナゾラム、アラプロクラート、アミネプチン、アミトリプチリン/クロルジアゼポキシドの組合わせ、アチパメゾール、アザミアンセリン、バジナプリン、ベフラリン、ビフェメラン、ビノダリン、ビペナモール、ブロファロミン、カロキサゾン、セリクラミン、シアノプラミン、シモキサトン、シタロプラム、クレメプロール、クロボキサミン、ダゼピニル、デアノール、デメキシプチリン、ジベンゼピン、ドチエピン、ドロキシドパ、エネフェキシン、エスタゾラム、エトペリドン、フェモキセチン、フェンガビン、フェゾラミン、フルオトラセン、イダゾキサン、インダルピン、インデロキサジン、イプリンドール、レボプロチリン、リチウム、リトキセチン、ロフェプラミン、メジホキサミン、メタプラミン、メトラリンドール、ミアンセリン、ミルナシプラン、ミナプリン、ミルタザピン、モンチレリン、ネブラセタム、ネホパム、ニアラミド、ノミフェンシン、ノルフルオキセチン、オロチレリン、オキサフロザン、ピナゼパム、ピルリンドール、ピゾチリン、リタンセリン、ロリプラム、セルクロレミン、セチプチリン、シブトラミン、スルブチアミン、スルピリド、テニロキサジン、トザリノン、チロリベリン、チアネプチン、チフルカルビン、トラゾドン、トフェナシン、トフィソパム、トロキサトン、トモキセチン、ベラリプリド、ビロキサジン、ビクアリン、ジメリジン、またはゾメタピンである、項60に記載の方法。
項69
さらに前記哺乳動物に抗てんかん薬を投与するステップを含む、項39に記載の方法。
項70
前記抗てんかん薬がカルバマゼピン、フルピルチン、ガバペンチン、ラモトリジン、オクスカルバゼピン、フェニトイン、レチガビン、トピラメート、またはバルプロエートである、項69に記載の方法。
項71
さらに前記哺乳動物に非ステロイド抗炎症性薬物(NSAID)またはアセトアミノフェンを投与するステップを含む、項39に記載の方法。
項72
前記NSAIDがアセメタシン、アスピリン、セレコキシブ、デラコキシブ、ジクロフェナク、ジフルニサル、エテンザミド、エトフェナマート、エトリコキシブ、フェノプロフェン、フルフェナム酸、フルビプロフェン、ロナゾラク、ロルノキシカム、イブプロフェン、インドメタシン、イソキシカム、ケブゾン、ケトプロフェン、ケトロラク、ナプロキセン、ナブメトン、ニフルム酸、スリンダク、トルメチン、ピロキシカム、メクロフェナム酸、メフェナム酸、メロキシカム、メタミゾール、モフェブタゾン、オキシフェンブタゾン、パレコキシブ、フェニドン、フェニルブタゾン、ピロキシカム、プロパセタモール、プロピフェナゾン、ロフェコキシブ、サリチルアミド、スプロフェン、チアプロフェン酸、テノキシカム、バルデコキシブ、4-(4-シクロヘキシル-2-メチルオキサゾール-5-イル)-2-フルオロベンゼンスルホンアミド、N-[2-(シクロヘキシルオキシ)-4-ニトロフェニル]メタンスルホンアミド、2-(3,4-ジフルオロフェニル)-4-(3-ヒドロキシ-3-メチルブトキシ)-5-[4-(メチルスルホニル)フェニル]-3(2H)-ピリダジノン、および2-(3,5-ジフルオロフェニル)-3-[4-(メチルスルホニル)フェニル]-2-シクロペンテン-1-オン)である、項71に記載の方法。
項73
さらに前記哺乳動物に抗不整脈薬、GABA-Bアンタゴニスト、またはα-2-アドレナリン受容体アゴニストを投与するステップを含む、項39に記載の方法。
項74
さらに前記哺乳動物にセロトニン5HT 1B/1D アゴニストを投与するステップを含む、項39に記載の方法。
項75
前記セロトニン5HT 1B/1D アゴニストがエレトリプタン、フロバトリプタン、ナラトリプタン、リザトリプタン、スマトリプタン、ドニトリプタン、またはゾルミトリプタンである、項74に記載の方法。
項76
さらに前記哺乳動物にN-メチル-D-アスパラギン酸アンタゴニストまたはグルタミン酸受容体アンタゴニストを投与するステップを含む、項39に記載の方法。
項77
前記N-メチル-D-アスパラギン酸アンタゴニストまたはグルタミン酸受容体アンタゴニストが、アマンタジン;アプチガネル;ベソンプロジル;ブジピン;コナントキンG;デルセミン;デキサナビノール;デキストロメトルファン;デキストロプロポキシフェン;フェルバメート;フルオロフェルバメート;ガシクリジン;グリシン;イペノキサゾン;カイトセファリン;ケタミン;ケトベミドン;ラニセミン;リコスチネル;ミダホテル;メマチン;D-メタドン;D-モルヒネ;ミルナシプラン;ネラメキサン;オルフェナドリン;レマセミド;スルファゾシン;FPL-12,495(レマセミド代謝物);トピラメート;(αR)-α-アミノ-5-クロロ-1-(ホスホノメチル)-1H-ベンゾイミダゾール-2-プロパン酸;1-アミノシクロペンタン-カルボン酸;[5-(アミノメチル)-2-[[[(5S)-9-クロロ-2,3,6,7-テトラヒドロ-2,3-ジオキソ-1H-,5H-ピリド[1,2,3-de]キノキサリン-5-イル]アセチル]アミノ]フェノキシ]-酢酸;α-アミノ-2-(2-ホスホノエチル)-シクロヘキサンプロパン酸;α-アミノ-4-(ホスホノメチル)-ベンゼン酢酸;(3E)-2-アミノ-4-(ホスホノメチル)-3-ヘプテン酸;3-[(1E)-2-カルボキシ-2-フェニルエテニル]-4,6-ジクロロ-1H-インドール-2-カルボン酸;8-クロロ-2,3-ジヒドロピリダジノ[4,5-b]キノリン-1,4-ジオン5-オキシドの2-ヒドロキシ-N,N,N-トリメチル-エタンアミニウムとの塩;N'-[2-クロロ-5-(メチルチオ)フェニル]-N-メチル-N-[3-(メチルチオ)フェニル]-グアニジン;N'-[2-クロロ-5-(メチルチオ)フェニル]-N-メチル-N-[3-[(R)-メチルスルフィニル]フェニル]-グアニジン;6-クロロ-2,3,4,9-テトラヒドロ-9-メチル-2,3-ジオキソ-1H-インデノ[1,2-b]ピラジン-9-酢酸;7-クロロチオキヌレン酸;(3S,4aR,6S,8aR)-デカヒドロ-6-(ホスホノメチル)-3-イソキノリンカルボン酸;(-)-6,7-ジクロロ-1,4-ジヒドロ-5-[3-(メトキシメチル)-5-(3-ピリジニル)-4-H-1,2,4-トリアゾール-4-イル]-2,3-キノキサリンジオン;4,6-ジクロロ-3-[(E)-(2-オキソ-1-フェニル-3-ピロリジニリデン)メチル]-1H-インドール-2-カルボン酸;(2R,4S)-rel-5,7-ジクロロ-1,2,3,4-テトラヒドロ-4-[[(フェニルアミノ)カルボニル]アミノ]-2-キノリンカルボン酸;(3R,4S)-rel-3,4-ジヒドロ-3-[4-ヒドロキシ-4-(フェニルメチル)-1-ピペリジニル]-2H-1-ベンゾピラン-4,7-ジオール;2-[(2,3-ジヒドロ-1H-インデン-2-イル)アミノ]-アセトアミド;1,4-ジヒドロ-6-メチル-5-[(メチルアミノ)メチル]-7-ニトロ-2,3-キノキサリンジオン;[2-(8,9-ジオキソ-2,6-ジアザビシクロ[5.2.0]ノン-1(7)-エン-2-イル)エチル]-ホスホン酸;(2R,6S)-1,2,3,4,5,6-ヘキサヒドロ-3-[(2S)-2-メトキシプロピル]-6,11,11-トリメチル-2,6-メタノ-3-ベンゾアゾシン-9-オール;2-ヒドロキシ-5-[[(ペンタフルオロフェニル)メチル]アミノ]-安息香酸;1-[2-(4-ヒドロキシフェノキシ)エチル]-4-[(4-メチルフェニル)メチル]-4-ピペリジノール;1-[4-(1H-イミダゾール-4-イル)-3-ブチニル]-4-(フェニルメチル)-ピペリジン;2-メチル-6-(フェニルエチニル)-ピリジン;3-(ホスホノメチル)-L-フェニルアラニン;または3,6,7-テトラヒドロ-2,3-ジオキソ-N-フェニル-1H,5H-ピリド[1,2,3-de]キノキサリン-5-アセトアミドである、項76に記載の方法。
項78
さらに前記哺乳動物にコレシストキニンBアンタゴニストを投与する、項39に記載の方法。
項79
さらに前記哺乳動物にサブスタンスPアンタゴニストを投与する、項39に記載の方法。
項80
さらに前記哺乳動物に抗炎症性化合物を投与する、項39に記載の方法。
項81
前記抗炎症性化合物がアスピリン、セレコキシブ、コルチゾン、デラコキシブ、ジフルニサル、エトリコキシブ、フェノプロフェン、イブプロフェン、ケトプロフェン、ナプロキセン、プレドニゾロン、スリンダク、トルメチン、ピロキシカム、メフェナム酸、メロキシカム、フェニルブタゾン、ロフェコキシブ、スプロフェン、バルデコキシブ、4-(4-シクロヘキシル-2-メチルオキサゾール-5-イル)-2-フルオロベンゼンスルホンアミド、N-[2-(シクロヘキシルオキシ)-4-ニトロフェニル]メタンスルホンアミド、2-(3,4-ジフルオロフェニル)-4-(3-ヒドロキシ-3-メチルブトキシ)-5-[4-(メチルスルホニル)フェニル]-3(2H)-ピリダジノン、または 2-(3,5-ジフルオロフェニル)-3-[4-(メチルスルホニル)フェニル]-2-シクロペンテン-1-オンである、項80に記載の方法。
項82
さらに前記哺乳動物に、DHP感受性L型カルシウムチャネルアンタゴニスト、ω-コノトキシン感受性N型カルシウムチャネルアンタゴニスト、P/Q型カルシウムチャネルアンタゴニスト、アデノシンキナーゼアンタゴニスト、アデノシン受容体A 1 アゴニスト、アデノシン受容体A 2a アンタゴニスト、アデノシン受容体A 3 アゴニスト、アデノシンデアミナーゼ阻害剤、アデノシンヌクレオシド輸送阻害剤、バニロイドVR1受容体アゴニスト、カンナビノイドCB1/CB2アゴニスト、AMPA受容体アンタゴニスト、カイニン酸受容体アンタゴニスト、ナトリウムチャネル遮断剤、ニコチン性アセチルコリン受容体アゴニスト、K ATP カリウムチャネル-、K v1.4 カリウムチャネル-、Ca 2+ -活性化カリウムチャネル-、SKカリウムチャネル-、BKカリウムチャネル-、IKカリウムチャネル-、またはKCNQ2/3カリウムチャネル開放剤、ムスカリン性M3アンタゴニスト、ムスカリン性M1アゴニスト、ムスカリン性M2/M3部分アゴニスト/アンタゴニスト、または抗酸化剤を投与するステップを含む、項39に記載の方法。
項83
さらに前記哺乳動物に抗精神病薬を投与するステップを含む、項39に記載の方法。
項84
前記抗精神病薬がプロマジン、クロルプロマジン、クロルプロチキセン、
チオリダジン、アセトフェナジン、メソリダジン、ドロペリドール、ロキサピン、モリンドン、ペルフェナジン、プロクロルペラジン、チオチキセン、トリフルオペラジン、フルフェナジン、ピモジド、フルペンチキソール、メトトリメプラジン、ピポチアジン、セルチンドール、クロザピン、オランザピン、リスペリドン、アリピプラゾール、クエチアピン、ハロペリドール、ジプラシドン、またはイロペリドンである、項83に記載の方法。
項85
さらに前記哺乳動物にドーパミン受容体パーキンソン病薬を投与するステップを含む、項39に記載の方法。
項86
前記パーキンソン病薬がレボドパまたはプラミペキソールである、項85に記載の方法。
項87
さらに前記哺乳動物に脂肪酸アミド加水分解酵素(FAAH)阻害剤を投与するステップを含む、項39に記載の方法。
Claims (18)
- 式:
Qは-O-(CHR6)1-3または-S-(CHR6)1-3-であり;
R1およびそれぞれのR6は、独立して、H、任意に置換されたC1-6アルキル、任意に置換されたC1-4アルカリール、任意に置換されたC1-4アルクヘテロシクリル、任意に置換されたC2-9ヘテロシクリル、任意に置換されたC3-8シクロアルキル、任意に置換されたC1-4アルクシクロアルキルまたは-(CR1AR1B)nNR1CR1Dであり;
R1AおよびR1Bは、独立して、H、ヒドロキシ、ハロ、任意に置換されたC1-6アルキル、任意に置換されたC1-6アルコキシ、任意に置換されたC1-4アルクシクロアルキル、任意に置換されたC1-4アルカリール、任意に置換されたC1-4アルクヘテロシクリル、任意に置換されたC1-4アルクヘテロアリール、任意に置換されたC3-8シクロアルキル、または任意に置換されたC2-9ヘテロシクリルであるか、またはR1AおよびR1Bは一緒に=Oを形成し;
R1CおよびR1Dは、独立して、H、任意に置換されたC1-6アルキル、任意に置換されたC1-6アルコキシ、任意に置換されたC1-4アルクシクロアルキル、任意に置換されたC1-4アルカリール、任意に置換されたC1-4アルクヘテロシクリル、任意に置換されたC1-4アルクヘテロアリール、任意に置換されたC3-8シクロアルキル、任意に置換されたC2-9ヘテロシクリル、もしくはホルミル、アセチル、プロピオニル、ピバロイル、t-ブチルアセチル、2-クロロアセチル、2-ブロモアセチル、トリフルオロアセチル、トリクロロアセチル、o-ニトロフェノキシアセチル、α-クロロブチリル、ベンゾイル、4-クロロベンゾイル、4-ブロモベンゾイル、4-ニトロベンゾイル、アラニニル、ロイシニル、フェニルアラニニル、ベンゼンスルホニル、p-トルエンスルホニル、ベンジルオキシカルボニル、p-クロロベンジルオキシカルボニル、p-メトキシベンジルオキシカルボニル、p-ニトロベンジルオキシカルボニル、2-ニトロベンジルオキシカルボニル、p-ブロモベンジルオキシカルボニル、3,4-ジメトキシベンジルオキシカルボニル、3,5-ジメトキシベンジルオキシカルボニル、2,4-ジメトキシベンジルオキシカルボニル、4-メトキシベンジルオキシカルボニル、2-ニトロ-4,5-ジメトキシベンジルオキシカルボニル、3,4,5-トリメトキシベンジルオキシカルボニル、1-(p-ビフェニリル)-1-メチルエトキシカルボニル、α,α-ジメチル-3,5-ジメトキシベンジルオキシカルボニル、ベンズヒドリルオキシカルボニル、t-ブチルオキシカルボニル、ジイソプロピルメトキシカルボニル、イソプロピルオキシカルボニル、エトキシカルボニル、メトキシカルボニル、アリルオキシカルボニル、2,2,2,-トリクロロエトキシカルボニル、フェノキシカルボニル、4-ニトロフェノキシカルボニル、フルオレニル-9-メトキシカルボニル、シクロペンチルオキシカルボニル、アダマンチルオキシカルボニル、シクロヘキシルオキシカルボニル、フェニルチオカルボニル、ベンジル、トリフェニルメチル、ベンジルオキシメチルおよびトリメチルシリルからなる群から選択されるN-保護基であるか、またはR1CおよびR1Dは一緒に任意に置換されたC2-9ヘテロシクリルを形成し;
nは整数1〜6であり;
R2およびR3のそれぞれは、独立して、H、hal、任意に置換されたC1-6アルキル、任意に置換されたC6-10アリール、任意に置換されたC1-6アルカリール、任意に置換されたC2-9ヘテロシクリル、ヒドロキシ、任意に置換されたC1-6アルコキシ、任意に置換されたC1-6チオアルコキシ、(CH2)r2NHC(NH)R2A、または(CH2)r2NHC(S)NHR2B、または任意に置換されたC1-4アルクヘテロシクリルであり、
ここで、r2は整数0〜2であり、R2Aは任意に置換されたC1-6アルキル、任意に置換されたC6-10アリール、任意に置換されたC1-4アルカリール、任意に置換されたC2-9ヘテロシクリル、任意に置換されたC1-4アルクヘテロシクリル、任意に置換されたC1-6チオアルコキシ、任意に置換されたC1-4チオアルカリール、任意に置換されたアリーロイル、任意に置換されたC1-4チオアルクヘテロシクリル、または置換されたアミノであり;R2Bは任意に置換されたC1-4アルカリール、任意に置換されたC2-9ヘテロシクリル、置換されたC1-4アルクヘテロシクリル、任意に置換されたC1-6チオアルコキシ、任意に置換されたC1-4チオアルカリール、任意に置換されたアリーロイル、任意に置換されたC1-4チオアルクヘテロシクリル、または任意に置換されたアミノであり;
R4およびR5のそれぞれは独立してH、hal、(CH2)r2NHC(NH)R2A、または(CH2)r2NHC(S)NHR2Bであり;
ここで、Y1およびY2はそれぞれHであるかまたはY1およびY2は一緒に=Oであるか、またはY1およびY2は独立してH、任意に置換されたC1-6アルキル、任意に置換されたC6-10アリール、任意に置換されたC1-6アルカリール、任意に置換されたC2-9ヘテロシクリル、ヒドロキシ、任意に置換されたC1-6アルコキシ、任意に置換されたC1-6チオアルコキシ、または任意に置換されたC1-4アルクヘテロシクリルであり;
ここで、R2、R3、R4、およびR5のうちのただ1つだけは(CH2)r2NHC(NH)R2Aまたは(CH2)r2NHC(S)NHR2Bであり;
ここで、アルキルの任意の置換基は、(1)1〜6個の炭素原子のアルコキシ;(2)1〜6個の炭素原子のアルキルスルフィニル;(3)1〜6個の炭素原子のアルキルスルホニル;(4)アミノ;(5)アリール;(6)アリールアルコキシ;(7)アリーロイル;(8)アジド;(9)カルボキサルデヒド(carboxaldehyde);(10)3〜8個の炭素原子のシクロアルキル;(11)hal;(12)ヘテロシクリル;(13)(複素環)オキシ;(14)(複素環)オイル;(15)ヒドロキシル;(16)N-保護アミノ;(17)ニトロ;(18)オキソ;(19)3〜8個の炭素原子のスピロシクリル;(20)1〜6個の炭素原子のチオアルコキシ;(21)チオール;(22)-CO 2 R A (R A は、(a)アルキル、(b)アリール、(c)アルカリール、および(d)水素(アルキレン基は、1〜6個の炭素原子を有する)からなる群から選択される);(23)-C(O)NR B R C (R B およびR C の各々は、独立に、(a)水素、(b)アルキル、(c)アリールおよび(d)アルカリール(アルキレン基は、1〜6個の炭素原子を有する)からなる群から選択される);(24)-SO 2 R D (R D は、(a)アルキル、(b)アリールおよび(c)アルカリール(アルキレン基は、1〜6個の炭素原子を有する)からなる群から選択される);(25)-SO 2 NR E R F (R E およびR F の各々は、独立に、(a)水素、(b)アルキル、(c)アリールおよび(d)アルカリール(アルキレン基は、1〜6個の炭素原子を有する)からなる群から選択される);および(26)-NR G R H (R G およびR H の各々は、独立に、(a)水素;(b)N-保護基;(c)1〜6個の炭素原子のアルキル;(d)2〜6個の炭素原子のアルケニル;(e)2〜6個の炭素原子のアルキニル;(f)アリール;(g)アルカリール(アルキレン基は、1〜6個の炭素原子を有する);(h)3〜8個の炭素原子のシクロアルキル;および(i)アルクシクロアルキル(シクロアルキル基は、3〜8個の炭素原子を有し、アルキレン基は、1〜10個の炭素原子を有する)からなる群から選択される)から選択され;
アリールおよびアリーロイルの任意の置換基は、(1)1〜6個の炭素原子のアルカノイル;(2)1〜6個の炭素原子のアルキル;(3)1〜6個の炭素原子のアルコキシ;(4)アルコキシアルキル(アルキルおよびアルキレン基は、独立に、1〜6個の炭素原子を有する);(5)1〜6個の炭素原子のアルキルスルフィニル;(6)アルキルスルフィニルアルキル(アルキルおよびアルキレン基は、独立に、1〜6個の炭素原子を有する);(7)1〜6個の炭素原子のアルキルスルホニル;(8)アルキルスルホニルアルキル(アルキルおよびアルキレン基は、独立に、1〜6個の炭素原子を有する);(9)アリール;(10)アミノ;(11)1〜6個の炭素原子のアミノアルキル;(12)ヘテロアリール;(13)アルカリール(アルキレン基は、1〜6個の炭素原子を有する);(14)アリーロイル;(15)アジド;(16)1〜6個の炭素原子のアジドアルキル;(17)カルボキサルデヒド;(18)(カルボキサルデヒド)アルキル(アルキレン基は、1〜6個の炭素原子を有する);(19)3〜8個の炭素原子のシクロアルキル;(20)アルクシクロアルキル(シクロアルキル基は、3〜8個の炭素原子を有し、アルキレン基は、1〜10個の炭素原子を有する);(21)hal;(22)1〜6個の炭素原子のハロアルキル;(23)ヘテロシクリル;(24)(ヘテロシクリル)オキシ;(25)(ヘテロシクリル)オイル;(26)ヒドロキシ;(27)1〜6個の炭素原子のヒドロキシアルキル;(28)ニトロ;(29)1〜6個の炭素原子のニトロアルキル;(30)N-保護アミノ;(31)N-保護アミノアルキル(アルキレン基は、1〜6個の炭素原子を有する);(32)オキソ;(33)1〜6個の炭素原子のチオアルコキシ;(34)チオアルコキシアルキル(アルキルおよびアルキレン基は、独立に、1〜6個の炭素原子を有する);(35)-(CH 2 ) q CO 2 R A (qは、0〜4の整数であり、R A は、(a)アルキル、(b)アリール、(c)アルカリール、および(d)水素(アルキレン基は、1〜6個の炭素原子を有する)からなる群から選択される);(36)-(CH 2 ) q CONR B R C (qは、0〜4の整数であり、R B およびR C は、(a)水素、(b)アルキル、(c)アリール、および(d)アルカリール(アルキレン基は、1〜6個の炭素原子を有する)からなる群から独立に選択される);(37)-(CH 2 ) q SO 2 R D (qは、0〜4の整数であり、R D は、(a)アルキル、(b)アリール、および(c)アルカリール(アルキレン基は、1〜6個の炭素原子を有する)からなる群から選択される);(38)-(CH 2 ) q SO 2 NR E R F (qは、0〜4の整数であり、R E およびR F の各々は、独立に、(a)水素、(b)アルキル、(c)アリール、および(d)アルカリール(アルキレン基は、1〜6個の炭素原子を有する)からなる群から選択される);(39)-(CH 2 ) q NR G R H (qは、0〜4の整数であり、R G およびR H の各々は、独立に、(a)水素;(b)N-保護基;(c)1〜6個の炭素原子のアルキル;(d)2〜6個の炭素原子のアルケニル;(e)2〜6個の炭素原子のアルキニル;(f)アリール;(g)アルカリール(アルキレン基は、1〜6個の炭素原子を有する);(h)3〜8個の炭素原子のシクロアルキル;および(i)アルクシクロアルキル(シクロアルキル基は、3〜8個の炭素原子を有し、アルキレン基は、1〜10個の炭素原子を有する)からなる群から選択される);(40)チオール;(41)ペルフルオロアルキル;(42)ペルフルオロアルコキシ;(43)アリールオキシ;(44)シクロアルコキシ;(45)シクロアルキルアルコキシ;および(46)アリールアルコキシから選択され;
シクロアルキルの任意の置換基は、(1)1〜6個の炭素原子のアルカノイル;(2)1〜6個の炭素原子のアルキル;(3)1〜6個の炭素原子のアルコキシ;(4)アルコキシアルキル(アルキルおよびアルキレン基は、独立に、1〜6個の炭素原子を有する);(5)1〜6個の炭素原子のアルキルスルフィニル;(6)アルキルスルフィニルアルキル(アルキルおよびアルキレン基は、独立に、1〜6個の炭素原子を有する);(7)1〜6個の炭素原子のアルキルスルホニル;(8)アルキルスルホニルアルキル(アルキルおよびアルキレン基は、独立に、1〜6個の炭素原子を有する);(9)アリール;(10)アミノ;(11)1〜6個の炭素原子のアミノアルキル;(12)ヘテロアリール;(13)アルカリール(アルキレン基は、1〜6個の炭素原子を有する);(14)アリーロイル;(15)アジド;(16)1〜6個の炭素原子のアジドアルキル;(17)カルボキサルデヒド;(18)(カルボキサルデヒド)アルキル(アルキレン基は、1〜6個の炭素原子を有する);(19)3〜8個の炭素原子のシクロアルキル;(20)アルクシクロアルキル(シクロアルキル基は、3〜8個の炭素原子を有し、アルキレン基は、1〜10個の炭素原子を有する);(21)hal;(22)1〜6個の炭素原子のハロアルキル;(23)ヘテロシクリル;(24)(ヘテロシクリル)オキシ;(25)(ヘテロシクリル)オイル;(26)ヒドロキシ;(27)1〜6個の炭素原子のヒドロキシアルキル;(28)ニトロ;(29)1〜6個の炭素原子のニトロアルキル;(30)N-保護アミノ;(31)N-保護アミノアルキル(アルキレン基は、1〜6個の炭素原子を有する);(32)オキソ;(33)1〜6個の炭素原子のチオアルコキシ;(34)チオアルコキシアルキル(アルキルおよびアルキレン基は、独立に、1〜6個の炭素原子を有する);(35)-(CH 2 ) q CO 2 R A (qは、0〜4の整数であり、R A は、(a)アルキル、(b)アリール、(c)アルカリール、および(d)水素(アルキレン基は、1〜6個の炭素原子を有する)からなる群から選択される);(36)-(CH 2 ) q CONR B R C (qは、0〜4の整数であり、R B およびR C は、(a)水素、(b)アルキル、(c)アリール、および(d)アルカリール(アルキレン基は、1〜6個の炭素原子を有する)からなる群から独立に選択される);(37)-(CH 2 ) q SO 2 R D (qは、0〜4の整数であり、R D は、(a)アルキル、(b)アリール、および(c)アルカリール(アルキレン基は、1〜6個の炭素原子を有する)からなる群から選択される);(38)-(CH 2 ) q SO 2 NR E R F (qは、0〜4の整数であり、R E およびR F の各々は、独立に、(a)水素、(b)アルキル、(c)アリール、および(d)アルカリール(アルキレン基は、1〜6個の炭素原子を有する)からなる群から選択される);(39)-(CH 2 ) q NR G R H (qは、0〜4の整数であり、R G およびR H の各々は、独立に、(a)水素;(b)N-保護基;(c)1〜6個の炭素原子のアルキル;(d)2〜6個の炭素原子のアルケニル;(e)2〜6個の炭素原子のアルキニル;(f)アリール;(g)アルカリール(アルキレン基は、1〜6個の炭素原子を有する);(h)3〜8個の炭素原子のシクロアルキル;および(i)アルクシクロアルキル(シクロアルキル基は、3〜8個の炭素原子を有し、アルキレン基は、1〜10個の炭素原子を有する)からなる群から選択され、ただし、2つの基は、カルボニル基またはスルホニル基を介して窒素原子に結合していない);(40)チオール;(41)ペルフルオロアルキル;(42)ペルフルオロアルコキシ;(43)アリールオキシ;(44)シクロアルコキシ;(45)シクロアルキルアルコキシ;および(46)アリールアルコキシから選択され;ならびに
ヘテロシクリルまたはヘテロアリールの任意の置換基は、(1)1〜6個の炭素原子のアルカノイル;(2)1〜6個の炭素原子のアルキル;(3)1〜6個の炭素原子のアルコキシ;(4)アルコキシアルキル(アルキルおよびアルキレン基は、独立に、1〜6個の炭素原子を有する);(5)1〜6個の炭素原子のアルキルスルフィニル;(6)アルキルスルフィニルアルキル(アルキルおよびアルキレン基は、独立に、1〜6個の炭素原子を有する);(7)1〜6個の炭素原子のアルキルスルホニル;(8)アルキルスルホニルアルキル(アルキルおよびアルキレン基は、独立に、1〜6個の炭素原子を有する);(9)アリール;(10)アミノ;(11)1〜6個の炭素原子のアミノアルキル;(12)ヘテロアリール;(13)アルカリール(アルキレン基は、1〜6個の炭素原子を有する);(14)アリーロイル;(15)アジド;(16)1〜6個の炭素原子のアジドアルキル;(17)カルボキサルデヒド;(18)(カルボキサルデヒド)アルキル(アルキレン基は、1〜6個の炭素原子を有する);(19)3〜8個の炭素原子のシクロアルキル;(20)アルクシクロアルキル(シクロアルキル基は、3〜8個の炭素原子を有し、アルキレン基は、1〜10個の炭素原子を有する);(21)ハロ;(22)1〜6個の炭素原子のハロアルキル;(23)ヘテロシクリル;(24)(ヘテロシクリル)オキシ;(25)(ヘテロシクリル)オイル;(26)ヒドロキシ;(27)1〜6個の炭素原子のヒドロキシアルキル;(28)ニトロ;(29)1〜6個の炭素原子のニトロアルキル;(30)N-保護アミノ;(31)N-保護アミノアルキル(アルキレン基は、1〜6個の炭素原子を有する);(32)オキソ;(33)1〜6個の炭素原子のチオアルコキシ;(34)チオアルコキシアルキル(アルキルおよびアルキレン基は、独立に、1〜6個の炭素原子を有する);(35)-(CH 2 ) q CO 2 R A (qは、0〜4の整数であり、R A は、(a)アルキル、(b)アリール、(c)アルカリール、および(d)水素(アルキレン基は、1〜6個の炭素原子を有する)からなる群から選択される);(36)-(CH 2 ) q CONR B R C (qは、0〜4の整数であり、R B およびR C は、(a)水素、(b)アルキル、(c)アリール、および(d)アルカリール(アルキレン基は、1〜6個の炭素原子を有する)からなる群から独立に選択される);(37)-(CH 2 ) q SO 2 R D (qは、0〜4の整数であり、R D は、(a)アルキル、(b)アリール、および(c)アルカリール(アルキレン基は、1〜6個の炭素原子を有する)からなる群から選択される);(38)-(CH 2 ) q SO 2 NR E R F (qは、0〜4の整数であり、R E およびR F の各々は、独立に、(a)水素、(b)アルキル、(c)アリール、および(d)アルカリール(アルキレン基は、1〜6個の炭素原子を有する)からなる群から選択される);(39)-(CH 2 ) q NR G R H (qは、0〜4の整数であり、R G およびR H の各々は、独立に、(a)水素;(b)N-保護基;(c)1〜6個の炭素原子のアルキル;(d)2〜6個の炭素原子のアルケニル;(e)2〜6個の炭素原子のアルキニル;(f)アリール;(g)アルカリール(アルキレン基は、1〜6個の炭素原子を有する);(h)3〜8個の炭素原子のシクロアルキル;および(i)アルクシクロアルキル(シクロアルキル基は、3〜8個の炭素原子を有し、アルキレン基は、1〜10個の炭素原子を有する)からなる群から選択される);(40)チオール;(41)ペルフルオロアルキル;(42)ペルフルオロアルコキシ;(43)アリールオキシ;(44)シクロアルコキシ;(45)シクロアルキルアルコキシ;および(46)アリールアルコキシから選択される]
を有する化合物またはその製薬上許容される塩。 - QはO-(CHR6)1-2またはS-(CHR6)1-2であり;R1およびそれぞれのR6は、独立して、H、任意に置換されたC1-6アルキル、任意に置換されたC1-4アルカリール、任意に置換されたC1-4アルクヘテロシクリル、または任意に置換されたC2-9ヘテロシクリルである、請求項1に記載の化合物。
- R2、R3、R4、またはR5は式:
を有し、
R2Aは式:
X1、X2、X4、およびX5のそれぞれは独立してO、S、NR7、N、またはCR8から選択され;
X3はNまたはCから選択され;
R7はH、または任意に置換されたC1-6アルキルであり;
R8はH、hal、任意に置換されたC1-6アルキル、ヒドロキシ、任意に置換されたC1-6アルコキシ、または任意に置換されたC1-6チオアルコキシであり、
ここで、X1、X2、X4、およびX5の少なくとも1つはCR8でないか、
R2Aは式:
X1およびX2のそれぞれは独立してO、S、NH、N、またはCHから選択され;
ここでX1およびX2の少なくとも1つはCHでない、請求項1または2に記載の化合物。 - Y1およびY2はそれぞれHであり、かつQはO-CHR6であるか、
Y1およびY2はそれぞれHであり、かつQはS-CHR6であるか、
Y1およびY2は一緒に=Oであり、かつQはO-CHR6であるか、
Y1およびY2は一緒に=Oであり、かつQはS-CHR6であるか、
Y1およびY2は一緒に=Oであり、かつQはO-(CHR6)2であるか、
Y1およびY2はそれぞれHであり、かつQはS-(CHR6)2であるか、
Y1およびY2は一緒に=Oであり、かつQはS-(CHR6)2であるか、
Y1およびY2はそれぞれHであり、かつQはO-(CHR6)2であるか、
Y1およびY2は一緒に=Oであり、かつQはO-(CHR6)3であるか、
Y1およびY2はそれぞれHであり、かつQはS-(CHR6)3であるか、
Y1およびY2は一緒に=Oであり、かつQはS-(CHR6)3であるか、あるいは
Y1およびY2はそれぞれHであり、かつQはO-(CHR6)3である、請求項1に記載の化合物。 - R1が、(i)任意に置換されたC1-6アルキル、または任意に置換されたアミノC1-6アルキルであるか、(ii)任意に置換されたC2-9ヘテロシクリル、任意に置換されたピロリジニル、任意に置換されたピペリジニル、または
(iii)任意に置換されたC1-4アルクヘテロシクリル、または任意に置換されたC1-4アルクヘテロシクリル(ここで前記ヘテロシクリルは5または6員の環状アミンであり、前記環状アミンがカルボン酸、C1-6エステル、またはアミドで置換されている)である、請求項1〜5のいずれか1項に記載の化合物。 - R1が、(i)任意に置換されたC3-C8シクロアルキル、もしくはアミノにより置換されたC3-C8シクロアルキル、(ii)-(CR1AR1B)nNR1CR1D(式中、R1AおよびR1BがそれぞれHであり、かつnが2または3であり、R1CがHでありかつR1Dが-CH3、-CH2CH3、-(CH2)2OH、または-CH2CO2Hであるか、R1CおよびR1Dは結合して、任意に置換されたピロリジニルまたは任意に置換されたピペリジニルを形成する)、あるいは(iii)-CH2CH2N(CH3)2または-CH2CH2NHCH3である、請求項1および請求項3〜6のいずれか1項に記載の化合物。
- R4またはR5の1つがHまたはFである、請求項1〜7のいずれか1項に記載の化合物。
- 請求項1〜11のいずれか1項に記載の化合物、またはその製薬上許容される塩、および製薬上許容される賦形剤を含むものである医薬組成物。
- 一酸化窒素シンターゼ(NOS)の作用により引き起こされる哺乳動物における症状を治療または予防するための医薬組成物であって、請求項1〜11のいずれか1項に記載の化合物、またはその製薬上許容される塩の有効量を含むものである前記医薬組成物。
- 前記症状が頭痛、中枢感作の根底をなす機構に伴う頭痛、神経因性疼痛、慢性炎症性疼痛、内臓疼痛、神経炎症、薬物誘発性痛覚過敏および/またはアロディニア、急性疼痛、慢性疼痛、中枢感作の成分を有する慢性疼痛、骨癌疼痛;化学物質依存症または嗜癖、CNS障害、神経変性疾患または神経傷害、心血管関連症状、あるいは消化器障害である、請求項13に記載の医薬組成物。
- 前記頭痛が片頭痛頭痛(前兆を伴うまたは伴わない)、慢性緊張型頭痛(CTTH)、アロディニアを伴う片頭痛、薬物乱用頭痛、群発性頭痛、慢性頭痛、または変容性片頭痛であり、
前記慢性疼痛が神経因性疼痛、AIDS関連有痛性ニューロパチー、中枢性卒中後痛(CPSP)、糖尿病性ニューロパチー、化学療法誘発性神経因性疼痛またはパクリタキセル、シスプラチン、もしくはドキソルビシンにより誘発される化学療法誘発性神経因性疼痛、帯状疱疹後神経痛、または三叉神経の神経痛であり、
前記慢性炎症性疼痛が骨関節炎、慢性関節リウマチ、強直性脊椎炎、乾癬性関節炎、未分化脊椎関節症、または反応性関節炎から生じるものであり、
前記薬物誘発性痛覚過敏またはアロディニアがオピオイド誘発性痛覚過敏/アロディニアまたはトリプタン(5-HT1D/1Bアゴニスト)誘発性痛覚過敏もしくはアロディニアであり、
前記化学物質依存症または嗜癖が薬物嗜癖、コカイン嗜癖、ニコチン嗜癖、メタンフェタミン誘発性神経毒性、エタノール耐性、依存、もしくは離脱、またはモルヒネ/オピオイド誘発性耐性、依存、痛覚過敏、もしくは離脱であり、
前記CNS障害が癲癇、不安、うつ病、注意欠陥機能亢進障害(ADHD)、精神病、または認知症であり、
前記神経変性疾患または神経傷害が急性脊椎損傷、AIDS関連認知症、パーキンソン病、アルツハイマー病、筋萎縮性側索硬化症(ALS)、ハンチントン舞踏病、多発性硬化症、神経毒性、または頭部外傷であり、
前記心血管関連症状が脳卒中、冠動脈バイパス移植(CABG)関連神経障害、低体温心停止(HCA)、卒中後痛、心原性ショック、再灌流傷害、または血管性認知症であり、あるいは
前記消化器障害が回腸造瘻術に関連する下痢、またはダンピング症候群である、請求項14に記載の医薬組成物。 - 前記症状が脳卒中、再灌流傷害、神経変性、頭部外傷、CABG、アロディニアを伴う片頭痛、中枢性卒中後痛(CPSP)、またはモルヒネ/オピオイド誘導性痛覚過敏である、請求項13に記載の医薬組成物。
- さらにオピオイド、抗うつ薬、抗てんかん薬、非ステロイド抗炎症性薬物(NSAID)、アセトアミノフェン、抗不整脈薬、GABA-Bアンタゴニスト、α-2-アドレナリン受容体アゴニスト、セロトニン5HT1B/1Dアゴニスト、N-メチル-D-アスパラギン酸アンタゴニスト、グルタミン酸受容体アンタゴニスト、コレシストキニンBアンタゴニスト、サブスタンスPアンタゴニスト、抗炎症性化合物、DHP感受性L型カルシウムチャネルアンタゴニスト、ω-コノトキシン感受性N型カルシウムチャネルアンタゴニスト、P/Q型カルシウムチャネルアンタゴニスト、アデノシンキナーゼアンタゴニスト、アデノシン受容体A1アゴニスト、アデノシン受容体A2aアンタゴニスト、アデノシン受容体A3アゴニスト、アデノシンデアミナーゼ阻害剤、アデノシンヌクレオシド輸送阻害剤、バニロイドVR1受容体アゴニスト、カンナビノイドCB1/CB2アゴニスト、AMPA受容体アンタゴニスト、カイニン酸受容体アンタゴニスト、ナトリウムチャネル遮断剤、ニコチン性アセチルコリン受容体アゴニスト、KATPカリウムチャネル開放剤、Kv1.4カリウムチャネル開放剤、Ca2+-活性化カリウムチャネル開放剤、SKカリウムチャネル開放剤、BKカリウムチャネル開放剤、IKカリウムチャネル開放剤、KCNQ2/3カリウムチャネル開放剤、ムスカリン性M3アンタゴニスト、ムスカリン性M1アゴニスト、ムスカリン性M2/M3部分アゴニスト/アンタゴニスト、抗酸化剤、抗精神病薬、ドーパミン受容体パーキンソン病薬、または脂肪酸アミド加水分解酵素(FAAH)阻害剤を含む、請求項13に記載の医薬組成物。
- 前記オピオイドが、アルフェンタニル、ブトルファノール 、ブプレノルフィン、デキストロモラミド、デゾシン、デキストロプロポキシフェン、コデイン、ジヒドロコデイン、ジフェノキシレート、エトルフィン、フェンタニル、ヒドロコドン、ヒドロモルフォン、ケトベミドン、ロペラミド、レボルファノール、レボメタドン、メプタジノール、メタドン、モルヒネ、モルヒネ-6-グルクロニド、ナルブフィン、ナロキソン、オキシコドン、オキシモルフォン、ペンタゾシン、ペチジン、ピリトラミド、プロポキシフェン、レミフェンタニル、スルフェンタニル、チリジン、またはトラマドールであり、
前記抗うつ薬が選択的セロトニン再取込み阻害剤、ノルエピネフリン再取込み阻害剤、デュアルセロトニン/ノルエピネフリン再取込み阻害剤、モノアミンオキシダーゼ阻害剤、可逆的モノアミンオキシダーゼA型阻害剤、または三環系であり、前記選択的セロトニン再取込み阻害剤がシタロプラム、エスシタロプラム、フルオキセチン、フルボキサミン、パロキセチン、またはセルトラリンであり、前記ノルエピネフリン再取込み阻害剤がアミトリプチリン、アトモキセチン、ブプロピオン、デスメチルアミトリプチリン、クロミプラミン、ドキセピン、イミプラミン、イミプラミンオキシド、トリミプラミン;アジナゾラム、アミルトリプチルイノキシド、アモキサピン、デシプラミン、マプロチリン、ノルトリプチリン、プロトリプチリン、アミネプチン、ブトリプチリン、デメキシプチリン、ジベンゼピン、ジメタクリン、ドチエピン、フルアシジン、イプリンドール、ロフェプラミン、メリトラセン、メタプラミン、ノルクロミプラミン、ノキシプチリン、オピプラモール、ペルラピン、ピゾチリン、プロピゼピン、キヌプラミン、レボキセチン、チアネプチン、またはトモキセチンであり、前記デュアルセロトニン/ノルエピネフリン再取込み阻害剤がデュロキセチン、ミルナシプラン、ミルタザピン、ネファゾドン、ベンラファキシン、またはデスベンラファキシンであり、前記モノアミンオキシダーゼ阻害剤がアミフラミン、イプロニアジド、イソカルボキサジド、M-3-PPC(Draxis)、モクロベミド、パルギリン、フェネルジン、トラニルシプロミン、またはバノキセリンであり、前記可逆的モノアミンオキシダーゼA型阻害剤がバジナプリン、ベフロキサトン、ブロファロミン、シモキサトン、またはクロルジリンであり、前記三環系がアミトリプチリン、クロミプラミン、デシプラミン、ドキセピン、イミプラミン、マプロチリン、ノルトリプチリン、プロトリプチリン、またはトリミプラミンであり、前記抗うつ薬がアジナゾラム、アラプロクラート、アミネプチン、アミトリプチリン/クロルジアゼポキシドの組合わせ、アチパメゾール、アザミアンセリン、バジナプリン、ベフラリン、ビフェメラン、ビノダリン、ビペナモール、ブロファロミン、カロキサゾン、セリクラミン、シアノプラミン、シモキサトン、シタロプラム、クレメプロール、クロボキサミン、ダゼピニル、デアノール、デメキシプチリン、ジベンゼピン、ドチエピン、ドロキシドパ、エネフェキシン、エスタゾラム、エトペリドン、フェモキセチン、フェンガビン、フェゾラミン、フルオトラセン、イダゾキサン、インダルピン、インデロキサジン、イプリンドール、レボプロチリン、リチウム、リトキセチン、ロフェプラミン、メジホキサミン、メタプラミン、メトラリンドール、ミアンセリン、ミルナシプラン、ミナプリン、ミルタザピン、モンチレリン、ネブラセタム、ネホパム、ニアラミド、ノミフェンシン、ノルフルオキセチン、オロチレリン、オキサフロザン、ピナゼパム、ピルリンドール、ピゾチリン、リタンセリン、ロリプラム、セルクロレミン、セチプチリン、シブトラミン、スルブチアミン、スルピリド、テニロキサジン、トザリノン、チロリベリン、チアネプチン、チフルカルビン、トラゾドン、トフェナシン、トフィソパム、トロキサトン、トモキセチン、ベラリプリド、ビロキサジン、ビクアリン、ジメリジン、またはゾメタピンであり、
前記抗てんかん薬がカルバマゼピン、フルピルチン、ガバペンチン、ラモトリジン、オクスカルバゼピン、フェニトイン、レチガビン、トピラメート、またはバルプロエートであり、
前記NSAIDがアセメタシン、アスピリン、セレコキシブ、デラコキシブ、ジクロフェナク、ジフルニサル、エテンザミド、エトフェナマート、エトリコキシブ、フェノプロフェン、フルフェナム酸、フルビプロフェン、ロナゾラク、ロルノキシカム、イブプロフェン、インドメタシン、イソキシカム、ケブゾン、ケトプロフェン、ケトロラク、ナプロキセン、ナブメトン、ニフルム酸、スリンダク、トルメチン、ピロキシカム、メクロフェナム酸、メフェナム酸、メロキシカム、メタミゾール、モフェブタゾン、オキシフェンブタゾン、パレコキシブ、フェニドン、フェニルブタゾン、ピロキシカム、プロパセタモール、プロピフェナゾン、ロフェコキシブ、サリチルアミド、スプロフェン、チアプロフェン酸、テノキシカム、バルデコキシブ、4-(4-シクロヘキシル-2-メチルオキサゾール-5-イル)-2-フルオロベンゼンスルホンアミド、N-[2-(シクロヘキシルオキシ)-4-ニトロフェニル]メタンスルホンアミド、2-(3,4-ジフルオロフェニル)-4-(3-ヒドロキシ-3-メチルブトキシ)-5-[4-(メチルスルホニル)フェニル]-3(2H)-ピリダジノン、または2-(3,5-ジフルオロフェニル)-3-[4-(メチルスルホニル)フェニル]-2-シクロペンテン-1-オン)であり、
前記セロトニン5HT1B/1Dアゴニストがエレトリプタン、フロバトリプタン、ナラトリプタン、リザトリプタン、スマトリプタン、ドニトリプタン、またはゾルミトリプタンであり、
前記N-メチル-D-アスパラギン酸アンタゴニストまたはグルタミン酸受容体アンタゴニストが、アマンタジン;アプチガネル;ベソンプロジル;ブジピン;コナントキンG;デルセミン;デキサナビノール;デキストロメトルファン;デキストロプロポキシフェン;フェルバメート;フルオロフェルバメート;ガシクリジン;グリシン;イペノキサゾン;カイトセファリン;ケタミン;ケトベミドン;ラニセミン;リコスチネル;ミダホテル;メマンチン;D-メタドン;D-モルヒネ;ミルナシプラン;ネラメキサン;オルフェナドリン;レマセミド;スルファゾシン;FPL-12,495(レマセミド代謝物);トピラメート;(αR)-α-アミノ-5-クロロ-1-(ホスホノメチル)-1H-ベンゾイミダゾール-2-プロパン酸;1-アミノシクロペンタン-カルボン酸;[5-(アミノメチル)-2-[[[(5S)-9-クロロ-2,3,6,7-テトラヒドロ-2,3-ジオキソ-1H-,5H-ピリド[1,2,3-de]キノキサリン-5-イル]アセチル]アミノ]フェノキシ]-酢酸;α-アミノ-2-(2-ホスホノエチル)-シクロヘキサンプロパン酸;α-アミノ-4-(ホスホノメチル)-ベンゼン酢酸;(3E)-2-アミノ-4-(ホスホノメチル)-3-ヘプテン酸;3-[(1E)-2-カルボキシ-2-フェニルエテニル]-4,6-ジクロロ-1H-インドール-2-カルボン酸;8-クロロ-2,3-ジヒドロピリダジノ[4,5-b]キノリン-1,4-ジオン5-オキシドの2-ヒドロキシ-N,N,N-トリメチル-エタンアミニウムとの塩;N'-[2-クロロ-5-(メチルチオ)フェニル]-N-メチル-N-[3-(メチルチオ)フェニル]-グアニジン;N'-[2-クロロ-5-(メチルチオ)フェニル]-N-メチル-N-[3-[(R)-メチルスルフィニル]フェニル]-グアニジン;6-クロロ-2,3,4,9-テトラヒドロ-9-メチル-2,3-ジオキソ-1H-インデノ[1,2-b]ピラジン-9-酢酸;7-クロロチオキヌレン酸;(3S,4aR,6S,8aR)-デカヒドロ-6-(ホスホノメチル)-3-イソキノリンカルボン酸;(-)-6,7-ジクロロ-1,4-ジヒドロ-5-[3-(メトキシメチル)-5-(3-ピリジニル)-4-H-1,2,4-トリアゾール-4-イル]-2,3-キノキサリ
ンジオン;4,6-ジクロロ-3-[(E)-(2-オキソ-1-フェニル-3-ピロリジニリデン)メチル]-1H-インドール-2-カルボン酸;(2R,4S)-rel-5,7-ジクロロ-1,2,3,4-テトラヒドロ-4-[[(フェニルアミノ)カルボニル]アミノ]-2-キノリンカルボン酸;(3R,4S)-rel-3,4-ジヒドロ-3-[4-ヒドロキシ-4-(フェニルメチル)-1-ピペリジニル]-2H-1-ベンゾピラン-4,7-ジオール;2-[(2,3-ジヒドロ-1H-インデン-2-イル)アミノ]-アセトアミド;1,4-ジヒドロ-6-メチル-5-[(メチルアミノ)メチル]-7-ニトロ-2,3-キノキサリンジオン;[2-(8,9-ジオキソ-2,6-ジアザビシクロ[5.2.0]ノン-1(7)-エン-2-イル)エチル]-ホスホン酸;(2R,6S)-1,2,3,4,5,6-ヘキサヒドロ-3-[(2S)-2-メトキシプロピル]-6,11,11-トリメチル-2,6-メタノ-3-ベンゾアゾシン-9-オール;2-ヒドロキシ-5-[[(ペンタフルオロフェニル)メチル]アミノ]-安息香酸;1-[2-(4-ヒドロキシフェノキシ)エチル]-4-[(4-メチルフェニル)メチル]-4-ピペリジノール;1-[4-(1H-イミダゾール-4-イル)-3-ブチニル]-4-(フェニルメチル)-ピペリジン;2-メチル-6-(フェニルエチニル)-ピリジン;3-(ホスホノメチル)-L-フェニルアラニン;または3,6,7-テトラヒドロ-2,3-ジオキソ-N-フェニル-1H,5H-ピリド[1,2,3-de]キノキサリン-5-アセトアミドであり、
前記抗炎症性化合物がアスピリン、セレコキシブ、コルチゾン、デラコキシブ、ジフルニサル、エトリコキシブ、フェノプロフェン、イブプロフェン、ケトプロフェン、ナプロキセン、プレドニゾロン、スリンダク、トルメチン、ピロキシカム、メフェナム酸、メロキシカム、フェニルブタゾン、ロフェコキシブ、スプロフェン、バルデコキシブ、4-(4-シクロヘキシル-2-メチルオキサゾール-5-イル)-2-フルオロベンゼンスルホンアミド、N-[2-(シクロヘキシルオキシ)-4-ニトロフェニル]メタンスルホンアミド、2-(3,4-ジフルオロフェニル)-4-(3-ヒドロキシ-3-メチルブトキシ)-5-[4-(メチルスルホニル)フェニル]-3(2H)-ピリダジノン、または 2-(3,5-ジフルオロフェニル)-3-[4-(メチルスルホニル)フェニル]-2-シクロペンテン-1-オンであり、
前記抗精神病薬がプロマジン、クロルプロマジン、クロルプロチキセン、チオリダジン、アセトフェナジン、メソリダジン、ドロペリドール、ロキサピン、モリンドン、ペルフェナジン、プロクロルペラジン、チオチキセン、トリフルオペラジン、フルフェナジン、ピモジド、フルペンチキソール、メトトリメプラジン、ピポチアジン、セルチンドール、クロザピン、オランザピン、リスペリドン、アリピプラゾール、クエチアピン、ハロペリドール、ジプラシドン、またはイロペリドンであり、あるいは
前記パーキンソン病薬がレボドパまたはプラミペキソールである、
請求項17に記載の医薬組成物。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US13388708P | 2008-07-03 | 2008-07-03 | |
| US61/133,887 | 2008-07-03 | ||
| PCT/CA2009/000923 WO2010000073A1 (en) | 2008-07-03 | 2009-07-03 | Benzoxazines, benzothiazines, and related compounds having nos inhibitory activity |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2011526251A JP2011526251A (ja) | 2011-10-06 |
| JP2011526251A5 JP2011526251A5 (ja) | 2012-08-16 |
| JP5572157B2 true JP5572157B2 (ja) | 2014-08-13 |
Family
ID=41465440
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011515041A Expired - Fee Related JP5572157B2 (ja) | 2008-07-03 | 2009-07-03 | Nos阻害活性を有するベンゾオキサジン類、ベンゾチアジン類、および関係化合物 |
Country Status (20)
| Country | Link |
|---|---|
| US (3) | US8106043B2 (ja) |
| EP (1) | EP2310386A4 (ja) |
| JP (1) | JP5572157B2 (ja) |
| KR (1) | KR20110036607A (ja) |
| CN (1) | CN102143961B (ja) |
| AR (1) | AR072471A1 (ja) |
| AU (1) | AU2009266386B2 (ja) |
| BR (1) | BRPI0913915A2 (ja) |
| CA (1) | CA2729246C (ja) |
| CL (1) | CL2010001633A1 (ja) |
| EA (1) | EA021798B1 (ja) |
| IL (1) | IL210195A (ja) |
| MX (1) | MX2011000124A (ja) |
| MY (1) | MY158796A (ja) |
| NZ (1) | NZ590727A (ja) |
| SG (1) | SG192470A1 (ja) |
| TW (1) | TWI458726B (ja) |
| UA (1) | UA105182C2 (ja) |
| WO (1) | WO2010000073A1 (ja) |
| ZA (1) | ZA201100436B (ja) |
Families Citing this family (117)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8829020B2 (en) | 2009-07-16 | 2014-09-09 | Mallinckrodt Llc | Compounds and compositions for use in phototherapy and in treatment of ocular neovascular disease and cancers |
| CN101830894B (zh) * | 2010-06-01 | 2013-05-29 | 上海交通大学 | 一类苯并[d]噁唑化合物及其制备方法 |
| WO2013076590A1 (en) * | 2011-11-23 | 2013-05-30 | Oxygen Healthcare Research Pvt. Ltd | Benzothiazine compounds as h3 receptor ligands |
| CN102491919B (zh) * | 2011-12-15 | 2014-03-19 | 南京友杰医药科技有限公司 | 去甲维拉帕米的合成方法 |
| WO2015023675A2 (en) | 2013-08-12 | 2015-02-19 | Pharmaceutical Manufacturing Research Services, Inc. | Extruded immediate release abuse deterrent pill |
| US10864209B2 (en) | 2013-11-05 | 2020-12-15 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11123343B2 (en) | 2013-11-05 | 2021-09-21 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US10966942B2 (en) | 2019-01-07 | 2021-04-06 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US9867819B2 (en) | 2013-11-05 | 2018-01-16 | Antecip Bioventures Ii Llc | Compositions and methods for increasing the metabolic lifetime of dextromethorphan and related pharmacodynamic effects |
| US11213521B2 (en) | 2013-11-05 | 2022-01-04 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US10772850B2 (en) | 2013-11-05 | 2020-09-15 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11541048B2 (en) | 2013-11-05 | 2023-01-03 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US20200338022A1 (en) | 2019-01-07 | 2020-10-29 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US10874664B2 (en) | 2013-11-05 | 2020-12-29 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11364233B2 (en) | 2013-11-05 | 2022-06-21 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11020389B2 (en) | 2013-11-05 | 2021-06-01 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US10894047B2 (en) | 2013-11-05 | 2021-01-19 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US10813924B2 (en) | 2018-03-20 | 2020-10-27 | Antecip Bioventures Ii Llc | Bupropion and dextromethorphan for treating nicotine addiction |
| US11524007B2 (en) | 2013-11-05 | 2022-12-13 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US10881657B2 (en) | 2013-11-05 | 2021-01-05 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11541021B2 (en) | 2013-11-05 | 2023-01-03 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US10980800B2 (en) | 2013-11-05 | 2021-04-20 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US10874665B2 (en) | 2013-11-05 | 2020-12-29 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11497721B2 (en) | 2013-11-05 | 2022-11-15 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US9763932B2 (en) | 2013-11-05 | 2017-09-19 | Antecip Bioventures Ii Llc | Compositions and methods for increasing the metabolic lifetime of dextromethorphan and related pharmacodynamic effects |
| US11617728B2 (en) | 2013-11-05 | 2023-04-04 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11433067B2 (en) | 2013-11-05 | 2022-09-06 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US10512643B2 (en) | 2013-11-05 | 2019-12-24 | Antecip Bioventures Ii Llc | Compositions and methods for increasing the metabolic lifetime of dextromethorphan and related pharmacodynamic effects |
| US11253492B2 (en) | 2013-11-05 | 2022-02-22 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11382874B2 (en) | 2013-11-05 | 2022-07-12 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11534414B2 (en) | 2013-11-05 | 2022-12-27 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US10966941B2 (en) | 2013-11-05 | 2021-04-06 | Antecip Bioventures Ii Llp | Bupropion as a modulator of drug activity |
| US11129826B2 (en) | 2013-11-05 | 2021-09-28 | Axsome Therapeutics, Inc. | Bupropion as a modulator of drug activity |
| US11096937B2 (en) | 2013-11-05 | 2021-08-24 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US9700528B2 (en) | 2013-11-05 | 2017-07-11 | Antecip Bioventures Ii Llc | Compositions and methods for increasing the metabolic lifetime of dextromethorphan and related pharmacodynamic effects |
| US11207281B2 (en) | 2013-11-05 | 2021-12-28 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11596627B2 (en) | 2013-11-05 | 2023-03-07 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11058648B2 (en) | 2013-11-05 | 2021-07-13 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US10874663B2 (en) | 2013-11-05 | 2020-12-29 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US9968568B2 (en) | 2013-11-05 | 2018-05-15 | Antecip Bioventures Ii Llc | Compositions and methods for increasing the metabolic lifetime of dextromethorphan and related pharmacodynamic effects |
| US11617747B2 (en) | 2013-11-05 | 2023-04-04 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11065248B2 (en) | 2013-11-05 | 2021-07-20 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US9198905B2 (en) | 2013-11-05 | 2015-12-01 | Antecip Bioventures Ii Llc | Compositions and methods for reducing dextrorphan plasma levels and related pharmacodynamic effects |
| US10945973B2 (en) | 2013-11-05 | 2021-03-16 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US10894046B2 (en) | 2013-11-05 | 2021-01-19 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11576909B2 (en) | 2013-11-05 | 2023-02-14 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11234946B2 (en) | 2013-11-05 | 2022-02-01 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US9408815B2 (en) | 2013-11-05 | 2016-08-09 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11197839B2 (en) | 2013-11-05 | 2021-12-14 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11969421B2 (en) | 2013-11-05 | 2024-04-30 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US9457023B1 (en) | 2013-11-05 | 2016-10-04 | Antecip Bioventures Ii Llc | Compositions and methods for increasing the metabolic lifetime of dextromethorphan and related pharmacodynamic effects |
| US11007189B2 (en) | 2013-11-05 | 2021-05-18 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11590124B2 (en) | 2013-11-05 | 2023-02-28 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11439636B1 (en) | 2013-11-05 | 2022-09-13 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11517543B2 (en) | 2013-11-05 | 2022-12-06 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US20220233470A1 (en) | 2013-11-05 | 2022-07-28 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11123344B2 (en) | 2013-11-05 | 2021-09-21 | Axsome Therapeutics, Inc. | Bupropion as a modulator of drug activity |
| US11571399B2 (en) | 2013-11-05 | 2023-02-07 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US10966974B2 (en) | 2013-11-05 | 2021-04-06 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11291665B2 (en) | 2013-11-05 | 2022-04-05 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11285146B2 (en) | 2013-11-05 | 2022-03-29 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US10799497B2 (en) | 2013-11-05 | 2020-10-13 | Antecip Bioventures Ii Llc | Combination of dextromethorphan and bupropion for treating depression |
| US11229640B2 (en) | 2013-11-05 | 2022-01-25 | Antecip Bioventures Ii Llc | Combination of dextromethorphan and bupropion for treating depression |
| US11478468B2 (en) | 2013-11-05 | 2022-10-25 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11141416B2 (en) | 2013-11-05 | 2021-10-12 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11344544B2 (en) | 2013-11-05 | 2022-05-31 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11419867B2 (en) | 2013-11-05 | 2022-08-23 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11426370B2 (en) | 2013-11-05 | 2022-08-30 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US10780064B2 (en) | 2019-01-07 | 2020-09-22 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11576877B2 (en) | 2013-11-05 | 2023-02-14 | Antecip Bioventures Ii Llc | Bupropion as modulator of drug activity |
| US9861595B2 (en) | 2013-11-05 | 2018-01-09 | Antecip Bioventures Ii Llc | Compositions and methods for increasing the metabolic lifetime of dextromethorphan and related pharmacodynamic effects |
| US10933034B2 (en) | 2013-11-05 | 2021-03-02 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11510918B2 (en) | 2013-11-05 | 2022-11-29 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US9474731B1 (en) | 2013-11-05 | 2016-10-25 | Antecip Bioventures Ii Llc | Compositions and methods for increasing the metabolic lifetime of dextromethorphan and related pharmacodynamic effects |
| US11273133B2 (en) | 2013-11-05 | 2022-03-15 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US9402843B2 (en) | 2013-11-05 | 2016-08-02 | Antecip Bioventures Ii Llc | Compositions and methods of using threohydroxybupropion for therapeutic purposes |
| US11185515B2 (en) | 2013-11-05 | 2021-11-30 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11311534B2 (en) | 2013-11-05 | 2022-04-26 | Antecip Bio Ventures Ii Llc | Bupropion as a modulator of drug activity |
| US20160324807A1 (en) | 2013-11-05 | 2016-11-10 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US9707191B2 (en) | 2013-11-05 | 2017-07-18 | Antecip Bioventures Ii Llc | Compositions and methods for increasing the metabolic lifetime of dextromethorphan and related pharmacodynamic effects |
| US11291638B2 (en) | 2013-11-05 | 2022-04-05 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US10940124B2 (en) | 2019-01-07 | 2021-03-09 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US10105327B2 (en) | 2013-11-05 | 2018-10-23 | Antecip Bioventures Ii Llc | Compositions and methods for increasing the metabolic lifetime of dextromethorphane and related pharmacodynamic effects |
| US11357744B2 (en) | 2013-11-05 | 2022-06-14 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11298351B2 (en) | 2013-11-05 | 2022-04-12 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11253491B2 (en) | 2013-11-05 | 2022-02-22 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11571417B2 (en) | 2013-11-05 | 2023-02-07 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11090300B2 (en) | 2013-11-05 | 2021-08-17 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11426401B2 (en) | 2013-11-05 | 2022-08-30 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11191739B2 (en) | 2013-11-05 | 2021-12-07 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11273134B2 (en) | 2013-11-05 | 2022-03-15 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US10786469B2 (en) | 2013-11-05 | 2020-09-29 | Antecip Bioventures Ii Llc | Compositions and methods for increasing the metabolic lifetime of dextromethorphan and related pharmacodynamic effects |
| US11298352B2 (en) | 2013-11-05 | 2022-04-12 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US11285118B2 (en) | 2013-11-05 | 2022-03-29 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US10080727B2 (en) | 2013-11-05 | 2018-09-25 | Antecip Bioventures Ii Llc | Compositions and methods for increasing the metabolic lifetime of dextromethorphan and related pharmacodynamic effects |
| US20160361305A1 (en) | 2013-11-05 | 2016-12-15 | Antecip Bioventures Ii Llc | Compositions and methods comprising bupropion or related compounds for sustained delivery of dextromethorphan |
| US10688066B2 (en) | 2018-03-20 | 2020-06-23 | Antecip Bioventures Ii Llc | Bupropion and dextromethorphan for treating nicotine addiction |
| US11147808B2 (en) | 2013-11-05 | 2021-10-19 | Antecip Bioventures Ii Llc | Method of decreasing the fluctuation index of dextromethorphan |
| US10105361B2 (en) | 2013-11-05 | 2018-10-23 | Antecip Bioventures Ii Llc | Compositions and methods for increasing the metabolic lifetime of dextromethorphan and related pharmacodynamic effects |
| US9457025B2 (en) | 2013-11-05 | 2016-10-04 | Antecip Bioventures Ii Llc | Compositions and methods comprising bupropion or related compounds for sustained delivery of dextromethorphan |
| US10898453B2 (en) | 2013-11-05 | 2021-01-26 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| US9492444B2 (en) | 2013-12-17 | 2016-11-15 | Pharmaceutical Manufacturing Research Services, Inc. | Extruded extended release abuse deterrent pill |
| WO2015095391A1 (en) | 2013-12-17 | 2015-06-25 | Pharmaceutical Manufacturing Research Services, Inc. | Extruded extended release abuse deterrent pill |
| CN103990106A (zh) * | 2014-06-11 | 2014-08-20 | 河北医科大学 | 八肽胆囊收缩素在制药中的应用 |
| WO2016010771A1 (en) | 2014-07-17 | 2016-01-21 | Pharmaceutical Manufacturing Research Services, Inc. | Immediate release abuse deterrent liquid fill dosage form |
| EP2985036A3 (en) * | 2014-08-14 | 2016-03-09 | Fraunhofer Gesellschaft zur Förderung der angewandten Forschung e.V. | CYP2J2 antagonists in the treatment of pain |
| JP2017531026A (ja) | 2014-10-20 | 2017-10-19 | ファーマシューティカル マニュファクチュアリング リサーチ サービシズ,インコーポレーテッド | 徐放性乱用抑止性液体充填剤形 |
| FR3030513B1 (fr) * | 2014-12-19 | 2016-12-23 | Oreal | Derives de benzoxazine cationiques et utilisation en coloration capillaire. |
| CN106279139B (zh) * | 2016-08-08 | 2018-12-28 | 湘潭大学 | 可用作sglt2抑制剂的化合物及其制备方法和用途 |
| CN106632353A (zh) * | 2016-11-18 | 2017-05-10 | 山东友帮生化科技有限公司 | 3‑硝基‑6‑氯咪唑并[1,2‑b]哒嗪的合成方法 |
| US11439632B2 (en) | 2018-12-05 | 2022-09-13 | Northwestern University | Use of neuronal nitric oxide synthase inhibitors for immunotherapy in melanoma patients |
| US10925842B2 (en) | 2019-01-07 | 2021-02-23 | Antecip Bioventures Ii Llc | Bupropion as a modulator of drug activity |
| CN109771386B (zh) * | 2019-01-10 | 2021-10-08 | 广东赛烽医药科技有限公司 | 一种氟哌噻吨美利曲辛片剂及其制备方法 |
| US20240000806A1 (en) * | 2020-11-20 | 2024-01-04 | University Of Pittsburgh - Of The Commonwealth System Of Higher Education | Methods and materials for inhibiting cb1 activity |
| IL308282A (en) * | 2021-05-10 | 2024-01-01 | Yissum Res Dev Co Of Hebrew Univ Jerusalem Ltd | Pharmaceutical compositions for the treatment of neurological diseases |
| US11717518B1 (en) | 2022-06-30 | 2023-08-08 | Antecip Bioventures Ii Llc | Bupropion dosage forms with reduced food and alcohol dosing effects |
| US11730706B1 (en) | 2022-07-07 | 2023-08-22 | Antecip Bioventures Ii Llc | Treatment of depression in certain patient populations |
Family Cites Families (108)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3862114A (en) | 1971-11-22 | 1975-01-21 | Ici Australia Ltd | Analogs of substance p |
| US3912711A (en) | 1972-07-03 | 1975-10-14 | Susan E Leeman | Synthetically produced undecapeptide, Substance P |
| US4481139A (en) | 1983-04-13 | 1984-11-06 | Board Of Regents, The University Of Texas System | Peptide antagonists of substance P |
| US4472305A (en) | 1983-05-17 | 1984-09-18 | Sterling Drug Inc. | Hexapeptide amides |
| US4680283A (en) | 1984-09-26 | 1987-07-14 | Merck & Co., Inc. | Analogs of substance P and eledoisin |
| US4839465A (en) | 1987-01-20 | 1989-06-13 | Sterling Drug Inc. | Di-(D-tryptophyl and/or tetrahydropyridoindolylcarbonyl)-containing peptide amides and process for preparation thereof |
| DE3711335A1 (de) | 1987-04-03 | 1988-10-20 | Merck Patent Gmbh | Aminosaeurederivate |
| US5410019A (en) | 1987-09-24 | 1995-04-25 | The Administrators Of The Tulane-Educational Fund | Therapeutic peptides |
| US5378803A (en) | 1987-12-11 | 1995-01-03 | Sterling Winthrop Inc. | Azole-fused peptides and processes for preparation thereof |
| GB8807921D0 (en) | 1988-04-05 | 1988-05-05 | Fujisawa Pharmaceutical Co | Ws-9326 & its derivatives |
| GB8802229D0 (en) | 1988-02-02 | 1988-03-02 | Fujisawa Pharmaceutical Co | Ws-9326 & its derivatives |
| US5187156A (en) | 1988-03-16 | 1993-02-16 | Fujisawa Pharmaceutical Co., Ltd. | Peptide compounds, processes for preparation thereof and pharmaceutical composition comprising the same |
| EP0360390A1 (en) | 1988-07-25 | 1990-03-28 | Glaxo Group Limited | Spirolactam derivatives |
| WO1990005525A1 (en) | 1988-11-23 | 1990-05-31 | Pfizer Inc. | Quinuclidine derivatives as substance p antagonists |
| ATE94384T1 (de) | 1989-04-14 | 1993-10-15 | Merz & Co Gmbh & Co | Verwendung von adamantan-derivaten zur praevention und behandlung der cerebralen ischaemie. |
| US5164372A (en) | 1989-04-28 | 1992-11-17 | Fujisawa Pharmaceutical Company, Ltd. | Peptide compounds having substance p antagonism, processes for preparation thereof and pharmaceutical composition comprising the same |
| IE903957A1 (en) | 1989-11-06 | 1991-05-08 | Sanofi Sa | Aromatic amine compounds, their method of preparation and¹pharmaceutical compositions in which they are present |
| FR2654725B1 (fr) | 1989-11-23 | 1992-02-14 | Rhone Poulenc Sante | Nouveaux derives de l'isoindolone, leur preparation et les compositions pharmaceutiques qui les contiennent. |
| GB8929070D0 (en) | 1989-12-22 | 1990-02-28 | Fujisawa Pharmaceutical Co | Peptide compounds,processes for preparation thereof and pharmaceutical composition comprising the same |
| WO1991009844A1 (en) | 1990-01-04 | 1991-07-11 | Pfizer Inc. | Substance p antagonists |
| US5232929A (en) | 1990-11-28 | 1993-08-03 | Pfizer Inc. | 3-aminopiperidine derivatives and related nitrogen containing heterocycles and pharmaceutical compositions and use |
| WO1991012266A1 (en) | 1990-02-15 | 1991-08-22 | Fujisawa Pharmaceutical Co., Ltd. | Peptide compound |
| DE4007869A1 (de) | 1990-03-13 | 1991-09-19 | Merck Patent Gmbh | Aminosaeurederivate |
| ATE113947T1 (de) | 1990-06-01 | 1994-11-15 | Pfizer | 3-amino-2-arylchinuclidine, verfahren zu ihrer herstellung und diese enthaltende pharmazeutische zubereitungen. |
| DE69106365T2 (de) | 1990-07-23 | 1995-05-04 | Pfizer | Chinuclidinderivate. |
| DK0550635T3 (da) | 1990-09-28 | 1995-09-04 | Pfizer | Cykliske forbindelser med kondeserede ringe, som er analoger til nitrogenholdige ikke-aromatiske het erocykliske forbindelser |
| US5420297A (en) | 1990-10-24 | 1995-05-30 | Fujisawa Pharmaceutical Co., Ltd. | Peptides having substance P antagonistic activity |
| DE4034829A1 (de) | 1990-11-02 | 1992-05-07 | Merck Patent Gmbh | Cyclopeptide |
| WO1992012151A1 (en) | 1991-01-10 | 1992-07-23 | Pfizer Inc. | N-alkyl quinuclidinium salts as substance p antagonists |
| ATE154354T1 (de) | 1991-02-11 | 1997-06-15 | Merck Sharp & Dohme | Azabicyclische verbindungen, diese enthaltende pharmazeutische zubereitungen und ihre therapeutische verwendung |
| ATE115581T1 (de) | 1991-03-01 | 1994-12-15 | Pfizer | 1-azabicyclo(3.2.2>nonan-3-aminderivate. |
| US5484886A (en) | 1991-04-25 | 1996-01-16 | Merck & Co., Inc. | Human neurokinin-1 receptor |
| FR2676054B1 (fr) | 1991-05-03 | 1993-09-03 | Sanofi Elf | Nouveaux composes n-alkylenepiperidino et leurs enantiomeres, procede pour leur preparation et compositions pharmaceutiques les contenant. |
| FR2676055B1 (fr) | 1991-05-03 | 1993-09-03 | Sanofi Elf | Composes polycycliques amines et leurs enantiomeres, procede pour leur preparation et compositions pharmaceutiques les contenant. |
| FR2676053B1 (fr) | 1991-05-03 | 1993-08-27 | Sanofi Elf | Nouveaux composes dialkylenepiperidino et leurs enantiomeres, procede pour leur preparation et compositions pharmaceutiques les contenant. |
| FR2676442B1 (fr) | 1991-05-17 | 1993-08-06 | Rhone Poulenc Rorer Sa | Nouveau derives de perhydroisoindole, leur preparation et les compositions pharmaceutiques qui les contiennent. |
| FR2676446B1 (fr) | 1991-05-17 | 1993-08-06 | Rhone Poulenc Rorer Sa | Nouveaux derives du thiopyranopyrrole, leur preparation et les compositions pharmaceutiques qui les contiennent. |
| US5292726A (en) | 1991-05-22 | 1994-03-08 | Merck & Co., Inc. | N,N-diacylpiperazines |
| DE9290057U1 (de) | 1991-05-22 | 1994-01-05 | Pfizer | Substituierte 3-Aminochinuclidine |
| KR100214905B1 (ko) | 1991-05-31 | 1999-08-02 | 디. 제이. 우드, 스피겔 알렌 제이 | 퀴누클리딘 유도체 |
| GB9113219D0 (en) | 1991-06-19 | 1991-08-07 | Fujisawa Pharmaceutical Co | Peptide compound,processes for preparation thereof and pharmaceutical composition comprising the same |
| ES2092113T3 (es) | 1991-06-20 | 1996-11-16 | Pfizer | Derivados fluoroalcoxibencilamino de heterociclos que contienen nitrogeno. |
| US5242944A (en) | 1991-06-20 | 1993-09-07 | Korea Research Institute Of Chemical Technology | Phenylacetamide derivatives and pharmaceutical compositions thereof |
| TW202432B (ja) | 1991-06-21 | 1993-03-21 | Pfizer | |
| US5288730A (en) | 1991-06-24 | 1994-02-22 | Merck Sharp & Dohme Limited | Azabicyclic compounds, pharmaceutical compositions containing them and their use in therapy |
| US5472978A (en) | 1991-07-05 | 1995-12-05 | Merck Sharp & Dohme Ltd. | Aromatic compounds, pharmaceutical compositions containing them and their use in therapy |
| IE72090B1 (en) | 1991-07-05 | 1997-03-12 | Merck Sharp & Dohme | Aromatic compounds pharmaceutical compositions containing them and their use in therapy |
| US5495047A (en) | 1991-07-10 | 1996-02-27 | Merck, Sharp & Dohme (Ltd.) | Fused tricyclic compounds, pharmaceutical compositions containing them and their use in therapy |
| JPH06509090A (ja) | 1991-07-10 | 1994-10-13 | メルク シヤープ エンド ドーム リミテツド | 芳香族化合物、それらを含む組成物、及び治療におけるそれらの使用 |
| MY110227A (en) | 1991-08-12 | 1998-03-31 | Ciba Geigy Ag | 1-acylpiperindine compounds. |
| EP0600952B1 (en) | 1991-08-20 | 1996-04-17 | MERCK SHARP & DOHME LTD. | Azacyclic compounds, processes for their preparation and pharmaceutical compositions containing them |
| CA2118704C (en) | 1991-09-26 | 1997-01-21 | John A. Lowe, Iii | Fused tricyclic nitrogen containing heterocycles as substance p receptor antagonists |
| CA2324959C (en) | 1991-11-12 | 2002-11-12 | Pfizer Limited | Phthalimido compounds as intermediates for producing substance p receptor antagonists |
| GB9201179D0 (en) | 1992-01-21 | 1992-03-11 | Glaxo Group Ltd | Chemical compounds |
| JP2656702B2 (ja) | 1992-03-23 | 1997-09-24 | ファイザー製薬株式会社 | ペプチド性キヌクリジン |
| FR2689888B1 (fr) | 1992-04-10 | 1994-06-10 | Rhone Poulenc Rorer Sa | Nouveaux derives de perhydroisoindole, leur preparation et les compositions pharmaceutiques qui les contiennent. |
| PT655055E (pt) | 1992-08-13 | 2001-03-30 | Warner Lambert Co | Antagonistas de taquiquinina |
| DK0655996T3 (da) | 1992-08-19 | 2001-12-27 | Pfizer | Substituerede benzylamino-nitrogenholdige, ikke-aromatiske, heterocykliske forbindelser |
| FR2696178B1 (fr) | 1992-09-30 | 1994-12-30 | Sanofi Elf | Amides basiques quaternaires, procédé pour leur préparation et compositions pharmaceutiques en contenant. |
| JP2656699B2 (ja) | 1992-10-21 | 1997-09-24 | ファイザー製薬株式会社 | 置換ベンジルアミノキヌクリジン |
| EP0670309A1 (en) | 1992-11-20 | 1995-09-06 | Japan Tobacco Inc. | Compound with prolyl endopeptidase inhibitor activity and pharmaceutical use thereof |
| US5338845A (en) | 1992-12-02 | 1994-08-16 | Sterling Winthrop Inc. | Aspergillus species, cyclic dimeric dipeptide derivative substance P antagonist biosynthetic products thereof, and process for preparation thereof |
| US5408308A (en) | 1993-01-29 | 1995-04-18 | Corning Incorporated | Method for monitoring hermetically-coated fibers |
| US5635510A (en) | 1993-05-06 | 1997-06-03 | Merrell Pharmaceuticals Inc. | Substituted pyrrolidin-3-yl-alkyl-piperidines |
| CA2163995A1 (en) | 1993-06-07 | 1994-12-22 | Malcolm Maccoss | Spiro-substituted azacycles as neurokinin antagonists |
| EP0634402A1 (en) | 1993-07-14 | 1995-01-18 | Takeda Chemical Industries, Ltd. | Isochinolinone derivatives, their production and use |
| WO1995003281A1 (en) | 1993-07-26 | 1995-02-02 | Pfizer Inc. | Tetrahydro-1h-benzazepinones and hexahydroazepinones as selective cholecystokinin-b receptor antagonists |
| TW365603B (en) | 1993-07-30 | 1999-08-01 | Rhone Poulenc Rorer Sa | Novel perhydroisoindole derivatives, their preparation and pharmaceutical compositions which contain them |
| AU7856194A (en) | 1993-10-26 | 1995-05-22 | Ciba-Geigy Ag | N-benzoyl-4-oxy/thio-2-substituted piperidines as substance-p receptor antagonists |
| US6403577B1 (en) | 1993-11-17 | 2002-06-11 | Eli Lilly And Company | Hexamethyleneiminyl tachykinin receptor antagonists |
| EP0683160A1 (en) * | 1994-04-04 | 1995-11-22 | Sumitomo Chemical Company, Limited | Iminothiazoline derivatives and herbicides containing them as active ingredients |
| JPH07324079A (ja) * | 1994-04-04 | 1995-12-12 | Sumitomo Chem Co Ltd | イミノチアゾリン誘導体およびその用途 |
| FR2719312B1 (fr) | 1994-04-28 | 1996-06-14 | Adir | Nouveau pseudopeptides dérivés de neurokinines, leur procédé de préparation et les compositions pharmaceutiques qui les contiennent. |
| DE4424787A1 (de) * | 1994-07-14 | 1996-01-18 | Bayer Ag | Substituierte Aryliminoheterocyclen |
| US5576317A (en) | 1994-12-09 | 1996-11-19 | Pfizer Inc. | NK-1 receptor antagonists and 5HT3 receptor antagonists for the treatment of emesis |
| DE19531152A1 (de) * | 1994-12-15 | 1996-06-20 | Bayer Ag | Substituierte N-Aryl-Stickstoffheterocyclen |
| RU2156250C2 (ru) | 1995-04-24 | 2000-09-20 | Новартис Аг | Производные хромона, способ их получения и фармацевтическая композиция |
| EP0851759A4 (en) | 1995-09-05 | 2000-12-06 | Smithkline Beecham Corp | COMPOUNDS AND RELATED METHODS |
| GB9524157D0 (en) | 1995-11-25 | 1996-01-24 | Pfizer Ltd | Therapeutic agents |
| TW382017B (en) | 1995-12-27 | 2000-02-11 | Janssen Pharmaceutica Nv | 1-(1,2-disubstituted piperidinyl)-4-(fused imidazole)-piperidine derivatives |
| PT891332E (pt) | 1996-03-29 | 2004-07-30 | Pfizer | Derivados de 6-fenilpiridil-2-amina |
| AU2611297A (en) | 1996-04-12 | 1997-11-07 | Eli Lilly And Company | Bisindoles for treating pain or nociception |
| AU3716997A (en) | 1996-07-17 | 1998-02-09 | Merck & Co., Inc. | Alteration of circadian rhythmicity with a tachykinin antagonist |
| MY132550A (en) | 1996-08-22 | 2007-10-31 | Novartis Ag | Acylaminoalkenylene-amide derivatives as nk1 and nk2 antogonists |
| AU4261697A (en) | 1996-09-09 | 1998-03-26 | Smithkline Beecham Corporation | Compounds and methods |
| BR9712023A (pt) | 1996-09-10 | 1999-08-31 | Thomae Gmbh Dr K | Aminoácidos derivados, medicamentos contendo esses compostos e processos para a sua preparação. |
| HN1997000027A (es) | 1996-12-06 | 1997-06-05 | Pfizer Prod Inc | Derivados de 6-fenil piridil - 2 amina |
| BR9811093A (pt) | 1997-02-10 | 2000-07-18 | Pfizer Prod Inc | Piridinas substituìdas com 2-amino-6-(4-fenóxi 2-substituìdo) |
| WO1998056779A1 (en) | 1997-06-13 | 1998-12-17 | Smithkline Beecham Corporation | 4-sulfinyl benzamides as calcitonin gene-related peptide receptor antagonists |
| US6071966A (en) | 1997-06-30 | 2000-06-06 | Merz + Co. Gmbh & Co. | 1-amino-alkylcyclohexane NMDA receptor antagonists |
| CA2292558C (en) | 1997-06-30 | 2006-09-19 | Merz + Co. Gmbh & Co. | 1-amino-alkylcyclohexane nmda receptor antagonists |
| HN1998000118A (es) | 1997-08-27 | 1999-02-09 | Pfizer Prod Inc | 2 - aminopiridinas que contienen sustituyentes de anillos condensados. |
| HN1998000125A (es) | 1997-08-28 | 1999-02-09 | Pfizer Prod Inc | 2-aminopiridinas con sustituyentes alcoxi ramificados |
| ES2235475T3 (es) | 1998-06-03 | 2005-07-01 | Pfizer Products Inc. | 2-aminopiridinas que contienen sustituyentes de anillos condensados como inhibidores de oxido nitrico sintasa. |
| DE19844291A1 (de) * | 1998-09-18 | 2000-03-23 | Schering Ag | Benzoxazin- und Benzothiazin-Derivate und deren Verwendung in Arzneimitteln |
| CA2345357A1 (en) | 1998-09-30 | 2000-04-06 | Merck Sharp & Dohme Limited | Benzimidazolinyl piperidines as cgrp ligands |
| AU4249700A (en) * | 1999-04-19 | 2000-11-02 | Sumitomo Pharmaceuticals Company, Limited | Hydroxamic acid derivative |
| DE19952146A1 (de) | 1999-10-29 | 2001-06-07 | Boehringer Ingelheim Pharma | Arylalkane, Arylalkene und Aryl-azaalkane, diese Verbindungen enthaltende Arzneimittel und Verfahren zu ihrer Herstellung |
| DE19952147A1 (de) | 1999-10-29 | 2001-05-03 | Boehringer Ingelheim Pharma | Neue Cyclopropane, diese Verbindungen enthaltende Arzneimittel und Verfahren zu ihrer Herstellung |
| DE10020667A1 (de) * | 2000-04-19 | 2001-11-22 | Schering Ag | Neue Benzoxazin- und Benzothiazin-Derivate und deren Verwendung in Arzneimitteln |
| US20030082225A1 (en) | 2001-10-19 | 2003-05-01 | Mason Paul Arthur | Sterile, breathable patch for treating wound pain |
| DK1539724T3 (da) | 2002-08-07 | 2008-02-11 | Neuraxon Inc | Aminobenzothiazolforbindelser med NOS-inhiberende aktivitet |
| CN101247853B (zh) * | 2005-04-13 | 2014-11-12 | 轴突公司 | 具有nos抑制活性的取代的吲哚化合物 |
| AR054045A1 (es) * | 2005-05-18 | 2007-05-30 | Neuraxon Inc | Compuestos benzoimidazol sustituidos con actividad dual no inhibitoria y mu opioide agonista |
| US7700592B2 (en) * | 2005-08-25 | 2010-04-20 | Schering Corporation | α2C adrenoreceptor agonists |
| DE602006016303D1 (de) * | 2005-08-25 | 2010-09-30 | Pharmacopeia Llc | 3,4-dihydro-2H-benzoÄ1,4Üoxazin- und 3,4-dihydro-2H-benzoÄ1,4Üthiazin-VERBINDUNGEN ALS ALPHA2C-ADRENOREZEPTOR-ANTAGONISTEN |
| AR060451A1 (es) * | 2006-04-13 | 2008-06-18 | Neuraxon Inc | Compuestos de indol 1,5 y 3,6-sustituidos con actividad inhibitoria de nos |
| CA2705833A1 (en) | 2007-11-16 | 2009-05-22 | Subhash C. Annedi | 3,5-substituted indole compounds having nos and norepinephrine reuptake inhibitory activity |
-
2009
- 2009-03-07 UA UAA201101136A patent/UA105182C2/ru unknown
- 2009-07-03 SG SG2013051644A patent/SG192470A1/en unknown
- 2009-07-03 AR ARP090102506A patent/AR072471A1/es unknown
- 2009-07-03 KR KR1020117002783A patent/KR20110036607A/ko not_active Application Discontinuation
- 2009-07-03 CA CA2729246A patent/CA2729246C/en not_active Expired - Fee Related
- 2009-07-03 NZ NZ590727A patent/NZ590727A/xx not_active IP Right Cessation
- 2009-07-03 JP JP2011515041A patent/JP5572157B2/ja not_active Expired - Fee Related
- 2009-07-03 WO PCT/CA2009/000923 patent/WO2010000073A1/en active Application Filing
- 2009-07-03 EP EP09771883A patent/EP2310386A4/en not_active Withdrawn
- 2009-07-03 MX MX2011000124A patent/MX2011000124A/es active IP Right Grant
- 2009-07-03 TW TW098122515A patent/TWI458726B/zh not_active IP Right Cessation
- 2009-07-03 AU AU2009266386A patent/AU2009266386B2/en not_active Ceased
- 2009-07-03 CN CN200980134295.9A patent/CN102143961B/zh not_active Expired - Fee Related
- 2009-07-03 EA EA201170130A patent/EA021798B1/ru not_active IP Right Cessation
- 2009-07-03 MY MYPI2010006341A patent/MY158796A/en unknown
- 2009-07-03 BR BRPI0913915A patent/BRPI0913915A2/pt not_active IP Right Cessation
- 2009-07-06 US US12/498,185 patent/US8106043B2/en not_active Expired - Fee Related
-
2010
- 2010-12-23 IL IL210195A patent/IL210195A/en not_active IP Right Cessation
- 2010-12-30 CL CL2010001633A patent/CL2010001633A1/es unknown
-
2011
- 2011-01-17 ZA ZA2011/00436A patent/ZA201100436B/en unknown
-
2012
- 2012-01-27 US US13/360,029 patent/US8618286B2/en not_active Expired - Fee Related
-
2013
- 2013-12-11 US US14/103,446 patent/US20140163016A1/en not_active Abandoned
Also Published As
| Publication number | Publication date |
|---|---|
| JP2011526251A (ja) | 2011-10-06 |
| MY158796A (en) | 2016-11-15 |
| US20120122855A1 (en) | 2012-05-17 |
| US20140163016A1 (en) | 2014-06-12 |
| CA2729246A1 (en) | 2010-01-07 |
| EA201170130A1 (ru) | 2011-08-30 |
| EA021798B1 (ru) | 2015-09-30 |
| AR072471A1 (es) | 2010-09-01 |
| US8106043B2 (en) | 2012-01-31 |
| EP2310386A4 (en) | 2012-04-11 |
| US20100009975A1 (en) | 2010-01-14 |
| KR20110036607A (ko) | 2011-04-07 |
| BRPI0913915A2 (pt) | 2015-10-13 |
| ZA201100436B (en) | 2012-10-31 |
| TWI458726B (zh) | 2014-11-01 |
| IL210195A (en) | 2015-08-31 |
| US8618286B2 (en) | 2013-12-31 |
| CN102143961B (zh) | 2014-11-05 |
| CA2729246C (en) | 2018-08-21 |
| UA105182C2 (ru) | 2014-04-25 |
| IL210195A0 (en) | 2011-03-31 |
| NZ590727A (en) | 2012-12-21 |
| SG192470A1 (en) | 2013-08-30 |
| MX2011000124A (es) | 2011-02-24 |
| EP2310386A1 (en) | 2011-04-20 |
| AU2009266386A1 (en) | 2010-01-07 |
| AU2009266386B2 (en) | 2015-02-19 |
| CN102143961A (zh) | 2011-08-03 |
| TW201002701A (en) | 2010-01-16 |
| WO2010000073A1 (en) | 2010-01-07 |
| CL2010001633A1 (es) | 2011-05-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5572157B2 (ja) | Nos阻害活性を有するベンゾオキサジン類、ベンゾチアジン類、および関係化合物 | |
| TWI417099B (zh) | 具抑制一氧化氮合成酶活性之喹諾酮、四氫喹啉及其相關化合物 | |
| US20090131503A1 (en) | 3,5 - substituted indole compounds having nos and norepinephrine reuptake inhibitory activity | |
| JP5833804B2 (ja) | Nos阻害活性を有する置換インドール化合物 | |
| US7919510B2 (en) | Substituted benzimidazole compounds with dual NOS inhibitory activity and mu opioid agonist activity | |
| JP5350219B2 (ja) | Nos阻害活性を有する1,5および3,6−置換インドール化合物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20110615 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120702 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20120702 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20140204 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20140501 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20140603 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20140627 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5572157 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| LAPS | Cancellation because of no payment of annual fees |