JP5489725B2 - 生分解性エンドプロテーゼおよび製造方法 - Google Patents
生分解性エンドプロテーゼおよび製造方法 Download PDFInfo
- Publication number
- JP5489725B2 JP5489725B2 JP2009546550A JP2009546550A JP5489725B2 JP 5489725 B2 JP5489725 B2 JP 5489725B2 JP 2009546550 A JP2009546550 A JP 2009546550A JP 2009546550 A JP2009546550 A JP 2009546550A JP 5489725 B2 JP5489725 B2 JP 5489725B2
- Authority
- JP
- Japan
- Prior art keywords
- polymer
- biodegradable
- tubular body
- item
- stent
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
- A61L31/14—Materials characterised by their function or physical properties, e.g. injectable or lubricating compositions, shape-memory materials, surface modified materials
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2/00—Filters implantable into blood vessels; Prostheses, i.e. artificial substitutes or replacements for parts of the body; Appliances for connecting them with the body; Devices providing patency to, or preventing collapsing of, tubular structures of the body, e.g. stents
- A61F2/82—Devices providing patency to, or preventing collapsing of, tubular structures of the body, e.g. stents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2/00—Filters implantable into blood vessels; Prostheses, i.e. artificial substitutes or replacements for parts of the body; Appliances for connecting them with the body; Devices providing patency to, or preventing collapsing of, tubular structures of the body, e.g. stents
- A61F2/82—Devices providing patency to, or preventing collapsing of, tubular structures of the body, e.g. stents
- A61F2/86—Stents in a form characterised by the wire-like elements; Stents in the form characterised by a net-like or mesh-like structure
- A61F2/90—Stents in a form characterised by the wire-like elements; Stents in the form characterised by a net-like or mesh-like structure characterised by a net-like or mesh-like structure
- A61F2/91—Stents in a form characterised by the wire-like elements; Stents in the form characterised by a net-like or mesh-like structure characterised by a net-like or mesh-like structure made from perforated sheets or tubes, e.g. perforated by laser cuts or etched holes
- A61F2/915—Stents in a form characterised by the wire-like elements; Stents in the form characterised by a net-like or mesh-like structure characterised by a net-like or mesh-like structure made from perforated sheets or tubes, e.g. perforated by laser cuts or etched holes with bands having a meander structure, adjacent bands being connected to each other
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
- A61L31/04—Macromolecular materials
- A61L31/06—Macromolecular materials obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
- A61L31/14—Materials characterised by their function or physical properties, e.g. injectable or lubricating compositions, shape-memory materials, surface modified materials
- A61L31/148—Materials at least partially resorbable by the body
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G63/00—Macromolecular compounds obtained by reactions forming a carboxylic ester link in the main chain of the macromolecule
- C08G63/02—Polyesters derived from hydroxycarboxylic acids or from polycarboxylic acids and polyhydroxy compounds
- C08G63/06—Polyesters derived from hydroxycarboxylic acids or from polycarboxylic acids and polyhydroxy compounds derived from hydroxycarboxylic acids
- C08G63/08—Lactones or lactides
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L67/00—Compositions of polyesters obtained by reactions forming a carboxylic ester link in the main chain; Compositions of derivatives of such polymers
- C08L67/04—Polyesters derived from hydroxycarboxylic acids, e.g. lactones
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2/00—Filters implantable into blood vessels; Prostheses, i.e. artificial substitutes or replacements for parts of the body; Appliances for connecting them with the body; Devices providing patency to, or preventing collapsing of, tubular structures of the body, e.g. stents
- A61F2/82—Devices providing patency to, or preventing collapsing of, tubular structures of the body, e.g. stents
- A61F2002/823—Stents, different from stent-grafts, adapted to cover an aneurysm
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2/00—Filters implantable into blood vessels; Prostheses, i.e. artificial substitutes or replacements for parts of the body; Appliances for connecting them with the body; Devices providing patency to, or preventing collapsing of, tubular structures of the body, e.g. stents
- A61F2/82—Devices providing patency to, or preventing collapsing of, tubular structures of the body, e.g. stents
- A61F2002/825—Devices providing patency to, or preventing collapsing of, tubular structures of the body, e.g. stents having longitudinal struts
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2210/00—Particular material properties of prostheses classified in groups A61F2/00 - A61F2/26 or A61F2/82 or A61F9/00 or A61F11/00 or subgroups thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2230/00—Geometry of prostheses classified in groups A61F2/00 - A61F2/26 or A61F2/82 or A61F9/00 or A61F11/00 or subgroups thereof
- A61F2230/0002—Two-dimensional shapes, e.g. cross-sections
- A61F2230/0004—Rounded shapes, e.g. with rounded corners
- A61F2230/0013—Horseshoe-shaped, e.g. crescent-shaped, C-shaped, U-shaped
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2250/00—Special features of prostheses classified in groups A61F2/00 - A61F2/26 or A61F2/82 or A61F9/00 or A61F11/00 or subgroups thereof
- A61F2250/0014—Special features of prostheses classified in groups A61F2/00 - A61F2/26 or A61F2/82 or A61F9/00 or A61F11/00 or subgroups thereof having different values of a given property or geometrical feature, e.g. mechanical property or material property, at different locations within the same prosthesis
- A61F2250/0036—Special features of prostheses classified in groups A61F2/00 - A61F2/26 or A61F2/82 or A61F9/00 or A61F11/00 or subgroups thereof having different values of a given property or geometrical feature, e.g. mechanical property or material property, at different locations within the same prosthesis differing in thickness
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10T—TECHNICAL SUBJECTS COVERED BY FORMER US CLASSIFICATION
- Y10T428/00—Stock material or miscellaneous articles
- Y10T428/13—Hollow or container type article [e.g., tube, vase, etc.]
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10T—TECHNICAL SUBJECTS COVERED BY FORMER US CLASSIFICATION
- Y10T428/00—Stock material or miscellaneous articles
- Y10T428/13—Hollow or container type article [e.g., tube, vase, etc.]
- Y10T428/1352—Polymer or resin containing [i.e., natural or synthetic]
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10T—TECHNICAL SUBJECTS COVERED BY FORMER US CLASSIFICATION
- Y10T428/00—Stock material or miscellaneous articles
- Y10T428/13—Hollow or container type article [e.g., tube, vase, etc.]
- Y10T428/1352—Polymer or resin containing [i.e., natural or synthetic]
- Y10T428/139—Open-ended, self-supporting conduit, cylinder, or tube-type article
Landscapes
- Health & Medical Sciences (AREA)
- Heart & Thoracic Surgery (AREA)
- Vascular Medicine (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Surgery (AREA)
- Epidemiology (AREA)
- Biomedical Technology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Cardiology (AREA)
- Organic Chemistry (AREA)
- Medicinal Chemistry (AREA)
- Oral & Maxillofacial Surgery (AREA)
- Transplantation (AREA)
- Polymers & Plastics (AREA)
- Physics & Mathematics (AREA)
- Optics & Photonics (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Urology & Nephrology (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Pharmacology & Pharmacy (AREA)
- Materials For Medical Uses (AREA)
- Prostheses (AREA)
- Media Introduction/Drainage Providing Device (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Biological Depolymerization Polymers (AREA)
- Surgical Instruments (AREA)
Description
本発明は、概して、医療デバイスおよびそれらの製造のための方法に関する。特に、本発明は、強化された強度および移植後の制御された持続性を有する、ステント等の生分解性エンドプロテーゼ(endoprosthesis)の製造に関する。
ステントに使用されるフィラメントおよび他の構成要素の熱焼鈍および他の処理は、特許文献1、特許文献2、および特許文献3に記載されている。ポリマーステント被覆の熱処理は、米国を指定する、共同所有された同時係属中出願のPCT/US07/81996に記載されている。
本発明は、例えば、以下を提供する。
(項目1)
生分解性プロテーゼを製造する方法であって、
初期の直径を有する管状本体を提供することであって、該管状本体は、少なくとも部分的に、実質的に非晶質の生分解性ポリマーから成る、ことを含み、
該管状本体は、該ポリマーの結晶化度を増加させるように改質を受ける、方法。
(項目2)
上記管状本体は、半径方向の収縮または拡張が可能な構造へのパターン形成を受ける、項目1に記載の方法。
(項目3)
上記改質は、上記ポリマーのガラス転移温度より高く、かつ該ポリマーの融点より低い温度まで、上記管状本体を加熱することを含む、項目1に記載の方法。
(項目4)
上記改質は、加熱、冷却、加圧、架橋結合、および添加物の添加のうちの少なくとも1つを含む、項目1に記載の方法。
(項目5)
生分解性プロテーゼを製造する方法であって、
初期の直径を有する管状本体を提供することであって、該管状本体は、少なくとも部分的に、実質的に非晶質の生分解性ポリマーから成るとともに、該直径は、実質的に不変のままである、ことと、
該ポリマーのガラス転移温度より高く、かつ該ポリマーの融点より低い温度まで該管状本体を加熱することと、
該ポリマーの結晶化度を増加させるために、該管状本体を冷却することと、
該管状本体を、半径方向の収縮および拡張が可能である構造にパターン形成することと
を含む、方法。
(項目6)
上記実質的に非晶質のポリマーは、加熱および冷却の前に、10重量%以下の結晶化度を有する、項目5に記載の方法。
(項目7)
上記ポリマーは、加熱および冷却後に、元の結晶化度の少なくとも20%だけ増加した結晶化度を有する、項目6に記載の方法。
(項目8)
上記ポリマーは、加熱および冷却後に、元の結晶化度の少なくとも100%だけ増加した結晶化度を有する、項目6に記載の方法。
(項目9)
上記管状本体を提供することは、押出、鋳造、および浸漬から成る群より選択される工程によって、該管状本体を形成することを含む、項目5に記載の方法。
(項目10)
上記管状本体を提供することは、溶媒中に溶解された上記ポリマーを円筒形構造上に吹き付けることを含む、項目5に記載の方法。
(項目11)
添加物は、上記溶媒中に溶解される、項目10に記載の方法。
(項目12)
上記管状本体は、2mmから10mmまでの範囲の外径、0.01mmから0.5mmまでの範囲の長さ、および5mmから40mmまでの範囲の肉厚を有する、項目5に記載の方法。
(項目13)
上記ポリマーは、ポリ−DL−ラクチド、ポリラクチド−コ−グリコラクチド;ポリラクチド−コ−ポリカプロラクトン、ポリ(L−ラクチド−コ−炭酸トリメチレン)、ポリ炭酸トリメチレンおよび共重合体;ポリヒドロキシ酪酸および共重合体;ポリヒドロキシ吉草酸および共重合体、ポリオルトエステルおよび共重合体、ポリ無水物および共重合体、ポリイミノカーボネートおよび共重合体、から成る群より選択される、項目5に記載の方法。
(項目14)
上記ポリマーは、L−ラクチドとグリコリドとの共重合体を備える、項目5に記載の方法。
(項目15)
上記共重合体は、85重量%のL−ラクチドと15重量%のグリコリドとである、項目14に記載の方法。
(項目16)
上記管状本体は、1分間から3時間までの範囲の期間の間、上記ガラス転移温度より少なくとも10℃高く、かつ上記融解温度より少なくとも5℃低い温度まで加熱される、項目5に記載の方法。
(項目17)
上記管状本体は、周囲温度またはそれより低い温度で冷却される、項目16に記載の方法。
(項目18)
上記管状本体は、加熱または冷却後にパターン形成される、項目5に記載の方法。
(項目19)
上記管状本体は、加熱または冷却前にパターン形成される、項目5に記載の方法。
(項目20)
パターン形成することは、レーザ切断を含む、項目5に記載の方法。
(項目21)
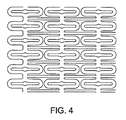
上記切断された管状構造は、複数の軸方向に連結された蛇行リングを備える、項目20に記載の方法。
(項目22)
上記管状本体は、パターン形成後に、少なくとも1つの追加サイクルを介して加熱および冷却される、項目5に記載の方法。
(項目23)
物質を上記管状本体に組み込むことをさらに含む、項目5に記載の方法。
(項目24)
上記物質は、血管の再狭窄を抑制するように選択される薬剤を備える、項目23に記載の方法。
(項目25)
上記物質は、上記プロテーゼの強度を強化するように選択される添加物である、項目23に記載の方法。
(項目26)
上記添加物は、ナノクレイ、ナノチューブ、ナノ粒子、剥離物、繊維、ウィスカ、小板状体、ナノ粉末、フラーレン、ナノスフィア、およびゼオライトから成る群より選択される、項目25に記載の方法。
(項目27)
上記添加物は、モンモリロナイト、スメクタイト、タルク、小板状体、および改質粘土から成る群より選択される、項目25に記載の方法。
(項目28)
上記添加物は、Cloisite NA、93A、30B、25A、15A、および10Aから成る群より選択される、粘土である、項目25に記載の方法。
(項目29)
上記添加物は、リネン、綿、レーヨン、アセテート;羊毛、絹;植物繊維;ガラス繊維;炭素繊維;金属繊維;セラミック繊維;および吸収性繊維から成る群より選択される、繊維である、項目25に記載の方法。
(項目30)
上記添加物は、ヒドロキシアパタイトウィスカ、リン酸三カルシウムウィスカから成る群より選択される、ウィスカである、項目25に記載の方法。
(項目31)
上記添加物は、化工澱粉、大豆、ヒアルロン酸、ヒドロキシアパタイト、およびリン酸トリカーボネートから成る群より選択される、項目25に記載の方法。
(項目32)
上記添加物は、ドデシル硫酸ナトリウム、および塩化トリエチレンベンジルアンモニウムから成る群より選択される、陰イオン性または陽イオン性の界面活性剤である、項目25に記載の方法。
(項目33)
上記添加物は、催分解剤、光分解性添加物、および酸化性添加物から成る群より選択される、項目25に記載の方法。
(項目34)
上記添加物は、電気活性ポリマー、電解質ポリマー、含水ポリマー、および乾燥剤から成る群より選択される、項目25に記載の方法。
(項目35)
上記添加物は、酸、過塩素酸塩、硝酸塩、過マンガン酸塩、およびそれらの塩から成る群より選択される、酸化剤である、項目25に記載の方法。
(項目36)
上記添加物は、蜜蝋および低分子量ポリエチレンから成る群より選択される、撥水ポリマーである、項目25に記載の方法。
(項目37)
上記添加物は、ポリビニルアルコール、ポリエチレンオキシド、グリセロール、カフェイン、およびリドカインから成る群より選択される、水誘引剤である、項目25に記載の方法。
(項目38)
少なくとも部分的に、実質的に非晶質の生分解性ポリマーから成る管状本体を備え、該生分解性ポリマーは、実質的に非晶質であるが、元の結晶化度の少なくとも20%だけ結晶化度を増加させるように改質を受けている、生分解性プロテーゼ。
(項目39)
10%から40%までの範囲の結晶化度を有する、項目38に記載の生分解性プロテーゼ。
(項目40)
上記ポリマーは、ポリ−DL−ラクチド、ポリラクチド−コ−グリコラクチド;ポリラクチド−コ−ポリカプロラクトン、ポリ(L−ラクチド−コ−炭酸トリメチレン)、炭酸ポリトリメチレンおよび共重合体;ポリヒドロキシ酪酸および共重合体;ポリヒドロキシ吉草酸および共重合体、ポリオルトエステルおよび共重合体、ポリ無水物および共重合体、ポリイミノカーボネートおよび共重合体から成る群より選択される、項目38に記載の生分解性プロテーゼ。
(項目41)
上記ポリマーは、L−ラクチドとグリコリドとの共重合体を備える、項目40に記載の生分解性プロテーゼ。
(項目42)
上記共重合体は、85重量%のL−ラクチドと15%重量のグリコリドとを備える、項目41に記載の生分解性プロテーゼ。
(項目43)
上記改質は、加熱および冷却の少なくとも1つのサイクルを含む、項目38に記載の生分解性プロテーゼ。
(項目44)
上記改質は、少なくとも、加熱および冷却の複数のサイクルを含む、項目42に記載の生分解性プロテーゼ。
Claims (25)
- 生分解性の移植可能な医療用プロテーゼを製造する方法であって、
該方法は、
初期の直径を有する管状本体を提供することであって、該管状本体は、少なくとも部分的に非晶質生分解性ポリマーから構成される、こと
を含み、
該管状本体は、押出、鋳造、浸漬または吹付によって形成され、
該管状本体は、該ポリマーが、10重量%から30重量%までの範囲の結晶化度を有するように、改質を受け、該改質は、加熱、冷却、加圧、架橋結合、および添加物の添加のうちの少なくとも1つを含む、方法。 - 前記管状本体は、改質の前または後に、半径方向の収縮または拡張が可能な構造へのパターン形成を受ける、請求項1に記載の方法。
- 前記改質は、前記ポリマーのガラス転移温度より高く、かつ該ポリマーの融点より低い温度まで、前記管状本体を加熱することを含む、請求項1に記載の方法。
- 前記生分解性プロテーゼは、クリンプされた直径から拡張可能なバルーンである、請求項1に記載の方法。
- 前記生分解性プロテーゼは、ステントである、請求項1に記載の方法。
- 前記管状本体は、前記生分解性プロテーゼの意図される配備直径の約1倍から1.3倍までにおけるパターン形成を受ける、請求項1に記載の方法。
- パターン形成における前記管状本体の直径は、前記初期の直径と同じである、請求項6に記載の方法。
- 前記生分解性プロテーゼは、Tg未満の温度において拡張状態まで拡張可能であり、かつ血管を支持するために十分な強度を有する、請求項1に記載の方法。
- 前記強度は、少なくとも3psiである、請求項8に記載の方法。
- 前記生分解性プロテーゼは、Tg未満の温度において拡張状態まで拡張可能であり、かつクリンプ状態から拡張状態までの拡張の後に、10%未満のリコイルを有する、請求項1に記載の方法。
- 前記生分解性プロテーゼは、0.01重量%から25重量%までの量の添加物をさらに含む、請求項1に記載の方法。
- 前記添加物は、モノマーである、請求項11に記載の方法。
- 前記モノマーは、前記生分解性ポリマーのモノマーである、請求項12に記載の方法。
- 前記生分解性ポリマーは、少なくとも0.5GPaの弾性係数を有する、請求項1に記載の方法。
- 前記ポリマーは、改質の後に、元の結晶化度の少なくとも20%だけ増加した結晶化度を有する、請求項1に記載の方法。
- 前記吹付は、溶媒中に溶解された前記ポリマーを円筒形構造上に吹き付けることを含む、請求項1に記載の方法。
- 前記ポリマーは、ポリ−DL−ラクチド、ポリラクチド−コ−グリコラクチド;ポリラクチド−コ−ポリカプロラクトン、ポリ(L−ラクチド−コ−炭酸トリメチレン)、ポリ炭酸トリメチレンおよび共重合体;ポリヒドロキシ酪酸および共重合体;ポリヒドロキシ吉草酸および共重合体、ポリオルトエステルおよび共重合体、ポリ無水物および共重合体、ポリイミノカーボネートおよび共重合体、ポリ乳酸および共重合体から成る群より選択される、請求項1に記載の方法。
- 前記管状本体は、1分間から3時間までの範囲の期間の間、ガラス転移温度より少なくとも10℃高く、かつ融解温度より少なくとも5℃低い温度まで加熱される、請求項1に記載の方法。
- 前記管状本体は、レーザ切断によってパターン形成される、請求項1に記載の方法。
- 切断された管状構造は、複数の軸方向に連結された蛇行リングを備える、請求項19に記載の方法。
- 前記管状本体は、少なくとも2つの改質サイクルを受ける、請求項1に記載の方法。
- 前記生分解性プロテーゼは、物質をさらに含む、請求項1に記載の方法。
- 前記物質は、血管の再狭窄を抑制するように選択される薬剤を備える、請求項22に記載の方法。
- 前記物質は、前記プロテーゼの強度を強化するように選択される添加物である、請求項22に記載の方法。
- 前記ポリマーは、L−ラクチドとグリコリドとの共重合体を備える、請求項1に記載の方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US88570007P | 2007-01-19 | 2007-01-19 | |
| US60/885,700 | 2007-01-19 | ||
| PCT/US2008/051479 WO2008089434A2 (en) | 2007-01-19 | 2008-01-18 | Biodegradable endoprostheses and methods for their fabrication |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013135191A Division JP5749296B2 (ja) | 2007-01-19 | 2013-06-27 | 生分解性エンドプロテーゼおよび製造方法 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2010516347A JP2010516347A (ja) | 2010-05-20 |
| JP2010516347A5 JP2010516347A5 (ja) | 2012-10-04 |
| JP5489725B2 true JP5489725B2 (ja) | 2014-05-14 |
Family
ID=39636746
Family Applications (8)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2009546552A Expired - Fee Related JP5355420B2 (ja) | 2007-01-19 | 2008-01-18 | 支持特徴を有するエンドプロテーゼ構造体 |
| JP2009546550A Expired - Fee Related JP5489725B2 (ja) | 2007-01-19 | 2008-01-18 | 生分解性エンドプロテーゼおよび製造方法 |
| JP2013135191A Expired - Fee Related JP5749296B2 (ja) | 2007-01-19 | 2013-06-27 | 生分解性エンドプロテーゼおよび製造方法 |
| JP2013181436A Expired - Fee Related JP5762486B2 (ja) | 2007-01-19 | 2013-09-02 | 支持特徴を有するエンドプロテーゼ構造体 |
| JP2014141094A Withdrawn JP2014195734A (ja) | 2007-01-19 | 2014-07-09 | 生分解性エンドプロテーゼおよび製造方法 |
| JP2014236223A Pending JP2015071056A (ja) | 2007-01-19 | 2014-11-21 | 支持特徴を有するエンドプロテーゼ構造体 |
| JP2016182603A Withdrawn JP2016221352A (ja) | 2007-01-19 | 2016-09-20 | 生分解性エンドプロテーゼおよび製造方法 |
| JP2016197807A Pending JP2017035511A (ja) | 2007-01-19 | 2016-10-06 | 支持特徴を有するエンドプロテーゼ構造体 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2009546552A Expired - Fee Related JP5355420B2 (ja) | 2007-01-19 | 2008-01-18 | 支持特徴を有するエンドプロテーゼ構造体 |
Family Applications After (6)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013135191A Expired - Fee Related JP5749296B2 (ja) | 2007-01-19 | 2013-06-27 | 生分解性エンドプロテーゼおよび製造方法 |
| JP2013181436A Expired - Fee Related JP5762486B2 (ja) | 2007-01-19 | 2013-09-02 | 支持特徴を有するエンドプロテーゼ構造体 |
| JP2014141094A Withdrawn JP2014195734A (ja) | 2007-01-19 | 2014-07-09 | 生分解性エンドプロテーゼおよび製造方法 |
| JP2014236223A Pending JP2015071056A (ja) | 2007-01-19 | 2014-11-21 | 支持特徴を有するエンドプロテーゼ構造体 |
| JP2016182603A Withdrawn JP2016221352A (ja) | 2007-01-19 | 2016-09-20 | 生分解性エンドプロテーゼおよび製造方法 |
| JP2016197807A Pending JP2017035511A (ja) | 2007-01-19 | 2016-10-06 | 支持特徴を有するエンドプロテーゼ構造体 |
Country Status (7)
| Country | Link |
|---|---|
| US (6) | US8182890B2 (ja) |
| EP (3) | EP2783710B1 (ja) |
| JP (8) | JP5355420B2 (ja) |
| CN (7) | CN105534627A (ja) |
| BR (2) | BRPI0806623A2 (ja) |
| ES (1) | ES2605731T3 (ja) |
| WO (2) | WO2008089446A2 (ja) |
Families Citing this family (99)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8741378B1 (en) | 2001-06-27 | 2014-06-03 | Advanced Cardiovascular Systems, Inc. | Methods of coating an implantable device |
| US9517149B2 (en) | 2004-07-26 | 2016-12-13 | Abbott Cardiovascular Systems Inc. | Biodegradable stent with enhanced fracture toughness |
| US8747879B2 (en) | 2006-04-28 | 2014-06-10 | Advanced Cardiovascular Systems, Inc. | Method of fabricating an implantable medical device to reduce chance of late inflammatory response |
| US7971333B2 (en) | 2006-05-30 | 2011-07-05 | Advanced Cardiovascular Systems, Inc. | Manufacturing process for polymetric stents |
| US7731890B2 (en) | 2006-06-15 | 2010-06-08 | Advanced Cardiovascular Systems, Inc. | Methods of fabricating stents with enhanced fracture toughness |
| US8597716B2 (en) | 2009-06-23 | 2013-12-03 | Abbott Cardiovascular Systems Inc. | Methods to increase fracture resistance of a drug-eluting medical device |
| US20150174864A1 (en) * | 2011-10-14 | 2015-06-25 | Midsun Group Inc. | Self-fusing carbon fiber silicone perforated tape |
| EP1834606B1 (en) * | 2006-03-16 | 2013-04-24 | CID S.p.A. | Stents |
| EP3009477B1 (en) | 2006-07-20 | 2024-01-24 | Orbusneich Medical Pte. Ltd | Bioabsorbable polymeric composition for a medical device |
| US8460362B2 (en) | 2006-07-20 | 2013-06-11 | Orbusneich Medical, Inc. | Bioabsorbable polymeric medical device |
| US7959942B2 (en) | 2006-10-20 | 2011-06-14 | Orbusneich Medical, Inc. | Bioabsorbable medical device with coating |
| US8814930B2 (en) | 2007-01-19 | 2014-08-26 | Elixir Medical Corporation | Biodegradable endoprosthesis and methods for their fabrication |
| US8182890B2 (en) | 2007-01-19 | 2012-05-22 | Elixir Medical Corporation | Biodegradable endoprostheses and methods for their fabrication |
| US20130150943A1 (en) | 2007-01-19 | 2013-06-13 | Elixir Medical Corporation | Biodegradable endoprostheses and methods for their fabrication |
| US8002817B2 (en) * | 2007-05-04 | 2011-08-23 | Abbott Cardiovascular Systems Inc. | Stents with high radial strength and methods of manufacturing same |
| WO2009018475A1 (en) * | 2007-08-01 | 2009-02-05 | Prescient Medical, Inc. | Expandable prostheses for treating atherosclerotic lesions including vulnerable plaques |
| US8252215B2 (en) * | 2008-03-31 | 2012-08-28 | Abbott Cardiovascular Systems Inc. | Method for fabricating a stent with nucleating agent |
| US20090269480A1 (en) * | 2008-04-24 | 2009-10-29 | Medtronic Vascular, Inc. | Supercritical Fluid Loading of Porous Medical Devices With Bioactive Agents |
| US8206635B2 (en) | 2008-06-20 | 2012-06-26 | Amaranth Medical Pte. | Stent fabrication via tubular casting processes |
| US10898620B2 (en) | 2008-06-20 | 2021-01-26 | Razmodics Llc | Composite stent having multi-axial flexibility and method of manufacture thereof |
| US8206636B2 (en) | 2008-06-20 | 2012-06-26 | Amaranth Medical Pte. | Stent fabrication via tubular casting processes |
| US8394317B2 (en) * | 2008-08-11 | 2013-03-12 | Abbott Cardiovascular Systems Inc. | Method of improving fracture toughness of implantable medical devices through annealing |
| US8372332B2 (en) | 2008-08-11 | 2013-02-12 | Abbott Cardiovascular Systems Inc. | Fabricating an implantable medical device from an amorphous or very low crystallinity polymer construct |
| US8765040B2 (en) | 2008-08-11 | 2014-07-01 | Abbott Cardiovascular Systems Inc. | Medical device fabrication process including strain induced crystallization with enhanced crystallization |
| US8337739B2 (en) * | 2008-08-12 | 2012-12-25 | Abbott Cardiovascular Systems Inc. | Improving fracture toughness of medical devices with a stereocomplex nucleating agent |
| US9572692B2 (en) * | 2009-02-02 | 2017-02-21 | Abbott Cardiovascular Systems Inc. | Bioabsorbable stent that modulates plaque geometric morphology and chemical composition |
| US8968818B2 (en) * | 2009-02-21 | 2015-03-03 | Covidien Lp | Medical devices having activated surfaces |
| US8147744B2 (en) | 2009-04-10 | 2012-04-03 | Abbott Cardiovascular Systems Inc. | Method of making a stent formed from crosslinked bioabsorbable polymer |
| WO2010132899A1 (en) * | 2009-05-15 | 2010-11-18 | Orbusneich Medical, Inc. | Bioabsorbable polymeric compositions and medical devices |
| US9265633B2 (en) * | 2009-05-20 | 2016-02-23 | 480 Biomedical, Inc. | Drug-eluting medical implants |
| US9889238B2 (en) * | 2009-07-21 | 2018-02-13 | Abbott Cardiovascular Systems Inc. | Biodegradable stent with adjustable degradation rate |
| US8119704B2 (en) * | 2009-07-21 | 2012-02-21 | Abbott Cardiovascular Systems Inc. | Implantable medical device comprising copolymer of L-lactide with improved fracture toughness |
| US8889823B2 (en) | 2009-07-21 | 2014-11-18 | Abbott Cardiovascular Systems Inc. | Method to make poly(L-lactide) stent with tunable degradation rate |
| US8207240B2 (en) * | 2009-09-14 | 2012-06-26 | Abbott Cardiovascular Systems Inc | Method to minimize molecular weight drop of poly(L-lactide) stent during processing |
| US8852268B2 (en) * | 2009-09-16 | 2014-10-07 | Bentley Surgical Gmbh | Stent having expandable elements |
| US8729171B2 (en) | 2010-01-22 | 2014-05-20 | Wayne State University | Supercritical carbon-dioxide processed biodegradable polymer nanocomposites |
| US8568471B2 (en) | 2010-01-30 | 2013-10-29 | Abbott Cardiovascular Systems Inc. | Crush recoverable polymer scaffolds |
| US8808353B2 (en) * | 2010-01-30 | 2014-08-19 | Abbott Cardiovascular Systems Inc. | Crush recoverable polymer scaffolds having a low crossing profile |
| TWI407942B (zh) * | 2010-02-09 | 2013-09-11 | Univ Nat Taiwan | 具預防血管狹窄之心血管支架 |
| WO2011100263A1 (en) * | 2010-02-10 | 2011-08-18 | Exploramed Iii, Inc. | Methods, systems and devices for treatment of cerebrospinal venous insufficiency and multiple sclerosis |
| US8685433B2 (en) | 2010-03-31 | 2014-04-01 | Abbott Cardiovascular Systems Inc. | Absorbable coating for implantable device |
| US8613880B2 (en) * | 2010-04-21 | 2013-12-24 | Abbott Cardiovascular Systems Inc. | Post electron beam conditioning of polymeric medical devices |
| WO2012015825A2 (en) | 2010-07-27 | 2012-02-02 | Incept, Llc | Methods and apparatus for treating neurovascular venous outflow obstruction |
| EP2415489B1 (de) | 2010-08-03 | 2016-07-06 | Biotronik AG | Polylactid-beschichtetes Implantat aus einer biokorrodierbaren Magnesiumlegierung |
| US8539663B2 (en) | 2010-08-23 | 2013-09-24 | Abbott Cardiovascular Systems Inc. | Reducing crimping damage to polymer scaffold |
| US20120059451A1 (en) | 2010-09-08 | 2012-03-08 | Qiang Zhang | Method of Manufacturing a Polymeric Stent Having Reduced Recoil |
| US8920867B2 (en) * | 2010-10-19 | 2014-12-30 | Covidien Lp | Methods of forming self-supporting films for delivery of therapeutic agents |
| US20120158123A1 (en) * | 2010-12-15 | 2012-06-21 | Biotronik Ag | Polymer stent |
| CA2988760A1 (en) | 2011-01-12 | 2012-07-19 | The Board Of Trustees Of The Leland Stanford Junior University | Composite laminated structures and methods for manufacturing and using the same |
| US8545546B2 (en) * | 2011-05-13 | 2013-10-01 | Abbott Cardiovascular Systems Inc. | Bioabsorbable scaffolds made from composites |
| US8487017B2 (en) | 2011-06-27 | 2013-07-16 | Covidien Lp | Biodegradable materials for orthopedic devices based on polymer stereocomplexes |
| JP6505438B2 (ja) * | 2011-06-30 | 2019-04-24 | エリクシアー メディカル コーポレイション | 生分解性内部人工器官およびその作製方法 |
| US8726483B2 (en) | 2011-07-29 | 2014-05-20 | Abbott Cardiovascular Systems Inc. | Methods for uniform crimping and deployment of a polymer scaffold |
| US9839537B2 (en) | 2012-03-07 | 2017-12-12 | Abbott Cardiovascular Systems Inc. | Bioresorbable polymer scaffold treatment of coronary and peripheral artery disease in diabetic patients |
| WO2013136965A1 (ja) * | 2012-03-15 | 2013-09-19 | テルモ株式会社 | 生体内留置用ステントおよびステントデリバリーシステム |
| KR101231197B1 (ko) * | 2012-09-20 | 2013-02-07 | 썬텍 주식회사 | 고분자 스텐트 |
| GB2512016A (en) | 2012-09-24 | 2014-09-24 | Arterius Ltd | Methods |
| US9724219B2 (en) | 2012-10-04 | 2017-08-08 | Abbott Cardiovascular Systems Inc. | Method of uniform crimping and expansion of medical devices |
| US10143574B2 (en) * | 2013-03-14 | 2018-12-04 | Vactronix Scientific, Llc | Monolithic medical devices, methods of making and using the same |
| TWI510225B (zh) * | 2013-06-25 | 2015-12-01 | Univ Nat Cheng Kung | Stent |
| US9364350B2 (en) | 2013-07-09 | 2016-06-14 | Abbott Cardiovascular Systems Inc. | Stent with eased corner feature |
| HK1216509A1 (zh) | 2014-02-04 | 2016-11-18 | Abbott Cardiovascular Systems, Inc. | 具有基於novolimus和丙交酯的塗層使得novolimus與塗層具有最小鍵合量的藥物遞送支架或支撐件 |
| CN103948459B (zh) * | 2014-05-27 | 2016-05-25 | 辽宁生物医学材料研发中心有限公司 | 一种低回弹高支撑冠状动脉可降解支架 |
| US9259339B1 (en) | 2014-08-15 | 2016-02-16 | Elixir Medical Corporation | Biodegradable endoprostheses and methods of their fabrication |
| US9730819B2 (en) | 2014-08-15 | 2017-08-15 | Elixir Medical Corporation | Biodegradable endoprostheses and methods of their fabrication |
| US9855156B2 (en) * | 2014-08-15 | 2018-01-02 | Elixir Medical Corporation | Biodegradable endoprostheses and methods of their fabrication |
| US9480588B2 (en) | 2014-08-15 | 2016-11-01 | Elixir Medical Corporation | Biodegradable endoprostheses and methods of their fabrication |
| US9381103B2 (en) * | 2014-10-06 | 2016-07-05 | Abbott Cardiovascular Systems Inc. | Stent with elongating struts |
| JP2016077354A (ja) | 2014-10-10 | 2016-05-16 | 住友ゴム工業株式会社 | プレフィルドシリンジ用ガスケット |
| US10617847B2 (en) | 2014-11-04 | 2020-04-14 | Orbusneich Medical Pte. Ltd. | Variable flexibility catheter support frame |
| EP4008389B1 (en) | 2014-11-04 | 2025-07-02 | OrbusNeich Medical Pte. Ltd. | Progressive flexibility catheter support frame |
| US9931231B2 (en) | 2014-12-29 | 2018-04-03 | Cook Medical Technologies Llc | Support structures for prostheses with branching portions |
| WO2017200956A1 (en) | 2016-05-16 | 2017-11-23 | Elixir Medical Corporation | Uncaging stent |
| CN105641751B (zh) * | 2016-03-09 | 2018-11-30 | 山东中恒碳纤维科技发展有限公司 | 一种三维编织复合材料假肢及其制备方法 |
| WO2019033121A1 (en) | 2017-08-11 | 2019-02-14 | Elixir Medical Corporation | Uncaging stent |
| US11622872B2 (en) * | 2016-05-16 | 2023-04-11 | Elixir Medical Corporation | Uncaging stent |
| WO2017223526A1 (en) * | 2016-06-23 | 2017-12-28 | Poly-Med, Inc. | Medical implants having managed biodegradation |
| US20190175326A1 (en) * | 2016-08-25 | 2019-06-13 | Mico Innovations, Llc | Neurovascular Stent |
| US10660773B2 (en) | 2017-02-14 | 2020-05-26 | Abbott Cardiovascular Systems Inc. | Crimping methods for thin-walled scaffolds |
| JP6953034B2 (ja) * | 2017-03-08 | 2021-10-27 | 国立大学法人山口大学 | 双安定構造を持つ管腔臓器への留置器具 |
| RU2668130C2 (ru) * | 2017-03-09 | 2018-09-26 | Акционерное общество "Военно-промышленная корпорация "Научно-производственное объединение машиностроения" | Чашка эндопротеза тазобедренного сустава |
| RU2668132C9 (ru) * | 2017-03-09 | 2018-11-19 | Акционерное общество "Военно-промышленная корпорация "Научно-производственное объединение машиностроения" | Головка эндопротеза тазобедренного сустава |
| RU2669352C9 (ru) * | 2017-03-09 | 2018-11-21 | Акционерное общество "Военно-промышленная корпорация "Научно-производственное объединение машиностроения" | Имплантат для замещения костных дефектов |
| RU2668131C9 (ru) * | 2017-03-09 | 2018-11-21 | Акционерное общество "Военно-промышленная корпорация "Научно-производственное объединение машиностроения" | Ножка эндопротеза тазобедренного сустава |
| EP3605206A4 (en) * | 2017-04-17 | 2020-03-04 | Guangdong Oppo Mobile Telecommunications Corp., Ltd. | DISPLAY DEVICE, ELECTRONIC EQUIPMENT, AND METHOD FOR MANUFACTURING DISPLAY DEVICE |
| CN107137168B (zh) * | 2017-06-21 | 2019-07-05 | 青岛容商天下网络有限公司 | 可降解可收回4d打印线型有机人体支架及其使用方法 |
| US10555825B2 (en) | 2017-11-09 | 2020-02-11 | Abbott Cardiovascular Systems Inc. | Rotation of a medical device during crimping |
| CN117481869A (zh) | 2018-01-25 | 2024-02-02 | 爱德华兹生命科学公司 | 在部署后用于辅助置换瓣膜重新捕获和重新定位的递送系统 |
| US10500078B2 (en) * | 2018-03-09 | 2019-12-10 | Vesper Medical, Inc. | Implantable stent |
| KR102328579B1 (ko) * | 2018-06-11 | 2021-11-18 | 주식회사 삼양홀딩스 | 열 안정성이 향상된 체내 삽입용 생분해성 의료용 장치 및 그 제조 방법 |
| US10967556B2 (en) | 2018-06-11 | 2021-04-06 | Abbott Cardiovascular Systems Inc. | Uniform expansion of thin-walled scaffolds |
| AU2019383400B2 (en) | 2018-11-21 | 2025-08-14 | Hollister Incorporated | Hydration solutions containing volatile solutes and medical device products including the same |
| US10702407B1 (en) | 2019-02-28 | 2020-07-07 | Renata Medical, Inc. | Growth stent for congenital narrowings |
| WO2020185851A1 (en) * | 2019-03-11 | 2020-09-17 | The Board Of Supervisors Of Louisiana State University And Agricultural And Mechanical College | Anastomosing stent and methods of use |
| MY198964A (en) * | 2019-04-29 | 2023-10-05 | Medical And Pharmaceutical Industry Tech And Development Center | Medical implant |
| RU2707551C1 (ru) * | 2019-08-02 | 2019-11-28 | Федеральное государственное бюджетное учреждение науки Институт органического синтеза им. И.Я. Постовского Уральского отделения Российской академии наук | Способ изготовления биоразлагаемого лакопротеза |
| EP4498944A4 (en) | 2022-03-28 | 2026-03-11 | Elixir Medical Corp | EXTENDABLE DISTAL TIP SUCTION CATHETERS |
| JP2026500175A (ja) | 2022-12-09 | 2026-01-06 | レナータ メディカル インコーポレイテッド | 経カテーテル成長デバイス、並びにノーウッド、グレン、及びフォンタン治療のための方法 |
| CN117618160B (zh) * | 2024-01-11 | 2024-04-09 | 北京迈迪顶峰医疗科技股份有限公司 | 瓣膜支架、瓣膜支架的加工方法和人工瓣膜 |
Family Cites Families (113)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3867190A (en) * | 1971-10-18 | 1975-02-18 | American Cyanamid Co | Reducing capillarity of polyglycolic acid sutures |
| AU7998091A (en) * | 1990-05-17 | 1991-12-10 | Harbor Medical Devices, Inc. | Medical device polymer |
| NL9001984A (nl) | 1990-09-10 | 1992-04-01 | Stamicarbon | Werkwijze voor het produceren van een voorwerp van een copolymeer van lactide en epsilon-caprolacton voor medische toepassingen. |
| CA2060635A1 (en) * | 1991-02-12 | 1992-08-13 | Keith D'alessio | Bioabsorbable medical implants |
| US5441483A (en) * | 1992-11-16 | 1995-08-15 | Avitall; Boaz | Catheter deflection control |
| US5741329A (en) * | 1994-12-21 | 1998-04-21 | Board Of Regents, The University Of Texas System | Method of controlling the pH in the vicinity of biodegradable implants |
| FI98136C (fi) * | 1995-09-27 | 1997-04-25 | Biocon Oy | Kudosolosuhteissa hajoava materiaali ja menetelmä sen valmistamiseksi |
| US6241760B1 (en) * | 1996-04-26 | 2001-06-05 | G. David Jang | Intravascular stent |
| US5670161A (en) * | 1996-05-28 | 1997-09-23 | Healy; Kevin E. | Biodegradable stent |
| US5922020A (en) * | 1996-08-02 | 1999-07-13 | Localmed, Inc. | Tubular prosthesis having improved expansion and imaging characteristics |
| US20030093143A1 (en) * | 1999-03-01 | 2003-05-15 | Yiju Zhao | Medical device having surface depressions containing nitric oxide releasing compound |
| US5911732A (en) * | 1997-03-10 | 1999-06-15 | Johnson & Johnson Interventional Systems, Co. | Articulated expandable intraluminal stent |
| US6033433A (en) * | 1997-04-25 | 2000-03-07 | Scimed Life Systems, Inc. | Stent configurations including spirals |
| DE29825178U1 (de) * | 1997-04-25 | 2005-10-06 | Boston Scientific Ltd., St. Michael | Verbesserte Stentkonfigurationen |
| US6610764B1 (en) * | 1997-05-12 | 2003-08-26 | Metabolix, Inc. | Polyhydroxyalkanoate compositions having controlled degradation rates |
| DE19722384A1 (de) | 1997-05-28 | 1998-12-03 | Gfe Ges Fuer Forschung Und Ent | Flexible expandierbare Gefäßstütze |
| CA2241558A1 (en) * | 1997-06-24 | 1998-12-24 | Advanced Cardiovascular Systems, Inc. | Stent with reinforced struts and bimodal deployment |
| US5980564A (en) * | 1997-08-01 | 1999-11-09 | Schneider (Usa) Inc. | Bioabsorbable implantable endoprosthesis with reservoir |
| US6245103B1 (en) * | 1997-08-01 | 2001-06-12 | Schneider (Usa) Inc | Bioabsorbable self-expanding stent |
| US5964798A (en) * | 1997-12-16 | 1999-10-12 | Cardiovasc, Inc. | Stent having high radial strength |
| US6626939B1 (en) * | 1997-12-18 | 2003-09-30 | Boston Scientific Scimed, Inc. | Stent-graft with bioabsorbable structural support |
| US6293967B1 (en) * | 1998-10-29 | 2001-09-25 | Conor Medsystems, Inc. | Expandable medical device with ductile hinges |
| EP1020166A1 (en) * | 1999-01-12 | 2000-07-19 | Orbus Medical Technologies, Inc. | Expandable intraluminal endoprosthesis |
| US6248363B1 (en) * | 1999-11-23 | 2001-06-19 | Lipocine, Inc. | Solid carriers for improved delivery of active ingredients in pharmaceutical compositions |
| US6224803B1 (en) * | 1999-04-28 | 2001-05-01 | Advanced Cardiovascular Systems, Inc. | Method of forming a thin walled member by extrusion and medical device produced thereby |
| US6540774B1 (en) * | 1999-08-31 | 2003-04-01 | Advanced Cardiovascular Systems, Inc. | Stent design with end rings having enhanced strength and radiopacity |
| DE60121141T2 (de) * | 2000-03-09 | 2007-05-31 | Design & Performance - Cyprus Ltd. | Stent mit hüllenbefestigungen |
| ATE516826T1 (de) | 2000-03-13 | 2011-08-15 | Kyoto Iryo Sekkei Kk | Drahtstangen für gefässprothesen und gefässprothesen unter anwendung derselben |
| DE10012460A1 (de) * | 2000-03-15 | 2001-09-20 | Biotronik Mess & Therapieg | Stent |
| US6527801B1 (en) * | 2000-04-13 | 2003-03-04 | Advanced Cardiovascular Systems, Inc. | Biodegradable drug delivery material for stent |
| US6602282B1 (en) * | 2000-05-04 | 2003-08-05 | Avantec Vascular Corporation | Flexible stent structure |
| WO2001095834A1 (en) * | 2000-06-13 | 2001-12-20 | Scimed Life Systems, Inc. | Disintegrating stent and method of making same |
| US20020161168A1 (en) * | 2000-10-27 | 2002-10-31 | Shalaby Shalaby W. | Amorphous polymeric polyaxial initiators and compliant crystalline copolymers therefrom |
| US20030033007A1 (en) * | 2000-12-22 | 2003-02-13 | Avantec Vascular Corporation | Methods and devices for delivery of therapeutic capable agents with variable release profile |
| US6607548B2 (en) | 2001-05-17 | 2003-08-19 | Inion Ltd. | Resorbable polymer compositions |
| US6585755B2 (en) * | 2001-06-29 | 2003-07-01 | Advanced Cardiovascular | Polymeric stent suitable for imaging by MRI and fluoroscopy |
| CN2517403Y (zh) * | 2001-07-27 | 2002-10-23 | 微创医疗器械(上海)有限公司 | 非均一波形结构的冠状动脉支架 |
| CN1131074C (zh) | 2001-08-10 | 2003-12-17 | 中国人民解放军总医院 | 一种用于微创快速血管吻合技术的速溶支架的制备方法 |
| US6997944B2 (en) * | 2001-08-13 | 2006-02-14 | Advanced Cardiovascular Systems, Inc. | Apparatus and method for decreasing stent gap size |
| BR0213279A (pt) * | 2001-10-15 | 2004-10-26 | Hemoteq Gmbh | Revestimento de stents para impedir a restenose |
| US7572287B2 (en) * | 2001-10-25 | 2009-08-11 | Boston Scientific Scimed, Inc. | Balloon expandable polymer stent with reduced elastic recoil |
| US20030088307A1 (en) * | 2001-11-05 | 2003-05-08 | Shulze John E. | Potent coatings for stents |
| US6866805B2 (en) * | 2001-12-27 | 2005-03-15 | Advanced Cardiovascular Systems, Inc. | Hybrid intravascular stent |
| US7029493B2 (en) * | 2002-01-25 | 2006-04-18 | Cordis Corporation | Stent with enhanced crossability |
| US7354450B2 (en) * | 2002-01-30 | 2008-04-08 | Boston Scientific Scimed, Inc. | Stent with wishbone connectors and serpentine bands |
| CN2532867Y (zh) * | 2002-03-22 | 2003-01-29 | 维科医疗器械(苏州)有限公司 | 零短缩结构冠状动脉扩张支架 |
| EP1501424B1 (en) | 2002-04-18 | 2018-06-06 | Helmholtz-Zentrum Geesthacht Zentrum für Material- und Küstenforschung GmbH | Biodegradable shape memory polymeric sutures |
| US7261734B2 (en) * | 2002-04-23 | 2007-08-28 | Boston Scientific Scimed, Inc. | Resorption-controllable medical implants |
| EP1549254A4 (en) * | 2002-09-27 | 2007-11-07 | Medlogics Device Corp | IMPLANTABLE STENT WITH MODIFIED ENDS |
| US7223283B2 (en) * | 2002-10-09 | 2007-05-29 | Boston Scientific Scimed, Inc. | Stent with improved flexibility |
| JP3988619B2 (ja) * | 2002-10-31 | 2007-10-10 | 東レ株式会社 | ポリ乳酸系樹脂組成物およびそれからなる成形品 |
| US20040098090A1 (en) * | 2002-11-14 | 2004-05-20 | Williams Michael S. | Polymeric endoprosthesis and method of manufacture |
| US20050187615A1 (en) * | 2004-02-23 | 2005-08-25 | Williams Michael S. | Polymeric endoprostheses with enhanced strength and flexibility and methods of manufacture |
| US20040111144A1 (en) * | 2002-12-06 | 2004-06-10 | Lawin Laurie R. | Barriers for polymeric coatings |
| US6863757B1 (en) * | 2002-12-19 | 2005-03-08 | Advanced Cardiovascular Systems, Inc. | Method of making an expandable medical device formed of a compacted porous polymeric material |
| US7316710B1 (en) * | 2002-12-30 | 2008-01-08 | Advanced Cardiovascular Systems, Inc. | Flexible stent |
| US6932930B2 (en) | 2003-03-10 | 2005-08-23 | Synecor, Llc | Intraluminal prostheses having polymeric material with selectively modified crystallinity and methods of making same |
| GB0310300D0 (en) * | 2003-05-06 | 2003-06-11 | Univ Belfast | Nanocomposite drug delivery composition |
| US7112216B2 (en) * | 2003-05-28 | 2006-09-26 | Boston Scientific Scimed, Inc. | Stent with tapered flexibility |
| US6979348B2 (en) * | 2003-06-04 | 2005-12-27 | Medtronic Vascular, Inc. | Reflowed drug-polymer coated stent and method thereof |
| BRPI0411431B8 (pt) * | 2003-06-13 | 2021-06-22 | Gkss Forschungszentrum Geesthacht Gmbh | stents biodegradáveis |
| CN1835723B (zh) * | 2003-06-16 | 2011-06-22 | 洛马林达大学医学中心 | 可展开的多功能止血剂 |
| JP2006527628A (ja) * | 2003-06-16 | 2006-12-07 | ナンヤン・テクノロジカル・ユニバーシティー | ポリマー材のステントおよび製造方法 |
| EP1958657A1 (en) * | 2003-07-18 | 2008-08-20 | Boston Scientific Limited | Medical devices |
| US8029755B2 (en) * | 2003-08-06 | 2011-10-04 | Angstrom Medica | Tricalcium phosphates, their composites, implants incorporating them, and method for their production |
| US7247166B2 (en) * | 2003-09-29 | 2007-07-24 | Advanced Cardiovascular Systems, Inc. | Intravascular stent with extendible end rings |
| US7377939B2 (en) * | 2003-11-19 | 2008-05-27 | Synecor, Llc | Highly convertible endolumenal prostheses and methods of manufacture |
| US8157855B2 (en) * | 2003-12-05 | 2012-04-17 | Boston Scientific Scimed, Inc. | Detachable segment stent |
| CN1242818C (zh) * | 2003-12-08 | 2006-02-22 | 华中科技大学 | 一种可降解的复合支架材料及其制备方法 |
| US7258697B1 (en) * | 2003-12-22 | 2007-08-21 | Advanced Cardiovascular Systems, Inc. | Stent with anchors to prevent vulnerable plaque rupture during deployment |
| DE10361940A1 (de) * | 2003-12-24 | 2005-07-28 | Restate Patent Ag | Degradationssteuerung biodegradierbarer Implantate durch Beschichtung |
| US7709570B2 (en) * | 2004-04-02 | 2010-05-04 | Alps South, LLC | Surface modification of triblock copolymer elastomers |
| AU2004318159B8 (en) * | 2004-04-02 | 2011-05-26 | Sahajanand Medical Technologies Private Limited | Polymer-based stent assembly |
| JP2005298617A (ja) * | 2004-04-09 | 2005-10-27 | Mitsubishi Plastics Ind Ltd | 射出成形体 |
| US8007737B2 (en) * | 2004-04-14 | 2011-08-30 | Wyeth | Use of antioxidants to prevent oxidation and reduce drug degradation in drug eluting medical devices |
| CN1569270B (zh) | 2004-04-29 | 2011-06-29 | 上海瑞邦生物材料有限公司 | 一种表面设有药物涂层的心血管支架的制备方法 |
| US20050261757A1 (en) * | 2004-05-21 | 2005-11-24 | Conor Medsystems, Inc. | Stent with contoured bridging element |
| US8747878B2 (en) | 2006-04-28 | 2014-06-10 | Advanced Cardiovascular Systems, Inc. | Method of fabricating an implantable medical device by controlling crystalline structure |
| US7971333B2 (en) * | 2006-05-30 | 2011-07-05 | Advanced Cardiovascular Systems, Inc. | Manufacturing process for polymetric stents |
| US7731890B2 (en) | 2006-06-15 | 2010-06-08 | Advanced Cardiovascular Systems, Inc. | Methods of fabricating stents with enhanced fracture toughness |
| US8268228B2 (en) * | 2007-12-11 | 2012-09-18 | Abbott Cardiovascular Systems Inc. | Method of fabricating stents from blow molded tubing |
| US8747879B2 (en) * | 2006-04-28 | 2014-06-10 | Advanced Cardiovascular Systems, Inc. | Method of fabricating an implantable medical device to reduce chance of late inflammatory response |
| US7875233B2 (en) * | 2004-09-30 | 2011-01-25 | Advanced Cardiovascular Systems, Inc. | Method of fabricating a biaxially oriented implantable medical device |
| CN2768714Y (zh) * | 2004-11-22 | 2006-04-05 | 微创医疗器械(上海)有限公司 | 一种柔软的血管支架 |
| JP4820551B2 (ja) * | 2005-01-14 | 2011-11-24 | テルモ株式会社 | 生体内留置物 |
| US7655254B2 (en) * | 2005-02-03 | 2010-02-02 | Intarcia Therapeutics, Inc. | Implantable device for continuous delivery of interferon |
| JP5247984B2 (ja) * | 2005-02-10 | 2013-07-24 | コーディス・コーポレイション | 機械的強度および薬理機能を強化した生分解性医療用具 |
| US20060193891A1 (en) * | 2005-02-25 | 2006-08-31 | Robert Richard | Medical devices and therapeutic delivery devices composed of bioabsorbable polymers produced at room temperature, method of making the devices, and a system for making the devices |
| US7291166B2 (en) * | 2005-05-18 | 2007-11-06 | Advanced Cardiovascular Systems, Inc. | Polymeric stent patterns |
| US7622070B2 (en) * | 2005-06-20 | 2009-11-24 | Advanced Cardiovascular Systems, Inc. | Method of manufacturing an implantable polymeric medical device |
| US20070043427A1 (en) * | 2005-08-19 | 2007-02-22 | Medlogics Device Corporation | Lumen-supporting stents |
| US20070132155A1 (en) | 2005-12-13 | 2007-06-14 | Robert Burgermeister | Polymeric stent having modified molecular structures in selected regions of the hoops and method for increasing elongation at break |
| US20070200271A1 (en) | 2006-02-24 | 2007-08-30 | Vipul Dave | Implantable device prepared from melt processing |
| US20070225798A1 (en) * | 2006-03-23 | 2007-09-27 | Daniel Gregorich | Side branch stent |
| US20070233233A1 (en) * | 2006-03-31 | 2007-10-04 | Boston Scientific Scimed, Inc | Tethered expansion columns for controlled stent expansion |
| US7594928B2 (en) * | 2006-05-17 | 2009-09-29 | Boston Scientific Scimed, Inc. | Bioabsorbable stents with reinforced filaments |
| US20070290412A1 (en) | 2006-06-19 | 2007-12-20 | John Capek | Fabricating a stent with selected properties in the radial and axial directions |
| US7922758B2 (en) * | 2006-06-23 | 2011-04-12 | Boston Scientific Scimed, Inc. | Nesting twisting hinge points in a bifurcated petal geometry |
| US9072820B2 (en) | 2006-06-26 | 2015-07-07 | Advanced Cardiovascular Systems, Inc. | Polymer composite stent with polymer particles |
| US20080001330A1 (en) | 2006-06-28 | 2008-01-03 | Bin Huang | Fabricating polymer stents with injection molding |
| US7740791B2 (en) | 2006-06-30 | 2010-06-22 | Advanced Cardiovascular Systems, Inc. | Method of fabricating a stent with features by blow molding |
| US9089627B2 (en) | 2006-07-11 | 2015-07-28 | Abbott Cardiovascular Systems Inc. | Stent fabricated from polymer composite toughened by a dispersed phase |
| US7794495B2 (en) | 2006-07-17 | 2010-09-14 | Advanced Cardiovascular Systems, Inc. | Controlled degradation of stents |
| US20080033540A1 (en) | 2006-08-01 | 2008-02-07 | Yunbing Wang | Methods to prepare polymer blend implantable medical devices |
| US9265866B2 (en) | 2006-08-01 | 2016-02-23 | Abbott Cardiovascular Systems Inc. | Composite polymeric and metallic stent with radiopacity |
| US7923022B2 (en) | 2006-09-13 | 2011-04-12 | Advanced Cardiovascular Systems, Inc. | Degradable polymeric implantable medical devices with continuous phase and discrete phase |
| EP2076211A4 (en) | 2006-10-20 | 2015-07-22 | Elixir Medical Corp | LUMINAL PROSTHESIS AND COATING METHOD THEREFOR |
| US20080103584A1 (en) * | 2006-10-25 | 2008-05-01 | Biosensors International Group | Temporal Intraluminal Stent, Methods of Making and Using |
| US8182890B2 (en) | 2007-01-19 | 2012-05-22 | Elixir Medical Corporation | Biodegradable endoprostheses and methods for their fabrication |
| US8002817B2 (en) | 2007-05-04 | 2011-08-23 | Abbott Cardiovascular Systems Inc. | Stents with high radial strength and methods of manufacturing same |
| US7829008B2 (en) * | 2007-05-30 | 2010-11-09 | Abbott Cardiovascular Systems Inc. | Fabricating a stent from a blow molded tube |
| US7666342B2 (en) * | 2007-06-29 | 2010-02-23 | Abbott Cardiovascular Systems Inc. | Method of manufacturing a stent from a polymer tube |
| US7824601B1 (en) * | 2007-11-14 | 2010-11-02 | Abbott Cardiovascular Systems Inc. | Process of making a tubular implantable medical device |
-
2008
- 2008-01-17 US US12/016,085 patent/US8182890B2/en active Active
- 2008-01-17 US US12/016,077 patent/US20080177373A1/en not_active Abandoned
- 2008-01-18 EP EP14174864.0A patent/EP2783710B1/en not_active Not-in-force
- 2008-01-18 BR BRPI0806623-0A patent/BRPI0806623A2/pt not_active IP Right Cessation
- 2008-01-18 CN CN201610065786.4A patent/CN105534627A/zh active Pending
- 2008-01-18 CN CN200880006660.3A patent/CN101636126B/zh not_active Expired - Fee Related
- 2008-01-18 JP JP2009546552A patent/JP5355420B2/ja not_active Expired - Fee Related
- 2008-01-18 CN CN201410172099.3A patent/CN104042375B/zh not_active Expired - Fee Related
- 2008-01-18 ES ES08727927.9T patent/ES2605731T3/es active Active
- 2008-01-18 EP EP08727927.9A patent/EP2124816B2/en not_active Not-in-force
- 2008-01-18 WO PCT/US2008/051497 patent/WO2008089446A2/en not_active Ceased
- 2008-01-18 CN CN201410343171.4A patent/CN104127270A/zh active Pending
- 2008-01-18 BR BRPI0806617-5A patent/BRPI0806617A2/pt not_active Application Discontinuation
- 2008-01-18 EP EP08727944.4A patent/EP2109416A4/en not_active Withdrawn
- 2008-01-18 WO PCT/US2008/051479 patent/WO2008089434A2/en not_active Ceased
- 2008-01-18 CN CN201410347826.5A patent/CN104096271B/zh not_active Expired - Fee Related
- 2008-01-18 CN CN201610065690.8A patent/CN105616044A/zh active Pending
- 2008-01-18 CN CN200880006680A patent/CN101621971A/zh active Pending
- 2008-01-18 JP JP2009546550A patent/JP5489725B2/ja not_active Expired - Fee Related
-
2012
- 2012-03-29 US US13/434,555 patent/US20120187606A1/en not_active Abandoned
- 2012-05-16 US US13/473,354 patent/US8323760B2/en active Active
-
2013
- 2013-06-27 JP JP2013135191A patent/JP5749296B2/ja not_active Expired - Fee Related
- 2013-09-02 JP JP2013181436A patent/JP5762486B2/ja not_active Expired - Fee Related
-
2014
- 2014-07-09 JP JP2014141094A patent/JP2014195734A/ja not_active Withdrawn
- 2014-08-01 US US14/450,137 patent/US20140350659A1/en not_active Abandoned
- 2014-11-21 JP JP2014236223A patent/JP2015071056A/ja active Pending
-
2015
- 2015-11-18 US US14/945,253 patent/US20160067389A1/en not_active Abandoned
-
2016
- 2016-09-20 JP JP2016182603A patent/JP2016221352A/ja not_active Withdrawn
- 2016-10-06 JP JP2016197807A patent/JP2017035511A/ja active Pending
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5489725B2 (ja) | 生分解性エンドプロテーゼおよび製造方法 | |
| EP2004104B1 (en) | Improved methods of polymeric stent surface smoothing and resurfacing to reduce biologically active sites | |
| US8267990B2 (en) | Controlled degradation of stents | |
| AU2014400542B2 (en) | Thin strut stent from bioabsorbable polymer with high fatigue and radial strength and method to manufacture thereof | |
| US20090105800A1 (en) | Methods of minimizing stent contraction following deployment | |
| US10518003B2 (en) | Method to manufacture thin strut stent from bioabsorbable polymer with high fatigue and radial strength | |
| US10603833B2 (en) | Method to manufacture thin strut stent from bioabsorbable polymer | |
| US10675387B2 (en) | Multi stage radial deformation for manufacturing thin strut stent from bioabsorbable polymer |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20101227 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20111220 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120820 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130111 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20130410 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20130417 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20130510 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20130517 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20130610 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20130617 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130627 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20130805 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20131202 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20140107 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20140130 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20140225 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5489725 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |