JP5129959B2 - 生産細胞の再クローン化方法 - Google Patents
生産細胞の再クローン化方法 Download PDFInfo
- Publication number
- JP5129959B2 JP5129959B2 JP2006523593A JP2006523593A JP5129959B2 JP 5129959 B2 JP5129959 B2 JP 5129959B2 JP 2006523593 A JP2006523593 A JP 2006523593A JP 2006523593 A JP2006523593 A JP 2006523593A JP 5129959 B2 JP5129959 B2 JP 5129959B2
- Authority
- JP
- Japan
- Prior art keywords
- cells
- cell
- cho cells
- serum
- free
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 238000000034 method Methods 0.000 title claims description 113
- 238000004519 manufacturing process Methods 0.000 title claims description 29
- 210000004027 cell Anatomy 0.000 claims abstract description 647
- 108090000623 proteins and genes Proteins 0.000 claims abstract description 125
- 238000010367 cloning Methods 0.000 claims abstract description 47
- 102000004169 proteins and genes Human genes 0.000 claims abstract description 38
- 239000000203 mixture Substances 0.000 claims abstract description 19
- 230000010076 replication Effects 0.000 claims abstract description 18
- 210000004978 chinese hamster ovary cell Anatomy 0.000 claims description 58
- 239000002609 medium Substances 0.000 claims description 53
- 239000000047 product Substances 0.000 claims description 35
- 108091006047 fluorescent proteins Proteins 0.000 claims description 30
- 102000034287 fluorescent proteins Human genes 0.000 claims description 29
- 238000004113 cell culture Methods 0.000 claims description 23
- 210000002966 serum Anatomy 0.000 claims description 20
- 238000001943 fluorescence-activated cell sorting Methods 0.000 claims description 17
- 230000003362 replicative effect Effects 0.000 claims description 17
- 230000001464 adherent effect Effects 0.000 claims description 13
- 210000004748 cultured cell Anatomy 0.000 claims description 13
- 238000012258 culturing Methods 0.000 claims description 13
- 230000000394 mitotic effect Effects 0.000 claims description 13
- 239000000725 suspension Substances 0.000 claims description 13
- 238000004114 suspension culture Methods 0.000 claims description 13
- 239000012679 serum free medium Substances 0.000 claims description 11
- 102000007056 Recombinant Fusion Proteins Human genes 0.000 claims description 6
- 108010008281 Recombinant Fusion Proteins Proteins 0.000 claims description 6
- 239000006143 cell culture medium Substances 0.000 claims description 6
- 239000012228 culture supernatant Substances 0.000 claims description 5
- 239000012528 membrane Substances 0.000 claims description 5
- 230000005855 radiation Effects 0.000 claims description 4
- 210000004962 mammalian cell Anatomy 0.000 abstract description 97
- 241000699800 Cricetinae Species 0.000 abstract description 41
- 206010035226 Plasma cell myeloma Diseases 0.000 abstract description 28
- 201000000050 myeloid neoplasm Diseases 0.000 abstract description 28
- 238000000151 deposition Methods 0.000 abstract description 3
- 239000004017 serum-free culture medium Substances 0.000 abstract 1
- 241000699666 Mus <mouse, genus> Species 0.000 description 35
- 235000018102 proteins Nutrition 0.000 description 34
- 230000012010 growth Effects 0.000 description 18
- 108090000765 processed proteins & peptides Proteins 0.000 description 16
- 239000003623 enhancer Substances 0.000 description 15
- 238000010790 dilution Methods 0.000 description 13
- 239000012895 dilution Substances 0.000 description 13
- 241000282414 Homo sapiens Species 0.000 description 12
- 239000012634 fragment Substances 0.000 description 12
- 102000004196 processed proteins & peptides Human genes 0.000 description 12
- IQFYYKKMVGJFEH-XLPZGREQSA-N Thymidine Chemical compound O=C1NC(=O)C(C)=CN1[C@@H]1O[C@H](CO)[C@@H](O)C1 IQFYYKKMVGJFEH-XLPZGREQSA-N 0.000 description 10
- 230000000670 limiting effect Effects 0.000 description 10
- 229920001184 polypeptide Polymers 0.000 description 10
- 210000004408 hybridoma Anatomy 0.000 description 9
- 239000003550 marker Substances 0.000 description 9
- 238000010370 cell cloning Methods 0.000 description 8
- 150000007523 nucleic acids Chemical class 0.000 description 8
- 230000035897 transcription Effects 0.000 description 8
- 238000013518 transcription Methods 0.000 description 8
- 238000001890 transfection Methods 0.000 description 8
- 241000699798 Cricetulus Species 0.000 description 7
- 108020004414 DNA Proteins 0.000 description 7
- 108010076504 Protein Sorting Signals Proteins 0.000 description 7
- 239000003242 anti bacterial agent Substances 0.000 description 7
- 230000001939 inductive effect Effects 0.000 description 7
- 102000039446 nucleic acids Human genes 0.000 description 7
- 108020004707 nucleic acids Proteins 0.000 description 7
- 230000001105 regulatory effect Effects 0.000 description 7
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 6
- 241000699678 Mesocricetus Species 0.000 description 6
- NWIBSHFKIJFRCO-WUDYKRTCSA-N Mytomycin Chemical compound C1N2C(C(C(C)=C(N)C3=O)=O)=C3[C@@H](COC(N)=O)[C@@]2(OC)[C@@H]2[C@H]1N2 NWIBSHFKIJFRCO-WUDYKRTCSA-N 0.000 description 6
- 150000001413 amino acids Chemical group 0.000 description 6
- 229940088710 antibiotic agent Drugs 0.000 description 6
- 230000000694 effects Effects 0.000 description 6
- FDGQSTZJBFJUBT-UHFFFAOYSA-N hypoxanthine Chemical compound O=C1NC=NC2=C1NC=N2 FDGQSTZJBFJUBT-UHFFFAOYSA-N 0.000 description 6
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 description 6
- 230000008488 polyadenylation Effects 0.000 description 6
- DWRXFEITVBNRMK-UHFFFAOYSA-N Beta-D-1-Arabinofuranosylthymine Natural products O=C1NC(=O)C(C)=CN1C1C(O)C(O)C(CO)O1 DWRXFEITVBNRMK-UHFFFAOYSA-N 0.000 description 5
- 241000699802 Cricetulus griseus Species 0.000 description 5
- 239000012981 Hank's balanced salt solution Substances 0.000 description 5
- 108700009124 Transcription Initiation Site Proteins 0.000 description 5
- 241001512733 Zoanthus sp. Species 0.000 description 5
- 235000001014 amino acid Nutrition 0.000 description 5
- 239000000427 antigen Substances 0.000 description 5
- 102000036639 antigens Human genes 0.000 description 5
- 108091007433 antigens Proteins 0.000 description 5
- IQFYYKKMVGJFEH-UHFFFAOYSA-N beta-L-thymidine Natural products O=C1NC(=O)C(C)=CN1C1OC(CO)C(O)C1 IQFYYKKMVGJFEH-UHFFFAOYSA-N 0.000 description 5
- 230000027455 binding Effects 0.000 description 5
- 239000003795 chemical substances by application Substances 0.000 description 5
- 239000013604 expression vector Substances 0.000 description 5
- 239000003102 growth factor Substances 0.000 description 5
- 230000001965 increasing effect Effects 0.000 description 5
- 230000008569 process Effects 0.000 description 5
- 230000001225 therapeutic effect Effects 0.000 description 5
- 229940104230 thymidine Drugs 0.000 description 5
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 4
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 4
- 108700028146 Genetic Enhancer Elements Proteins 0.000 description 4
- 108010067060 Immunoglobulin Variable Region Proteins 0.000 description 4
- 241001465754 Metazoa Species 0.000 description 4
- 239000004098 Tetracycline Substances 0.000 description 4
- 108010022394 Threonine synthase Proteins 0.000 description 4
- OIRDTQYFTABQOQ-KQYNXXCUSA-N adenosine Chemical compound C1=NC=2C(N)=NC=NC=2N1[C@@H]1O[C@H](CO)[C@@H](O)[C@H]1O OIRDTQYFTABQOQ-KQYNXXCUSA-N 0.000 description 4
- 229940024606 amino acid Drugs 0.000 description 4
- 210000004102 animal cell Anatomy 0.000 description 4
- 239000012298 atmosphere Substances 0.000 description 4
- 230000015572 biosynthetic process Effects 0.000 description 4
- 102000004419 dihydrofolate reductase Human genes 0.000 description 4
- 239000003814 drug Substances 0.000 description 4
- 229940079593 drug Drugs 0.000 description 4
- 230000004927 fusion Effects 0.000 description 4
- 230000001900 immune effect Effects 0.000 description 4
- 238000002955 isolation Methods 0.000 description 4
- 108020004999 messenger RNA Proteins 0.000 description 4
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 4
- 210000001672 ovary Anatomy 0.000 description 4
- 108091033319 polynucleotide Proteins 0.000 description 4
- 102000040430 polynucleotide Human genes 0.000 description 4
- 239000002157 polynucleotide Substances 0.000 description 4
- 238000002360 preparation method Methods 0.000 description 4
- 108020003175 receptors Proteins 0.000 description 4
- 102000005962 receptors Human genes 0.000 description 4
- 241000894007 species Species 0.000 description 4
- 239000000126 substance Substances 0.000 description 4
- 229960002180 tetracycline Drugs 0.000 description 4
- 229930101283 tetracycline Natural products 0.000 description 4
- 235000019364 tetracycline Nutrition 0.000 description 4
- 150000003522 tetracyclines Chemical class 0.000 description 4
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 3
- 241000006271 Discosoma sp. Species 0.000 description 3
- 108010043121 Green Fluorescent Proteins Proteins 0.000 description 3
- 102000004144 Green Fluorescent Proteins Human genes 0.000 description 3
- UGQMRVRMYYASKQ-UHFFFAOYSA-N Hypoxanthine nucleoside Natural products OC1C(O)C(CO)OC1N1C(NC=NC2=O)=C2N=C1 UGQMRVRMYYASKQ-UHFFFAOYSA-N 0.000 description 3
- 108010021625 Immunoglobulin Fragments Proteins 0.000 description 3
- 102000008394 Immunoglobulin Fragments Human genes 0.000 description 3
- 102000017727 Immunoglobulin Variable Region Human genes 0.000 description 3
- 102000004877 Insulin Human genes 0.000 description 3
- 108090001061 Insulin Proteins 0.000 description 3
- 108090000723 Insulin-Like Growth Factor I Proteins 0.000 description 3
- 241001529936 Murinae Species 0.000 description 3
- 102000006601 Thymidine Kinase Human genes 0.000 description 3
- 108020004440 Thymidine kinase Proteins 0.000 description 3
- 108091023040 Transcription factor Proteins 0.000 description 3
- 102000040945 Transcription factor Human genes 0.000 description 3
- 102000009618 Transforming Growth Factors Human genes 0.000 description 3
- 108010009583 Transforming Growth Factors Proteins 0.000 description 3
- 108060008682 Tumor Necrosis Factor Proteins 0.000 description 3
- 102000000852 Tumor Necrosis Factor-alpha Human genes 0.000 description 3
- 235000021120 animal protein Nutrition 0.000 description 3
- -1 antibodies Proteins 0.000 description 3
- 238000013459 approach Methods 0.000 description 3
- 229910052786 argon Inorganic materials 0.000 description 3
- 229960000074 biopharmaceutical Drugs 0.000 description 3
- 229910002091 carbon monoxide Inorganic materials 0.000 description 3
- 238000011109 contamination Methods 0.000 description 3
- 238000005138 cryopreservation Methods 0.000 description 3
- 238000011161 development Methods 0.000 description 3
- 230000018109 developmental process Effects 0.000 description 3
- 238000009826 distribution Methods 0.000 description 3
- 238000005516 engineering process Methods 0.000 description 3
- 102000037865 fusion proteins Human genes 0.000 description 3
- 108020001507 fusion proteins Proteins 0.000 description 3
- 239000005090 green fluorescent protein Substances 0.000 description 3
- 230000002779 inactivation Effects 0.000 description 3
- 229940125396 insulin Drugs 0.000 description 3
- 239000007788 liquid Substances 0.000 description 3
- 229960004857 mitomycin Drugs 0.000 description 3
- 239000013587 production medium Substances 0.000 description 3
- 238000000746 purification Methods 0.000 description 3
- 230000002285 radioactive effect Effects 0.000 description 3
- 239000002356 single layer Substances 0.000 description 3
- 238000003153 stable transfection Methods 0.000 description 3
- 238000010186 staining Methods 0.000 description 3
- 238000011144 upstream manufacturing Methods 0.000 description 3
- 230000035899 viability Effects 0.000 description 3
- DIGQNXIGRZPYDK-WKSCXVIASA-N (2R)-6-amino-2-[[2-[[(2S)-2-[[2-[[(2R)-2-[[(2S)-2-[[(2R,3S)-2-[[2-[[(2S)-2-[[2-[[(2S)-2-[[(2S)-2-[[(2R)-2-[[(2S,3S)-2-[[(2R)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[2-[[(2S)-2-[[(2R)-2-[[2-[[2-[[2-[(2-amino-1-hydroxyethylidene)amino]-3-carboxy-1-hydroxypropylidene]amino]-1-hydroxy-3-sulfanylpropylidene]amino]-1-hydroxyethylidene]amino]-1-hydroxy-3-sulfanylpropylidene]amino]-1,3-dihydroxypropylidene]amino]-1-hydroxyethylidene]amino]-1-hydroxypropylidene]amino]-1,3-dihydroxypropylidene]amino]-1,3-dihydroxypropylidene]amino]-1-hydroxy-3-sulfanylpropylidene]amino]-1,3-dihydroxybutylidene]amino]-1-hydroxy-3-sulfanylpropylidene]amino]-1-hydroxypropylidene]amino]-1,3-dihydroxypropylidene]amino]-1-hydroxyethylidene]amino]-1,5-dihydroxy-5-iminopentylidene]amino]-1-hydroxy-3-sulfanylpropylidene]amino]-1,3-dihydroxybutylidene]amino]-1-hydroxy-3-sulfanylpropylidene]amino]-1,3-dihydroxypropylidene]amino]-1-hydroxyethylidene]amino]-1-hydroxy-3-sulfanylpropylidene]amino]-1-hydroxyethylidene]amino]hexanoic acid Chemical compound C[C@@H]([C@@H](C(=N[C@@H](CS)C(=N[C@@H](C)C(=N[C@@H](CO)C(=NCC(=N[C@@H](CCC(=N)O)C(=NC(CS)C(=N[C@H]([C@H](C)O)C(=N[C@H](CS)C(=N[C@H](CO)C(=NCC(=N[C@H](CS)C(=NCC(=N[C@H](CCCCN)C(=O)O)O)O)O)O)O)O)O)O)O)O)O)O)O)N=C([C@H](CS)N=C([C@H](CO)N=C([C@H](CO)N=C([C@H](C)N=C(CN=C([C@H](CO)N=C([C@H](CS)N=C(CN=C(C(CS)N=C(C(CC(=O)O)N=C(CN)O)O)O)O)O)O)O)O)O)O)O)O DIGQNXIGRZPYDK-WKSCXVIASA-N 0.000 description 2
- GLCCHZQEWYMOBT-UHFFFAOYSA-N 2,5-diazatetracyclo[7.4.0.02,7.04,6]trideca-1(9),3,5,7,11-pentaene-10,13-dione Chemical compound O=C1C=CC(=O)C2=C1C=C1N2C=C2N=C21 GLCCHZQEWYMOBT-UHFFFAOYSA-N 0.000 description 2
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 2
- BFSVOASYOCHEOV-UHFFFAOYSA-N 2-diethylaminoethanol Chemical compound CCN(CC)CCO BFSVOASYOCHEOV-UHFFFAOYSA-N 0.000 description 2
- UZOVYGYOLBIAJR-UHFFFAOYSA-N 4-isocyanato-4'-methyldiphenylmethane Chemical compound C1=CC(C)=CC=C1CC1=CC=C(N=C=O)C=C1 UZOVYGYOLBIAJR-UHFFFAOYSA-N 0.000 description 2
- 108010085238 Actins Proteins 0.000 description 2
- 241000242764 Aequorea victoria Species 0.000 description 2
- 241000894006 Bacteria Species 0.000 description 2
- 239000002126 C01EB10 - Adenosine Substances 0.000 description 2
- 241000283707 Capra Species 0.000 description 2
- 108020004705 Codon Proteins 0.000 description 2
- 102000004127 Cytokines Human genes 0.000 description 2
- 108090000695 Cytokines Proteins 0.000 description 2
- 101150074155 DHFR gene Proteins 0.000 description 2
- 102000053602 DNA Human genes 0.000 description 2
- 102000004163 DNA-directed RNA polymerases Human genes 0.000 description 2
- 108090000626 DNA-directed RNA polymerases Proteins 0.000 description 2
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 2
- 239000007995 HEPES buffer Substances 0.000 description 2
- 101000610605 Homo sapiens Tumor necrosis factor receptor superfamily member 10A Proteins 0.000 description 2
- 102000002265 Human Growth Hormone Human genes 0.000 description 2
- 108010000521 Human Growth Hormone Proteins 0.000 description 2
- 239000000854 Human Growth Hormone Substances 0.000 description 2
- 108060003951 Immunoglobulin Proteins 0.000 description 2
- 108010054477 Immunoglobulin Fab Fragments Proteins 0.000 description 2
- 102000001706 Immunoglobulin Fab Fragments Human genes 0.000 description 2
- 102000014150 Interferons Human genes 0.000 description 2
- 108010050904 Interferons Proteins 0.000 description 2
- 102000015696 Interleukins Human genes 0.000 description 2
- 108010063738 Interleukins Proteins 0.000 description 2
- 239000007760 Iscove's Modified Dulbecco's Medium Substances 0.000 description 2
- 108010025815 Kanamycin Kinase Proteins 0.000 description 2
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 2
- QIVBCDIJIAJPQS-VIFPVBQESA-N L-tryptophane Chemical compound C1=CC=C2C(C[C@H](N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-VIFPVBQESA-N 0.000 description 2
- 241000124008 Mammalia Species 0.000 description 2
- 241000699673 Mesocricetus auratus Species 0.000 description 2
- 102000003792 Metallothionein Human genes 0.000 description 2
- 108090000157 Metallothionein Proteins 0.000 description 2
- 206010028980 Neoplasm Diseases 0.000 description 2
- 108090000099 Neurotrophin-4 Proteins 0.000 description 2
- 102100033237 Pro-epidermal growth factor Human genes 0.000 description 2
- 239000004365 Protease Substances 0.000 description 2
- 239000012980 RPMI-1640 medium Substances 0.000 description 2
- 241000242743 Renilla reniformis Species 0.000 description 2
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- 102000013275 Somatomedins Human genes 0.000 description 2
- 108700012411 TNFSF10 Proteins 0.000 description 2
- 102000036693 Thrombopoietin Human genes 0.000 description 2
- 108010041111 Thrombopoietin Proteins 0.000 description 2
- 102000003978 Tissue Plasminogen Activator Human genes 0.000 description 2
- 108090000373 Tissue Plasminogen Activator Proteins 0.000 description 2
- 108090000901 Transferrin Proteins 0.000 description 2
- 102000004338 Transferrin Human genes 0.000 description 2
- 102100024598 Tumor necrosis factor ligand superfamily member 10 Human genes 0.000 description 2
- 102100040113 Tumor necrosis factor receptor superfamily member 10A Human genes 0.000 description 2
- 102000005789 Vascular Endothelial Growth Factors Human genes 0.000 description 2
- 108010019530 Vascular Endothelial Growth Factors Proteins 0.000 description 2
- 241000700605 Viruses Species 0.000 description 2
- 229960005305 adenosine Drugs 0.000 description 2
- 102000006646 aminoglycoside phosphotransferase Human genes 0.000 description 2
- 239000011324 bead Substances 0.000 description 2
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 2
- 239000000872 buffer Substances 0.000 description 2
- 229910052792 caesium Inorganic materials 0.000 description 2
- TVFDJXOCXUVLDH-UHFFFAOYSA-N caesium atom Chemical compound [Cs] TVFDJXOCXUVLDH-UHFFFAOYSA-N 0.000 description 2
- 239000001506 calcium phosphate Substances 0.000 description 2
- 229910000389 calcium phosphate Inorganic materials 0.000 description 2
- 235000011010 calcium phosphates Nutrition 0.000 description 2
- 125000003917 carbamoyl group Chemical group [H]N([H])C(*)=O 0.000 description 2
- 230000008859 change Effects 0.000 description 2
- 238000003776 cleavage reaction Methods 0.000 description 2
- 229910017052 cobalt Inorganic materials 0.000 description 2
- 239000010941 cobalt Substances 0.000 description 2
- GUTLYIVDDKVIGB-UHFFFAOYSA-N cobalt atom Chemical compound [Co] GUTLYIVDDKVIGB-UHFFFAOYSA-N 0.000 description 2
- 238000002474 experimental method Methods 0.000 description 2
- MHMNJMPURVTYEJ-UHFFFAOYSA-N fluorescein-5-isothiocyanate Chemical compound O1C(=O)C2=CC(N=C=S)=CC=C2C21C1=CC=C(O)C=C1OC1=CC(O)=CC=C21 MHMNJMPURVTYEJ-UHFFFAOYSA-N 0.000 description 2
- 230000008014 freezing Effects 0.000 description 2
- 238000007710 freezing Methods 0.000 description 2
- 238000010353 genetic engineering Methods 0.000 description 2
- 239000008103 glucose Substances 0.000 description 2
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 description 2
- 238000004128 high performance liquid chromatography Methods 0.000 description 2
- 239000005556 hormone Substances 0.000 description 2
- 229940088597 hormone Drugs 0.000 description 2
- 108010002685 hygromycin-B kinase Proteins 0.000 description 2
- 102000018358 immunoglobulin Human genes 0.000 description 2
- 238000011534 incubation Methods 0.000 description 2
- 239000000411 inducer Substances 0.000 description 2
- 238000003780 insertion Methods 0.000 description 2
- 230000037431 insertion Effects 0.000 description 2
- 229940079322 interferon Drugs 0.000 description 2
- 229940047122 interleukins Drugs 0.000 description 2
- 230000001404 mediated effect Effects 0.000 description 2
- 238000000520 microinjection Methods 0.000 description 2
- 230000035772 mutation Effects 0.000 description 2
- 229910052757 nitrogen Inorganic materials 0.000 description 2
- 239000002777 nucleoside Substances 0.000 description 2
- 125000003835 nucleoside group Chemical group 0.000 description 2
- 239000002773 nucleotide Substances 0.000 description 2
- 125000003729 nucleotide group Chemical group 0.000 description 2
- 235000015097 nutrients Nutrition 0.000 description 2
- 238000005457 optimization Methods 0.000 description 2
- 239000002243 precursor Substances 0.000 description 2
- 238000001742 protein purification Methods 0.000 description 2
- RXWNCPJZOCPEPQ-NVWDDTSBSA-N puromycin Chemical compound C1=CC(OC)=CC=C1C[C@H](N)C(=O)N[C@H]1[C@@H](O)[C@H](N2C3=NC=NC(=C3N=C2)N(C)C)O[C@@H]1CO RXWNCPJZOCPEPQ-NVWDDTSBSA-N 0.000 description 2
- 230000007017 scission Effects 0.000 description 2
- 230000028327 secretion Effects 0.000 description 2
- 230000035939 shock Effects 0.000 description 2
- 239000006228 supernatant Substances 0.000 description 2
- 101150024821 tetO gene Proteins 0.000 description 2
- 229960000187 tissue plasminogen activator Drugs 0.000 description 2
- 239000011573 trace mineral Substances 0.000 description 2
- 235000013619 trace mineral Nutrition 0.000 description 2
- 230000005030 transcription termination Effects 0.000 description 2
- 239000012581 transferrin Substances 0.000 description 2
- 238000013519 translation Methods 0.000 description 2
- 230000014621 translational initiation Effects 0.000 description 2
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 2
- ZISSAWUMDACLOM-UHFFFAOYSA-N triptane Chemical compound CC(C)C(C)(C)C ZISSAWUMDACLOM-UHFFFAOYSA-N 0.000 description 2
- 241000701161 unidentified adenovirus Species 0.000 description 2
- MZOFCQQQCNRIBI-VMXHOPILSA-N (3s)-4-[[(2s)-1-[[(2s)-1-[[(1s)-1-carboxy-2-hydroxyethyl]amino]-4-methyl-1-oxopentan-2-yl]amino]-5-(diaminomethylideneamino)-1-oxopentan-2-yl]amino]-3-[[2-[[(2s)-2,6-diaminohexanoyl]amino]acetyl]amino]-4-oxobutanoic acid Chemical compound OC[C@@H](C(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H](CC(O)=O)NC(=O)CNC(=O)[C@@H](N)CCCCN MZOFCQQQCNRIBI-VMXHOPILSA-N 0.000 description 1
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 1
- NWUYHJFMYQTDRP-UHFFFAOYSA-N 1,2-bis(ethenyl)benzene;1-ethenyl-2-ethylbenzene;styrene Chemical compound C=CC1=CC=CC=C1.CCC1=CC=CC=C1C=C.C=CC1=CC=CC=C1C=C NWUYHJFMYQTDRP-UHFFFAOYSA-N 0.000 description 1
- QRBLKGHRWFGINE-UGWAGOLRSA-N 2-[2-[2-[[2-[[4-[[2-[[6-amino-2-[3-amino-1-[(2,3-diamino-3-oxopropyl)amino]-3-oxopropyl]-5-methylpyrimidine-4-carbonyl]amino]-3-[(2r,3s,4s,5s,6s)-3-[(2s,3r,4r,5s)-4-carbamoyl-3,4,5-trihydroxy-6-(hydroxymethyl)oxan-2-yl]oxy-4,5-dihydroxy-6-(hydroxymethyl)- Chemical compound N=1C(C=2SC=C(N=2)C(N)=O)CSC=1CCNC(=O)C(C(C)=O)NC(=O)C(C)C(O)C(C)NC(=O)C(C(O[C@H]1[C@@]([C@@H](O)[C@H](O)[C@H](CO)O1)(C)O[C@H]1[C@@H]([C@](O)([C@@H](O)C(CO)O1)C(N)=O)O)C=1NC=NC=1)NC(=O)C1=NC(C(CC(N)=O)NCC(N)C(N)=O)=NC(N)=C1C QRBLKGHRWFGINE-UGWAGOLRSA-N 0.000 description 1
- 102000007469 Actins Human genes 0.000 description 1
- 108010059616 Activins Proteins 0.000 description 1
- 241000242763 Anemonia Species 0.000 description 1
- 241001512986 Anemonia majano Species 0.000 description 1
- 241000242762 Anemonia sulcata Species 0.000 description 1
- 241000242757 Anthozoa Species 0.000 description 1
- 244000105975 Antidesma platyphyllum Species 0.000 description 1
- 102100023927 Asparagine synthetase [glutamine-hydrolyzing] Human genes 0.000 description 1
- 108010070255 Aspartate-ammonia ligase Proteins 0.000 description 1
- 102100026189 Beta-galactosidase Human genes 0.000 description 1
- 108010006654 Bleomycin Proteins 0.000 description 1
- 108010039209 Blood Coagulation Factors Proteins 0.000 description 1
- 102000015081 Blood Coagulation Factors Human genes 0.000 description 1
- 102000004506 Blood Proteins Human genes 0.000 description 1
- 108010017384 Blood Proteins Proteins 0.000 description 1
- 102000004219 Brain-derived neurotrophic factor Human genes 0.000 description 1
- 108090000715 Brain-derived neurotrophic factor Proteins 0.000 description 1
- 102100021943 C-C motif chemokine 2 Human genes 0.000 description 1
- 102100031092 C-C motif chemokine 3 Human genes 0.000 description 1
- 101710155856 C-C motif chemokine 3 Proteins 0.000 description 1
- 102100032367 C-C motif chemokine 5 Human genes 0.000 description 1
- 108010029697 CD40 Ligand Proteins 0.000 description 1
- 102100032937 CD40 ligand Human genes 0.000 description 1
- 101100289995 Caenorhabditis elegans mac-1 gene Proteins 0.000 description 1
- 108010067225 Cell Adhesion Molecules Proteins 0.000 description 1
- 241000282693 Cercopithecidae Species 0.000 description 1
- 108010055166 Chemokine CCL5 Proteins 0.000 description 1
- 241000006719 Clavularia Species 0.000 description 1
- 241000006720 Clavularia sp. Species 0.000 description 1
- 102100022641 Coagulation factor IX Human genes 0.000 description 1
- 102100023804 Coagulation factor VII Human genes 0.000 description 1
- 108091026890 Coding region Proteins 0.000 description 1
- 241000701022 Cytomegalovirus Species 0.000 description 1
- 102100039498 Cytotoxic T-lymphocyte protein 4 Human genes 0.000 description 1
- 230000004544 DNA amplification Effects 0.000 description 1
- 229920002307 Dextran Polymers 0.000 description 1
- 241000006867 Discosoma Species 0.000 description 1
- 241001512730 Discosoma striata Species 0.000 description 1
- 238000002965 ELISA Methods 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 101800003838 Epidermal growth factor Proteins 0.000 description 1
- 241000206602 Eukaryota Species 0.000 description 1
- 108010076282 Factor IX Proteins 0.000 description 1
- 108010023321 Factor VII Proteins 0.000 description 1
- 108010054218 Factor VIII Proteins 0.000 description 1
- 102000001690 Factor VIII Human genes 0.000 description 1
- 108010008177 Fd immunoglobulins Proteins 0.000 description 1
- 241000233866 Fungi Species 0.000 description 1
- 102100039619 Granulocyte colony-stimulating factor Human genes 0.000 description 1
- 102100039620 Granulocyte-macrophage colony-stimulating factor Human genes 0.000 description 1
- 101000889276 Homo sapiens Cytotoxic T-lymphocyte protein 4 Proteins 0.000 description 1
- 101000746367 Homo sapiens Granulocyte colony-stimulating factor Proteins 0.000 description 1
- 101000746373 Homo sapiens Granulocyte-macrophage colony-stimulating factor Proteins 0.000 description 1
- 101000599852 Homo sapiens Intercellular adhesion molecule 1 Proteins 0.000 description 1
- 101000599858 Homo sapiens Intercellular adhesion molecule 2 Proteins 0.000 description 1
- 101000998146 Homo sapiens Interleukin-17A Proteins 0.000 description 1
- 101001012157 Homo sapiens Receptor tyrosine-protein kinase erbB-2 Proteins 0.000 description 1
- 101100369992 Homo sapiens TNFSF10 gene Proteins 0.000 description 1
- 101000610604 Homo sapiens Tumor necrosis factor receptor superfamily member 10B Proteins 0.000 description 1
- 101000610602 Homo sapiens Tumor necrosis factor receptor superfamily member 10C Proteins 0.000 description 1
- 101000610609 Homo sapiens Tumor necrosis factor receptor superfamily member 10D Proteins 0.000 description 1
- 101000798130 Homo sapiens Tumor necrosis factor receptor superfamily member 11B Proteins 0.000 description 1
- 101000597785 Homo sapiens Tumor necrosis factor receptor superfamily member 6B Proteins 0.000 description 1
- 241000701024 Human betaherpesvirus 5 Species 0.000 description 1
- 102000026633 IL6 Human genes 0.000 description 1
- 108010091135 Immunoglobulin Fc Fragments Proteins 0.000 description 1
- 102000018071 Immunoglobulin Fc Fragments Human genes 0.000 description 1
- 102000012745 Immunoglobulin Subunits Human genes 0.000 description 1
- 108010079585 Immunoglobulin Subunits Proteins 0.000 description 1
- 102100026818 Inhibin beta E chain Human genes 0.000 description 1
- 108020005350 Initiator Codon Proteins 0.000 description 1
- 102000004218 Insulin-Like Growth Factor I Human genes 0.000 description 1
- 108090001117 Insulin-Like Growth Factor II Proteins 0.000 description 1
- 102000048143 Insulin-Like Growth Factor II Human genes 0.000 description 1
- 102000008607 Integrin beta3 Human genes 0.000 description 1
- 108010020950 Integrin beta3 Proteins 0.000 description 1
- 108010064600 Intercellular Adhesion Molecule-3 Proteins 0.000 description 1
- 102100037877 Intercellular adhesion molecule 1 Human genes 0.000 description 1
- 102100037872 Intercellular adhesion molecule 2 Human genes 0.000 description 1
- 102100037871 Intercellular adhesion molecule 3 Human genes 0.000 description 1
- 102000003814 Interleukin-10 Human genes 0.000 description 1
- 108090000174 Interleukin-10 Proteins 0.000 description 1
- 102000003815 Interleukin-11 Human genes 0.000 description 1
- 108090000177 Interleukin-11 Proteins 0.000 description 1
- 102000013462 Interleukin-12 Human genes 0.000 description 1
- 108010065805 Interleukin-12 Proteins 0.000 description 1
- 102000003816 Interleukin-13 Human genes 0.000 description 1
- 108090000176 Interleukin-13 Proteins 0.000 description 1
- 102000003812 Interleukin-15 Human genes 0.000 description 1
- 108090000172 Interleukin-15 Proteins 0.000 description 1
- 102000049772 Interleukin-16 Human genes 0.000 description 1
- 101800003050 Interleukin-16 Proteins 0.000 description 1
- 102100033461 Interleukin-17A Human genes 0.000 description 1
- 102000003810 Interleukin-18 Human genes 0.000 description 1
- 108090000171 Interleukin-18 Proteins 0.000 description 1
- 108020004684 Internal Ribosome Entry Sites Proteins 0.000 description 1
- 108091092195 Intron Proteins 0.000 description 1
- ZQISRDCJNBUVMM-UHFFFAOYSA-N L-Histidinol Natural products OCC(N)CC1=CN=CN1 ZQISRDCJNBUVMM-UHFFFAOYSA-N 0.000 description 1
- ZQISRDCJNBUVMM-YFKPBYRVSA-N L-histidinol Chemical compound OC[C@@H](N)CC1=CNC=N1 ZQISRDCJNBUVMM-YFKPBYRVSA-N 0.000 description 1
- ROHFNLRQFUQHCH-YFKPBYRVSA-N L-leucine Chemical compound CC(C)C[C@H](N)C(O)=O ROHFNLRQFUQHCH-YFKPBYRVSA-N 0.000 description 1
- 108091026898 Leader sequence (mRNA) Proteins 0.000 description 1
- ROHFNLRQFUQHCH-UHFFFAOYSA-N Leucine Natural products CC(C)CC(N)C(O)=O ROHFNLRQFUQHCH-UHFFFAOYSA-N 0.000 description 1
- 102000008072 Lymphokines Human genes 0.000 description 1
- 108010074338 Lymphokines Proteins 0.000 description 1
- 102000009571 Macrophage Inflammatory Proteins Human genes 0.000 description 1
- 108010009474 Macrophage Inflammatory Proteins Proteins 0.000 description 1
- 102100028123 Macrophage colony-stimulating factor 1 Human genes 0.000 description 1
- 101710127797 Macrophage colony-stimulating factor 1 Proteins 0.000 description 1
- 101710091439 Major capsid protein 1 Proteins 0.000 description 1
- 241001430197 Mollicutes Species 0.000 description 1
- 241000699660 Mus musculus Species 0.000 description 1
- 101100335081 Mus musculus Flt3 gene Proteins 0.000 description 1
- 101100341510 Mus musculus Itgal gene Proteins 0.000 description 1
- 101000969137 Mus musculus Metallothionein-1 Proteins 0.000 description 1
- 241000699670 Mus sp. Species 0.000 description 1
- 229930193140 Neomycin Natural products 0.000 description 1
- 108090000028 Neprilysin Proteins 0.000 description 1
- 102000003729 Neprilysin Human genes 0.000 description 1
- 108010025020 Nerve Growth Factor Proteins 0.000 description 1
- 102000007072 Nerve Growth Factors Human genes 0.000 description 1
- 102000004230 Neurotrophin 3 Human genes 0.000 description 1
- 108090000742 Neurotrophin 3 Proteins 0.000 description 1
- 102000003683 Neurotrophin-4 Human genes 0.000 description 1
- 102100033857 Neurotrophin-4 Human genes 0.000 description 1
- 108090000095 Neurotrophin-6 Proteins 0.000 description 1
- 108091028043 Nucleic acid sequence Proteins 0.000 description 1
- 108090000526 Papain Proteins 0.000 description 1
- 102000057297 Pepsin A Human genes 0.000 description 1
- 108090000284 Pepsin A Proteins 0.000 description 1
- 108091005804 Peptidases Proteins 0.000 description 1
- 102000035195 Peptidases Human genes 0.000 description 1
- 102000007079 Peptide Fragments Human genes 0.000 description 1
- 108010033276 Peptide Fragments Proteins 0.000 description 1
- LTQCLFMNABRKSH-UHFFFAOYSA-N Phleomycin Natural products N=1C(C=2SC=C(N=2)C(N)=O)CSC=1CCNC(=O)C(C(O)C)NC(=O)C(C)C(O)C(C)NC(=O)C(C(OC1C(C(O)C(O)C(CO)O1)OC1C(C(OC(N)=O)C(O)C(CO)O1)O)C=1NC=NC=1)NC(=O)C1=NC(C(CC(N)=O)NCC(N)C(N)=O)=NC(N)=C1C LTQCLFMNABRKSH-UHFFFAOYSA-N 0.000 description 1
- 108010035235 Phleomycins Proteins 0.000 description 1
- 101710098940 Pro-epidermal growth factor Proteins 0.000 description 1
- 101800004937 Protein C Proteins 0.000 description 1
- 102000017975 Protein C Human genes 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- 102100030086 Receptor tyrosine-protein kinase erbB-2 Human genes 0.000 description 1
- 102100029986 Receptor tyrosine-protein kinase erbB-3 Human genes 0.000 description 1
- 101710100969 Receptor tyrosine-protein kinase erbB-3 Proteins 0.000 description 1
- 102100029981 Receptor tyrosine-protein kinase erbB-4 Human genes 0.000 description 1
- 101710100963 Receptor tyrosine-protein kinase erbB-4 Proteins 0.000 description 1
- 241000714474 Rous sarcoma virus Species 0.000 description 1
- 240000004808 Saccharomyces cerevisiae Species 0.000 description 1
- 101000849522 Saccharomyces cerevisiae (strain ATCC 204508 / S288c) 40S ribosomal protein S13 Proteins 0.000 description 1
- 101800001700 Saposin-D Proteins 0.000 description 1
- 229920005654 Sephadex Polymers 0.000 description 1
- 239000012507 Sephadex™ Substances 0.000 description 1
- 102000007562 Serum Albumin Human genes 0.000 description 1
- 108010071390 Serum Albumin Proteins 0.000 description 1
- 108091081024 Start codon Proteins 0.000 description 1
- 108091008874 T cell receptors Proteins 0.000 description 1
- 102000016266 T-Cell Antigen Receptors Human genes 0.000 description 1
- 210000001744 T-lymphocyte Anatomy 0.000 description 1
- 241000053227 Themus Species 0.000 description 1
- 108091036066 Three prime untranslated region Proteins 0.000 description 1
- 108700029229 Transcriptional Regulatory Elements Proteins 0.000 description 1
- 102000006747 Transforming Growth Factor alpha Human genes 0.000 description 1
- 101800004564 Transforming growth factor alpha Proteins 0.000 description 1
- 108090000631 Trypsin Proteins 0.000 description 1
- 102000004142 Trypsin Human genes 0.000 description 1
- 102100031988 Tumor necrosis factor ligand superfamily member 6 Human genes 0.000 description 1
- 108050002568 Tumor necrosis factor ligand superfamily member 6 Proteins 0.000 description 1
- 102100040112 Tumor necrosis factor receptor superfamily member 10B Human genes 0.000 description 1
- 102100040115 Tumor necrosis factor receptor superfamily member 10C Human genes 0.000 description 1
- 102100040110 Tumor necrosis factor receptor superfamily member 10D Human genes 0.000 description 1
- 102100032236 Tumor necrosis factor receptor superfamily member 11B Human genes 0.000 description 1
- 102100035284 Tumor necrosis factor receptor superfamily member 6B Human genes 0.000 description 1
- 102000044159 Ubiquitin Human genes 0.000 description 1
- 108090000848 Ubiquitin Proteins 0.000 description 1
- 208000036142 Viral infection Diseases 0.000 description 1
- 108010084455 Zeocin Proteins 0.000 description 1
- 241001512728 Zoanthus Species 0.000 description 1
- 230000021736 acetylation Effects 0.000 description 1
- 238000006640 acetylation reaction Methods 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 239000000488 activin Substances 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- GFFGJBXGBJISGV-UHFFFAOYSA-N adenyl group Chemical class N1=CN=C2N=CNC2=C1N GFFGJBXGBJISGV-UHFFFAOYSA-N 0.000 description 1
- 239000000556 agonist Substances 0.000 description 1
- 230000003698 anagen phase Effects 0.000 description 1
- 239000005557 antagonist Substances 0.000 description 1
- 230000001580 bacterial effect Effects 0.000 description 1
- 210000000270 basal cell Anatomy 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 108010005774 beta-Galactosidase Proteins 0.000 description 1
- 230000001588 bifunctional effect Effects 0.000 description 1
- 230000003115 biocidal effect Effects 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 230000008033 biological extinction Effects 0.000 description 1
- 238000010352 biotechnological method Methods 0.000 description 1
- 229960001561 bleomycin Drugs 0.000 description 1
- OYVAGSVQBOHSSS-UAPAGMARSA-O bleomycin A2 Chemical compound N([C@H](C(=O)N[C@H](C)[C@@H](O)[C@H](C)C(=O)N[C@@H]([C@H](O)C)C(=O)NCCC=1SC=C(N=1)C=1SC=C(N=1)C(=O)NCCC[S+](C)C)[C@@H](O[C@H]1[C@H]([C@@H](O)[C@H](O)[C@H](CO)O1)O[C@@H]1[C@H]([C@@H](OC(N)=O)[C@H](O)[C@@H](CO)O1)O)C=1N=CNC=1)C(=O)C1=NC([C@H](CC(N)=O)NC[C@H](N)C(N)=O)=NC(N)=C1C OYVAGSVQBOHSSS-UAPAGMARSA-O 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- 239000008280 blood Substances 0.000 description 1
- 210000000601 blood cell Anatomy 0.000 description 1
- 239000003114 blood coagulation factor Substances 0.000 description 1
- 239000003130 blood coagulation factor inhibitor Substances 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 238000004364 calculation method Methods 0.000 description 1
- 201000011510 cancer Diseases 0.000 description 1
- 239000003729 cation exchange resin Substances 0.000 description 1
- 102000008395 cell adhesion mediator activity proteins Human genes 0.000 description 1
- 230000005779 cell damage Effects 0.000 description 1
- 208000037887 cell injury Diseases 0.000 description 1
- 239000013592 cell lysate Substances 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 210000000349 chromosome Anatomy 0.000 description 1
- 210000001728 clone cell Anatomy 0.000 description 1
- 238000000975 co-precipitation Methods 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- 230000003750 conditioning effect Effects 0.000 description 1
- 239000002577 cryoprotective agent Substances 0.000 description 1
- 125000000151 cysteine group Chemical group N[C@@H](CS)C(=O)* 0.000 description 1
- 210000001151 cytotoxic T lymphocyte Anatomy 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 238000012217 deletion Methods 0.000 description 1
- 230000037430 deletion Effects 0.000 description 1
- 230000008021 deposition Effects 0.000 description 1
- KVEAILYLMGOETO-UHFFFAOYSA-H dicalcium magnesium diphosphate Chemical compound P(=O)([O-])([O-])[O-].[Mg+2].[Ca+2].[Ca+2].P(=O)([O-])([O-])[O-] KVEAILYLMGOETO-UHFFFAOYSA-H 0.000 description 1
- 230000029087 digestion Effects 0.000 description 1
- 238000006471 dimerization reaction Methods 0.000 description 1
- 238000005315 distribution function Methods 0.000 description 1
- CETRZFQIITUQQL-UHFFFAOYSA-N dmso dimethylsulfoxide Chemical compound CS(C)=O.CS(C)=O CETRZFQIITUQQL-UHFFFAOYSA-N 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 101150097231 eg gene Proteins 0.000 description 1
- 238000004520 electroporation Methods 0.000 description 1
- 238000000295 emission spectrum Methods 0.000 description 1
- 229940088598 enzyme Drugs 0.000 description 1
- 229940116977 epidermal growth factor Drugs 0.000 description 1
- 238000012869 ethanol precipitation Methods 0.000 description 1
- 210000003527 eukaryotic cell Anatomy 0.000 description 1
- 230000005284 excitation Effects 0.000 description 1
- 238000000695 excitation spectrum Methods 0.000 description 1
- 229960004222 factor ix Drugs 0.000 description 1
- 229940012413 factor vii Drugs 0.000 description 1
- 229960000301 factor viii Drugs 0.000 description 1
- 238000000855 fermentation Methods 0.000 description 1
- 230000004151 fermentation Effects 0.000 description 1
- 210000002950 fibroblast Anatomy 0.000 description 1
- 238000000684 flow cytometry Methods 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 238000012215 gene cloning Methods 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- 239000003862 glucocorticoid Substances 0.000 description 1
- 102000005396 glutamine synthetase Human genes 0.000 description 1
- 108020002326 glutamine synthetase Proteins 0.000 description 1
- 230000013595 glycosylation Effects 0.000 description 1
- 238000006206 glycosylation reaction Methods 0.000 description 1
- 235000009424 haa Nutrition 0.000 description 1
- 229910001385 heavy metal Inorganic materials 0.000 description 1
- 239000000710 homodimer Substances 0.000 description 1
- 210000005260 human cell Anatomy 0.000 description 1
- 244000052637 human pathogen Species 0.000 description 1
- 229940072221 immunoglobulins Drugs 0.000 description 1
- 230000001976 improved effect Effects 0.000 description 1
- 239000000893 inhibin Substances 0.000 description 1
- ZPNFWUPYTFPOJU-LPYSRVMUSA-N iniprol Chemical compound C([C@H]1C(=O)NCC(=O)NCC(=O)N[C@H]2CSSC[C@H]3C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@H](C(N[C@H](C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=4C=CC(O)=CC=4)C(=O)N[C@@H](CC=4C=CC=CC=4)C(=O)N[C@@H](CC=4C=CC(O)=CC=4)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](C)C(=O)NCC(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CSSC[C@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C)NC(=O)[C@H](CO)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CC=4C=CC=CC=4)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CCCCN)NC(=O)[C@H](C)NC(=O)[C@H](CCCNC(N)=N)NC2=O)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CSSC[C@H](NC(=O)[C@H](CC=2C=CC=CC=2)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H]2N(CCC2)C(=O)[C@@H](N)CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(O)=O)C(=O)N2[C@@H](CCC2)C(=O)N2[C@@H](CCC2)C(=O)N[C@@H](CC=2C=CC(O)=CC=2)C(=O)N[C@@H]([C@@H](C)O)C(=O)NCC(=O)N2[C@@H](CCC2)C(=O)N3)C(=O)NCC(=O)NCC(=O)N[C@@H](C)C(O)=O)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@H](C(=O)N[C@@H](CC=2C=CC=CC=2)C(=O)N[C@H](C(=O)N1)C(C)C)[C@@H](C)O)[C@@H](C)CC)=O)[C@@H](C)CC)C1=CC=C(O)C=C1 ZPNFWUPYTFPOJU-LPYSRVMUSA-N 0.000 description 1
- 230000010354 integration Effects 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 238000005342 ion exchange Methods 0.000 description 1
- 230000001678 irradiating effect Effects 0.000 description 1
- 210000002510 keratinocyte Anatomy 0.000 description 1
- 210000003734 kidney Anatomy 0.000 description 1
- 210000003292 kidney cell Anatomy 0.000 description 1
- 102000005861 leptin receptors Human genes 0.000 description 1
- 108010019813 leptin receptors Proteins 0.000 description 1
- 239000002502 liposome Substances 0.000 description 1
- 238000009630 liquid culture Methods 0.000 description 1
- 239000006166 lysate Substances 0.000 description 1
- 210000002540 macrophage Anatomy 0.000 description 1
- GVALZJMUIHGIMD-UHFFFAOYSA-H magnesium phosphate Chemical compound [Mg+2].[Mg+2].[Mg+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O GVALZJMUIHGIMD-UHFFFAOYSA-H 0.000 description 1
- 239000004137 magnesium phosphate Substances 0.000 description 1
- 229910000157 magnesium phosphate Inorganic materials 0.000 description 1
- 229960002261 magnesium phosphate Drugs 0.000 description 1
- 235000010994 magnesium phosphates Nutrition 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 230000002503 metabolic effect Effects 0.000 description 1
- 238000010369 molecular cloning Methods 0.000 description 1
- 229960004927 neomycin Drugs 0.000 description 1
- 229940032018 neurotrophin 3 Drugs 0.000 description 1
- 231100000028 nontoxic concentration Toxicity 0.000 description 1
- 238000010899 nucleation Methods 0.000 description 1
- 235000019834 papain Nutrition 0.000 description 1
- 229940055729 papain Drugs 0.000 description 1
- 244000052769 pathogen Species 0.000 description 1
- 229940111202 pepsin Drugs 0.000 description 1
- CWCMIVBLVUHDHK-ZSNHEYEWSA-N phleomycin D1 Chemical compound N([C@H](C(=O)N[C@H](C)[C@@H](O)[C@H](C)C(=O)N[C@@H]([C@H](O)C)C(=O)NCCC=1SC[C@@H](N=1)C=1SC=C(N=1)C(=O)NCCCCNC(N)=N)[C@@H](O[C@H]1[C@H]([C@@H](O)[C@H](O)[C@H](CO)O1)O[C@@H]1[C@H]([C@@H](OC(N)=O)[C@H](O)[C@@H](CO)O1)O)C=1N=CNC=1)C(=O)C1=NC([C@H](CC(N)=O)NC[C@H](N)C(N)=O)=NC(N)=C1C CWCMIVBLVUHDHK-ZSNHEYEWSA-N 0.000 description 1
- 230000026731 phosphorylation Effects 0.000 description 1
- 238000006366 phosphorylation reaction Methods 0.000 description 1
- 238000000053 physical method Methods 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 230000001124 posttranscriptional effect Effects 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- 230000001737 promoting effect Effects 0.000 description 1
- 235000019419 proteases Nutrition 0.000 description 1
- 229960000856 protein c Drugs 0.000 description 1
- 230000020978 protein processing Effects 0.000 description 1
- 230000002797 proteolythic effect Effects 0.000 description 1
- 210000001938 protoplast Anatomy 0.000 description 1
- 229950010131 puromycin Drugs 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 230000002829 reductive effect Effects 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 230000000284 resting effect Effects 0.000 description 1
- 238000004366 reverse phase liquid chromatography Methods 0.000 description 1
- 238000004007 reversed phase HPLC Methods 0.000 description 1
- 229920002477 rna polymer Polymers 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 230000011664 signaling Effects 0.000 description 1
- 239000000377 silicon dioxide Substances 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 235000002639 sodium chloride Nutrition 0.000 description 1
- 210000004989 spleen cell Anatomy 0.000 description 1
- 230000002269 spontaneous effect Effects 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 210000000130 stem cell Anatomy 0.000 description 1
- 238000006467 substitution reaction Methods 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 229940037128 systemic glucocorticoids Drugs 0.000 description 1
- 230000005100 tissue tropism Effects 0.000 description 1
- 238000004448 titration Methods 0.000 description 1
- 230000005758 transcription activity Effects 0.000 description 1
- 238000003151 transfection method Methods 0.000 description 1
- 230000014723 transformation of host cell by virus Effects 0.000 description 1
- 230000001052 transient effect Effects 0.000 description 1
- 238000003146 transient transfection Methods 0.000 description 1
- 230000005945 translocation Effects 0.000 description 1
- 230000032258 transport Effects 0.000 description 1
- 239000013638 trimer Substances 0.000 description 1
- 239000012588 trypsin Substances 0.000 description 1
- 210000004881 tumor cell Anatomy 0.000 description 1
- 239000010981 turquoise Substances 0.000 description 1
- 108010087967 type I signal peptidase Proteins 0.000 description 1
- 238000009281 ultraviolet germicidal irradiation Methods 0.000 description 1
- VBEQCZHXXJYVRD-GACYYNSASA-N uroanthelone Chemical compound C([C@@H](C(=O)N[C@H](C(=O)N[C@@H](CS)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CS)C(=O)N[C@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)NCC(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H](CO)C(=O)NCC(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CS)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(O)=O)C(C)C)[C@@H](C)O)NC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@@H](NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H](CCSC)NC(=O)[C@H](CS)NC(=O)[C@@H](NC(=O)CNC(=O)CNC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CS)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)CNC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CS)NC(=O)CNC(=O)[C@H]1N(CCC1)C(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC(N)=O)C(C)C)[C@@H](C)CC)C1=CC=C(O)C=C1 VBEQCZHXXJYVRD-GACYYNSASA-N 0.000 description 1
- 230000009385 viral infection Effects 0.000 description 1
- 230000003612 virological effect Effects 0.000 description 1
- 108010047303 von Willebrand Factor Proteins 0.000 description 1
- 102100036537 von Willebrand factor Human genes 0.000 description 1
- 229960001134 von willebrand factor Drugs 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0693—Tumour cells; Cancer cells
- C12N5/0694—Cells of blood, e.g. leukemia cells, myeloma cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0693—Tumour cells; Cancer cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2500/00—Specific components of cell culture medium
- C12N2500/90—Serum-free medium, which may still contain naturally-sourced components
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2502/00—Coculture with; Conditioned medium produced by
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2502/00—Coculture with; Conditioned medium produced by
- C12N2502/30—Coculture with; Conditioned medium produced by tumour cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2510/00—Genetically modified cells
- C12N2510/02—Cells for production
Landscapes
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Life Sciences & Earth Sciences (AREA)
- Biomedical Technology (AREA)
- Wood Science & Technology (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Genetics & Genomics (AREA)
- Biotechnology (AREA)
- Zoology (AREA)
- Oncology (AREA)
- Biochemistry (AREA)
- Microbiology (AREA)
- General Engineering & Computer Science (AREA)
- General Health & Medical Sciences (AREA)
- Cell Biology (AREA)
- Hematology (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Description
本発明は、細胞培養技術の分野に関係し、細胞、好ましくはバイオ医薬品の生産に重要な細胞系を複製/クローン化する方法に関する。本発明は、個々の細胞を置く(depositことによって得、かつ複製した細胞を用いてタンパク質を調製する方法にも関し、個々の細胞の複製を可能にする組成物にも関するものである。
哺乳類細胞内での生物活性タンパク質又は治療用タンパク質、いわゆるバイオ医薬品のバイオテクノロジー生産では、生物活性タンパク質(又はそのサブユニット)をコードするDNAで、対応する哺乳類細胞を安定してトランスフェクトする。トランスフェクションプロセス後、通常、いろいろにトランスフェクトされた数百万個の細胞のプールが得られる。従って、効率的な生産細胞系の調製で重要なステップは、一方では非常に安定して成長し、他方では治療用タンパク質の高特異的生産性(産物形成など)を示す細胞クローンの選択と複製にある。数百万個の異なる産物-発現細胞があるので、非常に力強く成長し、かつ高い産物タイターも与える適切な候補(単一細胞クローン)を選別できるように、高処理能力で、かつ自動化によって多数の細胞を個々に分析できることが重要である。この単一細胞の単離及び継代培養プロセスはクローン化又は再クローン化として知られる。
しかしながら、マウス骨髄腫(NS0)、ハムスター卵巣(CHO)、又はハムスター腎臓細胞(BHK)のような典型的な組換え生産細胞(特にそれら細胞が血清フリー懸濁培養、すなわち、最近の生産関連細胞培養条件下、個々に培養容器内、例えばマイクロタイタープレートのウェル内、血清フリー培養条件下での成長に適応している場合)を置き、かつ効率的にそれらを複製(再クローン化)するという問題がある。数個の細胞、例えば5個未満の細胞を血清フリー条件下で培養容器に置いた場合、これら細胞はまったく複製できず、或いは少なくとも効率的に複製できない。この理由は、細胞と細胞の接触がないこと、低い細胞密度ではより多くの栄養/成長因子が必要であること及び/又は拡散性のシグナル因子及び条件付け(conditioning)因子がないか若しくは非常に低濃度なことだと考えられる。
これとは別に、現在、血清適応性付着細胞を個々に置くことよって、生産関連細胞系の単一細胞クローンを生成できるだけである。Mengら(2000)は、例えば、血清含有培地で個々の付着して成長するCHO細胞を置く方法を述べている。しかしながら、Mengらによって開示された方法は大きな欠点がある。すなわち、細胞の付着のため、骨の折れるその細胞を基質から酵素的に脱着すること(トリプシン処理)は相当な細胞損傷につながり、再クローン化細胞の成長特徴及び生産性が変わる。さらに、対応して得られる個々のクローンは懸濁培養での血清フリー成長に適応させなければならず、これは通常時間がかかる操作であり、細胞の生産性及び産物の質に影響を与える(この主題については、とりわけKaufmannら, 2001; Muellerら, 1999を参照されたい)。
異種フィーダー細胞を使用する場合、一般的にフィーダー細胞を逆-選択する必要がある。生産細胞は例えば培地への添加剤(G418のような抗生物質)及び/又は不完全培地(ヒポキサンチン、チミジンの非存在)の使用の結果として一般的に選択圧になりやすい。この選択圧が、例えば組換えタンパク質に対応する遺伝情報を吸収かつ組み込んだ細胞の選択を可能にする。このようにして生産細胞に適応させて生成された培地は、フィーダー細胞の成長に重大な影響を及ぼし、その他の点では非適合性の生産培地と共にフィーダー細胞の非常に迅速な乾燥をもたらす。結果として、もはやフィーダー細胞の機能は保証されない。
本発明の1つの目的は、5個未満の細胞、好ましくは1個の単一細胞から開始して血清フリー条件下かつ懸濁培養で生産関連哺乳類細胞を複製できる効率的な再クローン化法を見出すことだった。特に、この目的は、元来ハムスターから単離したCHO又はBHK細胞及び元来マウスから単離した骨髄腫細胞、例えばNS0細胞の再クローン化に対応する方法を提供することだった。
本発明のさらなる目的は、この対応する再クローン化法、特にハムスター細胞又はマウス骨髄腫細胞を再クローン化する方法の実施を可能にする組成物を提供することだった。
これら目的は、特許請求の範囲で定義した本発明の主題によって達成される。一局面では、本発明は、細胞のクローン化方法であって、5個未満、好ましくは1個又は2個の哺乳類細胞、好ましくはハムスター細胞又はマウス骨髄腫細胞を、フィーダー細胞、好ましくは自家起源のフィーダー細胞の存在下、血清フリー条件下で培養容器に置いて、血清フリー条件下で培養かつ複製することを特徴とする方法に関する。一特定局面では、本発明は、CHO若しくはBHK細胞(ハムスター細胞)又はNS0細胞(マウス骨髄腫細胞)(好ましくは、これら細胞が懸濁培養での血清フリー成長に適応している細胞の場合)の再クローン化に対応する方法に関する。
本発明の別の態様は、置かれて、かつクローン化される哺乳類細胞がハムスター細胞、特にCHO又はBHK細胞である場合にフィーダー細胞としてハムスター細胞を使用することに関する。置かれて、かつクローン化すべき細胞がNS0細胞の場合、好ましくはフィーダー細胞としてマウス骨髄腫細胞を使用する。
本発明の方法は、特に個々に置かれた細胞について10%より高い、好ましくは20%より高い良い再クローン化効率を特徴とする。別の態様によれば、本発明の再クローン化法は、30%より高い、好ましくは40%より高い、特に好ましくは50%より高い、さらに好ましくは60%より高い、なおさらに好ましくは70%より高い、なおさらに好ましくは80%より高い再クローン化効率を有する。
この場合、個々に置かれたCHO細胞の再クローン化では10%乃至65%より高い再クローン化効率、個々に置かれたBHK細胞の再クローン化では10%乃至50%より高い再クローン化効率、個々に置かれたNS0細胞の再クローン化では10%乃至45%より高い再クローン化効率が効率的とみなされる。1培養皿当たり1個より多い細胞、例えば2、3又は4個の細胞を置いている場合、問題の細胞の再クローン化効率はCHO、BHK及びNS0細胞の再クローン化について規定した上記値より高い。
別の局面では、本発明は、哺乳類細胞、特にハムスター細胞又はマウス骨髄腫細胞をクローン化に対応する方法であって、クローン化される細胞が1mlの培地当たり100〜200,000個のフィーダー細胞の存在下で複製される方法に関する。
a)問題の細胞を複製できる血清フリー条件下、対象遺伝子産物を発現する哺乳類細胞を培養する工程;
b)5個未満、好ましくは1又は2個の対応する哺乳類細胞を、血清フリー条件下で1つの細胞培養容器に置く工程;
c)対応して置かれた細胞を、血清フリー条件下、自家フィーダー細胞の存在下で複製する工程;
d)この複製された置かれた細胞を、対象遺伝子が発現される血清フリー条件下で培養する工程;及び
e)膜を含む細胞又は培養上清から、対象遺伝子でコードされている遺伝子産物を回収かつ精製する工程。
例えば、手動又はFACSベースソーティングによって哺乳類細胞を分離して、フィーダー細胞と共に細胞培養容器に置くことができる。好ましくは、非付着性培養フィーダー細胞を使用する。
本発明は、ハムスター細胞、特にCHO又はBHK細胞及びマウス骨髄腫細胞、特にNS0型細胞のフィーダー細胞としての基本的使用にも関する。好ましい態様では、本発明は、血清フリー培養条件に適応させた対応する細胞の使用に関する。
本発明は、血清フリー細胞培地と、分裂可能な5個未満の哺乳類細胞と、この分裂可能な哺乳類細胞について自家性のフィーダー細胞とから成る組成物にも関する。本発明のさらなる局面により、前記分裂可能な哺乳類細胞は、懸濁培養として血清フリー成長に適応している細胞である。特定態様では、本組成物は、前記培地中に分裂可能な哺乳類細胞を1又は2個だけ含有する。分裂可能な哺乳類細胞は、好ましくは、例えばCHO若しくはBHK細胞のようなハムスター細胞、又はマウス骨髄腫細胞、例えばNS0細胞である。
本発明の別の局面では、分裂可能な哺乳類細胞がCHO細胞の場合、組成物はフィーダー細胞としてハムスター細胞、好ましくはCHO細胞を含有する。分裂可能な哺乳類細胞がBHK細胞の場合、組成物はフィーダー細胞としてもハムスター細胞、好ましくはBHK細胞を含有する。分裂可能な哺乳類細胞がマウス骨髄腫細胞、例えばNS0細胞の場合、組成物はフィーダー細胞としてもマウス骨髄腫細胞を含有し、NS0細胞の場合はフィーダー細胞としても好ましくはNS0細胞を含有する。
本発明の方法は、血清フリー、タンパク質フリー又は化学的に規定した生産培地中の細胞に、対応する哺乳類細胞を置くことができるようにするので、普通は必要な血清フリー又はタンパク質フリー生産培地への適応化を行う必要がない。このことが生産関連細胞系の確立における開発時間の実質的な短縮(約50%)につながる。さらに、単一細胞を置くこと、安定した均質の細胞クローンをもたらし、このことはバイオ医薬品の生産で非常に重要であり、薬物としてのそれらの使用許可の規定要件について特に重要である。さらに、生産関連CHO、BHK又はNS0細胞の再クローン化用に自家フィーダー細胞を使用すること、例えば、ハムスター細胞、好ましくはCHO若しくはBHK細胞、又はマウス骨髄腫細胞、好ましくはNS0細胞の使用は、ヒト細胞又はあまりよく特徴づけされていない細胞の使用より、ヒト病原についてのコンタミネーションのリスクをかなり低減する。
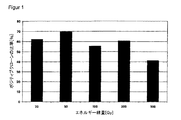
図1は、フィーダー細胞の生産で用いたエネルギー線量と、自動的に置かれた単一CHO-DG-44細胞の再クローン化におけるクローン化効率との関係を示す。各場合、約2000個の不活性な自家フィーダー細胞上にCHO-DG-44細胞を置く。グラフは、20〜500Gyのエネルギー線量で照射されたフィーダー細胞は未だ十分な因子を培地に放出し、50Gyで置かれた単一クローンの65%より多くをコロニーに成長させることを示している。
図2は、限界希釈(左側の列)又は単一細胞を置くこと(右側の列)によって得られた抗体発現CHO-DG-44培養の生産性を示す。左側の列は、限界希釈によって得られた6つの培養の生産性を示す。右側の列は、自動的に単一細胞を置くことから得られた6つの単一クローンの生産性を示す。生産性を決定するため、細胞クローン/培養毎に3とおりの平行実験を行った。限界希釈によるクローン化と対照的に、単一クローンを自動的に置くことによるクローン化は、生産性の実質的変化が少なかった。平行して培養し、かつ単一クローンから誘導した二次培養はその生産性について限界希釈で得た二次培養に比べて実質的に高い均質性を示す。
図3aは、種々の基準に従って貯蔵し、かつ個々に置かれたCHO-DG-44細胞クローンの産物タイターを示す。下段のグラフでは、“生きている細胞”という選別基準だけを満たす単一細胞を置いた。この基準はフローサイトメーターでのフォワードサイドスキャター記録を用いて定義した。細胞は蛍光では選択されなかった。他方、中段のグラフBと上段のグラフCでは、“生きている細胞”という選別基準にさらに“細胞の蛍光”という選別基準を論理的につなげた。“細胞の蛍光”という選別基準はさらに蛍光強度を用いても定義した。これを行うため、一方でトップ20%の蛍光性細胞クローンと、他方でトップ5%の蛍光性細胞クローンを個々に置いた。棒グラフCにおける右へのシフトは、トップ5%の蛍光性細胞の基準を用いた場合、A及びBで用いた他の選別基準に比べて高発現性の細胞クローンの比率が有意に増加することを示している。
図3bは、図3aに示したデータに基づいている。平均の2倍の生産性を有するプロデューサー(=高プロデューサー)を得る確率(%)を示す。すべての生細胞で得られたデータに正規分布を調和させ、平均タイターを決定した。次に、正規分布の分布関数から、個々に細胞を置くことで得られた細胞クローンが前記タイターの2倍以上であるパーセンテージを計算した。図3bにはこのパーセンテージが示されている。グラフは、“生きている細胞”という基準だけの使用に比べてさらにトップ5%という基準を使用した場合、高プロデューサーの確率が20倍を超えて高くなることを示している。
以下の非限定的な例示態様を用いて本発明をさらに詳細に説明する前に、不定冠詞、例えば“a”又は“an”と、定冠詞、すなわち“the”の使用は、問題の用語の単数と複数の二形式の一方を明白に除外し、特定形成(単数又は複数)に言及していない限り、両形式を包含することに注意すべきである。従って、用語“細胞(a cell)”は、単数の細胞だけを意味すると明白に述べていない限り、自動的に“複数の細胞”を包含する。例えば、“a”又は“one”が(1)で補足されている場合、明白に単数を意味する。
〔定義〕
細胞培養に関する用語“クローン化/再クローン化”、“クローン化/再クローン化する”は、元の細胞から同一細胞の細胞集団を得ることができる技術を意味する。従って、“細胞クローン化”又は“単一細胞クローン化”は、異なる遺伝子型の細胞のある細胞プールから単一細胞を同定かつ単離してから複製して、複数の遺伝子的に同一の細胞から成る細胞集団を形成することができるプロセスを意味する。細胞を個々に、すなわち1つの培養容器につき1個だけの細胞を置いてから増量させて同一細胞の細胞集団を形成する場合、このプロセスは“直接的単一細胞クローン化”である。いくつかの細胞を同時に培養容器に置いて、増量させて細胞集団を形成し、これを反復希釈(限界希釈)によって同一細胞の細胞集団に分裂する場合、これは“間接的クローン化”法と記述される。
単一クローンは、1個の単一細胞に由来する遺伝的に同一の細胞である。従って、以後、同起源の同一細胞から成る細胞集団を“モノクロナール細胞集団”と称する。同起源の細胞の培養中にそのゲノムに自発的変化、例えば、突然変異及び/又はトランスロケーションがあっても、本発明の目的では、この細胞集団の個々の細胞は未だ同一細胞とみなされ、該培養はモノクロナール細胞集団とみなされる。対照的に、安定してトランスフェクトされた細胞(トランスフェクタント)のプールは同じ血統の細胞クローンではない。すなわち、遺伝的に同一の出発細胞が同一の核酸でトランスフェクトされた場合でさえ、それらはモノクロナール細胞集団ではない。
“有効又は効率的な再クローン化”とは、少なくとも10%、好ましくは少なくとも20%、さらに好ましくは少なくとも30%、なおさらに好ましくは少なくとも40%のクローン化効率を意味する。本発明の特に好ましい態様では、用語効率的な再クローン化は、少なくとも50%、好ましくは少なくとも60%、最も好ましくは少なくとも70%、なおさらに好ましくは少なくとも80%の効率のクローン化を意味する。
用語“クローン化効率”は、置いた後好ましくは50個を超える細胞の活発な細胞集団を形成できる細胞のパーセンテージとして定義される。例えば、細胞選別操作で50個の細胞を50個の培養容器に分布させ、これら50個の個々に置かれた細胞の25個が成長して培養を形成した場合、このクローン化効率は50%(50から25)である。
本発明の目的での用語“分裂できる/増量可能な”は、細胞/細胞集団の無限に、少なくとも2回より多く、好ましくは4回の継代で分裂する可能性を示す。この可能性は、例えば[137]Csによる照射又はマイトマイシンC処理によって減少させ、或いは全部破壊することができる。
用語“派生物/子孫”は、遺伝的に特定の出発細胞にさかのぼることのできる細胞を指し、例えば継代培養(選択圧がある場合とない場合)によって形成され、及び/又遺伝子操作で生成される。同じ細胞型の細胞の再単離も用語“派生物/子孫”に包含される。従って、例えば、すべてのCHO細胞系は、継代培養、再単離又は遺伝子操作のいずれによって得られたかとは関係なく、Puckら(1958)によってチャイニーズハムスター(Cricetulus griseus)から単離されたハムスター卵巣細胞の派生物/子孫である。
用語“タンパク質フリー”は、培地が如何なる動物タンパク質をも含有しないことを意味する。ここで、細菌、酵母菌又は真菌から単離されるタンパク質は動物タンパク質とはみなさない。
用語“化学的に規定した”は、血清フリー、好ましくはタンパク質フリーでもあり、かつ化学的に規定した物質から成る細胞培地を示す。従って、化学的に規定した培地は、顕著に純粋な個々の物質の混合物から成る。化学的に規定した培地の一例は、Messrs Invitrogen (Carlsbad, CA, US)製のCD-CHO培地である。
表現“懸濁状態で培養されうる細胞”は、液体培養(“懸濁培養”)での成長に適応し、かつ容器、例えば細胞培養皿又はフラスコの表面に付着するその能力が制限され、或いは失われている細胞を指す。血清フリー成長と懸濁状態での成長の両方に適応している細胞を“血清フリー培地に適応した非付着性細胞”と称する。このような培養からフィーダー細胞を調製した場合、これら細胞を“血清フリー培地に適応した非付着性フィーダー細胞”と定義する。
本発明は、細胞のクローン化方法であって、5個未満、例えば、4、3、2又は1個の哺乳類細胞を、フィーダー細胞、好ましくは自家フィーダー細胞の存在下、培養容器、好ましくは血清フリー条件下の培養容器に置いて、血清フリー条件下で培養かつ複製することを特徴とする方法に関する。好ましい態様では、本発明は、哺乳類細胞のクローン化に対応する方法であって、1つの培養容器につき1又は2個の哺乳類細胞を血清フリー条件下で置いて、かつ血清フリー条件下、自家フィーダー細胞の存在下で培養することを特徴とする方法に関する。好ましい態様は、単一細胞のクローン化方法であって、血清フリー条件下、自家フィーダー細胞の存在下、培養容器に1個の単一哺乳類細胞を置いて、血清フリー条件下で培養かつ複製することを特徴とする方法に関する。別の好ましい態様では、置かれた被培養細胞が懸濁培養で成長する細胞である。
1つの培養容器に1個だけの細胞を置いて、複製して細胞集団を形成する場合、それぞれ個々に成長する細胞集団はモノクロナール細胞集団であり、このプロセスは直接的単一細胞クローン化法である。各培養容器に1個より多くの単一細胞、例えば2、3又は4個の細胞を置いて複製する場合、成長する細胞集団はいわゆる混合クローンである。これらは、直接的単一細胞クローン化又は常法、例えば細胞集団の反復希釈(=限界希釈)によって、いわゆる統計的なモノクロナール細胞集団に変換することができる(例えば、Morgan, Kultur tierischer Zellen [culture of animal cells], pages 113 and 114, Spektrum Akademischer Verlag 1994参照)。
特に好ましい態様では、Cricetulus属(中国の矮小ハムスター)のハムスター細胞及びこの属から単離した安定な細胞系又はこの単離細胞由来の細胞系、例えば、CHO、CHO-K1、CHO-DUKX、CHO-DUKX B1又はCHO-DG-44細胞及びこれら細胞系の派生物/子孫のハムスター細胞を複製/クローン化する方法である。特に好ましい本発明の方法は、自家フィーダー細胞の存在下でCHO-DG-44、CHO-DUKX、及びCHO-K1、特にCHO-DG-44及びCHO-DUKX細胞を複製かつクローン化する方法である。本発明の方法を用いて、Mesocricetus auratus(シリアハムスター)及びそれから単離された安定な細胞系又はその細胞系由来の細胞系、例えば、BHK21又はBHK TK-細胞及びこれら細胞系の派生物/子孫を本発明で述べる方法で複製かつクローン化することもできる。結果として、本発明は、好ましくはCHO又はBHK細胞、及びその派生物/子孫を複製かつクローン化する方法であって、5個未満、例えば、4、3、2、又は好ましくは1個の細胞を血清フリー条件下、自家フィーダー細胞の存在下、培養容器に置いて、血清フリー条件下で培養かつ複製することを特徴とする方法に関する。
本発明で複製及びクローン化しうるハムスター細胞及びマウス細胞のさらなる例を下表1に示す。これら細胞/細胞系の派生物及び子孫に加え、ヒト、マウス、ラット、モンキー、又はマウス以外のげっ歯類及びハムスター由来の細胞系を含む他の哺乳類細胞を本発明の方法で複製又はクローン化することができる。
対照的に、別の態様では、本発明は、付着性自家フィーダー細胞を用いるか、或いは別の好ましい態様では、懸濁状態でも維持される自家フィーダー細胞を用いて、懸濁状態で成長する細胞を複製することができる。フィーダー細胞と被培養細胞の両者が同じ基本細胞に由来する場合、例えば両細胞が元来懸濁状態での成長に適応させた細胞である場合、懸濁状態で維持される自家フィーダー細胞の使用が特に好ましい。従って、本発明は、上述した哺乳類細胞を複製/クローン化する方法であって、懸濁状態で維持される自家フィーダー細胞の存在下で被培養細胞を置き、培養及び複製することを特徴とする方法にも関する。被培養細胞が懸濁状態での成長に適応した細胞であることを特徴とする対応方法が特に好ましい。この関係では、細胞を置くこと及び置かれた哺乳類細胞の複製を血清フリー及び/又はタンパク質フリー及び/又は化学的に規定した懸濁培養で行うことも好ましい。
用語“自家フィーダー細胞”の定義により、本発明は、哺乳類細胞の複製/クローン化方法であって、複製/クローン化される置かれた哺乳類細胞がCHO又はBHK細胞の場合、フィーダー細胞としてハムスター細胞、好ましくはキヌゲネズミ亜科の細胞、さらに好ましくはCricetulus属又はMesocricetus属の細胞を使用し、複製/クローン化される置かれた哺乳類細胞がNS0細胞の場合、フィーダー細胞としてマウス骨髄腫細胞を使用することを特徴とする方法に関する。また、哺乳類細胞の複製/クローン化方法であって、複製/クローン化される置かれた哺乳類細胞がCHO細胞の場合、フィーダー細胞としてCHO細胞を使用し、複製/クローン化される置かれた哺乳類細胞がBHK細胞の場合、フィーダー細胞としてBHK細胞を使用し、複製/クローン化される置かれた哺乳類細胞がNS0細胞の場合、フィーダー細胞としてNS0細胞を使用することを特徴とする方法が好ましい。
本方法は、置かれた哺乳類細胞が元々置かれていた培養容器内で、1×105〜4×106/ml(培地)の密度まで前記置かれた哺乳類細胞を複製するのに好適である。好ましくは、第1継代は2×105〜8×105/ml(培地)の細胞密度、特に2×105〜5×105/ml(培地)の細胞密度で起こる。
ここで述べる本発明の哺乳類細胞の複製/クローン化方法は高レベルの再クローン化効率を特徴とし、本発明は、哺乳類細胞の複製/クローン化方法であって、クローン化効率が少なくとも10%、好ましくは少なくとも20%、さらに好ましくは少なくとも30%、なおさらに好ましくは少なくとも40%であることを特徴とする方法に関する。特に好ましい態様では、本発明は、哺乳類細胞の複製/クローン化方法であって、クローン化効率が少なくとも50%、好ましくは少なくとも60%、特に好ましくは少なくとも70%、なおさらに好ましくは少なくとも80%であることを特徴とする方法に関する。
本明細書で述べる実施例では、CHO細胞について65%以上の再クローン化効率が得られた。従って、本発明は、CHO細胞の複製/クローン化方法であって、置かれたCHO細胞を再クローン化するときの再クローン化効率が10%乃至65%より高く、好ましくは20%より高く、最も好ましくは30%より高く、さらに好ましくは40%より高く、なおさらに好ましくは50%より高く、特に60%より高いことを特徴とする方法にも関する。しかし、本発明は、細胞タイプについて規定した再クローン化効率よりいくらか低い方法にも関する。
生成される対象遺伝子は、宿主細胞に天然に存在する遺伝子でよく、或いは宿主細胞に人工的に導入される遺伝子でもよい。定義上、細胞に導入される各配列又は遺伝子は、その導入される配列又は遺伝子が前記細胞の内因性配列又は内因性遺伝子と同一である場合でさえ、この細胞との関係では、“異種配列”又は“異種遺伝子”と呼ばれる。例えば、ハムスター細胞に導入されるハムスターアクチン遺伝子は、定義上異種遺伝子である。この異種遺伝子が対象遺伝子をコードする場合、それを“異種対象遺伝子”とも称する。
用語“プロモーター”は、それに機能的に連結された遺伝子又は配列の転写を可能にし、かつ調節するポリヌクレオチド配列を意味する。プロモーターは、RNAポリメラーゼを結合するための認識配列と、転写の開始部位(転写開始部位)とを含む。特定の細胞型又は宿主細胞内で所望の配列を発現させるためには、適切な機能性プロモーターを選択しなければならない。当業者は種々の起源由来の種々のプロモーターに精通しており、構成性プロモーター、誘発性プロモーター及び抑制性プロモーターが挙げられる。これらプロモーターは、例えばGenbankのようなデータバンクに寄託されており、商業的又は個人的供給元から単独要素として又はポリヌクレオチド配列内にクローン化された要素として入手することができる。誘発性プロモーターでは、プロモーターの活性はシグナルに応じて増減しうる。誘発性プロモーターの一例はテトラサイクリン(tet)プロモーターである。これは、テトラサイクリン調節型トランス活性化因子(tTA)によって誘導されうるテトラサイクリンオペレーター配列(tetO)を含む。テトラサイクリンの存在下でtTAのtetOへの結合が阻害される。他の誘発性プロモーターの例は、jun、fos、メタロチオネイン及び熱ショックプロモーターである(Sambrook et al., 1989; Gossen et al., 1994も参照されたい)。真核生物での高発現に特に好適なプロモーターには、例えば、ハムスターのユビキチン/S27aプロモーター(WO 97/15664)、SV40初期プロモーター、アデノウイルス主要後期プロモーター、マウスメタロチオネイン-Iプロモーター、ラウス肉腫ウイルスのLTR領域及びヒトサイトメガロウイルスの初期プロモーターがある。他の異種哺乳類プロモーターの例は、アクチン、免疫グロブリン又は熱ショックプロモーターである。
用語エンハンサーは、プロモーターの活性にシス配置で作用して、このプロモーターに機能的に連結している遺伝子の転写を刺激するポリヌクレオチドを意味する。プロモーターとは異なり、エンハンサーの効果は位置や向きに無関係なので、イントロン内又はコード領域内でさえ、転写単位の前又は後ろに位置してもよい。
エンハンサーは、転写単位のすぐ近位に位置してもよく、プロモーターからかなり離れていてもよい。プロモーターと物理的及び機能的オーバーラップを有していてもよい。当業者は、種々の起源由来の多くのエンハンサー(及びGenbankのようなデータバンクに寄託されている例えばSV40エンハンサー、CMVエンハンサー、ポリオーマエンハンサー、アデノウイルスエンハンサー)に精通しており、それらは独立した要素として、又はポリヌクレオチド配列内にクローン化された要素として入手可能である(例えば、ATCCに寄託されており或いは商業的及び個人的供給元から)。頻繁に使用されるCMVプロモーターのようないくつかのプロモーター配列はエンハンサー配列をも含む。ヒトCMVエンハンサーは、これまでに同定されている最強のエンハンサーの1つである。誘発性エンハンサーの一例は、メタロチオネインエンハンサーであり、グルココルチコイド又は重金属で刺激されうる。
用語“転写開始部位”は、一次転写物(すなわちmRNA前駆体)に組み込まれる第1核酸に相当する該構築物中の核酸を指す。転写開始部位はプロモーター配列と重なりうる。
用語“転写終止部位”は、通常は対象遺伝子の3'末端又は転写される遺伝子部分の3'末端にあり、かつRNAポリメラーゼによる転写の終了を惹起するヌクレオチド配列を意味する。
“ポリアデニル化シグナル”は、真核生物のmRNAの3'末端の特定部位での切断と、この切断した3'末端での約100〜200アデニンヌクレオチドの配列の転写後組込みを引き起こすシグナル配列である。ポリアデニル化シグナルは、切断部位の約10〜30ヌクレオチド上流の配列AATAAAと、下流に位置する配列を含む。tk polyA、SV40後期及び初期polyA又はBGH polyAのような種々のポリアデニル化要素が知られている(例えばUS 5,122,458に記載されている)。
対象遺伝子産物として、タンパク質/ポリペプチド、例えば、抗体、酵素、サイトカイン、リンホカイン、接着分子、受容体及びその派生物又はフラグメントが挙げられるが、これらに限定されない。一般的に、アゴニスト又はアンタゴニストとして作用し、及び/又は治療若しくは診断用途のあるすべてのポリペプチドは価値がある。
用語“ポリペプチド”はアミノ酸配列又はタンパク質について用いられ、いずれの長さのアミノ酸のポリマーをも指す。この用語は、グリコシル化、リン酸化、アセチル化又はタンパク質プロセシングのような反応によって、翻訳後修飾されたタンパク質をも包含する。ポリペプチドの構造は、例えば、アミノ酸の置換、欠失又は挿入によって、またその生物活性を保持しながら他のタンパク質との融合によって修飾することができる。
Fabフラグメント(フラグメント抗原結合=Fab)は、両鎖が隣接定常部で一緒に保持されている可変部から成る。Fabフラグメントは、例えばパパインのようなプロテアーゼによる処理、又はDNAクローン化によって通常の抗体から生成されうる。他の抗体フラグメントは、ペプシンによるタンパク質分解消化によって生成されうるF(ab')2である。
遺伝子クローン化によって、重鎖(VH)及び軽鎖(VL)の可変部のみから成る短縮抗体フラグメントを調製することもできる。これらはFvフラグメント(可変フラグメント(fragment variable)=可変部のフラグメント)として知られる。これらFvフラグメントでは定常鎖のシステイン基による共有結合がありえないので、何らかの他の方法で安定化されることが多い。この目的では、約10〜30アミノ酸、好ましくは15アミノ酸の短ペプチドフラグメントを用いて可変部の重鎖と軽鎖を一緒に接合する場合が多い。これによってVHとAVがペプチドリンカーで一緒に接合された単一ポリペプチド鎖が生成する。このような抗体フラグメントは単鎖Fvフラグメント(scFv)とも呼ばれる。scFv抗体の例は周知であり、また開示されており、例えば、Hustonら, 1988を参照されたい。
本技術では用語“ジアボデイ”を用いて二価のホモダイマーscFv派生物を表す。scFv分子内のペプチドリンカーを5〜10アミノ酸に短縮すると、VH/VL鎖を重ねることでホモダイマーの形成となる。ジスルフィド結合を挿入することでジアボデイをさらに安定化することができる。ジアボデイの例は文献(例えば、Perisic et al., 1994)で見出される。
本技術では用語“ミニボデイ(minibody)”を用いて二価のホモダイマーscFv派生物を表す。ミニボデイは融合タンパク質であり、二量体化領域として免疫グロブリン、好ましくはIgG、最も好ましくはIgG1のCH3領域を含む。この領域がヒンジ部(これもやはりIgGの)とリンカー部を用いてscFvフラグメントを連結する。このようなミニボデイの例は、Huら(1996)によって開示されている。
本技術では用語トリアボデイを用いて三価のホモトリマーscFv派生物を表す(Kortt et al., 1997)。リンカー配列を使用しないVH-VLの直接融合がトリマーの形成につなる。
二価、三価又は四価構造を有するミニ抗体として技術的に公知のフラグメントもscFvフラグメントの派生物である。多量体化は、二価、三価又は四価コイルドコイル構造によって達成される(Pack et al., 1993及び1995;Lovejoy et al., 1993)。
例えば細菌β-ガラクトシダーゼ、細胞表面マーカー又は蛍光タンパク質を用いて蛍光活性化セルソーティング(FACS)でトランスフェクトされた細胞を選択することもできる。蛍光タンパク質は、個々の哺乳類細胞のFACSベース単離をも可能にする。対応して検出された細胞は単一細胞又は複数細胞として、例えばレーザー(例えばアルゴンレーザー(488nm))及び例えばオートクローン装置を備えたフローサイトメーター(Coulter EPICS Altra, Beckman-Coulter, Miami, FL, USA)で培養容器に自動的に置くことができる。好ましい態様では、このようにして自家フィーダー細胞を含有する細胞培養皿に1個だけ、又は多くとも2個の細胞を置く。個々の細胞を1個だけ置くことが特に有利である。さらに、磁気ビーズを用いて選別を行うことができる。このためには、例えば、磁気ビーズに結合した抗体を用いて細胞を標識する。これにより、特異的性質で細胞を選別することができる。
ここで述べた方法の1つに従って置かれて、かつ蛍光タンパク質と対象遺伝子を共発現する細胞クローンのFACSベース単離を行うことが特に有利である。好ましくは、蛍光タンパク質と対象遺伝子の発現は、相互に機能的に連係している。このような機能的連係は、例えば、これら2つの遺伝子が一緒に近接して配置されていることから成り、それで例えば宿主細胞の過渡的又は安定的トランスフェクション後、2つの遺伝子の発現率が相互的関係をもつ。このような機能的連係は、例えば、いわゆるIRES要素(internal ribosome entry site)又はRNAスプライシングによっても得られ、2つの遺伝子(対象遺伝子と蛍光タンパク質の遺伝子)がビシストロン(bicistronic)mRNAとして合成される。このようにして蛍光タンパク質と対象遺伝子の発現率の間に直接的関係がある。蛍光タンパク質の高発現を示す対応細胞クローンは、機能的連係の結果として対象遺伝子の高い発現率をも有する。
蛍光タンパク質は、例えば、緑色、青緑色、青色、黄色又は他の色の蛍光タンパク質でよい。1つの特定例は、Aequorea victoria又はRenilla reniformisから得た緑色蛍光タンパク質(GFP)及びそれらから発生した変異体である(例えば、Bennet et al., 1998; Chalfie et al., 1994; WO 01/04306及びこれらが引用している文献を参照されたい)。他の蛍光タンパク質及びそれをコードしている遺伝子は、WO 00/34318、WO 00/34326、WO 00/34526及びWO 01/27150(参照によって本明細書に取り込まれる)に記載されている。これら蛍光タンパク質は、種花虫網(Anthozoa)、例えばAnemonia majano、Clavularia sp.、Zoanthus sp. I、Zoanthus sp. II、Discosoma striata、 Discosoma sp. "赤"、Discosoma sp. "緑"、Discosoma sp. "マゼンタ"、Anemonia sulcataの非生物発光生体の発蛍光団である。使用する蛍光タンパク質は、野生型タンパク質、天然又は遺伝子操作した変異体及び変種、それらのフラグメント派生物又は例えば他のタンパク質又はペプチドと融合した変種から成りうる。使用する突然変異は、例えば励起スペクトル又は発光スペクトル、発色団の形成、タンパク質の吸光係数又は安定性を変えうる。また、コドンの最適化によって哺乳類細胞又は他の種における発現を高めることができる。本発明により、選択可能マーカー、好ましくは例えばジヒドロ葉酸レダクターゼ(DHFR)のような増幅性選択可能マーカーとの融合でも蛍光タンパク質を使用することができる。
再クローン化細胞内で1つ以上の対象遺伝子産物を生じさせるためには、対象遺伝子の発現を可能にする条件下、血清フリー培地内及び懸濁培養で再クローン化細胞を成長させることが好ましい。例えば、対象遺伝子が構成性プロモーターの制御下にある場合、特別な誘発因子を添加する必要はない。対象遺伝子が誘発性プロモーターの制御下にある場合、例えば対応する誘発因子を十分であるが無毒の濃度で細胞培地に添加しなければならない。複数回の継代によって細胞を所望どおりに増やして適切な細胞培養容器に移すことができる。遺伝子細胞は、細胞性産物、膜結合産物又は分泌産物として生成される。
また、再クローン化哺乳類細胞内で1種以上の組換え産物の生産に対応する方法であって、哺乳類細胞がハムスター細胞又はマウス骨髄腫細胞、好ましくはCHO、BHK又はNS0、及びこれら細胞系の派生物/子孫である、方法が好ましい。この方法の別の態様は、フィーダー細胞を血清フリー培地に適応させ、かつフィーダー細胞は非付着性培養細胞であることを特徴とする。また、上記生産方法の関係では、置かれる被複製/クローン化哺乳類細胞がCHO又はBHK細胞の場合、フィーダー細胞としてハムスター細胞を使用し、置かれる被複製/クローン化哺乳類細胞がNS0細胞の場合、フィーダー細胞としてマウス骨髄腫細胞を使用することが好ましい。特に好ましくは、置かれる被複製/クローン化哺乳類細胞がCHO細胞の場合、フィーダー細胞としてCHO細胞を使用し、置かれる被複製/クローン化哺乳類細胞がBHK細胞の場合、フィーダー細胞としてBHK細胞を使用し、置かれる被複製/クローン化哺乳類細胞がNS0細胞の場合、フィーダー細胞としてNS0細胞を使用する方法である。
他の好ましい組成物は、分裂可能な哺乳類細胞がCHO若しくはBHK細胞又はその派生物/子孫の場合、フィーダー細胞としてハムスター細胞、好ましくはキヌゲネズミ亜科の細胞、最も好ましくはCricetulus属又はMesocricetus属の細胞を含む。また、別の好ましい組成物は、分裂可能な哺乳類細胞がマウス骨髄腫細胞、好ましくはNS0又はその派生物/子孫の場合、フィーダー細胞としてマウス細胞、好ましくはMurinae亜科、最も好ましくは属Musの細胞を含む。特に好ましい組成物は、分裂可能な哺乳類細胞がCHO細胞の場合、フィーダー細胞としてCHO細胞を含み、分裂可能な哺乳類細胞がBHK細胞の場合、フィーダー細胞としてBHK細胞を含み、分裂可能な哺乳類細胞がNS0細胞の場合、フィーダー細胞としてNS0細胞を含むことを特徴とする。
理論的に、本発明は、5個未満、好ましくは4、3、2又は1個の生産関連ハムスター細胞(例えばCHO又はBHK細胞のような)及び生産関連マウス骨髄腫細胞(例えばNS0細胞のような)を、血清フリー条件下、哺乳類由来のフィーダー細胞の存在下で置いて複製できる組成物にも関する。
〔略語〕
ATCC 米国菌培養収集所(American Type Culture Collection)
BHK ベビーハムスター腎臓(Baby Hamster Kidney)
60Co コバルト同位元素60
137Cs セシウム同位元素137
CHO チャイニーズハムスター卵巣
CMV サイトメガロウイルス
DE 独国
DEAE ジエチルアミノエチル
DMSO ジメチルスルホキシド
DNA デオキシリボ核酸
FACS 蛍光活性化セルソーター
FITC フルオレッセイン-イソチオシアネート
Gy グレイ(Gray)
HBSS ハンクス液(Hank's balanced salt solution)
HPLC 高速液体クロマトグラフィー
mRNA メッセンジャーリボ核酸
NS0 マウスハイブリドーマ細胞
polyA ポリアデニル化配列
Sp2/0 マウスハイブリドーマ細胞
SV40 サルウイルス No.40
1.細胞培養
細胞CHO-DG44/dhfr-/-(Urlaub et al., 1983)を湿り大気及び5%のCO2中37℃で培養フラスコ内でヒポキサンチン及びチミジンで補充した血清フリーCHO-S-SFMII培地(Invitrogen GmbH, Karlsruhe, DE)中、懸濁細胞として持続的に培養した。CEDEX Cell Counter(Innovatis, DE)又はトリプタンブルー染色で細胞の数と生存度を測定してから細胞を1〜3×105/mLの濃度で播き、2〜3日毎に継代した。単一細胞クローン化のため、蛍光タンパク質(例えばZoanthus sp.由来のZS-Green)又は蛍光タンパク質とヒト若しくはヒト化モノクロナール抗体を発現する組換えCHO-DG44/dhfr-/-を使用した。これら細胞と同様にクローン化組換え細胞を培養した。使用した培地はやはりCHO-S-SFMII培地(Invitrogen GmbH, Karlsruhe, DE)であるが、ヒポキサンチン及びチミジンなしである。
BHK細胞は、湿り大気中5%のCO2下37℃で培養フラスコ内で血清フリーOpti Pro SFM培地(Invitrogen GmbH, Karlsruhe, DE)中、懸濁培養としてを持続的に培養できる。CEDEX Cell Counter(Innovatis, DE)又はトリプタンブルー染色で細胞の数と生存度を測定でき、次いで細胞を1〜3×105/mLの濃度で播き、2〜3日毎に継代する。BHK細胞と同様にクローン化細胞を培養する。
NS0細胞は、湿り大気中5%のCO2下37℃で培養フラスコ内で血清フリーハイブリドーマ培地(Sigma, Aldrich, St. Louis, USA)中、懸濁培養としてを持続的に培養できる。CEDEX Cell Counter(Innovatis, DE)又はトリプタンブルー染色で細胞の数と生存度を測定でき、次いで細胞を1〜3×105/mLの濃度で播き、2〜3日毎に継代する。NS0細胞と同様にクローン化細胞を培養する。培地としてハイブリドーマ培地、動物成分フリー培地(Sigma, Aldrich, St. Louis, USA)を使用する。
血清フリーかつタンパク質フリーで成長する懸濁CHO基本細胞(非トランスフェクト細胞)を10分間180gで遠心分離し、HBSS(ハンクス液)中1×106/mlの細胞濃度に調整した。
次に、4Gy/分のエネルギー線量出力の放射性照射源(Cs137ラジエーター,Gammacell 2000, Messrs Molsgaard Medical A/S, Denmark)で細胞を照射した。5分〜125分の照射時間で20〜500Gyのエネルギー線量が得られた。照射後、この細胞に特異的なCHO-S-SFMII培地に約2000細胞/ウェル(=培養容器)の割合で96-ウェルマイクロタイタープレートに細胞を播き、インキュベートチャンバー雰囲気内約37℃かつ5%のCO2で貯蔵した。この方法をBHK及びNS0細胞について同様に行い、該細胞に特異的な培地でフィーダー細胞を維持又は播種した。
このようにして製造したフィーダー細胞は-150℃未満で凍結保存することができる。凍結保存はプログラム制御可能フリーザー(Consarctic BV25, Consarctic, Schollkrippen, DE)を用いて問題の細胞培地内で行う。凍結保護剤として10%(v/v)DMSOを培地に添加する。凍結速度1℃/分で0℃〜-20℃に下げ、0.4℃/分で温度をさらに下げる。凍結が完了したら、気相内、液体窒素中でフィーダー細胞を凍結保存する。
4.自動化された、細胞を置くこと(automated cell deposition)
アルゴンレーザー(488nm)を備えたフローサイトメーター(Coulter EPICS Altra (Messrs Beckman-Coulter, Miami, FL, US))でオートクローン装置を用いて細胞を自動的に置くこと(単数又は複数個)を行う。指数的成長期の間、細胞を遠心分離機にかけ、HBSSに取り、細胞濃度を1〜1.5×107/mlにする。次に“ハイパーソートオプション”を用いて散乱光内の細胞の位置に応じて8000〜12000細胞/秒の速度で細胞を選別する。代わりに、蛍光タンパク質を発現する細胞は、細胞内発現した蛍光タンパク質の関係でその蛍光強度によって選別することができる。フィーダー細胞を含有する96-ウェルマイクロタイタープレートに細胞を1個ずつ置く。例えばBHK細胞はOptiPro SFM培地(Invitrogen GmbH, Karlsruhe, DE)に置く。選別されたNS0細胞を例えばハイブリドーマ培地、動物成分フリー培地(Sigma, Aldrich, St. Louis, USA)に置く。
CHO細胞の選別ではCHO-S-SFM-II(Invitrogen GmbH, Karlsruhe, DE)に細胞を置いた。ヒト又はヒト化モノクロナール抗体及びZoanthus sp.由来のZSグリーンを共発現する組換えCHO-DG-44細胞を置いた。細胞選別は、上述したように488nmのアルゴンレーザーで行った。
5.組換え発現遺伝子産物の生産性の決定(mAb-発現CHO-DGH-44を使用した場合)
安定してトランスフェクトされたCHO-DG-44細胞(ヒト又はヒト化モノクロナール抗体を発現する)の上清の抗体タイターは、一方でヤギ抗-ヒトIgG Fcフラグメント(Dianova, Hamburg, DE)を用い、他方でAP-抱合ヤギ抗-ヒトκ軽鎖抗体(Sigma)を用いて標準的方法(Ausubel et al., 1994, updated)に従ってELISAで定量した。精製抗体を標準物質として用いた。式pg/((CtCo)t/ln(CtCo))(式中、Co及びCtは播種時又は収集時の細胞数を表し、tは培養時間を示す)に従って生産性(pg/細胞/日)を計算した。
再クローン化効率に及ぼすフィーダー細胞生産中のエネルギー線量の影響を調べるため、方法“細胞の培養”で述べたようにCHO-DG-44細胞を成長させた。方法“照射によるフィーダー細胞の調製”で述べたように、20Gy、50Gy、100Gy、200Gy及び500Gyのエネルギー線量で照射してフィーダー細胞を調製した。照射後、約2000細胞/ウェルの細胞数で96-ウェルマイクロタイタープレートにフィーダー細胞を播いた。次に、方法“自動化された、単一細胞を置くこと”で述べたように、蛍光タンパク質を発現する組換えCHO-DG-44細胞により、単一細胞を自動的に置くことを行った。各ウェルのフィーダー細胞上に1個の細胞を置いた。再クローン化効率の目標値は、ポジティブウェル、すなわちクローンが成長して3週間のインキュベーション期間後に細胞集団を形成したウェルの数だった。達成された再クローン化効率は、組換えCHO-DG-44細胞の再クローン化で40〜70%だった(図1参照)。
細胞クローンの均質性を比較するため、一方では標準的な“限界希釈”法で組換え抗体発現CHO-DG-44細胞を置いてクローン化し、他方では自家フィーダー細胞の存在下、本明細書で述べた単一細胞を置く方法で置いてクローン化した(図2参照)。このため、限界希釈法で、トランスフェクトされた抗体発現CHO-DG-44細胞の6つの細胞プールを培養し、並行して“細胞の培養”で述べたように自動的に単一細胞を置いた後、“自動化された単一細胞を置くこと”で述べたように細胞をクローン化した。このようにして生成されたクローンを“細胞の培養”で述べたように培養し、方法“組換え発現遺伝子産物の生産性の決定”によって3回の継代の過程にわたって産物タイターを決定した。これら3回の継代で得られた平均を用いてグラフにプロットした。
産物遺伝子(組換え抗体)と蛍光タンパク質(Zoanthus sp.由来のZSグリーン)というビシストロン発現をコードする発現ベクターでCHO DG44細胞をトランスフェクトすることによって、前記抗体と前記蛍光タンパク質を両方とも共発現する細胞プールを得た。上述した方法で、自家性CHO DG44フィーダー細胞の存在下、マイクロタイタープレートにこれら細胞を個々に置いて培養した。次の3つの異なる基準でクローンを置くことを行った。
A.)すべての生きている細胞を置く
B.)20%の最も強い蛍光性細胞を置く
C.)5%の最も強い蛍光性細胞を置く
次に、“細胞の培養”で述べたように、得られたクローンを24-ウェルマクロタイタープレートに移して3回の継代で培養した。各継代の最後に、“組換え発現遺伝子産物の生産性の決定”で述べた方法で上清中の抗体のタイターを決定した。これら3回の継代から得られた平均値を用いてグラフにプロットした。これを行うため、指定タイターカテゴリーにわたって得られたクローン数をプロットし、正規分布に調和させた。
Ausubel, F.M. et al., Current Protocols in molecular biology. New York: Greene Publishing Associates and Wiley-Interscience. 1994 (updated)
Bennett, R.P. et al., BioTechniques 1998, 24, 478 - 482
Brodin et al., Journal of Immunological Methods, 1988, 2, 245-251
Butcher et al., Journal of Immunological Methods, 1988, 107, 245-251
Chalfie, M. et al., Science 1994, 263, 802 - 805
Chamov, S.M. et al., Antibody Fusion Proteins, Wiley-Liss Inc., 1999
Freshney RI, (eds.), Animal cell culture: A Practical Approach, IRL Press, Oxford 1986
Gossen, M. et al., Curr Opi Biotech 1994, 5, 516 - 520
Grigoriev et al., Analytical Biochemistry, 1996, 236, 250-254
Harris et al., Protein Purification: A Practical Approach, Pickwood and Hames, eds., IRL Press, Oxford, 1995
Hlinak A. et al., Folia Biologica (Praha) 1987, 34, 105.117
Hu, S. et al., Cancer Res. 1996, 56 (13), 3055 - 3061
Huston, C. et al., Proc Natl Acad Sci USA 1988, 85 (16), 5879 - 5883
Kaufmann H. et al., Biotechnology and Bioengineering 2001, 72, 592-602
Kortt, A.A. et al., Protein Engineering 1997, 10 (4), 423 - 433
Long et al., Journal of Immunological Methods, 1986, 86, 89-93
Lovejoy, B. et al., Science 1993, 259, 1288 - 1293
Meng YG., et al., Gene 2000, 242, 201-207
Morgan (eds.), Kultur tierischer Zellen, Spektrum Akademischer Verlag, Heidelberg, 1994
Mueller et al., Biotechnology and Bioengineering 1999, 65, 529532
Pack, P. et al., Biotechnology 1993, 11, 1271 1277
Pack, P. et al., J Mol Biol 1995, 246 (11), 28 - 34
Peng et al., Biotechnology and Bioengineering, 1996, 50, 479-492
Perisic, O. et al., Structure 1994, 2, 1217 - 1226
Pintus et al., Journal of Immunological Methods, 1983, 61, 195-200
Puck, TT et al., J Exp Med 1958, 108, 945 - 956
Rexroad et al., Molecular Reproduction and Development, 1997, 48, 238-245
Rheinwald, JG and Green, Cell 1975, 6, 331-344
Sambrook, J., Fritsch, E.F. & Maniatis, T.,Molecular Cloning: A Laboratory Manual Cold Spring Harbor Laboratory, Cold Spring Harbor, New York, 1989
Sanchez et al., Journal of Imunological Methods, 1991, 145, 193-197
Scopes, R., Protein Purification, Springer Verlag, 1988
Shapiro, Practical Flow Cytometry, 1995, John Wiley and Sons, Inc., New York, 3rd. edition
Shneyour et al., Plant Science Letters, 1984, 33, 293-302
Strick-Marchand et al., Mechanisms of Development, 2003, 120, 89-98
Urlaub, G. et al., Cell 1983, 33, 405 412
Wee Eng Lim et al., Proteomics 2002, 2, 1187-1203
Williams RL., et al., Nature 1988, 336, 684-687
Claims (14)
- CHO細胞のクローン化方法であって、
血清フリー条件下、放射線を照射したCHO細胞の存在下、培養容器に5個未満のCHO細胞を置き、血清フリー条件下で培養かつ複製すること、
置かれたCHO細胞を血清フリー懸濁培養で複製すること、
放射線を照射したCHO細胞が、血清フリー培地に適応した非付着性培養細胞であること、及び
置かれたCHO細胞の再クローン化の間、再クローン化効率が10%乃至65%より高いこと
を特徴とする方法。 - 血清フリー条件下、培養容器に1又は2個だけのCHO細胞を置き、血清フリー条件下、放射線を照射したCHO細胞の存在下で培養かつ複製することを特徴とする請求項1記載の方法。
- 血清フリー条件下、放射線を照射したCHO細胞の存在下、培養容器に1個の単一CHO細胞を置き、血清フリー条件下で培養かつ複製することを特徴とする請求項1記載の方法。
- 置かれたCHO細胞を、培地1ml当たり100〜200,000個の放射線を照射したCHO細胞の存在下で複製することを特徴とする請求項1〜3のいずれか1項に記載の方法。
- 置かれたCHO細胞を、培地1ml当たり4×106個の細胞密度まで培養かつ複製することを特徴とする請求項1〜4のいずれか1項に記載の方法。
- 血清フリー条件下、CHO細胞内でタンパク質を生産する方法であって、
(a)CHO細胞が、対象タンパク質をコードする対象遺伝子を含み;
(b)前記CHO細胞の複製を許容する血清フリー条件下で該CHO細胞を成長させ;
(c)血清フリー条件下、細胞培養容器に、各場合5個未満の前記CHO細胞を置き;
(d)適切に置かれたCHO細胞を、血清フリー懸濁条件下、放射線を照射したCHO細胞の存在下で複製し、ここで、該放射線を照射したCHO細胞が、血清フリー培地に適応した非付着性培養細胞であり;
(e)複製した細胞を、前記対象遺伝子が発現する血清フリー条件下で培養し;かつ
(f)膜を含む前記細胞又は培養上清から遺伝子産物を単離して精製する;
ことを特徴とする方法。 - 血清フリー条件下、CHO細胞内で組換えタンパク質を調製する方法であって、
(a)対象タンパク質をコードする対象遺伝子でCHO細胞をトランスフェクトし;
(b)このトランスフェクトされた細胞の複製を許容する血清フリー条件下で前記トランスフェクトされたCHO細胞を成長させ;
(c)血清フリー条件下、放射線を照射したCHO細胞のある細胞培養容器に、各場合5個未満の前記トランスフェクトされたCHO細胞を置き;
(d)置かれた細胞を、血清フリー懸濁条件下、放射線を照射したCHO細胞の存在下で複製し、ここで、該放射線を照射したCHO細胞が、血清フリー培地に適応した非付着性培養細胞であり;
(e)この複製された細胞を、前記対象遺伝子が発現する血清フリー条件下で成長させ;かつ
(f)前記細胞又は培養上清から遺伝子産物を単離して精製する;
ことを特徴とする方法。 - 前記ポイント(c)において、1個だけの単一CHO細胞を各細胞培養容器に置くことを特徴とする請求項6又は7記載の方法。
- 前記置かれたCHO細胞がさらに蛍光タンパク質をコードしており、かつ、この置かれたCHO細胞を血清フリー条件下、細胞培養容器に、FACSベースセルソーティングで置くことを特徴とする請求項6〜8のいずれか1項に記載の方法。
- ソートして置かれたCHO細胞を、培地1ml当たり100〜200,000個の放射線を照射したCHO細胞の存在下で複製することを特徴とする請求項6〜9のいずれか1項に記載の方法。
- ソートして置かれたCHO細胞を、培地1ml当たり4×106個の細胞密度まで培養することを特徴とする請求項6〜10のいずれか1項に記載の方法。
- 血清フリー懸濁条件下でのCHO細胞のクローン化におけるフィーダー細胞としての放射線を照射したCHO細胞の使用であって、該放射線を照射したCHO細胞が、血清フリー培地に適応した非付着性培養細胞である、使用。
- 血清フリー細胞培地と、5個未満の分裂可能なCHO細胞と、放射線を照射したCHO細胞であり、かつ、血清フリー培地に適応した非付着性培養細胞であるフィーダー細胞とから成る組成物。
- 該組成物が、前記培地中に1又は2個だけの分裂可能なCHO細胞を含有する、請求項13記載の組成物。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE10338531.2 | 2003-08-19 | ||
| DE10338531A DE10338531A1 (de) | 2003-08-19 | 2003-08-19 | Verfahren zur Reklonierung von Produktionszellen |
| PCT/EP2004/009204 WO2005019442A2 (de) | 2003-08-19 | 2004-08-17 | Verfahren zur reklonierung von produktionszellen |
Publications (4)
| Publication Number | Publication Date |
|---|---|
| JP2007502608A JP2007502608A (ja) | 2007-02-15 |
| JP2007502608A6 JP2007502608A6 (ja) | 2007-05-10 |
| JP2007502608A5 JP2007502608A5 (ja) | 2007-10-04 |
| JP5129959B2 true JP5129959B2 (ja) | 2013-01-30 |
Family
ID=34201814
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2006523593A Expired - Fee Related JP5129959B2 (ja) | 2003-08-19 | 2004-08-17 | 生産細胞の再クローン化方法 |
Country Status (11)
| Country | Link |
|---|---|
| US (1) | US7833787B2 (ja) |
| EP (2) | EP1658365B1 (ja) |
| JP (1) | JP5129959B2 (ja) |
| KR (1) | KR101184572B1 (ja) |
| AT (2) | ATE515565T1 (ja) |
| CA (1) | CA2536239C (ja) |
| DE (2) | DE10338531A1 (ja) |
| DK (2) | DK1658365T3 (ja) |
| ES (2) | ES2368772T3 (ja) |
| TW (1) | TWI337201B (ja) |
| WO (1) | WO2005019442A2 (ja) |
Families Citing this family (40)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20060223183A1 (en) * | 2005-03-11 | 2006-10-05 | Bates Steven E | Gamma irradiation of frozen feeder cells |
| WO2008031873A1 (en) * | 2006-09-15 | 2008-03-20 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | Methods of selecting cell clones |
| EP1901068A1 (en) * | 2006-09-15 | 2008-03-19 | Boehringer Ingelheim Pharma GmbH & Co. KG | Methods of selecting cell clones |
| WO2009115495A1 (de) * | 2008-03-19 | 2009-09-24 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | Methode zur steigerung der reklonierungseffizienz |
| JP5304275B2 (ja) * | 2009-01-29 | 2013-10-02 | Jnc株式会社 | アポクライティン−iiをコードするコドン最適化核酸およびその使用方法 |
| HUE045635T2 (hu) | 2009-04-09 | 2020-01-28 | Sartorius Stedim Cellca Gmbh | Eljárás továbbfejlesztett egysejtes klónozásra |
| JP5697042B2 (ja) | 2009-11-19 | 2015-04-08 | 国立大学法人 岡山大学 | 遺伝子発現を上昇させるシステム及び該システムを保持したベクター |
| AU2012328530A1 (en) | 2011-10-28 | 2014-06-26 | Prothena Biosciences Limited | Humanized antibodies that recognize alpha-synuclein |
| EP2807188B1 (en) | 2012-01-27 | 2019-09-11 | Prothena Biosciences Limited | Humanized antibodies that recognize alpha-synuclein |
| UA118441C2 (uk) | 2012-10-08 | 2019-01-25 | Протена Біосаєнсиз Лімітед | Антитіло, що розпізнає альфа-синуклеїн |
| SG10201707855YA (en) | 2013-03-13 | 2017-10-30 | Prothena Biosciences Ltd | Tau immunotherapy |
| US10513555B2 (en) | 2013-07-04 | 2019-12-24 | Prothena Biosciences Limited | Antibody formulations and methods |
| WO2015004633A1 (en) | 2013-07-12 | 2015-01-15 | Neotope Biosciences Limited | Antibodies that recognize islet-amyloid polypeptide (iapp) |
| WO2015004632A1 (en) | 2013-07-12 | 2015-01-15 | Neotope Biosciences Limited | Antibodies that recognize iapp |
| WO2015075635A2 (en) | 2013-11-19 | 2015-05-28 | Prothena Biosciences Limited | Monitoring immunotherapy of lewy body disease from constipation symptoms |
| ES2744526T3 (es) | 2014-03-12 | 2020-02-25 | Prothena Biosciences Ltd | Anticuerpos anti-MCAM y métodos de uso asociados |
| JP2017514458A (ja) | 2014-03-12 | 2017-06-08 | プロセナ バイオサイエンシーズ リミテッド | Lg4−5に対して特異的な抗−ラミニン4抗体 |
| TW201623331A (zh) | 2014-03-12 | 2016-07-01 | 普羅帝納生物科學公司 | 抗黑色素瘤細胞黏著分子(mcam)抗體類及使用彼等之相關方法 |
| US20170158755A1 (en) | 2014-03-12 | 2017-06-08 | Prothena Biosciences Limited | Anti-laminin4 antibodies specific for lg1-3 |
| CA2944402A1 (en) | 2014-04-08 | 2015-10-15 | Prothena Biosciences Limited | Blood-brain barrier shuttles containing antibodies recognizing alpha-synuclein |
| TWI718121B (zh) | 2015-01-28 | 2021-02-11 | 愛爾蘭商普羅佘納生物科技有限公司 | 抗甲狀腺素運送蛋白抗體 |
| TWI769570B (zh) | 2015-01-28 | 2022-07-01 | 愛爾蘭商普羅佘納生物科技有限公司 | 抗甲狀腺素運送蛋白抗體 |
| TWI786505B (zh) | 2015-01-28 | 2022-12-11 | 愛爾蘭商普羅佘納生物科技有限公司 | 抗甲狀腺素運送蛋白抗體 |
| WO2017046774A2 (en) | 2015-09-16 | 2017-03-23 | Prothena Biosciences Limited | Use of anti-mcam antibodies for treatment or prophylaxis of giant cell arteritis, polymyalgia rheumatica or takayasu's arteritis |
| EP3350226A2 (en) | 2015-09-16 | 2018-07-25 | Prothena Biosciences Limited | Use of anti-mcam antibodies for treatment or prophylaxis of giant cell arteritis, polymyalgia rheumatica or takayasu's arteritis |
| WO2017149513A1 (en) | 2016-03-03 | 2017-09-08 | Prothena Biosciences Limited | Anti-mcam antibodies and associated methods of use |
| WO2017153955A1 (en) | 2016-03-09 | 2017-09-14 | Prothena Biosciences Limited | Use of anti-mcam antibodies for treatment or prophylaxis of granulomatous lung diseases |
| WO2017153953A1 (en) | 2016-03-09 | 2017-09-14 | Prothena Biosciences Limited | Use of anti-mcam antibodies for treatment or prophylaxis of granulomatous lung diseases |
| BR112018072394A2 (pt) | 2016-05-02 | 2019-02-19 | Prothena Biosciences Limited | anticorpos que reconhecem a tau |
| EP3452508A1 (en) | 2016-05-02 | 2019-03-13 | Prothena Biosciences Limited | Antibodies recognizing tau |
| CA3022673A1 (en) | 2016-05-02 | 2017-11-09 | Prothena Biosciences Limited | Tau immunotherapy |
| WO2017208210A1 (en) | 2016-06-03 | 2017-12-07 | Prothena Biosciences Limited | Anti-mcam antibodies and associated methods of use |
| JP7016470B2 (ja) | 2016-07-02 | 2022-02-07 | プロセナ バイオサイエンシーズ リミテッド | 抗トランスサイレチン抗体 |
| JP7076711B2 (ja) | 2016-07-02 | 2022-05-30 | プロセナ バイオサイエンシーズ リミテッド | 抗トランスサイレチン抗体 |
| WO2018007924A2 (en) | 2016-07-02 | 2018-01-11 | Prothena Biosciences Limited | Anti-transthyretin antibodies |
| IL270375B1 (en) | 2017-05-02 | 2024-08-01 | Prothena Biosciences Ltd | Antibodies that recognize tau |
| CA3076313A1 (en) | 2017-09-28 | 2019-04-04 | Prothena Biosciences Limited | Dosing regimes for treatment of synucleinopathies |
| WO2020112687A2 (en) | 2018-11-26 | 2020-06-04 | Forty Seven, Inc. | Humanized antibodies against c-kit |
| TW202100550A (zh) | 2019-03-03 | 2021-01-01 | 愛爾蘭商普羅帝納生物科學公司 | 識別tau之抗體 |
| IL299329A (en) | 2020-06-24 | 2023-02-01 | Prothena Biosciences Ltd | Antibodies recognizing sortilin |
Family Cites Families (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE3584341D1 (de) | 1984-08-24 | 1991-11-14 | Upjohn Co | Rekombinante dna-verbindungen und expression von polypeptiden wie tpa. |
| US5008198A (en) | 1984-09-14 | 1991-04-16 | Scripps Clinic And Research Foundation | Merozoite surface glycoproteins |
| EP0557459B1 (en) | 1990-11-13 | 1997-10-22 | Immunex Corporation | Bifunctional selectable fusion genes |
| US5459058A (en) * | 1991-03-28 | 1995-10-17 | Benjamin Rich | Cell culture system |
| EP0804590A1 (en) | 1993-05-21 | 1997-11-05 | Targeted Genetics Corporation | Bifunctional selectable fusion genes based on the cytosine deaminase (cd) gene |
| DE19539493A1 (de) | 1995-10-24 | 1997-04-30 | Thomae Gmbh Dr K | Starker homologer Promotor aus Hamster |
| SK286870B6 (sk) | 1998-04-17 | 2009-06-05 | Soci�T� Des Produits Nestl� S.A. | Ľudská keratinocytová bunková línia, in vitro spôsob imortalizácie ľudských kožných buniek, použitie ľudskej bunkovej línie a umelá koža s jej obsahom |
| WO2000034325A1 (en) | 1998-12-11 | 2000-06-15 | Clontech Laboratories, Inc. | Fluorescent proteins from non-bioluminescent species of class anthozoa, genes encoding such proteins and uses thereof |
| WO2000034326A1 (en) | 1998-12-11 | 2000-06-15 | Clontech Laboratories, Inc. | Fluorescent proteins from non-bioluminescent species of class anthozoa, genes encoding such proteins and uses thereof |
| ES2361971T3 (es) | 1998-12-11 | 2011-06-24 | Clontech Laboratories Inc. | Proteínas fluorescentes de especies sin bioluminiscencia de la clase de los antozoos, genes codificantes de tales proteínas y sus usos. |
| WO2001004306A1 (en) | 1999-07-12 | 2001-01-18 | Genentech, Inc. | Expression vectors and methods |
| WO2001011021A1 (de) * | 1999-08-05 | 2001-02-15 | Baxter Aktiengesellschaft | Rekombinanter stabiler zellklon, seine herstellung und verwendung |
| US7456017B2 (en) * | 1999-10-01 | 2008-11-25 | University Of North Carolina At Chapel Hill | Processes for clonal growth of hepatic progenitor cells |
| JP2003527833A (ja) | 1999-10-14 | 2003-09-24 | クロンテック・ラボラトリーズ・インコーポレーテッド | 花虫類に由来する発色団/蛍光体、およびそれらの使用法 |
| CA2424779C (en) * | 2000-10-03 | 2016-08-23 | University Of North Carolina At Chapel Hill | Processes for clonal growth of hepatic progenitor cells |
| US20030073234A1 (en) * | 2001-10-12 | 2003-04-17 | Michal Amit | Clonal human embryonic stem cell lines and methods of generating same |
-
2003
- 2003-08-19 DE DE10338531A patent/DE10338531A1/de not_active Ceased
-
2004
- 2004-08-17 CA CA2536239A patent/CA2536239C/en not_active Expired - Fee Related
- 2004-08-17 ES ES08151018T patent/ES2368772T3/es not_active Expired - Lifetime
- 2004-08-17 JP JP2006523593A patent/JP5129959B2/ja not_active Expired - Fee Related
- 2004-08-17 EP EP04764194A patent/EP1658365B1/de not_active Expired - Lifetime
- 2004-08-17 DK DK04764194T patent/DK1658365T3/da active
- 2004-08-17 EP EP08151018A patent/EP1918364B1/de not_active Expired - Lifetime
- 2004-08-17 ES ES04764194T patent/ES2317023T3/es not_active Expired - Lifetime
- 2004-08-17 KR KR1020067003371A patent/KR101184572B1/ko not_active IP Right Cessation
- 2004-08-17 AT AT08151018T patent/ATE515565T1/de active
- 2004-08-17 WO PCT/EP2004/009204 patent/WO2005019442A2/de active Application Filing
- 2004-08-17 DE DE502004008542T patent/DE502004008542D1/de not_active Expired - Lifetime
- 2004-08-17 AT AT04764194T patent/ATE415471T1/de active
- 2004-08-17 DK DK08151018.2T patent/DK1918364T3/da active
- 2004-08-18 TW TW093124872A patent/TWI337201B/zh not_active IP Right Cessation
- 2004-08-19 US US10/922,577 patent/US7833787B2/en not_active Expired - Lifetime
Also Published As
| Publication number | Publication date |
|---|---|
| EP1918364B1 (de) | 2011-07-06 |
| WO2005019442A2 (de) | 2005-03-03 |
| EP1918364A3 (de) | 2008-05-14 |
| ATE415471T1 (de) | 2008-12-15 |
| TWI337201B (en) | 2011-02-11 |
| WO2005019442A3 (de) | 2005-10-06 |
| EP1918364A2 (de) | 2008-05-07 |
| CA2536239A1 (en) | 2005-03-03 |
| EP1658365B1 (de) | 2008-11-26 |
| ES2317023T3 (es) | 2009-04-16 |
| US20050059146A1 (en) | 2005-03-17 |
| US7833787B2 (en) | 2010-11-16 |
| JP2007502608A (ja) | 2007-02-15 |
| ES2368772T3 (es) | 2011-11-22 |
| CA2536239C (en) | 2014-05-27 |
| ATE515565T1 (de) | 2011-07-15 |
| DK1918364T3 (da) | 2011-08-29 |
| EP1658365A2 (de) | 2006-05-24 |
| DK1658365T3 (da) | 2009-02-02 |
| KR20060065706A (ko) | 2006-06-14 |
| DE502004008542D1 (de) | 2009-01-08 |
| KR101184572B1 (ko) | 2012-09-21 |
| DE10338531A1 (de) | 2005-04-07 |
| TW200516148A (en) | 2005-05-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5129959B2 (ja) | 生産細胞の再クローン化方法 | |
| JP2007502608A6 (ja) | 生産細胞の再クローン化方法 | |
| CA2616799C (en) | Improved methods and compositions for increasing longevity and protein yield from a cell culture | |
| US20140308703A1 (en) | Mammalian Cell Lines for Increasing Longevity and Protein Yield from a Cell Culture | |
| US20020098551A1 (en) | Production of multimeric protein by cell fusion method | |
| JP7344949B2 (ja) | グルタミンシンセターゼ遺伝子内相補ベクターを用いた高レベルのヘテロマータンパク質発現細胞の直接選択 | |
| US9657310B2 (en) | Expression vector | |
| CN105378071B (zh) | 用于产生稳定转染细胞的方法和组合物 | |
| CN106170554B (zh) | 过表达n-糖基化途径调节基因以调节重组蛋白的糖基化 | |
| US7604989B2 (en) | Inhibition of apoptosis process and improvement of cell performance | |
| JP2017501749A (ja) | 組換えタンパク質の高マンノースグリコフォーム含有量を操作するためのオルニチン代謝の調節 | |
| JP2012525826A (ja) | Cho/cert細胞系 | |
| US8669109B2 (en) | Methods of producing proteins in Chinese hamster ovary (CHO) cells | |
| JP2006507829A (ja) | 発現ベクター、異種遺伝子生成物の製造方法およびこのような生成物を高濃度で製造する組換え細胞の選別方法 | |
| JP2008520250A (ja) | 哺乳動物細胞を生成するための方法 | |
| US8597909B2 (en) | Use of HSA-producing cells | |
| US8563303B2 (en) | Method for increasing recloning efficiency | |
| WO2023180398A1 (en) | Bacterial glutamine synthetase as selection marker in mammalian cells | |
| TW200907062A (en) | Methods of gene amplification and expression | |
| EA043386B1 (ru) | Прямой отбор клеток, экспрессирующих высокие уровни гетеромерных белков, с использованием глутаминсинтетазных векторов внутригенной комплементации | |
| EA047078B1 (ru) | Сверхэкспрессия регуляторов пути n-гликозилирования для модуляции гликозилирования рекомбинантных белков |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20070816 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20070816 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20100510 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20100806 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20100813 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20101110 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20110912 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20111202 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20111209 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20111227 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20120110 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20120210 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20120217 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120312 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20121009 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20121105 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20151109 Year of fee payment: 3 |
|
| LAPS | Cancellation because of no payment of annual fees |