JP5044398B2 - 固形製剤 - Google Patents
固形製剤 Download PDFInfo
- Publication number
- JP5044398B2 JP5044398B2 JP2007520212A JP2007520212A JP5044398B2 JP 5044398 B2 JP5044398 B2 JP 5044398B2 JP 2007520212 A JP2007520212 A JP 2007520212A JP 2007520212 A JP2007520212 A JP 2007520212A JP 5044398 B2 JP5044398 B2 JP 5044398B2
- Authority
- JP
- Japan
- Prior art keywords
- solid preparation
- tablet
- powder
- trade name
- mixed
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/16—Agglomerates; Granulates; Microbeadlets ; Microspheres; Pellets; Solid products obtained by spray drying, spray freeze drying, spray congealing,(multiple) emulsion solvent evaporation or extraction
- A61K9/1605—Excipients; Inactive ingredients
- A61K9/1617—Organic compounds, e.g. phospholipids, fats
- A61K9/1623—Sugars or sugar alcohols, e.g. lactose; Derivatives thereof; Homeopathic globules
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2095—Tabletting processes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
- A61K31/536—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines ortho- or peri-condensed with carbocyclic ring systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/16—Agglomerates; Granulates; Microbeadlets ; Microspheres; Pellets; Solid products obtained by spray drying, spray freeze drying, spray congealing,(multiple) emulsion solvent evaporation or extraction
- A61K9/1605—Excipients; Inactive ingredients
- A61K9/1629—Organic macromolecular compounds
- A61K9/1652—Polysaccharides, e.g. alginate, cellulose derivatives; Cyclodextrin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2009—Inorganic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2013—Organic compounds, e.g. phospholipids, fats
- A61K9/2018—Sugars, or sugar alcohols, e.g. lactose, mannitol; Derivatives thereof, e.g. polysorbates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2022—Organic macromolecular compounds
- A61K9/205—Polysaccharides, e.g. alginate, gums; Cyclodextrin
- A61K9/2054—Cellulose; Cellulose derivatives, e.g. hydroxypropyl methylcellulose
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2072—Pills, tablets, discs, rods characterised by shape, structure or size; Tablets with holes, special break lines or identification marks; Partially coated tablets; Disintegrating flat shaped forms
- A61K9/2077—Tablets comprising drug-containing microparticles in a substantial amount of supporting matrix; Multiparticulate tablets
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/28—Dragees; Coated pills or tablets, e.g. with film or compression coating
- A61K9/2806—Coating materials
- A61K9/2833—Organic macromolecular compounds
- A61K9/286—Polysaccharides, e.g. gums; Cyclodextrin
- A61K9/2866—Cellulose; Cellulose derivatives, e.g. hydroxypropyl methylcellulose
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/04—Anorexiants; Antiobesity agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/06—Antihyperlipidemics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/12—Antihypertensives
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Epidemiology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Organic Chemistry (AREA)
- Diabetes (AREA)
- Biophysics (AREA)
- Molecular Biology (AREA)
- Obesity (AREA)
- Hematology (AREA)
- Heart & Thoracic Surgery (AREA)
- Cardiology (AREA)
- Inorganic Chemistry (AREA)
- Vascular Medicine (AREA)
- Endocrinology (AREA)
- Emergency Medicine (AREA)
- Child & Adolescent Psychology (AREA)
- Urology & Nephrology (AREA)
- Medicinal Preparation (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Description
例えば、水難溶性低融点物質であるシクランデレートを加熱溶融し、微細末の合成ケイ酸アルミニウム又は(及び)二酸化ケイ素の薬効を奏しない量を加えることを特徴とする固形製剤の製造方法が報告されている(特公昭51−16491号公報参照)。
本発明者らは、この問題を克服するための製剤組成を種々研究した結果、水難溶性低融点物質を多量に配合した場合でも、製造中および保存中において、凝集、溶融、融着などを起こさず安定性に優れ、かつ、経口投与後の消化管内で、迅速に水を引き込み、膨潤、崩壊して、速やかに水難溶性低融点物質を放出できる固形製剤を見出し、本発明の固形製剤を完成するに至った。
すなわち、本発明は、以下の[1]〜[17]に関する。
[1]以下の1)〜3)の特徴を有する固形製剤。
1)水難溶性低融点物質、糖類、ならびに結晶セルロースおよび低置換度ヒドロキシプロピルセルロースから選ばれるセルロース類を含む。
2)糖類/セルロース類の重量比が2を超える。
3)セルロース類の含量が5重量%以上である。
[2]水難溶性低融点物質の37℃での水に対する溶解度が10mg/L以下である上記[1]の固形製剤。
[3]水難溶性低融点物質の融点が10〜100℃である上記[1]の固形製剤。
[4]水難溶性低融点物質の平均粒子径が1〜100μmである上記[1]の固形製剤。
[5]水難溶性低融点物質がリパーゼ阻害剤である上記[1]の固形製剤。
[6]リパーゼ阻害剤が2−ヘキサデシルオキシ−6−メチル−4H−3,1−ベンズオキサジン−4−オンまたはその塩である上記[5]の固形製剤。
[7]糖類が糖アルコール類である上記[1]の固形製剤。
[8]糖アルコール類がマンニトールである上記[7]の固形製剤。
[9]セルロース類が結晶セルロースである上記[1]の固形製剤。
[10]水難溶性低融点物質の含量が5〜60重量%である上記[1]の固形製剤。
[11]糖類の含量が30〜75重量%である上記[1]記載の固形製剤。
[12]セルロース類の含量が5〜15重量%である上記[1]記載の固形製剤。
[13]糖類/セルロース類の重量比が3〜9である上記[1]記載の固形製剤。
[14]錠剤である上記[1]の固形製剤。
[15]37℃の水中での崩壊時間が30分以内である上記[1]の固形製剤。
[16]水難溶性低融点物質、糖類、ならびに結晶セルロースおよび低置換度ヒドロキシプロピルセルロースから選ばれるセルロース類を含む混合物を造粒することを含む、上記[1]の固形製剤の製造方法。
[17]前記造粒が流動層造粒機を用いて行われる、上記[16]の方法。
[発明の効果]
本発明の固形製剤では、製造中および保存中に通常観察される、水難溶性低融点物質の凝集、溶融、融着などが抑制されている。したがって、本発明の固形製剤は、経口投与後の崩壊特性および水難溶性低融点物質の放出特性に優れている。
また、本発明の固形製剤は、水難溶性低融点物質を多量に含んでいても、製造中および保存中の安定性に優れ、かつ経口投与後の崩壊特性および水難溶性低融点物質の放出特性に優れている。
本発明の製造方法は、水難溶性低融点物質の融点以下となる温度条件下で行うことができるため、水難溶性低融点物質を加熱溶融する必要がない。したがって、本発明の製造方法は、水難溶性低融点物質を分解させることなく、固形製剤を製造するための簡便な製造方法として極めて有用である。
本発明の固形製剤は、以下の1)〜3)を特徴とする。
1)水難溶性低融点物質、糖類、ならびに結晶セルロースおよび低置換度ヒドロキシプロピルセルロースから選ばれるセルロース類を含む。
2)糖類/セルロース類の重量比が2を超える。
3)セルロース類の含量が5重量%以上である。
本発明の固形製剤に用いる水難溶性低融点物質の水難溶性とは、水に溶解しにくい性質を示す。本発明では、例えば、水難溶性低融点物質の37℃での水に対する溶解度が通常10mg/L以下、好ましくは1mg/L以下、より好ましくは0.5mg/L以下である。
ここでいう溶解度は、次のように求める。まず、精製水(5ml)に水難溶性低融点物質物質を過剰量添加する。得られる混合液を、37℃の恒温槽に30分静置後、ボルテックスミキサーで攪拌する。この静置および攪拌の操作をさらに3回繰り返し、得られた懸濁液を、シリンジフィルター(日本ポール社製、商品名:アクロディスクLC25、PVDF、孔径0.2μm)で濾過する。このようにして得られた濾液中の水難溶性低融点物質の濃度(mg/L)を溶解度とする。
また、水難溶性低融点物質の低融点とは、通常10℃〜100℃、好ましくは20℃〜90℃、より好ましくは30℃〜90℃の範囲内にある融点を意味する。融点は、例えば、日本薬局方に既定される融点測定方法により測定することができる。
上記水難溶性低融点物質の平均粒子径は、通常1μm〜100μm、好ましくは1μm〜70μm、より好ましくは1μm〜60μm、特に好ましくは10μm〜50μmである。本明細書中、平均粒子径とは、乾式レーザー回折計(HELOS,Sympatec GmbH)を用いて測定した累積50%粒径値(X50)である。
上記水難溶性低融点物質の固形製剤中の含量は、通常5重量%〜60重量%、好ましくは5重量%〜55重量%、より好ましくは5重量%〜50重量%である。
上記水難溶性低融点物質としては、例えば、リパーゼ阻害剤、消炎鎮痛剤(例、イブプロフェン、ケトプロフェン)、電子伝達系補酵素剤(例、コエンザイムQ10、イデベノン)などが挙げられるが、好ましくはリパーゼ阻害剤である。
リパーゼ阻害剤としては、例えばオルリスタット、米国特許第6624161号明細書に記載された下式化合物が挙げられる。
[式中、R1は分岐または非分岐状C10−20アルキル(該C10−20アルキルは1または2個の酸素原子でインタラプト(interrupt)されていてよく、また、アリール、アリールオキシ、ヘテロアリール、ヘテロアリールオキシ、シアノ、ニトロ、−CO2R3、−NR3R4、−CONR3R4、OHおよびハロゲン原子から選ばれる1個以上の置換基で置換されていてよい。R3およびR4は、互いに独立して、水素原子またはC1−6アルキルを示す。)を、R8、R9、R10およびR11は、互いに独立して、水素原子、ハロゲン原子、ヒドロキシ、アミノ、ニトロ、シアノ、チオール、C1−10アルキル、C1−10アルコキシ、C3−10シクロアルキル、C3−10シクロアルコキシ、C(O)R5、C(O)NR5R6、S(O)R5またはハロC1−10アルキルを、R5およびR6は、互いに独立して、水素原子またはC1−10アルキルを示す。]
上記化合物のなかでも、2−ヘキサデシルオキシ−6−メチル−4H−3,1−ベンズオキサジン−4−オン(以下、単に化合物Aという)が好ましい。
本発明の固形製剤に用いられる水難溶性低融点物質は塩であってもよく、このような塩としては、例えば金属塩、アンモニウム塩、有機塩基との塩、無機酸との塩、有機酸との塩、塩基性または酸性アミノ酸との塩などが挙げられる。金属塩の好適な例としては、ナトリウム塩、カリウム塩などのアルカリ金属塩;カルシウム塩、マグネシウム塩、バリウム塩などのアルカリ土類金属塩;アルミニウム塩などが挙げられる。有機塩基との塩の好適な例としては、トリメチルアミン、トリエチルアミン、ピリジン、ピコリン、2,6−ルチジン、エタノールアミン、ジエタノールアミン、トリエタノールアミン、シクロヘキシルアミン、ジシクロヘキシルアミン、N,N’−ジベンジルエチレンジアミンなどとの塩が挙げられる。無機酸との塩の好適な例としては、塩酸、臭化水素酸、硝酸、硫酸、リン酸などとの塩が挙げられる。有機酸との塩の好適な例としては、ギ酸、酢酸、トリフルオロ酢酸、フタル酸、フマル酸、シュウ酸、酒石酸、マレイン酸、クエン酸、コハク酸、リンゴ酸、メタンスルホン酸、ベンゼンスルホン酸、p−トルエンスルホン酸などとの塩が挙げられる。塩基性アミノ酸との塩の好適な例としては、アルギニン、リジン、オルニチンなどとの塩が挙げられ、酸性アミノ酸との塩の好適な例としては、アスパラギン酸、グルタミン酸などとの塩が挙げられる。
このうち、薬学的に許容し得る塩が好ましい。
本発明の固形製剤に用いられる糖類としては、例えば、糖アルコール類(例、マンニトール(マンニット)、エリスリトール、キシリトール、マルチトール、ソルビトール)、二糖類(例、マルトース、スクロース、セルビオース、ラクトース)、単糖類(例、アラビノース、キシロース、リボース、2−デオキシリボース、ブドウ糖、果糖、ガラクトース、マンノース、ソルボース、ラムノース、フコース)、オリゴ糖(例、マルトトリオース、ラフィノース糖、スタキオース)などが挙げられるが、固形製剤の崩壊特性および当該固形製剤からの水難溶性低融点物質の放出特性という観点から、好ましくは糖アルコール類であり、より好ましくはマンニトールである。
本発明の固形製剤における糖類の含量の範囲は、通常10重量%〜75重量%、好ましくは20重量%〜75重量%、より好ましくは30重量%〜75重量%である。糖類をこの範囲内で含有することにより、固形製剤への水の浸透速度が上昇し、固形製剤の崩壊特性および水難溶性低融点物質の放出特性が向上する。
本発明の固形製剤に用いられるセルロース類は、結晶セルロースおよび低置換度ヒドロキシプロピルセルロースから選ばれるが、固形製剤からの水難溶性低融点物質の放出を速やかにするという観点から、結晶セルロースが好ましい。
また、固形製剤の成型性を向上させるという観点からも、セルロース類としては、結晶セルロースが好ましい。
ここで、固形製剤の成型性を向上させるということは、成型時に必要な圧力を減弱して、固形製剤の圧縮密度を下げても、該固形製剤が使用に耐える十分な硬度を維持しうることを意味する。
本発明の固形製剤において、結晶セルロースを用いることにより、該固形製剤を製造する過程で発生する、水難溶性低融点物質の凝集、溶融、融着などを防止することができる。このような防止効果は、水難溶性低融点物質の含量が高い固形製剤(例、水難溶性低融点物質の固形製剤中の含量が20重量%以上である固形製剤)において顕著に得られる。
特に、水難溶性低融点物質の含量が高い固形製剤(例、水難溶性低融点物質の固形製剤中の含量が20重量%以上である固形製剤)の製造時には、水難溶性低融点物質の凝集、溶融、融着などが発生する可能性が高いため、成型時に必要な圧力を減弱して、固形製剤の圧縮密度を下げ空隙率を上げても、固形製剤の十分な硬度を得ることができる本発明の固形製剤では、水難溶性低融点物質の凝集、溶融、融着などの防止効果が顕著に得られる。
また、本発明の固形製剤において、結晶セルロースを用いることにより、該固形製剤を保存する過程で発生する、水難溶性低融点物質の凝集、溶融、融着などを防止することができる。
特に、水難溶性低融点物質の含量が高い固形製剤(例、水難溶性低融点物質の固形製剤中の含量が20重量%以上である固形製剤)の保存時には、水難溶性低融点物質の凝集、溶融、融着などが発生する可能性が高いため、このような水難溶性低融点物質の凝集、溶融、融着などの防止効果が顕著に得られる。
本発明の製剤においては、上記糖類/セルロース類の重量比が2を超え、好ましくは2を超え15までの範囲であり、より好ましくは3〜9の範囲であり、最も好ましくは4〜7である。糖類/セルロース類の重量比が15以上であると、固形製剤への水の取り込み速度が不十分であるという理由により好ましくない。一方、上記糖類/セルロース類の重量比が2以下であると、通常、固形製剤が吸湿して膨れて扱いにくくなる。通常、錠剤の厚みは打錠工程で調整するが、打錠後に膨れて錠剤の厚みが増加すると品質管理上の錠剤の厚みに制御することが困難になる問題がある。特に、フィルムコーティング工程を経る場合は、錠剤(素錠)が膨れるときに錠剤表面に凹凸ができてしまい品質上問題が生じる。また、該固形製剤自体がもろくなるため、割れ、欠けなどの品質上の問題がおこる可能性がある。特に、フィルムコーティング工程を経る場合は、工程中にわずかな錠数でも、割れ、欠けなどの品質上の問題が起こると、製造バッチ全体に悪影響する。
また、本発明の固形製剤においては、セルロース類の含量は通常5重量%以上、好ましくは5重量%〜30重量%、より好ましくは5重量%〜25重量%、特に好ましくは5重量%〜15重量%である。本発明の固形製剤においてセルロース類の含量が5重量%未満であると、目的とする崩壊特性および放出特性を達成することができないので好ましくない。一方、本発明の固形製剤においてセルロース類の含量が30重量%を超えると、得られた固形製剤が膨れて扱いにくくなり、また、該固形製剤自体がもろくなるため、割れ、欠けなどの品質上の問題が起こる可能性がある。
また、本発明の固形製剤においては、水難溶性低融点物質と糖類との重量比は1:50〜50:1、好ましくは1:15〜10:1、より好ましくは1:15〜5:1である。
本発明の固形製剤の剤形としては、例えば顆粒剤、丸剤、錠剤、カプセル剤などが挙げられ、なかでも錠剤が好ましい。ここで、錠剤の形状は特に限定されず、円形錠剤、オーバル型錠剤、オブロング型錠剤などの錠剤の素錠およびその被覆錠剤などのいずれであってもよい。また、本発明の固形製剤は、二種類以上の顆粒を混合して成錠した群分け錠;二層錠、三層錠などの多層錠;有核錠;プレスコーティング錠などであってもよい。
また、本発明の固形製剤は、上記水難溶性低融点物質、糖類、ならびに結晶セルロースおよび低置換度ヒドロキシプロピルセルロースから選ばれるセルロース類に加えて、固形製剤の崩壊特性および固形製剤からの水難溶性低融点物質の放出特性を損なわない範囲内で、薬学的に許容され得る担体、具体的には医薬製剤に通常用いられる賦形剤、崩壊剤、結合剤、滑沢剤、着色剤、香料、遮光剤、可塑剤、安定化剤などの各種添加剤を含んでもよい。
賦形剤としては、例えば、軽質無水ケイ酸、炭酸マグネシウム、炭酸カルシウム、リン酸カルシウム、硫酸カルシウム、ケイ酸アルミニウム、メタケイ酸アルミニウムなどが挙げられる。
崩壊剤としては、例えばカルメロースカルシウム、クロスカルメロースナトリウム、カルボキシメチルスターチナトリウム、クロスリンクドインソルブルポリビニルピロリドンなどが挙げられる。
結合剤としては、例えば、ヒドロキシプロピルセルロース、ヒドロキシプロピルメチルセルロース、α化デンプン、ゼラチン、アラビアゴム粉末、ポリビニルピロリドン、デキストリン、プルランなどが挙げられる。
滑沢剤としては、例えばステアリン酸、ステアリン酸カルシウム、ステアリン酸マグネシウム、タルク、コロイドシリカなどが挙げられる。
着色剤としては、例えば黄色三二酸化鉄、三二酸化鉄などが挙げられる。
香料としては、合成物および天然物のいずれでもよく、例えばレモンフレーバー、ライムフレーバー、オレンジフレーバー、ストロベリーフレーバー、メントールなどが挙げられる。
遮光剤としては、例えば酸化チタン、タルク、炭酸カルシウム、炭酸マグネシウムなどが挙げられる。
可塑剤としては、例えばポリエチレングリコール(マクロゴール)、プロピレングリコール、コポリビドンなどが挙げられる。
安定化剤としては、例えばアスコルビン酸、アスコルビン酸ナトリウム、エリソルビン酸などが挙げられる。
なお、水難溶性低融点物質としてリパーゼ阻害剤を用いる場合、本発明の固形製剤は、必要に応じて、国際公開パンフレット第00/09122号などに記載の油吸着剤(例、メチルセルロース、キサンタンガム)を含んでいてもよい。
[製造方法]
本発明の固形製剤は、その剤形に応じて採用される公知の方法を組み合わせることによって、製造することができる。各工程の条件は、常法に従い決定すればよい。
好ましくは、本発明の固形製剤は、水難溶性低融点物質、糖類、ならびに結晶セルロースおよび低置換度ヒドロキシプロピルセルロースから選ばれるセルロース類を含む混合物を造粒することを含む方法(以下、本発明の製造方法と略記することがある)により製造される。造粒は通常用いられる造粒機(例、流動層造粒機、ハイスピードミキサー、ニーダー)のいずれを用いても行うことができるが、水難溶性低融点物質の変質防止という理由から、流動層造粒機を用いて造粒することが好ましい。
上記造粒は、造粒工程中の品温が、用いられる水難溶性低融点物質の融点以下となる温度条件下で行うことが好ましい。なお、水難溶性低融点物質と賦形剤とが共存する場合に、水難溶性低融点物質の融点が通常の融点以下に低下することがあるが、その場合は低下した融点以下に品温を制御して造粒することが好ましい。用いられる水難溶性低融点物質、糖類およびセルロース類の量は、それぞれ上述したとおりである。
上記造粒によって得られる顆粒は、50μm〜1.5mmの粒子を50%以上(好ましくは150μm〜1.0mmの粒子を50%以上)含む。得られた顆粒は、必要に応じて、水分の除去の目的で、約0.01時間〜72時間、乾燥してもよい。また、得られた顆粒は必要に応じてさらに整粒してもよい。整粒には通常、パワーミルなどの市販の整粒機が用いられる。整粒後の顆粒は約50μm〜1.5mmの粒子を50%以上(好ましくは150μm〜1.0mmの粒子を50%以上)含む。これらに、さらにクロスカルメロースナトリウムなどの崩壊剤およびステアリン酸マグネシウムなどの滑沢剤を加えてもよい。これらの混合には通常、タンブラー混合機などの市販の混合機が用いられる。用いられる崩壊剤および滑沢剤の含量は、それぞれ約0.1重量%〜25重量%および約0.1重量%〜10重量%である。
得られた顆粒は、顆粒剤としてそのまま用いてもよいが、通常、丸剤、錠剤、カプセル剤などの剤形に仕立てられる。
例えば錠剤の成形には、錠剤機などの市販の成形機が用いられる。錠剤に成形する際の打錠圧は、通常、約1kN〜25kNである。円形錠剤は、通常、直径約5mm〜20mm、厚さ約1mm〜10mmである。オーバル型錠剤は、通常、長径約7mm〜20mm、短径約5mm〜15mm、厚さ約1mm〜10mmである。オブロング型錠剤は、通常、長径約7mm〜20mm、短径約5mm〜15mm、厚さ約1mm〜10mmである。
上記で得られた錠剤は、さらにフィルムコーティングなどの被覆を施して、フィルムコーティング錠などの各種被覆製剤としてもよい。
フィルムコーティング操作には通常、パンコーティング装置などが使用される。フィルムコーティング錠としては、円形錠剤をフィルムコーティングしたものやオーバル型錠剤をフィルムコーティングしたもの、オブロング型錠剤をフィルムコーティングしたものが挙げられる。
上記フィルムコーティングに用いるフィルムコーティング液は、例えばヒドロキシプロピルメチルセルロースなどのフィルムコーティング用高分子を、例えば水などの溶媒に溶解または懸濁することによって調製することができる。該フィルムコーティング液には、さらに、着色剤、遮光剤などを配合することが好ましい。フィルムコーティング液を噴霧する時の製品(錠剤)温度は通常約10℃〜100℃にコントロールするが、約30℃〜80℃にコントロールすることがより好ましく、約35℃〜60℃にコントロールすることがさらに好ましい。
本発明の製造方法は、水難溶性低融点物質の融点以下となる温度条件下で行うことができるため、水難溶性低融点物質を加熱溶融する必要がない。したがって、本発明の製造方法は、水難溶性低融点物質を分解させることなく、固形製剤を製造するための簡便な製造方法として極めて有用である。
上記のように得られた本発明の固形製剤は、所望の崩壊特性を有する。具体的には、例えば、37℃の水中での崩壊時間が通常30分以内、好ましくは20分以内、より好ましくは10分以内である。
上記のように得られた本発明の固形製剤は、崩壊特性および経口投与後の水難溶性低融点物質の放出特性に優れている。
特に、化合物Aのようなリパーゼ阻害剤は、抗肥満作用を有する一方で毒性が低く安全であるので、本発明の固形製剤が水難溶性低融点物質としてリパーゼ阻害剤を含む場合、このような固形製剤は、哺乳動物(例えば、ヒト、ラット、マウス、ネコ、イヌ、ウサギ、ウシ、ブタ、ハムスター、ヒツジ、サル)に対して、例えば、肥満症、高脂血症(例、高トリグリセリド血症、高コレステロール血症、低HDL血症、食後高脂血症)、高血糖症(2型糖尿病、耐糖能不全(Impaired Glucose Tolerance))、高血圧、心血管疾患、卒中、消化器疾患などの各種疾患あるいはこれら疾患の合併症(例、2型糖尿病合併肥満症、高脂血症合併肥満症、メタボリックシンドローム)の安全な予防・治療剤として使用することができる。
本発明の固形製剤の投与量は、水難溶性低融点物質の種類、含量、剤形、薬物放出の持続時間、投与対象動物(例、ヒト、ラット、マウス、ネコ、イヌ、ウサギ、ウシ、ブタ、ハムスター、ヒツジ、サルなどの哺乳動物)、投与目的、症状、患者の年令などによっても異なるが、例えば成人患者(体重:60kg)に経口的に投与する場合、通常、1日当たり約1mg〜500mgである。
また、例えば、水難溶性低融点物質としてリパーゼ阻害剤(好ましくは化合物A)を含む固形製剤を肥満症またはその合併症(例、2型糖尿病合併肥満症、高脂血症合併肥満症)に罹患した成人患者(体重:60kg)に経口的に投与する場合、1日当たり水難溶性低融点物質として約1mg〜500mg、好ましくは約5mg〜250mg、さらに好ましくは約5mg〜100mgを含む本発明の固形製剤を、1〜3回に分割投与すればよい。
本発明の固形製剤は、必要に応じて、放出特性を損なわない範囲で、水難溶性低融点物質以外の薬物を適量配合してもよいし、または他の薬物と併用して使用することもできる。
水難溶性低融点物質とともに本発明の固形製剤に配合し得るまたは本発明の固形製剤と併用し得る薬物(以下、併用薬物と略記する)としては、例えば、以下のようなものが用いられる。
(1)糖尿病治療剤
インスリン製剤〔例、ウシ、ブタなどの膵臓から抽出された動物インスリン製剤;大腸菌、イーストを用い、遺伝子工学的に合成したヒトインスリン製剤;インスリン亜鉛;プロタミンインスリン亜鉛;インスリンのフラグメントまたは誘導体(例、INS−1);経口インスリン製剤〕、インスリン抵抗性改善剤(例、ピオグリタゾンまたはその塩(好ましくは塩酸塩)、ロシグリタゾンまたはその塩(好ましくはマレイン酸塩)、レグリキサン(Reglixane)、ネトグリタゾン(Netoglitazone)、FK−614、リボグリタゾン(Rivoglitazone)、DRF−2593、エダグリタゾン(Edaglitazone)(BM−13.1258)、R−119702、WO01/38325に記載の化合物、テサグリタザール(Tesaglitazar)、ラガグリタザール(Ragaglitazar)、ムラグリタザール(Muraglitazar)、ONO−5816、LM−4156、メタグリダセン(Metaglidasen)(MBX−102)、ナベグリタザール(Naveglitazar)(LY−519818)、MX−6054、LY−510929、バラグリタゾン(Balaglitazone)、T−131またはその塩、THR−0921)、α−グルコシダーゼ阻害剤(例、ボグリボース、アカルボース、ミグリトール、エミグリテート)、ビグアナイド剤(例、フェンホルミン、メトホルミン、ブホルミンまたはそれらの塩(例、塩酸塩、フマール酸塩、コハク酸塩))、インスリン分泌促進剤(スルホニルウレア剤(例、トルブタミド、グリベンクラミド、グリクラジド、クロルプロパミド、トラザミド、アセトヘキサミド、グリクロピラミド、グリメピリド、グリピザイド、グリブゾール)、レパグリニド、セナグリニド、ナテグリニド、ミチグリニドまたはそのカルシウム塩水和物)、GPR40アゴニスト、GLP−1受容体アゴニスト[例、GLP−1、GLP−1MR剤、NN−2211、AC−2993(exendin−4)、BIM−51077、Aib(8,35)hGLP−1(7,37)NH2、CJC−1131]、ジペプチジルペプチダーゼIV阻害剤(例、NVP−DPP−278、PT−100、P32/98、ヴィルダグリプチン(Vildagliptin)(LAF−237)、P93/01、TS−021、シタグリプチン フォスフェート(Sitagliptin phosphate)(MK−431)、サクサグリプチン(Saxagliptin)(BMS−477118)、E−3024、T−6666(TA−6666)、823093、825964、815541)、β3アゴニスト(例、AJ−9677)、アミリンアゴニスト(例、プラムリンチド)、フォスフォチロシンホスファターゼ阻害剤(例、バナジン酸ナトリウム)、糖新生阻害剤(例、グリコーゲンホスホリラーゼ阻害剤、グルコース−6−ホスファターゼ阻害剤、グルカゴン拮抗剤)、SGLT(sodium−glucose cotransporter)阻害剤(例、T−1095)、11β−HSD1阻害薬(例、BVT−3498)、アジポネクチンまたはその作動薬、IKK阻害薬(例、AS−2868)、レプチン抵抗性改善薬、ソマトスタチン受容体作動薬(例、WO01/25228、WO03/42204、WO98/44921、WO98/45285、WO99/22735に記載の化合物)、グルコキナーゼ活性化薬(例、Ro−28−1675)など。
(2)糖尿病性合併症治療剤
アルドース還元酵素阻害剤(例、トルレスタット、エパルレスタット、ゼナレスタット、ゾポルレスタット、フィダレスタット、ミナルレスタット、ラニレスタット、CT−112)、神経栄養因子およびその増加薬(例、NGF、NT−3、BDNF、WO01/14372に記載のニューロトロフィン産生・分泌促進剤(例、4−(4−クロロフェニル)−2−(2−メチル−1−イミダゾリル)−5−[3−(2−メチルフェノキシ)プロピル]オキサゾール))、神経再生促進薬(例、Y−128、VX853、prosaptide)、PKC阻害剤(例、ルボキシスタウリン メシレート(ruboxistaurin mesylate))、AGE阻害剤(例、ALT−945、ピマゲジン、N−フェナシルチアゾリウムブロミド(ALT−766)、EXO−226、ALT−711、ピリドリン(Pyridorin)、ピリドキサミン)、活性酸素消去薬(例、チオクト酸)、脳血管拡張剤(例、チアプリド)、ソマトスタチン受容体作動薬(例、BIM23190)、アポトーシスシグナルレギュレーティングキナーゼ−1(ASK−1)阻害薬など。
(3)抗高脂血症剤
HMG−CoA還元酵素阻害剤(例、プラバスタチン、シンバスタチン、ロバスタチン、アトルバスタチン、フルバスタチン、ピタバスタチン、ロスバスタチンまたはそれらの塩(例、ナトリウム塩、カルシウム塩))、スクアレン合成酵素阻害剤(例、WO97/10224に記載の化合物、例えば、N−[[(3R,5S)−1−(3−アセトキシ−2,2−ジメチルプロピル)−7−クロロ−5−(2,3−ジメトキシフェニル)−2−オキソ−1,2,3,5−テトラヒドロ−4,1−ベンゾオキサゼピン−3−イル]アセチル]ピペリジン−4−酢酸)、フィブラート系化合物(例、ベザフィブラート、クロフィブラート、シムフィブラート、クリノフィブラート)、ACAT阻害剤(例、アバシマイブ(Avasimibe)、エフルシマイブ(Eflucimibe))、陰イオン交換樹脂(例、コレスチラミン)、プロブコール、ニコチン酸系薬剤(例、ニコモール(nicomol)、ニセリトロール(niceritrol))、イコサペント酸エチル、植物ステロール(例、ソイステロール(Soysterol)、ガンマオリザノール(γ−oryzanol))など。
(4)降圧剤
アンジオテンシン変換酵素阻害剤(例、カプトプリル、エナラプリル、デラプリル、リシノプリル)、アンジオテンシンII拮抗剤(例、ロサルタン、カンデサルタン シレキセチル、エプロサルタン、バルサルタン、テルミサルタン、イルベサルタン、タソサルタン、1−[[2’−(2,5−ジヒドロ−5−オキソ−4H−1,2,4−オキサジアゾール−3−イル)ビフェニル−4−イル]メチル]−2−エトキシ−1H−ベンズイミダゾール−7−カルボン酸)、カルシウム拮抗剤(例、マニジピン、ニフェジピン、アムロジピン、エホニジピン、ニカルジピン)、カリウムチャンネル開口薬(例、レブクロマカリム、L−27152、AL 0671、NIP−121)、α1遮断薬(例、塩酸プラゾシン、塩酸テラゾシン、塩酸ブナゾシン)、β遮断薬(例、塩酸プロプラノロール、ピンドロール、アテノロール、塩酸セリプロロール、酒石酸メトプロロール)、α1、β遮断薬(例、塩酸ラベタロール、カルベジロール、塩酸ブニトロロール)クロニジンなど。
(5)抗肥満剤
中枢性抗肥満薬(例、デキスフェンフルアミン、フェンフルラミン、フェンテルミン、シブトラミン、アンフェプラモン、デキサンフェタミン、マジンドール、フェニルプロパノールアミン、クロベンゾレックス;MCH受容体拮抗薬(例、SB−568849;SNAP−7941;WO01/82925およびWO01/87834に記載の化合物);ニューロペプチドY拮抗薬(例、CP−422935);カンナビノイド受容体拮抗薬(例、SR−141716、SR−147778);グレリン拮抗薬)、β3アゴニスト(例、AJ−9677)、ペプチド性食欲抑制薬(例、レプチン、CNTF(毛様体神経栄養因子))、コレシストキニンアゴニスト(例、リンチトリプト、FPL−15849)、摂食抑制薬(例、P−57)など。
(6)利尿剤
キサンチン誘導体(例、サリチル酸ナトリウムテオブロミン、サリチル酸カルシウムテオブロミン)、チアジド系製剤(例、エチアジド、シクロペンチアジド、トリクロルメチアジド、ヒドロクロロチアジド、ヒドロフルメチアジド、ベンジルヒドロクロロチアジド、ペンフルチジド、ポリチアジド、メチクロチアジド)、抗アルドステロン製剤(例、スピロノラクトン、トリアムテレン)、炭酸脱水酵素阻害剤(例、アセタゾラミド)、クロルベンゼンスルホンアミド系製剤(例、クロルタリドン、メフルシド、インダパミド)、アゾセミド、イソソルビド、エタクリン酸、ピレタニド、ブメタニド、フロセミド、メチクランなど。
(7)化学療法剤
アルキル化剤(例、サイクロフォスファミド、イフォスファミド)、代謝拮抗剤(例、メソトレキセート、5−フルオロウラシルまたはその誘導体(例、フルツロン、ネオフルツロン))、抗癌性抗生物質(例、マイトマイシン、アドリアマイシン)、植物由来抗癌剤(例、ビンクリスチン、ビンデシン、タキソール)、シスプラチン、カルボプラチン、エトポシドなど。
(8)免疫療法剤
微生物または細菌成分(例、ムラミルジペプチド誘導体、ピシバニール)、免疫増強活性のある多糖類(例、レンチナン、シゾフィラン、クレスチン)、遺伝子工学的手法で得られるサイトカイン(例、インターフェロン、インターロイキン(例、IL−1、IL−2、IL−12))、コロニー刺激因子(例、顆粒球コロニー刺激因子、エリスロポエチン)など。
(9)抗血栓剤
ヘパリン(例、ヘパリンナトリウム、ヘパリンカルシウム、ダルテパリンナトリウム(dalteparin sodium))、ワルファリン(例、ワルファリンカリウム)、抗トロンビン薬(例、アルガトロバン(aragatroban))、血栓溶解薬(例、ウロキナーゼ(urokinase)、チソキナーゼ(tisokinase)、アルテプラーゼ(alteplase)、ナテプラーゼ(nateplase)、モンテプラーゼ(monteplase)、パミテプラーゼ(pamiteplase))、血小板凝集抑制薬(例、塩酸チクロピジン(ticlopidine hydrochloride)、シロスタゾール(cilostazol)、イコサペント酸エチル、ベラプロストナトリウム(beraprost sodium)、塩酸サルポグレラート(sarpogrelate hydrochloride))など。
(10)悪液質改善剤
プロゲステロン誘導体(例、メゲステロールアセテート)、メトクロプラミド系薬剤、テトラヒドロカンナビノール系薬剤、脂肪代謝改善剤(例、エイコサペンタエン酸)、成長ホルモン、IGF−1、あるいは悪液質を誘導する因子であるTNF−α、LIF、IL−6、オンコスタチンMに対する抗体など。
(11)消炎剤
ステロイド剤(例、デキサメサゾン)、ヒアルロン酸ナトリウム、シクロオキシゲナーゼ阻害剤(例、インドメタシン、ケトプロフェン、ロキソプロフェン、メロキシカム、アムピロキシカム、セレコキシブ、ロフェコキシブ)など。
(12)その他
糖化阻害剤(例、ALT−711)、抗うつ薬(例、デシプラミン、アミトリプチリン、イミプラミン、フロキセチン、パロキセチン、ドキセピン)、抗てんかん薬(例、ラモトリジン、カルバマゼピン)、抗不整脈薬(例、メキシレチン)、アセチルコリン受容体リガンド(例、ABT−594)、エンドセリン受容体拮抗薬(例、ABT−627)、モノアミン取り込み阻害薬(例、トラマドル)、インドールアミン取り込み阻害薬(例、フロキセチン、パロキセチン)、麻薬性鎮痛薬(例、モルヒネ)、GABA受容体作動薬(例、ギャバペンチン)、GABA取り込み阻害薬(例、チアガビン)、α2受容体作動薬(例、クロニジン)、局所鎮痛薬(例、カプサイシン)、抗不安薬(例、ベンゾジアゼピン類)、ホスホジエステラーゼ阻害薬(例、シルデナフィル)、ドーパミン受容体作動薬(例、アポモルフィン)、ドーパミン受容体拮抗薬(例、ハロペリドール)、セロトニン受容体作動薬(例、クエン酸タンドスピロン、スマトリプタン)、セロトニン受容体拮抗薬(例、塩酸シプロヘプタジン、オンダンセトロン)、セロトニン取り込み阻害薬(例、マレイン酸フルボキサミン、フロキセチン、パロキセチン)、睡眠導入剤(例、トリアゾラム、ゾルピデム)、抗コリン剤、α1受容体遮断薬(例、タムスロシン)、筋弛緩薬(例、バクロフェン)、アルツハイマー病予防・治療薬(例、ドネペジル、リバスチグミン、ガランタミン)、パーキンソン病治療薬(例、L−ドーパ)、多発性硬化症予防・治療薬(例、インターフェロンβ−1a)、ヒスタミンH1受容体阻害薬(例、塩酸プロメタジン)、プロトンポンプ阻害薬(例、ランソプラゾール、オメプラゾール、ラベプラゾールまたはその塩(例、ナトリウム塩))、NK−2受容体アンタゴニスト、HIV感染症治療薬(例、サキナビル、ジドブジン、ラミブジン、ネビラビン)、慢性閉塞性肺疾患治療薬(例、サルメテロール、チオトロピウムブロミド、シロミラスト)など。
抗コリン剤としては、例えば、アトロピン、スコポラミン、ホマトロピン、トロピカミド、シクロペントラート、臭化ブチルスコポラミン、臭化プロパンテリン、臭化メチルベナクチジウム、臭化メペンゾラート、フラボキサート、ピレンセビン、臭化イプラトピウム、トリヘキシフェニジル、オキシブチニン、プロピベリン、ダリフェナシン、トルテロジン、テミベリン、塩化トロスピウムまたはその塩(例、硫酸アトロピン、臭化水素酸スコポラミン、臭化水素酸ホマトロピン、塩酸シクロペントラート、塩酸フラボキサート、塩酸ピレンセビン、塩酸トリヘキシフェニジル、塩化オキシブチニン、酒石酸トルテロジン)などが用いられ、なかでも、オキシブチニン、プロピベリン、ダリフェナシン、トルテロジン、テミベリン、塩化トロスピウムまたはその塩(例、塩化オキシブチニン、酒石酸トルテロジン)が好適である。また、アセチルコリンエステラーゼ阻害薬(例、ジスチグミン)なども使用することができる。
NK−2受容体アンタゴニストとしては、例えば、GR159897、GR149861、SR48968(saredutant)、SR144190、YM35375、YM38336、ZD7944、L−743986、MDL105212A、ZD6021、MDL105172A、SCH205528、SCH62373、R−113281などのピペリジン誘導体;RPR−106145などのペルヒドロイソインドール誘導体;SB−414240などのキノリン誘導体;ZM−253270などのピロロピリミジン誘導体;MEN11420(nepadutant)、SCH217048、L−659877、PD−147714(CAM−2291)、MEN10376、S16474などのプソイドペプチド誘導体;その他、GR100679、DNK333、GR94800、UK−224671、MEN10376、MEN10627、またはそれらの塩などが挙げられる。
水難溶性低融点物質がリパーゼ阻害剤(好ましくは化合物A)である場合、併用薬物としては、インスリン製剤、インスリン抵抗性改善剤(好ましくはピオグリタゾンまたはその塩(好ましくは塩酸塩))、α−グルコシダーゼ阻害剤(好ましくはボグリボース)、ビグアナイド剤(好ましくはメトフォルミン)、インスリン分泌促進剤(好ましくはスルホニルウレア剤、ミチグリニドまたはそのカルシウム塩水和物)、HMG−CoA還元酵素阻害剤(好ましくはシンバスタチン、アトルバスタチン)などが好ましい。
水難溶性低融点物質と併用薬物とを配合または併用する本発明の固形製剤には、(1)水難溶性低融点物質と併用薬物とを含有する医薬組成物として単一に製剤化されたもの、(2)水難溶性低融点物質を含む医薬組成物と併用薬物とが別個に製剤化されたもののいずれも含まれる。以下、これらを総称して本発明の併用剤と略記する。
本発明の併用剤は、水難溶性低融点物質および併用薬物の有効成分を、別々にあるいは同時に、そのまま若しくは薬学的に許容され得る担体などと混合し、上述した本発明の固形製剤と同様の方法により製剤化することができる。
本発明の併用剤の一日投与量は、症状、人種、投与対象の年齢、性別、体重、投与形態、有効成分の種類などによって異なるが、副作用の問題とならない範囲であれば特に限定されない。本発明の併用剤の一日投与量は、例えば経口投与の場合、水難溶性低融点物質と併用薬物との合計投与量として、通常、哺乳動物1kg体重あたり約0.005〜100mg、好ましくは約0.05〜50mgであり、更に好ましくは約0.2〜30mgであり、これを通常1日1〜3回に分けて投与する。
本発明の併用剤を投与するに際しては、本発明の固形製剤と併用薬物とを同時期に投与してもよいが、併用薬物を先に投与した後、本発明の固形製剤を投与してもよいし、本発明の固形製剤を先に投与し、その後で併用薬物を投与してもよい。時間差をおいて投与する場合、時間差は投与する有効成分、剤形、投与方法により異なるが、例えば、併用薬物を先に投与する場合、併用薬物を投与した後1分〜3日以内、好ましくは10分〜1日以内、より好ましくは15分〜1時間以内に本発明の固形製剤を投与する方法が挙げられる。本発明の固形製剤を先に投与する場合、本発明の固形製剤を投与した後、1分〜1日以内、好ましくは10分〜6時間以内、より好ましくは15分から1時間以内に併用薬物を投与する方法が挙げられる。
本発明の併用剤において、併用剤全体に対する本発明の固形製剤の含有量は、併用剤の形態によって相違するが、通常、0.3重量%〜65重量%、好ましくは0.1重量%〜50重量%、さらに好ましくは0.5重量%〜20重量%程度である。
なお、以下の実施例および比較例において、ステアリン酸マグネシウムなどの各種添加剤としては、日本薬局方第14改正適合品あるいは医薬品添加物規格2003適合品を用いた。
また、以下の実施例および比較例において記載する錠剤の硬度(破壊硬度)は、ファルマテスト(PHARMA TEST APPARATEBAU GMBH、WHT 2ME)を用いて測定した。
[実施例1]
化合物A 660.0g(平均粒子径:20〜50μm)、マンニトール3196g(メルク)、結晶セルロース591.8g(旭化成、商品名:セオラス、グレードPH101)および軽質無水ケイ酸50.6g(日本アエロジル)の混合粉体を流動層造粒機に投入し流動させながら、6%(wt./v)のヒドロキシプロピルセルロース(日本曹達、HPC、グレードL)水溶液 2457gを噴霧して造粒および乾燥し造粒末を得た。得られた造粒末を、1.5mmφパンチングスクリーンを装着したパワーミルで解砕して整粒末とした。この整粒末3911gに対し、クロスカルメロースナトリウム(旭化成、商品名:Ac−Di−Sol)210.9gおよびステアリン酸マグネシウム40.7g(太平洋科学)を添加混合して打錠用顆粒とした。得られた顆粒を打錠機で直径8mmの円型R面の杵を用いて打錠し錠剤重量225mgの素錠を得た。得られた素錠をフィルムコーティング機に投入し、酸化チタン、マクロゴール6000(三洋化成)、三二酸化鉄およびヒドロキシプロピルメチルセルロース2910(信越化学、商品名:TC−5、グレードRW)を精製水に溶解または分散した液を噴霧し、1錠当たり化合物A30mg、マンニトール145.5mg、結晶セルロース26.9mg、軽質無水ケイ酸2.3mg、ヒドロキシプロピルセルロース6.7mg、クロスカルメロースナトリウム11.4mg、ステアリン酸マグネシウム2.2mg、ヒドロキシプロピルメチルセルロース2910 7.2mg、マクロゴール6000 1.6mg、酸化チタン1.0mgおよび三二酸化鉄0.2mgを含有するフィルムコーティング錠、約13500錠を得た。
[実施例2]
化合物A 1140.0g(平均粒子径:20〜50μm)、マンニトール2187g(メルク)、結晶セルロース511.1g(旭化成、商品名:セオラス、グレードPH101)および軽質無水ケイ酸43.7g(日本アエロジル)の混合粉体を流動層造粒機に投入し流動させながら、6%(wt./v)のヒドロキシプロピルセルロース(日本曹達、HPC、グレードL)水溶液 2122gを噴霧して造粒および乾燥し造粒末を得た。得られた造粒末を、1.5mmφパンチングスクリーンを装着したパワーミルで解砕して整粒末とした。この整粒末6828gに対し、クロスカルメロースナトリウム(旭化成、商品名:Ac−Di−Sol)368.2gおよびステアリン酸マグネシウム71.06g(太平洋科学)を添加混合して打錠用顆粒とした。得られた顆粒を打錠機で直径8mmの円型R面の杵を用いて打錠し錠剤重量225mgの素錠を得た。得られた素錠をフィルムコーティング機に投入し、酸化チタン、マクロゴール6000(三洋化成)、三二酸化鉄およびヒドロキシプロピルメチルセルロース2910(信越化学、商品名:TC−5、グレードRW)を精製水に溶解または分散した液を噴霧し、1錠当たり化合物A60mg、マンニトール115.5mg、結晶セルロース26.9mg、軽質無水ケイ酸2.3mg、ヒドロキシプロピルセルロース6.7mg、クロスカルメロースナトリウム11.4mg、ステアリン酸マグネシウム2.2mg、ヒドロキシプロピルメチルセルロース2910 7.2mg、マクロゴール6000 1.6mg、酸化チタン1.0mgおよび三二酸化鉄0.2mgを含有するフィルムコーティング錠、約22500錠を得た。
[実施例3]
化合物A 600.0g(平均粒子径:20〜50μm)、マンニトール2910g(メルク)、結晶セルロース538g(旭化成、商品名:セオラス、グレードPH101)および軽質無水ケイ酸46g(日本アエロジル)の混合粉体を流動層造粒機に投入し流動させながら、6%(wt./v)のヒドロキシプロピルセルロース(日本曹達、HPC、グレードL)水溶液 2234gを噴霧して造粒および乾燥し造粒末を得た。得られた造粒末を、1.5mmφパンチングスクリーンを装着したパワーミルで解砕して整粒末とした。この整粒末3700gに対し、クロスカルメロースナトリウム(旭化成、商品名:Ac−Di−Sol)199.5gおよびステアリン酸マグネシウム38.5g(太平洋科学)を添加混合して打錠用顆粒とした。得られた顆粒を打錠機で直径8mmの円型R面の杵を用いて打錠し錠剤重量225mgの素錠を得た。得られた素錠をフィルムコーティング機に投入し、酸化チタン、マクロゴール6000(三洋化成)、三二酸化鉄およびヒドロキシプロピルメチルセルロース2910(信越化学、商品名:TC−5、グレードRW)を精製水に溶解または分散した液を噴霧し、1錠当たり化合物A30mg、マンニトール145.5mg、結晶セルロース26.9mg、軽質無水ケイ酸2.3mg、ヒドロキシプロピルセルロース6.7mg、クロスカルメロースナトリウム11.4mg、ステアリン酸マグネシウム2.2mg、ヒドロキシプロピルメチルセルロース2910 7.2mg、マクロゴール6000 1.6mg、酸化チタン1.0mgおよび三二酸化鉄0.2mgを含有するフィルムコーティング錠、約15000錠を得た。
[実施例4]
化合物A 1200.0g(平均粒子径:20〜50μm)、マンニトール2310g(メルク)、結晶セルロース538g(旭化成、商品名:セオラス、グレードPH101)および軽質無水ケイ酸46g(日本アエロジル)の混合粉体を流動層造粒機に投入し流動させながら、6%(wt./v)のヒドロキシプロピルセルロース(日本曹達、HPC、グレードL)水溶液 2234gを噴霧して造粒および乾燥し造粒末を得た。得られた造粒末を、1.5mmφパンチングスクリーンを装着したパワーミルで解砕して整粒末とした。この整粒末3700gに対し、クロスカルメロースナトリウム(旭化成、商品名:Ac−Di−Sol)199.5gおよびステアリン酸マグネシウム38.5g(太平洋科学)を添加混合して打錠用顆粒とした。得られた顆粒を打錠機で直径8mmの円型R面の杵を用いて打錠し錠剤重量225mgの素錠を得た。得られた素錠をフィルムコーティング機に投入し、酸化チタン、マクロゴール6000(三洋化成)、三二酸化鉄およびヒドロキシプロピルメチルセルロース2910(信越化学、商品名:TC−5、グレードRW)を精製水に溶解または分散した液を噴霧し、1錠当たり化合物A60mg、マンニトール115.5mg、結晶セルロース26.9mg、軽質無水ケイ酸2.3mg、ヒドロキシプロピルセルロース6.7mg、クロスカルメロースナトリウム11.4mg、ステアリン酸マグネシウム2.2mg、ヒドロキシプロピルメチルセルロース2910 7.2mg、マクロゴール6000 1.6mg、酸化チタン1.0mgおよび三二酸化鉄0.2mgを含有するフィルムコーティング錠、約15000錠を得た。
[実施例5]
化合物A 36.0g(平均粒子径:20〜50μm)、乳糖390.5g(メグレ)および結晶セルロース64.6g(旭化成、商品名:セオラス、グレードPH101)の混合粉体を流動層造粒機に投入し流動させながら、8%(wt./v)のヒドロキシプロピルメチルセルロース2910(信越化学、商品名:TC−5、グレードRW)水溶液 209.9gを噴霧して造粒および乾燥し造粒末を得た。得られた造粒末を16メッシュの篩いでし過して整粒末とした。この整粒末190.3gに対し、クロスカルメロースナトリウム(旭化成、商品名:Ac−Di−Sol)10.3gおよびステアリン酸マグネシウム2.0g(太平洋科学)を添加混合して打錠用顆粒とした。得られた顆粒を打錠機で直径8mmの円型R面の杵を用いて打錠し錠剤重量225mgの素錠を得た。得られた素錠をフィルムコーティング機に投入し、酸化チタン、マクロゴール6000(三洋化成)、三二酸化鉄およびヒドロキシプロピルメチルセルロース2910(信越化学、商品名:TC−5、グレードRW)を精製水に溶解または分散した液を噴霧し、1錠当たり化合物A15mg、乳糖162.8mg、結晶セルロース26.9mg、ヒドロキシプロピルメチルセルロース2910 13.9mg、クロスカルメロースナトリウム11.4mg、ステアリン酸マグネシウム2.2mg、マクロゴール6000 1.6mg、酸化チタン1.0mgおよび三二酸化鉄0.2mgを含有するフィルムコーティング錠、約600錠を得た。
[実施例6]
化合物A 33.0g(平均粒子径:20〜50μm)、マンニトール160.1g(メルク)、結晶セルロース29.6g(旭化成、商品名:セオラス、グレードPH101)および軽質無水ケイ酸2.5g(日本アエロジル)の混合粉体を流動層造粒機に投入し流動させながら、6%(wt./v)のヒドロキシプロピルセルロース(日本曹達、HPC、グレードL)水溶液 115.9gを噴霧して造粒および乾燥し造粒末を得た。得られた造粒末を16メッシュの篩いでし過して整粒末とした。この整粒末200.8gに対し、クロスカルメロースナトリウム(旭化成、商品名:Ac−Di−Sol)10.8gおよびステアリン酸マグネシウム2.1g(太平洋科学)を添加混合して打錠用顆粒とした。得られた顆粒を打錠機で直径8mmの円型R面の杵を用いて打錠し錠剤重量225mgの素錠を得た。得られた素錠をフィルムコーティング機に投入し、酸化チタン、マクロゴール6000(三洋化成)、三二酸化鉄およびヒドロキシプロピルメチルセルロース2910(信越化学、商品名:TC−5、グレードRW)を精製水に溶解または分散した液を噴霧し、1錠当たり化合物A30mg、マンニトール145.5mg、結晶セルロース26.9mg、軽質無水ケイ酸2.3mg、ヒドロキシプロピルセルロース6.7mg、クロスカルメロースナトリウム11.4mg、ステアリン酸マグネシウム2.2mg、ヒドロキシプロピルメチルセルロース2910 7.2mg、マクロゴール6000 1.6mg、酸化チタン1.0mgおよび三二酸化鉄0.2mgを含有するフィルムコーティング錠、約600錠を得た。
[実施例7]
化合物A 85.0g(平均粒子径:20〜50μm)、乳糖410.8g(メグレ)および結晶セルロース85.0g(旭化成、商品名:セオラス、グレードPH101)の混合粉体を流動層造粒機に投入し流動させながら、6%(wt./v)のヒドロキシプロピルセルロース(日本曹達、HPC、グレードL)水溶液 549.0gを噴霧して造粒および乾燥し造粒末を得た。得られた造粒末を16メッシュの篩いでし過して整粒末とした。この整粒末450.0gに対し、クロスカルメロースナトリウム(旭化成、商品名:Ac−Di−Sol)25.5gおよびステアリン酸マグネシウム2.55g(太平洋科学)を添加混合して打錠用顆粒とした。得られた顆粒を打錠機で直径8mmの円型R面の杵を用いて打錠し錠剤重量225mgの素錠を得た。得られた素錠をフィルムコーティング機に投入し、酸化チタン、マクロゴール6000(三洋化成)、三二酸化鉄およびヒドロキシプロピルメチルセルロース2910(信越化学、商品名:TC−5、グレードRW)を精製水に溶解または分散した液を噴霧し、1錠当たり化合物A30mg、乳糖147.8mg、結晶セルロース26.9mg、ヒドロキシプロピルセルロース6.7mg、クロスカルメロースナトリウム11.4mg、ステアリン酸マグネシウム2.2mg、ヒドロキシプロピルメチルセルロース2910 7.2mg、マクロゴール6000 1.6mg、酸化チタン1.0mgおよび三二酸化鉄0.2mgを含有するフィルムコーティング錠、約1200錠を得た。
[実施例8]
化合物A 85.0g(平均粒子径:20〜50μm)、マンニトール410.8g(ロケット)および結晶セルロース85.0g(旭化成、商品名:セオラス、グレードPH101)の混合粉体を流動層造粒機に投入し流動させながら、6%(wt./v)のヒドロキシプロピルセルロース(日本曹達、HPC、グレードL)水溶液 549.0gを噴霧して造粒および乾燥し造粒末を得た。得られた造粒末を16メッシュの篩いでし過して整粒末とした。この整粒末450.0gに対し、クロスカルメロースナトリウム(旭化成、商品名:Ac−Di−Sol)25.5gおよびステアリン酸マグネシウム2.55g(太平洋科学)を添加混合して打錠用顆粒とした。得られた顆粒を打錠機で直径8mmの円型R面の杵を用いて打錠し錠剤重量225mgの素錠を得た。得られた素錠をフィルムコーティング機に投入し、酸化チタン、マクロゴール6000(三洋化成)、三二酸化鉄およびヒドロキシプロピルメチルセルロース2910(信越化学、商品名:TC−5、グレードRW)を精製水に溶解または分散した液を噴霧し、1錠当たり化合物A30mg、マンニトール147.8mg、結晶セルロース26.9mg、ヒドロキシプロピルセルロース6.7mg、クロスカルメロースナトリウム11.4mg、ステアリン酸マグネシウム2.2mg、ヒドロキシプロピルメチルセルロース2910 7.2mg、マクロゴール6000 1.6mg、酸化チタン1.0mgおよび三二酸化鉄0.2mgを含有するフィルムコーティング錠、約1200錠を得た。
[実施例9]
化合物A 85.0g(平均粒子径:20〜50μm)、マンニトール410.8g(ロケット)および結晶セルロース85.0g(旭化成、商品名:セオラス、グレードPH101)の混合粉体を流動層造粒機に投入し流動させながら、6%(wt./v)のヒドロキシプロピルセルロース(日本曹達、HPC、グレードL)水溶液 549.0gを噴霧して造粒および乾燥し造粒末を得た。得られた造粒末を16メッシュの篩いでし過して整粒末とした。この整粒末21.18gに対し、低置換度ヒドロキシプロピルセルロース(信越化学、商品名:L−HPC)1.2gおよびステアリン酸マグネシウム0.12g(太平洋科学)を添加混合して打錠用顆粒とした。得られた顆粒を打錠機で直径8.5mmの隅角平面の杵を用いて打錠し錠剤重量225mgの素錠を約1500錠得た。得られた素錠は、1錠当たり化合物A30mg、マンニトール147.8mg、結晶セルロース26.9mg、ヒドロキシプロピルセルロース6.7mg、低置換度ヒドロキシプロピルセルロース11.4mgおよびステアリン酸マグネシウム2.2mgを含有した。
[実施例10]
化合物A 85.0g(平均粒子径:20〜50μm)、マンニトール410.8g(ロケット)および結晶セルロース85.0g(旭化成、商品名:セオラス、グレードPH101)の混合粉体を流動層造粒機に投入し流動させながら、6%(wt./v)のヒドロキシプロピルセルロース(日本曹達、HPC、グレードL)水溶液 549.0gを噴霧して造粒および乾燥し造粒末を得た。得られた造粒末を16メッシュの篩いでし過して整粒末とした。この整粒末21.18gに対し、カルボキシメチルスターチナトリウム1.2gおよびステアリン酸マグネシウム0.12g(太平洋科学)を添加混合して打錠用顆粒とした。得られた顆粒を打錠機で直径8.5mmの隅角平面の杵を用いて打錠し錠剤重量225mgの素錠を約1200錠得た。得られた素錠は、1錠当たり化合物A30mg、マンニトール147.8mg、結晶セルロース26.9mg、ヒドロキシプロピルセルロース6.7mg、カルボキシメチルスターチナトリウム11.4mgおよびステアリン酸マグネシウム2.2mgを含有した。
[実施例11]
化合物A 108.0g(平均粒子径:20〜50μm)、マンニトール207.9g(ロケット)、結晶セルロース48.4g(旭化成、商品名:セオラス、グレードPH101)および軽質無水ケイ酸(日本アエロジル)の混合粉体を流動層造粒機に投入し流動させながら、6%(wt./v)のヒドロキシプロピルセルロース(日本曹達、HPC、グレードL)水溶液 189.0gを噴霧して造粒および乾燥し造粒末を得た。得られた造粒末を16メッシュの篩いでし過して整粒末とした。この整粒末317.1gに対し、クロスカルメロースナトリウム(旭化成、商品名:Ac−Di−Sol)17.1gおよびステアリン酸マグネシウム3.3g(太平洋科学)を添加混合して打錠用顆粒とした。得られた顆粒を打錠機で直径8mmの丸型の杵を用いて打錠し錠剤重量225mgの素錠を得た。得られた素錠をフィルムコーティング機中に投入し、酸化チタン、マクロゴール6000(三洋化成)、三二酸化鉄およびヒドロキシプロピルメチルセルロース2910(信越化学、商品名:TC−5、グレードRW)を精製水に溶解または分散した液を噴霧し、1錠当たり化合物A60mg、マンニトール115.5mg、結晶セルロース26.9mg、軽質無水ケイ酸2.3mg、ヒドロキシプロピルセルロース6.7mg、クロスカルメロースナトリウム11.4mg、ステアリン酸マグネシウム2.2mg、ヒドロキシプロピルメチルセルロース2910 7.2mg、マクロゴール6000 1.6mg、酸化チタン1.0mgおよび三二酸化鉄0.2mgを含有するフィルムコーティング錠、約800錠を得た。
[実施例12]
化合物A 108.0g(平均粒子径:20〜50μm)、マンニトール207.9g(ロケット)、結晶セルロース48.4g(旭化成、商品名:セオラス、グレードPH101)および軽質無水ケイ酸(日本アエロジル)の混合粉体を流動層造粒機に投入し流動させながら、6%(wt./v)のヒドロキシプロピルセルロース(日本曹達、HPC、グレードL)水溶液 189.0gを噴霧して造粒および乾燥し造粒末を得た。得られた造粒末を16メッシュの篩いでし過して整粒末とした。この整粒末317.1gに対し、クロスカルメロースナトリウム(旭化成、商品名:Ac−Di−Sol)17.1gおよびステアリン酸マグネシウム3.3g(太平洋科学)を添加混合して打錠用顆粒とした。得られた顆粒を打錠機で直径8.5mmの隅角平面の杵を用いて打錠し錠剤重量225mgの素錠を約1000錠得た。得られた素錠は、1錠当たり化合物A60mg、マンニトール115.5mg、結晶セルロース26.9mg、軽質無水ケイ酸2.3mg、ヒドロキシプロピルセルロース6.7mg、クロスカルメロースナトリウム11.4mgおよびステアリン酸マグネシウム2.2mgを含有した。
[実施例13]
化合物A 120.0g(平均粒子径:20〜50μm)、乳糖234.8g(メグレ)および結晶セルロース53.8g(旭化成、商品名:セオラス、グレードPH101)の混合粉体を流動層造粒機に投入し流動させながら、6%(wt./v)のヒドロキシプロピルセルロース(日本曹達、HPC、グレードL)水溶液 210.0gを噴霧して造粒および乾燥し造粒末を得た。得られた造粒末を16メッシュの篩いでし過して整粒末とした。この整粒末370.0gに対し、クロスカルメロースナトリウム(旭化成、商品名:Ac−Di−Sol)20.3gおよびステアリン酸マグネシウム3.9g(太平洋科学)を添加混合して打錠用顆粒とした。得られた顆粒を打錠機で直径8mmの丸型の杵を用いて打錠し錠剤重量225mgの素錠を得た。得られた素錠をフィルムコーティング機に投入し、酸化チタン、マクロゴール6000(三洋化成)、三二酸化鉄およびヒドロキシプロピルメチルセルロース2910(信越化学、商品名:TC−5、グレードRW)を精製水に溶解または分散した液を噴霧し、1錠当たり化合物A60mg、乳糖117.8mg、結晶セルロース26.9mg、ヒドロキシプロピルセルロース6.7mg、クロスカルメロースナトリウム11.4mg、ステアリン酸マグネシウム2.2mg、ヒドロキシプロピルメチルセルロース2910 7.2mg、マクロゴール6000 1.6mg、酸化チタン1.0mgおよび三二酸化鉄0.2mgを含有するフィルムコーティング錠、約600錠を得た。
[実施例14]
化合物A 120.0g(平均粒子径:20〜50μm)、乳糖230.2g(メグレ)、結晶セルロース53.8g(旭化成、商品名:セオラス、グレードPH101)および軽質無水ケイ酸4.6g(日本アエロジル)の混合粉体を流動層造粒機に投入し流動させながら、6%(wt./v)のヒドロキシプロピルセルロース(日本曹達、HPC、グレードL)水溶液 210.0gを噴霧して造粒および乾燥し造粒末を得た。得られた造粒末を16メッシュの篩いでし過して整粒末とした。この整粒末370.0gに対し、クロスカルメロースナトリウム(旭化成、商品名:Ac−Di−Sol)20.0gおよびステアリン酸マグネシウム3.9g(太平洋科学)を添加混合して打錠用顆粒とした。得られた顆粒を打錠機で直径8mmの丸型の杵を用いて打錠し錠剤重量225mgの素錠を得た。得られた素錠をフィルムコーティング機に投入し、酸化チタン、マクロゴール6000(三洋化成)、三二酸化鉄およびヒドロキシプロピルメチルセルロース2910(信越化学、商品名:TC−5、グレードRW)を精製水に溶解または分散した液を噴霧し、1錠当たり化合物A60mg、乳糖115.5mg、結晶セルロース26.9mg、軽質無水ケイ酸2.3mg、ヒドロキシプロピルセルロース6.7mg、クロスカルメロースナトリウム11.4mg、ステアリン酸マグネシウム2.2mg、ヒドロキシプロピルメチルセルロース2910 7.2mg、マクロゴール6000 1.6mg、酸化チタン1.0mgおよび三二酸化鉄0.2mgを含有するフィルムコーティング錠、約600錠を得た。
[実施例15]
化合物A 120.0g(平均粒子径:20〜50μm)、乳糖234.8g(メグレ)および結晶セルロース53.8g(旭化成、商品名:セオラス、グレードPH101)の混合粉体を流動層造粒機に投入し流動させながら、8%(wt./v)のヒドロキシプロピルメチルセルロース2910(信越化学、商品名:TC−5、グレードRW)水溶液 154.2gを噴霧して造粒および乾燥し造粒末を得た。得られた造粒末を16メッシュの篩いでし過して整粒末とした。この整粒末370.0gに対し、クロスカルメロースナトリウム(旭化成、商品名:Ac−Di−Sol)20.0gおよびステアリン酸マグネシウム3.9g(太平洋科学)を添加混合して打錠用顆粒とした。得られた顆粒を打錠機で直径8mmの円型R面の杵を用いて打錠し錠剤重量225mgの素錠を得た。得られた素錠をフィルムコーティング機に投入し、酸化チタン、マクロゴール6000(三洋化成)、三二酸化鉄およびヒドロキシプロピルメチルセルロース2910(信越化学、商品名:TC−5、グレードRW)を精製水に溶解または分散した液を噴霧し、1錠当たり化合物A60mg、乳糖117.8mg、結晶セルロース26.9mg、ヒドロキシプロピルメチルセルロース2910 13.9mg、クロスカルメロースナトリウム11.4mg、ステアリン酸マグネシウム2.2mg、マクロゴール6000 1.6mg、酸化チタン1.0mgおよび三二酸化鉄0.2mgを含有するフィルムコーティング錠、約600錠を得た。
[実施例16]
化合物A 120.0g(平均粒子径:20〜50μm)、乳糖234.8g(メグレ)および結晶セルロース53.8g(旭化成、商品名:セオラス、グレードPH101)の混合粉体を流動層造粒機に投入し流動させながら、8%(wt./v)のヒドロキシプロピルメチルセルロース2910(信越化学、商品名:TC−5、グレードRW)水溶液 154.2gを噴霧して造粒および乾燥し造粒末を得た。得られた造粒末を16メッシュの篩いでし過して整粒末とした。この整粒末370.0gに対し、クロスカルメロースナトリウム(旭化成、商品名:Ac−Di−Sol)20.0gおよびステアリン酸マグネシウム3.9g(太平洋科学)を添加混合して混合末とした。得られた混合末11.25gにアスコルビン酸0.25gを添加混合し打錠用顆粒とした。得られた顆粒を打錠機で直径8mmの円型R面の杵を用いて打錠し錠剤重量230mgの素錠を約1200錠得た。得られた素錠は、1錠当たり化合物A60mg、乳糖117.8mg、結晶セルロース26.9mg、ヒドロキシプロピルメチルセルロース2910 6.7mg、アスコルビン酸5mg、クロスカルメロースナトリウム11.4mgおよびステアリン酸マグネシウム2.2mgを含有した。
[実施例17]
化合物A 120.0g(平均粒子径が20〜50μm)、乳糖234.8g(メグレ)および結晶セルロース53.8g(旭化成、商品名:セオラス、グレードPH101)の混合粉体を流動層造粒機に投入し流動させながら、8%(wt./v)のヒドロキシプロピルメチルセルロース2910(信越化学、商品名:TC−5、グレードRW)水溶液 154.2gを噴霧して造粒および乾燥し造粒末を得た。得られた造粒末を16メッシュの篩いでし過して整粒末とした。この整粒末370.0gに対し、クロスカルメロースナトリウム(旭化成、商品名:Ac−Di−Sol)20.0gおよびステアリン酸マグネシウム3.9g(太平洋科学)を添加混合して混合末とした。得られた混合末11.25gにアスコルビン酸ナトリウム0.25gを添加混合し打錠用顆粒とした。得られた顆粒を打錠機で直径8mmの円型R面の杵を用いて打錠し錠剤重量230mgの素錠を約1200錠得た。得られた素錠は、1錠当たり化合物A60mg、乳糖117.8mg、結晶セルロース26.9mg、ヒドロキシプロピルメチルセルロース2910 6.7mg、アスコルビン酸ナトリウム5mg、クロスカルメロースナトリウム11.4mgおよびステアリン酸マグネシウム2.2mgを含有した。
[実施例18]
化合物A 120.0g(平均粒子径が20〜50μm)、乳糖234.8g(メグレ)および結晶セルロース53.8g(旭化成、商品名:セオラス、グレードPH101)の混合粉体を流動層造粒機に投入し流動させながら、8%(wt./v)のヒドロキシプロピルメチルセルロース2910(信越化学、商品名:TC−5、グレードRW)水溶液 154.2gを噴霧して造粒および乾燥し造粒末を得た。得られた造粒末を16メッシュの篩いでし過して整粒末とした。この整粒末370.0gに対し、クロスカルメロースナトリウム(旭化成、商品名:Ac−Di−Sol)20.0gおよびステアリン酸マグネシウム3.9g(太平洋科学)を添加混合して混合末とした。得られた混合末11.25gにエリソルビン酸0.25gを添加混合し打錠用顆粒とした。得られた顆粒を打錠機で直径8mmの円型R面の杵を用いて打錠し錠剤重量230mgの素錠を約1200錠得た。得られた素錠は、1錠当たり化合物A60mg、乳糖117.8mg、結晶セルロース26.9mg、ヒドロキシプロピルメチルセルロース2910 6.7mg、エリソルビン酸5mg、クロスカルメロースナトリウム11.4mgおよびステアリン酸マグネシウム2.2mgを含有した。
[実施例19]
化合物A 120.0g(平均粒子径:20〜50μm)、乳糖234.8g(メグレ)および結晶セルロース53.8g(旭化成、商品名:セオラス、グレードPH101)の混合粉体を流動層造粒機に投入し流動させながら、8%(wt./v)のヒドロキシプロピルメチルセルロース2910(信越化学、商品名:TC−5、グレードRW)水溶液 154.2gを噴霧して造粒および乾燥し造粒末を得た。得られた造粒末を16メッシュの篩いでし過して整粒末とした。この整粒末370.0gに対し、クロスカルメロースナトリウム(旭化成、商品名:Ac−Di−Sol)20.0gおよびステアリン酸マグネシウム3.9g(太平洋科学)を添加混合して混合末とした。得られた混合末11.25gに2,6−ジ−t−ブチル−4−メチルフェノール0.25gを添加混合し打錠用顆粒とした。得られた顆粒を打錠機で直径8mmの円型R面の杵を用いて打錠し錠剤重量230mgの素錠を約1200錠得た。得られた素錠は、1錠当たり化合物A60mg、乳糖117.8mg、結晶セルロース26.9mg、ヒドロキシプロピルメチルセルロース2910 6.7mg、2,6−ジ−t−ブチル−4−メチルフェノール5mg、クロスカルメロースナトリウム11.4mgおよびステアリン酸マグネシウム2.2mgを含有した。
[実施例20]
化合物A 45.0g(平均粒子径:20〜50μm)、マンニトール220.5g(メルク)および結晶セルロース40.2g(旭化成、商品名:セオラス、グレードPH101)を混合し流動層造粒機に投入し流動させながら、5%(wt./v)のヒドロキシプロピルセルロース(日本曹達、HPC、グレードL)水溶液 214.2gを噴霧して造粒および乾燥し造粒末を得た。得られた造粒末を16メッシュの篩いでし過して整粒末とした。この整粒末273.8gに対し、クロスカルメロースナトリウム(旭化成、商品名:Ac−Di−Sol)14.6gおよびステアリン酸マグネシウム2.9g(太平洋科学)を添加混合して混合末とした。得られた混合末を打錠機で直径6.5mmの円型R面の杵を用いて打錠し錠剤重量112.0mgの素錠を約2000錠得た。得られた素錠は、1錠当たり化合物A15mg、マンニトール73.5mg、結晶セルロース13.4mg、ヒドロキシプロピルセルロース3.4mg、クロスカルメロースナトリウム5.6mgおよびステアリン酸マグネシウム1.1mgを含有した。
[実施例21]
化合物A 75.0g(平均粒子径:20〜50μm)、マンニトール146.3g(メルク)および結晶セルロース33.5g(旭化成、商品名:セオラス、グレードPH101)を混合し流動層造粒機に投入し流動させながら、5%(wt./v)のヒドロキシプロピルセルロース(日本曹達、HPC、グレードL)水溶液 161.5gを噴霧して造粒および乾燥し造粒末を得た。得られた造粒末を16メッシュの篩いでし過して整粒末とした。この整粒末226.4gに対し、クロスカルメロースナトリウム(旭化成、商品名:Ac−Di−Sol)12gおよびステアリン酸マグネシウム2.4g(太平洋科学)を添加混合して混合末とした。得られた混合末を打錠機で直径8mmの隅角平面の杵を用いて打錠し錠剤重量224.0mgの素錠を約1250錠得た。得られた素錠は、1錠当たり化合物A30mg、マンニトール58.5mg、結晶セルロース13.4mg、ヒドロキシプロピルセルロース3.4mg、クロスカルメロースナトリウム5.6mgおよびステアリン酸マグネシウム1.1mgを含有した。
[実施例22]
化合物A 660.0g(平均粒子径:20〜50μm)、マンニトール3226g(メルク)および結晶セルロース589.6g(旭化成、商品名:セオラス、グレードPH101)を混合し流動層造粒機に投入し流動させながら、6%(wt./v)のヒドロキシプロピルセルロース(日本曹達、HPC、グレードL)水溶液に黄色三二酸化鉄4.4gを懸濁した液 2490gを噴霧して造粒および乾燥し造粒末を得た。得られた造粒末を、1.5mmφパンチングスクリーンを装着したパワーミルで解砕して整粒末とした。この整粒末3896gに対し、クロスカルメロースナトリウム(旭化成、商品名:Ac−Di−Sol)207.2gおよびステアリン酸マグネシウム40.7g(太平洋科学)を添加混合して混合末とした。得られた混合末を打錠機で直径6.5mmの隅角平面の杵を用いて打錠し錠剤重量112.0mgの素錠を約20000錠得た。得られた素錠は、1錠当たり化合物A15mg、マンニトール73.4mg、結晶セルロース13.4mg、黄色三二酸化鉄0.1mg、ヒドロキシプロピルセルロース3.5mg、クロスカルメロースナトリウム5.6mgおよびステアリン酸マグネシウム1.1mgを含有した。
[実施例23]
化合物A 1320g(平均粒子径:20〜50μm)、マンニトール2563g(メルク)および結晶セルロース589.6g(旭化成、商品名:セオラス、グレードPH101)を混合し流動層造粒機に投入し流動させながら、6%(wt./v)のヒドロキシプロピルセルロース(日本曹達、HPC、グレードL)水溶液に黄色三二酸化鉄4.4gを懸濁した液 2490gを噴霧して造粒および乾燥し造粒末を得た。得られた造粒末を、1.5mmφパンチングスクリーンを装着したパワーミルで解砕して整粒末とした。この整粒末3896gに対し、クロスカルメロースナトリウム(旭化成、商品名:Ac−Di−Sol)207.2gおよびステアリン酸マグネシウム40.7g(太平洋科学)を添加混合して混合末とした。得られた混合末を打錠機で直径6.5mmの隅角平面の杵を用いて打錠し錠剤重量112.0mgの素錠を約20000錠得た。得られた素錠は、1錠当たり化合物A30mg、マンニトール58.4mg、結晶セルロース13.4mg、黄色三二酸化鉄0.1mg、ヒドロキシプロピルセルロース3.5mg、クロスカルメロースナトリウム5.6mgおよびステアリン酸マグネシウム1.1mgを含有した。
また、得られた素錠の硬度は、70Nであった。
[実施例24]
化合物A 1320g(平均粒子径:20〜50μm)、マンニトール2563g(メルク)および結晶セルロース589.6g(旭化成、商品名:セオラス、グレードPH101)を混合し流動層造粒機に投入し流動させながら、6%(wt./v)のヒドロキシプロピルセルロース(日本曹達、HPC、グレードL)水溶液に黄色三二酸化鉄4.4gを懸濁した液 2495gを噴霧して造粒および乾燥し造粒末を得た。得られた造粒末を、1.5mmφパンチングスクリーンを装着したパワーミルで解砕して整粒末とした。この整粒末3896gに対し、クロスカルメロースナトリウム(旭化成、商品名:Ac−Di−Sol)207.2gおよびステアリン酸マグネシウム40.7g(太平洋科学)を添加混合して混合末とした。得られた混合末を打錠機で直径8.5mmの隅角平面の杵を用いて打錠し錠剤重量224.0mgの素錠を約10000錠得た。得られた素錠は、1錠当たり化合物A60mg、マンニトール116.8mg、結晶セルロース26.8mg、黄色三二酸化鉄0.2mg、ヒドロキシプロピルセルロース7.0mg、クロスカルメロースナトリウム11.2mgおよびステアリン酸マグネシウム2.2mgを含有した。
[実施例25]
化合物A1320g(平均粒子径が20〜50μm)、マンニトール2563g(メルク)、および結晶セルロース589.6g(旭化成、商品名:セオラス、グレードPH101)を混合し流動層造粒機に投入し流動させながら、6%(wt./v)のヒドロキシプロピルセルロース(日本曹達、HPC、グレードL)水溶液に黄色三二酸化鉄4.4gを懸濁した液 2495gを噴霧して造粒および乾燥し造粒末を得た。得られた造粒末を、1.5mmφパンチングスクリーンを装着したパワーミルで解砕して整粒末Aとした。一方、マンニトール3306g(メルク)、および結晶セルロース501.2g(旭化成、商品名:セオラス、グレードPH101)を混合し流動層造粒機に投入し流動させながら、6%(wt./v)のヒドロキシプロピルセルロース(日本曹達、HPC、グレードL)水溶液に黄色三二酸化鉄4.4gを懸濁した液 2117gを噴霧して造粒および乾燥し造粒末を得た。得られた造粒物を、1.5mmφパンチングスクリーンを装着したパワーミルで解砕して整粒末Pとした。
整粒末A731.8gに対し、整粒末P2196gを均一に混合し、クロスカルメロースナトリウム(旭化成、商品名:Ac−Di−Sol)155.7gとステアリン酸マグネシウム30.6g(太平洋科学)を添加混合して混合末とした。得られた混合末を打錠機で直径6.5mmの隅角平面の杵を用いて打錠し錠剤重量112.0mgの素錠を約10000錠得た。得られた素錠は、1錠当たり化合物A7.5mg、マンニトール80.9mg、結晶セルロース13.4mg、黄色三二酸化鉄0.1mg、ヒドロキシプロピルセルロース3.4mg、クロスカルメロースナトリウム5.6mgおよびステアリン酸マグネシウム1.1mgを含有した。
[実施例26]
実施例25の整粒末A1464gに対し、整粒末P1464gを均一に混合し、クロスカルメロースナトリウム(旭化成、商品名:Ac−Di−Sol)155.7gとステアリン酸マグネシウム30.6g(太平洋科学)を添加混合して混合末とした。得られた混合末を打錠機で直径6.5mmの隅角平面の杵を用いて打錠し錠剤重量112.0mgの素錠を約10000錠得た。得られた素錠は、1錠当たり化合物A15.0mg、マンニトール73.4mg、結晶セルロース13.4mg、黄色三二酸化鉄0.1mg、ヒドロキシプロピルセルロース3.4mg、クロスカルメロースナトリウム5.6mgおよびステアリン酸マグネシウム1.1mgを含有した。
[実施例27]
化合物A18000g、マンニトール34980g(ロケット)、および結晶セルロース8040g(旭化成、商品名:セオラス、グレードPH101)を混合し流動層造粒機に投入し流動させながら、ヒドロキシプロピルセルロース2040g(日本曹達、HPC、グレードL)を精製水24Lに溶解した液に、黄色三二酸化鉄60gを精製水7.86Lに懸濁した液を混合した液を、噴霧して造粒および乾燥し造粒末を得た。得られた造粒末を、1.5mmφパンチングスクリーンを装着したパワーミルで解砕して整粒末Aとした。
一方、マンニトール52980g、および結晶セルロース8040g(旭化成、商品名:セオラス、グレードPH101)を混合し流動層造粒機に投入し流動させながら、ヒドロキシプロピルセルロース4080g(日本曹達、HPC、グレードL)を精製水54.4Lに溶解した液に、黄色三二酸化鉄120gを精製水9.32Lに懸濁した液を混合した液を、噴霧して造粒および乾燥し造粒末を得た。得られた造粒物を、1.5mmφパンチングスクリーンを装着したパワーミルで解砕して整粒末Pとした。
整粒末A14990gおよび整粒末P44970gを均一に混合し、クロスカルメロースナトリウム(商品名:Ac−Di−Sol)3249gとステアリン酸マグネシウム627g(太平洋科学)を添加混合して混合末とした。得られた混合末を打錠機で直径6.5mmの隅角平面の杵を用いて打錠し錠剤重量112.0mgの素錠を約550000錠得た。得られた素錠は、1錠当たり化合物A7.5mg、マンニトール80.8mg、結晶セルロース13.4mg、黄色三二酸化鉄0.1mg、ヒドロキシプロピルセルロース3.4mg、クロスカルメロースナトリウム5.7mgおよびステアリン酸マグネシウム1.1mgを含有した。
[実施例28]
実施例27で得た整粒末A29980gおよび整粒末P29980gを均一に混合し、クロスカルメロースナトリウム(商品名:Ac−Di−Sol)3249gとステアリン酸マグネシウム627g(太平洋科学)を添加混合して混合末とした。得られた混合末を打錠機で直径6.5mmの隅角平面の杵を用いて打錠し錠剤重量112.0mgの素錠を約550000錠得た。得られた素錠は、1錠当たり化合物A15.0mg、マンニトール73.3mg、結晶セルロース13.4mg、黄色三二酸化鉄0.1mg、ヒドロキシプロピルセルロース3.4mg、クロスカルメロースナトリウム5.7mgおよびステアリン酸マグネシウム1.1mgを含有した。
[実施例29]
化合物A18000g、マンニトール34980g(ロケット)、および結晶セルロース8040g(旭化成、商品名:セオラス、グレードPH101)を混合し流動層造粒機に投入し流動させながら、ヒドロキシプロピルセルロース2040g(日本曹達、HPC、グレードL)を精製水24Lに溶解した液に、黄色三二酸化鉄60gを精製水7.86Lに懸濁した液を混合した液を、噴霧して造粒および乾燥し造粒末を得た。得られた造粒末を、1.5mmφパンチングスクリーンを装着したパワーミルで解砕して整粒末とした。得られた整粒末55760gに、クロスカルメロースナトリウム(商品名:Ac−Di−Sol)3021gとステアリン酸マグネシウム583g(太平洋科学)を添加混合して混合末とした。得られた混合末を打錠機で直径6.5mmの隅角平面の杵を用いて打錠し錠剤重量112.0mgの素錠を約510000錠得た。得られた素錠は、1錠当たり化合物A30mg、マンニトール58.3mg、結晶セルロース13.4mg、黄色三二酸化鉄0.1mg、ヒドロキシプロピルセルロース3.4mg、クロスカルメロースナトリウム5.7mgおよびステアリン酸マグネシウム1.1mgを含有した。
[実施例30]
化合物A18000g、マンニトール34980g(ロケット)、および結晶セルロース8040g(旭化成、商品名:セオラス、グレードPH101)を混合し流動層造粒機に投入し流動させながら、ヒドロキシプロピルセルロース4080g(日本曹達、HPC、グレードL)を精製水54Lに溶解した液に、黄色三二酸化鉄120gを精製水9.72Lに懸濁した液を混合した液を、噴霧して造粒および乾燥し造粒末を得た。得られた造粒末を、1.5mmφパンチングスクリーンを装着したパワーミルで解砕して整粒末とした。この操作を2回繰り返した。得られた整粒末111500gに、クロスカルメロースナトリウム(商品名:Ac−Di−Sol)6042gとステアリン酸マグネシウム1166g(太平洋科学)を添加混合して混合末とした。得られた混合末を打錠機で直径8.5mmの隅角平面の杵を用いて打錠し錠剤重量224.0mgの素錠を約510000錠得た。得られた素錠は、1錠当たり化合物A60mg、マンニトール116.6mg、結晶セルロース26.8mg、黄色三二酸化鉄0.2mg、ヒドロキシプロピルセルロース6.8mg、クロスカルメロースナトリウム11.4mgおよびステアリン酸マグネシウム2.2mgを含有した。
[実施例31]
実施例29で得られた整粒末2.104gにステアリン酸マグネシウム0.022g(太平洋科学)を添加混合して混合末とした。得られた混合末を打錠機で直径6.5mmの隅角平面の杵を用いて打錠し錠剤重量106.3mgの素錠を約20錠得た。得られた素錠は、1錠当たり化合物A30mg、マンニトール58.3mg、結晶セルロース13.4mg、黄色三二酸化鉄0.1mg、ヒドロキシプロピルセルロース3.4mg、ステアリン酸マグネシウム1.1mgを含有した。
また、得られた素錠の硬度は52Nであり、該素錠が十分な硬度を有することが確認された。
比較例1
化合物A 94.9g、マンニトール184.5g、および結晶セルロース9.5g(旭化成、商品名:セオラス、グレードPH101)を混合し流動層造粒機に投入し流動させながら、ヒドロキシプロピルセルロース10.8g(日本曹達、HPC、グレードL)を精製水204.4mLに溶解した液に、黄色三二酸化鉄0.3gを懸濁した液を噴霧して造粒および乾燥し造粒末を得た。得られた造粒末を16メッシュの篩いでし過して整粒末とした。得られた整粒末1.896gに、ステアリン酸マグネシウム0.018g(太平洋科学)を添加混合して混合末とした。得られた混合末を打錠機で直径6.5mmの隅角平面の杵を用いて打錠し錠剤重量95.7mgの素錠を約20錠得た。得られた素錠は、1錠当たり化合物A30mg、マンニトール58.3mg、結晶セルロース3mg、ヒドロキシプロピルセルロース3.4mg、黄色三二酸化鉄0.1mg、ステアリン酸マグネシウム0.9mgを含有した。
また、得られた素錠の硬度は、57Nであった。
比較例2
化合物A 85.5g、マンニトール102.3g、および結晶セルロース102.3g(旭化成、商品名:セオラス、グレードPH101)を混合し流動層造粒機に投入し流動させながら、ヒドロキシプロピルセルロース9.7g(日本曹達、HPC、グレードL)を精製水184mLに溶解した液に、黄色三二酸化鉄0.3gを懸濁した液を噴霧して造粒および乾燥し造粒末を得た。得られた造粒末を16メッシュの篩いでし過して整粒末とした。得られた整粒末2.106gに、ステアリン酸マグネシウム0.03g(太平洋科学)を添加混合して混合末とした。得られた混合末を打錠機で直径6.5mmの隅角平面の杵を用いて打錠し錠剤重量106.8mgの素錠を約20錠得た。得られた素錠は、1錠当たり化合物A30mg、マンニトール35.9mg、結晶セルロース35.9mg、ヒドロキシプロピルセルロース3.4mg、黄色三二酸化鉄0.1mg、ステアリン酸マグネシウム1.1mgを含有した。
また、得られた素錠の硬度は、60Nであった。
実験例1
実施例および比較例で得られた錠剤について、第14改正日本薬局方記載の崩壊試験を行い、崩壊時間を測定した。なお、試験液としては水を使用し、補助板は使用しなかった。結果を表1に示す。表中の崩壊時間は、錠剤6個の平均値である。
実験例2
実施例23で得られた錠剤について、一定期間保存後に、実験例1と同様にして、崩壊時間を測定した。
その結果、「イニシャル(保存前)」、「6ヶ月間、40℃乾燥剤入りガラス瓶密栓保存後」および「6ヶ月間、40℃で相対湿度(RH)75%の環境に開栓保存後」の崩壊時間(各錠剤5個の平均値)は、それぞれ5.6分、4.8分、4.6分であった。
すなわち、本発明の固形製剤は、保存前と長期保存後で同等の崩壊時間を有しており、優れた保存安定性を有することが示された。
実験例3
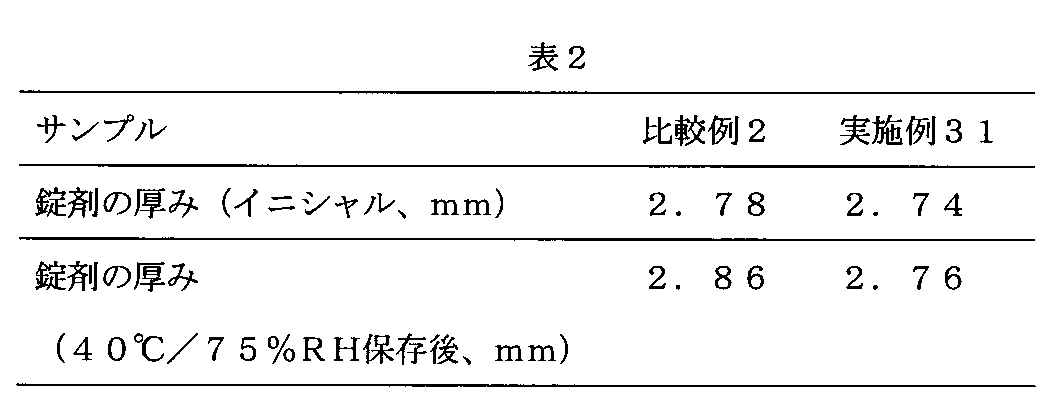
実施例および比較例で得られた錠剤について、40℃/75%RHの環境に開栓条件で3日間保存後の外観変化を評価した。外観変化の評価は、錠剤の厚みを厚みゲージで測定し、保存前の錠剤の厚みと比較することにより行った。結果を表2に示す。表中の厚みは、錠剤5個の平均値である。
すなわち、本発明の固形製剤は、同等の硬度および厚みを有する対照製剤と比較して、優れた保存安定性(吸湿による製剤の膨れの抑制)を有することが示された。
また、本発明の固形製剤は、水難溶性低融点物質を多量に含んでいても、製造中および保存中の安定性に優れ、かつ経口投与後の崩壊特性および水難溶性低融点物質の放出特性に優れている。
本発明の製造方法は、水難溶性低融点物質の融点以下となる温度条件下で行うことができるため、水難溶性低融点物質を加熱溶融する必要がない。したがって、本発明の製造方法は、水難溶性低融点物質を分解させることなく、固形製剤を製造するための簡便な製造方法として極めて有用である。
本出願は、2005年6月9日に日本で出願された特願2005−170172を基礎としており、その内容は本明細書中に援用される。
Claims (11)
- 以下の1)〜3)の特徴を有する固形製剤。
1)2−ヘキサデシルオキシ−6−メチル−4H−3,1−ベンズオキサジン−4−オンまたはその塩、糖アルコール類、ならびに結晶セルロースを含む。
2)糖アルコール類/結晶セルロースの重量比が2を超える。
3)結晶セルロースの含量が5重量%以上である。 - 2−ヘキサデシルオキシ−6−メチル−4H−3,1−ベンズオキサジン−4−オンまたはその塩の平均粒子径が1〜100μmである請求項1記載の固形製剤。
- 糖アルコール類がマンニトールである請求項1記載の固形製剤。
- 2−ヘキサデシルオキシ−6−メチル−4H−3,1−ベンズオキサジン−4−オンまたはその塩の含量が5〜60重量%である請求項1記載の固形製剤。
- 糖アルコール類の含量が30〜75重量%である請求項1記載の固形製剤。
- 結晶セルロースの含量が5〜15重量%である請求項1記載の固形製剤。
- 糖アルコール類/結晶セルロースの重量比が3〜9である請求項1記載の固形製剤。
- 錠剤である請求項1記載の固形製剤。
- 37℃の水中での崩壊時間が30分以内である請求項1記載の固形製剤。
- 2−ヘキサデシルオキシ−6−メチル−4H−3,1−ベンズオキサジン−4−オンまたはその塩、糖アルコール類、ならびに結晶セルロースを含む混合物を造粒することを含む、請求項1記載の固形製剤の製造方法。
- 前記造粒が流動層造粒機を用いて行われる、請求項10記載の方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2007520212A JP5044398B2 (ja) | 2005-06-09 | 2006-06-09 | 固形製剤 |
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2005170172 | 2005-06-09 | ||
| JP2005170172 | 2005-06-09 | ||
| JP2007520212A JP5044398B2 (ja) | 2005-06-09 | 2006-06-09 | 固形製剤 |
| PCT/JP2006/312078 WO2006132440A1 (ja) | 2005-06-09 | 2006-06-09 | 固形製剤 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPWO2006132440A1 JPWO2006132440A1 (ja) | 2009-01-08 |
| JP5044398B2 true JP5044398B2 (ja) | 2012-10-10 |
Family
ID=37498616
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2007520212A Expired - Fee Related JP5044398B2 (ja) | 2005-06-09 | 2006-06-09 | 固形製剤 |
Country Status (10)
| Country | Link |
|---|---|
| US (2) | US20090208584A1 (ja) |
| EP (1) | EP1897558B1 (ja) |
| JP (1) | JP5044398B2 (ja) |
| CA (1) | CA2611451C (ja) |
| DK (1) | DK1897558T3 (ja) |
| ES (1) | ES2434072T3 (ja) |
| PL (1) | PL1897558T3 (ja) |
| PT (1) | PT1897558E (ja) |
| SI (1) | SI1897558T1 (ja) |
| WO (1) | WO2006132440A1 (ja) |
Families Citing this family (21)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2008136392A1 (ja) * | 2007-04-27 | 2008-11-13 | Ajinomoto Co., Inc. | 経口投与用製剤 |
| JP2010529142A (ja) | 2007-06-08 | 2010-08-26 | アドレネクス・ファーマシューティカルズ,インコーポレイテッド | アドレナリン調節異常症を治療する徐放性の製剤および方法 |
| US20100172991A1 (en) * | 2007-06-08 | 2010-07-08 | Henry Joseph Horacek | Extended Release Formulation and Methods of Treating Adrenergic Dysregulation |
| US8486452B2 (en) * | 2007-07-20 | 2013-07-16 | Mylan Pharmaceuticals Inc. | Stabilized tolterodine tartrate formulations |
| EP2233129B1 (en) | 2007-12-28 | 2014-05-07 | Sawai Pharmaceutical Co., Ltd. | Oral cavity disintegrating tablet and method of producing the same |
| AR072883A1 (es) * | 2008-07-31 | 2010-09-29 | Takeda Pharmaceutical | COMPOSICIoN FARMACÉUTICA SoLIDA CON EL COMPUESTO (5-METIL-2-OXO-1,3-DIOXOL-4-IL)METIL2-ETOXI-1-{[2' -(5-OXO-4,5-DIHIDRO-1,2,4-OXADIAZOL-3-IL)BIFENIL-4-IL]METIL}-1H-BENCIMIDAZOL-7-CARBOXILATO Y UN DIURÉTICO PARA LA PROFILAXIS O TRATAMIENTO DE ENFERMEDADES DEL APARATO CIRCULATORIO. |
| TW201014850A (en) * | 2008-09-25 | 2010-04-16 | Takeda Pharmaceutical | Solid pharmaceutical composition |
| JP2010254623A (ja) | 2009-04-24 | 2010-11-11 | Takeda Chem Ind Ltd | ベンゾオキサジノン化合物の結晶 |
| EP2460523B1 (en) * | 2009-07-28 | 2017-01-04 | Takeda Pharmaceutical Company Limited | Tablet |
| EP2366378A1 (en) | 2010-03-01 | 2011-09-21 | Dexcel Pharma Technologies Ltd. | Sustained-release donepezil formulations |
| TWI511967B (zh) | 2010-06-16 | 2015-12-11 | Takeda Pharmaceutical | 醯胺化合物之結晶 |
| MX2014000253A (es) * | 2011-07-07 | 2014-10-17 | Arqule Inc | Formulaciones de pirroloquinolinil-pirrolidin-2,5-diona y metodos para preparar y utilizar las mismas. |
| CN103889908B (zh) * | 2011-10-19 | 2016-04-06 | 日本曹达株式会社 | 尿石抑制剂 |
| GB201122213D0 (en) * | 2011-12-23 | 2012-02-01 | Norgine Bv | Compositions |
| AU2012101841A4 (en) * | 2011-12-23 | 2013-01-17 | Norgine Bv | Compositions comprising cetilistat |
| WO2013092786A1 (en) * | 2011-12-23 | 2013-06-27 | Norgine B.V. | Compositions comprising cetilistat |
| WO2013122260A1 (en) * | 2012-02-15 | 2013-08-22 | Takeda Pharmaceutical Company Limited | Tablet |
| DE202012104963U1 (de) | 2012-12-19 | 2013-01-14 | Norgine B.V. | Cetilistat aufweisende Zusammensetzungen |
| JP5686452B2 (ja) * | 2013-03-01 | 2015-03-18 | 塩野義製薬株式会社 | イルベサルタンを含有する錠剤 |
| CN104971051A (zh) * | 2014-04-11 | 2015-10-14 | 刘小斌 | 一种赛利司他片及制备方法 |
| CN106310287B (zh) * | 2015-06-25 | 2019-03-19 | 山东省药学科学院 | 新利司他药用组合物及其制备方法 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH0753409A (ja) * | 1993-08-05 | 1995-02-28 | F Hoffmann La Roche Ag | 医薬調製物 |
| JP2000273039A (ja) * | 1999-01-20 | 2000-10-03 | Taisho Pharmaceut Co Ltd | 口腔内崩壊性組成物 |
| WO2004060401A1 (en) * | 2002-12-17 | 2004-07-22 | The Procter & Gamble Company | Compositions, methods, and kits useful for the alleviation of gastrointestinal side effects of lipase inhibitors |
Family Cites Families (37)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB224671A (en) | 1923-10-03 | 1924-11-20 | Ismay Annie Fownes | Improvements in and relating to wire-netting fencing |
| JPS5116491B2 (ja) | 1971-10-08 | 1976-05-25 | ||
| US4623588A (en) * | 1984-02-06 | 1986-11-18 | Biotek, Inc. | Controlled release composite core coated microparticles |
| JP2842244B2 (ja) * | 1993-09-21 | 1998-12-24 | 武田薬品工業株式会社 | イデベノン粒剤およびその製造法 |
| JP3532999B2 (ja) * | 1995-03-24 | 2004-05-31 | 株式会社ロッテ | 新規なタンニン類およびこれを有効成分とするリパーゼ阻害剤 |
| AU6944296A (en) | 1995-09-13 | 1997-04-01 | Takeda Chemical Industries Ltd. | Benzoxazepine compounds, their production and use as lipid lowering agents |
| EP0839526A3 (en) * | 1996-10-31 | 1999-01-07 | Takeda Chemical Industries, Ltd. | Solid pharmaceutical preparation with fast buccal disintegration or dissolution |
| JPH10182436A (ja) * | 1996-10-31 | 1998-07-07 | Takeda Chem Ind Ltd | 固形医薬製剤 |
| US6172095B1 (en) * | 1996-11-25 | 2001-01-09 | The Procter & Gamble Company | Guanidinylamino heterocycle compounds useful as alpha-2 adrenoceptor agonists |
| US6004996A (en) * | 1997-02-05 | 1999-12-21 | Hoffman-La Roche Inc. | Tetrahydrolipstatin containing compositions |
| US6057338A (en) | 1997-04-04 | 2000-05-02 | Merck & Co., Inc. | Somatostatin agonists |
| US6025372A (en) | 1997-04-04 | 2000-02-15 | Merck & Co., Inc. | Somatostatin agonists |
| JP3926888B2 (ja) * | 1997-05-27 | 2007-06-06 | 株式会社カネカ | コレステロール低下剤 |
| AU1285499A (en) | 1997-10-30 | 1999-05-24 | Merck & Co., Inc. | Somatostatin agonists |
| ATE291418T1 (de) * | 1998-07-28 | 2005-04-15 | Takeda Pharmaceutical | Leicht zerfallende feste zubereitung |
| TR200100471T2 (tr) | 1998-08-14 | 2001-07-23 | F.Hoffmann-La Roche Ag | Lipaz inhibitörleri içeren farmasötik bileşimler |
| US7815937B2 (en) * | 1998-10-27 | 2010-10-19 | Biovail Laboratories International Srl | Quick dissolve compositions and tablets based thereon |
| AR022204A1 (es) * | 1999-01-08 | 2002-09-04 | Norgine Bv | Compuesto, proceso para su preparacion, composicion farmaceutica y producto comestible que lo comprende. |
| US6740339B1 (en) * | 1999-06-18 | 2004-05-25 | Takeda Chemical Industries, Ltd. | Quickly disintegrating solid preparations |
| AR035016A1 (es) | 1999-08-25 | 2004-04-14 | Takeda Chemical Industries Ltd | Composicion de azol promotor de produccion/secrecion de neurotrofina, compuesto prodroga del mismo, composicion farmaceutica que lo comprende y uso del mismo para preparar esta ultima. |
| AR025587A1 (es) * | 1999-09-13 | 2002-12-04 | Hoffmann La Roche | Formulaciones en dispersion que contienen inhibidores de lipasa |
| EP1227090A4 (en) | 1999-10-07 | 2002-11-20 | Tadeka Chemical Ind Ltd | AMINE DERIVATIVES |
| HK1045991B (en) | 1999-11-10 | 2004-12-10 | Takeda Pharmaceutical Company Limited | 5-membered n-heterocyclic compounds with hypoglycemic and hypolipidemic activity |
| EP1285651B1 (en) | 2000-04-28 | 2010-09-01 | Takeda Pharmaceutical Company Limited | Melanin concentrating hormone antagonists |
| JP2001316249A (ja) * | 2000-05-11 | 2001-11-13 | Lion Corp | 錠剤型医薬組成物 |
| US7229986B2 (en) | 2000-05-16 | 2007-06-12 | Takeda Pharmaceutical Company Ltd. | Melanin-concentrating hormone antagonist |
| JP2001335469A (ja) * | 2000-05-26 | 2001-12-04 | Lion Corp | 固体製剤の製造方法 |
| NZ523684A (en) * | 2000-07-28 | 2005-04-29 | F | New pharmaceutical composition |
| US6967212B2 (en) * | 2001-05-30 | 2005-11-22 | Bristol-Myers Squibb Company | Substituted azole acid derivatives useful as antidiabetic and antiobesity agents and method |
| US20030027786A1 (en) * | 2001-06-06 | 2003-02-06 | Karsten Maeder | Lipase inhibiting composition |
| WO2003042204A1 (en) | 2001-10-19 | 2003-05-22 | Takeda Chemical Industries, Ltd. | Amine derivative |
| WO2003039516A1 (en) * | 2001-11-07 | 2003-05-15 | Fujisawa Pharmaceuticla Co., Ltd. | Method for improving dissolution of poorly dispersible medicaments |
| SI21301A (sl) * | 2002-09-11 | 2004-04-30 | LEK farmacevtska dru�ba d.d. | Farmacevtska oblika z nadzorovanim sproščanjem |
| EP1593681A4 (en) * | 2003-02-07 | 2007-09-05 | Takeda Pharmaceutical | TRICYCLIC COMPOUND, PROCESS FOR THEIR PREPARATION AND USE |
| US20050143441A1 (en) * | 2003-10-27 | 2005-06-30 | Jochen Antel | Novel medical combination treatment of obesity involving 4,5-dihydro-1H-pyrazole derivatives having CB1-antagonistic activity |
| JP2005170172A (ja) | 2003-12-10 | 2005-06-30 | Ogura Clutch Co Ltd | 車両室内用遮蔽装置 |
| US20060246141A1 (en) * | 2005-04-12 | 2006-11-02 | Elan Pharma International, Limited | Nanoparticulate lipase inhibitor formulations |
-
2006
- 2006-06-09 SI SI200631694T patent/SI1897558T1/sl unknown
- 2006-06-09 ES ES06747305T patent/ES2434072T3/es active Active
- 2006-06-09 CA CA2611451A patent/CA2611451C/en not_active Expired - Fee Related
- 2006-06-09 EP EP06747305.8A patent/EP1897558B1/en not_active Not-in-force
- 2006-06-09 DK DK06747305.8T patent/DK1897558T3/da active
- 2006-06-09 WO PCT/JP2006/312078 patent/WO2006132440A1/ja not_active Ceased
- 2006-06-09 PT PT67473058T patent/PT1897558E/pt unknown
- 2006-06-09 JP JP2007520212A patent/JP5044398B2/ja not_active Expired - Fee Related
- 2006-06-09 PL PL06747305T patent/PL1897558T3/pl unknown
- 2006-06-09 US US11/921,664 patent/US20090208584A1/en not_active Abandoned
-
2014
- 2014-02-26 US US14/190,528 patent/US20140178477A1/en not_active Abandoned
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH0753409A (ja) * | 1993-08-05 | 1995-02-28 | F Hoffmann La Roche Ag | 医薬調製物 |
| JP2000273039A (ja) * | 1999-01-20 | 2000-10-03 | Taisho Pharmaceut Co Ltd | 口腔内崩壊性組成物 |
| WO2004060401A1 (en) * | 2002-12-17 | 2004-07-22 | The Procter & Gamble Company | Compositions, methods, and kits useful for the alleviation of gastrointestinal side effects of lipase inhibitors |
Also Published As
| Publication number | Publication date |
|---|---|
| SI1897558T1 (sl) | 2014-03-31 |
| PL1897558T3 (pl) | 2014-01-31 |
| EP1897558A4 (en) | 2012-09-12 |
| US20140178477A1 (en) | 2014-06-26 |
| US20090208584A1 (en) | 2009-08-20 |
| WO2006132440A1 (ja) | 2006-12-14 |
| CA2611451A1 (en) | 2006-12-14 |
| PT1897558E (pt) | 2013-11-06 |
| ES2434072T3 (es) | 2013-12-13 |
| DK1897558T3 (da) | 2013-12-09 |
| CA2611451C (en) | 2014-04-22 |
| EP1897558B1 (en) | 2013-09-04 |
| EP1897558A1 (en) | 2008-03-12 |
| JPWO2006132440A1 (ja) | 2009-01-08 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5044398B2 (ja) | 固形製剤 | |
| JP5284967B2 (ja) | 打錠障害を生じない錠剤製剤 | |
| JP5432720B2 (ja) | 2−[[6−[(3r)−3−アミノ−1−ピペリジニル]−3,4−ジヒドロ−3−メチル−2,4−ジオキソ−1(2h)−ピリミジニル]メチル]−4−フルオロベンゾニトリルを含む固形製剤 | |
| JP5276991B2 (ja) | 固形製剤 | |
| JP5162475B2 (ja) | ピオグリタゾンを含有する経口剤 | |
| KR20090109115A (ko) | 알로그립틴 및 피오글리타존을 포함하는 고형 제제 | |
| KR20100036367A (ko) | 알로그립틴 및 메트포르민 히드로클로라이드를 포함하는 고체 제제 | |
| JP5179363B2 (ja) | 固形製剤 | |
| CN102482235B (zh) | 苯并噁嗪酮化合物的结晶 | |
| CA2738147C (en) | Solid pharmaceutical composition | |
| KR20060016787A (ko) | 고형 약학 제제 | |
| EP1677792B1 (en) | Solid preparation comprising pioglitazone, glimepiride and a polyoxyethylene sorbitan fatty acid ester | |
| JPWO2005099760A1 (ja) | 固形製剤 | |
| JP4361461B2 (ja) | 固形製剤 | |
| JP2005220024A (ja) | 被覆製剤の製造方法 | |
| JP2005015477A (ja) | 固形製剤 | |
| JP2008222646A (ja) | 固形製剤 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20090415 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20120417 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120604 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20120703 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20120713 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5044398 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20150720 Year of fee payment: 3 |
|
| R153 | Grant of patent term extension |
Free format text: JAPANESE INTERMEDIATE CODE: R153 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |