JP4828112B2 - プロトン伝導性高分子材料並びにこれを用いた固体電解質膜、電気化学セル及び燃料電池 - Google Patents
プロトン伝導性高分子材料並びにこれを用いた固体電解質膜、電気化学セル及び燃料電池 Download PDFInfo
- Publication number
- JP4828112B2 JP4828112B2 JP2004308139A JP2004308139A JP4828112B2 JP 4828112 B2 JP4828112 B2 JP 4828112B2 JP 2004308139 A JP2004308139 A JP 2004308139A JP 2004308139 A JP2004308139 A JP 2004308139A JP 4828112 B2 JP4828112 B2 JP 4828112B2
- Authority
- JP
- Japan
- Prior art keywords
- group
- sulfonic acid
- substituent
- carboxylic acid
- proton
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 239000012528 membrane Substances 0.000 title claims abstract description 79
- 239000007784 solid electrolyte Substances 0.000 title claims abstract description 75
- 229920001940 conductive polymer Polymers 0.000 title claims abstract description 63
- 239000000446 fuel Substances 0.000 title claims abstract description 39
- -1 ELECTROCHEMICAL CELL Substances 0.000 title claims description 71
- 239000002861 polymer material Substances 0.000 title claims description 39
- 150000001875 compounds Chemical group 0.000 claims abstract description 81
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 claims abstract description 71
- 239000002322 conducting polymer Substances 0.000 claims abstract description 12
- 239000000463 material Substances 0.000 claims abstract description 11
- 229920000642 polymer Polymers 0.000 claims description 112
- 125000001424 substituent group Chemical group 0.000 claims description 112
- 125000000542 sulfonic acid group Chemical group 0.000 claims description 74
- 125000004432 carbon atom Chemical group C* 0.000 claims description 49
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 39
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 claims description 38
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 claims description 32
- 125000002252 acyl group Chemical group 0.000 claims description 31
- 125000003545 alkoxy group Chemical group 0.000 claims description 31
- 125000005843 halogen group Chemical group 0.000 claims description 31
- 125000003277 amino group Chemical group 0.000 claims description 30
- 125000004093 cyano group Chemical group *C#N 0.000 claims description 30
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 30
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 claims description 30
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 claims description 30
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 claims description 29
- 125000003262 carboxylic acid ester group Chemical group [H]C([H])([*:2])OC(=O)C([H])([H])[*:1] 0.000 claims description 29
- 125000002843 carboxylic acid group Chemical group 0.000 claims description 29
- 125000005034 trifluormethylthio group Chemical group FC(S*)(F)F 0.000 claims description 29
- 125000002130 sulfonic acid ester group Chemical group 0.000 claims description 25
- 125000001567 quinoxalinyl group Chemical group N1=C(C=NC2=CC=CC=C12)* 0.000 claims description 24
- 125000000217 alkyl group Chemical group 0.000 claims description 20
- 125000000732 arylene group Chemical group 0.000 claims description 15
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 15
- 239000000178 monomer Substances 0.000 claims description 15
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 claims description 14
- 125000003118 aryl group Chemical group 0.000 claims description 14
- 239000002253 acid Substances 0.000 claims description 13
- 239000003792 electrolyte Substances 0.000 claims description 13
- 150000002391 heterocyclic compounds Chemical group 0.000 claims description 13
- 239000000203 mixture Substances 0.000 claims description 13
- 125000003785 benzimidazolyl group Chemical group N1=C(NC2=C1C=CC=C2)* 0.000 claims description 11
- 239000007772 electrode material Substances 0.000 claims description 11
- 125000005842 heteroatom Chemical group 0.000 claims description 10
- 125000002883 imidazolyl group Chemical group 0.000 claims description 10
- 229910052757 nitrogen Inorganic materials 0.000 claims description 10
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 claims description 9
- 150000007513 acids Chemical class 0.000 claims description 9
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 claims description 8
- 125000003342 alkenyl group Chemical group 0.000 claims description 8
- 229910000147 aluminium phosphate Inorganic materials 0.000 claims description 8
- 229920001400 block copolymer Polymers 0.000 claims description 8
- 125000002947 alkylene group Chemical group 0.000 claims description 7
- 125000001570 methylene group Chemical group [H]C([H])([*:1])[*:2] 0.000 claims description 7
- 239000007773 negative electrode material Substances 0.000 claims description 7
- FERIUCNNQQJTOY-UHFFFAOYSA-N Butyric acid Chemical compound CCCC(O)=O FERIUCNNQQJTOY-UHFFFAOYSA-N 0.000 claims description 6
- XBDQKXXYIPTUBI-UHFFFAOYSA-N dimethylselenoniopropionate Natural products CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 claims description 6
- IUVKMZGDUIUOCP-BTNSXGMBSA-N quinbolone Chemical compound O([C@H]1CC[C@H]2[C@H]3[C@@H]([C@]4(C=CC(=O)C=C4CC3)C)CC[C@@]21C)C1=CCCC1 IUVKMZGDUIUOCP-BTNSXGMBSA-N 0.000 claims description 6
- 125000000472 sulfonyl group Chemical group *S(*)(=O)=O 0.000 claims description 6
- 239000007774 positive electrode material Substances 0.000 claims description 5
- PNGLEYLFMHGIQO-UHFFFAOYSA-M sodium;3-(n-ethyl-3-methoxyanilino)-2-hydroxypropane-1-sulfonate;dihydrate Chemical compound O.O.[Na+].[O-]S(=O)(=O)CC(O)CN(CC)C1=CC=CC(OC)=C1 PNGLEYLFMHGIQO-UHFFFAOYSA-M 0.000 claims description 5
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 claims description 4
- 150000002460 imidazoles Chemical class 0.000 claims description 4
- 229910017604 nitric acid Inorganic materials 0.000 claims description 4
- KGBXLFKZBHKPEV-UHFFFAOYSA-N boric acid Chemical compound OB(O)O KGBXLFKZBHKPEV-UHFFFAOYSA-N 0.000 claims description 3
- 239000004327 boric acid Substances 0.000 claims description 3
- 150000004652 butanoic acids Chemical class 0.000 claims description 3
- 235000019260 propionic acid Nutrition 0.000 claims description 3
- 125000004185 ester group Chemical group 0.000 claims description 2
- GYPCWHHQAVLMKO-XXKQIVDLSA-N (7s,9s)-7-[(2r,4s,5s,6s)-4-amino-5-hydroxy-6-methyloxan-2-yl]oxy-6,9,11-trihydroxy-9-[(e)-n-[(1-hydroxy-2,2,6,6-tetramethylpiperidin-4-ylidene)amino]-c-methylcarbonimidoyl]-4-methoxy-8,10-dihydro-7h-tetracene-5,12-dione;hydrochloride Chemical group Cl.O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(\C)=N\N=C1CC(C)(C)N(O)C(C)(C)C1)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 GYPCWHHQAVLMKO-XXKQIVDLSA-N 0.000 claims 2
- 125000001273 sulfonato group Chemical group [O-]S(*)(=O)=O 0.000 claims 2
- 150000007942 carboxylates Chemical group 0.000 claims 1
- 150000001735 carboxylic acids Chemical class 0.000 claims 1
- 125000000623 heterocyclic group Chemical group 0.000 claims 1
- XSCHRSMBECNVNS-UHFFFAOYSA-N quinoxaline Chemical compound N1=CC=NC2=CC=CC=C21 XSCHRSMBECNVNS-UHFFFAOYSA-N 0.000 abstract description 42
- 238000012360 testing method Methods 0.000 description 25
- 238000000034 method Methods 0.000 description 24
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 21
- 238000005259 measurement Methods 0.000 description 20
- 238000006277 sulfonation reaction Methods 0.000 description 19
- 238000005227 gel permeation chromatography Methods 0.000 description 16
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 15
- 239000003054 catalyst Substances 0.000 description 15
- 238000006243 chemical reaction Methods 0.000 description 15
- 239000007864 aqueous solution Substances 0.000 description 14
- 238000000921 elemental analysis Methods 0.000 description 13
- 238000006116 polymerization reaction Methods 0.000 description 13
- 239000002994 raw material Substances 0.000 description 13
- 238000002329 infrared spectrum Methods 0.000 description 12
- 239000013076 target substance Substances 0.000 description 12
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 11
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 10
- SIKJAQJRHWYJAI-UHFFFAOYSA-N Indole Chemical compound C1=CC=C2NC=CC2=C1 SIKJAQJRHWYJAI-UHFFFAOYSA-N 0.000 description 9
- 229910052799 carbon Inorganic materials 0.000 description 9
- 230000000694 effects Effects 0.000 description 9
- 238000011156 evaluation Methods 0.000 description 9
- 239000000243 solution Substances 0.000 description 9
- 239000004693 Polybenzimidazole Substances 0.000 description 8
- 239000012298 atmosphere Substances 0.000 description 8
- 229920002480 polybenzimidazole Polymers 0.000 description 8
- 239000002904 solvent Substances 0.000 description 8
- 239000003990 capacitor Substances 0.000 description 7
- 229920001577 copolymer Polymers 0.000 description 7
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 7
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 6
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 6
- 239000001257 hydrogen Substances 0.000 description 6
- 229910052739 hydrogen Inorganic materials 0.000 description 6
- 239000003273 ketjen black Substances 0.000 description 6
- RLSSMJSEOOYNOY-UHFFFAOYSA-N m-cresol Chemical compound CC1=CC=CC(O)=C1 RLSSMJSEOOYNOY-UHFFFAOYSA-N 0.000 description 6
- 229910052760 oxygen Inorganic materials 0.000 description 6
- 239000001301 oxygen Substances 0.000 description 6
- 239000007787 solid Substances 0.000 description 6
- AZQWKYJCGOJGHM-UHFFFAOYSA-N 1,4-benzoquinone Chemical compound O=C1C=CC(=O)C=C1 AZQWKYJCGOJGHM-UHFFFAOYSA-N 0.000 description 5
- HSTOKWSFWGCZMH-UHFFFAOYSA-N 3,3'-diaminobenzidine Chemical compound C1=C(N)C(N)=CC=C1C1=CC=C(N)C(N)=C1 HSTOKWSFWGCZMH-UHFFFAOYSA-N 0.000 description 5
- 230000002378 acidificating effect Effects 0.000 description 5
- 239000011149 active material Substances 0.000 description 5
- 239000008151 electrolyte solution Substances 0.000 description 5
- PZOUSPYUWWUPPK-UHFFFAOYSA-N indole Natural products CC1=CC=CC2=C1C=CN2 PZOUSPYUWWUPPK-UHFFFAOYSA-N 0.000 description 5
- RKJUIXBNRJVNHR-UHFFFAOYSA-N indolenine Natural products C1=CC=C2CC=NC2=C1 RKJUIXBNRJVNHR-UHFFFAOYSA-N 0.000 description 5
- 229920000172 poly(styrenesulfonic acid) Polymers 0.000 description 5
- 229940005642 polystyrene sulfonic acid Drugs 0.000 description 5
- 239000000758 substrate Substances 0.000 description 5
- HYZJCKYKOHLVJF-UHFFFAOYSA-N 1H-benzimidazole Chemical compound C1=CC=C2NC=NC2=C1 HYZJCKYKOHLVJF-UHFFFAOYSA-N 0.000 description 4
- LSNNMFCWUKXFEE-UHFFFAOYSA-M Bisulfite Chemical compound OS([O-])=O LSNNMFCWUKXFEE-UHFFFAOYSA-M 0.000 description 4
- 230000015572 biosynthetic process Effects 0.000 description 4
- 230000000052 comparative effect Effects 0.000 description 4
- 238000006479 redox reaction Methods 0.000 description 4
- 238000003756 stirring Methods 0.000 description 4
- 239000000126 substance Substances 0.000 description 4
- 125000001140 1,4-phenylene group Chemical group [H]C1=C([H])C([*:2])=C([H])C([H])=C1[*:1] 0.000 description 3
- 239000002033 PVDF binder Substances 0.000 description 3
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 3
- 239000012752 auxiliary agent Substances 0.000 description 3
- 239000011230 binding agent Substances 0.000 description 3
- 238000007600 charging Methods 0.000 description 3
- 239000003795 chemical substances by application Substances 0.000 description 3
- 238000007796 conventional method Methods 0.000 description 3
- 230000018044 dehydration Effects 0.000 description 3
- 238000006297 dehydration reaction Methods 0.000 description 3
- 238000007599 discharging Methods 0.000 description 3
- 238000001035 drying Methods 0.000 description 3
- 238000007654 immersion Methods 0.000 description 3
- 150000007522 mineralic acids Chemical class 0.000 description 3
- 239000003960 organic solvent Substances 0.000 description 3
- 229910052697 platinum Inorganic materials 0.000 description 3
- 229920002981 polyvinylidene fluoride Polymers 0.000 description 3
- 229910052717 sulfur Inorganic materials 0.000 description 3
- 239000011593 sulfur Substances 0.000 description 3
- 239000013638 trimer Substances 0.000 description 3
- 125000006736 (C6-C20) aryl group Chemical group 0.000 description 2
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 description 2
- 125000003358 C2-C20 alkenyl group Chemical group 0.000 description 2
- 0 CCC(C)(C*)C(CC*(C)=C1N)CC1=*(C)C Chemical compound CCC(C)(C*)C(CC*(C)=C1N)CC1=*(C)C 0.000 description 2
- FXHOOIRPVKKKFG-UHFFFAOYSA-N N,N-Dimethylacetamide Chemical compound CN(C)C(C)=O FXHOOIRPVKKKFG-UHFFFAOYSA-N 0.000 description 2
- 238000004458 analytical method Methods 0.000 description 2
- IZALUMVGBVKPJD-UHFFFAOYSA-N benzene-1,3-dicarbaldehyde Chemical compound O=CC1=CC=CC(C=O)=C1 IZALUMVGBVKPJD-UHFFFAOYSA-N 0.000 description 2
- 239000002134 carbon nanofiber Substances 0.000 description 2
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 2
- 239000002800 charge carrier Substances 0.000 description 2
- 239000002131 composite material Substances 0.000 description 2
- 239000004020 conductor Substances 0.000 description 2
- 238000007334 copolymerization reaction Methods 0.000 description 2
- 238000002484 cyclic voltammetry Methods 0.000 description 2
- 238000010586 diagram Methods 0.000 description 2
- POULHZVOKOAJMA-UHFFFAOYSA-N dodecanoic acid Chemical compound CCCCCCCCCCCC(O)=O POULHZVOKOAJMA-UHFFFAOYSA-N 0.000 description 2
- 239000007789 gas Substances 0.000 description 2
- 239000011521 glass Substances 0.000 description 2
- 229910002804 graphite Inorganic materials 0.000 description 2
- 239000010439 graphite Substances 0.000 description 2
- 239000003014 ion exchange membrane Substances 0.000 description 2
- 125000005647 linker group Chemical group 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 239000011812 mixed powder Substances 0.000 description 2
- 238000002156 mixing Methods 0.000 description 2
- 238000000465 moulding Methods 0.000 description 2
- 150000007524 organic acids Chemical class 0.000 description 2
- 230000033116 oxidation-reduction process Effects 0.000 description 2
- 150000003016 phosphoric acids Chemical class 0.000 description 2
- 229920000767 polyaniline Polymers 0.000 description 2
- 230000000379 polymerizing effect Effects 0.000 description 2
- 229920001343 polytetrafluoroethylene Polymers 0.000 description 2
- 239000004810 polytetrafluoroethylene Substances 0.000 description 2
- 239000000843 powder Substances 0.000 description 2
- 150000003839 salts Chemical class 0.000 description 2
- 150000003460 sulfonic acids Chemical class 0.000 description 2
- 238000001308 synthesis method Methods 0.000 description 2
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 2
- 229920002554 vinyl polymer Polymers 0.000 description 2
- NLVXSWCKKBEXTG-UHFFFAOYSA-N vinylsulfonic acid Chemical compound OS(=O)(=O)C=C NLVXSWCKKBEXTG-UHFFFAOYSA-N 0.000 description 2
- NAWXUBYGYWOOIX-SFHVURJKSA-N (2s)-2-[[4-[2-(2,4-diaminoquinazolin-6-yl)ethyl]benzoyl]amino]-4-methylidenepentanedioic acid Chemical compound C1=CC2=NC(N)=NC(N)=C2C=C1CCC1=CC=C(C(=O)N[C@@H](CC(=C)C(O)=O)C(O)=O)C=C1 NAWXUBYGYWOOIX-SFHVURJKSA-N 0.000 description 1
- 125000003837 (C1-C20) alkyl group Chemical group 0.000 description 1
- HOTVNKKFZIDWCI-UHFFFAOYSA-N 1-phenyl-2h-quinoxaline Chemical compound C1C=NC2=CC=CC=C2N1C1=CC=CC=C1 HOTVNKKFZIDWCI-UHFFFAOYSA-N 0.000 description 1
- SMZOUWXMTYCWNB-UHFFFAOYSA-N 2-(2-methoxy-5-methylphenyl)ethanamine Chemical compound COC1=CC=C(C)C=C1CCN SMZOUWXMTYCWNB-UHFFFAOYSA-N 0.000 description 1
- NIXOWILDQLNWCW-UHFFFAOYSA-N 2-Propenoic acid Natural products OC(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 1
- 125000004174 2-benzimidazolyl group Chemical group [H]N1C(*)=NC2=C([H])C([H])=C([H])C([H])=C12 0.000 description 1
- MLMGJTAJUDSUKA-UHFFFAOYSA-N 2-ethenyl-1h-imidazole Chemical group C=CC1=NC=CN1 MLMGJTAJUDSUKA-UHFFFAOYSA-N 0.000 description 1
- BHNHHSOHWZKFOX-UHFFFAOYSA-N 2-methyl-1H-indole Chemical compound C1=CC=C2NC(C)=CC2=C1 BHNHHSOHWZKFOX-UHFFFAOYSA-N 0.000 description 1
- AGBXYHCHUYARJY-UHFFFAOYSA-N 2-phenylethenesulfonic acid Chemical compound OS(=O)(=O)C=CC1=CC=CC=C1 AGBXYHCHUYARJY-UHFFFAOYSA-N 0.000 description 1
- HHTJIEZVBFZGJC-UHFFFAOYSA-N 4-bromo-2-methylbenzenesulfonic acid Chemical compound CC1=CC(Br)=CC=C1S(O)(=O)=O HHTJIEZVBFZGJC-UHFFFAOYSA-N 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 1
- 229920000049 Carbon (fiber) Polymers 0.000 description 1
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 1
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 1
- 239000005639 Lauric acid Substances 0.000 description 1
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 1
- UEZVMMHDMIWARA-UHFFFAOYSA-N Metaphosphoric acid Chemical compound OP(=O)=O UEZVMMHDMIWARA-UHFFFAOYSA-N 0.000 description 1
- CERQOIWHTDAKMF-UHFFFAOYSA-N Methacrylic acid Chemical compound CC(=C)C(O)=O CERQOIWHTDAKMF-UHFFFAOYSA-N 0.000 description 1
- 229920000557 Nafion® Polymers 0.000 description 1
- 229930192627 Naphthoquinone Natural products 0.000 description 1
- 229910021607 Silver chloride Inorganic materials 0.000 description 1
- 229920002125 Sokalan® Polymers 0.000 description 1
- 238000010669 acid-base reaction Methods 0.000 description 1
- 150000007933 aliphatic carboxylic acids Chemical class 0.000 description 1
- 125000004414 alkyl thio group Chemical group 0.000 description 1
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 1
- PYKYMHQGRFAEBM-UHFFFAOYSA-N anthraquinone Natural products CCC(=O)c1c(O)c2C(=O)C3C(C=CC=C3O)C(=O)c2cc1CC(=O)OC PYKYMHQGRFAEBM-UHFFFAOYSA-N 0.000 description 1
- 150000004056 anthraquinones Chemical class 0.000 description 1
- 125000005428 anthryl group Chemical group [H]C1=C([H])C([H])=C2C([H])=C3C(*)=C([H])C([H])=C([H])C3=C([H])C2=C1[H] 0.000 description 1
- 125000005110 aryl thio group Chemical group 0.000 description 1
- 238000006664 bond formation reaction Methods 0.000 description 1
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 1
- 229910052794 bromium Inorganic materials 0.000 description 1
- 239000004917 carbon fiber Substances 0.000 description 1
- 239000003575 carbonaceous material Substances 0.000 description 1
- 238000005341 cation exchange Methods 0.000 description 1
- 239000007810 chemical reaction solvent Substances 0.000 description 1
- 229910052801 chlorine Inorganic materials 0.000 description 1
- 239000000460 chlorine Substances 0.000 description 1
- 238000006482 condensation reaction Methods 0.000 description 1
- 239000002482 conductive additive Substances 0.000 description 1
- 229920000547 conjugated polymer Polymers 0.000 description 1
- 230000021615 conjugation Effects 0.000 description 1
- 238000010281 constant-current constant-voltage charging Methods 0.000 description 1
- 125000004122 cyclic group Chemical group 0.000 description 1
- 238000000354 decomposition reaction Methods 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 238000007580 dry-mixing Methods 0.000 description 1
- 238000010828 elution Methods 0.000 description 1
- BNKAXGCRDYRABM-UHFFFAOYSA-N ethenyl dihydrogen phosphate Chemical compound OP(O)(=O)OC=C BNKAXGCRDYRABM-UHFFFAOYSA-N 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 238000011049 filling Methods 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 150000002222 fluorine compounds Chemical class 0.000 description 1
- UQSQSQZYBQSBJZ-UHFFFAOYSA-N fluorosulfonic acid Chemical compound OS(F)(=O)=O UQSQSQZYBQSBJZ-UHFFFAOYSA-N 0.000 description 1
- 229920000578 graft copolymer Polymers 0.000 description 1
- 238000007731 hot pressing Methods 0.000 description 1
- 238000006460 hydrolysis reaction Methods 0.000 description 1
- 239000003999 initiator Substances 0.000 description 1
- 150000002484 inorganic compounds Chemical class 0.000 description 1
- 229910010272 inorganic material Inorganic materials 0.000 description 1
- 239000011630 iodine Substances 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- 238000005342 ion exchange Methods 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 125000000468 ketone group Chemical group 0.000 description 1
- 229910052744 lithium Inorganic materials 0.000 description 1
- 238000012423 maintenance Methods 0.000 description 1
- VNWKTOKETHGBQD-UHFFFAOYSA-N methane Chemical compound C VNWKTOKETHGBQD-UHFFFAOYSA-N 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 150000002762 monocarboxylic acid derivatives Chemical class 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000001280 n-hexyl group Chemical group C(CCCCC)* 0.000 description 1
- 125000000740 n-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 150000002791 naphthoquinones Chemical class 0.000 description 1
- 125000001624 naphthyl group Chemical group 0.000 description 1
- 150000002815 nickel Chemical class 0.000 description 1
- 150000002894 organic compounds Chemical class 0.000 description 1
- MHYFEEDKONKGEB-UHFFFAOYSA-N oxathiane 2,2-dioxide Chemical compound O=S1(=O)CCCCO1 MHYFEEDKONKGEB-UHFFFAOYSA-N 0.000 description 1
- 238000004806 packaging method and process Methods 0.000 description 1
- 229920000553 poly(phenylenevinylene) Polymers 0.000 description 1
- 229920001197 polyacetylene Polymers 0.000 description 1
- 239000004584 polyacrylic acid Substances 0.000 description 1
- 238000012643 polycondensation polymerization Methods 0.000 description 1
- 238000006068 polycondensation reaction Methods 0.000 description 1
- 229920000414 polyfuran Polymers 0.000 description 1
- 239000005518 polymer electrolyte Substances 0.000 description 1
- 239000003505 polymerization initiator Substances 0.000 description 1
- 229920000098 polyolefin Polymers 0.000 description 1
- 229920000128 polypyrrole Polymers 0.000 description 1
- 229920000123 polythiophene Polymers 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 150000004053 quinones Chemical class 0.000 description 1
- 150000003252 quinoxalines Chemical class 0.000 description 1
- 150000003254 radicals Chemical class 0.000 description 1
- 229920005604 random copolymer Polymers 0.000 description 1
- 230000035484 reaction time Effects 0.000 description 1
- 230000009257 reactivity Effects 0.000 description 1
- 230000002468 redox effect Effects 0.000 description 1
- 238000010992 reflux Methods 0.000 description 1
- 229920005989 resin Polymers 0.000 description 1
- 239000011347 resin Substances 0.000 description 1
- 229920006395 saturated elastomer Polymers 0.000 description 1
- 238000007650 screen-printing Methods 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- HKZLPVFGJNLROG-UHFFFAOYSA-M silver monochloride Chemical compound [Cl-].[Ag+] HKZLPVFGJNLROG-UHFFFAOYSA-M 0.000 description 1
- 239000002002 slurry Substances 0.000 description 1
- 238000002336 sorption--desorption measurement Methods 0.000 description 1
- 125000001174 sulfone group Chemical group 0.000 description 1
- 150000003459 sulfonic acid esters Chemical class 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 238000002411 thermogravimetry Methods 0.000 description 1
- 238000001075 voltammogram Methods 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M8/00—Fuel cells; Manufacture thereof
- H01M8/10—Fuel cells with solid electrolytes
- H01M8/1016—Fuel cells with solid electrolytes characterised by the electrolyte material
- H01M8/1018—Polymeric electrolyte materials
- H01M8/1041—Polymer electrolyte composites, mixtures or blends
- H01M8/1044—Mixtures of polymers, of which at least one is ionically conductive
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08J—WORKING-UP; GENERAL PROCESSES OF COMPOUNDING; AFTER-TREATMENT NOT COVERED BY SUBCLASSES C08B, C08C, C08F, C08G or C08H
- C08J5/00—Manufacture of articles or shaped materials containing macromolecular substances
- C08J5/20—Manufacture of shaped structures of ion-exchange resins
- C08J5/22—Films, membranes or diaphragms
- C08J5/2206—Films, membranes or diaphragms based on organic and/or inorganic macromolecular compounds
- C08J5/2218—Synthetic macromolecular compounds
- C08J5/2256—Synthetic macromolecular compounds based on macromolecular compounds obtained by reactions other than those involving carbon-to-carbon bonds, e.g. obtained by polycondensation
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0564—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of organic materials only
- H01M10/0565—Polymeric materials, e.g. gel-type or solid-type
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M8/00—Fuel cells; Manufacture thereof
- H01M8/10—Fuel cells with solid electrolytes
- H01M8/1016—Fuel cells with solid electrolytes characterised by the electrolyte material
- H01M8/1018—Polymeric electrolyte materials
- H01M8/102—Polymeric electrolyte materials characterised by the chemical structure of the main chain of the ion-conducting polymer
- H01M8/1025—Polymeric electrolyte materials characterised by the chemical structure of the main chain of the ion-conducting polymer having only carbon and oxygen, e.g. polyethers, sulfonated polyetheretherketones [S-PEEK], sulfonated polysaccharides, sulfonated celluloses or sulfonated polyesters
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M8/00—Fuel cells; Manufacture thereof
- H01M8/10—Fuel cells with solid electrolytes
- H01M8/1016—Fuel cells with solid electrolytes characterised by the electrolyte material
- H01M8/1018—Polymeric electrolyte materials
- H01M8/102—Polymeric electrolyte materials characterised by the chemical structure of the main chain of the ion-conducting polymer
- H01M8/1027—Polymeric electrolyte materials characterised by the chemical structure of the main chain of the ion-conducting polymer having carbon, oxygen and other atoms, e.g. sulfonated polyethersulfones [S-PES]
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M8/00—Fuel cells; Manufacture thereof
- H01M8/10—Fuel cells with solid electrolytes
- H01M8/1016—Fuel cells with solid electrolytes characterised by the electrolyte material
- H01M8/1018—Polymeric electrolyte materials
- H01M8/102—Polymeric electrolyte materials characterised by the chemical structure of the main chain of the ion-conducting polymer
- H01M8/103—Polymeric electrolyte materials characterised by the chemical structure of the main chain of the ion-conducting polymer having nitrogen, e.g. sulfonated polybenzimidazoles [S-PBI], polybenzimidazoles with phosphoric acid, sulfonated polyamides [S-PA] or sulfonated polyphosphazenes [S-PPh]
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08J—WORKING-UP; GENERAL PROCESSES OF COMPOUNDING; AFTER-TREATMENT NOT COVERED BY SUBCLASSES C08B, C08C, C08F, C08G or C08H
- C08J2379/00—Characterised by the use of macromolecular compounds obtained by reactions forming in the main chain of the macromolecule a linkage containing nitrogen with or without oxygen, or carbon only, not provided for in groups C08J2361/00 - C08J2377/00
- C08J2379/04—Polycondensates having nitrogen-containing heterocyclic rings in the main chain; Polyhydrazides; Polyamide acids or similar polyimide precursors
- C08J2379/06—Polyhydrazides; Polytriazoles; Polyamino-triazoles; Polyoxadiazoles
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2300/00—Electrolytes
- H01M2300/0017—Non-aqueous electrolytes
- H01M2300/0065—Solid electrolytes
- H01M2300/0082—Organic polymers
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/30—Hydrogen technology
- Y02E60/50—Fuel cells
Landscapes
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Manufacturing & Machinery (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Electrochemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Sustainable Development (AREA)
- Sustainable Energy (AREA)
- Crystallography & Structural Chemistry (AREA)
- Inorganic Chemistry (AREA)
- Polymers & Plastics (AREA)
- Organic Chemistry (AREA)
- General Physics & Mathematics (AREA)
- Physics & Mathematics (AREA)
- Composite Materials (AREA)
- Materials Engineering (AREA)
- Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Dispersion Chemistry (AREA)
- Condensed Matter Physics & Semiconductors (AREA)
- Fuel Cell (AREA)
- Conductive Materials (AREA)
- Battery Electrode And Active Subsutance (AREA)
- Compositions Of Macromolecular Compounds (AREA)
- Macromolecular Compounds Obtained By Forming Nitrogen-Containing Linkages In General (AREA)
- Electric Double-Layer Capacitors Or The Like (AREA)
- Primary Cells (AREA)
Description
また本発明は、前記キノキサリン系化合物の構造が、下記一般式(2)で表されるキノキサリン構造単位である上記のプロトン伝導性高分子材料に関する。
また本発明は、前記キノキサリン系化合物の構造を持つ単位と、前記イミダゾール系化合物の構造を持つ単位と、これらの単位の少なくともいずれかに結合するプロトン放出機能を持つ置換基とを有し、且つ前記キノキサリン系化合物の構造のキノキサリン縮合環が主鎖を構成している重合体を含む上記のプロトン伝導性高分子材料に関する。
また本発明は、下記一般式(8)で表される、キノキサリン構造とイミダゾール構造とプロトン放出機能を持つ置換基とを持つ単位を有する重合体を含む上記のプロトン伝導性高分子材料に関する。
また本発明は、前記プロトン放出機能を持つ置換基が、スルホン酸基又はスルホン酸基を有する置換基である上記のプロトン伝導性高分子材料に関する。
(a)キノキサリン系化合物の骨格を持つ単位とイミダゾール系化合物の骨格を持つ単位とを有するランダム共重合構造。
(b)キノキサリン系化合物の骨格を持つ単位の連鎖と、イミダゾール系化合物の骨格を持つ単位の連鎖とが結合したブロック構造。
(c)キノキサリン系化合物の骨格を持つ単位とイミダゾール系化合物の骨格を持つ単位とを有するランダム共重合連鎖と、キノキサリン系化合物の骨格を持つ単位の連鎖と、イミダゾール系化合物の骨格を持つ単位の連鎖とが結合したブロック構造。
(d)キノキサリン系化合物の骨格を持つ単位を含む幹高分子(主鎖)に対し、イミダゾール系化合物の骨格を持つ側鎖(分岐鎖)またはイミダゾール系化合物が結合したグラフト構造。
(e)キノキサリン系化合物の骨格を持つ単位の連鎖と、イミダゾール系化合物の骨格を持つ単位の連鎖とを有するブロック重合体からなる幹高分子(主鎖)に対し、イミダゾール系化合物の骨格を持つ側鎖(分岐鎖)またはイミダゾール系化合物が結合したグラフト構造。
(f)キノキサリン系化合物の骨格を持つ単位とイミダゾール系化合物の骨格を持つ単位とを有するランダム共重合連鎖と、キノキサリン系化合物の骨格を持つ単位の連鎖と、イミダゾール系化合物の骨格を持つ単位の連鎖とを有するブロック重合体からなる幹高分子(主鎖)に対し、イミダゾール系化合物の骨格を持つ側鎖(分岐鎖)またはイミダゾール系化合物が結合したグラフト構造。
ここで言うX、Y及びmの「それぞれ独立に」とは、各繰り返し単位においてすべてが同じでも良く、また、すべてが異なっていても良いことを意味し、さらに、重合体のそれぞれの構造においても独立であることを示している。
目的化合物の確認は、生成物の収率の算出、CHNS元素分析およびIR測定を行い、化学構造とスルホン化度を確認した。重量平均分子量は、GPC(ゲルパーミエーションクロマトグラフィー)測定により得た(J.Polymer Science,part B,Polymer Physics,第38巻,1348頁,2000年、Chemistry Letters,1049頁,2000年)。収率は、重合前後の仕込み原料の濃度差より算出した。この収率が96%以上であれば、ほぼ目的化合物が生成できているものと判断できる。
固体電解質膜の強度は、引っ張り強度試験により測定した。
作製した固体電解質膜のイオン伝導度は、交流インピーダンス法にて測定した。具体的には、固体電解質膜を白金の不活性電極ではさみ、25℃、6Mの燐酸中において交流を印加し、インピーダンスの周波数特性で測定した。
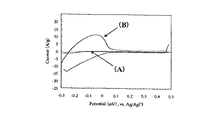
作製したプロトン伝導性高分子化合物の耐久性は、サイクリックボルタンメトリー法(以下CV法)によるCVサイクル試験を行い評価した。
スルホン化度2のキノキサリン−ベンズイミダゾール重合体を以下の反応式(28)に従って調製した。
実施例1で作製したプロトン伝導性高分子化合物の粉末をm−クレゾールに完全に溶解させ、この溶液をスクリーン印刷機を用いてガラス基盤上に成膜した。次いで、常温から徐々に80℃まで昇温し、最終的に120℃で1時間乾燥させm−クレゾールを揮発させた。これにより、膜厚50μmの茶黄色の固体電解質膜を得た。
正極活物質としてプロトン伝導型化合物である6−カルボン酸メチルインドール三量体を選択し、導電補助剤として繊維状カーボン(商品名:VGCF、昭和電工(株)製)、結着剤としてPVDF(平均分子量:1100)を選択し、これらをこの記載順に69:23:8の重量比で秤取り、ブレンダーを用いて攪拌・混合した。次に、この混合粉末を1cm2角の金型に入れ、200℃で加圧成形することにより正極電極を得た。
実施例2において作製した厚み50μmの固体電解質膜をセパレータとして用い、負極活物質としてポリフェニルキノキサリン(一般式(27)において全てのRがHである高分子化合物)を用いた以外は、実施例3と同様にして電池を作製し、放電容量を測定した。
実施例2において作製した厚み50μmの固体電解質膜を用い、定法に従い、その両側に白金触媒が担持された多孔質導電性炭素電極を設置し、燃料電池用積層体を作製した。この積層体の両側に水素供給室と空気供給室を設けて燃料電池を作製した。
下記式(29)で表されるスルホン化度4のキノキサリン−ベンズイミダゾール重合体を調製した。
下記式(30)で表されるスルホン化度4のキノキサリン−ベンズイミダゾール重合体を調製した。
実施例5と同様にして燃料電池を作製し、起電力を測定した結果、200mAで0.78Vの起電力が得られた。また、1Aでは0.66Vの起電力が得られた。
下記式(31)で表される連鎖構造を有するキノキサリン−ベンズイミダゾールブロック共重合体を調製した。
実施例5と同様にして燃料電池を作製し、起電力を測定した結果、200mAで0.67Vの起電力が得られた。また、1Aでは0.53Vの起電力が得られた。
下記式(32)で表されるスルホン化度2のキノキサリン−ベンズイミダゾールグラフト重合体を調製した。
実施例5と同様にして燃料電池を作製し、起電力を測定した結果、200mAで0.71Vの起電力が得られた。また、1Aでは0.59Vの起電力が得られた。
実施例2にて調製した固体電解質膜を、常温下、60wt%硫酸に24時間浸漬して、硫酸をドーピングした。浸漬前後において、膜の色が茶黄色から赤色に変化し、硫酸がドーピングされたことが確認された。
実施例2にて調製した固体電解質膜を、常温下、30wt%ポリスチレンスルホン酸水溶液に24時間浸漬して、ポリスチレンスルホン酸をドーピングした。浸漬前後において、膜の色が茶黄色から薄赤色に変化し、ポリスチレンスルホン酸がドーピングされたことが確認された。
反応式(14)で表される定法に従い、スルホン化度2のポリフェニルキノキサリンを調製した。得られた重合物の収率は92.4%であった。また、CHNSの元素分析値およびIRスペクトルから目的の物質であることが確認され、GPC測定による重量平均分子量は11,000であった。
実施例5と同様にして燃料電池を作製し、起電力を測定した結果、200mAで0.57Vの起電力が得られた。また、1Aでは0.43Vの起電力が得られた。
〔実施例13〕
定法に従い、無置換体のポリフェニルキノキサリン(一般式(27)において全てのRがHである高分子化合物)を調製した。すなわち、テトラカルボニル化合物と3,3’−ジアミノベンジジンをDMFに溶解させ、30分攪拌した後、大気中で、120℃で10時間攪拌し、反応させた。得られた黄色の固形物をろ過し、メタノールで洗浄した後、120℃で10時間減圧乾燥して重合物を得た。収率は、99.4%であった。また、CHNSの元素分析値およびIRスペクトルから目的の物質であることが確認され、GPC測定による重量平均分子量は45,000であった。
実施例13と同様にして、無置換のポリフェニルキノキサリン(一般式(27)において全てのRがHである高分子化合物)を調製した。収率は99.4%であった。また、CHNSの元素分析値およびIRスペクトルから目的の物質であることが確認され、GPC測定による重量平均分子量は45,000であった。
反応式(14)に示される定法に従い、スルホン化度2のポリフェニルキノキサリンを調製した。すなわち、テトラカルボニル化合物のスルホン化体と3,3’−ジアミノベンジジンをDMFに溶解させ、30分攪拌した後、大気中で、120℃で10時間攪拌し、反応させた。得られた黄色の固形物をろ過し、メタノールで洗浄した後、120℃で10時間減圧乾燥して重合物を得た。収率は92.4%であった。また、CHNS元素分析値およびIRスペクトルから目的の物質であることが確認され、GPC測定による重量平均分子量は11,000であった。
スルホン酸基を持たないテトラカルボニル化合物を用いた以外は実施例1と同様にして、スルホン酸基を持たないキノキサリン−ベンズイミダゾール重合体を調製した。収率は98.1%であった。また、CHNSの元素分析値およびIRスペクトルから目的の物質であることが確認され、GPC測定による重量平均分子量は64,000であった。
2 正極電極
3 負極電極
4 負極集電体
5 セパレータ
6 ガスケット
7 燃料極セパレータ
8 燃料極触媒層
9 プロトン伝導性固体電解質膜
10 空気極触媒層
11 空気極セパレータ
Claims (18)
- キノキサリン構造を持つ単位の連鎖であって、この単位の繰り返し数が2以上である連鎖と、
ベンズイミダゾール骨格またはベンズビスイミダゾール骨格を有するイミダゾール系化合物の構造を持つ単位の連鎖であって、この単位の繰り返し数が2以上である連鎖と、
前記キノキサリン構造を持つ単位に結合するプロトン放出機能を持つ置換基と、
前記イミダゾール系化合物の構造を持つ単位のイミダゾール環窒素原子に結合するプロトン放出機能を持つ置換基とを有するブロック共重合体であって、
前記プロトン放出機能を持つ置換基が、スルホン酸基又はスルホン酸基を有する置換基であり、
前記キノキサリン構造を持つ単位は、下記一般式(9a)で表される単位であり、
前記イミダゾール系化合物の構造を持つ単位は、下記一般式(10a)で表される単位、あるいは下記一般式(3)〜(5)のいずれかで表されるベンズイミダゾール骨格を持つ単位、もしくは下記一般式(6)で表されるベンズビスイミダゾール骨格を持つ単位である、プロトン伝導性高分子材料。
- キノキサリン構造を持つ単位を有し、この単位の繰り返し数が2以上の重合体である第1の高分子化合物と、
ベンズイミダゾール骨格またはベンズビスイミダゾール骨格を有するイミダゾール系化合物の構造を持つ単位を有し、この単位の繰り返し数が2以上の重合体である第2の高分子化合物とを含む混合物であって、
前記第2の高分子化合物は、前記イミダゾール系化合物の構造を持つ単位のイミダゾール環窒素原子に結合するプロトン放出機能を持つ置換基を有し、
前記プロトン放出機能を持つ置換基が、スルホン酸基又はスルホン酸基を有する置換基であり、
前記キノキサリン構造を持つ単位は、下記一般式(9a)又は(9b)で表される単位であり、
前記イミダゾール系化合物の構造を持つ単位は、下記一般式(10a)で表される単位、あるいは下記一般式(3)〜(5)のいずれかで表されるベンズイミダゾール骨格を持つ単位、もしくは下記一般式(6)で表されるベンズビスイミダゾール骨格を持つ単位である、プロトン伝導性高分子材料。
- 下記一般式(8)で表される、キノキサリン構造を持つ単位とイミダゾール構造を持つ単位とを含む単位を有し、この単位の繰り返し数が2以上である重合体であって、
前記キノキサリン構造を持つ単位に結合するプロトン放出機能を持つ置換基と、前記イミダゾール構造を持つ単位のイミダゾール環窒素原子に結合するプロトン放出機能を持つ置換基とを有し、
前記プロトン放出機能を持つ置換基が、スルホン酸基又はスルホン酸基を有する置換基である、プロトン伝導性高分子材料。
- 前記重合体の重量平均分子量が500〜100,000である、請求項1〜4のいずれかに記載のプロトン伝導性高分子材料。
- 請求項1〜5のいずれかのプロトン伝導性高分子材料を含む電極活物質。
- 請求項1〜5のいずれかのプロトン伝導性高分子材料を含む固体電解質。
- さらに酸性化合物を含む請求項7に記載の固体電解質。
- 前記酸性化合物が、硫酸、塩酸、硝酸、酢酸、ほう酸、四フッ化ほう酸、リン酸、六フッ化リン酸、プロピオン酸、フッ化プロピオン酸、酪酸、フッ化酪酸からなる群から選択される少なくとも一種以上である請求項8に記載の固体電解質。
- 前記酸性化合物が、スルホン酸系化合物、カルボン酸系化合物及びリン酸系化合物からなるモノマー並びにこれらのポリマーからなる群から選択される少なくとも1種以上である請求項8に記載の固体電解質。
- 請求項7〜10のいずれかに記載の固体電解質からなる固体電解質膜。
- 膜の厚みが10〜200μmである請求項11に記載の固体電解質膜
- 請求項1〜5のいずれかのプロトン伝導性高分子材料を電極活物質として用いた電気化学セル。
- 一対の電極と、これらの電極の間に設置されたセパレータを有する電気化学セルであって、
プロトン源を含む電解質を含有し、
正極活物質および負極活物質としてそれぞれプロトン伝導型化合物を含有し、
前記負極活物質のプロトン伝導型化合物として請求項1〜5のいずれかのプロトン伝導性高分子材料を含む、電気化学セル。 - 一対の電極と、これらの電極の間に設置された請求項11又は12に記載の固体電解質膜とを有する電気化学セル。
- プロトン源を含む電解質を含有し、
正極活物質および負極活物質としてそれぞれプロトン伝導型化合物を含有する、請求項15に記載の電気化学セル。 - 前記負極活物質のプロトン伝導型化合物として請求項1〜5のいずれかのプロトン伝導性高分子材料を含む、請求項16に記載の電気化学セル。
- 燃料極と、空気極と、これらの電極の間に設置された請求項11又は12に記載の固体電解質膜とを有する燃料電池。
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2004308139A JP4828112B2 (ja) | 2004-10-22 | 2004-10-22 | プロトン伝導性高分子材料並びにこれを用いた固体電解質膜、電気化学セル及び燃料電池 |
| US11/255,552 US20060088750A1 (en) | 2004-10-22 | 2005-10-21 | Proton-conducting polymer material, and solid electrolyte membrane, electrochemical cell and fuel cell therewith |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2004308139A JP4828112B2 (ja) | 2004-10-22 | 2004-10-22 | プロトン伝導性高分子材料並びにこれを用いた固体電解質膜、電気化学セル及び燃料電池 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2006117828A JP2006117828A (ja) | 2006-05-11 |
| JP4828112B2 true JP4828112B2 (ja) | 2011-11-30 |
Family
ID=36206542
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2004308139A Expired - Fee Related JP4828112B2 (ja) | 2004-10-22 | 2004-10-22 | プロトン伝導性高分子材料並びにこれを用いた固体電解質膜、電気化学セル及び燃料電池 |
Country Status (2)
| Country | Link |
|---|---|
| US (1) | US20060088750A1 (ja) |
| JP (1) | JP4828112B2 (ja) |
Families Citing this family (23)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB0505087D0 (en) * | 2005-03-12 | 2005-04-20 | Acal Energy Ltd | Fuel cells |
| JP4835026B2 (ja) * | 2005-04-15 | 2011-12-14 | 株式会社村田製作所 | ジフェニルキノキサリン骨格を有する化合物を含む導電性組成物 |
| IN266777B (ja) | 2006-03-24 | 2015-06-01 | Acal Energy Ltd | |
| GB0608079D0 (en) * | 2006-04-25 | 2006-05-31 | Acal Energy Ltd | Fuel cells |
| GB0614337D0 (en) * | 2006-07-19 | 2006-08-30 | Acal Energy Ltd | Fuel Cells |
| GB0614338D0 (en) * | 2006-07-19 | 2006-08-30 | Acal Energy Ltd | Fuel cells |
| US7846610B2 (en) | 2006-10-23 | 2010-12-07 | Canon Kabushiki Kaisha | Electrolyte membrane, production method thereof, and fuel cell |
| JP5247113B2 (ja) * | 2006-10-23 | 2013-07-24 | キヤノン株式会社 | 電解質膜、電解質膜の製造方法および燃料電池 |
| JP2008117648A (ja) * | 2006-11-06 | 2008-05-22 | Nec Tokin Corp | 電気化学セル |
| JP5376485B2 (ja) * | 2007-02-21 | 2013-12-25 | 独立行政法人日本原子力研究開発機構 | アルキルグラフト鎖からなる高分子電解質膜、及び、その製造方法 |
| GB0718349D0 (en) * | 2007-09-20 | 2007-10-31 | Acal Energy Ltd | Fuel cells |
| GB0718577D0 (en) * | 2007-09-24 | 2007-10-31 | Acal Energy Ltd | Fuel cells |
| GB0801198D0 (en) * | 2008-01-23 | 2008-02-27 | Acal Energy Ltd | Fuel cells |
| GB0801195D0 (en) * | 2008-01-23 | 2008-02-27 | Acal Energy Ltd | Fuel cells |
| GB0801199D0 (en) * | 2008-01-23 | 2008-02-27 | Acal Energy Ltd | Fuel cells |
| US20110033776A1 (en) * | 2009-08-10 | 2011-02-10 | Board of regents of the Nevada System of Higher Education, on Behalf of the University of | Proton exchange membranes |
| JP5599819B2 (ja) * | 2009-12-04 | 2014-10-01 | プルーデント エナジー インク | ポリマーブレンドプロトン交換膜及びこれを製造する方法 |
| JP5392778B2 (ja) * | 2010-01-14 | 2014-01-22 | 独立行政法人産業技術総合研究所 | 電池およびキャパシタの電極材料 |
| TWI424882B (zh) | 2010-12-29 | 2014-02-01 | Ind Tech Res Inst | 具含氮化合物修飾之金屬觸媒組成物 |
| WO2013089498A1 (ko) * | 2011-12-14 | 2013-06-20 | 주식회사 엘지화학 | 케이블형 이차전지 |
| JP2014209555A (ja) * | 2013-03-26 | 2014-11-06 | 船井電機株式会社 | 電気二重層キャパシタ用電極及び電気二重層キャパシタ |
| JP6093728B2 (ja) * | 2014-03-25 | 2017-03-08 | 富士フイルム株式会社 | スチレン系高分子機能性膜およびその製造方法 |
| JP7656824B2 (ja) * | 2021-05-18 | 2025-04-04 | 国立大学法人山梨大学 | リバーシブル燃料電池 |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE4241150C1 (de) * | 1992-12-07 | 1994-06-01 | Fraunhofer Ges Forschung | Elektrodenmembran-Verbund, Verfahren zu dessen Herstellung sowie dessen Verwendung |
| US5525436A (en) * | 1994-11-01 | 1996-06-11 | Case Western Reserve University | Proton conducting polymers used as membranes |
| US5599639A (en) * | 1995-08-31 | 1997-02-04 | Hoechst Celanese Corporation | Acid-modified polybenzimidazole fuel cell elements |
| JP2000195528A (ja) * | 1998-12-25 | 2000-07-14 | Aventis Res & Technol Gmbh & Co Kg | 高分子電解質膜の製造方法及び燃料電池 |
| EP1388906A3 (en) * | 2002-08-05 | 2006-10-11 | Nec Tokin Corporation | Cell electrode and electrochemical cell therewith |
| DE10301810A1 (de) * | 2003-01-20 | 2004-07-29 | Sartorius Ag | Membran-Elektroden-Einheit, Polymermembranen für eine Membran-Elektroden-Einheit und Polymerelektrolyt-Brennstoffzellen sowie Verfahren zur Herstellung derselben |
| JP2005126476A (ja) * | 2003-10-21 | 2005-05-19 | Tosoh Corp | 新規ポリキノキサリン共重合体及びその製造方法 |
| WO2005063799A2 (en) * | 2003-12-31 | 2005-07-14 | F.Hoffmann-La Roche Ag | Peptide synthesis and deprotection with co-solvent |
| JP2005209576A (ja) * | 2004-01-26 | 2005-08-04 | Nec Tokin Corp | 共重合体化合物及びそれを用いた電気化学セル |
-
2004
- 2004-10-22 JP JP2004308139A patent/JP4828112B2/ja not_active Expired - Fee Related
-
2005
- 2005-10-21 US US11/255,552 patent/US20060088750A1/en not_active Abandoned
Also Published As
| Publication number | Publication date |
|---|---|
| JP2006117828A (ja) | 2006-05-11 |
| US20060088750A1 (en) | 2006-04-27 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4828112B2 (ja) | プロトン伝導性高分子材料並びにこれを用いた固体電解質膜、電気化学セル及び燃料電池 | |
| US7537711B2 (en) | Electrically conductive polyaniline composition and method | |
| KR101016276B1 (ko) | 고분자 전해질과 그 제조방법, 및 전기 화학 소자 | |
| Che et al. | The effect of grafted alkyl side chains on the properties of poly (terphenyl piperidinium) based high temperature proton exchange membranes | |
| US7230069B2 (en) | Polymers and electrochemical cell therewith | |
| KR100800921B1 (ko) | 전기 화학 캐패시터 | |
| JP2014139927A (ja) | 蓄電デバイス、およびそれに用いる電極並びに多孔質シート | |
| CN100593027C (zh) | 可交联的磺化共聚物和包括其聚合组分的燃料电池 | |
| US20080226985A1 (en) | Electrochemical cell | |
| JP2005226035A (ja) | 共重合化合物及びこれを用いた電気化学セル | |
| CN119890430B (zh) | 一种基于十二重氢键的自修复聚合物固态电解质材料的制备方法和应用 | |
| TWI246222B (en) | Electrochemical cell | |
| JP4397117B2 (ja) | 燃料電池 | |
| JP2014127445A (ja) | 非水電解液二次電池 | |
| Miyatake et al. | All‐Solid‐State Rechargeable Air Batteries with Naphthoquinone‐Based Negative Electrodes: Improved Performance and Cyclability | |
| Rase et al. | Design enhancement in hydroxide ion conductivity of viologen–bakelite organic frameworks for a flexible rechargeable zinc–air battery | |
| JP4048063B2 (ja) | プロトン伝導性高分子固体電解質、該電解質の製造方法、該電解質からなる電解質膜、該電解質膜の製造方法、該電解質及び/又は該電解質膜を用いた電気化学素子並びに該電気化学素子の製造方法 | |
| JP2003203641A (ja) | 燃料電池 | |
| JP2003203642A (ja) | 燃料電池 | |
| KR102728980B1 (ko) | 이온전달 고분자, 이의 제조방법 및 이를 포함하는 전해질막 | |
| JP2004342595A (ja) | 電気化学セル用電極およびそれを用いた電気化学セル | |
| RU2373592C1 (ru) | Полимерный электролит, способ его получения и электрохимический элемент | |
| JP2006049866A (ja) | 電気化学キャパシタ | |
| JP2004146358A (ja) | 燃料電池 | |
| JPS63285863A (ja) | 導電性高分子電極材及びリチウム二次電池 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20070405 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20090827 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20090902 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20091029 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20100317 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100517 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20100714 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100903 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20110831 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20110914 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20140922 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 4828112 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| S533 | Written request for registration of change of name |
Free format text: JAPANESE INTERMEDIATE CODE: R313533 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |