JP3985263B2 - 負極活物質及びその製造方法、並びに非水電解質二次電池 - Google Patents
負極活物質及びその製造方法、並びに非水電解質二次電池 Download PDFInfo
- Publication number
- JP3985263B2 JP3985263B2 JP2001345326A JP2001345326A JP3985263B2 JP 3985263 B2 JP3985263 B2 JP 3985263B2 JP 2001345326 A JP2001345326 A JP 2001345326A JP 2001345326 A JP2001345326 A JP 2001345326A JP 3985263 B2 JP3985263 B2 JP 3985263B2
- Authority
- JP
- Japan
- Prior art keywords
- metal
- carbon
- negative electrode
- active material
- electrode active
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
Description
【発明の属する技術分野】
本発明は、リチウムと電気化学反応可能な金属を含む負極活物質及びその製造方法、並びに当該負極活物質を用いた非水電解質二次電池に関する。
【0002】
【従来の技術】
近年、カメラ一体型VTR、携帯電話、ラップトップコンピュータ等のポータブル電子機器が多く登場し、その小型軽量化が図られている。そして、これらの電子機器のポータブル電源として、電池、特に二次電池について、エネルギー密度を向上させるための研究開発が活発に進められている。
【0003】
なかでも、リチウムイオン二次電池は、従来の水系電解液二次電池である鉛電池、ニッケルカドミウム電池と比較して大きなエネルギー密度が得られるため、期特が大きい。
【0004】
リチウムイオン二次電池に使用される負極活物質としては、難黒鉛化性炭素や黒鉛等の炭素系負極活物質が、比較的高容量を示し良好なサイクル特性を発現することから広く用いられている。
【0005】
【発明が解決しようとする課題】
近年の高容量化に伴い、炭素系負極活物質の更なる高容量化が課題となっている。例えば特開平8−315825号公報では、炭素化原料と作製条件を選ぶことにより炭素質材料負極で高容量を達成している。
【0006】
しかしながら、負極放電電位が対リチウム0.8V〜1.0Vであり、電池を構成した時の電池放電電圧が低くなり電池エネルギー密度では大きな向上が見込めなかった。さらに充放電曲線形状にヒステリシスが大きく、各充放電サイクルでのエネルギー効率が低いという欠点があった。
【0007】
一方、高容量負極としては、ある種の金属がリチウムと電気化学的に合金化し、これが可逆的に生成/分解することを応用した材料が広く研究されてきた。例えばLi−Al合金を用いた高容量負極が広く研究され、米国特許第4950566号にはSi合金を用いた高容量負極が開示されている。しかし、充放電に伴ってLi−AlまたはLi−Si合金は膨張収縮し、充放電サイクルを繰り返すたびに負極は微粉化し、サイクル特性が極めて悪かった。
【0008】
このような微粉化によって、負極材料同志や材料と集電体との電子的なつながりが阻害され、充放電反応が進行し難くなることが、サイクル特性劣化の主要因の一つである。
【0009】
本発明は、このような従来の実情に鑑みて提案されたものであり、サイクル特性を向上させた負極活物質及びその製造方法、並びに当該負極活物質を用いた非水電解質二次電池を提供することを目的とする。
【0010】
【課題を解決するための手段】
本発明の負極活物質は、リチウムと電気化学反応可能な金属Mが、炭素を内包しており、かつ、当該金属Mの表面に炭素又はリチウムと電気化学反応しない金属Rが機械的な固着方法により固着されていることを特徴とする。
【0011】
上述したような本発明に係る負極活物質では、上記金属Mが炭素を内包し、さらに、金属Mの表面に炭素又は上記金属Rが機械的な固着方法により固着されているので、電気化学反応中の膨張収縮によって微粉化しても、リチウムと電気化学反応可能な金属Mの内部及び表面での電子伝導の低下が抑えられる。
【0012】
また、本発明の負極活物質の製造方法は、リチウムと電気化学反応可能な金属Mが、炭素を内包しており、かつ、当該金属Mの表面に炭素又はリチウムと電気化学反応しない金属Rが固着されている負極活物質を製造する方法であって、金属Rを、機械的な固着方法により金属Mの表面に固着させる工程を含むことを特徴とする。
【0013】
上述したような本発明に係る負極活物質の製造方法では、金属Rを、機械的な固着方法により金属Mの表面に固着させる工程を含むようにしたので、電気化学反応中の膨張収縮によって微粉化しても、リチウムと電気化学反応可能な金属Mの内部及び表面での電子伝導の低下が抑えられる。さらに、上記金属Mに炭素を内包する過程において、非酸化性雰囲気中で処理される工程を有するようにすれば、炭素の酸化が抑えられる。
【0014】
また、本発明の非水電解質二次電池は、LiMxOy(MはCo、Ni、Mn、Fe、Cr、Al、Tiから選ばれた少なくとも一つの元素である。)で表わされるリチウム複合酸化物を正極活物質として有する正極と、負極活物質を有する負極と、正極と負極との間に介在された非水電解質とを備え、上記負極活物質は、リチウムと電気化学反応可能な金属Mが、炭素を内包しており、かつ、当該金属Mの表面に炭素又はリチウムと電気化学反応しない金属Rが機械的な固着方法により固着されてなることを特徴とする。
【0015】
上述したような本発明に係る非水電解質二次電池では、上記金属Mが炭素を内包し、さらに、金属Mの表面に炭素又は上記金属Rが機械的な固着方法により固着されてなる負極活物質を用いているので、電気化学反応中の膨張収縮によって微粉化しても、リチウムと電気化学反応可能な金属Mの内部及び表面での電子伝導の低下が抑えられる。
【0016】
【発明の実施の形態】
以下、本発明を適用した負極活物質及びその製造方法、並びにその負極活物質を用いた非水電解質二次電池の実施の形態について、図面を参照しながら具体的に説明する。
【0017】
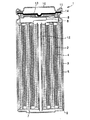
図1は、本発明の非水電解質二次電池の一構成例を示す縦断面図である。この非水電解液電池1は、フィルム状の正極2と、フィルム状の負極3とが、セパレータ4を介して密着状態で巻回された巻層電極体が、電池缶5内部に装填されてなる。
【0018】
上記正極2は、正極活物質と結着剤とを含有する正極合剤を集電体上に塗布、乾燥することにより作製される。集電体には例えばアルミニウム箔等の金属箔が用いられる。
【0019】
正極活物質には、目的とする電池の種類に応じて金属酸化物、金属硫化物又は特定の高分子を用いることができる。
【0020】
具体的には、例えばTiS2、MoS2、NbSe2、V2O5等のリチウムを含有しない金属硫化物あるいは酸化物や、LixMO2(式中、Mは一種以上の遷移金属を表し、xは電池の充放電状態によって異なり、通常0.05≦x≦1.10である。)を主体とするリチウム複合酸化物等を使用することができる。このリチウム複合酸化物を構成する遷移金属Mとしては、Co、Ni、Mn等が好ましい。
【0021】
このようなリチウム複合酸化物の具体例としては、LiCoO2、LiNiO2、LixNiyCo1−yO2(式中、x、y、は電池の充放電状態によって異なり、通常0<x<1、0.7<y<1.02である。)、スピネル型構造を有するリチウムマンガン複合酸化物等を上げることができる。これらリチウム複合酸化物は、高電圧を発生でき、エネルギー密度的に優れた正極活物質となる。正極には、これらの正極活物質の複数種を混合して使用してもよい。
【0022】
また、上記正極合剤の結着剤としては、通常、電池の正極合剤に用いられている公知の結着剤を用いることができるほか、上記正極合剤に導電剤等、公知の添加剤を添加することができる。
【0023】
負極3は、負極活物質と結着剤とを含有する負極合剤を、集電体上に塗布、乾燥することにより作製される。上記集電体には、例えば銅箔等の金属箔が用いられる。
【0024】
ここで、本発明では、負極活物質として、リチウムと電気化学反応可能な金属Mの組織中に炭素を内包しており、かつ、当該金属の表面に炭素またはリチウムと電気化学反応しない金属Rを固着させてなるものを用いている。
【0025】
本発明者らは、上述した問題を解決するため鋭意検討した結果、リチウムと電気化学反応可能な金属Mを作製する過程で、炭素粒子を内包させ、かつ、当該金属Mの表面に、炭素またはリチウムと電気化学反応しない金属Rを固着した負極活物質を用いることで、電気化学反応中の膨張収縮によって微粉化しても、リチウムと電気化学反応可能な金属Mの内部及び表面での電子伝導の低下が抑えられることを見出した。これにより非水電解液電池1のサイクル劣化を抑制できる。
【0026】
電気化学的にリチウムと合金を形成可能な金属Mとしては、元素単体及びその合金化合物が挙げられる。ここでいう合金化合物とは、リチウムと合金形成可能なある金属元素をMとしたとき、化学式MxM’yLiz(式中、M’は、Li元素及びM元素以外の1つ以上の金属元素、xは0より大きい数値であり、y,zは0以上の数値である。)で表される化合物である。
【0027】
さらに本明細書では、半導体元素であるB、Si、As等の元素も金属Mに含めることとする。例示するならば、Hg、B、Al、Ga、In、Si、Ge、Sn、Pb、Sb、Bi、Cd、Ag、Zn、Hf、Zr、Yの各金属とそれらの合金化合物、Li−Al、Li−Al−M(Mは、2A、3B、4B遷移金属元素のうち1つ以上からなる。)AlSb、CuMgSb等である。
【0028】
また、リチウムと合金形成可能な金属Mとしては、3B族典型元素を用いるのが好ましく、好ましくはSiまたはSn、更に好ましくはSiである。例示するなら、MxNySi(Mは各々、SiまたはSnを除く1つ以上の金属元素である。)で表される化合物であり、具体的には、SiB4、SiB6、Hg2Si、Hg2Sn、Ni2Si、TiSi2、MoSi2、CoSi2、NiSi2、CaSi2、CrSi2、Cu5Si、FeSi2、MnSi2、NbSi2、TaSi2、VSi2、WSi2、ZnSi2等が挙げられる。さらに複数種類の金属の組み合わせが可能で、この中には電気化学的にリチウムと合金を形成しない金属が含まれる。
【0029】
上述したような金属Mに内包させる炭素としては、ハードカーボン、ソフトカーボン、グラファイト、カーボンブラックの少なくとも一種以上を用いることができる。また、その形状としては、繊維状、球状、粒状、鱗片状の少なくとも一種以上を用いることができる。
【0030】
本発明において、金属Mに炭素を内包させる目的は、微粉化した金属においても電子伝導性を確保することにあるため、炭素は金属の利用形態によって適宜選択可能である。例えば、より高い電子伝導性を得るためには、高結晶性のグラファイトが好ましく、膨張収縮を抑えたい場合はハードカーボンが好ましい。また、構造破壊を抑えたい場合は繊維状炭素が好ましく、分散性を向上させたい場合はカーボンブラックが好ましい。また、その形状については、炭素の充填性を上げたければ粒状、または球状が好ましい。さらには、上記組み合わせの効果を得るため、2種以上を混合して適宜用いることができる。
【0031】
このような炭素の含有量は、炭素系負極に対して負極としての容量が勝る範囲で用いることができる。金属Mに対しての含有量は0.3重量%〜90重量%の範囲が好ましい。さらに好ましい範囲としては0.5重量%〜80重量%であり、最も好ましい範囲は1重量%〜70重量%である。
【0032】
金属Mの表面に固着させる炭素としては、金属Mに内包させる炭素と同様の特性を特つものが好ましい。
【0033】
金属Mの表面に固着させる金属Rとしては、リチウムと電気化学的に反応しない金属であればどのようなものでも使用可能であるが、具体的にはCr、Mn、Fe、Co、Ni、Cu、Mo、Nb、Nd、Sm、Ta、Ti、V等の金属が挙げられる。また、金属Rは必ずしも元素単体である必要はなく、合金、金属間化合物であっても構わない。また、それらを2種以上混合することも可能である。つまり、金属Rはリチウムと電気化学的に反応せず、電子伝導性を有するものであればどのようなものでも好適に使用可能である。
【0034】
金属Mの表面に固着させる炭素や金属Rは、金属Mに対して、0.5重量%〜20重量%の範囲であることが好ましく、さらに好ましくは1重量%〜10重量%の範囲である。また、炭素や金属Rは金属Mの表面全体を覆っても一部のみを覆っても構わない。
【0035】
炭素を金属M中に内包させる方法は、如何なる方法でも行うことはできるが、工業的には、金属を溶融状態にして炭素を金属中に分散させる方法が好ましい。その際、機械的に攪拌しても良く、誘導加熱等の自己攪拌作用を利用しても良い。
【0036】
当然の事ながら、金属が溶融するのはかなりの高温なので、炭素の酸化あるいは燃焼が起るおそれがある。そのため、いずれの作製過程においても、炭素が金属から露出する等して酸化するおそれがある場合は、非酸化性雰囲気中にて作製することが好ましい。
【0037】
金属の溶融前に乾式で混合する場合は、加熱前に真空あるいは非酸化性雰囲気に置換すればよい。
【0038】
また、金属Rを金属Mの表面に固着させる方法としては、ハイブリダイゼーション、メカノフュージョンのように機械的に固着させる方法やある種の結着剤で固着させる方法、メッキを施す方法が挙げられる。
【0039】
さらに、金属Rで金属Mの表面に固着させた後、金属Mと金属Rの融点のうち低い方の融点よりも50℃〜100℃低い温度で、かつ、真空あるいは非酸化性雰囲気中で熱処理すると、金属Rと金属Mがより強固に固着するため、電子伝導性がさらに向上するため好ましい。
【0040】
炭素が金属Mに内包されていることや炭素や金属Rが金属Mに固着しているかどうかは、例えば何れかの方法で金属を切断し、その断面を分析電子顕微鏡等で観察分析することにより確認することができる。ここで、本発明における内包の定義は、炭素が金属内に固着していることであり、金属表面から炭素が露出していてもその効果を得ることができる。
【0041】
以上のようにして得られる本発明の負極活物質は、炭素系負極材料と混合して用いても良く、炭素系負極に対して負極としての容量が勝る範囲で用いることができる。この場合の炭素の機能としては、導電助剤としての機能や負極材料としての機能が考えられるが、所定の電池特性を得るために、2種以上の如何なる組み合わせにおいても使用可能である。
【0042】
このような炭素材料としては、ハードカーボン、ソフトカーボン、グラファイト、カーボンブラックの少なくとも一種以上を用いることができる。また、その形状としては、繊維状、球状、粒状、鱗片状の少なくとも一種以上を用いることができる。また、炭素材料の混合量は、金属成分に対して1重量%〜95重量%の範囲が好ましい。
【0043】
そして、このような負極活物質を用いて負極を作製するに際しては、負極合剤の結着剤としては、通常リチウムイオン電池の負極合剤に用いられている公知の結着剤を用いることができるほか、上記負極合剤に公知の添加剤等を添加することができる。
【0044】
上記負極へのリチウムのドープは電池作製後に電池内で電気化学的に行われても良く、電池作製後あるいは電池作製前に、正極あるいは正極以外のリチウム源から供給され電気化学的にドープされても構わない。あるいは材料合成の際にリチウム含有材料として合成され、電池作製時に負極に含有されていても構わない。
【0045】
非水電解液は、電解質を非水溶媒に溶解して調製される。
【0046】
電解質としては、通常、電池電解液に用いられている公知の電解質を使用することができる。具体的には、LiClO4、LiAsF6、LiPF6、LiBF4、LiB(C6H5)4、CH3SO3Li、CF3SO3Li、LiCl、LiBr等が挙げられる。
【0047】
また、非水溶媒としては、従来より非水電解液に使用されている種々の非水溶媒を使用することができる。例えば、プロピレンカーボネート、エチレンカ一ボネート、ジエチルカーボネート、ジメチルカーボネート、1,2−ジメトキシエタン、1,2−ジエトキシエタン、γ−プチロラクトン、テトラヒドロフラン、2−メチルテトラヒドロフラン、1,3−ジオキソラン、4−メチル−1,3−ジオキソラン、ジエチルエーテル、スルホラン、メチルスルホラン、アセトニトリル、プロピオニトリル、アニソール、酢酸エステル、酪酸エステル、プロピオン酸エステル等が挙げられる。これらの非水溶媒は単独で使用してもよく、複数種を混合して使用してもよい。
【0048】
上述したような正極2と、負極3とは、セパレータ4を介して密着して渦巻型に多数回巻回されて巻層電極体を構成する。そして、内側にニッケルメッキを施した鉄製の電池缶5の底部に絶縁板6が配されており、絶縁板6上に上記巻層電極体が収納されている。
【0049】
そして、負極の集電をとるための、例えばニッケルからなる負極リード7の一端が負極3に圧着され、他端が電池缶5に溶接されている。これにより、電池缶5は負極3と導通をもつこととなり、非水電解液電池1の外部負極となる。
【0050】
また、正極2の集電をとるための、例えばアルミニウムからなる正極リード8の一端が正極2に取り付けられ、他端が電流遮断用薄板9を介して電池蓋10と電気的に接続されているる。この電流遮断用薄板9は、電池内圧に応じて電流を遮断するものである。これにより、電池蓋10は正極2と導通をもつこととなり、非水電解液電池1の外部正極となる。
【0051】
そして、この電池缶5の中には非水電解液が注入されており、巻回体を浸している。そして、アスファルトを塗布した絶縁封口ガスケット11を介して電池缶5がかしめられており、これにより電池蓋10が固定されている。
【0052】
なお、この非水電解液電池1においては、図1に示すように、負極リード7及び正極リード8に接続するセンターピン12が設けられているとともに、電池内部の圧力が所定値よりも高くなったときに内部の気体を抜くための安全弁装置13及び電池内部の温度上昇を防止するためのPTC素子14が設けられている。
【0053】
以上説明したように、本発明に係る非水電解液電池1では、負極活物質として、リチウムと電気化学反応可能な金属Mに炭素粒子が内包されており、かつ、当該金属Mの表面に、炭素またはリチウムと電気化学反応しない金属Rを固着したものを用いているので、負極活物質が電気化学反応中の膨張収縮によって微粉化しても、リチウムと電気化学反応可能な金属Mの内部及び表面での電子伝導の低下を抑えることができる。これにより非水電解液電池1は、電極劣化による電池内部抵抗の上昇が抑えられ、サイクル劣化を抑制することができ、高容量でかつサイクル特性に優れたものとなる。
【0054】
なお、上述した実施の形態では、非水電解質として、非水溶媒に電解質塩を溶解させた非水電解液を用いた場合を例に挙げて説明したが、本発明はこれに限定されるものではなく、電解質塩を含有させた固体電解質、マトリクスポリマ中に上記非水電解液を含浸させたゲル状電解質のいずれも用いることができる。
【0055】
固体電解質としては、リチウムイオン導電性を有する材料であれば無機固体電解質、高分子固体電解質いずれも用いることができる。無機固体電解質として、窒化リチウム、よう化リチウムが挙げられる。高分子固体電解質は電解質塩とそれを溶解する高分子化合物がらなり、その高分子化合物はポリ(エチレンオキサイド)や同架橋体などのエーテル系高分子、ポリ(メタクリレート)エステル系、アクリレート系などを単独あるいは分子中に共重合、または混合して用いることができる。
【0056】
ゲル状電解質のマトリックスポリマとしては、上記非水電解液を吸収してゲル化するものであれば種々の高分子が利用できる。たとえばポリ(ビニリデンフルオロライド)やポリ(ビニリデンフルオロライド−co−ヘキサフルオロプロピレン)などのフッ素系高分子、ポリ(エチレンオキサイド)や同架橋体などのエーテル系高分子、またポリ(アクリロニトリル)などを使用できる。特に酸化還元安定性から、フッ素系高分子を用いることが望ましい。
【0057】
本発明の電池は、電池形状については特に限定されることはない。円筒型、角型、コイン型、ボタン型等の種々の形状、大きさにすることができる。また、電池系内に存在するリチウムは必ずしもすべて正極あるいは負極から供給される必要はなく、電極あるいは電池の製造過程で、電気化学的に正極あるいは負極にドープされても良い。
【0058】
【実施例】
以下、本発明の効果を確認するために行った実施例及び比較例について説明する。なお、以下の説明では、具体的な物質名や数値等を挙げて説明しているが、本発明はこれらの例に限定されるものではないことは言うまでもない。
【0059】
〈実施例1〉
まず、負極をつぎのようにして作製した。
【0060】
リチウムと電気化学反応可能な金属MであるSi粉末を、非酸化性雰囲気中1500℃で加熱し溶融させ、ここに内包させる炭素として、Si粉末に対し10重量部のMCM6−28(大阪ガスケミカル製)を、雰囲気を変更せずに添加し、しばらく混合した。その後、Arガス雰囲気中に噴霧してアトマイズ粉を得た。得られた粉末を97重量部と、アセチレンブラックを3重量部とをハイブリダイゼーション装置に投入し、アセチレンブラックが表面に固着したアトマイズ粉を得た。得られた粉末を200メッシュで分級し、篩下を金属負極活物質として用いた。
【0061】
この金属負極活物質とリン片状黒鉛(ティミカル製KS−44)を50:50の重量比で混合し、結着剤として、上記混合物に対し8重量部のポリフッ化ビニリデンを加え、さらに溶媒としてN−メチルピロリドンを加えスラリー状の負極合剤を得た。この負極合剤を帯状の銅箔集電体の両面に均一に塗布し、乾燥後、ロールプレス機で圧縮成型し、帯状負極を得た。
【0062】
一方、正極をつぎのようにして作製した。
【0063】
正極活物質(LiCoO2)を得るために、炭酸リチウムと炭酸コバルトとを0.5モル:1モルの比率で混合し、空気中900℃で5時間焼成した。次に、得られたLiCoO2を91重量部と、導電剤としてグラファイトを6重量部と、結着剤としてポリフッ化ビニリデン(PVdF)を3重量部とを混合し、さらにこれをN一メチル−2−ピロリドンに分散させてスラリー状の正極合剤を得た。
【0064】
そして、この正極合剤を帯状の正極集電体である厚さ20μmのアルミニウム箔の両面に均一に塗布し、乾燥後、ロールプレス機で圧縮成型し、帯状正極を得た。
【0065】
帯状負極、帯状正極及び厚さ25μmの微多孔性ポリプロピレンフィルムよりなるセパレータを負極、セパレータ、正極、セパレータの順に積層してから、この積層体を渦巻型に多数回巻回し、最外周のセパレータ最終端部をテープで固定し巻層電極体を作製した。
【0066】
このようにして作製した巻層電極体を、内部にニッケルめっきを施した直径18mm、高さ65mmの鉄製電池缶(内径17.38mm、缶肉厚0.31mm)に収納した。巻層電極体の上下両端面には絶縁板を配設した。また、アルミニウム製正極リードを正極集電体から導出して電池蓋に溶接し、ニッケル製負極リードを負極集電体から導出して電池缶に溶接した。この電池缶の中に電解液を注入した。この電解液は、エチレンカーボネートとジメチルカーボネートとの等容量混合溶媒中にLiPF6を1モル/1の割合で溶解して調製した。
【0067】
アスファルトで表面を塗布した絶縁封口ガスケットを介して電池缶をかしめることにより、電池蓋を固定し、電池内の気密性を保特させた。以上のようにして、円筒型非水電解液二次電池を作製した。
【0068】
〈実施例2〉
実施例1と同様にして得たアトマイズ粉と、Cu粉をハイブリダイゼーションして金属負極活物質を作製し、この金属負極活物質を用いたこと以外は、実施例1と同様にして円筒型非水電解液二次電池を作製した。
【0069】
〈実施例3〉
Siの融点は1414℃であり、Cuの融点は1085℃であるので、実施例2のようにして作製したCuが表面に固着したアトマイズ粉をArガス雰囲気中1000℃で5時間熱処理した後、粉砕し、200メッシュで分級し、篩下を金属負極活物質として得た。この金属負極活物質を用いたこと以外は、実施例2と同様にして円筒型非水電解液二次電池を作製した。
【0070】
〈比較例1〉
金属M中に炭素を内包させなかった金属負極活物質を用いたこと以外は、実施例1と同様にして円筒型非水電解液二次電池を作製した。
【0071】
〈比較例2〉
炭素を内包した金属Mの周囲にアセチレンブラックをハイブリダイゼーションさせなかった金属負極活物質を用いたこと以外は、実施例1と同様にして円筒型非水電解液二次電池を作製した。
【0072】
以上のようにして作製された実施例及び比較例の電池に対して充放電サイクル試験を行い、サイクル特性を評価した。
【0073】
まず、各電池に対して、最大電圧4.2V、定電流1A、充電時間5hの条件で定電流定電圧充電し、その後、定電流1Aで終止電圧2.5Vまで放電する充放電サイクルを繰り返した。1サイクル目の放電容量を初期容量とし、その初期容量を100とした場合の50サイクル目の放電容量維特率(%)を求めた。
【0074】
各電池についての初期容量および50サイクル目の容量維特率を表1に示す。
【0075】
【表1】
【0076】
表1から明らかなように、金属M中に炭素を内包していない比較例1、金属Mの周囲に炭素が固着されていない比較例2の電池では、電子伝導性に劣るため、1サイクル目の充電時から充放電不能となる金属Mが生じ始めてしまう。そして、サイクルに伴い充放電不能となる金属Mの量が多くなり、初期容量、容量維特率ともに劣ってしまっていることがわかる。
【0077】
一方、金属M中に炭素が内包され、金属Mの周囲に炭素又は金属Rが機械的な固着方法により固着されている金属負極活物質を用いた実施例1〜実施例3の電池においては、金属負極活物質の電子伝導性が十分に確保されているため、初期容量も大きく容量維特率も高いことがわかる。特に、熱処理により十分な電子伝導性が確保されている実施例3の電池が最も大きな初期容量と高い容量維特率を示した。
【0078】
以上の結果より、金属Mに炭素粒子が内包され、かつ、当該金属Mの表面に炭素または金属Rを機械的な固着方法により固着したものを負極活物質として用いることで、負極活物質が電気化学反応中の膨張収縮によって微粉化しても、リチウムと電気化学反応可能な金属Mの内部及び表面での電子伝導の低下を抑えることができる。そして、このような負極活物質を用いた非水電解質電池は、電極劣化による電池内部抵抗の上昇が抑えられ、サイクル劣化を抑制することができ、高容量でかつサイクル特性に優れたものとなることがわかった。
【0079】
【本発明の効果】
本発明では、負極活物質として、リチウムと電気化学反応可能な金属Mに炭素粒子が内包されており、かつ、当該金属Mの表面に、炭素またはリチウムと電気化学反応しない金属Rを機械的な固着方法により固着したものを用いているので、負極活物質が電気化学反応中の膨張収縮によって微粉化しても、リチウムと電気化学反応可能な金属Mの内部及び表面での電子伝導の低下を抑えることができる。
【0080】
これにより、本発明では、電極劣化による電池内部抵抗の上昇が抑えられ、サイクル劣化を抑制することができ、高容量でかつサイクル特性に優れた非水電解質二次電池を実現することができる。
【図面の簡単な説明】
【図1】本発明の非水電解液電池の一構成例を示す縦断面図である。
【符号の説明】
1 非水電解液電池、 2 正極、 3 負極、 4 セパレータ、 5 電池缶、 6 絶縁板、 7 負極リード、 8 正極リード、 9 電流遮断用薄板、 10 電池蓋、 11 絶縁封口ガスケット、 12 センターピン、13 安全弁装置、 14 PTC素子
Claims (22)
- リチウムと電気化学反応可能な金属Mが、炭素を内包しており、かつ、当該金属Mの表面に炭素又はリチウムと電気化学反応しない金属Rが機械的な固着方法により固着されていることを特徴とする負極活物質。
- 前記機械的な固着方法は、ハイブリダイゼーションまたはメカノフュージョンであることを特徴とする請求項1記載の負極活物質。
- 上記金属Mが、リチウムと電気化学的に反応する金属と、反応しない金属との混合物であることを特徴とする請求項1記載の負極活物質。
- 上記金属M中に内包される炭素が、ハードカーボン、ソフトカーボン、グラファイト、カーボンブラックの少なくとも一種以上からなることを特徴とする請求項1記載の負極活物質。
- 上記金属M中に内包される炭素の形状が、繊維状、球状、粒状、鱗片状の少なくとも一種以上であることを特徴とする請求項1記載の負極活物質。
- 上記金属Mの表面に固着されている炭素が、ハードカーボン、ソフトカーボン、グラファイト、カーボンブラックの少なくとも一種以上であることを特徴とする請求項1記載の負極活物質。
- 上記金属Rが、Cr、Mn、Fe、Co、Ni、Cu、Mo、Nb、Nd、Sm、Ta、Ti、Vの中から選ばれた少なくとも1種以上の金属の混合物または合金化合物であることを特徴とする請求項1記載の負極活物質。
- リチウムと電気化学反応可能な金属Mが、炭素を内包しており、かつ、当該金属Mの表面に炭素又はリチウムと電気化学反応しない金属Rが固着されている負極活物質を製造する方法であって、
前記金属Rを、機械的な固着方法により前記金属Mの表面に固着させる工程を含む
ことを特徴とする負極活物質の製造方法。 - 前記機械的な固着方法として、ハイブリダイゼーションまたはメカノフュージョンを用いることを特徴とする請求項8記載の負極活物質の製造方法。
- 上記金属Mに炭素を内包する過程において、非酸化性雰囲気中で処理される工程を含むことを特徴とする請求項8記載の負極活物質の製造方法。
- 上記金属Mとして、リチウムと電気化学的に反応する金属と、反応しない金属との混合物を用いることを特徴とする請求項8記載の負極活物質の製造方法。
- 上記金属M中に内包する炭素として、ハードカーボン、ソフトカーボン、グラファイト、カーボンブラックの少なくとも一種以上を用いることを特徴とする請求項8記載の負極活物質の製造方法。
- 上記金属M中に内包する炭素として、繊維状、球状、粒状、鱗片状の少なくとも一種以上の形状のものを用いることを特徴とする請求項8記載の負極活物質の製造方法。
- 上記金属Mの表面に固着する炭素として、ハードカーボン、ソフトカーボン、グラファイト、カーボンブラックの少なくとも一種以上を用いることを特徴とする請求項8記載の負極活物質の製造方法。
- 上記金属Rとして、Cr、Mn、Fe、Co、Ni、Cu、Mo、Nb、Nd、Sm、Ta、Ti、Vの中から選ばれた少なくとも1種以上の金属の混合物または合金化合物を用いることを特徴とする請求項8記載の負極活物質の製造方法。
- LiMxOy(MはCo、Ni、Mn、Fe、Cr、Al、Tiの群から選ばれた少なくとも一つの元素である。)で表わされるリチウム複合酸化物を正極活物質として有する正極と、負極活物質を有する負極と、正極と負極との間に介在された非水電解質とを備え、上記負極活物質は、リチウムと電気化学反応可能な金属Mが、炭素を内包しており、かつ、当該金属Mの表面に炭素又はリチウムと電気化学反応しない金属Rが機械的な固着方法により固着されてなることを特徴とする非水電解質二次電池。
- 前記機械的な固着方法は、ハイブリダイゼーションまたはメカノフュージョンであることを特徴とする請求項16記載の非水電解質二次電池。
- 上記金属Mが、リチウムと電気化学的に反応する金属と、反応しない金属との混合物であることを特徴とする請求項16記載の非水電解質二次電池。
- 上記金属M中に内包される炭素が、ハードカーボン、ソフトカーボン、グラファイト、カーボンブラックの少なくとも一種以上からなることを特徴とする請求項16記載の非水電解質二次電池。
- 上記金属M中に内包される炭素の形状が、繊維状、球状、粒状、鱗片状の少なくとも一種以上であることを特徴とする請求項16記載の非水電解質二次電池。
- 上記金属Mの表面に固着されている炭素が、ハードカーボン、ソフトカーボン、グラファイト、カーボンブラックの少なくとも一種以上であることを特徴とする請求項16記載の非水電解質二次電池。
- 上記金属Rが、Cr、Mn、Fe、Co、Ni、Cu、Mo、Nb、Nd、Sm、Ta、Ti、Vの中から選ばれた少なくとも1種以上の金属の混合物または合金化合物であることを特徴とする請求項16記載の非水電解質二次電池。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2001345326A JP3985263B2 (ja) | 2001-11-09 | 2001-11-09 | 負極活物質及びその製造方法、並びに非水電解質二次電池 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2001345326A JP3985263B2 (ja) | 2001-11-09 | 2001-11-09 | 負極活物質及びその製造方法、並びに非水電解質二次電池 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2003151544A JP2003151544A (ja) | 2003-05-23 |
| JP2003151544A5 JP2003151544A5 (ja) | 2005-06-09 |
| JP3985263B2 true JP3985263B2 (ja) | 2007-10-03 |
Family
ID=19158677
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2001345326A Expired - Fee Related JP3985263B2 (ja) | 2001-11-09 | 2001-11-09 | 負極活物質及びその製造方法、並びに非水電解質二次電池 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP3985263B2 (ja) |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5156195B2 (ja) * | 2006-03-28 | 2013-03-06 | Jfeケミカル株式会社 | リチウムイオン二次電池用負極材料およびその製造方法、リチウムイオン二次電池用負極、ならびにリチウムイオン二次電池 |
| JP5254825B2 (ja) * | 2009-01-29 | 2013-08-07 | 三洋電機株式会社 | 非水電解液二次電池 |
| CN109326792B (zh) * | 2018-10-08 | 2021-09-21 | 电子科技大学 | 一种锂合金负极材料及其制备方法 |
-
2001
- 2001-11-09 JP JP2001345326A patent/JP3985263B2/ja not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| JP2003151544A (ja) | 2003-05-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US9972831B2 (en) | Negative material for nonaqueous electrolyte secondary battery and nonaqueous electrolyte secondary battery using the negative material | |
| JP4022889B2 (ja) | 電解液および電池 | |
| JP3726958B2 (ja) | 電池 | |
| JP2002203553A (ja) | 正極活物質及び非水電解質二次電池 | |
| JP2001148248A (ja) | 負極材料の製造方法および二次電池の製造方法 | |
| JP2000030703A (ja) | 非水電解質二次電池用負極材料とそれら負極材料を用いた非水電解質二次電池 | |
| JP2001345101A (ja) | 二次電池 | |
| WO2003090296A1 (fr) | Pile | |
| JP3755506B2 (ja) | 二次電池用負極材料およびそれを用いた二次電池 | |
| JP2006134758A (ja) | 二次電池 | |
| JP4701595B2 (ja) | リチウムイオン二次電池 | |
| JP2000348722A (ja) | 非水電解質電池 | |
| JP2004006188A (ja) | 非水電解質電池 | |
| JP2004335439A (ja) | 非水電解質二次電池 | |
| JP2005317447A (ja) | 電池 | |
| JP2002203556A (ja) | 非水電解質二次電池 | |
| JP2004111150A (ja) | 負極材料およびそれを用いた電池 | |
| JP3985263B2 (ja) | 負極活物質及びその製造方法、並びに非水電解質二次電池 | |
| JP4424477B2 (ja) | 電解液およびリチウムイオン二次電池 | |
| JP2002151065A (ja) | 負極活物質及び非水電解質電池 | |
| JP2004342459A (ja) | 非水電解質電池 | |
| JP2004186035A (ja) | 非水電解質電池 | |
| JP2003151543A (ja) | 負極活物質及び非水電解質二次電池 | |
| JPH08180878A (ja) | リチウム二次電池 | |
| JP2004335379A (ja) | 電池用負極、非水電解質電池 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20040831 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20040831 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20060901 |
|
| RD02 | Notification of acceptance of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7422 Effective date: 20070124 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20070221 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20070227 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20070427 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20070618 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20070701 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20100720 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20100720 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20110720 Year of fee payment: 4 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20110720 Year of fee payment: 4 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20120720 Year of fee payment: 5 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20120720 Year of fee payment: 5 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130720 Year of fee payment: 6 |
|
| LAPS | Cancellation because of no payment of annual fees |