JP3671209B2 - 配位子及びそれを用いた不斉触媒 - Google Patents
配位子及びそれを用いた不斉触媒 Download PDFInfo
- Publication number
- JP3671209B2 JP3671209B2 JP2001169922A JP2001169922A JP3671209B2 JP 3671209 B2 JP3671209 B2 JP 3671209B2 JP 2001169922 A JP2001169922 A JP 2001169922A JP 2001169922 A JP2001169922 A JP 2001169922A JP 3671209 B2 JP3671209 B2 JP 3671209B2
- Authority
- JP
- Japan
- Prior art keywords
- group
- metal
- asymmetric catalyst
- catalyst
- ligand
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
- 239000011982 enantioselective catalyst Substances 0.000 title claims description 43
- 239000003446 ligand Substances 0.000 title claims description 31
- 239000000126 substance Substances 0.000 claims description 37
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 claims description 34
- 238000006243 chemical reaction Methods 0.000 claims description 29
- 150000002576 ketones Chemical class 0.000 claims description 28
- 239000003054 catalyst Substances 0.000 claims description 25
- 229910052751 metal Inorganic materials 0.000 claims description 24
- 239000002184 metal Substances 0.000 claims description 24
- 239000010936 titanium Substances 0.000 claims description 19
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 claims description 17
- YCIMNLLNPGFGHC-UHFFFAOYSA-N catechol Chemical group OC1=CC=CC=C1O YCIMNLLNPGFGHC-UHFFFAOYSA-N 0.000 claims description 16
- -1 enone Chemical compound 0.000 claims description 15
- KWOLFJPFCHCOCG-UHFFFAOYSA-N Acetophenone Chemical compound CC(=O)C1=CC=CC=C1 KWOLFJPFCHCOCG-UHFFFAOYSA-N 0.000 claims description 14
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 claims description 14
- 239000002904 solvent Substances 0.000 claims description 14
- 229910052719 titanium Inorganic materials 0.000 claims description 11
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical compound [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 claims description 10
- 125000003118 aryl group Chemical group 0.000 claims description 10
- 125000001424 substituent group Chemical group 0.000 claims description 10
- LEIMLDGFXIOXMT-UHFFFAOYSA-N trimethylsilyl cyanide Chemical compound C[Si](C)(C)C#N LEIMLDGFXIOXMT-UHFFFAOYSA-N 0.000 claims description 10
- 238000000034 method Methods 0.000 claims description 8
- 229910052761 rare earth metal Inorganic materials 0.000 claims description 8
- 150000002910 rare earth metals Chemical class 0.000 claims description 8
- 229910052698 phosphorus Inorganic materials 0.000 claims description 7
- LCHWKMAWSZDQRD-UHFFFAOYSA-N silylformonitrile Chemical compound [SiH3]C#N LCHWKMAWSZDQRD-UHFFFAOYSA-N 0.000 claims description 7
- 229910052785 arsenic Inorganic materials 0.000 claims description 6
- 150000004696 coordination complex Chemical class 0.000 claims description 6
- 229910052688 Gadolinium Inorganic materials 0.000 claims description 5
- 125000006575 electron-withdrawing group Chemical group 0.000 claims description 5
- XTHFKEDIFFGKHM-UHFFFAOYSA-N Dimethoxyethane Chemical compound COCCOC XTHFKEDIFFGKHM-UHFFFAOYSA-N 0.000 claims description 4
- 229910052772 Samarium Inorganic materials 0.000 claims description 4
- 229910052769 Ytterbium Inorganic materials 0.000 claims description 4
- QCWXUUIWCKQGHC-UHFFFAOYSA-N Zirconium Chemical compound [Zr] QCWXUUIWCKQGHC-UHFFFAOYSA-N 0.000 claims description 4
- 150000004703 alkoxides Chemical group 0.000 claims description 4
- CATSNJVOTSVZJV-UHFFFAOYSA-N heptan-2-one Chemical compound CCCCCC(C)=O CATSNJVOTSVZJV-UHFFFAOYSA-N 0.000 claims description 4
- QNXSIUBBGPHDDE-UHFFFAOYSA-N indan-1-one Chemical compound C1=CC=C2C(=O)CCC2=C1 QNXSIUBBGPHDDE-UHFFFAOYSA-N 0.000 claims description 4
- KRIOVPPHQSLHCZ-UHFFFAOYSA-N propiophenone Chemical compound CCC(=O)C1=CC=CC=C1 KRIOVPPHQSLHCZ-UHFFFAOYSA-N 0.000 claims description 4
- NAWDYIZEMPQZHO-UHFFFAOYSA-N ytterbium Chemical compound [Yb] NAWDYIZEMPQZHO-UHFFFAOYSA-N 0.000 claims description 4
- 229910052726 zirconium Inorganic materials 0.000 claims description 4
- RIFKADJTWUGDOV-UHFFFAOYSA-N 1-cyclohexylethanone Chemical compound CC(=O)C1CCCCC1 RIFKADJTWUGDOV-UHFFFAOYSA-N 0.000 claims description 3
- XSAYZAUNJMRRIR-UHFFFAOYSA-N 2-acetylnaphthalene Chemical compound C1=CC=CC2=CC(C(=O)C)=CC=C21 XSAYZAUNJMRRIR-UHFFFAOYSA-N 0.000 claims description 3
- 229910052684 Cerium Inorganic materials 0.000 claims description 3
- 229910052692 Dysprosium Inorganic materials 0.000 claims description 3
- 229910052691 Erbium Inorganic materials 0.000 claims description 3
- 229910052693 Europium Inorganic materials 0.000 claims description 3
- GYHNNYVSQQEPJS-UHFFFAOYSA-N Gallium Chemical compound [Ga] GYHNNYVSQQEPJS-UHFFFAOYSA-N 0.000 claims description 3
- 229910052689 Holmium Inorganic materials 0.000 claims description 3
- 229910052779 Neodymium Inorganic materials 0.000 claims description 3
- 229910052777 Praseodymium Inorganic materials 0.000 claims description 3
- CWAKIXKDPQTVTA-UHFFFAOYSA-N [tert-butyl(dimethyl)silyl]formonitrile Chemical compound CC(C)(C)[Si](C)(C)C#N CWAKIXKDPQTVTA-UHFFFAOYSA-N 0.000 claims description 3
- 229910052782 aluminium Inorganic materials 0.000 claims description 3
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 claims description 3
- 229910052733 gallium Inorganic materials 0.000 claims description 3
- 229910052746 lanthanum Inorganic materials 0.000 claims description 3
- MKMPBMJIGMMCPB-UHFFFAOYSA-N triethylsilylformonitrile Chemical compound CC[Si](CC)(CC)C#N MKMPBMJIGMMCPB-UHFFFAOYSA-N 0.000 claims description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 16
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 12
- XYFCBTPGUUZFHI-UHFFFAOYSA-N Phosphine Chemical compound P XYFCBTPGUUZFHI-UHFFFAOYSA-N 0.000 description 8
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 7
- AUONHKJOIZSQGR-UHFFFAOYSA-N oxophosphane Chemical compound P=O AUONHKJOIZSQGR-UHFFFAOYSA-N 0.000 description 7
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 6
- 238000005481 NMR spectroscopy Methods 0.000 description 6
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 6
- 238000004519 manufacturing process Methods 0.000 description 6
- CZDYPVPMEAXLPK-UHFFFAOYSA-N tetramethylsilane Chemical compound C[Si](C)(C)C CZDYPVPMEAXLPK-UHFFFAOYSA-N 0.000 description 6
- 230000001965 increasing effect Effects 0.000 description 5
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 5
- 238000011160 research Methods 0.000 description 5
- 230000003197 catalytic effect Effects 0.000 description 4
- 229910052804 chromium Inorganic materials 0.000 description 4
- 239000011651 chromium Substances 0.000 description 4
- 230000000694 effects Effects 0.000 description 4
- 150000002739 metals Chemical class 0.000 description 4
- 238000010534 nucleophilic substitution reaction Methods 0.000 description 4
- 230000003647 oxidation Effects 0.000 description 4
- 238000007254 oxidation reaction Methods 0.000 description 4
- FDPIMTJIUBPUKL-UHFFFAOYSA-N pentan-3-one Chemical compound CCC(=O)CC FDPIMTJIUBPUKL-UHFFFAOYSA-N 0.000 description 4
- 229910000073 phosphorus hydride Inorganic materials 0.000 description 4
- 229910052708 sodium Inorganic materials 0.000 description 4
- 239000011734 sodium Substances 0.000 description 4
- LCGLNKUTAGEVQW-UHFFFAOYSA-N Dimethyl ether Chemical compound COC LCGLNKUTAGEVQW-UHFFFAOYSA-N 0.000 description 3
- 239000002841 Lewis acid Substances 0.000 description 3
- 239000002879 Lewis base Substances 0.000 description 3
- DHKHKXVYLBGOIT-UHFFFAOYSA-N acetaldehyde Diethyl Acetal Natural products CCOC(C)OCC DHKHKXVYLBGOIT-UHFFFAOYSA-N 0.000 description 3
- 150000001241 acetals Chemical class 0.000 description 3
- 230000015572 biosynthetic process Effects 0.000 description 3
- 125000002485 formyl group Chemical class [H]C(*)=O 0.000 description 3
- 150000007517 lewis acids Chemical class 0.000 description 3
- 239000007858 starting material Substances 0.000 description 3
- NUCWENGKGHLSAT-UHFFFAOYSA-N titanium(4+) tetracyanide Chemical compound [Ti+4].[C-]#N.[C-]#N.[C-]#N.[C-]#N NUCWENGKGHLSAT-UHFFFAOYSA-N 0.000 description 3
- YYROPELSRYBVMQ-UHFFFAOYSA-N 4-toluenesulfonyl chloride Chemical compound CC1=CC=C(S(Cl)(=O)=O)C=C1 YYROPELSRYBVMQ-UHFFFAOYSA-N 0.000 description 2
- XFXPMWWXUTWYJX-UHFFFAOYSA-N Cyanide Chemical compound N#[C-] XFXPMWWXUTWYJX-UHFFFAOYSA-N 0.000 description 2
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 2
- 239000007818 Grignard reagent Substances 0.000 description 2
- 239000002253 acid Substances 0.000 description 2
- 239000013543 active substance Substances 0.000 description 2
- 125000000217 alkyl group Chemical group 0.000 description 2
- 150000001412 amines Chemical class 0.000 description 2
- 150000001720 carbohydrates Chemical class 0.000 description 2
- 238000010586 diagram Methods 0.000 description 2
- 125000005982 diphenylmethyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])(*)C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 2
- 230000002708 enhancing effect Effects 0.000 description 2
- 150000002466 imines Chemical class 0.000 description 2
- 229910052763 palladium Inorganic materials 0.000 description 2
- 230000000704 physical effect Effects 0.000 description 2
- 150000003138 primary alcohols Chemical class 0.000 description 2
- 239000002994 raw material Substances 0.000 description 2
- 238000003786 synthesis reaction Methods 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- VXUYXOFXAQZZMF-UHFFFAOYSA-N titanium(IV) isopropoxide Chemical compound CC(C)O[Ti](OC(C)C)(OC(C)C)OC(C)C VXUYXOFXAQZZMF-UHFFFAOYSA-N 0.000 description 2
- 238000001644 13C nuclear magnetic resonance spectroscopy Methods 0.000 description 1
- 238000005160 1H NMR spectroscopy Methods 0.000 description 1
- HGUFODBRKLSHSI-UHFFFAOYSA-N 2,3,7,8-tetrachloro-dibenzo-p-dioxin Chemical compound O1C2=CC(Cl)=C(Cl)C=C2OC2=C1C=C(Cl)C(Cl)=C2 HGUFODBRKLSHSI-UHFFFAOYSA-N 0.000 description 1
- RNVNKNCCKYVVFR-UHFFFAOYSA-N 2-(diphenylphosphorylmethyl)-4-(2-methoxyphenyl)-3-phenylmethoxyoxane Chemical compound COC1=CC=CC=C1C1C(OCC=2C=CC=CC=2)C(CP(=O)(C=2C=CC=CC=2)C=2C=CC=CC=2)OCC1 RNVNKNCCKYVVFR-UHFFFAOYSA-N 0.000 description 1
- LBLYYCQCTBFVLH-UHFFFAOYSA-N 2-Methylbenzenesulfonic acid Chemical compound CC1=CC=CC=C1S(O)(=O)=O LBLYYCQCTBFVLH-UHFFFAOYSA-N 0.000 description 1
- 125000004204 2-methoxyphenyl group Chemical group [H]C1=C([H])C(*)=C(OC([H])([H])[H])C([H])=C1[H] 0.000 description 1
- AZOGWRDZLKUPBG-UHFFFAOYSA-N 2-methyl-4-phenyl-2-trimethylsilyloxybutanenitrile Chemical compound C[Si](C)(C)OC(C#N)(C)CCC1=CC=CC=C1 AZOGWRDZLKUPBG-UHFFFAOYSA-N 0.000 description 1
- 238000004679 31P NMR spectroscopy Methods 0.000 description 1
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 1
- IZVCCRWLZFWKLV-UHFFFAOYSA-N [4-(2-methoxyphenyl)-3-phenylmethoxyoxan-2-yl]methanol Chemical compound COC1=CC=CC=C1C1C(OCC=2C=CC=CC=2)C(CO)OCC1 IZVCCRWLZFWKLV-UHFFFAOYSA-N 0.000 description 1
- RRCSCQBFPHXRFC-UHFFFAOYSA-N [4-methoxy-3-[(2-phenyl-4,4a,6,7,8,8a-hexahydropyrano[3,2-d][1,3]dioxin-8-yl)oxy]phenyl]-phenylmethanone Chemical compound COC1=CC=C(C(=O)C=2C=CC=CC=2)C=C1OC(C1O2)CCOC1COC2C1=CC=CC=C1 RRCSCQBFPHXRFC-UHFFFAOYSA-N 0.000 description 1
- MKIPGUZOUZJLPK-UHFFFAOYSA-N [Ti+].[C-]#N Chemical compound [Ti+].[C-]#N MKIPGUZOUZJLPK-UHFFFAOYSA-N 0.000 description 1
- 238000009825 accumulation Methods 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 150000008365 aromatic ketones Chemical class 0.000 description 1
- 125000005002 aryl methyl group Chemical group 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- 125000003236 benzoyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C(*)=O 0.000 description 1
- 150000001728 carbonyl compounds Chemical class 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 230000009918 complex formation Effects 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- 238000010276 construction Methods 0.000 description 1
- 230000017858 demethylation Effects 0.000 description 1
- 238000010520 demethylation reaction Methods 0.000 description 1
- 238000010511 deprotection reaction Methods 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- VILAVOFMIJHSJA-UHFFFAOYSA-N dicarbon monoxide Chemical compound [C]=C=O VILAVOFMIJHSJA-UHFFFAOYSA-N 0.000 description 1
- RXKJFZQQPQGTFL-UHFFFAOYSA-N dihydroxyacetone Chemical compound OCC(=O)CO RXKJFZQQPQGTFL-UHFFFAOYSA-N 0.000 description 1
- 230000009977 dual effect Effects 0.000 description 1
- 125000004185 ester group Chemical group 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- DZGCGKFAPXFTNM-UHFFFAOYSA-N ethanol;hydron;chloride Chemical compound Cl.CCO DZGCGKFAPXFTNM-UHFFFAOYSA-N 0.000 description 1
- 238000001704 evaporation Methods 0.000 description 1
- 150000004795 grignard reagents Chemical class 0.000 description 1
- ORTFAQDWJHRMNX-UHFFFAOYSA-N hydroxidooxidocarbon(.) Chemical class O[C]=O ORTFAQDWJHRMNX-UHFFFAOYSA-N 0.000 description 1
- 238000002372 labelling Methods 0.000 description 1
- 150000007527 lewis bases Chemical class 0.000 description 1
- NIXOIRLDFIPNLJ-UHFFFAOYSA-M magnesium;benzene;bromide Chemical compound [Mg+2].[Br-].C1=CC=[C-]C=C1 NIXOIRLDFIPNLJ-UHFFFAOYSA-M 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- 239000000203 mixture Substances 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- 229910052760 oxygen Inorganic materials 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- 125000004430 oxygen atom Chemical group O* 0.000 description 1
- 239000011574 phosphorus Substances 0.000 description 1
- 239000002798 polar solvent Substances 0.000 description 1
- 239000012041 precatalyst Substances 0.000 description 1
- BDERNNFJNOPAEC-UHFFFAOYSA-N propan-1-ol Chemical compound CCCO BDERNNFJNOPAEC-UHFFFAOYSA-N 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 230000035484 reaction time Effects 0.000 description 1
- 125000003808 silyl group Chemical group [H][Si]([H])([H])[*] 0.000 description 1
- 238000001308 synthesis method Methods 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- FPGGTKZVZWFYPV-UHFFFAOYSA-M tetrabutylammonium fluoride Chemical compound [F-].CCCC[N+](CCCC)(CCCC)CCCC FPGGTKZVZWFYPV-UHFFFAOYSA-M 0.000 description 1
- ISXOBTBCNRIIQO-UHFFFAOYSA-N tetrahydrothiophene 1-oxide Chemical compound O=S1CCCC1 ISXOBTBCNRIIQO-UHFFFAOYSA-N 0.000 description 1
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 1
- JRSZVSQBYSJBKF-UHFFFAOYSA-N trimethylstannylformonitrile Chemical compound C[Sn](C)(C)C#N JRSZVSQBYSJBKF-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/66—Arsenic compounds
- C07F9/70—Organo-arsenic compounds
- C07F9/74—Aromatic compounds
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J31/00—Catalysts comprising hydrides, coordination complexes or organic compounds
- B01J31/16—Catalysts comprising hydrides, coordination complexes or organic compounds containing coordination complexes
- B01J31/18—Catalysts comprising hydrides, coordination complexes or organic compounds containing coordination complexes containing nitrogen, phosphorus, arsenic or antimony as complexing atoms, e.g. in pyridine ligands, or in resonance therewith, e.g. in isocyanide ligands C=N-R or as complexed central atoms
- B01J31/1845—Catalysts comprising hydrides, coordination complexes or organic compounds containing coordination complexes containing nitrogen, phosphorus, arsenic or antimony as complexing atoms, e.g. in pyridine ligands, or in resonance therewith, e.g. in isocyanide ligands C=N-R or as complexed central atoms the ligands containing phosphorus
- B01J31/1875—Phosphinites (R2P(OR), their isomeric phosphine oxides (R3P=O) and RO-substitution derivatives thereof)
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J31/00—Catalysts comprising hydrides, coordination complexes or organic compounds
- B01J31/16—Catalysts comprising hydrides, coordination complexes or organic compounds containing coordination complexes
- B01J31/22—Organic complexes
- B01J31/2204—Organic complexes the ligands containing oxygen or sulfur as complexing atoms
- B01J31/2208—Oxygen, e.g. acetylacetonates
- B01J31/2226—Anionic ligands, i.e. the overall ligand carries at least one formal negative charge
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J31/00—Catalysts comprising hydrides, coordination complexes or organic compounds
- B01J31/16—Catalysts comprising hydrides, coordination complexes or organic compounds containing coordination complexes
- B01J31/22—Organic complexes
- B01J31/2204—Organic complexes the ligands containing oxygen or sulfur as complexing atoms
- B01J31/2208—Oxygen, e.g. acetylacetonates
- B01J31/2226—Anionic ligands, i.e. the overall ligand carries at least one formal negative charge
- B01J31/223—At least two oxygen atoms present in one at least bidentate or bridging ligand
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic Table
- C07F7/003—Compounds containing elements of Groups 4 or 14 of the Periodic Table without C-Metal linkages
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/547—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom
- C07F9/655—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having oxygen atoms, with or without sulfur, selenium, or tellurium atoms, as the only ring hetero atoms
- C07F9/6552—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having oxygen atoms, with or without sulfur, selenium, or tellurium atoms, as the only ring hetero atoms the oxygen atom being part of a six-membered ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/547—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom
- C07F9/6596—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having atoms other than oxygen, sulfur, selenium, tellurium, nitrogen or phosphorus as ring hetero atoms
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2231/00—Catalytic reactions performed with catalysts classified in B01J31/00
- B01J2231/30—Addition reactions at carbon centres, i.e. to either C-C or C-X multiple bonds
- B01J2231/34—Other additions, e.g. Monsanto-type carbonylations, addition to 1,2-C=X or 1,2-C-X triplebonds, additions to 1,4-C=C-C=X or 1,4-C=-C-X triple bonds with X, e.g. O, S, NH/N
- B01J2231/341—1,2-additions, e.g. aldol or Knoevenagel condensations
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2531/00—Additional information regarding catalytic systems classified in B01J31/00
- B01J2531/20—Complexes comprising metals of Group II (IIA or IIB) as the central metal
- B01J2531/26—Zinc
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2531/00—Additional information regarding catalytic systems classified in B01J31/00
- B01J2531/20—Complexes comprising metals of Group II (IIA or IIB) as the central metal
- B01J2531/27—Cadmium
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2531/00—Additional information regarding catalytic systems classified in B01J31/00
- B01J2531/20—Complexes comprising metals of Group II (IIA or IIB) as the central metal
- B01J2531/28—Mercury
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2531/00—Additional information regarding catalytic systems classified in B01J31/00
- B01J2531/30—Complexes comprising metals of Group III (IIIA or IIIB) as the central metal
- B01J2531/32—Gallium
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2531/00—Additional information regarding catalytic systems classified in B01J31/00
- B01J2531/30—Complexes comprising metals of Group III (IIIA or IIIB) as the central metal
- B01J2531/38—Lanthanides other than lanthanum
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Inorganic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- Molecular Biology (AREA)
- Catalysts (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Description
【0001】
【発明の属する技術分野】
本発明は、配位子及びその配位子を用いた不斉触媒に関し、特に、ケトンのシアノシリル化反応を高エナンチオ選択的に促進する不斉触媒に関する。
【0002】
【従来の技術】
不斉触媒は、触媒自体が光学活性物質を生成する能力を持つ触媒で、エナンチオ区別触媒のことを意味する。不斉触媒を用いて得られる各種生成物を、出発物質等に利用して簡便に種々の生成物を得ることができる。
【0003】
現在では、アルデヒド、イミン、及びケトンなどのカルボニル化合物に対するシアンの不斉触媒の研究が集中的に行われている。化学触媒を用いた例として、アリールメチルケトンについて、最高でも72%程度のエナンチオマー過剰率が得られる触媒が知られている。
【0004】
【発明が解決しようとする課題】
しかしながら、ケトンの実用的な不斉触媒はこれまで報告されていない。また、事実、前述の化学触媒を用いた例においても、エチルケトン(30%)や脂肪族ケトンには適用できないという問題点がある。エチルケトンや脂肪族ケトンを含めケトン全般に作用できる不斉触媒を得ることができれば、医学及び薬学の研究などに大量に要求される4級α-ヒドロキシカルボン酸、4級β-アミノアルコール等の有用物質を大量に、かつ、簡便に合成することが可能となる。それゆえ、ケトンの有効的な触媒的シアノシリル化の開発が長く待ち望まれていた。しかし、このような不斉触媒は、これまで存在しない。
【0005】
そこで、本発明は、広くケトン全般に作用し得る不斉触媒を提供することを目的とする。
【0006】
【課題を解決するための手段】
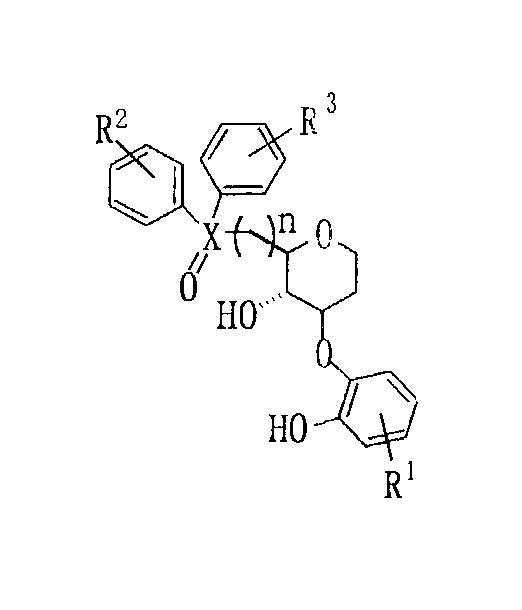
上記目的を達成するために、発明者らは、アルデヒドやイミン等の触媒的不斉シアノシリル化反応等の基礎研究を積み重ねた結果、本発明の化合物を見出すに至った。本発明の配位子は、
【化8】
(但し、[化8]中R1、R2、R3は、芳香族環上の置換基であり、Xは、P又はAsである。nは1〜3である。)で表されることを特徴とする。
本発明の配位子は、
【化9】
(式中R1、R2、R3は、芳香族環上の置換基であり、R4は、電子吸引基を示す。Xは、P又はAsである。nは1〜3である。)で表されることを特徴とする。
【0007】
本発明の配位子は、前記電子吸引基が、−NH3、−CF3、−CCl3、−NO2、−CN、−CHO4、−COCH3、−COCH3、−CO2H、−SO2CH3、下記式
【化10】
下記式
【化11】
下記式
【化12】
及び下記式
【化13】
(但し、[化10]中、R5は、芳香族環上の置換基を示す。)からなる群から選択される少なくとも1つからなることを特徴とする。
本発明の不斉触媒は、前記配位子のカテコール部分と金属とが結合していることを特徴とする。
【0008】
本発明の不斉触媒は、金属が、金属錯体として結合していることを特徴とする。
【0009】
本発明の不斉触媒は、金属錯体が、
【化14】
に示す構造からなることを特徴とする。
【0010】
本発明の不斉触媒の好ましい実施態様としては、金属が、チタン、ジルコニウム、イッテルビウム、アルミニウム、ガリウムからなる群から選択される少なくとも1種であることを特徴とする。
【0011】
本発明の不斉触媒の好ましい実施態様としては、金属が、希土類金属であることを特徴とする。
【0012】
本発明の不斉触媒の好ましい実施態様としては、希土類金属が、La、Ce、Pr、Nd,Pm、Sm、Eu、Gd、Dy、Ho、Erからなる群から選択される少なくとも1種であることを特徴とする。
【0013】
本発明のシロキシニトリルの製法としては、上記不斉触媒の存在下、ケトンとシリルシアニドとを反応させて得ることを特徴とする。
【0014】
本発明のシロキシニトリルの製法の好ましい実施態様としては、ケトンが、アセトフェノン、アセトナフトン、プロピオフェノン、インダノン、エノン、シクロヘキシルメチルケトン、n−アルカノン、2−ペプタノンからなる群から選択される少なくとも1種であることを特徴とする。
【0015】
本発明のシロキシニトリルの製法の好ましい実施態様としては、シリルシアニドが、トリメチルシリルシアニド、トリエチルシリルシアニド、tブチルジメチルシリルシアニドからなる群から選択される少なくとも1種であることを特徴とする。
【0016】
本発明のシロキシニトリルの製法の好ましい実施態様としては、反応を、配位性溶媒の存在下で行うことを特徴とする。
【0017】
本発明のシロキシニトリルの製法の好ましい実施態様としては、配位性溶媒が、テトラヒドロフラン(THF)、ジメトキシエタン、エーテルからなる群から選択されることを特徴とする。
【0018】
【発明の実施の形態】
本発明の配位子は、次式、
【化15】
(式中R1、R2、R3は、芳香族環上の置換基であり、Xは、P又はAsである。nは1〜3である。)で表される。nは、整数に限定されない。従って、nが異なる複数の配位子を用いて、触媒を同時に行うこともできる。
また、本発明の配位子は、次式、
【化16】
(式中R1、R2、R3は、芳香族環上の置換基であり、R4は、電子吸引基を示す。Xは、P又はAsである。nは1〜3である。)で表される。nは、整数に限定されない。従って、nが異なる複数の配位子を用いて、触媒を同時に行うこともできる。
【0019】
本発明者らは、機能性触媒の概念から新規不斉触媒を開発するための研究過程中、ルイス酸(Al)−ルイス塩基(ホスフィンオキシド)触媒(図2に示す。)がアセトフェノンのシアノシリル化を促進することができることを見出したが、エナンチオマー過剰率が低い(20%)ものであった。より高いエナンチオ選択性を得るために、C3ヒドロキシル基にてカテコール部分を導入することを試みた。C3でのエーテル酸素の配位は、例えば図3のような複合体の形成を可能とする。したがって、カテコールのフェニル基を、触媒のα側(リンと反対側、凹部側)で固定しなければならず、それゆえ、β側、ルイス塩基ホスフィンオキシドと同じ側で、ケトンの結合する位置を規定することを考えた。その結果、創作されたのが上式[化15]及び[化16]で示されるような配位子である。
【0020】
上記式[化15]の骨格となる配位子は、例えば、以下のように合成することができる。合成過程における反応を[化17]に示した。
【化17】
【0021】
アルコール1をナトリウム アルコキシドとした後、アレン−クロム錯体への求核置換反応により、アルコール1の水酸基にカテコール部分を導入した2を得る。出発原料となるアルコールとしては、特に限定されないが、例えば、糖を原料とするアルコールを挙げることができる。2のアセタールを、DIBAL−Hにより還元し3とした後、アルコールをトシル化し4とする。4とPh2PKを反応させ、生じたホスフィンをH2O2で酸化することで、5とする。5をパラジウム(Pd/C)触媒により還元的に脱ベンジル化し、その後AlCl3−EtSHでメチルエーテルを脱保護し、1-Lを得ることができる。
【0022】
このように、配位子1−Lを、[化17]に示すように既知のアルコールから5g程度のスケールで容易に合成することができる。
特に、R4として、[化3]で示される場合の合成方法について説明すると、以下のようになる。合成過程における反応を[化18]に示した。
【化18】
なお、[化18]中の反応条件及び試薬については、(a) 7, NaH, THF;I2, 84%(b)TBAF, THF, 99%;(c)PDC, MS4A, CH2Cl2、94%;(d) PhMgBr, THF, 95%;(e) PDC, MS 4A, CH2Cl2, 88%;(f)TsOH・MeOH, 97%;(g)TsCl, py, 83%;(h)ph2PK(2.2equiv.), THF;(i)H2O2, MeOH・H2O, 40%(2
Steps);(j)LiI, DMF, 150℃, 80%.である。
アルコール6をナトリウム アルコキシドとした後、アレン−クロム錯体への求核置換反応により、アルコール6の水酸基にカテコール部分を導入した8を得る。出発原料となるアルコールとしては、特に限定されないが、例えば、糖を原料とするアルコールを挙げることができる。TBS基を除去した後、酸化、グリニャール試薬の付加、酸化により9を合成した。9のアセタールを酸により脱保護し一級アルコールを選択的にトシル化し、10とする。10とPh2PKを反応させ、生じたホスフィンをH2O2で酸化し、その後、脱メチル化により2−Lを得ることができる。
【0023】
R1、R2、R3及びR5は、芳香族環上の置換基であり、特に限定されるものではない。置換基として、具体的には、アルキル、エーテル、アミン、エステル等を挙げることができる。R1として、ルイス酸性を高めるという観点から、好ましくは、エステル基、R2、R3として、ルイス塩基性を高めるという観点から、好ましくは、エーテル、アミン、アルキル基を挙げることができる。R5としては、立体的に大きなものという観点から、好ましくは、t‐ブチル基を挙げることができる。
【0024】
本発明の不斉触媒は、[化1]又は[化2]の配位子のカテコール部分に金属が結合する。不斉触媒とは、触媒自体が光学活性物質を生成する能力をもつ触媒で、正しくは、エナンチオ区別触媒のことを意味する。金属は、配位子のカテコール部分のヒドロキシル基にて金属錯体を形成することが可能である。
【0025】
カテコール部分に結合する金属としては、チタン、ジルコニウム、イッテルビウム、アルミニウム、ガリウムからなる群から選択される少なくとも1種を挙げることができる。これらの金属を単独で、又は組み合わせて使用することができる。エナンチオ選択性が高いという観点から、金属としては、チタンを挙げることができる。
また、カテコール部分に結合する金属としては、希土類金属を挙げることができる。希土類金属としては、例えば、La、Ce、Pr、Nd,Pm、Sm、Eu、Gd、Dy、Ho、Erからなる群から選択される少なくとも1種を挙げることができる。高いエナンチオ選択性が得られるという観点から、希土類金属としては、好ましくは、Gd、Smを挙げることができる。
【0026】
本発明の不斉触媒としては、金属錯体が、下記式
【化19】
に示す構造からなることができる。
【0027】
チタン、ジルコニウム等の場合、[化19]に示す構造を取り得る。R6としては、アルコキシド、CN、Cl、F、Br、Iなどを挙げることができる。R6として、これらアルコキシド、CN、Cl、F、Br、又はIを用いた配位子により、不斉触媒の安定化を図ることができる。なお、イッテルビウム等の場合のように、結合形態から、CNなどの配位子を必要としないものも存在する。
【0028】
本発明の不斉触媒は、ケトンのシアノシリル化反応を触媒することができる。シアノシリル化とは、カルボニル炭素にシアニドが求核付加をし、生じたアルコキシドがシリル基により補足されることをいう。
【0029】
本発明の製法によれば、シロキシニトリルは、上記不斉触媒の存在下、ケトンとシリルシアニドとを反応させて得ることができる。
【0030】
ケトンのシアノシリル化反応によって得られるシロキシニトリルは、4級α−ヒドロキシカルボン酸などの有用物質を、一工程で得ることを可能とする。
【0031】
ここで、本発明の不斉触媒の対象となるケトンは特に限定されない。従って、対象となるケトンとしては、脂肪族ケトン、芳香族ケトンなどを含めケトン全般を挙げることができる。例えば、ケトンとして、アセトフェノン、アセトナフトン、プロピオフェノン、インダノン、エノン、シクロヘキシルメチルケトン、n−アルカノンからなる群から選択される少なくとも1種を挙げることができる。n−アルカノンとしては、2−ヘプタノンなどを挙げることができる。
【0032】
シリルシアニドとしては、例えば、トリメチルシリルシアニド(TMSCN)、トリエチルシリルシアニド、t−ブチルジメチルシリルシアニド等を挙げることができる。なお、同様に適用してシロキシニトリルが得られる物質としては、シリルシアニド以外に、HCN、トリメチルすずシアニド等を挙げることができる。
【0033】
また、ケトンのシアノシリル化反応に用いる溶媒は、特に限定されるものではない。溶媒としては、例えば、トルエン、CH2Cl2などの低極性溶媒、テトラヒドロフラン(THF)、ジメトキシエタン、エーテルなどの配位性溶媒を挙げることができる。反応速度を上げ、高エナンチオ選択性を得るという観点から、溶媒としては、好ましくは、テトラヒドロフラン(THF)、ジメトキシエタン、エーテルなどの配位性溶媒を挙げることができる。
【0034】
シアノシリル化反応の反応温度は、室温でもよく特に限定されないが、高エナンチオ選択性を得るという観点から、−50〜室温℃、好ましくは、−50〜0℃、さらに好ましくは、−50〜−20℃である。下限を−50としたのは、エナンチオ選択性を高めるという理由からであり、上限を室温としたのは、反応速度をあげるという理由からである。
【0035】
また、ケトンの濃度は、目的とする生成物に応じて適宜変更することができ、特に限定されない。ケトンの濃度が高いほど反応速度が高いという傾向がある。
【0036】
【実施例】
ここで、本発明の一実施例を説明するが、本発明は、下記の実施例に限定して解釈されるものではない。また、本発明の要旨を逸脱することなく、適宜変更することが可能であることは言うまでもない。
実施例1
[3−ベンジルオキシ−4−(2−メトキシフェニル)−テトラハイドロ−ピラノ[3,2−d][1,3]ジオキシン−8−オールアルコール(以下、1とする)をナトリウム アルコキシドとした後、アレン−クロム錯体への求核置換反応により、アルコールの水酸基にカテコール部分を導入した8−(2−メトキシフェニル)−2−フェニル−ヘキサハイドロ−ピラノ[3,2−d][1,3]ジオキシン(以下、2とする)を得る。2のアセタールを、DIBAL−Hにより還元し[3−ベンジルオキシ−4−(2−メトキシフェニル)−テトラハイドロピラン−2−イル]メタノール(以下、3とする)とした後、アルコールをトシル化しトルエン−4−スルホン酸 3−ベンジルオキシ−4−(2−メトキシフェニル)−テトラハイドロピラン−2−イル−メチルエステル(以下、4とする)とする。4とPh2PKを反応させ、生じたホスフィンをH2O2で酸化することで、3−ベンジルオキシ−2−(ジフェニルホスフィノイルメチル)−4−(2−メトキシフェニル)−テトラハイドロピラン(以下、5とする)とする。5をパラジウム(Pd/C)触媒により還元的に脱ベンジル化し、その後AlCl3−EtSHでメチルエーテルを脱保護し、本発明の配位子1-Lを得ることができる。
【0037】
得られた配位子の1-Lの物性値を以下に示す。
融点 219−220℃
1H NMR(500MHz、CDCl3)δ1.94(m、1H)、2.14(m、1H)、2.69(ddd、J=9.8、15.0,15.0Hz、1H)、2.84(ddd、J=2.8,9.5、15.3Hz、1H)、3.23(ddd、J=1.9、12.2、12.2Hz、1H)、3.34(dddd、J=2.8,7.0,9.4,9.8Hz、1H)、3.55(ddd、J=5.5、8.9,11.6Hz、1H)、3.73(dd、J=8.9,9.4Hz、1H)、3.90(ddd、J=1.2、5.7、12.2Hz、1H)、6.71(ddd、J=1.9,7.4、7.4Hz、1H)、6.96(m、3H)、7.51(m、6H)、7.75(m、4H)、8.92(s、1H);13C NMR (125MHz、CDCl3) δ31.62,37.61(d、J=68Hz)、65.50,74.96、76.11、84.84,117.22、119.14、122.45、125.50、128.90、129.00、129.03、129.13、130.60(d、J=10Hz)、131.11(d、J=9Hz)、132.47、145.89、150.15:31P NMR(202MHz、CDCl3)、δ34.0
IR 3422、1156、1103cm-1
C25H27O5Pとしての分析値:C、67.67;H、6.10%.
実測値:C、67.92;H、5.94%
【0038】
実施例2
各種金属を用いて、エナンチオマー選択性を調べた。具体的には、アセトフェノンにTMS(テトラメチルシラン)CNを添加する触媒について配位子1−Lと結合した異なる金属について調査した。反応を、以下の[化20]に示す。
【化20】
【0039】
各種金属についてエナンチオマー選択性の結果を表1に示す。
【表1】
表1中、eeは、エナンチオマー過剰率を示す。また、R/Sは、生成物の絶対配置を示す。 Yb触媒は、著しい活性を示したが、Ti触媒は、最もよいエナンチオマー過剰率を示した。さらに、反応を、−20℃で行ったとき、エナンチオマー過剰率は73%まで増加した。
【0040】
実施例3
次に、不斉触媒の溶媒に対する影響を調べた。その結果を表2に示す。また、反応を以下の[化21]に示す。
【化21】
【0041】
興味深いことに、反応速度とエナンチオ選択性の双方は、CH2Cl2又はトルエンなどの低極性溶媒と比較してテトラヒドロフラン(以下、THFという。)などの配位性溶媒において増加した。興味あることに、より濃縮した条件下で使用すると(アセトフェノンの条件で3M)、反応は、−30℃で36時間の間より効率的に行われ、85%の収率と92%ccの生成物を与えた。反応条件を10mol%の Ti(OiPr)4及びTHF溶媒中の配位子1−Lを含むとした場合、最も良い結果を得た。
【0042】
【表2】
【0043】
実施例4
この新しく開発した不斉触媒は、芳香族及び脂肪族ケトンを含む、様々なケトンに対して幅広い適用性を高エナンチオ選択性で示す。その結果を表3に示す。また、反応を下記[化22]に示す。
【化22】
具体的に、プロピオフェノン9fやインダノン9eなどの反応性の低いケトンは、収率が、それぞれ89%と72%であり、エナンチオマー過剰率が、それぞれ91%と69%の生産物を与えた。エノン9gは、完全な選択性で付加生成物を与えた。簡単なn―アルカノン9jでさえ、76%のエナンチオマー過剰率を持つ生成物を与えた。
【0044】
また、エナンチオマー過剰率をおとさずに、2−トリメチルシロキシ−2−(2’−ナフチル)−プロパンニトリル(生成物10d)を、単一工程で第4級ヒドロキシエステル(HCl−EtOH、90℃にて3時間)又はアルデヒド(DIBAL−H)に変えることができた。
【0045】
【表3】
【0046】
実施例 5
不斉触媒の構造を確認するため、NMR解析を行った。Ti(OiPr)4及び1−Lの混合物を、トルエン中で75℃にて1時間加熱したとき、2当量のiPrOHの精製を1HNMRにおいて観察した。したがって、この段階にて、予備触媒は、チタン イソプロポキシド(1:Mtl=Ti(OiPr)2)を含む。トルエンを蒸発させた後、THF及びTMSCN(Tiに対して2当量)を加えた。その後、TMSOiPrに対応するピーク(0.19、1.21及び4.1ppm)が現われ、チタンシアニドの生成を示した。室温にて1時間後、約70%のチタンがモノシアニドを含むと考えられ、それは、残部のTMSCN(0.44ppm)と発生したTMSOPrの集積率から推測できる。アセトフェノン(Tiに対して10当量)及びTMSCN(Tiに対して15当量)を更に加えることにより反応が始まり、ほとんど完全にモノシアニドに変化する。したがって、不斉触媒は、チタンモノシアノモノイソプロポキシド(1:Mtl=Ti(CN)(OiPr)からなる複合体として存在することが可能である。後述するように、チタンモノシアニドの複合体形成は、1当量のTMSCNを使用してより長い反応時間(10h)によっても行える。
【0047】
この反応の性質についてさらなる識見を得るために、反応速度論的な研究を行い、触媒に対する反応次数を決定した。
【0048】
さらに、TMS13CNを使用した標識試験から、シアニドは、チタンシアニドからではなく、TMSCNから反応したと考えられた。すなわち、Ti(OiPr)4、1-L(1当量)及びTMS12CN(1当量)から12CNを含む活性チタン触媒を調整した(室温で10時間)。TMS12CNの完全な消費をH NMRで確認した後、9a(1当量)とTMS13CN(1当量)を加えた。生成物10aに13CNが77%取込まれていることを、C NMRで確認した。これらの結果は、チタンシアニドは、CN源としてでなくルイス酸としてだけ作用することを示唆した。
【0049】
そして、エナンチオ選択におけるホスフィンオキシドの役割を解明するためにホスフィンオキシドの代わりにジフェニルメチル基を有する触媒をした。その結果、ジフェニルメチル基を有する触媒では、非常にゆっくりと室温にて反応が進行し、2−トリメチルシロキシ−2−フェニルプロパニトリル([化22]の10a)、及び2−トリメチルシロキシ−2−メチル−4−フェニルブタンニトリル([化22]の10i)を、双方とも2%のエナンチオマー過剰率にて31%及び33%の収率(80時間)でそれぞれ得た。これらの観点、我々の従来の研究結果とから、チタンとホスフィンオキシドの酸素原子が、それぞれルイス酸、及びルイス塩基としてケトン、及びTMSCNを活性化する、触媒による二重活性機構である事が分かる(図1)。
【0050】
実施例6
[3−ベンジルオキシ−4−(2−メトキシフェニル)−テトラハイドロ−ピラノ[3,2−d][1,3]ジオキシン−8−オールアルコール(以下、1とする)をナトリウム アルコキシドとした後、アレン−クロム錯体への求核置換反応により、アルコールの水酸基にカテコール部分を導入したジ‐t‐ブチル‐[4−メトキシ−3−(2−フェニル−ヘキサヒドロ−ピラノ[3,2−d][1,3]ジオキシン−8−イロキシ)−ベンジロキシ]−メチル−シラン を得る。TBSを除去した後、酸化、フェニルグリニャール試薬の付加、酸化により[4−メトキシ−3−(2フェニル−ヘキサヒドロ−ピラノ[3,2−d][1,3]ジオキシン8−イロキシ)−フェニル]−フェニル−メタノン([化18]中の9に相当)とする。9のアセタールを脱保護し、一級アルコールを選択的にトシル化し、トルエンスルホン酸4−(5−ベンゾイル−2−メトキシ−フェノキシ−3−ヒドロキシ−テトラヒドロ−ピラン−2−イルメチルエステル(10に相当)とする。10とPh2PKを反応させ、生じたホスフィンをH2O2で酸化し、メチルエーテルを脱保護し、配位子2-Lを得ることができる。
【0051】
本発明の配位子2−Lの物性値を以下に示す。
1H−NMR(500MHz, CDCl3);δ1.94(m,1H)、2.16(m、1H)、2.72(ddd,J=9.45, 15.0, 15.0Hz, 1H)、2.84(ddd, J=3.35, 9.45、15.3Hz, 1H), 3.23(m、1H), 3.38(ddd, J=3.05, 9.15, 16.5Hz, 1H)、3.60(ddd, J=5.20, 8.90, 11.3Hz, 1H)、3.74(dd, J=8.90, 9.20Hz, 1H)、3.89(m, 1H)、6.98(d, J=8.25Hz, 1H)、7.43−7.80(m, 18H)、9.73(s, 1H):
13C−NMR(125.65MHz, CDCl3);δ31.5、36.0(d、J=68.2 Hz)、65.3, 74.7, 75.8, 84.8, 116.5, 123.8, 128.0, 128.7, 128.8, 128.8, 128.9, 129.0, 129.0, 129.6,130.0, 130.5, 130.6、130.8, 130.9, 131.0, 131.2, 131.7, 132.1, 132.3, 138.3、 145.7, 154.8, 195.1:
31P−NMR(202.35MHz, CDCl3);δ34.5
旋光度[α]D 27+13.2(c=2.34, CHCl3)
【0052】
実施例7
金属としてチタンを、R4としてベンゾイル基をそれぞれ用いて、エナンチオマー選択性を調べた。反応式を以下に示す。
【化23】
エナンチオマー選択性の結果を表4に示す。
【0053】
【表4】
表4中、eeは、エナンチオマー過剰率を示す。また、R/Sは、生成物の絶対配置を示す。R7として、フェニル基及びn−C5H11を用いた場合、それぞれ、97%及86%と高いエナンチオマー過剰率を示した。
【0054】
実施例8
次に、[化2]のR4が、フェニル基、n−C5H11、及び[化4]、[化5]、及び[化6]の場合のエナンチオマー選択性を調べた。結果を表5に示す。
【0055】
【表5】
R4が、フェニル基、n−C5H11、及び[化4]、[化5]、及び[化6]のいずれの場合においても、高いエナンチオマー選択性を示した。
【0056】
実施例9
次に、新規不斉触媒のエナンチオ選択性の結果を、種々のケトンを用いて調べた。その結果を表6に示す。
【0057】
【表6】
この結果、いずれも高いエナンチオマー過剰率を示した。
実施例10
次に、金属として、種々の希土類金属を用いた場合について、新規不斉触媒のエナンチオマー選択性を調べた。反応式を以下に示す。エナンチオマー選択性の結果を表7に示す。
【0058】
【表7】
表7中、eeは、エナンチオマー過剰率を示す。また、R/Sは、生成物の絶対配置を示す。表7に示す金属:配位子のモル比の不斉触媒を用いて、試験を行った。
その結果、R7として、フェニル基、PhCHCH基、m−C5H11を用いた場合、高いエナンチオマー過剰率を示した。
実施例11
次に、本発明の不斉触媒を用いて、種々のケトンのシアノシリル化を試みた。結果を表8に示す。
【表8】
表8中、eeは、エナンチオマー過剰率を示す。ケトンのシアノシリル化には、5mol%のGd(OiPr)と、10mol%の配位子1-Lとから構成される不斉触媒を用いた。溶媒として、THFを用いた。
表8からも明らかなように、いずれも良好なエナンチオマー過剰率を示した。
【0059】
【発明の効果】
本発明の配位子によれば、不斉触媒の配位子として有効に使用することができるという有利な効果を奏する。
【0060】
また、本発明の不斉触媒によれば、金属とホスフィンオキシドを含む新規多点認識触媒によって、ケトンの高エナンチオ選択的シアノシリル化を達成することができる。生成物(キラルシアノヒドリン)は、不斉4級αヒドロキシカルボニル誘導体、β−アミノアルコールに効果的に変換することができる。これは、不斉4級ヒドロキシカルボニル誘導体中心の構築に対する新規な合成法を与え、4級αヒドロキシカルボニル酸を使用する生化学研究を容易にすることができるという有利な効果を奏する。
【図面の簡単な説明】
【図1】 金属とホスフィンオキシドを含む本発明の不斉触媒の触媒作用についての一例を示す図である。
【図2】 ホスフィンオキシド触媒を示す図である。
【図3】 アルコールのC3ヒドロキシル基にて、カテコール部分を導入した触媒を示す図である。
【発明の属する技術分野】
本発明は、配位子及びその配位子を用いた不斉触媒に関し、特に、ケトンのシアノシリル化反応を高エナンチオ選択的に促進する不斉触媒に関する。
【0002】
【従来の技術】
不斉触媒は、触媒自体が光学活性物質を生成する能力を持つ触媒で、エナンチオ区別触媒のことを意味する。不斉触媒を用いて得られる各種生成物を、出発物質等に利用して簡便に種々の生成物を得ることができる。
【0003】
現在では、アルデヒド、イミン、及びケトンなどのカルボニル化合物に対するシアンの不斉触媒の研究が集中的に行われている。化学触媒を用いた例として、アリールメチルケトンについて、最高でも72%程度のエナンチオマー過剰率が得られる触媒が知られている。
【0004】
【発明が解決しようとする課題】
しかしながら、ケトンの実用的な不斉触媒はこれまで報告されていない。また、事実、前述の化学触媒を用いた例においても、エチルケトン(30%)や脂肪族ケトンには適用できないという問題点がある。エチルケトンや脂肪族ケトンを含めケトン全般に作用できる不斉触媒を得ることができれば、医学及び薬学の研究などに大量に要求される4級α-ヒドロキシカルボン酸、4級β-アミノアルコール等の有用物質を大量に、かつ、簡便に合成することが可能となる。それゆえ、ケトンの有効的な触媒的シアノシリル化の開発が長く待ち望まれていた。しかし、このような不斉触媒は、これまで存在しない。
【0005】
そこで、本発明は、広くケトン全般に作用し得る不斉触媒を提供することを目的とする。
【0006】
【課題を解決するための手段】
上記目的を達成するために、発明者らは、アルデヒドやイミン等の触媒的不斉シアノシリル化反応等の基礎研究を積み重ねた結果、本発明の化合物を見出すに至った。本発明の配位子は、
【化8】
(但し、[化8]中R1、R2、R3は、芳香族環上の置換基であり、Xは、P又はAsである。nは1〜3である。)で表されることを特徴とする。
本発明の配位子は、
【化9】
(式中R1、R2、R3は、芳香族環上の置換基であり、R4は、電子吸引基を示す。Xは、P又はAsである。nは1〜3である。)で表されることを特徴とする。
【0007】
本発明の配位子は、前記電子吸引基が、−NH3、−CF3、−CCl3、−NO2、−CN、−CHO4、−COCH3、−COCH3、−CO2H、−SO2CH3、下記式
【化10】
下記式
【化11】
下記式
【化12】
及び下記式
【化13】
(但し、[化10]中、R5は、芳香族環上の置換基を示す。)からなる群から選択される少なくとも1つからなることを特徴とする。
本発明の不斉触媒は、前記配位子のカテコール部分と金属とが結合していることを特徴とする。
【0008】
本発明の不斉触媒は、金属が、金属錯体として結合していることを特徴とする。
【0009】
本発明の不斉触媒は、金属錯体が、
【化14】
に示す構造からなることを特徴とする。
【0010】
本発明の不斉触媒の好ましい実施態様としては、金属が、チタン、ジルコニウム、イッテルビウム、アルミニウム、ガリウムからなる群から選択される少なくとも1種であることを特徴とする。
【0011】
本発明の不斉触媒の好ましい実施態様としては、金属が、希土類金属であることを特徴とする。
【0012】
本発明の不斉触媒の好ましい実施態様としては、希土類金属が、La、Ce、Pr、Nd,Pm、Sm、Eu、Gd、Dy、Ho、Erからなる群から選択される少なくとも1種であることを特徴とする。
【0013】
本発明のシロキシニトリルの製法としては、上記不斉触媒の存在下、ケトンとシリルシアニドとを反応させて得ることを特徴とする。
【0014】
本発明のシロキシニトリルの製法の好ましい実施態様としては、ケトンが、アセトフェノン、アセトナフトン、プロピオフェノン、インダノン、エノン、シクロヘキシルメチルケトン、n−アルカノン、2−ペプタノンからなる群から選択される少なくとも1種であることを特徴とする。
【0015】
本発明のシロキシニトリルの製法の好ましい実施態様としては、シリルシアニドが、トリメチルシリルシアニド、トリエチルシリルシアニド、tブチルジメチルシリルシアニドからなる群から選択される少なくとも1種であることを特徴とする。
【0016】
本発明のシロキシニトリルの製法の好ましい実施態様としては、反応を、配位性溶媒の存在下で行うことを特徴とする。
【0017】
本発明のシロキシニトリルの製法の好ましい実施態様としては、配位性溶媒が、テトラヒドロフラン(THF)、ジメトキシエタン、エーテルからなる群から選択されることを特徴とする。
【0018】
【発明の実施の形態】
本発明の配位子は、次式、
【化15】
(式中R1、R2、R3は、芳香族環上の置換基であり、Xは、P又はAsである。nは1〜3である。)で表される。nは、整数に限定されない。従って、nが異なる複数の配位子を用いて、触媒を同時に行うこともできる。
また、本発明の配位子は、次式、
【化16】
(式中R1、R2、R3は、芳香族環上の置換基であり、R4は、電子吸引基を示す。Xは、P又はAsである。nは1〜3である。)で表される。nは、整数に限定されない。従って、nが異なる複数の配位子を用いて、触媒を同時に行うこともできる。
【0019】
本発明者らは、機能性触媒の概念から新規不斉触媒を開発するための研究過程中、ルイス酸(Al)−ルイス塩基(ホスフィンオキシド)触媒(図2に示す。)がアセトフェノンのシアノシリル化を促進することができることを見出したが、エナンチオマー過剰率が低い(20%)ものであった。より高いエナンチオ選択性を得るために、C3ヒドロキシル基にてカテコール部分を導入することを試みた。C3でのエーテル酸素の配位は、例えば図3のような複合体の形成を可能とする。したがって、カテコールのフェニル基を、触媒のα側(リンと反対側、凹部側)で固定しなければならず、それゆえ、β側、ルイス塩基ホスフィンオキシドと同じ側で、ケトンの結合する位置を規定することを考えた。その結果、創作されたのが上式[化15]及び[化16]で示されるような配位子である。
【0020】
上記式[化15]の骨格となる配位子は、例えば、以下のように合成することができる。合成過程における反応を[化17]に示した。
【化17】
【0021】
アルコール1をナトリウム アルコキシドとした後、アレン−クロム錯体への求核置換反応により、アルコール1の水酸基にカテコール部分を導入した2を得る。出発原料となるアルコールとしては、特に限定されないが、例えば、糖を原料とするアルコールを挙げることができる。2のアセタールを、DIBAL−Hにより還元し3とした後、アルコールをトシル化し4とする。4とPh2PKを反応させ、生じたホスフィンをH2O2で酸化することで、5とする。5をパラジウム(Pd/C)触媒により還元的に脱ベンジル化し、その後AlCl3−EtSHでメチルエーテルを脱保護し、1-Lを得ることができる。
【0022】
このように、配位子1−Lを、[化17]に示すように既知のアルコールから5g程度のスケールで容易に合成することができる。
特に、R4として、[化3]で示される場合の合成方法について説明すると、以下のようになる。合成過程における反応を[化18]に示した。
【化18】
なお、[化18]中の反応条件及び試薬については、(a) 7, NaH, THF;I2, 84%(b)TBAF, THF, 99%;(c)PDC, MS4A, CH2Cl2、94%;(d) PhMgBr, THF, 95%;(e) PDC, MS 4A, CH2Cl2, 88%;(f)TsOH・MeOH, 97%;(g)TsCl, py, 83%;(h)ph2PK(2.2equiv.), THF;(i)H2O2, MeOH・H2O, 40%(2
Steps);(j)LiI, DMF, 150℃, 80%.である。
アルコール6をナトリウム アルコキシドとした後、アレン−クロム錯体への求核置換反応により、アルコール6の水酸基にカテコール部分を導入した8を得る。出発原料となるアルコールとしては、特に限定されないが、例えば、糖を原料とするアルコールを挙げることができる。TBS基を除去した後、酸化、グリニャール試薬の付加、酸化により9を合成した。9のアセタールを酸により脱保護し一級アルコールを選択的にトシル化し、10とする。10とPh2PKを反応させ、生じたホスフィンをH2O2で酸化し、その後、脱メチル化により2−Lを得ることができる。
【0023】
R1、R2、R3及びR5は、芳香族環上の置換基であり、特に限定されるものではない。置換基として、具体的には、アルキル、エーテル、アミン、エステル等を挙げることができる。R1として、ルイス酸性を高めるという観点から、好ましくは、エステル基、R2、R3として、ルイス塩基性を高めるという観点から、好ましくは、エーテル、アミン、アルキル基を挙げることができる。R5としては、立体的に大きなものという観点から、好ましくは、t‐ブチル基を挙げることができる。
【0024】
本発明の不斉触媒は、[化1]又は[化2]の配位子のカテコール部分に金属が結合する。不斉触媒とは、触媒自体が光学活性物質を生成する能力をもつ触媒で、正しくは、エナンチオ区別触媒のことを意味する。金属は、配位子のカテコール部分のヒドロキシル基にて金属錯体を形成することが可能である。
【0025】
カテコール部分に結合する金属としては、チタン、ジルコニウム、イッテルビウム、アルミニウム、ガリウムからなる群から選択される少なくとも1種を挙げることができる。これらの金属を単独で、又は組み合わせて使用することができる。エナンチオ選択性が高いという観点から、金属としては、チタンを挙げることができる。
また、カテコール部分に結合する金属としては、希土類金属を挙げることができる。希土類金属としては、例えば、La、Ce、Pr、Nd,Pm、Sm、Eu、Gd、Dy、Ho、Erからなる群から選択される少なくとも1種を挙げることができる。高いエナンチオ選択性が得られるという観点から、希土類金属としては、好ましくは、Gd、Smを挙げることができる。
【0026】
本発明の不斉触媒としては、金属錯体が、下記式
【化19】
に示す構造からなることができる。
【0027】
チタン、ジルコニウム等の場合、[化19]に示す構造を取り得る。R6としては、アルコキシド、CN、Cl、F、Br、Iなどを挙げることができる。R6として、これらアルコキシド、CN、Cl、F、Br、又はIを用いた配位子により、不斉触媒の安定化を図ることができる。なお、イッテルビウム等の場合のように、結合形態から、CNなどの配位子を必要としないものも存在する。
【0028】
本発明の不斉触媒は、ケトンのシアノシリル化反応を触媒することができる。シアノシリル化とは、カルボニル炭素にシアニドが求核付加をし、生じたアルコキシドがシリル基により補足されることをいう。
【0029】
本発明の製法によれば、シロキシニトリルは、上記不斉触媒の存在下、ケトンとシリルシアニドとを反応させて得ることができる。
【0030】
ケトンのシアノシリル化反応によって得られるシロキシニトリルは、4級α−ヒドロキシカルボン酸などの有用物質を、一工程で得ることを可能とする。
【0031】
ここで、本発明の不斉触媒の対象となるケトンは特に限定されない。従って、対象となるケトンとしては、脂肪族ケトン、芳香族ケトンなどを含めケトン全般を挙げることができる。例えば、ケトンとして、アセトフェノン、アセトナフトン、プロピオフェノン、インダノン、エノン、シクロヘキシルメチルケトン、n−アルカノンからなる群から選択される少なくとも1種を挙げることができる。n−アルカノンとしては、2−ヘプタノンなどを挙げることができる。
【0032】
シリルシアニドとしては、例えば、トリメチルシリルシアニド(TMSCN)、トリエチルシリルシアニド、t−ブチルジメチルシリルシアニド等を挙げることができる。なお、同様に適用してシロキシニトリルが得られる物質としては、シリルシアニド以外に、HCN、トリメチルすずシアニド等を挙げることができる。
【0033】
また、ケトンのシアノシリル化反応に用いる溶媒は、特に限定されるものではない。溶媒としては、例えば、トルエン、CH2Cl2などの低極性溶媒、テトラヒドロフラン(THF)、ジメトキシエタン、エーテルなどの配位性溶媒を挙げることができる。反応速度を上げ、高エナンチオ選択性を得るという観点から、溶媒としては、好ましくは、テトラヒドロフラン(THF)、ジメトキシエタン、エーテルなどの配位性溶媒を挙げることができる。
【0034】
シアノシリル化反応の反応温度は、室温でもよく特に限定されないが、高エナンチオ選択性を得るという観点から、−50〜室温℃、好ましくは、−50〜0℃、さらに好ましくは、−50〜−20℃である。下限を−50としたのは、エナンチオ選択性を高めるという理由からであり、上限を室温としたのは、反応速度をあげるという理由からである。
【0035】
また、ケトンの濃度は、目的とする生成物に応じて適宜変更することができ、特に限定されない。ケトンの濃度が高いほど反応速度が高いという傾向がある。
【0036】
【実施例】
ここで、本発明の一実施例を説明するが、本発明は、下記の実施例に限定して解釈されるものではない。また、本発明の要旨を逸脱することなく、適宜変更することが可能であることは言うまでもない。
実施例1
[3−ベンジルオキシ−4−(2−メトキシフェニル)−テトラハイドロ−ピラノ[3,2−d][1,3]ジオキシン−8−オールアルコール(以下、1とする)をナトリウム アルコキシドとした後、アレン−クロム錯体への求核置換反応により、アルコールの水酸基にカテコール部分を導入した8−(2−メトキシフェニル)−2−フェニル−ヘキサハイドロ−ピラノ[3,2−d][1,3]ジオキシン(以下、2とする)を得る。2のアセタールを、DIBAL−Hにより還元し[3−ベンジルオキシ−4−(2−メトキシフェニル)−テトラハイドロピラン−2−イル]メタノール(以下、3とする)とした後、アルコールをトシル化しトルエン−4−スルホン酸 3−ベンジルオキシ−4−(2−メトキシフェニル)−テトラハイドロピラン−2−イル−メチルエステル(以下、4とする)とする。4とPh2PKを反応させ、生じたホスフィンをH2O2で酸化することで、3−ベンジルオキシ−2−(ジフェニルホスフィノイルメチル)−4−(2−メトキシフェニル)−テトラハイドロピラン(以下、5とする)とする。5をパラジウム(Pd/C)触媒により還元的に脱ベンジル化し、その後AlCl3−EtSHでメチルエーテルを脱保護し、本発明の配位子1-Lを得ることができる。
【0037】
得られた配位子の1-Lの物性値を以下に示す。
融点 219−220℃
1H NMR(500MHz、CDCl3)δ1.94(m、1H)、2.14(m、1H)、2.69(ddd、J=9.8、15.0,15.0Hz、1H)、2.84(ddd、J=2.8,9.5、15.3Hz、1H)、3.23(ddd、J=1.9、12.2、12.2Hz、1H)、3.34(dddd、J=2.8,7.0,9.4,9.8Hz、1H)、3.55(ddd、J=5.5、8.9,11.6Hz、1H)、3.73(dd、J=8.9,9.4Hz、1H)、3.90(ddd、J=1.2、5.7、12.2Hz、1H)、6.71(ddd、J=1.9,7.4、7.4Hz、1H)、6.96(m、3H)、7.51(m、6H)、7.75(m、4H)、8.92(s、1H);13C NMR (125MHz、CDCl3) δ31.62,37.61(d、J=68Hz)、65.50,74.96、76.11、84.84,117.22、119.14、122.45、125.50、128.90、129.00、129.03、129.13、130.60(d、J=10Hz)、131.11(d、J=9Hz)、132.47、145.89、150.15:31P NMR(202MHz、CDCl3)、δ34.0
IR 3422、1156、1103cm-1
C25H27O5Pとしての分析値:C、67.67;H、6.10%.
実測値:C、67.92;H、5.94%
【0038】
実施例2
各種金属を用いて、エナンチオマー選択性を調べた。具体的には、アセトフェノンにTMS(テトラメチルシラン)CNを添加する触媒について配位子1−Lと結合した異なる金属について調査した。反応を、以下の[化20]に示す。
【化20】
【0039】
各種金属についてエナンチオマー選択性の結果を表1に示す。
【表1】
表1中、eeは、エナンチオマー過剰率を示す。また、R/Sは、生成物の絶対配置を示す。 Yb触媒は、著しい活性を示したが、Ti触媒は、最もよいエナンチオマー過剰率を示した。さらに、反応を、−20℃で行ったとき、エナンチオマー過剰率は73%まで増加した。
【0040】
実施例3
次に、不斉触媒の溶媒に対する影響を調べた。その結果を表2に示す。また、反応を以下の[化21]に示す。
【化21】
【0041】
興味深いことに、反応速度とエナンチオ選択性の双方は、CH2Cl2又はトルエンなどの低極性溶媒と比較してテトラヒドロフラン(以下、THFという。)などの配位性溶媒において増加した。興味あることに、より濃縮した条件下で使用すると(アセトフェノンの条件で3M)、反応は、−30℃で36時間の間より効率的に行われ、85%の収率と92%ccの生成物を与えた。反応条件を10mol%の Ti(OiPr)4及びTHF溶媒中の配位子1−Lを含むとした場合、最も良い結果を得た。
【0042】
【表2】
【0043】
実施例4
この新しく開発した不斉触媒は、芳香族及び脂肪族ケトンを含む、様々なケトンに対して幅広い適用性を高エナンチオ選択性で示す。その結果を表3に示す。また、反応を下記[化22]に示す。
【化22】
具体的に、プロピオフェノン9fやインダノン9eなどの反応性の低いケトンは、収率が、それぞれ89%と72%であり、エナンチオマー過剰率が、それぞれ91%と69%の生産物を与えた。エノン9gは、完全な選択性で付加生成物を与えた。簡単なn―アルカノン9jでさえ、76%のエナンチオマー過剰率を持つ生成物を与えた。
【0044】
また、エナンチオマー過剰率をおとさずに、2−トリメチルシロキシ−2−(2’−ナフチル)−プロパンニトリル(生成物10d)を、単一工程で第4級ヒドロキシエステル(HCl−EtOH、90℃にて3時間)又はアルデヒド(DIBAL−H)に変えることができた。
【0045】
【表3】
【0046】
実施例 5
不斉触媒の構造を確認するため、NMR解析を行った。Ti(OiPr)4及び1−Lの混合物を、トルエン中で75℃にて1時間加熱したとき、2当量のiPrOHの精製を1HNMRにおいて観察した。したがって、この段階にて、予備触媒は、チタン イソプロポキシド(1:Mtl=Ti(OiPr)2)を含む。トルエンを蒸発させた後、THF及びTMSCN(Tiに対して2当量)を加えた。その後、TMSOiPrに対応するピーク(0.19、1.21及び4.1ppm)が現われ、チタンシアニドの生成を示した。室温にて1時間後、約70%のチタンがモノシアニドを含むと考えられ、それは、残部のTMSCN(0.44ppm)と発生したTMSOPrの集積率から推測できる。アセトフェノン(Tiに対して10当量)及びTMSCN(Tiに対して15当量)を更に加えることにより反応が始まり、ほとんど完全にモノシアニドに変化する。したがって、不斉触媒は、チタンモノシアノモノイソプロポキシド(1:Mtl=Ti(CN)(OiPr)からなる複合体として存在することが可能である。後述するように、チタンモノシアニドの複合体形成は、1当量のTMSCNを使用してより長い反応時間(10h)によっても行える。
【0047】
この反応の性質についてさらなる識見を得るために、反応速度論的な研究を行い、触媒に対する反応次数を決定した。
【0048】
さらに、TMS13CNを使用した標識試験から、シアニドは、チタンシアニドからではなく、TMSCNから反応したと考えられた。すなわち、Ti(OiPr)4、1-L(1当量)及びTMS12CN(1当量)から12CNを含む活性チタン触媒を調整した(室温で10時間)。TMS12CNの完全な消費をH NMRで確認した後、9a(1当量)とTMS13CN(1当量)を加えた。生成物10aに13CNが77%取込まれていることを、C NMRで確認した。これらの結果は、チタンシアニドは、CN源としてでなくルイス酸としてだけ作用することを示唆した。
【0049】
そして、エナンチオ選択におけるホスフィンオキシドの役割を解明するためにホスフィンオキシドの代わりにジフェニルメチル基を有する触媒をした。その結果、ジフェニルメチル基を有する触媒では、非常にゆっくりと室温にて反応が進行し、2−トリメチルシロキシ−2−フェニルプロパニトリル([化22]の10a)、及び2−トリメチルシロキシ−2−メチル−4−フェニルブタンニトリル([化22]の10i)を、双方とも2%のエナンチオマー過剰率にて31%及び33%の収率(80時間)でそれぞれ得た。これらの観点、我々の従来の研究結果とから、チタンとホスフィンオキシドの酸素原子が、それぞれルイス酸、及びルイス塩基としてケトン、及びTMSCNを活性化する、触媒による二重活性機構である事が分かる(図1)。
【0050】
実施例6
[3−ベンジルオキシ−4−(2−メトキシフェニル)−テトラハイドロ−ピラノ[3,2−d][1,3]ジオキシン−8−オールアルコール(以下、1とする)をナトリウム アルコキシドとした後、アレン−クロム錯体への求核置換反応により、アルコールの水酸基にカテコール部分を導入したジ‐t‐ブチル‐[4−メトキシ−3−(2−フェニル−ヘキサヒドロ−ピラノ[3,2−d][1,3]ジオキシン−8−イロキシ)−ベンジロキシ]−メチル−シラン を得る。TBSを除去した後、酸化、フェニルグリニャール試薬の付加、酸化により[4−メトキシ−3−(2フェニル−ヘキサヒドロ−ピラノ[3,2−d][1,3]ジオキシン8−イロキシ)−フェニル]−フェニル−メタノン([化18]中の9に相当)とする。9のアセタールを脱保護し、一級アルコールを選択的にトシル化し、トルエンスルホン酸4−(5−ベンゾイル−2−メトキシ−フェノキシ−3−ヒドロキシ−テトラヒドロ−ピラン−2−イルメチルエステル(10に相当)とする。10とPh2PKを反応させ、生じたホスフィンをH2O2で酸化し、メチルエーテルを脱保護し、配位子2-Lを得ることができる。
【0051】
本発明の配位子2−Lの物性値を以下に示す。
1H−NMR(500MHz, CDCl3);δ1.94(m,1H)、2.16(m、1H)、2.72(ddd,J=9.45, 15.0, 15.0Hz, 1H)、2.84(ddd, J=3.35, 9.45、15.3Hz, 1H), 3.23(m、1H), 3.38(ddd, J=3.05, 9.15, 16.5Hz, 1H)、3.60(ddd, J=5.20, 8.90, 11.3Hz, 1H)、3.74(dd, J=8.90, 9.20Hz, 1H)、3.89(m, 1H)、6.98(d, J=8.25Hz, 1H)、7.43−7.80(m, 18H)、9.73(s, 1H):
13C−NMR(125.65MHz, CDCl3);δ31.5、36.0(d、J=68.2 Hz)、65.3, 74.7, 75.8, 84.8, 116.5, 123.8, 128.0, 128.7, 128.8, 128.8, 128.9, 129.0, 129.0, 129.6,130.0, 130.5, 130.6、130.8, 130.9, 131.0, 131.2, 131.7, 132.1, 132.3, 138.3、 145.7, 154.8, 195.1:
31P−NMR(202.35MHz, CDCl3);δ34.5
旋光度[α]D 27+13.2(c=2.34, CHCl3)
【0052】
実施例7
金属としてチタンを、R4としてベンゾイル基をそれぞれ用いて、エナンチオマー選択性を調べた。反応式を以下に示す。
【化23】
エナンチオマー選択性の結果を表4に示す。
【0053】
【表4】
表4中、eeは、エナンチオマー過剰率を示す。また、R/Sは、生成物の絶対配置を示す。R7として、フェニル基及びn−C5H11を用いた場合、それぞれ、97%及86%と高いエナンチオマー過剰率を示した。
【0054】
実施例8
次に、[化2]のR4が、フェニル基、n−C5H11、及び[化4]、[化5]、及び[化6]の場合のエナンチオマー選択性を調べた。結果を表5に示す。
【0055】
【表5】
R4が、フェニル基、n−C5H11、及び[化4]、[化5]、及び[化6]のいずれの場合においても、高いエナンチオマー選択性を示した。
【0056】
実施例9
次に、新規不斉触媒のエナンチオ選択性の結果を、種々のケトンを用いて調べた。その結果を表6に示す。
【0057】
【表6】
この結果、いずれも高いエナンチオマー過剰率を示した。
実施例10
次に、金属として、種々の希土類金属を用いた場合について、新規不斉触媒のエナンチオマー選択性を調べた。反応式を以下に示す。エナンチオマー選択性の結果を表7に示す。
【0058】
【表7】
表7中、eeは、エナンチオマー過剰率を示す。また、R/Sは、生成物の絶対配置を示す。表7に示す金属:配位子のモル比の不斉触媒を用いて、試験を行った。
その結果、R7として、フェニル基、PhCHCH基、m−C5H11を用いた場合、高いエナンチオマー過剰率を示した。
実施例11
次に、本発明の不斉触媒を用いて、種々のケトンのシアノシリル化を試みた。結果を表8に示す。
【表8】
表8中、eeは、エナンチオマー過剰率を示す。ケトンのシアノシリル化には、5mol%のGd(OiPr)と、10mol%の配位子1-Lとから構成される不斉触媒を用いた。溶媒として、THFを用いた。
表8からも明らかなように、いずれも良好なエナンチオマー過剰率を示した。
【0059】
【発明の効果】
本発明の配位子によれば、不斉触媒の配位子として有効に使用することができるという有利な効果を奏する。
【0060】
また、本発明の不斉触媒によれば、金属とホスフィンオキシドを含む新規多点認識触媒によって、ケトンの高エナンチオ選択的シアノシリル化を達成することができる。生成物(キラルシアノヒドリン)は、不斉4級αヒドロキシカルボニル誘導体、β−アミノアルコールに効果的に変換することができる。これは、不斉4級ヒドロキシカルボニル誘導体中心の構築に対する新規な合成法を与え、4級αヒドロキシカルボニル酸を使用する生化学研究を容易にすることができるという有利な効果を奏する。
【図面の簡単な説明】
【図1】 金属とホスフィンオキシドを含む本発明の不斉触媒の触媒作用についての一例を示す図である。
【図2】 ホスフィンオキシド触媒を示す図である。
【図3】 アルコールのC3ヒドロキシル基にて、カテコール部分を導入した触媒を示す図である。
Claims (14)
- 請求項1〜3項に記載の前記配位子のカテコール部分に金属が結合している不斉触媒。
- 金属が、金属錯体として結合している請求項4記載の不斉触媒。
- 金属が、チタン、ジルコニウム、イッテルビウム、アルミニウム、ガリウムからなる群から選択される少なくとも1種である請求項4〜6項のいずれか1項に記載の不斉触媒。
- 金属が、希土類金属であることを特徴とする請求項4〜6項のいずれか1項に記載の不斉触媒。
- 希土類金属が、La、Ce、Pr、Nd,Pm、Sm、Eu、Gd、Dy、Ho、Erからなる群から選択される少なくとも1種であることを特徴とする請求項8項に記載の不斉触媒。
- 請求項4〜9に記載の不斉触媒の存在下、ケトンと、シリルシアニドとを反応させて得ることを特徴とする、シロキシニトリルの製法。
- ケトンが、アセトフェノン、アセトナフトン、プロピオフェノン、インダノン、エノン、シクロヘキシルメチルケトン、n−アルカノン、2−ヘプタノンからなる群から選択される少なくとも1種である請求項10記載の製法。
- シリルシアニドが、トリメチルシリルシアニド、トリエチルシリルシアニド、t-ブチルジメチルシリルシアニドからなる群から選択される少なくとも1種である請求項10記載の製法。
- 反応を、配位性溶媒の存在下で行う請求項10〜12のいずれか1項に記載の製法。
- 配位性溶媒が、テトラヒドロフラン(THF)、ジメトキシエタン、エーテルからなる群から選択されることを特徴とする請求項13記載の製法。
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2001169922A JP3671209B2 (ja) | 2000-06-28 | 2001-06-05 | 配位子及びそれを用いた不斉触媒 |
| US10/070,724 US6677461B2 (en) | 2000-06-28 | 2001-06-21 | Ligands and asymmetric catalysts made by using the same |
| CA002383203A CA2383203C (en) | 2000-06-28 | 2001-06-21 | Ligands and asymmetric catalysts made by using the same |
| PCT/JP2001/005323 WO2002000668A1 (fr) | 2000-06-28 | 2001-06-21 | Ligands, et catalyseurs asymetriques les contenant |
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2000194212 | 2000-06-28 | ||
| JP2000395514 | 2000-12-26 | ||
| JP2000-194212 | 2000-12-26 | ||
| JP2000-395514 | 2000-12-26 | ||
| JP2001169922A JP3671209B2 (ja) | 2000-06-28 | 2001-06-05 | 配位子及びそれを用いた不斉触媒 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2002255985A JP2002255985A (ja) | 2002-09-11 |
| JP3671209B2 true JP3671209B2 (ja) | 2005-07-13 |
Family
ID=27343873
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2001169922A Expired - Lifetime JP3671209B2 (ja) | 2000-06-28 | 2001-06-05 | 配位子及びそれを用いた不斉触媒 |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US6677461B2 (ja) |
| JP (1) | JP3671209B2 (ja) |
| CA (1) | CA2383203C (ja) |
| WO (1) | WO2002000668A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2007100086A1 (ja) | 2006-03-03 | 2007-09-07 | The University Of Tokyo | 配位子及びその製造方法、並びに該配位子を用いた触媒 |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN101039898B (zh) | 2004-10-15 | 2012-01-11 | 三井化学株式会社 | 钛化合物及光学活性羟腈类的制备方法 |
-
2001
- 2001-06-05 JP JP2001169922A patent/JP3671209B2/ja not_active Expired - Lifetime
- 2001-06-21 CA CA002383203A patent/CA2383203C/en not_active Expired - Fee Related
- 2001-06-21 WO PCT/JP2001/005323 patent/WO2002000668A1/ja active Application Filing
- 2001-06-21 US US10/070,724 patent/US6677461B2/en not_active Expired - Fee Related
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2007100086A1 (ja) | 2006-03-03 | 2007-09-07 | The University Of Tokyo | 配位子及びその製造方法、並びに該配位子を用いた触媒 |
Also Published As
| Publication number | Publication date |
|---|---|
| CA2383203C (en) | 2006-01-03 |
| US20030119659A1 (en) | 2003-06-26 |
| US6677461B2 (en) | 2004-01-13 |
| WO2002000668A1 (fr) | 2002-01-03 |
| CA2383203A1 (en) | 2002-01-03 |
| JP2002255985A (ja) | 2002-09-11 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| TWI803692B (zh) | 用於製備6-(2,4-二氯苯基)-5-[4-[(3s)-1-(3-氟丙基)吡咯啶-3-基]氧基苯基]-8,9-二氫-7h-苯并[7]輪烯-2-甲酸甲酯之方法 | |
| Fujimori et al. | Stereoselective conjugate addition reactions using in situ metallated terminal alkynes and the development of novel chiral P, N-ligands | |
| JP2009535350A (ja) | シナカルセット塩基の調製法 | |
| JP2009539823A (ja) | シナカルセットの調製のために有用な中間体化合物を調製するためのプロセス | |
| JP4169801B2 (ja) | 亜鉛触媒存在下でのシランによるカルボニル化合物の還元 | |
| CN113896674B (zh) | 一种阿普斯特的合成方法 | |
| JP3671209B2 (ja) | 配位子及びそれを用いた不斉触媒 | |
| JP3890404B2 (ja) | 配位子及びそれを用いた不斉触媒 | |
| CN114057712A (zh) | 一种合成手性苯基噁唑烷-2-酮的方法 | |
| WO2005073156A1 (ja) | 光学活性ヒドロキシメチル化化合物の製法 | |
| JP2850068B2 (ja) | ルテニウム−ホスフィン錯体及びこれを触媒とする光学活性1−置換−1,3−プロパンジオールの製造方法 | |
| CN112979523B (zh) | 一种手性1,4-二苯基-2-羟基-1,4-二丁酮类化合物的制备方法 | |
| JP2005200347A (ja) | ケトイミンのシアノ化、及び当該シアノ化によるシロキシニトリルの製法 | |
| JP6011769B2 (ja) | ポリスチレン担持ピリジンビスオキサゾリン誘導体−カルシウム触媒 | |
| JP4725760B2 (ja) | 光学活性リン酸エステル誘導体及びその用途 | |
| JP3847653B2 (ja) | キラルジルコニウム触媒とアンチ選択性非対称アルドール反応方法 | |
| JP2003342229A (ja) | オキシブチニン及びその誘導体の製法 | |
| Fu et al. | Bifunctional Lewis Base Catalysis with Dual Activation of X 3 Si–Nu and C= O (n→ σ*) | |
| CN108276256A (zh) | (2r,3r)-2,3-二甲氧基-1,1,4,4-四苯基-1,4-丁二醇的制法 | |
| JP4316854B2 (ja) | 光学活性多価フェノール誘導体、その製造方法及びその用途 | |
| TW200416216A (en) | Chiral chelating agents and chiral catalysts | |
| JP4231277B2 (ja) | 環状カーボネートの製造法 | |
| JPS5973536A (ja) | α,β―不飽和カルボニル化合物の製造方法 | |
| RU2236414C1 (ru) | Способ получения n-замещённых этил-(2-диалкоксифосфорил-4циано)-бутанимидатов | |
| JPS6225677B2 (ja) |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A712 Effective date: 20040715 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20050322 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 3671209 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| EXPY | Cancellation because of completion of term |