JP2017511591A - 柔らかい固体結晶電解質組成物 - Google Patents
柔らかい固体結晶電解質組成物 Download PDFInfo
- Publication number
- JP2017511591A JP2017511591A JP2017502759A JP2017502759A JP2017511591A JP 2017511591 A JP2017511591 A JP 2017511591A JP 2017502759 A JP2017502759 A JP 2017502759A JP 2017502759 A JP2017502759 A JP 2017502759A JP 2017511591 A JP2017511591 A JP 2017511591A
- Authority
- JP
- Japan
- Prior art keywords
- composition
- crystal
- organic compound
- compound
- ionic
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0564—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of organic materials only
- H01M10/0565—Polymeric materials, e.g. gel-type or solid-type
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/052—Li-accumulators
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0564—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of organic materials only
- H01M10/0566—Liquid materials
- H01M10/0568—Liquid materials characterised by the solutes
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0564—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of organic materials only
- H01M10/0566—Liquid materials
- H01M10/0569—Liquid materials characterised by the solvents
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M6/00—Primary cells; Manufacture thereof
- H01M6/14—Cells with non-aqueous electrolyte
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M6/00—Primary cells; Manufacture thereof
- H01M6/14—Cells with non-aqueous electrolyte
- H01M6/16—Cells with non-aqueous electrolyte with organic electrolyte
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M6/00—Primary cells; Manufacture thereof
- H01M6/30—Deferred-action cells
- H01M6/36—Deferred-action cells containing electrolyte and made operational by physical means, e.g. thermal cells
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2300/00—Electrolytes
- H01M2300/0017—Non-aqueous electrolytes
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2300/00—Electrolytes
- H01M2300/0085—Immobilising or gelification of electrolyte
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
Abstract
Description
本出願は、2014年3月25日に出願された米国仮特許出願第61/970,146号の優先権を主張し、その全体を参照により本明細書に組み込む。
本発明は、自然科学基金により授与された譲渡証明書DMR1207221及びCBET−1437814のもと政府支援により行われる。政府は、然るべき本発明の権利を有す。
J of Physics及びChemistry of Solids 18,1−8;Sherwood,1979,The Plastically Crystalline State: Orientationally Disordered Crystals,Wiley,Chichester,UK;MacFarlane 及び Forsyth,2001,Advanced Materials 13,957−966;Pringleら.,2010,J of Materials Chemistry 20,2056−2062;Cooper 及び Angell,1986,Solid State Ionics 18−9,570−576;Yoshizawa−Fujitaら.,2007,Electrochemistry Communications 9,1202−1205.)、及び低分子量グリムを含む(Hendersonら.,2003,Chemistry of Materials 15,4679−4684;Hendersonら.,2003,Chemistry of Materials 15,4685−4690;Seneviratneら.,2004,J of Physical Chemistry B 108,8124−8128;Andreevら.,2005,Chemistry of Materials 17,767−772;Hendersonら.,2005,Chemistry of Materials 17,2284−2289;Henderson,2006,J of Physical Chemistry B 110,13177−13183;Zhangら.,2007,Angewandte Chemie−International Edition 46,2848−2850;Zhangら.,2007,J of the American Chemical Society 129,8700−8701)。柔らかい固体電解質物質の他の例は、NAFION(商標)ポリマーで、アニオン塗装(通常−SO3−)浸透クラスターを含み、移動し得る逆荷電イオンと通すチャンネルを有する(Mauritz 及び Moore,2004,Chemical Reviews 104,4535−4586)。
本発明は、有機マトリクスに取り囲まれたイオン化合物を含む組成物及び当該組成物を製造する方法に関する。組成物は、独特の低親和性イオンチャンネルを含み、概して、室温で固体である。一つの実施形態において、組成物は、電池に用いられ得るリチウムまたはナトリウムのようなイオンを含む柔らかい固体電解質である。別の実施形態において、組成物は、リチウムまたはナトリウム以外のイオンを含むことができ、及び水質浄化、燃料電池及び触媒装置のような非電池技術用として用いられ得る。特に、本発明の組成物は、一般に様々な産業において用いる安価な有機溶媒用途に調製され得る。イオンチャンネルを有するイオン化合物及び有機化合物の共結晶の成功裡の形成の最初の実証をここに記述する。
本発明は、塩の共結晶、即ち、イオン化合物及び有機化合物を含む組成物に関する。結晶は、概して、柔らかい固体であり、有機化合物により形成されたマトリクス内に含まれる塩のイオンチャンネルを有する。
本発明の組成物は、以下に記述するように合成され得る。当該組成物の伝導は、有機マトリクス分子と共に散在する塩の単結晶成長で始まる。本発明の方法は、LiX及びNaXのような塩用電解質マトリクスとしての利用に適合する一般の有効な有機化合物を用いて達成され得る。結果の組成物は、概して、優れたイオン伝導を有する柔軟で可撓性固体物質である。
本発明は、さらに以下の実験実施例を参照して詳細に記述される。当該実施例は、説明のためのみで提供され、特に規定がない限り限定されることをする意図しない。従って、本発明は、決して以下の例に限定されるものとして解釈するのではなく、むしろ提供した本明細書の教授の結果として、事象に現れるあらゆる及び全ての変化を包含するものとして解釈されるべきである。
結晶状柔らかい固体電解質は、一般の非高価実験用溶媒から調製される。結晶状有機マトリクス中のLi+及びCl−の固溶体の調製は、塩化リチウム溶液からの共結晶の沈殿で達成される。塩化リチウムは、DMFまたはピリジンいずれかの溶媒の最少量中に溶解する。ジエチルエーテル沈殿剤の添加で、塩化リチウムの純粋な白色共結晶沈殿及びそれぞれの溶媒に至る。本溶媒組合せは、溶媒DMF及びピリジンの両方は、Et2O中に溶解(混和)し、一方塩化リチウムは、Et2O中に不溶解であるため、純粋物質の単離用に理想的である。推定上、Li+及びCl−は、溶液中に溶媒付加物として存在し、従ってEt2Oが添加されると、塩化リチウムは、純粋な塩ではないが、その溶媒を含む付加物として沈殿し、結果的に結晶状、固体溶媒マトリクス中に固体Li+及びCl−に至る。
単結晶は、DMFまたはピリジン中のいずれかの無水LiClの溶解により得た。結晶は、二重ガラス器具内で室温において当該溶液中へのEt2O蒸気拡散により成長させた。
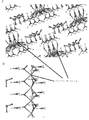
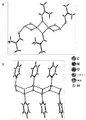
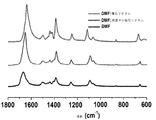
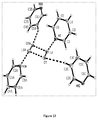
単結晶X線回析は、固体がそれぞれの溶媒の分子を有する1:1 LiClの付加物であることを確認する。図6を参照して、構造は、リチウム原子とDMFまたはピリジン配位子(それぞれ酸素および窒素)の柔らかいルイスドナーとの間の弱いルイス酸/塩基付加物を通じて格子と相互作用する1−Dイオン結合Li2Cl2斜面体の形成を示す。図7を参照して、DMF:LiClの固体状態AT−IRスペクトル中のレッドシフトC=Oストレッチ(1640cm−1)は、リチウムイオンと柔らかいカルボニル酸素ドナーとの間のC=O‐‐Liコンタクトの存在を確証する。斜方体モチーフは、さらに、CH−Cl水素結合(示さないが、H−Cl距離は2.8−2.9Å)を通じて隣接等価配位子通じて相互作用する。CH−Cl水素結合は、例外的であるが、以前に報告されている(Aakeroyら.,1999,New J of Chemistry 23,145−152)。
概略寸法0.045mm×0.090mm×0.250mmのC5H5ClLiNの試験片は、X線結晶分析に用いた。X線強度データを測定した。
概略寸法0.055mm×0.132mm×0.255mmのC3H7ClLiNOの試験片は、X線結晶解析に用いた。X線強度データを測定した。
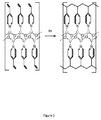
ジフェニルメタン(DPM)‐LiCl共結晶組成物を調製した。ジフェニルメタン(DPM)‐LiCl共結晶の化学構造を図2に示した。本構造は、Li+イオンに関し、2−Dチャンネル(44度で)交叉チャンネルを、しかし、Cl−に関し非交叉チャンネルを有する炭化水素中の塩の固溶体の顕著な例を表わす。一次系におけるイオン伝導度は、チャンネル内の僅かに少数の不純物または欠陥によって制限され得るため、高次元チャンネルを有する結晶は、イオン移動のためにより多数の通路を提供する(Kudo 及びFueki,1990,Solid State Ionics,Kodansha Ltd;VCH:Tokyo;Weinheim)。ジフェニルメタンは、(DMF及びピリジンのように)極性ではないが、アレーンは、分極性であり、マトリクスとLi及びClイオンとの間の双極子−双極子相互作用を可能にし、イオン分子マトリクスを形成させる。DPM−LiCl結晶は、それらが無極性C−H結合に隣接して位置するため、マトリクスと顕著なイオン−双極子相互作用を示さない。当該C−H結合は、分極化に必要であると同時に、イオンに対する双極子−双極子接触を提供し(Aakeroyら.,1999,New J of Chemistry 23,(2),145−152;Youmら.,2006,Polyhedron 25,(14),2717−2720)、イオンに関し、マトリクスの親和力は、DMF,Pyまたはグリム系中のヘテロ原子に関する親和力よりもより低そうで(Zhangら.,2007,Angewandte Chemie−International Edition,46,(16),2848−2850;Zhangら.,2007,J of the American Chemical Society 129,(28),8700−8701;Moriyaら.,2012,Chemistry−a European J 18,(48),15305−15309)、潜在的に低障壁イオン移動に立至る。
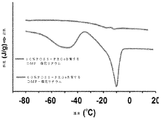
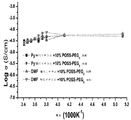
固体膜は、POSS−PEG8(POSS−PEG8の化学構造は、図15に示す)をジエチルエーテル中に溶解し、DMF−LiClまたはPy−LiClいずれかの結晶を懸濁させることにより調製し、それでジエチルエーテルを蒸発させた後に10重量%のPOSS−PEG8となる。全ての調製は、アルゴンでパージしながらグローブボックス内で実施した。蒸発後、膜は、−78℃では硬質固体で及び−30℃では、ゴム状固体である。DSCデータは、何らPOSS−PEG8の結晶化及びLi+溶解性を示すTgにおける増加ならびに正味サンプルと同じDMF−LiClの結晶構造を示していない。DMF−LiClまたはPy−LiCl及びPOSS−PEG8を含む薄膜の分析からのデータは、図16(DSC描画)及び17(温度依存伝導度描画)に示す。
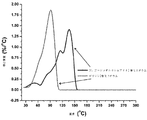
LiClとN,N−ジメチルホルムアミド(DMF)の共結晶化は、組成物LiCl・DMFを有す結晶に立至る。当該結晶は、結晶学的a方向において、イオンの線形、平行チャンネルを形成する。電気化学インピーダンス分光法による伝導度測定は、有機固体電解質に関して観察される最高の室温伝導度、1.3×10−4S/cmの値を与えた。本物質は、さらに、−15から25℃の周囲温度領域において、14kJ/molの低活性化障壁及びイオン輸率番号0.25を表した。異なる圧力下で調製されたペレット及び伝導性結合剤ペンタシクロ[9.5.1.13,9.15,15.17,13]オクタシロキサン−ポリエチレングリコール(POSS−PEG8)を含むサンプルで測定した伝導度は、伝導が凍結した当該層として測定した固有抵抗の主要な源を表す、結晶粒界でのLiCl/DMF液層の浸出を伴ってバルク結晶相において生じることを示した。
活性化エネルギー(Ea)は、アレニウス式を用いて、二つの異なる温度領域において計算される。高温度領域(25℃から−15℃)において、Ea=14.2kJ/mol、低温度領域(−20℃から−60℃)において、Ea=48kJ/mol、及び全温度範囲(25℃から−60℃)にわたって、Ea=45kJ/molである。全ては、〔CH3O(CH2CH2O)nCH3〕:LiAsF6(n=3,4)で作られた結晶状固体グリム錯体に関して得た値未満で、0から50℃の温度間隔にわたって、Ea=55kJ/mol(n=3)または68kJ/mol(n=4)である。理論に拘束されることを望むものではないが、log(σ)対1/Tの直線変化は、伝導のメカニズムが、VIF式(Zhangら、.2007、J.of the Am.Chem.Soc.,129(28):p.8700−8701)により、よく記述されたイオンとポリマー骨格運動との間の結晶動力学よりはむしろ、固体部位間のイオンホッピングであることを示唆している。
DMF:LiClに関する輸率は、15℃で対称リチウムブロッキング電極を用いて測定した(図20)。DMFがリチウム金属に対し腐食性であるため、DMFとリチウムとの接触を制限するために結合剤として、10%POSS−PEGを添加した。Vincent及び共同研究者によって開発された方法(Evansら.,1987,Polymer,28(13):p.2324−8)を以下のように輸率を計算するために用いた(Appetecchiら.,1995,Electrochimica Acta,40(8):p.991−997;Heoら.,2004,Electrochimica Acta,50(2−3)p.345−349)。
各サイクルにおいて、リチウムは失われ電解質とアノード(リチウム)との間に固体電解質界面(SEI)層と呼ばれる界面を形成する。10%POSS−PEG8を有するDMF:LiClに関しては、界面抵抗は、ほぼ6時間増加し、及び次に50時間で減少し(図20C)ならびに残りは一定(別に100時間試験した)である。酸素をパージしながら、グローブボックス内でセルを開放することにより、リチウム金属は、暗色(初期の光沢、金属光沢のない)に見え、電解質がLio金属と反応し、界面抵抗が40kΩから80kΩへと大きく増加する理由を表している。
Claims (45)
- イオン化合物及び有機化合物の共結晶を含む、柔らかい固体電解質組成物。
- 前記共結晶は、イオンチャンネルを含む、請求項1記載の前記組成物。
- 前記イオン化合物は、リチウム塩である、請求項1記載の前記組成物。
- 前記リチウム塩は、塩化リチウムである、請求項1記載の前記組成物。
- 前記イオン化合物は、ナトリウム塩である、請求項1記載の前記組成物。
- 前記ナトリウム塩は、過塩素酸ナトリウムである、請求項5記載の前記組成物。
- 前記ナトリウム塩は、ヘキサフルオロリン酸ナトリウムである、請求項5記載の前記組成物。
- 前記有機化合物は、有機溶媒である、請求項1記載の前記組成物。
- 前記有機化合物は、N,N−メチルホルムアミド(DMF)である、請求項8記載の前記組成物。
- 前記有機溶媒は、ピリジンである、請求項8記載の前記組成物。
- 前記有機溶媒は、イソキノリンである、請求項8記載の前記組成物。
- 前記有機化合物は、カルボニル化合物である、請求項1記載の前記組成物。
- 前記カルボニル化合物は、ベンゾフェノン、アセトフェノン及びフェニルベンゾエートから成るグループから選ばれる、請求項12記載の前記組成物。
- 前記有機化合物は、芳香族炭化水素である、請求項1記載の前記組成物。
- 前記芳香族炭化水素は、ジフェニルメタン(DPM)、トリフェニルメタン、ビベンジル、ビフェニル及びナフタレンから成るグループから選ばれる、請求項14記載の前記組成物。
- 前記有機化合物は、柔らかいルイスドナーである、請求項1記載の前記組成物。
- 請求項1から請求項16のいずれかに記載の任意の柔らかい固体電解質、及び結合剤を含む自立薄膜電解質組成物。
- 前記結合剤は、ポリエチレンオキサイド(PEO)である、請求項17記載の前記組成物。
- 前記結合剤は、八つのポリエチレングリコール鎖で官能化したポリ八面体シルセスキオキサン(POSS−PEG8)である、請求項17記載の前記組成物。
- 柔らかい固体電解質組成物を作る方法であり、溶液を形成するために、イオン化合物を有機化合物中に溶解し、前記溶液に沈殿剤を添加するステップを含み、前記イオン化合物及び有機化合物の共結晶が前記溶液から沈殿する、前記方法。
- 柔らかい固体電解質組成物を作る方法であり、溶液を形成するために、イオン化合物を有機化合物中に溶解し、前記溶液の温度を降温するステップを含み、前記イオン化合物及び有機化合物の共結晶が冷却により前記溶液から沈殿する、前記方法。
- 柔らかい固体電解質組成物を作る方法であり、混合物を形成するために、イオン化合物と有機化合物を混合し、前記有機化合物中の前記イオン化合物の溶液を形成するために、前記混合物を加熱し及び前記溶液を冷却するステップを含み、前記イオン化合物及び有機化合物の共結晶が冷却により前記溶液から沈殿する、前記方法。
- 前記共結晶を分離するステップをさらに含む、請求項20から請求項22のいずれかに記載の前記方法。
- 前記共結晶を空気から保護するステップをさらに含む、請求項20から請求項22のいずれかに記載の前記方法。
- 前記共結晶を水から保護するステップをさらに含む、請求項20から請求項22のいずれかに記載の前記方法。
- 前記イオン化合物は、リチウム塩である、請求項20から請求項22のいずれかに記載の前記方法。
- 前記リチウム塩は、塩化リチウムである、請求項20から請求項22のいずれかに記載の前記方法。
- 前記イオン化合物は、ナトリウム塩である、請求項20から請求項22のいずれかに記載の前記方法。
- 前記ナトリウム塩は、過塩素酸ナトリウムまたはヘキサフルオロリン酸ナトリウムである、請求項28記載の前記方法。
- 前記有機化合物は、有機溶媒である、請求項20から請求項22のいずれかに記載の前記方法。
- 前記有機化合物は、N,N−メチルホルムアミド(DMF)である、請求項30記載の前記方法。
- 前記有機溶媒は、ピリジンである、請求項30記載の前記方法。
- 前記有機化合物は、カルボニル化合物である、請求項20から請求項22のいずれかに記載の前記方法。
- 前記カルボニル化合物は、ベンゾフェノン、アセトフェノン、フェニルベンゾエート及びイソキノリンから成るグループから選ばれる、請求項33記載の前記方法。
- 前記有機化合物は、芳香族炭化水素である、請求項20から請求項22のいずれかに記載の前記方法。
- 前記芳香族炭化水素は、ジフェニルメタン(DPM)、トリフェニルメタン、ビベンジル、ビフェニル及びナフタレンから成るグループから選ばれる、請求項35記載の前記方法。
- 前記有機化合物は、高分子化可能である、請求項20から請求項22のいずれかに記載の前記方法。
- 少なくとも共結晶の一部分を高分子化するステップをさらに含む、請求項37記載の前記方法。
- 前記共結晶は、イオンチャンネルを含む、請求項20から請求項22のいずれかに記載の前記方法。
- 前記沈殿剤は、ジエチルエーテル(Et2O)である、請求項20記載の前記方法。
- 自立薄膜電解質組成物を作る方法であり、
溶液を形成するために、結合剤と溶媒を混合し、
柔らかい固体電解質組成物を前記溶液に添加し、
自立薄膜を形成するために、前記溶媒を除去するステップを含む、
前記方法。 - 前記柔らかい固体電解質組成物は、請求項1から請求項16のいずれかに記載の前記組成物である、請求項41記載の前記方法。
- 前記溶媒は、ジエチルエーテルである、請求項41記載の前記方法。
- 前記結合剤は、PEOまたはPOSS−PEG8である、請求項41記載の前記方法。
- 少なくとも約1×10‐5S/cmの伝導度を有する、請求項1から請求項19のいずれかに記載の前記組成物。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201461970146P | 2014-03-25 | 2014-03-25 | |
| US61/970,146 | 2014-03-25 | ||
| PCT/US2015/021725 WO2015148300A1 (en) | 2014-03-25 | 2015-03-20 | Soft-solid crystalline electrolyte compositions |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2017511591A true JP2017511591A (ja) | 2017-04-20 |
| JP2017511591A5 JP2017511591A5 (ja) | 2018-04-19 |
Family
ID=54196248
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2017502759A Pending JP2017511591A (ja) | 2014-03-25 | 2015-03-20 | 柔らかい固体結晶電解質組成物 |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US10381684B2 (ja) |
| EP (1) | EP3130021B1 (ja) |
| JP (1) | JP2017511591A (ja) |
| KR (1) | KR20160138207A (ja) |
| CN (1) | CN106463691A (ja) |
| CA (1) | CA2944008A1 (ja) |
| MX (1) | MX371416B (ja) |
| WO (1) | WO2015148300A1 (ja) |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2016196879A1 (en) * | 2015-06-05 | 2016-12-08 | Dana-Farber Cancer Institute, Inc. | Compounds and methods for treating cancer |
| CN109659604B (zh) * | 2017-10-12 | 2020-09-01 | 北京大学深圳研究生院 | 一种固体电解质复合材料及其制备方法和应用 |
| WO2019087752A1 (ja) * | 2017-10-30 | 2019-05-09 | 富士フイルム株式会社 | 固体電解質組成物、固体電解質含有シート及び全固体二次電池並びに固体電解質含有シート及び全固体二次電池の製造方法 |
| CN109638350B (zh) * | 2018-12-18 | 2022-08-16 | 西北工业大学 | 一种对锂稳定的丁二腈基固态电解质、制备方法及其应用 |
| CN113508446B (zh) * | 2019-03-29 | 2022-09-27 | 日本贵弥功株式会社 | 固体电解质、蓄电设备及固体电解质的制造方法 |
| CN113540394B (zh) * | 2021-07-19 | 2022-09-02 | 远景动力技术(江苏)有限公司 | 正极片其制备方法、固态锂离子电池、半固态锂离子电池及其制备方法 |
| WO2023234715A1 (ko) * | 2022-05-31 | 2023-12-07 | 주식회사 엘지에너지솔루션 | 고분자 고체 전해질 제조방법 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3977900A (en) * | 1975-06-05 | 1976-08-31 | Board Of Control, Michigan Technological University | Thermally activated electrochemical cell including an alkali metal salt solvate electrolyte |
| JP2008522376A (ja) * | 2004-12-02 | 2008-06-26 | オクシス・エナジー・リミテッド | リチウム・硫黄電池用電解質及びこれを使用するリチウム・硫黄電池 |
| JP2011238599A (ja) * | 2010-04-12 | 2011-11-24 | Nippon Soda Co Ltd | 不織布複合高分子固体電解質シート |
Family Cites Families (22)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AT374625B (de) | 1981-10-08 | 1984-05-10 | Inst Fiz Khim Pisarzhev An | Chemische stromquelle |
| US5354496A (en) * | 1987-07-27 | 1994-10-11 | Elliott Stanley B | Lyotropic liquid crystal salt/inorganic compound complexation products |
| JPH0311564A (ja) * | 1989-06-09 | 1991-01-18 | Komatsu Ltd | プラスチック電池 |
| US5102510A (en) * | 1990-08-23 | 1992-04-07 | Ensr Corporation | Process for electrochemical dehalogenation of organic contaminants |
| RU2066901C1 (ru) | 1993-07-01 | 1996-09-20 | Жуковский Владимир Михайлович | Твердый литийпроводящий электролит и способ его получения |
| SG103298A1 (en) * | 2000-06-16 | 2004-04-29 | Nisshin Spinning | Polymer battery and method of manufacture |
| US20020110735A1 (en) | 2000-12-18 | 2002-08-15 | Farnham William B. | Additive for lithium-ion battery |
| US6841303B2 (en) | 2001-01-17 | 2005-01-11 | Skc Co., Ltd. | High ionic conductivity gel polymer electrolyte for rechargeable polymer batteries |
| US20070218371A1 (en) * | 2006-03-14 | 2007-09-20 | Tda Research, Inc. | Nanoporous polymer electrolyte |
| DE102006046787A1 (de) * | 2006-10-02 | 2008-04-03 | Basf Ag | Elektrolyt für Lithiumionenbatterien |
| WO2008098137A2 (en) | 2007-02-07 | 2008-08-14 | Zettacore, Inc. | Liquid composite compositions using non-volatile liquids and nanoparticles and uses thereof |
| CN101617427B (zh) * | 2007-02-21 | 2012-07-18 | 旭化成电子材料株式会社 | 高分子电解质组合物、高分子电解质膜、膜电极接合体及固体高分子电解质型燃料电池 |
| KR20090064862A (ko) * | 2007-12-17 | 2009-06-22 | 광주과학기술원 | 피리딘을 기능성 그룹으로 함유한 스티렌 유도체의 음이온중합 방법 |
| JP2009256654A (ja) * | 2008-03-27 | 2009-11-05 | Sumitomo Chemical Co Ltd | 高分子電解質組成物 |
| GB0820865D0 (en) * | 2008-11-14 | 2008-12-24 | Membrane Extraction Tech Ltd | Degradable supports for tide synthesis |
| US20110143218A1 (en) | 2009-12-14 | 2011-06-16 | Issaev Nikolai N | Battery |
| WO2012012743A1 (en) | 2010-07-22 | 2012-01-26 | University Of Central Florida Research Foundation, Inc. | Alkali metal-copper storage battery |
| JP5752412B2 (ja) * | 2010-12-27 | 2015-07-22 | 株式会社アルバック | 薄膜リチウム二次電池の製造方法及び薄膜リチウム二次電池 |
| JP2014508814A (ja) | 2011-03-24 | 2014-04-10 | ユニバーシティ・オブ・サウス・フロリダ | リチウム組成物 |
| KR101502500B1 (ko) * | 2011-07-01 | 2015-03-16 | 주식회사 엘지화학 | 비수 전해액 및 이를 이용한 리튬 이차전지 |
| FR2977887B1 (fr) * | 2011-07-12 | 2018-01-26 | Commissariat A L'energie Atomique Et Aux Energies Alternatives | Phosphate de manganese lithie et materiau composite le comprenant |
| KR102461717B1 (ko) * | 2015-05-12 | 2022-11-01 | 삼성전자주식회사 | 에너지 저장장치용 전해질막, 이를 포함하는 에너지 저장장치, 및 상기 에너지 저장장치용 전해질막의 제조방법 |
-
2015
- 2015-03-20 CN CN201580021692.0A patent/CN106463691A/zh active Pending
- 2015-03-20 CA CA2944008A patent/CA2944008A1/en not_active Abandoned
- 2015-03-20 MX MX2016012562A patent/MX371416B/es active IP Right Grant
- 2015-03-20 KR KR1020167029714A patent/KR20160138207A/ko unknown
- 2015-03-20 EP EP15769204.7A patent/EP3130021B1/en active Active
- 2015-03-20 WO PCT/US2015/021725 patent/WO2015148300A1/en active Application Filing
- 2015-03-20 US US15/129,342 patent/US10381684B2/en active Active
- 2015-03-20 JP JP2017502759A patent/JP2017511591A/ja active Pending
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3977900A (en) * | 1975-06-05 | 1976-08-31 | Board Of Control, Michigan Technological University | Thermally activated electrochemical cell including an alkali metal salt solvate electrolyte |
| JP2008522376A (ja) * | 2004-12-02 | 2008-06-26 | オクシス・エナジー・リミテッド | リチウム・硫黄電池用電解質及びこれを使用するリチウム・硫黄電池 |
| JP2011238599A (ja) * | 2010-04-12 | 2011-11-24 | Nippon Soda Co Ltd | 不織布複合高分子固体電解質シート |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2015148300A1 (en) | 2015-10-01 |
| KR20160138207A (ko) | 2016-12-02 |
| MX371416B (es) | 2020-01-29 |
| US10381684B2 (en) | 2019-08-13 |
| EP3130021A1 (en) | 2017-02-15 |
| CN106463691A (zh) | 2017-02-22 |
| CA2944008A1 (en) | 2015-10-01 |
| EP3130021B1 (en) | 2018-12-26 |
| MX2016012562A (es) | 2017-04-13 |
| EP3130021A4 (en) | 2017-11-08 |
| US20170179524A1 (en) | 2017-06-22 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2017511591A (ja) | 柔らかい固体結晶電解質組成物 | |
| Jaschin et al. | A materials perspective on magnesium-ion-based solid-state electrolytes | |
| Wang et al. | Covalently linked metal–organic framework (MOF)-polymer all-solid-state electrolyte membranes for room temperature high performance lithium batteries | |
| Wang et al. | Coordination polymer-based conductive materials: ionic conductivity vs. electronic conductivity | |
| Devaux et al. | Comparison of single-ion-conductor block-copolymer electrolytes with Polystyrene-TFSI and Polymethacrylate-TFSI structural blocks | |
| Gou et al. | One-pot synthesis of a metal–organic framework as an anode for Li-ion batteries with improved capacity and cycling stability | |
| Nguyen et al. | 3-D coordination polymers based on the tetrathiafulvalenetetracarboxylate (TTF-TC) derivative: synthesis, characterization, and oxidation issues | |
| Lu et al. | Zwitterionic impetus on single lithium-ion conduction in solid polymer electrolyte for all-solid-state lithium-ion batteries | |
| Armand et al. | Polymer electrolytes | |
| Panda et al. | Li+ Ion-Conducting Sulfonate-Based Neutral Metal–Organic Framework | |
| Verma et al. | Chelating ligands as electrolyte solvent for rechargeable zinc-ion batteries | |
| Liu et al. | Synergistic effect of lithium salts with fillers and solvents in composite electrolytes for superior room-temperature solid-state lithium batteries | |
| Gebreyesus et al. | Preparation and characterization of lithium ion conducting polymer electrolytes based on a blend of poly (vinylidene fluoride-co-hexafluoropropylene) and poly (methyl methacrylate) | |
| Ma et al. | Class of Solid-like Electrolytes for Rechargeable Batteries Based on Metal–Organic Frameworks Infiltrated with Liquid Electrolytes | |
| Chen et al. | Electrochemical reactivity of lithium chloranilate vs Li and crystal structures of the hydrated phases | |
| Han et al. | High-efficiency lithium-ion transport in a porous coordination chain-based hydrogen-bonded framework | |
| Martínez Casado et al. | Anhydrous lithium acetate polymorphs and its hydrates: three-dimensional coordination polymers | |
| Tseng et al. | Polymer electrolytes based on Poly (VdF-co-HFP)/ionic liquid/carbonate membranes for high-performance lithium-ion batteries | |
| CN109585754A (zh) | 用于锂电池的复合膜、用于锂电池的正极以及包括所述复合膜的锂电池 | |
| JP2020510983A (ja) | 高分子電解質及びこの製造方法 | |
| Iwano et al. | Effect of molecular weights of confined single-chain poly (allylamine) toward proton conduction in inorganic frameworks based on Preyssler-type polyoxometalate | |
| Wang et al. | Study of a novel gel electrolyte based on poly-(methoxy/hexadecyl-poly (ethylene glycol) methacrylate) co-polymer plasticized with 1-butyl-3-methylimidazolium tetrafluoroborate | |
| Fall et al. | Crystal structure and ionic conductivity of the soft solid crystal: isoquinoline 3•(LiCl) 2 | |
| Fall et al. | A Soft-Solid Co-Crystalline Electrolyte Combining Advantages of Organics and Ceramics: Thermally, Electrochemically Stable, Highly Conductive (Adiponitrile) 2LiPF6 | |
| Wen et al. | Syntheses, Characterization, and Electrochemical Lithium‐Ion Storage Properties of Two Cobalt (II) Coordination Polymers Containing 5‐Hydroxyisophthalic Acid and Bis‐benzoimidazole Ligands |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20180309 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20180309 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20190306 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20190409 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20190708 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20191210 |