JP2016538325A - エレクトロクロミック性の単核及び2核ビオロゲン並びにそれらを含有する光学物品 - Google Patents
エレクトロクロミック性の単核及び2核ビオロゲン並びにそれらを含有する光学物品 Download PDFInfo
- Publication number
- JP2016538325A JP2016538325A JP2016543383A JP2016543383A JP2016538325A JP 2016538325 A JP2016538325 A JP 2016538325A JP 2016543383 A JP2016543383 A JP 2016543383A JP 2016543383 A JP2016543383 A JP 2016543383A JP 2016538325 A JP2016538325 A JP 2016538325A
- Authority
- JP
- Japan
- Prior art keywords
- aryl
- alkyl
- substituted
- alkylene
- compound
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- 230000003287 optical effect Effects 0.000 title claims abstract description 18
- -1 polyalkyleneoxy Chemical group 0.000 claims description 127
- 150000001875 compounds Chemical class 0.000 claims description 123
- 239000000203 mixture Substances 0.000 claims description 63
- 125000000217 alkyl group Chemical group 0.000 claims description 55
- 125000003118 aryl group Chemical group 0.000 claims description 50
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 38
- 125000001072 heteroaryl group Chemical group 0.000 claims description 34
- 229910052736 halogen Inorganic materials 0.000 claims description 27
- 150000002367 halogens Chemical class 0.000 claims description 27
- 125000000753 cycloalkyl group Chemical group 0.000 claims description 26
- 125000001424 substituent group Chemical group 0.000 claims description 24
- 125000003545 alkoxy group Chemical group 0.000 claims description 21
- 125000001188 haloalkyl group Chemical group 0.000 claims description 21
- 125000002947 alkylene group Chemical group 0.000 claims description 20
- 125000004438 haloalkoxy group Chemical group 0.000 claims description 19
- 229910052739 hydrogen Inorganic materials 0.000 claims description 16
- 125000004453 alkoxycarbonyl group Chemical group 0.000 claims description 14
- 125000000732 arylene group Chemical group 0.000 claims description 12
- 125000003107 substituted aryl group Chemical group 0.000 claims description 12
- 125000002993 cycloalkylene group Chemical group 0.000 claims description 11
- 229910052757 nitrogen Inorganic materials 0.000 claims description 11
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 claims description 10
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 claims description 10
- 125000004414 alkyl thio group Chemical group 0.000 claims description 10
- 125000004093 cyano group Chemical group *C#N 0.000 claims description 10
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 claims description 8
- 125000003710 aryl alkyl group Chemical group 0.000 claims description 8
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 claims description 8
- 125000005549 heteroarylene group Chemical group 0.000 claims description 8
- 229910052760 oxygen Inorganic materials 0.000 claims description 8
- 239000001301 oxygen Substances 0.000 claims description 8
- 229910052717 sulfur Inorganic materials 0.000 claims description 8
- 239000011593 sulfur Substances 0.000 claims description 8
- 125000002837 carbocyclic group Chemical group 0.000 claims description 7
- 125000004423 acyloxy group Chemical group 0.000 claims description 6
- 125000003342 alkenyl group Chemical group 0.000 claims description 6
- 125000000592 heterocycloalkyl group Chemical group 0.000 claims description 6
- 125000002768 hydroxyalkyl group Chemical group 0.000 claims description 6
- 239000004973 liquid crystal related substance Substances 0.000 claims description 6
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 6
- 125000004433 nitrogen atom Chemical group N* 0.000 claims description 6
- 125000003435 aroyl group Chemical group 0.000 claims description 5
- 125000005842 heteroatom Chemical group 0.000 claims description 5
- 150000002500 ions Chemical class 0.000 claims description 5
- 239000007788 liquid Substances 0.000 claims description 5
- 125000000843 phenylene group Chemical group C1(=C(C=CC=C1)*)* 0.000 claims description 5
- 229920000642 polymer Polymers 0.000 claims description 5
- ITMCEJHCFYSIIV-UHFFFAOYSA-M triflate Chemical compound [O-]S(=O)(=O)C(F)(F)F ITMCEJHCFYSIIV-UHFFFAOYSA-M 0.000 claims description 5
- 125000000590 4-methylphenyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1*)C([H])([H])[H] 0.000 claims description 4
- 125000004390 alkyl sulfonyl group Chemical group 0.000 claims description 4
- 125000000304 alkynyl group Chemical group 0.000 claims description 4
- 239000007864 aqueous solution Substances 0.000 claims description 4
- 125000004391 aryl sulfonyl group Chemical group 0.000 claims description 4
- 125000004104 aryloxy group Chemical group 0.000 claims description 4
- 125000001589 carboacyl group Chemical group 0.000 claims description 4
- 125000004957 naphthylene group Chemical group 0.000 claims description 4
- 150000002825 nitriles Chemical class 0.000 claims description 4
- 239000003960 organic solvent Substances 0.000 claims description 4
- 150000003839 salts Chemical class 0.000 claims description 4
- 229920006395 saturated elastomer Polymers 0.000 claims description 4
- 239000000758 substrate Substances 0.000 claims description 4
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical group [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 claims description 3
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 claims description 3
- 229910052799 carbon Inorganic materials 0.000 claims description 3
- 125000001316 cycloalkyl alkyl group Chemical group 0.000 claims description 3
- 125000004995 haloalkylthio group Chemical group 0.000 claims description 3
- 125000005885 heterocycloalkylalkyl group Chemical group 0.000 claims description 3
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 claims description 3
- XOJVVFBFDXDTEG-UHFFFAOYSA-N pristane Chemical compound CC(C)CCCC(C)CCCC(C)CCCC(C)C XOJVVFBFDXDTEG-UHFFFAOYSA-N 0.000 claims description 3
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 claims description 3
- 229920002554 vinyl polymer Polymers 0.000 claims description 3
- 125000004765 (C1-C4) haloalkyl group Chemical group 0.000 claims description 2
- ZXMGHDIOOHOAAE-UHFFFAOYSA-N 1,1,1-trifluoro-n-(trifluoromethylsulfonyl)methanesulfonamide Chemical compound FC(F)(F)S(=O)(=O)NS(=O)(=O)C(F)(F)F ZXMGHDIOOHOAAE-UHFFFAOYSA-N 0.000 claims description 2
- LBLYYCQCTBFVLH-UHFFFAOYSA-M 2-methylbenzenesulfonate Chemical compound CC1=CC=CC=C1S([O-])(=O)=O LBLYYCQCTBFVLH-UHFFFAOYSA-M 0.000 claims description 2
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 claims description 2
- 229920000106 Liquid crystal polymer Polymers 0.000 claims description 2
- 239000004977 Liquid-crystal polymers (LCPs) Substances 0.000 claims description 2
- 229910002651 NO3 Inorganic materials 0.000 claims description 2
- NHNBFGGVMKEFGY-UHFFFAOYSA-N Nitrate Chemical compound [O-][N+]([O-])=O NHNBFGGVMKEFGY-UHFFFAOYSA-N 0.000 claims description 2
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 claims description 2
- 239000002168 alkylating agent Substances 0.000 claims description 2
- 229940100198 alkylating agent Drugs 0.000 claims description 2
- 238000005349 anion exchange Methods 0.000 claims description 2
- 150000007942 carboxylates Chemical class 0.000 claims description 2
- 125000003754 ethoxycarbonyl group Chemical group C(=O)(OCC)* 0.000 claims description 2
- 150000004820 halides Chemical class 0.000 claims description 2
- VLTRZXGMWDSKGL-UHFFFAOYSA-M perchlorate Inorganic materials [O-]Cl(=O)(=O)=O VLTRZXGMWDSKGL-UHFFFAOYSA-M 0.000 claims description 2
- VLTRZXGMWDSKGL-UHFFFAOYSA-N perchloric acid Chemical compound OCl(=O)(=O)=O VLTRZXGMWDSKGL-UHFFFAOYSA-N 0.000 claims description 2
- 230000001588 bifunctional effect Effects 0.000 claims 1
- 150000003871 sulfonates Chemical class 0.000 claims 1
- 239000000463 material Substances 0.000 abstract description 10
- 238000002834 transmittance Methods 0.000 abstract description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 72
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 63
- 239000000243 solution Substances 0.000 description 56
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 40
- 239000002904 solvent Substances 0.000 description 34
- 238000003756 stirring Methods 0.000 description 34
- 239000000843 powder Substances 0.000 description 32
- 238000010992 reflux Methods 0.000 description 30
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 29
- 230000015572 biosynthetic process Effects 0.000 description 24
- 238000003786 synthesis reaction Methods 0.000 description 24
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 19
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 19
- 229910020808 NaBF Inorganic materials 0.000 description 19
- 150000003254 radicals Chemical class 0.000 description 16
- 239000002244 precipitate Substances 0.000 description 15
- 239000000047 product Substances 0.000 description 12
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 11
- 125000001570 methylene group Chemical group [H]C([H])([*:1])[*:2] 0.000 description 11
- 235000019439 ethyl acetate Nutrition 0.000 description 9
- GBMDVOWEEQVZKZ-UHFFFAOYSA-N methanol;hydrate Chemical compound O.OC GBMDVOWEEQVZKZ-UHFFFAOYSA-N 0.000 description 9
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 9
- 239000007787 solid Substances 0.000 description 8
- 238000001816 cooling Methods 0.000 description 7
- 238000000862 absorption spectrum Methods 0.000 description 6
- 125000004432 carbon atom Chemical group C* 0.000 description 6
- 238000000034 method Methods 0.000 description 6
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 6
- 229910001495 sodium tetrafluoroborate Inorganic materials 0.000 description 6
- 125000002950 monocyclic group Chemical group 0.000 description 5
- 125000004642 (C1-C12) alkoxy group Chemical group 0.000 description 4
- KGKAYWMGPDWLQZ-UHFFFAOYSA-N 1,2-bis(bromomethyl)benzene Chemical compound BrCC1=CC=CC=C1CBr KGKAYWMGPDWLQZ-UHFFFAOYSA-N 0.000 description 4
- WJFKNYWRSNBZNX-UHFFFAOYSA-N 10H-phenothiazine Chemical compound C1=CC=C2NC3=CC=CC=C3SC2=C1 WJFKNYWRSNBZNX-UHFFFAOYSA-N 0.000 description 4
- MWVTWFVJZLCBMC-UHFFFAOYSA-N 4,4'-bipyridine Chemical compound C1=NC=CC(C=2C=CN=CC=2)=C1 MWVTWFVJZLCBMC-UHFFFAOYSA-N 0.000 description 4
- 0 C*(CC1)(C=C*1(C)NC(*)(*)*(C=CC=C)=CC=Cc1cc*(*)cc1)c1cc*(C(*)(*)*)cc1 Chemical compound C*(CC1)(C=C*1(C)NC(*)(*)*(C=CC=C)=CC=Cc1cc*(*)cc1)c1cc*(C(*)(*)*)cc1 0.000 description 4
- 230000004913 activation Effects 0.000 description 4
- 125000002619 bicyclic group Chemical group 0.000 description 4
- 239000003086 colorant Substances 0.000 description 4
- 239000006071 cream Substances 0.000 description 4
- 239000003480 eluent Substances 0.000 description 4
- 238000010438 heat treatment Methods 0.000 description 4
- 150000002430 hydrocarbons Chemical group 0.000 description 4
- 229950000688 phenothiazine Drugs 0.000 description 4
- RUOJZAUFBMNUDX-UHFFFAOYSA-N propylene carbonate Chemical compound CC1COC(=O)O1 RUOJZAUFBMNUDX-UHFFFAOYSA-N 0.000 description 4
- 239000000377 silicon dioxide Substances 0.000 description 4
- 239000011734 sodium Substances 0.000 description 4
- NQXDAKVRYHXNPE-UHFFFAOYSA-N (2,4-dinitrophenyl) 4-methylbenzenesulfonate Chemical compound C1=CC(C)=CC=C1S(=O)(=O)OC1=CC=C([N+]([O-])=O)C=C1[N+]([O-])=O NQXDAKVRYHXNPE-UHFFFAOYSA-N 0.000 description 3
- 125000004641 (C1-C12) haloalkyl group Chemical group 0.000 description 3
- XTFIVUDBNACUBN-UHFFFAOYSA-N 1,3,5-trinitro-1,3,5-triazinane Chemical compound [O-][N+](=O)N1CN([N+]([O-])=O)CN([N+]([O-])=O)C1 XTFIVUDBNACUBN-UHFFFAOYSA-N 0.000 description 3
- AAAXMNYUNVCMCJ-UHFFFAOYSA-N 1,3-diiodopropane Chemical compound ICCCI AAAXMNYUNVCMCJ-UHFFFAOYSA-N 0.000 description 3
- LHKFFORGJVELPC-UHFFFAOYSA-N 2,3-bis(bromomethyl)quinoxaline Chemical compound C1=CC=C2N=C(CBr)C(CBr)=NC2=C1 LHKFFORGJVELPC-UHFFFAOYSA-N 0.000 description 3
- ZWEHNKRNPOVVGH-UHFFFAOYSA-N 2-Butanone Chemical compound CCC(C)=O ZWEHNKRNPOVVGH-UHFFFAOYSA-N 0.000 description 3
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 3
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 3
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 3
- JJURIQWVNOUVLK-UHFFFAOYSA-M [I-].[I-].CCCCCC[n+]1ccc(cc1)-c1cc[nH+]cc1 Chemical compound [I-].[I-].CCCCCC[n+]1ccc(cc1)-c1cc[nH+]cc1 JJURIQWVNOUVLK-UHFFFAOYSA-M 0.000 description 3
- JFDZBHWFFUWGJE-UHFFFAOYSA-N benzonitrile Chemical compound N#CC1=CC=CC=C1 JFDZBHWFFUWGJE-UHFFFAOYSA-N 0.000 description 3
- 229910052801 chlorine Inorganic materials 0.000 description 3
- 230000005684 electric field Effects 0.000 description 3
- 238000005562 fading Methods 0.000 description 3
- 229910052731 fluorine Inorganic materials 0.000 description 3
- ARRNBPCNZJXHRJ-UHFFFAOYSA-M hydron;tetrabutylazanium;phosphate Chemical compound OP(O)([O-])=O.CCCC[N+](CCCC)(CCCC)CCCC ARRNBPCNZJXHRJ-UHFFFAOYSA-M 0.000 description 3
- 229910052697 platinum Inorganic materials 0.000 description 3
- 125000004400 (C1-C12) alkyl group Chemical group 0.000 description 2
- 125000004643 (C1-C12) haloalkoxy group Chemical group 0.000 description 2
- HTRYWXJIGDXDLF-UHFFFAOYSA-L 1-(2,4-dinitrophenyl)-4-[1-(2,4-dinitrophenyl)pyridin-1-ium-4-yl]pyridin-1-ium;dichloride Chemical compound [Cl-].[Cl-].[O-][N+](=O)C1=CC([N+](=O)[O-])=CC=C1[N+]1=CC=C(C=2C=C[N+](=CC=2)C=2C(=CC(=CC=2)[N+]([O-])=O)[N+]([O-])=O)C=C1 HTRYWXJIGDXDLF-UHFFFAOYSA-L 0.000 description 2
- CGAIDPLAURANFI-UHFFFAOYSA-N 1-[4-(trifluoromethoxy)phenyl]-4-[1-[3-[4-[1-[4-(trifluoromethoxy)phenyl]pyridin-1-ium-4-yl]pyridin-1-ium-1-yl]propyl]pyridin-1-ium-4-yl]pyridin-1-ium Chemical compound FC(F)(F)Oc1ccc(cc1)-[n+]1ccc(cc1)-c1cc[n+](CCC[n+]2ccc(cc2)-c2cc[n+](cc2)-c2ccc(OC(F)(F)F)cc2)cc1 CGAIDPLAURANFI-UHFFFAOYSA-N 0.000 description 2
- QXBUYALKJGBACG-UHFFFAOYSA-N 10-methylphenothiazine Chemical compound C1=CC=C2N(C)C3=CC=CC=C3SC2=C1 QXBUYALKJGBACG-UHFFFAOYSA-N 0.000 description 2
- YBYIRNPNPLQARY-UHFFFAOYSA-N 1H-indene Chemical compound C1=CC=C2CC=CC2=C1 YBYIRNPNPLQARY-UHFFFAOYSA-N 0.000 description 2
- 125000001917 2,4-dinitrophenyl group Chemical group [H]C1=C([H])C(=C([H])C(=C1*)[N+]([O-])=O)[N+]([O-])=O 0.000 description 2
- HLCPWBZNUKCSBN-UHFFFAOYSA-N 2-aminobenzonitrile Chemical compound NC1=CC=CC=C1C#N HLCPWBZNUKCSBN-UHFFFAOYSA-N 0.000 description 2
- LODRGECCKZZTEQ-UHFFFAOYSA-N 2-benzylpropane-1,3-diol Chemical compound OCC(CO)CC1=CC=CC=C1 LODRGECCKZZTEQ-UHFFFAOYSA-N 0.000 description 2
- AEIOZWYBDBVCGW-UHFFFAOYSA-N 2-tert-butylaniline Chemical compound CC(C)(C)C1=CC=CC=C1N AEIOZWYBDBVCGW-UHFFFAOYSA-N 0.000 description 2
- MZSAMHOCTRNOIZ-UHFFFAOYSA-N 3-[4-(aminomethyl)-6-(trifluoromethyl)pyridin-2-yl]oxy-N-phenylaniline Chemical compound NCC1=CC(=NC(=C1)C(F)(F)F)OC=1C=C(NC2=CC=CC=C2)C=CC=1 MZSAMHOCTRNOIZ-UHFFFAOYSA-N 0.000 description 2
- UJBOOUHRTQVGRU-UHFFFAOYSA-N 3-methylcyclohexan-1-one Chemical compound CC1CCCC(=O)C1 UJBOOUHRTQVGRU-UHFFFAOYSA-N 0.000 description 2
- YEJRWHAVMIAJKC-UHFFFAOYSA-N 4-Butyrolactone Chemical compound O=C1CCCO1 YEJRWHAVMIAJKC-UHFFFAOYSA-N 0.000 description 2
- PAYRUJLWNCNPSJ-UHFFFAOYSA-N Aniline Chemical compound NC1=CC=CC=C1 PAYRUJLWNCNPSJ-UHFFFAOYSA-N 0.000 description 2
- KAKZBPTYRLMSJV-UHFFFAOYSA-N Butadiene Chemical group C=CC=C KAKZBPTYRLMSJV-UHFFFAOYSA-N 0.000 description 2
- 125000001313 C5-C10 heteroaryl group Chemical group 0.000 description 2
- TXDOIMQUPJIUMQ-UHFFFAOYSA-N CCCC.I.I.I.I Chemical compound CCCC.I.I.I.I TXDOIMQUPJIUMQ-UHFFFAOYSA-N 0.000 description 2
- XTHFKEDIFFGKHM-UHFFFAOYSA-N Dimethoxyethane Chemical compound COCCOC XTHFKEDIFFGKHM-UHFFFAOYSA-N 0.000 description 2
- KMTRUDSVKNLOMY-UHFFFAOYSA-N Ethylene carbonate Chemical compound O=C1OCCO1 KMTRUDSVKNLOMY-UHFFFAOYSA-N 0.000 description 2
- UXOZBJYVQNECML-UHFFFAOYSA-N FC(F)(F)S(=O)(=O)OCC(COS(=O)(=O)C(F)(F)F)Cc1ccccc1 Chemical compound FC(F)(F)S(=O)(=O)OCC(COS(=O)(=O)C(F)(F)F)Cc1ccccc1 UXOZBJYVQNECML-UHFFFAOYSA-N 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 2
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 2
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 2
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 2
- ABRVLXLNVJHDRQ-UHFFFAOYSA-N [2-pyridin-3-yl-6-(trifluoromethyl)pyridin-4-yl]methanamine Chemical compound FC(C1=CC(=CC(=N1)C=1C=NC=CC=1)CN)(F)F ABRVLXLNVJHDRQ-UHFFFAOYSA-N 0.000 description 2
- AMNPXXIGUOKIPP-UHFFFAOYSA-N [4-(carbamothioylamino)phenyl]thiourea Chemical compound NC(=S)NC1=CC=C(NC(N)=S)C=C1 AMNPXXIGUOKIPP-UHFFFAOYSA-N 0.000 description 2
- JQIDFSBEOWFSHF-UHFFFAOYSA-L [Cl-].[Cl-].CC(C)(C)c1cccc(c1)-[n+]1ccc(cc1)-c1cc[n+](cc1)-c1cccc(c1)C(C)(C)C Chemical compound [Cl-].[Cl-].CC(C)(C)c1cccc(c1)-[n+]1ccc(cc1)-c1cc[n+](cc1)-c1cccc(c1)C(C)(C)C JQIDFSBEOWFSHF-UHFFFAOYSA-L 0.000 description 2
- PDHAIJRRRQGEDD-UHFFFAOYSA-L [Cl-].[Cl-].CC(C)(C)c1ccccc1-[n+]1ccc(cc1)-c1cc[n+](cc1)-c1ccccc1C(C)(C)C Chemical compound [Cl-].[Cl-].CC(C)(C)c1ccccc1-[n+]1ccc(cc1)-c1cc[n+](cc1)-c1ccccc1C(C)(C)C PDHAIJRRRQGEDD-UHFFFAOYSA-L 0.000 description 2
- ZJZURHCCBVSJAQ-UHFFFAOYSA-M [Cl-].[Cl-].CC(C)(C)c1ccccc1-[n+]1ccc(cc1)-c1cc[nH+]cc1 Chemical compound [Cl-].[Cl-].CC(C)(C)c1ccccc1-[n+]1ccc(cc1)-c1cc[nH+]cc1 ZJZURHCCBVSJAQ-UHFFFAOYSA-M 0.000 description 2
- SOZOCIORXAPNBN-UHFFFAOYSA-M [Cl-].[Cl-].CC(C)c1ccccc1-[n+]1ccc(cc1)-c1cc[nH+]cc1 Chemical compound [Cl-].[Cl-].CC(C)c1ccccc1-[n+]1ccc(cc1)-c1cc[nH+]cc1 SOZOCIORXAPNBN-UHFFFAOYSA-M 0.000 description 2
- SEYCGVCIXJZZKJ-UHFFFAOYSA-L [Cl-].[Cl-].N#Cc1ccccc1-[n+]1ccc(cc1)-c1cc[n+](cc1)-c1ccccc1C#N Chemical compound [Cl-].[Cl-].N#Cc1ccccc1-[n+]1ccc(cc1)-c1cc[n+](cc1)-c1ccccc1C#N SEYCGVCIXJZZKJ-UHFFFAOYSA-L 0.000 description 2
- ZIHQUWYJSTVYAT-UHFFFAOYSA-N [NH-][N+]([O-])=O Chemical compound [NH-][N+]([O-])=O ZIHQUWYJSTVYAT-UHFFFAOYSA-N 0.000 description 2
- 238000010521 absorption reaction Methods 0.000 description 2
- 125000003282 alkyl amino group Chemical group 0.000 description 2
- 125000004644 alkyl sulfinyl group Chemical group 0.000 description 2
- 239000008346 aqueous phase Substances 0.000 description 2
- 150000004945 aromatic hydrocarbons Chemical class 0.000 description 2
- 125000001769 aryl amino group Chemical group 0.000 description 2
- 125000005135 aryl sulfinyl group Chemical group 0.000 description 2
- 125000005110 aryl thio group Chemical group 0.000 description 2
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 2
- 229910052794 bromium Inorganic materials 0.000 description 2
- 239000012230 colorless oil Substances 0.000 description 2
- 125000004663 dialkyl amino group Chemical group 0.000 description 2
- 125000004986 diarylamino group Chemical group 0.000 description 2
- ZUOUZKKEUPVFJK-UHFFFAOYSA-N diphenyl Chemical group C1=CC=CC=C1C1=CC=CC=C1 ZUOUZKKEUPVFJK-UHFFFAOYSA-N 0.000 description 2
- 230000000694 effects Effects 0.000 description 2
- 125000006575 electron-withdrawing group Chemical group 0.000 description 2
- 239000000706 filtrate Substances 0.000 description 2
- 125000002485 formyl group Chemical group [H]C(*)=O 0.000 description 2
- GAEKPEKOJKCEMS-UHFFFAOYSA-N gamma-valerolactone Chemical compound CC1CCC(=O)O1 GAEKPEKOJKCEMS-UHFFFAOYSA-N 0.000 description 2
- 239000011521 glass Substances 0.000 description 2
- AMGQUBHHOARCQH-UHFFFAOYSA-N indium;oxotin Chemical compound [In].[Sn]=O AMGQUBHHOARCQH-UHFFFAOYSA-N 0.000 description 2
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 2
- 239000012074 organic phase Substances 0.000 description 2
- 230000033116 oxidation-reduction process Effects 0.000 description 2
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 2
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 2
- 125000003944 tolyl group Chemical group 0.000 description 2
- WJKHJLXJJJATHN-UHFFFAOYSA-N triflic anhydride Chemical compound FC(F)(F)S(=O)(=O)OS(=O)(=O)C(F)(F)F WJKHJLXJJJATHN-UHFFFAOYSA-N 0.000 description 2
- 125000000876 trifluoromethoxy group Chemical group FC(F)(F)O* 0.000 description 2
- 125000006702 (C1-C18) alkyl group Chemical group 0.000 description 1
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 description 1
- 125000004191 (C1-C6) alkoxy group Chemical group 0.000 description 1
- JGTNAGYHADQMCM-UHFFFAOYSA-M 1,1,2,2,3,3,4,4,4-nonafluorobutane-1-sulfonate Chemical compound [O-]S(=O)(=O)C(F)(F)C(F)(F)C(F)(F)C(F)(F)F JGTNAGYHADQMCM-UHFFFAOYSA-M 0.000 description 1
- 125000001399 1,2,3-triazolyl group Chemical group N1N=NC(=C1)* 0.000 description 1
- 125000001376 1,2,4-triazolyl group Chemical group N1N=C(N=C1)* 0.000 description 1
- OXHOPZLBSSTTBU-UHFFFAOYSA-N 1,3-bis(bromomethyl)benzene Chemical compound BrCC1=CC=CC(CBr)=C1 OXHOPZLBSSTTBU-UHFFFAOYSA-N 0.000 description 1
- RBZMSGOBSOCYHR-UHFFFAOYSA-N 1,4-bis(bromomethyl)benzene Chemical compound BrCC1=CC=C(CBr)C=C1 RBZMSGOBSOCYHR-UHFFFAOYSA-N 0.000 description 1
- ROUYUBHVBIKMQO-UHFFFAOYSA-N 1,4-diiodobutane Chemical compound ICCCCI ROUYUBHVBIKMQO-UHFFFAOYSA-N 0.000 description 1
- GCZOMCDXYFMAGP-UHFFFAOYSA-N 1,8-bis(bromomethyl)naphthalene Chemical compound C1=CC(CBr)=C2C(CBr)=CC=CC2=C1 GCZOMCDXYFMAGP-UHFFFAOYSA-N 0.000 description 1
- UVCIVGWTJICGFA-UHFFFAOYSA-N 1-(2,4-dinitrophenyl)-4-[1-(2,4-dinitrophenyl)pyridin-1-ium-4-yl]pyridin-1-ium Chemical compound [O-][N+](=O)C1=CC([N+](=O)[O-])=CC=C1[N+]1=CC=C(C=2C=C[N+](=CC=2)C=2C(=CC(=CC=2)[N+]([O-])=O)[N+]([O-])=O)C=C1 UVCIVGWTJICGFA-UHFFFAOYSA-N 0.000 description 1
- ZDEMMLQKXKSOIW-UHFFFAOYSA-L 1-(2,4-dinitrophenyl)-4-[1-(2-propan-2-ylphenyl)pyridin-1-ium-4-yl]pyridin-1-ium 4-methylbenzenesulfonate Chemical compound Cc1ccc(cc1)S([O-])(=O)=O.Cc1ccc(cc1)S([O-])(=O)=O.CC(C)c1ccccc1-[n+]1ccc(cc1)-c1cc[n+](cc1)-c1ccc(cc1[N+]([O-])=O)[N+]([O-])=O ZDEMMLQKXKSOIW-UHFFFAOYSA-L 0.000 description 1
- OOQZNBUFTPBFBM-UHFFFAOYSA-M 1-(2,4-dinitrophenyl)-4-pyridin-1-ium-4-ylpyridin-1-ium;dichloride Chemical compound [Cl-].[Cl-].[O-][N+](=O)C1=CC([N+](=O)[O-])=CC=C1[N+]1=CC=C(C=2C=C[NH+]=CC=2)C=C1 OOQZNBUFTPBFBM-UHFFFAOYSA-M 0.000 description 1
- VDXGURZGBXUKES-UHFFFAOYSA-N 1-(bromomethyl)-2-[2-(bromomethyl)phenyl]benzene Chemical group BrCC1=CC=CC=C1C1=CC=CC=C1CBr VDXGURZGBXUKES-UHFFFAOYSA-N 0.000 description 1
- SWDIVDODDINILB-UHFFFAOYSA-L 1-hexyl-4-(1-hexylpyridin-1-ium-4-yl)pyridin-1-ium;diiodide Chemical compound [I-].[I-].C1=C[N+](CCCCCC)=CC=C1C1=CC=[N+](CCCCCC)C=C1 SWDIVDODDINILB-UHFFFAOYSA-L 0.000 description 1
- ANOOTOPTCJRUPK-UHFFFAOYSA-N 1-iodohexane Chemical compound CCCCCCI ANOOTOPTCJRUPK-UHFFFAOYSA-N 0.000 description 1
- DGYYJSHANXEPSK-UHFFFAOYSA-N 1-methyl-10h-phenothiazine Chemical compound S1C2=CC=CC=C2NC2=C1C=CC=C2C DGYYJSHANXEPSK-UHFFFAOYSA-N 0.000 description 1
- CJAOGUFAAWZWNI-UHFFFAOYSA-N 1-n,1-n,4-n,4-n-tetramethylbenzene-1,4-diamine Chemical compound CN(C)C1=CC=C(N(C)C)C=C1 CJAOGUFAAWZWNI-UHFFFAOYSA-N 0.000 description 1
- TZMSYXZUNZXBOL-UHFFFAOYSA-N 10H-phenoxazine Chemical compound C1=CC=C2NC3=CC=CC=C3OC2=C1 TZMSYXZUNZXBOL-UHFFFAOYSA-N 0.000 description 1
- QUTSYCOAZVHGGT-UHFFFAOYSA-N 2,6-bis(bromomethyl)pyridine Chemical compound BrCC1=CC=CC(CBr)=N1 QUTSYCOAZVHGGT-UHFFFAOYSA-N 0.000 description 1
- ZFCOUBUSGHLCDT-UHFFFAOYSA-N 2-(trifluoromethoxy)aniline Chemical compound NC1=CC=CC=C1OC(F)(F)F ZFCOUBUSGHLCDT-UHFFFAOYSA-N 0.000 description 1
- YKOLZVXSPGIIBJ-UHFFFAOYSA-N 2-Isopropylaniline Chemical compound CC(C)C1=CC=CC=C1N YKOLZVXSPGIIBJ-UHFFFAOYSA-N 0.000 description 1
- FPPLREPCQJZDAQ-UHFFFAOYSA-N 2-methylpentanedinitrile Chemical compound N#CC(C)CCC#N FPPLREPCQJZDAQ-UHFFFAOYSA-N 0.000 description 1
- NJXPYZHXZZCTNI-UHFFFAOYSA-N 3-aminobenzonitrile Chemical compound NC1=CC=CC(C#N)=C1 NJXPYZHXZZCTNI-UHFFFAOYSA-N 0.000 description 1
- CMJLMPKFQPJDKP-UHFFFAOYSA-N 3-methylthiolane 1,1-dioxide Chemical compound CC1CCS(=O)(=O)C1 CMJLMPKFQPJDKP-UHFFFAOYSA-N 0.000 description 1
- DPKTVUKEPNBABS-UHFFFAOYSA-N 3-tert-butylaniline Chemical compound CC(C)(C)C1=CC=CC(N)=C1 DPKTVUKEPNBABS-UHFFFAOYSA-N 0.000 description 1
- RDKAUIFVYMXTCH-UHFFFAOYSA-L 4-[1-(2-tert-butylphenyl)pyridin-1-ium-4-yl]-1-(2,4-dinitrophenyl)pyridin-1-ium 4-methylbenzenesulfonate Chemical compound Cc1ccc(cc1)S([O-])(=O)=O.Cc1ccc(cc1)S([O-])(=O)=O.CC(C)(C)c1ccccc1-[n+]1ccc(cc1)-c1cc[n+](cc1)-c1ccc(cc1[N+]([O-])=O)[N+]([O-])=O RDKAUIFVYMXTCH-UHFFFAOYSA-L 0.000 description 1
- OTLNPYWUJOZPPA-UHFFFAOYSA-M 4-nitrobenzoate Chemical compound [O-]C(=O)C1=CC=C([N+]([O-])=O)C=C1 OTLNPYWUJOZPPA-UHFFFAOYSA-M 0.000 description 1
- IVURTNNWJAPOML-UHFFFAOYSA-N 5,10-dihydrophenazine Chemical compound C1=CC=C2NC3=CC=CC=C3NC2=C1 IVURTNNWJAPOML-UHFFFAOYSA-N 0.000 description 1
- 101710134784 Agnoprotein Proteins 0.000 description 1
- PBGDIBQPASXECU-UHFFFAOYSA-N Br.Br.I.I Chemical compound Br.Br.I.I PBGDIBQPASXECU-UHFFFAOYSA-N 0.000 description 1
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 1
- UKAUPIBZGYUUCW-UHFFFAOYSA-N C1=C[NH+]=CC=C1C2=CC=[NH+]C=C2.C1=C[NH+]=CC=C1C2=CC=[NH+]C=C2.[Br-].[Br-].[I-].[I-] Chemical compound C1=C[NH+]=CC=C1C2=CC=[NH+]C=C2.C1=C[NH+]=CC=C1C2=CC=[NH+]C=C2.[Br-].[Br-].[I-].[I-] UKAUPIBZGYUUCW-UHFFFAOYSA-N 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 1
- 229910020366 ClO 4 Inorganic materials 0.000 description 1
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 1
- KRHYYFGTRYWZRS-UHFFFAOYSA-M Fluoride anion Chemical compound [F-] KRHYYFGTRYWZRS-UHFFFAOYSA-M 0.000 description 1
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 1
- RJUFJBKOKNCXHH-UHFFFAOYSA-N Methyl propionate Chemical group CCC(=O)OC RJUFJBKOKNCXHH-UHFFFAOYSA-N 0.000 description 1
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 1
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 1
- 239000002033 PVDF binder Substances 0.000 description 1
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 1
- 239000001089 [(2R)-oxolan-2-yl]methanol Substances 0.000 description 1
- WWFMINHWJYHXHF-UHFFFAOYSA-N [6-(hydroxymethyl)pyridin-2-yl]methanol Chemical compound OCC1=CC=CC(CO)=N1 WWFMINHWJYHXHF-UHFFFAOYSA-N 0.000 description 1
- HIEFKFUTIOYUQD-UHFFFAOYSA-L [I-].C(CCCCC)[N+]1(CC=CC=C1)[N+]1=CC=CC=C1.[I-] Chemical compound [I-].C(CCCCC)[N+]1(CC=CC=C1)[N+]1=CC=CC=C1.[I-] HIEFKFUTIOYUQD-UHFFFAOYSA-L 0.000 description 1
- MGYIIQCUXMRSFB-UHFFFAOYSA-J [I-].[I-].[I-].[I-].CCC.C(CCCCC)[N+]1(CC=CC=C1)[N+]1=CC=CC=C1.C(CCCCC)[N+]1(CC=CC=C1)[N+]1=CC=CC=C1 Chemical compound [I-].[I-].[I-].[I-].CCC.C(CCCCC)[N+]1(CC=CC=C1)[N+]1=CC=CC=C1.C(CCCCC)[N+]1(CC=CC=C1)[N+]1=CC=CC=C1 MGYIIQCUXMRSFB-UHFFFAOYSA-J 0.000 description 1
- BLFMVIFQJWAIQH-UHFFFAOYSA-J [I-].[I-].[I-].[I-].CCCCCC[n+]1ccc(cc1)-c1cc[n+](CCC[n+]2ccc(cc2)-c2cc[n+](CCCCCC)cc2)cc1 Chemical compound [I-].[I-].[I-].[I-].CCCCCC[n+]1ccc(cc1)-c1cc[n+](CCC[n+]2ccc(cc2)-c2cc[n+](CCCCCC)cc2)cc1 BLFMVIFQJWAIQH-UHFFFAOYSA-J 0.000 description 1
- 238000002835 absorbance Methods 0.000 description 1
- 230000032900 absorption of visible light Effects 0.000 description 1
- 125000002252 acyl group Chemical group 0.000 description 1
- 125000002877 alkyl aryl group Chemical group 0.000 description 1
- 230000002152 alkylating effect Effects 0.000 description 1
- 125000005529 alkyleneoxy group Chemical group 0.000 description 1
- 150000001450 anions Chemical class 0.000 description 1
- 125000002178 anthracenyl group Chemical group C1(=CC=CC2=CC3=CC=CC=C3C=C12)* 0.000 description 1
- 125000004653 anthracenylene group Chemical group 0.000 description 1
- 150000004056 anthraquinones Chemical class 0.000 description 1
- SRSXLGNVWSONIS-UHFFFAOYSA-M benzenesulfonate Chemical group [O-]S(=O)(=O)C1=CC=CC=C1 SRSXLGNVWSONIS-UHFFFAOYSA-M 0.000 description 1
- 229940077388 benzenesulfonate Drugs 0.000 description 1
- 125000003785 benzimidazolyl group Chemical group N1=C(NC2=C1C=CC=C2)* 0.000 description 1
- 125000003354 benzotriazolyl group Chemical group N1N=NC2=C1C=CC=C2* 0.000 description 1
- 230000005540 biological transmission Effects 0.000 description 1
- 235000010290 biphenyl Nutrition 0.000 description 1
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 1
- 150000004649 carbonic acid derivatives Chemical class 0.000 description 1
- 239000003638 chemical reducing agent Substances 0.000 description 1
- 125000000259 cinnolinyl group Chemical group N1=NC(=CC2=CC=CC=C12)* 0.000 description 1
- 238000002484 cyclic voltammetry Methods 0.000 description 1
- 125000004977 cycloheptylene group Chemical group 0.000 description 1
- 125000005725 cyclohexenylene group Chemical group 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000004956 cyclohexylene group Chemical group 0.000 description 1
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000004979 cyclopentylene group Chemical group 0.000 description 1
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 1
- 125000004980 cyclopropylene group Chemical group 0.000 description 1
- 238000010908 decantation Methods 0.000 description 1
- 125000002704 decyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- ICZLTZWATFXDLP-UHFFFAOYSA-N diethyl 2-benzylpropanedioate Chemical compound CCOC(=O)C(C(=O)OCC)CC1=CC=CC=C1 ICZLTZWATFXDLP-UHFFFAOYSA-N 0.000 description 1
- SBZXBUIDTXKZTM-UHFFFAOYSA-N diglyme Chemical compound COCCOCCOC SBZXBUIDTXKZTM-UHFFFAOYSA-N 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- ZYBWTEQKHIADDQ-UHFFFAOYSA-N ethanol;methanol Chemical compound OC.CCO ZYBWTEQKHIADDQ-UHFFFAOYSA-N 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- KTWOOEGAPBSYNW-UHFFFAOYSA-N ferrocene Chemical compound [Fe+2].C=1C=C[CH-]C=1.C=1C=C[CH-]C=1 KTWOOEGAPBSYNW-UHFFFAOYSA-N 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- RMBPEFMHABBEKP-UHFFFAOYSA-N fluorene Chemical compound C1=CC=C2C3=C[CH]C=CC3=CC2=C1 RMBPEFMHABBEKP-UHFFFAOYSA-N 0.000 description 1
- 125000002541 furyl group Chemical group 0.000 description 1
- ZTOMUSMDRMJOTH-UHFFFAOYSA-N glutaronitrile Chemical compound N#CCCCC#N ZTOMUSMDRMJOTH-UHFFFAOYSA-N 0.000 description 1
- 125000005843 halogen group Chemical group 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- 125000002883 imidazolyl group Chemical group 0.000 description 1
- 125000003453 indazolyl group Chemical group N1N=C(C2=C1C=CC=C2)* 0.000 description 1
- 125000001041 indolyl group Chemical group 0.000 description 1
- 239000012442 inert solvent Substances 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- 239000002608 ionic liquid Substances 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000002183 isoquinolinyl group Chemical group C1(=NC=CC2=CC=CC=C12)* 0.000 description 1
- 125000000842 isoxazolyl group Chemical group 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- NSBIQPJIWUJBBX-UHFFFAOYSA-N n-methoxyaniline Chemical compound CONC1=CC=CC=C1 NSBIQPJIWUJBBX-UHFFFAOYSA-N 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000001624 naphthyl group Chemical group 0.000 description 1
- 125000005186 naphthyloxy group Chemical group C1(=CC=CC2=CC=CC=C12)O* 0.000 description 1
- 230000000269 nucleophilic effect Effects 0.000 description 1
- NIHNNTQXNPWCJQ-UHFFFAOYSA-N o-biphenylenemethane Natural products C1=CC=C2CC3=CC=CC=C3C2=C1 NIHNNTQXNPWCJQ-UHFFFAOYSA-N 0.000 description 1
- 125000002971 oxazolyl group Chemical group 0.000 description 1
- 125000005564 oxazolylene group Chemical group 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 125000001792 phenanthrenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3C=CC12)* 0.000 description 1
- 125000005560 phenanthrenylene group Chemical group 0.000 description 1
- 125000004592 phthalazinyl group Chemical group C1(=NN=CC2=CC=CC=C12)* 0.000 description 1
- 239000000049 pigment Substances 0.000 description 1
- 229920000191 poly(N-vinyl pyrrolidone) Polymers 0.000 description 1
- 229920003229 poly(methyl methacrylate) Polymers 0.000 description 1
- 229920000058 polyacrylate Polymers 0.000 description 1
- 125000003367 polycyclic group Chemical group 0.000 description 1
- 239000004926 polymethyl methacrylate Substances 0.000 description 1
- 229920001451 polypropylene glycol Polymers 0.000 description 1
- 229920002635 polyurethane Polymers 0.000 description 1
- 239000004814 polyurethane Substances 0.000 description 1
- 229920002689 polyvinyl acetate Polymers 0.000 description 1
- 239000011118 polyvinyl acetate Substances 0.000 description 1
- 229920002981 polyvinylidene fluoride Polymers 0.000 description 1
- FVSKHRXBFJPNKK-UHFFFAOYSA-N propionitrile Chemical compound CCC#N FVSKHRXBFJPNKK-UHFFFAOYSA-N 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 125000003373 pyrazinyl group Chemical group 0.000 description 1
- 125000005550 pyrazinylene group Chemical group 0.000 description 1
- 125000002098 pyridazinyl group Chemical group 0.000 description 1
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 1
- 125000004076 pyridyl group Chemical group 0.000 description 1
- 125000005551 pyridylene group Chemical group 0.000 description 1
- 125000000714 pyrimidinyl group Chemical group 0.000 description 1
- 125000005576 pyrimidinylene group Chemical group 0.000 description 1
- 125000000168 pyrrolyl group Chemical group 0.000 description 1
- 239000010453 quartz Substances 0.000 description 1
- 125000002294 quinazolinyl group Chemical group N1=C(N=CC2=CC=CC=C12)* 0.000 description 1
- 125000002943 quinolinyl group Chemical group N1=C(C=CC2=CC=CC=C12)* 0.000 description 1
- 125000001567 quinoxalinyl group Chemical group N1=C(C=NC2=CC=CC=C12)* 0.000 description 1
- 150000005839 radical cations Chemical class 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 239000012279 sodium borohydride Substances 0.000 description 1
- 229910000033 sodium borohydride Inorganic materials 0.000 description 1
- HXJUTPCZVOIRIF-UHFFFAOYSA-N sulfolane Chemical compound O=S1(=O)CCCC1 HXJUTPCZVOIRIF-UHFFFAOYSA-N 0.000 description 1
- 125000000542 sulfonic acid group Chemical group 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- KBLZDCFTQSIIOH-UHFFFAOYSA-M tetrabutylazanium;perchlorate Chemical compound [O-]Cl(=O)(=O)=O.CCCC[N+](CCCC)(CCCC)CCCC KBLZDCFTQSIIOH-UHFFFAOYSA-M 0.000 description 1
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 1
- BSYVTEYKTMYBMK-UHFFFAOYSA-N tetrahydrofurfuryl alcohol Chemical compound OCC1CCCO1 BSYVTEYKTMYBMK-UHFFFAOYSA-N 0.000 description 1
- FHCPAXDKURNIOZ-UHFFFAOYSA-N tetrathiafulvalene Chemical compound S1C=CSC1=C1SC=CS1 FHCPAXDKURNIOZ-UHFFFAOYSA-N 0.000 description 1
- 125000000335 thiazolyl group Chemical group 0.000 description 1
- 125000005557 thiazolylene group Chemical group 0.000 description 1
- 125000001544 thienyl group Chemical group 0.000 description 1
- 125000005556 thienylene group Chemical group 0.000 description 1
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 1
- HTSABYAWKQAHBT-UHFFFAOYSA-N trans 3-methylcyclohexanol Natural products CC1CCCC(O)C1 HTSABYAWKQAHBT-UHFFFAOYSA-N 0.000 description 1
- 238000001665 trituration Methods 0.000 description 1
- 238000001429 visible spectrum Methods 0.000 description 1
- 239000008096 xylene Substances 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/06—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom containing only hydrogen and carbon atoms in addition to the ring nitrogen atom
- C07D213/22—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom containing only hydrogen and carbon atoms in addition to the ring nitrogen atom containing two or more pyridine rings directly linked together, e.g. bipyridyl
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D241/00—Heterocyclic compounds containing 1,4-diazine or hydrogenated 1,4-diazine rings
- C07D241/36—Heterocyclic compounds containing 1,4-diazine or hydrogenated 1,4-diazine rings condensed with carbocyclic rings or ring systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/06—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K9/00—Tenebrescent materials, i.e. materials for which the range of wavelengths for energy absorption is changed as a result of excitation by some form of energy
- C09K9/02—Organic tenebrescent materials
-
- G—PHYSICS
- G02—OPTICS
- G02C—SPECTACLES; SUNGLASSES OR GOGGLES INSOFAR AS THEY HAVE THE SAME FEATURES AS SPECTACLES; CONTACT LENSES
- G02C7/00—Optical parts
- G02C7/10—Filters, e.g. for facilitating adaptation of the eyes to the dark; Sunglasses
- G02C7/101—Filters, e.g. for facilitating adaptation of the eyes to the dark; Sunglasses having an electro-optical light valve
-
- G—PHYSICS
- G02—OPTICS
- G02F—OPTICAL DEVICES OR ARRANGEMENTS FOR THE CONTROL OF LIGHT BY MODIFICATION OF THE OPTICAL PROPERTIES OF THE MEDIA OF THE ELEMENTS INVOLVED THEREIN; NON-LINEAR OPTICS; FREQUENCY-CHANGING OF LIGHT; OPTICAL LOGIC ELEMENTS; OPTICAL ANALOGUE/DIGITAL CONVERTERS
- G02F1/00—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics
- G02F1/01—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour
- G02F1/15—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour based on an electrochromic effect
- G02F1/1503—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour based on an electrochromic effect caused by oxidation-reduction reactions in organic liquid solutions, e.g. viologen solutions
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1007—Non-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1011—Condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1029—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom
-
- G—PHYSICS
- G02—OPTICS
- G02F—OPTICAL DEVICES OR ARRANGEMENTS FOR THE CONTROL OF LIGHT BY MODIFICATION OF THE OPTICAL PROPERTIES OF THE MEDIA OF THE ELEMENTS INVOLVED THEREIN; NON-LINEAR OPTICS; FREQUENCY-CHANGING OF LIGHT; OPTICAL LOGIC ELEMENTS; OPTICAL ANALOGUE/DIGITAL CONVERTERS
- G02F1/00—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics
- G02F1/01—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour
- G02F1/15—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour based on an electrochromic effect
- G02F1/1514—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour based on an electrochromic effect characterised by the electrochromic material, e.g. by the electrodeposited material
- G02F1/1516—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour based on an electrochromic effect characterised by the electrochromic material, e.g. by the electrodeposited material comprising organic material
- G02F2001/1517—Cyano complex compounds, e.g. Prussian blue
-
- G—PHYSICS
- G02—OPTICS
- G02F—OPTICAL DEVICES OR ARRANGEMENTS FOR THE CONTROL OF LIGHT BY MODIFICATION OF THE OPTICAL PROPERTIES OF THE MEDIA OF THE ELEMENTS INVOLVED THEREIN; NON-LINEAR OPTICS; FREQUENCY-CHANGING OF LIGHT; OPTICAL LOGIC ELEMENTS; OPTICAL ANALOGUE/DIGITAL CONVERTERS
- G02F1/00—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics
- G02F1/01—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour
- G02F1/15—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour based on an electrochromic effect
- G02F1/1514—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour based on an electrochromic effect characterised by the electrochromic material, e.g. by the electrodeposited material
- G02F1/1516—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour based on an electrochromic effect characterised by the electrochromic material, e.g. by the electrodeposited material comprising organic material
- G02F2001/1518—Ferrocene compounds
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Physics & Mathematics (AREA)
- Nonlinear Science (AREA)
- Optics & Photonics (AREA)
- General Physics & Mathematics (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Health & Medical Sciences (AREA)
- Ophthalmology & Optometry (AREA)
- General Health & Medical Sciences (AREA)
- Plural Heterocyclic Compounds (AREA)
- Electrochromic Elements, Electrophoresis, Or Variable Reflection Or Absorption Elements (AREA)
- Pyridine Compounds (AREA)
- Eyeglasses (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
Description
Zは、
アルキレン;
シクロアルキレン;及び
式−R7−Y−R8、(ここで、
R7及びR8は、各々独立して、単結合、アルキレン及びシクロアルキレンから選択され、及び
Yは、アリーレン、シクロアルキレン、ヘテロアリーレン、アリーレン−アリーレン又はアリーレン−CR’R’’−アリーレンから選択され、R’及びR’’はそれらが結合している炭素と一緒に炭素環基を形成する)の2価の基から選択され、
前記アルキレン、シクロアルキレン、アリーレン、ヘテロアリーレン、及び炭素環基は、ハロゲン、アルキル、アルコキシ、アルキルチオ、ヒドロキシアルキル、アシルオキシ、シクロアルキル、アリール、置換アリール、アリールオキシ、ヘテロアリール及び置換ヘテロアリールから選択される1つ又は複数の置換基で置換されてもよく;
mは、0又は1であり;
R1及びR2は、
Yがアリーレン−アリーレン又はアリーレン−アルキレン−アリーレンである場合、R1及びR2は、フェニルでない;mが0である場合、R1及びR2は、各々独立して、任意選択により置換されるフェニル基から選択され、R1及びR2の少なくとも1つは、置換フェニル基から選択され、R1及びR2は、各々独立して、置換フェニル基から選択されるのが好ましい
とする条件で
各々独立して、C6〜C7アルキル、及び任意選択により置換されたフェニルから選択され;
R3、R4、R5及びR6は、各々独立して、H、アルキル、アルコキシ、アルキルチオ、ハロアルキル、ハロアルコキシ、ハロアルキルチオ、ポリアルキレンオキシ、アルコキシカルボニル、アリール、置換アリール、ヘテロアリール及び置換ヘテロアリールから選択され、ここでアルキル基は、アルコキシ、シクロアルキル、アリール、置換アリール、ヘテロアリール及び置換ヘテロアリールから選択される1つ又は複数の置換基で置換されてもよく;
n、p、q及びrは、各々独立して0〜4の整数であり、n、p、q及びrが2以上である場合、各R3、各R4、各R5又は各R6は、同一でも異なってもよく、及び
X−は、対イオンである]
によって表されるエレクトロクロミック化合物に関する。
H、ハロゲン、シアノ、ニトロ、アルキル、ハロアルキル、ハロアルコキシ、(ハロアルコキシ)アルキル、アリールアルキル、シクロアルキル、(シクロアルキル)アルキル及び(ヘテロシクロアルキル)アルキル、アルケニル、アルキニル、アリル、ビニル、アリール、置換アリール、ヘテロアリール、置換ヘテロアリール、−N(アリール)2、−N(アリール)CO(アリール)、−CO−アリール及び−CO−置換アリール;
−OR9、−SR9、−S(O)R9、−S(O2)R9、−S(O2)NR9R10、−NR9R10、−NR9COR10、−NR9CO(アリール)、−NR9アリール、−CH2OR9、−CH2SR9、−CH2R9、−CO−R9及び−CO2R10(R9及びR10は、独立してH、アルキル、ハロアルキル、アリールアルキル、シクロアルキル、シクロアルキルアルキル及びヘテロシクロアルキルアルキルから選択される);
−S(O2)NR11R12及び−NR11R12(R11及びR12は、それらが結合している窒素原子と一緒に、窒素原子に加えて、酸素、窒素及び硫黄から選択されるヘテロ原子をさらに1個含んでもよく、ハロゲン、−R9、−OR9、及び−NR9R10から選択される同一の又は異なる1個又は2個の基により任意選択により置換されてもよく、R9及びR10は、上に定義した通りである、飽和5〜7員のヘテロシクロアルキルを形成する);
−V−W−R13(式中、
Vは、酸素、−N(R9)−、硫黄、−S(O)−及び−S(O2)−(R9は上に定義した通りである)から選択され
Wは、アルキレンであり、ハロゲン及びアルコキシから選択される基により置換されてもよく;
R13は、−OR9、−NR9(アルキル)及び−SR9(R9は上に定義した通りである)から選択され;
OC(O)−R14{ここで、R14は、アルキル、ハロアルキル、アルケニル、−W−R13、及びアリール基(ハロゲン、−R9、−OR9、−SR9、−NR9R10、−NR11R12、−CO−R9、−CO2R9(ここで、R9、R10、R11、R12、R13及びWは、上に定義した通りである)から選択される1〜4個の基により置換されてもよい)から選択される}
から選択される]により表される。
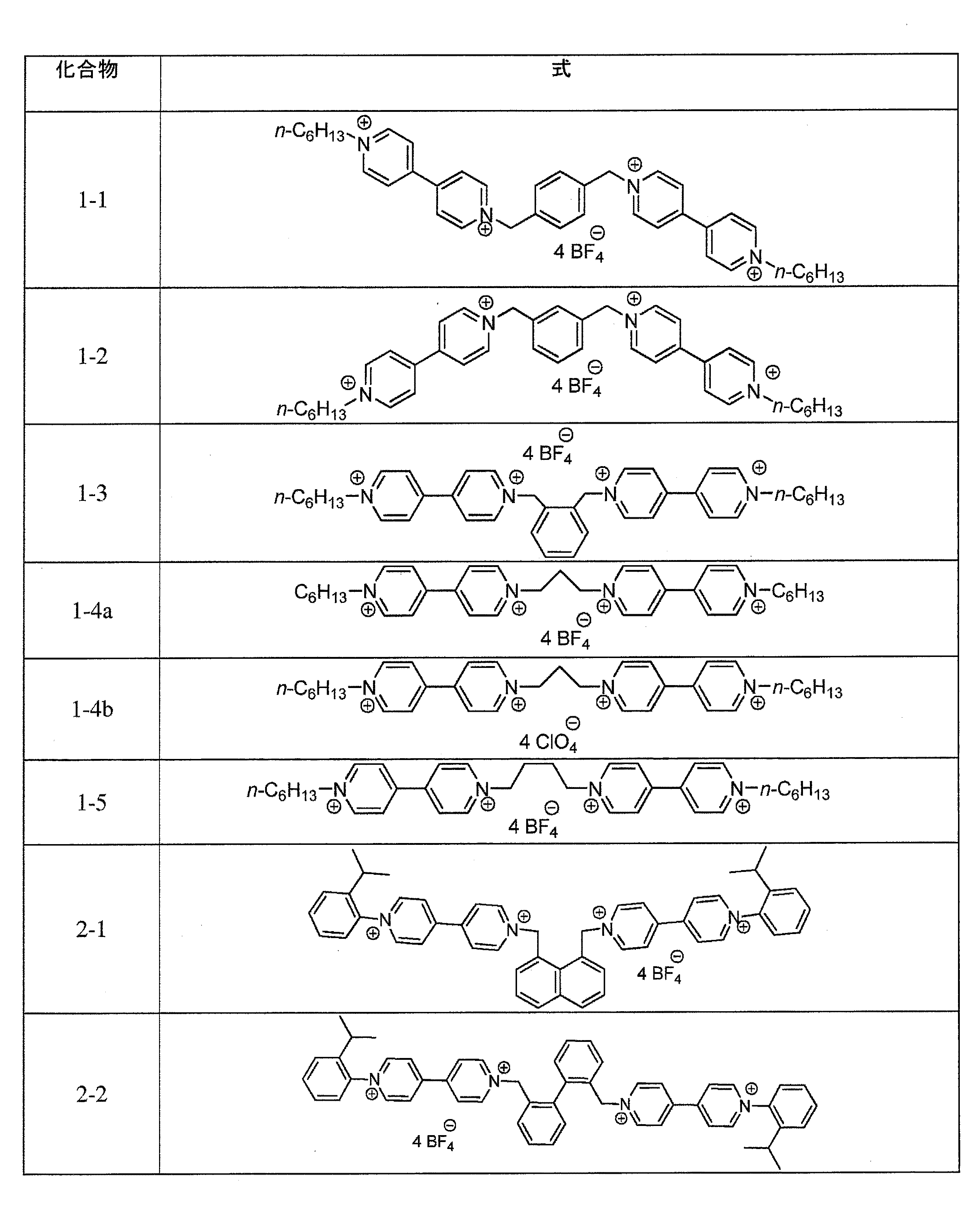
化合物2−1の合成:1’,1’’’−[ナフタレン−1,8−ジイル−ビス(メチレン)]−ビス{1−(2−イソプロピルフェニル)−[4,4’−ビピリジン]−1,1’−ジイウム}テトラキス(テトラフルオロボレート)
1−(2,4−ジニトロフェニル)−4,4’−ビピリジニウムクロリド(15g、41.8ミリモル)と2−イソプロピルアニリン(16.95g、125.5ミリモル)を水(300mL)中に含む混合物を4時間還流した後、冷却し、濾過し、濾液をCHCl3で3回洗浄した。CHCI3抽出物を廃棄し、水を減圧下で除去した。残渣をアセトンで洗浄して、黄色粉末として1−(2−イソプロピルフェニル)−4,4’−ビピリジニウムクロリド(9.17g、91%)を得た。
δΗ(400MHz,CD3OD−D2O)9.30(4H,d,J=6.8Hz),9.19(4H,d,J=6.8Hz),8.83(4H,d,J=6.8Hz),8.79(4H,d,J=6.8Hz),7.90−7.50(10H,m),7.26(2H,d,J=7.2Hz),6.69(4H,s),2.58(2H,sept,J=6.8Hz),1.27(12H,d,J=6.8Hz).
実施例2
化合物2−2の合成:1’,1’’’−{[1,1’−ビフェニル]−22’−ジイルビス(メチレン)}ビス(1−(2−イソプロピルフェニル)−[4,4’−ビピリジン]−1,1’−ジイウム)テトラキス(テトラフルオロボレート)
1−(2−イソプロピルフェニル)−4,4’−ビピリジニウムテトラフルオロボレート(3.19g、2.9ミリモル)(実施例1に基づいて得た)と2,2’−ビス(ブロモメチル)−1,1’−ビフェニル(1g、2.9ミリモル)をMeCN(40mL)に溶かした溶液を60時間還流し、冷却し、濾過し、Et2O(2×50ML)で洗浄し、空気乾燥した。得られた粉末をMeOH(20mL)に溶解させ、水(50mL)に溶かしたNaBF4溶液(3.88g、35ミリモル)に撹拌しながら滴下した。溶媒を減少させ、デカンテーションした。残渣を温水(30mL)に溶解させ、冷却し、デカンテーションし、真空下で乾燥し、黄色粉末として化合物2−2(1.61g、51%)を得た。
δH(400MHz,D2O)9.15(4H,d,J=6.8Hz),8.54(4H,d,J=6.8Hz),8.49(4H,d,J=6.8Hz),8.30(4H,d,J=6.8Hz),7.76(2H,d,J=7.6Hz),7.64(4H,bs),7.57(2H,t,J=7.6Hz),7.41(4H,bs),7.28(2H,t,J=7.2Hz),6.70(2H,J=7.6Hz),5.82(2H,d,J=15Hz),5.61(2H,d,J=15Hz),2.41(2H,sept,J=6.8Hz),1.09(12H,d,J=6.8Hz).
実施例3
化合物1−1の合成:1,1’’’−ジヘキシル−1,1’’−[1,4−フェニレンビス(メチレン)]ビス−4,4’−ビピリジニウムテトラキス(テトラフルオロボレート)
4,4’−ビピリジン(40g、256ミリモル)と1−ヨードヘキサン(54.36g、256ミリモル)をMeCN(200mL)に溶かした溶液を加熱還流した。16時間後、溶媒を減圧下で除去し、残渣を温EtOHに溶解させ、0℃まで3時間冷却した後、濾過した。濾液をEtOHから結晶化し、1,1’−ジヘキシル−4,4’−ビピリジニウムジヨージド(14.6g、10%)を得た。溶媒を減圧下で除去し、残渣を温DCMに溶解させ、ヘキサン(1L)を添加し、混合物を濾過し、そのプロセスを繰り返した。得られた沈殿物を、MeOH(DCM中において0〜3%)を溶離液として用いてシリカを介して濾過した。第1バンドを収集し、溶媒を減圧下で除去し、淡黄色粉末として1−ヘキシル−4,4’−ビピリジニウムヨージド(57g、60%)を得た。
δΗ(400MHz,DMSO−d6)9.47(2H,d,J=6.8Hz),9.36(2H,d,J=6.8Hz),8.77(2H,d,J=6.8Hz),8.72(2H,d,J=6.8Hz),7.70(4H,s),5.95(4H,s),4.69(4H,t,J=7.6Hz),1.98(4H,br.t),1.32(12H,br.s),0.88(6H,t,J=6.8Hz).
1,3−ジ(ブロモメチル)−ベンゼンと1,2−ジ(ブロモメチル)−ベンゼンをそれぞれ用いて、化合物1−2及び1−3を類似の手順で得ることができる。
化合物2−3の合成:1’1’’’−(プロパン−1,3−ジイル)ビス{1−(2−イソプロピルフェニル)−[4,4’−ビピリジン]−1,1’ージイウム}テトラキス(テトラフルオロボレート)
1,3−ジヨードプロパン(0.82g、2.8ミリモル)と1−(2−イソプロピルフェニル)−4,4’−ビピリジニウムテトラフルオロボレート(2.5g、6.9ミリモル)との混合物をMeCN(30mL)中で還流した。3日後、混合物を冷却し、濾過し、残渣をMeCNで洗浄し、赤色粉末として1’1’’’−(プロパン−1,3−ジイル)ビス{1−(2−イソプロピルフェニル)−[4,4’−ビピリジン]−1,1’−ジイウム}ビス(テトラフルオロボレート)ジヨージド(1.93g、68%)を得た。
δΗ(300MHz,DMSO―d6)9.63(4H,d,J=6.9Hz),9.42(4H,d,J=6.9Hz),9.00−8.90(8H,m),7.80−7.50(8H,m),8.7.90―7.60(8H,m),4.87(4H,t,J=7.2Hz),2.83(2H,quin,J=7.2Hz),2.46(2H,sept,J=6.6Hz),1.21(12H,d,J=6.6Hz).
実施例5
化合物2−4の合成:1’,1’’’−(プロパン−1,3−ジイル)ビス{1−(2−(トリフルオロメトキシ)フェニル)−[4,4’−ビピリジン]−1,1’−ジイウム}テトラキス(テトラフルオロボレート)
1−(2−(トリフルオロメトキシ)フェニル)−4,4’−ビピリジニウムテトラフルオロボレート(5.13g、12.7ミリモル)と1,3−ジヨードプロパン(1.48g、5ミリモル)をMeCN(40mL)に溶かした溶液を24時間加熱還流した後、冷却し、Et2O(30ml)で希釈した。混合物を、5分間撹拌した後、0.5時間静置し、濾過した。残渣を4℃でMeOHから結晶化し、塩の混合物(2.18g)を得た。この物質をMeOH−H2O(10ml、1:1)に溶解させ、NaBF4(4.34g、39ミリモル)をH2O(30mL)に溶かした溶液に撹拌しながら滴下した。撹拌を0.5時間継続した。混合物を濾過し、水(2×5L)で洗浄し、空気乾燥し、黄色粉末として化合物2−4(1.51g、29%)を得た。
δΗ(300MHz,DMSO−d6)9.31(4H,d,J=7.0Hz),9.20(4H,d,J=7.0Hz),8.72(4H,d,J=7.0Hz),8.64(4H,d,J=7.0Hz),7.90−7.60(8H,m),4.958(4H,t,J=7.8Hz),2.92(2H,quin,J=7.8Hz).
δF(282MHz,CD3OD−D2O)−59.10−−59.26(bs),−152.40−−151.60(bs).
実施例6
化合物2−5の合成:1’,1’’’−(プロパン−1,3−ジイル)ビス{1−(4−(トリフルオロメトキシ)フェニル)−[4,4’−ビピリジン]−1,1’−ジイウム}テトラキス(テトラフルオロボレート)
1,3−ジヨードプロパン(1.12g、3.8ミリモル)と1−[4−(トリフルオロメトキシ)フェニル]−4,4’−ビピリジニウムテトラフルオロボレート(3.68g、9.1ミリモル)とをMeCN(20mL)中に含む混合物を還流下で加熱した。16時間後、混合物を冷却し、濾過し、残渣を空気乾燥し、暗赤色針状物として1’,1’’’−(プロパン−1,3−ジイル)ビス{1−(4−(トリフルオロメトキシ)フェニル)−[4,4’−ビピリジン]−1,1’−ジイウム}ジヨージドビス(テトラフルオロボレート)(0.89g、20%)を得た。
δΗ(400MHz,CD3OD−D2O)9.45(4H,d,J=7.1Hz),9.30(4H,d,J=7.1Hz),8.80(4H,d,J=7.1Hz),8.75(4H,d,J=7.1Hz),8.03(4H,d,J=8.4Hz),7.75(4H,d,J=8.4Hz),5.03(4H,t,J=7.8Hz),2.98(2H,quin,J=7.8Hz).
δF(376MHz,CD3OD−D2O)−58.77(s),−151.60−−151.80(bs).
実施例7
化合物2−6の合成:1’,1’’’−(2−ベンジルプロパン−1,3−ジイル)ビス(1−(2−イソプロピルフェニル)−[4,4’−ビピリジン]−1,1’−ジイウム)テトラキス(テトラフルオロボレート)
1,2−ジメトキシエタン(70mL)中にNaBH4(6.08g、160ミリモル)を含む懸濁液に、臭素(11.26g、70ミリモル)を−20℃、N2下で撹拌しながら滴下した。添加後、混合物を0℃で2時間撹拌し、−5℃まで冷却し、2−ベンジルマロン酸ジエチル(8g、32ミリモル)を添加した。混合物を一晩かけて室温まで温め、5℃で迅速に撹拌しながら、注意深くHCl(1M、100mL)及びEtOAc(100mL)上に注いだ。水相を分離し、EtOAc(100mL)で抽出した。一緒にした有機相をNa2CO3(2×100mL)、水(100mL)で洗浄し、乾燥し(Na2SO4)、溶媒を減圧下で除去した。残渣を、EtOAc(ヘキサン中に40〜100%)を溶離液として用いてシリカを介して濾過した。第3バンド(Rf=0.05;ヘキサンに溶かした40%EtOAc)を回収し、溶媒を減圧下で除去し、無色オイル(静置すると凝固した)として2−ベンジルプロパン−1,3−ジオール(2.87g、54%)を得た。
δH(400MHz,CDC13)7.10−7.4(5H,m),3.83(2H,dd,J=4,11Hz),3.69(2H,dd,J=7,11Hz),2.64(2H,d,J=7Hz),2.35(2H,bs),2.02−2.16(1H,m).
δc(100MHz,CDC13)139.85,129.01,128.48,126.17,65.64,43.84.
トリフリン酸無水物(5.60g、19.8ミリモル)と2−ベンジルプロパン−1,3−ジオール(1.5g、9ミリモル)をDCM(50mL)に溶かした溶液に、ピリジン(1.57g、19.8ミリモル)を0℃で撹拌しながら滴下した。1時間撹拌を継続し、得られた混合物を水(100mL)に注入し、分離させ、水相をDCM(2×50mL)で抽出した。一緒にした有機相を乾燥(Na2SO4)し、溶媒を減圧下で除去した。残渣を、DCMを溶離液として用いてシリカのショートプラグを介して濾過し、溶媒を減圧下で除去し、無色オイルとして2−ベンジルプロパン−1,3−ジイルビス(トリフルオロメタンスルホネート)(3.35g、86%)を得た。
δH(400MHz,CDC13)7.10−7.50(5H,m),4.60(2H,dd,J=4,11Hz),4.50(2H,dd,J=7,11Hz),2.82(2H,d,J=7Hz),2.55−2.70(1H,m).
δF(376MHz,CDC13)−74.25。
δΗ(400MHz,CD3OD−D2O)9.30(4H,d,J=7.2Hz),9.23(4H,d,J=7.2Hz),8.74(4H,d,J=7.2Hz),8.60(4H,d,J=7.2Hz),7.74−8.87(4H,m),7.54−7.66(4H,m)7.15(5H,br.s),4.90−5.22(4H,m),3.67−3.80(1H,m),3.09(2H,d,J=7.2Hz),2.52−2.66(2H,m),1.28(12H,d,J=7.2Hz).
δF(376MHz,CD3OD−D2O)−79.65(br.s)及び−151.81−−151.92(br.s).
NaBF4(1.43g、13ミリモル)を水(30mL)に溶かした溶液に、1’,1’’’−(2−ベンジルプロパン−1,3−ジイル)ビス(1−(2−イソプロピルフェニル)−[4,4’−ビピリジン]−1,1’−ジイウム)ビス(トリフル酸)ビス(テトラフルオロボレート)(1.5g、1.3ミリモル)を水−MeOH(10mL、1:1)に溶かした溶液を撹拌しながら滴下した。混合物を加熱して溶解させ、迅速に撹拌しながら冷却し、濾過し、残渣を温水から結晶化し、濾過し、水(2×5mL)で洗浄し、空気乾燥した。水(30mL)に溶かしたNaBF4(1.43g、13ミリモル)に残渣を再び添加し、加熱して溶解させ、冷却し、濾過し、温水から結晶化し、濾過し、空気乾燥し、クリーム色粉末として化合物2−6(1.01g、75%)を得た。
δΗ(400MHz,CD3OD−D2O)9.27(4H,d,J=7.2Hz),9.20(4H,d,J=7.2Hz),8.72(4H,d,J=7.2Hz),8.57(4H,d,J=7.2Hz),7.75−7.83(4H,m),7.55−7.63(4H,m)7.130(5H,br.s),4.94−5.19(4H,m),3.63−3.81(1H,m),3.08(2H,d,J=7.2Hz),2.49−2.66(2H,m),1.26(12H,d,J=7.2Hz).
δF(376MHz,CD3OD−D2O)−152.36−−152.46(br.s).
実施例8
化合物2−7の合成:1’1’’’−[1,2−フェニレンビス(メチレン)]ビス{1−(2−イソプロピルフェニル)−[4,4’−ビピリジン]−1,1’−ジイウム}テトラキス(テトラフルオロボレート)
1−(2−イソプロピルフェニル)−4,4’−ビピリジニウムテトラフルオロボレート(3.43g、9.5ミリモル)と1,2ービス(ブロモメチル)ベンゼン(1.00g、3.8ミリモル)をMeCN(40mL)に溶かした溶液を、16時間加熱還流した。冷却後、混合物を濾過し、MeCN(2×5mL)で洗浄し、空気乾燥した。得られた吸湿性の黄色固体を水(20mL)に溶解させ、NaBF4(2.50g、22.7ミリモル)を水(30mL)に溶かした溶液に撹拌しながら滴下した。得られた混合物を加熱溶解させ、迅速に撹拌しながら室温まで冷却し、濾過し、水(2×5mL)で洗浄し、空気乾燥し、無色粉末として化合物2−7(1.40g、37%)を得た。
δΗ(400MHz,CD3OD−D2O),9.27(4H,d,J=6.5Hz),9.20(4H,d,J=6.5Hz),8.80(4H,d,J=6.5Hz),8.76(4H,d,J=6.5Hz),7.790(4H,br.s),7.65−7.75(2H,m),7.58(4H,br.s),7.40−7.50(2H,m),6.20(4H,s),2.57(2H,m)及び1.25(12H,d,J=6.8Hz)
δF(376MHz,CD3OD−D2O),−151.12−−151.27(br.s)。
化合物2−8の合成:1’1’’’−[1,2−フェニレンビス(メチレン)]ビス{1−(2−(トリフルオロメトキシ)フェニル)−[4,4’−ビピリジン]−1,1’−ジイウム}テトラキス(テトラフルオロボレート)
1−[2−(トリフルオロメトキシ)フェニル]−4,4’−ビピリジニウムテトラフルオロボレート(3.83g、9.5ミリモル)と1,2−ビス(ブロモメチル)ベンゼン(1.00g、3.8ミリモル)をMeCN(40mL)に溶かした溶液を、16時間加熱還流した。冷却後、混合物を濾過し、MeCN(2×5mL)で洗浄し、空気乾燥した。得られた黄色固体を、水(20mL)に溶解させ、NaBF4(2.50g、22.7ミリモル)を水(30mL)に溶かした溶液に撹拌しながら滴下した。0.5時間撹拌を継続し、得られた沈殿物を濾過し、水(2×5mL)で洗浄し、空気乾燥し、無色粉末として化合物2−8(1.73g、43%)を得た。
δΗ(400MHz,CD3OD−D2O),9.43(4H,d,J=6.8Hz),9.23(4H,d,J=6.8Hz),8.88(4H,d,J=6.8Hz),8.79(4H,d,J=6.8Hz),7.93−8.01(4H,m),7.82−7.88(4H,t,J=7.6Hz),7.67−7.74(2H,m),7.40−7.48(2H,m)及び6.23(4H,s)
δF,(376MHz,CD3OD−D2O),−58.98(s),151.87−−151.97(br.s)
実施例10
化合物1−4aの合成:1,3−ビス(1’−ヘキシル−4,4’−ビピリジニウム−1−イル)プロパンテトラキス(テトラフルオロボレート)
1−ヘキシル−4,4’−ビピリジニウムヨージド(1.68g、4.6ミリモル)と1,3−ジヨードプロパン(0.60g、0.45ミリモル)をMeCN(50mL)に溶かした溶液を4日間加熱還流した。混合物を冷却した後、濾過し、残渣をDCMで洗浄し、橙色粉末として1,3−ビス(1’−ヘキシル−4,4’−ビピリジニウム−1−イル)プロパンテトラヨージド(1.29g、62%)を得た。
δΗ(400MHz,DMSO−d6,)9.50−9.30(8H,m),8.85(4H,d,J=6.8Hz),8.79(4H,d,J=6.8Hz),4.82(4H,t,J=7.2Hz),4.70(4H,t,J=7.2Hz),2.90−2.70(2H,m),2.10−1.90(4H,m),1.40−1.20(12H,m),0.88(6H,t,J=6.8Hz).
対イオンをClO4 −で置換して、化合物1−4bを同一の手順により得ることができる。
化合物1−5の合成:1,4−ビス(1’−ヘキシル−4,4,−ビピリジニウム−1−イル)ブタンテトラキス(テトラフルオロボレート)
1−ヘキシルビピリジニウムヨージド(3.68g、10ミリモル)と1,4−ジヨードブタン(1.24g、4ミリモル)をMeCN(80mL)に溶かした溶液を、2週間加熱還流した。混合物を冷却した後、濾過し、残渣をMeCNで洗浄し、橙色粉末として1,4−ビス(1’−ヘキシル−4,4,−ビピリジニウム−1−イル)ブタンテトラヨージド(3.32g、79%)を得た。
δΗ(400MHz,DMSO−d6,)9.50−9.20(8H,m),8.90−8.70(8H,m),4.77(4H,br.s),4.70(4H,t,J=7.6Hz),2.10(4H,br.s),1.99(4H,br.s),1.33(12H,br.s),1.00−0.80(6H,m).
実施例12
化合物2−9の合成:1’1’’’−[1,2−フェニレンビス(メチレン)]ビス{1−(2−シアノフェニル)−[4,4’−ビピリジン]−1,1’−ジイウム}テトラキス(テトラフルオロボレート)
1−(2−シアノフェニル)−4,4’−ビピリジニウムテトラフルオロボレート(2g、5.8ミリモル)と1,2−ビス(ブロモメチル)ベンゼン(0.61g、2.3ミリモル)をMeCN(40mL)に溶かした溶液を16時間加熱還流し、冷却し、濾過した。生成物をMeCN(2×5mL)で洗浄し、空気乾燥した。得られた固体及びNaBF4(2.64g、30ミリモル)を、水(100mL)とMeOH(100mL)中で溶解するまで加熱し、セライトを介して濾過し、冷却し、溶媒を減少させた。得られた沈殿物を濾過し、水(2×30mL)で洗浄し、空気乾燥し、クリーム色粉末として化合物2−9(1.41g、63%)を得た。
δΗ(400MHz,DMSO−d6)9.83(4H,d,J=6.5Hz),9.47(4H,d,J=6.5Hz),9.11(4H,d,J=6.5Hz),9.00(4H,d,J=6.5Hz),8.38(2H,d,J=7.6Hz),8.10−8.25(4H,m),8.03(2H,t,J=7.2Hz),7.50−7.65(2H,m),7.25−7.35(2H,m),6.24(s,4H).
δF(376MHz,DMSO−d6)−148.0−−148.2(br.s).
実施例13
化合物2−10の合成:1’1’’’−[キノキサリン−2,3−ジイルビス(メチレン)]ビス{1−(2−シアノフェニル)−[4,4’−ビピリジン]−1,1’−ジイウム}テトラキス(テトラフルオロボレート)
1−(2−シアノフェニル)−4,4’−ビピリジニウムテトラフルオロボレート(2.73g、7.9ミリモル)と2,3−ビス(ブロモメチル)キノキサリン(1.00g,3.2ミリモル)をMeCN(40mL)に溶かした溶液を16時間加熱還流し、冷却した。生成物を濾過し、MeCN(2×5mL)で洗浄し、空気乾燥した。温水(40mL)及びMeOH(40mL)に溶かした緑色固体を水(40mL)に溶かしたNaBF4(4.18g、38ミリモル)に撹拌しながら滴下した。混合物を溶解するまで加熱し、セライトを介して濾過し、冷却した後、濾過し、水(2×10mL)で洗浄し、空気乾燥した。残渣を温水−MeOHから結晶化し、濾過し、MeOH(5mL)で洗浄し、空気乾燥し、淡黄色粉末として化合物2−10(1.47g、48%)を得た。
δΗ(400MHz,DMSO−d6)9.60(4H,d,J=6.8Hz),9.44(4H,d,J=6.8Hz),9.01(4H,d,J=6.8Hz),8.93(4H,d,J=6.5Hz),8.26(2H,d,J=7.5Hz),8.00−8.20(6H,m),7.80−7.95(4H,m)及び6.72(4H,m).
δF(376MHz,DMSO−d6)−151.1−−151.2(br.s).
実施例14
化合物2−11の合成:1’,1’’’−[キノキサリン−2,3−ジイルビス(メチレン)]ビス{1−(2−(トリフルオロメトキシ)フェニル)−[4,4’−ビピリジン]−1,1’−ジイウム}テトラキス(テトラフルオロボレート)
1−(2−トリフルオロメトキシフェニル)−4,4’−ビピリジニウムテトラフルオロボレート(3.07g、7.9ミリモル)と2,3−ビス(ブロモメチル)キノキサリン(1.00g、3.2ミリモル)をMeCN(40mL)に溶かした溶液を16時間加熱還流した後、冷却した。生成物を濾過し、MeCN(2×5mL)で洗浄し、空気乾燥した。温水(30mL)とMeOH(20mL)に溶かした緑色固体を水(30mL)に溶かしたNaBF4(4.18g、38ミリモル)に撹拌しながら滴下した。0.5時間撹拌を継続し、得られた沈殿物を濾過し、水(2×10mL)で洗浄した。残渣を温水−MeOHから結晶化し、濾過し、MeOH(5mL)で洗浄し、空気乾燥し、黄緑色プレートとして化合物2−11(2.25g、67%)を得た。
δΗ(400MHz,DMSO−d6)9.81(4H,d,J=6.5Hz),9.50(4H,d,J=6.5Hz),9.15(4H,d,J=6.5Hz),9.11(4H,d,J=6.5Hz),8.13(2H,d,J=7.7Hz),7.80−8.05(10H,m)及び6.65(4H,s).
δF(376MHz,DMSO−d6)−57.03(s)及び−148.1_−148.2(br.s).
実施例15
化合物2−12の合成:1’,1’’’−[キノキサリン−2,3−ジイルビス(メチレン)]ビス{1−(2−イソプロピルフェニル)−[4,4’−ビピリジン]−1,1’−ジイウム}テトラキス(テトラフルオロボレート)
1−(2−イソプロピルフェニル)−4,4’−ビピリジニウムテトラフルオロボレート(2.07g,7.9ミリモル)と2,3−ビス(ブロモメチル)キノキサリン(1.00g,3.2ミリモル)をMeCN(40mL)に溶かした溶液を、16時間加熱還流し、冷却した。生成物を濾過し、MeCN(2×5mL)で洗浄し、空気乾燥した。黄色固体及びNaBF4(4.18g、38ミリモル)を水(20mL)及びMeOH(10mL)中に加熱して溶解させ、冷却した。生成物を濾過し、水(2×5mL)、アセトン(4mL)で洗浄し、空気乾燥し、淡黄色粉末として化合物2−12(1.28g、37%)を得た。
δΗ(400MHz,DMSO−d6)9.69(4H,d,J=6.5Hz),9.49(4H,d,J=6.5Hz),9.00−9.20(8H,m),7.70−7.95(10H,m),7.55−7.65(2H,m),6.51(4H,s),2.48(2H,m)及び1.24(12H,t,J=7.2Hz).
δF(376MHz,DMSO−d6)−148.1−148.2(br.s).
実施例16
化合物2−13の合成:1’,1’’’−[ピリジン−2,6−ジイルビス(メチレン)]ビス{1−(2−イソプロピルフェニル)−[4,4’−ビピリジン]−1,1’−ジイウム}テトラキス(テトラフルオロボレート)
2,6−ビス(ブロモメチル)ピリジン
ピリジン−2,6−ジカルボン酸ジメチル(5.5g、28ミリモル)を乾燥EtOH(85mL)に溶かした溶液に、水素化ホウ素ナトリウム(5g,131ミリモル)を0℃、N2下で撹拌しながら数回に分けて添加した。得られた混合物を室温まで温め、3時間撹拌した後、10時間加熱還流した。その後、混合物を冷却し、溶媒を減圧下で除去した。水(200mL)を添加し、得られた溶液をEtOAc(20×50mL)で抽出した。乾燥(Na2SO4)後、EtOAcを溶離液として用いてシリカを介して抽出物を濾過し、溶媒を減圧下で除去した。残渣をEt2Oで粉末化し、空気乾燥した。得られた無色粉末をHBr(48%水溶液、15mL)に溶解させ、2時間加熱還流した後、冷却し、0℃で濃NaOH水溶液で中和した。生成物を濾過し、水(2×10mL)で洗浄し、空気乾燥し、無色粉末として2,6−ビス(ヒドロキシメチル)ピリジン(1.39g、19%)を得た。
1−(2−イソプロピルフェニル)−4,4’−ビピリジニウムテトラフルオロボレート(5.74g、15.8ミリモル)をMeCN(50mL)に溶かした還流溶液に、2,6−ビス(ブロモメチル)ピリジン(0.70g、2.6ミリモル)をMeCN(50mL)に溶かした溶液をN2下で撹拌しながら2時間にわたって滴下した。加熱を2時間を超えて続けた後、溶液を冷却し、撹拌しながらゆっくりとEt2Oで希釈した。得られた沈殿物をデカンテーションで分離し、ガム状の残渣が残った。残渣をMeCNに溶解させ、アセトンを添加した。得られた沈殿物を濾過し、アセトンで洗浄し、乾燥し、明黄色の吸湿性固体を得た。その固体を水(20mL)に溶解させ、水(50mL)に溶かした溶液に、NaBF4(5.81g、52.8ミリモル)を撹拌しながら滴下した。得られた沈殿物を加熱して溶解させた後、溶液を迅速に撹拌しながら冷却した。沈殿物を濾別した後、温水(10mL)に溶解させ、迅速に撹拌しながら再び冷却し、沈殿生成物を濾過し、水(5mL)で洗浄し、空気乾燥し、無色粉末として化合物2−13(0.80g、30%)を得た。
δΗ[400MHz,(CD3)2CO]:9.30−9.15(8H,m),8.79(4H,d,J=6.8Hz),8.73(4H,d,J=6.8Hz),8.13(1H,t,J=8.0Hz),8.85−8.72(6H,m),8.64−8.52(4H,d,J=8.0Hz),6.05(4H,s),2.60(2H,2×sept.,J=6.8Hz),1.25(12H,d,J=6.8Hz)
δF(376MHz,(CD3)2CO]:151.75(s)及び151.62(t,J=1Hz)
δ13C[100.6MHz,(CD3)2CO]:152.19,151.27,150.71,146.89,146.46,142.99,140.49,140.10,132.53,127.92,127.69,127.27,127.11,125.50,124.11,64.60,27.74,22.92.
実施例17
化合物3−1の合成:1,1’−ビス−(3−tert−ブチルフェニル)−4,4’−ビピリジニウムビス(テトラフルオロボレート)
3−tert−ブチルアニリン(4.78g、32ミリモル)を水(50mL)に溶かした還流溶液に、1,1’−ビス−(2,4−ジニトロフェニル)−4,4’−ビピリジニウムジクロリド(3g、5.3ミリモル)を温水(50mL)に溶かした溶液を滴下した。得られた混合物を2時間加熱還流し、冷却し、CHCl3(3×50mL)で洗浄し、溶媒を減圧下で除去した。残渣をMeOHに溶解させ、アセトンを添加した。得られた沈殿物を濾過し、アセトンで洗浄し、淡黄色粉末として直接次の段階で用いる1,1’−ビス−(3−tert−ブチルフェニル)−4,4’−ビピリジニウムジクロリド(1.85g、70%)を得た。
δΗ(400MHz,DMSO−d6)9.39(4H,d,J=6.4Hz),8.79(4H,d,J=6.4Hz),7.80−7.95(4H,m),7.57−7.75(4H,m)及び1.39(18H,s).
δF(376MHz,DMSO−d6)−155.4−−155.8(bs).
実施例18
化合物3−2の合成:1−(2−トリフルオロメトキシフェニル)−1’−(2−イソプロピルフェニル)−4,4’−ビピリジニウムビス(テトラフルオロボレート)
1−(2−イソプロピルフェニル)−4,4’−ビピリジニウムテトラフルオロボレート(4g、11ミリモル)と2,4−ジニトロフェニルp−トルエンスルホネート(6.94g、20.5ミリモル)をMeCN(40mL)に溶かした溶液を、2日間加熱還流した。溶媒を減少させ、残渣を0℃まで急冷し、得られた沈殿物を濾過し、冷MeCN(5mL)で洗浄し、空気乾燥し、1−(2,4−ジニトロフェニル)−1’−(2−イソプロピルフェニル)−4,4’−ビピリジニウムジトシレート(3.00g、35%)を得た。溶媒を除去し、残渣を水−CHCl3(200mL、1:1)に溶解させ、濃HCl(0.8mL)を添加し、混合物を濾過した。残渣を温MeOH−水(80mL、1:1)に溶解させ、NaBF4(7.47g、68ミリモル)を水(100mL)に溶かした溶液中で迅速に撹拌しながら濾過した。0.5時間後、得られた沈殿物を濾過し、水(2×10mL)で洗浄し、空気乾燥し、淡黄色粉末として1−(2,4−ジニトロフェニル)−1’−(2−イソプロピルフェニル)−4,4’−ビピリジニウムビス(テトラフルオロボレート)(2.72g、40%)を得た。
δΗ(300MHz,CD3OD)9.56(2H,d,J=6.9Hz),9.42(2H,d,J=6.9Hz),8.96(2H,d,J=6.9Hz),8.91(2H,d,J=6.9Hz),7.91−9.10(2H,m),7.73−7.89(4H,m),7.52−7.70(2H,m),2.64(1H,m),1.30(6H,d,J=6.8Hz).
δF(282MHz,CD3OD)−59.49(s),−154.05−154.15(br.s).
実施例19
化合物3−3の合成:1−(2−トリフルオロメトキシフェニル)−1’−(4−トリフルオロメトキシフェニル)−4,4’−ビピリジニウムビス(テトラフルオロボレート)
1−(2−トリフルオロメトキシフェニル)−4,4’−ビピリジニウムテトラフルオロボレート(2.30g、5.7ミリモル)と2,4−ジニトロフェニルp−トルエンスルホネート(2.87g、8.5ミリモル)をMeCN(40mL)に溶かした溶液を16時間加熱還流した。溶媒を減圧下で除去し、残渣を水(200mL)に溶解させ、CHCI3(3×50mL)で洗浄した。溶媒を減圧下で除去し、残渣をEtOHで洗浄し、空気乾燥し、緑黄色粉末として1−(2,4−ジニトロフェニル)−1’−(2−トリフルオロメトキシフェニル)−4,4’−ビピリジニウムビス(テトラフルオロボレート)(1.42g、38%)を得た。
δΗ(300MHz,CD3OD)9.45−9.65(4H,m),8.80−9.03(4H,m),7.66−8.17(8H,m).
δF(282MHz,CD3OD)−59.49(s),−59.52(s),−154.00−154.10(br.s).
実施例20
化合物3−4の合成:1,1’−ビス−(2−シアノフェニル)−4,4’−ビピリジニウムビス(テトラフルオロボレート)
2−アミノベンゾニトリル(10.1g、85.6ミリモル)を水(150mL)に溶かした還流溶液に、1,1’−ビス−(2,4−ジニトロフェニル)−4,4’−ビピリジニウムジクロリド(8g、14.3ミリモル)を温水(150mL)に溶かした溶液を滴下した。得られた混合物を16時間加熱還流した後、冷却した。生成物を濾過し、CHCl3(3×100mL)で洗浄し、溶媒を減圧下で除去した。残渣をアセトンで洗浄し、黄褐色粉末として1,1’−ビス−(2−シアノフェニル)−4,4’−ビピリジニウムジクロリド(5.96g、97%)を得た。
δΗ(300MHz,DMSO−d6)9.85(4H,d,J=6.7Hz),9.22(4H,d,J=6.7Hz),8.36(2H,d,J=7.5Hz),8.10−8.25(4H,m),8.96−8.08(2H,m).
δF(282MHz,DMSO−d6)−148.2−−148.4(br.s).
実施例21
化合物3−5の合成:1−(3−シアノフェニル)−1’−(2−イソプロピルフェニル)−4,4’−ビピリジニウムビス(テトラフルオロボレート)
1−(2,4−ジニトロフェニル)−1’−(2−イソプロピルフェニル)−4,4’−ビピリジニウムビス(テトラフルオロボレート)(1.5g、2.4ミリモル)と3−アミノベンゾニトリル(0.57g、4.8ミリモル)をMeOH−EtOH(40mL、1:1)に溶かした溶液を3時間加熱還流し、冷却し、溶媒を減圧下で除去した。残渣を温EtOHで粉末化し、冷却し、濾過し、淡黄色粉末として化合物3−5(1.25g、93%)を得た。
δΗ(300MHz,CD3OD)9.52(2H,d,J=6.9Hz),9.33(2H,d,J=6.9Hz),8.84−8.97(4H,m),8.36−8.43(1H,m),8.17−8.32(2H,m),7.98−8.08(1H,t,J=8Hz),7.74−7.84(2H,m),7.55−7.67(2H,m),2.61(1H,m),1.28(6H,d,J=6.8Hz).
δF(282MHz,CD3OD)−152.33−152.45(br.s).
実施例22
化合物3−6の合成:1−(2−tert−ブチルフェニル)−1’−フェニル−4,4’−ビピリジニウムビス(テトラフルオロボレート)
1−(2,4−ジニトロフェニル)−4,4’−ビピリジニウムクロリド(5g、13.9ミリモル)と2−tert−ブチルアニリン(6.23g、41.9ミリモル)を水(150mL)に溶かした溶液を、7日間加熱還流した。冷却後、混合物を濾過し、CHCl3(3×100mL)で洗浄した。溶媒を減圧下で除去し、残渣をアセトンで洗浄し、淡黄色粉末として1−(2−tert−ブチルフェニル)−4,4’−ビピリジニウムクロリド(3.14g、69%)を得た。
δΗ(300MHz,CD3OD−D2O)9.43−9.53(4H,m),8.85−8.92(4H,m),7.90−7.98(3H,m),7.82−7.88(3H,m),7.77(1H,t,J=7.5Hz),7.58(1H,t,J=7.9Hz),7.47(1H,t,J=7.9Hz)1.26(9H,s).
δF(282MHz,CD3OD−D2O)−152.34−152.44(br.s).
実施例23
化合物3−7の合成:1,1’−ビス−(2−tert−ブチルフェニル)−4,4’−ビピリジニウムビス(テトラフルオロボレート)
2−tert−ブチルアニリン(9.56g、64.2ミリモル)を水(100mL)に溶かした還流溶液に、1,1’−ビス−(2,4−ジニトロフェニル)−4,4’−ビピリジニウムジクロリド(6g、10.7ミリモル)を温水(100mL)に溶かした溶液を滴下した。得られた混合物を20日間加熱還流し、冷却した後、CHCl3(2×50mL)で洗浄した。溶媒を減圧下で除去し、残渣をMeOHに溶解させ、EtOAcで沈殿させ、淡黄色粉末として1,1’−ビス−(2−tert−ブチルフェニル)−4,4’−ビピリジニウムジクロリド(2.30g、44%)を得た。
δΗ(400MHz,DMSO−d6)9.56(4H,d,J=6.9Hz),8.89(4H,d,J=6.9Hz),7.94(2H,dd,J=1.1,8.2Hz),7.76(2H,dd,J=1.1,8.2Hz),7.42−7.62(4H,m),1.28(18H,s).
実施例24
化合物3−8の合成:1−(2−シアノフェニル)−1’−(2−イソプロピルフェニル)−4,4’−ビピリジニウムビス(テトラフルオロボレート)
1−(2,4−ジニトロフェニル)−1’−(2−イソプロピルフェニル)−4,4’−ビピリジニウムビス(テトラフルオロボレート)(1.5g、2.4ミリモル)と2−アミノベンゾニトリル(5.7g、48ミリモル)をイソプロパノール(40mL)に溶かした溶液を2日間加熱還流した。冷却後、溶媒を減圧下で除去した。残渣を温EtOHで粉末化し、冷却し、濾過して、無色粉末として化合物3−8(1.08g、81%)を得た。
δΗ(300MHz,CD3OD)9.577(2H,d,J=6.9Hz),9.33(2H,d,J=6.9Hz),9.00(2H,d,J=6.9Hz),8.91(2H,d,J=6.9Hz),8.00−8.30(4H,m),7.72−7.88(2H,m),7.54−7.67(2H,m),2.61(1H,m),1.28(6H,d,J=6.8Hz).
δF(282MHz,CD3OD)−152.79−152.90(br.s).
実施例25
本発明の化合物の酸化還元電位及び吸収スペクトルの評価
3つの電極を用いてサイクリックボルタンメトリー法により、化合物の酸化還元電位を測定する。
1つの白金作用電極
1つの白金補助電極又は対電極
1つの白金基準電極(アセトニトリルに溶かした0.01MのAgNO3+0.1MのTBAP(過塩素酸テトラブチルアンモニウム)からなる溶液に浸されている)
である。
Claims (18)
- 式1
Zは、
アルキレン;
シクロアルキレン;及び
式−R7−Y−R8(ここで、
R7及びR8は、各々独立して、単結合、アルキレン及びシクロアルキレンから選択され、及び
Yは、アリーレン、シクロアルキレン、ヘテロアリーレン、アリーレン−アリーレン又はアリーレン−CR’R’’−アリーレンから選択され、R’及びR’’はそれらが結合している炭素と一緒に炭素環基を形成する)の2価の基から選択され、
前記アルキレン、シクロアルキレン、アリーレン、ヘテロアリーレン、及び炭素環基は、ハロゲン、アルキル、アルコキシ、アルキルチオ、ヒドロキシアルキル、アシルオキシ、シクロアルキル、アリール、置換アリール、アリールオキシ、ヘテロアリール及び置換ヘテロアリールから選択される1つ又は複数の置換基で置換されてもよく;mは、0又は1であり;
R1及びR2は、
Yがアリーレン−アリーレン又はアリーレン−アルキレン−アリーレンである場合、R1及びR2は、フェニルでない;mが0である場合、R1及びR2は、各々独立して、任意選択により置換されるフェニル基から選択され、R1及びR2の少なくとも1つは、置換フェニル基から選択され、R1及びR2は、各々独立して、置換フェニル基から選択されるのが好ましい
とする条件で
各々独立して、C6〜C7アルキル、及び任意選択により置換されたフェニルから選択され;
R3、R4、R5及びR6は、各々独立して、H、アルキル、アルコキシ、アルキルチオ、ハロアルキル、ハロアルコキシ、ハロアルキルチオ、ポリアルキレンオキシ、アルコキシカルボニル、アリール、置換アリール、ヘテロアリール及び置換ヘテロアリールから選択され、ここで、アルキル基は、アルコキシ、シクロアルキル、アリール、置換アリール、ヘテロアリール及び置換ヘテロアリールから選択される1つ又は複数の置換基で置換されてもよく;
n、p、q及びrは、各々独立して0〜4の整数であり、n、p、q及びrが2以上である場合、各R3、各R4、各R5又は各R6は、同一でも異なってもよく、及び
X−は、対イオンである]の化合物。 - Zが、C1〜C12アルキレン、アリール置換のC1〜C12アルキレン、フェニレン、ナフチレン、(C1〜C4アルキレン)−フェニレン−(C1〜C4アルキレン)、(C1〜C4アルキレン)−ナフチレン−(C1〜C4アルキレン)、キノキサリン−2,3−ジイル、(C1〜C4アルキレン)−キノキサリン−2,3−ジイル−(C1〜C4アルキレン)、フェニレン−フェニレン、(C1〜C4アルキレン)−フェニレン−フェニレン−(C1〜C4アルキレン)及びフェニレン−フルオレニレン−フェニレンから選択され、Zが、−CH2−、−(CH2)2−、−(CH2)3−、−(CH2)4−、−(CH2)5−、−CH2−CH(CH3)−CH2−、−CH2−CH(CH2フェニル)−CH2−、−(CH2)2−CH(CH3)−CH2−、−(CH2)3−CH(CH3)−CH2−、−(CH2)2−CH(CH3)−(CH2)2−、
- R3、R4、R5及びR6が、各々独立して、C1〜C4アルキル、C1〜C4アルコキシカルボニル、アルカノイル、アロイル、ニトリル、アルキルスルホニル、アリールスルホニル、アリール及びヘテロアリールから選択され、前記アリール及びヘテロアリールが、C1〜C4アルキル及びC1〜C4ハロアルキルから選択される1つ又は複数の置換基により置換されてもよく、R3、R4、R5及びR6が、各々独立して、メチル、エトキシカルボニル、フェニル、p−メチルフェニル及びp−トリフルオロメチルフェニルから選択されるのが好ましい請求項1又は2に記載の化合物。
- 前記対イオンX−が、ハライド、テトレフルオロボレート、テトラフェニルボレート、ヘキサフルオロホスフェート、ニトレート、メタンスルホネート、トリフルオロメタンスルホネート、トルエンスルホネート、ヘキサクロロアンチモネート、ビス(トリフルオロメタンスルホニル)イミド、パークロレート、アセテート及びスルフェートから選択される請求項1〜3のいずれか1項に記載の化合物。
- mが、1であり、且つR1及びR2が、C6〜C7アルキル、好ましくはC6H13、さらに好ましくはn−C6H13である請求項1〜4のいずれか1項に記載の化合物。
- R1及びR2が、独立して、式(II)
H、ハロゲン、シアノ、ニトロ、アルキル、ハロアルキル、ハロアルコキシ、(ハロアルコキシ)アルキル、アリールアルキル、シクロアルキル、(シクロアルキル)アルキル及び(ヘテロシクロアルキル)アルキル、アルケニル、アルキニル、アリル、ビニル、アリール、置換アリール、ヘテロアリール、置換ヘテロアリール、−N(アリール)2、−N(アリール)CO(アリール)、−CO−アリール及び−CO−置換アリール;
−OR9、−SR9、−S(O)R9、−S(O2)R9、−S(O2)NR9R10、−NR9R10、−NR9COR10、−NR9CO(アリール)、−NR9アリール、−CH2OR9、−CH2SR9、−CH2R9、−CO−R9及び−CO2R10(ここで、R9及びR10は、独立してH、アルキル、ハロアルキル、アリールアルキル、シクロアルキル、シクロアルキルアルキル及びヘテロシクロアルキルアルキルから選択される);
−S(O2)NR11R12及び−NR11R12(ここで、R11及びR12は、それらが結合している窒素原子と一緒に、窒素原子に加えて、酸素、窒素及び硫黄から選択されるヘテロ原子をさらに1個含んでもよく、ハロゲン、−R9、−OR9、及び−NR9R10から選択される同一の又は異なる1個又は2個の基により任意選択により置換されてもよく、R9及びR10は、上に定義した通りである、飽和5〜7員のヘテロシクロアルキルを形成する);
−V−W−R13(式中、
Vは、酸素、−N(R9)−、硫黄、−S(O)−及び−S(O2)−(ここで、R9は上に定義した通りである)から選択され
Wは、アルキレンであり、ハロゲン及びアルコキシから選択される基により置換されてもよく;
R13は、−OR9、−NR9(アルキル)及び−SR9(ここで、R9は上に定義した通りである)から選択され;
OC(O)−R14{ここで、R14は、アルキル、ハロアルキル、アルケニル、−W−R13、及びアリール基(ハロゲン、−R9、−OR9、−SR9、−NR9R10、−NR11R12、−CO−R9、−CO2R9(ここで、R9、R10、R11、R12、R13及びWは、上に定義した通りである)から選択される1〜4個の基により置換されてもよい)から選択される}
から選択される]の任意選択により置換されるフェニル基から選択される請求項1〜4のいずれか1項に記載の化合物。 - Ra、Rb、Rc、Rd及びReが、各々独立してH、シアノ、ハロゲン、ニトロ、ヒドロキシル、アルキル、好ましくはC4〜C12アルキル、ハロアルキル、アルコキシ、ハロアルコキシ、アルコキシカルボニル、シクロアルキル、アリル、アリール、及びヘテロアリールから選択される請求項6に記載の化合物。
- Reが、Hであり、Ra、Rb、Rc、及びRdの少なくとも1つが、Hでなく、Ra及びRbの少なくとも1つが、Hでないのが好ましい請求項6又は7に記載の化合物。
- 請求項1〜9に定義した少なくとも1種の化合物を含むエレクトロクロミック組成物。
- 前記組成物が、液体、メソ形又はゲルのホスト媒体を含む請求項10に記載のエレクトロクロミック組成物。
- 前記液体又はメソ形のホスト媒体が、有機溶媒、液晶、ポリマー、液晶ポリマー及びそれらの混合物からなる群から選択される請求項11に記載のエレクトロクロミック組成物。
- 請求項1〜9のいずれか1項に記載の化合物又は請求項10〜12のいずれか1項に記載の組成物を含むエレクトロクロミック素子。
- 前記素子が、機械的に安定な環境において前記化合物又は前記組成物を保持するための機構を含む請求項13に記載のエレクトロクロミック素子。
- 前記素子が、前記化合物又は前記組成物を収容するためにその間にギャップを有する1対の対向した基材と、互いに隣接する前記の1対の基材を保持するためのフレームとを含む請求項14に記載のエレクトロクロミック素子。
- 前記素子が、それらの表面に平行な方向に並置された少なくとも1つの透明なセルの配置を備える光学部品を含み、各セルが、強固に近接されており、前記化合物又は前記組成物を含有する請求項14に記載のエレクトロクロミック素子。
- 前記エレクトロクロミック素子が、光学物品、好ましくは光学レンズ又は光学フィルタ、ウインドー、とりわけ航空機用ウインドー、サンバイザ、ミラー及びディスプレー、さらに好ましくは光学レンズから選択される光学物品、最も好ましくは眼用レンズから選択される光学物品から選択される請求項11〜16のいずれか1項に記載のエレクトロクロミック素子。
- 式(Ia)
H、ハロゲン、シアノ、ニトロ、アルキル、ハロアルキル、ハロアルコキシ、(ハロアルコキシ)アルキル、アリールアルキル、シクロアルキル、(シクロアルキル)アルキル及び(ヘテロシクロアルキル)アルキル、アルケニル、アルキニル、アリル、ビニル、アリール、置換アリール、ヘテロアリール、置換ヘテロアリール、−N(アリール)2、−N(アリール)CO(アリール)、−CO−アリール及び−CO−置換アリール;
−OR9、−SR9、−S(O)R9、−S(O2)R9、−S(O2)NR9R10、−NR9R10、−NR9COR10、−NR9CO(アリール)、−NR9アリール、−CH2OR9、−CH2SR9、−CH2R9、−CO−R9及び−CO2R10(ここで、R9及びR10は、独立してH、アルキル、ハロアルキル、アリールアルキル、シクロアルキル、シクロアルキルアルキル及びヘテロシクロアルキルアルキルから選択される);
−S(O2)NR11R12及び−NR11R12(ここで、R11及びR12は、それらが結合している窒素原子と一緒に、窒素原子に加えて、酸素、窒素及び硫黄から選択されるヘテロ原子をさらに1個含んでもよく、ハロゲン、−R9、−OR9、及び−NR9R10から選択される同一の又は異なる1個又は2個の基により任意選択により置換されてもよく、R9及びR10は、上に定義した通りである、飽和5〜7員のヘテロシクロアルキルを形成する);
−V−W−R13(式中、
Vは、酸素、−N(R9)−、硫黄、−S(O)−及び−S(O2)−(ここで、R9は上に定義した通りである)から選択され
Wは、アルキレンであり、ハロゲン及びアルコキシから選択される基により置換されてもよく;
R13は、−OR9、−NR9(アルキル)及び−SR9(ここで、R9は上に定義した通りである)から選択され;
OC(O)−R14{ここで、R14は、アルキル、ハロアルキル、アルケニル、−W−R13、及びアリール基(ハロゲン、−R9、−OR9、−SR9、−NR9R10、−NR11R12、−CO−R9、−CO2R9(ここで、R9、R10、R11、R12、R13及びWは、上に定義した通りである)から選択される1〜4個の基により置換されてもよい)から選択される}
から選択される]の化合物を調製する方法であって
2種のビピリジニウム塩(1)又は(1’)を、離脱基がスルホネート及びカルボキシレートから選択される二官能性アルキル化剤ZL2でアルキル化する工程(i)と、所望の対イオンX−の水溶液でのアニオン交換の工程(ii)とを備える方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2018229306A JP6892852B2 (ja) | 2013-09-17 | 2018-12-06 | エレクトロクロミック性の単核及び2核ビオロゲン並びにそれらを含有する光学物品 |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP13184771.7A EP2848667B1 (en) | 2013-09-17 | 2013-09-17 | Electrochromic single and two-core viologens and optical articles containing them |
| EP13184771.7 | 2013-09-17 | ||
| PCT/EP2014/069737 WO2015040033A2 (en) | 2013-09-17 | 2014-09-16 | Electrochromic single and two-core viologens and optical articles containing them |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018229306A Division JP6892852B2 (ja) | 2013-09-17 | 2018-12-06 | エレクトロクロミック性の単核及び2核ビオロゲン並びにそれらを含有する光学物品 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2016538325A true JP2016538325A (ja) | 2016-12-08 |
| JP6751022B2 JP6751022B2 (ja) | 2020-09-02 |
Family
ID=49223596
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016543383A Active JP6751022B2 (ja) | 2013-09-17 | 2014-09-16 | エレクトロクロミック性の単核及び2核ビオロゲン並びにそれらを含有する光学物品 |
| JP2018229306A Active JP6892852B2 (ja) | 2013-09-17 | 2018-12-06 | エレクトロクロミック性の単核及び2核ビオロゲン並びにそれらを含有する光学物品 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018229306A Active JP6892852B2 (ja) | 2013-09-17 | 2018-12-06 | エレクトロクロミック性の単核及び2核ビオロゲン並びにそれらを含有する光学物品 |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US9823534B2 (ja) |
| EP (1) | EP2848667B1 (ja) |
| JP (2) | JP6751022B2 (ja) |
| KR (1) | KR102347082B1 (ja) |
| CN (1) | CN105555911B (ja) |
| AU (1) | AU2014323167B2 (ja) |
| BR (1) | BR112016005305B1 (ja) |
| WO (1) | WO2015040033A2 (ja) |
Families Citing this family (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ES2662377T3 (es) | 2013-09-17 | 2018-04-06 | Essilor International | Composición electrocrómica |
| EP2848667B1 (en) | 2013-09-17 | 2019-04-10 | Essilor International | Electrochromic single and two-core viologens and optical articles containing them |
| ES2661512T3 (es) | 2013-09-17 | 2018-04-02 | Essilor International | Composición electrocrómica |
| EP2848668B1 (en) | 2013-09-17 | 2019-01-09 | Essilor International | Electrochromic two-core viologen derivatives and optical articles containing them |
| US10294415B2 (en) | 2014-06-09 | 2019-05-21 | iGlass Technology, Inc. | Electrochromic composition and electrochromic device using same |
| US10344208B2 (en) | 2014-06-09 | 2019-07-09 | iGlass Technology, Inc. | Electrochromic device and method for manufacturing electrochromic device |
| CN107924098A (zh) | 2015-07-10 | 2018-04-17 | 依视路国际公司 | 具有改善的振幅变化单元的眼科装置 |
| CN108474988B (zh) * | 2015-10-07 | 2021-08-17 | 伊格拉斯科技有限公司 | 电致变色组合物和使用其的电致变色装置 |
| EP3386599B1 (en) | 2015-12-10 | 2021-07-21 | Emory University | Polymers of polyoxometalates and hydroxy-terminated monomer units and uses in degrading noxious agents |
| EP3345981B1 (en) | 2017-01-09 | 2020-09-09 | Essilor International | Electrochromic compounds and optical articles containing them |
| KR102170391B1 (ko) * | 2017-02-10 | 2020-10-27 | 주식회사 엘지화학 | 피리딘 염 화합물, 이를 이용한 유기 발광 소자 및 이의 제조방법 |
| EP3367160B1 (en) | 2017-02-22 | 2020-12-16 | Essilor International | Spectacle lens comprising an activable optical filter |
| EP3418795A1 (en) | 2017-06-22 | 2018-12-26 | Essilor International | Multifunctional device for an ophthalmic lens |
| EP3923064A1 (en) | 2020-06-12 | 2021-12-15 | Essilor International | Electrochromic solution |
| CN111793062B (zh) * | 2020-07-30 | 2022-09-27 | 南京邮电大学 | 一类新型非对称紫精化合物及其制备方法与应用 |
| EP3985046A1 (en) | 2020-10-15 | 2022-04-20 | Essilor International | Crosslinked gel formulation |
| EP4016178A1 (en) | 2020-12-16 | 2022-06-22 | Essilor International | Multilayer structure, electrochromic cell and ophthalmic device incorporating it, and methods for manufacturing the same |
| EP4020066A1 (en) | 2020-12-23 | 2022-06-29 | Essilor International | Optical device forming an electrochromic ophthalmic lens, spectacle glasses incorporating it and method for manufacturing the same |
| EP4194935A1 (en) | 2021-12-10 | 2023-06-14 | Essilor International | Electro-active ophthalmic device satisfying a prescription for power correction(s), manufacturing method and use of a semi-finished hybrid lens |
Citations (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH11106376A (ja) * | 1997-10-01 | 1999-04-20 | Fuji Photo Film Co Ltd | ビオローゲン誘導体の製造方法 |
| US6037471A (en) * | 1997-04-02 | 2000-03-14 | Gentex Corporation | Electrochromic compounds |
| JP2001519922A (ja) * | 1997-04-02 | 2001-10-23 | ジェンテクス・コーポレーション | 予め選択された色を生ずることのできる改良されたエレクトロクロミック媒体 |
| JP2003128654A (ja) * | 2001-10-26 | 2003-05-08 | Fuji Photo Film Co Ltd | 4,4’−ビピリジニウム誘導体の製造方法 |
| JP2003168246A (ja) * | 2001-11-29 | 2003-06-13 | Fuji Photo Film Co Ltd | 光情報記録媒体 |
| JP2006181908A (ja) * | 2004-12-28 | 2006-07-13 | Fuji Photo Film Co Ltd | 光情報記録媒体及び光情報記録方法 |
| JP2008504583A (ja) * | 2004-07-02 | 2008-02-14 | エシロール アンテルナシオナル (コンパニー ジェネラレ ドプテイク) | 透明な光学素子の製造方法、この製造方法に関わる光学部品および得られた光学素子 |
| CN102234505A (zh) * | 2010-04-29 | 2011-11-09 | 比亚迪股份有限公司 | 一种电致变色材料及其制备方法、及防眩目汽车后视镜 |
| WO2011142329A1 (ja) * | 2010-05-13 | 2011-11-17 | 協和発酵ケミカル株式会社 | 錯化合物およびそれを含有する光記録媒体 |
| WO2012008468A1 (ja) * | 2010-07-14 | 2012-01-19 | 協和発酵ケミカル株式会社 | 錯化合物およびそれを含有する光記録媒体 |
| JP2012505426A (ja) * | 2008-10-09 | 2012-03-01 | エシロル アンテルナショナル(コンパーニュ ジェネラル ドプテーク) | 透明電気活性システム |
Family Cites Families (28)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB1514466A (en) * | 1974-06-21 | 1978-06-14 | Ici Ltd | Preparation of bipyridilium compounds |
| US4116535A (en) * | 1976-05-10 | 1978-09-26 | U.S. Philips Corporation | Picture display cell with memory effect |
| JPS5437080A (en) * | 1977-08-30 | 1979-03-19 | Nippon Chem Ind Co Ltd:The | Display material |
| JPS5554381A (en) * | 1978-10-18 | 1980-04-21 | Hitachi Ltd | Electrochromic material for display device |
| JPS5757779A (en) | 1980-09-22 | 1982-04-07 | Mitsubishi Electric Corp | Electrochromic display composition |
| JPS61107323A (ja) * | 1984-10-31 | 1986-05-26 | Sony Corp | エレクトロクロミツク表示装置 |
| US5278693A (en) | 1992-01-13 | 1994-01-11 | Gentex Corporation | Tinted solution-phase electrochromic devices |
| US5366940A (en) | 1994-01-28 | 1994-11-22 | Bausch & Lomb Incorporated | Transparent, fixed tint glass lenses |
| US5929093A (en) * | 1996-06-13 | 1999-07-27 | Mayo Foundation For Medical Education And Research | Bifunctional acetylcholinesterase reactivators |
| US6141137A (en) | 1998-08-26 | 2000-10-31 | Gentex Corporation | Electrochromic media for producing a preselected color |
| WO1998050314A1 (en) | 1997-05-07 | 1998-11-12 | Corning Incorporated | Ir and uv absorbing brown solar glasses, ophthalmic lenses |
| JPH1125505A (ja) * | 1997-05-09 | 1999-01-29 | Fuji Photo Film Co Ltd | 情報記録媒体及びオキソノール化合物 |
| DE10023765A1 (de) | 2000-05-15 | 2001-11-22 | Bayer Ag | Elektrochrome Vorrichtung |
| DE10023744A1 (de) | 2000-05-15 | 2001-12-13 | Bayer Ag | Elektrochrome Anzeigevorrichtung mit hoher Kantenschärfe |
| US7342706B2 (en) * | 2004-03-09 | 2008-03-11 | Fujifilm Corporation | Electrochromic element, optical density changing element, optical element and photographing unit |
| FR2872589B1 (fr) * | 2004-07-02 | 2006-10-27 | Essilor Int | Procede de realisation d'un element optique transparent, composant optique intervenant dans ce procede et element optique ainsi obtenu |
| US7855821B2 (en) | 2004-11-15 | 2010-12-21 | Gentex Corporation | Electrochromic compounds and associated media and devices |
| WO2008029194A1 (en) | 2006-09-06 | 2008-03-13 | Essilor International (Compagnie Générale d'Optique) | 6-(biphenyl-ester) -3h-naphtho [2, 1-b] pyrans as photochromic dichroic dyes and optical article containing them |
| JP2009073750A (ja) | 2007-09-20 | 2009-04-09 | Fujifilm Corp | ビピリジニウム化合物およびその合成中間体の製造方法、色素化合物の製造方法、ならびに新規ビピリジニウム化合物およびそれを含む新規色素化合物 |
| JPWO2011016523A1 (ja) * | 2009-08-07 | 2013-01-17 | 和光純薬工業株式会社 | ビス第4級アンモニウム塩の製造法及び新規中間体 |
| FR2950710B1 (fr) | 2009-09-28 | 2012-03-16 | Essilor Int | Systemes electrochromes transparents a plusieurs electrodes de polarisation |
| JP2013516430A (ja) | 2009-12-30 | 2013-05-13 | ザ ステイト オブ オレゴン アクティング バイ アンド スルー ザ ステイト ボード オブ ハイヤー エデュケーション オン ビハーフ オブ ポートランド ステイト ユニバーシティー | チオール検出 |
| KR101735570B1 (ko) * | 2010-03-26 | 2017-05-15 | 삼성전자주식회사 | 전기 변색 물질 및 이를 포함하는 전기 변색 소자 |
| US8610991B2 (en) * | 2010-07-14 | 2013-12-17 | Samsung Electronics Co., Ltd. | Electrochromic material and electrochromic device including the same |
| EP2848667B1 (en) * | 2013-09-17 | 2019-04-10 | Essilor International | Electrochromic single and two-core viologens and optical articles containing them |
| ES2661512T3 (es) | 2013-09-17 | 2018-04-02 | Essilor International | Composición electrocrómica |
| EP2848668B1 (en) | 2013-09-17 | 2019-01-09 | Essilor International | Electrochromic two-core viologen derivatives and optical articles containing them |
| ES2662377T3 (es) | 2013-09-17 | 2018-04-06 | Essilor International | Composición electrocrómica |
-
2013
- 2013-09-17 EP EP13184771.7A patent/EP2848667B1/en active Active
-
2014
- 2014-09-16 CN CN201480050706.7A patent/CN105555911B/zh active Active
- 2014-09-16 JP JP2016543383A patent/JP6751022B2/ja active Active
- 2014-09-16 US US15/022,784 patent/US9823534B2/en active Active
- 2014-09-16 KR KR1020167005699A patent/KR102347082B1/ko active IP Right Grant
- 2014-09-16 AU AU2014323167A patent/AU2014323167B2/en active Active
- 2014-09-16 BR BR112016005305-2A patent/BR112016005305B1/pt active IP Right Grant
- 2014-09-16 WO PCT/EP2014/069737 patent/WO2015040033A2/en active Application Filing
-
2018
- 2018-12-06 JP JP2018229306A patent/JP6892852B2/ja active Active
Patent Citations (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6037471A (en) * | 1997-04-02 | 2000-03-14 | Gentex Corporation | Electrochromic compounds |
| JP2001519922A (ja) * | 1997-04-02 | 2001-10-23 | ジェンテクス・コーポレーション | 予め選択された色を生ずることのできる改良されたエレクトロクロミック媒体 |
| JPH11106376A (ja) * | 1997-10-01 | 1999-04-20 | Fuji Photo Film Co Ltd | ビオローゲン誘導体の製造方法 |
| JP2003128654A (ja) * | 2001-10-26 | 2003-05-08 | Fuji Photo Film Co Ltd | 4,4’−ビピリジニウム誘導体の製造方法 |
| JP2003168246A (ja) * | 2001-11-29 | 2003-06-13 | Fuji Photo Film Co Ltd | 光情報記録媒体 |
| JP2008504583A (ja) * | 2004-07-02 | 2008-02-14 | エシロール アンテルナシオナル (コンパニー ジェネラレ ドプテイク) | 透明な光学素子の製造方法、この製造方法に関わる光学部品および得られた光学素子 |
| JP2006181908A (ja) * | 2004-12-28 | 2006-07-13 | Fuji Photo Film Co Ltd | 光情報記録媒体及び光情報記録方法 |
| JP2012505426A (ja) * | 2008-10-09 | 2012-03-01 | エシロル アンテルナショナル(コンパーニュ ジェネラル ドプテーク) | 透明電気活性システム |
| CN102234505A (zh) * | 2010-04-29 | 2011-11-09 | 比亚迪股份有限公司 | 一种电致变色材料及其制备方法、及防眩目汽车后视镜 |
| WO2011142329A1 (ja) * | 2010-05-13 | 2011-11-17 | 協和発酵ケミカル株式会社 | 錯化合物およびそれを含有する光記録媒体 |
| WO2012008468A1 (ja) * | 2010-07-14 | 2012-01-19 | 協和発酵ケミカル株式会社 | 錯化合物およびそれを含有する光記録媒体 |
Non-Patent Citations (3)
| Title |
|---|
| JOURNAL OF MEDICINAL CHEMISTRY, vol. 53, no. 9, JPN6018013885, 2010, pages 3480 - 3488, ISSN: 0003976381 * |
| JOURNAL OF ORGANIC CHEMISTRY, vol. 65, no. 2, JPN6018013887, 2000, pages 593 - 595, ISSN: 0003976379 * |
| JOURNAL OF POLYMER SCIENCE, PART A: POLYMER CHEMISTRY, vol. 26, no. 2, JPN6018013888, 1988, pages 653 - 656, ISSN: 0003976380 * |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2015040033A3 (en) | 2015-06-11 |
| JP6892852B2 (ja) | 2021-06-23 |
| KR20160055796A (ko) | 2016-05-18 |
| US20160231635A1 (en) | 2016-08-11 |
| EP2848667B1 (en) | 2019-04-10 |
| JP2019089765A (ja) | 2019-06-13 |
| KR102347082B1 (ko) | 2022-01-04 |
| CN105555911B (zh) | 2018-02-27 |
| JP6751022B2 (ja) | 2020-09-02 |
| AU2014323167B2 (en) | 2018-04-19 |
| BR112016005305A2 (ja) | 2017-08-01 |
| AU2014323167A1 (en) | 2016-03-10 |
| BR112016005305A8 (pt) | 2018-08-14 |
| US9823534B2 (en) | 2017-11-21 |
| EP2848667A1 (en) | 2015-03-18 |
| BR112016005305B1 (pt) | 2022-02-15 |
| WO2015040033A2 (en) | 2015-03-26 |
| CN105555911A (zh) | 2016-05-04 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6892852B2 (ja) | エレクトロクロミック性の単核及び2核ビオロゲン並びにそれらを含有する光学物品 | |
| JP6456964B2 (ja) | エレクトロクロミック性2核ビオロゲン誘導体及びそれらを含有する光学物品 | |
| JP6841657B2 (ja) | エレクトロクロミック組成物 | |
| CN107922830B (zh) | 电致变色化合物以及含有它们的光学物品 | |
| JP6898100B2 (ja) | エレクトロクロミック組成物 | |
| CN110114438B (zh) | 电致变色化合物以及含有它们的光学制品 | |
| Crossley | 94220 Charenton le Pont (FR) 94220 Charenton-le-Pont (FR)(72) Inventors:(74) Representative: Cabinet Plasseraud | |
| Aiken et al. | University of |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20160318 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20170616 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20180424 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A711 Effective date: 20180425 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20180723 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20180807 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20181206 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20181214 |
|
| A912 | Re-examination (zenchi) completed and case transferred to appeal board |
Free format text: JAPANESE INTERMEDIATE CODE: A912 Effective date: 20190215 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20191223 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200331 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20200813 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6751022 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |