JP2016113444A - 固形組成物 - Google Patents
固形組成物 Download PDFInfo
- Publication number
- JP2016113444A JP2016113444A JP2015231570A JP2015231570A JP2016113444A JP 2016113444 A JP2016113444 A JP 2016113444A JP 2015231570 A JP2015231570 A JP 2015231570A JP 2015231570 A JP2015231570 A JP 2015231570A JP 2016113444 A JP2016113444 A JP 2016113444A
- Authority
- JP
- Japan
- Prior art keywords
- solid composition
- onji
- sinapoyl
- sucrose ester
- mass
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Landscapes
- Medicinal Preparation (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines Containing Plant Substances (AREA)
Abstract
Description
(1)3’,6-di-O-sinapoyl-sucrose ester、並びに、カルボキシメチルスターチナトリウム、ソルビトール、ステビア、グリチルリチン酸二カリウム、マルチトール、及びサッカリンナトリウムからなる群から選ばれる少なくとも1種を含有することを特徴とする固形組成物、
(2)オンジを含有する(1)に記載の固形組成物、
(3)オンジが、オンジ末、オンジエキス、又はオンジエキス末である(2)に記載の固形組成物、
(4)固形組成物が内服用である、(1)〜(3)のいずれかに記載の固形組成物、
(5)固形組成物が錠剤、顆粒剤、散剤、カプセル剤、チュアブル錠剤、口腔内崩壊錠又はドライシロップ剤である、(1)〜(4)のいずれかに記載の固形組成物、
(6)3’,6-di-O-sinapoyl-sucrose esterの経時的な含量低下を抑制するために、カルボキシメチルスターチナトリウム、ソルビトール、ステビア、グリチルリチン酸二カリウム、マルチトール、及びサッカリンナトリウムからなる群から選ばれる少なくとも1種を使用する方法、
(7)カルボキシメチルスターチナトリウム、ソルビトール、ステビア、グリチルリチン酸二カリウム、マルチトール、及びサッカリンナトリウムからなる群から選ばれる少なくとも1種を添加することによって、3’,6-di-O-sinapoyl-sucrose esterの経時的な含量低下を抑制する方法、
である。
本発明のソルビトールは粒状のものでも粉末状のものであってもよく、市販品としてはNEOSORB(ロケットジャパン)、ソルビトール(三栄源エフエフアイ)、ソルビット(新日本理化)等が使用できる。ソルビトールの含有量は、本発明の固形組成物全体の1質量%〜90質量%が好ましく、3質量%〜70質量%が更に好ましい。また、本発明の固形組成物中にオンジを含む場合は、発明の効果の点からオンジ1質量部に対し、0.3〜1質量部が好ましい。
本発明のステビアは粒状のものでも粉末状のものであってもよく、市販品としてはステビMZ(丸善製薬)、ステビロンC(守田化学工業)等が使用できる。ステビアの含有量は、本発明の固形組成物全体の0.005質量%〜20質量%が好ましく、0.01質量%〜10質量%が更に好ましい。また、本発明の固形組成物中にオンジを含む場合は、発明の効果の点からオンジ1質量部に対し、0.001〜0.1質量部が好ましい。
本発明のグリチルリチン酸二カリウムは粒状のものでも粉末状のものであってもよく、市販品としてはグリチルリチン酸二カリウム(ALPS薬品工業)、グリチルリチン酸二カリウム(丸善製薬)等が使用できる。グリチルリチン酸二カリウムの含有量は、本発明の固形組成物全体の0.001質量%〜90質量%が好ましく、0.01質量%〜70質量%が更に好ましい。また、本発明の固形組成物中にオンジを含む場合は、発明の効果の点からオンジ1質量部に対し、0.001〜1質量部が好ましい。
本発明のマルチトールは粒状のものでも粉末状のものであってもよく、市販品としてはアマルティ(三菱商事フードテック)、レシス(三菱商事フードテック)等が使用できる。マルチトールの含有量は、本発明の固形組成物全体の1質量%〜90質量%が好ましく、3質量%〜70質量%が更に好ましい。また、本発明の固形組成物中にオンジを含む場合は、発明の効果の点からオンジ1質量部に対し、0.3〜1質量部が好ましい。
本発明のサッカリンナトリウムは粒状のものでも粉末状のものであってもよく、市販品としてはサッカリンナトリウム(大和化成)等を使用できる。サッカリンナトリウムの含有量は、本発明の固形組成物全体の0.005質量%〜20質量%が好ましく、0.01質量%〜10質量%が更に好ましい。また、本発明の固形組成物中にオンジを含む場合は、発明の効果の点から、オンジ1質量部に対し、0.001〜0.1質量部が好ましい。
以下表1に実施例1〜2及び比較例1〜4の処方を示す。オンジ(原生薬換算量約857mg)と各成分をガラス瓶内で混合し、固形組成物を調製した。
実施例1〜2及び比較例1〜4について25℃60%RH条件下で48時間静置したのち密閉し、65℃条件下で7日保存した。
保存後の固形組成物について、それぞれ組成物中の3’,6-di-O-sinapoyl-sucrose ester含有量を測定し、直後品中の3’,6-di-O-sinapoyl-sucrose ester量に対する残存率を(%)求め、比較例1における3’,6-di-O-sinapoyl-sucrose ester残存率との差を、各組成物における残存率改善度(%)とした。なお、直後品中に含まれる3’,6-di-O-sinapoyl-sucrose esterの含有量は0.85質量%であった。
実施例3〜6及び比較例5〜8について25℃60%RH条件下で48時間静置したのち密閉し、65℃条件下で7日保存した。
保存後の固形組成物について、それぞれ組成物中の3’,6-di-O-sinapoyl-sucrose ester含有量を測定し、直後品中の3’,6-di-O-sinapoyl-sucrose ester量に対する残存率を(%)求め、比較例5における3’,6-di-O-sinapoyl-sucrose ester残存率との差を、各組成物における残存率改善度(%)とした。
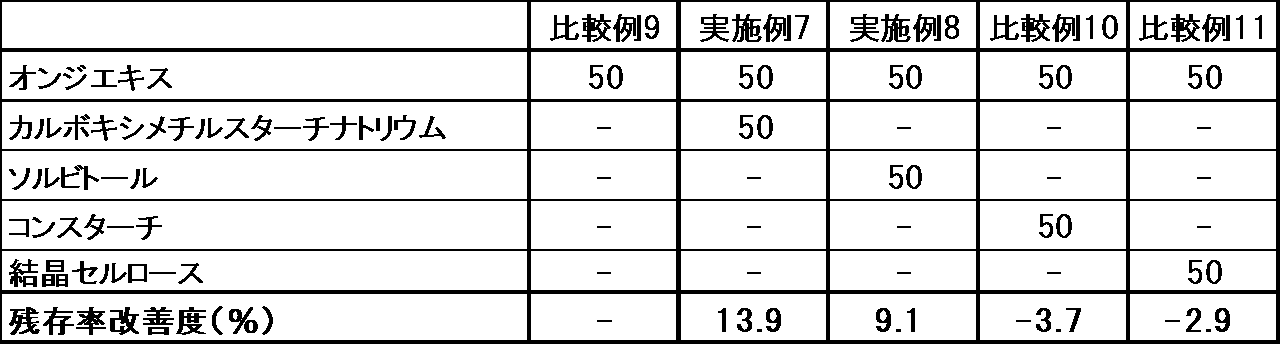
実施例7〜8及び比較例9〜11について25℃60%RH条件下で48時間静置したのち密閉し、65℃条件下で7日保存した。
保存後の固形組成物について、それぞれ組成物中の3’,6-di-O-sinapoyl-sucrose ester含有量を測定し、直後品中の3’,6-di-O-sinapoyl-sucrose ester量に対する残存率を(%)求め、比較例9における3’,6-di-O-sinapoyl-sucrose ester残存率との差を、各組成物における残存率改善度(%)とした。
Claims (7)
- 3’,6-di-O-sinapoyl-sucrose ester、並びに、カルボキシメチルスターチナトリウム、ソルビトール、ステビア、グリチルリチン酸二カリウム、マルチトール、及びサッカリンナトリウムからなる群から選ばれる少なくとも1種を含有することを特徴とする固形組成物。
- オンジを含有する請求項1に記載の固形組成物。
- オンジが、オンジ末、オンジエキス又はオンジエキス末である請求項2に記載の固形組成物。
- 固形組成物が内服用である、請求項1〜3のいずれかに記載の固形組成物。
- 固形組成物が錠剤、顆粒剤、散剤、カプセル剤、チュアブル錠剤、口腔内崩壊錠又はドライシロップ剤である、請求項1〜4のいずれかに記載の固形組成物。
- 3’,6-di-O-sinapoyl-sucrose esterの経時的な含量低下を抑制するために、カルボキシメチルスターチナトリウム、ソルビトール、ステビア、グリチルリチン酸二カリウム、マルチトール、及びサッカリンナトリウムからなる群から選ばれる少なくとも1種を使用する方法。
- カルボキシメチルスターチナトリウム、ソルビトール、ステビア、グリチルリチン酸二カリウム、マルチトール、及びサッカリンナトリウムからなる群から選ばれる少なくとも1種を添加することによって、3’,6-di-O-sinapoyl-sucrose esterの経時的な含量低下を抑制する方法。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2014252310 | 2014-12-12 | ||
| JP2014252310 | 2014-12-12 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2016113444A true JP2016113444A (ja) | 2016-06-23 |
| JP6668706B2 JP6668706B2 (ja) | 2020-03-18 |
Family
ID=56140890
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015231570A Active JP6668706B2 (ja) | 2014-12-12 | 2015-11-27 | 固形組成物 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP6668706B2 (ja) |
Citations (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS5758610A (en) * | 1980-09-26 | 1982-04-08 | Lion Corp | Composition for oral cavity |
| JPH09110708A (ja) * | 1995-08-11 | 1997-04-28 | Taisho Pharmaceut Co Ltd | 滋養強壮用生薬配合製剤 |
| CN1857694A (zh) * | 2006-04-13 | 2006-11-08 | 贵州信邦制药股份有限公司 | 一种痫愈片中药复方制剂及其制备方法 |
| CN101327296A (zh) * | 2008-07-23 | 2008-12-24 | 武汉理工大学 | 用于治疗和改善失眠症状的复方中药制剂及其制备方法 |
| CN101628076A (zh) * | 2008-07-16 | 2010-01-20 | 王跃进 | 一种失眠用中药茶颗粒 |
| CN103141742A (zh) * | 2013-03-29 | 2013-06-12 | 王新民 | 一种改善智力的压片糖果 |
| CN103690751A (zh) * | 2013-12-20 | 2014-04-02 | 青岛琴诚医药技术有限公司 | 一种舒心宁片的应用及制备方法 |
| CN103860941A (zh) * | 2014-04-01 | 2014-06-18 | 李佃场 | 一种治疗精神分裂症的中药及其制备方法 |
| CN104147460A (zh) * | 2014-09-02 | 2014-11-19 | 杭州金培科技有限公司 | 一种治疗帕金森病的中药制剂及其制备方法 |
| JP2016108327A (ja) * | 2014-12-05 | 2016-06-20 | 大正製薬株式会社 | 固形組成物 |
| JP2016108328A (ja) * | 2014-12-05 | 2016-06-20 | 大正製薬株式会社 | 固形組成物 |
-
2015
- 2015-11-27 JP JP2015231570A patent/JP6668706B2/ja active Active
Patent Citations (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS5758610A (en) * | 1980-09-26 | 1982-04-08 | Lion Corp | Composition for oral cavity |
| JPH09110708A (ja) * | 1995-08-11 | 1997-04-28 | Taisho Pharmaceut Co Ltd | 滋養強壮用生薬配合製剤 |
| CN1857694A (zh) * | 2006-04-13 | 2006-11-08 | 贵州信邦制药股份有限公司 | 一种痫愈片中药复方制剂及其制备方法 |
| CN101628076A (zh) * | 2008-07-16 | 2010-01-20 | 王跃进 | 一种失眠用中药茶颗粒 |
| CN101327296A (zh) * | 2008-07-23 | 2008-12-24 | 武汉理工大学 | 用于治疗和改善失眠症状的复方中药制剂及其制备方法 |
| CN103141742A (zh) * | 2013-03-29 | 2013-06-12 | 王新民 | 一种改善智力的压片糖果 |
| CN103690751A (zh) * | 2013-12-20 | 2014-04-02 | 青岛琴诚医药技术有限公司 | 一种舒心宁片的应用及制备方法 |
| CN103860941A (zh) * | 2014-04-01 | 2014-06-18 | 李佃场 | 一种治疗精神分裂症的中药及其制备方法 |
| CN104147460A (zh) * | 2014-09-02 | 2014-11-19 | 杭州金培科技有限公司 | 一种治疗帕金森病的中药制剂及其制备方法 |
| JP2016108327A (ja) * | 2014-12-05 | 2016-06-20 | 大正製薬株式会社 | 固形組成物 |
| JP2016108328A (ja) * | 2014-12-05 | 2016-06-20 | 大正製薬株式会社 | 固形組成物 |
Non-Patent Citations (4)
| Title |
|---|
| アドレニンエースシロップ 添付文書, JPN6019047668, 8 May 2014 (2014-05-08), ISSN: 0004168238 * |
| エナックロイヤル 添付文書, JPN6019047669, 4 February 2014 (2014-02-04), ISSN: 0004168239 * |
| フスコンZ液 添付文書, JPN6019047670, October 2011 (2011-10-01), ISSN: 0004168240 * |
| 新化粧品ハンドブック, JPN6019034797, 30 October 2006 (2006-10-30), pages 545, ISSN: 0004168241 * |
Also Published As
| Publication number | Publication date |
|---|---|
| JP6668706B2 (ja) | 2020-03-18 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6327237B2 (ja) | 固形組成物 | |
| JP5059142B2 (ja) | ケイアルデヒド含有量の保持方法 | |
| TWI503122B (zh) | Oral administration of pharmaceutical compositions | |
| JP6701689B2 (ja) | 固形組成物 | |
| CN106551946B (zh) | 一种含三氟胸苷和盐酸替比嘧啶的药物组合物及制备方法 | |
| JP2015024986A (ja) | 固形製剤 | |
| JP6668706B2 (ja) | 固形組成物 | |
| JP6485120B2 (ja) | 固形製剤 | |
| JP6179515B2 (ja) | 安定化された内服用固形製剤 | |
| JP6157214B2 (ja) | 解熱鎮痛薬組成物 | |
| JP6844394B2 (ja) | 固形組成物 | |
| JP6971060B2 (ja) | 医薬品組成物 | |
| JP6838474B2 (ja) | 固形組成物 | |
| JP6439503B2 (ja) | 固形製剤 | |
| JP6907515B2 (ja) | 固形組成物 | |
| JP7205074B2 (ja) | 固形組成物 | |
| JP2015229664A (ja) | メクリジン含有医薬組成物 | |
| JP2022007461A (ja) | トルバプタン含有口腔内崩壊錠 | |
| JP2013147488A (ja) | 固形製剤 | |
| JP5553522B2 (ja) | 経口投与用医薬組成物 | |
| JP2015157797A (ja) | 固形製剤 | |
| JP6075043B2 (ja) | 固形製剤 | |
| NZ710967A (en) | Pharmaceutical compositions containing dexketoprofen and tramadol | |
| JP2015024987A (ja) | 錠剤 | |
| JP2015229665A (ja) | メクリジン含有医薬組成物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20181120 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20190910 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20191028 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20191210 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200116 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20200128 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20200210 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6668706 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |