JP2010512792A - 髄膜炎菌性疾患の予防および処置のための新規な免疫原性組成物 - Google Patents
髄膜炎菌性疾患の予防および処置のための新規な免疫原性組成物 Download PDFInfo
- Publication number
- JP2010512792A JP2010512792A JP2009542957A JP2009542957A JP2010512792A JP 2010512792 A JP2010512792 A JP 2010512792A JP 2009542957 A JP2009542957 A JP 2009542957A JP 2009542957 A JP2009542957 A JP 2009542957A JP 2010512792 A JP2010512792 A JP 2010512792A
- Authority
- JP
- Japan
- Prior art keywords
- polypeptide
- seq
- composition
- nos
- acid sequence
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/02—Bacterial antigens
- A61K39/095—Neisseria
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/04—Immunostimulants
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/195—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from bacteria
- C07K14/22—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from bacteria from Neisseriaceae (F)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/54—Medicinal preparations containing antigens or antibodies characterised by the route of administration
- A61K2039/541—Mucosal route
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Immunology (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- General Chemical & Material Sciences (AREA)
- Microbiology (AREA)
- Epidemiology (AREA)
- Mycology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Molecular Biology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Genetics & Genomics (AREA)
- Biophysics (AREA)
- Biochemistry (AREA)
- Gastroenterology & Hepatology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Communicable Diseases (AREA)
- Oncology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Abstract
Description
配列番号1 天然のリーダー配列と組み合わされた時のCDC1135菌株由来の成熟2086タンパク質についてのアミノ酸配列をコードする核酸配列。
本発明は、2086サブファミリーAタンパク質および2086サブファミリーBタンパク質を含むナイセリアORF2086タンパク質(「2086タンパク質」)を提供する。2086タンパク質の各々は、Neisseria meningitidis(セログループA、B、C、D、W−135、X、Y、Zおよび29E)、Neisseria gonorrhoeae、およびNeisseria lactamicaの菌株を含む、天然のナイセリア菌株から単離され得るタンパク質である。2086タンパク質はまた、組換え技術を用いて調製されてもよい。
タンパク質、免疫原性部分および生物学等価物
本発明により提供される2086タンパク質は、単離されたタンパク質またはポリペプチドである。用語「単離された(isolated)」は、天然状態から人の手によって変更されたことを意味する。もし「単離された」組成物または物質が自然界で生ずるのであれば、それはすでにその本来の環境から変化しているかまたは取り除かれているか、あるいはその両方である。例えば、生きている動物中に天然に存在するポリペプチドまたはポリヌクレオチドは「単離され」てはいないが、同じポリペプチドまたはポリヌクレオチドがその天然の状態の共存物質から分離されていれば、本明細書中で使用される用語「単離され」と同じく「単離され」ている。したがって、本明細書中で用いられるように、用語「単離されたタンパク質(isolated protein)」は、天然供給源から単離されたタンパク質および組換え技術を用いて調製されたタンパク質、ならびに、他の抗原および/または例えば薬学的に許容される担体、バッファー、アジュバント等の添加物と組み合わされた時の上記のようなタンパク質を包含する。
na=xa−(xa・y)
式中、naはアミノ酸改変の数であり、xaは偶数番号の配列番号2−12中のアミノ酸の総数であり、yは、例えば70%については0.70、80%については0.80、85%については0.85等であり、xaとyとのどのような非整数積も、これをxaから引く前に最も近い整数に丸められる。
抗体
配列番号2−12のアミノ酸配列を含む本発明のタンパク質、それらのフラグメント、およびそれらの類似体、またはそれらを発現させる細胞はまた、本発明のポリペプチドについて免疫特異性の抗体を産生するための免疫原として用いられる。本発明は、免疫特異性のポリペプチドに対する抗体およびN.meningitidisの存在を検出し、受動的保護を提供あるいは細胞、組織抽出物、または生体液中のポリペプチドの量もしく濃度を測定するためのそのような抗体の使用を含む。
ポリヌクレオチド
本発明のタンパク質と同様に、本発明のポリヌクレオチドは、奇数番号の配列番号1−11の基準配列のうちのいずれかと同一、すなわち100%同一の核酸配列を含んでもよく、または、基準配列と比較していくつかのヌクレオチド改変を含んでもよい。そのような改変は、少なくとも1つのヌクレオチド欠失、転位および転換を含む置換、または挿入からなる群から選ばれ、前記改変は、基準ヌクレオチド配列の5’もしくは3’末端位置において、あるいは個別に基準アミノ酸配列中か基準アミノ酸配列内の1つ以上の隣接する群中のアミノ酸間に散在されて、それらの末端位置間のどこかで生じる。ヌクレオチド変更の数は、奇数番号の配列番号1−11のいずれかの中のヌクレオチド総数にそれぞれのパーセント同一性(100で割られる)を乗じ、その積を前記配列中の前記総数から引くことにより求められる。
nn=xn−(xn・y)、
式中、xnは、奇数番号の配列番号1−11のいずれかの核酸の総数であり、yは、0.95の値を有し、xnとyとのどのような非整数積も、そのような積をxnから引く前に最も近い整数に丸められる。当然、yは、95%について0.95の値等を有することもできる。偶数番号配列配列番号2−12のいずれかのアミノ酸配列を含むポリペプチドをコードするポリヌクレオチド配列の改変は、このコーディング配列中にナンセンス、ミスセンスまたはフレームシフト突然変異を作り出し、それによって、そのような改変に続いてポリヌクレオチドによってコードされるポリペプチドを改変することがある。
融合タンパク質
本発明はまた、融合タンパク質に関する。「融合タンパク質(fusion protein)」は、2つの、しばしば無関係な、融合遺伝子またはそのフラグメントによりコードされたタンパク質を意味する。例えば、免疫グロブリン分子の定常領域の様々な部分を別の免疫原性タンパク質またはその部分と共に含む融合タンパク質である。多くの場合、免疫グロブリンFc領域を融合タンパク質の一部として使用することは、治療および診断での使用に有利であり、例えば、改善された薬物動態学特性という結果になる(例えば、欧州特許出願公開第0232262号参照)。他方、用途によっては、融合タンパク質が発現され、検出され、精製された後に、Fc部分を欠失させることができることが望ましいであろう。本発明の2086ポリヌクレオチドは、本発明のポリペプチドの組換え産生に用いられ、ポリヌクレオチドは、それ自体で、成熟ポリペプチドのためのコード配列、あるいは、リーダーまたは分泌配列、プレもしくはプロないしはプレプロタンパク質配列、または他の融合ペプチド部分をコードするコード配列のような、他のコード配列を持つリーディングフレーム中の成熟ポリペプチドのためのコード配列を含み得る。例えば、2086ポリペプチドまたは融合ポリペプチドの精製を容易にするマーカー配列がコードされ得る(参照によりその全体が本明細書に組み込まれる、Gentzら、1989参照)。したがって、発現産物のHisタグ精製を可能にする融合ポリペプチドをコードするポリヌクレオチドの調製が本発明の実施において考慮される。ポリヌクレオチドはまた、転写された、非翻訳配列、スプライシングおよびポリアデニル化シグナルのような、非コーディング5’および3’配列を含み得る。そのような融合ポリペプチドは、形質変換/形質移入されたまたは感染させられたもしくは以下に記載されるように組換えDNAクローニングビークルで感染させられた宿主細胞により産生されることができ、そのような融合ペプチドはその後、宿主細胞から単離され、他の宿主細胞タンパク質を実質的に含まない融合ポリペプチドを提供することができる。
免疫原性組成物
本発明の1つの態様は、少なくとも1つの2086タンパク質または前記タンパク質をコードする核酸を含む免疫原性組成物を提供する。上記のものは、(1)複数の菌株への殺菌抗体を引き出し、(2)複数の菌株の表面と反応し、(3)生菌攻撃に対する受動的保護を付与し、および/または、(4)コロニー形成を防止する能力を有する。そのような免疫原性組成物の製剤は、当業者によく知られている。ある一定の実施形態において、本発明の組成物は、薬学的に許容される担体および/または希釈剤を含む。適切な薬学的に許容される担体および/または希釈剤としては、あらゆるすべての従来の溶媒、分散媒、フィラー、固体担体、水溶液、コーティング、抗菌性および抗真菌性薬剤、等張性および吸収遅延薬剤等が含まれる。適切な薬学的に許容される担体としては、例えば、1つ以上の水、食塩水、リン酸緩衝食塩水、デキストロース、グリセリロール、エタノール等、ならびにそれらの組み合わせが含まれる。薬学的に許容される担体はさらに、湿潤または乳化剤、防腐剤またはバッファーのような抗体の保存期間または有効性を向上する少量の補助物質をさらに含み得る。薬学的に許容される担体の調製および使用は、技術的によく知られている。いずれかの従来の培地または薬剤が活性成分と不和合である限りを除き、本発明の免疫原性組成物におけるそれらの使用は考慮される。本発明のある一定の実施形態によれば、薬学的に許容される担体は、担体タンパク質である。
担体タンパク質
担体タンパク質は、好ましくは非毒性かつ非反応原性であり、さらに十分な量および純度で入手可能なタンパク質である。担体タンパク質は、標準の接合手順に適用できるべきである。本発明の特定の実施形態において、CRM197が担体タンパク質として用いられる。
アジュバント
本明細書中で記載されるような免疫原性組成物はまた、ある一定の実施形態において、1つ以上のアジュバントを含む。アジュバントは、免疫原または抗原と共に投与された時に、免疫応答を増大させる物質である。いくつかのサイトカインおよびリンホカインは、免疫調整活性を有することが示されており、したがってアジュバントとして有用であり、インターロイキン1−α、1−β、2、4、5、6、7、8、10、12(例えば、米国特許第5,723,127号参照)、13、14、15、16、17および 18(ならびにその突然変異体);インターフェロン−α、βおよびγ;顆粒状マクロファージコロニー刺激因子(GM−CSF)(例えば、米国特許第5,078,996号およびATCC受入番号39900参照)、マクロファージコロニー刺激因子(M−CSF);顆粒状コロニー刺激因子(G−CSF)、ならびに腫瘍壊死因子αおよびβが含まれるが、これらに限定されない。本明細書中で記載される免疫原性組成物と共に有用な他のアジュバントとしては、MCP−1、MIP−1α、MIP−1βおよびRANETSを制限無く含むケモカイン;セレクチン、例えば、L−セレクチン、P−セレクチンおよびE−セレクチンのような接着分子;ムチン様分子、例えば、CD34、GlyCAM−1およびMadCAM−1;LFA−1、VLA−1、Mac−1およびp150.95のようなインテグリンファミリーの一つ;PECAM、ICAMs、例えば、ICAM−1、ICAM−2およびICAM−3、CD2およびLFA−3のような免疫グロブリンスーパーファミリーの一つ;CD40およびCD40Lのような共刺激分子;血管成長因子、神経成長因子、神経芽細胞成長因子、表皮成長因子、B7.2、PDGF、BL−1、ならびに血管内皮成長因子を含む成長因子;Fas、TNF受容体、Flt、Apo−1、p55、WSL−1、DR3、TRAMP、Apo−3、AIR、LARD、NGRF、DR4、DR5、KILLER、TRAIL−R2、TRICK2、およびDR6を含む受容体分子;ならびにカスパーゼ(ICE)が含まれる。
投与様式
そのような免疫原性組成物は、非経口的に、例えば、皮下注射か筋肉内注射により、ならびに経口的または鼻腔内的に投与され得る。筋肉内免疫化の方法は、WolffらおよびSedegahらにより記載されている。他の投与様式は、例えば、経口製剤、肺製剤、座薬、および経皮適用を用いるが、それらに限定されない。経口製剤としては、例えば、製薬グレードのマンニトール、乳糖、デンプン、ステアリン酸マグネシウム、サッカリンナトリウム、セルロース、炭酸マグネシウム等の通常用いられる賦形剤が含まれるが、それらに限定されない。
多重抗原
本発明のタンパク質、ポリヌクレオチドおよび等価物を含む免疫原性薬剤は、免疫原性組成物中の唯一の能動免疫原として投与されてもよく、代わりに、組成物は、他のNeisseria sp.免疫原性ポリペプチド、または1つ以上の他の微生物病原体(例えば、ウイルス、プリオン、細菌、真菌、ただしこれらに限定されない)の免疫学的活性なタンパク質もしくは莢膜多糖を含む他の能動免疫原を含んでもよい。組成物は、選ばれた徴候について要求されるように、1つ以上の所望のタンパク質、フラグメントまたは製薬化合物を含み得る。同様に、免疫原性組成物中に1つ以上の核酸を使用する本発明の組成物は、上記のように、同じ多様なタンパク質群をコードする核酸も含み得る。
ウイルスベクターおよび非ウイルスベクター
特にin vitoroおよびin vivo細胞アッセイのための好ましいベクターは、レンチウイルス、レトロウイルス、ヘルペスウイルス、アデノウイルス、アデノ随伴ウイルス、ワクシニアウイルス、バキュロウイルス、および望ましい細胞指向性を持つ他の組換えウイルスのようなウイルスベクターである。したがって、2086タンパク質またはその免疫原性フラグメントをコードする核酸は、ウイルスベクターを用いてまたはDNAの直接導入により、in vivo、ex vivo、またはin vitroで導入され得る。標的組織中での発現は、ウイルスベクターまたは受容体リガンドにより、または組織特異性プロモーターを用いて、あるいはその両方により、トランスジェニックベクターを特定の細胞特定に向けることにより行われ得る。標的遺伝子送達は、国際公開第95/28494号に記載され、これは、参照によりその全体が本明細書に組み入れられる。
細菌発現系およびプラスミド
本発明はまた、ベクターまたはプラスミドのような組換えDNA分子を提供し、これは、プロモーター配列およびイニシエーター配列ならびに本発明のポリペプチドをコードするヌクレオチド配列を有する発現制御配列を含み、ヌクレオチド配列は、プロモーターおよびイニシエーター配列に対して3’に位置する。さらに別の態様において、本発明は、プロモーター配列およびイニシエーター配列を有する発現制御配列、ならびに2086ポリペプチドをコードするヌクレオチド配列を含有する、2086ポリペプチドを発現することができる組換えDNAクローニングビヒクルを提供し、ヌクレオチド配列は、プロモーターおよびイニシエーター配列に対し3’に位置する。さらなる態様において、上記で記載されるような組換えDNAクローニングビークルおよび/または組換えDNA分子を含む宿主細胞が提供される。適切な発現制御配列および宿主細胞/クローニングビークルの組み合わせは、技術的によく知られており、Sambrookら(1989)に例証として記載されている。
異種菌株に対する殺菌抗体を引き出すことが可能なナイセリア膜タンパク質抽出物の同定:
以下の表IIを参照すると、LOS(脂質オリゴ糖)除去外膜タンパク質調製物は、殺菌抗体を引き出すことが示されている。これらの抗体は、それぞれの菌株のPorAに向けられることが多くある。セログループB髄膜炎菌株8529(B:15:P1.7b,3)由来のLOS除去外膜調製物は、このように普通ではない。なぜならば、それらの調製物は、いくつかの異種菌株に対する殺菌抗体を引き出すからである。
菌株および培養条件
凍結したガラスびんからのN.meningitidis菌株8529を、GCプレート上に筋状に塗った。(髄膜炎菌株8529は、The RIVM,Bilthoven,The Netherlandsから受領した)。プレートを、36C/5%CO2で7.5時間インキュベートした。いくつかのコロニーを用い、50mLの修正フランツ培地+GCサプリメントを含むフラスコに接種した。フラスコを36℃にてエアシェーカー中でインキュベートし、200RPMで4.5時間撹拌した。5mLを用いて、450mLの修正フランツ培地+GCサプリメントを含むフェルンバッハフラスコに接種した。フラスコを36℃にてエアシェーカー中でインキュベートし、100RPMで11時間撹拌した。450mL全部を用いて、10L発酵槽中の8.5Lの修正フランツ培地+GCサプリメントに接種した。
修正フランツ培地の組成:
グルタミン酸 1.3g/L
システイン 0.02
リン酸水素二ナトリウム・7水和物 10
塩化カリウム 0.09
塩化ナトリウム 6
塩化アンモニウム 1.25
透析酵母抽出物(YE) 40ml
(5容量のdH2Oに対して一晩透析し、次いでオートクレーブした25%YE溶液)
GCサプリメント100X、フィルタ殺菌
デキストロース 400g/L
グルタミン酸 10
コカルボキシラーゼ 0.02
硝酸第二鉄 0.5
以下のパラメータを発酵中制御した:温度=36℃;pH=7.4;溶存酸素=20%。数滴のP−2000消泡剤を添加して発泡を制御した。培養物を定常期まで生育させた。細胞を、OD650=5.25において遠心分離により収集した。一般に、全部で100〜300グラムの湿潤細胞ペーストが、〜8.5Lの培養物から収集される。
異種殺菌抗体を引き出す髄膜炎菌由来の外膜タンパク質画分の部分的精製:
湿重量100グラムの細胞を、10mM HEPES−NaOH、pH7.4、1mN Na2EDTAで湿重量の5倍の体積に縣濁させ、そしてチャンバを備える110Yマイクロフルイダイザーを約18,000psiで通過させて溶解させた。細胞ライゼートを清澄にし、300,000×gで1時間の遠心分離により細胞エンベロープを単離した。細胞エンベロープを、同じバッファーでホモジナイザーを用いて縣濁し、続いて上記のように遠心分離して2回洗浄した。次に細胞エンベロープを、10mM HEPES−NaOH、pH7.4、1mN MgCl2中の1%(w/v)Triton X−100 320mLで抽出した。以下の表IIIを参照すると、Triton X−100およびZwittergent3−14を用いた逐次ディファレンシャル界面活性剤抽出、続いてのマウスの免疫化の結果により、Triton抽出物が、対象となる候補を最適に抽出したと確認することができた。次に、表IIIに列記された5つの菌株のうち4つに対して殺菌抗体応答を引き出すこのTriton X−100抽出物を、BioRad Rotophorユニット中での調製用等電点分離(IEF)により分画した。両性電解質濃度は、1%pH4〜6と混合された1%pH3〜10であった。表IIIに示されるように、いくつかの画分は、異種殺菌性応答を引き出すことが見出された。IEFから得られた画分は、5.5〜7.8のpH範囲で集束したものであり、殺菌アッセイにより確認されるように大部分の菌株に対する異種応答を引き出した。プールしたIEF画分を濃縮し、両性電解質をエタノール沈降により除去した。約5.5〜7.8のpH範囲で得られたタンパク質のいくらかを陰イオン交換カラムに吸着させ、吸着タンパク質および非吸着タンパク質でマウスを免疫化した後に得られる殺菌活性を比較することにより、さらなる精製が達成された。表IIを再度参照すると、多くのタンパク質が陰イオン交換樹脂に吸着された一方、カラムにより吸着されなかったタンパク質はより多くの異種殺菌抗体を引き出した。
N.meningitidis A Sangerゲノム配列は、ZaugurskyおよびRussel,2001,BioTechniques,31:636−659に記載される方法およびアルゴリズムを用いて分析した。このマイニング分析により、12,000以上の考え得るオープンリーディングフレーム(ORF)がもたらされた。上述の直接配列データおよび質量スペクトルデータは、非吸着画分の主要成分が、Sangerデータベースの分析中に存在するいくつかのORFの生成物であることを示した。この方法論により同定された3つの主なタンパク質は、ORF4431、5163および2086に対応する(図1Bおよび3参照)。
免疫原性方法:
抗血清の調製:
言及される場合を除き、タンパク質組成物/ワクチンは、25μgの総タンパク質で製剤し、20μgQS−21をアジュバントとした。0.2mLの用量を皮下(臀部)注射により、6〜8週齢雌スイスウェブスターマウスに0週目および4週目に投与した。0週目および4週目に血液を採取し、最終瀉血を6週目に実行した。
殺菌アッセイ:
殺菌アッセイは、本質的に記載されたように実行した(Mountzouros and Howell,2000,J.Clin.Microbiol.38(8):2878−2884参照)。SBAについての補体媒介抗体依存性の殺菌力価は、アッセイに導入された標的分子の≧50%を致死させる試験血清の最高希釈の逆数として表した(BC50力価)。
2086タンパク質の同定に用いた方法:
臭化シアン開裂およびフラグメントの直接的配列決定:
陰イオン交換非吸着画分(AEUF)の臭化シアン開裂。AEUFを90%冷エタノールにより沈降させ、70%蟻酸中の10mg/mL臭化シアンを用いて1mg/mLのタンパク質濃度に可溶化した。反応は、暗所において室温で夜通し実行した。開裂生成物を高速真空によって乾燥させ、ペレットを、HE/0.1%還元TX−100で可溶化した。SDS−PAGE、続いてN末端アミノ酸配列決定を用いて、この画分の成分を同定した。
成分を同定するためのプロテアーゼ消化/逆相/N末端配列決定:
AEUFを、GluC(V8)、LysCまたはArgCで消化した。タンパク質と酵素の比は、30μgタンパク質と1μg酵素であった。消化は夜通し37℃にて実行した。消化されたタンパク質混合物(30μg)を、7ミクロンAquapore RF−300カラムに通し、0.1%トリフルオロ酢酸中の10〜95%アセトニトリルの勾配で溶出し、ピークを手作業で収集した。無タンパク質ブランクも走らせ、これからのピークを試料クロマトグラムから減じた。試料ランにおいてのみ生じるピークを質量分析器により分析し、明確な質量を与える試料をN末端アミノ酸配列決定について分析した。
N末端アミノ酸配列決定:
ブロットから切り出されたバンドの場合、タンパク質試料を、SDSゲルからPVDF膜に移し、アミドブラック(脱イオン水中の10%酢酸、0.1%アミドブラック)で染色し、10%酢酸中で脱色した。次に所望のタンパク質バンドを、メタノールで洗浄した円刃刀またはミニ−Exactoナイフを用いて全10レーンから切り出し、Applied Biosystems477Aタンパク質シークエンサーの反応カートリッジに入れた。溶液中の試料の直接配列決定の場合、Prosorbカートリッジを集め、PVDFを60μLのメタノールで湿らせた。PVDFを50μLの脱イオン水で洗浄し、試料(50μL)をPVDFに置いた。50μLの脱イオン水を使用して試料を洗浄した後、Prosorb PVDFを押し抜き、乾燥し、Applied Biosystems477Aタンパク質シークエンサーの反応カートリッジに入れた。両方の方法について、Applied Biosystems N末端シークエンサーを、最適ブロット条件下で12サイクル以上(1サイクル ブランク、1サイクル 標準、および所望の残基同定のための10サイクル以上)走らせ、PTH−アミノ酸検出をApplied Biosystems 120A PTHアナライザーで行った。サイクルは、アナログチャートレコーダーおよび計測器ソフトウェアを介してデジタル式の両方で収集した。アミノ酸の帰属は、アナログおよびデジタルデータの両方を使用して、PTH−アミノ酸の標準セットとアナライザー上でのそれら個々の保持時間の比較により行った(システイン残基は変換中に破壊され、検出されなかった)。複数の配列情報を単一の残基から得ることが可能であり、一次対二次帰属はシグナル強度に基づいて行われた。
LC−MS/MS
IEFにより精製されたタンパク質試料を、SDSポリアクリルアミドゲル電気泳動によりさらに分析した。タンパク質は、クーマシーブルー染色により視覚化し、対象となるバンドを手動で切り出し、その後還元し、アルキル化し、そして自動in−gelトリプシン消化ロボット(1)を用いてin situでトリプシンにより消化(Promega,Madison,WI)した。消化後、ペプチド抽出物を、Savant Speed Vac Concentrator(ThermoQuest,Holdbrook,NY)を使用して、最終容積10〜20μLに濃縮した。
マイクロキャピラリーHPLC−質量分析:
in−gel消化物由来の抽出ペプチドを、マイクロエレクトロスプレイHPLCシステムにより0〜50%溶媒Bの50分間勾配(A:0.1M HOAc、B:90% MeCN/0.1M HOAc)を用いて分離した。ペプチド分析は、スプレイ電位1.5kVで作動し、加熱キャピラリー温度150℃を使用したFinnigan LCQイオントラップ質量分析器(ThermoQuest,San Jose,CA)で行った。データは、機器と共に提供されたデータ取得ソフトウェアを使用して、自動MS/MSモードで得た。取得方法は、1MSスキャン(375〜1200m/z)、続いてMSスキャン中の最も豊富な3種のイオンのMS/MSスキャンを包含した。動的排除関数および同位体排除関数を使用して分析されるペプチドイオンの数を増加させた(設定:3amu=排除幅、3分=排除期間、30秒=排除前期間、3amu=同位体排除幅)。MS/MSデータの自動分析は、N.meningitidisの完全ゲノム由来のタンパク質データベース(Sangerより)を使用して、Finnigan Bioworksデータ解析パッケージに含まれたSEQUESTコンピュータアルゴリズム(ThermoQuest,San Jose,CA)を使用して実行した。研究の結果を図3に示す。
(実施例2)
組換え脂質化P2086(RLP2086)のクローニング:
A.)天然のリーダー配列:
供給源物質:
ORF2086遺伝子を、8529と呼ばれるセログループB Neisseria meningitidis株の臨床分離菌からPCRにより増幅させた。この菌株のセログループ、セロタイプおよびセロサブタイプは、括弧内に示される;8529(B:15、P1:7b、3)。この髄膜炎菌株は、The RIVM,Bilthoven,The Netherlandsから得た。
PCR増幅およびクローニング戦略:
ORF2086の目視検査は、この遺伝子が潜在的なリポタンパク質シグナル配列を有することを示した。特許権によって保護されている隠れマルコフモデルリポタンパク質アルゴリズム(Hidden Markov Model Lipoprotein algorithm)を使用した付加的な解析は、ORF2086がリポタンパク質シグナル配列を含むことを確認した。より自然に近い立体配座でP2086を組換え発現させるために、オリゴヌクレオチドプライマーは、リポタンパク質シグナル配列を持つ全長遺伝子を増幅するように設計し、そしてN.meningitidis A ORF2086のSanger配列の分析に基づいた。2086遺伝子を、ポリメラーゼ連鎖反応(PCR)[ABI2400サーマルサイクラー,Applied Biosystems,Foster City,CA]によりN.meningitidis菌株8529から増幅した。正しいサイズの増幅産物を結合し、pCR2.1−TOPO(Invitrogen)にクローニングした。プラスミドDNAを、NdeIおよびBamHIで制限消化し、ゲル精製し、pET−27b(+)ベクター(Novagen)に結合した。
天然のリーダー配列を使用したrLP2086タンパク質発現:
図5を参照すると、プラスミドpPX7340をBLR(DE3)pLysS宿主細胞(Life Sciences)に形質転換/形質移入、または感染させた。1つの形質転換体を選択し、2%グルコース、カナマイシン(30μg/mL)、クロラムフェニコール(30μg/mL)、およびテトラサイクリン(12μg/mL)を含有するテリフィックブロス(Terrific Broth)50mLに接種した。一晩培養した培養物のOD600は6.0であった。一晩培養した培養物を、1%グリセロールおよび同じ抗生物質を含有するテリフィックブロス1リットルで希釈した。出発OD600は、0.4であった。2時間後、OD600は1.6であり、誘導前試料を採取した。OD600=1に等価の細胞は遠心分離し、上澄みを除去した。全細胞ペレットを150μLのTris−EDTAバッファーおよび150μLの2xSDS−PAGE試料バッファーに再懸濁した。IPTGを添加し、最終濃度1mMとした。3.5時間後、記載されるように誘導後試料を採取し、SDS−PAGEで分析した(図4参照)。
rLP2086の精製:
rLP2086を、ディファレンシャル界面活性剤抽出後にE.coliから可溶化した。天然環境にあるP2086とは異なり、rLP2086は、Triton X−100またはZwittergent 3−12によって著しく可溶化されなかった。rLP2086のバルクをサルコシルで可溶化し、それはN.meningitidisにおける相互作用とは異なってE.coliの外膜成分と相互作用することを示唆した。ひとたび可溶化されると、rLP2086は天然タンパク質と同様に精製され、その中に混在する多くのE.coliタンパク質はアニオン交換樹脂にpH=8で吸着させることにより除去した。その理論的pIより2分の1pH単位上であるにもかかわらず、rLP2086はpH8で吸着されないままであった。それ以上の精製は、pH4.5におけるカチオン交換樹脂へのrLP2086の吸着により達成された。
精製方法:
P2086を発現するBLR DE3 pLysS細胞の凍結ペレットを、20mL/g細胞湿重量で10mM HEPES−NaOH/1mM EDTA/1μg/mL Pefabloc SCプロテアーゼ阻害剤(Roche)pH7.4(HEP)に再懸濁し、マイクロフルイダイザー(Microfluidics Corporation Model 110Y)により溶解した。細胞ライゼートは150,000×gで1時間遠心分離した。ペレットはHEPで2回洗浄し、2回遠心分離し、得られた膜ペレットは一晩凍結した。該ペレットは10mM HEPES−NaOH/1mM MgCl2/1%TX−100 pH7.4で30分間可溶化し、続いて150,000xgで30分間遠心分離した。これを3回繰り返した。膜ペレットは上記のように50mM Tris−HCl/5mM EDTA/1%Zwittergent3−12 pH8で2回洗浄し、続いて50mM Tris−HCl/5mM EDTA/1%Zwittergent3−14 pH8および50mM Tris−HCl/5mM EDTA/1%Zwittergent3−14/0.5M NaCl pH8のそれぞれで2回洗浄した。
rLP2086サブファミリーBに対する抗血清の表面反応性および殺菌活性:
表VIIを参照すると、サブファミリーB菌株8526由来の精製rLP2086に対する抗血清は、全細胞ELISAにより試験した10種の2086サブファミリーB菌株すべてに対して表面反応性を示した。殺菌活性は異種セロサブタイプ抗原、PorAを発現する10種の2086サブファミリーB菌株のうち9種に対して検出された。これらの菌株は西ヨーロッパ、アメリカ、オーストラリア、およびニュージーランド全体にわたってセログループB髄膜炎菌性疾患を引き起こす代表的な菌株である。殺菌アッセイで致死されなかった唯一の菌株、870227は、全細胞ELISAにより抗rLP2086(サブファミリーB)血清と強く反応し、この菌株がP2086に共通のエピトープを持つタンパク質を発現することを示した。
免疫原性方法:
抗血清の調製:
ワクチンを、前に実施例1に記載されるように製剤した。しかしながら、10μg投与量を使用した。
全細胞酵素結合免疫吸着アッセイ(ELISA):
N.meningitidis全細胞懸濁液を、無菌0.01M ホスフェート、0.137M NaCl、0.002M KCl(PBS)中、620nmにおける吸光度0.1に希釈した。この懸濁液から、0.1mLをNunc Bac T96ウェルプレート(Cat# 2−69620)の各々のウェルに添加した。細胞は室温で3日間、プレート上で乾燥し、その後覆い、反転させ、4℃で保存した。プレートは洗浄バッファー(0.01M Tris−HCl、0.139M NaCl/KCl、0.1%ドデシルポリ(オキシエチレレングリコールエーテル)n n=23(Brij−35(登録商標)、ICI Americas,Inc.,Wilmington,Delawareから入手可能)、pH7.0〜7.4)で3回洗浄した。抗血清の希釈物を、PBS、0.05%Tween−20/アジドで調製し、そして0.1mLを被覆したプレートに移した。プレートを2時間37℃でインキュベートした。プレートは洗浄バッファーで3回洗浄した。ヤギ−抗マウスIgG AP(Southern Biotech)をPBS/0.05%Tween−20で1:1500に希釈し、0.1mLを各々のウェルに添加し、プレートを37℃で2時間インキュベートした。プレートは(上記のように)洗浄した。基質溶液は、1M ジエタノールアミン/0.5mM MgCl2中にp−ニトロフェニルホスフェート(Sigma)を1mg/mLに溶解することにより調製した。基質はウェルあたり0.1mLでプレートに添加し、室温で1時間インキュベートした。反応は50μL/ウェルの3N NaOHで停止させ、プレートは、690nmを基準として、405nmで読み取った。
B.)P4リーダー配列:
PCR増幅およびクローニング法:
rLP2086発現を最適化するために、2086遺伝子を型分類不能なHaemophilus influenzaeのP4シグナル配列の後にクローニングした(Greenら、1991)。リポタンパク質クローニングに使用されたプライマーが表IVに列挙してあり、化合物番号:5658、5660、6473、6543および6385によって識別される。ORF2086は、以下の化合物番号5658および5660を持つプライマーを使用してN.meningitidisセログループB菌株8529から増幅された。ORF2086は、以下の化合物番号6385および5660を持つプライマーを使用してN.meningitidisセログループB菌株CDC1573から増幅された。ORF2086は、以下の化合物番号6473および6543を持つプライマーを使用してN.meningitidisセログループB菌株2996から増幅された。N末端(5’)プライマーは、2086遺伝子の成熟領域(システインのすぐ下流のアミノ酸位置3のセリン残基において開始)に相同であるように設計した。制限部位BamHI(GGATTC)はそれぞれのN−末端プライマーの5’末端に組み込まれ、アミノ酸位置2において成熟タンパク質にグリシン残基が挿入された。C末端(3’)プライマーは2086遺伝子のC−末端に相同であるように設計され、終止コドンおよびクローニングのためにSphI部位を含有した。各N.meningitidis B菌株から増幅されたフラグメントを、中間ベクターにクローニングし、配列分析によってスクリーニングした。
[P4シグナル配列]−TGT GGA TCC−[残存2086成熟核酸配列]
[P4シグナル配列]−Cys Gly Ser−[残存2086成熟アミノ酸配列]
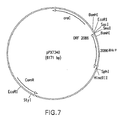
図7を参照すると、各増幅されたフラグメントはP4リーダー配列を含有する改変pBAD18−Cmベクターにクローニングされた。発酵はrP4LP2086(組換えP4脂質化2086)を発現する組換えE.coli BLR pPX7343で行い、付加的グルコースの添加により細胞密度増大を試みた。発酵装置は、1%グルコースを補足したSambrookの完全M9最小培地10Lで満たした。
非脂質化成熟2086タンパク質の発生遺伝学:
2086タンパク質の免疫原性をさらに評価するため、P2086の非脂質化型のクローニングおよび発現を行った。
ORF2086のPCR遺伝子増幅:
様々な染色由来の2086遺伝子が、参照により本明細書に組み込まれる国際出願PCT/US02/32369号(2003年8月7日、国際公開第03/063766号として公開)、および国際出願PCT/US04/11901号(2004年11月4日、国際公開第04/094596号として公開)に記載されるように、プライマーで増幅され得る。
非脂質化2086発現のための産生菌株または細胞系統の調製:
2086遺伝子は、髄膜炎菌株8529に由来する染色体DNAからポリメラーゼ連鎖反応(PCR)[AmpliTaq and ABI2400サーマルサイクラー,Applied Biosystems,Foster City,CA]により増幅した。2086遺伝子のPCR増幅は、それぞれの反応において化合物番号6474および5135によって同定された2種のオリゴヌレオチドプライマーを使用した。増幅された2086PCR産物はTOPO−PCR2.1クローニングベクターに直接クローニングし、100μg/mlアンピシリンおよび20μg/ml X−Galを補ったテリフィックブロス寒天培地で選択した。白色コロニーを選択し、培養した。プラスミドDNAは、Qiagen miniprepキットを使用して調製し、該プラスミドをPCRフラグメントインサートに関してスクリーニングした。PCRインサートプラスミドを、DNA配列決定にかけた(ABI377シークエンサーでのBig Dye化学,Applied Biosystems,Foster City,CA)。
非脂質化2086タンパク質の産生:
精製プラスミドDNAを用い、発現菌株BLR(DE3)pLysSを形質転換した。プラスミドを持つBLR(DE3)pLysS細胞は、カナマイシン耐性で、1mM IPTGの添加により高レベルのPorAタンパク質を発現するように誘導することができる。rP2086T7融合タンパク質は、E.coli細胞系統BLR(DE3)pLysS中に不溶性封入体として、全タンパク質の約40%において発現させることができる。この精製融合タンパク質は、マウスを免疫するために用いられ、異種髄膜炎菌株に対する有意レベルの殺菌抗体を生成した(表V参照)。
2086非脂質化遺伝子変異誘発:
PCRプライマー変異誘発は2086遺伝子の5’末端で行われた。成熟rP2086T7の高発現レベルを示しつつT7−タグを除去できるかどうかを確かめるための発現研究が進行中である。
非脂質化rP2086T7の精製:
非脂質化rP2086T7を発現するE.coliBLR(DE3)pLysS細胞を、10mM HEPES−NaOH/5mM EDTA/1mM Pefabloc SC pH7.4中で、マイクロフルイダイザーにより溶解した。細胞ライゼートを18,000xgで30分間遠心分離した。封入体ペレットを50mM Tris−HCl/5mM EDTA/1%Triton X−100 pH8で3回洗浄し、都度24,000xgで30分間遠心分離した。次に封入体ペレットを50mM Tris−HCl/5mM EDTA/1%Zwittergent3−14 pH8で2回洗浄し、都度24,000xgで15分間遠心分離した。続いて封入体ペレットを50mM Tris−HCl/5mM EDTA/4M 尿素 pH8で2時間可溶化し、その後不溶性物質を遠心分離により除去した。上澄み(可溶化rP2086T7)を4つの等しい試料に分けた。保存溶液を使用して、1つは50mM Tris−HCl/5mM EDTA/250mM NaCl/2M 尿素 pH8(界面活性剤を含まない)に調整し、1つは50mM Tris−HCl/5mM EDTA/250mM NaCl/2M 尿素/1%水素化Triton X−100 pH8(TX−100)に調整し、1つは50mM Tris−HCl/5mM EDTA/250mM NaCl/2M 尿素/1%Zwittergent3−12 pH8(Z3−12)に調整し、そして1つは50mM Tris−HCl/5mM EDTA/250mM NaCl/2M 尿素/1%Zwittergent3−14 pH8(Z3−14)に調整した。尿素を除去するために、尿素を含まないそれぞれのバッファーに対して試料を透析した。次に尿素を含まずに60mM NaClを含むそれぞれのバッファーに対して試料を透析し、NaCl濃度を減少させた。不溶性物質は2,000xgで15分間遠心分離することにより除去し、得られた上澄み(再生rP2086T7)をその後の実験に使用した。rP2086T7の均一性は、クーマシー染色したSDS−PAGEおよびレーザーデンシトメトリーを使用して測定し、91〜95%であることが見出された。
この精製融合タンパク質を使用してマウスを免疫化し、異種髄膜炎菌株に対する有意レベルの殺菌抗体を生成した。(以下の表V参照):
(実施例4)
ORF2086のキメラクローンの開発
菌株CDC−1573由来の2086タンパク質N末端領域は、菌株8529および2996由来の2086遺伝子には存在しない反復部分を含有する(図8参照)。この反復部分は、E.coliベースの2つの発現系(pETおよびpBAD)由来の高レベルの組換え2086タンパク質発現に関与すると考えられる。pETおよびpBAD発現系におけるCDC−1573 2086遺伝子由来の組換えタンパク質発現レベルは、同じ系を使用した菌株8529および2996による2086遺伝子由来の組換え体発現レベルに比較して有意に良好であった。3種すべての菌株に由来する2086遺伝子のN末端領域は、この反復部分以外は比較的相同である。したがって、pETおよびpBAD系を使用した場合、菌株8529および2996由来の2086遺伝子にCDC−1573N末端を融合することにより、これらの遺伝子から発現される組換え2086タンパク質レベルが増大すると考えることは妥当である。
材料および方法:
菌株8529および2996由来の染色体DNAを精製し、キメラ2086遺伝子のPCR増幅のための鋳型として使用した。化合物番号6721および5135を持つPCRプライマーを使用して菌株8529由来のキメラ2086遺伝子を増幅し、化合物番号6721および6605を持つPCRプライマーを使用して、菌株2996由来のキメラ2086遺伝子を増幅した。PCR産物は、InvitrogenのPCR2.1 TOPOベクターに直接クローニングし、次にDNA配列分析によりスクリーニングして、無傷のキメラ2086遺伝子を同定した。次にその遺伝子をBglIIによりPCR2.1ベクターから開裂し、BglIIフラグメントをpET9aプラスミドのBamHI部位に挿入した。プラスミドインサートが適切な配向であることをスクリーニングした後、NdeI消化にかけた。線状NdeIフラグメントは自己連結し、pET9aベクターによって与えられたT7−タグ配列を含有する小NdeIフラグメントの欠失が達成された。この欠失は、キメラ2086遺伝子の5’末端にT7プロモーターを直接結合する。NdeI欠失プラスミドをE.coli菌株BL21(DE3)に形質転換し、カナマイシン耐性コロニーをIPTG誘導によるキメラ2086タンパク質発現に関してスクリーニングした。
(実施例5)
N.meningitidis菌株の2086PCRスクリーニング:
臨床分離菌間の2086遺伝子の保存を確かめるために、88のN.meningitidis菌株にPCR増幅を行った。
(実施例6)
髄膜炎菌株に対するrLP2086抗血清の反応性:
以下の表、表VIIは、上述のrLP2086の交差反応性および交差保護能力を示す。表に示すように、rLP2086は、全細胞ELISA(WCE)力価、殺菌アッセイ(BCA)および幼若ラット(IR)アッセイを含む、多様な手法を使用して処理および分析して、2086タンパク質に対して引き起こされたポリクローナル抗体の細菌表面反応性を確認した。
− 菌血病において10分の1減少より小
(実施例7)
ORF2086タンパク質を発現させるための種々の構築物を調製した。以下の表、表VIIIは、例を示し、本発明の実施を例示するために提供されるr2086構築物表であるが、それらに限定されない。
LOS除去外膜タンパク質を用いたさらなる研究から、異種セロサブタイプを発現する菌株に殺菌抗体を誘導することができる、PorA以外の外膜タンパク質(単数または複数)を産生する付加的な菌株を同定した。以下に、本発明の一実施態様による付加的なタンパク質、具体的には髄膜炎菌免疫原性組成物に必要なタンパク質の数を減少させることができる外膜リポタンパク質を同定するためのさらなる研究を記載する。これらのさらなる研究は、以前の実施例に記載された研究を補足する。
以下の表、表Xはおよび表XIは、サブファミリーAおよびサブファミリーB両方の組換え脂質化P2086(rLP2086)の精製および特徴の概要を示す。
サブファミリーA rLP2086精製
2 SDS−PAGEおよびコロイド状クーマシー染色バンド(Simply Blue染色)のレーザーデンシトメトリーにより確認した純度
同種および異種菌株に対して試験された、サブファミリーBメンバー、rLP2086−8529の免疫原性。
b 吸光度=0.1における希釈度の逆数として表したエンドポイント力価
c 生細胞数を50%減少させる抗血清の希釈度の逆数として表したBC50力価。0週目の正常マウス血清のBC50力価は<10であった。
b 吸光度=0.1における希釈度の逆数として表したエンドポイント力価
c 生細胞数を50%減少させる抗血清の希釈度の逆数として表した殺菌性(BC50)力価。0週目の正常マウス血清のBC50力価は<10であった。
c 適切な1価対照:rLP2086−8529、rLP2086−2996、rP1.5−1,2−2またはrP1.22−1,14−1抗血清
以下に上記の研究の結果を概説する。抗rLP2086抗血清は、13/16の試験菌株に対して殺菌性である。異なるセロサブタイプを発現する11種の菌株は抗P2086血清により致死する。抗rLP2086血清の殺菌活性は抗rPorA血清に相補的である。P2086とPorAとの混合物は、マウスに相補的殺菌抗体を誘導する。ディファレンシャル界面活性剤抽出、精製および免疫、ならびに多くの菌株に対する機能的抗体アッセイを使用して、新規ワクチン候補を同定することができる。P2086は、P2086およびrPorAの両方において異種の菌株に対し殺菌抗体を誘導するワクチン候補として同定されている。したがって、タンパク質の2086ファミリーは、単独で、または別の髄膜炎菌抗原と組み合わせて有用なワクチンであり得る。
(実施例9)
変化するセログループの髄膜炎菌株を、ORF2086遺伝子の存在についてPCRによりスクリーニングした。結局、100種以上の髄膜炎菌株をスクリーニングした。
N.meningitidisA、B、C,W135、Y
N.lactamica
N.gonorrhoeaeFA1090
いくつかのORF2086遺伝子は、クローニングされ、組換え発現されている
P2086の脂質化バージョンは、種々の髄膜炎菌株から発現された。
(実施例11)
参考文献一覧
本明細書中で参照した参考文献が以下に記載され、それらは、参照によりその全体が本明細書に組み込まれる:
Claims (84)
- ポリヌクレオチドであって、
(a) 配列番号1−11の奇数番号配列のいずれかと少なくとも約95%配列同一性を有するヌクレオチド配列、または
(b) 配列番号2−12の偶数番号配列のいずれかのアミノ酸配列と少なくとも約95%配列同一性を有するアミノ酸配列を含むポリペプチドをコードするヌクレオチド、
を含む
ポリヌクレオチド。 - 前記ヌクレオチド配列が、配列番号1−11の奇数番号配列のいずれかと少なくとも約95%配列同一性を有する、請求項1に記載のポリヌクレオチド。
- 前記ヌクレオチド配列が、配列番号1−11の奇数番号配列のいずれかを含む、請求項1に記載のポリヌクレオチド。
- 前記ヌクレオチド配列が、配列番号2−12の偶数番号配列のいずれかのアミノ酸配列と少なくとも約95%配列同一性を有するアミノ酸配列を含むポリペプチドをコードする、請求項1に記載のポリヌクレオチド。
- 前記ヌクレオチド配列が、配列番号2−12の偶数番号配列のうちのいずれかを含むポリペプチドをコードする、請求項1に記載のポリヌクレオチド。
- 前記ヌクレオチド配列が、配列番号1−5の奇数番号配列のいずれかと少なくとも約95%配列同一性を有する、請求項1に記載のポリヌクレオチド。
- 前記ヌクレオチド配列が、配列番号1−5の奇数番号配列のいずれかを含む、請求項1に記載のポリヌクレオチド。
- 前記ヌクレオチド配列が、配列番号2−6の偶数番号配列のいずれかのアミノ酸配列と少なくとも約95%配列同一性を有するアミノ酸配列を含むポリペプチドをコードする、請求項1に記載のポリヌクレオチド。
- 前記ヌクレオチド配列が、配列番号2−6の偶数番号配列のうちのいずれかを含むポリペプチドをコードする、請求項1に記載のポリヌクレオチド。
- 前記ヌクレオチド配列が、配列番号7−11の奇数番号配列のいずれかと少なくとも約95%配列同一性を有する、請求項1に記載のポリヌクレオチド。
- 前記ヌクレオチド配列が、配列番号7−11の奇数番号配列のうちのいずれかを含むポリペプチドをコードする、請求項1に記載のポリヌクレオチド。
- 前記ヌクレオチド配列が、配列番号8−12の偶数番号配列のいずれかのアミノ酸配列と少なくとも約95%配列同一性を有するアミノ酸配列を含むポリペプチドをコードする、請求項1に記載のポリヌクレオチド。
- 前記ヌクレオチド配列が、配列番号8−12の偶数番号配列のいずれかを含むポリペプチドをコードする、請求項1に記載のポリヌクレオチド。
- 前記ポリヌクレオチドが、N.meningitidisセログループBに対する抗体を誘導するポリペプチドをコードする、請求項1に記載のポリヌクレオチド。
- 前記ポリヌクレオチドが、N.meningitidisセログループBサブファミリーAに対する抗体を誘導するポリペプチドをコードする、請求項1に記載のポリヌクレオチド。
- 前記ポリヌクレオチドが、N.meningitidisセログループBサブファミリーBに対する抗体を誘導するポリペプチドをコードする、請求項1に記載のポリヌクレオチド。
- 前記ポリヌクレオチドが組換えポリヌクレオチドである、請求項1〜16のいずれかに記載のポリヌクレオチド。
- 前記ポリヌクレオチドが天然供給源から単離される、請求項1〜16のいずれかに記載のポリヌクレオチド。
- 請求項1〜18のいずれかに記載のポリヌクレオチドを含むベクター。
- 前記ベクターがプラスミドである、請求項19に記載のベクター。
- 前記ベクターがファージである、請求項19に記載のベクター。
- 前記ベクターがバクテリオファージである、請求項19に記載のベクター。
- 前記ベクターが穏和ファージ(moderate phage)である、請求項19に記載のベクター。
- 請求項19〜23のいずれかに記載のベクターを含む、組換え細胞。
- 前記組換え細胞がハイブリドーマである、請求項24に記載の組換え細胞。
- 前記組換え細胞がトリオーマである、請求項24に記載の組換え細胞。
- ポリペプチドであって、
(a) 配列番号2−12の偶数番号配列のいずれかと少なくとも95%配列同一性を有するアミノ酸配列、
(b) 配列番号1−11の奇数番号配列のいずれかと少なくとも95%配列同一性を有するヌクレオチド配列によってコードされるアミノ酸配列、
(c) (a)もしくは(b)に記載されたアミノ酸配列の少なくとも1つの免疫原性部分、あるいは
(d) (a)もしくは(b)に記載されたアミノ酸配列または(c)に記載された免疫原性部分の少なくとも1つの生物学的等価物、
を含む
ポリペプチド。 - 前記ポリペプチドが、配列番号2−12の偶数番号配列のいずれかと少なくとも95%配列同一性を有するアミノ酸配列を含む、請求項27に記載のポリペプチド。
- 前記ポリペプチドが、配列番号2−12の偶数番号配列のいずれかのアミノ酸配列を含む、請求項27に記載のポリペプチド。
- 前記ポリペプチドが、配列番号1−11の奇数番号配列のいずれかと少なくとも95%配列同一性を有するヌクレオチド配列によってコードされるアミノ酸配列を含む、請求項27に記載のポリペプチド。
- 前記ポリペプチドが、配列番号1−11の奇数番号配列のいずれかの核酸配列によってコードされるアミノ酸配列を含む、請求項27に記載のポリペプチド。
- 前記ポリペプチドが、配列番号2−6の偶数番号配列のいずれかと少なくとも95%配列同一性を有するアミノ酸配列を含む、請求項27に記載のポリペプチド。
- 前記ポリペプチドが、配列番号2−6の偶数番号配列のいずれかのアミノ酸配列を含む、請求項27に記載のポリペプチド。
- 前記ポリペプチドが、配列番号1−5の奇数番号配列のいずれかと少なくとも95%配列同一性を有するヌクレオチド配列によってコードされるアミノ酸配列を含む、請求項27に記載のポリペプチド。
- 前記ポリペプチドが、配列番号1−5の奇数番号配列のいずれかの核酸配列によってコードされるアミノ酸配列を含む、請求項27に記載のポリペプチド。
- 前記ポリペプチドが、配列番号8−12の偶数番号配列のいずれかと少なくとも95%配列同一性を有するアミノ酸配列を含む、請求項27に記載のポリペプチド:。
- 前記ポリペプチドが、配列番号8−12の偶数番号配列のいずれかのアミノ酸配列を含む、請求項27に記載のポリペプチド。
- 前記ポリペプチドが、配列番号7−11の奇数番号配列のいずれかと少なくとも95%配列同一性を有するヌクレオチド配列によってコードされるアミノ酸配列を含む、請求項27に記載のポリペプチド。
- 前記ポリペプチドが、配列番号7−11の奇数番号配列のいずれかの核酸配列によってコードされるアミノ酸配列を含む、請求項27に記載のポリペプチド。
- 少なくとも1種のPorA、PorB、トランスフェリン結合タンパク質、または不透明タンパク質(opacity protein)(Opc)をさらに含む、請求項27に記載のポリペプチド。
- Neisseria speciesの少なくとも1種の付加的な表面抗原をさらに含み、該付加的な表面抗原が、非ORF2086タンパク質である、請求項27に記載のポリペプチド。
- 前記ポリペプチドが、質量分析により測定される場合に、約26,000〜約30,000の分子量を有する、請求項27に記載のポリペプチド。
- 前記ポリペプチドが、10%−20%SDSポリアクリルアミドゲル上で測定される場合に、約28〜35kDaの分子量を有する、請求項27に記載のポリペプチド。
- 前記ポリペプチドが非脂質化タンパク質である、請求項27に記載のポリペプチド。
- 前記ポリペプチドが組換えタンパク質である、請求項27に記載のポリペプチド。
- 前記ポリペプチドが天然のNeisseria speciesから単離される、請求項27に記載のポリペプチド。
- 抗体であって、
(a) 偶数番号の配列番号2−12のいずれかのアミノ酸配列を含むポリペプチドと免疫特異的に結合するポリペプチド、または
(b) (a)に記載されたポリペプチドの少なくとも1つの免疫原性部分、または
(c) (a)に記載されたポリペプチドもしくは(b)に記載された1つの免疫原性部分の少なくとも1つの生物学的等価物、
のいずれかを含む
抗体。 - 少なくとも1つの抗体がモノクローナル抗体である、請求項47に記載の抗体。
- ポリヌクレオチド、ベクター、組換え細胞、ポリペプチドまたは請求項1〜48のいずれかに記載の抗体を含む、組成物。
- 前記組成物が、薬学的に許容されるバッファー、希釈剤、およびアジュバントまたは担体をさらに含む、請求項49に記載の組成物。
- 前記組成物が担体をさらに含む、請求項49に記載の組成物。
- 前記組成物がアジュバントをさらに含む、請求項49に記載の組成物。
- 前記アジュバントが液体を含む、請求項52に記載の組成物。
- 前記ポリペプチドがリポタンパク質である、請求項49に記載の組成物。
- 前記組成物が多糖をさらに含む、請求項49に記載の組成物。
- 前記組成物が、前記ポリペプチドと結合体を形成する付加的なペプチド、ポリペプチドまたはタンパク質を含む、請求項49に記載の組成物。
- 前記付加的なペプチド、ポリペプチドまたはタンパク質が、哺乳動物において2種以上の細菌に対する免疫応答を引き起こす結合体を形成する、請求項56に記載の組成物。
- 前記組成物が、付加的なペプチド、ポリペプチドまたはタンパク質をコードする核酸配列をさらに含む、請求項49に記載の組成物。
- 組成物であって、
(a) 配列番号1−5の奇数番号配列のいずれかと少なくとも約95%配列同一性または配列番号2−6の偶数番号配列のいずれかのアミノ酸配列をコードするヌクレオチド配列と少なくとも約95%配列同一性を有するヌクレオチド配列を含む第1のポリヌクレオチドと、
(b) 配列番号7−11の奇数番号配列のいずれかと少なくとも約95%配列同一性または配列番号8−12の偶数番号配列のいずれかのアミノ酸配列をコードするヌクレオチド配列と少なくとも約95%配列同一性を有するヌクレオチド配列を含む第2のポリヌクレオチドと、
を含む、
組成物。 - 前記第1のポリヌクレオチドが、配列番号1−5の奇数番号配列のいずれかを含む、請求項59に記載の組成物。
- 前記第2のポリヌクレオチド配列が、配列番号7−11の奇数番号配列のいずれか含む、請求項59に記載の組成物。
- 組成物であって、
(a) 配列番号2−6の偶数番号配列のいずれかと少なくとも約95%配列同一性を有するアミノ酸配列を含む第1のポリペプチドと、
(b) 配列番号8−12の偶数番号配列のいずれかと少なくとも約95%配列同一性を有するアミノ酸配列を含む第2のポリペプチドと、
を含む
組成物。 - 前記第1のポリペプチドが、配列番号2−6の偶数番号配列のいずれかのアミノ酸配列を含む、請求項62に記載の組成物。
- 前記第2のポリペプチドが、配列番号8−12の偶数番号配列のいずれかのアミノ酸配列を含む、請求項62に記載の組成物。
- 組成物であって、
(a) 偶数番号の配列番号2−12のいずれかのアミノ酸配列を含むポリペプチド、
(b) 奇数番号の配列番号1−11のいずれかの核酸配列を含むポリヌクレオチドによりコードされたポリペプチド、
(c) (a)または(b)に記載されたポリペプチドの免疫原性部分、あるいは
(d) (a)もしくは(b)に記載されたポリペプチドまたは(c)に記載された免疫原性フラグメントの生物学的等価物
のいずれかを、
Neisseria speciesから単離および精製、または組換えにより調製するステップを含むプロセスにより調製される
組成物。 - 哺乳動物において免疫応答を引き起こすための薬剤の調製における、請求項49〜65にいずれかに記載の組成物の使用。
- 前記組成物が非経口的に投与される、請求項66に記載の使用。
- 前記組成物が粘膜的に投与される、請求項66に記載の使用。
- 哺乳動物における細菌性髄膜炎に対して効果的な薬剤における、請求項49〜65のいずれかに記載の組成物の使用。
- 前記組成物が非経口的に投与される、請求項69に記載の組成物の使用。
- 前記組成物が粘膜的に投与される、請求項69に記載の組成物の使用。
- 前記組成物が皮下または筋肉内注射により投与される、請求項69に記載の組成物の使用。
- 組成物を調製する方法であって、
本明細書中で記載されるポリペプチドのいずれかをコードする核酸配列を宿主細胞中で発現させるステップを含む、
方法。 - 前記核酸配列がin vivoで発現される、請求項73に記載の方法。
- 前記核酸配列がin vitroで発現される、請求項73に記載の方法。
- 前記ポリペプチドを発現させるためにP4リーダー配列を前記核酸配列と関連付けるステップをさらに含む、請求項73に記載の方法。
- 抗体組成物を調製する方法であって、
本明細書中で記載されるポリペプチド、タンパク質、免疫原性部分または生物学的等価物のいずれかを含む組成物を動物に導入した後、該動物から抗体を回収するステップを含む、
方法。 - 哺乳動物において免疫応答を引き起こす方法であって、
請求項49〜65に記載の1種以上の組成物の有効量を該哺乳動物に投与するステップを含む、
方法。 - 前記組成物が非経口的に投与される、請求項78に記載の方法。
- 前記組成物が粘膜的に投与される、前記の請求項78に記載の方法。
- 哺乳動物において細菌性髄膜炎を予防または処置する方法であって、
請求項49〜65に記載の1種以上の組成物の有効量を該哺乳動物に投与するステップを含む、
方法。 - 前記組成物が非経口的に投与される、請求項81に記載の方法。
- 前記組成物が粘膜的に投与される、請求項81に記載の方法。
- 前記組成物が皮下または筋肉内注射により投与される、請求項81に記載の方法。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US87648606P | 2006-12-22 | 2006-12-22 | |
| PCT/US2007/026238 WO2008079372A2 (en) | 2006-12-22 | 2007-12-21 | Novel immunogenic compositions for the prevention and treatment of meningococcal disease |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010512792A true JP2010512792A (ja) | 2010-04-30 |
| JP2010512792A5 JP2010512792A5 (ja) | 2011-02-17 |
Family
ID=39563116
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2009542957A Pending JP2010512792A (ja) | 2006-12-22 | 2007-12-21 | 髄膜炎菌性疾患の予防および処置のための新規な免疫原性組成物 |
Country Status (12)
| Country | Link |
|---|---|
| US (1) | US8574597B2 (ja) |
| EP (1) | EP2094294A2 (ja) |
| JP (1) | JP2010512792A (ja) |
| CN (1) | CN101631858A (ja) |
| AR (1) | AR064642A1 (ja) |
| AU (1) | AU2007338690B2 (ja) |
| BR (1) | BRPI0721003B8 (ja) |
| CA (1) | CA2673515C (ja) |
| CL (1) | CL2007003771A1 (ja) |
| MX (1) | MX2009006760A (ja) |
| TW (1) | TW200844226A (ja) |
| WO (1) | WO2008079372A2 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016515104A (ja) * | 2013-03-08 | 2016-05-26 | ファイザー・インク | 免疫原性融合ポリペプチド |
Families Citing this family (35)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2261343A3 (en) | 1998-05-01 | 2012-01-18 | Novartis Vaccines and Diagnostics, Inc. | Neisseria meningitidis antigens and compositions |
| CA2929348A1 (en) | 1999-05-19 | 2000-11-30 | Novartis Vaccines And Diagnostics S.R.L. | Combination neisserial compositions |
| ES2543736T3 (es) | 1999-10-29 | 2015-08-21 | Glaxosmithkline Biologicals Sa | Péptidos antigénicos de Neisseria |
| PT2270030E (pt) * | 2000-02-28 | 2012-07-24 | Novartis Vaccines & Diagnostic | Expressão heteróloga de proteínas de neisseria |
| GB0118249D0 (en) | 2001-07-26 | 2001-09-19 | Chiron Spa | Histidine vaccines |
| GB0121591D0 (en) | 2001-09-06 | 2001-10-24 | Chiron Spa | Hybrid and tandem expression of neisserial proteins |
| MX339524B (es) | 2001-10-11 | 2016-05-30 | Wyeth Corp | Composiciones inmunogenicas novedosas para la prevencion y tratamiento de enfermedad meningococica. |
| GB0227346D0 (en) | 2002-11-22 | 2002-12-31 | Chiron Spa | 741 |
| GB0408977D0 (en) | 2004-04-22 | 2004-05-26 | Chiron Srl | Immunising against meningococcal serogroup Y using proteins |
| GB0524066D0 (en) | 2005-11-25 | 2006-01-04 | Chiron Srl | 741 ii |
| US8466259B2 (en) | 2007-12-07 | 2013-06-18 | National Health Research Institutes | Adjuvants |
| US8426163B2 (en) | 2007-12-07 | 2013-04-23 | National Health Research Institutes | Production of lipidated proteins in E. coli |
| US9579372B2 (en) | 2008-02-21 | 2017-02-28 | Glaxosmithkline Biologicals Sa | Meningococcal fHBP polypeptides |
| PL2411048T3 (pl) | 2009-03-24 | 2020-11-16 | Glaxosmithkline Biologicals Sa | Adjuwantowe meningokokowe białko wiążące czynnik h |
| US8287880B2 (en) | 2009-06-02 | 2012-10-16 | National Health Research Institutes | Lipidated vaccine against dengue virus infection |
| CN102482327B (zh) | 2009-06-22 | 2014-10-29 | 财团法人卫生研究院 | 脂质化肿瘤相关抗原及其免疫治疗的组成物及方法 |
| CN102724988B (zh) | 2009-09-30 | 2014-09-10 | 诺华股份有限公司 | 脑膜炎球菌fHBP多肽的表达 |
| CA2779506A1 (en) * | 2009-10-02 | 2011-04-07 | University Of Iowa Research Foundation | Methods of improving vaccine immunogenicity |
| EP2585106A1 (en) * | 2010-06-25 | 2013-05-01 | Novartis AG | Combinations of meningococcal factor h binding proteins |
| KR101594228B1 (ko) | 2010-08-23 | 2016-02-15 | 와이어쓰 엘엘씨 | 네이세리아 메닌기티디스 rLP2086 항원의 안정한 제제 |
| AU2011300409B2 (en) | 2010-09-10 | 2015-03-26 | Wyeth Llc | Non-lipidated variants of Neisseria meningitidis ORF2086 antigens |
| TW201221642A (en) * | 2010-11-15 | 2012-06-01 | Nat Health Research Institutes | Method of producing lipidated polypeptides |
| TWI507413B (zh) | 2010-11-15 | 2015-11-11 | Nat Health Research Institutes | 脂質化多抗原表位疫苗 |
| BR112014016223A8 (pt) | 2011-12-29 | 2017-07-04 | Novartis Ag | combinações adjuvantes de proteínas de ligação de fator h meningocócico |
| KR101763625B1 (ko) | 2012-03-09 | 2017-08-01 | 화이자 인코포레이티드 | 수막염균 조성물 및 이의 사용 방법 |
| SA115360586B1 (ar) | 2012-03-09 | 2017-04-12 | فايزر انك | تركيبات لعلاج الالتهاب السحائي البكتيري وطرق لتحضيرها |
| WO2013186753A1 (en) * | 2012-06-14 | 2013-12-19 | Novartis Ag | Vaccines for serogroup x meningococcus |
| AU2013295242C1 (en) | 2012-07-27 | 2018-08-09 | Institut National De La Sante Et De La Recherche Medicale | CD147 as receptor for pilus-mediated adhesion of meningococci to vascular endothelia |
| US9822150B2 (en) | 2013-09-08 | 2017-11-21 | Pfizer Inc. | Neisseria meningitidis compositions and methods thereof |
| EP3782643A1 (en) | 2014-02-28 | 2021-02-24 | GlaxoSmithKline Biologicals SA | Modified meningococcal fhbp polypeptides |
| EA201692552A1 (ru) | 2014-07-17 | 2017-06-30 | Глаксосмитклайн Байолоджикалс С.А. | МОДИФИЦИРОВАННЫЕ МЕНИНГОКОККОВЫЕ ПОЛИПЕПТИДЫ fHbp |
| BR112017000519A2 (pt) | 2014-07-17 | 2017-11-21 | Glaxosmithkline Biologicals Sa | "composição imunogênica, e, método para proteger um mamífero contra uma infecção meningocócica" |
| KR20170103009A (ko) | 2015-02-19 | 2017-09-12 | 화이자 인코포레이티드 | 나이세리아 메닌지티디스 조성물 및 그의 방법 |
| PE20191107A1 (es) | 2017-01-31 | 2019-08-26 | Pfizer | Composiciones de neisseria meningitidis y metodos respectivos |
| GB202016604D0 (en) * | 2020-10-20 | 2020-12-02 | Univ Of Oxford | Compositions and methods for inducing an immune response |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2004048404A2 (en) * | 2002-11-22 | 2004-06-10 | Chiron Srl | Multiple variants of meningococcal protein nmb1870 |
| WO2006081259A2 (en) * | 2005-01-27 | 2006-08-03 | Children's Hospital & Research Center At Oakland | Gna1870-based vesicle vaccines for broad spectrum protection against diseases caused by neisseria meningitidis |
Family Cites Families (144)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4376110A (en) | 1980-08-04 | 1983-03-08 | Hybritech, Incorporated | Immunometric assays using monoclonal antibodies |
| US4554101A (en) | 1981-01-09 | 1985-11-19 | New York Blood Center, Inc. | Identification and preparation of epitopes on antigens and allergens on the basis of hydrophilicity |
| CH660375A5 (it) | 1983-02-08 | 1987-04-15 | Sclavo Spa | Procedimento per la produzione di proteine correlate alla tossina difterica. |
| US4816567A (en) | 1983-04-08 | 1989-03-28 | Genentech, Inc. | Recombinant immunoglobin preparations |
| US4650764A (en) | 1983-04-12 | 1987-03-17 | Wisconsin Alumni Research Foundation | Helper cell |
| JPS6147500A (ja) | 1984-08-15 | 1986-03-07 | Res Dev Corp Of Japan | キメラモノクロ−ナル抗体及びその製造法 |
| EP0173494A3 (en) | 1984-08-27 | 1987-11-25 | The Board Of Trustees Of The Leland Stanford Junior University | Chimeric receptors by dna splicing and expression |
| GB8422238D0 (en) | 1984-09-03 | 1984-10-10 | Neuberger M S | Chimeric proteins |
| GB8424757D0 (en) | 1984-10-01 | 1984-11-07 | Pasteur Institut | Retroviral vector |
| SE8405493D0 (sv) | 1984-11-01 | 1984-11-01 | Bror Morein | Immunogent komplex samt sett for framstellning derav och anvendning derav som immunstimulerande medel |
| FR2573436B1 (fr) | 1984-11-20 | 1989-02-17 | Pasteur Institut | Adn recombinant comportant une sequence nucleotidique codant pour un polypeptide determine sous le controle d'un promoteur d'adenovirus, vecteurs contenant cet adn recombinant, cellules eucaryotes transformees par cet adn recombinant, produits d'excretion de ces cellules transformees et leurs applications, notamment a la constitution de vaccins |
| JPS61134325A (ja) | 1984-12-04 | 1986-06-21 | Teijin Ltd | ハイブリツド抗体遺伝子の発現方法 |
| US4797368A (en) | 1985-03-15 | 1989-01-10 | The United States Of America As Represented By The Department Of Health And Human Services | Adeno-associated virus as eukaryotic expression vector |
| US4666829A (en) | 1985-05-15 | 1987-05-19 | University Of California | Polypeptide marker for Alzheimer's disease and its use for diagnosis |
| EP0232262A4 (en) | 1985-08-15 | 1989-09-19 | Stauffer Chemical Co | MICROORGANISM PRODUCING TRYPTOPHANE. |
| US5078996A (en) | 1985-08-16 | 1992-01-07 | Immunex Corporation | Activation of macrophage tumoricidal activity by granulocyte-macrophage colony stimulating factor |
| US5139941A (en) | 1985-10-31 | 1992-08-18 | University Of Florida Research Foundation, Inc. | AAV transduction vectors |
| DE3689123T2 (de) | 1985-11-01 | 1994-03-03 | Xoma Corp | Modulare einheit von antikörpergenen, daraus hergestellte antikörper und verwendung. |
| US4861719A (en) | 1986-04-25 | 1989-08-29 | Fred Hutchinson Cancer Research Center | DNA constructs for retrovirus packaging cell lines |
| US5514581A (en) | 1986-11-04 | 1996-05-07 | Protein Polymer Technologies, Inc. | Functional recombinantly prepared synthetic protein polymer |
| US4980289A (en) | 1987-04-27 | 1990-12-25 | Wisconsin Alumni Research Foundation | Promoter deficient retroviral vector |
| US5057540A (en) | 1987-05-29 | 1991-10-15 | Cambridge Biotech Corporation | Saponin adjuvant |
| JPH01144977A (ja) | 1987-11-30 | 1989-06-07 | Agency Of Ind Science & Technol | 新規組換えプラスミドpTPGIF2 |
| AU3069189A (en) | 1988-02-05 | 1989-08-25 | Trustees Of Columbia University In The City Of New York, The | Retroviral packaging cell lines and processes of using same |
| US4912094B1 (en) | 1988-06-29 | 1994-02-15 | Ribi Immunochem Research Inc. | Modified lipopolysaccharides and process of preparation |
| CA1339354C (en) | 1988-09-01 | 1997-08-26 | The Whitehead Institute For Biomedical Research | Recombinant retroviruses with amphotropic and ecotropic host ranges |
| US5124263A (en) | 1989-01-12 | 1992-06-23 | Wisconsin Alumni Research Foundation | Recombination resistant retroviral helper cell and products produced thereby |
| ATE195076T1 (de) | 1989-03-09 | 2000-08-15 | American Cyanamid Co | Verfahren zur isolierung von haemopnilus influenzae protein-e |
| US5354844A (en) | 1989-03-16 | 1994-10-11 | Boehringer Ingelheim International Gmbh | Protein-polycation conjugates |
| US5703055A (en) | 1989-03-21 | 1997-12-30 | Wisconsin Alumni Research Foundation | Generation of antibodies through lipid mediated DNA delivery |
| US5399346A (en) | 1989-06-14 | 1995-03-21 | The United States Of America As Represented By The Department Of Health And Human Services | Gene therapy |
| US5585362A (en) | 1989-08-22 | 1996-12-17 | The Regents Of The University Of Michigan | Adenovirus vectors for gene therapy |
| CA2039921A1 (en) | 1990-04-16 | 1991-10-17 | Xandra O. Breakefield | Transfer and expression of gene sequences into central nervous system cells using herpes simplex virus mutants with deletions in genes for viral replication |
| US5264618A (en) | 1990-04-19 | 1993-11-23 | Vical, Inc. | Cationic lipids for intracellular delivery of biologically active molecules |
| WO1991018088A1 (en) | 1990-05-23 | 1991-11-28 | The United States Of America, Represented By The Secretary, United States Department Of Commerce | Adeno-associated virus (aav)-based eucaryotic vectors |
| EP0467714A1 (en) | 1990-07-19 | 1992-01-22 | Merck & Co. Inc. | The class II protein of the outer membrane of neisseria meningitidis |
| AU658836B2 (en) | 1990-09-25 | 1995-05-04 | Xenova Research Limited | Viral defective vaccine produced by transcomplementing cell line |
| US5173414A (en) | 1990-10-30 | 1992-12-22 | Applied Immune Sciences, Inc. | Production of recombinant adeno-associated virus vectors |
| IL101715A (en) | 1991-05-02 | 2005-06-19 | Amgen Inc | Recombinant dna-derived cholera toxin subunit analogs |
| WO1993007897A1 (en) | 1991-10-21 | 1993-04-29 | Medimmune, Inc. | Bacterial expression vectors containing dna encoding secretion signals of lipoproteins |
| US5252479A (en) | 1991-11-08 | 1993-10-12 | Research Corporation Technologies, Inc. | Safe vector for gene therapy |
| WO1993015115A1 (en) | 1992-01-24 | 1993-08-05 | Cornell Research Foundation, Inc. | E. coli dna polymerase iii holoenzyme and subunits |
| EP0911413A3 (en) | 1992-12-03 | 2000-11-15 | Genzyme Corporation | Minimal adenovirus-based gene therapy vector |
| DE69434079T2 (de) | 1993-03-05 | 2005-02-24 | Wyeth Holdings Corp. | Plasmid zur Herstellung von CRM-Protein und Diphtherie-Toxin |
| JPH08507784A (ja) | 1993-03-19 | 1996-08-20 | キャンタブ ファーマシューティカルズ リサーチ リミティド | ウイルス・ワクチン |
| ES2145072T3 (es) | 1993-05-13 | 2000-07-01 | American Cyanamid Co | Preparacion y usos de proteinas de membranas externas carentes de los de cocos gramnegativos. |
| FR2705361B1 (fr) | 1993-05-18 | 1995-08-04 | Centre Nat Rech Scient | Vecteurs viraux et utilisation en thérapie génique. |
| FR2705686B1 (fr) | 1993-05-28 | 1995-08-18 | Transgene Sa | Nouveaux adénovirus défectifs et lignées de complémentation correspondantes. |
| SK282843B6 (sk) | 1993-07-13 | 2002-12-03 | Rhone-Poulenc Rorer S. A. | Defektný rekombinantný adenovírus a farmaceutický prostriedok s jeho obsahom |
| AU7477394A (en) | 1993-07-30 | 1995-03-27 | University Of Medicine And Dentistry Of New Jersey | Efficient gene transfer into primary lymphocytes |
| FR2708622B1 (fr) | 1993-08-02 | 1997-04-18 | Raymond Hamers | Vecteur recombinant contenant une séquence d'un gène de lipoprotéine de structure pour l'expression de séquences de nucléotides. |
| US5550213A (en) | 1993-12-27 | 1996-08-27 | Rutgers, The State University Of New Jersey | Inhibitors of urokinase plasminogen activator |
| FR2714830B1 (fr) | 1994-01-10 | 1996-03-22 | Rhone Poulenc Rorer Sa | Composition contenant des acides nucléiques, préparation et utilisations. |
| US5589118A (en) * | 1994-01-21 | 1996-12-31 | Covol Technologies, Inc. | Process for recovering iron from iron-containing material |
| FR2715847B1 (fr) | 1994-02-08 | 1996-04-12 | Rhone Poulenc Rorer Sa | Composition contenant des acides nucléiques, préparation et utilisations. |
| FR2716459B1 (fr) | 1994-02-22 | 1996-05-10 | Univ Paris Curie | Système hôte-vecteur utilisable en thérapie génique. |
| AU2194895A (en) | 1994-03-25 | 1995-10-17 | Uab Research Foundation, The | Composition and methods for creating syngeneic recombinant virus-producing cells |
| US5739118A (en) | 1994-04-01 | 1998-04-14 | Apollon, Inc. | Compositions and methods for delivery of genetic material |
| EP0753069A1 (en) | 1994-04-15 | 1997-01-15 | Targeted Genetics Corporation | Gene delivery fusion proteins |
| US5571515A (en) | 1994-04-18 | 1996-11-05 | The Wistar Institute Of Anatomy & Biology | Compositions and methods for use of IL-12 as an adjuvant |
| US6207646B1 (en) | 1994-07-15 | 2001-03-27 | University Of Iowa Research Foundation | Immunostimulatory nucleic acid molecules |
| US5565204A (en) | 1994-08-24 | 1996-10-15 | American Cyanamid Company | Pneumococcal polysaccharide-recombinant pneumolysin conjugate vaccines for immunization against pneumococcal infections |
| US5837533A (en) | 1994-09-28 | 1998-11-17 | American Home Products Corporation | Complexes comprising a nucleic acid bound to a cationic polyamine having an endosome disruption agent |
| GB9422096D0 (en) | 1994-11-02 | 1994-12-21 | Biocine Spa | Combined meningitis vaccine |
| FR2727679B1 (fr) | 1994-12-05 | 1997-01-03 | Rhone Poulenc Rorer Sa | Nouveaux agents de transfection et leurs applications pharmaceutiques |
| IL116816A (en) | 1995-01-20 | 2003-05-29 | Rhone Poulenc Rorer Sa | Cell for the production of a defective recombinant adenovirus or an adeno-associated virus and the various uses thereof |
| FR2730637B1 (fr) | 1995-02-17 | 1997-03-28 | Rhone Poulenc Rorer Sa | Composition pharmaceutique contenant des acides nucleiques, et ses utilisations |
| IL117483A (en) | 1995-03-17 | 2008-03-20 | Bernard Brodeur | MENINGITIDIS NEISSERIA shell protein is resistant to proteinase K. |
| WO1996039036A1 (en) | 1995-06-05 | 1996-12-12 | The University Of Alabama At Birmingham Research Foundation | Composition and methods for creating syngeneic recombinant virus-producing cells |
| PT832093E (pt) | 1995-06-07 | 2006-12-29 | Sanofi Pasteur Inc | Expressão de lipoproteínas |
| FR2741358B1 (fr) | 1995-11-17 | 1998-01-02 | Centre Nat Rech Scient | Production de vecteurs retroviraux par l'intermediaire de vecteurs viraux a base de virus a adn |
| US6355255B1 (en) | 1998-12-07 | 2002-03-12 | Regents Of The University Of Minnesota | Streptococcal C5a peptidase vaccine |
| US5846547A (en) | 1996-01-22 | 1998-12-08 | Regents Of The University Of Minnesota | Streptococcal C5a peptidase vaccine |
| ATE252602T1 (de) | 1996-08-27 | 2003-11-15 | Chiron Corp | Meningokokkus b-epitop ausbildende monoklonale antikoerper und deren verwendung zur herstellung von impfstoffzusammenstellungen |
| ATE208629T1 (de) | 1996-08-27 | 2001-11-15 | Chiron Corp | Neisseria meningitidis serogruppe b glykokonjugate und verfahren zu deren verwendung |
| AU5426098A (en) | 1996-10-24 | 1998-05-15 | Emory University | Invasion associated genes from (neisseria meningitidis) serogroup |
| US6113918A (en) | 1997-05-08 | 2000-09-05 | Ribi Immunochem Research, Inc. | Aminoalkyl glucosamine phosphate compounds and their use as adjuvants and immunoeffectors |
| DE69826124T3 (de) | 1997-06-30 | 2007-10-11 | Institut Gustave Roussy | Verabreichung der nukleinsäure in den quergestreiften muskel |
| JP2002515816A (ja) | 1997-06-30 | 2002-05-28 | アバンテイス・フアルマ・エス・アー | in vivo組織に核酸ベクターを最適に電気導入する装置 |
| HUP0004728A3 (en) | 1997-06-30 | 2003-08-28 | Centre Nat Rech Scient | Improved method for transferring nucleic acid into multicelled eukaryotic organism cells and combination therefor |
| PT1630168E (pt) | 1997-08-27 | 2011-07-20 | Novartis Vaccines & Diagnostic | Compostos miméticos moleculares de péptidos de meningococos do serogrupo b |
| EP1900818A3 (en) | 1997-11-06 | 2008-06-11 | Novartis Vaccines and Diagnostics S.r.l. | Neisserial antigens |
| TWI239847B (en) | 1997-12-02 | 2005-09-21 | Elan Pharm Inc | N-terminal fragment of Abeta peptide and an adjuvant for preventing and treating amyloidogenic disease |
| CA2317815A1 (en) | 1998-01-14 | 1999-07-22 | Chiron S.P.A. | Neisseria meningitidis antigens |
| JP4290875B2 (ja) | 1998-02-03 | 2009-07-08 | センター フォア ディズィーズ コントロール アンド プリヴェンション | 組換え脂質化PsaAタンパク質、調製法および使用 |
| GB9808734D0 (en) | 1998-04-23 | 1998-06-24 | Smithkline Beecham Biolog | Novel compounds |
| GB9808932D0 (en) | 1998-04-27 | 1998-06-24 | Chiron Spa | Polyepitope carrier protein |
| EP2261343A3 (en) * | 1998-05-01 | 2012-01-18 | Novartis Vaccines and Diagnostics, Inc. | Neisseria meningitidis antigens and compositions |
| DE69937571T2 (de) | 1998-09-30 | 2008-09-04 | The Government Of The United States Of America As Represented By The Uniformed Services University Of The Health Sciences | Mutiertes cholera holotoxin als hilfsmittel |
| JP2004511201A (ja) | 1998-10-09 | 2004-04-15 | カイロン コーポレイション | ナイセリアゲノム配列およびそれらの使用方法 |
| GB9902084D0 (en) | 1999-01-29 | 1999-03-24 | Smithkline Beecham Biolog | Novel compounds |
| CA2371032A1 (en) | 1999-04-30 | 2000-11-09 | Chiron Corporation | Neisseria genomic sequences and methods of their use |
| CA2929348A1 (en) | 1999-05-19 | 2000-11-30 | Novartis Vaccines And Diagnostics S.R.L. | Combination neisserial compositions |
| GB9928196D0 (en) | 1999-11-29 | 2000-01-26 | Chiron Spa | Combinations of B, C and other antigens |
| PT2270030E (pt) | 2000-02-28 | 2012-07-24 | Novartis Vaccines & Diagnostic | Expressão heteróloga de proteínas de neisseria |
| RU2413520C2 (ru) | 2000-06-08 | 2011-03-10 | Интерселл Аг | Вакцинная композиция, содержащая иммуностимулирующие олигодезоксинуклеотиды |
| AT410635B (de) | 2000-10-18 | 2003-06-25 | Cistem Biotechnologies Gmbh | Vakzin-zusammensetzung |
| GB0103424D0 (en) | 2001-02-12 | 2001-03-28 | Chiron Spa | Gonococcus proteins |
| WO2002079246A2 (en) | 2001-03-30 | 2002-10-10 | Geneprot, Inc. | Human arginine-rich protein-related compositions |
| DE60234695D1 (de) | 2001-06-07 | 2010-01-21 | Univ Colorado | Mutantenformen von cholera holotoxin als adjuvans |
| CA2449670A1 (en) | 2001-06-07 | 2002-12-12 | Wyeth Holdings Corporation | Mutant forms of cholera holotoxin as an adjuvant |
| CA2460546A1 (en) | 2001-09-14 | 2003-03-27 | Invitrogen Corporation | Dna polymerases and mutants thereof |
| CN1599866A (zh) | 2001-10-03 | 2005-03-23 | 因特拉迪格姆公司 | 用体内系统验证或识别靶的多元方法 |
| MX339524B (es) | 2001-10-11 | 2016-05-30 | Wyeth Corp | Composiciones inmunogenicas novedosas para la prevencion y tratamiento de enfermedad meningococica. |
| DE60328481D1 (de) | 2002-05-14 | 2009-09-03 | Novartis Vaccines & Diagnostic | Schleimhautapplizierter impfstoff, der das adjuvanz chitosan und menigokokkenantigene enthält |
| GB0220198D0 (en) | 2002-08-30 | 2002-10-09 | Chiron Spa | Modified saccharides,conjugates thereof and their manufacture |
| US7785608B2 (en) * | 2002-08-30 | 2010-08-31 | Wyeth Holdings Corporation | Immunogenic compositions for the prevention and treatment of meningococcal disease |
| GB0220194D0 (en) | 2002-08-30 | 2002-10-09 | Chiron Spa | Improved vesicles |
| AU2003274511B2 (en) | 2002-10-11 | 2009-06-04 | Glaxosmithkline Biologicals S.A. | Polypeptide-vaccines for broad protection against hypervirulent meningococcal lineages |
| DE60332477D1 (de) | 2002-11-15 | 2010-06-17 | Novartis Vaccines & Diagnostic | Unerwartete oberflächenproteine in neisseria meningitidis |
| CN102302776B (zh) | 2003-01-30 | 2014-06-18 | 诺华疫苗和诊断有限公司 | 抗多种脑膜炎球菌血清组的可注射性疫苗 |
| WO2004083251A2 (en) | 2003-03-17 | 2004-09-30 | Wyeth Holdings Corporation | Mutant cholera holotoxin as an adjuvant and an antigen carrier protein |
| CA2522751A1 (en) | 2003-04-16 | 2004-11-04 | Wyeth Holdings Corporation | Novel immunogenic compositions for the prevention and treatment of meningococcal disease |
| PT1631264E (pt) | 2003-06-02 | 2009-11-03 | Novartis Vaccines & Diagnostic | Composições imunogénicas à base de micropartículas biodegradáveis que compreendem um toxóide de difteria e do tétano |
| MXPA05014171A (es) | 2003-06-23 | 2007-02-21 | Sanofi Pasteur Inc | Metodo de inmunizacion contra neisseria meningitidis serogrupos a y c. |
| GB0316560D0 (en) | 2003-07-15 | 2003-08-20 | Chiron Srl | Vesicle filtration |
| GB0323103D0 (en) | 2003-10-02 | 2003-11-05 | Chiron Srl | De-acetylated saccharides |
| BRPI0415025A (pt) | 2003-10-02 | 2006-12-12 | Chiron Srl | vacinas lìquidas para sorogrupos meningocócicos múltiplos |
| GB0406013D0 (en) | 2004-03-17 | 2004-04-21 | Chiron Srl | Analysis of saccharide vaccines without interference |
| GB0408978D0 (en) | 2004-04-22 | 2004-05-26 | Chiron Srl | Meningococcal fermentation for preparing conjugate vaccines |
| GB0408977D0 (en) | 2004-04-22 | 2004-05-26 | Chiron Srl | Immunising against meningococcal serogroup Y using proteins |
| RU2379052C2 (ru) | 2004-04-30 | 2010-01-20 | Чирон С.Р.Л. | Вакцинация менингококковыми конъюгатами |
| GB0409745D0 (en) | 2004-04-30 | 2004-06-09 | Chiron Srl | Compositions including unconjugated carrier proteins |
| GB0500787D0 (en) | 2005-01-14 | 2005-02-23 | Chiron Srl | Integration of meningococcal conjugate vaccination |
| GB0410220D0 (en) | 2004-05-07 | 2004-06-09 | Kirkham Lea Ann | Mutant pneumolysin proteins |
| GB0411387D0 (en) | 2004-05-21 | 2004-06-23 | Chiron Srl | Analysis of saccharide length |
| GB0413868D0 (en) | 2004-06-21 | 2004-07-21 | Chiron Srl | Dimensional anlaysis of saccharide conjugates |
| CA2574375C (en) | 2004-07-23 | 2015-03-17 | Chiron Srl | Polypeptides for oligomeric assembly of antigens |
| GB0419408D0 (en) | 2004-09-01 | 2004-10-06 | Chiron Srl | 741 chimeric polypeptides |
| GB0419846D0 (en) | 2004-09-07 | 2004-10-13 | Chiron Srl | Vaccine adjuvants for saccharides |
| GB0424092D0 (en) | 2004-10-29 | 2004-12-01 | Chiron Srl | Immunogenic bacterial vesicles with outer membrane proteins |
| GB0428394D0 (en) | 2004-12-24 | 2005-02-02 | Chiron Srl | Saccharide conjugate vaccines |
| US20070014842A1 (en) | 2005-03-07 | 2007-01-18 | Denis Martin | Pharmaceutical liposomal compositions |
| JP2008540398A (ja) | 2005-05-06 | 2008-11-20 | ノバルティス ヴァクシンズ アンド ダイアグノスティクス エスアールエル | 髄膜炎a型ワクチンのための免疫原 |
| US8329184B2 (en) | 2005-06-27 | 2012-12-11 | Glaxosmithkline Biologicals S.A. | Process for manufacturing vaccines |
| CA2621023C (en) | 2005-09-01 | 2019-07-02 | Novartis Vaccines And Diagnostics Gmbh & Co. Kg | Multiple vaccination including serogroup c meningococcus |
| ATE485516T1 (de) | 2005-09-05 | 2010-11-15 | Glaxosmithkline Biolog Sa | Bakterizidie-serumtest für n. meningitidis spezifische antiseren |
| GB0524066D0 (en) * | 2005-11-25 | 2006-01-04 | Chiron Srl | 741 ii |
| JP2009520771A (ja) | 2005-12-23 | 2009-05-28 | グラクソスミスクライン バイオロジカルズ ソシエテ アノニム | コンジュゲートワクチン |
| WO2007111940A2 (en) | 2006-03-22 | 2007-10-04 | Novartis Ag | Regimens for immunisation with meningococcal conjugates |
| DE602007003596D1 (de) | 2006-06-12 | 2010-01-14 | Glaxosmithkline Biolog Sa | Impfstoff |
| GB0612854D0 (en) | 2006-06-28 | 2006-08-09 | Novartis Ag | Saccharide analysis |
| WO2008001224A2 (en) * | 2006-06-29 | 2008-01-03 | Novartis Ag | Polypeptides from neisseria meningitidis |
| SI2061897T1 (sl) | 2006-07-27 | 2020-07-31 | Wyeth Llc | Postopek fermentacije s tehniko dohranjevalne šarže za celice z visoko gostoto za proizvajanje rekombinantnega proteina |
-
2007
- 2007-12-20 AR ARP070105809A patent/AR064642A1/es unknown
- 2007-12-21 CN CN200780047494A patent/CN101631858A/zh active Pending
- 2007-12-21 US US12/004,869 patent/US8574597B2/en active Active
- 2007-12-21 EP EP07853461A patent/EP2094294A2/en not_active Withdrawn
- 2007-12-21 AU AU2007338690A patent/AU2007338690B2/en active Active
- 2007-12-21 MX MX2009006760A patent/MX2009006760A/es active IP Right Grant
- 2007-12-21 JP JP2009542957A patent/JP2010512792A/ja active Pending
- 2007-12-21 WO PCT/US2007/026238 patent/WO2008079372A2/en active Application Filing
- 2007-12-21 BR BRPI0721003A patent/BRPI0721003B8/pt active IP Right Grant
- 2007-12-21 TW TW096149621A patent/TW200844226A/zh unknown
- 2007-12-21 CL CL200703771A patent/CL2007003771A1/es unknown
- 2007-12-21 CA CA2673515A patent/CA2673515C/en active Active
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2004048404A2 (en) * | 2002-11-22 | 2004-06-10 | Chiron Srl | Multiple variants of meningococcal protein nmb1870 |
| WO2006081259A2 (en) * | 2005-01-27 | 2006-08-03 | Children's Hospital & Research Center At Oakland | Gna1870-based vesicle vaccines for broad spectrum protection against diseases caused by neisseria meningitidis |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016515104A (ja) * | 2013-03-08 | 2016-05-26 | ファイザー・インク | 免疫原性融合ポリペプチド |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2008079372A2 (en) | 2008-07-03 |
| CL2007003771A1 (es) | 2008-03-14 |
| BRPI0721003B1 (pt) | 2020-08-18 |
| EP2094294A2 (en) | 2009-09-02 |
| BRPI0721003A2 (pt) | 2015-05-05 |
| BRPI0721003B8 (pt) | 2021-05-25 |
| US20110189187A1 (en) | 2011-08-04 |
| US8574597B2 (en) | 2013-11-05 |
| AU2007338690A1 (en) | 2008-07-03 |
| CA2673515A1 (en) | 2008-07-03 |
| MX2009006760A (es) | 2009-08-20 |
| TW200844226A (en) | 2008-11-16 |
| CN101631858A (zh) | 2010-01-20 |
| WO2008079372A9 (en) | 2009-02-12 |
| AR064642A1 (es) | 2009-04-15 |
| WO2008079372A3 (en) | 2009-04-16 |
| CA2673515C (en) | 2014-11-18 |
| AU2007338690B2 (en) | 2011-10-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5997400B2 (ja) | 髄膜炎性疾患の予防および治療のための新規免疫原性組成物 | |
| JP2010512792A (ja) | 髄膜炎菌性疾患の予防および処置のための新規な免疫原性組成物 | |
| JP2006525330A (ja) | 髄膜炎菌性疾患の予防および処置のための新規免疫原性組成物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20101217 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20101217 |
|
| RD03 | Notification of appointment of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7423 Effective date: 20110523 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20110527 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110603 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20120926 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20121121 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20121221 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20130104 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130125 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20131015 |