JP2010177207A - 非水電解質二次電池 - Google Patents
非水電解質二次電池 Download PDFInfo
- Publication number
- JP2010177207A JP2010177207A JP2010086144A JP2010086144A JP2010177207A JP 2010177207 A JP2010177207 A JP 2010177207A JP 2010086144 A JP2010086144 A JP 2010086144A JP 2010086144 A JP2010086144 A JP 2010086144A JP 2010177207 A JP2010177207 A JP 2010177207A
- Authority
- JP
- Japan
- Prior art keywords
- positive electrode
- active material
- secondary battery
- electrolyte secondary
- electrode active
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
Abstract
【課題】遷移金属としてNi及びMnを少なくとも含有し、かつ層状構造を有するリチウム遷移金属複合酸化物を正極活物質として用いた非水電解質二次電池において、充放電サイクルにおける放電電圧及び容量の低下を抑制し、サイクル特性を向上させる。
【解決手段】遷移金属としてNi及びMnを少なくとも含有し、かつ層状構造を有するリチウム遷移金属複合酸化物に、ジルコニウムをさらに含有させたものを正極活物質として用いることを特徴としている。
【選択図】図1
【解決手段】遷移金属としてNi及びMnを少なくとも含有し、かつ層状構造を有するリチウム遷移金属複合酸化物に、ジルコニウムをさらに含有させたものを正極活物質として用いることを特徴としている。
【選択図】図1
Description
本発明は、非水電解質二次電池に関するものである。
近年、金属リチウム、リチウムイオンを吸蔵・放出し得る合金、もしくは炭素材料などを負極活物質とし、化学式:LiMo2(Mは遷移金属)で表わされるリチウム遷移金属複合酸化物を正極活物質とする非水電解質二次電池が、高エネルギー密度を有する電池として注目されている。
上記リチウム遷移金属複合酸化物の例としては、リチウムコバルト酸化物(LiCoO2)が代表的なものとして挙げられ、既に非水電解質二次電池の正極活物質として実用化されている。
しかしながら、遷移金属としてMnを含むものやNiを含むものも検討されており、また、Mn、Ni及びCoの全てを含む材料も盛んに検討がなされている(例えば、特許文献1、特許文献2、非特許文献1など)。
また、Mn、Ni及びCoを含むリチウム遷移金属酸化物の中で、MnとNiの組成が等しい化学式:LiMnxNixCo(1-2x)O2で表わされる材料が、充電状態(高い酸化状態)でも特異的に高い熱的安定性を示すことが報告されている(非特許文献2など)。
また、NiとMnが実質的に等しい複合酸化物が、LiCoO2と同等の4V近傍の電圧を有し、かつ高容量で優れた充放電効率を示すことが報告されている(特許文献3)。
このようなMnとNiとCoを含み、層状構造を有するリチウム遷移金属複合酸化物(例えば、化学式:LiaMnbNibCo(1-2b)O2(0≦a≦1.1,0<b≦0.5)を主材(50重量%以上)とする正極を用いた電池は、充電時の高い熱的安定性を有することから電池の信頼性が飛躍的に向上することが期待できる。さらに、このようなMnとNiとCoを含み、層状構造を有するリチウム遷移金属複合酸化物は、その高い構造安定性から、現状の充電電圧より高く設定しても(正極の電位で4.5V(vs.Li/Li+)以上)、現在使用されているLiCoO2などより良好なサイクル特性を示すことが報告されている(非特許文献3)。
現在、リチウム遷移金属複合酸化物(例えば、LiCoO2)を正極に用い、負極に炭素材料を用いる非水電解質二次電池では、その充電終止電圧は、一般に4.1〜4.2Vとなっているが、この場合正極は理論容量に対して50〜60%しか利用されていない。従って、MnとNiとCoを含み、層状構造を有するリチウム遷移金属複合酸化物を用いれば、充電電圧を高く設定しても熱的安定性を大きく低下させることなく、正極の容量を理論容量に対して70%以上利用することも可能であり、電池の高容量化及び高エネルギー密度化が可能となる。
Jornal of Power Sources 90(2000)176-181
Electrochemical and Solid-State Letters,4(12) A200-A203(2001)
Chemistry Letters, 2001,P.642-643
しかしながら、MnとNiとCoを含み、層状構造を有するリチウム遷移金属複合酸化物を正極活物質として用いた場合でも、依然として充放電サイクルに伴う放電電圧及び放電容量の低下がみられた。特に、正極の充電電位が4.5V(vs.Li/Li+)以上となるような高い電位の充電状態では、充放電サイクル後の放電電圧及び放電容量の低下が大きく、エネルギー密度の低下が問題となっていた。すなわち、電池の充放電サイクル特性、特に満充電状態での正極の電位が4.5V(vs.Li/Li+)以上となる電池(例えば、負極の充電電位が0.1V(vs.Li/Li+)である炭素負極を用いる場合であれば、充電電圧が4.4V以上となる電池)の充放電サイクル特性に問題があった。
本発明の目的は、遷移金属としてNi及びMnを少なくとも含有し、層状構造を有するリチウム遷移金属複合酸化物を正極活物質として含む正極を用いた非水電解質二次電池において、充放電サイクルにおける放電電圧及び容量の低下を抑制することができ、サイクル特性を高めることができる非水電解質二次電池を提供することにある。
本発明の非水電解質二次電池は、正極活物質を含む正極と、負極活物質を含む負極と、非水電解質とを備え、正極活物質が、遷移金属としてNi及びMnを少なくとも含有し、かつ層状構造を有するリチウム遷移金属複合酸化物であり、ジルコニウムをさらに含有していることを特徴としている。
本発明においては、上記リチウム遷移金属複合酸化物にジルコニウムが含まれることにより、充放電サイクルにおける放電電圧及び容量の低下を抑制することができる。この理由の詳細については明らかでないが、後述するように、充放電サイクル後の正極及び負極を解析した結果、以下のことがわかった。
(1)ジルコニウム(Zr)を含まないリチウム遷移金属複合酸化物の場合、サイクル前後のXRDパターンを調べた結果、両者において殆ど差は認められなかった。
(2)充放電サイクル後の負極の表面に析出(または堆積)したマンガン量を調べた結果、ジルコニウム(Zr)を含まないリチウム遷移金属複合酸化物を正極活物質とした電池では、ジルコニウム(Zr)を含む本発明の場合と比較して、多量のマンガンが負極の表面上に析出(堆積)していた。
上記のことから、ジルコニウムを含まないリチウム遷移金属複合酸化物を正極活物質として用いた電池の充放電サイクルによる特性低下は、正極活物質の構造の崩壊ではなく、正極活物質の表面からマンガンが溶解したことによるものと思われる。この結果として、正極−電解液界面の抵抗が上昇し、放電電圧及び放電容量が低下したものと考えられる。本発明に従い、ジルコニウムを上記リチウム遷移金属複合酸化物に添加したものを正極活物質として用いることにより、正極活物質の表面からのマンガンの溶解が抑制され、この結果、正極−電解液界面の抵抗の上昇を抑制することができ、放電電圧及び放電容量の低下を抑制することができるものと考えられる。
充放電サイクルに対するジルコニウム添加の効果は、正極の電位が4.3V(vs.Li/Li+)の充電状態でも確認されるが、4.5V(vs.Li/Li+)以上の高い電位の充電状態の場合、特に放電電位の低下抑制の効果が大きくなる。
特許文献4においては、LiCoO2にジルコニウムを添加することが提案されているが、段落番号〔0008〕に記載されているように、その作用効果は、LiCoO2粒子の表面が酸化ジルコニウムもしくはリチウムとジルコニウムとの複合酸化物Li2ZrO3により覆われることによって安定化されるため、電解液の分解や結晶破壊が生じなくなるというものであり、本発明とは全く異なる作用効果であると考えられる。
本発明において、正極活物質中に含まれるジルコニウムの量は、リチウム遷移金属複合酸化物中の遷移金属の合計量に対して、0.1モル%以上、5モル%以下であることが好ましい。ジルコニウムの量が少な過ぎると、サイクル特性を高める本発明の効果が十分に得られず、一方ジルコニウムの量が多過ぎると正極の放電特性に悪影響を及ぼすおそれがある。
本発明において用いる負極活物質としては、非水電解質二次電池に用いることができる負極活物質であれば特に限定されるものではないが、例えば、黒鉛などの炭素材料、シリコン、アルミニウム、錫などのリチウムと合金化する材料、チタン酸リチウムなどを用いることができる。例えば、負極の充電電位が0.1V(vs.Li/Li+)である炭素材料を負極活物質として用いた場合、満充電状態での正極の電位を4.5V(vs.Li/Li+)以上とすると、充電終止電圧は4.4V以上となる。本発明における限定された局面における非水電解質二次電池は、このような二次電池である。
すなわち、本発明に従う限定された局面に従う非水電解質二次電池は、正極活物質を含む正極と、負極活物質として炭素材料を含む負極と、非水電解質とを備え、4.4V以上の充電終止電圧で充電されるように設計された非水電解質二次電池であり、正極活物質が、遷移金属としてNi及びMnを少なくとも含有し、かつ層状構造を有するリチウム遷移金属複合酸化物であり、ジルコニウムをさらに含有していることを特徴としている。
本発明において、正極及び負極の対向する部分の容量比(負極/正極)は、1.0〜1.3の範囲内となるように設計されることが好ましい。この容量比が1.0より小さくなると、負極の表面に金属リチウムが析出し、電池のサイクル特性や安全性が著しく低下する場合がある。また、容量比が1.3を超えると、反応に関与しない余分な負極が増えるため、電池のエネルギー密度が低下する。
本発明においては、上述のように、充電状態での正極の電位は、4.5V(vs.Li/Li+)以上であることが好ましい。さらに好ましくは、充電状態での正極の電位は、4.5〜5.2V(vs.Li/Li+)である。正極の電位が、5.2V(vs.Li/Li+)を超える領域まで充電すると、活物質中のリチウムの脱離反応よりも電極表面での電解液の分解反応の方が顕著になるため好ましくない場合がある。
本発明において、ジルコニウムを含有するリチウム遷移金属複合酸化物としては、化学式:LiaMnxNiyCozO2(a、x、y及びzは、0≦a≦1.2、x+y+z=1、0<x≦0.5、0<y≦0.5、及びz≧0を満足する。)で表わされるものであることが好ましい。
また、本発明においては、リチウム遷移金属複合酸化物中にNiとMnが実質的に等しいモル量含有されていることが好ましい。実質的に等しいモル量とは、上記の化学式において、x及びyが以下の式を満足するという意味である。
0.45≦x/(x+y)≦0.55
0.45≦y/(x+y)≦0.55
ニッケルは、容量は大きいが充電時の熱的安定性が低いという性質を有しており、マンガンは、容量は小さいが充電時の熱的安定性が高いという性質を有している。従って、これらの元素が実質的に等しいモル量含まれることにより、これらの特性をバランスよく備えることができる。
0.45≦y/(x+y)≦0.55
ニッケルは、容量は大きいが充電時の熱的安定性が低いという性質を有しており、マンガンは、容量は小さいが充電時の熱的安定性が高いという性質を有している。従って、これらの元素が実質的に等しいモル量含まれることにより、これらの特性をバランスよく備えることができる。
本発明において正極活物質の比表面積は0.1〜2.0m2/gの範囲であることが好ましい。このような範囲内とすることにより、高い電位における正極活物質と電解液との反応を抑制することができる。
本発明においては、正極に導電剤を含有させることができる。導電剤として炭素材料が含まれる場合には、該炭素材料の含有量が正極活物質と導電剤と結着剤の合計に対して5重量%以下であることが好ましい。正極が高い電位となった場合、導電剤としての炭素材料の表面で電解液の酸化分解が最も進行し易くなる。このため、導電剤としての炭素材料は、上記の範囲内とすることが好ましい。
本発明において用いる非水電解質の溶媒としては、従来より非水電解質二次電池の電解質の溶媒として用いられているものを用いることができる。これらの中でも、環状カーボネートと鎖状カーボネートの混合溶媒が特に好ましく用いられる。環状カーボネートとしては、エチレンカーボネート、プロピレンカーボネート、ブチレンカーボネート、ビニレンカーボネートなどが挙げられる。鎖状カーボネートとしては、ジメチルカーボネート、メチルエチルカーボネート、ジエチルカーボネートなどが挙げられる。
一般に、環状カーボネートは、高い電位において分解を生じやすいので、溶媒中の環状カーボネートの含有割合は10〜50体積%の範囲内であることが好ましく、さらに好ましくは10〜30体積%の範囲内である。
本発明における非水電解質の溶質としては、非水電解質二次電池において一般に溶質として用いられるリチウム塩を用いることができる。このようなリチウム塩としては、LiPF6、LiBF4、LiCF3SO3、LiN(CF3SO2)2、LiN(C2F5SO2)2、LiN(CF3SO2)(C4F9SO2)、LiC(CF3SO2)3、LiC(C2F5SO2)3、LiAsF6、LiClO4、Li2B10Cl10、Li2B12Cl12など及びそれらの混合物が例示される。これらの中でも、LiPF6(ヘキサフルオロリン酸リチウム)が好ましく用いられる。高い充電電圧で充電する場合、正極の集電体であるアルミニウムが溶解しやすくなるが、LiPF6の存在下では、LiPF6が分解することにより、アルミニウム表面に被膜が形成され、この被膜によってアルミニウムの溶解を抑制することができる。従って、リチウム塩としては、LiPF6を用いることが好ましい。
本発明によれば、遷移金属としてNi及びMnを少なくとも含有し、かつ層状構造を有するリチウム遷移金属複合酸化物を用いた非水電解質二次電池において、充放電サイクルにおける放電電圧及び容量の低下を抑制することができ、サイクル特性を高めることができる。特に、満充電状態における正極の電位が、4.5V(vs.Li/Li+)以上としたときに、大きな特性改善の効果が得られる。
以下、本発明を実施例に基づきさらに詳細に説明するが、本発明は、以下の実施例に何ら限定されるものではなく、その要旨を変更しない範囲において適宜変更して実施することが可能なものである。
<実験1>
(実施例1)
〔正極活物質の作製〕
LiOHと、Mn0.33Ni0.33Co0.34(OH)2で表わされる共沈水酸化物を、Liと遷移金属全体のモル比が1:1となるように、石川式らいかい乳鉢にて混合した後、酸化ジルコニウム(IV)を、LiMn0.33Ni0.33Co0.34O2中の遷移金属の合計に対し、ジルコニウムとして0.5モル%となるように添加し、空気雰囲気中にて1000℃で20時間熱処理した後粉砕し、平均粒子径が約10μmのLiMn0.33Ni0.33Co0.34O2で表わされるリチウム遷移金属複合酸化物にジルコニウムを添加した正極活物質を得た。得られた正極活物質のBET比表面積は0.67m2/gであった。
(実施例1)
〔正極活物質の作製〕
LiOHと、Mn0.33Ni0.33Co0.34(OH)2で表わされる共沈水酸化物を、Liと遷移金属全体のモル比が1:1となるように、石川式らいかい乳鉢にて混合した後、酸化ジルコニウム(IV)を、LiMn0.33Ni0.33Co0.34O2中の遷移金属の合計に対し、ジルコニウムとして0.5モル%となるように添加し、空気雰囲気中にて1000℃で20時間熱処理した後粉砕し、平均粒子径が約10μmのLiMn0.33Ni0.33Co0.34O2で表わされるリチウム遷移金属複合酸化物にジルコニウムを添加した正極活物質を得た。得られた正極活物質のBET比表面積は0.67m2/gであった。
〔作用極の作製〕
上記のようにして得られた正極活物質に、導電剤としての炭素と、結着剤としてのポリフッ化ビニリデンと、分散媒としてのN−メチル−2−ピロリドンを、活物質と導電剤と結着剤の重量比が90:5:5の比率となるように加えた後に混練して、正極スラリーを作製した。作製したスラリーを集電体としてのアルミニウム箔上に塗布した後、乾燥し、その後圧延ローラーを用いて圧延し、集電タブを取り付けて作用極とした。
上記のようにして得られた正極活物質に、導電剤としての炭素と、結着剤としてのポリフッ化ビニリデンと、分散媒としてのN−メチル−2−ピロリドンを、活物質と導電剤と結着剤の重量比が90:5:5の比率となるように加えた後に混練して、正極スラリーを作製した。作製したスラリーを集電体としてのアルミニウム箔上に塗布した後、乾燥し、その後圧延ローラーを用いて圧延し、集電タブを取り付けて作用極とした。
〔電解液の作製〕
エチレンカーボネート(EC)とエチルメチルカーボネート(EMC)とを体積比3:7で混合した溶媒に、ヘキサフルオロリン酸リチウム(LiPF6)を濃度が1モル/リットルとなるように溶解して電解液を作製した。
エチレンカーボネート(EC)とエチルメチルカーボネート(EMC)とを体積比3:7で混合した溶媒に、ヘキサフルオロリン酸リチウム(LiPF6)を濃度が1モル/リットルとなるように溶解して電解液を作製した。
〔三電極式ビーカーセルの作製〕
アルゴン雰囲気下のグローブボックス中にて、図6に示す三電極式ビーカーセルを作製した。容器内には電解液4が入れられており、電解液4中に、作用極1、対極2及び参照極3が浸漬されている。対極2及び参照極3としては、リチウム金属を用いた。
アルゴン雰囲気下のグローブボックス中にて、図6に示す三電極式ビーカーセルを作製した。容器内には電解液4が入れられており、電解液4中に、作用極1、対極2及び参照極3が浸漬されている。対極2及び参照極3としては、リチウム金属を用いた。
〔初期充放電特性の評価〕
作製した三電極式ビーカーセルを、室温にて、0.75mA/cm2(約0.3C)の定電流で、作用極の電位が4.3V(vs.Li/Li+)に達するまで充電し、さらに0.25mA/cm2(約0.1C)の定電流で、電位が4.3V(vs.Li/Li+)に達するまで充電した後、0.75mA/cm2(約0.3C)の定電流で、電位が2.75V(vs.Li/Li+)に達するまで放電することにより、初期の充放電特性を評価した。
作製した三電極式ビーカーセルを、室温にて、0.75mA/cm2(約0.3C)の定電流で、作用極の電位が4.3V(vs.Li/Li+)に達するまで充電し、さらに0.25mA/cm2(約0.1C)の定電流で、電位が4.3V(vs.Li/Li+)に達するまで充電した後、0.75mA/cm2(約0.3C)の定電流で、電位が2.75V(vs.Li/Li+)に達するまで放電することにより、初期の充放電特性を評価した。
〔充放電サイクル特性の評価〕
初期充放電サイクル特性を評価した後、室温にて、初期充放電特性の評価と同じ条件にて、充放電を15サイクル行い、16サイクルでの容量維持率を以下の式で求めた。また、1サイクル目の放電曲線と16サイクル目の放電曲線を比較し、放電開始時の電位の低下を求めた。
初期充放電サイクル特性を評価した後、室温にて、初期充放電特性の評価と同じ条件にて、充放電を15サイクル行い、16サイクルでの容量維持率を以下の式で求めた。また、1サイクル目の放電曲線と16サイクル目の放電曲線を比較し、放電開始時の電位の低下を求めた。
容量維持率(%)=(16サイクル目の放電容量)÷(1サイクル目の放電容量)×100
(実施例2)
正極活物質の作製において、ジルコニウムの量をリチウム遷移金属複合酸化物中の遷移金属の合計に対し、1.0モル%となるように添加したこと以外は、実施例1と同様にして三電極式ビーカーセルを作製した。なお、得られた正極活物質のBET比表面積は0.64m2/gであった。初期充放電特性及び充放電サイクル特性は、実施例1と同様にして評価した。
正極活物質の作製において、ジルコニウムの量をリチウム遷移金属複合酸化物中の遷移金属の合計に対し、1.0モル%となるように添加したこと以外は、実施例1と同様にして三電極式ビーカーセルを作製した。なお、得られた正極活物質のBET比表面積は0.64m2/gであった。初期充放電特性及び充放電サイクル特性は、実施例1と同様にして評価した。
(実施例3)
実施例1と同様にして三電極式ビーカーセルを作製した。初期充放電特性及び充放電サイクル特性の評価において、作用極の充電電位を4.6V(vs.Li/Li+)とした以外は、実施例1と同様にして評価した。
実施例1と同様にして三電極式ビーカーセルを作製した。初期充放電特性及び充放電サイクル特性の評価において、作用極の充電電位を4.6V(vs.Li/Li+)とした以外は、実施例1と同様にして評価した。
(実施例4)
実施例2と同様にして三電極式ビーカーセルを作製した。初期充放電特性及び充放電サイクル特性の評価において、作用極の充電電位を4.6V(vs.Li/Li+)とした以外は、実施例1と同様にして評価した。
実施例2と同様にして三電極式ビーカーセルを作製した。初期充放電特性及び充放電サイクル特性の評価において、作用極の充電電位を4.6V(vs.Li/Li+)とした以外は、実施例1と同様にして評価した。
(比較例1)
正極活物質の作製において、LiOHとMn0.33Ni0.33Co0.34(OH)2で表わされる共沈水酸化物を、Liと遷移金属全体のモル比が1:1となるようにして、石川式らいかい乳鉢にて混合し、これをそのまま熱処理したこと以外は、実施例1と同様にして三電極式ビーカーセルを作製して、実施例1と同様にして初期充放電特性及び充放電サイクル特性を評価した。
正極活物質の作製において、LiOHとMn0.33Ni0.33Co0.34(OH)2で表わされる共沈水酸化物を、Liと遷移金属全体のモル比が1:1となるようにして、石川式らいかい乳鉢にて混合し、これをそのまま熱処理したこと以外は、実施例1と同様にして三電極式ビーカーセルを作製して、実施例1と同様にして初期充放電特性及び充放電サイクル特性を評価した。
(比較例2)
比較例1と同様にして、三電極式ビーカーセルを作製した。初期充放電特性及び充放電サイクル特性の評価において、作用極の充電電位を4.6V(vs.Li/Li+)とした以外は、実施例1と同様にして評価した。
比較例1と同様にして、三電極式ビーカーセルを作製した。初期充放電特性及び充放電サイクル特性の評価において、作用極の充電電位を4.6V(vs.Li/Li+)とした以外は、実施例1と同様にして評価した。
上記の実施例1〜4(ビーカーセルA1〜A4)、並びに比較例1及び2(ビーカーセルX1及びX2)の評価結果を表1及び表2に示す。なお、表1には、用いた正極活物質のBET比表面積も併せて示す。
表2から明らかなように、ジルコニウムを添加することにより、充放電サイクルにおける容量維持率が向上し、放電開始電位の低下が抑制されている。
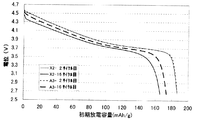
図1は、実施例1の電池A1と比較例1の電池X1の2サイクル目及び16サイクル目の充放電曲線を示しており、図2は、実施例2の電池A2と比較例1のX1の2サイクル目及び16サイクル目の充放電曲線を示している。図1及び図2において、充電終止電位は4.3V(vs.Li/Li+)である。
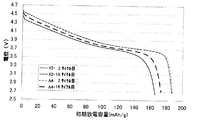
図3は、実施例3の電池A3と比較例2の電池X2の2サイクル目及び16サイクル目の充放電曲線を示しており、図4は、実施例4の電池A4と比較例2の電池X2の2サイクル目及び16サイクル目の充放電曲線を示している。図3及び図4において、充電終止電位は4.6V(vs.Li/Li+)である。
図1と図3及び図2と図4を比較することにより、充電終止電位を4.6V(vs.Li/Li+)とした方が充放電サイクル特性の改善の効果が大きいことがわかる。また、このことは表2からも明らかである。
<実験2>
(実施例5)
〔正極の作製〕
実施例2で作製した正極活物質と、導電剤としての炭素と、結着剤としてのポリフッ化ビニリデンと、分散媒としてのN−メチル−2−ピロリドンを、活物質と導電剤と結着剤の重量比が90:5:5の比率となるようにして加えた後混練して、正極スラリーを作製した。作製したスラリーを集電体としてのアルミニウム箔上に塗布した後、乾燥し、その後圧延ローラーを用いて圧延し、集電タブを取り付けることにより正極を作製した。
(実施例5)
〔正極の作製〕
実施例2で作製した正極活物質と、導電剤としての炭素と、結着剤としてのポリフッ化ビニリデンと、分散媒としてのN−メチル−2−ピロリドンを、活物質と導電剤と結着剤の重量比が90:5:5の比率となるようにして加えた後混練して、正極スラリーを作製した。作製したスラリーを集電体としてのアルミニウム箔上に塗布した後、乾燥し、その後圧延ローラーを用いて圧延し、集電タブを取り付けることにより正極を作製した。
〔負極の作製〕
増粘剤であるカルボキシメチルセルロースを水に溶かした水溶液に、負極活物質としての人造黒鉛と、結着剤としてのスチレン−ブタジエンゴムとを、活物質と結着剤と増粘剤の重量比が95:3:2の比率となるようにして加えた後混練して、負極スラリーを作製した。作製したスラリーを集電体としての銅箔上に塗布した後、乾燥し、その後圧延ローラーを用いて圧延し、集電タブを取り付けることにより負極を作製した。
増粘剤であるカルボキシメチルセルロースを水に溶かした水溶液に、負極活物質としての人造黒鉛と、結着剤としてのスチレン−ブタジエンゴムとを、活物質と結着剤と増粘剤の重量比が95:3:2の比率となるようにして加えた後混練して、負極スラリーを作製した。作製したスラリーを集電体としての銅箔上に塗布した後、乾燥し、その後圧延ローラーを用いて圧延し、集電タブを取り付けることにより負極を作製した。
〔電解液の作製〕
エチレンカーボネート(EC)とエチルメチルカーボネート(EMC)とを体積比3:7で混合した溶媒に対し、LiPF6を濃度が1モル/リットル溶解して電解液を作製した。
エチレンカーボネート(EC)とエチルメチルカーボネート(EMC)とを体積比3:7で混合した溶媒に対し、LiPF6を濃度が1モル/リットル溶解して電解液を作製した。
〔電池の作製〕
正極及び負極を、セパレータを介して対向するように巻き取って巻取り体を作製し、アルゴン雰囲気下のグローブボックス中にて巻取り体を電解液と共に、アルミニウムラミネートに封入することにより、電池規格サイズとして、厚み3.6mm×幅3.5cm×長さ6.2cmの非水電解質二次電池A5を得た。なお、正極及び負極の対向容量比は1.15とした。
正極及び負極を、セパレータを介して対向するように巻き取って巻取り体を作製し、アルゴン雰囲気下のグローブボックス中にて巻取り体を電解液と共に、アルミニウムラミネートに封入することにより、電池規格サイズとして、厚み3.6mm×幅3.5cm×長さ6.2cmの非水電解質二次電池A5を得た。なお、正極及び負極の対向容量比は1.15とした。
(比較例3)
比較例1で用いた正極活物質を用いた以外は、実施例5と同様にして電池X3を作製し、評価した。
比較例1で用いた正極活物質を用いた以外は、実施例5と同様にして電池X3を作製し、評価した。
〔電池の初期充放電特性の評価〕
作製した非水電解質二次電池を、室温にて、650mA(約1C)の定電流で、電圧が4.5Vに達するまで充電し、さらに4.5Vの定電圧で電流値が32mA(約0.05C)になるまで充電した後、650mAの定電流で電圧が2.75Vに達するまで放電することにより、電池の放電容量(mAh)を測定した。
作製した非水電解質二次電池を、室温にて、650mA(約1C)の定電流で、電圧が4.5Vに達するまで充電し、さらに4.5Vの定電圧で電流値が32mA(約0.05C)になるまで充電した後、650mAの定電流で電圧が2.75Vに達するまで放電することにより、電池の放電容量(mAh)を測定した。
〔充放電サイクル特性の評価〕
上記電池の初期充放電特性を評価した後、同じ条件で充放電サイクル試験を行い、50サイクル目での容量維持率と放電開始電圧の変化を求め、結果を表3に示した。なお、容量維持率は以下の式により算出した。
上記電池の初期充放電特性を評価した後、同じ条件で充放電サイクル試験を行い、50サイクル目での容量維持率と放電開始電圧の変化を求め、結果を表3に示した。なお、容量維持率は以下の式により算出した。
容量維持率(%)=(50サイクル目の放電容量)÷(1サイクル目の放電容量)×100
表3から明らかなように、ジルコニウムを添加した本発明に従う実施例5の電池A5は、ジルコニウムを添加していない比較例3の電池X3よりも、50サイクル後の容量維持率及びサイクル後の放電開始電圧の低下が改善されていることがわかる。
<実験3>
ここでは、リチウム遷移金属複合酸化物の充放電サイクルによる放電電圧の低下及び放電容量の低下の要因、並びにジルコニウムを含有させることによる作用効果を調べるため以下の実験を行った。
ここでは、リチウム遷移金属複合酸化物の充放電サイクルによる放電電圧の低下及び放電容量の低下の要因、並びにジルコニウムを含有させることによる作用効果を調べるため以下の実験を行った。
(1)充放電サイクル前後での正極活物質のXRDパターンの測定
比較例3の電池X3について、充放電サイクルを行う前及びサイクル後の正極を回収し、CuKαを線源とするX線回折(XRD)パターンを測定した。その結果を図5に示す。また、格子定数とGauss法を用いて半価幅を算出した。結果を表4に示す。
比較例3の電池X3について、充放電サイクルを行う前及びサイクル後の正極を回収し、CuKαを線源とするX線回折(XRD)パターンを測定した。その結果を図5に示す。また、格子定数とGauss法を用いて半価幅を算出した。結果を表4に示す。
図5から明らかなように、充放電サイクル前後の電池の正極活物質のX線回折パターンにおいて、大きな違いは認められなかった。また、表4から明らかなように、サイクル前後の電池の正極活物質の半値幅においても大きな差は認められなかった。これらのことから、サイクル後の電池の正極活物質において、結晶構造の崩壊などは起こっていないものと考えられる。
(2)サイクル後の電池の負極上へのマンガン析出量の評価
実施例5の電池A5及び比較例3の電池X3を充放電サイクル後、解体して負極を回収し、ロジウムを線源とする蛍光X線分析により、負極表面へのマンガンの析出量を測定した。検出範囲は0〜40keVである。結果を表5に示す。
実施例5の電池A5及び比較例3の電池X3を充放電サイクル後、解体して負極を回収し、ロジウムを線源とする蛍光X線分析により、負極表面へのマンガンの析出量を測定した。検出範囲は0〜40keVである。結果を表5に示す。
表5から明らかなように、ジルコニウムを添加した実施例5の電池A5においては、充放電サイクル後に負極表面上に析出するマンガンの量が、ジルコニウムを含まない比較例3の電池X3よりも10%以上少なくなっていることがわかる。
以上のことから、リチウム遷移金属複合酸化物の充放電サイクルによる放電電圧の低下と放電容量の低下の要因は、充放電サイクルによる正極活物質の結晶構造の崩壊ではなく、充放電サイクルによる正極活物質からのマンガンの溶出及びこれに起因する正極−電解液界面の抵抗の増加であると考えられる。本発明に従い、リチウム遷移金属複合酸化物にジルコニウムを含有させた正極活物質を用いることにより、正極活物質からのマンガンの溶出が抑制され、充放電サイクルによる放電電圧の低下及び容量の低下が抑制されるものと考えられる。
1…作用極
2…対極
3…参照極
4…電解液
2…対極
3…参照極
4…電解液
Claims (8)
- 正極活物質を含む正極と、負極活物質を含む負極と、非水電解質とを備える非水電解質二次電池において、前記正極活物質が、遷移金属としてNi及びMnを少なくとも含有し、かつ層状構造を有するリチウム遷移金属複合酸化物であり、ジルコニウムをさらに含有していることを特徴とする非水電解質二次電池。
- 電池を満充電状態したときの正極の電位が、4.5V(vs.Li/Li+)以上となることを特徴とする請求項1に記載の非水電解質二次電池。
- 正極活物質を含む正極と、負極活物質として炭素材料を含む負極と、非水電解質とを備え、4.4V以上の充電終止電圧で充電されるように設計された非水電解質二次電池において、
前記正極活物質が、遷移金属としてNi及びMnを少なくとも含有し、かつ層状構造を有するリチウム遷移金属複合酸化物であり、ジルコニウムをさらに含有していることを特徴とする非水電解質二次電池。 - 前記正極活物質中に含まれるジルコニウムの量が、遷移金属の合計量に対して0.1モル%以上、5モル%以下であることを特徴とする請求項1〜3のいずれか1項に記載の非水電解質二次電池。
- 前記正極及び前記負極の対向する部分の容量比(負極/正極)が1.0〜1.3の範囲内であることを特徴とする請求項1〜4のいずれか1項に記載の非水電解質二次電池。
- 前記リチウム遷移金属複合酸化物が、化学式:LiaMnxNiyCozO2(a、x、y及びzは、0≦a≦1.2、x+y+z=1、0<x≦0.5、0<y≦0.5、及びz≧0を満足する。)で表わされるものであることを特徴とする請求項1〜5のいずれか1項に記載の非水電解質二次電池。
- 前記リチウム遷移金属複合酸化物のニッケル量とマンガン量が、実質的に等しいことを特徴とする請求項1〜6のいずれか1項に記載の非水電解質二次電池。
- 前記正極活物質の比表面積が0.1〜2.0m2/gであることを特徴とする請求項1〜7のいずれか1項に記載の非水電解質二次電池。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2010086144A JP2010177207A (ja) | 2010-04-02 | 2010-04-02 | 非水電解質二次電池 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2010086144A JP2010177207A (ja) | 2010-04-02 | 2010-04-02 | 非水電解質二次電池 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2003206878A Division JP5036121B2 (ja) | 2003-08-08 | 2003-08-08 | 非水電解質二次電池 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010177207A true JP2010177207A (ja) | 2010-08-12 |
| JP2010177207A5 JP2010177207A5 (ja) | 2012-08-30 |
Family
ID=42707900
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2010086144A Pending JP2010177207A (ja) | 2010-04-02 | 2010-04-02 | 非水電解質二次電池 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2010177207A (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8139929B2 (en) | 1996-02-28 | 2012-03-20 | Panasonic Corporation | High-resolution optical disk for recording stereoscopic video, optical disk reproducing device, and optical disk recording device |
| JP2012113823A (ja) * | 2010-11-19 | 2012-06-14 | Nippon Chem Ind Co Ltd | リチウム二次電池用正極活物質、その製造方法及びリチウム二次電池 |
Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2002151076A (ja) * | 2000-11-14 | 2002-05-24 | Japan Storage Battery Co Ltd | 非水電解質二次電池用正極活物質およびそれを用いた非水電解質二次電池 |
| JP2002358962A (ja) * | 2001-05-31 | 2002-12-13 | Sanyo Electric Co Ltd | 非水電解質二次電池 |
| WO2003044881A1 (fr) * | 2001-11-22 | 2003-05-30 | Yuasa Corporation | Materiau actif d'electrode positive pour cellule secondaire au lithium et cellule secondaire associee |
| JP2003168430A (ja) * | 2001-11-30 | 2003-06-13 | Sanyo Electric Co Ltd | 非水電解質二次電池 |
| JP2003197190A (ja) * | 2001-12-25 | 2003-07-11 | Yuasa Corp | 非水電解質二次電池 |
| JP2004006229A (ja) * | 2001-12-07 | 2004-01-08 | Nichia Chem Ind Ltd | リチウムイオン二次電池用正極活物質 |
| WO2004082046A1 (ja) * | 2003-03-14 | 2004-09-23 | Seimi Chemical Co., Ltd. | リチウム二次電池用正極活物質粉末 |
-
2010
- 2010-04-02 JP JP2010086144A patent/JP2010177207A/ja active Pending
Patent Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2002151076A (ja) * | 2000-11-14 | 2002-05-24 | Japan Storage Battery Co Ltd | 非水電解質二次電池用正極活物質およびそれを用いた非水電解質二次電池 |
| JP2002358962A (ja) * | 2001-05-31 | 2002-12-13 | Sanyo Electric Co Ltd | 非水電解質二次電池 |
| WO2003044881A1 (fr) * | 2001-11-22 | 2003-05-30 | Yuasa Corporation | Materiau actif d'electrode positive pour cellule secondaire au lithium et cellule secondaire associee |
| JP2003168430A (ja) * | 2001-11-30 | 2003-06-13 | Sanyo Electric Co Ltd | 非水電解質二次電池 |
| JP2004006229A (ja) * | 2001-12-07 | 2004-01-08 | Nichia Chem Ind Ltd | リチウムイオン二次電池用正極活物質 |
| JP2003197190A (ja) * | 2001-12-25 | 2003-07-11 | Yuasa Corp | 非水電解質二次電池 |
| WO2004082046A1 (ja) * | 2003-03-14 | 2004-09-23 | Seimi Chemical Co., Ltd. | リチウム二次電池用正極活物質粉末 |
Cited By (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8139929B2 (en) | 1996-02-28 | 2012-03-20 | Panasonic Corporation | High-resolution optical disk for recording stereoscopic video, optical disk reproducing device, and optical disk recording device |
| US8150240B2 (en) | 1996-02-28 | 2012-04-03 | Panasonic Corporation | High-resolution optical disk for recording stereoscopic video, optical disk reproducing device, and optical disk recording device |
| US8184961B2 (en) | 1996-02-28 | 2012-05-22 | Panasonic Corporation | High-resolution optical disk for recording stereoscopic video, optical disk reproducing device, and optical disk recording device |
| US8200064B2 (en) | 1996-02-28 | 2012-06-12 | Panasonic Corporation | High-resolution optical disk for recording stereoscopic video, optical disk reproducing device, and optical disk recording device |
| US8391692B2 (en) | 1996-02-28 | 2013-03-05 | Panasonic Corporation | High-resolution optical disk for recording stereoscopic video, optical disk reproducing device, and optical disk recording device |
| US8391689B2 (en) | 1996-02-28 | 2013-03-05 | Panasonic Corporation | High-resolution optical disk for recording stereoscopic video, optical disk reproducing device, and optical disk recording device |
| JP2012113823A (ja) * | 2010-11-19 | 2012-06-14 | Nippon Chem Ind Co Ltd | リチウム二次電池用正極活物質、その製造方法及びリチウム二次電池 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4660164B2 (ja) | 非水電解質二次電池 | |
| JP4841116B2 (ja) | 非水電解質二次電池 | |
| JP4721729B2 (ja) | 非水電解質二次電池 | |
| JP5036121B2 (ja) | 非水電解質二次電池 | |
| JP6443441B2 (ja) | 非水電解質二次電池用正極活物質及び非水電解質二次電池用正極 | |
| JP4841133B2 (ja) | 非水電解質二次電池 | |
| JP4798964B2 (ja) | 非水電解質二次電池 | |
| JP2007234565A (ja) | 非水電解質二次電池 | |
| JP4307962B2 (ja) | 非水電解質二次電池 | |
| JP4424949B2 (ja) | 非水電解質二次電池 | |
| JP2008091236A (ja) | 非水電解質二次電池 | |
| JP2009217981A (ja) | 非水電解質二次電池 | |
| JP4297709B2 (ja) | 非水電解質二次電池 | |
| JP4297704B2 (ja) | 非水電解質二次電池 | |
| CN107112527B (zh) | 正极活性物质和非水电解质二次电池 | |
| JP6522661B2 (ja) | 非水電解質二次電池用正極活物質及び非水電解質二次電池 | |
| JP2009266791A (ja) | 非水電解質二次電池 | |
| JP2005085566A (ja) | 非水電解質二次電池の充放電制御方法 | |
| JP5089097B2 (ja) | 非水電解質二次電池及びその充放電方法 | |
| JP2010177207A (ja) | 非水電解質二次電池 | |
| US10873085B2 (en) | Positive electrode for lithium ion secondary battery and lithium ion secondary battery using the same | |
| JP2005339886A (ja) | 非水電解質二次電池 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120713 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20121113 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20130716 |