JP2010031048A - 有機リン酸化合物の製造方法 - Google Patents
有機リン酸化合物の製造方法 Download PDFInfo
- Publication number
- JP2010031048A JP2010031048A JP2009256364A JP2009256364A JP2010031048A JP 2010031048 A JP2010031048 A JP 2010031048A JP 2009256364 A JP2009256364 A JP 2009256364A JP 2009256364 A JP2009256364 A JP 2009256364A JP 2010031048 A JP2010031048 A JP 2010031048A
- Authority
- JP
- Japan
- Prior art keywords
- meth
- acrylic acid
- phosphoric acid
- diol
- monophosphate
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- 238000004519 manufacturing process Methods 0.000 title claims description 79
- 150000001875 compounds Chemical class 0.000 title description 42
- -1 phosphate compound Chemical class 0.000 claims abstract description 168
- 238000006243 chemical reaction Methods 0.000 claims abstract description 78
- 238000000034 method Methods 0.000 claims abstract description 71
- 239000011541 reaction mixture Substances 0.000 claims abstract description 57
- 239000000243 solution Substances 0.000 claims abstract description 56
- 125000004432 carbon atom Chemical group C* 0.000 claims abstract description 46
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims abstract description 44
- 238000005406 washing Methods 0.000 claims abstract description 35
- 239000002994 raw material Substances 0.000 claims abstract description 31
- 239000002253 acid Substances 0.000 claims abstract description 28
- 229910019142 PO4 Inorganic materials 0.000 claims abstract description 20
- 239000010452 phosphate Substances 0.000 claims abstract description 20
- 239000007864 aqueous solution Substances 0.000 claims abstract description 19
- 125000001183 hydrocarbyl group Chemical group 0.000 claims abstract 2
- CERQOIWHTDAKMF-UHFFFAOYSA-N Methacrylic acid Chemical compound CC(=C)C(O)=O CERQOIWHTDAKMF-UHFFFAOYSA-N 0.000 claims description 185
- 150000002009 diols Chemical class 0.000 claims description 111
- XHXFXVLFKHQFAL-UHFFFAOYSA-N phosphoryl trichloride Chemical compound ClP(Cl)(Cl)=O XHXFXVLFKHQFAL-UHFFFAOYSA-N 0.000 claims description 102
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 58
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 claims description 41
- 150000004712 monophosphates Chemical class 0.000 claims description 38
- 150000001412 amines Chemical class 0.000 claims description 35
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 claims description 28
- 230000015572 biosynthetic process Effects 0.000 claims description 28
- 150000001728 carbonyl compounds Chemical class 0.000 claims description 28
- 238000005886 esterification reaction Methods 0.000 claims description 21
- 230000007062 hydrolysis Effects 0.000 claims description 20
- 238000006460 hydrolysis reaction Methods 0.000 claims description 20
- 150000002148 esters Chemical class 0.000 claims description 19
- 239000008151 electrolyte solution Substances 0.000 claims description 17
- ZUQABTLQDXJZFK-UHFFFAOYSA-N 10-hydroxydecyl 2-methylprop-2-enoate Chemical group CC(=C)C(=O)OCCCCCCCCCCO ZUQABTLQDXJZFK-UHFFFAOYSA-N 0.000 claims description 14
- NIXOWILDQLNWCW-UHFFFAOYSA-N 2-Propenoic acid Natural products OC(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 claims description 14
- 230000008569 process Effects 0.000 claims description 14
- IXCSERBJSXMMFS-UHFFFAOYSA-N hydrogen chloride Substances Cl.Cl IXCSERBJSXMMFS-UHFFFAOYSA-N 0.000 claims description 13
- 229910000041 hydrogen chloride Inorganic materials 0.000 claims description 13
- 125000000962 organic group Chemical group 0.000 claims description 13
- 229920005862 polyol Polymers 0.000 claims description 13
- BYMMIQCVDHHYGG-UHFFFAOYSA-N Cl.OP(O)(O)=O Chemical compound Cl.OP(O)(O)=O BYMMIQCVDHHYGG-UHFFFAOYSA-N 0.000 claims description 12
- 230000032050 esterification Effects 0.000 claims description 12
- 239000011260 aqueous acid Substances 0.000 claims description 10
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 claims description 9
- FOTKYAAJKYLFFN-UHFFFAOYSA-N decane-1,10-diol Chemical compound OCCCCCCCCCCO FOTKYAAJKYLFFN-UHFFFAOYSA-N 0.000 claims description 9
- 229910052698 phosphorus Inorganic materials 0.000 claims description 9
- 239000011574 phosphorus Substances 0.000 claims description 9
- 230000002378 acidificating effect Effects 0.000 claims description 8
- OMDKOSBNXJTIDL-UHFFFAOYSA-N C(C=C)(=O)O.Cl.P(O)(O)(O)=O Chemical compound C(C=C)(=O)O.Cl.P(O)(O)(O)=O OMDKOSBNXJTIDL-UHFFFAOYSA-N 0.000 claims description 7
- SMZOUWXMTYCWNB-UHFFFAOYSA-N 2-(2-methoxy-5-methylphenyl)ethanamine Chemical compound COC1=CC=C(C)C=C1CCN SMZOUWXMTYCWNB-UHFFFAOYSA-N 0.000 claims description 6
- 238000000926 separation method Methods 0.000 claims description 4
- 125000002947 alkylene group Chemical group 0.000 claims description 3
- 239000003479 dental cement Substances 0.000 abstract description 60
- 238000003860 storage Methods 0.000 abstract description 41
- 238000002834 transmittance Methods 0.000 abstract description 34
- 125000002467 phosphate group Chemical group [H]OP(=O)(O[H])O[*] 0.000 abstract description 11
- 238000002360 preparation method Methods 0.000 abstract description 7
- 239000003792 electrolyte Substances 0.000 abstract description 6
- NBIIXXVUZAFLBC-UHFFFAOYSA-N phosphoric acid Substances OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 465
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 237
- 239000000178 monomer Substances 0.000 description 128
- CFKBCVIYTWDYRP-UHFFFAOYSA-N 10-phosphonooxydecyl 2-methylprop-2-enoate Chemical compound CC(=C)C(=O)OCCCCCCCCCCOP(O)(O)=O CFKBCVIYTWDYRP-UHFFFAOYSA-N 0.000 description 92
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 87
- 239000000203 mixture Substances 0.000 description 82
- RTZKZFJDLAIYFH-UHFFFAOYSA-N ether Substances CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 66
- 239000000126 substance Substances 0.000 description 55
- 239000000853 adhesive Substances 0.000 description 51
- 230000001070 adhesive effect Effects 0.000 description 50
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 37
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 36
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 33
- 150000005690 diesters Chemical class 0.000 description 32
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 27
- 239000012044 organic layer Substances 0.000 description 26
- 210000004268 dentin Anatomy 0.000 description 24
- 238000001879 gelation Methods 0.000 description 24
- 150000002430 hydrocarbons Chemical group 0.000 description 24
- 239000000047 product Substances 0.000 description 24
- NIXOWILDQLNWCW-UHFFFAOYSA-M acrylate group Chemical group C(C=C)(=O)[O-] NIXOWILDQLNWCW-UHFFFAOYSA-M 0.000 description 23
- 230000000052 comparative effect Effects 0.000 description 23
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 description 22
- 238000003786 synthesis reaction Methods 0.000 description 22
- 239000010410 layer Substances 0.000 description 21
- 239000002904 solvent Substances 0.000 description 20
- 239000007788 liquid Substances 0.000 description 19
- HMUNWXXNJPVALC-UHFFFAOYSA-N 1-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]piperazin-1-yl]-2-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethanone Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)N1CCN(CC1)C(CN1CC2=C(CC1)NN=N2)=O HMUNWXXNJPVALC-UHFFFAOYSA-N 0.000 description 18
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 16
- 239000012535 impurity Substances 0.000 description 15
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 15
- 238000006116 polymerization reaction Methods 0.000 description 15
- 235000010354 butylated hydroxytoluene Nutrition 0.000 description 13
- 238000000746 purification Methods 0.000 description 13
- 238000003756 stirring Methods 0.000 description 13
- 239000006227 byproduct Substances 0.000 description 12
- 238000004040 coloring Methods 0.000 description 12
- 239000012153 distilled water Substances 0.000 description 12
- 238000004811 liquid chromatography Methods 0.000 description 12
- 238000000605 extraction Methods 0.000 description 11
- 239000000706 filtrate Substances 0.000 description 11
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 10
- 239000003112 inhibitor Substances 0.000 description 10
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 10
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 9
- 150000003839 salts Chemical class 0.000 description 9
- WZFUQSJFWNHZHM-UHFFFAOYSA-N 2-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]piperazin-1-yl]-1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethanone Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)N1CCN(CC1)CC(=O)N1CC2=C(CC1)NN=N2 WZFUQSJFWNHZHM-UHFFFAOYSA-N 0.000 description 8
- CONKBQPVFMXDOV-QHCPKHFHSA-N 6-[(5S)-5-[[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]piperazin-1-yl]methyl]-2-oxo-1,3-oxazolidin-3-yl]-3H-1,3-benzoxazol-2-one Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)N1CCN(CC1)C[C@H]1CN(C(O1)=O)C1=CC2=C(NC(O2)=O)C=C1 CONKBQPVFMXDOV-QHCPKHFHSA-N 0.000 description 8
- 238000001914 filtration Methods 0.000 description 8
- 239000011521 glass Substances 0.000 description 8
- 239000003960 organic solvent Substances 0.000 description 8
- 238000012360 testing method Methods 0.000 description 8
- 241000283690 Bos taurus Species 0.000 description 7
- 125000005647 linker group Chemical group 0.000 description 7
- 239000011259 mixed solution Substances 0.000 description 7
- NWVVVBRKAWDGAB-UHFFFAOYSA-N p-methoxyphenol Chemical compound COC1=CC=C(O)C=C1 NWVVVBRKAWDGAB-UHFFFAOYSA-N 0.000 description 7
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N silicon dioxide Inorganic materials O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 7
- SPSPIUSUWPLVKD-UHFFFAOYSA-N 2,3-dibutyl-6-methylphenol Chemical compound CCCCC1=CC=C(C)C(O)=C1CCCC SPSPIUSUWPLVKD-UHFFFAOYSA-N 0.000 description 6
- VZSRBBMJRBPUNF-UHFFFAOYSA-N 2-(2,3-dihydro-1H-inden-2-ylamino)-N-[3-oxo-3-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)propyl]pyrimidine-5-carboxamide Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)C(=O)NCCC(N1CC2=C(CC1)NN=N2)=O VZSRBBMJRBPUNF-UHFFFAOYSA-N 0.000 description 6
- 239000004342 Benzoyl peroxide Substances 0.000 description 6
- OMPJBNCRMGITSC-UHFFFAOYSA-N Benzoylperoxide Chemical compound C=1C=CC=CC=1C(=O)OOC(=O)C1=CC=CC=C1 OMPJBNCRMGITSC-UHFFFAOYSA-N 0.000 description 6
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 6
- WTDHULULXKLSOZ-UHFFFAOYSA-N Hydroxylamine hydrochloride Chemical compound Cl.ON WTDHULULXKLSOZ-UHFFFAOYSA-N 0.000 description 6
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 6
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 6
- 238000004458 analytical method Methods 0.000 description 6
- 235000019400 benzoyl peroxide Nutrition 0.000 description 6
- 239000003054 catalyst Substances 0.000 description 6
- 239000003153 chemical reaction reagent Substances 0.000 description 6
- 238000004128 high performance liquid chromatography Methods 0.000 description 6
- 238000005259 measurement Methods 0.000 description 6
- ILWRPSCZWQJDMK-UHFFFAOYSA-N triethylazanium;chloride Chemical compound Cl.CCN(CC)CC ILWRPSCZWQJDMK-UHFFFAOYSA-N 0.000 description 6
- 150000001768 cations Chemical class 0.000 description 5
- 238000004440 column chromatography Methods 0.000 description 5
- 239000000805 composite resin Substances 0.000 description 5
- 239000000945 filler Substances 0.000 description 5
- 230000006872 improvement Effects 0.000 description 5
- 238000002156 mixing Methods 0.000 description 5
- 239000003505 polymerization initiator Substances 0.000 description 5
- NLBSQHGCGGFVJW-UHFFFAOYSA-N 2-carboxyethylphosphonic acid Chemical compound OC(=O)CCP(O)(O)=O NLBSQHGCGGFVJW-UHFFFAOYSA-N 0.000 description 4
- WOBHKFSMXKNTIM-UHFFFAOYSA-N Hydroxyethyl methacrylate Chemical compound CC(=C)C(=O)OCCO WOBHKFSMXKNTIM-UHFFFAOYSA-N 0.000 description 4
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 4
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 4
- OHFJNBZCEQRLFV-UHFFFAOYSA-N [3-[10-(2-methylprop-2-enoyloxy)decoxy]-3-oxopropyl]phosphonic acid Chemical compound CC(=C)C(=O)OCCCCCCCCCCOC(=O)CCP(O)(O)=O OHFJNBZCEQRLFV-UHFFFAOYSA-N 0.000 description 4
- 125000001931 aliphatic group Chemical group 0.000 description 4
- AYJRCSIUFZENHW-UHFFFAOYSA-L barium carbonate Chemical compound [Ba+2].[O-]C([O-])=O AYJRCSIUFZENHW-UHFFFAOYSA-L 0.000 description 4
- 239000012267 brine Substances 0.000 description 4
- 210000004027 cell Anatomy 0.000 description 4
- 238000004821 distillation Methods 0.000 description 4
- 238000011156 evaluation Methods 0.000 description 4
- 238000011835 investigation Methods 0.000 description 4
- 239000002808 molecular sieve Substances 0.000 description 4
- 239000002685 polymerization catalyst Substances 0.000 description 4
- 230000009467 reduction Effects 0.000 description 4
- URGAHOPLAPQHLN-UHFFFAOYSA-N sodium aluminosilicate Chemical compound [Na+].[Al+3].[O-][Si]([O-])=O.[O-][Si]([O-])=O URGAHOPLAPQHLN-UHFFFAOYSA-N 0.000 description 4
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 4
- 238000004448 titration Methods 0.000 description 4
- LDXJRKWFNNFDSA-UHFFFAOYSA-N 2-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)-1-[4-[2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidin-5-yl]piperazin-1-yl]ethanone Chemical compound C1CN(CC2=NNN=C21)CC(=O)N3CCN(CC3)C4=CN=C(N=C4)NCC5=CC(=CC=C5)OC(F)(F)F LDXJRKWFNNFDSA-UHFFFAOYSA-N 0.000 description 3
- JQMFQLVAJGZSQS-UHFFFAOYSA-N 2-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]piperazin-1-yl]-N-(2-oxo-3H-1,3-benzoxazol-6-yl)acetamide Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)N1CCN(CC1)CC(=O)NC1=CC2=C(NC(O2)=O)C=C1 JQMFQLVAJGZSQS-UHFFFAOYSA-N 0.000 description 3
- YLZOPXRUQYQQID-UHFFFAOYSA-N 3-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)-1-[4-[2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidin-5-yl]piperazin-1-yl]propan-1-one Chemical compound N1N=NC=2CN(CCC=21)CCC(=O)N1CCN(CC1)C=1C=NC(=NC=1)NCC1=CC(=CC=C1)OC(F)(F)F YLZOPXRUQYQQID-UHFFFAOYSA-N 0.000 description 3
- YGTVWCBFJAVSMS-UHFFFAOYSA-N 5-hydroxypentyl 2-methylprop-2-enoate Chemical compound CC(=C)C(=O)OCCCCCO YGTVWCBFJAVSMS-UHFFFAOYSA-N 0.000 description 3
- IIADORUTWJKWKW-UHFFFAOYSA-N 6-phosphonooxyhexyl 2-methylprop-2-enoate Chemical compound CC(=C)C(=O)OCCCCCCOP(O)(O)=O IIADORUTWJKWKW-UHFFFAOYSA-N 0.000 description 3
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 3
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 3
- 230000001476 alcoholic effect Effects 0.000 description 3
- 125000003118 aryl group Chemical group 0.000 description 3
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 3
- 239000003795 chemical substances by application Substances 0.000 description 3
- 238000004042 decolorization Methods 0.000 description 3
- 239000011350 dental composite resin Substances 0.000 description 3
- 239000005548 dental material Substances 0.000 description 3
- TXFOLHZMICYNRM-UHFFFAOYSA-N dichlorophosphoryloxybenzene Chemical compound ClP(Cl)(=O)OC1=CC=CC=C1 TXFOLHZMICYNRM-UHFFFAOYSA-N 0.000 description 3
- 238000011049 filling Methods 0.000 description 3
- 239000012467 final product Substances 0.000 description 3
- 230000001678 irradiating effect Effects 0.000 description 3
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 3
- 229910052760 oxygen Inorganic materials 0.000 description 3
- 239000001301 oxygen Substances 0.000 description 3
- 239000011347 resin Substances 0.000 description 3
- 229920005989 resin Polymers 0.000 description 3
- 229910000029 sodium carbonate Inorganic materials 0.000 description 3
- 239000011780 sodium chloride Substances 0.000 description 3
- 238000007711 solidification Methods 0.000 description 3
- 230000008023 solidification Effects 0.000 description 3
- 239000000725 suspension Substances 0.000 description 3
- FANCTJAFZSYTIS-IQUVVAJASA-N (1r,3s,5z)-5-[(2e)-2-[(1r,3as,7ar)-7a-methyl-1-[(2r)-4-(phenylsulfonimidoyl)butan-2-yl]-2,3,3a,5,6,7-hexahydro-1h-inden-4-ylidene]ethylidene]-4-methylidenecyclohexane-1,3-diol Chemical compound C([C@@H](C)[C@@H]1[C@]2(CCCC(/[C@@H]2CC1)=C\C=C\1C([C@@H](O)C[C@H](O)C/1)=C)C)CS(=N)(=O)C1=CC=CC=C1 FANCTJAFZSYTIS-IQUVVAJASA-N 0.000 description 2
- SHAHPWSYJFYMRX-GDLCADMTSA-N (2S)-2-(4-{[(1R,2S)-2-hydroxycyclopentyl]methyl}phenyl)propanoic acid Chemical compound C1=CC([C@@H](C(O)=O)C)=CC=C1C[C@@H]1[C@@H](O)CCC1 SHAHPWSYJFYMRX-GDLCADMTSA-N 0.000 description 2
- 229920002818 (Hydroxyethyl)methacrylate Polymers 0.000 description 2
- ATOUXIOKEJWULN-UHFFFAOYSA-N 1,6-diisocyanato-2,2,4-trimethylhexane Chemical compound O=C=NCCC(C)CC(C)(C)CN=C=O ATOUXIOKEJWULN-UHFFFAOYSA-N 0.000 description 2
- JUVSRZCUMWZBFK-UHFFFAOYSA-N 2-[n-(2-hydroxyethyl)-4-methylanilino]ethanol Chemical compound CC1=CC=C(N(CCO)CCO)C=C1 JUVSRZCUMWZBFK-UHFFFAOYSA-N 0.000 description 2
- 125000000954 2-hydroxyethyl group Chemical group [H]C([*])([H])C([H])([H])O[H] 0.000 description 2
- GMCNAQYARMUGJX-UHFFFAOYSA-N 4-phosphonooxybutyl 2-methylprop-2-enoate Chemical compound CC(=C)C(=O)OCCCCOP(O)(O)=O GMCNAQYARMUGJX-UHFFFAOYSA-N 0.000 description 2
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 2
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 2
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 2
- QIGBRXMKCJKVMJ-UHFFFAOYSA-N Hydroquinone Chemical compound OC1=CC=C(O)C=C1 QIGBRXMKCJKVMJ-UHFFFAOYSA-N 0.000 description 2
- TZYWCYJVHRLUCT-VABKMULXSA-N N-benzyloxycarbonyl-L-leucyl-L-leucyl-L-leucinal Chemical compound CC(C)C[C@@H](C=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(C)C)NC(=O)OCC1=CC=CC=C1 TZYWCYJVHRLUCT-VABKMULXSA-N 0.000 description 2
- 238000005481 NMR spectroscopy Methods 0.000 description 2
- ATUOYWHBWRKTHZ-UHFFFAOYSA-N Propane Chemical compound CCC ATUOYWHBWRKTHZ-UHFFFAOYSA-N 0.000 description 2
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 2
- MSULGOISLPYHNA-UHFFFAOYSA-N [3-[5-(2-methylprop-2-enoyloxy)pentoxy]-3-oxopropyl]phosphonic acid Chemical compound CC(=C)C(=O)OCCCCCOC(=O)CCP(O)(O)=O MSULGOISLPYHNA-UHFFFAOYSA-N 0.000 description 2
- 239000003377 acid catalyst Substances 0.000 description 2
- 239000003463 adsorbent Substances 0.000 description 2
- 239000003125 aqueous solvent Substances 0.000 description 2
- FQUNFJULCYSSOP-UHFFFAOYSA-N bisoctrizole Chemical compound N1=C2C=CC=CC2=NN1C1=CC(C(C)(C)CC(C)(C)C)=CC(CC=2C(=C(C=C(C=2)C(C)(C)CC(C)(C)C)N2N=C3C=CC=CC3=N2)O)=C1O FQUNFJULCYSSOP-UHFFFAOYSA-N 0.000 description 2
- 238000007664 blowing Methods 0.000 description 2
- RDHPKYGYEGBMSE-UHFFFAOYSA-N bromoethane Chemical compound CCBr RDHPKYGYEGBMSE-UHFFFAOYSA-N 0.000 description 2
- 230000008859 change Effects 0.000 description 2
- 239000007795 chemical reaction product Substances 0.000 description 2
- 239000003638 chemical reducing agent Substances 0.000 description 2
- 239000013078 crystal Substances 0.000 description 2
- 230000018044 dehydration Effects 0.000 description 2
- 238000006297 dehydration reaction Methods 0.000 description 2
- 239000002274 desiccant Substances 0.000 description 2
- 238000007865 diluting Methods 0.000 description 2
- 230000000694 effects Effects 0.000 description 2
- JMJWCUOIOKBVNQ-UHFFFAOYSA-N ethyl 3-diethoxyphosphorylpropanoate Chemical compound CCOC(=O)CCP(=O)(OCC)OCC JMJWCUOIOKBVNQ-UHFFFAOYSA-N 0.000 description 2
- 125000005843 halogen group Chemical group 0.000 description 2
- 238000010438 heat treatment Methods 0.000 description 2
- XXMIOPMDWAUFGU-UHFFFAOYSA-N hexane-1,6-diol Chemical compound OCCCCCCO XXMIOPMDWAUFGU-UHFFFAOYSA-N 0.000 description 2
- 239000012456 homogeneous solution Substances 0.000 description 2
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 2
- 230000003301 hydrolyzing effect Effects 0.000 description 2
- 230000002209 hydrophobic effect Effects 0.000 description 2
- 150000002500 ions Chemical class 0.000 description 2
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 2
- 235000019341 magnesium sulphate Nutrition 0.000 description 2
- 239000000463 material Substances 0.000 description 2
- 125000005395 methacrylic acid group Chemical group 0.000 description 2
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 2
- GVOISEJVFFIGQE-YCZSINBZSA-N n-[(1r,2s,5r)-5-[methyl(propan-2-yl)amino]-2-[(3s)-2-oxo-3-[[6-(trifluoromethyl)quinazolin-4-yl]amino]pyrrolidin-1-yl]cyclohexyl]acetamide Chemical compound CC(=O)N[C@@H]1C[C@H](N(C)C(C)C)CC[C@@H]1N1C(=O)[C@@H](NC=2C3=CC(=CC=C3N=CN=2)C(F)(F)F)CC1 GVOISEJVFFIGQE-YCZSINBZSA-N 0.000 description 2
- 238000006386 neutralization reaction Methods 0.000 description 2
- ABLZXFCXXLZCGV-UHFFFAOYSA-N phosphonic acid group Chemical group P(O)(O)=O ABLZXFCXXLZCGV-UHFFFAOYSA-N 0.000 description 2
- 150000003016 phosphoric acids Chemical class 0.000 description 2
- 239000000843 powder Substances 0.000 description 2
- 238000011403 purification operation Methods 0.000 description 2
- 229940005657 pyrophosphoric acid Drugs 0.000 description 2
- 238000011160 research Methods 0.000 description 2
- 239000000741 silica gel Substances 0.000 description 2
- 229910002027 silica gel Inorganic materials 0.000 description 2
- 239000000377 silicon dioxide Substances 0.000 description 2
- 235000017557 sodium bicarbonate Nutrition 0.000 description 2
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 2
- 229910052938 sodium sulfate Inorganic materials 0.000 description 2
- 235000011152 sodium sulphate Nutrition 0.000 description 2
- CHLCPTJLUJHDBO-UHFFFAOYSA-M sodium;benzenesulfinate Chemical compound [Na+].[O-]S(=O)C1=CC=CC=C1 CHLCPTJLUJHDBO-UHFFFAOYSA-M 0.000 description 2
- 125000006850 spacer group Chemical group 0.000 description 2
- 239000003381 stabilizer Substances 0.000 description 2
- 238000000967 suction filtration Methods 0.000 description 2
- 230000002194 synthesizing effect Effects 0.000 description 2
- 150000003512 tertiary amines Chemical class 0.000 description 2
- HBENZIXOGRCSQN-VQWWACLZSA-N (1S,2S,6R,14R,15R,16R)-5-(cyclopropylmethyl)-16-[(2S)-2-hydroxy-3,3-dimethylpentan-2-yl]-15-methoxy-13-oxa-5-azahexacyclo[13.2.2.12,8.01,6.02,14.012,20]icosa-8(20),9,11-trien-11-ol Chemical compound N1([C@@H]2CC=3C4=C(C(=CC=3)O)O[C@H]3[C@@]5(OC)CC[C@@]2([C@@]43CC1)C[C@@H]5[C@](C)(O)C(C)(C)CC)CC1CC1 HBENZIXOGRCSQN-VQWWACLZSA-N 0.000 description 1
- AQSYSSDRYRRQKN-UHFFFAOYSA-N (2,3-dichlorophenyl)phosphonic acid Chemical compound OP(O)(=O)C1=CC=CC(Cl)=C1Cl AQSYSSDRYRRQKN-UHFFFAOYSA-N 0.000 description 1
- IGVKWAAPMVVTFX-BUHFOSPRSA-N (e)-octadec-5-en-7,9-diynoic acid Chemical compound CCCCCCCCC#CC#C\C=C\CCCC(O)=O IGVKWAAPMVVTFX-BUHFOSPRSA-N 0.000 description 1
- JNPGUXGVLNJQSQ-BGGMYYEUSA-M (e,3r,5s)-7-[4-(4-fluorophenyl)-1,2-di(propan-2-yl)pyrrol-3-yl]-3,5-dihydroxyhept-6-enoate Chemical compound CC(C)N1C(C(C)C)=C(\C=C\[C@@H](O)C[C@@H](O)CC([O-])=O)C(C=2C=CC(F)=CC=2)=C1 JNPGUXGVLNJQSQ-BGGMYYEUSA-M 0.000 description 1
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 1
- VNQXSTWCDUXYEZ-UHFFFAOYSA-N 1,7,7-trimethylbicyclo[2.2.1]heptane-2,3-dione Chemical compound C1CC2(C)C(=O)C(=O)C1C2(C)C VNQXSTWCDUXYEZ-UHFFFAOYSA-N 0.000 description 1
- QBBZFXVSQSPGDF-UHFFFAOYSA-N 10-[hydroxy-[10-(2-methylprop-2-enoyloxy)decoxy]phosphoryl]oxydecyl 2-methylprop-2-enoate Chemical compound CC(=C)C(=O)OCCCCCCCCCCOP(O)(=O)OCCCCCCCCCCOC(=O)C(C)=C QBBZFXVSQSPGDF-UHFFFAOYSA-N 0.000 description 1
- SFRDXVJWXWOTEW-UHFFFAOYSA-N 2-(hydroxymethyl)propane-1,3-diol Chemical compound OCC(CO)CO SFRDXVJWXWOTEW-UHFFFAOYSA-N 0.000 description 1
- SXAMGRAIZSSWIH-UHFFFAOYSA-N 2-[3-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]-1,2,4-oxadiazol-5-yl]-1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethanone Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)C1=NOC(=N1)CC(=O)N1CC2=C(CC1)NN=N2 SXAMGRAIZSSWIH-UHFFFAOYSA-N 0.000 description 1
- ZRPAUEVGEGEPFQ-UHFFFAOYSA-N 2-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]pyrazol-1-yl]-1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethanone Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)C=1C=NN(C=1)CC(=O)N1CC2=C(CC1)NN=N2 ZRPAUEVGEGEPFQ-UHFFFAOYSA-N 0.000 description 1
- JVKRKMWZYMKVTQ-UHFFFAOYSA-N 2-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]pyrazol-1-yl]-N-(2-oxo-3H-1,3-benzoxazol-6-yl)acetamide Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)C=1C=NN(C=1)CC(=O)NC1=CC2=C(NC(O2)=O)C=C1 JVKRKMWZYMKVTQ-UHFFFAOYSA-N 0.000 description 1
- UEKHZPDUBLCUHN-UHFFFAOYSA-N 2-[[3,5,5-trimethyl-6-[2-(2-methylprop-2-enoyloxy)ethoxycarbonylamino]hexyl]carbamoyloxy]ethyl 2-methylprop-2-enoate Chemical compound CC(=C)C(=O)OCCOC(=O)NCCC(C)CC(C)(C)CNC(=O)OCCOC(=O)C(C)=C UEKHZPDUBLCUHN-UHFFFAOYSA-N 0.000 description 1
- ABUNWJIUMMKITG-UHFFFAOYSA-N 2-prop-2-enoyloxyethyl 1,3-dioxo-2-benzofuran-4-carboxylate Chemical compound C=CC(=O)OCCOC(=O)c1cccc2C(=O)OC(=O)c12 ABUNWJIUMMKITG-UHFFFAOYSA-N 0.000 description 1
- LZHCVNIARUXHAL-UHFFFAOYSA-N 2-tert-butyl-4-ethylphenol Chemical compound CCC1=CC=C(O)C(C(C)(C)C)=C1 LZHCVNIARUXHAL-UHFFFAOYSA-N 0.000 description 1
- GPNYZBKIGXGYNU-UHFFFAOYSA-N 2-tert-butyl-6-[(3-tert-butyl-5-ethyl-2-hydroxyphenyl)methyl]-4-ethylphenol Chemical compound CC(C)(C)C1=CC(CC)=CC(CC=2C(=C(C=C(CC)C=2)C(C)(C)C)O)=C1O GPNYZBKIGXGYNU-UHFFFAOYSA-N 0.000 description 1
- BMYNFMYTOJXKLE-UHFFFAOYSA-N 3-azaniumyl-2-hydroxypropanoate Chemical compound NCC(O)C(O)=O BMYNFMYTOJXKLE-UHFFFAOYSA-N 0.000 description 1
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 1
- YKXAYLPDMSGWEV-UHFFFAOYSA-N 4-hydroxybutyl 2-methylprop-2-enoate Chemical compound CC(=C)C(=O)OCCCCO YKXAYLPDMSGWEV-UHFFFAOYSA-N 0.000 description 1
- XFOFBPRPOAWWPA-UHFFFAOYSA-N 6-hydroxyhexyl 2-methylprop-2-enoate Chemical compound CC(=C)C(=O)OCCCCCCO XFOFBPRPOAWWPA-UHFFFAOYSA-N 0.000 description 1
- IISBACLAFKSPIT-UHFFFAOYSA-N Bisphenol A Natural products C=1C=C(O)C=CC=1C(C)(C)C1=CC=C(O)C=C1 IISBACLAFKSPIT-UHFFFAOYSA-N 0.000 description 1
- LSNNMFCWUKXFEE-UHFFFAOYSA-M Bisulfite Chemical compound OS([O-])=O LSNNMFCWUKXFEE-UHFFFAOYSA-M 0.000 description 1
- NLZUEZXRPGMBCV-UHFFFAOYSA-N Butylhydroxytoluene Chemical compound CC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 NLZUEZXRPGMBCV-UHFFFAOYSA-N 0.000 description 1
- ZMGJIQOKJQBMQN-UHFFFAOYSA-N C(CCCCCCCCCO)O.C(C(=C)C)(=O)OCCCCCCCCCCO Chemical compound C(CCCCCCCCCO)O.C(C(=C)C)(=O)OCCCCCCCCCCO ZMGJIQOKJQBMQN-UHFFFAOYSA-N 0.000 description 1
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 1
- MKYBYDHXWVHEJW-UHFFFAOYSA-N N-[1-oxo-1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)propan-2-yl]-2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidine-5-carboxamide Chemical compound O=C(C(C)NC(=O)C=1C=NC(=NC=1)NCC1=CC(=CC=C1)OC(F)(F)F)N1CC2=C(CC1)NN=N2 MKYBYDHXWVHEJW-UHFFFAOYSA-N 0.000 description 1
- IJJNKOSXHZXKCH-UHFFFAOYSA-N P(OCC)(OCC)OCC.C(C)OP(=O)(OCC)CCC(=O)OCC Chemical compound P(OCC)(OCC)OCC.C(C)OP(=O)(OCC)CCC(=O)OCC IJJNKOSXHZXKCH-UHFFFAOYSA-N 0.000 description 1
- AMFGWXWBFGVCKG-UHFFFAOYSA-N Panavia opaque Chemical compound C1=CC(OCC(O)COC(=O)C(=C)C)=CC=C1C(C)(C)C1=CC=C(OCC(O)COC(=O)C(C)=C)C=C1 AMFGWXWBFGVCKG-UHFFFAOYSA-N 0.000 description 1
- ALQSHHUCVQOPAS-UHFFFAOYSA-N Pentane-1,5-diol Chemical compound OCCCCCO ALQSHHUCVQOPAS-UHFFFAOYSA-N 0.000 description 1
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 1
- QYKIQEUNHZKYBP-UHFFFAOYSA-N Vinyl ether Chemical group C=COC=C QYKIQEUNHZKYBP-UHFFFAOYSA-N 0.000 description 1
- ULQMPOIOSDXIGC-UHFFFAOYSA-N [2,2-dimethyl-3-(2-methylprop-2-enoyloxy)propyl] 2-methylprop-2-enoate Chemical compound CC(=C)C(=O)OCC(C)(C)COC(=O)C(C)=C ULQMPOIOSDXIGC-UHFFFAOYSA-N 0.000 description 1
- XVYONSOXJYXMGT-UHFFFAOYSA-N [2-[2-(2-methylprop-2-enoyloxy)ethyl]phenyl]phosphonic acid Chemical compound CC(=C)C(=O)OCCC1=CC=CC=C1P(O)(O)=O XVYONSOXJYXMGT-UHFFFAOYSA-N 0.000 description 1
- 238000002835 absorbance Methods 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 125000003647 acryloyl group Chemical group O=C([*])C([H])=C([H])[H] 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 150000001299 aldehydes Chemical class 0.000 description 1
- 239000003513 alkali Substances 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 150000001340 alkali metals Chemical class 0.000 description 1
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 230000003466 anti-cipated effect Effects 0.000 description 1
- 229910052788 barium Inorganic materials 0.000 description 1
- DSAJWYNOEDNPEQ-UHFFFAOYSA-N barium atom Chemical compound [Ba] DSAJWYNOEDNPEQ-UHFFFAOYSA-N 0.000 description 1
- 159000000009 barium salts Chemical class 0.000 description 1
- WAKZZMMCDILMEF-UHFFFAOYSA-H barium(2+);diphosphate Chemical compound [Ba+2].[Ba+2].[Ba+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O WAKZZMMCDILMEF-UHFFFAOYSA-H 0.000 description 1
- 239000002585 base Substances 0.000 description 1
- 150000001555 benzenes Chemical class 0.000 description 1
- VEZXCJBBBCKRPI-UHFFFAOYSA-N beta-propiolactone Chemical compound O=C1CCO1 VEZXCJBBBCKRPI-UHFFFAOYSA-N 0.000 description 1
- 230000001588 bifunctional effect Effects 0.000 description 1
- 230000005540 biological transmission Effects 0.000 description 1
- 239000002639 bone cement Substances 0.000 description 1
- 229930006711 bornane-2,3-dione Natural products 0.000 description 1
- OSVHLUXLWQLPIY-KBAYOESNSA-N butyl 2-[(6aR,9R,10aR)-1-hydroxy-9-(hydroxymethyl)-6,6-dimethyl-6a,7,8,9,10,10a-hexahydrobenzo[c]chromen-3-yl]-2-methylpropanoate Chemical compound C(CCC)OC(C(C)(C)C1=CC(=C2[C@H]3[C@H](C(OC2=C1)(C)C)CC[C@H](C3)CO)O)=O OSVHLUXLWQLPIY-KBAYOESNSA-N 0.000 description 1
- 210000000692 cap cell Anatomy 0.000 description 1
- 150000001721 carbon Chemical group 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 1
- 125000002843 carboxylic acid group Chemical group 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 239000004568 cement Substances 0.000 description 1
- 239000000919 ceramic Substances 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 239000002131 composite material Substances 0.000 description 1
- 238000009833 condensation Methods 0.000 description 1
- 230000005494 condensation Effects 0.000 description 1
- 238000006482 condensation reaction Methods 0.000 description 1
- 238000010276 construction Methods 0.000 description 1
- 238000011109 contamination Methods 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 238000004132 cross linking Methods 0.000 description 1
- 125000004093 cyano group Chemical group *C#N 0.000 description 1
- INSRQEMEVAMETL-UHFFFAOYSA-N decane-1,1-diol Chemical compound CCCCCCCCCC(O)O INSRQEMEVAMETL-UHFFFAOYSA-N 0.000 description 1
- 238000000354 decomposition reaction Methods 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 230000007547 defect Effects 0.000 description 1
- 238000007033 dehydrochlorination reaction Methods 0.000 description 1
- 208000002925 dental caries Diseases 0.000 description 1
- 239000004851 dental resin Substances 0.000 description 1
- 238000001514 detection method Methods 0.000 description 1
- 230000006866 deterioration Effects 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-M dihydrogenphosphate Chemical compound OP(O)([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-M 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- XPPKVPWEQAFLFU-UHFFFAOYSA-N diphosphoric acid Chemical compound OP(O)(=O)OP(O)(O)=O XPPKVPWEQAFLFU-UHFFFAOYSA-N 0.000 description 1
- 238000002845 discoloration Methods 0.000 description 1
- 231100000676 disease causative agent Toxicity 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 239000003480 eluent Substances 0.000 description 1
- 238000004945 emulsification Methods 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 238000005530 etching Methods 0.000 description 1
- 125000001301 ethoxy group Chemical group [H]C([H])([H])C([H])([H])O* 0.000 description 1
- 239000000284 extract Substances 0.000 description 1
- 239000010419 fine particle Substances 0.000 description 1
- 235000019253 formic acid Nutrition 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 238000004817 gas chromatography Methods 0.000 description 1
- 238000007429 general method Methods 0.000 description 1
- 235000011187 glycerol Nutrition 0.000 description 1
- 229910052736 halogen Inorganic materials 0.000 description 1
- 150000002367 halogens Chemical class 0.000 description 1
- 125000001165 hydrophobic group Chemical group 0.000 description 1
- 125000002768 hydroxyalkyl group Chemical group 0.000 description 1
- 229910052588 hydroxylapatite Inorganic materials 0.000 description 1
- 239000012442 inert solvent Substances 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 239000011256 inorganic filler Substances 0.000 description 1
- 229910003475 inorganic filler Inorganic materials 0.000 description 1
- 239000013067 intermediate product Substances 0.000 description 1
- 238000004255 ion exchange chromatography Methods 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 239000002075 main ingredient Substances 0.000 description 1
- 239000012046 mixed solvent Substances 0.000 description 1
- 210000000214 mouth Anatomy 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 239000012454 non-polar solvent Substances 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- 150000002894 organic compounds Chemical class 0.000 description 1
- 150000002903 organophosphorus compounds Chemical class 0.000 description 1
- 239000007800 oxidant agent Substances 0.000 description 1
- 238000006146 oximation reaction Methods 0.000 description 1
- 150000002923 oximes Chemical class 0.000 description 1
- 125000004430 oxygen atom Chemical group O* 0.000 description 1
- XYJRXVWERLGGKC-UHFFFAOYSA-D pentacalcium;hydroxide;triphosphate Chemical compound [OH-].[Ca+2].[Ca+2].[Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O XYJRXVWERLGGKC-UHFFFAOYSA-D 0.000 description 1
- 230000035699 permeability Effects 0.000 description 1
- 150000002978 peroxides Chemical class 0.000 description 1
- 150000003014 phosphoric acid esters Chemical class 0.000 description 1
- 230000000704 physical effect Effects 0.000 description 1
- 239000003495 polar organic solvent Substances 0.000 description 1
- 238000005498 polishing Methods 0.000 description 1
- 229920003229 poly(methyl methacrylate) Polymers 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 239000004926 polymethyl methacrylate Substances 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 239000013615 primer Substances 0.000 description 1
- 239000002987 primer (paints) Substances 0.000 description 1
- 239000001294 propane Substances 0.000 description 1
- 229960000380 propiolactone Drugs 0.000 description 1
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 1
- 239000010453 quartz Substances 0.000 description 1
- 238000010992 reflux Methods 0.000 description 1
- 238000002390 rotary evaporation Methods 0.000 description 1
- 238000005070 sampling Methods 0.000 description 1
- 239000003566 sealing material Substances 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 159000000000 sodium salts Chemical class 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 238000001228 spectrum Methods 0.000 description 1
- 229910001220 stainless steel Inorganic materials 0.000 description 1
- 239000010935 stainless steel Substances 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 229910052712 strontium Inorganic materials 0.000 description 1
- CIOAGBVUUVVLOB-UHFFFAOYSA-N strontium atom Chemical compound [Sr] CIOAGBVUUVVLOB-UHFFFAOYSA-N 0.000 description 1
- 125000003011 styrenyl group Chemical group [H]\C(*)=C(/[H])C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- BUUPQKDIAURBJP-UHFFFAOYSA-N sulfinic acid Chemical compound OS=O BUUPQKDIAURBJP-UHFFFAOYSA-N 0.000 description 1
- 229910052717 sulfur Inorganic materials 0.000 description 1
- 125000004434 sulfur atom Chemical group 0.000 description 1
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 1
- 238000012719 thermal polymerization Methods 0.000 description 1
- 125000003396 thiol group Chemical group [H]S* 0.000 description 1
- 230000036962 time dependent Effects 0.000 description 1
- 238000005809 transesterification reaction Methods 0.000 description 1
- IMFACGCPASFAPR-UHFFFAOYSA-N tributylamine Chemical compound CCCCN(CCCC)CCCC IMFACGCPASFAPR-UHFFFAOYSA-N 0.000 description 1
- ZIBGPFATKBEMQZ-UHFFFAOYSA-N triethylene glycol Chemical compound OCCOCCOCCO ZIBGPFATKBEMQZ-UHFFFAOYSA-N 0.000 description 1
- 239000006097 ultraviolet radiation absorber Substances 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/06—Phosphorus compounds without P—C bonds
- C07F9/08—Esters of oxyacids of phosphorus
- C07F9/09—Esters of phosphoric acids
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/06—Phosphorus compounds without P—C bonds
- C07F9/08—Esters of oxyacids of phosphorus
- C07F9/09—Esters of phosphoric acids
- C07F9/091—Esters of phosphoric acids with hydroxyalkyl compounds with further substituents on alkyl
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/06—Phosphorus compounds without P—C bonds
- C07F9/08—Esters of oxyacids of phosphorus
- C07F9/09—Esters of phosphoric acids
- C07F9/098—Esters of polyphosphoric acids or anhydrides
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/06—Phosphorus compounds without P—C bonds
- C07F9/08—Esters of oxyacids of phosphorus
- C07F9/09—Esters of phosphoric acids
- C07F9/12—Esters of phosphoric acids with hydroxyaryl compounds
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/28—Phosphorus compounds with one or more P—C bonds
- C07F9/38—Phosphonic acids [RP(=O)(OH)2]; Thiophosphonic acids ; [RP(=X1)(X2H)2(X1, X2 are each independently O, S or Se)]
- C07F9/3804—Phosphonic acids [RP(=O)(OH)2]; Thiophosphonic acids ; [RP(=X1)(X2H)2(X1, X2 are each independently O, S or Se)] not used, see subgroups
- C07F9/3808—Acyclic saturated acids which can have further substituents on alkyl
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/28—Phosphorus compounds with one or more P—C bonds
- C07F9/38—Phosphonic acids [RP(=O)(OH)2]; Thiophosphonic acids ; [RP(=X1)(X2H)2(X1, X2 are each independently O, S or Se)]
- C07F9/40—Esters thereof
- C07F9/4071—Esters thereof the ester moiety containing a substituent or a structure which is considered as characteristic
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- Molecular Biology (AREA)
- Dental Preparations (AREA)
- Addition Polymer Or Copolymer, Post-Treatments, Or Chemical Modifications (AREA)
Abstract
【解決手段】ラジカル重合可能な二重結合、及び1又は2基のヒドロキシル基を有するリン酸残基をそれぞれ少なくとも1個有し、かつ分子内に炭素数4以上の炭化水素基を少なくとも一つ有する、特定の電気伝導度及び/又は特定の光透過率を有する有機リン酸化合物及び原料の反応率を制御して反応を行い、得られた反応混合物に対して酸の水溶液による洗浄及び電解質水溶液による洗浄を行う工程を含む、その製造方法。
【選択図】なし
Description
前記ステップ(I)で得られる反応混合物には、未反応ジオール、後のリン酸モノエステルの合成において必要な(メタ)アクリル酸モノエステルの他に、目的物でない(メタ)アクリル酸ジエステルが相当量含まれている。本発明者らの検討では、その比はモノエステル/ジエステル/未反応ジオール=0.8〜2/1/0.5〜1.5の範囲であった。(メタ)アクリル酸ジエステルに消費されたジオールは無駄となり、経済的とはいえない。特にジオールが高価な場合、コスト的に大きな問題となる。
上記の製造方法等により得られ得るリン酸モノエステルは、液体クロマトグラフィーによる分析では十分高い純度を有している。しかし、精製するに従ってリン酸モノエステルに淡黄色から淡褐色の着色がみられる場合がある。このような着色したリン酸モノマーを配合してなる歯科用接着剤においては、該接着剤の色調を審美的に優れた所望の色調に調節することが難しく、該接着剤を用いて修復した部分の色が周囲の歯と適合していないという不都合な面がある。
前記リン酸モノマー自体、或いはリン酸モノマーを含有してなる歯科用接着剤が、長期間保存されている間に粘度が上昇してゲル化や固化を起こす場合がある。さらにゲル化や固化を起こした後の該接着剤は接着力が低下する等、製品の性能低下を起こす問題がある。
〔1〕 (メタ)アクリル酸1モルに対して炭素数4〜30のジオールを1〜5モル反応させるとともに、(メタ)アクリル酸の反応率を60〜90モル%とし、ジオールの(メタ)アクリル酸モノエステル/ジオールの(メタ)アクリル酸ジエステルのモル生成比が2〜8である反応混合物を得、さらに得られたジオールの(メタ)アクリル酸モノエステルにオキシ塩化リンを反応させて、(メタ)アクリル酸モノエステルモノリン酸エステルを製造することを特徴とする、(メタ)アクリル酸モノエステルモノリン酸エステルの製造方法;
〔2〕 1つの水酸基と少なくとも1つの(メタ)アクリル基を有し、かつ少なくとも1つの炭素数4〜30の炭化水素基を有する有機残基からなるモノヒドロキシ(メタ)アクリル酸エステルに、アミン化合物の存在下でオキシ塩化リンを反応させ、(メタ)アクリル酸エステルモノリン酸エステル、(メタ)アクリル酸エステルモノリン酸エステル塩化物及びアミン塩を含有する反応混合物を得、該反応混合物を酸性水溶液で洗浄してアミン塩を水層に抽出分離し、分離して得た反応混合物を(メタ)アクリル酸エステルモノリン酸エステル塩化物の加水分解で生成する塩化水素により酸性とした電解質水溶液で洗浄することを特徴とする、(メタ)アクリル酸エステルモノリン酸エステルの製造方法;
〔3〕 (メタ)アクリル酸エステルモノリン酸エステル、(メタ)アクリル酸エステルモノリン酸エステル塩化物及びアミン塩を含有する反応混合物を得る工程が、該モノヒドロキシ(メタ)アクリル酸エステルとオキシ塩化リンをアミン化合物の存在下で反応させて(メタ)アクリル酸エステルモノリン酸エステル塩化物を得、次いで該(メタ)アクリル酸エステルモノリン酸エステル塩化物と水をアミン化合物の存在下で反応させて(メタ)アクリル酸エステルモノリン酸エステル及び微量の(メタ)アクリル酸エステルモノリン酸エステル塩化物を含有する反応混合物を得る工程である、前記〔2〕記載の製造方法;
〔4〕 分子内に炭素数が4以上の有機基と2個以上の水酸基を有するポリオール化合物を、(メタ)アクリル酸誘導体を用いて、少なくとも1個以上の水酸基を残して(メタ)アクリル酸エステル化を行って得られた、水酸基を少なくとも1個以上有する(メタ)アクリレート化合物を原料とし、該原料の水酸基をオキシハロゲン化リンを用いてリン酸エステル化する有機リン酸化合物の製造方法であって、ポリオール化合物中のカルボニル化合物の含有量が0.1モル%以下であることを特徴とする、有機リン酸化合物の製造方法;
〔5〕 ポリオール化合物が、炭素数4〜30を有するジオールである、前記〔4〕記載の製造方法;
〔6〕 (メタ)アクリル酸1モルに対して、カルボニル化合物の含有量が0.1モル%以下でありかつ炭素数4〜30を有するジオールを1〜5モル反応させて、ジオールの(メタ)アクリル酸モノエステルとジオールの(メタ)アクリル酸ジエステルを含む反応混合物を得、次いで得られた(メタ)アクリル酸モノエステルにアミン化合物の存在下でオキシ塩化リンを反応させて(メタ)アクリル酸モノエステルモノリン酸エステルを含む反応混合物を得、該反応混合物に対して酸の水溶液による洗浄及び電解質水溶液による洗浄を行って(メタ)アクリル酸モノエステルモノリン酸エステルを製造することを特徴とする、(メタ)アクリル酸モノエステルモノリン酸エステルの製造方法;
〔7〕 (メタ)アクリル酸モノエステルモノリン酸エステルを含む反応混合物を得、該反応混合物に対して酸の水溶液による洗浄及び電解質水溶液による洗浄を行なう工程が、ジオールの(メタ)アクリル酸モノエステルにアミン化合物の存在下でオキシ塩化リンを反応させて(メタ)アクリル酸モノエステルモノリン酸エステル塩化物を得、次いで該(メタ)アクリル酸モノエステルモノリン酸エステル塩化物と水をアミン化合物の存在下で反応させて(メタ)アクリル酸モノエステルモノリン酸エステル及び微量の(メタ)アクリル酸モノエステルモノリン酸エステル塩化物を含有する反応混合物を得、次いで酸の水溶液で洗浄してアミン塩を水層に抽出除去し、分離して得た反応混合物を(メタ)アクリル酸モノエステルモノリン酸エステル塩化物の加水分解で生成する塩化水素により酸性とした電解質水溶液で洗浄する工程である、前記〔6〕記載の製造方法;
〔8〕 (メタ)アクリル酸の反応率を60〜90モル%とする、前記〔6〕又は〔7〕記載の製造方法;
〔9〕 化学量論量以下のアミンの存在下で反応させることによって(メタ)アクリル酸モノエステルモノリン酸エステル塩化物を反応混合物内に含有させる、前記〔2〕、〔3〕、〔6〕又は〔7〕いずれか記載の製造方法;
〔10〕 pH3以下の酸性条件下で水溶液洗浄を行う、前記〔2〕、〔3〕、〔6〕又は〔7〕いずれか記載の製造方法;
〔11〕 ジオール中のカルボニル化合物の含有量が0.05モル%以下である、前記〔5〕〜〔7〕いずれか記載の製造方法;
〔12〕 炭素数8〜16のアルキレン基を有するジオールを使用する、前記〔1〕又は〔4〕〜〔7〕いずれか記載の製造方法;
〔13〕 ジオールが1,10−デカンジオールである、前記〔1〕又は〔5〕〜〔7〕いずれか記載の製造方法;
〔14〕 モノヒドロキシ(メタ)アクリル酸エステルが、10−メタクリロイルオキシデカン−1−オールである、前記〔2〕又は〔3〕記載の製造方法;に関する。
の構造単位のことを指す。また、2基のヒドロキシル基を有するリン酸残基とは、−P(O)(OH)2
の構造単位のことを指し、いずれもリン酸基およびホスホン酸基が該当する。
〔H2C=C(R1)COO−〕p−X−(Z)q−P(O)(OH)2
および〔H2C=C(R1)COO−〕p−X−(Z)q−P(O)(OH)−(Z)r−A
[式中、R1は水素原子またはメチル基で、pは1〜4の整数、qおよびrは0または1をあらわす。Xは炭素数が4以上の炭化水素基を含むp+1価の有機基、Zは酸素原子または硫黄原子、Aは1価の有機残基]で示されるリン酸モノマーである。Xで示される有機基(スペーサー)の例を示せば以下の通りである。
リン酸モノマーは、前記したように淡黄色から淡褐色に着色している。第一に、この原因は、製造したリン酸モノマー中の不純物の影響であると考えた。本出願人により提案されたリン酸モノマーの製造方法はいくつかあるが、例えば、特開昭59−139392号公報に示した方法で、デカンジオールのようなアルキルジオールからヒドロキシアルキルモノメタクリレートを経て、リン酸モノエステルであるメタクリロキシアルキルジハイドロジェンフォスフェートを製造する場合、目的とするリン酸モノエステル自体の純度は90〜96%で、この純度はNMRやHPLC分析により把握される。
まず、前記(1)と同様、製造して得られたリン酸モノマー中の不純物の分析を行った。しかし、本発明者らの検討により、NMRやHPLC分析の結果からみたリン酸モノマーの純度や、上記の不純物の種類や含有量は、本問題に対して相関性を殆ど持っていないことが明らかとなった。
n=9〜16
の化合物から合成したリン酸モノエステルは、優れた接着力と高度の耐水性を有する歯科用重合性組成物の原料として好適に用いられる。
(メタ)アクリル酸とジオールのエステル化反応を、無溶媒またはベンゼン、トルエン、ハロゲン化ベンゼン等の不活性溶媒中で酸触媒存在下130℃以下で行い、(メタ)アクリル酸モノエステルを合成する。その際に得られる反応混合物中のジオールの(メタ)アクリル酸モノエステル/ジオールの(メタ)アクリル酸ジエステルのモル比は、最終的に得られるリン酸モノエステルの収率を向上させる観点から、2〜8とするのが好ましい。ここでジオールの仕込み量が(メタ)アクリル酸に対して極端に少ない場合は、最終的に不必要になる(メタ)アクリル酸ジエステルが副生しやすくなり、生成する(メタ)アクリル酸エステル混合物中のモノエステル/ジエステルのモル比が2以下になりやすくなるため望ましくない。それゆえ、(メタ)アクリル酸1モルに対してジオール1〜5モル、より好ましくは1〜3モルを仕込むことが望ましい。
未反応ジオールを回収後、(メタ)アクリル酸モノエステルの水酸基をリン酸エステル化する。基本的には多数知られている公知の技術のいずれを利用しても良いが、簡単で収率の良い方法としてオキシ塩化リンを利用する次の方法がある。この工程は次に示す(i)、(ii)のように二段階に分けて考えることができる。
(アミンの第一滴下工程)反応式を化学式(m)で示す。
X−O−R−OH+P(O)Cl3
→X−O−R−O−P(O)Cl2+HCl (m)
(X−O−R−OHは(メタ)アクリル酸モノエステルを表し、Xは(メタ)アクリロイル基、Rは炭素数4〜30を有する有機残基を表す。)
(アミン第二滴下工程)反応式を化学式(n)で示す。
X−O−R−O−P(O)Cl2+H2O
→X−O−R−O−P(O)(OH)2+2HCl (n)
(X、Rは化学式(m)と同じ。)
(i)、(ii)の工程で得られる反応混合物には、リン酸モノエステルとアルカリ金属やアミンとの塩、アミン塩酸塩、塩酸、リン酸等のイオン性物質が含まれており、特にリン酸モノエステルの塩が最も多量に存在することが判明した。
リン酸モノエステルの1gに、メタノール(和光純薬特級)を加え、10重量%の希釈液とし、25℃に維持して電気伝導度を測定した。測定機器はデジタル伝導率計CM−117型(京都電子工業製)を用いた。
45℃で14日間保存したリン酸モノエステルを光路長10mmの分光光度計用ガラスセルに適量入れ、可視紫外分光光度計UV−2400型((株)島津製作所製)により、25℃にて455nmにおける光透過率%を測定した。
ジオール40gを精秤し、これをトルエン:中性エタノール=1:1の体積比である混合溶媒160ml中に加えて攪拌溶解し、この溶液に5wt/v%塩酸ヒドロキシルアミン溶液10mlを加え、1時間放置後に電位差自動滴定装置AT−410型(京都電子工業(株)製)を用いて1/10Nアルコール性KOHで滴定を行い、カルボニル基の数としての該ジオールに対するモル比(%)を下記の式により求めた。
[(A−B)×f×M]/(100×S)=カルボニル化合物(カルボニル基の数として)の対ジオールモル比(%)
A:サンプルの滴定量(ml)
B:ブランクの滴定量(ml)
S:試料採取量(g)
M:ジオールの分子量
f:1/10N アルコール性KOHファクター
150μmの幅の溝を有する歯科充填用コンポジットレジン「クリアフィルAP−X」((株)クラレ製)の硬化物(以下「レジン硬化物」と称する)を作製し、リン酸モノエステルを配合した歯科用接着剤を前記の歯科用レジン硬化物の溝に充填する。溝の上から歯科用可視光線照射器「ライテルII」(ウシオ電機(株)製)を用いて10秒間光を照射して歯科用接着剤を硬化させた。蛍光灯下約1000Lxにおいてレジン硬化物に対し、歯科用接着剤の硬化物が目立つかどうかを目視で確認し、色調適合性を良、不良の2段階で評価した。
リン酸モノエステルを配合した歯科用接着剤5gをガラス瓶に入れ、25℃の室内環境下で保存して毎日観察した。時間の経過とともにゲル状の透明な不純物が細かい粒子となって析出したものがあったが、目視でこの様な不溶物が認められた時点をゲル化までの日数とした。
下記に示すエタノール溶液を調製した。
成分(重量部)
エタノール(100)
N,N−ジエタノール−p−トルイジン(2)
ベンゼンスルフィン酸ナトリウム(4)
オキシ塩化リン18.4g(0.12モル)とジエチルエーテル100mlの混合溶液を、メカニカルスターラーと滴下漏斗をセットしたセパラブルフラスコに入れ、−40〜−30℃(内部温度)に冷却した。10−ヒドロキシデシルメタクリレート24.2g(0.1モル)とトリエチルアミン12.1g(0.12モル)とジエチルエーテル100mlの混合溶液を滴下漏斗に入れ、攪拌しながら上記の混合溶液に1時間かけて滴下した(第一滴下工程)。
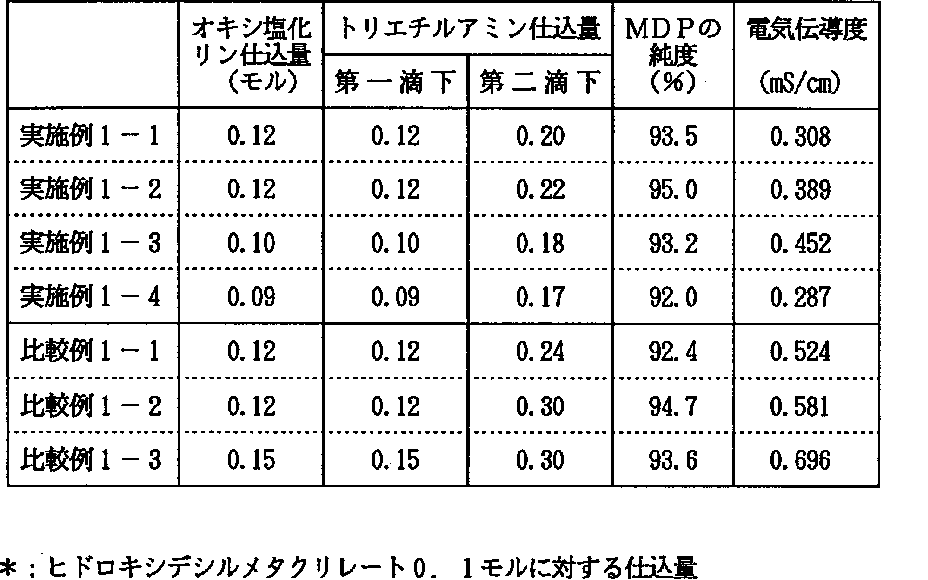
上述した第一滴下工程と第二滴下工程のオキシ塩化リンとトリエチルアミンを、それぞれ表1に記載の使用量で用いた以外は、実施例1−1と同様にしてMDPを製造した。得られたMDPの、HPLCによる純度と電気伝導度を表1にまとめた。
比較例1−1の方法で得られた電気伝導度の高いMDPの10gに、蒸留水200mlを加えて激しく攪拌振蕩するとコロイド状の懸濁液となった。この液を室温で10時間攪拌した後、該懸濁液にジエチルエーテルを加えてMDPをエーテル層に抽出した。エーテルを減圧留去するとMDPが約9g回収された。この操作を2回繰り返してイオン性物質を除去すると、電気伝導度が0.356mS/cmのMDPが得られた。
実施例1−1と同様な方法で、ジエチルエーテルを溶媒とし、10−ヒドロキシデシルメタクリレート48.4g(0.2モル)とオキシ塩化リン36.8g(0.24モル)を、トリエチルアミン24.3g(0.24モル)を用いて反応させた(第一滴下)。さらに引き続き、蒸留水12.6g(0.7モル)とトリエチルアミン40.5g(0.4モル)を用いて第二滴下反応を行った。
実施例1−6と同様なスケールと操作で、第二滴下反応までを行った。滴下終了後、さらにこの状態で2時間攪拌した。トリエチルアミンの塩酸塩を濾紙で吸引濾過し、分液漏斗を用いて濾液を水で洗浄した(200mlで3回)。有機層を無水硫酸ナトリウムで脱水乾燥しエーテルを減圧留去すると、MDPを主成分とするリン酸モノエステルが得られた。得られた生成物の電気伝導度は、0.632mS/cmであった。
(1)原料のモノヒドロキシ(メタ)アクリレート化合物(10−メタクリロイルオキシデカン−1−オール)の合成
メタクリル酸21.8g(0.25モル)と1,10−デカンジオール52.9g(0.30モル)を、80℃で反応させてエステルを合成した。この際、触媒としてp−トルエンスルホン酸3.6g、重合禁止剤として2,2'−メチレンビス(4−エチル−6−tert−ブチルフェノール)0.2gを加えた。
上記エステル混合物51.5g(10−メタクリロイルオキシデカン−1−オールを0.14モル含有)とトリエチルアミン17.1g(0.17モル)をジエチルエーテル100mlに溶解し、滴下ロートに入れて反応容器に接続した。反応容器内にオキシ塩化リン25.8g(0.17モル)をジエチルエーテル100mlに溶解して入れ、内部温度−40℃まで冷却した。オキシ塩化リン溶液を激しく攪拌し、滴下ロート内の10−メタクリロイルオキシデカン−1−オールとトリエチルアミンの溶液をゆっくり1時間かけてオキシ塩化リン溶液に滴下した。滴下終了後、−20℃でさらに30分間反応液を攪拌した。
(2)工程で得た反応液を0℃まで昇温してさらに1時間攪拌し、蒸留水15.3g(0.85モル)とトリエチルアミン28.5g(0.28モル。第一滴下工程で使用した量と合計してアミン総量は0.45モルになり、対オキシ塩化リン2.65倍モル量)の混合液を滴下し、0℃に保って30分間ゆっくり加水分解を行った。
析出してきたトリエチルアミンの塩酸塩を0.4N塩酸100mlで3回洗浄して抽出除去し、さらに2%食塩水100mlで2回洗浄した。
水を抽出後の有機層に活性炭5g((株)和光純薬工業製)を加えて1時間攪拌して脱色し、濾紙で活性炭を取り除いた有機層に重合禁止剤としてBHTを100mg添加して減圧留去すると、粘度の高い液体残渣約61.0gを得た。液体クロマトグラフィーで上記液体を同定した結果、該液体は10−メタクリロイルオキシデカン−1−オールのリン酸モノエステルであるMDPと1,10−デカンジオールのメタクリル酸ジエステルの混合物であった。
実施例2−1と同様のスケールで(4)の洗浄工程までを行った後、有機層に蒸留水200mlを加え、室温で12時間攪拌した(残存リン酸モノエステル塩化物の加水分解)。次いで実施例2−1の(5)以降の精製工程を同様に行ってMDPを合成したところ、MDPの電気伝導度は0.245mS/cmであった。
オキシ塩化リンに対するトリエチルアミンの総滴下量を表3に記載の使用量で使用した以外は、実施例2−2と同様の操作でMDPを合成した。得られたMDPの電気伝導度を表3にまとめた。
(1)(メタ)アクリル酸モノエステル(10−メタクリロイルオキシデカン−1−オール)の合成
メタクリル酸71.7g(0.83モル)とカルボニル価0.03%の1,10−デカンジオール174.0g(1.00モル、対メタクリル酸1.2倍モル量)を三ツ口フラスコに入れ、触媒としてp−トルエンスルホン酸12g、重合禁止剤として2,2’−メチレンビス(4−エチル−6−tert−ブチルフェノール)0.5gを加えた。80℃まで加熱して均一溶液とし、フラスコ内の混合物を液体クロマトグラフィー(カラム:ジーエル サイエンス社製 Unisil QC18、以下同様)で逐次追跡した。
上記エステル混合物108.7g(10−メタクリロイルオキシデカン−1−オールを0.33モル含有)とトリエチルアミン39.9g(0.40モル)をジエチルエーテル120mlに溶解し、滴下ロートに入れて反応容器に接続した。反応容器内にオキシ塩化リン60.4g(0.40モル)をジエチルエーテル120mlに溶解して入れ、内部温度−40℃まで冷却した。オキシ塩化リン溶液を激しく攪拌し、滴下ロート内のエステル混合物とトリエチルアミンの溶液を、ゆっくり1時間かけてオキシ塩化リン溶液に滴下した。滴下終了後、−20℃でさらに30分間反応液を攪拌した。
(2)工程で得た反応液を0℃まで昇温してさらに1時間攪拌し、蒸留水30g(1.67モル)とトリエチルアミン65.8g(0.65モル。第一滴下工程で使用した量と合計してアミン総量は1.06モルになり、対オキシ塩化リン2.65倍モル量)の混合液を滴下し、0℃に保って30分間ゆっくり加水分解を行った。
析出してきたトリエチルアミンの塩酸塩を0.4N塩酸100mlで3回洗浄して抽出除去し、さらに2%食塩水100mlで2回洗浄した。その後、有機層に蒸留水200mlを加え、室温で12時間攪拌した(残存リン酸モノエステル塩化物の加水分解)。
水を抽出後の有機層に活性炭100mgを加えて、室温で12時間放置した。活性炭を濾過で取り除いた有機層に重合禁止剤としてBHTを100mg添加して減圧留去すると、粘度の高い液体残渣約131.1gが得られた。液体クロマトグラフィーで上記液体を同定した結果、該液体はリン酸モノエステル(MDP)と1,10−デカンジオールのメタクリル酸ジエステルの混合物であった。また、MDP/メタクリル酸ジエステルのモル比は3.5であり、前述のメタクリル酸モノエステル/メタクリル酸ジエステルのモル比と等しく、リン酸エステル化によってメタクリル酸モノエステルがすべてMDPに転化したことが分かった。
カルボニル価0.07モル%の1,10−デカンジオールを使用し、メタクリル酸の反応率を85%、オキシ塩化リンに対するトリエチルアミンの総滴下量を2.83倍モル量にする以外は、実施例3−1と同様の条件でMDPを合成した。
カルボニル価0.14モル%の1,10−デカンジオールを使用し、メタクリル酸の反応率を98%、オキシ塩化リンに対するトリエチルアミンの総滴下量を3.23倍モル量にする以外は、実施例3−1と同様の条件でMDPを合成した。
メタクリル酸を表6に記載の反応率で反応させた以外は、実施例3−1と同様の操作でMDPを合成した。MDP/ジエステルのモル比、MDP生成量、MDP純度、ジエステル副生量、並びに未反応ジオール量について、表6にまとめた。
メタクリル酸に対してジオールを0.6倍モル量反応させ、メタクリル酸反応率を83%とした以外は、実施例3−1と同様の操作でMDPを合成した。MDP/ジエステルのモル比、MDP生成量、MDP純度、ジエステル副生量、未反応ジオール量について、表6にまとめた。
メタクリル酸に対してジオールを2.5倍モル量反応させ、メタクリル酸反応率が89%とする以外は、実施例3−1と同様にしてメタクリル酸エステル化反応を行い、モノエステルとジエステルの混合物を得た。さらに回収した未反応ジオールに対して、1回目の合成と同様にジオールがメタクリル酸に対して2.5倍モル量になるようにメタクリル酸を仕込み、メタクリル酸の反応率89%で反応させた。
表7に示すように、実施例3−1とはカルボニル価の異なるジオールを用いて、実施例3−1と同様の操作でMDPを合成した。MDPの光透過率、および前記のようにしてMDPを用いて調合した歯科用接着剤の色調適合性を評価し、これらの結果を表7にまとめた。
光透過率が低かった比較例3−5のMDPにつき、活性炭による精製を行った。比較例3−5のMDPをエタノール中に約10重量%溶解し、活性炭素粉末をエタノール溶液に対して5重量%分散させて攪拌後、活性炭素粉末を吸引濾過により濾別し、濾液のエタノールをロータリーエバポレーターにより留去して油状のMDPを得た。MDPの光透過率、および前記のようにしてMDPを用いて調合した歯科用接着剤の色調適合性を評価し、結果を表7にまとめた。
光透過率が低かった比較例3−5のMDPにつき、カラムクロマトグラフィーによる精製を行った。逆相クロマトグラフ用担体としてWakoge1 40C18((株)和光純薬工業製)を用い、溶離液として水/メタノール=3/7を用いて比較例3−5のMDPを処理し、ロータリーエバポレーターにより溶媒を留去して油状のMDPを得た。MDPの光透過率、および前記のようにしてMDPを用いて調合した歯科用接着剤の色調適合性を評価し、結果を表7にまとめた。
実施例3−1と同様の操作で(4)の洗浄工程までを行った後、残存リン酸モノエステル塩化物の加水分解を行わずに(5)以降の精製工程を同様に行ってMDPを合成した。MDPの電気伝導度、MDPを用いた歯科用接着剤のゲル化までの日数、該接着剤による調製直後(保存前)と50℃で30日間保存した後の象牙質接着力を表8にまとめた。
オキシ塩化リンに対するトリエチルアミンの総滴下量を表8に記載の使用量で使用した以外は、実施例3−1と同様の操作でMDPを合成した。MDPの電気伝導度、MDPを用いた歯科用接着剤のゲル化までの日数、該接着剤による調製直後(保存前)と50℃で30日間保存した後の象牙質接着力を表8にまとめた。
(1)(メタ)アクリル酸モノエステル(6−メタクリロイルオキシヘキサン−1−オール)の合成
メタクリル酸71.7g(0.83モル)とカルボニル価0.03モル%の1,6−ヘキサンジオール(表10の化合物6a)118.18g(1.00モル、対メタクリル酸1.2倍モル量)を三ツ口フラスコに入れ、触媒としてp−トルエンスルホン酸12g、重合禁止剤として2,2’−メチレンビス(4−エチル−6−tert−ブチルフェノール)0.5gを加えた。80℃まで加熱して均一溶液とし、フラスコ内の混合物を液体クロマトグラフィー(カラム:ジーエル サイエンス社製 Unisil QC18、以下同様)で逐次追跡した。
上記エステル混合物85.0g(6−メタクリロイルオキシヘキサン−1−オールを0.32モル含有)とトリエチルアミン39.9g(0.40モル)をジエチルエーテル120mlに溶解し、滴下ロートに入れて反応容器に接続した。反応容器内にオキシ塩化リン60.4g(0.40モル)をジエチルエーテル120mlに溶解して入れ、内部温度−40℃まで冷却した。オキシ塩化リン溶液を激しく攪拌し、滴下ロート内のエステル混合物とトリエチルアミンの溶液を、ゆっくり1時間かけてオキシ塩化リン溶液に滴下した。滴下終了後、−20℃でさらに30分間反応液を攪拌した。
(2)工程で得た反応液を0℃まで昇温してさらに1時間攪拌し、蒸留水30g(1.67モル)とトリエチルアミン65.8g(0.65モル。第一滴下工程で使用した量と合計してアミン総量は1.06モルになり、対オキシ塩化リン2.65倍モル量)の混合液を滴下し、0℃に保って30分間ゆっくり加水分解を行った。
析出してきたトリエチルアミンの塩酸塩を0.4N塩酸100mlで3回洗浄して抽出除去し、さらに2%食塩水100mlで2回洗浄した。その後、有機層に蒸留水200mlを加え、室温で12時間攪拌した(残存リン酸モノエステル塩化物の加水分解)。
水を抽出後の有機層に活性炭100mgを加えて、室温で12時間放置した。活性炭を濾過で取り除いた有機層に重合禁止剤としてジブチルヒドロキシトルエンを100mg添加して減圧留去すると、粘度の高い液体残渣約112gが得られた。液体クロマトグラフィーで上記液体を同定した結果、該液体はリン酸モノエステル(6−メタクリロイルオキシヘキシルジハイドロジェンホスフェート)と1,6−ヘキサンジオールのメタクリル酸ジエステルの混合物であった。また、リン酸モノエステル/メタクリル酸ジエステルのモル比は3.2であった。
4−メタクリロイルオキシブタン−1−オール(47.4g、0.30モル)を、実施例4−1の(2)アミン第1滴下工程の出発原料(エステル化合物)として用いて実施例4−1の(2)以降と同様の手順とモル比で反応を行い、4−メタクリロイルオキシブチルジハイドロジェンホスフェート(1e)を得た。この化合物について実施例4−1と同様に光透過率、電気伝導度、及び歯科用接着剤のゲル化までの日数を測定し、その結果を表11にまとめた。
2−ヒドロキシエチルメタクリレート54.9g(0.42モル)と、脱塩酸剤として用いるトリエチルアミン44.8g(0.44モル)をジエチルエーテル中に溶解して滴下ロートに入れた。2−ヒドロキシエチルメタクリレートに対して1.05倍モル量のジクロロリン酸フェニル93.3gをジエチルエーテル溶液に溶解して反応容器中に入れ、−20℃に冷却して激しく攪拌し、滴下ロート内の混合物をゆっくりと滴下した。さらにトリエチルアミン55.6g(0.55モル)の水溶液を滴下して反応を完結させた。使用したトリエチルアミンは、ジクロロリン酸フェニルに対して2.25倍モル量を使用した。反応液にジエチルエーテルを加えて析出してきたトリエチルアミンの塩酸塩を濾別し、有機層をイオン交換水で2回洗浄した。濾液にジブチルヒドロキシトルエンを加えてトルエンで抽出し、トルエンを減圧留去後、目的物である2−メタクリロイルオキシエチルフェニルアシドホスフェート(3a)96.5gを得た。
実施例5−1のトリエチルアミンの塩酸塩の濾過工程まで同一とし、濾液にジブチルヒドロキシトルエンを添加後、ロータリーエバポレーターで溶剤を除去した。蒸留水に濃縮した濾液を投入し、攪拌しながら炭酸バリウムを少しずつ添加して全量として66.5g(0.34モル)を添加後、15分攪拌した。ひきつづき室温で15分攪拌してリン酸バリウム塩とした。未反応の炭酸バリウムを濾過し、濾液をトルエンで3回洗浄して6N塩酸を加えた後、トルエンで抽出した。分離した有機層に活性炭を添加して12時間放置後、活性炭を濾別した。有機層をイオン交換水で4回洗浄した後、トルエンを留去して目的物である2−メタクリロイルオキシエチルフェニルアシドホスフェート(3a)を得た。
実施例5−2の製造方法において、使用原料であるジクロロリン酸フェニルに代わりジクロロフェニルホスホン酸を用い、実施例5−2と同様の原料モル比、手順で製造し、目的物である2−メタクリロイルオキシエチルフェニルホスホン酸(3b)を得た。得られたリン酸モノマーについての光透過率、及び電気伝導度、歯科用接着剤のゲル化日数、牛歯象牙質接着力、及び色調適合性を実施例5−1と同様に評価した(表12)。
実施例3−1と同じ手順により製造を行った。実施例3−1の(2)において、該混合物中のメタクリル酸モノエステルに対し、オキシ塩化リンを0.8倍モル量として反応させた。その他の原料のモル比は実施例3−1と同一とした。得られたリン酸モノエステル/リン酸ジエステルの混合物をHPLCで分析した結果、リン酸モノエステル/リン酸ジエステルのモル比が58/42であった。得られたリン酸モノマーについての光透過率、及び電気伝導度、歯科用接着剤のゲル化日数、牛歯象牙質接着力、及び色調適合性を実施例5−1と同様に評価した(表12)。
(1)5−ヒドロキシペンチルメタクリレートの製造
1,5−ペンタンジオールを原料として実施例4−1(1)と同じ手順、および原料モル比で製造し、得られたモノエステル体とジエステル体をカラムクロマトグラフィーで精製し、モノエステル体である5−ヒドロキシペンチルメタクリレートを得た。
亜リン酸トリエチルとβ−プロピオラクトンを等モル混合し、160℃にて18時間還流し反応させた。反応混合物を減圧蒸留し、130〜135℃(267〜533Pa)の留分を採取し、3−ジエチルホスホノプロピオン酸エチルを得た。
上記(2)で得られた3−ジエチルホスホノプロピオン酸エチル100g(0.42モル)、48%臭化水素酸300g、及び蟻酸200gを混合し、90℃にて加水分解しながら生成した臭化エチルを留去した。臭化エチルが生成しなくなった後、さらに加熱して濃縮し、反応混合物を氷冷して生成物の結晶を析出させた。この結晶を吸引濾過し、少量のアセトンで洗浄後、真空乾燥して2−カルボキシエチルホスホン酸を得た。
上記(1)で得た5−ヒドロキシペンチルメタクリレートを68.8g(0.40モル)を、上記(3)で得た2−カルボキシエチルホスホン酸96.3g(0.35モル)、p−トルエンスルホン酸3.5g、ジブチルヒドロキシトルエン3.5g、トルエン80gを反応容器に入れて約40kPa減圧下、約80℃で攪拌して反応させた。6時間反応後、室温まで冷却し、反応混合物を分液ロートに移して酢酸エチルを加え、水で2回洗浄した。分離した有機層に無水硫酸ナトリウムを加えて脱水し、減圧留去して油状物を得た。この油状物に炭酸ナトリウム水溶液を加えて水層に目的物を抽出し、水層に6N塩酸を加えて酸性とし、ジエチルエーテルで3回抽出した。エーテル層に活性炭を添加て12時間放置後、活性炭を濾別し、さらにイオン交換水で4回洗浄した後、エーテルを減圧留去して目的物である5−メタクリロイルオキシペンチル−3−ホスホノプロピオネート(5a)48gを得た。
(1)10−ヒドロキシデシルメタクリレートの製造
実施例5−1(1)と同様に反応を行い、得られたモノエステル体/ジエステル体の混合物をカラムクロマトグラフィーにて精製し、10−ヒドロキシデシルメタクリレートを得た。
上記(1)で得られた10−ヒドロキシデシルメタクリレートを58.3g(0.24モル)、2−カルボキシエチルホスホン酸30.7g(0.20モル)、p−トルエンスルホン酸3.5g、ジブチルヒドロキシトルエン0.35gを約40kPa、約100℃にて攪拌し、エステル化反応を行った。以降は実施例7−1と同様な処理を行い、目的物である10−メタクリロイルオキシデシル−3−ホスホノプロピオネート(5b)を28g得た。
〔1〕 ラジカル重合可能な二重結合、及び1又は2基のヒドロキシル基を有するリン酸残基をそれぞれ少なくとも1個有し、かつ分子内に炭素数4以上の炭化水素基を少なくとも一つ有する有機リン酸化合物であって、該有機リン酸化合物の10重量%メタノール溶液の25℃での電気伝導度が0.5mS/cm以下及び/又は該有機リン酸化合物の455nmにおける光透過率が90%以上であることを特徴とする有機リン酸化合物。
〔2〕 炭素数4以上の炭化水素基、(メタ)アクリレート基を有する有機基、及び1基のヒドロキシル基がリン酸残基に結合した有機リン酸化合物である前記〔1〕記載の有機リン酸化合物。
〔3〕 (メタ)アクリレート基、及び1又は2基のヒドロキシル基を有するリン酸残基が炭素数4以上の炭化水素基を少なくとも1つ有する連結基で結合された有機リン酸化合物である前記〔1〕記載の有機リン酸化合物。
〔4〕 連結基が炭素数4以上の脂肪族基である前記〔3〕記載の有機リン酸化合物。
〔5〕 (メタ)アクリレート基、及び2基のヒドロキシル基を有するリン酸残基が炭素数8〜16の脂肪族基を少なくとも1つ有する連結基で結合された有機リン酸化合物である前記〔3〕記載の有機リン酸化合物。
〔6〕 連結基が炭素数8以上で、芳香族基を少なくとも1つ含む有機基である前記〔3〕記載の有機リン酸化合物。
〔7〕 10重量%メタノール溶液の25℃での電気伝導度が、0.4mS/cm以下である前記〔1〕〜〔6〕いずれか記載の有機リン酸化合物。
〔8〕 ラジカル重合可能な二重結合、及び1又は2基のヒドロキシル基を有するリン酸残基をそれぞれ少なくとも1個有し、かつ分子内に炭素数4以上の炭化水素基を少なくとも一つ有する有機リン酸化合物であって、該有機リン酸化合物の10重量%メタノール溶液の25℃での電気伝導度が0.5mS/cm以下及び/又は該有機リン酸化合物の455nmにおける光透過率が90%以上である有機リン酸化合物、及び該有機リン酸化合物と共重合しうる重合性単量体からなることを特徴とする歯科用重合性組成物。
〔9〕 (メタ)アクリル酸1モルに対して炭素数4〜30のジオールを1〜5モル反応させるとともに、(メタ)アクリル酸の反応率を60〜90モル%とし、ジオールの(メタ)アクリル酸モノエステル/ジオールの(メタ)アクリル酸ジエステルのモル生成比が2〜8である反応混合物を得、さらに得られたジオールの(メタ)アクリル酸モノエステルにオキシ塩化リンを反応させて、(メタ)アクリル酸モノエステルモノリン酸エステルを製造することを特徴とする、(メタ)アクリル酸モノエステルモノリン酸エステルの製造方法。
〔10〕 1つの水酸基と少なくとも1つの(メタ)アクリル基を有し、かつ少なくとも1つの炭素数4〜30の炭化水素基を有する有機残基からなるモノヒドロキシ(メタ)アクリル酸エステルに、アミン化合物の存在下でオキシ塩化リンを反応させ、(メタ)アクリル酸エステルモノリン酸エステル、(メタ)アクリル酸エステルモノリン酸エステル塩化物及びアミン塩を含有する反応混合物を得、該反応混合物を酸性水溶液で洗浄してアミン塩を水層に抽出分離し、分離して得た反応混合物を(メタ)アクリル酸エステルモノリン酸エステル塩化物の加水分解で生成する塩化水素により酸性とした電解質水溶液で洗浄することを特徴とする、(メタ)アクリル酸エステルモノリン酸エステルの製造方法。
〔11〕 (メタ)アクリル酸エステルモノリン酸エステル、(メタ)アクリル酸エステルモノリン酸エステル塩化物及びアミン塩を含有する反応混合物を得る工程が、該モノヒドロキシ(メタ)アクリル酸エステルとオキシ塩化リンをアミン化合物の存在下で反応させて(メタ)アクリル酸エステルモノリン酸エステル塩化物を得、次いで該(メタ)アクリル酸エステルモノリン酸エステル塩化物と水をアミン化合物の存在下で反応させて(メタ)アクリル酸エステルモノリン酸エステル及び微量の(メタ)アクリル酸エステルモノリン酸エステル塩化物を含有する反応混合物を得る工程である、前記〔10〕記載の製造方法。
〔12〕 分子内に炭素数が4以上の有機基と2個以上の水酸基を有するポリオール化合物を、(メタ)アクリル酸誘導体を用いて、少なくとも1個以上の水酸基を残して(メタ)アクリル酸エステル化を行って得られた、水酸基を少なくとも1個以上有する(メタ)アクリレート化合物を原料とし、該原料の水酸基をオキシハロゲン化リンを用いてリン酸エステル化する有機リン酸化合物の製造方法であって、ポリオール化合物中のカルボニル化合物の含有量が0.1モル%以下であることを特徴とする、有機リン酸化合物の製造方法。
〔13〕 ポリオール化合物が、炭素数4〜30を有するジオールである、前記〔12〕記載の製造方法。
〔14〕 (メタ)アクリル酸1モルに対して、カルボニル化合物の含有量が0.1モル%以下でありかつ炭素数4〜30を有するジオールを1〜5モル反応させて、ジオールの(メタ)アクリル酸モノエステルとジオールの(メタ)アクリル酸ジエステルを含む反応混合物を得、次いで得られた(メタ)アクリル酸モノエステルにアミン化合物の存在下でオキシ塩化リンを反応させて(メタ)アクリル酸モノエステルモノリン酸エステルを含む反応混合物を得、該反応混合物に対して酸の水溶液による洗浄及び電解質水溶液による洗浄を行って(メタ)アクリル酸モノエステルモノリン酸エステルを製造することを特徴とする、(メタ)アクリル酸モノエステルモノリン酸エステルの製造方法。
〔15〕 (メタ)アクリル酸モノエステルモノリン酸エステルを含む反応混合物を得、該反応混合物に対して酸の水溶液による洗浄及び電解質水溶液による洗浄を行なう工程が、ジオールの(メタ)アクリル酸モノエステルにアミン化合物の存在下でオキシ塩化リンを反応させて(メタ)アクリル酸モノエステルモノリン酸エステル塩化物を得、次いで該(メタ)アクリル酸モノエステルモノリン酸エステル塩化物と水をアミン化合物の存在下で反応させて(メタ)アクリル酸モノエステルモノリン酸エステル及び微量の(メタ)アクリル酸モノエステルモノリン酸エステル塩化物を含有する反応混合物を得、次いで酸の水溶液で洗浄してアミン塩を水層に抽出除去し、分離して得た反応混合物を(メタ)アクリル酸モノエステルモノリン酸エステル塩化物の加水分解で生成する塩化水素により酸性とした電解質水溶液で洗浄する工程である、前記〔14〕記載の製造方法。
〔16〕 (メタ)アクリル酸の反応率を60〜90モル%とする、前記〔14〕又は〔15〕記載の製造方法。
〔17〕 化学量論量以下のアミンの存在下で反応させることによって(メタ)アクリル酸モノエステルモノリン酸エステル塩化物を反応混合物内に含有させる、前記〔10〕、〔11〕、〔14〕又は〔15〕いずれか記載の製造方法。
〔18〕 pH3以下の酸性条件下で水溶液洗浄を行う、前記〔10〕、〔11〕、〔14〕又は〔15〕いずれか記載の製造方法。
〔19〕 ジオール中のカルボニル化合物の含有量が0.05モル%以下である、前記〔13〕〜〔15〕いずれか記載の製造方法。
〔20〕 炭素数8〜16のアルキレン基を有するジオールを使用する、前記〔9〕又は〔12〕〜〔15〕いずれか記載の製造方法。
〔21〕 ジオールが1,10−デカンジオールである、前記〔9〕又は〔13〕〜〔15〕いずれか記載の製造方法。
〔22〕 モノヒドロキシ(メタ)アクリル酸エステルが、10−メタクリロイルオキシデカン−1−オールである、前記〔10〕又は〔11〕記載の製造方法。
Claims (14)
- (メタ)アクリル酸1モルに対して炭素数4〜30のジオールを1〜5モル反応させるとともに、(メタ)アクリル酸の反応率を60〜90モル%とし、ジオールの(メタ)アクリル酸モノエステル/ジオールの(メタ)アクリル酸ジエステルのモル生成比が2〜8である反応混合物を得、さらに得られたジオールの(メタ)アクリル酸モノエステルにオキシ塩化リンを反応させて、(メタ)アクリル酸モノエステルモノリン酸エステルを製造することを特徴とする、(メタ)アクリル酸モノエステルモノリン酸エステルの製造方法。
- 1つの水酸基と少なくとも1つの(メタ)アクリル基を有し、かつ少なくとも1つの炭素数4〜30の炭化水素基を有する有機残基からなるモノヒドロキシ(メタ)アクリル酸エステルに、アミン化合物の存在下でオキシ塩化リンを反応させ、(メタ)アクリル酸エステルモノリン酸エステル、(メタ)アクリル酸エステルモノリン酸エステル塩化物及びアミン塩を含有する反応混合物を得、該反応混合物を酸性水溶液で洗浄してアミン塩を水層に抽出分離し、分離して得た反応混合物を(メタ)アクリル酸エステルモノリン酸エステル塩化物の加水分解で生成する塩化水素により酸性とした電解質水溶液で洗浄することを特徴とする、(メタ)アクリル酸エステルモノリン酸エステルの製造方法。
- (メタ)アクリル酸エステルモノリン酸エステル、(メタ)アクリル酸エステルモノリン酸エステル塩化物及びアミン塩を含有する反応混合物を得る工程が、該モノヒドロキシ(メタ)アクリル酸エステルとオキシ塩化リンをアミン化合物の存在下で反応させて(メタ)アクリル酸エステルモノリン酸エステル塩化物を得、次いで該(メタ)アクリル酸エステルモノリン酸エステル塩化物と水をアミン化合物の存在下で反応させて(メタ)アクリル酸エステルモノリン酸エステル及び微量の(メタ)アクリル酸エステルモノリン酸エステル塩化物を含有する反応混合物を得る工程である、請求項2記載の製造方法。
- 分子内に炭素数が4以上の有機基と2個以上の水酸基を有するポリオール化合物を、(メタ)アクリル酸誘導体を用いて、少なくとも1個以上の水酸基を残して(メタ)アクリル酸エステル化を行って得られた、水酸基を少なくとも1個以上有する(メタ)アクリレート化合物を原料とし、該原料の水酸基をオキシハロゲン化リンを用いてリン酸エステル化する有機リン酸化合物の製造方法であって、ポリオール化合物中のカルボニル化合物の含有量が0.1モル%以下であることを特徴とする、有機リン酸化合物の製造方法。
- ポリオール化合物が、炭素数4〜30を有するジオールである、請求項4記載の製造方法。
- (メタ)アクリル酸1モルに対して、カルボニル化合物の含有量が0.1モル%以下でありかつ炭素数4〜30を有するジオールを1〜5モル反応させて、ジオールの(メタ)アクリル酸モノエステルとジオールの(メタ)アクリル酸ジエステルを含む反応混合物を得、次いで得られた(メタ)アクリル酸モノエステルにアミン化合物の存在下でオキシ塩化リンを反応させて(メタ)アクリル酸モノエステルモノリン酸エステルを含む反応混合物を得、該反応混合物に対して酸の水溶液による洗浄及び電解質水溶液による洗浄を行って(メタ)アクリル酸モノエステルモノリン酸エステルを製造することを特徴とする、(メタ)アクリル酸モノエステルモノリン酸エステルの製造方法。
- (メタ)アクリル酸モノエステルモノリン酸エステルを含む反応混合物を得、該反応混合物に対して酸の水溶液による洗浄及び電解質水溶液による洗浄を行なう工程が、ジオールの(メタ)アクリル酸モノエステルにアミン化合物の存在下でオキシ塩化リンを反応させて(メタ)アクリル酸モノエステルモノリン酸エステル塩化物を得、次いで該(メタ)アクリル酸モノエステルモノリン酸エステル塩化物と水をアミン化合物の存在下で反応させて(メタ)アクリル酸モノエステルモノリン酸エステル及び微量の(メタ)アクリル酸モノエステルモノリン酸エステル塩化物を含有する反応混合物を得、次いで酸の水溶液で洗浄してアミン塩を水層に抽出除去し、分離して得た反応混合物を(メタ)アクリル酸モノエステルモノリン酸エステル塩化物の加水分解で生成する塩化水素により酸性とした電解質水溶液で洗浄する工程である、請求項6記載の製造方法。
- (メタ)アクリル酸の反応率を60〜90モル%とする、請求項6又は7記載の製造方法。
- 化学量論量以下のアミンの存在下で反応させることによって(メタ)アクリル酸モノエステルモノリン酸エステル塩化物を反応混合物内に含有させる、請求項2、3、6又は7いずれか記載の製造方法。
- pH3以下の酸性条件下で水溶液洗浄を行う、請求項2、3、6又は7いずれか記載の製造方法。
- ジオール中のカルボニル化合物の含有量が0.05モル%以下である、請求項5〜7いずれか記載の製造方法。
- 炭素数8〜16のアルキレン基を有するジオールを使用する、請求項1又は4〜7いずれか記載の製造方法。
- ジオールが1,10−デカンジオールである、請求項1又は5〜7いずれか記載の製造方法。
- モノヒドロキシ(メタ)アクリル酸エステルが、10−メタクリロイルオキシデカン−1−オールである、請求項2又は3記載の製造方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2009256364A JP5225964B2 (ja) | 1999-03-31 | 2009-11-09 | 有機リン酸化合物の製造方法 |
Applications Claiming Priority (11)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP1999090662 | 1999-03-31 | ||
| JP9165399 | 1999-03-31 | ||
| JP9066299 | 1999-03-31 | ||
| JP1999091653 | 1999-03-31 | ||
| JP1999095145 | 1999-04-01 | ||
| JP9514599 | 1999-04-01 | ||
| JP12131999 | 1999-04-28 | ||
| JP1999121319 | 1999-04-28 | ||
| JP14100499 | 1999-05-21 | ||
| JP1999141004 | 1999-05-21 | ||
| JP2009256364A JP5225964B2 (ja) | 1999-03-31 | 2009-11-09 | 有機リン酸化合物の製造方法 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2000094720A Division JP4637994B2 (ja) | 1999-03-31 | 2000-03-30 | 歯科用接着剤 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010031048A true JP2010031048A (ja) | 2010-02-12 |
| JP5225964B2 JP5225964B2 (ja) | 2013-07-03 |
Family
ID=27525493
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2000094720A Expired - Lifetime JP4637994B2 (ja) | 1999-03-31 | 2000-03-30 | 歯科用接着剤 |
| JP2009256364A Expired - Fee Related JP5225964B2 (ja) | 1999-03-31 | 2009-11-09 | 有機リン酸化合物の製造方法 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2000094720A Expired - Lifetime JP4637994B2 (ja) | 1999-03-31 | 2000-03-30 | 歯科用接着剤 |
Country Status (14)
| Country | Link |
|---|---|
| US (1) | US6458868B1 (ja) |
| EP (1) | EP1084131B1 (ja) |
| JP (2) | JP4637994B2 (ja) |
| KR (1) | KR100684090B1 (ja) |
| CN (1) | CN1153775C (ja) |
| AT (1) | ATE255116T1 (ja) |
| AU (1) | AU764607B2 (ja) |
| BR (1) | BR0006009A (ja) |
| CA (1) | CA2333580C (ja) |
| DE (1) | DE60006757T2 (ja) |
| ES (1) | ES2209846T3 (ja) |
| NO (1) | NO20006057L (ja) |
| TW (1) | TWI262922B (ja) |
| WO (1) | WO2000058316A1 (ja) |
Families Citing this family (100)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2001038449A1 (en) * | 1999-11-22 | 2001-05-31 | Kuraray Co., Ltd. | Adhesive composition |
| DE10242106A1 (de) * | 2002-09-11 | 2004-04-15 | Fraunhofer-Gesellschaft zur Förderung der angewandten Forschung e.V. | Phosphorgruppenhaltige Carbonsäurederivate mit organisch polymerisierbaren Gruppen |
| US20040206932A1 (en) | 2002-12-30 | 2004-10-21 | Abuelyaman Ahmed S. | Compositions including polymerizable bisphosphonic acids and methods |
| US6797767B2 (en) * | 2003-01-03 | 2004-09-28 | Pulpdent Corporation | Polymerizable composite material |
| WO2005018581A2 (en) * | 2003-08-12 | 2005-03-03 | 3M Innovative Properties Company | Self-etching dental compositions and methods |
| US7030169B2 (en) * | 2003-09-26 | 2006-04-18 | 3M Innovative Properties Company | Arylsulfinate salts in initiator systems for polymeric reactions |
| US7250452B2 (en) | 2003-09-26 | 2007-07-31 | 3M Innovative Properties Company | Dental compositions and methods with arylsulfinate salts |
| US7026367B2 (en) * | 2003-09-26 | 2006-04-11 | 3M Innovative Properties Company | Photoiniators having triarylsulfonium and arylsulfinate ions |
| US7064152B2 (en) * | 2003-09-26 | 2006-06-20 | 3M Innovative Properties Company | Arylsulfinate salts in photoinitiator systems for polymerization reactions |
| US7090722B2 (en) * | 2004-05-17 | 2006-08-15 | 3M Innovative Properties Company | Acid-reactive dental fillers, compositions, and methods |
| US7090721B2 (en) * | 2004-05-17 | 2006-08-15 | 3M Innovative Properties Company | Use of nanoparticles to adjust refractive index of dental compositions |
| US7649029B2 (en) * | 2004-05-17 | 2010-01-19 | 3M Innovative Properties Company | Dental compositions containing nanozirconia fillers |
| US7156911B2 (en) * | 2004-05-17 | 2007-01-02 | 3M Innovative Properties Company | Dental compositions containing nanofillers and related methods |
| EP1784154A1 (en) | 2004-07-08 | 2007-05-16 | 3M Innovative Properties Company | Dental methods, compositions, and kits including acid-sensitive dyes |
| CA2575976A1 (en) | 2004-08-11 | 2006-02-23 | 3M Innovative Properties Company | Self-adhesive compositions including a plurality of acidic compounds |
| DE602005023509D1 (de) | 2004-11-16 | 2010-10-21 | 3M Innovative Properties Co | Dentalfüllstoffe, verfahren, zusammensetzungen mit einem caseinat |
| EP2832342A3 (en) | 2004-11-16 | 2015-02-11 | 3M Innovative Properties Company of 3M Center | Dental compositions with calcium phosphorus releasing glass |
| KR101366911B1 (ko) | 2004-11-16 | 2014-02-24 | 쓰리엠 이노베이티브 프로퍼티즈 컴파니 | 인-함유 표면 처리제를 포함하는 치과용 충전제, 및 그의조성물 및 방법 |
| DE602005025682D1 (de) | 2004-11-16 | 2011-02-10 | 3M Innovative Properties Co | Dentalfüllstoffe und zusammensetzungen mit phosphatsalzen |
| US20060204452A1 (en) * | 2005-03-10 | 2006-09-14 | Velamakanni Bhaskar V | Antimicrobial film-forming dental compositions and methods |
| US20060205838A1 (en) * | 2005-03-10 | 2006-09-14 | Velamakanni Bhaskar V | Hardenable antimicrobial dental compositions and methods |
| US7655722B2 (en) * | 2005-04-19 | 2010-02-02 | Kuraray Medical Inc. | Adhesive composition |
| KR101330957B1 (ko) | 2005-05-09 | 2013-11-18 | 쓰리엠 이노베이티브 프로퍼티즈 컴파니 | 하이브리드 단량체를 함유하는 치과용 조성물 |
| CN101170986B (zh) * | 2005-05-09 | 2011-07-27 | 3M创新有限公司 | 聚合收缩性低的可硬化牙科组合物 |
| DE102005022172A1 (de) | 2005-05-13 | 2006-11-16 | Voco Gmbh | Haftverbessernde Additive für polymerisierbare Zusammensetzungen |
| DE602006015475D1 (de) | 2005-08-05 | 2010-08-26 | 3M Espe Ag | Dentalzusammensetzungen mit einem oberflächenmodifizierten füllstoff |
| US7495054B2 (en) * | 2005-09-19 | 2009-02-24 | 3M Innovative Properties Company | Curable compositions containing dithiane monomers |
| US8026296B2 (en) | 2005-12-20 | 2011-09-27 | 3M Innovative Properties Company | Dental compositions including a thermally labile component, and the use thereof |
| US7776940B2 (en) | 2005-12-20 | 2010-08-17 | 3M Innovative Properties Company | Methods for reducing bond strengths, dental compositions, and the use thereof |
| US7896650B2 (en) | 2005-12-20 | 2011-03-01 | 3M Innovative Properties Company | Dental compositions including radiation-to-heat converters, and the use thereof |
| CN101351182B (zh) * | 2005-12-29 | 2016-01-20 | 3M创新有限公司 | 牙科用组合物和具有多环芳族组分的引发剂体系 |
| US8071662B2 (en) * | 2005-12-29 | 2011-12-06 | 3M Innovative Properties Company | Dental compositions with surface-treated filler for shelf stability |
| WO2007079144A1 (en) * | 2005-12-29 | 2007-07-12 | 3M Innovative Properties Company | Dental compositions with a water scavenger |
| US20070183986A1 (en) * | 2006-02-06 | 2007-08-09 | Ultradent Products, Inc. | Methods and systems for mixing a multi-part fluoride varnish composition |
| EP1849449A1 (en) | 2006-04-26 | 2007-10-31 | 3M Innovative Properties Company | Filler containing composition and process for production and use thereof |
| US7776010B2 (en) | 2006-05-01 | 2010-08-17 | Ultradent Products, Inc. | Syringe-in-syringe hollow inner barrel/plunger with integral seal and rupturable membrane and related kits, systems, and methods |
| ATE477283T1 (de) * | 2006-05-31 | 2010-08-15 | 3M Innovative Properties Co | Polymerisierbare zusammensetzungen enthaltend salze aus barbitursäure-derivaten |
| WO2008038651A1 (en) | 2006-09-27 | 2008-04-03 | Mitsui Chemicals, Inc. | Phosphate ester compound, metal salt thereof, dental material, and demtal composition |
| US20080096150A1 (en) | 2006-10-23 | 2008-04-24 | 3M Innovative Properties Company | Dental articles, methods, and kits including a compressible material |
| US9539065B2 (en) | 2006-10-23 | 2017-01-10 | 3M Innovative Properties Company | Assemblies, methods, and kits including a compressible material |
| CN101529957B (zh) * | 2006-11-01 | 2012-07-04 | 富士通株式会社 | 无线通信装置和无线通信方法 |
| WO2008076739A2 (en) | 2006-12-13 | 2008-06-26 | 3M Innovative Properties Company | Methods of using a dental composition having an acidic component and a photobleachable dye |
| EP2114351B1 (en) * | 2006-12-28 | 2016-07-13 | 3M Innovative Properties Company | Dental compositions with natural tooth fluorescence |
| WO2008082929A2 (en) | 2006-12-28 | 2008-07-10 | 3M Innovative Properties Company | Adhesive composition for hard tissue |
| WO2008082881A1 (en) * | 2006-12-28 | 2008-07-10 | 3M Innovative Properties Company | (meth)acryloyl-containing materials, compositions, and methods |
| US8454558B2 (en) | 2007-02-09 | 2013-06-04 | Ultradent Products, Inc. | Syringe-in-syringe hollow inner barrel/plunger with integral seal and rupturable membrane and related kits, systems and methods |
| US20110229838A1 (en) * | 2007-10-01 | 2011-09-22 | Kalgutkar Rajdeep S | Orthodontic composition with polymeric fillers |
| EP2214622B1 (en) * | 2007-11-01 | 2014-12-03 | 3M Innovative Properties Company | Dental compositions and initiator systems with color-stable amine electron donors |
| ATE546107T1 (de) * | 2007-12-13 | 2012-03-15 | 3M Innovative Properties Co | Kieferorthopädische artikel mit einer teilweise gehärteten zusammensetzung und anwendungs- und herstellungsverfahren |
| US8383163B2 (en) | 2008-01-29 | 2013-02-26 | Ultradent Products, Inc. | Fluoride varnish compositions including an organo phosphoric acid adhesion promoting agent |
| EP2133063A1 (en) * | 2008-06-10 | 2009-12-16 | 3M Innovative Properties Company | Initiator system with biphenylene derivates, method of production and use thereof |
| JP2010000465A (ja) * | 2008-06-20 | 2010-01-07 | Tokyo Univ Of Agriculture & Technology | 重金属吸着材及びその製造方法 |
| BRPI0913521A2 (pt) * | 2008-09-04 | 2015-10-13 | 3M Innovative Properties Co | composição dental endurecível e artigo dental |
| US20110171591A1 (en) * | 2008-09-30 | 2011-07-14 | Amos David T | Orthodontic composition with heat modified minerals |
| CN102224106A (zh) * | 2008-10-15 | 2011-10-19 | 3M创新有限公司 | 具有氧化锆和二氧化硅纳米粒子的填料和复合材料 |
| WO2010045096A2 (en) | 2008-10-15 | 2010-04-22 | 3M Innovative Properties Company | Dental compositions with fluorescent pigment |
| EP2376573B1 (en) * | 2008-10-22 | 2019-12-18 | 3M Innovative Properties Company | Dental composition comprising biphenyl di(meth)acrylate monomer comprising urethane moieties |
| WO2010068359A1 (en) | 2008-12-11 | 2010-06-17 | 3M Innovative Properties Company | Surface-treated calcium phosphate particles suitable for oral care and dental compositions |
| JP2011111432A (ja) * | 2009-11-30 | 2011-06-09 | Fujifilm Corp | リン酸エステルの精製方法、ポリマーの製造方法、及び、平版印刷版用版面処理剤 |
| EP2412361A1 (en) | 2010-07-29 | 2012-02-01 | 3M Innovative Properties Company | Kit of parts, method of producing and use thereof |
| US9370404B2 (en) | 2010-08-11 | 2016-06-21 | Bhaskar V. Velamakanni | Aesthetic and abrasion resistant coated dental articles and methods of making the same |
| US9044292B2 (en) | 2010-08-11 | 2015-06-02 | 3M Innovative Properties Company | Dental articles including a ceramic and microparticle coating and method of making the same |
| US20130137064A1 (en) | 2010-08-11 | 2013-05-30 | 3M Innovative Properties Company | Coated dental crowns and method of making the same |
| EP2603160A2 (en) | 2010-08-11 | 2013-06-19 | 3M Innovative Properties Company | Polymer coated dental articles and method of making the same |
| JP5691372B2 (ja) * | 2010-10-14 | 2015-04-01 | 東洋紡株式会社 | 触媒燃焼装置および触媒再生方法 |
| EP2450025B1 (de) | 2010-11-08 | 2012-11-28 | VOCO GmbH | Polymerisierbare Phosphorsäurederivate umfassend ein polyalicyclisches Strukturelement |
| WO2012078827A1 (en) * | 2010-12-10 | 2012-06-14 | Synthes Usa, Llc | Fixating two or more anatomical bodies |
| EP2658469B1 (en) | 2010-12-30 | 2019-11-27 | 3M Innovative Properties Company | Bondable dental assemblies and methods including a compressible material |
| JP2012140597A (ja) * | 2010-12-31 | 2012-07-26 | Rohm & Haas Co | リンの酸を含むモノマーからポリマービーズを製造する方法 |
| EP2688508A1 (en) | 2011-03-24 | 2014-01-29 | 3M Innovative Properties Company | Dental adhesive comprising a coated polymeric component |
| EP2578200B1 (de) | 2011-10-04 | 2018-03-28 | VOCO GmbH | Zusammensetzungen zum Infiltrieren und/oder Versiegeln von Zahnhartsubstanz und entsprechende Verfahren |
| ES2546064T3 (es) | 2011-11-22 | 2015-09-18 | Heraeus Medical Gmbh | Esterilización de monómeros polimerizables |
| BR112014013111A2 (pt) | 2011-12-01 | 2017-06-13 | 3M Innovative Properties Co | composição dental autoadesiva de componente único, processo de produção e utilização do mesmo |
| US9527931B2 (en) | 2012-02-16 | 2016-12-27 | Bisco, Inc. | Hydrophobic self-etch dental adhesive compositions |
| US10028894B2 (en) | 2013-09-09 | 2018-07-24 | 3M Innovative Properties Company | Dental composition containing polyoxometalates, process of production and use thereof |
| WO2015050767A1 (en) * | 2013-10-03 | 2015-04-09 | 3M Innovative Properties Company | Ligand-functionalized substrates with enhanced binding capacity |
| WO2015126865A1 (en) | 2014-02-18 | 2015-08-27 | 3M Innovative Properties Company | Adhesive bonding composition and use thereof |
| JP6616310B2 (ja) | 2014-02-18 | 2019-12-04 | スリーエム イノベイティブ プロパティズ カンパニー | 歯科用組成物及びその使用 |
| EP3107523B1 (en) | 2014-02-18 | 2018-10-17 | 3M Innovative Properties Company | Dental composition and use thereof |
| JP2015168672A (ja) * | 2014-03-10 | 2015-09-28 | サンメディカル株式会社 | 歯科用組成物 |
| RU2683315C2 (ru) | 2014-07-10 | 2019-03-28 | 3М Инновейтив Пропертиз Компани | Двухкомпонентный самоклеящийся стоматологический состав, способ его изготовления и применения |
| CN104151350B (zh) * | 2014-08-18 | 2016-05-04 | 长春工业大学 | 口腔粘接剂甲基丙烯酰癸基二氢磷酸酯的合成方法 |
| WO2017100231A1 (en) | 2015-12-08 | 2017-06-15 | 3M Innovative Properties Company | Two-component self-adhesive dental composition, storage stable initiator system, and use thereof |
| EP3522817B1 (en) | 2016-10-05 | 2021-12-08 | 3M Innovative Properties Company | Application device with redox initiator system, method of production and use thereof |
| WO2018148238A1 (en) | 2017-02-13 | 2018-08-16 | 3M Innovative Properties Company | Self-adhesive dental resin composition and use thereof |
| US11160733B2 (en) | 2017-05-15 | 2021-11-02 | 3M Innovative Properties Company | Dental adhesive composition, preparation and use thereof |
| US11612548B2 (en) | 2017-11-08 | 2023-03-28 | 3M Innovative Properties Company | Radiopaque dental composition |
| US10932995B2 (en) | 2017-11-08 | 2021-03-02 | 3M Innovative Properties Company | Dental composition with high E-modulus |
| WO2019132849A2 (en) * | 2017-12-29 | 2019-07-04 | Yildiz Teknik Universitesi | Production of antibacterial and regenerative dental composite using supportive phases (fillers) antibacterial and bioactive properties of which are improved |
| JP7199425B2 (ja) * | 2018-04-20 | 2023-01-05 | クラレノリタケデンタル株式会社 | 歯科用接着性組成物 |
| CN112055579B (zh) | 2018-05-02 | 2024-01-23 | 3M创新有限公司 | 用于固定牙科用复合材料的单组分牙科用粘合剂组合物 |
| EP3880156B1 (en) | 2018-11-14 | 2025-08-20 | Solventum Intellectual Properties Company | Storage stable two-component dual cure dental composition |
| JP2021088512A (ja) * | 2019-12-02 | 2021-06-10 | 株式会社トクヤマデンタル | 歯科用リン酸エステル系メタクリルモノマーの製造方法 |
| EP4106710A1 (en) | 2020-02-19 | 2022-12-28 | 3M Innovative Properties Company | Ascorbic acid component for use in a method of treating the surface of a prepared tooth |
| JP7455363B2 (ja) * | 2020-02-25 | 2024-03-26 | 株式会社トクヤマデンタル | リン酸モノマー組成物およびその製造方法、並びに歯科用接着性組成物 |
| KR102123279B1 (ko) * | 2020-03-02 | 2020-06-16 | 표상현 | 부분(메트)아크릴레이트화 폴리올의 분리 방법 및 이를 이용하여 제조된 (메트)아크릴레이트로 관능화된 우레탄-계 물질 |
| WO2022003470A1 (en) | 2020-07-03 | 2022-01-06 | 3M Innovative Properties Company | Process for producing a surface-modified dental article |
| CN116710023A (zh) | 2020-12-30 | 2023-09-05 | 3M创新有限公司 | 可粘合的畸齿矫正组件和用于粘合的方法 |
| CN117580559A (zh) | 2021-06-28 | 2024-02-20 | 3M创新有限公司 | 牙科用粘固剂组合物、组件套盒及其用途 |
| JP2025540069A (ja) | 2022-12-06 | 2025-12-11 | ソルベンタム インテレクチュアル プロパティズ カンパニー | 表面処理された充填剤、このような充填剤を含有する歯科用組成物、その製造方法及び使用 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS5821687A (ja) * | 1981-07-29 | 1983-02-08 | Kuraray Co Ltd | (メタ)アクリロイルオキシアルキルジハイドロジエンホスフエ−ト |
| JPS58128393A (ja) * | 1982-01-28 | 1983-07-30 | Kuraray Co Ltd | 新規な重合性リン酸モノエステル |
| JPH03294286A (ja) * | 1990-04-12 | 1991-12-25 | Shiyoufuu:Kk | 接着剤組成物 |
| JP2002523525A (ja) * | 1998-08-18 | 2002-07-30 | バイオマット サイエンス,インク. | 人体硬質組織用接着性組成物 |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3855364A (en) * | 1973-01-05 | 1974-12-17 | Alcolac Inc | Phosphate esters of hydroxyalkyl acrylates and hydroxyalkyl methacrylates |
| GB1569021A (en) | 1976-03-17 | 1980-06-11 | Kuraray Co | Adhesive cementing agents containing partial phosphonic orphosphonic acid esters |
| JPS5846156B2 (ja) * | 1977-03-15 | 1983-10-14 | 株式会社クラレ | 硬質組織用接着剤 |
| JPS59129278A (ja) * | 1983-01-14 | 1984-07-25 | Kuraray Co Ltd | 歯科・整形外科用接着剤 |
| DE3269173D1 (en) | 1981-07-29 | 1986-03-27 | Kuraray Co | Adhesive composition |
| DE68904665T2 (de) | 1988-03-17 | 1993-09-02 | Kuraray Co | Haertbare harzzusammensetzung. |
| JPH0853506A (ja) * | 1994-08-11 | 1996-02-27 | Okura Ind Co Ltd | 嫌気硬化性組成物の空気接触面の硬化方法 |
| JPH11209214A (ja) * | 1998-01-16 | 1999-08-03 | Gc Corp | 歯科用修復材 |
| JP4198237B2 (ja) * | 1998-08-20 | 2008-12-17 | 株式会社クラレ | 抗菌性歯科用接着剤システム |
| US6315566B1 (en) * | 1999-05-18 | 2001-11-13 | 3M Innovative Properties Company | Dental materials |
| US6350839B2 (en) * | 2000-04-17 | 2002-02-26 | Ivoclar Vivadent Ag | Hydrolysis-stable and polymerizable acrylophosphonic acid monoesters |
-
2000
- 2000-03-30 KR KR1020007013518A patent/KR100684090B1/ko not_active Expired - Fee Related
- 2000-03-30 US US09/701,374 patent/US6458868B1/en not_active Expired - Lifetime
- 2000-03-30 AU AU34552/00A patent/AU764607B2/en not_active Ceased
- 2000-03-30 CA CA002333580A patent/CA2333580C/en not_active Expired - Fee Related
- 2000-03-30 EP EP00912957A patent/EP1084131B1/en not_active Expired - Lifetime
- 2000-03-30 WO PCT/JP2000/002002 patent/WO2000058316A1/en not_active Ceased
- 2000-03-30 CN CNB008010072A patent/CN1153775C/zh not_active Expired - Lifetime
- 2000-03-30 BR BR0006009-7A patent/BR0006009A/pt not_active Application Discontinuation
- 2000-03-30 AT AT00912957T patent/ATE255116T1/de not_active IP Right Cessation
- 2000-03-30 ES ES00912957T patent/ES2209846T3/es not_active Expired - Lifetime
- 2000-03-30 DE DE60006757T patent/DE60006757T2/de not_active Expired - Lifetime
- 2000-03-30 JP JP2000094720A patent/JP4637994B2/ja not_active Expired - Lifetime
- 2000-03-31 TW TW089106100A patent/TWI262922B/zh active
- 2000-11-29 NO NO20006057A patent/NO20006057L/no not_active Application Discontinuation
-
2009
- 2009-11-09 JP JP2009256364A patent/JP5225964B2/ja not_active Expired - Fee Related
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS5821687A (ja) * | 1981-07-29 | 1983-02-08 | Kuraray Co Ltd | (メタ)アクリロイルオキシアルキルジハイドロジエンホスフエ−ト |
| JPS58128393A (ja) * | 1982-01-28 | 1983-07-30 | Kuraray Co Ltd | 新規な重合性リン酸モノエステル |
| JPH03294286A (ja) * | 1990-04-12 | 1991-12-25 | Shiyoufuu:Kk | 接着剤組成物 |
| JP2002523525A (ja) * | 1998-08-18 | 2002-07-30 | バイオマット サイエンス,インク. | 人体硬質組織用接着性組成物 |
Also Published As
| Publication number | Publication date |
|---|---|
| AU3455200A (en) | 2000-10-16 |
| BR0006009A (pt) | 2001-03-06 |
| US6458868B1 (en) | 2002-10-01 |
| TWI262922B (en) | 2006-10-01 |
| WO2000058316A1 (en) | 2000-10-05 |
| AU764607B2 (en) | 2003-08-28 |
| NO20006057D0 (no) | 2000-11-29 |
| HK1037375A1 (en) | 2002-02-08 |
| DE60006757T2 (de) | 2004-09-30 |
| CN1310720A (zh) | 2001-08-29 |
| EP1084131B1 (en) | 2003-11-26 |
| ATE255116T1 (de) | 2003-12-15 |
| CA2333580A1 (en) | 2000-10-05 |
| JP2001039992A (ja) | 2001-02-13 |
| JP5225964B2 (ja) | 2013-07-03 |
| KR100684090B1 (ko) | 2007-02-16 |
| ES2209846T3 (es) | 2004-07-01 |
| CN1153775C (zh) | 2004-06-16 |
| NO20006057L (no) | 2001-01-29 |
| JP4637994B2 (ja) | 2011-02-23 |
| CA2333580C (en) | 2009-06-02 |
| DE60006757D1 (de) | 2004-01-08 |
| KR20010043945A (ko) | 2001-05-25 |
| EP1084131A1 (en) | 2001-03-21 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5225964B2 (ja) | 有機リン酸化合物の製造方法 | |
| JP4921979B2 (ja) | 一液型自己エッチング自己プライマー処理の歯科用接着剤組成物 | |
| Moszner et al. | Monomers for adhesive polymers, 2. Synthesis and radical polymerisation of hydrolytically stable acrylic phosphonic acids | |
| EP1296634B1 (de) | Phosphonsäuren enthaltendes dentalmaterial | |
| EP0074708A2 (en) | Adhesive composition | |
| Moszner et al. | Monomers for adhesive polymers, 3. Synthesis, radical polymerization and adhesive properties of hydrolytically stable phosphonic acid monomers | |
| US20100024683A1 (en) | Phosphate compound, metal salt thereof, dental material and dental composition | |
| EP2482787A2 (en) | Novel multifunctional molecules for dental bonding applications having improved adhesion | |
| EP1601679B1 (en) | A poymerizable phosphoric acid ester derivative and a dental composition employing it. | |
| Ogliari et al. | Synthesis of phosphate monomers and bonding to dentin: esterification methods and use of phosphorus pentoxide | |
| JP5008852B2 (ja) | トリシクロデカン誘導体の異性体混合物 | |
| JPS58128393A (ja) | 新規な重合性リン酸モノエステル | |
| EP1537130B1 (de) | Phosphorgruppenhaltige carbonsäurederivate mit organisch polymerisierbaren gruppen | |
| RU2241003C2 (ru) | Способы получения фосфатоорганического соединения, фосфатоорганическое соединение и зубная полимеризуемая композиция на его основе | |
| JP5570229B2 (ja) | リン酸エステル化合物及びそれを含む重合性組成物 | |
| KR20170033085A (ko) | 카테콜 유도체 기반의 접착성 조성물 및 이의 제조방법 | |
| JP4507580B2 (ja) | シリコーン化合物の製造方法およびシリコーン剤 | |
| JP7723413B2 (ja) | 双性イオン化合物の製造方法 | |
| JP4509323B2 (ja) | リン酸モノエステルの精製方法 | |
| Nikolic | Synthesis and evaluation of novel MAPO-based photoinitiators | |
| EP1462080B1 (en) | Self-adhesive polymerizable monomer and dental/medical compositions therefrom | |
| JP2021088512A (ja) | 歯科用リン酸エステル系メタクリルモノマーの製造方法 | |
| JP2020066578A (ja) | リン酸化合物を含有する組成物及びその製造方法 | |
| WO2013105049A1 (fr) | Composes fluorophosphonyles, composition les contenant et leur utilisation pour restaurer les dents |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20091111 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20120627 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120820 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20130304 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20130313 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5225964 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20160322 Year of fee payment: 3 |
|
| LAPS | Cancellation because of no payment of annual fees |