JP2007534702A - 胃腸毒性の低い治療薬としてのインドール酢酸、及びインデン酢酸誘導体 - Google Patents
胃腸毒性の低い治療薬としてのインドール酢酸、及びインデン酢酸誘導体 Download PDFInfo
- Publication number
- JP2007534702A JP2007534702A JP2007509739A JP2007509739A JP2007534702A JP 2007534702 A JP2007534702 A JP 2007534702A JP 2007509739 A JP2007509739 A JP 2007509739A JP 2007509739 A JP2007509739 A JP 2007509739A JP 2007534702 A JP2007534702 A JP 2007534702A
- Authority
- JP
- Japan
- Prior art keywords
- alkyl
- group
- substituted
- hydrogen atom
- compound
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- MLKXDPUZXIRXEP-MFOYZWKCSA-N CC1=C(CC(O)=O)c2cc(F)ccc2/C1=C\c(cc1)ccc1S(C)=O Chemical compound CC1=C(CC(O)=O)c2cc(F)ccc2/C1=C\c(cc1)ccc1S(C)=O MLKXDPUZXIRXEP-MFOYZWKCSA-N 0.000 description 1
- DXPXXIRHSZUEBE-DEDYPNTBSA-N CSc1ccc(/C=C(\C=C(CC(NCc2ccccc2)=O)c2c3)/c2ccc3F)cc1 Chemical compound CSc1ccc(/C=C(\C=C(CC(NCc2ccccc2)=O)c2c3)/c2ccc3F)cc1 DXPXXIRHSZUEBE-DEDYPNTBSA-N 0.000 description 1
- CGIGDMFJXJATDK-UHFFFAOYSA-N Cc1c(CC(O)=O)c2cc(OC)ccc2[n]1C(c(cc1)ccc1Cl)=O Chemical compound Cc1c(CC(O)=O)c2cc(OC)ccc2[n]1C(c(cc1)ccc1Cl)=O CGIGDMFJXJATDK-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C233/00—Carboxylic acid amides
- C07C233/01—Carboxylic acid amides having carbon atoms of carboxamide groups bound to hydrogen atoms or to acyclic carbon atoms
- C07C233/02—Carboxylic acid amides having carbon atoms of carboxamide groups bound to hydrogen atoms or to acyclic carbon atoms having nitrogen atoms of carboxamide groups bound to hydrogen atoms or to carbon atoms of unsubstituted hydrocarbon radicals
- C07C233/11—Carboxylic acid amides having carbon atoms of carboxamide groups bound to hydrogen atoms or to acyclic carbon atoms having nitrogen atoms of carboxamide groups bound to hydrogen atoms or to carbon atoms of unsubstituted hydrocarbon radicals with carbon atoms of carboxamide groups bound to carbon atoms of an unsaturated carbon skeleton containing six-membered aromatic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/40—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil
- A61K31/403—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil condensed with carbocyclic rings, e.g. carbazole
- A61K31/404—Indoles, e.g. pindolol
- A61K31/405—Indole-alkanecarboxylic acids; Derivatives thereof, e.g. tryptophan, indomethacin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C235/00—Carboxylic acid amides, the carbon skeleton of the acid part being further substituted by oxygen atoms
- C07C235/02—Carboxylic acid amides, the carbon skeleton of the acid part being further substituted by oxygen atoms having carbon atoms of carboxamide groups bound to acyclic carbon atoms and singly-bound oxygen atoms bound to the same carbon skeleton
- C07C235/32—Carboxylic acid amides, the carbon skeleton of the acid part being further substituted by oxygen atoms having carbon atoms of carboxamide groups bound to acyclic carbon atoms and singly-bound oxygen atoms bound to the same carbon skeleton the carbon skeleton containing six-membered aromatic rings
- C07C235/34—Carboxylic acid amides, the carbon skeleton of the acid part being further substituted by oxygen atoms having carbon atoms of carboxamide groups bound to acyclic carbon atoms and singly-bound oxygen atoms bound to the same carbon skeleton the carbon skeleton containing six-membered aromatic rings having the nitrogen atoms of the carboxamide groups bound to hydrogen atoms or to acyclic carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C247/00—Compounds containing azido groups
- C07C247/02—Compounds containing azido groups with azido groups bound to acyclic carbon atoms of a carbon skeleton
- C07C247/12—Compounds containing azido groups with azido groups bound to acyclic carbon atoms of a carbon skeleton being further substituted by carboxyl groups
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C317/00—Sulfones; Sulfoxides
- C07C317/44—Sulfones; Sulfoxides having sulfone or sulfoxide groups and carboxyl groups bound to the same carbon skeleton
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C323/00—Thiols, sulfides, hydropolysulfides or polysulfides substituted by halogen, oxygen or nitrogen atoms, or by sulfur atoms not being part of thio groups
- C07C323/50—Thiols, sulfides, hydropolysulfides or polysulfides substituted by halogen, oxygen or nitrogen atoms, or by sulfur atoms not being part of thio groups containing thio groups and carboxyl groups bound to the same carbon skeleton
- C07C323/62—Thiols, sulfides, hydropolysulfides or polysulfides substituted by halogen, oxygen or nitrogen atoms, or by sulfur atoms not being part of thio groups containing thio groups and carboxyl groups bound to the same carbon skeleton having the sulfur atom of at least one of the thio groups bound to a carbon atom of a six-membered aromatic ring of the carbon skeleton
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/02—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom condensed with one carbocyclic ring
- C07D209/04—Indoles; Hydrogenated indoles
- C07D209/10—Indoles; Hydrogenated indoles with substituted hydrocarbon radicals attached to carbon atoms of the hetero ring
- C07D209/18—Radicals substituted by carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals
- C07D209/26—Radicals substituted by carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals with an acyl radical attached to the ring nitrogen atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2601/00—Systems containing only non-condensed rings
- C07C2601/12—Systems containing only non-condensed rings with a six-membered ring
- C07C2601/14—The ring being saturated
Abstract
【選択図】図1
Description
本特許出願は、2004年4月26日に出願された米国仮出願番号第60/565,489号の利益を主張し、その全内容は、本明細書中に引用により取り込まれている。
(助成金の記述)
本研究は、米国国立衛生研究所の助成金番号CA89450によりサポートされている。従って、米国政府は、本開示主題において特定の権利を有する。
一般的に、本開示主題は、シクロオキシゲナーゼ酵素を阻害する能力を低下するように改質されている、非ステロイド性抗炎症薬(NSAID)の誘導体に関するものである。また、シクロオキシゲナーゼ阻害化合物の特異性の変更方法、及び様々な生物活性を調節する該改質された化合物の使用方法を提供する。
15d−PGJ2 − 15−デオキシ−12,14−プロスタグランジンJ2
AA − アラキドン酸
AD − アルツハイマー病
APP − アミロイド前駆体タンパク質
ATCC − 米国微生物系統保存機関(American Type Culture Collection)
CCDB − ケンブリッジ結晶学データバンク(Cambridge Crystallographic Data Bank)
CNS − 中枢神経系
COX − シクロオキシゲナーゼ
COX−1 − シクロオキシゲナーゼ−1
COX−2 − シクロオキシゲナーゼ−2
DMAP − ジメチルアミノピリジン
DMEM − ダルベッコの改質イーグル培地
DM−INDO − 2−デス−メチルインドメタシン
DMSO − ジメチルスルホキシド
DTT − ジチオスレイトール
EBA − ブロモ酢酸エチル
ED50 − 細胞生存率を50%に減少する化合物濃度
EDCI − N−(3−ジメチルアミノプロピル)−N’−エチルカルボジイミド
EDTA − エチレンジアミン四酢酸
ESI−MS − エレクトロスプレーイオン化
Et2O − ジエチルエーテル
EtOAc − 酢酸エチル
FBS − ウシ胎児血清
GI − 胃腸
HOAc − 酢酸
IC50 − 酵素又は細胞活動を50%に減少する阻害剤濃度
INDO − インドメタシン
mCOX−2 − マウスCOX−2
MODY − 若年者の成人発症型糖尿病
NSAID − 非ステロイド性抗炎症薬
oCOX−1 − ヒツジCOX−1
PG − プロスタグランジン
PMA − リンモリブデン酸
PMTBA − p−メチルチオベンズアルデヒド
PPA − ポリリン酸
PPAR − ペルオキシソーム増殖因子[s]-活性化受容体
ppm − 100万分の1
PTSA − p−トルエンスルホン酸・H2O
SDS − ドデシル硫酸ナトリウム
SDS−PAGE − ドデシル硫酸ナトリウム−ポリアクリルアミドゲル電気泳動
S.E. − 標準誤差
TMS − テトラメチルシラン
非ステロイド性抗炎症薬(NSAID)は、抗炎症性、及び解熱性のために広く使用され、ヒトの窮迫、及び病気を治療する治療薬類である。典型的なNSAIDには、アスピリン、イブプロフェン、アセトアミノフェン、インドメタシン、及びナプロキセンなどがある。
NSAIDの抗炎症活性、及び解熱活性は、該シクロオキシゲナーゼ(COX)酵素に結合し、かつその作用を阻害する、これらの化合物の能力に由来する。COX活性は、シクロオキシゲナーゼ−1(COX−1)、及びシクロオキシゲナーゼ−2(COX−2; DeWitt & Smith, 1988; Yokoyama & Tanabe, 1989; Hla & Neilson, 1992を参照されたい。)と呼ばれる2つの異なった、独立に制御される酵素に由来する。COX−1は、構成イソ型であり、主に、胃腸(GI)路の細胞保護的プロスタグランジンの合成に応答し、血小板の凝集を引き起こす(Allisonらの論文, 1992)。一方、COX−2は、誘発性であり、かつ短命である。その発現は、内毒素、サイトカイン、及びマイトジェンに応答して刺激される(Kujubuらの論文, 1991; Leeらの論文, 1992; O'Sullivanらの論文, 1993)。NSAIDは、COX−1、及びCOX−2の選択性の変化を示すが、一般に、多くは、両酵素に対して阻害活性を示す(Meadeらの論文, 1993)。
本要旨は、本開示主題の幾つかの実施態様を記載し、多くの場合において、これらの実施態様の変更、及び置換を記載する。本要旨は、単に、多くの例証であり、かつ実施態様は変更される。所定の実施態様の1以上の代表的特徴の言及は、同様に、例証である。前記実施態様は、通常、言及された特徴の有無にかかわらず存在し得る;同様に、これらの特徴は、この要旨に記載されていてもいなくても、本開示主題の他の実施態様に適用され得る。必要以上の反復を避けるために、本要旨には、前記特徴の可能な組合せ全てを記載、又は提示しない。
また、本開示主題は、癌、神経変性疾患、及び糖尿病からなる群から選択される、対象の疾患の治療方法を提供する。幾つかの実施態様において、該方法は、該対象に、化合物の誘導体の治療有効量を投与することを含み、該化合物は、2’メチル基を有するインドール酢酸、又はインデン酢酸官能基を含むシクロオキシゲナーゼ阻害剤であり、かつ該誘導体は、該2’メチル基を、水素原子;ハロ;メチル基の少なくとも1つの水素原子がハロゲンで置換されたハロメチル;C2〜C6アルキル;C2〜C6分岐アルキル;及びC2〜C6置換アルキルからなる群から選択された成分に改質した結果として、シクロオキシゲナーゼ阻害活性を実質的に欠くものである。幾つかの実施態様において、該シクロオキシゲナーゼ阻害剤は、インデン酢酸官能基を含み、かつ該成分は、水素原子、及びフッ素原子からなる群から選択されたものである。幾つかの実施態様において、該対象は、哺乳動物である、幾つかの実施態様において、該哺乳動物は、ヒトである。
また、本開示主題は、対象の腫瘍増殖の抑制方法を提供する。幾つかの実施態様において、該方法は、腫瘍を有する対象に、化合物の誘導体を投与することを含み、該化合物は、2’メチル基を有するインドール酢酸、又はインデン酢酸官能基を含むシクロオキシゲナーゼ阻害剤であり、かつ該誘導体は、該2’メチル基を、水素原子;ハロ;メチル基の少なくとも1つの水素原子がハロゲンで置換されたハロメチル;C2〜C6アルキル;C2〜C6分岐アルキル;及びC2〜C6置換アルキルからなる群から選択された成分に改質した結果として、シクロオキシゲナーゼ阻害活性を実質的に欠くものである。幾つかの実施態様において、該シクロオキシゲナーゼ阻害剤は、インデン酢酸官能基を含み、かつ該成分は、水素原子、及びフッ素原子からなる群から選択されたものである。幾つかの実施態様において、該対象は、哺乳動物である、幾つかの実施態様において、該哺乳動物は、ヒトである。
また、本開示主題は、細胞のアポトーシスの誘発方法を提供する。幾つかの実施態様において、該方法は、該細胞を、化合物の誘導体と接触させることを含み、該化合物は、2’メチル基を有するインドール酢酸、又はインデン酢酸官能基を含むシクロオキシゲナーゼ阻害剤であり、かつ該誘導体は、該2’メチル基を、水素原子;ハロ;メチル基の少なくとも1つの水素原子がハロゲンで置換されたハロメチル;C2〜C6アルキル;C2〜C6分岐アルキル;及びC2〜C6置換アルキルからなる群から選択された成分に改質した結果として、シクロオキシゲナーゼ阻害活性を実質的に欠くものである。幾つかの実施態様において、該シクロオキシゲナーゼ阻害剤は、インデン酢酸官能基を含み、かつ該成分は、水素原子、及びフッ素原子からなる群から選択されたものである。幾つかの実施態様において、該細胞は、培養液中の細胞である。幾つかの実施態様において、該細胞は、癌細胞である。幾つかの実施態様において、該細胞は、対象内に存在するものである。幾つかの実施態様において、該対象は、哺乳動物である、幾つかの実施態様において、該哺乳動物は、ヒトである。
また、本開示主題は、ペルオキシソーム増殖因子活性化受容体(PPAR)イソ型の活性を調節する方法を提供する。幾つかの実施態様において、該方法は、該PPARイソ型を、化合物の誘導体と接触させることを含み、該化合物は、2’メチル基を有するインドール酢酸、又はインデン酢酸官能基を含むシクロオキシゲナーゼ阻害剤であり、かつ該誘導体は、該2’メチル基を、水素原子;ハロ;メチル基の少なくとも1つの水素原子がハロゲンで置換されたハロメチル;C2〜C6アルキル;C2〜C6分岐アルキル;及びC2〜C6置換アルキルからなる群から選択された成分に改質した結果として、シクロオキシゲナーゼ阻害活性を実質的に欠くものである。幾つかの実施態様において、該シクロオキシゲナーゼ阻害剤は、インデン酢酸官能基を含み、かつ該成分は、水素原子、及びフッ素原子からなる群から選択されたものである。幾つかの実施態様において、該PPARイソ型は、PPARγである。幾つかの実施態様において、該PPARイソ型は、対象内に存在する。幾つかの実施態様において、該対象は、哺乳動物である、幾つかの実施態様において、該哺乳動物は、ヒトである。
また、本開示主題は、シクロオキシゲナーゼ阻害化合物の特異性を変更する方法を提供する。幾つかの実施態様において、該方法は、(a)2’メチル基を有するインドール酢酸、又はインデン酢酸官能基を含む、シクロオキシゲナーゼ阻害活性を有する化合物を提供すること;及び(b)該2’メチル基を、水素原子;ハロ;メチル基の少なくとも1つの水素原子がハロゲンで置換されたハロメチル;C2〜C6アルキル;C2〜C6分岐アルキル;及びC2〜C6置換アルキルからなる群から選択された成分で置換し、シクロオキシゲナーゼ阻害活性を実質的に欠く誘導体を作り出すことを含む。幾つかの実施態様において、該化合物は、非ステロイド性抗炎症薬である。幾つかの実施態様において、該非ステロイド性抗炎症薬は、インドメタシン、及びスリンダク、及びそれらの医薬として許容し得る塩、及びそれらの組合せからなる群から選択されたものである。幾つかの実施態様において、該誘導体は、2−デス−メチルインドメタシン、及びエインデニック酸スルフィド(eindenic acid sulfide)、エインデニック酸スルホキシド(eindenic acid sulfoxide)、及びエインデニック酸スルホン(eindenic acid sulfone)からなる群から選択されたものである。幾つかの実施態様において、該誘導体は、エインデニック酸スルフィドである。幾つかの実施態様において、該方法は、前記化合物上に存在するカルボン酸成分を、エステル、又はアミドに誘導体化することをさらに含む。
R2は、水素原子、ハロ、CF3;SCH3;SOCH3;SO2CH3;SO2NH2;CONH2;C1〜C6アルキル、分岐アルキル、又は置換アルキル;C1〜C6アルコキシ、分岐アルコキシ、又は置換アルコキシ;ベンジルオキシ;C1〜C6アルキルカルボン酸、分岐アルキルカルボン酸、又は置換アルキルカルボン酸;及びCH2N3からなる群から選択され;
R5は、水素原子、C1〜C6アルキル、分岐アルキル、又は置換アルキル及び=Oからなる群から選択され;
R7は、水素原子;C1〜C6アルキル、分岐アルキル、又は置換アルキルであり;
R8は、水素原子、ハロ、C1〜C6アルキル、分岐アルキル、及び置換アルキル;C1〜C6アルコキシ、分岐アルコキシ、及び置換アルコキシ;C1〜C6アルキルカルボン酸、分岐アルキルカルボン酸、又は置換アルキルカルボン酸;アミノ;ニトロ;CF3;ブロモアセトアミジル;ベンゾイル;又は2−フェニル−オキシラニルであり;
Xは、O、又はNR9であって、ここでR9は、水素原子、又はアルキルであり;かつm、n、及びtは、それぞれ独立に0、1、2、3、4、又は5である。);
Aは、炭素原子、及び窒素原子からなる群から選択され;
p、及びqは、双方とも独立に0、1、2、3、又は4であり;
R5に結合した炭素原子と該インデン環との間の結合は、単結合、又は二重結合であり;かつ
R1が結合した6員環は、シクロへキシル、又はフェニルである。
本開示主題の目的は上記で規定され、他の目的は、説明が進むにつれて、及び下記で最適なものが記載されるにつれて、明らかになるであろう。
本主題は、添付の実施例を参照して、本開示主題の代表的な実施態様を示す下文でさらに完全に記載される。しかし、本開示主題は、異なる形態を具体化することができるものであり、かつ本明細書中で説明する実施態様に制限されるものとして解釈されるべきではない。むしろ、これらの実施態様は、本開示が、十分かつ完全になり、かつ本開示主題の範囲を当業者に完全に伝えるように提供される。
本明細書中で言及される全ての公報、特許出願、特許、及び他の引例は、これらの全体において本明細書中に取り込まれている。
本明細書、及び特許請求の範囲を通して、所定の化学式、又は名称は、全ての光学異性体、及び立体異性体、並びに前記異性体、及びラセミ混合物を、そのような異性体、及び混合物が存在する場合、含むであろう。
非ステロイド性抗炎症薬(NSAID)は、とりわけ、炎症抑制、疼痛抑制、熱低下、腫瘍増殖阻害、アルツハイマー病抑制、及び神経変性疾患における認知機能の改善を含む一連の生物活性を発揮する。これらの効果の幾つかは、シクロオキシゲナーゼ酵素(COX−1、及びCOX−2)の阻害により媒介され、他のものは、他の分子標的の調節により媒介される。後者には、ペルオキシソーム増殖因子活性化受容体(PPAR)の活性化、γ−セクレターゼの調節、c−GMPホスホジエステラーゼサブタイプの阻害、及びRho活性化の阻害があるが、これらに限定されない。シクロオキシゲナーゼ関連、及び非シクロオキシゲナーゼ関連応答、双方に活性を示す化合物は、インドメタシン、及びスリンダクスルフィドの2つがある。インドメタシンは、ヒトに投与した後に直接的に活性化し、一方、スリンダクスルフィドは、不活性プロドラッグであるスリンダクとして投与される。スリンダクは、胃腸路で還元され、活性薬剤スリンダクスルフィドに変換される。
下記用語は、当業者に十分に理解されると考えられるが、下記定義は、本開示主題の説明を容易にするために説明されるものである。
他に規定しない限り、本明細書中に使用される全ての技術及び科学用語は、本開示主題が属する当業者に一般に理解される意味と同じ意味を有する。本明細書中に記載したものと類似又は同等の全ての方法、装置、及び物質を、本開示主題の実施、又は試験に使用することができるが、今回、代表的な方法、装置、及び物質を記載した。
長年にわたる特許法の慣習に従って、“a”、“an”、及び“the”の用語は、特許請求の範囲を含む本出願において使用される場合、“1以上”を意味する。従って、例えば、“ベクター(a vector)”の言及は、複数の前記ベクターなどを含む。
さらに、アミノ酸残基配列の開始又は末端でのダッシュ記号は、1以上のアミノ酸残基のさらなる配列へのペプチド結合、或いは、NH2又はアセチルなどのアミノ末端基、又はCOOHなどのカルボキシ末端基への共有結合を示す。
本明細書中に使用されるように、用語“酵素活性”は、基質の産物への変換を触媒する酵素の能力を意味する。該酵素の基質は、該酵素の天然基質を含むことができるが、該天然基質の類似体も含むことができる。これらは、該酵素により産物、又は産物の類似体に変換され得る。該酵素の活性は、例えば、特定の反応時間後の産物量を決定することにより、又は特定時間後の反応混合物中に残った基質量を決定することにより測定される。また、該酵素活性は、特定時間後の反応混合物中に残った、該反応の未使用コファクター量を決定することにより、又は特定時間後の反応混合物中の、使用されたコファクター量を決定することにより測定され得る。また、該酵素の活性は、特定時間後の該反応混合物中に残った自由エネルギー、又は高エネルギー分子(例えば、ATP、ホスホエノールピルビン酸、アセチルリン酸、又はホスホクレアチン)の供与体量を決定することにより、又は特定時間後の該反応混合物中の自由エネルギー、又は高エネルギー分子(例えば、ADP、ピルビン酸、酢酸、又はクレアチン)の使用される供与体量を決定することにより測定され得る。
本明細書中に使用されるように、用語“相互作用する”は、分子間の“結合”相互作用、及び“会合”を含む。例えば、相互作用は、本質的に、タンパク質−タンパク質、タンパク質−小分子、タンパク質−核酸、及び核酸−核酸であり得る。
該相互作用が異なる度合いが正反対であるという要求がないことが理解されるに違いない。言い換えれば、該用語の選択的調節因子は、所定のポリペプチドにのみ結合する分子だけでなく、関連ファミリー群を含む。また、該用語は、対象の及び異なる度合いが小さい関連ファミリー群由来のポリペプチドとの相互作用により特徴付けられる調節因子を含むことが意図される。例えば、選択的調節因子は、その条件が、異なるファミリー群由来のポリペプチドと対比して、該調節因子の対象ポリペプチドへの結合における生物学的に関連した相違を与えること(該調節因子に存在する天然置換基など)を見い出すことを可能にする調節因子を含む。
本明細書中に使用されるように、用語“変異”は、その従来の意味を有し、かつ核酸、又はポリペプチド配列中に、変化、遺伝、自然発生、又は導入されたものを意味し、かつ当業者に一般的に公知の意味として使用される。
本明細書中に使用されるように、用語“有意な増加”は、測定技術に固有の誤差範囲よりも大きい活性(例えば、酵素活性)増加、基準活性(例えば、該阻害剤存在下の野生型酵素の活性)の約2倍以上、幾つかの実施態様において5倍以上、また幾つかの実施態様において10倍以上の増加を意味する。
本明細書中に使用されるように、用語“治療有効量”、“治療的有効量”、及び“治療量”は、同義的に使用され、測定可能な応答(例えば、標的化された対象の生物学的、又は臨床的に関連した応答)を生じるのに十分な治療組成物量を意味する。本開示主題の医薬組成物中の活性成分の実際の投与量レベルは、特定の対象に対する所望の治療反応の達成に有効な該活性化合物量を投与するために変更することができる。該選択された投与量レベルは、該治療組成物の活性、投与経路、他の薬剤又は治療との組合せ、治療される状態の重症度、並びに、治療される対象の状態及び前の病歴に依存するであろう。しかし、該化合物の投与は、所望の治療効果を達成するのに要求されるレベルよりも低いレベルで開始され、所望の効果が達成されるまで該投与量が徐々に増加されることは、技術的範囲内である。
本開示主題の本明細書中の開示の検討後に、当業者は、特定の製剤、該組成物に使用される投与方法、及び他の因子を考慮して、個々の対象に対して投与量を調整することができる。さらに、投与量の計算は、対象の身長及び体重、症状の重症度及び段階、並びに、付加的な有害な物理的状態の存在を考慮し得る。このような調整、又は変更、並びに、前記調整又は変更をする場合、及びその仕方は、医学の技術者に周知である。
(III.A 一般的考察)
シクロオキシゲナーゼ(COX)は、非ステロイド性抗炎症薬の治療標的である。インドメタシン(INDO)は、機能的に不可逆な、時間依存性阻害剤として特徴付けられた最初の非ステロイド性抗炎症薬の1つであった。しかし、この影響の根底にある分子的機序は、不確定である。COX−2に結合したINDOの結晶構造において、小さい疎水性ポケットが、INDOの2’メチル基を囲うことが確認された。該ポケットは、残基Ala-527、Val-349、Ser-530、及びLeu-531により形成される。このポケットの阻害への寄与が、Val-349の変異誘発によるその容積の変更により評価された。V349A変異は、該ポケットを拡大し、かつINDOの効力を増加した。一方、V349L変異は、該ポケットのサイズを減少し、かつINDOの効力を低下した。該V349L変異のINDO阻害の可逆性が、特に著しかった。
インビボにおけるPPAR、及び/又はセクレターゼを調節するNSAIDの使用は、該NSAIDの高投与量投与により誘発される有意な胃腸毒性の存在を併せ持つ。この効果は、該胃腸(GI)路の細胞保護的プロスタグランジンの産生、及び放出の低下の結果生じる、COX−1の阻害のためであるように見える。GI毒性低下への1つのアプローチは、COX−1、及び/又はCOX−2に結合し、さらに他の標的ポリペプチドを調節する能力を維持する、NSAIDの能力を低下することである。
R2は、水素原子、ハロ、CF3;SCH3;SOCH3;SO2CH3;SO2NH2;CONH2;C1〜C6アルキル、分岐アルキル、又は置換アルキル;C1〜C6アルコキシ、分岐アルコキシ、又は置換アルコキシ;ベンジルオキシ;C1〜C6アルキルカルボン酸、分岐アルキルカルボン酸、又は置換アルキルカルボン酸;及びCH2N3からなる群から選択され;
R5は、水素原子、C1〜C6アルキル、分岐アルキル、又は置換アルキル及び=Oからなる群から選択され;
R7は、水素原子;C1〜C6アルキル、分岐アルキル、又は置換アルキルであり;
R8は、水素原子、ハロ、C1〜C6アルキル、分岐アルキル、及び置換アルキル;C1〜C6アルコキシ、分岐アルコキシ、及び置換アルコキシ;C1〜C6アルキルカルボン酸、分岐アルキルカルボン酸、又は置換アルキルカルボン酸;アミノ;ニトロ;CF3;ブロモアセトアミジル;ベンゾイル;又は2−フェニル−オキシラニルであり;
Xは、O、又はNR9であって、ここでR9は、水素原子、又はアルキルであり;かつm、n、s、及びtは、それぞれ独立に0、1、2、3、4、又は5である。);
Aは、炭素原子、及び窒素原子からなる群から選択され;
p、及びqは、双方とも独立に0、1、2、3、又は4であり;
R5に結合した炭素原子と該インデン環との間の結合は、単結合、又は二重結合であり;かつ
R1が結合した6員環は、シクロへキシル、又はフェニルである。)。
本明細書中に使用されるように、用語“アルキル”は、C1−10含有(すなわち、炭素原子1、2、3、4、5、6、7、8、9、又は10個を含む炭素鎖、また幾つかの実施態様において、C1−10含有)直鎖、分岐、又は環状、飽和、又は不飽和(すなわち、アルケニル、及びアルキニル)炭化水素鎖を意味し、例えば、メチル、エチル、プロピル、イソプロピル、ブチル、イソブチル、tert−ブチル、ペンチル、ヘキシル、エテニル、プロペニル、ブテニル、ペンテニル、ヘキセニル、ブタジエニル、プロピニル、ブチニル、ペンチニル、ヘキシニル、及びアレニル基を含む。
本明細書中に使用される用語“アルコキシ”は、--OZ1ラジカルを意味し。Z1は、本明細書中に記載されるように、アルキル、置換アルキル、シクロアルキル、置換シクロアルキル、ヘテロシクロアルキル、置換へテロシクロアルキル、シリル基、及びこれらの組合せからなる群から選択される。適切なアルコキシラジカルは、例えば、メトキシ、エトキシ、ベンジルオキシ、t-ブトキシなどを含む。関連用語として“アリールオキシ”があり、Z1が、アリール、置換アリール、ヘテロアリール、置換ヘテロアリール、及びこれらの組合せからなる群から選択されるものである。適切なアリールオキシラジカルの例を挙げると、フェノキシ、置換フェノキシ、2-ピリジンオキシ、及び8-キナリンオキシなどがある。
本明細書に用いられているように、用語“アシル”は、カルボキシル基の−OHが他の置換基で置換された有機酸基(すなわち、Rが、本明細書に定められるアルキル、又はアリール基であるRCO−で表される)を意味する。そのように、用語“アシル”は、具体的には、アセチルフラン、及びフェナシル基のようなアリールアシル基を含む。アシル基の具体例としては、アセチル、及びベンゾイルが挙げられる。
“環状”、及び“シクロアルキル”は、約3〜約10個、例えば3、4、5、6、7、8、9、又は10個の炭素原子を有する非芳香族の単又は多環式環系を意味する。該シクロアルキル基は、任意に部分的不飽和であり得る。また、該シクロアルキル基は、本明細書に定められているアルキル置換基、オキソ、及び/又はアルキレンで任意に置換され得る。該環状アルキル鎖に沿って、1以上の酸素、硫黄、あるいは置換、又は無置換の窒素原子を任意に挿入することが可能であり、その窒素置換基は、水素原子、低級アルキル、又はアリールであり、従って、複素環基が与えられる。代表的な単環シクロアルキル環としては、シクロプロピル、シクロブチル、シクロペンチル、シクロヘキシル、及びシクロヘプチルが挙げられる。多環式シクロアルキル環としては、アダマンチル、オクタヒドロナフチル、デカリン、カンファー、カンファン、及びノルアダマンチルが挙げられる。
“ジアルキルアミノ”は、−NRR’基(式中、R、及びR’の各々は、独立に、先述したアルキル基である)を意味する。例示的なアルキルアミノ基としては、エチルメチルアミノ、ジメチルアミノ、及びジエチルアミノが挙げられる。
“アルコキシカルボニル”は、アルキル−O−CO−基を意味する。例示的なアルコキシカルボニル基としては、メトキシカルボニル、エトキシカルボニル、ブチルオキシカルボニル、及びt−ブチルオキシカルボニルが挙げられる。
“アラルコキシカルボニル”とは、アラルキル−O−CO−基を意味する。例示的なアラルコキシカルボニル基としては、ベンジルオキシカルボニルがある。
“カルバモイル”とは、H2N−CO−基を意味する。
“アルキルカルバモイル”は、R’RN−CO−基(式中、R、及びR’の一方が水素原子であり、R、及びR’の他方が、先述したアルキルである)を意味する。
“アシルオキシル”とは、アシル−O−基(式中、アシルは先述した通りである)を意味する。
“アシルアミノ”とは、アシル−NH−基(式中、アシルは先述の通りである)を意味する。
“アロイルアミノ”は、アロイル−NH−基(アロイルは先述した通りである)を意味する。
用語“アミノ”は、−NH2基を意味する。
用語“カルボキシル”は、−COOH−基を意味する。
本明細書中に使用されるように、用語“ハロ”、“ハライド”、又は“ハロゲン”は、フルオロ、クロロ、ブロモ、及びヨード基を意味する。
用語“ハロメチル”は、少なくとも1つの水素原子をハロゲンで置換したメチル基を意味する。
用語“ヒドロキシル”は、―OH基を意味する。
用語“ヒドロキシアルキル”は、―OH基で置換されたアルキル基を意味する。
用語“ニトロ”は、−NO2基を意味する。
用語“オキソ”は、炭素原子が酸素原子で置き換えられた、本明細書で既に述べた化合物を意味する。
用語“チオ”は、炭素、又は酸素原子が硫黄原子で置き換えられた、本明細書で既に述べた化合物を意味する。
用語“スルフェート”は、−SO4基を意味する。
式Iに示すように、“A”は、炭素原子、又は窒素原子を示す。
糖尿病は、対象のグルコース恒常性が不安定になり、かつ全身高血糖状態になる状態である。糖尿病状態には、I型とII型の2つの形態がある。通常、I型糖尿病は、約20歳の個人に発症し、インシュリン依存性となり、ケトアシドーシスを伴い、かつ糖尿病患者の約10%を示す。II型糖尿病は、アメリカの成人の約5パーセントが発症し、糖尿病患者の約90%を示す。通常、II型糖尿病は、肥満症に関連し、一般に、約40歳の個人に発症し、かつ非インシュリン依存性である。II型糖尿病の一部は、若い個人に発症し得る。これは、若年者の成人発症型糖尿病(MODY)と呼ばれる。
幾つかの実施態様において、本開示主題は、PPAR(例えば、PPARγ)の活性を調節する方法を提供する。この実施態様において、本開示主題の誘導体の治療有効量を、PPARを有する対象に投与し、それによって、該PPARを調節する。
ペルオキシソーム増殖因子活性化受容体(PPAR)は、アテローム性動脈硬化症、炎症、肥満症、糖尿病、免疫応答、及び老化に関わる様々な病的状態に関連している。受容体PPARγのこのファミリーのある特定の一員の活性は、特定種の癌細胞において、15−デオキシ-Δ12,14-プロスタグランジンJ2(15d−PGJ2)などのシクロペンテノンプロスタグランジン(PG)により、抗増殖、アポトーシス、分化、及び抗炎症応答を引き起こす。
幾つかの実施態様において、本開示主題は、PPAR(例えば、PPARγ)の活性を調節する方法を提供する。この実施態様において、本開示主題の誘導体の治療的有効量を、PPARを有する対象に投与し、それによって、該PPARの活性を調節する。
上記で詳細に論じたように、セクレターゼは、アルツハイマー病の病因と言われているAβ42の発生を含む、Aβペプチドの処理に関与する。幾つかの実施態様において、本開示主題は、セクレターゼ(例えば、γ−セクレターゼ)の活性を調節する方法を提供する。この実施態様において、本開示主題の誘導体の治療有効量を、セクレターゼを有する対象に投与し、それによって、該セクレターゼの活性を調節する。
(IV.A 対象)
また、本開示主題は、癌、神経変性疾患、及び糖尿病からなる群から選択される、対象の疾患の治療方法を提供し、該方法は、該対象に、化合物の誘導体の治療有効量を投与することを含み、該化合物は、2’メチル基を有するインドール酢酸、又はインデン酢酸官能基を含むシクロオキシゲナーゼ阻害剤であり、かつ該誘導体は、該2’メチル基を、水素原子、ハロ、及びC2〜C6アルキル又は分岐アルキルからなる群から選択された成分に改質した結果として、シクロオキシゲナーゼ阻害活性を実質的に欠くものである。
さらに詳細には、ヒトなどの哺乳動物、並びに絶滅の危機のある重要な哺乳動物(シベリア虎など)、ヒトにとって経済的に重要な動物(ヒトによって消費される農園で飼育される動物)、及び/又は社会的に重要な動物(ペットとして、又は動物園で保護される動物)、例えば、ヒト以外の食肉動物(猫、及び犬など)、豚(豚、雄豚、野豚)、反芻動物(畜牛、雄牛、羊、キリン、鹿、山羊、バイソン、ラクダなど)、及び馬などの治療が本明細書中に提供される。また、本明細書中には、動物園に保護された絶滅の危機のある鳥、ならびに、家禽、さらに詳細には家畜化した家禽、すなわち、七面鳥、鶏、カモ、ガチョウ、ホロホロ鳥(guinea fowl)等の家禽の種類の鳥の治療を含む、鳥の治療が提供され、それらはまた、全てヒトにとって経済的に重要である。従って、本明細書中に記載される方法の実施態様は、家畜化した豚(豚、及び雄豚)、反芻動物、馬、家禽等を含むがこれらに限定されない家畜の治療を含む。
本開示主題の組成物は、幾つかの実施態様において、キャリア、特にその医薬として許容し得るキャリアを含む組成物である。全ての適切な医薬製剤を使用して、対象への投与用の組成物を調製することができる。
例えば、適切な製剤は、酸化防止剤、緩衝液、静菌剤、殺菌性抗生物質、及び所定の受け手の体液で該製剤を等張性にする溶質を含み得る、水性、及び非水性滅菌注射液;及び懸濁化剤、及び増粘剤を含み得る、水性、及び非水性滅菌注射液を含み得る。該製剤は、例えば、密閉アンプル及びバイアルなどの単位投与量、又は複数投与量の容器中に存在することができ、かつ使用直前に、例えば注射用水などの滅菌液体キャリアの添加のみを要求する、凍結、又はフリーズドライ(凍結乾燥)条件下で保存することができる。幾つかの例示的成分は、SDSであり、一例においては、0.1〜10mg/mlの範囲、他の例においては、約2.0mg/mlであり;かつ/又はマンニトール又は他の糖であり、例えば、10〜100mg/mlの範囲、他の例においては、約30mg/mlであり;かつ/又はリン酸緩衝食塩水(PBS)である。
本開示主題の治療法、及び組成物は、制限されないが、サイトカイン、及び他の免疫調節化合物を含む、他の追加のアジュバント、又は生物反応修飾物質とともに使用することができる。
本開示主題の組成物の投与を、当業者に公知の全ての方法によって行うことができる。これらは、静脈内投与、滑液嚢内投与、経皮的投与、筋肉内投与、皮下投与、局所投与、直腸投与、膣内投与、腫瘍内投与、経口投与、口腔投与、経鼻投与、非経口投与、吸入、及び吹送投与を含むが、これらに限定されない。幾つかの実施態様において、本開示主題の組成物の適切な投与方法は、制限されないが、静脈注射である。本開示主題の組成物の特定の投与様式は、処置される細胞の分布、及び数、使用される化合物、該化合物の付加的な組織、又は細胞標的特徴、及び代謝機序、又は投与部位からの該化合物の除去を含む、様々な因子に依存する。
本開示主題の組成物の有効投与量が、それを必要とする対象に投与される。“治療有効量”、又は“治療量”は、測定可能な応答(例えば、標的化された対象の生物学的、又は臨床的に関連した応答)を生じるのに十分な治療組成物量である。幾つかの実施態様において、アミロイド凝集体形成の阻害活性が測定される。本開示主題の組成物中の活性成分の実際の投与量レベルは、特定の対象に対する所望の治療反応の達成に有効な該活性化合物量を投与するために変更することができる。該選択された投与量レベルは、該治療組成物の活性、投与経路、他の薬剤又は治療との組合せ、治療される状態の重症度、並びに、治療される対象の状態及び前の病歴に依存するであろう。しかし、該化合物の投与は、所望の治療効果を達成するのに要求されるレベルよりも低いレベルで開始され、所望の効果が達成されるまで該投与量が徐々に増加されることは、技術的範囲内である。治療組成物の効力を変更することができ、従って、“治療的有効量”を変更することができる。しかし、当業者は、本開示主題の候補化合物の効力、及び効果を評価し、かつ適宜に治療法を調整することができる。
(mCOX−2の変異誘発、及び精製)
マウスCOX−2(mCOX−2)核酸、及びペプチドの特定部位の変異誘発、発現、及び精製を、Rowlinsonらの文献, 1999に記載されているように行った。簡潔に言うと、QUIKCHANGE(登録商標)特定部位変異誘発キットを用いて、BLUESCRIPT(登録商標)ベクターに存在する配列をコードしているmCOX−2に対して、PCR−介在の特定部位の変異誘発を行った。野生型mCOX−2の位置335にバリンをコードしているGTGコドン(本明細書中にでは、上述した従来の番号付与に基づきVal-349と呼ぶ。)を、アラニン、ロイシン、又はイソロイシンをコードするように変化させ、mCOX−2ポリペプチドをコードしている3つの変異核酸を作成した。これらは、本明細書中でそれぞれ、mCOX−2V349A又はV349A、mCOX−2V349L又はV339L、及びmCOX−2V349I又はV349Iと呼ぶ。
次に、野生型、及び変異タンパク質を、Sf9細胞(EMD Biosciences社 - Novagen, マディソン, ウィスコンシン州, アメリカ合衆国)内にBACULOGOLD(商標)ベクター(BD Biosciences PharMingen)を有するmCOX−2z/pVL1393ベクターの相同的組換えにより発現した。ウイルス増幅後に、Sf9細胞4リットル(95〜100%生存)を、10%ウシ胎児血清(FBS; HyClone, ローガン, ユタ州, アメリカ合衆国)、1% L-グルタミン、及び0.1% (v/v) プルロニックF68を加えたTNM-FH培地で増殖し、次に、新しいウイルスストックで感染させた。生存率が65〜70%になった時に、該4リットル総量を、Sorvall RC-3B遠心分離機内で、2500rpmで遠心分離することにより収集し、かつ該ペレットを、氷温リン酸緩衝食塩水で洗浄し、かう再び遠心分離した。該最終細胞ペレットを、−80℃で保存した。
(試薬、及び溶媒)
未ラベル化アラキドン酸(AA)を、Nu Chek Prep (Elysian, ミネソタ州, アメリカ合衆国)から購入し、かつ[1-14C]-AAを、PerkinElmer Life Sciences社(ボストン, マサチューセッツ州, アメリカ合衆国)から購入した。雄ヒツジ精嚢を、Oxford Biomedical Research (オックスフォード, ミシガン州, アメリカ合衆国)から購入した。オリゴヌクレオチドを、Qiagen社(Valencia, カリフォルニア州, アメリカ合衆国)から購入し、かつ全ての分子生物学酵素を、New England Biolabs (べバリー, マサチューセッツ州, アメリカ合衆国)から得た。バキュロウイルス試薬を、BD Biosciences Pharmingen (サンディエゴ, カリフォルニア州, アメリカ合衆国)から購入した。特に明記しない限り、他の全ての化学物質を、Sigma/Aldrich (セントルイス, ミズーリ州, アメリカ合衆国)から得た。カラムクロマトグラフィーに使用するHPLC等級溶媒を、Fischer Scientific (ピッツバーグ, ペンシルベニア州, アメリカ合衆国)から得た。N,N-ジメチルホルムアミドを、水素化カルシウムから蒸留した。他の全ての化学物質を、さらに精製することなく使用した。薄層クロマトグラフィーを、Analtech (ニューワーク, デラウェア州, アメリカ合衆国; プレコートSilica Gel 60 F254)から得たシリカゲルで行った。該プレートを、UV蛍光(254nm)で読み取るか、又はリンモリブデン酸(PMA)で染色後に加熱して読み取った。カラムクロマトグラフィーを、シリカゲル200-300メッシュ(Fisher Scientific)を用いて行った。
(機器分析)
マススペクトルを、Finnigan TSQ 7000 トリプル四重極分光計(Thermo Electron社, ウォルサム, マサチューセッツ州, アメリカ合衆国)のエレクトロスプレーイオン化(ESI−MS)により得た。1H−NMRは、溶媒としてCDCl3、又はDMSO−d6、内部標準としてテトラメチルシランを用いて、Bruker AC 300 NMR分光計(Bruker BioSpin Corporation, ビルリカ, マサチューセッツ州, アメリカ合衆国)で得た。全ての化学シフトは、TMSからの100万分の1(ppm)低磁場で記録し、かつカップリング定数は、ヘルツで記録した。
(2-デス-メチルインドメタシンの合成)
2-デス-メチルインドメタシンを、図6に概説した段階に従って合成した。これらの段階を、下記にさらに詳細に示す。
(N-エチリデン-N'-(4-メトキシ-フェニル)-ヒドラゾン(図6中の化合物A))
4-メトキシフェニルヒドラジン(10.34 g, 0.075 mol)を、フレーム乾燥丸底フラスコ中のトルエン(76 mL)に溶解した。該フラスコを、アルゴンでパージし、かつ0℃に冷却した。アセトアルデヒド(8.4 mL, 0.15 mol)のトルエン(17 mL)溶液を滴下して加え、室温で30分間撹拌した。該溶液を、ろ紙を通して丸底フラスコに注ぎ、減圧下で濃縮することにより、粗ヒドラゾン(図6中の化合物A)を11.2 g得た。
アルゴン下、該粗ヒドラゾン(図6中の化合物A;0.424 g, 2.58 mmol)のピリジン(2.2 mL)溶液に、0℃で、4-クロロベンゾイルクロライド(0.904 g, 5.17 mmol)を一度に加えた。該反応混合液を、室温で3時間撹拌した。水(25 mL)を加え、該溶液を、CH2Cl2(3 x 20 mL)で抽出した。合わせた有機相を乾燥し(MgSO4)、濾過し、かつ減圧下で濃縮した。フラッシュクロマトグラフィー(ヘキサン/酢酸エチル 3:1)で精製し、表題化合物(図6中の化合物B)を橙色固体(0.266 g)として得た。1H NMR (CDCl3) δ 7.70 (d, J = 7.2 Hz, 2H), 7.36 (d, J = 8.2 Hz, 2H), 7.11 (d, J = 8.7 Hz, 2H), 7.01 (d, J = 8.5 Hz, 2H), 6.82 (d, J = 5.0 Hz, 1H), 3.84 (s, 3H), 1.89 (d, J = 5.0 Hz, 3H); ESI-CID 325, 327 (M-Na+[35/37Cl]).
凝縮器を備えた2口フラスコ内で、該ヒドラジド(図6中の化合物A;0.166 g, 0.55 mmol)を、トルエン(6.6 mL)、及びメタノール(0.33 mL)に溶解した。該混合液を0℃に冷却し、HClガスを1.5時間バブリングした。該過剰ガス、及び溶媒を、減圧下で除去した。トルエンで該固体をスワールし、濾過して、白色固体を得た。該固体を、酢酸エチルで洗浄し、該塩酸塩(図6中の化合物C)を、さらに精製することなく得た(0.131 g, 76%)。1H NMR (DMSO-d6) δ 7.41 (m, 4H), 7.33 (d, J = 8.4 Hz, 2H), 6.92 (d, J = 8.9 Hz), 3.74 (s, 3H).
該塩酸塩(図6中の化合物C;0.111 g, 0.35 mmol)、及びコハク酸セミアルデヒド (0.047 g, 0.46 mmol)を、酢酸(AcOH;2 mL)に溶解し、かつ4時間加熱還流した。該反応を一晩室温に冷却させた。水(5 mL)、及びCH2Cl2(5 mL)を加え、該有機相を除去した。該水相を、CH2Cl2のさらなる部分で抽出し、かつ該合わせた有機相を水で洗浄し、かつNaHCO3(2 x 20 mL)の飽和溶液で抽出した。該合わせた水相を、15% HClで酸性化し、得られた混合液を、CH2Cl2(3 x 20 mL)で抽出した。該合わせた有機相を乾燥し(MgSO4)、濾過し、かつ減圧下で濃縮した。粗生成物を再結晶化(イソプロパノール)し、表題化合物(すなわち、[1-(4-クロロ-ベンゾイル)-5-メトキシ-1H-インドール-3-イル]-酢酸;図6中の化合物D)を、灰色固体として得た(0.058 g, 48%)。1H NMR (DMSO-d6) δ 8.24 (d, J = 8.9 Hz, 1H), 7.82 (d, J = 8.5 Hz, 2H), 7.73 (d, J = 8.4 Hz, 2H), 7.39 (s, 1H), 7.19 (d, J = 2.3 Hz, 1H), 7.06 (dd, J = 2.4, 8.9 Hz, 1H), 3.87 (s, 3H), 3.73 (s, 2H); ESI-CID 342, 344 (M-H-[35/37Cl]). Anal. 計算値C18H14ClNO4: C, 62.89; H, 4.10; N, 4.07; Cl 10.31. 観測値: C, 62.80; H, 4.11; N, 4.06; Cl, 10.12.
(エインデニック酸スルフィドの合成)
エインデニック酸スルフィドを、図7に概説した段階に従って合成した。これらの段階を、下記にさらに詳細に示す。
(6-フルオロ-インダン-1-オン(図7中の化合物F))
3-(4-フルオロ-フェニル)-プロピオン酸(5 g, 29.7 mmol;図7中の化合物E)を、50℃で、ポリリン酸(PPA; 65.4 g, 0.654 mol)に加えた。該粘性混合液を、2時間90℃で加熱した。該シロップを、氷水に注ぎ、かつ30分間撹拌した。該水相をエーテルで抽出し(3 x 50 mL)、かつ該合わせた有機物を、H2O(2 x 50 mL)、及びNaHCO3で中和されるまで洗浄した。得られた有機相を、H2O(50 mL)で洗浄し、乾燥し(MgSO4)、濾過し、かつ減圧下で濃縮した。フラッシュクロマトグラフィー(7:1 ヘキサン/酢酸エチル(EtOAc))を用いて精製し、該インダノン(図7中の化合物F)を、黄色固体として得た(2.06 g, 46%)。1H NMR (CDCl3) δ 7.45 (ddd, J = 0.5, 4.5, 8.4 Hz, 1H), 7.39 (ddd, J = 0.3, 2.6, 7.8 Hz, 1H), 7.30 (td, J = 2.6, 8.6 Hz, 1H), 3.12 (t, J = 5.7 Hz, 2H), 2.75 (m, 2H); ESI-CID 151 (M-H+).
該インダノン(図7中の化合物F;2.06 g, 13.7 mmol)、及びブロモ酢酸エチル(EBA; 3.44 g, 20.6 mmol)のベンゼン(10 mL)溶液を、ベンゼン(21 mL)、及びエーテル(10 mL)中の活性亜鉛(3.77 g, 57.7 mmol)に、5分間かけて加えた。少量のヨウ素の結晶を加え、該反応を開始し、かつ該皇后液を、還流した。3時間間隔で、二回、亜鉛(1.8 g, 27.5 mmol)、及びブロモ酢酸エチル(EBA; 1.8 g, 10.8 mmol)を加え、かつ該混合液を一晩還流した。該溶液を室温に冷却し、かつエタノール(5 mL)、及び酢酸(23 mL)を加えた。該溶液を、1:1 水 酢酸 (100 mL)に注ぎ、かつ該有機相を分離した。該水相を、ジエチルエーテル (Et2O; 2 x 25 mL)で抽出し、かつ該合わせた有機物を、NaHCO3、水で洗浄し、乾燥し(MgSO4)、濾過し、かつ減圧下で濃縮して、粗生成物(図7中の化合物G;3.55 g)を得た。
トルエン(66 mL)中の該粗(6-フルオロ-1-ヒドロキシ-インダン-1-イル)-酢酸エチルエステル(図7中の化合物G;3.55 g)、p-トルエンスルホン酸・H2O(PTSA;5.67 g, 29.8 mmol)、及びCaCl2(4.13 g, 37.2 mmol)を、一晩還流した。該溶液を濾過し、かつ該固体残渣をベンゼンで洗浄した。該合わせた有機物を、水、NaHCO3、水で洗浄し、乾燥し(MgSO4)、濾過し、かつ減圧下で濃縮した。フラッシュクロマトグラフィ(13:1 ヘキサン/EtOAc)を用いた精製により、表題化合物(図7中の化合物H)を、橙色固体として得た(0.703 g)。1H NMR (CDCl3) δ 7.25 (m, 2H), 7.06 (m, 1H), 6.25 (d, J = 2.3 Hz, 1H), 4.24 (q, J = 7.0 Hz, 2H), 3.32 (s, 2H), 3.03 (s, 2H), 1.33 (t, J = 7.1 Hz, 3H); ESI-CID 221 (M-H+).
該(6-フルオロ-3H-インデン-1-イル)-酢酸エチルエステル(図7中の化合物H;0.668 g, 3.0 mmol)、及びp-メチルチオベンズアルデヒド(PMTBA;0.508 g, 3.3 mmol)のMeOH(18 mL)溶液に、1N NaOH(9 mL)を加えた。該混合液を、2時間還流して撹拌した。該溶液を冷却し、水で希釈し、かつエーテル(3x)で抽出した。残渣エーテルを、窒素で水相から飛ばし、かつ該水相溶液を、50%酢酸で酸性化した。沈殿生成物を濾過し、かつH2Oで洗浄した。メタノールからの再結晶により、表題化合物(すなわち、[6-フルオロ-3-(4-メチルスルファニル-ベンジリデン)-3H-インデン-1-イル]-酢酸、すなわち、エインデニック酸スルフィド;図7中の化合物I)を、橙色固体として得た(0.163 g, 17%)。1H NMR (DMSO-d6) δ 7.83 (dd, J = 5.2, 8.4 Hz, 1H), 7.64 (d, J = 8.4 Hz, 2H), 7.59 (s, 1H), 7.36 (d, J = 8.4 Hz, 2H), 7.16 (dd, J = 2.4, 9.6 Hz, 1H), 7.13 (s, 1H), 7.06 (td, J = 2.4, 9.6 Hz, 1H), 3.68 (s, 2H), 2.54 (s, 3H); ESI-CID 325 (M-H-).
(エインデニック酸スルフィドの誘導体の合成)
[6-フルオロ-3-(4-メチルスルファニル-ベンジリデン)-3H-インデン-1-イル]-酢酸(図7中の化合物I;0.02 g, 0.06 mmol))の乾燥CH2Cl2(1.5 mL)溶液に、N-(3-ジメチルアミノプロピル)-N'-エチルカルボジイミド(EDCI;0.014 g, 0.07 mmol)、ジメチルアミノピリジン(DMAP;0.75 mg, 0.006 mmol)、及びベンジルアミン(7.9 mg, 0.07 mmol)を加えた。該反応液を、室温で一晩撹拌した。該混合液を、水で希釈し、かつCH2Cl2(2x)で抽出した。該合わせた有機物を、H2Oで洗浄し、乾燥し(MgSO4)、濾過し、かつ減圧下で濃縮した。フラッシュクロマトグラフィー(5:2 ヘキサン/EtOAc)を用いた精製により、表題化合物(N-ベンジル-2-[6-フルオロ-3-(4-メチルスルファニル-ベンジリデン)-3H-インデン-1-イル]-アセトアミド;図7中の化合物J)を、橙色固体として得た(0.02 g, 79%)。
(シクロオキシゲナーゼ調製、及びアッセイ)
(COX阻害スクリーニングアッセイ)
PCRは、実施例1に概説した、位置349(ヒツジCOX−1 番号付与)のバリンをアラニン、イソロイシン、又はロイシンに変えた、部位特異的変異誘発マウスCOX−2をベースとした。これらの変異遺伝子を使用して、Sf9細胞内の大規模発現のためのバキュロウイルス構築体を作成した。発現COX−2タンパク質の精製は、従来の細胞分別、及び古典的なカラムクロマトグラフィーを介して行った。活性、又は阻害アッセイは、500μM フェノールを含む100 mM Tris−HCl緩衝液中でヘマチン−再構成タンパク質を用いて行った。シクロオキシゲナーゼ活性の定量化は、サーモスタットキュベット中、37℃で、5300酸素モニターとともにポーラログラフ電極を用いて(Yellow Springs Instrument Co. Inc., イエロースプリングス, オハイオ, アメリカ合衆国)、基質(アラキドン酸、又は酸素)消費量をモニタリングすることにより行った。全ての阻害剤、及び基質を、ジメチルスルホキシド(DMSO)中で可溶化した。活性、又は阻害アッセイは、500μM フェノールを含む100 mM Tris−HCl緩衝液中でヘマチン−再構成タンパク質を用いて行った。最大反応速度データを、酸素消費曲線の直線部分から得て、該データを、Prism 4.0 (GraphPad Software, サンディエゴ, カリフォルニア州, アメリカ合衆国)で非線形回帰により分析した。
競合的阻害アッセイは、基質、及び阻害剤を、タンパク質添加による反応の開始前に加えることを除き、同様の方法で行った。精製タンパク質のペルオキシダーゼ活性は、Markeyらの文献, 1987に記載されているように、グアヤコール法により測定した。COX活性、及びCOX−2変異体の相対的ペルオキシダーゼ活性に対するKm、及びVmaxを、表4に示した。
アッセイを終了させ、薄層クロマトグラフィーにより基質消費量を分析した。50% 酵素活性 (IC50)に対する全ての阻害剤濃度は、少なくとも2回の独立した測定の平均である。時間依存性COX阻害反応を、様々な阻害剤濃度で、時間長さを変えて(0〜30分)、37℃で前保温した。全ての反応は、[1-14C]-AAを用いて、37℃で30秒間行い、反応を終了させ、かつ上述のように分析した。
(時間依存性COX阻害アッセイ)
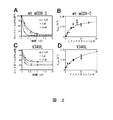
実施例1に記載したように、2’メチル基とメチル結合ポケットとの相互作用を調査するために、mCOX−2の位置349で、一連の変異を行い、該ポケットの容積を増加、又は減少させ (Val → Ala, Ile, Leu)、かつINDOによるこれらの酵素の阻害速度を測定した。最初に、時間依存性IC50アッセイを使用し、50μM AAの添加前に、該酵素を阻害剤とともに20分間前保温した。該COX反応を、終了前に30秒間進行させた。該IC50は、INDOの有効性が、該ポケット容積の増加時に増加し(V349A)、該ポケット容積の減少時に低下する(V349I, V349L;表5)。
野生型mCOX−2の速度パラメータ(表6)は、先に報告されたKI値(5 μM)、及びk2値(0.045 s-1;Gierseらの文献, 1999)とよい一致を示した。oCOX−1の値は、INDOが高い親和性(KI = 1.7μM)、及び不活性化の速い速度(k2 = 0.25 s-1;Kulmacz & Lands, 1985)を示すことを表す。これらの観察は、oCOX−1の方へのINDOの高い有効性により、さらに支持される(表5)。INDOのV349AのKIは、ほぼ4倍低下した。これは、結合の高い親和性示唆している。また、この変異は、k2をわずかに増加させた。これは、V349A酵素に対するINDOのIC50の3倍低下と一致する(表5)。表5で注目されるように、V349I変異は、INDOの速度パラメータへの影響はほとんどない。V349Lは、KIの3倍増加、及び測定可能なk−2を有し、阻害に対して最も大きな効果を示した。k2のわずかな上昇は、平衡への速い速度を示唆している。これは、k−2の出現に起因する(図2C)。
(DM−INDOによる時間依存性COX阻害)
実施例7、及び8に記載の実験は、該疎水性ポケット内へのINDOの2’メチル基の挿入が、阻害の時間依存に対して重要な一因であることを示唆している。これをさらに試験するために、DM−INDO(図1C)を、図6に示したスキームに従って合成した。該時間依存性IC50アッセイにおいて、DM−INDOは、野生型mCOX−2、及びV349Iをわずかに阻害した。しかし、V349A、V349L、及び野生型oCOX−1の20%未満の阻害を示した(表5)。野生型酵素、及びV349L変異体の阻害の時間、及び濃度依存は、両酵素に対して30%残存活性の平坦域を示した。これは、測定可能なk−2と一致する(図4)。重要なことには、V349Lは、野生型mCOX−2の阻害レベルと同様のレベルを得るために、ほぼ10倍高いDM−INDO濃度を要求したことである。DM−INDOによる野生型酵素阻害のデータ分析により、KI、k2、及びk-2値に対して、それぞれ26±7μM、0.80±0.03 s-1、及び0.05±0.02 s-1が得られた。従って、オン速度定数(k2)は、INDOよりもDM−INDOに対して約14倍速く、一方、オフ速度定数(k−2)は、該オン速度よりも14倍遅い。
DM−INDOによるV349L阻害の速度論は、式(2)を用いた分析のために修正されない。なぜならば、該グラフは、平坦域がないためである。線形回帰分析は、k−2のy切片値0.0025±0.0003 s-1を与えた(Copeland, 2000)。V349Lに対するDM−INDOのKIは、第二段階の平衡定数よりもさらに大きくなるに違いない。従って、式(1)の第一段階は、E−IのE−I*への時間依存性異性化を供給しない。
(Cox阻害の可逆性)
(INDOによるCOX阻害の可逆性)
式(1)中の第二段階の可逆性は、基質との長時間保温後に回復する酵素活性量により直接評価することができる。INDO阻害の可逆性を試験するために、野生型mCOX−2、及び3つのVal-349変異体を、時間依存性IC50アッセイに使用される同条件に曝した。50μM AAの添加前に、該酵素を、DMSO、又は10μM INDOとともに20分間前保温した。AAの添加後に、時間長さを変えて、酸素化反応を進行させた。INDO結合が可逆である場合、反応時間が増えるにつれて、阻害程度が低下した。AA酸素化が回復する時間経過は、一次指数関数に一致する(図3A)。予測されるように、INDO阻害の有意な可逆性は、V349L変異体に対して観察されたが、野生型、V349A、又はV349I酵素に対しては観察されなかった。該活性回復アッセイから計算されたk−2値(0.01 s-1)は、INDOに対する時間依存性阻害アッセイから計算されたk−2値(0.008 s-1;表6)と厳密に一致した。この関連性は、時間依存性機序における第二段階の可逆性が、50μM AA存在下のINDOによる阻害の原理決定因子であることを示唆している。
(DM−INDOによるCOX阻害の可逆性)
DM−INDO阻害の可逆性を、活性回復アッセイ(図3)を用いて、INDOと同様に評価した。該実験、及び分析を、上記のように行った。DM−INDOは、野生型mCOX−2、及びV349Iに対して阻害可逆性を示した。これらは、それぞれ、0.023±0.001 s-1、及び0.015±0.005 s-1のk-2値を有する(図3B)。10μM DM−INDOとの前保温によるV349A、及びV349Lのわずかな量の活性損失は、50μM AA添加により迅速に回復した(図3B)。
(COXの本質的な発光の定常状態消光)
INDO、及びDM−INDOを用いた蛍光消光実験は、Houtzagerらの文献, 1996に記載されているように、Spex Fluorolog-3分光蛍光光度計(Jobin Yvon Inc., エディソン, ニュージャージー州, アメリカ合衆国)を用いて行った。励起(280 nm)、及び発光(327 nm)のバンド幅を、それぞれ4 nm、及び6 nmにした。定常状態測定を、蛍光キュベット中で持続的に撹拌しながら37°Cで行った。全てのアポタンパク質を、200 nMに希釈し、かつホロ酵素等量の2%未満の活性を示した。240、又は360秒に渡って、2秒の積分時間でデータを集めた。消光の可逆性は、競合剤として50μM AAを用いて、同じ方法で分析した。該リガンドを、緩衝液中にさらに希釈する前にDMSO中に溶解した。該緩衝液中の有機成分は、0.4%以下であった。
(INDO、及びDM−INDOによる、COXの本質的な蛍光の消光)
Houtzagerらは、該アポタンパク質の蛍光消光により、COX−2に結合する阻害剤をモニターし、かつ該結合速度が、該阻害速度と密接に類似していることを示した(Houtzagerらの文献, 1996)。このアッセイは、INDO、及びDM−INDOのCOXへの結合を直接モニターする方法を提供する。様々な濃度のINDO、及びDM−INDOを、アポタンパク質に加え、かつ蛍光低下の割合を、時間に対してモニターした。該混合物が平衡に達した後、競合剤として50μMのAAを加え、結合の可逆性をモニターした。消光の動的データを、阻害に対する方法と同じ方法で分析した。明確にするために、蛍光消光の第一段階の平衡定数を、Kdと呼び、かつ消光の第二段階からのk2、及びk−2を、それぞれ、k'2、及びk'−2と表した。
(2-デス-メチル誘導体によるCOX酵素の阻害)
INDOの2-デス-メチル類似体(DM−INDO)を、実施例4に示したように合成し、かつ野生型COX−1、及びCOX−2、並びにVal-349変異体に対して、実施例7に記載したように試験した。DM−INDOは、試験した全ての酵素に結合したが、野生型mCOX−2、及びV349I酵素に対してのみ阻害効力を示した。該活性サイト内にDM−INDOを固着する該2’メチル基がなければ、該化合物は、アラキドン酸(AA)により、該酵素から離れて容易に競合される。阻害速度は、蛍光消光により評価された結合速度に相当する。これらの結果は、COXの時間依存性結合、及びCOX阻害において、INDOの2’メチル基と"メチル−結合ポケット"との間の接触の重要性に関係している。
RKO、及びHCT-116細胞(ヒト結腸直腸癌細胞株)を、5〜8×104細胞、及び化学物質の最終濃度(1-500μM)を含む、100μl培地の最終体積において、マイクロタイタープレート(組織培養等級,96ウェル平板)中で培養した。細胞を、8〜24時間、加湿雰囲気下で保温した。該培養液に、10μlの細胞増殖試薬WST−1(Roche Applied Science, インディアナポリス, インディアナ州, アメリカ合衆国)を加え、かつ1〜2時間、再度保温した。マイクロタイタープレートリーダーを用いて、該試料の吸光度を、バックグラウンド対照に対して405-450 nmの波長で測定した。参照波長は620 nmとした。テトラゾリウム塩WST−1(4-[3-(4-ヨードフェニル)-2-(4-ニトロフェニル)-2H-5-テトラゾリオ]-1,3-ベンゼンジスルホネート)を、"コハク酸テトラゾリウム還元酵素"系によるホルマザンに代謝させた。これは、ミトコンドリア内に存在し、かつ生存細胞にのみ活性を示す。従って、ホルマザンの形成(暗黄色)は、生存細胞数に比例する。この実験結果を、図8に示した。
(誘導体のED50値の測定)
表9中に示した各誘導体を用いて、実施例13に記載した細胞生存率アッセイを使用した。ED50値は、生じたデータ点を使用して、非線形回帰を用いるS字状の用量応答曲線により計算した。評価されたED50は、統計分析プログラムPRISM(登録商標)(GraphPad Software, Inc., サンディエゴ, カリフォルニア州, アメリカ合衆国)を用いて計算した。
該誘導体のED50値は、表9に示した。また、ED50値は、上述の細胞生存率アッセイを用いて、インドメタシン、及びスリンダクスルフィドに対して計算した。スリンダクスルフィドのED50値は、RKO細胞において98.2±1.4μM、及びHCT-116細胞において109.4±10.0μMであった。インドメタシンのED50値は、RKO細胞において162.2±11.0μM、及びHCT-116細胞において448.7±97.6μMであった。
(カスパーゼ-3比色分析アッセイ)
様々な時期に、試験化合物で試験されている、RKO、HCT-116(別のヒト結腸直腸癌細胞株)、及びH1299(ヒト非小細胞癌株)細胞を、氷冷PBSで2度洗浄し、かつ氷上で10分間、溶解緩衝液(BioVision)に溶解し、続いて、15,000×gで10分間、遠心分離した。アポトーシス細胞死の開始が決定される目安であるカスパーゼ-3活性は、基質としてp-ニトロアニリドラベル化ペプチドDEVD-pNAを用いる比色分析アッセイキット(BioVision Inc., パロアルト, カリフォルニア州, アメリカ合衆国)により、該上清中において測定した。カスパーゼ-3活性を、基質からのp-ニトロアニリドの放出により、405 nmでモニターした。カスパーゼ-3活性の倍増加を図9に示し、かつビヒクル試験コントロール、及びスリンダクスルフィド及びその類似体で試験したものからのp-ニトロアニリドの吸光度と比較することにより計算した。
(タンパク質ライセートの調製、及びウェスタンブロット分析)
様々な時期に試験化合物で試験されている細胞を、氷冷リン酸緩衝食塩水(PBS)で2度洗浄し、かつ30分間4℃で、キナーゼ溶解緩衝液[50 mM Tris緩衝液(pH 7.5) 150 mM NaCl, 0.1% トリトン X-100, 0.1% ノニデット P-40, 4 mM エチレンジアミン四酢酸 (EDTA), 50 mM NaF, 0.1 mMオルトバナジン酸ナトリウム, 1 mM ジチオスレイトール(DTT)、及びプロテアーゼ阻害剤:アンチパイン、ロイペプチン、ペプスタチンA、及びキモスタチン(5μg/mL)、フッ化フェニルメチルスルホニル(50μg/mL)、及び4-(2-アミノエチル)-ベンゼンスルホニルフルオライド(100μg/mL)]中に溶解した。細胞ライセートを、15,000gで15分間の遠心分離により透明にし、かつ該得られた上清を回収した。細胞タンパク質(30-50μg)を、等量の2X Laemmliサンプル緩衝液[125 mM Tris (pH 6.8)、10% β-メルカプトエタノール、20% グリセロール、4% ドデシル硫酸ナトリウム(SDS)、及び0.05% ブロモフェノールブルー]で混合し、かつ5分間、煮沸した。該タンパク質を、ドデシル硫酸ナトリウム-ポリアクリルアミドゲル電気泳動(SDS−PAGE)により分離し、かつポリビニリデンジフルオライド膜(Millipore Corp., ベッドフォード, マサチューセッツ州, アメリカ合衆国)上に、電気泳動的に移動させた。該膜を、0.1% Tween 20を含むTris緩衝食塩水(50 mM Tris pH 7.5, 150 mM NaCl)中の5%ノンファットミルクでブロックし、次に、抗ポリ(ADPリボース)ポリメラーゼ(PharMingen, サンディエゴ, カリフォルニア州, アメリカ合衆国)で1時間、保温した。次に、一次抗体を、ロバ抗ウサギ、又はヤギ抗マウス西洋わさびペルオキシダーゼ接合二次抗体で染色した。増強した化学発光を行い(ECL ウェスタンブロット検出系:Amersham Biosciences, Piscataway, ニュージャージー州, アメリカ合衆国)、かつタンパク質バンドを、オートラジオグラフィーにより検出した。開裂ポリ(ADPリボース)ポリメラーゼに対応するバンドの検出は、アポトーシス細胞死の開始を示した。
(PPARγレポーターアッセイ)
ヒト胎児腎臓細胞(HEK293細胞)を、American Type Culture Collection (ATCC)から購入し、かつ5% CO2恒湿37°Cインキュベーター中、GIBCO(商標)GLUTAMAX(商標)(Invitrogen Corp., Carlsbad, カリフォルニア州, アメリカ合衆国)、及び10%熱不活性化FBS (Atlas Biological, Fort Collins, Colorado, アメリカ合衆国)、又は10%チャコール処理FBS(charcoal-stripped FBS)(HyClone, ローガン, ユタ州, アメリカ合衆国)を有する、ダルベッコの改質イーグル培地(DMEM)中で保持した。9x105 HEK293細胞は、チャコール処理FBSを供給したDMEM中で平板培養した。平板培養18時間後に、細胞を、3 mLのDMEM + 10%チャコール処理FBS中の1 μg DNAにつき、8 μLのEffectene Transfection Reagent (Qiagen Inc., バレンシア, カリフォルニア州, アメリカ合衆国)の脂質比を用いて、コントロールRenilla発光酵素発現プラスミド(Promega Corp.のpCMV-renilla発光酵素0.2μg, マディソン, ウィスコンシン州, アメリカ合衆国)、0.4μg PPARγ-GAL4、及び0.4μg UAS-tk-lucでトランスフェクトした。トランスフェクション培地を、DMEM + 対象のリガンド又はビヒクル(0.1% DMSO)を含む10%チャコール処理血清で置き換えるまで、細胞をトランスフェクション混合物中に残存させた。
培養液中のトランスフェクト細胞において、2-デス-メチルインドメタシン、及びエインデニック酸スルフィド、及び一連の構造類似体を、培養癌細胞のアポトーシスを誘発する能力に対して、及びPPARγ媒介転写を活性化する能力に対して試験した。両化合物が、元の薬剤と同じ活性か、又はそれよりも活性があることを示した。事実、エインデニック酸スルフィドは、両アッセイにおいて、スリンダクスルフィドよりも相当に活性がある。同様の結果が、エインデニック酸スルフィドの類似体を用いて得られた。共同発明者らは、作用の特定の理論全てに限定されることを望まないが、2-デス-メチル類似体の増強された生物活性は、該2’メチル基の除去の結果生じる構造変化のためであろう。
(インビボの2-デス-メチルインドメタシンの毒性)
インドメタシン、及び2-デス-メチルインドメタシンの毒性を、C57/BL6マウスにおいて比較した。これは、インドメタシンにより胃腸毒性に非常に感受性がある。一連の濃度のインドメタシン、及び2-デス-メチルインドメタシンの毎日注射は、2-デス-メチルインドメタシンが、インドメタシンよりも少なくとも25倍毒性が小さいことを示し、高濃度2-デス-メチル類似体を投与できることを立証した。従って、インドメタシン、及びスリンダクスルフィドの2-デス-メチル類似体、並びに任意のプロドラッグ形態(例えば、エインデニック酸スルホキシド)は、一連の疾患を標的とする薬剤の魅力的な候補体であるように見える。
下記に示した引用文献、並びに、本明細書中に引用した全ての引用文献は、本明細書中に引用により組み込まれており、その内容は、本明細書中で使用した方法論、技術、及び/又は組成物を補充、説明、背景提供、又は教示するものである。
Bowden DW, Sale M, Howard TD, Qadri A, Spray BJ, Rothschild CB, Akots G, Rich SS & Freedman BI (1997) 「糖尿病性腎症の経歴を有する白人同胞対における、NIDDMへのヒト染色体20、及び12上の遺伝子マーカーの結合」 diabetes 46:882-86.
Celi FS & Shuldiner AR (2002) 「糖尿病、及び肥満症における、ペルオキシソーム増殖因子-活性化受容体ガンマの役割」 Curr Diab Rep 2:179-85.
Copeland RA (2000) 「酵素:構造、機序、及びデータ分析への実用的な導入」, Wiley-VCH, New York, New York, United States of America.
DeWitt DL & Smith WL (1988) 「相補的DNA配列から決定された、ヒツジ精嚢由来のプロスタグランジンG/Hシンターゼの一次構造」Proc Natl Acad Sci U S A 85:1412-1416.
Doege H, Schurmann A, Bahrenberg G, Brauers A & Joost HG (2000) GLUT8, 「グルコース輸送活性を有する糖輸送促進体ファミリーの新規メンバー」 J Biol Chem 275:16275-80.
Ghosh S, Watanabe RM, Hauser ER, Valle T, Magnuson VL, Erdos MR, Langefeld CD, Balow J Jr, Ally DS, Kohtamaki Kらの論文 (1999) 「2型糖尿病:同胞対に影響される716フィンランド人の染色体20上の結合の証拠」 Proc Natl Acad Sci U S A 96:2198-2203.
Hanis CL, Boerwinkle E, Chakraborty R, Ellsworth DL, Concannon P, Stirling B, Morrison VA, Wapelhorst B, Spielman RS, Gogolin-Ewens KJらの論文 (1996) 「ヒト非インシュリン依存(2型)糖尿病遺伝子の全ゲノム調査は、染色体2上の主要感受性遺伝子座を明らかにする。」 Nat Genet 13:161-66.
Hansen T, Andersen CB, Echwald SM, Urhammer SA, Clausen JO, Vestergaard H, Owens D, Hansen L & Pedersen O (1997) 「ホスファチジルイノシトール3-キナーゼのp85調節サブユニット内の共通アミノ酸多型の同定」 diabetes 46:494501.
Hla T & Neilson K (1992) 「ヒトシクロオキシゲナーゼ-2 cDNA」 Proc Natl Acad Sci U S A 89:7384-7388.
Ibberson M, Uldry M & Thorens B (2000) 「GLUTX1, 中枢神経系、及びインシュリン感受性組織中に発現される、新規な哺乳動物グルコース輸送体」 J Biol Chem 275:4607-12.
Kalgutkar AS, Crews BC, Rowlinson SW, Marnett AB, Kozak KR, Remmel RP & Marnett LJ (2000a) 「生化学を基礎とした、シクロオキシゲナーゼ−2(COX−2)阻害剤の設計:非ステロイド性抗炎症薬の強力かつ高度選択的なCOX−2阻害剤への容易な変換」 Proc Natl Acad Sci U S A 97, 925-30.
Kalgutkar AS, Marnett AB, Crews BC, Remmel RP & Marnett LJ (2000b) 「選択的シクロオキシゲナーゼ-2阻害剤としての非ステロイド性抗炎症薬インドメタシンのエステル、及びアミド誘導体」 J Med Chem 43, 2860-70.
Kersten S, Desvergne B & Wahli W (2000) 「健康、及び疾患におけるPPARの役割」 Nature 405:421-4.
Kujubu DA, Fletcher BS, Varnum BC, Lim RW & Herschman HR (1991) 「TIS10, Swiss 3T3細胞由来のホルボールエステル腫瘍プロモーター誘発性mRNA, 新規プロスタグランジンシンターゼ/シクロオキシゲナーゼ相同体をコードする。」 J Biol Chem 266:12866-12872.
Kurumbail RG, Stevens AM, Gierse JK, McDonald JJ, Stegeman RA, Pak JY, Gildehaus D, Miyashiro JM, Penning TD, Seibert K, Isakson PC & Stallings WC (1996) 「抗炎症薬によるシクロオキシゲナーゼ-2の選択的阻害の構造的基礎. Nature 384:644-648」
Kusari J, Verma US, Buse JB, Henry RR & Olefsky JM (1991) 「共通型非インシュリン依存糖尿病である対象の、インシュリン受容体、及びインシュリン感受性グルコース輸送体(GLUT-4)の遺伝子配列分析」 J Clin Invest 88:1323-30.
Lee SH, Soyoola E, Chanmugam P, Hart S, Sun W, Zhong H, Liou S, Simmons D & Hwang D (1992) 「リポ多糖類で刺激したマクロファージにおける、マイトジェン誘発性シクロオキシゲナーゼの選択的発現」 J Biol Chem 267:25934-25938.
Mahtani MM, Widen E, Lehto M, Thomas J, McCarthy M, Brayer J, Bryant B, Chan G, Daly M, Forsblom C, Kanninen T, Kirby A, Kruglyak L, Munnelly K, Parkkonen M, Reeve-Daly MP, Weaver A, Brettin T, Duyk G, Lander ES, Groop LC (1996) 「フィンランド人ファミリーのゲノムスキャンによるインシュリン分泌物検出に関連した、2型糖尿病に対する遺伝子マッピング」 Nat Genet 14:90-4.
Markey CM, Alward A, Weller PE & Marnett LJ (1987) 「プロスタグランジンHシンターゼによるヒドロペルオキシド還元の定量的研究. ペルオキシダーゼの基質特異性、及びその関連性を、シクロオキシゲナーゼ活性に還元すること」 J Biol Chem 262, 6266-79.
O'Sullivan MG, Huggins EM Jr. & McCall CE (1993) 「肺胞マクロファージにおける、プロスタグランジンHシンターゼ-2のリポ多糖類誘発性発現は、デキサメタゾンにより阻害され、アスピリンにより阻害されない。」 Biochem Biophys Res Commun 191:1294-1300.
Rome LH & Lands WE (1975) 「抗炎症薬を用いた、プロスタグランジンHシンターゼの相互作用の化学量論、及び速度論」 Proc Natl Acad Sci U S A 72:4863-5.
Schneider C, Boeglin WE, Prusakiewicz JJ, Rowlinson SW, Marnett LJ, Samel N & Brash AR (2002) 「シクロオキシゲナーゼ-1、及び-2による、15炭素でのロスタグランジン立体化学の制御. セリン530、及びバリン349の重要な役割」 J Biol Chem 277:478-85.
Shepherd PR & Kahn BB (1999) グルコース輸送体、及びインシュリン作用:インシュリン抵抗性と糖尿病との関連. N Engl J Med 341:248-57.
Timofeevski SL, Prusakiewicz JJ, Rouzer CA & Marnett LJ (2002) 「リアルタイム蛍光、阻害速度、及び特定部位の変異誘発により研究された、インドメタシンアミドを用いたシクロオキシゲナーゼ-2のイソ型選択的相互作用」 Biochemistry 41:9654-62.
Vaag A (1999) 「病態生理学に基づく遅発性非インシュリン依存糖尿病. 現在の議論、及び新しい洞察」 Dan Med Bull 46:197-234.
Weggen S, Eriksen JL, Das P, Sagi SA, Wang R, Pietrzik CU, Findlay KA, Smith TE, Murphy MP, Bulter T, Kang DE, Marquez-Sterling N, Golde TE & Koo EH (2001) 「シクロオキシゲナーゼ活性に独立的な、NSAID低アミロイド生成性Abeta42のサブセット」 Nature 414:212-6.
Yokoyama C & Tanabe T (1989) 「プロスタグランジンエンドペルオキシドシンターゼ、及び該酵素の一次構造をコードしているヒト遺伝子のクローニング」 Biochem Biophys Res Commun 165:888-894.
Zierler K (1999) 「全身グルコース代謝」 Am J Physiol 276:E409-26.
Zouali H, Hani EH, Philippi A, Vionnet N, Beckmann JS, Demenais F & Froguel P (1997) 「ホスホエノールピルビン酸カルボキシキナーゼ遺伝子に近接した、染色体20qへの早期発症型非インシュリン依存(2型)糖尿病マップの感受性遺伝子座」 Hum Mol Genet 6:1401-8.
Claims (60)
- 細胞を化合物の誘導体と接触させることを含む、細胞の増殖阻害方法であって、該化合物は、2’メチル基を有するインドール酢酸、又はインデン酢酸官能基を含むシクロオキシゲナーゼ阻害剤であり、かつ該誘導体は、該2’メチル基を、水素原子;ハロ;メチル基の少なくとも1つの水素原子がハロゲンで置換されたハロメチル;C2〜C6アルキル;C2〜C6分岐アルキル;及びC2〜C6置換アルキルからなる群から選択された成分に改質した結果として、シクロオキシゲナーゼ阻害活性を実質的に欠くものである、前記方法。
- 前記シクロオキシゲナーゼ阻害剤が、インデン酢酸官能基を含み、かつ前記成分が、水素原子、及びフッ素原子からなる群から選択されたものである、請求項1記載の方法。
- 前記細胞が、対象内に存在するものである、請求項1記載の方法。
- 前記細胞が、腫瘍細胞である、請求項3記載の方法。
- 前記対象が、哺乳動物である、請求項4記載の方法。
- 前記哺乳動物が、ヒトである、請求項5記載の方法。
- 前記化合物が、非ステロイド性抗炎症薬である、請求項1記載の方法。
- 前記非ステロイド性抗炎症薬が、インドメタシン、スリンダク、及びそれらの医薬として許容し得る塩からなる群から選択されたものである、請求項6記載の方法。
- 対象に化合物の誘導体の治療有効量を投与することを含む、癌、神経変性疾患、及び糖尿病からなる群から選択される対象の疾患の治療方法であって、該化合物は、2’メチル基を有するインドール酢酸、又はインデン酢酸官能基を含むシクロオキシゲナーゼ阻害剤であり、かつ該誘導体は、該2’メチル基を、水素原子;ハロ;メチル基の少なくとも1つの水素原子がハロゲンで置換されたハロメチル;C2〜C6アルキル;C2〜C6分岐アルキル;及びC2〜C6置換アルキルからなる群から選択された成分に改質した結果として、シクロオキシゲナーゼ阻害活性を実質的に欠くものである、前記方法。
- 前記シクロオキシゲナーゼ阻害剤が、インデン酢酸官能基を含み、かつ前記成分が、水素原子、及びフッ素原子からなる群から選択されたものである、請求項9記載の方法。
- 前記対象が、哺乳動物である、請求項9記載の方法。
- 前記哺乳動物が、ヒトである、請求項11記載の方法。
- 前記神経変性疾患が、アルツハイマー病である、請求項9記載の方法。
- 前記化合物が、非ステロイド性抗炎症薬である、請求項9記載の方法。
- 前記非ステロイド性抗炎症薬が、インドメタシン、及びスリンダク、それらの医薬として許容し得る塩、及びそれらの組合せからなる群から選択されたものである、請求項14記載の方法。
- 前記誘導体が、前記化合物よりも実質的に少ない胃腸毒性を生じる、請求項9記載の方法。
- 腫瘍を有する対象に化合物の誘導体を投与することを含む、対象の腫瘍増殖の抑制方法であって、該化合物は、2’メチル基を有するインドール酢酸、又はインデン酢酸官能基を含むシクロオキシゲナーゼ阻害剤であり、かつ該誘導体は、該2’メチル基を、水素原子;ハロ;メチル基の少なくとも1つの水素原子がハロゲンで置換されたハロメチル;C2〜C6アルキル;C2〜C6分岐アルキル;及びC2〜C6置換アルキルからなる群から選択された成分に改質した結果として、シクロオキシゲナーゼ阻害活性を実質的に欠くものである、前記方法。
- 前記シクロオキシゲナーゼ阻害剤が、インデン酢酸官能基を含み、かつ前記成分が、水素原子、及びフッ素原子からなる群から選択されたものである、請求項17記載の方法。
- 前記対象が、哺乳動物である、請求項17記載の方法。
- 前記哺乳動物が、ヒトである、請求項19記載の方法。
- 前記化合物が、非ステロイド性抗炎症薬である、請求項17記載の方法。
- 前記非ステロイド性抗炎症薬が、インドメタシン、及びスリンダク、それらの医薬として許容し得る塩、及びそれらの組合せからなる群から選択されたものである、請求項17記載の方法。
- 前記誘導体が、前記化合物よりも実質的に少ない胃腸毒性を生じる、請求項17記載の方法。
- 細胞を化合物の誘導体と接触させることを含む、細胞のアポトーシスの誘発方法であって、該化合物は、2’メチル基を有するインドール酢酸、又はインデン酢酸官能基を含むシクロオキシゲナーゼ阻害剤であり、かつ該誘導体は、該2’メチル基を、水素原子;ハロ;メチル基の少なくとも1つの水素原子がハロゲンで置換されたハロメチル;C2〜C6アルキル;C2〜C6分岐アルキル;及びC2〜C6置換アルキルからなる群から選択された成分に改質した結果として、シクロオキシゲナーゼ阻害活性を実質的に欠くものである、前記方法。
- 前記シクロオキシゲナーゼ阻害剤が、インデン酢酸官能基を含み、かつ前記成分が、水素原子、及びフッ素原子からなる群から選択されたものである、請求項24記載の方法。
- 前記細胞が、培養液中の細胞である、請求項24記載の方法。
- 前記細胞が、癌細胞である、請求項24記載の方法。
- 前記細胞が、対象内に存在するものである、請求項24記載の方法。
- 前記対象が、哺乳動物である、請求項28記載の方法。
- 前記哺乳動物が、ヒトである、請求項29記載の方法。
- 前記化合物が、非ステロイド性抗炎症薬である、請求項24記載の方法。
- 前記非ステロイド性抗炎症薬が、インドメタシン、及びスリンダク、それらの医薬として許容し得る塩、及びそれらの組合せからなる群から選択される、請求項31記載の方法。
- ペルオキシソーム増殖因子活性化受容体(PPAR)イソ型を、化合物の誘導体と接触させることを含む、PPARイソ型の活性を調節する方法であって、該化合物は、2’メチル基を有するインドール酢酸、又はインデン酢酸官能基を含むシクロオキシゲナーゼ阻害剤であり、かつ該誘導体は、該2’メチル基を、水素原子;ハロ;メチル基の少なくとも1つの水素原子がハロゲンで置換されたハロメチル;C2〜C6アルキル;C2〜C6分岐アルキル;及びC2〜C6置換アルキルからなる群から選択された成分に改質した結果として、シクロオキシゲナーゼ阻害活性を実質的に欠くものである、前記方法。
- 前記シクロオキシゲナーゼ阻害剤が、インデン酢酸官能基を含み、かつ前記成分が、水素原子、及びフッ素原子からなる群から選択されたものである、請求項33記載の方法。
- 前記ペルオキシソーム増殖因子活性化受容体(PPAR)イソ型が、PPARγである、請求項33記載の方法。
- 前記ペルオキシソーム増殖因子活性化受容体(PPAR)イソ型が、対象内に存在するものである、請求項33記載の方法。
- 前記対象が、哺乳動物である、請求項36記載の方法。
- 前記哺乳動物が、ヒトである、請求項37記載の方法。
- 前記化合物が、非ステロイド性抗炎症薬である、請求項33記載の方法。
- 前記非ステロイド性抗炎症薬が、インドメタシン、及びスリンダク、それらの医薬として許容し得る塩、及びそれらの組合せからなる群から選択されたものである、請求項33記載の方法。
- 前記誘導体が、前記化合物よりも実質的に少ない胃腸毒性を生じる、請求項33記載の方法。
- シクロオキシゲナーゼ阻害化合物の特異性を変更する方法であって:
(a)2’メチル基を有するインドール酢酸、又はインデン酢酸官能基を含む、シクロオキシゲナーゼ阻害活性を有する化合物を提供すること;及び
(b)該2’メチル基を、水素原子;ハロ;メチル基の少なくとも1つの水素原子がハロゲンで置換されたハロメチル;C2〜C6アルキル;C2〜C6分岐アルキル;及びC2〜C6置換アルキルからなる群から選択された成分で置換し、シクロオキシゲナーゼ阻害活性を実質的に欠く誘導体を作り出すことを含む、前記方法。 - 前記化合物が、インデン酢酸官能基を含み、かつ前記成分が、水素原子、及びフッ素原子からなる群から選択されたものである、請求項42記載の方法。
- 前記化合物が、非ステロイド性抗炎症薬である、請求項42記載の方法。
- 前記非ステロイド性抗炎症薬が、インドメタシン、及びスリンダク、それらの医薬として許容し得る塩、及びそれらの組合せからなる群から選択されたものである、請求項44記載の方法。
- 前記誘導体が、下記式を有する、請求項1、9、17、24、及び33のいずれか1項記載の方法:
R2は、水素原子、ハロ、CF3;SCH3;SOCH3;SO2CH3;SO2NH2;CONH2;C1〜C6アルキル、分岐アルキル、又は置換アルキル;C1〜C6アルコキシ、分岐アルコキシ、又は置換アルコキシ;ベンジルオキシ;C1〜C6アルキルカルボン酸、分岐アルキルカルボン酸、又は置換アルキルカルボン酸;及びCH2N3からなる群から選択され;
R3、及びR4は、それぞれ独立に、水素原子;ハロ;CF3;C1〜C6アルキル、分岐アルキル、又は置換アルキル;C1〜C6アルコキシ、分岐アルコキシ、又は置換アルコキシ;アリール; 置換アリール; ベンジルオキシ;SCH3;SOCH3;SO2CH3;及びSO2NH2からなる群から選択され;
R5は、水素原子、C1〜C6アルキル、分岐アルキル、又は置換アルキル、及び=Oからなる群から選択され;
R6は、水素原子;C1〜C6アルキル、分岐アルキル、又は置換アルキル;C1〜C6アルコキシ、分岐アルコキシ、又は置換アルコキシ;ベンジルオキシ;C1〜C6アルキルカルボン酸、分岐アルキルカルボン酸、又は置換アルキルカルボン酸;及び下記構造のものからなる群から選択され:
R7は、水素原子;C1〜C6アルキル、分岐アルキル、又は置換アルキルであり;
R8は、水素原子、ハロ、C1〜C6アルキル、分岐アルキル、及び置換アルキル;C1〜C6アルコキシ、分岐アルコキシ、及び置換アルコキシ;C1〜C6アルキルカルボン酸、分岐アルキルカルボン酸、又は置換アルキルカルボン酸;アミノ;ニトロ;CF3;ブロモアセトアミジル;ベンゾイル;又は2−フェニル−オキシラニルであり;
Xは、O、又はNR9であって、ここでR9は、水素原子、又はアルキルであり;かつm、n、及びtは、それぞれ独立に0、1、2、3、4、又は5である。);
Yは、水素原子;ハロ;メチル基の少なくとも1つの水素原子がハロゲンで置換されたハロメチル;C2〜C6アルキル;C2〜C6分岐アルキル;及びC2〜C6置換アルキルからなる群から選択され;
Aは、炭素原子、及び窒素原子からなる群から選択され;
p、及びqは、双方とも独立に0、1、2、3、又は4であり;
R5に結合した炭素原子と該インデン環との間の結合は、単結合、又は二重結合であり;かつ
R1が結合した6員環は、シクロへキシル、又はフェニルである。)。 - 前記誘導体が、2−デス−メチルインドメタシン、エインデニック酸スルフィド、エインデニック酸スルホキシド、及びエインデニック酸スルホンからなる群から選択されたものである、請求項46記載の方法。
- 前記誘導体が、エインデニック酸スルフィドである、請求項46記載の方法。
- 前記化合物上に存在するカルボン酸成分を、エステル、又はアミドに誘導体化することをさらに含む、請求項46記載の方法。
- 前記エステル、又はアミドが、表3中に存在する構造を有するものである、請求項49記載の方法。
- 下記式の化合物:
R2は、水素原子、ハロ、CF3;SCH3;SOCH3;SO2CH3;SO2NH2;CONH2;C1〜C6アルキル、分岐アルキル、又は置換アルキル;C1〜C6アルコキシ、分岐アルコキシ、又は置換アルコキシ;ベンジルオキシ;C1〜C6アルキルカルボン酸、分岐アルキルカルボン酸、又は置換アルキルカルボン酸;及びCH2N3からなる群から選択され;
R3、及びR4は、それぞれ独立に、水素原子;ハロ;CF3;C1〜C6アルキル、分岐アルキル、又は置換アルキル;C1〜C6アルコキシ、分岐アルコキシ、又は置換アルコキシ;アリール; 置換アリール; ベンジルオキシ;SCH3;SOCH3;SO2CH3;及びSO2NH2からなる群から選択され;
R5は、水素原子、C1〜C6アルキル、分岐アルキル、又は置換アルキル、及び=Oからなる群から選択され;
R6は、水素原子;C1〜C6アルキル、分岐アルキル、又は置換アルキル;C1〜C6アルコキシ、分岐アルコキシ、又は置換アルコキシ;ベンジルオキシ;C1〜C6アルキルカルボン酸、分岐アルキルカルボン酸、又は置換アルキルカルボン酸;及び下記構造のものからなる群から選択され:
R7は、水素原子;C1〜C6アルキル、分岐アルキル、又は置換アルキルであり;
R8は、水素原子、ハロ、C1〜C6アルキル、分岐アルキル、及び置換アルキル;C1〜C6アルコキシ、分岐アルコキシ、及び置換アルコキシ;C1〜C6アルキルカルボン酸、分岐アルキルカルボン酸、又は置換アルキルカルボン酸;アミノ;ニトロ;CF3;ブロモアセトアミジル;ベンゾイル;又は2−フェニル−オキシラニルであり;
Xは、O、又はNR9であって、ここでR9は、水素原子、又はアルキルであり;かつm、n、及びtは、それぞれ独立に0、1、2、3、4、又は5である。);
Yは、水素原子;ハロ;メチル基の少なくとも1つの水素原子がハロゲンで置換されたハロメチル;C2〜C6アルキル;C2〜C6分岐アルキル;及びC2〜C6置換アルキルからなる群から選択され;
Aは、炭素原子、及び窒素原子からなる群から選択され;
p、及びqは、双方とも独立に0、1、2、3、又は4であり;
R5に結合した炭素原子と該インデン環との間の結合は、単結合、又は二重結合であり;かつ
R1が結合した6員環は、シクロへキシル、又はフェニルである。)。 - R1が、C1〜C6アルキルカルボン酸、及び分岐C1〜C6アルキルカルボン酸からなる群から選択され;
R2が、ハロ、C1〜C6アルキル又は分岐アルキル、SCH3、SOCH3、SO2CH3、及びSO2NH2からなる群から選択され;かつ
R3〜R5、及びR7〜R10が、それぞれ独立に、水素原子、C1〜C6アルキル又は分岐アルキル、及びハロからなる群から選択された、請求項51記載の化合物。 - R*が、単又は多置換アリールであり、各置換基が、ハロゲン、NH2、OCH3、CF3、OH、C1〜C4アルキル又は分岐アルキル、NO2、ベンゾイル、2−フェニル−オキシラン、及びNH−CO−CH2Brからなる群から選択された、請求項56記載の化合物。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US56548904P | 2004-04-26 | 2004-04-26 | |
| PCT/US2005/014328 WO2005112921A2 (en) | 2004-04-26 | 2005-04-26 | Indoleacetic acid and indenacetic acid derivatives as therapeutic agents with reduced gastrointestinal toxicity |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2007534702A true JP2007534702A (ja) | 2007-11-29 |
| JP2007534702A5 JP2007534702A5 (ja) | 2008-06-26 |
Family
ID=35428831
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2007509739A Pending JP2007534702A (ja) | 2004-04-26 | 2005-04-26 | 胃腸毒性の低い治療薬としてのインドール酢酸、及びインデン酢酸誘導体 |
Country Status (7)
| Country | Link |
|---|---|
| US (2) | US7491744B2 (ja) |
| EP (1) | EP1744747A4 (ja) |
| JP (1) | JP2007534702A (ja) |
| CN (1) | CN101031289A (ja) |
| AU (1) | AU2005244770A1 (ja) |
| CA (1) | CA2562783A1 (ja) |
| WO (1) | WO2005112921A2 (ja) |
Cited By (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2009541311A (ja) * | 2006-06-22 | 2009-11-26 | アストラゼネカ・アクチエボラーグ | Baceインヒビターとしての置換イソインドール類及びそれらの使用 |
| JP2018501261A (ja) * | 2014-12-16 | 2018-01-18 | エーディーティー ファーマシューティカルズ,エルエルシー | Ras阻害インデニルアセトアミド化合物、組成物、およびその使用 |
| JP2018505145A (ja) * | 2014-12-16 | 2018-02-22 | エーディーティー ファーマシューティカルズ,エルエルシー | インデニル化合物、医薬組成物、およびその医学的使用 |
| US11104658B2 (en) | 2014-12-16 | 2021-08-31 | Adt Pharmaceuticals, Llc | Method of treating or preventing Ras-mediated diseases |
| JP2021524836A (ja) * | 2018-04-13 | 2021-09-16 | ヒールクス リミテッドHealx Limited | 脆弱x症候群の治療 |
| US11186596B2 (en) | 2018-04-26 | 2021-11-30 | Adt Pharmaceuticals, Llc | Anticancer indenes, indanes, azaindenes, azaindanes, pharmaceutical compositions and uses |
Families Citing this family (21)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2477604A1 (en) | 2002-03-13 | 2003-09-25 | Signum Biosciences, Inc. | Modulation of protein methylation and phosphoprotein phosphate |
| AU2004253159A1 (en) * | 2003-06-25 | 2005-01-06 | Vanderbilt University | COX-2-targeted imaging agents |
| CA2562783A1 (en) * | 2004-04-26 | 2005-12-01 | Vanderbilt University | Indoleacetic acid and indenacetic acid derivatives as therapeutic agents with reduced gastrointestinal toxicity |
| US20080139449A1 (en) * | 2005-01-04 | 2008-06-12 | Wolfgang Jahnke | X-Ray Structure of Human Fpps and Use For Selecting Fpps Binding Compounds |
| US7923041B2 (en) | 2005-02-03 | 2011-04-12 | Signum Biosciences, Inc. | Compositions and methods for enhancing cognitive function |
| US8221804B2 (en) | 2005-02-03 | 2012-07-17 | Signum Biosciences, Inc. | Compositions and methods for enhancing cognitive function |
| US8399666B2 (en) | 2005-11-04 | 2013-03-19 | Panmira Pharmaceuticals, Llc | 5-lipoxygenase-activating protein (FLAP) inhibitors |
| GB2431927B (en) | 2005-11-04 | 2010-03-17 | Amira Pharmaceuticals Inc | 5-Lipoxygenase-activating protein (FLAP) inhibitors |
| US7977359B2 (en) | 2005-11-04 | 2011-07-12 | Amira Pharmaceuticals, Inc. | 5-lipdxygenase-activating protein (FLAP) inhibitors |
| US8044048B2 (en) * | 2006-01-04 | 2011-10-25 | Southern Research Institute | Derivatives of sulindac, use thereof and preparation thereof |
| CA2657691A1 (en) | 2006-06-19 | 2007-12-27 | Vanderbilt University | Methods and compositions for diagnostic and therapeutic targeting of cox-2 |
| WO2009132051A1 (en) | 2008-04-21 | 2009-10-29 | Signum Biosciences, Inc. | Compounds, compositions and methods for making the same |
| CN102137858B (zh) | 2008-05-23 | 2014-07-23 | 潘米拉制药有限责任公司 | 5-脂氧合酶-活化蛋白抑制剂 |
| US8546431B2 (en) | 2008-10-01 | 2013-10-01 | Panmira Pharmaceuticals, Llc | 5-lipoxygenase-activating protein (FLAP) inhibitors |
| WO2013059245A1 (en) * | 2011-10-17 | 2013-04-25 | Vanderbilt University | Indomethacin analogs for the treatment of castrate-resistant prostate cancer |
| WO2014088982A1 (en) | 2012-12-07 | 2014-06-12 | Albert Einstein College Of Medicine Of Yeshiva University | Gut barrier dysfunction treatment and prevention |
| CN103630519A (zh) * | 2013-12-03 | 2014-03-12 | 华东理工大学 | 应用pH敏感的比率荧光蛋白检测酶-前药反应的方法 |
| US10329249B1 (en) | 2018-10-03 | 2019-06-25 | King Saud University | Sulindac derivatives |
| CN110554129B (zh) * | 2019-09-12 | 2020-09-25 | 浙江省农业科学院 | 一种特级初榨橄榄油中潜在抗炎活性成分的筛选方法 |
| CN111402948A (zh) * | 2020-04-02 | 2020-07-10 | 江苏食品药品职业技术学院 | 基于人工智能和动物实验数据集的药物代谢动力预测模型 |
| US20230227407A1 (en) * | 2021-12-30 | 2023-07-20 | ATAI Life Sciences AG | Dimethyltryptamine analogues as nitric oxide delivery drugs |
Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3196162A (en) * | 1961-03-13 | 1965-07-20 | Merck & Co Inc | Indolyl aliphatic acids |
| WO2002008188A1 (en) * | 2000-07-25 | 2002-01-31 | Merck & Co., Inc. | N-substituted indoles useful in the treatment of diabetes |
| WO2002020478A1 (en) * | 2000-08-24 | 2002-03-14 | Dublin City University | N-benzylindole-3-acetic acid derivatives for use in the treatment of drug resistan cancer |
| DE10163426A1 (de) * | 2001-12-21 | 2003-07-03 | Max Planck Gesellschaft | Pharmakologisch wirksame Inden-Derivate |
| US20030195244A1 (en) * | 2001-12-13 | 2003-10-16 | Hsing-Pang Hsieh | Indole compounds |
| WO2004020409A1 (en) * | 2002-08-29 | 2004-03-11 | Merck & Co., Inc. | Indoles having anti-diabetic activity |
| JP2004510762A (ja) * | 2000-10-02 | 2004-04-08 | メルク エンド カムパニー インコーポレーテッド | プレニル−蛋白質トランスフェラーゼの阻害剤 |
Family Cites Families (63)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AT290523B (de) * | 1962-01-05 | 1971-06-11 | Merck & Co Inc | Verfahren zur Herstellung neuer α-(3-Indolyl)-carbonsäuren |
| US3285908A (en) * | 1963-04-30 | 1966-11-15 | Merck & Co Inc | Indolyl acid amides |
| US3336194A (en) * | 1963-04-30 | 1967-08-15 | Merck & Co Inc | Indolyl acid amides |
| US3470203A (en) * | 1964-02-01 | 1969-09-30 | Merck & Co Inc | Intermediates for preparing 1-aroylindole-3-alkanoic acids |
| US3725548A (en) * | 1970-05-01 | 1973-04-03 | Merck & Co Inc | Substituted indenyl acetic acids in the treatment of pain, fever or inflammation |
| US3654349A (en) * | 1970-05-01 | 1972-04-04 | Merck & Co Inc | Substituted indenyl acetic acids |
| ES432545A1 (es) | 1974-12-03 | 1976-11-16 | Alter Sa | Un procedimiento de preparacion de ciertos esteres metile- nicos mixtos del acido 1-(p-clorobenzoil)-5-metoxi-2-meti- indol-3-acetico. |
| FR2392008A1 (fr) | 1977-05-02 | 1978-12-22 | Fabre Sa Pierre | Nouvelles formes modulees de medicaments utilisant les n-hydroxy alcoyl pyridine carboxamides comme vecteurs |
| DE2735537A1 (de) | 1977-08-06 | 1979-02-22 | Troponwerke Gmbh & Co Kg | Indolacetoxyacetylaminosaeurederivate, verfahren zu ihrer herstellung und ihre verwendung als arzneimittel |
| JPS5490174A (en) | 1977-12-27 | 1979-07-17 | Kanebo Ltd | Novel indomethacin derivatives and their preparation |
| US4229447A (en) * | 1979-06-04 | 1980-10-21 | American Home Products Corporation | Intraoral methods of using benzodiazepines |
| DE2926472A1 (de) | 1979-06-30 | 1981-01-15 | Thomae Gmbh Dr K | Neue benzoylderivate, deren herstellung und deren verwendung als arzneimittel |
| US4412994A (en) * | 1980-04-24 | 1983-11-01 | Interx Research Corporation | Mannich-base hydroxamic acid prodrugs, compositions and use |
| US4381307A (en) | 1980-10-31 | 1983-04-26 | Merck & Co., Inc. | Soft tertiary amine esters of bio-affecting carboxylic acids |
| PL131389B1 (en) | 1980-11-13 | 1984-11-30 | Krakowskie Zaklady Pharma | Method of obtaining n-acyl derivatives of triptamines |
| JPS5872560A (ja) | 1981-10-27 | 1983-04-30 | Teikoku Chem Ind Corp Ltd | インドメタシンフエニルエステル誘導体 |
| DE3145465A1 (de) | 1981-11-16 | 1983-05-19 | Krakowskie Zakłady Farmaceutyczne "Polfa", Kraków | Verfahren zur herstellung von n-acylderivaten der tryptamine |
| CA1187488A (en) | 1982-02-02 | 1985-05-21 | Yoichiro Ogawa | Indoleacetic ester derivatives and process for preparing same |
| DE3206885A1 (de) | 1982-02-26 | 1983-09-15 | Troponwerke GmbH & Co KG, 5000 Köln | Indolderivate, verfahren zu ihrer herstellung und ihre verwendung als arzneimittel |
| JPS58201763A (ja) | 1982-05-17 | 1983-11-24 | Kowa Co | インド−ルアセトキシ酢酸エステル |
| IL67445A (en) * | 1982-12-09 | 1985-11-29 | Teva Pharma | Ethoxycarbonyloxy ethyl esters of non-steroidal anti-inflammatory carboxylic acids |
| JPS59161358A (ja) | 1983-03-04 | 1984-09-12 | Ss Pharmaceut Co Ltd | 新規なインド−ル酢酸エステル誘導体及びその製造法 |
| JPS60112760A (ja) | 1983-11-18 | 1985-06-19 | Green Cross Corp:The | インド−ル酢酸誘導体及びその脂肪乳剤 |
| JPS60152462A (ja) | 1984-01-20 | 1985-08-10 | Terumo Corp | インド−ル酢酸アミド誘導体の製造方法 |
| JPS60214768A (ja) | 1984-04-07 | 1985-10-28 | Fujisawa Pharmaceut Co Ltd | オリゴペプチド化合物 |
| JPS6160649A (ja) | 1984-08-31 | 1986-03-28 | Ss Pharmaceut Co Ltd | 新規なエステル誘導体及びその製造法 |
| US5016652A (en) * | 1985-04-25 | 1991-05-21 | The Regents Of The University Of California | Method and apparatus for aiding in the reduction of incidence of tobacco smoking |
| JPS63196598A (ja) | 1987-02-09 | 1988-08-15 | Ss Pharmaceut Co Ltd | 新規なプレドニゾロンエステル誘導体 |
| JPS63275593A (ja) | 1987-05-08 | 1988-11-14 | Fujirebio Inc | β−アミノエチルリン酸エステル誘導体 |
| US5002935A (en) | 1987-12-30 | 1991-03-26 | University Of Florida | Improvements in redox systems for brain-targeted drug delivery |
| EP0335545B2 (en) | 1988-03-29 | 1998-09-23 | University Of Florida | Pharmaceutical formulations for parenteral use |
| DE3811120A1 (de) | 1988-03-31 | 1989-10-12 | Merckle Gmbh | Neopentylesterderivate, verfahren zu ihrer herstellung und ihre verwendung als arzneimittel |
| US4943587A (en) | 1988-05-19 | 1990-07-24 | Warner-Lambert Company | Hydroxamate derivatives of selected nonsteroidal antiinflammatory acyl residues and their use for cyclooxygenase and 5-lipoxygenase inhibition |
| US5504086A (en) * | 1989-10-17 | 1996-04-02 | Ellinwood, Jr.; Everett H. | Intraoral dosing method of administering trifluorobenzodiazepines, propoxyphene, and nefazodone |
| US5032588A (en) * | 1989-12-08 | 1991-07-16 | Abbott Laboratories | Thiazole lipoxygenase-inhibiting compounds derived from non-steroidal antiinflammatory carboxylic acids |
| US5093356A (en) * | 1990-01-16 | 1992-03-03 | Merck Frosst Canada, Inc. | Indenyl hydroxamic acids and hydroxy ureas as inhibitors of 5-lipoxygenase |
| US5681964A (en) * | 1990-10-23 | 1997-10-28 | University Of Kentucky Research Foundation | Permeable, non-irritating prodrugs of nonsteroidal and steroidal agents |
| GB9200114D0 (en) * | 1992-01-04 | 1992-02-26 | Scras | Dual inhibitors of no synthase and cyclooxygenase |
| US6048850A (en) * | 1992-09-22 | 2000-04-11 | Young; Donald A. | Method of inhibiting prostaglandin synthesis in a human host |
| US5436265A (en) * | 1993-11-12 | 1995-07-25 | Merck Frosst Canada, Inc. | 1-aroyl-3-indolyl alkanoic acids and derivatives thereof useful as anti-inflammatory agents |
| NZ269773A (en) | 1993-08-02 | 1997-11-24 | Commw Scient Ind Res Org | Therapeutic compound conjugates; such conjugates comprise a compound bound to one to three acyl groups derived from fatty acids |
| US5475021A (en) * | 1993-12-03 | 1995-12-12 | Vanderbilt University | Compounds and compositions for inhibition of cyclooxygenase activity |
| CA2182228C (en) | 1994-01-28 | 2008-09-16 | Paul Ashton | Codrugs as a method of controlled drug delivery |
| HUT76133A (en) | 1994-02-22 | 1997-06-30 | Merrell Pharma Inc | Novel indole derivatives useful to treat estrogen-related neoplasms and disorders pharmaceutical compositions containing them and process for producing them |
| US5643943A (en) * | 1994-12-23 | 1997-07-01 | Alcon Laboratories, Inc. | Systemic administration of esters and amides of antioxidants which may be used as antioxidant prodrug therapy for oxidative and inflammatory pathogenesis |
| US5607966A (en) * | 1994-12-23 | 1997-03-04 | Alcon Laboratories, Inc. | Esters and amides of non-steroidal anti-inflammatory carboxylic acids which may be used as anti-oxidants, 5-lipoxygenase inhibitors and non-steroidal anti-inflammatory prodrugs |
| US5510368A (en) * | 1995-05-22 | 1996-04-23 | Merck Frosst Canada, Inc. | N-benzyl-3-indoleacetic acids as antiinflammatory drugs |
| AU716582B2 (en) * | 1995-10-17 | 2000-03-02 | G.D. Searle & Co. | Method of detecting cyclooxygenase-2 |
| US5922742A (en) * | 1996-04-23 | 1999-07-13 | Merck Frosst Canada | Pyridinyl-2-cyclopenten-1-ones as selective cyclooxygenase-2 inhibitors |
| US5965619A (en) * | 1996-06-13 | 1999-10-12 | Cell Pathways Inc. | Method for treating patients having precancerous lesions with substituted indene derivatives |
| US5861419A (en) * | 1996-07-18 | 1999-01-19 | Merck Frosst Canad, Inc. | Substituted pyridines as selective cyclooxygenase-2 inhibitors |
| US5973191A (en) * | 1996-12-30 | 1999-10-26 | Vanderbilt University | Selective inhibitors of prostaglandin endoperoxide synthase-2 |
| GB2321455A (en) | 1997-01-24 | 1998-07-29 | Norsk Hydro As | Lipophilic derivatives of biologically active compounds |
| US5811425A (en) * | 1997-03-04 | 1998-09-22 | Abbott Laboratories | Heterocyclic compounds as COX-2 inhibitors |
| US6277878B1 (en) * | 1998-09-07 | 2001-08-21 | Pfizer Inc | Substituted indole compounds as anti-inflammatory and analgesic agents |
| IL144126A0 (en) | 1999-01-07 | 2002-05-23 | Univ Vanderbilt | A method of altering the specificity of cyclooxygenase-inhibiting compounds |
| US6207700B1 (en) | 1999-01-07 | 2001-03-27 | Vanderbilt University | Amide derivatives for antiangiogenic and/or antitumorigenic use |
| US6762182B1 (en) * | 1999-01-07 | 2004-07-13 | Vanderbilt University | Converting cox inhibition compounds that are not COX-2 selective inhibitors to derivatives that are COX-2 selective inhibitors |
| US6306890B1 (en) * | 1999-08-30 | 2001-10-23 | Vanderbilt University | Esters derived from indolealkanols and novel amides derived from indolealkylamides that are selective COX-2 inhibitors |
| ES2376161T3 (es) * | 2001-01-29 | 2012-03-09 | Janssen Pharmaceuticals, Inc. | Indoles sustituidos y su utilización como antagonistas de integrinas. |
| AU2004253159A1 (en) * | 2003-06-25 | 2005-01-06 | Vanderbilt University | COX-2-targeted imaging agents |
| CA2562783A1 (en) | 2004-04-26 | 2005-12-01 | Vanderbilt University | Indoleacetic acid and indenacetic acid derivatives as therapeutic agents with reduced gastrointestinal toxicity |
| CA2657691A1 (en) * | 2006-06-19 | 2007-12-27 | Vanderbilt University | Methods and compositions for diagnostic and therapeutic targeting of cox-2 |
-
2005
- 2005-04-26 CA CA002562783A patent/CA2562783A1/en not_active Abandoned
- 2005-04-26 EP EP05778497A patent/EP1744747A4/en not_active Withdrawn
- 2005-04-26 WO PCT/US2005/014328 patent/WO2005112921A2/en active Application Filing
- 2005-04-26 US US11/114,921 patent/US7491744B2/en not_active Expired - Fee Related
- 2005-04-26 JP JP2007509739A patent/JP2007534702A/ja active Pending
- 2005-04-26 AU AU2005244770A patent/AU2005244770A1/en not_active Abandoned
- 2005-04-26 CN CNA2005800213878A patent/CN101031289A/zh active Pending
-
2009
- 2009-01-05 US US12/319,262 patent/US8168656B2/en not_active Expired - Fee Related
Patent Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3196162A (en) * | 1961-03-13 | 1965-07-20 | Merck & Co Inc | Indolyl aliphatic acids |
| WO2002008188A1 (en) * | 2000-07-25 | 2002-01-31 | Merck & Co., Inc. | N-substituted indoles useful in the treatment of diabetes |
| WO2002020478A1 (en) * | 2000-08-24 | 2002-03-14 | Dublin City University | N-benzylindole-3-acetic acid derivatives for use in the treatment of drug resistan cancer |
| JP2004510762A (ja) * | 2000-10-02 | 2004-04-08 | メルク エンド カムパニー インコーポレーテッド | プレニル−蛋白質トランスフェラーゼの阻害剤 |
| US20030195244A1 (en) * | 2001-12-13 | 2003-10-16 | Hsing-Pang Hsieh | Indole compounds |
| DE10163426A1 (de) * | 2001-12-21 | 2003-07-03 | Max Planck Gesellschaft | Pharmakologisch wirksame Inden-Derivate |
| WO2004020409A1 (en) * | 2002-08-29 | 2004-03-11 | Merck & Co., Inc. | Indoles having anti-diabetic activity |
Non-Patent Citations (4)
| Title |
|---|
| JPN6011031029; Touhey,S. et al: European Journal of Cancer Vol.38, 2002, p.1661-1670 * |
| JPN6011031032; Bahner,CT. et al: Journal odf Medicinal Chemistry Vol.16, No.4, 1973, p.421-425 * |
| JPN6011031035; Hare,L.E. et al: Journal of Pharmaceutical Sciences Vol.66, No.3, 1977, p.414-417 * |
| JPN6011031038; Nixon,J.B. et al: Prostaglandins, Leukotrienes and Essential Fatty Acids Vol.68, 2003, p.323-330 * |
Cited By (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2009541311A (ja) * | 2006-06-22 | 2009-11-26 | アストラゼネカ・アクチエボラーグ | Baceインヒビターとしての置換イソインドール類及びそれらの使用 |
| US10981886B2 (en) | 2014-12-16 | 2021-04-20 | Adt Pharmaceuticals, Llc | Indenyl compounds, pharmaceutical compositions, and medical uses thereof |
| JP2021185193A (ja) * | 2014-12-16 | 2021-12-09 | エーディーティー ファーマシューティカルズ,エルエルシー | インデニル化合物、医薬組成物、およびその医学的使用 |
| US10526307B2 (en) | 2014-12-16 | 2020-01-07 | Adt Pharmaceuticals, Llc | Indenyl compounds, pharmaceutical compositions, and medical uses thereof |
| JP2020079307A (ja) * | 2014-12-16 | 2020-05-28 | エーディーティー ファーマシューティカルズ,エルエルシー | インデニル化合物、医薬組成物、およびその医学的使用 |
| US10975054B2 (en) | 2014-12-16 | 2021-04-13 | Adt Pharmaceuticals, Llc | Indenyl compounds, pharmaceutical compositions, and medical uses thereof |
| JP2018501261A (ja) * | 2014-12-16 | 2018-01-18 | エーディーティー ファーマシューティカルズ,エルエルシー | Ras阻害インデニルアセトアミド化合物、組成物、およびその使用 |
| US11104658B2 (en) | 2014-12-16 | 2021-08-31 | Adt Pharmaceuticals, Llc | Method of treating or preventing Ras-mediated diseases |
| US11407727B2 (en) | 2014-12-16 | 2022-08-09 | Adt Pharmaceuticals, Llc | Indenyl compounds, pharmaceutical compositions, and medical uses thereof |
| US11130744B2 (en) | 2014-12-16 | 2021-09-28 | Adt Pharmaceuticals, Llc | Indenyl compounds, pharmaceutical compositions, and medical uses thereof |
| US11198679B2 (en) | 2014-12-16 | 2021-12-14 | Adt Pharmaceuticals, Llc | Method of treating or preventing Ras-mediated diseases |
| JP2018505145A (ja) * | 2014-12-16 | 2018-02-22 | エーディーティー ファーマシューティカルズ,エルエルシー | インデニル化合物、医薬組成物、およびその医学的使用 |
| JP2021524836A (ja) * | 2018-04-13 | 2021-09-16 | ヒールクス リミテッドHealx Limited | 脆弱x症候群の治療 |
| US11186596B2 (en) | 2018-04-26 | 2021-11-30 | Adt Pharmaceuticals, Llc | Anticancer indenes, indanes, azaindenes, azaindanes, pharmaceutical compositions and uses |
| US11680073B2 (en) | 2018-04-26 | 2023-06-20 | Adt Pharmaceuticals, Llc | Anticancer indenes, indanes, azaindenes, azaindanes, pharmaceutical compositions and uses |
Also Published As
| Publication number | Publication date |
|---|---|
| CN101031289A (zh) | 2007-09-05 |
| US20090118290A1 (en) | 2009-05-07 |
| EP1744747A2 (en) | 2007-01-24 |
| US7491744B2 (en) | 2009-02-17 |
| CA2562783A1 (en) | 2005-12-01 |
| AU2005244770A1 (en) | 2005-12-01 |
| EP1744747A4 (en) | 2009-12-02 |
| US20050250839A1 (en) | 2005-11-10 |
| US8168656B2 (en) | 2012-05-01 |
| WO2005112921A3 (en) | 2007-04-26 |
| WO2005112921A2 (en) | 2005-12-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2007534702A (ja) | 胃腸毒性の低い治療薬としてのインドール酢酸、及びインデン酢酸誘導体 | |
| JP5498940B2 (ja) | サーチュイン調節性チアゾロピリジン化合物 | |
| AU2014306451B2 (en) | Substituted hydroxamic acid compounds | |
| US10398678B2 (en) | Indomethacin analogs for the treatment of castrate-resistant prostate cancer | |
| JP2023061995A (ja) | 発毛を調節するための組成物及び方法 | |
| IL111670A (en) | Isoxazoline compounds as anti-inflammatory substances | |
| JP6038773B2 (ja) | サーチュイン活性化因子および活性化アッセイ | |
| JPH11509519A (ja) | 非ステロイド系抗炎症剤誘導毒性を予防する組成物および方法 | |
| JP2009509932A (ja) | Ppar活性化合物 | |
| JP2002502815A (ja) | 抗菌剤 | |
| CA2332713C (en) | Hydroxamic acid derivatives as antibacterials | |
| US20090069428A1 (en) | Catalytic antioxidants and methods of use | |
| US20090082435A1 (en) | Methods, Compositions, And Compounds For Modulation Of Monoacylglycerol Lipase, Pain, And Stress-Related Disorders | |
| JP5913651B2 (ja) | 疼痛および他の疾患の処置のための化合物および方法 | |
| Chao et al. | Discovery of aliphatic-chain hydroxamates containing indole derivatives with potent class I histone deacetylase inhibitory activities | |
| JP5511676B2 (ja) | 寄生虫疾患を治療するためのシステインプロテアーゼ阻害剤 | |
| CN113272292B (zh) | (2,5-二氧代吡咯烷-1-基)(苯基)-乙酰胺衍生物及其在治疗神经系统疾病中的用途 | |
| JP2008525356A (ja) | 抗腫瘍活性を有するインドール誘導体 | |
| US6492550B2 (en) | Alpha-substituted thio, -oxo trifluoromethylketones as phospholipase inhibitors | |
| Kadhim | Synthesis and Evaluation of 4-Thiazolidinone Derivatives of Naproxen as Potential Improvement of it is Anti-Inflammatory Effect | |
| Kalin | Elucidation of the Histone Deacetylase 6 Pharmacophore | |
| MXPA00011225A (en) | Hydroxamic acid derivatives as antibacterials |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20080425 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20080425 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20110705 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20111003 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20111011 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120104 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20120515 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20120814 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20120821 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20130226 |