DE69937372T2 - Piperidin-indol derivate mit 5-ht6 affinität - Google Patents
Piperidin-indol derivate mit 5-ht6 affinität Download PDFInfo
- Publication number
- DE69937372T2 DE69937372T2 DE69937372T DE69937372T DE69937372T2 DE 69937372 T2 DE69937372 T2 DE 69937372T2 DE 69937372 T DE69937372 T DE 69937372T DE 69937372 T DE69937372 T DE 69937372T DE 69937372 T2 DE69937372 T2 DE 69937372T2
- Authority
- DE
- Germany
- Prior art keywords
- methyl
- pyridinyl
- tetrahydro
- indole
- mmol
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
- XVTILWLVPDMCSO-UHFFFAOYSA-N 1h-indole;piperidine Chemical class C1CCNCC1.C1=CC=C2NC=CC2=C1 XVTILWLVPDMCSO-UHFFFAOYSA-N 0.000 title 1
- 150000001875 compounds Chemical class 0.000 claims abstract description 100
- -1 C3-7cycloalkyloxy Chemical group 0.000 claims abstract description 69
- 229910052739 hydrogen Inorganic materials 0.000 claims abstract description 22
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 claims abstract description 14
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims abstract description 9
- 125000001624 naphthyl group Chemical group 0.000 claims abstract description 8
- 229920002554 vinyl polymer Polymers 0.000 claims abstract description 8
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 claims abstract description 7
- 201000000980 schizophrenia Diseases 0.000 claims abstract description 7
- 125000001424 substituent group Chemical group 0.000 claims abstract description 7
- 125000000876 trifluoromethoxy group Chemical group FC(F)(F)O* 0.000 claims abstract description 7
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 claims abstract description 7
- 125000001544 thienyl group Chemical group 0.000 claims abstract description 6
- 239000003814 drug Substances 0.000 claims abstract description 4
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims abstract description 4
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 claims abstract description 4
- 125000004076 pyridyl group Chemical group 0.000 claims abstract description 4
- 125000002943 quinolinyl group Chemical group N1=C(C=CC2=CC=CC=C12)* 0.000 claims abstract description 4
- 150000003839 salts Chemical class 0.000 claims description 26
- 125000000217 alkyl group Chemical group 0.000 claims description 25
- 125000003545 alkoxy group Chemical group 0.000 claims description 13
- 125000005843 halogen group Chemical group 0.000 claims description 13
- 229910052736 halogen Inorganic materials 0.000 claims description 11
- 150000002367 halogens Chemical class 0.000 claims description 11
- VVJULHDUNRLYJQ-UHFFFAOYSA-N 1-(4-chlorophenyl)sulfonyl-5,7-difluoro-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)indole Chemical compound C1N(C)CCC(C=2C3=CC(F)=CC(F)=C3N(C=2)S(=O)(=O)C=2C=CC(Cl)=CC=2)=C1 VVJULHDUNRLYJQ-UHFFFAOYSA-N 0.000 claims description 9
- MGOGWDKJDBVEDO-UHFFFAOYSA-N 1-(4-fluorophenyl)sulfonyl-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)indole Chemical compound C1N(C)CCC(C=2C3=CC=CC=C3N(C=2)S(=O)(=O)C=2C=CC(F)=CC=2)=C1 MGOGWDKJDBVEDO-UHFFFAOYSA-N 0.000 claims description 9
- PKIHTVNKQQSTNS-UHFFFAOYSA-N 5,7-difluoro-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-1-(4-methylphenyl)sulfonylindole Chemical compound C1N(C)CCC(C=2C3=CC(F)=CC(F)=C3N(C=2)S(=O)(=O)C=2C=CC(C)=CC=2)=C1 PKIHTVNKQQSTNS-UHFFFAOYSA-N 0.000 claims description 9
- BRCYJQJWECITRH-UHFFFAOYSA-N 5,7-difluoro-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-1-naphthalen-1-ylsulfonylindole Chemical compound C1N(C)CCC(C=2C3=CC(F)=CC(F)=C3N(C=2)S(=O)(=O)C=2C3=CC=CC=C3C=CC=2)=C1 BRCYJQJWECITRH-UHFFFAOYSA-N 0.000 claims description 9
- MMCUNKYUYLGXTO-UHFFFAOYSA-N 5,7-difluoro-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-1-naphthalen-2-ylsulfonylindole Chemical compound C1N(C)CCC(C=2C3=CC(F)=CC(F)=C3N(C=2)S(=O)(=O)C=2C=C3C=CC=CC3=CC=2)=C1 MMCUNKYUYLGXTO-UHFFFAOYSA-N 0.000 claims description 9
- DQFFAMCAKICAAE-UHFFFAOYSA-N 1-(4-bromophenyl)sulfonyl-5,7-difluoro-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)indole Chemical compound C1N(C)CCC(C=2C3=CC(F)=CC(F)=C3N(C=2)S(=O)(=O)C=2C=CC(Br)=CC=2)=C1 DQFFAMCAKICAAE-UHFFFAOYSA-N 0.000 claims description 8
- IZLTUOGTOXAMIB-UHFFFAOYSA-N 3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-1-(4-methylphenyl)sulfonyl-5-(trifluoromethoxy)indole Chemical compound C1N(C)CCC(C=2C3=CC(OC(F)(F)F)=CC=C3N(C=2)S(=O)(=O)C=2C=CC(C)=CC=2)=C1 IZLTUOGTOXAMIB-UHFFFAOYSA-N 0.000 claims description 8
- NRSSAGIHBHUFQT-UHFFFAOYSA-N 5-chloro-1-(4-fluorophenyl)sulfonyl-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)indole Chemical compound C1N(C)CCC(C=2C3=CC(Cl)=CC=C3N(C=2)S(=O)(=O)C=2C=CC(F)=CC=2)=C1 NRSSAGIHBHUFQT-UHFFFAOYSA-N 0.000 claims description 8
- CFERLOIPASCQHX-UHFFFAOYSA-N 5-fluoro-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-1-(4-methylphenyl)sulfonylindole Chemical compound C1N(C)CCC(C=2C3=CC(F)=CC=C3N(C=2)S(=O)(=O)C=2C=CC(C)=CC=2)=C1 CFERLOIPASCQHX-UHFFFAOYSA-N 0.000 claims description 8
- 229910052799 carbon Inorganic materials 0.000 claims description 8
- MIQZZXFQEUOVNN-UHFFFAOYSA-N 1-(2,5-dichlorophenyl)sulfonyl-5-fluoro-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)indole Chemical compound C1N(C)CCC(C=2C3=CC(F)=CC=C3N(C=2)S(=O)(=O)C=2C(=CC=C(Cl)C=2)Cl)=C1 MIQZZXFQEUOVNN-UHFFFAOYSA-N 0.000 claims description 7
- CZTXZSUGDKLCIJ-UHFFFAOYSA-N 1-(2-bromophenyl)sulfonyl-5-fluoro-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)indole Chemical compound C1N(C)CCC(C=2C3=CC(F)=CC=C3N(C=2)S(=O)(=O)C=2C(=CC=CC=2)Br)=C1 CZTXZSUGDKLCIJ-UHFFFAOYSA-N 0.000 claims description 7
- VCPHSKRMQVIJMW-UHFFFAOYSA-N 1-(4-bromophenyl)sulfonyl-5-fluoro-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)indole Chemical compound C1N(C)CCC(C=2C3=CC(F)=CC=C3N(C=2)S(=O)(=O)C=2C=CC(Br)=CC=2)=C1 VCPHSKRMQVIJMW-UHFFFAOYSA-N 0.000 claims description 7
- LUSZBABHUTXFPZ-UHFFFAOYSA-N 1-(4-chlorophenyl)sulfonyl-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-5-(trifluoromethoxy)indole Chemical compound C1N(C)CCC(C=2C3=CC(OC(F)(F)F)=CC=C3N(C=2)S(=O)(=O)C=2C=CC(Cl)=CC=2)=C1 LUSZBABHUTXFPZ-UHFFFAOYSA-N 0.000 claims description 7
- FOTRJEJEYZUGRU-UHFFFAOYSA-N 1-(4-chlorophenyl)sulfonyl-5-fluoro-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)indole Chemical compound C1N(C)CCC(C=2C3=CC(F)=CC=C3N(C=2)S(=O)(=O)C=2C=CC(Cl)=CC=2)=C1 FOTRJEJEYZUGRU-UHFFFAOYSA-N 0.000 claims description 7
- RJJMTJRTYASUEA-UHFFFAOYSA-N 1-(4-methoxyphenyl)sulfonyl-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)indole Chemical compound C1=CC(OC)=CC=C1S(=O)(=O)N1C2=CC=CC=C2C(C=2CCN(C)CC=2)=C1 RJJMTJRTYASUEA-UHFFFAOYSA-N 0.000 claims description 7
- CGSFFLVTUXMRJK-UHFFFAOYSA-N 5-fluoro-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-1-naphthalen-1-ylsulfonylindole Chemical compound C1N(C)CCC(C=2C3=CC(F)=CC=C3N(C=2)S(=O)(=O)C=2C3=CC=CC=C3C=CC=2)=C1 CGSFFLVTUXMRJK-UHFFFAOYSA-N 0.000 claims description 7
- YWMPUMZWTSQNNE-UHFFFAOYSA-N 1-(4-chloro-3-nitrophenyl)sulfonyl-5-fluoro-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)indole Chemical compound C1N(C)CCC(C=2C3=CC(F)=CC=C3N(C=2)S(=O)(=O)C=2C=C(C(Cl)=CC=2)[N+]([O-])=O)=C1 YWMPUMZWTSQNNE-UHFFFAOYSA-N 0.000 claims description 6
- HTJVVYKIAWUXOG-UHFFFAOYSA-N 5-cyclohexyloxy-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-1-(4-methylphenyl)sulfonylindole Chemical compound C1N(C)CCC(C=2C3=CC(OC4CCCCC4)=CC=C3N(C=2)S(=O)(=O)C=2C=CC(C)=CC=2)=C1 HTJVVYKIAWUXOG-UHFFFAOYSA-N 0.000 claims description 6
- LUWRUMKCMCRQSG-UHFFFAOYSA-N 5-fluoro-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-1-(2,4,6-trimethylphenyl)sulfonylindole Chemical compound C1N(C)CCC(C=2C3=CC(F)=CC=C3N(C=2)S(=O)(=O)C=2C(=CC(C)=CC=2C)C)=C1 LUWRUMKCMCRQSG-UHFFFAOYSA-N 0.000 claims description 6
- 208000028017 Psychotic disease Diseases 0.000 claims description 6
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 6
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 6
- 238000011282 treatment Methods 0.000 claims description 6
- OJWPQFHMHCVSPZ-UHFFFAOYSA-N 1-(4-fluorophenyl)sulfonyl-3-(1-methylpiperidin-4-yl)indole Chemical compound C1CN(C)CCC1C1=CN(S(=O)(=O)C=2C=CC(F)=CC=2)C2=CC=CC=C12 OJWPQFHMHCVSPZ-UHFFFAOYSA-N 0.000 claims description 5
- ITEXYDLMZZDEAJ-UHFFFAOYSA-N 5,7-difluoro-1-(4-fluorophenyl)sulfonyl-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)indole Chemical compound C1N(C)CCC(C=2C3=CC(F)=CC(F)=C3N(C=2)S(=O)(=O)C=2C=CC(F)=CC=2)=C1 ITEXYDLMZZDEAJ-UHFFFAOYSA-N 0.000 claims description 5
- KRPRYAUWVONDJD-UHFFFAOYSA-N 5-chloro-1-(4-fluorophenyl)sulfonyl-3-(1-methylpiperidin-4-yl)indole Chemical compound C1CN(C)CCC1C1=CN(S(=O)(=O)C=2C=CC(F)=CC=2)C2=CC=C(Cl)C=C12 KRPRYAUWVONDJD-UHFFFAOYSA-N 0.000 claims description 5
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 claims description 5
- 239000012453 solvate Substances 0.000 claims description 5
- DYCHFLNCHRGUEX-UHFFFAOYSA-N 1-(4-methoxyphenyl)sulfonyl-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-5-(trifluoromethyl)indole;hydrochloride Chemical compound Cl.C1=CC(OC)=CC=C1S(=O)(=O)N1C2=CC=C(C(F)(F)F)C=C2C(C=2CCN(C)CC=2)=C1 DYCHFLNCHRGUEX-UHFFFAOYSA-N 0.000 claims description 4
- QBNIMUXPAWGZNZ-UHFFFAOYSA-N 3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-1-(4-methylphenyl)sulfonyl-5-(trifluoromethyl)indole;hydrochloride Chemical compound Cl.C1N(C)CCC(C=2C3=CC(=CC=C3N(C=2)S(=O)(=O)C=2C=CC(C)=CC=2)C(F)(F)F)=C1 QBNIMUXPAWGZNZ-UHFFFAOYSA-N 0.000 claims description 4
- RCEAKXLHZYPIPN-UHFFFAOYSA-N 5-cyclohexyloxy-1-(4-methylphenyl)sulfonyl-3-(1-methylpiperidin-4-yl)indole Chemical compound C1CN(C)CCC1C(C1=C2)=CN(S(=O)(=O)C=3C=CC(C)=CC=3)C1=CC=C2OC1CCCCC1 RCEAKXLHZYPIPN-UHFFFAOYSA-N 0.000 claims description 4
- BLRHAPSCUXJJFG-UHFFFAOYSA-N 5-fluoro-1-(4-fluorophenyl)sulfonyl-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)indole Chemical compound C1N(C)CCC(C=2C3=CC(F)=CC=C3N(C=2)S(=O)(=O)C=2C=CC(F)=CC=2)=C1 BLRHAPSCUXJJFG-UHFFFAOYSA-N 0.000 claims description 4
- XUTVZCRVQBUPJO-UHFFFAOYSA-N 5-fluoro-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-1-[2,4,6-tri(propan-2-yl)phenyl]sulfonylindole Chemical compound CC(C)C1=CC(C(C)C)=CC(C(C)C)=C1S(=O)(=O)N1C2=CC=C(F)C=C2C(C=2CCN(C)CC=2)=C1 XUTVZCRVQBUPJO-UHFFFAOYSA-N 0.000 claims description 4
- 210000003169 central nervous system Anatomy 0.000 claims description 4
- JGSMAGQXWDWGNH-UHFFFAOYSA-N 1-(4-chlorophenyl)sulfonyl-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-5-(trifluoromethyl)indole;hydrochloride Chemical compound Cl.C1N(C)CCC(C=2C3=CC(=CC=C3N(C=2)S(=O)(=O)C=2C=CC(Cl)=CC=2)C(F)(F)F)=C1 JGSMAGQXWDWGNH-UHFFFAOYSA-N 0.000 claims description 3
- KZXDLYKFEIDQMO-UHFFFAOYSA-N 1-(4-fluorophenyl)sulfonyl-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-5-(trifluoromethyl)indole;hydrochloride Chemical compound Cl.C1N(C)CCC(C=2C3=CC(=CC=C3N(C=2)S(=O)(=O)C=2C=CC(F)=CC=2)C(F)(F)F)=C1 KZXDLYKFEIDQMO-UHFFFAOYSA-N 0.000 claims description 3
- QTCLTSOWXICWPZ-UHFFFAOYSA-N 1-(4-tert-butylphenyl)sulfonyl-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-5-(trifluoromethyl)indole;hydrochloride Chemical compound Cl.C1N(C)CCC(C=2C3=CC(=CC=C3N(C=2)S(=O)(=O)C=2C=CC(=CC=2)C(C)(C)C)C(F)(F)F)=C1 QTCLTSOWXICWPZ-UHFFFAOYSA-N 0.000 claims description 3
- BXWABEHSUKIMAP-UHFFFAOYSA-N 5,7-difluoro-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-1-(2,4,6-trimethylphenyl)sulfonylindole Chemical compound C1N(C)CCC(C=2C3=CC(F)=CC(F)=C3N(C=2)S(=O)(=O)C=2C(=CC(C)=CC=2C)C)=C1 BXWABEHSUKIMAP-UHFFFAOYSA-N 0.000 claims description 3
- 208000024827 Alzheimer disease Diseases 0.000 claims description 3
- 208000020925 Bipolar disease Diseases 0.000 claims description 3
- 208000023105 Huntington disease Diseases 0.000 claims description 3
- 208000026139 Memory disease Diseases 0.000 claims description 3
- 208000012902 Nervous system disease Diseases 0.000 claims description 3
- 208000025966 Neurological disease Diseases 0.000 claims description 3
- 208000018737 Parkinson disease Diseases 0.000 claims description 3
- 206010002026 amyotrophic lateral sclerosis Diseases 0.000 claims description 3
- 208000028683 bipolar I disease Diseases 0.000 claims description 3
- 125000000000 cycloalkoxy group Chemical group 0.000 claims description 3
- 150000004677 hydrates Chemical class 0.000 claims description 3
- 125000001637 1-naphthyl group Chemical group [H]C1=C([H])C([H])=C2C(*)=C([H])C([H])=C([H])C2=C1[H] 0.000 claims description 2
- 125000004201 2,4-dichlorophenyl group Chemical group [H]C1=C([H])C(*)=C(Cl)C([H])=C1Cl 0.000 claims description 2
- 125000006276 2-bromophenyl group Chemical group [H]C1=C([H])C(Br)=C(*)C([H])=C1[H] 0.000 claims description 2
- 125000004182 2-chlorophenyl group Chemical group [H]C1=C([H])C(Cl)=C(*)C([H])=C1[H] 0.000 claims description 2
- 125000004800 4-bromophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C([H])=C1Br 0.000 claims description 2
- 125000001255 4-fluorophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C([H])=C1F 0.000 claims description 2
- 125000000590 4-methylphenyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1*)C([H])([H])[H] 0.000 claims description 2
- 125000001309 chloro group Chemical group Cl* 0.000 claims description 2
- 125000003854 p-chlorophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C([H])=C1Cl 0.000 claims description 2
- 230000002265 prevention Effects 0.000 claims description 2
- 238000004519 manufacturing process Methods 0.000 claims 1
- 150000002475 indoles Chemical class 0.000 abstract description 14
- 230000005764 inhibitory process Effects 0.000 abstract description 2
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 abstract 7
- 125000000229 (C1-C4)alkoxy group Chemical group 0.000 abstract 5
- 125000001475 halogen functional group Chemical group 0.000 abstract 5
- 108091005435 5-HT6 receptors Proteins 0.000 abstract 2
- QZAYGJVTTNCVMB-UHFFFAOYSA-N serotonin Chemical compound C1=C(O)C=C2C(CCN)=CNC2=C1 QZAYGJVTTNCVMB-UHFFFAOYSA-N 0.000 description 86
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 48
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 48
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 41
- 102000005962 receptors Human genes 0.000 description 34
- 108020003175 receptors Proteins 0.000 description 34
- JLSQOXYKMJPCKL-UHFFFAOYSA-N 5-cyclohexyloxy-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-1h-indole Chemical compound C1N(C)CCC(C=2C3=CC(OC4CCCCC4)=CC=C3NC=2)=C1 JLSQOXYKMJPCKL-UHFFFAOYSA-N 0.000 description 32
- XFERGYRFFJXSGI-UHFFFAOYSA-N 5-fluoro-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-1h-indole Chemical compound C1N(C)CCC(C=2C3=CC(F)=CC=C3NC=2)=C1 XFERGYRFFJXSGI-UHFFFAOYSA-N 0.000 description 31
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 28
- BFXHJFKKRGVUMU-UHFFFAOYSA-N 4-fluorobenzenesulfonyl chloride Chemical compound FC1=CC=C(S(Cl)(=O)=O)C=C1 BFXHJFKKRGVUMU-UHFFFAOYSA-N 0.000 description 24
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 20
- 239000000203 mixture Substances 0.000 description 19
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 18
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 18
- VZROZUHJFVYRNB-UHFFFAOYSA-N 5,7-difluoro-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-1h-indole Chemical compound C1N(C)CCC(C=2C3=CC(F)=CC(F)=C3NC=2)=C1 VZROZUHJFVYRNB-UHFFFAOYSA-N 0.000 description 16
- 238000006243 chemical reaction Methods 0.000 description 15
- SIKJAQJRHWYJAI-UHFFFAOYSA-N Indole Chemical compound C1=CC=C2NC=CC2=C1 SIKJAQJRHWYJAI-UHFFFAOYSA-N 0.000 description 14
- 239000003153 chemical reaction reagent Substances 0.000 description 14
- RWRDLPDLKQPQOW-UHFFFAOYSA-N Pyrrolidine Chemical compound C1CCNC1 RWRDLPDLKQPQOW-UHFFFAOYSA-N 0.000 description 13
- ACEZXSPOZHQNPS-UHFFFAOYSA-N 3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-5-(trifluoromethoxy)-1h-indole Chemical compound C1N(C)CCC(C=2C3=CC(OC(F)(F)F)=CC=C3NC=2)=C1 ACEZXSPOZHQNPS-UHFFFAOYSA-N 0.000 description 12
- KGZVKFBGRBPYCW-UHFFFAOYSA-N 3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-5-(trifluoromethyl)-1h-indole Chemical compound C1N(C)CCC(C=2C3=CC(=CC=C3NC=2)C(F)(F)F)=C1 KGZVKFBGRBPYCW-UHFFFAOYSA-N 0.000 description 12
- 239000000243 solution Substances 0.000 description 12
- 239000002904 solvent Substances 0.000 description 12
- YYROPELSRYBVMQ-UHFFFAOYSA-N 4-toluenesulfonyl chloride Chemical compound CC1=CC=C(S(Cl)(=O)=O)C=C1 YYROPELSRYBVMQ-UHFFFAOYSA-N 0.000 description 11
- ZLYBFBAHAQEEQQ-UHFFFAOYSA-N 4-chlorobenzenesulfonyl chloride Chemical compound ClC1=CC=C(S(Cl)(=O)=O)C=C1 ZLYBFBAHAQEEQQ-UHFFFAOYSA-N 0.000 description 10
- DTJVECUKADWGMO-UHFFFAOYSA-N 4-methoxybenzenesulfonyl chloride Chemical compound COC1=CC=C(S(Cl)(=O)=O)C=C1 DTJVECUKADWGMO-UHFFFAOYSA-N 0.000 description 10
- WRIKHQLVHPKCJU-UHFFFAOYSA-N sodium bis(trimethylsilyl)amide Chemical compound C[Si](C)(C)N([Na])[Si](C)(C)C WRIKHQLVHPKCJU-UHFFFAOYSA-N 0.000 description 10
- IUENQRYBZHHPBN-UHFFFAOYSA-N 3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-1h-indole Chemical compound C1N(C)CCC(C=2C3=CC=CC=C3NC=2)=C1 IUENQRYBZHHPBN-UHFFFAOYSA-N 0.000 description 9
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 9
- 239000002253 acid Substances 0.000 description 9
- 239000002585 base Substances 0.000 description 9
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical class CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 9
- VHYFNPMBLIVWCW-UHFFFAOYSA-N 4-Dimethylaminopyridine Chemical compound CN(C)C1=CC=NC=C1 VHYFNPMBLIVWCW-UHFFFAOYSA-N 0.000 description 8
- YEZADZMMVHWFIY-UHFFFAOYSA-N 4-tert-butylbenzenesulfonyl chloride Chemical compound CC(C)(C)C1=CC=C(S(Cl)(=O)=O)C=C1 YEZADZMMVHWFIY-UHFFFAOYSA-N 0.000 description 8
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 8
- 239000003446 ligand Substances 0.000 description 8
- KDLHZDBZIXYQEI-UHFFFAOYSA-N palladium Substances [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 8
- XVYXWSODSCHHHB-UHFFFAOYSA-N 5-(trifluoromethoxy)-1h-indole Chemical compound FC(F)(F)OC1=CC=C2NC=CC2=C1 XVYXWSODSCHHHB-UHFFFAOYSA-N 0.000 description 7
- 239000003937 drug carrier Substances 0.000 description 7
- 235000019439 ethyl acetate Nutrition 0.000 description 7
- 238000000034 method Methods 0.000 description 7
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 7
- 125000006239 protecting group Chemical group 0.000 description 7
- PVJZBZSCGJAWNG-UHFFFAOYSA-N 2,4,6-trimethylbenzenesulfonyl chloride Chemical compound CC1=CC(C)=C(S(Cl)(=O)=O)C(C)=C1 PVJZBZSCGJAWNG-UHFFFAOYSA-N 0.000 description 6
- KMMHZIBWCXYAAH-UHFFFAOYSA-N 4-bromobenzenesulfonyl chloride Chemical compound ClS(=O)(=O)C1=CC=C(Br)C=C1 KMMHZIBWCXYAAH-UHFFFAOYSA-N 0.000 description 6
- CXKIOPZKRMEFOU-UHFFFAOYSA-N 5-chloro-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-1h-indole Chemical compound C1N(C)CCC(C=2C3=CC(Cl)=CC=C3NC=2)=C1 CXKIOPZKRMEFOU-UHFFFAOYSA-N 0.000 description 6
- NLDSVLMGLXEPPV-UHFFFAOYSA-N 5-cyclohexyloxy-1h-indole Chemical compound C1CCCCC1OC1=CC=C(NC=C2)C2=C1 NLDSVLMGLXEPPV-UHFFFAOYSA-N 0.000 description 6
- ZJHSPAMSFOLWGE-UHFFFAOYSA-N 6-bromo-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-1h-indole Chemical compound C1N(C)CCC(C=2C3=CC=C(Br)C=C3NC=2)=C1 ZJHSPAMSFOLWGE-UHFFFAOYSA-N 0.000 description 6
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 6
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 6
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 6
- 239000012043 crude product Substances 0.000 description 6
- PZOUSPYUWWUPPK-UHFFFAOYSA-N indole Natural products CC1=CC=CC2=C1C=CN2 PZOUSPYUWWUPPK-UHFFFAOYSA-N 0.000 description 6
- RKJUIXBNRJVNHR-UHFFFAOYSA-N indolenine Natural products C1=CC=C2CC=NC2=C1 RKJUIXBNRJVNHR-UHFFFAOYSA-N 0.000 description 6
- 238000002844 melting Methods 0.000 description 6
- 230000008018 melting Effects 0.000 description 6
- DASJFYAPNPUBGG-UHFFFAOYSA-N naphthalene-1-sulfonyl chloride Chemical compound C1=CC=C2C(S(=O)(=O)Cl)=CC=CC2=C1 DASJFYAPNPUBGG-UHFFFAOYSA-N 0.000 description 6
- OPECTNGATDYLSS-UHFFFAOYSA-N naphthalene-2-sulfonyl chloride Chemical compound C1=CC=CC2=CC(S(=O)(=O)Cl)=CC=C21 OPECTNGATDYLSS-UHFFFAOYSA-N 0.000 description 6
- 239000003921 oil Substances 0.000 description 6
- 235000019198 oils Nutrition 0.000 description 6
- 239000008194 pharmaceutical composition Substances 0.000 description 6
- 239000000725 suspension Substances 0.000 description 6
- GBJSCSVGBRFBAK-UHFFFAOYSA-N 1-(2-bromophenyl)sulfonyl-5-cyclohexyloxy-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)indole Chemical compound C1N(C)CCC(C=2C3=CC(OC4CCCCC4)=CC=C3N(C=2)S(=O)(=O)C=2C(=CC=CC=2)Br)=C1 GBJSCSVGBRFBAK-UHFFFAOYSA-N 0.000 description 5
- RDGLYGKGEAGSEQ-UHFFFAOYSA-N 5-cyclohexyloxy-1-(4-methoxyphenyl)sulfonyl-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)indole Chemical compound C1=CC(OC)=CC=C1S(=O)(=O)N1C2=CC=C(OC3CCCCC3)C=C2C(C=2CCN(C)CC=2)=C1 RDGLYGKGEAGSEQ-UHFFFAOYSA-N 0.000 description 5
- YRKLSYVATYZBNV-UHFFFAOYSA-N 5-cyclohexyloxy-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-1-naphthalen-1-ylsulfonylindole Chemical compound C1N(C)CCC(C=2C3=CC(OC4CCCCC4)=CC=C3N(C=2)S(=O)(=O)C=2C3=CC=CC=C3C=CC=2)=C1 YRKLSYVATYZBNV-UHFFFAOYSA-N 0.000 description 5
- CEKQLOAFHHLVTR-UHFFFAOYSA-N 5-cyclohexyloxy-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-1-naphthalen-2-ylsulfonylindole Chemical compound C1N(C)CCC(C=2C3=CC(OC4CCCCC4)=CC=C3N(C=2)S(=O)(=O)C=2C=C3C=CC=CC3=CC=2)=C1 CEKQLOAFHHLVTR-UHFFFAOYSA-N 0.000 description 5
- LJVVPQKRJWDQSJ-UHFFFAOYSA-N 5-fluoro-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-1-(3-nitrophenyl)sulfonylindole Chemical compound C1N(C)CCC(C=2C3=CC(F)=CC=C3N(C=2)S(=O)(=O)C=2C=C(C=CC=2)[N+]([O-])=O)=C1 LJVVPQKRJWDQSJ-UHFFFAOYSA-N 0.000 description 5
- CCWVHMHEZWALRN-UHFFFAOYSA-N 5-fluoro-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-1-naphthalen-2-ylsulfonylindole Chemical compound C1N(C)CCC(C=2C3=CC(F)=CC=C3N(C=2)S(=O)(=O)C=2C=C3C=CC=CC3=CC=2)=C1 CCWVHMHEZWALRN-UHFFFAOYSA-N 0.000 description 5
- POJVEMDUIHHPTN-UHFFFAOYSA-N 6-bromo-1-(4-fluorophenyl)sulfonyl-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)indole Chemical compound C1N(C)CCC(C=2C3=CC=C(Br)C=C3N(C=2)S(=O)(=O)C=2C=CC(F)=CC=2)=C1 POJVEMDUIHHPTN-UHFFFAOYSA-N 0.000 description 5
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 5
- 239000005557 antagonist Substances 0.000 description 5
- 239000000460 chlorine Substances 0.000 description 5
- 150000003840 hydrochlorides Chemical class 0.000 description 5
- 238000011534 incubation Methods 0.000 description 5
- 239000012442 inert solvent Substances 0.000 description 5
- 239000002609 medium Substances 0.000 description 5
- 238000002360 preparation method Methods 0.000 description 5
- 238000012360 testing method Methods 0.000 description 5
- HUKXPALBUQHURI-UHFFFAOYSA-N 1-(4-bromophenyl)sulfonyl-5-cyclohexyloxy-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)indole Chemical compound C1N(C)CCC(C=2C3=CC(OC4CCCCC4)=CC=C3N(C=2)S(=O)(=O)C=2C=CC(Br)=CC=2)=C1 HUKXPALBUQHURI-UHFFFAOYSA-N 0.000 description 4
- CUFPUJPXSPMOSV-UHFFFAOYSA-N 1-(4-chlorophenyl)sulfonyl-5-cyclohexyloxy-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)indole Chemical compound C1N(C)CCC(C=2C3=CC(OC4CCCCC4)=CC=C3N(C=2)S(=O)(=O)C=2C=CC(Cl)=CC=2)=C1 CUFPUJPXSPMOSV-UHFFFAOYSA-N 0.000 description 4
- CXLPPGQUHADSEC-UHFFFAOYSA-N 1-(4-fluorophenyl)sulfonyl-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-5-(trifluoromethoxy)indole Chemical compound C1N(C)CCC(C=2C3=CC(OC(F)(F)F)=CC=C3N(C=2)S(=O)(=O)C=2C=CC(F)=CC=2)=C1 CXLPPGQUHADSEC-UHFFFAOYSA-N 0.000 description 4
- CPUSZPLZVYECNZ-UHFFFAOYSA-N 1-(4-tert-butylphenyl)sulfonyl-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-5-(trifluoromethoxy)indole Chemical compound C1N(C)CCC(C=2C3=CC(OC(F)(F)F)=CC=C3N(C=2)S(=O)(=O)C=2C=CC(=CC=2)C(C)(C)C)=C1 CPUSZPLZVYECNZ-UHFFFAOYSA-N 0.000 description 4
- YWSVTPLQEHIADB-UHFFFAOYSA-N 1-(4-tert-butylphenyl)sulfonyl-5-cyclohexyloxy-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)indole Chemical compound C1N(C)CCC(C=2C3=CC(OC4CCCCC4)=CC=C3N(C=2)S(=O)(=O)C=2C=CC(=CC=2)C(C)(C)C)=C1 YWSVTPLQEHIADB-UHFFFAOYSA-N 0.000 description 4
- JAPYIBBSTJFDAK-UHFFFAOYSA-N 2,4,6-tri(propan-2-yl)benzenesulfonyl chloride Chemical compound CC(C)C1=CC(C(C)C)=C(S(Cl)(=O)=O)C(C(C)C)=C1 JAPYIBBSTJFDAK-UHFFFAOYSA-N 0.000 description 4
- BXCOSWRSIISQSL-UHFFFAOYSA-N 2,5-dichlorobenzenesulfonyl chloride Chemical compound ClC1=CC=C(Cl)C(S(Cl)(=O)=O)=C1 BXCOSWRSIISQSL-UHFFFAOYSA-N 0.000 description 4
- VFPWGZNNRSQPBT-UHFFFAOYSA-N 2-bromobenzenesulfonyl chloride Chemical compound ClS(=O)(=O)C1=CC=CC=C1Br VFPWGZNNRSQPBT-UHFFFAOYSA-N 0.000 description 4
- KYSCKYJNMTUJPA-UHFFFAOYSA-N 3-(1-methylpiperidin-4-yl)-1h-indole Chemical compound C1CN(C)CCC1C1=CNC2=CC=CC=C12 KYSCKYJNMTUJPA-UHFFFAOYSA-N 0.000 description 4
- MWWNNNAOGWPTQY-UHFFFAOYSA-N 3-nitrobenzenesulfonyl chloride Chemical compound [O-][N+](=O)C1=CC=CC(S(Cl)(=O)=O)=C1 MWWNNNAOGWPTQY-UHFFFAOYSA-N 0.000 description 4
- SEWNAJIUKSTYOP-UHFFFAOYSA-N 4-chloro-3-nitrobenzenesulfonyl chloride Chemical compound [O-][N+](=O)C1=CC(S(Cl)(=O)=O)=CC=C1Cl SEWNAJIUKSTYOP-UHFFFAOYSA-N 0.000 description 4
- NIHPABZCGXPCNX-UHFFFAOYSA-N 5-cyclohexyloxy-1-(4-fluorophenyl)sulfonyl-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)indole Chemical compound C1N(C)CCC(C=2C3=CC(OC4CCCCC4)=CC=C3N(C=2)S(=O)(=O)C=2C=CC(F)=CC=2)=C1 NIHPABZCGXPCNX-UHFFFAOYSA-N 0.000 description 4
- UEISPMVVZNJELF-UHFFFAOYSA-N 5-cyclohexyloxy-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-1-(3-nitrophenyl)sulfonylindole Chemical compound C1N(C)CCC(C=2C3=CC(OC4CCCCC4)=CC=C3N(C=2)S(=O)(=O)C=2C=C(C=CC=2)[N+]([O-])=O)=C1 UEISPMVVZNJELF-UHFFFAOYSA-N 0.000 description 4
- YILDEVIQZDLSGL-UHFFFAOYSA-N 5-cyclohexyloxy-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-1-[3-nitro-4-(trifluoromethyl)phenyl]sulfonylindole Chemical compound C1N(C)CCC(C=2C3=CC(OC4CCCCC4)=CC=C3N(C=2)S(=O)(=O)C=2C=C(C(=CC=2)C(F)(F)F)[N+]([O-])=O)=C1 YILDEVIQZDLSGL-UHFFFAOYSA-N 0.000 description 4
- FIHMHSFARLUHRI-UHFFFAOYSA-N 5-cyclohexyloxy-3-(1-methylpiperidin-4-yl)-1h-indole Chemical compound C1CN(C)CCC1C(C1=C2)=CNC1=CC=C2OC1CCCCC1 FIHMHSFARLUHRI-UHFFFAOYSA-N 0.000 description 4
- QBQNOLXBAYSVNM-UHFFFAOYSA-N 5-fluoro-3-(1-methylpiperidin-4-yl)-1h-indole Chemical compound C1CN(C)CCC1C1=CNC2=CC=C(F)C=C12 QBQNOLXBAYSVNM-UHFFFAOYSA-N 0.000 description 4
- 108091032151 5-hydroxytryptamine receptor family Proteins 0.000 description 4
- YLKWPAQKNZFZNX-UHFFFAOYSA-N 6-bromo-1-(4-methoxyphenyl)sulfonyl-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)indole Chemical compound C1=CC(OC)=CC=C1S(=O)(=O)N1C2=CC(Br)=CC=C2C(C=2CCN(C)CC=2)=C1 YLKWPAQKNZFZNX-UHFFFAOYSA-N 0.000 description 4
- UZUDWBTXINULIE-UHFFFAOYSA-N 6-chloro-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-1h-indole Chemical compound C1N(C)CCC(C=2C3=CC=C(Cl)C=C3NC=2)=C1 UZUDWBTXINULIE-UHFFFAOYSA-N 0.000 description 4
- NACVPZPBIPYRPS-UHFFFAOYSA-N 6-chloro-3-(1-methylpiperidin-4-yl)-1h-indole Chemical compound C1CN(C)CCC1C1=CNC2=CC(Cl)=CC=C12 NACVPZPBIPYRPS-UHFFFAOYSA-N 0.000 description 4
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 4
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 4
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 4
- MZRVEZGGRBJDDB-UHFFFAOYSA-N N-Butyllithium Chemical compound [Li]CCCC MZRVEZGGRBJDDB-UHFFFAOYSA-N 0.000 description 4
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 4
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 4
- 239000000443 aerosol Substances 0.000 description 4
- 239000000556 agonist Substances 0.000 description 4
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 4
- 229910052794 bromium Inorganic materials 0.000 description 4
- 230000000694 effects Effects 0.000 description 4
- 239000012458 free base Substances 0.000 description 4
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 4
- 238000010992 reflux Methods 0.000 description 4
- 239000007787 solid Substances 0.000 description 4
- 239000003826 tablet Substances 0.000 description 4
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 4
- WYNHJUCDIBBCRK-UHFFFAOYSA-N 1-(4-chloro-3-nitrophenyl)sulfonyl-5-cyclohexyloxy-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)indole Chemical compound C1N(C)CCC(C=2C3=CC(OC4CCCCC4)=CC=C3N(C=2)S(=O)(=O)C=2C=C(C(Cl)=CC=2)[N+]([O-])=O)=C1 WYNHJUCDIBBCRK-UHFFFAOYSA-N 0.000 description 3
- HUUPVABNAQUEJW-UHFFFAOYSA-N 1-methylpiperidin-4-one Chemical compound CN1CCC(=O)CC1 HUUPVABNAQUEJW-UHFFFAOYSA-N 0.000 description 3
- 125000006418 4-methylphenylsulfonyl group Chemical group 0.000 description 3
- WZPOGQRJXZGSMH-UHFFFAOYSA-N 5,7-difluoro-1h-indole Chemical compound FC1=CC(F)=C2NC=CC2=C1 WZPOGQRJXZGSMH-UHFFFAOYSA-N 0.000 description 3
- UVGVFOXMUYGAIA-UHFFFAOYSA-N 5-chloro-3-(1-methylpiperidin-4-yl)-1h-indole Chemical compound C1CN(C)CCC1C1=CNC2=CC=C(Cl)C=C12 UVGVFOXMUYGAIA-UHFFFAOYSA-N 0.000 description 3
- NGUBSASZLGYKSY-UHFFFAOYSA-N 5-cyclohexyloxy-1-(2,5-dichlorophenyl)sulfonyl-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)indole Chemical compound C1N(C)CCC(C=2C3=CC(OC4CCCCC4)=CC=C3N(C=2)S(=O)(=O)C=2C(=CC=C(Cl)C=2)Cl)=C1 NGUBSASZLGYKSY-UHFFFAOYSA-N 0.000 description 3
- DOOQYNYDKOUFKX-UHFFFAOYSA-N 5-cyclohexyloxy-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-1-(2,4,6-trimethylphenyl)sulfonylindole Chemical compound C1N(C)CCC(C=2C3=CC(OC4CCCCC4)=CC=C3N(C=2)S(=O)(=O)C=2C(=CC(C)=CC=2C)C)=C1 DOOQYNYDKOUFKX-UHFFFAOYSA-N 0.000 description 3
- HFALWEVWTIGVJK-UHFFFAOYSA-N 5-cyclohexyloxy-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-1-[2,4,6-tri(propan-2-yl)phenyl]sulfonylindole Chemical compound CC(C)C1=CC(C(C)C)=CC(C(C)C)=C1S(=O)(=O)N1C2=CC=C(OC3CCCCC3)C=C2C(C=2CCN(C)CC=2)=C1 HFALWEVWTIGVJK-UHFFFAOYSA-N 0.000 description 3
- 102000014630 G protein-coupled serotonin receptor activity proteins Human genes 0.000 description 3
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 3
- 239000004480 active ingredient Substances 0.000 description 3
- 238000003556 assay Methods 0.000 description 3
- CBHOOMGKXCMKIR-UHFFFAOYSA-N azane;methanol Chemical compound N.OC CBHOOMGKXCMKIR-UHFFFAOYSA-N 0.000 description 3
- 239000002775 capsule Substances 0.000 description 3
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 3
- 238000005859 coupling reaction Methods 0.000 description 3
- 238000010511 deprotection reaction Methods 0.000 description 3
- 208000035475 disorder Diseases 0.000 description 3
- 239000002552 dosage form Substances 0.000 description 3
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 3
- 239000000543 intermediate Substances 0.000 description 3
- 239000007788 liquid Substances 0.000 description 3
- 239000012528 membrane Substances 0.000 description 3
- 229910052751 metal Inorganic materials 0.000 description 3
- 239000002184 metal Substances 0.000 description 3
- 150000007522 mineralic acids Chemical class 0.000 description 3
- 150000007524 organic acids Chemical class 0.000 description 3
- 229910052697 platinum Inorganic materials 0.000 description 3
- 229940076279 serotonin Drugs 0.000 description 3
- 239000012679 serum free medium Substances 0.000 description 3
- 239000000741 silica gel Substances 0.000 description 3
- 229910002027 silica gel Inorganic materials 0.000 description 3
- 238000010561 standard procedure Methods 0.000 description 3
- 208000024891 symptom Diseases 0.000 description 3
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 3
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 3
- ACTVJANMKLGALF-UHFFFAOYSA-N 1-(4-methoxyphenyl)sulfonyl-3-(1-methyl-3,6-dihydro-2H-pyridin-4-yl)-5-(trifluoromethoxy)indole Chemical compound COC1=CC=C(C=C1)S(=O)(=O)N1C=C(C2=CC(=CC=C12)OC(F)(F)F)C=1CCN(CC=1)C ACTVJANMKLGALF-UHFFFAOYSA-N 0.000 description 2
- LLHGZQNIHTVMHZ-UHFFFAOYSA-N 1-(4-tert-butylphenyl)sulfonyl-4-fluoro-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)indole Chemical compound C1N(C)CCC(C=2C3=C(F)C=CC=C3N(C=2)S(=O)(=O)C=2C=CC(=CC=2)C(C)(C)C)=C1 LLHGZQNIHTVMHZ-UHFFFAOYSA-N 0.000 description 2
- MINLLGMYMCKNKJ-UHFFFAOYSA-N 1-(4-tert-butylphenyl)sulfonyl-5-fluoro-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)indole Chemical compound C1N(C)CCC(C=2C3=CC(F)=CC=C3N(C=2)S(=O)(=O)C=2C=CC(=CC=2)C(C)(C)C)=C1 MINLLGMYMCKNKJ-UHFFFAOYSA-N 0.000 description 2
- NGYQNOJBJMUUDF-UHFFFAOYSA-N 1-(benzenesulfonyl)-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)indole Chemical compound C1N(C)CCC(C=2C3=CC=CC=C3N(C=2)S(=O)(=O)C=2C=CC=CC=2)=C1 NGYQNOJBJMUUDF-UHFFFAOYSA-N 0.000 description 2
- COILYGISKGVZAT-UHFFFAOYSA-N 2-(4-methoxyphenyl)sulfonyl-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-5-(trifluoromethoxy)-1h-indole Chemical compound C1=CC(OC)=CC=C1S(=O)(=O)C1=C(C=2CCN(C)CC=2)C2=CC(OC(F)(F)F)=CC=C2N1 COILYGISKGVZAT-UHFFFAOYSA-N 0.000 description 2
- DWLZJKNCWVJFOO-UHFFFAOYSA-N 2-sulfonylindole Chemical compound C1=CC=CC2=NC(=S(=O)=O)C=C21 DWLZJKNCWVJFOO-UHFFFAOYSA-N 0.000 description 2
- OFCNTYBPPAQCRE-UHFFFAOYSA-N 3-(2-aminoethyl)-3h-indol-5-ol Chemical compound C1=C(O)C=C2C(CCN)C=NC2=C1 OFCNTYBPPAQCRE-UHFFFAOYSA-N 0.000 description 2
- GDJPESFQLZUZMS-UHFFFAOYSA-N 3-nitro-4-(trifluoromethyl)benzenesulfonyl chloride Chemical compound [O-][N+](=O)C1=CC(S(Cl)(=O)=O)=CC=C1C(F)(F)F GDJPESFQLZUZMS-UHFFFAOYSA-N 0.000 description 2
- FJKROLUGYXJWQN-UHFFFAOYSA-N 4-hydroxybenzoic acid Chemical compound OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 2
- LCFDJWUYKUPBJM-UHFFFAOYSA-N 5-(trifluoromethyl)-1h-indole Chemical compound FC(F)(F)C1=CC=C2NC=CC2=C1 LCFDJWUYKUPBJM-UHFFFAOYSA-N 0.000 description 2
- MYTGFBZJLDLWQG-UHFFFAOYSA-N 5-chloro-1h-indole Chemical compound ClC1=CC=C2NC=CC2=C1 MYTGFBZJLDLWQG-UHFFFAOYSA-N 0.000 description 2
- SVAZZDDFPRCYEP-UHFFFAOYSA-N 5-fluoro-1-(4-fluorophenyl)sulfonyl-3-(1-methylpiperidin-4-yl)indole Chemical compound C1CN(C)CCC1C1=CN(S(=O)(=O)C=2C=CC(F)=CC=2)C2=CC=C(F)C=C12 SVAZZDDFPRCYEP-UHFFFAOYSA-N 0.000 description 2
- ODFFPRGJZRXNHZ-UHFFFAOYSA-N 5-fluoroindole Chemical compound FC1=CC=C2NC=CC2=C1 ODFFPRGJZRXNHZ-UHFFFAOYSA-N 0.000 description 2
- LMIQERWZRIFWNZ-UHFFFAOYSA-N 5-hydroxyindole Chemical compound OC1=CC=C2NC=CC2=C1 LMIQERWZRIFWNZ-UHFFFAOYSA-N 0.000 description 2
- YTYIMDRWPTUAHP-UHFFFAOYSA-N 6-Chloroindole Chemical compound ClC1=CC=C2C=CNC2=C1 YTYIMDRWPTUAHP-UHFFFAOYSA-N 0.000 description 2
- MAWGHOPSCKCTPA-UHFFFAOYSA-N 6-bromo-1h-indole Chemical compound BrC1=CC=C2C=CNC2=C1 MAWGHOPSCKCTPA-UHFFFAOYSA-N 0.000 description 2
- ONXIWBNOVOJCCN-UHFFFAOYSA-N 6-chloro-1-(4-fluorophenyl)sulfonyl-3-(1-methylpiperidin-4-yl)indole Chemical compound C1CN(C)CCC1C1=CN(S(=O)(=O)C=2C=CC(F)=CC=2)C2=CC(Cl)=CC=C12 ONXIWBNOVOJCCN-UHFFFAOYSA-N 0.000 description 2
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 2
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 2
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 2
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 2
- 102000004190 Enzymes Human genes 0.000 description 2
- 108090000790 Enzymes Proteins 0.000 description 2
- AEMRFAOFKBGASW-UHFFFAOYSA-N Glycolic acid Chemical compound OCC(O)=O AEMRFAOFKBGASW-UHFFFAOYSA-N 0.000 description 2
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 2
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 2
- 102000003992 Peroxidases Human genes 0.000 description 2
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 2
- 239000002202 Polyethylene glycol Substances 0.000 description 2
- LCTONWCANYUPML-UHFFFAOYSA-N Pyruvic acid Chemical compound CC(=O)C(O)=O LCTONWCANYUPML-UHFFFAOYSA-N 0.000 description 2
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 2
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 2
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 2
- GDCXPPXOHLRQSD-UHFFFAOYSA-N [5-fluoro-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)indol-1-yl]-phenylmethanone Chemical compound C1N(C)CCC(C=2C3=CC(F)=CC=C3N(C(=O)C=3C=CC=CC=3)C=2)=C1 GDCXPPXOHLRQSD-UHFFFAOYSA-N 0.000 description 2
- 230000002378 acidificating effect Effects 0.000 description 2
- 150000007513 acids Chemical class 0.000 description 2
- 230000001476 alcoholic effect Effects 0.000 description 2
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 2
- 150000001412 amines Chemical class 0.000 description 2
- 239000003125 aqueous solvent Substances 0.000 description 2
- 239000012298 atmosphere Substances 0.000 description 2
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 2
- 239000003054 catalyst Substances 0.000 description 2
- 235000010980 cellulose Nutrition 0.000 description 2
- 229920002678 cellulose Polymers 0.000 description 2
- 229910052801 chlorine Inorganic materials 0.000 description 2
- 238000004440 column chromatography Methods 0.000 description 2
- 230000008878 coupling Effects 0.000 description 2
- 238000010168 coupling process Methods 0.000 description 2
- HPXRVTGHNJAIIH-UHFFFAOYSA-N cyclohexanol Chemical compound OC1CCCCC1 HPXRVTGHNJAIIH-UHFFFAOYSA-N 0.000 description 2
- 125000002933 cyclohexyloxy group Chemical group C1(CCCCC1)O* 0.000 description 2
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 2
- 239000006185 dispersion Substances 0.000 description 2
- 239000006196 drop Substances 0.000 description 2
- 238000002474 experimental method Methods 0.000 description 2
- 239000012894 fetal calf serum Substances 0.000 description 2
- 238000001914 filtration Methods 0.000 description 2
- 238000003818 flash chromatography Methods 0.000 description 2
- 125000001153 fluoro group Chemical group F* 0.000 description 2
- 238000009472 formulation Methods 0.000 description 2
- 239000001530 fumaric acid Substances 0.000 description 2
- 239000007903 gelatin capsule Substances 0.000 description 2
- 235000011187 glycerol Nutrition 0.000 description 2
- 229940093915 gynecological organic acid Drugs 0.000 description 2
- 239000001257 hydrogen Substances 0.000 description 2
- 238000005984 hydrogenation reaction Methods 0.000 description 2
- SUMDYPCJJOFFON-UHFFFAOYSA-N isethionic acid Chemical compound OCCS(O)(=O)=O SUMDYPCJJOFFON-UHFFFAOYSA-N 0.000 description 2
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 2
- ZCSHNCUQKCANBX-UHFFFAOYSA-N lithium diisopropylamide Chemical compound [Li+].CC(C)[N-]C(C)C ZCSHNCUQKCANBX-UHFFFAOYSA-N 0.000 description 2
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 2
- 231100000252 nontoxic Toxicity 0.000 description 2
- 230000003000 nontoxic effect Effects 0.000 description 2
- 235000005985 organic acids Nutrition 0.000 description 2
- 239000012044 organic layer Substances 0.000 description 2
- 229910052763 palladium Inorganic materials 0.000 description 2
- NFHFRUOZVGFOOS-UHFFFAOYSA-N palladium;triphenylphosphane Chemical compound [Pd].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 NFHFRUOZVGFOOS-UHFFFAOYSA-N 0.000 description 2
- 238000007911 parenteral administration Methods 0.000 description 2
- 108040007629 peroxidase activity proteins Proteins 0.000 description 2
- 125000000951 phenoxy group Chemical group [H]C1=C([H])C([H])=C(O*)C([H])=C1[H] 0.000 description 2
- 239000002953 phosphate buffered saline Substances 0.000 description 2
- 229920001223 polyethylene glycol Polymers 0.000 description 2
- 229910000027 potassium carbonate Inorganic materials 0.000 description 2
- 239000003380 propellant Substances 0.000 description 2
- 238000000746 purification Methods 0.000 description 2
- 239000002287 radioligand Substances 0.000 description 2
- 239000011541 reaction mixture Substances 0.000 description 2
- YGSDEFSMJLZEOE-UHFFFAOYSA-N salicylic acid Chemical compound OC(=O)C1=CC=CC=C1O YGSDEFSMJLZEOE-UHFFFAOYSA-N 0.000 description 2
- 239000003751 serotonin 6 antagonist Substances 0.000 description 2
- 239000000377 silicon dioxide Substances 0.000 description 2
- 239000011734 sodium Substances 0.000 description 2
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 2
- 235000017557 sodium bicarbonate Nutrition 0.000 description 2
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 2
- QAEDZJGFFMLHHQ-UHFFFAOYSA-N trifluoroacetic anhydride Chemical compound FC(F)(F)C(=O)OC(=O)C(F)(F)F QAEDZJGFFMLHHQ-UHFFFAOYSA-N 0.000 description 2
- RIOQSEWOXXDEQQ-UHFFFAOYSA-N triphenylphosphine Chemical compound C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 RIOQSEWOXXDEQQ-UHFFFAOYSA-N 0.000 description 2
- 238000010792 warming Methods 0.000 description 2
- BJEPYKJPYRNKOW-REOHCLBHSA-N (S)-malic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O BJEPYKJPYRNKOW-REOHCLBHSA-N 0.000 description 1
- UWYVPFMHMJIBHE-OWOJBTEDSA-N (e)-2-hydroxybut-2-enedioic acid Chemical compound OC(=O)\C=C(\O)C(O)=O UWYVPFMHMJIBHE-OWOJBTEDSA-N 0.000 description 1
- 0 *c1c(C2CCN(*)CC2)c(c(*)c(*=C)c(*)c2*)c2[n]1[Al] Chemical compound *c1c(C2CCN(*)CC2)c(c(*)c(*=C)c(*)c2*)c2[n]1[Al] 0.000 description 1
- WBYWAXJHAXSJNI-VOTSOKGWSA-M .beta-Phenylacrylic acid Natural products [O-]C(=O)\C=C\C1=CC=CC=C1 WBYWAXJHAXSJNI-VOTSOKGWSA-M 0.000 description 1
- AVFZOVWCLRSYKC-UHFFFAOYSA-N 1-methylpyrrolidine Chemical compound CN1CCCC1 AVFZOVWCLRSYKC-UHFFFAOYSA-N 0.000 description 1
- IIZPXYDJLKNOIY-JXPKJXOSSA-N 1-palmitoyl-2-arachidonoyl-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCC\C=C/C\C=C/C\C=C/C\C=C/CCCCC IIZPXYDJLKNOIY-JXPKJXOSSA-N 0.000 description 1
- RJXOVESYJFXCGI-UHFFFAOYSA-N 2,4-difluoro-1-nitrobenzene Chemical compound [O-][N+](=O)C1=CC=C(F)C=C1F RJXOVESYJFXCGI-UHFFFAOYSA-N 0.000 description 1
- JGYMIVIOMGCKTM-UHFFFAOYSA-N 2,4-difluoro-1h-indole Chemical compound C1=CC=C2NC(F)=CC2=C1F JGYMIVIOMGCKTM-UHFFFAOYSA-N 0.000 description 1
- PKRSYEPBQPFNRB-UHFFFAOYSA-N 2-phenoxybenzoic acid Chemical compound OC(=O)C1=CC=CC=C1OC1=CC=CC=C1 PKRSYEPBQPFNRB-UHFFFAOYSA-N 0.000 description 1
- WLJVXDMOQOGPHL-PPJXEINESA-N 2-phenylacetic acid Chemical compound O[14C](=O)CC1=CC=CC=C1 WLJVXDMOQOGPHL-PPJXEINESA-N 0.000 description 1
- YRNWIFYIFSBPAU-UHFFFAOYSA-N 4-[4-(dimethylamino)phenyl]-n,n-dimethylaniline Chemical compound C1=CC(N(C)C)=CC=C1C1=CC=C(N(C)C)C=C1 YRNWIFYIFSBPAU-UHFFFAOYSA-N 0.000 description 1
- 125000004172 4-methoxyphenyl group Chemical group [H]C1=C([H])C(OC([H])([H])[H])=C([H])C([H])=C1* 0.000 description 1
- XHAJMVPMNOBILF-UHFFFAOYSA-N 5-(trifluoromethoxy)-1h-indole-2,3-dione Chemical compound FC(F)(F)OC1=CC=C2NC(=O)C(=O)C2=C1 XHAJMVPMNOBILF-UHFFFAOYSA-N 0.000 description 1
- VXWVFZFZYXOBTA-UHFFFAOYSA-N 5-bromo-1h-indole Chemical compound BrC1=CC=C2NC=CC2=C1 VXWVFZFZYXOBTA-UHFFFAOYSA-N 0.000 description 1
- IRJNNZSKGXPISD-UHFFFAOYSA-N 5-bromo-3-(1-methyl-3,6-dihydro-2h-pyridin-4-yl)-1h-indole Chemical compound C1N(C)CCC(C=2C3=CC(Br)=CC=C3NC=2)=C1 IRJNNZSKGXPISD-UHFFFAOYSA-N 0.000 description 1
- 102000040125 5-hydroxytryptamine receptor family Human genes 0.000 description 1
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 1
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 1
- 241000416162 Astragalus gummifer Species 0.000 description 1
- 239000005711 Benzoic acid Substances 0.000 description 1
- WBYWAXJHAXSJNI-SREVYHEPSA-N Cinnamic acid Chemical compound OC(=O)\C=C/C1=CC=CC=C1 WBYWAXJHAXSJNI-SREVYHEPSA-N 0.000 description 1
- 229910020323 ClF3 Inorganic materials 0.000 description 1
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- 229910021589 Copper(I) bromide Inorganic materials 0.000 description 1
- 206010012239 Delusion Diseases 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 1
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 1
- 238000011891 EIA kit Methods 0.000 description 1
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- 102000018899 Glutamate Receptors Human genes 0.000 description 1
- 108010027915 Glutamate Receptors Proteins 0.000 description 1
- 208000004547 Hallucinations Diseases 0.000 description 1
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- 235000010643 Leucaena leucocephala Nutrition 0.000 description 1
- 240000007472 Leucaena leucocephala Species 0.000 description 1
- AHVYPIQETPWLSZ-UHFFFAOYSA-N N-methyl-pyrrolidine Natural products CN1CC=CC1 AHVYPIQETPWLSZ-UHFFFAOYSA-N 0.000 description 1
- 102000003840 Opioid Receptors Human genes 0.000 description 1
- 108090000137 Opioid Receptors Proteins 0.000 description 1
- 102000016979 Other receptors Human genes 0.000 description 1
- 235000019483 Peanut oil Nutrition 0.000 description 1
- 239000004793 Polystyrene Substances 0.000 description 1
- OFOBLEOULBTSOW-UHFFFAOYSA-N Propanedioic acid Natural products OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 1
- 229910018105 SCl2 Inorganic materials 0.000 description 1
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 1
- 229920001615 Tragacanth Polymers 0.000 description 1
- NPKCKCVQUHCEEI-UHFFFAOYSA-N [N].N1CCCC=C1 Chemical compound [N].N1CCCC=C1 NPKCKCVQUHCEEI-UHFFFAOYSA-N 0.000 description 1
- ZXYNGLRGFYLTQZ-UHFFFAOYSA-M [Zn]Cl Chemical compound [Zn]Cl ZXYNGLRGFYLTQZ-UHFFFAOYSA-M 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 102000030621 adenylate cyclase Human genes 0.000 description 1
- 108060000200 adenylate cyclase Proteins 0.000 description 1
- 239000002671 adjuvant Substances 0.000 description 1
- 239000004479 aerosol dispenser Substances 0.000 description 1
- 229910001854 alkali hydroxide Inorganic materials 0.000 description 1
- 150000008044 alkali metal hydroxides Chemical class 0.000 description 1
- 125000004453 alkoxycarbonyl group Chemical group 0.000 description 1
- 125000004448 alkyl carbonyl group Chemical group 0.000 description 1
- BJEPYKJPYRNKOW-UHFFFAOYSA-N alpha-hydroxysuccinic acid Natural products OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 1
- 239000003708 ampul Substances 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 229940054051 antipsychotic indole derivative Drugs 0.000 description 1
- 239000008365 aqueous carrier Substances 0.000 description 1
- 239000012223 aqueous fraction Substances 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- YCOXTKKNXUZSKD-UHFFFAOYSA-N as-o-xylenol Natural products CC1=CC=C(O)C=C1C YCOXTKKNXUZSKD-UHFFFAOYSA-N 0.000 description 1
- 235000010323 ascorbic acid Nutrition 0.000 description 1
- 239000011668 ascorbic acid Substances 0.000 description 1
- 229960005070 ascorbic acid Drugs 0.000 description 1
- 125000004429 atom Chemical group 0.000 description 1
- 230000006399 behavior Effects 0.000 description 1
- CSKNSYBAZOQPLR-UHFFFAOYSA-N benzenesulfonyl chloride Chemical compound ClS(=O)(=O)C1=CC=CC=C1 CSKNSYBAZOQPLR-UHFFFAOYSA-N 0.000 description 1
- 235000010233 benzoic acid Nutrition 0.000 description 1
- PASDCCFISLVPSO-UHFFFAOYSA-N benzoyl chloride Chemical compound ClC(=O)C1=CC=CC=C1 PASDCCFISLVPSO-UHFFFAOYSA-N 0.000 description 1
- 239000012267 brine Substances 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 230000001593 cAMP accumulation Effects 0.000 description 1
- 230000003491 cAMP production Effects 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 230000003197 catalytic effect Effects 0.000 description 1
- 206010007776 catatonia Diseases 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 208000015114 central nervous system disease Diseases 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- 239000003638 chemical reducing agent Substances 0.000 description 1
- KYKAJFCTULSVSH-UHFFFAOYSA-N chloro(fluoro)methane Chemical compound F[C]Cl KYKAJFCTULSVSH-UHFFFAOYSA-N 0.000 description 1
- 235000013985 cinnamic acid Nutrition 0.000 description 1
- 229930016911 cinnamic acid Natural products 0.000 description 1
- 235000015165 citric acid Nutrition 0.000 description 1
- 238000010367 cloning Methods 0.000 description 1
- QZUDBNBUXVUHMW-UHFFFAOYSA-N clozapine Chemical compound C1CN(C)CCN1C1=NC2=CC(Cl)=CC=C2NC2=CC=CC=C12 QZUDBNBUXVUHMW-UHFFFAOYSA-N 0.000 description 1
- 229960004170 clozapine Drugs 0.000 description 1
- 229940110456 cocoa butter Drugs 0.000 description 1
- 235000019868 cocoa butter Nutrition 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 230000021615 conjugation Effects 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- NKNDPYCGAZPOFS-UHFFFAOYSA-M copper(i) bromide Chemical compound Br[Cu] NKNDPYCGAZPOFS-UHFFFAOYSA-M 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- 231100000868 delusion Toxicity 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 201000010099 disease Diseases 0.000 description 1
- BNIILDVGGAEEIG-UHFFFAOYSA-L disodium hydrogen phosphate Chemical compound [Na+].[Na+].OP([O-])([O-])=O BNIILDVGGAEEIG-UHFFFAOYSA-L 0.000 description 1
- 239000002270 dispersing agent Substances 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 238000005538 encapsulation Methods 0.000 description 1
- YFXCNIVBAVFOBX-UHFFFAOYSA-N ethenylboronic acid Chemical compound OB(O)C=C YFXCNIVBAVFOBX-UHFFFAOYSA-N 0.000 description 1
- 239000000706 filtrate Substances 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 235000011087 fumaric acid Nutrition 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 239000000499 gel Substances 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 229930195712 glutamate Natural products 0.000 description 1
- 239000001963 growth medium Substances 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 238000003018 immunoassay Methods 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- 230000002401 inhibitory effect Effects 0.000 description 1
- 238000011221 initial treatment Methods 0.000 description 1
- PNDPGZBMCMUPRI-UHFFFAOYSA-N iodine Chemical compound II PNDPGZBMCMUPRI-UHFFFAOYSA-N 0.000 description 1
- SNHMUERNLJLMHN-UHFFFAOYSA-N iodobenzene Chemical compound IC1=CC=CC=C1 SNHMUERNLJLMHN-UHFFFAOYSA-N 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 239000004310 lactic acid Substances 0.000 description 1
- 235000014655 lactic acid Nutrition 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 239000000787 lecithin Substances 0.000 description 1
- 235000010445 lecithin Nutrition 0.000 description 1
- 229940067606 lecithin Drugs 0.000 description 1
- 239000012669 liquid formulation Substances 0.000 description 1
- 239000012280 lithium aluminium hydride Substances 0.000 description 1
- 239000007937 lozenge Substances 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- RMGJCSHZTFKPNO-UHFFFAOYSA-M magnesium;ethene;bromide Chemical compound [Mg+2].[Br-].[CH-]=C RMGJCSHZTFKPNO-UHFFFAOYSA-M 0.000 description 1
- 238000011418 maintenance treatment Methods 0.000 description 1
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 1
- 239000011976 maleic acid Substances 0.000 description 1
- 239000001630 malic acid Substances 0.000 description 1
- 235000011090 malic acid Nutrition 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 229910052987 metal hydride Inorganic materials 0.000 description 1
- 150000004681 metal hydrides Chemical class 0.000 description 1
- 229940098779 methanesulfonic acid Drugs 0.000 description 1
- WBYWAXJHAXSJNI-UHFFFAOYSA-N methyl p-hydroxycinnamate Natural products OC(=O)C=CC1=CC=CC=C1 WBYWAXJHAXSJNI-UHFFFAOYSA-N 0.000 description 1
- 230000001722 neurochemical effect Effects 0.000 description 1
- 238000002414 normal-phase solid-phase extraction Methods 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- 150000003891 oxalate salts Chemical class 0.000 description 1
- 238000010651 palladium-catalyzed cross coupling reaction Methods 0.000 description 1
- 239000000312 peanut oil Substances 0.000 description 1
- 239000008188 pellet Substances 0.000 description 1
- 239000000546 pharmaceutical excipient Substances 0.000 description 1
- 125000003386 piperidinyl group Chemical group 0.000 description 1
- 239000011505 plaster Substances 0.000 description 1
- 229920002223 polystyrene Polymers 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- CHKVPAROMQMJNQ-UHFFFAOYSA-M potassium bisulfate Chemical compound [K+].OS([O-])(=O)=O CHKVPAROMQMJNQ-UHFFFAOYSA-M 0.000 description 1
- 229910000343 potassium bisulfate Inorganic materials 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 230000002335 preservative effect Effects 0.000 description 1
- 208000020016 psychiatric disease Diseases 0.000 description 1
- 229940107700 pyruvic acid Drugs 0.000 description 1
- 229960004889 salicylic acid Drugs 0.000 description 1
- 208000022610 schizoaffective disease Diseases 0.000 description 1
- 239000008159 sesame oil Substances 0.000 description 1
- 235000011803 sesame oil Nutrition 0.000 description 1
- 238000007086 side reaction Methods 0.000 description 1
- 150000004760 silicates Chemical class 0.000 description 1
- 229910000029 sodium carbonate Inorganic materials 0.000 description 1
- 229910052938 sodium sulfate Inorganic materials 0.000 description 1
- 235000011152 sodium sulphate Nutrition 0.000 description 1
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 1
- 238000004611 spectroscopical analysis Methods 0.000 description 1
- 238000004544 sputter deposition Methods 0.000 description 1
- 229910000080 stannane Inorganic materials 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 108010028621 stem cell inhibitory factor Proteins 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 235000000346 sugar Nutrition 0.000 description 1
- 150000003460 sulfonic acids Chemical class 0.000 description 1
- YBBRCQOCSYXUOC-UHFFFAOYSA-N sulfuryl dichloride Chemical class ClS(Cl)(=O)=O YBBRCQOCSYXUOC-UHFFFAOYSA-N 0.000 description 1
- 239000006228 supernatant Substances 0.000 description 1
- 239000000829 suppository Substances 0.000 description 1
- 239000002511 suppository base Substances 0.000 description 1
- 239000000375 suspending agent Substances 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 239000006188 syrup Substances 0.000 description 1
- 235000020357 syrup Nutrition 0.000 description 1
- 239000011975 tartaric acid Substances 0.000 description 1
- 235000002906 tartaric acid Nutrition 0.000 description 1
- DYHSDKLCOJIUFX-UHFFFAOYSA-N tert-butoxycarbonyl anhydride Chemical compound CC(C)(C)OC(=O)OC(=O)OC(C)(C)C DYHSDKLCOJIUFX-UHFFFAOYSA-N 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 239000000196 tragacanth Substances 0.000 description 1
- 235000010487 tragacanth Nutrition 0.000 description 1
- 229940116362 tragacanth Drugs 0.000 description 1
- 150000003628 tricarboxylic acids Chemical class 0.000 description 1
- ITMCEJHCFYSIIV-UHFFFAOYSA-M triflate Chemical compound [O-]S(=O)(=O)C(F)(F)F ITMCEJHCFYSIIV-UHFFFAOYSA-M 0.000 description 1
- 238000003828 vacuum filtration Methods 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P21/00—Drugs for disorders of the muscular or neuromuscular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
- A61P25/16—Anti-Parkinson drugs
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/18—Antipsychotics, i.e. neuroleptics; Drugs for mania or schizophrenia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/22—Anxiolytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/24—Antidepressants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
Landscapes
- Health & Medical Sciences (AREA)
- Organic Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Neurology (AREA)
- Veterinary Medicine (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- General Chemical & Material Sciences (AREA)
- Biomedical Technology (AREA)
- Neurosurgery (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Psychiatry (AREA)
- Hospice & Palliative Care (AREA)
- Pain & Pain Management (AREA)
- Psychology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Physical Education & Sports Medicine (AREA)
- Plural Heterocyclic Compounds (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Indole Compounds (AREA)
- Hydrogenated Pyridines (AREA)
Description
- Diese Erfindung bezieht sich auf Indolverbindungen mit einer Affinität für den Serotonin-5-HT6-Rezeptor, auf pharmazeutische Zusammensetzungen, die sie enthalten, und auf ihre medizinische Verwendung, insbesondere bei der Behandlung von ZNS-Leiden.
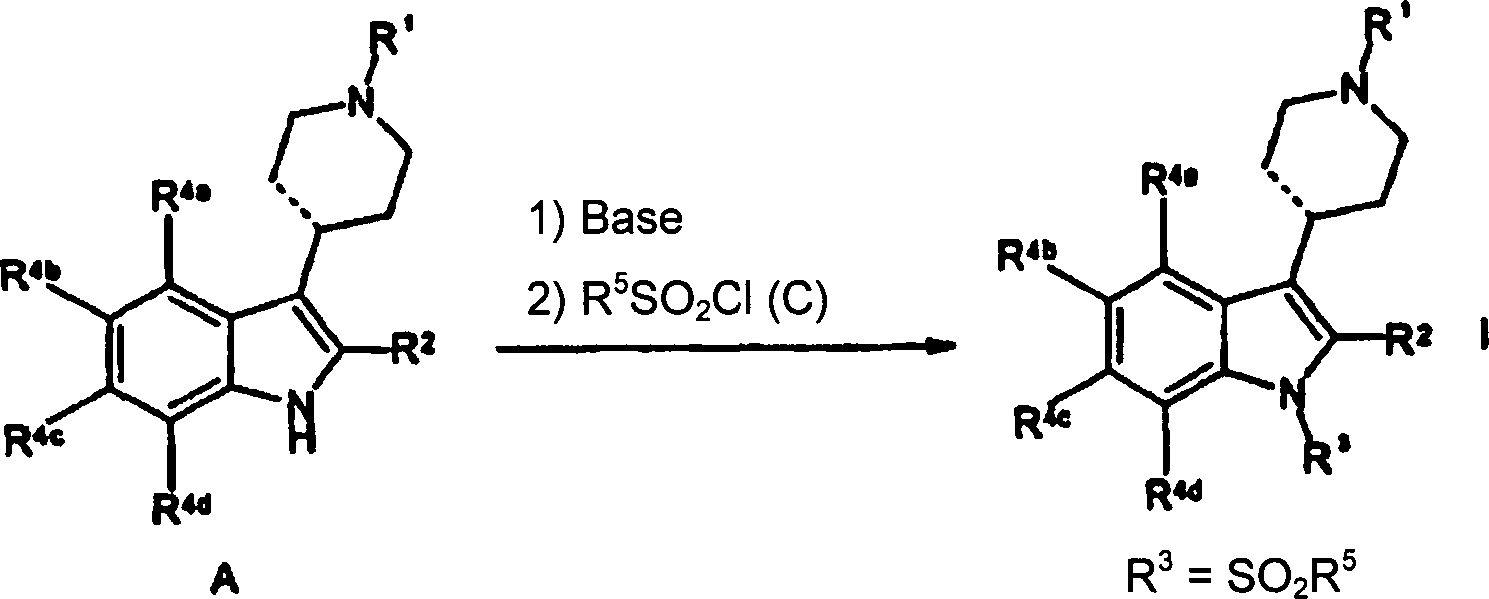
- Gemäß einem Aspekt der Erfindung werden Verbindungen der Formel I und Salze, Solvate oder Hydrate davon bereitgestellt: worin:
R1 ausgewählt ist aus der Gruppe bestehend aus H und C1-4-Alkyl;
R2 ausgewählt ist aus der Gruppe bestehend aus H, C1-4-Alkyl und Benzyl;
--- eine Einfach- oder Doppelbindung bedeutet;
R3 SO2R5 bedeutet;
R4a ausgewählt ist aus der Gruppe bestehend aus H, OH, Halogen, C1-4-Alkyl und C1-4-Alkoxy;
R4b ausgewählt ist aus der Gruppe bestehend aus H, Hydroxy, Halogen, C3-7-Cycloalkyloxy, C1-4-Alkoxy, C1-4-Alkyl, Benzyloxy, Phenoxy, Trifluormethyl, Trifluormethoxy und Vinyl;
R4c ausgewählt ist aus der Gruppe bestehend aus H, OH, Halogen, C1-4-Alkyl und C1-4-Alkoxy;
R4d ausgewählt ist aus der Gruppe bestehend aus H, OH, Halogen, C1-4-Alkyl und C1-4-Alkoxy; und
R5 ausgewählt ist aus der Gruppe bestehend aus Phenyl, Pyridyl, Thienyl, Chinolinyl und Naphthyl, welche gegebenenfalls substituiert sind mit 1-4 Substituenten, ausgewählt aus C1-4-Alkoxy, C1-4-Alkyl, Halogen, Nitro, Trifluormethyl, Trifluormethoxy, 1,2-Methylendioxy, C1-4-Alkylcarbonyl, C1-4-Alkoxycarbonyl und C1-4-AlkylS-. - Gemäß einem weiteren Aspekt der Erfindung wird eine pharmazeutische Zusammensetzung bereitgestellt, die eine Verbindung der Formel I in einer Menge, die den 5-HT6-Rezeptor wirksam antagonisiert, und einen pharmazeutisch annehmbaren Träger umfasst.
- In einem weiteren Aspekt der vorliegenden Erfindung werden Zusammensetzungen bereitgestellt, welche die Verbindungen der vorliegenden Erfindung in Mengen zur pharmazeutischen Verwendung zum Behandeln von ZNS-Zuständen bzw. Leiden, bei denen ein 5-HT6-Ligand beteiligt ist, enthalten, z. B. für die Behandlung oder Verhütung von Störungen des Zentralnervensystems wie eine Psychose, Schizophrenie, manische Depression, Depression, neurologische Störungen, Gedächtnisstörungen, die Parkinson-Krankheit, die amyotrophe Lateralsklerose, die Alzheimer-Krankheit und Chorea Huntington. Diese und andere Aspekte der vorliegenden Erfindung werden nachstehend ausführlicher beschrieben.
- Zum Stand der Technik, welcher Indolderivate, die eine neurochemische inhibitorische Aktivität aufweisen oder anderweitig für 5HT-Rezeptoren relevant sind, offenbart, gehören die folgenden:
-
WO-A-97/47302 -
EP-A-0200322 -
EP-A-0465398 -
WO-A-92/13856 - Mol. Pharmacol. 43, 320 (1993)
- Med. Chem. Res. 4, 16 (1964)
- Exp. Opin. Ther. Patents 8, 1217 (1998)
- Trends Pharmacol. Sci. 19, 2 (1998)
- Neuropharmacol. 36, 419 (1994)
- Pharmacol. Rev. 46, 157 (1992)
- Der Begriff "Halo" bedeutet so, wie er in dieser Anmeldung verwendet wird, Halogen und schließt Fluor, Chlor, Brom und dergleichen ein.
- Der Begriff "pharmazeutisch annehmbares Salz" bedeutet ein Säureadditionssalz, welches mit der Behandlung von Patienten vereinbar ist.
- Ein "pharmazeutisch annehmbares Säureadditionssalz" ist ein beliebiges nicht-toxisches organisches oder anorganisches Säureadditionssalz der Basenverbindungen, die durch Formel I wiedergegeben werden, oder ein beliebiges Zwischenprodukt davon. Zu beispielhaften anorganischen Säuren, welche geeignete Salze bilden, gehören Chlorwasserstoffsäure, Bromwasserstoffsäure, Schwefelsäure und Phosphorsäure und saure Metallsalze wie Natrium monohydrogenorthophosphat und Kalium hydrogensulfat. Zu beispielhaften organischen Säuren, welche geeignete Salze bilden, gehören die Mono-, Di- und Tricarbonsäuren. Beispielhaft für solche Säuren sind z. B. Essigsäure, Glycolsäure, Milchsäure, Brenztraubensäure, Malonsäure, Bernsteinsäure, Glutarsäure, Fumarsäure, Äpfelsäure, Weinsäure, Citronensäure, Ascorbinsäure, Maleinsäure, Hydroxymaleinsäure, Benzoesäure, Hydroxybenzoesäure, Phenylessigsäure, Zimtsäure, Salicylsäure, 2-Phenoxybenzoesäure, p-Toluolsulfonsäure und andere Sulfonsäuren wie Methansulfonsäure und 2-Hydroxyethansulfonsäure. Entweder die Mono- oder Disäuresalze können gebildet werden und solche Salze können entweder in einer hydratisierten, solvatisierten oder im Wesentlichen wasserfreien Form vorkommen. Im Allgemeinen sind die Säureadditionssalze von diesen Verbindungen in Wasser und verschiedenen hydrophilen organischen Lösungsmitteln besser löslich und weisen im Allgemeinen höhere Schmelzpunkte im Vergleich zu ihren Freie-Base-Formen auf. Die Auswahlkriterien für das geeignete Salz sind dem Fachmann bekannt.
- "Solvat" bedeutet eine Verbindung der Formel I oder das pharmazeutisch annehmbare Salz von einer Verbindung der Formel I, worin Moleküle eines geeigneten Lösungsmittels in einem Kristallgitter eingebaut sind. Ein geeignetes Lösungsmittel ist bei der als das Solvat verabreichten Dosierung physiologisch tolerierbar. Beispiele für geeignete Lösungsmittel sind Ethanol und dergleichen.
- Der Begriff "Stereoisomere" ist ein allgemeiner Begriff für alle Isomere der einzelnen Moleküle, welche sich nur durch die Orientierung ihrer Atome im Raum unterscheiden. Er schließt Spiegelbildisomere (Enantiomere), geometrische (cis/trans) Isomere und Isomere von Verbindungen mit mehr als einem chiralen Zentrum, welche nicht Spiegelbilder voneinander sind, (Diastereomere) ein.
- Der Begriff "behandelt" oder "behandeln" bedeutet das Lindern von Symptomen, das Beseitigen der Ursache der Symptome entweder auf einer temporären oder permanenten Basis oder das Verhüten oder Verlangsamen des Auftretens von Symptomen der genannten Störung oder des genannten Zustands bzw. Leidens.
- Der Begriff "therapeutisch wirksame Menge" bedeutet eine Menge der Verbindung, welche die genannte Störung oder den genannten Zustand bzw. das genannte Leiden wirksam behandelt.
- Der Begriff "pharmazeutisch annehmbarer Träger" bedeutet ein nicht-toxisches Lösungsmittel, Dispergiermittel, Excipiens, Adjuvans oder anderes Material, welches mit dem Wirkstoff vermischt wird, um die Bildung einer pharmazeutischen Zusammensetzung, d. h. einer Dosierungsform, die dem Patienten verabreicht werden kann, zu gestatten. Ein Beispiel für einen solchen Träger ist ein pharmazeutisch annehmbares Öl, das typischerweise für eine parenterale Verabreichung verwendet wird.
- Der Begriff "Schizophrenie" bedeutet eine Schizophrenie, schizophrenieforme Störung, schizoaffektive Störung und psychotische Störung, wobei sich der Begriff "psychotisch" auf Wahnideen, markante Halluzinationen, desorganisierte Sprache oder desorganisiertes oder katatonisches Verhalten bezieht. Siehe Diagnostic and Statistical Manual of Mental Disorder, 4. Auflage, American Psychiatric Association, Washington, D.C.
- In Ausführungsformen der Erfindung schließen Verbindungen der Formel I solche ein, bei denen R1 ausgewählt ist aus H und C1-4-Alkyl. Vorzugsweise ist R1 Methyl. Im Rahmen der Erfindung liegen auch Verbindungen der Formel I, worin R2 ausgewählt ist aus H, C1-4-Alkyl und Benzyl. In bevorzugten Ausführungsformen ist R2 H.
- Zu Verbindungen der Erfindung gehören Verbindungen der Formel I, worin R3 SO2R5 ist. Innerhalb von R3 ist R5 ausgewählt aus Phenyl, Pyridyl, Thienyl, Chinolinyl und Naphthyl, welche gegebenenfalls mit 1-4 Substituenten, ausgewählt aus C1-4-Alkoxy, C1-4-Alkyl, Halogen, Nitro, Trifluormethyl, Trifluormethoxy, 1,2-Methylendioxy, C1-4-Alkylcarbonyl, C1-4-Alkoxycarbonyl und C1-4-AlkylS-, substituiert sind. R5 ist speziell ausgewählt aus Phenyl, Naphthyl und Thienyl, welche alle gegebenenfalls mit 1-3 Gruppen, unabhängig voneinan der ausgewählt aus Methyl, Methoxy, Halogen, Trifluormethyl und 1,2-Methylendioxy, substituiert sind. In bevorzugten Ausführungsformen ist, wenn R3 SO2R5 ist, R5 ausgewählt aus der Gruppe bestehend aus Naphthyl und Phenyl, gegebenenfalls substituiert mit 1-3 Substituenten, die unabhängig voneinander ausgewählt sind aus Chlor, Brom, Fluor, Nitro, Methyl und Methoxy. In mehr bevorzugten Ausführungsformen ist, wenn R3 SO2R5 ist, R5 ausgewählt aus der Gruppe bestehend aus Phenyl, 2-Chlorphenyl, 2-Bromphenyl, 1-Naphthyl, 4-Fluorphenyl, 4-Chlorphenyl, 4-Bromphenyl, 2,4-Dichlorphenyl, 3-Nitro-4-chlorphenyl, 2,4,6-Trimethylphenyl, 4-Methoxyphenyl und 4-Methylphenyl.
- In weiteren Ausführungsformen der Erfindung ist R4b ausgewählt aus H, Hydroxy, Halogen, C3-7-Cycloalkyloxy, C1-4-Alkoxy, C1-4-Alkyl, Benzyloxy, Phenoxy, Trifluormethyl, Trifluormethoxy und Vinyl. In spezifischen Ausführungsformen ist R4b ausgewählt aus H, Halogen, Cyclohexyloxy, Trifluormethoxy und Trifluormethyl. Vorzugsweise ist R4b ausgewählt aus Chlor, Trifluormethoxy, Trifluormethyl und Fluor.
- In anderen Ausführungsformen der Erfindung sind R4a, R4c und R4d jeweils unabhängig voneinander ausgewählt aus H, OH, Halogen, C1-4-Alkyl und C1-4-Alkoxy. In spezifischen Ausführungsformen sind R4a und R4c beide H und ist R4d Halogen oder ist R4c Halogen und sind R4a, R4b, R4d alle H. In einer bevorzugten Ausführungsform sind R4a, R4c und R4d alle H.
- In einer anderen Ausführungsform der Erfindung bedeutet --- eine Einfach- oder Doppelbindung. Vorzugsweise bedeutet --- eine Doppelbindung.
- In Ausführungsformen der Erfindung gehören zu den Verbindungen der Formel I:
5-Fluor-1-(4-methylphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(4-Methoxyphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(4-Fluorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(4-Bromphenylsulfonyl)-5-fuor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
5-Fluor-1-(2,5-dichlorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(4-Chlor-3-nitrophenylsulfonyl)-5-fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(2,4,6-trimethylphenylsulfonyl)indol;
5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(2,4,6-triisopropylphenylsulfonyl)indol;
5-Cyclohexyloxy-1-(4-methylphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
6-Brom-1-(4-methoxyphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
6-Brom-1-(4-fluorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
5-Cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(1-naphthylsulfonyl)indol;
5-Cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(2-naphthylsulfonyl)indol;
1-(2-Bromphenylsulfonyl)-5-cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
5-Cyclohexyloxy-1-(2,5-dichlorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
5-Cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(2,4,6-trimethylphenylsulfonyl)indol;
5-Cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(2,4,6-triisopropylphenylsulfonyl)indol;
5-Cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(3-nitrophenylsulfonyl)indol;
1-(4-Chlor-3-nitrophenylsulfonyl)-5-cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
5-Cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(3-nitro-4-trifluormethylphenylsulfonyl)indol;
1-(4-Bromphenylsulfonyl)-5-cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
5-Cyclohexyloxy-1-(4-methoxyphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
5-Cyclohexyloxy-1-(4-fluorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(4-Chlorphenylsulfonyl)-5-cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(4-t-Butylphenylsulfonyl)-5-cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(2-Bromphenylsulfonyl)-5-fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(4-Fluorphenylsulfonyl)-5-fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(4-Chlorphenylsulfonyl)-5-fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(4-t-Butylphenylsulfonyl)-4-fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(3-nitrophenylsulfonyl)indol;
5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(1-naphthylsulfonyl)indol;
5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(2-naphthylsulfonyl)indol;
5-Chlor-1-(4-fluorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(4-Fluorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethoxyindol;
1-(4-t-Butylphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethoxyindol;
1-(4-Chlorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethoxyindol;
1-(4-Methylphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethoxyindol;
(4-Methoxyphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethoxyindol;
1-(4-Fluorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethylindolhydrochlorid;
1-(4-t-Butylphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethylindolhydrochlorid;
1-(4-Chlorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethylindolhydrochlorid;
1-(4-Methoxyphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethylindolhydrochlorid;
1-(4-Methylphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethylindolhydrochlorid;
5-Cyclohexyloxy-1-(4-methylphenylsulfonyl)-3-(1-methyl-4-piperidinyl)indol;
5-Chlor-1-(4-fluorphenylsulfonyl)-3-(1-methyl-4-piperidinyl)indol;
1-(4-Fluorphenylsulfonyl)-3-(1-methyl-4-piperidinyl)indol;
1-(4-Fluorphenylsulfonyl)-6-chlor-3-(1-methyl-4-piperidinyl)indol;
1-(4-Fluorphenylsulfonyl)-5-fluor-3-(1-methyl-4-piperidinyl)indol;
5,7-Difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(4-methylphenylsulfonyl)indol;
5,7-Difluor-1-(4-fluorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(4-Bromphenylsulfonyl)-5,7-difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(4-Chlorphenylsulfonyl)-5,7-difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
5,7-Difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(1-naphthylsulfonyl)indol;
5,7-Difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(2-naphthylsulfonyl)indol; und
5,7-Difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(2,4,6-trimethylphenyl)sulfonylindol. - In speziellen Ausführungsformen der Erfindung gehören zu den Verbindungen der Formel I:
5-Fluor-1-(4-methylphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(4-Methoxyphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(4-Fluorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(4-Bromphenylsulfonyl)-5-fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
5-Fluor-1-(2,5-dichlorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(4-Chlor-3-nitrophenylsulfonyl)-5-fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(2,4,6-trimethylphenylsulfonyl)indol;
5-Cyclohexyloxy-1-(4-methylphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
6-Brom-1-(4-methoxyphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
6-Brom-1-(4-fluorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
5-Cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(1-naphthylsulfonyl)indol;
5-Cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(2-naphthylsulfonyl)indol;
1-(2-Bromphenylsulfonyl)-5-cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
5-Cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(3-nitrophenylsulfonyl)indol;
5-Cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(3-nitro-4-trifluormethylphenylsulfonyl)indol;
1-(4-Bromphenylsulfonyl)-5-cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
5-Cyclohexyloxy-1-(4-methoxyphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
5-Cyclohexyloxy-1-(4-fluorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(4-Chlorphenylsulfonyl)-5-cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(4-t-Butylphenylsulfonyl)-5-cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(2-Bromphenylsulfonyl)-5-fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(4-Fluorphenylsulfonyl-5-fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(4-Chlorphenylsulfonyl)-5-fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(4-t-Butylphenylsulfonyl)-4-fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(3-nitrophenylsulfonyl)indol;
5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(1-naphthylsulfonyl)indol;
5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(2-naphthylsulfonyl)indol;
5-Chlor-1-(4-fluorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(4-Fluorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethoxyindol;
1-(4-t-Butylphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethoxyindol;
1-(4-Chlorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethoxyindol;
1-(4-Methylphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethoxyindol;
(4-Methoxyphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethoxyindol;
1-(4-Fluorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethylindolhydrochlorid;
1-(4-t-Butylphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethylindolhydrochlorid;
1-(4-Chlorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethylindolhydrochlorid;
1-(4-Methoxyphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethylindolhydrochlorid;
1-(4-Methylphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethylindolhydrochlorid;
5-Chlor-1-(4-fluorphenylsulfonyl)-3-(1-methyl-4-piperidinyl)indol;
1-(4-Fluorphenylsulfonyl)-3-(1-methyl-4-piperidinyl)indol;
1-(4-Fluorphenylsulfonyl)-6-chlor-3-(1-methyl-4-piperidinyl)indol;
5,7-Difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(4-methylphenylsulfonyl)indol;
5,7-Difluor-1-(4-fluorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(4-Chlorphenylsulfonyl)-5,7-difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
5,7-Difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(1-naphthylsulfonyl)indol;
5,7-Difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(2-naphthylsulfonyl)indol; und
5,7-Difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(2,4,6-trimethylphenyl)sulfonylindol. - In spezielleren Ausführungsformen der Erfindung gehören zu den Verbindungen der Formel I:
5-Fluor-1-(4-methylphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(4-Methoxyphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(4-Fluorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(4-Bromphenylsulfonyl)-5-fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
5-Fluor-1-(2,5-dichlorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(4-Chlor-3-nitrophenylsulfonyl)-5-fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(2,4,6-trimethylphenylsulfonyl)indol;
5-Cyclohexyloxy-1-(4-methylphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
6-Brom-1-(4-fluorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
5-Cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(1-naphthylsulfonyl)indol;
5-Cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(2-naphthylsulfonyl)indol;
1-(2-Bromphenylsulfonyl)-5-cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
5-Cyclohexyloxy-1-(4-methoxyphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(2-Bromphenylsulfonyl)-5-fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(4-Fluorphenylsulfonyl-5-fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(4-Chlorphenylsulfonyl)-5-fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(3-nitrophenylsulfonyl)indol;
5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(1-naphthylsulfonyl)indol;
5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(2-naphthylsulfonyl)indol;
5-Chlor-1-(4-fluorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(4-Chlorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethoxyindol;
1-(4-Methylphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethoxyindol;
1-(4-Chlorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethylindolhydrochlorid;
1-(4-Methoxyphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethylindolhydrochlorid;
1-(4-Methylphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethylindolhydrochlorid;
5,7-Difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(4-methylphenylsulfonyl)indol;
1-(4-Bromphenylsulfonyl)-5,7-difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(4-Chlorphenylsulfonyl)-5,7-difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
5,7-Difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(1-naphthylsulfonyl)indol; und
5,7-Difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(2-naphthylsulfonyl)indol. - In den speziellsten Ausführungsformen der Erfindung gehören zu den Verbindungen der Formel I:
5-Fluor-1-(4-methylphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(4-Fluorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(2-Bromphenylsulfonyl)-5-fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(4-Fluorphenylsulfonyl-5-fuor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(4-Chlorphenylsulfonyl)-5-fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(1-naphthylsulfonyl)indol;
5-Chlor-1-(4-fluorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(4-Chlorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethoxyindol;
1-(4-Methylphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethoxyindol;
5,7-Difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(4-methylphenylsulfonyl)indol;
1-(4-Bromphenylsulfonyl)-5,7-difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
1-(4-Chlorphenylsulfonyl)-5,7-difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol;
5,7-Difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(1-naphthylsulfonyl)indol; und
5,7-Difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(2-naphthylsulfonyl)indol. - Säureadditionssalze der Verbindungen der Formel I werden am zweckmäßigsten aus pharmazeutisch annehmbaren Säuren gebildet und zu ihnen gehören z. B. solche, die mit anorganischen Säuren, z. B. Chlorwasserstoffsäure, Schwefelsäure oder Phosphorsäure, und organischen Säuren, z. B. Bernsteinsäure, Maleinsäure, Essigsäure oder Fumarsäure gebildet werden. Weitere nicht pharmazeutisch annehmbare Salze, z. B. Oxalate, können z. B. bei der Isolierung von Verbindungen der Formel I für Laborzwecke oder zur anschließenden Umwandlung in ein pharmazeutisch annehmbares Säureadditionssalz verwendet werden. Im Rahmen der Erfindung liegen auch Solvate und Hydrate der Erfindung.
- Die Umwandlung eines bestimmten Salzes der Verbindung in ein gewünschtes Salz der Verbindung wird durch Anwendung von Standardmethoden erreicht, in welchen eine wässrige Lösung des bestimmten Salzes mit einer Lösung einer Base, z. B. Natriumcarbonat oder Kaliumhydroxid, behandelt wird, um die freie Base freizusetzen, welche dann in ein geeignetes Lösungsmittel wie etwa Ether extrahiert wird. Die freie Base wird dann von dem wässri gen Anteil abgetrennt, getrocknet und mit der erforderlichen Säure behandelt, um das gewünschte Salz zu ergeben.
- Verbindungen der vorliegenden Erfindung können in ihrer Struktur ein chirales Zentrum aufweisen. Die Erfindung erstreckt sich auf alle strukturellen und optischen Isomere der verschiedenen Verbindungen sowie racemische Gemische davon.
- In Übereinstimmung mit anderen Aspekten der Erfindung können die Verbindungen der vorliegenden Erfindung durch Verfahren hergestellt werden, die den im Fachgebiet etablierten Verfahren analog sind. Zum Beispiel können, wie in Schema 1 gezeigt, Verbindungen der Formel I hergesellt werden, indem zunächst Verbindungen der Formel A, worin R1 C1-4-Alkyl ist und R2 und R4a-d wie in Formel I definiert sind, mit einer geeigneten Base behandelt werden, gefolgt von der Zugabe eines Reagenzes der Formel C, welches eine Verbindung der Formel I ergibt, worin R3 SO2R5 ist. Deshalb ergibt z. B. die Behandlung von Verbindungen der Formel A mit einer starken Base wie Lithiumdiisopropylamid, n-Butyllithium oder Natriumbis(trimethylsilyl)amid in einem inerten Lösungsmittel wie Tetrahydrofuran oder Hexanen bei einer Temperatur im Bereich von –100 bis 0°C oder alternativ einem organischen Amin in Gegenwart von 4-Dimethylaminopyridin (DMAP) in einem inerten Lösungsmittel wie Methylenchlorid oder Chloroform bei einer Temperatur im Bereich von 0-60°C, gefolgt von der Zugabe von Sulfonylchloriden der Formel C, worin R5 wie in Formel I definiert ist, Verbindungen der Formel I, worin R3 COR5 ist. Bevorzugte Bedingungen sind Natriumbis(trimethylsilyl)amid in Tetrahydrofuran bei –78°C, gefolgt von Aufwärmen auf Raumtemperatur, oder Triethylamin und DMAP in Methylenchlorid bei Raumtemperatur. Die Reagenzien C sind kommerziell erhältlich oder können unter Verwendung von Standardverfahren hergestellt werden, die dem Fachmann bekannt sind. Die Herstellung von Verbindungen der Formel A ist nachstehend beschrieben.
- Verbindungen der Formel I, worin R1 H ist, können durch Behandeln einer Verbindung der Formel A, worin R1 eine geeignete Schutzgruppe wie etwa t-Butoxycarbonyl (t-BOC) ist, mit Reagenzien der Formel C wie vorstehend beschrieben hergestellt werden. Das Entfernen der Schutzgruppe kann unter Standardbedingungen erfolgen, z. B. unter Verwendung von sauren Bedingungen wie HCl in Ethylacetat, um die t-BOC-Gruppe zu entfernen, um Verbindungen der Formel I bereitzustellen, worin R1 H ist.
- Verbindungen der Formel I, worin R2 aus C1-4-Alkyl und Benzyl ausgewählt ist, R1 C1-4-Alkyl ist, R3 SO2R5 ist und R4a-d wie in Formel I definiert sind, können ebenfalls durch Behandeln von Verbindungen der Formel I, worin R2 H ist, R1 aus C1-4-Alkyl ausgewählt ist, R3 SO2R5 ist und R4a-d wie in Formel I definiert sind, mit einer starken Base, wie n-Butyllithium, in einem inerten Lösungsmittel, wie Tetrahydrofuran, bei einer Temperatur im Bereich von –100-0°C (vorzugsweise –78°C), gefolgt von der Zugabe eines Reagenzes mit der Formel R2-X, worin R2 aus C1-4-Alkyl und Benzyl ausgewählt ist und X eine geeignete Abgangsgruppe wie etwa Brom ist, gefolgt vom Aufwärmen auf Raumtemperatur hergestellt werden. Die vorstehende Reaktion kann auch an einer Verbindung der Formel I durchgeführt werden, worin R2 H ist, R1 eine geeignete Schutzgruppe, wie etwa t-Butoxycarbonyl, ist, R3 SO2R5 ist und R4a-d wie in Formel I definiert sind, welche nach dem Entfernen der Schutzgruppe unter Verwendung von Standardbedingungen zum Entfernen von Schutzgruppen (z. B. HCl in Ethylacetat zum Entfernen der t-Butoxycarbonyl-Schutzgruppe) eine Verbindung der Formel I ergibt, worin R2 aus C1-4-Alkyl und Benzyl ausgewählt ist, R1 H ist, R3 SO2R5 ist und R4a-c wie in Formel I definiert sind.
- Verbindungen der Formel A, worin R1, R2 und R4a-d wie in Formel I definiert sind, können wie in Schema 2 gezeigt hergestellt werden. Indol D, worin R2 und R4a-d wie in Formel I definiert sind, können mit einem Reagenz der Formel E, worin R1 wie in Formel I definiert ist, in Gegenwart einer Base in einem geeigneten Lösungsmittel bei Temperaturen im Bereich von 25-100°C, vorzugsweise 60-90°C kondensiert werden, um Verbindungen der Formel A bereitzustellen, worin R1, R2, R4a-d wie in Formel I definiert sind und --- eine Doppelbindung bedeutet. Zu geeigneten Basen gehören organische Amine wie Pyrrolidin oder Triethylamin und zu geeigneten Lösungsmitteln gehören Methanol, Ethanol und dergleichen. Bevorzugte Bedingungen sind Pyrrolidin in Ethanol bei Rückflusstemperatur. Verbindungen der Formel A, worin R1, R2, R4a-d wie in Formel I definiert sind und --- eine Doppelbindung bedeutet, können unter Verwendung von Standardhydrierungsbedingungen oder unter Verwendung von Metallhydridreduktionsmitteln reduziert werden, um Verbindungen der Formel A bereitzustellen, worin R1, R2, R4a-d wie in Formel I definiert sind und --- eine Einfachbindung bedeutet, wie in Schema 2 gezeigt ist. Bevorzugt ist eine Reduktion durch Hydrierung unter Verwendung eines geeigneten Katalysators wie Palladium oder Platin auf Kohlenstoff in Methanol bei Raumtemperatur.
- Reagenzien der Formel A, worin R1 eine Schutzgruppe ist und R2 und R4a-d wie in Formel I definiert sind, sind erhältlich durch Behandeln von Reagenzien der Formel A, worin R1 H ist, R2 und R4a-d wie in Formel I definiert sind und --- eine Einfach- oder Doppelbindung bedeutet, unter Standardbedingungen, um eine Schutzgruppe an dem Piperidin- oder Tetrahydropyridinstickstoff einzuführen. Zum Beispiel würde eine Reaktion von Indol A, worin R1 H ist, in Gegenwart von Di-t-butyldicarbonat und einer Base, wie Natriumhydroxid, Verbindungen der Formel A ergeben, worin R1 die t-BOC-Schutzgruppe ist, R2 und R4a-d wie in Formel I definiert sind und --- eine Einfach- oder Doppelbindung bedeutet.
- Die Indole der Formel D sind entweder kommerziell erhältlich oder können unter Verwendung von Standardverfahren hergestellt werden. Zum Beispiel können Verbindungen der Formel D wie in Schema 3 gezeigt hergestellt werden. 4-substituierte Aniline der Formel E, worin R4a-d wie in Formel I definiert sind, können mit Reagenzien der Formel F, worin R2 wie in Formel I definiert ist, in Gegenwart einer Base wie Natriumhydrogencarbonat oder Kaliumcarbonat in einem alkoholischen Lösungsmittel bei Temperaturen im Bereich von 60-100°C behandelt werden, um Zwischenprodukte der Formel G bereitzustellen. Bevorzugte Bedingungen sind Natriumhydrogencarbonat in Ethanol bei ungefähr 80°C. Zwischenprodukte der Formel G können in Gegenwart von Reagenzien der Formel H, worin R z. B. Methyl oder Trifluormethyl (welches bevorzugt ist) bedeutet, bei Temperaturen im Bereich von 60-100°C zyklisiert werden, um Indole der Formel J bereitzustellen. Die bevorzugten Bedingungen sind Trifluoressigsäureanhydrid und Trifluoressigsäure bei Rückflusstemperaturen. Schließlich können Verbindungen der Formel J unter Standardbedingungen zum Entfernen von Schutzgruppen behandelt werden, z. B. mit Alkalihydroxiden in einem alkoholischen Lösungsmittel, um Indole der Formel D bereitzustellen, worin R2 und R4a-d wie in Formel I definiert sind. Bevorzugte Bedingungen für diese Reaktion sind Kaliumhydroxid in Ethanol bei Raumtemperatur. Die Reagenzien der Formel E und F sind entweder kommerziell erhältlich oder können unter Verwendung von Verfahren hergestellt werden, die den im Fachgebiet etablierten Verfahren analog sind.
- Ein alternatives Verfahren zum Herstellen von Indolen der Formel D, worin R4b Vinyl oder Ethyl ist, ist in Schema 4 gezeigt. Indole der Formel K, worin Y eine geeignete Abgangsgruppe wie Halogen oder Triflat (vorzugsweise Brom) bedeutet und R2 wie in Formel I definiert ist, können mit einem Vinyltrialkylstannan beispielsweise mit der Formel L unter Standardbedingungen für eine palladiumkatalysierte Kreuzkupplung gekuppelt werden, um Indole der Formel D bereitzustellen, worin R4b Vinyl ist und R2 wie in Formel I definiert ist. Es ist klar, dass andere Metallkupplungsreagenzien anstelle des Vinylstannans verwendet werden können, z. B. eine Vinylboronsäure, Chlorzink und dergleichen. Zu bevorzugten Kupplungsbedingungen gehören das Erhitzen des Indols und des Vinylmetallreagenzes in einem inerten Lösungsmittel wie Dimethylformamid oder Toluol in Gegenwart von Tetrakis(triphenylphosphin)palladium (0) bei Rückflusstemperaturen. Im Anschluss an die Kupplungsreaktion kann die Doppelbindung der Vinylgruppe unter Verwendung katalytischer Mengen von Palladium auf Kohlenstoff in einem inerten Lösungsmittel (vorzugsweise Ethylacetat) in einer Wasserstoffatmosphäre bei Raumtemperatur hydriert werden, um Indole der Formel D bereitzustellen, worin R4b Ethyl bedeutet. Dieses Verfahren könnte auch zum Herstellen von Verbindungen der Formel D verwendet werden, worin R4a, R4c oder R4d Ethyl bedeuten, indem das geeignet substituierte Indol L wie vorstehend beschrieben umgesetzt wird.
- Indole der Formel D, worin R4b Cyclooxy oder Phenoxy ist und R2 wie in Formel I definiert ist, sind ebenfalls aus dem entsprechenden 5-Hydroxyindol M wie in Schema 5 gezeigt erhältlich. Eine Reaktion von Indol M beispielsweise mit Cyclohexanol N unter Standard-Mitsunobu-Bedingungen (Mitsunobu, O. Synthesis, 1981: 1-28) ergibt Reagenzien der Formel D, worin R4b Cyclohexyloxy ist und R2 wie in Formel I definiert ist. Eine Reaktion von Indol M mit einem Reagenz der Formel O, worin Y eine geeignete Abgangsgruppe wie Halogen, vorzugsweise Iod, ist, unter Standard Ulman-Bedingungen (Fanta, F. E., Chem. Rev., 64, 1964: 613) ergibt Indole der Formel D, worin R4b Phenoxy ist und R2 wie in Formel I definiert ist. Bevorzugte Bedingungen sind Iodbenzol in Gegenwart von Kaliumcarbonat, Kupfer(I)-bromid und Kupferpulver in N-Methylpyrrolidin bei 170°C.
- Die in den Schemata 4 und 5 gezeigten Reaktionen könnten auch auf Indole angewandt werden, bei denen die Gruppe in 3-Stellung vorhanden ist. In einigen Fällen müssen die vorstehend skizzierten chemischen Reaktionen modifiziert werden, z. B. durch Verwendung von Schutzgruppen, um Nebenreaktionen aufgrund von reaktiven Gruppen, wie etwa reaktiven Gruppen, die als Substituenten gebunden sind, zu vermeiden.
- Die Verbindungen der vorliegenden Erfindung können verwendet werden, um 5-HT6-Rezeptoren von anderen Rezeptorsubtypen, z. B. Glutamat- oder Opioidrezeptoren, innerhalb einer Population von Rezeptoren zu unterscheiden und insbesondere um zwischen den 5-HT6 und anderen 5-HT-Rezeptorsubtypen zu unterscheiden. Letzteres kann erreicht werden durch Inkubieren von Präparationen des 5-HT6-Rezeptors und eines der anderen 5-HT-Rezeptorsubtypen (z. B. 5-HT2A) mit einer 5-HT6-selektiven Verbindung der Erfindung und anschließendes Inkubieren der resultierenden Präparation mit einem radioaktiv markierten Serotoninrezeptorliganden, z. B. [3H]-Serotonin. Die 5-HT6-Rezeptoren werden dann durch Bestimmen des Unterschieds der membrangebundenen Aktivität unterschieden, wobei der 5-HT6-Rezeptor weniger Radioaktivität, d. h. weniger [3H]-Serotoninbindung aufweist als der andere 5-HT-Rezeptorsubtyp.
- Die Verbindung kann in markierter Form, wie etwa radioaktiv markierter Form, z. B. durch Einbau von 3H oder 14C in seine Struktur oder durch Konjugation an 125I markiert, bereitgestellt werden. Die Verbindungen in markierter Form können verwendet werden, um 5-HT6-Rezeptorliganden durch im Fachgebiet übliche Methoden zu identifizieren. Dies kann erreicht werden durch Inkubieren des Rezeptors oder Gewebes in Gegenwart eines Ligandenkandidaten und anschließendes Inkubieren der resultierenden Präparation mit einer äquimolaren Menge einer radioaktiv markierten Verbindung der Erfindung wie [3H]-5-Fluor-1-(4-methylphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol. 5-HT6-Rezeptorliganden werden somit als diejenigen kenntlich gemacht, welche nicht signifikant durch die radioaktiv markierte Verbindung der vorliegenden Erfindung verdrängt werden. Alternativ können 5-HT6-Rezeptorligandenkandidaten identifiziert werden, indem zunächst eine radioaktiv markierte Form einer Verbindung der Erfindung inkubiert wird und anschließend die resultierende Präparation in Gegenwart des Kandidatenliganden inkubiert wird. Ein stärkerer 5-HT6-Rezeptorligand verdrängt bei äquimolarer Konzentration die radioaktiv markierte Verbindung der Erfindung.
- Die Verbindungen der vorliegenden Erfindung sind als Pharmazeutika für die Behandlung von verschiedenen Zuständen bzw. Leiden brauchbar, bei denen die Verwendung eines 5-HT6-Antagonisten angezeigt ist, wie etwa bei einer Psychose, Schizophrenie, manischen Depression, Depression, neurologischen Störungen, Gedächtnisstörungen, Parkinson-Krankheit, amyotropher Lateralsklerose, Alzheimer-Krankheit und Chorea Huntington. In einem weiteren ihrer Aspekte stellt die vorliegende Erfindung pharmazeutische Zusammensetzungen bereit, die zum Behandeln von mit 5-HT6 zusammenhängenden medizinischen Zuständen bzw. Leiden brauchbar sind, in welchen eine Verbindung der Formel I in einer Menge, die die Stimulierung des 5-HT6-Rezeptors wirksam antagonisiert, zusammen mit einem pharmazeutisch annehmbaren Träger vorhanden ist. Die Verbindungen sind brauchbar zum Behandeln von medizinischen Zuständen bzw. Leiden, für die ein 5-HT6-Rezeptorantagonist angezeigt ist, wobei das Behandeln den Schritt des Verabreichens einer Menge einer Verbindung der Formel I, die die Stimulierung des 5-HT6-Rezeptors wirksam antagonisiert, und eines pharmazeutisch annehmbaren Trägers dafür an den Patienten umfasst.
- Zur Verwendung in der Medizin können die Verbindungen der vorliegenden Erfindung in einer pharmazeutischen Standardzusammensetzung verabreicht werden. Die vorliegende Erfindung stellt deshalb in einem weiteren Aspekt pharmazeutische Zusammensetzungen bereit, die einen pharmazeutisch annehmbaren Träger und eine Verbindung der Formel I oder ein pharmazeutisch annehmbares Salz, Solvat oder Hydrat davon in einer Menge umfassen, welche zum Behandeln der Zielindikation wirksam ist.
- Die Verbindungen der vorliegenden Erfindung können auf jedem zweckmäßigen Weg, z. B. durch orale, parenterale, bukkale, sublinguale, nasale, rektale oder transdermale Verabreichung oder Verabreichung mittels eines Pflasters oder einer Pumpe verabreicht werden und die pharmazeutischen Zusammensetzungen können entsprechend formuliert werden.
- Verbindungen der Formel I und ihre pharmazeutisch annehmbaren Salze, welche aktiv sind, wenn sie oral verabreicht werden, können als Flüssigkeiten, z. B. Sirupe, Suspensionen oder Emulsionen, oder als feste Formen wie Tabletten, Kapseln und Trochisken formuliert werden. Eine flüssige Formulierung besteht im Allgemeinen aus einer Suspension oder Lösung der Verbindung oder des pharmazeutisch annehmbaren Salzes in einem geeigneten flüssigen pharmazeutischen Träger, z. B. Ethanol, Glycerin, nicht-wässriges Lösungsmittel, z. B. Polyethylenglycol, Öle, oder Wasser mit einem Suspendiermittel, Konservierungsmittel, Aromastoff oder Färbemittel. Eine Zusammensetzung in Form einer Tablette kann unter Verwendung eines beliebigen pharmazeutischen Trägers hergestellt werden, der routinemäßig zum Herstellen von festen Formulierungen verwendet wird. Zu Beispielen für solche Träger gehören Magnesiumstearat, Stärke, Lactose, Sucrose und Cellulose. Eine Zusammensetzung in Form einer Kapsel kann unter Verwendung von routinemäßigen Einkapselungsverfahren hergestellt werden. Zum Beispiel können Pellets, die den Wirkstoff enthalten, unter Verwendung von Standardträgern hergestellt werden und anschließend in eine Hartgelatinekapsel eingefüllt werden; alternativ kann eine Dispersion oder Suspension unter Verwendung eines geeigneten pharmazeutischen Trägers, z. B. wässrige Gummen, Cellulosen, Silikate oder Öle, hergestellt werden und die Dispersion oder Suspension in eine Weichgelatinekapsel eingefüllt werden.
- Typische parenterale Zusammensetzungen bestehen aus einer Lösung oder Suspension der Verbindung oder des pharmazeutisch annehmbaren Salzes in einem sterilen wässrigen Träger oder parenteral annehmbaren Öl, z. B. Polyethylenglycol, Polyvinylpyrrolidon, Lecithin, Erdnussöl oder Sesamöl. Alternativ kann die Lösung lyophilisiert und anschließend mit einem geeigneten Lösungsmittel unmittelbar vor der Verabreichung rekonstituiert werden.
- Zusammensetzungen für eine nasale Verabreichung können zweckmäßigerweise als Aerosole, Tropfen, Gele und Pulver formuliert werden. Aerosolformulierungen umfassen typischerweise eine Lösung oder feine Suspension der aktiven Substanz in einem physiologisch annehmbaren wässrigen oder nicht-wässrigen Lösungsmittel und werden gewöhnlich in Einzel- oder Mehrfachdosenmengen in steriler Form in einem verschlossenen Behälter dargeboten, welcher die Form einer Patrone oder Nachfüllpackung zur Verwendung mit einer Zerstäubungsvorrichtung annehmen kann. Alternativ kann der verschlossene Behälter eine einheitliche Abgabevorrichtung wie etwa ein nasaler Einzeldosis-Inhalator oder eine Aerosolabgabevorrichtung sein, die mit einem Dosierventil ausgestattet ist, welche nach der Verwendung weggeworfen werden soll. Wenn die Dosierungsform eine Aerosolabgabevorrichtung umfasst, enthält sie ein Treibmittel, welches ein komprimiertes Gas wie komprimierte Luft oder ein organisches Treibmittel wie Fluorchlorkohlenwasserstoff sein kann. Die Aerosoldosierungsformen können auch die Form eines Pumpenzerstäubers annehmen.
- Zu Zusammensetzungen, die für eine bukkale oder sublinguale Verabreichung geeignet sind, gehören Tabletten, Trochisken und Pastillen, wobei der Wirkstoff mit einem Träger wie Zucker, Akaziengummi, Traganth oder Gelatine und Glycerin formuliert wird. Zusammenset zungen für eine rektale Verabreichung liegen zweckmäßigerweise in Form von Zäpfchen vor, die eine herkömmliche Zäpfchengrundlage wie Kakaobutter enthalten.
- Vorzugsweise liegt die Zusammensetzung in Form einer Einheitsdosis wie etwa eine Tablette, Kapsel oder Ampulle vor. Geeignete Dosierungseinheiten, d. h. therapeutisch wirksame Mengen, können während klinischer Versuche bestimmt werden, die für jeden Zustand bzw. jedes Leiden, für welchen bzw. welches die Verabreichung einer ausgewählten Verbindung angezeigt ist, zweckmäßig entworfen werden, und sie schwanken natürlich in Abhängigkeit von dem gewünschten klinischen Endpunkt. Jede Dosierungseinheit für eine orale Verabreichung kann 0,01 bis 500 mg/kg (und für eine parenterale Verabreichung 0,1 bis 50 mg) einer Verbindung der Formel I oder eines pharmazeutisch annehmbaren Salzes davon, berechnet als die freie Base, enthalten und wird in einer Häufigkeit verabreicht, die für eine Initialbehandlung und eine Erhaltungsbehandlung zweckmäßig ist. Für die Verwendung im Labor können die Verbindungen der vorliegenden Erfindung in abgepackter Form zur Rekonstitution und Verwendung aufbewahrt werden.
- Experimentalbeispiele
- Informationsbeispiel 1: 5-Cyclohexyloxy-1H-indol
- Triphenylphosphin (10,3 g, 39,4 mmol) und 5-Hydroxy-1H-indol (5 g, 36,9 mmol) wurden zu einer Lösung von Cyclohexanol (3,7 ml, 35,7 mmol) in THF (200 ml) bei 0°C zugegeben. DEAD (5,9 ml, 39,4 mmol) wurde langsam zugegeben und die resultierende Lösung wurde 1 Woche bei Raumtemperatur gerührt. Das Lösungsmittel wurde im Vakuum entfernt und eine Flash-Chromatografie (Silicagel, 10% Ethylacetat in Hexan) ergab 5-Cyclohexyloxy-1H-indol (3,2 g, 40%).
- Informationsbeispiel 2: 5-Trifluormethoxy-1H-indol
- Lithiumaluminiumhydrid (10,4 ml, 1 M in THF, 10,4 mmol) wurde zu einer Lösung von 5-Trifluormethoxyisatin (0,8 g, 3,45 mmol) in THF bei Raumtemperatur zugegeben und das Gemisch wurde über Nacht refluxiert. Das Reaktionsgemisch wurde gekühlt und Na2SO4·10H2O wurde sehr vorsichtig portionsweise zugegeben, gefolgt von Ethylacetat. Das Reaktionsgemisch wurde dann filtriert und das Filtrat wurde eingedampft. Das zurückbleibende Öl wurde durch Säulenchromatografie mit Ethylacetat in Hexanen (2:98) gereinigt, wobei 5-Trifluormethoxy-1H-indol (0,162 g, 23%) erhalten wurde.
- Informationsbeispiel 3: 5,7-Difluor-1H-indol
- Vinylmagnesiumbromid (30 ml, 1 M in THF, 30 mmol) wurde tropfenweise zu einer Lösung von 2,4-Difluornitrobenzol (1,6 g, 10 mmol) in THF bei –40°C zugegeben. Das Gemisch wurde 30 min gerührt und dann in CH2Cl2-verdünnte HCl gegossen. Die organische Schicht wurde abgetrennt und getrocknet (Na2SO4). Nachdem das Lösungsmittel im Vakuum entfernt worden war, wurde das zurückbleibende Öl durch Säulenchromatografie mit EtOAc/Hexanen (2:98) gereinigt, wobei 2,4-Difluor-1H-indol (189 mg, 12%) erhalten wurde.
- Beispiel I (a): 5-Brom-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol
- 5-Brom-1H-indol (4,31 g, 22 mmol), 1-Methyl-4-piperidon (2,46 ml, 20 mmol) und Pyrrolidin (17 ml, 200 mmol) wurden in Ethanol (30 ml) vermischt und 72 Stunden refluxiert. Das Gemisch wurde auf Raumtemperatur gekühlt und der resultierende Feststoff durch Filtration gesammelt, mit Methanol gewaschen und getrocknet, wobei die Titelverbindung als ein weißer Feststoff erhalten wurde (4,40 g, 76%). Schmelzpunkt >230°C, Zers.
- Auf ähnliche Weise wurden die folgenden weiteren Verbindungen hergestellt:
- (b) 5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol: aus 5-Fluor-1H-indol;
- (c) 5-Cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol: aus 5-Cyclohexyloxy-1H-indol (Beispiel 1);
- (d) 5-Chlor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol: aus 5-Chlor-1H-indol;
- (e) 3-(1-Methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol: aus 1H-Indol;
- (f) 6-Brom-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol: aus 6-Brom-1H-indol;
- (g) 5,7-Difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol: (176,8 mg, 58%); aus 5,7-Difluorindol (Informationsbeispiel 3, 188 mg, 1,23 mmol) und N-Methyl-4-piperidon (153,4 mg, 1,23 mmol) mit Pyrrolidin (875 mg, 12,3 mmol) in Ethanol (1,5 ml) am Rückfluss. Schmelzpunkt 215-21°C, HRMS-FAB+ für C14H14N2F2: ber. MH+: 249,12033; gefunden: 249,12095;
- (h) 3-(1-Methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethoxy-1H-indol: aus 5-Trifluormethoxy-1H-indol (Beispiel 2);
- (i) 3-(1-Methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethyl-1H-indol:
aus 5-Trifluormethyl-1H-indol
(hergestellt nach Miyano, et al.,
JP-60204759 - (j) 6-Chlor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol: aus 6-Chlor-1H-indol.
- Referenzbeispiel 2 (a): 5-Cyclohexyloxy-3-(1-methyl-4-piperidinyl)-1H-indol
- Palladium auf Kohlenstoff (10%, 31 mg) wurde zu einer Lösung von 5-Cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ic, 48,4 mg, 0,16 mmol) in Methanol (5 ml) zugegeben und das Gemisch wurde unter einer Wasserstoffatmosphäre 8 h gerührt. Das Entfernen des Katalysators durch Filtration wurde Celite und Siliciumdioxid (20% 2 M methanolisches Ammoniak in Dichlormethan) ergab 5-Cyclohexyloxy-3-(1-methyl-4-piperidinyl)-1H-indol (quantitativ, HRMS-FAB+ für C20H28N20: berechnet MH+: 313,22800; gefunden MH+: 313,23083).
- Auf ähnliche Weise wurden die folgenden weiteren Verbindungen hergestellt:
- (b) 6-Chlor-3-(1-methyl-4-piperidinyl)-1H-indol: (0,815 g, 81%); aus 6-Chlor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ij, 1,0 g, 4 mmol) und 5% Pt/C (0,78 g, 0,2 mmol) in Ethanol unter H2; Schmelzpunkt 218-24°C.
- (c) 5-Fluor-3-(1-methyl-4-piperidinyl)-1H-indol: (0,64 g, 64%); aus 5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ib, 1,0 g, 4,34 mmol) und 5% Pt/C (0,43 g, 0,4 mmol) in Ethanol unter H2; Schmelzpunkt 158-61°C. HRMS-FAB+ für C14H17N2F berechnet MH+: 233,14540, gefunden: 233,13193.
- (d) 3-(1-Methyl-4-piperidinyl)-1H-indol: (0,92 g, 91%); aus 3-(1-Methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ie, 1,0 g, 4,69 mmol) und 10% Pd/C auf Kohlenstoff (0,5 g, 0,47 mmol) in Ethanol unter H2; Schmelzpunkt 174-6°C; HRMS-FAB+ für C14H18N2, berechnet MH+: 215,15483, gefunden: 215,15356.
- (e) 5-Chlor-3-(1-methyl-4-piperidinyl)indol: (0,89 g, 88%); aus 5-Chlor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol (Beispiel Id, 1,0 g, 4 mmol) und 5% Pt/C (0,78 g, 0,2 mmol) in Methanol unter H2; Schmelzpunkt 192-4°C; HRMS-FAB+ für C14H17N2Cl berechnet MH+: 249,11584, gefunden: 249,11529.
- Referenzbeispiel 3 (a): 1-Benzoyl-5-fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol
- Benzoylchlorid (33,3 mg, 0,24 mmol) wurde zu einer Lösung von 5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol (Beispiel Ib, 49,6 mg, 0,215 mmol), Triethylamin (0,15 ml, 1,1 mmol) und DMAP (5 mg) in Dichlormethan (2 ml) zugegeben. Das Gemisch wurde bei Raumtemperatur gerührt, bevor es mit Wasser versetzt wurde, um die Reaktion zu beenden, und in Dichlormethan extrahiert wurde. Die organische Schicht wurde mit Salzlösung gewaschen und über Natriumsulfat getrocknet. Eine Reinigung durch Flash-Chromatografie (Silicagel, 2 M methanolisches Ammoniak in Chloroform) ergab 1-Benzoyl-5-fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol (27,8 mg, 39%, HRMS-FAB+ für C21H20N2OF berechnet MH+: 335,15598; gefunden: 335,15457).
- Auf ähnliche Weise wurden die folgenden weiteren Verbindungen hergestellt:
Beispiel 3 (b) 5-Fluor-1-(4-methylphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol: (7,2 mg, 8%), aus 5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol: (Beispiel Ib, 52,0 mg, 0,226 mmol) und 4-Methylphenylsulfonylchlorid (48,0 mg, 0,25 mmol); HRMS-FAB+ für C21H22N2O2SF: berechnet MH+: 385,13861; gefunden: 385,14053. - Beispiel 4 (a): 3-(1-Methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-phenylsulfonylindol
- Natriumbis(trimethylsilyl)amid (0,23 ml, 1 M in THF, 0,23 mmol) wurde zu einer Lösung von 3-(1-Methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol (Beispiel Ie, 25,0 mg, 0,12 mmol) in THF (1,5 ml) bei –78°C zugegeben und das Gemisch wurde 1 h gerührt. Phenylsulfonylchlorid (30 μl, 0,24 mmol) wurde zugegeben und das Gemisch 2 h bei Raumtemperatur gerührt, bevor es mit Wasser (4 Tropfen) und Silicagel (~1 g) versetzt wurde, um die Reaktion zu beenden. Eine Reinigung unter Verwendung von Festphasenextraktionsröhrchen (1000 mg Siliciumdioxid, wobei mit 0-10% 2 M methanolischem Ammoniak in Dichlormethan eluiert wurde) ergab 3-(1-Methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-phenylsulfonylindol (9,0 mg, 22%, HRMS-FAB+ für C20H20N2O2S: berechnet MH+: 353,13239; gefunden: 353,13235).
- Auf ähnliche Weise wurden die folgenden weiteren Verbindungen hergestellt:
- (b) 1-(4-Methoxyphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol: (9,0 mg, 20%); aus 3-(1-Methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ie, 24,8 mg, 0,12 mmol) und 4-Methoxyphenylsulfonylchlorid (48,2 mg, 0,23 mmol); HRMS-FAB+ für C21H22N2O3S: berechnet MH+: 383,14294; gefunden 383,14276.
- (c) 1-(4-Fluorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol: (9,0 mg, 21%); aus 3-(1-Methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ie, 24,8 mg, 0,12 mmol) und 4-Fluorphenylsulfonylchlorid (46,5 mg, 0,24 mmol); HRMS-FAB+ für C20H19N2O2SF: berechnet MH+: 371,12296; gefunden: 371,12323.
- (d) 1-(4-Bromphenylsulfonyl)-5-fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol: (43,8 mg, 90%) aus 5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ib, 25,0 mg, 0,108 mmol) und 4-Bromphenylsulfonylchlorid (56,4 mg, 0,22 mmol); HRMS-FAB+ für C20H18N2O2SFBr: berechnet MH+: 449,03348; gefunden: 449,03297.
- (e) 5-Fluor-1-(2,5-dichlorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol: (36,5 mg, 76%); aus 5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ib, 25,3 mg, 0,110 mmol) und 2,5-Dichlorphenylsulfonylchlorid (55,6 mg, 0,23 mmol); HRMS-FAB+ für C20H17N2O2SFCl2: berechnet MH+: 439,04501; gefunden: 439,04294.
- (f) 1-(4-Chlor-3-nitrophenylsulfonyl)-5-fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol: (39,1 mg, 79%); aus 5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ib, 25,4 mg, 0,110 mmol) und 4-Chlor-3-nitrophenylsulfonylchlorid (57,6 mg, 0,22 mmol); HRMS-FAB+ für C20H17N2O4SFCl: berechnet MH+: 450,06906; gefunden: 450,07176.
- (g) 5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(2,4,6-trimethylphenylsulfonyl)indol: (34,7 mg, 76%); aus 5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ib, 25,5 mg, 0,110 mmol) und 2,4,6-Trimethylphenylsulfonylchlorid (48,4 mg, 0,22 mmol); HRMS-FAB+ für C23H25N2O2SF: berechnet MH+: 413,16989; gefunden: 413,17396.
- (h) 5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(2,4,6-triisopropylphenylsulfonyl)indol: (25,8 mg, 48%); aus 5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ib, 24,9 mg, 0,108 mmol) und 2,4,6-Triisopropylphenylsulfonylchlorid (68,8 mg, 0,23 mmol); HRMS-FAB+ für C29H37N2O2SF: berechnet MH+: 497,26379; gefunden: 497,26112.
- (i) 5-Cyclohexyloxy-1-(4-methylphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol: (49,0 mg, 94%); aus 5-Cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4- pyridinyl)-1H-indol (Beispiel Ic, 35,0 mg, 0,112 mmol) und 4-Methylphenylsulfonylchlorid (41 mg, 0,22 mmol); HRMS-FAB+ für C27H32N2O3S: berechnet MH+: 465,22119; gefunden: 465,22309.
- (j) 6-Brom-1-(4-methoxyphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol: (24,5 mg, 62%); aus 6-Brom-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)1H-indol (Beispiel If, 25,0 mg, 0,086 mmol) und 4-Methoxyphenylsulfonylchlorid (35 mg, 0,17 mmol); HRMS-FAB+ für C21H21N2O3BrS: berechnet MH+: 461,05344; gefunden: 461,04886.
- (k) 6-Brom-1-(4-fluorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-indol: (20,9 mg, 54%); aus 6-Brom-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel If, 25,1 mg, 0,086 mmol) und 4-Fluorphenylsulfonylchlorid (35 mg, 0,18 mmol); HRMS-FAB+ für C20H18N2O2BrSF: berechnet MH+: 449,03348; gefunden: 449,02907.
- (l) 5-Cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(1-naphthylsulfonyl)indol: (35,9 mg, 87%); aus 5-Cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ic, 25,5 mg, 0,082 mmol) und 1-Naphthylsulfonylchlorid (37,7 mg, 0,17 mmol); HRMS-FAB+ für C30H32N2O3S: berechnet MH+: 501,22119; gefunden: 501,21807.
- (m) 5-Cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(2-naphthylsulfonyl)indol: (37,4 mg, 92%); aus 5-Cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ic, 25,2 mg, 0,081 mmol) und 2-Naphthylsulfonylchlorid (38,5 mg, 0,17 mmol); HRMS-FAB+ für C30H32N2O3S: berechnet MH+: 501,22119; gefunden: 501,22101.
- (n) 1-(2-Bromphenylsulfonyl)-5-cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol: (34,4 mg, 82%); aus 5-Cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ic, 24,5 mg, 0,079 mmol) und 2-Bromphenylsulfonylchlorid (40,2 mg, 0,16 mmol); HRMS-FAB+ für C26H29N2O3SBr: berechnet MH+: 529,11603; gefunden: 529,11380.
- (o) 5-Cyclohexyloxy-1-(2,5-dichlorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol: (37,3 mg, 89%); aus 5-Cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ic, 25,5 mg, 0,082 mmol) und 2,5-Dichlorphenylsulfonylchlorid (42,0 mg, 0,17 mmol); HRMS-FAB+ für C26H28N2O3SCl2: berechnet MH+: 519,12762; gefunden: 519,12579.
- (p) 5-Cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(2,4,6-trimethylphenylsulfonyl)indol: (31,6 mg, 78%); aus 5-Cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ic, 25,5 mg, 0,082 mmol) und 2,4,6-Trimethylphenylsulfonylchlorid (36,8 mg, 0,17 mmol); HRMS-FAB+ für C29H36N2O3S: berechnet MH+: 493,25250; gefunden: 493,25329.
- (q) 5-Cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(2,4,6-triisopropylphenylsulfonyl)indol: (23,3 mg, 50%); aus 5-Cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ic, 25,2 mg, 0,081 mmol) und 2,4,6-Triisopropylphenylsulfonylchlorid (53,7 mg, 0,18 mmol); HRMS-FAB+ für C35H48N2O3S: berechnet MH+: 577,34637; gefunden: 577,34710.
- (r) 5-Cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(3-nitrophenylsulfonyl)indol: (38,0 mg, 96%); aus 5-Cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ic, 24,8 mg, 0,080 mmol) und 3-Nitrophenylsulfonylchlorid (35,3 mg, 0,159 mmol); HRMS-FAB+ für C26H29N3O5S: berechnet MH+: 496,19061; gefunden: 496,19042.
- (s) 1-(4-Chlor-3-nitrophenylsulfonyl)-5-cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol: (37,4 mg, 87%); aus 5-Cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ic, 25,1 mg, 0,081 mmol) und 4-Chlor-3-nitrophenylsulfonylchlorid (42,7 mg, 0,17 mmol); HRMS-FAB+ für C26H28N3O5SCl: berechnet MH+: 530,15167; gefunden: 530,14727.
- (t) 5-Cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(3-nitro-4-trifluormethylphenylsulfonyl)indol: (33,9 mg, 75%); aus 5-Cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ic, 24,8 mg, 0,080 mmol) und 3-Nitro-4-trifluormethylphenylsulfonylchlorid (48,4 mg, 0,167 mmol); HRMS-FAB+ für C27H28N3O5SF3: berechnet MH+: 564,17798; gefunden: 564,17855.
- (u) 1-(4-Bromphenylsulfonyl)-5-cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol: (31,4 mg, 72%); aus 5-Cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ic, 25,7 mg, 0,083 mmol) und 4-Bromphenylsulfonylchlorid (43 mg, 0,17 mmol); HRMS-FAB+ für C26H29N2O3SBr: berechnet MH+: 529,11603; gefunden: 529,11817.
- (v) 5-Cyclohexyloxy-1-(4-methoxyphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol: (34,8 mg, 89%); aus 5-Cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ic, 25,2 mg, 0,081 mmol) und 4-Methoxyphenylsulfonylchlorid (34,1 mg, 0,165 mmol); HRMS-FAB+ für C27H32N2O4S: berechnet MH+: 481,21609; gefunden: 481,21625.
- (w) 5-Cyclohexyloxy-1-(4-fluorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol: (34,0 mg, 88%); aus 5-Cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ic, 25,5 mg, 0,082 mmol) und 4-Fluorphenylsulfonylchlorid (30,8 mg, 0,16 mmol); HRMS-FAB+ für C26H29N2O3SF: berechnet MH+: 469,19611; gefunden: 469,19626.
- (x) 1-(4-Chlorphenylsulfonyl)-5-cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol: (37,7 mg, 94%); aus 5-Cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ic, 25,5 mg, 0,082 mmol) und 4-Chlorphenylsulfonylchlorid (35,6 mg, 0,169 mmol); HRMS-FAB+ für C26H29N2O3SCl: berechnet MH+: 485,16656; gefunden: 485,16480.
- (y) 1-(4-t-Butylphenylsulfonyl)-5-cyclohexyloxy-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol: (34,0 mg, 81%); aus 5-Cyclohexyloxy-3-(1-methyl-1,2,3-6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ic, 25,6 mg, 0,082 mmol) und 4-t-Butylphenylsulfonylchlorid (37,2 mg, 0,16 mmol); HRMS-FAB+ für C30H38N2O3S: berechnet MH+: 507,26813; gefunden: 507,27183.
- (z) 1-(2-Bromphenylsulfonyl)-5-fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol: (32 mg, 53%), aus 5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ib, 30,6 mg, 0,133 mmol) und 2-Bromphenylsulfonylchlorid (67,9 mg, 0,27 mmol); HRMS-FAB+ für C20H19N2SO2BrF berechnet MH+: 449,03348; gefunden: 449,03240.
- (aa) 1-(4-Fluorphenylsulfonyl)-5-fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol: (30 mg, 57%), aus 5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ib) und 4-Fluorphenylsulfonylchlorid (52,9 mg, 0,27 mmol); HRMS-FAB+ für C20H19N2O2SF2 berechnet MH+: 389,11353; gefunden: 389,11544.
- (bb) 1-(4-Chlorphenylsulfonyl)-5-fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol: (28,1 mg, 53%), aus 5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ib, 30,1 mg, 0,131 mmol) und 4-Chlorphenylsulfonylchlorid (55,3 mg, 0,26 mmol); HRMS-FAB+ für C20H19N2O2SClF berechnet MH+: 405,08998; gefunden: 405,08291.
- (cc) 1-(4-t-Butylphenylsulfonyl)-5-fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol: (23,0 mg, 42%), aus 5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ib, 29,4 mg, 0,128 mmol) und 4-t-Butylphenylsulfonylchlorid (59,6 mg, 0,26 mmol); HRMS-FAB+ für C24H28N2O2SF berechnet MH+: 427,18555; gefunden: 427,18680.
- (dd) 5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(3-nitrophenylsulfonyl)indol: (31,0 mg, 56%), aus 5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ib, 30,1 mg, 0,131 mmol) und 3-Nitrophenylsulfonylchlorid (58,1 mg, 0,26 mmol); HRMS-FAB+ für C20H19N3O4SF berechnet MH+: 416,10803; gefunden 416,10631.
- (ee) 5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(1-naphthylsulfonyl)indol: (28,2 mg, 52%), aus 5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ib, 29,4 mg, 0,128 mmol) und 1-Naphthylsulfonylchlorid (58 mg, 0,26 mmol); HRMS-FAB+ für C24H22N2O2SF berechnet MH+: 421,13861; gefunden: 421,14099.
- (ff) 5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(2-naphthylsulfonyl)indol: (32,3 mg, 56%), aus 5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ib, 31,4 mg, 0,136 mmol) und 2-Naphthylsulfonylchlorid (61,7 mg, 0,27 mmol); HRMS-FAB+ für C24H22N2O2SF berechnet MH+: 421,13861; gefunden: 421,13866.
- (gg) 5-Chlor-1-(4-fluorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol: aus 5-Chlor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Id, 25 mg, 0,1 mmol) und 4-Fluorphenylsulfonylchlorid (29,1 mg, 0,15 mmol). Der HCl-Salz-Ether (32,6 mg, 74%) wurde aus dem Rohprodukt hergestellt, wobei 1 M HCl in Ether verwendet wurde. Schmelzpunkt 256-7°C, HRMS-FAB+ für C20H18N2O2SClF·HCl, berechnet MW+(-HCl): 405,08398; gefunden: 405,0797.
- (hh) 1-(4-Fluorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethoxyindol: aus 3-(1-Methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethoxy-1H-indol (Beispiel Ih, 20 mg, 0,068 mmol) und 4-Fluorphenylsulfonylchlorid (20,8 mg, 0,11 mmol). Das HCl-Salz (24,0 mg, 69%) wurde aus dem Rohprodukt hergestellt, wobei 1 M HCl in Ether verwendet wurde. HRMS-FAB+ für C21H18N2O3SF4·HCl, berechnet MH+(-HCl): 455,10526; gefunden: 455,10735.
- (ii) 1-(4-t-Butylphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethoxyindol: aus 3-(1-Methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethoxy-1H-indol (Beispiel Ih, 20 mg, 0,068 mmol) und 4-t-Butylphenylsulfonylchlorid (24,9 mg, 0,11 mmol). Das HCl-Salz (9,4 mg, 25%) wurde aus dem Rohprodukt hergestellt, wobei 1 M HCl in Ether verwendet wurde. HRMS-FAB+ für C25H27N2O3SF3·HCl, berechnet MH+(-HCl): 493,17728; gefunden: 493,17565.
- (jj) 1-(4-Chlorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethoxyindol: aus 3-(1-Methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethoxy-1H-indol (Beispiel Ih, 20 mg, 0,068 mmol) und 4-Chlorphenylsulfonylchlorid (22,5 mg, 0,11 mmol). Das HCl-Salz (21,8 mg, 60%) wurde aus dem Rohprodukt hergestellt, wobei 1 M HCl in Ether verwendet wurde. HRMS-FAB+ für C21H18N2O3SClF3·HCl, berechnet MH+(-HCl): 473,07275; gefunden: 473,07154.
- (kk) 1-(4-Methylphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethoxyindol: aus 3-(1-Methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethoxy-1H-indol (Beispiel Ih, 20 mg, 0,068 mmol) und 4-Methylphenylsulfonylchlorid (20,4 mg, 0,11 mmol). Das HCl-Salz (17,0 mg, 49%) wurde aus dem Rohprodukt hergestellt, wobei 1 M HCl in Ether verwendet wurde. HRMS-FAB+ für C22H21N2O3SF3·HCl, berechnet MH+(-HCl): 451,13031; gefunden: 451,12820.
- (ll) 1-(4-Methoxyphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethoxyindol: aus 3-(1-Methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethoxy-1H-indol (Beispiel Ih, 20 mg, 0,068 mmol) und 4-Methoxyphenylsulfonylchlorid (22,1 mg, 0,11 mmol). Das HCl-Salz (15,8 mg, 44%) wurde aus dem Rohprodukt hergestellt, wobei 1 M HCl in Ether verwendet wurde. HRMS-FAB+ für C22H21N2O4SF3·HCl, berechnet MH+(-HCl): 467,12524; gefunden: 467,12526.
- (mm) 1-(4-Fluorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethylindol-hydrochlorid: (15,0 mg, 44%); aus 3-(1-Methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethyl-1H-indol (Beispiel Ii, 20 mg, 0,071 mmol) und 4-Fluorphenylsulfonylchlorid (20,8 mg, 0,107 mmol). HRMS-FAB+ für C21H18N2O2SF4·HCl, berechnet MH+(-HCl): 439,11035; gefunden: 439,10807.
- (nn) 1-(4-t-Butylphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethylindol-hydrochlorid: (8,7 mg, 24%); aus 3-(1-Methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethyl-1H-indol (Beispiel Ii, 20 mg, 0,071 mmol) und 4-t-Butylphenylsulfonylchlorid (24,9 mg, 0,11 mmol). HRMS-FAB+ für C25H27N2O2SF3·HCl, berechnet MH+(-HCl): 477,18237; gefunden: 477,18134.
- (oo) 1-(4-Chlorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethylindol-hydrochlorid: (11,5 mg, 33%); aus 3-(1-Methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethyl-1H-indol (Beispiel Ii, 20 mg, 0,071 mmol) und 4-Chlorphenylsulfonylchlorid (22,5 mg, 0,11 mmol). HRMS-FAB+ für C21H18ClF3N2O2S·HCl, berechnet MH+(-HCl): 455,08078; gefunden: 455,08266.
- (pp) 1-(4-Methoxyphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethylindol-hydrochlorid: (22,2 mg, 69%); aus 3-(1-Methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethyl-1H-indol (Beispiel Ii, 20 mg, 0,071 mmol) und 4-Methoxyphenylsulfonylchlorid (22,1 mg, 0,107 mmol). HRMS-FAB+ für C22H21N2O3SF3·HCl, berechnet MH+: 451,13031; gefunden: 451,13007.
- (qq) 1-(4-Methylphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethylindol-hydrochlorid: (14,8 mg, 48%); aus 3-(1-Methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethyl-1H-indol (Beispiel Ii, 20 mg, 0,071 mmol) und 4-Methylphenylsulfonylchlorid (20,4 mg, 0,107 mmol). HRMS-FAB+ für C22H21N2O2SF3HCl, berechnet MH+: 435,13541; gefunden: 435,13700.
- (rr) 5-Cyclohexyloxy-1-(4-methylphenylsulfonyl)-3-(1-methyl-4-piperidinyl)indol (12,0 mg, 51%); aus 5-Cyclohexyloxy-3-(1-methyl-4-piperidinyl)-1H-indol (Beispiel 2a, 15,7 mg, 0,05 mmol) und 4-Methylphenylsulfonylchlorid (50 mg, 0,26 mmol); HRMS-FAB+ für C27H34N2O3S: berechnet MH+: 467,23685; gefunden: 467,23882.
- (ss) 5-Chlor-1-(4-fluorphenylsulfonyl)-3-(1-methyl-4-piperidinyl)indol (18,4 mg, 45%) aus 5-Chlor-3-(1-methyl-4-piperidinyl)-1H-indol (Beispiel 2e, 25 mg, 0,1 mmol) und 4-Fluorphenylsulfonylchlorid (29,2 mg, 0,15 mmol), HRMS-FAB+ für C20H20N2O2SClF, berechnet MH+: 407,09964; gefunden: 407,09685.
- (tt) 1-(4-Fluorphenylsulfonyl)-3-(1-methyl-4-piperidinyl)indol: (17,0 mg, 46%), aus 3-(1-Methyl-4-piperidinyl)-1H-indol (Beispiel 2d, 21,5 mg, 0,1 mmol) und 4-Fluorphenylsulfonylchlorid (29,2 mg, 0,15 mmol), HRMS-FAB+ für C20H21N2O2SF, berechnet MH+: 373,13861; gefunden 373,13669.
- (uu) 1-(4-Fluorphenylsulfonyl)-6-chlor-3-(1-methyl-4-piperidinyl)indol: 26,8 mg, 65%), aus 6-Chlor-3-(1-methyl-4-piperidinyl)-1H-indol (Beispiel 2b, 25 mg, 0,10 mmol) und 4-Fluorphenylsulfonylchlorid (29,2 mg, 0,15 mmol), HRMS-FAB+ für C20H20N2O2SClF, berechnet MH+: 407,09964; gefunden: 407,09929.
- (vv) 1-(4-Fluorphenylsulfonyl)-5-fluor-3-(1-methyl-4-piperidinyl)indol: (22,6 mg, 58%) aus 5-Fluor-3-(1-methyl-4-piperidinyl)-1H-indol (Beispiel 2c, 25 mg, 0,1 mmol) und 4-Fluorphenylsulfonylchlorid (29,2 mg, 0,15 mmol), HRMS-FAB+ für C20H20N2O2SF2, berechnet MH+: 391,12918; gefunden 391,22926.
- (ww) 5,7-Difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(4-methylphenylsulfonyl)indol: (8,8 mg, 54%); aus 5,7-Difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ig, 10 mg, 0,04 mmol) und 4-Methylphenylsulfonylchlorid (11,4 mg, 0,06 mmol) mit 1 M NaN(TMS)2 (60 μl, 0,06 mmol) in THF (0,5 ml) bei RT.
- (xx) 5,7-Difluor-1-(4-fluorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol: (7,6 mg, 46,4%) aus 5,7-Difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ig, 10 mg, 0,04 mmol) und 4-Fluorphenylsulfonylchlorid (11,7 mg, 0,06 mmol) mit 1 M NaN(TMS)2 (60 μl, 0,06 mmol) in THF (0,5 ml) bei RT.
- (yy) 1-(4-Bromphenylsulfonyl)-5,7-difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol: (8,7 mg, 48%); aus 5,7-Difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ig, 10 mg, 0,04 mmol) und 4-Bromphenylsulfonylchlorid (15,3 mg, 0,06 mmol) mit 1 M NaN(TMS)2 (60 μl, 0,06 mmol) in THF (0,5 ml) bei RT.
- (zz) 1-(4-Chlorphenylsulfonyl)-5,7-difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol: (6,7 mg, 39%); aus 5,7-Difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ig, 10 mg, 0,04 mmol) und 4-Chlorphenylsulfonylchlorid (12,7 mg, 0,06 mmol) mit 1 M NaN(TMS)2 (60 μl, 0,06 mmol) in THF (0,5 ml) bei RT.
- (aaa) 5,7-Difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(1-naphthylsulfonyl)indol: (9,2 mg, 52%); aus 5,7 Difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ig, 10 mg, 0,04 mmol) und 1-Naphthalinsulfonylchlorid (13,6 mg, 0,06 mmol) mit 1 M NaN(TMS)2 (60 μl, 0,06 mmol) in THF (0,5 ml) bei RT.
- (bbb) 5,7-Difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(2-naphthylsulfonyl)indol: 5,1 mg, 29%); aus 5,7-Difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ig, 10 mg, 0,04 mmol) und 2-Naphthalinsulfonylchlorid (13,6 mg, 0,06 mmol) mit 1 M NaN(TMS)2 (60 μl, 0,06 mmol) in THF (0,5 ml) bei RT.
- (ccc) 5,7-Difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(2,4,6-trimethylphenyl)sulfonylindol: (5,7 mg, 33%); aus 5,7-Difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1H-indol (Beispiel Ig, 10 mg, 0,04 mmol) und 2,4,6-Trimethylphenylsulfonylchlorid (13,1 mg, 0,06 mmol) mit 1 M NaN(TMS)2 (60 μl, 0,06 mmol) in THF (0,5 ml).
- Beispiel 5: Bindungsaffinität für den 5-HT6-Rezeptor
- Alle Verbindungen der Erfindung wurden unter Verwendung von Zelltypen bewertet, die spezifisch für den 5-HT6-Rezeptor empfänglich sind (zur Klonierung und Charakterisierung des menschlichen 5-HT6-Rezeptors siehe Kohen, et al. J. Neurochemistry, 66, 1996: 47-56). Das Assayprotokoll umfasste im Allgemeinen die Inkubation von Membranen, die aus Zellen, welche den 5-HT6-Rezeptor exprimieren, hergestellt wurden, mit 3H-LSD. Zunehmende Spiegel der Testverbindung wurden mit dem Radioliganden inkubiert und die Membranhomogenate aus den rekombinanten Zellen hergestellt. Nach einer 60minütigen Inkubation bei 37°C wurde die Inkubation durch Vakuumfiltration beendet. Die Filter wurden mit Puffer gewaschen und die Filter wurden unter Verwendung einer Flüssigszintillationsspektrometrie auf Radioaktivität hin ausgezählt. Die Affinität der Testverbindung für den 5-HT6-Rezeptor wurde durch Computer-unterstützte Analyse der Daten und Bestimmen der Menge der Verbindung bestimmt, die zum Hemmen von 50% der Bindung des Radioliganden an den Rezeptor erforderlich ist. Es wurden Konzentrationen im Bereich von 10–11 M bis 10–5 M der Testverbindung bewertet. Zum Vergleich wurde die Affinität von Clozapin für den 5-HT6-Rezeptor (Ki ~3 nM) als Standard verwendet. Alle Verbindungen der Erfindung wiesen eine Affinität für den menschlichen 5-HT6-Rezeptor mit Ki-Werten von nicht mehr als 1000 nM auf. Bevorzugte Verbindungen, diejenigen der Beispiele 3b, 4a, 4b, 4c, 4d, 4e, 4f, 4g, 4i, 4k, 4z, 4aa, 4bb, 4ee, 4gg, 4jj, 4kk, 4gg, 4ww, 4yy, 4zz, 4aaa und 4bbb wiesen Ki-Werte von nicht mehr als 50 nM auf. Besonders bevorzugte Verbindungen, diejenigen der Beispiele 3b, 4a, 4c, 4z, 4aa, 4bb, 4ee, 4gg, 4jj, 4kk, 4ww, 4yy, 4zz, 4aaa, 4bbb wiesen Ki-Werte von nicht mehr als 5 nM auf. Die Verbindungen der Erfindung banden auch an den menschlichen 5-HT6-Rezeptor auf eine selektive Weise, bezogen auf die menschlichen 5-HT2c- und 5-HT7-Rezeptoren. Das heißt, die Verbindungen der Erfindung banden an den menschlichen 5-HT6-Rezeptor mit einer wenigstens 2fach größeren Affinität, bezogen auf die menschlichen 5-HT2C- und 5-HT7-Rezeptoren. Bevorzugte Verbindungen, z. B. diejenigen der Beispiele 3b, 4i, 4z, 4bb, 4ee und 4ff banden an den menschlichen 5-HT6-Rezeptor mit einer wenigstens 60fach größeren Affinität, bezogen auf die menschlichen 5-HT2C- und 5-HT7-Rezeptoren. Mehr bevorzugte Verbindungen, z. B. diejenigen von Beispiel 4ee, banden an den menschlichen 5-HT6-Rezeptor mit einer wenigstens 300fach größeren Affinität, bezogen auf die menschlichen 5-HT2C- und 5-HT7-Rezeptoren.
- Beispiel 6: Wirkung von Verbindungen auf die cAMP-Reaktion von menschlichen 5-HT6-Rezeptoren
- Die Antagonisteneigenschaft (oder Agonisteneigenschaft) von Verbindungen für menschliche 5-HT6-Rezeptoren wurde durch Testen ihrer Wirkung auf die cAMP-Akkumulation in stabil transfizierten HEK293-Zellen bestimmt.
- Das Binden eines Agonisten an den menschlichen 5-HT6-Rezeptor führt zu einer Zunahme der Adenylcyclase-Aktivität. Eine Verbindung, welche ein Agonist ist, zeigt eine Zunahme der cAMP-Produktion und eine Verbindung, welche ein Antagonist ist, blockiert die Agonistenwirkung.
- Zellassay: Menschliche 5-HT6-Rezeptoren wurden in HEK293-Zellen kloniert und stabil exprimiert. Diese Zellen wurden in Platten mit 6 Vertiefungen in DMEM/F12-Medium mit 10% fötalem Kälberserum (FCS) und 500 μg/ml G418 ausplattiert und bei 37°C in einem CO2-Inkubator inkubiert. Die Zellen wurden vor dem Beginn des Experiments bis zu ungefähr 70% Konfluenz wachsen gelassen.
- Am Tag des Experiments wurde das Kulturmedium entfernt und die Zellen wurden einmal mit serumfreiem Medium (SFM) gewaschen. Zwei ml SFM + IBMX-Medium wurden zugegeben und 10 min bei 37°C inkubiert. Das Medium wurde entfernt und frisches SMF + IBMX-Medium, das verschiedene Verbindungen enthielt, und 1 μM Serotonin (als Antagonist) wurde zu den entsprechenden Vertiefungen zugegeben und 30 min inkubiert. Nach der Inkubation wurde das Medium entfernt und die Zellen wurden einmal mit 1 ml PBS (Phosphatgepufferter Kochsalzlösung) gewaschen. Jede Vertiefung wurde mit 1 ml kaltem 95%igem Ethanol und 5 mM EDTA (2:1) bei 4°C 1 Stunde lang behandelt. Die Zellen wurden dann abgekratzt und in Eppendorf-Röhrchen überführt. Die Röhrchen wurden 5 min bei 4°C zentrifugiert und die Überstände wurden bis zum Test bei 4°C aufbewahrt.
- cAMP-Messung: der cAMP-Gehalt wurde durch EIA (Enzym-Immunassay) unter Verwendung des Amersham Biotrak cAMP EIA-Kits (Amersham RPN 225) bestimmt. Das verwendete Verfahren ist wie für den Kit beschrieben. Kurz gesagt wird cAMP bestimmt durch die Konkurrenz zwischen unmarkiertem cAMP und einer festgesetzten Menge von Peroxidasemarkiertem cAMP um die Bindungsstellen an einem Anti-cAMP-Antikörper. Der Antikörper ist auf Polystyrol-Mikrotiterplatten-Vertiefungen immobilisiert, die mit einem zweiten Antikörper vorbeschichtet sind. Die Reaktion wird durch Zugeben von 50 μl Peroxidase-markiertem cAMP zu der Probe (100 μl), die mit dem Antiserum (100 μl) 2 Stunden bei 4°C vorinkubiert wurde, gestartet. Nach 1 Stunde Inkubation bei 4°C wird der ungebundene Ligand durch ein einfaches Waschverfahren abgetrennt. Dann wird ein Enzymsubstrat, Tetramethylbenzidin (TMB), zugegeben und 60 min bei Raumtemperatur inkubiert. Die Reaktion wird durch die Zugabe von 100 μl 1,0 M Schwefelsäure angehalten und die resultierende Farbe mit einem Mikrotiterplatten-Spektrofotometer bei 450 nM innerhalb von 30 Minuten abgelesen.
- Alle Verbindungen der Erfindung, welche in den vorstehenden Assays getestet wurden, erwiesen sich als Antagonisten. Die Stärke der Verbindungen der Erfindung als Antagonisten ist als ein EC50-Wert angegeben, welcher die Konzentration ist, die eine 50%ige Hemmung der Serotonin-stimulierten cAMP-Reaktion verursacht.
Claims (14)
- Verbindung nach Formel I und Salze, Solvate oder Hydrate davon: worin: R1 ausgewählt ist aus der Gruppe bestehend aus H und C1-4-Alkyl; R2 ausgewählt ist aus der Gruppe bestehend aus H, C1-4-Alkyl und Benzyl; --- eine Einfach- oder Doppelbindung bedeutet; R3 SO2R5 bedeutet; R4a ausgewählt ist aus der Gruppe bestehend aus H, OH, Halogen, C1-4-Alkyl und C1-4-Alkoxy; R4b ausgewählt ist aus der Gruppe bestehend aus H, Hydroxy, Halogen, C3-7-Cycloalkyloxy, C1-4-Alkoxy, C1-4-Alkyl, Benzyloxy, Phenoxy, Trifluormethyl, Trifluormethoxy und Vinyl; R4c ausgewählt ist aus der Gruppe bestehend aus H, OH, Halogen, C1-4-Alkyl und C1-4-Alkoxy; R4d ausgewählt ist aus der Gruppe bestehend aus H, OH, Halogen, C1-4-Alkyl und C1-4-Alkoxy; und R5 ausgewählt ist aus der Gruppe bestehend aus Phenyl, Pyridyl, Thienyl, Chinolinyl und Naphthyl, welche gegebenenfalls substituiert sind mit 1-4 Substituenten, ausgewählt aus C1-4-Alkoxy, C1-4-Alkyl, Halogen, Nitro, Trifluormethyl, Trifluormethoxy, 1,2-Methylendioxy, C1-4-Alkylcarbonyl, C1-4-Alkoxycarbonyl und C1-4-AlkylS-.
- Verbindung nach Anspruch 1, worin R1 Methyl ist.
- Verbindung nach Anspruch 1, worin R2 H ist.
- Verbindung nach Anspruch 1, worin R5 ausgewählt ist aus der Gruppe bestehend aus Phenyl, Naphthyl und Thienyl, welche alle gegebenenfalls mit 1-3 Gruppen substituiert sind, die unabhängig voneinander ausgewählt sind aus Methyl, Methoxy, Halogen, Trifluormethyl und 1,2-Methylendioxy.
- Verbindung nach Anspruch 4, worin R5 ausgewählt ist aus der Gruppe bestehend aus Naphthyl und Phenyl, gegebenenfalls substituiert mit 1-3 Substituenten, die unabhängig voneinander ausgewählt sind aus Chlor, Brom, Fluor, Nitro, Methyl und Methoxy.
- Verbindung nach Anspruch 5, worin R5 ausgewählt ist aus der Gruppe bestehend aus 2-Chlorphenyl, 2-Bromphenyl, 1-Naphthyl, 4-Fluorphenyl, 4-Chlorphenyl, 4-Bromphenyl, 2,4-Dichlorphenyl, 3-Nitro-4-chlorphenyl, 2,4,6-Trimethylphenyl, 4-Methyoxyphenyl und 4-Methylphenyl.
- Verbindung nach Anspruch 1, worin R4a, R4c und R4d H sind und R4b ausgewählt ist aus H, Halogen, Methyl, Trifluormethyl und Methoxy.
- Verbindung nach Anspruch 1, worin F4b und R4d Halogen sind.
- Verbindung nach Anspruch 1, worin --- eine Doppelbindung bedeutet.
- Verbindung nach Anspruch 1, welche ausgewählt ist aus: 5-Fluor-1-(4-methylphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol; 1-(4-Methoxyphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol; 1-(4-Fluorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol; 1-(4-Bromphenylsulfonyl)-5-fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol; 5-Fluor-1-(2,5-dichlorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol; 1-(4-Chlor-3-nitrophenylsulfonyl)-5-fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol; 5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(2,4,6-trimethylphenylsulfonyl)indol; 5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(2,4,6-triisopropylphenylsulfonyl)indol; 5-Cyclohexyloxy-1-(4-methylphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol; 1-(4-Fluorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethylindol-hydrochlorid; 1-(4-t-Butylphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethylindol-hydrochlorid; 1-(4-Chlorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethylindol-hydrochlorid; 1-(4-Methoxyphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethylindol-hydrochlorid; 1-(4-Methylphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethylindol-hydrochlorid; 5-Cyclohexyloxy-1-(4-methylphenylsulfonyl)-3-(1-methyl-4-piperidinyl)indol; 5-Chlor-1-(4-fluorphenylsulfonyl)-3-(1-methyl-4-piperidinyl)indol; 1-(4-Fluorphenylsulfonyl)-3-(1-methyl-4-piperidinyl)indol; 1-(4-Fluorphenylsulfonyl)-6-chlor-3-(1-methyl-4-piperidinyl)indol; 1-(4-Fluorphenylsulfonyl)-5-fluor-3-(1-methyl-4-piperidinyl)indol; 5,7-Difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(4-methylphenylsulfonyl)indol; 5,7-Difluor-1-(4-fluorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol; 1-(4-Bromphenylsulfonyl)-5,7-difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol; 1-(4-Chlorphenylsulfonyl)-5,7-difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol; 5,7-Difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(1-naphthylsulfonyl)indol; 5,7-Difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(2-naphthylsulfonyl)indol; und 5,7-Difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(2,4,6-trimethylphenyl)sulfonylindol.
- Verbindung nach Anspruch 1, welche ausgewählt ist aus: 5-Fluor-1-(4-methylphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol; 1-(4-Methoxyphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol; 1-(4-Fluorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol; 1-(4-Bromphenylsulfonyl)-5-fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol; 5-Fluor-1-(2,5-dichlorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol; 5-Chlor-1-(4-fluorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol; 1-(4-Chlorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethoxyindol; 1-(4-Methylphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethoxyindol; 1-(4-Chlorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethylindol-hydrochlorid; 1-(4-Methoxyphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethylindol-hydrochlorid; 1-(4-Methylphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethylindol-hydrochlorid; 5,7-Difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(4-methylphenylsulfonyl)indol; 1-(4-Bromphenylsulfonyl)-5,7-difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol; 1-(4-Chlorphenylsulfonyl)-5,7-difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol; 5,7-Difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(2-naphthylsulfonyl)indol; und 5,7-Difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(1-naphthylsulfonyl)indol.
- Verbindung nach Anspruch 1, welche ausgewählt ist aus: 5-Fluor-1-(4-methylphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol; 1-(4-Fluorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol; 1-(2-Bromphenylsulfonyl)-5-fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol; 1-(4-Fluorphenylsulfonyl)-5-fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol; 1-(4-Chlorphenylsulfonyl)-5-fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol; 5-Fluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(1-naphthylsulfonyl)indol; 5-Chlor-1-(4-fluorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol; 1-(4-Chlorphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethoxyindol; 1-(4-Methylphenylsulfonyl)-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-5-trifluormethoxyindol; 5,7-Difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(4-methylphenylsulfonyl)indol; 1-(4-Bromphenylsulfonyl)-5,7-difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol; 1-(4-Chlorphenylsulfonyl)-5,7-difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)indol; 5,7-Difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(1-naphthylsulfonyl)indol; und 5,7-Difluor-3-(1-methyl-1,2,3,6-tetrahydro-4-pyridinyl)-1-(2-naphthylsulfonyl)indol.
- Verwendung der Verbindung nach einem der Ansprüche 1 bis 12 bei der Herstellung eines Medikaments für die Behandlung oder Verhütung von Störungen des Zentralnervensystems.
- Verwendung nach Anspruch 13, wobei die Störungen des Zentralnervensystems eine Psychose, Schizophrenie, manische Depression, Depression, die Parkinson-Krankheit, neurologische Störungen, Gedächtnisstörungen, die amyotrophe Lateralsklerose, die Alzheimer-Krankheit oder Chorea Huntington sind.
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| PCT/CA1999/000342 WO2000063203A1 (en) | 1999-04-21 | 1999-04-21 | Piperidine-indole compounds having 5-ht6 affinity |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| DE69937372D1 DE69937372D1 (de) | 2007-11-29 |
| DE69937372T2 true DE69937372T2 (de) | 2008-06-26 |
Family
ID=4173364
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE69937372T Expired - Lifetime DE69937372T2 (de) | 1999-04-21 | 1999-04-21 | Piperidin-indol derivate mit 5-ht6 affinität |
Country Status (9)
| Country | Link |
|---|---|
| EP (1) | EP1173432B9 (de) |
| JP (1) | JP4597386B2 (de) |
| AT (1) | ATE375990T1 (de) |
| AU (1) | AU778682B2 (de) |
| CA (1) | CA2370147C (de) |
| DE (1) | DE69937372T2 (de) |
| ES (1) | ES2291024T4 (de) |
| MX (1) | MXPA01010655A (de) |
| WO (1) | WO2000063203A1 (de) |
Families Citing this family (30)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1803720A1 (de) * | 2000-12-22 | 2007-07-04 | Wyeth a Corporation of the State of Delaware | Hetorocyclindazole und -Azaindazole Verbindungen als 5-Hydroxytryptamine-6 Liganden |
| MXPA03005432A (es) * | 2000-12-22 | 2003-09-10 | Wyeth Corp | Compuestos de heterociclilindazol y -azaindazol como ligandos de 5-hidroxitriptamina-6. |
| ATE340795T1 (de) | 2001-01-30 | 2006-10-15 | Lilly Co Eli | Benzolsulfonsäureester-indol-5-yl als 5-ht6 rezeptor-antagonisten |
| EP1401813B1 (de) * | 2001-06-07 | 2007-02-07 | F. Hoffman-la Roche AG | Neue indolderivate mit affinität zum 5-ht6-rezeptor |
| ITRM20010356A1 (it) * | 2001-06-21 | 2002-12-23 | Sigma Tau Ind Farmaceuti | "5-alogeno derivati della triptamina utili come ligandi del recettore5-ht6 e/o 5-ht7 della serotonina. |
| TW200301251A (en) * | 2001-12-20 | 2003-07-01 | Wyeth Corp | Azaindolylalkylamine derivatives as 5-hydroxytryptamine-6 ligands |
| WO2003065046A2 (en) * | 2002-02-01 | 2003-08-07 | Bayer Healthcare Ag | Diagnostics and therapeutics for diseases associated with a new human 5-ht6 receptor |
| BRPI0308696B8 (pt) * | 2002-03-27 | 2021-05-25 | Axovant Sciences Gmbh | composto derivado de quinolina, seu processo de preparação, sua composição farmacêutica e seus usos |
| BRPI0315959C1 (pt) * | 2002-11-28 | 2021-05-25 | Suven Life Sciences Ltd | composto, composição farmacêutica, uso do composto, método para o tratamento, método para reduzir a morbidez e a mortalidade associadas com o excesso de peso e processo para a preparação do composto |
| EP1592690A1 (de) | 2003-02-14 | 2005-11-09 | Wyeth | Heterocyclyl-3-sulfonylazaindol- oder -azaindazolderivate als 5-hydroxytryptamin-6-liganden |
| WO2005005439A1 (en) * | 2003-07-09 | 2005-01-20 | Suven Life Sciences Limited | Benzothiazino indoles |
| PT1558582E (pt) | 2003-07-22 | 2006-05-31 | Arena Pharm Inc | Derivados de diaril- e aril-heteroaril-ureia como moduladores do receptor de serotonina 5-ht2a uteis para a profilaxia e tratamento de desordens relacionadas com o mesmo |
| GB0321473D0 (en) * | 2003-09-12 | 2003-10-15 | Glaxo Group Ltd | Novel compounds |
| CA2637531A1 (en) * | 2006-02-17 | 2007-08-30 | Memory Pharmaceuticals Corporation | Compounds having 5-ht6 receptor affinity |
| AU2007343063B2 (en) | 2007-01-08 | 2011-02-17 | Suven Life Sciences Limited | 5-(Heterocyclyl)alkyl-N-(arylsulfonyl)indole compounds and their use as 5-HT6 ligands |
| US8507469B2 (en) | 2007-03-23 | 2013-08-13 | Abbott Gmbh & Co. Kg | Azetidin compounds suitable for treating disorders that respond to modulation of the serotonin 5-HT6 receptor |
| BRPI0809873A2 (pt) | 2007-05-03 | 2018-11-13 | Suven Life Sciences Ltd | "composto, processo para a preparação do composto, método para o tratamento de uma desordem do sistema nervoso central, composição farmacêutica, uso do composto, método para testar antagonistas e antagonistas com seletividade para o receptor 5-th6 e método de tratamento" |
| CN101835748B (zh) | 2007-10-26 | 2012-11-14 | 苏文生命科学有限公司 | 氨基芳基磺胺化合物及其作为5-ht6配体的用途 |
| EP2508177A1 (de) | 2007-12-12 | 2012-10-10 | Glaxo Group Limited | Kombinationen mit 3-phenylsulfonyl-8-piperazinyl-1yl-chinolin |
| WO2009123714A2 (en) | 2008-04-02 | 2009-10-08 | Arena Pharmaceuticals, Inc. | Processes for the preparation of pyrazole derivatives useful as modulators of the 5-ht2a serotonin receptor |
| WO2010032257A1 (en) | 2008-09-17 | 2010-03-25 | Suven Life Sciences Limited | Aryl indolyl sulfonamide compounds and their use as 5-ht6 ligands |
| EP2346847B1 (de) | 2008-09-17 | 2013-05-15 | Suven Life Sciences Limited | Arylsulfonamidaminverbindungen und deren verwendung als 5-ht6-liganden |
| WO2010062321A1 (en) | 2008-10-28 | 2010-06-03 | Arena Pharmaceuticals, Inc. | Processes useful for the preparation of 1-[3-(4-bromo-2-methyl-2h-pyrazol-3-yl)-4-methoxy-phenyl]-3-(2,4-difluoro-phenyl)-urea and crystalline forms related thereto |
| CA2786072C (en) | 2010-01-05 | 2014-10-28 | Suven Life Sciences Limited | Sulfone compounds as 5-ht6 receptor ligands |
| WO2015090233A1 (en) | 2013-12-20 | 2015-06-25 | Sunshine Lake Pharma Co., Ltd. | Aromatic heterocyclic compounds and their application in pharmaceuticals |
| EP3166924B1 (de) | 2014-07-08 | 2019-02-20 | Sunshine Lake Pharma Co., Ltd. | Aromatische heterocyclische derivate und pharmazeutische anwendungen davon |
| WO2016201373A1 (en) | 2015-06-12 | 2016-12-15 | Axovant Sciences Ltd. | Diaryl and arylheteroaryl urea derivatives useful for the prophylaxis and treatment of rem sleep behavior disorder |
| WO2017011767A2 (en) | 2015-07-15 | 2017-01-19 | Axovant Sciences Ltd. | Diaryl and arylheteroaryl urea derivatives as modulators of the 5-ht2a serotonin receptor useful for the prophylaxis and treatment of hallucinations associated with a neurodegenerative disease |
| CN116917305A (zh) * | 2020-12-07 | 2023-10-20 | 明德赛特制药公司 | 用于治疗cns病症的作为血清素能剂的3-环状胺-吲哚衍生物 |
| CA3229361A1 (en) * | 2021-08-20 | 2023-02-23 | Abdelmalik Slassi | 3-cycloamino-indole compounds as serotonergic agents useful for the treatment of disorders related thereto |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| IE58370B1 (en) * | 1985-04-10 | 1993-09-08 | Lundbeck & Co As H | Indole derivatives |
| DK158590D0 (da) * | 1990-07-02 | 1990-07-02 | Lundbeck & Co As H | Indolderivater |
| TW263508B (de) * | 1991-02-12 | 1995-11-21 | Pfizer | |
| US5846982A (en) * | 1996-06-14 | 1998-12-08 | Eli Lilly And Company | Inhibition of serotonin reuptake |
-
1999
- 1999-04-21 AT AT99915418T patent/ATE375990T1/de not_active IP Right Cessation
- 1999-04-21 WO PCT/CA1999/000342 patent/WO2000063203A1/en not_active Ceased
- 1999-04-21 DE DE69937372T patent/DE69937372T2/de not_active Expired - Lifetime
- 1999-04-21 JP JP2000612293A patent/JP4597386B2/ja not_active Expired - Fee Related
- 1999-04-21 MX MXPA01010655A patent/MXPA01010655A/es active IP Right Grant
- 1999-04-21 AU AU34035/99A patent/AU778682B2/en not_active Ceased
- 1999-04-21 CA CA002370147A patent/CA2370147C/en not_active Expired - Fee Related
- 1999-04-21 ES ES99915418T patent/ES2291024T4/es not_active Expired - Lifetime
- 1999-04-21 EP EP99915418A patent/EP1173432B9/de not_active Expired - Lifetime
Also Published As
| Publication number | Publication date |
|---|---|
| ATE375990T1 (de) | 2007-11-15 |
| CA2370147A1 (en) | 2000-10-26 |
| AU778682B2 (en) | 2004-12-16 |
| AU3403599A (en) | 2000-11-02 |
| EP1173432A1 (de) | 2002-01-23 |
| DE69937372D1 (de) | 2007-11-29 |
| ES2291024T3 (es) | 2008-02-16 |
| EP1173432B9 (de) | 2008-10-15 |
| CA2370147C (en) | 2009-07-28 |
| ES2291024T4 (es) | 2009-03-01 |
| EP1173432B1 (de) | 2007-10-17 |
| JP2002542241A (ja) | 2002-12-10 |
| MXPA01010655A (es) | 2002-11-04 |
| JP4597386B2 (ja) | 2010-12-15 |
| WO2000063203A1 (en) | 2000-10-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DE69937372T2 (de) | Piperidin-indol derivate mit 5-ht6 affinität | |
| DE69911798T2 (de) | Bicyclische piperidin- und piperazin-verbindungen mit 5-ht6-rezeptor-affinität | |
| DE69233038T2 (de) | Anxiolytisch wirkende Piperidin-Derivate | |
| DE68920482T2 (de) | 1-Indolylalkyl-4-(substituierte Pyridinyl)-Piperazine. | |
| US6100291A (en) | Pyrrolidine-indole compounds having 5-HT6 affinity | |
| DE60014083T2 (de) | Substituierte heterocyclylkondensierte gamma carboline | |
| DE69929704T2 (de) | Tetrahydrobenzazepin-derivate verwendbar als dopamin-d3-rezeptor-modulatoren (antipsychotische mittel) | |
| DE602005005167T2 (de) | 1-isopropyl-2-oxo-1,2-dihydropyridin-3-carbonsäureamidderivate mit agonistischer wirkung am 5-ht4-rezeptor | |
| DE69922186T2 (de) | 1-(1-subst.-4-piperidinyl)methyl]-4-piperidin-derivate, verafhren zu deren herstellung, pharmazeutische mixturen und intermediate zu deren herstellung | |
| US5834493A (en) | Indole derivatives as 5-HT1A and/or 5-HT2 ligands | |
| DE69531476T2 (de) | Serotonergische Modulatoren | |
| DE69108461T2 (de) | 1-Indolylalkyl-4-(alkoxy-pyrimidinyl)piperazine. | |
| DE69433984T2 (de) | Arylpiperazinderivate von indol als liganden der rezeptoren 5 ht1-like, 5 ht1b und 5 ht1d | |
| EP0683166B1 (de) | 3-Indolylpiperidine | |
| EP1228059B1 (de) | Neue cyclopropane als cgrp-antagonisten, diese verbindungen enthaltende arzneimittel und verfahren zu ihrer herstellung | |
| US6133287A (en) | Piperidine-indole compounds having 5-HT6 affinity | |
| RU2158264C2 (ru) | 3-азетидинилалкилпиперидины или пирролидины в качестве антагонистов тахикинина, способы их получения, промежуточные соединения, фармацевтическая композиция на их основе и способ лечения | |
| DE60011269T2 (de) | Azaidole mit serotonin rezeptor affinität | |
| DE69105659T2 (de) | 3-Arylindol- und 3-Arylindazolderivate. | |
| HUP0105108A2 (hu) | Amidvegyületek, eljárás az előállításukra és ezeket tartalmazó gyógyszerkészítmények | |
| DE69704060T2 (de) | Tetrahydroisochinolinderivate und ihre pharmazeutische anwendung | |
| DE69911238T2 (de) | Indolderivate und ihre verwendung als serotoninrezeptor-liganden | |
| DE69311165T2 (de) | Kondensierte heterocyclische Ketonderivate, ihre Herstellung und ihre Verwendung | |
| DE69815700T2 (de) | Tetrahydro gamma-carboline | |
| DE69829317T2 (de) | Tetrahydrobenzindol-derivate |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 8364 | No opposition during term of opposition | ||
| 8327 | Change in the person/name/address of the patent owner |
Owner name: NPS PHARMACEUTICALS, INC. (N.D.GES.D. STAATES , US |