DE69936635T2 - Verwendundung von Rhamnolipiden als Kosmetika - Google Patents
Verwendundung von Rhamnolipiden als Kosmetika Download PDFInfo
- Publication number
- DE69936635T2 DE69936635T2 DE69936635T DE69936635T DE69936635T2 DE 69936635 T2 DE69936635 T2 DE 69936635T2 DE 69936635 T DE69936635 T DE 69936635T DE 69936635 T DE69936635 T DE 69936635T DE 69936635 T2 DE69936635 T2 DE 69936635T2
- Authority
- DE
- Germany
- Prior art keywords
- chr
- rhamnopyranosyl
- formula
- treatment
- composition
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
- 239000002537 cosmetic Substances 0.000 title claims description 11
- 238000000034 method Methods 0.000 claims abstract description 15
- 239000000203 mixture Substances 0.000 claims abstract description 14
- 230000037303 wrinkles Effects 0.000 claims abstract description 6
- FCBUKWWQSZQDDI-UHFFFAOYSA-N rhamnolipid Chemical compound CCCCCCCC(CC(O)=O)OC(=O)CC(CCCCCCC)OC1OC(C)C(O)C(O)C1OC1C(O)C(O)C(O)C(C)O1 FCBUKWWQSZQDDI-UHFFFAOYSA-N 0.000 claims description 10
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 claims description 7
- 239000000969 carrier Substances 0.000 claims description 2
- 150000001875 compounds Chemical class 0.000 claims description 2
- 239000003085 diluting agent Substances 0.000 claims description 2
- 230000000699 topical effect Effects 0.000 claims description 2
- 206010016654 Fibrosis Diseases 0.000 abstract description 4
- 230000004761 fibrosis Effects 0.000 abstract description 3
- 239000004480 active ingredient Substances 0.000 abstract description 2
- 230000032683 aging Effects 0.000 abstract description 2
- 230000002265 prevention Effects 0.000 abstract 2
- 201000001320 Atherosclerosis Diseases 0.000 abstract 1
- 208000020401 Depressive disease Diseases 0.000 abstract 1
- 206010052779 Transplant rejections Diseases 0.000 abstract 1
- 210000000056 organ Anatomy 0.000 abstract 1
- 201000000980 schizophrenia Diseases 0.000 abstract 1
- 230000035939 shock Effects 0.000 abstract 1
- 230000029663 wound healing Effects 0.000 abstract 1
- 208000027418 Wounds and injury Diseases 0.000 description 14
- 206010052428 Wound Diseases 0.000 description 13
- 230000001605 fetal effect Effects 0.000 description 10
- KIUKXJAPPMFGSW-DNGZLQJQSA-N (2S,3S,4S,5R,6R)-6-[(2S,3R,4R,5S,6R)-3-Acetamido-2-[(2S,3S,4R,5R,6R)-6-[(2R,3R,4R,5S,6R)-3-acetamido-2,5-dihydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-2-carboxy-4,5-dihydroxyoxan-3-yl]oxy-5-hydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-3,4,5-trihydroxyoxane-2-carboxylic acid Chemical compound CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@H](O[C@H]2[C@@H]([C@@H](O[C@H]3[C@@H]([C@@H](O)[C@H](O)[C@H](O3)C(O)=O)O)[C@H](O)[C@@H](CO)O2)NC(C)=O)[C@@H](C(O)=O)O1 KIUKXJAPPMFGSW-DNGZLQJQSA-N 0.000 description 8
- 229920002674 hyaluronan Polymers 0.000 description 8
- 229960003160 hyaluronic acid Drugs 0.000 description 8
- 210000002540 macrophage Anatomy 0.000 description 8
- 239000002674 ointment Substances 0.000 description 7
- 108090000695 Cytokines Proteins 0.000 description 6
- 102000004127 Cytokines Human genes 0.000 description 6
- 230000000694 effects Effects 0.000 description 6
- 239000003102 growth factor Substances 0.000 description 6
- 210000001519 tissue Anatomy 0.000 description 6
- 102000008186 Collagen Human genes 0.000 description 5
- 108010035532 Collagen Proteins 0.000 description 5
- 229920001436 collagen Polymers 0.000 description 5
- 206010040954 Skin wrinkling Diseases 0.000 description 4
- 230000001684 chronic effect Effects 0.000 description 4
- 210000003754 fetus Anatomy 0.000 description 4
- 210000002950 fibroblast Anatomy 0.000 description 4
- 230000035755 proliferation Effects 0.000 description 4
- 230000008439 repair process Effects 0.000 description 4
- 210000003491 skin Anatomy 0.000 description 4
- 102000004887 Transforming Growth Factor beta Human genes 0.000 description 3
- 108090001012 Transforming Growth Factor beta Proteins 0.000 description 3
- 210000004207 dermis Anatomy 0.000 description 3
- ZRKFYGHZFMAOKI-QMGMOQQFSA-N tgfbeta Chemical compound C([C@H](NC(=O)[C@H](C(C)C)NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CC(C)C)NC(=O)CNC(=O)[C@H](C)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](NC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)[C@@H](NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](N)CCSC)C(C)C)[C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](C)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C)C(=O)N[C@@H](CC(C)C)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(O)=O)C1=CC=C(O)C=C1 ZRKFYGHZFMAOKI-QMGMOQQFSA-N 0.000 description 3
- 102000016942 Elastin Human genes 0.000 description 2
- 108010014258 Elastin Proteins 0.000 description 2
- 102000010834 Extracellular Matrix Proteins Human genes 0.000 description 2
- 108010037362 Extracellular Matrix Proteins Proteins 0.000 description 2
- 102000003886 Glycoproteins Human genes 0.000 description 2
- 108090000288 Glycoproteins Proteins 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 210000004027 cell Anatomy 0.000 description 2
- 210000002808 connective tissue Anatomy 0.000 description 2
- 230000006378 damage Effects 0.000 description 2
- 229920002549 elastin Polymers 0.000 description 2
- 210000002744 extracellular matrix Anatomy 0.000 description 2
- 210000000987 immune system Anatomy 0.000 description 2
- 239000011159 matrix material Substances 0.000 description 2
- 125000001160 methoxycarbonyl group Chemical group [H]C([H])([H])OC(*)=O 0.000 description 2
- 230000005012 migration Effects 0.000 description 2
- 238000013508 migration Methods 0.000 description 2
- 230000008569 process Effects 0.000 description 2
- 231100000241 scar Toxicity 0.000 description 2
- 230000037390 scarring Effects 0.000 description 2
- 208000027930 type IV hypersensitivity disease Diseases 0.000 description 2
- 102000019034 Chemokines Human genes 0.000 description 1
- 108010012236 Chemokines Proteins 0.000 description 1
- 102000009123 Fibrin Human genes 0.000 description 1
- 108010073385 Fibrin Proteins 0.000 description 1
- BWGVNKXGVNDBDI-UHFFFAOYSA-N Fibrin monomer Chemical compound CNC(=O)CNC(=O)CN BWGVNKXGVNDBDI-UHFFFAOYSA-N 0.000 description 1
- 102000018233 Fibroblast Growth Factor Human genes 0.000 description 1
- 108050007372 Fibroblast Growth Factor Proteins 0.000 description 1
- 229920002683 Glycosaminoglycan Polymers 0.000 description 1
- 101000611183 Homo sapiens Tumor necrosis factor Proteins 0.000 description 1
- 108010003272 Hyaluronate lyase Proteins 0.000 description 1
- 102000001974 Hyaluronidases Human genes 0.000 description 1
- 206010020751 Hypersensitivity Diseases 0.000 description 1
- 206010061218 Inflammation Diseases 0.000 description 1
- 108010002352 Interleukin-1 Proteins 0.000 description 1
- -1 Kollagen Polymers 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- 206010039580 Scar Diseases 0.000 description 1
- 210000001744 T-lymphocyte Anatomy 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 239000000853 adhesive Substances 0.000 description 1
- 230000001070 adhesive effect Effects 0.000 description 1
- 239000000427 antigen Substances 0.000 description 1
- 230000007503 antigenic stimulation Effects 0.000 description 1
- 102000036639 antigens Human genes 0.000 description 1
- 108091007433 antigens Proteins 0.000 description 1
- 210000004204 blood vessel Anatomy 0.000 description 1
- 230000037319 collagen production Effects 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 239000006071 cream Substances 0.000 description 1
- 230000003111 delayed effect Effects 0.000 description 1
- 230000008021 deposition Effects 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 238000004090 dissolution Methods 0.000 description 1
- 230000008030 elimination Effects 0.000 description 1
- 238000003379 elimination reaction Methods 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 210000002889 endothelial cell Anatomy 0.000 description 1
- 230000003203 everyday effect Effects 0.000 description 1
- 238000000855 fermentation Methods 0.000 description 1
- 230000004151 fermentation Effects 0.000 description 1
- 230000008442 fetal wound healing Effects 0.000 description 1
- 229950003499 fibrin Drugs 0.000 description 1
- 229940126864 fibroblast growth factor Drugs 0.000 description 1
- 229960002773 hyaluronidase Drugs 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- 208000014674 injury Diseases 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 239000006210 lotion Substances 0.000 description 1
- 230000002085 persistent effect Effects 0.000 description 1
- 229920001184 polypeptide Polymers 0.000 description 1
- 230000003389 potentiating effect Effects 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 230000035935 pregnancy Effects 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 102000004196 processed proteins & peptides Human genes 0.000 description 1
- 108090000765 processed proteins & peptides Proteins 0.000 description 1
- 230000002250 progressing effect Effects 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 230000028327 secretion Effects 0.000 description 1
- 238000001356 surgical procedure Methods 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 230000002123 temporal effect Effects 0.000 description 1
- 229940098465 tincture Drugs 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7028—Compounds having saccharide radicals attached to non-saccharide compounds by glycosidic linkages
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7024—Esters of saccharides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/30—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds
- A61K8/60—Sugars; Derivatives thereof
- A61K8/602—Glycosides, e.g. rutin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/18—Antipsychotics, i.e. neuroleptics; Drugs for mania or schizophrenia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/24—Antidepressants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q19/00—Preparations for care of the skin
- A61Q19/08—Anti-ageing preparations
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Medicinal Chemistry (AREA)
- Chemical & Material Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Epidemiology (AREA)
- Dermatology (AREA)
- Molecular Biology (AREA)
- Immunology (AREA)
- Neurosurgery (AREA)
- Birds (AREA)
- Gerontology & Geriatric Medicine (AREA)
- Psychiatry (AREA)
- Biomedical Technology (AREA)
- Neurology (AREA)
- Transplantation (AREA)
- Pain & Pain Management (AREA)
- Urology & Nephrology (AREA)
- Heart & Thoracic Surgery (AREA)
- Cardiology (AREA)
- Vascular Medicine (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Cosmetics (AREA)
- Saccharide Compounds (AREA)
- Medicines Containing Plant Substances (AREA)
- Medicinal Preparation (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Description
- Die vorliegende Erfindung betrifft ein kosmetisches Verfahren zur Behandlung von Falten unter Verwendung von Rhamnolipiden.
- Üblicherweise heilt, wenn ein erwachsener Mensch eine Verletzung entweder durch eine Verbrennung von Gewebe oder durch einen Schnitt in das Hautgewebe erleidet, die Wunde unter Ausbildung einer Narbe ab. Dies ist auch bei einer Erholung nach einem chirurgischen Eingriff, wobei die Wunde mit Nähten (obwohl die Narbenbildung in solchen Fällen im Allgemeinen geringer ist) verschlossen wurde, der Fall. Bei Wunden von Föten trifft dies jedoch nicht zu. Es ist bekannt, dass bei Föten bis zu einem späten Stadium der Schwangerschaft Wunden schnell und im Allgemeinen ohne Narbenbildung heilen.
- Gründe hierfür schließen ein:
- 1. Bei Wunden von Erwachsenen ist die Dermis der Ort der Narbe. Mit fortschreitender Entwicklung wird Hautkollagen abgelagert und sulfatierte Glucosaminoglykane (GAG) ersetzen nicht sulfatierte GAG, wobei überwiegend Hyaluronsäure (HA) vorliegt.
- 2. Für fetales Gewebe scheint bei der Reparatur eine Minderung der Fibrose spezifisch zu sein und der vorherrschende fetale Zelltyp, der für eine solche Reparatur verantwortlich ist, kann der fetale Fibroblast sein.
- 3. Das fetale Immunsystem ist im Verhältnis zum adulten Immunsystem funktionell unreif und spielt bei der fetalen Wundheilung eine weitaus weniger herausragende Rolle.
- 4. Die fetale extrazelluläre Matrix (EZM) unterscheidet sich von der von Erwachsenen darin, dass sie HA, Kollagen, Elastin und Adhäsionsglycoproteine als wesentliche Bestandteile aufweist.
- Es wurde gezeigt, dass die Spiegel von Hyaluronsäure in Wunden sowohl von fetalen als auch von erwachsenen Schafen bis zu drei Tagen nach dem Setzen einer Wunde schnell ansteigen. Dieser erhöhte Spiegel bleibt beim Fötus mindestens 21 Tage lang nach dem Setzen der Wunde bestehen, wohingegen er beim adulten Tier schnell auf den Ausgangswert zurückfällt. In adulten Wunden wird HA binnen kurzem in einem Gerinnsel aus Fibrin und Plättchen abgelagert. Die HA wird von Hyaluronidase entfernt und diese provisorische Matrix wird mit Kollagen und sulfatierten Glucosaminoglykanen ersetzt. Die Ablagerung von Kollagen in fetalen Wunden erfolgt in einem hochgradig organisierten Muster, das sich von unverletzter fetaler Dermis nicht unterscheiden lässt. Einige der hauptsächlichen Unterschiede zwischen fetaler und adulter Reparatur sind die temporalen Muster von in der Wunde vorliegenden Adhäsionsglycoproteinen, die im frühesten Stadium der Reparatur vorgefunden werden. Diese Unterschiede können zu Unterschieden bei der Mobilität, Migration, Adhäsion und Proliferation der Zellen führen.
- Zytokine. Transformierender Wachstumsfaktor beta (TGF-beta) ruft Fibroplasie hervor und steigert die Reißfestigkeit in adulten Wunden. Ähnliche Wirkungen wurden bei fetalen Wunden registriert. Bei Erwachsenen modifizieren die Produkte von aktivierten Makrophagen wie zum Beispiel Zytokine und Wachstumsfaktoren fortschreitend die lokale Gewebsumgebung, wobei sie anfänglich zur Gewebszerstörung führen und später, das heißt bei chronischen Überempfindlichkeitsreaktionen vom verzögerten Typ (DTH), einen Ersatz durch Bindegewebe verursachen. Die Wirkungen von Zytokinen und von Wachstumsfaktoren, die von Makrophagen stammen, treten in zwei Phasen auf. TNF, IL-1 und Chemokine, die von Makrophagen stammen, steigern intensiv inflammatorische Reaktionen, die von T-Zellen eingeleitet wurden. Die gleichen Zytokine stimulieren auch chronisch die Proliferation von Fibroblasten und die Kollagenproduktion. Diese langsamen Wirkungen von Zytokinen werden durch die Wirkungen von Polypeptid-Wachstumsfaktoren, die von Makrophagen stammen, verstärkt. Plättchen-Wachstumsfaktor, der von aktivierten Makrophagen produziert wird, ist ein stark wirksamer Stimulator der Proliferation von Fibroblasten, wohingegen von Makrophagen stammender Wachstumsfaktor (TGF-beta) die Kollagensynthese steigert. Die Sezernierung von Fibroblasten-Wachstumsfaktor durch Makrophagen führt zur Wanderung und Proliferation von Endothelzellen, was zur Bildung neuer Blutgefäße führt. Die Auswirkungen dieser langsamen Wirkungen von Zytokinen und Wachstumsfaktoren bestehen darin, dass eine anhaltende Aktivierung von Makrophagen in einem Gewebe, zum Beispiel im Milieu einer chronischen, antigenen Stimulation, zum Ersatz von differenziertem Gewebe durch Bindegewebe führt. Die Folge von chronischer DTH ist Fibrose, wenn die Elimination des Antigens und eine schnelle Auflösung erfolglos sind.
- Somit besteht ein Bedarf, ein kosmetisches Verfahren zur Behandlung von Falten zu entwickeln, wobei das Verfahren Folgendes umfasst:
Verabreichen einer wirksamen Menge einer Zusammensetzung, die eine oder mehrere Rhamnolipide der Formel 1 umfasst, an eine Person, die dessen bedarf: wobei R1 = H, unsubstituiertes α-L-Rhamnopyranosyl, α-L-Rhamnopyranosyl, an der Position 2 substituiert mit einer Gruppe der Formel -O-C(=O)-CH=CH-R5, oder -O-C(=O)-CH=CH-R5;
R2 = H, lineares oder verzweigtes C1-C6 Alkyl, -CHR4-CH2-COOH oder -CHR4-CH2-COOR6;
R3 = -(CH2)x-CH3, wobei x = 4-19;
R4 = -(CH2)y-CH3, wobei y = 1-19;
R5 = -(CH2)z-CH3, wobei z = 1-12 und
R6 = lineares oder verzweigtes C1-C6 Alkyl. - Man wird leicht zu einem kompletteren Verständnis der Erfindung und vieler der sie begleitenden Vorteile gelangen, wenn sie unter Bezug auf die folgende ausführliche Beschreibung besser verstanden wird.
- Die vorliegende Erfindung betrifft ein kosmetisches Verfahren zur Behandlung von Falten durch Verabreichen von kosmetischen Zubereitungen und Zusammensetzungen, welche ein oder mehrere Rhamnolipide der Formel 1 als Wirkstoffe umfassen: wobei R1 = H, α-L-Rhamnopyranosyl (entweder unsubstituiert oder an der Position 2 substituiert mit einer Gruppe der Formel -O-C(=O)-CH=CH-R5) oder -O-C(=O)-CH=CH-R5;
R2 = H, lineares oder verzweigtes C1-C6 Alkyl, vorzugsweise -CH3, -CHR4-CH2-COOH oder -CHR4-CH2-COOR6;
R3 = -(CH2)x-CH3, wobei x = 4-19;
R4 = -(CH2)y-CH3, wobei y = 1-19;
R5 = -(CH2)z-CH3, wobei z = 1-12 und
R6 = lineares oder verzweigtes C1-C6 Alkyl, vorzugsweise -CH3. - Die Rhamnolipide der vorliegenden Erfindung können mittels herkömmlicher Verfahren hergestellt werden, vorzugsweise mittels Fermentation, Isolierung und Reinigung wie in den
U.S. Patenten 5.455.232 ,5.466.675 und5.514.661 und auch inBE 1005704 A4 CA 2.129.542 ,JP 5-512946 EP 93914523.1 -
- Andere bevorzugte Rhamnolipide schließen diejenigen ein, bei denen:
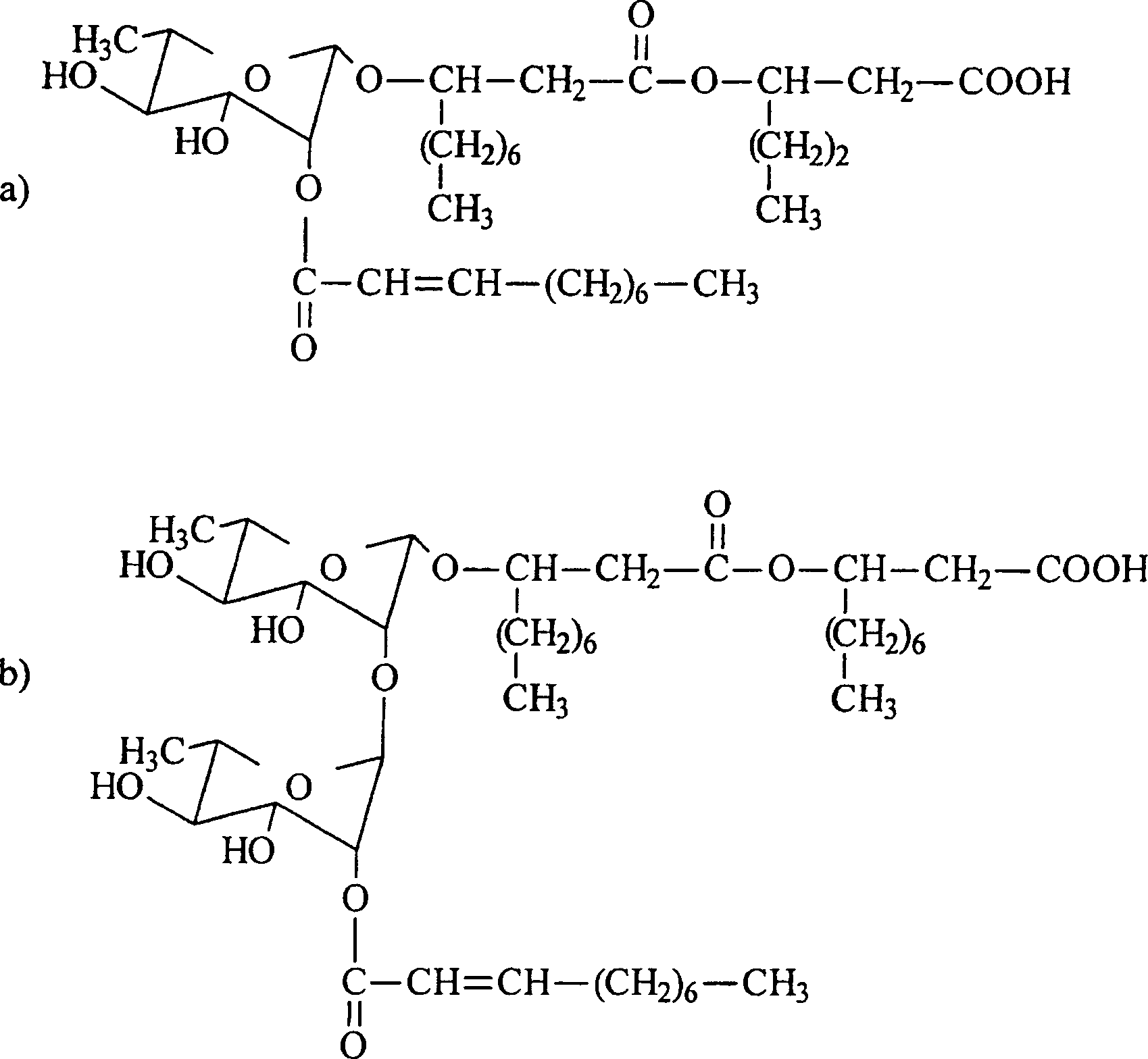
- a) R1 = -O-C(=O)-CH=CH-R5; R2 = -CHR4-CH2-COOH; R3 = -(CH2)6-CH3; R4 = -(CH2)2-CH3 und R5 = -(CH2)6-CH3 oder
- b) R1 = α-L-Rhamnopyranosyl, an der Position 2 substituiert durch -O-C(=O)-CH=CH-R5; R2 = -CHR4-CH2-COOH; R3 = -(CH2)6-CH3; R4 = -(CH2)6-CH3 und R5 = -(CH2)6-CH3 oder
- c) R1 = -O-C(=O)-CH=CH-R5; R2 = -CHR4-CH2-COOCH3; R3 = -(CH2)6-CH3; R4 = -(CH2)2-CH3 und R5 = -(CH2)6-CH3 oder
- d) R1 = α-L-Rhamnopyranosyl, an der Position 2 substituiert durch -O-C(=O)-CH=CH-R5; R2 = -CHR4-CH2-COOCH3; R3 = -(CH2)6-CH3; R4 = -(CH2)6-CH3 und R5 = -(CH2)6-CH3.
-
- Die Toxizität und die Wirksamkeit dieser Verbindungen können weiter modifiziert werden, indem man die R-Gruppen nach Bedarf im Rahmen von Formel 1 variiert.
- Es wurde nun festgestellt, dass diese Rhamnolipide bei der Reepithelialisierung der Haut wirksam sind. Vorzugsweise ist das im kosmetischen Verfahren verwendete Rhamnolipid das oben beschriebene Rhamnolipid BAC-3. Die Zusammensetzung, welche das Rhamnolipid umfasst, kann in Form einer unverdünnten Flüssigkeit, einer Suspension, einer Dispersion, einer Emulsion, einer Creme, einer Tinktur, eines Pulvers, einer Salbe oder einer Lotion vorliegen. Vorzugsweise liegt die Zusammensetzung in einer Salbe vor. Die Menge von Rhamnolipid, die in der Behandlung eingesetzt wird, beträgt 0,001 % in der Salbe bis zu 5 % in der Salbe, vorzugsweise von 0,01 bis 1 % in der Salbe, bevorzugter von 0,05 bis 0,5 % in der Salbe. (Soweit nicht anders gekenn zeichnet sind alle Prozentsätze Gewichtsprozent, basierend auf dem Gesamtgewicht der Zusammensetzung.) Die Salbe wird über eine Dauer von 1 Tag bis zu 6 Wochen 1-5 Mal täglich, vorzugsweise 2-3 Mal täglich direkt auf das Testareal aufgetragen.
- Die Zusammensetzung, die Rhamnolipid enthält und im dem Verfahren, auf das aktuell Anspruch erhoben wird, verwendet wird, umfasst ein oder mehrere der Rhamnolipide in einer Menge, die zum Behandeln von Falten als Zeichen des Alterns wirksam sind. Eine solche kosmetische Zusammensetzung würde von 1 bis 3 Mal am Tag auf das betroffene Areal aufgetragen werden. Die kosmetische Zusammensetzung könnte in jeder der oben erwähnten topischen Formen vorliegen und ähnliche Mengen von Rhamnolipid(en) enthalten.
- Die Zusammensetzung, welche das eine oder mehrere Rhamnolipide umfasst, kann ferner, falls erwünscht, einen oder mehrere Träger und/oder Verdünnungsmittel, die üblicherweise in der pharmazeutischen und/oder kosmetischen Industrie verwendet werden, enthalten.
Claims (6)
- Kosmetisches Verfahren zur Behandlung von Falten, wobei das Verfahren Folgendes umfasst: Verabreichen einer wirksamen Menge einer Zusammensetzung an eine bedürftige Person, die ein oder mehrere Rhamnolipide der Formel 1 umfasst: wobei R1 = H, unsubstituiertes α-L-Rhamnopyranosyl, α-L-Rhamnopyranosyl, an der Position 2 substituiert mit einer Gruppe der Formel -O-C(=O)-CH=CH-R5 oder -O-C(=O)-CH=CH-R5: R2 = H, lineares oder verzweigtes C1-C6 Alkyl, -CHR4-CH2-COOH oder -CHR4-CH2-COOR6; R3 = -(CH2)x-CH3, wobei x = 4-19 ist; R4 = -(CH2)y-CH3, wobei y = 1-19 ist; R5 = -(CH2)z-CH3, wobei z = 1-12 ist; und R6 = lineares oder verzweigtes C1-C6 Alkyl ist.
- Verfahren nach Anspruch 1, wobei das/die genannte(n) eine oder mehreren Rhamnolipid(e) der Formel 1 ausgewählt ist/sind aus der Gruppe bestehend aus Verbindungen der Formel 1, wobei: R1 = -O-C(=O)-CH=CH-R5, R2 = -CHR4-CH2-COOH, R3 = -(CH2)6-CH3, R4 = -(CH2)2-CH3, und R5 = -(CH2)6-CH3; R1 = α-L-Rhamnopyranosyl, substituiert an der Position 2 durch -O-C(=O)-CH=CH-R5, R2 = -CHR4-CH2-COOH, R3 = -(CH2)6-CH3, R4 = -(CH2)6-CH3, und R5 = -(CH2)6-CH3; R1 = -O-C(=O)-CH=CH-R5, R2 = -CHR4-CH2-COOCH3, R3 = -(CH2)6-CH3, R4 = -(CH2)2-CH3, und R5 = -(CH2)6-CH3; und R1 = α-L-Rhamnopyranosyl, substituiert an der Position 2 durch -O-C(=O)-CH=CH-R5, R2 = -CHR4-CH2-COOCH3, R3 = -(CH2)6-CH3, R4 = –(CH2)6-CH3, und R5 = -(CH2)6-CH3.
- Verfahren nach einem der vorherigen Ansprüche, wobei die Zusammensetzung 1 bis 3 Mal täglich angewendet wird.
- Verfahren nach einem der vorherigen Ansprüche, wobei die Zusammensetzung in topischer Form vorliegt.
- Verfahren nach einem der vorherigen Ansprüche, wobei die Zusammensetzung ferner einen oder mehrere Träger und/oder Verdünnungsmittel umfasst.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US7595998P | 1998-02-24 | 1998-02-24 | |
| US75959P | 1998-02-24 | ||
| PCT/US1999/003714 WO1999043334A1 (en) | 1998-02-24 | 1999-02-24 | Use of rhamnolipids in wound healing, treating burn shock, atherosclerosis, organ transplants, depression, schizophrenia and cosmetics |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| DE69936635D1 DE69936635D1 (de) | 2007-09-06 |
| DE69936635T2 true DE69936635T2 (de) | 2008-05-08 |
Family
ID=22129018
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE69936635T Expired - Lifetime DE69936635T2 (de) | 1998-02-24 | 1999-02-24 | Verwendundung von Rhamnolipiden als Kosmetika |
Country Status (10)
| Country | Link |
|---|---|
| US (2) | US20070155678A1 (de) |
| EP (1) | EP1056462B1 (de) |
| JP (2) | JP2002504513A (de) |
| AT (1) | ATE367797T1 (de) |
| AU (1) | AU747088B2 (de) |
| CA (1) | CA2321926C (de) |
| DE (1) | DE69936635T2 (de) |
| DK (1) | DK1056462T3 (de) |
| ES (1) | ES2291036T3 (de) |
| WO (1) | WO1999043334A1 (de) |
Families Citing this family (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ATE473749T1 (de) | 1999-08-05 | 2010-07-15 | Paradigm Biomedical Inc | Verwendung von rhamnolipiden zur wundheilung, behandlung und vorbeugung einer zahnfleischerkrankung und periodontaler regeneration |
| WO2008013899A2 (en) * | 2006-07-27 | 2008-01-31 | Aurora Advance Beauty Labs | Rhamnolipid-based formulations |
| NZ575806A (en) * | 2006-10-17 | 2011-09-30 | Idemitsu Kosan Co | Animal feed comprising mannosylerythritol and rhamnolipds |
| JO3416B1 (ar) | 2009-04-27 | 2019-10-20 | Jeneil Biosurfactant Co Llc | تركيبات مضادة للبكتيريا وطرق استخدامها |
| US9474283B2 (en) | 2010-12-09 | 2016-10-25 | Y&B Mother's Choice Ltd. | Formulations comprising saponins and uses thereof |
| WO2012077120A2 (en) | 2010-12-09 | 2012-06-14 | Y&B Mother's Choice Ltd. | Natural formulations |
| US10434058B2 (en) | 2010-12-09 | 2019-10-08 | Y&B Mother's Choice Ltd. | Natural formulations |
| EP2723348B1 (de) * | 2011-06-21 | 2019-08-14 | Anton Leighton | Verfahren zur behandlung von adipositas |
| EP2967053A4 (de) | 2013-03-15 | 2016-10-26 | Jeneil Biosurfactant Co Llc | Antimikrobielle zusammensetzungen und zugehörige verfahren zur verwendung |
| EP2988829B1 (de) | 2013-04-25 | 2017-03-22 | Unilever PLC, a company registered in England and Wales under company no. 41424 of | Reingiungszusammensetzungne mit verbesserten abgabe- und suspensionseigenschaften |
| IL229836A0 (en) | 2013-12-08 | 2014-03-31 | Y & B Mother S Choice Ltd | Formulations to reduce or suppress irritation to eye tissue |
| CN105326848A (zh) * | 2015-11-26 | 2016-02-17 | 浙江大学 | 一种鼠李糖脂在制备抗纤维化药物制剂中的用途 |
| BR102017000578B1 (pt) | 2017-01-11 | 2019-04-02 | Natura Cosméticos S.A. | Processo de obtenção de ramnolipídeo produzido por pseudomonas ou enterobacter utilizando o resíduo de semente de andiroba ou murumuru |
| WO2020247808A1 (en) | 2019-06-07 | 2020-12-10 | Dale Biotech, Llc | Method for treating dupuytren's disease |
| WO2021155143A1 (en) | 2020-01-31 | 2021-08-05 | Jeneil Biosurfactant Company, Llc | Antimicrobial compositions for modulation of fruit and vegetable tissue necrosis |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE3405664A1 (de) * | 1984-02-17 | 1985-09-05 | Wintershall Ag, 3100 Celle | Verfahren zur biotechnischen herstellung von rhamnolipiden und rhamnolipide mit nur einem ss-hydroxidecancarbonsaeurerest im molekuel |
| JPS63182029A (ja) * | 1987-01-22 | 1988-07-27 | Agency Of Ind Science & Technol | リポソ−ム |
| US4933281A (en) * | 1987-03-17 | 1990-06-12 | The University Of Iowa Research Foundation | Method for producing rhamnose |
| JPS63253025A (ja) * | 1987-04-09 | 1988-10-20 | Yamanouchi Pharmaceut Co Ltd | ホスホリパ−ゼa↓2阻害剤 |
| EP0288965A2 (de) * | 1987-04-29 | 1988-11-02 | Hoechst Aktiengesellschaft | Peptide mit Phospholipase A2- hemmender Wirkung |
| DE4030262A1 (de) * | 1990-09-25 | 1992-03-26 | Suedzucker Ag | Verfahren zur herstellung von rhamnose aus rhamnolipiden |
| BE1005704A4 (nl) * | 1992-02-04 | 1993-12-21 | Piljac Goran & Piljac Visnja | Farmaceutisch preparaat op basis van rhamnolipide. |
| US5455232A (en) * | 1992-02-04 | 1995-10-03 | Piljac; Goran | Pharmaceutical preparation based on rhamnolipid |
| US5466675A (en) * | 1992-02-04 | 1995-11-14 | Piljac; Goran | Immunological activity of rhamnolipids |
-
1999
- 1999-02-24 EP EP99936031A patent/EP1056462B1/de not_active Expired - Lifetime
- 1999-02-24 DE DE69936635T patent/DE69936635T2/de not_active Expired - Lifetime
- 1999-02-24 AT AT99936031T patent/ATE367797T1/de not_active IP Right Cessation
- 1999-02-24 DK DK99936031T patent/DK1056462T3/da active
- 1999-02-24 AU AU33048/99A patent/AU747088B2/en not_active Ceased
- 1999-02-24 WO PCT/US1999/003714 patent/WO1999043334A1/en not_active Ceased
- 1999-02-24 CA CA2321926A patent/CA2321926C/en not_active Expired - Fee Related
- 1999-02-24 JP JP2000533130A patent/JP2002504513A/ja not_active Withdrawn
- 1999-02-24 ES ES99936031T patent/ES2291036T3/es not_active Expired - Lifetime
-
2007
- 2007-02-02 US US11/701,860 patent/US20070155678A1/en not_active Abandoned
-
2009
- 2009-05-11 US US12/463,801 patent/US20090220603A1/en not_active Abandoned
-
2010
- 2010-08-19 JP JP2010183906A patent/JP2011001373A/ja active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| AU747088B2 (en) | 2002-05-09 |
| WO1999043334A1 (en) | 1999-09-02 |
| JP2002504513A (ja) | 2002-02-12 |
| CA2321926A1 (en) | 1999-09-02 |
| CA2321926C (en) | 2010-04-27 |
| ATE367797T1 (de) | 2007-08-15 |
| ES2291036T3 (es) | 2008-02-16 |
| EP1056462A4 (de) | 2004-12-01 |
| AU3304899A (en) | 1999-09-15 |
| EP1056462A1 (de) | 2000-12-06 |
| US20070155678A1 (en) | 2007-07-05 |
| DK1056462T3 (da) | 2007-12-03 |
| US20090220603A1 (en) | 2009-09-03 |
| EP1056462B1 (de) | 2007-07-25 |
| JP2011001373A (ja) | 2011-01-06 |
| DE69936635D1 (de) | 2007-09-06 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DE69936635T2 (de) | Verwendundung von Rhamnolipiden als Kosmetika | |
| DE69627680T2 (de) | Verwendung von Kohlenhydraten zur Förderung der Abschuppung der Haut | |
| DE69726001T2 (de) | Verminderung des haarwuchhses | |
| DE3874813T2 (de) | Zusammensetzung zur behandlung der haut. | |
| DE68901992T2 (de) | Kosmetisches praeparat. | |
| DE69917526T2 (de) | Verwendung mindestens eines Hydroxystilben in einer Zusammensetzung, die die Abschuppung der Haut fördern soll, und Hydroxystilbenhaltige Zusammensetzung | |
| DE3752176T2 (de) | Vernetzte Ester von Hyaluronsäure | |
| DE68902565T2 (de) | Assoziat, bestehend aus pyrimidin-derivaten und harnstoff- und/oder allantoin-derivaten zum induzieren und stimulieren des haarwuchses und zum vermindern des haarausfalles. | |
| DE69324006T2 (de) | Zubereitungen von hyaluronsaeure mit niedrigem molekulargewicht zur foerderung der knochenbildung | |
| DE69032182T2 (de) | Verfahren zur Verhütung der Hautalterung mittels Retinoiden | |
| DE69009748T2 (de) | Fgf enthaltende stabilisierte zubereitungen. | |
| DE3726176C2 (de) | Mittel in Form eines Gels zur Förderung und Stimulierung des Haarwachstums und zur Verringerung von Haarausfall auf Basis von Piperidino-Pyrimidin-Derivaten | |
| EP0500602B1 (de) | Mittel zur neutralisierung der tumorzellen-assoziierten prokoagulant-aktivität | |
| DE69106110T2 (de) | Kosmetische Verwendung eines Mittels gegen Erytheme. | |
| DE69426932T2 (de) | Verwendung von oligosacchariden zur verhütung und behandlung von alterung der haut | |
| DE3873889T2 (de) | Mischung, bestehend aus 1,8-hydroxy-und/oder acyloxyanthracen oder anthron- und pyrimidinderivaten zum induzieren und stimulieren des haarwuchses und zum vermindern des haarausfalls. | |
| DE69528637T2 (de) | Hautbehandlungsmittel gegen akne | |
| EP0312913A2 (de) | Verwendung von paf-Acether-Antagonisten zur Herstellung eines Arzneimittels und Verfahren zu deren Wirksamkeitsbestimmung | |
| DE69312948T2 (de) | Verwendung von lectinen für die behandlung von krankheiten | |
| DE69531150T2 (de) | Verwendung von biopolymeren zur behandlung der muskeln | |
| DE2153386C3 (de) | Haarpflegemittel, enthaltend Lab | |
| DE60116338T2 (de) | Eine mischung von nicht-sulfatierten oligosacchariden auf der basis von fukose, eine diese mischung enthaltende, kosmetische oder pharmazeutische zusammensetzung und deren verwendungen in der kosmetik und pharmazie | |
| DE68902511T2 (de) | Dermato-kosmetische zusammensetzung zur behandlung des hautalterns und zur verhuetung von falten. | |
| EP0493662A1 (de) | Verwendung von Superoxiddismutasen für die Herstellung von Arzneimitteln zur Prophylaxe und/oder Behandlung von Organversagen bei Risikopatienten mit Polytrauma als Unfallfolge | |
| EP0107846B1 (de) | Mittel zur Pflege oder Behandlung der menschlichen Haut |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 8327 | Change in the person/name/address of the patent owner |
Owner name: PARADIGM BIOMEDICAL, INC., ST. PETERSBURG, FLA, US |
|
| 8364 | No opposition during term of opposition |