CN115931687A - 用于成像流式细胞术的设备、系统和方法 - Google Patents
用于成像流式细胞术的设备、系统和方法 Download PDFInfo
- Publication number
- CN115931687A CN115931687A CN202310087156.7A CN202310087156A CN115931687A CN 115931687 A CN115931687 A CN 115931687A CN 202310087156 A CN202310087156 A CN 202310087156A CN 115931687 A CN115931687 A CN 115931687A
- Authority
- CN
- China
- Prior art keywords
- flow channel
- flow
- particles
- region
- illumination
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 238000003384 imaging method Methods 0.000 title claims description 64
- 238000000034 method Methods 0.000 title abstract description 77
- 238000000684 flow cytometry Methods 0.000 title abstract description 34
- 239000002245 particle Substances 0.000 claims abstract description 237
- 238000005286 illumination Methods 0.000 claims description 145
- 230000003287 optical effect Effects 0.000 claims description 65
- 238000001514 detection method Methods 0.000 claims description 35
- 239000012530 fluid Substances 0.000 claims description 33
- 230000000694 effects Effects 0.000 claims description 7
- 238000004891 communication Methods 0.000 claims description 5
- 230000006854 communication Effects 0.000 claims description 5
- 238000004458 analytical method Methods 0.000 abstract description 12
- 210000004027 cell Anatomy 0.000 description 86
- 239000000975 dye Substances 0.000 description 19
- 230000008859 change Effects 0.000 description 13
- 239000000523 sample Substances 0.000 description 13
- 239000011324 bead Substances 0.000 description 12
- 230000008901 benefit Effects 0.000 description 10
- 238000013459 approach Methods 0.000 description 7
- 230000007423 decrease Effects 0.000 description 7
- 230000005284 excitation Effects 0.000 description 7
- 230000003247 decreasing effect Effects 0.000 description 6
- 239000000463 material Substances 0.000 description 6
- 238000012545 processing Methods 0.000 description 6
- 238000013461 design Methods 0.000 description 5
- 238000005516 engineering process Methods 0.000 description 5
- 230000008569 process Effects 0.000 description 5
- 239000002131 composite material Substances 0.000 description 4
- 210000003743 erythrocyte Anatomy 0.000 description 4
- 230000006870 function Effects 0.000 description 4
- 230000003993 interaction Effects 0.000 description 4
- 238000000926 separation method Methods 0.000 description 4
- 239000007787 solid Substances 0.000 description 4
- 230000004075 alteration Effects 0.000 description 3
- 230000002596 correlated effect Effects 0.000 description 3
- 230000000875 corresponding effect Effects 0.000 description 3
- 230000005684 electric field Effects 0.000 description 3
- 239000004615 ingredient Substances 0.000 description 3
- 210000004940 nucleus Anatomy 0.000 description 3
- 239000010453 quartz Substances 0.000 description 3
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N silicon dioxide Inorganic materials O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 3
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 2
- GLNADSQYFUSGOU-GPTZEZBUSA-J Trypan blue Chemical compound [Na+].[Na+].[Na+].[Na+].C1=C(S([O-])(=O)=O)C=C2C=C(S([O-])(=O)=O)C(/N=N/C3=CC=C(C=C3C)C=3C=C(C(=CC=3)\N=N\C=3C(=CC4=CC(=CC(N)=C4C=3O)S([O-])(=O)=O)S([O-])(=O)=O)C)=C(O)C2=C1N GLNADSQYFUSGOU-GPTZEZBUSA-J 0.000 description 2
- 238000002835 absorbance Methods 0.000 description 2
- 201000009310 astigmatism Diseases 0.000 description 2
- 230000009286 beneficial effect Effects 0.000 description 2
- 239000011248 coating agent Substances 0.000 description 2
- 238000000576 coating method Methods 0.000 description 2
- 230000001276 controlling effect Effects 0.000 description 2
- 238000013500 data storage Methods 0.000 description 2
- 238000009826 distribution Methods 0.000 description 2
- 239000007850 fluorescent dye Substances 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- 239000006249 magnetic particle Substances 0.000 description 2
- 239000000203 mixture Substances 0.000 description 2
- 238000012758 nuclear staining Methods 0.000 description 2
- 230000005855 radiation Effects 0.000 description 2
- 229910052710 silicon Inorganic materials 0.000 description 2
- 239000010703 silicon Substances 0.000 description 2
- 230000002123 temporal effect Effects 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- 101000738771 Homo sapiens Receptor-type tyrosine-protein phosphatase C Proteins 0.000 description 1
- 108010052285 Membrane Proteins Proteins 0.000 description 1
- 102000018697 Membrane Proteins Human genes 0.000 description 1
- 102100037422 Receptor-type tyrosine-protein phosphatase C Human genes 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 230000004308 accommodation Effects 0.000 description 1
- 230000001464 adherent effect Effects 0.000 description 1
- 230000000274 adsorptive effect Effects 0.000 description 1
- 238000003556 assay Methods 0.000 description 1
- 230000008033 biological extinction Effects 0.000 description 1
- 238000005415 bioluminescence Methods 0.000 description 1
- 230000029918 bioluminescence Effects 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 230000003915 cell function Effects 0.000 description 1
- 210000000170 cell membrane Anatomy 0.000 description 1
- 210000003855 cell nucleus Anatomy 0.000 description 1
- 230000008614 cellular interaction Effects 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 230000000295 complement effect Effects 0.000 description 1
- 238000013329 compounding Methods 0.000 description 1
- 230000003750 conditioning effect Effects 0.000 description 1
- 238000010226 confocal imaging Methods 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 238000012937 correction Methods 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 210000000805 cytoplasm Anatomy 0.000 description 1
- 238000013480 data collection Methods 0.000 description 1
- 230000007812 deficiency Effects 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 238000002073 fluorescence micrograph Methods 0.000 description 1
- 238000001506 fluorescence spectroscopy Methods 0.000 description 1
- 238000001943 fluorescence-activated cell sorting Methods 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- 238000003780 insertion Methods 0.000 description 1
- 230000037431 insertion Effects 0.000 description 1
- 230000010354 integration Effects 0.000 description 1
- 230000008611 intercellular interaction Effects 0.000 description 1
- 230000001788 irregular Effects 0.000 description 1
- 238000004020 luminiscence type Methods 0.000 description 1
- 238000007898 magnetic cell sorting Methods 0.000 description 1
- 239000003550 marker Substances 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 238000000691 measurement method Methods 0.000 description 1
- 229910044991 metal oxide Inorganic materials 0.000 description 1
- 150000004706 metal oxides Chemical class 0.000 description 1
- 230000000116 mitigating effect Effects 0.000 description 1
- 239000003607 modifier Substances 0.000 description 1
- 210000003463 organelle Anatomy 0.000 description 1
- 238000005086 pumping Methods 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 238000005464 sample preparation method Methods 0.000 description 1
- 239000004065 semiconductor Substances 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 239000011343 solid material Substances 0.000 description 1
- 230000003595 spectral effect Effects 0.000 description 1
- 238000001228 spectrum Methods 0.000 description 1
- 238000010186 staining Methods 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 230000008685 targeting Effects 0.000 description 1
- 230000007704 transition Effects 0.000 description 1
- 238000011144 upstream manufacturing Methods 0.000 description 1
- 230000000007 visual effect Effects 0.000 description 1
- 238000012800 visualization Methods 0.000 description 1
Images
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L3/00—Containers or dishes for laboratory use, e.g. laboratory glassware; Droppers
- B01L3/50—Containers for the purpose of retaining a material to be analysed, e.g. test tubes
- B01L3/502—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures
- B01L3/5027—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip
- B01L3/502761—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip specially adapted for handling suspended solids or molecules independently from the bulk fluid flow, e.g. for trapping or sorting beads, for physically stretching molecules
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume, or surface-area of porous materials
- G01N15/10—Investigating individual particles
- G01N15/14—Electro-optical investigation, e.g. flow cytometers
- G01N15/1434—Electro-optical investigation, e.g. flow cytometers using an analyser being characterised by its optical arrangement
- G01N15/1436—Electro-optical investigation, e.g. flow cytometers using an analyser being characterised by its optical arrangement the optical arrangement forming an integrated apparatus with the sample container, e.g. a flow cell
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01J—MEASUREMENT OF INTENSITY, VELOCITY, SPECTRAL CONTENT, POLARISATION, PHASE OR PULSE CHARACTERISTICS OF INFRARED, VISIBLE OR ULTRAVIOLET LIGHT; COLORIMETRY; RADIATION PYROMETRY
- G01J3/00—Spectrometry; Spectrophotometry; Monochromators; Measuring colours
- G01J3/28—Investigating the spectrum
- G01J3/44—Raman spectrometry; Scattering spectrometry ; Fluorescence spectrometry
- G01J3/4406—Fluorescence spectrometry
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume, or surface-area of porous materials
- G01N15/02—Investigating particle size or size distribution
- G01N15/0205—Investigating particle size or size distribution by optical means, e.g. by light scattering, diffraction, holography or imaging
- G01N15/0227—Investigating particle size or size distribution by optical means, e.g. by light scattering, diffraction, holography or imaging using imaging, e.g. a projected image of suspension; using holography
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume, or surface-area of porous materials
- G01N15/02—Investigating particle size or size distribution
- G01N15/0272—Investigating particle size or size distribution with screening; with classification by filtering
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume, or surface-area of porous materials
- G01N15/10—Investigating individual particles
- G01N15/14—Electro-optical investigation, e.g. flow cytometers
- G01N15/1404—Fluid conditioning in flow cytometers, e.g. flow cells; Supply; Control of flow
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume, or surface-area of porous materials
- G01N15/10—Investigating individual particles
- G01N15/14—Electro-optical investigation, e.g. flow cytometers
- G01N15/1429—Electro-optical investigation, e.g. flow cytometers using an analyser being characterised by its signal processing
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume, or surface-area of porous materials
- G01N15/10—Investigating individual particles
- G01N15/14—Electro-optical investigation, e.g. flow cytometers
- G01N15/1434—Electro-optical investigation, e.g. flow cytometers using an analyser being characterised by its optical arrangement
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume, or surface-area of porous materials
- G01N15/10—Investigating individual particles
- G01N15/14—Electro-optical investigation, e.g. flow cytometers
- G01N15/1456—Electro-optical investigation, e.g. flow cytometers without spatial resolution of the texture or inner structure of the particle, e.g. processing of pulse signals
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume, or surface-area of porous materials
- G01N15/10—Investigating individual particles
- G01N15/14—Electro-optical investigation, e.g. flow cytometers
- G01N15/1456—Electro-optical investigation, e.g. flow cytometers without spatial resolution of the texture or inner structure of the particle, e.g. processing of pulse signals
- G01N15/1459—Electro-optical investigation, e.g. flow cytometers without spatial resolution of the texture or inner structure of the particle, e.g. processing of pulse signals the analysis being performed on a sample stream
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume, or surface-area of porous materials
- G01N15/10—Investigating individual particles
- G01N15/14—Electro-optical investigation, e.g. flow cytometers
- G01N15/1468—Electro-optical investigation, e.g. flow cytometers with spatial resolution of the texture or inner structure of the particle
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume, or surface-area of porous materials
- G01N15/10—Investigating individual particles
- G01N15/14—Electro-optical investigation, e.g. flow cytometers
- G01N15/1468—Electro-optical investigation, e.g. flow cytometers with spatial resolution of the texture or inner structure of the particle
- G01N15/147—Electro-optical investigation, e.g. flow cytometers with spatial resolution of the texture or inner structure of the particle the analysis being performed on a sample stream
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/17—Systems in which incident light is modified in accordance with the properties of the material investigated
- G01N21/47—Scattering, i.e. diffuse reflection
- G01N21/49—Scattering, i.e. diffuse reflection within a body or fluid
- G01N21/53—Scattering, i.e. diffuse reflection within a body or fluid within a flowing fluid, e.g. smoke
- G01N21/532—Scattering, i.e. diffuse reflection within a body or fluid within a flowing fluid, e.g. smoke with measurement of scattering and transmission
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N21/645—Specially adapted constructive features of fluorimeters
- G01N21/6456—Spatial resolved fluorescence measurements; Imaging
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2200/00—Solutions for specific problems relating to chemical or physical laboratory apparatus
- B01L2200/06—Fluid handling related problems
- B01L2200/0647—Handling flowable solids, e.g. microscopic beads, cells, particles
- B01L2200/0652—Sorting or classification of particles or molecules
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2400/00—Moving or stopping fluids
- B01L2400/08—Regulating or influencing the flow resistance
- B01L2400/082—Active control of flow resistance, e.g. flow controllers
-
- G01N15/149—
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume, or surface-area of porous materials
- G01N2015/0003—Determining electric mobility, velocity profile, average speed or velocity of a plurality of particles
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume, or surface-area of porous materials
- G01N2015/0007—Investigating dispersion of gas
- G01N2015/0011—Investigating dispersion of gas in liquids, e.g. bubbles
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume, or surface-area of porous materials
- G01N2015/03—Electro-optical investigation of a plurality of particles, the analyser being characterised by the optical arrangement
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume, or surface-area of porous materials
- G01N15/10—Investigating individual particles
- G01N2015/1006—Investigating individual particles for cytology
-
- G01N2015/1028—
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume, or surface-area of porous materials
- G01N15/10—Investigating individual particles
- G01N15/14—Electro-optical investigation, e.g. flow cytometers
- G01N15/1404—Fluid conditioning in flow cytometers, e.g. flow cells; Supply; Control of flow
- G01N2015/1415—Control of particle position
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume, or surface-area of porous materials
- G01N15/10—Investigating individual particles
- G01N15/14—Electro-optical investigation, e.g. flow cytometers
- G01N15/1404—Fluid conditioning in flow cytometers, e.g. flow cells; Supply; Control of flow
- G01N2015/142—Acoustic or ultrasonic focussing
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume, or surface-area of porous materials
- G01N15/10—Investigating individual particles
- G01N15/14—Electro-optical investigation, e.g. flow cytometers
- G01N15/1404—Fluid conditioning in flow cytometers, e.g. flow cells; Supply; Control of flow
- G01N2015/1422—Electrical focussing
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume, or surface-area of porous materials
- G01N15/10—Investigating individual particles
- G01N15/14—Electro-optical investigation, e.g. flow cytometers
- G01N15/1434—Electro-optical investigation, e.g. flow cytometers using an analyser being characterised by its optical arrangement
- G01N2015/1438—Using two lasers in succession
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume, or surface-area of porous materials
- G01N15/10—Investigating individual particles
- G01N15/14—Electro-optical investigation, e.g. flow cytometers
- G01N15/1434—Electro-optical investigation, e.g. flow cytometers using an analyser being characterised by its optical arrangement
- G01N2015/144—Imaging characterised by its optical setup
- G01N2015/1445—Three-dimensional imaging, imaging in different image planes, e.g. under different angles or at different depths, e.g. by a relative motion of sample and detector, for instance by tomography
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume, or surface-area of porous materials
- G01N15/10—Investigating individual particles
- G01N15/14—Electro-optical investigation, e.g. flow cytometers
- G01N15/1434—Electro-optical investigation, e.g. flow cytometers using an analyser being characterised by its optical arrangement
- G01N2015/1452—Adjustment of focus; Alignment
Abstract
本公开提供了用于在相对高的事件率下通过流式细胞术进行颗粒分析以及用于收集颗粒的高分辨率图像的设备、系统和方法。
Description
本申请是申请号为201880028673.4、申请日为2018年3月30日、发明名称为“用于成像流式细胞术的设备、系统和方法”的发明专利申请的分案申请。
技术领域
本公开涉及用于流体流动中细胞和其它微粒的成像设备、系统和方法的领域。
背景技术
流式细胞术是以高速度对颗粒进行的分析,其中细胞或颗粒传输通过高度聚焦的激光束,在所述激光束中,积分的荧光和散射光由一组检测器收集。这通常以高度并行的方式进行,其中颗粒在其行进通过系统期间横越多个激光器/检测组。所得数据用于确定性质(如表面蛋白质、内部标记物、颗粒形状的粗略估计等)的存在或不存在。在典型的细胞计数器中,这种分析以每秒100到100,000个细胞的速率进行。
期望收集与尽可能多的细胞相关联的光,但是在操作中,必须避免称为重合的情况。当多于一个细胞/颗粒同时处于激光束中时,重合就会发生。重合率与颗粒在激光器中花费的时间(探询时间)成正比。一般来说,探询时间越短,重合概率就越低。为此,通常采用非常低的占空比(<10%)和几微秒级的短探询时间以努力使重合事件最小化。
然而,在收集足够的光子以进行检测时,微秒级的探询时间造成困难。为了克服这个问题,采用高功率激光器、光电子倍增检测器(如光电倍增管(PMT)和雪崩光电二极管(APD))以及快速电子器件的组合。几十年来,这一直是流式细胞术设计的标准。当信号是由整个细胞生成的积分响应时,这些超短探询时间通常是可接受的,就像传统流式细胞术方法中所做的那样。然而,如果需要更高的空间分辨率数据,如以允许细胞膜、细胞核、细胞质和/或细胞器可视化的方式对细胞进行成像,那么这样短的时间是有问题的。
由于高分析速率所需的短探询时间,因此流式细胞术中的高分辨率成像受到限制。如与从整个细胞收集积分信号相反,如相机等成像检测器必须逐个像素地对来自细胞上的更小位置的光进行检测。以高速度收集单细胞高分辨率图像的挑战是困难的,因为由每个像素生成的光子计数远低于积分光子计数。为此,在流式细胞仪中进行的成像通常以较长的探询时间进行以增加光子计数。然而,较长的探询时间大大降低了事件率,并且因此成像流式细胞术主要用于利基应用。因此,本领域长期需要用于成像流式细胞术的设备、系统和方法,所述设备、系统和方法能够操作以便以相对缓慢和相对较快的探询时间收集信息。
发明内容
一方面,本公开提供了系统,其包括:流动通道,所述流动通道具有入口,并且所述流动通道限定了流体通过其连通的流动路径;第一光具组,所述第一光具组包括第一照明源和第一检测模块,所述第一检测模块被安置成接收与由所述第一照明源照亮的所述流动通道的第一区域相关的信号,所述第一区域定位在距所述流动通道的所述入口的第一距离处;第二光具组,所述第二光具组包括第二照明源和第二检测模块,所述第二检测模块被安置成与由所述第二照明源照亮的所述流动通道的第二区域相关的信号,所述第二区域定位在距所述流动通道的所述入口的第二距离处,所述第二距离大于所述第一距离,并且(a)其中所述流动通道的所述第一区域限定第一横截面面积,其中所述流动通道的所述第二区域限定第二横截面面积,并且其中所述第一横截面面积和所述第二横截面面积在面积上、形状上或在面积和形状两者上彼此不同,或(b)其中(i)所述系统包括进入所述流动通道的所述入口与所述流动通道的所述第一区域之间的所述流动通道的导管,(ii)所述系统包括进入所述流动通道的所述第一区域与所述第二区域之间的所述流动通道的导管,或(i)和(ii)两者,(c)其中所述系统包括流速调节器,所述流速调节器被配置成调节所述流动路径中的速度,或(d)所述系统进一步包括场模块,所述场模块被配置成增加或减少所述流动通道的区域处的场,以便使所述流动通道中的流动中的至少一些颗粒移动并且对从所述流动通道中的所述流动内的颗粒速度的速度流线S0到所述流动通道中的所述流动内的颗粒速度的速度流线S1的场敏感,其中在所述流动通道的第一区域与第二区域之间,系统操作期间S0处的所述颗粒速度不同于S1处的颗粒速度,或(a)、(b)、(c)、或(d)的任何组合。
另一方面,本公开提供了方法,其包括:使颗粒群流动通过流动通道;使用第一光具组,在所述流动通道的第一区域处照亮所述颗粒群中的至少一些并收集与所述照明有关的第一信号;使用第二光具组,在所述流动通道的第二区域处照亮所述颗粒群中的至少一些并收集与所述照明有关的第二信号,所述流动通道的所述第一区域处的颗粒速度不同于所述流动通道的所述第二区域处的颗粒速度,并且所述第一信号不同于所述第二信号。
进一步提供了方法,其包括:在从流动通道的第一区域朝向所述流动通道的第二区域的方向上使颗粒群传送通过所述流动通道;使用第一光具组,在所述流动通道的所述第一区域处照亮所述颗粒群中的至少一些并收集与所述照明有关的第一信号;使用第二光具组,在所述流动通道的所述第二区域处照亮所述颗粒群中的至少一些并收集与所述照明有关的第二信号;增加或减少所述流动通道的所述第一区域与所述第二区域之间的颗粒子集上的场,增加或减少所述场,以便将所述颗粒子集从所述流动通道内的颗粒速度的速度流线S0移动到所述流动通道内的颗粒速度的速度流线S1,其中S0处的所述颗粒速度不同于S1处的所述颗粒速度。
附图说明
当结合附图阅读时,将进一步理解发明内容以及以下具体实施方式。出于说明本技术的目的,在附图中示出了本发明的示例性和优选实施例;然而,本公开不限于所公开的具体方法、组合物和装置。另外,附图不一定按比例绘制,并且附图的各个部分上的文本标签仅是说明性的并不限制所公开的技术。在附图中:
图1提供了以不同速度横越不同探询区的颗粒的图示;
图2描绘了具有不同横截面的流动池可以如何改变不同探询位置之间的颗粒的速度;
图3A提供了流动池,所述流动池通过在探询区之间注入或移除鞘液来操作,以便在探询区之间产生颗粒的速度差;
图3B提供了流动池,所述流动池通过在探询区之间采用流速调节器来操作,以便在探询区之间产生颗粒的速度差;
图3C提供了流动池,所述流动池通过在探询区之间采用场模块来操作,以便在探询区之间产生颗粒的速度差;
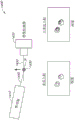
图4提供了流动池,所述流动池被配置成沿着颗粒流动的方向收集图像;
图5提供了流动池,所述流动池被配置成沿着颗粒的流动路径收集图像;并且其中通过增大流动通道尺寸来减小颗粒的速度,并且可以通过适当调整输出端口的大小来进一步减小颗粒的速度以调整颗粒轨迹;
图6描绘了常规流式细胞术数据(高度、面积和宽度)以及还有若干颗粒中的每一个颗粒的图像数据的集合;
图7描绘了流式细胞仪,所述收流式细胞仪收集常规流式细胞术数据并在颗粒被分选之前捕获所述颗粒的一个或多个图像;
图8描绘了流式细胞仪,所述流式细胞仪在颗粒/细胞被分选之后捕获颗粒/细胞的一个或多个图像或其它数据;并且其中分选后区域可以进一步包括阱和/或其它用于经过分选的颗粒/细胞的下游操纵的装置;
图9描绘了一种系统,所述系统被配置成捕获合成图像,如收集同一图像内的明场和荧光数据两者;
图10描绘了由成像光学器件产生的会聚波形;并且还有其中二色性选择性地允许光以产生无像差的图像的方式通过或反射,同时使用多个相机;
图11提供了实施例的图示,在所述实施例中,石英板的插入将焦距延伸到图像检测器之一;
图12提供了实施例,在所述实施例中,成像光学器件将多个目标平面用于轨迹与通过成像系统的轨迹略微不同的颗粒;对于具有浅景深的成像系统,这种布置可以减少对高精度颗粒定位的要求,并且还可以增加常规流动光学器件的景深,从而扩展了有用的高数值孔径(NA)光学设计的范围;
图13提供了实施例,在所述实施例中,由照明光具组使用的多个焦面在更大的焦深上产生更均匀的照明,由此提高图像质量、减少激光散斑并降低对物体定位的灵敏度;
图14提供了实施例,在所述实施例中,光学系统内的照明和成像的光轴线偏移角度α,以在所得图像内产生阴影区域,所述阴影区域提供增强的对比度;
图15提供了拍摄的以4米/秒(曝光时间为1微秒)行进的红细胞的图像-如图所示,图像是模糊的并且难以辨别细胞边界;
图16提供了用与图15相同的设置以慢四倍的速度(1米/秒)拍摄的红细胞的图像-如图所示,运动模糊减少并且细胞的外部边界易于区分;
图17提供了以约1米/秒行进的珠粒的图像(珠粒在焦点上);并且
图18提供了以约8米/秒行进的珠粒的图像(珠粒是模糊的)。
具体实施方式
除非另有定义,否则本文所使用的所有技术术语和科学术语具有与本领域普通技术人员通常理解的含义相同的含义。在有冲突的情况下,将以本文件,包含定义为准。虽然与本文所述的那些方法和材料类似或相当的方法和材料可以用于实践或测试中,但是以下描述了优选的方法和材料。本文所提及的所有出版物、专利申请、专利和其它参考通过引用以其整体并入。本文所公开的材料、方法和实例仅是说明性的而不旨在是限制性的。
除非上下文另外清楚地指明,否则单数形式“一个(a)”、“一种(an)”和“所述(the)”包含复数指示物。如说明书和权利要求书所使用的,术语“包括”可以包含“由……组成”和“基本上由……组成”的实施例。如本文所使用的,术语“包括(comprise(s))”、“包含(include(s))”、“具有(having)”、“具有(has)”、“可以”、“含有(contain(s))”及其变体旨在是需要指定材料/步骤存在并且允许其它材料/步骤存在的开放式过渡性短语、术语或词语。然而,此类描述应被解释为还将组合物或方法描述为“由所枚举成分/步骤组成”和“基本上由所枚举成分/步骤组成”,这允许仅存在所述成分/步骤连同可能由此产生的任何杂质,并排除其它成分/步骤。应该理解的是,本文所使用的术语仅出于描述特定方面的目的,而不旨在是限制性的。如说明书和权利要求书所使用的,术语“包括(comprising)”可能包含“由……组成”和“基本上由……组成”的实施例。除非另外定义,否则本文使用的所有技术术语和科学术语具有与本公开所属领域的普通技术人员通常所理解的含义相同的含义。在本说明书和随后的权利要求中,将参考应在本文中定义的一些术语。
本申请的说明书和权利要求中的数值反映了平均值。此外,除非相反指出,否则数值应被理解为包含与当减少到有效数字的相同数量时相同的数值以及与所述值的差异小于属于在本申请中被描述为用于确定值的类型的传统测量技术的实验误差的数值。
本文所公开的所有范围包含所述的端点并且可独立地组合(例如,“2克(g)到10克”的范围包含端点、2克和10克以及所有中间值)。本文所公开的范围的端点和任何值不限于精确的范围或值;它们非常不精确以包含近似这些范围和/或值的值。
如本文所使用的,可以应用近似语言来修饰任何定量表示,所述定量表示可以在不导致与其相关的基本功能的变化的情况下发生变化。因此,在一些情况下,由一个或多个术语(如“约”和“基本上”)修饰的值可能不限于指定的精确值。在至少一些情况下,近似语言可以对应于用于测量值的仪器的精度。修饰语“约”还应该被视为公开了由两个端点的绝对值限定的范围。例如,表达“约2到约4”还公开了“2到4”的范围。术语“约”可以指代所指示的数字的加或减10%。例如,“约10%”可以表示9%到11%的范围,并且“约1”可以意指0.9到1.1。“约”的其它含义可以从上下文显而易见,如四舍五入,因此,例如“约1”还可以意指0.5到1.4。
术语
如本文所使用的,“照明”是指辐射(可见或不可见),所述辐射可以应用于颗粒、细胞或其它所关注的分析物。应该理解的是,术语“照明”包含荧光染料或其它部分的激发,并且还包含在亮场、暗场、相衬照明等的背景下辐射的应用。类似地,“照明源”是执行照明的装置或允许执行照明的装置或系统的一个或多个部件。激光器、灯、发光二极管等被认为是照明源的非限制性实例。
如本文所使用的,“检测”是指光的集合,无论是反射的、波长移位的还是未反射的,都包含发射光(包含荧光)或与样品相互作用的光。作为一个实例,收集可见图像的相机执行“检测”。类似地,“检测器”是指执行检测的装置或允许执行检测的装置或系统的一个或多个部件。光电倍增管(PMT)、硅光电倍增管(SiPM)、光子计数器、雪崩光电二极管(APD)等被认为是检测器的非限制性实例。
如本文所使用的,术语“图像检测器”是指允许产生颗粒图像的任何类型的检测器或检测方法。像素化检测器、狭缝扫描光学器件、频率多路复用成像、时间拉伸方法等被认为是能够产生颗粒图像的“图像检测器”。
如本文所使用的,与术语“常规流式细胞术数据”可互换使用的术语“传统流式细胞术数据”是指由于光与流动流中的颗粒相互作用而从光中收集的数据,例如脉冲高度、面积和宽度。这种传统流式细胞术数据在历史上并不包含成像数据,因为传统流式细胞仪在历史上并没有成像能力。如本文所使用的,术语“传统流式细胞仪”和“常规流式细胞仪”可互换使用。
如本文所解释的,期望具有能够以高事件率和低重合度收集传统流式细胞术数据同时还产生颗粒的高分辨率图像的仪器。已经有成像流式细胞术的多个实例。这些现有方法中的大多数采用常规流式细胞仪设计中的图像检测器。然而,由于常规流式细胞仪设计和可用成像技术的不足,在流动中对颗粒进行成像的尝试导致低图像捕获和低分析速率。目前,有解决成像流式细胞术的更高数据速率的若干种技术。一种技术使用时间延迟积分(TDI)阵列。TDI阵列累积移动物体的多次曝光,由此增加探询时间。该技术需要精确的颗粒速度知识,以允许检测器跟踪颗粒的横越。使用该技术的当前系统具有每秒仅几千个颗粒的最大事件率。另外,通过在图像中找到细胞并在经过计算的细胞边界内进行积分来处理常规流式细胞术数据(积分信号)。该处理是存储器密集的且耗费时间的,从而迫使数据显示和分析在数据收集后执行。
第二种技术是使用频率多路复用的方法。在该方法中,照明光被频率多路复用成小像素的大阵列。通过使颗粒与该光束阵列相互作用产生的时域签名由PMT收集。然后通过在频域中处理信号并将像素位置分配给特定光谱值来构建图像。该系统以与频率多路复用显微镜非常类似的方式操作。
频率多路复用成像相对于流式细胞仪中的基于相机的系统具有优势,因为常规流式细胞术数据(积分信号)更容易获取。与分析图像相反,通过对时域信号进行积分来获得积分数据。但是,为了减少图像中移动细胞的模糊,必须限制颗粒速度以获取高分辨率图像。虽然用该方法对常规流式细胞仪数据进行的处理可以快速完成,但是对较低速度的要求导致比常规流式细胞仪更低的数据速率。
与频率多路复用成像类似,已经开发了类似的方法来在空间上拉伸光脉冲。所述照明包括光脉冲,所述光脉冲具有跨光束延伸的频谱。在与细胞相互作用之后,所收集的光行进通过分散元件,所述分散元件在时间上扩散作为频率函数的光脉冲。一旦捕获了时域签名,就通过将像素分配到特定时间收集的光量来重建图像。
理论上,通过在较高浓度和较低速度下运行样品,可以提高与这些成像技术相关联的较低数据速率。这是可能的,因为增加的空间分辨率可以用于更好地区分图像中的单个细胞,从而通过图像处理减少重合事件的数量,代价是增加处理负担和数据时延。
然而,在实践中,增加的样品浓度并不总是实用的或期望的。为了达到常规流式细胞仪的数据速率而需要更高的样品浓度,这就需要改变样品制备方法以产生浓度超过典型工作条件的样品。高浓度还导致更多细胞彼此粘附,特别是对于粘附样品。
使在较低速度下分析的浓度较高样品的问题更为复杂的是与成像系统相关联的浅景深。由于高放大率光学器件所需的景深有限,因此高质量高分辨率图像需要在图像平面上对颗粒进行紧密定位。通常,通过利用鞘液与样品流体的高比率来实现这种精确定位。因此,为了精确定位颗粒以适应浅景深,需要进一步限制事件率的相对低的体积样品输入速率。
随着快速、高灵敏度成像检测器(如电子倍增电荷耦合装置(EMCCD)、强化电荷耦合装置(ICCD)、互补金属氧化物半导体(CMOS)装置等)与快速、廉价电子器件的组合,穿过照明探询区的细胞图像可以以接近常规流式细胞仪中的那些的相对高的速度进行处理。本发明描述了用于创建和采用混合流式细胞仪的设备、系统和方法,所述混合流式细胞仪能够以常规流式细胞仪的高事件率收集积分颗粒数据,同时还获得颗粒的高分辨率图像。以下描述了各种不同的实施例。
多个速度区
通过将不同的颗粒速度与每个区相关联,可以通过在系统内创建单独的颗粒探询区来增强混合成像流式细胞仪的吞吐量和数据质量。图1提供了一种创建单独的颗粒探询区的方式。如图1所示,系统100可以包含第一照明源102(在这种情况下,照明源),所述第一照明源被安置成在第一照明源102与检测器104之间的位置处照亮第一位置180a处的颗粒。在第一位置180a处,颗粒经历速度V1。
然后,颗粒传送到第二位置180b,所述第二位置被安置在第二照明源106与图像检测器110之间,所述图像检测器在此被描述为相机。在第二位置180b处,颗粒经历速度V2,其中速度V2小于速度V1。较高速度区(V1)允许较短的探询时间和传统流式细胞仪的低重合。较低速度区(V2)允许较长的探询时间,所述较长的探询时间增加了积分光子计数并减少了成像装置的模糊。除了成像方法的优点之外,可以对所得图像进行处理以解决与第一位置180a相关联的重合事件。
沿颗粒路径创建不同速度区的一种方式是改变流动通道的横截面。图2描绘了系统200,其中改变了两个区域之间的流动通道220的横截面面积。第一区域290a定位在第一照明源202与检测器204之间。第二区域290b定位在第二照明源206与图像检测器210之间。当颗粒从第一区域290a内的第一位置280a传送到第二区域290b内的第二位置280b时,颗粒经历速度降低(第一位置280a处的V1和第二位置280b处的较小V2),由于流动通道220在第二区域290b内的横截面面积相对于第一区域290a增大。
由于颗粒的速度可以与流动的横截面面积成比例地缩放,因此正方形横截面流动的尺寸的2倍变化(例如,100μm x 100μm的横截面变为200μm x 200μm的横截面)可以导致颗粒速度变化4倍。在此实例中,总光子计数增加了四倍,明显提高了图像检测器的信噪比。另外,降低的速度减少了图像中的模糊,从而允许在平行于颗粒移动的维度上具有更高的分辨率。
随着探询时间的增加,流动池尺寸的增加还增加了颗粒位置的变化。这可以增加对扩展焦深的要求,所述扩展焦深可能降低图像质量。与流动池尺寸在其它方向上的扩展相比,这可以通过在垂直于物面的方向上将流动池尺寸扩展相对较小的量来减轻。可替代地,可以采用其它缓解方法,如使用如声学聚焦等场聚焦技术以更好地将颗粒聚焦在图像平面中。
用于改变探询区之间的颗粒速度的替代性方法采用改变探询区之间的流动特性。增加或减少两个探询区之间的体积流动可以产生速度差。图3A中示出了这种系统的实例。
如图3A所示,系统300包含流动通道320,在所述流动通道内,颗粒从第一区域390a内的第一位置380a(所述第一位置安置在第一照明源302与图像检测器306之间)传送到第二区域390b内的第二位置380b(所述第二位置安置在第二照明源304与检测器308之间)。在第一区域390a与第二区域390b之间,流动通道320可以包含侧通道340和侧通道342,所述侧通道用作导管以允许引入和/或抽出额外流体(例如,鞘液),以便增大或减小第一位置380a与第二位置380b之间的流动速度。如图3A所示,通过侧通道340和侧通道342引入额外的流体—鞘液提供了与在第一位置380a处的较早的较小速度V1相比在第二位置380b处具有较大速度V2的颗粒。
在替代性实施例中,与引入流体相反,侧通道340和侧通道342从流动通道320中抽出流体。在此类实施例中,从第一位置380a与第二位置380b之间的流动通道320移除流体具有降低颗粒速度的效果,使得V1大于V2。对于这些替代性实施例,可能期望至少交换图像检测器306和检测器308的位置(即,使得图像检测器306在第二位置380b处获得颗粒的图像)。这将为图像检测器306带来益处,因为在此类实施例中,考虑到较低速度V2,可以收集更多的光子。在此类实施例中,根据各自的能力和所期望的输出,还可能期望交换第一照明源302和第二照明源304的位置。
此外,对于使用侧通道从流动通道320引入和/或抽出流体的实施例,某些实施例可以仅利用一对探询区之间的一个侧通道或导管(例如,系统300仅使用侧通道340,而不使用侧通道342)。在此类实施例中,采用一个侧通道的效果将是使颗粒更靠近流动通道320的一个侧壁移动。如本领域中已知的,流动通道中的流体和颗粒的速度在通道的中心处最高,并且随着流体和颗粒接近通道的壁而减小。单个侧通道实施例的这种使用可以有助于例如当接近经受图像检测器的流动通道区域时减慢颗粒的速度,从而能够收集由于通道壁附近较低颗粒速度而数目增加的光子。
用于改变探询区之间颗粒速度的替代性方法采用在探询区之间使用流速调节器。图3B示出了此类系统的实例。
如图3B所示,系统300包含流动通道320,在所述流动通道内,颗粒从第一区域390a内的第一位置380a(所述第一位置安置在第一照明源302与图像检测器306之间)传送到第二区域390b内的第二位置380b(所述第二位置安置在第二照明源304与检测器308之间)。在第一区域390a与第二区域390b之间,系统300可以包含流速调节器350和流速调节器352,所述流速调节器允许第一位置380a与第二位置380b之间的流动速率增大或减小。流速调节器可以包括例如泵、阀等。如图3B所示,使用流速调节器350和流速调节器352将额外的流体泵入到流动通道320中提供了与在第一位置380a处较早的较小速度V1相比在第二位置380b处具有更大速度V2的颗粒。
在图3B的替代性实施例中,流速调节器350和/或流速调节器352可以包括阀,当打开时,所述阀用于从流动通道320中移除流体。此类实施例将提供与在第一位置380a处的较早的较高速度V1相比在第二位置380b处具有较小速度V2的颗粒。如果期望将图像检测器306定位到颗粒将具有较小速度的流动通道320的区域,则此类实施例还可以交换图像检测器306和检测器308的位置。与图3A的某些替代性替代实施例一样,图3B的替代性实施例中仅采用单个流速调节器。例如,流速调节器350可以用作阀,以在打开时从流动通道320中移除流体,并且不需要任何对应的流速调节器352。在此实例中,颗粒还将更靠近流动通道320的侧壁移动,从而进一步降低其速度。
用于改变探询区之间颗粒速度的替代性方法采用在探询区之间使用场模块。图3C示出了此类系统的实例。
如图3C所示,系统300包含流动通道320,在所述流动通道内,颗粒从第一区域390a内的第一位置380a(所述第一位置安置在第一照明源302与图像检测器306之间)传送到第二区域390b内的第二位置380b(所述第二位置安置在第二照明源304与检测器308之间)。在第一区域390a与第二区域390b之间,系统300可以包含场模块360,所述场模块被配置成增大或减小流动通道320的区域处的场,以便将受场影响的颗粒重新定位到流动通道320内的流动的不同速度流线中。(尽管图3C中仅示出了一个场模块,但是应该理解的是,所公开的技术设想使用单个场模块以及使用多个场模块两者。作为一个实例,根据本公开的系统可能包含磁场模块并且还包含声场模块。如图3C所描述的,在第一位置380a处时,颗粒处于速度流线370内,并且在颗粒通过场模块360移动到速度流线375中之后在颗粒处于第二位置380b处时移动到速度流线375中。颗粒的这种重定位的效果是,颗粒在第二位置380b处的速度V2小于颗粒在第一位置380a处的速度V1。场模块360可以生成磁场、电场、声场或其任何组合。如果采用不同场的组合,则除了场模块360之外,系统300可以采用一个或多个另外的场模块。因此,可以使用一个或多个场模块,使得给定的颗粒在流动室内的不同区域处经历不同的速度。
如在各个实施例的上述描述中可以看到的,正如由尺寸变化引起的较慢流动一样,来自较低体积速度的较慢流动导致样品颗粒的位置分布较宽。这种较慢的流动可以类似地通过在一个维度上增加或减少比另一个维度上更多的流动来控制在两个维度上,并且还可以类似地受益于基于场的聚焦。如果提供了差分地控制增加或减少的流动的方法,则这种方法还可以用于调整颗粒位置,以实现更好的图像聚焦。改变体积速率的方法的优点在于每个速度区都可以如特定应用可能期望的单独地调整或拨入。例如,从单个孔口注入或移除流体从而将颗粒重定位到较低速度的流动流中可能导致较低的颗粒速度。流体的注入/移除可以手动或以自动方式实现。流体的注入/移除可以是恒定的或随时间推移而变化。
应该理解的是,根据本公开的系统可以包含将流动池的尺寸变化与体积流动速率的增加或减少组合。将这两种方法组合起来允许以最大灵活性设计具有所期望的颗粒速度、颗粒分布、流动通道物理尺寸和整个系统配置(包含光源和检测器)的流动区域。
通过选择颗粒经历速度区的顺序,可以实现某些优点。例如,在较慢速度之前具有较快速度的优点在于,在较高速度区中生成的较低存储器密集数据(例如,来自整个细胞的积分信号)可以更容易地用于基于积分信号数据选择性地触发图像捕获。通过仅选择性地触发图像捕获装置,所收集和处理的数据量减少,尤其是对于罕见的事件。例如,可以利用该特征来允许针对更少数量的细胞的更高分辨率增加内容图像。该特征还可以与受益于较低占空比的图像技术一起使用,如使用多通道板或条纹管的图像增强器或需要等待时间段来下载或处理数据的图像检测器,当以非常高的重复率使用时,所述图像增强器可能使电子耗尽。应该理解的是,所公开的技术非常适合于涉及罕见事件的应用,例如,以0.01%和以下的频率发生的事件。所公开的技术可以用于检测以0.01%和以下频率(例如,0.01%到0.001%或甚至0.01%到0.00001%)发生的事件。
在一些实施例中,根据本公开的系统可以使颗粒经受较低速度部分,然后是较高速度部分。此类实施例在人们可能希望以较低速度部分对颗粒成像(例如,以便提高图像分辨率)并且然后增加颗粒速度以进行随后的分选和/或常规流动分析的情况下可能是有用的。参考图1,此类施例将是V2大于V1的实施例,并且其中图像检测器(例如,相机或其它成像器)存在于V1上游位置处,并且检测器存在于下游V2位置处。
应该理解的是,所公开技术的实施例可以包含多于两个速度区。例如,当细胞被许多不同的检测器系统探询时,若干连续的速度变化可能是有利的。作为一个实例,系统可以包含常规流动数据、低分辨率图像数据和高分辨率图像数据的顺序生成。作为另一个实例,系统可以包含用于成像的慢速度区、用于常规流动的相当快的速度区以及用于在分选期间更好地分离的仍相当更快的速度区。根据本公开的系统可以具有例如三个、四个或甚至更多个速度区。
各种其它实施例可以包含检测器和/或照明源的朝向的变化和/或流动方向的变化。例如,图4示出了系统400,所述系统包含具有物镜的图像检测器408,所述物镜被配置成沿着通道420中的流动轴线捕获图像。
如图所示,颗粒可以从第一区域490a中的第一位置480a(所述第一位置安置在照明源402与检测器404之间)传送到第二区域490b中的第二位置480b,其中颗粒可能经受来自照明源406和/或来自照明源460的照明。如图4所示,照明源460被配置成提供落射照明。如图所示,颗粒在第一区域490a处经历速度V1,所述速度V1可以大于颗粒在第二区域490b处经历的速度V2。第二区域490中的颗粒的照明可以任选地与图像检测器408的物镜分离和/或它可以使用图像检测器408的物镜本身。
图5提供了系统500,所述系统具有针对图4的替代性配置,其中第二区域590b内的流动比第一区域590a内的流动慢。如图5所示,颗粒可以在流动通道520内从第一位置580a传送到第二位置580b,其中所述颗粒在第二位置580b处的速度V2小于在第一位置580a处的速度V1。如图所示,在第一位置580a处,颗粒安置在照明源502与检测器504之间。在第二位置580b处,颗粒可以从照明源550和/或照明源555接收照明,其中对应的图像数据由图像检测器560收集。如图5所描述的,照明源555处于epi配置中。照明可以任选地与图像检测器560的物镜分离和/或它可以使用图像检测器560的物镜本身。如前述等几何形状变化对于检测器或照明元件的物理容纳并且还对于控制由照明配置产生的杂散光可能是期望的。
另外,在照射轴线垂直或接近垂直于颗粒移动并且图像采集轴线接近平行于颗粒移动的配置中,严格的景深要求可以大大降低,因为当颗粒将流过由景深限定的整个区域时,景深不再与垂直于流动方向的平面中的颗粒位置相关联。在此类实施例中,选择适当的时间(与控制侧向位置相反)是捕获期望平面中的图像所需的全部。
应该理解的是,尽管上述实施例应用于流动成像,但该技术对于将标准高速流动数据与任何难以用常规方法检测到的低光度现象组合具有实用性。例如,在常规流速下难以检测单细胞化学发光和生物发光。在此类替代性实施例中,成像元件(如图4内的图像检测器408或图5内的图像检测器560)可能不存在,因为替代性实施例还可以采用没有成像能力的检测器,因为此类检测器还将受益于在较低流速下从这些低功率信号收集的增加数量的光子。
重合门控
在传统流式细胞仪中,数据是通过将来自检测区域内整个细胞的散射光/荧光进行积分而形成的。为了确定事件是否重合,通常针对可以包含脉冲高度、脉冲宽度或脉冲面积的若干不同参数来绘制数据。然后利用该数据来确定可能的重合。该方法可以用作确定重合事件的近似值。
然而,在重合很重要的实验中,需要改进的方法来确定重合。将图像生成装置或系统添加到常规流式细胞仪可以允许大大改进的重合检测。图像包含用于确定检测区域中多于一个细胞的存在的空间信息。
图6提供了具有示例性配置的系统600,其中常规流动数据和图像数据从颗粒收集。如图所示,颗粒可以从第一位置620a传送到第二位置620b并传送到第三位置620c,其中第一位置经受第一照明源630和第一检测器660,第二位置经受第二照明源632和第二检测器662,并且第三位置经受照明源620和图像检测器650。如所描述的,常规流动数据由从检测器收集的光脉冲中收集的若干参数组成。这些参数可以包含脉冲高度(H)、脉冲面积(A)和脉冲宽度(W)。无论探询区之间是否存在速度变化,该配置都是有益的。
通过添加颗粒的图像,用户可以以若干不同方式利用这些数据来确定当存在另一个细胞时是否收集来自具体细胞或颗粒的数据。例如,通过观察图像,可以评估给定事件的重合,从而提供数据质量的零阶确定。以更复杂的方式,可以对图像进行处理以确定整个数据集中的任何数据点是否存在重合事件。在这种情况下,用户可以根据具体的一组规则处理图像数据,以确定在数据集内的重合条件期间收集了哪些事件。然后,用户可以丢弃与重合事件相关联的数据,以节省数据存储空间或进行另外的分析。
值得注意的是,重合并不总是不利的。存在两个接触的细胞可能代表所关注的细胞-细胞相互作用的情况。由于空间数据在常规流式细胞仪中受到限制,因此难以检测此类相互作用。向常规流式细胞仪添加成像能力允许用户通过查看或处理图像来确定这种情况。然后,该信息可以与收集的常规流式细胞术数据内的具体事件相关联。
基于图像的分选
流式细胞术分选涉及从单独细胞收集传统流式细胞术数据(积分信号)以决定对细胞进行分选。对于用户来说,具有已经分选的对应图像将是有利的。通过添加与常规流式细胞术检测器符合的成像能力,如图7所示,图像可以与已经分选的颗粒相关联。所述图像将包含常规流式细胞术数据中不存在的信息,如细胞形态、核大小/形状、重合相互作用等。
如说明性图7中的系统700所示,颗粒可以从第一位置720a传送到第二位置720b并传送到第三位置720c,其中第一位置经受第一照明源714和第一检测器770,第二位置经受第二照明源712和第二检测器模块772,并且第三位置经受第三照明源710和图像检测器774。如所描述的,流动数据可以包含从由检测器收集的光脉冲收集的若干参数。这些参数可以包含脉冲高度(H)、脉冲面积(A)和脉冲宽度(W)。无论探询区之间是否存在速度变化,该配置都是有益的。
图7的系统可以进一步包含分选模块790,所述分选模块可以基于表示一个或多个具体标记物、细胞功能、物理特性等的存在、不存在或水平的存在、不存在或数据水平来对颗粒进行分选。一些示例性分选模块包含基于机械的分选器,例如捕集管分选器、阀分选器等。液滴分选器和气泡分选器也是合适的,因为基于场的分选器(如基于电场、声场和磁场的分选器)还是合适的。场的大小可以是恒定的,但还可以根据用户的需要随时间推移而调整或改变。
使用常规流式细胞术数据执行分选决策并且然后捕获图像的系统对于流式细胞术用户是有利的。在一些实施例中,在此类系统内可以使用分选触发器来触发相机,使得仅保存经过分选的颗粒的图像。在此类方法中,用户可以绘制门控来选择具有属于这些门控的特性的任何颗粒。当用户希望数据落在所选定的门控之外时,还可能出现负值。可以实时分析数据以确定分选和成像决策。通过选择性地对门控进行分选和成像,可以大大减少数据存储空间的需求。另外,用于分析数据的处理负担也大大降低。
在图像或其它分析后进行分选
如果分选的动作将颗粒或细胞移动到具有不同速度的例如(i)不同的流动通道、(ii)不同的腔室、或(iii)不同的流动部分,则分选过程本身可以用作切换分析区域的工具。该技术对于稀有细胞尤其有利,在所述稀有细胞中,细胞的速度可以大大降低或甚至停止。物理细胞阱或基于场的细胞阱还可以用于在成像/分析区域中或在此类区域之后收集细胞。
如图8中的系统800所示,颗粒可以从第一位置820a(其中颗粒经受来自第一照明源834的照明和第一检测器840)传送到第二位置820b,其中颗粒经受第二照明源832和第二检测器842。然后,分选模块830可以用于在特定基础上对颗粒进行分选,使得经过分选的颗粒(例如,在位置820e处示出的颗粒)在一个方向上路由(例如,在相同的流动通道中继续),并未经分选的颗粒或不满足可适用的分选标准的颗粒(例如,位置820d处的颗粒)在另一个方向上路由(例如,被路由到单独的流动通道中)。图像检测器850(例如,相机)可以收集经过分选的颗粒的图像。
当然,系统可以被配置成包含多个分选器,所述多个分选器可以用于基于不同的颗粒特性对颗粒进行分选。例如,系统可以包含第一分选器和第二分选器,所述第一分选器用于基于尺寸对颗粒进行分选,所述第二分选器基于颗粒的电荷对颗粒进行分选。系统还可以包含一个或多个成像器,以允许在分选阶段之前或之后收集颗粒图像。
在一些实施例中,通道可以从“主干”区域分成多个“分支”区域。主干中的流速可能比分支区域中的流速慢,即使这不是必需的。此类实施例可以适用于存在颗粒分选的应用(例如,其中细胞通过流动数据进行分选,并且然后对可能关注的细胞进行成像,同时将不关注的细胞引导到替代性分支)。在一些实施例中,一个或多个分支区域可以包含其自己的照明源和/或检测器,以便允许样品的多路复用分析。
然后,可以采用可能以其它方式受限制的成像技术来收集更高的内容信息。可以从采用本文所公开的实施例中大大受益的此类成像技术的实例包含时间分辨成像、3D共焦成像和3D全息成像。在此类装置中,可以通过交换缓冲液/添加其它试剂来对所收集的细胞进一步进行下游操纵以为其它分析做准备。
重叠、合成图像和彩色图像
操作常规流式细胞仪的流式细胞仪操作者可以同时对细胞进行若干不同的测定。例如,研究人员可能对细胞上的CD4、CD8和CD45表达感兴趣。这需要若干检测通道来识别每个相关联标签的贡献。同样地,在对细胞进行成像时,所关注的是有能力运行显示细胞相互作用发生的位置的若干不同的标签。
传统上,空间识别是通过在不同波长下创建若干图像来完成的。例如,存在在成像阵列上或甚至在单个像素化检测器上创建多个单独图像的方法。类似地,已经提出了利用频率多路复用方法的流式细胞术成像方法,其中波长滤波的光被收集在单独的PMT上并且稍后被处理以创建图像。
从同一图像收集若干条信息(例如,散射和荧光)可能是有利的,从而降低系统的复杂性、成本和所需的存储空间。在一种方法中,可以在同一图像内同时收集包含不同信息的若干信号以创建合成图像。例如,有许多染料在空间上在细胞的特定区域(例如,核染色)中染色,所述染料可以用于创建图像对比度。通过使用适当的滤波器,可以在不同的细胞结构之间创建对比度。
图9提供了示例性系统900。如图所示,颗粒可以从第一位置920a(经受第一照明源940和第一检测器970)传送到第二位置920b(经受第二照明源942和第二检测器972)、传送到第三位置920c(其中颗粒可以经受第三照明源944和图像检测器960(例如,如图9中所描述的相机))。一个或多个滤波器950(例如,激光衰减、带通)可以被安置成调整由图像检测器960接收的光。
作为一个实例,用户可以用适当的染料对核进行染色并收集明场或暗场图像。使用适当的滤波器,可以为细胞核提供另外的对比度。在这种情况下,滤波器可以包含用于减少散射信号的激光衰减滤波器和用于将核染色与其它荧光信号隔离的带通滤波器。为了进一步增加对比度,可以用不平行于成像轴线的照明光束照亮目标,从而还减少来自照明源的光到达图像传感器的量。
如细胞的大小、形态和粒度等测量结果还可以由合成图像以及细胞内的核大小和位置来确定。随着极亮染料(例如,可以附接到特异性抗体的聚合物染料)的出现,基于抗体的染料缀合物还可以用于在图像内创建对比度。
在上述实例和所公开技术的各个实施例中,存在各种可以在合成图像内创建特定对比度的染料和染色剂。可以包含染色剂以照亮隔室、结构和细胞边界。在这些情况下,使用适当的滤波器,可以包含单个图像内的若干种染色剂。另外,增强的对比度可以通过使用吸附染料来隔离和增强特定空间实体的对比度来创建。
在类似方法中,可以使用彩色染料收集复合信息。例如,台盼蓝(Trypan Blue)可以用作活/死染色剂。通过使用如以上所讨论的彩色相机或适当的一组滤波器,蓝色染色剂可以叠加在明场或暗场图像的顶部上。
使用如激光等单色光源还基于在用于激发的一个或多个波长处吸收特定染料而创建染料的吸收对比度。多于一个激发源的吸光度信息可以用滤波器解析,或可替代地用激发源的空间或时间分离来解析。还应该注意的是,许多荧光染料具有可以通过吸光度增加空间对比度的强消光系数。进一步地,已经开发了使用靶向化学部分(例如,点击化学)的技术,所述技术允许对所期望结构进行特定设计的颜色染色,所述所期望的结构被制成结合这些化学反应位点。
用于标记细胞内的结构和体积的无数染料和染色剂很多,并且存在许多可以用于从合成图像或彩色图像获得有用的信息的组合。图像可以包含明场、暗场、荧光或彩色图像、或前述的任何组合。
像散矫正
流式细胞术中的典型成像方法使用透镜来准直从物体接收的光。然后,该准直光在成像到检测器上之前穿过一系列二向色和带通滤波器。有利的是,直接对物体进行成像而不需要准直横穿光分散/调节滤波器元件的光。这是有问题的,因为通过倾斜的二向色镜传递聚焦或会聚光由于倾斜的几何形状而在传播路径中引入不对称性。这导致如像散等像差。
图10提供了系统1000,所述系统被配置成使用具有二向色涂层的固体元件而不是使用倾斜的二向色镜在两个方向上分光。如针对系统1000的图中所示,位置1020处的颗粒经受照明源1030。成像光学器件1070和不在传播路径中引入不对称性的二向色镜1040(例如,如图10中所描述的立方体等固体元件内的二向色涂层)被配置成处理然后由图像检测器1050和图像检测器1060收集的光。对于二向色镜1040的其它固体元件配置也是可能的,如引入很少或没有像差的立方体配置。此外,如图10所描述的,成像光学器件1070包含会聚元件(例如,会聚透镜)。在此类配置中,会聚波形在传播路径中不经历空间不对称。以这种方式,在两个传播方向上产生几乎无像差的图像。另外,使用此类布置,有可能创建几何形状,在所述几何形状中,多于两个图像检测器可以用在单独的位置处并且仍然促进在不产生像差的不同波长下创建质量图像。
以类似的方式,可以使用固体二向色元件和/或透明元件来改变会聚光束的焦距。通过将具有不同光传播速度的材料插入到光路中,焦距可以沿着所述路径改变。
图11提供了系统1100,所述系统被配置成改变与系统内的一个图像检测器相关联的焦距,同时采用单个聚焦透镜以创建会聚波形。如图11所示,系统1100可以包含二向色镜1140(例如,如所展示的二向色立方体),所述二向色镜与成像光学器件1120和图像检测器1150光学连接。如先前关于图10所讨论的,二向色镜1140被描绘为立方体,但可以具有如立方体配置等其它配置。另外的图像检测器1170与二向色镜1140光学连接,插入物1160(例如,石英板插入物)存在于二向色镜1140与图像检测器1170之间以增加焦距。不受任何特定理论的束缚,通过将如石英等固体材料插入物插入到传播路径中,光束的焦点长度将增加灵活性,以允许其中可能无法与图像检测器相等的光路长度的配置。
扩展景深
景深是成像流式细胞术中较难解决的效应之一。由于需要较大的放大倍数,所以景深通常相当小。较小的景深值要求以较高精确度将颗粒放置在物面中。这在流动系统中是一个挑战,因为之后必须以微米范围内的公差使颗粒对齐,以确保来自流过传感器的所有颗粒的图像均处于焦点上。
解决此问题的一种方法是产生具有多个物面的系统。可以通过在图像捕获期间移动图像平面来完成这一点。通过横越物面,图像将在扫描期间的某个点处于焦点上。可以通过快速改变成像系统的特性来实现物面的移动。可以通过移动光具组内的元件或通过快速操纵光学元件之一以有效地改变物面的位置从而实现这一点。图12示出了通过多个图像平面进行成像的实例。
如图12所示,在操作期间,系统1200可以包含进入流动通道1210的颗粒1202、1204和1206。还示出了不同的物面(例如,第一物面1212和第二物面1214)。成像光具组1220可以操作以便在多个物面处扫描和收集图像,然后由图像检测器1240收集所述图像。可以通过机械装置移动图像平面,如快速移动成像光学器件,或通过使用可以快速改变系统的焦距的光学部件(例如,变焦透镜)。可替代地,可以使用透镜阵列同时收集多个平面。此外,虽然图12描绘了第一物面1212和第二物面1214,但是替代性实施例可以基于特定系统的配置、期望的性能能力和与系统1200的其它方面的相容性(例如,成像光具组1220的能力)而具有多于两个物面(例如,3个、4个、5个等)。系统1200可以另外包含根据本文所公开的其它实施例的未明确描述的其它方面,如一个或多个照明源。
还可以在常规流式细胞术光学器件中使用此相同方法以扩展景深,由此增加颗粒定位公差并允许使用景深通常较浅的、放大倍数较高的、数值孔径(NA)较高的物镜。
照明的扩展景深
类似地,可以通过快速扫描源的焦腰(focal waist)来扩展照明光的焦点。此技术可以产生更均匀的照明并且潜在地改变束相干性,从而减少如散斑等不期望的效果。此技术对于成像是有用的,并且其还可以应用于常规流式细胞术,在所述常规流式细胞术中,期望均匀的照明以获得更高精度的定量荧光和散射数据。图13中展示了此类技术的实例。
如图13所示,在操作期间,系统1300可以包含在不同物面(例如,第一焦面1312和第二焦面1314)处进入流动通道1310的颗粒1302、1304和1306。照明光具组1320可以操作以便在多个焦面处扫描和收集数据,其中照明由照明源1340供应。可以通过机械装置移动焦面,如快速移动成像光学器件,或通过使用可以快速改变系统的焦距的光学部件(例如,变焦透镜)。此外,虽然图13描绘了第一焦面1312和第二焦面1314,但是替代性实施例可以基于特定系统的配置、期望的性能能力和与系统1300的其它方面的相容性(例如,照明光具组1320的能力)而具有多于两个焦面(例如,3个、4个、5个等)。系统1300可以另外包含根据本文公开的其它实施例的未明确描绘的其它方面,如一个或多个检测器(包含一个或多个图像检测器)。
还可以在常规流式细胞术光学器件中使用此相同方法以扩展景深,由此增加颗粒定位公差并允许使用景深通常较浅的、放大倍数较高的、NA较高的物镜。
非法向照明
在大多数成像系统中,照明光平行于系统的光轴。存在需要较大对比度的应用,尤其是在图像相对于周围介质提供的对比度不高的情况下。在这种情况下,显微镜可以使用结构化照明,如用光锥照亮样品以消除平行于成像轴线的光。可以通过使用轴对称的光锥进行照明来实现这一点。
如图14所示,在操作期间,系统1400可以包含颗粒1430。系统1400包括被配置成照亮颗粒1430的照明源1410,以及被配置成收集由颗粒1430的照明产生的信号的图像检测器1420。通过用不与成像系统的光轴平行并且不关于所述轴线对称的光(倾斜入射)照亮颗粒1430,可以在图像内产生阴影区域并且因此增加图像中的细胞/颗粒特征的对比度。
通过限制与如细胞结构等图像中特征相邻的区域中的照明量,阴影区域可以产生更高的对比度。另外,轴外照明还会减少到达图像检测器的照明光的量,从而进一步增加图像对比度。可以通过所述两条轴线之间的偏移角度来控制阴影的深度。
图14显示了照明轴线1440与成像轴线1450偏移角度α的配置。另外,可以操纵照明,使得存在于流动池中的反射照明被引导远离也有可能存在的其它探询区,如被设计成收集常规流式细胞术数据的那些探询区。
如以上所讨论的,图10-14示出了根据本公开的各种光学元件部分配置。应该理解的是,图10-14所示的部件配置中的任何部件配置可以与图1-9中所示的流动系统配置中的任何流动系统配置一起使用。
示例性图像
以下结果仅是说明性的,并且不应理解为限制本说明书的范围。
如本文其它地方所解释的,通常使用相对较高的颗粒速度来收集常规流动数据。此类方法的一个特征是颗粒在探询区中花费的时间越少,两个颗粒被同时探询并且因此产生错误的结果的概率就越低。然而,为了对颗粒进行成像,较低的速度有利于使颗粒的运动最小化。图15和图16展示了这一点。
图15提供了对以4米/秒行进的红血球拍摄的图像,其中曝光时间为1微秒。如图所示,图像相对模糊,并且难以识别细胞边界。
通过比较,图16提供了用与图15的设置相同的设置拍摄的红细胞图像,但是细胞的行进速度比图15所示的细胞速度慢四倍(即,1米/秒)。如图16所示,与图15的细胞相比,运动模糊减少并且细胞的外部边界更容易辨别。
图17和图18提供了以1米/秒和8米/秒(分别地)的速度行进的珠粒的图像。如图所示,以1米/秒行进的珠粒的图像是处于焦点中并且易于识别。相比之下,以8米/秒行进的珠粒是模糊的。此测试的基本参数是(i)珠粒直径:15微米;(ii)速度:1米/秒或8米/秒;(iii)快门时间:1微秒;(iv)透镜放大倍数:50x;(v)配置:明场;(vi)照明:LED;(viii)流动在图像中为从左到右。
在图17和图18中,在约1米/秒的速度下,珠粒在快门循环期间移动约1微米。在8米/秒下,珠粒将在快门期间移动约8微米。因为珠粒的直径为约15微米,所以在快门循环期间珠粒的移动距离将略微超过其直径的一半。根据本公开的系统可以被配置成使得颗粒在快门循环期间的移动距离小于其直径的4倍、或在快门循环期间的移动距离小于其直径的2倍、在快门循环期间的移动距离小于其直径的约1倍、或甚至在快门循环期间的移动距离小于其直径约0.75倍。
示例性方面
以下方面仅是说明性的,并且不应理解为限制本说明书或所附权利要求的范围。
方面1.一种系统,其包括:
流动通道,所述流动通道具有入口,并且所述流动通道限定了流体通过其连通的流动路径;
第一光具组,所述第一光具组包括第一照明源和第一检测模块,所述第一检测模块被安置成接收与由所述第一照明源照亮的所述流动通道的第一区域相关的信号,所述第一区域定位在距所述流动通道的所述入口的第一距离处;
第二光具组,所述第二光具组包括第二照明源和第二检测模块,所述第二检测模块被安置成接收与由所述第二照明源照亮的所述流动通道的第二区域相关的信号,所述第二区域定位在距所述流动通道的所述入口的第二距离处,所述第二距离大于所述第一距离,并且
(a)其中所述流动通道的所述第一区域限定第一横截面面积,其中所述流动通道的所述第二区域限定第二横截面面积,并且其中所述第一横截面面积和所述第二横截面面积在面积上、形状上或在面积和形状两者上彼此不同,或
(b)其中(i)所述系统包括进入所述流动通道的所述入口与所述流动通道的所述第一区域之间的所述流动通道的导管,(ii)所述系统包括进入所述流动通道的所述第一区域与所述第二区域之间的所述流动通道的导管,或(i)和(ii)两者,或
(c)其中所述系统包括流速调节器,所述流速调节器被配置成调节所述流动路径中的速度,或
(d)所述系统进一步包括场模块,
所述场模块被配置成增加或减少所述流动通道的区域处的场,以便使所述流动通道中的流动中的至少一些颗粒移动并且对从所述流动通道中的所述流动内的颗粒速度的速度流线S0到所述流动通道中的所述流动内的颗粒速度的速度流线S1的场敏感,其中在所述流动通道的所述第一区域与所述第二区域之间,系统操作期间S0处的所述颗粒速度不同于S1处的所述颗粒速度,或
(a)、(b)、(c)或(d)的任何组合。
流动通道可以具有圆形横截面,但其横截面也可以是椭圆形、多边形或不规则的。矩形或方形横截面被认为是特别适合的,但不是必需的。通道的横截面尺寸(例如,直径)可以处于约50微米到约10,000微米的范围内。
适合的第一照明和检测模块在本文其它地方描述。
所述系统的所述第一区域可以是所述流动通道的区域,所述区域安置在所述第一照明源与所述第一检测模块之间,例如,所述流动通道的一部分,可能由所述第一照明源照亮的颗粒处于所述流动通道的一部分内,并且所述照明(或与其相关的信号,如荧光)可以由所述第一检测模块检测。
类似地,所述系统的所述第二区域可以是所述流动通道的区域,所述区域安置在所述第二照明源与所述第二检测模块之间,例如,所述流动通道的一部分,可能由所述第二照明源照亮的颗粒处于所述流动通道的一部分内,并且所述照明(或与其相关的信号,如荧光)可以由所述第二检测模块检测。
如从所述流动通道的所述入口沿所述流动通道测量的,所述第一区域和所述第二区域适当地安置在不同的距离处。所述第一区域与所述第二区域之间的间隔可以为例如约100微米到约10mm,即使这不是必需的。
在一些实施例中,所述第二区域可以被描述为相对于所述第一区域的下游。在一些实施例中,所述第一区域可以被描述为相对于所述第二区域的下游。如本文其它地方所描述的,流动通道可以从主干部分分支成两个或更多个流动分支。可替代地,流动通道可以从两个或更多个分支会聚到主干部分。主干部分中的流速可以与分支部分中的流速不同。
方面2.根据方面1所述的系统,其中所述第一横截面面积和所述第二横截面面积彼此不同,并且所述第一横截面面积与第二横截面面积的比率为约100:1到约1:100,不包括1:1。作为一些非限制性实例,所述第一横截面面积与所述第二横截面面积的比率可以为约100:1到约1:100、或约98:1到约1:98、或约90:1到约1:90、或约80:1到约1:80、或约70:1到约1:70、或约60:1到约1:60、或约50:1到约1:50、或约40:1到约1:40、或约30:1到约1:30、或约20:1到约1:20、或约10:1到约1:10、或约8:1到约1:8、或约6:1到约1:6、或约5:1到约1:5、或约4:1到约1:4、或约3:1到约1:3、或约2:1到约1:2、或约1.8:1到约1:1.8、或约1.5:1到约1:1.5、或约1.3:1到约1:1.3、或约1.1:1到约1:1.1。
以这种方式,所述系统在操作期间在所述第一区域和所述第二区域处实现不同的颗粒速度。在一个实施例中,颗粒可以以速度v1通过所述第一区域,并且然后以速度v2通过所述第二区域,其中v2<v1,由于所述流动通道在所述第一区域处的横截面面积大于所述流动通道在所述第二区域处的横截面面积。较大的速度可以为例如较低速度的1.0001倍到约1000倍、或较低速度的1.001倍到约100倍、或较低速度的1.01倍到约10倍、或较低速度的1.01到约5倍。
方面3.根据方面1到2中任一方面所述的系统,其中所述流动通道限定了主轴线。这可以例如在圆柱形流动通道中,其中所述主轴线是所述圆柱形通道的中心轴线。
方面4.根据方面3所述的系统,其中所述第一照明源和所述第二照明源中的至少一个被配置成提供基本上平行于所述流动通道的所述主轴线的照明。在一些实施例中,所述第一照明源和所述第二照明源中的至少一个被配置成提供基本上垂直于所述流动通道的所述主轴线的照明。当然,所述照明可以成一定角度,所述角度处于平行于所述流动通道的所述主轴线与垂直于所述流动通道的所述主轴线之间。仅举几例,所述照明可以相对于所述流道通道的所述主轴线成约1度到约89度、或相对于所述流动通道的所述主轴线成约3度到约86度、或相对于所述流动通道的所述主轴线成约7度到约81度、或相对于所述流动通道的所述主轴线成约11度到约77度、或相对于所述流动通道的所述主轴线成约17度到约70度、或相对于所述流动通道的所述主轴线成约23度到约65度、或相对于所述流动通道的所述主轴线成约30度到约58度、或相对于所述流动通道的所述主轴线成约37度到约50度、或相对于所述流动通道的所述主轴线成约40度到约44度。
方面5.根据方面1到4中任一方面所述的系统,其中所述流动路径至少部分是非线性的。此类流动路径可以是例如弯曲的、扭结的,或甚至包括拐角。(图5中示出了一个此类实施例,所述图提供了具有非线性、扭结的流动路径的流动通道520。)流动路径可以包含小于90度、小于80度、小于70度、小于60度、小于50度、小于40度、小于30度、小于20度、或甚至小于10度的弯曲或扭结。
流动路径可以从单个通道分叉成多个通道,并且还可以从多个通道会聚成更少的通道或甚至会聚成单个通道。
方面6.根据方面1到5中任一方面所述的系统,其进一步包括与所述流动通道流体连通的颗粒分离器。
方面7.根据方面6所述的系统,其中所述分离器被配置成基于颗粒大小、颗粒形状、颗粒质量、与一个或多个颗粒相关联的信号或其任何组合来使颗粒转向。适合的此类分离器是本领域普通技术人员已知的那些分离器。一些示例性分离器包含例如单细胞分选、荧光活化细胞分选、磁性细胞分选、浮力活化细胞分选等。
方面8.根据方面7所述的系统,其中所述分离器被配置成基于与一个或多个颗粒相关联的信号使所述流动通道内的颗粒转向。作为一个实例,分离器可以被配置成使在特定波长或特定波长范围处展现出至少一定强度的荧光的颗粒转向。
方面9.根据方面6到8中任一方面所述的系统,其中所述系统被配置成收集经过分离的颗粒的一个或多个图像。例如,系统可以具有装置(例如,相机、CCD),所述装置被配置成对转向到替代性流动通道或流动流的颗粒进行成像。
方面10.根据方面1到9中任一方面所述的系统,其中所述第一检测模块或所述第二检测模块中的至少一个包括多个检测器。
方面11.根据方面1到10中任一方面所述的系统,其进一步包括与至少一个检测模块光连通的光反射器、分光器或两者。
图11提供了示例性的此类系统。如图11所示,示例性系统可以包含与图像检测器1150和图像检测器1170光连通的二向色镜1140(具有反射特性和分离特性)。
方面12.根据方面1到11中任一方面所述的系统,其中所述第一光具组或所述第二光具组中的一个或两个被配置成在所述流动通道内的两个或更多个平面处实现成像。
方面13.根据方面12所述的系统,其中所述第一光具组或所述第二光具组中的一个或两个被配置成在两个或更多个焦面处收集图像。
方面14.根据方面12到13中任一方面所述的系统,其中所述第一光具组或所述第二光具组中的一个或两个被配置成在两个或更多个平面处聚焦照明。
方面15.根据方面1到12中任一方面所述的系统,其中所述第一光具组被配置成使得来自所述第一照明源的照明轴线偏离所述第一检测模块一定角度,其中所述第二光具组被配置成使得来自所述第二照明源的照明轴线偏离所述第二检测模块一定角度,或两者。偏移角度可以为例如约1度到约90度,例如,约1度、5度、10度、15度、20度、25度、30度、35度、40度、45度、50度、55度、60度、65度、70度、75度、80度、85度或甚至约90度。
方面16.根据方面1到15中任一方面所述的系统,其中所述第一照明源、所述第二照明源或两者包括激光器、灯、发光二极管(LED)等。
方面17.根据方面1到16中任一方面所述的系统,其中所述第一检测模块、所述第二检测模块或两者包括光电倍增管(PMT)、雪崩光电二极管(APD)、相机、硅光电倍增管(SiPM)等。
方面18.根据方面1到17中任一方面所述的系统,其中所述系统被配置成使得(a)所述第二光具组的操作、(b)所述分离器的操作,如果存在的话或(a)和(b)两者与由所述第一光具组收集的信号有关。
方面19.根据方面1到18中任一方面所述的系统,其中所述场模块包括磁场源、电场源、声场源或其任何组合。
方面20.一种方法,其包括:
使颗粒群流动通过流动通道;
使用第一光具组,在所述流动通道的第一区域处照亮所述颗粒群中的至少一些并收集与所述照明有关的第一信号或其缺乏;
使用第二光具组,在所述流动通道的第二区域处照亮所述颗粒群中的至少一些并收集与所述照明有关的第二信号或其缺乏;
所述流动通道的所述第一区域处的颗粒速度与所述流动通道的所述第二区域处的颗粒速度不同,并且
所述第一信号与所述第二信号不同。
在一些实施例中,所述第一信号和所述第二信号的强度、波长或两者不同。作为一个实例,一个信号可以是与染料的激发有关的荧光信号,并且另一个信号可以是在可见光下聚集的呼叫的视觉图像。作为另一个实例,一个信号可以是与第一染料的激发有关的荧光信号,并且另一个信号可以是与第二种不同染料的激发有关的荧光信号。
在又另一个实例中,第一检测器可以收集与第一染料的荧光有关的信号,所述第一染料定位在受第一照明器照亮的区域中。第二检测器可以检测与第二染料的荧光有关的光子的不存在,所述第二染料定位在受第二照明器照亮的区域中,所述光子的不存在可以被认为是信号。
方面21.根据方面20所述的方法,其中所述流动通道的所述第一区域的横截面面积与所述流动通道的所述第二区域的横截面面积在面积、形状或两者上不同。
方面22.根据方面20到21中任一方面所述的方法,其进一步包括在所述流动通道的所述第一区域与所述第二区域之间的位置处引入流体或从所述流动通道中移除流体。
可以引入流体,使得所述第二区域处的流体的体积流动速率与所述第一区域处的体积流动速率的比率为例如1.0001:1到约5:1、10:1、20:1或甚至约40:1。可以抽出流体,使得所述第二区域处的流体的体积流动速率与所述第一区域处的体积流动速率的比率为例如1:1.0001到约1:5、1:10、1:20或甚至约1:40。
所述第一区域和所述第二区域处的颗粒的探询时间可以变化,并且可以为约0.1微秒到例如一毫秒或甚至数十毫秒。作为一个实例,用于从颗粒收集荧光信号的激光探询可以具有处于一微秒到数十微秒范围内的探询时间。用于收集颗粒的标准图像的可见光探询可以具有处于一毫秒到几十毫秒范围内的探询时间。所述第一区域中的颗粒探询时间与所述第二区域中的颗粒探询时间的比率可以处于例如约1:100,000到约100,000:1(例如,10,000:1到1:10,000)以及所有中间值的范围内。
方面23.根据方面20到22中任一方面所述的方法,其中所述流动通道限定了主轴线。
方面24.根据方面23所述的方法,其中在所述流动通道的所述第一区域处照亮所述颗粒群中的至少一些,其中在所述流动通道的所述第二区域处照亮所述颗粒群中的至少一些或两者是通过基本上平行于所述主轴线的照明来实现的。
方面25.根据方面20到24中任一方面所述的方法,其中所述流动通道限定了至少部分非线性的流动路径。
方面26.根据方面20到25中任一方面所述的方法,其进一步包括基于所述第一信号、所述第二信号或两者分离所述颗粒群中的至少一些。
方面27.根据方面20到26中任一方面所述的方面,其进一步包括收集一个或多个经过分离的颗粒的图像。应该理解的是,这可以包括收集满足分离标准或不满足分离标准的颗粒的一个或多个图像。
方面28.根据方面20到27中任一方面所述的方法,其进一步包括用照明反射器、照明分离器或两者引导来自所述第一光具组的照明。
方面29.根据方面20到28中任一方面所述的方法,其进一步包括用照明反射器、照明分离器或两者引导来自所述第二光具组的照明。
方面30.根据方面20到29中任一方面所述的方法,其进一步包括操作所述第一光具组、所述第二光具组或两者以便在所述流动通道内的两个或更多个平面处收集信号。
方面31.根据方面20到30中任一方面所述的方法,其进一步包括操作所述第一光具组、所述第二光具组或两者以便在所述流动通道内的两个或更多个平面处聚焦照明。
方面32.根据方面20到31中任一方面所述的方法,其中来自所述第一光具组的照明源的照明轴线偏离所述第一光具组的检测模块一定角度,其中来自所述第二光具组的照明源的照明偏离来自第二光具组的检测模块一定角度,或两者。
方面33.根据方面20到32中任一方面所述的方法,其中所述第一信号、所述第二信号或两者是荧光信号、荧光图像、发光图像、相衬图像、全息图像、明场图像、暗场图像、散射信号或其任何组合。
方面34.根据方面20到33中任一方面所述的方法,其中所述第二光具组的操作与由所述第一光具组收集的所述第一信号有关。作为一个实例,除非某个阈值信号(例如,一定水平的荧光)由所述第一光具组收集,否则所述第二光具组可能不操作以进行照明或检测。以这种方式,所述第二光具组可以操作以仅聚集关于已经满足由所述第一光具组聚集的一个或多个标准的细胞或其它颗粒的信息。
方面35.根据方面20到34中任一方面所述的方法,其进一步包括使所述第一信号、所述第二信号或两者与所述颗粒群中的至少一个的一个或多个特性相关。作为一个实例,可以使特定染料的存在与细胞的活/死状态相关,如本文其它地方所描述的。还可以例如使信号(例如,荧光)的强度与细胞中标记物或其它染料的水平相关。
方面36.根据方面20到35中任一方面所述的方法,其中所述颗粒群以第一流体流速在第一区域处流动并且以第二流体流速在所述第二区域处流动,并且其中所述第一流体流速与所述第二流体流速的比率为约40:1到约1:40,不包括1:1。
示例性颗粒速度(在第一区域或第二区域中)的范围可以为例如厘米/秒到数十米/秒,例如,约0.1米/秒到约10米/秒、约0.5到约5米/秒、约1到约2.5米/秒或甚至以约1.5米/秒。
同样不受任何特定理论的束缚,所公开的系统可以以例如约10μl/min(微升/分钟)到约1000微升每分钟的体积流动速率操作。约10到约1000μl/min、或约50到约700μl/min、或约100到约500μl/min、或约200到约400μl/min的流速都被认为是适合的。
根据本公开的系统可以以例如约10到约100,000个细胞/秒的速率操作。约10到约100,000个细胞/秒、或约50到约50,000个细胞/秒、或约100到约10,000个细胞/秒、或甚至约500到约5,000个细胞/秒的速率都被认为是适合的。
还应该理解的是,根据本公开的系统可以以约10到约100,000事件/秒的速率操作。约10到约100,000事件/秒、或约50到约50,000事件/秒、或约100到约10,000事件/秒、或甚至约500到约5,000事件/秒的速率都被认为是适合的。通过应用分选和/或门控,系统可以被配置成排除样品中的某些细胞/颗粒并仅分析未排除的细胞/颗粒,以便仅在样品的亚群上利用系统资源。但是,作为一个实例,如果系统能够以50,000个事件每秒操作,则系统将需要10秒来分析500,000个细胞的群。但是,如果系统被配置成排除样品中50%的细胞,则系统可以在5秒内分析250.000个所关注的细胞。
方面37.一种方法,其包括:
在从流动通道的第一区域朝向所述流动通道的第二区域的方向上使颗粒群传送通过所述流动通道;
使用第一光具组,在所述流动通道的所述第一区域处照亮所述颗粒群中的至少一些并收集与所述照明有关的第一信号;
使用第二光具组,在所述流动通道的所述第二区域处照亮所述颗粒群中的至少一些并收集与所述照明有关的第二信号;
增加或减少所述流动通道的所述第一区域与第二区域之间的颗粒子集上的场,
增加或减少所述场,以便将所述颗粒子集从所述流动通道内的颗粒速度的速度流线S0移动到所述流动通道内的颗粒速度的速度流线S1,其中S0处的所述颗粒速度不同于S1处的所述颗粒速度。
不受任何特定理论的束缚,可以执行该操作以便将颗粒(所述颗粒经受场)从流动通道中心处的第一速度流线移动到流动通道壁处的第二速度流线,其中与所述流动通道中心处的流量相比,流动-根据标准泊肃叶定律流动(Poiseuille law flow)-在壁处相对较慢。以这种方式,当颗粒更靠近流动通道壁移动时,颗粒可以以比颗粒传送到第一区域时所具有的速度更低的速度传送到第二区域。
方面38.根据方面37所述的方法,其中所述场包括磁场、电场、声场、重力场、介电场或其任何组合。
方面39.根据方面37到38中任一方面所述的方法,其进一步包括将所述颗粒子集耦合到对所述场敏感的实体。实例实体包含例如磁性颗粒、具有不同介电性质的颗粒、具有不同密度的颗粒以及具有不同可压缩性的颗粒。
方面40.根据方面39所述的方法,其中所述实体包括磁性颗粒。
方面41.根据方面39所述的方法,其中所述实体包括介电颗粒。
方面42.一种方法,其包括使颗粒群流动通过根据方面1到19中任一方面所述的系统。
方面43.一种方法,其包括操作根据方面1到19中任一方面所述的系统。
Claims (18)
1.一种系统,其包括:
流动通道,
所述流动通道具有入口,并且
所述流动通道限定了通过其连通的流体的流动路径;
第一光具组,所述第一光具组包括第一照明源和第一检测模块,
所述第一检测模块被安置成接收与由所述第一照明源照亮的所述流动通道的第一区域相关的信号,所述第一区域位于距所述流动通道的所述入口的第一距离处;
第二光具组,所述第二光具组包括第二照明源和第二检测模块,
所述第二检测模块被安置成接收与由所述第二照明源照亮的(i)所述流动通道的第二区域或者(ii)第二流动通道的区域相关的信号,
所述流动通道的第二区域或者所述第二流动通道的区域位于距所述流动通道的所述入口的第二距离处;
所述第二距离大于所述第一距离,并且
(a)其中所述流动通道的所述第一区域限定第一横截面面积,其中所述流动通道的所述第二区域限定第二横截面面积,并且其中所述第一横截面面积和所述第二横截面面积在面积上、形状上或在面积和形状两者上彼此不同,或
(b)其中(i)所述系统包括进入位于所述流动通道的所述入口和所述流动通道的所述第一区域之间的所述流动通道的导管,(ii)所述系统包括进入位于所述流动通道的所述第一区域和所述第二区域之间的所述流动通道的导管,或(i)和(ii)两者。
2.根据权利要求1所述的系统,其中所述第一横截面面积和所述第二横截面面积在面积上彼此不同,并且所述第一横截面面积与第二横截面面积的比率为约100:1到约1:100,但不包括1:1。
3.根据权利要求2所述的系统,其中所述第一横截面面积和所述第二横截面面积在面积上彼此不同,并且所述第一横截面面积与第二横截面面积的比率为约20:1到约1:20,但不包括1:1。
4.根据权利要求1所述的系统,其中所述流动通道限定了主轴线。
5.根据权利要求4所述的系统,其中所述第一照明源和所述第二照明源中的至少一个被配置成提供基本上平行于所述流动通道的所述主轴线的照明。
6.根据权利要求1所述的系统,其中所述流动路径至少部分是非线性的。
7.根据权利要求1所述的系统,其进一步包括颗粒分离器,所述颗粒分离器与所述流动通道流体连通。
8.根据权利要求7所述的系统,其中所述分离器被配置成基于颗粒大小、颗粒形状、颗粒质量、与一个或多个颗粒相关联的信号,或其任何组合来使颗粒转向。
9.根据权利要求8所述的系统,其中所述分离器被配置成基于与一个或多个颗粒相关联的所述信号使所述流动通道内的颗粒转向。
10.根据权利要求7所述的系统,其中所述系统被配置成收集分离的颗粒的一个或多个图像。
11.根据权利要求1所述的系统,其中所述第一检测模块或所述第二检测模块中的至少一个包括多个检测器。
12.根据权利要求1所述的系统,其进一步包括与至少一个检测模块光连通的光反射器、分光器或两者。
13.根据权利要求1所述的系统,其中所述第一光具组或所述第二光具组中的一个或两个被配置成在所述流动通道内的两个或更多个平面处实现成像。
14.根据权利要求13所述的系统,其中所述第一光具组或所述第二光具组中的一个或两个被配置成在两个或更多个焦面处收集图像。
15.根据权利要求13所述的系统,其中所述第一光具组或所述第二光具组中的至少一个被配置成在两个或更多个平面处聚焦照明。
16.根据权利要求1所述的系统,其中所述第一光具组被配置成使得来自所述第一照明源的照明轴线偏离所述第一检测模块一定角度,其中所述第二光具组被配置成使得来自所述第二照明源的照明轴线偏离所述第二检测模块一定角度,或两者。
17.根据权利要求1所述的系统,其中所述第一照明源、所述第二照明源或两者包括激光器、灯、发光二极管,或其任何组合。
18.根据权利要求7所述的系统,其中所述系统被配置成使得(a)所述第二光具组的操作、(b)所述颗粒分离器的操作,或(a)和(b)两者,与由所述第一光具组收集的信号有关。
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201762479734P | 2017-03-31 | 2017-03-31 | |
| US62/479,734 | 2017-03-31 | ||
| PCT/US2018/025538 WO2018183939A1 (en) | 2017-03-31 | 2018-03-30 | Apparatuses, systems and methods for imaging flow cytometry |
| CN201880028673.4A CN110573858B (zh) | 2017-03-31 | 2018-03-30 | 用于成像流式细胞术的设备、系统和方法 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201880028673.4A Division CN110573858B (zh) | 2017-03-31 | 2018-03-30 | 用于成像流式细胞术的设备、系统和方法 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN115931687A true CN115931687A (zh) | 2023-04-07 |
Family
ID=62017615
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202310087156.7A Pending CN115931687A (zh) | 2017-03-31 | 2018-03-30 | 用于成像流式细胞术的设备、系统和方法 |
| CN201880028673.4A Active CN110573858B (zh) | 2017-03-31 | 2018-03-30 | 用于成像流式细胞术的设备、系统和方法 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201880028673.4A Active CN110573858B (zh) | 2017-03-31 | 2018-03-30 | 用于成像流式细胞术的设备、系统和方法 |
Country Status (7)
| Country | Link |
|---|---|
| US (8) | US10386290B2 (zh) |
| EP (1) | EP3602003A1 (zh) |
| JP (2) | JP7187474B2 (zh) |
| KR (1) | KR102585276B1 (zh) |
| CN (2) | CN115931687A (zh) |
| SG (1) | SG11201908847TA (zh) |
| WO (1) | WO2018183939A1 (zh) |
Families Citing this family (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| HUE061715T2 (hu) * | 2015-12-23 | 2023-08-28 | Siemens Healthcare Gmbh | Áramlási cella részecskék elemzéséhez egy vizsgálni kívánt folyadékban, eljárás és alkalmazás |
| EP3821227B1 (en) * | 2018-07-10 | 2024-03-13 | Gerrit Jan Van Den Engh | System, apparatus and method for off-axis illumination in flow cytometry |
| CN109470672A (zh) * | 2018-12-06 | 2019-03-15 | 大连海事大学 | 多光强激发检测单个微藻细胞活性的装置与方法 |
| WO2020241226A1 (ja) * | 2019-05-30 | 2020-12-03 | ソニーセミコンダクタソリューションズ株式会社 | 光学測定装置及び光学測定システム |
| JP6745559B1 (ja) * | 2020-03-24 | 2020-08-26 | 株式会社Cybo | イメージングフローサイトメーター、ソート方法、及びキャリブレーション方法 |
| KR102559634B1 (ko) * | 2020-08-26 | 2023-07-26 | 한국전자통신연구원 | 다파장 광원에 기반한 pcr 진단을 위한 장치 및 방법 |
| JPWO2022107557A1 (zh) * | 2020-11-18 | 2022-05-27 | ||
| WO2022132667A1 (en) * | 2020-12-14 | 2022-06-23 | Life Technologies Corporation | Systems and methods for improved imaging and fluorescence in flow cytometry and other applications |
| US11639895B2 (en) | 2021-03-09 | 2023-05-02 | Globalfoundries U.S. Inc. | Device including optofluidic sensor with integrated photodiode |
| CN117581087A (zh) * | 2021-07-01 | 2024-02-20 | 索尼集团公司 | 生物样品分析系统、信息处理装置、信息处理方法以及生物样品分析方法 |
| US20230366802A1 (en) * | 2022-05-13 | 2023-11-16 | Bio-Rad Laboratories, Inc. | Method and system for detection of particles focused asymmetrically |
Family Cites Families (131)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS499288B1 (zh) * | 1968-12-19 | 1974-03-04 | ||
| US4171159A (en) | 1977-07-14 | 1979-10-16 | White Matthew B | Optical homodyne microscope |
| US4195221A (en) | 1978-07-03 | 1980-03-25 | The United States Of America As Represented By The Secretary Of The Navy | Scanning focused local oscillator optical heterodyne imaging system |
| US4193088A (en) | 1978-08-02 | 1980-03-11 | The United States Of America As Represented By The Secretary Of The Navy | Optical heterodyne system for imaging in a dynamic diffusive medium |
| FR2477184A1 (fr) * | 1980-02-28 | 1981-09-04 | Onera (Off Nat Aerospatiale) | Procede pour augmenter la duree de vie d'une piece en materiau refractaire a fibres paralleles de darbure metallique noyees dans une matrice metallique |
| JPS59184841A (ja) * | 1983-04-05 | 1984-10-20 | ベクトン・デイツキンソン・アンド・カンパニ− | サンプル中の白血球のサブクラスを識別する方法および装置 |
| US4786165A (en) | 1986-07-10 | 1988-11-22 | Toa Medical Electronics Co., Ltd. | Flow cytometry and apparatus therefor |
| JP3084296B2 (ja) | 1991-02-27 | 2000-09-04 | シスメックス株式会社 | フローイメージサイトメータ |
| JPH0734012B2 (ja) | 1991-02-27 | 1995-04-12 | 東亜医用電子株式会社 | フローイメージサイトメータ |
| JP3084295B2 (ja) | 1991-02-27 | 2000-09-04 | シスメックス株式会社 | フローイメージサイトメータ |
| US5412466A (en) | 1991-07-26 | 1995-05-02 | Toa Medical Electronics Co., Ltd. | Apparatus for forming flattened sample flow for analyzing particles |
| JP3212647B2 (ja) | 1991-10-24 | 2001-09-25 | シスメックス株式会社 | イメージングフローサイトメータ |
| JP3102935B2 (ja) | 1991-11-20 | 2000-10-23 | シスメックス株式会社 | イメージングフローサイトメータ |
| JP3102938B2 (ja) | 1991-12-30 | 2000-10-23 | シスメックス株式会社 | 粒子画像分析装置 |
| JP3187129B2 (ja) | 1992-04-01 | 2001-07-11 | シスメックス株式会社 | 粒子分析装置 |
| JP3145487B2 (ja) | 1992-06-12 | 2001-03-12 | シスメックス株式会社 | 粒子分析装置 |
| JP3145486B2 (ja) | 1992-06-12 | 2001-03-12 | シスメックス株式会社 | イメージングフローサイトメータ |
| JP3215175B2 (ja) | 1992-08-10 | 2001-10-02 | シスメックス株式会社 | 粒子分析装置 |
| JPH06186156A (ja) | 1992-10-21 | 1994-07-08 | Toa Medical Electronics Co Ltd | 粒子分析装置 |
| JP3052665B2 (ja) * | 1993-01-26 | 2000-06-19 | 株式会社日立製作所 | フローセル装置 |
| US5418371A (en) | 1993-02-01 | 1995-05-23 | Aslund; Nils R. D. | Apparatus for quantitative imaging of multiple fluorophores using dual detectors |
| JPH07120375A (ja) | 1993-10-21 | 1995-05-12 | Hitachi Ltd | フロー式粒子画像解析方法及び装置 |
| JPH07270301A (ja) * | 1994-03-31 | 1995-10-20 | Hitachi Ltd | フロー式粒子画像解析方法およびその装置 |
| DE69533469T2 (de) | 1994-12-26 | 2005-09-22 | Sysmex Corp. | Durchflusszytometer |
| US5694216A (en) | 1996-04-25 | 1997-12-02 | University Of Central Florida | Scanning heterodyne acousto-optical interferometers |
| US5908599A (en) * | 1996-07-30 | 1999-06-01 | Bayer Corporation | Heated reaction chamber in a unified fluid circuit of a hematology diagnostic instrument |
| US5872627A (en) * | 1996-07-30 | 1999-02-16 | Bayer Corporation | Method and apparatus for detecting scattered light in an analytical instrument |
| US6831781B2 (en) | 1998-02-26 | 2004-12-14 | The General Hospital Corporation | Confocal microscopy with multi-spectral encoding and system and apparatus for spectroscopically encoded confocal microscopy |
| US6151127A (en) | 1998-05-28 | 2000-11-21 | The General Hospital Corporation | Confocal microscopy |
| JP3871456B2 (ja) | 1998-12-10 | 2007-01-24 | シスメックス株式会社 | 粒子画像分析装置 |
| US6256096B1 (en) | 1999-01-11 | 2001-07-03 | Softray | Flow cytometry apparatus and method |
| US20010006416A1 (en) | 1999-01-11 | 2001-07-05 | Johnson Paul E. | Ribbon flow cytometry apparatus and methods |
| US7057732B2 (en) | 1999-01-25 | 2006-06-06 | Amnis Corporation | Imaging platform for nanoparticle detection applied to SPR biomolecular interaction analysis |
| US8131053B2 (en) | 1999-01-25 | 2012-03-06 | Amnis Corporation | Detection of circulating tumor cells using imaging flow cytometry |
| US8005314B2 (en) | 2005-12-09 | 2011-08-23 | Amnis Corporation | Extended depth of field imaging for high speed object analysis |
| US7450229B2 (en) | 1999-01-25 | 2008-11-11 | Amnis Corporation | Methods for analyzing inter-cellular phenomena |
| US6249341B1 (en) | 1999-01-25 | 2001-06-19 | Amnis Corporation | Imaging and analyzing parameters of small moving objects such as cells |
| US6671044B2 (en) | 1999-01-25 | 2003-12-30 | Amnis Corporation | Imaging and analyzing parameters of small moving objects such as cells in broad flat flow |
| US6309886B1 (en) | 1999-06-04 | 2001-10-30 | The Regents Of The University Of California | High throughput analysis of samples in flowing liquid |
| US6813017B1 (en) | 1999-10-20 | 2004-11-02 | Becton, Dickinson And Company | Apparatus and method employing incoherent light emitting semiconductor devices as particle detection light sources in a flow cytometer |
| US6934408B2 (en) | 2000-08-25 | 2005-08-23 | Amnis Corporation | Method and apparatus for reading reporter labeled beads |
| US6608680B2 (en) | 2000-08-25 | 2003-08-19 | Amnis Corporation | TDI imaging system for kinetic studies |
| US6778263B2 (en) | 2000-08-25 | 2004-08-17 | Amnis Corporation | Methods of calibrating an imaging system using calibration beads |
| US6875973B2 (en) | 2000-08-25 | 2005-04-05 | Amnis Corporation | Auto focus for a flow imaging system |
| US6583865B2 (en) | 2000-08-25 | 2003-06-24 | Amnis Corporation | Alternative detector configuration and mode of operation of a time delay integration particle analyzer |
| US6532061B2 (en) | 2000-08-25 | 2003-03-11 | Amnis Corporation | Measuring the velocity of small moving objects such as cells |
| WO2002031467A1 (en) | 2000-10-12 | 2002-04-18 | Amnis Corporation | Multipass cavity for illumination and excitation of moving objects |
| WO2002031583A1 (en) | 2000-10-12 | 2002-04-18 | Amnis Corporation | System and method for high numeric aperture imaging systems |
| WO2002059254A2 (en) * | 2001-01-09 | 2002-08-01 | Ppg Industries Ohio, Inc. | Method and device for detecting and controlling the level of biological contaminants in a coating process |
| US6467350B1 (en) | 2001-03-15 | 2002-10-22 | The Regents Of The University Of California | Cylindrical acoustic levitator/concentrator |
| CA2445044C (en) | 2001-04-25 | 2011-02-15 | Amnis Corporation | Method and apparatus for correcting crosstalk and spatial resolution for multichannel imaging |
| WO2002103335A1 (en) | 2001-06-18 | 2002-12-27 | Amnis Corporation | Spectral deconvolution of fluorescent markers |
| WO2003009579A2 (en) | 2001-07-17 | 2003-01-30 | Amnis Corporation | Computational methods for the segmentation of images of objects from background in a flow imaging instrument |
| WO2003052389A1 (en) | 2001-12-18 | 2003-06-26 | University Of Wyoming | Apparatus and methods for high throughput analysis of particles in a translucent flowing liquid |
| EP1327865A1 (de) * | 2002-01-14 | 2003-07-16 | Abb Research Ltd. | Verfahren zur thermischen Durchflussmessung mit nicht konstanten Heizpulsen |
| US7161665B2 (en) | 2002-12-18 | 2007-01-09 | University Of Wyoming | High resolution imaging fountain flow cytometry |
| WO2004065544A2 (en) | 2003-01-15 | 2004-08-05 | Amnis Corporation | Cell suspension rotating fluidic pump |
| DE10304653B4 (de) * | 2003-02-05 | 2005-01-27 | Evotec Technologies Gmbh | Mehrparametrige Detektion in einem fluidischen Mikrosystem |
| DE10320956B4 (de) | 2003-02-05 | 2005-02-17 | Evotec Technologies Gmbh | Untersuchungsverfahren für biologische Zellen und zugehörige Untersuchungseinrichtung |
| DK2305172T3 (en) * | 2003-03-28 | 2016-08-22 | Inguran Llc | DEVICE AND PROCEDURES TO PROVIDE SEXUAL ANIMAL SEED |
| JP3816072B2 (ja) * | 2003-10-28 | 2006-08-30 | ローム株式会社 | 光導波路型センサおよびそれを用いた測定装置 |
| EP1800124B1 (en) | 2004-03-16 | 2011-12-21 | Amnis Corporation | Image based quantitation of molecular translocation |
| CA2596101A1 (en) | 2004-03-16 | 2005-09-29 | Amnis Corporation | Method for imaging and differential analysis of cells |
| US7340957B2 (en) | 2004-07-29 | 2008-03-11 | Los Alamos National Security, Llc | Ultrasonic analyte concentration and application in flow cytometry |
| US7074622B2 (en) | 2004-11-15 | 2006-07-11 | Eastman Kodak Company | Method and system for sorting and separating particles |
| DE102004055662A1 (de) | 2004-11-18 | 2006-06-01 | Evotec Technologies Gmbh | Mikrofluidisches System mit einer Kanalaufweitung |
| US7307721B2 (en) | 2005-04-13 | 2007-12-11 | Brightwell Technologies | Particle imaging system with a varying flow rate |
| JP2007148981A (ja) * | 2005-11-30 | 2007-06-14 | Univ Waseda | 微粒子分別マイクロシステムおよび微粒子分別方法 |
| US7464356B2 (en) * | 2005-12-15 | 2008-12-09 | International Business Machines Corporation | Method and apparatus for diffusion based cell placement migration |
| US7460248B2 (en) | 2006-05-15 | 2008-12-02 | Carestream Health, Inc. | Tissue imaging system |
| US7835000B2 (en) | 2006-11-03 | 2010-11-16 | Los Alamos National Security, Llc | System and method for measuring particles in a sample stream of a flow cytometer or the like |
| US7804594B2 (en) | 2006-12-29 | 2010-09-28 | Abbott Laboratories, Inc. | Method and apparatus for rapidly counting and identifying biological particles in a flow stream |
| KR100871097B1 (ko) | 2007-01-08 | 2008-11-28 | 김태근 | 결맞음 주파수영역 반사파 계측법에 기초한 광영상 시스템 |
| EP2479552B1 (en) | 2007-04-02 | 2015-09-02 | Acoustic Cytometry Systems, Inc. | Methods for enhanced analysis of acoustic field focused cells and particles |
| US7837040B2 (en) | 2007-04-09 | 2010-11-23 | Los Alamos National Security, Llc | Acoustic concentration of particles in fluid flow |
| US8083068B2 (en) | 2007-04-09 | 2011-12-27 | Los Alamos National Security, Llc | Apparatus for separating particles utilizing engineered acoustic contrast capture particles |
| US8702945B2 (en) | 2007-05-18 | 2014-04-22 | University Of Washington | Time-varying flows for microfluidic particle separation |
| JP5259154B2 (ja) | 2007-10-24 | 2013-08-07 | オリンパス株式会社 | 走査型レーザ顕微鏡 |
| US8263407B2 (en) | 2007-10-24 | 2012-09-11 | Los Alamos National Security, Llc | Method for non-contact particle manipulation and control of particle spacing along an axis |
| US8528406B2 (en) | 2007-10-24 | 2013-09-10 | Los Alamos National Security, LLP | Method for non-contact particle manipulation and control of particle spacing along an axis |
| US8266950B2 (en) | 2007-12-19 | 2012-09-18 | Los Alamos National Security, LLP | Particle analysis in an acoustic cytometer |
| JP4909288B2 (ja) * | 2008-01-10 | 2012-04-04 | 日本電信電話株式会社 | 浮遊粒子状物質測定装置 |
| US8714014B2 (en) | 2008-01-16 | 2014-05-06 | Life Technologies Corporation | System and method for acoustic focusing hardware and implementations |
| DE102008017119A1 (de) | 2008-04-02 | 2009-10-08 | Polytec Gmbh | Vibrometer und Verfahren zur optischen Vermessung eines Objekts |
| US7796256B2 (en) | 2008-05-05 | 2010-09-14 | Fluid Imaging Technologies, Inc. | Oil-immersion enhanced imaging flow cytometer |
| US9013692B2 (en) | 2008-06-12 | 2015-04-21 | East Carolina University | Flow cytometer apparatus for three dimensional difraction imaging and related methods |
| US8440952B2 (en) | 2008-11-18 | 2013-05-14 | The Regents Of The University Of California | Methods for optical amplified imaging using a two-dimensional spectral brush |
| WO2010108020A1 (en) * | 2009-03-20 | 2010-09-23 | Bio-Rad Laboratories, Inc. | Serial-line-scan-encoded multi-color fluorescence microscopy and imaging flow cytometry |
| DE102009017151A1 (de) * | 2009-04-15 | 2010-10-21 | Eisenmann Anlagenbau Gmbh & Co. Kg | Anlage zur Tauchbehandlung |
| US8610085B2 (en) | 2009-08-20 | 2013-12-17 | Bio-Rad Laboratories, Inc. | High-speed cellular cross sectional imaging |
| US8451524B2 (en) | 2009-09-29 | 2013-05-28 | Amnis Corporation | Modifying the output of a laser to achieve a flat top in the laser's Gaussian beam intensity profile |
| JP2011095181A (ja) | 2009-10-30 | 2011-05-12 | Sysmex Corp | 粒子分析装置 |
| US20110134426A1 (en) | 2009-12-04 | 2011-06-09 | Life Technologies Corporation | Apparatuses, systems, methods, and computer readable media for acoustic flow cytometry. |
| US9217635B2 (en) | 2010-01-07 | 2015-12-22 | Shilat Optronics Ltd. | Three dimensional measurement system |
| US9023294B2 (en) | 2010-02-24 | 2015-05-05 | Kanagawa Academy Of Science And Technology | Cell analyzer |
| US9068916B2 (en) | 2010-03-15 | 2015-06-30 | Bio-Rad Laboratories, Inc. | Microassembled imaging flow cytometer |
| DE102010013829A1 (de) | 2010-03-26 | 2011-09-29 | Carl Zeiss Microlmaging Gmbh | Mikroskop und Verfahren zur Erfassung von Probenlicht |
| US8817115B1 (en) | 2010-05-05 | 2014-08-26 | Amnis Corporation | Spatial alignment of image data from a multichannel detector using a reference image |
| US9274042B2 (en) * | 2010-05-07 | 2016-03-01 | Stc.Unm | Spatially correlated light collection from multiple sample streams excited with a line focused light source |
| JP2013531816A (ja) | 2010-06-21 | 2013-08-08 | ザ、リージェンツ、オブ、ザ、ユニバーシティ、オブ、カリフォルニア | 微分干渉コントラストの連続した時間でエンコードされた増幅顕微鏡検査法 |
| US20120002029A1 (en) | 2010-06-30 | 2012-01-05 | Fluid Imaging Technologies, Inc. | System and method for sweeping mirror enhanced imaging flow cytometry |
| US8736818B2 (en) | 2010-08-16 | 2014-05-27 | Ball Aerospace & Technologies Corp. | Electronically steered flash LIDAR |
| US8761486B2 (en) | 2011-02-22 | 2014-06-24 | Bio-Rad Laboratories, Inc. | Line scan cytometry systems and methods |
| JP5973471B2 (ja) | 2011-03-03 | 2016-08-23 | ライフ テクノロジーズ コーポレーション | サンプリングプローブ、システム、装置、および方法 |
| US20140147860A1 (en) | 2011-06-27 | 2014-05-29 | Life Technologies Corporation | Acoustic Cytometry Methods and Protocols |
| JP5849503B2 (ja) * | 2011-08-01 | 2016-01-27 | 株式会社Ihi | 粒子観察装置及びマニピュレート装置 |
| JP6047870B2 (ja) | 2011-10-14 | 2016-12-21 | ソニー株式会社 | 3dデータ解析のための装置、方法及びプログラムと、微小粒子解析システム |
| WO2013132344A2 (en) * | 2012-03-09 | 2013-09-12 | University Of Manitoba | Split-sensor dielectrophoretic/magnetophoretic cytometer |
| US8879797B2 (en) | 2012-05-25 | 2014-11-04 | Fluid Imaging Technologies, Inc. | System and method for total internal reflection enhanced imaging flow cytometry |
| EP2864762A4 (en) * | 2012-06-21 | 2016-01-20 | Stc Unm | SPATIALLY CORRELATED COLLECTION OF MULTIPLE SAMPLES TREATED WITH A LINE-FOCUSED LIGHT SOURCE |
| US9201008B2 (en) | 2012-06-26 | 2015-12-01 | Universite Laval | Method and system for obtaining an extended-depth-of-field volumetric image using laser scanning imaging |
| JP6396911B2 (ja) * | 2012-10-15 | 2018-09-26 | ナノセレクト バイオメディカル, インコーポレイテッド | 粒子を選別するためのシステム、装置、および、方法 |
| EP4075104A1 (en) * | 2012-10-16 | 2022-10-19 | Xtralis Technologies Ltd | Addressability in particle detection |
| JP6338597B2 (ja) | 2013-01-09 | 2018-06-06 | ザ リージェンツ オブ ザ ユニバーシティ オブ カリフォルニアThe Regents Of The University Of California | 無線周波数多重励起を用いた蛍光イメージングのための装置及び方法 |
| JP2014174139A (ja) * | 2013-03-13 | 2014-09-22 | Sony Corp | 流路デバイス、粒子分取装置、粒子流出方法、及び粒子分取方法 |
| BR112015021902B1 (pt) | 2013-03-15 | 2021-06-15 | Iris International, Inc | Líquido para alinhamento de partícula e organela intracelular |
| KR102055474B1 (ko) * | 2013-03-15 | 2019-12-12 | 아이리스 인터내셔널 인크. | 혈액 샘플에서의 입자 분석을 위한 플로우셀 시스템 및 방법 |
| EP2984468B1 (en) * | 2013-04-12 | 2021-11-17 | Becton, Dickinson and Company | Automated set-up for cell sorting |
| US9372143B2 (en) | 2013-05-15 | 2016-06-21 | Captl Llc | Scanning image flow cytometer |
| JP6717741B2 (ja) * | 2013-05-28 | 2020-07-08 | シェモメテック・アクティーゼルスカブChemometec A/S | 画像形成サイトメータ |
| CN103308440A (zh) | 2013-05-28 | 2013-09-18 | 香港浸会大学深圳研究院 | 一种流式荧光显微成像装置及方法 |
| US10061111B2 (en) * | 2014-01-17 | 2018-08-28 | The Trustees Of Columbia University In The City Of New York | Systems and methods for three dimensional imaging |
| US9726593B2 (en) | 2014-02-28 | 2017-08-08 | Life Technologies Corporation | Systems, methods, and apparatuses for optical systems in flow cytometers |
| AU2015225730A1 (en) | 2014-03-06 | 2016-10-27 | Life Technologies Corporation | Systems and methods for diagnosing a fluidics system and determining data processing settings for a flow cytometer |
| JP6104475B2 (ja) * | 2014-08-28 | 2017-04-05 | シスメックス株式会社 | 粒子撮像装置および粒子撮像方法 |
| CN104266956A (zh) * | 2014-09-02 | 2015-01-07 | 上海凯度机电科技有限公司 | 高内涵图像流式生物显微分析方法 |
| CN104535481B (zh) * | 2014-12-29 | 2017-04-05 | 中国科学院长春光学精密机械与物理研究所 | 成像流式细胞仪 |
| EP3259371B1 (en) | 2015-02-19 | 2020-09-02 | Becton, Dickinson and Company | High-throughput single-cell analysis combining proteomic and genomic information |
| JP6030740B1 (ja) | 2015-12-03 | 2016-11-24 | リオン株式会社 | パーティクルカウンタ |
| CN108474729B (zh) | 2015-12-30 | 2020-12-29 | 生命技术公司 | 提供稳定流体流的系统和方法 |
| US20180059005A1 (en) * | 2016-05-26 | 2018-03-01 | Redshift Bioanalytics, Inc. | Microfluidic Methods and Apparatus for Analysis of Analyte Bearing Fluids |
-
2018
- 2018-03-30 CN CN202310087156.7A patent/CN115931687A/zh active Pending
- 2018-03-30 KR KR1020197030723A patent/KR102585276B1/ko active IP Right Grant
- 2018-03-30 JP JP2019553505A patent/JP7187474B2/ja active Active
- 2018-03-30 EP EP18718661.4A patent/EP3602003A1/en active Pending
- 2018-03-30 WO PCT/US2018/025538 patent/WO2018183939A1/en active Application Filing
- 2018-03-30 SG SG11201908847T patent/SG11201908847TA/en unknown
- 2018-03-30 US US15/941,791 patent/US10386290B2/en active Active
- 2018-03-30 CN CN201880028673.4A patent/CN110573858B/zh active Active
-
2019
- 2019-06-18 US US16/444,232 patent/US10545085B2/en active Active
-
2020
- 2020-01-06 US US16/734,676 patent/US10969326B2/en active Active
-
2021
- 2021-03-04 US US17/191,780 patent/US11566995B2/en active Active
-
2022
- 2022-11-30 JP JP2022191046A patent/JP7464685B2/ja active Active
- 2022-12-21 US US18/069,324 patent/US20230221237A1/en active Pending
- 2022-12-21 US US18/069,281 patent/US11940371B2/en active Active
-
2023
- 2023-09-08 US US18/463,411 patent/US20230417649A1/en active Pending
- 2023-09-08 US US18/463,429 patent/US20230417650A1/en active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| US20180284009A1 (en) | 2018-10-04 |
| JP7464685B2 (ja) | 2024-04-09 |
| US10969326B2 (en) | 2021-04-06 |
| JP2020513103A (ja) | 2020-04-30 |
| EP3602003A1 (en) | 2020-02-05 |
| US20230417649A1 (en) | 2023-12-28 |
| WO2018183939A1 (en) | 2018-10-04 |
| SG11201908847TA (en) | 2019-10-30 |
| US20230221237A1 (en) | 2023-07-13 |
| KR102585276B1 (ko) | 2023-10-05 |
| US10386290B2 (en) | 2019-08-20 |
| JP7187474B2 (ja) | 2022-12-12 |
| JP2023036596A (ja) | 2023-03-14 |
| CN110573858B (zh) | 2023-02-17 |
| US10545085B2 (en) | 2020-01-28 |
| CN110573858A (zh) | 2019-12-13 |
| KR20190135012A (ko) | 2019-12-05 |
| US20230131332A1 (en) | 2023-04-27 |
| US20200141860A1 (en) | 2020-05-07 |
| US11566995B2 (en) | 2023-01-31 |
| US20210364411A1 (en) | 2021-11-25 |
| US20230417650A1 (en) | 2023-12-28 |
| US11940371B2 (en) | 2024-03-26 |
| US20190301997A1 (en) | 2019-10-03 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN110573858B (zh) | 用于成像流式细胞术的设备、系统和方法 | |
| Schonbrun et al. | Microfabricated multiple field of view imaging flow cytometry | |
| EP3671180B1 (en) | Method of using an apparatus configured to separate biological particles | |
| US7161665B2 (en) | High resolution imaging fountain flow cytometry | |
| US9464977B2 (en) | System and method for deforming, imaging and analyzing particles | |
| KR102162213B1 (ko) | 이미지 형성 세포 계수기 | |
| US20130314526A1 (en) | Cell analysis device | |
| US9772282B2 (en) | System for wide field-of-view, highly oblique illumination microscopy for scatter-based discrimination of cells | |
| JP2007263983A (ja) | 画像化システム及びその方法 | |
| CN108700500A (zh) | 用于颗粒的光学检测系统 | |
| JP2007502419A (ja) | 時間遅延積分による対象を撮像するための装置および方法 | |
| EP2111539A2 (en) | Images acquisition system in 2d and reconstructed tomographically in 3d of single cell/particles in flow carrier (laminar and non). | |
| US20220299420A1 (en) | Systems and methods for image cytometry | |
| AU2015224429B2 (en) | Apparatuses, systems, methods, and computer readable media for acoustic flow cytometry | |
| WO2024077266A2 (en) | Systems, devices and methods for sorting moving particles |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination |