CN115925931A - 抗tigit抗体 - Google Patents
抗tigit抗体 Download PDFInfo
- Publication number
- CN115925931A CN115925931A CN202210784461.7A CN202210784461A CN115925931A CN 115925931 A CN115925931 A CN 115925931A CN 202210784461 A CN202210784461 A CN 202210784461A CN 115925931 A CN115925931 A CN 115925931A
- Authority
- CN
- China
- Prior art keywords
- antibody
- seq
- antigen
- amino acid
- acid sequence
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
- A61K39/39533—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals
- A61K39/3955—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals against proteinaceous materials, e.g. enzymes, hormones, lymphokines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
- A61K39/39533—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals
- A61K39/39558—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals against tumor tissues, cells, antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
- A61K39/39533—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals
- A61K39/39566—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals against immunoglobulins, e.g. anti-idiotypic antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/57—Medicinal preparations containing antigens or antibodies characterised by the type of response, e.g. Th1, Th2
- A61K2039/572—Medicinal preparations containing antigens or antibodies characterised by the type of response, e.g. Th1, Th2 cytotoxic response
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/34—Identification of a linear epitope shorter than 20 amino acid residues or of a conformational epitope defined by amino acid residues
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/30—Non-immunoglobulin-derived peptide or protein having an immunoglobulin constant or Fc region, or a fragment thereof, attached thereto
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02A—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE
- Y02A50/00—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE in human health protection, e.g. against extreme weather
- Y02A50/30—Against vector-borne diseases, e.g. mosquito-borne, fly-borne, tick-borne or waterborne diseases whose impact is exacerbated by climate change
Abstract
本发明涉及抗TIGIT抗体。还涉及这些抗体在治疗疾病诸如癌症和感染性疾病中的用途。
Description
本申请是申请日为2016年8月9日的中国专利申请 201680059753.7“抗TIGIT抗体”的分案申请。
相关申请的交叉引用
本申请要求享有于2015年8月14日提交的美国临时申请号62/205,048的权益,且所述美国临时申请以其整体并入本文。
关于电子提交的序列表
本申请的序列表作为ASCII格式的序列表经由EFS-Web电子提交,所述序列表具有文件名“24178WOPCTSEQ.txt”,创建于2016年7月29日,且大小为111KB。经由EFS-Web提交的该序列表是本说明书的一部分,并且以其整体通过引用并入本文。
技术领域
本发明涉及抗TIGIT抗体,以及这些抗体在治疗疾病诸如癌症和感染性疾病中的用途。
背景技术
用于实现肿瘤免疫疗法的一种关键因子从以下发现出现:一般充当免疫检查点以维持自身耐受性的抑制性免疫调节受体(IMR)对肿瘤微环境逃避免疫的能力而言是重要的。抑制性IMR的阻断似乎比用活化细胞因子或肿瘤疫苗直接刺激肿瘤免疫更有效地释放有效肿瘤特异性免疫反应,且所述方法具有转换人类癌症疗法的潜能。针对该潜能,现在出现一个重大暗示和机会,开发针对其它IMR的新抗体拮抗剂且组合针对多于一种IMR的拮抗性抗体,以增加肿瘤学临床试验中反应者的比例,以及扩大其中肿瘤免疫疗法治疗有效的肿瘤学适应症。
值得注目地,抑制性IMR和调节细胞免疫的配体通常在肿瘤细胞和肿瘤相关巨噬细胞(TAM)上过表达。值得注意地,肿瘤中PD-L1的过表达与肿瘤特异性T细胞耗尽和不良预后相关联。在临床试验中PD-1/PD-L1接合的阻断导致相当大比例的患者中持久的肿瘤消退反应。近期的报导表明与表达单独任一IMR的细胞相比,黑色素瘤患者来源的肿瘤特异性CD8+ T细胞中PD-1和另一抑制性IMR (TIM-3)的共表达与功能更加失常的T细胞耗尽表型相关联。此外,使用临床前肿瘤模型的几个报导表明与单独拮抗性PD-1相比,多种IMR(包括PD-1、TIM-3、LAG-3和CTLA-4)的阻断更有效地诱导抗肿瘤反应。这些结果强调进一步研究IMR途径的重要性。
TIGIT(具有Ig和ITIM结构域的T细胞免疫受体)是一种主要在活化T细胞和NK细胞上表达的免疫调节受体。TIGIT也称为VSIG9;VSTM3;和WUCAM。其结构显示一个细胞外免疫球蛋白结构域、1型跨膜区和两个ITIM基序。TIGIT形成由T细胞上的阳性(CD226)和阴性(TIGIT)免疫调节受体和APC上表达的配体(CD155和CD112)组成的共刺激网络的一部分。
TIGIT结构中的一个重要特征是其胞质尾结构域中存在基于免疫受体酪氨酸的抑制基序(ITIM)。如同PD-1和CTLA-4,预测TIGIT的胞质区中的ITIM结构域募集酪氨酸磷酸酶,诸如SHP-1和SHP-2,且随后用T细胞受体(TCR)亚基上的基于免疫受体酪氨酸的活化基序(ITAM)将酪氨酸残基去磷酸化。因此,TIGIT与肿瘤细胞或TAMS表达的受体-配体CD155和CD112的接合可有助于抑制对建立有效抗肿瘤免疫而言必要的TCR信号传导和T细胞活化。因此,对TIGIT具有特异性的拮抗性抗体可抑制CD155和CD112诱导的T细胞反应的抑制且增强抗肿瘤免疫。本发明的一个目标是获得可单独或与其它试剂组合用于治疗癌症的抗TIGIT抗体。
发明内容
本发明提供包含以下指定的结构和功能特征的抗TIGIT抗体和其抗原结合片段。
在一个实施方案中,本发明提供结合人TIGIT的抗体或其抗原结合片段,其包含:包含SEQ ID NO:3、19、45、46或47的氨基酸序列的重链可变区CDR3。 在进一步的实施方案中,抗体或其抗原结合片段任选地具有以下特征中的至少一种:(i)以如通过表面等离子共振(例如,BIACORE)或类似技术(例如,KinExa或OCTET)所测定的约1 x 10-9M至约1 x 10-12M的KD值结合人TIGIT;(ii)与食蟹猴和恒河猴TIGIT交叉反应;(iii)阻断人TIGIT与人CD155和人CD112的结合;(iv)增加T细胞活化;(v)刺激IL-2和IFNγ的抗原特异性T细胞产生;(vi)阻断由TIGIT与同源配体CD155和CD112接合所诱导的T细胞活化抑制的诱导。
在另一个实施方案中,本发明提供结合人TIGIT的抗体或其抗原结合片段,其包含:包含SEQ ID NO:6、22、57、58、59、60、61或62的氨基酸序列的轻链可变区CDR3。 在进一步的实施方案中,抗体任选地具有以下特征中的至少一种:(i)以如通过表面等离子共振(例如,BIACORE)或类似技术(例如,KinExa或OCTET)所测定的约1 x 10-9M至约1 x 10-12M的KD值结合人TIGIT;(ii)与食蟹猴和恒河猴TIGIT交叉反应;(iii)阻断人TIGIT与人CD155和人CD112的结合;(iv)增加T细胞活化;(v)刺激IL-2和IFNγ的抗原特异性T细胞产生;(vi)阻断由TIGIT与同源配体CD155和CD112接合所诱导的T细胞活化抑制的诱导。
在另一个实施方案中,本发明提供结合人TIGIT的抗体或其抗原结合片段,其包含:(i)包含SEQ ID NO:1的氨基酸序列的重链可变区CDR1;(ii)包含SEQ ID NO:2的氨基酸序列的重链可变区CDR2;和(iii)包含SEQ ID NO: 3、45、46或47的氨基酸序列的重链可变区CDR3。在进一步的实施方案中,抗体或其抗原结合片段任选地具有以下特征中的至少一种:(i)以如通过表面等离子共振(例如,BIACORE)或类似技术(例如,KinExa或OCTET)所测定的约1 x 10-9M至约1 x 10-12M的KD值结合人TIGIT;(ii)与食蟹猴和恒河猴TIGIT交叉反应;(iii)阻断人TIGIT与人CD155和人CD112的结合;(iv)增加T细胞活化;(v)刺激IL-2和IFNγ的抗原特异性T细胞产生;(vi)阻断由TIGIT与同源配体CD155和CD112接合所诱导的T细胞活化抑制的诱导。
在另一个实施方案中,本发明提供结合人TIGIT的抗体或其抗原结合片段,其包含:(i)包含SEQ ID NO:17的氨基酸序列的重链可变区CDR1;(ii)包含SEQ ID NO:18、81、82、83、84、85、86、87或88的氨基酸序列的重链可变区CDR2;和(iii)包含SEQ ID NO:19的氨基酸序列的重链可变区CDR3。在进一步的实施方案中,抗体或其抗原结合片段任选地具有以下特征中的至少一种:(i)以如通过表面等离子共振(例如,BIACORE)或类似技术(例如,KinExa或OCTET)所测定的约1 x 10-9M至约1 x 10-12M的KD值结合人TIGIT;(ii)与食蟹猴和恒河猴TIGIT交叉反应;(iii)阻断人TIGIT与人CD155和人CD112的结合;(iv)增加T细胞活化;(v)刺激IL-2和IFNγ的抗原特异性T细胞产生;(vi)阻断由TIGIT与同源配体CD155和CD112接合所诱导的T细胞活化抑制的诱导。
在另一个实施方案中,本发明提供结合人TIGIT的抗体或其抗原结合片段,其包含:(i)包含SEQ ID NO: 4的氨基酸序列的轻链可变区CDR1;(ii)包含SEQ ID NO: 5的氨基酸序列的轻链可变区CDR2;和(iii)包含SEQ ID NO: 6、57、58、59、60、61或62的氨基酸序列的轻链可变区CDR3。在进一步的实施方案中,抗体或其抗原结合片段任选地具有以下特征中的至少一种:(i)以如通过表面等离子共振(例如,BIACORE)或类似技术(例如,KinExa或OCTET)所测定的约1 x 10-9M至约1 x 10-12M的KD值结合人TIGIT;(ii)与食蟹猴和恒河猴TIGIT交叉反应;(iii)阻断人TIGIT与人CD155和人CD112的结合;(iv)增加T细胞活化;(v)刺激IL-2和IFNγ的抗原特异性T细胞产生;(vi)阻断由TIGIT与同源配体CD155和CD112接合所诱导的T细胞活化抑制的诱导。
在另一个实施方案中,本发明提供结合人TIGIT的抗体或其抗原结合片段,其包含:(i)包含SEQ ID NO: 20的氨基酸序列的轻链可变区CDR1;(ii)包含SEQ ID NO: 21的氨基酸序列的轻链可变区CDR2;和(iii)包含SEQ ID NO: 22的氨基酸序列的轻链可变区CDR3。在进一步的实施方案中,抗体或其抗原结合片段任选地具有以下特征中的至少一种:(i)以如通过表面等离子共振(例如,BIACORE)或类似技术(例如,KinExa或OCTET)所测定的约1 x 10-9M至约1 x 10-12M的KD值结合人TIGIT;(ii)与食蟹猴和恒河猴TIGIT交叉反应;(iii)阻断人TIGIT与人CD155和人CD112的结合;(iv)增加T细胞活化;(v)刺激IL-2和IFNγ的抗原特异性T细胞产生;(vi)阻断由TIGIT与同源配体CD155和CD112接合所诱导的T细胞活化抑制的诱导。
在另一个实施方案中,本发明提供结合人TIGIT的抗体或其抗原结合片段,其包含:(i)包含SEQ ID NO: 1的氨基酸序列的重链可变区CDR1;(ii)包含SEQ ID NO: 2的氨基酸序列的重链可变区CDR2;(iii)包含SEQ ID NO: 3、45、46或47的氨基酸序列的重链可变区CDR3;(iv)包含SEQ ID NO: 4的氨基酸序列的轻链可变区CDR1;(v)包含SEQ ID NO: 5的氨基酸序列的轻链可变区CDR2;和(vi)包含SEQ ID NO: 6、57、58、59、60、61或62的氨基酸序列的轻链可变区CDR3。在一个实施方案中,所述抗体或其抗原结合片段是人源化的。在另一个实施方案中,抗体或其抗原结合片段包含具有SEQ ID NO:9的氨基酸序列的重链可变区;和具有SEQ ID NO:13的氨基酸序列的轻链可变区。在一个实施方案中,所述抗体或其抗原结合片段包含选自SEQ ID NO: 10、11、12、48、49、50、51、52、53、54、55和56的重链可变区;和选自SEQ ID NO: 14、15、16、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79和80的轻链可变区。在一个实施方案中,所述抗体或其抗原结合片段包含:包含与SEQ IDNO: 10、11、12、48、49、50、51、52、53、54、55或56中任一个具有至少90%、95%、96%、97%、98%或99%同一性的重链可变区;和包含于SEQ ID NO: 14、15、16、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79或80中任一个具有至少90%、95%、96%、97%、98%或99%同一性的轻链可变区。在一个实施方案中,所述抗体或其抗原结合片段包含:包含与SEQ ID NO: 10、11、12、48、49、50、51、52、53、54、55或56中任一个具有至少90%、95%、96%、97%、98%或99%同一性的重链可变区;和包含与SEQ ID NO: 14、15、16、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79或80中任一个具有至少90%、95%、96%、97%、98%或99%同一性的轻链可变区,其中任何序列变化发生在所述抗体的构架区中。在前述进一步的实施方案中,抗体或其抗原结合片段任选地具有以下特征中的至少一种:(i)以如通过表面等离子共振(例如,BIACORE)或类似技术(例如,KinExa或OCTET)所测定的约1 x 10-9M至约1 x 10-12M的KD值结合人TIGIT;(ii)与食蟹猴和恒河猴TIGIT交叉反应;(iii)阻断人TIGIT与人CD155和人CD112的结合;(iv)增加T细胞活化;(v)刺激IL-2和IFNγ的抗原特异性T细胞产生;(vi)阻断由TIGIT与同源配体CD155和CD112接合所诱导的T细胞活化抑制的诱导。
在另一个实施方案中,本发明提供结合人TIGIT的抗体或其抗原结合片段,其包含:(i)包含SEQ ID NO: 17的氨基酸序列的重链可变区CDR1;(ii)包含SEQ ID NO: 18、81、82、83、84、85、86、87或88的氨基酸序列的重链可变区CDR2;(iii)包含SEQ ID NO: 19的氨基酸序列的重链可变区CDR3;(iv)包含SEQ ID NO: 20的氨基酸序列的轻链可变区CDR1;(v)包含SEQ ID NO: 21的氨基酸序列的轻链可变区CDR2;和(vi)包含SEQ ID NO: 22的氨基酸序列的轻链可变区CDR3。在一个实施方案中,所述抗体或其抗原结合片段是人源化的。在另一个实施方案中,所述抗体或其抗原结合片段包含具有SEQ ID NO: 25的氨基酸序列的重链可变区;和具有SEQ ID NO: 29的氨基酸序列的轻链可变区。在进一步的实施方案中,所述抗体或其抗原结合片段包含选自SEQ ID NO: 26、27、28、89、90、91、92、93、94、95、96、97、98、99、100、101、102、103、104、105、106、107、108、109、110、111和112的重链可变区和选自SEQ ID NO:30、31和32的轻链可变区。在上文所述的进一步的实施方案中,所述抗体或其抗原结合片段包含:包含与SEQ ID NO: 26、27、28、89、90、91、92、93、94、95、96、97、98、99、100、101、102、103、104、105、106、107、108、109、110、111或112中任一个具有至少90%、95%、96%、97%、98%或99%同一性的重链可变区;和包含与SEQ ID NO:30、31或32中任一个具有至少90%、95%、96%、97%、98%或99%同一性的轻链可变区。在上文所述的进一步的实施方案中,所述抗体或其抗原结合片段包含:包含与SEQ ID NO: 26、27、28、89、90、91、92、93、94、95、96、97、98、99、100、101、102、103、104、105、106、107、108、109、110、111或112中任一个具有至少90%、95%、96%、97%、98%或99%同一性的重链可变区;和包含与SEQ ID NO:30、31或32中任一个具有至少90%、95%、96%、97%、98%或99%同一性的轻链可变区,其中任何序列变化发生在所述抗体的构架区中。在前述进一步的实施方案中,抗体或其抗原结合片段任选地具有以下特征中的至少一种:(i)以如通过表面等离子共振(例如,BIACORE)或类似技术(例如,KinExa或OCTET)所测定的约1 x 10-9M至约1 x 10-12M的KD值结合人TIGIT;(ii)与食蟹猴和恒河猴TIGIT交叉反应;(iii)阻断人TIGIT与人CD155和人CD112的结合;(iv)增加T细胞活化;(v)刺激IL-2和IFNγ的抗原特异性T细胞产生;(vi)阻断由TIGIT与同源配体CD155和CD112接合所诱导的T细胞活化抑制的诱导。
在另一个实施方案中,本发明提供结合人TIGIT的抗体或其抗原结合片段,其包含:(i)包含SEQ ID NO:1的氨基酸序列的重链可变区CDR1;(ii)包含SEQ ID NO:2的氨基酸序列的重链可变区CDR2;(iii)包含SEQ ID NO:3、45、46或47的氨基酸序列的重链可变区CDR3;(iv)包含SEQ ID NO:4的氨基酸序列的轻链可变区CDR1;(v)包含SEQ ID NO:5的氨基酸序列的轻链可变区CDR2;和(vi)包含SEQ ID NO:6、57、58、59、60、61或62的氨基酸序列的轻链可变区CDR3;其中所述抗体或其抗原结合片段包含:包含与选自SEQ ID No:9、10、11、12、48、49、50、51、52、53、54、55和56的重链可变区具有至少90%、95%、96%、97%、98%或99%同一性的重链可变区和包含与选自SEQ ID No:13、14、15、16、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79和80的轻链可变区具有至少90%、95%、96%、97%、98%或99%同一性的轻链可变区。在该前述实施方案中,序列变化发生在构架区中。在一个实施方案中,抗体以如通过表面等离子共振(例如,BIACORE)或类似技术(例如,KinExa或OCTET)所测定的约1x 10-9M至约1 x 10-12M的KD值结合人TIGIT。
在另一个实施方案中,本发明提供结合人TIGIT的抗体或其抗原结合片段,其包含:(i)包含SEQ ID NO:17的氨基酸序列的重链可变区CDR1;(ii)包含SEQ ID NO:18、81、82、83、84、85、86、87或86的氨基酸序列的重链可变区CDR2;(iii)包含SEQ ID NO:19的氨基酸序列的重链可变区CDR3;(iv)包含SEQ ID NO:20的氨基酸序列的轻链可变区CDR1;(v)包含SEQ ID NO:21的氨基酸序列的轻链可变区CDR2;和(vi)包含SEQ ID NO:22的氨基酸序列的轻链可变区CDR3;其中所述抗体或其抗原结合片段包含:包含与选自SEQ ID No:25、26、27、28、89、90、91、92、93、94、95、96、97、98、99、100、101、102、103、104、105、106、107、108、109、110、111和112的重链可变区具有至少90%、95%、96%、97%、98%或99%同一性的重链可变区和包含与选自SEQ ID No:29、30、31和32的轻链可变区具有至少90%、95%、96%、97%、98%或99%同一性的轻链可变区。在该前述实施方案中,序列变化发生在构架区中。在一个实施方案中,抗体以如通过表面等离子共振(例如,BIACORE)或类似技术(例如,KinExa或OCTET)所测定的约1 x 10-9M至约1 x 10-12M的KD值结合人TIGIT。
在另一个实施方案中,本发明还提供结合人TIGIT的抗体或其抗原结合片段,其包含:(i)包含SEQ ID NO: 1的氨基酸序列的重链可变区CDR1;(ii)包含SEQ ID NO: 2的氨基酸序列的重链可变区CDR2;(iii)包含SEQ ID NO: 3、45、46或47的氨基酸序列的重链可变区CDR3;(iv)包含SEQ ID NO: 4的氨基酸序列的轻链可变区CDR1;(v)包含SEQ ID NO: 5的氨基酸序列的轻链可变区CDR2;和(vi)包含SEQ ID NO: 6、57、58、59、60、61或62的氨基酸序列的轻链可变区CDR3。在一个实施方案中,抗体或其抗原结合片段包含重链CDR(SEQ IDNO:1、2、3、45、46或47)中和/或轻链CDR(SEQ ID NO:4、5、6、57、58、59、60、61或62)中的1、2或3个氨基酸取代。在一个实施方案中,抗体以如通过表面等离子共振(例如,BIACORE)或类似技术(例如,KinExa或OCTET)所测定的约1 x 10-9M至约1 x 10-12M的KD值结合人TIGIT。
在另一个实施方案中,本发明还提供结合人TIGIT的抗体或其抗原结合片段,其包含:(i)包含SEQ ID NO: 17的氨基酸序列的重链可变区CDR1;(ii)包含SEQ ID NO: 18、81、82、83、84、85、86、87和88的氨基酸序列的重链可变区CDR2;(iii)包含SEQ ID NO: 19的氨基酸序列的重链可变区CDR3;(iv)包含SEQ ID NO: 20的氨基酸序列的轻链可变区CDR1;(v)包含SEQ ID NO: 21的氨基酸序列的轻链可变区CDR2;和(vi)包含SEQ ID NO: 22的氨基酸序列的轻链可变区CDR3。在一个实施方案中,抗体或其抗原结合片段包含重链CDR(SEQID NO:17、18、19、81、82、83、84、85、86、87和88)中和/或轻链CDR(SEQ ID NO:20、21或22)中的1、2或3个氨基酸取代。在一个实施方案中,抗体以如通过表面等离子共振(例如,BIACORE)或类似技术(例如,KinExa或OCTET)所测定的约1 x 10-9M至约1 x 10-12M的KD值结合人TIGIT。
在另一个实施方案中,本发明提供了抗体或其抗原结合片段,其包含:包含SEQ IDNO: 7的氨基酸序列的可变重链和/或选自包含SEQ ID NO: 8的氨基酸序列的可变轻链,其中所述抗体或其抗原结合片段结合人TIGIT。在一个实施方案中,抗体以如通过表面等离子共振(例如,BIACORE)或类似技术(例如,KinExa或OCTET)所测定的约1 x 10-9M至约1 x 10-12M的KD值结合人TIGIT。
在另一个实施方案中,本发明提供了抗体或其抗原结合片段,其包含:包含SEQ IDNO: 23的氨基酸序列的可变重链和/或选自包含SEQ ID NO: 24的氨基酸序列的可变轻链,其中所述抗体或其抗原结合片段结合人TIGIT。在一个实施方案中,抗体以如通过表面等离子共振(例如,BIACORE)或类似技术(例如,KinExa或OCTET)所测定的约1 x 10-9M至约1 x10-12M的KD值结合人TIGIT。在一个实施方案中,本发明涉及结合人TIGIT的分离的抗体或抗原结合片段,其包含:包含SEQ ID NO:7的氨基酸序列的重链或包含至多30个氨基酸取代的其变体,和/或包含SEQ ID NO:8的氨基酸序列的轻链或包含至多12个氨基酸取代的其变体。
在另一个实施方案中,本发明涉及结合人TIGIT的分离的抗体或抗原结合片段,其包含:包含SEQ ID No:10、11、12、48、49、50、51、52、53、54、55、56的氨基酸序列的重链或包含至多12(1、2、3、4、5、6、7、8、9、10、11或12)个氨基酸取代的其变体,和/或包含SEQ ID NO:14、15、16、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80的氨基酸序列的轻链或包含至多8(1、2、3、4、5、6、7或8)个氨基酸取代的其变体。在进一步的实施方案中,本发明涉及结合人TIGIT的分离的抗体或抗原结合片段,其包含:包含SEQ ID No:10、11、12、48、49、50、51、52、53、54、55、56的氨基酸序列的重链或包含至多11个氨基酸取代的其变体,和/或包含SEQ ID NO:14、15、16、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80的氨基酸序列的轻链或包含至多8个氨基酸取代的其变体。在进一步的实施方案中,所述取代出现在重可变链和轻可变链的构架区中。
在另一个实施方案中,本发明涉及结合人TIGIT的分离的抗体或抗原结合片段,其包含:包含SEQ ID No:10的氨基酸序列的重链或包含至多12(1、2、3、4、5、6、7、8、9、10、11或12)个氨基酸取代的其变体,和/或包含SEQ ID NO:14的氨基酸序列的轻链或包含至多8(1、2、3、4、5、6、7或8)个氨基酸取代的其变体。在进一步的实施方案中,本发明涉及结合人TIGIT的分离的抗体或抗原结合片段,其包含:包含SEQ ID NO:10的氨基酸序列的重链或包含至多11个氨基酸取代的其变体,和/或包含SEQ ID NO:14的氨基酸序列的轻链或包含至多8个氨基酸取代的其变体。在进一步的实施方案中,所述取代出现在重可变链和轻可变链的构架区中。
在一个实施方案中,本发明涉及结合人TIGIT的分离的抗体或抗原结合片段,其包含:包含SEQ ID NO:23的氨基酸序列的重链或包含至多24个氨基酸取代的其变体,和/或包含SEQ ID NO:8的氨基酸序列的轻链或包含至多12个氨基酸取代的其变体。
在另一个实施方案中, 本发明涉及结合人TIGIT的分离的抗体或抗原结合片段,其包含:包含SEQ ID No:26、27、28、89、90、91、92、93、94、95、96、97、98、99、100、101、102、103、104、105、106、107、108、109、110、111、112的氨基酸序列的重链或包含至多12(1、2、3、4、5、6、7、8、9、10、11或12)个氨基酸取代的其变体,和/或包含SEQ ID NO:30、31、32的氨基酸序列的轻链或包含至多8(1、2、3、4、5、6、7或8)个氨基酸取代的其变体。在进一步的实施方案中, 本发明涉及结合人TIGIT的分离的抗体或抗原结合片段,其包含:包含SEQ ID No:26、27、28、89、90、91、92、93、94、95、96、97、98、99、100、101、102、103、104、105、106、107、108、109、110、111、112的氨基酸序列的重链或包含至多11个氨基酸取代的其变体,和/或包含SEQ ID NO:30、31、32的氨基酸序列的轻链或包含至多8个氨基酸取代的其变体。在进一步的实施方案中,所述取代出现在重可变链和轻可变链的构架区中。在进一步的实施方案中, 本发明涉及结合人TIGIT的分离的抗体或抗原结合片段,其包含:包含SEQ ID No:26的氨基酸序列的重链或包含至多12(1、2、3、4、5、6、7、8、9、10、11或12)个氨基酸取代的其变体,和/或包含SEQ ID NO:30的氨基酸序列的轻链或包含至多8(1、2、3、4、5、6、7或8)个氨基酸取代的其变体。在进一步的实施方案中,本发明涉及结合人TIGIT的分离的抗体或抗原结合片段,其包含:包含SEQ ID No:26的氨基酸序列的重链或包含至多11个氨基酸取代的其变体,和/或包含SEQ ID NO:30的氨基酸序列的轻链或包含至多4个氨基酸取代的其变体。在进一步的实施方案中,所述取代出现在重可变链和轻可变链的构架区中。
在以上实施方案中的任一个中,所述抗体或其抗原结合片段是分离的。
在以上实施方案中的任一个中,所述抗体或其抗原结合片段是重组抗体。
在以上实施方案中的任一个中,所述抗体或其抗原结合片段是全长抗体。
在以上实施方案中的任一个中,所述抗体或其抗原结合片段是人源化抗体。
在任意上述实施方案中,所述抗体或其抗原结合片段是包含两条重链和两条轻链的人源化抗体。在一个实施方案中,所述重链是IgG1同种型且轻链为κ轻链。在上述实施方案中的任一个中,本发明的抗体或其抗原结合片段可包含由以下组成的可变重链区:(a)上述可变重链中的任一种和(b)前导肽(例如SEQ ID NO:40的前导肽)。在上述实施方案中的任一个中,本发明的抗体或其抗原结合片段可包含由以下组成的可变轻链区:(a)上述可变轻链中的任一种和(b)前导肽(例如SEQ ID NO:41的前导肽)。
在上述实施方案中的任一个中,本发明的抗体或其抗原结合片段是包含上述可变重链中的任一种和任何人重链恒定结构域的抗体。在一个实施方案中,本发明的抗体或其抗原结合片段为IgG同种型,且包含人IgG1、IgG2、IgG3或IgG4人重链恒定结构域。在一个实施方案中,本发明的抗体或其抗原结合片段包含人重链IgG1恒定结构域(SEQ ID NO:44)或其变体,其中所述变体包含至多20个修饰的氨基酸取代。在一个实施方案中,本发明的抗体或其抗原结合片段是包含含有SEQ ID NO:44的氨基酸序列的人重链IgG1恒定结构域的抗体。在一个实施方案中,本发明的抗体或其抗原结合片段包含人重链IgG1恒定结构域,其中IgG1恒定结构域被无岩藻糖基化。在一个实施方案中,本发明的抗体或其抗原结合片段包含人重链IgG4恒定结构域或其变体,其中所述变体包含至多20个修饰的氨基酸取代。在另一个实施方案中,本发明的抗体或其抗原结合片段包含人重链IgG4恒定结构域,其中位置228的氨基酸(使用EU编号方案)已从Ser取代为Pro。在一个实施方案中,本发明的抗体或其抗原结合片段包含含有SEQ ID NO:42的氨基酸序列的人重链IgG4恒定结构域。
在进一步的实施方案中,与人IgG1、IgG2、IgG3或IgG4同种型的天然重链恒定结构域的氨基酸序列相比,所述恒定结构域可以包含1、2、3、4、5、6、7、8、9或10个氨基酸取代、添加、缺失或其组合。在具体的方面,所述恒定结构域可以包含C-端赖氨酸或可以缺少C-端赖氨酸。
在进一步的实施方案中,所述抗体包含人IgG1、IgG2、IgG3或IgG4同种型的重链恒定结构域或相比天然人IgG1、IgG2、IgG3或IgG4同种型的氨基酸序列包含1、2、3、4、5、6、7、8、9或10个氨基酸取代、添加、缺失或其组合的其变体,其中抗体或抗原结合片段结合TIGIT。在进一步的方面,所述恒定结构域可以包含C-端赖氨酸或可以缺少C-端赖氨酸。
在进一步的实施方案中,所述抗体包含人IgG1或IgG4同种型的重链恒定结构域。在进一步的方面,重链恒定结构域是IgG4同种型的且进一步包括在位置228(EU编号)的丝氨酸至脯氨酸取代,其对应于SEQ ID NO:42的位置108(在位置108的丝氨酸)。在进一步的方面,所述恒定结构域可以包含C-端赖氨酸或可以缺少C-端赖氨酸。
在进一步的实施方案中,所述抗体包含含有SEQ ID NO:42中所示氨基酸序列的人IgG4重链恒定结构域。在进一步的方面中,所述恒定结构域可以包含1、2、3、4、5、6、7、8、9或10个氨基酸取代、添加、缺失或其组合。在进一步的方面,所述恒定结构域可以包含C-端赖氨酸或可以缺少C-端赖氨酸。
在进一步的实施方案中,所述抗体包含含有SEQ ID NO:44中所示氨基酸序列的人IgG1重链恒定结构域。在进一步的方面中,所述恒定结构域可以包含1、2、3、4、5、6、7、8、9或10个氨基酸取代、添加、缺失或其组合。在进一步的方面,所述恒定结构域可以包含C-端赖氨酸或可以缺少C-端赖氨酸。
在上述实施方案中的任一个中,本发明的抗体或其抗原结合片段可包含上述可变轻链中的任一种和人轻链恒定结构域。在一个实施方案中,本发明的抗体或其抗原结合片段包含人κ轻链恒定结构域或其变体,其中所述变体包含至多20个修饰的氨基酸取代。在另一个实施方案中,本发明的抗体或其抗原结合片段包含人λ轻链恒定结构域或其变体,其中所述变体包含至多20个修饰的氨基酸取代。在一个实施方案中,本发明的抗体或其抗原结合片段包含含有SEQ ID NO:43的氨基酸序列的人κ轻链恒定结构域。
本发明进一步提供了结合在TIGIT上的包含氨基酸序列SSTTAQVNWEQQDQL (SEQID NO:113)、 ICN、 IYHTYPGT (SEQ ID NO:114)和GRIFL (SEQ ID NO:115)的表位的抗体或抗原结合片段。在一个实施方案中,本发明进一步提供了结合在TIGIT上的基本上由氨基酸序列SSTTAQVNWEQQDQL (SEQ ID NO:113)、 ICN、 IYHTYPGT (SEQ ID NO:114)和GRIFL(SEQ ID NO:115)组成的表位的抗体或抗原结合片段。
在进一步的实施方案中,所述抗体包含人IgG1、IgG2、IgG3或IgG4恒定结构域或其经修饰的衍生物。
在进一步的实施方案中,人IgG1、IgG2、IgG3或IgG4恒定结构域与天然人IgG1、IgG2、IgG3或IgG4同种型的氨基酸序列相比,是包含至少1、2、3、4、5、6、7、8、9或10个氨基酸取代、添加、缺失或其组合的变体。
在进一步的实施方案中,所述IgG1、IgG2、IgG3或IgG4恒定结构域与天然人IgG1、IgG2、IgG3或IgG4同种型的氨基酸序列相比,是包含至少1、2、3个氨基酸取代、添加、缺失或其组合的变体。
在进一步的实施方案中,所述IgG4恒定结构域是包含如本文所示用脯氨酸残基取代位置228(EU编号)或位置108的丝氨酸中至少一个的变体。
在进一步的实施方案中,所述IgG1、IgG2、IgG3或IgG4恒定结构域是至少缺乏在C-端的赖氨酸的变体。
在进一步的实施方案中,所述抗体或抗原结合片段包含含有人抗体的构架特征的可变结构域序列。
本发明进一步提供了结合在TIGIT上的包含氨基酸序列SSTTAQVNWEQQDQL (SEQID NO:113)、ICN、IYHTYPGT (SEQ ID NO:114)和GRIFL (SEQ ID NO:115)的表位的抗体或抗原结合片段,其中所述抗体或其抗原结合片段包含人IgG1或IgG4恒定结构域或其经修饰的衍生物。
在进一步的实施方案中,人IgG1或IgG4恒定结构域与天然人IgG1、IgG2、IgG3或IgG4同种型的氨基酸序列相比,是包含至少1、2、3、4、5、6、7、8、9或10个氨基酸取代、添加、缺失或其组合的变体。
在进一步的实施方案中,人IgG1或IgG4恒定结构域与天然人IgG1、IgG2、IgG3或IgG4同种型的氨基酸序列相比,是包含至少1、2、3、4、5、6、7、8、9或10个氨基酸取代、添加、缺失或其组合的变体。
在进一步的实施方案中,所述IgG4恒定结构域是包含如本文所示用脯氨酸残基取代位置228(EU编号)或位置108的丝氨酸中至少一个的变体。
在进一步的实施方案中,所述IgG1或IgG4恒定结构域是至少缺乏在C-端的赖氨酸的变体。
在进一步的实施方案中,所述抗体或抗原结合片段包含含有人抗体的构架特征的可变结构域序列。
在一个实施方案中,本发明的抗TIGIT抗体包含具有两条轻链和两条重链的四聚体结构,其中每条轻链包含:包含SEQ ID NO:16、17、18、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79或80中任一个的可变区和人κ轻链恒定区(SEQ ID NO:43);且每条重链包含:包含SEQ ID NO:9、10、11、12、48、49、50、51、52、53、54、55或56中任一个的可变区和人IgG1恒定区(SEQ ID NO: 44)。
在一个实施方案中,本发明的抗TIGIT抗体包含具有两条轻链和两条重链的四聚体结构,其中每条轻链包含:包含SEQ ID NO:29、30、31或32中任一个的可变区和人κ轻链恒定区(SEQ ID NO:43);且每条重链包含:包含SEQ ID NO:25、26、27、28、89、90、91、92、93、94、95、96、97、98、99、100、101、102、103、104、105、106、107、108、109、110、111或112中任一个的可变区和人IgG1恒定区(SEQ ID NO: 44)。
在一个实施方案中,本发明的抗TIGIT抗体包含具有两条轻链和两条重链的四聚体结构,其中每条轻链包含:包含SEQ ID NO:13-16或29-32中任一个的可变区和人κ轻链恒定区(SEQ ID NO:43);且每条重链包含:包含SEQ ID NO:9-13或25-28中任一个的可变区和人IgG1恒定区(SEQ ID NO: 44)。
在上述实施方案中的任一个中,本发明的抗TIGIT抗体或其抗原结合片段可以与至少一种治疗剂缀合。在一个实施方案中,其中所述治疗剂包含第二抗体或其片段、免疫调节剂、激素、细胞毒性剂、酶、放射性核素、缀合至至少一种免疫调节剂、酶、放射性标记、激素、反义寡核苷酸或细胞毒性剂的第二抗体或其组合。
本发明还提供分离的多肽,其包含SEQ ID NO:1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98、99、100、101、102、103、104、105、106、107、108、109、110、111、112中的任一氨基酸序列,或任何所述序列的片段。
本发明还提供分离的核酸,其编码任一本发明的抗TIGIT抗体或抗原结合片段。在一个实施方案中,本发明提供分离的核酸,其编码SEQ ID NO:1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98、99、100、101、102、103、104、105、106、107、108、109、110、111或112的任一多肽,其中所述多肽可任选地包含前导序列。本发明还提供表达载体,其包含编码SEQ ID NO:1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98、99、100、101、102、103、104、105、106、107、108、109、110、111或 112的任一多肽的核酸(其中所述多肽可任选地包含前导序列)。这些分离的核酸和包含其的表达载体可用于在重组宿主细胞中表达本发明的抗体或其抗原结合片段。因此,本发明还提供包含编码SEQ ID NO:1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98、99、100、101、102、103、104、105、106、107、108、109、110、111或 112的任一多肽的分离的核酸的宿主细胞(其中所述多肽可任选地包含前导序列)。在一个实施方案中,宿主细胞为中国仓鼠卵巢细胞。在一个实施方案中,宿主细胞为酵母细胞,例如毕赤酵母(Pichia)细胞或巴斯德毕赤酵母(Pichia pastoris)宿主细胞。
本发明还提供药物组合物,其包含本发明的抗体或抗原结合片段和药学上可接受的载体或稀释剂。在一个实施方案中,组合物包含另一治疗剂。在一个实施方案中,另一治疗剂选自:抗PD1抗体或其抗原结合片段;抗LAG3抗体或其抗原结合片段;抗VISTA抗体或其抗原结合片段;抗BTLA抗体或其抗原结合片段;抗TIM3抗体或其抗原结合片段;抗CTLA4抗体或其抗原结合片段;抗HVEM抗体或其抗原结合片段;抗CD27抗体或其抗原结合片段;抗CD137抗体或其抗原结合片段;抗OX40抗体或其抗原结合片段;抗CD28抗体或其抗原结合片段;抗PDL1抗体或其抗原结合片段;抗PDL2抗体或其抗原结合片段;抗GITR抗体或其抗原结合片段;抗ICOS抗体或其抗原结合片段;抗SIRPα抗体或其抗原结合片段;抗ILT2抗体或其抗原结合片段;抗ILT3抗体或其抗原结合片段;抗ILT4抗体或其抗原结合片段;和抗ILT5抗体或其抗原结合片段;抗4-1BB抗体或其抗原结合片段。在一个实施方案中,所述抗PD1抗体或其抗原结合片段选自:派姆单抗(pembrolizumab)或其抗原结合片段和尼鲁单抗(nivolumab)或其抗原结合片段。
在一个实施方案中,本发明的抗TIGIT抗体或抗原结合片段包含:(i)包含SEQ IDNO: 1的氨基酸序列的重链可变区CDR1;(ii)包含SEQ ID NO: 2的氨基酸序列的重链可变区CDR2;(iii)包含SEQ ID NO: 3、45、46或47的氨基酸序列的重链可变区CDR3;(iv)包含SEQ ID NO: 4的氨基酸序列的轻链可变区CDR1;(v)包含SEQ ID NO: 5的氨基酸序列的轻链可变区CDR2;和(vi)包含SEQ ID NO: 6、57、58、59、60、61或62的氨基酸序列的轻链可变区CDR3。在一个实施方案中,所述抗TIGIT抗体或其抗原结合片段包含:(i)包含SEQ ID NO:17的氨基酸序列的重链可变区CDR1;(ii)包含SEQ ID NO: 18、81、82、83、84、85、86、87或88的氨基酸序列的重链可变区CDR2;(iii)包含SEQ ID NO: 19的氨基酸序列的重链可变区CDR3;(iv)包含SEQ ID NO: 20的氨基酸序列的轻链可变区CDR1;(v)包含SEQ ID NO: 21的氨基酸序列的轻链可变区CDR2;和(vi)包含SEQ ID NO: 22的氨基酸序列的轻链可变区CDR3。
在一个实施方案中,本发明提供组合物,其包含:(i)本发明的抗TIGIT抗体或抗原结合片段;和(ii)包含SEQ ID NO:36的重链序列和SEQ ID NO:37的轻链可变序列的抗PD1抗体。在另一个实施方案中,本发明提供组合物,其包含:(a)本发明的抗TIGIT抗体或抗原结合片段;和(b)包含SEQ ID NO:38的重链序列和SEQ ID NO:39的轻链可变序列的抗PD1抗体。在一个实施方案中,所述抗PDI抗体在施用抗TIGIT抗体前施用。在一个实施方案中,所述抗PD1抗体在施用抗TIGIT抗体前4-10天施用。在一个实施方案中,用抗PD1抗体预处理治疗可调节免疫细胞,导致增强的抗TIGIT抗体的Fc介导的功能。在一个实施方案中,本发明的抗TIGIT抗体或抗原结合片段包含:(i)包含SEQ ID NO: 1的氨基酸序列的重链可变区CDR1;(ii)包含SEQ ID NO: 2的氨基酸序列的重链可变区CDR2;(iii)包含SEQ ID NO: 3、45、46或47的氨基酸序列的重链可变区CDR3;(iv)包含SEQ ID NO: 4的氨基酸序列的轻链可变区CDR1;(v)包含SEQ ID NO: 5的氨基酸序列的轻链可变区CDR2;和(vi)包含SEQ IDNO: 6、57、58、59、60、61或62的氨基酸序列的轻链可变区CDR3。在一个实施方案中,所述抗TIGIT抗体或其抗原结合片段包含:(i)包含SEQ ID NO: 17的氨基酸序列的重链可变区CDR1;(ii)包含SEQ ID NO: 18、81、82、83、84、85、86、87或88的氨基酸序列的重链可变区CDR2;(iii)包含SEQ ID NO: 19的氨基酸序列的重链可变区CDR3;(iv)包含SEQ ID NO: 20的氨基酸序列的轻链可变区CDR1;(v)包含SEQ ID NO: 21的氨基酸序列的轻链可变区CDR2;和(vi)包含SEQ ID NO: 22的氨基酸序列的轻链可变区CDR3。
本发明还包括包含本发明的抗TIGIT抗体或抗原结合片段与一种、两种或更多种治疗剂组合的组合;其中第二治疗剂选自:抗PD1抗体或其抗原结合片段;抗LAG3抗体或其抗原结合片段;抗VISTA抗体或其抗原结合片段;抗BTLA抗体或其抗原结合片段;抗TIM3抗体或其抗原结合片段;抗CTLA4抗体或其抗原结合片段;抗HVEM抗体或其抗原结合片段;抗CD27抗体或其抗原结合片段;抗CD137抗体或其抗原结合片段;抗OX40抗体或其抗原结合片段;抗CD28抗体或其抗原结合片段;抗PDL1抗体或其抗原结合片段;抗PDL2抗体或其抗原结合片段;抗GITR抗体或其抗原结合片段;抗ICOS抗体或其抗原结合片段;抗SIRPα抗体或其抗原结合片段;抗ILT2抗体或其抗原结合片段;抗ILT3抗体或其抗原结合片段;抗ILT4抗体或其抗原结合片段;抗ILT5抗体或其抗原结合片段;和抗4-1BB抗体或其抗原结合片段。在一个实施方案中,本发明的抗TIGIT抗体或抗原结合片段包含:(i)包含SEQ ID NO: 1的氨基酸序列的重链可变区CDR1;(ii)包含SEQ ID NO: 2的氨基酸序列的重链可变区CDR2;(iii)包含SEQ ID NO: 3、45、46或47的氨基酸序列的重链可变区CDR3;(iv)包含SEQ IDNO: 4的氨基酸序列的轻链可变区CDR1;(v)包含SEQ ID NO: 5的氨基酸序列的轻链可变区CDR2;和(vi)包含SEQ ID NO: 6、57、58、59、60、61或62的氨基酸序列的轻链可变区CDR3。在一个实施方案中,所述抗TIGIT抗体或其抗原结合片段包含:(i)包含SEQ ID NO: 17的氨基酸序列的重链可变区CDR1;(ii)包含SEQ ID NO: 18、81、82、83、84、85、86、87或88的氨基酸序列的重链可变区CDR2;(iii)包含SEQ ID NO: 19的氨基酸序列的重链可变区CDR3;(iv)包含SEQ ID NO: 20的氨基酸序列的轻链可变区CDR1;(v)包含SEQ ID NO: 21的氨基酸序列的轻链可变区CDR2;和(vi)包含SEQ ID NO: 22的氨基酸序列的轻链可变区CDR3。
本发明还提供容器或注射装置,其包含本发明的任一抗TIGIT抗体或抗原结合片段。在一个实施方案中,本发明的抗TIGIT抗体或抗原结合片段包含:(i)包含SEQ ID NO: 1的氨基酸序列的重链可变区CDR1;(ii)包含SEQ ID NO: 2的氨基酸序列的重链可变区CDR2;(iii)包含SEQ ID NO: 3、45、46或47的氨基酸序列的重链可变区CDR3;(iv)包含SEQID NO: 4的氨基酸序列的轻链可变区CDR1;(v)包含SEQ ID NO: 5的氨基酸序列的轻链可变区CDR2;和(vi)包含SEQ ID NO: 6、57、58、59、60、61或62的氨基酸序列的轻链可变区CDR3。在一个实施方案中,所述抗TIGIT抗体或其抗原结合片段包含:(i)包含SEQ ID NO:17的氨基酸序列的重链可变区CDR1;(ii)包含SEQ ID NO: 18、81、82、83、84、85、86、87或88的氨基酸序列的重链可变区CDR2;(iii)包含SEQ ID NO: 19的氨基酸序列的重链可变区CDR3;(iv)包含SEQ ID NO: 20的氨基酸序列的轻链可变区CDR1;(v)包含SEQ ID NO: 21的氨基酸序列的轻链可变区CDR2;和(vi)包含SEQ ID NO: 22的氨基酸序列的轻链可变区CDR3。
本发明还提供产生本发明的抗TIGIT抗体或抗原结合片段其的方法,其包括:将包含编码本发明抗体的重链和/或轻链(或其抗原结合片段)的多核苷酸的宿主细胞在有利于表达所述多核苷酸的条件下培养;且任选地,从宿主细胞和/或培养基回收抗体或抗原结合片段。在一个实施方案中,编码重链的多核苷酸和编码轻链的多核苷酸在单一载体中。在另一个实施方案中,编码重链的多核苷酸和编码轻链的多核苷酸在不同载体中。在一个实施方案中,编码重链的多核苷酸和编码轻链的多核苷酸编码包含以下的抗体或抗原结合片段:(i)包含SEQ ID NO: 1的氨基酸序列的重链可变区CDR1;(ii)包含SEQ ID NO: 2的氨基酸序列的重链可变区CDR2;(iii)包含SEQ ID NO: 3、45、46或47的氨基酸序列的重链可变区CDR3;(iv)包含SEQ ID NO: 4的氨基酸序列的轻链可变区CDR1;(v)包含SEQ ID NO: 5的氨基酸序列的轻链可变区CDR2;和(vi)包含SEQ ID NO: 6、57、58、59、60、61或62的氨基酸序列的轻链可变区CDR3。在另一个实施方案中,编码重链的多核苷酸和编码轻链的多核苷酸编码包含以下的抗体或抗原结合片段:(i)包含SEQ ID NO: 17的氨基酸序列的重链可变区CDR1;(ii)包含SEQ ID NO: 18、81、82、83、84、85、86、87或88的氨基酸序列的重链可变区CDR2;(iii)包含SEQ ID NO: 19的氨基酸序列的重链可变区CDR3;(iv)包含SEQ ID NO: 20的氨基酸序列的轻链可变区CDR1;(v)包含SEQ ID NO: 21的氨基酸序列的轻链可变区CDR2;和(vi)包含SEQ ID NO: 22的氨基酸序列的轻链可变区CDR3。
本发明还提供治疗有需要的个体的癌症的方法,其包括向所述个体施用有效量的本发明的抗TIGIT抗体或抗原结合片段,其任选地与另一治疗剂或治疗程序联合。在一个实施方案中,所治疗的个体为人类个体。在一个实施方案中,另一治疗剂选自:抗PD1抗体或其抗原结合片段;抗LAG3抗体或其抗原结合片段;抗VISTA抗体或其抗原结合片段;抗BTLA抗体或其抗原结合片段;抗TIM3抗体或其抗原结合片段;抗CTLA4抗体或其抗原结合片段;抗HVEM抗体或其抗原结合片段;抗CD27抗体或其抗原结合片段;抗CD137抗体或其抗原结合片段;抗OX40抗体或其抗原结合片段;抗CD28抗体或其抗原结合片段;抗PDL1抗体或其抗原结合片段;抗PDL2抗体或其抗原结合片段;抗GITR抗体或其抗原结合片段;抗ICOS抗体或其抗原结合片段;抗SIRPα抗体或其抗原结合片段;抗ILT2抗体或其抗原结合片段;抗ILT3抗体或其抗原结合片段;抗ILT4抗体或其抗原结合片段;抗ILT5抗体或其抗原结合片段;和抗4-1BB抗体或其抗原结合片段。在一个实施方案中,抗PD1抗体或其抗原结合片段选自:派姆单抗或其抗原结合片段和尼鲁单抗或其抗原结合片段。在一个实施方案中,本发明的抗TIGIT抗体或抗原结合片段包含:(i)包含SEQ ID NO: 1的氨基酸序列的重链可变区CDR1;(ii)包含SEQ ID NO: 2的氨基酸序列的重链可变区CDR2;(iii)包含SEQ ID NO: 3、45、46或47的氨基酸序列的重链可变区CDR3;(iv)包含SEQ ID NO: 4的氨基酸序列的轻链可变区CDR1;(v)包含SEQ ID NO: 5的氨基酸序列的轻链可变区CDR2;和(vi)包含SEQ ID NO: 6、57、58、59、60、61或62的氨基酸序列的轻链可变区CDR3。在一个实施方案中,所述抗TIGIT抗体或其抗原结合片段包含:(i)包含SEQ ID NO: 17的氨基酸序列的重链可变区CDR1;(ii)包含SEQID NO: 18、81、82、83、84、85、86、87或88的氨基酸序列的重链可变区CDR2;(iii)包含SEQID NO: 19的氨基酸序列的重链可变区CDR3;(iv)包含SEQ ID NO: 20的氨基酸序列的轻链可变区CDR1;(v)包含SEQ ID NO: 21的氨基酸序列的轻链可变区CDR2;和(vi)包含SEQ IDNO: 22的氨基酸序列的轻链可变区CDR3。
本发明还提供治疗有需要的个体的癌症的方法,其包括向所述个体施用有效量的本发明的抗TIGIT抗体或抗原结合片段,且进一步施用抗PD1抗体或其抗原结合片段。在一个实施方案中,抗PD1抗体或其抗原结合片段选自:派姆单抗或其抗原结合片段和尼鲁单抗或其抗原结合片段。在一个实施方案中,本发明的抗TIGIT抗体或抗原结合片段包含:(i)包含SEQ ID NO: 1的氨基酸序列的重链可变区CDR1;(ii)包含SEQ ID NO: 2的氨基酸序列的重链可变区CDR2;(iii)包含SEQ ID NO: 3、45、46或47的氨基酸序列的重链可变区CDR3;(iv)包含SEQ ID NO: 4的氨基酸序列的轻链可变区CDR1;(v)包含SEQ ID NO: 5的氨基酸序列的轻链可变区CDR2;和(vi)包含SEQ ID NO: 6、57、58、59、60、61或62的氨基酸序列的轻链可变区CDR3。在一个实施方案中,所述抗TIGIT抗体或其抗原结合片段包含:(i)包含SEQ ID NO: 17的氨基酸序列的重链可变区CDR1;(ii)包含SEQ ID NO: 18、81、82、83、84、85、86、87或88的氨基酸序列的重链可变区CDR2;(iii)包含SEQ ID NO: 19的氨基酸序列的重链可变区CDR3;(iv)包含SEQ ID NO: 20的氨基酸序列的轻链可变区CDR1;(v)包含SEQID NO: 21的氨基酸序列的轻链可变区CDR2;和(vi)包含SEQ ID NO: 22的氨基酸序列的轻链可变区CDR3。
本发明还提供治疗个体的感染或感染性疾病的方法,其包括向所述个体施用有效量的本发明的抗体或抗原结合片段,其任选地与另一治疗剂或治疗程序联合。在一个实施方案中,所治疗的个体为人类个体。在一个实施方案中,另一治疗剂选自:抗PD1抗体或其抗原结合片段;抗LAG3抗体或其抗原结合片段;抗VISTA抗体或其抗原结合片段;抗BTLA抗体或其抗原结合片段;抗TIM3抗体或其抗原结合片段;抗CTLA4抗体或其抗原结合片段;抗HVEM抗体或其抗原结合片段;抗CD27抗体或其抗原结合片段;抗CD137抗体或其抗原结合片段;抗OX40抗体或其抗原结合片段;抗CD28抗体或其抗原结合片段;抗PDL1抗体或其抗原结合片段;抗PDL2抗体或其抗原结合片段;抗GITR抗体或其抗原结合片段;抗ICOS抗体或其抗原结合片段;抗SIRPα抗体或其抗原结合片段;抗ILT2抗体或其抗原结合片段;抗ILT3抗体或其抗原结合片段;抗ILT4抗体或其抗原结合片段;抗ILT5抗体或其抗原结合片段;和抗4-1BB抗体或其抗原结合片段。在一个实施方案中,所述抗PD1抗体或其抗原结合片段选自:派姆单抗或其抗原结合片段和尼鲁单抗或其抗原结合片段。在一个实施方案中,本发明的抗TIGIT抗体或抗原结合片段包含:(i)包含SEQ ID NO: 1的氨基酸序列的重链可变区CDR1;(ii)包含SEQ ID NO: 2的氨基酸序列的重链可变区CDR2;(iii)包含SEQ ID NO: 3、45、46或47的氨基酸序列的重链可变区CDR3;(iv)包含SEQ ID NO: 4的氨基酸序列的轻链可变区CDR1;(v)包含SEQ ID NO: 5的氨基酸序列的轻链可变区CDR2;和(vi)包含SEQ ID NO: 6、57、58、59、60、61或62的氨基酸序列的轻链可变区CDR3。在一个实施方案中,所述抗TIGIT抗体或其抗原结合片段包含:(i)包含SEQ ID NO: 17的氨基酸序列的重链可变区CDR1;(ii)包含SEQ ID NO: 18、81、82、83、84、85、86、87或88的氨基酸序列的重链可变区CDR2;(iii)包含SEQ ID NO: 19的氨基酸序列的重链可变区CDR3;(iv)包含SEQ ID NO: 20的氨基酸序列的轻链可变区CDR1;(v)包含SEQ ID NO: 21的氨基酸序列的轻链可变区CDR2;和(vi)包含SEQ ID NO: 22的氨基酸序列的轻链可变区CDR3。
本发明还提供疫苗,其包含本发明的抗体或抗原结合片段。在一个实施方案中,本发明的抗TIGIT抗体或抗原结合片段包含:(i)包含SEQ ID NO: 1的氨基酸序列的重链可变区CDR1;(ii)包含SEQ ID NO: 2的氨基酸序列的重链可变区CDR2;(iii)包含SEQ ID NO:3、45、46或47的氨基酸序列的重链可变区CDR3;(iv)包含SEQ ID NO: 4的氨基酸序列的轻链可变区CDR1;(v)包含SEQ ID NO: 5的氨基酸序列的轻链可变区CDR2;和(vi)包含SEQ IDNO: 6、57、58、59、60、61或62的氨基酸序列的轻链可变区CDR3。在一个实施方案中,所述抗TIGIT抗体或其抗原结合片段包含:(i)包含SEQ ID NO: 17的氨基酸序列的重链可变区CDR1;(ii)包含SEQ ID NO: 18、81、82、83、84、85、86、87或88的氨基酸序列的重链可变区CDR2;(iii)包含SEQ ID NO: 19的氨基酸序列的重链可变区CDR3;(iv)包含SEQ ID NO: 20的氨基酸序列的轻链可变区CDR1;(v)包含SEQ ID NO: 21的氨基酸序列的轻链可变区CDR2;和(vi)包含SEQ ID NO: 22的氨基酸序列的轻链可变区CDR3。在一个实施方案中,所述疫苗进一步包含抗原。
本发明还提供了用于检测样品中TIGIT肽或其片段存在的方法,其包括将所述样品与本发明的抗体或其抗原结合片段接触,并且检测抗体或片段与所述肽的复合物的存在;其中所述复合物的存在指示了TIGIT肽的存在。在一个实施方案中,本发明的抗TIGIT抗体或抗原结合片段包含:(i)包含SEQ ID NO: 1的氨基酸序列的重链可变区CDR1;(ii)包含SEQ ID NO: 2的氨基酸序列的重链可变区CDR2;(iii)包含SEQ ID NO: 3、45、46或47的氨基酸序列的重链可变区CDR3;(iv)包含SEQ ID NO: 4的氨基酸序列的轻链可变区CDR1;(v)包含SEQ ID NO: 5的氨基酸序列的轻链可变区CDR2;和(vi)包含SEQ ID NO: 6、57、58、59、60、61或62的氨基酸序列的轻链可变区CDR3。在一个实施方案中,所述抗TIGIT抗体或其抗原结合片段包含:(i)包含SEQ ID NO: 17的氨基酸序列的重链可变区CDR1;(ii)包含SEQID NO: 18、81、82、83、84、85、86、87或88的氨基酸序列的重链可变区CDR2;(iii)包含SEQID NO: 19的氨基酸序列的重链可变区CDR3;(iv)包含SEQ ID NO: 20的氨基酸序列的轻链可变区CDR1;(v)包含SEQ ID NO: 21的氨基酸序列的轻链可变区CDR2;和(vi)包含SEQ IDNO: 22的氨基酸序列的轻链可变区CDR3。
本发明还提供增加免疫细胞的活性的方法,其包括使免疫细胞与本发明的任一抗体或抗原结合片段接触。在一个实施方案中,本发明提供增加免疫细胞的活性的方法,其包括向有需要的个体施用有效量的本发明的抗体或抗原结合片段。在一个实施方案中,所述方法用于:治疗癌症、治疗感染或感染性疾病或作为疫苗佐剂。在一个实施方案中,免疫细胞活性的增加可通过测量免疫细胞的增殖来检测。例如,T细胞活性的增加可通过测量T细胞的增殖来检测。在一个实施方案中,免疫细胞活性的增加可通过在来源于个体的样品中离体测量T细胞活化来检测。在一个实施方案中,T细胞活性的增加通过以下来测定:(i)测量混合淋巴细胞反应或诱导选自以下的细胞因子的产生的T细胞受体(TCR)信号传导的直接抗CD3 mAb刺激:IL-2、TNFα、IL-17、IFNγ、IL-1β、GM-CSF、RANTES、IL-6、IL-8、IL-5和IL-13;(ii)测量SEB诱导的一种或多种选自以下的细胞因子的产生:IL-2、TNFα、IL-17、IFNγ、GM-CSF、RANTES、IL-6、IL-8、IL-5和IL-13;或(iii)测量TT诱导的选自以下的细胞因子的产生:IL-2、TNFα、IL-17、IFNγ、GM-CSF、RANTES、IL-6、IL-8、IL-5和IL-13。在一个实施方案中,本发明的抗TIGIT抗体或抗原结合片段包含:(i)包含SEQ ID NO: 1的氨基酸序列的重链可变区CDR1;(ii)包含SEQ ID NO: 2的氨基酸序列的重链可变区CDR2;(iii)包含SEQ IDNO: 3、45、46或47的氨基酸序列的重链可变区CDR3;(iv)包含SEQ ID NO: 4的氨基酸序列的轻链可变区CDR1;(v)包含SEQ ID NO: 5的氨基酸序列的轻链可变区CDR2;和(vi)包含SEQ ID NO: 6、57、58、59、60、61或62的氨基酸序列的轻链可变区CDR3。在一个实施方案中,所述抗TIGIT抗体或其抗原结合片段包含:(i)包含SEQ ID NO: 17的氨基酸序列的重链可变区CDR1;(ii)包含SEQ ID NO: 18、81、82、83、84、85、86、87或88的氨基酸序列的重链可变区CDR2;(iii)包含SEQ ID NO: 19的氨基酸序列的重链可变区CDR3;(iv)包含SEQ ID NO:20的氨基酸序列的轻链可变区CDR1;(v)包含SEQ ID NO: 21的氨基酸序列的轻链可变区CDR2;和(vi)包含SEQ ID NO: 22的氨基酸序列的轻链可变区CDR3。
本发明还包括治疗个体的癌症或感染性疾病的方法,其包括向所述个体施用有效量的本发明的拮抗剂抗TIGIT抗体和拮抗剂抗PD1抗体,其中所述抗TIGIT抗体被无岩藻糖基化。在一个实施方案中,本发明的抗TIGIT抗体或抗原结合片段包含:(i)包含SEQ ID NO:1的氨基酸序列的重链可变区CDR1;(ii)包含SEQ ID NO: 2的氨基酸序列的重链可变区CDR2;(iii)包含SEQ ID NO: 3、45、46或47的氨基酸序列的重链可变区CDR3;(iv)包含SEQID NO: 4的氨基酸序列的轻链可变区CDR1;(v)包含SEQ ID NO: 5的氨基酸序列的轻链可变区CDR2;和(vi)包含SEQ ID NO: 6、57、58、59、60、61或62的氨基酸序列的轻链可变区CDR3。在一个实施方案中,所述抗TIGIT抗体或其抗原结合片段包含:(i)包含SEQ ID NO:17的氨基酸序列的重链可变区CDR1;(ii)包含SEQ ID NO: 18、81、82、83、84、85、86、87或88的氨基酸序列的重链可变区CDR2;(iii)包含SEQ ID NO: 19的氨基酸序列的重链可变区CDR3;(iv)包含SEQ ID NO: 20的氨基酸序列的轻链可变区CDR1;(v)包含SEQ ID NO: 21的氨基酸序列的轻链可变区CDR2;和(vi)包含SEQ ID NO: 22的氨基酸序列的轻链可变区CDR3。
附图说明
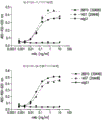
图1显示本发明的抗体与人和食蟹猴/恒河猴TIGIT的结合。
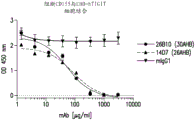
图2显示通过基于细胞的ELISA阻断测定确定本发明的抗体阻断hCD155与hTIGIT的相互作用。
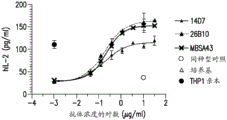
图3显示本发明的抗体在体外T细胞测定中的活性。
图4显示由小鼠抗-人TIGIT 14D7抗体结合的人TIGIT氨基酸残基的氘标记的不同热图。
具体实施方式
缩写
在本发明的详述和实施例中,将使用以下缩写:
ADCC 抗体依赖性细胞毒性
CDC 补体依赖性细胞毒性
CDR 免疫球蛋白可变区中的互补决定区,使用Kabat编号系统定义
CHO 中国仓鼠卵巢
ELISA 酶联免疫吸附测定
FR 抗体构架区:排除CDR区的免疫球蛋白可变区
HRP 辣根过氧化物酶
IFN 干扰素
IC50 导致50%抑制的浓度
IgG 免疫球蛋白G
Kabat 通过Elvin A. Kabat ((1991) Sequences of Proteins ofImmunological Interest,第5版Public Health Service, National Institutes ofHealth, Bethesda, Md.)开创的免疫球蛋白比对和编号系统
mAb或Mab或MAb 单克隆抗体
SEB 葡萄球菌肠毒素B
TT 破伤风类毒素
V区 不同抗体之间序列可变的IgG链的区段。其延伸至轻链中的Kabat残基109和重链中的Kabat残基113。
VH 免疫球蛋白重链可变区
VK 免疫球蛋白κ轻链可变区。
定义
为了可更容易理解本发明,在下文中具体地定义某些技术和科学术语。除非在本文件中别处具体地定义,否则本文所使用的所有其它技术和科学术语均具有本发明所属领域的本领域普通技术人员通常所理解的含义。
除非上下文另外清楚地规定,否则如本文所用,包括随附权利要求,词语单数形式诸如“一个/种(a)”、“一个/种(an)”和“该(the)”包括其对应的复数个提及物。
“施用”和“处理”在应用于动物、人类、实验个体、细胞、组织、器官或生物流体时是指外源性药物、治疗剂、诊断剂或组合物与所述动物、人类、个体、细胞、组织、器官或生物流体接触。细胞的处理涵盖使试剂与细胞的接触,以及试剂与流体的接触,其中所述流体与细胞接触。“施用”和“处理”也意指通过试剂、诊断剂、结合化合物或通过另一细胞例如体外和离体处理细胞。
“治疗(Treat)”或“治疗(treating)”意指在内部或外部向具有一种或多种疾病症状或怀疑患有疾病的药剂对其具有治疗活性的个体或患者施用治疗剂,诸如含有本发明的任一抗体或抗原结合片段的组合物。通常,药剂以有效缓解所治疗个体或群体中的一种或多种疾病症状的量施用,无论是通过任何临床上可测量的程度诱导此类症状的消退还是通过任何临床上可测量的程度抑制其进展。有效缓解任何特定疾病症状的治疗剂的量可根据因素诸如疾病状态、患者的年龄和体重以及药物在个体中引发所需反应的能力而变化。是否已缓解疾病症状可通过医师或其它熟练医疗护理提供者通常用于评价症状的严重程度或进展状态的任何临床测量来评价。
TIGIT
术语TIGIT包括人TIGIT、食蟹猴TIGIT和恒河猴TIGIT,以及其片段,诸如其缺乏信号肽的成熟片段。在本发明的一个实施方案中,人TIGIT的氨基酸序列包含Genbank登录号NP_776160.2 (SEQ ID NO: 33)的氨基酸残基25-244中公开的氨基酸序列。(SEQ ID NO:33的氨基酸残基1-24对应于前导肽,其从成熟TIGIT蛋白去除。)
在本发明的一个实施方案中,食蟹猴,例如食蟹猴(Macaca fascicularis)TIGIT的氨基酸序列包含(SEQ ID NO:34)中公开的氨基酸序列;还参见Genbank登录号XP_005548157。恒河猴TIGIT的氨基酸序列与食蟹猴TIGIT的氨基酸序列相同。(SEQ ID NO:34的氨基酸残基1-24对应于前导肽,其从成熟TIGIT蛋白去除。)
抗TIGIT抗体和其抗原结合片段
本发明提供结合人TIGIT的抗体或其抗原结合片段,和此类抗体或片段的用途。在一些实施方案中,抗TIGIT抗体是分离的。
如本文所用,抗TIGIT抗体或其抗原结合片段是指特异性结合人TIGIT的抗体或其抗原结合片段。“特异性结合人TIGIT”的抗体或其抗原结合片段为以约1nM的KD或更高亲和力(例如1nM-2pM、1nM、100pM、10pM或2pM)结合人TIGIT。例如,“特异性结合”人TIGIT的抗体不结合人CD226、人CD155和人CD112。作为另一实例,特异性结合人TIGIT的抗体或抗原结合片段可结合人TIGIT的FLAG®标记形式,但不会结合缺乏人TIGIT表位的其它FLAG®标记的蛋白。在一个实施方案中,特异性结合人TIGIT的本发明抗体还与食蟹猴和恒河猴TIGIT交叉反应。如本文所用,“交叉反应性”是指抗体与来自其它物种的同源蛋白反应的能力,其可以使用本领域已知的任何测定来确定。抗体是否特异性结合人TIGIT可使用本领域中已知的任何测定法确定。本领域中已知测定结合亲和力和交叉反应性的分析的实例包括表面等离子共振(例如,BIACORE)或类似技术(例如,KinExa或OCTET)。
本发明包括抗TIGIT抗体和其使用方法。如本文所用,术语“抗体”是指展现所需生物活性的抗体的任何形式。因此,其以最广泛意义使用,且具体涵盖,但不限于,单克隆抗体(包括包含两条轻链和两条重链的全长单克隆抗体)、多克隆抗体、多特异性抗体(例如双特异性抗体)、人源化抗体、完全人类抗体和嵌合抗体。
本发明包括非人类亲本(例如小鼠和啮齿动物)抗TIGIT抗体和其抗原结合片段以及其使用方法。这些抗体可针对预期用途而修饰,诸如将抗体人源化以用作人类治疗抗体或片段。
本发明包括抗TIGIT抗原结合片段和其使用方法。如本文所用,除非另外指明,否则“抗体片段”或“抗原结合片段”是指抗体的抗原结合片段,即保留特异性结合全长抗体所结合的抗原的能力的抗体片段,例如保留一个或多个CDR区的片段。抗原结合片段的实例包括,但不限于,Fab、Fab'、F(ab')2和Fv片段;双抗体(diabodies);线性抗体;单链抗体分子,例如sc-Fv;由全长抗体链或抗体片段形成的纳米抗体和多特异性抗体。
本发明包括抗TIGIT Fab片段和其使用方法。“Fab片段”包含一条轻链以及一条重链的CH1和可变区。Fab分子的重链无法与另一重链分子形成二硫键。“Fab片段”可以是抗体的木瓜蛋白酶切割的产物。
本发明包括抗TIGIT抗体和其包含Fc区的抗原结合片段以及其使用方法。“Fc”区含有两个包含抗体的CH1和CH2结构域的重链片段。两个重链片段通过两个或更多个二硫键和CH3结构域的疏水性相互作用保持在一起。
本发明包括抗TIGIT Fab片段和其使用方法。“Fab片段”含有一条轻链和一条重链的含有VH结构域和CH1结构域以及还有CH1和CH2结构域之间的区域的一部分或片段,使得在两个Fab片段的两条重链之间可形成链间二硫键以形成F(ab’)2分子。
本发明包括抗TIGIT F(ab’)2片段和其使用方法。“F(ab’)2片段”含有两条轻链和含有CH1结构域和CH2结构域之间的一部分恒定区的两条重链,使得在两条重链之间形成链间二硫键。因此,F(ab’)2片段由通过两条重链之间的二硫键保持在一起的两个Fab’片段构成。“F(ab’)2片段”可以是抗体的胃蛋白酶切割的产物。
本发明包括抗TIGIT Fv片段和其使用方法。“Fv区”包含来自重链和轻链的可变区,但缺乏恒定区。
本发明包括抗TIGIT scFv片段和其使用方法。术语“单链Fv”或“scFv”抗体是指包含抗体的VH和VL结构域的抗体片段,其中这些结构域存在于单一多肽链中。通常,Fv多肽在VH与VL结构域之间进一步包含多肽接头,其使得scFv能够形成用于抗原结合的所需结构。关于scFv的综述,参见Pluckthun (1994) The Pharmacology of MonoclonalAntibodies,第113卷,Rosenburg和Moore编辑,Springer-Verlag,New York,第269-315页。还参见国际专利申请公开号WO 88/01649和美国专利号4,946,778和5,260,203。
本发明包括抗TIGIT结构域抗体和其使用方法。“结构域抗体”是仅含有重链的可变区或轻链的可变区的免疫功能免疫球蛋白片段。在一些情况下,两个或更多个VH区用肽接头共价接合,以产生二价结构域抗体。二价结构域抗体的两个VH区可靶向相同或不同的抗原。
本发明包括抗TIGIT二价抗体和其使用方法。“二价抗体”包含两个抗原结合位点。在一些情况下,两个结合位点具有相同抗原特异性。然而,二价抗体可以是双特异性的(参见下文)。
本发明包括抗TIGIT双抗体和其使用方法。如本文所用,术语“双抗体”是指具有两个抗原结合位点的小抗体片段,所述片段包含重链可变结构域(VH)和与其在同一多肽链中连接的轻链可变结构域(VL)(VH-VL或VL-VH)。通过使用过短以使得同一链上的两个可变结构域之间不能配对的接头,迫使结构域与另一条链的互补结构域配对,且产生两个抗原结合位点。对双抗体的更全面描述在例如,EP 404,097;WO 93/11161;和 Holliger
等人(1993)
Proc. Natl. Acad. Sci. USA 90: 6444-6448中。关于工程改造的抗体变体的综述,一般参见Holliger和Hudson (2005) Nat. Biotechnol. 23:1126-1136。
通常,以一定方式修饰的本发明的抗体或抗原结合片段当活性以摩尔计表示时保留其结合活性的至少10%(当与亲本亲本相比时)。优选地,本发明的抗体或抗原结合片段保留亲本抗体的TIGIT结合亲和力的至少20%、50%、70%、80%、90%、95%或100%或更多。还意欲本发明的抗体或抗原结合片段可包括不实质上改变其生物活性的保守或非保守氨基酸取代(称为抗体的“保守变体”或“功能保守变体”)。
本发明包括分离的抗TIGIT抗体和其抗原结合片段和其使用方法。“分离”的抗体或其抗原结合片段至少部分不含来自产生其的细胞或细胞培养物的其它生物分子。此类生物分子包括核酸、蛋白、脂质、碳水化合物或其它物质,诸如细胞碎片和生长培养基。分离的抗体或抗原结合片段可进一步至少部分不含表达系统组分,诸如来自宿主细胞或其生长培养基的生物分子。通常,术语“分离的”不意指完全不存在此类生物分子或不存在水、缓冲剂或盐,或包括抗体或片段的药物制剂的组分。
本发明包括单克隆抗TIGIT抗体和其抗原结合片段以及包含多个分离单克隆抗体的单克隆组合物。如本文所用,术语“单克隆抗体”是指实质上均质抗体的群体,即除可能天然存在的可以少量存在的突变以外,构成该群体的抗体分子是氨基酸序列相同的。相比之下,常规(多克隆)抗体制备物通常包括在其可变结构域、尤其其CDR中具有不同氨基酸序列的许多不同抗体,其通常对不同表位是特异性的。修饰语“单克隆”指示抗体的特征为获得自实质上均质的抗体群体,且不应理解为需要通过任何特定方法产生所述抗体。例如,待根据本发明使用的单克隆抗体可通过Kohler等人(1975) Nature 256: 495首先描述的杂交瘤方法制备,或可通过重组DNA方法(参见例如美国专利号4,816,567)制备。“单克隆抗体”也可使用例如Clackson等人(1991) Nature 352: 624-628和Marks等人(1991) J. Mol.Biol. 222: 581-597中描述的技术分离自噬菌体抗体文库。还参见 Presta (2005) J.Allergy Clin. Immunol. 116:731。
本发明包括抗TIGIT嵌合抗体(例如人类恒定结构域/小鼠可变结构域)和其使用方法。如本文所用,“嵌合抗体”是具有来自第一抗体的可变结构域和来自第二抗体的恒定结构域的抗体,其中所述第一和第二抗体来自不同物种。(美国专利号4,816,567;和Morrison等人,(1984) Proc. Natl. Acad. Sci. USA 81: 6851-6855)。通常,可变结构域获得自来自实验动物诸如啮齿动物的抗体(“亲本抗体”),且恒定结构域序列获得自人类抗体,使得所得嵌合抗体与亲本(例如小鼠)抗体相比,将不太可能在人类个体中引发不良免疫反应。
本发明包括抗TIGIT人源化抗体和其抗原结合片段(例如已人源化的大鼠或小鼠抗体)和其使用方法。本发明包括14D7抗体(包含SEQ ID NO:7和8)或26B10抗体(包含SEQID NO:23和24)的任何人源化版本。如本文所用,术语“人源化抗体”是指含有来自人类和非人类(例如小鼠或大鼠)抗体的序列的抗体形式。通常,人源化抗体将包含至少一个且通常两个可变结构域的基本上全部,其中所有或实质上所有高变环对应于非人类免疫球蛋白的那些且所有或基本上所有构架(FR)区是人类免疫球蛋白序列的那些。人源化抗体可任选地包含人类免疫球蛋白恒定区(Fc)的至少一部分。
通常,基本抗体结构单元包含四聚体。各四聚体包括两个相同对的多肽链,各对具有一个“轻”链(约25kDa)和一个“重”链(约50-70kDa)。各链的氨基末端部分包括主要负责抗原识别的约100至110或更多个氨基酸的可变区。重链的羧基端部分可定义主要负责效应子功能的恒定区。通常,人轻链分类为κ和λ轻链。此外,人重链通常分类为μ、δ、γ、α或ε,且分别将抗体的同种型定义为IgM、IgD、IgG、IgA和IgE。在轻链和重链内,可变区和恒定区由约12个或更多个氨基酸的“J”区接合,其中重链还包括约10个以上氨基酸的“D”区。一般参见Fundamental Immunology 第7章(Paul, W.编辑,第2版Raven Press, N.Y. (1989)。
各轻链/重链对的可变区形成抗体结合位点。因此,通常,完整抗体具有两个结合位点。除了在双功能或双特异性抗体中,两个结合位点通常是相同的。
通常,重链和轻链两者的可变结构域包含三个高变区,也称为互补决定区(CDR),其位于相对保守构架区(FR)内。所述CDR通常通过所述构架区比对,使得能够结合特异性表位。通常,从N端至C端,轻链和重链可变结构域包含FR1、CDR1、FR2、CDR2、FR3、CDR3和FR4。氨基酸分配至各结构域通常根据以下的定义:Sequences of Proteins of ImmunologicalInterest, Kabat, 等人;National Institutes of Health, Bethesda, Md. ;第5版;NIH公开号91-3242 (1991);Kabat (1978) Adv. Prot. Chem. 32:1-75;Kabat, 等人,(1977) J. Biol. Chem. 252:6609-6616;Chothia, 等人, (1987) J Mol. Biol. 196:901-917或Chothia, 等人, (1989) Nature 342:878-883。
如本文所用,术语“高变区”是指负责抗原结合的抗体或其抗原结合片段的氨基酸残基。高变区包含来自“互补决定区”或“CDR”(即轻链可变结构域中的CDRL1、CDRL2和CDRL3,和重链可变结构域中的CDRH1、CDRH2和CDRH3)的氨基酸残基。参见Kabat等人(1991)Sequences of Proteins of Immunological Interest,第5版Public Health Service,National Institutes of Health, Bethesda, Md. (通过序列定义抗体的CDR区);还参见Chothia和Lesk (1987) J. Mol. Biol. 196: 901-917 (通过结构定义抗体的CDR区)。如本文所用,术语“构架”或“FR”残基是指除在本文中定义为CDR残基的高变区残基外的那些可变结构域残基。
“分离的核酸分子”或“分离的多核苷酸”意指基因组、mRNA、cDNA或合成来源的DNA或RNA或其一定组合,其不与在自然界中发现分离的多核苷酸的多核苷酸的全部或一部分缔合,或连接至其在自然界中不连接的多核苷酸。出于本发明的目的,应理解“包含特定核苷酸序列的核酸分子”不涵盖完整染色体。除指定序列之外,“包含”指定核酸序列的分离的核酸分子可包括多达十种或甚至多达二十种或更多种其它蛋白的编码序列或其部分或片段,或可包括控制所述核酸序列的编码区域的表达的可操作连接的调节序列,和/或可包括载体序列。
短语“控制序列”是指在特定宿主生物体中表达可操作连接的编码序列所需的DNA序列。适于原核生物的控制序列例如包括启动子、任选操纵子序列和核糖体结合位点。已知真核细胞使用启动子、聚腺苷酸化信号和增强子。
当核酸或多核苷酸置于与另一核酸序列的功能关系中时,其为“可操作连接的”。例如,如果前序列或分泌前导序列的DNA被表达为参与多肽分泌的前蛋白,则其与该多肽的DNA可操作连接;如果启动子或增强子影响编码序列的转录,则其与该序列可操作连接;或如果核糖体结合位点被定位以便有助于翻译,则其与编码序列可操作连接。通常,但未必总是,“可操作连接”意味着所连接的DNA序列相邻,并在分泌前导序列的情况下,相邻并在阅读相中。然而,增强子不必是连续的。连接通过在适宜限制性位点处连接来实现。如果此类位点不存在,则根据常规操作使用合成寡核苷酸适体或接头。
如本文所用,表述“细胞”、“细胞系”和“细胞培养物”可互换使用且所有此类名称均包括子代。因此,词语“转化体”和“转化细胞”包括原代个体细胞和来源于其的培养物,而无论转移次数。还应理解,由于有意或无意突变,不是所有子代都具有准确相同的DNA内含物。包括具有与最初转化细胞中所筛选相同的功能或生物活性的突变子代。在预期不同名称的情况下,其从上下文来看将是清楚的。
如本文所用,“种系序列”是指未重排的免疫球蛋白DNA序列的序列。可使用未重排的免疫球蛋白序列的任何合适来源。人类种系序列可获得自例如美国国立卫生研究院(theUnited States National Institutes of Health)的美国国立关节炎和肌肉骨骼和皮肤病研究所(the National Institute of Arthritis and Musculoskeletal and SkinDiseases)的网站上的JOINSOLVER种系数据库。小鼠种系序列可例如如Giudicelli等人(2005) Nucleic Acids Res. 33:D256-D261中所述获得。
示例性抗TIGIT抗体的物理和功能特性
本发明提供具有指定结构和功能特征的抗TIGIT抗体和其抗原结合片段,和所述抗体或其抗原结合片段用于治疗或预防疾病(例如癌症或感染性疾病)的方法。
“本发明的抗TIGIT抗体或其抗原结合片段”包括:本文中讨论的任何抗体或其抗原结合片段(例如14D7、26B10或这些抗体的人源化版本)。
交叉阻断抗体和其抗原结合片段可基于在标准结合测定(例如,BIACORE、ELISA、流式细胞术)中其与本发明抗体交叉竞争的能力来鉴定。例如,可使用标准ELISA测定,其中将重组TIGIT(例如人TIGIT)蛋白固定于板上,荧光标记抗体之一且评估未标记的抗体竞争掉标记抗体的结合的能力。或者或可替换地,BIAcore分析可用于评价抗体交叉竞争的能力。测试抗体抑制另一抗体(例如抗体14D7或26B10)与TIGIT(例如人TIGIT)结合的能力表明测试抗体可与另一抗体(例如14D7或26B10)竞争结合TIGIT(例如人TIGIT),且因此可在一些情况下结合TIGIT(例如人TIGIT)上与抗体14D7 或26B10相同的表位或重叠表位。
如上所述,结合与本发明的任一抗TIGIT抗体或其抗原结合片段相同的表位的抗体和片段也形成本发明的一部分。此外,结合与本发明的任一抗TIGIT抗体结合的表位重叠的表位的抗体也形成本发明的一部分。存在几种可用于定位靶抗原上的抗体表位的方法,包括:H/D-Ex质谱法、X射线结晶学、pepscan分析和定向诱变。例如,HDX(氢氘交换)与蛋白水解和质谱法的偶联可用于测定特定抗原Y上抗体的表位。HDX-MS依赖于当在D2O中在自身下和在其抗体存在的情况下以各种时间间隔孵育时抗原并入氘的准确测量和比较。氘与暴露区域中蛋白的酰胺主链上的氢交换,而结合抗体的抗原的区域将受保护,并将在通过蛋白水解片段的LC-MS/MS分析之后显示较少或不交换。
本发明的抗TIGIT抗体的免疫球蛋白链以及其CDR的实例包括但不限于表4中公开的那些。本发明包括包含SEQ ID NO:1、32、45-112的氨基酸序列或由其组成的任何多肽,和编码此类多肽的重组核苷酸。
本发明的范围包括分离的抗TIGIT抗体和其抗原结合片段(例如人源化抗体),其包含本文记载的免疫球蛋白链的变体,例如SEQ ID NO:716、48-56、63-80、23-32和89-112中的任一种;其中所述变体展现以下特性中的一种或多种:(i)结合人TIGIT;(ii)与食蟹猴和恒河猴TIGIT交叉反应;(iii)阻断人TIGIT与人CD155和人CD112的结合;(iv)增加T细胞活化;(v)刺激IL-2和IFNγ的抗原特异性T细胞产生;(vi)阻断由TIGIT与同源配体CD155和CD112接合所诱导的T细胞活化抑制的诱导。
在其它实施方案中,本发明提供抗体或其抗原结合片段,其结合人TIGIT(例如人源化抗体)且具有与SEQ ID NO:7-16、48-56、63-80、23-32和89-112具有至少80%、85%、90%、95%、96%、97%、98%或99%序列同一性的VL结构域和VH结构域;其中所述变体展现所需结合和特性,例如(i)以如通过表面等离子共振(例如,BIACORE)或类似技术(例如,KinExa或OCTET)所测定的约1 x 10-9M至约1 x 10-12M的KD值结合人TIGIT;(ii)与食蟹猴和恒河猴TIGIT交叉反应;(iii)阻断人TIGIT与人CD155和人CD112的结合;(iv)增加T细胞活化;(v)刺激IL-2和IFNγ的抗原特异性T细胞产生;(vi)阻断由TIGIT与同源配体CD155和CD112接合所诱导的T细胞活化抑制的诱导。
“保守修饰变体”或“保守取代”是指蛋白中的氨基酸被具有类似特征(例如电荷、侧链大小、疏水性/亲水性、主链构象和刚性等)的其它氨基酸取代,使得可频繁进行该变化,而不改变蛋白的生物活性。本领域技术人员认识到,通常,多肽的非必需区域中的单一氨基酸取代基本上不改变生物活性(参见例如 Watson等人(1987) Molecular Biology ofthe Gene, The Benjamin/Cummings Pub. Co.,第224页(第4版))。 另外,结构或功能相似氨基酸的取代不太可能破坏生物活性。示例性保守取代记载于表1中。
表1. 示例性保守氨基酸取代
| 初始残基 | 保守取代 |
| Ala (A) | Gly; Ser |
| Arg (R) | Lys; His |
| Asn (N) | Gln; His |
| Asp (D) | Glu; Asn |
| Cys (C) | Ser; Ala |
| Gln (Q) | Asn |
| Glu (E) | Asp; Gln |
| Gly (G) | Ala |
| His (H) | Asn; Gln |
| Ile (I) | Leu; Val |
| Leu (L) | Ile; Val |
| Lys (K) | Arg; His |
| Met (M) | Leu; Ile; Tyr |
| Phe (F) | Tyr; Met; Leu |
| Pro (P) | Ala |
| Ser (S) | Thr |
| Thr (T) | Ser |
| Trp (W) | Tyr; Phe |
| Tyr (Y) | Trp; Phe |
| Val (V) | Ile; Leu |
本发明还涵盖本发明抗体的功能保守变体。如本文所用,“功能保守变体”是指其中一个或多个氨基酸残基已改变、而不改变所需特性诸如抗原亲和力和/或特异性的抗体或片段。此类变体包括,但不限于,氨基酸被具有类似特性的氨基酸置换,诸如表1的保守氨基酸取代。还提供具有多达0、1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30或更多个氨基酸取代的包含本发明抗TIGIT抗体的VL结构域(例如SEQ ID NO:8、13-16、24、29-33、63-80)的分离的多肽和包含本发明抗TIGIT抗体的VH结构域的分离的多肽(例如SEQ ID NO:7, 9-12、24 26-29、48-56、89-112)。
在另一个实施方案中,提供抗体或其抗原结合片段,其结合TIGIT且具有与本文所述的VL结构域或VH结构域中的一种或多种具有至少99%、98%、97%、96%、95%、90%、85%、80%或75%序列同一性的VL结构域和VH结构域,且展现与TIGIT的特异性结合。在另一个实施方案中,本发明的结合抗体或其抗原结合片段包含具有多达0、1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30或更多个氨基酸取代的VL和VH结构域(具有和不具有信号序列),且展现与TIGIT的特异性结合。
多核苷酸和多肽
本发明进一步包含编码本发明的抗TIGIT抗体和其抗原结合片段的多肽或免疫球蛋白链中的任一种的多核苷酸。例如,本发明包括编码SEQ ID NO:1-32或45-112中描述的氨基酸的多核苷酸,以及与其杂交的多核苷酸,且此外,由此类杂交多核苷酸编码的任何多肽。
通常,多核苷酸在低、中等或高严格度条件下杂交,且编码维持结合TIGIT(人类、恒河猴和/或食蟹猴,例如食蟹猴)的能力的抗体或其抗原结合片段。当第一多核苷酸分子的单链形式可在适当温度和溶液离子强度条件下与第二多核苷酸分子退火时,第一多核苷酸分子与第二多核苷酸分子“可杂交”(参见Sambrook等人,同上)。温度和离子强度的条件决定杂交的“严格度”。典型的低严格度杂交条件包括55℃、5X SSC、0.1% SDS和无甲酰胺;或30%甲酰胺、5X SSC、0.5% SDS、在42℃下。典型中等严格度杂交条件为40%甲酰胺、5X或6XSSC和0.1% SDS、在42℃下。高严格度杂交条件为50%甲酰胺、5X或6X SSC、在42℃下或任选地在更高温度(例如57℃、59℃、60℃、62℃、63℃、65℃或68℃)下。通常,SSC为0.15M NaCl和0.015M柠檬酸钠。杂交要求两个多核苷酸含有互补序列,但是,取决于杂交的严格度,碱基之间的错配是可能的。用于杂交多核苷酸的适当严格度取决于多核苷酸的长度和互补程度、本领域中众所周知的变量。两个核苷酸序列之间的相似性或同源性程度越大,核酸可杂交的严格度越高。对于长度超过100个核苷酸的杂交物,已推导出用于计算熔融温度的方程(参见Sambrook等人,同上,9.50-9.51)。对于与更短多核苷酸、例如寡核苷酸的杂交,错配位置变得更重要,且寡核苷酸长度决定其特异性(参见Sambrook等人,同上,11.7-11.8)。
在另一个实施方案中,提供分离的多核苷酸,例如DNA,其编码本文记载的分离的抗体或抗原结合片段的多肽链。在一个实施方案中,分离的多核苷酸编码包含至少一个根据本发明的成熟免疫球蛋白轻链可变(VL)结构域和/或至少一个根据本发明的成熟免疫球蛋白重链可变(VH)结构域的抗体或其抗原结合片段。在一些实施方案中,分离的多核苷酸编码单一多核苷酸分子上的轻链与重链,且在其它实施方案中,编码分开的多核苷酸分子上的轻链和重链。在另一个实施方案中,多核苷酸进一步编码信号序列。
在一个实施方案中,本发明包含分离的多核苷酸,其编码包含CDR-H1(SEQ ID NO:1)、CDR-H2(SEQ ID NO:2)和CDR-H3(SEQ ID NO:3、45、46或47)的抗体重链可变(VH)结构域或其抗原结合片段。
在一个实施方案中,本发明包含分离的多核苷酸,其编码包含CDR-L1(SEQ ID NO:4)、CDR-L2(SEQ ID NO:5)和CDR-L3(SEQ ID NO:6、57、58、59、60、61、或62)的抗体轻链可变(VL)结构域或其抗原结合片段。
在一个实施方案中,本发明包含分离的多核苷酸,其编码SEQ ID NO:7的免疫球蛋白重链可变(VH)结构域。
在一个实施方案中,本发明包含分离的多核苷酸,其编码SEQ ID NO:8的免疫球蛋白重链可变(VL)结构域。
在一个实施方案中,本发明包含分离的多核苷酸,其编码SEQ ID NO:9-12中任一者的免疫球蛋白重链可变(VH)结构域。
在一个实施方案中,本发明包含分离的多核苷酸,其编码SEQ ID NO:48-56中任一者的免疫球蛋白重链可变(VH)结构域。
在一个实施方案中,本发明包含分离的多核苷酸,其编码SEQ ID NO:13-16中任一个的免疫球蛋白重链可变(VL)结构域。
在一个实施方案中,本发明包含分离的多核苷酸,其编码SEQ ID NO:63-80中任一个的免疫球蛋白重链可变(VL)结构域。
在一个实施方案中,本发明包含分离的多核苷酸,其编码包含CDR-H1(SEQ ID NO:17)、CDR-H2(SEQ ID NO:18、81、82、83、84、85、86、87或88)和CDR-H3(SEQ ID NO:19)的抗体重链可变(VH)结构域或其抗原结合片段。
在一个实施方案中,本发明包含分离的多核苷酸,其编码包含CDR-L1(SEQ ID NO:4)、CDR-L2(SEQ ID NO:5)和CDR-L3(SEQ ID NO:6、57、58、59、60、61或62)的抗体轻链可变(VL)结构域或其抗原结合片段。
在一个实施方案中,本发明包含分离的多核苷酸,其编码SEQ ID NO:23的免疫球蛋白重链可变(VH)结构域。
在一个实施方案中,本发明包含分离的多核苷酸,其编码SEQ ID NO:24的免疫球蛋白重链可变(VL)结构域。
在一个实施方案中,本发明包含分离的多核苷酸,其编码SEQ ID NO:25-28中任一者的免疫球蛋白重链可变(VH)结构域。
在一个实施方案中,本发明包含分离的多核苷酸,其编码SEQ ID NO:89-112中任一者的免疫球蛋白重链可变(VH)结构域。
在一个实施方案中,本发明包含分离的多核苷酸,其编码SEQ ID NO:29-32中任一个的免疫球蛋白重链可变(VL)结构域。
本发明还提供载体,例如表达载体,诸如质粒,其包含本发明的分离的多核苷酸,其中当宿主细胞用载体转染时该多核苷酸可操作连接至宿主细胞识别的控制序列。还提供包含本发明的载体的宿主细胞和用于产生本文公开的抗体或其抗原结合片段或多肽的方法,所述方法包括在培养基中培养携带编码抗体或其抗原结合片段的免疫球蛋白链的表达载体或核酸的宿主细胞,且从宿主细胞或培养基分离抗体或其抗原结合片段。
本发明中还包括当通过BLAST算法进行比较时,氨基酸序列与本文提供的抗体的氨基酸序列具有至少约75%同一性、具有80%同一性、更优选具有至少约90%同一性且最优选具有至少约95%(例如95%、96%、97%、98%、99%、100%)同一性的多肽,例如免疫球蛋白多肽,其中选择算法的参数以在相应参考序列的整个长度上在相应序列之间得到最大匹配(例如预期阈值:10;字长:3;查询范围中的最大匹配:0;BLOSUM 62矩阵;间隙成本:存在11、延伸1;条件性组成评分矩阵调整)。
序列同一性是指当最佳比对两个序列时两个多肽的氨基酸在等效位置相同的程度。
以下参考文献涉及经常用于序列分析的BLAST算法:BLAST ALGORITHMS:Altschul等人 (2005) FEBS J. 272(20): 5101-5109;Altschul, S.F.,等人, (1990) J.Mol. Biol. 215:403-410;Gish, W.,等人, (1993) Nature Genet. 3:266-272;Madden,T.L.,等人, (1996) Meth. Enzymol. 266:131-141;Altschul, S.F.,等人, (1997)Nucleic Acids Res. 25:3389-3402;Zhang, J.,等人, (1997) Genome Res. 7:649-656;Wootton, J.C.,等人, (1993) Comput. Chem. 17:149-163;Hancock, J.M.等人, (1994)Comput. Appl. Biosci. 10:67-70;ALIGNMENT SCORING SYSTEMS: Dayhoff, M.O.,等人,“A model of evolutionary change in proteins.” in Atlas of Protein Sequenceand Structure, (1978) 第5卷,增刊3. M.O. Dayhoff (编辑), 第345-352页, Natl.Biomed. Res. Found., Washington, DC;Schwartz, R.M.,等人, “Matrices fordetecting distant relationships.” in Atlas of Protein Sequence and Structure,(1978) 第5卷,增刊3.” M.O. Dayhoff (编辑), 第353-358页, Natl. Biomed. Res.Found., Washington, DC;Altschul, S.F., (1991) J. Mol. Biol. 219:555-565;States, D.J.,等人, (1991) Methods 3:66-70;Henikoff, S.,等人, (1992) Proc.Natl. Acad. Sci. USA 89:10915-10919;Altschul, S.F.,等人, (1993) J. Mol. Evol.36:290-300;ALIGNMENT STATISTICS: Karlin, S.,等人, (1990) Proc. Natl. Acad.Sci. USA 87:2264-2268;Karlin, S.,等人, (1993) Proc. Natl. Acad. Sci. USA 90:5873-5877;Dembo, A.,等人, (1994) Ann. Prob. 22:2022-2039;和Altschul, S.F.“Evaluating the statistical significance of multiple distinct localalignments.” Theoretical and Computational Methods in Genome Research (S.Suhai,编辑), (1997) 第1-14页, Plenum, New York。
结合亲和力
例如且不限于,本文公开的抗体和抗原结合片段可以如通过表面等离子共振(例如,BIACORE)或类似技术(例如,KinExa或OCTET)所测定的至少约1 x 10-9M的KD值(即1 x10-9M或更低的KD值)结合人TIGIT。在一个实施方案中,本文公开的抗体和抗原结合片段可以如通过表面等离子共振(例如,BIACORE)或类似技术(例如,KinExa或OCTET)所测定的至少约1 x 10-9M至约1 x 10-12M的KD值结合人TIGIT。在一个实施方案中,本文公开的抗体和抗原结合片段可以如通过表面等离子共振(例如,BIACORE)或类似技术(例如,KinExa或OCTET)所测定的至少约1 x 10-9M至约1 x 10-12M的KD值结合人TIGIT。在一个实施方案中,本文公开的抗体和抗原结合片段可以如通过BIACORE或类似技术所测定的至少约50pM的KD值(即约50pM或更低的KD值)结合人TIGIT。在一个实施方案中,本文公开的抗体和抗原结合片段可以如通过BIACORE或类似技术所测定的至少约10pM的KD值(即约10pM或更低的KD值)结合人TIGIT。在一个实施方案中,本发明的抗体和抗原结合片段可以如通过BIACORE或类似技术所测定的约50pM至约1pM的KD结合人TIGIT。
免疫细胞活化
在一些实施方案中,本发明的抗体或抗原结合片段增加免疫细胞的活性。免疫细胞活性的增加可使用本领域中已知的任何方法检测。在一个实施方案中,免疫细胞活性的增加可通过测量免疫细胞的增殖来检测。例如,T细胞活性的增加可通过测量T细胞的增殖或信号转导事件、诸如将信号传输至转录调节因子的免疫受体或下游激酶的酪氨酸磷酸化来检测。其它实施方案中,免疫细胞活性的增加可通过测量特定靶细胞上的CTL或NK细胞细胞毒性功能或与抗肿瘤免疫的刺激相关的IFNγ细胞因子反应来检测。在还有其它实施方案中,免疫细胞活性的增加可通过在来源于个体的样品中离体测量T细胞活化来检测。在一个实施方案中,T细胞活性的增加通过以下来测定:(i)测量SEB(葡萄球菌肠毒素B)诱导的一种或多种选自以下的促炎性细胞因子的产生:IL-2、TNFα、IL-17、IFNγ、IL-1β、GM-CSF、RANTES、IL-6、IL-8、IL-5和IL-13;或(ii)测量诱导选自以下的细胞因子的产生的T细胞受体(TCR)信号传导的混合淋巴细胞反应或直接抗CD3 mAb刺激:IL-2、TNFα、IL-17、IFNγ、IL-1β、GM-CSF、RANTES、IL-6、IL-8、IL-5和IL-13。 在某些实施方案中,本发明的抗TIGIT抗体或其抗原结合片段将使IL-2和/或IFNγ的抗原特异性T细胞产生刺激至少1.5倍。
本发明包括拮抗剂抗TIGIT抗体和其抗原结合片段和其使用方法,例如人源化、拮抗剂抗TIGIT抗体和片段。拮抗剂抗TIGIT抗体或其抗原结合片段诸如通过抑制TIGIT与CD155和CD112的结合,并在结合CD155和CD112后抑制TIGIT的功能性ITIM信号转导来拮抗人TIGIT的活性。抗TIGIT拮抗剂活性的测量可通过表明在通过TIGIT与同源配体CD155和CD112接合所诱导的TCR活化后T细胞抑制的阻断来评价。因此,在增加反应的一个实施方案中,用拮抗剂抗TIGIT抗体治疗能够将IL-2反应拯救至在未受TIGIT的CD155或CD112诱导抑制的T细胞中观察到的水平。在活化的一种更优选水平上,在用抗TIGIT拮抗抗体处理后,反应可增加至高于未受CD155或CD112抑制的T细胞反应的水平。
抗hTIGIT抗体阻断与hCD155和hCD112结合的能力
在一些实施方案中,本发明的抗TIGIT抗体或抗原结合片段能够阻断人TIGIT与人CD155和人CD112的结合。阻断人TIGIT与人CD155和人CD112的结合的能力可使用本领域中已知的任何方法测定。在一个实施方案中,抗体阻断人TIGIT与人CD155和人CD112的结合的能力使用如实施例2中所述的ELISA测定法来测定。
制备抗体和其抗原结合片段的方法
产生本文中讨论的亲本(例如大鼠或小鼠)单克隆抗TIGIT抗体或其抗原结合片段的杂交瘤细胞可通过本领域中通常已知的方法产生。此类分离的杂交瘤是本发明的一部分。这些方法包括,但不限于,最初由Kohler, 等人, (1975) (Nature 256:495-497)产生的杂交瘤技术,以及三源杂交瘤技术(Hering, 等人, (1988) Biomed. Biochim. Acta.47:211-216和Hagiwara, 等人, (1993) Hum. Antibod. Hybridomas 4:15)、人类B细胞杂交瘤技术(Kozbor, 等人, (1983) Immunology Today 4:72和Cote, 等人, (1983) Proc.Natl. Acad. Sci. U.S.A 80:2026-2030)、EBV-杂交瘤技术(Cole, 等人,MonoclonalAntibodies and Cancer Therapy, Alan R. Liss, Inc., 第77-96页, 1985)和使用CytoPulse大室细胞融合电穿孔器的基于电场的电融合(Cyto Pulse Sciences, Inc., GlenBurnie, MD)。优选地,分离小鼠脾细胞且与PEG融合,或通过基于标准方案与小鼠骨髓瘤细胞系电融合。然后可筛选所得杂交瘤以产生抗原特异性抗体。例如,来自免疫小鼠的脾淋巴细胞的单细胞悬浮液可用50% PEG与六分之一数目的P3X63-Ag8.653非分泌小鼠骨髓瘤细胞(ATCC,CRL 1580)融合。细胞可以约2 x 105个细胞/mL铺板于平底微量滴定板中,随后在含有20%胎克隆血清、18% “653”条件培养基、5% origen(IGEN)、4mM L-谷氨酰胺、1mM L-谷氨酰胺、1mM丙酮酸钠、5mM HEPES、0.055mM 2-巯基乙醇、50单位/ml青霉素、50mg/ml链霉素、50mg/ml庆大霉素和1X HAT(Sigma;在融合之后24小时添加HAT)的选择性培养基中孵育两周。在两周之后,可以在其中用HT置换HAT的培养基中培养细胞。然后可针对抗TIGIT单克隆IgG抗体,通过ELISA筛选个别孔。一旦发生大量杂交瘤生长,则通常可在10-14天之后观察培养基。可将分泌抗体的杂交瘤再次铺板,再次筛选,且如果仍然对人IgG为阳性,则抗TIGIT单克隆抗体可通过限制稀释法亚克隆至少两次。然后可体外培养稳定亚克隆以在组织培养基中产生少量抗体用于表征。
因此,本发明包括用于制备本发明的抗TIGIT抗体或其抗原结合片段的方法,其包括将表达抗体或片段的杂交瘤细胞在有利于此类表达的条件下培养,且任选地从杂交瘤和/或生长培养基(例如细胞培养基)分离抗体或片段。
本文公开的抗TIGIT抗体也可以重组产生(例如,在大肠杆菌/T7表达系统、哺乳动物细胞表达系统或低等真核生物表达系统中)。在该实施方案中,编码本发明的抗体免疫球蛋白分子(例如VH或VL)的核酸可插入基于pET的质粒中并在大肠杆菌/T7系统中表达。例如,本发明包括用于在宿主细胞(例如细菌宿主细胞,诸如大肠杆菌,诸如BL21或BL21DE3)中表达抗体或其抗原结合片段或其免疫球蛋白链的方法,其包括在还包括编码可操作连接至T7启动子的免疫球蛋白链的多核苷酸的细胞中表达T7 RNA聚合酶。例如,在本发明的一个实施方案中,细菌宿主细胞,诸如大肠杆菌,包括编码可操作连接至lac启动子的T7 RNA聚合酶基因的多核苷酸,且聚合酶和链的表达通过宿主细胞与IPTG(异丙基-β-D-硫代半乳糖苷)一起孵育来诱导。
存在几种产生重组抗体的本领域中已知的方法。重组产生抗体的方法的一个实例公开于美国专利号4,816,567中。
转化可通过任何已知用于将多核苷酸引入宿主细胞中的方法。用于将异源多核苷酸引入哺乳动物细胞的方法是本领域中众所周知的,且包括葡聚糖介导的转染、磷酸钙沉淀、凝聚胺介导的转染、原生质体融合、电穿孔、多核苷酸封装在脂质体中、基因枪注射和DNA直接显微注射至核中。另外,核酸分子可通过病毒载体引入哺乳动物细胞中。细胞转化方法是本领域中众所周知的。参见例如美国专利号4,399,216;4,912,040;4,740,461和4,959,455。
因此,本发明包括用于制备本发明的抗TIGIT抗体或其抗原结合片段或其免疫球蛋白链的重组方法,其包括引入编码抗体或片段的一条或多条免疫球蛋白链(例如免疫球蛋白重链和/或轻链)的多核苷酸;在有利于此类表达的条件下培养宿主细胞(例如CHO或毕赤酵母或巴斯德毕赤酵母),且任选地从宿主细胞和/或其中宿主细胞生长的培养基分离抗体或片段或链。
抗TIGIT抗体也可通过美国专利号6,331,415中记载的任一方法合成。
真核和原核宿主细胞,包括哺乳动物细胞作为用于表达本文公开的抗体或片段或免疫球蛋白链的宿主,是本领域中众所周知的,且包括许多可得自美国典型培养物保藏中心(American Type Culture Collection,ATCC)的永生化细胞系。这些尤其包括中国仓鼠卵巢(CHO)细胞、NSO、SP2细胞、HeLa细胞、幼仓鼠肾(BHK)细胞、猴肾细胞(COS)、人类肝细胞癌细胞(例如Hep G2)、A549细胞、3T3细胞、HEK-293细胞和许多其它细胞系。哺乳动物宿主细胞包括人类、小鼠、大鼠、狗、猴、猪、山羊、牛、马和仓鼠细胞。特别优先的细胞系通过确定哪些细胞系具有高表达水平来选择。可使用的其它细胞系为昆虫细胞系,诸如Sf9细胞、两栖动物细胞、细菌细胞、植物细胞和真菌细胞。真菌细胞包括酵母和丝状真菌细胞,包括例如巴斯德毕赤酵母、芬兰毕赤酵母(Pichia finlandica)、喜海藻糖毕赤酵母(Pichiatrehalophila)、考拉姆毕赤酵母(Pichia koclamae)、膜醭毕赤酵母(Pichiamembranaefaciens)、微小毕赤酵母(Pichia minuta)(Ogataea minuta、林氏毕赤酵母(Pichia lindneri))、Pichia opuntiae、耐热毕赤酵母(Pichia thermotolerans)、Pichiasalictaria、Pichia guercuum、皮杰普氏毕赤酵母(Pichia pijperi)、Pichia stiptis、甲醇毕赤酵母(Pichia methanolica)、毕赤酵母属(Pichia sp.)、酿酒酵母(Saccharomycescerevisiae)、酵母属(Saccharomyces sp.)、多形汉逊酵母(Hansenula polymorpha)、克鲁维酵母属(Kluyveromyces sp.)、乳酸克鲁维酵母(Kluyveromyces lactis)、白色念珠菌(Candida albicans)、构巢曲霉菌(Aspergillus nidulans)、黑曲霉(Aspergillusniger)、米曲霉(Aspergillus oryzae)、里氏木霉(Trichoderma reesei)、金孢子菌(Chrysosporium lucknowense)、镰刀菌属(Fusarium sp.)、禾谷镰孢菌(Fusariumgramineum)、镰孢霉(Fusarium venenatum)、小立碗藓(Physcomitrella patens)和粗糙脉孢菌(Neurospora crassa)。毕赤酵母属,任何酵母属、多形汉逊酵母、任何克鲁维酵母属、白色念珠菌、任何曲霉菌属、里氏木菌、金孢子菌、任何镰刀菌属、解脂耶氏酵母和粗糙脉孢菌。当将编码重链或其抗原结合部分或片段、轻链和/或其抗原结合片段的重组表达载体引入哺乳动物宿主细胞中时,抗体通过将宿主细胞培养一段足以允许抗体或片段或链在宿主细胞中表达或分泌至宿主细胞生长的培养基中的时间来产生。
抗体和其抗原结合片段和免疫球蛋白链可使用标准蛋白纯化方法来从培养基回收。此外,可使用许多已知的技术增强本发明的抗体和其抗原结合片段和免疫球蛋白链(或来自其的其它部分)从产生细胞系的表达。例如,谷氨酰胺合成酶基因表达系统(GS系统)为用于增强在某些条件下表达的常用方法。GS系统整体或部分结合欧洲专利号0 216 846、0256 055和0 323 997和欧洲专利申请号89303964.4进行讨论。因此,在本发明的一个实施方案中,哺乳动物宿主细胞(例如CHO)缺乏谷氨酰胺合成酶基因并在培养基中不存在谷氨酰胺的情况下生长,其中然而,编码免疫球蛋白链的多核苷酸包含补充宿主细胞中基因的缺乏的谷氨酰胺合成酶基因。
本发明包括用于纯化本发明的抗TIGIT抗体或其抗原结合片段的方法,其包括将包含抗体或片段的样品引入纯化培养基(例如阳离子交换培养基、阴离子交换培养基、疏水性交换培养基、亲和力纯化培养基(例如蛋白-A、蛋白-G、蛋白-A/G、蛋白-L))且从不结合培养基的所述样品的流过级分收集纯化的抗体或片段;或丢弃流过级分且洗脱来自培养基的结合抗体或片段且收集洗脱液。在本发明的一个实施方案中,培养基在施加样品的柱中。在本发明的一个实施方案中,在抗体或片段在宿主细胞中重组表达之后进行纯化方法,例如其中宿主细胞首先裂解且任选地在培养基上纯化前纯化裂解物以除去不溶材料。
通常,在特定细胞系或转基因动物中产生的糖蛋白将具有细胞系或转基因动物中产生的糖蛋白特征性的糖基化模式。因此,抗体的特定糖基化模式将取决于用于产生抗体的特定细胞系或转基因动物。然而,由本文提供的核酸分子编码或包含本文提供的氨基酸序列的所有抗体均构成本发明,其不依赖于抗体可具有的糖基化模式。类似地,在具体实施方案中,具有仅仅包含未岩藻糖基化N-聚糖的糖基化模式的抗体可以是有利的,因为这些抗体已显示通常在体外和体内显示比其岩藻糖基化对应物更有效的功效(参见例如Shinkawa等人,J. Biol. Chem. 278: 3466-3473 (2003);美国专利号6,946,292和7,214,775)。具有未岩藻糖基化N-聚糖的这些抗体因为其碳水化合物结构为人类血清IgG中存在的群体的正常组分而不可能是免疫原性的。
本发明包括多克隆抗TIGIT抗体和其抗原结合片段,例如包含多种抗TIGIT抗体和片段的组合物,其包括一种或多种本发明的抗TIGIT抗体或其抗原结合片段,和其使用方法。多克隆抗体是在一种或多种其它不相同抗体中或存在的情况下产生的抗体。通常,多克隆抗体由不同B淋巴细胞集合,例如用目标免疫原处理的动物的B淋巴细胞产生,所述B淋巴细胞产生不同抗体的群体,但其均针对免疫原。通常,多克隆抗体直接从免疫动物、例如脾、血清或腹水获得。
本发明包括对TIGIT和另一抗原诸如例如PD-1或PD-L1或LAG-3具有结合特异性的双特异性和双抗体和抗原结合片段,和其使用方法。在本发明的一个实施方案中,抗TIGIT链包含表4中所述的任一VH/VL序列,且PD1链包含SEQ ID NO:36和37或SEQ ID NO:38和39的氨基酸序列(或任一所述序列的抗原结合片段)。双特异性或双抗体为具有两个不同重链/轻链对和两个不同结合位点的人工杂交抗体。双特异性抗体可通过包括杂交瘤的融合或Fab’片段的连接的多种方法产生。参见例如Songsivilai, 等人, (1990) Clin. Exp.Immunol. 79: 315-321,Kostelny, 等人, (1992) J Immunol. 148:1547- 1553。另外,双特异性抗体可形成为“双抗体”(Holliger, 等人, (1993) PNAS USA 90:6444-6448)或为“Janusins” (Traunecker, 等人, (1991) EMBO J. 10:3655-3659和Traunecker, 等人,(1992) Int. J. Cancer Suppl. 7:51-52)。
本发明进一步包括本文公开的抗TIGIT抗体的抗TIGIT抗原结合片段。抗体片段包括F(ab)2片段,其可通过经由例如胃蛋白酶对IgG进行酶促切割来产生。Fab片段可通过例如用二硫苏糖醇或巯基乙胺还原F(ab)2来产生。
免疫球蛋白可根据其重链的恒定结构域的氨基酸序列而分成不同类别。存在至少五个主要类别的免疫球蛋白:IgA、IgD、IgE、IgG和IgM,且这些中的几种可进一步分成亚类(同种型),例如IgG1、IgG2、IgG3和IgG4;IgA1和IgA2。本发明包含抗体的这些类别或亚类中任一种的抗体和抗原结合片段。
在一个实施方案中,抗体或抗原结合片段包含重链恒定区,例如人类恒定区,诸如γ1、γ2、γ3或γ4人重链恒定区或其变体。在另一个实施方案中,抗体或抗原结合片段包含轻链恒定区,例如人轻链恒定区,诸如λ或κ人轻链区或其变体。例如且不限于,人重链恒定区可以是γ4,且人轻链恒定区可以是κ。在一个替代实施方案中,抗体的Fc区为具有Ser228Pro突变的γ4 (Schuurman, J 等人, Mol. Immunol. 38: 1-8, 2001)。
在一个实施方案中,抗体或抗原结合片段包含IgG1亚型的重链恒定区。
在一些实施方案中,不同恒定结构域可附接至衍生自本文提供的CDR的人源化VL和VH区。例如,如果本发明的抗体(或片段)的特定意欲用途需要改变效应子功能,则可使用除人IgG1外的重链恒定结构域,或可利用杂合IgG1/IgG4。
虽然人IgG1抗体提供长半衰期和效应子功能,诸如补体活化和抗体依赖性细胞毒性,但此类活性可能不是抗体的所有用途所需的。在此类情况下,可使用例如人IgG4恒定结构域。本发明包括包含IgG4恒定结构域的抗TIGIT抗体和其抗原结合片段,例如拮抗剂、人源化抗TIGIT抗体和片段,和其使用方法。在一个实施方案中,IgG4恒定结构域可在对应于EU系统中的位置228和KABAT系统中的位置241的位置不同于天然人IgG4恒定结构域(Swiss-Prot登录号P01861.1),其中天然Ser108被Pro置换,以防止Cys106和Cys109之间可干扰适当链内二硫键形成的潜在链间二硫键形成(对应于EU系统中的位置Cys 226和Cys229和KABAT系统中的位置Cys 239和Cys 242)。参见Angal等人(1993) Mol. Imunol. 30:105。在其它情况下,可使用已修饰以增加半衰期或降低效应子功能的修饰的IgG1恒定结构域。
抗体工程改造
进一步包括其中抗TIGIT抗体和其抗原结合片段是工程改造以包括对亲本(例如小鼠或大鼠)单克隆抗体的可变结构域内构架残基的修饰,例如改善抗体或片段的特性的抗体的实施方案。通常,进行此类构架修饰以降低抗体或片段的免疫原性。这通常通过将亲本(例如啮齿动物)抗体或片段(供体抗体或片段)中可变结构域中的非CDR残基(即构架残基)用来自其中将使用抗体的物种的免疫库的类似残基、例如在人类治疗剂的情况下人类残基(受体抗体)置换来实现。此抗体或片段被称为“人源化”抗体或片段。在一些情况下,需要增加或减少工程改造(例如人源化)的抗体的亲和力或改变其特异性。需要的免疫球蛋白特征可以通过选择和组合来自亲本抗体和受体抗体的构架残基来实现。一种方法是使一个或多个构架残基突变成相应种系序列。更具体地,已经历体细胞突变的抗体或片段可含有不同于抗体所来源的人种系序列的构架残基。此类残基可通过比较亲本抗体或片段构架序列与人抗体或片段所来源的种系序列来鉴定,并将抗体中一个或多个框架残基突变为相应的人种系序列。另一方法是在工程改造(例如人源化)抗体的一个或多个位置上回复(“反向突变(backmutate)”)至原始亲本(例如啮齿动物)残基,例如以恢复在置换构架残基的过程中可能失去的结合亲和力。(参见例如美国专利号5,693,762、美国专利号5,585,089、美国专利号5,530,101、WO9222653和WO9404679。)。
在某些实施方案中,抗TIGIT抗体和其抗原结合片段被工程改造(例如人源化)以在构架和/或CDR中包括修饰,以改善其特性。此类工程改造的变化可基于分子建模。亲本(非人类)抗体序列的可变区的分子模型可被构建以理解抗体的结构特征并用于鉴定可与抗原相互作用的抗体上的潜在区域。常规CDR基于比对免疫球蛋白序列和鉴定可变区。Kabat等人,(1991) Sequences of Proteins of Immunological Interest, Kabat,等人;National Institutes of Health, Bethesda, Md.;第5版;NIH公开号91-3242;Kabat(1978) Adv. Prot. Chem. 32:1-75;Kabat等人,(1977) J. Biol. Chem. 252:6609-6616。Chothia和同事小心地检查抗体的晶体结构中环的构型且提出高变环。Chothia等人,(1987) J Mol. Biol. 196:901-917或Chothia等人,(1989) Nature 342:878-883。归类为“CDR”和“高变环”的区域之间存在变化。 后来的研究(Raghunathan等人,(2012) J. MolRecog. 25, 3, 103-113)分析几种抗体-抗原晶体复合物且观察到抗体中的抗原结合区不必严格地与“CDR”残基或“高变”环一致。非人类抗体的可变区的分子模型可用于引导可潜在结合抗原的区域的选择。实际上,基于模型的潜在抗原结合区不同于常规“CDR”或“高变”环。商业科学软件诸如MOE (Chemical Computing Group)可用于分子建模。人类构架可基于构架中和CDR中与非人类序列的最佳匹配来选择。对于VH中的FR4(构架4),将人类种系的VJ区与对应非人类区域相比较。在VL中的FR4(构架4)的情况下,将人类种系序列的J-κ和J-λ区与对应非人类区相比较。一旦鉴定合适的人类构架,就将CDR移植至所选人类构架中。在一些情况下,VL-VH界面中的某些残基可如非人类(亲本)序列中保留。分子模型也可用于鉴定可潜在地改变CDR构型且因此改变与抗原的结合的残基。在一些情况下,这些残基如非人类(亲本)序列中得到保留。分子模型也可用于鉴定溶剂暴露的氨基酸,其可导致不必要作用,诸如糖基化、脱酰胺和氧化。可在设计阶段早期引入可开发性过滤器以消除/最小化这些潜在问题。
构架修饰的另一类型涉及将构架区内或甚至一个或多个CDR区内的一个或多个残基突变以去除T细胞表位,由此降低抗体的潜在免疫原性。该方法也称为“去免疫”,且进一步详细描述于美国专利号7,125,689中。
在具体实施方案中,需要将含有暴露的侧链的某些氨基酸改变成另一氨基酸残基,以提供最终抗体的更大化学稳定性,以避免脱酰胺或异构化。天冬酰胺的脱酰胺可在NG、DG、NG、NS、NA、NT、QG或QS序列上进行,且导致产生异天冬氨酸残基,其将扭结引入多肽链中且降低其稳定性(异天冬氨酸作用)。异构化可在DG、DS、DA或DT序列进行。在某些实施方案中,本发明的抗体不含脱酰胺或天冬酰胺异构位点。
例如,天冬酰胺(Asn)残基可改变成Gln或Ala以降低任何Asn-Gly序列、特别CDR内形成异天冬氨酸的潜能。相似问题可在Asp-Gly序列发生。Reissner和Aswad (2003) Cell.Mol. Life Sci. 60:1281。异天冬氨酸形成可减弱或完全废除抗体与其靶抗原的结合。参见Presta (2005) J. Allergy Clin. Immunol. 116:731第734页。在一个实施方案中,天冬酰胺改变成谷氨酰胺(Gln)。也可能需要改变与天冬酰胺(Asn)或谷氨酰胺(Gln)残基相邻的氨基酸以降低脱酰胺的可能性,当小氨基酸与天冬酰胺或谷氨酰胺相邻出现时脱酰胺以更大速率发生。参见Bischoff & Kolbe (1994) J. Chromatog. 662:261。另外,CDR中任何甲硫氨酸残基(通常溶剂暴露的Met)或色氨酸残基可改变成Lys、Leu、Ala或Phe或其它氨基酸以减小甲硫氨酸硫会氧化的可能性,其可降低抗原结合亲和力且还有助于最终抗体制备中的分子异质性。
同上。另外,为了预防或最小化潜在易切断的Asn-Pro肽键,可能需要将在CDR中发现的任何Asn-Pro组合改变成Gln-Pro、Ala-Pro或Asn-Ala。随后筛选具有此类取代的抗体以确保所述取代不使抗体对TIGIT的亲和力或特异性或其它所需生物活性降低至不可接受的水平。
表2. 示例性稳定CDR变体
。
Fc区的抗体工程改造
本文公开的抗体(例如人源化抗体)和其抗原结合片段(例如14D7、26B10和其人源化版本)也可工程改造以在Fc区内包括修饰,通常改变抗体的一种或多种特性,诸如血清半衰期、补体结合、Fc受体结合和/或效应子功能(例如抗原依赖性细胞毒性)。此外,本文公开的抗体和其抗原结合片段(例如14D7、26B10和其人源化版本)可被化学修饰(例如一种或多种化学部分可附接至抗体)或被修饰以改变其糖基化,再次改变抗体或片段的一种或多种特性。这些实施方案各自进一步详细描述于下文中。Fc区中的残基的编号是Kabat EU索引的编号。
本文公开的抗体和其抗原结合片段(例如14D7、26B10和其人源化版本)也包括具有修饰(或阻断)的Fc区以提供改变的效应子功能的抗体和片段。参见例如美国专利号5,624,821;WO2003/086310;WO2005/120571;WO2006/0057702。此类修饰可用于增强或抑制免疫系统的各种反应,其具有诊断和疗法中的可能有益作用。Fc区的改变包括氨基酸变化(取代、缺失和插入)、糖基化或去糖基化和添加多个Fc区。Fc的改变也可改变治疗抗体中抗体的半衰期,实现不太频繁的给药且因此增加便利性且物质使用减少。参见Presta (2005)J. Allergy Clin. Immunol. 116:731第734-35页。
在一个实施方案中,本发明的抗体或抗原结合片段(例如14D7、26B10或其人源化版本)是在重链恒定区的铰链区中对应于位置228的位置包含丝氨酸至脯氨酸突变(S228P;EU索引)的IgG4同种型抗体或片段。已报导该突变消除铰链区中重链间二硫桥的异质性(Angal等人,同上;位置241基于Kabat编号系统)。
在本发明的一个实施方案中,CH1的铰链区被修饰,使得铰链区中的半胱氨酸残基的数目增加或减少。该方法进一步描述于美国专利号5,677,425中。CH1的铰链区中半胱氨酸残基的数目被改变,例如以促进轻链和重链的组装或增加或降低抗体的稳定性。
在另一个实施方案中,本发明的抗体或抗原结合片段(例如14D7、26B10或其人源化版本)的Fc铰链区被突变,以缩短抗体或片段的生物半衰期。更具体地,将一个或多个氨基酸突变引入Fc铰链片段的CH2-CH3结构域界面区,使得抗体或片段具有相对于天然Fc-铰链结构域SpA结合受损的葡萄球菌蛋白A(SpA)结合。此方法进一步详细描述于美国专利号6,165,745中。
在另一个实施方案中,本发明的抗体或抗原结合片段(例如14D7、26B10或其人源化版本)被修饰以增加其生物半衰期。各种方法为可能的。例如,可引入以下突变中的一种或多种:T252L、T254S、T256F,如美国专利号6,277,375中所述。或者,为了增加生物半衰期,抗体可在CH1或CL区内改变以含有结合取自IgG的Fc区的CH2结构域的两个环的表位的拯救受体,如美国专利号5,869,046和6,121,022中所述。
在还有其它实施方案中,Fc区通过将至少一个氨基酸残基用不同氨基酸残基置换以改变抗体或抗原结合片段的效应子功能。例如,选自氨基酸残基234、235、236、237、297、318、320和322的一个或多个氨基酸可被不同氨基酸残基置换,使得抗体具有改变的对效应子配体的亲和力且保留亲本抗体的抗原结合能力。亲和力改变的效应子配体可以是例如Fc受体或补体的C1组分。该方法进一步详细描述于美国专利号5,624,821和5,648,260中。
在另一个实例中,选自氨基酸残基329、331和322的一个或多个氨基酸可被不同氨基酸残基置换,使得抗体具有改变的C1q结合和/或降低或消除的补体依赖性细胞毒性(CDC)。此方法进一步详细描述于美国专利号6,194,551中。
在另一个实例中,氨基酸位置123和239内的一个或多个氨基酸残基被改变,由此改变抗体固定补体的能力。在另一个实例中,氨基酸位置123和239内的一个或多个氨基酸残基被改变,由此改变抗体固定补体的能力。该方法进一步描述于PCT公开WO 94/29351中。
在又另一个实例中,Fc区通过在以下位置修饰一个或多个氨基酸而被修饰以降低本发明的抗体或抗原结合片段(例如14D7、26B10或其人源化版本)介导抗体依赖性细胞毒性(ADCC)的能力和/或降低抗体或片段对Fcγ受体的亲和力:238、239、243、248、249、252、254、255、256、258、264、265、267、268、269、270、272、276、278、280、283、285、286、289、290、292、293、294、295、296、298、301、303、305、307、309、312、315、320、322、324、326、327、329、330、331、333、334、335、337、338、340、360、373、376、378、382、388、389、398、414、416、419、430、434、435、437、438或439。该方法进一步描述于PCT公开WO 00/42072中。此外,已定位人IgG1上对FcγR1、FcγRII、FcγRIII和FcRn的结合位点且已描述具有提高结合的变体(参见Shields等人(2001) J. Biol. Chem. 276:6591-6604)。
在本发明的一个实施方案中,Fc区通过修饰残基243和264而被修饰以降低本发明抗体(例如14D7、26B10和其人源化版本)介导效应子功能的能力和/或增加抗炎特性。在一个实施方案中,抗体或片段的Fc区通过将位置243和264的残基改变成丙氨酸来修饰。在一个实施方案中,Fc区通过修饰残基243、264、267和328而被修饰以降低抗体或片段介导效应子功能的能力和/或增加抗炎特性。
效应子功能增强
在一些实施方案中,抗TIGIT抗体的Fc区被修饰以增加抗体或抗原结合片段介导效应子功能的能力和/或增加其与Fcγ受体(FcγR)的结合。
如本文所用,术语“效应子功能”意指以下中的一种或多种:抗体依赖性细胞介导的细胞毒性活性(ADCC)、补体依赖性细胞毒性活性(CDC)介导的反应、Fc介导的吞噬作用或抗体依赖性细胞吞噬作用(ADCP)和经由FcRn受体的抗体再循环。
据信抗原结合蛋白的恒定区和各种Fc受体(FcR)(包括FcγRI(CD64)、FcγRII(CD32)和FcγRIII(CD16))之间的相互作用介导抗原结合蛋白的效应子功能,诸如ADCC和CDC。Fc受体对于抗体交联也是重要的,所述抗体交联对于抗肿瘤免疫性可以是重要的。
效应子功能可用许多方式、包括例如经由FcγRIII与天然杀伤细胞的结合或经由FcγRI与单核细胞/巨噬细胞的结合来测量以测量ADCC效应子功能。例如,可在天然杀伤细胞测定中评估本发明的抗原结合蛋白的ADCC效应子功能。此类测定的实例可见于Shields等人,2001 J. Biol. Chem. ,第276卷,第6591-6604页;Chappel等人, 1993 J. Biol.Chem. ,第268卷,第25124-25131页;Lazar等人, 2006 PNAS, 103; 4005-4010。
本发明抗体的ADCC或CDC特性或其交联特性可以许多方式增强。
已显示在残基Asn297上含有特定突变或改变的糖基化的人IgG1恒定区增强与Fc受体的结合。在一些情况下,这些突变也已显示增强ADCC和CDC(Lazar等人PNAS 2006,103; 4005-4010;Shields等人J Biol Chem 2001, 276;6591-6604;Nechansky等人MolImmunol, 2007, 44; 1815-1817)。
在本发明的一个实施方案中,此类突变在选自239、332和330(IgG1)的一个或多个位置中,或其它IgG同种型中的同等位置中。合适突变的实例为S239D和I332E和A330L。在一个实施方案中,本文所述的本发明的抗原结合蛋白在位置239和332突变,例如S239D和I332E,或在另一个实施方案中,其在选自239和332和330的三个或更多个位置(例如S239D和I332E和A330L)突变。(EU索引编号)。
在本发明的一个替代实施方案中,提供抗体,其包含具有改变的糖基化模式的重链恒定区,使得所述抗原结合蛋白具有增强的效应子功能。例如,其中抗体具有增强的ADCC或增强的CDC或其中其具有增强的ADCC和CDC效应子功能。产生具有改变的糖基化概况的抗原结合蛋白的合适方法的实例描述于WO2003011878、WO2006014679和EP1229125中。
在另一个方面,本发明提供“未岩藻糖基化”或“无岩藻糖基化”抗体。未岩藻糖基化抗体具有无岩藻糖残基的Fc的复合物型N-聚糖的三甘露糖基核心结构。归因于FcγRIIIa结合能力的增强,这些缺乏来自Fc N-聚糖的核心岩藻糖残基的糖工程改造的抗体可表现出比岩藻糖基化同等物更强的ADCC。
本发明还提供产生根据本发明的抗体的方法,其包括以下步骤:a)培养包含含有如本文所述的分离的核酸的表达载体的重组宿主细胞,其中所述重组宿主细胞不包含α-1,6-岩藻糖基转移酶;和b)回收抗原结合蛋白。重组宿主细胞通常可不含编码α-1,6-岩藻糖基转移酶的基因(例如酵母宿主细胞,诸如毕赤酵母属)或可已被遗传修饰以使α-1,6-岩藻糖基转移酶失活。可获得已经遗传修饰以使编码α-1,6-岩藻糖基转移酶的FUT8基因失活的重组宿主细胞。参见例如可得自BioWa, Inc. (Princeton, N.J.)的POTELLIGENT™技术系统,其中缺乏FUT8基因的功能拷贝的CHOK1SV细胞产生具有增强的抗体依赖性细胞介导的细胞毒性(ADCC)活性的单克隆抗体,所述ADCC活性相对于在具有功能性FUT8基因的细胞中产生的相同单克隆抗体增加。POTELLIGENT™技术系统的方面描述于US7214775、US6946292、WO0061739和WO0231240中。本领域技术人员将显而易见,此类修饰不仅可单独使用,而且也可彼此组合使用,以进一步增强效应子功能。
本领域技术人员将显而易见,此类修饰不仅可单独使用,而且也可彼此组合使用,以进一步增强效应子功能。
具有修饰的糖基化的抗体的产生
在再一个实施方案中,本发明的抗体或抗原结合片段(例如14D7、26B10和其人源化版本)包含特定糖基化模式。例如,可制备无岩藻糖基化或无糖基化抗体或片段(即抗体分别缺乏岩藻糖或糖基化)。抗体或片段的糖基化模式可被改变,以例如增加抗体或片段对TIGIT抗原的亲和力或亲合力。此类修饰可通过例如改变抗体或片段序列内的一个或多个糖基化位点来实现。例如,可进行一个或多个氨基酸取代,其导致去除一个或多个可变区构架糖基化位点,由此消除该位点的糖基化。此类无糖基化可增加抗体或片段对抗原的亲和力或亲合力。参见例如美国专利号5,714,350和6,350,861。
本文公开的抗体和抗原结合片段(例如14D7、26B10和其人源化版本)可进一步包括在低级真核生物宿主细胞中产生的抗体和抗原结合片段,特别是真菌宿主细胞诸如酵母和丝状真菌已被遗传工程改造以产生具有哺乳动物或人类样糖基化模式的糖蛋白(参见例如Choi等人(2003) Proc. Natl. Acad. Sci. 100: 5022-5027;Hamilton等人,(2003)Science 301: 1244-1246;Hamilton等人,(2006) Science 313: 1441-1443;Nett等人,Yeast 28(3):237-52 (2011);Hamilton等人,Curr Opin Biotechnol. Oct;18(5):387-92(2007))。这些遗传修饰的宿主细胞相对于当前使用的哺乳动物细胞系的一个特定优势是能够控制在细胞中产生的糖蛋白的糖基化概况,使得可产生其中特定N-聚糖结构占优势的糖蛋白的组合物(参见例如美国专利号7,029,872和美国专利号7,449,308)。这些遗传修饰的宿主细胞已用于产生主要具有特定N-聚糖结构的抗体(参见例如Li等人(2006) Nat.Biotechnol. 24: 210-215)。
在具体实施方案中,本文公开的抗体和其抗原结合片段(例如14D7、26B10和其人源化版本)进一步包括在低级真核宿主细胞中产生的抗体和其抗原结合片段且其包含岩藻糖基化和未岩藻糖基化的杂合和复合N-聚糖,包括二等分和多天线物质,包括,但不限于,N-聚糖,诸如GlcNAc(1-4)Man3GlcNAc2;Gal(1-4)GlcNAc(1-4)Man3GlcNAc2;NANA(1-4)Gal(1-4)GlcNAc(1-4)Man3GlcNAc2。
在具体实施方案中,本文提供的抗体和其抗原结合片段(例如14D7、26B10和其人源化版本)包含具有至少一个选自以下的杂合N-聚糖的抗体和片段包含复合N-聚糖,其中至少50%、60%、70%、80%、90%、95%、97%、98%、99%或100%的复合N-聚糖包含结构NANA2Gal2GlcNAc2Man3GlcNAc2,其中此类结构被无岩藻糖基化。此类结构可例如在工程改造的巴斯德毕赤酵母宿主细胞中产生。
如本文所用,术语“N-聚糖”和“糖型”可互换使用且是指N-连接的寡糖,例如通过天冬酰胺-N-乙酰基葡糖胺键附接至多肽的天冬酰胺残基的N-连接的寡糖。N-连接的糖蛋白含有在蛋白中连接至天冬酰胺残基的酰胺氮的N-乙酰基葡糖胺残基。在糖蛋白上发现的主要糖为葡萄糖、半乳糖、甘露糖、岩藻糖、N-乙酰基半乳糖胺(GalNAc)、N-乙酰基葡糖胺(GlcNAc)和唾液酸(例如N-乙酰基-神经氨酸(NANA))。对于N-连接的糖蛋白,糖基团的处理与翻译同时在ER的内腔中发生,并在翻译后在高尔基体中继续。
N-聚糖具有Man3GlcNAc2 的常用五糖核心(“Man”是指甘露糖;“Glc”是指葡萄糖;且“NAc”是指N-乙酰基;GlcNAc是指N-乙酰基葡糖胺)。通常,N-聚糖结构以非还原末端在左边且还原性末端在右边来呈现。N-聚糖的还原性末端为附接至蛋白上包含糖基化位点的Asn残基的末端。N-聚糖在包含添加至Man3GlcNAc2 (“Man3”)核心结构(其也称为“三甘露糖核心”、“五糖核心”或“寡甘露糖”核心)的周围糖(例如GlcNAc、半乳糖、岩藻糖和唾液酸)的分枝(天线)数目方面不同。N-聚糖根据其分枝组分(例如高甘露糖、复合型或杂合型)分类。“高甘露糖”型N-聚糖具有五个或更多个甘露糖残基。“复合”型N-聚糖通常具有至少一个附接至“三甘露糖”核心的1,3甘露糖臂的GlcNAc和至少一个附接至“三甘露糖”核心的1,6甘露糖臂的GlcNAc。复合N-聚糖也可具有任选地被唾液酸或衍生物(例如“NANA”或“NeuAc”,其中“Neu”是指神经氨酸且“Ac”是指乙酰基)修饰的半乳糖(“Gal”)或N-乙酰基半乳糖胺(“GalNAc”)残基。复合N-聚糖也可具有包含“二等分”GlcNAc和核心岩藻糖(“Fuc”)的链内取代。复合N-聚糖也可在“三甘露糖核心”上具有多个天线,经常被称为“多天线聚糖”。“杂合”N-聚糖在三甘露糖核心的1,3甘露糖臂的末端上具有至少一个GlcNAc并在三甘露糖核心的1,6甘露糖臂上具有零或多个甘露糖。各种N-聚糖也称为“糖型”。
抗体物理特性
本文公开的抗体和其抗原结合片段(例如14D7、26B10和其人源化版本)可在轻链或重链免疫球蛋白可变区中进一步含有一个或多个糖基化位点。此类糖基化位点可导致增加的抗体或片段的免疫原性,或由于改变的抗原结合而改变抗体的pK(Marshall等人(1972) Annu Rev Biochem 41:673-702;Gala和Morrison (2004) J Immunol 172:5489-94;Wallick等人(1988) J Exp Med 168:1099-109;Spiro (2002) Glycobiology 12:43R-56R;Parekh等人(1985) Nature 316:452-7;Mimura等人(2000) Mol Immunol 37:697-706)。已知糖基化在含有N-X-S/T序列的基序进行。
各抗体或抗原结合片段(例如14D7、26B10或其人源化版本)将具有独特等电点(pI),其通常落在在6和9.5之间的pH范围内。IgG1抗体的pI通常落在7-9.5的pH范围内,且IgG4抗体的pI通常落在6-8的pH范围内。
各抗体或抗原结合片段(例如14D7、26B10或其人源化版本)将具有特征性熔融温度,其中较高熔融温度指示更大的体内整体稳定性(Krishnamurthy R和Manning MC(2002) Curr Pharm Biotechnol 3:361-71)。通常,TM1(初始解折叠温度)可超过60℃、超过65℃或超过70℃。抗体或片段的熔点可使用差示扫描量热法(Chen等人(2003) PharmRes 20:1952-60;Ghirlando等人(1999) Immunol Lett 68:47-52)或圆二色性(Murray等人(2002) J. Chromatogr Sci 40:343-9)测量。
在另一个实施方案中,选择不迅速降解的抗体和其抗原结合片段(例如14D7、26B10和其人源化版本)。可使用毛细管电泳(CE)和MALDI-MS测量抗体或片段的降解(Alexander AJ和Hughes DE (1995) Anal Chem 67:3626-32)。
在另一个实施方案中,选择具有最小聚集作用的抗体(例如14D7、26B10和其人源化版本)和其抗原结合片段,所述聚集作用可导致不必要免疫反应的触发和/或改变或不利的药代动力学特性。通常,聚集度为25%或更少、20%或更少、15%或更少、10%或更少或5%或更少的抗体和片段是可接受的。聚集可通过几种技术、包括尺寸排阻柱(SEC)、高效液相色谱(HPLC)和光散射来测量。
抗体缀合物
本文公开的抗TIGIT抗体和其抗原结合片段(例如14D7、26B10和其人源化版本)也可缀合至化学部分。化学部分可尤其为聚合物、放射性核素或细胞毒性因子。在具体实施方案中,化学部分是增加抗体或片段在个体体内的半衰期的聚合物。合适的聚合物包括,但不限于,亲水性聚合物,其包括,但不限于,聚乙二醇(PEG)(例如分子量为2kDa、5kDa、10kDa、12kDa、20kDa、30kDa或40kDa的PEG)、葡聚糖和单甲氧基聚乙二醇(mPEG)。Lee等人(1999)(Bioconj. Chem. 10:973-981)公开PEG缀合的单链抗体。Wen等人(2001) (Bioconj.Chem. 12:545-553)公开了用附接至放射金属螯合剂(二乙烯三胺五乙酸(DTPA))的PEG缀合抗体。
本文公开的抗体和其抗原结合片段(例如14D7、26B10和其人源化版本)也可用标记缀合,所述标记诸如99Tc,90Y、111In、32P、14C、125I、3H、131I、11C、15O、13N、18F、35S、51Cr、57To、226Ra、60Co、59Fe、57Se、152Eu、67CU、217Ci、211At、212Pb、47Sc、109Pd、234Th、and 40K、157Gd、55Mn、52Tr和56Fe。
本文公开的抗体和抗原结合片段(例如14D7、26B10和其人源化版本)也可聚乙二醇化,例如以增加其生物(例如血清)半衰期。为了将抗体或片段聚乙二醇化,通常使抗体或片段与聚乙二醇(PEG)的反应形式,诸如PEG的反应性酯或醛衍生物在其中一个或多个PEG基团变得附接至抗体或抗体片段的条件下反应。在具体实施方案中,聚乙二醇化经由与反应性PEG分子(或类似反应性水溶性聚合物)的酰化反应或烷基化反应进行。如本文所用,术语“聚乙二醇”意欲涵盖已用于衍生其它蛋白的任一种PEG形式,诸如单(C1-C10)烷氧基-或芳氧基-聚乙二醇或聚乙二醇-马来酰亚胺。在某些实施方案中,待聚乙二醇化的抗体或片段是无糖基化的抗体或片段。用于聚乙二醇化蛋白的方法是本领域中已知的,且可应用于本发明的抗体。参见例如EP 0 154 316和EP 0 401 384。
本文公开的抗体和抗原结合片段(例如14D7、26B10和其人源化版本)也可与荧光或化学发光标记缀合,所述标记包括荧光团,诸如稀土螯合物、荧光素和其衍生物、若丹明和其衍生物、异硫氰酸酯、藻红蛋白、藻蓝蛋白、别藻蓝蛋白、邻苯二甲醛、荧光胺、152Eu、丹磺酰基、伞酮、荧光素、鲁米那标记、异鲁米那标记、芳族吖啶酯标记、咪唑标记、吖啶盐标记、草酸酯标记、水母素标记、2,3-二氢酞嗪二酮、生物素/抗生素蛋白、旋转标记和稳定自由基。
本发明的抗体和其抗原结合片段(例如14D7、26B10和其人源化版本)也可缀合至细胞毒性因子,诸如白喉毒素、绿脓假单胞菌外毒素A链、蓖麻毒素A链、相思豆毒素A链、蒴莲素A链、α-八叠球菌、油桐(Aleurites fordii)蛋白和化合物(例如脂肪酸)、香石竹毒蛋白、美洲商陆(Phytoiacca americana)蛋白PAPI、PAPII和PAP-S、苦瓜(momordicacharantia)抑制剂、麻风树毒蛋白、巴豆毒素、肥皂草(saponaria officinalis)抑制剂、有丝分裂素(mitogellin)、局限曲菌素、酚霉素和伊诺霉素(enomycin)。
可采用本领域中已知的用于将本发明的抗体和其抗原结合片段(例如14D7、26B10和其人源化版本)缀合至各种部分的任何方法,包括由Hunter等人(1962) Nature 144:945;David等人(1974) Biochemistry 13:1014;Pain等人(1981) J. Immunol. Meth. 40:219;和Nygren, J., (1982) Histochem. and Cytochem. 30:407描述的方法。用于缀合抗体和片段的方法是本领域中常规和非常众所周知的。
抗TIGIT抗体的治疗用途
进一步提供用于治疗需要用本文公开的分离的抗体或其抗原结合片段(例如14D7、26B10和其人源化版本)治疗的个体、包括人类个体的方法。在本发明的一个实施方案中,此类个体患有感染或感染性疾病。在本发明的另一个实施方案中,此类个体患有癌症。在一个实施方案中,癌症是通过表达TIGIT的肿瘤浸润性淋巴细胞浸润的实体瘤。在一个实施方案中,癌症是例如骨肉瘤、横纹肌肉瘤、神经母细胞瘤、肾癌、白血病、肾移行细胞癌、膀胱癌、维尔姆氏癌(Wilm’s cancer)、卵巢癌、胰脏癌、乳癌、前列腺癌、骨癌、肺癌(例如非小细胞肺癌)、胃癌、结肠直肠癌、子宫颈癌、滑膜肉瘤、头颈癌、鳞状细胞癌、多发性骨髓瘤、肾细胞癌、视网膜母细胞瘤、肝母细胞瘤、肝细胞癌、黑色素瘤、肾横纹肌样瘤、尤因氏肉瘤(Ewing’s sarcoma)、软骨肉瘤、脑癌、胶质母细胞瘤、脑膜瘤、垂体腺瘤、前庭神经鞘瘤、原始神经外胚层瘤、成神经管细胞瘤、星形细胞瘤、退行性星形细胞瘤、少突神经胶质瘤、室管膜瘤、脉络丛乳头状瘤、真性红细胞增多症、血小板增多症、特发性骨髓纤维化、软组织肉瘤、甲状腺癌、子宫内膜癌、类癌瘤癌或肝癌、乳癌或胃癌。在本发明的一个实施方案中,癌症是转移性癌症,例如上述种类的转移性癌症。
在一个实施方案中,本发明提供使用本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10和其人源化版本)治疗个体的方法,其中所述个体患有病毒感染。在一个实施方案中,所述病毒感染是被选自以下的病毒感染:人类免疫缺乏病毒(HIV)、肝炎病毒(A、B或C)、疱疹病毒(例如VZV、HSV-I、HAV-6、HSV-II和CMV、Epstein-Barr病毒)、腺病毒、流感病毒、黄病毒、艾柯病毒、鼻病毒、柯萨奇病毒、冠状病毒、呼吸道合胞病毒、腮腺炎病毒、轮状病毒、麻疹病毒、风疹病毒、细小病毒、牛痘病毒、HTLV病毒、登革热病毒、乳头状瘤病毒、软疣病毒、脊髓灰质炎病毒、狂犬病病毒、JC病毒或虫媒病毒性脑炎病毒。
在一个实施方案中,本发明提供使用本发明的抗TIGIT抗体或其抗原结合片段治疗个体的方法,其中所述个体患有细菌感染。在一个实施方案中,细菌感染是被选自以下的细菌感染:衣原体(Chlamydia)、立克次体细菌(rickettsial bacteria)、分枝杆菌(mycobacteria)、葡萄球菌(staphylococci)、链球菌(streptococci)、肺炎球菌(pneumonococci)、脑膜炎球菌(meningococci)和淋球菌(gonococci)、克雷伯氏菌(klebsiella)、变形杆菌(proteus)、沙雷氏菌属(serratia)、假单胞菌(pseudomonas)、军团杆菌属(Legionella)、白喉棒状杆菌(Corynebacterium diphtheriae)、沙门氏菌(Salmonella)、芽孢杆菌(bacilli)、霍乱弧菌(Vibrio cholerae)、破伤风梭菌(Clostridium tetan)、肉毒梭状芽孢杆菌(Clostridium botulinum)、炭疽芽孢杆菌(Bacillus anthricis)、鼠疫耶尔森菌(Yersinia pestis)、麻风分支杆菌(Mycobacteriumleprae)、弥漫型麻风分枝杆菌(Mycobacterium lepromatosis)和包柔氏螺旋体(Borriella)。
在一个实施方案中,本发明提供使用本发明的抗TIGIT抗体或其抗原结合片段治疗个体的方法,其中所述个体患有真菌感染。在一个实施方案中,真菌感染是被选自以下的真菌感染:念珠菌属(Candida)(白色念珠菌(albicans)、克鲁斯氏念珠菌(krusei)、光滑念珠菌(glabrata)、热带念珠菌(tropicalis)等)、新型隐球菌(Cryptococcus neoformans)、曲霉菌属(Aspergillus)(烟曲霉(fumigatus)、黑曲霉(niger)等)、毛霉菌属(GenusMucorales)(白霉菌属(mucor)、犁头霉属(absidia)、根霉菌属(rhizopus))、申克氏胞丝菌(Sporothrix schenkii)、皮炎芽生菌(Blastomyces dermatitidis)、巴西副球孢子菌(Paracoccidioides brasiliensis)、粗球孢子菌(Coccidioides immitis)和荚膜组织胞浆菌(Histoplasma capsulatum)。
在一个实施方案中,本发明提供使用本发明的抗TIGIT抗体或其抗原结合片段治疗个体的方法,其中所述个体患有寄生虫感染。在一个实施方案中,寄生虫感染是被选自以下的寄生虫感染:溶组织内阿米巴(Entamoeba histolytica)、结肠小袋纤毛虫(Balantidium coli)、福氏纳格里阿米巴原虫(Naegleria fowleri)、棘阿米巴虫属(Acanthamoeba)、篮氏贾第鞭毛虫(Giardia lambia)、隐胞子虫属(Cryptosporidium)、卡氏肺孢子虫(Pneumocystis carinii)、间日疟原虫(Plasmodium vivax)、微小巴贝虫(Babesia microti)、布氏锥虫(Trypanosoma brucei)、克氏锥虫(Trypanosoma cruzi)、杜氏利什曼原虫(Leishmania donovani)、刚地弓形虫(Toxoplasma gondii)和巴西日圆线虫(Nippostrongylus brasiliensis)。
另外,本发明提供在个体(例如人类)中防止或抑制TIGIT结合MHC II类、增强抗原特异性T细胞活化或刺激白介素-2的T细胞产生的方法,例如其中所述个体患有癌症或感染性疾病(例如如本文中所讨论),所述方法包括施用有效量的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10和其人源化版本),其任选地与另一化学治疗剂联合。
“个体”可以是哺乳动物,诸如人类、犬、猫、马、牛、小鼠、大鼠、猴(例如食蟹猴,例如食蟹猴)或兔。在本发明的优选实施方案中,所述个体为人类个体。
在具体实施方案中,本文公开的抗体或其抗原结合片段(例如14D7、26B10和其人源化版本)可单独或与其它另外治疗剂和/或治疗程序联合使用,用于治疗或预防需要此类治疗或预防的个体中的任何疾病诸如癌症,例如如本文中所讨论。包含此类抗体和片段与另外治疗剂联合的组合物,例如包含药学上可接受的载体的药物组合物,也是本发明的一部分。
在具体实施方案中,本文公开的抗体或其抗原结合片段(例如14D7、26B10和其人源化版本)可单独或与肿瘤疫苗联合使用。
在具体实施方案中,本文公开的抗体或其抗原结合片段(例如14D7、26B10和其人源化版本)可单独或与化学治疗剂联合使用。
在具体实施方案中,本文公开的抗体或其抗原结合片段(例如14D7、26B10和其人源化版本)可单独或与放射疗法联合使用。
在具体实施方案中,本文公开的抗体或其抗原结合片段(例如14D7、26B10和其人源化版本)可单独或与靶向疗法联合使用。靶向疗法的实例包括:激素疗法、信号转导抑制剂(例如EGFR抑制剂,诸如西妥昔单抗(Erbitux)和埃罗替尼(Tarceva));HER2抑制剂(例如曲妥珠单抗(Herceptin)和帕妥珠单抗(Perjeta));BCR-ABL抑制剂(诸如伊马替尼(Gleevec)和达沙替尼(Sprycel));ALK抑制剂(诸如克里唑替尼(Xalkori)和色瑞替尼(Zykadia));BRAF抑制剂(诸如维罗非尼(Zelboraf)和达拉菲尼(Tafinlar))、基因表达调节剂、细胞凋亡诱导剂(例如硼替佐米(Velcade)和卡非佐米(Kyprolis))、血管生成抑制剂(例如贝伐单抗(Avastin)和雷莫芦单抗(Cyramza))、附接至毒素的单克隆抗体(例如brentuximab vedotin (Adcetris)和阿多曲妥珠单抗恩他新(ado-trastuzumabemtansine)(Kadcyla))。
在具体实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10和其人源化版本)可与抗癌治疗剂或免疫调节药物,诸如免疫调节受体抑制剂,例如特异性结合受体的抗体或其抗原结合片段组合使用。
因此,本发明包括包含本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10和其人源化版本)与派姆单抗联合的组合物;以及用于治疗或预防个体中的癌症的方法,其包括向所述个体施用有效量的抗TIGIT抗体或其抗原结合片段和派姆单抗。任选地,所述个体还施用另一治疗剂。
在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10和其人源化版本)与含有包含SEQ ID NO:36的氨基酸序列的免疫球蛋白重链和包含SEQ ID NO:37的氨基酸序列的免疫球蛋白轻链的分离的抗体联合。SEQ ID NO:36和37编码派姆单抗的重链和轻链。
在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10和其人源化版本)与含有包含SEQ ID NO:38的氨基酸序列的免疫球蛋白重链和包含SEQ ID NO:39的氨基酸序列的免疫球蛋白轻链的分离的抗体联合。SEQ ID NO:38和39编码尼鲁单抗的重链和轻链。
在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10和其人源化版本)与以下中的一种或多种联合:抗PD1抗体(例如派姆单抗、尼鲁单抗、皮立珠单抗(pidilizumab)(CT-011))、抗PDL1抗体、抗CTLA4抗体、抗CS1抗体(例如埃罗妥珠单抗(elotuzumab))、抗KIR2DL1/2/3抗体(例如利瑞鲁单抗(lirilumab))、抗CD137抗体(例如乌鲁单抗(urelumab))、抗GITR抗体(例如TRX518)、抗PD-L1抗体(例如BMS-936559、MSB0010718C或MPDL3280A)、抗PD-L2抗体、抗ILT1抗体、抗ILT2抗体、抗ILT3抗体、抗ILT4抗体、抗ILT5抗体、抗ILT6抗体、抗ILT7抗体、抗ILT8抗体、抗CD40抗体、抗OX40抗体、抗ICOS、抗SIRPα、抗KIR2DL1抗体、抗KIR2DL2/3抗体、抗KIR2DL4抗体、抗KIR2DL5A抗体、抗KIR2DL5B抗体、抗KIR3DL1抗体、抗KIR3DL2抗体、抗KIR3DL3抗体、抗NKG2A抗体、抗NKG2C抗体、抗NKG2E抗体、抗4-1BB抗体(例如PF-05082566)、抗TSLP抗体、抗IL-10抗体、IL-10或聚乙二醇化的IL-10或此类靶标的任何小有机分子抑制剂。
在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与抗PD1抗体联合。在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与抗PDL1抗体(例如BMS-936559、MSB0010718C或MPDL3280A)联合。在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与抗CTLA4抗体联合。在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与抗CS1抗体联合。在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与抗KIR2DL1/2/3抗体联合。在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与抗CD137(例如乌鲁单抗(urelumab))抗体联合。在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与抗GITR(例如TRX518)抗体联合。在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与抗PD-L2抗体联合。在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与抗ITL1抗体联合。在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与抗ITL2抗体联合。在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与抗ITL3抗体联合。在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与抗ITL4抗体联合。在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与抗ITL5抗体联合。在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与抗ITL6抗体联合。在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与抗ITL7抗体联合。在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与抗ITL8抗体联合。在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与抗CD40抗体联合。在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与抗OX40抗体联合。在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与抗KIR2DL1抗体联合。在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与抗KIR2DL2/3抗体联合。在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与抗KIR2DL4抗体联合。在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或或其人源化版本)与抗KIR2DL5A抗体联合。在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与抗KIR2DL5B抗体联合。在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与抗KIR3DL1抗体联合。在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与抗KIR3DL2抗体联合。在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与抗KIR3DL3抗体联合。在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与抗NKG2A抗体联合。在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与抗NKG2C抗体联合。在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与抗ICOS抗体联合。在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与抗SIRPα抗体联合。在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与抗4-1BB抗体联合。在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与抗IL-10抗体联合。在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与抗TSLP抗体联合。在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与IL-10或聚乙二醇化IL-10联合。
在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与诸如以下的抑制剂(例如小有机分子或抗体或其抗原结合片段)中的一种或多种联合:MTOR(哺乳动物雷帕霉素靶标)抑制剂、细胞毒性剂、铂剂、EGFR抑制剂、VEGF抑制剂、微管稳定剂、紫杉烷、CD20抑制剂、CD52抑制剂、CD30抑制剂、RANK(核因子κ-B的受体活化物)抑制剂、RANKL(核因子κ-B配体的受体活化物)抑制剂、ERK抑制剂、MAP激酶抑制剂、AKT抑制剂、MEK抑制剂、PI3K抑制剂、HER1抑制剂、HER2抑制剂、HER3抑制剂、HER4抑制剂、Bcl2抑制剂、CD22抑制剂、CD79b抑制剂、ErbB2抑制剂或法呢基蛋白转移酶抑制剂。
在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与以下中的任何一种或多种联合:13-顺-视黄酸、(3-[5-(甲基磺酰基哌啶甲基)-吲哚基]-喹诺酮)、4-羟基他莫昔芬、5-脱氧尿苷、5'-脱氧-5-氟尿苷、5-氟尿嘧啶、6-巯基嘌呤、7-羟基星孢菌素、A-443654、醋酸阿比特龙、abraxane、ABT-578、阿考比芬、ADS-100380、ALT-110、六甲蜜胺、阿米福汀、氨鲁米特、氨柔比星、安吖啶、阿那格雷、阿那曲唑、血管生长抑制因子、AP-23573、ARQ-197、阿佐昔芬、AS-252424、AS-605240、天冬酰胺酶、AT-9263、阿曲生坦、阿西替尼、AZD1152、卡介(Bacillus Calmette-Guerin,BCG)疫苗、batabulin、BC-210、besodutox、贝伐单抗、比卡鲁胺、Bio111、BIO140、博莱霉素、BMS-214662、BMS-247550、BMS-275291、BMS-310705、硼替佐米、布舍瑞林、白消安、骨化三醇、喜树碱、卡奈替尼、卡培他滨、卡铂、卡莫司汀、CC8490、西地尼布、CG-1521、CG-781、查米多星(chlamydocin)、苯丁酸氮芥、氯毒素、西仑吉肽、西米替丁、顺铂、克拉屈滨、氯屈膦酸盐、COL-3、CP-724714、环磷酰胺、环丙孕酮、醋酸环丙氯地孕酮、阿糖胞苷(cytarabine)、阿糖胞苷(cytosinearabinoside)、达卡巴嗪、达西司特、放线菌素D、dalotuzumab、达鲁舍替、达沙替尼(dasatanib)、道诺霉素、地卡塔尼(decatanib)、鱼藤素、地尼白介素、脱氧柯福霉素、缩酚肽、二芳基丙腈、二乙基己烯雌酚、diftitox、多西他赛、多韦替尼、阿霉素、屈洛昔芬、艾特咔林(edotecarin)、钇90标记的艾多替德(yttrium-90 labeled-edotreotide)、艾多替德(edotreotide)、EKB-569、EMD121974、内皮抑素、恩杂鲁胺、enzastaurin、表柔比星、埃博霉素B、ERA-923、Erbitux、埃罗替尼、雌二醇、雌氮芥、依托泊苷、依维莫司、依西美坦、ficlatuzumab、非那雄胺、夫拉平度、氟尿苷、氟达拉宾、氟氢可的松、氟甲睾酮、氟他胺、FOLFOX方案、氟维司群、galeterone、吉非替尼、吉西他滨、吉马替康、戈舍瑞林、乙酸戈舍瑞林、棉酚、GSK461364、GSK690693、HMR-3339、己酸羟孕酮、羟基脲、IC87114、伊达比星、idoxyfene、异环磷酰胺、IM862、伊马替尼、IMC-1C11、INCB24360、INO1001、干扰素、白介素-12、伊匹单抗、伊立替康、JNJ-16241199、酮康唑、KRX-0402、拉帕替尼、拉索昔芬、来曲唑、甲酰四氢叶酸、亮丙瑞林、乙酸亮丙瑞林、左旋咪唑、脂质体包覆的紫杉醇、洛莫司汀、洛那法尼、硫蒽酮、LY292223、LY292696、LY293646、LY293684、LY294002、LY317615、马立马司他、氮芥(mechlorethamine)、甲羟孕酮乙酸酯、甲地孕酮乙酸酯、美法仑、巯基嘌呤、美司钠、甲氨蝶呤、光神霉素、丝裂霉素、米托坦、米托蒽醌、陶扎色替、MLN8054、癌立消(neovastat)、来那替尼、neuradiab、尼罗替尼、nilutimide、诺拉曲特、NVP-BEZ235、oblimersen、奥曲肽、奥法木单抗、奥戈伏单抗、orteronel、奥沙利铂、紫杉醇、帕博西尼、帕米膦酸盐、帕尼单抗、帕唑帕尼、PD0325901、PD184352、PEG-干扰素、培美曲塞、喷司他丁、哌立福新、苯丙氨酸氮芥、PI-103、pictilisib、PIK-75、哌喷昔芬、PKI-166、普卡霉素、卟吩姆(porfimer)、泼尼松、丙卡巴肼、孕酮、PX-866、R-763、雷洛昔芬、雷替曲塞、razoxin、地磷莫司、利妥昔单抗、罗米地辛、RTA744、鲁比替康、scriptaid、Sdx102、seliciclib、司美替尼、司马沙尼(semaxanib)、SF1126、西罗莫司、SN36093、索拉非尼、螺内酯、角鲨胺、SR13668、链脲菌素、SU6668、辛二酰苯胺异羟肟酸(suberoylanalide hydroxamic acid)、舒尼替尼、合成雌激素、他仑帕奈、塔利拉维(talimogene laherparepvec)、他莫昔芬、替莫唑胺、坦罗莫司、替尼泊苷、替米利芬、睾酮(testosterone)、粉防己碱(tetrandrine)、TGX-221、沙利多胺、硫鸟嘌呤、噻替派、替西单抗(ticilimumab)、替吡法尼、替沃扎尼(tivozanib)、TKI-258、TLK286、拓朴替康、柠檬酸托瑞米芬、曲贝替定、曲妥珠单抗、维甲酸、曲古抑菌素A、磷酸曲西立滨单水合物、双羟萘酸曲普瑞林、TSE-424、尿嘧啶氮芥、丙戊酸、戊柔比星、凡德他尼、瓦他拉尼(vatalanib)、VEGF捕获物、长春花碱、长春新碱、长春地辛、长春瑞滨、vitaxin、vitespan、伏立诺他(vorinostat)、VX-745、渥曼青霉素、Xr311、zanolimumab、ZK186619、ZK-304709、ZM336372、ZSTK474。
在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与一种或多种止吐药联合,所述止吐药包括,但不限于:卡索匹坦(GlaxoSmithKline)、奈妥吡坦(Netupitant)(MGI-Helsinn)和其它NK-1受体拮抗剂、帕洛诺司琼(由MGI Pharma作为Aloxi销售)、阿瑞匹坦(由Merck and Co.作为Emend销售;Rahway, NJ)、苯海拉明(由Pfizer作为Benadryl®销售;New York, NY)、安泰乐(由Pfizer作为Atarax®销售;New York, NY)、甲氧氯普胺(由AH Robins Co.作为Reglan®销售;Richmond, VA)、劳拉西泮(由Wyeth作为Ativan®销售;Madison, NJ)、阿普唑仑(由Pfizer作为Xanax®销售;New York, NY)、氟哌啶醇(由Ortho-McNeil作为Haldol®销售;Raritan, NJ)、氟哌利多(Inapsine®)、屈大麻酚(由Solvay Pharmaceuticals, Inc.作为Marinol®销售;Marietta,GA)、地塞米松(由Merck and Co.作为Decadron®销售;Rahway,NJ)、甲基泼尼龙(由Pfizer作为Medrol®销售;New York, NY);丙氯拉嗪(由Glaxosmithkline作为Compazine®销售;Research Triangle Park, NC)、格拉司琼(由Hoffmann-La Roche Inc.作为Kytril®销售;Nutley, NJ)、昂丹司琼(由Glaxosmithkline作为Zofran®销售;Research Triangle Park, NC)、多拉司琼(由Sanofi-Aventis作为Anzemet®销售;New York, NY)、托烷司琼(由Novartis作为Navoban®销售;EastHanover, NJ)。
癌症治疗的其它副作用包括红细胞和白细胞缺乏。因此,在本发明的一个实施方案中,抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与治疗或预防此类缺乏的药剂(诸如非格司亭(filgrastim)、PEG-非格司亭、红细胞生成素、阿法依泊汀(epoetin alfa)或阿法达贝泊汀(darbepoetin alfa))联合。
在本发明的一个实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)与抗癌放射疗法联合施用。例如,在本发明的一个实施方案中,放射疗法为外部束疗法(EBT):用于递送一束高能X射线至肿瘤位置的方法。所述束在患者外面产生(例如通过线性加速器)且靶向在肿瘤部位。这些X射线可破坏癌细胞且小心的治疗计划允许绕过周围正常组织。不将放射性源置于患者体内。在本发明的一个实施方案中,放射疗法是质子束疗法:以质子代替X-射线轰击患病组织的一种类型的适形疗法。在本发明的一个实施方案中,放射疗法是适形外部束放射疗法:使用先进技术将放射疗法针对个体身体结构调整的程序。在本发明的一个实施方案中,放射疗法为短程疗法:放射性物质暂时置于体内,通常用以将超剂量或增强剂量的放射给予区域。
在本发明的一个实施方案中,与抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)联合施用的手术程序是手术肿瘤切除术。
术语“联合”指示在本发明的方法中施用的组分(例如抗TIGIT抗体(例如人源化抗体)或其抗原结合片段(例如14D7、26B10或其人源化版本)连同派姆单抗)可配制成单一组合物以同时递送,或分开配制成两种或更多种组合物(例如试剂盒)。各组分可在不同于施用其它组分的时间向个体施用;例如,每次施用可经给定时间段以几种时间间隔非同时给予(例如分开或依次)。此外,分开的组分可通过相同或不同途径向个体施用。
实验和诊断用途
本文公开的抗TIGIT抗体和其抗原结合片段(例如14D7、26B10和其人源化版本)可用作亲和力纯化试剂。在该过程中,抗TIGIT抗体和其抗原结合片段使用本领域中众所周知的方法固定在固相诸如Sephadex、玻璃或琼脂糖树脂或滤纸上。使固定抗体或片段与待纯化的含有TIGIT蛋白(或其片段)的样品接触,且此后将支持物用合适溶剂洗涤,其将去除除结合固定的抗体或片段的TIGIT蛋白外的样品中实质上所有物质。最终,将支持物用洗脱结合的TIGIT的溶剂(例如蛋白A)洗涤。此类固定抗体和片段形成本发明的一部分。
进一步提供用于产生可用于例如进行Western印迹和本文中讨论的其它免疫测定的二级抗体的抗原。具体而言,公开包含本文公开的治疗抗体(例如14A6、28H5或31C6)的可变区和/或CDR序列且可用于产生用于特异性检测例如在治疗背景下抗体存在的抗独特型抗体的多肽。
抗TIGIT抗体(例如人源化抗体)和其抗原结合片段也可用于TIGIT蛋白的诊断测定中,例如检测其在特定细胞、组织或血清,例如肿瘤细胞,诸如黑色素瘤细胞中的表达。此类诊断方法可用于各种疾病诊断。
本发明包括ELISA测定(酶联免疫吸附测定法),其并入本文公开的抗TIGIT抗体或其抗原结合片段(例如14A6或其人源化版本)的使用。
例如,此类方法包括以下步骤:
(a)用抗TIGIT抗体或其抗原结合片段包被基板(例如微量滴定板孔的表面,例如塑料板);
(b)将待测试TIGIT的存在的样品施加至基板;
(c)洗涤该板,使得去除样品中未结合的物质;
(d)施加也对TIGIT抗原特异性的可检测标记的抗体(例如酶联抗体);
(e)洗涤该基板,使得去除未结合的标记抗体;
(f)如果酶联标记的抗体,则施加通过酶转化成荧光信号的化学物质;以及
(g)检测标记抗体的存在。
检测与基板缔合的标记指示TIGIT蛋白的存在。
在另一个实施方案中,标记的抗体或其抗原结合片段用过氧化酶标记,所述过氧化酶与ABTS(例如2,2’-次偶氮基-双(3-乙基苯并噻唑啉-6-磺酸))或3,3’,5,5’-四甲基联苯胺反应,以产生可检测的颜色变化。或者,标记的抗体或片段用可检测的放射性同位素(例如3H)标记,所述放射性同位素可通过闪烁计数器在闪烁体存在的情况下检测。
本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)可用于Western印迹或免疫-蛋白印迹程序中。此类程序形成本发明的一部分且包括例如:
(1)任选地使用本领域中已知的方法(例如半干印迹法或罐印迹法)从待测试TIGIT的存在的样品(例如从样品中蛋白的PAGE或SDS-PAGE电泳分离)转移蛋白至膜或其它固体基板上;使待测试结合的TIGIT或其片段的存在的膜或其它固体基板与本发明的抗TIGIT抗体或其抗原结合片段接触。
此类膜可采取硝酸纤维素或基于乙烯基的(例如聚偏二氟乙烯(PVDF))膜的形式,待在非变性PAGE(聚丙烯酰胺凝胶电泳)凝胶或SDS-PAGE(十二烷基硫酸钠聚丙烯酰胺凝胶电泳)凝胶中测试TIGIT的存在的蛋白已转移至该膜 (例如在凝胶中电泳分离后)。在膜与抗TIGIT抗体或片段接触前,该膜任选地用例如脱脂奶粉等封闭以便结合膜上的非特异性蛋白结合位点。
(2)将膜洗涤一次或多次以去除未结合的抗TIGIT抗体或片段和其它未结合的物质;和
(3)检测结合的抗TIGIT抗体或片段。
结合的抗体或片段的检测指示TIGIT蛋白存在于膜或基板上和样品中。合的抗体或片段的检测可通过抗体或片段与可检测标记的二级抗体(一种抗免疫球蛋白抗体)结合,且然后检测二级抗体的存在。
本文公开的抗TIGIT抗体和其抗原结合片段(例如14D7、26B10和其人源化版本)也可用于免疫组织化学。此类方法形成本发明的一部分且包含例如:
(1)使待测试TIGIT蛋白的存在的细胞(例如肿瘤细胞,诸如黑色素瘤细胞)与本发明的抗TIGIT抗体或其抗原结合片段接触;和
(2)检测细胞上或细胞中的抗体或片段。
如果可检测标记抗体或片段本身,则其可直接检测。或者,抗体或片段可由可检测标记的二级抗体结合,检测所述二级抗体。
某些本文公开的抗TIGIT抗体和其抗原结合片段(例如14D7、26B10和其人源化版本)也可用于体内肿瘤成像。此类方法可包括将放射性标记的抗TIGIT抗体或其抗原结合片段注射至待测试与TIGIT表达相关的肿瘤(例如其例如在肿瘤细胞表面上表达TIGIT)的存在的患者体内,随后对患者身体进行核成像,以检测例如包含结合肿瘤的高浓度抗体或片段的位点上标记的抗体或片段的存在。位点的检测指示TIGIT+肿瘤和肿瘤细胞的存在。
成像技术包括SPECT成像(单光子发射计算机断层摄影术)或PET成像(正电子发射断层摄影术)。标记包括例如碘-123(123I)和锝-99m(99mTc),例如结合SPECT成像或 11C、13N、15O或18F,例如结合PET成像或铟-111(参见例如Gordon等人,(2005) International Rev.Neurobiol. 67:385-440)。
药物组合物和施用
为了制备本发明的抗TIGIT抗体和抗原结合片段(例如14D7、26B10和其人源化版本)的药物或无菌组合物,将抗体或其抗原结合片段与药学上可接受的载体或赋形剂混合。参见例如 Remington’s Pharmaceutical Sciences and U.S. Pharmacopeia: NationalFormulary, Mack Publishing Company, Easton, PA (1984)。
治疗和诊断剂的制剂可通过以例如冻干粉末、浆液、水性溶液或悬浮液的形式与可接受的载体、赋形剂或稳定剂混合来制备(参见例如Hardman等人(2001) Goodman andGilman’s The Pharmacological Basis of Therapeutics, McGraw-Hill, New York,NY; Gennaro (2000) Remington: The Science and Practice of Pharmacy,Lippincott, Williams, and Wilkins, New York, NY; Avis, 等人(编辑) (1993)Pharmaceutical Dosage Forms: Parenteral Medications, Marcel Dekker, NY;Lieberman, 等人(编辑) (1990) Pharmaceutical Dosage Forms: Tablets, MarcelDekker, NY; Lieberman, 等人(编辑) (1990) Pharmaceutical Dosage Forms:Disperse Systems, Marcel Dekker, NY; Weiner和Kotkoskie (2000) ExcipientToxicity and Safety, Marcel Dekker, Inc., New York, NY)。
单独或与另一治疗剂组合施用的本发明抗体的毒性和治疗功效可通过标准药物程序在细胞培养物或实验动物中测定,例如测定LD50(群体的50%致死的剂量)和ED50 (群体的50%中治疗有效的剂量)。毒性和治疗作用之间的剂量比率为治疗指数(LD50/ ED50)。从这些细胞培养物测定和动物研究获得的数据可用于配制用于人类的剂量范围。此类化合物的剂量优选在循环浓度的范围内,其包括活性很小或无毒性的ED50。剂量可根据所采用的剂型和施用途径而在该范围内变化。
在另一个实施方案中,根据Physicians’ Desk Reference 2003 (ThomsonHealthcare;第57版(2002年11月1日))另一治疗剂与本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10)联合向个体施用。
施用模式可变化。施用途径包括经口、直肠、经粘膜、经肠、肠胃外;肌肉内、皮下、皮内、髓内、鞘内、直接心室内、静脉内、腹膜内、鼻内、眼内、吸入、吹入、局部、皮肤、经皮或动脉内。
在具体实施方案中,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10和其人源化版本)可通过侵袭性途径、诸如通过注射来施用。在本发明的其它实施方案中,抗TIGIT抗体或其抗原结合片段或其药物组合物静脉内、皮下、肌肉内、动脉内、瘤内或通过吸入、气溶胶递送来施用。通过非侵袭性途径(例如经口;例如在丸剂、胶囊或锭剂中)施用也在本发明的范围内。
本发明提供容器(例如塑料或玻璃小瓶,例如具有盖或色谱柱、中空孔针或注射器圆筒),其包含任一本发明的抗体或抗原结合片段(例如14D7、26B10和其人源化版本)或其药物组合物。本发明还提供注射装置,其包含任一本发明的抗体或抗原结合片段(例如14D7、26B10和其人源化版本)或其药物组合物。注射装置是经由肠胃外途径,例如肌肉内、皮下或静脉内,将物质引入患者体内的装置。例如,注射装置可以是注射器(例如预填充有药物组合物,诸如自动注射器),其例如包括用于容纳待注射的流体(例如抗体或片段或其药物组合物)的针筒或圆筒、用于刺穿皮肤和/或血管以注射流体的针;以及用于推动流体从针筒出来且穿过针孔的栓塞。在本发明的一个实施方案中,包含本发明的抗体或其抗原结合片段或其药物组合物的注射装置为静脉内(IV)注射装置。此类装置包括套管或套管针/针中的抗体或片段或其药物组合物,所述套管或套管针/针可附接至管,所述管可附接至用于容纳通过套管或套管针/针引入患者体内的流体(例如盐水;或包含NaCl、乳酸钠、KCl、CaCl2且任选地包括葡萄糖的乳酸化林格氏溶液)的袋子或储器。在本发明的一个实施方案中,一旦将套管针和套管插入个体静脉中,抗体或片段或其药物组合物可引入装置中,且从插入套管移除套管针。IV装置可例如插入周围静脉(例如手或臂中);上腔静脉或下腔静脉,或心脏右心房内(例如中央IV);或锁骨下、颈内静脉或股静脉,且例如前进至心脏,直至其达到上腔静脉或右心房(例如中央静脉)。在本发明的一个实施方案中,注射装置为自动注射器;喷射注射器或外部输注泵。喷射喷射器使用液体的高压狭窄喷射,其穿透表皮层以将抗体或片段或其药物组合物引入患者体内。外部输注泵为将抗体或片段或其药物组合物以受控量递送至患者体内的医学装置。外部输注泵可以是电动或机械动力的。不同泵以不同方式操作,例如注射泵保持流体在注射器储器中,且可移动活塞控制流体递送,弹性泵保持流体在可拉伸的气球储器中,且来自气球的弹性壁的压力驱动流体递送。在蠕动泵中,一组滚筒在柔性导管长度上向下挤压,推动流体向前。在多通道泵中,流体可从多个储器以多个速率递送。
本文公开的药物组合物也可用无针皮下注射装置施用;诸如美国专利号6,620,135;6,096,002;5,399,163;5,383,851;5,312,335;5,064,413;4,941,880;4,790,824或4,596,556中公开的装置。此类包含药物组合物的无针装置也是本发明的一部分。本文公开的药物组合物也可通过输注施用。众所周知用于施用药物组合物的植入物和模块的实例包括以下中公开的那些:美国专利号4,487,603,其公开以受控速率分配药物的可植入微输注泵;美国专利号4,447,233,其公开以精确输注速率递送药物的药物输注泵;美国专利号4,447,224,其公开用于连续药物递送的可变流量可植入输注设备;美国专利号4,439,196,其公开具有多腔室隔室的渗透药物递送系统。 许多其它此类植入物、递送系统和模块是本领域技术人员众所周知的,且包含本发明的药物组合物的那些植入物、递送系统和模块在本发明的范围内。
或者,可以局部而非全身性方式,例如经由直接注射抗体或片段至肿瘤,例如TIGIT+肿瘤来施用本发明的抗TIGIT抗体或抗原结合片段(例如14D7、26B10或其人源化版本)。此外,可在靶向药物递送系统中,例如在用靶向例如肿瘤,例如TIGIT+肿瘤(例如通过免疫病理学表征)的组织特异性抗体包被的脂质体中施用所述抗体或片段。将脂质体靶向至患病组织且通过患病组织选择性吸收。此类方法和脂质体是本发明的一部分。
施用方案取决于几个因素,包括治疗抗体或抗原结合片段的血清或组织转换率、症状水平、治疗抗体的免疫原性和生物基质中靶细胞的可接近性。优选地,施用方案递送足够治疗抗体或片段以实现目标疾病状况的改善,同时最小化不希望的副作用。因此,递送的生物制剂的量部分地取决于特定治疗抗体和所治疗的病况的严重程度。可获得关于选择治疗抗体或片段的适当剂量的指导(参见例如Wawrzynczak (1996) Antibody Therapy,Bios Scientific Pub. Ltd, Oxfordshire, UK; Kresina (编辑) (1991) MonoclonalAntibodies, Cytokines and Arthritis, Marcel Dekker, New York, NY; Bach (编辑)(1993) Monoclonal Antibodies and Peptide Therapy in Autoimmune Diseases,Marcel Dekker, New York, NY; Baert, 等人 (2003) New Engl. J. Med. 348:601-608; Milgrom 等人(1999) New Engl. J. Med. 341:1966-1973; Slamon et al. (2001)New Engl. J. Med. 344:783-792; Beniaminovitz 等人(2000) New Engl. J. Med.342:613-619; Ghosh等人 (2003) New Engl. J. Med. 348:24-32; Lipsky等人(2000)New Engl. J. Med. 343:1594-1602)。
适当剂量的测定通过临床医师,例如使用本领域中已知或怀疑影响治疗的参数或因素进行。通常,剂量以略小于最佳剂量的量开始,且其随后以较小增量增加,直至相对于任何负面的副作用实现所要或最佳作用。重要的诊断量度包括例如炎症的症状或所产生炎性细胞因子的水平的量度。通常,期望将使用的生物制剂来源于与靶向治疗的动物相同的物种,由此最小化对试剂的任何免疫反应。在人类个体的情况下,例如人源化和完全人类抗体可以是期望的。
本文公开的抗体或其抗原结合片段(例如14D7、26B10和其人源化版本)可通过连续输注或通过施用的剂量,例如每日、每周1-7次、每周、每两周、每个月、每两个月、每季、每半年、每年等提供。可例如静脉内、皮下、局部、经口、经鼻、经直肠、肌肉内、颅内、脊椎内或通过吸入提供剂量。总每周剂量通常为至少0.05μg/kg体重,更通常至少0.2μg/kg、0.5μg/kg、1μg/kg、10μg/kg、100μg/kg、0.25mg/kg、1.0mg/kg、2.0mg/kg、5.0mg/ml、10mg/kg、25mg/kg、50mg/kg或更多体重(参见例如Yang等人(2003) New Engl. J. Med. 349:427-434;Herold, 等人(2002) New Engl. J. Med. 346:1692-1698; Liu, 等人(1999) J.Neurol.Neurosurg. Psych. 67:451-456; Portielji, 等人 (20003) Cancer Immunol.Immunother. 52:151-144)。也可提供剂量以实现个体血清中抗TIGIT抗体的预定靶浓度,诸如0.1、0.3、1、3、10、30、100、300μg/ml或更多。在其它实施方案中,本发明的抗TIGIT抗体例如皮下或静脉内,每周、每两周、“每4周”、每个月、每两个月或每季以10、20、50、80、100、200、500、1000或2500 mg/个体施用。
如本文所用,术语“有效量”是指本发明的抗TIGIT或其抗原结合片段(例如人源化14A6或人源化28H5)当单独或与其它治疗剂组合施用至细胞、组织或个体时有效引起疾病的一种或多种症状、例如癌症或癌症进展引起可测量的改善的量。有效剂量进一步是指抗体或片段足以导致症状的至少部分改善、例如肿瘤缩小或消除、肿瘤生长的缺乏、增加存活时间的量。当应用单独施用的个别活性成分时,有效剂量是指单独的成分。当应用于组合时,有效剂量是指无论组合连续还是同时施用,导致治疗效应的活性成分的组合量。有效量的治疗剂将导致诊断量度或参数改善至少10%;通常至少20%;优选至少约30%;更优选至少40%且最优选至少50%。在主观量度用于评价疾病严重程度的情况下,有效量也可导致主观量度的改善。
试剂盒
进一步提供包含一种或多种组分的试剂盒,所述一种或多种组分包括,但不限于,如本文中所讨论的抗TIGIT抗体或抗原结合片段(例如人源化14D7或人源化26B10)与一种或多种包括但不限于如本文中所讨论的药学上可接受的载体和/或的治疗剂的其它组分联合。抗体或片段和/或治疗剂可配制为纯组合物或与药学上可接受的载体组合于药物组合物中。
在一个实施方案中,所述试剂盒包括一个容器中(例如无菌玻璃或塑料小瓶中)的本发明的抗TIGIT抗体或其抗原结合片段(例如人源化14D7或人源化26B10)或其药物组合物和另一容器中(例如无菌玻璃或塑料小瓶中)的其药物组合物和/或治疗剂。
在另一个实施方案中,所述试剂盒包含本发明的组合,其在单一常用容器中包括本发明的抗TIGIT抗体或其抗原结合片段(例如人源化14D7或人源化26B10)连同药学上可接受的载体,任选地与一种或多种治疗剂组合,任选地一起配制于药物组合物中。
如果试剂盒包括用于向个体肠胃外施用的药物组合物,则所述试剂盒可包括用于进行此类施用的装置。例如,所述试剂盒可包括如上文所讨论的一种或多种皮下针或其它注射装置。
所述试剂盒可包括包装插页,其包括关于试剂盒中的药物组合物和剂型的信息。通常,此类信息帮助患者和医师有效且安全地使用封装的药物组合物和剂型。例如,以下关于本发明的组合的信息可供应于该插页中:药代动力学、药效动力学、临床研究、功效参数、适应症和用法、禁忌症、警告信息、注意事项、不良反应、过剂量、适当剂量和施用、如何供应、适当储存条件、参考文献、制造商/经销商信息和专利信息。
检测试剂盒和治疗试剂盒
为了方便起见,本发明的抗TIGIT抗体或其抗原结合片段(例如14D7、26B10或其人源化版本)可提供于试剂盒中,即预定量的试剂与用于进行诊断或检测测定的说明书的包装组合。在抗体或片段用酶标记的情况下,试剂盒将包括酶所需的底物和辅因子(例如提供可检测发色团或荧光团的底物前体)。另外,可包括其它添加剂,诸如稳定剂、缓冲剂(例如阻断缓冲液或裂解缓冲液)等等。各种试剂的相对量可广泛变化以提供实质上优化测定灵敏度的溶液中试剂的浓度。具体地,试剂可作为干燥粉末提供,其通常冻干,包括赋形剂,其在溶解后,将提供具有适当浓度的试剂溶液。
还提供包含一种或多种此类试剂的诊断或检测试剂和试剂盒,其用于多种检测测定中,包括例如免疫测定,诸如ELISA(夹心型或竞争形式)。试剂盒的组分可预附接至固体支持物,或可以当使用试剂盒时施加至固体支持物的表面。在本发明的一些实施方案中,信号产生装置可与本发明的抗体或片段预缔合,或在使用前可能需要组合一种或多种组分,例如缓冲剂、抗体-酶缀合物、酶底物等。试剂盒也可包括额外试剂,例如用于减少与固相表面的非特异性结合的封闭试剂、洗涤试剂、酶底物等。固相表面可呈管、珠粒、微量滴定板、微球体或适合于固定蛋白、肽或多肽的其它材料的形式。在具体方面,催化化学发光或发色产物形成或化学发光或发色底物的还原的酶是信号产生装置的组分。此类酶是本领域中众所周知的。试剂盒可包含任一本文所述的捕获试剂和检测试剂。任选地,试剂盒也可包含用于进行本发明的方法的说明书。
还提供试剂盒,其包含包装在容器诸如小瓶或瓶中的抗TIGIT抗体(例如人源化抗体)或其抗原结合片段,且进一步包含附接至容器或与容器一起包装的标签,所述标签描述容器的内含物且提供适应症和/或关于使用容器内含物治疗如本文所述的一种或多种疾病状态的说明书。
在一个方面,试剂盒用于治疗癌症且包含抗TIGIT抗体(例如人源化抗体)或其抗原结合片段和另一治疗剂或疫苗。试剂盒可任选地进一步包括用于肠胃外,例如静脉内施用的注射器。在另一个方面,试剂盒包含抗TIGIT抗体(例如人源化抗体)或其抗原结合片段和描述抗体或片段与疫苗或其它治疗剂的使用的附接至容器或与容器一起包装的标签。在又一个方面,试剂盒包含疫苗或其它治疗剂和描述疫苗或其它治疗剂与抗TIGIT抗体或片段的使用的附接至容器或与容器一起包装的标签。在某些实施方案中,抗TIGIT抗体和疫苗或其它治疗剂在分开小瓶中或一起组合在相同药物组合物中。
如上文在组合疗法章节中所讨论,两种治疗剂的同时施用不要求药剂同时或通过相同途径施用,只要药剂发挥其治疗作用的时间段存在重叠。涵盖同时或依次施用,如在不同日或周施用。
也可制备包含本文公开的抗体、肽、抗原结合片段或多核苷酸中的至少一种和关于使用组合物作为检测试剂或治疗剂的说明书的本文公开的治疗和检测试剂盒。用于此类试剂盒中的容器通常可包含至少一个小瓶、试管、烧瓶、瓶、注射器或其它适合容器,检测和/或治疗组合物中的一种或多种可置于其中,且优选适当等分。在还提供第二治疗剂的情况下,试剂盒也可含有第二不同容器,其中可放置该第二检测和/或治疗组合物。
或者,多种化合物可制备成单一药物组合物,且可包装在单一容器装置诸如小瓶、烧瓶、注射器、瓶或其它适合单一容器中。本文公开的试剂盒通常还将包括用于严密地容纳小瓶用于商业销售的装置,诸如例如其中保持期望小瓶的注塑或吹塑塑料容器。在放射性标记、发色、荧光生成或其它类型的可检测标记或检测装置包括在试剂盒内的情况下,标记试剂可提供于与检测或治疗组合物本身相同的容器中,或者可置于其中可放置且适当等分该第二组合物的第二不同容器装置中。或者,检测试剂和标记可制备于单一容器装置中,并且在大多数情况下,试剂盒也通常包括用于严密地容纳小瓶用于商业销售和/或便于包装和递送的装置。
还提供用于进行本文所述的检测或监测方法的装置或设备。此类设备可包括其中可输入样品的腔室或管、任选地包括阀或泵以引导样品流过装置的流体处理系统、任选将血浆或血清与血液分开的过滤器、用于添加捕获试剂或检测试剂的混合腔室和任选检测结合捕获试剂免疫复合物的可检测标记的量的检测装置。样品流可以是被动的(例如通过毛细管、流体静力学或一旦施加样品就不需要进一步操纵装置的其它力)或主动的(例如通过施加经由机械泵、电渗泵、离心力或增加气压所产生的力)或通过主动力和被动力的组合。
在进一步实施方案中,还提供处理器、计算机可读存储器和存储在计算机可读存储器上且经调整以在处理器上执行以进行本文所述的任一方法的例行程序。合适计算系统、环境和/或配置的实例包括个人计算机、服务器计算机、手持式或膝上型装置、多处理器系统、基于微处理器的系统、机顶盒、可编程的消费性电子产品、网络PC、小型计算机、大型计算机、包括以上系统或装置中任一种的分布式计算环境或本领域中已知的任何其它系统。
一般方法
分子生物学中的标准方法描述于:Sambrook, Fritsch和Maniatis (1982 & 1989第2版,2001第3版) Molecular Cloning, A Laboratory Manual, Cold Spring HarborLaboratory Press, Cold Spring Harbor, NY;Sambrook和Russell (2001) MolecularCloning, 第3版, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, NY;Wu (1993) Recombinant DNA, 第217卷, Academic Press, San Diego, CA) 。标准方法还出现于Ausbel, 等人(2001) Current Protocols in Molecular Biology, 第1-4卷,John Wiley and Sons, Inc. New York, NY,其描述细菌细胞中的克隆和DNA诱变(第1卷)、哺乳动物细胞和酵母中的克隆(第2卷)、糖缀合物和蛋白表达(第3卷)和生物信息(第4卷)。
描述了用于蛋白纯化的方法,包括免疫沉淀、色谱法、电泳、离心和结晶(Coligan等人(2000) Current Protocols in Protein Science,第1卷, John Wiley and Sons,Inc., New York)。描述了化学分析、化学修饰、翻译后修饰、融合蛋白的产生、蛋白的糖基化(参见例如Coligan等人(2000) Current Protocols in ProteinScience,第2卷 ,JohnWiley and Sons, Inc., New York;Ausubel等人(2001) Current Protocols inMolecular Biology,第3卷 ,John Wiley and Sons,Inc., NY, NY,第16.0.5-16.22.17页;Sigma-Aldrich, Co. (2001) Products for Life Science Research, St. Louis,MO;第45-89页;Amersham Pharmacia Biotech(2001) BioDirectory, Piscataway, N.J.,第384-391页)。描述了多克隆和单克隆抗体的产生、纯化和片段化(Coligan等人(2001)Current Protcols in Immunology,第1卷 ,John Wiley and Sons, Inc., New York;Harlow和Lane(1999) Using Antibodies, Cold Spring Harbor Laboratory Press,Cold Spring Harbor, NY;Harlow和Lane,同上)。用于表征配体/受体相互作用的标准技术是可得的(参见例如Coligan等人(2001) Current Protocols in Immunology,第4卷 ,John Wiley, Inc., New York)。
可制备单克隆、多克隆和人源化抗体(参见例如Sheperd和Dean(编辑) (2000)Monoclonal Antibodies, Oxford Univ. Press, New York, NY;Kontermann和Dubel(编辑) (2001) Antibody Engineering, Springer-Verlag, New York;Harlow和Lane(1988)Antibodies A Laboratory Manual, Cold Spring Harbor Laboratory Press, ColdSpring Harbor, NY,第139-243页;Carpenter等人(2000) J. Immunol. 165:6205;He等人(1998) J. Immunol. 160:1029;Tang等人(1999) J. Biol. Chem. 274:27371-27378;Baca等人(1997) J. Biol. Chem. 272:10678-10684;Chothia等人(1989) Nature 342:877-883;Foote和Winter (1992) J. Mol. Biol. 224:487-499;美国专利号6,329,511)。
人源化的一种替代方案是在转基因小鼠中使用在噬菌体或人类抗体文库上展示的人类抗体文库(Vaughan等人(1996) Nature Biotechnol. 14:309-314;Barbas (1995)Nature Medicine 1:837-839;Mendez等人(1997) Nature Genetics 15:146-156;Hoogenboom和Chames (2000) Immunol. Today 21:371-377;Barbas等人(2001) PhageDisplay: A Laboratory Manual, Cold Spring Harbor Laboratory Press, ColdSpring Harbor, New York;Kay等人(1996) Phage Display of Peptides and Proteins:A Laboratory Manual, Academic Press, San Diego, CA;de Bruin等人(1999) NatureBiotechnol. 17:397-399)。
描述了单链抗体和双抗体(参见例如Malecki等人(2002) Proc. Natl. Acad.Sci. USA 99:213-218; Conrath等人(2001) J. Biol. Chem. 276:7346-7350; Desmyter等人(2001) J. Biol. Chem. 276:26285-26290; Hudson和Kortt (1999) J. Immunol.Methods 231:177-189;和美国专利号4,946,778)。提供了双抗体(参见例如Mack, 等人(1995) Proc. Natl. Acad. Sci. USA 92:7021-7025;Carter (2001) J. Immunol.Methods 248:7-15;Volkel, 等人(2001) Protein Engineering 14:815-823;Segal, 等人(2001) J. Immunol. Methods 248:1-6;Brennan, 等人 (1985) Science 229:81-83;Raso, 等人(1997) J. Biol. Chem. 272:27623;Morrison (1985) Science 229:1202-1207;Traunecker, 等人(1991) EMBO J. 10:3655-3659;和美国专利号5,932,448、5,532,210和6,129,914)。
还提供了双特异性抗体(参见例如Azzoni等人(1998) J. Immunol. 161:3493;Kita等人(1999) J. Immunol. 162:6901;Merchant等人(2000) J. Biol. Chem. 74:9115;Pandey等人(2000) J. Biol. Chem. 275:38633;Zheng等人(2001) J. Biol Chem.276:12999;Propst等人(2000) J. Immunol. 165:2214;Long (1999) Ann. Rev.Immunol. 17:875)。
抗原的纯化不是抗体产生所必需的。动物可用携带目标抗原的细胞免疫。然后可以从免疫的动物分离脾细胞,且脾细胞可与骨髓瘤细胞系融合以产生杂交瘤(参见例如Meyaard等人(1997)Immunity 7:283-290;Wright等人(2000) Immunity13:233-242;Preston等人,同上;Kaithamana等人(1999) J. Immunol. 163:5157-5164)。
抗体可缀合至例如小药物分子、酶、脂质体、聚乙二醇(PEG)。抗体可用于治疗、诊断、试剂盒或其它目的,且包括偶联至例如染料、放射性同位素、酶或金属(例如胶态金)的抗体(参见例如Le Doussal等人(1991) J. Immunol. 146:169-175;Gibellini等人(1998)J. Immunol. 160:3891-3898;Hsing和Bishop (1999) J. Immunol. 162:2804-2811;Everts等人(2002) J. Immunol. 168:883-889)。
用于流式细胞术的方法,包括荧光活化的细胞分选(FACS),是可得的(参见例如Owens, 等人 (1994) Flow Cytometry Principles for Clinical LaboratoryPractice, John Wiley and Sons, Hoboken, NJ; Givan (2001) Flow Cytometry, 第2版 ;Wiley-Liss, Hoboken, NJ; Shapiro (2003) Practical Flow Cytometry, JohnWiley and Sons, Hoboken, NJ)。用作例如诊断试剂的适用于修饰核酸,包括核酸引物和探针、多肽和抗体的荧光试剂是可得的(Molecular Probes (2003) Catalogue,Molecular Probes, Inc., Eugene, OR; Sigma-Aldrich (2003) Catalogue, St.Louis, MO)。
描述了免疫系统的组织学的标准方法(参见例如Muller-Harmelink (编辑)(1986) Human Thymus: Histopathology and Pathology, Springer Verlag, New York,NY;Hiatt等人(2000) Color Atlas of Histology, Lippincott, Williams, andWilkins, Phila, PA;Louis等人(2002) Basic Histology: Text and Atlas, McGraw-Hill, New York, NY)。
用于测定例如抗原片段、前导序列、蛋白折叠、功能结构域、糖基化位点和序列比对的软件包和数据库是可得的(参见例如GenBank, Vector NTI® Suite (Informax,Inc, Bethesda, MD);GCG Wisconsin Package (Accelrys, Inc., San Diego, CA);DeCypher® (TimeLogic Corp., Crystal Bay, Nevada);Menne, 等人(2000)Bioinformatics 16: 741-742;Menne, 等人(2000) Bioinformatics Applications Note16:741-742;Wren, 等人 (2002) Comput. Methods Programs Biomed. 68:177-181;vonHeijne (1983) Eur. J. Biochem. 133:17-21;von Heijne (1986) Nucleic Acids Res.14:4683-4690)。
实施例1
小鼠抗hTIGIT抗体的产生
为了产生针对人TIGIT的抗体,用人类Fc标记的人TIGIT重组蛋白、使用RIBI佐剂和足垫注射以两周一次时间表来免疫Balb/C小鼠。将免疫的动物取血并使用基于细胞的ELISA(下文描述)测定结合人TIGIT转染的CHOK1细胞的血清滴度。用重组蛋白给予具有最高滴度的动物最终加强,其中四天后分离引流腘淋巴结。通过使用Cytopulse Hybrimmune电融合系统将分离的淋巴细胞与骨髓瘤融合配偶体P3X63-AG8.653电融合来产生杂交瘤。将融合细胞铺板在96孔板中DMEM/F12、15% BCS、HAT、IL-6、OPI补充物和庆大霉素中。
使用基于细胞的ELISA形式,测定杂交瘤上清液与表达人TIGIT的CHOK1细胞的结合和与表达食蟹猴和恒河猴TIGIT的CHO细胞的交叉反应性。将表达人TIGIT和食蟹猴/恒河猴TIGIT的CHO-K1细胞铺板在96孔组织培养板中50μl DMEM/F12、10% BCS和庆大霉素(CHO-K1培养基)中。将细胞在测定前两天以2x104个细胞/孔铺板或在测定前一天以4x104个细胞/孔铺板。在测定前从孔去除培养基并添加50μl杂交瘤上清液。将杂交瘤上清液在室温下孵育30-60分钟并使用细胞ELISA洗涤方案,在Biotek EL405x Select CW洗板机上用PBS/0.05% Tween 20洗涤3次。五十微升检测抗体(HRP缀合的山羊抗大鼠IgG(SouthernBiotech目录号3030-05)或HRP缀合的山羊抗小鼠IgG(Southern Biotech目录号1043-05))以1:2000稀释度添加至CHO-K1培养基中并在室温下孵育30-60分钟。如上洗涤测定板并用TMB显色,并用TMB终止溶液(KPL目录号50-85-06)或0.1N磷酸终止。测定450nm-620nm下的吸光度。阳性克隆对人TIGIT和食蟹猴/恒河猴TIGIT转染的CHO-K1细胞反应,且对于与亲本CHO-K1细胞的结合为阴性。在这些测定中,如果抗体显示与亲本(未转染)CHO-K1细胞的结合,则我们在筛选中由于对TIGIT无特异性而丢弃该抗体。
阳性杂交瘤通过限制稀释法来亚克隆或通过将杂交瘤铺板在半固体培养基中来亚克隆,并在ClonePix® (Genetix)上挑取克隆。对亲本杂交瘤进行两轮亚克隆。使最终亚克隆在无血清的杂交瘤产生培养基中在小规模培养物中生长,并纯化以产生纯化抗体用于进一步表征。
实施例2
抗hTIGIT抗体的表征
在基于细胞的ELISA形式中测试来自阳性克隆的上清液阻断重组人CD155-huFc蛋白结合hTIGIT CHOK1细胞的能力。将人TIGIT-CHO-K1细胞如上所述铺板在96孔板中。从培养板去除培养基,并将50μl杂交瘤上清液与人TIGIT CHO-K1细胞在4℃下一起孵育30分钟。将五十微升人CD155-huFc添加至培养板中,人CD155-huFc的最终浓度为0.5μg/ml,并在4℃下孵育30分钟。如上将测定板用PBS/0.05% Tween-20洗涤3次。使用HRP-缀合物F(ab)’2山羊抗人IgG二级抗体(Jackson 109-036-098)以1:2000稀释度在CHO-K1培养基中检测人CD155-huFc与hTIGIT-CHOK1细胞的结合。如上所述,将板使用TMB显色,并使用TMB终止溶液终止,且测定A450-620nm。
根据上述方法产生的小鼠抗体被称为14D7,且来源于克隆MEB125.14D7。该小鼠抗体(14D7)为IgG1/κ同种型且包含SEQ ID NO:6的重链可变区和SEQ ID NO:7的轻链可变区。使用上述方法,如通过基于细胞的ELISA所测定(结合人TIGIT和食蟹猴/恒河猴TIGIT-CHOK1细胞)(图1),纯化的14D7抗体结合人TIGIT和食蟹猴/恒河猴TIGIT。使用基于细胞的ELISA阻断测定法(图2),使用上述方法,纯化的14D7 抗体也可阻断hTIGIT和hCD155相互作用。
根据上述方法产生的另一种小鼠抗体被称为26B10,且来源于克隆MEB125.26B10。该小鼠抗体(26B10)为IgG1/κ同种型且包含SEQ ID NO:23的重链可变区和SEQ ID NO:24的轻链可变区。使用上述方法,如通过基于细胞的ELISA所测定(结合人TIGIT和食蟹猴/恒河猴TIGIT-CHOK1细胞)(图1),纯化的26B10抗体结合人TIGIT和食蟹猴/恒河猴TIGIT。使用基于细胞的ELISA阻断测定法(图2),使用上述方法,纯化的26B10抗体也阻断hTIGIT和hCD155相互作用。
亲本(非人类)抗TIGIT抗体与人TIGIT重组蛋白的结合的亲和力测定:通过表面等离子共振、使用Biacore T200系统(Biacore, GE Healthcare, Piscataway, NJ)测量抗人TIGIT抗体14D7 和26B10(如实施例1中所述制备)和商业抗体MBSA43的动力学结合活性。约5000RU抗小鼠IgG(GE Healthcare目录号BR-1008-38)或约13,000RU片段特异性的山羊抗大鼠IgG Fcγ(Jackson ImmunoResearch目录号112-006-071)经由胺偶联化学法固定至Series S CM5传感器芯片(目录号BR-1005-30)上。将小鼠抗人TIGIT克隆14D7、26B10和MBSA43各自以1μg/mL注射在固定的抗小鼠表面上,捕获水平为40RU。HBS-EP+缓冲液(BR-1006-69)用作运行缓冲液,流速为30μL/min。将范围为0.29nM至40nM的不同浓度的人TIGIT-His蛋白以45μL/min的流速注射在抗体表面上。在每个小鼠抗人TIGIT注射周期后,使用10mM甘氨酸pH 1.7的一次三分钟注射,以10μL/min的流速,再生Series S CM5芯片表面。
背景减去结合传感图用于分析缔合(ka)和解离(kd)的速率常数和平衡解离常数KD。所得数据集用1:1朗缪尔结合模型(Langmuir Binding Model)使用Biacore T200评估软件(版本2.0)拟合。表3概述抗人TIGIT抗体对人TIGIT-His蛋白的亲和力。
表3:使用BIAcore的抗人TIGIT抗体对人TIGIT-His蛋白和TIGIT-Fc蛋白的亲和力的测量。
拮抗剂抗hTIGIT抗体的体外T细胞活性测定
我们开发以表征阻断人TIGIT受体的功能结果的一种测定法利用Jurkat细胞,一种人类T淋巴细胞细胞的永生化系(克隆,E6-1;ATCC TIB-152),其经工程改造以过表达人TIGIT (hTIGIT-Jurkat),其与THP-1细胞(一种人类单核细胞性细胞系)在TIGIT配体CD155和CD112之一存在或不存在的情况下共培养。与THP-1细胞共培养并用板结合的抗CD3 mAb刺激的hTIGIT-Jurkat细胞产生IL-2,但当将TIGIT配体(CD155或CD112)添加至共培养物时,IL-2水平以配体依赖性方式减少。使用阻断CD155-或CD112-TIGIT相互作用的抗体,诸如市售抗-hTIGIT Ab、克隆MBSA43 (eBioscience Cat# 12-9500-42; 10 μg/ml)处理将IL-2拯救至等于当活化的hTIGIT Jurkat细胞与THP-1在不存在CD155或CD112的情况下一起培养时的水平(图3)。
在4℃下将96孔平底板用小鼠抗人CD3抗体(1μg/ml,于PBS中;克隆HIT3a;BDPharmingen目录号555336)包被过夜。第二天,将hTIGIT-Jurkat细胞(50,000个)铺板于预包被板中并与各种浓度的mAb预孵育30-60分钟。将THP-1细胞(50,000个)添加至培养物,随后添加CD155-Fc(人CD155的ECD与人类Fc的融合体;1.0μg/ml)或CD112-Fc(人CD112的ECD与人类Fc的融合体;0.5μg/ml)。在37℃和5.0% CO2下孵育18-24小时之后,通过Meso Scale(人类IL-2组织培养MESO试剂盒:目录号K151AHB-2)评价培养物上清液中的IL-2水平。
如图3中所示,与使用该测定的0.23μg/ml的MBSA43相比,抗hTIGIT克隆14D7和26B10从30μg/ml向下滴定至0.04g/ml分别得到0.17μg/ml和0.19 g/ml的EC50。
实施例3
抗体人源化
使用本说明书中所述的方法将14D7和26B10小鼠抗体人源化。从抗体14D7,构建以下人源化可变重链:SEQ ID NO:9-12;且构建以下人源化可变轻链:SEQ ID NO:13-16。从小鼠抗体26B10,构建以下人源化可变重链:SEQ ID NO:25-28;且构建以下人源化可变轻链:SEQ ID NO:29-32。
实施例4
通过氢氘交换质谱法的人TIGIT 抗体的表位定位
抗TIGIT抗体14D7和人TIGIT之间的接触区域通过使用氢氘交换质谱(HDX-MS)分析来测定。HDX-MS测量氘与氢交换至蛋白的酰胺主链中。影响交换速率的一个因素是氢对溶剂的暴露。当结合抗体时抗原中的交换水平的比较可鉴定其中结合抗体的蛋白区域。
材料
● hTIGIT-His (SEQ ID NO:35) – 包含人TIGIT的细胞外结构域(SEQ ID NO:33的残基25-145)和组氨酸标签。
● 小鼠抗人TIGIT 14D7抗体(批号# 26AHB) (小鼠x [TIGIT_H] mAb(MEB125.14D7.C1.C1) IgG1 / κ(HY)) (包含 SEQ ID NO:6的重链可变区和 SEQ ID NO:7的轻链可变区)
液相色谱-质谱法
质谱仪为Thermo Scientific Orbitrap-Elite。为了测量氘标记的样品,质谱仪被设定为在轨道阱中在120,000分辨能力、1E6的靶离子数、500毫秒的最大离子注射时间和两次微扫描下获取一个完整扫描MS数据。为了获取MS/MS数据用于肽鉴定,质谱仪被设定为在120,000分辨能力下获取一个完整扫描光谱,随后在离子阱中获取十个数据依赖性MS/MS光谱。
液相色谱系统为用于分析柱梯度的Waters nanoAcquity和用于样品消化和上样的Waters 515等度泵。对于样品消化和上样,所用缓冲液为2%乙腈和0.05%三氟乙酸,流速为80 ul/分钟。对于分析梯度,缓冲液为缓冲液A) 水中的0.1%甲酸和缓冲液B) 乙腈中的0.1%甲酸。
梯度以40μl/分钟在10分钟内2% B至36% B,随后为80% B洗涤2分钟,和在2% B下重新平衡3分钟。然后通过在2%和80% B之间的梯度循环三次,每个步骤1分钟,随后在2% B下最终平衡5分钟来洗涤柱。捕获柱为Waters Vanguard CSH C18 1.7um保护柱且分析柱为Waters CSH C18, 1.7um 1x50mm柱。
用于氘标记的样品处理通过Leaptec H/D-X PAL系统进行。标记样品盘设定成25℃的温度,淬灭盘设定成1.5℃,且捕获器和分析柱室设定成1.5℃。固定的胃蛋白酶柱(Enzymate BEH Pepsin, Waters corporation)保持在柱室外室温下。
氘标记
将人TIGIT-His与抗体14D7混合至人TIGIT-His为30 µM 且14D7为15 µM的终浓度。通过将人TIGIT-His孵育在50 mM乙酸钠 pH5.5中制备未结合对照。将抗体结合的样品和未结合对照在室温下孵育1小时,然后开始标记实验。
为了氘标记样品,将2μl样品与25μl 氧化氘pH 7.6中的PBS混合。标记时间点为30、300、1500、4500和9000秒。在时间点之后,将25μl标记混合物添加至35μl冷淬灭缓冲液(8M脲、100mMTCEP)。将淬灭的样品在1.5℃下孵育一分钟。然后将50μl注射至柱冷却室中,其中样品通过胃蛋白酶柱且所得肽上样至捕获柱上。在两分钟之后,阀开关从管线中取出胃蛋白酶柱且将捕获器再洗涤90秒。然后将捕获器与分析柱内联切换且开始分析梯度和质谱数据获取。以随机化顺序一式三份获取每个时间点。
通过将2μl hTIGIT(60pmol/μL)与108μl氘化变性缓冲液(99.5%氧化氘中的4M脲、100mM TCEP、0.01% DDM)一起孵育来产生完全氘化的样品。将样品在室温下孵育过夜。然后将50μl直接注射至柱室且如前获取数据。
数据分析
获取未标记样品的LC-MS/MS数据并数据库搜索以验证蛋白的成功消化且从胃蛋白酶消化产生一系列肽。使用Proteome Discoverer 1.4和SEQUEST HT搜索算法(ThermoFisher Scientific)进行数据库搜索。所用蛋白数据库为串联至酵母酿酒酵母Uniprot(5/20/13)数据库的人TIGIT-His和抗人TIGIT抗体序列。
来自氘标记实验的MS数据通过HDExaminer(版本1.3,Sierra Analytics)处理。人工验证通过软件针对各肽选择的质量和保留时间。
结果
通过14D7抗体保护的人TIGIT肽说明于热图中(图4),且对应于(SEQ ID NO:33)所示的人TIGIT的氨基酸残基24-41 (SSTTAQVNWEQQDQL, SEQ ID NO:113)、44-46 (ICN)、85-93 (IYHTYPDGT, SEQ ID NO:114)和96-100 (GRIFL, SEQ ID NO:115)。
本文中引用的所有参考文献均通过引用并入,其程度如同各个别出版物、数据库条目(例如Genbank序列或GeneID条目)、专利申请或专利具体且个别地指示通过引用并入一样。申请人遵循37 C.F.R. §1.57(b)(1)关于各个和每一个别出版物、数据库条目(例如Genbank序列或GeneID条目)、专利申请或专利意欲该通过引用并入的陈述,其中各自均遵照37 C.F.R. §1.57(b)(2)明确鉴定,即使此类引用不直接接近通过引用并入的专用表述。通过引用并入的专用表述(如果存在)包括于本说明书内不会以任何方式弱化该通过引用并入的一般陈述。本文中参考文献的引用不意欲承认该参考文献为相关现有技术,关于这些出版物或文献的内容或日期,也不构成任何承认。
本发明的范围不受本文描述的具体实施方案所限制。实际上,从前述描述和附图,除了本文所述的修改之外,本发明的各种修改对本领域技术人员而言将变得显而易见。此类修改意欲落在所附权利要求的范围内。
前述书面说明书被认为足以能够使本领域技术人员实施本发明。除了本文所示和所述的修改之外,本发明的各种修改对本领域技术人员而言将变得显而易见且落在所附权利要求的范围内。
表4:序列信息
。
Claims (10)
1.抗体或其抗原结合片段,其结合人TIGIT,其中所述抗体或抗原结合片段选自:
a.包含以下的抗体或抗原结合片段:包含SEQ ID NO:1的氨基酸序列的重链可变区CDR1、包含SEQ ID NO:2的氨基酸序列的重链可变区CDR2、包含SEQ ID NO:3、45、46或47的氨基酸序列的重链可变区CDR3、包含SEQ ID NO:4的氨基酸序列的轻链可变区CDR1、包含SEQ ID NO:5的氨基酸序列的轻链可变区CDR2和包含SEQ ID NO:6、57、58、59、60、61或62的氨基酸序列的轻链可变区CDR3;和
b.包含以下的抗体或抗原结合片段:包含SEQ ID NO:17的氨基酸序列的重链可变区CDR1、包含SEQ ID NO:18、81、82、83、84、85、86、87或88的氨基酸序列的重链可变区CDR2、包含SEQ ID NO:19的氨基酸序列的重链可变区CDR3、包含SEQ ID NO:20的氨基酸序列的轻链可变区CDR1、包含SEQ ID NO:21的氨基酸序列的轻链可变区CDR2和包含SEQ ID NO:22的氨基酸序列的轻链可变区CDR3。
2.权利要求1的抗体或抗原结合片段,其中所述抗体含有包含SEQ ID NO:1的氨基酸序列的重链可变区CDR1、包含SEQ ID NO:2的氨基酸序列的重链可变区CDR2、包含SEQ ID NO:3、45、46或47的氨基酸序列的重链可变区CDR3、包含SEQ ID NO:4的氨基酸序列的轻链可变区CDR1、包含SEQ ID NO:5的氨基酸序列的轻链可变区CDR2和包含SEQ ID NO:6、57、58、59、60、61或62的氨基酸序列的轻链可变区CDR3。
3.权利要求1的抗体或抗原结合片段,其中所述抗体含有包含SEQ ID NO:17的氨基酸序列的重链可变区CDR1、包含SEQ ID NO:18、81、82、83、84、85、86、87或88的氨基酸序列的重链可变区CDR2、包含SEQ ID NO:19的氨基酸序列的重链可变区CDR3、包含SEQ ID NO:20的氨基酸序列的轻链可变区CDR1、包含SEQ ID NO:21的氨基酸序列的轻链可变区CDR2和包含SEQ ID NO:22的氨基酸序列的轻链可变区CDR3。
4.抗体或其抗原结合片段,其结合人TIGIT,其包含选自以下的轻链免疫球蛋白、重链免疫球蛋白或轻链和重链免疫球蛋白:
a.含有包含SEQ ID NO:7的氨基酸序列的可变重链和/或包含SEQ ID NO:8的氨基酸序列的可变轻链的抗体或其抗原结合片段;
b.含有包含SEQ ID NO:9的氨基酸序列的可变重链和/或包含SEQ ID NO:13的氨基酸序列的可变轻链的抗体或其抗原结合片段;
c.含有包含SEQ ID NO:23的氨基酸序列的可变重链和/或包含SEQ ID NO:24的氨基酸序列的可变轻链的抗体或其抗原结合片段;
d.含有包含SEQ ID NO:25的氨基酸序列的可变重链和/或包含SEQ ID NO:29的氨基酸序列的可变轻链的抗体或其抗原结合片段;
e.抗体或其抗原结合片段包含选自SEQ ID NO: 10、11、12、48、49、50、51、52、53、54、55或56的可变重链和/或选自SEQ ID NO: 14、15、16、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79或80中任一者的可变轻链;
f.抗体或其抗原结合片段包含选自SEQ ID NO: 26、27、28、89、90、91、92、93、94、95、96、97、98、99、100、101、102、103、104、105、106、107、108、109、110、111和112的可变重链和/或选自SEQ ID NO:30、31和32中任一者的可变轻链;
g.抗体或其抗原结合片段包含:包含与SEQ ID NO: 10、11、12、48、49、50、51、52、53、54、55或56中任一者具有至少90%、95%、96%、97%、98%或99%同一性的可变重链和/或包含与SEQ ID NO: 14、15、16、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79或80中任一者具有至少90%、95%、96%、97%、98%或99%同一性的可变轻链;
h.抗体或其抗原结合片段包含:包含与SEQ ID NO: 26、27、28、89、90、91、92、93、94、95、96、97、98、99、100、101、102、103、104、105、106、107、108、109、110、111或112中任一者具有至少90%、95%、96%、97%、98%或99%同一性的可变重链和/或包含与SEQ ID NO:30、31或32中任一者具有至少90%、95%、96%、97%、98%或99%同一性的可变轻链;
i.抗体或其抗原结合片段包含:包含与SEQ ID NO: 10、11、12、48、49、50、51、52、53、54、55或56中任一者具有至少90%、95%、96%、97%、98%或99%同一性的可变重链和/或包含与SEQ ID NO: 14、15、16、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79或80中任一者具有至少90%、95%、96%、97%、98%或99%同一性的可变轻链,其中任何序列变化发生在所述抗体的构架区中;和
j.抗体或其抗原结合片段包含:包含与SEQ ID NO: 26、27、28、89、90、91、92、93、94、95、96、97、98、99、100、101、102、103、104、105、106、107、108、109、110、111或112中任一者具有至少90%、95%、96%、97%、98%或99%同一性的可变重链和/或包含与SEQ ID NO:30、32或32中任一者具有至少90%、95%、96%、97%、98%或99%同一性的可变轻链,其中任何序列变化发生在所述抗体的构架区中。
5.权利要求1-5中任一项的抗体或抗原结合片段,其中所述抗体以如通过表面等离子共振(例如,BIACORE)或类似技术(例如,KinExa或OCTET)所测定的约1 x 10-9M至约1 x 10-12M的KD值结合人TIGIT。
6.上述权利要求中任一项的抗体或抗原结合片段,其为包含两条重链和两条轻链的人源化抗体。
7.上述权利要求中任一项的抗体或抗原结合片段,其为人源化抗体,其中所述抗体包含人IgG1恒定结构域和人类κ恒定结构域。
8.上述权利要求中任一项的抗体或抗原结合片段,其为抗体,其中所述抗体在CHO细胞中产生。
9.分离的多肽,其包含SEQ ID NO:7、8、9、10、11、12、13、14、15、16、23、24、25、26、27、28、29、30、31、32、48、49、50、51、52、53、54、55、56、63、54、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、 89、90、91、92、93、9495、96、97、98、99、100、101、102、103、104、105、106、107、108、109、110、111或112中的任一种的氨基酸序列。
10.分离的核酸,其编码:权利要求1-8的抗体或抗原结合片段中的任一种,或权利要求9的多肽中的任一种。
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201562205048P | 2015-08-14 | 2015-08-14 | |
| US62/205048 | 2015-08-14 | ||
| PCT/US2016/046100 WO2017030823A2 (en) | 2015-08-14 | 2016-08-09 | Anti-tigit antibodies |
| CN201680059753.7A CN108290936B (zh) | 2015-08-14 | 2016-08-09 | 抗tigit抗体 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201680059753.7A Division CN108290936B (zh) | 2015-08-14 | 2016-08-09 | 抗tigit抗体 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN115925931A true CN115925931A (zh) | 2023-04-07 |
Family
ID=58051810
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201680059753.7A Active CN108290936B (zh) | 2015-08-14 | 2016-08-09 | 抗tigit抗体 |
| CN202210784461.7A Pending CN115925931A (zh) | 2015-08-14 | 2016-08-09 | 抗tigit抗体 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201680059753.7A Active CN108290936B (zh) | 2015-08-14 | 2016-08-09 | 抗tigit抗体 |
Country Status (7)
| Country | Link |
|---|---|
| US (2) | US10766957B2 (zh) |
| EP (1) | EP3334757A4 (zh) |
| JP (1) | JP6976241B2 (zh) |
| CN (2) | CN108290936B (zh) |
| AU (1) | AU2016307845B2 (zh) |
| CA (1) | CA2994555A1 (zh) |
| WO (1) | WO2017030823A2 (zh) |
Families Citing this family (65)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2855098C (en) | 2007-06-18 | 2018-02-27 | Merck Sharp & Dohme B.V. | Antibodies to human programmed death receptor pd-1 |
| GB201403775D0 (en) | 2014-03-04 | 2014-04-16 | Kymab Ltd | Antibodies, uses & methods |
| TWI715587B (zh) | 2015-05-28 | 2021-01-11 | 美商安可美德藥物股份有限公司 | Tigit結合劑和彼之用途 |
| EP3334757A4 (en) * | 2015-08-14 | 2019-04-03 | Merck Sharp & Dohme Corp. | ANTI-TIGIT ANTIBODIES |
| KR102543118B1 (ko) | 2016-05-27 | 2023-06-14 | 아게누스 인코포레이티드 | 항-tim-3 항체 및 이의 사용 방법 |
| CN109475603B (zh) | 2016-06-20 | 2023-06-13 | 科马布有限公司 | 抗pd-l1抗体 |
| US9567399B1 (en) | 2016-06-20 | 2017-02-14 | Kymab Limited | Antibodies and immunocytokines |
| TWI760352B (zh) | 2016-08-09 | 2022-04-11 | 英商克馬伯有限公司 | 抗icos抗體 |
| US10844119B2 (en) | 2016-10-11 | 2020-11-24 | Agenus Inc. | Anti-LAG-3 antibodies and methods of use thereof |
| WO2018083248A1 (en) | 2016-11-03 | 2018-05-11 | Kymab Limited | Antibodies, combinations comprising antibodies, biomarkers, uses & methods |
| NZ753515A (en) | 2016-11-30 | 2022-02-25 | Oncomed Pharm Inc | Methods for treatment of cancer comprising tigit-binding agents |
| JP2020510422A (ja) * | 2017-02-28 | 2020-04-09 | シアトル ジェネティックス, インコーポレイテッド | 抗tigit抗体 |
| HUE062927T2 (hu) * | 2017-05-01 | 2023-12-28 | Agenus Inc | Anti-TIGIT ellenanyagok és alkalmazási eljárásaik |
| AU2018263868A1 (en) | 2017-05-02 | 2019-12-12 | Merck Sharp & Dohme Llc | Formulations of anti-LAG3 antibodies and co-formulations of anti-LAG3 antibodies and anti-PD-1 antibodies |
| JOP20190260A1 (ar) | 2017-05-02 | 2019-10-31 | Merck Sharp & Dohme | صيغ ثابتة لأجسام مضادة لمستقبل الموت المبرمج 1 (pd-1) وطرق استخدامها |
| AU2018276140A1 (en) | 2017-06-01 | 2019-12-19 | Compugen Ltd. | Triple combination antibody therapies |
| WO2018229163A1 (en) | 2017-06-14 | 2018-12-20 | King's College London | Methods of activating v delta 2 negative gamma delta t cells |
| GB201709808D0 (en) | 2017-06-20 | 2017-08-02 | Kymab Ltd | Antibodies |
| KR20200100589A (ko) * | 2017-07-27 | 2020-08-26 | 아이테오스 테라퓨틱스 에스에이 | 항-tigit 항체 |
| JP7317272B2 (ja) | 2017-09-29 | 2023-07-31 | ジエンス ヘンルイ メデイシンカンパニー リミテッド | Tigit抗体、その抗原結合断片及びその医療用途 本願は、2019年9月29日に出願された出願番号cn201710908565.3に基づいたものであり、その優先権を主張する。その開示は、その全体が参照により本明細書に組み込まれる。 |
| EP3728314A1 (en) | 2017-12-19 | 2020-10-28 | Kymab Limited | Bispecific antibody for icos and pd-l1 |
| TWI816729B (zh) * | 2017-12-30 | 2023-10-01 | 英屬開曼群島商百濟神州有限公司 | 抗tigit抗體及其作為治療和診斷的用途 |
| KR102224556B1 (ko) * | 2018-02-06 | 2021-03-09 | 아이-맵 바이오파마 유에스 리미티드 | Ig 및 itim 도메인을 갖는 t 세포 면역 수용체 (tigit)에 대한 항체 및 이것의 사용 |
| KR20200136454A (ko) | 2018-03-27 | 2020-12-07 | 브리스톨-마이어스 스큅 컴퍼니 | 자외선 신호를 사용한 단백질 농도의 실시간 모니터링 |
| TWI754157B (zh) * | 2018-07-25 | 2022-02-01 | 大陸商信達生物製藥(蘇州)有限公司 | 抗tigit抗體及其用途 |
| JP2021534196A (ja) * | 2018-08-23 | 2021-12-09 | シージェン インコーポレイテッド | 抗tigit抗体 |
| CN109384846B (zh) * | 2018-09-25 | 2020-03-03 | 合肥瑞达免疫药物研究所有限公司 | 能够结合tigit的抗体或其抗原结合片段及用途 |
| CN113614109A (zh) | 2018-12-21 | 2021-11-05 | Ose免疫疗法公司 | 双功能抗pd-1/il-7分子 |
| WO2020165374A1 (en) | 2019-02-14 | 2020-08-20 | Ose Immunotherapeutics | Bifunctional molecule comprising il-15ra |
| US20220135619A1 (en) | 2019-02-24 | 2022-05-05 | Bristol-Myers Squibb Company | Methods of isolating a protein |
| CN109734806B (zh) * | 2019-03-15 | 2022-07-01 | 安徽安科生物工程(集团)股份有限公司 | 一种全人源抗huTIGIT单克隆抗体及其应用 |
| US20220220430A1 (en) | 2019-05-23 | 2022-07-14 | Bristol-Myers Squibb Company | Methods of monitoring cell culture media |
| BR112022000628A2 (pt) * | 2019-07-15 | 2022-03-03 | Shanghai Junshi Biosciences Co Ltd | Anticorpos anti-tigit e aplicação dos mesmos |
| EP4054722A1 (en) * | 2019-11-05 | 2022-09-14 | Merck Patent GmbH | Anti-tigit antibodies and uses thereof |
| CA3160313A1 (en) * | 2019-11-15 | 2021-05-20 | Surface Oncology, Inc. | Compositions and methods for immunotherapy |
| WO2021122866A1 (en) | 2019-12-17 | 2021-06-24 | Ose Immunotherapeutics | Bifunctional molecules comprising an il-7 variant |
| MX2022008412A (es) | 2020-01-07 | 2022-08-08 | Univ Texas | Variantes de enzima que agotan metiltioadenosina/adenosina mejorada humana para terapia de cancer. |
| WO2021180205A1 (zh) | 2020-03-13 | 2021-09-16 | 江苏恒瑞医药股份有限公司 | Pvrig结合蛋白及其医药用途 |
| US20230258645A1 (en) | 2020-05-07 | 2023-08-17 | Institut Curie | Antxr1 as a biomarker of immunosuppressive fibroblast populations and its use for predicting response to immunotherapy |
| KR20230024368A (ko) | 2020-06-18 | 2023-02-20 | 제넨테크, 인크. | 항-tigit 항체 및 pd-1 축 결합 길항제를 사용한 치료 |
| WO2021258337A1 (en) * | 2020-06-24 | 2021-12-30 | Huahui Health Ltd. | Human monoclonal antibodies against tigit for immune related diseases |
| TW202216778A (zh) | 2020-07-15 | 2022-05-01 | 美商安進公司 | Tigit及cd112r阻斷 |
| WO2022044010A1 (en) | 2020-08-26 | 2022-03-03 | Yissum Research Development Company Of The Hebrew University Of Jerusalem Ltd. | Anti-t-cell immunoglobulin and itim domain (tigit) antibodies for the treatment of fungal infections |
| WO2022076318A1 (en) | 2020-10-05 | 2022-04-14 | Bristol-Myers Squibb Company | Methods for concentrating proteins |
| TWI815220B (zh) * | 2020-11-23 | 2023-09-11 | 大陸商廣東菲鵬制藥股份有限公司 | 抗tigit抗體或其抗原結合片段及其生產方法與應用,以及包含其的核酸、載體、細胞、藥物組合物及試劑盒 |
| WO2022112198A1 (en) | 2020-11-24 | 2022-06-02 | Worldwide Innovative Network | Method to select the optimal immune checkpoint therapies |
| WO2022124864A1 (ko) * | 2020-12-10 | 2022-06-16 | 주식회사 유틸렉스 | 항-tigit 항체 및 이의 용도 |
| WO2022148781A1 (en) | 2021-01-05 | 2022-07-14 | Institut Curie | Combination of mcoln activators and immune checkpoint inhibitors |
| CN114762678B (zh) * | 2021-01-14 | 2024-03-15 | 上海君实生物医药科技股份有限公司 | 抗tigit抗体药物组合物及其用途 |
| EP4320156A1 (en) | 2021-04-09 | 2024-02-14 | Ose Immunotherapeutics | Scaffold for bifunctioanl molecules comprising pd-1 or cd28 and sirp binding domains |
| AU2022253351A1 (en) | 2021-04-09 | 2023-10-12 | Ose Immunotherapeutics | New scaffold for bifunctional molecules with improved properties |
| TW202304965A (zh) | 2021-05-04 | 2023-02-01 | 美商艾吉納斯公司 | 抗tigit抗體、抗cd96抗體及其使用方法 |
| WO2023010094A2 (en) | 2021-07-28 | 2023-02-02 | Genentech, Inc. | Methods and compositions for treating cancer |
| CA3227854A1 (en) * | 2021-07-28 | 2023-02-02 | Elpiscience (Suzhou) Biopharma, Ltd. | Novel anti-sirpa antibodies |
| CA3231320A1 (en) | 2021-09-15 | 2023-03-23 | Zhiliang CAO | Protein specifically binding to pd-1 and pharmaceutical use thereof |
| WO2023040935A1 (zh) | 2021-09-15 | 2023-03-23 | 江苏恒瑞医药股份有限公司 | 一种含抗pvrig/tigit双特异性抗体的药物组合物 |
| WO2023056403A1 (en) | 2021-09-30 | 2023-04-06 | Genentech, Inc. | Methods for treatment of hematologic cancers using anti-tigit antibodies, anti-cd38 antibodies, and pd-1 axis binding antagonists |
| WO2023138639A1 (zh) * | 2022-01-24 | 2023-07-27 | 原启生物科技(上海)有限责任公司 | 靶向tigit的抗原结合蛋白及其用途 |
| WO2023173011A1 (en) | 2022-03-09 | 2023-09-14 | Bristol-Myers Squibb Company | Transient expression of therapeutic proteins |
| WO2023178192A1 (en) | 2022-03-15 | 2023-09-21 | Compugen Ltd. | Il-18bp antagonist antibodies and their use in monotherapy and combination therapy in the treatment of cancer |
| WO2023211868A1 (en) * | 2022-04-29 | 2023-11-02 | Merck Sharp & Dohme Llc | Stable formulations of anti-ilt4 antibodies or antigen-binding fragments thererof in combination with anti-pd-1 antibodies and methods of use thereof |
| WO2023240058A2 (en) | 2022-06-07 | 2023-12-14 | Genentech, Inc. | Prognostic and therapeutic methods for cancer |
| WO2024003360A1 (en) | 2022-07-01 | 2024-01-04 | Institut Curie | Biomarkers and uses thereof for the treatment of neuroblastoma |
| WO2024028386A1 (en) | 2022-08-02 | 2024-02-08 | Ose Immunotherapeutics | Multifunctional molecule directed against cd28 |
| WO2024041639A1 (en) * | 2022-08-26 | 2024-02-29 | Nanjing Legend Biotech Co., Ltd. | Antibodies targeting tigit and uses thereof |
Family Cites Families (48)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7368527B2 (en) | 1999-03-12 | 2008-05-06 | Human Genome Sciences, Inc. | HADDE71 polypeptides |
| WO2000058334A1 (en) | 1999-03-26 | 2000-10-05 | Human Genome Sciences, Inc. | 50 human secreted proteins |
| US7408041B2 (en) | 2000-12-08 | 2008-08-05 | Alexion Pharmaceuticals, Inc. | Polypeptides and antibodies derived from chronic lymphocytic leukemia cells and uses thereof |
| EP1575480A4 (en) | 2002-02-22 | 2008-08-06 | Genentech Inc | COMPOSITIONS AND METHODS FOR TREATING DISEASES RELATED TO THE IMMUNE SYSTEM |
| US7193069B2 (en) | 2002-03-22 | 2007-03-20 | Research Association For Biotechnology | Full-length cDNA |
| CA2497337A1 (en) | 2002-09-11 | 2004-03-25 | Genentech, Inc. | Novel composition and methods for the treatment of psoriasis |
| EP1539228B1 (en) | 2002-09-11 | 2010-12-29 | Genentech, Inc. | Novel composition and methods for the treatment of immune related diseases |
| DE60336406D1 (de) | 2002-10-16 | 2011-04-28 | Purdue Pharma Lp | Antikörper, die an zellassoziiertes ca 125/0722p binden, und verfahren zu deren anwendung |
| US7312320B2 (en) * | 2003-12-10 | 2007-12-25 | Novimmune Sa | Neutralizing antibodies and methods of use thereof |
| EP2399932B1 (en) | 2005-05-12 | 2016-11-16 | ZymoGenetics, Inc. | Compositions and methods for modulating immune responses |
| AU2006269458B2 (en) | 2005-07-08 | 2012-11-08 | Biogen Ma Inc. | Sp35 antibodies and uses thereof |
| FR2906533B1 (fr) * | 2006-09-28 | 2013-02-22 | Pf Medicament | Procede de generation d'anticorps actifs contre un antigene de resistance,anticorps obtenus par ledit procede et leurs utilisations |
| PT2520590T (pt) | 2007-04-03 | 2018-11-14 | Amgen Res Munich Gmbh | Domínio de ligação específico de espécies cruzadas |
| CN104655854A (zh) | 2008-04-09 | 2015-05-27 | 健泰科生物技术公司 | 用于免疫相关疾病的治疗的新组合物和方法 |
| AU2015202123B2 (en) * | 2008-04-09 | 2017-06-15 | Genentech, Inc. | Novel compositions and methods for the treatment of immune related diseases |
| US8722856B2 (en) * | 2008-10-28 | 2014-05-13 | National University Corporation Hokkaido University | Anti-MUC1 antibody |
| EP2462161B1 (en) * | 2009-08-06 | 2017-03-08 | Immunas Pharma, Inc. | Antibodies that specifically bind to a beta oligomers and use thereof |
| JP2013507378A (ja) | 2009-10-09 | 2013-03-04 | メルク・シャープ・エンド・ドーム・コーポレイション | 抗her3抗体の製造、特徴づけ及びその用途 |
| WO2011066995A1 (en) * | 2009-12-05 | 2011-06-09 | Universität Heidelberg | Malaria vaccines based on apicomplexan ferlins, ferlin-like proteins and other c2-domain containing proteins |
| JP2013531982A (ja) | 2010-06-09 | 2013-08-15 | ザイモジェネティクス, インコーポレイテッド | 二量体vstm3融合タンパク質および関連組成物および方法 |
| NZ629913A (en) | 2010-08-23 | 2016-01-29 | Univ Texas | Anti-ox40 antibodies and methods of using the same |
| UA112434C2 (uk) * | 2011-05-27 | 2016-09-12 | Ґлаксо Ґруп Лімітед | Антигензв'язувальний білок, який специфічно зв'язується з всма |
| US9205144B2 (en) | 2011-06-03 | 2015-12-08 | Dana-Farber Cancer Institute, Inc. | Identification of conserved peptide blocks in homologous polypeptides |
| KR20130062168A (ko) * | 2011-12-02 | 2013-06-12 | 고려대학교 산학협력단 | 재조합 형광 단백질 나노입자 |
| MD20140108A2 (ro) | 2012-02-29 | 2015-03-31 | Gilead Biologics, Inc. | Anticorpi împotriva metaloproteinazei 9 matriciale |
| US20150086570A1 (en) * | 2012-03-29 | 2015-03-26 | Biogen Idec Ma Inc. | Biomarkers for use in integrin therapy applications |
| WO2013151999A1 (en) | 2012-04-02 | 2013-10-10 | President And Fellows Of Harvard College | Cancer treatment and immune system regulation through fat10 pathway inhibition |
| EP3202419A1 (en) | 2012-06-06 | 2017-08-09 | OncoMed Pharmaceuticals, Inc. | Pvrig binding agents that modulate the hippo pathway and uses thereof |
| SI2925350T1 (sl) | 2012-12-03 | 2019-04-30 | Bristol-Myers Squibb Company | Izboljšanje protirakave aktivnosti imunomodulatornih FC fuzijskih proteinov |
| EP2928483A4 (en) | 2012-12-04 | 2016-06-08 | Oncomed Pharm Inc | IMMUNOTHERAPY BY LIAISON AGENTS |
| CN103073644B (zh) * | 2012-12-31 | 2014-03-12 | 中国科学技术大学 | 特异性抗小鼠tigit的单克隆抗体及其制备方法、鉴定及应用 |
| US20140314741A1 (en) * | 2013-04-18 | 2014-10-23 | Developmen Center For Biotechnology | Human Antibody against Interleukin-20 and Treatment for Inflammatory Diseases |
| KR20230118704A (ko) * | 2013-07-16 | 2023-08-11 | 제넨테크, 인크. | Pd-1 축 결합 길항제 및 tigit 억제제를 사용한 암을치료하는 방법 |
| MX2016009858A (es) * | 2014-02-21 | 2017-01-26 | Medimmune Llc | Fusiones anti proteína convertasa subtilisina/kexina tipo 9 (anti-pcsk9)n péptido 1 similar a glucagón (glp-1) y métodos de uso. |
| AU2015289621A1 (en) | 2014-07-16 | 2017-01-12 | Genentech, Inc. | Methods of treating cancer using TIGIT inhibitors and anti-cancer agents |
| UA122395C2 (uk) | 2014-08-19 | 2020-11-10 | Мерк Шарп Енд Доум Корп. | Антитіло проти tigit |
| SG11201703376QA (en) | 2014-11-06 | 2017-05-30 | Genentech Inc | Combination therapy comprising ox40 binding agonists and tigit inhibitors |
| MX2017006323A (es) | 2014-11-21 | 2017-08-21 | Bristol Myers Squibb Co | Anticuerpos que comprenden regiones constantes pesadas modificadas. |
| KR102644115B1 (ko) | 2014-12-23 | 2024-03-05 | 브리스톨-마이어스 스큅 컴퍼니 | Tigit에 대한 항체 |
| EP3334757A4 (en) * | 2015-08-14 | 2019-04-03 | Merck Sharp & Dohme Corp. | ANTI-TIGIT ANTIBODIES |
| WO2017218707A2 (en) * | 2016-06-14 | 2017-12-21 | Xencor, Inc. | Bispecific checkpoint inhibitor antibodies |
| US9567399B1 (en) * | 2016-06-20 | 2017-02-14 | Kymab Limited | Antibodies and immunocytokines |
| US10793632B2 (en) * | 2016-08-30 | 2020-10-06 | Xencor, Inc. | Bispecific immunomodulatory antibodies that bind costimulatory and checkpoint receptors |
| RU2019138519A (ru) * | 2017-05-02 | 2021-06-02 | Мерк Шарп И Доум Корп. | Стабильные составы антител против tigit, отдельно и в комбинации с антителами против рецептора 1 программируемой смерти (pd-1), и способы их применения |
| US10981992B2 (en) * | 2017-11-08 | 2021-04-20 | Xencor, Inc. | Bispecific immunomodulatory antibodies that bind costimulatory and checkpoint receptors |
| US11312770B2 (en) * | 2017-11-08 | 2022-04-26 | Xencor, Inc. | Bispecific and monospecific antibodies using novel anti-PD-1 sequences |
| CN113811549A (zh) * | 2019-02-21 | 2021-12-17 | Xencor股份有限公司 | 非靶向和靶向性il-10 fc融合蛋白 |
| WO2023018677A1 (en) * | 2021-08-10 | 2023-02-16 | Merck Sharp & Dohme Llc | A therapeutic combination comprising a t1git antagonist, a pd-1 antagonist, and a chemotherapeutic agent(s) |
-
2016
- 2016-08-09 EP EP16837506.1A patent/EP3334757A4/en active Pending
- 2016-08-09 CN CN201680059753.7A patent/CN108290936B/zh active Active
- 2016-08-09 WO PCT/US2016/046100 patent/WO2017030823A2/en active Application Filing
- 2016-08-09 JP JP2018507015A patent/JP6976241B2/ja active Active
- 2016-08-09 CN CN202210784461.7A patent/CN115925931A/zh active Pending
- 2016-08-09 US US15/751,618 patent/US10766957B2/en active Active
- 2016-08-09 AU AU2016307845A patent/AU2016307845B2/en active Active
- 2016-08-09 CA CA2994555A patent/CA2994555A1/en active Pending
-
2020
- 2020-07-27 US US16/939,883 patent/US11958902B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| EP3334757A4 (en) | 2019-04-03 |
| US20210017276A1 (en) | 2021-01-21 |
| US11958902B2 (en) | 2024-04-16 |
| CA2994555A1 (en) | 2017-02-23 |
| WO2017030823A3 (en) | 2017-03-30 |
| AU2016307845A1 (en) | 2018-03-08 |
| JP6976241B2 (ja) | 2021-12-08 |
| AU2016307845B2 (en) | 2020-10-15 |
| WO2017030823A2 (en) | 2017-02-23 |
| CN108290936B (zh) | 2022-07-12 |
| US20180371083A1 (en) | 2018-12-27 |
| EP3334757A2 (en) | 2018-06-20 |
| US10766957B2 (en) | 2020-09-08 |
| CN108290936A (zh) | 2018-07-17 |
| JP2018527919A (ja) | 2018-09-27 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN108290936B (zh) | 抗tigit抗体 | |
| JP7066777B2 (ja) | 抗tigit抗体 | |
| JP6843174B2 (ja) | 抗lag3抗体および抗原結合性フラグメント |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination |