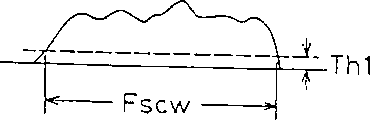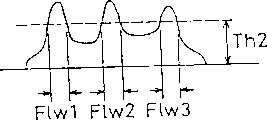CN1155824C - 尿液中有形成分分析装置及其方法 - Google Patents
尿液中有形成分分析装置及其方法 Download PDFInfo
- Publication number
- CN1155824C CN1155824C CNB961232897A CN96123289A CN1155824C CN 1155824 C CN1155824 C CN 1155824C CN B961232897 A CNB961232897 A CN B961232897A CN 96123289 A CN96123289 A CN 96123289A CN 1155824 C CN1155824 C CN 1155824C
- Authority
- CN
- China
- Prior art keywords
- haemolysis
- anticipation
- distribution plan
- split screen
- screen zone
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/483—Physical analysis of biological material
- G01N33/487—Physical analysis of biological material of liquid biological material
- G01N33/493—Physical analysis of biological material of liquid biological material urine
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume, or surface-area of porous materials
- G01N15/10—Investigating individual particles
- G01N15/14—Electro-optical investigation, e.g. flow cytometers
- G01N15/1456—Electro-optical investigation, e.g. flow cytometers without spatial resolution of the texture or inner structure of the particle, e.g. processing of pulse signals
Abstract
高精度地分类和计数尿液中含有的红血球数的尿液中有形成分分析装置和方法。本发明的分析装置具有用鞘液包裹包含尿液中有形成分、经过染色处理的试样液从而形成试样流的鞘流单元、向试样流照射光的光源、从各有形成分检测荧光强度和散射光信息的光检测部和根据检测的光学信息分析有形成分的分析部,而分析部具有从检测的光学信息中抽出与强度和发光时间有关的参量的参量抽出部、生成与上述多参量有关的第一和第二分布图的分布图生成部、存储预想分画面区域的设定条件存储部和确定非溶血红血球、溶血红血球的分布区域的分画面区域确定部和根据生成的第一、第二分布图计算关于有形成分的分析数据的运算部,计算的分析数据为溶血红血球数。
Description
技术领域
本发明涉及尿液中有形成分分析装置及其方法,例如,检测尿液中含有的血球、管型、上皮细胞、细菌等的装置及其方法。
背景技术
对于先有的粒子分析装置,已知的有向经过染色的粒子照射光、测量前方或侧面的荧光和散射光生成散射图对粒子进行分类的光学式装置和在电阻式的粒子计数器中将针状的部件插入测流孔内计数各种尺寸的粒子的装置等(例如,参见特开平4-337459号公报和在欧洲申请公开的公报第242971 A2号)。
使用这种先有的分析装置分析尿液中的红血球时,由于溶血红血球流出内容物后发生收缩,所以,在散射图中便出现在与通常的红血球(非溶血红血球)出现的区域不同的区域。
另外,通常的红血球随着时间的推移变化为溶血红血球,从而分布在与细菌及小的酵母样真菌重叠的区域。因此,高精度地检测尿液中的红血球并不是容易的事情。
发明内容
本发明就是考虑了这种情况而完成的,目的旨在提供可以检测溶血红血球和非溶血红血球从而可以高精度地计算红血球总数的尿液中有形成分分析装置及其方法。
本发明提供了一种尿液中有形成分分析装置,其特征在于包括:用鞘液包裹包含尿液中有形成分、经过染色处理的试样液,从而形成试样流的鞘流单元;向试样流照射光的光源;从各有形成分检测荧光信息和散射光信息的光检测部,和根据检测出的荧光信息和散射光信息分析有形成分的分析部,其中,所述分析部具有:从检测出的荧光信息和散射光信息中抽出与强度和发光时间有关的参量的参量抽出部;生成以散射光强度和荧光强度为所述参量的第一分布图和以荧光强度和散射光脉冲宽度为所述参量的第二分布图的分布图生成部;存储第1预想分画面区域、第2预想分画面区域和第3预想分画面区域的设定条件存储部,所述第1预想分画面区域预想在第一分布图存在非溶血红血球的分布的频数极大点,所述第2预想分画面区域预想在第一分布图存在溶血红血球的分布的频数极大点,所述第3预想分画面区域预想在第2分布图存在溶血红血球的分布的频数极大点;分画面区域确定部,用于根据由所述设定条件存储部读出的第1预想分画面区域和第1分布图的第1预想分画面区域内的频数极大点确定非溶血红血球的分布区域,根据由所述设定条件存储部读出的第2预想分画面区域和第1分布图的第2预想分画面区域内的频数极大点确定第1溶血红血球分布区域,根据从所述设定条件存储部读出的第3预想分画面区域和第2分布图的第3预想分画面区域内的频数极大点确定第2溶血红血球分布区域;以及根据第一分布图和第二分布图计算关于有形成分的分析数据的运算部,所述运算部对非溶血红血球数R和溶血红血球数r进行计数,利用R+r计算总红血球数作为分析数据。
本发明的分析装置中的被检测粒子(有形成分)主要是人的尿液中包含的血球、管型(cast)、粘液丝(mucous)和上皮细胞那样的粒子,这些粒子最好是预先利用荧光染料及荧光标识试剂处理过的。
所谓管型,就是Tomm-Horsfall粘蛋白在少量血清蛋白存在的条件下在肾小管腔内凝固沉淀成为基质而血液细胞及肾小管上皮细胞等埋入到该基质内形成的有形成分。
由于管型根据其形状是以圆筒或尿道细管腔为铸模形成的,所以称为cast(管型的存在,意味着尿道细管腔有暂时堵塞的现象,作为预示有肾障碍的角度看,是重要的,特别是包含血液细胞、上皮管型等内容物的管型,在临床上的意义是很高的)。
本发明的鞘流单元最好使用由通过细孔连通的上下2个单元构成,通过将包含粒子的试样液包到鞘液内流动,利用流体力学效应形成试样液的流动,使粒子成一串地通过细孔。本发明使用的鞘流单元,例如是使试样液以大约0.5~10m/sec的速度通过细孔。
光源是对正在通过细孔的、通过之前的或通过之后的粒子从鞘流单元的外部照射光束的光源,为此,最好将聚焦用透镜附加到连续发光(非脉冲发光式的光源)的激光光源上。照射的光束宽度(流动方向)最好为5~30μm。
光检测部是检测从接受光束的粒子发出的光学信息即散射光及荧光并将其变换为脉冲状的电信号的检测装置,为此,可以使用光电二极管、光电晶体管或光电倍增管等。分析部最好利用由CPU、ROM和RAM构成的微型计算机及个人计算机构成。
参量抽出部从关于检测的荧光及散射光的脉冲信号的各峰值分别抽出荧光强度F1和散射光强度Fsc,从脉冲宽度抽出荧光发光时间(荧光脉冲宽度)F1w和散射光发光时间(散射光脉冲宽度)Fscw等,峰值的抽出可以使用峰值保持电路,脉冲宽度的抽出可以使用计数电路。
抽出的参量变换为参量空间的分布数据F(X)。分布数据作为由根据需要从参量X1,X2,…,Xn中选择的m个(例如2个)参量X1,X2,…Xm规定的m维特征参量空间的坐标(X1,X2,…,Xm)的频数F(X1,X2,…,Xm)而形成。因此,分布图生成部生成以参量X1,X,…,Xm为轴的频数分布图(直方图和散射图)。
以尿液中有形成分作为分析对象时,能出现的有形成分的种类很多,另外,出现时的数量幅度也相当大,有形成分的出现形态很多(损伤的程度不同等),随着采样时间的经过,有形成分的形态及数量容易发生变化(细菌的繁殖、红血球溶血的进行、结晶的析出等)等,由于上述尿液特有的这些情况,与血液的情况相比,根据分布图分类分析有形成分是不容易的。例如,对于红血球,在健康人的尿液中几乎不出现,而在血尿的情况下,则出现数十个~数千个/μl以上(这以分布图中出现频数的不同进行表示)。另外,对于尿液中的红血球,是从损伤程度少、保持内容物的(非溶血)状态的红血球到内容物几乎全部溶出的(溶血)状态的红血球(这作为分布图的出现位置不同进行表示,或者以分布区域的广度进行表示)。进而,当溶血的红血球与其他有形成分(例如细菌)重叠分布时,这些粒子的分类就不容易进行。即使在细菌中,特别是当链杆菌非常多、大部分红血球溶血时,分类便非常困难,对于分类异常,必须表明是可靠性低的数据。
因此,本发明的运算部可高精度地计算包含溶血红血球数的红血球数作为分析数据,另外,还具有可靠性保证的指标,其原理如下:
即,计数非溶血红血球数和溶血红血球数,求出总红血球数。根据溶血红血球与总红血球数的比例判断分画面的异常/正常。若以散射光强度Fsc来看,非溶血红血球分布在高水平区域,溶血红血球分布在低水平区域。这时,溶血红血球与细菌可以相互重叠分布。但是,若以散射光发光时间(脉冲宽度)Fscw来看,溶液血红血球的散射光发光时间Fscw比非溶血红血球的小若干、而比细菌(除链杆菌外)的大,所以,两者可以识别。另一方面,若以散射光强度Fsc来看,可知链杆菌分布在某一阈值以下,所以,该阈值以下的链杆菌与该阈值以上的溶血红血球可以识别。
具体地说,就是测量尿液中的有形成分,生成以散射光强度Fsc和荧光强度F1为参量的第1分布图和以荧光强度F1和散射光脉冲宽度Fscw为参量的第2分布图。并且,在第1分布图中,分别设置主要出现非溶血红血球的区域A、主要出现Fsc水平比区域A低的溶血红血球的区域B和存在Fsc比区域A低的低水平的链杆菌的可能性小的区域C。
在第2分布图中,设定主要存在溶血红血球的区域D,分别求出在区域A出现的非溶血红血球数R、在区域B出现的溶血红血球数r1、根据在区域C(溶血红血球和其他粒子混合存在但不存在连锁杆菌的区域)出现的有形成分和在区域D(溶血红血球和链杆菌混合存在的区域)出现的有形成分的逻辑积得到的溶血红血球数r2,计算总红血球数RBC=R+r1+r2。
进而,计算溶血红血球比例h=(r1+r2)/(R+r1+r2),将该比例与预先设定的阈值进行比较,当大于阈值时,就视为分画面异常。这是利用由于作为将区域D的链杆菌除外的方法是采用求与区域C的逻辑积,有可能漏掉Fsc水平比区域C低的溶血红血球,从而溶血红血球比例越高越增大Fsc水平比区域C低的红血球的比例的性质。
因此,按照本发明的分析装置,可以将溶血红血球数与细菌区别、进行高精度的计数。另外,当溶血红血球与总红血球数的比例大(溶血红血球的漏计率高)时,就判定为分画面(分析)异常,所以,对溶血红血球及总红血球数的测量数据的可靠性不会降低。
本发明提供了一种尿液中有形成分分析方法,其特征在于包括下列步骤:用鞘液包裹包含尿液中有形成分、经过染色处理的试样液从而形成试样流;向试样流照射光并从各有形成分检测荧光信息和散射光;从检测出的荧光信息和散射光中抽出与强度和发光时间有关的参量;生成以散射光强度和荧光强度为参量的第一分布图和以荧光强度和散射光脉冲宽度为参量的第二分布图;从设定条件存储部读出预想在第一分布图存在非溶血红血球的分布频数极大点的第1预想分画面区域、预想在第一分布图存在溶血红血球的分布频数极大点的第2预想分画面区域和预想在第2分布图存在溶血红血球的分布频数极大点的第3预想分画面区域;根据由所述设定条件存储部读出的第1预想分画面区域和第1分布图的第1预想分画面区域内的频数极大点确定非溶血红血球的分布区域,根据由所述设定条件存储部读出的第2预想分画面区域和第1分布图的第2预想分画面区域内的频数极大点确定第1溶血红血球分布区域,根据从所述设定条件存储部读出的第3预想分画区域和第2分布图的第3预想分画面区域内的频数极大点确定第2溶血红血球分布区域;以及根据所述第一和第二分布图计算关于有形成分的分析数据,其中,上述计算分析数据的运算步骤包括对非溶血红血球数R和溶血红血球数r计数,从而计算出总红血球数作为分析数据的步骤。
附图说明
图1是本发明的一个实施例的结构图。
图2是图1的主要部分的断面图。
图3是表示实施例的主要部分的框图。
图4是表示图3的主要部分的框图。
图5是表示实施例的主要部分的动作的流程图。
图6是表示实施例的动作的分布图。
图7是表示实施例的动作的分布图。
图8是表示实施例的动作的分布图。
图9是表示实施例的动作的说明图。
图10是表示实施例的动作的说明图。
图11是表示实施例的动作的说明图。
图12是表示实施例的动作的分布图。
图13是表示实施例的动作的分布图。
图14是表示实施例的动作的分布图。
图15是表示实施例的动作的分布图。
图16是表示实施例的动作的分布图。
图17是表示实施例的动作的分布图。
图18是表示实施例的直方图。
图19是实施例的红血球的直方图。
图20是表示实施例的散射图的分布区域的说明图。
图21是表示管型的外形图。
图22是实施例的散射光脉冲的波形图。
图23是实施例的荧光脉冲的波形图。
图24是实施例的非溶血红血球和溶血红血球及细菌的直方图。
图25是实施例的非溶血红血球和溶血红血球及细菌的直方图。
具体实施方式
下面,根据附图所示的实施例详细说明本发明。但并不因此而限制本发明。
图1是表示分析装置的主要部分的结构的说明图,1和2是阀,3是从试样液容器(图中未示出)中吸引经过稀释、染色等前处理的试样液的吸管,4是注射器,5是流动单元,6是试样喷嘴,7a是第1单元,7a是第1单元,7b是第2单元,8是阀,9是鞘液容器,10是将鞘液向第1单元7a供给的供给口,11是具有图2所示的断面的连接第1单元7a和第2单元7b的细孔,包括测流孔状的部分(以后,称为测流孔进行说明)。
12是设在第1单元7a上的不锈钢制的电极,13是设在第2单元7b上的白金制的电极,14是设在第2单元7b上的排液口,15是以电极12为阴极、以电极13为阳极连接在电极12和电极13之间的直流恒流电源,16是将电源15的输出电压放大作为信号29而输出的放大器。
另外,17是氩激光光源,18是聚光器,19是光束挡板,20是聚焦透镜,21是针孔,22是分色镜,23是滤光器,24是光电倍增管,25是光电二极管,26是从试样喷嘴6喷出的试样液流,30是具有针孔21的遮光板。
在这样的结构中,首先,将阀1、2打开指定时间时,利用负压试样液(在本实施例中,包含尿液中有形成分的试样液)从吸管3充满阀1、2之间。
其次,通过注射器4以一定流量将阀1、2之间的试样液向试样喷嘴6内推压,试样液从试样喷嘴6向第1单元7a排出。
与此同时,通过打开阀8,向第1电源7a供给鞘液。
这样,试样液便被鞘液所包裹,进而由测流孔11细束从而形成鞘流。测流孔11的断面形状如图2所示,具有一边d为100~300μm的方孔,用光学玻璃(也包括石英玻璃)作成。
这样,通过形成鞘流,便可使试样液中预先包含的粒子一个一个地通过测流孔11排列成一串流动。通过测流孔11的试样液和鞘液从设在第2单元7b上的排液口14排出。
电极12、13间的电阻由鞘液的电导率、测流孔11的孔尺寸(截面面积)和孔长度、试样液的电导率、试样液的液流的直径决定。
通过使恒定电流从直流恒流电源15流过电极12、13之间,产生由电极12、13间的电阻和电流值决定的直流电压。另外,当粒子通过测流孔11时,由于测流孔11的两端的电阻发生变化,所以,在电极12、13间发生的电压只在粒子通过中变化为脉冲状,其变化部分的最大值(脉冲的峰值)与通过测流孔11的粒子的大小成正比。该变化部分由放大器16放大后作为电阻信号29(脉冲状的模拟信号)输出。
另一方面,从激光光源17发出的激光由聚光器18聚焦为椭圆形向流过测流孔11的试样液流26照射。该椭圆形的尺寸在试样的流动方向上与被检测粒子直径同量级,例如约为10μm,在与试样的流动方向正交的方向上远远大于被检测粒子直径,例如约为100~400μm。
未照射到试样液中的粒子上而直接透过流单元5的激光被光束挡板19挡住。从受到激光照射的粒子发出的前方散射光和前方荧光由聚焦透镜20聚焦后通过遮光板30的针孔21。并且,到达分色镜22。
波长比散射光长的荧光直接透过分色镜22,由滤光器23进一步滤除散射光后,由光电倍增管24检测,作为荧光信号27(脉冲状的模拟信号)输出。另外,散射光由分色镜22反射后由光电二极管25接收,作为散射光信号28(脉冲状的模拟信号)输出。
图3是处理按上述方式得到的荧光信号27、散射光信号28和电阻信号29的分析部100的框图,参量运算部200具有放大器31~33、直流再生电路34,35、比较器37,39、峰值保持电路38,50、时钟脉冲发生器52、计数器42,44、A/D变换器43,45,51和计数器用控制电路46。47是数据存储部,48是数据处理部,49是显示部。
下面,说明这种结构的信号处理动作的简要情况。
脉冲状的散射光信号28由放大器32放大后,由直流再生电路35固定为直流电平。从直流再生电路35输出的脉冲信号S2在比较器39中与阈值Th1(参见图22)进行比较,超过阈值Th1的期间(脉冲宽度)Fscw由计数器44作为散射光发光时间(散射光脉冲宽度)进行计时。散射光发光的最大值取入峰值保持电路50,由A/D变换器51进行A/D变换后获得散射光强度Fsc。脉冲状的荧光信号27由放大器31放大后,由直流再生电路34固定为直流电平作为信号S1输出。信号S1由比较器37与阈值Th2(参见图23)进行比较,超过阈值Th2的期间由计数器42进行计时,成为荧光发光时间(荧光脉冲宽度)F1w。
同时,荧光信号27的最大值由峰值保持电路38取入,由A/D变换器43进行A/D变换后,获得荧光强度F1。
脉冲状的电阻信号29由放大器33放大后,由采样保持电路40保持峰值(脉冲峰值),由A/D变换器45变换为数字值。
数字化的各计数器42、44和A/D变换器43、45、51的输出信号存储到数据存储部47内,同时传送给直方图及数据处理部48,进行粒子的辨别处理。
即,根据分布图(直方图或散射图)进行红血球、管型、透明管型、有封入体的管型等的分类。并且,对经过分类的粒子进行计数,并换算为每1微升试样的数量。另外,该结果与各种分布图一起在显示部49上进行显示。
图4是表示数据处理部48的结构的框图。图4中,61是用于预先设定各种值及预想区域等条件的数据输入部,例如由键盘及鼠标器构成。
另外,61a是存储设定的各种条件的设定条件存储部。62是根据数据存储部47存储的参量信息生成分布图即生成关于F1-Fsc、Fscw-F1、Fscw-F1w的各散射图及关于F1、Fsc、F1w、Fscw等的各直方图的分布图生成部,63是从由分布图生成部62生成的分布图抽出坐标及区域的抽出部。
64是在由分布图生成部62生成的分布图中决定各粒子的分画面区域的分画面区域生成部,65是进行分画面区域内的粒子数的计数及各种运算的运算部,66是当在分画面及计数的结果中检测到异常时发出警告的警告部,67是判断在确定的分画面区域中存在的粒子的种类的判断部。并且,运算部65的运算结果和警告部66发出的警告与由分布图生成部62生成的分布图一样在显示部49上进行显示。
下面,详细说明数据处理部48的主要动作。
(1)分布图中分画面区域的确定
该分析装置为了将检测的粒子进行分类,在分布图中确定分画面区域,这里使用图5的流程图说明该处理的一例。
首先,利用分布图生成部62生成F1-Fsc分布图(散射图),若显示为图6所示的那样时(S1),如果存在设定条件存储部61a存储的红血球的分布的频数极大点,就呼叫预想的预想分画面区域S0,如图7所示那样进行设定(S2)。
另外,使用者也可以使用输入部61改变预想分画面区域S0。
其次,抽出部63在区域S0中设定阈值,如图8所示的那样抽出频数超过该阈值具有比周围大的频数的点即极大点P1、P2……(S3)。
并且,对该极大点P1如图9所示的那样附加上假定是构成要求的分画面区域的一个点的标志(在图9中,用黑点表示)(S4)。
然后,带标志的点(黑点)与其周围的点按频数进行比较,频数低的点如图10所示的那样附加上标志(S5~S7)。反复进行该处理,当带标志的点的周围没有了频数低的点时(S6),如图11所示,就将带标志的点的集合确定为区域S1。
对于有多个极大点的情况,也进行同样的处理。对于极大点P2,确定区域S2(S9~S13),如图12所示,将区域S1和区域S2合并的区域确定为红血球分画面区域(S14)。
对于其他种类的粒子(有形成分),同样也确定各分画面区域,利用分画面区域进行了分类的粒子的频数由运算部65进行计数,并在显示部49进行显示。
如上所述,本发明的分画面方式是开始先确定1个以上的极大点,然后利用与各相邻点的频数的比较来扩大区域的方式,所以,即使分布形状复杂,即使存在多个频数的极大点,另外,即使分布数少,也可以不受这些因素的影响而确定分画面区域。
另外,即使分布随分析装置的灵敏度变化等多少发生偏离,也可以不受其影响而确定分画面区域。
此外,只要预先将分布图的坐标合并,便可减少处理对象的坐标,所以,可以简化处理程序,实现高速化分析。例如,如果将4×4的坐标合并为1个,分布图的坐标数就减少为1/16。
(2)溶血红血球的分析
在本发明中,进行以往未进行的溶血红血球的分析,所以,下面说明其分析顺序。
首先,分画面区域确定部64对由分布图生成部62生成的F1-Fsc的分布图如图13所示的那样确定主要存在非溶血红血球的区域A和主要存在散射光强度Fsc比区域A的红血球低的溶血红血球的区域B。
其次,利用输入部61设定存在散射光强度Fsc比区域A的红血球低的溶血红血球的区域C(但是,在区域C中,链杆菌的出现频度低)。
然后,分画面区域确定部64对由分布图生成部62生成的Fscw-F1分布图如图14所示的那样确定存在溶血红血球的区域D(但是,在区域D中能出现链杆菌)。
并且,运算部65分别计算在区域A中存在的非溶血红血球数R、在区域B中存在的溶血红血球数r1、以及在区域C和区域D中同时存在的溶血红血球数r2。
并且,利用下式计算溶血红血球数r和总红血球数RBC。
r=r1+r2 (1)
RBC=R+r (2)
溶血红血球数r随时间而变化。例如,用Fsc的直方图(图24)观察时,即使非溶血红血球数R与溶血红血球数r的比率是80%对20%,该比率也随时间而变化,如图25所示,成为20%和80%。
在图25中,由于细菌的频数分布J与溶血红血球数r的分布重叠部分大,所以,在图25那样的状态下,即使计数溶血红血球数r,也不可能高精度地进行计数。即,当溶血红血球数r的计数值大于指定值时,就认为该计数值是不正确的值。
因此,区域C考虑溶血红血球随时间的变化,利用输入部61进行半固定地设定。
另外,运算部65按照h=r/(R+r)计算溶血红血球比率h,当h大于指定值时,由溶血红血球的分布区域与细菌的分布区域相互重叠,所以,就视为分画面异常,警告部66就使显示部49显示该异常。
这样,按照本发明,由于计数了以往未测量的溶血红血球,所以,可以求出尿液中的总红血球数。另外,还可以跟踪其随时间的变化高精度地测量溶血红血球数。
(3)分析异常(分画面)的警告
该分析装置具有警告上述分析(分画面)异常的功能,此外,当判定在同一分画面区域混合存在不同种类的粒子时,就视为不能进行分画面并进行警告。首先以草酸钙和红血球为例说明该处理顺序。
当利用分布图生成部62生成F1-Fsc分布图且分画面区域确定部64如图16那样确定了分画面区域X时,分画面区域确定部64就与预先设定的预想存在红血球的区域S0进行比较。草酸钙的区域X与区域S0几乎完全重叠,与区域S0相比,由于Fsc直到高水平存在,所以,当二者之差大于指定水平时,警告部66就发出由于存在草酸钙不可能进行红血球的分画面处理的警告。
另外,当存在DHA结晶时,如图17的F1-Fsc分布图所示的那样,由于横切设定的预想区域S0而存在,所以,只有红血球不能正确地进行分画面处理。
这时,对于由分布图生成部62生成的F1的直方图(图18),警告部66将其频数的峰值a与a/5的频数的分布宽度b之比b/a和指定值进行比较。该指定值根据通常的红血球的直方图(图19)进行设定。因此,当b/a大于指定值时,警告部66就发出由于存在DHA结晶不可能进行红血球的分画面处理的警告。
(4)管型的检测和细分类
利用对细胞膜和细胞核染色的染色法预先对尿液中的有形成分(粒子)进行染色时,对于血球、上皮、细菌和结晶,散射光发光时间Fscw和荧光发光时间F1w的比率基本上是相同的值,但是,管型的蛋白质部分由于染色微弱,其比率不同。
另外,包含内容物的管型由于内容物被进行了染色,所以,其比率将随内容物的密度而变化。
利用这种特性在该分析装置中进行管型的分类,同时将管型分为包含内容物的管型和不包含内容物的管型(透明管型)。
具体地说,就是如果图21所示的管型Z的尺寸L与图22所示的散射光脉冲宽度Fscw成正比,并且管型Z预先进行了染色,则内容物Z1、Z2、Z3的尺寸L1、L2、L3分别与图23所示的荧光信号的脉冲宽度F1w1、F1w2、F1w3成正比。
另外,图22和图23的Th1和Th2是预先设定在图3的比较器39、37内的阈值。
因此,在该分析装置中,令
Flw=Flw1+Flw2+Flw3 (3)
即,对于1个管型,当获得荧光脉冲宽度F1w1、F1w2、……F1wn时,就按下式计算从1个管型获得的脉冲宽度F1w
在分布图生成部62根据这样获得的F1w生成的Fscw-F1w分布图中,如图20所示,红血球分布区域T1、白血球分布区域T2和上皮细胞分布区域T3基本上排列在直线L1上,管型的分布区域T4则以直线L2为界远离区域T1~T3而存在。
因此,判断部67将分布在直线L2下侧的区域T4确定为管型的分布区域。
另外,对于散射图的各坐标,当F1w/Fscw的值小于直线L2的斜率时,也可以将该坐标所属的区域确定为管型区域。
另外,通常根据内容物的含量多少将管型分为含内容物管型和不含内容物管型(透明管型)。
因此,如果利用输入部61将成为分类基准的直线L3设定为图20所示的那样,则判断部67就以该直线L3为界将上侧区域T4a判定为含内容物管型的分布区域,将下侧区域T4b判定为透明管型的分布区域。
按照本发明,可以识别溶血红血球与细菌,所以,可以计数溶血红血球和总红血球数。
Claims (8)
1.一种尿液中有形成分分析装置,其特征在于包括:
用鞘液包裹包含尿液中有形成分、经过染色处理的试样液,从而形成试样流的鞘流单元;
向试样流照射光的光源;
从各有形成分检测荧光信息和散射光信息的光检测部,和
根据检测出的荧光信息和散射光信息分析有形成分的分析部,
其中,所述分析部具有:从检测出的荧光信息和散射光信息中抽出与强度和发光时间有关的参量的参量抽出部;
生成以散射光强度和荧光强度为所述参量的第一分布图和以荧光强度和散射光脉冲宽度为所述参量的第二分布图的分布图生成部;
存储第1预想分画面区域、第2预想分画面区域和第3预想分画面区域的设定条件存储部,所述第1预想分画面区域预想在第一分布图存在非溶血红血球的分布的频数极大点,所述第2预想分画面区域预想在第一分布图存在溶血红血球的分布的频数极大点,所述第3预想分画面区域预想在第二分布图存在溶血红血球的分布的频数极大点;
分画面区域确定部,用于根据由所述设定条件存储部读出的第1预想分画面区域和第一分布图的第1预想分画面区域内的频数极大点确定非溶血红血球的分布区域,根据由所述设定条件存储部读出的第2预想分画面区域和第一分布图的第2预想分画面区域内的频数极大点确定第1溶血红血球分布区域,根据从所述设定条件存储部读出的第3预想分画面区域和第二分布图的第3预想分画面区域内的频数极大点确定第2溶血红血球分布区域;以及
根据第一分布图和第二分布图计算关于有形成分的分析数据的运算部,
所述运算部对非溶血红血球数R和溶血红血球数r进行计数,利用R+r计算总红血球数作为分析数据。
2.按权利要求1所述的尿液中有形成分分析装置,其特征在于:所述运算部利用h=r/(R+r)计算溶血红血球比h。
3.按权利要求2所述的尿液中有形成分分析装置,其特征在于:所述分析部进而还具有当h大于指定值时发出警告的警告部。
4.按权利要求1~3的任一项所述的尿液中有形成分分析装置,其特征在于:抽出的参量由荧光强度F1、散射光强度Fsc和散射光发光时间Fscw构成,利用根据F1-Fsc的分布图计数的溶血红血球数r1与根据F1-Fsc的分布图及Fscw-F1的分布图计数的溶血红血球数r2之和计算溶血红血球数r。
5.一种尿液中有形成分分析方法,其特征在于包括下列步骤:
用鞘液包裹包含尿液中有形成分、经过染色处理的试样液从而形成试样流;
向试样流照射光并从各有形成分检测荧光信息和散射光;
从检测出的荧光信息和散射光中抽出与强度和发光时间有关的参量;
生成以散射光强度和荧光强度为参量的第一分布图和以荧光强度和散射光脉冲宽度为参量的第二分布图;
从设定条件存储部读出预想在第一分布图存在非溶血红血球的分布频数极大点的第1预想分画面区域、预想在第一分布图存在溶血红血球的分布频数极大点的第2预想分画面区域和预想在第二分布图存在溶血红血球的分布频数极大点的第3预想分画面区域;
根据由所述设定条件存储部读出的第1预想分画面区域和第一分布图的第1预想分画面区域内的频数极大点确定非溶血红血球的分布区域,根据由所述设定条件存储部读出的第2预想分画面区域和第一分布图的第2预想分画面区域内的频数极大点确定第1溶血红血球分布区域,根据从所述设定条件存储部读出的第3预想分画区域和第二分布图的第3预想分画面区域内的频数极大点确定第2溶血红血球分布区域;以及
根据所述第一和第二分布图计算关于有形成分的分析数据,
其中,上述计算分析数据的运算步骤包括对非溶血红血球数R和溶血红血球数r计数,从而计算出总红血球数作为分析数据的步骤。
6.按权利要求5所述的尿液中有形成分分析方法,其特征在于:计算分析数据的步骤进而还包括利用h=r/(R+r)计算溶血红血球比h的步骤。
7.按权利要求6所述的尿液中有形成分分析方法,其特征在于:还包括当h大于指定值时发出警告的步骤。
8.按权利要求5~7的任一项所述的尿液中有形成分分析方法,其特征在于:抽出的参量由荧光强度F1、散射光强度Fsc和散射光发光时间Fscw构成,利用根据F1-Fsc的分布图计数的溶血红血球数r1与根据F1-Fsc的分布图及Fscw-F1的分布图计数的溶血红血球数r2之和计算溶血红血球数r。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP35071295 | 1995-12-19 | ||
| JP350712/1995 | 1995-12-19 | ||
| JP350712/95 | 1995-12-19 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN1159583A CN1159583A (zh) | 1997-09-17 |
| CN1155824C true CN1155824C (zh) | 2004-06-30 |
Family
ID=18412345
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CNB961232897A Expired - Fee Related CN1155824C (zh) | 1995-12-19 | 1996-12-19 | 尿液中有形成分分析装置及其方法 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US5731867A (zh) |
| EP (1) | EP0780680B1 (zh) |
| JP (1) | JP3313291B2 (zh) |
| KR (1) | KR970048450A (zh) |
| CN (1) | CN1155824C (zh) |
| DE (1) | DE69630005T2 (zh) |
| TW (1) | TW438973B (zh) |
Families Citing this family (34)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6133995A (en) * | 1997-05-09 | 2000-10-17 | Sysmex Corporation | Particle measuring apparatus |
| US6295146B1 (en) * | 1998-01-14 | 2001-09-25 | Mci Communications Corporation | System and method for sharing a spare channel among two or more optical ring networks |
| JP3867880B2 (ja) * | 1998-04-08 | 2007-01-17 | シスメックス株式会社 | 尿中赤血球の鑑別装置および方法 |
| CA2640578A1 (en) | 1998-05-14 | 1999-11-18 | Luminex Corporation | Multi-analyte diagnostic system and computer implemented process for same |
| US6087182A (en) | 1998-08-27 | 2000-07-11 | Abbott Laboratories | Reagentless analysis of biological samples |
| JP4101994B2 (ja) | 1999-01-21 | 2008-06-18 | シスメックス株式会社 | 粒子分析装置および自動粒子分析方法 |
| JP3817091B2 (ja) * | 1999-07-02 | 2006-08-30 | テルモ株式会社 | 細胞数測定装置 |
| US6631211B1 (en) * | 1999-07-08 | 2003-10-07 | Perkinelmer Las, Inc. | Interactive system for analyzing scatter plots |
| JP4708605B2 (ja) * | 2000-07-24 | 2011-06-22 | シスメックス株式会社 | 粒子分析装置とその粒子分画方法 |
| JP4659252B2 (ja) * | 2001-03-29 | 2011-03-30 | シスメックス株式会社 | フローサイトメータ |
| US6979570B2 (en) * | 2001-07-26 | 2005-12-27 | Sysmex Corporation | Particle analyzer and particle analyzing method |
| US9429509B2 (en) * | 2002-01-28 | 2016-08-30 | Sysmex Corporation | Particle analyzer and particle analysis method |
| US7319907B2 (en) * | 2002-11-18 | 2008-01-15 | International Remote Imaging Systems, Inc. | Multi-level controller system |
| JP4057539B2 (ja) * | 2004-01-09 | 2008-03-05 | 浜松ホトニクス株式会社 | シースフローセルキュベット及びその製造方法 |
| JP4563743B2 (ja) * | 2004-07-15 | 2010-10-13 | シスメックス株式会社 | 尿中有形成分分析装置と方法 |
| JP4733949B2 (ja) | 2004-09-17 | 2011-07-27 | シスメックス株式会社 | 分析装置、プログラムおよびそのプログラムを記録した記録媒体 |
| JP4413120B2 (ja) * | 2004-09-30 | 2010-02-10 | シスメックス株式会社 | 検体中粒子分析方法及び分析装置 |
| US20070037135A1 (en) * | 2005-08-08 | 2007-02-15 | Barnes Russell H | System and method for the identification and quantification of a biological sample suspended in a liquid |
| JP4817442B2 (ja) * | 2006-07-31 | 2011-11-16 | シスメックス株式会社 | 粒子分析装置用光学系、及びそれを用いた粒子分析装置 |
| JP4817450B2 (ja) * | 2007-01-31 | 2011-11-16 | シスメックス株式会社 | 血液分析装置、血液分析方法およびコンピュータプログラム |
| JP5259305B2 (ja) * | 2007-10-03 | 2013-08-07 | シスメックス株式会社 | 細胞分析装置及び細胞分析方法 |
| JP2011501132A (ja) * | 2007-10-10 | 2011-01-06 | ポカード・ディアグノスティクス・リミテッド | 尿中のバクテリアの同定を行うためのシステム |
| JP5685378B2 (ja) * | 2010-01-08 | 2015-03-18 | シスメックス株式会社 | 検体分析装置および検体分析方法 |
| EP2348301B1 (en) | 2010-01-08 | 2013-08-21 | Sysmex Corporation | Sample analyzer |
| CN101900737A (zh) * | 2010-06-10 | 2010-12-01 | 上海理工大学 | 基于支持向量机的尿沉渣有形成分自动识别系统 |
| DK2658965T3 (da) * | 2010-12-31 | 2016-06-13 | Universität Für Bodenkultur Wien | Fremgangsmåde til fremstilling af inducerede pluripotente stamceller og differentierede celler |
| WO2014078741A1 (en) * | 2012-11-16 | 2014-05-22 | Beckman Coulter, Inc. | Flow cytometry data segmentation result evaluation systems and methods |
| JP6317976B2 (ja) * | 2014-03-31 | 2018-04-25 | シスメックス株式会社 | 尿検体分析方法及び尿検体分析装置 |
| CN105090810A (zh) * | 2014-05-16 | 2015-11-25 | 科宝智慧医疗科技(上海)有限公司 | 一种照明装置 |
| DE102015002750A1 (de) * | 2015-03-05 | 2016-09-08 | Mann + Hummel Gmbh | Messeinrichtung zur Ermittlung von Partikeln in einem Messfluid |
| JP6352871B2 (ja) * | 2015-08-28 | 2018-07-04 | シスメックス株式会社 | 尿検体分析装置および尿検体分析方法 |
| JP6680492B2 (ja) * | 2015-09-11 | 2020-04-15 | シスメックス株式会社 | 細胞分析装置および細胞分析方法 |
| CN109297946A (zh) * | 2018-11-28 | 2019-02-01 | 浙江瑞宝生物科技有限公司 | 健康监护型智能座便器装置及其潜血检测方法 |
| CN109612911B (zh) * | 2018-12-26 | 2023-07-21 | 深圳天依生命健康科技有限公司 | 全自动精子细胞检测仪 |
Family Cites Families (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3844662A (en) * | 1971-07-13 | 1974-10-29 | Froreich A Von | Sedimentation instrument for body fluids and method of microscopic examination of the sediment |
| JPS55136958A (en) * | 1979-04-14 | 1980-10-25 | Olympus Optical Co Ltd | Automatic analyzer |
| US4667830A (en) * | 1981-06-15 | 1987-05-26 | The Board Of Trustees Of The Leland Stanford Junior University | Method and means for sorting individual particles into containers for culturing, cloning, analysis, or the like |
| US4992365A (en) * | 1984-04-23 | 1991-02-12 | Hyman Edward S | Method of detecting bacteria in urine |
| GB8606299D0 (en) * | 1986-03-14 | 1986-04-23 | Holley J E F | Scanner |
| US4845653A (en) * | 1987-05-07 | 1989-07-04 | Becton, Dickinson And Company | Method of displaying multi-parameter data sets to aid in the analysis of data characteristics |
| JP2935529B2 (ja) * | 1990-03-01 | 1999-08-16 | シスメックス株式会社 | 白血球分類方法および試薬 |
| US5047321A (en) * | 1988-06-15 | 1991-09-10 | Becton Dickinson & Co. | Method for analysis of cellular components of a fluid |
| JPH0222537A (ja) * | 1988-07-11 | 1990-01-25 | Omron Tateisi Electron Co | 細胞分折装置 |
| JP3070968B2 (ja) * | 1991-05-14 | 2000-07-31 | シスメックス株式会社 | 尿中の細胞分析用試薬及び方法 |
| JP3098273B2 (ja) * | 1991-05-14 | 2000-10-16 | シスメックス株式会社 | 尿中の細胞分析装置 |
| JP3213334B2 (ja) * | 1991-05-14 | 2001-10-02 | シスメックス株式会社 | 尿中の細胞分析装置 |
| JP3145486B2 (ja) * | 1992-06-12 | 2001-03-12 | シスメックス株式会社 | イメージングフローサイトメータ |
-
1996
- 1996-11-13 TW TW085113825A patent/TW438973B/zh not_active IP Right Cessation
- 1996-11-28 JP JP31802596A patent/JP3313291B2/ja not_active Expired - Fee Related
- 1996-12-04 KR KR1019960061525A patent/KR970048450A/ko not_active Application Discontinuation
- 1996-12-17 US US08/767,782 patent/US5731867A/en not_active Expired - Fee Related
- 1996-12-18 EP EP96402791A patent/EP0780680B1/en not_active Expired - Lifetime
- 1996-12-18 DE DE69630005T patent/DE69630005T2/de not_active Expired - Fee Related
- 1996-12-19 CN CNB961232897A patent/CN1155824C/zh not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| EP0780680A3 (en) | 1999-12-15 |
| CN1159583A (zh) | 1997-09-17 |
| EP0780680B1 (en) | 2003-09-17 |
| JPH09229926A (ja) | 1997-09-05 |
| DE69630005D1 (de) | 2003-10-23 |
| TW438973B (en) | 2001-06-07 |
| DE69630005T2 (de) | 2004-07-15 |
| JP3313291B2 (ja) | 2002-08-12 |
| US5731867A (en) | 1998-03-24 |
| EP0780680A2 (en) | 1997-06-25 |
| KR970048450A (ko) | 1997-07-29 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN1155824C (zh) | 尿液中有形成分分析装置及其方法 | |
| CN1153063C (zh) | 尿液中有形成分分析装置 | |
| CN1121612C (zh) | 尿液中有形成分分析装置 | |
| US5719666A (en) | Particle analyzer classifying particles of various biological types using a correlation of measurements | |
| JP5323829B2 (ja) | 細胞の識別およびソーティング方法およびその装置 | |
| US10337975B2 (en) | Method and system for characterizing particles using a flow cytometer | |
| EP0515099B1 (en) | Apparatus for analyzing cells in urine | |
| EP0681177A1 (en) | Method and apparatus for cell counting and cell classification | |
| EP0514178B1 (en) | Apparatus for analyzing cells in urine | |
| US20170102310A1 (en) | Flow cytometer and a multi-dimensional data classification method and an apparatus thereof | |
| JP2021522491A (ja) | 粒子分析器のための特性評価および選別 | |
| CN114813522A (zh) | 基于显微放大数字图像的血液细胞分析方法及系统 | |
| CN110226083A (zh) | 红细胞碎片识别方法和装置、血液细胞分析仪及分析方法 | |
| US20230011382A1 (en) | Off-focus microscopic images of a sample | |
| JP3642658B2 (ja) | 尿中有形成分分析装置および分析方法 | |
| CN112432948A (zh) | 一种外周血细胞形态学自动检测方法 | |
| JP3504030B2 (ja) | 粒子判定基準の決定方法およびその装置並びにその判定基準を用いた粒子分析装置 | |
| EP3244191A1 (en) | Method and system for characterizing particles using a flow cytometer | |
| EP2937681A1 (en) | Particle detection device and particle detection method | |
| CN116324383A (zh) | 信息处理装置、粒子分析装置、粒子筛分装置以及信息处理方法 | |
| JP3325447B2 (ja) | 粒子分析装置およびその方法 | |
| EP4348222A1 (en) | Methods and systems for classifying flow cyometer data | |
| CN114414442A (zh) | 样本检测方法、装置及计算机可读存储介质 | |
| CN114907960A (zh) | 一种基于液滴微流控的无标记活细胞筛选系统和方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C14 | Grant of patent or utility model | ||
| GR01 | Patent grant | ||
| C19 | Lapse of patent right due to non-payment of the annual fee | ||
| CF01 | Termination of patent right due to non-payment of annual fee |