CN109642009B - 硅烷官能的聚合聚氨酯 - Google Patents
硅烷官能的聚合聚氨酯 Download PDFInfo
- Publication number
- CN109642009B CN109642009B CN201780048302.8A CN201780048302A CN109642009B CN 109642009 B CN109642009 B CN 109642009B CN 201780048302 A CN201780048302 A CN 201780048302A CN 109642009 B CN109642009 B CN 109642009B
- Authority
- CN
- China
- Prior art keywords
- groups
- reaction
- group
- isocyanate
- compound
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/28—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen characterised by the compounds used containing active hydrogen
- C08G18/40—High-molecular-weight compounds
- C08G18/62—Polymers of compounds having carbon-to-carbon double bonds
- C08G18/6216—Polymers of alpha-beta ethylenically unsaturated carboxylic acids or of derivatives thereof
- C08G18/625—Polymers of alpha-beta ethylenically unsaturated carboxylic acids; hydrolyzed polymers of esters of these acids
- C08G18/6258—Polymers of alpha-beta ethylenically unsaturated carboxylic acids; hydrolyzed polymers of esters of these acids the acid groups being esterified with polyhydroxy compounds or epoxy compounds during or after polymerization
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/70—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen characterised by the isocyanates or isothiocyanates used
- C08G18/72—Polyisocyanates or polyisothiocyanates
- C08G18/80—Masked polyisocyanates
- C08G18/8061—Masked polyisocyanates masked with compounds having only one group containing active hydrogen
- C08G18/8083—Masked polyisocyanates masked with compounds having only one group containing active hydrogen with compounds containing at least one heteroatom other than oxygen or nitrogen
- C08G18/809—Masked polyisocyanates masked with compounds having only one group containing active hydrogen with compounds containing at least one heteroatom other than oxygen or nitrogen containing silicon
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/08—Processes
- C08G18/16—Catalysts
- C08G18/22—Catalysts containing metal compounds
- C08G18/227—Catalysts containing metal compounds of antimony, bismuth or arsenic
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/08—Processes
- C08G18/16—Catalysts
- C08G18/22—Catalysts containing metal compounds
- C08G18/24—Catalysts containing metal compounds of tin
- C08G18/244—Catalysts containing metal compounds of tin tin salts of carboxylic acids
- C08G18/246—Catalysts containing metal compounds of tin tin salts of carboxylic acids containing also tin-carbon bonds
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/28—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen characterised by the compounds used containing active hydrogen
- C08G18/2805—Compounds having only one group containing active hydrogen
- C08G18/288—Compounds containing at least one heteroatom other than oxygen or nitrogen
- C08G18/289—Compounds containing at least one heteroatom other than oxygen or nitrogen containing silicon
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/28—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen characterised by the compounds used containing active hydrogen
- C08G18/40—High-molecular-weight compounds
- C08G18/4009—Two or more macromolecular compounds not provided for in one single group of groups C08G18/42 - C08G18/64
- C08G18/4063—Mixtures of compounds of group C08G18/62 with other macromolecular compounds
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/28—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen characterised by the compounds used containing active hydrogen
- C08G18/40—High-molecular-weight compounds
- C08G18/42—Polycondensates having carboxylic or carbonic ester groups in the main chain
- C08G18/4205—Polycondensates having carboxylic or carbonic ester groups in the main chain containing cyclic groups
- C08G18/4208—Polycondensates having carboxylic or carbonic ester groups in the main chain containing cyclic groups containing aromatic groups
- C08G18/4211—Polycondensates having carboxylic or carbonic ester groups in the main chain containing cyclic groups containing aromatic groups derived from aromatic dicarboxylic acids and dialcohols
- C08G18/4219—Polycondensates having carboxylic or carbonic ester groups in the main chain containing cyclic groups containing aromatic groups derived from aromatic dicarboxylic acids and dialcohols from aromatic dicarboxylic acids and dialcohols in combination with polycarboxylic acids and/or polyhydroxy compounds which are at least trifunctional
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/28—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen characterised by the compounds used containing active hydrogen
- C08G18/40—High-molecular-weight compounds
- C08G18/62—Polymers of compounds having carbon-to-carbon double bonds
- C08G18/6216—Polymers of alpha-beta ethylenically unsaturated carboxylic acids or of derivatives thereof
- C08G18/625—Polymers of alpha-beta ethylenically unsaturated carboxylic acids; hydrolyzed polymers of esters of these acids
- C08G18/6254—Polymers of alpha-beta ethylenically unsaturated carboxylic acids and of esters of these acids containing hydroxy groups
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/28—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen characterised by the compounds used containing active hydrogen
- C08G18/67—Unsaturated compounds having active hydrogen
- C08G18/68—Unsaturated polyesters
- C08G18/683—Unsaturated polyesters containing cyclic groups
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/70—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen characterised by the isocyanates or isothiocyanates used
- C08G18/71—Monoisocyanates or monoisothiocyanates
- C08G18/718—Monoisocyanates or monoisothiocyanates containing silicon
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/70—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen characterised by the isocyanates or isothiocyanates used
- C08G18/72—Polyisocyanates or polyisothiocyanates
- C08G18/73—Polyisocyanates or polyisothiocyanates acyclic
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/70—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen characterised by the isocyanates or isothiocyanates used
- C08G18/72—Polyisocyanates or polyisothiocyanates
- C08G18/74—Polyisocyanates or polyisothiocyanates cyclic
- C08G18/75—Polyisocyanates or polyisothiocyanates cyclic cycloaliphatic
- C08G18/751—Polyisocyanates or polyisothiocyanates cyclic cycloaliphatic containing only one cycloaliphatic ring
- C08G18/752—Polyisocyanates or polyisothiocyanates cyclic cycloaliphatic containing only one cycloaliphatic ring containing at least one isocyanate or isothiocyanate group linked to the cycloaliphatic ring by means of an aliphatic group
- C08G18/753—Polyisocyanates or polyisothiocyanates cyclic cycloaliphatic containing only one cycloaliphatic ring containing at least one isocyanate or isothiocyanate group linked to the cycloaliphatic ring by means of an aliphatic group containing one isocyanate or isothiocyanate group linked to the cycloaliphatic ring by means of an aliphatic group having a primary carbon atom next to the isocyanate or isothiocyanate group
- C08G18/755—Polyisocyanates or polyisothiocyanates cyclic cycloaliphatic containing only one cycloaliphatic ring containing at least one isocyanate or isothiocyanate group linked to the cycloaliphatic ring by means of an aliphatic group containing one isocyanate or isothiocyanate group linked to the cycloaliphatic ring by means of an aliphatic group having a primary carbon atom next to the isocyanate or isothiocyanate group and at least one isocyanate or isothiocyanate group linked to a secondary carbon atom of the cycloaliphatic ring, e.g. isophorone diisocyanate
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/70—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen characterised by the isocyanates or isothiocyanates used
- C08G18/72—Polyisocyanates or polyisothiocyanates
- C08G18/77—Polyisocyanates or polyisothiocyanates having heteroatoms in addition to the isocyanate or isothiocyanate nitrogen and oxygen or sulfur
- C08G18/78—Nitrogen
- C08G18/79—Nitrogen characterised by the polyisocyanates used, these having groups formed by oligomerisation of isocyanates or isothiocyanates
- C08G18/797—Nitrogen characterised by the polyisocyanates used, these having groups formed by oligomerisation of isocyanates or isothiocyanates containing carbodiimide and/or uretone-imine groups
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09D—COATING COMPOSITIONS, e.g. PAINTS, VARNISHES OR LACQUERS; FILLING PASTES; CHEMICAL PAINT OR INK REMOVERS; INKS; CORRECTING FLUIDS; WOODSTAINS; PASTES OR SOLIDS FOR COLOURING OR PRINTING; USE OF MATERIALS THEREFOR
- C09D175/00—Coating compositions based on polyureas or polyurethanes; Coating compositions based on derivatives of such polymers
- C09D175/04—Polyurethanes
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09D—COATING COMPOSITIONS, e.g. PAINTS, VARNISHES OR LACQUERS; FILLING PASTES; CHEMICAL PAINT OR INK REMOVERS; INKS; CORRECTING FLUIDS; WOODSTAINS; PASTES OR SOLIDS FOR COLOURING OR PRINTING; USE OF MATERIALS THEREFOR
- C09D175/00—Coating compositions based on polyureas or polyurethanes; Coating compositions based on derivatives of such polymers
- C09D175/04—Polyurethanes
- C09D175/14—Polyurethanes having carbon-to-carbon unsaturated bonds
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09J—ADHESIVES; NON-MECHANICAL ASPECTS OF ADHESIVE PROCESSES IN GENERAL; ADHESIVE PROCESSES NOT PROVIDED FOR ELSEWHERE; USE OF MATERIALS AS ADHESIVES
- C09J175/00—Adhesives based on polyureas or polyurethanes; Adhesives based on derivatives of such polymers
- C09J175/04—Polyurethanes
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09J—ADHESIVES; NON-MECHANICAL ASPECTS OF ADHESIVE PROCESSES IN GENERAL; ADHESIVE PROCESSES NOT PROVIDED FOR ELSEWHERE; USE OF MATERIALS AS ADHESIVES
- C09J175/00—Adhesives based on polyureas or polyurethanes; Adhesives based on derivatives of such polymers
- C09J175/04—Polyurethanes
- C09J175/14—Polyurethanes having carbon-to-carbon unsaturated bonds
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G2150/00—Compositions for coatings
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G2170/00—Compositions for adhesives
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G2190/00—Compositions for sealing or packing joints
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Materials Engineering (AREA)
- Engineering & Computer Science (AREA)
- Life Sciences & Earth Sciences (AREA)
- Wood Science & Technology (AREA)
- Polyurethanes Or Polyureas (AREA)
- Sealing Material Composition (AREA)
- Paints Or Removers (AREA)
- Adhesives Or Adhesive Processes (AREA)
- Silicon Polymers (AREA)
- Addition Polymer Or Copolymer, Post-Treatments, Or Chemical Modifications (AREA)
Abstract
本发明涉及用于制备含硅烷基团的聚氨酯的方法、通过所述方法可得到的产物以及其用于制备特别是用于漆料原料、密封剂原料或胶粘剂原料的可交联的粘合剂的用途。
Description
本发明涉及用于制备含硅烷基团的聚氨酯的方法、通过此方法可得的含硅烷基团的聚氨酯、其在可交联的漆料原料、密封剂原料或胶粘剂原料中作为粘合剂的用途以及具有本发明的含硅烷基团的聚氨酯的可交联的粘合剂。
硅烷官能的聚氨酯作为用于胶粘剂、密封剂或涂料的粘合剂已经久为人知且已经描述过多次。
带有硅烷基团的聚氨酯可以以各种方式制备,例如通过多异氰酸酯或异氰酸酯官能的预聚物与对于异氰酸酯基团呈反应性的硅烷化合物,例如仲氨基烷基硅烷或巯基烷基硅烷的反应。
由于其产生具有特别低粘度的硅烷官能的聚氨酯而常常优选的一种方法是使羟基官能的化合物,例如聚醚多元醇、聚氨酯多元醇或聚酯多元醇与异氰酸根合有机硅烷,例如US 3,494,951或EP-A 0 649 850中描述的异氰酸根合烷基烷氧基硅烷反应。通过使用该类异氰酸根合烷基硅烷,可以例如由羟基官能的聚氨酯预聚物或聚醚多元醇制备低粘度的硅烷封端的聚氨酯预聚物,其可充当用于湿交联的胶粘剂和密封剂的粘合剂(见例如EP-A0 070 475和EP-A 0 372 561)。
根据WO 2009/115079的教导,异氰酸根合丙基三甲氧基硅烷或异氰酸根合丙基三乙氧基硅烷与多元醇的反应产生含烷氧基硅烷基团的聚氨酯,其可以在合适的催化剂存在下甚至在排除水的情况下热固化,并且使得例如能够配制具有非常高耐刮擦性的汽车漆料。一个实施例具体描述了由两种聚丙烯酸酯多元醇和低分子量1,6-己二醇组成的多元醇混合物与HDI缩二脲和异氰酸根合丙基三甲氧基硅烷的反应。
异氰酸根合烷基烷氧基硅烷,例如异氰酸根合丙基三甲氧基硅烷和含有最多20个碳原子的低分子量支化二醇或多元醇的加合物以及其作为自交联粘合剂或在双组分涂料体系中作为羟基官能的粘合剂的固化剂的用途是EP-A 2 641 925的主题。除了低分子量支化二醇或多元醇之外,在加合物的制备中还可以共同使用最多40重量%含量的其它二醇和/或多元醇,也包括例如含羟基的聚酯或聚丙烯酸酯。
WO 2013/189882描述了异氰酸根合三烷氧基硅烷和多元醇的加合物作为非水性双组分聚氨酯漆(双组分PUR)中的另外的交联剂。优选地,所用的多元醇是低分子量支化二醇和/或多元醇,其还可含有最多40重量%含量的含羟基的聚合物,例如聚酯多元醇或聚丙烯酸酯多元醇。
WO 2014/180623描述了湿交联的涂料,其含有异氰酸根合硅烷在羟基官能的化合物上的至少一种加合物、含锡的催化剂和氨基硅烷。作为用于制备加合物的合适的羟基官能化合物,提及一元或多元醇以及多元醇,其包括一长列合适的聚合多元醇以及羟基官能的聚丙烯酸酯。然而,在此公开物的实施例中,通过Vestanat M 95仅使用异氰酸根合丙基三甲氧基硅烷和1,9-壬二醇的低分子量2:1加合物(摩尔)。
WO 2008/034409例如描述了可商购的聚酯多元醇Desmophen 1145(CovestroDeutschland AG)与不足量的异氰酸根合丙基三乙氧基硅烷的部分反应。由于所选择的当量比,最初存在于多元醇中的羟基的小于15%被氨基甲酸酯化。
WO 2014/037265描述了通过多元醇与贫单体二异氰酸酯/巯基硅烷加合物的反应来制备具有硫代氨基甲酸酯结构的硅烷官能的粘合剂。实施例中提到的聚合的聚丙烯酸酯多元醇和聚酯多元醇仅以与基于羟基当量计相当大量的低分子量二醇的混合物进行反应。
迄今尚无描述聚合的聚酯多元醇和/或聚丙烯酸酯多元醇的所有羟基与异氰酸根合烷氧基硅烷优选在不共同使用较大量低分子量、低官能度的醇的情况下的完全反应。如自己的实验表明,在常规反应条件下,例如在高于60℃的温度下仅使用聚合多元醇时,甚至在氨基甲酸酯化反应结束之前就发生反应批料的胶凝。
因此,本发明的目的是提供一种制备烷氧基硅烷改性的聚氨酯的新方法,该方法使得聚合多元醇,例如聚酯多元醇和/或聚丙烯酸酯多元醇,优选甚至在不共同使用低分子量醇的情况下可以与异氰酸根合烷氧基硅烷以安全和可重复的方式完全反应。通过此方法可得到的产物应当适用于硅烷官能的聚氨酯的所有使用领域,尤其是作为用于湿交联或可热固化的胶粘剂、密封剂或涂料的粘合剂。
此目的可以通过在下文更详细描述的本发明的方法来实现。本发明的方法基于以下令人惊讶的观察:聚合的聚酯多元醇和/或聚丙烯酸酯多元醇(如其例如作为双组分PUR漆料的粘合剂组分商购可得)在聚合物中所含的羧基优选完全地化学反应后(优选甚至在不存在低分子量醇的情况下)毫无问题地与异氰酸根合硅烷反应,特别优选完全地反应以得到硅烷官能的聚氨酯。
本发明提供了一种制备含硅烷基团的聚氨酯的方法,其包括A)与B)的反应以获得反应产物以及所述反应产物与C)的反应:
A)至少一种聚合多元醇,其具有根据DIN EN ISO 2114:2002-06测定的0.01至30.0mg KOH/g的酸值,基于固含量计,
B)至少一种化合物,其具有至少一个对于羧基呈反应性的基团且含有至少一个环氧基团、碳二亚胺基团和/或2-噁唑啉基团,
C)至少一种烷氧基硅烷官能的异氰酸酯。
在第一个优选的实施方案中,聚合多元醇A)是至少双官能的聚合多元醇,其具有的数均分子量Mn为270至22000g/mol,优选500至18000g/mol,特别优选800至12000g/mol。同样优选、与上述数均分子量组合时特别优选的是,聚合多元醇A)是至少一种双官能多元醇并且具有根据DIN EN ISO 2114:2002-06测定的酸值为0.01至30mg KOH/g,优选0.1至25.0mg KOH/g,特别优选0.2至20.0mg KOH/g,在每种情况下基于固含量计。
在本文件中,“聚合多元醇”理解为是指具有至少两个羟基的分子,其由多个相同或不同的重复基础单元形成,并且可通过本身已知的大分子化学方法,例如通过聚合、缩聚或加聚来制备。术语“聚合多元醇”还应包括所谓的低聚多元醇,其通常仅由少数,例如3至20个基础单元形成,其中从低聚物至低分子量聚合物的转变是流畅的。
本文件中提及的聚合多元醇A)的数均分子量Mn借助凝胶渗透色谱法(GPC)通过使用聚苯乙烯标准物和四氢呋喃作为洗脱液根据DIN 55672-1:2016-03测定。
根据本发明,术语“包含”或“含有”优选表示“基本上由......组成”,特别优选表示“由......组成”。
用于本发明方法的合适的聚合多元醇A)特别是聚酯多元醇、聚碳酸酯多元醇和/或聚丙烯酸酯多元醇。优选地,这些多元醇具有的平均OH官能度为2至6,特别优选平均官能度为2至4。
合适的聚酯多元醇A)例如是在EP-A 0 978 523,第5页第17行-第47行,或EP-A 0659 792 第 6页第32行-第45行中提到的那些类型,只要它们在官能度和分子量方面满足上面所述的说明。特别优选的聚酯多元醇是多元醇与不足量的多元羧酸或羧酸酐的缩合产物,其中所述多元醇例如1,2-乙二醇、1,2-丙二醇、二乙二醇、1,4-丁二醇、1,6-己二醇、新戊二醇、环己烷-1,4-二甲醇、1,4-环己二醇、全氢双酚、1,1,1-三羟甲基丙烷、1,2,3-丙三醇、季戊四醇和/或山梨糖醇,所述多元醇羧酸或羧酸酐例如琥珀酸、己二酸、癸二酸、十二烷二酸、戊二酸酐、马来酸酐、邻苯二甲酸酐、间苯二甲酸、对苯二甲酸、偏苯三酸、六氢邻苯二甲酸酐和/或四氢邻苯二甲酸酐,或如以本身已知的方式由内酯例如ε-己内酯和简单的一元醇例如上面示例性提及的那些作为起始剂分子通过开环可得到的那些。
合适的聚碳酸酯多元醇A)特别是二元醇,例如上文在多元醇列表中举例提及的那些与碳酸二芳基酯,例如碳酸二苯酯、碳酸二甲酯或光气的本身已知的反应产物。合适的聚碳酸酯多元醇A)还包括除了含有碳酸酯结构外还含有酯基的那些。其特别是本身已知的聚酯碳酸酯二醇,其如例如根据DE-AS 1 770 245的教导通过二元醇与内酯,如特别是ε-己内酯的反应以及在此所得的聚酯二醇与碳酸二苯酯或碳酸二甲酯的随后反应可得到。同样合适的聚碳酸酯多元醇A)是除了含有碳酸酯结构外还含有醚基的那些。其特别是本身已知的聚醚碳酸酯多元醇,如例如根据EP-A 2 046 861的方法通过环氧烷(环氧化物)和二氧化碳在H-官能的起始剂物质存在下的催化反应可得到。
合适的聚丙烯酸酯多元醇A)例如是在WO 2011/124710,第10页第32行-第13页第18行中提到的那些类型,只要它们在官能度和分子量方面满足上面所述的说明。特别优选的聚丙烯酸酯多元醇A)是丙烯酸或甲基丙烯酸的羟烷基酯任选地与丙烯酸烷基酯和/或甲基丙烯酸烷基酯、苯乙烯或其它可共聚的烯属不饱和单体一起的聚合物或共聚物,其中所述丙烯酸或甲基丙烯酸的羟烷基酯例如丙烯酸羟乙酯、丙烯酸羟丙酯、丙烯酸羟丁酯、甲基丙烯酸羟乙酯、甲基丙烯酸羟丙酯或甲基丙烯酸羟丁酯,所述丙烯酸烷基酯和/或甲基丙烯酸烷基酯例如丙烯酸甲酯、丙烯酸乙酯、丙烯酸正丁酯、丙烯酸异丁酯、丙烯酸2-乙基己酯、丙烯酸环己酯、丙烯酸异冰片酯、丙烯酸月桂酯、甲基丙烯酸甲酯、甲基丙烯酸乙酯、甲基丙烯酸正丁酯、甲基丙烯酸异丁酯、甲基丙烯酸2-乙基己酯、甲基丙烯酸环己酯、甲基丙烯酸异冰片酯、甲基丙烯酸月桂酯。
合适的多元醇A)还例如是通过简单二醇与甲醛的反应可得的已知聚缩醛多元醇,或通过环状缩醛例如三噁烷的缩聚制备的聚缩醛,所述简单二醇例如二乙二醇、三乙二醇、4,4'-二((2-羟基乙氧基)苯基)-二甲基甲烷(2摩尔环氧乙烷在双酚A上的加合物)或己二醇。
另外合适的多元醇A)还例如是EP-A 0 689 556和EP-A 0 937 110中描述的、例如通过环氧化的脂肪酸酯与脂族或芳族多元醇通过环氧化物开环的反应可得的特定多元醇。
同样可用作多元醇A)的是含羟基的聚丁二烯。
所述聚合多元醇A)可以在本发明的方法中单独使用或以相互的任意混合物的形式使用。它们既可以是不含溶剂的形式,也可以是溶解在常规溶剂中的形式。
合适的溶剂尤其是对于所述烷氧基硅烷官能的异氰酸酯C)的反应性基团呈惰性的那些,例如已知的常规非质子漆料溶剂,例如乙酸乙酯、乙酸丁酯、乙二醇单甲基-或-乙基醚乙酸酯、乙酸1-甲氧基丙-2-基酯、乙酸3-甲氧基-正丁酯、丙酮、2-丁酮、4-甲基-2-戊酮、环己酮、甲苯、二甲苯、氯苯、石油溶剂油、具有较高取代度的芳族化合物,如例如以溶剂石脑油、Solvesso®、Isopar®、Nappar®(Deutsche EXXON CHEMICAL GmbH,Köln, DE)和Shellsol® (Deutsche Shell Chemie GmbH, Eschborn, DE)的名称市购可得,以及溶剂如丙二醇二乙酸酯、二乙二醇二甲醚、二丙二醇二甲醚、二乙二醇乙基-和-丁基醚乙酸酯、乙氧基丙酸乙酯、碳酸亚丙酯、N-甲基吡咯烷酮和N-甲基己内酰胺,或该类溶剂的任意混合物。
在本发明的方法中使用的组分B)是这样的任意化合物,其具有至少一个对于羧基呈反应性的基团且含有至少一个环氧基团、碳二亚胺基团和/或2-噁唑啉基团并优选具有数均分子量为44至2000,优选128至1500,特别优选250至1000,例如如在漆料技术中通常称为酸清除剂(Säurefänger)的那些。
在另一个优选的实施方案中,具有至少一个对于羧基呈反应性的基团的化合物B)含有一至三个,特别优选一个或两个,非常特别优选恰好一个环氧基团、碳二亚胺基团和/或2-噁唑啉基团。
合适的含环氧基团的化合物B)例如是1,2-环氧乙烷、1,2-环氧丙烷、1,2-环氧丁烷、1,2-环氧己烷、1,2-环氧庚烷、1,2-环氧癸烷、1,2-环氧十二烷、1,2-环氧十四烷、1,2-环氧十六烷、1,2-环氧十八烷、1,2-环氧环戊烷、1-甲基-1,2-环氧环戊烷、1,2-环氧环己烷、1,2-环氧环庚烷、1,2-环氧环辛烷、氧化异佛尔酮、氧化苯乙烯、(2,3-环氧丙基)苯、反式均二苯代乙烯氧化物、3-环氧丙氧基丙基三甲氧基硅烷、3-环氧丙氧基丙基三乙氧基硅烷、3-环氧丙氧基丙基甲基二乙氧基硅烷、2-(3,4-环氧环己基)乙基三甲氧基硅烷、2-(3,4-环氧环己基)乙基三乙氧基硅烷、1,2,7,8-二环氧辛烷、1,2,5,6-二环氧环辛烷、丁基缩水甘油醚、2-乙基己基缩水甘油醚、Versatic酸缩水甘油酯、六氢邻苯二甲酸二缩水甘油酯、双酚-A-二缩水甘油醚(BADGE)、甘油缩水甘油醚和异氰脲酸三缩水甘油酯(TGIC)。
合适的含碳二亚胺基团的化合物B)原则上是任意的单体或聚合碳二亚胺,其如例如以本身已知的方式通过脂族、脂环族、芳脂族和/或芳族单-和/或二异氰酸酯的催化热缩聚可得。
它们例如是脂环族碳二亚胺,例如二环己基碳二亚胺或在DE 2 301 725、DE 2358 038和EP 0 890 604中描述的基于1-异氰酸根合-3,3,5-三甲基-5-异氰酸根合甲基环己烷(异佛尔酮二异氰酸酯;IPDI)、2,4'-和4,4'-二异氰酸根合二环己基甲烷和/或环己基异氰酸酯的碳二亚胺;是由叔(tertiär)键合的异氰酸酯基团制成的碳二亚胺,例如US 4419 294中描述的基于1,3-双(1-异氰酸根合-1-甲基乙基)苯(TMXDI)和1-异氰酸根合-4-(1-异氰酸根合-1-甲基乙基)-1-甲基-环己烷的碳二亚胺;是芳族碳二亚胺,例如基于2,4-和2,6-甲苯二异氰酸酯、2,4'-和4,4'-二苯基甲烷二异氰酸酯、1,3-和1,4-苯二异氰酸酯的那些;特别是基于芳族异氰酸酯的那些,其各自在异氰酸酯基团的至少一个邻位上带有具有1至6个碳原子的脂族取代基,优选异丙基,例如邻甲苯基异氰酸酯、2,6-二异丙基苯基异氰酸酯和/或1,3,5-三异丙基苯-2,4-二异氰酸酯。
合适的含噁唑啉基团的化合物B)例如是2-甲基-2-噁唑啉、2-羟基乙基-2-噁唑啉、2-羟基丙基-2-噁唑啉、5-羟基戊基-2-噁唑啉和/或1,3-亚苯基双-2-噁唑啉。
特别优选的具有对于羧基呈反应性的基团的化合物B)是基于2,6-二异丙基苯基异氰酸酯和/或1,3,5-三异丙基苯-2,4-二异氰酸酯的单-和多碳二亚胺,其如例如由Rheinchemie Rheinau GmbH(德国)公司以商品名Stabaxol®获得。非常特别优选使用二-(2,6-二异丙基苯基)-碳二亚胺(Stabaxol® I)。
具有对于羧基呈反应性的基团的化合物B)在本发明的方法中既可以作为单组分使用,也可以以相互的任意混合物的形式使用。取决于所用多元醇A)和具有对于羧基呈反应性的基团的化合物B)的性质,甚至与摩尔不足量的对于羧基呈反应性的基团反应也可足以实现根据本发明的稳定效果。然而,在另一个优选的实施方案中,聚合多元醇A)与至少一种具有对于羧基呈反应性的基团的化合物B)的反应在遵循羧基与对于羧基呈反应性的基团的如下当量比的情况下进行:1.5:1 - 1:5,优选1.2:1 - 1:2,特别优选1.1:1 - 1:1.1。
非常特别优选地,化合物B)的计量加入以如下量进行,以使得对于聚合多元醇A)的每个羧基存在至少一个对于羧基呈反应性的基团。
在本发明的方法中,在所述反应之后,优选在聚合多元醇A)与对于羧基呈反应性的化合物B)的反应后,所得反应产物在进一步的方法步骤中与至少一种烷氧基硅烷官能的异氰酸酯C)反应。任选地在与C)反应之前,由A)与B)的反应获得的反应产物可以经历进一步的任意的中间步骤,只要在与至少一种烷氧基硅烷官能的异氰酸酯C)反应过程中在反应产物中还存在足够量的羟基。但是特别优选地,所述反应产物与烷氧基硅烷官能的异氰酸酯C)的反应在没有中间步骤的情况下进行。
烷氧基硅烷官能的异氰酸酯C)是任意的化合物,其中至少一个,优选恰好一个异氰酸酯基团和至少一个,优选恰好一个具有至少一个烷氧基取代基的硅烷基团彼此同时存在。烷氧基硅烷官能的异氰酸酯C)在下文中也称为异氰酸根合烷氧基硅烷C)。
合适的异氰酸根合烷氧基硅烷C)例如是异氰酸根合烷基烷氧基硅烷,其如例如可根据US 3 494 951、EP-A 0 649 850、WO 2014/063895和WO 2016/010900中描述的方法通过无光气的途径通过相应的氨基甲酸酯或脲的热裂解而获得。
在另一个优选的实施方案中,所用的烷氧基硅烷官能的异氰酸酯C)是至少一种通式(I)的化合物
其中
R1、R2和R3彼此独立地表示相同或不同的、饱和或不饱和的、线性或支化的、脂族或脂环族的或任选地取代的具有最多18个碳原子的芳族或芳脂族基团,其可任选地含有最多3个选自氧、硫、氮的杂原子,优选在每种情况下具有最多6个碳原子的烷基和/或具有最多6个碳原子的烷氧基,其可含有最多3个氧原子,特别优选在每种情况下甲基、甲氧基和/或乙氧基,条件是基团R1、R2和R3中的至少一个通过氧原子与硅原子连接,且
X表示具有最多6个,优选1至4个碳原子的线性或支化的有机基团,特别优选亚丙基(-CH2-CH2-CH2-)。
这种异氰酸根合烷氧基硅烷的实例是异氰酸根合甲基三甲氧基硅烷、异氰酸根合甲基三乙氧基硅烷、异氰酸根合甲基三异丙氧基硅烷、2-异氰酸根合乙基三甲氧基硅烷、2-异氰酸根合乙基三乙氧基硅烷、2-异氰酸根合乙基三异丙氧基硅烷、3-异氰酸根合丙基三甲氧基硅烷、3-异氰酸根合丙基三乙氧基硅烷、3-异氰酸根合丙基甲基二甲氧基硅烷、3-异氰酸根合丙基甲基二乙氧基硅烷、3-异氰酸根合丙基乙基二乙氧基硅烷、3-异氰酸根合丙基二甲基乙氧基硅烷、3-异氰酸根合丙基二异丙基乙氧基硅烷、3-异氰酸根合丙基三丙氧基硅烷、3-异氰酸根合丙基三异丙氧基硅烷、3-异氰酸根合丙基三丁氧基硅烷、3-异氰酸根合丙基甲基二丁氧基硅烷、3-异氰酸根合丙基苯基二甲氧基硅烷、3-异氰酸根合丙基苯基二乙氧基硅烷、3-异氰酸根合丙基三(甲氧基乙氧基乙氧基)硅烷、2-异氰酸根合异丙基三甲氧基硅烷、4-异氰酸根合丁基三甲氧基硅烷、4-异氰酸根合丁基三乙氧基硅烷、4-异氰酸根合丁基三异丙氧基硅烷、4-异氰酸根合丁基甲基二甲氧基硅烷、4-异氰酸根合丁基甲基二乙氧基硅烷、4-异氰酸根合丁基乙基二甲氧基硅烷、4-异氰酸根合丁基乙基二乙氧基硅烷、4-异氰酸根合丁基二甲基甲氧基硅烷、4-异氰酸根合丁基苯基二甲氧基硅烷、4-异氰酸根合丁基苯基二乙氧基硅烷、4-异氰酸根合(3-甲基丁基)三甲氧基硅烷、4-异氰酸根合(3-甲基丁基)三乙氧基硅烷、4-异氰酸根合(3-甲基丁基)甲基二甲氧基硅烷、4-异氰酸根合(3-甲基丁基)甲基二乙氧基硅烷和11-异氰酸根合十一烷基三甲氧基硅烷或这种异氰酸根合烷氧基硅烷的任意混合物。
合适的异氰酸根合烷氧基硅烷C)还例如是具有硫代氨基甲酸酯结构的异氰酸根合硅烷,其例如可根据WO2014/037279中的方法通过任意的脂族、脂环族、芳脂族或芳族二异氰酸酯与任意的巯基硅烷以6:1至40:1的NCO:SH比的反应和随后通过薄层蒸馏除去过量的未转化的单体二异氰酸酯。
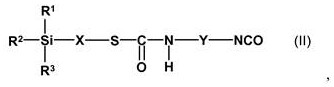
在另一个优选的实施方案中,所用的异氰酸根合烷氧基硅烷C)是至少一种通式(II)的化合物
其以与次要量的通式(III)的硅烷官能的化合物的混合物存在,
其中在式(II)和(III)中
R1、R2和R3彼此独立地表示相同或不同的、饱和或不饱和的、线性或支化的、脂族或脂环族的或任选地取代的具有最多18个碳原子的芳族或芳脂族基团,其可任选地含有最多3个选自氧、硫、氮的杂原子,优选在每种情况下具有最多6个碳原子的烷基和/或具有最多6个碳原子的烷氧基,其可含有最多3个氧原子,特别优选在每种情况下甲基、甲氧基和/或乙氧基,条件是基团R1、R2和R3中的至少一个通过氧原子与硅原子连接,
X表示具有最多6个,优选1至4个碳原子的线性或支化的有机基团,特别优选亚丙基(-CH2-CH2-CH2-),且
Y 表示具有4至18个碳原子的线性或支化的脂族或脂环族基团或具有6至18个碳原子的任选地取代的芳族或芳脂族基团,优选具有6至13个碳原子的线性或支化的脂族或脂环族基团,且
其中通式(III)的化合物优选占通式(II)和(III)的化合物的总质量的2至15重量%,特别优选2至10重量%的含量。
具有硫代氨基甲酸酯结构的这种异氰酸根合硅烷的特别优选的实例是2-巯基乙基三甲基硅烷、2-巯基乙基甲基二甲氧基硅烷、2-巯基乙基三甲氧基硅烷、2-巯基乙基三乙氧基硅烷、3-巯基丙基甲基二甲氧基硅烷、3-巯基丙基二甲基甲氧基硅烷、3-巯基丙基三甲氧基硅烷、3-巯基丙基甲基二乙氧基硅烷、 3-巯基丙基三乙氧基硅烷、3-巯基丙基乙基二甲氧基硅烷、3-巯基丙基乙基二乙氧基硅烷和/或4-巯基丁基三甲氧基硅烷与1,5-二异氰酸根合戊烷、1,6-二异氰酸根合己烷、1-异氰酸根合-3,3,5-三甲基-5-异氰酸根合甲基环己烷、2,4’-和/或4,4’-二异氰酸根合二环己基甲烷或这些二异氰酸酯的任意混合物的反应产物。
同样合适的异氰酸根合烷氧基硅烷C)还例如是具有甲酰基脲结构的那些,其例如可根据WO2014/113923的方法通过含甲酰胺基团的硅烷与摩尔过量的任意的脂族、脂环族、芳脂族或芳族二异氰酸酯的反应和随后蒸馏分离出未转化的单体二异氰酸酯来获得。
在另一个优选的实施方案中,所用的异氰酸根合烷氧基硅烷C)是至少一种通式(IV)的化合物
其以与次要量的通式(V)的硅烷官能的化合物的混合物存在,
其中在式(IV)和(V)中
R1、R2和R3彼此独立地表示相同或不同的、饱和或不饱和的、线性或支化的、脂族或脂环族的或任选地取代的具有最多18个碳原子的芳族或芳脂族基团,其可任选地含有最多3个选自氧、硫、氮的杂原子,优选在每种情况下具有最多6个碳原子的烷基和/或具有最多6个碳原子的烷氧基,其可含有最多3个氧原子,特别优选在每种情况下甲基、甲氧基和/或乙氧基,条件是基团R1、R2和R3中的至少一个通过氧原子与硅原子连接,
X表示具有最多6个,优选1至4个碳原子的线性或支化的有机基团,特别优选亚丙基(-CH2-CH2-CH2-),且
Y 表示具有4至18个碳原子的线性或支化的脂族或脂环族基团或具有6至18个碳原子的任选地取代的芳族或芳脂族基团,优选具有6至13个碳原子的线性或支化的脂族或脂环族基团,且
其中通式(V)的化合物优选占通式(IV)和(V)的化合物的总质量的2至15重量%,特别优选2至10重量%的含量。
具有甲酰基脲结构的这种异氰酸根合硅烷的实例是甲酰胺硅烷的反应产物,其例如可根据WO 2015/113923中公开的方法通过带伯氨基的氨基硅烷,特别是3-氨基丙基三甲氧基硅烷和/或3-氨基丙基三乙氧基硅烷与甲酸烷基酯,优选与甲酸甲酯和/或甲酸乙酯在消去醇的情况下的反应,与脂族和/或脂环族二异氰酸酯,优选1,5-二异氰酸根合戊烷、1,6-二异氰酸根合己烷、1-异氰酸根合-3,3,5-三甲基-5-异氰酸根合甲基环己烷、2,4'-和/或4,4'-二异氰酸根合二环己基甲烷或这些二异氰酸酯的任意混合物的反应获得。
其它合适的异氰酸根合烷氧基硅烷C)还例如是根据EP-A 1 136 495制备的二异氰酸酯和特定仲氨基烷基烷氧基硅烷的1:1单加合物、由EP-A 0 596 360已知的通过马来酸二烷基酯与氨基硅烷的反应可获得的天冬氨酸酯,其中共反应物通过使用大摩尔过量的异氰酸酯相互反应,随后通过蒸馏分离出未转化的单体二异氰酸酯。
用于本发明方法的优选的烷氧基硅烷官能的异氰酸酯C)是异氰酸根合甲基三甲氧基硅烷、异氰酸根合甲基三乙氧基硅烷、3-异氰酸根合丙基三甲氧基硅烷和3-异氰酸根合丙基三乙氧基硅烷、根据WO2014/037279的方法通过3-巯基丙基三甲氧基硅烷和/或3-巯基丙基三乙氧基硅烷与1,5-二异氰酸根合戊烷、1,6-二异氰酸根合己烷、1-异氰酸根合-3,3,5-三甲基-5-异氰酸根合甲基环己烷、2,4'-和/或4,4'-二异氰酸根合二环己基甲烷的反应可获得的具有硫代氨基甲酸酯结构的异氰酸根合硅烷以及这种异氰酸根合硅烷的任意混合物。
特别优选使用上述的具有硫代氨基甲酸酯结构的异氰酸根合硅烷。
为了进行本发明的方法,至少一种聚合多元醇A)在第一方法步骤中与至少一种对于多元醇A)的羧基呈反应性的化合物B)反应。该反应优选在20℃至200℃,优选30℃至120℃,特别优选40℃至100℃的温度下进行,在每种情况下任选地在上述非质子溶剂中的至少一种的存在下以及在每种情况下优选遵循上述的羧基与对于羧基呈反应性的基团的当量比。取决于所选的共反应物A)和B)的性质和所选的反应温度,反应以不同的速率进行,并且通常在5分钟至48小时,优选在10分钟至12小时,特别优选在15分钟至4小时的时间后终止。
聚合多元醇A)和对于羧基呈反应性的化合物B)的本反应产物在进一步的步骤中与至少一种烷氧基硅烷官能的异氰酸酯C)反应。产生含硅烷基团的聚氨酯的此反应优选在20℃至200℃,优选40℃至160℃,特别优选60℃至120℃的温度下进行,在每种情况下任选地在上述非质子溶剂中的至少一种的存在下。这里并且通常作为进一步优选的实施方案,所述反应产物的羟基与烷氧基硅烷官能的异氰酸酯C)的反应在遵循异氰酸酯基团与羟基的如下当量比的情况下进行:0.7:1至1.5:1,优选0.8:1至1.2:1,特别优选0.9:1至1.1:1,并非常特别优选为1:1至1.05:1。
本发明的方法可以以未催化的方式进行。然而,特别是为了加速氨基甲酸酯化反应,任选地也可以共同使用异氰酸酯化学中常规的催化剂。在此的实例包括叔胺,例如三乙胺、三丁胺、二甲基苄胺、二乙基苄胺、吡啶、甲基吡啶、二环己基甲胺、二甲基环己胺、N,N,N',N'-四甲基二氨基二乙醚、双(二甲基氨基丙基)脲、N-甲基-或N-乙基吗啉、N-椰油基吗啉、N-环己基吗啉、N,N,N',N'-四甲基亚乙基二胺、N,N,N',N'-四甲基-1,3-丁二胺、N,N,N',N'-四甲基-1,6-己二胺、五甲基二亚乙基三胺、N-甲基哌啶、N-二甲基氨基乙基哌啶、N,N'-二甲基哌嗪、N-甲基-N'-二甲基氨基哌嗪、1,2-二甲基咪唑、2-甲基咪唑、N,N-二甲基咪唑-β-苯基乙胺、1,4-二氮杂双环[2.2.2]辛烷(DABCO)和己二酸双(N,N-二甲基氨基乙基)酯,脒,例如1,5-二氮杂双环[4.3.0]壬烯(DBN)、1,8-二氮杂双环[5.4.0]十一碳-7-烯(DBU)和2,3-二甲基-3,4,5,6-四氢嘧啶,烷醇胺化合物,例如三乙醇胺、三异丙醇胺、N-甲基二乙醇胺、N-乙基二乙醇胺、二甲基氨基乙醇和2-(N,N-二甲基氨基乙氧基)乙醇,N,N',N"-三(二烷基氨基烷基)六氢三嗪,例如N,N',N"-三(二甲基氨基丙基)-均-六氢三嗪、双(二甲基氨基乙基)醚和金属盐,例如铁、铅、铋、锌和/或锡的金属常规氧化态的无机和/或有机化合物,例如氯化铁(II)、氯化铁(III)、2-乙基己酸铋(III)、铋(III)、辛酸铋(III)、新癸酸铋(III)、庚二酸镱(III)、乙酰丙酮镱(III)和氯化镱(III)、氯化锌、2-乙基己酸锌、辛酸锡(II)、乙基己酸锡(II)、棕榈酸锡(II)、二月桂酸二丁基锡(IV)(DBTL)、二氯化二丁基锡(IV)或辛酸铅。
优选使用的催化剂是所述类型的铋化合物和锡化合物。特别优选的催化剂是2-乙基己酸铋(III)和二月桂酸二丁基锡(IV)(DBTL)。
在本发明的方法中,这些催化剂可以单独使用或以相互的任意混合物的形式使用,且在此如果使用的话,按照所用的催化剂的总重量计算以0.001至1.0重量%,优选0.01至0.5重量%的量使用,基于共反应物A)、B)和C)的总重量计。
为了在本发明方法的过程中防止硅烷基团的过早交联,可有利地加入水清除剂,例如原甲酸酯,例如原甲酸三乙酯,或乙烯基硅烷,例如乙烯基三甲氧基硅烷。如果使用的话,按照所用的水清除剂的总重量计算以最多5重量%,优选最多2重量%的量使用所述水清除剂,基于共反应物A)、B)和C)的总重量计。
在本发明方法的一个优选实施方案中,任选地在惰性气体,例如氮气下和任选地在所述类型的合适溶剂存在下,在20-100℃的温度下预先放置烷氧基硅烷官能的异氰酸酯C)。随后,聚合多元醇A)或聚合多元醇A)的混合物与一种或多种对于羧基呈反应性的化合物B)的反应产物任选地与其它溶剂一起以任意的顺序相继地、或以上面提及的异氰酸酯基团与羟基的当量比的混合物的形式加入,并且用于氨基甲酸酯化的反应温度任选地通过使用合适的措施(加热或冷却)设定为40℃至160℃。在共同使用催化剂和/或水清除剂的情况下,可以将其在实际的氨基甲酸酯化反应开始之前就加入到烷氧基硅烷官能的异氰酸酯C)和/或A)和B)的反应产物中。然而,也可以在氨基甲酸酯化反应过程中或结束后的任意时间点将这些助剂加入到所述反应混合物中。为了除去多元醇组分A)中的残余水分,优选地在实际的反应开始之前向其中加入任选地共同使用的水清除剂。
在本发明的方法中,可以例如通过根据DIN EN ISO 11909:2007-05滴定测定NCO含量或通过IR光谱法来跟踪氨基甲酸酯化反应的进程。在氨基甲酸酯化反应后,优选在异氰酸酯基团和羟基完全反应之后,获得本发明的含硅烷基团的聚氨酯作为本发明方法的产物。
本发明进一步提供了根据本发明的方法制备或可制备的含硅烷基团的聚氨酯。
本发明的含硅烷基团的聚氨酯是用于制备经由硅烷结构可交联的漆料原料、密封剂原料或胶粘剂原料的有价值的粘合剂。
本发明进一步提供了本发明的含硅烷基团的聚氨酯在制备特别是用于漆料原料、密封剂原料或胶粘剂原料的可交联粘合剂中的用途,以及包含本发明的含硅烷基团的聚氨酯的可交联粘合剂。
本发明的含硅烷基团的聚氨酯可以以无溶剂形式用作制备漆料原料、密封剂原料或胶粘剂原料的粘合剂,但是如果要求的话,也可以在本发明的方法中通过常规溶剂,例如上面提及的在本发明方法中任选地共同使用的惰性漆料溶剂进行稀释而不浑浊。
本发明的含硅烷基团的聚氨酯的固化既可以在溶胶-凝胶反应的范畴中通过湿交联进行,也可以通过热,例如在没有湿气的情况下进行。
这里也可以共同使用如下催化剂,其加速烷氧基硅烷基团的水解和缩合或热诱导的缩合。
除上述的氨基甲酸酯化催化剂外,这种催化剂还例如是酸,例如有机羧酸,例如乙酸和三氟乙酸、硫酸、对甲苯磺酸、三氟甲磺酸、十二烷基苯磺酸、磷酸,磷酸单酯和磷酸二酯,例如磷酸二丁酯、磷酸2-乙基己酯、磷酸苯酯和磷酸双(2-乙基己基)酯,以及例如WO2007/033786中描述的膦酸、膦酸二酯和二膦酸二酯。
同样适合作为硅烷交联的催化剂的还有碱,例如N-取代的脒1,5-二氮杂双环[4.3.0]壬-5-烯(DBN)和1,5-二氮杂双环[5.4.0]十一碳-7-烯 (DBU),或金属盐和金属螯合物,例如钛酸四异丙酯、钛酸四丁酯、乙酰丙酮钛(IV)、三仲丁醇铝、乙酰丙酮铝、三氟甲磺酸铝、三氟甲磺酸锡或乙基乙酰乙酸锆,例如如WO 2006/042658中所述。
用于硅烷交联的合适催化剂还是上述类型的磷酸酯和膦酸酯,其为以胺,优选以叔胺封端的形式存在。特别优选的这类催化剂是在80℃至150℃的温度范围内通过封端胺的消除而再次释放构成实际活性催化剂的酸性磷酸酯和膦酸酯的那些。例如,WO 2008/074489和WO 2009/077180中描述了合适的胺封端的磷酸催化剂。
用于硅烷交联的同样合适的催化剂是上述类型的有机磺酸,其以封端形式,例如以胺中和的形式,或作为环氧化物上的加合物(如DE 2 356 768 B1中所述)使用并在高于例如80℃时再次释放催化活性的磺酸。
适用于硅烷基团交联的其它催化剂是羧酸四烷基铵,例如甲酸四甲基铵、乙酸四甲基铵、丙酸四甲基铵、丁酸四甲基铵、苯甲酸四甲基铵、甲酸四乙基铵、乙酸四乙基铵、丙酸四乙基铵、丁酸四乙基铵、苯甲酸四乙基铵、甲酸四丙基铵、乙酸四丙基铵、丙酸四丙基铵、丁酸四丙基铵、苯甲酸四丙基铵、甲酸四丁基铵、乙酸四丁基铵、丙酸四丁基铵、丁酸四丁基铵和/或苯甲酸四丁基铵。
适用于硅烷基团交联的催化剂还是季铵多氟化物和鏻多氟化物,其例如由EP-A 0798 299、EP-A 0 896 009和EP-A 0 962 455作为异氰酸酯基团的三聚催化剂已知。
用于硅烷交联的合适催化剂最后还是锌-脒配合物,其可根据WO 2014/016019的方法通过一种或多种双羧酸锌(II)与脒的反应制备。
用于交联硅烷基团的优选催化剂是所述类型的酸性磷酸酯、膦酸酯和磺酸(其可任选地为胺封端的形式),脒碱以及所述类型的羧酸四烷基铵。
如果有的话,这些催化剂的用量为最高5重量%,优选最高2重量%,按照使用的催化剂的总重量计算,基于用作粘合剂的含硅烷基团的聚氨酯的重量计。取决于所用催化剂的类型和量,由本发明的方法产物配制的涂料、密封剂或胶粘剂的固化可在宽温度范围内,例如-20℃至200℃,优选0℃至180℃,特别优选20℃至160℃下进行。
也可以任选地向用本发明的含硅烷基团的聚氨酯配制的涂料、密封剂或胶粘剂加入任意的其它可水解的硅烷化合物,例如四甲氧基硅烷、四乙氧基硅烷、甲基三甲氧基硅烷、甲基三乙氧基硅烷、乙基三乙氧基硅烷、异丁基三甲氧基硅烷、异丁基三乙氧基硅烷、辛基三乙氧基硅烷、辛基三甲氧基硅烷、3-氨基丙基三甲氧基硅烷、3-氨基丙基三乙氧基硅烷、(3-环氧丙氧基丙基)甲基二乙氧基硅烷、(3-环氧丙氧基丙基)三甲氧基硅烷、苯基三甲氧基硅烷、苯基三乙氧基硅烷或US 4 499 150中所述类型的硅烷官能的共聚物,或该类硅烷化合物的混合物作为共反应物。
在配制漆料、密封剂或胶粘剂时,也可以向本发明的含硅烷基团的聚氨酯加入任意的其它常规助剂和添加剂,例如UV稳定剂、抗氧化剂、水清除剂、滑爽添加剂、消泡剂、流平剂、流变剂、阻燃剂、填料和/或颜料。
除了用作单独的粘合剂之外,本发明的方法产物也可以例如作为添加剂加入到常规的单组分或双组分聚氨酯体系中,例如以实现非常特定的性能,例如用于改进粘附性。
通过使用本发明的含硅烷基团的聚氨酯配制的涂料、密封剂或胶粘剂的施用可以通过本身已知的方法进行,例如通过喷涂、涂抹、浸渍、流涂,或借助于辊或刮刀以一层或多层进行。可考虑的基底包括任意的基底,例如金属、木材、玻璃、石头、陶瓷材料、混凝土、硬质和软质塑料、皮革和纸张,其在涂覆之前也可以任选地配备有常规的底漆。
因此,本发明还提供了涂有本发明的含硅烷基团的聚氨酯的上述基底。
下面借助实施例和对比例更详细地阐述本发明,但本发明并不限于此。
实施例
所有百分率数据基于重量,除非另外声明。
NCO含量根据DIN EN ISO 11909:2007-05通过滴定法测定。
OH值根据DIN53240-2:2007-11通过滴定法测定,酸值根据DIN EN ISO 2114:2002-06测定。所示的OH含量由通过分析测定的OH值计算。在每种情况下,所示的值与基于包括任选使用的溶剂的各自组合物的总重量。
所有的粘度测量都用Anton Paar Germany GmbH (DE)公司的Physica MCR 51流变仪根据DIN EN ISO 3219:1994-10以剪切速率250 s-1进行。
残余单体含量根据DIN EN ISO 10283:2007-11通过气相色谱法使用内标测量。
双加合物(由两分子巯基硅烷和一分子二异氰酸酯制成)在烷氧基硅烷官能的异氰酸酯C)中的含量通过凝胶渗透色谱法基于DIN 55672-1:2016-03 (凝胶渗透色谱法(GPC) - 部分1:四氢呋喃(THF)作为洗脱溶剂)测定,其中的改变是通过流速0.6 ml/min而不是1.0 ml/min操作。由色谱图所取的以面积%表示的双加合物含量(其通过软件帮助确定)各自大致等于以重量%表示的含量并且以基于单-和双加合物的总量计的那样示出。
起始化合物
聚合多元醇A)
聚合多元醇A1)
在乙酸丁酯中以70%溶解的聚丙烯酸酯多元醇,其由34.0%的甲基丙烯酸羟乙酯、25.1%丙烯酸正丁酯、40.0%苯乙烯和0.9%丙烯酸制备。
OH值(OH含量) 98 mg KOH/g (3.0%)
当量重量: 572 g/当量OH
酸值: 7.5 mg KOH/g
粘度(23℃): 3500 mPas。
聚合多元醇A2)
在溶剂石脑油100中以60%溶解的聚丙烯酸酯多元醇,其由23.2%的甲基丙烯酸羟丙酯、29.6%丙烯酸正丁酯、44.7%苯乙烯和1.9%甲基丙烯酸甲酯和0.6%丙烯酸制备。
OH值(OH含量) 53 mg KOH/g (1.6%)
当量重量: 1062 g/当量OH
酸值: 4.0 mg KOH/g
粘度(23℃): 2800 mPas。
聚合多元醇A3)
在乙酸丁酯/二甲苯(3:1)中以65%溶解的来自63重量份聚丙烯酸酯多元醇与37重量份聚酯多元醇的混合物,所述聚丙烯酸酯多元醇由32.5%甲基丙烯酸羟乙酯、24.5%丙烯酸正丁酯、41.9%苯乙烯和1.1%丙烯酸制备,所述聚酯多元醇由10.0%己二酸、20.2%2-乙基己酸、41.2%三羟甲基丙烷、27.0%邻苯二甲酸酐和1.6%马来酸酐制备。
OH值(OH含量) 96 mg KOH/g (2.9%)
当量重量: 585 g/当量OH
酸值: 9.0 mg KOH/g
粘度(23℃): 3000 mPas。
聚合多元醇A4)
不含溶剂的聚酯多元醇,其由11.9%己二酸、33.7%间苯二甲酸、10.7%三羟甲基丙烷、37.7% 1,6-己二醇和6.0%邻苯二甲酸酐制备。
OH值(OH含量) 143 mg KOH/g (4.3%)
当量重量: 392 g/当量OH
酸值: 1 mg KOH/g
粘度(23℃): 3500 mPas。
对于羧基呈反应性的化合物B)
对于羧基呈反应性的化合物B1)
二(2,6-二异丙基苯基)碳二亚胺(Stabaxol® I,德国Rheinchemie Rheinau GmbH公司)
碳二亚胺含量: 20.4% (按照-N=C=N-,分子量 = 40计算)。
对于羧基呈反应性的化合物B2)
2-乙基己基缩水甘油基醚(德国Sigma-Aldrich Chemie GmbH公司)
环氧化物含量: 23.1% (按照C2H3O,分子量 = 43计算)。
烷氧基硅烷官能的异氰酸酯C)
烷氧基硅烷官能的异氰酸酯C1)
向1680 g (10 mol)六亚甲基二异氰酸酯(HDI)在80℃的温度下在干燥的氮气下加入196 g(1.0 mol)巯基丙基三甲氧基硅烷,并在加入0.05 g (25 ppm)1,4-二氮杂双环[2.2.2]辛烷(DABCO)后搅拌1小时直到达到42.5%的NCO含量,这对应于完全发应。随后,在薄层蒸发器上在140℃的温度和0.1mbar的压力下分离出未转化的单体HDI。得到几乎无色、清澈的异氰酸根合硅烷,其具有下面的特征数据:
NCO含量: 11.2%
单体HDI: 0.19%
粘度(23℃): 80 mPas
双加合物的含量: 4.1%
Si含量(计算值): 8.1%。
烷氧基硅烷官能的异氰酸酯C2)
向1680 g (10 mol)六亚甲基二异氰酸酯(HDI)在80℃的温度下在干燥的氮气下加入238 g (1.0 mol)巯基丙基三乙氧基硅烷,并在加入0.05 g (25 ppm)1,4-二氮杂双环[2.2.2]辛烷(DABCO)后搅拌1小时,直到达到41.6%的NCO含量,这对应于完全发应。随后,在薄层蒸发器上在140℃的温度和0.1mbar的压力下分离出未转化的单体HDI。得到几乎无色、清澈的异氰酸根合硅烷,其具有下面的特征数据:
NCO含量: 9.8%
单体HDI: 0.15%
粘度(23℃): 92 mPas
双加合物的含量: 7.8%
Si含量(计算值): 7.6%。
烷氧基硅烷官能的异氰酸酯C3)
向2220 g (10 mol)异佛尔酮二异氰酸酯(IPDI)在80℃的温度下在干燥的氮气下加入196 g (1.0 mol)巯基丙基三甲氧基硅烷,并在加入0.06 g (25 ppm)二月桂酸二丁基锡(IV)(DBTL)后搅拌3小时,直到达到33.0%的NCO含量,这对应于完全发应。随后,在薄层蒸发器上在150℃的温度和0.1mbar的压力下分离出未转化的单体IPDI。得到几乎无色、清澈的异氰酸根合硅烷,其具有下面的特征数据:
NCO含量: 9.7%
单体IPDI: 0.23%
粘度(23℃): 5400 mPas
双加合物的含量: 4.8%
Si含量(计算值): 6.9%。
烷氧基硅烷官能的异氰酸酯C4)
3-异氰酸根合丙基三甲氧基硅烷(Geniosil® GF 40, 德国Wacker Chemie AG公司)
NCO含量: 20.1 % (理论值:20.4 %)
Si含量(计算值): 13.6%。
实施例1(非本发明)
在干燥氮气下在80℃下将375.0g(1.0当量)烷氧基硅烷官能的异氰酸酯C1)和345g乙酸丁酯、作为水清除剂的9.5g原甲酸三乙酯和作为催化剂的0.06g二月桂酸二丁基锡(IV)(DBTL)一起预先放置,在30分钟内加入572g(1.0当量)聚合多元醇A1),在添加结束后在该温度下继续搅拌。在约2小时的反应时间后,可观察到反应批料的显著粘度增加。2.5小时后,反应混合物完全胶凝并且不再可搅拌。
实施例2(本发明)
将572g(1.0当量)聚合多元醇A1)用200g乙酸丁酯稀释,并在加入15g的Stabaxol®I后(其对应于羧基与对于羧基呈反应性的基团的当量比为1:1)在干燥氮气下在50℃下搅拌3小时。
随后在30分钟内将由此获得的混合物滴加到在干燥氮气下在80℃下预先放置的375.0g(1.0当量)烷氧基硅烷官能的异氰酸酯C1)、9.5g原甲酸三乙酯和0.06g DBTL在145g乙酸丁酯中的溶液中,这对应于异氰酸酯基与羟基的当量比为1:1。在添加结束后在80℃下进一步搅拌,直至约8小时后通过IR光谱不再能检测到异氰酸酯。冷却至室温后,本发明的含硅烷基团的聚氨酯以无色溶液的形式存在。
固含量: 60%
粘度(23℃): 1450 mPas
Si含量(计算值): 3.8 % (基于固体计)。
实施例3(非本发明)
在干燥氮气下在80℃下将375.0g(1.0当量)烷氧基硅烷官能的异氰酸酯C1)和250g乙酸丁酯、作为水清除剂的10 g原甲酸三乙酯和作为催化剂的0.08 g DBTL一起预先放置,在30分钟内加入1062 g(1.0当量)聚合多元醇A2),在添加结束后在该温度下继续搅拌。在1.5小时的反应时间后,可观察到反应批料的显著粘度增加。2小时后,反应混合物完全胶凝并且不再可搅拌。
实施例4(本发明)
将1062 g(1.0当量)聚合多元醇A2)用200g乙酸丁酯稀释,并在加入14.8 g的Stabaxol® I后(其对应于羧基与对于羧基呈反应性的基团的当量比为1:1)在干燥氮气下在50℃下搅拌3小时。
随后在30分钟内将由此获得的混合物滴加到在干燥氮气下在80℃下预先放置的375.0g(1.0当量)烷氧基硅烷官能的异氰酸酯C1)、10 g原甲酸三乙酯和0.06g DBTL在60g乙酸丁酯中的溶液中,这对应于异氰酸酯基与羟基的当量比为1:1。在添加结束后在80℃下进一步搅拌,直至约8小时后通过IR光谱不再能检测到异氰酸酯。冷却至室温后,本发明的含硅烷基团的聚氨酯以无色溶液的形式存在。
固含量: 60%
粘度(23℃): 3250 mPas
Si含量(计算值): 2.9 % (基于固体计)。
实施例5(非本发明)
在干燥氮气下在80℃下将209.0 g(1.0当量)3-异氰酸根合丙基三甲氧基硅烷(烷氧基硅烷官能的异氰酸酯C4))和238 g乙酸丁酯、作为水清除剂de 6.0 g原甲酸三乙酯和作为催化剂e 0.05 g二月桂酸二丁基锡(IV)(DBTL)一起预先放置,在30分钟内加入572g(1.0当量)聚合多元醇A1),在添加结束后在该温度下继续搅拌。在约1小时的反应时间后,可观察到反应批料的显著粘度增加。2小时后,反应混合物完全胶凝并且不再可搅拌。
实施例6(本发明)
将572g(1.0当量)聚合多元醇A1)用200g乙酸丁酯稀释,并在加入15g的Stabaxol®I后(其对应于羧基与对于羧基呈反应性的基团的当量比为1:1)在干燥氮气下在50℃下搅拌3小时。
随后在30分钟内将由此获得的混合物滴加到在干燥氮气下在80℃下预先放置的209.0 g(1.0当量)3-异氰酸根合丙基三甲氧基硅烷(烷氧基硅烷官能的异氰酸酯C4))、6.0g原甲酸三乙酯和0.05 g DBTL在48 g乙酸丁酯中的溶液中,这对应于异氰酸酯基与羟基的当量比为1:1。在添加结束后在80℃下进一步搅拌,直至约6小时后通过IR光谱不再能检测到异氰酸酯。冷却至室温后,本发明的含硅烷基团的聚氨酯以无色溶液的形式存在。
固含量: 60%
粘度(23℃): 1320 mPas
Si含量(计算值) 4.5 % (基于固体计)。
非本发明的实施例1、3和5与本发明的实施例2、4和6的比较表明,在聚合物中所含的羧基与对于羧基呈反应性的化合物反应后,由聚合的聚丙烯酸酯多元醇可以毫无问题地制备完全硅烷官能化的聚氨酯(实施例2、4和6),而使相同的聚丙烯酸酯多元醇在没有所述预反应的情况下(实施例1、3和5)与硅烷官能化的异氰酸酯反应的实验导致反应批料的胶凝。
实施例7(本发明)
将585 g(1.0当量)聚合多元醇A3)用200g乙酸丁酯稀释,并在加入18.4 g的Stabaxol® I后(其对应于羧基与对于羧基呈反应性的基团的当量比为1:1)在干燥氮气下在50℃下搅拌3小时。
随后在30分钟内将由此获得的混合物滴加到在干燥氮气下在80℃下预先放置的375.0g(1.0当量)烷氧基硅烷官能的异氰酸酯C1)、8 g原甲酸三乙酯和0.06g DBTL在115 g乙酸丁酯中的溶液中,这对应于异氰酸酯基与羟基的当量比为1:1。在添加结束后在80℃下进一步搅拌,直至约8小时后通过IR光谱不再能检测到异氰酸酯。冷却至室温后,本发明的含硅烷基团的聚氨酯以无色溶液的形式存在。
固含量: 60%
粘度(23℃): 2900 mPas
Si含量(计算值): 3.9 % (基于固体计)。
实施例8(本发明)
将392 g(1.0当量)聚合多元醇A4)用350 g乙酸丁酯稀释,并在加入1.4 g的Stabaxol® I后(其对应于羧基与对于羧基呈反应性的基团的当量比为1:1)在干燥氮气下在50℃下搅拌3小时。
随后在30分钟内将由此获得的混合物滴加到在干燥氮气下在80℃下预先放置的375.0g(1.0当量)烷氧基硅烷官能的异氰酸酯C1)、8 g原甲酸三乙酯和0.06g DBTL在162 g乙酸1-甲氧基-2-丙基酯中的溶液中,这对应于异氰酸酯基与羟基的当量比为1:1。在添加结束后在80℃下进一步搅拌,直至约8小时后通过IR光谱不再能检测到异氰酸酯。冷却至室温后,本发明的含硅烷基团的聚氨酯以无色溶液的形式存在。
固含量: 60%
粘度(23℃): 2450 mPas
Si含量(计算值): 3.9 % (基于固体计)。
实施例9(本发明)
将572g(1.0当量)聚合多元醇A1)用200g乙酸丁酯稀释,并在加入15g的Stabaxol®I后(其对应于羧基与对于羧基呈反应性的基团的当量比为1:1)在干燥氮气下在50℃下搅拌3小时。
随后在30分钟内将由此获得的混合物滴加到在干燥氮气下在80℃下预先放置的428.5 g(1.0当量)烷氧基硅烷官能的异氰酸酯C2)、10.0 g原甲酸三乙酯和0.06g DBTL在190 g乙酸丁酯中的溶液中,这对应于异氰酸酯基与羟基的当量比为1:1。在添加结束后在80℃下进一步搅拌,直至约8小时后通过IR光谱不再能检测到异氰酸酯。冷却至室温后,本发明的含硅烷基团的聚氨酯以无色溶液的形式存在。
固含量: 60%
粘度(23℃): 1450 mPas
Si含量(计算值): 3.9 % (基于固体计)。
实施例10(本发明)
将572g(1.0当量)聚合多元醇A1)用200g乙酸丁酯稀释,并在加入15g的Stabaxol®I后(其对应于羧基与对于羧基呈反应性的基团的当量比为1:1)在干燥氮气下在50℃下搅拌3小时。
随后在30分钟内将由此获得的混合物滴加到在干燥氮气下在80℃下预先放置的262.5 g(0.7当量)烷氧基硅烷官能的异氰酸酯C1)、129.9g(0.3当量)烷氧基硅烷官能的异氰酸酯C3)、12.0 g原甲酸三乙酯和0.06g DBTL在175 g乙酸丁酯中的溶液中,这对应于异氰酸酯基与羟基的当量比为1:1。在添加结束后在80℃下进一步搅拌,直至约8小时后通过IR光谱不再能检测到异氰酸酯。冷却至室温后,本发明的含硅烷基团的聚氨酯以无色溶液的形式存在。
固含量: 60%
粘度(23℃): 1840 mPas
Si含量(计算值): 3.7 % (基于固体计)。
实施例11(本发明)
将572g(1.0当量)聚合多元醇A1)用200g乙酸丁酯稀释,并在加入13.5 g(0.077当量) 的2-乙基己基缩水甘油醚后(其对应于羧基与对于羧基呈反应性的基团的当量比为1:1)在干燥氮气下在50℃下搅拌3小时。
随后在30分钟内将由此获得的混合物滴加到在干燥氮气下在80℃下预先放置的403.9 g(1.077当量)烷氧基硅烷官能的异氰酸酯C1)、9.5 g原甲酸三乙酯和0.06g DBTL在165 g乙酸丁酯中的溶液中,这对应于异氰酸酯基与羟基的当量比为1:1(考虑到在羧基/环氧化物反应过程中形成的额外的羟基)。在添加结束后在80℃下进一步搅拌,直至约8小时后通过IR光谱不再能检测到异氰酸酯。冷却至室温后,本发明的含硅烷基团的聚氨酯以无色溶液的形式存在。
固含量: 60%
粘度(23℃): 1370 mPas
Si含量(计算值): 4.0 % (基于固体计)。
Claims (24)
1.制备含硅烷基团的聚氨酯的方法,其包括A)与B)的反应以获得反应产物以及所述反应产物与C)的反应:
A)至少一种聚合多元醇,其具有根据DIN EN ISO 2114:2002-06测定的0.01至30.0mgKOH/g的酸值,基于固含量计,
B)至少一种具有至少一个对于羧基呈反应性的基团的化合物,其含有至少一个环氧基团、碳二亚胺基团和/或2-噁唑啉基团,
C)至少一种烷氧基硅烷官能的异氰酸酯。
2.如权利要求1所述的方法,其特征在于:聚合多元醇A)是至少双官能的聚合多元醇,其具有的数均分子量Mn为270-22000g/mol。
3.如权利要求1或2所述的方法,其特征在于:聚合多元醇A)是聚酯多元醇、聚碳酸酯多元醇和/或聚丙烯酸酯多元醇。
4.如权利要求1或2所述的方法,其特征在于:具有至少一个对于羧基呈反应性的基团的化合物B)是至少一种基于2,6-二异丙基苯基异氰酸酯和/或1,3,5-三异丙基苯-2,4-二异氰酸酯的单-或多碳二亚胺。
5.如权利要求4所述的方法,其特征在于:具有至少一个对于羧基呈反应性的基团的化合物B)是二(2,6-二异丙基苯基)碳二亚胺。
6.根据权利要求1或2所述的方法,其特征在于:聚合多元醇A)与具有至少一个对于羧基呈反应性的基团的化合物B)的反应在遵循羧基与对于羧基呈反应性的基团的如下当量比的情况下进行:1.5:1 - 1:5。
7.根据权利要求1或2所述的方法,其特征在于:聚合多元醇A)与具有至少一个对于羧基呈反应性的基团的化合物B)的反应在遵循羧基与对于羧基呈反应性的基团的如下当量比的情况下进行:1.2:1 - 1:2。
8.根据权利要求1或2所述的方法,其特征在于:聚合多元醇A)与具有至少一个对于羧基呈反应性的基团的化合物B)的反应在遵循羧基与对于羧基呈反应性的基团的如下当量比的情况下进行:1.1:1 - 1:1.1。
9.如权利要求1或2所述的方法,其特征在于:所用的烷氧基硅烷官能的异氰酸酯C)是至少一种包含恰好一个异氰酸酯基团和恰好一个具有至少一个烷氧基取代基的硅烷基团的化合物。
11.如权利要求10所述的方法,其特征在于:在式(I)中
R1、R2和R3彼此独立地表示相同或不同的具有最多6个碳原子的烷基和/或具有最多6个碳原子的烷氧基,其可含有最多3个氧原子,前提条件是基团R1、R2或R3中的至少一个表示烷氧基,且
X 表示具有1至4个碳原子的线性或支化的有机基团。
13.如权利要求12所述的方法,其特征在于:在式(II)和(III)中
R1、R2、R3和X具有权利要求11中对于式(I)所给出的定义。
14.如权利要求12所述的方法,其特征在于:所用的烷氧基硅烷官能的异氰酸酯C)是3-巯基丙基三甲氧基硅烷和/或3-巯基丙基三乙氧基硅烷与1,5-二异氰酸根合戊烷、1,6-二异氰酸根合己烷、1-异氰酸根合-3,3,5-三甲基-5-异氰酸根合甲基环己烷、2,4'-和/或4,4'-二异氰酸根合二环己基甲烷或这些二异氰酸酯的任意混合物的至少一种反应产物。
16.如权利要求15所述的方法,其特征在于:其中在式(IV)和(V)中
R1、R2、R3和X具有权利要求11中对于式(I)所给出的定义。
17.根据权利要求1或2所述的方法,其特征在于:所述反应产物与烷氧基硅烷官能的异氰酸酯C)的反应在遵循异氰酸酯基团与羟基的如下当量比的情况下进行:0.7:1 - 1.5:1。
18.根据权利要求1或2所述的方法,其特征在于:所述反应产物与烷氧基硅烷官能的异氰酸酯C)的反应在遵循异氰酸酯基团与羟基的如下当量比的情况下进行:0.8:1 - 1.2:1。
19.根据权利要求1或2所述的方法,其特征在于:所述反应产物与烷氧基硅烷官能的异氰酸酯C)的反应在遵循异氰酸酯基团与羟基的如下当量比的情况下进行:0.9:1 - 1.1:1。
20.根据权利要求1或2所述的方法,其特征在于:所述反应产物与烷氧基硅烷官能的异氰酸酯C)的反应在遵循异氰酸酯基团与羟基的如下当量比的情况下进行:1:1 - 1.05 :1。
21.含硅烷基团的聚氨酯,其通过如权利要求1至20中任一项所述的方法制备。
22.如权利要求21所述的含硅烷基团的聚氨酯用于制备可交联的粘合剂的用途。
23.如权利要求22所述的用途,用于制备可交联的漆料原料、密封剂原料或胶粘剂原料。
24.可交联的粘合剂,其含有如权利要求21所述的含硅烷基团的聚氨酯。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP16183429.6 | 2016-08-09 | ||
| EP16183429 | 2016-08-09 | ||
| PCT/EP2017/070078 WO2018029197A1 (de) | 2016-08-09 | 2017-08-08 | Silanfunktionelle polymere polyurethane |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN109642009A CN109642009A (zh) | 2019-04-16 |
| CN109642009B true CN109642009B (zh) | 2021-12-10 |
Family
ID=56618039
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201780048302.8A Active CN109642009B (zh) | 2016-08-09 | 2017-08-08 | 硅烷官能的聚合聚氨酯 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US10844161B2 (zh) |
| EP (1) | EP3497146B1 (zh) |
| JP (1) | JP6997761B2 (zh) |
| KR (1) | KR102442964B1 (zh) |
| CN (1) | CN109642009B (zh) |
| ES (1) | ES2927985T3 (zh) |
| WO (1) | WO2018029197A1 (zh) |
Families Citing this family (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2676694C9 (ru) | 2013-01-23 | 2019-06-25 | Альдейра Терапьютикс, Инк. | Заболевания, связанные с токсичным альдегидом, и их лечение |
| CN110540795B (zh) * | 2018-05-28 | 2021-10-15 | 广东华润涂料有限公司 | 非异氰酸酯固化的溶剂型双组分涂料组合物 |
| US11326017B2 (en) * | 2018-09-10 | 2022-05-10 | Evonik Operations Gmbh | Tin-free catalysis of silane-functional polyurethane crosslinkers |
| CN113056497A (zh) | 2018-10-30 | 2021-06-29 | 科思创知识产权两合公司 | 具有改善的层粘附的多层漆构造 |
| WO2020089019A1 (de) | 2018-10-30 | 2020-05-07 | Covestro Deutschland Ag | Verfahren zur herstellung eines mehrschicht-lackaufbaus mit einer deckschicht aus silangruppen-enthaltenden prepolymeren |
| CN109651578B (zh) * | 2018-12-12 | 2021-09-17 | 中昊北方涂料工业研究设计院有限公司 | 一种耐烧蚀阻燃有机-无机树脂及其制备 |
| EP3722346A1 (de) | 2019-04-09 | 2020-10-14 | Covestro Deutschland AG | 2-komponenten-polyurethanbeschichtungen mit verbesserter topfzeit ohne einbusse in der witterungsstabilität |
| CN112812680A (zh) * | 2021-01-26 | 2021-05-18 | 广东爱上体育产业股份有限公司 | 一种强渗透型提升水泥混凝土强度的密封底漆及其制备方法 |
| CN116239741A (zh) * | 2021-12-07 | 2023-06-09 | 万华化学集团股份有限公司 | 一种环氧改性水性聚氨酯树脂、制备方法及其应用 |
| CN116102930B (zh) * | 2022-12-29 | 2023-09-12 | 广东邦固化学科技有限公司 | 一种冷烫印膜用保护层涂料及其制备方法 |
Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DD132969A1 (de) * | 1977-07-29 | 1978-11-22 | Klaus Walter | Herstellungsverfahren fuer stabilisierte polyesterpolyole und estergruppen aufweisende kunststoffe |
| CN1942500A (zh) * | 2005-03-23 | 2007-04-04 | 德古萨公司 | 含脲二酮基团的低粘度聚加成化合物、其制备方法和应用 |
| CN101311201A (zh) * | 2007-05-22 | 2008-11-26 | 拜尔材料科学股份公司 | 聚酯预聚物 |
| DE102010015683A1 (de) * | 2010-04-21 | 2011-10-27 | Basf Coatings Gmbh | Beschichtungsmittel mit hohem Festkörpergehalt und gutem Verlauf sowie daraus hergestellte Mehrschichtlackierungen und deren Verwendung |
| CN104350077A (zh) * | 2012-05-03 | 2015-02-11 | 莱茵化学莱瑙有限公司 | 用于改进聚氨酯(pu)基体系的耐水解性的方法 |
| CN104583260A (zh) * | 2012-09-04 | 2015-04-29 | 拜耳材料科技股份有限公司 | 具有硫代氨基甲酸酯结构的硅烷官能的粘合剂 |
| WO2015113923A1 (de) * | 2014-01-31 | 2015-08-06 | Bayer Materialscience Ag | Silanmodifizierte formamide |
Family Cites Families (37)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3494951A (en) | 1967-09-20 | 1970-02-10 | Gen Electric | Nitrogen-containing organosilicon materials and methods for producing them |
| DE1770245C3 (de) | 1968-04-23 | 1979-11-15 | Bayer Ag, 5090 Leverkusen | Verfahren zur Herstellung von gegebenenfalls vernetzten Polyurethanen |
| DE2301725A1 (de) | 1973-01-13 | 1974-07-18 | Bayer Ag | Verfahren zur herstellung von carbodiimiden |
| FR2250808B1 (zh) | 1973-11-14 | 1978-10-13 | Huels Chemische Werke Ag | |
| DE2358038A1 (de) | 1973-11-21 | 1975-05-28 | Bayer Ag | Verfahren zur herstellung von carbodiimiden |
| US4345053A (en) | 1981-07-17 | 1982-08-17 | Essex Chemical Corp. | Silicon-terminated polyurethane polymer |
| US4419294A (en) | 1982-03-08 | 1983-12-06 | American Cyanamid Company | Carbodiimide oligomers of tertiary aliphatic isocyanates |
| US4499150A (en) | 1983-03-29 | 1985-02-12 | Ppg Industries, Inc. | Color plus clear coating method utilizing addition interpolymers containing alkoxy silane and/or acyloxy silane groups |
| US5068304A (en) | 1988-12-09 | 1991-11-26 | Asahi Glass Company, Ltd. | Moisture-curable resin composition |
| DE4237468A1 (de) | 1992-11-06 | 1994-05-11 | Bayer Ag | Alkoxysilan- und Aminogruppen aufweisende Verbindungen |
| DE4308097A1 (de) | 1993-03-15 | 1994-09-22 | Henkel Kgaa | Polyol für ein Isocyanat-Gießharz und Beschichtungen |
| US5393910A (en) | 1993-10-20 | 1995-02-28 | Osi Specialties, Inc. | Process for making isocyanatoorganosilanes |
| US5502147A (en) | 1993-12-21 | 1996-03-26 | Bayer Corporation | Aliphatic rim elastomers |
| DE19611849A1 (de) | 1996-03-26 | 1997-10-02 | Bayer Ag | Neue Isocyanattrimerisate und Isocyanattrimerisatmischungen, deren Herstellung und Verwendung |
| DE19646424A1 (de) | 1996-11-11 | 1998-05-14 | Henkel Kgaa | Verwendung von Polyolen für Isocyanat-Gießharze und -Beschichtungsmassen |
| US5973024A (en) | 1997-07-09 | 1999-10-26 | Nisshinbo Industries, Inc. | Method for control of biodegradation rate of biodegradable plastic |
| DE19734048A1 (de) | 1997-08-06 | 1999-02-11 | Bayer Ag | Verfahren zur Herstellung von Polyisocyanaten, damit hergestellte Polyisocyanate und deren Verwendung |
| DE59902995D1 (de) | 1998-06-02 | 2002-11-14 | Bayer Ag | Verfahren zur Herstellung Iminooxadiazindiongruppen enhaltender Polyisocyanate |
| DE19835113A1 (de) | 1998-08-04 | 2000-02-10 | Basf Ag | Verfahren zur Herstellung von kompakten, transparenten Polyisocyanat-Polyadditionsprodukten |
| DE10013628A1 (de) | 2000-03-18 | 2001-09-20 | Degussa | Stabile 1:1-Monoaddukte aus sekundären Aminoalkylalkoxysilanen und Diisocyanaten sowie ein Verfahren zu ihrer Herstellung |
| US7635388B1 (en) * | 2000-05-04 | 2009-12-22 | Tyler Thomas D | Device and method for incremental correction of sight disorders and occular diseases |
| DE102004050748A1 (de) | 2004-10-19 | 2006-04-20 | Basf Coatings Aktiengesellschaft | Hochkratzfeste und hochelastische Beschichtungsmittel auf Basis von Alkoxysilanen |
| DE102005045228A1 (de) | 2005-09-22 | 2007-04-05 | Basf Coatings Ag | Verwendung von Phosphonsäurediestern und Diphosphonsäurediestern sowie silangruppenhaltige, härtbare Gemische, enthaltend Phosphonsäurediester und Diphosphonsäurediester |
| US7977501B2 (en) | 2006-07-24 | 2011-07-12 | Bayer Materialscience Llc | Polyether carbonate polyols made via double metal cyanide (DMC) catalysis |
| DE102006044310A1 (de) | 2006-09-18 | 2008-03-27 | Nano-X Gmbh | Silanbeschichtungsmaterial und Verfahren zur Herstellung eines Silanbeschichtungsmaterials |
| PL2102263T3 (pl) | 2006-12-19 | 2011-12-30 | Basf Coatings Gmbh | Środek powłokowy o wysokiej odporności na zadrapania i odporności na działanie czynników atmosferycznych |
| DE102007061854A1 (de) | 2007-12-19 | 2009-06-25 | Basf Coatings Ag | Beschichtungsmittel mit hoher Kratzbeständigkeit und Witterungsstabilität |
| EP2254960A1 (de) | 2008-03-18 | 2010-12-01 | Nano-X GmbH | Verfahren zur herstellung eines hoch abriebfesten fahrzeuglackes, fahrzeuglack und dessen verwendung |
| JP2012111786A (ja) * | 2009-03-17 | 2012-06-14 | Asahi Glass Co Ltd | 粘着体 |
| EP2556100A1 (de) | 2010-04-09 | 2013-02-13 | Basf Se | Durch energieeintrag reparable beschichtungen |
| DE102012204290A1 (de) | 2012-03-19 | 2013-09-19 | Evonik Degussa Gmbh | Addukte aus Isocyanatoalkyl-trialkoxysilanen und aliphatischen, alkyl-verzweigten Diolen oder Polyolen |
| PL2864383T3 (pl) | 2012-06-20 | 2020-04-30 | Evonik Degussa Gmbh | Środek powlekający o wysokiej odporności na zarysowania |
| PL2877515T3 (pl) | 2012-07-25 | 2018-12-31 | Basf Coatings Gmbh | Kompozycja poliuretanowego środka powłokowego, wieloetapowy sposób powlekania |
| HUE042411T2 (hu) | 2012-09-04 | 2019-06-28 | Covestro Deutschland Ag | Izocianátoszilán tiouretán-szerkezettel |
| DE102012219324A1 (de) | 2012-10-23 | 2014-04-24 | Evonik Industries Ag | Zusammensetzungen umfassend alkoxysilanhaltige Isocyanateund saure Stabilisatoren |
| DE102013208356A1 (de) | 2013-05-07 | 2014-11-13 | Evonik Industries Ag | Vernetzung von IPMS Addukten mit Aminosilanen |
| JP6878267B2 (ja) | 2014-07-14 | 2021-05-26 | モメンティブ パフォーマンス マテリアルズ インコーポレイテッドMomentive Performance Materials Inc. | 低着色および色安定なイソシアネートオルガノシランの製造プロセスおよびそれにより得られる生成物 |
-
2017
- 2017-08-08 KR KR1020197003583A patent/KR102442964B1/ko active IP Right Grant
- 2017-08-08 EP EP17749466.3A patent/EP3497146B1/de active Active
- 2017-08-08 WO PCT/EP2017/070078 patent/WO2018029197A1/de unknown
- 2017-08-08 US US16/323,604 patent/US10844161B2/en active Active
- 2017-08-08 CN CN201780048302.8A patent/CN109642009B/zh active Active
- 2017-08-08 ES ES17749466T patent/ES2927985T3/es active Active
- 2017-08-08 JP JP2019506726A patent/JP6997761B2/ja active Active
Patent Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DD132969A1 (de) * | 1977-07-29 | 1978-11-22 | Klaus Walter | Herstellungsverfahren fuer stabilisierte polyesterpolyole und estergruppen aufweisende kunststoffe |
| CN1942500A (zh) * | 2005-03-23 | 2007-04-04 | 德古萨公司 | 含脲二酮基团的低粘度聚加成化合物、其制备方法和应用 |
| CN101311201A (zh) * | 2007-05-22 | 2008-11-26 | 拜尔材料科学股份公司 | 聚酯预聚物 |
| DE102010015683A1 (de) * | 2010-04-21 | 2011-10-27 | Basf Coatings Gmbh | Beschichtungsmittel mit hohem Festkörpergehalt und gutem Verlauf sowie daraus hergestellte Mehrschichtlackierungen und deren Verwendung |
| CN104350077A (zh) * | 2012-05-03 | 2015-02-11 | 莱茵化学莱瑙有限公司 | 用于改进聚氨酯(pu)基体系的耐水解性的方法 |
| CN104364284A (zh) * | 2012-05-03 | 2015-02-18 | 莱茵化学莱瑙有限公司 | 用于控制(延长)基于扩链的聚氨酯(pu)的体系中的适用期的方法 |
| CN104583260A (zh) * | 2012-09-04 | 2015-04-29 | 拜耳材料科技股份有限公司 | 具有硫代氨基甲酸酯结构的硅烷官能的粘合剂 |
| WO2015113923A1 (de) * | 2014-01-31 | 2015-08-06 | Bayer Materialscience Ag | Silanmodifizierte formamide |
Non-Patent Citations (2)
| Title |
|---|
| Kinetics of the reaction between polyester acid and carbodiimide in dry polyester diols and in a polyester polyurethane;Daniel W. Brown等;《Macromolecules》;19810501;第14卷(第3期);659-663 * |
| 碳化二亚胺的制备及其水解稳定作用;徐海涛 等;《弹性体》;20031231;第13卷(第6期);71-73 * |
Also Published As
| Publication number | Publication date |
|---|---|
| US20190202973A1 (en) | 2019-07-04 |
| EP3497146A1 (de) | 2019-06-19 |
| US10844161B2 (en) | 2020-11-24 |
| ES2927985T3 (es) | 2022-11-14 |
| CN109642009A (zh) | 2019-04-16 |
| KR102442964B1 (ko) | 2022-09-14 |
| JP6997761B2 (ja) | 2022-01-18 |
| JP2019524957A (ja) | 2019-09-05 |
| KR20190039505A (ko) | 2019-04-12 |
| EP3497146B1 (de) | 2022-08-31 |
| WO2018029197A1 (de) | 2018-02-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN109642009B (zh) | 硅烷官能的聚合聚氨酯 | |
| JP6602794B2 (ja) | シラン基含有のチオアロファネートポリイソシアネート | |
| JP5751789B2 (ja) | アロファネート基及びシラン基を含む高官能性ポリイソシアネート | |
| JP6892825B2 (ja) | 1,5−ジイソシアナトペンタンを基礎とするシラン基含有のポリイソシアネート | |
| JP5311904B2 (ja) | アロファネート基およびシラン基を含むポリイソシアネート | |
| US9353210B2 (en) | Silane functional binder with thiourethane structure | |
| EP2160424B1 (en) | Curable silyl-containing polymer composition containing paint adhesion additive | |
| US7060750B2 (en) | Moisture-curable, polyether urethanes and their use in sealant, adhesive and coating compositions | |
| US10040808B2 (en) | Silane-modified formamides | |
| KR20220099536A (ko) | 선택적 폴리우레탄 예비폴리머 합성 | |
| CN106414463B (zh) | 硅烷改性的甲酰胺 | |
| CN112638978A (zh) | 用于湿固化组合物的干燥剂 | |
| CN117545786A (zh) | 涂料组合物和可由其获得的具有改进的抗污性和(自)清洁性能的涂层 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| GR01 | Patent grant | ||
| GR01 | Patent grant |