BRPI0917147B1 - Composto ou sal deste, uso de um composto ou sal deste, e, processo para fabricar um composto - Google Patents
Composto ou sal deste, uso de um composto ou sal deste, e, processo para fabricar um composto Download PDFInfo
- Publication number
- BRPI0917147B1 BRPI0917147B1 BRPI0917147-9A BRPI0917147A BRPI0917147B1 BR PI0917147 B1 BRPI0917147 B1 BR PI0917147B1 BR PI0917147 A BRPI0917147 A BR PI0917147A BR PI0917147 B1 BRPI0917147 B1 BR PI0917147B1
- Authority
- BR
- Brazil
- Prior art keywords
- compound
- salt
- pyridin
- benzofuran
- nitro
- Prior art date
Links
- 150000001875 compounds Chemical class 0.000 title claims abstract description 140
- 238000000034 method Methods 0.000 title claims abstract description 64
- 150000003839 salts Chemical class 0.000 title claims abstract description 63
- 230000008569 process Effects 0.000 title claims abstract description 34
- 239000002243 precursor Substances 0.000 claims abstract description 20
- 238000004519 manufacturing process Methods 0.000 claims abstract description 5
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 claims description 29
- YDLUIXGYKWYMMC-UHFFFAOYSA-N tert-butyl n-[5-[5-(ethoxymethoxy)-1-benzofuran-2-yl]-6-nitropyridin-2-yl]-n-methylcarbamate Chemical compound C=1C2=CC(OCOCC)=CC=C2OC=1C1=CC=C(N(C)C(=O)OC(C)(C)C)N=C1[N+]([O-])=O YDLUIXGYKWYMMC-UHFFFAOYSA-N 0.000 claims description 23
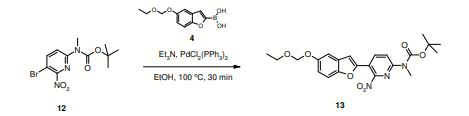
- DHKRJJDNEABPBH-UHFFFAOYSA-N tert-butyl n-[6-[5-(ethoxymethoxy)-1-benzofuran-2-yl]-2-nitropyridin-3-yl]-n-methylcarbamate Chemical compound C=1C2=CC(OCOCC)=CC=C2OC=1C1=CC=C(N(C)C(=O)OC(C)(C)C)C([N+]([O-])=O)=N1 DHKRJJDNEABPBH-UHFFFAOYSA-N 0.000 claims description 20
- 238000002441 X-ray diffraction Methods 0.000 claims description 14
- 230000005855 radiation Effects 0.000 claims description 14
- WRIKHQLVHPKCJU-UHFFFAOYSA-N sodium bis(trimethylsilyl)amide Chemical compound C[Si](C)(C)N([Na])[Si](C)(C)C WRIKHQLVHPKCJU-UHFFFAOYSA-N 0.000 claims description 13
- 229940125898 compound 5 Drugs 0.000 claims description 8
- 239000002168 alkylating agent Substances 0.000 claims description 7
- YNHIGQDRGKUECZ-UHFFFAOYSA-L bis(triphenylphosphine)palladium(ii) dichloride Chemical compound [Cl-].[Cl-].[Pd+2].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 YNHIGQDRGKUECZ-UHFFFAOYSA-L 0.000 claims description 4
- XKXIQBVKMABYQJ-UHFFFAOYSA-N tert-butyl hydrogen carbonate Chemical compound CC(C)(C)OC(O)=O XKXIQBVKMABYQJ-UHFFFAOYSA-N 0.000 claims description 4
- 125000003277 amino group Chemical group 0.000 claims description 3
- MYNQXTDIPMCJCR-HUYCHCPVSA-N 2-[2-fluoranyl-6-(methylamino)pyridin-3-yl]-1-benzofuran-5-ol Chemical compound [18F]C1=NC(NC)=CC=C1C1=CC2=CC(O)=CC=C2O1 MYNQXTDIPMCJCR-HUYCHCPVSA-N 0.000 claims description 2
- FXERARHKNULYEN-HUYCHCPVSA-N 2-[6-(18F)fluoranyl-5-(methylamino)pyridin-2-yl]-1-benzofuran-5-ol Chemical compound [18F]C1=C(C=CC(=N1)C=1OC2=C(C=1)C=C(C=C2)O)NC FXERARHKNULYEN-HUYCHCPVSA-N 0.000 claims description 2
- 229910002483 Cu Ka Inorganic materials 0.000 claims description 2
- 239000000203 mixture Substances 0.000 abstract description 28
- 238000003384 imaging method Methods 0.000 abstract description 19
- 208000024827 Alzheimer disease Diseases 0.000 abstract description 18
- 208000037259 Amyloid Plaque Diseases 0.000 abstract description 18
- 238000001727 in vivo Methods 0.000 abstract description 10
- 238000002600 positron emission tomography Methods 0.000 abstract description 10
- 210000004556 brain Anatomy 0.000 abstract description 9
- 238000011282 treatment Methods 0.000 abstract description 4
- 239000003795 chemical substances by application Substances 0.000 abstract description 2
- 238000003745 diagnosis Methods 0.000 abstract description 2
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 66
- -1 [5- (5-ethoxymethoxy-benzofuran-2-yl) -6-nitro-pyridin-2-yl] -methyl Chemical group 0.000 description 58
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 54
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 53
- 239000002904 solvent Substances 0.000 description 46
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 36
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 35
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 32
- 239000000243 solution Substances 0.000 description 30
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 27
- 239000003153 chemical reaction reagent Substances 0.000 description 25
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 24
- 239000011541 reaction mixture Substances 0.000 description 22
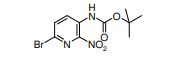
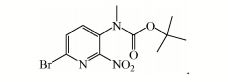
- RXEWOIDRYSEUGT-UHFFFAOYSA-N tert-butyl n-(5-bromo-6-nitropyridin-2-yl)-n-methylcarbamate Chemical compound CC(C)(C)OC(=O)N(C)C1=CC=C(Br)C([N+]([O-])=O)=N1 RXEWOIDRYSEUGT-UHFFFAOYSA-N 0.000 description 22
- 239000000523 sample Substances 0.000 description 19
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 17
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 16
- 229910000104 sodium hydride Inorganic materials 0.000 description 16
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 15
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 15
- 239000002585 base Substances 0.000 description 14
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 14
- 239000002253 acid Substances 0.000 description 13
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 12
- 239000003643 water by type Substances 0.000 description 12
- IZFOPMSVNDORMZ-UHFFFAOYSA-N 1-benzofuran-5-ol Chemical compound OC1=CC=C2OC=CC2=C1 IZFOPMSVNDORMZ-UHFFFAOYSA-N 0.000 description 11
- 238000005160 1H NMR spectroscopy Methods 0.000 description 11
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 11
- 230000015572 biosynthetic process Effects 0.000 description 11
- 239000012267 brine Substances 0.000 description 11
- 238000001514 detection method Methods 0.000 description 11
- 239000000284 extract Substances 0.000 description 11
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 11
- PCLIMKBDDGJMGD-UHFFFAOYSA-N N-bromosuccinimide Chemical compound BrN1C(=O)CCC1=O PCLIMKBDDGJMGD-UHFFFAOYSA-N 0.000 description 10
- 230000027455 binding Effects 0.000 description 10
- 238000000113 differential scanning calorimetry Methods 0.000 description 10
- 239000000047 product Substances 0.000 description 10
- PSMKEFBZOUIMJQ-UHFFFAOYSA-N tert-butyl n-(5-bromo-6-nitropyridin-2-yl)carbamate Chemical compound CC(C)(C)OC(=O)NC1=CC=C(Br)C([N+]([O-])=O)=N1 PSMKEFBZOUIMJQ-UHFFFAOYSA-N 0.000 description 10
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 10
- QFLWZFQWSBQYPS-AWRAUJHKSA-N (3S)-3-[[(2S)-2-[[(2S)-2-[5-[(3aS,6aR)-2-oxo-1,3,3a,4,6,6a-hexahydrothieno[3,4-d]imidazol-4-yl]pentanoylamino]-3-methylbutanoyl]amino]-3-(4-hydroxyphenyl)propanoyl]amino]-4-[1-bis(4-chlorophenoxy)phosphorylbutylamino]-4-oxobutanoic acid Chemical compound CCCC(NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](Cc1ccc(O)cc1)NC(=O)[C@@H](NC(=O)CCCCC1SC[C@@H]2NC(=O)N[C@H]12)C(C)C)P(=O)(Oc1ccc(Cl)cc1)Oc1ccc(Cl)cc1 QFLWZFQWSBQYPS-AWRAUJHKSA-N 0.000 description 9
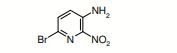
- LZAGKOUCASAJII-UHFFFAOYSA-N 5-bromo-6-nitropyridin-2-amine Chemical compound NC1=CC=C(Br)C([N+]([O-])=O)=N1 LZAGKOUCASAJII-UHFFFAOYSA-N 0.000 description 9
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 9
- 239000012043 crude product Substances 0.000 description 9
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 9
- 238000002360 preparation method Methods 0.000 description 9
- 239000007858 starting material Substances 0.000 description 9
- 238000003756 stirring Methods 0.000 description 9
- 238000002411 thermogravimetry Methods 0.000 description 9
- JWUJQDFVADABEY-UHFFFAOYSA-N 2-methyltetrahydrofuran Chemical compound CC1CCCO1 JWUJQDFVADABEY-UHFFFAOYSA-N 0.000 description 8
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 8
- 206010002022 amyloidosis Diseases 0.000 description 8
- ILAHWRKJUDSMFH-UHFFFAOYSA-N boron tribromide Chemical compound BrB(Br)Br ILAHWRKJUDSMFH-UHFFFAOYSA-N 0.000 description 8
- RIOQSEWOXXDEQQ-UHFFFAOYSA-N triphenylphosphine Chemical compound C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 RIOQSEWOXXDEQQ-UHFFFAOYSA-N 0.000 description 8
- ISJLVVQDIUZTQX-UHFFFAOYSA-N 5-(ethoxymethoxy)-1-benzofuran Chemical compound CCOCOC1=CC=C2OC=CC2=C1 ISJLVVQDIUZTQX-UHFFFAOYSA-N 0.000 description 7
- JJXPTUWJVQUHKN-UHFFFAOYSA-N 5-methoxy-1-benzofuran Chemical compound COC1=CC=C2OC=CC2=C1 JJXPTUWJVQUHKN-UHFFFAOYSA-N 0.000 description 7
- 229940125773 compound 10 Drugs 0.000 description 7
- 229940126214 compound 3 Drugs 0.000 description 7
- 201000010099 disease Diseases 0.000 description 7
- ZLVXBBHTMQJRSX-VMGNSXQWSA-N jdtic Chemical compound C1([C@]2(C)CCN(C[C@@H]2C)C[C@H](C(C)C)NC(=O)[C@@H]2NCC3=CC(O)=CC=C3C2)=CC=CC(O)=C1 ZLVXBBHTMQJRSX-VMGNSXQWSA-N 0.000 description 7
- 229910000027 potassium carbonate Inorganic materials 0.000 description 7
- 239000002287 radioligand Substances 0.000 description 7
- 238000002603 single-photon emission computed tomography Methods 0.000 description 7
- 239000007787 solid Substances 0.000 description 7
- 238000003786 synthesis reaction Methods 0.000 description 7
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 6
- IAZDPXIOMUYVGZ-WFGJKAKNSA-N Dimethyl sulfoxide Chemical compound [2H]C([2H])([2H])S(=O)C([2H])([2H])[2H] IAZDPXIOMUYVGZ-WFGJKAKNSA-N 0.000 description 6
- 206010016202 Familial Amyloidosis Diseases 0.000 description 6
- MZRVEZGGRBJDDB-UHFFFAOYSA-N N-Butyllithium Chemical compound [Li]CCCC MZRVEZGGRBJDDB-UHFFFAOYSA-N 0.000 description 6
- KEAYESYHFKHZAL-UHFFFAOYSA-N Sodium Chemical compound [Na] KEAYESYHFKHZAL-UHFFFAOYSA-N 0.000 description 6
- 239000003849 aromatic solvent Substances 0.000 description 6
- 239000003054 catalyst Substances 0.000 description 6
- 238000004440 column chromatography Methods 0.000 description 6
- 238000002330 electrospray ionisation mass spectrometry Methods 0.000 description 6
- 238000011503 in vivo imaging Methods 0.000 description 6
- SIAPCJWMELPYOE-UHFFFAOYSA-N lithium hydride Chemical compound [LiH] SIAPCJWMELPYOE-UHFFFAOYSA-N 0.000 description 6
- 229910000103 lithium hydride Inorganic materials 0.000 description 6
- 210000000056 organ Anatomy 0.000 description 6
- 235000011181 potassium carbonates Nutrition 0.000 description 6
- 238000000746 purification Methods 0.000 description 6
- AOJFQRQNPXYVLM-UHFFFAOYSA-N pyridin-1-ium;chloride Chemical compound [Cl-].C1=CC=[NH+]C=C1 AOJFQRQNPXYVLM-UHFFFAOYSA-N 0.000 description 6
- 239000012312 sodium hydride Substances 0.000 description 6
- 210000001519 tissue Anatomy 0.000 description 6
- ZPTCUFQLPDXXGM-UHFFFAOYSA-N 6-bromo-2-nitropyridin-3-amine Chemical compound NC1=CC=C(Br)N=C1[N+]([O-])=O ZPTCUFQLPDXXGM-UHFFFAOYSA-N 0.000 description 5
- FGUUSXIOTUKUDN-IBGZPJMESA-N C1(=CC=CC=C1)N1C2=C(NC([C@H](C1)NC=1OC(=NN=1)C1=CC=CC=C1)=O)C=CC=C2 Chemical compound C1(=CC=CC=C1)N1C2=C(NC([C@H](C1)NC=1OC(=NN=1)C1=CC=CC=C1)=O)C=CC=C2 FGUUSXIOTUKUDN-IBGZPJMESA-N 0.000 description 5
- 238000005481 NMR spectroscopy Methods 0.000 description 5
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 5
- 230000003941 amyloidogenesis Effects 0.000 description 5
- 230000031709 bromination Effects 0.000 description 5
- 238000005893 bromination reaction Methods 0.000 description 5
- 229910052799 carbon Inorganic materials 0.000 description 5
- 238000006243 chemical reaction Methods 0.000 description 5
- 229940125782 compound 2 Drugs 0.000 description 5
- INQOMBQAUSQDDS-UHFFFAOYSA-N iodomethane Chemical compound IC INQOMBQAUSQDDS-UHFFFAOYSA-N 0.000 description 5
- 239000000463 material Substances 0.000 description 5
- 238000002156 mixing Methods 0.000 description 5
- 108090000623 proteins and genes Proteins 0.000 description 5
- 238000004611 spectroscopical analysis Methods 0.000 description 5
- NHDIQVFFNDKAQU-UHFFFAOYSA-N tripropan-2-yl borate Chemical compound CC(C)OB(OC(C)C)OC(C)C NHDIQVFFNDKAQU-UHFFFAOYSA-N 0.000 description 5
- AUNUJMUXMFAWNR-UHFFFAOYSA-N (5-bromo-6-nitropyridin-2-yl)-methylcarbamic acid Chemical compound OC(=O)N(C)C1=CC=C(Br)C([N+]([O-])=O)=N1 AUNUJMUXMFAWNR-UHFFFAOYSA-N 0.000 description 4
- FXERARHKNULYEN-UHFFFAOYSA-N 2-[6-fluoro-5-(methylamino)pyridin-2-yl]-1-benzofuran-5-ol Chemical compound N1=C(F)C(NC)=CC=C1C1=CC2=CC(O)=CC=C2O1 FXERARHKNULYEN-UHFFFAOYSA-N 0.000 description 4
- GNFTZDOKVXKIBK-UHFFFAOYSA-N 3-(2-methoxyethoxy)benzohydrazide Chemical compound COCCOC1=CC=CC(C(=O)NN)=C1 GNFTZDOKVXKIBK-UHFFFAOYSA-N 0.000 description 4
- JMAGBGSWLILKOC-UHFFFAOYSA-N 6-nitropyridin-2-amine Chemical compound NC1=CC=CC([N+]([O-])=O)=N1 JMAGBGSWLILKOC-UHFFFAOYSA-N 0.000 description 4
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 4
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 4
- 241000124008 Mammalia Species 0.000 description 4
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 4
- 101100030361 Neurospora crassa (strain ATCC 24698 / 74-OR23-1A / CBS 708.71 / DSM 1257 / FGSC 987) pph-3 gene Proteins 0.000 description 4
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 4
- YTAHJIFKAKIKAV-XNMGPUDCSA-N [(1R)-3-morpholin-4-yl-1-phenylpropyl] N-[(3S)-2-oxo-5-phenyl-1,3-dihydro-1,4-benzodiazepin-3-yl]carbamate Chemical compound O=C1[C@H](N=C(C2=C(N1)C=CC=C2)C1=CC=CC=C1)NC(O[C@H](CCN1CCOCC1)C1=CC=CC=C1)=O YTAHJIFKAKIKAV-XNMGPUDCSA-N 0.000 description 4
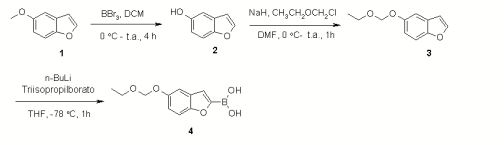
- AZFJZNXXAWDHES-UHFFFAOYSA-N [5-(ethoxymethoxy)-1-benzofuran-2-yl]boronic acid Chemical compound CCOCOC1=CC=C2OC(B(O)O)=CC2=C1 AZFJZNXXAWDHES-UHFFFAOYSA-N 0.000 description 4
- 150000001335 aliphatic alkanes Chemical class 0.000 description 4
- 150000001408 amides Chemical class 0.000 description 4
- 230000000694 effects Effects 0.000 description 4
- 150000002170 ethers Chemical class 0.000 description 4
- 239000012467 final product Substances 0.000 description 4
- 239000012535 impurity Substances 0.000 description 4
- 238000000338 in vitro Methods 0.000 description 4
- 238000002595 magnetic resonance imaging Methods 0.000 description 4
- SKTCDJAMAYNROS-UHFFFAOYSA-N methoxycyclopentane Chemical compound COC1CCCC1 SKTCDJAMAYNROS-UHFFFAOYSA-N 0.000 description 4
- 229910052757 nitrogen Inorganic materials 0.000 description 4
- 239000000843 powder Substances 0.000 description 4
- 238000000634 powder X-ray diffraction Methods 0.000 description 4
- 102000004169 proteins and genes Human genes 0.000 description 4
- 229920006395 saturated elastomer Polymers 0.000 description 4
- 238000001228 spectrum Methods 0.000 description 4
- 238000004809 thin layer chromatography Methods 0.000 description 4
- 239000008096 xylene Substances 0.000 description 4
- MYNQXTDIPMCJCR-UHFFFAOYSA-N 2-[2-fluoro-6-(methylamino)pyridin-3-yl]-1-benzofuran-5-ol Chemical compound FC1=NC(NC)=CC=C1C1=CC2=CC(O)=CC=C2O1 MYNQXTDIPMCJCR-UHFFFAOYSA-N 0.000 description 3
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 3
- DYHSDKLCOJIUFX-UHFFFAOYSA-N Di-tert-butyl dicarbonate Substances CC(C)(C)OC(=O)OC(=O)OC(C)(C)C DYHSDKLCOJIUFX-UHFFFAOYSA-N 0.000 description 3
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 3
- BZLVMXJERCGZMT-UHFFFAOYSA-N Methyl tert-butyl ether Chemical compound COC(C)(C)C BZLVMXJERCGZMT-UHFFFAOYSA-N 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- UJLXRMRGINDKCA-UHFFFAOYSA-N [5-[5-(ethoxymethoxy)-1-benzofuran-2-yl]-6-nitropyridin-2-yl]-methylcarbamic acid Chemical compound C(C)OCOC=1C=CC2=C(C=C(O2)C=2C=CC(=NC=2[N+](=O)[O-])N(C(O)=O)C)C=1 UJLXRMRGINDKCA-UHFFFAOYSA-N 0.000 description 3
- 238000011888 autopsy Methods 0.000 description 3
- FCYRSDMGOLYDHL-UHFFFAOYSA-N chloromethoxyethane Chemical compound CCOCCl FCYRSDMGOLYDHL-UHFFFAOYSA-N 0.000 description 3
- 229940125904 compound 1 Drugs 0.000 description 3
- 239000006185 dispersion Substances 0.000 description 3
- 150000002148 esters Chemical class 0.000 description 3
- 238000001704 evaporation Methods 0.000 description 3
- 230000008020 evaporation Effects 0.000 description 3
- 238000001914 filtration Methods 0.000 description 3
- 208000017105 hereditary amyloidosis Diseases 0.000 description 3
- HMSWAIKSFDFLKN-UHFFFAOYSA-N hexacosane Chemical compound CCCCCCCCCCCCCCCCCCCCCCCCCC HMSWAIKSFDFLKN-UHFFFAOYSA-N 0.000 description 3
- 238000004128 high performance liquid chromatography Methods 0.000 description 3
- 238000005259 measurement Methods 0.000 description 3
- 150000007522 mineralic acids Chemical class 0.000 description 3
- 239000012299 nitrogen atmosphere Substances 0.000 description 3
- 231100000252 nontoxic Toxicity 0.000 description 3
- 230000003000 nontoxic effect Effects 0.000 description 3
- 238000009206 nuclear medicine Methods 0.000 description 3
- 229910052763 palladium Inorganic materials 0.000 description 3
- 150000003384 small molecules Chemical class 0.000 description 3
- 239000011780 sodium chloride Substances 0.000 description 3
- 230000009885 systemic effect Effects 0.000 description 3
- 238000003325 tomography Methods 0.000 description 3
- GHYOCDFICYLMRF-UTIIJYGPSA-N (2S,3R)-N-[(2S)-3-(cyclopenten-1-yl)-1-[(2R)-2-methyloxiran-2-yl]-1-oxopropan-2-yl]-3-hydroxy-3-(4-methoxyphenyl)-2-[[(2S)-2-[(2-morpholin-4-ylacetyl)amino]propanoyl]amino]propanamide Chemical compound C1(=CCCC1)C[C@@H](C(=O)[C@@]1(OC1)C)NC([C@H]([C@@H](C1=CC=C(C=C1)OC)O)NC([C@H](C)NC(CN1CCOCC1)=O)=O)=O GHYOCDFICYLMRF-UTIIJYGPSA-N 0.000 description 2
- UNILWMWFPHPYOR-KXEYIPSPSA-M 1-[6-[2-[3-[3-[3-[2-[2-[3-[[2-[2-[[(2r)-1-[[2-[[(2r)-1-[3-[2-[2-[3-[[2-(2-amino-2-oxoethoxy)acetyl]amino]propoxy]ethoxy]ethoxy]propylamino]-3-hydroxy-1-oxopropan-2-yl]amino]-2-oxoethyl]amino]-3-[(2r)-2,3-di(hexadecanoyloxy)propyl]sulfanyl-1-oxopropan-2-yl Chemical compound O=C1C(SCCC(=O)NCCCOCCOCCOCCCNC(=O)COCC(=O)N[C@@H](CSC[C@@H](COC(=O)CCCCCCCCCCCCCCC)OC(=O)CCCCCCCCCCCCCCC)C(=O)NCC(=O)N[C@H](CO)C(=O)NCCCOCCOCCOCCCNC(=O)COCC(N)=O)CC(=O)N1CCNC(=O)CCCCCN\1C2=CC=C(S([O-])(=O)=O)C=C2CC/1=C/C=C/C=C/C1=[N+](CC)C2=CC=C(S([O-])(=O)=O)C=C2C1 UNILWMWFPHPYOR-KXEYIPSPSA-M 0.000 description 2
- MTJGVAJYTOXFJH-UHFFFAOYSA-N 3-aminonaphthalene-1,5-disulfonic acid Chemical compound C1=CC=C(S(O)(=O)=O)C2=CC(N)=CC(S(O)(=O)=O)=C21 MTJGVAJYTOXFJH-UHFFFAOYSA-N 0.000 description 2
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonia chloride Chemical class [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 2
- 229910015845 BBr3 Inorganic materials 0.000 description 2
- GDVJVIMFXITKLU-UHFFFAOYSA-N C1=CC(=NC(=C1NC(=O)O)[N+](=O)[O-])Br Chemical compound C1=CC(=NC(=C1NC(=O)O)[N+](=O)[O-])Br GDVJVIMFXITKLU-UHFFFAOYSA-N 0.000 description 2
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 2
- 206010012289 Dementia Diseases 0.000 description 2
- KRHYYFGTRYWZRS-UHFFFAOYSA-M Fluoride anion Chemical compound [F-] KRHYYFGTRYWZRS-UHFFFAOYSA-M 0.000 description 2
- 208000005531 Immunoglobulin Light-chain Amyloidosis Diseases 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- LRHPLDYGYMQRHN-UHFFFAOYSA-N N-Butanol Chemical compound CCCCO LRHPLDYGYMQRHN-UHFFFAOYSA-N 0.000 description 2
- PXHVJJICTQNCMI-UHFFFAOYSA-N Nickel Chemical compound [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 2
- XYFCBTPGUUZFHI-UHFFFAOYSA-N Phosphine Chemical compound P XYFCBTPGUUZFHI-UHFFFAOYSA-N 0.000 description 2
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 2
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 2
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 2
- 238000009825 accumulation Methods 0.000 description 2
- 229940100198 alkylating agent Drugs 0.000 description 2
- 150000001412 amines Chemical class 0.000 description 2
- 238000006254 arylation reaction Methods 0.000 description 2
- 230000009286 beneficial effect Effects 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- IANQTJSKSUMEQM-UHFFFAOYSA-N benzofuran Natural products C1=CC=C2OC=CC2=C1 IANQTJSKSUMEQM-UHFFFAOYSA-N 0.000 description 2
- 239000011230 binding agent Substances 0.000 description 2
- 229940125797 compound 12 Drugs 0.000 description 2
- 150000001907 coumarones Chemical class 0.000 description 2
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 2
- 208000035475 disorder Diseases 0.000 description 2
- 239000003814 drug Substances 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- 150000002500 ions Chemical class 0.000 description 2
- 229910052751 metal Inorganic materials 0.000 description 2
- 239000002184 metal Substances 0.000 description 2
- HHQJWDKIRXRTLS-UHFFFAOYSA-N n'-bromobutanediamide Chemical compound NC(=O)CCC(=O)NBr HHQJWDKIRXRTLS-UHFFFAOYSA-N 0.000 description 2
- ONNRHLDBKGPEAC-UHFFFAOYSA-N n-methyl-6-nitropyridin-2-amine Chemical compound CNC1=CC=CC([N+]([O-])=O)=N1 ONNRHLDBKGPEAC-UHFFFAOYSA-N 0.000 description 2
- 238000002610 neuroimaging Methods 0.000 description 2
- 150000007524 organic acids Chemical class 0.000 description 2
- 235000005985 organic acids Nutrition 0.000 description 2
- 239000008194 pharmaceutical composition Substances 0.000 description 2
- 239000002953 phosphate buffered saline Substances 0.000 description 2
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 2
- SCVFZCLFOSHCOH-UHFFFAOYSA-M potassium acetate Chemical compound [K+].CC([O-])=O SCVFZCLFOSHCOH-UHFFFAOYSA-M 0.000 description 2
- NROKBHXJSPEDAR-UHFFFAOYSA-M potassium fluoride Chemical compound [F-].[K+] NROKBHXJSPEDAR-UHFFFAOYSA-M 0.000 description 2
- 238000001556 precipitation Methods 0.000 description 2
- 108090000765 processed proteins & peptides Proteins 0.000 description 2
- 238000000159 protein binding assay Methods 0.000 description 2
- 238000011002 quantification Methods 0.000 description 2
- 238000011894 semi-preparative HPLC Methods 0.000 description 2
- 239000000741 silica gel Substances 0.000 description 2
- 229910002027 silica gel Inorganic materials 0.000 description 2
- 229910052938 sodium sulfate Inorganic materials 0.000 description 2
- 235000011152 sodium sulphate Nutrition 0.000 description 2
- 239000012453 solvate Substances 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- 235000011149 sulphuric acid Nutrition 0.000 description 2
- 208000024891 symptom Diseases 0.000 description 2
- 231100000419 toxicity Toxicity 0.000 description 2
- 230000001988 toxicity Effects 0.000 description 2
- LWIHDJKSTIGBAC-UHFFFAOYSA-K tripotassium phosphate Chemical compound [K+].[K+].[K+].[O-]P([O-])([O-])=O LWIHDJKSTIGBAC-UHFFFAOYSA-K 0.000 description 2
- 235000012141 vanillin Nutrition 0.000 description 2
- MWOOGOJBHIARFG-UHFFFAOYSA-N vanillin Chemical compound COC1=CC(C=O)=CC=C1O MWOOGOJBHIARFG-UHFFFAOYSA-N 0.000 description 2
- FGQOOHJZONJGDT-UHFFFAOYSA-N vanillin Natural products COC1=CC(O)=CC(C=O)=C1 FGQOOHJZONJGDT-UHFFFAOYSA-N 0.000 description 2
- 239000003039 volatile agent Substances 0.000 description 2
- FLUWIAPINGEFQX-UHFFFAOYSA-N (5-bromo-6-nitropyridin-2-yl)carbamic acid Chemical compound BrC=1C=CC(=NC1[N+](=O)[O-])NC(O)=O FLUWIAPINGEFQX-UHFFFAOYSA-N 0.000 description 1
- KZPYGQFFRCFCPP-UHFFFAOYSA-N 1,1'-bis(diphenylphosphino)ferrocene Chemical compound [Fe+2].C1=CC=C[C-]1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=C[C-]1P(C=1C=CC=CC=1)C1=CC=CC=C1 KZPYGQFFRCFCPP-UHFFFAOYSA-N 0.000 description 1
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 1
- FCEHBMOGCRZNNI-UHFFFAOYSA-N 1-benzothiophene Chemical class C1=CC=C2SC=CC2=C1 FCEHBMOGCRZNNI-UHFFFAOYSA-N 0.000 description 1
- MICMHFIQSAMEJG-UHFFFAOYSA-N 1-bromopyrrolidine-2,5-dione Chemical compound BrN1C(=O)CCC1=O.BrN1C(=O)CCC1=O MICMHFIQSAMEJG-UHFFFAOYSA-N 0.000 description 1
- MEKOFIRRDATTAG-UHFFFAOYSA-N 2,2,5,8-tetramethyl-3,4-dihydrochromen-6-ol Chemical compound C1CC(C)(C)OC2=C1C(C)=C(O)C=C2C MEKOFIRRDATTAG-UHFFFAOYSA-N 0.000 description 1
- GZBKVUGZEAJYHH-UHFFFAOYSA-N 2-nitropyridin-3-amine Chemical compound NC1=CC=CN=C1[N+]([O-])=O GZBKVUGZEAJYHH-UHFFFAOYSA-N 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- 208000023769 AA amyloidosis Diseases 0.000 description 1
- 208000023761 AL amyloidosis Diseases 0.000 description 1
- 108700028369 Alleles Proteins 0.000 description 1
- USFZMSVCRYTOJT-UHFFFAOYSA-N Ammonium acetate Chemical compound N.CC(O)=O USFZMSVCRYTOJT-UHFFFAOYSA-N 0.000 description 1
- 239000005695 Ammonium acetate Substances 0.000 description 1
- 102000013455 Amyloid beta-Peptides Human genes 0.000 description 1
- 108010090849 Amyloid beta-Peptides Proteins 0.000 description 1
- 102000009091 Amyloidogenic Proteins Human genes 0.000 description 1
- 108010048112 Amyloidogenic Proteins Proteins 0.000 description 1
- 108010060159 Apolipoprotein E4 Proteins 0.000 description 1
- 230000007082 Aβ accumulation Effects 0.000 description 1
- 208000035143 Bacterial infection Diseases 0.000 description 1
- BTBUEUYNUDRHOZ-UHFFFAOYSA-N Borate Chemical compound [O-]B([O-])[O-] BTBUEUYNUDRHOZ-UHFFFAOYSA-N 0.000 description 1
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 1
- COVZYZSDYWQREU-UHFFFAOYSA-N Busulfan Chemical compound CS(=O)(=O)OCCCCOS(C)(=O)=O COVZYZSDYWQREU-UHFFFAOYSA-N 0.000 description 1
- FNUGUIQDFBBQSP-UHFFFAOYSA-N CCOCOC1=CC2=C(C=C1)OC(=C2)C3=NC(=C(C(=C3)C(C)(C)C)N(C)C(=O)O)[N+](=O)[O-] Chemical compound CCOCOC1=CC2=C(C=C1)OC(=C2)C3=NC(=C(C(=C3)C(C)(C)C)N(C)C(=O)O)[N+](=O)[O-] FNUGUIQDFBBQSP-UHFFFAOYSA-N 0.000 description 1
- OKTJSMMVPCPJKN-OUBTZVSYSA-N Carbon-13 Chemical compound [13C] OKTJSMMVPCPJKN-OUBTZVSYSA-N 0.000 description 1
- 241000557626 Corvus corax Species 0.000 description 1
- 208000011231 Crohn disease Diseases 0.000 description 1
- YZCKVEUIGOORGS-OUBTZVSYSA-N Deuterium Chemical compound [2H] YZCKVEUIGOORGS-OUBTZVSYSA-N 0.000 description 1
- 201000010374 Down Syndrome Diseases 0.000 description 1
- 206010016207 Familial Mediterranean fever Diseases 0.000 description 1
- 206010019233 Headaches Diseases 0.000 description 1
- 208000017604 Hodgkin disease Diseases 0.000 description 1
- 208000010747 Hodgkins lymphoma Diseases 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- 206010061218 Inflammation Diseases 0.000 description 1
- 206010024229 Leprosy Diseases 0.000 description 1
- 239000002841 Lewis acid Substances 0.000 description 1
- 208000034578 Multiple myelomas Diseases 0.000 description 1
- FXHOOIRPVKKKFG-UHFFFAOYSA-N N,N-Dimethylacetamide Chemical compound CN(C)C(C)=O FXHOOIRPVKKKFG-UHFFFAOYSA-N 0.000 description 1
- 229910017917 NH4 Cl Inorganic materials 0.000 description 1
- 208000012902 Nervous system disease Diseases 0.000 description 1
- 208000025966 Neurological disease Diseases 0.000 description 1
- 206010053159 Organ failure Diseases 0.000 description 1
- 206010031252 Osteomyelitis Diseases 0.000 description 1
- 238000012879 PET imaging Methods 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 208000037581 Persistent Infection Diseases 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 1
- 206010035226 Plasma cell myeloma Diseases 0.000 description 1
- 206010036673 Primary amyloidosis Diseases 0.000 description 1
- 206010037660 Pyrexia Diseases 0.000 description 1
- 208000035977 Rare disease Diseases 0.000 description 1
- 206010039811 Secondary amyloidosis Diseases 0.000 description 1
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 1
- VMHLLURERBWHNL-UHFFFAOYSA-M Sodium acetate Chemical compound [Na+].CC([O-])=O VMHLLURERBWHNL-UHFFFAOYSA-M 0.000 description 1
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical class [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 1
- GKLVYJBZJHMRIY-OUBTZVSYSA-N Technetium-99 Chemical compound [99Tc] GKLVYJBZJHMRIY-OUBTZVSYSA-N 0.000 description 1
- HEDRZPFGACZZDS-MICDWDOJSA-N Trichloro(2H)methane Chemical compound [2H]C(Cl)(Cl)Cl HEDRZPFGACZZDS-MICDWDOJSA-N 0.000 description 1
- 206010044688 Trisomy 21 Diseases 0.000 description 1
- YZCKVEUIGOORGS-NJFSPNSNSA-N Tritium Chemical compound [3H] YZCKVEUIGOORGS-NJFSPNSNSA-N 0.000 description 1
- 230000002159 abnormal effect Effects 0.000 description 1
- 125000000218 acetic acid group Chemical group C(C)(=O)* 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 230000002152 alkylating effect Effects 0.000 description 1
- 208000026935 allergic disease Diseases 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 235000019257 ammonium acetate Nutrition 0.000 description 1
- 229940043376 ammonium acetate Drugs 0.000 description 1
- 230000006933 amyloid-beta aggregation Effects 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 239000008346 aqueous phase Substances 0.000 description 1
- 238000000376 autoradiography Methods 0.000 description 1
- 208000022362 bacterial infectious disease Diseases 0.000 description 1
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid group Chemical group C(C1=CC=CC=C1)(=O)O WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 1
- 238000001574 biopsy Methods 0.000 description 1
- XGIUDIMNNMKGDE-UHFFFAOYSA-N bis(trimethylsilyl)azanide Chemical compound C[Si](C)(C)[N-][Si](C)(C)C XGIUDIMNNMKGDE-UHFFFAOYSA-N 0.000 description 1
- 230000008499 blood brain barrier function Effects 0.000 description 1
- 210000001218 blood-brain barrier Anatomy 0.000 description 1
- 230000037396 body weight Effects 0.000 description 1
- 210000001185 bone marrow Anatomy 0.000 description 1
- 201000006491 bone marrow cancer Diseases 0.000 description 1
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 1
- 229910052794 bromium Inorganic materials 0.000 description 1
- FJDQFPXHSGXQBY-UHFFFAOYSA-L caesium carbonate Chemical compound [Cs+].[Cs+].[O-]C([O-])=O FJDQFPXHSGXQBY-UHFFFAOYSA-L 0.000 description 1
- 229910000024 caesium carbonate Inorganic materials 0.000 description 1
- GTCAXTIRRLKXRU-UHFFFAOYSA-N carbamic acid methyl ester Natural products COC(N)=O GTCAXTIRRLKXRU-UHFFFAOYSA-N 0.000 description 1
- 238000001460 carbon-13 nuclear magnetic resonance spectrum Methods 0.000 description 1
- 150000004649 carbonic acid derivatives Chemical class 0.000 description 1
- 150000001735 carboxylic acids Chemical class 0.000 description 1
- 230000002490 cerebral effect Effects 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- 208000037976 chronic inflammation Diseases 0.000 description 1
- 208000037893 chronic inflammatory disorder Diseases 0.000 description 1
- 238000011260 co-administration Methods 0.000 description 1
- 230000003920 cognitive function Effects 0.000 description 1
- 239000012230 colorless oil Substances 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 238000012937 correction Methods 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- 239000002178 crystalline material Substances 0.000 description 1
- 238000002447 crystallographic data Methods 0.000 description 1
- DEZRYPDIMOWBDS-UHFFFAOYSA-N dcm dichloromethane Chemical compound ClCCl.ClCCl DEZRYPDIMOWBDS-UHFFFAOYSA-N 0.000 description 1
- 230000007423 decrease Effects 0.000 description 1
- 230000002950 deficient Effects 0.000 description 1
- 230000007850 degeneration Effects 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 230000008021 deposition Effects 0.000 description 1
- 229910052805 deuterium Inorganic materials 0.000 description 1
- 239000010432 diamond Substances 0.000 description 1
- 235000005911 diet Nutrition 0.000 description 1
- 230000037213 diet Effects 0.000 description 1
- IJKVHSBPTUYDLN-UHFFFAOYSA-N dihydroxy(oxo)silane Chemical compound O[Si](O)=O IJKVHSBPTUYDLN-UHFFFAOYSA-N 0.000 description 1
- VAYGXNSJCAHWJZ-UHFFFAOYSA-N dimethyl sulfate Chemical compound COS(=O)(=O)OC VAYGXNSJCAHWJZ-UHFFFAOYSA-N 0.000 description 1
- UXGNZZKBCMGWAZ-UHFFFAOYSA-N dimethylformamide dmf Chemical compound CN(C)C=O.CN(C)C=O UXGNZZKBCMGWAZ-UHFFFAOYSA-N 0.000 description 1
- 208000016097 disease of metabolism Diseases 0.000 description 1
- 238000004090 dissolution Methods 0.000 description 1
- CETRZFQIITUQQL-UHFFFAOYSA-N dmso dimethylsulfoxide Chemical compound CS(C)=O.CS(C)=O CETRZFQIITUQQL-UHFFFAOYSA-N 0.000 description 1
- 239000002552 dosage form Substances 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- OCLXJTCGWSSVOE-UHFFFAOYSA-N ethanol etoh Chemical compound CCO.CCO OCLXJTCGWSSVOE-UHFFFAOYSA-N 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- 238000003818 flash chromatography Methods 0.000 description 1
- 239000012458 free base Substances 0.000 description 1
- 230000006870 function Effects 0.000 description 1
- 230000004927 fusion Effects 0.000 description 1
- 210000005095 gastrointestinal system Anatomy 0.000 description 1
- 238000007429 general method Methods 0.000 description 1
- 231100000869 headache Toxicity 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 210000002216 heart Anatomy 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 125000001072 heteroaryl group Chemical group 0.000 description 1
- 125000000623 heterocyclic group Chemical group 0.000 description 1
- FFUAGWLWBBFQJT-UHFFFAOYSA-N hexamethyldisilazane Chemical compound C[Si](C)(C)N[Si](C)(C)C FFUAGWLWBBFQJT-UHFFFAOYSA-N 0.000 description 1
- 150000004677 hydrates Chemical class 0.000 description 1
- 239000012216 imaging agent Substances 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 239000003999 initiator Substances 0.000 description 1
- 229910052500 inorganic mineral Inorganic materials 0.000 description 1
- 238000001361 intraarterial administration Methods 0.000 description 1
- 238000007917 intracranial administration Methods 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- 238000007913 intrathecal administration Methods 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 238000007914 intraventricular administration Methods 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- 239000011630 iodine Substances 0.000 description 1
- 230000007794 irritation Effects 0.000 description 1
- 210000001503 joint Anatomy 0.000 description 1
- 210000003734 kidney Anatomy 0.000 description 1
- 238000002372 labelling Methods 0.000 description 1
- 230000002045 lasting effect Effects 0.000 description 1
- 150000007517 lewis acids Chemical class 0.000 description 1
- 239000003446 ligand Substances 0.000 description 1
- 210000004185 liver Anatomy 0.000 description 1
- 229920002521 macromolecule Polymers 0.000 description 1
- 238000001819 mass spectrum Methods 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- 230000003340 mental effect Effects 0.000 description 1
- COTNUBDHGSIOTA-UHFFFAOYSA-N meoh methanol Chemical compound OC.OC COTNUBDHGSIOTA-UHFFFAOYSA-N 0.000 description 1
- QSHDDOUJBYECFT-UHFFFAOYSA-N mercury Chemical compound [Hg] QSHDDOUJBYECFT-UHFFFAOYSA-N 0.000 description 1
- 229910052753 mercury Inorganic materials 0.000 description 1
- 208000030159 metabolic disease Diseases 0.000 description 1
- 229910052987 metal hydride Inorganic materials 0.000 description 1
- 150000004681 metal hydrides Chemical class 0.000 description 1
- 235000010755 mineral Nutrition 0.000 description 1
- 239000011707 mineral Substances 0.000 description 1
- 239000002480 mineral oil Substances 0.000 description 1
- 235000010446 mineral oil Nutrition 0.000 description 1
- 238000012544 monitoring process Methods 0.000 description 1
- WOOWBQQQJXZGIE-UHFFFAOYSA-N n-ethyl-n-propan-2-ylpropan-2-amine Chemical compound CCN(C(C)C)C(C)C.CCN(C(C)C)C(C)C WOOWBQQQJXZGIE-UHFFFAOYSA-N 0.000 description 1
- 210000000653 nervous system Anatomy 0.000 description 1
- 229910052759 nickel Inorganic materials 0.000 description 1
- FEMOMIGRRWSMCU-UHFFFAOYSA-N ninhydrin Chemical compound C1=CC=C2C(=O)C(O)(O)C(=O)C2=C1 FEMOMIGRRWSMCU-UHFFFAOYSA-N 0.000 description 1
- 150000002825 nitriles Chemical class 0.000 description 1
- 239000012457 nonaqueous media Substances 0.000 description 1
- 230000009871 nonspecific binding Effects 0.000 description 1
- 239000003921 oil Substances 0.000 description 1
- 239000004533 oil dispersion Substances 0.000 description 1
- 239000012074 organic phase Substances 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- YJVFFLUZDVXJQI-UHFFFAOYSA-L palladium(ii) acetate Chemical compound [Pd+2].CC([O-])=O.CC([O-])=O YJVFFLUZDVXJQI-UHFFFAOYSA-L 0.000 description 1
- 210000000496 pancreas Anatomy 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 238000010951 particle size reduction Methods 0.000 description 1
- 230000008506 pathogenesis Effects 0.000 description 1
- 230000001575 pathological effect Effects 0.000 description 1
- 235000021317 phosphate Nutrition 0.000 description 1
- 235000011007 phosphoric acid Nutrition 0.000 description 1
- 150000003013 phosphoric acid derivatives Chemical class 0.000 description 1
- 229910000073 phosphorus hydride Inorganic materials 0.000 description 1
- 229910052697 platinum Inorganic materials 0.000 description 1
- 235000011056 potassium acetate Nutrition 0.000 description 1
- IUBQJLUDMLPAGT-UHFFFAOYSA-N potassium bis(trimethylsilyl)amide Chemical compound C[Si](C)(C)N([K])[Si](C)(C)C IUBQJLUDMLPAGT-UHFFFAOYSA-N 0.000 description 1
- 235000015320 potassium carbonate Nutrition 0.000 description 1
- 239000011698 potassium fluoride Substances 0.000 description 1
- 235000003270 potassium fluoride Nutrition 0.000 description 1
- 229910000160 potassium phosphate Inorganic materials 0.000 description 1
- 235000011009 potassium phosphates Nutrition 0.000 description 1
- 238000004237 preparative chromatography Methods 0.000 description 1
- 208000022256 primary systemic amyloidosis Diseases 0.000 description 1
- 230000000750 progressive effect Effects 0.000 description 1
- BDERNNFJNOPAEC-UHFFFAOYSA-N propan-1-ol Chemical compound CCCO BDERNNFJNOPAEC-UHFFFAOYSA-N 0.000 description 1
- FVSKHRXBFJPNKK-UHFFFAOYSA-N propionitrile Chemical compound CCC#N FVSKHRXBFJPNKK-UHFFFAOYSA-N 0.000 description 1
- 125000006239 protecting group Chemical group 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 150000003242 quaternary ammonium salts Chemical class 0.000 description 1
- 230000002285 radioactive effect Effects 0.000 description 1
- 238000000163 radioactive labelling Methods 0.000 description 1
- 238000001953 recrystallisation Methods 0.000 description 1
- 230000000306 recurrent effect Effects 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 210000002345 respiratory system Anatomy 0.000 description 1
- 206010039073 rheumatoid arthritis Diseases 0.000 description 1
- 229910021332 silicide Inorganic materials 0.000 description 1
- FVBUAEGBCNSCDD-UHFFFAOYSA-N silicide(4-) Chemical compound [Si-4] FVBUAEGBCNSCDD-UHFFFAOYSA-N 0.000 description 1
- 229910052710 silicon Inorganic materials 0.000 description 1
- 239000010703 silicon Substances 0.000 description 1
- 210000003491 skin Anatomy 0.000 description 1
- 239000002002 slurry Substances 0.000 description 1
- 210000000813 small intestine Anatomy 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 239000001632 sodium acetate Substances 0.000 description 1
- 235000017281 sodium acetate Nutrition 0.000 description 1
- 229910000029 sodium carbonate Inorganic materials 0.000 description 1
- 235000017550 sodium carbonate Nutrition 0.000 description 1
- RMBAVIFYHOYIFM-UHFFFAOYSA-M sodium methanethiolate Chemical compound [Na+].[S-]C RMBAVIFYHOYIFM-UHFFFAOYSA-M 0.000 description 1
- 239000001488 sodium phosphate Substances 0.000 description 1
- 229910000162 sodium phosphate Inorganic materials 0.000 description 1
- 235000011008 sodium phosphates Nutrition 0.000 description 1
- 210000000952 spleen Anatomy 0.000 description 1
- 239000007921 spray Substances 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 229940056501 technetium 99m Drugs 0.000 description 1
- LEDGEFAUSJYBHL-UHFFFAOYSA-N tert-butyl n-(6-bromo-2-nitropyridin-3-yl)carbamate Chemical compound CC(C)(C)OC(=O)NC1=CC=C(Br)N=C1[N+]([O-])=O LEDGEFAUSJYBHL-UHFFFAOYSA-N 0.000 description 1
- FQFILJKFZCVHNH-UHFFFAOYSA-N tert-butyl n-[3-[(5-bromo-2-chloropyrimidin-4-yl)amino]propyl]carbamate Chemical compound CC(C)(C)OC(=O)NCCCNC1=NC(Cl)=NC=C1Br FQFILJKFZCVHNH-UHFFFAOYSA-N 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- WHRNULOCNSKMGB-UHFFFAOYSA-N tetrahydrofuran thf Chemical compound C1CCOC1.C1CCOC1 WHRNULOCNSKMGB-UHFFFAOYSA-N 0.000 description 1
- CZDYPVPMEAXLPK-UHFFFAOYSA-N tetramethylsilane Chemical compound C[Si](C)(C)C CZDYPVPMEAXLPK-UHFFFAOYSA-N 0.000 description 1
- WROMPOXWARCANT-UHFFFAOYSA-N tfa trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F.OC(=O)C(F)(F)F WROMPOXWARCANT-UHFFFAOYSA-N 0.000 description 1
- 229940124597 therapeutic agent Drugs 0.000 description 1
- JADVWWSKYZXRGX-UHFFFAOYSA-M thioflavine T Chemical class [Cl-].C1=CC(N(C)C)=CC=C1C1=[N+](C)C2=CC=C(C)C=C2S1 JADVWWSKYZXRGX-UHFFFAOYSA-M 0.000 description 1
- 230000000699 topical effect Effects 0.000 description 1
- LGQXXHMEBUOXRP-UHFFFAOYSA-N tributyl borate Chemical compound CCCCOB(OCCCC)OCCCC LGQXXHMEBUOXRP-UHFFFAOYSA-N 0.000 description 1
- WLPUWLXVBWGYMZ-UHFFFAOYSA-N tricyclohexylphosphine Chemical compound C1CCCCC1P(C1CCCCC1)C1CCCCC1 WLPUWLXVBWGYMZ-UHFFFAOYSA-N 0.000 description 1
- WRECIMRULFAWHA-UHFFFAOYSA-N trimethyl borate Chemical compound COB(OC)OC WRECIMRULFAWHA-UHFFFAOYSA-N 0.000 description 1
- LTEHWCSSIHAVOQ-UHFFFAOYSA-N tripropyl borate Chemical compound CCCOB(OCCC)OCCC LTEHWCSSIHAVOQ-UHFFFAOYSA-N 0.000 description 1
- RYFMWSXOAZQYPI-UHFFFAOYSA-K trisodium phosphate Chemical compound [Na+].[Na+].[Na+].[O-]P([O-])([O-])=O RYFMWSXOAZQYPI-UHFFFAOYSA-K 0.000 description 1
- 229910052722 tritium Inorganic materials 0.000 description 1
- 238000007794 visualization technique Methods 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/04—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K51/00—Preparations containing radioactive substances for use in therapy or testing in vivo
- A61K51/02—Preparations containing radioactive substances for use in therapy or testing in vivo characterised by the carrier, i.e. characterised by the agent or material covalently linked or complexing the radioactive nucleus
- A61K51/04—Organic compounds
- A61K51/041—Heterocyclic compounds
- A61K51/044—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine, rifamycins
- A61K51/0455—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine, rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4427—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems
- A61K31/443—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems containing a five-membered ring with oxygen as a ring hetero atom
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K51/00—Preparations containing radioactive substances for use in therapy or testing in vivo
- A61K51/02—Preparations containing radioactive substances for use in therapy or testing in vivo characterised by the carrier, i.e. characterised by the agent or material covalently linked or complexing the radioactive nucleus
- A61K51/04—Organic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07B—GENERAL METHODS OF ORGANIC CHEMISTRY; APPARATUS THEREFOR
- C07B59/00—Introduction of isotopes of elements into organic compounds ; Labelled organic compounds per se
- C07B59/002—Heterocyclic compounds
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/60—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D213/72—Nitrogen atoms
- C07D213/75—Amino or imino radicals, acylated by carboxylic or carbonic acids, or by sulfur or nitrogen analogues thereof, e.g. carbamates
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/60—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D213/72—Nitrogen atoms
- C07D213/76—Nitrogen atoms to which a second hetero atom is attached
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D307/00—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom
- C07D307/77—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom ortho- or peri-condensed with carbocyclic rings or ring systems
- C07D307/78—Benzo [b] furans; Hydrogenated benzo [b] furans
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F5/00—Compounds containing elements of Groups 3 or 13 of the Periodic Table
- C07F5/02—Boron compounds
- C07F5/025—Boronic and borinic acid compounds
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07B—GENERAL METHODS OF ORGANIC CHEMISTRY; APPARATUS THEREFOR
- C07B2200/00—Indexing scheme relating to specific properties of organic compounds
- C07B2200/05—Isotopically modified compounds, e.g. labelled
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07B—GENERAL METHODS OF ORGANIC CHEMISTRY; APPARATUS THEREFOR
- C07B2200/00—Indexing scheme relating to specific properties of organic compounds
- C07B2200/13—Crystalline forms, e.g. polymorphs
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Physics & Mathematics (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Optics & Photonics (AREA)
- Neurosurgery (AREA)
- Biomedical Technology (AREA)
- Engineering & Computer Science (AREA)
- Neurology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Hospice & Palliative Care (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Psychiatry (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Plural Heterocyclic Compounds (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Pyridine Compounds (AREA)
- Furan Compounds (AREA)
Abstract
COMPOSTO OU SAL DESTE USO DE UM COMPOSTO OU SAL DESTE, E, PROCESSO PARA FABRICAR UM COMPOSTO. A presente invenção diz respeito a novos derivados que são adequados como percursores para compostos que são úteis para formação de imagem de depósitos de amilóide em pacientes vivos, as suas composições métodos de uso e processos para fabricar tais componentes. Os compostos que derivam destes precursores dão úteis nos métodos de formação de imagem de depósitos de amilóide no cérebro in vivo para permitir diagnóstico anterior á morte da doença de Alzheimer pela tomografia de emissão de positron (PET) assi, como medir a eficácia clínica de agentes terapêuticos para a doença de Alzheimer. Além disso, a presente invenção também divulga os compostos precursores na forma cristalina.
Description
[001] Esta patente reivindica o benefício do Pedido Provisório US N- 61/092.851 (depositado em 29 de agosto de 2008). O texto completo do pedido de patente aludido acima é incorporado por referência nesta patente.
[002] A presente invenção diz respeito a novos derivados que são adequados como precursores para compostos úteis para a formação de imagem de depósitos de amilóide em mamíferos tais como pacientes vivos, suas composições, métodos de uso e processos para fabricar tais compostos. Os compostos que derivam destes precursores são úteis nos métodos de formação de imagem de depósitos de amilóide no cérebro in vivo para permitir o diagnóstico anterior à morte da doença de Alzheimer com técnicas de formação de imagem tais como a tomografia de emissão de positron (PET). Os compostos também podem ser usados para medir a eficácia clínica de agentes terapêuticos para a doença de Alzheimer. Além disso, a presente invenção também divulga os compostos precursores na forma cristalina.
[003] A amiloidose é uma doença metabólica progressiva, incurável de causa desconhecida caracterizada pelos depósitos anormais de proteína em um ou mais órgãos ou sistemas corporais. As proteínas amilóides são fabricadas, por exemplo, pelo mal funcionamento da medula óssea. A amiloidose, que ocorre quando depósitos de amilóide acumulados prejudicam o funcionamento normal do corpo, pode causar a insuficiência de órgão ou morte. A mesma é uma doença rara, que ocorre em cerca de oito de cada 1.000.000 pessoas. A mesma afeta homens e mulheres igualmente e usualmente se desenvolve depois da idade de 40. Pelo menos 15 tipos de amiloidose foram identificados. Cada um está associado com depósitos de um tipo diferente de proteína.
[004] As formas principais de amiloidose são amiloidose primária sistêmica, secundária, e familiar ou hereditária.
[005] Existe também uma outra forma de amiloidose, que está associada com a doença de Alzheimer. A amiloidose sistêmica primária usualmente se desenvolve entre as idades de 50 e 60. Com cerca de 2.000 novos casos diagnosticados anualmente, a amiloidose primária sistêmica é a forma mais comum desta doença nos Estados Unidos. Também conhecida como amiloidose relacionada com a cadeia leve, também pode ocorrer em associação com mieloma múltiplo (câncer ósseo da medula). A amiloidose secundária é um resultado da infecção crônica ou doença inflamatória. A mesma está frequentemente associada com a febre Mediterrânea Familiar (uma infecção bacteriana caracterizada por calafrios, fraqueza, dor de cabeça, e febre recorrente), ileíte granulomatosa (inflamação do intestino delgado), doença de Hodgkin, Lepra, Osteomielite e Artrite reumatóide.
[006] A amiloidose familiar ou hereditária é a única forma herdada da doença. A mesma ocorre em membros da maioria dos grupos étnicos, e cada família tem um padrão distintivo de sintomas e envolvimento de órgão. A Amiloidose hereditária é considerada ser dominante autossômica, que significa que apenas uma cópia do gene defeituoso é necessária para causar a doença. Uma criança de um pai com amiloidose familiar tem um risco de 50- 50 de desenvolver a doença.
[007] A amiloidose pode envolver qualquer órgão ou sistema no corpo. O coração, rins, sistema gastrointestinal, e sistema nervoso são afetados mais frequentemente. Outros sítios comuns de acúmulo de amilóide incluem o cérebro, juntas, fígado, baço, pâncreas, sistema respiratório, e pele.
[008] A doença de Alzheimer (AD) é a forma mais comum de demência, uma doença neurológica caracterizada pela perda de capacidade mental severa o bastante para interferir com as atividades normais da vida diária, durando pelo menos seis meses, e não presente do nascimento. A AD usualmente ocorre na idade avançada, e é marcada por um declínio nas funções cognitivas tais como lembrança, raciocínio, e planejamento.
[009] Entre dois e quatro milhões de americanos têm AD; este número é esperado crescer até tanto quanto 14 milhões em meados do século 21 conforme a população como um todo envelhece. Embora um número pequeno de pessoas nos seus 40 e 50 anos desenvolvam a doença, a AD predominantemente afeta os idosos. A AD afeta cerca de 3 % de todas as pessoas entre as idades de 65 e 74, cerca de 20 % daquelas entre 75 e 84, e cerca de 50 % daquelas acima de 85.
[0010] O acúmulo de peptídeo amilóide Aβ no cérebro é uma marca patológica de toda as formas de AD. E no geral aceito que a deposição de peptídeo Aβ amilóide cerebral é a influência primária que leva à patogênese da AD. (Hardy J e Selkoe D. J., Science. 297: 353-356, 2002).
[0011] As técnicas de formação de imagem, tais como a tomografia de emissão de positron (PET) e tomografia computadorizada de emissão de fóton único (SPECT), são eficazes no monitoramento do acúmulo de depósitos de amilóide no cérebro e técnicas úteis para medir a correlação com a progressão da AD (ver por exemplo, Miller, Science, 2006, 313, 1376). A aplicação destas técnicas requer radioligantes que facilmente entrem no cérebro e seletivamente se liguem aos depósitos de amilóide in vivo.
[0012] Uma necessidade existe quanto a compostos que liguem amilóide que possam cruzar a barreira hemato-encefálica, e consequentemente, possam ser usados em diagnósticos. Além disso, é importante monitorar a eficácia do tratamento dado aos pacientes com AD, medindo-se o efeito do dito tratamento medindo-se as mudanças dos níveis de placa AD.
[0013] As propriedades de interesse particular de um composto que ligue amilóide detectável, além de alta afinidade para os depósitos de amilóide in vivo e alta e rápida entrada no cérebro, incluem baixa ligação não específica ao tecido normal e rápida depuração do mesmo. Estas propriedades são habitualmente dependentes da lipofilicidade do composto (Coimbra et al. Curr. Top. Med. Chem. 2006, 6, 629). Entre as moléculas pequenas propostas para a formação de imagem das placas de amilóide, alguns análogos não carregados de tioflavina T foram sintetizados (Mathis et al.J. Med. Chem. 2003, 46, 2740). Os heterociclos isoestéricos diferentes são relatados como ligantes de ligação de amilóide potenciais (Cai et al.J. Med. Chem. 2004, 47, 2208; Kung et al.J. Med. Chem. 2003, 46, 237). Os derivados de benzofurano foram anteriormente descritos para o uso como agentes de formação de imagem (Ono et al.J. Med. Chem. 2006, 49, 2725; Lockhart et al. J. Biol. Chem. 2005, 280(9), 7677; Kung et al. Nuclear Med. Biol. 2002, 29(6), 633; W02003051859 e para o uso na prevenção da agregação de Abeta (Twyman et al. Tetrahedron Lett. 1999, 40(52), 9383; Howlett et al. Biochemical Journal 1999, 340(1), 283; Choi et al. Archives of Pharmacal Research 2004, 27(1), 19; Twyman et al. Bioorg. Med. Chem. Lett. 2001, 11(2), 255; WO9517095).
[0014] Em uma forma de realização da presente invenção, é fornecido o éster terc-butílico do ácido [6-(5-etoximetóxi-benzofuran-2-il)-2-nitro- piridin-3-il]-metil-carbâmico ou sais deste. Em uma outra forma de realização o sal é um sal farmaceuticamente aceitável.
[0015] Em uma outra forma de realização da presente invenção, é fornecido o composto éster terc-butílico do ácido [5-(5-etoximetóxi- benzofuran-2-il)-6-nitro-piridin-2-il]-metil-carbâmico ou sal deste. Em uma outra forma de realização o sal é um sal farmaceuticamente aceitável.
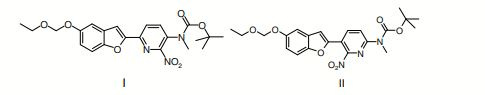
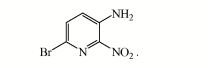
[0017] O composto I refere-se ao éster terc-butílico do ácido [6-(5- etoximetóxi-benzofuran-2-il)-2-nitro-piridin-3-il]-metil-carbâmico e o composto n refere-se ao éster terc-butílico do ácido [5-(5-etoximetóxi- benzofuran-2-il)-6-nitro-piridin-2-il]-metil-carbâmico.
[0018] Um composto pode ser esperado ser mais quimicamente estável em um estado cristalino em comparação com o mesmo composto em um estado amorfo, como descrito em Haleblian e McCrone J. Pharm. Sei 1969, 58, p911-929, especialmente p913. Esta observação é comum para as moléculas pequenas (isto é, não proteínas) mas nem sempre verdadeira para as macromoléculos como as proteínas, como descrito em Pikal e Rigsbee, Pharm. Res. 1997, 14, p 1379-1387, especialmente pl379. Um estado cristalino é assim benéfico para as moléculas pequenas tais como o éster terc- butílico do ácido [6-(5-etoximetóxi-benzofuran-2-il)-2-nitro-piridin-3-il]- metil-carbâmico e o éster terc-butílico do ácido (5-Bromo-6-nitro-piridin-2- il)-metil-carbâmico respectivamente.
[0019] Os raios X serão dispersos pelos elétrons em átomos em um composto. O material cristalino desviará os raios X por meio da difração dando picos nas direções de interferência construtiva. As direções são determinadas pela estrutura cristalina, incluindo o tamanho e forma da célula unitária. Todos os valores °2theta do pico de difração aqui divulgado e/ou reivindicado refere-se à radiação de Cu Kα. Um material amorfo (não cristalino) não dará tais picos de difração. Ver por exemplo, Klug, H. P. &Alexander, L. E., X-Ray Diffraction Procedures For Polycrystaline and Amorphous Materials, 1974, John Wiley & Sons.
[0020] A capacidade para um composto para agregar-se entre si ou formar bolo sem controle aumentará se o composto é aquecido até próximo à sua temperatura de fusão. Os grumos e bolos terão propriedades de fluxo diferente e de dissolução diferentes quando comparados com um pó. O tratamento mecânico de um pó, tal como durante a redução do tamanho de partícula, levará energia para o material e assim dá uma possibilidade para elevar a temperatura. A armazenagem de um composto assim como o transporte de um composto pode involuntariamente também levar a uma temperatura aumentada.
[0021] A fusão é um evento endotérmico. Os eventos endotérmicos podem ser medidos, por exemplo, pela calorimetria de varredura diferencial.
[0022] É assim benéfico para o éster terc-butílico do ácido [6-(5- etoximetóxi-benzofuran-2-il)-2-nitro-piridin-3-il]-metil-carbâmico ou sal deste; e para o éster terc-butílico do ácido [5-(5-etoximetóxi-benzofuran-2-il)- 6-nitro-piridin-2-il]-metil-carbâmico ou sal deste respectivamente ter tais eventos endotérmicos em uma temperatura mais alta do que a temperatura máxima esperada durante o uso normal para impedir os ditos compostos de formar um grumo ou bolo indesejados.
[0023] Em uma outra forma de realização da presente invenção, é fornecido o éster terc-butílico do ácido [6-(5-etoximetóxi-benzofuran-2-il)-2- nitro-piridin-3-il]-metil-carbâmico ou sal deste; e o éster terc-butílico do ácido [5-(5-etoximetóxi-benzofuran-2-il)-6-nitro-piridin-2-il]-metil- carbâmico ou sal deste, na forma cristalina.
[0024] Em uma outra forma de realização da presente invenção, é fornecido éster terc-butílico do ácido [6-(5-etoximetóxi-benzofuran-2-il)-2- nitro-piridin-3-il]-metil-carbâmico ou sal deste; e éster terc-butílico do ácido [5-(5-etoximetóxi-benzofuran-2-il)-6-nitro-piridin-2-il]-metil-carbâmico ou sal deste, na forma cristalina, que compreende picos de difração de raio X distintos e tendo pelo menos um evento endotérmico com início entre 70 °C e 300 °C.
[0025] Em uma outra forma de realização da presente invenção, é fornecido o composto éster terc-butílico do ácido [6-(5-etoximetóxi- benzofuran-2-il)-2-nitro-piridin-3-il]-metil-carbâmico ou sal deste, na forma cristalina, tendo um padrão de difração de raio X com pelo menos um pico de difração específico em cerca de 2-teta = 13,51°.
[0026] Em uma outra forma de realização da presente invenção, é fornecido o composto éster terc-butílico do ácido [6-(5-etoximetóxi- benzofuran-2-il)-2-nitro-piridin-3-il]-metil-carbâmico ou sal deste, na forma cristalina, que compreende os seguintes picos de difração: 11,27, 12,00, 13,51, 15,53, 16,82, 17,91 e 23,72 °2teta.
[0027] Em uma outra forma de realização a dita forma cristalina compreende os seguintes picos de difração: 6,97, 9,24, 11,27, 12,00, 13,51, 15,53, 16,82, 17,91 e 23,72 °2teta.
[0028] Em uma outra forma de realização da presente invenção, é fornecido o composto éster terc-butílico do ácido [5-(5-etoximetóxi- benzofuran-2-il)-6-nitro-piridin-2-il]-metil-carbâmico ou sal deste, na forma cristalina, tendo um padrão de difração de raio X com pelo menos um pico de difração específico em cerca de 2-teta = 6,18°.
[0029] Em uma outra forma de realização da presente invenção, é fornecido o composto éster terc-butílico do ácido [5-(5-etoximetóxi- benzofuran-2-il)-6-nitro-piridin-2-il]-metil-carbâmico ou sal deste, na forma cristalina, que compreende os seguintes picos de difração: 6,18, 9,14, 11,67, 14,98 e 16,44 °2teta.
[0030] Em uma outra forma de realização a dita forma cristalina compreende os seguintes picos de difração: 6,18, 9,14, 11,67, 12,32, 14,65, 14,98, 16,44, 17,52 e 20,66 °2teta.
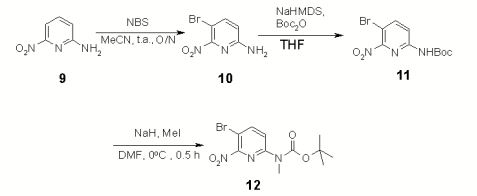
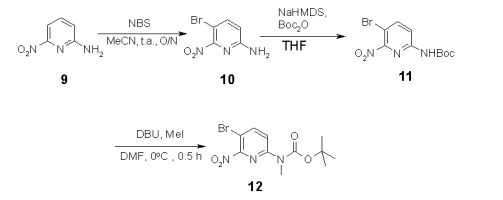
[0031] Em uma outra forma de realização da presente invenção, é fornecido o uso do éster terc-butílico do ácido [6-(5-etoximetóxi-benzofuran- 2-il)-2-nitro-piridin-3-il]-metil-carbâmico ou sal deste e do éster terc-butílico do ácido [5-(5-etoximetóxi-benzofuran-2-il)-6-nitro-piridin-2-il]-metil- carbâmico ou sal deste, como um precursor sintético, na fabricação de um composto final útil para a formação de imagem de depósitos de amilóide em mamíferos tais como pacientes vivos. Em uma forma de realização, o éster terc-butílico do ácido [6-(5-etoximetóxi-benzofuran-2-il)-2-nitro-piridin-3-il]- metil-carbâmico ou sal deste ou o éster terc-butílico do ácido [5-(5- etoximetóxi-benzofuran-2-il)-6-nitro-piridin-2-il]-metil-carbâmico ou sal deste estão na forma cristalina. Em uma outra forma de realização os ditos compostos têm um padrão de difração descrito acima.
[0032] Em uma outra forma de realização da presente invenção, é fornecido o uso do éster terc-butílico do ácido [6-(5-etoximetóxi-benzofuran- 2-il)-2-nitro-piridin-3-il]-metil-carbâmico ou sal deste ou do éster terc- butílico do ácido [5-(5-etoximetóxi-benzofuran-2-il)-6-nitro-piridin-2-il]- metil-carbâmico ou sal deste, como um precursor sintético, em um processo para a preparação de um composto rotulado. Em uma outra forma de realização o rótulo é um átomo 18F. Em uma forma de realização, o éster terc- butílico do ácido [6-(5-etoximetóxi-benzofuran-2-il)-2-nitro-piridin-3-il]- metil-carbâmico ou sal deste ou o éster terc-butílico do ácido [5-(5- etoximetóxi-benzofuran-2-il)-6-nitro-piridin-2-il]-metil-carbâmico ou sal deste estão na forma cristalina. Em uma outra forma de realização os ditos compostos têm um padrão de difração descrito acima.
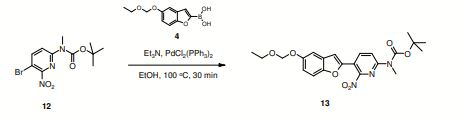
[0033] Os compostos éster terc-butílico do ácido [6-(5-etoximetóxi- benzofuran-2-il)-2-nitro-piridin-3-il]-metil-carbâmico ou sal deste e éster terc- butílico do ácido [5-(5-etoximetóxi-benzofuran-2-il)-6-nitro-piridin-2-il]- metil-carbâmico ou sal deste são úteis na preparação de compostos (radio)rotulados das seguintes fórmulas:
[0036] Em uma forma de realização, o éster terc-butílico do ácido [6- (5-etoximetóxi-benzofuran-2-il)-2-nitro-piridin-3-il]-metil-carbâmico ou sal deste ou do éster terc-butílico do ácido [5-(5-etoximetóxi-benzofuran-2-il)-6- nitro-piridin-2-il]-metil-carbâmico ou sal deste estão na forma cristalina. Em uma outra forma de realização os ditos compostos têm um padrão de difração descrito acima.
[0037] Em uma outra forma de realização da presente invenção, é fornecido o uso do éster terc-butílico do ácido [6-(5-etoximetóxi-benzofuran- 2-il)-2-nitro-piridin-3-il]-metil-carbâmico ou sal deste ou do éster terc- butílico do ácido [5-(5-etoximetóxi-benzofuran-2-il)-6-nitro-piridin-2-il]- metil-carbâmico ou sal deste, na preparação dos compostos 2-(6-[18F]-fluoro- 5-metilamino-piridin-2-il)-benzofuran-5-ol e 2-(2-[18F]-fluoro-6-metilamino- piridin-3-il)-benzofuran-5-ol.
[0038] Em uma forma de realização, o éster terc-butílico do ácido [6- (5-etoximetóxi-benzofuran-2-il)-2-nitro-piridin-3-il]-metil-carbâmico ou sal deste ou o éster terc-butílico do ácido [5-(5-etoximetóxi-benzofuran-2-il)-6- nitro-piridin-2-il]-metil-carbâmico ou sal deste estão na forma cristalina. Em uma outra forma de realização os ditos compostos têm um padrão de difração descrito acima.
[0039] Em uma outra forma de realização o sal do éster terc-butílico do ácido [6-(5-etoximetóxi-benzofuran-2-il)-2-nitro-piridin-3-il]-metil- carbâmico e do éster terc-butílico do ácido [5-(5-etoximetóxi-benzofuran-2- il)-6-nitro-piridin-2-il]-metil-carbâmico são sais farmaceuticamente aceitáveis.
[0040] Em uma forma de realização, a dita detecção é realizada por uma técnica selecionada de formação de imagem gama, tomografia de emissão de positron (PET), formação de imagem pela ressonância magnética e espectroscopia de ressonância magnética.
[0041] A Figura 1 representa o padrão de difração de raio X do éster terc-butílico do ácido [6-(5-etoximetóxi-benzofuran-2-il)-2-nitro-piridin-3-il]- metil-carbâmico. O eixo vertical representa intensidade (contagens) e o eixo horizontal representa a posição (°2teta para a radiação de Cu Kα).
[0042] A Figura 2 representa o padrão de difração de raio X do éster terc-butílico do ácido [6-(5-etoximetóxi-benzofuran-2-il)-2-nitro-piridin-3-il]- metil-carbâmico em uma escala diferente no eixo horizontal comparado com a Figura 1. O eixo vertical representa intensidade (contagens) e o eixo horizontal representa a posição (°2teta para a radiação Cu Kα).
[0043] A Figura 3 retrata o padrão de difração de raio X do éster terc- butílico do ácido [5-(5-etoximetóxi-benzofuran-2-il)-6-nitro-piridin-2-il]- metil-carbâmico. o eixo vertical representa a intensidade (contagens) e o eixo horizontal representa a posição (°2teta para a radiação Cu Kα).
[0044] A Figura 4 retrata o padrão de difração de raio X do éster terc- butílico do ácido [5-(5-etoximetóxi-benzofuran-2-il)-6-nitro-piridin-2-il]- metil-carbâmico em uma escala diferente no eixo horizontal comparado com a Figura 1. O eixo vertical representa a intensidade (contagens) e o eixo horizontal representa a posição (°2teta para a radiação Cu Kα).
[0045] A Figura 5 retrata os padrões de difração de raio X do éster terc-butílico do ácido [6-(5-etoximetóxi-benzofuran-2-il)-2-nitro-piridin-3-il]- metil-carbâmico (A); éster terc-butílico do ácido [5-(5-etoximetóxi- benzofuran-2-il)-6-nitro-piridin-2-il]-metil-carbâmico (B); Sulfato de sódio (C); e Cloreto de sódio (D). O eixo vertical representa intensidade (contagens) e o eixo horizontal representa posição (°2teta para a radiação Cu Kα).
[0046] Uma forma de realização diz respeito ao composto éster terc- butílico do ácido [6-(5-etoximetóxi-benzofuran-2-il)-2-nitro-piridin-3-il]- metil-carbâmico como descrito na figura 1.
[0047] Uma outra forma de realização diz respeito ao composto éster terc-butílico do ácido [5-(5-etoximetóxi-benzofuran-2-il)-6-nitro-piridin-2-il]- metil-carbâmico como descrito na figura 3.
[0048] Como aqui usado, “farmaceuticamente aceitável” é utilizado para se referir a aqueles compostos e/ou materiais, composições, e/ou formas de dosagem que são, dentro do escopo do julgamento médico criterioso, adequado para o uso em contato com os tecidos de mamíferos sem toxicidade, irritação, respostas alérgicas excessivas, ou outro problema ou complicação e comensurado com uma razão de benefício/risco razoável.
[0049] Como aqui usado, “uma base livre ou um sal farmaceuticamente aceitável” refere-se a ansolvates, incluindo anidratos e solvatos dessolvatados, e solvatos, incluindo hidratos.
[0050] Como aqui usado, “sais farmaceuticamente aceitáveis” refere- se a derivados dos compostos divulgados em que o composto precursor é modificado fabricando-se os sais de ácido ou de base ou cocristais destes. Os exemplos de sais farmaceuticamente aceitáveis incluem, mas não são limitados a, sais de ácido mineral ou orgânico de resíduos básicos tais como aminas; sais alcalinos ou orgânicos de resíduos ácidos tais como ácidos carboxílicos; e outros. Os sais farmaceuticamente aceitáveis incluem os sais não tóxicos convencionais ou os sais de amónio quaternários do composto precursor formado, por exemplo, a partir de ácidos inorgânicos ou orgânicos não tóxicos. Por exemplo, tais sais não tóxicos convencionais incluem aqueles derivados de ácidos inorgânicos tais como clorídrico, fosfórico, e outros; e os sais preparados a partir de ácidos orgânicos tais como láctico, maléico, cítrico, benzóico, metanossulfônico, e outros.
[0051] Os sais farmaceuticamente aceitáveis dos compostos da presente invenção podem ser sintetizados a partir do composto precursor que contém uma porção básica ou ácida pelos métodos químicos convencionais. No geral, tais sais podem ser preparados reagindo-se as formas de ácido ou base livres destes compostos com uma quantidade estequiométrica da base ou ácido apropriados em água ou em um solvente orgânico, ou em uma mistura dos dois; No geral, meios não aquosos como éter, acetato de etila, etanol, isopropanol, ou acetonitrila são usados.
[0052] Um composto ou agente “isotopicamente rotulado”, “radio- rotulado”, “rotulado”, “detectável” ou “ligação de amilóide detectável”, ou um “radioligante” é um composto onde um ou mais átomos são trocados ou substituídos por um átomo tendo uma massa atômica ou número de massa diferentes da massa atômica ou número de massa tipicamente encontrados na natureza (isto é, que ocorrem naturalmente). Uma exceção não limitante é 19F, que permite a detecção de uma molécula que contém este elemento sem enriquecimento a um grau mais alto do que é de ocorrência natural. Os compostos que carregam o substituinte 19F pode assim ser também aludido como “rotulado” ou semelhante. Os radionuclídeos adequados (isto é, “isótopos detectáveis”) que podem ser incorporados nos compostos da presente invenção incluem mas não são limitados a 2H (também escrito como D para deutério), 3H (também escrito como T para trítio), nC, 13C, 14C, 13N, 15N, 15O, 17O, 18O, 18F, 35S, 36C1,82Br, 75Br, 76Br, 77Br, 123I, 124I, 125I e 131I. Deve ser entendido que um composto isotopicamente rotulado precisa apenas ser enriquecido com um isótopo detectável até o, ou acima, do grau que possibilita a detecção com um técnica adequada para a aplicação particular, por exemplo, em um composto detectável rotulado com nC, o átomo de carbono do grupo rotulado do composto rotulado pode ser constituído pelo 12C ou outros isótopos do carbono em uma fração das moléculas. O radionuclídeo que é incorporado nos compostos radiorrotulados dependerá da aplicação específica deste composto radiorrotulado. Por exemplo, para a rotulação de placa ou receptor in vitroe em ensaio de competição, os compostos que incorporam 3H, 14C, ou 125I no geral serão mais úteis. Para aplicações na formação de imagem in vivonC, 13C, 18F, 19F, 120I, 123I, 131I, 75Br, ou 76Br no geral serão mais úteis.
[0053] Os exemplos de uma “quantidade eficaz” incluem quantidades que possibilitam a formação de imagem de depósito(s) de amilóide in vivo em níveis de biodisponibilidade para uso farmacêutico ou de formação de imagem, e/ou prevenir a degeneração e toxicidade celulares associadas com a formação de fibrila.
[0054] Os compostos da presente invenção podem ser usados como precursores para um radioligante ou como um radioligante, para determinar a presença, localização e/ou quantidade de um ou mais depósito(s) de amilóide em um órgão ou área corporal, incluindo o cérebro, de um animal ou ser humano. O(s) depósito(s) de amilóide incluem, sem limitação, depósito(s) de Aβ (amilóide beta). Permitindo-se que a sequência temporal da deposição de amilóide seja seguida, os compostos da invenção, como precursores para um radioligante ou como um radioligante, podem ser usados ainda para correlacionar a deposição de amilóide com o início de sintomas clínicos associados com uma doença, distúrbio ou condição. Os compostos da invenção por fim podem ser usados para tratar, e para diagnosticar uma doença, distúrbio ou condição caracterizados pela deposição de amilóide, tais como AD, AD familiar, síndrome de Down, amiloidose e homozigotos para o alelo E4 de apolipoproteína.
[0055] Os compostos da invenção, como precursores para um radioligante ou como um radioligante, podem assim ser usados em um método in vivo para medir depósitos de amilóide em um mamífero, que compreende as etapas de: (a) administrar uma quantidade detectável de uma composição farmacêutica como apresentada no parágrafo acima, e (b): detectar a ligação do composto ao depósito de amilóide no indivíduo.
[0056] O método determina a presença e localização de depósitos de amilóide em um órgão ou área corporal, preferivelmente no cérebro de um paciente. O presente método compreende a administração de uma quantidade detectável de uma composição farmacêutica que contém um composto de ligação de amilóide da presente invenção chamado de um “composto detectável,” ou um sal deste farmaceuticamente aceitável solúvel em água deste, a um paciente.
[0057] Uma “quantidade detectável” significa que a quantidade do composto detectável que é administrada é suficiente para possibilitar a detecção da ligação do composto ao amilóide. Uma “quantidade eficaz na formação de imagem” significa que a quantidade do composto detectável que é administrada é suficiente para permitir a formação de imagem da ligação do composto ao amilóide.
[0058] A invenção utiliza sondas de amilóide que, em conjunção com técnicas de formação de neuroimagem não invasivas tais como a espectroscopia de ressonância magnética (MRS) ou formação de imagem (MINI), ou formação de imagem gama tal como na tomografia de emissão de positron (PET) ou tomografia computadorizada de emissão de fóton único (SPECT), são usados para quantificar a deposição de amilóide in vivo. O termo “formação de imagem in vivo”, ou “formação de imagem”, refere-se a qualquer método que permite a detecção de um benzofurano substituído rotulado com heteroarila ou derivados de benzotiofeno como aqui descrito. Para a formação de imagem gama, a radiação emitida a partir do órgão ou área que é examinada é medida e expressada como ligação total ou como uma razão em que a ligação total em um tecido é normalizado (por exemplo, dividido por) para a ligação total em um outro tecido do mesmo indivíduo durante o mesmo procedimento de formação de imagem in vivo. A ligação total in vivo é definida como o sinal inteiro detectado em um tecido por uma técnica de formação de imagem in vivo sem a necessidade quanto a correção por uma segunda injeção de uma quantidade idêntica de composto rotulado junto com um excesso grande de composto não rotulado, mas de outro modo quimicamente idêntico. Um “indivíduo” é um mamífero, preferivelmente um ser humano, e mais preferivelmente um ser humano suspeito de ter demência.
[0059] Para os propósitos de formação de imagem in vivo, o tipo de instrumento de detecção disponível é um fator principal na seleção de um dado rótulo. Por exemplo, isótopos radioativos e 19F são particularmente adequados para a formação de imagem in vivo. O tipo de instrumento usado orientará a seleção do radionuclídeo ou isótopo estável. Por exemplo, o radionuclídeo escolhido deve ter um tipo de decaimento detectável por um dado tipo de instrumento.
[0060] Uma outra consideração diz respeito à meia-vida do radionuclídeo. A meia-vida deve ser longa o bastante de modo que seja ainda detectável no momento de captação máxima pelo alvo, mas curto o bastante de modo que o hospedeiro não carregue radiação nociva. Os compostos radiorrotulados da invenção podem ser detectados usando a formação de imagem gama em que a irradiação gama emitida do comprimento de onda apropriado seja detectada. Os métodos de formação de imagem gama incluem, mas não são limitados a, SPECT e PET. Preferivelmente, para a detecção SPECT, o radiorrótulo escolhido carece de uma emissão particulada, mas produzirá um número grande de fótons em uma faixa de 140 a 200 keV.
[0061] Para a detecção de PET, o radiorrótulo será um radionuclídeo que emite positron, tal como 18F ou nC, que exterminar-se-á para formar dois raios gama, que serão detectados pela câmara de PET.
[0062] Na presente invenção, precursores para compostos/sondas de ligação de amilóide são fabricados e estes compostos/sondas são úteis para a formação de imagem in vivo e quantificação da deposição de amilóide. Estes compostos devem ser usados em conjunção com técnicas de formação de neuroimagem não invasivas tais como a espectroscopia de ressonância magnética (MRS) ou formação de imagem (MRI), tomografia de emissão de positron (PET), e tomografia computadorizada de emissão de fóton único (SPECT). De acordo com esta invenção, os derivados de benzofurano substituídos por 2-heteroarila podem ser rotulados com 19F ou 13C para MRS/MRI pelas técnicas da química orgânica geral conhecidas na técnica. Os compostos também podem ser radiorrotulados com, por exemplo, 18F, nC, 75Br, 76Br, ou 120I para PET pelas técnicas bem conhecidas no ramo tais como descritas por Fowler, J. e Wolf, A. em “Positron Emisssion Tomography and Autoradiography” 391-450 (Raven Press, 1986). Os compostos também podem ser radiorrotulado com 123I e 131I para SPECT por qualquer uma de diversas técnicas conhecidas no ramo. Ver, por exemplo, Kulkarni, Int. J. Rad. Appl. & Inst. (Parte B) 18: 647 (1991). Os compostos também podem ser radiorrotulados com radiorrótulos de metal conhecidos, tais como Tecnécio-99m (99mTc). O composto radiorrotulado com metal pode ser usado para detectar depósitos de amilóide. A preparação de derivados radiorrotulados de Tc-99m é bem conhecida na técnica. Ver, por exemplo, Zhuang et al. Nuclear Medicine &Biology 26(2): 217-24, (1999); Oya et al. Nuclear Medicine &Biology 25(2): 135-40, (1998), e Horn et al. Nuclear Medicine &Biology 24(6): 485-98, (1997). Além disso, os compostos podem ser rotulados com 3H, 14C e 125I, pelos métodos bem conhecidos por uma pessoa habilitada na técnica, para a detecção de placa de amilóide in vitro e amostras e autópsia. Além disso, os compostos fluorescentes podem ser usados para a detecção das placas presentes in vitroe amostras de autópsia pela utilização de técnicas bem conhecidas com base na detecção da fluorescência.
[0063] Os elementos particularmente úteis na espectroscopia de ressonância magnética incluem 19F e 13C.
[0064] Os radioisótopos adequados para os propósitos desta invenção incluem emissores beta, emissores gama, emissores de positron e emissores de raio x. Estes radioisótopos incluem 120I, 123I, 131I, 125I, 18F, nC, 75Br, e 76Br. Os isótopos estáveis adequados para o uso na Formação de Imagem pela Ressonância Magnética (MRI) ou Espectroscopia (MRS), de acordo com esta invenção, incluem 19F e 13C. Os radioisótopos adequados para a quantificação in vitrode amilóide em homogenados de biópsia ou tecido de autópsia incluem 125I, 14C, e 3H. Os radiorrótulos preferidos são nC e 18F para o uso na formação de imagem in vivo de PET, 123I para o uso na formação de imagem de SPECT, 19F para MRS/MRI, e 3H e 14C para estudos in vitro.Entretanto, qualquer método convencional para visualizar sondas de diagnóstico podem ser utilizados de acordo com esta invenção.
[0065] Os compostos finais, radiorrotulados que derivam dos compostos da presente invenção podem ser administrados por qualquer um dos meios conhecidos por uma pessoa de habilidade comum na técnica. Por exemplo, a administração ao animal podem ser local ou sistêmica e realizada oral, parenteral, pela inalação pulverização, tópica, retal, inalado, nasal, bucal, vaginalmente, ou via um reservatório implantado. O termo “parenteral” como aqui usado inclui a injeção subcutânea, intravenosa, intraarterial, intramuscular, intraperitoneal, intratecal, intraventricular, intraesternal, intracraniana, e intraóssea e técnicas de infusão.
[0066] Os níveis de dose podem variar de cerca de 0,001 pg/kg/dia a cerca de 10.000 mg/kg/dia. Em uma forma de realização, o nível de dose é de cerca de 0,001 pg/kg/dia a cerca de 10 g/kg/dia. Em uma outra forma de realização, o nível de dose é de cerca de 0,01 pg/kg/dia a cerca de 1,0 g/kg/dia. Ainda em uma outra forma de realização, o nível de dose é de cerca de 0,1 mg/kg/dia a cerca de 100 mg/kg/dia.
[0067] O protocolo de administração exato e os níveis de dose variarão dependendo de vários fatores incluindo a idade, peso corporal, saúde geral, sexo e dieta do paciente; a determinação de procedimentos de administração específicos são rotina para qualquer pessoa de habilidade comum na técnica.
[0068] O regime pode incluir o pré-tratamento e/ou a co- administração com compostos adicionais tais como por exemplo agente(s) terapêuticos.
[0070] Uma forma de realização da invenção diz respeito a um processo para fabricar o ácido 5-etoximetóxi-benzofuran-2-borônico, em que o processo compreende: converter o composto 1 no composto 2 com um reagente de desproteção em um solvente; converter o composto 2 no composto 3 com uma base e um reagente de proteção em um solvente; e converter o composto 3 no ácido 5-etoximetóxi-benzofuran-2- borônico por um processo que compreende desprotonar o composto 3 com uma base e misturar o produto desprotonado com um borato de trialquila em um solvente, em que; o composto 1 corresponde a: o composto 2 corresponde a: o composto 3 corresponde a: O produto final das etapas de reação diferentes pode ser purificado ainda ou recristalizado se necessário.
[0071 ] Os solventes adequados para a etapa a) são por exemplo, mas não limitados a, solventes clorados tais como diclorometano, solvente aromático, tal como tolueno, amidas tais como dimetilformamida e N- metilpirrolidona e alcanos tais como hexano e heptano, ou misturas destes.
[0072] Os solventes adequados para a etapa b) são por exemplo, mas não limitado a, solventes clorados tais como diclorometano, solventes aromáticos tais como tolueno, amidas tais como dimetilformamida e N- metilpirrolidona, éteres tais como tetraidrofurano, 2-metiltetraidrofurano, éter terc-butilmetílico, éter ciclopentil metílico e éter dietílico, e alcanos tais como hexano e heptano, ou misturas destes.
[0073] Os solventes adequados para a etapa c) são por exemplo, mas não limitados a, solventes aromáticos tais como tolueno e xileno, éteres tais como tetraidrofurano, 2-metiltetraidrofurano, éter terc-butilmetílico, éter ciclopentil metílico e éter dietílico, e alcanos tais como hexano e heptano, ou misturas destes.
[0074] Em uma forma de realização o solvente usado na etapa a) é diclorometano, tolueno ou N-metilpirrolidona.
[0075] Em uma outra forma de realização o solvente usado na etapa b) é o éter ciclopentil metílico, tetraidrofurano ou 2-metil tetraidrofurano.
[0076] Em uma outra forma de realização o solvente usado na etapa c) é hexano, tetraidrofurano ou 2-metil tetraidrofurano.
[0077] A quantidade total de solventes usados nas etapas a-c pode variar na faixa de cerca de 2 a 100 (v/p) volumes em peso de material de partida, particularmente na faixa de 6 a 20 (v/p) volumes em peso de material de partida.
[0078] Os reagentes adequados para a etapa a) são por exemplo, mas não limitados a, ácidos de Lewis tais como BBr3 e BC13, alquiltiolatos tais como tiometilato de sódio e tiooctilato de sódio e cloridreto de piridina.
[0079] Os reagentes adequados para a etapa b) são por exemplo, mas não limitados a, haletos de etóxi metóxi tais como brometo de etóxi metóxi ou cloreto de etóxi metóxi e hidretos metálicos tais como hidreto de sódio ou hidreto de lítio.
[0080] Os reagentes adequados para a etapa c) são por exemplo, mas não limitados a, reagentes de alquillítio tais como metillítio, butillítio e hexillítio e trialquilboratos tais como borato de trimetila, borato de tripropila, borato de triisopropila e borato de tributila.
[0081] Em uma forma de realização os reagentes usados na etapa a) são BBr3 ou cloridreto de piridina
[0082] Em uma outra forma de realização os reagentes usados na etapa b) são cloreto de etóxi metóxi com hidreto de sódio ou hidreto de lítio.
[0083] Em uma outra forma de realização os reagentes usados na etapa c) são bultillítio e borato de triisopropila.
[0084] Em uma forma de realização o reagente na etapa a) é tribrometo de boro.
[0085] Em uma outra forma de realização o reagente na etapa a) é cloridreto de piridina.
[0086] Em uma outra forma de realização os reagentes na etapa b) são hidreto de sódio em mistura com éter clorometil etílico.
[0087] Em uma outra forma de realização os reagentes na etapa b) são Hidreto de lítio em mistura com éter clorometil etílico.
[0088] Em uma outra forma de realização os reagentes na etapa c) são n-butillítio em mistura com borato de triisopropila.
[0089] Uma outra forma de realização diz respeito ao processo descrito acima no esquema 1 em que o processo compreende: converter o composto 1 no composto 2 usando BBr, em diclorometano; converter o composto 2 no composto 3 usando NaH e CH3CH2OCH2CI em dimetilformamida; e converter o composto 3 no ácido 5-etoximetóxi-benzofuran-2- borônico por um processo que compreende desprotonar o composto 3 usando n-butillítio e misturando o produto desprotonado com borato de triisopropila em tetraidrofurano.
[0090] A temperatura para as etapas a-c pode estar na faixa de cerca de -78 a 250 °C, particularmente na faixa de cerca de -25 a 200 °C.
[0091] Esquema 2. Síntese de éster terc-butílico do ácido [6-(5- etoximetóxi-benzofuran-2-il)-2-nitro-piridin-3-il]-metil-carbâmico (8)
[0092] Uma forma de realização da invenção diz respeito a um processo para fabricar éster terc-butílico do ácido [6-(5-etoximetóxi- benzofuran-2-il)-2-nitro-piridin-3-il]-metil-carbâmico, em que o processo compreende: converter o composto 5 no composto 6 por um processo que compreende proteger o grupo amino no composto 5 usando um grupo de proteção na presença de uma base; converter o composto 6 no composto 7 por um processo que compreende alquilar o composto 6 usando um agente de alquilação na presença de uma base; e reagir o composto 7 e o composto 4 na presença de um catalisador de paládio e base em um solvente; em que; o composto 4 corresponde a: o composto 5 corresponde a: o composto 6 corresponde a: o composto 7 corresponde a: O produto final das etapas de reação diferentes pode ser ainda purificado ou recristalizado se necessário.
[0093] Os solventes adequados são por exemplo, mas não limitados a, na etapa d) THF ou éter dietílico; na etapa e) DMF ou THF; na etapa f) etanol ou DMF, ou misturas destes.
[0094] Em uma forma de realização o solvente na etapa d) é THF.
[0095] Em uma outra forma de realização o solvente na etapa e) é DMF.
[0096] Em uma outra forma de realização o solvente na etapa f) é etanol.
[0097] As bases adequadas são por exemplo, mas não limitadas a, na etapa d) NaHMDS, KHMDS, ou NaH, na etapa e) NaH, NaHMDS; na etapa f) Et3-N ou K2CO3.
[0098] Em uma outra forma de realização a base na etapa d) é NaHMDS.
[0099] Em uma forma de realização a base na etapa e) é NaH.
[00100] Em uma outra forma de realização a base na etapa f) é Et3-N.
[00101] Os catalisadores adequados para a etapa f) são por exemplo mas não limitados a, Pd(PPh3)2C12 ou Pd(dppf)C12
[00102] Uma outra forma de realização diz respeito ao processo descrito acima no esquema 2 em que o processo compreende: converter o composto 5 no composto 6 por um processo que compreende proteger o grupo amino no composto 5 usando bicarbonato de t- butila na presença de hexametildissilazida de sódio; converter o composto 6 no composto 7 por um processo que compreende alquilar o composto 6 usando CH3I na presença de NaH; e reagir o composto 7 e o composto 4 na presença de diclorobis(trifenilfosfina)paládio(II) e (CH/CfUhN em etanol. As temperaturas de reação para as etapas d-f estão entre -80 até a temperatura ambiente.
[00103] Esquema 3. Síntese do éster terc-butílico do ácido (5-Bromo- 6-nitro-piridin-2-il)-metil-carbâmico (12)
[00104] Uma forma de realização da invenção diz respeito a um processo para fabricar o éster terc-butílico do ácido (5-bromo-6-nitro-piridin- 2-il)-metil-carbâmico, em que o processo compreende: converter o composto 9 no composto 10 por um processo que compreende a bromação do composto 9 em um solvente usando um reagente de bromação; converter o composto 10 no composto 11 por um processo que compreende combinar o composto 10 e o composto 11 em um solvente na presença de uma base seguido pela adição de bicarbonato de t-butila; e converter o composto 11 no éster terc-butílico do ácido (5- bromo-6-nitro-piridin-2-il)-metil-carbâmico por um processo que compreende alquilar o composto 11 em um solvente usando um agente de alquilação na presença de uma base; em que; o composto 9 corresponde a: o composto 10 corresponde a: o composto 11 corresponde a: O produto final das etapas de reação diferentes pode ser ainda purificado ou recristalizado se necessário.
[00105] Os solventes adequados para as etapas g-i são por exemplo, mas não limitados a, nitrilas tais como acetonitrila e propionitrila, solventes clorados tais como diclorometano, solventes aromáticos tais como tolueno e xileno, éteres tais como tetraidrofurano, 2-metil-tetraidrofurano, éter terc- butilmetílico, éter ciclopentil metílico e éter dietílico, amidas tais como dimetilformamida e N-metilpirrolidona e alcanos tais como hexano e heptano, ou misturas destes.
[00106] Em uma forma de realização o solvente usado na etapa g) é água, acetonitrila (MeCN), tolueno, tetraidrofurano, ou misturas destes.
[00107] Em uma outra forma de realização o solvente usado na etapa h) é tetraidrofurano, heptano, 2-metil tetraidrofurano, ou misturas destes.
[00108] Em uma outra forma de realização o solvente usado na etapa i) é água, hexano, acetonitrila, dimetil formamida, tetraidrofurano, 2-metil tetraidrofurano, ou misturas destes.
[00109] Em uma forma de realização o solvente na etapa g) é MeCN misturado com água.
[00110] Em uma outra forma de realização o solvente na etapa h) é THF misturado com heptano.
[00111] Em uma outra forma de realização o solvente na etapa h) é THF misturado com hexano.
[00112] Em uma outra forma de realização o solvente na etapa i) é DMF misturado com água.
[00113] Em uma outra forma de realização o solvente na etapa i) é THF misturado com heptano.
[00114] Em uma outra forma de realização o solvente na etapa i) é MeCN misturado com água.
[00115] A quantidade total de solventes usados nas etapas g) a i) pode variar na faixa de cerca de 2 a 100 (v/p) volumes em peso de material de partida, particularmente na faixa de 6 a 20 (v/p) volumes em peso de material de partida.
[00116] Os reagentes adequados para a etapa g) são por exemplo, mas não limitados a reagentes de bromação tais como N-bromossuccinimida.
[00117] Os reagentes adequados para a etapa h) são por exemplo, mas não limitados a, bicarbonato de di-terc-butila e base tal como bis(trimetilsilil)amida de sódio, hidreto de sódio ou hidreto de lítio.
[00118] Em uma forma de realização os reagentes usados na etapa h) são bicarbonato de di-terc-butila com hidreto de sódio, hidreto de lítio ou bis(trimetilsilil)amida de sódio.
[00119] Os reagentes adequados para a etapa i) são por exemplo, mas não limitados a, reagentes de alquilação tais como iodeto de metila e sulfato de dimetila, e base tai como hidreto de sódio, hidreto de litio, bis(trimetilsilil)amida de sódio e l,8-Diazabiciclo[5,4,0]undec-7-eno.
[00120] Em uma outra forma de realização o reagente na etapa g) é N- bromossuccinimida.
[00121] Em uma forma de realização a base na etapa h) é NaHMDS e BocoO.
[00122] Em uma outra forma de realização a base na etapa i) é DBU.
[00123] Em uma outra forma de realização a base na etapa i) é NaH.
[00124] Uma outra forma de realização diz respeito ao processo descrito acima no esquema 3 em que o processo compreende: converter o composto 9 no composto 10 por um processo que compreende a bromação do composto 9 em CH3CN usando n- bromossuccinimida; converter o composto 10 no composto 11 por um processo que compreende combinar o composto 10 e o composto 11 em um solvente na presença de hexametildissilazida de sódio seguido pela adição de bicarbonato de t-butila; e converter 0 composto 11 no éster terc-butílico do ácido (5- bromo-6-nitro-piridin-2-il)-metil-carbâmico por um processo que compreende alquilar o composto 11 em dimetilformamida usando CH3I na presença de NaH.
[00125] A temperatura para as etapas g-i pode estar na faixa de cerca de -78 a 150 °C, particularmente na faixa de cerca de 0o a 50 °C.
[00126] O produto na etapa i), o éster terc-butílico do ácido (5-Bromo- 6-nitro-piridin-2-il)-metil-carbâmico (12) pode ser purificado pela precipitação a partir de uma mistura de DMF/ água ou a partir de uma mistura de MeCN/ água.
[00127] Em uma forma de realização o éster terc-butílico do ácido (5- Bromo-6-nitro-piridin-2-il)-metil-carbâmico (12) é purificado a partir de uma mistura de MeCN/água.
[00128] Esquema 4. Vias alternativas para o éster terc-butílico do ácido (5-Bromo-6-nitro-piridin-2-il)-metil-carbâmico (12):
[00129] O éster terc-butílico do ácido (5-Bromo-6-nitro-piridin-2-il)- metil-carbâmico (12) pode ser preparado por duas vias alternativas. Por exemplo o composto 12 pode ser preparado a partir de 6-nitro-piridin-2- ilamina (9), por intermédio da N-metil-6-nitropiridin-2-amina (14) ou (6- nitropiridin-2-il)carbamato de terc-butil metila (16), onde a bromação é introduzida no final em ambas as sequências.
[00130] Esquema 4. Síntese do éster terc-butílico do ácido [5-(5- etoximetóxi-benzofuran-2-il)-6-nitro-piridin-2-il]-metil-carbâmico (13)
[00131] Uma forma de realização da invenção diz respeito a um processo para a preparação do composto 13 misturando-se o composto 12 e o composto 4 em um solvente adequado usando uma base adequada na presença de um catalisador adequado seguido pela extração.
[00132] O produto final pode ser ainda purificado ou recristalizado se necessário.
[00133] Os solventes adequados são por exemplo, mas não limitados a, álcoois tais como metanol, etanol, propanol, isopropanol e butanol, éteres tais como dioxano, tetraidrofurano e 2-metiltetraidrofurano e solventes aromáticos tais como benzeno, tolueno e xileno, ou misturas destes.
[00134] Em uma forma de realização o solvente na etapa j) é etanol.
[00135] A quantidade total de solventes usados na etapa j) pode variar na faixa de cerca de 2 a 100 (v/p) volumes em peso de material de partida, particularmente na faixa de 6 a 20 (v/p) volumes em peso de material de partida.
[00136] Os reagentes adequados são por exemplo, mas não limitados a, aminas, tais como trietilamina, carbonatos tais como carbonato de césio, carbonato de potássio e carbonato de sódio, fosfatos tais como fosfato de potássio e fosfato de sódio ou fluoreto de potássio junto com catalisadores de paládio. Também, uma pletora de ligantes de fosfina adequados e ligantes de imidazol-2-ilideno podem ser considerados.
[00137] Em uma outra forma de realização os reagentes na etapa j) são trietilamina e PdCEtPPhsA
[00138] A temperatura para a etapa j) podem estar na faixa de cerca de -0 °C a 150 °C, particularmente na faixa de cerca de 25 °C a 100 °C.
[00139] Esquema 5. A síntese alternativa de éster terc-butílico do ácido [5-(5-etoximetóxi-benzofuran-2-il)-6-nitro-piridin-2-il]-metil-carbâmico (13) via arilação direta.
[00140] O éster terc-butílico do ácido [5-(5-etoximetóxi-benzofuran-2- il)-6-nitro-piridin-2-il]-metil-carbâmico (13) pode ser fabricado por intermédio de uma arilação direta de 5-etoximetóxi-benzofurano (3) com éster terc-butílico do ácido (5-Bromo-6-nitro-piridin-2-il)-metil-carbâmico (12) na presença de um catalisador adequado.
[00141] Os solventes adequados são por exemplo, mas não limitados a, amidas tais como dimetilacetamida, solventes aromáticos tais como tolueno, e xileno.
[00142] A quantidade total de solventes usados nas etapas de g a i pode variar na faixa de cerca de 2 a 100 (v/p) volumes em peso de material de partida, particularmente na faixa de 6 a 20 (v/p) volumes em peso de material de partida.
[00143] Os reagentes adequados são por exemplo, mas não limitados a, sistemas de catalisador de paládio tais como Pd(PPh3)4 com acetato de potássio ou acetato de paládio com triciclohexilfosfina, álcool pivaloílico e carbonato de potássio.
[00144] Abaixo seguem vários exemplos não limitantes de compostos precursores da invenção.
[00145] Todos os solventes usados foram comercialmente disponíveis e foram usados sem outra purificação. As reações foram tipicamente conduzidas usando solventes anidros sob uma atmosfera inerte de nitrogênio.
[00146] Os espectros de e 13C RMN foram registrados a 400 MHz para próton e 100 MHz para carbono-13 em um Espectrômetro de RMN Varian Mercury Plus 400 equipado com uma sonda Varian 400 ATB PFG. Todos os solventes deuterados contiveram tipicamente 0,03 % a 0,05 % v/v de tetrametilsilano, que foi usada como o sinal de referência (ajustado em δ 0,00 tanto para ’H quanto para 13C).
[00147] Os espectros de massa foram registrados em um Waters MS consistindo de um Alliance 2795 (LC) e detetor Waters Micromass ZQ a 120 °C. O espectrômetro de massa foi equipado com uma fonte de íon de eletropulverização (ES) operado em um modo de íon positivo ou negativo. O espectrômetro de massa foi escaneado entre m/z 100 a 1000 com um tempo de varredura de 0,3 s.
[00148] As análises pela HPLC foram realizadas em um sistema Waters 600 Controller com um Autoamostrador Waters 717 Plus e um Detetor de Arranjo de Fotodiodo Waters 2996. A coluna usada foi uma ACE Cis, 5 pm, 4 60X150 mm. Em uma condução de 20 min, um gradiente linear foi aplicado partindo de 95 % A (A: 0,1 % de H3PO4 em água) e terminando a 90 % de C (C: MeCN) em 6 min, mantendo em 90 % de C por 4 min e depois terminando de volta a 95 % de A. A coluna estava na temperatura ambiente com a taxa de fluxo de 1,0 ml/min. O Detetor de Arranjo de Diodo foi escaneado de 200 a 400 nm.
[00149] O aquecimento de microonda foi realizado em um CEM Discover LabMate ou em um Biotage Initiator System na temperatura indicada nos tubos de microonda recomendados.
[00150] A cromatografia de camada fina (TLC) foi realizada em Alugram® (Gel de Sílica 60 F254) da Mancherey-Nagel e a UV foi tipicamente usada para visualizar as manchas. Os métodos de visualização adicionais foram também utilizados em alguns casos. Nestes casos a placa de TLC foi desenvolvida com iodo (gerado pela adição de aproximadamente 1 g de I2 para 10 g de gel de sílica e misturando completamente), vanilina (gerada dissolvendo-se cerca de 1 g de vanilina em 100 ml de H2SO4 a 10 %), ninhidrina (comercialmente disponível da Aldrich), ou Magic Stain (gerado misturando-se completamente 25 g de (NH4)6Mθ7θ24.4H2θ, 5 g de (NH4)2Ce(IV)(NOa)6, 450 ml de H2O e 50 ml de H2SO4 concentrado) para visualizar o composto. A cromatografia cintilante foi pré-formada usando gel de sílica de 40 a 63 pm (230 a 400 malhas) da Silicide seguindo técnicas análogas àquelas divulgadas em Still, W. C.; Kahn, M.; e Mitra, M. Journal of Organic Chemistry, 1978, 43, 2923 a 2925. Os solventes típicos usados para a cromatografia cintilante ou cromatografia de camada fina foram misturas de diclorometano/metanol, acetato de etila/metanol e hexanos/ acetato de etila.
[00151] A cromatografia preparativa foi realizada em um Sistema Waters Prep LC 4000 usando um Arranjo de Diodo Waters 2487 ou em um Waters LC Module 1 plus. A coluna usada foi uma Waters XTerra Prep Cis, 5 |um, 30 X 100 mm (taxa de fluxo de 40 ml/min) ou um Fenomenex Luna Cis, 5 pm, 21,6 X 250 mm (taxa de fluxo 20 ml/min). Gradientes estreitos com acetonitrila/ água, com a água contendo 0,1 % de ácido trifluoroacético ou 10 mM de acetato de amónio, foram usados para eluir o composto em um tempo de condução total entre 20 e 30 min.
[00152] Os padrões de Difração de Raio X no Pó (XRPD) foram coletados em um sistema PANalytical X’Pert PRO MPD teta-teta usando radiação de Cu Kα de foco fino longo (40 kV, 50 mA) e um detetor X’Celerator. Uma fenda de divergência programável e uma fenda anti- dispersão programável dando um comprimento irradiado de 20 mm foram usados. Fendas de Soller de 0,02 rad foram usadas no caminho de feixe incidente e no difratado. Uma máscara fixa de 20 mm foi usada no caminho de feixe incidente e um filtro de níquel foi colocado em frente do detetor. Amostras planas finas foram preparadas em placas de fundo zero de silício plano usando uma espátula. As placas foram montadas em suportes de amostras e giradas em uma posição horizontal durante a medição. Os padrões de difração foram coletados entre 2°2teta e 80°2teta em um modo de varredura contínua. O tempo total para uma varredura foi de 25 minutos 30 segundos. A pessoa habilitada na difração de raio X no pó constatará que a intensidade relativa dos picos pode ser afetada, por exemplo, pelos grãos aproximadamente acima de 30 micrômetros no tamanho e razões de aspecto não unitárias, que podem afetar a análise da amostra. Além disso, deve ser entendido que as intensidades podem flutuar dependendo das condições experimentais e preparação da amostra tais como orientação preferida das partículas na amostra. O uso das fendas de divergência automáticas ou fixas também influenciará nos cálculos da intensidade relativa. Uma pessoa habilitada na técnica pode manejar tais efeitos quando da comparação dos padrões de difração.
[00153] A pessoa habilitada também constatará que a posição das reflexões pode ser afetada pela altura exata na qual a amostra se situa no difratômetro, temperatura e a calibração do zero do difratômetro. A planaridade da superfície da amostra também pode ter um efeito pequeno. O valor exato para a posição de uma reflexão pode variar levemente entre as amostras, por exemplo, devido às diferenças na cristalinidade do material. O uso do programas de descobrimento de picos automáticos ou manuais, subjetivos, a determinação de pico também pode afetar levemente a posição relatada de uma reflexão. É óbvio para a pessoa habilitada que diferenças no desempenho do instrumento pode influencia a resolução de pico. Consequentemente os dados de padrão de difração apresentados não devem ser interpretados como valores absolutos.
[00154] No geral, um erro de medição de um ângulo de difração em um difratograma de raio X no pó é de cerca de 5 % ou menos, em particular dentro da faixa de mais 0,5° 2-teta a menos 0,5° 2-teta quando do uso da radiação Cu Ka, e tal grau de um erro de medição deve ser levado em conta quando da consideração dos padrões de difração de raio X nas figuras 1 a 5 e quando da leitura das Tabelas 1 e 2.
[00155] A pessoa habilitada também constatará que traços de quaisquer impurezas cristalinas da preparação do material de amostra, por exemplo, resíduos salinos tais como sulfato de sódio ou cloreto de sódio das etapas de secagem, precipitação por saturação de sal e/ou ajuste de pH, podem fazer com que a difração e aqueles picos que têm ângulos de difração próximos aos picos esperados de tais impurezas cristalinas emanem total ou parcialmente de tais impurezas cristalinas.
[00156] Os padrões de difração de muitos compostos podem ser simulados, por exemplo, a partir das bases de dados tais como as bases de dados da Powder Diffraction File (PDF) do International Centre for Diffraction Data (ICDD). A pessoa habilitada pode comparar tais padrões de difração simulados com os padrões experimentais.
[00157] A calorimetria de varredura diferencial (DSC) de 30 °C a 300 °C foi realizada sob nitrogênio em copos de amostra de alumínio com tampas perfuradas usando um instrumento Perkin Elmer Diamond DSC. A taxa de varredura foi de 10 °C por minuto. O tamanho da amostra foi menor do que 1 mg. É bem conhecido que as temperaturas de início e pico da DSC assim como valores de energia podem variar devido, por exemplo, à pureza da amostra e tamanho da amostra e devido aos parâmetros instrumentais, especialmente a taxa de varredura da temperatura. Consequentemente os dados de DSC apresentados não devem ser interpretados como valores absolutos.
[00158] Uma pessoa habilitada na técnica pode ajustar os parâmetros instrumentais para um calorímetro de varredura diferencial de modo que os dados comparáveis com os dados aqui apresentados possam ser coletados de acordo com métodos padrão, por exemplo aqueles descritos em Hõhne, G. W. H. et al (1996), Differential Scanning Calorimetry, Springer, Berlim.
[00159] A análise termogravimétrica (TGA) da temperatura ambiente até 250 °C foi realizada sob nitrogênio em um copo de amostra de platina usando um analisador termogravimétrico Perkin Elmer Piris 1 TGA. A taxa de varredura foi de 10 °C por minuto. O tamanho da amostra foi menor do que 1 mg. É bem conhecido que o traço de TGA possa variar devido a, por exemplo, o tamanho da amostra e devido aos parâmetros instrumentais, especialmente a taxa de varredura da temperatura. Consequentemente os dados de TGA apresentados não devem ser interpretados como valores absolutos. As seguintes abreviações foram usadas: Ac acetila; aq. aquoso; BOC2O bicarbonato de di-terc-butila; DCM diclorometano; DIPEA N,N-Diisopropiletilamina; DMF N,N-dimetilformamida; DMSO sulfóxido de dimetila; DSC Calorimetria de Varredura Diferencial EtOH etanol; MeOH metanol; HMDS bis(trimetilsilil)amida; NBS N-bromossuccinimida; r.t. temperatura ambiente; THF tetraidrofurano; TFA ácido trifluoroacético; TGA Análise Termogravimétrica XRPD Difração de Raio X no Pó DBU l,8-Diazabiciclo[5,4,0]undec-7-eno Et?,N Trietilamina Os materiais de partida usados foram disponíveis de fontes comerciais ou preparados de acordo com procedimentos da literatura e tiveram dados experimentais de acordo com aqueles relatados.
[00161] A uma solução agitada de 5-metoxibenzofurano (1) (0,50 g, 3,38 mmol) em diclorometano (15 ml), tribrometo de boro (16,87 ml, 16,87 mmol, solução 1 M em diclorometano) foi adicionada lentamente a 0 °C. A mistura de reação foi aquecida até a temperatura ambiente e agitada por 4 horas. A mistura de reação foi depois esfriada até 0 °C, extinta com solução saturada aquosa de NaHCCh e extraída com diclorometano (3 x 50 ml). Os extratos orgânicos combinados foram lavados com salmoura (25 ml), secados em NajSOzt, e concentrados sob pressão reduzida para dar o composto (2) como um sólido branco amarelado (300 mg) que foi usado na etapa seguinte sem outra purificação.
[00162] 1H RMN (400 MHz, CLOROFÓRMIO-d) δ: 7,59 (d, J = 1,95 Hz, 1 H), 7,35 (d, J = 8,59 Hz, 1 H), 7,00 (d, J = 2,73 Hz, 1 H), 6,80 (dd, 8,59, 2,74 Hz, 1 H), 6,67 (m, 1 H), 4,66 (s, 1 H)
[00163] A uma solução agitada de benzofuran-5-ol (2) (257 mg, 1,92 mmol) em DMF (3 ml), NaH (81 mg, 1,92 mmol, dispersão a 57 % em óleo) foi adicionado a 0 °C. A mistura de reação foi aquecida até a temperatura ambiente e agitada 1 hora. O éter clorometil etílico (214 pl, 2,30 mmol) foi depois adicionado às gotas até 0 °C e a mistura foi agitada na temperatura ambiente por um adicional de 1 hora. A água (10 ml) foi adicionada e a mistura de reação foi extraída com acetato de etila (2 x 50 ml). Os extratos orgânicos foram lavados com água, salmoura, secados em Na2SÜ4, e concentrados a vácuo. A purificação do produto bruto pela cromatografia de coluna cintilante usando acetato de etila a 10 % em hexano produziu o composto (3) (273 mg) como um óleo incolor.
[00164] 1H RMN (400 MHz, CLOROFÓRMIO-d) δ: 7,59 (d, J = 1,95 Hz, 1 H), 7,39 (d, J = 8,16 Hz, 1 H), 7,27 (d, J = 2,73 Hz, 1 H), 6,99 (dd, J = 8,98, 2,34 Hz, 1H), 6,70 (m, 1 H), 5,24 (s, 2 H), 3,77 (q, J = 7,03 Hz, 2 H), 1,25 (t, J = 7,03 Hz, 3 H).
[00165] A uma solução agitada de 5-etoximetóxi-benzofurano (3) (265 mg, 1,38 mmol) em THF (5 ml) a -78 °C, n-butillitio (solução em hexano 2,5 M, 0,56 ml, 1,44 mmol) foi adicionado às gotas. Depois a mistura de reação foi agitada por 1 hora, borato de triisopropila (0,635 ml, 2,76 mmol) foi adicionado lentamente e a agitação foi continuada por um adicional de 20 minutes a -78 °C. A mistura de reação foi extinta com a solução saturada de cloreto de amónio (10 ml) e foi deixada aquecer até a temperatura ambiente. A água (10 ml) foi adicionada e a mistura resultante foi extraída em éter dietílico (2 x 50 ml). Os extratos combinados foram lavados com salmoura, secados em MgSCE, e concentrados sob pressão reduzida. A purificação do produto bruto pela recristalização a partir de acetato de etila e hexano produziu o composto desejado (4) (170 mg) como um sólido branco.
[00166] 1H RMN (DMSO-d6 ,400 MHz) δ: 8,54 (s, 2 H), 7,48 (d, J = 8,6 Hz, 1 H), 7,39 (s, 1 H), 7,30 (d, J = 2,7 Hz, 1 H), 7,02 (dd, J = 8,8, 2,5 Hz, 1 H), 5,23 (s, 2 H), 3,68 (q, J = 7,0 Hz, 2 H), 1,14 (t, J = 7,0 Hz, 3 H)
[00167] Exemplo precursor final 1: Síntese do éster terc-butílico do ácido [6-(5-etoximetóxi-benzofuran-2-il)-2-nitro-piridin-3-il]-metil- carbâmico (8)
[00169] A uma suspensão agitada de 2-nitro-piridin-3-ilamina (5,06 g, 36,40 mmol) e acetato de sódio (2,99 g, 36,46 mmol) em ácido acético (40 ml), uma solução de bromo (2,5 ml, 48,79 mmol) em ácido acético (8 ml) foi adicionada às gotas e a mistura de reação foi agitada durante a noite. O ácido acético foi removido sob pressão reduzida. O resíduo foi esfriado até 0 °C, neutralizado com solução saturada de bicarbonato de sódio para ajustar até o pH ~ 7, e extraída com acetato de etila (4 x 50 ml). Os extratos orgânicos combinados foram lavados com salmoura, secados em Na2SÜ4 anidro, e concentrados sob pressão reduzida. O resíduo foi triturado com acetato de etila para produzir o composto (5) (5,1 g) como um sólido amarelo.
[00170] 1H RMN (DMSO-dô, 400 MHz) δ: 7,66 (d, J = 8,6 Hz, 1 H), 7,58 (s, 2 H), 7,49 (d, J = 8,6 Hz, 1 H) ESMS: m/z 216,33 [M - 1]’ d) Éster terc-butílico do ácido de (6-Bromo-2-nitro-piridin-3-il)-carbâmico (6)
[00171] A uma solução agitada de 6-bromo-2-nitro-piridin-3-ilamina (5) (854 mg, 3,92 mmol) em THF (50 ml), NaHMDS (5,09 ml, 5,09 mmol, 1 M em THF) foi adicionado a 0 °C. Depois agitado por 15 minutos, uma solução de bicarbonato de di-terc-butila (853 mg, 3,91 mmol) em THF (5 ml) foi adicionada em um período de 30 minutos. A mistura de reação foi agitada por 3,5 horas na temperatura ambiente e depois NaHCCb saturado aquoso foi adicionado. A mistura de reação foi extraída com acetato de etila (3 x 50 ml). Os extratos combinados foram lavados com água, salmoura, secados em Na2SÜ4, e concentrados sob pressão reduzida. O produto bruto foi purificado pela cromatografia de coluna cintilante usando acetato de etila a 10 % em hexano para produzir o composto (6) (293 mg) como um sólido branco amarelado.
[00172] 1H RMN (400 MHz, CLOROFÓRMIO-d) δ: 9,41 (br. s., 1 H), 9,00 (d, J = 8,6 Hz, 1 H), 7,73 (d, J = 9,0 Hz, 1 H), 1,55 ppm (s, 9 H) ESMS: m/z 318,36 [M + 1]+ e) Éster terc-butílico do ácido (6-Bromo-2-nitro-piridin-3-il)-metil-carbâmico (7)
[00173] A uma solução agitada de éster terc-butílico do ácido (6- bromo-2-nitro-piridin-3-il)-carbâmico (6) (290 mg, 0,91 mmol) em DMF (10 ml), NaH (57 mg, 1,36 mmol, dispersão a 57 % em óleo) foi adicionado a 0 °C. Depois de agitar por 15 minutos, iodeto de metila (79 pl, 1,27 mmol) foi adicionado e a mistura de reação foi agitada por 1 hora. A mistura de reação foi depois extinta com a solução saturada de cloreto de amónio (15 ml) e extraída com acetato de etila (2 x 40 ml). Os extratos orgânicos combinados foram lavados com água, salmoura, secados em MgSOzt, e concentrada a vácuo. O resíduo foi purificado pela cromatografia de coluna cintilante usando acetato de etila a 20 % em hexano para dar o composto (7) (268 mg) como um sólido amarelo claro.
[00174] 1H RMN (400 MHz, CLOROFÓRMIO-d) δ: 7,78 (d, J = 8,2 Hz, 1 H), 7,66 (d, J = 8,2 Hz, 1 H), 3,29 (s, 3 H), 1,39 (br. s., 9 H) ESMS: m/z 276,36 [M - 56]’ f) Éster terc-butílico do ácido [6-(5-etoximetóxi-benzofuran-2-il)-2-nitro- piridin-3-il]-metil-carbâmico (8)
[00175] A uma solução desgaseificada de ácido 5-etoximetóxi- benzofurano benzóico (4) (140 mg, 0,593 mmol) em etanol (10 ml), éster terc-butílico do ácido (6-bromo-2-nitro-piridin-3-il)-metil-carbâmico (7) (151 mg, 0,455 mmol), Pd(PPh3)2Cl2 (42 mg, 0,059 mmol) e Et3N (127 pl, 0,909 mmol) foram adicionados. A mistura de reação foi agitada a 100 °C por 30 minutos em um reator de microonda. Os voláteis foram removidos sob pressão reduzida. O resíduo foi diluído com água (15 ml) e a mistura foi extraída com acetato de etila (3 x 50 ml). Os extratos orgânicos combinados foram lavados com água, salmoura, secados em Na2SÜ4, e concentrados sob pressão reduzida. O produto bruto foi purificado pela cromatografia de coluna cintilante usando acetato de etila a 20 % em hexano. A evaporação do solvente deu o composto do título 8 (170 mg) como um sólido amarelo claro.
[00176] RMN (400 MHz, CLOROFÓRMIO-d) δ : 8,10 (d, J = 8,20 Hz, 1 H), 7,84 (d, J = 8,20 Hz, 1 H), 7,50 (s, 1 H), 7,45 (d, J = 8,98 Hz, 1 H), 7,32 (d, J = 1,95 Hz, 1 H), 7,02 - 7,16 (m, 1 H), 5,27 (s, 2 H), 3,78 (q, J = 6,63 Hz, 2 H), 3,32 (s, 3 H), 1,36 (br. s., 9 H), 1,26 (t, J = 7,22 Hz, 3 H) ESMS: m/z 444,51 [M + 1]+ DSC: evento endotérmico com início a 109,5 °C e o pico a 110,8 °C. ΔH 89,6 Jg1 TGA: nenhum evento percebido entre a temperatura ambiente e160 °C Tabela 1 Picos de Difração de Raio X no Pó Representativos para o éster terc-butílico do ácido [6-(5-etoximetóxi-benzofuran-2-il)-2-nitro-piridin-3-il]-metil- carbâmico vs = muito forte s = forte w = fraco
[00177] Exemplo intermediário 2: éster terc-butílico do ácido (5- Bromo-6-nitro-piridin-2-il)-metil-carbâmico (12) g) 5-Bromo-6-nitro-piridin-2-ilamina (10)
[00178] A uma solução agitada de 6-nitro-piridin-2-ilamina (1,0 g, 7,18 mmol) em CH3CN (100 ml), protegida da luz e sob atmosfera de nitrogênio, N-bromossuccinamida (636 mg, 3,59 mmol) foi adicionada a 0 °C. Depois de 1 hora, uma outra porção de N-bromossuccinamida (636 mg, 3,59 mmol) foi adicionada. A mistura de reação foi deixada aquecer até a temperatura ambiente e a agitação continuou durante a noite. A mistura de reação foi depois extinta pela adição de ^2826)3 saturado aquoso e extraída com acetato de etila (3 x 30 ml). Os extratos orgânicos combinados foram lavados com água, salmoura, secados em MgSÜ4 (anidro) e concentrados a vácuo. O produto bruto foi purificado pela Biotage usando acetato de etila a 10 % em hexano para produzir 1,2 g de 5-bromo-6-nitro-piridin-2-ilamina (10).
[00179] 1H RMN (400 MHz, DMSO-d6) δ ppm: 7,84 (d, J = 8,98 Hz, 1 H), 7,03 (s, 2 H), 6,66 (d, J = 8,98 Hz, 1 H) h) Éster terc-butílico do ácido (5-Bromo-6-nitro-piridin-2-il)-carbâmico (11)
[00180] A uma solução de 5-bromo-6-nitro-piridin-2-ilamina (900 mg, 4,12 mmol) em THF seco (40 ml), NaHMDS (1 M em THF, 5,8 ml) foi adicionado 0 °C. Depois agitado por 15 minutos, uma solução de BOC2O (901 mg, 4,12 mmol) em THF (5 ml) foi adicionada lentamente a 0 °C em 30 minutos. A mistura resultante foi aquecida até a temperatura ambiente, agitada por 3 horas, extinta com NaHCCb saturado aquoso e extraída com acetato de etila (3 x 30 ml). Os extratos combinados foram lavados com água e salmoura, secados em Na2SÜ4 e concentrados sob pressão reduzida. O resíduo foi purificado pela Biotage usando 5 a 10 % de acetato de etila em hexano para dar 786 mg do éster terc-butílico do ácido (5-bromo-6-nitro- piridin-2-il)-carbâmico (11).
[00181] 1H RMN (400 MHz, CLOROFÓRMIO-d) δ ppm: 8,14 (d, J = 8,98 Hz, 1 H), 8,03 (d, J = 8,59 Hz, 1 H), 7,52 (s, 1 H), 1,53 (s, 9 H) i) éster terc-butílico do ácido (5-Bromo-6-nitro-piridin-2-il)-metil-carbâmico (12)
[00182] A uma solução de éster terc-butílico do ácido (5-bromo-6- nitro-piridin-2-il)-carbâmico (11) (800 mg, 2,52 mmol) em DMF seco (15 ml), NaH (60 % dispersão óleo mineral, 191 mg, 4,53 mmol) foi adicionado a 0 °C. A mistura resultante foi agitada por 30 minutos a 0 °C e iodeto de metila (0,23 ml, 3,68 mmol) foi depois adicionado. Depois de agitar a mistura de reação por 30 minutos a 10 °C, NH4CI saturado aquoso (15 ml) foi adicionado. A mistura de reação foi extraída com acetato de etila (3 x 30 ml). Os extratos combinados foram lavados com água, salmoura, secados em MgSÜ4 (anidro) e concentrados sob pressão reduzida. O produto bruto foi purificado pela Biotage usando acetato de etila a 10 % em hexano para produzir éster terc-butílico do ácido (5-Bromo-6-nitro-piridin-2-il)-metil- carbâmico 12 (789 mg).
[00183] 1H RMN (400 MHz, CLOROFÓRMIO-d) δ ppm: 8,12 (d, J = 8,60 Hz, 1 H), 7,95 (d, J = 8,99 Hz, 1 H), 3,40 (s, 3 H), 1,55 (s, 9 H) ou procedimento alternativo para éster terc-butílico do ácido (5-Bromo-6-nitro-piridin-2-il)-metil-carbâmico (12): g) 5-Bromo-6-nitro-piridin-2-ilamina (10)
[00184] A uma solução agitada de 6-nitro-piridin-2-ilamina (9) (5,1 g, 18,4 mmol) em MeCN (125 ml) sob atmosfera de nitrogênio, N- bromossuccinimida (3,43 g, 19,3 mmol) foi adicionada a 0 °C. Depois de 1 hora, uma outra porção de N-bromossuccinimida (3,57 g, 20,1 mmol) foi adicionada. A mistura de reação foi deixada aquecer até a temperatura ambiente e a agitação continuou durante a noite. O produto foi precipitado pela adição de água (125 ml). A pasta fluida foi esfriada até 0 °C e o produto precipitado foi isolado pela filtração, lavado com MeCN:água (1:1) pré- misturados e secados sob vácuo a 40 °C para produzir 3,8 g de 5-bromo-6- nitro-piridin-2-ilamina (2).
[00185] 1H RMN (400 MHz, DMSO-d6) δ ppm: 7,84 (d, J = 8,98 Hz, 1 H), 7,03 (s, 2 H), 6,66 (d, J = 8,98 Hz, 1 H) h) Éster terc-butílico do ácido (5-Bromo-6-nitro-piridin-2-il)-carbâmico (11)
[00186] A uma solução de 5-bromo-6-nitro-piridin-2-ilamina (10) (3,8 g, 18,4 mmol) em THF seco (40 ml), NaHMDS (1 M em THF, 45 ml, 45 mmol) foi adicionado a 0 °C. Depois de agitar por 15 minutos, uma solução de BOC2O (28,3 % em peso em THF, 14,2 g, 18,4 mmol) foi adicionada lentamente a 0 °C em 1 hora. A mistura resultante foi extinta com NaHSCU aquoso (1 M, 110 ml, 110 mmol) e aquecida até a temperatura ambiente. A fase aquosa foi descartada e o produto contendo a fase orgânica foi concentrado sob pressão reduzida. O resíduo foi dissolvido em THF (40 ml) e impurezas foram precipitadas na adição de heptano (160 ml) e removidas pela filtração. O produto filtrado claro contendo a solução foi evaporado até a secura produzindo 4,2 g do éster terc-butílico do ácido (5-bromo-6-nitro- piridin-2-il)-carbâmico (11) como um resíduo escuro, marrom avermelhado que foi usado sem outra purificação na etapa seguinte.
[00187] ]H RMN (400 MHz, CLOROFÓRMIO-d) δ ppm: 8,14 (d, J = 8,98 Hz, 1 H), 8,03 (d, J = 8,59 Hz, 1 H), 7,52 (s, 1 H), 1,53 (s, 9 H) i) éster terc-butílico do ácido (5-Bromo-6-nitro-piridin-2-il)-metil-carbâmico (12)
[00188] A uma solução de éster terc-butílico do ácido (5-bromo-6- nitro-piridin-2-il)-carbâmico (11) (4,2 g, 13,2 mmol) em DMF seco (21 ml), DBU (5,02 g, 33,0 mmol)! foi adicionado a 0 °C. Iodeto de metila (3,75 g, 26,4 mmol) foi adicionado lentamente a 0 °C. Depois de agitar por 3 horas a 0 °C a mistura de reação foi extinta e o produto foi precipitado na adição de NaHSCU (1M) aquoso. O produto bruto foi isolado pela filtração e purificado pela recristalização de uma mistura de MeCN e água para produzir éster terc- butílico do ácido (5-Bromo-6-nitro-piridin-2-il)-metil-carbâmico 12 (1,55 g).
[00189] 1H RMN (400 MHz, CLOROFÓRMIO-d) δ ppm: 8,12 (d, J = 8,60 Hz, 1 H), 7,95 (d, J = 8,99 Hz, 1 H), 3,40 (s, 3 H), 1,55 (s, 9 H)
[00190] Exemplo precursor final 2: Síntese do éster terc-butílico do ácido [5-(5-etoximetóxi-benzofuran-2-il)-6-nitro-piridin-2-il]-metil- carbâmico (13) j) éster terc-butílico do ácido [5-(5-etoximetóxi-benzofuran-2-il)-6-nitro- piridin-2-il] -metil-carbâmico (13)
[00191] Seguindo-se o mesmo procedimento como descrito no Exemplo 1 (etapa d), foi preparado usando éster terc-butílico do ácido (5- Bromo-6-nitro-piridin-2-il)-metil-carbâmico (12) (100 mg, 0,30 mmol) e ácido 5-etóxi-metóxi-benzofuran-2-benzóico (4) (92,5 mg, 0,39 mmol). O trabalho como descrito no Exemplo ld, seguido pela purificação do produto bruto pela cromatografia de coluna cintilante usando de 10 a 25 % de acetato de etila em hexano. A evaporação do solvente produziu 120 mg do composto desejado (13) como sólido amarelado.
[00192] RMN (400 MHz, acetona) δ ppm: 8,48 (d, J = 8,59 Hz, 1 H), 8,36 (d, J = 8,98 Hz, 1 H), 7,48 (d, J = 8,98 Hz, 1 H), 7,37 (d, J = 2,73 Hz, 1 H), 7,23 (s, 1 H), 7,09 (dd, J = 8,98, 2,34 Hz, 1 H), 5,28 (s, 2 H), 3,74 (q, J = 7,02 Hz, 2 H), 3,43 (s, 3 H), 1,58 (s, 9 H), 1,19 (t, J = 7,02 Hz, 3 H) ESMS: m/z 444,44 [M + 1]+; 388,45 [(M - 56) +1]+ DSC: evento endotérmico com início a 81,0 °C e o pico a 83,4 °C. ΔH 76,4 Jg1 TGA: nenhum evento percebido entre a temperatura ambiente e 160 °C.
[00193] Ou uma alternativa para o éster terc-butílico do ácido [5-(5- etoximetóxi-benzofuran-2-il)-6-nitro-piridin-2-il]-metil-carbâmico (13) j) éster terc-butílico do ácido [5-(5-etoximetóxi-benzofuran-2-il)-6-nitro- piridin-2-il]-metil-carbâmico (13)
[00194] A uma solução des gaseificada de ácido 5-etoximetóxi- benzofurano benzóico (4) (0,69 g, 2,63 mmol) em etanol (17,5 ml), éster terc- butílico do ácido (5-Bromo-6-nitro-piridin-2-il)-metil-carbâmico 12 (0,50 g, 1,51 mmol), Pd(PPh3)2Cl2 (0,14 g, 0,20 mmol) e Et3N (0,48 ml, 3,46 mmol) foram adicionados. A mistura de reação foi agitada a 90 °C por 30 minutos. A mistura de reação foi esfriada até 0 °C e filtrada clara. Os voláteis foram removidos sob pressão reduzida. O resíduo foi diluído com água e a mistura foi extraída com acetato de etila. O extrato orgânico foi lavado com salmoura e concentrados sob pressão reduzida. O produto bruto foi purificado pela cromatografia de coluna cintilante. A evaporação do solvente deu o composto do título 13 (58 % de rendimento).
[00195] RMN (400 MHz, acetona) δ ppm: 8,48 (d, J = 8,59 Hz, 1 H), 8,36 (d, J = 8,98 Hz, 1 H), 7,48 (d, J = 8,98 Hz, 1 H), 7,37 (d, J = 2,73 Hz, 1 H), 7,23 (s, 1 H), 7,09 (dd, J = 8,98, 2,34 Hz, 1 H), 5,28 (s, 2 H), 3,74 (q, J = 7,02 Hz, 2 H), 3,43 (s, 3 H), 1,58 (s, 9 H), 1,19 (t, J = 7,02 Hz, 3 H) ESMS: m/z 444,44 [M + 1]+; 388,45 [(M-56) +1]+ Tabela 2 Picos de Difração de Raio X no Pó Representativos para o éster terc-butílico do ácido [5-(5-etoximetóxi-benzofuran-2-il)-6-nitro-piridin-2-il]-metil- carbâmico. vs = muito forte s = forte w = fraco vw = muito fraco
[00196] O procedimento para a preparação de [18F](2-(2-18F-fluoro-6- (metilamino)piridin-3-il)benzofuran-5-ol a partir do éster terc-butílico do ácido [5-(5-etoximetóxi-benzofuran-2-il)-6-nitro-piridin-2-il]-metil- carbâmico.
[00197] O Fluoreto 18F foi isolado em linha a partir da solução alvo do ciclotron em um cartucho QMA SepPak Eight (Waters) que foi pré- condicionado com carbonato de potássio aquoso (0,5 M, 10 ml) e água (18 MΩ, 15 ml). Depois de 3 min, o QMA SepPak Light foi fluxado com uma porção de 2 ml de uma solução de kryptofix (4,7,13,16,21,24-hexaoxa-l,10- diazobiciclo[8,8,8]hexacosano) (99 mg, 0,26 mmol) e carbonato de potássio (16 mg, 0,12 mmol) em água (0,85 ml) e acetonitrila seca (20 ml). O eluído foi aquecido a 160 °C sob fluxo de nitrogênio (110 ml/min) até seco, esfriado até a temperatura ambiente e uma solução de 5-(5-(etoximetóxi)benzofuran-2- il)-6-nitropiridin-2-il(metil)carbamato de terc-butila (3 mg, 6,8 pmol) em DMSO (1 ml) foi adicionada. A mistura foi aquecida a 85 °C por 15 min, depois esfriada a 70 °C e ácido clorídrico (6 M, 0,25 ml) foi adicionado. Depois de 30 min, a mistura de reação foi diluída com água (0,5 ml) e carregada em uma coluna de HPLC semi-preparativa (coluna ACE C-18, 5*250 mm, 5 pm), que foi eluída com MeOH/HCO2NH4 (0,1 M) (50:50 (v/v)) a 6 ml/min. A fração que elui a 34 min foi coletada, evaporada até a secura, o resíduo foi redissolvido em uma mistura de solução salina tamponada com fosfato (pH 7,4) e etanol (70 %) em propileno glicol, 5:3 (v/v) e filtrada através de um filtro estéril (0,22 pm, Millipore). Rendimento radioquímico estimado: 3 %. Pureza Radioquímica (HPLC): > 99 %. O espectro de MS/MS do produto está de acordo com o espectro do 2-(2-fluoro- 6-metilamino-piridin-3-il)-benzofuran-5-ol não rotulado autêntico.
[00198] O 2-(2-fluoro-6-metilamino-piridin-3-il)-benzofuran-5-ol não rotulado demonstra uma IC50 de 13 nM no ensaio de ligação de competição descrito na W02007/086800.
[00199] Procedimento para a preparação de [18F]2-(6-fluoro-5- metilamino-2-piridil)benzofuran-5-ol a partir do N-[6-[5-(etoximetóxi) benzofuran-2-il]-2-nitro-3-piridil]-N-metil-carbamato de terc-butila
[00200] O Fluoreto 18F foi isolado on-lineda solução alvo do ciclotron em um cartucho QMA SepPak Light (Waters) que foi pré-condicionado com carbonato de potássio aquoso (0,5 M, 10 ml) e água (18 MΩ, 15 ml). Depois de 3 min, o QMA SepPak Light foi fluxado com uma porção de 2 ml de uma solução de kryptofix (4,7,13,16,21,24-hexaoxa-l,10-diazobiciclo[8,8,8]- hexacosano) (99 mg, 0,26 mmol) e carbonato de potássio (16 mg, 0,12 mmol) em água (0,85 ml) e acetonitrila seco (20 ml). O eluído foi aquecido a 160 °C sob fluxo de nitrogênio (110 ml/min) até seco, esfriado até a temperatura ambiente e uma solução de 6-(5-(etoximetóxi)benzofuran-2-il)-2-nitropiridin- 3-il(metil)carbamato de terc-butila (2,7 mg, 0,26 mmol) em acetonitrila (1 ml) foi adicionada. A mistura foi aquecida a 85 °C por 15 min, depois esfriada a 70 °C e ácido clorídrico (2 M, 1 ml) foi adicionado. Depois de 30 min, a mistura de reação foi diluída com água (0,5 ml) e carregada em uma coluna de HPLC semi-preparativa (Coluna Waters pBondapak C-18, 7,8*300 mm, 10 pm), que foi eluída com MeOH/HCChNfL (0,1 M) (30:70 (v/v)) a 6 ml/min. A fração que elui em 24 min foi coletada, evaporada até a secura, e o resíduo foi redissolvido em solução salina tamponada com fosfato (pH 7,4) e filtrada através de um filtro estéril (0,22 pm, Millipore). Rendimento Radioquímico: 11 %. Pureza Radioquímica (HPLC): > 99 %. O espectro de MS/MS do produto está de acordo com o espectro do 2-(6-fluoro-5- metilamino-2-piridil)benzofuran-5-ol não rotulado autêntico.
[00201] O 2-(6-fluoro-5-metilamino-2-piridil)benzofuran-5-ol não rotulado demonstra uma IC50 de 44 nM no ensaio de ligação de competição descrito na WO 2007/086800.
Claims (17)
1. Composto ou sal deste, caracterizadopelo fato de que o composto é éster terc-butílico do ácido [6-(5-etoximetóxi-benzofuran-2-il)-2- nitro-piridin-3-il]-metil-carbâmico.
2. Composto ou sal deste de acordo com a reivindicação 1, caracterizadopelo fato de que estão na forma cristalina.
3. Composto ou sal deste de acordo com a reivindicação 2, caracterizadopelo fato de que a forma cristalina tem pelo menos um evento endotérmico com início entre 70° C e 300° C.
4. Composto ou sal deste de acordo com a reivindicação 1, caracterizadopelo fato de que têm uma forma cristalina tendo um padrão de difração de raio X que compreende pelo menos um pico de difração específico de 2-teta = 13,5Io para radiação de Cu Ka.
5. Composto ou sal deste de acordo com a reivindicação 4, caracterizadopelo fato de que têm uma forma cristalina que compreende os seguintes picos de difração: 11,27, 12,00, 13,51, 15,53, 16,82, 17,91, e 23,72 °2teta para radiação de Cu Ka.
6. Uso de um composto ou sal deste como definido na reivindicação 1 ou 2 como um precursor sintético, caracterizadopelo fato de ser para fabricar um composto rotulado.
7. Uso de acordo com a reivindicação 6, caracterizadopelo fato de que o rótulo é um átomo de 18F.
8. Uso de acordo com a reivindicação 6 ou 7, caracterizado pelo fato de que o composto rotulado é o 2-(6-[18F]-fluoro-5-metilamino- piridin-2-il)-benzofuran-5-ol ou um sal deste.
9. Processo para fabricar um composto, o composto sendo éster terc-butílico do ácido [6-(5-etoximetóxi-benzofuran-2-il)-2-nitro-piridin- 3-il]-metil-carbâmico, o processo caracterizadopelo fato de que compreende: converter o composto 5 no composto 6 por um processo que compreende proteger o grupo amino no composto 5 usando bicarbonato de t- butila na presença de hexametildissilazida de sódio; converter o composto 6 no composto 7 por um processo que compreende alquilar o composto 6 usando CH3I na presença de NaH; e reagir o composto 7 e o composto 4 na presença de diclorobis(trifenilfosfina)paládio(II) e (CHiC^hN em etanol; em que; o composto 4 corresponde a: o composto 5 corresponde a: o composto 6 corresponde a: o composto 7 corresponde a:
10. Composto ou sal deste, caracterizadopelo fato de que o composto é éster terc-butílico do ácido [5-(5-etoximetóxi-benzofuran-2-il)-6- nitro-piridin-2-il]-metil-carbâmico.
11. Composto ou sal deste de acordo com a reivindicação 10, caracterizadopelo fato de que está na forma cristalina.
12. Composto ou sal deste de acordo com a reivindicação 11, caracterizadopelo fato de que a forma cristalina tem pelo menos um evento endotérmico com início entre 70° C e 300° C.
13. Composto ou sal deste de acordo com a reivindicação 11, caracterizado pelo fato de que uma forma cristalina tendo um padrão de difração de raio X que compreende pelo menos um pico de difração específico de 2-teta = 6,18° para radiação de Cu Kα.
14. Composto ou sal deste de acordo com a reivindicação 13, caracterizado pelo fato de que está em uma forma cristalina compreendendo os seguintes picos de difração: 6,18, 9,14, 11,67, 14,98, e 16,44° 2teta para radiação de Cu Kα.
15. Uso do composto ou sal deste como definido na reivindicação 10 ou 11 como um precursor sintético, caracterizado pelo fato de ser para fabricar um composto rotulado.
16. Uso de acordo com a reivindicação 15, caracterizado pelo fato de que o rótulo é um átomo de 18F.
17. Uso de acordo com a reivindicação 15 ou 16, caracterizado pelo fato de que o composto rotulado é o 2-(2-[18F]-fluoro-6-metilamino- piridin-3-il)-benzofuran-5-ol ou um sal deste.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US9285108P | 2008-08-29 | 2008-08-29 | |
| US61/092851 | 2008-08-29 | ||
| PCT/SE2009/050972 WO2010024769A1 (en) | 2008-08-29 | 2009-08-28 | New benzofurans suitable as precursors to compounds that are useful for imaging amyloid deposits |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| BRPI0917147A2 BRPI0917147A2 (pt) | 2015-11-17 |
| BRPI0917147B1 true BRPI0917147B1 (pt) | 2020-09-15 |
| BRPI0917147B8 BRPI0917147B8 (pt) | 2021-05-25 |
Family
ID=41721733
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI0917147A BRPI0917147B8 (pt) | 2008-08-29 | 2009-08-28 | composto ou sal deste, uso de um composto ou sal deste, e, processo para fabricar um composto |
Country Status (22)
| Country | Link |
|---|---|
| US (3) | US8193363B2 (pt) |
| EP (1) | EP2328891B1 (pt) |
| JP (1) | JP5613669B2 (pt) |
| KR (1) | KR101648848B1 (pt) |
| CN (3) | CN104447710A (pt) |
| AR (2) | AR073230A1 (pt) |
| AU (1) | AU2009286176B2 (pt) |
| BR (1) | BRPI0917147B8 (pt) |
| CA (1) | CA2735497C (pt) |
| CL (1) | CL2011000420A1 (pt) |
| CO (1) | CO6341628A2 (pt) |
| EA (1) | EA019093B1 (pt) |
| EC (1) | ECSP11010850A (pt) |
| ES (1) | ES2627769T3 (pt) |
| IL (1) | IL211188A0 (pt) |
| MX (1) | MX2011001918A (pt) |
| NZ (1) | NZ591446A (pt) |
| PE (1) | PE20110393A1 (pt) |
| TW (1) | TW201014848A (pt) |
| UY (1) | UY32076A (pt) |
| WO (1) | WO2010024769A1 (pt) |
| ZA (1) | ZA201102284B (pt) |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8193363B2 (en) | 2008-08-29 | 2012-06-05 | Astrazeneca Ab | Compounds suitable as precursors to compounds that are useful for imaging amyloid deposits |
| JP5825608B2 (ja) * | 2010-08-06 | 2015-12-02 | 国立大学法人京都大学 | ピリジルベンゾフラン誘導体 |
| US10098859B2 (en) | 2012-09-05 | 2018-10-16 | Amri Ssci, Llc | Cocrystals of p-coumaric acid |
| WO2014097474A1 (ja) | 2012-12-21 | 2014-06-26 | 独立行政法人放射線医学総合研究所 | 脳内に蓄積したタウタンパク質をイメージングするための新規化合物 |
| US10913736B2 (en) | 2014-08-22 | 2021-02-09 | University Of Washington | Specific inhibitors of methionyl-tRNA synthetase |
| US20180344881A1 (en) * | 2015-11-20 | 2018-12-06 | Navidea Biopharmaceuticals, Inc. | Formulations for 2-heteroaryl substituted benzofurans |
| WO2021097243A1 (en) | 2019-11-13 | 2021-05-20 | Aprinoia Therapeutics Inc. | Compounds for degrading tau protein aggregates and uses thereof |
Family Cites Families (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB1041525A (en) | 1964-11-11 | 1966-09-07 | Belge Produits Chimiques Sa | Benzofuran derivatives and processes for preparing the same |
| JPH09507071A (ja) | 1993-12-21 | 1997-07-15 | イーライ・リリー・アンド・カンパニー | アミロイド原性ペプチドに関連した状態を治療又は予防する方法 |
| NZ518037A (en) * | 1999-10-15 | 2004-04-30 | F | Benzodiazepine derivatives useful as metabotropic glutamate receptors |
| FR2800069A1 (fr) * | 1999-10-22 | 2001-04-27 | Centre Nat Rech Scient | 3-amino-2,2-di-c-alkyl-1,4-butyrolactones et 1,4- thiobutyrolactones n-substituees utiles comme stimulant de l'activite de l'acide gamma-aminobutyrique et leur procede de preparation |
| WO2002055496A1 (en) | 2001-01-15 | 2002-07-18 | Glaxo Group Limited | Aryl piperidine and piperazine derivatives as inducers of ldl-receptor expression |
| JP4307001B2 (ja) | 2001-03-14 | 2009-08-05 | キヤノン株式会社 | 金属配位化合物、電界発光素子及び表示装置 |
| GB0130305D0 (en) * | 2001-12-19 | 2002-02-06 | Amersham Plc | Compounds for imaging alzheimers disease |
| WO2004012736A1 (en) | 2002-08-02 | 2004-02-12 | Genesoft Pharmaceuticals, Inc. | Biaryl compounds having anti-infective activity |
| EP1631561B1 (en) * | 2003-05-07 | 2010-08-18 | General Electric Company | Compositions and methods for non-invasive imaging of soluble beta-amyloid |
| US20040223912A1 (en) * | 2003-05-07 | 2004-11-11 | Montalto Michael Christopher | Compositions and methods for non-invasive imaging of soluble beta-amyloid |
| WO2005003101A2 (en) | 2003-07-02 | 2005-01-13 | Biofocus Discovery Limited | Pyrazine and pyridine derivatives as rho kinase inhibitors |
| WO2006020049A2 (en) * | 2004-07-15 | 2006-02-23 | Amr Technology, Inc. | Aryl-and heteroaryl-substituted tetrahydroisoquinolines and use thereof to block reuptake of norepinephrine, dopamine, and serotonin |
| WO2006099379A2 (en) * | 2005-03-14 | 2006-09-21 | Transtech Pharma, Inc. | Benzazole derivatives, compositions, and methods of use as b-secretase inhibitors |
| ES2375929T3 (es) | 2005-07-04 | 2012-03-07 | High Point Pharmaceuticals, Llc | Antagonistas del receptor histamina h3. |
| ES2379987T3 (es) * | 2005-10-11 | 2012-05-07 | University Of Pittsburgh - Of The Commonwealth System Of Higher Education | Compuestos de benzofurano marcados isotópicamente como radiotrazadores para proteínas amiloidógenas |
| TW200736252A (en) * | 2006-01-27 | 2007-10-01 | Astrazeneca Ab | Novel heteroaryl substituted benzothiazoles |
| KR20090087037A (ko) * | 2006-12-05 | 2009-08-14 | 고쿠리츠다이가쿠호진 나가사키다이가쿠 | 오론 유도체 함유 진단용 조성물 |
| JP4328820B2 (ja) | 2007-01-10 | 2009-09-09 | 田辺三菱製薬株式会社 | 医薬組成物 |
| TW200901998A (en) * | 2007-03-06 | 2009-01-16 | Astrazeneca Ab | Novel 2-heteroaryl substituted benzothiophenes and benzofuranes |
| US8193363B2 (en) * | 2008-08-29 | 2012-06-05 | Astrazeneca Ab | Compounds suitable as precursors to compounds that are useful for imaging amyloid deposits |
-
2009
- 2009-08-20 US US12/544,556 patent/US8193363B2/en active Active
- 2009-08-27 UY UY0001032076A patent/UY32076A/es not_active Application Discontinuation
- 2009-08-27 TW TW098128873A patent/TW201014848A/zh unknown
- 2009-08-28 EP EP09810319.5A patent/EP2328891B1/en active Active
- 2009-08-28 EA EA201100267A patent/EA019093B1/ru not_active IP Right Cessation
- 2009-08-28 CA CA2735497A patent/CA2735497C/en active Active
- 2009-08-28 MX MX2011001918A patent/MX2011001918A/es active IP Right Grant
- 2009-08-28 AR ARP090103323A patent/AR073230A1/es active IP Right Grant
- 2009-08-28 KR KR1020117004579A patent/KR101648848B1/ko active IP Right Grant
- 2009-08-28 WO PCT/SE2009/050972 patent/WO2010024769A1/en active Application Filing
- 2009-08-28 JP JP2011524942A patent/JP5613669B2/ja active Active
- 2009-08-28 AU AU2009286176A patent/AU2009286176B2/en active Active
- 2009-08-28 CN CN201410655681.5A patent/CN104447710A/zh active Pending
- 2009-08-28 NZ NZ591446A patent/NZ591446A/xx not_active IP Right Cessation
- 2009-08-28 BR BRPI0917147A patent/BRPI0917147B8/pt active IP Right Grant
- 2009-08-28 CN CN200980142788.7A patent/CN102197036B/zh active Active
- 2009-08-28 PE PE2011000219A patent/PE20110393A1/es not_active Application Discontinuation
- 2009-08-28 ES ES09810319.5T patent/ES2627769T3/es active Active
- 2009-08-28 CN CN201410653507.7A patent/CN104478862B/zh active Active
-
2011
- 2011-02-10 IL IL211188A patent/IL211188A0/en unknown
- 2011-02-21 CO CO11020875A patent/CO6341628A2/es not_active Application Discontinuation
- 2011-02-25 CL CL2011000420A patent/CL2011000420A1/es unknown
- 2011-02-28 EC EC2011010850A patent/ECSP11010850A/es unknown
- 2011-03-28 ZA ZA2011/02284A patent/ZA201102284B/en unknown
-
2012
- 2012-06-04 US US13/487,349 patent/US8653274B2/en active Active
-
2014
- 2014-01-07 US US14/149,563 patent/US9309267B2/en active Active
-
2018
- 2018-11-12 AR ARP180103297A patent/AR114029A2/es unknown
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US9309267B2 (en) | Compounds suitable as precursors to compounds that are useful for imaging amyloid deposits | |
| EP2436666B1 (en) | Method for obtaining novel derivatives of naphtalene for the in vivo diagnosis of alzheimer 's disease | |
| JP2009532328A (ja) | 5−ht1b受容体の放射性リガンド | |
| BRPI0808503B1 (pt) | Composto, uso de um composto, e, composição farmacêutica | |
| MX2008015718A (es) | Nuevos benzoxazoles sustituidos con heteroarilo. | |
| KR20230111272A (ko) | 방사성 표지된 전립선-특이적 막 항원(PSMA) 억제제[18F]DCFPyL의 개선된 합성 | |
| JP2022548018A (ja) | 放射性標識化合物 | |
| WO2002040060A2 (en) | Conjugates of an antioxidants with metal chelating ligands | |
| JP2010520275A (ja) | 新規な2−ヘテロアリール置換インドール695 | |
| JP5618042B2 (ja) | アイソトープ標識化合物及びアイソトープ標識化合物前駆体 | |
| JP7438197B2 (ja) | 多環式芳香族アミンの第四級アンモニウム塩の放射標識化合物、陽電子放射断層撮影の診断方法における放射標識化合物の使用、及び多環式芳香族アミンの第四級アンモニウム塩の放射標識化合物を含有する医薬組成物 | |
| JP2021102593A (ja) | タウを画像化する新規化合物 | |
| RU2472789C2 (ru) | Новые 2-гетероарил-замещенные бензотиофены и бензофураны 709 | |
| AU2015200027A1 (en) | Contrast agents for applications including perfusion imaging | |
| WO2011124713A1 (en) | Labelled huprine derivatives and their use in medical imaging |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B07D | Technical examination (opinion) related to article 229 of industrial property law [chapter 7.4 patent gazette] | ||
| B07E | Notification of approval relating to section 229 industrial property law [chapter 7.5 patent gazette] | ||
| B06U | Preliminary requirement: requests with searches performed by other patent offices: procedure suspended [chapter 6.21 patent gazette] | ||
| B06A | Patent application procedure suspended [chapter 6.1 patent gazette] | ||
| B09A | Decision: intention to grant [chapter 9.1 patent gazette] | ||
| B16A | Patent or certificate of addition of invention granted [chapter 16.1 patent gazette] |
Free format text: PRAZO DE VALIDADE: 10 (DEZ) ANOS CONTADOS A PARTIR DE 15/09/2020, OBSERVADAS AS CONDICOES LEGAIS. |
|
| B16C | Correction of notification of the grant [chapter 16.3 patent gazette] |
Free format text: PRAZO DE VALIDADE: 20 (VINTE) ANOS CONTADOS A PARTIR DE 28/08/2009 OBSERVADAS AS CONDICOES LEGAIS. PATENTE CONCEDIDA CONFORME ADI 5.529/DF |