CAMPO TÉCNICO
[0001] A presente invenção diz respeito à composição farmacêutica compreendendo um derivado de pirazina ou um sal do mesmo e um ou mais inibidor(es) de neuraminidase, que é usado no tratamento (por exemplo, terapia ou prevenção) de doenças virais. Além disso, a presente invenção diz respeito a um método para usar um derivado de pirazina ou um sal do mesmo e inibidor(es) de neuraminidase em combinação para tratamento (por exemplo, terapia ou prevenção) de influenza.
FUNDAMENTOS DA TÉCNICA
[0002] Infecção por vírus da influenza (daqui em diante referido como influenza) causada por vírus da influenza é frequentemente uma doença fatal. Recentemente, vírus, tal como influenza aviária ocorreram, que apresentou forte patogenicidade aos humanos. Influenza aviária ameaça ser pandêmico.
[0003] Entretanto, medicamentos aplicáveis à influenza são muito menos que agentes antimicrobianos ou similares. Por exemplo, amantadina e oseltamivir atualmente usados têm problemas, tal como resistência a eles.
[0004] Um método para usar agentes anti-vírus da influenza em combinação foi discutido com o propósito de reduzir resistência ao medicamento de vírus da influenza, melhorar os efeitos terapêuticos e/ou reduzir efeitos colaterais, etc. Entretanto, os medicamentos usados em combinação são limitados em número e nem sempre produzem efeitos satisfatórios.
[0005] Por exemplo, inibidores de neuraminidase são conhecidos como medicamentos que apresentam efeitos no vírus da influenza. Neuraminidase, que é uma glicoproteína da espícula encontrada na superfície do vírus da influenza, é requerida para células que infectam o vírus da influenza da garganta ou brônquio e proliferação para espalhar para suas células vizinhas. A inibição da neuraminidase pode suprimir o espalhamento de tal vírus da influenza para as células vizinhas. Por exemplo, um inibidor da neuraminidase oseltamivir é convertido na sua forma ativa GS-4071 in vivo, que apresenta efeitos antivirais, de maneira tal que iniba a neuraminidase no vírus da influenza (DOCUMENTO NÃO PATENTE 1). Oseltamivir e zanamivir são comercialmente disponíveis como inibidores de neuraminidase. Tais medicamentos ainda tem que ser desenvolvidos e estudados.
[0006] Por outro lado, um derivado de pirazina tendo atividades antivirais é conhecido (DOCUMENTO PATENTE 1). Sabe-se que este derivado de pirazina apresenta efeitos antivirais em ribosilfosforilação intracelular, de maneira tal que ele apresente RNA polimerase de vírus (DOCUMENTO PATENTE 2).
[0007] Entretanto, nem uma composição farmacêutica compreendendo um inibidor da neuraminidase e um derivado de pirazina nem um método para usar um inibidor da neuraminidase e um derivado de pirazina em combinação são até agora conhecidos. DOCUMENTO PATENTE 1: Folheto de WO00/10569 DOCUMENTO PATENTE 2: Folheto de WO03/015798 DOCUMENTO NÃO PATENTE 1: Japanese Journal of Clinical Medicine, 2003, vol. 61, p. 1975-1979
DESCRIÇÃO DA INVENÇÃO
[0008] PROBLEMAS A SER RESOLVIDOS PELA INVENÇÃO
[0009] Existe uma demanda para uma composição farmacêutica que tem fortes atividades anti-vírus da influenza com poucos efeitos colaterais e seja usada para o tratamento (por exemplo, terapia ou prevenção) de influenza e para um método de tratar influenza.
MEIOS PARA RESOLVER OS PROBLEMAS
[0010] Em tais circunstâncias, o presente inventor conduziu estudos de aplicação e consequentemente completou a presente invenção preceituando que uma composição farmacêutica compreendendo um derivado de pirazina representado pela seguinte fórmula geral [1] ou um sal do mesmo e um ou mais inibidor(es) de neuraminidase: [Fórmula 1]
em que R1 e R2são os mesmos ou diferentes e cada um representa um átomo de hidrogênio ou um átomo de halogênio; e R3 representa um átomo de hidrogênio ou um grupo que protege amino, tem fortes atividades anti-vírus da influenza e é usado para o tratamento de influenza, e que um método para usar estes compostos em combinação é usado como um método de tratamento de influenza.
[0011] Uma composição farmacêutica compreendendo um derivado de pirazina ou um sal do mesmo e um ou mais inibidor(es) de neuraminidase tem fortes atividades sinergísticas anti-vírus da influenza e é usada para o tratamento (por exemplo, terapia ou prevenção) de influenza. Um método para usar estes compostos em combinação é usado como um método de tratamento (por exemplo, terapia ou prevenção) de influenza.
MELHOR MODO DE REALIZAR A INVENÇÃO
[0012] Daqui em diante, a presente invenção ser descrita em detalhe.
[0013] Na presente especificação, a menos que de outra forma especificado, um átomo de halogênio significa átomos de flúor, cloro, bromo e iodo; um grupo acila significa, por exemplo, um grupo formila, um grupo alcanoíla C2-C12 reto ou ramificado (por exemplo, acetila, propionila, butirila, isovalerila, e pivaloíla), um grupo alquilcarbonila ar-C1-6 (por exemplo, benzilcarbonila), um grupo carbonila de hidrocarboneto cíclico (por exemplo, benzoíla e naftoíla), um grupo carbonila heterocíclico (por exemplo, nicotinoíla, tenoíla, pirrolidinocarbonila, e furoíla), um grupo succinila, um grupo glutarila, um grupo maleoíla, um grupo ftaloíla, e um grupo -aminoalquila reto ou ramificado (que pode ser N-terminalmente protegido) derivado de aminoácidos (exemplos dos aminoácidos incluem glicina, alanina, valina, leucina, isoleucina, serina, treonina, cisteína, metionina, ácido aspártico, ácido glutâmico, asparagina, glutamina, arginina, lisina, histidina, hidroxilisina, fenilalanina, tirosina, triptofano, prolina, e hidroxiprolina); um grupo alquiloxicarbonila significa, por exemplo, um grupo alquiloxicarbonila C1-12 reto ou ramificado, tais como metoxicarbonila, etoxicarbonila, 1,1-dimetilpropoxicarbonila, isopropoxicarbonila, 2-etilexiloxicarbonila, terc-butoxicarbonila, e terc- pentiloxicarbonila; um grupo aralquiloxicarbonila significa, por exemplo, um grupo alquiloxicarbonila ar-C1-6, tais como grupos benziloxicarbonila e fenetiloxicarbonila; um grupo atiloxicarbonila significa, por exemplo, um grupo feniloxicarbonila; um grupo aralquila significa, por exemplo, um grupo alquila ar-C1-6, tais como benzila, difenilmethila, tritila, phenethila, e naftilmetila; um grupo alcoxialquila significa, por exemplo, um grupo alcóxi C1-6 alquila C1-6, tais como metoximetilae 1-etoxietila; um grupo aralquiloxialquila significa, por exemplo, um grupo ar-alquilóxi C1-6 alquila C1-6, tais como benziloximetila e fenetiloximetila.
[0014] Um grupo ariltio significa, por exemplo, um grupo feniltio; um grupo alquilsulfonila significa, por exemplo, um grupo alquilsulfonila C1-6, tais como metilsulfonila, etilsulfonila, e propilsulfonila; um grupo arilsulfonila significa, por exemplo, benzenossulfonila, toluenossulfonila, e grupos naftalenossulfonila; um grupo dialquilaminoalquilideno significa, por exemplo, N,N-dimetilaminometileno e grupos N,N-dietilaminometileno; um grupo aralquilideno significa, por exemplo, grupos benzilideno e naftilmetileno; um grupo alquilideno heterocíclico contendo nitrogênio significa, por exemplo, um grupo 3-hidróxi-4-piridilmetileno; um grupo cicloalquilideno significa, por exemplo, grupos ciclopentilideno e cicloexilideno; um grupo diarilfosforila significa, por exemplo, um grupo difenilfosforila; um grupo diaralquilfosforila significa, por exemplo, um grupo dibenzilfosforila; um grupo alquila heterocíclico contendo oxigênio significa, por exemplo, um grupo 5-metil-2-oxo-2H- 1,3-dioxol-4-ilmetila; e um grupo silila substituído significa, por exemplo, grupos trimetilsilila, trietilsilila, e tributilsilila.
[0015] Um grupo que protege amino engloba todos os grupos disponíveis como grupos que protegem amino usuais. Exemplos destes incluem grupos descritos em W. Greene et al., Protective Groups in Organic Synthesis, 3rd ed., p. 494-653, 1999, John Wiley & Sons, INC. Exemplos específicos destes incluem um grupo acila, um grupo alquiloxicarbonila, um grupo aralquiloxicarbonila, um grupo atiloxicarbonila, um grupo aralquila, um grupo alcoxialquila, um grupo aralquiloxialquila, um grupo ariltio, um grupo alquilsulfonila, um grupo arilsulfonila, um grupo dialquilaminoalquilideno, um grupo aralquilideno, um grupo alquilideno heterocíclico contendo nitrogênio, um grupo cicloalquilideno, um grupo diarilfosforila, um grupo diaralquilfosforila, um grupo alquila heterocíclico contendo oxigênio, e um grupo silila substituído.
[0016] Exemplos de um sal do composto da fórmula geral [1] usado na presente invenção podem incluir sais conhecidos de grupos hidroxila. Exemplos destes podem incluir: sais com metais alcalinos, tais como sódio e potássio; sais com metais alcalinos terrosos, tais como cálcio e magnésio; sais de amônio; e sais com bases orgânicas contendo nitrogênio, tais como trimetilamina, trietilamina, tributilamina, N-metilpiperidina, N-metilmorpholina, dietilamina, dicicloexilamina, procaína, dibenzilamina, N-benzil-β-fenetilamina, 1-efenamina, e N,N'- dibenziletilenodiamina.
[0017] Exemplos desejáveis do sal incluem sais farmacologicamente aceitáveis. Um sal com sódio é preferível.
[0018] Exemplos desejáveis do composto da fórmula geral [1] usados na presente invenção incluem os seguintes compostos: compostos representados pela fórmula geral [1] em que R1é um átomo de hidrogênio, R2é um átomo de flúor, e R3é um átomo de hidrogênio.
[0019] O composto da fórmula geral [1] usado na presente invenção é produzido combinando métodos conhecidos per se na técnica e pode ser produzido de acordo com, por exemplo, um método de produção descrito no DOCUMENTO PATENTE 1.
[0020] Exemplos de um inibidor da neuraminidase usados na presente invenção incluem compostos em si ou seus metabólitos in-vivo tendo efeitos inibitórios na neuraminidase, tais como oseltamivir, zanamivir, peramivir, CS-8958 e FRUNET. Oseltamivir e zanamivir são preferíveis. Oseltamivir é além do mais desejável.
[0021] A via de administração de uma composição farmacêutica da presente invenção não é particularmente limitada, e ela pode ser administrada intravenosa, oral, intramuscular, hipodermicamente, por inalação, por aspersão ou por meio de outras vias de administração. Além disso, o derivado de pirazina representado pela fórmula geral [1] ou o sal do mesmo pode ser administrado com o inibidor da neuraminidase simultaneamente ou em uma ordem particular.
[0022] A composição farmacêutica da presente invenção é usada para o tratamento (por exemplo, terapia ou prevenção) de influenza.
[0023] A composição farmacêutica da presente invenção permite o tratamento (por exemplo, terapia ou prevenção) de influenza mais severa. Além disso, os medicamentos individuais usados apresentam fortes efeitos anti-vírus da influenza mesmo quando eles são administrados em menores quantidades. Desta forma, seus respectivos efeitos colaterais podem ser reduzidos.
[0024] Quando a composição farmacêutica da presente invenção é usada, ela pode normalmente ser misturada apropriadamente com auxiliares farmacêuticos usados na formulação, tais como um excipiente, um veículo e um diluente. Estas formulações podem ser administradas oral ou parenteralmente em uma forma, tais como um comprimido, uma cápsula, um pó, um xarope, um grânulo, uma pílula, uma suspensão, uma emulsão, uma solução, uma preparação em pó, um supositório, colírios, gotas nasais, gotas para o ouvido, um adesivo, um unguento ou uma injeção de acordo com um método convencional. Além disso, um método de administração, uma dose, e a frequência de administração podem ser selecionados apropriadamente de acordo com a idade, peso corporal e sintoma de um paciente. Ele pode ser normalmente administrado oral ou parenteralmente (por exemplo, injeção, infusões intravenosas e administração a um sítio retal) a um adulto em uma a várias doses divididas nas doses de 0,01 a 1.000 mg/kg por dia.
[0025] EXEMPLOS
[0026] Em seguida, a presente invenção será descrita com referência aos exemplos de teste. Entretanto, a presente invenção não se destina a ser limitada por eles.
[0027] 6-Fluoro-3-hidróxi-2-pirazinacarboxamida (daqui em diante referido como T-705) foi selecionado como um composto de teste. GS-4071, que é uma forma ativa in-vivo de oseltamivir, e zanamivir foram selecionados como inibidores de neuraminidase. Neste contexto, GS-4071 usado nos presentes testes foi obtido por extração de Tamiflu (medicamento comercialmente disponível), seguido por hidrólise de acordo com um método convencional.
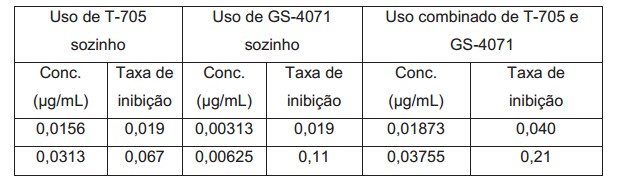
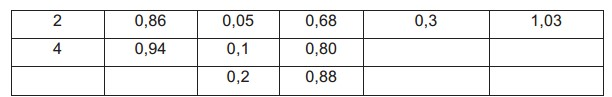
[0028] Exemplo de teste 1 T-705 foi selecionado como um composto de teste. GS-4071 foi selecionado como um inibidor da neuraminidase. (1) Cultura de células MDCK Células de rim canino Madin-Darby (daqui em diante referido como MDCK) subcultivadas a 37 °C em condições de dióxido de carbono 5 % em um meio MEM de Eagle suplementado com soro bovino fetal 10 % na solução de cultura foram dissociadas por um método de ácido etilenodiaminotetracético-tripsina e suspensas no mesmo meio anterior. A suspensão de célula preparada para conter 2 x 104 células em 100 μL foi, por sua vez, inoculada em uma placa de 96 poços. As células foram cultivadas durante toda a noite a 37 °C em condições de dióxido de carbono 5 % para obter uma monocamada de células MDCK. (2) Infecção por vírus da influenza e aumento de medicamento Um meio de teste usado foi um meio preparado adicionando tripsina tratada com L-1-tosilamido-2-feniletil clorometil cetona (TPCK) em uma concentração de 3 μg/mL a um meio MEM de Eagle contendo albumina de soro bovino 1 % suplementada com 60 μg/mL de canamicina e quarto vezes a concentração usual de vitaminas. As células MDCK obtidas no parágrafo (1) foram rinsadas com um meio MEM de Eagle depois da remoção do sobrenadante da cultura. Então, a cada poço, os seguintes agentes foram adicionados: 100 μL de um meio MEM de Eagle contendo albumina de soro bovino e vitaminas em duas vezes a concentração do meio de teste; 50 mL de uma solução de vírus da influenza (PR/8 (H1N1)) ajustada para 4,0 x 103 PFU/mL com um meio MEM de Eagle contendo tripsina tratada com TPCK em quatro vezes a concentração do meio de teste; e 50 mL de um meio MEM de Eagle contendo T-705 ou GS-4071 em quatro vezes a concentração alvo (concentração alvo de T-705 (μg/mL): 0,0156, 0,0313, 0,0625, 0,125, 0,25, 0,5, 1, 2, e 4; e concentração alvo de GS-4071 (μg/mL): 0,00313, 0,00625, 0,0125, 0,025, 0,05, 0,1, 0,2, 0,4, e 0,8) ou contendo uma mistura de T-705/GS-4071 (5:1 razão em peso da concentração) em quatro vezes a concentração alvo. Depois da adição de medicamento, as células foram cultivadas a 35 °C por 2 dias em condições de dióxido de carbono 5 %. (3) Ensaio de absorção de vermelho neutro O efeito citopático (CPE) observado junto com a proliferação do vírus da influenza foi estimado pelos métodos descritos em J. Virol. Methods, 2002, vol. 106, p. 71-79 e Proc. Natl. Acad. Sci., 1998, vol. 95, p. 8874-8849. Depois do final da cultura, uma solução de vermelho neutron 0,033 % diluída com um tampão de fosfato de Dulbecco sem calico/magnésio foi adicionada em um volume de 100 μL a cada poço. A placa foi repousou a 35 °C em condições de dióxido de carbono 5 %. Duas horas depois, as soluções nos poços foram removidas por aspiração. Depois de rinsar duas vezes com 100 mL de um tampão de fosfato de Dulbecco sem cálcio/magnésio, 100 mL de uma solução mista de um tampão (pH 4,2; composto de 0,1 mol/L de citrato de sódio e 0,1 mol/L de ácido clorídrico) e etanol numa razão 1:1 em volume foi adicionado a cada poço. A placa repousou a temperatura ambiente, protegida da luz. Trinta minutos depois, a absorbância (540 nm) foi medida usando um leitor de microplaca (BIO-RAD Model 550). Controles não infectados foram preparados adicionando, em vez da solução do vírus da influenza, 50 mL de um meio MEM de Eagle contendo tripsina tratada com TPCK em quatro vezes a concentração do meio de teste e submetidos aos mesmos procedimentos dos para o grupo de teste, seguido pela medição da absorbância. Para branco, poços sem ser inoculados com as células MDCK foram submetidos aos mesmos procedimentos para os controles não infectados, seguido pela medição da absorbância. Oito poços foram usados em cada concentração. Um valor médio foi usado, e um valor numérico obtido subtraindo a absorbância do branco do valor medido foi usado para o seguinte cálculo como absorbância. Um valor obtido subtraindo a absorbância de controles infectados do valor dos controles não infectados foi usado como um valor de inibição completa da proliferação do vírus. A taxa de inibição de proliferação de vírus em cada teste foi calculada de acordo com a seguinte fórmula: Taxa de inibição de proliferação do vírus = [(Absorbância do medicamento sozinho ou medicamentos combinados) - (Absorbância do controle infectado)]/[(Absorbância dos controle não infectado)-(Absorbância do controle infectado)]. (4) Análise dos efeitos de combinação A partir das concentrações de medicamentos sozinhos e dois medicamentos usados em combinação, a razão dos medicamentos de combinação, e a taxa de inibição de proliferação do vírus, os efeitos da combinação foram analisados usando SAS release 8.2 (SAS Institute Japan Ltd.) de acordo com o método de efeito mediano de Chou et al. Of methods shown in Advanced Enzyme Regulation, 1984, vol. 22, p. 27-55, uma equação para medicamentos cujos mecanismos de ação são completamente independente um do outro (medicamentos mutuamente não exclusivos) foi usada para calcular um valor CI. Os efeitos da combinação foram determinados com base em um valor CI em 50 % de inibição da proliferação do vírus de acordo com a descrição do papel de Taira et al. [Acta Medica Okayama., 2006, vol. 60, p. 25-34] em que CI <0,8 representa sinergismo, 0,8 < CI < 1,2 representa aditividade, e 1,2 <CI representa antagonismo. As taxas de inibição da proliferação do vírus de T-705 usado sozinho, GS- 4071 usado sozinho e a combinação destes medicamentos são mostradas na tabela 1. Os resultados da análise usando estes valores são mostrados na tabela 2.
[0031] A administração combinada de T-705 e GS-4071 (forma ativa in-vivo de oseltamivir) apresentou efeitos inibitórios sinergísticos mais excelentes na proliferação do vírus que a apresentada pela administração do medicamento sozinho.
[0032] Exemplo de teste 2 T-705 foi selecionado como um composto de teste. Zanamivir foi selecionado como um inibidor da neuraminidase. Um teste foi conduzido da mesma maneira que o método descrito no exemplo de teste 1. As taxas de inibição da proliferação do vírus de T-705 usado sozinho, zanamivir usado sozinho, e a combinação destes medicamentos são mostradas na tabela 3. Os resultados da análise usando estes valores são mostrados na tabela 4.
[0035] A administração combinada de T-705 e zanamivir apresentou efeitos inibitórios sinergísticos mais excelentes na proliferação do vírus que a apresentada pela administração do medicamento sozinho.
[0036] Exemplo de teste 3 T-705 foi selecionado como um composto de teste. GS-4071 foi selecionado como um inibidor da neuraminidase. Um teste foi conduzido da mesma maneira que o método descrito no exemplo de teste 1 usando Victoria/3/75 (H3N2) como vírus da influenza. As taxas de inibição da proliferação do vírus de T-705 usado sozinho, GS-4071 usado sozinho e a combinação destes medicamentos são mostradas na tabela 5. Os resultados da análise usando estes valores são mostrados na tabela 6.
[0039] A administração combinada de T-705 e GS-4071 (forma ativa in-vivo de oseltamivir) apresentou efeitos inibitórios sinergísticos mais excelentes na proliferação do vírus que a apresentada pela administração do medicamento sozinho.
[0040] Exemplo de teste 4 T-705 foi selecionado como um composto de teste. Zanamivir foi selecionado como um inibidor da neuraminidase. Um teste foi conduzido da mesma maneira que o método descrito no exemplo de teste 3. As taxas de inibição da proliferação do vírus de T-705 usado sozinho, zanamivir usado sozinho, e a combinação destes medicamentos são mostradas na tabela 7. Os resultados da análise usando estes valores são mostrados na tabela 8.
[0043] A administração combinada de T-705 e zanamivir apresentou efeitos inibitórios sinergísticos mais excelentes na proliferação do vírus que a apresentada pela administração do medicamento sozinho.
[0044] Conforme visto a partir dos resultados, a administração combinada de um derivado de pirazina representado pela fórmula geral [1] ou um sal do mesmo e vários inibidores de neuraminidase apresenta atividades anti-vírus da influenza sinergísticas e é efetiva para o tratamento (por exemplo, terapia ou prevenção) de influenza.
APLICABILIDADE INDUSTRIAL
[0045] Uma composição farmacêutica compreendendo um derivado de pirazina ou um sal do mesmo e um ou mais inibidor(es) de neuraminidase tem fortes atividades sinergísticas anti-vírus da influenza e é usada para o tratamento (por exemplo, terapia ou prevenção) de influenza. Um método para usar estes compostos em combinação é usado como um método de tratamento (por exemplo, terapia ou prevenção) de influenza.