Campo da Invenção
A invenção refere-se a formulações terapêuticas e métodos para alterar a distribuição de massa do corpo. Mais especificamente, a invenção refere-se às formulações terapêuticas que compreendem compostos, tais como flavonóides, polifenóis, polipeptídeos, leucina e outros aminoácidos de cadeia ramificada e bioativos lácteos, para serem utilizados em métodos para alterar a distribuição de massa do corpo.
Antecedentes da Invenção
Neste relatório descritivo onde um documento, ato ou item de conhecimento é mencionado ou discutido, essa referência ou discussão não é uma admissão de que o documento, ato ou item de conhecimento ou qualquer combinação dos mesmos seja na data de prioridade, publicamente disponível, conhecido pelo público, parte do conhecimento geral comum; ou conhecido como de relevância para uma tentativa de solucionar qualquer problema com o qual este relatório descritivo esteja relacionado.
Aumento da massa magra do corpo
Há uma série de doenças que envolvem a caquexia (fraqueza e perda de massa do corpo) como um sintoma em que o corpo perde quantidades significativas de massa magra do corpo. Os exemplos de tais doenças incluem o diabetes, o câncer, o mal de Alzheimer, a bulimia nervosa e a anorexia.
Desse modo, há uma necessidade quanto a um tratamento que permita que o corpo aumente a sua porcentagem da massa magra do corpo com um aumento mínimo, ou idealmente uma diminuição, na porcentagem da massa de gordura.
Polifenóis
Os polifenóis (compostos com dois ou mais grupos hidróxi fenólicos) constituem uma classe de fitoquímicos encontrados em uma variedade de fontes incluindo o vinho, as uvas, o cacau e a cana de açúcar. Todos os polifenóis (ou fenólicos) têm um componente químico básico comum, isto é, uma estrutura de anel fenólico. Há pelo menos 8.000 polifenóis identificados em uma série de subcategorias, tais como anticianinas e catequinas. Os polifenóis naturais podem variar de moléculas simples, tal como o ácido fenólico, a grandes compostos altamente polimerizados, tais como as taninas. As formas conjugadas de polifenóis são as mais comuns, onde várias moléculas de açúcar, ácidos orgânicos e os lipídios (gorduras) são ligados com a estrutura de anel fenólico. As diferenças nessa estrutura química conjugada são as responsáveis pelas diferentes classificações químicas e pela variação nos modos de ação e propriedades da saúde dos vários compostos.
Os polifenóis são considerados como provedores de uma série de benefícios de saúde, incluindo: atividade antioxidante; propriedades preventivas do câncer; proteção contra doenças do coração e hipertensão; atividade antibiótica/antiviral; atividade anti-inflamatória; propriedades oftamológicas; e protegendo o reforço dos vasos sangüíneos. Os polifenóis são os responsáveis pelos pigmentos de coloração brilhante de muitas frutas, legumes e flores (variando do cor-de-rosa ao escarlate, roxo e azul), eles protegem as plantas contra doenças e a luz ultravioleta e ajudam a impedir danos às sementes até que elas germinem.
Infelizmente, embora os dados epidemiológicos para a ingestão de frutas e legumes e a prevenção de doenças sejam intensos, os suplementos dietéticos que contêm antioxidantes fenólicos isolados não foram estudados extensamente em termos da prevenção de doenças. Produtos tais como o chá verde, o HCA (ácido hiroxicítrico) e a inulina reivindicam benefícios da perda de peso com base na suposição que esses produtos atrasam a absorção da glicose e/ou regulam a insulina para controlar o apetite. Isto ainda tem que ser provado em experimentações clínicas controladas com seres humanos (Functional Food Update 01, National Centre of Excellence in Functional Foods, Austrália, Junho de 2006).
Cana de açúcar
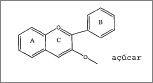
As anticianinas são sais polifenólicos de flavilium com unidades de açúcar unidas à molécula e são derivadas principalmente de seis antocianidas: pelargonidina, cianidina, delfinidina, peonidina, petunidina e malvidina. Esses compostos diferem na posição e no número de grupos hidroxila no anel B, mas todos têm uma unidade de açúcar na posição 3 e são solúveis em água. Com exceção do grupo petunidina, os representantes de todas as outras classes de anticianina foram localizados na cana de açúcar.
A estrutura básica comum a todas as anticianinas é tal como segue:
Apenas em segundo lugar depois da água, o chá é uma das bebidas mais amplamente consumidas no mundo. Aproximadamente 3,0 milhões de toneladas métricas de chá seco são produzidas anualmente, 20% das quais consiste em chá verde, 2% em chá oolong, e o restante consiste em chá preto (boletim anual de estatísticas de 2002 do Comitê Internacional do Chá) . Os chás preto, oolong e o chá verde são produzidos a partir das folhas da planta de chá Camellia, sinensis,um membro da família das Theaceae. Variedades diferentes do chá são produzidas ao variar o grau de oxidação das folhas. O chá verde é produzido ao cozinhar as folhas recém colhidas a altas temperaturas, inativando as enzimas oxidantes. Isto preserva o elevado teor de polifenol encontrado no chá verde. As folhas do chá preto são as mais oxidadas, ao passo que a oxidação das folhas do chá oolong é intermediária entre o chá verde e o chá preto.
A maior parte dos polifenóis no chá consiste em flavonõis, especificamente as catequinas. Essas moléculas pequenas reagem umas com as outras durante o processo de oxidação que produz os chás preto e oolong para formar compostos maiores altamente coloridos denominados teaflavinas e tearubiginas.
Recentemente, tem sido feita muita pesquisa quanto aos benefícios farmacêuticos potenciais dos polifenóis extraídos do chá. O agente quimiopreventivo mais potente normalmente extraído do chá é o (-)-epigalocatequina-3-gaiato (EGCG) . Também há reivindicações de que os polifenóis do chá verde podem ajudar com a perda do peso por causa de sua capacidade de aumentar o metabolismo e a queima de gordura observada enquanto foi estudado o efeito dos polifenóis nos níveis de colesterol no sangue. Os medicamentos feitos a partir de polifenóis do chá passaram a fazer parte do tratamento para a nefrite, a hepatite crônica e a leucemia na China. Em outros países, os suplementos de chá verde estão disponíveis.
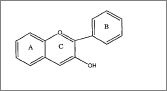
A estrutura básica comum a todas as catequinas é tal como segue:
O cacau Theobroma é uma fonte rica de flavonóides incluindo polifenóis. Um estudo sobre o consumo de chocolate escuro por seres humanos mostrou que o chocolate rico em flavonóides melhora a função endotelial e aumenta as concentrações de epicatequina do plasma. No entanto, esse estudo não encontrou nenhuma mudança nas medidas do stress oxidante, em perfis de lipídios, na pressão sangüínea, no peso do corpo ou no índice de massa do corpo [Engler et al., "Flavonoid-rich dark chocolate improves endothelial function and increases plasma epicatechin concentrations in healthy adults"J Am Coll Nutr 2004 ; 23 (3) : 197-204] .
Um outro estudo sobre o consumo do chocolate escuro não encontrou nenhuma mudança na capacidade antioxidante total do plasma ou na susceptibilidade à oxidação de lipídios 5 do soro. O estudo descobriu que os polifenóis do cacau podem aumentar a concentração de colesterol HDL, ao passo que os ácidos graxos do chocolate podem modificar a composição de ácidos graxos de LDL e torná-lo mais resistente aos danos oxidantes [Mursu et al. , "Dark chocolate consumption 10 increases HDL cholesterol concentration and chocolate fatty- acids inhibit lipid peroxidation in healthy humans"Free Radio Biol Med, 01 de novembro de 2004; 37(9):1351-9].
Inibidores de ACE
O ACE é uma parte importante do sistema renina- 15 angiotensina-aldosterona, um dos principais sistemas endócrinos no corpo. O ACE cliva a angiotensina I (ANG-I) no potente vasoconstrictor angiotensina II (ANG-II), o qual regula as principais funções fisiológicas do corpo incluindo a pressão sangüínea, o sódio do corpo e a homeostase fluida 20 que media a sua função através dos receptors celulares AT-1 e AT-2. Foi demonstrado que o inibidores de ACE são úteis na redução da pressão sangüínea e no tratamento da disfunção ventricular esquerda e da neuropatia diabética.
Há uma série de estudos sobre os vários papéis de 25 ANG-II: . organogênese (Oliverio MI, Madsen K, Best CF, Ito M, Maeda N, Smithies O, Coffman TM. "Renal growth and development in mice lacking AT1A receptors for angiotensin II". Am. J. Physiol. 1998; 274:F43-F50); 30 . formação de pré-adipócitos; os pré-adipócitos humanos expressam uma grande afinidade com os subtipos de receptores AT-1 (Crandall DL, Armellino DC, Busier DE, McHendry-Rinde B, Kral JG. ’’Angiotensin II receptors in human preadipocytes: role in cell cycle regulation". Endocrinology 1999; 140:154-158); o tecido adiposo branco foi relatado como um sítio importante de produção de angiotensinogênio (Cassis LA, Saye J, Peach MJ. "Location and development of rat angiotensin Messenger RNA". 1988; Hypertension 11:591-596); estimulação da adipogênese ou da formação de células de adipose (gordura) (Darimont C, Vassaux G, Alihaud G, Negrel R. "Differentiation of preadipose cells: paracrine role of prostaciclin upon stimulation of adipose cell by angiotensin-II". Endocrinology 1994; 135:2030-2036; Saint- Marc P. Kozak LP, Ailhaud G, Darimont C, Negrel R. "Angiotensin-II as a trophic factor of white adipose tissue: stimulation of adipose cell formation". Endocrinology 2001; 142:487-492); aumento da lipogênese e acumulação de trigliceridios em células de preadipose e adipócitos humanos (Jones BH, Standridge MK, Moustaid N. 11 Angiotensin-II increases lipogenesis in 3T3-L1 and human adipose cells". Endocrinology 1997; 138:15121519); os ratos tratados com um inibidor de ACE (losartan) apresentam uma redução no tamanho do adipócito (Zorad S, Fickova M, Zelezna B, L Macho, Kral JG. "The role of angiotensin-II and its receptors in regulation of adipose tissue metabolism and cellularity". Gen, Physiol. Biophys. 1995; 14:383-391).
Coletivamente, esses estudos indicam que a ANG-II desempenha um papel importante no desenvolvimento do tecido adiposo.
Os estudos também mostraram que os inibidores de ACE podem ser úteis na redução do ganho de peso.
Em camundongos com deficiência em angiotensinogênio, o ganho de peso é mais baixo do que nos camundongos do tipo selvagem normal a despeito da ingestão de alimento que é similar para ambos os genótipos (Massiera F, Seydoux J, Geloen A, Quignard_Boulange A, Turban S, Saint- saint-Marc P, Fukamizu A, Negrel R, Ailhaud G. e Teboul M. "Angiotensinogen-Deficient mice exhibit impairment of diet- induced weight gain with alteration in adipose tissue development and increase in locomotor activity". Endocrinology 2001; 142 (12) :5220-5225) . . A superalimentação de roedores conduz à produção aumentada de ANG-II e a infusão de ANG-II crônica resulta em uma redução dependente da dose no peso do corpo (Cassis LA, Marshall DE, Fettinger MJ, Rosenblut B, Lodder LA. "Mechanisms that contribute to angiotensin II regulation of body weight". Am. J. Physiol. Endocrinol. Metab. 1998; 274:E867-E876) . . Em pacientes hipertensivos humanos obesos, a ANG- II aumenta nos adipócitos e pode ser um fator que contribui com o desenvolvimento da resistência à insulina. Isto pode ser agravado pela inibição do recrutamento de pré-adipócitos, que resulta na redistribuição da gordura ao fígado e ao músculo esqueletal. Por essa razão, a inibição de ACE pode ter o potencial no retardamento do desenvolvimento de diabetes tipo 2 e papéis patofisiológicos do sistema receptor de renina-angiotensina de tecido adiposo na síndrome metabólica (Engeli S, Schling P, Gorzelniak K, Boschmann M, Janke J, Ailhaud G, Teboul M, Massiera F, Sharma AM. "The adipose tissue renin-angiotensin-aldosterone system: role in metabolic syndrome". The International Journal of Biochemistry & Cell Biology 2003; 35:807-825).
No entanto, nenhum desses estudos descreve um método para mudar a composição da massa do corpo, por exemplo, uma massa de gordura reduzida e uma massa de músculo magro aumentada. O aumento da massa magra do corpo não é associado necessariamente com uma perda de peso. Desse modo, ainda existe uma necessidade a tal método para ajudar os indivíduos que sofrem de caquexia.
Bioativos lácteos, leucina, peptídeos inibidores de ACE e outros aminoácidos de cadeia ramificada
Os bioativos do leite, a leucina e outros aminoácidos de cadeia ramificada são inibidores de enzima de conversão de angiotensina (ACE) naturais. Os peptídeos inibidores de ACE podem ser liberados pela proteólise de proteínas do leite pelas bactérias do ácido láctico durante a maturação do queijo. Eles também podem ser isolados do leite e do soro de leite coalhado durante a fermentação (Fitzgerald RJ, Murray BA. "Bioactive Peptides and lactic fermentations". International Journal of Dairy Technologie 2006; 59(2):118- 125) . Os peptídeos lácteos inibidores de ACE têm valores de IC50 > 520 |im, e quantidades suficientes podem ser aplicadas através de leites fermentados e extratos de produtos de laticínio fermentados. Embora a redução de peso tenha sido proposta mediante a utilização de produtos de laticínio (Zemel MB et al. "Dairy augmentation of total and central fat loss in obese subjects". Int. J. Obes. Relat. Metab. Disord, 2005; 29 (4) : 391-7) , o papel no gerenciamento do peso foi questionado recentemente (Gunter CW et al. "Dairy products do not lead to alterations in body weight or fat mass in Young women in a 1-y intervention". Am. J. Clin. Nutr. 2005; 81:751-756).
Obesidade
Um método para aumentar a proporção da massa magra do corpo também pode ser útil para o tratamento de indivíduos que sofrem de obesidade.
Cada pessoa tem e necessita de tecido gordo em seu corpo. Quando há gordura em demasia no corpo, o resultado é a obesidade. Há aproximadamente 300 milhões de adultos obesos, de acordo com a Organização Mundial da Saúde, e 1,1 bilhão de pessoas acima do peso em todo o mundo.
O número de americanos acima do peso e obesos continuou a aumentar desde 1960, uma tendência que não está desacelerando. Mais da metade dos adultos dos Estados Unidos está acima do peso (64,5 por cento) e quase um terço (30,5 por cento) são obesos. A cada ano, a obesidade causa pelo menos 300.000 mortes adicionais nos Estados Unidos, e os custos de cuidados com a saúde de adultos norte-americanos com obesidade atingem aproximadamente $100 bilhões. É a segunda causa principal de morte que pode ser prevenida depois do fumo.
A obesidade aumenta o risco de uma pessoa desenvolver condições tais como a pressão sangüínea elevada, diabetes (tipo 2) , doenças do coração, acidente vascular cardíaco, doença da bexiga e câncer de mama, da próstata e do cólon. A tendência para a obesidade é promovida pelo nosso ambiente: falta de atividade física combinada com alimentos de baixo custo e elevado teor de calorias. Se for mantida, até mesmo perdas de peso tão pequenas quanto 10 por cento do peso do corpo podem melhorar a saúde de uma pessoa.
Ser obeso e estar acima do peso não são a mesma condição. A sua balança do banheiro pode mostrar uma medida do seu peso e ajudar a acompanhar as mudanças no seu peso, mas não é a melhor maneira para determinar se você está acima do peso ou obeso, ou com o risco de desenvolver a obesidade e suas condições de saúde correlatas.
A fim de determinar se uma pessoa é obesa, o índice de massa do corpo (BMI) e a circunferência da cintura são necessários. Você pode ter um BMI que indique que você tem um peso saudável, mas ainda pode ter uma medida da cintura acima da faixa saudável. . BMI: é um número baseado na altura e no peso. Ele pode ajudar a determinar o grau em que uma pessoa pode estar acima do peso e dar uma avaliação razoável da gordura total do corpo para a população em geral. O BMI se correlaciona melhor com as condições de saúde tais como doenças do coração e diabetes tipo 2 do que o próprio peso. O BMI não ê perfeito. Algumas pessoas, tais como atletas, podem medir um BMI elevado mas terem mais músculos do que gordura. Os ’'pontos de corte" do BMI são números utilizados para ajudar a determinar se você está com um peso saudável, acima do peso, obeso ou seriamente obeso. É importante observar que o BMI é diferente para tabelas de Saúde/Peso. . 18,5 a 24,9 = peso saudável . 25 a 29,9 = peso excessivo . 30 a 34,9 = obesidade (classe 1) . 35 a 39,9 = obesidade (classe 2) . 40 ou mais = obesidade grave (classe 3) A medida da circunferência da cintura é utilizada para determinar os riscos de saúde relacionados especificamente à gordura abdominal. . Para Homens: 40 polegadas ou mais . Para Mulheres: 35 polegadas ou mais Se a sua medida da cintura for maior do que aquela listada acima, e se o seu BMI estiver entre 25 e 34,9, você tem um risco aumentado de desenvolver diabetes tipo 2, hipertensão e doença cardiovascular.
Causas da obesidade
Há muitos fatores que contribuem com a causa da obesidade, incluindo a genética, o ambiente e o comportamento.
Genes: Alguns indivíduos têm uma tendência genética de ganhar peso e de armazenar gordura. Embora nem todas as pessoas com essa tendência fiquem obesas, algumas pessoas sem predisposição genética ficam obesas. Vários genes foram identificados como contribuintes da obesidade, e os pesquisadores estão construindo um mapa humano do gene da obesidade para identificar alvos genéticos nos seres humanos que pode conduzir ao desenvolvimento de novos tratamentos. . Ambiente: Um ambiente que promove o peso saudável é aquele que incentiva o consumo de alimentos nutritivos em porções razoáveis e atividade física regular. Um ambiente saudável é importante para todos os indivíduos para a prevenção e o tratamento da obesidade e manter a perda do peso. A identificação e a prevenção consciente de situações de alto risco no ambiente podem ajudar nos esforços de controle do peso. . Comportamento: A adoção de hábitos saudáveis para o controle do peso durante toda a vida inclui a atividade física regular e a ingestão de alimentos nutritivos. As estratégias comportamentais específicas para a perda e a manutenção do peso incluem: início e acompanhamento de padrões de dieta e exercícios em uma dieta diária, ingerindo uma dieta baixa em calorias, a limitação da quantidade de calorias da gordura, o gasto de calorias rotineiramente através de exercícios, o monitoramento do peso regularmente, a proposição de objetivos realistas, e o desenvolvimento de uma rede de suporte social.
O número de pessoas obesas no mundo está aumentando apesar do conhecimento acima. Desse modo, existe uma necessidade quanto a métodos para modificar a distribuição da massa do corpo.
Descrição Resumida da Invenção
Surpreendentemente, foi verificado que alguns compostos irão alterar o processamento dos alimentos pelo corpo até uma extensão tal que a distribuição da massa do corpo total é alterada. Particularmente, a adição desses compostos ao alimento resulta em uma proporção aumentada da massa magra em relação à massa de gordura quando comparada ao consumo do mesmo alimento sem a adição desses compostos. Em outras palavras, esses compostos podem reduzir a quantidade de gordura que é produzida a partir do alimento consumido. Esses compostos que alteram a massa do corpo incluem polifenóis e bioativos do leite.
Também foi verificado que os flavonóides e os polifenóis podem ter uma atividade inibidora de ACE. Sem desejar ficar limitado pela teoria, acredita-se que a atividade de inibição de ACE está relacionada com a capacidade desses compostos de alterar a composição da massa do corpo. No entanto, é reconhecido que a capacidade desses compostos de alterar a composição da massa do corpo também pode estar relacionada com as propriedades antioxidantes (isto é, polifenóis) e/ou os efeitos de influxo de cálcio (isto é, proteínas do leite).
De acordo com um primeiro aspecto da invenção é apresentado um método para alterar a distribuição da massa do corpo pela diminuição da porcentagem de gordura total e/ou pelo aumento da proporção da massa magra em relação à massa de gordura, o qual compreende a administração a um indivíduo de uma quantidade eficaz de um ou mais compostos que têm pelo menos um grupo hidroxila e a capacidade de alterar a composição da massa do corpo, ou um derivado ou um pró- medicamento fisiologicamente aceitável dos mesmos. O primeiro aspecto da invenção também apresenta um método que compreende a administração a um indivíduo de uma formulação terapêutica que compreende uma quantidade eficaz de um ou mais compostos que têm pelo menos um grupo hidroxila e a capacidade de alterar a composição da massa do corpo, ou um derivado ou um pró-medicamento fisiologicamente aceitável dos mesmos e um veículo aceitável.
O primeiro aspecto da invenção também apresenta uma formulação terapêutica quando utilizada para alterar a distribuição da massa do corpo pela diminuição da porcentagem de gordura total e/ou pelo aumento da proporção da massa magra em relação à massa de gordura, a qual compreende uma quantidade eficaz de um ou mais compostos que têm pelo menos um grupo hidroxila e a capacidade de alterar a composição da massa do corpo ou um análogo fisiologicamente aceitável, o derivado ou pró-medicamento dos mesmos e um veículo aceitável.
O primeiro aspecto da invenção também apresenta o uso de uma quantidade eficaz de um ou mais compostos que têm pelo menos um grupo hidroxila e a capacidade de alterar a composição da massa do corpo ou um análogo, um derivado ou um pró-medicamento fisiologicamente aceitável dos mesmos conjuntamente com um veículo apropriado na manufatura de um medicamento para alterar a distribuição da massa do corpo pela diminuição da porcentagem de gordura total e/ou pelo aumento da proporção da massa magra em relação à massa de gordura.
Neste relatório descritivo, a expressão "compostos que têm pelo menos um grupo hidroxila e a capacidade de alterar a composição da massa do corpo"refere-se a qualquer composto que contém um grupo hidroxila que altera a composição da massa do corpo pela diminuição da porcentagem de gordura e/ou pelo aumento da proporção da massa magra em relação à massa de gordura. Os compostos podem ser extraídos naturalmente de animais ou de plantas ou podem ser manufaturados sinteticamente. Um exemplo de uma fonte animal é o veneno de serpente que contem peptídeos. Os exemplos de fontes de plantas incluem polifenóis do chá verde, do vinho, do cacau, da cana de açúcar, da beterraba, dos produtos residuais da cana de açúcar e da beterraba, do melaço e de ervas chinesas tais como Magnolia, liliflora e Magnolia officinalis.Outros exemplos de tais compostos incluem (i) flavonóides tais como anticianinas, catequinas, polifenóis, chalconas, flavonóis, flavonas e (ii) polipeptídeos, leucina e outros aminoácidos de cadeia ramificada e bioativos lácteos tais como extratos de soro de leite coalhado. De preferência, o composto que tem pelo menos um grupo hidroxila e a capacidade de alterar a composição da massa do corpo é selecionado do grupo que consiste em flavonóides, polifenóis, proteínas do leite, peptídeos inibidores de ACE, melaço, extratos de melaço, açúcares de elevado teor fenólico, e as misturas destes.
De acordo com um segundo aspecto da invenção, é apresentado um método para alterar a distribuição da massa do corpo pela diminuição da porcentagem de gordura total e/ou pelo aumento da proporção da massa magra em relação à massa de gordura, o qual compreende a administração a um indivíduo de uma quantidade eficaz de um ou mais compostos que têm a atividade de inibir ACE, ou um derivado ou um pró-medicamento fisiologicamente aceitável dos mesmos.
O segundo aspecto da invenção também apresenta um método que compreende a administração a um indivíduo de uma formulação terapêutica que compreende uma quantidade eficaz de um ou mais compostos que têm a atividade de inibição de ACE, ou um derivado ou um pró-medicamento fisiologicamente aceitável dos mesmos e um veículo aceitável.
O segundo aspecto da invenção também apresenta uma formulação terapêutica quando utilizada para alterar a distribuição da massa do corpo pela diminuição da porcentagem de gordura total e/ou pelo aumento da proporção da massa magra em relação à massa de gordura, o qual compreende uma quantidade eficaz de um ou mais compostos que têm a atividade de inibição de ACE, ou um análogo, derivado ou pró- medicamento fisiologicamente aceitável dos mesmos e um veículo aceitável.
O segundo aspecto da invenção também apresenta o uso de uma quantidade eficaz de um ou mais compostos que têm a atividade de inibição de ACE ou um análogo, um derivado ou um pró-medicamento fisiologicamente aceitável dos mesmos conjuntamente com um veículo apropriado na manufatura de um medicamento para alterar a distribuição da massa do corpo pela diminuição da porcentagem de gordura total e/ou pelo aumento da proporção da massa magra em relação ã massa de gordura.
Neste relatório descritivo, a expressão "compostos que têm a atividade de inibição de ACE"refere-se a qualquer composto que tem propriedades de inibição de ACE e a capacidade de alterar a composição da massa do corpo pela diminuição da porcentagem de gordura total e/ou pelo aumento da proporção da massa magra em relação à massa de gordura. Os compostos podem ser extraídos naturalmente de animais ou de plantas ou podem ser manufaturados sinteticamente. Um exemplo de uma fonte animal é o veneno de serpente que contém peptídeos. Os exemplos de fontes de plantas incluem polifenóis de cacau, da cana de açúcar, da beterraba, dos produtos residuais da cana de açúcar e da beterraba, melaço, uvas, vinho, frutas (bagas, drupas, pomos, frutas tropicais, sucos), vegetais (bulbos, raízes, túberos, folhas, hastes), ervas, temperos, favas, leguminosas, grãos (cevada, trigo mourisco, milho, painço, aveia, arroz, centeio, sorgo, trigo), castanhas (amêndoas, noz de areca, castanha de caju, avelãs, amendoins, noz pecan, nozes), sementes oleaginosas, óleos de plantas, chá, café, cerveja, cidra, sementes, chá verde, ervas chinesas tais como Magnolia liliflora e Magnolia officinalis,e as misturas destes. Outros exemplos de tais compostos incluem (i) flavonóides tais como anticianinas, catequinas, polifenóis, chalconas, flavonóis, flavonas e (ii) polipeptídeos, leucina e outros aminoácidos de cadeia ramificada e bioativos lácteos tais como extratos do soro de leite coalhado. De preferência, o composto que tem propriedades de inibição de ACE é selecionado do grupo que consiste em flavonóides, polifenóis, proteínas do leite, cacau, produtos de cacau, extratos de cacau, extratos de uva, melaço, extratos de melaço, açúcar de elevado teor fenólico, e as misturas destes.
De acordo com um terceiro aspecto da invenção, é apresentado um método para alterar a distribuição da massa do corpo pela diminuição da porcentagem de gordura total e/ou pelo aumento da proporção da massa magra em relação à massa de gordura, o qual compreende a administração a um indivíduo de uma quantidade eficaz de um ou mais polifenóis, ou um derivado ou um pró-medicamento fisiologicamente aceitável dos mesmos.
O terceiro aspecto da invenção também apresenta um método que compreende a administração a um indivíduo de uma formulação terapêutica que compreende uma quantidade eficaz de um ou mais polifenóis ou um derivado ou um pró-medicamento fisiologicamente aceitável dos mesmos e um veículo aceitável.
O terceiro aspecto da invenção também apresenta uma formulação terapêutica quando utilizada para alterar a distribuição da massa do corpo pela diminuição da porcentagem de gordura total e/ou pelo aumento da proporção da massa magra em relação à massa de gordura, o qual compreende uma quantidade eficaz de um ou mais polifenóis ou um análogo, derivado ou pró-medicamento fisiologicamente aceitável dos mesmos e um veículo aceitável.
O terceiro aspecto da invenção também apresenta o uso de uma quantidade eficaz de um ou mais polifenóis ou um análogo, um derivado ou um pró-medicamento fisiologicamente aceitável dos mesmos conjuntamente com um veículo apropriado na manufatura de um medicamento para alterar a distribuição da massa do corpo pela diminuição da porcentagem de gordura total e/ou pelo aumento da proporção da massa magra em relação à massa de gordura.
Neste relatório descritivo, a expressão "polifenóis” refere-se a todos os polifenóis extraídos ou derivados do cacau, da cana de açúcar, da beterraba, de produtos residuais da cana de açúcar e da beterraba, melaço, uvas, vinho, frutas (bagas, drupas, pomos, frutas tropicais, sucos), vegetais (bulbos, raízes, túberos, folhas, hastes), ervas, temperos, favas, leguminosas, grãos (cevada, trigo mourisco, milho, painço, aveia, arroz, centeio, sorgo, trigo), castanhas (amêndoas, noz de areca, castanha de caju, avelãs, amendoins, noz pecan, nozes), sementes oleaginosas, óleos de plantas, chá, café, cerveja, cidra, sementes, chá verde, ervas chinesas tais como Magnolia, liliflora e Magnolia officinalis, e as misturas destes. De preferência, o polifenol é extraído do melaço, de extratos de melaço, de açúcar de elevado teor fenólico, e das misturas destes. De preferência, os polifenóis têm uma alta atividade antioxidante.
De acordo com um quarto aspecto da invenção, é apresentado um método para alterar a distribuição da massa do corpo pela diminuição da porcentagem de gordura total e/ou pelo aumento da proporção da massa magra em relação à massa de gordura, o qual compreende administrando a um indivíduo de uma quantidade eficaz de melaço ou um extrato do mesmo.
O quarto aspecto da invenção também apresenta um método que compreende a administração a um indivíduo de uma formulação terapêutica que compreende uma quantidade eficaz de melaço ou um extrato do mesmo e um veículo aceitável.
O quarto aspecto da invenção também apresenta uma formulação terapêutica quando utilizada para alterar a distribuição da massa do corpo pela diminuição da porcentagem de gordura total e/ou pelo aumento da proporção da massa magra em relação à massa de gordura, a qual compreende uma quantidade eficaz de melaço ou um extrato do mesmo e um veículo aceitável.
O quarto aspecto da invenção também apresenta o uso de uma quantidade eficaz de melaço ou um extrato do mesmo conjuntamente com um veículo apropriado na manufatura de um medicamento para alterar a distribuição da massa do corpo pela diminuição da porcentagem de gordura total e/ou pelo aumento da proporção da massa magra em relação à massa de gordura.
A expressão "uma quantidade eficaz" é aqui empregada para se referir a uma quantidade que é suficiente para alterar a distribuição da massa do corpo mediante o aumento da massa magra ou a diminuição da massa de gordura. A proporção da massa magra em relação à massa de gordura é aumentada quando a quantidade de massa magra de um indivíduo aumenta ou a quantidade de massa de gordura do indivíduo diminui. Deve ser observado que uma mudança na proporção da massa magra em relação à massa de gordura envolve necessariamente uma mudança no peso total. Um exemplo de uma quantidade eficaz para animais é de 1 a 2% da dieta. Supondo que um ser humano consome normalmente 1.000 g de alimento por dia e o consumo normal de polifenóis é de 1 g/dia, a quantidade eficaz deve provavelmente ficar na faixa de 2 a 20 mg/dia, e com mais preferência de 2 a 10 g/dia.
A capacidade de um composto de diminuir o aumento da porcentagem de gordura e/ou a proporção da massa magra em relação à massa de gordura pode ser testada utilizando a experiência com camundongos discutido nos exemplos. Se uma mudança estatisticamente significativa for obtida quando comparada ao controle, então o composto pode ser utilizado na invenção. Um resultado típico na experiência com camundongos é uma diminuição na porcentagem de gordura de 8 para 12% ou um aumento na proporção da massa magra em relação à massa de gordura de 4 para 7%. Para os seres humanos que sofrem de caquexia, um aumento na proporção da massa magra em relação à massa de gordura de pelo menos 1 a 2% deve ser ideal.
A expressão "formulação terapêutica" é um termo amplo que inclui preparados farmacêuticos enterais e parenterais, nutracêuticos, suplementos, alimentos funcionais e preparados de ervas. Os exemplos de formulações apropriadas incluem comprimidos, pós, comprimidos mastigáveis, cápsulas, suspensões orais, suspensões, emulsões ou fluidos, formulações para crianças, alimentos enterais, nutracêuticos, supositórios, sprays nasais, bebidas e produtos alimentícios. O veículo pode conter quaisquer excipientes apropriados, tais como o amido ou aglutinantes poliméricos, adoçantes, agentes corantes, emulsificantes e revestimentos. De preferência, o veículo é um produto alimentício ou um ingrediente de alimento, tal como açúcar ou chocolate.
A formulação terapêutica pode estar em qualquer forma apropriada para a administração ao indivíduo. A formulação terapêutica pode ser administrada topicamente, oralmente ou por qualquer outra via de administração.
O termo "indivíduo", tal como aqui empregado, refere-se a um animal. Não há nenhuma limitação quanto ao tipo de animal que poderia se beneficiar das formulações e dos métodos atualmente descritos. De preferência, o indivíduo é um mamífero, e com mais preferência um ser humano. Um "animal" também inclui a espécie de animais domésticos, tais como bois, cavalos, carneiros, porcos, cabras, asnos e aves domésticas, tais como galinhas, patos, perus e gansos, ou animais domésticos tais como gatos e cães. Um indivíduo, independente do fato de se tratar de um ser humano ou um animal não-humano, também pode ser mencionado como um indivíduo, animal, paciente, hospedeiro ou receptor. As formulações e os métodos da presente invenção têm aplicações na medicina humana, nas indústrias de cosméticos e estética, na medicina veterinária, bem como na pecuária geral, de animais domésticos e selvagem.
Desenhos
Várias realizações/aspectos da invenção serão descritas agora com referência aos seguintes desenhos, nos quais (os asteriscos destacam diferenças significativas):
A Figura 1 mostra o método de extração utilizado no Exemplo 4.
A Figura 2 mostra os resultados do Teor Mineral no Osso do Exemplo 6.
A Figura 3 mostra os resultados da Massa de Músculo Magro do Exemplo 6.
A Figura 4 mostra os resultados da Massa de Gordura do Exemplo 6.
A Figura 5 mostra os resultados da Porcentagem de Gordura do Exemplo 6.
A Figura 6 mostra o Peso Total do Corpo por resultados de DEXA do Exemplo 6.
A Figura 7 mostra os resultados do Peso Total do Corpo do Exemplo 6.
A Figura 8 mostra o peso do corpo no momento dos resultados da carga de glicose para o Exemplo 8.
A Figura 9 mostra o peso do corpo no momento da análise DEXA para o Exemplo 8.
A Figura 10 mostra a porcentagem de massa de gordura no momento da análise DEXA para o Exemplo 8.
A Figura 11 mostra a massa de gordura em gramas no momento da análise DEXA para o Exemplo 8.
A Figura 12 mostra a massa magra em gramas no momento da análise DEXA para o Exemplo 8.
A Figura 13 mostra os resultados da glicose no sangue para o Exemplo 8.
A Figura 14 mostra os resultados da ingestão de alimento para o Exemplo 8.
A Figura 15 mostra os resultados da ingestão de fluido para o Exemplo 8.
A Figura 16 mostra os resultados da oxidação da gordura no fígado para o Exemplo 8.
A Figura 17 mostra o peso do corpo (A), a proporção da gordura do corpo (B) e a proporção da massa magra (C) em camundongos ACE +/+ (barras vazias) e ACE -/- (barras cheias). Os valores são a média + SEM (n = 7 por grupo), * p < 0,05;** p < 0,01; *** p < 0,001.
A Figura 18 mostra a ingestão de alimento (A) e de água (B) em camundongos ACE +/+ (barras vazias) e ACE -/- (barras cheias) . Os valores são a média + SEM (n = 7 por grupo), *** p < 0,001.
A Figura 19 mostra as imagens MRI axiais ponderadas de densidade de prótons através do corpo de camundongos ACE +/+ (A) e ACE -/- (B). As áreas brancas brilhantes denotam a gordura. Cada série de imagens representa os dados de um único animal. A cabeça da seta branca indica a gordura andróide.
A Figura 20 mostra a temperatura retal (A) , a atividade de roda de girar espontânea (a distância percorrida por dia (B) , a velocidade (C) e a proporção de gordura na matéria fecal (D) em camundongos ACE +/ + (barras vazias) e ACE -/- (barras cheias). Os valores são a média ± SEM (n = 5 por grupo para a temperatura retal, medições da atividade de roda de girar espontânea. ACE (-/-): n = 6 e ACE (+/+): n = 7 para a análise de gordura fecal).
Exemplos
Várias realizações da invenção serão descritas agora com referência aos seguintes exemplos não-limitadores.
Exemplo 1
Este exemplo compara o teor fenólico e as atividades antioxidantes de pós fenólicos que podem ser utilizados nos métodos da invenção.
Métodos
O teor fenólico e as atividades antioxidantes de três pós fenólicos, o pó fenólico de melaço produzido na TFT (International Food Technology Company), o pó fenólico de Extrato de Uva HW 65-10 da Hansen, e o pó de extrato de semente de uva Vinlife™, foram comparados. Os pós foram dissolvidos em metanol a 80% a uma concentração de 5 mg/ml. Uma diluição adicional com água foi requerida para obter as concentrações apropriadas para os respectivos ensaios. Os resultados desses ensaios são mostrados na Tabela 1 (abaixo).
Resultados
Os dados na Tabela 1 permitem que a eficiência antioxidante relativa dos pós seja comparada. A Tabela 2 mostra as atividades específicas dos três pós, ou seja, o número de unidades antioxidantes por unidade fenólica. Tabela 1: Teor fenólico e atividade antioxidante de três pós fenólicos
Tabela 2: Atividade antioxidante específica de três pós fenólicos
Esses resultados mostram que o pó de melaço tem um teor mais baixo de fenólicos do que os outros dois pós, e uma atividade antioxidante específica mais baixa. Isto é provavelmente devido às diferenças nos perfis fenólicos entre os vários pós. A análise de HPLC sugere que o pó de melaço não contém muitos dos ácidos fenólicos simples, tal como o ácido gálico, que são antioxidantes muito poderosos. Esses compostos parecem ser insuficientemente hidrofóbicos para se ligarem à resina XAD 16. No entanto, métodos diferentes de extração devem provavelmente ter a capacidade de extrair tais compostos hidrofílicos menores e eles podem ser incluídos em um extrato de melaço para ser utilizado em um método de acordo com a invenção.
Exemplo 2
Este exemplo investiga a capacidade antioxidante em chocolate fortificado com fenólicos em comparação ao chocolate não-fortifiçado.
Método
A capacidade antioxidante de seis pedaços de chocolate ao leite de controle (1 pedaço de cada fileira de um bloco de aproximadamente 100 g) e 12 pedaços de chocolate ao leite fortificado com fenólicos (2 pedaços de cada fileira alternando primeira e terceira, segunda e quarta) foram escolhidos para o ensaio. O chocolate ao leite foi fornecido pela Cool Health Pty Ltd. Uma amostra de cada um, pesando entre 1,7 e 2 g, foi pesada com precisão e adicionada a um tubo de 50 ml. As amostras de chocolate foram desengorduradas mediante a adição de 20 ml de heptano. As amostras foram centrifugadas e o heptano foi decantado. As amostras foram deixadas abertas em uma coifa para remover os resquícios de heptano. Os antioxidantes foram extraídos utilizando alíquotas de 2 x 20 ml de metanol a 8 0%, em primeiro lugar uma extração de duas horas e em segundo lugar uma extração durante toda a noite. Os extratos primário e secundário foram adicionados conjuntamente e ensaiados em duplicata utilizando o método da ABTS após uma diluição de cinco vezes em água. Resultados Tabela 3: Capacidade antioxidante no chocolate

A capacidade antioxidante do chocolate de controle era de 1,587 ± 0,039 mg de catequina equivalentes por grama (média ± desvio padrão). A capacidade antioxidante do chocolate fortificado com fenólicos era de 1,961 ± 0,142 mg de catequina equivalentes por grama. Isto representa um aumento de 21,2% em comparação com o chocolate de controle. É desse modo possível que uma quantidade eficaz de polifenóis seja adicionada e distribuída uniformemente em uma matriz de chocolate para produzir uma formulação apropriada para ser utilizada nos métodos de acordo com a invenção.
Exemplo 3
Este exemplo investigou o teor de polifenol dos extratos de vários produtos de cana de açúcar em estágios diferentes no processo de refino do açúcar. Foi feita uma avaliação de equivalentes de catequina do primeiro suco expresso, suco final, xarope, melaço, açúcar de baixo teor de polifenol, lama de moinho, talos de cana e espuma. Resultados Tabela 4: Potencial antioxidante de vários extratos de canade açúcar
Tabela 5: Potencial antioxidante de extratos de cana de açúcar versus outras fontes do polifenol
A análise revelou que os extratos de melaço e de lama de moinho contêm uma quantidade significativa de polifenóis e, desse modo, poderiam ser adicionados a uma formulação apropriada para ser utilizada nos métodos de 10 acordo com a invenção.
Exemplo 4
Este exemplo demonstra a obtenção de um produto de açúcar que contém polifenóis que pode ser utilizado em uma formulação para ser utilizada em um método de acordo com a 15 invenção.
O fluxograma na Figura 1 ilustra o processo utilizado para produzir um extrato de melaço de cana de açúcar de elevado teor de polifenóis. A extração do melaço de cana de açúcar é discutida mais detalhadamente no pedido de patente internacional número 2005/117608.
Uma base de sacarose de elevado teor de polifenol foi preparada, a qual compreendia 99% total de sacarose, glicose e frutose (em que a quantidade de glicose e frutose não era não maior do que 0,5%) e 1% de uma mistura de ácidos orgânicos, minerais, polifenóis, antioxidantes e polissacarídeos. Essa mistura consistia no seguinte: . 600 a 2.100 microgramas por grama de uma mistura de ácido trans-acotínico e ácidos oxálico, cis-acotínico, cítrico, fosfórico, glucônico, málico, succínico, láctico, fórmico e acético, em que a maior parte da mistura consistia em ácido trans-acotínico em uma quantidade na faixa de 200 a 600 microgramas por grama; . 15 0 a 600 microgramas por grama de minerais em que a relação entre cálcio, magnésio e potássio é de 50:15:35; 0,2 a 0,5 equivalente de mg de catequina por grama de polifenóis; antioxidantes, de modo que a atividade antioxidante se encontra na faixa de 0,4 a 1,2 micromoles por grama; e . 20 a 60 microgramas por grama de polissacarídeos.
Um adoçante de elevado teor de fenólicos foi preparado ao combinando a base de sacarose de elevado teor de polifenóis com o extrato de elevado teor de polifenóis obtido acima.
A Espectrometria de Massa de Eletroaspersão (ES/MS) foi realizada em uma Plataforma de Micromassa ES/MS. As amostras foram dissolvidas em Metanol/Água (80:20) e injetadas em um circuito de 20 pl e eluídas com metanol/água (80:20) a 20 nl/min. A análise de MS foi realizada no modo de ions negativos com uma voltagem de cone de 4 0 kV e uma faixa de massa de 50-700 Da.
O produto de açúcar continha uma quantidade significativa de polifenóis e, desse modo, pode ser adicionada a uma formulação apropriada para ser utilizada nos métodos de acordo com a invenção.
Exemplo 5
Este exemplo demonstra a obtenção de um produto comercial de chocolate que contém polifenóis que pode ser utilizado no método de acordo com a invenção.
Infusão de passas de Corinto
Mistura da Infusãot A seguinte mistura (25 litros) foi suficiente para a infusão de 125 kg de passas de Corinto que é suficiente para 1.000 kg de chocolate. . 20 litros de vinho, por exemplo Shiraz, Merlot ou Pinot Noir) . 5 litros de extrato de casca/semente de uva . 125 ml de flavorizante
Misturar bem os ingredientes acima em um vaso grande à temperatura ambiente. Agitar lentamente para se assegurar que o extrato de casca/semente de uva e o flavorizante fiquem bem misturados com o vinho.
O flavorizante pode ser qualquer sabor natural ou sintético, dependendo da nota e do perfil específicos desejados no chocolate final. O sabor pode ter um ingrediente alcoólico, monossacarídeo, polissacarídeo, polidextrose, uma polidextrina, dextrina, poliol, amido, propileno glicol, óleo óleo vegetal, triglicerídeo ou uma outra base/veículo apropriado.
Uma mistura de infusão não-alcoólica também pode ser utilizada se for requerido ao substituir a variedade de vinho por uma variedade desalcoolizada não-alcoólica. Além disso, uma gama de flavorizantes não-alcoólicos ou desalcoolizados também pode ser adicionada à mistura de infusão para melhorar o sabor e a capacidade de distribuição das passas de Corinto no chocolate.
Infusão das passas de Corinto: Combinar as passas de Corinto 5 e a mistura de infusão em um vaso que pode ser girado para misturar completamente o conteúdo. Girar o vaso regularmente pelas 24 horas seguintes. Filtrar/peneirar qualquer excesso de líquido e espalhar as passas de Corinto em infusão em uma estante de secagem e colocar em uma sala quente (40°C) com ar 10 fluindo através das passas de Corinto durante toda a noite. Preparação de chocolate que contém pó de semente de uva e flavorizante Receita de Chocolate Base (por 500 kg (batelada de 0,5 t)):
Adicionar para formar as conchas na seqüência I 15 correta e formar as conchas por 12-16 horas a 40°C até que o tamanho médio de partícula do chocolate atinja menos de 20 JLI (faixa de 18 jul ~ 2 0pi) . Ao chocolate foi então aplicado um flavorizante, tal como um dentre shiraz, pinot ou merlot. O chocolate tem uma razão entre gordura do leite e manteiga de 20 cacau de 0,13.
O sabor de vinho varietal real no chocolate pode ser realçado mediante a adição de uma gama de flavorizantes que não somente realçam o sabor mas servem para reduzir o amargor quando quantidades maiores do que as usuais de 25 polifenóis são adicionadas para promover saúde. Um elemento versado na técnica da química de flavorizantes saberá qual mistura de flavorizantes pode ser utilizada para melhorar a palatabilidade, a sensação na boca e outras propriedades organoléticas.
Preparação do pó de semente (para uma batelada de 0,5 tonelada de chocolate): Pesar 2,25 kg de pó de semente de uva Vinlife (Tarac Technologies) e adicionar a 5 kg de manteiga de cacau derretida (45°C). Adicionar lentamente com agitação e se assegurar que o pó seja disperso uniformemente por toda a manteiga de cacau. Evitar a incorporação de ar enquanto estiver misturando, mas se assegurar que o pó fique bem disperso na manteiga de cacau.
Adição do Pó de Semente ao Chocolate: A 0,5 tonelada (500 kg) de chocolate com flavorizante de vinho mantido em um tanque de contenção a 40 - 45 °C, adicionar os 5 kg de manteiga de cacau que contém o pó de semente disperso. Adicionar lentamente e misturar no tanque por cinco minutos ou até ficar disperso uniformemente.
Adição de Passas de Corinto em Infusão ao Chocolate
As passas de Corinto filtradas e drenadas (aproximadamente 5,5 - 5,8 kg) foram misturadas com 40 kg de chocolate flavorizado e moderado. A mistura deve ser bem misturada para assegurar uma distribuição uniforme das passas de Corinto.
A mistura de passas de Corinto/chocolate é então moldada e resfriada.
Ao utilizar passas de Corinto secas ou fruta em infusão com vinho e polifenóis solúveis em água dispersos em manteiga de cacau, as dificuldades experimentadas tipicamente com a adição a alimentos tais como o chocolate podem ser superadas. O sabor pode ser melhorado ainda mais ao utilizar flavorizantes de vinho e um produto singularmente palatável pode ser produzido com um teor incrementado de polif enol, antioxidante e uma atividade inibidora de ACE para ser utilizado nos métodos de acordo com a invenção.
Exemplo 6
Neste exemplo, polifenóis de açúcar ou o extrato de melaço do Exemplo 4 foram testados para determinar o efeito na distribuição da massa do corpo de camundongos.
Método
Nesta experiência, camundongos C57B1/6J com seis semanas de idade livres de doenças (n = 65) foram utilizados. Os camundongos foram adquiridos no Animal Resource Centre, Canning Vale, WA, Austrália.
Vários dias depois da chegada na casa dos animais, os camundongos foram passados de sua dieta de ração normal (3% de gordura) para uma dieta de elevado teor de carboidratos e elevado teor de gordura (21% de gordura, 20% de proteína, 49% de carboidratos, 5% de celulose, 5% de vitaminas e sais minerais). As dietas foram formuladas especialmente pela Specialty Feeds, Glen Forrest, WA, Austrália. Todos os animais foram abrigados em dois por grupo a 19-21°C com um ciclo lu-escuridão de 12:12.
Três grupos de camundongos (n = 13 camundongos por grupo) foram mantidos na dieta de elevado teor de carboidratos e elevado teor de gordura que contém (1) 1% de pó contendo polifenol; (2) 2% de pó contendo polifenol; (3) melaço; (4) 1% de sacarose (controle). As dietas utilizadas neste exemplo foram feitas ao combinar 98-99% da dieta base mais 1-2% dos aditivos indicados acima. Os animais foram alimentados nas dietas por nove semanas.
Durante o período de nove semanas, as ingestões de alimento e de água e o peso do corpo foram medidos semanalmente. Na semana 9, a composição do corpo dos camundongos foi determinada utilizando Absorbiometria de Raios X de Energia Dual (DEXA).
Absorbiometria de Raios X de Energia Dual (DEXA): A composição do corpo integral de camundongos foi avaliada utilizando DEXA (Norland XR-36) equipada com o pacote de software otimizado para animais pequenos. Os camundongos foram escaneados sob leve anestesia (Ketamil e Rompun) . Um 5 modo de varredura de corpo integral foi utilizado, fornecendo informações tais como a % de gordura do corpo, o teor de mineral no osso (BMC), a densidade mineral do osso (BMD), e a massa magra. Os animais foram colocados na posição apropriada no centro e em paralelo ao eixo longo da mesa de varredura.
Resultados e Discussão
O pó de polifenol e o melaço adicionados à dieta de elevado teor de gordura, ambos a 1 e 2% (PP1%, PP2%) , diminuíram a gordura do corpo (em gramas - vide a Figura 4, ou como uma % do peso do corpo - vide a Figura 5) e 15 aumentaram a massa magra (vide a Figura 3) . O peso do corpo e o teor de mineral no osso não foram alterados de maneira significativa (Figuras 2 e 6). A DEXA foi executada após nove semanas de intervenção dietética. O peso do corpo DEXA (soma da massa magra, do osso e da gordura) foi altamente 20 correlacionado com o peso do corpo medido em um equilíbrio (r = 0,98).
Nas Figuras 2 a 7, a análise estatística pela análise de variação de uma só via e o teste post hoc de Fisher LSD subseqüente; versus o controle, * p < 0,05; **p< 25 0,01; *** p < 0,001.
Não havia nenhuma diferença na ingestão de alimento ou de água (não mostrado) . As figuras atuais não mostram que o melaço diminuiu a gordura do corpo; isto é, a % de gordura, média (SEM), controle = 36,9 (2,3), melaço = 30,2 (1,7), PP1% 30 = 26,3 (1,6), PP2% = 25,0 (2,8).
Conclusão
Os resultados demonstram claramente que o pó de polifenol mudou a composição do corpo ao aumentar de maneira significativa a massa de músculo magro e ao diminuir de maneira significativa a porcentagem de gordura. A redução média de 11,9% de gordura e o aumento de 6% na massa de músculo magro devem melhorar de maneira significativa o prognóstico para as pessoas que sofrem de obesidade, diabetes e caquexia.
Exemplo 7
Neste exemplo, o extrato de melaço do Exemplo 4 e que foi utilizado no Exemplo 6 foi testado quanto à capacidade antioxidante (ORAC) e a influência na atividade de a-glucosidase e a-amilase.
Materiais e métodos
Preparação da Amostra: As amostras foram trituradas e aproximadamente 50 mg foram solubilizados em 5 ml de metanol. As amostras foram turbilhonadas, submetidas à sonicação por trinta minutos, e centrifugadas por cinco minutos (1900 RCF). O sobrenadante foi coletado e colocado para secar. As amostras foram solubilizadas novamente em metanol a 10 mg/ml.
As amostras do pó de melaço eram diretamente solúveis em água. O pó de melaço foi solubilizado em tampão de fosfato (pH 7,4) a uma concentração de 1 mg/ml, antes do ensaio de ORAC. A amostra do pó de melaço também foi extraída tal como acima, para fornecer dados comparativos de ORAC. O pó de melaço foi solubilizado em água antes dos ensaios de a- amilase e a-glucosidase.
Ensaio de Capacidade de Absorbância Radical de Oxigênio (ORAC): O ensaio de ORAC empregado neste estudo mediu a atividade de limpeza de antioxidante na amostra de teste, contra os radicais peroxila induzida por cloridreto de 2,2’- azobis(2-amidinopropano) (AAPH) a 37°C. A fluoresceína foi utilizada como sonda fluorescente. Os valores hidrofílicos de ORAC foram determinados para as amostras.
Os extratos/amostras foram analisados utilizando o procedimento de ORAC na diluição em série (x 4) com AWA (acetona: água: ácido acético; 70:29,5:0,5), e em quadruplicata, começando com a concentração correspondente ã amostra, dependendo da capacidade antioxidante aproximada de 5 uma tela inicial. Um extrato de chá verde foi incluído como um controle positivo, e o extrato foi preparado tal como para a preparação da amostra.
A amostra do pó de melaço foi solubilizada diretamente em tampão de fosfato (pH 7,4), e analisada, com 10 exceção do fato que AWA foi substituído por tampão de fosfato (pH 7,4) . Um extrato de chá verde metanólico foi incluído como um controle positivo, e também foi solubilizado em tampão de fosfato (pH 7,4).
Trolox, um análogo solúvel em água da vitamina E, 15 foi utilizado como um padrão de referência. Uma curva padrão do trolox foi estabelecida a partir dos padrões de trolox preparados a 100, 50, 25, e 12,5 pM em AWA.
Resumidamente, 20 p 1 de amostras/ padrões/ controle/ molde (AWA), 10 pl de fluoresceína (6,0 x 10'7 M) , e 20 170 ui de AAF (20 mM) foram adicionados a cada cavidade.
Imediatamente depois do carregamento, a placa foi transferida ao leitor de placas pré-ajustado em 37°C, e a fluorescência foi medida 35 vezes a intervalos de um minuto. As leituras da fluorescência fizeram referência às cavidades sem solvente. 25 Os valores ORAC finais foram calculados utilizando uma equação de regressão entre a concentração de Trolox e a área líquida sob a curva de deterioração de fluoresceína, e expressos como equivalentes de Trolox em micromoles (TE) por g da amostra.
Ensaios de inibição de enzima de metabolismo da glicose
a-Glucosidase: A amostra do pó de melaço foi solubilizada em água antes de ser utilizada neste ensaio. Fucoidan foi incluído como um controle positivo, e também foi solubilizado em água.
A enzima glucosidase foi solubilizada em tampão de acetato (50 mM, pH 4,5) a uma concentração de 0,7 mg/ml. Isto forneceu uma concentração final de 0,2 U/ml. A uma placa de 96 cavidades, 50 |il de enzima foram adicionados a cada cavidade. Um conjunto correspondente de cavidades também foi incluído, em que o tampão de acetato foi adicionado em vez da enzima. As amostras/controles foram então adicionados às cavidades (5 |il) , em triplicata, seguidos pelo substrato 4- Nitrofenil-a-D-glucopiranoside (concentração final de 2 mM) . A placa foi coberta, agitada e incubada então a 3 7°C por trinta minutos. A reação foi interrompida com a adição de Na2CO3 0,2 M (100 pl/cavidade) . A absorbância foi medida a 405 nm, utilizando uma leitora de placas Victor2.
A absorbância das cavidades contendo a amostra, o substrato e o tampão foi subtraída das cavidades correspondentes que contêm a enzima glucosidase, e a porcentagem de inibição pelas amostras foi calculada em comparação aos controles de solvente. a-Ainilase: A amostra do pó de melaço foi solubilizada em água. Acarbose foi incluída como um controle positivo. Tabletes de Acarbose foram esmagados e solubilizados em etanol aquoso a 50% (56 mg/ml) . A solução foi submetida à sonicação e centrifugada a 2.000 RCF por dez minutos. O sobrenadante foi coletado e armazenado a 4°C.
Um kit de ensaio Enzchek Ultra Amylase foi utilizado para determinar a influência da amostra 1 na atividade de a-amilase (Molecular Probes E33651). Resumidamente, um tampão de reação lx (fornecido com o kit) foi preparado ao diluir o material de partida 1:10 com água destilada. Um frasco de substrato de amido liofilizado (amido
DQ™ do milho, conjugado BODIPY® FL) foi preparado ao adicionar 100 |il de 50 mM de acetato de sódio (pH 4,0) e em seguida 900 p,l do tampão de reação lx, seguido pela diluição vinte vezes com o tampão de reação lx. Uma solução de partida de amilase foi preparada ao solubilizar 0,5 mg/ml de cc- amilase de suínos (Sigma A3176) em água destilada. O material de partida de amilase foi diluído então com o tampão de reação lx para obter uma concentração de 125 U/ml.
O ensaio foi executado utilizando um formato de placa de 96 cavidades. 10 0 |il da solução de enzima amilase foram adicionados a cada cavidade, seguidos pelas amostras e controles (5 p,l/cavidade) . A solução do substrato foi então adicionada (95 jjl/cavidade) , e a fluorescência (excitação a 485 nm, emissão a 530 nm) foi medida utilizando uma leitora de placas Victor.
Resultados e discussão
O rendimento de cada produto é apresentado na Tabela 6. Tabela 6: Rendimento de extrato de cada amostra
Capacidade Antioxidante-, As capacidades antioxidantes das amostras, preparadas mediante a formação de extratos metanólicos, são apresentadas na Tabela 7. A amostra do pó de melaço demonstrou a maior capacidade antioxidante, com um valor de ORAC de 4395 pmol de TE/da amostra quando um extrato foi gerado ou 5.020 pmol de TE/da amostra quando dissolvido diretamente em tampão (Tabela 8) . Ambos os valores eram consideravelmente mais elevados do que o extrato de chá verde correspondente. Tabela 7: Capacidade antioxidante do pó de melaço extraído com metanol, comparado a um extrato de chá verde metanólico (os valores são a média + erro padrão da média)
Tabela 8: Capacidade antioxidante do pó de melaço solubilizado diretamente em tampão de fosfato (pH 7,4), comparado a um extrato de chá verde metanólico (os valores são a média ± erro padrão da média)
Inibição de a-Glucosidase: A amostra de pó de melaço 1 inibiu a a-glucosidase até uma extensão limitada, comparada ao controle fucoidan (Tabela 9) . Os dados deste ensaio eram problemáticos, porque a amostra do pó de melaço exibiu uma elevada absorbância base, a qual foi subtraída das cavidades correspondentes que contêm a enzima glucosidase. Isto possivelmente causou uma super-estimativa da inibição na atividade de a-glucosidase, uma vez que a inibição é calculada comparada ao controle de solvente, que tinha uma absorbância base relativamente baixa. Tabela 9: Inibição (%) de a-glucosidase pela amostra 1,comparada a fucoidan (os valores são a média + SEM)
A amostra 1 não inibiu a atividade de a-amilase, comparada ao controle, acarbose (Tabela 10). Um valor de IC5o não podia ser calculado a partir destes dados porque a amostra 1 não inibiu suficientemente a atividade de a- amilase. Um valor de IC50poderia possivelmente ser calculado se a amostra fosse testada a concentrações muito mais elevadas, mas a relevância biológica de tal concentração é questionável. Tabela 10: Inibição (%) de oc-amilase pela amostra 1 comparada à acarbose (os valores são a média + SEM)
Este exemplo claramente suporta os Exemplos 1 e 4 ao demonstrar por um outro método a para medição da capacidade antioxidante que o extrato de melaço é um potente antioxidante. 0 potência relativa do pó de melaço é tal como segue: extrato de semente de uva>estrato de uva> pó de melaço>chá verde
Produtos tais como o chá verde, o HCA (ácido hidróxi cítrico) e a insulina reivindicam os benefícios da perda de peso com base na hipótese que o consumo desses produtos irá retardar a absorção de glicose e/ou regular a insulina para controlar o apetite. O absorção de glicose é controlada pelo glucosidase e pela amilase. O extrato de melaço tem uma atividade fraca de glucosidase e, portanto, parece que as mudanças na composição do corpo devem ser por outros mecanismos de ação. É mais provável que o mecanismo envolva a inibição de ACE.
Exemplo 8
Este exemplo investiga o efeito dos polifenóis extraídos do chá na distribuição da massa do corpo.
Método
Animais e tratamentos: Ratos Sprague Dawley machos (n = 48) foram adquiridos no Animal Resource Centre (Canning Valley, WA) em três semanas de idade. Os animais foram colocados para se aclimatar por uma semana com ração de ratos Purina e água. A partir de quatro semanas de idade, a todos os animais foi administrada uma dieta semi-sintética de elevado teor de gordura (15% de gordura, Tabela 6) (Specialty Feeds, Glen Forrest, WA) e administrado um de quatro tratamentos de fluido: Chá verde, chá preto, Gaiato de Epigalocatequina (EGCG) ou água. O chá e os extratos de chá foram administrados como 100% de sua ingestão de fluido. Os ratos foram mantidos na dieta de elevado teor de gordura e no tratamento com chá até a semana 29. As ingestões de alimento e fluido foram medidas diariamente e os pesos do corpo foram registrados semanalmente. Tabela 11; Composição da dieta de elevado teor de gordura
Chá verde e chá preto: Os sacos de chá verde e chá preto (Dilmah natural green tea™ e Dilmah black tea™) foram adquiridos de umas saída de varejo locais. Dez sacos de chá (chá leaves/bag de aproximadamente 2 g) foram embebidos em 1 litro de água da torneira em ebulição em um recipiente coberto por três minutos. Os sacos de chá foram então expelidos do chá em excesso e dos preparados de chá compostos até um volume de 2 litros com água fria da torneira. Isto se aproximou de 1 saco de chá por 200 ml de água. Os preparados de chá foram feitos frescos a cada segundo dia.
Gaiato de Epigalocatequina: Gaiato de Epigalocatequina (EGCG (98%), Sapphire Bioscience, VIC) foi dissolvido em água potável e administrado em uma dose de 1 mg/kg/dia. Os preparados de EGCG foram feitos frescos diariamente.
Teste de Tolerância à Glicose: Os animais jejuaram durante toda a noite com acesso ad libituma fluido. Na manhã seguinte, os ratos foi contidos e as caudas foram imersas em anestésico local (Xilocaina) por um minuto. Um segmento pequeno foi cortado da ponta da cauda, e a cauda foi massageada da base à ponta até aparecer uma pequena quantidade de sangue. As amostras de sangue foram coletadas (microcubetas hemocue) e as amostras de glicose no sangue basais jejuadas foram tomadas (analisador de glicose no sangue Hemocue Glucostat). Uma carga oral de glicose (40% de glicose, bolus, peso do corpo de 2 g/kg) foi então aplicada por meio de gavagem e a glicose no sangue foi medida a intervalos de trinta minutos por duas horas.
Absorb!ornetri a de Baios X de Energia Dual (DEXA) : A composição do corpo foi determinada pela absorbiometria de raios X de energia dual utilizando um Absorciômetro Hologic Qdr-4000/A. Os animais foram levemente anestesiados (Nembutal, I.P., 40 mg/kg) e colocados na posição supina na plataforma de varredura. As caudas foram presas com fita no lugar e uma varredura do corpo inteiro foi feita. A massa da gordura, magra e total foi medida, juntamente com a relação da porcentagem de gordura e o teor de minerais no osso. A massa total tal como medida por DEXA foi altamente 5 correlacionada com a massa medida ao pesar o animal (r = 0,99) •
Análise estatística: Os resultados do teste de tolerância à glicose foram comparados empregando a análise de variação de duas vias (medidas repetidas) e uma análise de variação de 10 uma via foi empregada para comparar os resultados de DEXA e de insulina no plasma. Ambas as análises foram seguidas pelo teste de LSD. A significância foi alcançada guando p < 0,05. Todos os resultados são apresentados como a média ± SEM.
Resultados e discussão
As Figuras 8 a 16 mostram os resultados obtidos. . Nenhuma mudança nos níveis de glucose no sangue foi observada em conseqüência da intervenção.
O peso do corpo para ratos em todos os tratamentos era similar. Os polifenóis não alteraram o peso 20 do corpo total. . Em 11 e 18 semanas, a porcentagem da massa de gordura para os tratamentos com chá verde e chá preto era significativamente mais baixa do que aquela para o controle de água. Em 18 semanas, a porcentagem do resultado da massa 25 de gordura para EGCG também era significativamente diferente.
Em 18 semanas, os gramas da massa de gordura eram significativamente mais baixos do que aqueles para o controle de água. Os polifenóis fizeram com que menos massa de gordura fosse produzida quando na mesma dieta de alimento que 30 o controle de água.
Em 11 e 18 semanas, os gramas da massa magra para os tratamentos com chá verde e EGCG eram significativamente mais elevados do que aqueles para o controle de água. Os polifenóis fizeram com que uma massa magra aumentada fosse produzida. A diferença no teor de polifenol entre o chá verde e o chá preto é provavelmente a razão para o fato que o chá preto não alterou significativamente a massa magra quando comparado ao controle de água.
Exemplo 9
Neste exemplo, foi feita a avaliação de camundongos knock-out (ACE -/-) de enzima de conversão de angiotensina para determinar se eles desenvolvem um fenótipo de massa de gordura reduzida.
Materiais e Métodos
Camundongos: Os camundongos knockout ACE (+/-) heterozigotos machos e fêmeas foram obtidos junto ao laboratório da Pierre Meneton, Insern, U3 67, Paris, França, eles foram mantidos em um fundo C57BL/6J na casa dos animais. Os camundongos heterozigotos (ACE +/-) foram desenvolvidos para produzir o tipo selvagem (ACE +/+) e a prole homozigótica ACE nulo (ACE -/-) . A reação em cadeia de polimerase em tempo real que incorpora a tecnologia de sonda dual-labelled-Taqman® (Applied Biosystems, Foster City, CA) foi utilizada para a obtenção de genótipos da prole de ACE (-/-) e ACE ('+/ + ). Os camundongos foram abrigados em gaiolas de plástico individuais com tampas de grade inclinadas (Wiretainers, Melbourne, Austrália). O alimento (Barastoc, cubos de Mouse Breeder, Barastoc Stockfeeds, Austrália) ficou disponível ad libitumna seção inclinada da tampa e havia acesso livre até a água de torneira. Os camundongos foram mantidos em um ciclo de doze horas de luz/escuridão. Pares de camundongos ACE (+/+) e ACE (-/-) machos de idades combinadas que tinham doze meses de idade e tinham sido mantidos nas mesmas condições de abrigo foram selecionados para o estudo. A quantidade de alimento e de água consumida foi monitorada diariamente por uma semana.
Visualização in vivo da distribuição de tecido adiposo pela Técnica de Formação de Imagem com Ressonância Magnética (MRI): A distribuição da gordura do corpo regional foi visualizada por formação de imagem com ressonância magnética (MRI) . As imagens foram adquiridas em um scanner Bruker BIOSPEC 47/30, equipado com um ímã horizontal 4.7 T Oxford. A densidade de prótons ponderou imagens axiais com os seguintes parâmetros: número de fatias, 20; espessura da fatia, 1 mm; campo de visão (FOV) , 6 cm; matriz, 256 x 256; tempo de repetição (TR) , 815 ms; tempo do eco (TE), 17,9 ms foram obtidos. Os camundongos foram anestesiados ao serem colocados em uma câmara de indução com uma exposição a uma concentração de Isoflurane (Abbott Australiasia Pty Ltd, Sydney, Austrália) de 5% em v/v em ar de grau médico e a redução subseqüente a uma concentração de 2%.
Análise da Composição do Corpo pela Absorbiometria de Raios X de Energia Dual (DEXA) : A avaliação da composição do corpo integral de camundongos ACE (-/-) e ACE (+/ + ) foi executada utilizando DEXA (Hologic QDR 4500, Hologic Inc. EUA) equipado com o pacote de software (versão 3.07) otimizado para animais pequenos. Os animais foram submetidos à varredura quando em uma posição apropriada sob leve anestesia (peso do corpo de 0,02 ml/g) com uma mistura de Ketamine (0,75 ml de 100 mg/ml de Ketaplex, Apex Lab.) e xilazina (0,25 ml de 2 0 mg/ml de Rompun, Bayer).
Análises do Sangue: No final da experiência, os camundongos foram sacrificados ao serem sangrados no coração sob anestesia através da injeção intraperitoneal de uma mistura de Ketamine e Xilazine descrita acima. O sangue foi coletado com seringas revestidas com heparina e a hematócrito foi medida imediatamente depois da aspiração de uma amostra a um tubo capilar seguida pela centrifugação em uma micro centrífuga (HERMLE Z 233 M-2, Medos Company Pty Ltd, Victoria, Austrália) por cinco minutos a 10.000 rpm. Subsequentemente, o plasma foi separado por meio de centrifugação a 3.000 rpm por quinze minutos em uma centrifuga refrigerada (Sorval-RT7) e armazenado a -80 graus Celsius até a análise bioquímica ser completada. Os triglicerídeos do plasma, os níveis totais de colesterol e glicose foram medidos por meio de espectrofotometria de acordo com os procedimentos descritos em kits comercialmente disponíveis (Beckman-Coulter Inc., Fulerton, CA, EUA). Nos camundongos ACE (-/-) e ACE ( + / + ) (n = ' 6) , a leptina do plasma foi medida tal como descrito anteriormente.
Medição da Temperatura do Corpo no Núcleo (temperatura retal): A temperatura foi medida por termopares do tipo K conectados a um termômetro eletrônico de canal duplo Fluke 52 (John Fluke Manufacturing). Para medir a temperatura retal, um termopar (revestido em silicone na ponta) foi inserido 2 cm no esfincter anal de cada camundongo. A ponta do termopar e os fios de conexão foram revestidas com 5% em peso/volume de gel de lidocaina (Xilocaina, Astra Pharmaceuticals) como um anestésico local e lubrificante. As medições da temperatura foram feitas ao mesmo tempo em quatro dias consecutivos e foi tirada a média dessas quatro medições.
Atividade Física Espontânea em Roda de Girar: Os animais tiveram acesso ad libitum por catorze dias às rodas de girar equipadas com um velocímetro (Sigma Sport BC 700 calibradas para raios de rodas de girar) fixado na gaiola de plástico individual com a tampa de grade. A distância (km) e a velocidade (km/h) do percurso foram medidas diariamente durante dez dias. Os camundongos tiveram acesso livre ao alimento e à água. Análise Para o Teor de Gordura Fecal: As fezes foram coletadas das gaiolas dos camundongos pelo período de uma semana e mantidos em um freezer (-20 graus Celsius) até a análise. Os lipídios foram extraídos de 5 g de fezes utilizando uma solução 2:1 de clorofórmio e metanol. O teor total de lipídios foi determinado gravimetricalmente após a extração por 24 horas à temperatura ambiente. O peso seco das fezes foi determinado no resíduo extraído de lipídio. O peso seco total das fezes foi determinado ao adicionar o peso do teor de gordura ao peso seco do resíduo fecal.
Análise Estatística: Todos os dados são indicados como média + /- SEM. As diferenças entre os dois grupos foram analisadas por um teste t de Student (Statistica, StatSoft, EUA) . Resultados Tabela 12: Composição de plasma e hematócrito de camundongos ACE +/+ e ACE -/-
Os valores são expressos como a média ± SEM; ★** p < 0,001 (ACE -/- versus ACE +/+).
Peso do Corpo, Gordura do Corpo e Ingestões de Alimento e de Ãgua: Em comparação com camundongos ACE (+/+), os camundongos ACE (-/-) pesaram 14-16% menos (p < 0,01); (Figura 17A) e tinham 50-55% a menos de gordura do corpo (p < 0,001; Figura 17B) . Os camundongos ACE (-/-) tinham uma proporção significativamente aumentada da massa magra do corpo em comparação com os camundongos ACE (+/ + ) (Figura 17C).
A ingestão de alimento era similar (Figura 18A) , mas o consumo de água dos camundongos ACE (-/-) era maior do que o dobro daquele dos camundongos ACE ( + / + ) (p < 0,001; Figura 18B). O nível de leptina no sangue de camundongos ACE (-/-) tendeu a ser mais baixo do que aquele dos camundongos ACE ( + / + ) (l,5+/-0,3 versus 8,l+/-2,8 nmol/1:F(1,4) df = 5,60, p < 0,07, n = 3 por grupo) e foi correlacionado com a gordura do corpo (r = 0,85, p < 0,05).
Osso - Nenhuma diferença significativa foi observada entre camundongos ACE (-/-) e ACE ( + / + ) em uma ou outra proporção do teor de mineral no osso (2,2+/-0,06 versus 2,1+/-0,05, n = 7 por grupo) ou densidade mineral do osso (0,076 + /- 0,002 versus 0,078+/-0,001 g/cm2, n = 7 por grupo).
Visualização de Massas de Gordura Regionais por MRI:As áreas brancas brilhantes em imagens de MRI ponderadas por densidade de prótons são gordas. A comparação visual da série de imagens axiais demonstrou que o tecido adiposo foi reduzido de maneira marcante em camundongos ACE (-/-) em comparação com camundongos ACE (+/ + ) (Figura 19) . Esse efeito era mais observável na massa de gordura abdominal, tal como indicado pela seta.
Temperatura do Corpo de Núcleo, Nível de Atividade Física Espontânea e Excreção de Gordura: Nenhuma diferença significativa foi observada entre camundongos ACE (-/-) e ACE (+/+) na temperatura do corpo de núcleo (Figura 20A), atividade espontânea (distância de percurso média, Figura 20B; velocidade, Figura 20C), ou proporção da gordura na matéria fecal (Figura 20D).
Hematócritos e Composição do Plasma: Em comparação com camundongos ACE ( + / + ), os camundongos ACE (-/-) tinham um hematócrito mais baixo (p < 0,001). Nenhuma diferença foi observada nos níveis totais de glicose, triglicerídeos (TG) ou colesterol no plasma (Tabela 12).
Conclusão
Em vista das mesmas mudanças fisiológicas que ocorreram utilizando modelos animais deficientes em ACE e várias fontes de polifenol (chá, melaço e extrato de melaço), os resultados suportam a inferência que os polifenóis estão agindo através de um mecanismo de inibição de ACE.
A palavra compreende1 e formas da palavra 'compreende1, tal como empregado nesta descrição e nas reivindicações, não limita a invenção reivindicada de modo a excluir quaisquer variantes ou adições.
As modificações e os aperfeiçoamentos na invenção 5 serão imediatamente aparentes aos elementos versados na técnica. Tais modificações e aperfeiçoamentos devem estar enquadrados dentro do âmbito da presente invenção.
As reivindicações que definem a invenção são tal como segue.