WO2022239676A1 - 負極活物質及びその製造方法 - Google Patents
負極活物質及びその製造方法 Download PDFInfo
- Publication number
- WO2022239676A1 WO2022239676A1 PCT/JP2022/019356 JP2022019356W WO2022239676A1 WO 2022239676 A1 WO2022239676 A1 WO 2022239676A1 JP 2022019356 W JP2022019356 W JP 2022019356W WO 2022239676 A1 WO2022239676 A1 WO 2022239676A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- negative electrode
- active material
- electrode active
- particles
- silicon compound
- Prior art date
Links
- 239000007773 negative electrode material Substances 0.000 title claims abstract description 192
- 238000004519 manufacturing process Methods 0.000 title claims description 27
- 239000002245 particle Substances 0.000 claims abstract description 186
- 150000003377 silicon compounds Chemical class 0.000 claims abstract description 103
- XGZVUEUWXADBQD-UHFFFAOYSA-L lithium carbonate Chemical compound [Li+].[Li+].[O-]C([O-])=O XGZVUEUWXADBQD-UHFFFAOYSA-L 0.000 claims abstract description 61
- 229910052808 lithium carbonate Inorganic materials 0.000 claims abstract description 60
- 229910052799 carbon Inorganic materials 0.000 claims abstract description 39
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 claims abstract description 35
- 238000002441 X-ray diffraction Methods 0.000 claims abstract description 32
- 229910052744 lithium Inorganic materials 0.000 claims abstract description 25
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 claims abstract description 24
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 claims abstract description 23
- 239000001301 oxygen Substances 0.000 claims abstract description 23
- 229910052760 oxygen Inorganic materials 0.000 claims abstract description 23
- 239000011248 coating agent Substances 0.000 claims abstract description 19
- 238000000576 coating method Methods 0.000 claims abstract description 19
- 239000010703 silicon Substances 0.000 claims abstract description 19
- 229910052710 silicon Inorganic materials 0.000 claims abstract description 17
- 229910001416 lithium ion Inorganic materials 0.000 claims description 47
- HBBGRARXTFLTSG-UHFFFAOYSA-N Lithium ion Chemical compound [Li+] HBBGRARXTFLTSG-UHFFFAOYSA-N 0.000 claims description 37
- 239000002131 composite material Substances 0.000 claims description 23
- 238000002156 mixing Methods 0.000 claims description 20
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 claims description 19
- 239000013078 crystal Substances 0.000 claims description 18
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 17
- 239000000203 mixture Substances 0.000 claims description 16
- ILRRQNADMUWWFW-UHFFFAOYSA-K aluminium phosphate Chemical compound O1[Al]2OP1(=O)O2 ILRRQNADMUWWFW-UHFFFAOYSA-K 0.000 claims description 15
- 239000011164 primary particle Substances 0.000 claims description 13
- 239000000463 material Substances 0.000 claims description 12
- 229910052757 nitrogen Inorganic materials 0.000 claims description 12
- 239000011149 active material Substances 0.000 claims description 11
- 239000006185 dispersion Substances 0.000 claims description 6
- 239000007788 liquid Substances 0.000 claims 1
- 239000002002 slurry Substances 0.000 abstract description 85
- 229910052814 silicon oxide Inorganic materials 0.000 abstract description 25
- 229910007562 Li2SiO3 Inorganic materials 0.000 abstract 2
- 230000005855 radiation Effects 0.000 abstract 1
- 239000010410 layer Substances 0.000 description 32
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N silicon dioxide Inorganic materials O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 32
- LIVNPJMFVYWSIS-UHFFFAOYSA-N silicon monoxide Chemical compound [Si-]#[O+] LIVNPJMFVYWSIS-UHFFFAOYSA-N 0.000 description 31
- -1 silane compound Chemical class 0.000 description 25
- 238000000034 method Methods 0.000 description 23
- 150000001875 compounds Chemical class 0.000 description 20
- 229910052751 metal Inorganic materials 0.000 description 20
- 239000002184 metal Substances 0.000 description 20
- 239000002904 solvent Substances 0.000 description 20
- 239000002409 silicon-based active material Substances 0.000 description 19
- 230000000052 comparative effect Effects 0.000 description 18
- 238000011156 evaluation Methods 0.000 description 17
- 150000003839 salts Chemical class 0.000 description 17
- AFCARXCZXQIEQB-UHFFFAOYSA-N N-[3-oxo-3-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)propyl]-2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidine-5-carboxamide Chemical compound O=C(CCNC(=O)C=1C=NC(=NC=1)NCC1=CC(=CC=C1)OC(F)(F)F)N1CC2=C(CC1)NN=N2 AFCARXCZXQIEQB-UHFFFAOYSA-N 0.000 description 15
- 239000007774 positive electrode material Substances 0.000 description 15
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 14
- 239000000243 solution Substances 0.000 description 14
- IJKVHSBPTUYDLN-UHFFFAOYSA-N dihydroxy(oxo)silane Chemical compound O[Si](O)=O IJKVHSBPTUYDLN-UHFFFAOYSA-N 0.000 description 12
- 239000008151 electrolyte solution Substances 0.000 description 11
- 239000007789 gas Substances 0.000 description 11
- 238000010438 heat treatment Methods 0.000 description 11
- 239000002388 carbon-based active material Substances 0.000 description 10
- 238000007599 discharging Methods 0.000 description 10
- 230000002427 irreversible effect Effects 0.000 description 10
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 8
- XTHFKEDIFFGKHM-UHFFFAOYSA-N Dimethoxyethane Chemical compound COCCOC XTHFKEDIFFGKHM-UHFFFAOYSA-N 0.000 description 8
- 229910004298 SiO 2 Inorganic materials 0.000 description 8
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 8
- 229910052782 aluminium Inorganic materials 0.000 description 8
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 8
- 239000003792 electrolyte Substances 0.000 description 8
- PXHVJJICTQNCMI-UHFFFAOYSA-N Nickel Chemical compound [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 7
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 7
- 238000006243 chemical reaction Methods 0.000 description 7
- 239000004020 conductor Substances 0.000 description 7
- 230000000694 effects Effects 0.000 description 7
- 239000011883 electrode binding agent Substances 0.000 description 7
- 229910052736 halogen Inorganic materials 0.000 description 7
- 150000002367 halogens Chemical class 0.000 description 7
- 230000014759 maintenance of location Effects 0.000 description 7
- 230000002829 reductive effect Effects 0.000 description 7
- 239000002344 surface layer Substances 0.000 description 7
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 6
- KMTRUDSVKNLOMY-UHFFFAOYSA-N Ethylene carbonate Chemical compound O=C1OCCO1 KMTRUDSVKNLOMY-UHFFFAOYSA-N 0.000 description 6
- 238000000354 decomposition reaction Methods 0.000 description 6
- ZUOUZKKEUPVFJK-UHFFFAOYSA-N diphenyl Chemical compound C1=CC=CC=C1C1=CC=CC=C1 ZUOUZKKEUPVFJK-UHFFFAOYSA-N 0.000 description 6
- 239000000843 powder Substances 0.000 description 6
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 5
- 239000004743 Polypropylene Substances 0.000 description 5
- 239000012298 atmosphere Substances 0.000 description 5
- 239000011230 binding agent Substances 0.000 description 5
- 150000005676 cyclic carbonates Chemical class 0.000 description 5
- SBZXBUIDTXKZTM-UHFFFAOYSA-N diglyme Chemical compound COCCOCCOC SBZXBUIDTXKZTM-UHFFFAOYSA-N 0.000 description 5
- IEJIGPNLZYLLBP-UHFFFAOYSA-N dimethyl carbonate Chemical compound COC(=O)OC IEJIGPNLZYLLBP-UHFFFAOYSA-N 0.000 description 5
- 239000011267 electrode slurry Substances 0.000 description 5
- 238000010828 elution Methods 0.000 description 5
- 239000011255 nonaqueous electrolyte Substances 0.000 description 5
- 229920001155 polypropylene Polymers 0.000 description 5
- 239000002994 raw material Substances 0.000 description 5
- 239000011871 silicon-based negative electrode active material Substances 0.000 description 5
- 239000000126 substance Substances 0.000 description 5
- 229910052723 transition metal Inorganic materials 0.000 description 5
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 4
- UFWIBTONFRDIAS-UHFFFAOYSA-N Naphthalene Chemical compound C1=CC=CC2=CC=CC=C21 UFWIBTONFRDIAS-UHFFFAOYSA-N 0.000 description 4
- 239000004698 Polyethylene Substances 0.000 description 4
- 229910004283 SiO 4 Inorganic materials 0.000 description 4
- MWPLVEDNUUSJAV-UHFFFAOYSA-N anthracene Chemical compound C1=CC=CC2=CC3=CC=CC=C3C=C21 MWPLVEDNUUSJAV-UHFFFAOYSA-N 0.000 description 4
- 239000003575 carbonaceous material Substances 0.000 description 4
- 150000005678 chain carbonates Chemical class 0.000 description 4
- WDECIBYCCFPHNR-UHFFFAOYSA-N chrysene Chemical compound C1=CC=CC2=CC=C3C4=CC=CC=C4C=CC3=C21 WDECIBYCCFPHNR-UHFFFAOYSA-N 0.000 description 4
- 239000010949 copper Substances 0.000 description 4
- VPUGDVKSAQVFFS-UHFFFAOYSA-N coronene Chemical compound C1=C(C2=C34)C=CC3=CC=C(C=C3)C4=C4C3=CC=C(C=C3)C4=C2C3=C1 VPUGDVKSAQVFFS-UHFFFAOYSA-N 0.000 description 4
- 230000006866 deterioration Effects 0.000 description 4
- JBTWLSYIZRCDFO-UHFFFAOYSA-N ethyl methyl carbonate Chemical compound CCOC(=O)OC JBTWLSYIZRCDFO-UHFFFAOYSA-N 0.000 description 4
- 239000011888 foil Substances 0.000 description 4
- 239000005001 laminate film Substances 0.000 description 4
- 230000004048 modification Effects 0.000 description 4
- 238000012986 modification Methods 0.000 description 4
- 230000033116 oxidation-reduction process Effects 0.000 description 4
- YNPNZTXNASCQKK-UHFFFAOYSA-N phenanthrene Chemical compound C1=CC=C2C3=CC=CC=C3C=CC2=C1 YNPNZTXNASCQKK-UHFFFAOYSA-N 0.000 description 4
- 229920000573 polyethylene Polymers 0.000 description 4
- 238000002360 preparation method Methods 0.000 description 4
- BBEAQIROQSPTKN-UHFFFAOYSA-N pyrene Chemical compound C1=CC=C2C=CC3=CC=CC4=CC=C1C2=C43 BBEAQIROQSPTKN-UHFFFAOYSA-N 0.000 description 4
- 239000000377 silicon dioxide Substances 0.000 description 4
- 235000012239 silicon dioxide Nutrition 0.000 description 4
- 239000002210 silicon-based material Substances 0.000 description 4
- 229920003048 styrene butadiene rubber Polymers 0.000 description 4
- ZUHZGEOKBKGPSW-UHFFFAOYSA-N tetraglyme Chemical compound COCCOCCOCCOCCOC ZUHZGEOKBKGPSW-UHFFFAOYSA-N 0.000 description 4
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 4
- 238000005011 time of flight secondary ion mass spectroscopy Methods 0.000 description 4
- 238000002042 time-of-flight secondary ion mass spectrometry Methods 0.000 description 4
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 3
- HMUNWXXNJPVALC-UHFFFAOYSA-N 1-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]piperazin-1-yl]-2-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethanone Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)N1CCN(CC1)C(CN1CC2=C(CC1)NN=N2)=O HMUNWXXNJPVALC-UHFFFAOYSA-N 0.000 description 3
- VZSRBBMJRBPUNF-UHFFFAOYSA-N 2-(2,3-dihydro-1H-inden-2-ylamino)-N-[3-oxo-3-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)propyl]pyrimidine-5-carboxamide Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)C(=O)NCCC(N1CC2=C(CC1)NN=N2)=O VZSRBBMJRBPUNF-UHFFFAOYSA-N 0.000 description 3
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 3
- OIFBSDVPJOWBCH-UHFFFAOYSA-N Diethyl carbonate Chemical compound CCOC(=O)OCC OIFBSDVPJOWBCH-UHFFFAOYSA-N 0.000 description 3
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- PFYQFCKUASLJLL-UHFFFAOYSA-N [Co].[Ni].[Li] Chemical compound [Co].[Ni].[Li] PFYQFCKUASLJLL-UHFFFAOYSA-N 0.000 description 3
- 239000000654 additive Substances 0.000 description 3
- 229910052783 alkali metal Inorganic materials 0.000 description 3
- 150000001340 alkali metals Chemical class 0.000 description 3
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 3
- 150000001342 alkaline earth metals Chemical class 0.000 description 3
- 230000015572 biosynthetic process Effects 0.000 description 3
- 235000010290 biphenyl Nutrition 0.000 description 3
- 239000004305 biphenyl Substances 0.000 description 3
- 235000010948 carboxy methyl cellulose Nutrition 0.000 description 3
- 239000011247 coating layer Substances 0.000 description 3
- 229910052802 copper Inorganic materials 0.000 description 3
- 238000000151 deposition Methods 0.000 description 3
- 238000011161 development Methods 0.000 description 3
- 239000004210 ether based solvent Substances 0.000 description 3
- 230000006870 function Effects 0.000 description 3
- 229910002804 graphite Inorganic materials 0.000 description 3
- 239000010439 graphite Substances 0.000 description 3
- 230000006872 improvement Effects 0.000 description 3
- 238000003780 insertion Methods 0.000 description 3
- 230000037431 insertion Effects 0.000 description 3
- PAZHGORSDKKUPI-UHFFFAOYSA-N lithium metasilicate Chemical compound [Li+].[Li+].[O-][Si]([O-])=O PAZHGORSDKKUPI-UHFFFAOYSA-N 0.000 description 3
- 229910052912 lithium silicate Inorganic materials 0.000 description 3
- 239000012046 mixed solvent Substances 0.000 description 3
- 229910052759 nickel Inorganic materials 0.000 description 3
- 239000003960 organic solvent Substances 0.000 description 3
- RUOJZAUFBMNUDX-UHFFFAOYSA-N propylene carbonate Chemical compound CC1COC(=O)O1 RUOJZAUFBMNUDX-UHFFFAOYSA-N 0.000 description 3
- 230000001681 protective effect Effects 0.000 description 3
- 238000001179 sorption measurement Methods 0.000 description 3
- 230000000087 stabilizing effect Effects 0.000 description 3
- 238000003756 stirring Methods 0.000 description 3
- WWSJZGAPAVMETJ-UHFFFAOYSA-N 2-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]-3-ethoxypyrazol-1-yl]-1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethanone Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)C=1C(=NN(C=1)CC(=O)N1CC2=C(CC1)NN=N2)OCC WWSJZGAPAVMETJ-UHFFFAOYSA-N 0.000 description 2
- WZFUQSJFWNHZHM-UHFFFAOYSA-N 2-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]piperazin-1-yl]-1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethanone Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)N1CCN(CC1)CC(=O)N1CC2=C(CC1)NN=N2 WZFUQSJFWNHZHM-UHFFFAOYSA-N 0.000 description 2
- YJLUBHOZZTYQIP-UHFFFAOYSA-N 2-[5-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]-1,3,4-oxadiazol-2-yl]-1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethanone Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)C1=NN=C(O1)CC(=O)N1CC2=C(CC1)NN=N2 YJLUBHOZZTYQIP-UHFFFAOYSA-N 0.000 description 2
- SBLRHMKNNHXPHG-UHFFFAOYSA-N 4-fluoro-1,3-dioxolan-2-one Chemical compound FC1COC(=O)O1 SBLRHMKNNHXPHG-UHFFFAOYSA-N 0.000 description 2
- CONKBQPVFMXDOV-QHCPKHFHSA-N 6-[(5S)-5-[[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]piperazin-1-yl]methyl]-2-oxo-1,3-oxazolidin-3-yl]-3H-1,3-benzoxazol-2-one Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)N1CCN(CC1)C[C@H]1CN(C(O1)=O)C1=CC2=C(NC(O2)=O)C=C1 CONKBQPVFMXDOV-QHCPKHFHSA-N 0.000 description 2
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 2
- KWOLFJPFCHCOCG-UHFFFAOYSA-N Acetophenone Chemical compound CC(=O)C1=CC=CC=C1 KWOLFJPFCHCOCG-UHFFFAOYSA-N 0.000 description 2
- 239000004215 Carbon black (E152) Substances 0.000 description 2
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 2
- QUSNBJAOOMFDIB-UHFFFAOYSA-N Ethylamine Chemical compound CCN QUSNBJAOOMFDIB-UHFFFAOYSA-N 0.000 description 2
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 2
- 229910013870 LiPF 6 Inorganic materials 0.000 description 2
- 238000005004 MAS NMR spectroscopy Methods 0.000 description 2
- BZLVMXJERCGZMT-UHFFFAOYSA-N Methyl tert-butyl ether Chemical compound COC(C)(C)C BZLVMXJERCGZMT-UHFFFAOYSA-N 0.000 description 2
- BAVYZALUXZFZLV-UHFFFAOYSA-N Methylamine Chemical compound NC BAVYZALUXZFZLV-UHFFFAOYSA-N 0.000 description 2
- 239000002033 PVDF binder Substances 0.000 description 2
- 229920000265 Polyparaphenylene Polymers 0.000 description 2
- 239000002174 Styrene-butadiene Substances 0.000 description 2
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 2
- SLGBZMMZGDRARJ-UHFFFAOYSA-N Triphenylene Natural products C1=CC=C2C3=CC=CC=C3C3=CC=CC=C3C2=C1 SLGBZMMZGDRARJ-UHFFFAOYSA-N 0.000 description 2
- QDAYJHVWIRGGJM-UHFFFAOYSA-B [Mo+4].[Mo+4].[Mo+4].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O Chemical compound [Mo+4].[Mo+4].[Mo+4].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QDAYJHVWIRGGJM-UHFFFAOYSA-B 0.000 description 2
- 150000008065 acid anhydrides Chemical class 0.000 description 2
- 230000000996 additive effect Effects 0.000 description 2
- 229910045601 alloy Inorganic materials 0.000 description 2
- 239000000956 alloy Substances 0.000 description 2
- 150000001412 amines Chemical class 0.000 description 2
- 239000003125 aqueous solvent Substances 0.000 description 2
- 239000000470 constituent Substances 0.000 description 2
- 239000011889 copper foil Substances 0.000 description 2
- 230000003247 decreasing effect Effects 0.000 description 2
- 230000008021 deposition Effects 0.000 description 2
- 238000007580 dry-mixing Methods 0.000 description 2
- GVEPBJHOBDJJJI-UHFFFAOYSA-N fluoranthrene Natural products C1=CC(C2=CC=CC=C22)=C3C2=CC=CC3=C1 GVEPBJHOBDJJJI-UHFFFAOYSA-N 0.000 description 2
- 230000004927 fusion Effects 0.000 description 2
- 229930195733 hydrocarbon Natural products 0.000 description 2
- 150000002430 hydrocarbons Chemical class 0.000 description 2
- 239000001257 hydrogen Substances 0.000 description 2
- 229910052739 hydrogen Inorganic materials 0.000 description 2
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 2
- 238000005470 impregnation Methods 0.000 description 2
- 150000002500 ions Chemical class 0.000 description 2
- 239000005453 ketone based solvent Substances 0.000 description 2
- 229910003002 lithium salt Inorganic materials 0.000 description 2
- 159000000002 lithium salts Chemical class 0.000 description 2
- 239000011572 manganese Substances 0.000 description 2
- 229910044991 metal oxide Inorganic materials 0.000 description 2
- 150000004706 metal oxides Chemical class 0.000 description 2
- TZIHFWKZFHZASV-UHFFFAOYSA-N methyl formate Chemical compound COC=O TZIHFWKZFHZASV-UHFFFAOYSA-N 0.000 description 2
- SLIUAWYAILUBJU-UHFFFAOYSA-N pentacene Chemical compound C1=CC=CC2=CC3=CC4=CC5=CC=CC=C5C=C4C=C3C=C21 SLIUAWYAILUBJU-UHFFFAOYSA-N 0.000 description 2
- 230000002093 peripheral effect Effects 0.000 description 2
- 239000012071 phase Substances 0.000 description 2
- 229920002981 polyvinylidene fluoride Polymers 0.000 description 2
- 239000011241 protective layer Substances 0.000 description 2
- 230000002441 reversible effect Effects 0.000 description 2
- 238000007789 sealing Methods 0.000 description 2
- 239000007787 solid Substances 0.000 description 2
- 238000001228 spectrum Methods 0.000 description 2
- 229910052717 sulfur Inorganic materials 0.000 description 2
- 239000011593 sulfur Substances 0.000 description 2
- 150000008053 sultones Chemical class 0.000 description 2
- 229920003002 synthetic resin Polymers 0.000 description 2
- 239000000057 synthetic resin Substances 0.000 description 2
- IFLREYGFSNHWGE-UHFFFAOYSA-N tetracene Chemical compound C1=CC=CC2=CC3=CC4=CC=CC=C4C=C3C=C21 IFLREYGFSNHWGE-UHFFFAOYSA-N 0.000 description 2
- YFNKIDBQEZZDLK-UHFFFAOYSA-N triglyme Chemical compound COCCOCCOCCOC YFNKIDBQEZZDLK-UHFFFAOYSA-N 0.000 description 2
- 125000005580 triphenylene group Chemical group 0.000 description 2
- 238000009834 vaporization Methods 0.000 description 2
- 230000008016 vaporization Effects 0.000 description 2
- 229910000166 zirconium phosphate Inorganic materials 0.000 description 2
- LEHFSLREWWMLPU-UHFFFAOYSA-B zirconium(4+);tetraphosphate Chemical compound [Zr+4].[Zr+4].[Zr+4].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O LEHFSLREWWMLPU-UHFFFAOYSA-B 0.000 description 2
- AVPYLKIIPLFMHQ-UHFFFAOYSA-N 1,2,6-oxadithiane 2,2,6,6-tetraoxide Chemical compound O=S1(=O)CCCS(=O)(=O)O1 AVPYLKIIPLFMHQ-UHFFFAOYSA-N 0.000 description 1
- ZZXUZKXVROWEIF-UHFFFAOYSA-N 1,2-butylene carbonate Chemical compound CCC1COC(=O)O1 ZZXUZKXVROWEIF-UHFFFAOYSA-N 0.000 description 1
- YJTKZCDBKVTVBY-UHFFFAOYSA-N 1,3-Diphenylbenzene Chemical group C1=CC=CC=C1C1=CC=CC(C=2C=CC=CC=2)=C1 YJTKZCDBKVTVBY-UHFFFAOYSA-N 0.000 description 1
- FSSPGSAQUIYDCN-UHFFFAOYSA-N 1,3-Propane sultone Chemical compound O=S1(=O)CCCO1 FSSPGSAQUIYDCN-UHFFFAOYSA-N 0.000 description 1
- VAYTZRYEBVHVLE-UHFFFAOYSA-N 1,3-dioxol-2-one Chemical compound O=C1OC=CO1 VAYTZRYEBVHVLE-UHFFFAOYSA-N 0.000 description 1
- DSMUTQTWFHVVGQ-UHFFFAOYSA-N 4,5-difluoro-1,3-dioxolan-2-one Chemical compound FC1OC(=O)OC1F DSMUTQTWFHVVGQ-UHFFFAOYSA-N 0.000 description 1
- BJWMSGRKJIOCNR-UHFFFAOYSA-N 4-ethenyl-1,3-dioxolan-2-one Chemical compound C=CC1COC(=O)O1 BJWMSGRKJIOCNR-UHFFFAOYSA-N 0.000 description 1
- 229910017119 AlPO Inorganic materials 0.000 description 1
- 238000007088 Archimedes method Methods 0.000 description 1
- 229910018871 CoO 2 Inorganic materials 0.000 description 1
- PIICEJLVQHRZGT-UHFFFAOYSA-N Ethylenediamine Chemical compound NCCN PIICEJLVQHRZGT-UHFFFAOYSA-N 0.000 description 1
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 1
- 229910013063 LiBF 4 Inorganic materials 0.000 description 1
- 229910010707 LiFePO 4 Inorganic materials 0.000 description 1
- 229910013716 LiNi Inorganic materials 0.000 description 1
- PWHULOQIROXLJO-UHFFFAOYSA-N Manganese Chemical compound [Mn] PWHULOQIROXLJO-UHFFFAOYSA-N 0.000 description 1
- 239000004677 Nylon Substances 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 1
- 238000001237 Raman spectrum Methods 0.000 description 1
- SOXUFMZTHZXOGC-UHFFFAOYSA-N [Li].[Mn].[Co].[Ni] Chemical compound [Li].[Mn].[Co].[Ni] SOXUFMZTHZXOGC-UHFFFAOYSA-N 0.000 description 1
- KXKVLQRXCPHEJC-UHFFFAOYSA-N acetic acid trimethyl ester Natural products COC(C)=O KXKVLQRXCPHEJC-UHFFFAOYSA-N 0.000 description 1
- 239000006230 acetylene black Substances 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 239000000853 adhesive Substances 0.000 description 1
- 230000001070 adhesive effect Effects 0.000 description 1
- 239000002313 adhesive film Substances 0.000 description 1
- MOVRNJGDXREIBM-UHFFFAOYSA-N aid-1 Chemical compound O=C1NC(=O)C(C)=CN1C1OC(COP(O)(=O)OC2C(OC(C2)N2C3=C(C(NC(N)=N3)=O)N=C2)COP(O)(=O)OC2C(OC(C2)N2C3=C(C(NC(N)=N3)=O)N=C2)COP(O)(=O)OC2C(OC(C2)N2C3=C(C(NC(N)=N3)=O)N=C2)COP(O)(=O)OC2C(OC(C2)N2C(NC(=O)C(C)=C2)=O)COP(O)(=O)OC2C(OC(C2)N2C3=C(C(NC(N)=N3)=O)N=C2)COP(O)(=O)OC2C(OC(C2)N2C3=C(C(NC(N)=N3)=O)N=C2)COP(O)(=O)OC2C(OC(C2)N2C3=C(C(NC(N)=N3)=O)N=C2)COP(O)(=O)OC2C(OC(C2)N2C(NC(=O)C(C)=C2)=O)COP(O)(=O)OC2C(OC(C2)N2C3=C(C(NC(N)=N3)=O)N=C2)COP(O)(=O)OC2C(OC(C2)N2C3=C(C(NC(N)=N3)=O)N=C2)COP(O)(=O)OC2C(OC(C2)N2C3=C(C(NC(N)=N3)=O)N=C2)COP(O)(=O)OC2C(OC(C2)N2C(NC(=O)C(C)=C2)=O)COP(O)(=O)OC2C(OC(C2)N2C3=C(C(NC(N)=N3)=O)N=C2)COP(O)(=O)OC2C(OC(C2)N2C3=C(C(NC(N)=N3)=O)N=C2)COP(O)(=O)OC2C(OC(C2)N2C3=C(C(NC(N)=N3)=O)N=C2)CO)C(O)C1 MOVRNJGDXREIBM-UHFFFAOYSA-N 0.000 description 1
- 239000005456 alcohol based solvent Substances 0.000 description 1
- 230000001476 alcoholic effect Effects 0.000 description 1
- IZJSTXINDUKPRP-UHFFFAOYSA-N aluminum lead Chemical compound [Al].[Pb] IZJSTXINDUKPRP-UHFFFAOYSA-N 0.000 description 1
- 229910021486 amorphous silicon dioxide Inorganic materials 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 239000012300 argon atmosphere Substances 0.000 description 1
- 150000001491 aromatic compounds Chemical class 0.000 description 1
- 229910021383 artificial graphite Inorganic materials 0.000 description 1
- 229910052788 barium Inorganic materials 0.000 description 1
- OJIJEKBXJYRIBZ-UHFFFAOYSA-N cadmium nickel Chemical compound [Ni].[Cd] OJIJEKBXJYRIBZ-UHFFFAOYSA-N 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 239000002041 carbon nanotube Substances 0.000 description 1
- 229910021393 carbon nanotube Inorganic materials 0.000 description 1
- 150000004649 carbonic acid derivatives Chemical class 0.000 description 1
- 239000001768 carboxy methyl cellulose Substances 0.000 description 1
- 239000008112 carboxymethyl-cellulose Substances 0.000 description 1
- 229920006184 cellulose methylcellulose Polymers 0.000 description 1
- 239000000919 ceramic Substances 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 229910017052 cobalt Inorganic materials 0.000 description 1
- 239000010941 cobalt Substances 0.000 description 1
- GUTLYIVDDKVIGB-UHFFFAOYSA-N cobalt atom Chemical compound [Co] GUTLYIVDDKVIGB-UHFFFAOYSA-N 0.000 description 1
- CKFRRHLHAJZIIN-UHFFFAOYSA-N cobalt lithium Chemical compound [Li].[Co] CKFRRHLHAJZIIN-UHFFFAOYSA-N 0.000 description 1
- 229910052681 coesite Inorganic materials 0.000 description 1
- 238000013329 compounding Methods 0.000 description 1
- 238000007906 compression Methods 0.000 description 1
- 230000006835 compression Effects 0.000 description 1
- 238000000748 compression moulding Methods 0.000 description 1
- 238000005336 cracking Methods 0.000 description 1
- 229910052906 cristobalite Inorganic materials 0.000 description 1
- 229910021419 crystalline silicon Inorganic materials 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 230000008025 crystallization Effects 0.000 description 1
- 125000004122 cyclic group Chemical group 0.000 description 1
- 238000009831 deintercalation Methods 0.000 description 1
- 230000036425 denaturation Effects 0.000 description 1
- 238000004925 denaturation Methods 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- VDGKFLGYHYBDQC-UHFFFAOYSA-N difluoromethyl methyl carbonate Chemical compound COC(=O)OC(F)F VDGKFLGYHYBDQC-UHFFFAOYSA-N 0.000 description 1
- 238000007323 disproportionation reaction Methods 0.000 description 1
- 238000010494 dissociation reaction Methods 0.000 description 1
- 230000005593 dissociations Effects 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 238000002848 electrochemical method Methods 0.000 description 1
- 230000008030 elimination Effects 0.000 description 1
- 238000003379 elimination reaction Methods 0.000 description 1
- 239000003759 ester based solvent Substances 0.000 description 1
- 229940093499 ethyl acetate Drugs 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 239000010419 fine particle Substances 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- PIQRQRGUYXRTJJ-UHFFFAOYSA-N fluoromethyl methyl carbonate Chemical compound COC(=O)OCF PIQRQRGUYXRTJJ-UHFFFAOYSA-N 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 239000012634 fragment Substances 0.000 description 1
- 238000007602 hot air drying Methods 0.000 description 1
- 230000002209 hydrophobic effect Effects 0.000 description 1
- 238000007654 immersion Methods 0.000 description 1
- 239000011261 inert gas Substances 0.000 description 1
- 238000009830 intercalation Methods 0.000 description 1
- 229910000765 intermetallic Inorganic materials 0.000 description 1
- 229910052742 iron Inorganic materials 0.000 description 1
- JMMWKPVZQRWMSS-UHFFFAOYSA-N isopropanol acetate Natural products CC(C)OC(C)=O JMMWKPVZQRWMSS-UHFFFAOYSA-N 0.000 description 1
- 229940011051 isopropyl acetate Drugs 0.000 description 1
- GWYFCOCPABKNJV-UHFFFAOYSA-N isovaleric acid Chemical compound CC(C)CC(O)=O GWYFCOCPABKNJV-UHFFFAOYSA-N 0.000 description 1
- 238000010030 laminating Methods 0.000 description 1
- HEPLMSKRHVKCAQ-UHFFFAOYSA-N lead nickel Chemical compound [Ni].[Pb] HEPLMSKRHVKCAQ-UHFFFAOYSA-N 0.000 description 1
- 239000011244 liquid electrolyte Substances 0.000 description 1
- GELKBWJHTRAYNV-UHFFFAOYSA-K lithium iron phosphate Chemical class [Li+].[Fe+2].[O-]P([O-])([O-])=O GELKBWJHTRAYNV-UHFFFAOYSA-K 0.000 description 1
- RSNHXDVSISOZOB-UHFFFAOYSA-N lithium nickel Chemical compound [Li].[Ni] RSNHXDVSISOZOB-UHFFFAOYSA-N 0.000 description 1
- 229910001496 lithium tetrafluoroborate Inorganic materials 0.000 description 1
- DVATZODUVBMYHN-UHFFFAOYSA-K lithium;iron(2+);manganese(2+);phosphate Chemical class [Li+].[Mn+2].[Fe+2].[O-]P([O-])([O-])=O DVATZODUVBMYHN-UHFFFAOYSA-K 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- 238000012423 maintenance Methods 0.000 description 1
- 229910052748 manganese Inorganic materials 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- KKQAVHGECIBFRQ-UHFFFAOYSA-N methyl propyl carbonate Chemical compound CCCOC(=O)OC KKQAVHGECIBFRQ-UHFFFAOYSA-N 0.000 description 1
- 239000013081 microcrystal Substances 0.000 description 1
- 238000002715 modification method Methods 0.000 description 1
- YKYONYBAUNKHLG-UHFFFAOYSA-N n-Propyl acetate Natural products CCCOC(C)=O YKYONYBAUNKHLG-UHFFFAOYSA-N 0.000 description 1
- 239000005543 nano-size silicon particle Substances 0.000 description 1
- 239000002114 nanocomposite Substances 0.000 description 1
- 229910021382 natural graphite Inorganic materials 0.000 description 1
- 229920001778 nylon Polymers 0.000 description 1
- 229920006284 nylon film Polymers 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 230000036961 partial effect Effects 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- 150000003013 phosphoric acid derivatives Chemical class 0.000 description 1
- 230000000704 physical effect Effects 0.000 description 1
- 229920005672 polyolefin resin Polymers 0.000 description 1
- 229920001343 polytetrafluoroethylene Polymers 0.000 description 1
- 239000004810 polytetrafluoroethylene Substances 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- BDERNNFJNOPAEC-UHFFFAOYSA-N propan-1-ol Chemical compound CCCO BDERNNFJNOPAEC-UHFFFAOYSA-N 0.000 description 1
- 229940090181 propyl acetate Drugs 0.000 description 1
- QQONPFPTGQHPMA-UHFFFAOYSA-N propylene Natural products CC=C QQONPFPTGQHPMA-UHFFFAOYSA-N 0.000 description 1
- 230000009257 reactivity Effects 0.000 description 1
- 238000006479 redox reaction Methods 0.000 description 1
- 238000002407 reforming Methods 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 238000004062 sedimentation Methods 0.000 description 1
- 229910000077 silane Inorganic materials 0.000 description 1
- 150000004760 silicates Chemical class 0.000 description 1
- 229910021332 silicide Inorganic materials 0.000 description 1
- FVBUAEGBCNSCDD-UHFFFAOYSA-N silicide(4-) Chemical compound [Si-4] FVBUAEGBCNSCDD-UHFFFAOYSA-N 0.000 description 1
- 239000011863 silicon-based powder Substances 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 238000005507 spraying Methods 0.000 description 1
- 230000006641 stabilisation Effects 0.000 description 1
- 238000011105 stabilization Methods 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 229910052682 stishovite Inorganic materials 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- BDHFUVZGWQCTTF-UHFFFAOYSA-M sulfonate Chemical compound [O-]S(=O)=O BDHFUVZGWQCTTF-UHFFFAOYSA-M 0.000 description 1
- 230000001629 suppression Effects 0.000 description 1
- 238000005979 thermal decomposition reaction Methods 0.000 description 1
- 239000002562 thickening agent Substances 0.000 description 1
- 229910052905 tridymite Inorganic materials 0.000 description 1
- NQPDZGIKBAWPEJ-UHFFFAOYSA-N valeric acid Chemical compound CCCCC(O)=O NQPDZGIKBAWPEJ-UHFFFAOYSA-N 0.000 description 1
- 239000012808 vapor phase Substances 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- 239000013585 weight reducing agent Substances 0.000 description 1
- 238000003466 welding Methods 0.000 description 1
- 238000004804 winding Methods 0.000 description 1
Images
Classifications
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/58—Selection of substances as active materials, active masses, active liquids of inorganic compounds other than oxides or hydroxides, e.g. sulfides, selenides, tellurides, halogenides or LiCoFy; of polyanionic structures, e.g. phosphates, silicates or borates
- H01M4/5825—Oxygenated metallic salts or polyanionic structures, e.g. borates, phosphates, silicates, olivines
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/58—Selection of substances as active materials, active masses, active liquids of inorganic compounds other than oxides or hydroxides, e.g. sulfides, selenides, tellurides, halogenides or LiCoFy; of polyanionic structures, e.g. phosphates, silicates or borates
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B33/00—Silicon; Compounds thereof
- C01B33/20—Silicates
- C01B33/32—Alkali metal silicates
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/362—Composites
- H01M4/366—Composites as layered products
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/38—Selection of substances as active materials, active masses, active liquids of elements or alloys
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/38—Selection of substances as active materials, active masses, active liquids of elements or alloys
- H01M4/386—Silicon or alloys based on silicon
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B32/00—Carbon; Compounds thereof
- C01B32/05—Preparation or purification of carbon not covered by groups C01B32/15, C01B32/20, C01B32/25, C01B32/30
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2002/00—Crystal-structural characteristics
- C01P2002/70—Crystal-structural characteristics defined by measured X-ray, neutron or electron diffraction data
- C01P2002/72—Crystal-structural characteristics defined by measured X-ray, neutron or electron diffraction data by d-values or two theta-values, e.g. as X-ray diagram
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2002/00—Crystal-structural characteristics
- C01P2002/70—Crystal-structural characteristics defined by measured X-ray, neutron or electron diffraction data
- C01P2002/74—Crystal-structural characteristics defined by measured X-ray, neutron or electron diffraction data by peak-intensities or a ratio thereof only
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2004/00—Particle morphology
- C01P2004/60—Particles characterised by their size
- C01P2004/61—Micrometer sized, i.e. from 1-100 micrometer
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M2004/026—Electrodes composed of, or comprising, active material characterised by the polarity
- H01M2004/027—Negative electrodes
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/62—Selection of inactive substances as ingredients for active masses, e.g. binders, fillers
- H01M4/624—Electric conductive fillers
- H01M4/625—Carbon or graphite
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
Definitions
- the present invention relates to a negative electrode active material and its manufacturing method, and more particularly to a negative electrode active material for a lithium ion secondary battery and its manufacturing method.
- lithium-ion secondary batteries are highly expected because they are small and easy to increase in capacity, and they can obtain higher energy density than lead-acid batteries and nickel-cadmium batteries.
- the lithium-ion secondary battery described above includes a positive electrode, a negative electrode, a separator, and an electrolytic solution, and the negative electrode contains a negative electrode active material involved in charge-discharge reactions.
- the negative electrode active material expands and contracts during charging and discharging, so cracking occurs mainly near the surface layer of the negative electrode active material.
- an ionic substance is generated inside the active material, making the negative electrode active material fragile.
- a new surface is generated thereby increasing the reaction area of the active material.
- a decomposition reaction of the electrolytic solution occurs on the new surface, and a film, which is a decomposition product of the electrolytic solution, is formed on the new surface, so that the electrolytic solution is consumed.
- cycle characteristics tend to deteriorate.
- silicon and amorphous silicon dioxide are simultaneously deposited using a vapor phase method (see Patent Document 1, for example).
- a carbon material electroconductive material
- an active material containing silicon and oxygen is produced, and an active material layer with a high oxygen ratio is formed in the vicinity of the current collector (for example, see Patent Document 3).
- oxygen is contained in the silicon active material, and the average oxygen content is 40 at % or less, and the oxygen content is increased near the current collector. (see, for example, Patent Document 4).
- a nanocomposite containing Si phase, SiO 2 , and M y O metal oxide is used to improve the initial charge/discharge efficiency (see, for example, Patent Document 5).
- the molar ratio of oxygen to silicon in the negative electrode active material is set to 0.1 to 1.2, and the difference between the maximum and minimum molar ratios near the interface between the active material and the current collector is 0.4 or less (see Patent Document 7, for example).
- a metal oxide containing lithium is used (see, for example, Patent Document 8).
- a hydrophobic layer such as a silane compound is formed on the surface layer of the silicon material (see, for example, Patent Document 9).
- Patent Document 10 silicon oxide is used, and conductivity is imparted by forming a graphite film on the surface layer.
- Patent Document 10 broad peaks appear at 1330 cm ⁇ 1 and 1580 cm ⁇ 1 with respect to the shift values obtained from the RAMAN spectrum of the graphite film, and their intensity ratio I 1330 /I 1580 is 1.5 ⁇ I 1330 /I 1580 ⁇ 3.
- particles having a silicon microcrystalline phase dispersed in silicon dioxide are used in order to increase battery capacity and improve cycle characteristics (see, for example, Patent Document 11).
- a silicon oxide in which the atomic ratio of silicon and oxygen is controlled to 1:y (0 ⁇ y ⁇ 2) is used (see Patent Document 12, for example).
- Non-Patent Document 1 Japanese Patent Document 1
- the silicon oxide proposed by Hohl is a composite of Si 0+ to Si 4+ and has various oxidation states (Non-Patent Document 2).
- Kapaklis also proposed a disproportionated structure in which silicon oxide is divided into Si and SiO 2 by applying a thermal load (Non-Patent Document 3).
- Non-Patent Document 4 Among silicon oxides having a disproportionated structure, Miyachi et al. focused on Si and SiO2 that contribute to charging and discharging (Non-Patent Document 4), and Yamada et al. (Non-Patent Document 5).
- Si and SiO 2 that constitute silicon oxide react with Li, and are divided into Li silicide, Li silicate, and partially unreacted SiO 2 .
- the Li silicate produced here is irreversible, and once formed, it is a stable substance that does not release Li.
- the capacity per mass calculated from this reaction formula has a value close to the experimental value, and is recognized as a reaction mechanism of silicon oxide.
- Kim et al. identified Li silicate, an irreversible component associated with charging and discharging of silicon oxide, as Li 4 SiO 4 using 7 Li-MAS-NMR and 29 Si-MAS-NMR (Non-Patent Document 6).
- This irreversible capacity is the weakest point of silicon oxide, and improvement is desired. Therefore, Kim et al. used a Li pre-doping method in which Li silicate is formed in advance to greatly improve the initial efficiency as a battery and create a negative electrode that can withstand practical use (Non-Patent Document 7).
- Patent Document 13 a method of treating the powder has been proposed, and the irreversible capacity has been improved.
- lithium-ion secondary batteries which are the main power source for these devices, have been required to have increased battery capacity.
- the development of a lithium ion secondary battery comprising a negative electrode using a silicon material as a main material is desired.
- lithium-ion secondary batteries using silicon materials are desired to have battery characteristics that are close to those of lithium-ion secondary batteries using carbon materials. Therefore, the cycle retention rate and initial efficiency of batteries have been improved by using silicon oxides modified by the insertion and partial elimination of Li as negative electrode active materials.
- the modified silicon oxide is modified using Li, it has relatively low water resistance.
- the slurry containing the silicon oxide after the modification which is prepared during the production of the negative electrode, is insufficiently stabilized, gas is generated due to changes in the slurry over time, or the particles of the silicon oxide and the binder component aggregate. Sedimentation (precipitation) may occur.
- the present invention has been made in view of the problems described above, and aims to provide a negative electrode active material that has a highly stable aqueous slurry, a high capacity, and good cycle characteristics and initial efficiency.
- Another object of the present invention is to provide a method for producing a negative electrode active material that has a highly stable aqueous slurry, a high capacity, and good cycle characteristics and initial efficiency.
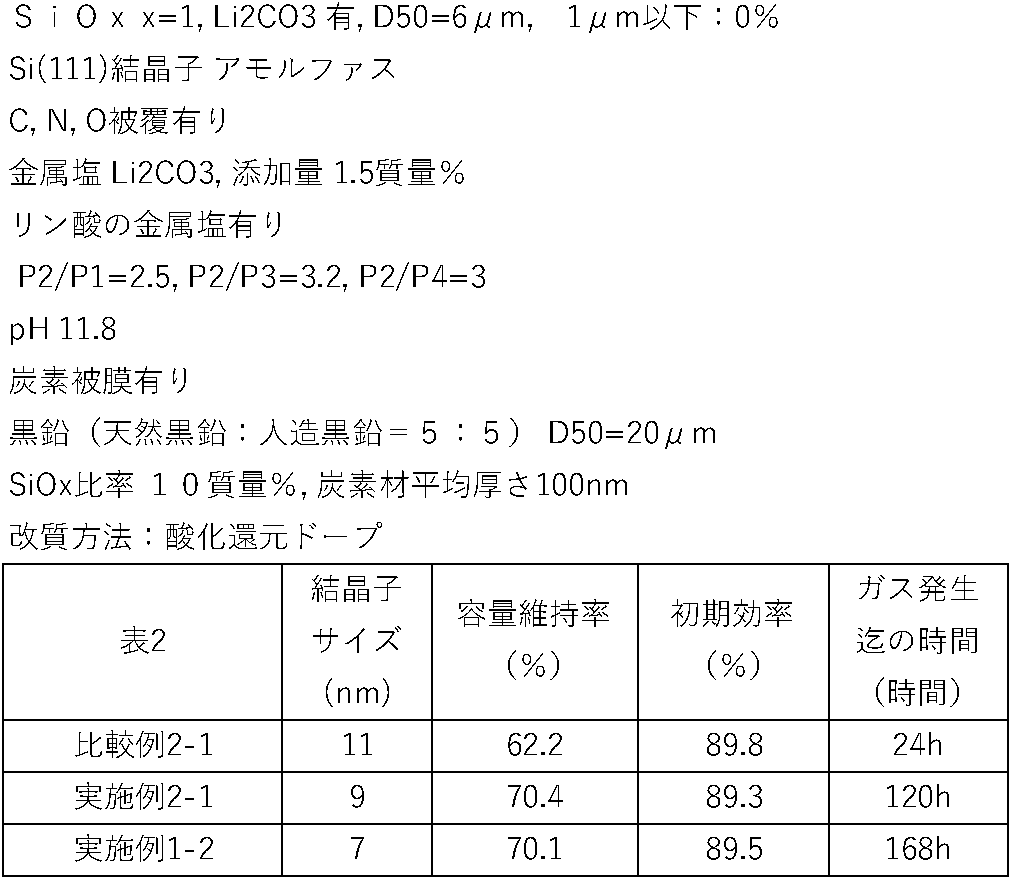
- a negative electrode active material containing negative electrode active material particles for a lithium ion secondary battery contains silicon compound particles made of a silicon compound containing lithium and oxygen, The ratio of oxygen to silicon constituting the silicon compound particles satisfies SiO x : 0.8 ⁇ X ⁇ 1.2, At least part of Li constituting the silicon compound particles is Li 2 SiO 3 ,
- the silicon compound particles have a crystallite size of 10 nm or less due to the Si (111) crystal face obtained by X-ray diffraction using CuK ⁇ rays, At least part of the surface of the silicon compound particles is coated with a carbon coating,
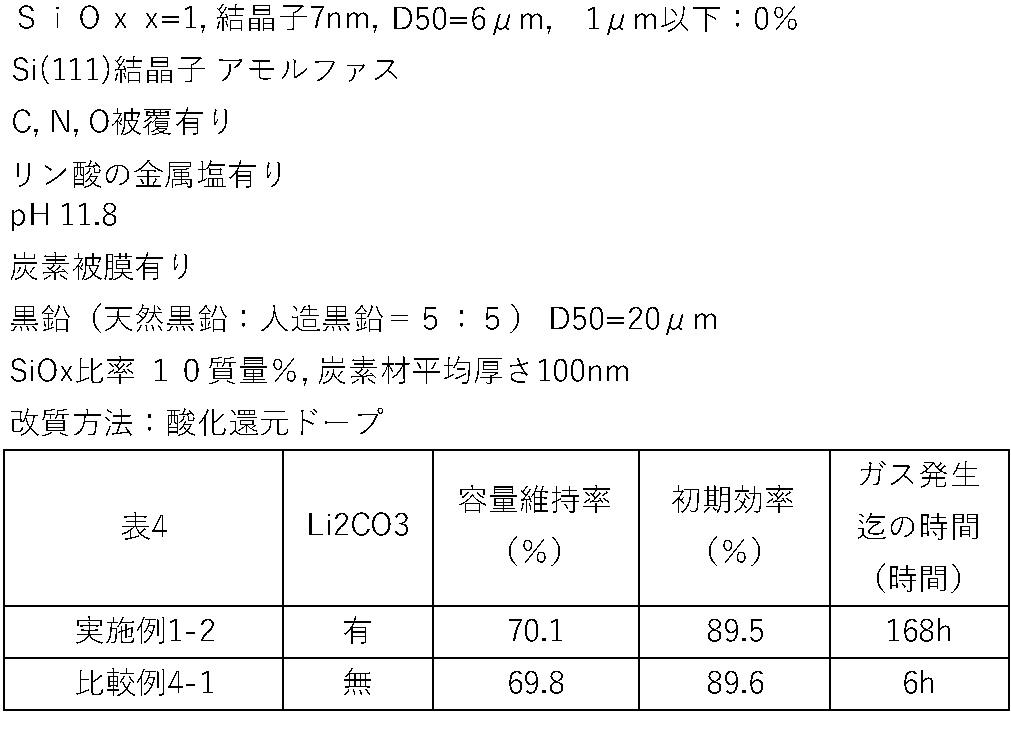
- the negative electrode active material particles contain lithium carbonate, At least part of the lithium carbonate has crystallinity,
- the negative electrode active material particles have a peak height P1 due to at least a part of lithium carbonate that appears in the range of diffraction angle 2 ⁇ of 20 to 21° by X-ray diffraction using CuK ⁇ rays, and
- the negative electrode active material of the present invention contains negative electrode active material particles containing silicon compound particles (also referred to as silicon-based active material particles), the battery capacity can be improved.
- the silicon compound particles contain Li 2 SiO 3 as a Li compound, the irreversible capacity generated during charging can be reduced. This can improve the initial efficiency and cycle characteristics of the battery.
- lithium carbonate is included together with the silicon compound particles, when the negative electrode active material is mixed with the aqueous slurry in the manufacturing process of the negative electrode, Li ions eluted from the silicon compound particles and the like in the aqueous slurry are generated in the presence of lithium carbonate.
- the crystallite size due to the Si (111) crystal plane obtained by X-ray diffraction using CuK ⁇ rays is 10 nm or less, thereby improving battery characteristics and stably generating Li compounds. can be done.
- the crystallite size resulting from the Si (111) crystal face obtained by X-ray diffraction using the CuK ⁇ ray is 8 nm or less. Moreover, it is preferable that the crystallite size resulting from the Si (111) crystal face obtained by X-ray diffraction using the CuK ⁇ ray is substantially amorphous.
- the outermost layer of the negative electrode active material particles is coated with a composite containing C, N and O.
- a negative electrode active material coated with such a composite can reduce the contact area between Li ions and water and improve slurry stability.
- the total amount of lithium carbonate present in the negative electrode active material particles is preferably in the range of 0.5% by mass or more and 2.5% by mass or less with respect to the total amount of the negative electrode active material particles.
- lithium carbonate has moderate reactivity with Li ions, so slurry stability can be further enhanced.
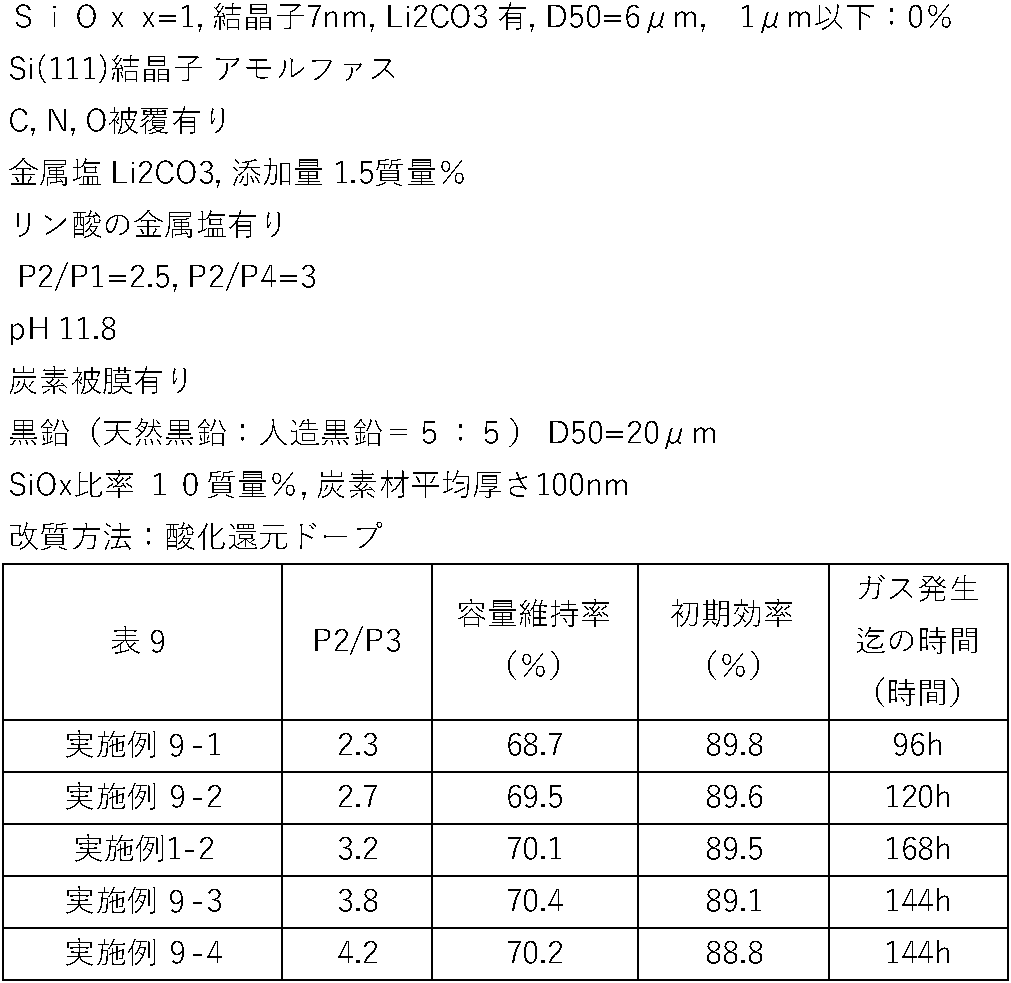
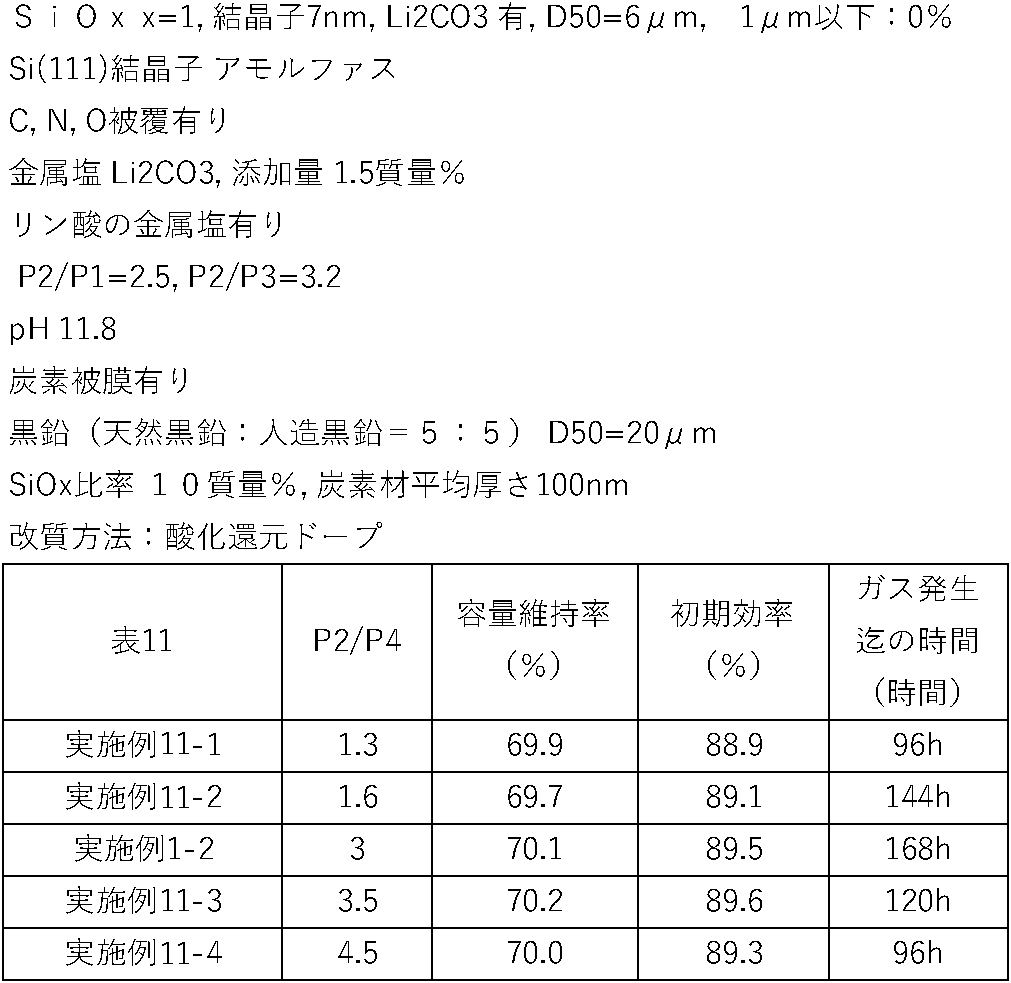
- the negative electrode active material particles have a peak height P2 due to at least a part of Li 2 SiO 3 appearing in a range of diffraction angles 2 ⁇ of 17 to 20° in X-ray diffraction using CuK ⁇ rays, and a diffraction angle It is preferable that the peak height P3 due to the Si (111) crystal plane appearing in the range of 2 ⁇ from 44 to 50° satisfies the relationship of 2.5 ⁇ P2/P3 ⁇ 4.
- the battery capacity can be improved and the effect of slurry stability can be sufficiently exhibited.
- the negative electrode active material particles further contain aluminum phosphate.
- the Li ions eluted in the aqueous slurry react with aluminum to form a film on the surface of the negative electrode active material particles, improving the stability of the slurry.
- the negative electrode active material particles have a peak height P4 due to at least a part of aluminum phosphate that appears in a diffraction angle 2 ⁇ range of 21 to 23°, and a diffraction angle 2 ⁇
- the peak height P2 caused by at least part of Li 2 SiO 3 appearing in the range of 17 to 20° preferably satisfies the relationship of 1.5 ⁇ P2/P4 ⁇ 4.
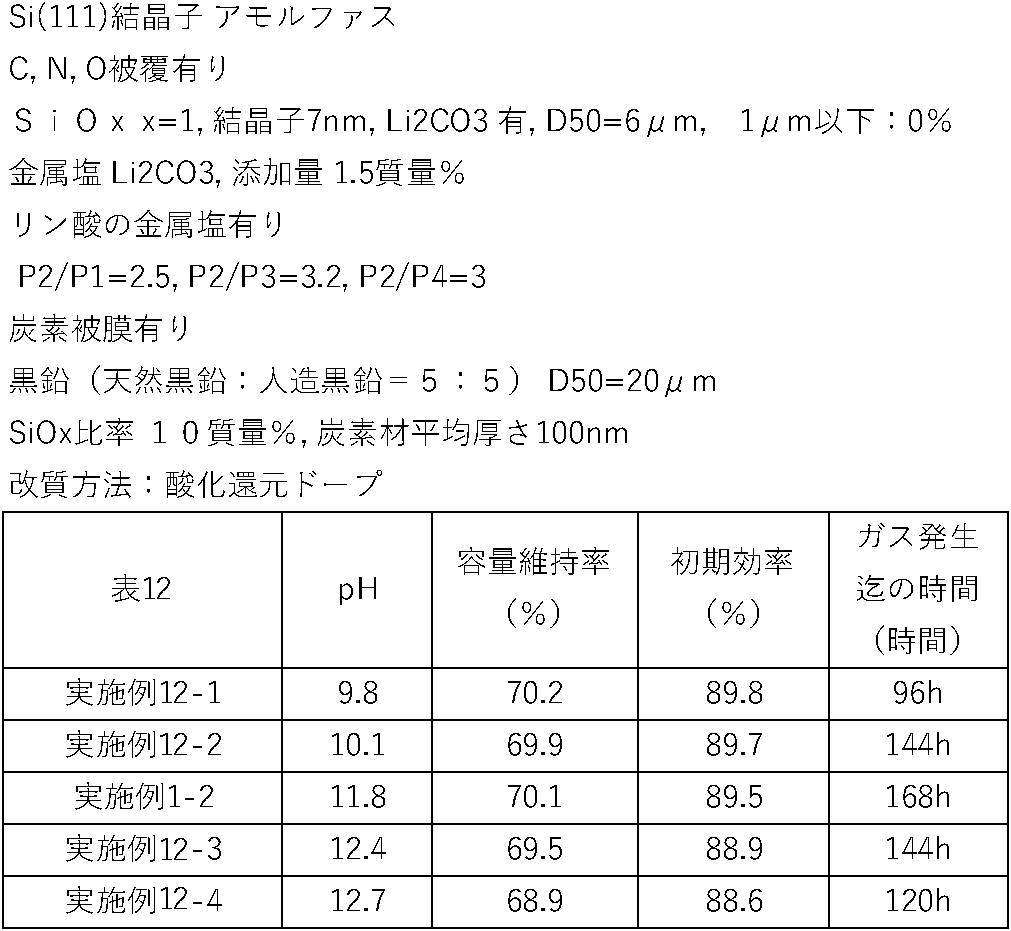
- the pH value of a dispersion obtained by dispersing 10% by mass of the negative electrode active material particles in pure water at 25° C. is 10 or more and 12.5 or less.
- the stability of the slurry can be further enhanced.
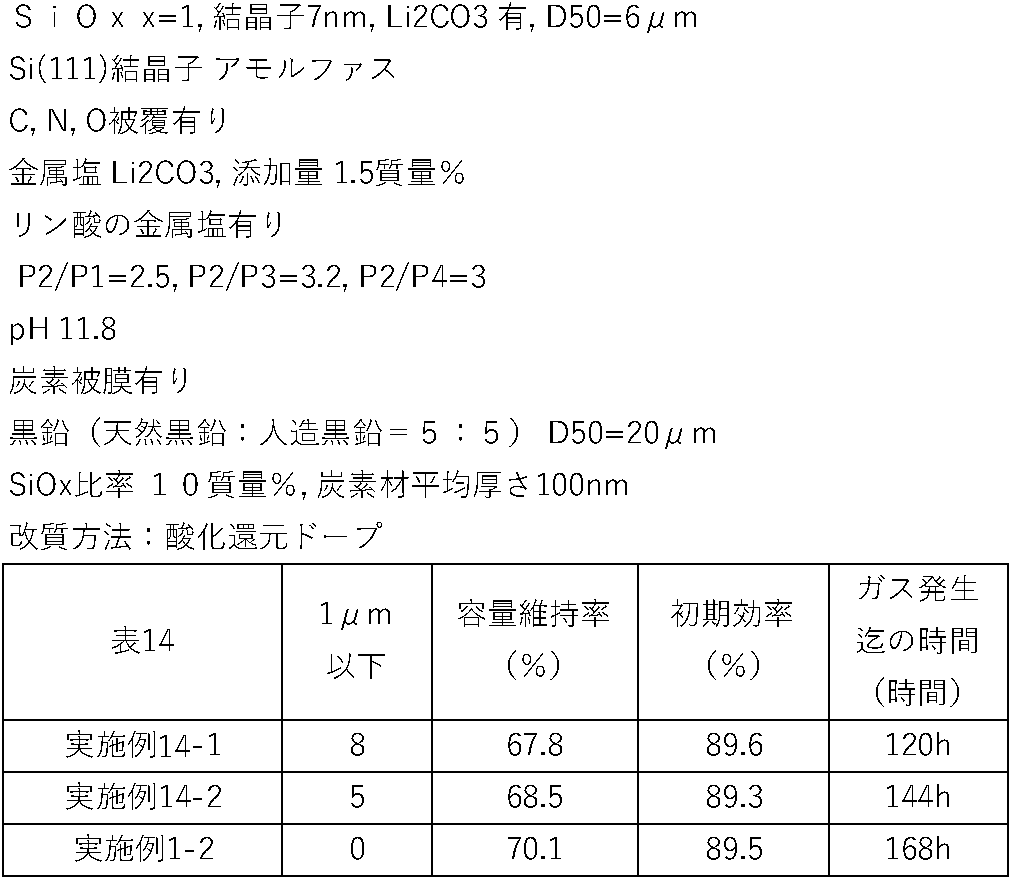
- the proportion of primary particles with a particle diameter of 1 ⁇ m or less among the primary particles of the silicon compound particles is 5% or less on a volume basis.
- the ratio of primary particles having a particle diameter of 1 ⁇ m or less is such, it is possible to suppress an increase in the irreversible capacity of the battery due to an increase in the surface area per mass.
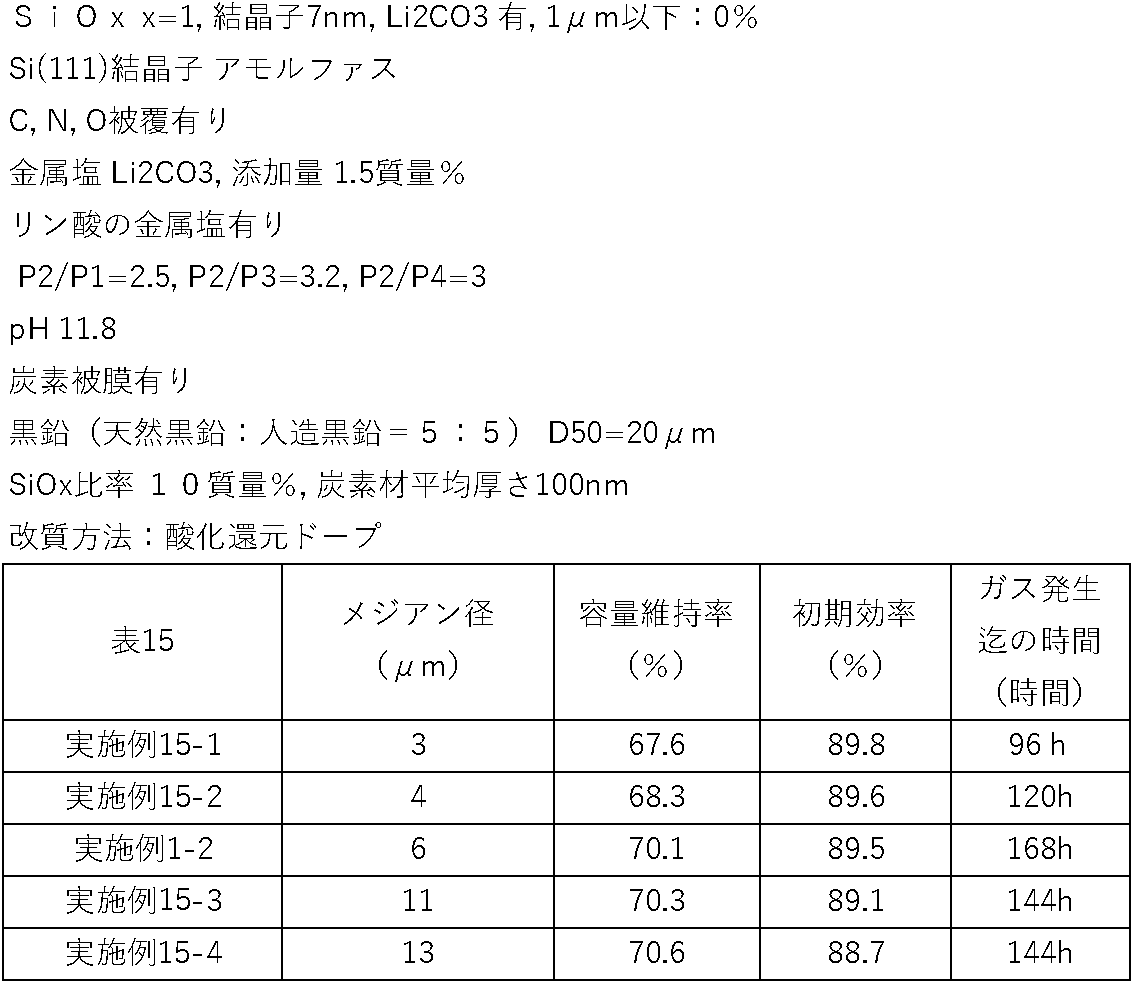
- the median diameter of the negative electrode active material particles is preferably 4.0 ⁇ m or more and 15 ⁇ m or less.
- the median diameter of the negative electrode active material particles is 4.0 ⁇ m or more, an increase in reversible capacity can be suppressed.
- the median diameter is 15 ⁇ m or less, the particles are less likely to break and new surfaces are less likely to appear, which is preferable.
- the present invention provides a negative electrode characterized by containing the above negative electrode active material.
- the negative electrode can be formed using a negative electrode active material with high stability of the aqueous slurry.
- the present invention A method for producing a negative electrode active material containing negative electrode active material particles for a lithium ion secondary battery, A step of producing silicon compound particles containing a silicon compound; a step of coating at least a portion of the silicon compound particles with a carbon layer; a step of inserting Li into the silicon compound particles and causing the silicon compound particles to contain Li 2 SiO 3 ; A step of blending lithium carbonate having crystallinity at least partially into the negative electrode active material particles thus produced, In the mixture of lithium carbonate, the negative electrode active material particles have a peak height P1 due to at least a part of lithium carbonate that appears at a diffraction angle 2 ⁇ in the range of 20 to 21 ° by X-ray diffraction using CuK ⁇ rays; Blending is performed so that the peak height P2 due to at least part of Li 2 SiO 3 appearing in the range of 17 to 20° of diffraction angle 2 ⁇ satisfies the relationship of 2 ⁇ P2/P1 ⁇ 3.5.
- the negative electrode active material of the present invention is capable of stabilizing the aqueous slurry prepared during the production of the negative electrode, and when used as the negative electrode active material of a lithium ion secondary battery, exhibits high capacity, good cycle characteristics and initial charging. Discharge characteristics are obtained.
- a mixed negative electrode active material containing this negative electrode active material can also provide the same effect.
- FIG. 1 is a diagram showing a structural example (laminate film type) of a lithium ion secondary battery containing the negative electrode active material of the present invention
- Lithium-ion secondary batteries using this silicon-based active material are desired to have slurry stability, initial charge/discharge characteristics, and cycle characteristics that are close to those of lithium-ion secondary batteries using a carbon-based active material.
- a silicon-based active material having slurry stability, initial charge/discharge characteristics, and cycle characteristics equivalent to those of a lithium-ion secondary battery using a carbon-based active material has not yet been proposed.
- the present inventors have devoted themselves to obtaining a silicon-based negative electrode active material that, when used in a lithium ion secondary battery, has a high battery capacity and good slurry stability, cycle characteristics, and initial efficiency. After repeated studies, the inventors have arrived at the present invention.
- a negative electrode active material of the present invention is a negative electrode active material containing negative electrode active material particles for a lithium ion secondary battery, wherein the negative electrode active material particles contain silicon compound particles made of a silicon compound containing lithium and oxygen. , the ratio of oxygen and silicon constituting the silicon compound particles satisfies SiO x : 0.8 ⁇ X ⁇ 1.2, and Li constituting the silicon compound particles is at least partially Li 2 SiO 3 wherein the silicon compound particles have a crystallite size of 10 nm or less due to the Si (111) crystal face obtained by X-ray diffraction using CuK ⁇ rays, and at least part of the surface of the silicon compound particles is a carbon coating.
- the negative electrode active material particles contain lithium carbonate, the lithium carbonate has crystallinity at least in part, and the negative electrode active material particles are X-ray diffraction using CuK ⁇ rays Due to the peak height P1 due to at least part of lithium carbonate appearing in the range of 20 to 21 ° with a diffraction angle 2 ⁇ and at least part of Li 2 SiO 3 appearing in the range of 17 to 20 ° with a diffraction angle 2 ⁇ due to and a peak height P2 satisfying the relationship 2 ⁇ P2/P1 ⁇ 3.5.
- the negative electrode active material of the present invention contains negative electrode active material particles (silicon-based active material particles) containing silicon compound particles, the battery capacity can be improved.
- the silicon compound particles contain Li 2 SiO 3 as a Li compound, the irreversible capacity generated during charging can be reduced. This can improve the initial efficiency and cycle characteristics of the battery.
- the crystallite size due to the Si (111) crystal plane obtained by X-ray diffraction using CuK ⁇ rays is 10 nm or less, thereby improving battery characteristics and stably generating Li compounds. can be done.
- the negative electrode active material of the present invention contains lithium carbonate together with the silicon compound particles
- the negative electrode active material of the present invention contains lithium carbonate together with the silicon compound particles
- Li eluted from the silicon compound particles and the like in the aqueous slurry Li eluted from the silicon compound particles and the like in the aqueous slurry.
- the ions partially react with the lithium carbonate particles in the presence of lithium carbonate to form a film on the surface of the negative electrode active material particles, suppress the reaction between Li ions and water, and improve the slurry stability.
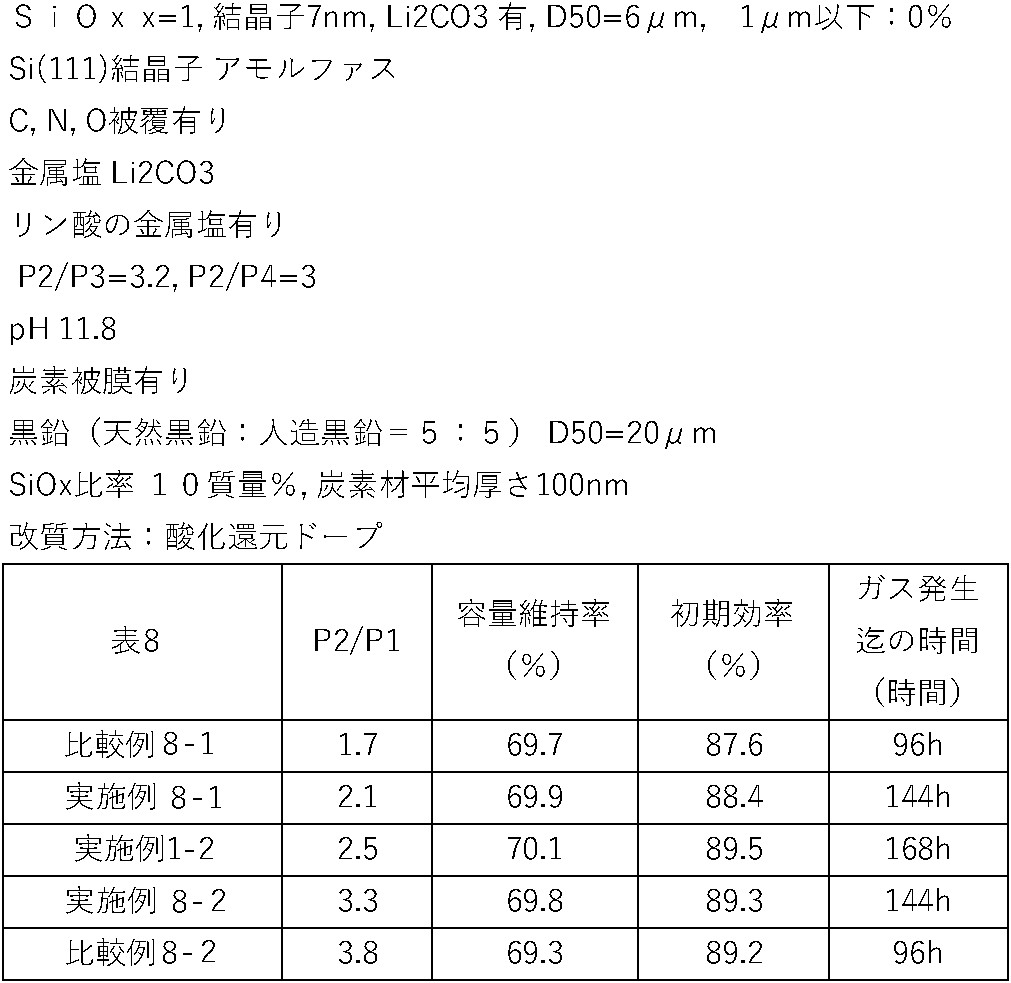
- the peak height P1 of the peak due to lithium carbonate in X-ray diffraction and the peak height P2 of the peak due to Li 2 SiO 3 satisfy 2 ⁇ P2.
- the ratio P2/P1 is less than 2, the ratio of lithium carbonate in the negative electrode active material increases, resulting in deterioration in initial charge/discharge characteristics. If the ratio P2/P1 exceeds 3.5, it becomes difficult to uniformly disperse lithium carbonate in the negative electrode active material, resulting in deterioration of slurry stability.
- FIG. 2 shows an example of an X-ray diffraction chart using CuK ⁇ rays measured from negative electrode active material particles (silicon-based negative electrode active material particles containing lithium carbonate) contained in the negative electrode active material of the present invention.
- negative electrode active material particles silicon-based negative electrode active material particles containing lithium carbonate
- FIG. 2 shows an example of an X-ray diffraction chart using CuK ⁇ rays measured from negative electrode active material particles (silicon-based negative electrode active material particles containing lithium carbonate) contained in the negative electrode active material of the present invention.
- the negative electrode active material containing lithium carbonate as in the present invention can improve slurry stability.
- the negative electrode active material of the present invention can improve the battery characteristics such as the initial efficiency and cycle characteristics of the secondary battery, and particularly significantly improve the cycle characteristics, compared to conventional negative electrode active materials.
- Negative Electrode for Nonaqueous Electrolyte Secondary Battery Next, the configuration of the negative electrode of the secondary battery containing the negative electrode active material of the present invention will be described.
- FIG. 1 shows a cross-sectional view of a negative electrode containing the negative electrode active material of the present invention.
- the negative electrode 10 has a structure in which a negative electrode active material layer 12 is provided on a negative electrode current collector 11 .
- the negative electrode active material layer 12 may be provided on both sides of the negative electrode current collector 11 or only on one side.
- the negative electrode current collector 11 may be omitted.
- the negative electrode current collector 11 is made of an excellent conductive material and has high mechanical strength.
- Examples of conductive materials that can be used for the negative electrode current collector 11 include copper (Cu) and nickel (Ni). This conductive material is preferably a material that does not form an intermetallic compound with lithium (Li).
- the negative electrode current collector 11 preferably contains carbon (C) and sulfur (S) in addition to the main elements. This is because the physical strength of the negative electrode current collector is improved. This is because, in particular, in the case of having an active material layer that expands during charging, if the current collector contains the above element, it has the effect of suppressing deformation of the electrode including the current collector.
- the contents of the above-mentioned contained elements are not particularly limited, they are preferably 100 ppm by mass or less. This is because a higher deformation suppression effect can be obtained.
- the surface of the negative electrode current collector 11 may or may not be roughened.
- Roughened negative electrode current collectors are, for example, electrolytically treated, embossed, or chemically etched metal foils.
- the non-roughened negative electrode current collector is, for example, a rolled metal foil.
- the negative electrode active material layer 12 contains the negative electrode active material (silicon-based active material) of the present invention, and may further contain, as the negative electrode active material, a carbon-based active material in addition to the silicon-based active material. Furthermore, in terms of battery design, it may contain other materials such as a thickener (also referred to as a "binder” or "binder") and a conductive aid. Moreover, the shape of the negative electrode active material may be particulate.
- the negative electrode active material of the present invention contains silicon compound particles containing a silicon compound containing oxygen.
- the ratio of silicon to oxygen constituting this silicon compound must be in the range of SiO x : 0.8 ⁇ X ⁇ 1.2. If X is 0.8 or more, the oxygen ratio is higher than that of simple silicon, so the cycle characteristics are good. If X is 1.2 or less, the resistance of the silicon oxide does not become too high.
- the crystallite size (crystallite size) must be 10 nm or less, more preferably 8 nm or less.
- the crystallite size resulting from the Si (111) crystal face obtained by X-ray diffraction using the CuK ⁇ ray is substantially amorphous.
- a substantially amorphous state can be defined as having a peak half width of 1.2° or more. Such a half-value width can be obtained as a numerical value using analysis software or the like, but it is considered that Si is actually in an amorphous state.
- Peak value 2 ⁇ (47.5°) Peak spread 2 ⁇ (measured half width - metal Si half width 0.089°*) *The half-value width of metal Si, 0.089°, varies depending on the XRD device. *Crystalline Si with no crystal strain is used to measure the half-value width of metal Si. This estimates the half-value width specific to the XRD device. By subtracting the Si half-value width from the measured half-value width, the half-value width due to the crystallite size can be obtained.
- ⁇ X-ray wavelength used (0.154 nm)
- K Scherrer coefficient: 0.9
- Such a negative electrode active material contains negative electrode active material particles containing silicon compound particles, the battery capacity can be improved.
- the silicon compound particles contain lithium silicate as described above, the irreversible capacity generated during charging can be reduced.
- the ratio of primary particles having a particle diameter of 1 ⁇ m or less among the primary particles of the silicon compound particles is 5% or less on a volume basis, the amount of fine powder of the silicon compound particles from which lithium is easily eluted is small, so that the water-based negative electrode It is possible to suppress the elution of lithium ions from the negative electrode active material during slurry preparation. As a result, the stability of the aqueous negative electrode slurry at the time of manufacturing the negative electrode is improved, and the initial efficiency and cycle characteristics are improved.
- Li 2 SiO 3 is a type of lithium silicate.
- the silicon compound particles may contain Li silicate other than Li 2 SiO 3 . Since Li silicate is relatively more stable than other Li compounds, a silicon-based active material containing Li silicate can provide more stable battery characteristics. Li silicate can be obtained by selectively changing a part of the SiO 2 component generated inside the silicon compound particles to a Li compound to modify the silicon compound particles.
- Li 4 SiO 4 is relatively soluble in water, and when an aqueous slurry is used, it is easily eluted during slurrying. Therefore, the Li compound contained in the silicon compound particles is preferably Li 2 SiO 3 , which is less soluble in water than Li 4 SiO 4 and exhibits relatively stable behavior in aqueous slurry.
- the negative electrode active material particles have a diffraction angle 2 ⁇ in the range of 17 to 20 ° in X - ray diffraction using CuK ⁇ rays. It is preferable that the height P2 and the peak height P3 due to the Si (111) crystal plane appearing in the diffraction angle 2 ⁇ range of 44 to 50° satisfy the relationship of 2.5 ⁇ P2/P3 ⁇ 4.
- the peak height ratio is 2.5 or more, Si crystal growth has not progressed excessively. Therefore, less Si is exposed on the particle surface, and slurry stability and cycle characteristics are improved.
- this ratio is 4 or less, the ratio of Li 2 SiO 3 is appropriate, and the initial charge/discharge characteristics are improved.
- the negative electrode active material of the present invention contains lithium carbonate together with the silicon compound particles.
- the mixed lithium carbonate is preferably in the range of 0.5% by mass or more and 2.5% by mass or less with respect to the total amount of the negative electrode active material particles.
- this ratio is 0.5% by mass or more, lithium carbonate can be easily dispersed uniformly in the negative electrode active material, thereby improving the slurry stability.
- this ratio is 2.5% by mass or less, the ratio of lithium carbonate is appropriate, and the initial charge/discharge characteristics are improved.
- metal salts composed of alkali metals and alkaline earth metals other than lithium carbonate may be mixed.
- Alkali metals and alkaline earth metals include Na, K, Mg, Ca and Ba in addition to Li.
- the elements other than Li are carbonates.
- the outermost layer of the negative electrode active material particles is preferably coated with a composite containing C, N and O.
- a negative electrode active material coated with such a composite can reduce the contact area between Li ions and water and improve slurry stability. Fragments of C, N, and O-based compounds can be detected in the spectrum obtained by time-of-flight secondary ion mass spectrometry (TOF-SIMS) in the composite coating containing C, N, and O. Also, such a composite coating can be formed, for example, by the method described below.
- the negative electrode active material particles may further contain a metal salt of phosphoric acid.
- a metal salt of phosphoric acid aluminum phosphate is preferable, but zirconium phosphate and molybdenum phosphate may also be used.
- the negative electrode active material particles contain a metal salt of phosphoric acid such as aluminum phosphate, the Li ions eluted in the aqueous slurry react with the metal such as aluminum to form a coating on the surface of the negative electrode active material particles. and improve slurry stability.
- the negative electrode active material particles are at least a portion of aluminum phosphate that appears in a diffraction angle 2 ⁇ in the range of 21 to 23° in X-ray diffraction using CuK ⁇ rays. and the peak height P2 due to at least a part of Li 2 SiO 3 appearing in the range of 17 to 20° with a diffraction angle 2 ⁇ of 1.5 ⁇ P2/P4 ⁇ 4. is preferably satisfied.
- the stability of the slurry can be enhanced. That is, when the ratio P2/P4 is 1.5 or more, the ratio of the aluminum phosphate particles in the negative electrode active material is appropriate, and the initial charge/discharge characteristics are improved.
- the ratio P2/P4 is 4 or less, lithium carbonate is easily dispersed uniformly in the negative electrode active material, and slurry stability is improved.
- the pH value of the dispersion obtained by dispersing 10% by mass of the negative electrode active material particles in pure water at 25° C. is 10 or more and 12.5 or less. is preferred.
- the pH of the water-based negative electrode slurry composition is 10 or more
- the silicate contained in the silicon compound particles does not accelerate the elution, so the stability of the slurry can be further enhanced.
- the pH of the water-based negative electrode slurry composition is 10 or more
- the silicate contained in the silicon compound particles does not accelerate the elution, so the stability of the slurry can be further enhanced.
- the pH of the water-based negative electrode slurry composition is 10 or more, the silicate contained in the silicon compound particles does not accelerate the elution, so the stability of the slurry can be further enhanced.
- denaturation of a binder component can be suppressed, a viscosity fall can be suppressed.
- the median diameter of the negative electrode active material particles is preferably 4.0 ⁇ m or more and 15 ⁇ m or less.
- the median diameter of the negative electrode active material particles is 4.0 ⁇ m or more, an increase in reversible capacity can be suppressed.
- the median diameter is 15 ⁇ m or less, the particles are less likely to break and new surfaces are less likely to appear, which is preferable.
- the negative electrode active material contained in the negative electrode is manufactured.
- the negative electrode active material can be produced by the production method of the present invention as follows.
- silicon compound particles containing a silicon compound are produced.
- the silicon compound preferably contains silicon and oxygen, and the ratio thereof is SiO x : 0.8 ⁇ X ⁇ 1.2.
- At least a portion of the silicon compound particles are then coated with a carbon layer.
- Li is inserted into the silicon compound particles to contain Li 2 SiO 3 in the silicon compound particles.
- a part of Li inserted into the silicon compound particles may be desorbed.
- at least a part of the produced negative electrode active material particles is blended with lithium carbonate having crystallinity.
- the negative electrode active material particles have a peak height P1 due to at least a part of lithium carbonate that appears at a diffraction angle 2 ⁇ in the range of 20 to 21° by X-ray diffraction using CuK ⁇ rays.
- peak height P2 due to at least part of Li 2 SiO 3 appearing in the range of diffraction angles 2 ⁇ of 17 to 20° satisfy the relationship of 2 ⁇ P2/P1 ⁇ 3.5.
- a negative electrode material and a negative electrode can be produced by mixing the negative electrode active material with a conductive aid or a binder.
- the negative electrode active material of the present invention is produced, for example, by the following procedure.
- silicon compound particles containing a silicon compound (SiO x : 0.8 ⁇ X ⁇ 1.2)
- a raw material that generates silicon oxide gas is heated to 900° C. to 1600° C. in the presence of an inert gas or under reduced pressure. to generate silicon oxide gas.
- the raw material is a mixture of metallic silicon powder and silicon dioxide powder.
- the Si crystallites in the produced particles are controlled by changing the preparation range and vaporization temperature, and by heat treatment after production.
- the generated gas is deposited on the adsorption plate. After the temperature inside the reactor is lowered to 100° C. or less, the deposit is taken out and pulverized into powder using a ball mill, jet mill, or the like.
- a carbon coating layer is formed on the surface layer of the obtained powder material (silicon compound particles and silicon oxide particles).
- the carbon coating layer is effective in improving the battery characteristics of the negative electrode active material.
- Pyrolytic CVD is desirable as a technique for forming a carbon coating layer on the surface layer of the powder material.
- powder materials are set in a furnace, and the furnace is filled with hydrocarbon gas to raise the temperature inside the furnace.
- the decomposition temperature is not particularly limited, 1200° C. or less is particularly desirable. A temperature of 950° C. or less is more desirable, and it is possible to suppress unintended disproportionation of silicon oxide.
- the hydrocarbon gas is not particularly limited, but preferably 3 ⁇ n in the C n H m composition. This is because the production cost is low and the physical properties of the decomposition products are good.
- the silicon compound particles are modified by inserting Li into the silicon compound particles.
- the silicon compound particles in this Li insertion, contain Li 2 SiO 3 .
- an electrochemical method, a modification method using an oxidation-reduction reaction, or the like can be used.
- lithium can be inserted by first immersing the silicon-based active material particles in a solution A in which lithium is dissolved in an ether-based solvent.
- This solution A may further contain a polycyclic aromatic compound or a linear polyphenylene compound.
- the Li compound can be stabilized by heat-treating the obtained silicon-based active material particles at 400° C. or higher and 700° C. or lower. As a result, the decomposed product of the solvent reacts with nitrogen to form a composite film composed of C, N and O on the outermost layer of the negative electrode active material. If the heat treatment temperature is 400° C.
- the Li silicate is stabilized and becomes more likely to function as an irreversible component during charge/discharge, thereby improving the initial charge/discharge characteristics.
- the heat treatment temperature is 700° C. or lower, the crystal growth of Si is not promoted, so slurry stability and cycle characteristics can be improved.
- active lithium may be desorbed from the silicon-based active material particles by immersing the silicon-based active material particles in a solution B containing a polycyclic aromatic compound or a derivative thereof.
- Solvents for this solution B can be, for example, ether solvents, ketone solvents, ester solvents, alcohol solvents, amine solvents, or mixed solvents thereof.
- ether solvent used for solution A diethyl ether, tertbutyl methyl ether, tetrahydrofuran, dioxane, 1,2-dimethoxyethane, diethylene glycol dimethyl ether, triethylene glycol dimethyl ether, tetraethylene glycol dimethyl ether, or a mixed solvent thereof is used. be able to. Among these, tetrahydrofuran, dioxane, 1,2-dimethoxyethane, and diethylene glycol dimethyl ether are particularly preferred. These solvents are preferably dehydrated and preferably deoxygenated.
- polycyclic aromatic compound contained in the solution A one or more of naphthalene, anthracene, phenanthrene, naphthacene, pentacene, pyrene, triphenylene, coronene, chrysene, and derivatives thereof can be used.
- linear polyphenylene compound one or more of biphenyl, terphenyl, and derivatives thereof can be used.
- polycyclic aromatic compound contained in solution B one or more of naphthalene, anthracene, phenanthrene, naphthacene, pentacene, pyrene, triphenylene, coronene, chrysene, and derivatives thereof can be used.
- Ether-based solvents for solution B include diethyl ether, tert-butyl methyl ether, tetrahydrofuran, dioxane, 1,2-dimethoxyethane, diethylene glycol dimethyl ether, triethylene glycol dimethyl ether, tetraethylene glycol dimethyl ether, or mixed solvents thereof. can be used.
- Acetone, acetophenone, etc. can be used as the ketone-based solvent.
- ester solvent methyl formate, methyl acetate, ethyl acetate, propyl acetate, isopropyl acetate, and the like can be used.
- alcoholic solvents methanol, ethanol, propanol, isopropylalconol, etc. can be used.
- amine-based solvent methylamine, ethylamine, ethylenediamine, etc. can be used.
- the produced negative electrode active material particles are blended with at least partly crystalline lithium carbonate to produce a negative electrode active material.
- the lithium carbonate used at this time may be in the form of particles or aggregates thereof.
- dry mixing such as stirring mixing, tumbling mixing, and shear mixing may be used, or a wet method in which lithium carbonate particles dispersed in a solution are sprayed onto the negative electrode active material particles. Mixing may also be used.
- the negative electrode active material particles are at least part of lithium carbonate that appears in a diffraction angle 2 ⁇ in the range of 20 to 21° by X-ray diffraction using CuK ⁇ rays.
- Blend to fill Specifically, it can be achieved by blending lithium carbonate while changing the amount of lithium carbonate during mixing.
- metal salts composed of alkali metals and alkaline earth metals other than lithium carbonate may be mixed by the same method.
- a metal salt of phosphoric acid may also be added.
- the metal salt of phosphoric acid aluminum phosphate is preferable, but zirconium phosphate and molybdenum phosphate may also be used.
- the method for mixing the metal salt of phosphoric acid may be dry mixing such as stirring mixing, tumbling mixing, or shear mixing. Wet mixing by spraying may also be used.
- the negative electrode of the non-aqueous electrolyte secondary battery of the present invention can be manufactured.
- Lithium ion secondary battery> a lithium ion secondary battery containing the negative electrode active material of the present invention will be described.
- a laminated film type lithium ion secondary battery is taken as an example.
- the wound electrode body 21 has a separator between the positive electrode and the negative electrode and is wound.
- a laminate is housed with a separator between the positive electrode and the negative electrode.
- a positive electrode lead 22 is attached to the positive electrode and a negative electrode lead 23 is attached to the negative electrode.
- the outermost periphery of the electrode body is protected by a protective tape.
- the positive and negative leads 22 and 23 are, for example, led out in one direction from the inside of the exterior member 25 toward the outside.
- the positive lead 22 is made of a conductive material such as aluminum
- the negative lead 23 is made of a conductive material such as nickel or copper.
- the exterior member 25 is, for example, a laminate film in which a fusion layer, a metal layer, and a surface protective layer are laminated in this order.
- the outer peripheral edges of the fusion layer are fused together or adhered to each other with an adhesive or the like.
- the fused portion is, for example, a film such as polyethylene or polypropylene, and the metal portion is aluminum foil or the like.
- the protective layer is, for example, nylon or the like.
- An adhesion film 24 is inserted between the exterior member 25 and the positive and negative leads to prevent outside air from entering.
- This material is, for example, polyethylene, polypropylene, polyolefin resin.
- the positive electrode has, for example, a positive electrode active material layer on both sides or one side of the positive electrode current collector, like the negative electrode 10 in FIG.
- the positive electrode current collector is made of a conductive material such as aluminum, for example.
- the positive electrode active material layer contains one or more of positive electrode materials capable of intercalating and deintercalating lithium ions. may contain In this case, the details of the positive electrode binder and the positive electrode conductive aid are the same as those of the negative electrode binder and the negative electrode conductive aid already described, for example.
- a lithium-containing compound is desirable as the positive electrode material.
- the lithium-containing compound includes, for example, a composite oxide composed of lithium and a transition metal element, or a phosphate compound having lithium and a transition metal element.
- positive electrode materials compounds containing at least one of nickel, iron, manganese and cobalt are preferred.
- These chemical formulas are represented by Li x M 1 O 2 or Li y M 2 PO 4 , for example.
- M 1 and M 2 represent at least one transition metal element.
- the values of x and y vary depending on the state of charge and discharge of the battery, they are generally represented by 0.05 ⁇ x ⁇ 1.10 and 0.05 ⁇ y ⁇ 1.10.
- Examples of composite oxides containing lithium and a transition metal element include lithium-cobalt composite oxides (Li x CoO 2 ), lithium-nickel composite oxides (Li x NiO 2 ), lithium-nickel-cobalt composite oxides, and the like. .
- Examples of lithium-nickel-cobalt composite oxides include lithium-nickel-cobalt-aluminum composite oxides (NCA) and lithium-nickel-cobalt-manganese composite oxides (NCM).
- Phosphate compounds containing lithium and a transition metal element include, for example, lithium iron phosphate compounds (LiFePO 4 ) and lithium iron manganese phosphate compounds (LiFe 1-u Mn u PO 4 (0 ⁇ u ⁇ 1)). is mentioned.
- LiFePO 4 lithium iron phosphate compounds
- LiFe 1-u Mn u PO 4 (0 ⁇ u ⁇ 1) lithium iron manganese phosphate compounds
- the negative electrode has the same configuration as the negative electrode 10 for a lithium ion secondary battery shown in FIG.
- the negative electrode preferably has a larger negative electrode charge capacity than the electric capacity (charge capacity as a battery) obtained from the positive electrode active material. This is because deposition of lithium metal on the negative electrode can be suppressed.
- the non-facing region that is, the region where the negative electrode active material layer and the positive electrode active material layer do not face each other, is hardly affected by charging and discharging. Therefore, the state of the negative electrode active material layer is maintained as it is immediately after formation. As a result, the composition of the negative electrode active material can be accurately investigated with good reproducibility regardless of the presence or absence of charge/discharge.
- the separator separates the positive electrode from the negative electrode and allows lithium ions to pass therethrough while preventing current short circuit due to contact between the two electrodes.
- This separator is formed of a porous film made of synthetic resin or ceramic, for example.
- the separator may have a laminated structure in which two or more kinds of porous films are laminated. Examples of synthetic resins include polytetrafluoroethylene, polypropylene, and polyethylene.
- Electrode At least part of the active material layer or the separator is impregnated with a liquid electrolyte (electrolytic solution).
- electrolytic solution has an electrolytic salt dissolved in a solvent, and may contain other materials such as additives.
- Non-aqueous solvents include, for example, ethylene carbonate, propylene carbonate, butylene carbonate, dimethyl carbonate, diethyl carbonate, ethylmethyl carbonate, methylpropyl carbonate, 1,2-dimethoxyethane, tetrahydrofuran and the like.
- ethylene carbonate, propylene carbonate, dimethyl carbonate, diethyl carbonate, and ethylmethyl carbonate it is desirable to use at least one of ethylene carbonate, propylene carbonate, dimethyl carbonate, diethyl carbonate, and ethylmethyl carbonate. This is because better characteristics can be obtained.
- halogen is not particularly limited, but fluorine is preferred. This is because it forms a better film than other halogens. Moreover, the larger the number of halogens, the better. This is because the coating obtained is more stable and the decomposition reaction of the electrolyte is reduced.
- halogenated chain carbonates include fluoromethylmethyl carbonate and difluoromethylmethyl carbonate.
- Halogenated cyclic carbonates include 4-fluoro-1,3-dioxolan-2-one and 4,5-difluoro-1,3-dioxolan-2-one.
- sultone cyclic sulfonate
- solvent additive examples include propane sultone and propene sultone.
- the solvent preferably contains an acid anhydride. This is because the chemical stability of the electrolytic solution is improved.
- Acid anhydrides include, for example, propanedisulfonic anhydride.
- the electrolyte salt can include, for example, any one or more of light metal salts such as lithium salts.
- lithium salts include lithium hexafluorophosphate (LiPF 6 ) and lithium tetrafluoroborate (LiBF 4 ).
- a negative electrode can be produced using the negative electrode active material produced by the method for producing a negative electrode active material of the present invention, and a lithium ion secondary battery can be produced using the produced negative electrode.
- a negative electrode is manufactured by forming a negative electrode active material layer on the negative electrode current collector using the same work procedure as that for manufacturing the negative electrode 10 for a lithium ion secondary battery described above.
- respective active material layers are formed on both surfaces of the positive electrode and the negative electrode current collector. At this time, the active material coating lengths on both sides of both electrodes may deviate (see FIG. 1). ).
- an adhesive film is inserted between the positive electrode lead and the negative electrode lead and the exterior member.
- a predetermined amount of the electrolytic solution prepared as described above is introduced through the opening, and vacuum impregnation is performed. After impregnation, the opening is adhered by a vacuum heat-sealing method.
- the laminated film type lithium ion secondary battery 20 can be manufactured.
- Example 1-1 The laminate film type lithium ion secondary battery 20 shown in FIG. 3 was produced by the following procedure.
- the positive electrode active material contains 95% by mass of LiNi 0.7 Co 0.25 Al 0.05 O, which is a lithium-nickel-cobalt composite oxide, 2.5% by mass of a positive electrode conductive aid (acetylene black), and a positive electrode binder.
- a positive electrode conductive aid acetylene black
- a positive electrode binder Polyvinylidene fluoride: PVDF
- PVDF Polyvinylidene fluoride
- NMP N-methyl-2-pyrrolidone
- the slurry was applied to both surfaces of the positive electrode current collector with a coating device having a die head, and dried with a hot air drying device. At this time, the positive electrode current collector used had a thickness of 15 ⁇ m.
- compression molding was performed using a roll press.
- a negative electrode active material (silicon-based active material) was produced as follows. A raw material (vaporization starting material) in which metal silicon and silicon dioxide are mixed is introduced into a reactor, vaporized in a vacuum atmosphere of 10 Pa, deposited on an adsorption plate, cooled sufficiently, and then the deposit is removed. It was pulverized with a take-out ball mill to obtain silicon compound particles. Among the primary particles of this silicon compound, the ratio of primary particles having a particle diameter of 1 ⁇ m or less was 0% on a volume basis. The value of x in SiOx of the silicon compound particles thus obtained was 0.9. Subsequently, the particle size of the silicon compound particles was adjusted by classification. After that, the surfaces of the silicon compound particles were coated with a carbon material by performing thermal decomposition CVD. The thickness of the carbon coating was 100 nm on average.
- the silicon compound particles coated with a carbon film (hereinafter also referred to as “carbon-coated silicon compound particles”) are doped with lithium by an oxidation-reduction method as described below to insert lithium into the silicon compound particles. and reformed.
- the carbon-coated silicon compound particles were washed, and the washed carbon-coated silicon compound particles were dried under reduced pressure.
- the washing treatment was carried out by stirring with an alkaline aqueous solution for 2 hours.
- the carbon-coated silicon compound particles were modified.
- carbon-coated silicon compound particles were produced.
- the number of microcrystals obtained by Scherrer's formula based on the half-value width of the diffraction peak attributed to Si (111) is The crystallite size was 7 nm. Also, P2/P1 was 2.5, P2/P3 was 3.2, and P2/P4 was 3.
- TOF-SIMS time-of-flight secondary ion mass spectrometry
- the median diameter of the negative electrode active material particles was 6 ⁇ m.
- the pH value of the dispersion was 11.8.
- this negative electrode active material was blended with the carbon-based active material so that the mass ratio of the silicon-based active material particles and the carbon-based active material particles was 1:9 to prepare a mixed negative electrode active material.
- the carbon-based active material a mixture of natural graphite coated with a pitch layer and artificial graphite at a mass ratio of 5:5 was used.
- the median diameter of the carbon-based active material was 20 ⁇ m.
- the mixed negative electrode active material conductive aid 1 (carbon nanotube, CNT), conductive aid 2 (carbon fine particles having a median diameter of about 50 nm), styrene-butadiene rubber (styrene-butadiene copolymer, hereinafter referred to as SBR), Carboxymethyl cellulose (hereinafter referred to as CMC) was mixed at a dry mass ratio of 92.5:1:1:2.5:3, and diluted with pure water to prepare an aqueous negative electrode slurry.
- SBR styrene-butadiene rubber
- CMC Carboxymethyl cellulose
- An electrolytic copper foil having a thickness of 15 ⁇ m was used as the negative electrode current collector.
- This electrolytic copper foil contained carbon and sulfur at a concentration of 70 mass ppm each.
- the aqueous negative electrode slurry was applied to the negative electrode current collector and dried in a vacuum atmosphere at 100° C. for 1 hour. After drying, the deposition amount of the negative electrode active material layer per unit area (also referred to as area density) on one side of the negative electrode was 5 mg/cm 2 .
- the electrolyte salt lithium hexafluorophosphate : LiPF 6
- the outer peripheral edges except for one side were heat-sealed to each other, and the electrode body was housed inside.
- An aluminum laminate film obtained by laminating a nylon film, an aluminum foil, and a polypropylene film was used as the exterior member.
- the prepared electrolytic solution was injected from the opening, impregnated in a vacuum atmosphere, and then heat-sealed and sealed.
- the cycle characteristics were investigated as follows. First, two cycles of charge and discharge were performed at 0.2C in an atmosphere of 25°C for battery stabilization, and the discharge capacity of the second cycle was measured. Subsequently, charging and discharging were performed until the total number of cycles reached 499 cycles, and the discharge capacity was measured each time. Finally, the discharge capacity at the 500th cycle obtained by charging and discharging at 0.2 C was divided by the discharge capacity at the second cycle to calculate the capacity retention rate (hereinafter simply referred to as retention rate). normal cycle. That is, from the 3rd cycle to the 499th cycle, charging and discharging were performed at 0.7C for charging and 0.5C for discharging.
- retention rate capacity retention rate
- initial efficiency (hereinafter sometimes referred to as initial efficiency) was calculated.
- the ambient temperature was the same as in the case of examining the cycle characteristics.
- the pot life of the slurry was evaluated as the time until gas was generated from the slurry. It can be said that the longer this time is, the more stable the slurry is.
- 10 g was aliquoted from the prepared slurry and sealed in an aluminum laminate pack, immediately after preparation (after 0 hours), after 6 hours, after 24 hours, after 48 hours, after 72 hours, after 96 hours. , after 120 hours, after 144 hours, and after 168 hours, the volumes were measured by the Archimedes method. The determination of gas generation was made when the volume change from immediately after preparation exceeded 1 ml.
- the slurry was stored at a temperature of 20°C.
- Table 1 shows the evaluation results of Comparative Examples 1-1, 1-2 and Examples 1-1 to 1-3.
- Example 2-1 A secondary battery was produced under the same conditions as in Example 1-2, except that the crystallite size of Si (111) of the silicon compound was changed as shown in Table 2, and the cycle characteristics, initial efficiency, and slurry stability were evaluated. did.
- the crystallite size of Si (111) was adjusted in the process of solidifying and depositing silicon oxide gas on an adsorption plate.
- Table 2 shows the evaluation results of Comparative Example 2-1 and Example 2-1.
- Example 3-1 A secondary battery was produced under the same conditions as in Example 1-2 except that the lithium silicate contained inside the silicon compound particles was not modified and the silicon compound did not contain lithium, and cycled. Properties, initial efficiency, and slurry stability were evaluated.
- Table 3 shows the evaluation results of Comparative Example 3-1.
- Example 4-1 A secondary battery was produced under the same conditions as in Example 1-2, except that lithium carbonate was not added to the negative electrode active material, and cycle characteristics, initial efficiency, and slurry stability were evaluated.
- Table 4 shows the evaluation results of Comparative Example 4-1.
- Example 5-1 A secondary battery was produced under the same conditions as in Example 1-2, except that the heat treatment time of the silicon-based active material particles modified by the oxidation-reduction method was extended to promote the crystallization of Si. , and slurry stability.
- Table 5 shows the evaluation results of Example 5-1.
- Example 6-1 A secondary battery was produced under the same conditions as in Example 1-2, except that the silicon-based active material particles modified by the oxidation-reduction method were heat-treated in an argon atmosphere instead of nitrogen, and cycle characteristics, initial efficiency, and slurry was evaluated for stability. This prevented the formation of a composite film of C, N, and O on the outermost surface of the silicon-based negative electrode active material particles.
- Table 6 shows the evaluation results of Example 6-1.
- Li is less likely to elute in the aqueous slurry than when there is no composite coating, and the stability of the slurry. improved.
- Examples 7-1 to 7-4 A secondary battery was produced under the same conditions as in Example 1-2, except that the addition rate of lithium carbonate was changed, and cycle characteristics, initial efficiency, and slurry stability were evaluated.
- Table 7 shows the evaluation results of Examples 7-1 to 7-4.
- Example 8-1 to 8-2 Comparative Examples 8-1 to 8-2
- a secondary battery was produced under the same conditions as in Example 1-2, except that the analytical peak intensity ratio P2/P1 of X-ray analysis was changed as shown in Table 8, and the cycle characteristics, initial efficiency, and slurry stability were evaluated. evaluated.
- Table 8 shows the evaluation results of Examples 8-1 and 8-2 and Comparative Examples 8-1 and 8-2.
- Example 9-1 to 9-4 A secondary battery was produced under the same conditions as in Example 1-2, except that the analytical peak intensity ratio P2/P3 of X-ray analysis was changed as shown in Table 9, and the cycle characteristics, initial efficiency, and slurry stability were evaluated. evaluated. This ratio was adjusted by changing the heat treatment temperature in the heat treatment for stabilizing the Li silicate.
- Table 9 shows the evaluation results of Examples 9-1 to 9-4.
- Example 10-1 A secondary battery was produced under the same conditions as in Example 1-2 except that the metal salt of phosphoric acid (aluminum phosphate) in the negative electrode material was not added, and the cycle characteristics, initial efficiency, and slurry stability were evaluated. .
- Table 10 shows the evaluation results of Example 10-1.
- Example 11-1 to 11-4 A secondary battery was produced under the same conditions as in Example 1-2, except that the analytical peak intensity ratio P2/P4 of X-ray analysis was changed as shown in Table 11, and the cycle characteristics, initial efficiency, and slurry stability were evaluated. evaluated. This ratio was adjusted by changing the heat treatment temperature in the heat treatment for stabilizing the Li silicate and by changing the compounding amount of aluminum phosphate.
- Table 11 shows the evaluation results of Examples 11-1 to 11-4.
- Example 12-1 to 12-4 A secondary battery was prepared under the same conditions as in Example 1-2, except that the pH value of the dispersion obtained by dispersing the negative electrode active material particles in pure water at 25° C. at a rate of 10% by mass as shown in Table 12 was changed. was prepared, and cycle characteristics, initial efficiency, and slurry stability were evaluated.
- Table 12 shows the evaluation results of Examples 12-1 to 12-4.
- Example 13-1 A secondary battery was produced under the same conditions as in Example 1-2, except that no carbon film was formed, and the cycle characteristics, initial efficiency, and slurry stability were evaluated.
- Table 13 shows the evaluation results of Comparative Example 13-1.
- the formation of the carbon coating improved the conductivity and improved the battery characteristics.
- a large amount of Li was eluted, making it difficult to prepare the slurry, so the evaluation was stopped.
- Example 14-1, 14-2 A secondary battery was produced under the same conditions as in Example 1-2, except that the ratio of primary particles of 1 ⁇ m or less among the primary particles of the silicon compound was changed as shown in Table 14. Stability was evaluated.
- Table 14 shows the evaluation results of Examples 14-1 and 14-2.
- Example 15-1 to 15-4 A secondary battery was produced under the same conditions as in Example 1-2, except that the median diameter of the silicon compound particles was changed as shown in Table 15, and the cycle characteristics, initial efficiency, and slurry stability were evaluated.
- Table 15 shows the evaluation results of Examples 15-1 to 15-4.
- the present invention is not limited to the above embodiments.
- the above embodiment is an example, and any device that has substantially the same configuration as the technical idea described in the claims of the present invention and produces similar effects is the present invention. It is included in the technical scope of the invention.
Landscapes
- Chemical & Material Sciences (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Electrochemistry (AREA)
- Inorganic Chemistry (AREA)
- Composite Materials (AREA)
- Organic Chemistry (AREA)
- Crystallography & Structural Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Battery Electrode And Active Subsutance (AREA)
- Materials Engineering (AREA)
- Manufacturing & Machinery (AREA)
- Silicates, Zeolites, And Molecular Sieves (AREA)
Abstract
Description
2SiO(Si+SiO2) + 6.85Li+ + 6.85e-
→ 1.4Li3.75Si + 0.4Li4SiO4 + 0.2SiO2
反応式ではケイ素酸化物を構成するSiとSiO2がLiと反応し、LiシリサイドとLiシリケート、一部未反応であるSiO2にわかれる。
リチウムイオン二次電池用の負極活物質粒子を含む負極活物質であって、
前記負極活物質粒子は、リチウムと酸素を含むケイ素化合物からなるケイ素化合物粒子を含有し、
前記ケイ素化合物粒子を構成する酸素とケイ素の比は、SiOX:0.8≦X≦1.2を満たし、
前記ケイ素化合物粒子を構成するLiは、少なくともその一部がLi2SiO3であり、
前記ケイ素化合物粒子は、CuKα線を用いたX線回折により得られるSi(111)結晶面に起因する結晶子サイズが10nm以下であり、
前記ケイ素化合物粒子の表面の少なくとも一部が炭素被膜で被覆されており、
前記負極活物質粒子は、炭酸リチウムを含み、
前記炭酸リチウムは少なくともその一部に結晶性を有しており、
前記負極活物質粒子は、CuKα線を用いたX線回折により回折角2θが20~21°の範囲に現れる炭酸リチウムの少なくとも一部に起因するピーク高さP1と、回折角2θが17~20°の範囲に現れるLi2SiO3の少なくとも一部に起因するピーク高さP2とが、2≦P2/P1≦3.5の関係を満たすことを特徴とする負極活物質を提供する。
リチウムイオン二次電池用の負極活物質粒子を含む負極活物質の製造方法であって、
ケイ素化合物を含むケイ素化合物粒子を作製する工程と、
前記ケイ素化合物粒子の少なくとも一部を炭素層で被膜する工程と、
前記ケイ素化合物粒子にLiを挿入し、該ケイ素化合物粒子にLi2SiO3を含有させる工程と、
前記作製した負極活物質粒子に、少なくとも一部に結晶性を有する炭酸リチウムを配合する工程と
を含み、
前記炭酸リチウムの配合において、前記負極活物質粒子が、CuKα線を用いたX線回折により回折角2θが20~21°の範囲に現れる炭酸リチウムの少なくとも一部に起因するピーク高さP1と、回折角2θが17~20°の範囲に現れるLi2SiO3の少なくとも一部に起因するピーク高さP2とが、2≦P2/P1≦3.5の関係を満たすように配合を行うことを特徴とする負極活物質の製造方法を提供する。
続いて、このような本発明の負極活物質を含む二次電池の負極の構成について説明する。
図1は、本発明の負極活物質を含む負極の断面図を表している。図1に示すように、負極10は、負極集電体11の上に負極活物質層12を有する構成になっている。この負極活物質層12は負極集電体11の両面、又は、片面だけに設けられていても良い。さらに、本発明の非水電解質二次電池の負極においては、負極集電体11はなくてもよい。
負極集電体11は、優れた導電性材料であり、かつ、機械的な強度に長けた物で構成される。負極集電体11に用いることができる導電性材料として、例えば銅(Cu)やニッケル(Ni)が挙げられる。この導電性材料は、リチウム(Li)と金属間化合物を形成しない材料であることが好ましい。
負極活物質層12は、本発明の負極活物質(ケイ素系活物質)を含んでおり、さらに、負極活物質として、ケイ素系活物質の他に炭素系活物質などを含んでいて良い。さらに、電池設計上、増粘剤(「結着剤」、「バインダー」とも呼称する)や導電助剤等の他の材料を含んでいても良い。また、負極活物質の形状は粒子状であって良い。
L=Kλ/(βcosθ)
L:結晶子径
β:半値幅:ピーク値から、おおよそ±5°(/2θ)の範囲を用いて求めた。
ピーク値:2θ(47.5°)
ピークの広がり2θ(測定半値幅-金属Si半値幅0.089°※)
※金属Si半値幅0.089°は、XRD装置により異なる。
※金属Si半値幅の測定には、結晶歪の無い結晶性Siを使用する。
これによりXRD装置固有の半値幅を見積もる。
測定半値幅から上記Si半値幅を差し引くことで結晶子サイズに起因する半値幅を求めることができる。
λ:使用X線波長(0.154nm)
K:シェラー係数:0.9
θ:回折角
続いて、非水電解質二次電池の負極の製造方法の一例を説明する。
次に、本発明の負極活物質を含むリチウムイオン二次電池について説明する。ここでは具体例として、ラミネートフィルム型のリチウムイオン二次電池を例に挙げる。
図3に示すラミネートフィルム型のリチウムイオン二次電池20は、主にシート状の外装部材25の内部に巻回電極体21が収納されたものである。この巻回電極体21は正極、負極間にセパレータを有し、巻回されたものである。また正極、負極間にセパレータを有し積層体を収納した場合も存在する。どちらの電極体においても、正極に正極リード22が取り付けられ、負極に負極リード23が取り付けられている。電極体の最外周部は保護テープにより保護されている。
正極は、例えば、図1の負極10と同様に、正極集電体の両面又は片面に正極活物質層を有している。
負極は、上記した図1のリチウムイオン二次電池用負極10と同様の構成を有し、例えば、集電体11の両面に負極活物質層12を有している。この負極は、正極活物質剤から得られる電気容量(電池として充電容量)に対して、負極充電容量が大きくなることが好ましい。負極上でのリチウム金属の析出を抑制することができるためである。
セパレータは正極と負極を隔離し、両極接触に伴う電流短絡を防止しつつ、リチウムイオンを通過させるものである。このセパレータは、例えば合成樹脂、あるいはセラミックからなる多孔質膜により形成されている。また、セパレータは2種以上の多孔質膜が積層された積層構造を有しても良い。合成樹脂として例えば、ポリテトラフルオロエチレン、ポリプロピレン、ポリエチレンなどが挙げられる。
活物質層の少なくとも一部、又は、セパレータには、液状の電解質(電解液)が含浸されている。この電解液は、溶媒中に電解質塩が溶解されており、添加剤など他の材料を含んでいても良い。
本発明では、上記の本発明の負極活物質の製造方法によって製造した負極活物質を用いて負極を作製でき、該作製した負極を用いてリチウムイオン二次電池を製造することができる。
最初に上記した正極材を用い正極電極を作製する。まず、正極活物質と、必要に応じて正極結着剤、正極導電助剤などを混合し正極合剤としたのち、有機溶剤に分散させ正極合剤スラリーとする。続いて、ナイフロール又はダイヘッドを有するダイコーターなどのコーティング装置で正極集電体に合剤スラリーを塗布し、熱風乾燥させて正極活物質層を得る。最後に、ロールプレス機などで正極活物質層を圧縮成型する。この時、加熱しても良く、また加熱又は圧縮を複数回繰り返しても良い。
を参照)。
以下の手順により、図3に示したラミネートフィルム型のリチウムイオン二次電池20を作製した。
ケイ素化合物のバルク内酸素量を調整したことを除き、実施例1-1と同様に、二次電池の製造を行った。この場合、ケイ素化合物の原料中の金属ケイ素と二酸化ケイ素との比率や加熱温度を変化させることで、酸素量を調整した。実施例1-2~1-3、比較例1-1、1-2における、SiOXで表されるケイ素化合物のXの値を表1中に示した。
ケイ素化合物のSi(111)の結晶子サイズを表2のように変更したこと以外、実施例1-2と同じ条件で二次電池を作製し、サイクル特性、初回効率、スラリーの安定性を評価した。Si(111)の結晶子サイズは酸化ケイ素ガスを吸着版に固化させて堆積させる工程で調整した。
ケイ素化合物粒子の内部に含ませるリチウムシリケートを、改質を行わず、ケイ素化合物にリチウムを含ませないように変更したこと以外、実施例1-2と同じ条件で二次電池を作製し、サイクル特性、初回効率、及びスラリーの安定性を評価した。
負極活物質中に炭酸リチウムを添加させないこと以外、実施例1-2と同じ条件で二次電池を作製し、サイクル特性、初回効率、及びスラリーの安定性を評価した。
酸化還元法で改質されたケイ素系活物質粒子の熱処理時間を延ばしてSiの結晶化を進めたこと以外、実施例1-2と同じ条件で二次電池を作製し、サイクル特性、初回効率、及びスラリーの安定性を評価した。
酸化還元法で改質されたケイ素系活物質粒子を窒素でなくアルゴン雰囲気下で熱処理すること以外、実施例1-2と同じ条件で二次電池を作製し、サイクル特性、初回効率、及びスラリーの安定性を評価した。これにより、ケイ素系負極活物質粒子の最表面にC、N、Oの複合物被膜が形成されないようにした。
炭酸リチウムの添加率を変えたこと以外、実施例1-2と同じ条件で二次電池を作製し、サイクル特性、初回効率、及びスラリーの安定性を評価した。
X線解析の解析ピーク強度比P2/P1を表8のように変更したこと以外、実施例1-2と同じ条件で二次電池を作製し、サイクル特性、初回効率、及びスラリーの安定性を評価した。
X線解析の解析ピーク強度比P2/P3を表9のように変更したこと以外、実施例1-2と同じ条件で二次電池を作製し、サイクル特性、初回効率、及びスラリーの安定性を評価した。この比率は、Liシリケートを安定化するための熱処理における熱処理温度を変化させることにより調整した。
負極材中のリン酸の金属塩(リン酸アルミニウム)を添加させないこと以外、実施例1-2と同じ条件で二次電池を作製し、サイクル特性、初回効率、及びスラリーの安定性を評価した。
X線解析の解析ピーク強度比P2/P4を表11のように変更したこと以外、実施例1-2と同じ条件で二次電池を作製し、サイクル特性、初回効率、及びスラリーの安定性を評価した。この比率は、Liシリケートを安定化するための熱処理における熱処理温度を変化させること、リン酸アルミニウムの配合量を変化させることにより調整した。
表12のように負極活物質粒子を10質量%の割合で25℃の純水中に分散させた分散液のpHの値を変更したこと以外、実施例1-2と同じ条件で二次電池を作製し、サイクル特性、初回効率、及びスラリーの安定性を評価した。
炭素被膜を形成しなかったこと以外、実施例1-2と同じ条件で二次電池を作製し、サイクル特性、初回効率、スラリーの安定性を評価した。
ケイ素化合物の一次粒子のうち、1μm以下の一次粒子の割合を表14のように変更したこと以外、実施例1-2と同じ条件で二次電池を作製し、サイクル特性、初回効率、スラリーの安定性を評価した。
ケイ素化合物粒子のメジアン径を表15のように変化させたこと以外、実施例1-2と同じ条件で二次電池を作製し、サイクル特性、初回効率、スラリーの安定性を評価した。
Claims (13)
- リチウムイオン二次電池用の負極活物質粒子を含む負極活物質であって、
前記負極活物質粒子は、リチウムと酸素を含むケイ素化合物からなるケイ素化合物粒子を含有し、
前記ケイ素化合物粒子を構成する酸素とケイ素の比は、SiOX:0.8≦X≦1.2を満たし、
前記ケイ素化合物粒子を構成するLiは、少なくともその一部がLi2SiO3であり、
前記ケイ素化合物粒子は、CuKα線を用いたX線回折により得られるSi(111)結晶面に起因する結晶子サイズが10nm以下であり、
前記ケイ素化合物粒子の表面の少なくとも一部が炭素被膜で被覆されており、
前記負極活物質粒子は、炭酸リチウムを含み、
前記炭酸リチウムは少なくともその一部に結晶性を有しており、
前記負極活物質粒子は、CuKα線を用いたX線回折により回折角2θが20~21°の範囲に現れる炭酸リチウムの少なくとも一部に起因するピーク高さP1と、回折角2θが17~20°の範囲に現れるLi2SiO3の少なくとも一部に起因するピーク高さP2とが、2≦P2/P1≦3.5の関係を満たすことを特徴とする負極活物質。 - 前記CuKα線を用いたX線回折により得られるSi(111)結晶面に起因する結晶子サイズが8nm以下であることを特徴とする請求項1に記載の負極活物質。
- 前記CuKα線を用いたX線回折により得られるSi(111)結晶面に起因する結晶子サイズが、実質的にアモルファス状態であることを示すことを特徴とする請求項1又は請求項2に記載の負極活物質。
- 前記負極活物質粒子は、その最表層が、C、N及びOを含む複合物に被覆されていることを特徴とする請求項1から請求項3のいずれか1項に記載の負極活物質。
- 前記負極活物質粒子に存在する前記炭酸リチウムの総量が、前記負極活物質粒子の総量に対して0.5質量%以上2.5質量%以下の範囲のものであることを特徴とする請求項1から請求項4のいずれか1項に記載の負極活物質。
- 前記負極活物質粒子は、CuKα線を用いたX線回折において、回折角2θが17~20°の範囲に現れるLi2SiO3の少なくとも一部に起因するピーク高さP2と、回折角2θが44~50°の範囲に現れるSi(111)結晶面に起因するピーク高さP3とが、2.5≦P2/P3≦4の関係を満たすことを特徴とする請求項1から請求項5のいずれか1項に記載の負極活物質。
- 前記負極活物質粒子が、さらに、リン酸アルミニウムを含むことを特徴とする請求項1から請求項6のいずれか1項に記載の負極活物質
- 前記負極活物質粒子は、CuKα線を用いたX線回折において、回折角2θが21~23°の範囲に現れるリン酸アルミニウムの少なくとも一部に起因するピーク高さP4と、回折角2θが17~20°の範囲に現れるLi2SiO3の少なくとも一部に起因するピーク高さP2とが、1.5≦P2/P4≦4の関係を満たすことを特徴とする請求項7に記載の負極活物質。
- 前記負極活物質粒子を10質量%の割合で25℃の純水中に分散させた分散液のpHの値が10以上12.5以下となるものであることを特徴とする請求項1から8のいずれか1項に記載の負極活物質。
- 前記ケイ素化合物粒子の一次粒子のうち、粒子径1μm以下の一次粒子の割合が体積基準で5%以下であることを特徴とする請求項1から請求項9のいずれか1項に記載の負極活物質。
- 前記負極活物質粒子のメジアン径は、4.0μm以上15μm以下であることを特徴とする請求項1から請求項10のいずれか1項に記載の負極活物質。
- 請求項1から請求項11のいずれか1項に記載の負極活物質を含むものであることを特徴とする負極。
- リチウムイオン二次電池用の負極活物質粒子を含む負極活物質の製造方法であって、
ケイ素化合物を含むケイ素化合物粒子を作製する工程と、
前記ケイ素化合物粒子の少なくとも一部を炭素層で被膜する工程と、
前記ケイ素化合物粒子にLiを挿入し、該ケイ素化合物粒子にLi2SiO3を含有させる工程と、
前記作製した負極活物質粒子に、少なくとも一部に結晶性を有する炭酸リチウムを配合する工程と
を含み、
前記炭酸リチウムの配合において、前記負極活物質粒子が、CuKα線を用いたX線回折により回折角2θが20~21°の範囲に現れる炭酸リチウムの少なくとも一部に起因するピーク高さP1と、回折角2θが17~20°の範囲に現れるLi2SiO3の少なくとも一部に起因するピーク高さP2とが、2≦P2/P1≦3.5の関係を満たすように配合を行うことを特徴とする負極活物質の製造方法。
Priority Applications (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020237038697A KR20240007153A (ko) | 2021-05-13 | 2022-04-28 | 부극 활물질 및 그 제조 방법 |
| EP22807378.9A EP4340070A1 (en) | 2021-05-13 | 2022-04-28 | Negative electrode active material and method for producing same |
| CN202280034125.9A CN117296168A (zh) | 2021-05-13 | 2022-04-28 | 负极活性物质及其制造方法 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2021-081941 | 2021-05-13 | ||
| JP2021081941A JP7457671B2 (ja) | 2021-05-13 | 2021-05-13 | 負極活物質及びその製造方法 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2022239676A1 true WO2022239676A1 (ja) | 2022-11-17 |
Family
ID=84028314
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2022/019356 WO2022239676A1 (ja) | 2021-05-13 | 2022-04-28 | 負極活物質及びその製造方法 |
Country Status (6)
| Country | Link |
|---|---|
| EP (1) | EP4340070A1 (ja) |
| JP (1) | JP7457671B2 (ja) |
| KR (1) | KR20240007153A (ja) |
| CN (1) | CN117296168A (ja) |
| TW (1) | TW202312537A (ja) |
| WO (1) | WO2022239676A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN117747803A (zh) * | 2023-12-20 | 2024-03-22 | 宣城矽立科新材料有限公司 | 一种提高导电性的硅氧负极材料及其制备方法 |
Citations (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH06325765A (ja) | 1992-07-29 | 1994-11-25 | Seiko Instr Inc | 非水電解質二次電池及びその製造方法 |
| JP2001185127A (ja) | 1999-12-24 | 2001-07-06 | Fdk Corp | リチウム2次電池 |
| JP2002042806A (ja) | 2000-07-19 | 2002-02-08 | Japan Storage Battery Co Ltd | 非水電解質二次電池 |
| JP2006114454A (ja) | 2004-10-18 | 2006-04-27 | Sony Corp | 電池 |
| JP2006164954A (ja) | 2004-11-11 | 2006-06-22 | Matsushita Electric Ind Co Ltd | リチウムイオン二次電池用負極、その製造方法、およびそれを用いたリチウムイオン二次電池 |
| JP2007234255A (ja) | 2006-02-27 | 2007-09-13 | Sanyo Electric Co Ltd | リチウム二次電池用負極及びその製造方法並びにリチウム二次電池 |
| JP2008177346A (ja) | 2007-01-18 | 2008-07-31 | Sanyo Electric Co Ltd | エネルギー貯蔵デバイス |
| JP2008251369A (ja) | 2007-03-30 | 2008-10-16 | Matsushita Electric Ind Co Ltd | リチウム二次電池用負極およびそれを備えたリチウム二次電池、ならびにリチウム二次電池用負極の製造方法 |
| JP2008282819A (ja) | 2008-07-10 | 2008-11-20 | Toshiba Corp | 非水電解質二次電池用負極活物質の製造方法およびこれによって得られる非水電解質電池用負極活物質 |
| JP2009070825A (ja) | 2007-09-17 | 2009-04-02 | Samsung Sdi Co Ltd | リチウム2次電池用負極活物質とその製造方法、リチウム2次電池用負極及びリチウム2次電池 |
| JP2009205950A (ja) | 2008-02-28 | 2009-09-10 | Shin Etsu Chem Co Ltd | 非水電解質二次電池用負極活物質、及びそれを用いた非水電解質二次電池 |
| JP2009212074A (ja) | 2008-02-07 | 2009-09-17 | Shin Etsu Chem Co Ltd | 非水電解質二次電池用負極材及びその製造方法並びにリチウムイオン二次電池及び電気化学キャパシタ |
| JP2015156355A (ja) | 2013-08-21 | 2015-08-27 | 信越化学工業株式会社 | 負極活物質、負極活物質材料、負極電極、リチウムイオン二次電池、負極電極の製造方法、負極活物質の製造方法、並びに、リチウムイオン二次電池の製造方法 |
| JP2017147057A (ja) * | 2016-02-15 | 2017-08-24 | 信越化学工業株式会社 | 負極活物質、混合負極活物質材料、非水電解質二次電池用負極、リチウムイオン二次電池、及び負極活物質の製造方法 |
| WO2017183286A1 (ja) * | 2016-04-18 | 2017-10-26 | 信越化学工業株式会社 | 負極活物質、混合負極活物質材料、負極活物質の製造方法 |
| JP2020077510A (ja) * | 2018-11-07 | 2020-05-21 | 信越化学工業株式会社 | 負極活物質、混合負極活物質、水系負極スラリー組成物、及び、負極活物質の製造方法 |
| CN111430677A (zh) * | 2019-09-30 | 2020-07-17 | 蜂巢能源科技有限公司 | 负极材料及其制备方法、负极和锂离子电池 |
-
2021
- 2021-05-13 JP JP2021081941A patent/JP7457671B2/ja active Active
-
2022
- 2022-04-28 KR KR1020237038697A patent/KR20240007153A/ko unknown
- 2022-04-28 EP EP22807378.9A patent/EP4340070A1/en active Pending
- 2022-04-28 WO PCT/JP2022/019356 patent/WO2022239676A1/ja active Application Filing
- 2022-04-28 CN CN202280034125.9A patent/CN117296168A/zh active Pending
- 2022-05-03 TW TW111116652A patent/TW202312537A/zh unknown
Patent Citations (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH06325765A (ja) | 1992-07-29 | 1994-11-25 | Seiko Instr Inc | 非水電解質二次電池及びその製造方法 |
| JP2001185127A (ja) | 1999-12-24 | 2001-07-06 | Fdk Corp | リチウム2次電池 |
| JP2002042806A (ja) | 2000-07-19 | 2002-02-08 | Japan Storage Battery Co Ltd | 非水電解質二次電池 |
| JP2006114454A (ja) | 2004-10-18 | 2006-04-27 | Sony Corp | 電池 |
| JP2006164954A (ja) | 2004-11-11 | 2006-06-22 | Matsushita Electric Ind Co Ltd | リチウムイオン二次電池用負極、その製造方法、およびそれを用いたリチウムイオン二次電池 |
| JP2007234255A (ja) | 2006-02-27 | 2007-09-13 | Sanyo Electric Co Ltd | リチウム二次電池用負極及びその製造方法並びにリチウム二次電池 |
| JP2008177346A (ja) | 2007-01-18 | 2008-07-31 | Sanyo Electric Co Ltd | エネルギー貯蔵デバイス |
| JP2008251369A (ja) | 2007-03-30 | 2008-10-16 | Matsushita Electric Ind Co Ltd | リチウム二次電池用負極およびそれを備えたリチウム二次電池、ならびにリチウム二次電池用負極の製造方法 |
| JP2009070825A (ja) | 2007-09-17 | 2009-04-02 | Samsung Sdi Co Ltd | リチウム2次電池用負極活物質とその製造方法、リチウム2次電池用負極及びリチウム2次電池 |
| JP2009212074A (ja) | 2008-02-07 | 2009-09-17 | Shin Etsu Chem Co Ltd | 非水電解質二次電池用負極材及びその製造方法並びにリチウムイオン二次電池及び電気化学キャパシタ |
| JP2009205950A (ja) | 2008-02-28 | 2009-09-10 | Shin Etsu Chem Co Ltd | 非水電解質二次電池用負極活物質、及びそれを用いた非水電解質二次電池 |
| JP2008282819A (ja) | 2008-07-10 | 2008-11-20 | Toshiba Corp | 非水電解質二次電池用負極活物質の製造方法およびこれによって得られる非水電解質電池用負極活物質 |
| JP2015156355A (ja) | 2013-08-21 | 2015-08-27 | 信越化学工業株式会社 | 負極活物質、負極活物質材料、負極電極、リチウムイオン二次電池、負極電極の製造方法、負極活物質の製造方法、並びに、リチウムイオン二次電池の製造方法 |
| JP2017147057A (ja) * | 2016-02-15 | 2017-08-24 | 信越化学工業株式会社 | 負極活物質、混合負極活物質材料、非水電解質二次電池用負極、リチウムイオン二次電池、及び負極活物質の製造方法 |
| WO2017183286A1 (ja) * | 2016-04-18 | 2017-10-26 | 信越化学工業株式会社 | 負極活物質、混合負極活物質材料、負極活物質の製造方法 |
| JP2020077510A (ja) * | 2018-11-07 | 2020-05-21 | 信越化学工業株式会社 | 負極活物質、混合負極活物質、水系負極スラリー組成物、及び、負極活物質の製造方法 |
| CN111430677A (zh) * | 2019-09-30 | 2020-07-17 | 蜂巢能源科技有限公司 | 负极材料及其制备方法、负极和锂离子电池 |
Non-Patent Citations (6)
| Title |
|---|
| "Journal of BATTERY ASSOCIATION OF JAPAN", DENCHI, 1 May 2010 (2010-05-01), pages 10 |
| A. HOHLT. WIEDERP. A. VAN AKENT. E. WEIRICHG. DENNINGERM. VIDALS. OSWALDC. DENEKEJ. MAYERH. FUESS, J. NON-CRYST. SOLIDS, vol. 320, 2003, pages 255 |
| HYE JIN KIMSUNGHUN CHOISEUNG JONG LEEMYUNG WON SEOJAE GOO LEEERHAN DENIZYONG JU LEEEUN KYUNG KIMJANG WOOK CHOI, NANO LETT, vol. 16, 2016, pages 282 - 288 |
| M. YAMADAM. INABAA. UEDAK. MATSUMOTOT. IWASAKIT. OHZUKU ET AL., J. ELECTROCHEM. SOC, vol. 159, 2012, pages A1630 |
| MARIKO MIYACHIHIRONORI YAMAMOTOHIDEMASA KAWAI, J. ELECTROCHEM. SOC, vol. 154, 2007, pages A1112 - A1117 |
| V. KAPAKLIS, J. NON-CRYSTALLINE SOLIDS, vol. 354, no. 2008, February 1961 (1961-02-01) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN117747803A (zh) * | 2023-12-20 | 2024-03-22 | 宣城矽立科新材料有限公司 | 一种提高导电性的硅氧负极材料及其制备方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP7457671B2 (ja) | 2024-03-28 |
| CN117296168A (zh) | 2023-12-26 |
| EP4340070A1 (en) | 2024-03-20 |
| TW202312537A (zh) | 2023-03-16 |
| KR20240007153A (ko) | 2024-01-16 |
| JP2022175518A (ja) | 2022-11-25 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7186099B2 (ja) | 非水電解質二次電池用負極活物質及びその製造方法 | |
| US11961997B2 (en) | Negative electrode active material, mixed negative electrode active material, aqueous negative electrode slurry composition, and method for producing negative electrode active material | |
| JP7368577B2 (ja) | 負極及びその製造方法 | |
| WO2016185663A1 (ja) | 非水電解質二次電池用負極活物質及び非水電解質二次電池並びに非水電解質二次電池用負極材の製造方法 | |
| JP7410259B2 (ja) | 非水電解質二次電池 | |
| TW202310474A (zh) | 負極及負極的製造方法 | |
| WO2022239676A1 (ja) | 負極活物質及びその製造方法 | |
| JP7175254B2 (ja) | 非水電解質二次電池負極用添加剤、及び、非水電解質二次電池用水系負極スラリー組成物 | |
| US20240351894A1 (en) | Negative electrode active material and method for manufacturing the same | |
| JP7325458B2 (ja) | 非水電解質二次電池用負極活物質及び非水電解質二次電池用負極活物質の製造方法 | |
| WO2023135970A1 (ja) | 負極活物質及び負極 | |
| JP7412372B2 (ja) | 非水電解質二次電池用負極活物質及びその製造方法並びに非水電解質二次電池 | |
| EP4379834A1 (en) | Negative electrode and method for producing same | |
| WO2023140072A1 (ja) | 非水電解質二次電池用負極活物質及びその製造方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 22807378 Country of ref document: EP Kind code of ref document: A1 |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 18290107 Country of ref document: US Ref document number: 202280034125.9 Country of ref document: CN |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2022807378 Country of ref document: EP |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| ENP | Entry into the national phase |
Ref document number: 2022807378 Country of ref document: EP Effective date: 20231213 |