WO2015020153A1 - ベラプロスト含有貼付剤 - Google Patents
ベラプロスト含有貼付剤 Download PDFInfo
- Publication number
- WO2015020153A1 WO2015020153A1 PCT/JP2014/070899 JP2014070899W WO2015020153A1 WO 2015020153 A1 WO2015020153 A1 WO 2015020153A1 JP 2014070899 W JP2014070899 W JP 2014070899W WO 2015020153 A1 WO2015020153 A1 WO 2015020153A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- patch
- beraprost
- weight
- water
- acid
- Prior art date
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/335—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin
- A61K31/34—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin having five-membered rings with one oxygen as the only ring hetero atom, e.g. isosorbide
- A61K31/343—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin having five-membered rings with one oxygen as the only ring hetero atom, e.g. isosorbide condensed with a carbocyclic ring, e.g. coumaran, bufuralol, befunolol, clobenfurol, amiodarone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/557—Eicosanoids, e.g. leukotrienes or prostaglandins
- A61K31/558—Eicosanoids, e.g. leukotrienes or prostaglandins having heterocyclic rings containing oxygen as the only ring hetero atom, e.g. thromboxanes
- A61K31/5585—Eicosanoids, e.g. leukotrienes or prostaglandins having heterocyclic rings containing oxygen as the only ring hetero atom, e.g. thromboxanes having five-membered rings containing oxygen as the only ring hetero atom, e.g. prostacyclin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/02—Inorganic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/10—Alcohols; Phenols; Salts thereof, e.g. glycerol; Polyethylene glycols [PEG]; Poloxamers; PEG/POE alkyl ethers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/12—Carboxylic acids; Salts or anhydrides thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/70—Web, sheet or filament bases ; Films; Fibres of the matrix type containing drug
- A61K9/7023—Transdermal patches and similar drug-containing composite devices, e.g. cataplasms
- A61K9/703—Transdermal patches and similar drug-containing composite devices, e.g. cataplasms characterised by shape or structure; Details concerning release liner or backing; Refillable patches; User-activated patches
- A61K9/7038—Transdermal patches of the drug-in-adhesive type, i.e. comprising drug in the skin-adhesive layer
- A61K9/7046—Transdermal patches of the drug-in-adhesive type, i.e. comprising drug in the skin-adhesive layer the adhesive comprising macromolecular compounds
- A61K9/7053—Transdermal patches of the drug-in-adhesive type, i.e. comprising drug in the skin-adhesive layer the adhesive comprising macromolecular compounds obtained by reactions only involving carbon to carbon unsaturated bonds, e.g. polyvinyl, polyisobutylene, polystyrene
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/70—Web, sheet or filament bases ; Films; Fibres of the matrix type containing drug
- A61K9/7023—Transdermal patches and similar drug-containing composite devices, e.g. cataplasms
- A61K9/703—Transdermal patches and similar drug-containing composite devices, e.g. cataplasms characterised by shape or structure; Details concerning release liner or backing; Refillable patches; User-activated patches
- A61K9/7038—Transdermal patches of the drug-in-adhesive type, i.e. comprising drug in the skin-adhesive layer
- A61K9/7046—Transdermal patches of the drug-in-adhesive type, i.e. comprising drug in the skin-adhesive layer the adhesive comprising macromolecular compounds
- A61K9/7053—Transdermal patches of the drug-in-adhesive type, i.e. comprising drug in the skin-adhesive layer the adhesive comprising macromolecular compounds obtained by reactions only involving carbon to carbon unsaturated bonds, e.g. polyvinyl, polyisobutylene, polystyrene
- A61K9/7061—Polyacrylates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/70—Web, sheet or filament bases ; Films; Fibres of the matrix type containing drug
- A61K9/7023—Transdermal patches and similar drug-containing composite devices, e.g. cataplasms
- A61K9/703—Transdermal patches and similar drug-containing composite devices, e.g. cataplasms characterised by shape or structure; Details concerning release liner or backing; Refillable patches; User-activated patches
- A61K9/7038—Transdermal patches of the drug-in-adhesive type, i.e. comprising drug in the skin-adhesive layer
- A61K9/7046—Transdermal patches of the drug-in-adhesive type, i.e. comprising drug in the skin-adhesive layer the adhesive comprising macromolecular compounds
- A61K9/7069—Transdermal patches of the drug-in-adhesive type, i.e. comprising drug in the skin-adhesive layer the adhesive comprising macromolecular compounds obtained otherwise than by reactions only involving carbon to carbon unsaturated bonds, e.g. polysiloxane, polyesters, polyurethane, polyethylene oxide
Abstract
Description
(1)樹脂、プラスチック、ゴムなどの非水溶性の天然または合成高分子化合物を主基剤とし、軟化剤、粘着付与樹脂等を加えた粘着基剤(油性基剤)に、有効成分を加え全体を均質とし、布またはプラスチックフィルムに展延もしくは封入して成形する、いわゆる油性貼付剤、
(2)水溶性高分子、吸水性高分子などの天然または合成高分子化合物、更にグリセリンなどを精製水(単に水と記す場合もある)と混和し練り合わせ、有効成分を加え全体を均質にし、布などに展延して成形する貼付剤(以下、水性貼付剤と称する)、ならびに、
(3)ポリアクリル酸と多価アルコールなどを混和し練り合わせ、有効成分を加え全体を均質にし、布などに展延して成形する実質的に水を含まない貼付剤(以下、非水性貼付剤と称する)に分類することができる。
(1)ベラプロストまたはその薬理学的に許容しうる塩、水溶性高分子、多価アルコール、および架橋剤を含有してなることを特徴とする貼付剤;
(2)膏体重量に対して、ベラプロストまたはその薬理学的に許容しうる塩を0.01~10重量%、水溶性高分子を1~30重量%、多価アルコールを5~95重量%、および架橋剤を0.01~5重量%含有することを特徴とする、上記(1)に記載の貼付剤;
(3)ベラプロストまたはその薬理学的に許容しうる塩がベラプロストナトリウムである、上記(1)または(2)に記載の貼付剤;
(4)水溶性高分子が、ポリアクリル酸、ポリアクリル酸塩、ポリアクリル酸部分中和物、カルメロースナトリウム、ポリビニルアルコール、ヒドロキシエチルセルロース、ヒドロキシプロピルセルロース、およびカルボキシビニルポリマーからなる群より選択される1種あるいは2種以上である、上記(1)~(3)のいずれか1つに記載の貼付剤;
(5)多価アルコールが、プロピレングリコール、グリセリン、D-ソルビトール、および1,3-ブチレングリコールからなる群より選択される1種あるいは2種以上である、上記(1)~(4)のいずれか1つに記載の貼付剤;ならびに
(6)架橋剤が、アルミニウムグリシネートおよびメタケイ酸アルミン酸マグネシウムからなる群より選択される1種あるいは2種である、上記(1)~(5)のいずれか1つに記載の貼付剤
に関する。
また、膏体中に水分を含有しない非水性貼付剤の場合、水溶性高分子としてポリアクリル酸を含むのが好ましく、その場合、使用するポリアクリル酸は、その10重量%水溶液の粘度が5000~150000(cps/25℃)を有するものがより好ましい。
ベラプロストまたはその薬理学的に許容しうる塩がベラプロストナトリウムであり、
水溶性高分子が、ポリアクリル酸、ポリアクリル酸塩、ポリアクリル酸部分中和物、カルメロースナトリウム、ポリビニルアルコール、ヒドロキシエチルセルロース、ヒドロキシプロピルセルロース、およびカルボキシビニルポリマーからなる群より選択される1種あるいは2種以上であり、
多価アルコールが、プロピレングリコール、グリセリン、D-ソルビトール、および1,3-ブチレングリコールからなる群より選択される1種あるいは2種以上であり、かつ
架橋剤が、アルミニウムグリシネートおよびメタケイ酸アルミン酸マグネシウムからなる群より選択される1種あるいは2種である貼付剤を提供する。
ベラプロストまたはその薬理学的に許容しうる塩がベラプロストナトリウムであり、
水溶性高分子が、ポリアクリル酸、ポリアクリル酸塩、ポリアクリル酸部分中和物、カルメロースナトリウム、ポリビニルアルコール、ヒドロキシエチルセルロース、ヒドロキシプロピルセルロース、およびカルボキシビニルポリマーからなる群より選択される2種以上であり、
多価アルコールが、プロピレングリコール、グリセリン、D-ソルビトール、および1,3-ブチレングリコールからなる群より選択される2種以上であり、かつ
架橋剤が、アルミニウムグリシネートおよびメタケイ酸アルミン酸マグネシウムからなる群より選択される1種である貼付剤を提供する。
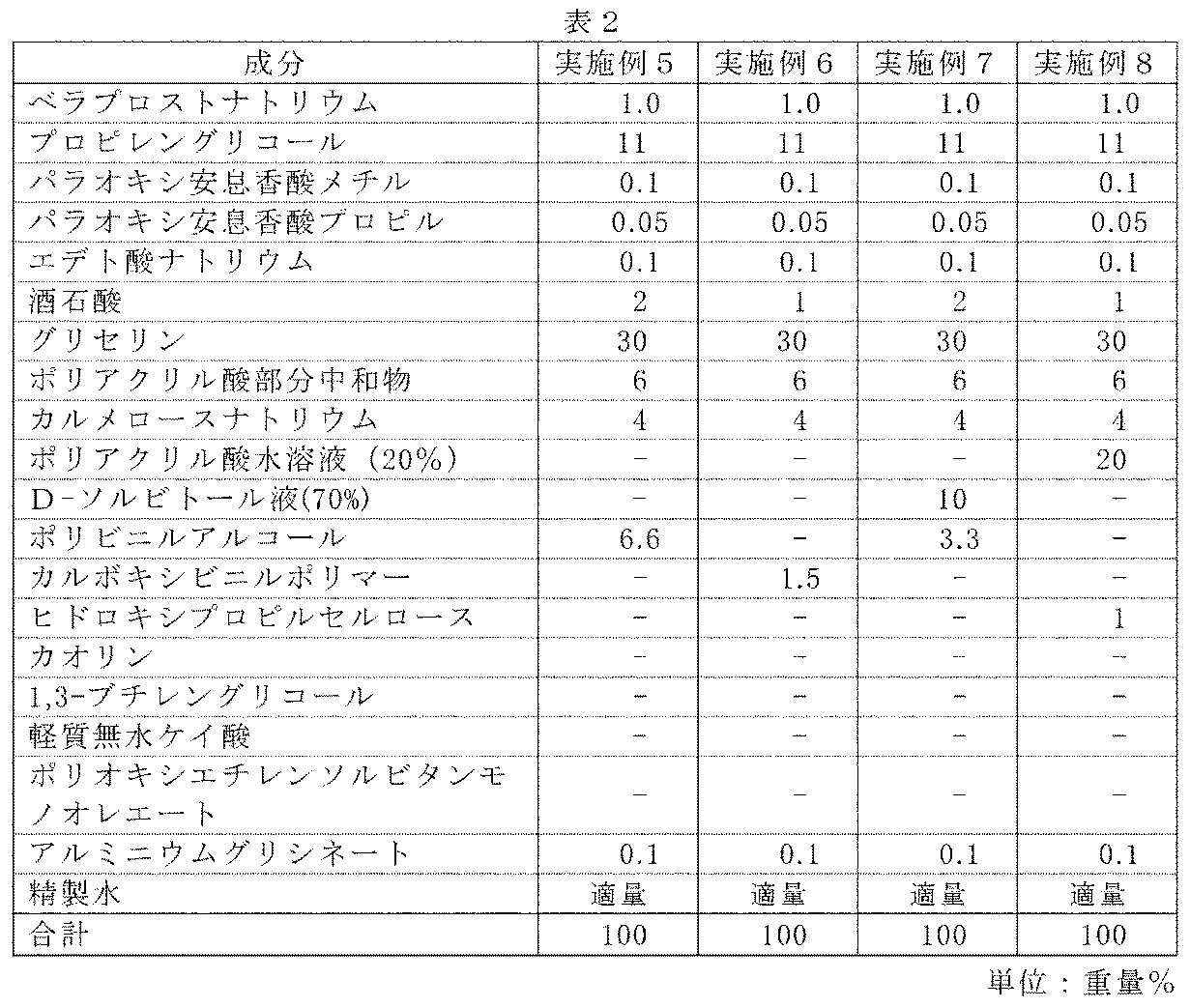
ベラプロストナトリウムをプロピレングリコールに溶解し主薬溶液とした。次に水溶性高分子、グリセリン、精製水、酒石酸、アルミニウムグリシネートおよびその他の成分を均一になるまで攪拌混合して粘着基剤を得た。最後に粘着基剤に主薬溶液を加え、均一に混合し、水性膏体を得た。この水性膏体を支持体上に500g/m2の塗布量にて均一に塗布した後、さらに剥離ライナーを被覆し、所望の大きさに裁断して本発明の貼付剤(水性貼付剤)を得た。なお、各成分の配合比は表1に示す通りである。
表1~表3に示す組成により、実施例1の製法に従い、各実施例の貼付剤を作製した。
ポリアクリル酸およびヒドロキシエチルセルロースをグリセリンに加えて加熱溶解した。冷却後、メタケイ酸アルミン酸マグネシウムをプロピレングリコールに分散させた溶液をこの液に加えて、攪拌混合し、粘着基剤を得た。最後にベラプロストナトリウムをプロピレングリコールに溶解させた主薬溶液を、粘着基剤に加え、均一に混合させ、非水性膏体を得た。この非水性膏体を支持体上に500g/m2の塗布量にて均一に塗布した後、さらに剥離ライナーを被覆し、所望の大きさに裁断して本発明の貼付剤(非水性貼付剤)を得た。なお、各成分の配合比は表4に示す通りである。
比較例1
ベラプロストナトリウムをメタノールに溶解後、酢酸エチルを添加し、主薬溶液を調製した。主薬溶液とアクリル系粘着剤(Duro-Tak 87-2516)を均一になるまで撹拌混合することによって得られた粘着剤溶液を、剥離ライナー上に伸展して酢酸エチルを乾燥除去させ、厚さ50μmの粘着剤層を形成後、支持体を貼り合わせることによりテープ剤を得た。なお、各成分の配合比は表5に示すとおりである。
ベラプロスト(遊離型)を酢酸エチルに溶解させ主薬溶液を調製した。この主薬溶液とアクリル系粘着剤(Duro-Tak 87-2516)を均一になるまで撹拌混合することによって得られた粘着剤溶液を、剥離ライナー上に伸展して溶媒を乾燥除去させ、厚さ50μmの粘着剤層を形成後、支持体を貼り合わせることによりテープ剤を得た。なお、各成分の配合比は表5に示すとおりである。
特許文献2に記載されている、実施例1の各成分の配合比、製法に従って貼付剤を作製した。なお、各成分の配合比は表5に示すとおりである。
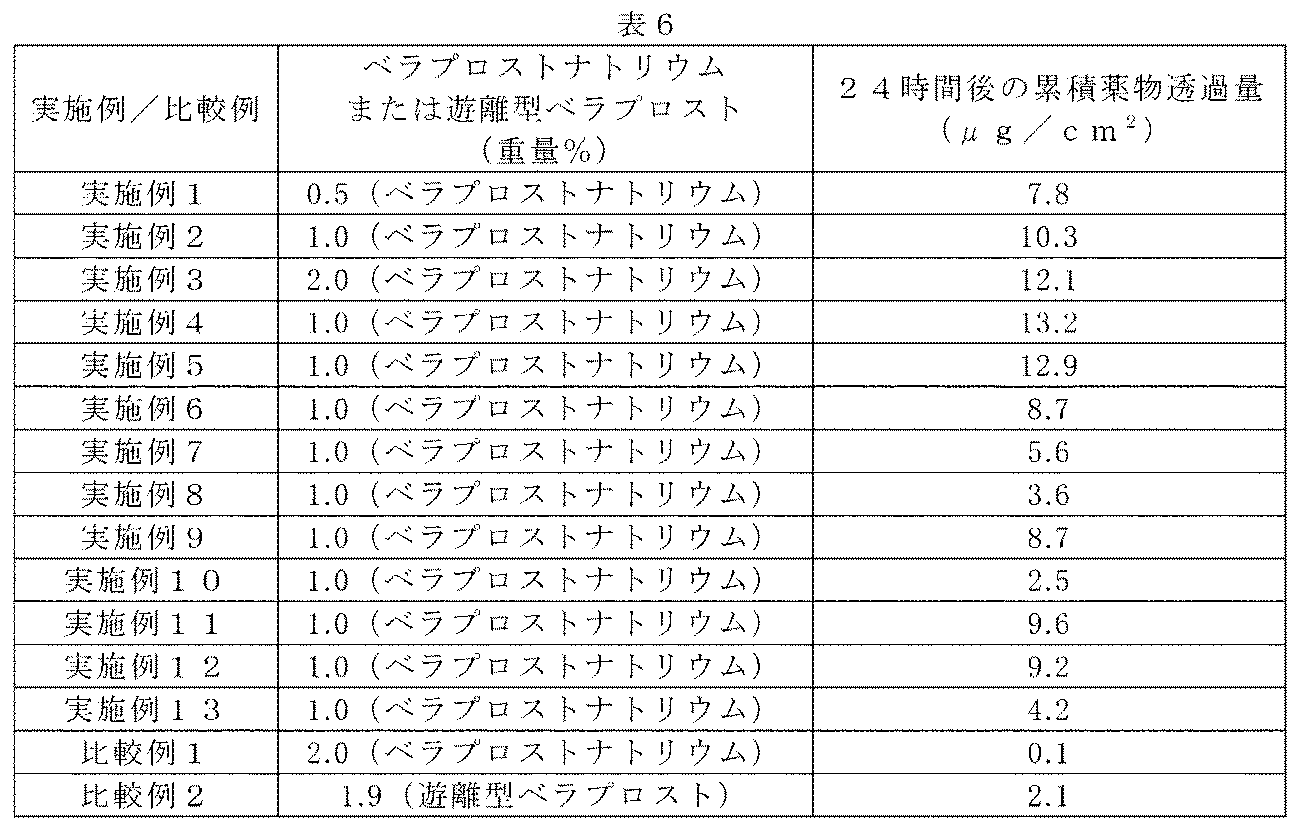
試験例1:インビトロヘアレスラット皮膚透過性試験
本発明の貼付剤におけるベラプロストの経皮吸収性を検討するため、各実施例、ならびに比較例1および2の製剤について、ヘアレスラットにおけるインビトロ皮膚透過性試験を行った。雄性ヘアレスラット(HWY系、7週齢)の腹部摘出皮膚をフランツ型拡散セルにセットし、円形(φ14mm)に裁断した各試験製剤を貼付した。レセプター側にはリン酸緩衝生理食塩水を満たし、ウォータージャケットには、37℃の温水を還流した。経時的にレセプター液をサンプリングし、皮膚を透過したベラプロスト量を液体クロマトグラフ法により測定し、その結果より、試験開始24時間後の累積透過量を算出した。その結果を、表6に示す。
各実施例および各比較例の製剤について、(1)凝集力、(2)指タック、実際に皮膚に貼付した時の(3)貼付性および(4)糊のこりの観点から各製剤の製剤物性を評価した。各試験方法は以下の通りである。
(1)凝集力:膏体面に指を押し当て、引き離した後の製剤表面の膏体の状態を目視にて観察した。
(2)指タック:膏体面に指を押し当て、引き離した時の粘着性を評価した。
(3)貼付性:各製剤を皮膚に貼付し、貼付中における製剤の浮き、ハガレ等を目視にて観察した。
(4)糊のこり:各製剤を一定時間皮膚に貼付したのち、剥離し、皮膚面に残留する膏体の有無を目視にて観察した。
各評価項目については、良好である場合には○印で示し、やや不良の場合は△印で示し、不良の場合は×印にて示した。その結果を、表7に示す。
Claims (6)
- ベラプロストまたはその薬理学的に許容しうる塩、水溶性高分子、多価アルコール、および架橋剤を含有してなることを特徴とする貼付剤。
- 膏体重量に対して、ベラプロストまたはその薬理学的に許容しうる塩を0.01~10重量%、水溶性高分子を1~30重量%、多価アルコールを5~95重量%、および架橋剤を0.01~5重量%含有することを特徴とする、請求項1に記載の貼付剤。
- ベラプロストまたはその薬理学的に許容しうる塩がベラプロストナトリウムである、請求項1または2に記載の貼付剤。
- 水溶性高分子が、ポリアクリル酸、ポリアクリル酸塩、ポリアクリル酸部分中和物、カルメロースナトリウム、ポリビニルアルコール、ヒドロキシエチルセルロース、ヒドロキシプロピルセルロース、およびカルボキシビニルポリマーからなる群より選択される1種あるいは2種以上である、請求項1~3のいずれか1項に記載の貼付剤。
- 多価アルコールが、プロピレングリコール、グリセリン、D-ソルビトール、および1,3-ブチレングリコールからなる群より選択される1種あるいは2種以上である、請求項1~4のいずれか1項に記載の貼付剤。
- 架橋剤が、アルミニウムグリシネートおよびメタケイ酸アルミン酸マグネシウムからなる群より選択される1種あるいは2種である、請求項1~5のいずれか1項に記載の貼付剤。
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CA2920284A CA2920284C (en) | 2013-08-09 | 2014-08-07 | Beraprost-containing patch |
| US14/910,738 US10335389B2 (en) | 2013-08-09 | 2014-08-07 | Beraprost-containing patch |
| JP2015530956A JP6444305B2 (ja) | 2013-08-09 | 2014-08-07 | ベラプロスト含有貼付剤 |
| EP14835157.0A EP3031459B1 (en) | 2013-08-09 | 2014-08-07 | Beraprost-containing patch |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2013-166302 | 2013-08-09 | ||
| JP2013166302 | 2013-08-09 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2015020153A1 true WO2015020153A1 (ja) | 2015-02-12 |
Family
ID=52461482
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2014/070899 WO2015020153A1 (ja) | 2013-08-09 | 2014-08-07 | ベラプロスト含有貼付剤 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US10335389B2 (ja) |
| EP (1) | EP3031459B1 (ja) |
| JP (1) | JP6444305B2 (ja) |
| CA (1) | CA2920284C (ja) |
| TW (1) | TWI643638B (ja) |
| WO (1) | WO2015020153A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2020066592A (ja) * | 2018-10-24 | 2020-04-30 | 帝國製薬株式会社 | 水性貼付剤 |
Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1996015793A1 (fr) | 1994-11-17 | 1996-05-30 | Toray Industries, Inc. | Preparation absorbable par voie percutanee |
| WO2004041270A1 (ja) * | 2002-11-05 | 2004-05-21 | Lead Chemical Co.,Ltd. | 3−メチル−1−フェニル−2−ピラゾリン−5−オン含有経皮吸収製剤 |
| WO2005046680A1 (ja) * | 2003-11-12 | 2005-05-26 | Lead Chemical Co., Ltd. | 経皮吸収型脳保護剤 |
| JP2006517224A (ja) * | 2003-02-07 | 2006-07-20 | テイコク ファーマ ユーエスエー インコーポレーテッド | 皮膚用薬の対象への投与方法 |
| WO2008146796A1 (ja) * | 2007-05-25 | 2008-12-04 | Lead Chemical Co., Ltd. | 5-メチル-1-フェニル-2-(1h)-ピリドン含有貼付剤 |
| WO2011111809A1 (ja) * | 2010-03-12 | 2011-09-15 | 帝國製薬株式会社 | ケトプロフェン含有水性貼付剤 |
| JP2013067584A (ja) | 2011-09-22 | 2013-04-18 | Hisamitsu Pharmaceut Co Inc | 貼付剤 |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20120220962A1 (en) * | 1999-12-16 | 2012-08-30 | Technology Recovery Systems, Llc | Transdermal and topical administration of vitamins using basic permeation enhancers |
| US7553867B2 (en) * | 2002-09-06 | 2009-06-30 | Takeda Pharmaceutical Company Limited | Furan or thiophene derivative and medicinal use thereof |
| EP2968362A4 (en) * | 2013-03-15 | 2016-10-05 | Gemmus Pharma Inc | BERAPROST ISOMER AS A MEANS FOR THE TREATMENT OF VIRUS INFECTIONS |
-
2014
- 2014-08-07 WO PCT/JP2014/070899 patent/WO2015020153A1/ja active Application Filing
- 2014-08-07 US US14/910,738 patent/US10335389B2/en active Active
- 2014-08-07 TW TW103127106A patent/TWI643638B/zh active
- 2014-08-07 JP JP2015530956A patent/JP6444305B2/ja active Active
- 2014-08-07 CA CA2920284A patent/CA2920284C/en active Active
- 2014-08-07 EP EP14835157.0A patent/EP3031459B1/en active Active
Patent Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1996015793A1 (fr) | 1994-11-17 | 1996-05-30 | Toray Industries, Inc. | Preparation absorbable par voie percutanee |
| WO2004041270A1 (ja) * | 2002-11-05 | 2004-05-21 | Lead Chemical Co.,Ltd. | 3−メチル−1−フェニル−2−ピラゾリン−5−オン含有経皮吸収製剤 |
| JP2006517224A (ja) * | 2003-02-07 | 2006-07-20 | テイコク ファーマ ユーエスエー インコーポレーテッド | 皮膚用薬の対象への投与方法 |
| WO2005046680A1 (ja) * | 2003-11-12 | 2005-05-26 | Lead Chemical Co., Ltd. | 経皮吸収型脳保護剤 |
| WO2008146796A1 (ja) * | 2007-05-25 | 2008-12-04 | Lead Chemical Co., Ltd. | 5-メチル-1-フェニル-2-(1h)-ピリドン含有貼付剤 |
| WO2011111809A1 (ja) * | 2010-03-12 | 2011-09-15 | 帝國製薬株式会社 | ケトプロフェン含有水性貼付剤 |
| JP2013067584A (ja) | 2011-09-22 | 2013-04-18 | Hisamitsu Pharmaceut Co Inc | 貼付剤 |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2020066592A (ja) * | 2018-10-24 | 2020-04-30 | 帝國製薬株式会社 | 水性貼付剤 |
Also Published As
| Publication number | Publication date |
|---|---|
| CA2920284C (en) | 2021-08-24 |
| TW201605496A (zh) | 2016-02-16 |
| US20160193178A1 (en) | 2016-07-07 |
| TWI643638B (zh) | 2018-12-11 |
| EP3031459A4 (en) | 2017-04-19 |
| EP3031459A1 (en) | 2016-06-15 |
| JPWO2015020153A1 (ja) | 2017-03-02 |
| EP3031459B1 (en) | 2019-01-09 |
| US10335389B2 (en) | 2019-07-02 |
| CA2920284A1 (en) | 2015-02-12 |
| JP6444305B2 (ja) | 2018-12-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5301190B2 (ja) | 貼付剤 | |
| ES2705028T3 (es) | Yeso a base de agua | |
| KR102000435B1 (ko) | 하이드로겔 패치 형태의 경피투여용 약학 조성물 | |
| AU2010204986A1 (en) | Transdermal administration of tamsulosin | |
| WO2006090782A1 (ja) | 含水系外用貼付剤用組成物及びこの組成物を用いた貼付剤 | |
| WO2019142940A1 (ja) | 皮膚貼付用粘着シート | |
| JP4879928B2 (ja) | ケトプロフェンリジン塩を含有する水性貼付剤 | |
| JP2001302502A (ja) | インドメタシン貼付剤 | |
| JP2011088862A (ja) | ジクロフェナクナトリウム含有水性貼付剤 | |
| JP4799783B2 (ja) | 伸縮性外用貼付剤 | |
| JP6444305B2 (ja) | ベラプロスト含有貼付剤 | |
| JP5319950B2 (ja) | 塩酸ブテナフィン含有水性貼付剤 | |
| JP4890856B2 (ja) | ジクロフェナク含有貼付剤 | |
| JP5358551B2 (ja) | フェニル酢酸誘導体類及びメントール類を含有する消炎鎮痛剤及び消炎鎮痛作用増強方法 | |
| JP3193161B2 (ja) | 経皮吸収性製剤 | |
| JP4237293B2 (ja) | 経皮吸収型貼付剤 | |
| JP2005529150A (ja) | 気管支拡張薬を有するマトリックスタイプパッチ | |
| JPS6116369B2 (ja) | ||
| JP2002029971A (ja) | インドメタシン水溶性貼付剤 | |
| WO2021192270A1 (ja) | 含水系貼付剤 | |
| TW202202147A (zh) | 貼附劑 | |
| WO2022065430A1 (ja) | 医薬品用含水系貼付剤 | |
| WO2022064608A1 (ja) | 非医薬品用含水系貼付剤 | |
| JP2020164471A (ja) | 貼付材 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 14835157 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2015530956 Country of ref document: JP Kind code of ref document: A |
|
| ENP | Entry into the national phase |
Ref document number: 2920284 Country of ref document: CA |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2014835157 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 14910738 Country of ref document: US |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |