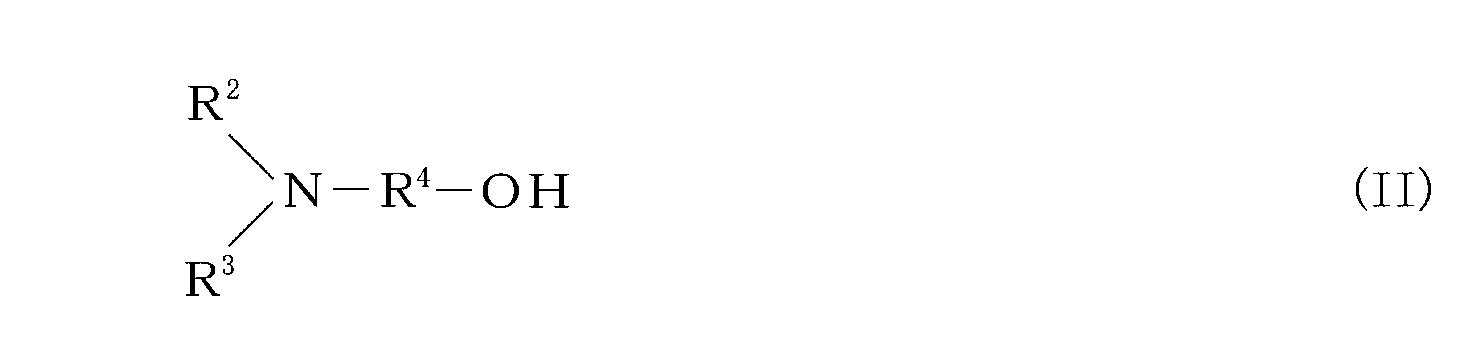WO2014208686A1 - (メタ)アクリル酸エステルの製造システム - Google Patents
(メタ)アクリル酸エステルの製造システム Download PDFInfo
- Publication number
- WO2014208686A1 WO2014208686A1 PCT/JP2014/067043 JP2014067043W WO2014208686A1 WO 2014208686 A1 WO2014208686 A1 WO 2014208686A1 JP 2014067043 W JP2014067043 W JP 2014067043W WO 2014208686 A1 WO2014208686 A1 WO 2014208686A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- distillation
- meth
- acrylic acid
- distillation column
- acid ester
- Prior art date
Links
Images
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D3/00—Distillation or related exchange processes in which liquids are contacted with gaseous media, e.g. stripping
- B01D3/009—Distillation or related exchange processes in which liquids are contacted with gaseous media, e.g. stripping in combination with chemical reactions
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C67/00—Preparation of carboxylic acid esters
- C07C67/03—Preparation of carboxylic acid esters by reacting an ester group with a hydroxy group
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D3/00—Distillation or related exchange processes in which liquids are contacted with gaseous media, e.g. stripping
- B01D3/42—Regulation; Control
- B01D3/4205—Reflux ratio control splitter
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C67/00—Preparation of carboxylic acid esters
- C07C67/48—Separation; Purification; Stabilisation; Use of additives
- C07C67/52—Separation; Purification; Stabilisation; Use of additives by change in the physical state, e.g. crystallisation
- C07C67/54—Separation; Purification; Stabilisation; Use of additives by change in the physical state, e.g. crystallisation by distillation
Definitions
- the present invention relates to a (meth) acrylic acid ester production system. More specifically, the present invention relates to a (meth) acrylic acid ester production system capable of efficiently producing a (meth) acrylic acid ester by a transesterification method.
- the (meth) acrylic acid ester is a compound useful as a raw material for, for example, a (meth) acrylic resin, a surfactant, an adhesive, or a paint, although depending on the type.
- (meth) acrylic acid ester means “acrylic acid ester” and / or “methacrylic acid ester”.
- methyl (meth) acrylate can be recovered from the bottom of the reactor, but after the methyl (meth) acrylate is recovered, it remains in the reactor (meta) ) Unable to recover methyl acrylate.
- an azeotropic solvent that forms an azeotropic composition with the by-produced alkyl alcohol is used as a method for producing the target compound (meth) acrylic acid ester by transesterification of the raw material (meth) acrylic acid alkyl ester and alcohol.
- an azeotropic solvent that forms an azeotropic composition with the by-produced alkyl alcohol is used as a method for producing the target compound (meth) acrylic acid ester by transesterification of the raw material (meth) acrylic acid alkyl ester and alcohol.
- the boiling point of the azeotropic solvent is not less than the azeotropic temperature of the azeotropic solvent and not more than 2 ° C higher than the azeotropic temperature, and the bottom temperature of the distillation column is not less than 10 ° C lower than the boiling point of the azeotropic solvent.
- a method for producing a (meth) acrylic acid ester has been proposed (see, for example, Patent Document 2).
- the present invention has been made in view of the prior art, and after producing a (meth) acrylic acid ester by a transesterification method, a raw material (meth) acrylic acid ester remaining in the reaction system, a solvent, A system for producing (meth) acrylic acid esters by a transesterification method that can efficiently recover and reuse by-produced alcohol, etc., and can efficiently produce the desired (meth) acrylic acid esters.
- the issue is to provide.
- the present invention (1) A (meth) acrylic acid ester production system used when producing a (meth) acrylic acid ester by transesterification, A reaction apparatus A having a distillation column and a distillation apparatus B having a distillation column;
- the upper part of the distillation column of the reaction apparatus A is connected to the condensing device via a pipe, and the condensing device and the upper part of the distillation column Is connected via a switching device, and the condenser and the liquid separation device are connected via the switching device in a pipe for sending the remainder of the condensate obtained by the condensing device to the liquid separation device,
- the upper part of the separator and the distillation tower are connected by a pipe for refluxing the upper liquid to the distillation tower.
- the lower part of the condensate separated by the separator is connected to the distillation tower.
- the lower part of the separator and the distillation device B are connected by piping for feeding the liquid to the distillation device B
- the upper part of the distillation column of the distillation apparatus B is connected to the condensing apparatus via a pipe, and the condensing apparatus and the upper part of the distillation column are connected to the upper part of the distillation column by a pipe for refluxing a part of the condensate obtained by the condensing apparatus to the upper part of the distillation column.
- a pipe for refluxing the residue present in the distillation apparatus B to the distillation tower of the reaction apparatus A is connected to the lower part of the distillation apparatus B and a pipe between the switching apparatus and the condensation apparatus of the reaction apparatus A.
- (Meth) acrylic acid ester production system (manufacturing equipment), and (2) (meth) acrylic acid ester production system used when producing (meth) acrylic acid ester by transesterification
- a reaction apparatus A having a distillation tower, a distillation apparatus B having a distillation tower, and a distillation apparatus C having a distillation tower
- the upper part of the distillation column of the reaction apparatus A is connected to the condensing device via a pipe
- the condensing device and the upper part of the distillation column Is connected via a switching device
- the condenser and the liquid separation device are connected via the switching device in a pipe for sending the remainder of the condensate obtained by the condensing device to the liquid separation device
- the upper part of the separator and the distillation tower are connected by a pipe for refluxing the upper liquid to the distillation tower.
- the lower part of the condensate separated by the separator is connected to the distillation tower.
- the lower part of the separator and the distillation device B are connected by piping for feeding the liquid to the distillation device B
- the upper part of the distillation column of the distillation apparatus B is connected to the condensing apparatus via a pipe, and the condensing apparatus and the upper part of the distillation column are connected to the upper part of the distillation column by a pipe for refluxing a part of the condensate obtained by the condensing apparatus to the upper part of the distillation column.
- the condenser and the recovery unit are connected via a switching device in a pipe for feeding to the recovery unit for recovering the remaining portion of the condensate obtained by the condensing device
- the lower part of the distillation apparatus B and the distillation apparatus C are connected by a pipe for sending the residue present in the distillation apparatus B to the distillation tower of the distillation apparatus C
- the upper part of the distillation column of the distillation apparatus C is connected to the condensing apparatus through a pipe, and the condensing apparatus and the upper part of the distillation tower are connected to the upper part of the distillation column by a pipe for refluxing a part of the condensate obtained by the condensing apparatus to the upper part of the distillation column.
- a pipe for sending the residue present in the distillation apparatus C to the distillation tower of the reaction apparatus A is connected to the lower part of the distillation apparatus C and a pipe between the switching apparatus and the condensation apparatus of the reaction apparatus A.
- the raw material (meth) acrylic acid ester remaining in the reaction system, the solvent, As a by-product alcohol and the like can be efficiently recovered and reused, an excellent effect that the target (meth) acrylic acid ester can be efficiently produced is exhibited.
- (meth) acrylic acid esters such as methyl (meth) acrylate are temperature-sensitive compounds and polymerize easily, so that a reactor is used to suppress the polymerization of the (meth) acrylic acid ester.
- a system in which the raw material (meth) acrylic acid ester remaining inside is recovered by distillation under reduced pressure at a low temperature is conceivable.
- a (meth) acrylic acid ester production system in which a system is functionally constructed using the reaction apparatus A having a distillation column and the distillation apparatus B having a distillation column.
- a (meth) acrylic ester production system in which a system is functionally constructed using a reaction apparatus A having a distillation column, a distillation apparatus B having a distillation column, and a distillation apparatus C having a distillation column can recover the (meth) acrylic acid ester used as a raw material remaining in the reaction apparatus A from the reaction apparatus A under normal pressure without using the decompression operation as described above.
- the recovered raw material (meth) acrylic acid ester is used when the raw material (meth) acrylic acid ester and the alcohol corresponding to the target compound (meth) acrylic acid ester are newly transesterified. It has also been found that it can be suitably used as a (meth) acrylic acid ester.
- the (meth) acrylic acid ester production system of the present invention there is no need to depressurize, and the raw material (meth) acrylic acid ester remaining in the reactor A even under normal pressure can be obtained. It can be efficiently recovered, and the solvent, by-product alcohol, etc. can be efficiently recovered and reused, and the desired (meth) acrylic acid ester can be efficiently manufactured, and further recovered The (meth) acrylic ester thus produced can be reused.
- the (meth) acrylic acid ester production system of the present invention is a (meth) acrylic acid ester production system excellent in industrial productivity.
- the (meth) acrylic acid ester production system of the present invention is a (meth) acrylic acid ester production system used when producing a (meth) acrylic acid ester by transesterification as described above.
- the production system for a (meth) acrylic acid ester of the present invention has a reaction apparatus A having a distillation tower and a distillation apparatus B having a distillation tower, and the upper part of the distillation tower of the reaction apparatus A is connected to a condensing apparatus via a pipe.
- Condensate obtained by the condenser by connecting the condenser and the upper part of the distillation tower via a switching device with a pipe for refluxing a part of the condensate obtained by the condenser to the upper part of the distillation tower.
- a condenser and a separator are connected via a switching device with a pipe for sending the remainder of the liquid to a separator, and the upper liquid of the condensed liquid separated by the separator is returned to the distillation column.
- the upper part of the separation device is connected to the distillation tower by piping for causing the lower part of the condensate separated by the separation device to flow to the distillation device B, and the lower part of the separation device is connected to the distillation device B.
- the condensing unit is connected to the upper part of the distillation column via a switching device and is connected to the upper part of the distillation column by a pipe for refluxing a part of the condensate obtained by the condensing unit to the upper part of the distillation column.
- the condensing unit and the recovery unit are connected via a switching device in a pipe for feeding the recovery unit for recovering the remaining condensate, and the residue present in the distillation unit B is removed from the distillation column of the reactor A.
- the lower part of the distillation apparatus B and the pipe between the switching device of the reaction apparatus A and the condensing apparatus are connected by a pipe for recirculating to the pipe.
- the (meth) acrylic acid ester production system includes a reaction apparatus A having a distillation tower, a distillation apparatus B having a distillation tower, and a distillation apparatus C having a distillation tower,
- the upper part of the distillation column of the apparatus A is connected to the condensing device via a pipe, and the condensing device and the upper part of the distilling column are connected by a pipe for refluxing a part of the condensate obtained by the condensing device to the upper part of the distillation column.
- the condenser and the separator are connected via the switching device by a pipe connected to the separator and connected to the separator by the piping for feeding the remaining portion of the condensate obtained by the condenser to the separator.
- the upper part of the separator is connected to the distillation tower by a pipe for refluxing the upper liquid to the distillation tower, and the lower part of the condensate separated by the separator is distilled.
- the lower part of the separator and the distillation unit B are connected by piping for feeding to B.
- the upper part of the distillation tower of the distillation apparatus B is connected to the condensing apparatus via a pipe, and the upper part of the condensing apparatus and the distillation tower is connected to the upper part of the distillation tower by refluxing a part of the condensate obtained by the condensing apparatus.
- a condenser and a recovery unit are connected via a switching device in a pipe for feeding to a recovery unit for recovering the remainder of the condensate obtained by the condensing device
- the lower part of the distillation apparatus B and the distillation apparatus C are connected by a pipe for sending the residue present in the distillation apparatus B to the distillation tower of the distillation apparatus C, and the upper part of the distillation tower of the distillation apparatus C is connected via the pipe.
- the condenser is connected to the condenser, and the condenser and the upper part of the distillation tower are connected via a switching device in a pipe for refluxing a part of the condensate obtained in the condenser to the upper part of the distillation tower.
- the condensing device and the recovery unit are connected via a switching device, and a pipe for feeding the residue present in the distillation device C to the distillation tower of the reaction device A, and the switching of the reaction device A.
- a pipe between the apparatus and the condenser is connected by a pipe.
- Examples of the (meth) acrylic acid ester used as a raw material in the (meth) acrylic acid ester production system of the present invention include (meth) acrylic having 1 to 8 carbon atoms in the alkyl group such as methyl (meth) acrylate. Although acid alkyl ester etc. are mentioned, this invention is not limited only to this illustration.
- the transesterification reaction between the (meth) acrylic acid ester used as a raw material and the alcohol corresponding to the (meth) acrylic acid ester of the target compound may be carried out by either a flow system or a batch system.
- a (meth) acrylic acid ester used as a raw material and an alcohol corresponding to the target compound (meth) acrylic acid ester are transesterified.
- the alcohol used when transesterifying the (meth) acrylic acid ester used as a raw material with the alcohol is appropriately selected according to the (meth) acrylic acid ester of the target compound. More specifically, an alcohol that forms an ester group of the (meth) acrylic acid ester of the target compound is used as the alcohol. As an example, for example, when the (meth) acrylic acid ester of the target compound is n-propyl (meth) acrylate, n-propyl alcohol is used as the alcohol that forms the propyl group.
- Examples of the alcohol corresponding to the target compound (meth) acrylic acid ester include ethyl alcohol, n-propyl alcohol, isopropyl alcohol, n-butyl alcohol, isobutyl alcohol, sec-butyl alcohol, tert-butyl alcohol, and n-pentyl.
- n-hexyl alcohol isohexyl alcohol, cyclohexyl alcohol, 3,3,5-trimethylcyclohexyl alcohol, 4-tert-butylcyclohexyl alcohol, n-heptyl alcohol, n-octyl alcohol, isooctyl alcohol, 2-ethylhexyl Alcohol, 3,4-dimethylhexyl alcohol, 3,4-dimethylheptyl alcohol, lauryl alcohol, nonyl alcohol, isononyl alcohol Stearyl alcohol, expressions such as 2-heptyl undecanoic-1-ol (I):
- Aliphatic or alicyclic alcohol represented by: aromatic alcohol such as phenol, benzyl alcohol, 1-phenylethyl alcohol, 2-phenylethyl alcohol, phenoxyethanol; dimethylaminoethyl alcohol, diethylaminoethyl alcohol, dipropylaminoethyl alcohol, Dibutylaminoethyl alcohol, dipentylaminoethyl alcohol, dihexylaminoethyl alcohol, dioctylaminoethyl alcohol, methylethylaminoethyl alcohol, methylpropylaminoethyl alcohol, methylbutylaminoethyl alcohol, methylhexylaminoethyl alcohol, ethylpropylaminoethyl alcohol, Ethylbutylaminoethyl alcohol, ethylpenty
- R 2 and R 3 each independently represents a hydrogen atom or an alkyl group having 1 to 8 carbon atoms, and R 4 represents an alkylene group having 1 to 4 carbon atoms
- the amount of (meth) acrylic ester used as a raw material per equivalent of hydroxyl group of alcohol corresponding to the (meth) acrylic ester of the target compound is determined by transesterification of (meth) acrylic ester used as the raw material with the alcohol. From the viewpoint of increasing the reaction rate of the reaction, it is preferably 0.3 equivalents or more, more preferably 0.5 equivalents or more, further preferably 0.8 equivalents or more, and a (meth) acrylic acid ester used as an unreacted raw material From the viewpoint of reducing the amount, the amount is preferably 5 equivalents or less, more preferably 4 equivalents or less, and even more preferably 3 equivalents or less.
- (Meth) acrylic acid acrylate may be mentioned as a (meth) acrylic acid ester used as a suitable raw material.
- a transesterification catalyst When the (meth) acrylic acid ester used as a raw material and the alcohol corresponding to the target compound (meth) acrylic acid ester are transesterified, a transesterification catalyst can be used.
- transesterification catalyst examples include lithium hydroxide, sodium hydroxide, potassium hydroxide, cesium hydroxide, magnesium hydroxide, calcium hydroxide, barium hydroxide, strontium hydroxide and the like; lithium hydrogen carbonate, carbonic acid Hydrogen carbonate compounds such as sodium hydrogen carbonate, potassium hydrogen carbonate, cesium hydrogen carbonate, magnesium hydrogen carbonate, calcium hydrogen carbonate, barium hydrogen carbonate, strontium hydrogen carbonate; lithium carbonate, sodium carbonate, potassium carbonate, cesium carbonate, magnesium carbonate, calcium carbonate, Carbonates such as barium carbonate and strontium carbonate; acetates such as lithium acetate, sodium acetate, potassium acetate, cesium acetate, magnesium acetate, calcium acetate, barium acetate and strontium acetate; lithium borohydride Boron hydride compounds such as sodium borohydride, potassium borohydride, cesium borohydride; lithium stearate, sodium stearate, potassium stearate, cesium stea
- Benzoates such as dilithium hydrogen phosphate, disodium hydrogen phosphate, dipotassium hydrogen phosphate, and cesium hydrogen phosphate; dilithium phenyl phosphate; Phenyl phosphate compounds such as disodium phenyl phosphate, dipotassium phenyl phosphate, and cesium phenyl phosphate; metal alkoxides such as sodium alkoxide and titanium alkoxide; tetramethoxy titanium, tetraethoxy titanium, tetrapropoxy titanium, tetrabutoxy titanium, etc.
- Tetraalkoxytitanium dialkyltin oxides such as dialkyltin oxide having 4 to 18 carbon atoms in the alkyl group such as dibutyltin oxide, dioctyltin oxide, dilauryltin oxide; titanium alcoholate, aluminum alcoholate, magnesium alcoholate Although metal alcoholates such as copper are listed, the present invention is not limited to such examples.
- dialkyltin oxides such as dialkyltin oxide having 4 to 18 carbon atoms in the alkyl group such as dibutyltin oxide, dioctyltin oxide, dilauryltin oxide
- titanium alcoholate aluminum alcoholate
- magnesium alcoholate metal alcoholates such as copper are listed, the present invention is not limited to such examples.
- These transesterification catalysts may be used alone or in combination of two or more.
- transesterification catalysts from the viewpoint of promoting the transesterification reaction, tetraalkoxytitanium and dialkyltin oxide having 4 to 12 carbon atoms in the alkyl group are preferable, and tetraalkoxytitanium and alkyl group having 4 to 4 carbon atoms. More preferred are 8 dialkyltin oxides, and tetramethoxytitanium, dibutyltin oxide and dioctyltin oxide are even more preferred.
- the amount of the transesterification catalyst varies depending on the type of the transesterification catalyst and cannot be determined unconditionally, it is preferably determined appropriately according to the type of the transesterification catalyst.
- the amount of the transesterification catalyst per mole of (meth) acrylic acid ester used as a raw material is preferably from the viewpoint of efficiently proceeding the transesterification reaction of (meth) acrylic acid ester used as a raw material with an alcohol. It is 0.00001 mol or more, more preferably 0.0001 mol or more, and from the viewpoint of improving economy, it is preferably 0.10 mol or less, more preferably 0.05 mol or less.
- a polymerization inhibitor when the (meth) acrylic acid ester used as a raw material and an alcohol are subjected to a transesterification reaction, a polymerization inhibitor can be used.
- the polymerization inhibitor include 4-hydroxy-2,2,6,6-tetramethylpiperidine-N-oxyl, 4-acetamino-2,2,6,6-tetramethylpiperidine-N-oxyl, 4- Benzoyloxy-2,2,6,6-tetramethylpiperidine-N-oxyl, 4-oxo-2,2,6,6-tetramethylpiperidine-N-oxyl, 2,2,6,6-tetramethylpiperidine N-oxy radical compounds such as —N-oxyl; paramethoxyphenol, 2,2′-methylenebis (4-ethyl-6-tert-butylphenol), 2,6-ditert-butyl-4-methylphenol, 2 , 6-Ditert-butyl-N, N-dimethylamino-p-cresol, 2,4-d
- the amount of the polymerization inhibitor per 100 parts by mass of the (meth) acrylic acid ester used as a raw material is from the viewpoint of suppressing polymerization of the (meth) acrylic acid ester used as the raw material and the (meth) acrylic acid ester of the target compound.
- it is 0.00001 parts by mass or more, more preferably 0.00005 parts by mass or more, and further preferably 0.0001 parts by mass or more, and preferably 0 from the viewpoint of increasing the purity of the (meth) acrylic acid ester of the target compound.
- (meth) acrylic used as a raw material as a solvent As a raw material, it azeotropes with the by-product alcohol at a temperature below the boiling point of the alcohol by-produced by the transesterification reaction between the acid ester and the alcohol corresponding to the (meth) acrylic acid ester of the target compound It is preferable to use an azeotropic solvent that azeotropes with the (meth) acrylic acid ester used as the raw material at a temperature below the boiling point of the (meth) acrylic acid ester used.
- the (meth) acrylic acid ester used as the raw material at a temperature lower than the boiling point of the (meth) acrylic acid ester used as a raw material is azeotroped with the by-product alcohol at a temperature lower than the boiling point of the by-product alcohol as a solvent.
- a transesterification reaction is carried out.
- the (meth) acrylic acid ester used as a raw material existing in the reactor can be efficiently recovered from the reactor A.
- the boiling solvent for example, when the (meth) acrylic acid ester used as a raw material is methyl (meth) acrylate, since the by-product alcohol is methyl (meth) acrylate, cyclohexane, n-hexane, etc.
- these azeotropic solvents may be used alone or in combination.
- cyclohexane is preferable from the viewpoint of shortening the reaction time of the transesterification reaction and efficiently recovering the (meth) acrylic acid ester used as a raw material.
- the amount of the solvent is not particularly limited, but is usually about 5 to 200 parts by mass per 100 parts by mass of the total amount of the (meth) acrylic acid ester used as a raw material and the alcohol corresponding to the (meth) acrylic acid ester of the target compound. If it is.
- solvents may be used as long as the object of the present invention is not impaired.
- examples of other solvents include n-pentane, n-hexane, isohexane, n-heptane, n-octane, 2,3-dimethylbutane, 2,5-dimethylhexane, and 2,2,4-trimethylpentane.
- examples include aliphatic hydrocarbon compounds having 5 to 8 carbon atoms other than cyclohexane, but the present invention is not limited to such examples.
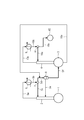
- FIG. 1 is a schematic explanatory view showing one embodiment of the (meth) acrylic acid ester production system of the present invention.
- the reaction apparatus A1 having the distillation column 2 is used. .
- Examples of the reaction apparatus A1 having the distillation column 2 include a reaction apparatus having a distillation column such as a rectification column, a fluidized bed, a fixed bed, and a reactive distillation column.
- a reaction apparatus having a distillation column such as a rectification column, a fluidized bed, a fixed bed, and a reactive distillation column.
- the present invention is limited only to such examples. It is not something.
- suitable distillation column 2 include a packed column type distillation column and a tray type distillation column.
- Examples of the tray type distillation column include a packed column type distillation machine, an Oldershaw type distillation column, a lift tray type distillation column, and the like, but the present invention is not limited to such examples.
- the number of theoretical plates of the distillation column 2 is preferably from the viewpoint of efficiently and stably proceeding the transesterification reaction between the (meth) acrylic acid ester used as a raw material and the alcohol corresponding to the (meth) acrylic acid ester of the target compound. It is 7 steps or more, more preferably 10 steps or more, and further preferably 15 steps or more. From the viewpoint of improving economy, it is preferably 100 steps or less, more preferably 70 steps or less, and even more preferably 50 steps or less.
- a condensing device 6 is disposed at the top of the distillation column 2 of the reactor A1, preferably at the top of the column via a pipe 5a. Further, in order to recirculate a part of the condensate obtained in the condensing device 6 to the upper part of the distillation column 2, preferably the top of the column, the condensing device 6 and the switching device 7 are connected via a pipe 5b. 7 and the upper part of the distillation column 2, preferably the top of the column are connected via a pipe 5c. Examples of the condensing device 6 include a capacitor, but the present invention is not limited to such an example.
- the switching device 7 is provided to send the condensate obtained by the condensing device 6 to the upper part of the distillation column 2, preferably the top of the column or the liquid separating device 8.
- Examples of the switching device 7 include a switching valve, a reflux distributor, an electromagnetic valve, and the like, but the present invention is not limited to such an example.
- the condensing device 6 and the switching device 7 are connected via a pipe 5b, and the switching device 7 and the liquid separating device 8 are connected. It is connected via a pipe 5d. Therefore, a part of the condensate obtained in the condensing device 6 is sent to the upper part of the distillation column 2, preferably the top of the column via the switching device 7, and the remainder of the condensate switches the switching device 7. Thus, the liquid is fed to the liquid separator 8.
- the separator 8 used when separating the condensate into two layers, an upper layer and a lower layer include a decanter, a separatory funnel, and an oil-moisture liquid device. It is not limited.
- the upper part of the separator 8 and the distillation tower 2 are connected via a pipe 5e in order to return the upper liquid of the condensed liquid separated by the separator 8 to the distillation tower 2.
- the position where the pipe 5e in the distillation column 2 is connected is not particularly limited, but the (meth) acrylic acid ester used as a raw material and the alcohol corresponding to the (meth) acrylic acid ester of the target compound are efficiently transesterified. From this viewpoint, it is preferable to supply to the middle part of the distillation column 2.
- the middle part of the distillation column 2 means a stage near the center of the multistage distillation column. For example, when the distillation column 2 is a distillation column having 15 theoretical plates, 6 to 9 plates correspond to the middle portion of the distillation column 2.
- the lower part of the liquid separator 8 and the distillation apparatus B3 are connected by a pipe 5f in order to send the lower liquid to the distillation apparatus B3.
- the distillation apparatus B3 having the distillation tower 4 may be either a batch type or a flow type.
- Examples of the distillation column 4 of the distillation apparatus B3 include a packed column and a tray-type distillation column, but the present invention is not limited to such examples.
- Examples of the packing used in the packed tower include a helipack, a McMahon, a cascade mini-ring, and the like, but the present invention is not limited to such examples.
- Examples of the tray type distillation column include a packed column type distillation machine, an Oldershaw type distillation column, a lift tray type distillation column, and the like, but the present invention is not limited to such examples.
- the upper part, preferably the top of the distillation column 4 of the distillation device B3 is connected to the condensing device 9 via a pipe 10a.
- the condensing device 9 and the switching device 11 are connected via a pipe 10b.
- the upper part of the distillation column 4, preferably the top of the column, is connected via a pipe 10c.
- the condensing device 9 and the switching device 11 are connected via a pipe 10b, and the switching device 11 and the collecting part 12 are connected via a pipe 10d. ing. Therefore, a part of the condensate obtained in the condensing device 9 is sent to the upper part of the distillation column 4, preferably the top of the column via the switching device 11, and the remainder of the condensate switches the switching device 11. Thus, the liquid is fed to the collection unit 12.
- the switching device 11 include a switching valve, a reflux distributor, an electromagnetic valve, and the like, but the present invention is not limited to such an example.
- the collection unit 12 may be a so-called receiver.
- a pipe 10e is connected to the lower part of the distillation apparatus B3, and the other end of the pipe 10e is a switching apparatus for the reaction apparatus A1.
- a three-way cock (not shown) or the like is connected to the pipe 5d between the separator 7 and the liquid separator 8.
- a reaction apparatus is obtained by azeotropically evaporating the solvent and the by-product alcohol.
- By-product alcohol vapor is preferably removed from the upper part of the distillation column 2 attached to A1, preferably from the top of the column.
- the top temperature of the distillation column 2 is preferably 5 ° C. higher than the azeotropic temperature from the azeotropic temperature of the by-product alcohol and the solvent. Is preferably adjusted to be in the temperature range up to 2 ° C. higher.
- the vapor is taken out from the upper part of the distillation column 2 and the vapor is condensed into the condenser 6.
- By-condensation, by-product alcohol can be recovered as a condensate.
- a part of the condensate obtained by the condenser 6 is refluxed to the distillation column 2 by operating the switching device 7 so that the pipe 5b and the pipe 5c communicate with each other.
- the remainder of the condensate is removed out of the system of the reaction apparatus A1 via the liquid separator 8 by operating the switching device 7 so that the piping 5b and the piping 5d communicate with each other.
- the heating temperature of the reaction device A1 is not controlled by operating the switching device 7 and refluxing the condensate obtained in the condensation device 6 to the distillation column 2 or removing it from the system of the reaction device A1.
- the temperature at the top of the distillation column 2 can be easily adjusted to the azeotropic temperature of the by-product alcohol and the solvent.
- the condensate removed from the reaction apparatus A1 by operating the switching device 7 so that the piping 5b and the piping 5d communicate with each other is sent to the separation device 8.
- the separation liquid By adding water to the condensate sent to the separation device 8, the separation liquid can be efficiently separated into two layers of an upper layer and a lower layer.
- the amount of water per 100 parts by volume of the condensate is not particularly limited, but usually it is preferably 10 parts by volume or more, more preferably 20 parts by volume or more from the viewpoint of efficiently separating the upper layer and the lower layer. From the viewpoint of reducing the amount of the lower layer, it is preferably 300 parts by volume or less, more preferably 200 parts by volume or less.
- the temperature of the condensate when water is added to the condensate is preferably 0 to 50 ° C., more preferably 0 to 40 ° C., from the viewpoint of efficiently separating the condensate into two layers of an upper layer and a lower layer. More preferably, it is 0 to 30 ° C.
- the upper layer mainly contains a solvent.
- the solvent contained in the upper layer can be effectively used as a solvent for the transesterification reaction between the (meth) acrylic acid ester used as a raw material and the alcohol corresponding to the (meth) acrylic acid ester of the target compound.
- the upper layer is supplied to the distillation column 2 from the viewpoint of effectively using the solvent contained in the upper layer.
- the upper layer is supplied to the distillation column 2 from the viewpoint of efficiently proceeding the transesterification reaction between the (meth) acrylic acid ester used as the raw material and the alcohol.
- the middle part of the distillation column 2 means a stage near the center of the multistage distillation column as described above. For example, when the distillation column 2 is a distillation column having 15 theoretical plates, 6 to 9 plates correspond to the middle portion of the distillation column.
- the fractionation ability of the distillation column 2 can be increased by refluxing a part of the condensate to the upper part of the distillation column 2, preferably the top of the column via the piping 5 d, the switching device 7 and the piping 5 c.
- the amount of the condensate refluxed to the upper part of the distillation column 2 is not particularly limited, but is about 20 to 95% by mass of the total amount of the condensate from the viewpoint of increasing the fractionating ability of the distillation column 2 and increasing the reaction rate. It is preferably about 50 to 90% by mass.
- the upper layer of the two separated layers mainly contains a solvent, it corresponds to the (meth) acrylate ester used as the raw material and the (meth) acrylate ester of the target compound in the same manner as described above. It can be effectively used as a reaction solvent when transesterifying the alcohol to be transesterified. In that case, it is preferable to supply the said upper layer to the middle stage part of the distillation column 2 similarly to the above from a viewpoint of making the transesterification reaction of (meth) acrylic acid ester used as a raw material and alcohol efficiently advance.
- the lower layer mainly contains by-product alcohol and water, but besides these components, the content of (meth) acrylic acid ester used as a solvent and a raw material is about 1 to 10% by mass, respectively. Included.
- the (meth) acrylic acid ester used as a solvent and a raw material contained in the lower layer azeotropes with the by-product alcohol, and therefore can be removed from the lower layer as an azeotrope.
- the condensate removed out of the system of the reactor A1 is sent to the separation device 8, and water is added to the condensate to separate it into two layers, an upper layer and a lower layer, and the lower layer of the separated two layers is separated.
- the solution is sent to the distillation apparatus B3 via a pipe 5f connecting the lower part of the apparatus 8 and the distillation apparatus B3 having the distillation column 4.
- the lower layer sent to the distillation apparatus B3 is distilled in the distillation apparatus B3.
- the temperature at the top of the distillation column 4 is adjusted to a predetermined temperature, for example, 64 ° C. or lower when the (meth) acrylic acid ester used as a raw material is methyl (meth) acrylate.
- a vapor containing a (meth) acrylic ester used as a raw material, a by-product alcohol and a solvent is generated, and then the temperature of the lower layer is set to a predetermined temperature, for example, the (meth) acrylic ester used as a raw material is (
- the temperature of the lower layer is set to a predetermined temperature, for example, the (meth) acrylic ester used as a raw material is (
- the temperature to 64 to 66 ° C. steam containing a by-product alcohol as a main component can be generated by transesterification. Any generated steam can be taken out from the upper part of the distillation column 4.
- the lower layer can be distilled using the distillation apparatus B3 having the distillation column 4 as described above.
- the distillation apparatus B3 may be either a batch type or a flow type.
- the pressure when distilling the lower layer may be either atmospheric pressure or reduced pressure.
- the number of theoretical plates of the distillation column 4 used for distillation is preferably 5 or more, more preferably 7 from the viewpoint of efficiently azeotropically evaporating the solvent, the (meth) acrylic acid ester used as a raw material and the by-product alcohol. From the viewpoint of improving economy, the number is preferably 10 or less, more preferably 70 or less, and even more preferably 50 or less.
- the distillation temperature when distilling the lower layer is preferably 20 ° C.
- (meth) acrylic acid ester used as a raw material is prevented.
- it is preferably 120 ° C. or lower, more preferably 110 ° C. or lower, and further preferably 105 ° C. or lower.
- the vapor containing the (meth) acrylic acid ester, by-product alcohol and solvent used as raw materials contains the solvent, the (meth) acrylic acid ester and by-product alcohol used as raw materials, It is possible to condense and use the resulting condensate as a raw material when transesterifying the (meth) acrylic acid ester used as a raw material with the alcohol corresponding to the (meth) acrylic acid ester of the target compound. It is preferable from the viewpoint of reducing. Moreover, after condensing the said vapor
- the separated by-product alcohol and water can be used, for example, as water to be added to the condensate removed from the system of the reactor A1.
- the by-product alcohol and water can be easily separated by, for example, distillation purification. Since the by-product alcohol separated from the water contained in the residue contains substantially no impurities other than moisture, the by-product alcohol is, for example, an industrial raw material in the same manner as a commonly used alcohol. It can be used as a solvent.
- the reaction temperature at the time of carrying out the transesterification reaction of (meth) acrylic acid ester and alcohol used as a raw material is preferably 70 ° C. or higher, more preferably 75 ° C. or higher, from the viewpoint of increasing the reaction rate. From the viewpoint of preventing polymerization of the (meth) acrylic acid ester used as the target compound and the (meth) acrylic acid ester of the target compound, it is preferably 140 ° C. or lower, more preferably 130 ° C. or lower, and further preferably 120 ° C. or lower.
- Atmosphere when performing transesterification reaction of (meth) acrylic acid ester used as raw material and alcohol is a viewpoint to prevent polymerization of (meth) acrylic acid ester used as raw material and (meth) acrylic acid ester of target compound Therefore, an atmosphere containing oxygen is preferable, and from the viewpoint of improving safety, a gas having an oxygen concentration of 5% by volume to atmospheric concentration is more preferable.
- the pressure of the atmosphere should just be atmospheric pressure normally, However, Pressurization or pressure reduction may be sufficient. For example, when the pressure of the atmosphere is reduced, the reflux temperature can be lowered, so that there is an advantage that side reactions can be suppressed.
- the transesterification reaction may be terminated when a predetermined reaction rate is reached. it can.
- the (meth) acrylic acid ester used as a raw material in the reactor A1 disappears by azeotropy with the solvent.
- the top temperature of the distillation column 2 finally reaches the boiling point of the solvent. Therefore, the disappearance of the (meth) acrylic acid ester used as a raw material can be confirmed by the column top temperature of the distillation column 2.
- the transesterification reaction between the (meth) acrylic ester used as a raw material and the alcohol is completed. be able to.
- the end point of the transesterification reaction of the (meth) acrylic acid ester used as a raw material and alcohol can be confirmed by, for example, gas chromatography, liquid chromatography, or the like.
- the reaction time for the transesterification reaction between the (meth) acrylic acid ester used as the raw material and the alcohol varies depending on the amount of the (meth) acrylic acid ester used as the raw material and the alcohol, the reaction temperature, etc. In general, the time until the target reaction rate is reached is selected.
- the (meth) acrylic acid ester of the target compound can be obtained by performing a transesterification reaction between the (meth) acrylic acid ester used as a raw material and the alcohol.
- the (meth) acrylic acid ester used as a raw material and the alcohol corresponding to the (meth) acrylic acid ester of the target compound are subjected to a transesterification reaction, and then the resulting reaction mixture is further heated, Vapor containing (meth) acrylic acid ester used as an unreacted raw material is taken out from the upper part.
- the reaction mixture in the reaction apparatus A1 is further heated, and steam containing (meth) acrylic acid ester used as an unreacted raw material from the upper part of the distillation column 2 is supplied. It can be taken out.
- the (meth) acrylic acid ester used as a raw material can be efficiently recovered from the reactor A1.
- the temperature of the transesterification reaction of (meth) acrylic acid ester and alcohol which is usually used as a raw material, is preferably 70 ° C. or higher, more preferably 75 ° C. or higher. From the viewpoint of preventing polymerization of the (meth) acrylic acid ester and the (meth) acrylic acid ester of the target compound, it is preferably 140 ° C. or lower, more preferably 130 ° C. or lower, and further preferably 120 ° C. or lower.
- the pressure at the time of heating the reaction mixture in reaction apparatus A1 can be made into atmospheric pressure, the apparatus for pressurization or pressure reduction is not required, but the said pressure is higher than atmospheric pressure if necessary. It may be a pressure or a pressure lower than atmospheric pressure.
- Vapor generated by heating the reaction mixture in the reaction apparatus A1 is taken out from the upper part of the reaction apparatus A1, preferably from the top of the reaction apparatus A1 to the outside of the reaction apparatus A1, and recovered as a condensed liquid by cooling. Can do.
- the reaction is performed together with the (meth) acrylic acid ester in which the solvent is used as a raw material. Since the amount of the solvent taken out from the apparatus A1 and present in the reaction apparatus A1 is reduced, in order to efficiently azeotrope the (meth) acrylic acid ester used as a raw material and the solvent, a reaction is performed as necessary. You may add the said solvent in apparatus A1.
- the amount of the solvent to be added is not particularly limited as long as it can azeotrope the (meth) acrylic acid ester used as a raw material and the solvent.
- the end point of the operation for azeotroping the (meth) acrylic acid ester used as the raw material and the solvent is not particularly limited, but the (meth) acrylic acid ester used as the raw material remaining in the reactor A1 is not particularly limited.
- the azeotropic temperature of the azeotrope approaches the boiling point of the solvent, so from the viewpoint of increasing the recovery efficiency of the (meth) acrylic acid ester used as a raw material, it is performed until the boiling point of the solvent is reached. preferable.
- the condensate recovered as described above mainly contains (meth) acrylic acid ester used as a recovered raw material, a solvent and a by-product alcohol by-produced by the transesterification reaction. Since the amount is very small compared to the amount of (meth) acrylic acid ester and solvent used as the recovered raw material, the condensate is used as a raw material when a new transesterification reaction is performed (meta ) It can be used effectively as an acrylic ester.
- the target compound (meth) acrylic acid ester is present in the reaction mixture in the reaction apparatus A1, and can be recovered, for example, by removing the reaction mixture from the lower part of the reaction apparatus A1.
- the reaction mixture contains the solvent used in the transesterification, a small amount of unreacted (meth) acrylate and by-product alcohol. If necessary, by removing these components, the target compound (meth) acrylic acid ester can be recovered. Removal of unreacted (meth) acrylic acid ester, solvent and by-product alcohol from the reaction mixture can be easily performed by, for example, distillation, extraction or the like.
- the (meth) acrylic acid ester is produced by the transesterification method, and then the raw material ( The (meth) acrylic acid ester, the solvent, the by-produced alcohol and the like can be efficiently recovered and reused, and the intended (meth) acrylic acid ester can be efficiently produced.
- FIG. 2 is a schematic explanatory view showing another embodiment of the (meth) acrylic acid ester production system of the present invention.
- the reaction apparatus A1 having the distillation column 2 shown in FIG. 2 may be the same as the reaction apparatus A1 having the distillation column 2 shown in FIG.
- distillation apparatus B3 having the distillation column 4 shown in FIG. 2 may be the same as the distillation apparatus B3 having the distillation column 4 shown in FIG.
- the distillation apparatus B3 may be provided with a heating device 15 such as a reboiler, for example, in order to heat the contents of the distillation apparatus B3, if necessary.
- the condensate removed from the reaction apparatus A1 is sent to the separator 8 and water is added to the condensate.
- the upper layer and the lower layer are separated into two layers, and the lower layer of the separated two layers is distilled into the distillation apparatus B3 having the distillation column 4 through the pipe 5f.
- the position of the distillation column 4 for feeding the lower layer may be supplied to the middle part of the distillation column 4 from the viewpoint of efficiently separating the solvent contained in the lower layer from the by-product alcohol and the by-produced water.
- the middle part of the distillation column 4 means a stage near the center of the multi-stage distillation column as described above. For example, when the distillation column 4 is a distillation column having 15 theoretical plates, 6 to 9 plates correspond to the middle portion of the distillation column.
- the temperature at the top of the distillation column 4 is adjusted to a predetermined temperature, for example, 64 ° C. or lower when the (meth) acrylic acid ester used as a raw material is methyl (meth) acrylate.
- a vapor containing a (meth) acrylic ester used as a raw material, a by-product alcohol and a solvent is generated, and then the temperature of the lower layer is set to a predetermined temperature, for example, a (meth) acrylic ester used as a raw material.
- a predetermined temperature for example, a (meth) acrylic ester used as a raw material.
- steam containing by-product alcohol as a main component can be generated by transesterification. Any generated steam can be taken out from the upper part of the distillation column 4.
- the pressure when distilling the lower layer may be either atmospheric pressure or reduced pressure.
- the number of theoretical plates of the distillation column 4 used for distillation is preferably 5 or more, more preferably 7 from the viewpoint of efficiently azeotropically evaporating the solvent, the (meth) acrylic acid ester used as a raw material and the by-product alcohol. From the viewpoint of improving economy, the number is preferably 10 or less, more preferably 70 or less, and even more preferably 50 or less.
- the distillation temperature when distilling the lower layer is preferably 20 ° C. or higher, more preferably 40 ° C. or higher, and further preferably 50 ° C. or higher. However, polymerization of (meth) acrylic acid ester used as a raw material is prevented. From this viewpoint, the temperature is preferably 120 ° C. or lower, more preferably 110 ° C. or lower, and further preferably 105 ° C. or lower.
- the vapor containing (meth) acrylic acid ester, by-product alcohol and solvent used as raw materials contains the solvent, (meth) acrylic acid ester and by-product alcohol used as raw materials. Therefore, the upper part, preferably the top of the distillation column 4 of the distillation apparatus B3 is connected to the condensing apparatus 9 via the pipe 10a, and a part of the condensate obtained in the condensing apparatus 9 is transferred to the upper part of the distillation column 4, preferably In order to recirculate to the top of the column, the condenser 9 and the switching device 11 are connected via a pipe 10b, and the switching device 11 and the upper part of the distillation column 4, preferably the top of the column, are connected via a pipe 10c. Yes.
- the condensing device 9 and the switching device 11 are connected via a pipe 10b, and the switching device 11 and the collecting part 12 are connected via a pipe 10d. ing.
- the condensate obtained by condensing the vapor with the condenser 9 mainly contains a solvent, (meth) acrylic acid ester and by-product alcohol used as raw materials. Therefore, the condensate is recovered by the recovery unit 12, and the condensate recovered by the recovery unit 12 is returned to the reaction apparatus A1 for effective use.
- a liquid mainly containing water and by-product alcohol is present at the bottom or bottom of the distillation apparatus B3 having the distillation column 4.
- the liquid is sent to a distillation apparatus C14 having a distillation column 13 through a pipe 16 connected to the lower stage or bottom of the distillation apparatus B3.
- the distillation apparatus C14 having the distillation tower 13 may be the same as the distillation apparatus B3 having the distillation tower 4 shown in FIG. Note that the distillation device C14 may be provided with a heating device 17 such as a reboiler, for example, in order to heat the contents of the distillation device C14, if necessary.
- a heating device 17 such as a reboiler, for example, in order to heat the contents of the distillation device C14, if necessary.
- the position of the distillation column 13 for feeding the liquid is preferably supplied to the middle part of the distillation column 13 from the viewpoint of efficiently separating water and by-product alcohol contained in the liquid.
- the middle part of the distillation column 13 means a stage near the center of the multi-stage distillation column as described above. For example, when the distillation column 13 is a distillation column having 15 theoretical plates, 6 to 9 plates correspond to the middle portion of the distillation column.
- the temperature of the top of the distillation column 13 is adjusted to a predetermined temperature, for example, 64 to 66 ° C. when the by-product alcohol is methanol.
- the generated steam can be taken out from the upper part of the distillation column 13.
- the distillation apparatus C14 may be either a batch type or a distribution type.
- Examples of the distillation apparatus C14 having a suitable distillation column 13 include a packed column and a tray-type distillation column.
- the present invention is not limited to such examples.
- Examples of the packing used in the packed tower include a helipack, a McMahon, a cascade mini-ring, and the like, but the present invention is not limited to such examples.
- Examples of the tray type distillation column include a packed column type distillation machine, an Oldershaw type distillation column, a lift tray type distillation column, and the like, but the present invention is not limited to such examples.
- the pressure at the time of distilling the liquid may be either atmospheric pressure or reduced pressure.
- the number of theoretical plates of the distillation column 13 used in the distillation is preferably 5 or more, more preferably 7 or more, and even more preferably 10 or more, from the viewpoint of efficiently azeotropically producing the by-product alcohol and water. From the viewpoint of improving economy, it is preferably 100 stages or less, more preferably 70 stages or less, and even more preferably 50 stages or less.
- the distillation temperature when distilling the liquid is preferably 20 ° C. or higher, more preferably 40 ° C. or higher, and still more preferably 50 ° C. or higher.
- the chemical stability of the target (meth) acrylate ester From the viewpoint of improving the temperature, it is preferably 120 ° C. or lower, more preferably 110 ° C. or lower, and further preferably 105 ° C. or lower.
- the upper part, preferably the top of the distillation column 13 of the distillation device C14 is connected to the condensing device 19 via a pipe 18a.
- the condensing device 19 and the switching device 20 are connected via a pipe 18b.
- the switching device 20 and the upper part of the distillation column 13, preferably the top of the column are connected via a pipe 18c.
- Examples of the switching device 20 include a switching valve, a reflux distributor, and a solenoid valve, but the present invention is not limited to such examples.
- the condensate obtained by condensing the steam with the condensing device 19 mainly contains by-product alcohol.
- the switching device 20 and the recovery unit 21 are connected to each other by connecting the condenser 19 and the switching device 20 via the pipe 18b and operating the switching device 20. It connects so that it may connect via the piping 18d.
- the by-product alcohol recovered by the recovery unit 21 can be effectively used as, for example, a raw material for preparing various fuels and various organic compounds.
- the collection unit 21 may be a so-called receiver.
- Water is mainly present at the bottom or bottom of the distillation apparatus C14 having the distillation column 13.
- the water can be effectively used in the separation device 8 disposed in the reaction device A1, for example, by connecting the lower stage or bottom of the distillation device C14 and the piping 5d via the piping 18e.
- the pipe 18e and the pipe 5d can be easily connected by, for example, a three-way cock (not shown).
- the (meth) acrylic acid ester is produced by the transesterification method, and then the raw material ( The (meth) acrylic acid ester, the solvent, the by-produced alcohol and the like can be efficiently recovered and reused, and the intended (meth) acrylic acid ester can be efficiently produced.
- (meth) acrylic acid ester used as the raw material is usually a substance that gives off a bad odor, and emits a strong odor when released into the atmosphere, so it is not discharged into the atmosphere or discharged into the atmosphere. It is desirable to reduce the amount as much as possible.
- the (meth) acrylic acid ester remaining in the reaction mixture after completion of the transesterification reaction and can be used as a raw material is azeotroped with a solvent under atmospheric pressure to react the reaction mixture. Therefore, the amount of (meth) acrylic acid ester used as a raw material in the atmosphere can be reduced as much as possible.
- the (meth) acrylic ester production system of the present invention is an environment-friendly production system in consideration of the environment.
- an alkali scrubber is installed at the air outlet provided in the reaction apparatus A1 to absorb (meth) acrylic ester used as a raw material, and the ( The release of the (meth) acrylic acid ester into the atmosphere may be suppressed.
- the (meth) acrylic acid ester production system of the invention is also useful as a system for preventing the (meth) acrylic acid ester used as a raw material from being mixed into the target compound (meth) acrylic acid ester.
- the (meth) acrylic acid ester production system of the present invention by-product alcohol can be recovered with high purity, and the (meth) acrylic acid ester by-produced by the transesterification reaction is effectively utilized. Since the replicated water can be effectively used, the (meth) acrylic acid ester production system of the present invention is a system (apparatus) excellent in industrial productivity of (meth) acrylic acid ester.
- the production system of the (meth) acrylic acid ester of the present invention is a so-called closed system, it is possible to reduce the amount of by-products discharged outside the reaction system, and the (meth) acrylic acid ester of the target compound. The yield of can be improved.
- the (meth) acrylic acid ester obtained by the (meth) acrylic acid ester production system of the present invention is useful as a raw material for, for example, (meth) acrylic resins, surfactants, adhesives, paints and the like.
- the yield of the (meth) acrylic acid ester of the target compound is the ratio of the actual (meth) acrylic acid ester production amount to the theoretical (meth) acrylic acid ester production amount of the target compound. I asked for it.
- the amounts of the raw material alcohol, the raw material alcohol (meth) acrylic ester, the solvent and the (meth) acrylic ester used as the raw material in the reaction mixtures of the following examples are all determined by gas chromatography (hereinafter, It was determined from the area percentage by GC using an analyzer (referred to as GC) (manufactured by Agilent, detector FID, column capillary DB-1: 30 m).
- Example 1 The (meth) acrylic ester production system shown in FIG. 1 was used.
- a reaction apparatus A having a distillation column a condensing apparatus is disposed at the top of the column, a 20-liter Oldershaw distillation column (theoretical plate number: 15) having a side tube, and a 2 L four-necked flask having an air introduction tube was used.
- 694 g (8.06 mol) of methyl acrylate, 552 g (6.20 mol) of N, N-dimethylaminoethanol, 1.76 g of phenothiazine, 22.1 g of dibutyltin oxide and 100 g of cyclohexane were charged.
- the transesterification reaction was performed while air was blown into the flask at a flow rate of 20 mL / min from the air introduction tube. More specifically, the vapor taken out from the top of the distillation column is condensed by a condenser, a part of the resulting condensate is refluxed to the top of the distillation column, and the remaining condensate is removed outside the flask. .
- the top temperature of the distillation column was adjusted to 54 to 56 ° C., which is the azeotropic temperature of methyl alcohol and cyclohexane, by adjusting the amount of the condensed liquid removed.
- the amount of the lower layer is 410 g.
- methyl acrylate 3.6% by mass (15 g) and water 48. 9% by mass (200 g) was contained.
- the upper layer was effectively used by supplying it to the position of the 10th stage from the bottom of the distillation tower, which is the middle stage of the distillation tower.
- the reaction temperature is 85 to 102 ° C, with appropriate addition of cyclohexane in the flask. Ended. After completion of the reaction, the amount of methyl acrylate contained in the reaction mixture obtained by the transesterification reaction was 160 g.
- the reaction mixture obtained by the transesterification reaction is further heated, the reflux ratio is set to 10 to 15, the vapor is taken out from the top of the distillation column, and the vapor is condensed to obtain a condensate. It was collected.
- cyclohexane was added to the flask so that the temperature of the reaction mixture in the flask was maintained at 85 to 100 ° C.
- the top temperature of the distillation tower gradually increased, and distillation was continued until the top temperature of the distillation tower reached 80 ° C., which is the boiling point of cyclohexane.
- the content of methyl acrylate in the reaction mixture in the flask was 0.1% by mass or less.
- the amount of the condensate taken out and recovered from the tower top was 490 g, and this condensate contained 5 g of methanol, 145 g of methyl acrylate, and 340 g of cyclohexane. This condensate contained most of the methyl acrylate used in excess.
- This recovered condensate could be used in the transesterification reaction between methyl acrylate and N, N-dimethylaminoethanol. From this, it was confirmed that the loss of methyl acrylate can be prevented by using the condensate in the transesterification reaction between methyl acrylate and N, N-dimethylaminoethanol.
- the yield of acrylic acid-N, N-dimethylaminoethyl was 852 g (based on N, N-dimethylaminoethanol). Yield of 96% by mass, yield based on the charged amount of methyl acrylate: 73.8% by mass, yield after reusing methyl acrylate recovered by azeotropy with cyclohexane after completion of the reaction Rate: 93.3% by mass).
- distillation apparatus B a 1 L four-necked flask having a 10-stage Oldershaw distillation column (theoretical plate number: 7 stages) having a reflux apparatus at the top of the column and having a side tube and an air introduction pipe was used. The lower layer obtained above was charged in the flask.
- fraction B had a composition of 99.9% by mass of methyl alcohol and 0.1% by mass of water, and it was not confirmed that methyl acrylate was contained.
- the composition of the residual liquid 203 g in the flask is 3% by mass of methyl alcohol and 97% by mass of water, and components contained in the other components are not detected by GC, and are mainly composed of water.
- the said residual liquid was able to be used as water at the time of mixing a condensate and water in Example 1.
- Example 2 The same reactor A as used in Example 1 was used. Into the flask, 517 g (6.00 mol) of methyl acrylate, 651 g (5.00 mol) of n-octyl alcohol, 1.76 g of phenothiazine, 0.72 g of tetramethyltitanium and 117 g of n-hexane were charged. The transesterification reaction was performed while air was blown into the flask at a flow rate of 20 mL / min from the air introduction tube. More specifically, the vapor taken out from the top of the distillation column was condensed, a part of the resulting condensate was refluxed to the top, and the remaining condensate was removed outside the flask. By adjusting the amount of the condensate removed outside the flask, the top temperature of the distillation column was adjusted to 48 to 50 ° C., which is the azeotropic temperature of methyl alcohol and n-hexane.
- the amount of the lower layer is 257 g.
- methyl acrylate 3.1% by mass (8 g) and water 38.9% by mass (100 g) was contained.
- the upper layer was effectively used by supplying it to the position of the 10th stage from the bottom of the distillation tower, which is the middle stage of the distillation tower.
- the reaction temperature in the transesterification reaction between methyl acrylate and n-octyl alcohol was 90 to 110 ° C., and the transesterification reaction was completed after 8 hours from the start of the reaction. After completion of the reaction, the amount of methyl acrylate contained in the reaction mixture obtained by the transesterification reaction was 86 g.
- the reaction mixture obtained by the transesterification reaction is further heated, the reflux ratio is set to 10 to 15, the vapor is taken out from the top of the distillation column, and the vapor is condensed to obtain a condensate. It was collected.
- n-hexane was added to the flask so that the temperature of the reaction mixture in the flask was maintained at 90 to 110 ° C.
- the top temperature of the distillation tower gradually increased, and distillation was continued until the top temperature of the distillation tower reached 68 ° C., the boiling point of n-hexane.
- the content of methyl acrylate in the reaction mixture in the flask was 0.2% by mass or less.
- the amount of the condensate taken out from the top of the column and recovered was 392 g.
- 3.8% by mass of methanol (15 g) 18.6% by mass of methyl acrylate (73 g) and 77. 6% by mass (304 g) was contained.
- This condensate contained most of the methyl acrylate used in excess.
- This recovered condensate could be used in the transesterification reaction between methyl acrylate and n-octyl alcohol. From this, it was confirmed that the loss of methyl acrylate can be prevented by using the condensate in the transesterification reaction between methyl acrylate and n-octyl alcohol.
- the yield of n-octyl acrylate was 912 g (yield based on n-octyl alcohol: 99.0% by mass, methyl acrylate The yield is 82.5% by mass based on the charged amount of styrene, and the yield when reusing methyl acrylate recovered by azeotropy with n-hexane after completion of the reaction is 96.0% by mass).
- distillation apparatus B a 2 L four-necked flask having a reflux apparatus at the top of the tower and having a 10-stage Oldershaw distillation column (theoretical plate number: 7 stages) having a side pipe and an air introduction pipe was used. The lower layer obtained above was charged in the flask.
- fraction A Distillation was performed with the reflux ratio set to 10 to 15, and fraction A was recovered when the column top temperature was 64 ° C. or lower. As a result, the amount of fraction A recovered was 32 g.
- the composition of A was 62.5 mass% (20 g) of methyl alcohol, 25.0 mass% (8 g) of methyl acrylate, 12.5 mass% (4 g) of n-hexane, and 0.1 mass% of water. This fraction A could be used in the transesterification reaction between methyl acrylate and n-octyl alcohol.
- the fraction B does not contain components other than methyl alcohol and a small amount of water, it was confirmed that it can be used effectively as an industrial raw material, a solvent, and the like. In addition, since methyl acrylate was not detected by GC in the fraction B, it was confirmed that there was almost no loss of methyl acrylate, so that the yield of n-octyl acrylate was not adversely affected.
- the composition of the residual liquid 103 g in the flask is 3% by mass (3 g) of methyl alcohol and 97% by mass (100 g) of water, and other components are not detected by GC, and are mainly composed of water. Therefore, the residual liquid could be used as water when mixing the condensate and water.
- Example 3 The same reactor A as used in Example 1 was used. Into the flask, 430 g (5.0 mol) of methyl acrylate, 675 g (7.5 mol) of 1,4-butanediol, 0.72 g of phenothiazine, 3.6 g of dioctyltin oxide and 100 g of cyclohexane were charged. The transesterification reaction was performed while air was blown into the flask at a flow rate of 20 mL / min from the air introduction tube. More specifically, the vapor taken out from the top of the distillation column was condensed, a part of the resulting condensate was refluxed to the top, and the remaining condensate was removed out of the reactor. The top temperature of the distillation column was adjusted to 54 to 56 ° C., which is the azeotropic temperature of methyl alcohol and cyclohexane, by adjusting the amount of condensate removed outside the reaction apparatus.
- the amount of the lower layer is 303 g.
- methyl acrylate 3.3% by mass (10 g) and water 46. 4 mass% (140 g) was contained.
- the upper layer was effectively used by supplying it to the position of the 10th stage from the bottom of the distillation tower, which is the middle stage of the distillation tower.
- the reaction was carried out while appropriately adding cyclohexane to the flask so that the reaction temperature in the transesterification reaction between methyl acrylate and 1,4-butanediol was 85 to 100 ° C. finished. After completion of the reaction, the amount of methyl acrylate contained in the reaction mixture obtained by the transesterification reaction was 20 g.
- the reaction mixture obtained by the transesterification reaction is further heated, the reflux ratio is set to 10 to 15, the vapor is taken out from the top of the distillation column, and the vapor is condensed to obtain a condensate. It was collected.
- cyclohexane was added to the flask so that the temperature of the reaction mixture in the flask was maintained at 85 to 100 ° C.
- the top temperature of the distillation tower gradually increased, and distillation was continued until the top temperature of the distillation tower reached 80 ° C., which is the boiling point of cyclohexane.
- the content of methyl acrylate in the reaction mixture in the flask was 0.2% by mass or less.
- the amount of the condensate taken out and recovered from the tower top was 75 g, and this condensate contained 5 g of methanol, 10 g of methyl acrylate and 60 g of cyclohexane. This condensate contained most of the methyl acrylate used in excess.
- the recovered condensate could be used in the transesterification reaction between methyl acrylate and 1,4-butanediol. From this, it was confirmed that the loss of methyl acrylate can be prevented by using the condensate in the transesterification reaction between methyl acrylate and 1,4-butanediol.
- distillation apparatus B a 1 L four-necked flask having a 10-stage Oldershaw distillation column (theoretical plate number: 7 stages) having a reflux apparatus at the top of the column and having a side tube and an air introduction pipe was used. The lower layer obtained above was charged in the flask.
- fraction B had a composition of 99.9% by mass of methyl alcohol and 0.1% by mass of water, and it was not confirmed that methyl acrylate was contained.
- the fraction B does not contain components other than methyl alcohol and a small amount of water, it was confirmed that it can be used effectively as an industrial raw material, a solvent, and the like. In addition, since methyl acrylate was not detected by GC in the fraction B, it was confirmed that there was no loss of methyl acrylate, so that the yield of 4-hydroxybutyl acrylate was not adversely affected.
- the composition of the residual liquid 142g in the flask is 3% by mass of methyl alcohol and 97% by mass of water, and components contained in the other components are not detected by GC, and are mainly composed of water.
- the residual liquid could be used as water when mixing the condensate and water.
- Example 4 In the same reactor A used in Example 1, 780.9 (7.80 mol) of methyl methacrylate, 372.4 g (6.00 mol) of N, N-dimethylaminoethanol and 1.89 g of phenothiazine were added. A transesterification reaction was carried out in the same manner as in Example 1 except that it was charged. After completion of the reaction, the amount of methyl methacrylate contained in the reaction mixture obtained by the transesterification reaction was 178 g.
- the lower layer of the decanter was distilled in the same manner as in Example 1 to recover 5 g of a fraction A.
- the composition of this fraction A was 86.9% by mass of methyl alcohol, 13.0% by mass of cyclohexane and 0.1% by mass of water.
- This fraction A could be used for a transesterification reaction between methyl methacrylate and N, N-dimethylaminoethanol.
- fraction B was recovered in the same manner as in Example 1, and the composition thereof was examined.
- the composition of this fraction B was 99.9% by mass of methyl alcohol and 0.1% by mass of water.
- Example 5 In the same reactor A used in Example 1, methyl methacrylate 1041.2 (10.4 mol), ethylene glycol 248.3 g (4.00 mol), phenothiazine 1.59 and lithium hydroxide 0.00. A transesterification reaction was carried out in the same manner as in Example 1 except that 96 g was charged. After completion of the reaction, the amount of methyl methacrylate contained in the reaction mixture obtained by the transesterification reaction was 235 g.
- the lower layer of the decanter was distilled in the same manner as in Example 1 to recover 5 g of a fraction A.
- the composition of this fraction A was 86.9% by mass of methyl alcohol, 13.0% by mass of cyclohexane and 0.1% by mass of water.
- This fraction A could be used for the transesterification reaction between methyl methacrylate and ethylene glycol.
- fraction B was recovered in the same manner as in Example 1, and the composition thereof was examined.
- the composition of this fraction B was 99.9% by mass of methyl alcohol and 0.1% by mass of water.
- Example 6 In Example 1, transesterification was performed in the same manner as in Example 1 except that 633.2 g (6.20 mol) of tetrahydrofurfuryl alcohol was used instead of N, N-dimethylaminoethanol. After completion of the reaction, the amount of methyl acrylate contained in the reaction mixture obtained by the transesterification reaction was 147 g.
- the composition of the fraction A was 62.3% by mass of methyl alcohol, 32.1% by mass of methyl acrylate, 5.5% by mass of cyclohexane, and 0% of water. It was 1 mass%.
- This fraction A could be used for a transesterification reaction between methyl acrylate and tetrahydrofurfuryl alcohol.
- the fraction B was recovered in the same manner as in Example 2, and the composition thereof was examined. As a result, the composition of the fraction B was 99.9% by mass of methyl alcohol and 0.1% by mass of water. Was not confirmed to be included.
- Example 7 A transesterification reaction was carried out in the same manner as in Example 1, except that 805.0 g (6.00 mol) of diethylene glycol monoethyl ether was used instead of N, N-dimethylaminoethanol. . After completion of the reaction, the amount of methyl acrylate contained in the reaction mixture obtained by the transesterification reaction was 140 g.
- the composition of the fraction A was 62.3% by mass of methyl alcohol, 32.3% by mass of methyl acrylate, 5.3% by mass of cyclohexane, and water. It was 0.1 mass%.
- This fraction A could be used for a transesterification reaction between methyl acrylate and diethylene glycol monoethyl ether.
- the fraction B was recovered in the same manner as in Example 2, and the composition thereof was examined. As a result, the composition of the fraction B was 99.9% by mass of methyl alcohol and 0.1% by mass of water. Was not confirmed to be included.
- Example 8 Example 1 Example 1 except that methyl acrylate 894.8 (5.20 mol), 1,6-hexanediol 472.7 g (4.00 mol) and dioctyltin oxide 3.7 g were used. A transesterification reaction was carried out in the same manner as described above. After completion of the reaction, the amount of methyl acrylate contained in the reaction mixture obtained by the transesterification reaction was 189 g.
- the content of methyl acrylate in the reaction mixture in the flask was examined.
- the content of methyl acrylate was 0.1% by mass. It was the following.
- the composition of the fraction A was 62.1% by mass of methyl alcohol, 32.4% by mass of methyl acrylate, 5.4% by mass of cyclohexane, and water. It was 0.1 mass%.
- This fraction A could be used for a transesterification reaction between methyl acrylate and 1,6-hexanediol.
- the fraction B was recovered in the same manner as in Example 1, and the composition thereof was examined.
- the composition of the fraction B was 99.9% by mass of methyl alcohol and 0.1% by mass of water. Was not confirmed to be included.
- Example 9 In the same manner as in Example 1, except that 1006.7 g (11.7 mol) of methyl acrylate, 402.5 g (3.00 mol) of trimethylolpropane and 8.4 g of dioctyltin oxide were used. The transesterification reaction was performed. After completion of the reaction, the amount of methyl acrylate contained in the reaction mixture obtained by the transesterification reaction was 216 g.
- the content of methyl acrylate in the reaction mixture in the flask was examined.
- the content of methyl acrylate was 0.1% by mass. It was the following.
- the composition of the fraction A was 62.1% by mass of methyl alcohol, 32.3% by mass of methyl acrylate, 5.5% by mass of cyclohexane, and water. It was 0.1 mass%.
- This fraction A could be used for a transesterification reaction between methyl acrylate and trimethylolpropane.
- the fraction B was recovered in the same manner as in Example 1, and the composition thereof was examined.
- the composition of the fraction B was 99.9% by mass of methyl alcohol and 0.1% by mass of water. Was not confirmed to be included.
- Example 10 In Example 1, methyl acrylate 559.3 (6.5 mol), 2-ethyl-2-methyl-1,3-dioxolane-4-methanol 1041.5 g (5.00 mol) and dioctyltin oxide 4. A transesterification reaction was carried out in the same manner as in Example 1 except that 7 g was used. After completion of the reaction, the amount of methyl acrylate contained in the reaction mixture obtained by the transesterification reaction was 117 g.
- the content of methyl acrylate in the reaction mixture in the flask was examined.
- the content of methyl acrylate was 0.1% by mass. It was the following.
- the composition of the fraction A was 62.5% by mass of methyl alcohol, 32.1% by mass of methyl acrylate, 5.3% by mass of cyclohexane, and water. It was 0.1 mass%.
- This fraction A could be used for a transesterification reaction between methyl acrylate and 2-ethyl-2-methyl-1,3-dioxolane-4-methanol.
- the fraction B was recovered in the same manner as in Example 2, and the composition thereof was examined. As a result, the composition of the fraction B was 99.9% by mass of methyl alcohol and 0.1% by mass of water. Was not confirmed to be included.
- Example 11 In Example 1, methyl acrylate 615.2 (7.15 mol), 3-ethyl-3-oxetanyl methyl alcohol 892.1 g (5.50 mol) and dioctyltin oxide 5. A transesterification reaction was carried out in the same manner as in Example 1 except that lg was used. After completion of the reaction, the amount of methyl acrylate contained in the reaction mixture obtained by the transesterification reaction was 123 g.
- the content of methyl acrylate in the reaction mixture in the flask was examined.
- the content of methyl acrylate was 0.1% by mass. It was the following.
- the composition of the fraction A was 62.3% by mass of methyl alcohol, 32.1% by mass of methyl acrylate, 5.5% by mass of cyclohexane, and water. It was 0.1 mass%.
- This fraction A could be used for the transesterification reaction between methyl acrylate and 3-ethyl-3-oxetanylmethyl alcohol.
- the fraction B was recovered in the same manner as in Example 2, and the composition thereof was examined. As a result, the composition of the fraction B was 99.9% by mass of methyl alcohol and 0.1% by mass of water. Was not confirmed to be included.
- Example 12 The (meth) acrylic acid ester production system shown in FIG. 2 was used.
- a reaction apparatus A having a distillation column a condensing apparatus is disposed at the top of the column, a 20-liter Oldershaw distillation column (theoretical plate number: 15) having a side tube, and a 2 L four-necked flask having an air introduction tube was used.
- 694 g (8.06 mol) of methyl acrylate, 552 g (6.20 mol) of N, N-dimethylaminoethanol, 1.76 g of phenothiazine, 22.1 g of dibutyltin oxide and 100 g of cyclohexane were charged.
- the transesterification reaction was performed while air was blown into the flask at a flow rate of 20 mL / min from the air introduction tube. More specifically, the vapor taken out from the top of the distillation column is condensed by a condenser, a part of the resulting condensate is refluxed to the top of the distillation column, and the remaining condensate is removed outside the flask. .
- the top temperature of the distillation column was adjusted to 54 to 56 ° C., which is the azeotropic temperature of methyl alcohol and cyclohexane, by adjusting the amount of the condensed liquid removed.
- the amount of the lower layer was 410 g, and the lower layer contained 48.5% by mass of methyl alcohol, 0.6% by mass of cyclohexane, 3.4% by mass of methyl acrylate, and 47.5% by mass of water.
- the upper layer was effectively used by supplying it to the position of the 10th stage from the bottom of the distillation tower, which is the middle stage of the distillation tower.
- the reaction temperature is 85 to 102 ° C, with appropriate addition of cyclohexane in the flask. Ended. After completion of the reaction, the amount of methyl acrylate contained in the reaction mixture obtained by the transesterification reaction was 160 g.
- the reaction mixture obtained by the transesterification reaction is further heated, the reflux ratio is set to 10 to 15, the vapor is taken out from the top of the distillation column, and the vapor is condensed to obtain a condensate. It was collected.
- cyclohexane was added to the flask so that the temperature of the reaction mixture in the flask was maintained at 85 to 100 ° C.
- the top temperature of the distillation tower gradually increased, and distillation was continued until the top temperature of the distillation tower reached 80 ° C., which is the boiling point of cyclohexane.
- the content of methyl acrylate in the reaction mixture in the flask was 0.1% by mass or less.
- the amount of the condensate taken out and recovered from the tower top was 490 g, and this condensate contained 5 g of methanol, 145 g of methyl acrylate, and 340 g of cyclohexane. This condensate contained most of the methyl acrylate used in excess.
- This recovered condensate could be used in the transesterification reaction between methyl acrylate and N, N-dimethylaminoethanol. From this, it was confirmed that the loss of methyl acrylate can be prevented by using the condensate in the transesterification reaction between methyl acrylate and N, N-dimethylaminoethanol.
- the yield of acrylic acid-N, N-dimethylaminoethyl was 852 g (based on N, N-dimethylaminoethanol). Yield of 96% by mass, yield based on the charged amount of methyl acrylate: 73.8% by mass, yield after reusing methyl acrylate recovered by azeotropy with cyclohexane after completion of the reaction Rate: 93.3% by mass).
- distillation apparatus B a 1 L four-necked flask having a reflux apparatus at the top of the tower, an Oldershaw 20-stage distillation tower having a side pipe, and an air introduction pipe was used.
- the lower layer obtained above was continuously charged into the middle stage (10 stages) of the Oldershaw type distillation column at a flow rate of 200 g / hr.
- the composition of the liquid taken out from the lower stage of the distillation apparatus B was examined, the composition of the liquid was 57.8% by mass of water and 42.2% by mass of methyl alcohol.
- distillation apparatus C a 1 L four-necked flask having a reflux apparatus at the top of the tower and having an Oldershaw 20-stage distillation tower having a side pipe and an air introduction pipe was used.
- the liquid obtained above was continuously charged into the middle stage (10 stages) of the Oldershaw distillation column at a flow rate of 184 g / hr.
- the composition of the liquid taken out from the lower stage of the distillation apparatus C was examined, the composition of the liquid was 100% by mass of water. This water could be suitably used in the separation apparatus of the reactor A.
- Comparative Example 1 The same reactor A as used in Example 1 was used. In the flask, 694 g (8.06 mol) of methyl acrylate, 552 g (6.20 mol) of N, N-dimethylaminoethanol, 1.76 g of phenothiazine, 22.1 g of dibutyltin oxide and 100 g of isohexane were charged.
- a transesterification reaction was performed at a reaction temperature of 76 to 93 ° C. while air was blown into the flask at a flow rate of 20 mL / min. More specifically, the vapor taken out from the top of the distillation column installed in the reactor is condensed, a part of the resulting condensate is refluxed to the top, and the remaining condensate is removed outside the reactor. .
- the top temperature of the distillation column was adjusted to 45 to 46 ° C., which is the azeotropic temperature of methyl alcohol and isohexane, by adjusting the amount of condensate removed outside the reaction apparatus.
- the amount of methyl acrylate remaining in the reaction apparatus when the steal exchange reaction was completed was 160 g.
- the reflux ratio was set to 10 to 15, and the condensate was taken out from the top of the column.
- the top temperature quickly reached 62 ° C., which is the boiling point of isohexane.
- the amount of condensate taken out from the top of the column was 300 g.
- the residual amount of methyl acrylate in the reaction apparatus was 10.8% by mass.
- 300 g of the condensate taken out from the top of the tower contained 5 g of methanol, 5 g of methyl acrylate, and 290 g of isohexane. From this, it was confirmed that the condensate contained almost no methyl acrylate used as a raw material, and most of the methyl acrylate remained in the reactor.
- the amount of methyl acrylate remaining in the reaction apparatus at the end of the reaction was 160 g. Further, in the operation after completion of the reaction, methyl acrylate was not azeotroped with isohexane, and only 5 g was recovered.
- Comparative Example 2 A 2 L four-necked flask equipped with a reflux apparatus at the top of the column and having a 20-stage Oldershaw distillation column (theoretical plate number: 15) having side tubes and an air introduction tube was used as the reaction apparatus.
- 694 g (8.06 mol) of methyl acrylate, 552 g (6.20 mol) of N, N-dimethylaminoethanol, 1.76 g of phenothiazine, 22.1 g of dibutyltin oxide and 100 g of cyclohexane were charged. .
- the transesterification reaction was performed while air was blown into the flask at a flow rate of 20 mL / min from the air introduction tube.
- the vapor extracted from the top of the distillation tower installed in the reactor is condensed, a part of the resulting condensate is refluxed to the top, and the remaining condensate is removed outside the reactor. did.
- the top temperature of the distillation column was adjusted to 54 to 56 ° C., which is the azeotropic temperature of methyl alcohol and cyclohexane, by adjusting the amount of condensate removed outside the reaction apparatus.
- the 700 g of the condensate removed from the top of the distillation column of the reaction apparatus and 200 g of water were mixed at a temperature of 20 ° C., and the resulting mixture was introduced into a decanter.
- This mixed solution was separated into two layers, an upper layer and a lower layer.
- Methyl alcohol contained in the condensate was extracted with water and contained in the lower layer, and cyclohexane contained in the condensate was contained in the upper layer of the extract.
- the amount of the lower layer is 410 g.
- methyl acrylate 3.6% by mass (15 g) and water 48.9 Mass% (200 g) was included.
- the reaction temperature is 85 to 102 ° C, with appropriate addition of cyclohexane in the flask. Ended.
- the yield of acrylic acid-N, N-dimethylaminoethyl was 96.0% by mass, and the yield based on methyl acrylate was 73.8% by mass.
- the composition of the aqueous layer from which methanol was extracted from the condensate was 48.0% by mass of methanol, 0.1% by mass of n-hexane and 3.6% by mass of methyl acrylate, but remained in the reactor.
- the residual amount of methyl acrylate was 160 g.
- the (meth) acrylic acid ester remaining after the (meth) acrylic acid ester and alcohol used as the raw material after the transesterification reaction is efficiently obtained. It can be recovered that the (meth) acrylic acid ester used as the recovered raw material can be reused when the (meth) acrylic acid ester used as the raw material and the alcohol are transesterified. .
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Crystallography & Structural Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
Description
(1)エステル交換反応によって(メタ)アクリル酸エステルを製造する際に使用される(メタ)アクリル酸エステルの製造システムであって、
蒸留塔を有する反応装置Aと蒸留塔を有する蒸留装置Bとを有し、
反応装置Aの蒸留塔の上部が配管を介して凝縮装置と接続され、凝縮装置で得られた凝縮液の一部を蒸留塔の上部に還流させるための配管で凝縮装置と蒸留塔の上部とが切換装置を介して接続され、凝縮装置で得られた凝縮液の残部を分液装置に送液するための配管で凝縮装置と分液装置とが切換装置を介して接続され、
分液装置で分離された凝縮液のうち上層の液を蒸留塔に還流させるための配管で分液装置の上部と蒸留塔とが接続され、分液装置で分離された凝縮液のうち下層の液を蒸留装置Bに送液するための配管で分液装置の下部と蒸留装置Bとが接続され、
蒸留装置Bの蒸留塔の上部が配管を介して凝縮装置と接続され、凝縮装置で得られた凝縮液の一部を蒸留塔の上部に還流させるための配管で凝縮装置と蒸留塔の上部とが切換装置を介して接続され、凝縮装置で得られた凝縮液の残部を回収するための回収部に送液するための配管で凝縮装置と回収部とが切換装置を介して接続され、
蒸留装置B内に存在する残渣を反応装置Aの蒸留塔に還流させるための配管で蒸留装置Bの下部と、反応装置Aの切換装置と凝縮装置との間の配管とが配管で接続されている(メタ)アクリル酸エステルの製造システム(製造装置)、および
(2)エステル交換反応によって(メタ)アクリル酸エステルを製造する際に使用される(メタ)アクリル酸エステルの製造システムであって、
蒸留塔を有する反応装置Aと蒸留塔を有する蒸留装置Bと蒸留塔を有する蒸留装置Cとを有し、
反応装置Aの蒸留塔の上部が配管を介して凝縮装置と接続され、凝縮装置で得られた凝縮液の一部を蒸留塔の上部に還流させるための配管で凝縮装置と蒸留塔の上部とが切換装置を介して接続され、凝縮装置で得られた凝縮液の残部を分液装置に送液するための配管で凝縮装置と分液装置とが切換装置を介して接続され、
分液装置で分離された凝縮液のうち上層の液を蒸留塔に還流させるための配管で分液装置の上部と蒸留塔とが接続され、分液装置で分離された凝縮液のうち下層の液を蒸留装置Bに送液するための配管で分液装置の下部と蒸留装置Bとが接続され、
蒸留装置Bの蒸留塔の上部が配管を介して凝縮装置と接続され、凝縮装置で得られた凝縮液の一部を蒸留塔の上部に還流させるための配管で凝縮装置と蒸留塔の上部とが切換装置を介して接続され、凝縮装置で得られた凝縮液の残部を回収するための回収部に送液するための配管で凝縮装置と回収部とが切換装置を介して接続され、
蒸留装置B内に存在する残渣を蒸留装置Cの蒸留塔に送液するための配管で蒸留装置Bの下部と、蒸留装置Cとが接続され、
蒸留装置Cの蒸留塔の上部が配管を介して凝縮装置と接続され、凝縮装置で得られた凝縮液の一部を蒸留塔の上部に還流させるための配管で凝縮装置と蒸留塔の上部とが切換装置を介して接続され、凝縮装置で得られた凝縮液の残部を回収するための回収部に送液するための配管で凝縮装置と回収部とが切換装置を介して接続され、
蒸留装置C内に存在する残渣を反応装置Aの蒸留塔に送液するための配管で蒸留装置Cの下部と、反応装置Aの切換装置と凝縮装置との間の配管とが配管で接続されている(メタ)アクリル酸エステルの製造システム(製造装置)
に関する。
で表わされる脂肪族または脂環式アルコール;フェノール、ベンジルアルコール、1-フェニルエチルアルコール、2-フェニルエチルアルコール、フェノキシエタノールなどの芳香族アルコール;ジメチルアミノエチルアルコール、ジエチルアミノエチルアルコール、ジプロピルアミノエチルアルコール、ジブチルアミノエチルアルコール、ジペンチルアミノエチルアルコール、ジヘキシルアミノエチルアルコール、ジオクチルアミノエチルアルコール、メチルエチルアミノエチルアルコール、メチルプロピルアミノエチルアルコール、メチルブチルアミノエチルアルコール、メチルヘキシルアミノエチルアルコール、エチルプロピルアミノエチルアルコール、エチルブチルアミノエチルアルコール、エチルペンチルアミノエチルアルコール、エチルオクチルアミノエチルアルコール、プロピルブチルアミノエチルアルコール、ジメチルアミノプロピルアルコール、ジエチルアミノプロピルアルコール、ジプロピルアミノプロピルアルコール、ジブチルアミノプロピルアルコール、ブチルペンチルアミノプロピルアルコールなどの式(II):
で表わされるアミノアルコール;2-メトキシエチルアルコール、エトキシエチルアルコール、ブトキシエチルアルコール、エチレングリコールモノメチルエーテル、エチレングリコールモノエチルエーテル(エチルカルビトール)、トリエチレングリコールモノメチルエーテル、テトラヒドロフルフリルアルコール、2-エチル-2-メチル-1,3-ジオキソラン-4-メチルアルコール、シクロヘキサンスピロ-2-1,3-ジオキソラン-4-メチルアルコール、3-エチル-3-オキセタニルメチルアルコール、3-エチル-3-オキセタニルメチルアルコールなどのアルコキシアルコール;アリルアルコール、メタリルアルコール、テトラヒドロフルフリルアルコールなどの一価アルコール;エチレングリコール、2,3-プロパンジオール、1,3-ブタンジオール、1,4-ブタンジオール、1,6-ヘキサンジオール、トリメチロールプロパン、シクロヘキサンジオールなどの二価アルコール;グリセリンなどの水酸基を3個以上有する多価アルコールなどが挙げられるが、本発明は、かかる例示のみに限定されるものではない。これらのアルコールは、それぞれ単独で用いてもよく、2種類以上を併用してもよい。
図1に示される(メタ)アクリル酸エステルの製造システムを使用した。蒸留塔を有する反応装置Aとして、塔頂部に凝縮装置が配設され、側管を有する20段オルダーショウ蒸留塔(理論段数:15段)と、空気導入管とを有する2L容の四つ口フラスコを用いた。当該フラスコ内に、アクリル酸メチル694g(8.06モル)、N,N-ジメチルアミノエタノール552g(6.20モル)、フェノチアジン1.76g、ジブチルスズオキサイド22.1gおよびシクロヘキサン100gを仕込んだ。空気導入管から空気を20mL/分の流量でフラスコ内に吹き込みながらエステル交換反応を行なった。より具体的には、蒸留塔の塔頂から取り出された蒸気を凝縮装置で凝縮し、得られた凝縮液の一部を蒸留塔の上部に還流させ、残りの凝縮液をフラスコ外に除去した。除去した凝縮液の量を調節することにより、蒸留塔の塔頂温度をメチルアルコールとシクロヘキサンとの共沸温度である54~56℃に調整した。
実施例1で用いたのと同じ反応装置Aを用いた。フラスコ内に、アクリル酸メチル517g(6.00モル)、n-オクチルアルコール651g(5.00モル)、フェノチアジン1.76g、テトラメチルチタン0.72gおよびn-ヘキサン117gを仕込んだ。空気導入管から空気を20mL/分の流量でフラスコ内に吹き込みながらエステル交換反応を行なった。より具体的には、蒸留塔の塔頂から取り出された蒸気を凝縮し、得られた凝縮液の一部を上部に還流させ、残りの凝縮液をフラスコ外に除去した。フラスコ外に除去した凝縮液の量を調節することにより、蒸留塔の塔頂温度をメチルアルコールとn-ヘキサンとの共沸温度である48~50℃に調整した。
実施例1で用いたのと同じ反応装置Aを用いた。フラスコ内に、アクリル酸メチル430g(5.0モル)、1,4-ブタンジオール675g(7.5モル)、フェノチアジン0.72g、ジオクチルスズオキサイド3.6gおよびシクロヘキサン100gを仕込んだ。空気導入管から空気を20mL/分の流量でフラスコ内に吹き込みながらエステル交換反応を行なった。より具体的には、蒸留塔の塔頂から取り出された蒸気を凝縮し、得られた凝縮液の一部を上部に還流させ、残りの凝縮液を反応装置外に除去した。反応装置外に除去した凝縮液の量を調節することにより、蒸留塔の塔頂温度をメチルアルコールとシクロヘキサンとの共沸温度である54~56℃に調整した。
実施例1で使用したのと同じ反応装置A内に、メタクリル酸メチル780.9(7.80モル)、N,N-ジメチルアミノエタノール372.4g(6.00モル)およびフェノチアジン1.89gを仕込んだこと以外は、実施例1と同様にしてエステル交換反応を行なった。反応終了後、エステル交換反応によって得られた反応混合物に含まれているメタクリル酸メチルの量は178gであった。
実施例1で使用したのと同じ反応装置A内に、メタクリル酸メチル1041.2(10.4モル)、エチレングリコール248.3g(4.00モル)、フェノチアジン1.59および水酸化リチウム0.96gを仕込んだこと以外は、実施例1と同様にしてエステル交換反応を行なった。反応終了後、エステル交換反応によって得られた反応混合物に含まれているメタクリル酸メチルの量は235gであった。
実施例1において、N,N-ジメチルアミノエタノールの代わりにテトラヒドロフルフリルアルコール633.2g(6.20モル)を用いたこと以外は、実施例1と同様にしてエステル交換反応を行なった。反応終了後、エステル交換反応によって得られた反応混合物に含まれているアクリル酸メチルの量は147gであった。
実施例1において、N,N-ジメチルアミノエタノールの代わりにジエチレングリコールモノエチルエ-テル805.0g(6.00モル)を用いたこと以外は、実施例1と同様にしてエステル交換反応を行なった。反応終了後、エステル交換反応によって得られた反応混合物に含まれているアクリル酸メチルの量は140gであった。
実施例1において、アクリル酸メチル894.8(5.20モル)、1,6-ヘキサンジオール472.7g(4.00モル)およびジオクチルスズオキサイド3.7gを用いたこと以外は、実施例1と同様にしてエステル交換反応を行なった。反応終了後、エステル交換反応によって得られた反応混合物に含まれているアクリル酸メチルの量は189gであった。
実施例1において、アクリル酸メチル1006.7g(11.7モル)、トリメチロールプロパン402.5g(3.00モル)およびジオクチルスズオキサイド8.4gを用いたこと以外は、実施例1と同様にしてエステル交換反応を行なった。反応終了後、エステル交換反応によって得られた反応混合物に含まれているアクリル酸メチルの量は216gであった。
実施例1において、アクリル酸メチル559.3(6.5モル)、2-エチル-2-メチル-1,3-ジオキソラン-4-メタノール1041.5g(5.00モル)およびジオクチルスズオキサイド4.7gを用いたこと以外は、実施例1と同様にしてエステル交換反応を行なった。反応終了後、エステル交換反応によって得られた反応混合物に含まれているアクリル酸メチルの量は117gであった。
実施例1において、アクリル酸メチル615.2(7.15モル)、3-エチル-3-オキセタニルメチルアルコール892.1g(5.50モル)およびジオクチルスズオキサイド5.lgを用いたこと以外は、実施例1と同様にしてエステル交換反応を行なった。反応終了後、エステル交換反応によって得られた反応混合物に含まれているアクリル酸メチルの量は123gであった。
図2に示される(メタ)アクリル酸エステルの製造システムを使用した。
蒸留塔を有する反応装置Aとして、塔頂部に凝縮装置が配設され、側管を有する20段オルダーショウ蒸留塔(理論段数:15段)と、空気導入管とを有する2L容の四つ口フラスコを用いた。当該フラスコ内に、アクリル酸メチル694g(8.06モル)、N,N-ジメチルアミノエタノール552g(6.20モル)、フェノチアジン1.76g、ジブチルスズオキサイド22.1gおよびシクロヘキサン100gを仕込んだ。空気導入管から空気を20mL/分の流量でフラスコ内に吹き込みながらエステル交換反応を行なった。より具体的には、蒸留塔の塔頂から取り出された蒸気を凝縮装置で凝縮し、得られた凝縮液の一部を蒸留塔の上部に還流させ、残りの凝縮液をフラスコ外に除去した。除去した凝縮液の量を調節することにより、蒸留塔の塔頂温度をメチルアルコールとシクロヘキサンとの共沸温度である54~56℃に調整した。
実施例1で用いたのと同じ反応装置Aを用いた。フラスコ内に、アクリル酸メチル694g(8.06モル)、N,N-ジメチルアミノエタノール552g(6.20モル)、フェノチアジン1.76g、ジブチルスズオキサイド22.1gおよびイソヘキサン100gを仕込んだ。
塔頂部に還流装置を備え、側管を有する20段オルダーショウ蒸留塔(理論段数:15段)と、空気導入管とを有する2L容の四つ口フラスコを反応装置として用いた。当該反応装置のフラスコ内に、アクリル酸メチル694g(8.06モル)、N,N-ジメチルアミノエタノール552g(6.20モル)、フェノチアジン1.76g、ジブチルスズオキサイド22.1gおよびシクロヘキサン100gを仕込んだ。空気導入管から空気を20mL/分の流量でフラスコ内に吹き込みながらエステル交換反応を行なった。
2 蒸留塔
3 蒸留装置B
4 蒸留塔
5a~5f 配管
6 凝縮装置
7 切換装置
8 分液装置
9 凝縮装置
10a~10e 配管
11 切換装置
12 回収部
13 蒸留塔
14 蒸留装置C
15 加熱装置
16 配管
17 加熱装置
18a~18e 配管
19 凝縮装置
20 切換装置
21 回収部
Claims (2)
- エステル交換反応によって(メタ)アクリル酸エステルを製造する際に使用される(メタ)アクリル酸エステルの製造システムであって、
蒸留塔を有する反応装置Aと蒸留塔を有する蒸留装置Bとを有し、
反応装置Aの蒸留塔の上部が配管を介して凝縮装置と接続され、凝縮装置で得られた凝縮液の一部を蒸留塔の上部に還流させるための配管で凝縮装置と蒸留塔の上部とが切換装置を介して接続され、凝縮装置で得られた凝縮液の残部を分液装置に送液するための配管で凝縮装置と分液装置とが切換装置を介して接続され、
分液装置で分離された凝縮液のうち上層の液を蒸留塔に還流させるための配管で分液装置の上部と蒸留塔とが接続され、分液装置で分離された凝縮液のうち下層の液を蒸留装置Bに送液するための配管で分液装置の下部と蒸留装置Bとが接続され、
蒸留装置Bの蒸留塔の上部が配管を介して凝縮装置と接続され、凝縮装置で得られた凝縮液の一部を蒸留塔の上部に還流させるための配管で凝縮装置と蒸留塔の上部とが切換装置を介して接続され、凝縮装置で得られた凝縮液の残部を回収するための回収部に送液するための配管で凝縮装置と回収部とが切換装置を介して接続され、
蒸留装置B内に存在する残渣を反応装置Aの蒸留塔に還流させるための配管で蒸留装置Bの下部と、反応装置Aの切換装置と凝縮装置との間の配管とが配管で接続されている(メタ)アクリル酸エステルの製造システム。 - エステル交換反応によって(メタ)アクリル酸エステルを製造する際に使用される(メタ)アクリル酸エステルの製造システムであって、
蒸留塔を有する反応装置Aと蒸留塔を有する蒸留装置Bと蒸留塔を有する蒸留装置Cとを有し、
反応装置Aの蒸留塔の上部が配管を介して凝縮装置と接続され、凝縮装置で得られた凝縮液の一部を蒸留塔の上部に還流させるための配管で凝縮装置と蒸留塔の上部とが切換装置を介して接続され、凝縮装置で得られた凝縮液の残部を分液装置に送液するための配管で凝縮装置と分液装置とが切換装置を介して接続され、
分液装置で分離された凝縮液のうち上層の液を蒸留塔に還流させるための配管で分液装置の上部と蒸留塔とが接続され、分液装置で分離された凝縮液のうち下層の液を蒸留装置Bに送液するための配管で分液装置の下部と蒸留装置Bとが接続され、
蒸留装置Bの蒸留塔の上部が配管を介して凝縮装置と接続され、凝縮装置で得られた凝縮液の一部を蒸留塔の上部に還流させるための配管で凝縮装置と蒸留塔の上部とが切換装置を介して接続され、凝縮装置で得られた凝縮液の残部を回収するための回収部に送液するための配管で凝縮装置と回収部とが切換装置を介して接続され、
蒸留装置B内に存在する残渣を蒸留装置Cの蒸留塔に送液するための配管で蒸留装置Bの下部と、蒸留装置Cとが接続され、
蒸留装置Cの蒸留塔の上部が配管を介して凝縮装置と接続され、凝縮装置で得られた凝縮液の一部を蒸留塔の上部に還流させるための配管で凝縮装置と蒸留塔の上部とが切換装置を介して接続され、凝縮装置で得られた凝縮液の残部を回収するための回収部に送液するための配管で凝縮装置と回収部とが切換装置を介して接続され、
蒸留装置C内に存在する残渣を反応装置Aの蒸留塔に送液するための配管で蒸留装置Cの下部と、反応装置Aの切換装置と凝縮装置との間の配管とが配管で接続されている(メタ)アクリル酸エステルの製造システム。
Priority Applications (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP14816822.2A EP3015449B1 (en) | 2013-06-27 | 2014-06-26 | (meth)acrylate production system |
| KR1020157027112A KR102219539B1 (ko) | 2013-06-27 | 2014-06-26 | (메타)아크릴산 에스테르의 제조 시스템 |
| JP2015524116A JP6363599B2 (ja) | 2013-06-27 | 2014-06-26 | (メタ)アクリル酸エステルの製造システム |
| CN201480036464.6A CN105339341B (zh) | 2013-06-27 | 2014-06-26 | (甲基)丙烯酸酯的制造系统 |
| US14/977,922 US20160136538A1 (en) | 2013-06-27 | 2015-12-22 | (meth)acrylate production system |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2013-134582 | 2013-06-27 | ||
| JP2013134582 | 2013-06-27 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| US14/977,922 Continuation US20160136538A1 (en) | 2013-06-27 | 2015-12-22 | (meth)acrylate production system |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2014208686A1 true WO2014208686A1 (ja) | 2014-12-31 |
Family
ID=52142012
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2014/067043 WO2014208686A1 (ja) | 2013-06-27 | 2014-06-26 | (メタ)アクリル酸エステルの製造システム |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US20160136538A1 (ja) |
| EP (1) | EP3015449B1 (ja) |
| JP (1) | JP6363599B2 (ja) |
| KR (1) | KR102219539B1 (ja) |
| CN (1) | CN105339341B (ja) |
| WO (1) | WO2014208686A1 (ja) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN105646201A (zh) * | 2015-12-30 | 2016-06-08 | 潍坊科麦化工有限公司 | 一种乙酰乙酸基甲基丙烯酸乙酯的合成方法 |
| CN106518815A (zh) * | 2015-09-11 | 2017-03-22 | 万华化学集团股份有限公司 | 一种连续酯化反应制备四氢呋喃丙烯酸酯的方法及其催化剂的制备方法 |
| CN109134245A (zh) * | 2018-10-22 | 2019-01-04 | 南京晓庄学院 | 一种酯交换法生产甲基丙烯酸羟乙酯的方法 |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN106966913B (zh) * | 2017-04-06 | 2020-07-10 | 青岛科技大学 | 一种甲基丙烯酸二烷氨基乙酯的制备方法 |
| CN108976136A (zh) * | 2017-05-31 | 2018-12-11 | 中国石油化工股份有限公司 | 一种甲基丙烯酸二烷氨基乙酯的合成方法 |
| CN110698437B (zh) * | 2019-10-29 | 2021-05-18 | 山东瑞博龙化工科技股份有限公司 | 丙烯酸(3-乙基-3-氧杂环丁烷基)甲酯的制备方法及应用 |
| CN114746518A (zh) * | 2019-11-29 | 2022-07-12 | 三菱化学株式会社 | 喷墨印刷用紫外线固化性水性印墨、喷墨印刷用紫外线固化性水性组合物及印刷物 |
| CN113831317A (zh) * | 2021-08-03 | 2021-12-24 | 中山市千佑化学材料有限公司 | 一种合成甘油缩丁酮丙烯酸酯的方法 |
| EP4299155A1 (en) * | 2022-06-27 | 2024-01-03 | Evonik Operations GmbH | Process to precisely calculate the raw material demand of intermediate batches within a production campaign |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH08268938A (ja) | 1995-03-29 | 1996-10-15 | Osaka Organic Chem Ind Ltd | アクリル酸メチルまたはメタクリル酸メチルとメタノールの分離方法 |
| JP2004189650A (ja) | 2002-12-10 | 2004-07-08 | Mitsubishi Rayon Co Ltd | (メタ)アクリル酸エステルの製造方法 |
| JP4520310B2 (ja) * | 2003-05-28 | 2010-08-04 | ダイヤニトリックス株式会社 | (メタ)アクリル酸n−アルキルアミノアルキルエステルの製造方法 |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB1373159A (en) * | 1972-08-29 | 1974-11-06 | Ici Ltd | Methanol |
| KR100342737B1 (ko) * | 1995-04-10 | 2002-12-11 | 오오사까유끼가가꾸고오교오가부시끼가이샤 | 아크릴산메틸또는메타크릴산메틸과메탄올의분리방법 |
| DE10063510A1 (de) * | 2000-12-20 | 2002-07-04 | Basf Ag | Verfahren und Vorrichtung zur kontinuierlichen Herstellung von Alkylacrylaten |
| US20050107629A1 (en) * | 2003-11-17 | 2005-05-19 | Hershberger Brian L. | Method for producing ethyl acrylate |
-
2014
- 2014-06-26 KR KR1020157027112A patent/KR102219539B1/ko active IP Right Grant
- 2014-06-26 WO PCT/JP2014/067043 patent/WO2014208686A1/ja active Application Filing
- 2014-06-26 JP JP2015524116A patent/JP6363599B2/ja active Active
- 2014-06-26 EP EP14816822.2A patent/EP3015449B1/en active Active
- 2014-06-26 CN CN201480036464.6A patent/CN105339341B/zh active Active
-
2015
- 2015-12-22 US US14/977,922 patent/US20160136538A1/en not_active Abandoned
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH08268938A (ja) | 1995-03-29 | 1996-10-15 | Osaka Organic Chem Ind Ltd | アクリル酸メチルまたはメタクリル酸メチルとメタノールの分離方法 |
| JP2004189650A (ja) | 2002-12-10 | 2004-07-08 | Mitsubishi Rayon Co Ltd | (メタ)アクリル酸エステルの製造方法 |
| JP4520310B2 (ja) * | 2003-05-28 | 2010-08-04 | ダイヤニトリックス株式会社 | (メタ)アクリル酸n−アルキルアミノアルキルエステルの製造方法 |
Non-Patent Citations (1)
| Title |
|---|
| See also references of EP3015449A4 |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN106518815A (zh) * | 2015-09-11 | 2017-03-22 | 万华化学集团股份有限公司 | 一种连续酯化反应制备四氢呋喃丙烯酸酯的方法及其催化剂的制备方法 |
| CN106518815B (zh) * | 2015-09-11 | 2019-06-18 | 万华化学集团股份有限公司 | 一种连续酯化反应制备四氢呋喃丙烯酸酯的方法及其催化剂的制备方法 |
| CN105646201A (zh) * | 2015-12-30 | 2016-06-08 | 潍坊科麦化工有限公司 | 一种乙酰乙酸基甲基丙烯酸乙酯的合成方法 |
| CN109134245A (zh) * | 2018-10-22 | 2019-01-04 | 南京晓庄学院 | 一种酯交换法生产甲基丙烯酸羟乙酯的方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP3015449A4 (en) | 2017-03-01 |
| CN105339341A (zh) | 2016-02-17 |
| KR102219539B1 (ko) | 2021-02-24 |
| EP3015449A1 (en) | 2016-05-04 |
| CN105339341B (zh) | 2018-02-13 |
| JP6363599B2 (ja) | 2018-07-25 |
| KR20160026829A (ko) | 2016-03-09 |
| EP3015449B1 (en) | 2018-10-10 |
| JPWO2014208686A1 (ja) | 2017-02-23 |
| US20160136538A1 (en) | 2016-05-19 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6363599B2 (ja) | (メタ)アクリル酸エステルの製造システム | |
| JP5582032B2 (ja) | (メタ)アクリル酸エステルの製造方法 | |
| KR101692682B1 (ko) | (메트)아크릴산 무수물의 제조 방법 및 보존 방법, 및 (메트)아크릴산 에스터의 제조 방법 | |
| JP6290460B2 (ja) | アクリル酸の製造方法 | |
| US5659072A (en) | Process for the manufacture of alkyl acrylates by direct esterification | |
| WO2013157597A1 (ja) | 4-ヒドロキシブチルアクリレートの製造方法 | |
| EP0968995B1 (en) | Process for continuously producing ester of acrylic or methacrylic acid | |
| TWI501945B (zh) | (甲基)丙烯酸羥烷基酯之製造方法 | |
| JP5093103B2 (ja) | (メタ)アクリル酸エステルの製造方法 | |
| JP6132570B2 (ja) | (メタ)アクリル酸エステルの製造方法 | |
| JP5964180B2 (ja) | (メタ)アクリル酸エステルの製造方法 | |
| JP6159538B2 (ja) | ヒドロキシアルキルアクリレートの製造方法 | |
| JP2007015956A (ja) | (メタ)アクリレートの製造方法及び製造装置 | |
| KR20090033711A (ko) | 하이드록시알킬 (메타)아크릴레이트 반응에서의 촉매분리방법 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WWE | Wipo information: entry into national phase |
Ref document number: 201480036464.6 Country of ref document: CN |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 14816822 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2015524116 Country of ref document: JP Kind code of ref document: A |
|
| ENP | Entry into the national phase |
Ref document number: 20157027112 Country of ref document: KR Kind code of ref document: A |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2014816822 Country of ref document: EP |