WO2006095836A1 - 多発性硬化症に伴う痒みに対する止痒剤 - Google Patents
多発性硬化症に伴う痒みに対する止痒剤 Download PDFInfo
- Publication number
- WO2006095836A1 WO2006095836A1 PCT/JP2006/304655 JP2006304655W WO2006095836A1 WO 2006095836 A1 WO2006095836 A1 WO 2006095836A1 JP 2006304655 W JP2006304655 W JP 2006304655W WO 2006095836 A1 WO2006095836 A1 WO 2006095836A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- carbon atoms
- epoxy
- hydrogen
- morphinan
- cyclopropylmethyl
- Prior art date
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D489/00—Heterocyclic compounds containing 4aH-8, 9 c- Iminoethano-phenanthro [4, 5-b, c, d] furan ring systems, e.g. derivatives of [4, 5-epoxy]-morphinan of the formula:
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/02—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains two hetero rings
- C07D491/10—Spiro-condensed systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/485—Morphinan derivatives, e.g. morphine, codeine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/04—Antipruritics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
Definitions
- the present invention relates to an antidiarrheal agent against itching associated with multiple sclerosis.
- MS Multiple sclerosis
- Intractable Disease Information Center which is jointly operated by the Ministry of Health, Labor and Welfare, Health Bureau, Disease Control Division and the Foundation for Research on Intractable Diseases.
- Non-Patent Document 2 One of the sensory disorders is severe itching (pruritus), which occurs when there is a disorder in the dorsal horn of the spinal cord (for example, Non-Patent Document 2).
- This itch is characterized by a few minutes of itch appearing several times a day.
- the site of itching is relatively bilateral, according to the segments of nerve branches such as the cervical and thoracic nerves.
- the feeling of itching is an unbearable itching after being stabbed by a small insect, and when it appears at night, it disturbs sleep (for example, Non-Patent Document 3). There is no rash on the skin, but sometimes the skin is eroded by intense whispering power.
- Non-Patent Document 5 Dermatologists express itch that does not stop even if they crawl, and itch that can be destroyed by self-injury, as a strange symptom (for example, Non-Patent Document 2).
- Opioid ⁇ having 4,5-epoxymorphinan skeleton Receptor agonist compounds include, for example, atopic dermatitis, neurodermatitis, contact dermatitis, seborrheic dermatitis, self-sensitizing dermatitis, caterpillar dermatitis, sebum deficiency, senile skin pruritus Dermatosis, insect bites, photosensitivity, urticaria, urticaria, shingles, impetigo, eczema, ringworm, lichen, psoriasis, scabies, acne vulgaris, and malignant tumors, diabetes, liver disease, It has been reported that it can be an antidiarrheal agent for the treatment of general pruritus such as renal failure, renal dialysis, and visceral diseases such as pregnancy (
- opioid ⁇ -receptor activity is not a cause of multiple sclerosis, which is caused by a neurological disease, not a skin disease or a medical disease, and whose characteristics and treatment are greatly different from those of normal itch. It was unclear whether the compound was effective.
- Patent Document 1 Japanese Patent No. 3531170
- Non-Patent Document 1 Research Group for Neurological and Muscle Disease (Immune Neurological Diseases), Stealing, Treatment Guidelines> Multiple Sclerosis A [online], June 20, 2005, Information Center for Intractable Diseases, [Heisei 18 February 27, 2005 ", Internet http://www.nanbyou.or.jp/sikkan/068 ⁇ htm>
- Non-Patent Document 2 “General Clinical” written by Seihiro Inoue, (Japan), 2004, 53rd, No. 5, p. 180
- Non-Patent Document 3 “Yumi Q & A” edited by Ryoji Kaji, (Japan), first edition, Pharmaceutical Journal, Inc., 1997, p. 86-87
- Non-patent literature 4 Seikei Inoue, “Nippon Medical News”, (Japan), 2003, No. 4157, p. 85
- Non-patent literature 5 Takashi Yamamura (supervised by National Institute of Neurology and Neurology), “ Overview of Multiple Sclerosis ”, [online], March 2004, Specified Nonprofit Corporation MS Cabin, [Search February 27, 2006], Internet http: http www.mscabin.org/ms08. html>
- Non-Patent Document 6 European Journal of Pharmacology, (Netherlands), 2002, No. 435, No. 2-3, p. 259-264
- An object of the present invention is to provide an antidiarrheal agent for itch caused by multiple sclerosis, which is not available in the prior art.
- the present inventors have obtained an opioid having a 4,5-epoxymorphinan skeleton.
- a kappa receptor agonist compound has an action to suppress bowel I beating behavior in MRL / lpr mice, which are widely used as an autoimmune disease model, and is particularly useful as an antidiarrheal agent for multiple sclerosis.
- the present invention has been completed. That is, the present invention provides the following general formula (I)
- R 1 is alkyl having 1 to 5 carbon atoms, cycloalkyl alkyl having 4 to 7 carbon atoms, cycloalkalkyl having 5 to 7 carbon atoms, 6 to 12 carbon atoms, aralkyl having 7 to 13 carbon atoms, carbon number 4 to 7 alkyl, aryl, furan 2-ylalkyl (the alkyl part has 1 to 5 carbon atoms) or thiophene 2-ylalkyl (the alkyl part has 1 to 5 carbon atoms),
- R 2 represents hydrogen, hydroxy, nitro, alkanoyloxy having 1 to 5 carbons, alkoxy having 1 to 5 carbons, alkyl having 1 to 5 carbons, or NR 9 R 1C)
- R 9 represents hydrogen or
- R 1G represents hydrogen, alkyl having 1 to 5 carbons, or
- R n represents hydrogen, phenol, or alkyl having 1 to 5 carbon atoms
- R 3 represents hydrogen, hydroxy, alkanoyloxy having 1 to 5 carbons, or alkoxy having 1 to 5 carbons;
- R 4 represents hydrogen, straight-chain or branched alkyl having 1 to 5 carbon atoms, or aryl having 6 to 12 carbon atoms, wherein R 4 May be the same or different
- B is a valence bond, straight-chain or branched alkylene having 1 to 14 carbon atoms (however, alkoxy having 1 to 5 carbon atoms, alkanoyloxy having 1 to 5 carbon atoms, hydroxy, fluorine, chlorine, bromine, iodine, amino Group power of nitro, trifluoromethyl, and phenoxy groups, which may be substituted with at least one selected substituent, or 1 to 3 methylene groups may be replaced by carbonyl groups)
- a C2-C14 linear or branched acyclic unsaturated hydrocarbon containing 1 to 3 double bonds and Z or triple bonds (provided that alkoxy having 1 to 5 carbons, alkano having 1 to 5 carbons) Substituted with at least one substituent selected from the group consisting of oxy, hydroxy, fluorine, chlorine, bromine, iodine, ami-containing nitro, cyan, trifluoromethyl and phenoxy.
- 1 to 3 methylene groups may be replaced by a carbocycle group), or 1 to 5 carbon atoms containing 1 to 5 thioether bonds, ether bonds and Z or amino bonds. 14 straight or min Saturated or unsaturated hydrocarbons (however, the heteroatom is not directly bonded to A, and 1 to 3 methylene groups are replaced by a carbonyl group! /, May! /) Represent,
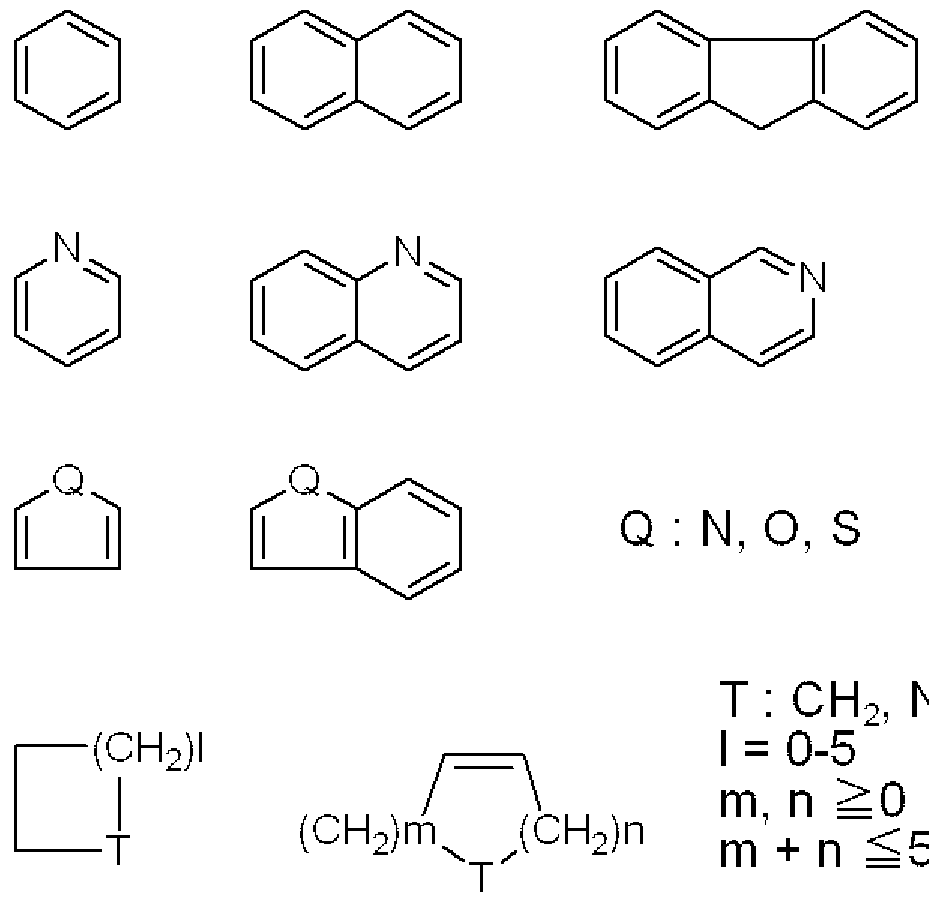
- R 5 is hydrogen or the following basic skeleton:
- Q represents N, O or S
- T represents CH, NH
- C 1 to C 5 alkoxy, C 1 to C 5 alkanoyloxy, hydroxy, fluorine, chlorine, bromine, iodine, ami-nitro, cyano, isothiocyanato, trifluoromethyl, trifluoromethoxy and Methylene dioxyca also represents a group force that may be substituted by at least one selected substituent, and
- R 6 is hydrogen
- R 7 is hydrogen, hydroxy, alkoxy having 1 to 5 carbon atoms or alkanoyloxy having 1 to 5 carbon atoms, or R 6 and R 7 together — 0—, —CH— Or — S
- R 8 represents hydrogen, alkyl having 1 to 5 carbons or alkanol having 1 to 5 carbons
- R 12 and R 13 are both hydrogen, or one of them is hydrogen and the other is hydroxy, or together represents oxo.
- the general formula (I) includes (+) body, (-) body, and (shi) body. ]
- a pharmacologically acceptable acid addition salt thereof as an active ingredient is provided as an antidiarrheal agent against itching associated with multiple sclerosis.
- the present invention also provides the use of a compound represented by the above general formula (I) or a pharmacologically acceptable acid addition salt thereof for the production of an antipruritic agent.
- the present invention relates to multiple sclerosis comprising administering to a patient with multiple sclerosis an effective amount of the compound represented by the above general formula (I) or a pharmaceutically acceptable acid addition salt thereof.
- a method is provided for preventing or reducing the associated itch.
- the present invention there has been provided a therapeutic agent for treating itch associated with multiple sclerosis, for which there has been no effective treatment.
- the antidiarrheal agent of the present invention has an excellent alleviating effect against itching associated with multiple sclerosis. Therefore, by administering the antidiarrheal agent of the present invention to a patient with multiple sclerosis, the patient's pruritus is reduced and the quality of life of the patient is improved.
- FIG. 1 is a graph showing the relationship between the age of the mouse and the serum IgG antibody value or serum IgE antibody value in the MRL / lpr mice used in the examples of the present invention.
- FIG. 2 is a graph showing the relationship between the age of the mouse and the serum IgG antibody level or serum IgE antibody level in the MRL / lpr mice used in the examples of the present invention.
- FIG. 2 is a graph showing the relationship between the dose of Compound 1 of the present invention and the number of pulling actions measured in the examples of the present invention, and the comparison compound anti-histamine drug chlorchloramine. It is a figure which shows the relationship between dosage and the frequency
- the antidiarrheal agent of the present invention contains the compound represented by the above general formula (I) or a pharmacologically acceptable acid addition salt thereof as an active ingredient.
- R 1 is alkyl having 1 to 5 carbons, cycloalkylmethyl having 4 to 7 carbons, cycloalkylmethyl having 5 to 7 carbons, or phenylalkyl having 7 to 13 carbons.
- Carbonyl, aryl, and furan 2-alkyl alkyls with 4 to 7 carbon atoms (the alkyl part has 1 to 5 carbon atoms) and thiophene 2-yl alkyls (with the alkyl part having 1 to 5 carbon atoms) are preferred.
- Methyl, ethyl, propyl, butyl, isobutyl, cyclopropylmethyl, allyl, benzyl and phenethyl are particularly preferred.
- R 2 is preferably hydrogen, hydroxy, nitro, acetoxy, methoxy, methyl, ethynole, propyl, dimethylamino-substituted acetylamino-substituted benzilamino, and more preferably hydrogen, hydroxy, nitro, acetoxy, methoxy, methyl, Particularly preferred are dimethylamido hydrogen, hydroxy, acetonitrile and methoxy.
- R 3 hydrogen, hydroxy, acetoxy, and methoxy are preferable, and hydroxy, acetoxy, and methoxy are particularly preferable.
- XC ( Y) Z—, one X—, or one XSO ⁇ (where X represents NR 4 , Y represents O or S, and Z represents NR 4
- R 4 is hydrogen, linear or branched alkyl having 1 to 5 carbon atoms, which is preferably straight-chain or branched alkyl having 1 to 5 carbon atoms, particularly methyl, ethyl, propyl, butyl, Isobutyl is particularly preferred.
- CH CH—, —C ⁇ C—, —CH 2 O, or —
- CH 2 S 1 CH ⁇ CH or 1 C ⁇ C— is preferred.
- R 5 is hydrogen or the following basic skeleton:
- An organic group having any one of the above (wherein, Q represents O or S, and each organic group is alkyl having 1 to 5 carbon atoms, alkoxy having 1 to 5 carbon atoms, or 1 carbon atom)
- each organic group is alkyl having 1 to 5 carbon atoms, alkoxy having 1 to 5 carbon atoms, or 1 carbon atom
- R 5 above hydrogen, phenol, chenyl, and furanyl (however, these organic groups are alkyl having 1 to 5 carbon atoms, alkoxy having 1 to 5 carbon atoms, and 1 carbon atom).
- More specific examples are hydrogen, phenol, 2-methylphenol, 3-methylphenol, 4-methylmethyl, 3,4-dimethylphenol, 3,5-dimethylmer, 2-methoxyphenyl. , 3-methoxyphenyl, 4-methoxyphenyl, 3,4-dimethoxyphenyl, 3-hydroxyphenyl, 4-hydroxyphenyl, 3,4 dihydroxyphenyl, 2 fluorophenol, 3-funoleolo Feninore, 4—Funoreolofeninore, 3, 4—Diphnorolerofeninore, Noffolet Rofeninole, 2 Kuroguchi Feninore, 3 Kuroguchi Feninore, 4 Kuroguchi Feninore, 2 , 4-dichrome mouth fenore, 3, 4, dichroic mouth cinnole, 2, 4, 5 trichrome mouth fenenore, 2, 4, 6 trichrome mouth fenore, 2 bromo p
- —O— is particularly preferable.
- R 8 a hydrogen, an alkyl having 1 to 5 carbon atoms, Arukanoiru is preferred signaling hydrogen having 1 to 5 carbon atoms, methyl, Echiru, propyl more Konomashigu hydrogen particularly preferred.
- R 12 and R 13 are both hydrogen, which force is hydroxy, together preferably oxo is preferred, and both hydrogen or either is more preferred, and hydrogen is particularly preferred.
- R 1 is methyl, ethyl, propyl, butyl, isobutyl, cyclopropylmethyl, allyl, benzyl or phenethyl
- R 2 , R 3 Are each independently hydrogen, hydroxy, acetoxy, methoxy
- X represents NR 4 , Y represents O or S, Z represents NR 4 or O, R 4 represents hydrogen or linear or branched alkyl having 1 to 5 carbon atoms), B Is a straight-chain alkylene having 1 to 3 carbon atoms, R 6 and R 7 are joined together — O, and R 8 is hydrogen, or a pharmacologically acceptable acid addition salt thereof.
- An antipruritic agent for itch caused by multiple sclerosis as a component is preferable.
- R 4 represents a straight-chain or branched alkyl having 1 to 5 carbon atoms) or a pharmacologically acceptable acid addition salt thereof as an active ingredient for an antipruritic agent against itching associated with multiple sclerosis
- R 5 is hydrogen or the following basic skeleton:
- Organic group represented by R 5 An organic group having any one of the above (wherein, Q represents O or S, and each organic group is alkyl having 1 to 5 carbon atoms, alkoxy having 1 to 5 carbon atoms, or 1 carbon atom) To 5 substituted with at least one substituent selected from the group consisting of alkanoyloxy, hydroxy, fluorine, chlorine, bromine, iodine, ami-nitro, cyano, isothiocyanato, trifluoromethyl, trifluoromethoxy and methylenedioxy Have been,)
- An antidiarrheal agent against itching associated with multiple sclerosis which comprises a compound or a pharmacologically acceptable acid addition salt thereof as an active ingredient is preferred.
- A is
- an antipruritic agent against itching associated with multiple sclerosis which comprises a compound or a pharmacologically acceptable acid addition salt thereof as an active ingredient.
- R 1 is methyl, ethyl, propyl, butyl, isobutyl, cyclopropylmethyl, aryl, benzyl or phenethyl
- R 2 and R 3 are each independently hydrogen, hydroxy, acetoxy or methoxy
- A is
- R 5 is hydrogen or the following basic skeleton: [0036]
- An organic group having any of the above (wherein, Q represents O or S, and each organic group is alkyl having 1 to 5 carbon atoms, alkoxy having 1 to 5 carbon atoms, or 1 to carbon atoms) Selected from the group consisting of 5 alkanoyloxy, hydroxy, fluorine, chlorine, bromine, iodine, nitro nitro, cyan, isothiocyanato, trifluoromethyl, trifluoromethoxy and methylenedioxy
- R 5 is hydrogen or the following basic skeleton:
- Q represents O or S
- each organic group is alkyl having 1 to 5 carbon atoms, alkoxy having 1 to 5 carbon atoms, or 1 to carbon atoms.
- an antipruritic agent against itching associated with multiple sclerosis which comprises a compound or a pharmacologically acceptable acid addition salt thereof as an active ingredient.
- the compound represented by the general formula (I) is known per se and can be produced by a known production method.
- those in which R 12 and R 13 are both hydrogen can be produced according to the method shown in Japanese Patent No. 2525552.
- compounds in which R 12 and R 13 are combined to form an oxo group are described in, for example, literature (Heterocycles, 63, 865 (2004), Bioorg. Med. Chem. Lett , 5, 1505 (1995)), and is produced according to the method described in Chem. Pharm. Bull. 52, 664 (2004) and Patent No. 2525552. be able to.
- Preferable examples of pharmacologically acceptable acid addition salts for the above-mentioned compounds include inorganic acid salts such as hydrochloride, sulfate, nitrate, hydrobromide, hydroiodide, and phosphate. , Acetate, lactate, citrate, oxalate, dartrate, malate, tartrate, fumarate, mandelate, maleate, benzoate, phthalate, etc.
- Organic sulfonates such as salts, methane sulfonate, ethane sulfonate, benzene sulfonate, p-toluene sulfonate, camphor sulfonate, and the like.
- hydrochloride, hydrobromide, Phosphate, tartrate, methanesulfonate, etc. are preferred, but of course not limited to these! /.
- the dosage form for oral administration can be selected from tablets, capsules, powders, granules, etc.
- parenteral administration can be selected from rapid intravenous infusion, continuous intravenous infusion, intramuscular injection, intradermal injection, subcutaneous injection, etc. ,Also Of course, it is not limited to this.
- the content of the present compound in the pharmaceutical composition is not particularly limited, but it is usually prepared to be 0.:g to: LOOmg at one time for both oral and parenteral administration.
- the dose can be appropriately selected according to the patient's symptoms and the like, but is usually 0.1 g to 20 mg, preferably 1 as the amount of the active ingredient represented by the general formula (1) per day for an adult. ⁇ g is about 10mg
- the compound of the present invention can also be used in combination with, for example, a drug used for the prevention or treatment of multiple sclerosis.
- corticosteroids intended for acute treatment such as cortisone acetate, hydrocortisone, hydroconoretisone phosphate, hydroconoretisone succinate, prednisolone, succinic acid Prednisolone, methylprednisolone, methylprednisolone acetate, methylprednisolone succinate, triamcinolone, triamcinolone acetate, dexamethasone, dexamethasone phosphate, dexamethasone normitate, betamethasone, betamethasone phosphate, parameterzone acetate, fluprecordone acetate, etc.
- Interferon used for the purpose of suppressing recurrence or progression such as interferon beta, interferon beta-lb (genetical recombination), etc. and immunosuppressive agents such as aza Opurine, mizoribine, mycofenol mofuethyl monosulfate, methotrexate, leflunomide, cyclophosphamide, cyclosporine, neoral, tac mouth limus hydrate, gusperimus hydrochloride, muromonab-CD3, nosiliximab, etc.
- immunosuppressive agents such as aza Opurine, mizoribine, mycofenol mofuethyl monosulfate, methotrexate, leflunomide, cyclophosphamide, cyclosporine, neoral, tac mouth limus hydrate, gusperimus hydrochloride, muromonab-CD3, nosiliximab, etc.
- Targeted muscle relaxants such as tolperisone hydrochloride, metcarbamol, fenprobamate, pridinol mesylate, chlorfenesine rubamate, noclofen, piracetam, eperisone hydrochloride, afloqualone, tizadine hydrochloride, squisametonium hydrochloride, dantrolene Sodium, panchrome bromide, bebromine bromide, etc., and antiepileptic drugs for the treatment of sensory disorders such as primidone, fetotoin, etotoin, trimetadione, sultiam, etosucci Acetylphenetride, clonazepam, diazepam, clobazam, carbamazepine, sodium valproate, zo-samide, etc.
- tolperisone hydrochloride metcarbamol, fenproba
- tricyclic antidepressants such as imibulamine hydrochloride, clomipramine hydrochloride, trimipramine maleate, amitriptyline hydrochloride, nortriptyline hydrochloride, hydrochloric acid Anti-cholinestera for the treatment of dysuria, including oral flavin, amoxapine, doslevine hydrochloride, etc.
- salt-and-bendum salt-and-bodeum
- distigmine bromide and frequent urine treatments
- flavoxate hydrochloride oxyptynine hydrochloride, propiverine hydrochloride, and mesna
- psychostimulants aimed at improving fatigue such as pemoline and dopamine release promoters, such as amantadine hydrochloride.
- EAE autoimmune encephalomyelitis
- MRL / lpr mice This strain is a model animal that is widely used as a model of autoimmune disease, and inflammation or nervous abnormal behavior of central tissues has been reported (Scand. J. Rheumatol. 12, 263-273 (1995) has been reported.
- MRL / lpr mice it was confirmed that it causes pulling behavior against itching as shown in Reference Example 1 described below.
- the serum IgG level which is an indicator of the activity level of the blood, is more prominent in females, which is a result reminiscent of multiple sclerosis occurring more frequently in women.
- the MRL / lpr mouse is the model that reflects the itchiness of multiple sclerosis among the existing evaluation systems, and the inventors have found that the compounds effective in this evaluation system are itchiness associated with multiple sclerosis. Found to be an antidiarrheal agent.
- mice The pulling action was measured as a series of movements from the time the mouse lifted the hind limb to start pulling and then lowered. The results are shown in Table 1.
- ** indicates that the difference from the control group (at the age of 8 weeks) is statistically significant (p 0.01) (multiple comparison test between time points of 1 group).
- female MRL / lpr mice showed significant pulling behavior even at 10 weeks of age, and the average number of pulling behaviors at 20 weeks of age exceeded 300. It was shown that it is desirable to use female mice for evaluation.
- IgG antibody titer correlates with the number of pulling behaviors.
- the blood IgE antibody titer was not more than g / mL on average, although a slight slight increase was observed in females. This result was similar to that of multiple sclerosis, where no significant increase in IgE antibody titer was observed.
- the ability to suppress the pulling behavior was evaluated.
- the evaluation was divided into 5 days, and on the first day, sterilized distilled water was orally administered 30 minutes before the start of shooting of the pulling behavior, and the number of pulling behaviors at the time of solvent administration was measured for 60 minutes.
- the eyes were orally administered to the same mice at 3 ⁇ g / kg 30 minutes before the start of shooting of the pulling behavior, and the number of bowing movements for 60 minutes was counted.
- each mouse is individually placed in one observation cage (1 division: 10 X 14 X 30cm), and then one hour of action is performed by video recording from above in an unattended environment.
- the videotape was reproduced and measured visually.
- the pulling action was measured as a series of movements until the mouse lifted the hind limb to start pulling and dropped.
- chlorfelamin an antihistamine
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Emergency Medicine (AREA)
- Epidemiology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Biomedical Technology (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Hospice & Palliative Care (AREA)
- Dermatology (AREA)
- Psychiatry (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Description
Claims
Priority Applications (9)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP06715476.5A EP1870413B1 (en) | 2005-03-10 | 2006-03-09 | Antipruritic agent for pruritus caused by multiple sclerosis |
| US11/885,946 US9051335B2 (en) | 2005-03-10 | 2006-03-09 | Antipruritic agent for pruritus caused by multiple sclerosis |
| PL06715476T PL1870413T3 (pl) | 2005-03-10 | 2006-03-09 | Środek przeciwświądowy w przypadku świądu spowodowanego stwardnieniem rozsianym |
| JP2007507193A JP5119919B2 (ja) | 2005-03-10 | 2006-03-09 | 多発性硬化症に伴う痒みに対する止痒剤 |
| ES06715476T ES2423004T3 (es) | 2005-03-10 | 2006-03-09 | Agente antiprurítico para el prurito provocado por la esclerosis múltiple |
| CA2604071A CA2604071C (en) | 2005-03-10 | 2006-03-09 | Antipruritic agent for pruritus caused by multiple sclerosis |
| CN2006800078067A CN101137658B (zh) | 2005-03-10 | 2006-03-09 | 用于与多发性硬化症伴随的搔痒的止痒剂 |
| AU2006221314A AU2006221314B2 (en) | 2005-03-10 | 2006-03-09 | Antipruritic agent for pruritus caused by multiple sclerosis |
| KR1020077020357A KR101324539B1 (ko) | 2005-03-10 | 2006-03-09 | 다발성 경화증에 따른 가려움의 치료에 사용하는 제품 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2005066666 | 2005-03-10 | ||
| JP2005-066666 | 2005-03-10 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2006095836A1 true WO2006095836A1 (ja) | 2006-09-14 |
Family
ID=36953428
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2006/304655 WO2006095836A1 (ja) | 2005-03-10 | 2006-03-09 | 多発性硬化症に伴う痒みに対する止痒剤 |
Country Status (11)
| Country | Link |
|---|---|
| US (1) | US9051335B2 (ja) |
| EP (1) | EP1870413B1 (ja) |
| JP (1) | JP5119919B2 (ja) |
| KR (1) | KR101324539B1 (ja) |
| CN (1) | CN101137658B (ja) |
| AU (1) | AU2006221314B2 (ja) |
| CA (1) | CA2604071C (ja) |
| ES (1) | ES2423004T3 (ja) |
| PL (1) | PL1870413T3 (ja) |
| PT (1) | PT1870413E (ja) |
| WO (1) | WO2006095836A1 (ja) |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2008133297A1 (ja) | 2007-04-24 | 2008-11-06 | Toray Industries, Inc. | ジスキネジアの治療または予防剤 |
| WO2009044883A1 (ja) | 2007-10-05 | 2009-04-09 | Toray Industries, Inc. | モルヒナン誘導体またはその薬理学的に許容される酸付加塩を有効成分とする皮膚性状改善治療薬 |
| WO2011093441A1 (ja) | 2010-01-29 | 2011-08-04 | 東レ株式会社 | 胆道疾患の治療又は予防剤 |
| US8183256B2 (en) | 2007-06-22 | 2012-05-22 | Toray Industries, Inc. | Remedy or preventive for integration dysfunction syndrome |
| WO2012105475A1 (ja) | 2011-01-31 | 2012-08-09 | 東レ株式会社 | 悪液質の治療又は予防剤 |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN102266317A (zh) * | 2011-06-24 | 2011-12-07 | 中国人民解放军第三军医大学 | 丙戊酸及其衍生物的应用 |
| CN102526732A (zh) * | 2011-12-20 | 2012-07-04 | 同济大学 | 靶向调节组蛋白乙酰化水平的药物在制备用于预防或治疗自身免疫性疾病的药物中的用途 |
| WO2016152953A1 (ja) * | 2015-03-24 | 2016-09-29 | 東レ株式会社 | モルヒナン誘導体及びその医薬用途 |
| AU2019229892A1 (en) | 2018-03-08 | 2020-09-03 | University Of Kansas | Treatment of demyelinating diseases |
| US11135197B2 (en) | 2020-02-07 | 2021-10-05 | Argentum Pharmaceuticals Llc | Dosage regimen of an S1P receptor modulator |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2001014383A1 (fr) * | 1999-08-24 | 2001-03-01 | Toray Industries, Inc. | Remedes contre les douleurs neuropathiques et modeles animaux de douleurs neuropathiques |
| JP2001163784A (ja) * | 1999-12-06 | 2001-06-19 | Toray Ind Inc | 角膜または結膜用止痒剤 |
| JP2002308769A (ja) * | 2001-04-12 | 2002-10-23 | Toray Ind Inc | 止痒剤 |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH0578243A (ja) * | 1990-12-11 | 1993-03-30 | Shiseido Co Ltd | 鎮痒剤及び鎮痒組成物 |
| ATE291429T1 (de) * | 1996-11-25 | 2005-04-15 | Toray Industries | Mittel gegen juckreiz |
| WO2001041705A2 (en) | 1999-11-29 | 2001-06-14 | Adolor Corporation | Novel methods for the treatment and prevention of dizziness and pruritus |
| EP1696877A4 (en) * | 2003-11-13 | 2010-06-09 | Gen Hospital Corp | PROCESS FOR PAIN TREATMENT |
-
2006
- 2006-03-09 WO PCT/JP2006/304655 patent/WO2006095836A1/ja active Application Filing
- 2006-03-09 CA CA2604071A patent/CA2604071C/en not_active Expired - Fee Related
- 2006-03-09 PL PL06715476T patent/PL1870413T3/pl unknown
- 2006-03-09 JP JP2007507193A patent/JP5119919B2/ja not_active Expired - Fee Related
- 2006-03-09 CN CN2006800078067A patent/CN101137658B/zh not_active Expired - Fee Related
- 2006-03-09 KR KR1020077020357A patent/KR101324539B1/ko active IP Right Grant
- 2006-03-09 ES ES06715476T patent/ES2423004T3/es active Active
- 2006-03-09 AU AU2006221314A patent/AU2006221314B2/en not_active Ceased
- 2006-03-09 PT PT67154765T patent/PT1870413E/pt unknown
- 2006-03-09 EP EP06715476.5A patent/EP1870413B1/en not_active Not-in-force
- 2006-03-09 US US11/885,946 patent/US9051335B2/en not_active Expired - Fee Related
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2001014383A1 (fr) * | 1999-08-24 | 2001-03-01 | Toray Industries, Inc. | Remedes contre les douleurs neuropathiques et modeles animaux de douleurs neuropathiques |
| JP2001163784A (ja) * | 1999-12-06 | 2001-06-19 | Toray Ind Inc | 角膜または結膜用止痒剤 |
| JP2002308769A (ja) * | 2001-04-12 | 2002-10-23 | Toray Ind Inc | 止痒剤 |
Non-Patent Citations (2)
| Title |
|---|
| "Sogo Rinsho", PARTIAL TRANSLATION OF KIYOHARU INOUE, vol. 53, no. 5, 2004, pages 1807 - 1811 |
| See also references of EP1870413A4 * |
Cited By (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2008133297A1 (ja) | 2007-04-24 | 2008-11-06 | Toray Industries, Inc. | ジスキネジアの治療または予防剤 |
| US8183256B2 (en) | 2007-06-22 | 2012-05-22 | Toray Industries, Inc. | Remedy or preventive for integration dysfunction syndrome |
| WO2009044883A1 (ja) | 2007-10-05 | 2009-04-09 | Toray Industries, Inc. | モルヒナン誘導体またはその薬理学的に許容される酸付加塩を有効成分とする皮膚性状改善治療薬 |
| EP2196206A1 (en) * | 2007-10-05 | 2010-06-16 | Toray Industries, Inc. | Remedy for relieving skin troubles comprising morphinan derivative or pharmacologically acceptable acid addition salt thereof as the active ingredient |
| EP2196206A4 (en) * | 2007-10-05 | 2010-09-22 | Toray Industries | MEDICAMENT FOR TREATING SKIN PROBLEMS WITH A MORPHINE DERIVATIVE OR PHARMACOLOGICALLY COMPATIBLE ACIDIC ACID SALT AS AN ACTIVE SUBSTANCE |
| AU2008308005B2 (en) * | 2007-10-05 | 2012-06-07 | Toray Industries, Inc. | Remedy for relieving skin troubles comprising morphinan derivative or pharmacologically acceptable acid addition salt thereof as the active ingredient |
| KR101173509B1 (ko) | 2007-10-05 | 2012-08-14 | 도레이 카부시키가이샤 | 모르피난 유도체 또는 그 약리학적으로 허용되는 산부가염을 유효 성분으로 하는 피부 성상 개선 치료약 |
| JP5613417B2 (ja) * | 2007-10-05 | 2014-10-22 | 東レ株式会社 | モルヒナン誘導体またはその薬理学的に許容される酸付加塩を有効成分とする皮膚性状改善治療薬 |
| WO2011093441A1 (ja) | 2010-01-29 | 2011-08-04 | 東レ株式会社 | 胆道疾患の治療又は予防剤 |
| US10131672B2 (en) | 2010-01-29 | 2018-11-20 | Toray Industries, Inc. | Therapeutic or prophylactic agent for biliary diseases |
| WO2012105475A1 (ja) | 2011-01-31 | 2012-08-09 | 東レ株式会社 | 悪液質の治療又は予防剤 |
| US9006262B2 (en) | 2011-01-31 | 2015-04-14 | Toray Industries, Inc. | Therapeutic or prophylactic agent for cachexia |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20070117574A (ko) | 2007-12-12 |
| AU2006221314B2 (en) | 2012-09-06 |
| ES2423004T3 (es) | 2013-09-17 |
| US9051335B2 (en) | 2015-06-09 |
| US20090170888A1 (en) | 2009-07-02 |
| JP5119919B2 (ja) | 2013-01-16 |
| CN101137658A (zh) | 2008-03-05 |
| PT1870413E (pt) | 2013-10-01 |
| EP1870413A1 (en) | 2007-12-26 |
| EP1870413B1 (en) | 2013-07-10 |
| CN101137658B (zh) | 2011-06-08 |
| AU2006221314A1 (en) | 2006-09-14 |
| KR101324539B1 (ko) | 2013-11-01 |
| CA2604071A1 (en) | 2006-09-14 |
| EP1870413A4 (en) | 2009-12-23 |
| PL1870413T3 (pl) | 2013-12-31 |
| CA2604071C (en) | 2013-10-08 |
| JPWO2006095836A1 (ja) | 2008-08-21 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| WO2006095836A1 (ja) | 多発性硬化症に伴う痒みに対する止痒剤 | |
| EP0897726B1 (en) | Antipruritic agent | |
| US6262062B1 (en) | Method of treating the syndrome of coronary heart disease risk factors in humans | |
| KR101732042B1 (ko) | 담도 질환의 치료 또는 예방제 | |
| KR101285645B1 (ko) | 진통제 | |
| KR101477043B1 (ko) | 디스키네시아의 치료 또는 예방제 | |
| JP4453254B2 (ja) | レストレス・レッグズ症候群治療薬 | |
| JP2011074018A (ja) | 線維筋痛症の治療剤又は予防剤 | |
| US8183256B2 (en) | Remedy or preventive for integration dysfunction syndrome | |
| JP2015520145A (ja) | 呼吸抑制の治療 | |
| WO2019100057A1 (en) | Use of morphinans for treating cocaine addiction, pruritis, and seizure disorders | |
| EP1645270A2 (en) | Control of pain with endogenous cannabinoids | |
| JP3007097B2 (ja) | 睡眠薬組成物 | |
| JP2005075747A (ja) | 痒み抑制剤 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WWE | Wipo information: entry into national phase |
Ref document number: 200680007806.7 Country of ref document: CN |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application | ||
| WWE | Wipo information: entry into national phase |
Ref document number: 2007507193 Country of ref document: JP Ref document number: 1020077020357 Country of ref document: KR |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2006221314 Country of ref document: AU Ref document number: 2006715476 Country of ref document: EP Ref document number: 2604071 Country of ref document: CA |
|
| NENP | Non-entry into the national phase |
Ref country code: RU |
|
| ENP | Entry into the national phase |
Ref document number: 2006221314 Country of ref document: AU Date of ref document: 20060309 Kind code of ref document: A |
|
| WWP | Wipo information: published in national office |
Ref document number: 2006221314 Country of ref document: AU |
|
| WWP | Wipo information: published in national office |
Ref document number: 2006715476 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 11885946 Country of ref document: US |