RU2661898C2 - Силансодержащие полимеры с карбоксильными концевыми группами - Google Patents
Силансодержащие полимеры с карбоксильными концевыми группами Download PDFInfo
- Publication number
- RU2661898C2 RU2661898C2 RU2015150052A RU2015150052A RU2661898C2 RU 2661898 C2 RU2661898 C2 RU 2661898C2 RU 2015150052 A RU2015150052 A RU 2015150052A RU 2015150052 A RU2015150052 A RU 2015150052A RU 2661898 C2 RU2661898 C2 RU 2661898C2
- Authority
- RU
- Russia
- Prior art keywords
- polymers
- formula
- copolymers
- mean
- butadiene
- Prior art date
Links
- 229920000642 polymer Polymers 0.000 title claims abstract description 108
- 229910000077 silane Inorganic materials 0.000 title claims abstract description 16
- BLRPTPMANUNPDV-UHFFFAOYSA-N Silane Chemical compound [SiH4] BLRPTPMANUNPDV-UHFFFAOYSA-N 0.000 title claims abstract description 14
- 239000000203 mixture Substances 0.000 claims abstract description 41
- 238000000034 method Methods 0.000 claims abstract description 22
- 229920001577 copolymer Polymers 0.000 claims abstract description 21
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 claims abstract description 18
- 150000001993 dienes Chemical class 0.000 claims abstract description 17
- 125000000217 alkyl group Chemical group 0.000 claims abstract description 16
- 229910052799 carbon Inorganic materials 0.000 claims abstract description 10
- 229910052739 hydrogen Inorganic materials 0.000 claims abstract description 9
- 150000007942 carboxylates Chemical class 0.000 claims abstract description 5
- 229920001971 elastomer Polymers 0.000 claims description 58
- 239000005060 rubber Substances 0.000 claims description 57
- KAKZBPTYRLMSJV-UHFFFAOYSA-N Butadiene Chemical compound C=CC=C KAKZBPTYRLMSJV-UHFFFAOYSA-N 0.000 claims description 28
- PPBRXRYQALVLMV-UHFFFAOYSA-N Styrene Chemical compound C=CC1=CC=CC=C1 PPBRXRYQALVLMV-UHFFFAOYSA-N 0.000 claims description 26
- 125000003118 aryl group Chemical group 0.000 claims description 23
- 229910052710 silicon Inorganic materials 0.000 claims description 23
- 229910052717 sulfur Inorganic materials 0.000 claims description 23
- 150000001875 compounds Chemical class 0.000 claims description 22
- 239000000945 filler Substances 0.000 claims description 19
- RRHGJUQNOFWUDK-UHFFFAOYSA-N Isoprene Chemical compound CC(=C)C=C RRHGJUQNOFWUDK-UHFFFAOYSA-N 0.000 claims description 18
- 238000006116 polymerization reaction Methods 0.000 claims description 17
- 125000005842 heteroatom Chemical group 0.000 claims description 15
- 229910052757 nitrogen Inorganic materials 0.000 claims description 15
- 229910052760 oxygen Inorganic materials 0.000 claims description 15
- 239000000178 monomer Substances 0.000 claims description 12
- 239000003795 chemical substances by application Substances 0.000 claims description 11
- HTDJPCNNEPUOOQ-UHFFFAOYSA-N hexamethylcyclotrisiloxane Chemical compound C[Si]1(C)O[Si](C)(C)O[Si](C)(C)O1 HTDJPCNNEPUOOQ-UHFFFAOYSA-N 0.000 claims description 11
- 239000005062 Polybutadiene Substances 0.000 claims description 10
- 125000002877 alkyl aryl group Chemical group 0.000 claims description 10
- 125000000753 cycloalkyl group Chemical group 0.000 claims description 10
- 229920002857 polybutadiene Polymers 0.000 claims description 10
- 150000004756 silanes Chemical class 0.000 claims description 10
- 125000004429 atom Chemical group 0.000 claims description 9
- 230000009477 glass transition Effects 0.000 claims description 7
- 239000003921 oil Substances 0.000 claims description 7
- 229910052751 metal Inorganic materials 0.000 claims description 6
- 239000002184 metal Substances 0.000 claims description 6
- 229920002554 vinyl polymer Polymers 0.000 claims description 6
- 230000032683 aging Effects 0.000 claims description 5
- 239000003112 inhibitor Substances 0.000 claims description 5
- 229910052719 titanium Inorganic materials 0.000 claims description 5
- XMSXQFUHVRWGNA-UHFFFAOYSA-N Decamethylcyclopentasiloxane Chemical compound C[Si]1(C)O[Si](C)(C)O[Si](C)(C)O[Si](C)(C)O[Si](C)(C)O1 XMSXQFUHVRWGNA-UHFFFAOYSA-N 0.000 claims description 4
- IUMSDRXLFWAGNT-UHFFFAOYSA-N Dodecamethylcyclohexasiloxane Chemical compound C[Si]1(C)O[Si](C)(C)O[Si](C)(C)O[Si](C)(C)O[Si](C)(C)O[Si](C)(C)O1 IUMSDRXLFWAGNT-UHFFFAOYSA-N 0.000 claims description 4
- 229910052779 Neodymium Inorganic materials 0.000 claims description 4
- 238000007334 copolymerization reaction Methods 0.000 claims description 4
- 229910052744 lithium Inorganic materials 0.000 claims description 4
- HMMGMWAXVFQUOA-UHFFFAOYSA-N octamethylcyclotetrasiloxane Chemical compound C[Si]1(C)O[Si](C)(C)O[Si](C)(C)O[Si](C)(C)O1 HMMGMWAXVFQUOA-UHFFFAOYSA-N 0.000 claims description 4
- 229920001195 polyisoprene Polymers 0.000 claims description 4
- 229910052726 zirconium Inorganic materials 0.000 claims description 4
- 229910052791 calcium Inorganic materials 0.000 claims description 3
- 229910052742 iron Inorganic materials 0.000 claims description 3
- 229910052749 magnesium Inorganic materials 0.000 claims description 3
- 229910052750 molybdenum Inorganic materials 0.000 claims description 3
- 229910052700 potassium Inorganic materials 0.000 claims description 3
- 229910052721 tungsten Inorganic materials 0.000 claims description 3
- 229910052720 vanadium Inorganic materials 0.000 claims description 3
- 229910052725 zinc Inorganic materials 0.000 claims description 3
- 229910052708 sodium Inorganic materials 0.000 claims description 2
- 229910052718 tin Inorganic materials 0.000 claims description 2
- 238000004519 manufacturing process Methods 0.000 abstract description 9
- 238000002360 preparation method Methods 0.000 abstract description 7
- 238000005299 abrasion Methods 0.000 abstract description 6
- 239000000126 substance Substances 0.000 abstract description 3
- 230000000694 effects Effects 0.000 abstract description 2
- 229920003048 styrene butadiene rubber Polymers 0.000 description 30
- 238000006243 chemical reaction Methods 0.000 description 17
- -1 alkali metal amides Chemical class 0.000 description 16
- MZRVEZGGRBJDDB-UHFFFAOYSA-N N-Butyllithium Chemical compound [Li]CCCC MZRVEZGGRBJDDB-UHFFFAOYSA-N 0.000 description 14
- 239000000243 solution Substances 0.000 description 13
- 239000006229 carbon black Substances 0.000 description 12
- 238000005096 rolling process Methods 0.000 description 12
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 11
- 239000002904 solvent Substances 0.000 description 11
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 8
- 125000000129 anionic group Chemical group 0.000 description 8
- 230000015572 biosynthetic process Effects 0.000 description 8
- 230000000052 comparative effect Effects 0.000 description 8
- 239000003999 initiator Substances 0.000 description 8
- 235000012239 silicon dioxide Nutrition 0.000 description 8
- 239000011593 sulfur Substances 0.000 description 8
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 6
- 239000000654 additive Substances 0.000 description 6
- 239000003054 catalyst Substances 0.000 description 6
- 125000000524 functional group Chemical group 0.000 description 6
- 238000002156 mixing Methods 0.000 description 6
- 239000004014 plasticizer Substances 0.000 description 6
- 238000003786 synthesis reaction Methods 0.000 description 6
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 6
- 239000002174 Styrene-butadiene Substances 0.000 description 5
- XLOMVQKBTHCTTD-UHFFFAOYSA-N Zinc monoxide Chemical compound [Zn]=O XLOMVQKBTHCTTD-UHFFFAOYSA-N 0.000 description 5
- 125000003545 alkoxy group Chemical group 0.000 description 5
- 238000010539 anionic addition polymerization reaction Methods 0.000 description 5
- 125000003710 aryl alkyl group Chemical group 0.000 description 5
- 238000005859 coupling reaction Methods 0.000 description 5
- SCPYDCQAZCOKTP-UHFFFAOYSA-N silanol Chemical compound [SiH3]O SCPYDCQAZCOKTP-UHFFFAOYSA-N 0.000 description 5
- 125000005624 silicic acid group Chemical class 0.000 description 5
- 239000003153 chemical reaction reagent Substances 0.000 description 4
- 239000012967 coordination catalyst Substances 0.000 description 4
- 238000013016 damping Methods 0.000 description 4
- 229920003244 diene elastomer Polymers 0.000 description 4
- 238000000605 extraction Methods 0.000 description 4
- 238000010528 free radical solution polymerization reaction Methods 0.000 description 4
- BXWNKGSJHAJOGX-UHFFFAOYSA-N hexadecan-1-ol Chemical compound CCCCCCCCCCCCCCCCO BXWNKGSJHAJOGX-UHFFFAOYSA-N 0.000 description 4
- 230000006872 improvement Effects 0.000 description 4
- 230000003993 interaction Effects 0.000 description 4
- GDOPTJXRTPNYNR-UHFFFAOYSA-N methylcyclopentane Chemical compound CC1CCCC1 GDOPTJXRTPNYNR-UHFFFAOYSA-N 0.000 description 4
- 239000012453 solvate Substances 0.000 description 4
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 3
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 3
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 3
- IAYPIBMASNFSPL-UHFFFAOYSA-N Ethylene oxide Chemical compound C1CO1 IAYPIBMASNFSPL-UHFFFAOYSA-N 0.000 description 3
- BPQQTUXANYXVAA-UHFFFAOYSA-N Orthosilicate Chemical compound [O-][Si]([O-])([O-])[O-] BPQQTUXANYXVAA-UHFFFAOYSA-N 0.000 description 3
- RWRDLPDLKQPQOW-UHFFFAOYSA-N Pyrrolidine Chemical compound C1CCNC1 RWRDLPDLKQPQOW-UHFFFAOYSA-N 0.000 description 3
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 3
- 125000005248 alkyl aryloxy group Chemical group 0.000 description 3
- 125000004104 aryloxy group Chemical group 0.000 description 3
- 239000007822 coupling agent Substances 0.000 description 3
- 125000000000 cycloalkoxy group Chemical group 0.000 description 3
- 238000007306 functionalization reaction Methods 0.000 description 3
- 230000007062 hydrolysis Effects 0.000 description 3
- 238000006460 hydrolysis reaction Methods 0.000 description 3
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 3
- 239000000543 intermediate Substances 0.000 description 3
- OFBQJSOFQDEBGM-UHFFFAOYSA-N n-pentane Natural products CCCCC OFBQJSOFQDEBGM-UHFFFAOYSA-N 0.000 description 3
- 230000000269 nucleophilic effect Effects 0.000 description 3
- 150000003254 radicals Chemical class 0.000 description 3
- RMAQACBXLXPBSY-UHFFFAOYSA-N silicic acid Chemical compound O[Si](O)(O)O RMAQACBXLXPBSY-UHFFFAOYSA-N 0.000 description 3
- 238000003860 storage Methods 0.000 description 3
- 239000011787 zinc oxide Substances 0.000 description 3
- 235000014692 zinc oxide Nutrition 0.000 description 3
- 125000006686 (C1-C24) alkyl group Chemical group 0.000 description 2
- MYRTYDVEIRVNKP-UHFFFAOYSA-N 1,2-Divinylbenzene Chemical compound C=CC1=CC=CC=C1C=C MYRTYDVEIRVNKP-UHFFFAOYSA-N 0.000 description 2
- KVNYFPKFSJIPBJ-UHFFFAOYSA-N 1,2-diethylbenzene Chemical compound CCC1=CC=CC=C1CC KVNYFPKFSJIPBJ-UHFFFAOYSA-N 0.000 description 2
- QRMPKOFEUHIBNM-UHFFFAOYSA-N 1,4-dimethylcyclohexane Chemical compound CC1CCC(C)CC1 QRMPKOFEUHIBNM-UHFFFAOYSA-N 0.000 description 2
- VXNZUUAINFGPBY-UHFFFAOYSA-N 1-Butene Chemical compound CCC=C VXNZUUAINFGPBY-UHFFFAOYSA-N 0.000 description 2
- GQBYMAJHDVRWAI-UHFFFAOYSA-N 2,2-dimethyl-1,4,2-oxathiasilinan-6-one Chemical compound C[Si]1(C)CSCC(=O)O1 GQBYMAJHDVRWAI-UHFFFAOYSA-N 0.000 description 2
- SDJHPPZKZZWAKF-UHFFFAOYSA-N 2,3-dimethylbuta-1,3-diene Chemical compound CC(=C)C(C)=C SDJHPPZKZZWAKF-UHFFFAOYSA-N 0.000 description 2
- FZLHAQMQWDDWFI-UHFFFAOYSA-N 2-[2-(oxolan-2-yl)propan-2-yl]oxolane Chemical compound C1CCOC1C(C)(C)C1CCCO1 FZLHAQMQWDDWFI-UHFFFAOYSA-N 0.000 description 2
- VVBLNCFGVYUYGU-UHFFFAOYSA-N 4,4'-Bis(dimethylamino)benzophenone Chemical compound C1=CC(N(C)C)=CC=C1C(=O)C1=CC=C(N(C)C)C=C1 VVBLNCFGVYUYGU-UHFFFAOYSA-N 0.000 description 2
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical compound [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 description 2
- RGSFGYAAUTVSQA-UHFFFAOYSA-N Cyclopentane Chemical compound C1CCCC1 RGSFGYAAUTVSQA-UHFFFAOYSA-N 0.000 description 2
- XTHFKEDIFFGKHM-UHFFFAOYSA-N Dimethoxyethane Chemical compound COCCOC XTHFKEDIFFGKHM-UHFFFAOYSA-N 0.000 description 2
- YNQLUTRBYVCPMQ-UHFFFAOYSA-N Ethylbenzene Chemical compound CCC1=CC=CC=C1 YNQLUTRBYVCPMQ-UHFFFAOYSA-N 0.000 description 2
- 244000043261 Hevea brasiliensis Species 0.000 description 2
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 2
- 229920000459 Nitrile rubber Polymers 0.000 description 2
- 239000006057 Non-nutritive feed additive Substances 0.000 description 2
- GOOHAUXETOMSMM-UHFFFAOYSA-N Propylene oxide Chemical compound CC1CO1 GOOHAUXETOMSMM-UHFFFAOYSA-N 0.000 description 2
- 229910002808 Si–O–Si Inorganic materials 0.000 description 2
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 2
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 2
- 150000004703 alkoxides Chemical class 0.000 description 2
- TZCXTZWJZNENPQ-UHFFFAOYSA-L barium sulfate Chemical compound [Ba+2].[O-]S([O-])(=O)=O TZCXTZWJZNENPQ-UHFFFAOYSA-L 0.000 description 2
- 239000011575 calcium Substances 0.000 description 2
- OSGAYBCDTDRGGQ-UHFFFAOYSA-L calcium sulfate Chemical compound [Ca+2].[O-]S([O-])(=O)=O OSGAYBCDTDRGGQ-UHFFFAOYSA-L 0.000 description 2
- 229960000541 cetyl alcohol Drugs 0.000 description 2
- DIOQZVSQGTUSAI-UHFFFAOYSA-N decane Chemical compound CCCCCCCCCC DIOQZVSQGTUSAI-UHFFFAOYSA-N 0.000 description 2
- 238000004821 distillation Methods 0.000 description 2
- IIEWJVIFRVWJOD-UHFFFAOYSA-N ethylcyclohexane Chemical compound CCC1CCCCC1 IIEWJVIFRVWJOD-UHFFFAOYSA-N 0.000 description 2
- 239000011152 fibreglass Substances 0.000 description 2
- 229910052736 halogen Inorganic materials 0.000 description 2
- 150000002367 halogens Chemical class 0.000 description 2
- WGOPGODQLGJZGL-UHFFFAOYSA-N lithium;butane Chemical compound [Li+].CC[CH-]C WGOPGODQLGJZGL-UHFFFAOYSA-N 0.000 description 2
- VCPPTNDHEILJHD-UHFFFAOYSA-N lithium;prop-1-ene Chemical class [Li+].[CH2-]C=C VCPPTNDHEILJHD-UHFFFAOYSA-N 0.000 description 2
- 239000011777 magnesium Substances 0.000 description 2
- 229910044991 metal oxide Inorganic materials 0.000 description 2
- UAEPNZWRGJTJPN-UHFFFAOYSA-N methylcyclohexane Chemical compound CC1CCCCC1 UAEPNZWRGJTJPN-UHFFFAOYSA-N 0.000 description 2
- 229920003052 natural elastomer Polymers 0.000 description 2
- 229920001194 natural rubber Polymers 0.000 description 2
- 229910052759 nickel Inorganic materials 0.000 description 2
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 2
- 150000002900 organolithium compounds Chemical class 0.000 description 2
- 150000002989 phenols Chemical class 0.000 description 2
- 230000021715 photosynthesis, light harvesting Effects 0.000 description 2
- 239000011164 primary particle Substances 0.000 description 2
- ODLMAHJVESYWTB-UHFFFAOYSA-N propylbenzene Chemical compound CCCC1=CC=CC=C1 ODLMAHJVESYWTB-UHFFFAOYSA-N 0.000 description 2
- 150000003335 secondary amines Chemical class 0.000 description 2
- 125000005372 silanol group Chemical group 0.000 description 2
- 150000004760 silicates Chemical class 0.000 description 2
- 239000010703 silicon Substances 0.000 description 2
- 125000001424 substituent group Chemical group 0.000 description 2
- 229920003051 synthetic elastomer Polymers 0.000 description 2
- 239000005061 synthetic rubber Substances 0.000 description 2
- GETQZCLCWQTVFV-UHFFFAOYSA-N trimethylamine Chemical compound CN(C)C GETQZCLCWQTVFV-UHFFFAOYSA-N 0.000 description 2
- 239000001993 wax Substances 0.000 description 2
- 239000011701 zinc Substances 0.000 description 2
- AHAREKHAZNPPMI-AATRIKPKSA-N (3e)-hexa-1,3-diene Chemical compound CC\C=C\C=C AHAREKHAZNPPMI-AATRIKPKSA-N 0.000 description 1
- PMJHHCWVYXUKFD-SNAWJCMRSA-N (E)-1,3-pentadiene Chemical compound C\C=C\C=C PMJHHCWVYXUKFD-SNAWJCMRSA-N 0.000 description 1
- SSAJVTUSTWLLBY-UHFFFAOYSA-N 1,1-dimethyl-2,1-benzoxasilol-3-one Chemical compound C1=CC=C2[Si](C)(C)OC(=O)C2=C1 SSAJVTUSTWLLBY-UHFFFAOYSA-N 0.000 description 1
- WVAFEFUPWRPQSY-UHFFFAOYSA-N 1,2,3-tris(ethenyl)benzene Chemical compound C=CC1=CC=CC(C=C)=C1C=C WVAFEFUPWRPQSY-UHFFFAOYSA-N 0.000 description 1
- WWOFGTSYQPBRHF-UHFFFAOYSA-N 1,2,4-tris(chloromethyl)benzene Chemical compound ClCC1=CC=C(CCl)C(CCl)=C1 WWOFGTSYQPBRHF-UHFFFAOYSA-N 0.000 description 1
- QLLUAUADIMPKIH-UHFFFAOYSA-N 1,2-bis(ethenyl)naphthalene Chemical compound C1=CC=CC2=C(C=C)C(C=C)=CC=C21 QLLUAUADIMPKIH-UHFFFAOYSA-N 0.000 description 1
- LZDKZFUFMNSQCJ-UHFFFAOYSA-N 1,2-diethoxyethane Chemical compound CCOCCOCC LZDKZFUFMNSQCJ-UHFFFAOYSA-N 0.000 description 1
- OWRCNXZUPFZXOS-UHFFFAOYSA-N 1,3-diphenylguanidine Chemical compound C=1C=CC=CC=1NC(=N)NC1=CC=CC=C1 OWRCNXZUPFZXOS-UHFFFAOYSA-N 0.000 description 1
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 1
- UWFRVQVNYNPBEF-UHFFFAOYSA-N 1-(2,4-dimethylphenyl)propan-1-one Chemical compound CCC(=O)C1=CC=C(C)C=C1C UWFRVQVNYNPBEF-UHFFFAOYSA-N 0.000 description 1
- UYMQPNRUQXPLCY-UHFFFAOYSA-N 1-(2-piperidin-1-ylethyl)piperidine Chemical compound C1CCCCN1CCN1CCCCC1 UYMQPNRUQXPLCY-UHFFFAOYSA-N 0.000 description 1
- HBIXFRSMLXSLQI-UHFFFAOYSA-N 1-(2-pyrrolidin-1-ylethyl)pyrrolidine Chemical compound C1CCCN1CCN1CCCC1 HBIXFRSMLXSLQI-UHFFFAOYSA-N 0.000 description 1
- KZVBBTZJMSWGTK-UHFFFAOYSA-N 1-[2-(2-butoxyethoxy)ethoxy]butane Chemical compound CCCCOCCOCCOCCCC KZVBBTZJMSWGTK-UHFFFAOYSA-N 0.000 description 1
- DURPTKYDGMDSBL-UHFFFAOYSA-N 1-butoxybutane Chemical compound CCCCOCCCC DURPTKYDGMDSBL-UHFFFAOYSA-N 0.000 description 1
- NVZWEEGUWXZOKI-UHFFFAOYSA-N 1-ethenyl-2-methylbenzene Chemical compound CC1=CC=CC=C1C=C NVZWEEGUWXZOKI-UHFFFAOYSA-N 0.000 description 1
- JZHGRUMIRATHIU-UHFFFAOYSA-N 1-ethenyl-3-methylbenzene Chemical compound CC1=CC=CC(C=C)=C1 JZHGRUMIRATHIU-UHFFFAOYSA-N 0.000 description 1
- RRQYJINTUHWNHW-UHFFFAOYSA-N 1-ethoxy-2-(2-ethoxyethoxy)ethane Chemical compound CCOCCOCCOCC RRQYJINTUHWNHW-UHFFFAOYSA-N 0.000 description 1
- QEDJMOONZLUIMC-UHFFFAOYSA-N 1-tert-butyl-4-ethenylbenzene Chemical compound CC(C)(C)C1=CC=C(C=C)C=C1 QEDJMOONZLUIMC-UHFFFAOYSA-N 0.000 description 1
- IGGDKDTUCAWDAN-UHFFFAOYSA-N 1-vinylnaphthalene Chemical compound C1=CC=C2C(C=C)=CC=CC2=C1 IGGDKDTUCAWDAN-UHFFFAOYSA-N 0.000 description 1
- XNMHBTAJRGKASU-UHFFFAOYSA-N 2,2,3,3-tetramethyl-1,4,2-dioxasilinan-6-one Chemical compound CC1(C)OCC(=O)O[Si]1(C)C XNMHBTAJRGKASU-UHFFFAOYSA-N 0.000 description 1
- DOHVHSKVGWOXJJ-UHFFFAOYSA-N 2,2,4,4-tetramethyl-1,2,4-oxadisilinan-6-one Chemical compound C[Si]1(C)CC(=O)O[Si](C)(C)C1 DOHVHSKVGWOXJJ-UHFFFAOYSA-N 0.000 description 1
- PDOFPKHKKSYLQZ-UHFFFAOYSA-N 2,2,4,5-tetramethyloxasilinan-6-one Chemical compound CC1C[Si](C)(C)OC(=O)C1C PDOFPKHKKSYLQZ-UHFFFAOYSA-N 0.000 description 1
- ZWTLIAXFPIFJBR-UHFFFAOYSA-N 2,2,4-trimethyl-1,4,2-oxazasilinan-6-one Chemical compound CN1CC(=O)O[Si](C)(C)C1 ZWTLIAXFPIFJBR-UHFFFAOYSA-N 0.000 description 1
- GGPLWEZGITVTJX-UHFFFAOYSA-N 2,2,4-trimethyl-1,4,2-oxazasilinane Chemical compound CN1CCO[Si](C)(C)C1 GGPLWEZGITVTJX-UHFFFAOYSA-N 0.000 description 1
- NIJAXGHSOVXAHH-UHFFFAOYSA-N 2,2,4-trimethyloxasilinan-6-one Chemical compound CC1CC(=O)O[Si](C)(C)C1 NIJAXGHSOVXAHH-UHFFFAOYSA-N 0.000 description 1
- IUHDPSMXSUADHI-UHFFFAOYSA-N 2,2,5-trimethyl-1,4,2-dioxasilinan-6-one Chemical compound CC1OC[Si](C)(C)OC1=O IUHDPSMXSUADHI-UHFFFAOYSA-N 0.000 description 1
- DXVCVFLSVFVXET-UHFFFAOYSA-N 2,2-diethoxy-4-methyl-1,4,2-oxazasilinan-6-one Chemical compound CCO[Si]1(OCC)CN(C)CC(=O)O1 DXVCVFLSVFVXET-UHFFFAOYSA-N 0.000 description 1
- BQVWMUVEFBAEOD-UHFFFAOYSA-N 2,2-diethoxyoxasilinan-6-one Chemical compound CCO[Si]1(CCCC(=O)O1)OCC BQVWMUVEFBAEOD-UHFFFAOYSA-N 0.000 description 1
- MQCGHVALBKCUIY-UHFFFAOYSA-N 2,2-diethyl-1,4,2-oxathiasilinan-6-one Chemical compound CC[Si]1(CC)CSCC(=O)O1 MQCGHVALBKCUIY-UHFFFAOYSA-N 0.000 description 1
- YRFQUVNVUDZEHM-UHFFFAOYSA-N 2,2-diethyloxasilinan-6-one Chemical compound CC[Si]1(CC)CCCC(=O)O1 YRFQUVNVUDZEHM-UHFFFAOYSA-N 0.000 description 1
- AKDDCUQIBIIUOE-UHFFFAOYSA-N 2,2-dimethyl-1,4,2-oxazasilinan-6-one Chemical compound C[Si]1(C)CNCC(=O)O1 AKDDCUQIBIIUOE-UHFFFAOYSA-N 0.000 description 1
- CZOBZBMNMAQGJR-UHFFFAOYSA-N 2,2-dimethyl-4-phenyloxasilolan-5-one Chemical compound O=C1O[Si](C)(C)CC1C1=CC=CC=C1 CZOBZBMNMAQGJR-UHFFFAOYSA-N 0.000 description 1
- WQJXYQLPILOJSD-UHFFFAOYSA-N 2,2-dimethyl-4-trimethylsilyl-1,4,2-oxazasilinan-6-one Chemical compound C[Si](C)(C)N1CC(=O)O[Si](C)(C)C1 WQJXYQLPILOJSD-UHFFFAOYSA-N 0.000 description 1
- DXYPCCTZWSLOMU-UHFFFAOYSA-N 2,2-dimethyloxasilepan-7-one Chemical compound C[Si]1(C)CCCCC(=O)O1 DXYPCCTZWSLOMU-UHFFFAOYSA-N 0.000 description 1
- SGUUUWRDDYWFOC-UHFFFAOYSA-N 2,2-dimethyloxasilinan-6-one Chemical compound C[Si]1(C)CCCC(=O)O1 SGUUUWRDDYWFOC-UHFFFAOYSA-N 0.000 description 1
- IBRRTCNKNFYOEH-UHFFFAOYSA-N 2,2-dimethyloxasilolan-5-one Chemical compound C[Si]1(C)CCC(=O)O1 IBRRTCNKNFYOEH-UHFFFAOYSA-N 0.000 description 1
- PWRTXQPJKPPNGQ-UHFFFAOYSA-N 2,2-ditert-butyloxasilolan-5-one Chemical compound CC(C)(C)[Si]1(CCC(=O)O1)C(C)(C)C PWRTXQPJKPPNGQ-UHFFFAOYSA-N 0.000 description 1
- SMZOUWXMTYCWNB-UHFFFAOYSA-N 2-(2-methoxy-5-methylphenyl)ethanamine Chemical compound COC1=CC=C(C)C=C1CCN SMZOUWXMTYCWNB-UHFFFAOYSA-N 0.000 description 1
- VUFKMYLDDDNUJS-UHFFFAOYSA-N 2-(ethoxymethyl)oxolane Chemical compound CCOCC1CCCO1 VUFKMYLDDDNUJS-UHFFFAOYSA-N 0.000 description 1
- YCRFDHHKONBVBR-UHFFFAOYSA-N 2-(hexoxymethyl)oxolane Chemical compound CCCCCCOCC1CCCO1 YCRFDHHKONBVBR-UHFFFAOYSA-N 0.000 description 1
- NIXOWILDQLNWCW-UHFFFAOYSA-N 2-Propenoic acid Natural products OC(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 1
- POAOYUHQDCAZBD-UHFFFAOYSA-N 2-butoxyethanol Chemical compound CCCCOCCO POAOYUHQDCAZBD-UHFFFAOYSA-N 0.000 description 1
- KWGJJEBPCVMBIG-UHFFFAOYSA-N 2-methyl-2-[2-[(2-methylpropan-2-yl)oxy]ethoxy]propane Chemical compound CC(C)(C)OCCOC(C)(C)C KWGJJEBPCVMBIG-UHFFFAOYSA-N 0.000 description 1
- RJMRCNBBTPROCR-UHFFFAOYSA-N 2-methyl-2-[2-[2-[(2-methylpropan-2-yl)oxy]ethoxy]ethoxy]propane Chemical compound CC(C)(C)OCCOCCOC(C)(C)C RJMRCNBBTPROCR-UHFFFAOYSA-N 0.000 description 1
- GAODDBNJCKQQDY-UHFFFAOYSA-N 2-methyl-4,6-bis(octylsulfanylmethyl)phenol Chemical compound CCCCCCCCSCC1=CC(C)=C(O)C(CSCCCCCCCC)=C1 GAODDBNJCKQQDY-UHFFFAOYSA-N 0.000 description 1
- RNBTWOBLBLMEQJ-UHFFFAOYSA-N 3,3-dimethyl-4H-2,3-benzoxasilin-1-one Chemical compound C[Si]1(C)Cc2ccccc2C(=O)O1 RNBTWOBLBLMEQJ-UHFFFAOYSA-N 0.000 description 1
- QRQKCMFVJWNKQI-UHFFFAOYSA-N 4-(2-morpholin-4-ylethyl)morpholine Chemical compound C1COCCN1CCN1CCOCC1 QRQKCMFVJWNKQI-UHFFFAOYSA-N 0.000 description 1
- JLBJTVDPSNHSKJ-UHFFFAOYSA-N 4-Methylstyrene Chemical compound CC1=CC=C(C=C)C=C1 JLBJTVDPSNHSKJ-UHFFFAOYSA-N 0.000 description 1
- VXEGSRKPIUDPQT-UHFFFAOYSA-N 4-[4-(4-methoxyphenyl)piperazin-1-yl]aniline Chemical compound C1=CC(OC)=CC=C1N1CCN(C=2C=CC(N)=CC=2)CC1 VXEGSRKPIUDPQT-UHFFFAOYSA-N 0.000 description 1
- 239000005995 Aluminium silicate Substances 0.000 description 1
- 239000004604 Blowing Agent Substances 0.000 description 1
- ZATOFRITFRPYBT-UHFFFAOYSA-N C1=CC=C2C([Li])=CC=CC2=C1 Chemical compound C1=CC=C2C([Li])=CC=CC2=C1 ZATOFRITFRPYBT-UHFFFAOYSA-N 0.000 description 1
- OQIRJAPODYUJRB-UHFFFAOYSA-N CC1CC(=O)O[Si]1(C)C Chemical compound CC1CC(=O)O[Si]1(C)C OQIRJAPODYUJRB-UHFFFAOYSA-N 0.000 description 1
- SFZKQXCVSIPTRO-UHFFFAOYSA-N CC1CC[Si](C)(C)OC1=O Chemical compound CC1CC[Si](C)(C)OC1=O SFZKQXCVSIPTRO-UHFFFAOYSA-N 0.000 description 1
- UCQCETDJODVHKV-UHFFFAOYSA-N CN1CC(=O)O[Si](C)(C1)c1ccccc1 Chemical compound CN1CC(=O)O[Si](C)(C1)c1ccccc1 UCQCETDJODVHKV-UHFFFAOYSA-N 0.000 description 1
- RVEBIOQKPDDWPD-UHFFFAOYSA-N C[Si]1(C)COCC(=O)O1 Chemical compound C[Si]1(C)COCC(=O)O1 RVEBIOQKPDDWPD-UHFFFAOYSA-N 0.000 description 1
- MJKMMLBDIWJLFL-UHFFFAOYSA-N C[Si]1(CC=C)CCC(=O)O1 Chemical compound C[Si]1(CC=C)CCC(=O)O1 MJKMMLBDIWJLFL-UHFFFAOYSA-N 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- 229920002209 Crumb rubber Polymers 0.000 description 1
- ZAFNJMIOTHYJRJ-UHFFFAOYSA-N Diisopropyl ether Chemical compound CC(C)OC(C)C ZAFNJMIOTHYJRJ-UHFFFAOYSA-N 0.000 description 1
- 241001441571 Hiodontidae Species 0.000 description 1
- 238000004566 IR spectroscopy Methods 0.000 description 1
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 1
- WHNWPMSKXPGLAX-UHFFFAOYSA-N N-Vinyl-2-pyrrolidone Chemical compound C=CN1CCCC1=O WHNWPMSKXPGLAX-UHFFFAOYSA-N 0.000 description 1
- ZWXPDGCFMMFNRW-UHFFFAOYSA-N N-methylcaprolactam Chemical compound CN1CCCCCC1=O ZWXPDGCFMMFNRW-UHFFFAOYSA-N 0.000 description 1
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 1
- WVWLMWKKQDYNLP-UHFFFAOYSA-N O=C1CSC[Si](O1)(c1ccccc1)c1ccccc1 Chemical compound O=C1CSC[Si](O1)(c1ccccc1)c1ccccc1 WVWLMWKKQDYNLP-UHFFFAOYSA-N 0.000 description 1
- 239000004793 Polystyrene Substances 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- 229920006978 SSBR Polymers 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 1
- 235000021355 Stearic acid Nutrition 0.000 description 1
- DHXVGJBLRPWPCS-UHFFFAOYSA-N Tetrahydropyran Chemical compound C1CCOCC1 DHXVGJBLRPWPCS-UHFFFAOYSA-N 0.000 description 1
- 229910021627 Tin(IV) chloride Inorganic materials 0.000 description 1
- FMRLDPWIRHBCCC-UHFFFAOYSA-L Zinc carbonate Chemical compound [Zn+2].[O-]C([O-])=O FMRLDPWIRHBCCC-UHFFFAOYSA-L 0.000 description 1
- XZKRXPZXQLARHH-XVNBXDOJSA-N [(1e)-buta-1,3-dienyl]benzene Chemical compound C=C\C=C\C1=CC=CC=C1 XZKRXPZXQLARHH-XVNBXDOJSA-N 0.000 description 1
- AKJDBMXGGIRWMV-UHFFFAOYSA-N [Li]C(C=C)N(Cc1ccccc1)Cc1ccccc1 Chemical compound [Li]C(C=C)N(Cc1ccccc1)Cc1ccccc1 AKJDBMXGGIRWMV-UHFFFAOYSA-N 0.000 description 1
- WEBPKKIECSQIFI-UHFFFAOYSA-N [Li]C(C=C)N(c1ccccc1)c1ccccc1 Chemical compound [Li]C(C=C)N(c1ccccc1)c1ccccc1 WEBPKKIECSQIFI-UHFFFAOYSA-N 0.000 description 1
- OHFYUJRGDSKCNF-UHFFFAOYSA-N [Li]C(C=C)N1CCCC1 Chemical compound [Li]C(C=C)N1CCCC1 OHFYUJRGDSKCNF-UHFFFAOYSA-N 0.000 description 1
- FYOQEFGAZKEPGG-UHFFFAOYSA-N [Li]C1=CC=C(C)C=C1 Chemical compound [Li]C1=CC=C(C)C=C1 FYOQEFGAZKEPGG-UHFFFAOYSA-N 0.000 description 1
- SEVZJBPKDJZGFW-UHFFFAOYSA-N [Li]C1=CC=C(CCCC)C=C1 Chemical compound [Li]C1=CC=C(CCCC)C=C1 SEVZJBPKDJZGFW-UHFFFAOYSA-N 0.000 description 1
- WXZIKFXSSPSWSR-UHFFFAOYSA-N [Li]CCCCC Chemical compound [Li]CCCCC WXZIKFXSSPSWSR-UHFFFAOYSA-N 0.000 description 1
- CPNOVDWZRIYWQV-UHFFFAOYSA-N [Li]CCCCCCCC Chemical compound [Li]CCCCCCCC CPNOVDWZRIYWQV-UHFFFAOYSA-N 0.000 description 1
- SHJXVDAAVHAKFB-UHFFFAOYSA-N [Li]CCCCCCCCCC Chemical compound [Li]CCCCCCCCCC SHJXVDAAVHAKFB-UHFFFAOYSA-N 0.000 description 1
- BZEZSORUWZUMNU-UHFFFAOYSA-N [Li]CCCC[Li] Chemical compound [Li]CCCC[Li] BZEZSORUWZUMNU-UHFFFAOYSA-N 0.000 description 1
- SDENQAIPKIPKCA-UHFFFAOYSA-N [Li]CCCO[Si](C)(C)C(C)(C)C Chemical compound [Li]CCCO[Si](C)(C)C(C)(C)C SDENQAIPKIPKCA-UHFFFAOYSA-N 0.000 description 1
- 239000012190 activator Substances 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 239000003513 alkali Substances 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 229910052915 alkaline earth metal silicate Inorganic materials 0.000 description 1
- 150000001342 alkaline earth metals Chemical class 0.000 description 1
- 150000001336 alkenes Chemical class 0.000 description 1
- 150000005215 alkyl ethers Chemical class 0.000 description 1
- XYLMUPLGERFSHI-UHFFFAOYSA-N alpha-Methylstyrene Chemical compound CC(=C)C1=CC=CC=C1 XYLMUPLGERFSHI-UHFFFAOYSA-N 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- WNROFYMDJYEPJX-UHFFFAOYSA-K aluminium hydroxide Chemical compound [OH-].[OH-].[OH-].[Al+3] WNROFYMDJYEPJX-UHFFFAOYSA-K 0.000 description 1
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 description 1
- 229910000323 aluminium silicate Inorganic materials 0.000 description 1
- 235000012211 aluminium silicate Nutrition 0.000 description 1
- 229920006318 anionic polymer Polymers 0.000 description 1
- 239000000010 aprotic solvent Substances 0.000 description 1
- 150000004982 aromatic amines Chemical class 0.000 description 1
- 150000004945 aromatic hydrocarbons Chemical class 0.000 description 1
- 229910052788 barium Inorganic materials 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- NTXGQCSETZTARF-UHFFFAOYSA-N buta-1,3-diene;prop-2-enenitrile Chemical compound C=CC=C.C=CC#N NTXGQCSETZTARF-UHFFFAOYSA-N 0.000 description 1
- 239000001273 butane Substances 0.000 description 1
- 229910000019 calcium carbonate Inorganic materials 0.000 description 1
- BRPQOXSCLDDYGP-UHFFFAOYSA-N calcium oxide Chemical compound [O-2].[Ca+2] BRPQOXSCLDDYGP-UHFFFAOYSA-N 0.000 description 1
- 239000000292 calcium oxide Substances 0.000 description 1
- ODINCKMPIJJUCX-UHFFFAOYSA-N calcium oxide Inorganic materials [Ca]=O ODINCKMPIJJUCX-UHFFFAOYSA-N 0.000 description 1
- 239000000378 calcium silicate Substances 0.000 description 1
- 229910052918 calcium silicate Inorganic materials 0.000 description 1
- OYACROKNLOSFPA-UHFFFAOYSA-N calcium;dioxido(oxo)silane Chemical compound [Ca+2].[O-][Si]([O-])=O OYACROKNLOSFPA-UHFFFAOYSA-N 0.000 description 1
- 150000001721 carbon Chemical group 0.000 description 1
- 150000004649 carbonic acid derivatives Chemical class 0.000 description 1
- 150000001735 carboxylic acids Chemical class 0.000 description 1
- 229910052804 chromium Inorganic materials 0.000 description 1
- 238000003776 cleavage reaction Methods 0.000 description 1
- 238000013329 compounding Methods 0.000 description 1
- 238000012718 coordination polymerization Methods 0.000 description 1
- 239000003431 cross linking reagent Substances 0.000 description 1
- LEKSIJZGSFETSJ-UHFFFAOYSA-N cyclohexane;lithium Chemical compound [Li]C1CCCCC1 LEKSIJZGSFETSJ-UHFFFAOYSA-N 0.000 description 1
- 230000006378 damage Effects 0.000 description 1
- 230000000593 degrading effect Effects 0.000 description 1
- GUJOJGAPFQRJSV-UHFFFAOYSA-N dialuminum;dioxosilane;oxygen(2-);hydrate Chemical compound O.[O-2].[O-2].[O-2].[Al+3].[Al+3].O=[Si]=O.O=[Si]=O.O=[Si]=O.O=[Si]=O GUJOJGAPFQRJSV-UHFFFAOYSA-N 0.000 description 1
- RJGHQTVXGKYATR-UHFFFAOYSA-L dibutyl(dichloro)stannane Chemical compound CCCC[Sn](Cl)(Cl)CCCC RJGHQTVXGKYATR-UHFFFAOYSA-L 0.000 description 1
- VILAVOFMIJHSJA-UHFFFAOYSA-N dicarbon monoxide Chemical group [C]=C=O VILAVOFMIJHSJA-UHFFFAOYSA-N 0.000 description 1
- 229940019778 diethylene glycol diethyl ether Drugs 0.000 description 1
- SBZXBUIDTXKZTM-UHFFFAOYSA-N diglyme Chemical compound COCCOCCOC SBZXBUIDTXKZTM-UHFFFAOYSA-N 0.000 description 1
- SMBQBQBNOXIFSF-UHFFFAOYSA-N dilithium Chemical compound [Li][Li] SMBQBQBNOXIFSF-UHFFFAOYSA-N 0.000 description 1
- HSUGRBWQSSZJOP-RTWAWAEBSA-N diltiazem Chemical compound C1=CC(OC)=CC=C1[C@H]1[C@@H](OC(C)=O)C(=O)N(CCN(C)C)C2=CC=CC=C2S1 HSUGRBWQSSZJOP-RTWAWAEBSA-N 0.000 description 1
- LIKFHECYJZWXFJ-UHFFFAOYSA-N dimethyldichlorosilane Chemical compound C[Si](C)(Cl)Cl LIKFHECYJZWXFJ-UHFFFAOYSA-N 0.000 description 1
- HNPSIPDUKPIQMN-UHFFFAOYSA-N dioxosilane;oxo(oxoalumanyloxy)alumane Chemical compound O=[Si]=O.O=[Al]O[Al]=O HNPSIPDUKPIQMN-UHFFFAOYSA-N 0.000 description 1
- POLCUAVZOMRGSN-UHFFFAOYSA-N dipropyl ether Chemical compound CCCOCCC POLCUAVZOMRGSN-UHFFFAOYSA-N 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- 239000000806 elastomer Substances 0.000 description 1
- 238000010891 electric arc Methods 0.000 description 1
- 239000003974 emollient agent Substances 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 238000007720 emulsion polymerization reaction Methods 0.000 description 1
- 150000002170 ethers Chemical class 0.000 description 1
- BLHLJVCOVBYQQS-UHFFFAOYSA-N ethyllithium Chemical compound [Li]CC BLHLJVCOVBYQQS-UHFFFAOYSA-N 0.000 description 1
- 238000011049 filling Methods 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 239000000446 fuel Substances 0.000 description 1
- 239000000499 gel Substances 0.000 description 1
- 239000012760 heat stabilizer Substances 0.000 description 1
- DMEGYFMYUHOHGS-UHFFFAOYSA-N heptamethylene Natural products C1CCCCCC1 DMEGYFMYUHOHGS-UHFFFAOYSA-N 0.000 description 1
- 229930195733 hydrocarbon Natural products 0.000 description 1
- 150000002430 hydrocarbons Chemical class 0.000 description 1
- 238000011065 in-situ storage Methods 0.000 description 1
- XEEYBQQBJWHFJM-UHFFFAOYSA-N iron Substances [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 1
- NLYAJNPCOHFWQQ-UHFFFAOYSA-N kaolin Chemical compound O.O.O=[Al]O[Si](=O)O[Si](=O)O[Al]=O NLYAJNPCOHFWQQ-UHFFFAOYSA-N 0.000 description 1
- 239000003446 ligand Substances 0.000 description 1
- 239000004611 light stabiliser Substances 0.000 description 1
- RLAWWYSOJDYHDC-BZSNNMDCSA-N lisinopril Chemical compound C([C@H](N[C@@H](CCCCN)C(=O)N1[C@@H](CCC1)C(O)=O)C(O)=O)CC1=CC=CC=C1 RLAWWYSOJDYHDC-BZSNNMDCSA-N 0.000 description 1
- AFRJJFRNGGLMDW-UHFFFAOYSA-N lithium amide Chemical class [Li+].[NH2-] AFRJJFRNGGLMDW-UHFFFAOYSA-N 0.000 description 1
- WYWICELSCKLXFP-UHFFFAOYSA-N lithium;dibenzylazanide Chemical compound [Li+].C=1C=CC=CC=1C[N-]CC1=CC=CC=C1 WYWICELSCKLXFP-UHFFFAOYSA-N 0.000 description 1
- XWWCTWQBCBOOAG-UHFFFAOYSA-N lithium;diphenylazanide Chemical compound [Li+].C=1C=CC=CC=1[N-]C1=CC=CC=C1 XWWCTWQBCBOOAG-UHFFFAOYSA-N 0.000 description 1
- CETVQRFGPOGIQJ-UHFFFAOYSA-N lithium;hexane Chemical compound [Li+].CCCCC[CH2-] CETVQRFGPOGIQJ-UHFFFAOYSA-N 0.000 description 1
- AXSMTZCJJBPZAA-UHFFFAOYSA-N lithium;morpholin-4-ide Chemical compound [Li]N1CCOCC1 AXSMTZCJJBPZAA-UHFFFAOYSA-N 0.000 description 1
- DWNRISLZVCBTRN-UHFFFAOYSA-N lithium;piperidin-1-ide Chemical compound [Li]N1CCCCC1 DWNRISLZVCBTRN-UHFFFAOYSA-N 0.000 description 1
- SZAVVKVUMPLRRS-UHFFFAOYSA-N lithium;propane Chemical compound [Li+].C[CH-]C SZAVVKVUMPLRRS-UHFFFAOYSA-N 0.000 description 1
- FJDQVJUXXNIHNB-UHFFFAOYSA-N lithium;pyrrolidin-1-ide Chemical compound [Li+].C1CC[N-]C1 FJDQVJUXXNIHNB-UHFFFAOYSA-N 0.000 description 1
- ZLNQQNXFFQJAID-UHFFFAOYSA-L magnesium carbonate Chemical compound [Mg+2].[O-]C([O-])=O ZLNQQNXFFQJAID-UHFFFAOYSA-L 0.000 description 1
- 239000001095 magnesium carbonate Substances 0.000 description 1
- 229910000021 magnesium carbonate Inorganic materials 0.000 description 1
- VTHJTEIRLNZDEV-UHFFFAOYSA-L magnesium dihydroxide Chemical compound [OH-].[OH-].[Mg+2] VTHJTEIRLNZDEV-UHFFFAOYSA-L 0.000 description 1
- 239000000347 magnesium hydroxide Substances 0.000 description 1
- 229910001862 magnesium hydroxide Inorganic materials 0.000 description 1
- HCWCAKKEBCNQJP-UHFFFAOYSA-N magnesium orthosilicate Chemical compound [Mg+2].[Mg+2].[O-][Si]([O-])([O-])[O-] HCWCAKKEBCNQJP-UHFFFAOYSA-N 0.000 description 1
- 239000000395 magnesium oxide Substances 0.000 description 1
- CPLXHLVBOLITMK-UHFFFAOYSA-N magnesium oxide Inorganic materials [Mg]=O CPLXHLVBOLITMK-UHFFFAOYSA-N 0.000 description 1
- 239000000391 magnesium silicate Substances 0.000 description 1
- 229910052919 magnesium silicate Inorganic materials 0.000 description 1
- 235000019792 magnesium silicate Nutrition 0.000 description 1
- AXZKOIWUVFPNLO-UHFFFAOYSA-N magnesium;oxygen(2-) Chemical compound [O-2].[Mg+2] AXZKOIWUVFPNLO-UHFFFAOYSA-N 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 229910000000 metal hydroxide Inorganic materials 0.000 description 1
- 150000004706 metal oxides Chemical class 0.000 description 1
- 150000002739 metals Chemical class 0.000 description 1
- 239000005055 methyl trichlorosilane Substances 0.000 description 1
- GYNNXHKOJHMOHS-UHFFFAOYSA-N methyl-cycloheptane Natural products CC1CCCCCC1 GYNNXHKOJHMOHS-UHFFFAOYSA-N 0.000 description 1
- DVSDBMFJEQPWNO-UHFFFAOYSA-N methyllithium Chemical compound C[Li] DVSDBMFJEQPWNO-UHFFFAOYSA-N 0.000 description 1
- JLUFWMXJHAVVNN-UHFFFAOYSA-N methyltrichlorosilane Chemical compound C[Si](Cl)(Cl)Cl JLUFWMXJHAVVNN-UHFFFAOYSA-N 0.000 description 1
- 229910052901 montmorillonite Inorganic materials 0.000 description 1
- IJDNQMDRQITEOD-UHFFFAOYSA-N n-butane Chemical compound CCCC IJDNQMDRQITEOD-UHFFFAOYSA-N 0.000 description 1
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 1
- TVMXDCGIABBOFY-UHFFFAOYSA-N octane Chemical compound CCCCCCCC TVMXDCGIABBOFY-UHFFFAOYSA-N 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 239000000546 pharmaceutical excipient Substances 0.000 description 1
- NHKJPPKXDNZFBJ-UHFFFAOYSA-N phenyllithium Chemical compound [Li]C1=CC=CC=C1 NHKJPPKXDNZFBJ-UHFFFAOYSA-N 0.000 description 1
- AQSJGOWTSHOLKH-UHFFFAOYSA-N phosphite(3-) Chemical class [O-]P([O-])[O-] AQSJGOWTSHOLKH-UHFFFAOYSA-N 0.000 description 1
- 230000000704 physical effect Effects 0.000 description 1
- 239000000049 pigment Substances 0.000 description 1
- PMJHHCWVYXUKFD-UHFFFAOYSA-N piperylene Natural products CC=CC=C PMJHHCWVYXUKFD-UHFFFAOYSA-N 0.000 description 1
- 239000002798 polar solvent Substances 0.000 description 1
- 229920001084 poly(chloroprene) Polymers 0.000 description 1
- 239000003505 polymerization initiator Substances 0.000 description 1
- 229920002223 polystyrene Polymers 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 230000005588 protonation Effects 0.000 description 1
- 239000000376 reactant Substances 0.000 description 1
- 230000035484 reaction time Effects 0.000 description 1
- 230000002441 reversible effect Effects 0.000 description 1
- 238000010058 rubber compounding Methods 0.000 description 1
- 230000007017 scission Effects 0.000 description 1
- 230000035939 shock Effects 0.000 description 1
- 238000007086 side reaction Methods 0.000 description 1
- 239000005049 silicon tetrachloride Substances 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 159000000000 sodium salts Chemical class 0.000 description 1
- 239000004071 soot Substances 0.000 description 1
- 239000008117 stearic acid Substances 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 238000006467 substitution reaction Methods 0.000 description 1
- QAZLUNIWYYOJPC-UHFFFAOYSA-M sulfenamide Chemical compound [Cl-].COC1=C(C)C=[N+]2C3=NC4=CC=C(OC)C=C4N3SCC2=C1C QAZLUNIWYYOJPC-UHFFFAOYSA-M 0.000 description 1
- 229940124530 sulfonamide Drugs 0.000 description 1
- 150000003456 sulfonamides Chemical class 0.000 description 1
- 150000003460 sulfonic acids Chemical class 0.000 description 1
- 150000003467 sulfuric acid derivatives Chemical class 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 150000003512 tertiary amines Chemical group 0.000 description 1
- 125000001302 tertiary amino group Chemical group 0.000 description 1
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 1
- 150000007970 thio esters Chemical class 0.000 description 1
- 150000003568 thioethers Chemical class 0.000 description 1
- KUAZQDVKQLNFPE-UHFFFAOYSA-N thiram Chemical compound CN(C)C(=S)SSC(=S)N(C)C KUAZQDVKQLNFPE-UHFFFAOYSA-N 0.000 description 1
- 229960002447 thiram Drugs 0.000 description 1
- HPGGPRDJHPYFRM-UHFFFAOYSA-J tin(iv) chloride Chemical compound Cl[Sn](Cl)(Cl)Cl HPGGPRDJHPYFRM-UHFFFAOYSA-J 0.000 description 1
- 231100000925 very toxic Toxicity 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Chemical compound O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
- 230000003313 weakening effect Effects 0.000 description 1
- 239000008096 xylene Substances 0.000 description 1
- 239000011667 zinc carbonate Substances 0.000 description 1
- 235000004416 zinc carbonate Nutrition 0.000 description 1
- 229910000010 zinc carbonate Inorganic materials 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F236/00—Copolymers of compounds having one or more unsaturated aliphatic radicals, at least one having two or more carbon-to-carbon double bonds
- C08F236/02—Copolymers of compounds having one or more unsaturated aliphatic radicals, at least one having two or more carbon-to-carbon double bonds the radical having only two carbon-to-carbon double bonds
- C08F236/04—Copolymers of compounds having one or more unsaturated aliphatic radicals, at least one having two or more carbon-to-carbon double bonds the radical having only two carbon-to-carbon double bonds conjugated
- C08F236/10—Copolymers of compounds having one or more unsaturated aliphatic radicals, at least one having two or more carbon-to-carbon double bonds the radical having only two carbon-to-carbon double bonds conjugated with vinyl-aromatic monomers
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B60—VEHICLES IN GENERAL
- B60C—VEHICLE TYRES; TYRE INFLATION; TYRE CHANGING; CONNECTING VALVES TO INFLATABLE ELASTIC BODIES IN GENERAL; DEVICES OR ARRANGEMENTS RELATED TO TYRES
- B60C1/00—Tyres characterised by the chemical composition or the physical arrangement or mixture of the composition
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B60—VEHICLES IN GENERAL
- B60C—VEHICLE TYRES; TYRE INFLATION; TYRE CHANGING; CONNECTING VALVES TO INFLATABLE ELASTIC BODIES IN GENERAL; DEVICES OR ARRANGEMENTS RELATED TO TYRES
- B60C1/00—Tyres characterised by the chemical composition or the physical arrangement or mixture of the composition
- B60C1/0016—Compositions of the tread
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08C—TREATMENT OR CHEMICAL MODIFICATION OF RUBBERS
- C08C19/00—Chemical modification of rubber
- C08C19/25—Incorporating silicon atoms into the molecule
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08C—TREATMENT OR CHEMICAL MODIFICATION OF RUBBERS
- C08C19/00—Chemical modification of rubber
- C08C19/30—Addition of a reagent which reacts with a hetero atom or a group containing hetero atoms of the macromolecule
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08C—TREATMENT OR CHEMICAL MODIFICATION OF RUBBERS
- C08C19/00—Chemical modification of rubber
- C08C19/30—Addition of a reagent which reacts with a hetero atom or a group containing hetero atoms of the macromolecule
- C08C19/34—Addition of a reagent which reacts with a hetero atom or a group containing hetero atoms of the macromolecule reacting with oxygen or oxygen-containing groups
- C08C19/36—Addition of a reagent which reacts with a hetero atom or a group containing hetero atoms of the macromolecule reacting with oxygen or oxygen-containing groups with carboxy radicals
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08C—TREATMENT OR CHEMICAL MODIFICATION OF RUBBERS
- C08C19/00—Chemical modification of rubber
- C08C19/30—Addition of a reagent which reacts with a hetero atom or a group containing hetero atoms of the macromolecule
- C08C19/42—Addition of a reagent which reacts with a hetero atom or a group containing hetero atoms of the macromolecule reacting with metals or metal-containing groups
- C08C19/44—Addition of a reagent which reacts with a hetero atom or a group containing hetero atoms of the macromolecule reacting with metals or metal-containing groups of polymers containing metal atoms exclusively at one or both ends of the skeleton
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F236/00—Copolymers of compounds having one or more unsaturated aliphatic radicals, at least one having two or more carbon-to-carbon double bonds
- C08F236/02—Copolymers of compounds having one or more unsaturated aliphatic radicals, at least one having two or more carbon-to-carbon double bonds the radical having only two carbon-to-carbon double bonds
- C08F236/04—Copolymers of compounds having one or more unsaturated aliphatic radicals, at least one having two or more carbon-to-carbon double bonds the radical having only two carbon-to-carbon double bonds conjugated
- C08F236/06—Butadiene
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G77/00—Macromolecular compounds obtained by reactions forming a linkage containing silicon with or without sulfur, nitrogen, oxygen or carbon in the main chain of the macromolecule
- C08G77/04—Polysiloxanes
- C08G77/045—Polysiloxanes containing less than 25 silicon atoms
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L25/00—Compositions of, homopolymers or copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by an aromatic carbocyclic ring; Compositions of derivatives of such polymers
- C08L25/02—Homopolymers or copolymers of hydrocarbons
- C08L25/04—Homopolymers or copolymers of styrene
- C08L25/08—Copolymers of styrene
- C08L25/10—Copolymers of styrene with conjugated dienes
Landscapes
- Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- General Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Mechanical Engineering (AREA)
- Compositions Of Macromolecular Compounds (AREA)
- Addition Polymer Or Copolymer, Post-Treatments, Or Chemical Modifications (AREA)
- Polyesters Or Polycarbonates (AREA)
- Silicon Polymers (AREA)
Abstract
Изобретение относится к полимерам с функционализованными концевыми группами, их получению и применению. Предложены полимеры с функционализованными концевыми группами, где полимеры являются диеновыми (со)полимерами, имеющими на конце полимерной цепи силансодержащую карбоксильную группу формулы (I), в которой R1, R2 являются одинаковыми или разными алкильными остатками, R3, R4 означают H, A означает двухвалентный органический остаток, который наряду с C и H содержит атом S, где силансодержащая карбоксильная группа связана с цепью полимера через один или несколько двухвалентных структурных элементов, производных от циклосилоксанов. Предложен также полимер, концевые группы которого имеют вид силансодержащих карбоксилатов, способ получения заявленных полимеров, использование в этом способе силолактонов, а также применение указанных полимеров для получения вулканизирующихся композиций, соответствующие композиции, их применение для получения шин и полученные шины. Технический результат – предложенные полимеры позволяют получить шины с улучшенными характеристиками в отношении заноса, имеющие при этом стойкость к истиранию. 8 н. и 9 з.п. ф-лы, 3 табл., 7 пр.
Description
Изобретение относится к полимерам с функционализованными концевыми группами, их получению и применению.
Важными свойствами, желательными для протекторов шины, являются хорошая адгезия на сухой и мокрой поверхности, низкое сопротивление качению, а также высокая стойкость к истиранию. При этом очень сложно улучшить устойчивость шины против заноса без одновременного ухудшения сопротивления качению и стойкости к истиранию. Низкое сопротивление качению важно для низкого расхода топлива, а высокая стойкость к истиранию является решающим фактором для высокого пробега шины.
Сцепление с мокрой дорогой и сопротивление качению протектора шины зависит по большей части от механико-динамических свойств каучуков, которые используются в рецептуре. В целях снижения сопротивления качению для протекторов шин применяются каучуки с высокой эластичностью по отскоку при повышенных температурах (60°C-100°C). С другой стороны, для улучшения сцепления с мокрой дорогой выгодны каучуки с высоким коэффициентом затухания при низких температурах (0-23°C) или низкой эластичностью по отскоку в интервале 0°C-23°C. Чтобы удовлетворить этим комплексным спецификациям, для протектора используют смеси разных каучуков. Обычно применяются смеси одного или нескольких каучуков с относительно высокой температурой стеклования, как бутадиен-стирольный каучук, и одного или нескольких каучуков с относительно низкой температурой стеклования, такие как полибутадиен с высоким содержанием цис-1,4-звеньев или бутадиен-стирольный каучук с низким содержанием стирола и низким содержанием винильных групп или полученный в растворе полибутадиен со средним содержанием 1,4-цис-связей и низким содержанием винильных групп.
Содержащие двойные связи каучуки, полученные анионной полимеризацией в растворе, такие как растворный полибутадиен и растворные бутадиен-стирольные каучуки, облают преимуществами по сравнению с соответствующими эмульсионными каучуками при получении протекторов шин с низким сопротивлением качению. Преимущества заключаются, помимо прочего, в возможности регулирования содержания винильных групп и связанных с этим температуры стеклования и разветвления молекул. Отсюда при практическом применении возникают особые преимущества в отношении сцепления с мокрой дорогой и сопротивления шин качению. Значительный вклад в рассеяние энергии и тем самым в сопротивление качению протектора шины вносят свободные концы полимерных цепей и обратимое образование и деструкция сетки, которую образует использующийся в рецептуре для протектора шины наполнитель (чаще всего кремниевая кислота и/или сажа).
Введение функциональных групп на концы и/или в начало полимерных цепей позволяет физически или химически связать эти концы или начала полимерных цепей с поверхностью наполнителя. В результате ограничивается их подвижность и, тем самым, снижается рассеяние энергии при динамических нагрузках на протектор шины. Одновременно эти функциональные группы улучшают диспергирование наполнителя в протекторе шины, что может привести к ослаблению сетки наполнителя и тем самым может привести к дальнейшему снижению сопротивления качению.
С этой целью было разработано много способов модифицирования концевых групп. Например, в документе EP0180141A1 описано применение 4,4'-бис(диметиламино)бензофенона или N-метилкапролактама в качестве функционализирующих агентов. Из EP0864606A1 известно также применение этиленоксида и N-винилпирролидона. Ряд других возможных функционализирующих агентов приводится в патенте US 4417029. Способы введения функциональных групп в начало полимерной цепи посредством функциональных инициаторов анионной полимеризации описаны, например, в EP0513217A1 и EP0675140A1 (инициаторы с защищенными гидроксильными группами), US 2008/0308204A1 (инициаторы, содержащие тиоэфиры), а также в US5792820, EP0590490A1 и EP0594107A1 (амиды щелочных металлов из вторичных аминов в качестве инициаторов полимеризации).
Карбоксильная группа как высокополярный бидентатный лиганд может особенно хорошо взаимодействовать с поверхностью силикатного наполнителя в каучуковой смеси. Способы введения карбоксильных групп вдоль полимерной цепи растворных диеновых каучуков известны и описаны, например, в заявках DE2653144A1, EP1000971 A1, EP1050545A1, WO2009034001A1. Эти способы не лишены некоторых недостатков, так, например, требуются большие времена реакции, превращение функционализирующих агентов является неполным, и в результате побочных реакций происходят изменения полимерных цепей, такие как разветвление. Кроме того, эти способы не позволяют достичь особо эффективной функционализации концов полимерных цепей.
Описано также (смотри, например, US 3242129) введение карбоксильных групп на концы цепей диеновых каучуков путем реакции анионных концов полимерных цепей с CO2. Недостатком этого способа является то, что полимерный раствор необходимо приводить в контакт с газообразным CO2, что из-за высокой вязкости и обусловленного этим плохого перемешивания оказывается сложным. Кроме того, протекают плохо контролируемые реакции сочетания из-за взаимодействия более одного конца полимерных цепей с атомом углерода CO2. Это сочетание можно предотвратить путем последовательной реакции карбанионных концов полимерной цепи сначала с этиленоксидом или пропиленоксидом и последующей реакции теперь алкоксидных концов цепей с циклическим ангидридом (US 4465809). Но и здесь также имеется тот недостаток, что в высоковязкий раствор каучука необходимо вводить газообразный и к тому же очень токсичный этиленоксид или пропиленоксид. Кроме того, в результате реакции алкоксидных концов цепей с циклическим ангидридом образуются гидролизирующиеся сложноэфирные соединения, которые могут отщепиться при переработке и при позднейшем применении.
В частности, силаны и циклосилоксаны, содержащие в общей сложности по меньшей мере два галогеновых, и/или алкокси-, и/или арилокси-заместителя на кремнии, хорошо подходят для функционализации концевых групп диеновых каучуков, так как один из указанных заместителей на атоме Si легко может быть заменен в быстрой реакции замещения анионным концом цепи диенового полимера, а второй или следующие из вышеуказанных заместителей на Si доступны как функциональные группы, которые, при необходимости после гидролиза, могут взаимодействовать с наполнителем в смеси для протектора шины. Примеры таких силанов можно найти в документах US3244664, US4185042, EP077831 1A1 и US20050203251A1.
Эти силаны содержат, как правило, функциональные группы, которые напрямую соединены с атомом Si или соединены через промежуточное звено и которые могут взаимодействовать с поверхностью силикатного наполнителя в каучуковой смеси. Под такими функциональными группами подразумеваются, как правило, алкокси-группы или галогены прямо на атоме Si, а также заместители третичные амины, которые соединены с Si через промежуточное звено. Недостатками этих силанов являются возможные реакции нескольких анионных концов полимерных цепей на одну молекулу силана, отщепление нежелательных компонентов и соединение с образованием связей Si-O-Si при переработке и хранении. Введение карбоксильных групп с помощью этих силанов не описывается.
В документе WO2012/065908A1 описываются 1-окса-2-силациклоалканы в качестве функционализирующих агентов для введения гидроксильных концевых групп в диеновые полимеры. Эти 1-окса-2-силациклоалканы не имеют недостатков силанов, описанных в предыдущем абзаце, таких как реакция нескольких анионных концов полимерных цепей на молекулу силана, отщепление нежелательных компонентов и соединение с образованием связей Si-O-Si при обработке и хранении. Правда, эти функционализирующие агенты также не позволяют вводить карбоксильные группы на концы полимерных цепей.
Таким образом, стоит задача разработать полимеры с карбоксильными концевыми группами, которые не имеют недостатков уровня техники и которые позволяют, в частности, использовать хорошую химическую активность силанов в отношении концов цепей анионных полимеров.
Для решения этой задачи предлагаются полимеры с функционализованными концевыми группами, которые на конце полимерной цепи имеют силансодержащую карбоксильную группу формулы (I)
в которой
R1, R2 являются одинаковыми или разными и означают H, алкильный, алкокси-, циклоалкильный, циклоалкокси-, арильный, арилокси-, алкарильный, алкарилокси-, аралкильный или аралкокси-остатки, которые могут содержать один или несколько гетероатомов, предпочтительно O, N, S или Si,
R3, R4 являются одинаковыми или разными и означают H, алкильный, циклоалкильный, арильный, алкарильный или аралкильный остатки, которые могут содержать один или несколько гетероатомов, предпочтительно O, N, S или Si,
A означает двухвалентный органический остаток, который наряду с C и H может содержать один или несколько гетероатомов, предпочтительно O, N, S или Si.
Предпочтительно, предлагаемые изобретением полимеры с функционализованными концевыми группами могут являются карбоксилатами с концевыми группами формулы (II):
в которой
R1, R2 являются одинаковыми или разными и означают H, алкильный, алкокси-, циклоалкильный, циклоалкокси-, арильный, арилокси-, алкарильный, алкарилокси-, аралкильный или аралкокси-остатки, которые могут содержать один или несколько гетероатомов, предпочтительно O, N, S или Si,
R3, R4 являются одинаковыми или разными и означают H, алкильный, циклоалкильный, арильный, алкарильный или аралкильный остатки, которые могут содержать один или несколько гетероатомов, предпочтительно O, N, S или Si,
A означает двухвалентный органический остаток, который наряду с C и H может содержать один или несколько гетероатомов, предпочтительно O, N, S или Si,
n означает целое число от 1 до 4,
M означает металл или получеталл с валентностью от 1 до 4, предпочтительно Li, Na, K, Mg, Ca, Zn, Fe, Co, Ni, AI, Nd, Ti, Sn, Si, Zr, V, Mo или W.
Предпочтительными полимерами для получения полимеров с функционализованными концевыми группами согласно изобретению являются диеновые полимеры и сополимеры диенов, полученные сополимеризацией диенов с винилароматическими мономерами.
В качестве диенов предпочтительны 1,3-бутадиен, изопрен, 1,3-пентадиен, 2,3-диметилбутадиен, 1-фенил-1,3-бутадиен и/или 1,3-гексадиен. Особенно предпочтительно использовать 1,3-бутадиен и/или изопрен.
В качестве винилароматических сомономеров можно применять, например, стирол, о-, м- и/или п-метилстирол, п-трет-бутилстирол, α-метилстирол, винилнафталин, дивинилбензол, тривинилбензол и/или дивинилнафталин. Особенно предпочтительно использовать стирол.
Эти полимеры получают предпочтительно анионной полимеризацией в растворе или полимеризацией на координационных катализаторах. Под координационными катализаторами в этой связи следует понимать катализаторы Циглера-Натта или монометаллические каталитические системы. Предпочтительные координационные катализаторы имеют в основе Ni, Co, Ti, Zr, Nd, V, Cr, Mo, W или Fe.
Инициаторы для анионной полимеризации в растворе являются инициаторы на основе щелочных или щелочноземельных металлов, например, метиллитий, этиллитий, изопропиллитий, н-бутиллитий, втор-бутиллитий, пентиллитий, н-гексиллитий, циклогексиллитий, октиллитий, дециллитий, 2-(6-литио-н-гексокси)тетрагидропиран, 3-(трет-бутилдиметилсилокси)-1-пропиллитий, фениллитий, 4-бутилфениллитий, 1-нафтиллитий, п-толуиллитий, а также аллиллитиевые соединения, производные от третичных N-аллиламинов, как [1-(диметиламино)-2-пропенил]литий, [1-[бис(фенилметил)амино]-2-пропенил]литий, [1-(дифениламино)-2-пропенил]литий, [1-(1-пирролидинил)-2-пропенил]литий, литийамиды вторичных аминов, как литийпирролидид, литийпиперидид, литийгексаметиленимид, литий-1-метилимидазолидид, литий-1-метилпиперазид, литийморфолид, литийдициклогексиламид, литийдибензиламид, литийдифениламид. Эти аллиллитиевые соединения и эти литийамиды могут быть получены также in situ реакцией литийорганического соединения с соответствующими третичными N-аллиламинами или с соответствующими вторичными аминами. Кроме того, можно использовать также би- и полифункциональные литийорганические соединения, например, 1,4-дилитиобутан, дилитийпиперазид. Предпочтительно использовать н-бутиллитий и втор-бутиллитий.
Кроме того, можно использовать известные агенты рандомизации и регулирования микроструктуры полимеров, например, следующие простые эфиры: диэтиловый эфир, ди-н-пропиловый эфир, диизопропиловый эфир, ди-н-бутиловый эфир, диметиловый эфир этиленгликоля, диэтиловый эфир этиленгликоля, ди-н-бутиловый эфир этиленгликоля, ди-трет-бутиловый эфир этиленгликоля, диметиловый эфир диэтиленгликоля, диэтиловый эфир диэтиленгликоля, ди-н-бутиловый эфир диэтиленгликоля, ди-трет-бутиловый эфир диэтиленгликоля, 2-(2-этоксиэтокси)-2-метилпропан, диметиловый эфир триэтиленгликоля, тетрагидрофуран, этилтетрагидрофурфуриловый эфир, гексилтетрагидрофурфуриловый эфир, 2,2-бис(2-тетрагидрофурил)пропан, диоксан, триметиламин, триэтиламин, Ν,Ν,Ν',Ν'-тетраметил-этилендиамин, N-метилморфолин, N-этилморфолин, 1,2-дипиперидинoэтан, 1,2-дипирролидиноэтан, 1,2-диморфолинoэтан, а также калиевые и натриевые соли спиртов, фенолов, карбоновых кислот, сульфокислот.
Такие типы растворной полимеризации известны и описаны, например, в работах I. Franta, Elastomers and Rubber Compounding Materials; Elsevier 1989, p. 113-131, Houben-Weyl, Methoden der Organischen Chemie, Thieme Verlag, Stuttgart, 1961, Band XIV/1 Seiten 645-673 или Band E 20 (1987), Seiten 114-134, Seiten 134-153, а также в Comprehensive Polymer Science, Vol. 4, Part II (Pergamon Press Ltd., Oxford 1989), p. 53-108.
Получение предпочтительных диеновых гомо- и сополимеров предпочтительно проводится в растворителе. В качестве растворителя для полимеризации предпочтительно используются инертные апротонные растворители, как, например, парафиновые углеводороды, такие как изомеры бутана, пентана, гексана, гептана, октана, декана, циклопентана, метилциклопентана, циклогексана, метилциклогексана, этилциклогексана или 1,4-диметилциклогексана, или алкены, как 1-бутен, или ароматические углеводороды, как бензол, толуол, этилбензол, ксилол, диэтилбензол или пропилбензол. Эти растворители можно применять по отдельности или в комбинации. Предпочтительны циклогексан, метилциклопентан и н-гексан. Возможно также смешение в полярными растворителями.
Количество растворителя в способе согласно изобретению составляет обычно от 100 до 1000 г, предпочтительно от 200 до 700 г, в расчете на 100 г суммарного количества используемых мономеров. Однако можно также проводить полимеризацию мономеров в отсутствие растворителей.
Полимеризацию можно проводить таким образом, чтобы сначала ввести мономеры и растворитель, а затем инициировать полимеризацию путем добавления инициатора или катализатора. Полимеризацию можно также осуществить способом подпитки, согласно которому реактор полимеризации заполняют путем подачи мономеров и растворителя, причем инициатор или катализатор уже присутствуют или добавляются с мономерами и растворителем. Возможны варианты, такие как сначала наполнение реактора растворителем, затем добавление инициатора или катализатора с последующим добавлением мономеров. Кроме того, полимеризацию можно вести в непрерывном режиме. Во всех случаях возможно добавка дополнительных мономеров и растворителя во время или в конце полимеризации.
Время полимеризации может колебаться в широких пределах, от нескольких минут до нескольких часов. Обычно продолжительность полимеризации составляет от 10 минут до 8 часов, предпочтительно от 20 минут до 4 часов. Она может проводиться как при нормальном давлении, так и при повышенном давлении (от 1 до 10 бар).
Неожиданно было установлено, что благодаря применению одного или нескольких силалактонов в качестве функционализирующих агентов можно получить полимеры с концевыми карбоксильными группами, не имеющие недостатков уровня техники.
Под силалактонами имеются в виду соединения формулы (III)
причем
R1, R2 являются одинаковыми или разными и означают H, алкильный, алкокси-, циклоалкильный, циклоалкокси-, арильный, арилокси-, алкарильный, алкарилокси-, аралкильный или аралкокси-остатки, которые могут содержать один или несколько гетероатомов, предпочтительно O, N, S или Si,
R3, R4 являются одинаковыми или разными и означают H, алкильный, циклоалкильный, арильный, алкарильный или аралкильный остатки, которые могут содержать один или несколько гетероатомов, предпочтительно O, N, S или Si,
A означает двухвалентный органический остаток, который наряду с C и H может содержать один или несколько гетероатомов, предпочтительно O, N, S или Si,
причем предпочтительно:
- R1, R2 являются одинаковыми или разными и означают H, (C1-C24)-алкильный, (C1-C24)-алкокси-, (C3-C24)-циклоалкильный, (C3-C24)-циклоалкокси-, (C6-C24)-арильный, (C6-C24)-арилокси-, (C6-C24)-алкарильный, (C6-C24)-алкарилокси-, (C6-C24)-аралкильный или (C6-C24)-аралкокси-остатки, которые могут содержать один или несколько гетероатомов, предпочтительно O, N, S или Si, и
- R3, R4 являются одинаковыми или разными и означают H, (C1-C24)-алкильный, (C3-C24)-циклоалкильный, (C6-C24)-арильный, (C6-C24)-алкарильный или (C6-C24)-аралкильный остатки, которые могут содержать один или несколько гетероатомов, предпочтительно O, N, S или Si.
Примерами соединений формулы (III) являются:
2,2-диметил-1-окса-2-силациклогексан-6-он (1), 2,2,4-триметил-1-окса-2-силациклогексан-6-он (2), 2,2,5-триметил-1-окса-2-силациклогексан-6-он (3), 2,2,4,5-тетраметил-1-окса-2-силациклогексан-6-он (4), 2,2-диэтил-1-окса-2-силациклогексан-6-он (5), 2,2-диэтокси-1-окса-2-силациклогексан-6-он (6), 2,2-диметил-1,4-диокса-2-силациклогексан-6-он (7), 2,2,5-триметил-1,4-диокса-2-силациклогексан-6-он (8), 2,2,3,3-тетраметил-1,4-диокса-2-силациклогексан-6-он (9), 2,2-диметил-1-окса-4-тиа-2-силациклогексан-6-он (10), 2,2-диэтил-1-окса-4-тиа-2-силациклогексан-6-он (11), 2,2-дифенил-1-окса-4-тиа-2-силациклогексан-6-он (12), 2-метил-2-этенил-1-окса-4-тиа-2-силациклогексан-6-он (13), 2,2,5-триметил-1-окса-4-тиа-2-силациклогексан-6-он (14), 2,2-диметил-1-окса-4-аза-2-силациклогексан-6-он (15), 2,2,4-триметил-1-окса-4-аза-2-силациклогексан-6-он (16), 2,4-диметил-2-фенил-1-окса-4-аза-2-силациклогексан-6-он (17), 2,2-диметил-4-триметилсилил-1-окса-4-аза-2-силациклогексан-6-он (18), 2,2-диэтокси-4-метил-1-окса-4-аза-2-силациклогексан-6-он (19), 2,2,4,4-тетраметил-1-окса-2,4-дисилациклогексан-6-он (20), 3,4-дигидро-3,3-диметил-1H-2,3-бензоксасилин-1-он (21), 2,2-диметил-1-окса-2-силациклопентан-5-он (22), 2,2,3-триметил-1-окса-2-силациклопентан-5-он (23), 2,2-диметил-4-фенил-1-окса-2-силациклопентан-5-он (24), 2,2-ди(трет-бутил)-1-окса-2-силациклопентан-5-он (25), 2-метил-2-(2-пропен-1-ил)-1-окса-2-силациклопентан-5-он (26), 1,1-диметил-2,1-бензоксасилол-3(1H)-он (27), 2,2-диметил-1-окса-2-силациклогептан-7-он (28).
Синтез таких силалактонов описан, например, в работах US 2,635,109; M. Wieber, M. Schmidt, Chemische Berichte 1963, 96 (10), 2822-5; J.M. Wolcott, F.K. Cartledge, Journal of Organic Chemistry 1974, 39 (16), 2420-4; M.P. Sibi, J.W. Christensen, Tetrahedron Letters 1995, 36 (35), 6213-6; T. Linker, M. Maurer, F. Rebien, Tetrahedron Letters 1996, 37 (46), 8363-6; M. Shindo et al., Angewandte Chemie, International Edition 2004, 43 (1), 104-6.
Было установлено, что предлагаемые изобретением полимеры с функционализованными концевыми группами можно получить реакцией реакционно-способных концов полимерных цепей с силалактонами и при необходимости с последующим протонированием образующихся при этом карбоксилатных концевых групп с образованием карбоксильных концевых групп.
Таким образом, применение силалактонов в качестве агентов функционализации для получения предлагаемых изобретением полимеров с функционализованными концевыми группами формулы (I) или (II) также является объектом изобретения.
При реакции полимеров, которые содержат очень химически активные нуклеофильные концы цепей, с соединениями формулы (III), связывание полимерных цепей может происходить не только на атоме Si функционализирующего агента, но дополнительно может возникать также связывание на карбонильном атоме углерода. Это ведет к линейному присоединению полимерных цепей (схема 1). В этом случае имеется смесь полимеров. Полимерами с высокоактивными концами цепей являются, например, диеновые гомо- и сополимеры, которые получены анионной полимеризацией или полимеризацией с координационными катализаторами.
Полимер-: полимерная цепь с реакционно-способным концом
M+: противоион, например, Li+
Схема 1
Такие реакции сочетания в некоторых случаях могут быть желательными, чтобы повысить полидисперсность и тем самым повлиять на реологические свойства полимеров, такие как вязкость по Муни и хладотекучесть. В других случаях может быть выгодным подавить реакцию сочетания, чтобы получить максимально высокое число функционализованных концов полимерных цепей, что должно положительно влиять на механико-динамические свойства вулканизатов, содержащих эти полимеры.
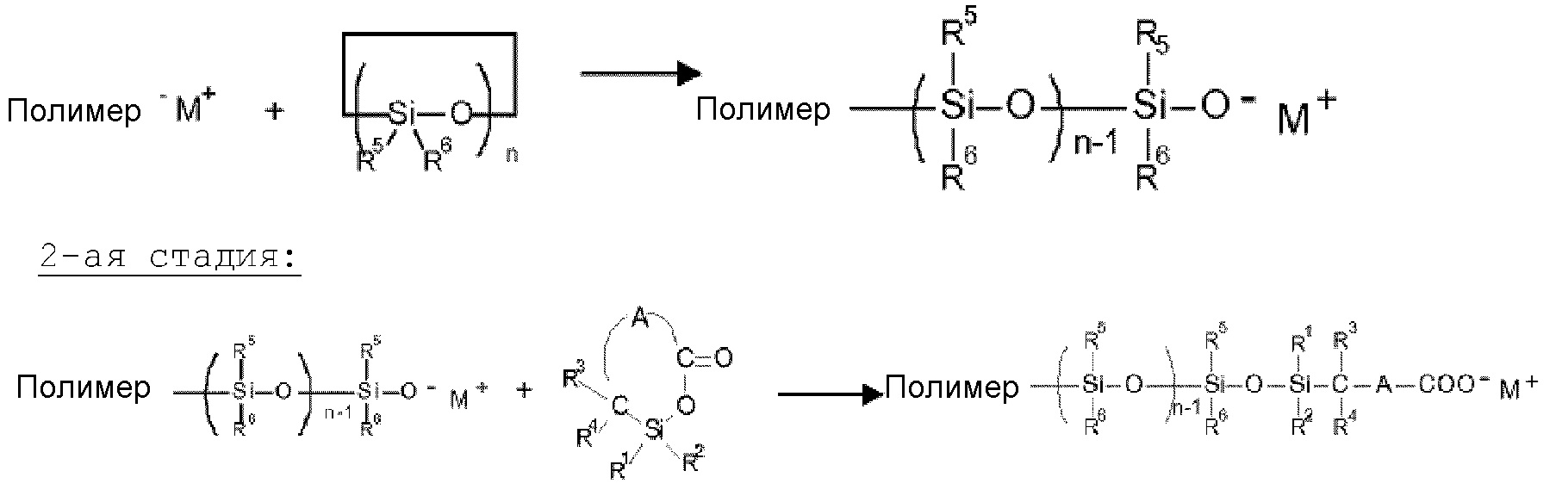
Теперь же неожиданно было обнаружено, что реакцию сочетания согласно схеме 1 можно почти полностью подавить (<5 вес.% от полного количества полимера), если полимерные цепи, содержащие очень химически активные нуклеофильные концы, на первой стадии привести в реакцию с реагентом, который ведет к полимерам с силанольными или силанолятными концевыми группами, а на второй стадии позволить этим полимерам с силанольными или силанолятными концевыми группами реагировать с соединениями формулы (III) (схема 2). Можно также целенаправленно устанавливать желательную степень сочетания, если на первой стадии реакцию реакционно-способных нуклеофильных концов полимерных цепей с реагентом, ведущим к полимерам с силанольными или силанолятными концевыми группами, проводить не до конца.
1-ая стадия:
Схема 2
Реагенты, какие используются на первой стадии, могут привести, напрямую или опосредованно (например, в результате последующего гидролиза групп Si-Cl) к силанольным или силанолятным концевым группам. Однако предпочтительны реагенты, которые дают силанолятные концевые группы в прямой реакции. В высшей степени предпочтительны циклосилоксаны формулы (IV)
причем R5, R6 в схеме 2 и в формуле (IV) являются одинаковыми или разными и означают H, алкильный, циклоалкильный, арильный, алкарильный и аралкильный остатки, которые могут содержать один или несколько гетероатомов, предпочтительно O, N, S или Si.
Предпочтительными являются гексаметилциклотрисилоксан, октаметилциклотетрасилоксан, декаметилциклопентасилоксан и додекаметилциклогексасилоксан, а также смеси циклосилоксанов с разной величиной цикла.
Промежуточные продукты, получаемые согласно схеме 2, можно выделить известными специалисту методами.
Полимеры с функционализованными концевыми группами согласно изобретению предпочтительно имеют средний молекулярный вес (среднечисленный, Mn) от 10000 до 2000000 г/моль, предпочтительно от 100000 до 1000000 г/моль и температуру стеклования от -110°C до +20°C, предпочтительно от -110°C до 0°C, а также вязкость по Муни [ML1+4 (100°C)] от 10 до 200, предпочтительно от 30 до 150 единиц Муни.
Следующим объектом изобретение является способ получения предлагаемых изобретением полимеров с функционализованными концевыми группами, в соответствии с которым одно или несколько соединений формулы (III), в виде чистого вещества, раствора или суспензии, добавляют в полимеры с реакционно-способными концами цепей. Добавление предпочтительно осуществлять по окончании полимеризации, но его можно также осуществить и до достижения полной конверсии мономеров. Реакцию соединений формулы (III) с полимерами с реакционно-способными концами цепей проводят при температурах, обычно применяемых для полимеризации. Продолжительность реакции соединений формулы (III) с реакционно-способными концами полимерных цепей может составлять от нескольких минут до нескольких часов.
Количество этих соединений можно выбирать так, чтобы все реакционно-способные концы полимерных цепей прореагировали с соединениями формулы (III), или эти соединения можно использовать в недостаточном количестве. Количество используемых соединений формулы (III) может варьироваться в широком диапазоне. Предпочтительные количества составляют от 0,005 до 2 вес.%, особенно предпочтительно от 0,01 до 1 вес.%, в расчете на количество полимера.
Следующим объектом изобретения является взаимодействие полимеров с карбанионными концами цепей (полученными в результате анионной или координационной полимеризации) сначала с циклосилоксанами формулы (IV) и на следующей стадии взаимодействие полученных на первой стадии полимеров с силанольными концевыми группами с соединениями формулы (III) с получением полимеров с карбоксилатными концевыми группами. Циклосилоксаны формулы (IV) могут использоваться самостоятельно или как смесь разных циклосилоксанов. Количество циклосилоксанов можно выбирать так, чтобы все реакционно-способные концы полимерных цепей прореагировали с циклосилоксанами формулы (IV), или эти соединения можно использовать в недостаточном количестве. Количества используемых циклосилоксанов формулы (IV) могут варьироваться в широких пределах. Предпочтительные количества составляют от 0,002 до 4 вес.%, особенно предпочтительно от 0,005 до 2 вес.%, в расчете на количество полимера. Количество соединений формулы (III) на следующей стадии в идеале следует выбирать так, чтобы все имеющиеся в известных случаях карбанионные концы полимерных цепей и все концы цепей с силанольными концевыми группами реагировали с соединениями формулы (III). Предпочтительное отношение в смеси силалактона к циклосилоксану составляет от 20:1 до 1:1, особенно предпочтительно это отношение составляет от 10:1 до 1:1, в высшей степени предпочтительно от 3:1 до 1:1.
В дополнение к соединениям формулы (III) и циклосилоксанам формулы (IV) можно также использовать типичные для анионной полимеризации диенов агенты сочетания для реакции с реакционно-способными концами цепей. Примерами таких агентов сочетания являются тетрахлорид кремния, метилтрихлорсилан, диметилдихлорсилан, тетрахлорид олова, хлорид дибутилолова, тетраалкоксисиланы, диглицидиловый эфир этиленгликоля, 1,2,4-трис(хлорметил)бензол. Такие агенты сочетания можно добавлять перед добавлением соединений формулы (III), вместе с ними или после них.
После добавления соединений формулы (III) и при необходимости после реакций сочетания, перед или во время обработки силансодержащих полимеров согласно изобретению с карбоксильными концевыми группами предпочтительно добавляют обычные ингибиторы старения, такие как стерически затрудненные фенолы, ароматические амины, фосфиты, тиоэфиры. Кроме того, можно добавить обычные, использующиеся для диеновых каучуков масла-пластификаторы, такие как масла DAE (Distillate Aromatic Extract = дистиллированный ароматический экстракт), TDAE (Treated Distillate Aromatic Extract = очищенный дистиллированный ароматический экстракт), MES (Mild Extraction Solvates = сольваты мягкой экстракции), RAE (Residual Aromatic Extract = остаточный ароматический экстракт), TRAE (Treated Residual Aromatic Extract = очищенный остаточный ароматический экстракт), нафтеновые и тяжелые нафтеновые масла. Возможна также добавка наполнителей, таких как сажа и кремниевая кислота, каучуков и вспомогательных добавок для каучуков.
Удаление растворителей из процесса полимеризации можно осуществить обычным способом, таким как дистилляция, отгонка водяным паром или приложением вакуума, при необходимости при повышенной температуре.
Следующим объектом изобретения является применение предлагаемых изобретением полимеров с функционализованными концевыми группами для получения вулканизующихся каучуковых композиций.
Эти вулканизующиеся каучуковые композиции предпочтительно включают дополнительные каучуки, наполнители, реагенты для взаимодействия с каучуками, технологические добавки и масла-пластификаторы.
Дополнительными каучуками являются, например, натуральный каучук, а также синтетические каучуки. Если таковые присутствуют, их количество обычно составляет от 0,5 до 95 вес.%, предпочтительно от 10 до 80 вес.% от полного количества полимеров в смеси. Количество дополнительно добавляемых каучуков определяется соответствующим назначением смесей по изобретению. Примерами таких синтетических каучуков являются BR (полибутадиен), сополимеры акриловой кислоты с алкиловым эфиром, IR (полиизопрен), E-SBR (бутадиен-стирольные сополимеры, полученные эмульсионной полимеризацией), S-SBR (бутадиен-стирольные сополимеры, полученные полимеризацией в растворе), IIR (сополимеры изобутилена с изопреном), NBR (сополимеры бутадиена с акрилонитрилом), HNBR (частично или полностью гидрированный NBR-каучук), EPDM (тройные сополимеры этилена, пропилена и диена), а также смеси этих каучуков. Для получения шин для автомобилей представляют интерес, в частности, натуральный каучук, E-SBR, а также S-SBR с температурой стеклования выше -60°C, полибутадиеновый каучук с высоким содержание цис-звеньев (>90%), который был получен с катализаторами на основе Ni, Co, Ti или Nd, а также полибутадиеновый каучук с содержанием винильных групп до 80%, а также их смеси.
В качестве наполнителей для каучуковых композиций согласно изобретению подходят все применяющиеся в резиновой промышленности наполнители. Сюда входят как активные, так и неактивные наполнители.
Можно упомянуть, например:
- высокодисперсные кремниевые кислоты, получаемые, например, осаждением из растворов силикатов или пламенным гидролизом галогенидов кремния, с удельными поверхностями 5-1000, предпочтительно 20-400 м2/г (поверхность по БЭТ) и с размером первичных частиц 10-400 нм. При необходимости кремниевые кислоты могут также находиться в виде смешанных оксидов с оксидами других металлов, как оксиды Al, Mg, Ca, Ba, Zn, Zr, Ti;
- синтетические силикаты, как алюмосиликат, силикат щелочноземельного металла, как силикат магния или силикат кальция, с поверхностями по БЭТ 20-400 м2/г и диаметрами первичных частиц 10-400 нм;
- природные силикаты, как каолин, монтмориллонит и другие кремниевые кислоты природного происхождения;
- стекловолокна и продукты из стекловолокон (маты, прутки) или микростеклошарики;
- оксиды металлов, как оксид цинка, оксид кальция, оксид магния, оксид алюминия;
- карбонаты металлов, как карбонат магния, карбонат кальция, карбонат цинка;
- гидроксиды металлов, как, например, гидроксид алюминия, гидроксид магния;
- сульфаты металлов, как сульфат кальция, сульфат бария;
- сажа: подходящей для применения в настоящем изобретении сажей является сажа, полученная огневым способом, канальным способом, печным способом, газовым способом, термическим способом получения сажи, способом получения ацетиленовой сажи или электродуговым способом, она имеет поверхность по БЭТ 9-200 м2/г, например, сажа SAF, ISAF-LS, ISAF-HM, ISAF-LM, ISAF-HS, CF, SCF, HAF-LS, HAF, HAF-HS, FF-HS, SPF, XCF, FEF-LS, FEF, FEF-HS, GPF-HS, GPF, APF, SRF-LS, SRF-LM, SRF-HS, SRF-HM и MT, например, сажи N110, N219, N220, N231, N234, N242, N294, N326, N327, N330, N332, N339, N347, N351, N356, N358, N375, N472, N539, N550, N568, N650, N660, N754, N762, N765, N774, N787 и N990 согласно ASTM;
- каучуковые гели, в частности, на основе BR, E-SBR и/или полихлоропрена с размером частиц от 5 до 1000 нм.
Предпочтительно, в качестве наполнителей используются высокодисперсные кремниевые кислоты и/или сажа.
Указанные наполнители могут применяться самостоятельно или в смеси. В одном особенно предпочтительном варианте осуществления каучуковые композиции содержат в качестве наполнителей смесь светлых наполнителей, таких как высокодисперсные кремниевые кислоты, и сажи, причем соотношение в смеси между светлыми наполнителями и сажей составляет от 0,01:1 до 50:1, предпочтительно от 0,05:1 до 20:1.
При этом наполнители используются в количестве от 10 до 500 весовых частей на 100 весовых частей каучука. Предпочтительно используются количества в диапазоне от 20 до 200 весовых частей.
В следующем варианте осуществления изобретения каучуковые композиции дополнительно содержат вспомогательные добавки для каучука, которые, например, улучшают технологические свойства каучуковых композиций, служат для сшивки каучуковых композиций, улучшают физические свойства вулканизатов, получаемых из каучуковых композиций согласно изобретению, для их конкретного назначения, улучшают взаимодействие между каучуком и наполнителем или служат для связывания каучука с наполнителем.
Вспомогательные добавки в каучук представляют собой, например, сшивающие агенты, как, например, сера или соединения - доноры серы, а также ускорители реакции, ингибиторы старения, термостабилизаторы, светостабилизаторы, антиозонанты, технологические добавки, пластификаторы, средства для повышения клейкости, порообразователи, красители, пигменты, воски, мягчители, органические кислоты, силаны, замедлители, оксиды металлов, масла-пластификаторы, как, например, масла DAE (Distillate Aromatic Extract = дистиллированный ароматический экстракт), TDAE (Treated Distillate Aromatic Extract = очищенный дистиллированный ароматический экстракт), MES (Mild Extraction Solvates = сольваты мягкой экстракции), RAE (Residual Aromatic Extract = остаточный ароматический экстракт), TRAE (Treated Residual Aromatic Extract = очищенный остаточный ароматический экстракт), нафтеновые и тяжелые нафтеновые масла, а также активаторы.
Полное количество вспомогательных добавок в каучук составляет от 1 до 300 весовых частей в расчете на 100 весовых частей всего каучука. Предпочтительно вспомогательные добавки в каучук используются в количестве от 5 до 150 весовых частей.
Получение вулканизующихся каучуковых композиций можно осуществить одностадийным или многостадийным способом, причем предпочтительны 2-3 ступени смешения. Так, например, добавление серы и ускорителя может происходить на отдельной ступени смешения, например, на валке, при этом предпочтительны температуры в диапазоне от 30°C до 90°C. Добавление серы и ускорителя предпочтительно проводится на последней ступени смешения.
Агрегатами, подходящими для получения вулканизующихся каучуковых композиций, являются, например, валки, пластикаторы, закрытые резиносмесители или смесительные экструдеры.
Таким образом, вулканизующиеся каучуковые композиции, содержащие полимеры с функционализованными концевыми группами формул (I) или (II), являются следующим объектом изобретения.
Следующим объектом изобретения является применение предлагаемых изобретением вулканизующихся каучуковых композиций для получения резины, в частности, для производства шин, в частности, протекторов шин, которые имеют особенно низкое сопротивление качению при высоком сцеплении с мокрой дорогой и высокой стойкостью к истиранию.
Вулканизующиеся каучуковые композиции согласно изобретению подходят также для получения формованных изделий, например, оболочек кабеля, шлангов, приводных ремней, конвейерных лент, покрытий валков, подошв для обуви, уплотнительных колец и амортизирующих элементов.
Следующие примеры служат для пояснения изобретения, однако не имеют при этом ограничительного характера.
Примеры
Пример 1: Синтез нефункционализованного бутадиен-стирольного сополимера (сравнительный пример)
В инертизированный 20-л реактор вводили 8,5 кг гексана, 1185 г 1,3-бутадиена, 315 г стирола, 8,6 ммоль 2,2-бис(2-тетрагидрофурил)пропана, а также 11,3 ммоль бутиллития и содержимое нагревали до 60°C. При перемешивании проводили полимеризацию 25 минут при 60°C. Затем добавляли 11,3 ммоль цетилового спирта для обрыва анионных концов полимерных цепей, сливали раствор каучука, стабилизировали добавлением 3 г Irganox® 1520 (2,4-бис(октилтиометил)-6-метилфенол)) и растворитель удаляли путем отгонки водяным паров. Каучуковую крошку сушили при 65°C в вакууме.
Пример 2: Синтез бутадиен-стирольного сополимера с силанoльными концевыми группами путем реакции с циклосилоксаном (сравнительный пример)
Действовали как в примере 1. Однако вместо цетилового спирта добавляли эквимолярное бутиллитию количество гексаметилциклотрисилоксана (в виде раствора в циклогексане) и затем содержимое реактора грели еще 20 минут при 60°C.
Пример 3: Синтез силансодержащего бутадиен-стирольного сополимера с концевыми карбоксильными группами путем реакции с циклосилоксаном, а затем с силалактоном (согласно изобретению)
Действовали как в примере 2. Через 20 минут после добавления гексаметилциклотрисилоксана дополнительно добавляли эквимолярное бутиллитию и гексаметилциклотрисилоксану количество 2,2-диметил-1-окса-4-тиа-2-силациклогексан-6-она (в виде раствора в толуоле) и грели еще 20 минут при 60°C.
Пример 4: Синтез силансодержащего бутадиен-стирольного сополимера с концевыми карбоксильными группами и с третичной аминогруппой в начале цепи путем реакции с циклосилоксаном, а затем с силалактоном (согласно изобретению)
Действовали как в примере 3. Однако перед добавлением бутиллития добавляли эквимолярное количество пирролидина.
Пример 5: Синтез силансодержащего бутадиен-стирольного сополимера с концевыми гидроксильными группами путем реакции с 1-окса-2-силациклоалканом (сравнительный пример)
Действовали как в примере 2. Однако вместо гексаметилциклотрисилоксана добавляли эквимолярное бутиллитию количество 2,2,4-триметил-1-окса-4-аза-2-силациклогексана (в виде раствора в гексане).
Полимерные свойства бутадиен-стирольных сополимеров из примеров 1-5 сведены в таблице 1. Из таблицы 1 видно, что силансодержащие полимеры с концевыми карбоксильными группами из примеров 3 и 4 согласно изобретению при том же уровне молекулярного веса и полидисперсности, что и полимеры из сравнительных примеров 1, 2 и 5, имеют заметно более высокую вязкость по Муни и заметно более низкие значения хладотекучести. Низкие значения хладотекучести выгодны, так как соответствующие каучуки при хранении имеют меньшую склонность к текучести и, тем самым, лучшую стабильность формы.
Примеры 6 a-e: Каучуковые композиции
Готовили каучуковые композиции для протектора шины, которые содержат бутадиен-стирольные сополимеры из примеров 1-5. Компоненты перечислены в таблице 2. Каучуковые композиции (без серы и ускорителя) получали в 1,5-литровом пластикаторе. Затем на валке при 40°C добавляли компоненты серу и ускоритель.
| Таблица 1 | ||||||||
| Свойства бутадиен-стирольных сополимеров из примеров 1-5 | ||||||||
| SSBR из примера | Функционализирующий агент | Содержание винила a) [вес.%] | Содержание стирола a) [вес.%] | Tg b) [°C] | Mn c) [kг/моль] | Mw/Mn c) | ML1+4 d) [ME] | Хладотекучесть e) [мг/мин] |
| 1 (сравнительный) | - | 51,5 | 20,9 | -23 | 244 | 1,10 | 42 | 21 |
| 2 (сравнительный) | гексаметил-циклотрисилоксан | 50,6 | 21,3 | -24 | 239 | 1,10 | 41 | 21 |
| 3 (согласно изобретению) | 1. гексаметил-циклотрисилоксан 2. силалактон |
50,7 | 21,0 | -24 | 246 | 1,09 | 79 | 0 |
| 4 (согласно изобретению) | 1. гексаметил-циклотрисилоксан 2. силалактон |
49,9 | 21,9 | -24 | 183 | 1,22 | 56 | 9 |
| 5 (сравнительный) | 1-окса-2-силациклоалкан | 50,9 | 21,5 | -23 | 220 | 1,15 | 37 | 25 |
| a) Определение содержаний винильных групп и стирола методом ИК-спектроскопии с Фурье-преобразованием b) Определение температуры стеклования методом ДСК c) Определение молекулярных масс Mn и полидисперсности Mw/Mn методом ГПХ (калибровка по полистиролу) d) Определение вязкости по Муни при 100°C e) Определение хладотекучести при 50°C |
||||||||
| Таблица 2 | |||||
| Компоненты каучуковых композиций для протекторов шин (данные в phr: весовые части на 100 весовых частей каучука) | |||||
| Ср. пример 6a | Ср. пример 6b | Пример 6с по изобретению | Пример 6d по изобретению | Ср. пример 6e | |
| бутадиен-стирольный сополимер из примера 1 | 70 | 0 | 0 | 0 | 0 |
| бутадиен-стирольный сополимер из примера 2 | 0 | 70 | 0 | 0 | 0 |
| бутадиен-стирольный сополимер из примера 3 | 0 | 0 | 70 | 0 | 0 |
| бутадиен-стирольный сополимер из примера 4 | 0 | 0 | 0 | 70 | 0 |
| бутадиен-стирольный сополимер из примера 5 | 0 | 0 | 0 | 0 | 70 |
| полибутадиен с высоким содержанием цис-звеньев (BUNA™ CB 24 от Lanxess Deutschland GmbH) | 30 | 30 | 30 | 30 | 30 |
| кремниевая кислота (Ultrasil® 7000) | 90 | 90 | 90 | 90 | 90 |
| сажа (Vulcan® J/N 375) | 7 | 7 | 7 | 7 | 7 |
| масло TDAE (Vivatec 500) | 36,3 | 36,3 | 36,3 | 36,3 | 36,3 |
| технологическая добавка (Aflux 37) | 3 | 3 | 3 | 3 | 3 |
| стеариновая кислота (Edenor C18 98-100) | 1 | 1 | 1 | 1 | 1 |
| ингибитор старения (Vulkanox® 4020/LG от Lanxess Deutschland GmbH) | 2 | 2 | 2 | 2 | 2 |
| ингибитор старения (Vulkanox® HS/LG от Lanxess Deutschland GmbH) | 2 | 2 | 2 | 2 | 2 |
| оксид цинка (цинковые белила липотон) | 3 | 3 | 3 | 3 | 3 |
| воск (Antilux 654) | 2 | 2 | 2 | 2 | 2 |
| силан (Si 69® от Evonik) | 7,2 | 7,2 | 7,2 | 7,2 | 7,2 |
| дифенилгуанидин (Rhenogran DPG-80) | 2,75 | 2,75 | 2,75 | 2,75 | 2,75 |
| сульфенамид (Vulkacit® NZ/EGC от Lanxess Deutschland GmbH) | 1,6 | 1,6 | 1,6 | 1,6 | 1,6 |
| сера (молотая сера 90/95 Chancel) | 1,6 | 1,6 | 1,6 | 1,6 | 1,6 |
| сульфонамид (Vulkalent® E/C) | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 |
Примеры 7a-e: Свойства вулканизата
Каучуковые композиции для протектора шины из примеров 6a-e согласно таблице 2 вулканизовали 20 минут при 160°C. Свойства соответствующих вулканизатов приведены в таблице 3 как примеры 7a-e. Свойствам вулканизованных образцов из сравнительного примера 7a с нефункционализованным бутадиен-стирольным сополимером был присвоен показатель 100. Все значения выше 100 в таблице 3 означают соответствующее процентное улучшение исследуемого свойства.
| Таблица 3 | |||||
| Свойства вулканизата | |||||
| Ср. пример 7a | Ср. пример 7b | Пример 7с по изобретению | Пример 7d по изобретению | Cр. пример 7e | |
| Бутадиенстирольный сополимер в вулканизате: | |||||
| бутадиен-стирольный сополимер из примера 1 | X | ||||
| бутадиен-стирольный сополимер из примера 2 | X | ||||
| бутадиен-стирольный сополимер из примера 3 | X | ||||
| бутадиен-стирольный сополимер из примера 4 | X | ||||
| бутадиен-стирольный сополимер из примера 5 | X | ||||
| Свойства вулканизата: | |||||
| tgδ при 0°C (динамическое демпфирование при 10 Гц) | 100 | 112 | 125 | 125 | 115 |
| tgδ при 60°C (динамическое демпфирование при 10 Гц) | 100 | 110 | 143 | 145 | 117 |
| tgδ-максимум (MTS-амплитудная модуляция при 1 Гц, 60°C) | 100 | 115 | 134 | 139 | 117 |
| δG* (G*@0,5% - G*@15% из MTS-амплитудной модуляции) [МПа] | 100 | 159 | 254 | 255 | 189 |
| эластичность по отскоку при 60°C [%] | 100 | 113 | 118 | 121 | 114 |
| износ (DIN 53516) [мм3] | 100 | 119 | 135 | 130 | 113 |
Эластичность по отскоку при 60°C, динамическое демпфирование tgδ при 60°C, максимальный tgδ при амплитудной модуляции, а также разность модулей δG* между низким и высоким удлинением в амплитудной модуляции являются индикаторами сопротивления качению шины. Как видно из таблицы 3, вулканизаты из примеров 7c и 7d согласно изобретению отличаются особенно значительным улучшением этих важных для сопротивления качению свойств.
Динамическое демпфирование tgδ при 0°C является индикатором для сцепления шин с мокрой дорогой. Как следует из таблицы 3, вулканизаты из примеров 7c и 7d согласно изобретению отличаются особенно значительным улучшением этих важного для сцепления с мокрой дорогой свойства.
Износ согласно стандарту DIN является показателем прочности на истирание протектора шины. Как видно из таблицы 3, вулканизаты из примеров 7c и 7d согласно изобретению отличаются особенно значительным улучшением этого свойства.
Claims (62)
1. Полимеры с функционализованными концевыми группами, отличающиеся тем, что указанные полимеры на конце полимерной цепи имеют силансодержащую карбоксильную группу формулы (I)
в которой
R1, R2 являются одинаковыми или разными и означают алкильный остаток,
R3, R4 означают H,
A означает двухвалентный органический остаток, который наряду с C и H содержит атом S,
где данная силансодержащая карбоксильная группа связана с цепью полимера через один или несколько двухвалентных структурных элементов формулы (V)
предпочтительно производных от циклосилоксанов, особенно предпочтительно циклосилоксанов формулы (IV)
причем R5, R6 в формуле (IV) являются одинаковыми или различными и означают H, алкильный, циклоалкильный, арильный, алкарильный или аралкильный остатки, которые могут содержать один или несколько гетероатомов, предпочтительно O, N, S или Si, и наиболее предпочтительно представляют собой гексаметилциклотрисилоксан, октаметилциклотетрасилоксан, декаметилциклопентасилоксан или додекаметилциклогексасилоксан, и
где полимеры являются диеновыми полимерами, предпочтительно полибутадиеном или полиизопреном, или диеновыми сополимерами, полученными сополимеризацией диенов с винилароматическими мономерами, предпочтительно сополимерами бутадиена и изопрена, сополимерами бутадиена и стирола, сополимерами изопрена и стирола или тройными сополимерами бутадиена, изопрена и стирола.
2. Полимеры с функционализованными концевыми группами, отличающиеся тем, что концевые группы полимеров имеют вид карбоксилатов формулы (II)
в которой
R1, R2 являются одинаковыми или разными и означают алкильный остаток,
R3, R4 означают H,
A означает двухвалентный органический остаток, который наряду с C и H содержит атом S,
n означает целое число от 1 до 4,
M означает металл или полуметалл с валентностью от 1 до 4, предпочтительно Li, Na, K, Mg, Ca, Zn, Fe, Co, Ni, AI, Nd, Ti, Sn, Si, Zr, V, Mo или W,
где данная силансодержащая карбоксильная группа связана с цепью полимера через один или несколько двухвалентных структурных элементов формулы (V)
предпочтительно производных от циклосилоксанов, особенно предпочтительно циклосилоксанов формулы (IV)
причем R5, R6 в формуле (IV) являются одинаковыми или различными и означают H, алкильный, циклоалкильный, арильный, алкарильный или аралкильный остатки, которые могут содержать один или несколько гетероатомов, предпочтительно O, N, S или Si, и наиболее предпочтительно представляют собой гексаметилциклотрисилоксан, октаметилциклотетрасилоксан, декаметилциклопентасилоксан или додекаметилциклогексасилоксан, и
где полимеры являются диеновыми полимерами, предпочтительно полибутадиеном или полиизопреном, или диеновыми сополимерами, полученными сополимеризацией диенов с винилароматическими мономерами, предпочтительно сополимерами бутадиена и изопрена, сополимерами бутадиена и стирола, сополимерами изопрена и стирола или тройными сополимерами бутадиена, изопрена и стирола.
3. Полимеры с функционализованными концевыми группами по п. 1 или 2, отличающиеся тем, что полимер получен реакцией реакционно-способных концов полимерных цепей с одним или несколькими функционализирующими агентами в виде силалактонов.
4. Полимеры с функционализованными концевыми группами по п. 3, отличающиеся тем, что силалактоны являются соединениями формулы (III)
в которой
R1, R2 являются одинаковыми или разными и означают алкильный остаток,
R3, R4 означают H,
A означает двухвалентный органический остаток, который наряду с C и H содержит атом S.
5. Полимеры с функционализованными концевыми группами по п. 1 или 2, отличающиеся тем, что полимеры имеют средний молекулярный вес (среднечисленный, Mn) от 10000 до 2000000 г/моль, предпочтительно от 100000 до 1000000 г/моль.
6. Полимеры с функционализованными концевыми группами по п. 1 или 2, отличающиеся тем, что полимеры имеют температуру стеклования от -110°C до +20°C, предпочтительно от -110°C до 0°C.
7. Применение силалактонов для получения полимеров с функционализованными концевыми группами по одному из пп. 1-6, где силалактоны являются соединениями формулы (III)
в которой
R1, R2 являются одинаковыми или разными и означают алкильный остаток,
R3, R4 означают H,
A означает двухвалентный органический остаток, который наряду с C и H содержит атом S.
8. Способ получения полимеров с функционализованными концевыми группами по одному из пп. 1-6, отличающийся тем, что к полимерам с реакционно-способными концами полимерных цепей добавляют один или несколько силалактонов, где полимеры являются диеновыми полимерами, предпочтительно полибутадиеном или полиизопреном, или диеновыми сополимерами, полученными сополимеризацией диенов с винилароматическими мономерами, предпочтительно сополимерами бутадиена и изопрена, сополимерами бутадиена и стирола, сополимерами изопрена и стирола или тройными сополимерами бутадиена, изопрена и стирола, и
силалактоны являются соединениями формулы (III)
в которой
R1, R2 означают алкильный остаток,
R3, R4 означают H,
A означает двухвалентный органический остаток, который наряду с C и H содержит атом S,
причем после полимеризации и перед добавлением силалактонов используют циклосилоксаны формулы (IV)
где R5, R6 в формуле (IV) являются одинаковыми или разными и означают H, алкильный, циклоалкильный, арильный, алкарильный или аралкильный остатки, которые могут содержать один или несколько гетероатомов, предпочтительно O, N, S или Si, и предпочтительно используют циклосилоксаны, представляющие собой гексаметилциклотрисилоксан, октаметилциклотетрасилоксан, декаметилциклопентасилоксан или додекаметилциклогексасилоксан.
9. Способ по п. 8, отличающийся тем, что добавление силалактонов проводят по окончании полимеризации.
10. Способ по п. 8 или 9, отличающийся тем, что силалактоны используются в избытке, стехиометрическом количестве или в недостатке по отношению к количеству полимера.
11. Способ по п. 8 или 9, отличающийся тем, что количество силалактонов составляет от 0,005 до 2 вес.%, предпочтительно от 0,01 до 1 вес.% в расчете на количество полимера.
12. Способ по п. 8 или 9, отличающийся тем, что количество циклосилоксанов формулы (IV) лежит в интервале от 0,002 до 4 вес.%, предпочтительно от 0,005 до 2 вес.%, в расчете на количество полимера.
13. Способ по п. 8 или 9, отличающийся тем, что количественное соотношение компонентов силалактона к циклосилоксану составляет от 20:1 до 1:1, предпочтительно от 10:1 до 1:1, особенно предпочтительно от 3:1 до 1:1.
14. Применение полимеров с функционализованными концевыми группами по любому из пп. 1-6 для получения вулканизирующихся каучуковых композиций.
15. Вулканизирующиеся каучуковые композиции, содержащие
a) полимеры с функционализованными концевыми группами по любому из пп. 1-6, а также
b) ингибиторы старения, масла, наполнители, каучуки и/или другие вспомогательные средства для каучука.
16. Применение вулканизирующихся каучуковых композиций по п. 15 для получения шин.
17. Формованные изделия, представляющие собой шины, которые могут быть получены из вулканизирующихся каучуковых композиций по п. 15.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP13165209.1 | 2013-04-24 | ||
| EP13165209.1A EP2796471A1 (de) | 2013-04-24 | 2013-04-24 | Silanhaltige carboxyterminierte Polymere |
| PCT/EP2014/057424 WO2014173706A1 (de) | 2013-04-24 | 2014-04-11 | Silanhaltige carboxyterminierte polymere |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2015150052A RU2015150052A (ru) | 2017-05-29 |
| RU2661898C2 true RU2661898C2 (ru) | 2018-07-23 |
Family
ID=48143213
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2015150052A RU2661898C2 (ru) | 2013-04-24 | 2014-04-11 | Силансодержащие полимеры с карбоксильными концевыми группами |
Country Status (17)
| Country | Link |
|---|---|
| US (1) | US9920149B2 (ru) |
| EP (2) | EP2796471A1 (ru) |
| JP (1) | JP6306688B2 (ru) |
| KR (1) | KR102254257B1 (ru) |
| CN (1) | CN105164163B (ru) |
| BR (1) | BR112015026742B1 (ru) |
| ES (1) | ES2623628T3 (ru) |
| HK (1) | HK1222187A1 (ru) |
| HU (1) | HUE033135T2 (ru) |
| MX (1) | MX365163B (ru) |
| MY (1) | MY179258A (ru) |
| PL (1) | PL2989129T3 (ru) |
| RU (1) | RU2661898C2 (ru) |
| SA (1) | SA515370039B1 (ru) |
| SG (1) | SG11201508109PA (ru) |
| TW (1) | TWI617612B (ru) |
| WO (1) | WO2014173706A1 (ru) |
Families Citing this family (29)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2796485A1 (de) * | 2013-04-24 | 2014-10-29 | LANXESS Deutschland GmbH | Cold Flow reduzierte Polymere mit gutem Verarbeitungsverhalten |
| DE102014111781B4 (de) * | 2013-08-19 | 2022-08-11 | Korea Atomic Energy Research Institute | Verfahren zur elektrochemischen Herstellung einer Silizium-Schicht |
| DE102015210421A1 (de) | 2015-06-08 | 2016-12-08 | Continental Reifen Deutschland Gmbh | Kautschukmischung und Fahrzeugreifen |
| DE102015210424A1 (de) | 2015-06-08 | 2016-12-08 | Continental Reifen Deutschland Gmbh | Kautschukmischung und Fahrzeugreifen |
| WO2018125733A1 (en) | 2016-12-28 | 2018-07-05 | Firestone Polymers, Llc | Methods of making polymers with reduced tack, and rubber compositions incorporating these polymers |
| EP3366709A1 (en) * | 2017-02-24 | 2018-08-29 | ARLANXEO Deutschland GmbH | In-chain phosphine- and phosphonium- containing diene-polymers |
| WO2019129797A1 (en) * | 2017-12-27 | 2019-07-04 | Borealis Ag | Ziegler-natta catalyst and preparation thereof |
| US11753486B2 (en) | 2017-12-28 | 2023-09-12 | Borealis Ag | Catalyst and preparation thereof |
| CN108610457B (zh) * | 2018-05-28 | 2020-11-06 | 青岛科技大学 | 一种含硅高乙烯基聚丁二烯的制备方法 |
| WO2021009154A1 (en) * | 2019-07-16 | 2021-01-21 | Arlanxeo Deutschland Gmbh | Carboxyterminated diene rubbers |
| WO2021186210A1 (en) * | 2020-03-16 | 2021-09-23 | Bridgestone Europe Nv/Sa | Rubber composition, rubber product and tyre |
| US20230098990A1 (en) * | 2020-03-26 | 2023-03-30 | Arlanxeo Deutschland Gmbh | Polydiene rubbers with functionalized end groups |
| US20220033627A1 (en) * | 2020-07-29 | 2022-02-03 | Fina Technology, Inc. | Silane modified styrene butadiene copolymer for high performance in dry adherence, wet adherence and rolling resistance |
| US20230303734A1 (en) | 2020-09-28 | 2023-09-28 | Arlanxeo Deutschland Gmbh | Partially hydrogenated diene polymers |
| EP4122984A1 (en) | 2021-07-22 | 2023-01-25 | Bridgestone Europe NV/SA | Rubber compositions |
| KR20240042433A (ko) | 2021-08-17 | 2024-04-02 | 아란세오 도이치란드 게엠베하 | 관능화된 중합체 |
| CN117897280A (zh) | 2021-08-27 | 2024-04-16 | 阿朗新科德国有限责任公司 | 包含有机酸和用包含羧酸基团的单元官能化的二烯橡胶的稳定聚合物组合物 |
| EP4163331A1 (en) | 2021-10-05 | 2023-04-12 | Bridgestone Corporation | Rubber compounds for use in producing vehicle tires |
| KR20240116707A (ko) | 2021-12-07 | 2024-07-30 | 아란세오 도이치란드 게엠베하 | 불포화된 실록산계 커플링제로 제조된 작용화된 디엔 고무 |
| WO2023152146A1 (en) | 2022-02-11 | 2023-08-17 | Arlanxeo Deutschland Gmbh | Modified diene rubbers |
| CN118696068A (zh) | 2022-04-08 | 2024-09-24 | 阿朗新科德国有限责任公司 | 支化的改性二烯橡胶 |
| WO2023217604A1 (en) | 2022-05-12 | 2023-11-16 | Arlanxeo Deutschland Gmbh | Tire compositions comprising functionalized rubbers based on ethylene-copolymers |
| WO2023227763A1 (en) | 2022-05-27 | 2023-11-30 | Arlanxeo Deutschland Gmbh | Rubber compounds of functionalized conjugated diene rubbers and silica fillers |
| WO2023247719A1 (en) | 2022-06-23 | 2023-12-28 | Arlanxeo Deutschland Gmbh | Alpha-omega-functionalized polymers |
| WO2024132167A1 (en) | 2022-12-22 | 2024-06-27 | Bridgestone Europe Nv/Sa | A tread band for a pneumatic tyre and tyre comprising the same |
| EP4438324A1 (en) | 2023-03-31 | 2024-10-02 | Bridgestone Europe NV/SA | Rubber composition for pneumatic tyre and pneumatic tyre produced therefrom |
| EP4438323A1 (en) | 2023-03-31 | 2024-10-02 | Bridgestone Europe NV/SA | Rubber composition for pneumatic tyre and pneumatic tyre produced therefrom |
| EP4438325A1 (en) | 2023-03-31 | 2024-10-02 | Bridgestone Europe NV/SA | Rubber composition for pneumatic tyre and pneumatic tyre produced therefrom |
| EP4438326A1 (en) | 2023-03-31 | 2024-10-02 | Bridgestone Europe NV/SA | Rubber composition for pneumatic tyre and pneumatic tyre produced therefrom |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SU200158A1 (ru) * | ||||
| US4788313A (en) * | 1983-12-23 | 1988-11-29 | Dow Corning Corporation | Silalactones and methods for their preparation and use |
| RU2299894C2 (ru) * | 2002-05-09 | 2007-05-27 | Родиа Шими | Кремнийорганическое соединение с дикарбоксигруппой и их применение |
Family Cites Families (32)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2635109A (en) | 1949-06-30 | 1953-04-14 | Dow Corning | Production of silalactones |
| US3244664A (en) | 1960-10-24 | 1966-04-05 | Phillips Petroleum Co | Silicon-containing polymers |
| US3242129A (en) | 1963-03-11 | 1966-03-22 | Phillips Petroleum Co | Carboxy terminated polymers as processing aids for polybutadiene |
| US4033731A (en) * | 1973-06-13 | 1977-07-05 | Rhone Poulenc S.A. | Partially crosslinked silalactone polymers, their preparation and their use |
| DE2653144C2 (de) | 1976-11-23 | 1984-12-20 | Bayer Ag, 5090 Leverkusen | Verfahren zur Herstellung von modifiziertem Polybutadien |
| GB1597500A (en) | 1977-12-29 | 1981-09-09 | Shell Int Research | Polymers |
| US4417029A (en) | 1981-08-03 | 1983-11-22 | Atlantic Richfield Company | Derivatization of star-block copolymers |
| US4465809A (en) | 1982-11-05 | 1984-08-14 | Phillips Petroleum Company | Conversion of polymer lithium to polymer carboxylate |
| US4616069A (en) | 1984-10-26 | 1986-10-07 | Nippon Zeon Co., Ltd. | Process for making diene polymer rubbers |
| US4604478A (en) * | 1985-05-17 | 1986-08-05 | Dow Corning Corporation | Method for silalactone preparation and use |
| JPS6210137A (ja) * | 1985-07-09 | 1987-01-19 | Nippon Oil & Fats Co Ltd | 分子の両末端にペルオキシエステル基を有するポリシロキサン化合物 |
| US5665829A (en) | 1990-02-08 | 1997-09-09 | The Secretary Of State For Defence In Her Britannic Majesty's Government Of The United Kingdom Of Gt. Britain & Northern Ireland | Process for the polymerization of olefinic-containing monomers employing anionic initiators |
| GB9002804D0 (en) | 1990-02-08 | 1990-04-04 | Secr Defence | Anionic polymerisation |
| US5332810A (en) | 1992-10-02 | 1994-07-26 | Bridgestone Corporation | Solubilized anionic polymerization initiator and preparation thereof |
| US6025450A (en) | 1992-10-02 | 2000-02-15 | Bridgestone Corporation | Amine containing polymers and products therefrom |
| US5625017A (en) | 1992-10-19 | 1997-04-29 | Bridgestone Corporation | Process for preparing a polymer using lithium initiator prepared by in situ preparation |
| CA2108594C (en) | 1992-10-19 | 2000-10-17 | Koichi Morita | Process for preparing a polymer using lithium initiator prepared by in situ preparation |
| DE4244951C2 (de) * | 1992-12-01 | 1998-08-06 | Minnesota Mining & Mfg | Fasersubstrat mit Wasser-, Öl-, Schmutzabweisungsvermögen und Weichgriffigkeit |
| US5416168A (en) | 1994-03-31 | 1995-05-16 | Shell Oil Company | Protected functional initiators for making terminally functionalized polymers |
| US5496940A (en) | 1995-02-01 | 1996-03-05 | Bridgestone Corporation | Alkyllithium compounds containing cyclic amines and their use in polymerization |
| FR2740778A1 (fr) | 1995-11-07 | 1997-05-09 | Michelin & Cie | Composition de caoutchouc a base de silice et de polymere dienique fonctionalise ayant une fonction silanol terminale |
| JP3622803B2 (ja) | 1995-11-28 | 2005-02-23 | 日本ゼオン株式会社 | ゴム組成物 |
| FR2763074B1 (fr) * | 1997-05-07 | 1999-06-25 | Michelin & Cie | Composition de caoutchouc a base de noir de carbone ayant de la silice fixee a sa surface et de polymere dyenique fonctionalise ou modifie par des fonctions silanols |
| EP1000971B1 (de) | 1998-11-16 | 2003-10-15 | Bayer Aktiengesellschaft | Carboxylgruppen-haltige Lösungskautschuke enthaltende Kautschukmischungen |
| ATE281473T1 (de) | 1999-05-05 | 2004-11-15 | Michelin Soc Tech | Verfahren zur herstellung von polymeren mit mindestens einer doppelbindung und carbonylgruppen entlang der kette |
| EP1479698B1 (en) * | 2003-05-22 | 2008-05-14 | JSR Corporation | Method for producing modified conjugated diene polymer and rubber composition |
| US20050203251A1 (en) | 2004-03-11 | 2005-09-15 | Sumitomo Chemical Company, Limited | Process for producing modified diene polymer rubber |
| US8063165B2 (en) | 2007-06-18 | 2011-11-22 | Bridgestone Corporation | Functional polymers prepared with sulfur-containing initiators |
| DE102007044175A1 (de) * | 2007-09-15 | 2009-03-19 | Lanxess Deutschland Gmbh | Funktionalisierte Hochvinyl-Dienkautschuke |
| EP2452951A1 (de) | 2010-11-16 | 2012-05-16 | LANXESS Deutschland GmbH | Silanhaltige carbinolterminierte Polymere |
| US8962745B2 (en) * | 2010-12-27 | 2015-02-24 | Bridgestone Corporation | Functionalized polymers and vulcanizates with reduced hysteretic loss |
| EP2796485A1 (de) * | 2013-04-24 | 2014-10-29 | LANXESS Deutschland GmbH | Cold Flow reduzierte Polymere mit gutem Verarbeitungsverhalten |
-
2013
- 2013-04-24 EP EP13165209.1A patent/EP2796471A1/de not_active Withdrawn
-
2014
- 2014-04-11 MY MYPI2016703699A patent/MY179258A/en unknown
- 2014-04-11 EP EP14716845.4A patent/EP2989129B1/de active Active
- 2014-04-11 ES ES14716845.4T patent/ES2623628T3/es active Active
- 2014-04-11 WO PCT/EP2014/057424 patent/WO2014173706A1/de active Application Filing
- 2014-04-11 RU RU2015150052A patent/RU2661898C2/ru active
- 2014-04-11 MX MX2015014855A patent/MX365163B/es active IP Right Grant
- 2014-04-11 SG SG11201508109PA patent/SG11201508109PA/en unknown
- 2014-04-11 BR BR112015026742-4A patent/BR112015026742B1/pt not_active IP Right Cessation
- 2014-04-11 KR KR1020157033443A patent/KR102254257B1/ko active IP Right Grant
- 2014-04-11 JP JP2016509375A patent/JP6306688B2/ja active Active
- 2014-04-11 PL PL14716845T patent/PL2989129T3/pl unknown
- 2014-04-11 CN CN201480023457.2A patent/CN105164163B/zh active Active
- 2014-04-11 US US14/786,205 patent/US9920149B2/en active Active
- 2014-04-11 HU HUE14716845A patent/HUE033135T2/en unknown
- 2014-04-22 TW TW103114450A patent/TWI617612B/zh not_active IP Right Cessation
-
2015
- 2015-10-22 SA SA515370039A patent/SA515370039B1/ar unknown
-
2016
- 2016-08-29 HK HK16110245.4A patent/HK1222187A1/zh not_active IP Right Cessation
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SU200158A1 (ru) * | ||||
| US4788313A (en) * | 1983-12-23 | 1988-11-29 | Dow Corning Corporation | Silalactones and methods for their preparation and use |
| RU2299894C2 (ru) * | 2002-05-09 | 2007-05-27 | Родиа Шими | Кремнийорганическое соединение с дикарбоксигруппой и их применение |
Also Published As
| Publication number | Publication date |
|---|---|
| BR112015026742A2 (pt) | 2017-07-25 |
| US20160075809A1 (en) | 2016-03-17 |
| WO2014173706A1 (de) | 2014-10-30 |
| CN105164163B (zh) | 2018-06-08 |
| MX2015014855A (es) | 2016-03-09 |
| MY179258A (en) | 2020-11-03 |
| SG11201508109PA (en) | 2015-11-27 |
| JP2016518492A (ja) | 2016-06-23 |
| MX365163B (es) | 2019-05-16 |
| KR20160018494A (ko) | 2016-02-17 |
| PL2989129T3 (pl) | 2017-08-31 |
| US9920149B2 (en) | 2018-03-20 |
| HK1222187A1 (zh) | 2017-06-23 |
| EP2989129A1 (de) | 2016-03-02 |
| ES2623628T3 (es) | 2017-07-11 |
| EP2989129B1 (de) | 2017-03-01 |
| BR112015026742B1 (pt) | 2020-07-21 |
| CN105164163A (zh) | 2015-12-16 |
| TWI617612B (zh) | 2018-03-11 |
| SA515370039B1 (ar) | 2016-07-31 |
| TW201504322A (zh) | 2015-02-01 |
| RU2015150052A (ru) | 2017-05-29 |
| HUE033135T2 (en) | 2017-11-28 |
| JP6306688B2 (ja) | 2018-04-04 |
| EP2796471A1 (de) | 2014-10-29 |
| KR102254257B1 (ko) | 2021-05-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2661898C2 (ru) | Силансодержащие полимеры с карбоксильными концевыми группами | |
| KR101716539B1 (ko) | 실란을 함유하는 메탄올-말단 중합체 | |
| RU2658908C2 (ru) | Полимеры со сниженной текучестью на холоде с хорошей перерабатываемостью | |
| JP6595699B2 (ja) | 重合開始剤、変性共役ジエン系重合体及びこれらの製造方法 | |
| JP6215310B2 (ja) | アミン含有カルビノール末端ポリマー | |
| JP6321630B2 (ja) | アリルアミン含有カルビノール末端ポリマー | |
| JP7403497B2 (ja) | 変性共役ジエン系重合体、およびそれを含むゴム組成物 | |
| US10421825B2 (en) | Methanol-terminated polymers containing ether | |
| KR102478240B1 (ko) | 변성 공액디엔계 중합체 및 이를 포함하는 고무 조성물 | |
| KR102527753B1 (ko) | 변성 공액디엔계 중합체, 이의 제조방법 및 이를 포함하는 고무 조성물 | |
| KR101716540B1 (ko) | 트리알킬실릴옥시-말단 중합체 | |
| EP3487890A1 (en) | Method for producing modified rubber by anionic solution polymerization, rubber composition comprising said rubber and use thereof |